Настоящая заявка относится к сополимерам изоолефина и мультиолефина и к способам их получения, включающим гидрофторированный олефиновый (HFO) разбавитель.
Бутилкаучук (IIR), статистический сополимер изобутилена и изопрена, хорошо известен за счет своей превосходной термостойкости, озоностойкости и хороших амортизационных характеристик. IIR получают в промышленности суспензионным способом, используя метилхлорид в качестве разбавителя и катализатор Фриделя-Крафта в качестве инициатора полимеризации. Метилхлорид имеет преимущество, заключающееся в том, что AlCl3, относительно недорогой катализатор Фриделя-Крафта, растворим в нем, как и сомономеры изобутилен и изопрен. Кроме того, бутилкаучуковый полимер нерастворим в метилхлориде и осаждается из раствора в виде мелких частиц. Полимеризацию обычно проводят при температурах от приблизительно -90°С до -100°С (смотрите патент США №2356128 и Ullmanns Encyclopedia of Industrial Chemistry, том A 23, 1993, страницы 288-295, полное содержание каждого из документов включено в настоящий документ ссылкой). Низкие температуры полимеризации требуются для получения молекулярных масс, которые достаточно высоки для применений каучука.
В последнее время был сделан упор на поиск альтернативных разбавителей вместо традиционного хлорированного углеводорода, метилхлорида. Гидрофторуглероды (HFC) имеют свойства, аналогичные хлорированным углеводородам, и известны как хладагенты (смотрите WO 2008/027518 и WO 2009/042847). Такие HFC, в частности насыщенные HFC, например, HFC-134a (1,1,1,2-тетрафторэтан), были определены как возможные заменители метилхлорида в процессах полимеризации, в которых используют высокие температуры (см. документы US 7723447, US 7582715, US 7425601, US 7423100, US 7332554, US 7232872, US 7214750, US 7699962, US 2008/0290049, US 7781547, US 7342079, US 2007/0117939, US 2007/0299190, US 2007/0299161, US 2008/0234447, US 2008/0262180, US 7414101, US 7402636 и US 7557170).
Однако, такие насыщенные HFC являются газами, вызывающими сильный парниковый эффект и их использование нежелательно. Наиболее изученным HFC является HFC-134a (1,1,1,2-тетрафторэтан), также известный как R134a, который производился в больших масштабах в качестве хладагента в 1990-е гг. для замены хлорфторуглеродов (CFC) и гидрохлорфторуглеродов (HCFC), которые являются разрушающими озон химическими продуктами. Увеличение использования HFC-134a теперь представляет собой значительную опасность для окружающей среды, поскольку такие HFC, как известно, являются газами, вызывающими сильный парниковый эффект. GWP (потенциал глобального потепления) HFC-134a составляет 1430. Было проведено несколько международных обсуждений в отношении внедрения программы контроля для прекращения производства HFC-134а.
Кроме того, циклические олигомеры образуются в значительных количествах при полимеризации бутилкаучука при использовании в качестве разбавителей или HFC-134a, или метилхлорид, или их смеси. Эти примеси нежелательны для фармацевтических применений, таких как резиновые крышки, из-за вероятности выделения олигомеров из каучука. Кроме того, изопреноидные (с короткоцепочечной разветвленностью) структуры образуются в значительных количествах при полимеризации бутилкаучука с использованием метилхлорида в качестве разбавителя. Изопреноидные структуры ограничивают эффективность последующих реакций галогенирования при получении галогенбутилкаучуков. Кроме того, когда желателен бутилкаучук с высоким содержанием изопрена, традиционные реакции требуют тщательного регулирования условий процесса для увеличения уровней изопрена в бутилкаучуке.
Таким образом, все еще существует необходимость в средах для полимеризации, которые являются относительно недорогими, не вносят значительный вклад в парниковый эффект и/или обеспечивают улучшения процесса полимеризации. Также все еще существует необходимость в бутил-каучуковых полимерах с низкими уровнями циклических олигомеров, низкими уровнями изопреноидных структур и/или высокими уровнями изопрена.
Неожиданно было обнаружено, что конкретный класс HFC, гидрофторированные олефины (HFO), и, в частности, класс HFO, известный как тетрафторированные пропены, являются превосходной средой для процессов получения бутилкаучука суспензионной полимеризацией. Обеспечивается способ получения сополимера, включающий: контакт по меньшей мере одного изоолефинового мономера по меньшей мере с одним мультиолефиновым и/или β-пиненовым мономером в присутствии по меньшей мере одной кислоты Льюиса и по меньшей мере одного инициатора в разбавителе, содержащем тетрафторированный пропен. Также обеспечивается сополимер, полученный способом настоящего изобретения.
Также было неожиданно обнаружено, что смеси HFO и других инертных растворителей в процессах получения бутилкаучука суспензионной полимеризацией дают полимеры с низкими уровнями изопреноидных (с короткоцепочечной разветвленностью) структур. Обеспечивается способ получения сополимера, включающий: контакт по меньшей мере одного изоолефинового мономера по меньшей мере с одним мультиолефиновым и/или β-пиненовым мономером в присутствии по меньшей мере одной кислоты Льюиса и по меньшей мере одного инициатора в разбавителе, содержащем смесь тетрафторированного пропена и инертного растворителя, отличного от тетрафторированного пропена.
Когда в качестве разбавителей используют определенные HFO, эти способы предпочтительно дают полимеры с высокими уровнями мультиолефина, включенного в них. Обеспечивается сополимер по меньшей мере одного изоолефинового мономера и по меньшей мере одного мультиолефинового и/или β-пиненового мономера, имеющий содержание мультиолефинового и/или β-пиненового мономера выше, чем в сопоставимом полимере, полученном в сларри-процессе получения бутилкаучука с использованием 1,1,1,2-тетрафторэтана в качестве разбавителя.
Когда в качестве разбавителей используют определенные HFO, эти способы предпочтительно дают полимеры с низкими уровнями циклических олигомеров и/или полимеры с предпочтительно низкими отношениями С21/С13-олигомеров. Обеспечивается сополимер по меньшей мере одного изоолефинового мономера и по меньшей мере одного мультиолефинового и/или β-пиненового мономера, имеющий содержание циклических олигомеров по меньшей мере на 10% ниже, чем в сопоставимом полимере, полученном в сларри-процессе получения бутилкаучука с использованием 1,1,1,2-тетрафторэтана в качестве разбавителя.
Когда в качестве разбавителей используют определенные HFO, эти способы предпочтительно дают полимеры с низкими уровнями изопреноидных (с короткоцепочечной разветвленностью) структур. Также обеспечивается сополимер по меньшей мере одного изоолефинового мономера и по меньшей мере одного мультиолефинового и/или β-пиненового мономера с содержанием изопреноида ниже, чем в сопоставимом полимере, полученном в сларри-процессе получения бутилкаучука с использованием 1,1,1,2-тетрафторэтана в качестве разбавителя.
Сополимер можно получать согласно способу, включающему: контакт по меньшей мере одного изоолефинового мономера по меньшей мере с одним мультиолефиновым и/или β-пиненовым мономером в присутствии по меньшей мере одной кислоты Льюиса и по меньшей мере одного инициатора в разбавителе. Сополимер можно получать при температуре меньшей или равной -75°С или меньшей или равной -95°С. Разбавитель предпочтительно содержит гидрофторированный олефин (HFO), содержащий по меньшей мере три атома углерода и по меньшей мере три атома фтора. Разбавитель может содержать по меньшей мере три атома углерода и/или по меньшей мере четыре атома фтора. Предпочтительный разбавитель содержит четыре атома фтора. Особенно предпочтительный разбавитель выбран из класса, известного как тетрафторированные пропены, и содержит три атома углерода и четыре атома фтора.
Гидрофторированные олефины, содержащие тетрафторированные пропены, являются лучшими разбавителями для катионной суспензионной полимеризации для получения бутилкаучука, чем насыщенные гидрофторуглероды. Например, HFO-1234yf (2,3,3,3-тетрафтор-1-пропен), как неожиданно было обнаружено, является намного лучшим разбавителем для катионной суспензионной полимеризации для получения бутилкаучука, чем HFC-134a (1,1,1,2-тетрафторэтан), в частности при низкой температуре (например, -95°С), а также при повышенной температуре (например, -75°С). Использование тетрафторированных пропенов (например, HFO-1234yf) в качестве разбавителя обеспечивает одно или более из следующих преимуществ: более высокий выход полимера; более высокое включение мультиолефина; полимерные цепочки с более высокой молекулярной массой; более узкое распределение молекулярной массы; меньше циклических олигомерных побочных продуктов; более предпочтительное отношение С21/С13-циклических олигомеров и/или более низкое содержание изопреноидных (с короткоцепочечной разветвленностью) структур.
Сополимеры могут иметь значительно более низкое содержание изопреноида, чем бутилкаучук, полученный в 1,1,1,2-тетрафторэтане, указывая на сниженную короткоцепочечную разветвленность, получающуюся в результате реакций передачи цепи в полимере при полимеризации. Бутил-каучук с более низким содержанием изопреноида будет иметь большую общую ненасыщенность, доступную в 1,4-конфигурации звеньев для дальнейшей химической модификации, и, как предполагается, будет иметь более высокую эффективность в последующих реакциях галогенирования для получения галогенбутилкаучука. Содержание изопреноидов может составлять менее чем приблизительно 15% в пересчете на общую ненасыщенность, присутствующую в полимере, предпочтительно менее чем приблизительно 12%, более предпочтительно приблизительно 11% или менее, еще более предпочтительно приблизительно 6% или менее. Общую ненасыщенность определяют как сумму мультиолефина (% мол.) и изопреноида (% мол.), где % мол. представлены в пересчете на общее число моль мономерных звеньев в сополимере. Содержание изопреноидов определяют как отношение изопреноида (% мол.) к общей ненасыщенности (% мол.).
Сополимер может иметь содержание циклических олигомеров по меньшей мере на 10% ниже, чем в сопоставимом полимере, полученном в сларри-процессе получения бутилкаучука с использованием 1,1,1,2-тетрафторэтана в качестве разбавителя. Содержание циклических олигомеров может составлять по меньшей мере на 25% меньше, по меньшей мере на 50% меньше, по меньшей мере на 60% меньше, по меньшей мере на 70% меньше или по меньшей мере на 75% меньше, чем в сопоставимом полимере, полученном в сларри-процессе получения бутилкаучука с использованием 1,1,1,2-тетрафторэтана в качестве разбавителя. Отношение С21/С13-олигомеров в сополимере может быть меньше или равняться 2,5, 2,0 или 1,5. Общее содержание циклических олигомеров может составлять менее 3200 ч.н.млн при отношении С21/С13-олигомеров менее 1,5. Эти сополимеры могут иметь содержание циклических олигомеров меньшее или равное 2000 ч.н.млн, меньшее или равное 1000 ч.н.млн, меньшее или равное 700 ч.н.млн или меньшее или равное 650 ч.н.млн.
Сополимер можно растворять в растворителе, подходящем для извлечения С13 циклических олигомерных продуктов. Растворитель можно удалять для отгонки растворителя и С13 циклических олигомерных продуктов из сополимера. Растворитель может быть неполярным и может содержать алкан, такой как гексан. Отгонку можно проводить при повышенной температуре, используя, например, пар в качестве средства для отгонки. Полимер можно заранее растворять в спирте, таком как этанол, перед стадией отгонки. Отношение С21/С13-олигомеров в полимере перед отгонкой может быть меньше или равно 7,9, 7,3, 2,5, 1,5 или 1,0.
Образование циклических олигомеров можно существенно снизить в присутствии гидрофторированных олефинов в качестве разбавителя, в частности при температуре -90°С или ниже (например, -95°С). Содержание олигомеров в полимерах настоящего изобретения может составлять по меньшей мере на 20% меньше, по меньшей мере на 30% меньше, по меньшей мере на 40% меньше, по меньшей мере на 50% меньше, по меньшей мере на 55% меньше, по меньшей мере на 60% меньше, по меньшей мере на 65% меньше, по меньшей мере на 70% меньше, по меньшей мере на 75% меньше, по меньшей мере на 80% меньше, по меньшей мере на 85% меньше, по меньшей мере на 90% меньше и/или на 95% меньше, чем с другими разбавителями, например, HFC-134a и/или метилхлоридом.
Содержание мультиолефинов (например, изопрена) в полимерах настоящего изобретения может находиться в диапазоне от 0,5 до 15% мол. в пересчете на массу полимера. Содержание мультиолефинов в полимерах может составлять на 5-10% больше, чем у полимеров, полученных при помощи разбавителей уровня техники (например, MeCl и/или HFC-134a) при аналогичной температуре и степени превращения. Более высокое содержание мультиолефинов особенно очевидно при сравнении использования HFO-1234yf с HFC-134a, в частности при температуре -75°С или ниже (например, -95°С). Большее включение мультиолефинов соответствует лучшему коэффициенту использования мультиолефина, подразумевая меньшее количество отходов и более низкую общую стоимость процесса. Включение мультиолефина можно сравнивать на основании отношения мономерного состава сырья (f=[M1]/[M2]) к составу сополимера (F=[M1]/[M2]). Отношение мономерного состава сырья к составу сополимера (f/F) в способе настоящего изобретения предпочтительно составляет больше чем приблизительно 0,7, более предпочтительно больше чем приблизительно 0,8, еще более предпочтительно приблизительно 0,85 или больше, еще более предпочтительно приблизительно 0,9 или больше.
Молекулярные массы полимеров настоящего изобретения аналогичны или значительно выше молекулярных масс полимеров, полученных при помощи разбавителей уровня техники (например, MeCl и/или HFC-134a). При более высоких температурах, например, около -75°С, молекулярные массы выше, но при температуре -90°С или ниже (например, -95°С) молекулярные массы полимеров настоящего изобретения, в частности полученных в HFO-1234yf, могут быть значительно выше, чем у полимеров, полученных в разбавителях уровня техники (например, MeCl и/или HFC-134a). Например, при -75°С среднемассовая молекулярная масса (Mw) может быть большей или равной 330000 г/моль или большей или равной 400000 г/моль, а при -95°С молекулярная масса может быть большей или равной 445000 г/моль или большей или равной 475000 г/моль. Это означает, что можно получать сополимер с желаемой молекулярной массой при более высокой температуре с тетрафторированными пропеновыми разбавителями, что приводит к снижению затрат на энергию, улучшению экономики процесса и снижению воздействия на окружающую среду.
Выход полимера, полученного способами настоящего изобретения, может быть, по меньшей мере, сравнимым с выходом, полученным при помощи разбавителей уровня техники (например, MeCl и/или HFC-134a), а в некоторых случаях может быть больше в 1,5 раза или даже в 2 раза. Большие выходы особенно очевидны при сравнении использования HFO-1234yf с HFC-134a, в частности при температуре -90°С или ниже (например, -95°С).
Таким образом, заданную молекулярную массу при использовании тетрафторированных пропеновых разбавителей настоящего изобретения можно получить при более высокой температуре, с более высокой степенью превращения и более эффективным коэффициентом использования изопрена, чем можно получить при помощи разбавителей уровня техники (например, MeCl и/или HFC-134a). Эта неожиданная комбинация предпочтительных признаков приводит к более низким общим стоимостям способа и улучшенным полимерам.
Кроме того, некоторые HFO характеризуются желательными свойствами, но не разрушают озон (озоноразрушающий потенциал, ODP=0), и характеризуются незначительным потенциалом для глобального потепления или не имеют его. Примеры таких более экологически безвредных гидрофторированных олефинов представляют собой тетрафторированные пропены HFO-1234fy (GWP=4) и HFO-1234ze (GWP=6), которые особенно заслуживают внимания в качестве возможных заменителей для HFC-134a (GWP=1430).
Дополнительные признаки настоящего изобретения будут раскрыты или станут очевидными в ходе следующего подробного описания.
Для того, чтобы настоящее изобретение можно было понять более ясно, его варианты осуществления будут теперь подробно описаны посредством примера со ссылкой на сопутствующие графические материалы, на которых:
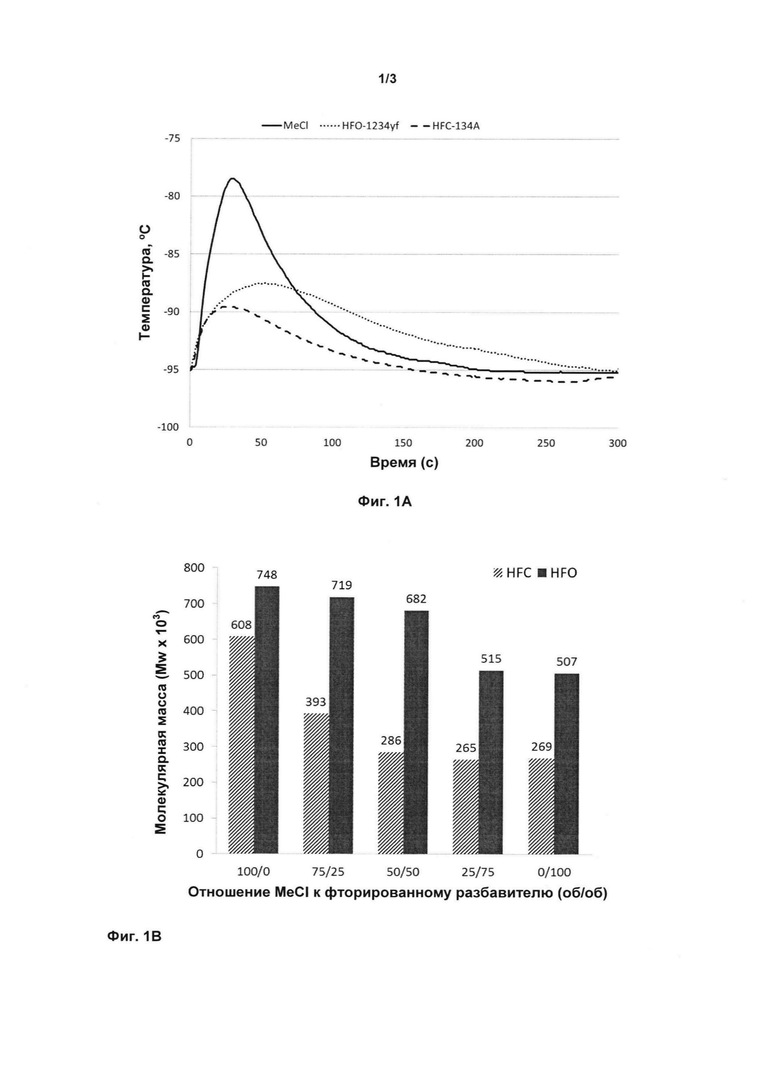
на фиг. 1А изображен профиль температуры реакции для реакций с компонентами на основе чистых разбавителей при -95°С;
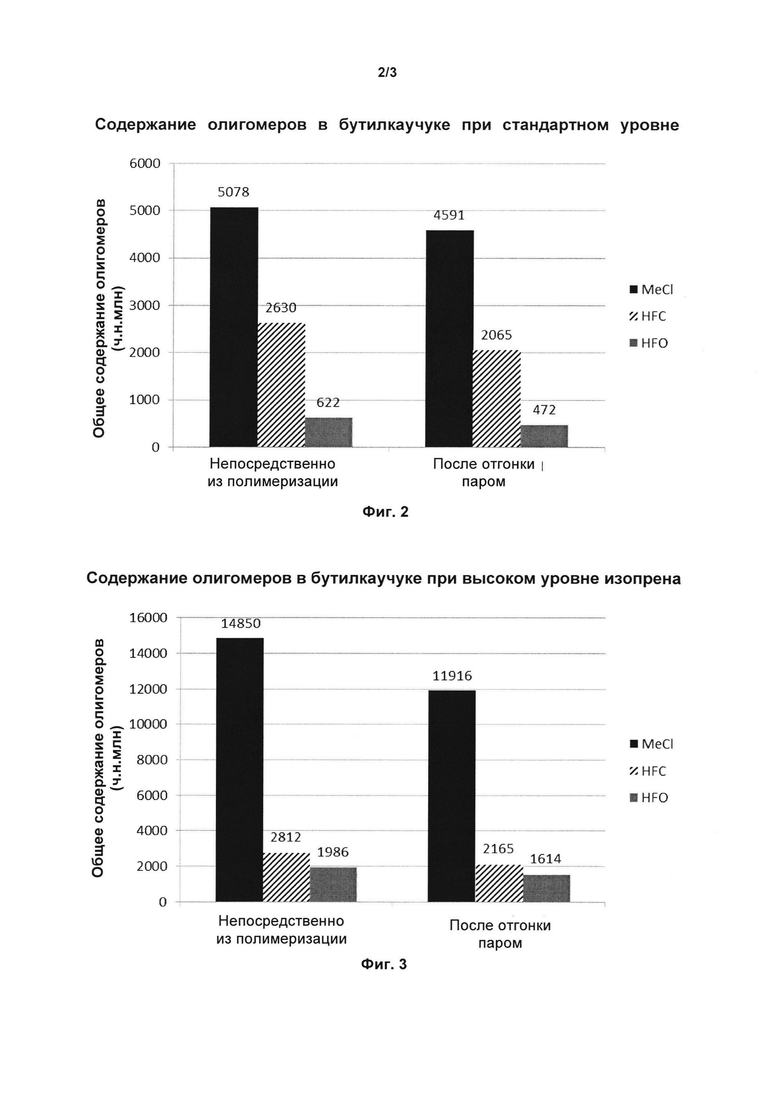
на фиг. 1В изображен график, показывающий молекулярную массу для полимеров, полученных в различных отношениях HFO-1234yf или HFC-134AcMeCl при -95°С;
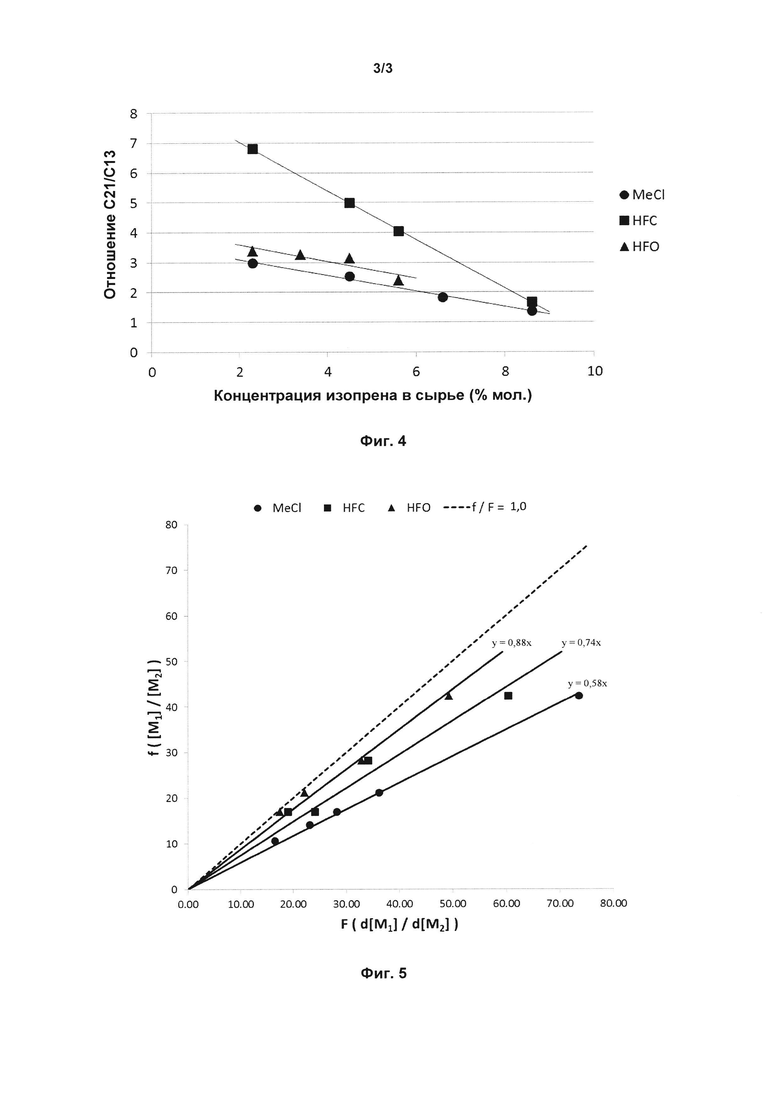
на фиг. 2 изображен график общего содержания олигомеров в бутилкаучуке, полученном в MeCl, HFC-134A и HFO-1234yf при стандартных уровнях изопрена (содержание в сырье 2,3% мол.);
на фиг. 3 изображен график общего содержания олигомеров в бутилкаучуке, полученном в MeCl, HFC-134A и HFO-1234yf при высоких уровнях изопрена (содержание в сырье 5,6% мол.);
на фиг. 4 изображен график, показывающий отношение С21/С13-олигомеров в бутилкаучуке, полученном в MeCl, HFC-134A и HFO-1234yf при -95°С, используя различные концентрации изопрена в сырье.
на фиг. 5 изображен график, показывающий отношение мономеров в сырье (f) по сравнению с отношением сополимеров (F) для полимеризаций, проводимых в MeCl, HFC-134A и HFO-1234yf при различных уровнях изопрена в сырье.
В настоящем описании, включая формулу изобретения, использование единственного числа в отношении объекта не означает исключение возможности включения множественного числа объекта согласно некоторым вариантам осуществления. Специалисту в данной области техники будет очевидно, что, по меньшей мере, в некоторых случаях в настоящем описании, включая приложенную формулу изобретения, можно будет включать множественное число объекта, по меньшей мере, в некоторых вариантах осуществления.
Бутилкаучуки образуются сополимеризацией по меньшей мере одного изоолефинового мономера и по меньшей мере одного мультиолефинового мономера и необязательно дополнительных сополимеризуемых мономеров.
Настоящее изобретение не ограничено конкретным изоолефином. Однако, предпочтительны изоолефины в диапазоне от 4 до 16 атомов углерода, предпочтительно 4-7 атомов углерода, такие как изобутен, 2-метил-1-бутен, 3-метил-1-бутен, 2-метил-2-бутен, 4-метил-1-пентен и их смеси. Более предпочтительным является изобутен.
Настоящее изобретение не ограничено конкретным мультиолефином. Можно использовать любой мультиолефин, сополимеризуемый с изоолефином, известный специалистам в данной области техники. Однако, можно использовать мультиолефины в диапазоне 4-14 атомов углерода, такие как изопрен, бутадиен, 2-метилбутадиен, 2,4-диметилбутадиен, пиперилен, 3-метил-1,3-пентадиен, 2,4-гексадиен, 2-неопентилбутадиен, 2-метил-1,5-гексадиен, 2,5-диметил-2,4-гексадиен, 2-метил-1,4-пентадиен, 2-метил-1,6-гептадиен, циклопентадиен, метилциклопентадиен, циклогексадиен, 1-винилциклогексадиен и их смеси, предпочтительно сопряженные диены. Предпочтительнее использовать изопрен. β-пинен можно также использовать в качестве сомономера для изоолефина.
Любой мономер, сополимеризуемый с изоолефинами и/или диенами, известный специалистам в данной области техники, можно использовать в качестве альтернативы вышеуказанным мультиолефинам или даже в дополнение к вышеуказанным мультиолефинам. Производные индена, стирола или их смеси можно использовать вместо мультиолефинов, перечисленных выше, или в качестве необязательных дополнительных мономеров. Предпочтительно используют α-метилстирол, п-метилстирол, хлор-стирол или их смеси. Предпочтительнее использовать п-метилстирол.
Полимеризацию для получения бутилкаучука проводят в присутствии кислоты Льюиса и инициатора, способного инициировать процесс полимеризации. Подходящими кислотами Льюиса являются такие, которые легко растворимы в выбранном разбавителе. Примеры подходящих кислот Льюиса включают дихлорид этилалюминия (EADC), хлорид диэтилалюминия (DEAC), тетрахлорид титана, тетрахлорид олова, трифторид бора, трихлорид бора, метилалюмоксан и/или их смеси. Согласно некоторым вариантам осуществления можно также использовать AlCl3. Подходящие инициаторы содержат источник протонов и/или катионогенное вещество. Источник протонов, подходящий для настоящего изобретения, содержит любое соединение, которое будет давать протон при добавлении в выбранную кислоту Льюиса. Протоны могут образовываться при реакции кислоты Льюиса с источниками протонов, такими как вода, соляная кислота (HCl), спирт или фенол, с получением протона и соответствующего побочного продукта. Такая реакция может быть предпочтительна в случае, когда реакция источника протонов быстрее с протонированной добавкой по сравнению с его реакцией с мономерами. Другие дающие протоны реагенты включают триолы, карбоновые кислоты и подобное. Наиболее предпочтительная кислота Льюиса содержит смесь EADC и DEAC, а наиболее предпочтительным источником протонов является HCl. Предпочтительные отношения EADC/DEAC к HCl составляют от 5:1 до 100:1 по массе.
В дополнение или вместо источника протонов можно использовать катионогенное вещество, способное инициировать процесс полимеризации. Подходящее катионогенное вещество включает любое соединение, которое образует карбокатион при существующих условиях. Предпочтительная группа катионогенных веществ включает карбокатионные соединения с формулой:
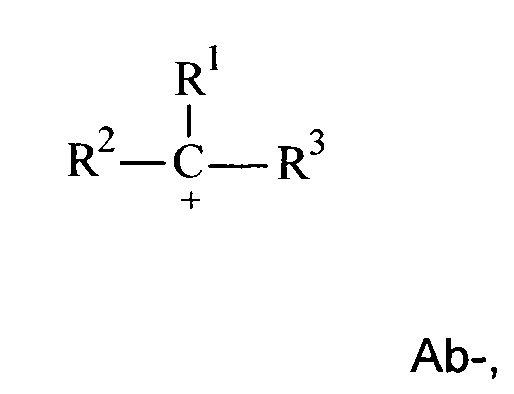
где R1, R2 и R3 независимо представляют собой водород или линейную, разветвленную или циклическую ароматическую или алифатическую группу при условии, что только один из R1, R2 и R3 может представлять собой водород. Предпочтительно R1, R2 и R3 независимо представляют собой ароматическую или алифатическую группу с 1-20 атомами углерода. Неограничивающие примеры подходящих ароматических групп представляют собой фенил, толил, ксилил и бифенил. Неограничивающие примеры подходящих алифатических групп включают метил, этил, пропил, бутил, пентил, гексил, октил, нонил, децил, додецил, 3-метилпентил и 3,5,5-триметилгексил.
Другая предпочтительная группа катионогенных веществ включает замещенные катионные соединения силилия с формулой:
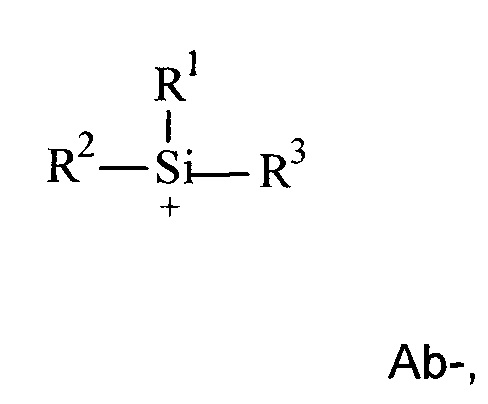
где R1, R2 и R3 независимо представляют собой водород или линейную, разветвленную или циклическую ароматическую или алифатическую группу при условии, что только один из R1, R2 и R3 может представлять собой водород. Предпочтительно ни одна из R1, R2 и R3 не является Н. Предпочтительно R1, R2 и R3 независимо представляют собой ароматическую или алифатическую группу с 1-20 атомами углерода. Более предпочтительно R1, R2 и R3 независимо представляют собой алкильную группу с 1-8 атомами углерода. Примеры пригодных ароматических групп представляют фенил, толил, ксилил и бифенил. Неограничивающие примеры пригодных алифатических групп включают метил, этил, пропил, бутил, пентил, гексил, октил, нонил, децил, додецил, 3-метилпентил и 3,5,5-триметилгексил. Предпочтительная группа реакционноспособных замещенных катионов силилия включает триметилсилилий, триэтилсилилий и бензилдиметилсилилий. Такие катионы можно получать, например, путем обмена гидридной группы соединения R1R2R3Si-H с некоординирующим анионом (NCA), таким как Ph3C+B(pfp)4-, давая композиции, такие как R1R2R3SiB(pfp)4, которые в подходящем растворителе дают катион.
Согласно настоящему изобретению Ab- означает анион. Предпочтительные анионы включают содержащие один координационный комплекс, имеющий несущий заряд металл или металлоидное ядро, которое отрицательно заряжено в степени, необходимой для уравнивания заряда на активных частицах катализатора, которые могут образовываться при объединении двух компонентов. Более предпочтительно Ab- соответствует соединению с общей формулой [MQ4]-, где М представляет собой бор, алюминий, галлий или индий с номинальной степенью окисления +3; a Q независимо представляет собой гидридный, диалкиламидо, галогенидный, гидрокарбильный, гидрокарбилоксидный, галогензамещенный гидрокар-бильный, галогензамещенный гидрокарбилоксидный или галогензамещенный силилгидрокарбильный радикалы.
Предпочтительно мономерная смесь для получения бутилкаучука содержит в диапазоне от приблизительно 80% масс. до приблизительно 99% масс. по меньшей мере одного изоолефинового мономера и в диапазоне от приблизительно 1,0% масс. до приблизительно 20% масс. по меньшей мере одного мультиолефинового мономера и/или β-пинена. Более предпочтительно мономерная смесь содержит в диапазоне от 83% масс. до 98% масс. по меньшей мере одного изоолефинового мономера и в диапазоне от 2,0% масс. до 17% масс. мультиолефинового мономера или β-пинена. Наиболее предпочтительно мономерная смесь содержит в диапазоне от 85% масс. до 97% масс. по меньшей мере одного изоолефинового мономера и в диапазоне от 3,0% масс. до 15% масс.по меньшей мере одного мультиолефинового мономера или β-пинена.
Мономеры обычно вступают в катионную полимеризацию предпочтительно при температурах в диапазоне от приблизительно -120°С до приблизительно -50°С, предпочтительно в диапазоне от приблизительно -100°С до приблизительно -70°С, более предпочтительно в диапазоне от приблизительно -98°С до приблизительно -75°С, например, от приблизительно -98°С до приблизительно -90°С. Рабочие температуры приблизительно -98°С и приблизительно -75°С особенно заслуживают внимания. Предпочтительные давления находятся в диапазоне от 0,1 до 4 бар.
Использование реактора непрерывного действия вместо реактора периодического действия, как представляется, имеет положительное влияние на процесс. Предпочтительно способ проводят по меньшей мере в одном реакторе непрерывного действия объемом от 0,1 м3 до 100 м3, более предпочтительно от 1 м3 до 10 м3. Непрерывный процесс предпочтительно проводят, по меньшей мере, со следующими сырьевыми потоками:
I) растворитель/разбавитель, содержащий тетрафторированный пропен+изоолефин (предпочтительно изобутен) + мультиолефин (предпочтительно диен, такой как изопрен); и
II) система инициаторов, содержащая кислоту Льюиса и источник протонов.
Для экономически выгодного производства желателен непрерывный процесс, проводимый в суспензии (взвеси) в разбавителе, как описано в патенте США №5417930, полное содержание которого включено в настоящий документ ссылкой.
Разбавитель предпочтительно содержит по меньшей мере один гидрофторированный олефин, содержащий по меньшей мере три атома углерода и по меньшей мере три атома фтора, как описывается формулой I:

где x представляет собой целое число со значением 3 или больше, z представляет собой целое число со значением 3 или больше, a y+z равняется 2x. Значение x предпочтительно составляет от 3 до 6, более предпочтительно от 3 до 5, еще более предпочтительно 3. Значение z предпочтительно составляет от 3 до 8, более предпочтительно от 4 до 6, еще более предпочтительно 4. Y представляет собой целое число со значением 2x-z и может находиться в диапазоне, например, от 2 до 10, от 3 до 9, от 4 до 8 или от 4 до 6. Значение у предпочтительно составляет 2.
Примеры подходящих разбавителей с тремя или более атомами углерода и тремя или более атомами фтора включают 1,1,2-трифторпропен; 1,1,3-трифторпропен; 1,2,3-трифторпропен; 1,3,3-трифторпропен; 2,3,3-трифторпропен; 3,3,3-трифторпропен; 1,3,3,3-тетрафтор-1-пропен; 2,3,3,3-тетрафтор-1-пропен; 1,1,3,3-тетрафтор-1-пропен, 1,1,2,3-тетрафтор-1-пропен, 1,2,3,3-тетрафтор-1-пропен, 1,1,2,3-тетрафтор-1-бутен; 1,1,2,4-тетрафтор-1-бутен; 1,1,3,3-тетрафтор-1-бутен; 1,1,3,4-тетрафтор-1-бутен; 1,1,4,4-тетрафтор-1-бутен; 1,2,3,3-тетрафтор-1-бутен; 1,2,3,4-тетрафтор-1-бутен; 1,2,4,4-тетрафтор-1-бутен; 1,3,3,4-тетрафтор-1-бутен; 1,3,4,4-тетрафтор-1-бутен; 1,4,4,4-тетрафтор-1-бутен; 2,3,3,4-тетрафтор-1-бутен; 2,3,4,4-тетрафтор-1-бутен; 2,4,4,4-тетрафтор-1-бутен; 3,3,4,4-тетрафтор-1-бутен; 3,4,4,4-тетрафтор-1-бутен; 1,1,2,3,3-пентафтор-1-бутен; 1,1,2,3,4-пентафтор-1-бутен; 1,1,2,4,4-пентафтор-1-бутен; 1,1,3,3,4-пентафтор-1-бутен; 1,1,3,4,4-пентафтор-1-бутен; 1,1,4,4,4-пентафтор-1-бутен; 1,2,3,3,4-пентафтор-1-бутен; 1,2,3,4,4-пентафтор-1-бутен; 1,2,4,4,4-пентафтор-1-бутен; 2,3,3,4,4-пентафтор-1-бутен; 2,3,4,4,4-пентафтор-1-бутен; 3,3,4,4,4-пентафтор-1-бутен; 1,1,2,3,3,4-гексафтор-1-бутен; 1,1,2,3,4,4-гексафтор-1-бутен; 1,1,2,4,4,4-гексафтор-1-бутен; 1,2,3,3,4,4-гексафтор-1-бутен; 1,2,3,4,4,4-гексафтор-1-бутен; 2,3,3,4,4,4-гексафтор-1-бутен; 1,1,2,3,3,4,4-гептафтор-1-бутен; 1,1,2,3,4,4,4-гептафтор-1-бутен; 1,1,3,3,4,4,4-гептафтор-1-бутен; 1,2,3,3,4,4,4-гептафтор-1-бутен; 1,1,1,2-тетрафтор-2-бутен; 1,1,1,3-тетрафтор-2-бутен; 1,1,1,4-тетрафтор-2-бутен; 1,1,2,3-тетрафтор-2-бутен; 1,1,2,4-тетрафтор-2-бутен; 1,2,3,4-тетрафтор-2-бутен; 1,1,1,2,3-пентафтор-2-бутен; 1,1,1,2,4-пентафтор-2-бутен; 1,1,1,3,4-пентафтор-2-бутен; 1,1,1,4,4-пентафтор-2-бутен; 1,1,2,3,4-пентафтор-2-бутен; 1,1,2,4,4-пентафтор-2-бутен; 1,1,1,2,3,4-гексафтор-2-бутен; 1,1,1,2,4,4-гексафтор-2-бутен; 1,1,1,3,4,4-гексафтор-2-бутен; 1,1,1,4,4,4-гексафтор-2-бутен; 1,1,2,3,4,4-гексафтор-2-бутен; 1,1,1,2,3,4,4-гептафтор-2-бутен; 1,1,1,2,4,4,4-гептафтор-2-бутен и их смеси.
Примеры HFO с четырьмя или более атомами фтора и тремя или более атомами углерода представляют собой 1,3,3,3-тетрафтор-1-пропен; 2,3,3,3-тетрафтор-1-пропен; 1,1,3,3-тетрафтор-1-пропен, 1,1,2,3-тетрафтор-1-пропен, 1,2,3,3-тетрафтор-1-пропен; 1,1,2,3-тетрафтор-1-бутен; 1,1,2,4-тетрафтор-1-бутен; 1,1,3,3-тетрафтор-1-бутен; 1,1,3,4-тетрафтор-1-бутен; 1,1,4,4-тетрафтор-1-бутен; 1,2,3,3-тетрафтор-1-бутен; 1,2,3,4- тетрафтор-1-бутен; 1,2,4,4-тетрафтор-1-бутен; 1,3,3,4-тетрафтор-1-бутен; 1,3,4,4-тетрафтор-1-бутен; 1,4,4,4-тетрафтор-1-бутен; 2,3,3,4-тетрафтор-1-бутен; 2,3,4,4-тетрафтор-1-бутен; 2,4,4,4-тетрафтор-1-бутен; 3,3,4,4-тетрафтор-1-бутен; 3,4,4,4-тетрафтор-1-бутен; 1,1,2,3,3-пентафтор-1-бутен; 1,1,2,3,4-пентафтор-1-бутен; 1,1,2,4,4-пентафтор-1-бутен; 1,1,3,3,4-пентафтор-1-бутен; 1,1,3,4,4-пентафтор-1-бутен; 1,1,4,4,4-пентафтор-1-бутен; 1,2,3,3,4-пентафтор-1-бутен; 1,2,3,4,4-пентафтор-1-бутен; 1,2,4,4,4-пентафтор-1-бутен; 2,3,3,4,4-пентафтор-1-бутен; 2,3,4,4,4-пентафтор-1-бутен; 3,3,4,4,4-пентафтор-1-бутен; 1,1,2,3,3,4-гексафтор-1-бутен; 1,1,2,3,4,4-гексафтор-1-бутен; 1,1,2,4,4,4-гексафтор-1-бутен; 1,2,3,3,4,4-гексафтор-1-бутен; 1,2,3,4,4,4-гексафтор-1-бутен; 2,3,3,4,4,4-гексафтор-1-бутен; 1,1,2,3,3,4,4-гептафтор-1-бутен; 1,1,2,3,4,4,4-гептафтор-1-бутен; 1,1,3,3,4,4,4-гептафтор-1-бутен; 1,2,3,3,4,4,4-гептафтор-1-бутен; 1,1,1,2-тетрафтор-2-бутен; 1,1,1,3-тетрафтор-2-бутен; 1,1,1,4-тетрафтор-2-бутен; 1,1,2,3-тетрафтор-2-бутен; 1,1,2,4-тетрафтор-2-бутен; 1,2,3,4-тетрафтор-2-бутен; 1,1,1,2,3-пентафтор-2-бутен; 1,1,1,2,4-пентафтор-2-бутен; 1,1,1,3,4-пентафтор-2-бутен; 1,1,1,4,4-пентафтор-2-бутен; 1,1,2,3,4-пентафтор-2-бутен; 1,1,2,4,4-пентафтор-2-бутен; 1,1,1,2,3,4-гексафтор-2-бутен; 1,1,1,2,4,4-гексафтор-2-бутен; 1,1,1,3,4,4-гексафтор-2-бутен; 1,1,1,4,4,4-гексафтор-2-бутен; 1,1,2,3,4,4-гексафтор-2-бутен; 1,1,1,2,3,4,4-гептафтор-2-бутен; 1,1,1,2,4,4,4-гептафтор-2-бутен и их смеси.
Тетрафторированные пропены с четырьмя атомами фтора и тремя атомами углерода следует особо отметить. Примеры представляют собой 1,3,3,3-тетрафтор-1-пропен (HFO-1234ze), 2,3,3,3-тетрафтор-1-пропен (HFO-1234yf), 1,1,3,3-тетрафтор-1-пропен, 1,1,2,3-тетрафтор-1-пропен, 1,2,3,3-тетрафтор-1-пропен и их смеси. Тетрафторированные пропены могут существовать или в Z-, или в Е-изомерных формах или в виде смеси Z-и Е-изомерных форм. 1,3,3,3-тетрафтор-1-пропен (HFO-1234ze) и 2,3,3,3-тетрафтор-1-пропен (HFO-1234yf) особенно предпочтительны. HFO-1234yf (2,3,3,3-тетрафтор-1-пропен) наиболее предпочтителен.
Разбавитель может также содержать один или более других инертных растворителей, известных специалисту в данной области техники для полимеризации бутилкаучука. Такие другие инертные растворители могут представлять собой, например, галогенированные углеводороды, отличные от гидрофторуглеродов (например, метилхлорид, дихлорметан или их смеси).
Примеры
Все полимеризации проводили в сухой, инертной атмосфере. Полимеризации проводили как периодические реакции в 600 мл реакционных емкостях из нержавеющей стали, оборудованных закрепленной сверху 4-лопастной мешалкой из нержавеющей стали, приводимой в движение внешним электрическим приводом. Температуру реакции измеряли посредством термопары. Реактор охлаждали до желаемой температуры реакции, указанной в таблицах, путем погружения собранного реактора в пентановую охлаждающую ванну. Температуру перемешанной углеводородной ванны контролировали до ±2°С. Все агрегаты находящиеся в жидкостном контакте с реакционной средой сушили при 150°С в течение по меньшей мере 6 часов и охлаждали перед использованием в камере с возможностью замены вакуума на атмосферу азота. Изобутен и метилхлорид высокой чистоты получали от промышленного предприятия LANXESS и использовали как есть. Гидрофторуглерод 1,1,1,2-тетрафторэтан (чистотой >99,9%) (HFC-134a, Genetron® 134а) и гидрофторолефины (Е)-1,3,3,3-тетрафтор-1-пропен (чистотой>99,99%) (HFO-1234ze, Solstice® 1234ze хладагент) и 2,3,3,3-тетрафтор-1-пропен (чистотой>99,99%) (HFO-1234yf, Solstice® 1234yf автомобильной марки) закупали у Honeywell и использовали в том виде, в котором получали. Все вещества конденсировали и собирали в виде жидкостей в вытяжном шкафу. Изопрен (Sigma-Aldrich, чистотой >99,5%) сушили над активированными молекулярными ситами 3А в течение нескольких дней и очищали в атмосфере азота. 1,0 М раствор дихлорида этилалюминия в гексанах (Sigma-Aldrich) использовали в том виде, в котором получали. Раствор HCl/CH2Cl2 готовили путем барботирования безводного газообразного HCl (Sigma-Aldrich, чистотой 99%) через предварительно высушенную бутылку Sure/Seal™, содержащую безводный CH2Cl2 (VWR). Раствор HCl/CH2Cl2 затем титровали при помощи стандартного раствора 0,1 н NaOH (VWR) для определения его концентрации.
Суспензионные полимеризации проводили путем загрузки мономера, сомономера и ожиженного разбавителя (определенного в каждом примере) в охлажденную реакционную емкость при температуре полимеризации и перемешивали при заранее определенной скорости перемешивания от 500 до 900 об/мин. Растворы инициатора/соинициатора готовили в метил-хлориде. Растворы инициатора/соинициатора готовили при таких же температурных условиях, как и реакционную емкость, путем разбавления раствора HCl/CH2Cl2 в аликвоте метилхлорида и добавления 1,0 М раствора дихлорида этилалюминия в мольном отношении HCl:EADC 1:4 с последующим аккуратным перемешиванием. Раствор инициатора/соинициатора использовали сразу же. Раствор инициатора/соинициатора добавляли в реакцию полимеризации при помощи охлажденной стеклянной пипетки Пастера. Реакции позволяли протекать в течение 5 минут и останавливали добавлением 2 мл 1% раствора гидроксида натрия в этаноле. Конверсию записывали в виде % масс. мономеров, превратившихся в полимер при температуре полимеризации.
Молекулярную массу полимеров определяли при помощи GPC (гель-проникающей хроматографии), используя сепарационный модуль Waters 2690/5 и детектор коэффициента преломления Waters 2414. Тетрагидро-фуран использовали в качестве элюента (0,8 мл/мин, 35°С) с серией из трех колонок Agilent PLgel 10 мкм Mixed-B LS 300 × 5,7 мм.
Включение изопрена определяли при помощи 1H-NMR спектрометрии. Измерения NMR получали при помощи спектрометра Bruker DRX 500 МГц (500,13 МГц), используя растворы полимеров в CDCl3, причем остаточный пик CHCl3 использовали в качестве внутреннего стандарта.
Определение уровней олигомеров проводили посредством GC-FID при помощи Agilent 6890 Series Plus, используя колонку Agilent J+W VF-1ms 30×0,25 (1,0) (на входе: 275°С, 22,5 фунта/кв. дюйм) и температуру FID 300°С, оборудованного автоинжектором серии HP 7683.
Пример А: Полимеризации с чистыми разбавителями при -95°С
В таблице 1 указаны результаты полимеризаций, проводимых при -95°С в метилхлориде (примеры 1 и 2), HFO-1234ze (примеры 3 и 4), HFO-1234yf (примеры 5 и 6) и HFC-134a (примеры 7 и 8). Все полимеризации проводили согласно указанному выше в 600 мл емкости из нержавеющей стали, используя HCl/EADC в качестве инициатора/соинициатора. Полимеризации проходили с 180 мл разбавителя, 20 мл изобутена и 0,6 мл изопрена (содержание изопрена в сырье = 2,3% мол.). Раствор инициатора/соинициатора готовили в 40 мл MeCl, используя 6 мл 0,16 М растворов HCl/CH2Cl2 и 4 мл 1,0 М раствора дихлорида этилалюминия (EADC) в гексане. Такой же объем раствора инициатора/соинициатора (5 мл) использовали во всех примерах в таблице 1, которая также обеспечивает больше подробностей об олигомерном составе в каждом примере.
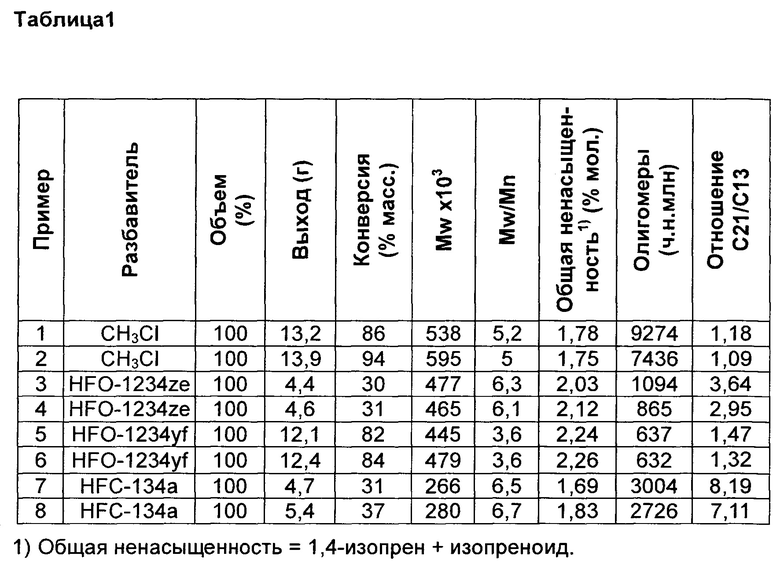
Ссылаясь на фиг. 1А, полимеризация в HFO-1234yf показывает превосходный профиль температуры с умеренным пиком температуры и увеличенным временем реакции по сравнению с полимеризациями в метилхлориде (MeCl).
Полимеризации с использованием MeCl давали значительное загрязнение стенок реакционной емкости, датчика температуры и вала мешалки, а также образование шариков каучука в реакционной среде. Полимеризации с использованием как гидрофторуглерода, так и гидрофторолефинов приводили к минимальному загрязнению реакционной емкости, датчика температуры и вала мешалки или его отсутствию. HFO-1234yf давал очень устойчивую, однородную суспензию каучука без агломерации полимера.
При таких же условиях реакции, при температуре реакции -95°С, активность полимеризации в HFO-1234yf превосходная (средняя конверсия 83%) и вполне сравнимая, хотя и несколько ниже, чем при использовании обычного разбавителя метилхлорида (средняя конверсия 90%). Однако, результаты показали заметную разницу активности полимеризации для гидрофторуглерода HFC-134a относительно гидрофторолефина HFO-1234yf. Реакции, проводимые в HFO-1234yf (средняя конверсия 83%), давали намного больший выход полимера, чем с HFC-134a (средняя конверсия 34%). Гидрофторлефиновый изомер (Е) HFO-1234ze показал активность полимеризации (средняя конверсия 30%), аналогичную таковой с HFC-134a.
В дополнение к высоким конверсиям полимера образцы бутилкаучука, полученного из разбавителя HFO-1234yf, давали наилучшую комбинацию свойств, таких как высокая молекулярная масса, узкое распределение молекулярных масс, высокое включение изопрена и низкие уровни циклических олигомерных побочных продуктов (таблица 1). Ясно видно, что каучук, полученный при помощи HFO-1234yf в качестве разбавителя, характеризуется значительно более высокой среднемассовой молекулярной массой (Mw), чем полученный в HFC-134A, аналогичной Mw полученному в HFO-1234ze и более низкой Mw, чем полученный в MeCl. При сравнении среднего значения дважды проведенных реакций Mw, полученная для полимеризаций в HFO-1234yf, проводимых при -95°С (пр. 5 и 6), составляла 462000 по сравнению со средними значениями 567000 для MeCl (пр. 1 и 2), 273000 для HFC-134A (пр. 7 и 8) и 471000 для HFO1234ze (пр. 3 и 4).
Хорошо известно, что циклические олигомеры, а именно соединения С13Н24 и С21Н40, по существу образуются в качестве побочных продуктов в процессе получения бутилкаучука полимеризацией. Молекулярные структуры этих циклических олигомеров показаны ниже на схеме 1, где изомер С13Н24 содержит 1 молекулу изопрена и 2 молекулы изобутилена, а изомер С21Н40 содержит 1 молекулу изопрена и 4 молекулы изобутилена. Эти циклические олигомеры существуют в следовых количествах в готовых продуктах из обычного бутилкаучука. Присутствие С13Н24 и C21H40 в бутилкаучуке представляет собой насущную проблему при фармацевтическом применении. Эти соединения являются основными экстрагируемыми веществами в определенных композициях фармацевтических резиновых пробок.
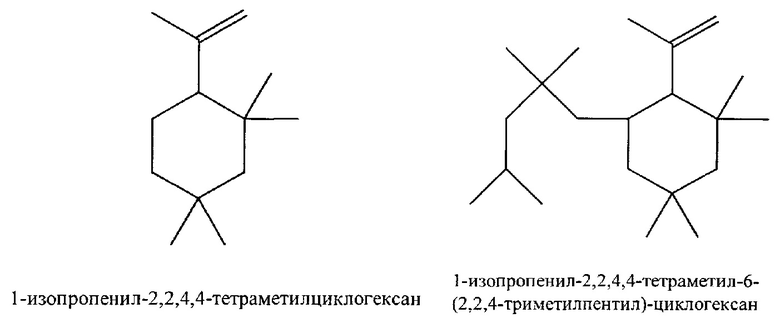
Схема 1 - Молекулярные структуры циклических олигомеров
В дополнение к обеспечению неожиданно низких уровней олигомеров использование тетрафторированных пропеновых разбавителей также дает неожиданно предпочтительное отношение С21/С13-олигомеров. Например, использование HFO-1234yf обеспечивает отношения 1,32 и 1,47, тогда как использование HFC-134a обеспечивает отношения 7,11 и 8,19. Поскольку низкомолекулярные С13-олигомеры предпочтительно удаляют при операциях отгонки паром и сушки каучука, низкое отношение предпочтительно, поскольку готовый продукт может быть получен с еще более низкими общими уровнями содержания олигомеров.
Хотя разбавитель HFO-1234ze, как правило, дает более низкие степени превращения сополимеров, образцы бутилкаучука, полученные из этого разбавителя, показывают превосходные свойства в отношении молекулярной массы, включения изопрена и содержания циклических олигомеров. В общем, оба тетрафторированных пропена, HFO-1234yf и HFO-1234ze, показывают лучшее поведение и являются более подходящими для получения бутилкаучука суспензионной полимеризацией, чем HFC-134а, при низких температурах.
Хотя данные NMR здесь не представлены, в общем было обнаружено, что возникала более низкая разветвленность полимера, когда использовали разбавители HFO-1234yf, тогда как разбавители HFO-1234ze давали полимеры с аналогичной разветвленностью, как у разбавителей HFC-134a.
Пример В: Полимеризации с чистыми разбавителями при -75°С
В таблице 2 указаны результаты полимеризаций, проводимых при -75°С в метилхлориде (примеры 9 и 10), HFO-1234ze (примеры 11 и 12), HFO-1234yf (примеры 13 и 14) и HFC-134a (примеры 15 и 16). Все полимеризации проводили согласно указанному выше в 600 мл емкости из нержавеющей стали, используя HCl/EADC и инициатор/соинициатор. Полимеризации проходили с 180 мл разбавителя, 20 мл изобутена и 0,6 мл изопрена (содержание изопрена в сырье = 2,3% мол.). Раствор инициатора/соинициатора готовили в 40 мл MeCl, используя 6 мл 0,16 М растворов HCl/CH2Cl2 и 4 мл 1,0 М раствора дихлорида этилалюминия (EADC) в гексане. Такой же объем раствора инициатора/соинициатора (5 мл) использовали для всех полимеризаций.
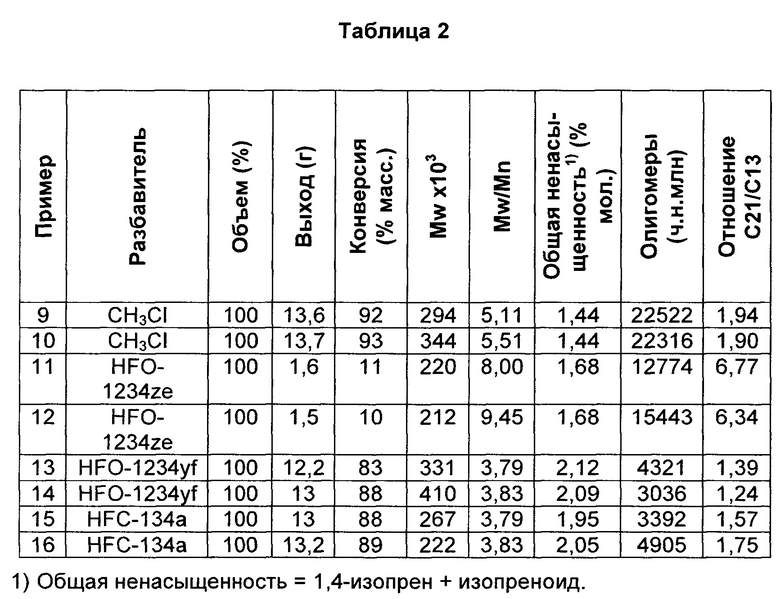
При более высокой температуре реакции -75°С полимеризация становилась намного более активной в HFC-134a, уровни конверсии (средняя конверсия 89%) теперь сравнимы с таковыми в HFO-1234yf (средняя конверсия 85%). Эксперименты, проводимые в HFC-134a и HFO-1234yf, показали сравнимую активность; однако, оба эти разбавителя показали несколько меньшие конверсии реакции, чем обычный разбавитель метилхлорид. Температура не имела влияния на HFO-1234ze, поскольку этот разбавитель все еще проявлял плохую активность, несмотря на более высокую температуру реакции.
При более высокой температуре полимеризации полимер, полученный в HFO-1234yf, обладал наивысшей Mw. При сравнении средних значений дважды проведенных полимеризаций, проводимых при -75°С, HFO-1234yf (пр. 13 и 14) давал полимер с Mw=371000, HFC-134A (пр. 15 и 16) с Mw=245000, HFO-1234ze (пр. 11 и 12) с Mw=216000, a MeCl (пр. 9 и 10) с Mw=319000. Это является важным преимуществом для непрерывного процесса получения бутилкаучука, поскольку высокая Mw и связанные желаемые физические свойства можно сохранять в продукте даже при более высоких температурах реактора.
Сравнивая данные, показанные в таблицах 1 и 2, общее влияние более высокой температуры реакции заключается в снижении молекулярных масс полимерных цепочек (Mw) и значительном увеличении содержания циклических олигомеров. Влияние проявляется в одинаковых тенденциях для всех разбавителей, однако, образцы бутилкаучука, полученные из HFO-1234yf, сохраняют более высокие молекулярные массы полимеров относительно HFC-134a. Уровень общей ненасыщенности несколько выше для HFO-1234yf (в среднем 2,1% мол.) относительно HFC-134a (в среднем 2,0% мол.), тогда как уровень циклических олигомеров ниже для HFO-1234yf (в среднем 3679 ч.н.млн) относительно HFC-134a (в среднем 4148 ч.н.млн). Отношение С21/С13 более предпочтительно с HFO-1234yf, чем с HFC-134a. То же самое можно наблюдать при сравнении HFO-1234yf с метилхлоридом в отношении молекулярных масс сополимера.
Уровень общей ненасыщенности и, таким образом, уровень изопрена намного выше в образцах бутилкаучука, полученного в HFO-1234yf относительно метилхлорида. Как видно в таблицах 1 и 2, каучук, полученный при помощи HFO-1234yf в качестве разбавителя, содержит значительно большую ненасыщенность от включенного изопрена по сравнению с другими разбавителями, когда используют равную концентрацию изопрена в смешанном сырье для реакции. При сравнении средних значений дважды проведенных реакций общая ненасыщенность, полученная для полимеризаций с HFO-1234yf, проводимых при -95°С (пр. 5 и 6), составляла 2,25% мол. по сравнению со средними значениями 1,77% мол. для MeCl (пр. 1 и 2), 1,76% мол. для HFC-134A (пр. 7 и 8) и 2,08% мол. для HFO-1234ze (пр. 3 и 4). Включение изопрена для HFC-134A ограничено при -95°С из-за низких конверсий при этой температуре. Такие же тенденции существуют при сравнении средних значений дважды проведенных полимеризаций, проводимых при высокой температуре (-75°С), причем HFO-1234yf (пр. 13 и 14) включает в среднем 2,11% мол. всего изопрена, HFC-134A (пр. 15 и 16) 2,00% мол., HFO-1234ze (пр. 11 и 12) 1,68% мол., a MeCl (пр. 9 и 10) 1,44% мол.. Включение изопрена для HFO-1234ze ограничено при -75°С из-за низких степеней превращения при этой температуре. Повышенное включение изопрена в бутилкаучук дает более низкую концентрацию изопрена, требуемую в сырьевом потоке для достижения эквивалентных уровней ненасыщенности в готовом продукте, что приводит к снижению затрат для непрерывного суспензионного процесса производства. Кроме того, уровни циклических олигомеров значительно выше в метилхлориде относительно HFO-1234yf и HFC-134a, а отношения С21/С13 также нежелательно выше. В общем, ход полимеризации и преимущества HFO-1234yf применимы при различных температурах реакции, т.е. при -95°С и -75°С.
Пример С: Полимеризации со смесями разбавителей 50:50 при -95°С
В таблице 3 указаны результаты полимеризаций, проводимых при -95°С в смеси 50:50 MeCl:HFO-1234ze (примеры 17 и 18) и смеси 50:50 MeCl:HFO-1234yf (примеры 19 и 20). Все полимеризации проводили согласно указанному выше в 600 мл емкости из нержавеющей стали, используя HCl/EADC и инициатор/соинициатор. Полимеризации проходили с 180 мл разбавителя, 20 мл изобутена и 0,6 мл изопрена (содержание изопрена в сырье = 2,3% мол.). Раствор инициатора/соинициатора готовили в 40 мл MeCl, используя 6 мл 0,16 М растворов HCl/CH2Cl2 и 4 мл 1,0 М раствора дихлорида этилалюминия (EADC) в гексане. Такой же объем раствора инициатора/соинициатора (5 мл) использовали для всех полимеризаций.
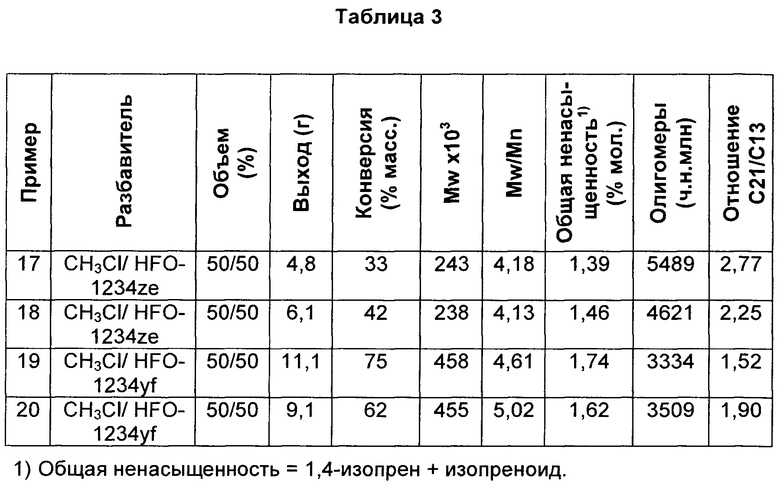
При температуре реакции -95°С полимеризации с использованием смесей разбавителей приводили, в общем, к тенденциям, аналогичным наблюдаемым в чистом разбавителе. Таким образом, реакции в смеси 50:50 метилхлорида/НРО-1234ут (средняя конверсия 68%) более активны, чем в смесях метилхлорида/НРО-1234ze (средняя конверсия 38%). Образцы бутилкаучука, полученные из метилхлорида/НРО-1234yf, также характеризовались более высокими молекулярными массами и более высоким включением изопрена, чем в смеси разбавителей метилхлорида/НРО-1234ze. Уровни циклических олигомеров ниже для метилхлорида/НРО-1234yf, чем в случае метилхлорида/НFО-1234ze. Кроме того, отношение С21/С13 ниже для метилхлорида/HFO-1234yf по сравнению со смесью разбавителей, содержащей метилхлорид/HFO-1234ze.
Бутилкаучук, полученный в смеси MeCl с HFO-1234yf, обладал значительно более высокой Mw, чем в HFO-1234ze. При сравнении средних значений дважды проведенных полимеризаций, проводимых при -95°С, смеси MeCl с HFO1234yf (пр. 19 и 20) давали полимер с Mw=457000, тогда как HFO1234ze (пр. 17 и 18) давал полимер с Mw=241000. Это является важным преимуществом для непрерывного суспензионного процесса получения бутилкаучука. Высокую Mw можно сохранять даже со смесью HFO-1234yf с MeCl, что приводит к более низким эксплуатационным затратам по сравнению с 100% HFO-1234yf без потери других преимуществ системы фторированных разбавителей. Во всех случаях наблюдали минимальное загрязнение на поверхностях, находящихся в контакте с реакционными смесями, или его отсутствие. При сравнении полимеризация в метилхлориде давала толстое покрытие полимера на стенках реактора, датчике температуры и вале мешалки, а также большие количества агломератов полимера в реакционной среде.
Пример D: Полимеризации со смесями разбавителей 50:50 при -75°С
В таблице 4 указаны результаты полимеризаций, проводимых при -75°С в смеси 50:50 MeCl:HFO-1234ze (примеры 21 и 22) и смеси 50:50 MeCl:HFO-1234yf (примеры 23 и 24). Все полимеризации проводили согласно указанному выше в 600 мл емкости из нержавеющей стали, используя HCl/EADC и инициатор/соинициатор. Полимеризации проходили с 180 мл разбавителя, 20 мл изобутена и 0,6 мл изопрена (содержание изопрена в сырье = 2,3% мол.). Раствор инициатора/соинициатора готовили в 61 мл MeCl, используя 11 мл 0,18 М растворов HCl/CH2Cl2 и 8 мл 1,0 М раствора дихлорида этилалюминия (EADC) в гексане. Такой же объем раствора инициатора/соинициатора (5 мл) использовали для всех полимеризаций.
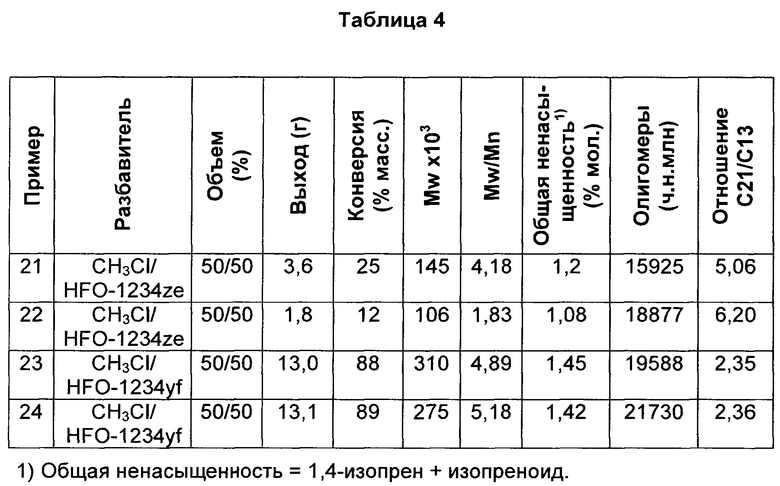
Полимеризации с использованием смеси разбавителей при -75°С давали значительное загрязнение для всех смесей разбавителей. Смесь MeCl/HFO-1234ze приводила к полимеру, создающему загрязнение только вокруг вала мешалки, тогда как MeCl/HFO-1234yf давала толстый слой загрязнения на валу мешалки вместе с образованием шариков каучука в реакционной среде. Для сравнения, полимеризация в метилхлориде приводила к толстому слою полимера на стенках реактора, датчике температуры и валу мешалки, а также к большим количествам агломератов полимера в реакционной среде.
Снова в этом случае температура имела относительно небольшое влияние на конверсии полимера для реакций, включающих метилхлорид/HFO-1234ze. Наибольшие конверсии и молекулярные массы получали с метил-хлоридом/HFO-1234yf.
Бутилкаучук, полученный в смеси с HFO-1234yf, характеризовался более высокой Mw, чем в HFO-1234ze. При сравнении средних значений дважды проведенных полимеризаций, проводимых при -75°С, смеси MeCl с HFO-1234yf (пр. 21 и 22) давали полимер с Mw=457000, тогда как HFO-1234ze (пр. 23 & 24) давал полимер с Mw=241000. Это является важным преимуществом для непрерывного суспензионного процесса получения бутилкаучука, доказывая, что высокая Mw сохраняется даже при более высоких температурах полимеризации со смесью HFO-1234yf в MeCl.
Пример Е: Влияние отгонки паром на полимеры в отношении снижения содержания С13 циклических олигомеров
Для полимеров, полученных согласно выбранным экспериментальным условиям, отгонку паром проводили в качестве конечной стадии для снижения содержания С13 циклических олигомеров и при этом снижения общего количества извлекаемых циклических олигомеров из полимера. Эта конечная стадия использует преимущество желательного низкого отношения С21/С13, наблюдаемого для полимеров, полученных при помощи HFO настоящего изобретения для получения полимеров с желаемым сниженным общим содержанием олигомеров.
Для каждого образца 2 г полимера (который ранее коагулировали в этаноле и выпаривали при комнатной температуре) растворяли в 20 мл гексана. Следует отметить, что стадия коагуляции в этаноле давала некоторое извлечение циклических олигомеров; это приводило к низким исходным общим уровням олигомеров и более высокому отношению С21/С13 для этих образцов, чем указано выше. Гексановый растворитель, растворяющий С13-олигомеры из образца и растворителя, удаляли вместе с олигомерами путем отгонки паром в течение тридцати минут. Полимер извлекали и повторно растворяли в гексане для последующего анализа на содержание олигомеров при помощи GC/MS. Результаты анализа представлены в таблице 5.
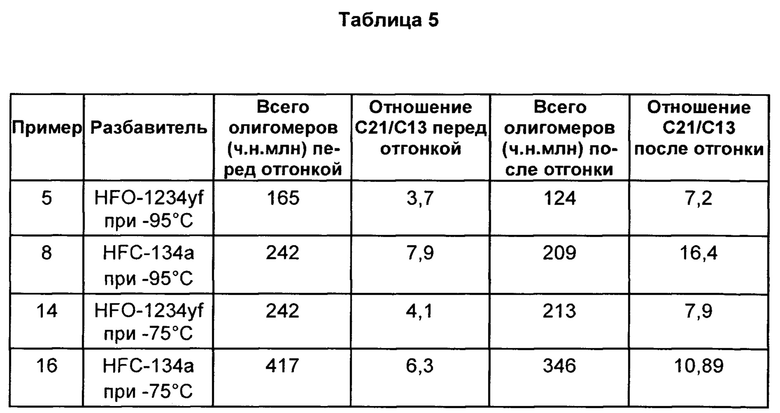
Путем использования отгонки паром в качестве конечного процесса обеспечивалась возможность получать полимеры с низким общим содержанием олигомеров из полимеров, полученных при помощи HFO-разбавителя. Как можно увидеть из таблицы 5, отгонка паром снижала общее содержание олигомеров в образцах, полученных при помощи разбавителя HFO-1234yf, до более низкого уровня, чем у полученных при помощи разбавителя HFC-134a. Хотя снижение уровней циклических олигомеров наблюдали для полимеров, полученных при всех температурах, оно было наиболее выраженным для полученных при более низкой температуре -95°С, поскольку отношение С21/С13 было благоприятным для HFO-разбавителей при этой температуре. Самые низкие общие уровни циклических олигомеров получали у полимера, полученного при помощи HFO-1234yf при -95°С.Используя процесс отгонки паром, получали бутил каучук с общим содержанием циклических олигомеров менее 125 ч.н.млн. Поскольку С13 извлекали, во всех случаях отношение С21/С13 увеличивалось после отгонки паром. Полимеры, полученные при помощи конечного процесса отгонки паром, являются новыми, поскольку они характеризуются наивысшей чистотой и самым низшим общим уровнем всех циклических олигомеров, что является предпочтительным в фармацевтических применениях.
Ряд полимеризаций проводили в метилхлориде (MeCl), HFC-134A и HFO1234yf в качестве разбавителей при различных содержаниях изопрена в реакционном сырье. Полимеризации проводили, как описано ранее, за исключением того, что 1,5 мл изопрена использовали в сырье для полимеризаций с высоким содержанием изопрена (содержание изопрена в сырье = 5,6% мол.). Содержание олигомеров измеряли для образцов полимера, взятых непосредственно из реакционной емкости или после отгонки паром реакционной смеси для имитации условий промышленного процесса производства. Результаты показаны в таблице 6.
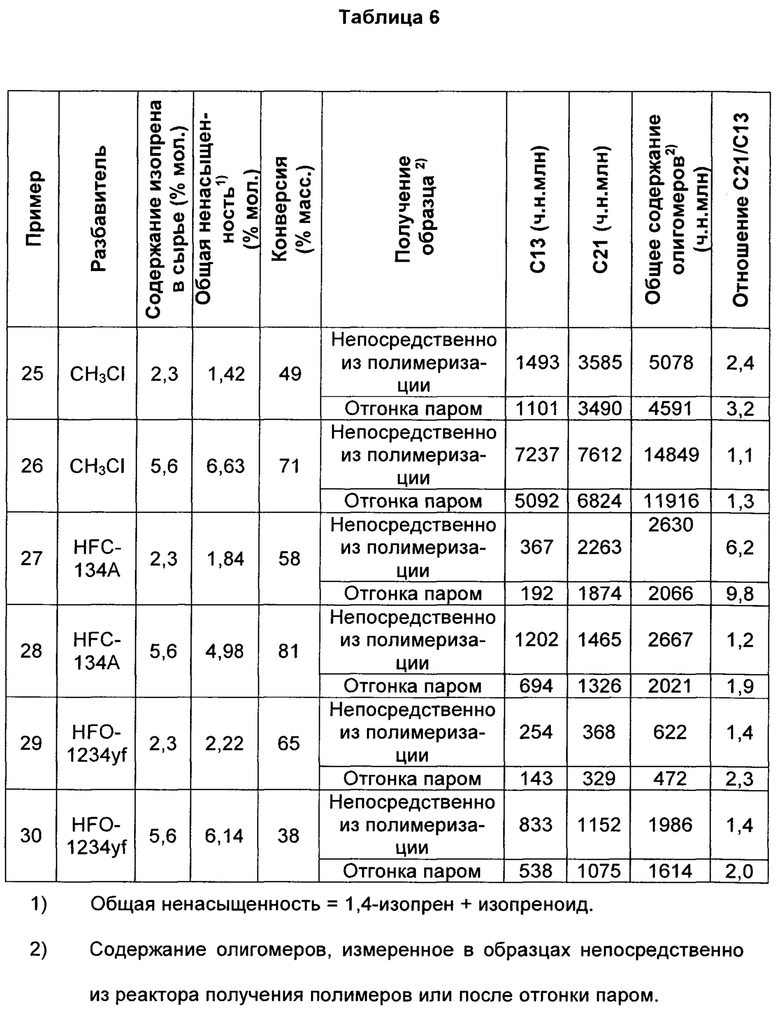
Как видно из таблицы 6, использование HFO1234yf в качестве разбавителя для полимеризации дает бутилкаучук со значительно более низкими количествами циклических олигомеров по сравнению с MeCl и HFC-134A. Уровни олигомеров, измеренные для образцов, взятых непосредственно из полимеризации, являются истинным значением общего содержания олигомеров, образованных при реакции. Данные для олигомеров, представленные в таблице 6 для образцов, взятых непосредственно из полимеризации, показали такие же тенденции, как наблюдались для данных таблицы 5. Очевидно, что каучук, полученный при помощи HFO1234yf (пр. 29) в качестве разбавителя, содержит значительно меньшее общее количество олигомеров, чем полученный в MeCl (пр. 25) или HFC-134A (пр. 27). На фиг. 2 сравнивается общее содержание олигомеров для реакций, проводимых со стандартными уровнями изопрена (примеры 25, 27 и 29). Стадию очистки отгонкой паром проводили для оценки очистки продукта, происходящей при непрерывном процессе производства бутилкаучука. Стадия отгонки паром, как наблюдали, снижает содержание С13 предпочтительнее для бутилкаучука, полученного во всех разбавителях при аналогичных значениях. Это предполагается, поскольку, как известно, С13-олигомеры можно отгонять паром при конечном процессе.
Как также видно из таблицы 6, использование HFO1234yf в качестве разбавителя для полимеризации дает бутилкаучук со значительно меньшими количествами циклических олигомеров по сравнению с MeCl и HFC-134A при более высоких уровнях включения изопрена. Полимеризации проводили в присутствии увеличенных концентраций изопрена в сырье с различными разбавителями для получения бутилкаучука с высоким содержанием включенного изопрена. Аналогично тому, что наблюдали для реакций, проводимых при стандартных уровнях изопрена, низкое содержание олигомеров обеспечивалось в разбавителе HFO-1234yf (пр. 30) по сравнению с MeCl (пр. 26) или HFC-134A (пр. 28). На фиг. 3 сравнивается общее содержание олигомеров для реакций с высоким содержанием изопрена в сырье. После отгонки паром полимер, образованный в разбавителе HFO-1234yf с высоким включением изопрена, содержал значительно меньше олигомера, чем измерено для очищенного полимера, полученного в HFC-134А и MeCl.
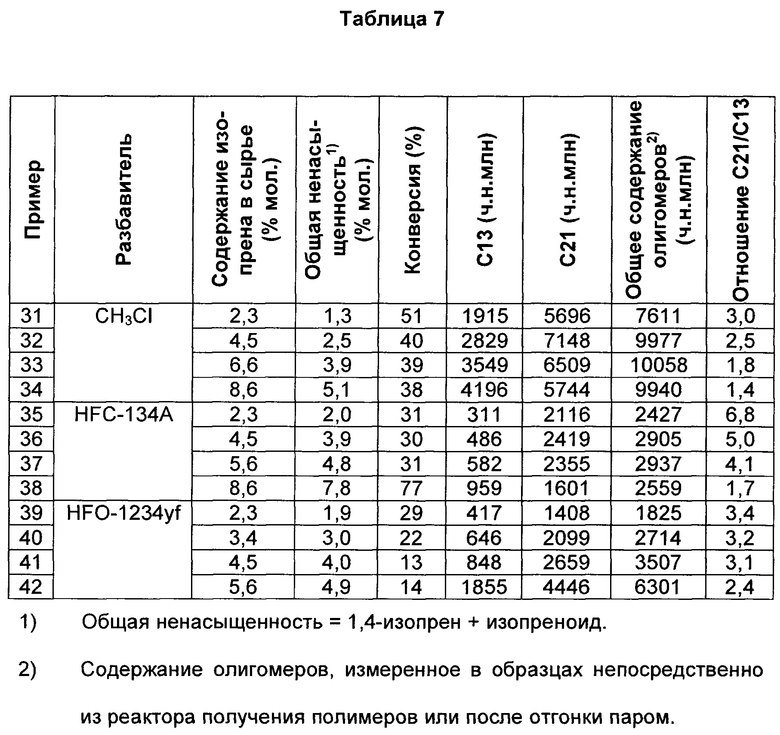
Как видно из таблицы 7 и фиг. 4, использование HFO-1234yf в качестве разбавителя в реакциях полимеризации дает более низкое отношение С21/С13-олигомеров по сравнению с HFC-134A в диапазоне содержаний изопрена 0-8% мол. Полимеризации проводили с различными отношениями изопрена в мономерном сырье, как указано в таблице 7 (примеры 31-42), и отношение С21- к С13-олигомерам измеряли для полимера, взятого непосредственно из реактора, по сравнению с полимеризациями, проводимыми с концентрациями изопрена в сырье, изменяющимися от 2,3 до 8,6% мол. на фиг. 4. Более низкое отношение С21/С13 наблюдали для бутилкаучука, полученного в HFO-1234yf по сравнению с HFC-134A при всех уровнях изопрена. Отношение С21/С13, как наблюдали, было практически аналогичным для материалов из HFO-1234yf по сравнению с реакциями, проводимыми в MeCl. Известно, что С13-олигомеры предпочтительно удаляли при процессах разделения и сушки каучука при непрерывном процессе производства бутилкаучука. Таким образом, более низкое отношение С21/С13 желательно для бутилкаучука, взятого непосредственно из реактора полимеризации, для получения готового продукционного бутилкаучука с низким общим содержанием олигомеров.
Пример F: Сниженное содержание изопреноида в бутилкаучуке
Бутилкаучуки, полученные в примерах 1-16, анализировали для определения влияния разбавителя на содержание изопреноида (с короткоцепочечной разветвленностью) в бутилкаучуке. Результаты представлены в таблице 8. Примеры 1-16 являются такими же, как в таблицах 1 и 2 выше.
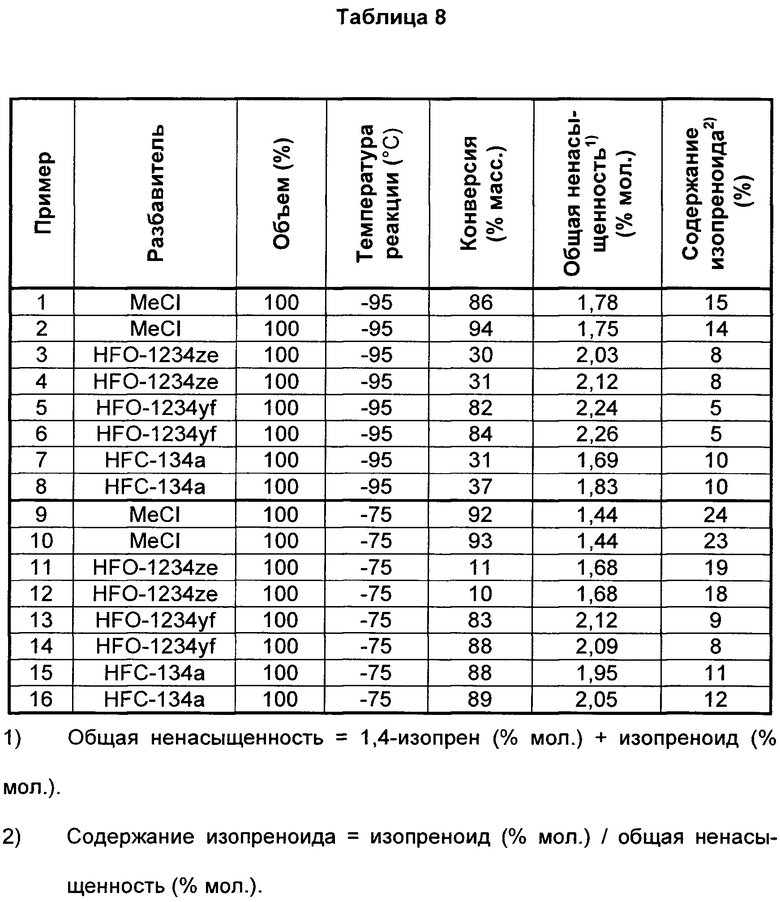
Как видно из таблицы 8, каучук, полученный при помощи 100% HFO-1234yf, HFC-134A или HFO-1234ze в качестве разбавителя, содержит более низкое измеренное содержание изопреноида (с короткоцепочечной разветвленностью) по сравнению с MeCl при использовании равной концентрации изопрена в смешанном сырье для реакции. Что еще более важно, видно при сравнении среднего значения проводимых дважды реакций, что полимеризации в HFO-1234yf дают значительно сниженные содержания изопреноида при -95°С. Содержание изопреноида для полимера, полученного в HFO-1234yf при -95°С (пр. 5 и 6), составляло 5,0% по сравнению со средними значениями 15% для MeCl (пр. 1 и 2), 10% для HFC-134A (пр. 7 и 8) и 8% для HFO-1234ze (пр. 3 и 4). Это важно, поскольку бутилкаучук с более низким содержанием изопреноида будет иметь большую общую ненасыщенность, доступную в 1,4-конфигурации звеньев для дальнейшей химической модификации и, как предполагается, будет иметь большую эффективность в последующих реакциях галогенирования для получения галогенбутилкаучука.
Короткоцепочечные ответвления возникают вследствие реакций передачи цепи реакционноспособной концевой группы цепи на саму себя с образованием 5-ти углеродных боковых цепочек, присоединенных к небольшому количеству 1,4-изопреновых звеньев вдоль основной цепи. Эти замещенные 1,4-изопреновые звенья в настоящем документе называются изопреноидными звеньями. Количество этих звеньев важно для получения галогенбутилкаучука, поскольку замещенный изопреноид не доступен для химической модификации галогенированием. Как видно из таблицы 8, при стандартных условиях полимеризации для получения бутилкаучука при помощи MeCl в качестве разбавителя содержание изопреноида в получаемом бутилкаучуке составляет 15%. Таким образом, при этих стандартных условиях только 85% добавленных изопреновых звеньев находятся в 1,4-конфигурации и доступны для участия в дальнейших реакциях модификации полимера, таких как галогенирование. Таким образом, предполагается, что процесс галогенирования будет происходить с большей эффективностью с сополимером бутилкаучука, имеющим более низкое содержание изопреноида, важный фактор для непрерывного процесса получения галогенбутилкаучука.
Такие же тенденции существуют при сравнении средних значений дважды проведенных полимеризаций, проводимых при высокой температуре (-75°С), причем материал, полученный в HFO-1234yf (пр. 13 и 14) содержит в среднем 9,0% изопреноида, HFC-134A (пр. 15 и 16) 12%, HFO-1234ze (пр. 11 и 12) 19%, a MeCl (пр. 9 и 10) 24%. Это показывает, что при более высоких температурах полимеризации, проводимые в HFO-1234yf или HFC-134А, также дают бутилкаучук, содержащий значительно меньше коротко-цепочечных разветвленностей, и, как предполагается, он будет подвергаться галогенированию более эффективно, чем материалы, полученные в других системах разбавителей.
Ряд полимеризаций проводили в чистых разбавителях с высоким содержанием изопрена в реакционном сырье для получения бутилкаучука с высоким содержанием изопрена. В таблице 9 представлены результаты полимеризаций, проводимых в чистых разбавителях при -95°С или со стандартным мольным отношением изопрена в сырье (2,3% мол.), или с высоким содержанием изопрена (5,6% мол.).
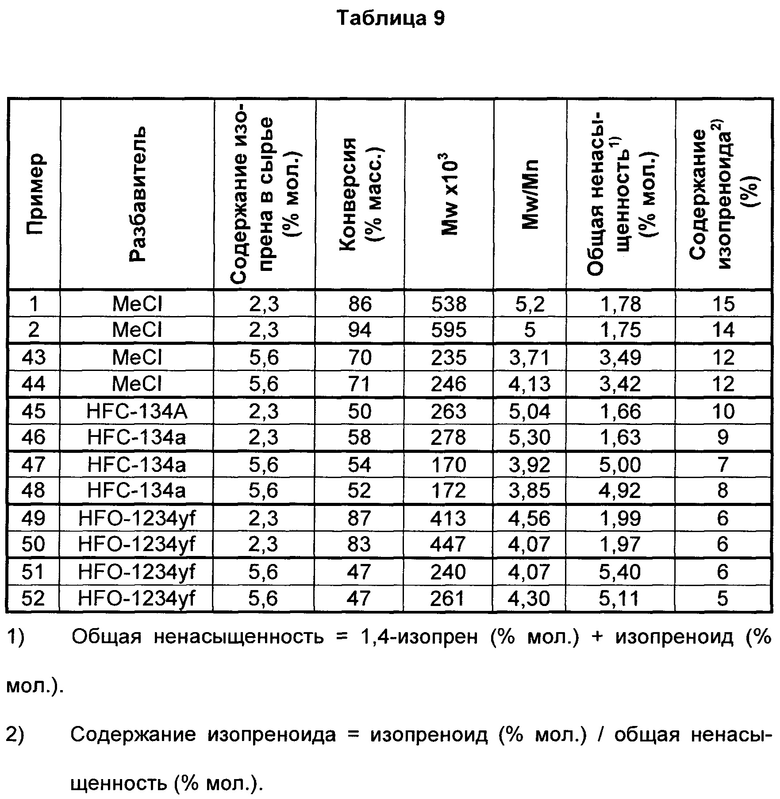
Как видно из таблицы 9, каучук, полученный при -95°С при помощи HFO-1234yf (пр. 49 и 50) или HFC-134A (пр. 45 и 46) в качестве разбавителя, имеет более низкое содержание изопреноида, чем с MeCl (пр. 1 и 2), при стандартном отношении изопрена в смешанном сырье (2,3% мол.). Также каучук, полученный при помощи HFO-1234yf в качестве разбавителя (пр. 49 и 50), имеет более низкое содержание изопреноида, чем с HFC-134A (пр. 45 и 46). Что еще более важно, тенденция сохраняется при высоком отношении изопрена в сырье (5,6% мол.), где HFO-1234yf и HFC-134A давали в среднем содержанием изопреноида 6% (пр. 51 и 52) и 8% (пр. 47 и 48), соответственно, по сравнению с 12% (пр. 43 и 44) для MeCl. Аналогично реакциям, проводимым при стандартных уровнях изопрена, бутилкаучук с высоким содержанием изопрена, полученный в HFO-1234yf, имел значительно более низкое содержание изопреноида по сравнению с полимеризациями, проводимыми в HFC-134A.
Полимеризации также проводили в смесях фторированного растворителя с MeCl в качестве разбавителя. Ряд полимеризаций проводили при помощи различных отношений HFO-1234yf и MeCl в смеси при стандартных условиях при -95°С, давая бутилкаучук со сниженным содержанием изопреноида при всех отношениях компонентов в смеси по сравнению с 100% MeCl. В таблице 10 представлены результаты полимеризаций, проводимых с различными отношениями HFO-1234yf и MeCl в смеси при -95°С.
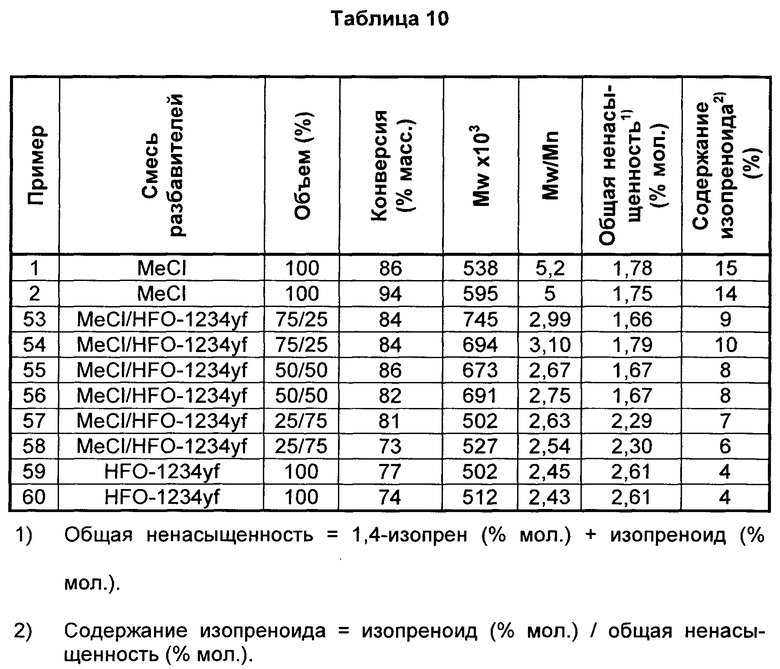
Как видно из таблицы 10, значительно более низкое содержание изопреноида получают при всех отношениях MeCl и HFO-1234yf в смеси по сравнению с 100% MeCl.
Кроме того, ряд полимеризаций проводили при помощи смесей 50/50 MeCl с HFO-1234yf в качестве разбавителя при температурах в диапазоне от -75°С до -95°С. Содержание изопрена в сырье составляло 2,3% мол. В таблице 11 представлены результаты полимеризаций, проводимых при отношениях 50/50 MeCl и HFO-1234yf в смеси при температурах в диапазоне от -75°С до -95°С. Как видно из таблицы 11, в диапазоне температур полимеризации, проводимые в смесях 50/50 HFO-1234yf с MeCl, давали бутилкаучук с более низким содержанием изопреноида из-за короткоцепочечной разветвленности вследствие реакций передачи цепи в полимере.
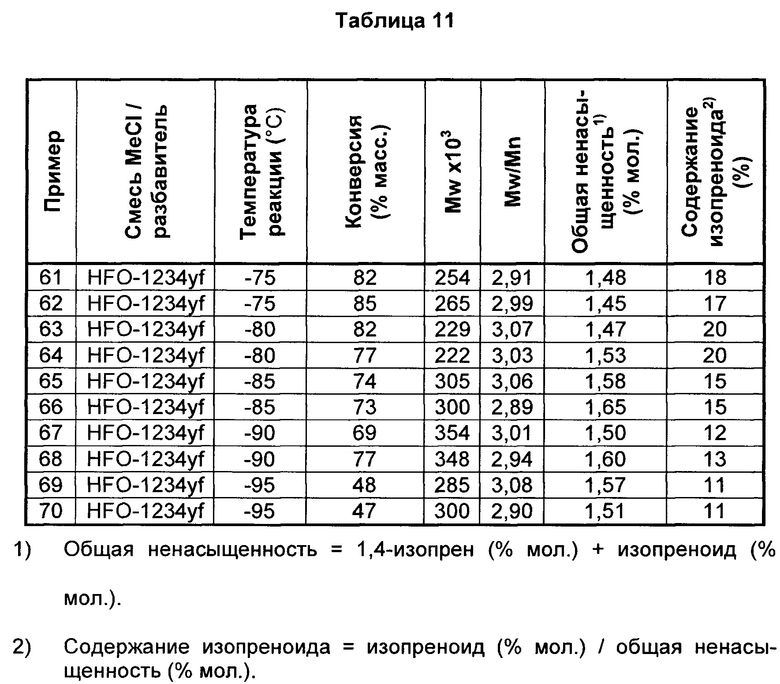
При сравнении полимеризаций при -95°С смесь HFO-1234yf с MeCl давала бутилкаучук, имеющий самое низкое содержание изопреноида (пр. 69 и 70, среднее = 11%) по сравнению с полимеризациями в чистом разбавителе MeCl (смотрите таблицу 8: среднее = 15%). Полимеризации, проводимые в смесях MeCl с HFO-1234yf, также давали бутилкаучук с низким содержанием изопреноида при -75°С (пр. 61 и 62, среднее = 18%). Материал на основе бутилкаучука, полученный при помощи смесей HFO-1234yf, имел сниженное содержание изопреноида по сравнению с 100% MeCl при всех температурах.
Пример G: Увеличенное содержание изопрена в бутилкаучуке
Ряд полимеризаций также проводили при помощи смесей 50/50 MeCl с HFO-1234ze или HFO-1234yf при стандартных условиях реакции при температурах в диапазоне от -75°С до -95°С. В таблице 12 представлены результаты полимеризаций, проводимых в смесях фторированных разбавителей с MeCl при различных температурах в диапазоне от -75°С до -95°С.
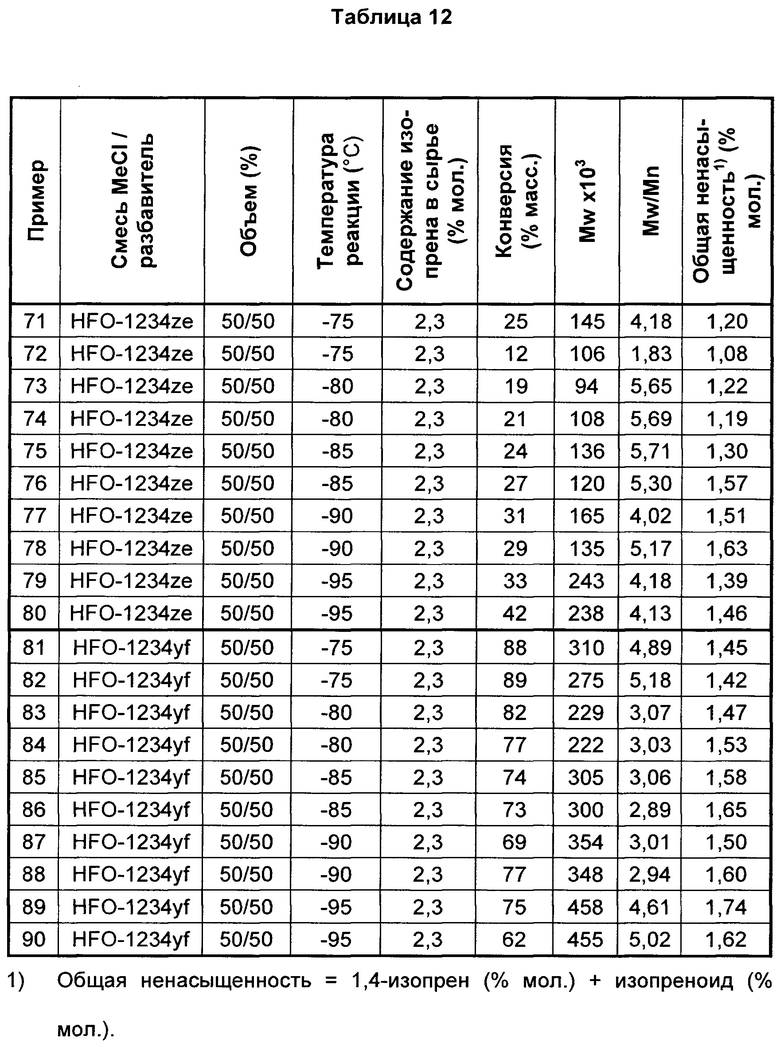
Как видно из таблицы 12, данные для смешанных систем разбавителей из фторированных растворителей с MeCl следуют такой же тенденции, что и данные, представленные в таблицах 1 и 2 для полимеризаций с чистым разбавителем. При аналогичной концентрации изопрена в реакционном сырье смесь MeCl/HFO-1234yf давала полимер с более высоким общим включением изопрена, чем полимеризации, проводимые со смесями MeCl с HFO-1234ze, при всех температурах ниже -75°С. Полимеризации, проводимые в смесях MeCl с HFO-1234yf, давали самый высокий уровень ненасыщенности полимера при всех температурах, аналогично результатам, наблюдаемым с чистыми разбавителями.
Включение изопрена сравнивали на основе отношения мономерного состава сырья (f=[M1]/[M2]) к составу сополимера (F=[М1]/[М2]). В литературе хорошо известно, что константы скорости для сополимеризации 2 мономеров могут быть описаны в Quirk R.P., Gomochak-Pickel D.L.; The Science and Technology of Rubber, 3rd Ed., Chap.2.
M1* + M1 → M1* (скорость = k11)
M1* + M2 → M2* (скорость = k12)
M2* + M2 → M2* (скорость = k22)
M2* + M1 → M1* (скорость = k21)
Константы сополимеризации мономеров получают из констант скорости следующим образом и выражают относительную активность каждого из двух типов растущих концевых групп цепи с их «собственным» типом мономера по сравнению с «другим» мономером:
r1=k11/k12; r2=k22/k12.
Текущий состав сополимера относительно концентраций мономеров в сырье можно определять при помощи следующего уравнения Майо-Льюиса:
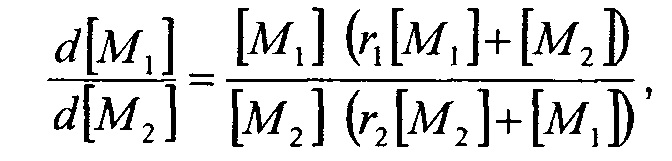
где:
f=[M1]/[M2] (отношение мономеров в сырье),
F=d[M1]/d[M2] (состав сополимера).
В случае, когда r1 >> 1 >> r2, будет происходить отклонение в составе полимера, образованного по реакции, причем предпочтительно мономер 1 раньше добавляют в реакцию. Второй мономер будет реагировать дальше на более поздних стадиях полимеризации, как только мономер 1 главным образом израсходуется. Конечно, хорошо известно, что константы сополимеризации для сополимеризации изобутилена/изопрена в MeCl составляют r1=2,5 и r2=0,4, давая отношение f/F близкое к 0,6. Для получения более статистического сополимера константы сополимеризации должны быть равными или близкими к 1 (r1=r2=1). В этом предельном случае f-отношение (f/F) будет ближе к 1,0.
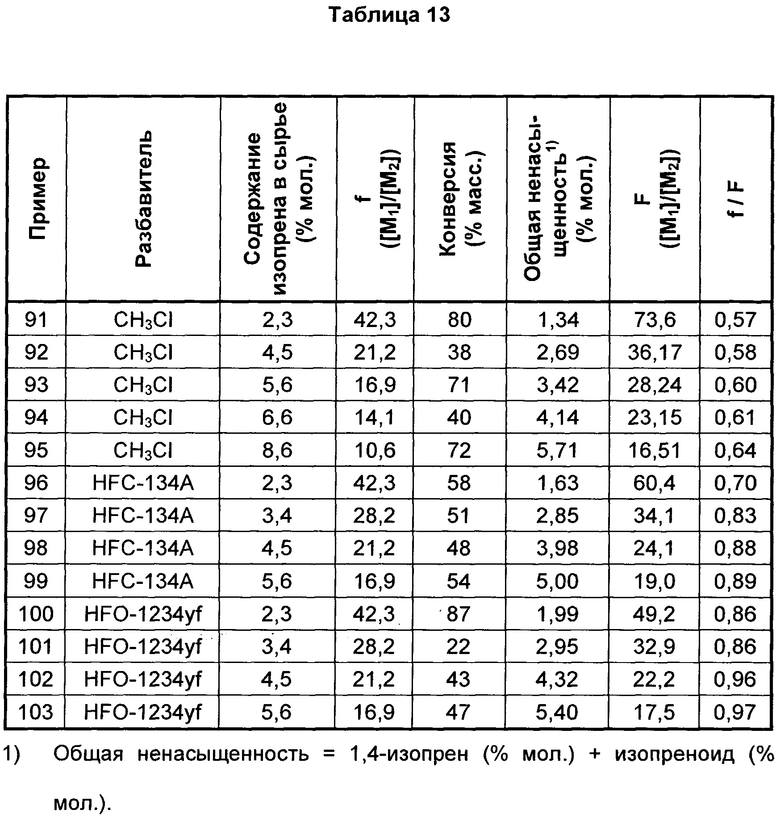
В таблице 13 представлены результаты полимеризаций, проводимых в чистых разбавителях при -95°С с содержаниями изопрена в сырье в диапазоне от 2,3 до 8,6% мол. Аналогично примерам в таблице 12, каучук, полученный при -95°С при помощи HFO-1234yf в качестве разбавителя, содержит значительно большую ненасыщенность из-за включенного изопрена по сравнению с другими системами разбавителей при всех содержаниях изопрена в сырье. На фиг. 5 сравниваются отношения мономеров в сырье и в сополимере (f-отношение) для полимеризаций в чистых разбавителях при -95°С. Наблюдали, что линия соответствия, построенная по данным, дает f-отношение 0,88 для бутилкаучука, полученного в HFO-1234yf. В сравнении линия соответствия f-отношения для HFC-134A составляет 0,74, а для MeCl - 0,58. Таким образом, очевидно, что константы сополимеризации в HFO-1234yf более точно подходят, давая повышенное включение изопрена при полимеризации и, таким образом, более статистический сополимер. HFO-1234yf дает увеличенное включение изопрена (f/F=0,9) по сравнению с HFC-134A (f/F=0,8) или MeCl (f/F=0,6).
Новые признаки настоящего изобретения станут очевидными специалистам в данной области техники при изучении подробного описания настоящего изобретения. Следует понимать, однако, что объем формулы изобретения не должен быть ограничен предпочтительными вариантам осуществления, указанными в примерах, но должен давать самое широкое толкование, согласующееся с описанием в целом.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОПОЛИМЕР С НИЗКИМ СОДЕРЖАНИЕМ ЦИКЛИЧЕСКИХ ОЛИГОМЕРОВ | 2015 |
|
RU2712144C2 |
| СОПОЛИМЕР С НИЗКИМ СОДЕРЖАНИЕМ ИЗОПРЕНОИДА | 2015 |
|
RU2687552C2 |
| СОПОЛИМЕР, ИМЕЮЩИЙ ВЫСОКОЕ СОДЕРЖАНИЕ МУЛЬТИОЛЕФИНА | 2015 |
|
RU2708081C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗООЛЕФИНОВЫХ ПОЛИМЕРОВ С ИСПОЛЬЗОВАНИЕМ ТРЕТИЧНОГО ПРОСТОГО ЭФИРА | 2019 |
|
RU2808455C2 |
| СПОСОБЫ ГАЛОИДИРОВАНИЯ | 2005 |
|
RU2422466C2 |
| 2, 3, 3, 3-ТЕТРАФТОР-1-ПРОПЕН В КАЧЕСТВЕ РАЗБАВИТЕЛЯ ДЛЯ ПОЛУЧЕНИЯ НОВЫХ БУТИЛКАУЧУКОВ | 2015 |
|
RU2699793C2 |
| РАЗБАВИТЕЛЬ ДЛЯ ПОЛУЧЕНИЯ БУТИЛКАУЧУКА | 2015 |
|
RU2674473C2 |
| СПОСОБ РАЗДЕЛЕНИЯ ФАЗ С ИСПОЛЬЗОВАНИЕМ ФТОРУГЛЕВОДОРОДА | 2007 |
|
RU2435791C2 |
| РАЗДЕЛЕНИЕ ПОЛИМЕРНЫХ СУСПЕНЗИЙ | 2008 |
|
RU2454432C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ УГЛЕВОДОРОДНОГО РЕЗИНОВОГО КЛЕЯ С ИСПОЛЬЗОВАНИЕМ ФТОРУГЛЕВОДОРОДНОГО РАЗБАВИТЕЛЯ | 2007 |
|
RU2445322C2 |
Изобретение относится к сополимерам изоолефина и мультиолефина и к способам их получения, включающим разбавитель тетрафторированный пропен. Способ получения сополимера включает полимеризацию по меньшей мере одного изоолефинового мономера с по меньшей мере одним мультиолефиновым мономером в присутствии по меньшей мере одной кислоты Льюиса и по меньшей мере одного инициатора в разбавителе, содержащем тетрафторированный пропен. Технический результат – поучение сополимеров с низкими уровнями циклических олигомеров, низкими уровнями изопреноидных структур и/или высокими уровнями изопреноида. 2 н. и 15 з.п. ф-лы, 6 ил., 13 табл., 103 пр.
1. Способ получения сополимера, причем способ включает полимеризацию по меньшей мере одного изоолефинового мономера, имеющего от 4 до 16 атомов углерода, по меньшей мере с одним мультиолефиновым мономером, имеющим от 4 до 14 атомов углерода, в присутствии по меньшей мере одной кислоты Льюиса и по меньшей мере одного инициатора и в разбавителе, содержащем тетрафторированный пропен.
2. Способ по п. 1, причем тетрафторированный пропен включает 1,3,3,3-тетрафтор-1-пропен (HFO-1234ze), 2,3,3,3-тетрафтор-1-пропен (HFO-1234yf), 1,1,3,3-тетрафтор-1-пропен, 1,1,2,3-тетрафтор-1-пропен, 1,2,3,3-тетрафтор-1-пропен или их смеси.
3. Способ по п. 1, причем тетрафторированный пропен включает 1,3,3,3-тетрафтор-1-пропен (HFO-1234ze), 2,3,3,3-тетрафтор-1-пропен (HFO-1234yf) или их смеси.
4. Способ по п. 1, причем тетрафторированный пропен включает 2,3,3,3-тетрафтор-1-пропен (HFO-1234yf).
5. Способ по п. 1, причем по меньшей мере один изоолефиновый мономер включает изоолефин, содержащий от 4 до 7 атомов углерода.
6. Способ по п. 5, причем по меньшей мере один изоолефиновый мономер включает изобутен, 2-метил-1-бутен, 3-метил-1-бутен, 2-метил-2-бутен, 4-метил-1-пентен или их смеси.
7. Способ по п. 1, причем по меньшей мере один мультиолефиновый мономер включает изопрен, бутадиен, 2,4-диметилбутадиен, пиперилен, 3-метил-1,3-пентадиен, 2,4-гексадиен, 2-неопентилбутадиен, 2-метил-1,5-гексадиен, 2,5-диметил-2,4-гексадиен, 2-метил-1,4-пентадиен, 2-метил-1,6-гептадиен, циклопентадиен, метилциклопентадиен, циклогексадиен, 1-винил-циклогексадиен или их смеси.
8. Способ по п. 1, дополнительно включающий полимеризацию по меньшей мере одного дополнительного мономера по меньшей мере с одним изоолефиновым мономером и по меньшей мере одним мультиолефиновым мономером, причем по меньшей мере один дополнительный мономер включает индол, α-метилстирол, п-метилстирол, хлорстирол или их смеси.
9. Способ по п. 1, причем кислота Льюиса включает дихлорид этилалюминия (EADC), хлорид диэтилалюминия (DEAC) и/или их смеси.
10. Способ по п. 1, причем инициатор включает источник протонов и/или катионоген.
11. Способ по п. 1, причем мономеры полимеризуют при температуре в диапазоне от приблизительно -120°С до приблизительно -50°С.
12. Способ по п. 1, причем мономеры полимеризуют при температуре в диапазоне от приблизительно -100°С до приблизительно -75°С.
13. Способ по п. 1, причем мономеры полимеризуют при температуре в диапазоне от приблизительно -98°С до приблизительно -90°C.
14. Способ по п. 1, причем мономеры полимеризуют при температуре в диапазоне от приблизительно -95°С до приблизительно -75°С.
15. Способ по любому из пп. 1-14, причем разбавитель дополнительно включает метилхлорид.
16. Способ по п. 15, причем отношение метилхлорида к тетрафторированному пропену в разбавителе равно приблизительно 50:50.
17. Сополимер, полученный способом, как определено в любом из пп. 1-16.
| СПОСОБЫ ПОЛИМЕРИЗАЦИИ | 2003 |
|
RU2362786C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ПОЧВООБРАБАТЫВАЮЩИЙ КАТОК | 2022 |
|
RU2787122C1 |
| ПОЛИМЕРЫ, ПО СУЩЕСТВУ СВОБОДНЫЕ ОТ ДЛИННОЦЕПОЧЕЧНОГО РАЗВЕТВЛЕНИЯ, ПЕРЕКРЕСТНЫЕ | 2003 |
|
RU2344145C2 |
Авторы
Даты
2019-07-25—Публикация
2015-04-28—Подача