Изобретение относится к области фармацевтической химии и технологии, а именно к синтезу 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана (1) в качестве исходного соединения для получения оксигенирующих эмульсий, используемых как терапевтические средства наружного применения (кремы, мази, линименты), а также как оксигенирующий компонент культуральных сред в биотехнологических процессах [1].
Ранее было показано, что оксигенирующие композиции для наружного применения, полученные на основе перфтордекалина и/или его смеси с перфторметилциклогексилпиперидином (препарат «Перфторан»), перфтороктилбромида, перфтортрипропиламина, при местном применении ускоряют процесс заживления зубных лунок, ожоговых ран и нарушения трофики [RU 2237473, RU 2225209, RU 2259819; КЛИГУНЕНКО Е.Н. и др. 1999; Хрупкин В.И. и др. 1997]. Ключевые механизмы: подавление развития патогенной анаэробной микрофлоры, значимое улучшение кровотока (микрокатализ с участием NO) у животных и у людей, а также трофики в целом, подавление вторичного повреждения, вызываемого активными формами кислорода, которые продуцируют гиперактивированные лейкоциты, уменьшение гнойной инфильтрации и соответствующее ускорение регенерации при подсадке лоскута, выдержанного сутки в оксигенирующей эмульсии (например, в перфторане).
В то же время вышеперечисленные фторуглероды и эмульсии на их основе имеют ряд существенных недостатков. Температуры кипения этих фторуглеродов лежат в интервале 130°C (перфтортрипропиламин) - 185°C (перфторметилциклогексилпиперидин), т.е. обладают достаточно высокой летучестью, а их эмульсии недостаточно стабильны при стерилизации в автоклаве при 120°C и длительном хранении (эмульсия перфторана должна храниться в замороженном состоянии при минусовых температурах).
Целью настоящего изобретения является синтез фторсодержащих соединений, обладающих, подобно другим фторуглеродам, высокой растворяющей способностью по отношению к кислороду и характеризующихся пониженной летучестью, повышенной, по сравнению с перфторалканами, липофильностью, и образующие эмульсии, устойчивые как при длительном хранении при плюсовых температурах, так и при стерилизации в автоклаве при 120°C.
Указанная цель достигается синтезом 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана формулы  образующегося при анодном окислении (электросинтезом Кольбе) 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты
образующегося при анодном окислении (электросинтезом Кольбе) 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты 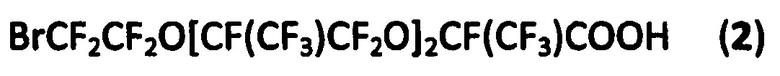 и характеризующегося низкой летучестью (т. кип. 117-119°C/1Torr):
и характеризующегося низкой летучестью (т. кип. 117-119°C/1Torr):
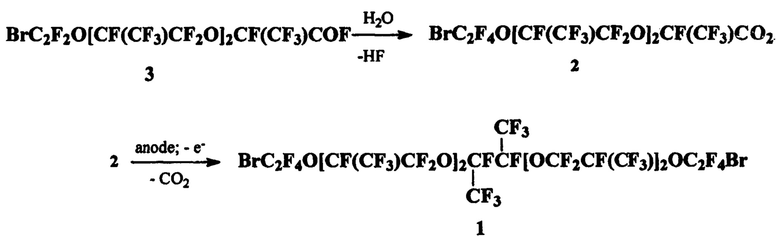
Кислота 2 легко получается омылением соответствующего фторангидрида формулы  описанного в [2]. Очистка дибромида 1 до фармакопейной чистоты (содержание фторид-иона не более 5×10-5 вес. %) достигается его обработкой 40%-ным водн. раствором K2CO3 с последующей перегонкой в вакууме.
описанного в [2]. Очистка дибромида 1 до фармакопейной чистоты (содержание фторид-иона не более 5×10-5 вес. %) достигается его обработкой 40%-ным водн. раствором K2CO3 с последующей перегонкой в вакууме.
Дибромид 1 характеризуется высокой растворяющей способностью по отношению к кислороду (53 об. % при рО2 760 мм. рт.ст.) и в присутствии эмульгаторов при экструзии под высоким давлением образует 10%-ные водные субмикронные эмульсии, стабильные при длительном хранении без замораживания при 8÷10°C, выдерживающие стерилизацию в автоклаве при 121°C.
При внутривенном введении прямых субмикронных эмульсий дибромида 1 в воде, полученных на гомогенизаторе модели «Донор» при давлении до 800 кг/см2 со средним диаметром частиц от 30 до 120 нм (по показаниям лазерного наносайзера Coulter 15 фирмы Becman-Coulte, США), лабораторным крысам линии Wistar в дозе 50 мл на кг массы тела признаков токсического воздействия на животных не обнаружено. После внутривенного введения полученных эмульсий в дозе 20 мл на кг кроликам - высокочувствительным к эмульсионным препаратам - также признаков повреждения не выявлено, и кролики прожили более года до искусственной?? (есть естественная?) эвтаназии.
Использование дибромида 1 в качестве оксигенирующего компонента питательной среды при глубинном культивировании S. purpurogeniscleroticus ВБМ 81 (по методике, описанной в работе [1]) привело к ускорению роста и увеличению выхода биомассы стрептомицета в ~3,5 раз и выхода даунорубицина в ~10 раз. Потери дибромида 1 в цикле культивирование-стерилизация составляют не более 0,5%. Таким образом, полученные данные свидетельствуют об эффективности применения дибромида 1 в биотехнологических процессах.
Для лучшего понимания настоящего изобретения приводим примеры получения дибромида 1 и эмульсий на его основе.
Пример 1. Получение кислоты 2.
К смеси 30 г (44 ммол) 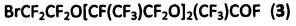 и 10 мл гептана прибавили 5 мл (280 ммол) воды, интенсивно перемешивали 30 мин, прибавили 5 мл H2SO4, органический слой отделили, перегнали в вакууме, собирая фракцию, кипящую в интервале 90-150°/1Torr. Повторной перегонкой получили 24,7 г (82,6%) 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты (2), т.кип. 133-135°/17Torr. Найдено %: С 20,00; Н 0,20; F 56,37; Br 11,36. C11BrHF20O5. Вычислено %: С 19,61; Н 0,15; F 56,43; Br 11,89.
и 10 мл гептана прибавили 5 мл (280 ммол) воды, интенсивно перемешивали 30 мин, прибавили 5 мл H2SO4, органический слой отделили, перегнали в вакууме, собирая фракцию, кипящую в интервале 90-150°/1Torr. Повторной перегонкой получили 24,7 г (82,6%) 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты (2), т.кип. 133-135°/17Torr. Найдено %: С 20,00; Н 0,20; F 56,37; Br 11,36. C11BrHF20O5. Вычислено %: С 19,61; Н 0,15; F 56,43; Br 11,89.
Пример 2. Получение дибромида 1.
В электролизер снабженный водяной рубашкой, магнитной мешалкой и обратным холодильником загружают 9.8 г (14 ммол) кислоты 2, 0,122 г (2,2 ммол) КОН, 1 мл H2O и 29 мл CH3CN. Анод - сплав платина +10% иридия (15 см2). Катод - нержавеющая сталь (2 см2). Плотность тока 51.6 мА.см-2. Ток - 0,8 А, температура электролиза 20°C. Теоретическое количество электричества в расчете на израсходование 11,8 ммол кислоты 2 составляет 0,32 А⋅час. Всего пропущено 0,37 А⋅час электричества. Исходное напряжение на электролизере 24 В. Конечное напряжение на электролизере после 28 минут электролиза составило 40 В. По окончании электролиза электролит промыли водой, 40%-ным водным раствором K2CO3, органический слой отделили, перегнали и получили 7,1 г (80% выход по веществу) и (72% выход по току) 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана 1, т. кип. 117-119°C/1Torr. Найдено %: С 19,09; F 60,43; Br 12,38. C20Br2F40O6. Вычислено %: С 19,11; F 60,51; Br 12,74.
Спектр 19F ЯМР1:
BrCF2CF2OCF(CF3)CF2OCF(CF3)CF2OCF(CF3)CF(CF3)OCF2CF(CF3)OCF2CF(CF3)OC F2CF2Br
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
-71,1 + -72,0 (2F1 + 2F20); -80,45÷-86,14 (группа сигналов 30F2+4+5+7+8+10+12+13+15+16+18+19);.-143,2 (1F9+1F11); -147-147.5 (1F3+6+14+17).
Масс-спектр 1 (M/Z, отнесение): 727 [C12BrF24O3]+; 705 [C12BrF22O4]+; 667 [C12F25O3]+; 611 [C12BrF22O3]+; 551 [C10F21O2]+; 529 [C10F19O3]+; 511 [C8BrF16O2]+; 395 [C6BrF12O2]+; 385 [C8BrF16O2]+; 345 [C5BrF10O]+; 335 [C6F13O]+; 313 [C6F11O2]+; 285 [C5F11O]+; 229 [C3BrF6]+; 219 [C4F9]+; 179 [C2BrF4]+ (100%); 147 [C3F5O]+; 131 [C3F5]+; 100 [C2F4]+; 69 [CF3]+.
Пример 3. Очистка дибромида 1.
Смесь 20 г дибромида 1 и 10 мл 40%-ного водн. раствора K2CO3 интенсивно перемешивали 5 час при 50-70°C, летучие продукты отогнали в охлаждаемый приемник (-78°C) в вакууме сначала водоструйного, а затем масляного насоса. Дистиллят отогрели, органический слой отделили, высушили над MgSO4 и перегонкой в вакууме получили 19 г дибромида 1 (т. кип. 117-119°C/1 Torr) с содержанием фторид-иона 1,5×10-5%.
Пример 4. Получение эмульсии на основе дибромида 1.
В 100 весовых частях дистиллированной воды растворяли 10 весовых частей неионогенного поверхносто-активного соединения Плюроника F68 и при постоянном интенсивном перемешивании на турбинной мешалке при скорости вращения 8000 оборотов в мин к полученному раствору добавляли 20 объемных частей дибромида 1. В результате получали грубодисперсную эмульсию с распределением частиц по размерам от 10 мкм до 1000 мкм. Грубодисперсную эмульсии измельчали путем экструзии по давлением от 350 до 800 ат (кг/см2) до достижения среднего размера 100 нм при распределении частиц по размерам от 30 нм до 160 нм. Далее полученную нанодисперную эмульсию, содержащую 20 об. % бромированного перфторуглерода, смешивали с равным объемом водно-солевого раствора. Таким образом получалась изотоничная биологическим жидкостям готовая форма, содержащую 10 об. % бромированного перфторуглерода, 4% Плюроника F68,100 mM NaCl, 5 mМ KCl, 1 mM MgCl2, 2 mM Na2HPO4,8 mM NaHCO3, (pH 7,3). NaCl - 5,85 g, KCl - 0,375 g, MgCl2 - 0,1 g, Na2HPO4 - 0,376 g, NaHCO3 - 0,67 g. (В расчете на 1 л. эмульсии)
Готовую форму 10% эмульсии хранили без замораживания при температуре  .
.
Пример 5. Получение эмульсии на основе бромида 1 (вариант 2).
Аналогично получена эмульсии на основе бромида 1 с использованием Проксанола 268 в качестве ПАВ со средним размером частиц 100 нм при распределении частиц в интервале 30-180 нм. Готовую форму 10% эмульсии хранили без замораживания при температуре 2÷6°C. Размер частиц контролировали с помощью лазерного наносайзера.
Пример 6. Применение эмульсии для лечения Ожеговых ран.
Полученную по примеру 4 наноэмульсию с содержанием 20 об % фторгулеродной фазы без солевого раствора со средним размером частиц 120 нм в количестве 50 мл добавляли порционно по 5 мл в официнальную мазь, предназначенной для стимуляции заживления кожных покровов, полученную согласно описанию патента Российского патентна №2026072, перемешивали с помощью механической мешалки до получения однородной массы. Полученную модифицированную мазь в количестве 1 г. наносили дважды с интервалом 2 дня на обожженную кожу крыс в межлопаточной области. В контрольных экспериментах, выполненных на 7 крысах-самцах линии Вистар общей массой 300 г, использовали мазь исходной рецептуры. В опытной группе, также состоящей из 7 животных использовали для лечения ожога модифицированную эмульсией мазь. При ежедневном контроле состояния ожоговой раны фиксировали изменение площади ожога и время освобождения раны от ожогового струпа. При использовании полученной согласно описанию модифицированной мази площадь ожога уменьшалась существенно быстрее так, что рана освободилась от струпа в опытной группе через 6-7 дней, тогда как в контрольной группе процесс эпителизации и освобождения раны от струпа занимал в среднем 11 дней.
Пример 7. Использование дибромида 1 в качестве компонента культуральных сред. Влияние дибромида 1 на биосинтез даунорубицина культурой S. Purpurogeniscleroticus ВБМ 81.
Культивирование стрептомицета S. Purpurogeniscleroticus ВБМ 81 в среде на основе соевой муки (исходная концентрация микробной культуры - 0,5 мг/см3, инкубирование выполняли на шуттеле в течение 10 суток при 28-29°C, 230 об/мин) в присутствии 2 об. % дибромида 1, что привело к увеличению биомассы стрептомицета в 3,5 раза и выхода даунорубицина в 10,2 раза по сравнению с контрольным опытом.
Литература
1. А.Ю. Плетнева, диссертация на соискание ученой степени кандидата биологических наук, М., МГА ветеринарной медицины и биотехнологии им. К.И. Скрябина, 2007.
2. RU 2237473 Дроботов В.Н. Кричевский А.Л. (RU); Галеев И.К. (RU); Лоскутников С.Ю. (RU); Казанин К.С. СПОСОБ ЛЕЧЕНИЯ РАН
3. RU 2225209 Захаров В.Ю. Горшков Ю.В. Дедов А.С. Любимов А.Н. Осипов А.П. Средство для лечения ожогов и ран.
4. RU 2259819 Кузнецова И.Н., Маевский Е.И., Германов Евгений Павлович. ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ
5. RU 2026072 Оксиноид О.Э„ Сидляров Д.П., Захаров В.В., Николаев А.В., Ахсянов У.У., Литвиненко Ю.А., Краснопольский Ю.М., Темиров Ю.П.. СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ РЕПАРАТИВНЫХ ПРОЦЕССОВ
6. КЛИГУНЕНКО Е.Н. и др. Местное применение перфторана в комплексном лечении длительно заживающих ран, в кн.: Перфторорганические соединения в биологии и медицине. - Пущино, 1999, с. 146-149.
7. Хрупкин В.И. Писаренко Л.В. Мороз В.В. Хоменчук А.И Использование эмульсии перфторуглеродов в местном лечении ран, осложненных хирургичекой инфекцией Вестник хирургии им. И.И. Грекова. 1997, T. 156, N4. C. 53-55.
8. RU 2497801 Михайлова З.А., Тютюнов А.А., Игумнов С.М., Стерлин С.Р. Окса- и полиоксаперфторалкилбромиды и способ их получения.
| название | год | авторы | номер документа |
|---|---|---|---|
| α,ω-ДИБРОМПОЛИОКСАПЕРФТОРАЛКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЭМУЛЬСИИ МЕДИКО-БИОЛОГИЧЕСКОГО НАЗНАЧЕНИЯ НА ИХ ОСНОВЕ | 2016 |
|
RU2707553C2 |
| α-БРОМ-ω-ГАЛОГЕНПЕРФТОРПОЛИЭФИРЫ В КАЧЕСТВЕ ОСНОВЫ ГАЗОТРАНСПОРТНЫХ КОМПОЗИЦИЙ МЕДИКО-БИОЛОГИЧЕСКОГО НАЗНАЧЕНИЯ | 2019 |
|
RU2707081C1 |
| 2-БРОМТЕТРАФТОРЭТИЛПЕРФТОРАЛКИЛОВЫЕ ЭФИРЫ ДЛЯ ПОЛУЧЕНИЯ ЭМУЛЬСИЙ МЕДИКО-БИОЛОГИЧЕСКОГО НАЗНАЧЕНИЯ | 2017 |
|
RU2696871C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ В ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА | 2016 |
|
RU2626600C1 |
| РЕАБИЛИТАЦИОННАЯ ПРОТИВОПРОЛЕЖНЕВАЯ КРОВАТЬ ДЛЯ ОЖОГОВЫХ БОЛЬНЫХ | 2012 |
|
RU2484804C1 |
| 2,3,5,6-Тетраазидопиридин-4-карбонитрил и способ его получения | 2016 |
|
RU2640415C2 |
| 3,4,5-Триазидопиридин-2,6-дикарбонитрил и способ его получения | 2016 |
|
RU2639303C2 |
| ШТАММ БАКТЕРИЙ STENOTROPHOMONAS SP. ВКМ В-2818D - ДЕСТРУКТОР НЕФТИ И НЕФТЕПРОДУКТОВ | 2018 |
|
RU2687154C1 |
| КОНТРАСТИРУЮЩИЙ АГЕНТ ДЛЯ ВВЕДЕНИЯ ФТОР-19 МЕТКИ В БЕЛКИ, СОДЕРЖАЩИЕ ОСТАТКИ ЛИЗИНА | 2015 |
|
RU2599500C1 |
| Способ получения 2,3,5,6,8-пентагидрокси-1,4-нафтохинона (спинохрома D) и промежуточные соединения, используемые в этом способе | 2016 |
|
RU2632668C2 |
Изобретение относится к области фармацевтической химии и технологии, а именно к синтезу 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана, используемого для получения оксигенирующих прямых эмульсий медицинского и биотехнологического назначения, например для лечения ожогов. Синтез 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана заключается в анодном окислении 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты. 2 н.п. ф-лы, 7 пр.
1. Способ получения 1,20-дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозана, заключающийся в анодном окислении 11-бром-3,6,9-триоксаперфтор-2,5,8-триметилундекановой кислоты.
2. 1,20-Дибром-3,6,9,12,15,18-гексаоксаперфтор-4,7,10,11,14,17-гексаметилэйкозан в качестве фторорганической основы эмульсий медико-биологического назначения.
| СПОСОБ ЛЕЧЕНИЯ РАН | 2003 |
|
RU2237473C1 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2004 |
|
RU2259819C1 |
| ОКСА- И ПОЛИОКСАПЕРФТОРАЛКИЛБРОМИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2497801C1 |
| Хрупкин В.И | |||
| и др | |||
| "Использование эмульсии перфторуглеродов в местном лечении ран, осложненных хирургической инфекцией" Вестник хирургии им | |||
| И.И.Грекова, 1997, т.156, 4, с | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
Авторы
Даты
2019-08-07—Публикация
2016-11-23—Подача