ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к микобактерии туберкулеза (Mycobacterium tuberculosis). В частности, настоящее изобретение относится к композициям и способу обнаружения Mycobacterium tuberculosis.
УРОВЕНЬ ТЕХНИКИ
Mycobacterium tuberculosis (МБТ) представляет собой серьезную угрозу здоровью населения во всем мире, и она находится на втором месте после ВИЧ/СПИД, на долю которого приходится наибольшее количество смертей от одного инфекционного агента по всему миру (Warren и др., Differentiation of Mycobacterium tuberculosis complex by PCR amplification of genomic regions of difference, 2006 Jul, Int J Tuberc Lung Dis, 10 (7):818-822). По сообщению Центра по контролю и профилактике заболеваний (CDC) в 2011 г. было зафиксировано 8,7 миллиона новых случаев МБТ (13% были коинфицированы ВИЧ); 1,4 миллиона людей погибли от МБТ, включая почти один миллион смертей ВИЧ-отрицательных индивидов и 430000 смертей людей, которые были ВИЧ-положительными. Всемирная Организация Здравоохранения (ВОЗ) сообщила, что в 2011 году МБТ была одним из ведущих факторов, приводящих к смерти женщин: 300000 смертей было зарегистрировано среди ВИЧ-отрицательных женщин и 200000 смертей - среди ВИЧ-положительных женщин. Она находится среди трех самых частых причин смерти женщин в возрасте от 15 до 44 лет. МБТ также является ведущим фактором, приводящим к смерти людей, живущих с ВИЧ, являясь причиной четверти всех их смертей. В 2011 году было зафиксировано 0,5 миллиона случаев и 64000 смертей среди детей. Распространенность заболеваемости МБТ с множественной лекарственной устойчивостью (МЛУ-БТ) растет, и она присутствует практически во всех исследованных странах. Географически распространенность МБТ наиболее высока в Азии и Африке. По сообщениям ВОЗ общая частота обнаружения случаев с МБТ все еще менее 60% в странах с низким уровнем доходов (LIC) и лишь 66% во всем мире. Другими словами, из приблизительно 8,7 миллиона людей, заболевших от МБТ в 2011 году, 2,9 миллиона с активным заболеванием не были диагностированы и зарегистрированы в государственных программах по контролю МБТ. Кроме того, лишь 19% случаев МЛУ-МБТ были надлежащим образом диагностированы и зарегистрированы. Менее чем у 1 из 20 вновь диагностированных пациентов с МБТ был доступ к тестированию устойчивости МБТ к лекарственным средствам. Вследствие риска распространения МБТ, потенциального возникновения устойчивых к лекарственным средствам штаммов и тяжести данного заболевания у пациентов, инфицированных ВИЧ-1, чрезвычайно важно разработать недорогой, быстрый и точный молекулярный тест на выявление МБТ. Обычное культивирование требует больших затрат времени и может занимать до шести недель. Исследование под микроскопом кислотоустойчивых мазков представляет собой наиболее быстрый способ обнаружения микобактерий, но этот способ нечувствителен и неспецифичен.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данной заявке предложены композиции и способы, подходящие для обнаружения МБТ. В частности, в данной заявке предложены наборы, реагенты, реакционные смеси и способы, в которых их применяют для процедур амплификации и обнаружения нуклеиновых кислот, которые позволяют специфично и чувствительно обнаружить МБТ в образцах. Такие композиции и способ включают праймеры, зонды, наборы праймеров, наборы праймеров и зондов, и способы обнаружения комплекса МБТ в различных образцах из человека, таких как мокрота, бронхоальвеолярный лаваж (БАЛ) и осадки образцов мокроты и БАЛ в N-ацетил-L-цистеине (NALC)-NaOH.
В некоторых вариантах реализации два или более из полинуклеотидных реагентов, представленных в данной заявке в виде последовательностей SEQ ID NO: 1-9, объединены в одной композиции (например, в комплекте, наборе реагентов, реакционной смеси и т.д.). В некоторых вариантах реализации один или более, или все реагенты на основе нуклеиновых кислот содержат детектируемую молекулу (например, синтетическую метку). В некоторых вариантах реализации указанные композиции содержат один или более праймеров с последовательностями SEQ ID NO: 1-4 или 7-8. В некоторых вариантах реализации указанные композиции содержат одну или более пар праймеров с последовательностями SEQ ID NO: 1 и 2, 3 и 4, или 7 и 8. В некоторых вариантах реализации указанные композиции содержат один или более зондов (например, меченых зондов) с последовательностями SEQ ID NO: 5, 6 или 9. В некоторых вариантах реализации указанные композиции содержат наборы праймеров и зондов: последовательности SEQ ID NO 1-2 и 5, 3-4 и 6, или 7-9. В некоторых вариантах реализации указанные композиции содержат реагенты для внутреннего контроля, такие как последовательности SEQ ID NO: 7-9. В некоторых вариантах реализации указанные композиции содержат систему двух зондов, включающую последовательности SEQ ID NO: 5 и 6.
В некоторых вариантах реализации в указанных композициях и способах используют комплекты реагентов, содержащие полинуклеотидный компонент, включающий праймеры, зонды, наборы праймеров и/или наборы зондов. В некоторых вариантах реализации указанный полинуклеотидный компонент в композиции состоит из комбинации праймеров, зондов, набора праймеров или набора зондов, описанных выше. Как реакционные смеси указанные композиции могут состоять из таких полинуклеотидов, а также из любых полинуклеотидов, содержащихся в образце (т.е. единственными не принадлежащими образцу молекулами нуклеиновых кислот являются полинуклеотиды, представленные в SEQ ID NO: 1-9, отдельно или в комбинациях (например, в комбинациях, описанных выше).
Наборы праймеров, предложенные в данной заявке, содержат два праймера, и они являются подходящими для амплификации целевых последовательностей, например, с помощью ПЦР. В некоторых вариантах реализации указанные композиции содержат по меньшей мере два праймера и один или более (например, два или более) зондов, которые позволяют обнаружить ампликоны, полученные с помощью праймеров.
Также в данной заявке предложены способы обнаружения МБТ в образце. В некоторых вариантах реализации указанные способы включают (а) получение реакционной смеси, содержащей реагенты для амплификации нуклеиновых кислот, по меньшей мере полинуклеотидный праймер или зонд, описанный в данной заявке, и тестируемый образец, потенциально содержащий по меньшей мере одну целевую последовательность; и (b) помещение смеси в условия амплификации с получением по меньшей мере одной копии последовательности нуклеиновой кислоты, комплементарной целевой последовательности. В некоторых вариантах реализации указанный способ дополнительно включает обнаружение полученных ампликонов. В некоторых вариантах реализации указанное обнаружение включает (с) гибридизацию зонда с последовательностью нуклеиновой кислоты, комплементарной целевой последовательности, с получением гибрида, содержащего зонд и последовательность нуклеиновой кислоты, комплементарную целевой последовательности; и (d) обнаружение, непосредственно или опосредованно, указанного гибрида, свидетельствующее о присутствии МБТ в тестируемом образце.
Кроме того, если амплификация представляет собой ПЦР, или аналогичный термоциклический процесс амплификации, то этап (b) можно повторить несколько раз, чтобы увеличить количество копий целевой последовательности.
Согласно другому варианту реализации обнаруживают как МБТ, так и один или более дополнительных инфекционных агентов (например, ВИЧ) или других молекул нуклеиновых кислот (например, человеческих последовательностей). Соответственно, в некоторых вариантах реализации композиции содержат реагенты для обнаружения таких других агентов или молекул нуклеиновых кислот.
В некоторых вариантах реализации в указанных композициях и способах дополнительно используют контрольные реагенты или компоненты набора (например, положительные контроли, отрицательные контроли). В некоторых вариантах реализации указанные контрольные реагенты включают синтетическую целевую нуклеиновую кислоту. В некоторых вариантах реализации указанные контрольные реагенты включают реагенты для обнаружения МБТ, человеческой или другой последовательности, которая, как ожидают, присутствует в образце. В некоторых вариантах реализации контрольную целевую нуклеиновую кислоту, либо синтетическую, либо эндогенно присутствующую в образце, выбирают таким образом, чтобы амплификационные праймеры, которые амплифицируют целевую нуклеиновую кислоту МБТ, также амплифицировали указанную контрольную целевую нуклеиновую кислоту. В некоторых таких вариантах реализации зонд, который позволяет обнаружить целевую нуклеиновую кислоту МБТ или ампликон, полученный из нее, не позволяет обнаружить контрольную мишень или ампликон, полученный из нее. В некоторых вариантах реализации предложен контрольный зонд, который позволяет обнаружить контрольную целевую нуклеиновую кислоту или ампликон, полученный из нее, но не позволяет обнаружить целевую нуклеиновую кислоту МБТ или ампликон, полученный из нее. В некоторых вариантах реализации предусмотрены внутренние стандарты для количественного анализа.
В некоторых вариантах реализации наборы, дополнительно к обсуждаемым выше реагентам, включают один или более подходящих контейнеров, инструкции по применению, программное обеспечение (например, программное обеспечение для анализа результатов) и тому подобное. В некоторых вариантах реализации наборы содержат реагенты для мечения полинуклеотидов. В некоторых вариантах реализации один или более компонентов в указанном наборе находится в лиофилизированной форме.
В вариантах реализации согласно настоящему описанию предложены композиции, наборы, системы и способы идентификации МБТ в сложных биологических образцах, таких как мокрота или бронхоальвеолярный лаваж и осадки перечисленных образцов. В некоторых вариантах реализации в указанных композициях и способах предложены инактивирующие реагенты и способы обнаружения в реальном времени с использованием одного зонда или нескольких зондов, которые позволяют специфично и точно выделить и идентифицировать МБТ.
Например, в некоторых вариантах реализации в настоящем описании предложена композиция, содержащая: по меньшей мере одну (например, одну, две или три) пару праймеров, выбранную из последовательностей SEQ ID NO: 1 и 2, последовательностей SEQ ID NO: 3 и 4, или последовательностей SEQ ID NO: 7 и 8. В некоторых вариантах реализации указанная композиция содержит последовательности SEQ ID NO: 1-4 и 7-8. В некоторых вариантах реализации указанная композиция дополнительно содержит по меньшей мере один зонд, выбранный из последовательностей SEQ ID NO: 5, 6 или 9.
В дополнительных вариантах реализации предложена композиция, содержащая: набор пар праймеров с последовательностями SEQ ID NO: 1 и 2 и последовательностями SEQ ID NO: 3 и 4. В некоторых вариантах реализации указанная композиция дополнительно содержит по меньшей мере один зонд, выбранный из последовательностей SEQ ID NO: 5, 6 или 9. В некоторых вариантах реализации указанная композиция дополнительно содержит пару праймеров с последовательностями SEQ ID NO: 7 и 8.
В дополнительных вариантах реализации предложена композиция, содержащая каждую из нуклеиновых кислот с последовательностями SEQ ID NO: 1-9. В некоторых вариантах реализации описанные выше композиции содержат или заменены на одну или более из последовательностей нуклеиновых кислот, выбранных из SEQ ID NO: 10-36.
В вариантах реализации согласно настоящему описанию предложен набор, содержащий: а) любую из упомянутых выше композиций, и b) по меньшей мере один реагент для проведения реакции амплификации нуклеиновых кислот (например, полимеразу нуклеиновых кислот; множество дНТФ, буфер или инактивирующий реагент). В некоторых вариантах реализации инактивирующий реагент содержит воду, детергент, спирт и NaOH (например, изопропанол, гидроксид натрия, TWEEN-20 и воду).
В других вариантах реализации согласно настоящему описанию предложена реакционная смесь, содержащая: любую из упомянутых выше композиций или нуклеиновых кислот, гибридизованных с нуклеиновой кислотой Microbacterium tuberculosis (МБТ). В некоторых вариантах реализации указанная целевая нуклеиновая кислота МБТ представляет собой одну или более (например, обе) из последовательностей вставки (IS) 6110 и белквого антигена B (РАВ).
В дополнительных вариантах реализации согласно настоящему описанию предложен способ идентификации нуклеиновой кислоты МБТ в биологическом образце, включающий: а) осуществление контакта биологического образца из субъекта с любым из упомянутых выше праймеров или зондов на основе нуклеиновых кислот, и b) непосредственное или опосредованное обнаружение связывания указанных праймеров или зондов на основе нуклеиновых кислот с нуклеиновой кислотой МБТ. В некоторых вариантах реализации указанный способ дополнительно включает этап с) установления присутствия МБТ в образце, если обнаружено связывание. В некоторых вариантах реализации указанное обнаружение осуществляют путем обнаружения с помощью ПЦР в реальном времени. В некоторых вариантах реализации указанный способ дополнительно включает этап инактивации МБТ в образце с применением инактивирующего буфера. В некоторых вариантах реализации указанный образец представляет собой мокроту, бронхоальвеолярный лаваж (БАЛ) или осадки мокроты и БАЛ в N-ацетил-L-цистеине (NALC). В некоторых вариантах реализации указанный способ дополнительно включает этап экстрагирования ДНК из образца после инактивации.
В других дополнительных вариантах реализации предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию биологического образца с помощью инактивирующего реагента с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с одной или более парами праймеров и одним или более зондами на основе нуклеиновых кислот; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в образце.
В дополнительных вариантах реализации предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию указанного биологического образца с помощью инактивирующего реагента, содержащего изопропанол, гидроксид натрия, TWEEN-20 и воду, с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с одной или более парами праймеров, выбранными из последовательностей SEQ ID NO: 1 и 2 и последовательностей SEQ ID NO: 3 и 4; и одним или более зондами на основе нуклеиновых кислот, выбранными из последовательностей SEQ ID NO: 5 и 6; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в указанном образце.
В дополнительных вариантах реализации предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию указанного биологического образца с помощью инактивирующего реагента с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с одной или более парами праймеров, выбранными из последовательностей SEQ ID NO: 1 и 2 и последовательностей SEQ ID NO: 3 и 4; и одним или более зондами на основе нуклеиновых кислот, выбранными из последовательностей SEQ ID NO: 5 и 6; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в образце.
В других вариантах реализации предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию биологического образца с помощью инактивирующего реагента с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с одной или более парами праймеров, выбранными из последовательностей SEQ ID NO: 1 и 2 и последовательностей SEQ ID NO: 3 и 4; и одним или более зондами на основе нуклеиновых кислот, выбранными из последовательностей SEQ ID NO: 5 и 6; d) проведение анализа методом ПЦР в реальном времени для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в образце.
В других дополнительных вариантах реализации предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию биологического образца с помощью инактивирующего реагента с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с одной или более парами праймеров, выбранными из последовательностей SEQ ID NO: 1 и 2 и последовательностей SEQ ID NO: 3 и 4; и одним или более зондами на основе нуклеиновых кислот, выбранными из последовательностей SEQ ID NO: 5 и 6; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ, выбранных из IS6110 и РАВ; и е) установление присутствия мишени в образце.
В некоторых вариантах реализации в настоящем описании предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию биологического образца с помощью инактивирующего реагента с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с указанными парами праймеров с последовательностями SEQ ID NO: 1 и 2 и последовательностями SEQ ID NO: 3 и 4; и с зондами на основе нуклеиновых кислот с последовательностями SEQ ID NO: 5 и 6; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в образце.
В некоторых вариантах реализации в настоящем описании предложен способ обнаружения нуклеиновой кислоты МБТ в биологическом образце, включающий: а) инактивацию биологического образца с помощью инактивирующего реагента, содержащего изопропанол, гидроксид натрия, TWEEN-20 и воду, с получением инактивированного образца; b) выделение ДНК из инактивированного образца; с) осуществление контакта указанной ДНК с указанными парами праймеров с последовательностями SEQ ID NO: 1 и 2 и последовательностями SEQ ID NO: 3 и 4; и с зондами на основе нуклеиновых кислот с последовательностями SEQ ID NO: 5 и 6; d) проведение реакции амплификации для амплификации одной или более целевых нуклеиновых кислот МБТ; и е) установление присутствия мишени в образце.
Дополнительные варианты реализации описаны в данной заявке.
ОПИСАНИЕ ФИГУР
На фигуре 1 показана диаграмма последовательности проведения анализа МБТ в некоторых вариантах реализации методики, предложенной в данной заявке.
На фигуре 2 показаны результаты обнаружения 46 филогенетически и географически разнообразных изолятов МБТ.
На фигуре 3 показана диаграмма последовательности проведения анализа МБТ для получения образца.
На фигуре 4 показаны средние значения количества циклов, определенные при исследовании геномных ДНК комплекса МБТ для определения полноты анализа.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данной заявке предложены композиции и способы, подходящие для обнаружения МБТ. В частности, в данной заявке предложены наборы, реагенты, реакционные смеси и способы, в которых их применяют для процедур амплификации и обнаружения нуклеиновых кислот, которые позволяют специфично и чувствительно обнаружить МБТ в образцах.
В некоторых вариантах реализации в данной заявке предложены полинуклеотиды, которые специфично гибридизуются с последовательностью нуклеиновой кислоты МБТ, или с комплементарной ей последовательностью. Данные полинуклеотиды можно применять для амплификации МБТ, если он присутствует в образце, и для специфичного обнаружения присутствия МБТ. Примеры полинуклеотидов описаны, например, в последовательностях SEQ ID NO: 1-9 или 10-36.
В некоторых вариантах реализации в анализах, описанных в данной заявке, используют несколько (например, два) различных наборов МБТ-специфичных праймеров/зондов. Например, в некоторых вариантах реализации первый набор разработан таким образом, чтобы он позволял обнаружить элемент многокопийной вставки IS6110 (Thierry D, и др., Nucleic Acids Res 1990;18:188), а второй набор - однокопийный ген РАВ (Anderson АВ, Hansen ЕВ, Infect Immun 1989; 57: 2481-2488). Так как были сообщения о штаммах МБТ, у которых отсутствует IS6110 (Mathema В и др., Clinical Microbiology Reviews 2006; 19: 658-685) или у которых есть делеция в гене РАВ (Gilpin СМ, и др., J Clin Microbiol 2002; 40: 2305-2307), применение обеих мишеней минимизирует риск ложноотрицательных результатов. Эксперименты, описанные в данной заявке, продемонстрировали, что стратегия двойной мишени приводит к обнаружению геномной ДНК МБТ с высокой достоверностью.
Клеточная стенка микобактерий устойчива к обычным методикам лизирования клеток вследствие ее сложной структуры, состоящей из липофильных молекул и полисахаридов. Таким образом, в некоторых вариантах реализации в анализах, позволяющих обнаружить МБТ, используют способ очистки на магнитных микрочастицах с гуанидинтиоцианатом при оптимизированных температурах инкубации и условиях смешивания для лизирования клеток МБТ и высвобождения геномной ДНК. Эксперименты, осуществленные в процессе разработки вариантов реализации анализов, описанных в данной заявке, показали, что указанный способ экстрагирования образца ДНК сравним по эффективности с механическим разрушением гранулами для лизирования клеток МБТ.
В дополнительных экспериментах продемонстрировали, что с помощью данного анализа были обнаружены все 66 ДНК комплекса МБТ (включая восемь различных видов комплекса МБТ). Достоверность указанного анализа оценивали четырьмя способами. Во-первых, специфичность анализа оценивали путем тестирования 80 потенциально различных перекрестных реагентов. Ни один из потенциальных перекрестных реагентов не был обнаружен. Во-вторых, осуществляли оценку переноса материала из другой пробы: при данном анализе высокоположительные образцы МБТ обрабатывали одновременно с отрицательными образцами, чтобы определить, будут ли зарегистрированы ложноположительные результаты, или перенос материала из другой пробы, в отрицательных образцах. Не наблюдали ложноположительных результатов. В-третьих, исследовали влияние различных веществ, потенциально препятствующих эффективности анализа. Такое мешающее действие наблюдали только в присутствии 8,3% и 5,0% бычьей слизи, но не в других случаях. Данное мешающее действие устраняли путем уменьшения концентрации слизи до ≤2,5%. При исследовании клинических образцов уровень образцов с неправильными результатами ВК составлял 0,3%, демонстрируя, что способы получения образца, описанные в данной заявке, позволяли эффективно удалить ингибиторы ПЦР. Это служит доказательством надежности протокола и свидетельствует о том, что вклад мешающего действия, вызванного бычьей слизью, вероятно несущественен для данного анализа. Наконец, проводили исследование воспроизводимости, в котором несколько пользователей применяли множество аппаратных систем m2000 для получения образца или получали образец вручную, чтобы протестировать низкоположительные (в три раза выше нижнего предела обнаружения) и отрицательные панели. Наблюдали 100% воспроизводимость. Полученные результаты свидетельствуют о надежности данного анализа при его применении для аналитических исследований и тестирования клинических образцов.
Клиническую ценность анализов, позволяющих обнаружить МБТ, оценивали путем тестирования образцов мокроты и NALC, собранных из пациентов, у которых подозревали наличие МБТ, из пяти стран, используя как образцы из архива, так и проспективно собранные образцы. Общая чувствительность анализа составляла 93%, при этом она составляла 99% в образцах с положительным мазком и положительной культурой и 81% в образцах с отрицательным мазком и положительной культурой. Специфичность составляла 97%. Все результаты аналитической проверки специфичности и тестирования образцов мокроты из популяции из США, в которой подозревают отсутствие МБТ, показали 100% специфичность. Клиническую специфичность определили на основании сравнения результатов анализа с результатами культивирования.
Варианты реализации методики, описанной в данной заявке, позволяют осуществить автоматизированное обнаружение МБТ с высокой пропускной способностью, высокой чувствительностью и специфичностью. По сравнению с обычными культуральными анализами описанная методика значительно улучшает быструю диагностику МБТ, позволяя непосредственное обнаружение микобактерий в клинических образцах. Указанные анализы обладают гораздо большей чувствительностью и специфичностью по сравнению с обычным исследованием кислотоустойчивых мазков под микроскопом. Пробелом в современных анализах для диагностики МБТ является отсутствие чувствительности по отношению к популяции с положительной культурой и отрицательным мазком (с низкой концентрацией МБТ в образцах). Варианты реализации методики, предложенной в данной заявке, заполняют данный пробел. Анализы, предложенные в данной заявке, надежные, с низким уровнем ингибирования, даже при сложности работы с образцами мокроты. Это уменьшает время, необходимое для повторного тестирования неправильно протестированных образцов. В некоторых вариантах реализации исследуют многокопийную мишень МБТ, что обеспечивает большую чувствительность к мишени и меньшую вероятность ложноотрицательных результатов анализа, вызванных мутациями/делециями в целевом участке. Варианты реализации дополнительно предлагают уникальные и эффективные способы инактивации МБТ.
Термин "специфично гибридизуются" в данном тексте относится к способности нуклеиновой кислоты связываться специфично и на обнаруживаемом уровне со второй нуклеиновой кислотой. Полинуклеотиды специфично гибридизуются с цепями целевой нуклеиновой кислоты при условиях гибридизации и промывки, которые минимизируют значительные обнаруживаемые уровни связывания с неспецифичными нуклеиновыми кислотами. Строгие условия, которые можно применять, чтобы добиться специфичной гибридизации, известны в данной области.
"Целевая последовательность" или "целевая последовательность нуклеиновой кислоты" в данном тексте означает последовательность нуклеиновой кислоты МБТ или другую последовательность, которую нужно обнаружить (например, ВИЧ), или комплементарную ей последовательность, которую амплифицировали, обнаружили или амплифицировали и обнаружили, применяя один или более из полинуклеотидов, предложенных в данной заявке. Кроме того, тогда как термин "целевая последовательность" иногда относится к двухцепочечной последовательности нуклеиновой кислоты, для специалистов в данной области будет очевидно, что целевая последовательность также может быть одноцепочечной. В случаях, когда мишень двухцепочечная, полинуклеотидные последовательности праймеров предпочтительно амплифицируют обе цепи целевой последовательности. Можно выбрать целевую последовательность, которая более менее специфична для конкретного организма. Например, целевая последовательность может быть специфична для всего рода, для более чем одного рода, для вида или подвида, серогруппы, ауксотипа, серотипа, штамма, изолята или другой подгруппы организмов.
Термин "тестируемый образец" в данном тексте означает образец, изъятый из организма, биологической жидкости, образец из окружающей среды или другой образец, в котором подозревают присутствие или потенциальное присутствие целевой последовательности МБТ. Тестируемый образец можно взять из любого биологического источника, такого как, например, ткань, кровь, слюна, мокрота, осадки мокроты в N-ацетил-L-цистеине (NALC)-NaOH, слизь, бронхоальвеолярный лаваж (БАЛ), пот, моча, мазки из уретры, мазки с шейки матки, урогенитальные или анальные мазки, конъюнктивальные мазки, жидкость камеры глаза, спинномозговая жидкость, молоко, свободная жидкость брюшной полости, синовиальная жидкость, перитонеальная жидкость, амниотическая жидкость, ферментативные бульоны, культуры клеток, химические реакционные смеси и тому подобные источники. Тестируемый образец можно применять (i) непосредственно в том виде, в котором он был получен из источника, или (ii) после предварительной обработки, изменяющей тип образца. Таким образом, тестируемый образец можно предварительной обработать перед применением, например, путем получения плазмы или сыворотки из крови, разрушения клеток или вирусных частиц, получения жидкостей из твердых материалов, разбавления вязких жидкостей, фильтрации жидкостей, дистиллирования жидкостей, концентрирования жидкостей, инактивации мешающих компонентов, добавления реагентов, очистки нуклеиновых кислот и тому подобными способами.
Термин "метка" в данном тексте означает молекулу или вещество, обладающие способностью или свойством, которые можно обнаружить и, возможно, количественно оценить. Метка может быть непосредственно детектируемой, как например (и без ограничения), радиоактивные изотопы, флуорофоры, хемилюминофоры, ферменты, коллоидные частицы, флуоресцентные микрочастицы и тому подобные метки; или метка может быть опосредованно детектируемой, как например участники специфического связывания. Очевидно, что для непосредственно детектируемых меток могут потребоваться дополнительные компоненты, такие как, например, субстраты, запускающие реакцию реагенты, гасящие реакцию молекулы, свет и тому подобное, чтобы позволить обнаружение и/или определение количества метки. При применении опосредованно детектируемых меток, их обычно используют в комбинации с "конъюгатом". Конъюгат обычно представляет собой участника специфического связывания, который был присоединен или связан с непосредственно детектируемой меткой. Химические способы связывания, подходящие для синтеза конъюгата, хорошо известны в данной области и могут включать, например, любые химические средства и/или физические средства, которые не нарушают способность к специфическому связыванию участника специфического связывания или свойства метки, позволяющие ее обнаружить. В данном тексте "участник специфического связывания" означает участника связывающейся пары, например, двух различных молекул, где одна из молекул, например, с помощью химических или физических способов, специфично связывается с другой молекулой. Дополнительно к специфично связывающимся парам антигена и антитела другие специфично связывающиеся пары включают, но не предполагается, что они ограничены перечисленными парами: авидин и биотин; гаптены и антитела, специфичные к гаптенам; комплементарные последовательности нуклеотидов; кофакторы ферментов или субстраты и ферменты; и тому подобные пары.
Полинуклеотид представляет собой полимер нуклеиновой кислоты: рибонуклеиновую кислоту (РНК), дезоксирибонуклеиновую кислоту (ДНК), модифицированную РНК или ДНК, или миметики РНК или ДНК (такие как, без ограничения, пептидилнуклеиновые кислоты (ПНК)), и производные и гомологи перечисленных полимеров. Таким образом, полинуклеотиды включают полимеры, состоящие из встречающихся в природе нуклеооснований, сахаров и ковалентных межнуклеозидных (каркасных) связей, а также полимеры, содержащие не встречающиеся в природе части, которые функционируют аналогичным образом. Такие модифицированные или содержащие заместители полимеры нуклеиновых кислот хорошо известны в данной области, и для целей настоящего изобретения их называют "аналогами". Для простоты получения и привычности для квалифицированного специалиста, полинуклеотиды предпочтительно представляют собой модифицированные или немодифицированные полимеры дезоксирибонуклеиновой кислоты или рибонуклеиновой кислоты.
Аналоги полинуклеотидов, подходящих для настоящего изобретения, включают полимеры с модифицированными остовами или неприродными межнуклеозидными связями. Модифицированные остовы включают такие остовы, в которых сохранился атом фосфора, такие как фосфоротиоаты, хиральные фосфоротиоаты, фосфородитиоаты, фосфотриэфиры, аминоалкилфосфотриэфиры, метилфосфонаты и фосфонаты другого алкила, а также такие остовы, в которых больше нет атома фосфора, такие как остовы, образованные межнуклеозидными связями алкила или циклоалкила с короткой цепью, межнуклеозидными связями смешанного гетероатома и алкила или циклоалкила, или межнуклеозидными связями одного или более гетероатомов или гетероциклов с короткой цепью. Пример такого не содержащего фосфор остова представляет собой морфолиновая связь (см., например, патенты США с номерами 5185444, 5034506 и 5142047, описания каждого из которых включены в данной заявку посредством ссылки). Модифицированные полимеры нуклеиновых кислот (аналоги) могут содержать одну или более модифицированных молекул сахара. Например, молекулы сахара могут быть модифицированы путем замены в положении 2' на 2-метоксиэтокси (2-МОЕ)-группу (см., например, Martin и др., (1995) Helv. Chim. Acta, 78: 486-504).
В вариантах реализации также предложены аналоги, которые представляют собой миметики РНК или ДНК, в которых как сахар, так и межнуклеозидная связь нуклеотидных единиц заменены на новые группы. В таких миметиках единицы оснований сохранены для гибридизации с целевой последовательностью. Пример такого миметика, у которого была показана превосходная способность к гибридизации, представляет собой пептидонуклеиновую кислоту (ПНК) (Nielsen и др., (1991) Science, 254: 1497-1500; международная заявка на патент WO 92/20702, которые включены в данную заявку посредством ссылки). В соединениях ПНК сахарный остов олигонуклеотида заменен на содержащий амид остов, например, аминоэтилглициновый остов. Нуклеооснования сохранены и связаны непосредственно или опосредованно с атомами аза-азота амидной части остова.
Предложенные полинуклеотиды могут дополнительно включать производные, в которых молекула нуклеиновой кислоты была ковалентно модифицирована путем замены, химическим, ферментативным или другими подходящими способами на молекулу, отличную от встречающегося в природе нуклеотида, например, на молекулу, которая выполняет функцию метки, описанной в данной заявке.
В объем настоящего изобретения дополнительно входят гомологи указанных полинуклеотидов, последовательности нуклеиновых кислот которых представлены в SEQ ID NO: 1-9 или 10-36. Гомологи представляют собой нуклеиновые кислоты, содержащие по меньшей мере одно изменение в первичной последовательности, представленной в любой из SEQ ID NO: 1-9 или 10-36, которое не нарушает способность полинуклеотида специфично гибридизоваться с целевой последовательностью, описанной выше. Соответственно, первичную последовательность можно изменить, например, путем вставки, добавления, делеции или замены одного или более нуклеотидов, например, в последовательностях SEQ ID NO: 1-9 или 10-36. Таким образом, гомологи, которые представляют собой фрагменты последовательности, описанной в SEQ ID NO: 1-9 или 10-36, могут представлять собой непрерывную последовательность из по меньшей мере приблизительно 7, 10, 13, 14, 15, 16, 17, 18, 19 20, 21, 22, 23 или более нуклеотидов последовательностей нуклеиновых кислот, представленных в SEQ ID NO: 1-9 или 10-36, и у них сохранится способность специфично гибридизоваться с целевой последовательностью, как описано выше. Обычно последовательности нуклеиновых кислот указанных гомологов будут идентичны по меньшей мере приблизительно на 50%, 60%, 70%, 80%, 85%, 90% или 95% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 1-9 или 10-36. Идентичность в отношении таких последовательностей в данной заявке означает процент нуклеотидов в кандидатной последовательности, которые идентичны известным полинуклеотидам после выравнивания указанных последовательностей и введения гэпов, при необходимости, для достижения максимального процента идентичности. Концевые (5' или 3') или внутренние делеции, удлинения или вставки в последовательность нуклеотидов не должны истолковываться как влияющие на идентичность.
В некоторых вариантах реализации указанные полинуклеотиды включают праймеры и зонды, которые специфично гибридизуются с целевой последовательностью МБТ, например, молекулы нуклеиновых кислот, имеющие любую из последовательностей нуклеиновых кислот, представленных в SEQ ID NO: 1-9 или 10 -36, включая аналоги и/или производные указанных последовательностей нуклеиновых кислот, и их гомологи, которые специфично гибридизуются с целевой последовательностью МБТ. Ниже описано, что полинуклеотиды можно применять в качестве праймеров и/или зондов для амплификации или обнаружения МБТ.
Указанные полинуклеотиды можно получить с помощью различных методик. Например, полинуклеотиды можно получить, применяя твердофазный синтез, с помощью доступного для приобретения устройства, такого как устройство, доступное для приобретения у Applied Biosystems USA Inc. (Фостер Сити, Калифорния), DuPont, (Уилмингтон, Делавэр) или Milligen (Бедфорд, Массачусетс). Модифицированные полинуклеотиды, такие как фосфоротиоаты и алкилированные производные, также можно легко получить (см., например, патенты США с номерами 5464746; 5424414 и 4948882).
Указанные полинуклеотиды можно непосредственно применять в качестве зондов для обнаружения или определения количества, или обнаружения и определения количества, нуклеиновых кислот МБТ в тестируемом образце. Тестируемый образец приводят в контакт с по меньшей мере одним из указанных полинуклеотидов при подходящих условиях гибридизации, а затем детектируют гибридизацию между целевой последовательностью и по меньшей мере одним из указанных полинуклеотидов. Детектирование может быть непосредственным или опосредованным. В некоторых вариантах реализации гибрид между зондом и мишенью детектируют напрямую. В некоторых вариантах реализации указанный гибрид детектируют опосредованно, например, путем обнаружения побочных продуктов реакции, которые образуются в результате ферментативной реакции, которая происходит в присутствии дуплекса между зондом и мишенью МБТ.
Полинуклеотиды могут содержать одну или более детектируемых меток. Детектируемые метки представляют собой молекулы или вещества, обладающие способностью или свойством, которые можно детектировать непосредственно или опосредованно, и их выбирают таким образом, чтобы они не оказывали негативного влияния на способность полинуклеотида гибридизоваться с целевой последовательностью.
Определение детектируемых меток аналогично ранее описанному определению "метки", и термин "захватывающие метки" обычно используют, чтобы отделить продукты удлинения, и зонды, связанные с любыми такими продуктами, от других веществ, участвующих в реакции амплификации. Участники специфического связывания (которым было дано определение выше) хорошо подходят для данной цели. Также зонды, используемые в соответствии с данным способом, можно блокировать по 3'-концам таким образом, чтобы они не удлинялись при условиях гибридизации. Способы предотвращения удлинения зонда хорошо известны, и конкретный способ выбирает специалист в данной области.
В случаях, когда метки используют для обнаружения амплифицированных с помощью праймеров продуктов, последовательности праймеров возможно могут быть помечены либо захватывающей меткой, либо детектирующей меткой. В некоторых вариантах реализации праймер содержит 3'-участок, который гибридизуется с целевой нуклеиновой кислотой МБТ, и 5'-участок, который внедряет не принадлежащую МБТ последовательность в полученные продукты удлинения. Такие 5'-участки могут содержать последовательность синтетической метки для применения, например, в технологиях секвенирования нового поколения.
В некоторых вариантах реализации зонд используют для гибридизации с продуктом удлинения или ампликоном, полученными с помощью последовательностей праймеров, и он обычно гибридизуется с последовательностью, которая не содержит последовательности праймеров. Аналогично последовательности праймера, последовательность зонда также можно пометить либо захватывающей меткой, либо детектирующей меткой с той оговоркой, что в некоторых вариантах реализации, в которых праймер помечен захватывающей меткой, зонд должен быть помечен детектирующей меткой, и наоборот. При образовании гибридов воспроизведенная последовательность/зонд можно использовать различные метки (т.е., захватывающие и детектирующие метки) на воспроизведенной последовательности и последовательности зонда, чтобы отделить и обнаружить такие гибриды.
Указанные полинуклеотиды также подходят для применения в качестве захватывающих зондов в анализах типа «сэндвич». Вкратце, полинуклеотидный захватывающий зонд присоединяют к твердой подложке и приводят в контакт с тестируемым образцом при подходящих условиях гибридизации таким образом, что образуется гибрид зонд : мишень между захватывающим зондом и любой целевой нуклеиновой кислотой, присутствующей в тестируемом образце. После одного или более подходящих этапов промывки гибрид зонд : мишень детектируют, обычно посредством второго "выявляющего" зонда или с помощью специфического антитела, которое распознает гибридную молекулу.
В вариантах реализации также предложено применение указанных полинуклеотидов в модифицированных анализах гибридизации нуклеиновых кислот. Например, в патенте США номер 5627030 описан способ усиления детектируемого сигнала в анализе гибридизации нуклеиновых кислот. В описанном анализе последовательность первого полинуклеотидного зонда гибридизуют при подходящих условиях с целевой последовательностью, гибрид зонд : мишень затем повергают иммунологическому захвату и иммобилизуют. Второй полинуклеотидный зонд, который содержит множество повторяющихся единиц последовательности, затем гибридизуют с первым зондом из гибрида зонд : мишень. Обнаружения добиваются путем гибридизации множества меченых последовательностей нуклеиновых кислот зондов, по одному с каждой из повторяющихся единиц последовательности, присутствующих во втором зонде. Присоединение множества меченых зондов ко второму зонду таким образом усиливает детектируемый сигнал и повышает чувствительность анализа.
Амплификация и обнаружение последовательностей нуклеотидов МБТ
Указанные полинуклеотиды можно применять в качестве праймеров или зондов для амплификации и/или обнаружения МБТ в тестируемом образце. Наборы праймеров/зондов, предложенные в данной заявке, включают по меньшей мере два праймера и по меньшей мере один зонд. Данные наборы праймеров/зондов можно использовать в соответствии с методиками амплификации нуклеиновых кислот. Следовательно, указанные праймеры в любом конкретном наборе праймеров/зондов можно применять для амплификации целевой последовательности. В большинстве случаев, зонд гибридизуется с копиями целевой последовательности, полученными с помощью одного или более из указанных праймеров, и, как правило, упрощает обнаружение любых копий целевой последовательности, полученных в процессе реакции амплификации. Все наборы праймеров/зондов можно использовать в соответствии с процедурами амплификации нуклеиновых кислот для того, чтобы специфично и чувствительно обнаружить МБТ при комбинировании подходящих праймеров и зондов. Предполагается, что отдельные праймеры и зонды из указанных наборов праймеров/зондов, предложенных в данной заявке, можно, в качестве альтернативы, применять в комбинации с праймерами и/или зондами, отличными от таковых, описанных в данных наборах праймеров/зондов, предложенных в данной заявке. В некоторых вариантах реализации наборы двух праймеров и зонда применяют для обнаружения двух различных целевых последовательностей МБТ.
Процедуры амплификации включают, но не ограничены перечисленными: полимеразную цепную реакцию (ПЦР), транскрипционную амплификацию (ТМА), амплификацию по типу катящегося кольца, амплификацию, основанную на последовательности нуклеиновых кислот (NASBA), и амплификацию с замещением цепи (SDA). Для специалиста в данной области должно быть очевидно, что для применения в некоторых методиках амплификации может потребоваться модификация указанных праймеров, например, праймер для SDA должен содержать дополнительные нуклеотиды около 5'-конца, которые представляют собой сайт узнавания для эндонуклеазы рестрикции. Аналогично, праймер для NASBA должен содержать дополнительные нуклеотиды около 5'-конца, которые представляют собой промотор для РНК-полимеразы.
В некоторых вариантах реализации при выборе праймера для реакции амплификации учитывают определенные критерии. Например, если требуется пара праймеров для реакции амплификации, то указанные праймеры следует выбирать таким образом, чтобы вероятность образования 3'-дуплексов была минимальной, и таким образом, чтобы температуры плавления (ТM) были достаточно близки, чтобы оптимизировать отжиг с целевой последовательностью и минимизировать степень неспецифического отжига.
В некоторых вариантах реализации способы амплификации включают: (а) получение реакционной смеси, содержащей реагенты для амплификации нуклеиновых кислот, по меньшей мере один набор праймеров/зондов и тестируемый образец, в котором подозревают наличие по меньшей мере одной целевой последовательности, и (b) помещение смеси в условия амплификации с получением по меньшей мере одной копии последовательности нуклеиновой кислоты, комплементарной целевой последовательности. Этап (b) описанных выше способов можно повторить любое подходящее количество раз (перед этапом (с) в способе обнаружения), например, путем циклической термообработки реакционной смеси от 10 до 100 раз, обычно от приблизительно 20 до приблизительно 60 раз, чаще от приблизительно 25 до приблизительно 45 раз.
Реагенты для амплификации нуклеиновых кислот включают, но не ограничены перечисленными: фермент, обладающий по меньшей мере активностью полимеразы, кофакторы фермента, такие как магний или марганец; соли; никотинамидадениндинуклеотид (NAD); и дезоксинуклеотидтрифосфаты (dNTP), такие как, например, дезоксиаденинтрифосфат, дезоксигуанинтрифосфат, дезоксицитозинтрифосфат и дезокситиминтрифосфат.
Условия амплификации представляют собой такие условия, которые, как правило, вызывают отжиг и удлинение одной или более последовательностей нуклеиновых кислот.
Конкретные ампликоны, полученные путем амплификации целевых последовательностей нуклеиновых кислот с применением полинуклеотидов, описанных выше, можно обнаружить с помощью различных способов. Например, один или более из праймеров, применяемых для реакций амплификации, можно пометить таким образом, что ампликон можно будет непосредственно обнаружить с помощью обычных методик после проведения реакции амплификации. В качестве альтернативы, после завершения реакции амплификации можно добавить зонд, представляющий собой меченый вариант одного из праймеров, использованных в реакции амплификации, или третий полинуклеотид, отличный от последовательностей праймеров, который пометили и который комплементарен некоторому участку амплифицированной последовательности. Указанную смесь затем подвергают воздействию подходящих условий гибридизации и промывки, и метку детектируют с помощью обычных способов.
Продукт амплификации, полученный, как описано выше, можно детектировать в процессе или после амплификации целевой последовательности. Способы обнаружения амплификации целевой последовательности в процессе амплификации (например, ПЦР в реальном времени) кратко изложены выше и описаны, например, в патенте США номер 5210015. В качестве альтернативы, продукты амплификации гибридизуют с зондами, затем отделяют от других компонентов реакции и детектируют, применяя микрочастицы и меченые зонды.
Должно быть очевидно, что процедура, которая позволяет как амплификацию, так и обнаружение целевых последовательностей нуклеиновых кислот, предпочтительно должна происходить одновременно в одном закрытом реакционном сосуде. Такая процедура позволяет избежать риска контаминации в результате переноса материала из другой пробы на этапах обработки после амплификации, а также способствует высокопроизводительному скринингу или анализам и приспособлению данной процедуры к автоматизации. Более того, такой тип процедуры позволяет контролировать реакцию амплификации "в реальном времени", а также контролировать "конечную точку". Примеры молекул зонда, которые особенно хорошо подходят для данного типа процедуры, включают зонды молекулярные маяки и зонды TAQMAN. Зонды TAQMAN, как правило, представляют собой меченые двумя метками флуорогенные зонды на основе нуклеиновых кислот, состоящие из полинуклеотида, комплементарного целевой последовательности, который помечен по 5'-концу флуорофором и по 3'-концу гасителем. В свободном зонде пространственная близость флуорофора и гасителя обеспечивает внутреннее гашение флуорофора. В ходе фазы удлинения реакции амплификации зонд расщепляется посредством 5'-нуклеазной активности полимеразы, и флуорофор высвобождается. Высвобожденный флуорофор затем может флуоресцировать и, таким образом, вырабатывает детектируемый сигнал.
В некоторых вариантах реализации применяют зонды "молекулярные маяки". Зонды молекулярные маяки описаны, например, в патентах США с номерами 6150097; 5925517 и 6103476 (полностью включены в данную заявку посредством ссылки). По существу, молекулярные маяки представляют собой полинуклеотидные зонды, способные образовывать шпилечную структуру («петля-на-стебле»). Петля представляет собой одноцепочечную структуру, содержащую последовательности, комплементарные целевой последовательности, тогда как стебель обычно не имеет отношения к целевой последовательности и самогибридизуется с образованием двухцепочечного участка. Также могут быть частью участка стебля как комплементарные целевой последовательности нуклеотиды, так и самогибридизующиеся нуклеотиды. К одному плечу стебля присоединена молекула флуорофора и к другому плечу присоединена молекула гасителя. Когда полинуклеотид принимает форму шпильки, флуорофор и гаситель находятся в пространственной близости, и энергия, излучаемая флуорофором, таким образом, поглощается гасителем и выделяется в виде тепла, что приводит к внутреннему гашению флуорофора. После связывания полинуклеотида с целевой последовательностью флуорофор и гаситель оказываются разделенными в пространстве, и флуорофор может флуоресцировать, производя детектируемый сигнал.
Примеры флуорофоров, которые обычно применяют, включают, но не ограничены перечисленными: флуоресцеин и производные флуоресцеина, такие как дигало-(с C1 по C8)диалкоксикарбоксифлуоресцеин, 5-(2'-аминоэтил)аминонафталин-1-сульфоновую кислоту (EDANS), кумарин и производные кумарина, люциферовый желтый, техасский красный, тетраметилродамин, тетрахлор-6-карбоксифлуоресцеин, 5-карбоксиродамин, цианиновые красители и тому подобные флуорофоры. Гасители включают, но не ограничены перечисленными: DABCYL, 4'-(4-диметиламинофенилазо)бензойную кислоту (DABSYL), 4-диметиламинофенилазофенил-4'-малеимид (DABMI), тетраметилродамин, карбокситетраметилродамин (TAMRA), гаситель «черная дыра» (BHQ) и тому подобные гасители.
В некоторых вариантах реализации используют количественные анализы. В некоторых таких вариантах реализации в данной реакции используют внутренние стандарты. Такие внутренние стандарты, как правило, включают контрольную целевую последовательность нуклеиновой кислоты и контрольный полинуклеотидный зонд. Внутренние стандарты необязательно могут дополнительно включать дополнительную пару праймеров. Первичная последовательность данных контрольных праймеров может не иметь отношения к полинуклеотидам МБТ и может быть специфична к контрольной целевой последовательности нуклеиновой кислоты. В качестве альтернативы, нет необходимости в применении дополнительного праймера, если контрольная целевая последовательность разработана таким образом, что она связывается с праймерами МБТ. Количество целевой нуклеиновой кислоты в тестируемом образце можно измерить, применяя способы "конечной точки" или способы "в реальном времени".
В некоторых вариантах реализации анализы, позволяющие обнаружить МБТ, предусмотрены в виде высокопроизводительных анализов. Для высокопроизводительных анализов компоненты реакции обычно размещают на носителе или платформе с множеством контейнеров, такой как многолуночный микротитрационный планшет, который позволяет отслеживать множество аналитических реакций, содержащих различные тестируемые образцы, в рамках одного анализа. В некоторых вариантах реализации высокоавтоматизированные высокопроизводительные анализы применяют для повышения эффективности скрининга или процесса анализа. На сегодняшний день для приобретения доступно множество систем высокопроизводительного скрининга или анализа, а также возможности автоматизации многих процедур, таких как пипетирование образца и реагента, дозирование жидкости, хронометрированное инкубирование, перевод образцов в формат микрочипов, проведение термоциклических реакций в микропланшетах и считывание микропланшетов в подходящем детекторе, что приводит к гораздо меньшему времени производственного цикла. В некоторых вариантах реализации реакции осуществляют в микрофлюидных устройствах (например, картах).
Указанные полинуклеотиды, способы и наборы являются подходящими в клинических или исследовательских форматах для обнаружения и/или определения количества нуклеиновых кислот МБТ. Таким образом, в данных форматах указанные полинуклеотиды можно применять в анализах для диагностики инфекции МБТ у субъекта или для отслеживания количества целевой последовательности нуклеиновой кислоты МБТ у субъекта, инфицированного МБТ. Контроль количества бактерий у субъекта особенно важен для обнаружения или контролирования ответа на антибактериальную терапию.
В некоторых вариантах реализации осуществляют анализ двойной мишени, применяя ПЦР в реальном времени, в комбинации с инактивацией образца. Хотя можно использовать различные образцы, наибольшую клиническую значимость имеют образцы, включающие образцы мокроты (индуцированной или откашлянной) с положительным мазком или отрицательным мазком, образцы бронхоальвеолярного лаважа (БАЛ) или обработанные N-ацетил-L-цистеином (NALC) осадки образцов мокроты и БАЛ. Проблемы, связанные с данными образцами, включают молекулярную сложность мокроты, которая содержит множество компонентов, которые могут препятствовать молекулярным анализам, лизису клеток и инактивации клеток.
В некоторых вариантах реализации осуществляют этап инактивации образца, чтобы снизить риск инфицирования, связанный с клиническими образцами, которые могут содержать МБТ. Снижения риска инфицирования добиваются, например, путем инкубации клинических образцов с инактивирующим реагентом (см. пример 3 ниже).
В некоторых вариантах реализации указанные анализы подходят для применения в них автоматизированной системы детектирования ПЦР в реальном времени, такой как система m2000sp Abbott. Таким образом, в некоторых вариантах реализации перед проведением анализа образцы подготавливают для применения с такими системами. Например, в некоторых вариантах реализации получение целевой ДНК осуществляют, применяя методику на основе магнитных микрочастиц (Abbott mSample Preparation SystemDNA). Это можно осуществить, применяя m2000sp Abbott для автоматизированного получения образцов или применяя протокол получения образцов вручную. В некоторых вариантах реализации внутренний контроль (ВК), положительный контроль и отрицательный контроль обрабатывают с момента начала обработки образцов, чтобы продемонстрировать, что данный процесс проходил правильно.
Для амплификации в некоторых вариантах реализации очищенную из образца ДНК и общую реакционную смесь добавляют в 96-луночный планшет для ПЦР, применяя устройство m2000sp Abbott, или вручную. После добавления каждый планшет запечатывают и переносят в m2000rt Abbott, где осуществляют ПЦР-амплификацию, применяя ДНК-полимеразу.
В некоторых вариантах реализации присутствие продуктов амплификации МБТ обнаруживают в ходе этапа отжига/удлинения по измерению флуоресцентного сигнала от МБТ-зондов в реальном времени. Присутствие продуктов амплификации ВК обнаруживают по измерению флуоресцентного сигнала в реальном времени от ВК-зонда. В некоторых вариантах реализации указанные МБТ- и ВК-зонды представляют собой одноцепочечные ДНК-олигонуклеотиды, состоящие из специфично связывающей мишень последовательности, флуоресцентной молекулы, ковалентно связанной с 5'-концом зонда, и молекулы гасителя, ковалентно связанной с 3'-концом зонда. В отсутствие целевых последовательностей МБТ или ВК, флуоресценция зонда гасится. В присутствии целевых последовательностей МБТ или ВК, МБТ или ВК-зонды специфично связываются с комплементарными последовательностями в мишенях в ходе этапа отжига/удлинения, позволяя излучение и обнаружение флуоресценции. В некоторых вариантах реализации МБТ-зонды помечены различными флуоресцентными красителями (FAM™ для зондов к мишени МБТ, Quasar® для ВК), таким образом позволяя одновременное обнаружение продуктов амплификации МБТ и ВК в одной реакции.
В некоторых вариантах реализации осуществляют этапы, позволяющие избежать контаминации нуклеиновыми кислотами. Например, в некоторых вариантах реализации контаминацию минимизируют благодаря тому, что: ПЦР-амплификация и гибридизация олигонуклеотидов происходят в запечатанных многолуночных планшетах; детектирование осуществляют автоматически, без необходимости открывать сосуды для проведения реакций (например, лунки планшета); для всех этапов пипетирования используют аэрозоль-устойчивые наконечники для пипетки; наконечники для пипетки выбрасывают после использования; и используют специальные изолированные зоны для проведения анализа МБТ.
В некоторых вариантах реализации перечисленные выше реагенты предусмотрены в виде набора и/или системы (например, систем, включающих устройства для автоматизированного манипулирования образцами и устройства анализа, описанные в данной заявке). Например, в некоторых вариантах реализации указанный набор включает, по существу состоит или состоит из следующих компонентов:
1. Внутренний контроль МБТ (4 пробирки, 0,4 мл в каждой пробирке): <0,01% неинфекционная линеаризованная плазмидная ДНК в буферном растворе с ДНК-носителем. Консерванты: азид натрия и 0,15% ProClin® 950.
2. Упаковка реагентов для амплификации (4 упаковки, 24 анализа в упаковке). Каждая упаковка реагентов содержит: 1 сосуд (0,078 мл) с ДНК-полимеразой (от 5,4 до 5,9 единиц/мкл) в буферном растворе со стабилизаторами. 1 сосуд (0,5314 мл) с реагентом для амплификации МБТ. <0,1% синтетические олигонуклеотиды (наборы праймеров и зонды для одной или более мишеней; набор праймеров и зонд для внутреннего контроля) и <0,6% дНТФ в буферном растворе с референсным красителем. Консерванты: азид натрия и 0,15% ProClin® 950. 1 сосуд (0,778 мл) с активирующим реагентом. 38 мМ хлорид магния в буферном растворе. Консерванты: азид натрия и 0,15% ProClin® 950.
3. Отрицательный контроль МБТ (8 пробирок по 1,6 мл в каждой пробирке); буферные растворы; консерванты: азид натрия и 0,15% ProClin® 950.
4. Положительный контроль МБТ (8 пробирок по 1,6 мл в каждой пробирке); <0,01% неинфекционная линеаризованная плазмидная ДНК в буферном растворе с ДНК-носителем. Консерванты: азид натрия и 0,15% ProClin® 950.
В некоторых вариантах реализации обнаруживают все формы МБТ (например, праймеры и зонды выбирают таким образом, чтобы определить все целевые последовательности нуклеиновых кислот МБТ, которые могут присутствовать в образце). В некоторых вариантах реализации обнаруживают последовательности определенных МБТ, такие как последовательности устойчивых к антибиотикам (например, рифампицину, изониазиду) штаммов.
ПРИМЕРЫ
Следующие примеры представлены исключительно с целью иллюстрирования, и они не должны рассматриваться как каким-либо образом ограничивающие объем настоящего изобретения.
ПРИМЕР 1
Пример последовательности проведения анализа
В данном примере описан специфичный, эффективный подход к проведению ПЦР в реальном времени для обнаружения МБТ в образце. В некоторых вариантах реализации способы проведения ПЦР в реальном времени включают или состоят из следующих этапов:
1. Инактивация МБТ в образцах (например, в мокроте, бронхоальвеолярном лаваже (БАЛ) и осадках мокроты и БАЛ в N-ацетил-L-цистеине (NALC)) с применением инактивирующего реагента (IR). В некоторых вариантах реализации инактивирующий реагент содержит или состоит из изопропанола, гидроксида натрия, TWEEN-20 и воды;
2. Получение образца, в ходе которого ДНК выделяют из указанных инактивированных образцов, применяя реагенты; получение образцов осуществляют, применяя автоматизированное устройство m2000sp (Abbott Molecular), или вручную;
3. Соединение компонентов ПЦР, при котором очищенные образцы и компоненты для анализа ПЦР добавляют вместе в оптический 96-луночный реакционный планшет или на другую реакционную подложку с множеством камер; это осуществляют, применяя m2000sp, или вручную;
4. Запечатывание оптического 96-луночного реакционного планшета вручную и перенос планшета в устройство m2000rt.
5. Амплификация и детектирование продуктов ПЦР с применением автоматизированного устройства m2000rt; результаты для пациента автоматически выводятся на рабочую станцию m2000rt.
Краткое графическое представление данной последовательности проведения анализа показано на фигуре 1.
ПРИМЕР 2
Выбор мишени и разработка праймеров/зондов
В некоторых вариантах реализации используют стратегию двойной мишени для обнаружения комплекса МБТ. Две указанные мишени включают: последовательность вставки (IS) 6110 и белквый антиген B (РАВ). См. таблицу 1 ниже:
Таблица 1. Выбор мишени для анализа Abbott RealTime МТБ:

Применение стратегии двойной мишени предотвращает ложноотрицательные результаты, обусловленные мутацией или делецией в целевых последовательностях.
Зонды и праймеры, которые можно применять для обнаружения целевых последовательностей IS6110 и РАВ, включают зонды и праймеры, представленные в таблице 2.
Таблица 2. Последовательности праймеров/зондов для анализа RealTime МТБ (FP = прямой праймер; RP = обратный праймер; #pdU = 5'-пропинил dU; *pdC = 5'-пропинил dC; Fam = краситель флуоресцеин; BHQ = гаситель «черная дыра»; ВК (IС) = внутренний контроль; probe = зонд):
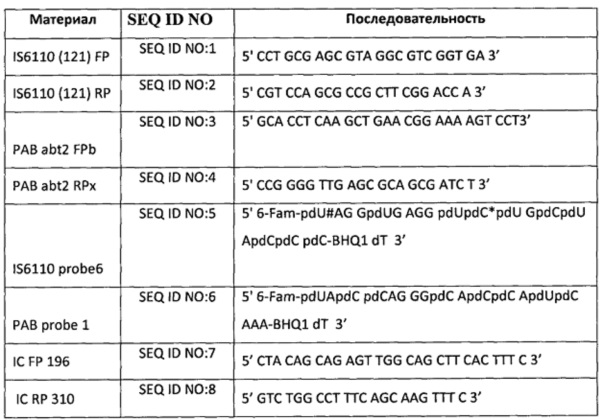
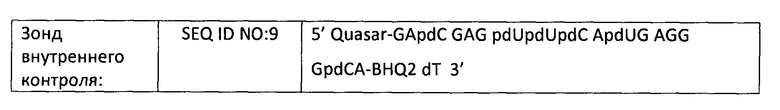
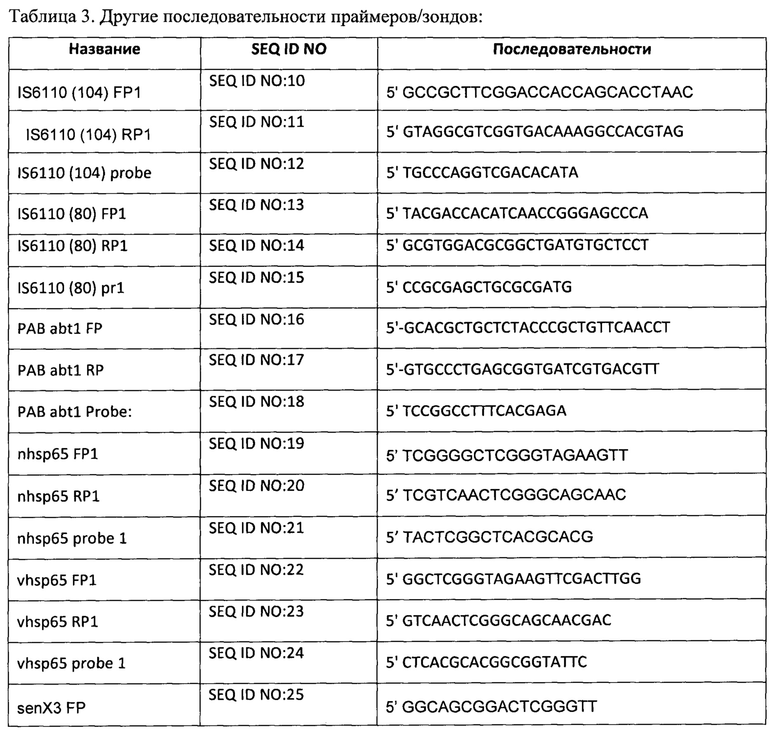
В таблице 3 приведены альтернативные праймеры и зонды для применения для обнаружения целевых последовательностей МБТ. Вдобавок к IS6110 и РАВ, дополнительные мишени включают rPOB (однокопийный ген, кодирующий β-субъединицу РНК-полимеразы, сайт, в котором происходит приблизительно 95% мутаций, приводящих к устойчивости к рифампицину), SenX3-RegXe (однокопийный ген, кодирующий регуляторные белки), hsp65 (однокопийный ген, кодирующий белок теплового шока), и МРВ64 (однокопийный ген, кодирующий белок размером 23 кДа).

ПРИМЕР 3
Инактивация образца
В данном примере описаны типичные реагенты и способы осуществления этапа инактивации образца.
Получение инактивирующего реагента (IR)
Используемые материалы:
• Полипропиленовый или стеклянный контейнер
• 10 M NaOH
• Изопропанол
• TWEEN-20
• Очищенная вода
Получение IR:
Объем материала, необходимый для 500 мл
10 M NaOH 20 мл
Очищенная вода 179,1 мл
Изопропанол 300 мл
TWEEN-20 0,9 мл
1. Добавляли 179,1 мл воды в пустой полипропиленовый или стеклянный контейнер (избегайте применения полистиролового контейнера).
2. Добавляли 0,9 мл TWEEN-20 в контейнер.
3. Добавляли 20 мл 10 М NaOH в контейнер.
4. Добавляли 300 мл изопропанола в контейнер.
5. Смешивали указанные компоненты путем переворачивания 20 раз.
Использовали или хранили при температуре окружающей среды в течение до 1 месяца.
Процедура инактивации:
1. Если образцы были заморожены, то разморозить их при температуре от 15 до 30°C.
2. Оценить объем образца, который нужно инактивировать.
3. Добавить IR при соотношении 1:3 (например, 1 мл образца + 3 мл IR) (предпочтительный объем образца составляет от 0,3 до 10 мл).
4. Перевернуть контейнер, чтобы обеспечить контакт IR и образца.
5. Встряхивать смесь на вортексе в течение от 20 до 30 секунд.
6. Инкубировать смесь при температуре окружающей среды в течение по меньшей мере 1 часа и предпочтительно не более 24 часов. Встряхивать смесь на вортексе один последний раз в течение от 20 до 30 секунд через 20-30 минут периода инкубации.
ПРИМЕР 4
Способ получения образца
В анализе МБТ из примера 1 используют автоматизированное устройство m2000sp Abbott или ручной способ обработки мокроты, БАЛ и осадка образцов мокроты или БАЛ в NALC-NaOH и используют автоматизированное устройство m2000rt Abbott для амплификации и обнаружения. Оба процесса включают выделение ДНК из образцов, обе очистки ДНК осуществляют, применяя реагенты для обработки образцов ДНК GPR (перечень 6К12-24) из системы пробоподготовки Abbott /mSample Preparation SystemDNA.
Реагенты для обработки образцов и способ (включая этап лизирования, этап промывки, этап элюирования, установку повторного использования наконечников и т.д.) оптимизировали, чтобы уменьшить ингибиторное влияние на реакции ПЦР ингибиторной мокроты или переноса из другой пробы инактивирующего МБТ реагента (IR): таким образом, центрифугирование для избавления от IR в обработанном IR образце не обязательно. Данную процедуру также оптимизировали, чтобы уменьшить следы высоко положительных проб в соседнем отрицательном образце. Обработку образцов также оптимизировали, чтобы гарантировать разрыв клетки МБТ для эффективного получения ДНК и проведения ПЦР.
ПЦР в реальном времени
После смешивания всех компонентов для реакции ПЦР в оптическом 96-луночном реакционном планшете (либо вручную, либо с помощью m2000sp), 96-луночный планшет вручную запечатывали и переносили в m2000rt для осуществления амплификации и реакции обнаружения флуоресценции в реальном времени. Результаты для пациента автоматически выводились на рабочую станцию m2000rt. Анализ МБТ позволяет обнаружить последовательность нуклеиновой кислоты внутреннего контроля в качестве контроля пригодности образца, контроля эффективности экстрагирования и амплификации образца. В таблице 4 приведены примеры условий проведения циклов ПЦР.
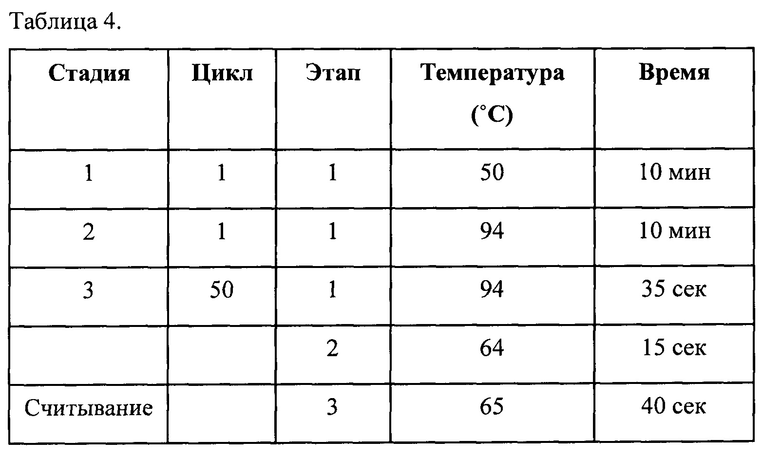
Для результатов, показанных в примерах ниже, использовали пороговое значение анализа, равное 42. Другими словами, образцы со значениями Ct<42 считали положительными по МБТ (обнаружен), тогда как образцы со значениями Ct>42 считали отрицательными по МБТ (не обнаружен).
Проведение анализов осуществляли на m2000rt, следуя протоколам, рекомендованным производителем. Один такой пример включал описанные ниже этапы.
1. В каждом запуске анализировали 96 обработанных IR образцов. В анализ включали один отрицательный контроль и один положительный контроль в каждом запуске, следовательно, в каждом запуске можно было обработать максимум 94 обработанных IR образца.
2. Перед применением обработанные IR образцы встряхивать на вортексе в течение от 3 до 5 секунд. Используя пипетку, перенести обработанные IR образцы в сосуды для проведения реакций. Минимизировать перенос видимых частиц в обработанные IR образцы в ходе данного этапа.
3. Разморозить контроли для анализа, ВК и реагенты для амплификации при температуре от 2 до 8°C или от 15 до 30°C. После размораживания ВК можно хранить закрытыми при температуре от 2 до 8°C в течение вплоть до 14 дней перед применением. После размораживания контроли можно хранить при температуре от 2 до 8°C в течение вплоть до 24 часов перед применением. Если не используется необязательная возможность более длительного применения реагентов для амплификации: разморозить новые реагенты для амплификации при температуре от 2 до 8°C или от 15 до 30°C. После размораживания указанные реагенты для амплификации можно хранить при температуре от 2 до 8°C в течение вплоть до 24 часов перед применением. Если используется необязательная возможность более длительного применения реагентов для амплификации: выбрать новые и/или частично использованные упаковки реагентов для амплификации для применения в данном запуске. Обратиться к руководству по эксплуатации (№ в перечне 9К20-06 или выше), рабочим инструкциям m2000sp Abbott для получения инструкций, касающихся учета запасов упаковок с реагентами для амплификации. У упаковок с реагентами для амплификации должен быть одинаковый номер партии.
4. Встряхивать на вортексе каждый контроль трижды в течение от 2 до 3 секунд каждый раз перед применением. Удостовериться в том, что не образовались пузырьки или пена. Если образовались, то удалить их с помощью нового стерильного наконечника пипетки для каждой пробирки. Удостовериться в том, что содержимое каждой пробирки находится на дне после встряхивания на вортексе, путем постукивания пробиркой по столу, чтобы жидкость опустилась на дно пробирки.
5. Аккуратно перевернуть сосуды mSample Preparation SystemDNA Abbott, чтобы убедиться в гомогенности раствора. Если после раскупоривания в любом из сосудов с реагентами наблюдаются кристаллы, то оставить реагенты для восстановления равновесия при комнатной температуре до исчезновения кристаллов. Не использовать реагенты до полного растворения кристаллов. Удостовериться, что не образовались пузырьки или пена; если они присутствуют, то удалить их с помощью стерильного наконечника пипетки, используя новый наконечник для каждого сосуда. ПРИМЕЧАНИЕ: Перед тем, как добавить mMicroparticlesDNA в 200 мл сосуд с реагентами, интенсивно перемешать их или встряхивать на вортексе до полного ресуспендирования mMicroparticlesDNA.
6. Встряхивать на вортексе пробирку с ВК трижды в течение от 2 до 3 секунд каждый раз перед применением. Удостовериться, что не образовались пузырьки или пена; если они присутствуют, то удалить их с помощью стерильного наконечника пипетки.
7. Используя калиброванную точную пипетку, предназначенную для применения только для внутреннего контроля, добавить 180 мкл ВК в 1 сосуд с буфером mLysisDNA. Перемешать путем аккуратного переворачиания контейнера от 5 до 10 раз, чтобы минимизировать пенообразование. Каждый сосуд с буфером mLysisDNA предназначен для получения до 48 образцов. Добавьте 180 мкл ВК во второй сосуд с буфером mLysisDNA для образцов с 49 по 96. Если используется необязательная возможность более длительного применения реагентов для амплификации, частично использованные пробирки с ВК можно закупорить и хранить при температуре от 2 до 8°C для повторного применения.
8. Добавить 25 мл 190-200-градусного этанола (от 95 до 100% этанола) фармацевтической чистоты (USP) в буфер mLysisDNA + сосуд с реагентом ВК. Не использовать этанол, который содержит денатуранты. Аккуратно перевернуть контейнер, чтобы удостовериться в гомогенности раствора. Для образцов с 49 по 96, добавить 25 мл этанола во второй сосуд с буфером mLysisDNA + ВК. Аккуратно перевернуть, чтобы убедиться в гомогенности раствора.
9. Добавить 70 мл 190-200-градусного этанола (от 95 до 100% этанола) фармацевтической чистоты (USP) в сосуд mWash 2DNA. Не использовать этанол, который содержит денатуранты. Каждый сосуд mWash 2DNA предназначен для проведения до 48 реакций. Аккуратно перевернуть, чтобы убедиться в гомогенности раствора.
10. Поместить отрицательный и положительный контроль и образцы из пациента в штатив для проб m2000sp Abbott.
11. Поместить сосуды для проведения реакций объемом 5 мл в штатив для реакционных пробирок m2000sp Abbott объемом 1 мл.
12. Загрузить штативы с пробирками, содержащими реагенты mSample Preparation SystsmDNA Abbott, и 96-луночный планшет с глубокими лунками Abbott на рабочий стол m2000sp Abbott, как описано в руководстве по эксплуатации, в рабочих инструкциях m2000sp Abbott.
13. На экране Запуск выделения образца выбрать и запустить протокол выделения образца, как описано в руководстве по эксплуатации, в рабочей инструкции m2000sp Abbott.
ПРИМЕЧАНИЕ: Сменить перчатки перед манипуляциями с реагентами для амплификации.
14. Загрузить упаковку реагентов для амплификации и пробирку с общей реакционной смесью (при необходимости) на рабочий стол m2000sp Abbott после завершения обработки образцов. Каждая упаковка реагентов для амплификации предназначена для проведения до 24 реакций. Разморозить 1 набор реагентов для образцов с 1 по 24, 2 комплекта для образцов с 25 по 48, 3 комплекта для образцов с 49 по 72 и 4 комплекта для образцов с 73 по 96. Перед применением удостовериться в том, что реагенты для амплификации полностью разморозились. Удостовериться в том, что содержимое находится на дне пробирок, путем постукивания пробирками по столу в вертикальном положении. Удалить крышки с пробирок с реагентами для амплификации. Если используется необязательная возможность более длительного применения реагентов для амплификации, то можно комбинировать новые и частично использованные упаковки с реагентами. Если не используется необязательная возможность более длительного применения реагентов для амплификации, то можно использовать только новые упаковки. Перед тем как открыть реагенты для амплификации, удостовериться в том, что содержимое новых упаковок с реагентами для амплификации находится на дне пробирок, путем постукивания пробирками по столу в вертикальном положении. Не постукивать частично использованными упаковками с реагентами для амплификации, которые используются второй раз. Постукивание может привести к потере объема общей реакционной смеси в крышке. Удалить крышки. Если новую упаковку реагентов для амплификации хранят для повторного применения, то пробирки закупоривают для хранения. Если планируется повторное использование исходных крышек для повторного закупоривания пробирок с реагентами, то исходные крышки сохраняют и используют. Если планируется использование новых крышек для повторного закупоривания пробирок с реагентами, то исходные крышки выбрасывают. Частично использованные упаковки загружают слева от новых упаковок с реагентами для амплификации на рабочий стол m2000sp Abbott. Удостовериться в том, что упаковки с реагентами для амплификации надежно установлены в устройство.
15. Выбрать подходящий планшет с глубокими лунками на экране запуска добавления общей реакционной смеси, который подходит для соответствующего экстрагирования образцов. Запустить протокол добавления общей реакционной смеси Abbott m2000sp. Следовать инструкциям, описанным в разделе рабочих инструкций руководства по эксплуатации m2000sp Abbott. ПРИМЕЧАНИЕ: Объединение общей реакционной смеси для амплификации и элюатов образцов в оптическом 96-луночном реакционном планшете Abbott (этап 15) необходимо осуществить в течение 1 часа после завершения получения образцов. ПРИМЕЧАНИЕ: Протокол m2000rt Abbott (этап 20) необходимо начать в течение 90 минут после запуска протокола добавления общей реакционной смеси. ПРИМЕЧАНИЕ: Если запуск прерывается по любой причине после этапа 15, то реагенты для амплификации следует выбросить, и необходимо использовать новый 96-луночный планшет для ПЦР, если нужно будет повторить протокол добавления общей реакционной смеси (этап 15) Abbott m2000sp.
16. Включить и установить m2000rt Abbott в помещении для амплификации. ПРИМЕЧАНИЕ: m2000rt Abbott требуется 15 минут, чтобы нагреться. ПРИМЕЧАНИЕ: Сменить лабораторные халаты и перчатки перед возвращением в зону обработки образцов.
17. Поместить оптический 96-луночный реакционный планшет Abbott в подставку, позволяющую избежать разбрызгивания (Splash-Free Support Base) Abbott, после того, как устройство m2000sp Abbott завершило добавление образцов и общей реакционной смеси.
18. Запечатать оптический 96-луночный реакционный планшет Abbott согласно разделу рабочих инструкций руководства по эксплуатации m2000sp Abbott. Экспортировать результаты, полученные в результате ПЦР для планшета, на CD (или непосредственно в отображенный m2000rt Abbott посредством сетевого соединения).
В некоторых вариантах реализации применяют способ обработки образцов вручную. Пример такого способа описан далее:
1. Разморозить реагенты для амплификации при температуре от 15 до 30°C или при температуре от 2 до 8°C. Данный этап можно начать до завершения процедуры обработки образцов.
2. В комплекте магнитных штативов можно обработать 12 образцов. Отрицательный контроль и положительный контроль включали в каждый запуск, следовательно, в каждом запуске можно было обработать максимум 10 образцов. Подготовить образцы к обработке, следуя описанным ниже этапам. ПРИМЕЧАНИЕ: Образцы от пациента необходимо инактивировать перед началом выделения образца.
3. Разморозить 1 пробирку отрицательного контроля МБТ, 1 пробирку положительного контроля МБТ и 1 пробирку внутреннего контроля МБТ при температуре от 15 до 30°C или при температуре от 2 до 8°C. Если ВК не обрабатывается сразу после размораживания, то храните его при температуре от 2 до 8°C в течение вплоть до 14 дней перед применением. Если контроли не обрабатываются сразу после размораживания, то храните их при температуре от 2 до 8°C в течение вплоть до 24 часов перед применением. Встряхивать на вортексе контроли и ВК трижды в течение от 2 до 3 секунд каждый раз перед применением. Удостовериться в том, что содержимое каждой пробирки находится на дне после встряхивания на вортексе, путем постукивания пробиркой по столу, чтобы жидкость опустилась на дно пробирки. Удостовериться, что не образовались пузырьки или пена; если они присутствуют, то удалить их с помощью стерильного наконечника пипетки, применяя новый наконечник для каждой пробирки.
4. Открыть упаковку(-и) с реагентами Abbott mSample Preparation SystemDNA. Если после раскупоривания в любом из сосудов с реагентами наблюдаются кристаллы, то оставить реагенты для восстановления равновесия при комнатной температуре до исчезновения кристаллов. Не использовать реагенты до полного растворения кристаллов.
5. Приготовить mWash 2DNA путем добавления 70 мл 190-200-градусного этанола (от 95 до 100% этанола) чистоты USP в сосуд с mWash 2DNA. Не использовать этанол, который содержит денатуранты. Аккуратно перевернуть, чтобы убедиться в гомогенности раствора. ПРИМЕЧАНИЕ: Промаркировать сосуд mWash 2DNA, чтобы указать, что этанол уже был добавлен, для дальнейшего использования.
6. Приготовить mLysisDNA путем добавления 25 мл 190-200-градусного этанола (от 95 до 100% этанола) чистоты USP в сосуд mLysisDNA. Не использовать этанол, который содержит денатуранты. Аккуратно перевернуть от 5 до 10 раз, чтобы перемешать и чтобы минимизировать пенообразование. ПРИМЕЧАНИЕ: Промаркировать сосуд mLysisDNA, чтобы указать, что этанол уже был добавлен, для дальнейшего использования.
7. Рассчитать объем раствора mLysisDNA, необходимого для запуска вручную: (1,85 мл mLysisDNA × количество образцов). Отобрать пипеткой необходимый объем раствора mLysisDNA в полипропиленовый контейнер, достаточно большой, чтобы вместить весь объем. Рассчитать объем ВК, необходимого для запуска вручную: (3,51 мкл ВК × количество образцов). Использовать точную пипетку, специально предназначенную только для внутреннего контроля, чтобы добавить необходимый объем ВК в полипропиленовый контейнер, содержащий раствор mLysisDNA, необходимый для запуска вручную. Смешать раствор mLysisDNA и смесь ВК путем аккуратного переворачивания от 10 до 15 раз, чтобы минимизировать пенообразование. После первоначального использования пробирки с частично израсходованным ВК можно хранить при температуре от 2 до 8°C в течение вплоть до 14 дней и использовать еще 1 раз.
8. Перед применением аккуратно перевернуть сосуды со всеми реагентами, за исключением сосуда mMicroparticlesDNA и сосуда mWash 1DNA, от 5 до 10 раз, чтобы удостовериться в гомогенности раствора. Сосуд mMicroparticlesDNA будет перемешан на этапе 11.
9. Включить терморегулируемый сухожаровой блок. Установить температуру первого блока на 58°C. Установить температуру второго блока на 80°C. ПРИМЕЧАНИЕ: Проверить температуру термостата. Не продолжать до тех пор, пока в термостате не установится нужная температура.
10. Промаркировать все необходимые пробирки: по одному реакционному сосуду объемом 5 мл для каждого образца для этапов лизирования, инкубации и промывки (mWash 1DNA). По одной микроцентрифужной пробирке объемом 1,5 мл для каждого образца для первого и второго этапов mWash 2DNA и элюирования. По одной микроцентрифужной пробирке объемом 1,5 мл для каждого образца или 96-луночный полипропиленовый планшет для элюата.
11. Поместить промаркированные сосуды для проведения реакций объемом 5 мл для каждого образца в ненагретую подставку. Ресуспендировать mMicroparticlesDNA путем встряхивания на вортексе или интенсивного встряхивания до тех пор, пока частицы не перейдут в суспензию, и осевшие частицы больше будут не видны на дне сосуда. После ресуспендирования частиц используйте точный дозатор и стерильный аэрозоль-устойчивый наконечник для пипетки объемом 200 мкл для добавления 50 мкл mMicroparticlesDNA в каждый сосуд для проведения реакций.
12. Используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, добавить 1,75 мл (2 × 875 мкл) mLysisDNA в сосуды для проведения реакций.
13. Добавить 0,8 мл контролей и образцы в подходящие сосуды для проведения реакций, применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца. Перемешать каждую смесь образец/mLysisDNA 5- - 10-кратным пипетированием (аспирацией и выпусканием обратно) объема 800 мкл до тех пор, пока не получится однородная суспензия. ПРИМЕЧАНИЕ: Аспирировать и выпускать жидкость медленно, чтобы избежать пенообразования.
14. Перенести сосуды для проведения реакций объемом 5 мл в термостат с температурой 58°C.
15. Запустить таймер и инкубировать в течение 15 минут.
16. После инкубации, используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, перемешать смесь 5-кратным пипетированием объема 800 мкл.
17. Запустить таймер и инкубировать в течение дополнительных 10 минут в термостате с температурой 58°C.
18. После инкубации, используя свежий, стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, перемешать смесь 5-кратным пипетированием объема 800 мкл.
19. Запустить таймер и инкубировать в течение дополнительных 10 минут в термостате с температурой 58°C.
20. После завершения инкубации поместить сосуды для проведения реакций в подставку для магнитного захвата на 2 минуты, чтобы частицы смогли примагнититься и осесть на стенках сосудов для проведения реакций.
21. Пока сосуды для проведения реакций находятся в магнитной подставке, использовать свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл или одноразовую пипетку для переноса для каждого образца, чтобы аккуратно удалить mLysisDNA из каждого сосуда для проведения реакций и отбросить жидкость в контейнер для жидких отходов. Полностью удалить жидкость, насколько это возможно. Не прикасаться к захваченным магнитным частицам и не аспирировать их.
22. Вынуть сосуды для проведения реакций из магнитного штатива и перенести в немагнитный штатив.
mWash 1DNA (промывка).
23. Применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, добавить 800 мкл mWash 1DNA в образцы и ресуспендировать магнитные частицы в жидкости для промывки путем аккуратного перемешивания 10-кратным пипетированием с помощью наконечника пипетки. Смыть частицы со стенок сосуда для проведения реакций при необходимости. ПРИМЕЧАНИЕ: При добавлении жидкости для промывки mWash 1DNA, выпускать жидкость медленно, чтобы избежать разбрызгивания.
24. Перенести жидкость для промывки и частицы в промаркированную 1,5 мл микроцентрифужную пробирку.
25. Поместить пробирки в подставку для магнитного захвата на 1 минуту, чтобы частицы смогли примагнититься и осесть на стенках пробирок.
26. Пока пробирки находятся в магнитной подставке, использовать свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, чтобы аккуратно удалить mWash 1DNA из каждой пробирки и отбросить жидкость в контейнер для жидких отходов. Полностью удалить жидкость, насколько это возможно. Не прикасаться к захваченным магнитным частицам и не аспирировать их.
27. Вынуть пробирки из магнитного штатива и перенести в немагнитный штатив. mWash 2DNA (первая промывка).
28. Применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, добавить 800 мкл mWash 2DNA в образцы и ресуспендировать магнитные частицы в жидкости для промывки путем аккуратного перемешивания 5- - 10-кратным пипетированием с помощью наконечника пипетки. Смыть частицы со стенок пробирки при необходимости. ПРИМЕЧАНИЕ: При добавлении промывки mWash 2DNA выпускать жидкость медленно, чтобы избежать разбрызгивания.
29. Поместить пробирки в подставку для магнитного захвата на 1 минуту, чтобы частицы смогли примагнититься и осесть на стенках пробирок.
30. Пока пробирки находятся в магнитной подставке, использовать свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, чтобы аккуратно удалить mWash 2DNA из каждой пробирки и отбросить жидкость в контейнер для жидких отходов. Полностью удалить жидкость, насколько это возможно. Не прикасаться к захваченным магнитным частицам и не аспирировать их.
31. Вынуть пробирки из магнитного штатива и перенести в немагнитный штатив. mWash 2DNA (вторая промывка).
32. Применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, добавить 800 мкл mWash 2DNA в образцы и ресуспендировать магнитные частицы в жидкости для промывки путем аккуратного перемешивания 5- - 10-кратным пипетированием с помощью наконечника пипетки. Смыть частицы со стенок пробирки при необходимости. ПРИМЕЧАНИЕ: При добавлении промывки mWash 2DNA выпускать жидкость медленно, чтобы избежать разбрызгивания.
33. Поместить пробирки в подставку для магнитного захвата на 1 минуту, чтобы частицы смогли примагнититься и осесть на стенках пробирок.
34. Пока пробирки находятся в магнитной подставке, использовать свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, чтобы аккуратно удалить mWash 2DNA из каждой пробирки и отбросить жидкость в контейнер для жидких отходов. Полностью удалить жидкость, насколько это возможно. Не прикасаться к захваченным магнитным частицам и не аспирировать их.
35. Вынуть пробирки из магнитного штатива, перенести в термостат с температурой 80°C и инкубируйте в течение 15 минут с открытыми крышками, чтобы позволить этанолу испариться.
36. Применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, добавить 250 мкл буфера для элюирования mElution BufferDNA в образцы и ресуспендировать магнитные частицы в жидкости путем пипетирования (аспирации и выпускания обратно) с помощью наконечника пипетки. Смыть частицы со стенок пробирки при необходимости.
37. Поместить пробирки в термостат с температурой 80°C, запустить таймер и инкубируйте в течение 4 минут.
38. Вынуть пробирки из термостата с температурой 80°C. Используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, смешать образец и смесь в mElution BufferDNA 4-кратным пипетированием объема 200 мкл.
39. Вернуть пробирки в термостат с температурой 80°C. Запустить таймер и инкубировать в течение 4 минут.
40. Вынуть пробирки из термостата с температурой 80°C и поместить в подставку для магнитного захвата на 1 минуту, чтобы частицы смогли примагнититься и осесть на стенках пробирок.
41. Пока пробирки находятся в магнитной подставке, использовать свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 1000 мкл для каждого образца, чтобы аккуратно удалить элюированный образец из пробирок. Не прикасаться к захваченным микрочастицам и не аспирировать их. Элюированный образец(-цы) можно поместить в свежую промаркированную 1,5 мл микроцентрифужную пробирку или в 96-луночный полипропиленовый планшет. ПРИМЕЧАНИЕ: Объединение общей реакционной смеси для амплификации и элюированных образцов в оптическом 96-луночном реакционном планшете Abbott (этап 48) необходимо осуществить в течение 1 часа после завершения получения образцов.
42. Включить и установить устройство m2000rt Abbott. ПРИМЕЧАНИЕ: m2000rt Abbott требуется 15 минут, чтобы нагреться.
43. Создать файл проведения реакции (test order) для m2000rt Abbott. Обратиться к разделу рабочих инструкций руководства по эксплуатации m2000rt Abbott. В окне протокола выбрать протокол выполнения анализа Realtime МТВ Abbott. ПРИМЕЧАНИЕ: Снять перчатки перед возвращением в зону подготовки реагентов.
44. Приготовить общую реакционную смесь для амплификации. ПРИМЕЧАНИЕ: Вся подготовка реагентов должна происходить в зоне, специально предназначенной для подготовки реагентов. Сменить перчатки перед манипуляциями с реагентами для амплификации. Не встряхивать на вортексе и не переворачивать упаковку с реагентами для амплификации. Каждая упаковка реагентов для амплификации предназначена для проведения до 24 реакций. Перед применением удостовериться в том, что реагенты для амплификации полностью разморозились. Перед тем, как открыть реагенты для амплификации, удостовериться в том, что содержимое упаковки реагентов для амплификации находится на дне, путем постукивания упаковкой с реагентами для амплификации в вертикальном положении по рабочему столу, чтобы жидкость опустилась на дно пробирок. Реагенты для амплификации подписаны следующим образом: активирующий реагент (Реагент 1); реагент для амплификации МБТ (Реагент 2); ДНК-полимераза (Реагент 3). Удалить и выбросить крышки. Используя калиброванную точную пипетку, предназначенную только для реагента, добавить 298 мкл активирующего реагента (Реагента 1) и 418 мкл реагента для амплификации МБТ (Реагента 2) в сосуд с ДНК-полимеразой (Реагент 3), чтобы получить общую реакционную смесь. Перемешать путем аккуратного 5-кратного пипетирования вверх и вниз. Избегать образования пены.
45. Перенести пипеткой всю общую реакционную смесь из сосуда с ДНК-полимеразой в микроцентрифужную пробирку объемом 1,5 мл (№ в перечне 4J71-50 или эквивалентный). Перемешать путем аккуратного 5-кратного пипетирования вверх и вниз. Избегать образования пены.
46. Поместить оптический 96-луночный реакционный планшет Abbott в подставку Abbott, позволяющую избежать разбрызгивания, чтобы предотвратить контаминацию. Загрязнение дна оптического 96-луночного реакционного планшета Abbott флуоресцентными материалами потенциально может препятствовать анализу МБТ. Оптический 96-луночный реакционный планшет Abbott следует держать и перемещать вместе с подставкой, позволяющей избежать разбрызгивания (Splash-Free Support Base) Abbott, чтобы минимизировать контаминацию.
47. Используя точную пипетку, специально предназначенную только для реагентов, распределить аликвоты объемом по 25 мкл общей реакционной смеси для амплификации в каждую лунку оптического 96-луночного реакционного планшета Abbott, который будет использоваться для анализа образцов и контролей. Можно применять калиброванный дозатор многократного дозирования (репитер). Добавить общую реакционную смесь в следующем порядке: начинать с колонки 1 (сверху вниз) и продвигаться к каждой последующей колонке слева направо. Визуально удостовериться в том, что в каждую лунку был добавлен объем 25 мкл. Перенести оптический 96-луночный реакционный планшет Abbott в подставке Abbott, позволяющей избежать разбрызгивания (Splash-Free Support Base), в зону обработки образцов.
48. Применяя точный дозатор и используя свежий стерильный аэрозоль-устойчивый наконечник для пипетки объемом 200 мкл для каждого образца, перенести 25 мкл каждого элюированного образца в оптический 96-луночный реакционный планшет Abbott. В процессе переноса каждого образца перемешать полученную реакционную смесь путем 3- - 5-кратного пипетирования вверх и вниз. Визуально удостовериться в том, что в каждую лунку был добавлен общий объем 50 мкл.
49. Запечатать оптический 96-луночный реакционный планшет Abbott, следуя инструкциям в разделе рабочих инструкций руководства по эксплуатации m2000rt Abbott.
50. Центрифугировали оптический 96-луночный реакционный планшет Abbott в подставке Abbott, позволяющей избежать разбрызгивания, при 5000 g в течение 5 минут.
51. Перенести оптический 96-луночный реакционный планшет Abbott в подставке Abbott, позволяющей избежать разбрызгивания, в зону для проведения амплификации. ПРИМЕЧАНИЕ: Протокол m2000rt Abbott (этап 52) необходимо начать в течение 90 минут после начала добавления общей реакционной смеси и подготовки планшета для ПЦР (этап 44).
52. Поместить оптический 96-луночный реакционный планшет Abbott в устройство m2000rt Abbott, выбрать файл проведения реакции (test order), созданный на этапе 43, и запустить протокол выполнения анализа Abbott Realtime МТВ, как описано в разделе рабочих инструкций руководства по эксплуатации m2000rt Abbott. После завершения запуска результаты анализа будут представлены в отчете m2000rt Abbott.
ПРИМЕР 5
Результаты эксперимента: инактивация
Оценивали, насколько эффективно IR убивал МБТ. В данном эксперименте образцы, содержащие МБТ (культивированный МБТ, который был разбавлен до известных концентраций МБТ перед инактивацией, а также содержащие МБТ осадки в NALC-NaOH), подвергали процедуре инактивации согласно примеру 3. После инактивации избыток инактивирующего реагента удаляли путем центрифугирования/промывки и выжившие клетки помещали в культуру MGIT на срок вплоть до 42 дней или шести недель. Эта продолжительность культивирования рекомендуется как наибольшее время выращивания культуры МБТ; для большинства МБТ-положительных образцов рост культуры можно обнаружить в течение 20 дней от момента инициирования культуры). В таблице 5 ниже проиллюстрированы результаты, полученные при тестировании культивированных образцов после инактивации. Для положительного контроля (ПК), который состоит из не инактивированного МБТ, продемонстрировали рост в течение ожидаемого 20-дневного периода времени, тогда как для отрицательного контроля (ОК) продемонстрировали отсутствие роста.
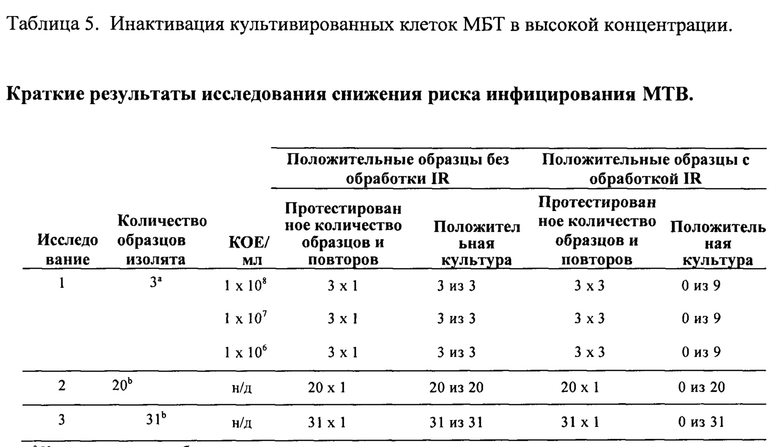
a Культивированные образцы изолята;
b Клинические образцы изолята.
Полученные результаты продемонстрировали эффективность процедуры инактивации в отношении инактивации МБТ.
ПРИМЕР 6
Инклюзивность анализа
Восемь подвидов и 20 образцов из комплекса МБТ (М. tuberculosis, М. Africanum, М. bovis, М. bovis BCG, М. canettii, М. microti, М. caprae, М. pinnipedii) получили от АТСС (М canettii получили от Научно-исследовательского института здравоохранения (Public Health Research Institute)) и исследовали при добавлении от 10 до 100 копий геномной ДНК/реакцию (см. таблицу 6). Все 8 подвидов были обнаружены при обоих указанных уровнях.
Таблица 6. Исследованные подвиды комплекса МБТ.

Исследовали ДНК сорока шести филогенетически и географически разнообразных изолятов МБТ (>50% с MDR), полученных от Public Health Research Institute, при добавлении от 25 до 100 копий геномной ДНК/реакцию (фигура 2). Были обнаружены все исследованные подвиды.
ПРИМЕР 7
Специфичность анализа
Очищенные нуклеиновые кислоты из различных микобактерий, вирусов и других микроорганизмов (n=80) при целевых концентрациях от 1е5 до 1е7 геномов/мл и культивированные микроорганизмы при концентрации 1×106 КОЕ/мл добавляли в отрицательный контроль МБТ, чтобы оценить влияние потенциально перекрестно реагирующих веществ на результаты анализа МБТ для МБТ-отрицательных образцов. Очищенные нуклеиновые кислоты из различных микобактерий, вирусов и других микроорганизмов при целевых концентрациях от 1×106 до 1×107 геномов в миллилитре и культивированные микроорганизмы при концентрации 1е6 КОЕ/мл добавляли к МБТ-положительным образцам, чтобы оценить влияние потенциально перекрестно реагирующих веществ на результаты анализа МБТ для МБТ-положительных образцов. МБТ-положительные образцы получали путем разбавления исходного раствора термоинактивированных клеток МБТ в отрицательном контроле до целевой концентрации, равной 1000 копий/мл (посчитали, используя кривую геномной ДНК). Ни один из МБТ-отрицательных образцов, исследованных с потенциально перекрестно реагирующими веществами, не был обнаружен. Все 80 МБТ-положительных образцов, исследованных с потенциально перекрестно реагирующими веществами, были обнаружены.

ПРИМЕР 8
Чувствительность анализа
Готовили серийные разведения панели МБТ, штамма H37Rv, при концентрации 40 КОЕ/мл в объединенной МБТ-отрицательной мокроте, чтобы получить панель чувствительности. Исследовали шестнадцать повторов каждого разведения. Наблюдали уровень обнаружения, равный 100%, при всех разведениях кратности 160 и ниже. Результаты показаны в таблице 8.
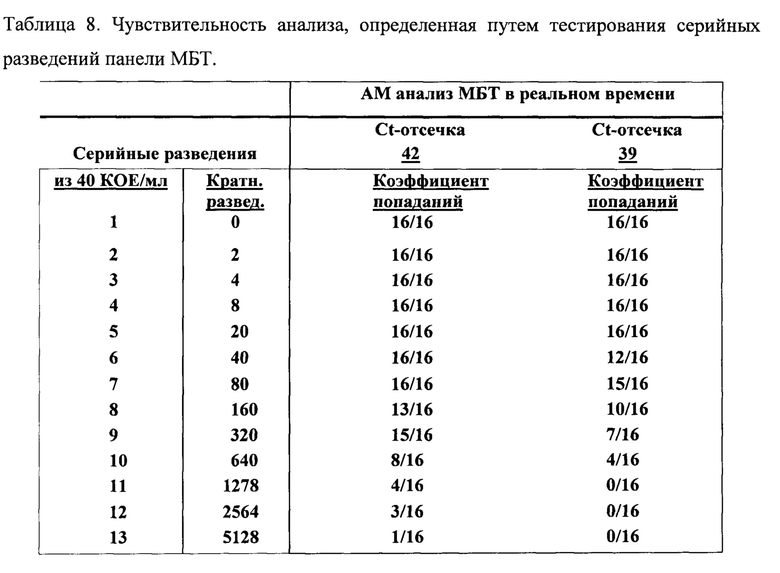
ПРИМЕР 9
Клиническая специфичность
Исследовали образцы NALC (n=155), образцы мокроты (n=23) и БАЛ (n=28) (образцы NALC принадлежали популяции, в которой подозревают наличие МБТ; образцы мокроты и БАЛ принадлежали пациентам без симптомов МБТ) с отрицательной культурой, чтобы определить клиническую специфичность (см. результаты, кратко представленные ниже в таблице 10). Специфичность для образцов мокроты и БАЛ составляла 100%. Специфичность для образцов NALC составляла 98,7%, при этом совокупная специфичность составляла 99%.
Таблица 9. Клиническая специфичность, которую определили путем тестирования МБТ-отрицательных образцов.
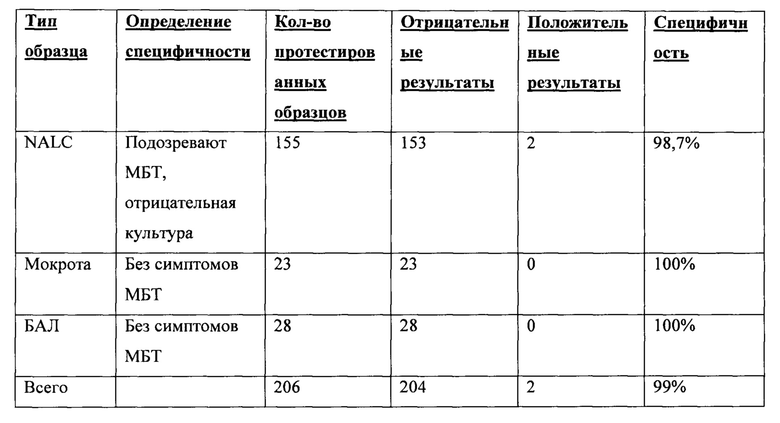
Таблица 10. Исследовали образцы с МБТ-положительной культурой (включая образцы как с положительным мазком, так и с отрицательным мазком) путем анализа МБТ (AM) и другого анализа для сравнения (Уровень сравнимости).
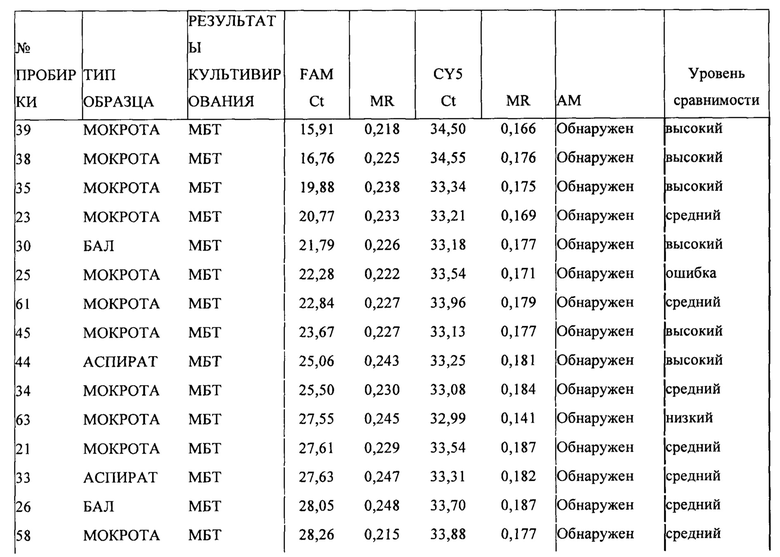
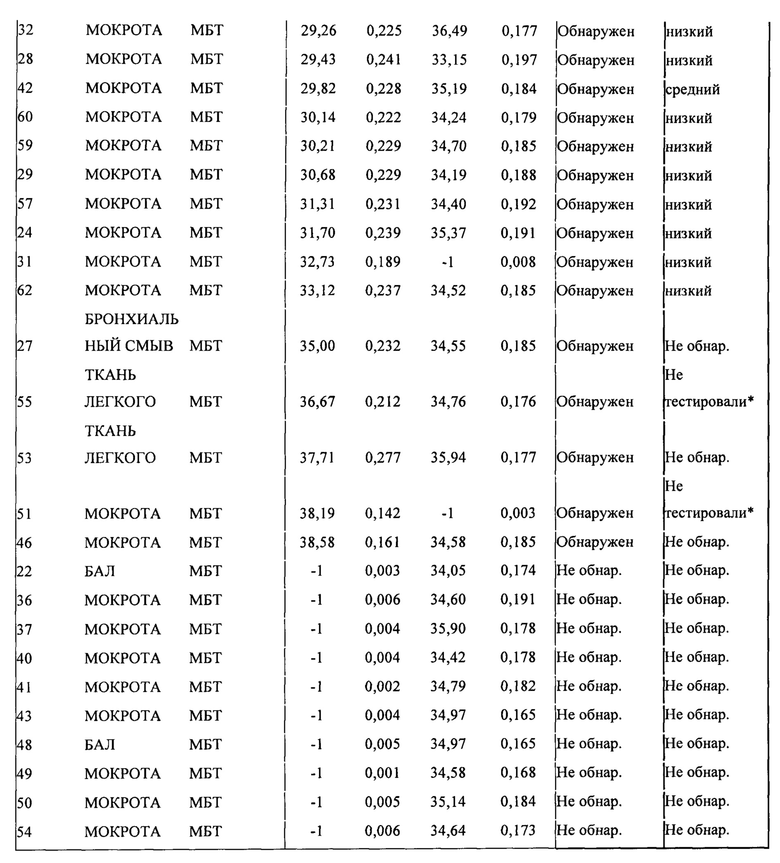
* "не тестировали" образец вследствие недостаточного объема
Для анализа МБТ в реальном времени показали лучшую чувствительность при тестировании образцов с низкой концентрацией по сравнению с сопоставляемым анализом.
ПРИМЕР 10
Аналитическая и клиническая эффективность анализа МБТ
В данном примере описана аналитическая эффективность анализа в реальном времени, позволяющего обнаружить МБТ.
Материалы и методы
Последовательность проведения анализа МБТ в реальном времени описана на фигуре 1.
Инактивация образца
500 мл инактивирующего реагента (IR) получали путем объединения следующих компонентов: 20 мл 10 М NaOH, 300 мл изопропанола, 0,9 мл Tween-20 и 179,1 мл очищенной воды. После получения IR, он был стабилен в течение вплоть до одного месяца при комнатной температуре. Если образцы были заморожены (необработанные образцы или обработанные NALC осадки) размораживали при температуре от 15° до 30°C. Приблизительно три объема IR добавляли в каждый объем образца (минимально допустимый объем образца составлял 0,3 мл). Такое же объемное отношение образец: IR поддерживали независимо от типа образца (необработанный образец или осадок в NALC). Смесь встряхивали на вортексе дважды, каждый раз в течение от 20 до 30 секунд, в течение первого часа инкубации при комнатной температуре. Одобренное время инкубации составляло от одного до 24 часов. Процесс инактивации осуществляли в вытяжном шкафу. После завершения инактивации инактивированные образцы вынимали из вытяжного шкафа, а затем осуществляли обработку образцов вне вытяжного шкафа. Продемонстрировали, что данный процесс инактивации эффективно снижал жизнеспособность МБТ в трех различных лабораториях, в которых использовали культивированные МБТ, добавленные к осадкам мокроты в NALC, МБТ-положительные клинические осадки в NALC и образцы мокроты с положительными на МБТ мазком/культурой (Qi С., и др., Effectiveness of the sample inactivation procedure employed by the new Abbott RealTime assay for the detection of Mycobacterium tuberculosis, 24-й Европейский конгресс по клинической микробиологии и инфекционным заболеваниям (ECCMID) 2014).
Обработка образца
Обработанные IR образцы и контроли для анализа загружали в устройство m2000sp, в котором выделяли ДНК, применяя методику магнитных микрочастиц с гуанидинтиоцианатом для захвата нуклеиновых кислот, с последующими промывками для удаления не связавшихся компонентов. Внутренний контроль (ВК) добавляли в начале обработки образцов. Связавшиеся нуклеиновые кислоты элюировали и переносили в 96-луночный планшет с глубокими лунками. По завершении обработки образцов использовали m2000sp для получения общей реакционной смеси для амплификации, состоящей из полимеразы AmpliTaq Gold, активирующего реагента хлорида магния и олигонуклеотидного реагента, содержащего праймеры, зонды и дНТФ. m2000sp также использовали для распределения аликвот объемом 25 мкл общей реакционной смеси, а затем аликвот объемом 25 мкл экстрагированных элюатов по оптическому 96-луночному реакционному планшету. Планшет запечатывали вручную и переносили в m2000rt для проведения ПЦР в реальном времени. В качестве альтернативы m2000sp, обработку образцов, получение общей реакционной смеси и распределение аликвот по планшету для ПЦР можно осуществить вручную.
Амплификация и детектирование
Устройство m2000 rt использовали для амплификации и обнаружения флуоресценции в реальном времени. Обнаружения представителей комплекса МБТ (Warren RM, и др., Int J Tuberc Lung Dis 2006; 10: 818-822) добивались путем применения двух комплектов праймеров: один был нацелен на элемент вставки IS6110 (Thierry D, и др., Nucleic Acids Res 1990; 18: 188), а другой-на ген РАВ (Anderson АВ, Hansen ЕВ Infect Immun 1989; 57: 2481-2488). Сигнал для обнаружения комплекса МБТ получали, применяя меченые флуоресцентными метками зонды. Каждый из зондов для обнаружения двойной мишени МБТ был помечен флуорофором FAM по 5'-концу и гасителем «черная дыра» (BHQ1) по 3'-концу. Таким образом, сигналы МБТ от обоих IS6110 и РАВ детектировали в одном и том же канале FAM. Цикл амплификации, в котором обнаруживают флуоресцентный сигнал FAM, прямо пропорционален логарифму концентрации ДНК МБТ, присутствующей в исходном образце. Зонд для внутреннего контроля (ВК) метили Quasar по 5'-концу и гасителем «черная дыра» BHQ2 по 3'-концу, чтобы сигналы ВК и мишени в одной лунке ПЦР можно было отличить.
Контроли для анализа
Использовали минимум один повтор отрицательного контроля и один повтор положительного контроля, чтобы определить правильность запуска. Отрицательный контроль состоял из буфера ТЕ и консервантов. Положительный контроль состоял из плазмидной ДНК, содержащей обе целевые последовательности IS6110 и РАВ, разбавленной в буфере ТЕ с добавлением 1,5 г/мл поли(dА:dТ) и консервантов. ВК состоял из плазмидной ДНК, содержащей вставку последовательности гидроксипируватредуктазы из тыквы (HPR), разбавленной в буфере ТЕ с добавлением 1,5 г/мл поли(dА:dТ) и консервантов. ВК добавляли в начале обработки образцов, и он служил в качестве контроля выхода получения образца, ингибирования образца и эффективности амплификации. ВК не выступал в качестве контроля для процедуры инактивации. Различия в значениях порогового цикла (Ct) ВК между каждым образцом и контролями запуска использовали, чтобы оценить достоверность результата для каждого образца.
Панели и клинические образцы
Подвиды комплекса МБТ
Образцы ДНК девятнадцати подвидов комплекса МБТ получили из Американской коллекции типовых культур (АТСС, Манассас, Виргиния) и один (М. canettii) был любезно предоставлен Ibis Biosciences (Карлсбад, Калифорния). Всего исследовали 20 штаммов комплекса МБТ, включая М. Africanum 25420, М. Africanum 35711, М. bovis 35735, М. bovis 19274, М. bovis BCG 35746, М. bovis BCG 35747D, М. canettii, М. caprae BAA-824D, М. microti 11152, М. microti 19422, М. pinnipedii BAA-688D, МБТ 25177D-5 (H37Ra), МБТ 25618D-5 (H37Rv), МБТ ВАА-2236D, МБТ BAA-2237D, МБТ 27294D, МБТ BAA-2234D, МБТ 35822D, МБТ 35838D, МБТ BAA-2235D. Кроме того, 46 штаммов подвидов МБТ, включая три основные генетические группы и девять генетических кластеров, получили от Dr. Barry Kreiswirth из University of Medicine and Dentistry New Jersey (Ньюарк, Нью-Джерси) (Mathema В, и др., Current Insights, Clinical Microbiology Reviews 2006; 19: 658-685). ДНК из 20 подвидов комплекса МБТ, полученную от АТСС и Ibis, исследовали напрямую, применяя указанные концентрации ДНК, определенные с помощью способа PicoGreen® NanoDrop. Концентрации других 46 ДНК определяли в Abbott Molecular, используя измерения PicoGreen® NanoDrop, за исключением трех образцов, для которых такие измерения не могли быть сделаны вследствие низкого объема и примесей. Данные три образца разбавляли в соотношении образца к воде 1:600 и исследовали напрямую.
Предел обнаружения (LOD). Панель МБТ H37Rv, нацеленную на 1×105 колониеобразующих единиц (КОЕ)/мл, получали в Zeptometrix (Буффало, Нью-Йорк). Три аликвоты по одному мл панели Zeptometrix объединяли и центрифугировали при 3000 g в течение 15 минут, чтобы удалить свободную ДНК МБТ в супернатанте. Осадок клеток ресуспендировали в трех мл буфера ТЕ, чтобы сохранить концентрацию 1×105 КОЕ/мл. Клетки затем добавляли в объединенную мокроту, которую гомогенизовали, применяя механическое разрушение гранулами, с получением следующих содержащих МБТ панелей разведения: 80 КОЕ/мл, 50 КОЕ/мл, 25 КОЕ/мл, 10 КОЕ/мл, 5 КОЕ/мл, 1 КОЕ/мл, 0,50 КОЕ/мл, 0,10 КОЕ/мл и 0,05 КОЕ/мл.
Специфичность анализа
Представителей панели специфичности анализа собирали, как описано далее: цитомегаловирус, вирус простого герпеса 1 и вирус ветряной оспы получили от Advanced Biotechnology Inc. (Колумбия, Мэриленд), 69 видов микобактерий и других микроорганизмов получили от АТСС, и восемь изолятов бактерий были культивированы в Abbott Molecular.
Потенциально интерферирующие вещества. Для данного анализа получили следующие материалы: кровь, ДНК из клеток человека, желудочную кислоту, гипертонический солевой раствор, физиологический солевой раствор, культуральные среды, материал осадка в NALC, пять лекарственных средств против МБТ (изониазид, рифампицин, стрептомицин, пиразинамид, этамбутол), и бычью слизь.
Перенос материала из другой пробы
Получали два образца: высоко положительный образец МБТ, содержащий 1×107 копий/мл плазмиды, содержащей целевые для данного анализа последовательности, и отрицательный образец.
Воспроизводимость
Получали два образца: положительный образец, содержащий МБТ в концентрации, ~ в три раза превышающей заявленный LOD анализа, и отрицательный образец.
Клинические образцы
198 образцов мокроты были собраны Discovery Life Sciences (Лос Осос, Калифорния) из пациентов, у которых подозревали наличие МБТ, из России, Южной Африки, Уганды и Вьетнама. 150 образцов мокроты из Вьетнама получили из банка образцов, которым управляет Foundation for Innovative New Diagnostics (FIND) (Женева, Швейцария). 234 образца NALC получили из Northwestern University Memorial Hospital (Чикаго, Иллинойс). Все образцы из пациентов собирали следуя этическим нормам. ВИЧ-статус пациентов не определяли. Для всех образцов тестирование мазков (если они были доступны) и культур проводили вблизи от места сбора, тогда как анализ МБТ в реальном времени Abbott осуществляли в Abbott Molecular.
Результаты
Обнаружение подвидов комплекса МБТ
Данное исследование проводили, чтобы определить позволят ли специфичные праймеры и зонды, используемые в анализах МБТ, обнаружить следующие восемь подвидов комплекса МБТ: М. Africanum, М. bovis, М. bovis BCG, М. canettii, М. caprae, М. microti, М. pinnipedii и М. tuberculosis. Исследовали два набора очищенных ДНК комплекса МБТ. Первый набор из 20 очищенных ДНК включал представителей ранее упомянутых подвидов МБТ. Каждую очищенную ДНК исследовали при двух концентрациях (100 и 10 геномов/реакцию), при этом каждую концентрацию исследовали в четырех повторах. При уровне 100 геномов МБТ на реакцию каждый из 20 штаммов МБТ был обнаружен во всех четырех повторах. При уровне 10 геномов МБТ на реакцию 17 штаммов были обнаружены во всех четырех повторах. Три штамма (два М. bovis и один М. bovis BCG) были обнаружены в двух из четырех повторов (фигура 4). Второй набор из 46 штаммов МБТ из подвидов МБТ исследовали при двух концентрациях: 100 геномов/реакцию и 25 геномов/реакцию. Каждую концентрацию каждой ДНК исследовали в четырех повторах. Все исследованные повторы были положительны при обеих концентрациях (фигура 2).
Предел обнаружения (LOD)
Получали девятикратное серийное разведение клеток штамма МБТ H37Rv, разбавленных гомогенизованной стеклянными гранулами объединенной мокротой. Целевые концентрации представителей панели после серийного разведения перечислены далее: 80 КОЕ/мл, 50 КОЕ/мл, 25 КОЕ/мл, 10 КОЕ/мл, 5 КОЕ/мл, 1 КОЕ/мл, 0,50 КОЕ/мл, 0,10 КОЕ/мл и 0,05 КОЕ/мл. Двадцать повторов каждого представителя панели исследовали в четырех запусках, применяя анализ МБТ в реальном времени Abbott. Исследование проводили, используя одну партию реагентов для анализа МБТ и контрольных реагентов. Уровень значимости для данного исследования составлял 0,05. Частоту обнаружения рассчитывали для каждой целевой концентрации (таблица 11). На основании целевых концентраций и частоты обнаружения применили модель пробит-регрессии, используя PROC PROBIT в SAS, где целевая концентрация (X) выступала в роли независимой переменной и частота обнаружения Р (Y=1) выступала в роли переменной отклика. Анализ результатов пробит позволил определить, что концентрация МБТ, обнаруживаемая с вероятностью 95%, составляла 2,45 КОЕ/мл (доверительный интервал (CI) 95%: 1,44-6,10 КОЕ/мл). Заявленная чувствительность анализа данного анализа МБТ в реальном времени Abbott составляла 17 КОЕ/мл в объединенной гомогенизованной мокроте при использовании штамма МБТ H37Rv.
Специфичность анализа
Исследовали каждое из 80 потенциально перекрестно реагирующих веществ как в МБТ-положительном образце, так и в МБТ-отрицательном образце. Нуклеиновую кислоту из каждой потенциально перекрестно реагирующей микобактерий, вируса или другого микроорганизма при целевой концентрации, равной от 1×105 до 1×107 копий или геномов в мл, добавляли в МБТ-положительные образцы (содержащие 1000 геномов МБТ/мл) и в МБТ-отрицательные образцы. Культивированные микроорганизмы при целевой концентрации, равной 1×106 КОЕ/мл, добавляли в МБТ-положительные образцы и в МБТ-отрицательные образцы. Результаты анализа для всех 80 отрицательных образцов были следующими: "МБТ не обнаружен". Результаты анализа для всех 80 образцов, содержащих МБТ, были следующими: "МБТ обнаружен" (таблица 7).
Потенциально препятствующие вещества
Оценивали потенциально влияющие на результаты анализа вещества, которые могут присутствовать в дыхательной системе. МБТ-отрицательные и МБТ-положительные (500 копий/мл) образцы исследовали в отсутствие или в присутствии каждого потенциально препятствующего вещества при повышенных уровнях бычьей слизи, крови, ДНК из клеток человека, желудочной кислоты, гипертонического солевого раствора, физиологического солевого раствора, культуральных сред, осажденного в NALC материала и пяти лекарственных средств против МБТ (изониазида, рифампицина, стрептомицина, пиразинамида, этамбутола) (таблица 12). Результаты показали отсутствие снижения эффективности анализа МБТ в присутствии высоких уровней крови, ДНК из клеток человека, желудочной кислоты, гипертонического солевого раствора, физиологического солевого раствора, культуральных сред, осажденного в NALC материала и пяти лекарственных средств против МБТ (изониазида, рифампицина, стрептомицина, пиразинамида, этамбутола). Препятствие анализу МБТ в реальном времени Abbott наблюдали в присутствии бычьей слизи при концентрациях 8,3% (все пять повторов были ложноотрицательными или ингибированными) и 5,0% (один из пяти повторов был ложноотрицательным). Не было обнаружено препятствия анализу при концентрации бычьей слизи 2,5% или менее.
Перенос материала из другой пробы
Чтобы оценить потенциальный перенос материала из высоко положительных образцов МБТ в отрицательные образцы при применении анализа МБТ в реальном времени Abbott, провели пять запусков в системе m2000, каждый из которых состоял из 96 образцов (положительный контроль, отрицательный контроль, 46 высоко положительных образцов при концентрации 1×107 копий/мл и 46 отрицательных образцов), при этом высоко положительные образцы были распределены между отрицательными образцами. Концентрация МБТ в высоко положительном образце, равная 1×107 копий/мл, приводила к значению Ct, которые было меньше, чем 95% или более результатов, полученных для образцов из МБТ-положительной популяции, исследованной с помощью анализа МБТ. В данном анализе не выявили переноса материала из высоко положительных образцов в 230 отрицательных образцов в пяти запусках. Запуск 96 образцов занимал менее 8 часов.
Воспроизводимость
Проводили тест на воспроизводимость, чтобы оценить воспроизводимость анализа МБТ в реальном времени Abbott в системе m2000 и совместимость устройства m2000sp Abbott со способом обработки образцов вручную. Исследование проводили с положительной панелью при концентрации, в три раза превышающей заявленный уровень LOD, и отрицательной панелью. Исследование проводили четыре оператора, использующие две партии реагентов для амплификации МБТ: два оператора проводили запуски, используя устройство m2000sp Abbott, и два оператора проводили запуски, используя обработку образцов вручную. Для каждого способа обработки образцов каждый из двух операторов использовал одну уникальную партию реагентов для амплификации МБТ в реальном времени Abbott, и исследовали каждого представителя панели в восьми повторах, один раз в день в течение пяти дней, всего протестировали 40 повторов каждого представителя панели (всего 80 повторов каждого представителя панели протестировано каждым способом; всего 160 протестировано с обработкой образцов с помощью устройства m2000sp и всего 160 протестировано с обработкой образцов вручную). Общее соответствие ожидаемым результатам составляло 100% (159/159, один образец оказался непригодным вследствие ошибки устройства) с наименьшим 95% CI, равным 98,1%, для образцов, полученных с помощью устройства m2000sp Abbott, или образцов, полученных путем обработки вручную. Анализ МБТ совместим как со способом обработки образцов в устройстве m2000sp Abbott, так и со способом обработки образцов вручную Abbott.
Клиническая чувствительность и специфичность
Исследовали одну мокроту или один осадок в NALC из каждого из 582 пациентов, у которых подозревали наличие МБТ. Образцы собирали из России, Южной Африки, Уганды, Соединенных Штатов и Вьетнама. Каждый образец разделяли, чтобы обеспечить возможность тестирования МБТ в одной аликвоте и получить мазок и культуру из второй аликвоты. Тестируемые образцы заслепляли, и расшифровку конечного результата осуществляла статистическая группа AM. При тестировании МБТ для двух образцов получили ошибочные результаты ВК, и для дополнительных четырех образцов получили коды ошибки m2000. Частота ошибочных результатов для клинических образцов вследствие ингибирования составляла 0,3% (2/582), тогда как частота ошибочных результатов вследствие как ингибирования, так и ошибок устройства составляла 1,0% (6/582). Пять образцов с отрицательной культурой, которые были положительны как по результатам анализа МБТ, описанного в данной заявке, так и по результатам доступного для приобретения анализа МБТ-NAAT, исключили из данного анализа. Всего 571 допустимый образец был включен для анализа результатов. Общая чувствительность к МБТ по сравнению с культурой составляла 93% (198/212). Чувствительность анализа составляла 99% (147/149) в образцах с положительным мазком и положительной культурой и 81% (51/63) в образцах с отрицательным мазком и положительной культурой. Специфичность составляла 97% (348/359) (таблица 13). 76 из МБТ-отрицательных образцов содержали не туберкулезные микобактерий (НТМ). Из них 38 представляли собой MAC (комплекс М. avium), семь представляли собой М. gordonae, пять представляли собой М. kansasii, пять представляли собой M.chelonae/abcessus, три представляли собой М. xenopi и 18 включали другие виды микобактерий. Результаты анализа МБТ, описанного в данной заявке, для всех образцов НТМ были следующими: "МБТ не обнаружен", - за исключением двух образцов, в которых результат был: "МБТ обнаружен", при поздних значениях CN (>38) по сравнению с пороговым в данном анализе значением, равным 40. Значение специфичности 97%, полученное в результате тестирования популяции НТМ, было аналогично специфичности, наблюдаемой при тестировании популяции, не принадлежащей к НТМ. Более того для 500 образцов мокроты, собранных из пациентов из популяции США, у которых не подозревали наличие МБТ, получили 100% МБТ-отрицательных результатов анализа.
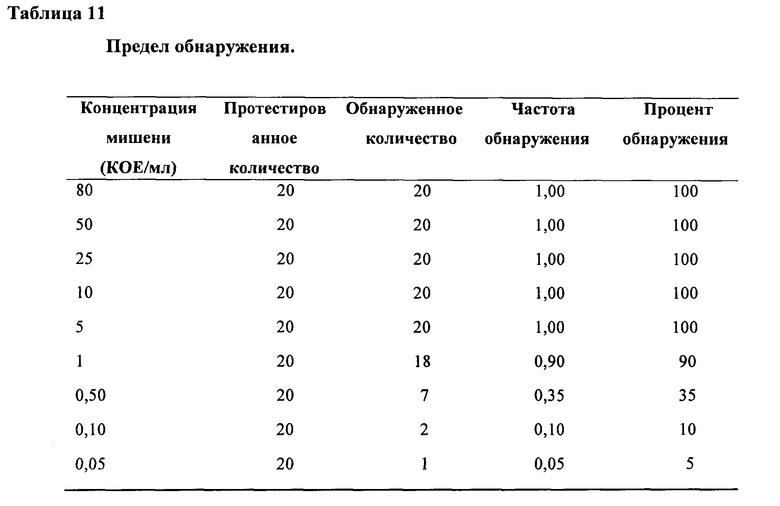
Пробит-анализ результатов анализа МБТ в реальном времени Abbott позволил определить, что концентрация МБТ, обнаруживаемая с вероятностью 95%, составляла 2,45 КОЕ/мл при пороговом значении CN, равном 40 (95% доверительный интервал 1,44-6,10 КОЕ/мл).



ПРИМЕР 11
Инактивирующие реагенты
В данном примере описаны инактивирующие реагенты для применения в анализах, позволяющих обнаружить МБТ. Указанный анализ представляет собой NAAT для обнаружения комплекса ДНК МБТ в образцах из дыхательной системы (мокроте, бронхоальвеолярном лаваже (БАЛ) и в осадках в N-ацетил-L-цистеине (NALC) мокроты и бронхоальвеолярного лаважа (БАЛ)). Инактивирующие образец реагент и процедура были разработаны для разжижения вязких образцов и снижения жизнеспособности МБТ, чтобы обеспечить возможность безопасного тестирования образцов за пределами боксов микробиологической безопасности. Данное исследование проводили, чтобы оценить эффективность процедуры инактивации образца и определить стабильность инактивирующего реагента (IR).
Для исследования уменьшения вязкости 150 образцов мокроты смешивали с IR (0,6% гидроксид натрия (масса/объем), 60% изопропанол (объем/объем) и 1,8% Tween-20 (объем/объем)) в соотношении 1:2 или 1:3. Смеси интенсивно встряхивали на вортексе и инкубировали при комнатной температуре. Смесь снова встряхивали на вортексе после 20-30 минут инкубации. Уменьшение вязкости оценивали путем визуального наблюдения после 30 минут, 60 минут и 24 часов инкубации.
Для исследования инактивации два клинических изолята МБТ и изолят МБТ АТСС 27294 использовали для получения имитации МБТ-положительных образцов из дыхательной системы путем смешивания одного мл суспензии клеток МБТ при концентрациях 1×106, 1×107 или 1×108 КОЕ/мл с четырьмя мл объединенного МБТ-отрицательного, обработанного NALC образца из дыхательной системы. Каждый имитирующий МБТ образец, обработанный NALC, затем смешивали с IR при соотношениях 1:2 или 1:3. Имитирующий образец, обработанный стерильным буфером ФБР при соотношении образца к ФБР 1:2, использовали в качестве положительного контроля. Отрицательные контроли получали путем добавления стерильного ФБР в объединенный МБТ-отрицательный образец, обработанный NALC, при соотношении ФБР к NALC 1:2. Все образцы/контроли интенсивно встряхивали на вортексе и инкубировали в течение 60 минут при комнатной температуре. Встряхивание на вортексе повторяли после 30 минут инкубации. По окончании инкубации обработанные IR образцы переносили в новые пробирки объемом 50 мл, встряхивали на вортексе и центрифугировали в течение 15 минут при 3000 × g. Полученный осадок ресуспендировали в 10 мл стерильного ФБР и центрифугировали в течение дополнительных 15 минут при 3000 × g. Каждый осадок ресуспендировали в 10 мл стерильного ФБР. Один мл полученной суспензии использовали для инокуляции индикаторной пробирки роста микобактерий (MGIT). Конечное количество МБТ, добавленное в каждую культуру MGIT, находилось в диапазоне от 1 - 2×104 до 1 - 2×106 КОЕ. Кроме того, исследовали рост всего 51 МБТ-положительного клинического осадка мокроты в NALC: 20 из Northwestern Memorial Hospital и 31 из Lancet Laboratories, после обработки IR при соотношении образца к IR, равном 1:3, с помощью такой же процедуры. Десять из 20 образцов из Northwestern Memorial Hospital обрабатывали при соотношении образца к IR, равном 1:2. Остальные 41 образец обрабатывали при соотношении образца к IR, равном 1:3. Культивирование осуществляли с помощью системы ВАСТЕС MGIT 960 (Becton Dickinson, Спаркс, Мэриленд) в течение 42 дней. Положительный рост обнаружили с помощью системы Gen-Probe Accuprobe® (Gen-Probe Inc, Сан-Диего, Калифорния). Также проводили первичные исследования для демонстрации эффективности инактивации образцов, непосредственно полученных из дыхательной системы (образцов мокроты с МБТ-положительными мазком и культурой), в комбинации с исследованием стабильности IR, описанным в следующем абзаце.
Для того, чтобы определить оптимальные условия хранения IR, три аликвоты IR хранили в течение 39 дней при условиях хранения 15-30°C и 33-37°C в стеклянных или полипропиленовых сосудах. Изучали изменения внешнего вида и объема каждой аликвоты IR при каждом из условий хранения и исследовали эффективность инактивации МБТ после 39 дней хранения на 12 образцах мокроты с положительными на МБТ мазком и культурой, полученных от SAGE Bio Networks (Дакка, Бангладеш) и из банка образцов МБТ Foundation for Innovative New Diagnostics (FIND), используя соотношение образца к IR, равное 1:3. Панель клеток штамма МБТ H37Rv, полученную от Zeptometrix Corporation (Буффало, Нью-Йорк), использовали в качестве положительного контроля.
При исследовании уменьшения вязкости показали, что 60 минут инкубации было достаточно для того, чтобы уменьшить вязкость образцов. При исследовании инактивации ни в одном из имитирующих МБТ образцов, полученных из трех изолятов МБТ при концентрации 1×108, 1×107 и 1×106 КОЕ/мл, не выявили рост МБТ после обработки IR при соотношении образца к IR, равном 1:3. В одном обработанном IR образце, полученном из МБТ при концентрации 1×107 КОЕ/мл и обработанном IR при соотношении образца к IR, равном 1:2, выявили рост после 27 дней инкубации, хотя для двух повторов при такой же концентрации бактерий результаты анализа роста были отрицательными. Ни в одном из 20 МБТ-положительных осадках мокроты в NALC не выявили рост МБТ после обработки IR при соотношении образца к IR, равном 1:2 или 1:3. Кроме того, в 31 клиническом осадке мокроты в NALC, результаты анализа роста МБТ в культурах, которые при предыдущем исследовании были положительными на МБТ, оказались отрицательными после обработки при соотношении образца к IR, равном 1:3.
Изменений внешнего вида после 39 дней хранения не наблюдали. Наблюдали потерю объема от 0 до 6% после 39 дней хранения. Наибольшую потерю объема, составляющую 6%, наблюдали, когда IR хранили в полипропиленовых контейнерах при 33-37°C. Тем не менее эффективность раствора IR в отношении инактивации МБТ не нарушалась после хранения. В 12 указанных МБТ-положительных образцах мокроты не выявили роста после обработки IR, который хранили при различных условиях, описанных выше.
Было отмечено, что некоторое количество МБТ в клинических образцах пережило процесс инактивации образца, рекомендуемый Cepheid GeneXpert MTB/RIF (период инкубации 15 минут и соотношение образца к инактивирующему реагенту 1:2) (Banada, P.P., и др., 2010. J. Clin. Microbiol. 48: 3551-3557). Авторы настоящего изобретения предположили, что для полной инактивации МБТ может потребоваться более длительное время инкубации. Результаты эксперимента, полученные в ходе исследования, описанного в данной заявке, продемонстрировали, что инактивации образца, осуществленной в течение 60 минут с использованием рекомендуемых этапов встряхивания на вортексе, было достаточно для полной инактивации МБТ.
При использовании соотношения образца к IR, равного 1:2, выявили рост в одном повторе при концентрации МБТ 1×107 КОЕ/мл культуры (2×105 КОЕ/мл в культуре MGIT) после 27 дней инкубации культуры MGIT. В предыдущем исследовании показали, что культуры MGIT, содержащие 10 КОЕ МБТ/мл, становились положительными после 16 дней инкубации, полученный результат позволил предположить, что очень малое количество МБТ выживало в процессе инактивации при использовании соотношения образца к IR, равного 1:2 (Tortoli, Е., Р. и др., J. Clin. Microbiol, 37 (11): 3578-3582; Wallis, и др., 1999. Antimicrobial Agents and Chemotherapy, 43: 2600-2606). Для достижения оптимальной эффективности инактивации использовали соотношение образца к IR, равное 1:3, для остальных экспериментов по инактивации.
В заключение, IR, который оценивали в данном исследовании, был способен разжижать образцы мокроты и приводить к эффективной инактивации МБТ в клинических образцах после обработки IR при соотношении образца к IR, равном 1:3, в течение 60 минут. Данная процедура инактивации позволяет безопасно проводить манипуляции над данными образцами за пределами бокса микробиологической безопасности после надлежащей процедуры инактивации.











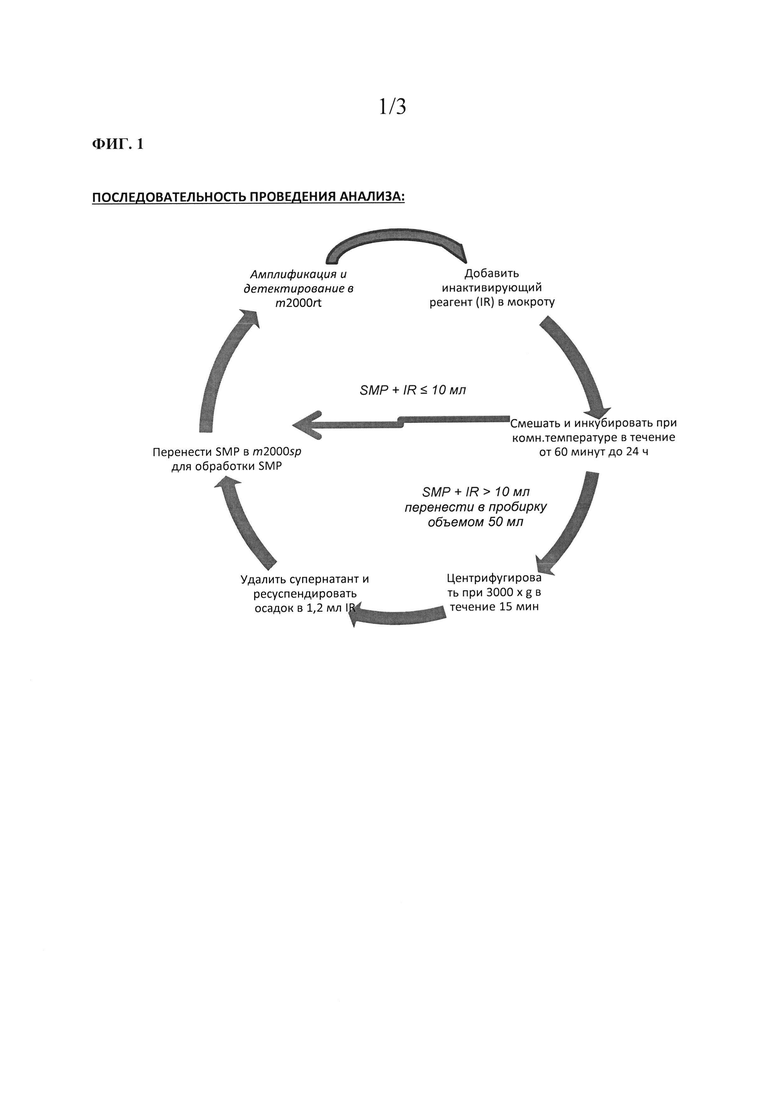
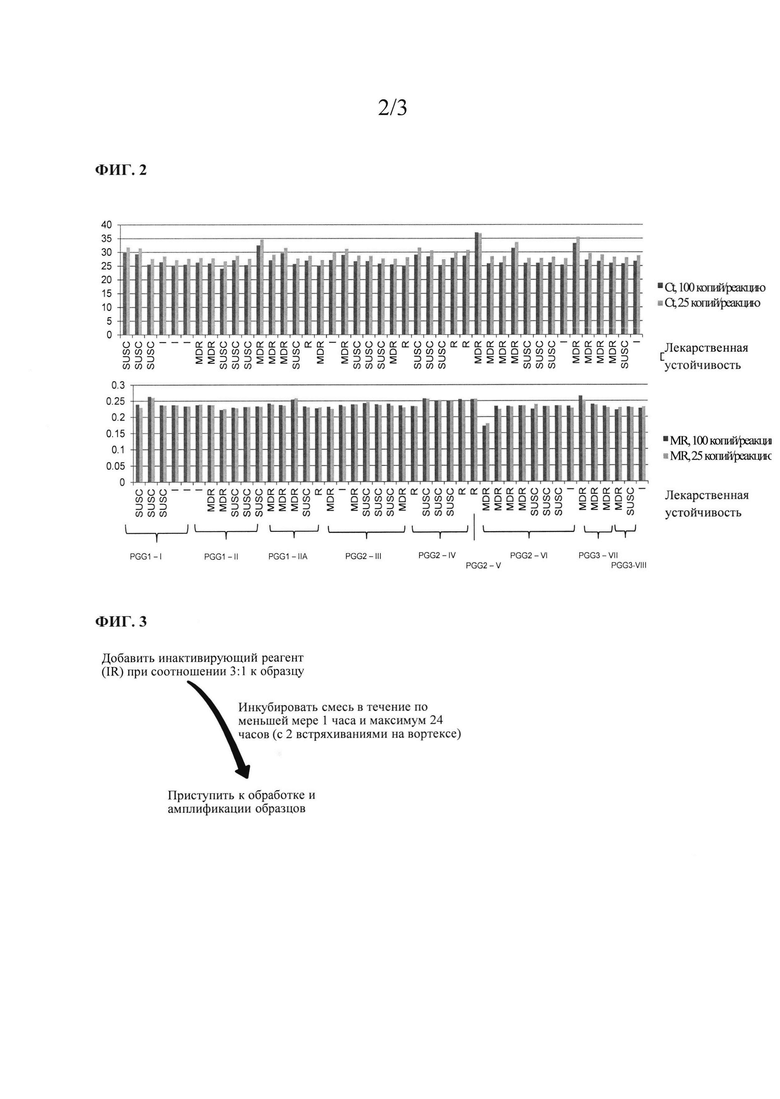
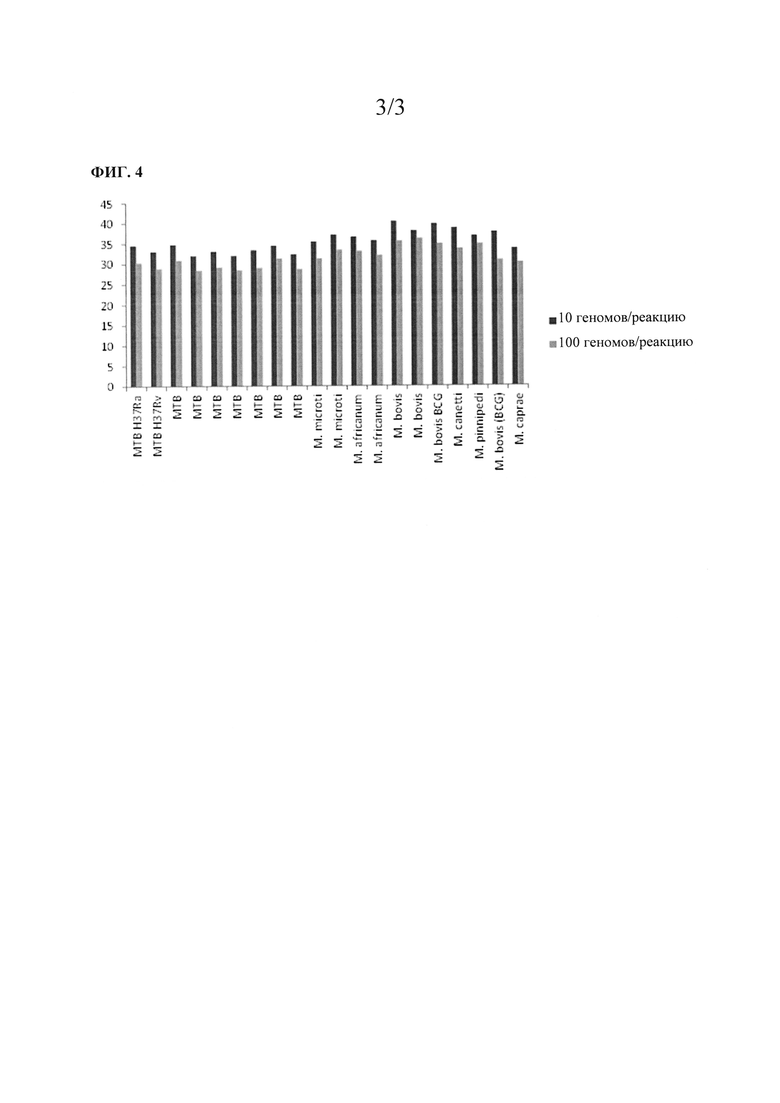
Изобретение относится к биотехнологии, в частности предложены композиции и способы, подходящие для обнаружения МБТ. В данном изобретении предложены наборы, реагенты, реакционные смеси и способы, в которых их применяют для процедур амплификации и обнаружения нуклеиновых кислот, которые позволяют специфично и чувствительно обнаружить МБТ в образцах. 5 н. и 9 з.п. ф-лы, 4 ил., 13 табл., 11 пр.
1. Композиция реакционной смеси для обнаружения микобактерии туберкулеза, содержащая по меньшей мере одну пару праймеров, выбранную из группы, состоящей из последовательностей SEQ ID NO: 1 и 2, последовательностей SEQ ID NO: 3 и 4 и последовательностей SEQ ID NO: 7 и 8.
2. Композиция по п. 1, отличающаяся тем, что указанная композиция содержит последовательности SEQ ID NO: 1-4 и 7-8.
3. Композиция по п. 1, отличающаяся тем, что указанная композиция дополнительно содержит по меньшей мере один зонд, выбранный из группы, состоящей из последовательностей SEQ ID NO: 5, 6 и 9.
4. Композиция реакционной смеси для обнаружения микобактерии туберкулеза, содержащая набор пар праймеров, содержащих:
а) последовательности SEQ ID NO: 1 и 2; и
б) последовательности SEQ ID NO: 3 и 4.
5. Композиция по п. 1, отличающаяся тем, что указанная композиция дополнительно содержит по меньшей мере один зонд, выбранный из группы, состоящей из последовательностей SEQ ID NO: 5, 6 и 9.
6. Композиция по п. 4 или 5, отличающаяся тем, что указанная композиция дополнительно содержит пару праймеров с последовательностями SEQ ID NO: 7 и 8.
7. Композиция реакционной смеси для обнаружения микобактерии туберкулеза, содержащая нуклеиновые кислоты с последовательностями SEQ ID NO: 1-9.
8. Композиция по любому из пп. 1-7, отличающаяся тем, что одна или более из перечисленных последовательностей SEQ ID NO содержит метку.
9. Композиция по п. 8, отличающаяся тем, что указанная метка включает флуорофор.
10. Композиция по любому из пп. 1-9, отличающаяся тем, что указанная композиция дополнительно содержит одну или более последовательностей нуклеиновых кислот, выбранных из группы, состоящей из последовательностей SEQ ID NO: 10 - 36.
11. Композиция по любому из пп. 1-10, отличающаяся тем, что указанная реакционная смесь содержит образец.
12. Композиция по п. 11, отличающаяся тем, что указанный образец содержит целевую нуклеиновую кислоту микобактерии туберкулеза (МБТ).
13. Набор для обнаружения микобактерии туберкулеза, содержащий:
a) композицию по любому из пп. 1-10; и
b) по меньшей мере один реагент для проведения реакции амплификации нуклеиновых кислот.
14. Способ идентификации нуклеиновой кислоты микобактерии туберкулеза (МБТ) в биологическом образце, включающий:
a) осуществление контакта биологического образца от субъекта с праймером или зондом на основе нуклеиновых кислот с последовательностями SEQ ID NO: 1-9, и
b) обнаружение связывания указанного праймера или зонда на основе нуклеиновых кислот с указанной нуклеиновой кислотой МБТ.
| Устройство для регулирования напряжения вспомогательного генератора локомотива | 1975 |
|
SU619375A1 |
| WO 2003070981 A2, 28.08.2003 | |||
| US 20130177914 A1, 11.07.2013 | |||
| СПОСОБ ДЕТЕКЦИИ ПАТОГЕННЫХ МИКОБАКТЕРИЙ В КЛИНИЧЕСКИХ ОБРАЗЦАХ | 2003 |
|
RU2338789C2 |
Авторы
Даты
2019-08-14—Публикация
2015-07-07—Подача