УРОВЕНЬ ТЕХНИКИ
Мутации киназы анапластической лимфомы (АЛК), как считается, вовлечены в развитие подмножеств многочисленных видов рака включая i) немелкоклеточный рак легкого; И) диффузную крупноклеточную В-клеточную лимфому; iii) плоскоклеточный рак пищевода; iv) анапластическую крупноклеточную лимфому; v) нейробластому (рак у детей, который возникает из развивающейся периферической нервной системы) и vi) саркомы, известные как воспалительные миофибробластные опухоли (ВМО). Результаты лечения пациентов со многими из этих злокачественных новообразований являются неудовлетворительными, отчасти вследствие позднего обнаружения рака из-за отсутствия эффективных клинических способов диагностики. Раннее выявление и диагностика АЛК-опосредованных видов раковых заболеваний резко повышает выживаемость в группе пациентов. Так, например, раннее выявление АЛК-положительной анапластической крупноклеточной лимфомы может привести к уровню выживаемости до 83%, тогда как позднее выявление связано в некоторых случаях с выживаемостью только 50% популяции пациентов. Технологии, которые позволили бы раннюю диагностику этих видов рака могут значительно облегчить медицинский менеджмент пациентов, страдающих от них, в конечном счете помогая улучшить исход их лечения. Как доклинические так и ранние клинические данные демонстрируют, что только те виды рака, которые экспрессируют активирующие АЛК мутации, ведущие к их развитию и прогрессированию, проявляют надежные противоопухолевые ответы на низкомолекулярные ингибиторы АЛК.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Способы и композиции, описанные здесь, относятся к области обнаружения и диагностики наличия заболевания или состояния, такого как рак; оценивания восприимчивости или риска развития заболевания или состояния, такого как рак; мониторинга прогрессии заболевания для таких заболеваний, как рак, а также определения чувствительности или устойчивости к терапевтическому лечению такого заболевания, как рак, где заболевание или состояние представляет собой рак, ассоциированный с вариациями, усечением нуклеиновой кислоты, или слиянием гена АЛК. Понятно, и в данном документе это рассматривается, что описанные здесь способы позволяют быстро и точно обнаруживать редкие мутации (т.е. нуклеотидные вариации, которые малочисленны), включая мутации, содержащие слияния полипептида в присутствии избытка нормальной ДНК, а также выявлять редкие усечения и аберрантные чрезмерные экспрессии генов дикого типа.
В соответствии с целью (целями) данного изобретения, как это реализовано и широко описано здесь, это изобретение, в одном аспекте, относится к способам определения наличия ракового заболевания путем выявления нуклеотидных изменений в интересующей нас нуклеиновой кислоте, включающий проведение полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) на мРНК, извлеченной из образца ткани субъекта с раком, где наличие амплификации продукта или увеличение амплификации продукта по сравнению с контролем свидетельствует о наличии слияния, нуклеотидной вариации, усечения, или чрезмерной экспрессии, таким образом, определяя наличие рака. В частности, изобретение, в одном аспекте, относится к способам определения наличия рака, путем обнаружения наличия одного или нескольких связанных с АЛК слияний и/или усиления экспрессии АЛК дикого типа, которые могут возникнуть при определенных раковых заболеваниях.
Дополнительные преимущества открытых способов и композиций будут изложены частично в нижеследующем описании, а частично будут понятны из описания, или могут быть изучены при использовании на практике открытых способов и композиций. Преимущества открытых способов и композиций будут реализованы и достигнуты посредством элементов и их комбинаций, детально указанных в формуле изобретения. Должно быть понятно, что как вышеупомянутое общее описание, так и последующее детальное описание являются только примерными и пояснительными и не ограничивающими формулу изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Сопроводительные чертежи, которые включены в данный документ и являются частью этой спецификации, иллюстрируют несколько вариантов воплощения открытых способов и композиций, и вместе с описанием, служат для объяснения принципов открытых способов и композиций.
Фигура 1 демонстрирует, репрезентативные белки АЛК слияния, хромосомные перестройки, которые их генерируют, их присутствие в АЛК-положительных лимфомах и воспалительных миофибробластических опухолях (ВМО) саркомах, и их субклеточные локализации. Частичный перечень наиболее распространенных онкогенных АЛК слияний показан (не показаны: ALO17-АЛК, CARS-АЛК, MYH9-АЛК, SEC31L1-AЛК, MSN-АЛК, и TFGXL-AЛК. С: цитозольное, N: ядерное, СМ: клеточная мембрана, NM: ядерные мембраны. ТРМ3: тропомиозин-3; ATIC: 5-аминоимидазол-4-карбоксамида рибонуклеотид формилтрансфераза / IMP циклогидролаза; CLTC: клатрина тяжелая цепь; TFG: TFG-ген слияния; ТРМ4; тропомиозин-4; MSN: моезин; RanBP2: Ran-связывающий белок 2; EML4: связанный с микротубулами протеиноподобный 4 иглокожих.
Фигура 2 демонстрирует, прямой и обратный праймеры для ОТ-ПЦР реакции для выявления слияния АЛК.
Фигура 3 демонстрирует примерное положение зонда и область поломки АЛК дикого типа и различных партнеров слияния в том числе семь вариантов ЕМL4-АЛК, NPM-АЛК, MSN-АЛК, CLTC-АЛК, ТРМ-АЛК, и КIF5В-АЛК.
Фигура 4 демонстрирует ОТ-ПЦР амплификацию целей слияния АЛК.
Фигура 5 демонстрирует обнаружение слияния АЛК и идентификацию ампликона при помощи ОТ-ПЦР. Фигура 5А демонстрирует, что образец от субъекта может быть получен и протестирован на наличие слияния АЛК (известного или неидентифицированного ранее), АЛК дикого типа, доменов АЛК киназы, а также элементов контроля реакции для нормализации упорядочивания между анализами (СОХ5В) и положительным и отрицательным контролем анализа. Фигура 5В демонстрирует примеры идентификации слияния или диких типов по размеру ампликона.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Прежде чем будут раскрыты и описаны настоящие соединения, композиции, статьи, устройства и/или способы, следует понять, что они не ограничиваются конкретными синтетическими способами или конкретными рекомбинантными биотехнологическими способами, если не указано иное, или определенными реагентами, если не указано иное, и как таковые могут, конечно, меняться. Также следует понимать, что терминология, используемая в настоящем документе, применяется только с целью описания конкретных вариантов воплощения изобретения, но не для какого бы то ни было ограничения.
Формы единственного числа, используемые в спецификации и формуле изобретения, включают множественное число референтов, если контекст ясно не диктует иное. Так, например, ссылка на "фармацевтический носитель" включает смеси двух или более таких носителей, и тому подобное.
Диапазоны могут быть выражены здесь, как в форме от "приблизительно" одного конкретного значения, и/или до "приблизительно" другого конкретного значения. При отображении такого диапазона другой вариант воплощения изобретения включает - от одного, конкретного значения и/или до другого конкретного значения. Аналогичным образом, когда значения выражаются приближенно, при использовании ранее упомянутого "приблизительно", будет понятно, что конкретное значение образует другой вариант воплощения изобретения. Далее станет понятно, что конечная точка каждого из диапазонов является показательной как по отношению к другой конечной точке, так и независимо от других конечных точек. Предполагается также, что есть ряд значений, описанных здесь, и что каждое значение также раскрывается здесь как "приблизительное", то есть конкретное значение в дополнение к самому значению. Например, если раскрывается значение "10", то также раскрываются значения "приблизительно 10". Также понятно, что, когда указывается значение, которое "меньше или равно значению ", больше или равно значению" и возможные диапазоны между значениями также раскрыты, это также понятно специалистам в данной области. Например, если значение "10" раскрывается как "меньше или равно 10", также раскрывается "больше или равно 10". Также понятно, что во всем приложении, данные представлены в нескольких различных форматах, и эти данные, представляет собой конечные точки и отправные точки, и диапазоны для любой комбинации точек данных. Например, если раскрыта конкретная точка данных "10" и конкретная точка данных 15, то понятно, что больше чем, больше или равно, меньше чем, меньше или равно, и равно 10 и 15 считаются раскрытыми, так же как диапазон между 10 и 15.
В этой спецификации и в формуле изобретения, которые следуют ниже, будут сделаны ссылки на ряд терминов, которые должны быть определены, как имеющие следующие значения:
"Необязательный" или "необязательно" означает, что описанные впоследствии события или обстоятельства могут произойти или не произойти, и что описание включает случаи, когда это событие или обстоятельство происходит и случаи, когда это не происходит.
Термин "увеличение" может относиться к любым изменениям, которые приводят к большему количеству композиции или соединения, такие как амплификация продукта по сравнению с контролем. Так, например, увеличение количества продуктов амплификации может включать, но не ограничивается увеличением на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, или 100 %. Кроме того, предполагается, что обнаружение увеличения экспрессии или избытка ДНК, мРНК или белка по сравнению с контролем, обязательно включает в себя обнаружение присутствия ДНК, мРНК или белка в ситуациях, когда ДНК, мРНК или белок не присутствует в контроле.
"Получение образца ткани" или "получить образец ткани" означает отобрать образец ткани у субъекта или измерить ткани у субъекта. Понятно, и в данном документе предполагается, что образцы тканей могут быть получены с помощью любых средств, известных в данной области техники, включая инвазивные и неинвазивные способы. Также понятно, что способы измерения могут быть прямыми или косвенными. Примеры способов получения или измерения образца ткани могут включать, но, не ограничиваясь, биопсию ткани, лаваж ткани, аспирацию, мазок ткани, спинномозговую пункцию, магнитно-резонансную томографию (МРТ), компьютерную томографию (КТ), позитронно-эмиссионную томографию (ПЭТ) сканирование и рентгеновское исследование (с контрастным веществом и без него).
Точное обнаружение мутации в известном сайте в ДНК можно легко произвести, используя существующие технологии. Аллель-специфичные праймеры могут быть направлены на целевую мутацию в известном месте, таким образом, что ее сигнал может быть предпочтительно усилен выше ДНК дикого типа. К сожалению, это невозможно с неизвестными мутациями, которые могут возникнуть в любом положении (основании) в последовательности-мишени.
Способы выявления AЛК-связанных видов рака
Раскрытые способы в одном из аспектов, относятся к способам выявления или диагностики наличия заболевания или состояния, такого как рак, оценки восприимчивости или риска развития заболевания или состояния, такого как рак, мониторингу прогрессирования заболевания или состояния, такого как рак, и определению чувствительности или устойчивости к терапевтическому лечению заболевания или состояния, такого как рак у субъекта, включающие выявление наличия или измерения уровня экспрессии мРНК из образца ткани от субъекта; где увеличение количества продукта амплификации по сравнению с контролем указывает на наличие рака, и где рак ассоциирован с вариациями, усечением нуклеиновой кислоты, либо слиянием гена АЛК.
Киназа анапластической лимфомы (АЛК)
Ген АЛК кодирует рецептор тирозин киназы (РТК) под названием АЛК (ПОСЛ. ID NO: 1) (GenBank регистрационный номер U62540 (кодирующая последовательность человека)) и, как правило, экспрессируется первоначально в центральной и периферической нервной системе. 1620аа АЛК полипептид содержит ЮЗОаа внеклеточный домен, который включает 2баа аминоконцевую сигнальную пептидную последовательность, и сайты связывания, расположенные между остатками 391 и 401. Кроме того, АЛК полипептид содержит домен киназы (остатки 1116-1383), который включает в себя три тирозина, ответственные за аутофосфорилирование в активационной петле на остатках 1278, 1282 и 1283. АЛК мутации, продемонстрировали конститутивную активацию киназной каталитической функции АЛК белка, с дерегулированием мутантной АЛК, в свою очередь, активирующей нисходящие клеточные сигнальные белки в проводящих путях, которые содействуют аберрантной клеточной пролиферации. Фактически, мутации, которые приводят к дизрегуляции активности АЛК киназы, связаны с несколькими видами рака.
АЛК слияния представляют собой наиболее распространенные мутации этой тирозинкиназы. Такие слияния включают, но не ограничиваясь, нуклеофозмин-АЛК (NPM-AЛK), 5-аминоимидазол-4-карбоксамида рибонуклеотид формилтрансферазу / IMP циклогидролазу (АТIС-АЛК), клатрина тяжелую цепь-АЛК (CLTC-АЛК), тяжелой цепи кинезина-1 ген-АЛК (КIF5В-АЛК); Ran-связывающий белок 2-АЛК (RАNВР2-АЛК), SEС31L1-АЛК, тропомиозин-3-АЛК (ТРМ3-АЛК), тропомиозин-4-АЛК (ТРМ4-АЛК), ТРК - слияния ген (болыдой)-АЛК (ТFGL-АЛК), ТРК - слияния ген (малый)-АЛК (TFGS-АЛК), CARS-АЛК, ЕМL4-АЛК, 5-аминоимидазол-4-карбоксамид рибонуклеотид формилтрансфераза / IMP циклогидролаза-АЛК (АТIС-АЛК), ALO17-АЛК, моезин-АЛК (MSN-АЛК), ген тяжелой цепи немышечного миозина-АЛК (МYН9-АЛК) и ТРК-слияния ген (экстра большой)-АЛК (TFGXL-АЛК). Шесть АЛК слияний, CARS-АЛК. CLTC-АЛК, RANBP2-AЛK, SЕС31L1-АЛК, ТРМ3-АЛК, и ТРМ4-АЛК были определены в ВМО. ТРМ3-АЛК, ТРМ4-АЛК и CLTC-АЛК слияния были обнаружены как в классической, Т - или нуль-клеточных лимфомах и ВМО саркомах, в то время как CARS-АЛК, RANBP2-AЛK, и SЕС31L1-АЛК происходят в ВМО. CLTC-АЛК и НПМ-АЛК также встречаются в В-клеточных плазмабластных/иммунобластных лимфомах. ТРМ4-АЛК слияние происходит при плоскоклеточном раке пищевода, и АЛК слияние ЕМL4-АЛК, TFG-АЛК и KIF5B-АЛК обнаруживают при немелкоклеточном раке легких. ЕМL4-АЛК слияние также недавно было выявлено при карциномах толстого кишечника и молочной железы. Таким образом, в одном аспекте, описанньми здесь являются способы выявления присутствия АЛК-связанного слияния, включающие выявление наличия или измерения количества нуклеиновых кислот, которые связаны со слиянием АЛК из образца ткани, полученной от субъекта, где присутствие нуклеиновой кислоты или увеличение нуклеиновой кислоты по сравнению с контролем показали наличие слияния АЛК.
АЛК слияния, ассоциированы с несколькими известными раковыми заболеваниями. Понятно, что одно или несколько слияний АЛК могут быть ассоциированы с определенным видом рака. Также понятно, что есть несколько видов рака, ассоциированных со слияниями АЛК, включая, но, не ограничиваясь анапластическую крупноклеточную лимфому (АККЛ), нейробластому, рак молочной железы, рак яичников, рак толстого кишечника, немелкоклеточный рак легкого, диффузную крупноклеточную В-клеточную лимфому, плоскоклеточный рак пищевода, анапластическую крупноклеточную лимфому, нейробластому, воспалительные миофибробластные опухоли, злокачественный гистиоцитоз, и глиобластомы.
АККЛ анапластические крупноклеточные лимфомы включают ~2,5% от всех НХЛ; в педиатрической возрастной группе в частности, ~13% от всех НХЛ (30-40% от всех крупноклеточных лимфом детского возраста) принадлежат к этому типу. Исследования пациентов АККЛ теперь делят эти НХД на АЛК-позитивные и АЛК-отрицательные подгруппы; ~60% всех АККЛ вызваны слияниями АЛК. По неясным причинам, АЛК-позитивные АККЛ пациенты достигают значительно лучшего результата после режима мультиагентной традиционной химиотерапии на основе CHOP, чем те, у которых АЛК-негативное заболевание (с уровнем общей 5-летней выживаемости ~75% по сравнению с ~35%, соответственно). Однако более чем треть пациентов страдает от множественных рецидивов после химиотерапии, таким образом, 5-летняя выживаемость без признаков заболевания АЛК-позитивных АККЛ составляет только ~40%.
АЛК+ Диффузная крупноклеточная В-клеточная лимфома. В 2003 году было показано, что АЛК слияния происходит в не-АККЛ форме НХЛ с описанием CLTC-АЛК или NPM-АЛК в диффузных крупноклеточных В-клеточных лимфомах (АЛК+ДККБКЛ). В соответствии со своим В-происхождением, эти НХЛ экспрессируют цитоплазматический IgA и маркеры плазматических клеток и обладают иммунобластной морфологией. Трансляционные научные исследования открыли t(2; 17) и CLTC-АЛК мРНК в большинстве этих лимфом, в то время как иммуномаркировки подтвердили зернистое окрашивание АЛК, идентичное такому, которое наблюдается в CLTC-АЛК-позитивных АККЛ. Что касается всех других партнерских белков АЛК слияния, мотив самоассоциации в CLTC части CLTC-АЛК выступает посредником конститутивной самоассоциации и активации киназы слияния для управления лимфомагенезом. АЛК+ДККБКЛ возникают преимущественно у взрослых, однако, t(2; 5) и NPM-АЛК мРНК в детских лимфомах фенотипически идентичны CLTC-АЛК-положительным В-НХЛ взрослых. Примерно 0,5-1% от всех ДККБКЛ считаются АЛК-положительными. Идентификация ДККБКЛ, вызванных мутантной АЛК является важной, потому что пациенты с этими лимфомами имеют результаты, которые значительно уступают результатам АЛК-негативных ДККБКЛ пациентов после схемы лечения на основе CHOP; таким образом, АЛК+ДККБКЛ пациенты должны решительно рассматриваться в качестве кандидатов на АЛК- нацеленную терапию ингибитором киназы.
АЛК+ системный гистиоцитоз. АЛК слияния были описаны в 2008 году при другом гемопоэтическом новообразовании, системном гистиоцитозе. Три случая этой ранее неохарактеризованной формы гистиоцитоза, которая присутствует в раннем детском возрасте, продемонстрировали АЛК иммунореактивность и один проанализированный случай молекулярно экспрессировал ТРМ3-АЛК.
В дополнение к вышеупомянутым гематологическим злокачественным заболеваниям, в которых конститутивно активированные АЛК слияния были продемонстрированны как причинный механизм, во многих случаях, происхождение подгрупп различных солидных опухолей, в некоторых случаях, очень часто опухолей человека, таких как немелкоклеточный рак легкого, рак толстого кишечника и рак молочной железы, как доказано в последнее время, связано с аберрантно активированной АЛК
Воспалительные миофибробластные опухоли. Первая обнаруженная не гемопоэтическая опухоль, экспрессирующая АЛК слияния была саркома, известная как воспалительная миофибробластная опухоль (ВМО), веретеноклеточная пролиферация в мягких тканях и внутренних органах детей и молодых людей (средний возраст на момент постановки диагноза ~10 лет). Многие ВМО являются неактивными и могут быть вылечены при помощи резекции. Тем не менее, местно-рецидивирующие, инвазивные и метастатические ВМО не являются редкостью, и современные виды химио- и радио-терапии являются абсолютно неэффективными. Описанным здесь является вовлечение хромосомы 2р23 (расположение АЛК гена) в ВМО, а также реаранжировка АЛК гена. Была продемонстрирована иммунореактивность АЛК в 7 из 11 ВМО, а в нескольких случаях были выявлены ТРМ3-АЛК и ТРМ4-АЛК. Кроме того, были идентифицированы два дополнительных слияния АЛК при ВМО, CLTC и RanВР2-АЛК. АЛК слияния были также изучены с помощью иммуноокрашивания в 73 ВМО, при этом обнаружилось, что 60% (44 из 73 случаев), являются АЛК-позитивными. Таким образом, дерегулирование АЛК имеет важное патогенное значение в большинстве ВМО.
Немелкоклеточный рак легкого. Кроме того, роль АЛК слияния при раке увеличилась с описанием нового ЕМL-АЛК химерного белка у 5 из 75 (6,7%) японских пациентов с немелкоклеточным раком легкого. Вскоре после этого, существование АЛК слияния при раке легкого было подтверждено на примере другой группы, в которой обнаружилось б из 137 (4,4%) китайских пациентов с раком легкого, которые экспрессировали АЛК слияние (ЕМL4-АЛК, 3 пациента; TFG-АЛК, 1 пациент; Х-АЛК. Возникли две общие темы - 1) АЛК слияния происходят преимущественно у пациентов с аденокарциномой (хотя наблюдаются случайные АЛК-положительные НМКРЛ с плоскоклеточной или смешанной гистологией), в основном у лиц с историей минимального курения/без курения, и 2) АЛК отклонения, как правило, происходят, исключая другие распространенные генетические аномалии (например, EGFR и KRAS мутации).Точный процент НМКРЛ, вызванных слияниями АЛК еще до конца не ясен, но оценки, основанные на докладах, в биомедицинской литературе предполагают диапазон ~5-10%.
Плоскоклеточный рак пищевода. У 45 иранских пациентов протеомический подход идентифицировал белки, которые недостаточно или чрезмерно представлены при плоскоклеточном раке пищевода (ПКРП); ТРМ4-АЛК входил в число чрезмерно представленных белков. Второе исследование ПКРП на протеомической основе - в данном случае, у китайских пациентов - также идентифицировало ТРМ4-АЛК в этих опухолях.
Рак толстого кишечника, рак молочной железы. Три типа опухолей человека - рак толстого кишечника, молочной железы, и немелкоклеточный рак легкого были исследованы на наличие EML4-AЛK слияния (другие мутации АЛК в данном исследовании не оценивались). Помимо подтверждения экспрессии EML4-AЛK в НМКРЛ (в 12 из 106 исследованных образцов, 11,3%), подгруппы рака груди (5 из 209 случаев, 2,4%) и рака толстого кишечника (2 из 83 случаев, 2,4%) были EML4-АЛК-положительными. В дополнение к известным ЕМL-АЛК вариантам 1 (Е13; А20) и 2 (Е20; А20), был обнаружен новый вариант (Е21; А20) при раке толстого кишечника.
АЛК в семейной и спорадической нейробластоме. Нейробластома является наиболее распространенной экстракраниальной солидной опухолью детского возраста и происходит из развивающегося неврального гребня. Небольшая часть (~1-2%) нейробластом проявляет семейную предрасположенность с аутосомно-доминантным типом наследования. Большинство пациентов с нейробластомой имеют агрессивное заболевание, ассоциированное с вероятностью выживания <40%, несмотря на интенсивную химио- и радиотерапию, а также заболевание составляет ~15% всей смертности от рака детского возраста. Ранее было установлено, что АЛК является конститутивно активированной также из-за высокого уровня чрезмерной экспрессии, как результата амплификации гена в небольшом количестве клеточных линий нейробластомы, по сути, АЛК амплификация происходит в ~15% нейробластом в дополнение к активизации точечных мутаций. Эти бессмысленные мутации в АЛК были подтверждены как активизирующие мутации, которые стимулируют рост нейробластомы, кроме того, инкубация клеточных линий нейробластомы с низкомолекулярными ингибиторами АЛК выявляет, что эти клетки с АЛК активацией (но не клеточные линии с нормальными уровнями экспрессии АЛК дикого типа) демонстрируют ясный цитотоксический ответ.
Недавние исследования демонстрируют, что ингибирование этих мутантных форм АЛК с низкомолекулярными лекарственньми кандидатурами аннулирует указанную ненормальную клеточную пролиферацию и способствует апоптозу в нейробластоме и других АЛК-управляемых линиях опухолевых клеток. Эти открытия выдвигают на первый план необходимость специализированного диагностического теста на АЛК мутации - теста, который будет иметь множественное клиническое применение. Например, такой анализ может быть использован для скрининга детей в семьях, пораженных наследственной нейробластомой, чтобы облегчить выявление опухолей на ранней стадии, когда они лучше поддаются лечению. Раннее выявление и диагностика АЛК-опосредованных видов рака резко повышает уровень выживаемости в популяции пациентов. Так, в одном аспекте данного изобретения представлены способы обнаружения или диагностики наличия заболевания или состояния, такого как рак, например рак; связанный с киназой анапластической лимфомы (АЛК), включающие обнаружение наличия или измерение уровня либо ДНК, кДНК, либо уровня экспрессии мРНК, ассоциированного с вариацией, усечением нуклеиновой кислоты, или АЛК слияниями из образца ткани от субъекта;
где увеличение количества продукта амплификации по сравнению с контролем указывает на наличие рака, связанного с АЛК. Также раскрываются способы оценки восприимчивости или риска развития заболевания или состояния, мониторинга прогрессирования заболевания, или определения чувствительности или устойчивости к терапевтическому лечению рака, ассоциированного с вариацией, усечением нуклеиновой кислоты или АЛК слияния у субъекта, включающий обнаружение наличия или измерение уровня или ДНК, кДНК, или уровня экспрессии мРНК из образца ткани субъекта; где увеличение количества продукта амплификации относительно контроля указывает на наличие ракового заболевания, связанного с АЛК.
Так, в одном аспекте, выявление последовательностей АЛК слияния указывает на наличие рака. Таким образом, описанными здесь являются способы диагностики рака, связанного с киназой анапластической лимфомы (АЛК) у субъекта, включающие выявление наличия или измерение уровня экспрессии мРНК из образца ткани субъекта; где мРНК является специфичной для слияния АЛК, и где увеличение количества мРНК по сравнению с контролем указывает на наличие видов рака, связанных с АЛК.
Раковые заболевания, связанные с АЛК слиянием, можно лечить с помощью ингибиторов АЛК киназы. Тем не менее, также были обнаружены виды рака, которые устойчивы к лечению ингибитором АЛК киназы. Эти виды рака представляют собой АЛК слияния, которые дополнительно содержат точечные мутации АЛК в семейных и спорадических формах рака (например, нейробластома, рак молочной железы, рак яичников, рак толстого кишечника, немелкоклеточный рак легкого, диффузная крупноклеточная В-клеточная лимфома, плоскоклеточный рак пищевода, анапластическая крупноклеточная лимфома, нейробластома, воспалительные миофибробластные опухоли, злокачественные гистиоцитоз и глиобластомы).
Мутации в АЛК приводят к конститутивной активации АЛК. Соответственно, формы рака, связанные с АЛК, движутся путем таких активированных точечных мутаций. Мутации в каталитическом домене тирозинкиназы M1166R, A1168P, I1171N, F1174I, F1174L, R1192P, F1245C, F1245V, F1245L, F1245I, I1250T и R1275Q и во внеклеточном домене на V476A ассоциированы с нейробластомой. Мутации в R401Q, А1168P и V757M были обнаружены при раке толстого кишечника. Кроме того, мутации на L560F были выявлены при раке молочной железы, и на A877S при раке яичников. Так, в одном аспекте, выявление наличия рака осуществляется путем выявления точечных мутаций в последовательности АЛК (то есть, путем выявления точечной мутации идентифицируют рак, связанный с АЛК). Таким образом, описанными здесь, являются способы обнаружения наличия рака, связанного с АЛК, где рак дополнительно содержит одну или несколько точечных мутаций в АЛК или повышение уровня АЛК дикого типа.
Раскрытые слияния АЛК также могут привести к дизрегуляции АЛК дикого типа. Дизрегуляция АЛК дикого типа может привести к увеличению производства вырабатываемой АЛК дикого типа, а также дизрегуляции каталитической активности киназы. Кроме того, рак может иметь первичную молекулярную патологию от другого рецептора тирозин киназы (РТК), такого как, сМЕТ или IGFR, но развить устойчивость к ингибиторам с помощью параллельных путей активации сигнальных путей, посредством АЛК. Таким образом, еще одним средством для обнаружения наличия рака является путь выявления увеличения экспрессии АЛК дикого типа. Кроме того, у усеченного гена АЛК дикого типа отсутствуют регуляторные регионы, что может привести к конститутивной каталитической функции АЛК киназы. Таким образом, описанными здесь, являются способы диагностики наличия рака, включающие выявление наличия или относительного увеличения экспрессии мРНК, связанных с усеченной АЛК последовательностью.
Понятно, и здесь рассматривается, что причина форм рака, связанных с АЛК, может быть обусловлена не только нарушением регуляции АЛК дикого типа или известных слияний АЛК, но одним или несколькими неопознанными слияниями АЛК. Способы, пригодные только для обнаружения известных слияний, будут непригодны для обнаружения ранее неизвестных слияний или мутаций АЛК. При помощи обнаружения не только наличия усечения, вариации нуклеиновой кислоты АЛК или слияния АЛК, но также обнаружения присутствия АЛК дикого типа и активности АЛК киназы, специалист в данной области может определить, является ли рак следствием дизрегуляции АЛК дикого типа, известного слияния АЛК, или ранее неизвестного слияния АЛК или мутации АЛК. Соответственно, описанными здесь являются способы для диагностики рака, оценки восприимчивости или риска развития рака, или обнаружения наличия нарушения регуляции АЛК дополнительно включающие определение наличия АЛК дикого типа и способы, еще дополнительно включающие определение наличия активности киназы АЛК, Так, например, описанными здесь являются способы диагностики АЛК-связанных форм рака, включающие обнаружение наличия нуклеиновых кислот, ассоциированных со слиянием АЛК, дикого типа АЛК и/или домена АЛК киназы из образца ткани субъекта.
Обнаружение и количественная оценка мРНК
Способы, описанные здесь, относятся к обнаружению вариаций формы нуклеиновой кислоты, например, точечных мутаций и усечения, или обнаружение экспрессии АЛК слияний, экспрессии аберрантной АЛК дикого типа или экспрессии мутантов усечения АЛК. Для этих последних определений уровней экспрессии, способы включают обнаружение либо численности, либо присутствия мРНК, или и то и другое вместе. Таким образом, описанными здесь, являются способы и композиции для диагностики у субъекта раковых заболеваний, связанных с киназой анапластической лимфомы (АЛК), включающие оценивание наличия или уровня мРНК из образца ткани от субъекта; где увеличение количества мРНК по сравнению с контролем указывает на наличие АЛК-связанного ракового заболевания.
Существует ряд широко используемых процедур для обнаружения и определения количества конкретной мРНК в общем или поли (А) образце РНК. Например, специфические мРНК могут быть обнаружены с помощью Нозерн-блоттинг анализа, анализов защиты нуклеазы (АЗН), гибридизации in situ, или обратной транскрипции-полимеразной цепной реакции (ОТ-ПЦР), и микроматрицы.
Теоретически, каждый из этих способов может быть использован для обнаружения специфических РНК и точного определения их уровня экспрессии. В общем, Нозерн-блоттинг анализ является единственным способом, который предоставляет информацию о размере транскрипта, в то время как АЗН являются самыми простыми способами одновременно изучать множественные месседжи. Гибридизация in situ используется для локализации экспрессии определенного гена в пределах типа ткани или типа клеток, и ОТ-ПЦР является наиболее точным способом обнаружения и количественной оценки экспрессии генов.
ОТ-ПЦР делает возможным обнаружение РНК-транскрипта любого гена, вне зависимости от недостаточного количества исходного материала или относительного обилия конкретных мРНК. В ОТ-ПЦР, шаблон РНК копируется в комплементарную ДНК (кДНК) с использованием ретровирусной обратной транскриптазы. Затем кДНК экспоненциально амплифицируют при помощи ПЦР с использованием ДНК-полимеразы. Обратная транскрипция и ПЦР-реакции могут происходить в одной и той же или в разных пробирках. ОТ-ПЦР является до некоторой степени толерантной к деградированной РНК. Пока РНК является интактной в регионе, в пределах праймеров, цель будет амплифицированна.
Относительный количественный анализ ОТ-ПЦР включает амплификацию внутреннего контроля одновременно с интересующим геном. Внутренний контроль используется для нормализации образцов. Как только образец нормализован, могут быть сделаны прямые сравнения относительного избытка специфических мРНК по образцам. Очень важно выбрать внутренний контроль с постоянным уровнем экспрессии во всех экспериментальных образцах (то есть, не находящихся под влиянием экспериментальной обработки). Используемые обычно процедуры внутреннего контроля (например, GAPDH, Р-актин, циклофилин) часто различаются по экспрессии и, следовательно, не могут быть подходящими видами внутреннего контроля. Кроме того, наиболее распространенные системы внутреннего контроля являются экспрессирующими при гораздо более высоких уровнях, чем мРНК, которая исследуется. Для того, чтобы результаты относительной ОТ-ПЦР имели смысл, все продукты реакции ПЦР должны быть проанализированы в линейном диапазоне амплификации. Это становится трудным для транскриптов, в значительной степени отличающихся уровнями численности.
Для абсолютного количественного определения используется конкурентная ОТ-ПЦР. Эта методика включает проектирование, синтез и точное количественное определение конкурента РНК, который можно отличить от эндогенной цели по небольшой разнице в размерах или последовательности. Известные количества конкурентов РНК добавляют в экспериментальные образцы и выполняют ОТ-ПЦР. Сигналы от эндогенной мишени сравнивают с сигналами от конкурентов, чтобы определить количество целей, присутствующих в образце.
Таким образом, описанными здесь, в одном аспекте являются способы диагностики у субъекта форм рака, которые связанны с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает в себя обратный праймер, способный на специфическую гибридизацию с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер; и где увеличение количества продукта амплификации по сравнению с контролем указывает на наличие АЛК-связанных раковых заболеваний. В равной степени, раскрытые способы могут быть использованы для обнаружения дикого типа АЛК, слияний АЛК и домена активности АЛК киназы, также здесь раскрыты способы диагностики форм рака, связанных с киназой анапластической лимфомы (АЛК), или обнаружение дизрегуляции АЛК киназы у субъекта, включающее проведение первой ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает в себя обратный праймер, способный специфически гибридизироваться с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер, где прямой праймер специфически гибридизируется с партнером слияния АЛК; проведение второй ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает прямой и обратный праймер, способный специфически гибридизироваться с одной или более последовательностями АЛК; проведение третьей ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает прямой и обратный праймер, способный специфически гибридизироваться с одним или несколькими доменами последовательности АЛК киназы; и где присутствие ампликона или увеличение количества продукта амплификации по сравнению с контролем указывает на наличие АЛК связанных раковых заболеваний и наличие дизрегуляции АЛК киназы. В частности, наличие ампликона АЛК слияния и ампликона домена киназы указывает на наличие известных АЛК слияний; наличие ампликона дикого типа и ампликона домена киназы служит признаком АЛК дикого типа, а наличие только ампликона домена киназы указывает на наличие ранее неизвестных АЛК слияний или мутировавших АЛК.
Нозерн анализ является самым простым способом определения размера транскрипта и для выявления альтернативного сплайсинга транскриптов и членов мультигенной семьи. Он также может быть использован для прямого сравнения относительного содержания данного месседжа между всеми образцами блота.
Процедура Нозерн-блоттинга проста и дает возможность для оценки прогресса в различных точках (например, интактность образца РНК, и насколько эффективно он был перемещен на мембрану). Образцы РНК вначале разделяют по размеру с помощью электрофореза в агарозном геле в денатурирующих условиях. Затем РНК перемещают на мембрану, сшитую и гибридизованную с меченым зондом. Неизотопные или меченые зонды высокой специфической активности могут быть использованы, включая ДНК-зонды случайных праймеров, ник-трансляции или ПЦР-генерирующие ДНК-зонды, РНК-зонды in vitro транскрипции, и олигонуклеотиды. Кроме того, последовательности только с частичной гомологией (например, кДНК из разных видов или геномные фрагменты ДНК, которые могут содержать экзон) могут быть использованы в качестве зондов.
Анализ защиты нуклеазы (АЗН) (включая как анализы защиты рибонуклеазы, так и анализы S1 нуклеазы) является чувствительным способом обнаружения и количественного определения специфических мРНК. Основой АЗН является раствор гибридизации антисмыслового зонда (меченого или неизотопного) с образцом РНК. После гибридизации одноцепочечный, негибридизированный зонд и РНК, деградируют нуклеазами. Остальные защищенные фрагменты разделяют на акриламидном геле. Гибридизация в растворе, как правило, более эффективна, чем мембранная гибридизация, и она может вместить до 100 мкг образцов РНК, по сравнению с максимумом 20-30 мкг при блот гибридизации. АЗН также являются менее чувствительными к деградации образца РНК, чем Нозерн-блот анализ, так как расщепление обнаруживается только в регионе частичного перекрытия с зондом (зонды, как правило, по длине равны приблизительно 100-400 оснований).
АЗН являются способом выбора для одновременного обнаружения нескольких видов РНК. Во время гибридизации в растворе и последующего анализа, индивидуальные зонд/мишень взаимодействия являются полностью независимыми друг от друга. Таким образом, несколько мишеней РНК и соответствующие процедуры контроля могут быть проанализированы одновременно (до двенадцати в такой же реакции), при условии, что отдельные зонды имеют различную длину. АЗН также часто используются для точного нанесения мРНК концов и интрон/экзон соединений.
Гибридизация in situ (ISH) является мощным и универсальным инструментом для локализации специфических мРНК в клетках или тканях. В отличие от Нозерн анализа и анализов защиты нуклеазы, ISH не требует изоляции или разделения РНК электрофорезом. Гибридизация зонда происходит внутри клетки или ткани. Так как клеточная структура сохраняется на протяжении всей процедуры, ISH предоставляет информацию о местонахождении мРНК в образце ткани.
Процедура начинается с фиксации образцов в нейтральном буферном формалине и заливки ткани в парафин. Образцы затем нарезают на тонкие секции и устанавливают на предметный столик микроскопа. (Кроме того, ткань можно разрезать замороженной и после фиксации в параформальдегиде.) После серии промываний, чтобы депарафинизировать и регидратировать срезы, проводится расщепление протеиназы К для увеличения доступности зонда, и меченый зонд затем гибридизируют со срезами образца. Меченые зонды визуализируются с жидкой пленкой, высушенной на срезах, в то время как неизотопно меченые зонды легко обнаруживают с помощью колориметрических или флуоресцентных реагентов.
Из-за ограничений технологии секвенирования, особенно чувствительности, в течение многих лет были разработаны многочисленные технологии сканирования для неизвестных мутаций: денатурирующая высокоэффективная жидкостная хроматография (дВЭЖХ) Xiao и Oefner, 2001, сканирование первичной структуры путем удаления оснований (СПУО), полиморфизм конформации одноцепочечной ДНК (ПКОЦ) (Orita et.al.,1989), гетеродуплексный (гибридизационный) анализ (ГА) (Nagamine et.al. 1989), конформационно-чувствительный гель-электрофорез (КЧГЭ) (Ganguly and Prockop, 1995; Ganguly et. al. 1993), электрофорез в градиенте денатурирующего геля (ДГГЭ) (Fodde and Losekoot, 1994), электрофорез в равномерном денатурирующем геле (РДГЭ) (Hovig et al. 1991), гель-электрофорез при временном градиенте температуры (ВТГЭ) (Chen et.al. 1999), метод химического расщепления некомплементарных сайтов (Cotton et al. 1988; Tabon et al. 2006), метод ферментного расщепления некомплементарных сайтов (Winter et al., 1985; Myers et al. 1985) и ферментное восстановление некомплементарных сайтов (Oldenburg and Siebert, 2000; Babon et. al. 1999; Youil et. al. 1996; Brow et. al. 1996; Lu и Hsu, 1992). Эти технологии еще не нашли широкого применения, вследствие одного или нескольких ограничений: трудоемкость, трудности автоматизации (низкая пропускная способность), низкая чувствительность или сложность воспроизведения. Большинство современных анализов точечных мутаций сосредоточены на обнаружении известных точечных мутаций в сайтах генов-мишеней. Для таких генов, как АЛК, тем не менее, спонтанные точечные мутации возникают в больших регионах ДНК, что требует технологии, которая может сканировать несколько сотен пар оснований. Несколько технологий неизвестных точечных мутаций были разработаны, но все или почти все имеют ограничения, которые исключают их использование для обнаружения редких генетических мутаций.
В отличие от вышеупомянутых технологий, шаблонная реакция обмена и экстензии (TEER™), использует на своих последних стадиях селективную амплификацию, чтобы увеличить чувствительность выявления редких и неизвестных мутаций. Это преимущество транслируется как способность обнаруживать болезни рано, а также как способность контролировать накопление дополнительных мутационных изменений при раке, поскольку они продолжают прогрессировать и видоизменяться. Кроме того, TEER™ является адаптируемой к нескольким платформам, включая ПЦР в реальном времени, фрагментный анализ и электрофорез. Например, TEER™, начинается от получения образца и длится до конечной точки обнаружения редких точечных мутаций активации АЛК из смешанных экземпляров клинического образца, который содержит обилие нормальной ДНК от загрязняющих, не опухолевых клеток. Весь процесс может быть завершен примерно за 5,5 часов.
Платформа TEER™ состоит из 5 основных шагов. 1. Аллель-специфический олигонуклеотид, содержащий флуоресцирующую последовательность метку флуоресцеина (FAM) и метку биотина для твердофазной очистки с захватом, используется для ПЦР-амплификации начального АЛК 270-Ьр шаблона, содержащего редкие или новые мутации. 2-Ампликон денатурируют теплом, а затем позволяют гибридизироваться вместе с денатурированным шаблоном АЛК дикого типа, позволяя происходить шаблонной реакции обмена. 3. Все существующие некомплементарные нуклеотиды затем расщеплются ферментативно с использованием одноцепочечной нуклеазы, CEL 1. 4. Цепочки ДНК содержащие удаленные некомплементарные основания удлиняют с Таg-полимеразой. 5. Специфичные ОТ-ПЦР праймеры затем используют для обнаружения единственного 5' региона расширенного шаблона. Объединение TEER™ амплификации и количественной оценки обеспечивает высокую пропускную способность и чувствительное выявление. Любые присутствующие (или отсутствующие) потенциальные мутации амплифицируются и количественно оцениваются с использованием уникального сайта обратного праймера, присутствующего только на расширенном TEER™ очищенном шаблоне. Фон, производный от загрязненых шаблонов дикого типа, сводят к минимуму с помощью биотинилированной последовательности с олиго захватом на начальном прямом праймере и использованием Ехо III, чтобы переварить любые двухцепочечные дуплексы, содержащие комплементарный 3' или 5' конец (патент США номер 6150105, который включен здесь в полном объеме для обучения шаблонной реакции обмена и экстензии).
Процесс TEER™ был изначально разработан в области онкологии для решения потребности в инструменте высокой производительности для обнаружения неисследованных генетических полиморфизмов в шаблонах от злокачественных клеток и тканей. TEER™ изначально продемонстрирована с помощью электрофореза в полиакриламидном геле (ПАГЭ). TEER™ предназначена для обнаружения генетических вариаций в ДНК шаблонах, которые могут содержать редкие, известные или новые мутации по сравнению с контролем, не мутировавшим ДНК шаблоном. Исходя из того, что секвенированные продукты являются уникальными для шаблонов, из которых они создаются, TEER™ была использована для сравнения "неизвестного" ДНК-шаблона, который потенциально содержит мутации, с шаблоном с подтвержденным отсутствием мутаций. Любые изменения в секвенированных продуктах отражают генетическую мутацию в неизвестном шаблоне ДНК и могут быть визуализированы с помощью гель-электрофореза. Совсем недавно TEER™ процесс был адаптирован к твердофазной платформе микротитровального обнаружения для разрешения высокопроизводительного анализа и повышения удобства использования. Контрольный и "неизвестный" шаблоны ДНК амплифицировали с использованием 5' биотинилированного праймера для получения биотинилированных продуктов ПЦР. После этого гомодуплексная и гетеродуплексная ДНК были сформированы с помощью гибридизации ампликонов ПЦР из контроля и "неизвестных" шаблонов ДНК. После гибридизации, гомодуплексная и гетеродуплексная ДНК были прикреплены к твердой фазе с помощью конъюгации с покрытыми стрептавидином лунками микропланшета, в котором все шаги TEER™ процеса могут быть легко выполнены, что значительно упрощает манипуляции и обработки образцов. TEER™ процесс является модифицированным анализом аллель-специфической олигонуклеотидной гибридизации и может быть связан с платформой ПЦР в реальном времени для высокой производительности и высокой чувствительности.
Обнаружение и количественная оценка ДНК
Способы, описанные здесь относятся к обнаружению изменений нуклеиновых кислот в форме, например, точечных мутаций и усечения, или обнаружению экспрессии АЛК слияний, аберрантной экспрессии АЛК дикого типа или экспрессии усеченных мутантов АЛК. Для этих последних обнаруженных уровней экспрессии, способы включают обнаружение либо избытка, либо присутствия мРНК, или того и другого. Кроме того, обнаружение может быть направлено на избыток или наличие ДНК, например, кДНК. Таким образом, описанными здесь, являются способы и композиции для диагностики у субъекта форм рака, связянных с киназой анапластической лимфомы (АЛК), включающие оценивание наличия или уровня ДНК из образца ткани от субъекта; где увеличение количества ДНК по сравнению с контролем указывает на наличие АЛК-связанного ракового заболевания.
Ряд широко используемых процедур существует для обнаружения и установления количества определенной ДНК в образце. Например, технология ПЦР позволяет выполнять амплификацию и последующее обнаружение мельчайших количеств целевой нуклеиновой кислоты. Подробности ПЦР хорошо описаны в данной области, в том числе, например, в патентах США под номерами 4683195 Mullis et al., 4683202 Mullis и 4965188 Mullis et al. Как правило, олигонуклеотидные праймеры отжигаются на денатурированных нитях целевой нуклеиновой кислоты, и продукты удлинения праймера образуются путем полимеризации дезоксинуклеозидтрифосфатов с помощью полимеразы. Типичный способ ПЦР включает повторяющиеся циклы шаблонной денатурации нуклеиновой кислоты, отжига праймеров и удлинения отожженных праймеров под действием термостабильной полимеразы. Процесс приводит к экспоненциальной амплификации целевых нуклеиновых кислот, и, таким образом, позволяет обнаружить цели, существующие в очень низкой концентрации в образце. Понятно, и здесь рассматривается, что есть варианты способов ПЦР, известные в данной области, которые также могут быть использованы в раскрытых способах, например, количественная ПЦР (КПЦР); микроматрицы, ПЦР в режиме реального времени;
ПЦР с использованием горячего старта, гнездовая ПЦР ; аллель-специфичная ПЦР и тачдаун ПЦР.
Микроматрицы
Матрица представляет собой упорядоченное расположение образцов, обеспечивая среду для приведения в соответствие известных и неизвестных образцов ДНК на основе правил спаривания оснований и автоматизации процесса выявления неизвестных. Матричный эксперимент может использовать общие системы анализа, такие как микропланшеты или мембраны стандартного блоттинга, а может быть создан вручную или использовать роботов для внесения образца. В общем, матрицы описывают как макроматрицы или микроматрицы, с разницей между ними, состоящей в размере пятен образца. Макроматрицы содержат образцы пятна размером около 300 микрон и больше и могут быть легко отображены существующими гелевыми и блот сканерами. Образец размеров пятна в микроматрицах может быть 300 микрон или меньше, но обычно не превышает 200 микрон в диаметре, и эти матрицы, как правило, содержат тысячи пятен. Микроматрицы требуют специальной робототехники и/или оборудования для создания изображений, как правило, не доступных коммерчески как целостная система. Терминология, которая была использована в литературе для описания этой технологии включает, но не ограничиваясь: биочип, ДНК чип, ДНК-микрочипы, GeneChip (Affymetrix, Inc. который относится к матрицам ДНК высокой плотности, на основе олигонуклеотидов), и генная матрица
ДНК-микроматрицы или ДНК-чипы, изготовленные высокоскоростной робототехникой, как правило, на стеклянных или нейлоновых подложках, для которых используются зонды с известной идентичностью, для определения комплементарных связей, делая возможной тем самым массовую параллельную экспрессию генов и исследования обнаружения генов. Эксперимент с единичным ДНК чипом может предоставить информацию о тысячах генов одновременно. Именно здесь рассматривается вопрос, что изобретенные микрочипы могут быть использованы для мониторинга экспрессии генов, диагностики заболеваний, генных открытий, открытий лекарственных препаратов (фармакогеномики), и токсикологических исследований или токсикогеномики.
Есть два варианта технологии ДНК-микроматриц, с точки зрения свойств матричной ДНК последовательности с известной идентичностью. Тип I микрочипов содержит зонд кДНК (500 ~5000 оснований в длину), который обездвижен на твердой поверхности, такой как стекло, использующий автоматическое устройство нанесения проб и подвергающийся комплексу задач, либо раздельно, либо в смешивании. Этот способ традиционно называют ДНК-микроматрица. С микроматрицами I типа, локализованные множественные копии одной или нескольких полинуклеотидных последовательностей, предпочтительно копий одной полинуклеотидной последовательности являются иммобилизованными на множестве определенных регионов поверхности подложки. Полинуклеотид относится к цепочке нуклеотидов в диапазоне от 5 до 10 тысяч нуклеотидов. Эти иммобилизованные копии полинуклеотидной последовательности пригодны для использования в качестве зондов при проведении экспериментов гибридизации.
Для подготовки бусин, покрытых иммобилизованными зондами, бусины погружают в раствор, содержащий желаемую последовательность зонда, а затем иммобилизуют на бусинах с помощью ковалентных или нековалентных способов. Кроме того, когда зонды иммобилизованы на стержнях, данный зонд может быть внесен в определенные регионы стержня. Типичные диспенсеры включают микропипетки, доставляющие растворы на подложку с помощью роботизированной системы для контроля положения микропипетки по отношению к подложке. Диспенсеры могут быть многочисленными, так что реагенты могут доставляться в регионы реакции одновременно. В одном варианте воплощения изобретения микроматрица формируется с помощью струйной технологии на основе пьезоэлектрического эффекта, при котором узкие пробирки, содержащие жидкость, представляющую интерес, как, например, реагенты олигонуклеотидного синтеза, окружены адаптером. Электрический заряд передается через адаптер, вызывая его расширение со скоростью, отличающейся от скорости расширения пробирки и форсирует небольшую каплю жидкости на подложку.
В качестве образцов может быть взят любой образец, содержащий полинуклеотиды (целевые полинуклеотиды), представляющие интерес и полученные из любой жидкости организма (кровь, моча, слюна, мокрота, желудочный сок и т.д.), культивированные клетки, биопсии или другие препараты из тканей. ДНК или РНК, могут быть выделены из образца в соответствии с любым из ряда способов, хорошо известных специалистам в данной области. В одном из вариантов воплощения изобретения, общую РНК выделяли с использованием реагента TRIzol изоляция общей РНК {Life Technologies, Inc, Роквилл, штат Мэриленд) и РНК выделяли с использованием олиго d(T) хроматографической колонки или стеклянных бус. После гибридизации и обработки, полученные сигналы гибридизации должны точно отражать количество контроля целевого полинуклеотида, добавленного к образцу.
Множество определенных регионов на подложке может быть расположено в разнообразных форматах. Например, регионы могут быть расположены перпендикулярно или параллельно к длине контейнера. Более того, цели не должны быть напрямую связаны с подложкой, а, скорее, могут быть связаны с подложкой через линкер группу. Линкер группы, как правило, могут варьироваться по длине от 6 до 50 атомов. Линкер группы включают олигомеры этиленгликоля, диамины, дикислоты и тому подобное. Реактивные группы на поверхности подложки, вступают в реакцию с одной из терминальных позиций линкера, чтобы связывать линкер с подложкой. Другая терминальная часть линкера затем функционирует для связывания зондов.
Образец полинуклеотидов может быть помечен одним или несколькими маркировочными фрагментами, предоставляющими возможность обнаружения гибридизированного зонда/ишени полинуклеотидных комплексов. Маркировочные фрагменты могут включать композиции, которые можно обнаружить с помощью спектроскопических, фотохимических, биохимических, биоэлектронных, иммунохимических, электрических, оптических или химических средств. Маркировочные фрагменты включают радиоизотопы, например, 32?, ^Р или ^S, хемилюминесцентные соединения, меченые связанные белки, атомы тяжелых металлов, спектроскопические маркеры, такие как флуоресцентные маркеры и красители, магнитные маркеры, связанные ферменты, метки для масс-спектрометрии, спиновые метки, доноры и акцепторы переноса электронов, биотин, и тому подобное.
Маркировка может быть выполнена во время реакции амплификации, такой как полимеразная цепная реакция и in vitro или in vivo реакции транскрипции. Кроме того, маркировочный фрагмент может быть включен после гибридизации, когда сформирован комплекс зонд-мишень. В одном из вариантов воплощения изобретения биотин сначала встраивают во время шага амплификации, как описано выше. После реакции гибридизации, несвязанные нуклеиновые кислоты смывают, так что только биотин оставшийся связаным с подложкой является присоединенным к целевым полинуклеотидам, которые гибридизуются с полинуклеотидными зондами. Затем, добавляют авидин-конъюгированный флуорофор, такой как авидин-фикоэритрин, который связывается с биотином с высоким сродством.
Гибридизация является причиной формирования стабильного дуплекса полинуклеотидным зондом и комплементарными мишенями через спаривание оснований. Способы гибридизация хорошо известны специалистам в данной области.
Обязательные условия для гибридизации могут быть определены концентрацией соли, температурой и другими химическими веществами и условиями. Различные дополнительные параметры, такие как время гибридизации, концентрация детергента (додецилсульфата натрия, НДС) или растворителя (формамид), а также включение или исключение носителя ДНК, являются хорошо известными специалистам в данной области. Дополнительные вариации этих условий будут очевидными для специалистов в данной области.
Способы для обнаружения комплексного образования, хорошо известны специалистам в данной области. В одном варианте воплощения изобретения полинуклеотидные зонды являются меченными флуоресцентной меткой и измерение уровней и паттернов образования комплекса достигается путем флуоресцентной микроскопии, предпочтительно конфокальной флуоресцентной микроскопии. Аргоновый ионный лазер возбуждает флуоресцентную метку, излучение направлено на фотоэлектронный умножитель и количество излучаемого света регистрируется и количественно оценивается. Регистрируемый сигнал должен быть пропорциональным количеству полинуклеотидного комплекса зонд/мишень на каждой позиции микроматрицы. Флуоресцентный микроскоп может быть ассоциирован со сканирующим устройством, которое управляется компьютером, для создания количественного двухмерного изображения интенсивности гибридизации. Отсканированное изображение исследуют, чтобы определить численное содержание/уровень экспрессии каждого гибридизированного целевого полинуклеотида.
В эксперименте дифференциальной гибридизации, полинуклеотидные мишени из двух или более различных биологических образцов являются помеченными двумя или более различными флуоресцентными метками с разными длинами волн излучения. Флуоресцентные сигналы определяют раздельно с помощью различных наборов фотоэлектронных умножителей для обнаружения определенных длин волн. Получают уровни избытка/экспрессии целевых полинуклеотидов в двух или более образцах. Как правило, интенсивность флуоресценции микроматрицы может быть нормализована с учетом изменения интенсивности гибридизации, когда в аналогичных условиях тестирования используется более одной микроматрицы. В одном из вариантов воплощения изобретения, индивидуальный полинуклеотидный зонд/интенсивность целевой комплексной гибридизации нормализуют с использованием интенсивности, полученной от внутреннего контроля нормализации, заключенного на каждой микроматрице.
Микроматрицы типа II содержат матрицу олигонуклеотидов (20 ~80-мерные олигонуклеотиды) или зонды пептидных нуклеиновых кислот (ПНК), которые синтезируются либо на месте (на чипе) или с помощью обычного синтеза, за которым следует иммобилизация на чипе. Матрицу подвергают воздействию меченого образца ДНК, гибридизируют и определяют тождественность/относительное содержание комплементарных последовательностей. Этот способ, "исторически" называемый ДНК-чипы, был разработан в компании Affymetrix, Inc, которая продает свою фотолитографически изготовленную продукцию под торговой маркой GeneChip®.
Основная концепция использования матриц типа II для экспрессии гена проста: меченые кДНК или кРНК мишени, производные от мРНК экспериментального образца, гибридизуют с зондами нуклеиновой кислоты, которые присоединены к твердой опоре. С помощью мониторинга количества метки, связанной с каждым месторасположением ДНК, можно сделать вывод о количестве каждого представленного вида мРНК. Хотя гибридизация использовалась десятилетиями для выявления и количественной оценки нуклеиновых кислот, сочетание миниатюризации технологии и большого и растущего количества информации о последовательностях, чрезвычайно расширило масштаб, в котором могут быть изучены экспрессии генов.
Производство микроматриц может начаться с 5-дюймовых квадратных кварцевых пластин. Первоначально кварц промывают для обеспечения унифицированного гидроксилирования по его поверхности. Поскольку кварц является по природе гидроксилированным, он обеспечивает прекрасный субстрат для прикрепления химических веществ, таких как линкер молекулы, которые в дальнейшем используются для позиционирования зондов на матрицах.
Пластину помещают в ванну с силаном, который вступает в реакцию с гидроксильными группами кварца, и формирует матрицу ковалентно связанных молекул. Расстояние между этими молекулами силана определяет плотность упаковки зондов, позволяя матрицам фиксировать более 500000 месторасположений зонда, или признаков, в бассейне 1,28 квадратных сантиметров. Каждый из этих признаков скапливает миллионы идентичных молекул ДНК. Пленка силана обеспечивает равномерную гидроксильную плотность для инициирования сборки зонда. Линкер молекул, прикрепленный к матрице силана, обеспечивает поверхность, которая может быть пространственно активизирована светом.
Синтез зонда происходит параллельно, в результате добавления А, С, Т, или G нуклеотида на несколько растущих цепей одновременно. Чтобы определить, какие олигонуклеотидные цепи получат нуклеотид в каждом шаге, фотолитографические маски, несущие окна от 18 до 20 квадратных микрон, что соответствует размерам индивидуальных свойств, располагают над покрытой пластиной. Окна распределены над маской, основанной на желаемой последовательности каждого зонда. Когда ультрафиолетовый свет светит над маской на первом этапе синтеза, подвергающиеся его воздействию линкеры становятся незащищенными и доступными для нуклеотидного соединения.
Как только желаемые свойства были активированы раствором, содержащим один тип дезоксинуклеотидов со сменной защитной группой, орошается поверхность пластины. Нуклеотиды присоединяются к активированным линкерам, инициируя процесс синтеза.
Хотя каждая позиция в последовательности олигонуклеотида может быть занята 1 из 4 нуклеотидов, в результате чего очевидна необходимость в 25×4 или 100, различных масках на пластине, может быть разработан процесс синтеза, чтобы значительно снизить это требование. Алгоритмы, которые помогают минимизировать использование маски, вычисляют, как лучше координировать рост зонда, регулируя скорость синтеза отдельных зондов и выявления ситуаций, когда ту же маску можно использовать несколько раз.
Некоторые из ключевых элементов отбора и разработки являются общими для производства всех микроматриц, независимо от предполагаемого применения. Стратегии, направленные на оптимизацию гибридизации зонда, например, неизменно включаются в процесс отбора зонда. Гибридизация при определенных условиях рН, соли и температуре может быть оптимизирована, принимая во внимание температуру плавления и использование эмпирических правил, которые коррелируют с желаемым поведением гибридизации.
Чтобы получить полное представление об активности гена, некоторые зонды выбирают из регионов, совместно используемых несколькими сплайсерами или вариантами полиаденилирования. В других случаях, являются предпочтительными уникальные зонды, которые обладают отличительными признаками между вариантами. Межзондовое расстояние также учитывается в процессе отбора.
Другой набор стратегий используют для выбора зондов для генотипирующих матриц, которые опираются на множество зондов, чтобы опросить отдельные нуклеотиды в последовательности. Идентичность целевого основания может быть выведена с помощью использования четырех идентичных зондов, которые изменяются только в целевой позиции, каждый из которых содержит одно из четырех возможных оснований.
Кроме того, наличие консенсусной последовательности может быть протестировано с помощью одного или двух зондов, представляющих специфичные аллели. Для генотипирования гетерозиготных или генетически смешанных образцов, матрицы с большим количеством зондов могут быть созданы для обеспечения избыточной информации, что приводит к четкому генотипированию. Кроме того, универсальные зонды могут быть использованы в некоторых аппликациях для максимальной гибкости. Некоторые зондовые матрицы, например, допускают разделение и анализ отдельных продуктов реакции из сложных смесей, таких, как те, которые используются в некоторых протоколах для выявления одиночных нуклеотидных полиморфизмов (ОНП).
ПЦР в режиме реального времени
ПЦР в режиме реального времени отслеживает флуоресценцию, испускаемую во время реакции, как показатель получения ампликона в течение каждого цикла ПЦР (т.е. в реальном времени), в отличие от конечной точки обнаружения. Прогрессирование реакции в режиме реального времени может быть просмотрено в некоторых системах. ПЦР в режиме реального времени не обнаруживает размер ампликона и, следовательно, не допускает дифференциации между амплификацией ДНК и кДНК, однако, это не зависит от неспецифической амплификации, за исключением случаев использования SYBR Green. Количественный ПЦР в режиме реального времени исключает переработку продуктов ПЦР после проведения ПЦР. Это помогает увеличить пропускную способность и уменьшить вероятность переноса загрязнений. ПЦР в режиме реального времени также предлагает широкий динамический диапазон, вплоть до 107-кратного. Динамический диапазон любого анализа определяет, насколько может меняться целевая концентрация, чтобы при этом все еще можно было провести количественную оценку. Широкий динамический диапазон означает, что широкий спектр соотношений мишени и нормализатора может быть проанализирован с одинаковой чувствительностью и специфичностью. Отсюда следует, что чем шире динамический диапазон, тем более точной является количественная оценка. В сочетании с ОТ-ПЦР, ПЦР реакция в режиме реального времени РВ_ПЦР сокращает время, необходимое для измерения количества ампликона, путем предоставления возможности для визуализации ампликона по мере прогрессирования процесса амплификации.
Система ПЦР в режиме реального времени основана на обнаружении и количественном определении флуоресценции репортера. Этот сигнал увеличивается в прямой зависимости от количества продукта ПЦР в реакции. Регистрируя количество эмиссии флуоресценции в каждом цикле, возможно мониторировать ПЦР-реакции во время экспоненциальной фазы, где первое значительное увеличение количества продукта ПЦР коррелирует с первоначальным количеством целевого шаблона. Чем выше начальное число копий целевых нуклеиновых кислот, тем скорее наблюдается значительное усиление флуоресценции. Значительное усиление флуоресценции выше базового уровня, измеренного во время 3-15 циклов, может указывать на обнаружение накопленных продуктов ПЦР.
Фиксированный порог флуоресценции устанавливается значительно выше базовых показателей, которые могут быть изменены оператором. Параметр Ст (пороговый цикл) определяется как номер цикла, при котором эмиссия флуоресценции превышает фиксированный порог.
Существуют три основных системы мониторинга флуоресценции для амплификации ДНК: (1) зонды гидролиза; (2) зонды гибридизации; и (3) ДНК-связывающие агенты. Зонды гидролиза включают TaqMan зонды, молекулярные "маячки" и "скорпионы". Они используют флуорогенную 5' экзонуклеазную активность Taq-полимеразы для измерения количества целевых последовательностей в образцах кДНК.
TaqMan зонды представляют собой олигонуклеотиды, которые длинее, чем праймеры (20-30 оснований в длину со значением Тm выше 10°С), содержащие флуоресцентный краситель обычно на 5' основании, и тушитель красителя (обычно TAMRA) как правило, на 3' основании. При облучении, возбужденный флуоресцентный краситель передает энергию в близлежащие молекулы тушителя красителя, а не в флуоресцирующие молекулы (это называется FRET = ФРПЭ = Флуоресцентная резонансная передача энергии по Фёрстеру ). Таким образом, непосредственная близость репортера и тушителя предотвращает эмиссию любой флуоресценции, в то время как зонд является интактным. TaqMan зонды предназначены для отжига на внутренние регионы ПЦР-продукта. Когда полимераза повторяет шаблон, с которым связан зонд TaqMan, ее 5' экзонуклеазная активность расщепляет зонд. На этом заканчивается активность тушителя (без ФРПЭ) и репортер-краситель начинает излучать флуоресценцию, которая увеличивается в каждом цикле пропорционально скорости расщепления зонда. Накопление продуктов ПЦР определяется с помощью мониторинга увеличения флуоресценции репортера-красителя (заметим, что праймеры не являются мечеными). TaqMan анализ использует универсальные тепловые циклические параметры и условия ПЦР-реакции. Поскольку расщепление происходит только если зонд гибридизуется к мишени, источником обнаруженной флуоресценции является специфическая амплификация. Процесс гибридизации и расщепления не пересекается с экспоненциальной аккумуляцией продукта. Одно из специфических требований для флуорогенных зондов является то, что на 5' конце не будет G. Соседний "G" к репортеру красителю может тушить репортер флуоресценции даже после расщепления.
Молекулярные "маячки" также содержат флуоресцентные красители (FAM, TAMRA, ТЕТ, ROX) и тушители (как правило, DABCYL) на обоих концах, но они разработаны, чтобы принимать структуры шпильки в то время как находятся свободными в растворе, чтобы привести флуоресцентный краситель и тушитель в непосредственную близость для совершения ФРПЭ. У них есть две ручки с комплементарными последовательностями, которые формируют очень стабильный гибрид или стержень. Непосредственная близость репортера и тушителя в этой конфигурации шпильки подавляет репортер флуоресценции. Когда маячок гибридизуется с мишенью во время отжига, репортер краситель отделяется от тушителя и репортер флуоресцирует (ФРПЭ не происходит). Молекулярные "маячки" остаются неизменными во время ПЦР и должны снова привязываться к мишени в каждом цикле для флуоресцентного излучения. Это коррелирует с количеством доступного ПЦР-продукта. Все химические процессы ПЦР в режиме реального времени позволяют обнаружить множество видов ДНК (мультиплексирования), при помощи разработки каждого зонда/маячка со спектрально уникальной парой флуоресцирующий агент/тушитель до тех пор, пока платформа подходит для анализа кривой плавления, если используется SYBR green. При помощи мультиплексирования, мишень(и) и эндогенный контроль могут быть амплифицированы в одной пробирке.
Со "Скорпион"-зондами, последовательность-специфический прайминг и обнаружение ПЦР-продукта достигается с помощью одного олигонуклеотида.
"Скорпион" - зонд сохраняет конфигурацию стержень-петля в негибридизированном состоянии. Флуорофор крепится к 5' концу и гасится фрагментом, связанным с 3' концом. 3' часть стержня также содержит последовательность, которая является комплементарной к удлиненному продукту праймера. Эта последовательность связана с 5' концом специфического праймера через не-амплифицируемый мономер. После удлинения праймера "Скорпиона" специфическая последовательность зонда способна связываться с его комплементом в рамках расширенного ампликона, открывая тем самым петлю шпильки. Это предотвращает флуоресценции от тушения, и наблюдается сигнал.
Другой альтернативой является связывание красящего химического вещества с двухцепочечной ДНК, что позволяет количественно определять продукцию ампликона (в том числе неспецифическую амплификацию и праймер-димер комплекс) за счет использования флуоресцентного интеркалирующего агента, не являющегося последовательность-специфичным (SYBR-green I или этидия бромид) . Он не связывается с оцДНК. SYBR зеленый являяется флуорогенным красителем, который связывается с малой бороздкой, и демонстрирует незначительную флуоресценцию в растворе, но излучает сильный флуоресцентный сигнал при связывании с двухцепочечной ДНК. Недостатки ПЦР в режиме реального времени на основе SYBR green вызывают потребность в широкой оптимизации. Кроме того, при неспецифических амплификациях требуются последующие анализы (анализ кривой точки плавления или анализ диссоциации) для идентификации ампликона. Способ был использован в HFE-C282Y генотипировании. Другая поддающаяся контролю проблема состоит в том, что более длинные ампликоны создают более сильный сигнал (в сочетании с другими факторами, это может привести к насыщению CDC камеры, см. ниже). Обычно SYBR green используется в одноплексной реакции, однако в сочетании с анализом температуры плавления, он может быть использован для мультиплексных реакций.
Пороговый цикл или значение СT представляет собой цикл, при котором впервые регистрируется значительное увеличение ΔRn (определение ΔRn, см. ниже). Пороговый цикл - это когда система начинает обнаруживать увеличение сигнала, связанного с экспоненциальным ростом продукта ПЦР во время лог-линейной фазы. Эта фаза предоставляет наиболее полезную информацию о реакции (безусловно, более важную, чем конечная точка). Наклон лог-линейной фазы является отражением эффективности амплификации. Эффективность (Eff) реакции можно рассчитать по формуле: Eff=10(-1/наклон)-1. Эффективность ПЦР должна составлять 90-100% (3,6>наклон>3,1). Число переменных может повлиять на эффективность ПЦР. Эти факторы включают длину ампликона, вторичную структуру и качество праймера. Хотя можно получить достоверные данные, которые выпадают из диапазона эффективности, должны быть дополнительно оптимизированы кОТ-ПЦР или разработаны альтернативные ампликоны. Для того чтобы наклон кривой был адекватным индикатором ПЦР (а не дрейфа сигнала), должна быть точка сгиба. Это та точка на кривой роста, где начинается лог-линейная фаза. Она также представляет наибольшую скорость изменения вдоль кривой роста (дрейф- сигнал характеризуется постепенным увеличением или уменьшением флуоресценции без амплификации продукта). Важным параметром для расчета количества является Ст. Чем выше начальное количество геномной ДНК, тем скорее накапливается продукт, регистрируемый в процессе ПЦР, и тем ниже значение Ст. Порог должен быть помещен выше любой активности базовой линии в пределах фазы экспоненциального роста (который выглядит линейно в логарифмическом преобразовании). Некоторое программное обеспечение позволяет определять порог цикла (Ст) с помощью математического анализа кривой роста. Это обеспечивает лучшую воспроизводимость от запуска к запуску. Значение Ст, равное 40, означает отсутствие амплификации, и такое значение не может быть включено в вычисления. Помимо применения для количественного анализа, значение Ст может быть использовано для качественного анализа, как измерение прошел/не прошел.
Мультиплексные анализы TaqMan могут быть выполнены с использованием нескольких красителей с различными длинами волн излучения. Доступными красителями для этой цели являются FAM, TET, VIC и JOE (самый дорогой). TAMRA зарезервирован в качестве тушителя на зонде и ROX в качестве пассивного стандарта. Для достижения наилучших результатов, рекомендовано сочетание FAM (цель) и VIC (эндогенный контроль), так как они обладают наибольшей разницей максимумов эмиссии, в то время как, JOE и VIC комбинировать не следует. Является важным, что если слой красителя был выбран неправильно, то машина будет по-прежнему считывать спектр других красителей. Например, и VIC и FAM флюоресцируют в близком диапазоне друг к другу и при действии одного красителя, лунки должны быть маркированы правильно. В случае мультиплексирования, спектральная компенсация должна быть включена для анализа, проводимого после выполнения реакции (по ABI 7700: Инструмент / Диагностика / Дополнительные настройки / Разное). Активация спектральной компенсации улучшает спектральное разрешение красителя.
Гнездная ПЦР
С помощью раскрытых способов можно дополнительно использовать гнездную ПЦР. Гнездная ПЦР увеличивает специфичность амплификации ДНК за счет снижения фона от неспецифической амплификации ДНК. Два комплекта праймеров используются в двух последовательных ПЦР. В первой реакции, одна пара праймеров используется для генерации ДНК-продуктов, которые помимо намеченной мишени, все же могут включать неспецифически амплифицированные фрагменты ДНК. Продукт(ы) затем используют во второй ПЦР с набором праймеров, чьи сайты связывания полностью или частично отличаются от и расположены на 3' каждого из праймеров, используемых в первой реакции. Гнездная ПЦР часто является более успешной в специфически амплифицированных длинных фрагментах ДНК, чем обычная ПЦР, но она требует более детального знания целевой последовательности.
Таким образом, описанными здесь в одном аспекте являются способы диагностики у субъекта форм рака, связанных с киназой анапластической лимфомы (АЛК), включающие проведение реакции ПЦР на ДНК из образца ткани от субъекта; где ПЦР реакция включает обратный праймер, способный к специфической гибридизации с одной или более последовательностями АЛК и, по меньшей мере, один прямой праймер, и где увеличение количества продукта амплификации по сравнению с контролем указывает на присутствие АЛК-связанных типов рака.
Праймеры и зонды
Используемый здесь термин "праймеры" означает подмножество зондов, которые способны поддерживать некоторые типы ферментативных манипуляций и которые могут гибридизироваться с целевой нуклеиновой кислотой, таким образом, что может произойти ферментативная манипуляция. Праймер может быть сделан из любой комбинации нуклеотидов или нуклеотидных производных или аналогов, доступных в данной области техники, которые не вмешиваются в ферментативную манипуляцию.
Используемый здесь термин "зонды" означает молекулы, способные взаимодействовать с целевой нуклеиновой кислотой, как правило, последовательность-специфическим образом, например, путем гибридизации. Гибридизация нуклеиновых кислот хорошо понятна в данной области техники и рассматривается в данном документе. Обычно зонд может быть сделан из любой комбинации нуклеотидов или нуклеотидных производных или аналогов, доступных в данной области техники.
Раскрываются композиции, включающие праймеры и зонды, которые способны взаимодействовать с раскрытыми нуклеиновыми кислотами, такими как ПОСЛ. ID NO: 1 или с ее комплементом. В некоторых вариантах воплощения изобретения праймеры используются для поддержки реакций удлинения нуклеиновых кислот, реакций репликации нуклеиновых кислот и/или реакций амплификации нуклеиновых кислот. Обычно праймеры смогут быть удлинены последовательность-специфичным образом. Удлинение праймера последовательность-специфичным образом включает любые способы, где последовательность и/или композиция молекулы нуклеиновой кислоты, с которой праймер гибридизирован или иным образом связан, руководит или влияет на композицию или последовательность продукта, произведенного путем удлинения праймера. Удлинение праймера последовательность-специфичным образом, следовательно, включает, но не ограничивается, ПЦР, секвенирование ДНК, ДНК-удлинение, ДНК-полимеризацию, РНК-транскрипцию или обратную транскрипцию. Способы и условия, которые амплифицируют праймер последовательность-специфичным образом являются раскрытыми. В некоторых вариантах воплощения изобретения праймеры используются для реакции амплификации ДНК, такой как ПЦР или прямое секвенирование. Понятно, что в некоторых вариантах воплощения изобретения праймеры также могут быть удлинены с помощью неферментативных способов, где, например, нуклеотиды или олигонуклеотиды, используемые для удлинения праймера, являются модифицированными таким образом, что они химически реагируют с удлиненным праймером последовательность-специфичным образом. Как правило, раскрытые праймеры гибридизуются с раскрытыми нуклеиновыми кислотами или регионом нуклеиновых кислот, или они гибридизируются с комплементом нуклеиновых кислот или комплементом региона нуклеиновых кислот. В качестве примера использования праймеров можно привести следующий: один или несколько праймеров могут использоваться для создания продуктов расширения из нуклеиновой кислоты и шаблона по первой нуклеиновой кислоте.
Праймеры или зонды для взаимодействия с нуклеиновыми кислотами могут быть любого размера, который поддерживает заданную ферментативную манипуляцию праймера, например амплификацию ДНК или простую гибридизацию зонда или праймера. Типичный праймер или зонд будет по меньшей мере составлять в длину 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61. 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1250, 1500, 1750, 2000, 2250, 2500, 2750, 3000, 3500, или 4000 нуклеотидов.
В других вариантах воплощения изобретения праймер или зонд могут быть в длину меньше или равны 6, 7, 8, 9, 10, 11, 12 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1250, 1500, 1750, 2000, 2250, 2500, 2750, 3000, 3500, или 4000 нуклеотидов.
Праймеры для интересующей нуклеиновой кислоты, как правило, будут использоваться для производства продуктов расширения и/или других реплицированных или амплифицированных продуктов, которые содержат регион интересующей нуклеиновой кислоты. Размер продукта может быть таким, чтобы размер мог быть точно определен с точностью до 3 или 2, или 1 нуклеотида.
В некоторых вариантах воплощения изобретения продукт может составлять в длину, например, по меньшей мере 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1250, 1500, 1750, 2000, 2250, 2500, 2750, 3000, 3500, или 4000 нуклеотидов.
В других вариантах воплощения изобретения продукт может быть в длину меньше или равным 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78. 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1250, 1500, 1750, 2000, 2250, 2500, 2750, 3000, 3500, или 4000 нуклеотидов.
Таким образом, понятно, и в этом документе рассматривается, что раскрытые ОТ-ПЦР и ПЦР-реакции требуют прямых и обратных праймеров для формирования пары праймеров. В этом документе раскрыто, что прямой праймер может быть выбран из группы, состоящей из, например, прямого праймера, который может быть внутриклеточным АЛК праймером, таким как, например, (праймер 100) 5'ACTACTGCTTTGCTGGCAAGACCT (ПОСЛ. ID NO: 6); внеклеточным ЕМЪ4-АЛК слияния праймером, такой как, например, (праймер 103) 5'TGTTCAAGATCGCCTGTCAGCTCT (ПОСЛ. ID NO: 3); внеклеточный WM-АЛК слияния праймер, такой как, например (праймер 102); 5TCTGTACAGCCAACGGTTTCCCTT (ПОСЛ. ID NO: 4); внеклеточный CTLC-АЛК слияния праймер, такой как, например, (праймер 105) 5'GAGAGTGCTTTGGAGCTTGTCTGT (ПОСЛ. ID NO: 5); или внеклеточный дикого типа АЛК праймер из негомологичного региона, такой как, например, (праймер 104) 5'TTCCTTCATCAGTCCACTGGGCAT (ПОСЛ. ID NO: 2). Дополнительные прямые и обратные праймеры, которые могут быть использованы в способах настоящего воплощения, можно найти в таблице 3.
Обратным праймером может быть, например, праймер 101: 5'TCGTCCTGTTCAGAGCACACTTCA (ПОСЛ. ID NO: 7). В качестве альтернативы, обратным праймером может быть ПОСЛ. ID NO: 32, ПОСЛ. ID NO: 46, ПОСЛ. ID NO: 47, ПОСЛ. ID NO: 56, ПОСЛ. ID NO: 57, или ПОСЛ. ID NO: 58. Понятно, что способы включают, по меньшей мере, один прямой праймер и обратный праймер. Таким образом, описанными здесь являются способы диагностики у субъекта форм рака, связанных с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает обратный праймер, способный к специфической гибридизации с одной или несколькими АЛК последовательностями и, по меньшей мере, один прямой праймер, где прямой праймер выбирается из группы, состоящей из КIF5В-АЛК праймера, NPM-АЛК праймера, АТIС-АЛК праймера, CLTC-АЛК праймера, RANBP2-AЛК праймера, SEC31L1-АЛК праймера, ТРМ3-АЛК праймера, ТРМ4-АЛК праймера, TАGL-АЛК праймера, TFGS-АЛК праймера, CARS-АЛК праймера, EML4-АЛК праймера, ALO17-АЛК праймера, MYH9-АЛК праймера, MSN-АЛК праймера, и TFGXL-AЛK праймера; и где увеличение количества продукта амплификации по сравнению с контролем указывает на присутствие АЛК-связанных раковых заболеваний. Таким образом, также раскрываются способы, в которых прямой праймер выбирается из группы, состоящей из ПОСЛ. ID NO: 2, ПОСЛ. ID NO: 3, ПОСЛ. ID NO: 4, ПОСЛ. ID NO: 5, ПОСЛ. ID NO: 6, ПОСЛ. ID NO: 35, ПОСЛ. ID NO: 36, ПОСЛ. ID NO: 37, ПОСЛ. ID NO: 38, ПОСЛ. ID NO: 39, ПОСЛ. ID NO: 40, ПОСЛ. ID NO; 41, ПОСЛ. ID NO: 42, ПОСЛ. ID NO: 43, ПОСЛ. ID NO: 44, ПОСЛ. ID NO: 45, ПОСЛ. ID NO: 48, ПОСЛ. ID NO: 49, ПОСЛ. ID NO: 50, ПОСЛ. ID NO: 51, ПОСЛ. ID NO: 52, ПОСЛ. ID NO: 53, ПОСЛ. ID NO: 54, ПОСЛ. ID NO: 55, и ПОСЛ. ID NO: 59. Например, описанными здесь являются способы диагностики у субъекта форм рака, связанных с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает обратный праймер, способный к специфической гибридизации с одной или несколькими АЛК последовательностями и, по меньшей мере, один прямой, где прямой праймер представляет собой NPM-АЛК слияния праймер, включающий ПОСЛ. ID NO: 4, и где увеличение количества продукта амплификации по сравнению с контролем указывает на присутствие АЛК-связанных раковых заболеваний.
В качестве дополнительных примеров пар праймеров, в частности, описанных здесь, являются способы, где прямой праймер представляет собой дикого типа АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой KIF5B-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой NPM-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой АТIС-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой CLTC-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой РАNВР2-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой SEC31L1-AЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой ТРМ3-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой ТРМ4-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой TFGL-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой TFGS-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой CARS-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой EML4-AЛK праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой ALO17-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; где прямой праймер представляет собой MYH-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7; или где прямой праймер представляет собой TFGXL-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 7. Также раскрытыми являются способы, где пара праймеров включает ПОСЛ. ID NO: 2 и 7, ПОСЛ. ID NO: 3 и 7, ПОСЛ. ID NO: 4 и 7, ПОСЛ. ID NO: 5 и 7, или ПОСЛ. ID NO: 6 и 7.
Дополнительными примерами пар праймеров, в частности, описанными здесь, являются способы, где прямой праймер представляет собой дикого типа АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой KIF5B-AЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой NРМ-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой АТIС-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой CLTC-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой RANBP2-AЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой SEC31L1-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой ТРМ3-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой ТРМ4-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой TFGL-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой TFGS-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой CARS-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой ЕМL4-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой ALO17-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; где прямой праймер представляет собой MYH9-AЛK праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46; или где прямой праймер представляет собой TFGXL-АЛК праймер и обратный праймер представляет собой ПОСЛ. ID NO: 46. Также раскрытыми являются способы, где пара праймеров включает ПОСЛ. ID NOS: 2 и 46. ПОСЛ. ID NOS: 3 и 46, ПОСЛ. ID NOS: 4 и 46, ПОСЛ. ID NOS: 5 и 46, ПОСЛ. ID NOS: 6 и 46; ПОСЛ. ID NOS; 33 и 46; ПОСЛ. ID NOS: 34 и 46; ПОСЛ. ID NOS: 35 и 46; ПОСЛ. ID NOS: 36 и 46; ПОСЛ. ID NOS: 37 и 46; ПОСЛ. ID NOS: 38 и 46; ПОСЛ. ID NOS: 39 и 46; ПОСЛ. ID NOS: 40 и 46; ПОСЛ. ID NOS: 41 и 46; ПОСЛ. ID NOS: 42 и 46; ПОСЛ. ID NOS: 43 и 46; ПОСЛ. ID NOS: 44 и 46; ПОСЛ. ID NOS: 45 и 46; ПОСЛ. ID NOS: 485 и 46; ПОСЛ. ID NOS: 49 и 46; ПОСЛ. ID NOS: 50 и 46; ПОСЛ. ID NOS: 51 и 46; ПОСЛ. ID NOS: 52 и 46; ПОСЛ. ID NOS: 53 и 46; ПОСЛ. ID NOS: 54 и 46; ПОСЛ. ID NOS: 55 и 46, или ПОСЛ. ID NO: 58 и 46.
Понятно, и в данном документе рассматривается, что существуют ситуации, когда может быть выгодно использовать более одной пары праймеров для обнаружения присутствия слияния, усечения, или чрезмерной экспрессии мутации. Такие ОТ-ПЦР или ПЦР реакции могут быть проведены раздельно, или в одной реакции. Когда несколько пар праймеров, помещают в одну реакцию, это называется "мультиплексная ПЦР", Например, реакция может состоять из праймера АЛК дикого типа в паре с обратным праймером, а также, праймера АЛК слияния в паре с тем же обратным праймером. Таким образом, описанными здесь являются способы диагностики у субъекта форм рака, связанных с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает обратный праймер способный к специфической гибридизации с одной или несколькими АЛК последовательностями и, по меньшей мере, два прямых праймера, и где увеличение количества продукта амплификации по сравнению с контролем указывает на присутствие АЛК-связанных раковых заболеваний. Аналогично раскрываются способы, содержащие, по меньшей мере, три прямых праймера. Понятно, и в данном документе рассматривается, что любая комбинация из двух или более или трех или более прямых праймеров, описанных здесь, может быть использована в мультиплексной реакции. Так, например, здесь раскрыты способы диагностики, где прямые праймеры представляют собой NPM-АЛК праймер и дикого типа АЛК праймер. Также раскрытыми, например, являются способы диагностики, где прямые праймеры представляют собой ELM4-AЛK праймер и дикого типа АЛК праймер.
Другие примеры наборов прямых праймеров для мультиплексной ПЦР включают, но не ограничиваются KIF5B-AЛK слияния праймер и дикого типа АЛК праймер, CLTC-АЛК слияния праймер и дикого типа АЛК праймер, RANBP2-АЛК слияния праймер и дикого типа АЛК праймер, ATIC-АЛК слияния праймер и дикого типа АЛК праймер, SEC31L1-AЛК слияния праймер и дикого типа АЛК праймер, ТРМ3-АЛК слияния праймер и дикого типа АЛК праймер, ТРМ4-АЛК слияния праймер и дикого типа АЛК праймер, TFGL-АЛК слияния праймер и дикого типа АЛК праймер, TFGS-АЛК слияния праймер и дикого типа АЛК праймер, CARS-АЛК слияния праймер и дикого типа АЛК праймер, ALO17-АЛК слияния праймер и дикого типа АЛК праймер, МYН9-АЛК слияния праймер и дикого типа АЛК праймер. MSN-АЛК слияния праймер и дикого типа АЛК праймер, усеченный АЛК праймер и дикого типа АЛК праймер, ЕLМ4-АЛК слияния праймер и усеченный АЛК праймер, NPM-АЛК слияния праймер и усеченный АЛК праймер, CLTC-АЛК слияния праймер и усеченный АЛК праймер. RANBP2-АЛК слияния праймер и усеченный АЛК праймер, ATIC-АЛК слияния праймер и усеченный АЛК праймер, SEC31L1-АЛК слияния праймер и усеченный АЛК праймер. ТРМ3-АЛК слияния праймер и усеченный АЛК праймер, ТРМ4-АЛК слияния праймер и усеченный АЛК праймер, ТFGL-АЛК слияния праймер и усеченный АЛК праймер, TFGS-АЛК слияния праймер и усеченный АЛК праймер, CARS-АЛК слияния праймер и усеченный АЛК праймер, ALO17-АЛК слияния праймер и усеченный АЛК праймер, MYH9-АЛК слияния праймер и усеченный АЛК праймер, и MSN-АЛК слияния праймер и усеченный АЛК праймер.
Дополнительные примеры включают, но не ограничиваются ЕLМ4-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; NPM-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; CLTC-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; RANBP2-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; ATIC-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; SEC31L1-AЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; ТРМ3-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; ТРМ4-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; TFGL-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; TFGL-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; CARS-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; ALO17-АЛК слияния праймер, дикого типа АЛК праймер и усеченный АЛК праймер; МYH9-АЛК слияния праймер, дикого типа АЛК праймер, и усеченный АЛК праймер; и MSN-АЛК слияния праймер, дикого типа АЛК праймер и усечетыиАЛК праймер.
Таким образом, в одном из аспектов, пробирка для одной реакции может включать прямой праймер, который гибридизуется к одному или нескольким АЛК слияниям, АЛК дикого типа или домену АЛК киназы, и обратный праймер, который гибридизуется с АЛК дикого типа. Понятно, что способы, описанные здесь, могут включать пробирки для множества реакций. Например, способы могут включать первую реакцию для обнаружения наличия известной АЛК слияния, которая содержит один или несколько прямых праймеров АЛК слияния и обратный АЛК праймер, который гибридизуется с диким типом АЛК (например, прямые праймеры ПОСЛ. ID NOs 2, 3, 4, 5, 6, 34,35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 48, 49, 50, 51, 52, 53, и 59 и обратные праймеры ПОСЛ. ID NOs: 7, 32, 46, 47, 56, 57, или 58); пробирка для второй реакции, которая содержит прямой и обратный праймер для обнаружения АЛК дикого типа (например, прямой праймер ПОСЛ. ID NOs: 33, 54, или 55 и обратный праймер ПОСЛ. ID NOs: 7, 32, 46, 47, 56, 57, или 58); прямой и обратный праймер для обнаружения наличия киназного домена АЛК (например, прямой праймер ПОСЛ. ID NOs: 45 или 48 и обратный праймер ПОСЛ. ID NOs: 7, 32, 46, 47, 56, 57, или 58); прямой и обратный праймер для обнаружения контроля; прямой и обратный праймер для позитивного кДНК контроля; и прямой и обратный праймер для негативного кДНК контроля. В способе с множественными реакциями в пробирке, РНК извлекается из образца ткани, полученного от субъекта; РНК обратно транскрибируется для получения кДНК; кДНК разделяется между одной или несколькими реакционными пробирками и выполняется ОТ-ПЦР или микроматричные анализы. При условии, что контроль выполнен в соответствии с планом, специалист в данной области техники может обнаружить продукт амплификации в пробирке слияния, пробирке дикого типа и пробирке киназы. В результате анализа в пробирке слияния и в киназной пробирке присутствует ампликон, но пробирка дикого типа не указывает на наличие известного слияния АЛК. Если пробирка слияния является отрицательной, но пробирки дикого типа и киназы положительными, то это означает, что присутствует только АЛК дикого типа. Если обе реакционные пробирки, дикого типа и слияния являются отрицательными, а пробирка киназы положительна, то это ознчает, что присутствуют ранее неизвестные слияния. Если пробирка киназы является отрицательной и либо пробирка слияния, либо пробирка дикого типа положительной, значит нет никаких функциональных АЛК и образец ткани не содержит АЛК-связанных типов рака (см. Фигура 5А). Понятно, что при измерении размера ампликона может быть определена идентичность конкретного АЛК слияния или АЛК дикого типа в образце (см. Фигура 5В). Там, где ампликон имеет размер, который не связан с конкретной АЛК слияния или АЛК дикого типа, значит ампликон представляет ранее неизвестное АЛК слияние.
Зонды и праймеры изменения флуоресценции
Зонды изменения флуоресценции и праймеры изменения флуоресценции относятся ко всем зондам и праймерам, которые включают изменение интенсивности флуоресценции или длины волны на основе изменения формы или конформации зонда или праймера и нуклеиновых кислот, чтобы быть обнаруженными, проанализированными или реплицированными. Примеры зондов и праймеров изменения флуоресценции включают молекулярные "маячки", Amplifluors, ФРПЭ зонды, расщепляемые ФРПЭ зонды, TaqMan зонды, "скорпион" праймеры, флуоресцентные триплекс олигонуклеотиды, включая, но не ограничиваясь, триплекс молекулярные "маячки" или триплекс ФРПЭ зонды, флуоресцентные водорастворимые конъюгированные полимеры, ПНК зонды и КПНК зонды.
Зонды и праймеры изменения флуоресценции могут быть классифицированы в зависимости от их структуры и/или функции. Зонды изменения флуоресценции включают зонды тушения шпилькой, зонды тушения расщеплением, зонды, активированные расщеплением, флуоресцентно активированные зонды.
Праймеры изменения флуоресценции включают праймеры тушения стержнем и праймеры тушения шпилькой.
Зонды тушения шпилькой представляют собой зонды, которые, когда не привязаны к целевой последовательности, формируют структуру шпильки (и, как правило, петлю), которая приносит флуоресцентную метку и фрагмент тушения в непосредственную близость, так что флуоресценция из метки является потушенной. Когда зонд связывается с целевой последовательностью, стержень разрывается, фрагмент тушения больше не находится в непосредственной близости от флуоресцентной метки и флуоресценция возрастает. Примерами зондов тушения шпилькой являются молекулярные "маячки", флуоресцентные триплекс олигонуклеотиды, триплекс молекулярные "маячки", триплекс ФРПЭ зонды, и КПНК зонды.
Зонды, активированные расщеплением, представляют собой зонды, где флуоресценция возрастает при расщеплении зонда. Зонды, активированные расщеплением могут включать флуоресцентную метку и фрагмент тушения в непосредственной близости, таким образом, что флуоресценция метки тушится. Когда зонд обрезается или переваривается (обычно с помощью 5'-3 'экзонуклеазной активности полимеразы при амплификации), фрагмент тушения больше не находится в непосредственной близости от флуоресцентной метки и флуоресценция возрастает. TaqMan зонды являются примером зондов, активированных расщеплением.
Зонды тушения расщеплением являются зондами, где флуоресценция уменьшается или измененяется при расщеплении зонда. Зонды тушения расщеплением могут включать акцепторную флуоресцентную метку и фрагмент-донор, такой, что, когда акцептор и донор находятся в непосредственной близости, флуоресцентная резонансная энергия переносится от донора к акцептору, вызывая флуоресценцию акцептора. Зонды, таким образом, флуоресцируют, например, при гибридизации с целевой последовательностью. Когда зонд обрезается или переваривается (обычно 5'-3' экзонуклеазной активностью полимеразы при амплификации), фрагмент-донор больше не находится в непосредственной близости от акцепторной флуоресцентной метки и флуоресценция акцептора уменьшается. Если фрагмент-донор сам по себе является флуоресцентной меткой, он может высвободить энергию флуоресценции (как правило, с другой длиной волны, чем флуоресценция акцептора), когда он не находится в непосредственной близости от акцептора. Общий эффект будет затем представлять собой снижение акцепторной флуоресценции и увеличение флуоресценции донора. Флуоресценция донора в случае зондов тушения расщеплением является эквивалентной флуоресценции, генерированной с помощью зондов, активированных расщеплением с акцептором, являющимся фрагментом тушения и донором, являющимся флуоресцентной меткой. Расщепляемые ФРПЭ (флуоресцентная резонансная передача энергии) зонды являются примером зондов тушения расщеплением.
Флуоресцентно активированные зонды представляют собой зонды или пары зондов, где флуоресценция увеличивается или измененяется путем гибридизации зонда к целевой последовательности. Флуоресцентно активированные зонды могут включать акцепторную флуоресцентную метку и фрагмент-донор, такой, что, когда акцептор и донор находятся в непосредственной близости (когда зонды гибридизированны к целевой последовательности), флуоресцентная резонансная энергия переносится от донора к акцептору вызывая флуоресценцию акцептора. Флуоресцентно активированные зонды, как правило, представляют собой пары зондов предназначенные для гибридизации с соседними последовательностями, таким образом, что акцептор и донор становятся приведенными в непосредственную близость. Флуоресцентно активированные зонды также могут быть единичными зондами, содержащими как донор, так и акцептор; когда зонд не гибридизуется с целевой последовательностью, донор и акцептор не находятся в непосредственной близости, но где донор и акцептор приведены в непосредственную близость, когда зонд гибридизируется с целевой последовательностью. Это может быть достигнуто, например, путем размещения донора и акцептора на противоположных концах зонда и размещения целевой комплементарной последовательности на каждом конце зонда, где целевая комплементарная последовательность является комплементарной к соседним последовательностям в целевой последовательности. Если фрагмент-донор Флуоресцентно активированного зонда сам по себе представляет флуоресцентную метку, он может высвободить энергию в виде флуоресценции (как правило, с другой длиной волны, чем флуоресценция акцептора), когда он не находится в непосредственной близости от акцептора (то есть, когда зонды не гибридизированы с целевой последовательностью). Когда зонды гибридизированы с целевой последовательностью, общий эффект будет затем проявляться снижением флуоресценции донора и увеличением акцепторной флуоресценции. ФРПЭ зонды представляют собой пример флуоресцентно активированных зондов.
Праймеры тушения стержнем представляют собой праймеры, которые, когда не гибридизуются с комплементарной последовательностью образуют структуру стержня (либо внутримолекулярную структуру стержня или межмолекулярную структуру стержня), которая доставляет флуоресцентную метку и фрагмент-тушитель в непосредственную близость, таким образом, что флуоресценция из метки угасает. Когда праймер связывается с комплементарной последовательностью, стержень разрывается, фрагмент тушения больше не находится в непосредственной близости от флуоресцентной метки и флуоресценция возрастает. В раскрытом способе, праймеры тушения стержнем используются в качестве праймеров для синтеза нуклеиновых кислот и таким образом встраиваются в синтезированную или амплифицированную нуклеиновую кислоту. Примерами праймеров тушения стержнем являются праймеры тушения пептидных нуклеиновых кислот и праймеры тушения шпилькой.
Праймеры тушения пептидных нуклеиновых кислот представляют собой праймеры связанные с тушителем пептидной нуклеиновой кислоты или фтором пептидной нуклеиновой кислоты, чтобы формировать стволовые структуры. Праймер содержит флуоресцентную метку или фрагмент тушения и ассоциирован либо с тушителем пептидной нуклеиновой кислоты или с фтором пептидной нуклеиновой кислоты, соответственно. Это ставит флуоресцентную метку в непосредственную близость к фрагменту тушения. Когда праймер реплицируется, пептидная нуклеиновая кислота перемещается, что позволяет флуоресцентной метке продуцировать флуоресцентный сигнал.
Праймеры тушения шпилькой представляют собой праймеры, которые, когда не гибридизированы с комплементарной последовательностью, формируют структуру шпильки (и, как правило, петлю), которая приносит флуоресцентную метку и фрагмент тушения в непосредственную близость, таким образом, что флуоресценция из метки является потушенной. Когда праймер связывается с комплементарной последовательностью, стержень разрывается, фрагмент тушения больше не находится в непосредственной близости от флуоресцентной метки и флуоресценция возрастает. Праймеры тушения шпилькой обычно используются в качестве праймеров для синтеза нуклеиновых кислот и таким образом встраиваются в синтезированные или амплифицированные нуклеиновые кислоты Примерами праймеров тушения шпилькой являются праймеры «амплифлюр» и «скорпионы».
Праймеры тушения расщеплением являются схожими с зондами тушения расщеплением, за исключением того, что они являются праймерами, которые встроены в реплицированные цепочки и затем являются впоследствии расщепленными.
Метки
Для помощи в выявлении и количественном определении нуклеиновых кислот, полученных с использованием раскрытых способов, метки могут быть непосредственно встроены в нуклеотиды и нуклеиновые кислоты или могут быть связаны с молекулами обнаружения, такими как зонды и праймеры. В данном случае, метка является любой молекулой, которая может быть связана с нуклеотидом или нуклеиновой кислотой, прямо или опосредованно, и которая приводит к измеримому, обнаруживаемому сигналу, прямо или косвенно. Многие такие метки для включения в нуклеотиды и нуклеиновые кислоты или соединенные с зондами нуклеиновой кислоты известны специалистам в данной области техники. Примеры меток, подходящих для использования в раскрытых способах, являются радиоактивными изотопами, флуоресцентными молекулами, фосфоресцирующими молекулами, ферментами, антителами, и лигандами. Флуоресцентные метки, особенно в контексте зондов и праймеров изменения флуоресцентции, пригодны для обнаружения амплификации в реальном времени.
Примеры подходящих флуоресцентных меток включают флуоресцеина изотиоцианат (FITC), 5,6-карбоксиметил флуоресцеин, техасский красный, нитробенз-2-окса-1,3-диазол-4-ил (NBD), кумарин, дансила хлорид, родамин, амино-метил кумарин (АМСА), эозин, эритрозин, BODIPY®, CASCADE Blue®, OREGON GREEN®, пирен, лиссамин, ксантены, акридины, оксазины, фикоэритрин, макроциклические хелаты лантанидных ионов, такие как quantum dye™, флуоресцентные красители передачи энергии, такие как тиазола оранжевого-этидия гетеродимер и цианиновые красители Су3, Су3.5, Су5, Су5.5 и Су7. Примеры других специфических флуоресцентных меток включают 3-гидроксипирен 5,8,10-трисульфоновой кислоты, 5-гидрокси триптамин {5-НТ), фуксинсернистую кислоту, ализарин комплексен, ализарин красный, аллофикоцианин, аминокумарин, антроил стеарат, астразон бриллиантовый красный 4G , астразон оранжевый R, астразон красной 6В, астразон желтый 7 GLL, атабрин, аурамин, аурофосфин, аурофосфин G, ВАО 9 (бисаминофенилоксадиазол), BCECF, берберин сульфат, бисбензамид, бланкофор FFG рвствор, бланкофор SV., BODIPY F1, бриллиантовый сульфофлавин FF, кальцеин синий, кальций зеленый, калкофтор RW раствор, калкофтор белый, калкофор белый АВТ раствор, калкофор белый стандартный раствор, карбостирил, каскад желтый, катехоламин, чайнакрин, корифосфин О, кумарин-фаллоидин, CY3.1 8, CY5.1 8, CY7, Данс (1-диметил амино нафалин 5 сульфоновая кислота), данса (диамино нафтил сульфоновая кислота), дансил NH-CH3, диамино фенил оксидиазол (DAO), диметиламино-5-сульфоновая кислота, дипиррометенборон дифторид, дифенил бриллиантовый флавин 7GFF, дофамин, эритрозин ITC, эукризин, ФИФ (формальдегид индуцированная флуоресценция), флазо оранжевый, флуоЗ, флуорескамин, фура-2, генакрил бриллиантовый красный В, генакрил бриллиантовый желтый 10GF, генакрил розовый 3G, генакрил желтый 5GF, глоксалиновая кислота, грануляр синий, гематопорфирин, индо-1, интравайт Cf жидкий, лейкофор PAF, лейкофор SF, лейкофор WS, лиссамин родамин В200 (RD200), люцифер желтый СН, люцифер желтый VS, магдала красный, синий марина, максилон бриллиантовый флавин 10 GFF, максилон бриллиантовый флавин 8 GFF, MPS (метил зеленый пиронин стильбен), митрамицин, NBD амин, нитробензоксадидол, норадреналин, ядерный быстрый красный, ядерный желтый, нилосан бриллиантовый флавин E8G, оксадиазол, пацифик синий, Pararosaniline (Фельген), форвайт АР раствор, форвайт BKL, форвайт Rev, форвайт РПА, фосфин 3R, фталоцианин, фикоэритрин R, фикоэритрин В, полиазаиндацен понтохром синий черный, порфирин, примулин, процион желтый, пиронин, пиронин В, пирозал бриллиантовый флавин 7GF, акрихин горчичный, родамин 123, родамин 5 GLD, родамин 6G, родамин В, родамин В 200, родамин В Extra, родамин ВВ, родамин BG, родамин WT, серотонин, севрон бриллиантовый красный 2В, севрон бриллиантовый красный 4G, севрон бриллиантовый красный В, севрон оранжевый, севрон желтый L, SITS (примулин), SITS (стильбен изотиосульфоновая кислота), стильбен, Snarf 1, сульфо родамин В кэн С, сульфо родамин G Extra, тетрациклин, тиазиновый красный R, тиофлавин S, тиофлавин TCN, тиофлавин 5, тиолит, тиозол оранжевый, тинопол CBS, настоящий синий цвет, ультралайт, уранин В, увитекс SFC, ксилол оранжевый и XRITC.
Абсорбция и эмиссия максимумов, соответственно, для некоторых из этих флуоресцирующих агентов составляет: FITC (490 нм; 520 нм), Су3 (554 нм; 568 нм), Су3.5 (581 нм; 588 нм), Су5 (652 нм: 672 нм), Су5.5 (682 нм; 703 нм) и Су7 (755 нм;
778 нм), тем самым позволяя их одновременное обнаружение. Другие примеры флуоресцеиновых красителей включают 6-карбоксифлуоресцеина (6-FAM), 2',4', 1,4,-тетрахлорфлуоросцеин (ТЕТ), 2',4',5',7',1,4-гексахлорфлуоросцеин (HEX), 2',7'-диметокси-4', 5'-дихлор-6-карбоксиродамин (JOE), 2'-хлор-5-фтор-7', 8'-слитый фенил-1,4-дихлор-6-карбоксифлуоресцеин (NED), и 2'-хлор-7'-фенил-1,4-дихлор-6-карбоксифлуоресцеин (VIC). Флуоресцентные метки могут быть получены из различных коммерческих источников, в том числе Amersham Pharmacia Biotech, Piscataway, NJ; Molecular Probes, Eugene, OR; и Research Organics, Cleveland, Ohio
Дополнительные метки представляющие интерес, включают те, которые обеспечивают сигнал только тогда, когда зонд с которыми они связаны специфически связан с молекулой-мишенью, где такие метки включают: молекулярные маячки , как описано в работе Tyagi & Kramer, Nature Biotechnology (1996) 14:303 and EP 0070685 В]. Другие метки, представляющие интерес, включают описанные в патенте США No 5563037, который упомянут здесь в качестве ссылки.
Маркированные нуклеотиды являются формой метки, которые могут быть непосредственно включены в продукты амплификации в процессе синтеза. Примеры меток, которые могут быть отнесены к амплифицированным нуклеиновым кислотам, включают нуклеотидные аналоги, такие как BrdUrd, аминоаллилдезоксиуридин, 5-метилцитозин, бромуридин и нуклеотиды, модифицированные с биотином или с подходящими гаптенами, такими как дигоксигенин. Подходящие флуоресцентно-меченые нуклеотиды представляют собой флуоресцеин-изотиоцианат-dUTP, цианин-3-dUTP и цианин-5-dUTP. Одним из примеров метки аналога нуклеотидов для ДНК является BrdUrd (бромдезоксиуридин, BrdUrd, BrdU, BUdR, Sigma-Aldrich Co). Другие примеры нуклеотидных аналогов для включения метки в ДНК являются АА-dUTP (аминоаллил-дезоксиуридина трифосфат, Sigma-Aldrich Со), и 5-метил- dCTP (Roche Molecular Biochemicals). Одним из примеров нуклеотидного аналога для включения метку в РНК является биотин-16-UTP (биотин-16-уридин-5'-трифосфат, Roche Molecular Biochemicals). Флуоресцеин, Су3 и Су5 могут быть связаны с dUTP для прямой маркировки. Су3.5 и Су7 являются доступными как авидин или анти-дигоксигенин конъюгаты для вторичного обнаружения биотин-или дигоксигенин-меченых зондов.
Метки, которые включены в амплифицированную нуклеиновую кислоту, такие как биотин, могут быть впоследствии обнаружены с помощью чувствительных способов, хорошо известных в данной области техники. Например, биотин может быть обнаружен с помощью конъюгата стрептавидин-щелочной фосфатазы (Tropix, Inc), который связан с биотином и впоследствии обнаруживается с помощью хемилюминесценции подходящих субстратов (например, хемилюминесцентный субстрат CSPD: динатрий, 3 (4-метоксиспиро-[1,2,-диоксетан-3-2'-(5'-хлор)трицикло[3.3.1.13,7]декан]-4-ил) фенил фосфат; Tropix, Inc.) Метки могут также быть ферментами, такими как щелочная фосфатаза, пероксидаза сои, пероксидаза хрена и полимеразы, которые могут быть обнаружены, например, с амплификацией химического сигнала или с помощью субстрата к ферменту, который производит свет (например, хемилюминесцентный 1, 2-диоксетан субстрат) или флуоресцентный сигнал.
Молекулы, которые объединяют две или более из этих меток, также считаются метками. Любая из известных меток может быть использована с зондами воплощения, тегами и способом для маркировки и обнаружения амплифицированной нуклеиновой кислоты с использованием способов воплощения. Способы обнаружения и измерения сигналов, генерируемые метками также известны специалистам в данной области техники. Например, радиоактивные изотопы могут быть обнаружены с помощью сцинтилляционного счета или прямой визуализации; флуоресцентные молекулы могут быть обнаружены с помощью флуоресцентных спектрофотометров, фосфоресцирующие молекулы могут быть обнаружены с помощью спектрофотометра или непосредственно визуализируются камерой; ферменты могут быть обнаружены путем выявления и визуализации продуктов в реакции, катализируемой ферментом; антитела могут быть обнаружены путем выявления вторичной метки, связанной с антителом. В данном случае, молекулы обнаружения являются молекулами, которые взаимодействуют с амплифицированной нуклеиновой кислотой и с которой связаны одна или несколько меток.
Понятно, и здесь предполагается, что одним способом оценки либо увеличения конкретной мРНК, либо произошедшей экспрессии мРНК, либо наличия конкретной мРНК является сравнение с контрольным образцом. Таким образом, предусмотренными в настоящем документе, являются способы диагностики рака у субъекта, включающие проведение ОТ-ПЦР или ПЦР-реакции с мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает в себя обратный праймер, способный на специфическую гибридизацию с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер; и где увеличение количества продукта амплификации по сравнению с контролем указывает на наличие АЛК-связанных раковых заболеваний и где полученная контрольная ткань является нераковой тканью. Предполагается также, что в отношении АЛК-связанных раковых заболеваний, использование контроля из нераковой ткани может применяться, но не является необходимым, поскольку раковые ткани из не-АЛК-связанных видов рака также могут использоваться. Таким образом, описанными здесь являются способы диагностики у субъекта форм рака, связанных с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР, с мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает в себя обратный праймер, способный специфически гибридизироваться с одной или несколькими последовательностями АЛК, и, по меньшей мере, один прямой праймер, и где увеличение количества продукта амплификации по сравнению с контролем указывает на наличие АЛК связанных форм рака, и где контрольная ткань является полученной не из АЛК-связанной раковой ткани.
Раскрытые способы могут быть использованы для диагностики любых заболеваний, где происходит неконтролируемая клеточная пролиферация и здесь называется "рак". Не ограничивающий перечень различных видов АЛК-связанных раковых заболеваний, выглядит следующим образом: лимфомы (Ходжкина и неходжкинские), лейкозы, рак, рак твердых тканей, плоскоклеточный рак, аденокарцинома, саркомы, глиомы, высокодифференцированные глиомы, бластомы, нейробластомы, плазмацитомы, гистиоцитомы, меланомы, аденомы, гипоксические опухоли, миеломы, лимфомы или саркомы связанные со СПИДом, метастатические раковые заболевания, или раковые заболевания в целом.
Репрезентативный, но не ограничивающий список раковых заболеваний, для диагностики которых могут быть использованы раскрытые способы является следующим: лимфома, В-клеточная лимфома, Т-клеточная лимфома, грибовидный микоз, болезнь Ходжкина, миелолейкоз, рак мочевого пузыря, рак мозга, рак нервной системы, рака головы и шеи, плоскоклеточный рак головы и шеи, рак почки, рак легких, также как мелкоклеточный рак легкого и немелкоклеточный рак легкого, нейробластома/глиобластома, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак печени, меланома, плоскоклеточный рак полости рта, горла, гортани и легких, рак толстой кишки, рак шейки матки, карцинома шейки матки, рак молочной железы, и эпителиальный рак, рак почки, мочеполовой рак, рака легкого, карцинома пищевода, головы и шеи карцинома, рак толстой кишки, рак системы кроветворения; рак яичек, рак толстой кишки и прямой кишки, рак предстательной железы, или рак поджелудочной железы.
Таким образом, описанными здесь являются способы диагностики рака, где рак выбран из группы, состоящей из немелкоклеточного рака легкого, диффузной крупноклеточной В-клеточной лимфомы, системного гистиоцитоза, рака молочной железы, рака толстого кишечника, плоскоклеточного рака пищевода, анапластической крупноклеточной лимфомы, нейробластомы, и воспалительных миофибробластных опухолей (ВМО). Например, описанными здесь являются способы диагностики у субъекта ракового заболевания, связанного с киназой анапластической лимфомы (АЛК), включающие проведение ОТ-ПЦР реакции на мРНК из образца ткани от субъекта; где полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) включает в себя обратный праймер, способный к специфической гибридизации с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер, где увеличение количества продукта амплификации относительно контроля указывает на присутствие АЛК-связанного ракового заболевания, и где рак выбран из группы, состоящей из немелкоклеточного рака легкого, диффузной крупноклеточной В-клеточной лимфомы, системного гистиоцитоза, рака молочной железы, рака толстого кишечника, плоскоклеточного рака пищевода, анапластической крупноклеточной лимфомы, нейробластомы, и воспалительных миофибробластных опухолей (ВМО).
Способы оценки пригодности АЛК-направленного лечения
Хоть и не желая быть связанными с современными теориями, мы считаем, что ингибирование этих форм АЛК генов низкомолекулярными кандидатурами лекарств отменяет связанную ненормальную пролиферацию клеток и способствует апоптозу при нейробластоме и других АЛК-связанных опухолевых клеточных линиях, более того, как доклинические животные модели, так и ранний клинический опыт с этими ингибиторами показывают, что низкомолекулярные ингибиторы АЛК обладают не только отмеченной противоопухолевой активностью в отношении АЛК-связанных раковых заболеваний, но и очень хорошо переносятся, с не ограничивающей токсичностью, ассоциированной с мишенью.
Эти открытия выводят на первый план необходимость специализированного диагностического теста на АЛК-мутации. Например, такой анализ может быть использован для скрининга детей в семьях, страдающих наследственной нейробластомой, чтобы помочь и облегчить выявление опухоли на ранней стадии, когда опухоль более легко поддается лечению. Таким образом, описанными здесь, являются способы оценки пригодности лечения рака у субъектов с помощью АЛК ингибиторов, включающие измерение мРНК из образца ткани от субъекта; где увеличение количества АЛК-последовательности мРНК по сравнению с контролем указывает, что рак можно лечить с помощью ингибитора АЛК.
Понятно, и здесь предполагается, что любая из раскрытых техник измерения мРНК, описанных здесь, может быть использована в этих способах. Так, например, раскрытыми здесь, являются способы оценки пригодности лечения рака у субъектов с помощью АЛК ингибиторов, включающие проведение ОТ-ПЦР реакцию с мРНК или ПЦР-реакции с ДНК из образца ткани от субъекта; где ОТ-ПЦР реакция включает обратный праймер, способный к специфической гибридизации с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер, где увеличение количества продукта амплификации относительно контроля указывает, что рак можно лечить с помощью ингибитора АЛК. Понятно также, что раскрытые выше способы могут дополнительно содержать любой из описанных здесь праймеров и использовать раскрытые техники мультиплексирования ПЦР.
Способы диагностики АЛК-связанных раковых заболеваний, развившихся из точечных мутаций АЛК и способы оценки устойчивости к АЛК ингибиторам.
Прогностическая важность и значимость влияния на принятие решений, касающихся лечения, следующих за выявлением минимальной остаточной болезни (МОБ) после терапии АЛК-связанных раковых заболеваний, может быть повышена за счет высокой чувствительности и легкости осуществления диагностических анализов, таких как те, которые предлагаются в настоящем документе. Доклинические исследования выявили спектр домена точечных мутаций АЛК киназы, которые придают устойчивость к низкомолекулярным ингибиторам, таким как NVP-TAE684 и PF-2341066. Такие анализы известны высокой прогностичностью клинически значимых мутаций резистентности к ингибитору на основе их использования для предсказания мутаций, которые придают устойчивость к ингибиторам, таким как Гливек, который используется клинически на протяжении многих лет.
Настоящее изобретение включает способы и композиции для чувствительных и специфичных АЛК диагностических тестов, которые могут использоваться для селективной прямой и целевой лекарственной терапии пациентов. Многочисленные технологии сканирования для неизвестных мутаций могут быть использованы в способах, описанных здесь, таких как: денатурирующая высокоэффективная жидкостная хроматография (дВЭЖХ), сканирование первичной структуры путем удаления оснований (СПУО), полиморфизм конформации одноцепочечной ДНК (ПКОЦ), гетеродуплексный (гибридизационный) анализ (ГА), конформационно-чувствительный гель-электрофорез (КЧГЭ), электрофорез в градиенте денатурирующего геля (ДГГЭ), электрофорез в равномерном денатурирующем геле (РДГЭ), гель-электрофорез при временном градиенте температуры (ВТГЭ), полиморфизм длин фрагментов, полученных при помощи переваривания кливазой (КПДФ), способ химического расщепления некомплементарных сайтов, метод ферментного расщепления некомплементарных сайтов и ферментное восстановление некомплементарных сайтов. В одном аспекте, описанными здесь, являются способы идентификации одного нуклеотида или других мутационных изменений, связанных с АЛК геном с использованием технологии шаблонной реакции обмена и экстензии (TEER™) для выявления онкогенных мутаций в АЛК или мутаций, которые придают лекарственную устойчивость АЛК-связанным видам рака. Технология TEER™ может идентифицировать такие АЛК мутации, присутствующие как на ранней стадии, так и при лекарственной устойчивости АЛК рака, включая даже редкие и новые мутации. TEER технология описана в патенте США №6610486, патенте США №6150105 и заявке США №12/152512, которые включены в данный,документ в качестве ссылки во всей полноте их учения в обнаружении нуклеотидных вариаций.
Способы для обнаружения АЛК связанных вариаций нуклеиновых кислот, описанные здесь, имеют множество применений, включая, но не ограничиваясь обнаружение или диагностику наличия заболевания или состояния, такого как рак, оценивание восприимчивости или риска развития заболевания или состояния, ассоциированного с вариациями нуклеиновых кислот, мониторинг прогрессии заболевания и определение чувствительности или устойчивости к терапии.
Понятно, и здесь предполагается, что могут быть встречаться различия между мутантами одного и того же типа (т.е. между двумя точечными мутациями или между двумя ЕМ1-Л-АЛК слияниями). Таким образом, следует понимать, что любой из раскрытых способов диагностики рака или оценки пригодности лечения может дополнительно содержать секвенирование любого ампликона, полученного в результате применения способа.
Способы скрининга
АЛК-слияния и точечные мутации, описанные здесь являются мишенями для лечения рака. Таким образом, раскрытыми здесь, являются способы скрининга на наличие агента, который ингибирует АЛК-связанные раковые заболевания у субъекта, включающие:
а) получение образца ткани от субъекта с АЛК-связанным раковым заболеванием;
б) контактирование образца ткани с агентом,
в) экстрагирование мРНК из образца ткани;
г) проведение ОТ-ПЦР реакции на мРНК из образца ткани;
где ОТ-ПЦР реакция включает обратный праймер, способный к специфической гибридизации с одной или несколькими последовательностями АЛК и, по меньшей мере, один прямой праймер; и где уменьшение количества продукта амплификации относительно нелеченного контроля указывает на агент, который может ингибировать АЛК-связанное раковое заболевание.
Нуклеиновые кислоты
Раскрытые способы и композиции используют различные нуклеиновые кислоты. Обычно, любая нуклеиновая кислота может быть использована в раскрытом способе. Например, раскрытые нуклеиновые кислоты, представляющие интерес, и раскрытые справочные нуклеиновые кислоты могут быть выбраны на основе желаемого анализа и информации, которые могут быть получены или оценены. Раскрытые способы также производят новые и измененные нуклеиновые кислоты. Характер и структура таких нуклеиновых кислот будут установлены таким образом, которым они производятся и регулируются различными способами. Так, например, продукты удлинения и гибридизированные нуклеиновые кислоты изготавливаются раскрытыми способами. Упоминаемые здесь, гибридизованные нуклеиновые кислоты являются гибридами продуктов удлинения и второй нуклеиновой кислоты.
Понятно, и в данном документе рассматривается, что нуклеиновой кислотой, представляющей интерес, может быть любая нуклеиновая кислота, в которой является желательным определение наличия или отсутствия нуклеотидной вариации. Так, например, нуклеиновая кислота, представляющая интерес, может содержать последовательность, которая соответствует последовательности дикого типа нуклеиновой кислоты-эталона. Кроме того, здесь описание, что указанные способы могут быть выполнены, если первая нуклеиновая кислота является нуклеиновой кислотой-эталоном, а вторая нуклеиновая кислота является нуклеиновой кислотой интереса, или если первая нуклеиновая кислота является нуклеиновой кислотой интереса, а вторая нуклеиновая кислота является нуклеиновой кислотой-эталоном.
Понятно, и в данном документе рассматривается, что нуклеиновой кислотой-эталоном может быть любая нуклеиновая кислота, с которой нуклеиновая кислота интереса будет сравниваться. Как правило, нуклеиновая кислота-эталон обладает известной последовательностью (и/или, как известно, имеет последовательность интереса в качестве эталона). Хотя этого и не требуется, может оказаться полезным, если последовательность эталона имеет известную или предполагаемую взаимосвязь с нуклеиновой кислотой, представляющей интерес. Например, если необходимо, чтобы была обнаружена вариация одного нуклеотида, последовательностью эталона может быть с пользой выбрана последовательность, которая является гомологом или близко соответствует нуклеиновой кислоте, представляющей интерес, такой, как нуклеиновая кислота, полученная из того же самого гена или генетический элемент из того же или родственного организма или индивидуума. Так, например, здесь рассматривается, что нуклеиновая кислота-эталон может включать последовательность дикого типа или альтернативно может включать известную мутацию, в том числе, например, мутации, наличие или отсутствие которых связано с заболеванием или устойчивостью к терапии. Так, например, предполагается, что указанные выше способы могут быть использованы для обнаружения или диагностики наличия известных мутаций в нуклеиновой кислоте интереса, путем сравнения нуклеиновой кислоты, представляющей интерес с нуклеиновой кислотой-эталоном, которая включает последовательность дикого типа (т.е. известной тем, что не обладает мутацией) и экспертизы на наличие или отсутствие изменений в нуклеиновой кислоте интереса, где отсутствие изменений будет означать отсутствие мутации. Кроме того, нуклеиновая кислота-эталон может обладать известной мутацией. Так, например, предполагается, что указанные выше способы могут быть использованы для определения восприимчивости к болезни или состоянию, при помощи сравнения нуклеиновой кислоты, представляющей интерес с нуклеиновой кислотой-эталоном, включающей известную мутацию, которая означает восприимчивость к болезни и для изучения на предмет наличия или отсутствия мутации, где наличие мутации означает болезнь.
Здесь, термин "нуклеотидная вариация" относится к любому изменению или различию в нуклеотидной последовательности нуклеиновых кислот интереса по сравнению к нуклеотидной последовательностью нуклеиновой кислоты-эталона. Таким образом, нуклеотидную вариацию называют произошедшей, когда последовательности между нуклеиновой кислотой-эталоном и нуклеиновой кислотой, представляющей интерес (или ее комплементом, как соответствует контексту) отличаются. Так, например, замещение аденина (А) на гуанин (G) в определенной позиции в нуклеиновой кислоте было бы нуклеотидной вариацией при условии, что нуклеиновая кислота-эталон включала бы А в соответствующей позиции. Понятно, и в данном документе рассматривается, что определение вариации основано на нуклеиновой кислоте-эталоне и не указывает, является ли последовательность или нет последовательностью дикого типа. Так, например, когда нуклеиновая кислота с известной мутацией используется в качестве нуклеиновой кислоты-эталона, нуклеиновая кислота, не обладающая мутацией (в том числе нуклеиновая кислота дикого типа), будет рассматриваться как обладающая нуклеотидной вариацией (относительно нуклеиновой кислоты-эталона).
Нуклеотиды
Раскрытые способы и композиции используют различные нуклеотиды. Через всю данную заявку и способы, описанные здесь, делается ссылка на тип основания для нуклеотида. Понятно, и здесь предусмотрено, что там, где делается ссылка на тип основания, это относится к основанию, которое в нуклеотиде в цепочке нуклеиновой кислоты способно к гибридизации (связывание), с определенным набором из одного или нескольких канонических оснований. Так, например, если делается ссылка на удлиненные продукты, которые удлинены в присутствии трех типов устойчивых к нуклеазе нуклеотидов, а не в присутствии нуклеотидов, которые содержат тот же тип основания, что и модифицированные нуклеотиды, это означает, что если, например,основание модифицированного нуклеотида было аденин (А), нуклеазо устойчивые нуклеотиды могут быть, например, гуанин (Г), тимин (Т) и цитозин (С). Каждое из этих оснований (которые представляют собой четыре канонических основания) способны к гибридизации с другим, одним из четырех канонических оснований и таким образом, каждое квалифицировано как другой тип основания, как это определено в настоящем документе. В качестве другого примера, основание инозин составляет пару в первую очередь с аденином и цитозином (в ДНК) и, следовательно, может считаться другим типом основания от аденина и от цитозина, который составляет пару основаниям с тимином и гуанином, соответственно, но не другой тип основания с гуанином и тимином, которые составляют пару оснований с цитозином и аденином, соответственно, потому что спаривание оснований гуанина и тимина перекрывается (то есть, ничем не отличается от) моделью гибридизации инозина.
Любой тип модифицированного или альтернативного основания может быть использован в раскрытых способах и композициях, как правило, ограниченных только возможностями ферментов, применяемых при использовании таких оснований. Многие модифицированные и альтернативные нуклеотиды и основания известны, некоторые из которых описаны ниже и в других местах в настоящем документе. Тип основания, которое представляет такие модифицированные и альтернативные основания можно определить по модели спаривания оснований для этого основания, как описано в настоящем документе. Так, например, если модифицированным нуклеотидом был аденин, любой аналог, производное, модифицированное основание или вариант основания, которое в первую очередь спаривается с тимином, будет считаться тем же типом основания, что и аденин. Другими словами, до тех пор пока аналог, производное, модифицированное основание или вариант имеет ту же модель спаривания оснований как другое основание, оно может рассматриваться, как тот же тип основания. Модификации могут быть внесены в сахарные или фосфатные группы нуклеотидов. Как правило, такие модификации не будут изменять модель спаривания основания. Однако модель спаривания оснований нуклеотида в цепочке нуклеиновой кислоты определяет тип основания в нуклеотиде.
Модифицированные нуклеотиды для включения в удлиненные продукты и для выборочной делении раскрытыми агентами в раскрытых способах могут быть любыми модифицированными нуклеотидами, которые функционируют по мере необходимости в раскрытых способах, как это описано в другом месте в настоящем документе. Модифицированные нуклеотиды также могут производиться в существующей цепочке нуклеиновой кислоты, такой как удлиненные продукты, путем, например, химической модификации, ферментативной модификации, или их комбинации.
Многие виды нуклеазо-устойчивых нуклеотидов известны и могут быть использованы в раскрытых способах. Например, нуклеотиды, имеющие модифицированные фосфатные группы и/или модифицированные группы Сахаров могут быть устойчивыми к одной или нескольким нуклеазам. Нуклеазная устойчивость определяется здесь как устойчивость к делеции из нуклеиновой кислоты какой-либо одной или нескольких нуклеаз. Как правило, нуклеазная резистентность конкретного нуклеотида может быть определена в пределах соответствующей нуклеазы. Так, например, если определенная нуклеаза используется в раскрытом способе, нуклеазо-устойчивым нуклеотидам нужно только быть устойчивым к данной нуклеазе. Примеры применимых нуклеазо-устойчивых нуклеотидов включают тио-модифицированные нуклеотиды и борано-модифицированные нуклеотиды.
Существует множество молекул на основе нуклеиновых кислот, описанных здесь. Неограничивающие примеры этих и других молекул, рассматриваются в настоящем документе. Понятно, что, например, нуклеотид представляет собой молекулу, которая содержит фрагмент основания, сахарный фрагмент и фосфатный фрагмент. Нуклеотиды могут быть связаны друг с другом через свои фосфатные фрагменты и фрагменты сахара, создавая межнуклеозидную связь. Фрагментом основания нуклеотида может быть аденин-9-ил (аденин А), цитозин-1-ил (цитозин С), гуанин-9-ил (гуанин, G), урацил-1-ил (урацил, U) и тимин-1-ил (тимин, Т). Сахарным фрагментом нуклеотида является рибоза или дезоксирибоза. Фосфатным фрагментом нуклеотида является пятивалентный фосфат. Неограничивающим примером нуклеотида мог бы быть 3'-АМФ (З'-аденозинмонофосфат) или 5'-ГМФ (5'-гуанозинмонофосфат).
Нуклеотидный аналог представляет собой нуклеотид, который содержит некоторый тип модификации либо фрагментов основания, сахара, или фосфата. Модификации фрагмента основания будут включать природные и синтетические модификации А, С, G и T/U, а также различных пуриновых или пиримидиновых оснований, таких как урацил-5-ил (ψ), гипоксантин-9-ил (инозин, I), и 2 аминоаденин-9-ил. Модифицированное основание включает, но не ограничивается 5-метилцитозин (5-ме-С), 5-гидроксиметил цитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил и другие алкильные производные аденина и гуанина, 2-пропил и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галоурацил и цитозин, 5-пропинил урацил и цитозин, 6-азо урацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацила, 8-гало, 8-амино, 8-тиол, 8-тиоалкил, 8-гидроксил и другие 8 замещенные аденины и гуанины, 5-гало, в частности 5-бром, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 8-азагуанин и 8-азааденин, 7-деазагуанин и 7-деазааденин и 3-деазагуанин и 3-деазааденин. Дополнительные модификации оснований можно найти, например, в патенте США № 3687808, который включен в данный документ в полном объеме благодаря идее модификаций оснований. Определенные нуклеотидные аналоги, такие как 5-замещенные пиримидины, 6 азапиримидины и N-2, N-6 и 0-6 замещенные пурины, в том числе 2-аминопропиладенин, 5-пропинилурацил и 5-пропинилцитозин. 5-метилцитозин может увеличить стабильность образования дуплекса. Часто по времени, модификации оснований могут быть объединены, например, с модификацией Сахаров, такой как 2'-0-метоксиэтил, для достижения уникальных свойств, таких как повышенная стабильность дуплекса. Существуют многочисленные патенты США, такие как под номерами 4845205, 5130302, 5134066, 5175273, 5367066, 5432272, 5457187, 5459255, 5484908, 5502177, 5525711, 5552540, 5587469, 5594121, 5596091, 5614617, и 5681941, которые детализируют и описывают диапазон модификаций оснований. Каждый из этих патентов приводится в настоящем документе в качестве ссылки.
Нуклеотидные аналоги могут также включать модификации сахарного фрагмента. Модификации в сахарном фрагменте будут включать природные модификации рибозы и дезоксирибозы, а также синтетические модификации. Модификации сахара включают, но не ограничиваются следующими модификациями в позиции 2': ОН; F; O-, S-, или N-алкил; O-, S-, или N-алкенил; O-, S- или N-алкинил; или О- алкил -О- алкил, где алкил, алкенил или алкинил могут быть замещенными или незамещенными от С1 до С 10, алкилом или от С2 до С 10 алкенилом и алкинилом. 2' модификации сахара также включают, но не ограничиваются -O[(CH2)n O]m CH3, -O(CH2)n OCH3, -O(CH2)n NH2, -O(СН2)n СН3, -O(CH2)n -ONH2, и -O(CH2)nON[(CH2)n СН3)]2, где n и m равны от 1 до приблизительно 10.
Другие модификации на позиции 2' включают, но не ограничиваются: С1 до С10 низший алкил, замещенный низший алкил, алкарил, аралкил, O-алкарил или 0-аралкил, SH, SCH3, OCN, Сl, Br, CN, CF3, OCF3, SOCH3, SO2 СН3, ONO2, NO2, N3, NH2, гетероциклоалкил, гетероциклоалкарил, аминоалкиламино, полиалкиламино, замещенный силил, группу РНК расщепления, репортер группу, интеркалятор, группу по улучшению фармакокинетических свойств олигонуклеотида или группу по улучшению фармакодинамические свойств олигонуклеотида, и другие заместители, имеющие аналогичные свойства. Подобные модификации могут быть также сделаны в других позициях на сахаре, в частности, 3' положении сахара на 3' терминальном нуклеотиде или в 2'-5' связанных олигонуклеотидах и в 5' позиции 5' терминального нуклеотида. Модифицированные сахара будут также включать те, что содержат модификации на мостовом кольце кислорода, такие как СН2 и S. Аналоги нуклеотидного сахара также могут иметь миметики сахара, такие как циклобутил фрагменты на месте сахара пентофуранозила. Существуют многочисленные патенты США, которые учат подготовке таких модифицированных структур сахара, такие как под номерами 4981957, 5118800, 5319080, 5359044, 5393878, 5446137, 5466786, 5514785, 5519134, 5567811, 5576427, 5591722, 5597909, 5610300, 5627053, 5639873, 5646265 ; 5658873; 5670633 и 5700920, каждый из которых включен в настоящий документ в качестве ссылки в полном объеме.
Нуклеотидные аналоги также может быть модифицированы в фосфатных фрагментах. Модифицированные фосфатные фрагменты включают, но не ограничиваются теми, которые могут быть изменены таким образом, что связь между двумя нуклеотидами содержит фосфоротиоат, хиральный фосфоротиоат, фосфородитиоат, фосфотриэфир, аминоалкилфосфотриэфир, метил и другие алкильные фосфонаты, в том числе 3'-алкиленфосфонат и хиральные фосфонаты, фосфинаты, фосфорамидаты, в том числе 3'-аминофосфорамидат и аминоалкилфосфорамидаты, тионофосфорамидаты, тионоалкилфосфонаты, тионоалкилфосфотриэфиры и боранофосфаты. Понятно, что эти фосфатные или модифицированные фосфатные связи между двумя нуклеотидами могут осуществляться через 3'-5' связь или 2'-5' связь, и связь может содержать инвертированную полярность, такую как 3'-5' к 5'-3' или 2'-5' к 5'-2'. Различные соли, смешанные соли и формы свободной кислоты также включены. Многочисленные патенты США учат, как сделать и использовать нуклеотиды, содержащие модифицированные фосфаты и включают, но не ограничиваясь этим, патенты под номерами 3687808, 4469863, 4476301, 5023243, 5177196, 5188897, 5264423, 5276019, 5278302, 5286717, 5321131, 5399676, 5405939, 5453496; 5455233; 5466677; 5476925; 5519126; 5536821; 5541306; 5550111; 5563253; 5571799; 5587361 и 5625050, каждый из которых включен в данный документ в качестве ссылки.
Понятно, что нуклеотидным аналогам, нужно содержать только одну модификацию, но они могут также содержать несколько модификаций в одном из фрагментов или между различными фрагментами.
Нуклеотидные заместители представляют собой молекулы, имеющие аналогичные нуклеотидам функциональные свойства, но которые не содержат фрагмент фосфатов, такие как пептидные нуклеиновые кислоты (ПНК). Нуклеотидные заместители представляют собой молекулы, которые будут опознавать нуклеиновые кислоты по модели Уотсона и Крика или Хугетина, но которые связаны друг с другом через фрагмент, отличающийся от фосфатного фрагмента. Нуклеотидные заместители способны соответствовать двойной структуре типа спирали при взаимодействии с соответствующей целевой нуклеиновой кислотой.
Нуклеотидные заместители представляют собой нуклеотиды или Нуклеотидные аналоги, которые имели замещение фрагмента фосфата и/или фрагментов сахара. Нуклеотидные заместители не содержат стандартный атом фосфора. Заместителями фосфата могут быть, например, алкил с короткой цепью или циклоалкильные межнуклеозидные связи, смешанный гетероатом и алкильные или циклоалкильные межнуклеозидные связи, или одна или более короткоцепочечные гетероатомные или гетероциклические межнуклеозидные связи. К ним относятся те, которые имеют морфолино связи (образуются частично из сахарной части нуклеозида); силоксановые каркасы; сульфидные, сульфоксидные и сульфоновые каркасы; формацетильные и тиоформацетильные каркасы; метиленовые формацетильные и тиоформацетильные каркасы; алкен содержащие каркасы; сульфаматные каркасы; метилениминовые и метиленгидразиновые каркасы; сульфанатные и сульфонамидные каркасы; амидные каркасы, а также другие, имеющие смешанные N, О, S и СН2 части компонента. Многочисленные патенты США раскрывают, как изготовить и использовать эти типы фосфатных замен и включают, но не ограничиваясь, патенты под номерами 5034506; 5166315; 5185444; 5214134; 5216141; 5235033; 5264562; 5264564; 5405938; 5434257; 5466677; 5470967; 5489677; 5541307; 5561225; 5596086; 5602240; 5610289; 5602240; 5608046; 5610289; 5618704; 5623070; 5663312; 5633360; 5677437 и 5677439, каждый из которых включен в данный документ в качестве ссылки.
Также понимается в нуклеотидном заместителе, что оба и сахарный и фосфатный фрагменты нуклеотида могут быть заменены, например, амидным типом связи (аминоэтилглицин) (ПНК). Патенты США под номерами 5539082, 5714331, и 5719262 учат, как приготовить и использовать ПНК молекулы, каждый из которых включен в данный документ в качестве ссылки.
Также возможно связать другие типы молекул (конъюгатов) с нуклеотидами или нуклеотидными аналогами. Конъюгаты могут быть химически связаны с нуклеотидом или нуклеотидными аналогами. Такие конъюгаты включают, но не ограничиваются липидные фрагменты, такие как холестериновый фрагмент, желчную кислоту, тиоэфир, например, гексил-8-тритилтиол, тиохолестерин, алифатическую цепь, например, остатки додекандиола или ундецила, фосфолипид, например, ди-гексадецил-рац-глицерин или триэтиламмония 1,2-ди-О-гексадецил-рац-глицеро-З-Н фосфонат, цепи полиамино или полиэтиленгликоля, или адамантана уксусную кислоту, фрагмент пальмитила, или октадециламина или гексиламино-карбонил-оксихолестериновый фрагмент. Многочисленные патенты США учат изготовлению таких конъюгатов и включают, но не ограничиваясь, патенты США под номерами 4828979; 4948882; 5218105; 5525465; 5541313; 5545730; 5552538; 5578717, 5580731, 5580731, 5591584, 5109124, 5118802, 5138045, 5414077, 5486603, 5512439, 5578718, 5608046, 4587044, 4605735, 4667025, 4762779, 4789737; 4824941; 4835263; 4876335; 4904582; 4958013; 5082830; 5112963; 5214136; 5082830; 5112963; 5214136; 5245022; 5254469; 5258506; 5262536; 5272250; 5292873; 5317098; 5371241, 5391723, 5416203, 5451463, 5510475, 5512667, 5514785; 5565552; 5567810; 5574142; 5585481; 5587371; 5595726; 5597696; 5599923; 5599928 и 5688941, каждый из которых включен в настоящий документ в качестве ссылки.
Взаимодействие Уотсона-Крика представляет собой по меньшей мере одно взаимодействие с лицевой поверхностью Уотсона-Крика нуклеотида, нуклеотидного аналога, или нуклеотидного зпместителя. Лицевая поверхность Уотсона-Крика нуклеотида, нуклеотидного аналога, или нуклеотидного зпместителя включает С2, N1, и С6 позиции нуклеотида, нуклеотидного аналога или нуклеотидного заместителя на основе пурина, и С2, N3, С4 позиции нуклеотида, нуклеотидного аналога или нуклеотидного заместителя на основе пиримидина.
Взаимодействие Хугстина представляет собой взаимодействие, которое имеет место на лицевой поверхности Хугстина нуклеотида или нуклеотидного аналога, которая является открытой в большой бороздке дуплексной ДНК. Лицевая поверхность Хугстина включает N7 позицию и реактивные группы (NH2 или О) в С6 позиции пуриновых нуклеотидов.
Гибридизация / Селективная Гибридизация
Термин "гибридизация" обычно означает управляемое последовательностью взаимодействие между, по меньшей мере, двумя молекулами нуклеиновой кислоты, такими как праймер, или зонд и ген. Управляемое последовательностью взаимодействие подразумевает взаимодействие, которое происходит между двумя нуклеотидами или нуклеотидными аналогами или нуклеотидными производными нуклеотидно специфическим образом. Например, G взаимодействие с С или взаимодействие А с Т является управляемыми последовательностью взаимодействиями. Обычно управляемые последовательностью взаимодействия происходят на поверхности Уотсона и Крика или поверхности Хугстина нуклеотида. Гибридизация двух нуклеиновых кислот находится под влиянием ряда условий и параметров, которые известны специалистам в данной области техники. Например, концентрации соли, уровни рН и температура реакции - все это влияет на то, будут ли две молекулы нуклеиновой кислоты гибридизироваться.
Параметры для селективной гибридизации между двумя молекулами нуклеиновой кислоты хорошо известны специалистам в данной области техники Например, в некоторых вариантах воплощения изобретения, условия селективной гибридизации могут быть определены как обязательные (жесткие) условия гибридизации. Например, жесткость гибридизации находится под контролем температуры и концентрации соли или обоими шагами гибридизации и промывки. Например, условия гибридизации для достижения селективной гибридизации могут вовлекать гибридизацию в растворе высокой ионной силы (6Х SSC или 6Х SSPE) при температуре, которая составляет приблизительно 12-25°С ниже Тт (температура плавления, при которой половина молекул диссоциирует от своих партнеров гибридизации) с последующей промывкой при комбинации температуры и концентрации соли, выбранных таким образом, что температура промывания составляет приблизительно от 5°С до 20°С ниже Тm. Условия уровня температуры и концентрации соли легко определяются эмпирически в предварительных экспериментах, в которых образцы ДНК-эталона, иммобилизованные на фильтрах, гибридизируют с меченой нуклеиновой кислотой интереса, а затем промывают в условиях различной точности. Температуры гибридизации являются, как правило, выше для ДНК-РНК и РНК-РНК гибридизации. Условия могут быть использованы, как описано выше для достижения точности, или так, как известно, в данной области техники. Предпочтительное точное условие для гибридизации для ДНК:ДНК гибридизации может быть при температуре 68°С (в водном растворе) в 6Х SSC или 6Х SSPE с последующей промывкой при температуре 68°С. Точность гибридизации и промывки, при желании, может быть уменьшена в соответствии с тем, насколько необходимо уменьшение степени комлиментарности, а в дальнейшем, в зависимости от изобилия G-C или А-Т любой области, в которой ищут изменчивость. Кроме того, точность гибридизации и промывки, при желании, может быть увеличена, в соответствии с тем, насколько необходимо увеличение гомологии, а в дальнейшем, в зависимости от изобилия G-C или А-Т любой области, в которой необходима высокая гомология, все, как известно в данной области техники.
Другим способом определения селективной гибридизации является определение количества (в процентах) одной из нуклеиновых кислот, связанной с другой нуклеиновой кислотой. Например, в некоторых вариантах воплощения изобретения условия селективной гибридизации были бы тогда, по меньшей мере около, 60, 65, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 процентов предельной нуклеиновой кислоты, будучи связанными с неограничивающей нуклеиновой кислотой. Как правило, неограничивающий праймер находится, например, в 10 или 100 или 1000-кратном избытке. Этот тип анализа может быть выполнен в условиях, когда оба ограничивающие и неограничивающие праймеры находятся, например, на уровне в 10 раз или 100 раз или 1000 раз ниже их ka, или, где только одна из молекул нуклеиновой кислоты находится на уровне в 10 раз или в 100 раз или в 1000 раз, или когда одна или обе молекулы нуклеиновых кислот находятся выше их k<i.
Другим путем для определения селективной гибридизации, необходимо определение процента праймера, который получает возможность ферментативного манипулирования в условиях, когда гибридизация, требуется для повышения желаемой ферментативной манипуляции. Например, в некоторых вариантах воплощения изобретения условия селективной гибридизации были бы тогда, по меньшей мере, около, 60, 65, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84,85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 процентов праймера, будучи ферментативно манипулированным в условиях, которые способствуют ферментативной манипуляции, например, если ферментативной манипуляцией является удлинение ДНК, то условия селективной гибридизации были бы, тогда, по меньшей мере, 60, 65, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 процентов молекул праймера, которые удлинены. Условия включают также те, что предложены производителем или указаны в данной области техники как подходящие для ферментного выполнения манипуляции.
Так же, как и с гомологией, следует понимать, что существуют различные способы, которые раскрываются здесь для определения уровня гибридизации между двумя молекулами нуклеиновых кислот. Понятно, что эти способы и условия могут обеспечить различные проценты гибридизации между двумя молекулами нуклеиновых кислот, но если не указано иное, соответствие параметрам любого из способов будет достаточно. Например, если требовалась гибридизация 80%, и до тех пор, пока гибридизация происходит в пределах требуемых параметров в любом из этих способов, она считается здесь раскрытой.
Понятно, что специалисты в данной области техники понимают, что если композиция или способ отвечает какому-либо одному из этих критериев для определения гибридизации либо вместе, либо разрозненно, это является композицией или способом, который раскрывается в настоящем документе.
Наборы
Раскрытыми в настоящем документе являются наборы, собранные из реагентов, которые могут быть использованы для применении на практике описанных здесь способов. В частности, наборы могут включать любой реагент или комбинацию реагентов, упоминаемых в данном документе, или тех, которые будут понятны как необходимые или благоприятные в осуществлении на практике раскрытых способов. Например, наборы могут включать один или несколько праймеров, описанных здесь, для выполнения реакции удлинения, репликации и амплификации, обсуждаемых в некоторых вариантах воплощения способов, а также буферы и ферменты, необходимые для использования праймеров, как предполагалось.
Понятно, что для обнаружения АЛК соответствующего слияния, может быть использован обратный праймер, который гибридизируется с АЛК дикого типа. Таким образом, описанньми здесь, являются наборы, которые включают, по меньшей мере, один обратный праймер, где обратный праймер гибридизируется с частью АЛК дикого типа, таким как домен киназы АЛК дикого типа. Примеры обратных праймеров, которые могут быть использованы в наборах настоящего изобретения, включают, но не ограничиваются ПОСЛ. ID NO. 7, ПОСЛ. ID NO: 32, ПОСЛ. ID NO: 46, ПОСЛ. ID NO: 47, ПОСЛ. ID NO: 56 и ПОСЛ. ID NO: 57. Кроме того, следует понимать, что наборы, описанные здесь, могут включать один или несколько прямых праймеров, которые специфически гибридизируются с партнером слияния АЛК или АЛК дикого типа. Так, например прямой праймер может гибридизироваться с АЛК дикого типа, 5-аминоимидазол-4-карбоксамид рибонуклеотидом формилтрансферазы/IMP циклогидролазы (ATIC), тяжелой цепью клатрина (CLTC), Ran-связывающим протеином 2 (RANBP2), SEC31L1, тропомиозином-3 (ТРМ3), тропомиозином-4 (ТРМ4), ТРК - слияния геном (большим) (TFGL), ТРК-слияния геном (малым) (TFGS), CARS, ALO17, моезином (MSN), геном тяжелой цепи немышечного миозина (MYH9) или ТРК - слияния геном (экстра большим) (ТFGXL). Неограничивающий список прямых праймеров, которые могут быть использованы в наборах, описанных здесь, включает, но не ограничивается ПОСЛ. ID NO: 2, ПОСЛ. ID NO: 3. ПОСЛ. ID NO: 4, ПОСЛ. ID NO: 5, ПОСЛ. ID NO: 6, ПОСЛ. ID NO: 35, ПОСЛ. ID NO: 36, ПОСЛ. ID NO: 37, ПОСЛ. ID NO: 38, ПОСЛ. ID NO: 39, ПОСЛ. ID NO: 40, ПОСЛ. ID NO: 41, ПОСЛ. ID NO: 42, ПОСЛ. ID NO: 43, ПОСЛ. ID NO: 44, ПОСЛ. ID NO: 45, ПОСЛ. ID NO: 48, ПОСЛ. ID NO: 49, ПОСЛ. ID NO: 50, ПОСЛ. ID NO: 51, ПОСЛ. ID NO: 52, ПОСЛ. ID NO: 53, ПОСЛ. ID NO: 54, ПОСЛ. ID NO: 55, и ПОСЛ. ID NO: 59. Специалист в данной области техники может оценить, что удобно иметь комплект, который состоит из более чем единственной пары праймера и может включать, например, один обратный праймер, такой как ПОСЛ. ID NO: 7, и несколько обратных праймеров. Таким образом, специально предусмотренными в настоящем документе являются наборы, включающие один или несколько прямых праймеров, которые специфически гибридизируются с АЛК дикого типа, 5-аминоимидазол-4-карбоксамид рибонуклеотидом формилтрансферазы/IMP циклогидролазы (ATIC), тяжелой цепью клатрина (CLTC), Ran-связывающим протеином 2 (RANBP2), SEC31L1, тропомиозином-3 (ТРМ3), тропомиозином-4 (ТРМ4), ТРК - слияния геном (большим) (TFGL), ТРК-слияния геном (малым) (TFGS), CARS, ALO17, моезином (MSN), геном тяжелой цепи немышечного миозина (MYH9), или ТРК - слияния геном (экстра большим) (TFGXL) и, по меньшей мере, один обратный праймер, где обратный праймер представляет собой АЛК дикого типа обратный праймер, такой как ПОСЛ. ID NO. 7, ПОСЛ. ID NO: 32, ПОСЛ. ID NO: 46, ПОСЛ. ID NO: 47. ПОСЛ. ID NO: 56, ПОСЛ. ID NO: 57 и ПОСЛ. ID NO: 58.
Понятно, что раскрытые наборы могут включать также элементы контроля для обеспечения правильного функционирования способов, описанных здесь и нормализации результатов между анализами. Так, например, описанными здесь, являются положительный кДНК контроль, негативный кДНК контроль и контрольные пары праймера. Например, раскрытые наборы могут включать контрольные пары праймера для обнаружения Homo sapiens АТР синтазы, Н+ транспортировки, митохондриального комплекса F1, О субъединицы (АТР50), ядерного гена, кодирующего митохондриальный белок мРНК; Homo sapiens NADH дегидрогеназы (убихинон) 1 альфа подкомплекса, 2, 8kDa (NDUFA2), мРНК; Homo sapiens глицеральдегид-3-фосфат дегидрогеназы (GAPDH), мРНК; Homo sapiens Н3 гистона, семьи 3А (H3F3A), мРНК; Homo sapiens протеасомы (просомы, макропейн) субъединицы, бета-тип, 4 (PSMB4), мРНК; Homo sapiens рибосомного белка S27a (RPS27A), транскрипта вариант 1, мРНК; Homo sapiens эукариотического фактора инициации трансляции 4А, изоформы 2 (EIF4A2), мРНК; Homo sapiens рибосомного белка L18 (RPL18), мРНК; Homo sapiens аденозиндезаминазы, РНК-специфические (ADAR), транскрипт вариант 1, мРНК, или Homo sapiens цитохрома с-оксидазы субъединицы Vb (COX5B), мРНК. Примеры пар праймеров включают, но не ограничиваясь, пары праймеров, приведенные в таблице 1.
Кроме того, следует понимать, что указанные выше наборы могут включать также другие реагенты и материалы для выполнения раскрытых способов, такие как ферменты (например, полимеразы), буферы, стерильную воду, реакционные пробирки. Кроме того, наборы могут включать также модифицированные нуклеотиды, нуклеазо-устойчивые нуклеотиды, и/или меченые нуклеотиды. Кроме того, раскрытые наборы могут включать инструкции по выполнению способов, описанных здесь и программное обеспечение, делающее возможным расчет наличия АЛК мутаций.
С одной стороны, наборы изобретения могут включать достаточный материал для применения в одном анализе одновременно, или по отдельности способов для определения, содержит ли проба АЛК дикого типа, известное АЛК слияние, или ранее неизвестные АЛК слияния. Наборы могут также включать достаточный материал, для проведения контрольных реакций. Таким образом, описанными здесь, в одном аспекте, являются наборы, содержащие, положительную кДНК контрольную реакционную пробирку, отрицательную кДНК контрольную реакционную пробирку, контрольную реакционную пробирку праймера, реакционную пробирку, для обнаружения известных АЛК слияний, реакционную пробирку, для обнаружения АЛК дикого типа, и реакционную пробирку для выявления активности киназы.
В другой конфигурации, набор настоящего изобретения может быть использован для определения статуса АЛК - либо экспрессии дикого типа, гиперэкспрессии домена киназы, либо гиперэкспрессии мутации слияния - на основе измерений, выполненных по отношению к генам внутреннего контроля. Под генами внутреннего контроля, описанными в других разделах настоящего изобретения, понимаются гены, экспрессирующие стабильно и конститутивно независимые от клеточного цикла, развития или факторов окружающей среды. Таким образом, в одном аспекте, статус АЛК можно определить, используя уравнение АЛК (числитель) / внутренний контроль (знаменатель), где в результате частное представляет собой диапазон результатов, которые указывают либо на АЛК положительные или АЛК отрицательные тестируемые ткани, клеточные линии или другие образцы. С пониманием того, что определенные ткани экспрессируют транскрипты внутреннего контроля на разных уровнях, соотношение и частное определяется для указания АЛК положительного или отрицательного статуса, который будет установлен отдельно для каждого типа ткани и образца.
Композиции, описанные здесь, и композиции, необходимые для выполнения раскрытых способов, могут быть изготовлены любым способом, известным специалистам в данной области техники для данного реагента или соединения, если иное не отмечено особо.
Синтез нуклеиновой кислоты
Раскрытые нуклеиновые кислоты, такие как олигонуклеотиды, чтобы использоваться в качестве праймеров, могут быть изготовлены с использованием стандартных способов химического синтеза или могут быть получены с использованием ферментативных способов, или любым другим известным способом. Такие способы могут варьироваться от стандартного ферментативного переваривания с последующей изоляцией нуклеотидного фрагмента чисто синтетическими способами, например, с помощью способа цианоэтил фосфорамидита с использованием ДНК синтезатора Milligen or Beckman System IPlus (например, модель 8700 автоматизированного синтезатора Milligen-Biosearch, Берлингтон, МА или ABI Модель 380В).
ПРИМЕРЫ
Следующие примеры используются, чтобы предоставить обычным специалистам в этой области техники полное изобретение и описание того, как соединения, композиции, статьи, устройства и/или способы, формулы изобретения изготавливаются и оцениваются, и предназначены, чтобы быть чисто образцовыми и не предназначены для ограничения изобретения. Были предприняты усилия для обеспечения точности в отношении чисел (например, количество, температура и т.д.), но необходимо принимать во внимание некоторые ошибки и отклонения. Если не указано иное, части являются массовыми частями, температура указана в °С или является комнатной температурой, а давление представляет собой атмосферное или около того.
А. Пример 1: гены АЛК слияния при онкогематологических заболеваниях и солидных опухолями (анапластическая крупноклеточная лимфома, АЛК+ диффузная крупноклеточная В-клеточная лимфома, АЛК+системный гистиоцитоз, ВМО саркома, немелкоклеточный рак легкого, плоскоклеточный рак пищевода, рак молочной железы, рак толстого кишечника).
Хотя точечные мутации АЛК происходят в нейробластоме, так называемые "АЛК слияния" на самом деле представляют собой наиболее распространенные мутации этой тирозинкиназы (Фигура 1). Подмножества каждой из гематологических (происхождения системы крови) и солидных опухолей, перечисленных выше в заголовке, вызваны слияниями АЛК. В качестве одного примера следует отметить, что новый белок ЕМL4-АЛК слияния находят почти у 7% японских пациентов с немелкоклеточным раком легкого. Для проведения ОТ-ПЦР обнаружения последовательностей АЛК слияния, получают образцы тканей от субъекта с раком. мРНК извлекают из образцов тканей. ОТ-ПЦР реакция использует, по меньшей мере, один прямой праймер и обратный праймер. Фигура 2 демонстрирует примеры различного образования пар праймерами. Например, прямой праймер может быть внутриклеточным АЛК праймером (праймер 100) 5'ACTACTGCTTTGCTGGCAAGACCT (ПОСЛ. ID NO: 6); внеклеточным ЕМL4-АЛК слияния праймером (праймер 103) 5'TGTTCAAGATCGCCTGTCAGCTCT (ПОСЛ. ID NO: 3); внеклеточным NPM-АЛК слияния праймером (праймер 102); 5'TCTGTACAGCCAACGGTTTCCCTT (ПОСЛ. ID NO: 4); внеклеточным CTLC-АЛК слияния праймером (праймер 105) 5'GAGAGTGCTTTGGAGCTTGTCTGT (ПОСЛ. ID NO: 5); или внеклеточным дикого типа АЛК праймером из негомологичного региона (праймер 104) 5'TTCCTTCATCAGTCCACTGGGCAT (ПОСЛ. ID NO: 2). Обратный праймер может быть праймером 101: 5TCGTCCTGTTCAGAGCACACTTCA (ПОСЛ. ID NO: 7). В результате ОТ-ПЦР реакции получают продукты амплификации (т.е., ампликоны) с размерами, продемонстрированными в таблице 2.
В. Пример 2: Шаблонная реакция обмена и экстензии (TEER)
Шаблонная реакция обмена и экстензии (TEER) относится к классу способов, которые могут сравнить неизвестную или несеквенированную нуклеиновую кислоту с секвенированным шаблоном, чтобы определить, являются ли они идентичными. Она основана на том факте, что секвенирование продуктов являются уникальным для шаблона, из которого они сгенерированы. Раскрытые способы и композиции связаны с конкретными формами TEER.
Первоначально шаблонная реакция обмена и экстензии (TEER) была разработана для распознавания неизвестных зародышевых и соматических мутаций, присутствующих в гомозиготном или гетерозиготном состоянии. Эта реакция была продемонстрирована путем электрофореза в полиакриламидном геле с последующим хемилюминесцентным обнаружением. Процесс был преобразован в формат обнаружения на основе микротитрования. В формате микротитровального планшета, она имеет намного более высокую пропускную способность и может использоваться для быстрого обнаружения ДНК мутации до секвенирования ДНК. В качестве способа сканирования последовательности, она является пригодной для скрининга большого образца групп населения, где вероятность мутации в гене для данного образца была достаточно низкой. TEER быстро исследует те образцы и сигналы, которые содержат такие мутации, которые могут быть секвенированы для выявления мутаций.
TEER продемонстрировала обнаружение мутаций в формате микропланшета. Покрытые стрептавидином лунки микропланшетов используют, чтобы прикрепить биотинилированный продукт ПЦР к твердой фазе. Гомо и гетеродуплексные молекулы образуются в процессе гибридизации в твердой фазе. Каждый шаг процесса легко осуществляется в микротитровальном планшете, это значительно упрощает оперирование образцами и обработку информации.
С. Пример 3: Обнаружение вставок и делеций
TEER может легко обнаружить вставки и делеций. Эти мутации создают несоответствие в точке вставки/делеции или только 3' мутации (на цепочке удлинения дикого типа), где рамка последовательности смещается. Обнаружение этих мутаций может быть блокировано в областях, где присутствует длинное удлинение тех же нуклеотидов или повторяющиеся последовательности. Можно привести следующий пример, когда удлинение достаточно длинное, петля шпильки может начать формироваться таким образом, что вставка или делеция выдавливается и не может быть обнаружена. Вставки или делеций около середины этих удлинений являются более проблематичными для обнаружения, чем те, которые находятся на концах.
D. Пример 4: Обнаружение TEER отобранных мутаций ПЦР в режиме реального времени
Во время перемещения химии к микропланшетам, было очевидно, что TEER была выборочной для мутантного сигнала, более чем для нормального или дикого типа сигнала. Она генерировала сигнал от одного "мутанта" из 60 "нормальных" удлинений одного основания. Усиление сигнала гетеродуплекса более гомодуплекса не было существенным, примерно, 4-кратным, но предоставило доказательства того, что процесс работает. И это, наряду с необходимостью увеличения соотношения сигнал-шум микропланшетного обнаружения, чтобы определить, может ли ПЦР быть использована для амплификации таких мутаций, таким образом, чтобы она могла быть дополнительно охарактеризована при помощи секвенирования ДНК. Использование ПЦР для амплификации мутации, во-первых, позволяет быстрое и чувствительных обнаружение редких мутаций. Образцы, которые являются положительными могут быть секвенированы, чтобы определить местонахождение и идентифицировать мутацию. Каждое из 4 оснований нацелено в отдельной реакции так, чтобы каждое основание в последовательности являлось проанализированным. После того как TEER произошла, четыре продукта реакций из образца могут быть объединены вместе и проанализированы в одной реакции обнаружения ПЦР в режиме реального времени.
Первым шагом в TEER является шаблонный обмен. Амплифицированную с помощью ПЦР ДНК дикого типа, которая была модифицированна случайно в специфическом основании гибридизируют с амплифицированной ДНК из образца с потенциальной мутацией. Дуплексная ДНК имеет несоответствия на одном конце для предотвращения деградации с Ехо III, а другой конец имеет углубленный (с выемкой) 3'конец, чтобы позволить лигирование линкер-зонда для присоединения твердой фазы. Линкер гарантирует, что все цели гибридизируются с его комплементом, и что это представляет собой продукт удлинения на полную длину. Любые продукты неполного удлинения не будут лигированы и будут легко удалены из планшета с помощью обязательного промывания. Гетеродуплексную ДНК обрабатывают ферментами или химическими веществами, которые специфически расщепляют у модифицированного нуклеотида только в цепи дикого типа. Комплементарная цепь, потенциально содержащая мутации не затрагивается. Это создает подмножество абазических сайтов, представляющих каждое появление основания в последовательности. Это, по сути, лестница секвенирования, с меньшим количеством целевого основания, на интактном полнодлинном шаблоне.
Следующим шагом в TEER является реакция удлинения с нуклеотидами с экзонуклеазной устойчивостью. Здесь используются альфа-тионуклеотиды. Понятно и в данном документе рассматривается, что бор нуклеотиды, также могут быть использованы. Смесь трех альфа-тио дезоксинуклеотид трифосфатов (dNTP), которые представляют три возможные нуклеотидные мутации, используются в реакции удлинения с Thermosequenase. dNTP, соответствующие целевым основаниям отсутствуют. Для примера следует отметить, если бы тимин (через урацил) был целевым основанием, то удлинение нуклеотидов было бы альфа-тио dATP, dCTP, и dGTP.
Экзонуклеаза III может использоваться для выбора мутации. Продукты удлинения, ограниченные тионуклеотидами, представляют мутации и устойчивы к экзонуклеазе III. Незащищенный шаблон дикого типа деградирован.
Редактированная цепь дикого типа сейчас содержит копию мутации. По мере того, как полимераза удлиняет ДНК, она использует сдвиг нити, или 5' к 3' экзонуклеазу, зависящую от полимеразы, чтобы перейти к концу мутантного шаблона. Этот процесс высвобождает мутантный дуплекс из твердой фазы. Высвобожденная ДНК может быть перемещена из микропланшета непосредственно в реакцию ПЦР в режиме реального времени.
Выбранный мутантный шаблон амплифицируется специфическим использованием флуоресцентного прямого праймера и обратного праймера в режиме реального времени. Для примера, могут быть использованы SYBR зеленый краситель или флуорогенный праймер шпилька, который флуоресцирует только после того, как был удлинен таким праймером как LUX (Invitrogen, Carlsbad, CA). Использование внутренних гибридизационных зондов для ПЦР в режиме реального времени, таких как Taqman или двойных меченых ФРПЭ зондов не рекомендуется, поскольку сайт мутации является неизвестным.
Е. Пример 5: Проектирование и изготовление микроматрицы
В этом документе описание развитие диагностических микроматриц для идентификации специфических мутаций АЛК. Здесь раскрывается изготовление ДНК-микроматриц, состоящих из 47 уникальных элементов, которые способны выявить 12 возможных мутаций и АЛК дикого типа как внутренний контроль.
Эмпирически может осуществляться два сценария для оптимизации введения зонда нуклеиновой кислоты, включающего обратную транскрипцию или обратную транскрипцию и ПЦР (ОТ-ПЦР). In vitro осуществимость на основе точного обнаружения слияний и вариантов субклонированной АЛК может быть продемонстрированна из плазмидной конструкции, и с использованием различных мутантов АЛК слияния, содержащих человеческие клеточные линии рака, смешаные в различных соотношениях с клеточными линиями, которые содержат АЛК дикого типа. АЛК мутации могут быть идентифицированы в образцах биопсии при раке легких. Эта работа может включать проведение сопоставительных [оценочных] испытаний по сравнению с имеющимися диагностическими стандартами, анализом АЛК FISH и анти-АЛК иммуногистохимии (ИГХ).
1. Дизайн олигонуклеотидов
Была разработана стратегия по выявлению АЛК мутаций и ее субвариантов по выявлению уникальных 5' регионов партнеров АЛК слияния. В целом, стратегия была основана на обратной транскрипции и удлинении и/или амплификации из региона в пределах 3' внутриклеточного региона АЛК мРНК, через весь соединительный сайт, и в 5' части партнера слияния. Сгенерированная кДНК или амплифицированная ДНК являются пост-меченными ковалентно связанным флюорозондом и предназначены для введения в микроматрицу. Два зонда, комплементарные различным регионам в пределах 5' региона партнера слияния или АЛК кДНК, отпечатанные в трех экземплярах, служат микроматричной ДНК захвата. Положение гибридизации и обнаружение сигнала определяет наличие АЛК и/или АЛК мутаций и их экспрессию по сравнению с набором из десяти транскриптов внутреннего контроля для служебных действий, (Фигура 3 и Таблица 3).
AGATCGCATAAAGCA AGCAGTCAGGTCA (ПОСЛ. ID NO: 23)
Каждый синтезированный зонд был оптимизирован для температуры плавления 65°С и уникального региона гибридизации в пределах 5' партнера слияния или АЛК с помощью программы OLIGOANLYZER 3.1®. Температура плавления и приблизительная длина 30 нуклеотидов были отобраны на основе зарегистрированных оптимальных условий микроматриц. 5' монометокситритил С-6 амино линкер был добавлен к зондам с тем, чтобы сделать возможной их очистку и конъюгацию с подготовленными стеклянными слайдами. Этот линкер был выбран на основе химической оптимизации. Наконец, два зонда для каждого партнера АЛК слияния, в идеале в различных регионах партнера слияния, были синтезированы для обеспечения альтернативного способа идентификации в случае, если бы зонд был лишен возможности привязки к региону путем конформационных ограничений третичной структуры ДНК. Эти критерии были также применены к разработке внутреннего контроля.
ПЦР праймеры
Каждый синтезированный праймер был снова оптимизирован для теоретической температуры плавления 60°С и уникальных регионов в рамках 5' партнера слияния и 3' внутриклеточного домена АЛК с помощью программы OLIGOANLYZER 3.1®. Праймер, определенный как "Универсальный АЛК обратный праймер", служит общим праймером для шага обратной транскрипции. Другие перечисленные праймеры допускают последующие шаги ПЦР и амплификацию предполагаемых целей. Эти критерии были также применены к разработке внутреннего контроля.
Оптимизация ОТ-ПЦР праймеров
Праймеры для ОТ-ПЦР были оптимизированы для связывания Тm 60°С в целях создания предполагаемой ДНК-мишени. Эти праймеры были оптимизированы как отдельные реакции ампликона, однако, несколько или все они могут быть сгруппированы с целью позволить мультиплексирование предполагаемой ДНК-мишени. Фигура 4 демонстрирует гель-электрофорез целевых ДНК, амплифицированных из каждого варианта АЛК и слияния, представляющие интерес. Протокол ПЦР-амплификации, использует 35 циклов с температурой 95°С в течение 15 мин; 94°С в течение 30 сек; 52°С в течение 1 мин; 72°С в течение 1 мин; 72°С в течение 15 мин и 4°С.
Для специалиста в данной области техники будет очевидно, что различные модификации и вариации могут быть сделаны в настоящем изобретении, не выходя за пределы масштаба или духа изобретения. Другие варианты воплощения изобретения будут очевидны специалистам в данной области техники после рассмотрения спецификаций и применения на практике изобретения, раскрытого в настоящем документе. Предполагается, что спецификация и примеры приведены только в качестве образца; истинныей объем и сущность изобретения указаны в следующей формуле изобретения.
Понятно, что раскрытые способ и композиции не ограничиваются описанными конкретной методологией, протоколами и реактивами, так как они могут варьироваться. Также следует понимать, что терминология используется в настоящем документе только с целью описания конкретных вариантов воплощения изобретения и не предназначена для лимитирования объема настоящего изобретения, который будет ограничен только прилагаемой формулой изобретения.
На протяжении описания и формулы изобретения данной спецификации слово "содержать" и вариации этого слова, такие как "содержащий" и "включает в себя", означает "включая, но не ограничиваясь этим," и не предназначено для исключения, к примеру, других добавлений, компонентов, целых чисел или шагов. Специалистам в данной области будет понятно, или они будут иметь возможность убедиться, используя не более чем рутинные эксперименты, что многие эквиваленты специфических вариантов способов и композиций описаны в настоящем документе. Такие эквиваленты включены в нижеследующую формулу изобретения.
Материалы, использованные при экспертизе заявки
Babon JJ, McKenzie M, Cotton RG. Mutation detection using fluorescent enzyme mismatch cleavage with T4 endonuclease VII. Electrophoresis 1999; 20(6):1162-70.
Brow MA, Oldenburg MC, Lyamichev V, et al. Differentiation of bacterial 16S rRNA genes and intergenic regions and Mycobacterium tuberculosis katG genes by structure-specific endonuclease cleavage. J Clin Microbiol 1996; 34(12):3129-37.
Chen TJ, Boles RG, Wong LJ. Detection of mitochondrial DNA mutations by temporal temperature gradient gel electrophoresis. Clin Chem 1999; 45(8 Pt 1):1162-7.
Cotton RG, Rodrigues NR, Campbell RD. Reactivity of cytosine and thymine in single-base-pair mismatches with hydroxylamine and osmium tetroxide and its application to the study of mutations. ProcNatI Acad Sci U S A 1988; 85(12):4397-401.
Fodde R, Losekoot M. Mutation detection by denaturing gradient gel electrophoresis (DGGE). Hum Mutat 1994; 3(2):83-94.
Ganguly A, Prockop DJ. Detection of mismatched bases in double stranded DNA by gel electrophoresis. Electrophoresis 1995; 16(10): 1830-5.
Ganguly A, Rock MJ, Prockop DJ. Conformation-sensitive gel electrophoresis for rapid detection of single-base differences in double-stranded PCR products and DNA fragments: evidence for solvent-induced bends in DNA heteroduplexes. Proc Nati Acad Sci USA 1993; 90(21):10325-9.
Gleason ВС, Homick JL. J Clin Pathol 2008 Apr; 61(4):428-37.
Hacia JG. Resequencing and mutational analysis using oligonucleotide microarrays. Nat Genet 1999; 21(1 Suppl):42-7.
Hovig E, Smith-Sorensen B, Brogger A, Borresen AL. Constant denaturant gel electrophoresis, a modification of электрофорез в градиенте денатурирующего геля, in mutation detection. Mutat Res 1991; 262(1):63-71.
Labeit S, Lehrach H, Goody RS. A new method of DNA sequencing using deoxynucleoside alpha-thiotriphosphates. Dna 1986; 5(2):173-7.
Labeit S, Lehrach H, Goody RS. DNA sequencing using alpha-thiodeoxynucleotides. Methods Enzymol 1987; 155:166-77.
Lamant L et al.. Genes Chromosomes Cancer. 2003 Aug; 37(4):427-32
Li R, Morris SW, Med Res Rev. 2008 May; 28(3):372-412.
Lu AL, Hsu 1C. Detection of single DNA base mutations with mismatch repair enzymes. Genomics 1992; 14(2):249-55.
Mano H., Cancer Sci. 2008 Dec; 99(12):2349-55
Myers RM, Larin Z, Maniatis T. Detection of single base substitutions by ribonuclease cleavage at mismatches in RNA:DNA duplexes. Science 1985; 230(4731):1242-6.
Nagamine CM, Chan K, Lau YF. A PCR artifact: generation of heteroduplexes. Am J Hum Genet 1989; 45(2):337-9.
Nakamaye K.L, Gish G, Eckstein F, Vosberg HP. Direct sequencing of polymerase chain reaction amplified DNA fragments through the incorporation of deoxynucleoside alpha-thiotriphosphates. Nucleic Acids Res 1988; 16(21):9947-59.
Novack DF, Casna NJ, Fischer SG, Ford JP. Detection of single base-pair mismatches in DNA by chemical modification followed by electrophoresis in 15% polyacrylamide gel. Proc Nati Acad Sci USA 1986; 83(3):586-90.
Oldenburg MC, Siebert M; New Cleavase Fragment Length Polymorphism method improves the mutation detection assay. Biotechniques 2000; 28(2):351-7.
Orita M, Suzuki Y, Sekiya T, Hayashi K. Rapid and sensitive detection of point mutations and DNA polymorphisms using the polymerase chain reaction. Genomics 1989; 5(4):874-9.
Pincas H, Pingle MR, Huang J, et al. High sensitivity EndoV mutation scanning through real-time ligase proofreading. Nucleic Acids Res 2004; 32(19):e148.
Porter KW, Briley JD, Shaw BR. Direct PCR sequencing with boronated nucleotides. Nucleic Acids Res 1997; 25(8):1611-7.
Rudzki Z et al., Pol J Pathol. 2005;56(1):37-45 Takeuchi K et al., Clin Cancer Res. 2009 May 1; 15(9):3143-9
Winter E, Yamamoto F, Almoguera C, Perucho M. A method to detect and characterize point mutations in transcribed genes: amplification and overexpression of the mutant c-Ki-ras allele in human tumor cells. Proc Nati Acad Sci USA 1985; 82(22):7575-9.
Xiao W, Oefner PJ. Denaturing high-performance liquid chromatography: A review. Hum Mutat2001; 17(6):439-74.
Youil R, Kemper B, Cotton RG. Detection of 81 of 81 known mouse beta-globin promoter mutations with T4 endonuclease VII-the EMC method. Genomics 1996, 32:431-5.
































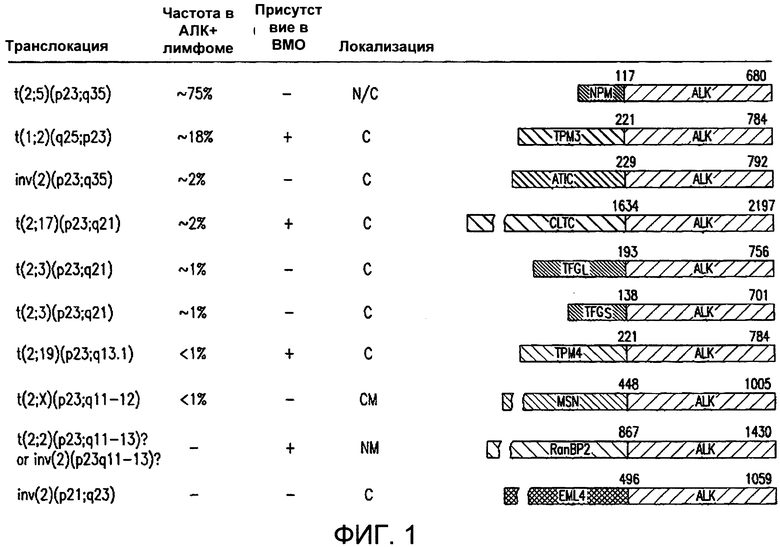
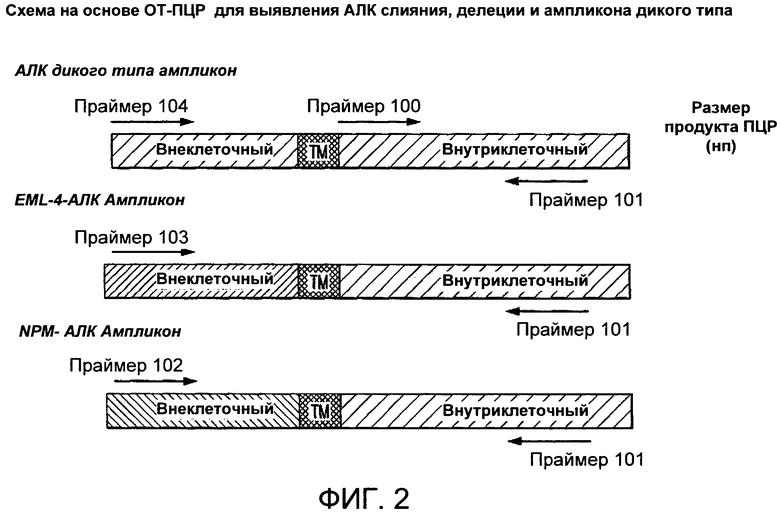
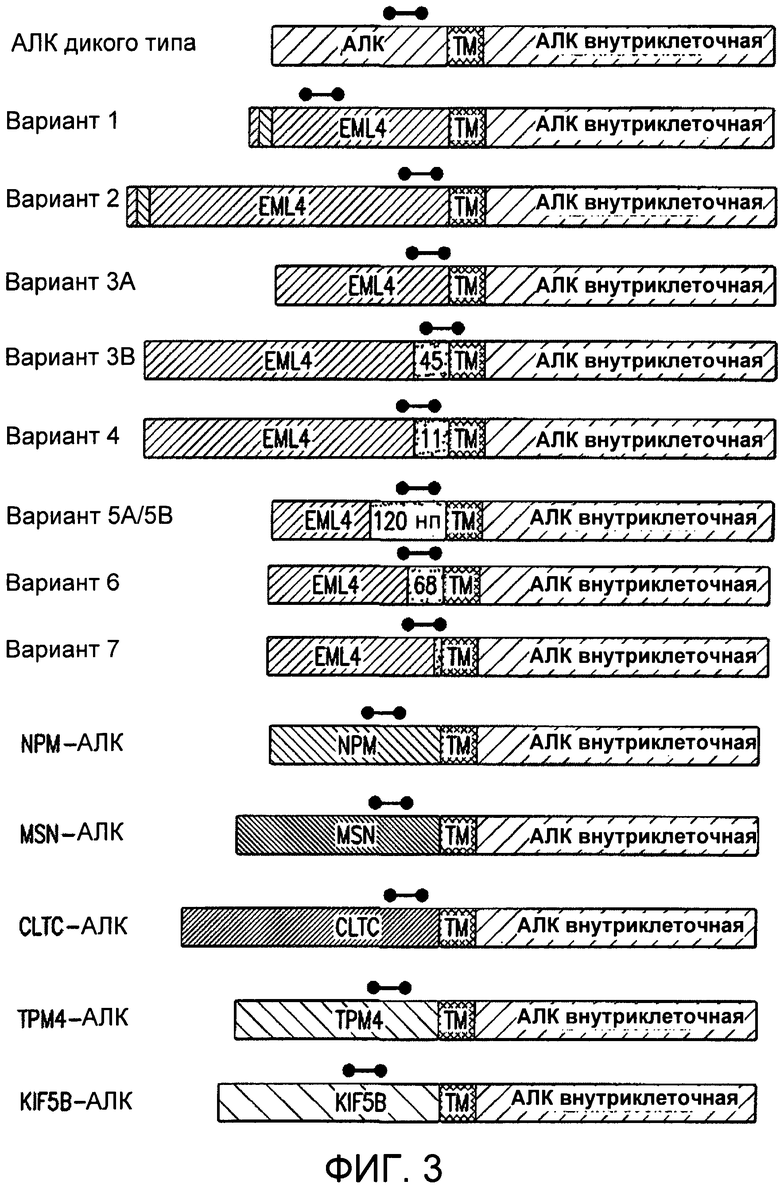
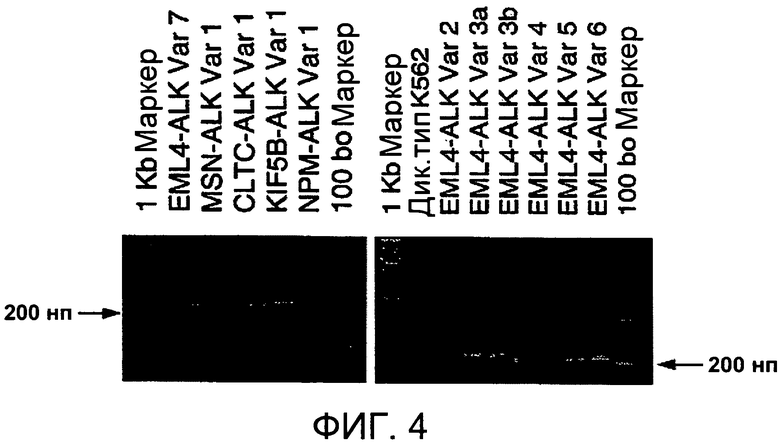
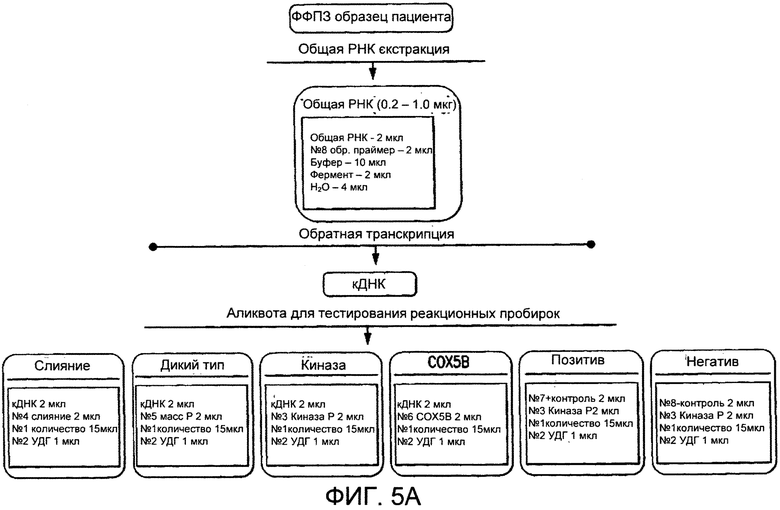
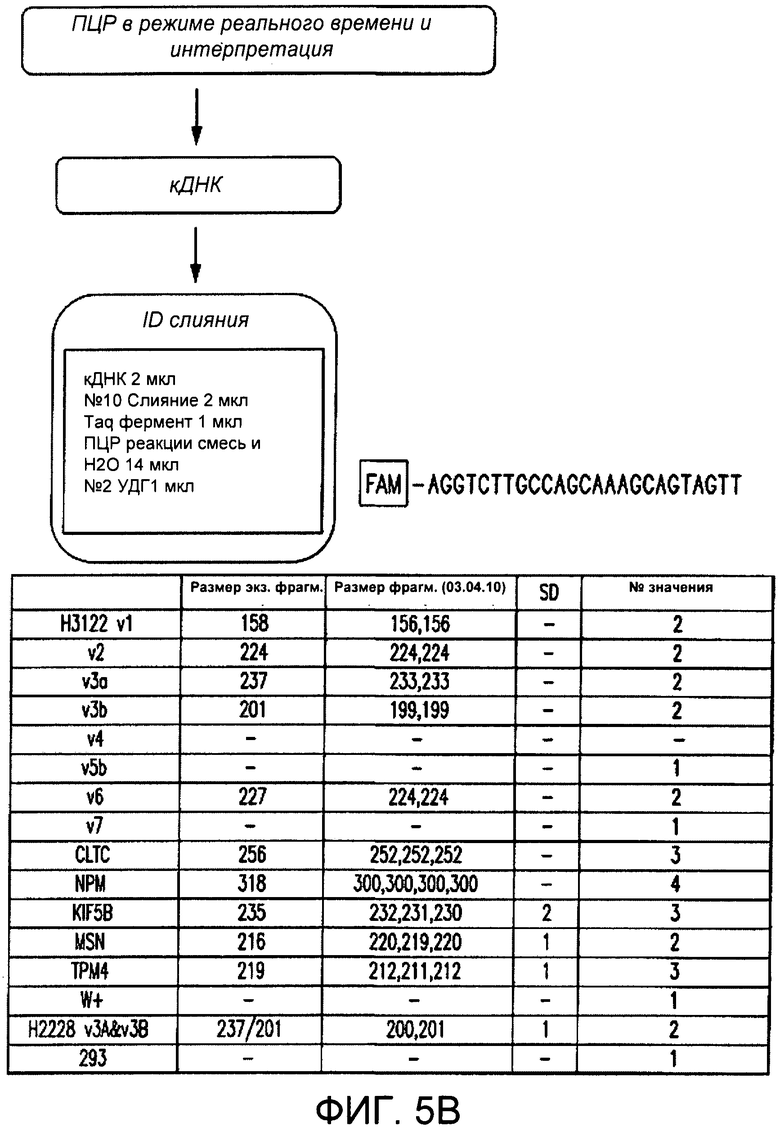
Изобретение относится к области биотехнологии. Раскрываются способы и композиции для определения наличия рака у субъекта и оценки эффективности лечения у него же. Раскрывается способ использования полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) и техники мультиплексной полимеразной цепной реакции, а также шаблонная реакция обмена и экстензии (TEER) для обнаружения наличия точечных мутаций, усечения или слияния киназы анапластической лимфомы. Предложенная группа изобретений может быть использована в медицине. 3 н. и 21 з.п. ф-лы, 6 ил., 3 табл., 5 пр.
1. Способ диагностики ракового заболевания, связанного со слиянием киназы анапластической лимфомы (АЛК) у субъекта, включающий проведение процесса амплификации нуклеиновых кислот из образца ткани от субъекта и обнаружение присутствия или измерение количества нуклеиновых кислот, ассоциированных с доменом АЛК дикого типа и киназным доменом АЛК дикого типа в образце ткани, где праймеры, используемые в процессе амплификации, состоят из праймеров, специфически гибридизующихся с АЛК дикого типа и киназным доменом АЛК дикого типа, при этом присутствие или повышение количества нуклеиновых кислот, ассоциированных с киназным доменом АЛК дикого типа, указывает на наличие ракового заболевания, связанного со слиянием АЛК у субъекта.
2. Способ по п. 1, в котором процесс амплификации нуклеиновых кислот представляет собой полимеразную цепную реакцию с обратной транскрипцией (ОТ-ПЦР) или ПЦР в реальном времени.
3. Способ по п. 2, в котором реакция ОТ-ПЦР или ПЦР в реальном времени включает пару, состоящую из прямого праймера и обратного праймера, которая специфически гибридизуется с АЛК дикого типа, и пару, состоящую из прямого праймера и обратного праймера, которая специфически гибридизуется с последовательностью киназного домена АЛК дикого типа.
4. Способ по п. 3, в котором по меньшей мере один обратный праймер представляет собой SEQ ID NO: 7, SEQ ID NO: 32, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 57, SEQ ID NO: 58 или SEQ ID NO: 66.
5. Способ по п. 3, в котором по меньшей мере один прямой праймер представляет собой SEQ ID NO: 2, SEQ ID NO: 6, SEQ ID NO: 31, SEQ ID NO: 33, SEQ ID NO: 45, SEQ ID NO: 48, SEQ ID NO: 54, SEQ ID NO: 55, SEQ ID NO: 65 или SEQ ID NO: 67.
6. Способ по п. 3, в котором по меньшей мере один прямой праймер гибридизуется с внеклеточной областью АЛК дикого типа.
7. Способ по п. 6, в котором прямой праймер представляет собой SEQ ID NO: 2, SEQ ID NO: 31, SEQ ID NO: 33, SEQ ID NO: 54, SEQ ID NO: 55 или SEQ ID NO: 65.
8. Способ по п. 2, в котором реакция ОТ-ПЦР или ПЦР в реальном времени включает прямой праймер, способный специфически гибридизоваться с доменом АЛК киназы.
9. Способ по п. 8, в котором прямой праймер представляет собой SEQ ID NO: 6, SEQ ID NO: 45, SEQ ID NO: 48 или SEQ ID NO: 67.
10. Способ по п. 1, в котором рак выбран из группы, состоящей из рака молочной железы, рака яичников, колоректального рака, немелкоклеточного рака легкого, диффузной крупноклеточной В-клеточной лимфомы, плоскоклеточного рака пищевода, анапластической крупноклеточной лимфомы, воспалительных миофибробластных опухолей, злокачественного гистиоцитоза и глиобластомы.
11. Способ по п. 10, в котором рак представляет собой колоректальный рак, который имеет одну или несколько АЛК-ассоциированных точечных мутаций, выбранных из группы, включающей R401Q, А1168Р и V757M.
12. Способ по п. 10, в котором рак представляет собой рак молочной железы, который имеет АЛК-ассоциированную точечную мутацию, причем точечная мутация представляет собой L560F.
13. Способ по п. 10, в котором рак представляет собой рак яичников, который имеет АЛК-ассоциированную точечную мутацию, причем точечная мутация представляет собой A877S.
14. Способ диагностики ракового заболевания, связанного со слиянием киназы анапластической лимфомы (АЛК) у субъекта, включающий проведение процесса амплификации нуклеиновых кислот из образца ткани от субъекта, где процесс амплификации нуклеиновых кислот состоит из обнаружения присутствия или измерения количества нуклеиновых кислот, ассоциированных с киназным доменом АЛК дикого типа в образце ткани, при этом присутствие или увеличение количества нуклеиновых кислот, ассоциированных с киназным доменом АЛК дикого типа, указывает на наличие ракового заболевания, связанного со слиянием АЛК у субъекта.
15. Способ определения присутствия слияния или гиперэкспрессии киназы анапластической лимфомы (АЛК) в образце ткани от субъекта-человека, у которого присутствует раковое заболевание, включающий получение образца ткани от субъекта, выделение нуклеиновых кислот из образца ткани, проведение полимеразной цепной реакции (ПЦР) с нуклеиновой кислотой, где ПЦР включает по меньшей мере один прямой и обратный праймер, который специфически гибридизуется с нуклеиновой кислотой, кодирующей киназный домен АЛК дикого типа, как показано в SEQ ID NO: 1, и определение присутствия или отсутствия киназного домена АЛК, где присутствие киназного домена АЛК указывает на наличие слияния или гиперэкспрессии АЛК.
16. Способ по п. 15, в котором прямой праймер выбран из группы, состоящей из SEQ ID NO: 6, SEQ ID NO: 45, SEQ ID NO: 48 и SEQ ID NO: 67.
17. Способ по п. 15, в котором обратный праймер выбран из группы, состоящей из SEQ ID NO: 7, SEQ ID NO: 32, SEQ ID NO: 46, SEQ ID NO: 47, SEQ ID NO: 57 и SEQ ID NO: 58.
18. Способ по п. 17, в котором прямой праймер представляет собой SEQ ID NO: 67, а обратный праймер представляет собой SEQ ID NO: 7.
19. Способ по п. 15, в котором дополнительно используется по меньшей мере один прямой праймер, который специфически гибридизуется с нуклеиновой кислотой, кодирующей внеклеточную область АЛК дикого типа, как показано в SEQ ID NO: 1.
20. Способ по п. 19, в котором прямой праймер, который специфически гибридизуется с нуклеиновой кислотой, кодирующей внеклеточную область АЛК дикого типа, выбран из группы праймеров, состоящей из SEQ ID NO: 2, SEQ ID NO: 31, SEQ ID NO: 33, SEQ ID NO: 54, SEQ ID NO: 55 и SEQ ID NO: 65.
21. Способ по п. 19, дополнительно включающий использование по меньшей мере одного обратного праймера, который специфически гибридизуется с нуклеиновой кислотой, кодирующей внеклеточную область АЛК дикого типа, как показано в SEQ ID NO: 1.
22. Способ по п. 22, в котором обратный праймер, который специфически гибридизуется с нуклеиновой кислотой, кодирующей внеклеточную область АЛК дикого типа, представляет собой SEQ ID NO: 66.
23. Способ по п. 15, в котором по меньшей мере один праймер представляет собой праймер-скорпион.
24. Способ по п. 15, в котором раковое заболевание выбрано из группы, состоящей из рака молочной железы, рака яичников, рака толстого кишечника, немелкоклеточного рака легкого, диффузной крупноклеточной В-клеточной лимфомы, плоскоклеточного рака пищевода, анапластической крупноклеточной лимфомы, воспалительных миофибробластных опухолей, злокачественного гистиоцитоза и глиобластомы.
| DIRKS W.G | |||
| et al., “Expression and functional analysis of the anaplastic lymphoma kinase (ALK) gene in tumor cell lines”, Int J Cancer | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| WO 2008127248 A1, 23.10.2008 | |||
| US 2008090776 A1, 17.04.2008 | |||
| US 2009055715 A1, 26.02.2009 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2015-09-10—Публикация
2010-05-17—Подача