ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] В данной заявке заявляется приоритет по предварительной заявке на патент США №62/083980, поданной 25 ноября 2014 г., описание которой включено в данный документ в полном объеме посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] В данном изобретении предложены стабилизированные композиции для офтальмологического применения, содержащие масла омега-3. Эти композиции могут быть эффективны, среди прочего, в качестве искусственных слез или в качестве композиций для офтальмологического применения для диагностирования, лечения или профилактики синдрома сухого глаза или кератоконъюнктивита у человека или другого млекопитающего, нуждающегося в таком диагностировании, лечении или профилактике.
УРОВЕНЬ ТЕХНИКИ
[0003] В изданной литературе часто упоминается о благоприятном воздействии масел омега-3 на здоровье глаз, а некоторые омега-3-жирные кислоты, как известно, являются важными компонентами глаза млекопитающего. См., например, Insight, Oct-Dec; 33 (4): 20-5 (2008). Большинство продуктов с маслами омега-3 разработаны в виде мягких или твердых желатиновых капсул, заполненных композициями на основе масел омега-3, которые предназначены для пероральной и системной доставки масел омега-3. На данный момент на рынке США нет коммерческих продуктов для офтальмологического применения, содержащих масла омега-3 для доставки на поверхность глаза. Эмульсии, как правило, являются предпочтительными лекарственными формами для доставки маслянистых компонентов на поверхность глаза, в которых масло диспергировано в водной фазе в виде капель, как правило, в субмикронном диапазоне, с использованием поверхностно-активных веществ и эмульгаторов.
[0004] Основным препятствием для разработки продукта для офтальмологического применения, содержащего масла омега-3, является химическая стабильность омега-3-компонентов, которые подвержены деградации за счет окисления и гидролиза. В публикациях патентов США №2007/0265341, 2008/0153909 и 2010/0305045, например, сообщается о нескольких композициях, содержащих масла омега-3, но не рассматривается вопрос о стабильности. В патенте США №2007/0265341 сообщается об использовании витамина Е в качестве антиоксиданта, но витамин Е не является эффективным для сохранения масел омега-3, как описано в данном документе. Таким образом, остается потребность в стабильных композициях для офтальмологического применения, содержащих масла омега-3.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] В данном изобретении предложены стабилизированные композиции для офтальмологического применения, содержащие масла омега-3 и один или более антиоксидантов. В частности, антиоксидант выбран из бутилированного гидроксианизола (БГА) и бутилированного гидрокситолуола (БГТ), по отдельности или в комбинации. Эти композиции можно использовать, среди прочего, в качестве искусственных слез или в качестве композиций для офтальмологического применения для диагностирования, лечения или профилактики кератоконъюнктивита или синдрома сухого глаза у человека или другого млекопитающего, нуждающегося в таком диагностировании, лечении или профилактике.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
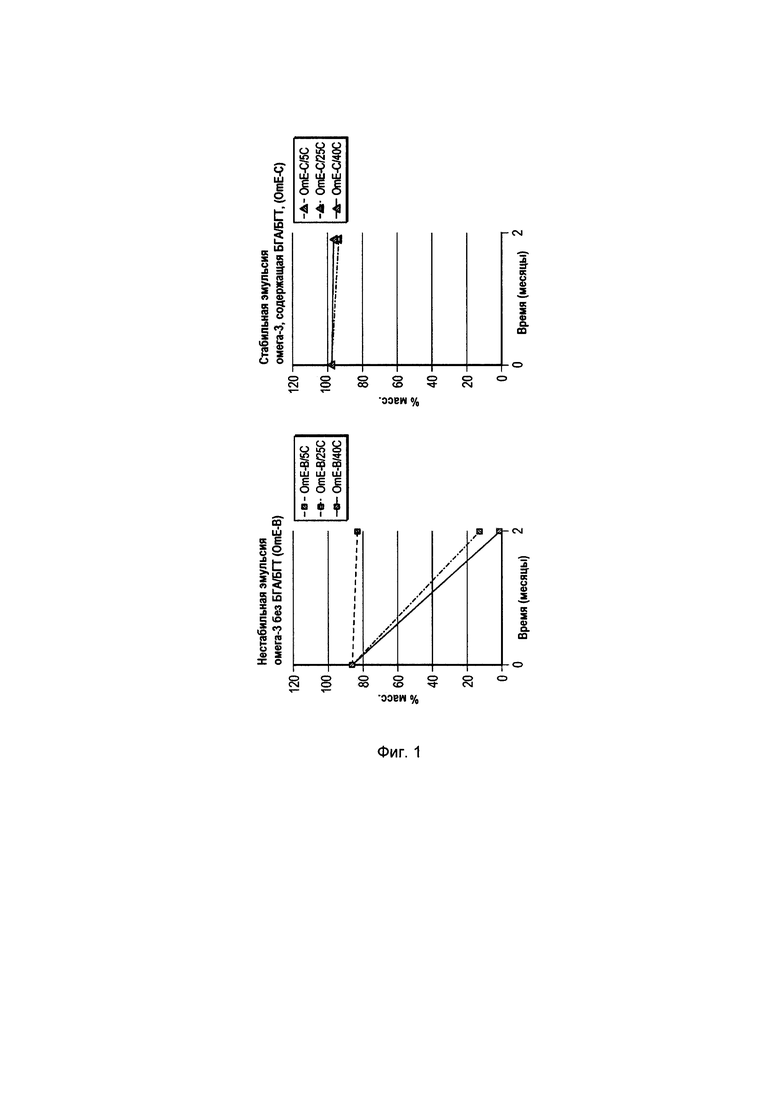
[0006] Фиг. 1 иллюстрирует повышение химической стабильности масел омега-3 в эмульсиях, содержащих БГА и БГТ, по сравнению с эмульсиями, содержащими масло омега-3 без БГА/БГТ.
[0007] Фиг. 2 иллюстрирует стабильность эмульсионного состава, содержащего льняное масло, с течением времени.
[0008] Фиг. 3 иллюстрирует результаты об in vivo переносимости эмульсий, содержащих масла омега-3.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0009] В данном изобретении предложены стабилизированные композиции для офтальмологического применения, содержащие масла омега-3 и один или более антиоксидантов. В частности, антиоксиданты выбраны из бутилированного гидроксианизола (БГА) и бутилированного гидрокситолуола (БГТ), по отдельности или в комбинации.
[0010] Бутилированный гидрокситолуол (БГТ) также известен как бутил гидрокситолуол, трет-бутилгидрокситолуол или 2,6-бис(1,1-диметилэтил)-4-метилфенол. Бутилированный гидроксианизол (БГА) также известен как бутилгидроксианизол или трет-бутилгидроксианизол. БГА обычно включает смесь 2-трет-бутил-4-гидроксианизола и 3-трет-бутил-4-гидроксианизола.
[0011] Авторы изобретения неожиданно обнаружили, что БГА, БГТ или их комбинации демонстрируют уникальное стабилизирующее действие на масла омега-3 по сравнению с другими известными антиоксидантами. Оценивали ряд композиций для офтальмологического применения, которые содержали антиоксиданты, с целью предотвратить деградацию масел омега-3. Типичной проблемой, связанной с маслами омега-3, является их склонность к деградации и прогорканию с течением времени. Неожиданно, много традиционно используемых антиоксидантов для масел, таких как аскорбилпальмитат, альфа-токоферол и витамин Е-ацетат, не продемонстрировали благоприятного влияния на защиту омега-3-компонентов от деградации. Еще более неожиданно, что в некоторых случаях эти антиоксиданты увеличивали скорости деградации масел омега-3. Установлено, что только БГА и БГТ обладают стабилизирующим влиянием на масла омега-3.
[0012] С применением этого стабилизирующего свойства БГА и БГТ было разработано несколько новых композиций составов для офтальмологических эмульсий, содержащих масла омега-3. Прототипы эмульсий разрабатывали с использованием ряда вспомогательных веществ, включая различные поверхностно-активные вещества, антиоксиданты и водные добавки. За физической и химической стабильностью этих прототипных составов следили в течение 3, 6 и/или 12 месяцев как в условиях ускоренного хранения, так и в условиях долгосрочного хранения. Установлено, что эмульсии, содержащие БГА и/или БГТ, были химически и физически стабильны в течение 3, 6 и/или 12 месяцев в условиях ускоренного и/или долгосрочного хранения. Добавление других маслорастворимых антиоксидантов, таких как витамин Е-ацетат, аскорбилпальмитат и альфа-токоферол, приводило к деградации масла омега-3, а также к изменению физических свойств эмульсий. Водорастворимые добавки, такие как ЭДТА, трегалоза и пируват, не влияли на стабильность эмульсий. Подробности этих исследований стабильности представлены в примерах в данном документе.
[0013] Композиции, представленные в данном документе, можно использовать, среди прочего, в качестве искусственных слез и/или в качестве композиций для офтальмологического применения для лечения сухости глаз или для диагностирования, лечения или профилактики кератоконъюнктивита или синдрома сухого глаза у людей или других животных. Композиции для офтальмологического применения, представленные в данном документе, могут также содержать один или более терапевтических агентов в дополнение к одному или более маслам омега-3.
[0014] В дополнение к маслам омега-3 и антиоксиданту, выбранному из БГА, БГТ и их смесей, композиции для офтальмологического применения, представленные в данном изобретении, могут содержать другие ингредиенты, пригодные для офтальмологического применения. Эти композиции также рассматриваются как офтальмологически приемлемые жидкости. Офтальмологически приемлемая жидкость включает жидкость, которая составлена так, что она является приемлемой для местного офтальмологического применения пациентом. Офтальмологически приемлемая жидкость может представлять собой раствор или эмульсию.
[0015] Для офтальмологического применения можно получить растворы или другие формы композиций/лекарственных препаратов, например, с использованием физиологического солевого раствора в качестве основного носителя. pH растворов или композиций для офтальмологического применения можно поддерживать в комфортном значении с применением подходящей буферной системы. Составы также могут содержать традиционные фармацевтически приемлемые консерванты, стабилизаторы и поверхностно-активные вещества.
[0016] В некоторых вариантах реализации изобретения композиция для офтальмологического применения, представленная в данном документе, содержит буферный агент. Буферный агент может меняться и может включать любую сопряженную слабую кислотно-основную пару для поддержания желаемого диапазона pH. Примеры включают, но не ограничиваясь ими, ацетатные буферные агенты, цитратные буферные агенты, фосфатные буферные агенты, боратные буферные агенты или их комбинацию. Для регулирования pH указанных составов при необходимости можно использовать кислоты или основания. Количество используемого буферного агента может быть различным. В некоторых вариантах реализации изобретения буферный агент может иметь концентрацию в диапазоне от около 1 нМ до около 100 мМ. pH буферного раствора можно увеличивать путем добавления NaOH или другого основания или уменьшать путем добавления HCl или другой кислоты. В некоторых вариантах реализации изобретения pH композиции может составлять от около 6,4 до около 7,8; от 6,8 до около 7,5; от 6,8 до около 7,4; от 6,8 до около 7,3; от 6,8 до около 7,2; от 6,9 до около 7,1; или около 6,8; около 6,9; около 7,0; около 7,1; около 7,2 или около 7,3.
[0017] Композиция для офтальмологического применения, представленная в данном документе, может содержать одно или более поверхностно-активных веществ. Поверхностно-активное вещество может изменяться и может включать любое вещество, которое является поверхностно-активным или может образовывать мицеллы. Поверхностно-активное вещество можно использовать для облегчения растворения вспомогательного вещества или активного агента, диспергирования твердого вещества или жидкости в композиции, усиления смачивания, изменения размера капель, стабилизации эмульсии или для ряда других задач. Пригодные поверхностно-активные вещества включают, но не ограничиваясь ими, поверхностно-активные вещества следующих классов: спирты; аминооксиды; блок-сополимеры; карбоксилированные этоксилаты спиртов или алкилфенолов; карбоновые кислоты/жирные кислоты; этоксилированные спирты; этоксилированные алкилфенолы; этоксилированные арилфенолы; этоксилированные жирные кислоты; этоксилированные сложные эфиры жирных кислот или масла (животные и растительные); сложные эфиры жирных кислот; этоксилаты метиловых эфиров жирных кислот; сложные эфиры глицерина; сложные эфиры гликоля; производные на основе ланолина; лецитин и производные лецитина; лигнин и производные лигнина; метиловые сложные эфиры; моноглицериды и их производные; полиэтиленгликоли; полимерные поверхностно-активные вещества; пропоксилированные и этоксилированные жирные кислоты, спирты или алкилфенолы; поверхностно-активные вещества на основе белков; производные саркозина; производные сорбитана; сложные эфиры сахарозы и глюкозы и их производные. В некоторых вариантах реализации изобретения поверхностно-активное вещество может включать полиэтиленгликоль(15)гидроксистеарат (№CAS 70142-34-6, доступен под названием Solutol HS 15® у BASF), блок-сополимер полиоксиэтилен-полиоксипропилен (№CAS 9003-11-6, доступен под названием Pluronic® F-68 у BASF), полиоксиэтилен(40)стеарат (ПОЭ(40)стеарат), полисорбат 80 или полиоксиэтилен(80)сорбитанмоноолеат (№CAS 9005-65-6), сорбитанмоностеарат (№CAS 1338-41-6, доступен под названием Span™ 60 у Croda International PLC), полиоксиэтиленглицеринтририцинолеат 35 (№CAS 61791-12-6, доступен под названием Cremophor EL® у BASF). Количество поверхностно-активного вещества может быть различным. В некоторых вариантах реализации изобретения количество любого поверхностно-активного вещества, такого как перечисленные выше, может составлять от около 0,001 до около 5%, от около 0,1% до около 2% или от около 0,1% до около 1%.
[0018] Композиция для офтальмологического применения, представленная в данном документе, может содержать один или более агентов, изменяющих вязкость, включая класс полимерных гидрогелей. Примеры агентов, изменяющих вязкость, включают, но не ограничиваясь ими, карбоксиметилцеллюлозу (КМЦ) и ее соли, целлюлозные полимеры, такие как гидроксипропилметилцеллюлоза (ГПМЦ), алкилакрилатные сшитые полимеры, такие как сшитый полимер акрилата/С10-30 алкилакрилата (например, Pemulen™), поливинилпирролидон (ПВП), гиалуроновую кислоту (ГК) и ее соли, гидроксиэтилцеллюлозу (ГЭЦ), этилгидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, метилцеллюлозу, декстран 70, желатин, глицерин, полиэтиленгликоли, полисорбат 80, пропиленгликоль, повидон, карбомеры, поливиниловый спирт, альгинаты, каррагинаны, гуаровую камедь, камедь карайи, агаровую камедь, камедь бобов рожкового дерева, трагакантовую камедь и ксантановую камедь.
[0019] В некоторых вариантах реализации изобретения полимерный гидрогель выбран из КМЦ и ее солей, ГПМЦ, ПВП, ГЭЦ, ГК и ее солей и их смесей. В некоторых вариантах реализации изобретения полимерный гидрогель представляет собой КМЦ натрия.
[0020] В некоторых вариантах реализации изобретения агент, изменяющий вязкость, может представлять собой комбинацию полимерного гидрогеля и алкилакрилатного сшитого полимера, такого как сшитый полимер акрилата/С10-30 алкилакрилата. Pemulen™ TR-2 (Lubrizol Corporation, Виклифф, Огайо) представляет собой имеющийся в продаже сшитый полимер акрилата/С10-30 алкилакрилата. В некоторых вариантах реализации изобретения количество сшитого полимера акрилата/С10-30 алкилакрилата составляет от около 0,5% до около 1,5%; или от около 0,8% до около 1,2%; или от около 0,9% до около 1,1%; или около 1,0%.
[0021] Композиция для офтальмологического применения, представленная в данном документе, может содержать один или более агентов, регулирующих тоничность. Агент, регулирующий тоничность, может изменяться и может включать любое соединение или вещество, которое пригодно для регулирования тоничности жидкости для офтальмологического применения. Примеры включают, но не ограничиваясь ими, соли, в частности, хлорид натрия, хлорид калия, хлорид магния и хлорид кальция; многоатомные спирты и сахара, такие как глицерин (глицерол), пропиленгликоль, эритрит, маннит, сорбит и трегалоза; аминокислоты, такие как карнитин (например, левокарнитин или L-карнитин) и бетаин; или любой другой подходящий офтальмологически приемлемый регулятор тоничности. Количество агента, регулирующего тоничность, может изменяться в зависимости от того, какая жидкость необходима: изотоническая, гипертоническая или гипотоническая. В некоторых вариантах реализации изобретения количество агента, регулирующего тоничность, такого как перечисленные выше, может составлять по меньшей мере от около 0,001% до около 1%, около 2% или около 5%. В некоторых вариантах реализации изобретения количество каждого агента, регулирующего тоничность, составляет около 0,125%, около 0,25%, около 0,4%, около 0,5%, около 0,6%, около 0,75%, около 1,0%, около 1,25%, около 1,5%, около 1,75% или около 2,0%.
[0022] В некоторых вариантах реализации изобретения агенты, регулирующие тоничность, используются в данном изобретении для получения практически изотонических или слегка гипотонических офтальмологически приемлемых композиций. В некоторых вариантах реализации изобретения осмолярность композиции составляет от 150 до 450 мосмоль/кг; от 250 до 330 мосмоль/кг; от 270 до 310 мосмоль/кг; или около 240 мосмоль/кг.
[0023] Композиция для офтальмологического применения, представленная в данном документе, может содержать один или более комплексообразующих агентов. Комплексообразующий агент может изменяться и может включать любое соединение или вещество, которое способно образовывать комплекс с металлом. Пригодный комплексообразующий агент представляет собой этилендиаминтетраацетат динатрия (ЭДТА), хотя вместо него или вместе с ним могут быть использованы также другие комплексообразующие агенты.
[0024] Хотя обычно растворы для офтальмологического применения содержат противомикробные консерванты, композиции, представленные в данном документе, не содержат такие консерванты. Примеры таких исключенных консервантов включают, но не ограничиваясь ими, катионные консерванты, такие как четвертичные аммониевые соединения, включая бензалкония хлорид, поликвад и тому подобное; консерванты на основе гуанидина, включая ПГМБ, хлоргексидин и тому подобное; хлорбутанол; ртутные консерванты, такие как тимеросал, ацетат фенилртути и нитрат фенилртути; и окисляющие консерванты, такие как стабилизированные оксихлоркомплексы (например, Purite®).
[0025] Композиции, представленные в данном документе, могут представлять собой водные растворы или эмульсии или некоторые другие приемлемые жидкие формы. В случае эмульсии в дополнение к маслам омега-3 в эмульсии можно использовать одно или более других масел. Пригодные масла включают, но не ограничиваясь ими, анисовое масло, касторовое масло, гвоздичное масло, кассиевое масло, коричное масло, миндальное масло, кукурузное масло, арахисовое масло, хлопковое масло, сафлоровое масло, маисовое масло, льняное масло, рапсовое масло, соевое масло, оливковое масло, тминное масло, розмариновое масло, масло земляного ореха, масло перечной мяты, подсолнечное масло, эвкалиптовое масло, сезамовое масло и тому подобное. В некоторых вариантах реализации изобретения дополнительное масло представляет собой касторовое масло.
[0026] Конкретные масла омега-3 включают, но не ограничиваясь ими, масла растительного происхождения, такие как масло семян льна (радиола или linum usitatissimum), чиа (шалфей испанский или salvia hispanica), киви (китайский крыжовник или actinidia chinensis), периллы (шисо или perilla frutescens), брусники (vaccinium vitis-idaea), рыжика (рыжик посевной или camelina sativa), портулака (портулак огородный или portulaca oleracea) и малины западной (rubus occidentalis); и жиры холодноводных рыб, такие как жир печени трески, лососевый жир, анчоусный жир и тунцовый жир. В некоторых вариантах реализации изобретения масло омега-3 представляет собой льняное масло.

[0028] Любая из композиций, представленных в данном документе, может содержать в качестве «масла омега-3» одну из омега-3-кислот из Таблицы 1 или их смесь, как из синтетических источников, так и выделенную из природного масла.
[0029] В Таблице 2 приведены примеры масла семян растений, которые можно использовать как источник омега-3-компонентов. Для эмульсионных составов в качестве источников масла омега-3 можно использовать одно или более масел, представленных в Таблице 2.

[0031] В конкретных вариантах реализации изобретения композиции для офтальмологического применения, представленные в данном документе, содержат одно или более масел омега-3, касторовое масло, БГТ и/или БГА, один или более гидрогелей, один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата и не содержат противомикробный консервант.
[0032] В других вариантах реализации изобретения композиции для офтальмологического применения, представленные в данном документе, содержат льняное масло, касторовое масло, БГТ и/или БГА, один или более гидрогелей, один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата и не содержат противомикробный консервант.
[0033] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло, касторовое масло, БГТ, один или более гидрогелей, один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата, причем композиция не содержит противомикробный консервант.
[0034] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло, касторовое масло, БГА, один или более гидрогелей, один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата, причем композиция не содержит противомикробный консервант.
[0035] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло, касторовое масло, БГТ, БГА, один или более гидрогелей, один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата, причем композиция не содержит противомикробный консервант.
[0036] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА; КМЦ или ее соль; один или более агентов, регулирующих тоничность, одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0037] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА, КМЦ или ее соль; один или более агентов, регулирующих тоничность, выбранных из карнитина, глицерина, эритрита и трегалозы; одно или более поверхностно-активных веществ и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0038] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА, КМЦ или ее соль; один или более агентов, регулирующих тоничность, выбранных из карнитина, глицерина, эритрита и трегалозы; одно или более поверхностно-активных веществ, выбранных из полисорбата 80 и ПОЭ(40)стеарата и сшитый полимер акрилата/С10-30 алкилакрилата, причем композиция не содержит противомикробный консервант.
[0039] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА; КМЦ натрия; один или более агентов, регулирующих тоничность, выбранных из карнитина, глицерина, эритрита и трегалозы; одно или более поверхностно-активных веществ, выбранных из полисорбата 80 и ПОЭ(40)стеарата и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0040] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА, КМЦ натрия; один или более агентов, регулирующих тоничность, выбранных из карнитина, глицерина, эритрита и трегалозы; полисорбат 80; ПОЭ(40)стеарат и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0041] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА; КМЦ натрия; карнитин; глицерин; эритрит; трегалозу; буферный агент; полисорбат 80; ПОЭ(40)стеарат и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0042] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ и/или БГА; КМЦ натрия; карнитин; глицерин; эритрит; трегалозу; борную кислоту; полисорбат 80; ПОЭ(40)стеарат и сшитый полимер акрилата/С10-30 алкилакрилата; причем композиция не содержит противомикробный консервант.
[0043] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ, КМЦ натрия; карнитин; глицерин; эритрит; трегалозу; борную кислоту; полисорбат 80; ПОЭ(40)стеарат; сшитый полимер акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0044] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая льняное масло; касторовое масло; БГТ; БГА; КМЦ натрия; карнитин; глицерин; эритрит; трегалозу; борную кислоту; полисорбат 80; ПОЭ(40)стеарат; сшитый полимер акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0045] Когда в данном документе используется термин «около», понимают, что он охватывает приемлемый диапазон отклонений от приведенной величины. Специалистам в данной области техники понятно, что приемлемое отклонение зависит от области техники и конкретных условий для заданной величины. В некоторых вариантах реализации изобретения «около» включает +/-30%-е отклонение от представленной величины. В некоторых вариантах реализации изобретения «около» включает +/-25%-е отклонение от представленной величины. В некоторых вариантах реализации изобретения «около» включает +/-10%-е отклонение от представленной величины. В некоторых вариантах реализации изобретения «около» включает +/-5%-е отклонение от представленной величины. В некоторых вариантах реализации изобретения «около» включает +/-1%-е отклонение от представленной величины.
[0046] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 1% мас. льняного масла; от около 0,1% до около 1% мас. касторового масла; от около 0,001% до около 0,05% мас. БГТ; от около 0,001% до около 0,05% мас. БГА; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,1% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 0,5% до около 3% мас. трегалозы; от около 0,1% до около 2% мас. борной кислоты; от около 0,1% до около 2% мас. полисорбата 80; от около 0,1% до около 2% мас. ПОЭ(40)стеарата; от около 0,1% до около 1% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0047] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 1% мас. льняного масла; от около 0,1% до около 1% мас. касторового масла; от около 0,001% до около 0,05% мас. БГТ; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,1% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 0,5% до около 3% мас. трегалозы; от около 0,1% до около 2% мас. борной кислоты; от около 0,1% до около 2% мас. полисорбата 80; от около 0,1% до около 2% мас. ПОЭ(40)стеарата; от около 0,05% до около 1% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0048] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 0,5% мас. льняного масла; от около 0,1% до около 0,5% мас. касторового масла; от около 0,005% до около 0,02% мас. БГТ; от около 0,005% до около 0,02% мас. БГА; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,5% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 1% до около 2% мас. трегалозы; от около 0,25% до около 1% мас. борной кислоты; от около 0,25% до около 1% мас. полисорбата 80; от около 0,1% до около 1% мас. ПОЭ(40)стеарата; от около 0,05% до около 0,25% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0049] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 0,5% мас. льняного масла; от около 0,1% до около 0,5% мас. касторового масла; от около 0,005% до около 0,02% мас. БГТ; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,5% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 1% до около 2% мас. трегалозы; от около 0,25% до около 1% мас. борной кислоты; от около 0,25% до около 1% мас. полисорбата 80; от около 0,1% до около 1% мас. ПОЭ(40)стеарата; от около 0,05% до около 0,25% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0050] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 0,25% мас. льняного масла; от около 0,1% до около 0,25% мас. касторового масла; от около 0,005% до около 0,02% мас. БГТ; от около 0,005% до около 0,02% мас. БГА; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,5% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 1% до около 2% мас. трегалозы; от около 0,25% до около 1% мас. борной кислоты; от около 0,25% до около 1% мас. полисорбата 80; от около 0,1% до около 1% мас. ПОЭ(40)стеарата; от около 0,05% до около 0,25% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0051] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая от около 0,1% до около 0,25% мас. льняного масла; от около 0,1% до около 0,25% мас. касторового масла; около 0,02% мас. БГТ; от около 0,25% до около 1% мас. КМЦ натрия; от около 0,1% до около 0,5% мас. карнитина; от около 0,5% до около 2% мас. глицерина; от около 0,1% до около 0,5% мас. эритрита; от около 1% до около 2% мас. трегалозы; от около 0,25% до около 1% мас. борной кислоты; от около 0,25% до около 1% мас. полисорбата 80; от около 0,1% до около 1% мас. ПОЭ(40)стеарата; от около 0,05% до около 0,25% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0052] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая по существу около 0,125% мас. льняного масла; около 0,125% мас. касторового масла; от около 0,005% до около 0,02% мас. БГТ; от около 0,005% до около 0,02% мас. БГА; около 0,5% мас. КМЦ натрия; около 0,25% мас. карнитина; около 1% мас. глицерина; около 0,25% мас. эритрита; около 1,5% мас. трегалозы; около 0,6% мас. борной кислоты; около 0,5% мас. полисорбата 80; от около 0,25% до около 0,5% мас. ПОЭ(40)стеарата; около 0,1% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
[0053] В одном варианте реализации в данном изобретении предложена композиция для офтальмологического применения, содержащая, по существу, около 0,125% мас. льняного масла; около 0,125% мас. касторового масла; около 0,02% мас. БГТ; около 0,5% мас. КМЦ натрия; около 0,25% мас. карнитина; около 1% мас. глицерина; около 0,25% мас. эритрита; около 1,5% мас. трегалозы; около 0,6% мас. борной кислоты; около 0,5% мас. полисорбата 80; от около 0,25% до около 0,5% мас. ПОЭ(40)стеарата; около 0,1% мас. сшитого полимера акрилата/С10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
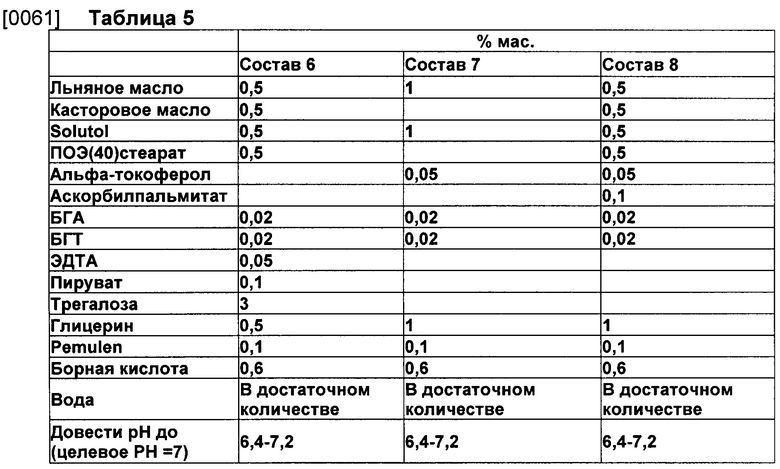
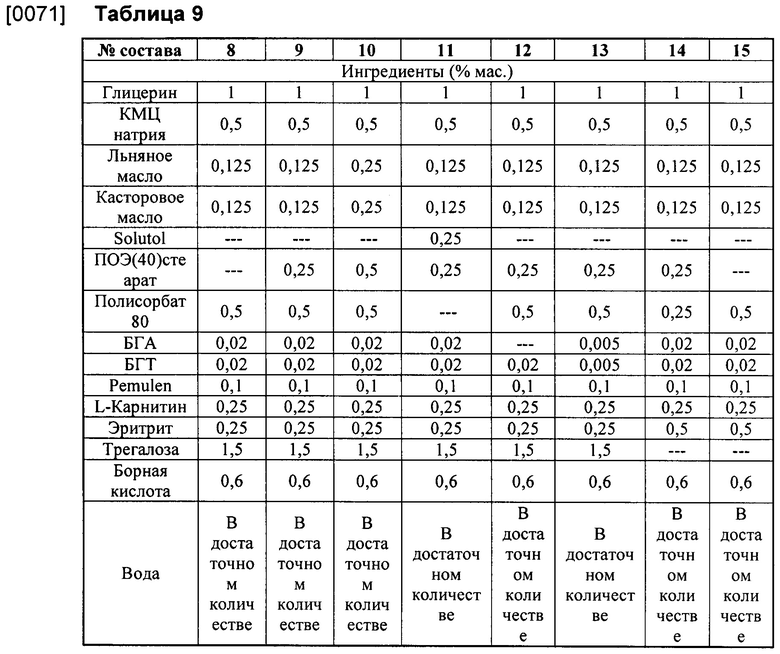
[0054] В других вариантах реализации изобретения композиция для офтальмологического применения содержит, состоит, по существу, из или состоит из конкретных типовых эмульсий, представленных в Таблицах 3-10 ниже. В каждом случае массовая доля может быть приблизительной, что означает, что каждый ингредиент присутствует в количестве около указанной массовой доли (т.е. массовая доля может изменяться на величины, определенные в данном документе словом «около»). В других вариантах реализации изобретения представленная массовая доля именно такая, как указана.
[0055] В Таблице 3 перечислены конкретные композиции, содержащие льняное масло (иначе называемое маслом из семян льна) в качестве источника омега-3-жирных кислот. Было установлено, что эти композиции демонстрируют превосходную химическую и физическую стабильность. Другие композиции с хорошей химической/физической стабильностью представлены в примерах ниже.


ПРИМЕРЫ
[0057] Следующие неограничивающие примеры представлены для иллюстративных целей. Каждый пример представляет по меньшей мере один вариант реализации изобретения, представленный в данном документе.
[0058] Пример 1. Добавление БГА и БГТ в масляную фазу эмульсии, обозначенной как «состав 5», улучшает химическую стабильность масел омега-3 в указанных эмульсиях по сравнению с «составом 4», который не содержит БГА или БГТ. См. фиг. 1. В эмульсиях, не содержащих БГА и БГТ (OmE-В), которые хранили как при комнатной температуре, так и при 40°С, наблюдается деградация масел омега-3 в течение двух месяцев, тогда как те эмульсии, которые содержали БГА и БГТ (OmE-С), стабильны при всех трех температурах в течение этого периода. Композиция состава 4 и состава 5 представлена в Таблице 4 ниже.

[0060] Пример 2. Добавление БГА и БГТ в масляную фазу улучшало физическую стабильность масел омега-3 в эмульсии. Состав 6, содержащий только БГА/БГТ в масляной фазе, сохранял свой белый опалесцирующий вид при всех условиях хранения (5°С, 25°С и 40°С) в течение 3 месяцев, тогда как для эмульсий, содержащих α-токоферол и аскорбилпальмитат, в течение того же периода наблюдалось изменение цвета (составы 7 и 8). Установлено, что изменение цвета происходило вследствие химической деградации омега-3-жирных кислот. Данные показаны для образцов, хранившихся при 40°С в течение 3 месяцев.
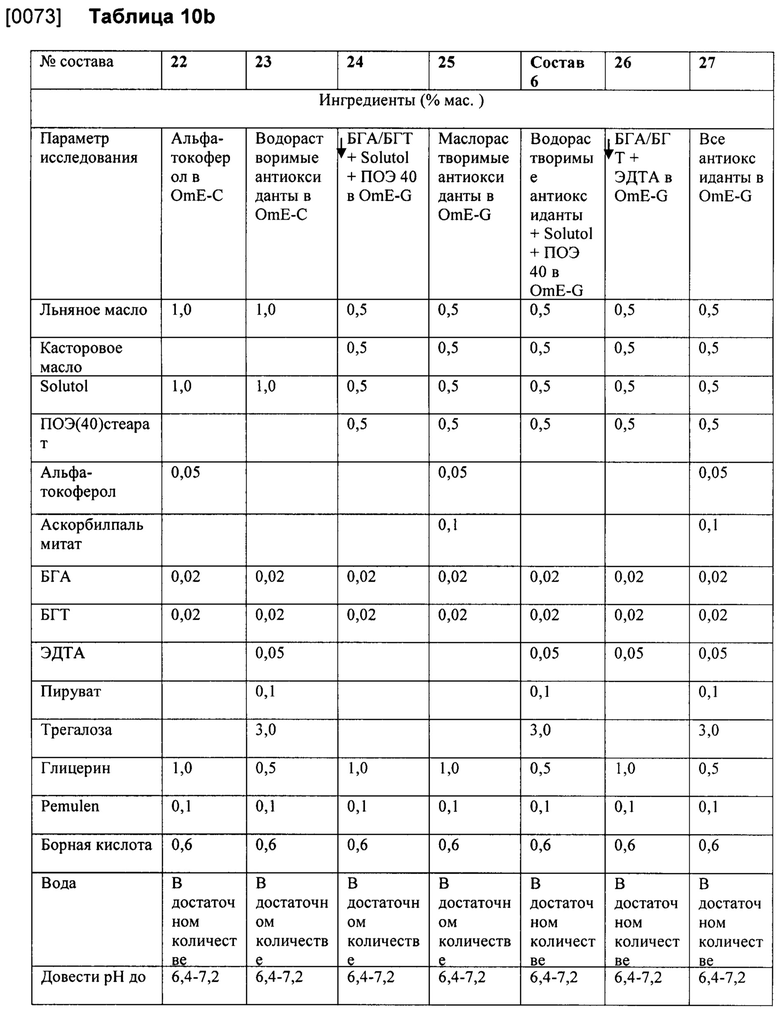
[0062] Пример 3. Включение вспомогательных веществ, которые, как сообщается в литературе, являются маслорастворимыми антиоксидантами, таких как альфа-токоферол и витамин Е-ацетат, неожиданно ухудшало химическую стабильность масел омега-3 в эмульсии. См. фиг. 2. Не наблюдалось значительного влияния водорастворимых добавок, таких как пируват или ЭДТА, на стабильность масел омега-3. Композиция каждой из исследованных эмульсий представлена в Таблице 10 в конце этих примеров.
[0063] Пример 4. Композиции составов были оптимизированы, чтобы выбрать ингредиенты, обеспечивающие максимальную стабильность композиций эмульсий, содержащих омега-3. Композиции двух типовых ключевых составов (состав 1 и состав 3) показаны в Таблице 6 ниже.

[0065] В Таблице 6 показана химическая/физическая стабильность типовых составов. Анализ льняного масла выполняли с помощью ЖХМС путем количественного определения триглицерида линоленовой кислоты (омега-3-компонент). Не наблюдалось значительной деградации триглицерида линоленовой кислоты, и все результаты были в пределах аналитической погрешности метода (±10%). Каждый из составов 1 и 3 оставался белого цвета/прозрачным без какого-либо изменения цвета, расслоения или отделения масла после хранения в течение 5 месяцев при 25°С и 40°С. См. Таблицу 6.
[0066] Пример 5. Для каждого из состава 1 и состава 3 выполняли анализ размера капель, чтобы дополнительно оценить стабильность омега-3-компонента. См. Таблицу 7 ниже. В течение трех месяцев наблюдений за стабильностью не наблюдалось изменений размера капель эмульсий. Эти результаты дополнительно подтверждают стабильность эмульсионных составов 1 и 3 и других подобных эмульсий на основе омега-3, содержащих БГТ и/или БГА.

[0068] Пример 6. Для того чтобы дополнительно оценить стабильность омега-3-компонентов в исследуемых составах, определяли рН и осмоляльность. См. Таблицу 8 ниже. Для исследуемых составов не наблюдалось никаких изменений в течение 3 месяцев наблюдений за стабильностью, что указывает на химическую и физическую стабильность эмульсий на основе омега-3.
[0069] Переносимость исследуемых эмульсий оценивали с использованием модели на кроликах. Было установлено, что составы 1 и 3 являются хорошо переносимыми. См. фиг. 3. Хотя каждая эмульсия была хорошо переносимой, состав 1 продемонстрировал наиболее низкий показатель дискомфорта in vivo, указывая на то, что данная эмульсия была особенно хорошо переносимой.


Способы лечения
[0074] В данном изобретении предложены способы диагностирования, лечения или профилактики кератоконъюнктивита или синдрома сухого глаза. Способы диагностирования, лечения или профилактики, описанные в данном документе, можно осуществлять путем местного нанесения композиции, представленной в данном документе, непосредственно на глаз или ткани, окружающие глаз.
[0075] Аномалии слезной пленки включают полный или частичный дефицит выработки слезной жидкости, известный как сухой кератоконъюнктивит, или СКК. Сухой кератоконъюнктивит, как правило, вызван недостаточной выработкой слезы. Слой слезной жидкости нарушен, что приводит к дефициту слезной жидкости или уменьшению секреции слез. Слезная железа не вырабатывает количество слезной жидкости, достаточное для полного покрытия всей конъюнктивы и роговицы. Это обычно происходит у людей, которые в остальном здоровы. Выработка слез уменьшается с возрастом. Это наиболее распространенный тип, который встречается у женщин после менопаузы. Причины включают идиопатические, врожденную алакремию, ксерофтальмию, удаление слезной железы и сенсорную денервацию. В редких случаях он может представлять собой симптом коллагеновых болезней, включая ревматоидный артрит, гранулематоз Вегенера и системную красную волчанку.
[0076] В относительно легких формах основной симптом сухого кератоконъюнктивита представляет собой ощущение постороннего предмета или легкое царапание. Это может прогрессировать в постоянное интенсивное жжение или ощущение раздражения, которое может быть изнуряющим для пациента. Более тяжелые формы могут приводить к развитию нитчатого кератита, болезненного патологического состояния, которое характеризуется появлением многочисленных нитей или волокон, прикрепленных к поверхности роговицы. Данные свидетельствуют, что эти волокна представляют разрывы в континууме нормальных эпителиальных клеток роговицы. Воздействие, возникающее при движении века, растягивает эти волокна, вызывая боль. Лечение этой стадии сухого кератоконъюнктивита является очень сложным.
[0077] Частым осложнением сухого кератоконъюнктивита является вторичная инфекция. По-видимому, происходит ряд нарушений в нормальных механизмах защиты глаза, которые, вероятно, связаны с уменьшением концентрации антибактериального лизоцима в слезной жидкости пациента, страдающего от сухого кератоконъюнктивита.
[0078] Хотя сухой кератоконъюнктивит может развиваться в отсутствие любой другой системной патологии, часто сухой кератоконъюнктивит связывают с системным заболеванием. Сухой кератоконъюктивит может являться частью большего системного патологического процесса, известного как синдром Шегрена. Обычно он состоит из сухости глаз, сухости во рту и артрита. Синдром Шегрена и аутоиммунные заболевания, связанные с синдромом Шегрена также являются патологическими состояниями, связанными с дефицитом слезной жидкости. Это патологическое состояние могут вызывать или ухудшать лекарственные средства, такие как изотретиноин, седативные средства, диуретические средства, трициклические антидепрессанты, гипотензивные средства, пероральные контрацептивы, антигистаминные средства, средства против заложенности носа, бета-блокаторы, фенотиазины, атропин и обезболивающие опиаты, такие как морфин. Также данное патологическое состояние может вызывать инфильтрация слезных желез при саркоидозе или опухолях или пострадиацинный фиброз слезных желез. Гистологически, при сухом кератоконъюнктивите (как часть синдром Шегрена или отдельно) первоначальные изменения, наблюдаемые в слезных железах, представляют собой фокальные инфильтраты из лимфоцитарных и плазматических клеток, связанные с разрушением ткани железы. Эти изменения напоминают те, которые наблюдаются при аутоиммунных заболеваниях в других тканях, что служит поводом для предположений о том, что сухой кератоконъюнктивит имеет аутоиммунную основу.
[0079] Сухой кератоконъюнктивит также может быть вызван аномальным составом слез, приводящим к быстрому испарению или преждевременному разрушению слез. Если он вызван быстрым испарением, его называют эвапоративным синдромом сухих глаз. При таком патологическом состоянии, хотя слезная железа вырабатывает достаточное количество слез, скорость испарения слез слишком высокая. Происходит потеря воды из слез, которая приводит к тому, что слезы становятся слишком «солеными» или гипертоническими. В результате конъюнктива и роговица не могут быть полностью покрыты слоем слезы во время некоторых видов деятельности или в некоторых условиях окружающей среды.
[0080] Как правило, симптомы сухости глаз могут быть вызваны старением, так как выработка слез имеет тенденцию уменьшаться с возрастом. Сухость глаз также может быть вызвана повреждением глаза, ожогами, диабетом или аденовирусами. Также сухость глаз может быть вызвана использованием контактных линз или хирургическим вмешательством на глазах.
[0081] Поэтому в некоторых вариантах реализации в данном изобретении предложены способы лечения сухого кератоконъюнктивита или синдрома сухого глаза у человека или другого млекопитающего с терапевтическими агентами или без них, который вызван любым одним или более вышеприведенными факторами или другими факторами, с использованием композиций для офтальмологического применения, описанных в данном документе. В некоторых вариантах реализации в данном изобретении предложены способы лечения сухого кератоконъюнктивита или синдрома сухого глаза у человека или другого млекопитающего с терапевтическими агентами или без них, который вызван любым одним или более вышеприведенными факторами или другими факторами, с помощью местного нанесения композиций для офтальмологического применения, описанных в данном документе.
[0082] Как предложено в настоящем документе, термин «лечение», при использовании в данном документе, относится к подходу (например, способу или режиму) для получения полезных или желаемых результатов, включая клинические результаты. «Лечение» заболевания, расстройства или патологического состояния означает, что степень или нежелательные клинические проявления заболевания, расстройства или патологического состояния, или и то и другое, снижены и/или динамика прогрессирования замедлена (т.е. растянута во времени) по сравнению с отсутствием лечения заболевания, расстройства или патологического состояния. В рамках способов, описанных в данном документе, полезные или желаемые клинические результаты включают, но не ограничиваясь ими, ослабление или уменьшение интенсивности одного или более симптомов (например, симптомов синдрома сухого глаза), уменьшение степени расстройства, стабилизацию (т.е. отсутствие ухудшения) состояния расстройства, задержку или замедление прогрессирования расстройства, ослабление или временное облегчение расстройства и ремиссию (частичную или полную), как явные, так и неявные.
[0083] Как предложено в настоящем документе, термины «эффективное количество», «терапевтически эффективное количество» и тому подобное в контексте композиций и способов, описанных в данном документе, в традиционном смысле относятся к количеству, которое достаточно для получения желаемого результата. Следовательно, терапевтически эффективное количество, применяемое при лечении, представляет собой количество, достаточное для уменьшения степени или нежелательных клинических проявлений заболевания, расстройства или патологического состояния, или и того и другого.
[0084] LASIK (лазерный кератомилез) и другие процедуры по коррекции зрения могут вызывать сухость глаз, после того, как с их помощью проникают через поверхность глаза и уменьшают чувствительность нервов роговицы. В некоторых случаях глаз затем не способен ощущать необходимость увлажнения, что приводит к недостаточной выработке слез. Следовательно, в данном изобретении предложены способы лечения сухости глаз, свойственной или вызванной хирургическим вмешательством на глазах. Хирургическое вмешательство на глазах включает, но не ограничиваясь ими, процедуры LASIK, экстракции лентикулы через малый разрез (SMILE) и хирургические процедуры при катаракте. См. Ocul. Surf., 8: 135-145 (2010); Ophthamology, 107: 2131-2135 (2000).
[0085] В одном варианте реализации изобретения способ лечения уменьшает интенсивность симптомов нарушения слезоотделения после LASIK. В другом варианте реализации изобретения способ лечения уменьшает интенсивность симптомов нарушения слезоотделения после хирургии катаракты. В другом варианте реализации изобретения способ лечения уменьшает интенсивность симптомов нарушения слезоотделения после хирургического вмешательства SMILE.
[0086] Термины в единственном числе и аналогичные термины, используемые в данном документе (особенно в контексте нижеследующей формулы изобретения), должны толковаться как охватывающие как единственное, так и множественное число, если в данном документе не указано иное, или это явно не противоречит контексту. Все описанные в данном документе способы могут быть осуществлены в любом подходящем порядке, если в данном документе не указано иное, или иное явным образом не противоречит контексту. Использование любых примеров или иллюстративной формы (например, «такой как») в данном документе предназначено только для лучшего раскрытия изобретения и не накладывает ограничений на объем любого пункта формулы изобретения. Ни одно выражение в описании не должно быть истолковано как указание на какой-либо незаявленный элемент, существенный для практического осуществления изобретения.
[0087] Группы альтернативных элементов или вариантов реализации изобретения, раскрытых в данном документе, не должны истолковываться как ограничения. Каждый член группы может быть указан и заявлен индивидуально или в любой комбинации с другими членами группы или другими элементами, находящимися в данном документе. Предполагается, что один или более членов группы могут быть включены в группу или удалены из нее из соображений удобства и/или патентоспособности. Когда происходит такое включение или удаление, считается, что описание содержит группу, модифицированную таким образом, что выполняется письменное описание всех групп Маркуша, используемых в прилагаемой формуле изобретения.
[0088] В заключение, следует понимать, что варианты реализации изобретения, описанные в данном документе, являются иллюстрацией принципов формулы изобретения. Другие модификации, которые могут быть использованы, находятся в рамках объема формулы изобретения. Таким образом, в качестве примера, а не ограничения, могут быть использованы альтернативные варианты реализации изобретения в соответствии с идеями, излагаемыми в данном документе. Соответственно, формула изобретения не ограничена вариантами реализации изобретения в точности, как они показаны и описаны.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ СУХОСТИ ГЛАЗА | 2012 |
|
RU2651046C2 |
| ИСКУССТВЕННЫЕ СЛЕЗЫ И ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2589837C2 |
| КОМПОЗИЦИИ ДЛЯ ЛИЧНОГО УХОДА, СОДЕРЖАЩИЕ ФУНКЦИОНАЛИЗИРОВАННЫЕ ПОЛИМЕРЫ | 2007 |
|
RU2420262C2 |
| КРЕМ-ГЕЛЬ, СОДЕРЖАЩИЙ ИВЕРМЕКТИН | 2005 |
|
RU2389494C2 |
| УСОВЕРШЕНСТВОВАННЫЙ ШАМПУНЬ ПРОТИВ ПЕРХОТИ | 1995 |
|
RU2154464C2 |
| ОЧИЩАЮЩИЕ КОМПОЗИЦИИ | 2008 |
|
RU2474413C1 |
| АНДРОГЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2012 |
|
RU2599036C2 |
| ТОПИЧЕСКИЕ КОСМЕТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ЦЕЛЛЮЛИТА | 2009 |
|
RU2478365C1 |
| СОСТАВ ДЛЯ ЭФФЕКТИВНОЙ ДОСТАВКИ ЛИПИДОВ В СЛЕЗНУЮ ПЛЕНКУ ЧЕЛОВЕКА С ИСПОЛЬЗОВАНИЕМ ЧУВСТВИТЕЛЬНОЙ К СОЛИ ЭМУЛЬСИОННОЙ СИСТЕМЫ | 2012 |
|
RU2772357C2 |
| КОМПОЗИЦИИ | 2015 |
|
RU2707282C2 |


Группа изобретений относится к фармацевтической промышленности, а именно к вариантам офтальмологической композиции и к способу лечения кератоконъюнктивита или синдрома сухого глаза путем введения человеку или другому млекопитающему эффективного количества предложенной офтальмологической композиции. В одном из вариантов композиция представляет собой эмульсию и содержит 0,1-1 мас.% льняного масла, 0,1-1 мас.% касторового масла, 0,001-0,05 мас.% бутилированного гидрокситолуола, 0,25-1 мас.% карбоксиметицеллюлозы натрия, 0,1-0,5 мас.% карнитина, 0,1-2 мас.% глицерина, 0,1-0,5 мас.% эритрита, 0,5-3 мас.% трегалозы, 0,1-2 мас.% борной кислоты, 0,1-2 мас.% полисорбата 80, 0,1-2 мас.% полиоксиэтилен(40)стеарата, 0,05-1 мас.% сшитого полимера акрилата/C10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант. В другом варианте предложена композиция с точечным содержанием указанных компонентов. В еще одном варианте композиция дополнительно содержит 0,001-0,05 мас.% бутилированного гидроксианизола. Группа изобретений обеспечивает стабилизированные составы на основе масел, являющихся источником омега-3-жирных кислот. 4 н. и 8 з.п. ф-лы, 6 пр., 10 табл., 3 ил.
1. Офтальмологическая композиция для лечения кератоконъюнктивита или синдрома сухого глаза, которая представляет собой эмульсию, содержащая около 0,125% мас. льняного масла, около 0,125% мас. касторового масла, около 0,02% мас. бутилированного гидрокситолуола (БГТ), около 0,5% мас. карбоксиметилцеллюлозы натрия (КМЦ натрия), около 1 мас.% глицерина, около 0,25% мас. карнитина, около 0,25% мас. эритрита, около 1,5% мас. трегалозы, около 0,25% мас. полиоксиэтилен(40)стеарата (ПОЭ(40)стеарат), около 0,5% мас. полисорбата 80, около 0,1% мас. сшитого полимера акрилата/C10-30 алкилакрилата, около 0,6% мас. борной кислоты и воду;
причем офтальмологическая композиция не содержит противомикробный консервант.
2. Офтальмологическая композиция по п. 1, отличающаяся тем, что композиция не содержит бутилированный гидроксианизол (БГА).
3. Офтальмологическая композиция по п. 1, содержащая 0,125% мас. льняного масла, 0,125% мас. касторового масла, 0,02% мас. БГТ, 0,5% мас. КМЦ натрия, 1% мас. глицерина, 0,25% мас. карнитина, 0,25% мас. эритрита, 1,5% мас. трегалозы, 0,25% мас. ПОЭ(40)стеарата, 0,5% мас. полисорбата 80, 0,1% мас. сшитого полимера акрилата/C10-30 алкилакрилата, 0,6% мас. борной кислоты и воду.
4. Офтальмологическая композиция по п. 1, состоящая из около 0,125% мас. льняного масла, около 0,125% мас. касторового масла, около 0,02% мас. БГТ, около 0,5% мас. КМЦ натрия, около 1% мас. глицерина, около 0,25% мас. карнитина, около 0,25% мас. эритрита, около 1,5% мас. трегалозы, около 0,25% мас. ПОЭ(40)стеарата, около 0,5% мас. полисорбата 80, около 0,1% мас. сшитого полимера акрилата/C10-30 алкилакрилата, около 0,6% мас. борной кислоты и воды в достаточном количестве до 100% мас.
5. Офтальмологическая композиция по п. 4, состоящая из 0,125% мас. льняного масла, 0,125% мас. касторового масла, 0,02% мас. БГТ, 0,5% мас. КМЦ натрия, 1% мас. глицерина, 0,25% мас. карнитина, 0,25% мас. эритрита, 1,5% мас. трегалозы, 0,25% мас. ПОЭ(40)стеарата, 0,5% мас. полисорбата 80, 0,1% мас. сшитого полимера акрилата/C10-30 алкилакрилата, 0,6% мас. борной кислоты и воды в достаточном количестве до 100% мас.
6. Офтальмологическая композиция для лечения кератоконъюнктивита или синдрома сухого глаза, которая представляет собой эмульсию, содержащая от около 0,1 до около 1% мас. льняного масла, от около 0,1 до около 1% мас. касторового масла, от около 0,001 до около 0,05% мас. БГТ, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,1 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 0,5 до около 3% мас. трегалозы, от около 0,1 до около 2% мас. борной кислоты, от около 0,1 до около 2% мас. полисорбата 80, от около 0,1 до около 2% мас. ПОЭ(40)стеарата, от около 0,05 до около 1% мас. сшитого полимера акрилата/C10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
7. Офтальмологическая композиция по п. 6, отличающаяся тем, что композиция содержит от около 0,1 до около 0,5% мас. льняного масла, от около 0,1 до около 0,5% мас. касторового масла, от около 0,005 до около 0,02% мас. БГТ, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,5 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 1 до около 2% мас. трегалозы, от около 0,25 до около 1% мас. борной кислоты, от около 0,25 до около 1% мас. полисорбата 80, от около 0,1 до около 1% мас. ПОЭ(40)стеарата и от около 0,05 до около 0,25% мас. сшитого полимера акрилата/C10-30 алкилакрилата.
8. Офтальмологическая композиция по п. 6, отличающаяся тем, что композиция содержит от около 0,1 до около 0,25% мас. льняного масла, от около 0,1 до около 0,25% мас. касторового масла, около 0,02% мас. БГТ, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,5 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 1 до около 2% мас. трегалозы, от около 0,25 до около 1% мас. борной кислоты, от около 0,25 до около 1% мас. полисорбата 80, от около 0,1 до около 1% мас. ПОЭ(40)стеарата и от около 0,05 до около 0,25% мас. сшитого полимера акрилата/C10-30 алкилакрилата.
9. Офтальмологическая композиция для лечения кератоконъюнктивита или синдрома сухого глаза, которая представляет собой эмульсию, содержащая от около 0,1 до около 1% мас. льняного масла, от около 0,1 до около 1% мас. касторового масла, от около 0,001 до около 0,05% мас. БГТ, от около 0,001 до около 0,05% мас. БГА, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,1 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 0,5 до около 3% мас. трегалозы, от около 0,1 до около 2% мас. борной кислоты, от около 0,1 до около 2% мас. полисорбата 80, от около 0,1 до около 2% мас. ПОЭ(40)стеарата, от около 0,1 до около 1% мас. сшитого полимера акрилата/C10-30 алкилакрилата и воду; причем композиция не содержит противомикробный консервант.
10. Офтальмологическая композиция по п. 9, отличающаяся тем, что композиция содержит от около 0,1 до около 0,5% мас. льняного масла, от около 0,1 до около 0,5% мас. касторового масла, от около 0,005 до около 0,02% мас. БГТ, от около 0,005 до около 0,02% мас. БГА, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,5 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 1 до около 2% мас. трегалозы, от около 0,25 до около 1% мас. борной кислоты, от около 0,25 до около 1% мас. полисорбата 80, от около 0,1 до около 1% мас. ПОЭ(40)стеарата и от около 0,05 до около 0,25% мас. сшитого полимера акрилата/C10-30 алкилакрилата.
11. Офтальмологическая композиция по п. 9, отличающаяся тем, что композиция содержит от около 0,1 до около 0,25% мас. льняного масла, от около 0,1 до около 0,25% мас. касторового масла, от около 0,005 до около 0,02% мас. БГТ, от около 0,005 до около 0,02% мас. БГА, от около 0,25 до около 1% мас. КМЦ натрия, от около 0,1 до около 0,5% мас. карнитина, от около 0,5 до около 2% мас. глицерина, от около 0,1 до около 0,5% мас. эритрита, от около 1 до около 2% мас. трегалозы, от около 0,25 до около 1% мас. борной кислоты, от около 0,25 до около 1% мас. полисорбата 80, от около 0,1 до около 1% мас. ПОЭ(40)стеарата и от около 0,05 до около 0,25% мас. сшитого полимера акрилата/C10-30 алкилакрилата.
12. Способ лечения сухого кератоконъюнктивита или синдрома сухого глаза у человека или другого млекопитающего, который включает введение эффективного количества офтальмологической композиции по любому из пп. 1-11 указанному человеку или другому млекопитающему.
| WO 2010106571 A2, 23.09.2010 | |||
| US 20100305045 A1, 02.12.2010 | |||
| Ruzhi Deng et al | |||
| Osmoprotectants suppress the production and activity of matrix metalloproteinases induced by hyperosmolarity in primary human corneal epithelial cells / Molecular Vision, September 2014, V.20, pp.1243-1252 | |||
| WO 2013090842 А2, 20.06.2013 | |||
| АППАРАТ ДЛЯ ПРИГОТОВЛЕНИЯ НАСТОЕВ, ДЕСТИЛЛЯЦИИ ВОДЫ, СТЕРИЛИЗАЦИИ РАСТВОРОВ И СНАБЖЕНИЯ ГОРЯЧЕЙ И ХОЛОДНОЙ ВОДОЙ | 1926 |
|
SU10437A1 |
Авторы
Даты
2019-08-21—Публикация
2015-11-23—Подача