Способ относится к области медицины и может быть использован для выявления группы больных раком молочной железы с экспрессией рецептора Her2/neu на мембране опухолевых клеток.
Выявление группы больных с гиперэкспрессией рецептора Her2/neu на мембране клеток рака молочной железы служит показанием для назначения этим больным лекарственного средства герцептин (трастузумаб), однако лечебное действие этого дорогостоящего препарата может отсутствовать или быть незначительно выраженным ввиду недостаточной чувствительности существующих методов оценки экспрессии Her2/neu раковыми клетками. Наиболее близким к заявляемому техническим решением является распространенный и стандартизованный способ иммуногистохимической диагностики Her2/neu-позитивного рака молочной железы по парафиновым блокам (Antonio C.W. et al. American Society of Clinical Oncology / College of American Pathologists Clinical Practice Guideline Update.: // Recommendation for Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer - 2014. - V. 138 - P. 241 - P. 256.).
Исследование проводится с использованием поли- или моноклональных антител. В настоящее время используются несколько типов антител: клон СВ11 (Novocastra, Ventana), TAB 250 (Zymed), кроличьи поликлональные антитела А0485 (DacoCytomation). Также для определения Her2/neu иммуногистохимическим методом используют кроличьи поликлональные антитела R60 и мышиные моноклональные антитела 10Н8. В то же время существует стандартный набор для определения Her2/neu - "HercepTest" (Dako), одобренный FDA в сентябре 1998 года для отбора пациентов, которым показано лечение трастузумабом. Набор включает кроличьи поликлональные антитела А0485 к рецептору Her2/neu. Антитела были получены путем иммунизации комплексом синтетического пептида, входящего в состав Her2/neu, и гемоцианина улитки. Пептид представляет собой часть онкобелка, кодируемого ERBB2 (мол. масса этого белка 185 kDa), называемого также HER2 или NEU. Антитело распознает эпитоп в цитоплазматической части мембраносвязанного с-erbB2 онкопротеина. Гиперэкспрессия с-erbB2 онкопротеина наблюдается в 25-30% рака молочной железы у человека (DAKO, Дания). Этот способ избран в качестве прототипа.
Прототип имеет следующие недостатки:
1. Оценка экспрессии антигена является полуколичественной как по проценту антиген-позитивных клеток, так и по уровням экспрессии антигена и выражается в баллах - 0, 1, 2, 3. 0 и 1 характеризуют отрицательную реакцию, 3 - положительную реакцию, при которой показано назначение с терапевтической целью гуманизированных моноклональных антител (герцептин, трастузумаб). Собственно для решения вопроса о целесообразности назначения герцептина и проводится иммуногистохимическое исследование экспрессии Her2/neu. В случаях, когда реакция оценивается на 2 балла, экспрессия оценивается как сомнительная, и требуются дополнительные исследования.
2. Иммуногистохимическая оценка Her2/neu с помощью HercepTest, оценивает цитоплазматическую детерминанту трансмембранного белка HER2, что позволяет лишь косвенно предполагать о наличии белка на мембране. Вместе с тем, терапевтические антитела распознают внеклеточную антигенную детерминанту рецептора. Герцептин связывает HER2 в С-концевой области домена IV. Область взаимодействия соответствует по площади 1,350  в виде длинного кармана и представляет собой необычайно высокую комплементарность формы (Lawrence М.С. et al, 1993) для взаимодействий антиген-антитело. Взаимодействие опосредуется тремя областями Her2 - петлями, сформированными аминокислотными остатками 557-561 и 570-573, а также основанием петли, сформированной остатками 593-603. Наибольшее значение во взаимодействии с Герцептином имеет 2-ая петля. Связывание Герцептина с юкстамембранной областью может существенно перекрестно связывать HER2 рецептор, что приводит к его усиленному эндоцитозу, в то же время предотвращая киназную активность рецептора за счет стерического барьера взаимодействий трансмембранных областей (Cho H.-S. et al., 2003). Следовательно, прямого соответствия того, что распознается иммуногистохимически и наличием мишени для антител нет.
в виде длинного кармана и представляет собой необычайно высокую комплементарность формы (Lawrence М.С. et al, 1993) для взаимодействий антиген-антитело. Взаимодействие опосредуется тремя областями Her2 - петлями, сформированными аминокислотными остатками 557-561 и 570-573, а также основанием петли, сформированной остатками 593-603. Наибольшее значение во взаимодействии с Герцептином имеет 2-ая петля. Связывание Герцептина с юкстамембранной областью может существенно перекрестно связывать HER2 рецептор, что приводит к его усиленному эндоцитозу, в то же время предотвращая киназную активность рецептора за счет стерического барьера взаимодействий трансмембранных областей (Cho H.-S. et al., 2003). Следовательно, прямого соответствия того, что распознается иммуногистохимически и наличием мишени для антител нет.
3. Недостатком прототипа также является необходимость проводить дополнительные исследования для подтверждения экспрессии HER2, среди которых наибольшее распространение получил метод FISH, который позволяет оценить амплификацию гена ERBB2. Данный метод, хотя и коррелирует с мембранной экспрессией HER2, но прямой информации об экспрессии белка на мембране не дает, а именно это необходимо для назначения Герцептина.
В заявленном способе решается задача повышения точности диагностики Her2/neu-позитивного рака молочной железы.
Задача решается тем, что антитела проверяют на предмет выявления антигена в заведомо антиген-позитивных случаях рака молочной железы методом проточной цитометрии, определяют рабочий титр антител; при окраске клеток для проточно-цитометрического определения HER2/neu используют наряду с FITC (флуоресцеин-изотиоцианат)-мечеными антителами к HER2/neu двойную и тройную флуоресцентную метку с целью исключения экспрессии антигена на лейкоцитах(CD45-PerCP) и подтверждения экспрессии антигена на эпителиальных клетках (CD326-PE); подсчитывают процент клеток позитивных по HER2/neu в гейте CD45-CD326+, указывают уровень экспрессии антигена на основании определения средней интенсивности флуоресценции по ранее проведенной калибровке; определяют мембранный эпитоп HER2, распознаваемый терапевтическими моноклональными антителами (герцептин, трастузумаб), оценивают количество антиген-позитивных клеток и уровней экспрессии мембранного антигена.
Способ осуществляется следующим образом.
1. Готовят флуоресцентно-меченый конъюгат гуманизированных антител против HER2/neu.
2. Антитела проверяют на предмет выявления антигена в заведомо антиген-позитивных случаях рака молочной железы методом проточной цитометрии. Определяют рабочий титр антител.
3. Для проведения проточно-цитометрического определения экспрессии антигена на опухолевых клетках фрагмент опухоли, удаленной в ходе хирургического вмешательства, переводят в суспензию клеток путем гомогенизации на приборе Medimashin (BD, USA), затем фильтруются через фильтры Partek (Германия) с диаметром пор 40 мкм.
4. При окраске клеток для проточно-цитометрического определения HER2/neu используют наряду с FITC (флуоресцеин-изотиоцианат)-мечеными антителами к HER2/neu двойную и тройную флуоресцентную метку с целью исключения экспрессии антигена на лейкоцитах(CD45-PerCP) и подтверждения экспрессии антигена на эпителиальных клетках (CD326-PE).
5. Сбор клеток осуществляют на проточном цитометре (типа FACScan). Собирается не менее 50000 событий.
6. С использованием программы WinMDI 2.8. подсчитывают процент клеток позитивных по HER2/neu в гейте CD45-CD326+, указывается уровень экспрессии антигена на основании определения средней интенсивности флуоресценции по ранее проведенной калибровке.
При отработке метода мы провели два вида сопоставлений:
1. Оценили возможность использования немеченых антител к HER2/neu с последующим докрашиванием флуоресцентно-мечеными IgG-антителами кролика против иммуноглобулинов человека при выявлении антигена на криосрезах.
2. Сопоставили метод проточной цитометрии с методом определения антигена на криостатных (свежезамороженных) срезах опухолевой ткани молочной железы.
3. Сравнили заявленный способ со стандартным иммуногистохимическим способом определения антигена.
Получены следующие выводы:
При использовании немеченых гуманизированных антител (герцептин) с последующим докрашиванием криостатных срезов FITC-мечеными кроличьими IgG в ряде случаев отмечается окраска соединительной ткани и сосудов за счет тканевых иммуноглобулинов человека, а также за счет Fc-рецептора. В этих случаях необходимо стандартное блокирование неспецифическго связывания. Неспецифического окрашивания опухолевых зон не отмечалось. В целом данный метод показал возможности использования гуманизированных антител к Her2/neu (Герцептин) для выявления мембранной экспрессии антигена-мишени на свежих срезах опухолевой ткани молочной железы, не подвергнутых фиксации и парафиновой заливке. Вместе с тем, использование немеченых антител имеет ряд ограничений: во-первых, необходимо использовать в ряде случаев блокирование неспецифического связывания FITC-меченых кроличьих антител, что удлиняет процедуру и требует отбора случаев, в которых блокирование показано. Во-вторых, использование немеченых антител невозможно при проведении проточно-цитометрических исследований, при которых стандартом является использование прямых конъюгатов.
По этим причинам в дальнейшей работе использовали прямые конъюгаты - FITC-меченые антитела трастузумаб. При использовании прямого метода иммунофлуоресценции с использованием FITC-меченых антител Герцептин на криостатных срезах отсутствовало неспецифическое связывание; визуализация антигена (HER2/neu) достаточно четкая, сигнал сильный. Лимитирующими параметрами при использовании данного метода, как и в случаях использования стандартного HercepTest, являются отсутствие точной количественной характеристики экспрессии антигена по числу позитивных клеток и уровням экспрессии HER2/neu. Метод определения антигена на криосрезах имеет преимущества перед стандартно-используемым иммуногистохимическим методом в том, что определяется мембранный антиген, а именно эпитоп, взаимодействующий с Герцептином.
При сравнении способа определения антигена по криосрезам и проточно-цитометрического способа определения HER2/neu на мембране клеток рака молочной железы, отмечено, что способы взаимно дополняют друг друга: метод проточной цитометрии позволяет количественно учитывать процент антиген-позитивных клеток, а также уровень экспрессии антигена на опухолевых клетках (MFI). В то же время метод прямой иммунофлуоресценции на криостатных срезах позволяет судить об экспрессии антигена на опухолевых клетках и оценивать антиген на инфильтративном компоненте. Оба способа имеют преимущества перед иммуногистохимией в том, что определяют мембранную экспрессию антигена - эпитоп, взаимодействующий с антителами Герцептин. Результаты исследования двумя способами (иммунофлуоресцентным по криосрезам и проточно-цитометрическим) практически полностью совпадали. Расхождение отмечено лишь в одном случае, в котором антиген был выявлен лишь проточной цитометрией (рассмотрено ниже).
Изобретение иллюстрируется фигурой 1 А-Г и таблицами 1 и 2.
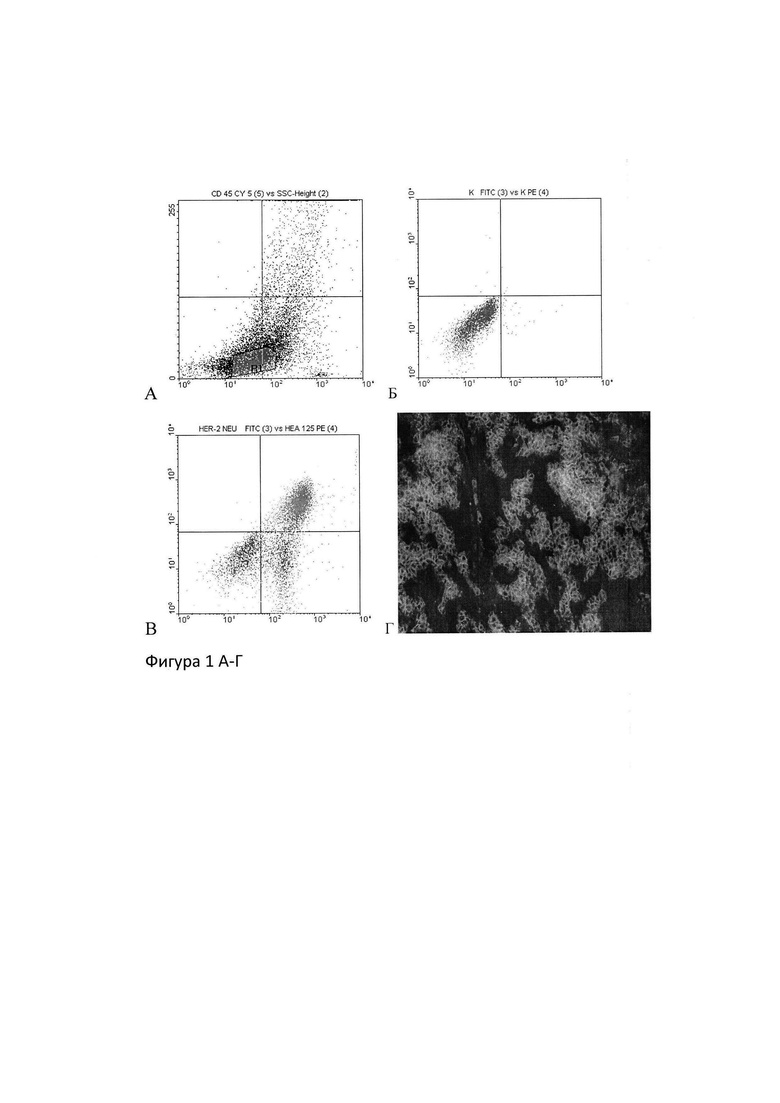
На фигуре 1 А-Г приведен пример экспрессии рецептора Her2/neu в люминисцентном методе и экспрессия антигена, вывляемого проточно-цитометрически.
Фигура 1.
А-В. Проточноцитометрическая оценка. А - выделение популяции клеток по характеристикам рассеяния света лазерного луча. Б - контрольное окрашивание (негативный контроль). В - экспрессия Her2/neu на опухолевых клетках (по оси абсцисс - уровни экспрессии Her2/neu, меченых FITC; по оси ординат - уровни экспрессии общеэпителиального антигена Egp34 (EpCam).
Г. Выявление антигена в иммунофлуоресцентном методе - положительные клетки окрашены черным цветом.
Результаты проведенной сравнительной оценки стандартного иммуногистохимического способа (Герцептест) и способа определения мембранной экспрессии антигена люминисцентным методом с использованием FITC-меченых антител трастузумаб представлены в таблице 1. В данной таблице наличие экспрессии в Герцептесте означает 3+, отсутствие - 0-2 (относительно случаев 2+) детальный анализ представлен в таблице 1.
Рассмотрим случаи несовпадения результатов. У 1 больной в иммунофлуоресцентном методе реакция отсутствовала - расценена как фоновая с наличием отдельных отчетливо позитивных клеток. У этой же больной для более точной оценки экспрессия антигена оценена проточно-цитометрическим методом. В этом случае 100% раковых клеток экспрессировали рецептор, однако, уровень экспрессии был достаточно низким (не на 3+). Данный пример иллюстрирует возможности проточно-цитометрической диагностики Her2/neu позитивного рака молочной железы. Вместе с тем, чувствительность люминисцентного метода оказалась недостаточной в сравнении с иммуногистохимией и проточной цитометрией.
Наибольший интерес представляет наблюдение, в котором иммунофлуоресцентный метод на криосрезах выявил положительную реакцию, а в иммуногистохимии экспрессия антигена была сомнительной (единственное наблюдение в нашей группе больных, в котором реакция иммуногистохимически была расценена на 2+). В этом случае у больной в иммунофлуоресцентом методе выявлялось 20% клеток, гиперэкспрессирующих (++++) на мембране Her2/neu. Проточно-цитометрическое определение рецептора в данном случае не проводили, так как к исследование проводили в непрямом иммунофлуоресцентном способе.
Сравнение предложенного проточно-цитометрического способа определения HER2/NEU со стандартным иммуногистохимическим приводится в таблице 2.
Сравнение способов указывает на высокое совпадение результатов, вместе с тем, во всех случаях заявляемый способ позволил подтвердить или, напротив, исключить экспрессию антигена.
ТЕХНИЧЕСКИЙ РЕЗУЛЬТАТ
Заявленный способ определения экспрессии HER2/neu имеет следующие преимущества перед прототипом. Во-первых, он позволяет определять мембранную экспрессию антигена. Во-вторых, выявляется тот же самый эпитоп, который выявляется терапевтическими антителами трастузумаб. В-третьих, определение проводится на нативных клетках без их повреждения фиксацией в формалине, парафиновой заливкой, поэтому «восстановления» антигена не требуется. Способ может быть особенно полезен при подтверждении наличия мембранной экспрессии антигена в случаях, расцененных иммуногистохимически как 2+, вместо дорогостоящего метода FISH-анализа.
Заявленный способ определения антигена на криосрезах имеет преимущества перед стандартно-используемым иммуногистохимическим методом в том, что определяется мембранный антиген, а именно эпитоп, взаимодействующий с Герцептином.

Совпадение методов достоверное: Хи-квадрат = 10,5; р=0,001.

Совпадение методов достоверное: Хи-квадрат = 15,0; р=0,000.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения прогноза эффективности терапии рака молочной железы | 2021 |
|
RU2757590C1 |
| Способ прогнозирования вероятности полной регрессии при проведении неоадъювантной химиотерапии у пациенток с трижды негативным молекулярно-генетическим субтипом рака молочной железы | 2016 |
|
RU2623118C1 |
| Биомедицинский клеточный продукт для терапии злокачественных новообразований | 2023 |
|
RU2813531C1 |
| Способ прогнозирования степени вероятности полной регрессии при проведении неоадъювантной химиотерапии у пациенток с люминальным В молекулярно-генетическим субтипом рака молочной железы | 2016 |
|
RU2632112C1 |
| Биомедицинский клеточный продукт со специфической противоопухолевой активностью, представленный популяциями лимфокин-активированных киллеров и анти-HER2 CAR-γδΤ-ОИЛ и анти-HER2 CAR-T-NK | 2022 |
|
RU2786210C1 |
| Конъюгат люминесцентных наночастиц диоксида кремния с рекомбинантными однодоменными нано - моноантителами C7b ламы, способными специфически взаимодействовать с рекомбинантным белком HER2/neu - аналогом природного рецептора эпидермального фактора роста EGFR/ERBB клеток человека | 2017 |
|
RU2679075C1 |
| Способ прогноза эффективности терапии меланомы | 2021 |
|
RU2766739C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ЦИРКУЛИРУЮЩИХ В КРОВИ ОПУХОЛЕВЫХ КЛЕТОК МЕТОДОМ МНОГОПАРАМЕТРОВОЙ ПРОТОЧНОЙ ЦИТОМЕТРИИ | 2024 |
|
RU2825188C2 |
| АНТИТЕЛО, СПЕЦИФИЧЕСКИ ВЗАИМОДЕЙСТВУЮЩЕЕ С ОНКОБЕЛКОМ HER2/neu | 2010 |
|
RU2425840C1 |
| ИДЕНТИФИКАЦИЯ ПАЦИЕНТОВ, НУЖДАЮЩИХСЯ В СОВМЕСТНОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ИНГИБИТОРА PD-L1 | 2013 |
|
RU2692773C2 |
Изобретение относится к области медицины. Предложен способ диагностики рака молочной железы с экспрессией рецептора Her2/neu на мембране опухолевых клеток. Способ включает проверку антител на предмет выявления антигена в заведомо антиген-позитивных случаях рака молочной железы методом проточной цитометрии и определе6ние рабочего титра антител. При окраске клеток для проточно-цитометрического определения HER2/neu используют наряду с FITC (флуоресцеин-изотиоцианат)-мечеными антителами к HER2/neu двойную и тройную флуоресцентные метки, а далее подсчитывают процент клеток, позитивных по HER2/neu, в гейте CD45-CD326+, указывают уровень экспрессии антигена на основании определения средней интенсивности флуоресценции по ранее проведенной калибровке, определяют распознаваемый терапевтическими моноклональными антителами мембранный эпитоп HER2 и оценивают количество антиген-позитивных клеток и уровней экспрессии мембранного антигена. Изобретение обеспечивает повышение точности диагностики Her2/neu-позитивного рака молочной железы. 1 ил., 2 табл.
Способ диагностики рака молочной железы с экспрессией рецептора Her2/neu на мембране опухолевых клеток, отличающийся тем, что антитела проверяют на предмет выявления антигена в заведомо антиген-позитивных случаях рака молочной железы методом проточной цитометрии, определяют рабочий титр антител; при окраске клеток для проточно-цитометрического определения HER2/neu используют наряду с FITC (флуоресцеин-изотиоцианат)-мечеными антителами к HER2/neu двойную и тройную флуоресцентные метки; подсчитывают процент клеток, позитивных по HER2/neu, в гейте CD45-CD326+, указывают уровень экспрессии антигена на основании определения средней интенсивности флуоресценции по ранее проведенной калибровке; определяют мембранный эпитоп HER2, распознаваемый терапевтическими моноклональными антителами, оценивают количество антиген-позитивных клеток и уровней экспрессии мембранного антигена.
| WOLFF A.C | |||
| et al., HER2 Testing in Breast Cancer:American Society of ClinicalOncology/College of AmericanPathologists Clinical PracticeGuideline FocusedUpdate Summary // Journal of Oncology Practice, Vol.14, Is.7, July 2018, с.437-442 | |||
| Cayre A | |||
| et al., Comparison of different commercial kits for HER2 testing in breast cancer: looking for the accurate cutoff for amplification // Breast Cancer Research, Vol.9, No.5, с.1-10 | |||
| ФРАНК Г.А | |||
| и др., HER2 - статус при раке молочной железы: тестирование, оценка прогноза при таргетной терапии // Ремедиум, тредны и брэнды, 32, апрель 2012, с.32-35 | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| СПОСОБЫ ДИАГНОСТИКИ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2013 |
|
RU2666627C2 |
Авторы
Даты
2019-09-25—Публикация
2018-09-18—Подача