Перечень последовательностей
Настоящее изобретение зарегистрировано вместе с перечнем последовательностей в электронном формате. Перечень последовательностей представлен в виде файла под названием BIOL0251WOSEQ_ST25.txt, созданного 28 апреля 2015 года, размером 204 Кб. Информация о перечне последовательностей в электронном формате в полном объеме включена в настоящий документ посредством ссылки.
Область техники
В вариантах реализации настоящего изобретения предложены способы, соединения и композиции для лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, посредством введения субъекту специфического ингибитора фактора комплемента В (CFB).
Уровень техники
Система комплемента представляет собой часть врожденной иммунной системы хозяина, участвующую в лизинге чужеродных клеток, усилении фагоцитоза антигенов, агрегации антиген-несущих агентов и привлечении макрофагов и нейтрофилов. Систему комплемента подразделяют на три пути инициации - классический, пектиновый и альтернативный пути - которые сходятся у компонента С3 с образованием ферментного комплекса, известного как С3-конвертаза, которая расщепляет С3 на С3а и C3b. C3b через CFB связывается с С3-конвертазой и приводит к образованию С5-конвертазы, которая расщепляет С5 на С5а и C5b, что инициирует мембраноатакующий каскад, приводящий к формированию мембраноатакующего комплекса (MAC), содержащего компоненты C5b, С6, С7, С8 и С9. Мембраноатакующий комплекс (MAC) образует трансмембранные каналы и разрушает двойной фосфолипидный слой клеток-мишеней, приводя к лизису клеток.
В гомеостатическом состоянии альтернативный путь непрерывно активируется на нижнем «холостом» уровне в результате активации альтернативного пути спонтанным гидролизом С3 и выработкой C3b, который образует С5-конвертазу.
Сущность изобретения
Система комплемента опосредует врожденный иммунитет и играет важную роль в нормальной воспалительной реакции на травму, но ее дисрегуляция может вызывать тяжелое повреждение. Активация альтернативного пути комплемента выше конститутивного «холостого» уровня может приводить к неограниченной гиперактивности и проявлению в форме заболеваний дисрегуляции комплемента.
Некоторые варианты реализации изобретения относятся к способам лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, у субъекта посредством введения специфического ингибитора фактора комплемента В (CFB). Некоторые варианты реализации, предложенные в настоящем документе, относятся к способу ингибирования экспрессии CFB у субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, посредством введения субъекту специфического ингибитора CFB. В некоторых вариантах реализации изобретения способ снижения или ингибирования накопления отложений С3 в глазу субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту специфического ингибитора CFB. В некоторых вариантах реализации изобретения способ снижения или ингибирования накопления отложения С3 в почках субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту специфического ингибитора CFB.
Подробное описание изобретения
Следует понимать, что изложенное выше общее описание и следующее подробное описание являются лишь примерными и пояснительными, и не являются ограничивающими заявленное изобретение. В настоящем документе использование единственного числа включает множественное число, если специально не указано иное. При использовании в настоящем документе, термин «или» означает «и/или», если не указано иное. Кроме того, использование термина «включая», а также других форм, таких как «включает» и «включенный», не является ограничивающим. Также, такие термины как «элемент» или «компонент» охватывают как элементы и компоненты, содержащие одну единицу, так и элементы и компоненты, которые содержат более одной субъединицы, если специально не указано иное.
Названия разделов, используемые в настоящем документе, предназначены лишь для организационных целей, и их не следует толковать как ограничение описанного объекта изобретения. Все документы или части документов, цитируемые в настоящей заявке, включая, но не ограничиваясь ими, патенты, патентные заявки, статьи, книги и трактаты, в явной форме включены в настоящий документ посредством ссылки в отношении частей документов, обсуждаемых в данном описании, а также в полном объеме.
При отсутствии конкретных определений, номенклатура, используемая в связи с ними, а также в связи с приемами и методиками аналитической химии, синтетической органической химии, а также медицинской и фармацевтической химии, описанная в настоящем документе, является общеизвестной и общепринятой в данной области техники. Для химического синтеза и химического анализа могут быть использованы стандартные методики. Некоторые такие методики и приемы представлены, например, в публикациях «Carbohydrate Modifications in Antisense Research» под редакцией Sangvi и Cook, American Chemical Society, федеральный округ Вашингтон, 1994; «Remington's Pharmaceutical Sciences,» Mack Publishing Co., Истон, штат Пенсильвания, 21е издание, 2005; и «Antisense Drug Technology, Principles, Strategies, and Applications» под редакцией Stanley Т. Crooke, CRC Press, Бока-Ратон, штат Флорида; а также в книге Sambrook et al., «Molecular Cloning, A laboratory Manual,» 2е издание. Cold Spring Harbor Laboratory Press, 1989, которые включены в настоящий документ посредством ссылки для всех целей. Если это допустимо, все патенты, заявки, опубликованные заявки и другие публикации, а также другие данные, упоминаемые в тексте настоящего описания, включены в настоящий документ посредством ссылки в полном объеме.
Если не указано иное, следующие термины имеют следующие значения:
«2'-F нуклеозид» относится к нуклеозиду, содержащему сахар, который содержит фтор в 2'-положении. Если не указано иное, то фтор в 2'-F нуклеозиде находится в рибо-положении (заменяя ОН природной рибозы).
«2'-O-метоксиэтил» (также 2'-МОЕ и 2'-O(CH2)2-OCH3) относится к O-метоксиэтил модификации в 2' положении фуранозного кольца. 2'-O-метоксиэтил-модифицированный сахар представляет собой модифицированный сахар.
«2'-МОЕ нуклеозид» (также 2'-O-метоксиэтил-нуклеозид) означает нуклеозид, содержащий 2'-МОЕ модифицированный сахарный фрагмент.
«2'-замещенный нуклеозид» означает нуклеозид, содержащий заместитель в 2'-положении фуранозного кольца, отличный от Н или ОН. В неких вариантах реализации 2'-замещенные нуклеозиды включают нуклеозиды с бициклическими сахарными модификациями.
«3' Сайт-мишень» обозначает нуклеотид нуклеиновой кислоты-мишени, комплементарный 3'-крайнему нуклеотиду конкретного антисмыслового соединения.
«5' Сайт-мишень» обозначает нуклеотид нуклеиновой кислоты-мишени, комплементарный 5'-крайнему нуклеотиду конкретного антисмыслового соединения.
«5-метилцитозин» означает цитозин модифицированный метильной группой в 5 положении. 5-метилцитозин представляет собой модифицированное азотистое основание.
«Около» означает в пределах ±10% от значения. Например, если указано, что «соединения вызывают по меньшей мере около 70% ингибирования CFB», подразумевается, что уровни CFB ингибируются в пределах 60-80%.
«Вводить» или «введение» относится к способам введения субъекту антисмыслового соединения, предложенного в настоящем документе, для выполнения его предназначенной функции. Пример способа введения, который может быть использован, включает, но не ограничивается им, парентеральное введение, такое как подкожная, внутривенная или внутримышечная инъекция или инфузия.
«Алкил» в данном контексте означает насыщенный прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода. Примеры алкильных групп включают, без ограничения, метил, этил, пропил, бутил, изопропил, н-гексил, октил, децил, додецил и т.п. Алкильные группы обычно содержат от 1 до около 24 атомов углерода, более часто от 1 до около 12 атомов углерода (С1-С12 алкил), более предпочтительно от 1 до около 6 атомов углерода.
В данном контексте «алкенил» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода и имеющий по меньшей мере одну двойную углерод-углеродную связь. Примеры алкенильных групп включают, без ограничения, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил, диены, такие как 1,3-бутадиен и т.п. Алкенильные группы обычно содержат от 2 до около 24 атомов углерода, более часто от 2 до около 12 атомов углерода, более предпочтительно от 2 до около 6 атомов углерода. Алкенильные группы, используемые в настоящем документе, могут необязательно содержать одну или более дополнительных групп заместителей.
В данном контексте «алкинил» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода и имеющий по меньшей мере одну тройную углерод-углеродную связь. Примеры алкинильных групп включают, без ограничения, этинил, 1-пропинил, 1-бутинил и т.п. Алкинильные группы обычно содержат от 2 до около 24 атомов углерода, более часто от 2 до около 12 атомов углерода, более предпочтительно от 2 до около 6 атомов углерода. Алкинильные группы, используемые в настоящем документе, могут необязательно содержать одну или более дополнительных групп заместителей.
В данном контексте «ацил» означает радикал, образованный за счет удаления гидроксильной группы от органической кислоты, и имеет общую формулу -С(O)-Х, где Х обычно является алифатическим, алициклическим или ароматическим. Примеры включают алифатические карбонилы, ароматические карбонилы, алифатические сульфонилы, ароматические сульфинилы, алифатические сульфинилы, ароматические фосфаты, алифатические фосфаты и т.п. Ацильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
В данном контексте «алициклическая» означает циклическую кольцевую систему, в которой кольцо является алифатическим. Кольцевая система может содержать одно или более колец, при этом по меньшей мере одно кольцо является алифатическим. Предпочтительные алициклические системы включают кольца, имеющие от около 5 до около 9 атомов углерода в кольце. Алициклические группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
В данном контексте «алифатический» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода, в котором насыщенность между любыми двумя атомами углерода представляет собой одинарную, двойную или тройную связь. Алифатическая группа предпочтительно содержит от 1 до около 24 атомов углерода, более часто от 1 до около 12 атомов углерода, более предпочтительно от 1 до около 6 атомов углерода. Прямая или разветвленная цепь алифатической группы может быть прервана одним или более гетероатомами, которые включают азот, кислород, серу и фосфор. Такие алифатические группы, прерванные гетероатомами, включают, без ограничения, полиалкокси, такие как полиалкиленгликоли, полиамины и полиимины. Алифатические группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
В данном контексте «алкокси» означает радикал, образованный между алкильной группой и атомом кислорода, при этом атом кислорода используется для присоединения алкокси-группы к исходной молекуле. Примеры алкокси-групп включают, без ограничения, метокси, этокси, пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, н-пентокси, неопентокси, н-гексокси и т.п. Алкокси-группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
В данном контексте «аминоалкил» означает аминозамещенный С1-С12 алкильный радикал. Алкильная часть указанного радикала образует ковалентную связь с исходной молекулой. Аминогруппа может быть расположена в любом положении, и аминоалкильная группа может быть замещена дополнительной группой заместителя в алкильной и/или амино-части.
В данном контексте «аралкил» и «арилалкил» означает ароматическую группу, которая ковалентно связана с С1-С12 алкильным радикалом. Часть алкильного радикала образовавшейся аралкильной (или арилалкильной) группы образует ковалентную связь с исходной молекулой. Примеры включают, без ограничения, бензил, фенетил и т.п. Аралкильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей, присоединенные к алкильной, арильной или к обеим группам, которые образуют указанную радикальную группу.
В данном контексте «арил» и «ароматический» означают радикалы моно- или полициклической карбоциклической кольцевой системы, имеющие одно или более ароматических колец. Примеры арильных групп включают, без ограничения, фенил, нафтил, тетрагидронафтил, инданил, инденил и т.п. Предпочтительные арильные кольцевые системы имеют от около 5 до около 20 атомов углерода в одном или более кольцах. Арильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
«Ослабление» относится к уменьшению по меньшей мере одного показателя, признака или симптома связанного заболевания, расстройства или патологического состояния. В некоторых вариантах реализации ослабление включает отсрочку или замедление развития одного или более показателей патологического состояния или заболевания. Степень тяжести показателей может быть определена субъективными или объективными показателями, которые известны специалистам в данной области техники.
«Животное» относится к человеку или животному, не являющемуся человеком, включающему, но не ограничивающемуся ими, мышей, крыс, кроликов, собак, кошек, свиней и приматов, включая, но не ограничиваясь ими, обезьян и шимпанзе.
«Антисмысловая активность» означает любую обнаруживаемую или поддающуюся измерению активность, обусловленную гибридизацией антисмыслового соединения с его нуклеиновой кислотой-мишенью. В неких вариантах реализации антисмысловая активность представляет собой уменьшение количества или экспрессии нуклеиновой кислоты-мишени или белка, кодируемого такой нуклеиновой кислотой-мишенью.
«Антисмысловое соединение» обозначает олигомерное соединение, которое способно к гибридизации с нуклеиновой кислотой-мишенью посредством водородной связи. Примеры антисмысловых соединений включают одноцепочечные и двухцепочечные соединения, такие как антисмысловые олигонуклеотиды, миРНК, мшРНК, оцРНК и соединения на их основе.
«Антисмысловое ингибирование» означает снижение уровней нуклеиновой кислоты-мишени в присутствии антисмыслового соединения, комплементарного нуклеиновой кислоте-мишени, по сравнению с уровнями нуклеиновой кислоты-мишени в отсутствие антисмыслового соединения.
«Антисмысловые механизмы» представляют собой все механизмы, принимающие участие в гибридизации соединения с нуклеиновой кислотой-мишенью, причем результат или эффект гибридизации представляет собой разложение мишени или оккупацию мишени с сопутствующей остановкой клеточного аппарата, включая, например, транскрипцию или сплайсинг.
«Антисмысловой олигонуклеотид» означает одноцепочечный олигонуклеотид, имеющий последовательность азотистых оснований, обеспечивающую возможность гибридизации с соответствующей областью или сегментом нуклеиновой кислоты-мишени.
«Комплементарность основания» относится к способности спаривания конкретной пары азотистых оснований антисмыслового олигонуклеотида с соответствующими азотистыми основаниями в нуклеиновой кислоте-мишени (т.е. гибридизации), опосредованной уотсон-криковским, хугстиновским или обратным хугстиновским водородным связыванием между соответствующими азотистыми основаниями.
«Бициклический сахарный фрагмент» означает модифицированный сахарный фрагмент, содержащий 4-7-членное кольцо (включая, но не ограничиваясь им, фуранозил), содержащее мостик, связывающий два атома 4-7-членного кольца с образованием второго кольца, что приводит к получению бициклической структуры. В некоторых вариантах реализации 4-7-членное кольцо представляет собой сахарное кольцо. В некоторых вариантах реализации 4-7-членное кольцо представляет собой фуранозил. В некоторых таких вариантах реализации мостик соединяет 2'-углерод и 4'-углерод фуранозила.
«Бициклическая нуклеиновая кислота» или «БНК» или «БНК нуклеозид» означает, что мономеры нуклеиновой кислоты имеют мостик, соединяющий два атома углерода между 4' и 2' положениями нуклеозидной сахарной единицы, тем самым образуя бициклический сахар. Примеры такого бициклического сахара включают, но не ограничиваются ими. А) α-L-метиленокси (4'-CH2-O-2') LNA, (В) β-D-метиленокси (4'-CH2-O-2') LNA, (С) этиленокси (4'-(CH2)2-O-2') LNA, (D) аминоокси (4'-CH2-O-N(R)-2') LNA и (Е) оксиамино (4'-CH2-N(R)-O-2') LNA, как показано ниже.
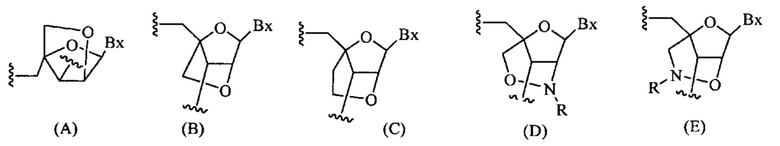
В данном контексте соединения LNA включают, но не ограничиваются ими, соединения, имеющие по меньшей мере один мостик между 4' и 2' положениями сахара, причем каждый из мостиков независимо содержит 1 или от 2 до 4 связанных групп, независимо выбранных из -[C(R1)(R2)]n-, -C(R1)=C(R2)-, -C(R1)=N-, -C(=NR1)-, -C(=O)-, -C(=S)-, -O-, -Si(R1)2-, -S(=O)x- и -N(R1)-; где х равен 0, 1 или 2; n равен 1, 2, 3 или 4; каждый R1 и R2 независимо представляет собой Н, защитную группу, гидроксил, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, С5-С20 арил, замещенный С5-С20 арил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, С5-С7 алициклический радикал, замещенный С5-С7 алициклический радикал, галоген, OJ1, NJ1J2, SJ1, N3, COOJ1, ацил (С(=O)-Н), замещенный ацил, CN, сульфонил (S(=O)2-J1) или сульфоксил (S(=O)-J1); и каждый J1 и J2 независимо представляет собой Н, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, С5-С20 арил, замещенный С5-С20 арил, ацил (С(=O)-Н), замещенный ацил, гетероциклический радикал, замещенный гетероциклический радикал, C1-C12 аминоалкил, замещенный C1-C12 аминоалкил или защитную группу.
Примеры 4'-2' мостиковых групп, входящих в определение LNA, включают, но не ограничиваются ими, одну из формул: -[C(R1)(R2)]n-, -[C(R1)(R2)]n-O-, -C(R1R2)-N(R1)-O- or -C(R1R2)-O-N(R1)-. Кроме того, другие мостиковые группы, входящие в определение LNA, представляют собой мостики 4'-CH2-2', 4'-(CH2)2-2', 4'-(CH2)3-2', 4'-CH2-O-2', 4'-(CH2)2-O-2', 4'-CH2-O-N(R1)-2' и 4'-CH2-N(R1)-O-2'-, где каждый R1 и R2 независимо представляет собой Н, защитную группу или C1-C12 алкил.
Также в определение LNA согласно настоящему изобретению включены LNA, в которых 2'-гидроксильная группа рибозильного сахарного кольца соединена с 4' атомом углерода сахарного кольца, с образованием таким образом мостика метиленокси (4'-CH2-O-2'), формируя бициклический сахарный фрагмент. Мостик также может быть метиленовой группой (-CH2-), соединяющей атом кислорода 2' и атом углерода 4', для которой используется термин метиленокси (4'-CH2-O-2') LNA. Кроме того, в случае бициклического сахарного фрагмента, содержащего этиленовую мостиковую группу в данном положении, применяется термин этиленокси (4'-CH2CH2-O-2') LNA. α-L-метиленокси (4'-CH2-O-2'), изомер метиленокси (4'-CH2-O-2') LNA, также попадает под определение LNA в данном контексте.
«Кэп-структура» или «кэп-терминальный фрагмент» означает химические модификации, которые были сделаны у любого конца антисмыслового соединения.
«Углевод» означает природный углевод, модифицированный углевод или производное углевода.
«Углеводный кластер» означает соединение, имеющее один или более углеводных остатков, присоединенных к скелету или линкерной группе, (см., например, Maier et al., «Synthesis of Antisense Oligonucleotides Conjugated to a Multivalent Carbohydrate Cluster for Cellular Targeting,» Bioconjugate Chemistry, 2003, (14): 18-29, полное содержание которой включено в настоящий документ посредством ссылки, или Rensen et al., «Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asiaglycoprotein Receptor», J. Med. Chem. 2004, (47): 5798-5808, где представлены примеры углеводных сопряженных кластеров).
«Производное углевода» означает любое соединение, которое может быть синтезировано с использованием углевода в качестве исходного материала или промежуточного соединения.
«cEt» или «стерически затрудненный этил» означает бициклический сахарный фрагмент, содержащий мостик, соединяющий 4'-углерод и 2'-углерод, причем мостик имеет формулу: 4'-СН(CH3)-O-2'.
«Химическая модификация» означает химическое отличие в соединении, по сравнению с природным аналогом. Химические модификации олигонуклеотидов включают нуклеозидные модификации (включая модификации сахарного фрагмента и модификации азотистого основания) и модификации межнуклеозидных линкеров. В отношении олигонуклеотида химическая модификация включает не только отличия в последовательности азотистых оснований.
«Расщепляемая связь» означает любую химическую связь, которая может быть расщеплена. В некоторых вариантах реализации расщепляемая связь выбрана из: амида, полиамида, сложного эфира, эфира, одного или обоих сложных эфиров фосфодиэфира, фосфатного сложного эфира, карбамата, дисульфида или пептида.
«Расщепляемый фрагмент» означает связь или группу, которая может быть расщеплена при физиологических условиях. В некоторых вариантах реализации расщепляемый фрагмент расщепляется внутри клетки или во внутриклеточных отделах, таких как лизосома. В некоторых вариантах реализации расщепляемый фрагмент расщепляется эндогенными ферментами, такими как нуклеазы. В некоторых вариантах реализации расщепляемый фрагмент содержит группу атомов, имеющую один, два, три, четыре или более четырех расщепляемых связей.
«Конъюгат» или «группа конъюгата» означает атом или группу атомов, связанную с олигонуклеотидом или олигомерным соединением. Как правило, группы конъюгата модифицируют одно или более свойств соединения, к которому они присоединены, включая, но не ограничиваясь ими, свойства фармакодинамики, фармакокинетики, связывания, поглощения, клеточного распределения, клеточного захвата, заряда и/или выведения.
«Линкер конъюгата» или «линкер» в контексте группы конъюгата означает часть группы конъюгата, содержащую любой атом или группу атомов и ковалентно связывающую (1) олигонуклеотид с другой частью группы конъюгата или (2) две или более частей группы конъюгата.
Группы конъюгата представлены в настоящем документе как радикалы, обеспечивающие связь для образования ковалентного присоединения к олигомерному соединению, такому как антисмысловой олигонуклеотид. В некоторых вариантах реализации точка присоединения в олигомерном соединении представляет собой 3'-атом кислорода 3'-гидроксильной группы 3'-концевого нуклеозида олигомерного соединения. В некоторых вариантах реализации точка присоединения у олигомерного соединения представляет собой 5'-атом кислорода 5'-гидроксильной группы 5'-концевого нуклеозида олигомерного соединения. В некоторых вариантах реализации связь для образования присоединения к олигомерному соединению представляет собой расщепляемую связь. В некоторых таких вариантах реализации такая расщепляемая связь составляет весь или часть расщепляемого фрагмента.
В некоторых вариантах реализации группы конъюгата содержат расщепляемый фрагмент (например, расщепляемую связь или расщепляемый нуклеозид) и часть углеводного кластера, такую как часть кластера GalNAc. Такая часть углеводного кластера содержит: нацеливающий фрагмент и необязательно линкер конъюгата. В некоторых вариантах реализации часть углеводного кластера определяют по количеству и сущности лиганда. Например, в некоторых вариантах реализации часть углеводного кластера содержит 3 группы GalNAc и обозначена «GalNAc3». В некоторых вариантах реализации часть углеводного кластера содержит 4 группы GalNAc и обозначена «GalNAc4». Конкретные части углеводных кластеров (имеющие конкретную связку, группы ветвления и линкера конъюгата) описаны в настоящем документе и обозначены римской цифрой с последующим нижним индексом «а». Соответственно, «GalNac3-1a» относится к конкретной части углеводного кластера группы конъюгата, имеющей 3 группы GalNac и конкретно определенную связку, группы ветвления и линкера Такой фрагмент углеводного кластера присоединен к олигомерному соединению через расщепляемый фрагмент, такой как расщепляемая связь или расщепляемый нуклеозид.
«Сопряженное соединение» означает любые атомы, группы атомов или группу связанных атомов, подходящую для применения в качестве группы конъюгата. В некоторых вариантах реализации сопряженные соединения могут обладать или влиять на одно или более свойств, включая, но не ограничиваясь ими, свойства фармакодинамики, фармакокинетики, связывания, абсорбции, клеточного распределения, клеточного захвата, заряда и/или выведения.
«Нуклеозид со стерически затрудненным этилом» (также cEt нуклеозид) означает нуклеозид, содержащий бициклический сахарный фрагмент, содержащий 4'-СН(CH3)-O-2' мостик.
«Фактор комплемента В (CFB)» означает любую нуклеиновую кислоту или белок CFB. «Нуклеиновая кислота CFB» означает любую нуклеиновую кислоту, кодирующую CFB. Например, в некоторых вариантах реализации нуклеиновая кислота CFB включает последовательность ДНК, кодирующую CFB, последовательность РНК, транскрибированную из ДНК, кодирующей CFB (включая геномную ДНК, содержащую интроны и экзоны), включая некодирующую белок (т.е. некодирующую) последовательность РНК, и последовательность мРНК, кодирующую CFB. «мРНК CFB» означает мРНК, кодирующую белок CFB.
«Специфический ингибитор CFB» относится к любому агенту, способному специфически ингибировать экспрессию РНК CFB и/или белка CFB или активность на молекулярном уровне. Например, CFB-специфические ингибиторы включают нуклеиновые кислоты (включая антисмысловые соединения), пептиды, антитела, низкомолекулярные соединения и другие агенты, способные ингибировать экспрессию РНК СFВ и/или белка CFB.
«Химически различимый участок» относится к участку антисмыслового соединения, который в некотором роде химически отличается от другого участка того же антисмыслового соединения. Например, участок, содержащий 2'-O-метоксиэтиловые нуклеозиды, является химически отличным от участка, содержащего нуклеозиды без 2'-O-метоксиэтиловых модификаций.
«Химерное антисмысловое соединение» означает антисмысловое соединение, которое имеет по меньшей мере 2 химически различных участка, каждая позиция имеет множество субъединиц.
«Комплементарность» означает способность спаривания азотистых оснований первой и второй нуклеиновых кислот.
«Включать», «включает» и «включающий» следует понимать как обозначение включения указанной стадии или элемента, или группы элементов или стадий, но не исключения любого другого элемента или стадии, или группы стадий или элементов.
«Непрерывные азотистые основания» означают азотистые основания, непосредственно примыкающие друг к другу.
«Дезоксинуклеозид» означает нуклеозид, содержащий 2'-Н фуранозильный сахарный фрагмент, находящийся в природных дезоксирибонуклеозидах (ДНК). В некоторых вариантах реализации 2'-дезоксинуклеозид может содержать модифицированное азотистое основание или может содержать азотистое основание РНК (например, урацил).
«Дезоксирибонуклеотид» означает нуклеотид, имеющий водород в 2' положении сахарной части нуклеотида. Дезоксирибонуклеотиды могут быть модифицированы с помощью любого из множества заместителей.
«Конструирование» или «разработка» относится к процессу конструирования олигомерного соединения, которое специфически гибридизуется с выбранной молекулой нуклеиновой кислоты.
«По-разному модифицированные» означает химические модификации или химические заместители, которые отличны друг от друга, включая отсутствие модификаций. Так, например, МОЕ нуклеозид и немодифицированный нуклеозид ДНК являются «по-разному модифицированными», даже несмотря на то, что нуклеозид ДНК не является модифицированным. Точно так же, ДНК и РНК являются «по-разному модифицированными», даже несмотря на то, что оба представляют собой природные не модифицированные нуклеозиды. Нуклеозиды, которые являются одинаковыми, но содержат различные азотистые основания, не являются по-разному модифицированными. Например, нуклеозид, содержащий 2'-ОМе модифицированный сахар и немодифицированное азотистое основание аденин, и нуклеозид, содержащий 2'-ОМе модифицированный сахар и немодифицированное азотистое основание тимин, не являются по-разному модифицированными.
«Двухцепочечные» относится к двум отдельным олигомерным соединениям, которые гибридизованы друг с другом. Такие двухцепочечные соединения могут иметь один или более негибридизованных нуклеозидов у одного или обоих концов одной или обеих цепей (выступы) и/или один или более внутренних негибридизованных нуклеозидов (несоответствий), при условии, что существует достаточная комплементарность для сохранения гибридизации при физиологически релевантных условиях.
«Эффективное количество» означает количество активного фармацевтического агента, достаточное для достижения желаемого физиологического результата у индивидуума, нуждающегося в таком агенте. Эффективное количество может варьировать среди индивидуумов в зависимости от здоровья и физического состояния индивидуума, подлежащего лечению, таксономической группы индивидуумов, подлежащих лечению, рецептуры композиции, оценки индивидуального состояния здоровья и других релевантных факторов.
«Эффективность» означает способность производить желаемый эффект.
«Экспрессия» включает в себя все функции, благодаря которым информация, закодированная в гене, преобразуется в структуры, присутствующие и функционирующие в клетке. Такие структуры включают, но не ограничиваются ими, продукты транскрипции и трансляции.
«Полностью комплементарный» или «100% комплементарный» означает, что каждое азотистое основание первой нуклеиновой кислоты имеет комплементарное азотистое основание во второй нуклеиновой кислоте. В некоторых вариантах реализации первая нуклеиновая кислота представляет собой антисмысловое соединение, а нуклеиновая кислота-мишень представляет собой вторую нуклеиновую кислоту.
«Фуранозил» означает структуру, содержащую 5-членное кольцо, содержащее четыре атома углерода и один атом кислорода.
«Гэпмер» означает химерное антисмысловое соединение, в котором внутренний участок, имеющий множество нуклеозидов, которые поддерживают расщепление РНКазой Н, располагается между внешними участками, имеющими один или несколько нуклеозидов, причем нуклеозиды, составляющие внутренние участки, химически отличаются от нуклеозида или нуклеозидов, составляющих внешние участки. Внутренний участок может быть описан как «гэп», а внешние участки могут быть описаны как «крылья».
«Гало» и «галоген» означают атом, выбранный из фтора, хлора, брома и йода.
«Гетероарил» и «гетероароматический» означают радикал, содержащий моно- или полициклическое ароматическое кольцо, кольцевую систему или конденсированную кольцевую систему, в которой по меньшей мере одно из колец является ароматическим и содержит один или более гетероатомов. Гетероарил включает также конденсированные кольцевые системы, включая системы, в которых одно или более из конденсированных колец не содержат гетероатомов. Гетероарильные группы, как правило, содержат один кольцевой атом, выбранный из серы, азота или кислорода. Примеры гетероарильных групп включают, без ограничения, пиридинил, пиразинил, пиримидинил, пирролил, пиразолил, имидазолил, тиазолил, оксазолил, изоксазолил, тиадиазолил, оксадиазолил, тиофенил, фуранил, хинолинил, изохинолинил, бензимидазолил, бензоксазолил, хиноксалинил и т.п. Гетероарильные радикалы могут быть присоединены к исходной молекуле напрямую или через линкерный фрагмент, такой как алифатическая группа или гетероатом. Гетероарильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
«Гибридизация» означает соединение комплементарных молекул нуклеиновых кислот. В некоторых вариантах реализации комплементарные молекулы нуклеиновых кислот включают, но не ограничиваются ими, антисмысловые соединения и нуклеиновую кислоту-мишень. В некоторых вариантах реализации комплементарные молекулы нуклеиновых кислот включают, но не ограничиваются ими, антисмысловой олигонуклеотид и нуклеиновую кислоту-мишень.
«Идентификация животного, страдающего или имеющего риск возникновения заболевания, расстройства и/или патологического состояния» обозначает идентификацию животного, которому поставлен диагноз заболевания, расстройства и/или патологического состояния, или идентификацию животного, предрасположенного к развитию заболевания, расстройства и/или патологического состояния. Такая идентификация может быть выполнена любым способом, включая оценку истории болезни индивидуума и стандартные клинические испытания или оценки.
«Непосредственно примыкающий» означает, что нет никаких промежуточных элементов между непосредственно примыкающими элементами.
«Индивидуум» означает человека или животное, не являющееся человеком, выбранное для лечения или терапии.
«Ингибирование экспрессии или активности» означает снижение, блокаду экспрессии или активности и не обязательно говорит о полном прекращении экспрессии или активности.
«Межнуклеозидная связь» относится к химической связи между нуклеозидами.
«Межнуклеозидная нейтральная линкерная группа» означает нейтральную линкерную группу, которая напрямую связывает два нуклеозида.
«Межнуклеозидная фосфорная линкерная группа» означает фосфорную линкерную группу, которая напрямую связывает два нуклеозида.
«Удлиненные» антисмысловые олигонуклеотиды представляют собой олигонуклеотиды, которые имеют один или более дополнительных нуклеозидов, по сравнению с антисмысловым олигонуклеотидом, описанным в настоящем документе.
«Линкерный мотив» означает характерный участок линкерных модификаций в олигонуклеотиде или его области. Нуклеозиды такого олигонуклеотида могут быть модифицированными или немодифицированными. Если не указано иное, мотивы, описывающие в настоящем документе только линкеры, представляют собой линкерные мотивы. Следовательно, в таких случаях нуклеозиды не ограничены.
«Связанный дезоксинуклеозид» означает основание нуклеиновой кислоты (A, G, С, Т, U), замещенное дезоксирибозой, связанной фосфатным эфиром, с образованием нуклеотида.
«Связанные нуклеозиды» означают соседние нуклеозиды, связанные между собой межнуклеозидной связью.
«Нуклеозид закрытой нуклеиновой кислоты» или «LNA» означает нуклеозид, содержащий бициклический сахарный фрагмент, который содержит мостик 4'-CH2-O-2'.
«Несоответствие» или «некомплементарное азотистое основание» относится к случаю, когда азотистое основание первой нуклеиновой кислоты не способно связываться с соответствующим азотистым основанием второй или нуклеиновой кислоты-мишени.
«Модифицированная Межнуклеозидная связь» обозначает замену или любое изменение природной межнуклеозидной связи (т.е. фосфодиэфирной межнуклеозидной связи).
«Модифицированное азотистое основание» означает любое азотистое основание, отличное от аденина, цитозина, гуанина, тимидина или урацила. «Немодифицированное азотистое основание» означает пуриновые основания: аденин (А) и гуанин (G), и пиримидиновые основания: тимин (Т), цитозин (С), и урацил (U).
«Модифицированный нуклеозид» обозначает нуклеозид, содержащий независимо модифицированный сахарный фрагмент и/или модифицированное азотистое основание.
«Модифицированный нуклеотид» означает нуклеотид, содержащий независимо модифицированный сахарный фрагмент, модифицированную межнуклеозидную связь или модифицированное азотистое основание.
«Модифицированный олигонуклеотид» обозначает олигонуклеотид, содержащий по меньшей мере одну модифицированную межнуклеозидную связь, модифицированный сахар, и/или модифицированное азотистое основание.
«Модифицированный сахар» означает замещение и/или измену любого из природных сахарных фрагментов.
«Модулирование» относится к изменению или регулированию характеристики в клетке, ткани, органе или организме. Например, модулирование мРНК CFB может означать увеличение или снижение уровня мРНК CFB и/или белка CFB в клетке, ткани, органе или организме. «Модулятор» вызывает изменение в клетке, ткани, органе или организме. Например, антисмысловое соединение CFB может представлять собой модулятор, который снижает количество мРНК CFB и/или белка CFB в клетке, ткани, органе или организме.
«Мономер» означает одно звено олигомера. Мономеры включают, но не ограничиваются ими, нуклеозиды и нуклеотиды, природные или модифицированные.
«Моно- или полициклическая кольцевая система» включает все кольцевые системы, выбранные из одиночных или полициклических радикальных кольцевых систем, в которых указанные кольца конденсированы или связаны, и включает одиночные или смешанные кольцевые системы, индивидуально выбранные из алифатических, алициклических, арильных, гетероарильных, аралкильных, арилалкильных, гетероциклических, гетероарильных, гетероароматических и гетероарилалкильных. Такие моно- и полициклические структуры могут содержать кольца, каждое из которых имеет одинаковую степень насыщенности, или каждое независимо имеет переменные степени насыщенности, включая полностью насыщенные, частично насыщенные или полностью ненасыщенные. Каждое кольцо может содержать кольцевые атомы, выбранные из С, N, О и S с образованием гетероциклических колец, а также колец, содержащих только кольцевые атомы С, которые могут быть представлены в смешанном мотиве, как, например, в бензимидазоле, в котором одно кольцо имеет только кольцевые атомы углерода, а конденсированное кольцо имеет два атома азота. Моно- или полициклическая кольцевая система может быть дополнительно замещена группами заместителей, как, например, фталимид, который имеет две группы =O, присоединенные к одному из колец. Моно- или полициклические кольцевые системы могут быть присоединены к исходным молекулам при помощи различных способов, таких как непосредственно через кольцевой атом, путем конденсации через несколько кольцевых атомов, через группу заместителя или через бифункциональный линкерный фрагмент.
«Мотив» означает конфигурацию из немодифицированных и модифицированных нуклеозидов в антисмысловом соединении.
«Природный сахарный фрагмент» означает фрагмент сахара, находящийся в ДНК (2'-Н) или РНК (2'-ОН).
«Природная межнуклеозидная связь» означает 3' к 5' фосфодиэфирную связь.
«Нейтральная линкерная группа» означает линкерную группу, которая не имеет заряда. Нейтральные линкерные группы включают, без ограничения, фосфотриэфиры, метилфосфонаты, MMI (-CH2-N(CH3)-O-), амид-3 (-CH2-C(=O)-N(H)-), амид-4 (-CH2-N(H)-C(=O)-), формацеталь (-O-CH2-O-) и тиоформацеталь (-S-CH2-O-). Дополнительные нейтральные группы включают неионные линкеры, содержащие силоксан (диалкилсилоксан), карбоксилатный эфир, карбоксамид, сульфид, сульфонатный эфир и амиды (см., например: Carbohydrate Modifications in Antisense Research; Y.S. Sanghvi and P.D. Cook Eds. ACS Symposium Series 580; главы 3 и 4, (сс. 40-65)). Дополнительные нейтральные линкерные группы включают неионные линкеры, содержащие смешанные составные части N, О, S и CH2.
«Некомплементарное азотистое основание» относится к паре азотистых оснований нуклеиновых кислот, которые не образуют водородных связей друг с другом или иным образом не поддерживают гибридизацию.
«Немежнуклеозидная нейтральная линкерная группа» означает нейтральную линкерную группу, которая не связывает напрямую два нуклеозида. В некоторых вариантах реализации немежнуклеозидная нейтральная линкерная группа связывает нуклеозид с группой, отличной от нуклеозида. В некоторых вариантах реализации немежнуклеозидная нейтральная линкерная группа связывает две группы, ни одна из которых не является нуклеозидом.
«Немежнуклеозидная фосфорная линкерная группа» означает фосфорную линкерную группу, которая не связывает напрямую два нуклеозида. В некоторых вариантах реализации немежнуклеозидная фосфорная линкерная группа связывает нуклеозид с группой, отличной от нуклеозида. В некоторых вариантах реализации немежнуклеозидная фосфорная линкерная группа связывает две группы, ни одна из которых не является нуклеозидом.
«Нуклеиновая кислота» означает молекулы, состоящие из мономерных нуклеотидов. Нуклеиновая кислота включает, но не ограничивается ими, рибонуклеиновые кислоты (РНК), дезоксирибонуклеиновой кислоты (ДНК), одноцепочечные нуклеиновые кислоты их двухцепочечные нуклеиновые кислоты.
«Азотистое основание» означает гетероциклический фрагмент, способный спариваться с основанием другой нуклеиновой кислоты.
«Комплементарность азотистого основания» относится к азотистому основанию, способному к спариванию с другим основанием. Например, в ДНК аденин (А) комплементарен тимину (Т). Например, в РНК аденин (А) комплементарен урацилу (U). В некоторых вариантах реализации комплементарное азотистое основание относится к азотистому основанию антисмыслового соединения, способному спариваться с азотистым основанием своей нуклеиновой кислоты-мишени. Например, если азотистое основание в определенном положении антисмыслового соединения способно к водородному связыванию с азотистым основанием в определенном положении нуклеиновой кислоты-мишени, то это положение водородного связывания между олигонуклеотидом и нуклеиновой кислотой-мишенью считается комплементарным по этой паре азотистых оснований.
«Мотив модификации азотистого основания» означает характерный участок модификаций азотистых оснований вдоль олигонуклеотида. Если не указано иное, то мотив модификации азотистого основания не зависит от последовательности азотистого основания.
«Последовательность азотистых оснований» означает порядок последовательных азотистых оснований, независимый от любого сахара, связи и/или модификации азотистого основания.
«Нуклеозид» означает азотистое основание, связанное с сахаром.
«Миметик нуклеозида» включает структуры, используемые для замены сахара или сахара и основания и необязательно связи в одном или нескольких положениях олигомерного соединения, например, такие как миметики нуклеозидов, содержащие морфолино, циклогексенил, циклогексил, тетрагидропиранил, бицикло или трицикло сахара-миметики, например, нефуранозные сахарные звенья. Нуклеотид-миметик включает в себя структуры, используемые для замены нуклеозида и связи в одном или более положениях олигомерного соединения, такие как, например, пептидные нуклеиновые кислоты или морфолино-соединения (морфолино-соединения, связанные -N(H)-C(=O)-O- или другой нефосфодиэфирной связью). Заменитель сахара пересекается более широким термином нуклеозид-миметик, но предназначен для обозначения замены только сахарной единицы (фуранозного кольца). Тетрагидропираниловые кольца, представленные в настоящем документе, иллюстрируют пример заменителя сахара, в котором сахарная фуранозная группа заменена тетрагидропираниловой кольцевой системой. «Миметик» относится к группам, которые заменяют сахар, азотистое основание и/или межнуклеозидную связь. Как правило, миметик используют вместо сахара или комбинации сахара с межнуклеозидной связью, а азотистое основание сохраняется для гибридизации с выбранной мишенью.
«Нуклеозидный мотив» означает характерный участок нуклеозидных модификаций в олигонуклеотиде или его области. Связи такого олигонуклеотида могут быть модифицированными или немодифицированными. Если не указано иное, мотивы, описывающие в настоящем документе только нуклеозиды, представляют собой нуклеозидные мотивы. Следовательно, в таких случаях связи не ограничены.
«Нуклеотид» означает нуклеозид, имеющий фосфатную группу, ковалентно связанную с сахарной частью нуклеозида.
«Олигомерное соединение» означает полимер из связанных мономерных субъединиц, которые способны к гибридизации с по меньшей мере областью молекулы нуклеиновой кислоты.
«Олигонуклеозид» означает олигонуклеотид, в котором ни одна из межнуклеозидных связей не содержит атома фосфора.
«Олигонуклеотид» означает полимер связанных нуклеозидов, каждый из которых может быть модифицированным или немодифицированным, независимо друг от друга.
«Парентеральное введение» означает введение путем инъекций или инфузии. Парентеральное введение включает подкожное введение, внутривенное введение, внутримышечное введение, внутриартериальное введение, внутрибрюшинное введение или внутричерепное введение, например, интратекальное или интрацеребровентрикулярное введение.
«Фармацевтическая композиция» означает смесь веществ, пригодных для введения индивидууму. Например, фармацевтическая композиция может содержать один или более активных фармацевтических агентов и стерильный водный раствор.
«Фармацевтически приемлемые соли» обозначает физиологически и фармацевтически приемлемые соли антисмысловых соединений, т.е. соли, которые сохраняют желательную биологическую активность исходного олигонуклеотида и не вызывают нежелательных токсикологических эффектов.
«Тиофосфатная связь» означает связь между нуклеозидами, где фосфодиэфирные связи модифицированы путем замены одного из немостиковых атомов кислорода на атом серы. Тиофосфатная связь представляет собой модифицированную межнуклеозидную связь.
«Фосфорная линкерная группа» означает линкерную группу, содержащую атом фосфора. Фосфорные линкерные группы включают, без ограничения, группы, имеющие формулу:
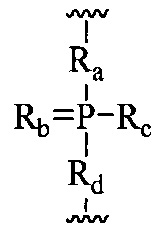
где
Ra и Rd, каждый независимо, представляют собой О, S, CH2, NH или NJ1, где J1 представляет собой C1-C6 алкил или замещенный C1-C6 алкил;
Rb представляет собой О или S;
Rc представляет собой ОН, SH, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, амино или замещенный амино; и
J1 представляет собой Rb представляет собой О или S.
Фосфорные линкерные группы включают, без ограничения, фосфодиэфир, тиофосфат, дитиофосфат, фосфонат, фосфорамидат, фосфортиоамидат, тионоалкилфосфонат, фосфотриэфиры, тионоалкил-фосфотриэфиры и боранофосфат.
«Часть» означает определенное количество смежных (т.е. связанных) азотистых оснований нуклеиновой кислоты. В некоторых вариантах реализации часть представляет собой определенное число смежных азотистых оснований нуклеиновой кислоты-мишени. В некоторых вариантах реализации часть представляет собой определенное число смежных азотистых оснований антисмыслового соединения.
«Предупреждать» относится к задержке или предотвращению появления, развития или прогрессирования заболевания, расстройства или патологического состояния в течение периода времени от нескольких минут до неопределенного срока. Предупреждение означает также снижение риска развития заболевания, расстройства или патологического состояния.
«Пролекарство» означает неактивную или менее активную форму соединения, которая при введении субъекту метаболизируется с образованием активного или более активного соединения (например, лекарства).
«Профилактически эффективное количество» означает такое количество фармацевтического агента, которое обеспечивает профилактический или превентивный эффект для животного.
«Защитная группа» означает любое соединение или защитную группу, известную специалистам в данной области техники. Неограничивающие примеры защитных групп представлены в книге «Protective Groups in Organic Chemistry», Т.W. Greene, P.G.M. Wuts, ISBN 0-471-62301-6, John Wiley & Sons, Inc, Нью-Йорк, полное содержание которой включено в настоящий документ посредством ссылки.
«Участок» определяют как фрагмент нуклеиновой кислоты-мишени, имеющий по меньшей мере одну идентифицируемую структуру, функцию или характеристику.
«Рибонуклеотид» означает нуклеотид, имеющий гидрокси-группу в 2' положении сахарного фрагмента нуклеотида. Рибонуклеотиды могут быть модифицированы с помощью любого из множества заместителей.
«Антисмысловое соединение на основе RISC» означает антисмысловое соединение, в котором по меньшей мере часть антисмысловой активности антисмыслового соединения обусловлена РНК-индуцируемым комплексом сайленсинга (RISC).
«Антисмысловое соединение на основе РНКазы Н» означает антисмысловое соединение, в котором по меньшей мере часть антисмысловой активности антисмыслового соединения обусловлена гибридизацией антисмыслового соединения с нуклеиновой кислотой-мишенью и последующим расщеплением нуклеиновой кислоты-мишени под действием РНКазы Н.
«Сегменты» определяют как меньшие или субфрагменты участков в составе нуклеиновой кислоты-мишени.
«Отдельные участки» означает части олигонуклеотида, в которых химические модификации или мотив химических модификаций любой из соседних частей содержит по меньшей мере одно отличие для обеспечения возможности различать участки друг от друга.
«Мотив последовательности» означает характерный участок азотистых оснований, расположенных вдоль олигонуклеотида или его части. Если не указано иное, то мотив последовательности не зависит от химических модификаций и, следовательно, может иметь любую комбинацию химических модификаций, включая отсутствие химических модификаций.
«Побочные эффекты» означают физиологическое заболевание и/или состояния, обусловленные лечением, которые отличны от желаемого эффекта. В некоторых вариантах реализации побочные эффекты включают реакции в месте инъекции, аномалии функциональных проб печени, отклонения в функциях почек, гепатотоксичность, нефротоксичность, аномалии центральной нервной системы, миопатии и недомогание. Например, повышение уровней аминотрансферазы в сыворотке может указывать на гепатотоксичность или нарушение функции печени. Например, повышенный билирубин может указывать на гепатотоксичность или нарушение функции печени.
«Сайты» в данном контексте определяют как уникальные положения азотистых оснований в нуклеиновой кислоте-мишени.
«Замедляет прогрессирование» означает ослабление развития указанного заболевания.
«Специфично гибридизуется» обозначает антисмысловое соединение, обладающее достаточной степенью комплементарности между антисмысловым олигонуклеотидом и нуклеиновой кислотой-мишенью, чтобы вызывать желаемый эффект, минимально или никак не влияния на нецелевые нуклеиновые кислоты в условиях, в которых специфическое связывание является желательным, т.е. в физиологических условиях в случае анализов in vivo и терапевтического лечения. «Строгие условия гибридизации» или «жесткие условия» означают условия, при которых олигомерное соединение гибридизируется со своей целевой последовательностью, но с минимальным количеством других последовательностей.
«Субъект» означает человека или животного, не являющегося человеком, выбранного для лечения или терапии.
«Заместитель» и «группа заместителя» означает атом или группу, которая вытесняет атом или группу указанного исходного соединения. Например, заместитель модифицированного нуклеозида представляет собой любой атом или группу, которая отлична от атома или группы, находящейся в природном нуклеозиде (например, модифицированный 2'-заместитель представляет собой любой атом или группу в 2'-положении нуклеозида, отличную от Н или ОН). Группы заместителей могут быть защищенными или незащищенными. В некоторых вариантах реализации соединения настоящего описания имеют заместители в одном или более чем в одном положении исходного соединения. Заместители также могут быть дополнительно замещены другими группами заместителей и могут быть присоединены напрямую или через линкерную группу, такую как алкильная или углеводородная группа, к исходному соединению.
Точно так же, в данном контексте «заместитель» в отношении химической функциональной группы означает атом или группу атомов, которая отлична от атома или группы атомов, обычно содержащихся в указанной функциональной группе. В некоторых вариантах реализации заместитель вытесняет атом водорода функциональной группы (например, в некоторых вариантах реализации заместитель замещенной метильной группы представляет собой атом или группу, отличную от водорода, которая вытесняет один или более атомов водорода незамещенной метильной группы). Если не указано иное, группы, которые могут быть использованы в качестве заместителей, включают, без ограничения, галоген, гидроксил, алкил, алкенил, алкинил, ацил (-C(O)Raa), карбоксил (-C(O)O-Raa), алифатические группы, алициклические группы, алкокси, замещенный окси (-O-Raa), арил, аралкил, гетероциклический радикал, гетероарил, гетероарилалкил, амино (N(Rbb)(Rcc)), имино (=NRbb), амидо (C(O)N(Rbb)(Rcc) или N(Rbb)C(O)Raa), азидо (-N3), нитро (NO2), пиано (-CN), карбамидо (OC(O)N(Rbb)(Rcc) или N(Rbb)C(O)ORaa), уреидо (N(Rbb)C(O)N(Rbb)(Rcc)), тиоуреидо (N(Rbb)C(S)N(Rbb)(Rcc)), гуанидинил (N(Rbb)C(=NRbb)N(Rbb)(Rcc)), амидинил (C(=NRbb)N(Rbb)(Rcc) или N(Rbb)C(=NRbb)(Raa)), тиол (-SRbb), сульфинил (S(O)Rbb), сульфонил (-S(O)2Rbb) и сульфонамидил (-S(O)2N(Rbb)(Rcc) или N(Rbb)S(O)2Rbb). Где каждый Raa, Rbb и Rcc независимо представляет собой Н, необязательно связанную химическую функциональную группу или дополнительную группу заместителя, при этом предпочтительный перечень включает, без ограничения, алкил, алкенил, алкинил, алифатические, алкокси, ацил, арил, аралкил, гетероарил, алициклические, гетероциклические и гетероарилалкил. Выбранные заместители в соединениях, описанных в настоящем документе, находятся в рекурсивной степени.
«Замещенный сахарный фрагмент» означает фуранозил, который не является природным сахарным фрагментом. Замещенные сахарные фрагменты включают, но не ограничиваются ими, фуранозилы, содержащие заместители в 2'-положении, 3'-положении, 5'-положении и/или 4'-положении. Некоторые замещенные сахарные фрагменты представляют собой бициклические сахарные фрагменты.
«Сахарный фрагмент» означает природный сахарный фрагмент или модифицированный сахарный фрагмент нуклеозида.
«Сахарный мотив» означает характерный участок сахарных модификаций в олигонуклеотиде или его области.
«Заменитель сахара» означает структуру, которая не содержит фуранозила и способна заменять природный сахарный фрагмент нуклеозида, так что образующиеся нуклеозидные субъединицы могут связываться вместе и/или связываться с другими нуклеозидами с образованием олигомерного соединения, которое может гибридизоваться с комплементарным олигомерным соединением. Такие структуры включают кольца, содержащие другое количество атомов, чем фуранозил (например, (например, 4, 6 или 7-членные кольца); замену кислорода фуранозила некислородным атомом (например, углеродом, серой или азотом); или одновременное изменение количества атомов и замену кислорода. Такие структуры также могут содержать замещения, соответствующие замещениям, описанным для замещенных сахарных фрагментов (например, 6-членные карбоциклические бициклические заменители сахара, необязательно содержащие дополнительные заместители). Заменители сахара включают также более сложные сахарные замены (например, некольцевые системы пептидной нуклеиновой кислоты). Заменители сахара включают, без ограничения, морфолино, циклогексенилы и циклогекситы.
«Мишень» обозначает белок, модуляция которого является желательной. «Ген-мишень» означает ген, кодирующий белок-мишень.
«Таргетинг» означает процесс конструирования и выбора антисмыслового соединения, которое будет специфически гибридизироваться с нуклеиновой кислотой-мишенью и вызывать желаемый эффект.
«Нуклеиновая кислота-мишень», «РНК-мишень», транскрипт РНК-мишени» и «целевая нуклеиновая кислота» означают нуклеиновую кислоту, способную подвергаться целевому воздействию антисмысловых соединений.
«Целевой участок» означает фрагмент целевой нуклеиновой кислоты, на который нацелено одно или более антисмысловых соединений.
«Целевой сегмент» означает последовательность нуклеотидов нуклеиновой кислоты-мишени, на который нацелено антисмысловое соединение. «5' целевой сайт» относится к 5'-крайнему нуклеотиду целевого сегмента. «3' целевой сайт» относится к 3'-крайнему нуклеотиду целевого сегмента.
«Концевая группа» означает один или более атомов, присоединенных к любому или к обоим 3'- или 5'-концам олигонуклеотида. В некоторых вариантах реализации концевая группа представляет собой группу конъюгата. В некоторых вариантах реализации концевая группа содержит один или более нуклеозидов концевой группы.
«Концевая межнуклеозидная связь» означает связь между последними двумя нуклеозидами олигонуклеотида или его определенной области.
«Терапевтически эффективное количество» означает количество фармацевтического агента, которое обеспечивает терапевтический эффект для индивидуума.
«Лечение» означает введение композиции животному для изменения или облегчения заболевания, расстройства или патологического состояния у животного. В некоторых вариантах реализации животному может быть введена одна или более фармацевтических композиций.
«Немодифицированные» азотистые основания означают пуриновые основания: аденин (А) и гуанин (G), и пиримидиновые основания: тимин (Т), цитозин (С) и урацил (U).
«Немодифицированный нуклеотид» означает нуклеотид, состоящий из природных азотистых оснований, сахарных фрагментов и межнуклеозидных связей. В некоторых вариантах реализации изобретения немодифицированный нуклеотид представляет собой РНК нуклеотид (т.е. β-D-рибонуклеозиды) или ДНК нуклеотид (т.е. β-D-дезоксирибонуклеозид).
Некоторые варианты реализации изобретения
В некоторых вариантах реализации изобретения предложены способы, соединения и композиции для ингибирования экспрессии фактора комплемента В (CFB).
В некоторых вариантах реализации предложены антисмысловые соединения, направленные на нуклеиновую кислоту CFB. В некоторых вариантах реализации нуклеиновая кислота CFB имеет последовательность с номером доступа GENBANK NM_001710.5 (включенную в настоящий документ как SEQ ID NO: 1), с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000 (включенную в настоящий документ как SEQ ID NO: 2), с номером доступа GENBANK NW_001116486.1, усеченную с нуклеотида 536000 по 545000 (включенную в настоящий документ как SEQ ID NO: 3), с номером доступа GENBANK XM_001113553.2 (включенную в настоящий документ как SEQ ID NO: 4) или с номером доступа GENBANK NM_008198.2 (включенную в настоящий документ как SEQ ID NO: 5).
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 9 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 10 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 11 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 12 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из последовательности азотистых оснований SEQ ID NO: 6-808.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, комплементарных азотистым основаниям 30-49, 48-63, 150-169, 151-170, 152-171, 154-169, 154-173, 156-171, 156-175, 157-176, 158-173, 158-177, 480-499, 600-619, 638-657, 644-663, 738-757, 1089-1108, 1135-1154, 1141-1160, 1147-1166, 1150-1169, 1153-1172, 1159-1178, 1162-1181, 1165-1184, 1171-1186, 1171-1190, 1173-1188, 1173-1192, 1175-1190, 1175-1194, 1177-1196, 1183-1202, 1208-1227, 1235-1254, 1298-1317, 1304-1323, 1310-1329, 1316-1335, 1319-1338, 1322-1341, 1328-1347, 1349-1368, 1355-1374, 1393-1412, 1396-1415, 1399-1418, 1405-1424, 1421-1440, 1621-1640, 1646-1665, 1646-1665, 1647-1666, 1689-1708, 1749-1768, 1763-1782, 1912-1931, 2073-2092, 2085-2104, 2166-2185, 2172-2191, 2189-2208, 2191-2210, 2193-2212, 2195-2210, 2195-2214, 2196-2215, 2197-2212, 2197-2216, 2202-2221, 2223-2238, 2223-2242, 2225-2240, 2226-2245, 2227-2242, 2227-2246, 2238-2257, 2241-2260, 2267-2286, 2361-2380, 2388-2407, 2397-2416, 2448-2467, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2459-2478, 2461-2476, 2461-2480, 2532-2551, 2550-2569, 2551-2566, 2551-2570, 2552-2568, 2552-2570, 2552-2571, 2553-2568, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2555-2570, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2573, 2557-2574, 2557-2575, 2557-2576, 2558-2575, 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2576, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2583, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2585, 2570-2587, 2570-2589, 2571-2586, 2571-2588, 2571-2590, 2572-2589. 2572-2590, 2572-2591, 2573-2590, 2573-2592, 2574-2590, 2574-2591, 2574-2593, 2575-2590. 2575-2591, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2595, 2577-2596, 2578-2594, 2578-2596, 2578-2597, 2579-2598, 2580-2596, 2580-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2582-2598, 2582-2599, 2582-2600, 2582-2601, 2583-2599, 2583-2600, 2583-2601, 2583-2602, 2584-2600, 2584-2601, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2601, 2586-2602, 2586-2604, 2586-2605, 2587-2602, 2587-2603, 2587-2605, 2587-2606, 2588-2603, 2588-2604, 2588-2605, 2588-2606, 2588-2607, 2589-2604, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2590-2609, 2591-2607, 2591-2608, 2591-2609, 2591-2610, 2592-2607, 2592-2608, 2592-2609, 2592-2610, 2592-2611, 2593-2608, 2593-2609, 2593-2610, 2593-2612, 2594-2609, 2594-2610, 2594-2611, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2612, 2596-2613, 2596-2614, 2596-2615, 2597-2612, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2618, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2631 или 2616-2631 SEQ ID NO: 1, и при этом указанный модифицированный олигонуклеотид по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарен SEQ ID NO: 1.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую часть из по меньшей мере 8 смежных азотистых оснований, комплементарную равной по длине части азотистых оснований 30-49, 48-63, 150-169, 151-170, 152-171, 154-169, 154-173, 156-171, 156-175, 157-176, 158-173, 158-177, 480-499, 600-619, 638-657, 644-663, 738-757, 1089-1108, 1135-1154, 1141-1160, 1147-1166, 1150-1169, 1153-1172, 1159-1178, 1162-1181, 1165-1184, 1171-1186, 1171-1190, 1173-1188, 1173-1192, 1175-1190, 1175-1194, 1177-1196, 1183-1202, 1208-1227, 1235-1254, 1298-1317, 1304-1323, 1310-1329, 1316-1335, 1319-1338, 1322-1341, 1328-1347, 1349-1368, 1355-1374, 1393-1412, 1396-1415, 1399-1418, 1405-1424, 1421-1440, 1621-1640, 1646-1665, 1646-1665, 1647-1666, 1689-1708, 1749-1768, 1763-1782, 1912-1931, 2073-2092, 2085-2104, 2166-2185, 2172-2191, 2189-2208, 2191-2210, 2193-2212, 2195-2210, 2195-2214, 2196-2215, 2197-2212, 2197-2216, 2202-2221, 2223-2238, 2223-2242, 2225-2240, 2226-2245, 2227-2242, 2227-2246, 2238-2257, 2241-2260, 2267-2286, 2361-2380, 2388-2407, 2397-2416, 2448-2467, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2459-2478, 2461-2476, 2461-2480, 2532-2551, 2550-2569, 2551-2566, 2551-2570, 2552-2568, 2552-2570, 2552-2571, 2553-2568, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2555-2570, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2573, 2557-2574, 2557-2575, 2557-2576, 2558-2575, 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2576, 2561-2578, 2561-2579. 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2583, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2585, 2570-2587, 2570-2589, 2571-2586, 2571-2588, 2571-2590, 2572-2589, 2572-2590, 2572-2591, 2573-2590, 2573-2592, 2574-2590, 2574-2591, 2574-2593, 2575-2590, 2575-2591, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2595, 2577-2596, 2578-2594, 2578-2596, 2578-2597, 2579-2598, 2580-2596, 2580-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2582-2598, 2582-2599, 2582-2600, 2582-2601, 2583-2599, 2583-2600, 2583-2601, 2583-2602, 2584-2600, 2584-2601, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2601, 2586-2602, 2586-2604, 2586-2605, 2587-2602, 2587-2603, 2587-2605, 2587-2606, 2588-2603, 2588-2604, 2588-2605, 2588-2606, 2588-2607, 2589-2604, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2590-2609, 2591-2607, 2591-2608, 2591-2609, 2591-2610, 2592-2607, 2592-2608, 2592-2609, 2592-2610, 2592-2611, 2593-2608, 2593-2609, 2593-2610, 2593-2612, 2594-2609, 2594-2610, 2594-2611, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2612, 2596-2613, 2596-2614, 2596-2615, 2597-2612, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2618, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2631 или 2616-2631 SEQ ID NO: 1, и при этом последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарна SEQ ID NO: 1.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, комлементарных азотистым основаниям 1608-1627, 1685-1704, 1686-1705, 1751-1770, 1769-1784, 1871-1890, 1872-1891, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1878-1897, 1879-1894, 1879-1898, 2288-2307, 2808-2827, 2846-2865, 2852-2871, 2946-2965, 3773-3792, 3819-3838, 3825-3844, 3831-3850, 3834-3853, 3837-3856, 3843-3862, 4151-4166, 4151-4170, 4153-4172, 4159-4178, 4184-4203, 4211-4230, 4609-4628, 4612-4631, 4615-4634, 4621-4640, 4642-4661, 4648-4667, 4686-4705, 4689-4708, 4692-4711, 4698-4717, 4714-4733, 5270-5289, 5295-5314, 5296-5315, 5830-5849, 5890-5909, 5904-5923, 6406-6425, 6662-6681, 6674-6693, 6954-6973, 6960-6979, 6977-6996, 6979-6998, 6981-7000, 6983-6998, 6983-7002, 6984-7003, 6985-7000, 6985-7004, 6990-7009, 7122-7141, 7125-7144, 7151-7170, 7353-7372, 7362-7381, 7683-7702, 7688-7707, 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7694-7713, 7696-7711, 7696-7715, 7767-7786, 7785-7804, 7786-7801, 7787-7803, 7787-7805, 7787-7806, 7788-7803, 7788-7805, 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7805, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7808, 7792-7809, 7792-7810, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7811, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7818, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7820, 7805-7822, 7805-7824, 7806-7821, 7806-7823, 7806-7825, 7807-7824, 7807-7825, 7807-7826, 7808-7825, 7808-7827, 7809-7825, 7809-7826, 7809-7828, 7810-7825, 7810-7826, 7810-7827, 7810-7829, 7811-7828, 7811-7830, 7812-7829, 7812-7830, 7812-7831, 7813-7829, 7813-7831, 7813-7832, 7814-7833, 7815-7831, 7815-7832, 7815-7833, 7815-7834, 7816-7832, 7816-7833, 7816-7834, 7816-7835, 7817-7833, 7817-7834, 7817-7835, 7817-7836, 7818-7834, 7818-7835, 7818-7836, 7818-7837, 7819-7835, 7819-7836, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7836, 7821-7837, 7821-7839, 7821-7840, 7822-7837, 7822-7838, 7822-7840, 7822-7841, 7823-7838, 7823-7839, 7823-7839, 7823-7840, 7823-7841, 7823-7842, 7824-7839, 7824-7840, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7843, 7825-7844, 7826-7842, 7826-7843, 7826-7844, 7826-7845, 7827-7842, 7827-7843, 7827-7844, 7827-7845, 7827-7846, 7828-7843, 7828-7844, 7828-7845, 7828-7847, 7829-7844, 7829-7845, 7829-7846, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7847, 7831-7848, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849. 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7853, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861 или 7846-7862 SEQ ID NO: 2, и где указанный модифицированный олигонуклеотид по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарен SEQ ID NO: 2.
В некоторых вариантах реализации предложено соединение, содержащее модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющий последовательность азотистых оснований, содержащую часть из по меньшей мере 8 смежных азотистых оснований, комплементарную равной по длине части азотистых оснований 1608-1627, 1685-1704, 1686-1705, 1751-1770, 1769-1784, 1871-1890, 1872-1891, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1878-1897, 1879-1894, 1879-1898, 2288-2307, 2808-2827, 2846-2865, 2852-2871, 2946-2965, 3773-3792, 3819-3838, 3825-3844, 3831-3850, 3834-3853, 3837-3856, 3843-3862, 4151-4166, 4151-4170, 4153-4172, 4159-4178, 4184-4203, 4211-4230, 4609-4628, 4612-4631, 4615-4634, 4621-4640, 4642-4661, 4648-4667, 4686-4705, 4689-4708, 4692-4711, 4698-4717, 4714-4733, 5270-5289, 5295-5314, 5296-5315, 5830-5849, 5890-5909, 5904-5923, 6406-6425, 6662-6681, 6674-6693, 6954-6973, 6960-6979, 6977-6996, 6979-6998, 6981-7000, 6983-6998, 6983-7002, 6984-7003, 6985-7000, 6985-7004, 6990-7009, 7122-7141, 7125-7144, 7151-7170, 7353-7372, 7362-7381, 7683-7702, 7688-7707, 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7694-7713, 7696-7711, 7696-7715, 7767-7786, 7785-7804, 7786-7801, 7787-7803, 7787-7805, 7787-7806, 7788-7803, 7788-7805, 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7805, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7808, 7792-7809, 7792-7810, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7811, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7818, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7820, 7805-7822, 7805-7824, 7806-7821, 7806-7823, 7806-7825, 7807-7824, 7807-7825, 7807-7826, 7808-7825, 7808-7827, 7809-7825, 7809-7826, 7809-7828, 7810-7825, 7810-7826, 7810-7827, 7810-7829, 7811-7828, 7811-7830, 7812-7829, 7812-7830, 7812-7831, 7813-7829, 7813-7831, 7813-7832, 7814-7833, 7815-7831, 7815-7832, 7815-7833, 7815-7834, 7816-7832, 7816-7833, 7816-7834, 7816-7835, 7817-7833, 7817-7834, 7817-7835, 7817-7836, 7818-7834, 7818-7835, 7818-7836, 7818-7837, 7819-7835, 7819-7836, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7836, 7821-7837, 7821-7839, 7821-7840, 7822-7837, 7822-7838, 7822-7840, 7822-7841, 7823-7838, 7823-7839, 7823-7839, 7823-7840, 7823-7841, 7823-7842, 7824-7839, 7824-7840, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7843, 7825-7844, 7826-7842, 7826-7843, 7826-7844, 7826-7845, 7827-7842, 7827-7843, 7827-7844, 7827-7845, 7827-7846, 7828-7843, 7828-7844, 7828-7845, 7828-7847, 7829-7844, 7829-7845, 7829-7846, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7847, 7831-7848, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7853, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861 и 7846-7862 SEQ ID NO: 2, и где последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарна SEQ ID NO: 2.
В некоторых вариантах реализации антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB. В некоторых вариантах реализации такие соединения или олигонуклеотиды, направленные на область нуклеиновой кислоты CFB, имеют часть смежных азотистых оснований, которая комплементарна равной по длине части азотистых оснований указанной области. Например, область может представлять собой часть из по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15 или 16 смежных азотистых оснований, комплементарную равной по длине части области, указанной в настоящем документе. В некоторых вариантах реализации соединение содержит или состоит из конъюгата и модифицированного олигонуклеотида, направленного на любые из следующих нуклеотидных областей SEQ ID NO: 1: 30-49, 48-63, 150-169, 151-170, 152-171, 154-169, 154-173, 156-171, 156-175, 157-176, 158-173, 158-177, 480-499, 600-619, 638-657, 644-663, 738-757, 1089-1108, 1135-1154, 1141-1160, 1147-1166, 1150-1169, 1153-1172, 1159-1178, 1162-1181, 1165-1184, 1171-1186, 1171-1190, 1173-1188, 1173-1192, 1175-1190, 1175-1194, 1177-1196, 1183-1202, 1208-1227, 1235-1254, 1298-1317, 1304-1323, 1310-1329, 1316-1335, 1319-1338, 1322-1341, 1328-1347, 1349-1368, 1355-1374, 1393-1412, 1396-1415, 1399-1418, 1405-1424, 1421-1440, 1621-1640, 1646-1665, 1646-1665, 1647-1666, 1689-1708, 1749-1768, 1763-1782, 1912-1931, 2073-2092, 2085-2104, 2166-2185, 2172-2191, 2189-2208, 2191-2210, 2193-2212, 2195-2210, 2195-2214, 2196-2215, 2197-2212, 2197-2216, 2202-2221, 2223-2238, 2223-2242, 2225-2240, 2226-2245, 2227-2242, 2227-2246, 2238-2257, 2241-2260, 2267-2286, 2361-2380, 2388-2407, 2397-2416, 2448-2467, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2459-2478, 2461-2476, 2461-2480, 2532-2551, 2550-2569, 2551-2566, 2551-2570, 2552-2568, 2552-2570, 2552-2571, 2553-2568, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2555-2570, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2573, 2557-2574, 2557-2575, 2557-2576, 2558-2575. 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2576, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2583, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2585, 2570-2587, 2570-2589, 2571-2586, 2571-2588, 2571-2590, 2572-2589, 2572-2590, 2572-2591. 2573-2590, 2573-2592, 2574-2590, 2574-2591, 2574-2593, 2575-2590, 2575-2591, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2595, 2577-2596, 2578-2594, 2578-2596, 2578-2597, 2579-2598, 2580-2596, 2580-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2582-2598, 2582-2599, 2582-2600, 2582-2601, 2583-2599, 2583-2600, 2583-2601, 2583-2602, 2584-2600, 2584-2601, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2601, 2586-2602, 2586-2604, 2586-2605, 2587-2602, 2587-2603, 2587-2605, 2587-2606, 2588-2603, 2588-2604, 2588-2605, 2588-2606, 2588-2607, 2589-2604, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2590-2609, 2591-2607, 2591-2608, 2591-2609, 2591-2610, 2592-2607. 2592-2608, 2592-2609. 2592-2610, 2592-2611, 2593-2608, 2593-2609, 2593-2610, 2593-2612, 2594-2609, 2594-2610. 2594-2611, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2612, 2596-2613, 2596-2614, 2596-2615, 2597-2612, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2618, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2631 и 2616-2631.
В некоторых вариантах реализации антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB. В некоторых вариантах реализации такие соединения или олигонуклеотиды, направленные на область нуклеиновой кислоты CFB, имеют часть смежных азотистых оснований, которая комплементарна равной по длине части азотистых оснований указанной области. Например, область может представлять собой часть из по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15 или 16 смежных азотистых оснований, комплементарную равной по длине части области, указанной в настоящем документе. В некоторых вариантах реализации соединение содержит или состоит из конъюгата и модифицированного олигонуклеотида, направленного на следующие нуклеотидные области SEQ ID NO: 2: 1608-1627, 1685-1704, 1686-1705, 1751-1770, 1769-1784, 1871-1890, 1872-1891, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1878-1897, 1879-1894, 1879-1898, 2288-2307, 2808-2827, 2846-2865, 2852-2871, 2946-2965, 3773-3792, 3819-3838, 3825-3844, 3831-3850, 3834-3853, 3837-3856, 3843-3862, 4151-4166, 4151-4170, 4153-4172, 4159-4178, 4184-4203, 4211-4230, 4609-4628, 4612-4631, 4615-4634, 4621-4640, 4642-4661, 4648-4667, 4686-4705, 4689-4708, 4692-4711, 4698-4717, 4714-4733, 5270-5289, 5295-5314, 5296-5315, 5830-5849, 5890-5909, 5904-5923, 6406-6425, 6662-6681, 6674-6693, 6954-6973, 6960-6979, 6977-6996, 6979-6998, 6981-7000, 6983-6998, 6983-7002, 6984-7003, 6985-7000, 6985-7004, 6990-7009, 7122-7141, 7125-7144, 7151-7170, 7353-7372, 7362-7381, 7683-7702, 7688-7707, 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7694-7713, 7696-7711, 7696-7715, 7767-7786, 7785-7804, 7786-7801, 7787-7803, 7787-7805, 7787-7806, 7788-7803, 7788-7805, 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7805, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7808, 7792-7809, 7792-7810, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7811, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7818, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7820, 7805-7822, 7805-7824, 7806-7821, 7806-7823, 7806-7825, 7807-7824, 7807-7825, 7807-7826, 7808-7825, 7808-7827, 7809-7825, 7809-7826, 7809-7828, 7810-7825, 7810-7826, 7810-7827, 7810-7829, 7811-7828, 7811-7830, 7812-7829, 7812-7830, 7812-7831, 7813-7829, 7813-7831, 7813-7832, 7814-7833, 7815-7831, 7815-7832, 7815-7833, 7815-7834, 7816-7832, 7816-7833, 7816-7834, 7816-7835, 7817-7833, 7817-7834, 7817-7835, 7817-7836, 7818-7834, 7818-7835, 7818-7836, 7818-7837, 7819-7835, 7819-7836, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7836, 7821-7837, 7821-7839, 7821-7840, 7822-7837, 7822-7838, 7822-7840, 7822-7841, 7823-7838, 7823-7839, 7823-7839, 7823-7840, 7823-7841, 7823-7842, 7824-7839, 7824-7840, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7843, 7825-7844, 7826-7842, 7826-7843, 7826-7844, 7826-7845, 7827-7842, 7827-7843, 7827-7844, 7827-7845, 7827-7846, 7828-7843, 7828-7844, 7828-7845, 7828-7847, 7829-7844, 7829-7845, 7829-7846, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7847, 7831-7848, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7853, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861 и 7846-7862.
В некоторых вариантах реализации соединение содержит или состоит из конъюгата и модифицированного олигонуклеотида, направленного на 3' НТО нуклеиновой кислоты CFB. В некоторых аспектах модифицированный олигонуклеотид направлен на диапазон нуклеотидов 2574-2626 нуклеиновой кислоты CFB, имеющей последовательность азотистых оснований SEQ ID NO: 1. В некоторых аспектах модифицированный олигонуклеотид имеет часть из по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15 или 16 смежных азотистых оснований, комплементарную равной по длине части в диапазоне нуклеотидов 2576-2626 нуклеиновой кислоты CFB, имеющей последовательность азотистых оснований SEQ ID NO: I.
В некоторых вариантах реализации соединение содержит или состоит из конъюгата и модифицированного олигонуклеотида, направленного на область нуклеиновой кислоты CFB, имеющую последовательность азотистых оснований SEQ ID NO: 1 в диапазоне азотистых оснований 2457-2631, 2457-2472, 2457-2474, 2457-2476, 2457-2566, 2457-2570, 2457-2571, 2457-2572, 2457-2573, 2457-2574, 2457-2575, 2457-2576, 2457-2577, 2457-2578, 2457-2579, 2457-2580, 2457-2581, 2457-2582, 2457-2583, 2457-2584, 2457-2585, 2457-2586, 2457-2587, 2457-2588, 2457-2589, 2457-2590, 2457-2591, 2457-2592, 2457-2593, 2457-2594, 2457-2595, 2457-2596, 2457-2597, 2457-2598, 2457-2599, 2457-2600, 2457-2601, 2457-2602, 2457-2603, 2457-2604, 2457-2605, 2457-2606, 2457-2607, 2457-2608, 2457-2609, 2457-2610, 2457-2611, 2457-2612, 2457-2613, 2457-2614, 2457-2615, 2457-2616, 2457-2617, 2457-2618, 2457-2619, 2457-2620, 2457-2621, 2457-2622, 2457-2623, 2457-2624, 2457-2625, 2457-2626, 2457-2627, 2457-2628, 2457-2629, 2457-2630, 2457-2631, 2459-2474, 2459-2476, 2459-2566, 2459-2570, 2459-2571, 2459-2572, 2459-2573, 2459-2574, 2459-2575, 2459-2576, 2459-2577, 2459-2578, 2459-2579, 2459-2580, 2459-2581, 2459-2582, 2459-2583, 2459-2584, 2459-2585, 2459-2586, 2459-2587, 2459-2588, 2459-2589, 2459-2590, 2459-2591, 2459-2592, 2459-2593, 2459-2594, 2459-2595, 2459-2596, 2459-2597, 2459-2598, 2459-2599, 2459-2600, 2459-2601, 2459-2602, 2459-2603, 2459-2604, 2459-2605, 2459-2606, 2459-2607, 2459-2608, 2459-2609, 2459-2610, 2459-2611, 2459-2612, 2459-2613, 2459-2614, 2459-2615, 2459-2616, 2459-2617, 2459-2618, 2459-2619, 2459-2620, 2459-2621, 2459-2622, 2459-2623, 2459-2624, 2459-2625, 2459-2626, 2459-2627, 2459-2628, 2459-2629, 2459-2630, 2459-2631, 2461-2476, 2461-2566, 2461-2570, 2461-2571, 2461-2572, 2461-2573, 2461-2574, 2461-2575, 2461-2576, 2461-2577, 2461-2578, 2461-2579, 2461-2580, 2461-2581, 2461-2582, 2461-2583, 2461-2584, 2461-2585, 2461-2586, 2461-2587, 2461-2588, 2461-2589, 2461-2590, 2461-2591, 2461-2592, 2461-2593, 2461-2594, 2461-2595, 2461-2596, 2461-2597, 2461-2598, 2461-2599, 2461-2600, 2461-2601, 2461-2602, 2461-2603, 2461-2604, 2461-2605, 2461-2606, 2461-2607, 2461-2608, 2461-2609, 2461-2610, 2461-2611, 2461-2612, 2461-2613, 2461-2614, 2461-2615, 2461-2616, 2461-2617, 2461-2618, 2461-2619, 2461-2620, 2461-2621, 2461-2622, 2461-2623, 2461-2624, 2461-2625, 2461-2626, 2461-2627, 2461-2628, 2461-2629, 2461-2630, 2461-2631, 2551-2566, 2551-2570, 2551-2571, 2551-2572, 2551-2573, 2551-2574, 2551-2575, 2551-2576, 2551-2577, 2551-2578, 2551-2579, 2551-2580, 2551-2581, 2551-2582, 2551-2583, 2551-2584, 2551-2585, 2551-2586, 2551-2587, 2551-2588, 2551-2589, 2551-2590, 2551-2591, 2551-2592, 2551-2593, 2551-2594, 2551-2595, 2551-2596, 2551-2597, 2551-2598, 2551-2599, 2551-2600, 2551-2601, 2551-2602. 2551-2603, 2551-2604, 2551-2605, 2551-2606, 2551-2607, 2551-2608, 2551-2609, 2551-2610, 2551-2611, 2551-2612, 2551-2613, 2551-2614, 2551-2615, 2551-2616, 2551-2617, 2551-2618, 2551-2619, 2551-2620, 2551-2621, 2551-2622, 2551-2623, 2551-2624, 2551-2625, 2551-2626, 2551-2627, 2551-2628, 2551-2629, 2551-2630, 2551-2631, 2553-2570, 2553-2571, 2553-2572, 2553-2573, 2553-2574, 2553-2575, 2553-2576, 2553-2577, 2553-2578, 2553-2579, 2553-2580, 2553-2581, 2553-2582, 2553-2583, 2553-2584, 2553-2585, 2553-2586, 2553-2587, 2553-2588, 2553-2589, 2553-2590, 2553-2591, 2553-2592, 2553-2593, 2553-2594, 2553-2595, 2553-2596, 2553-2597, 2553-2598, 2553-2599, 2553-2600, 2553-2601, 2553-2602, 2553-2603, 2553-2604, 2553-2605, 2553-2606, 2553-2607, 2553-2608, 2553-2609, 2553-2610, 2553-2611, 2553-2612, 2553-2613, 2553-2614, 2553-2615, 2553-2616, 2553-2617, 2553-2618, 2553-2619, 2553-2620, 2553-2621, 2553-2622, 2553-2623, 2553-2624, 2553-2625, 2553-2626, 2553-2627, 2553-2628, 2553-2629, 2553-2630, 2553-2631, 2554-2573, 2554-2574, 2554-2575, 2554-2576, 2554-2577, 2554-2578, 2554-2579, 2554-2580, 2554-2581, 2554-2582, 2554-2583, 2554-2584, 2554-2585, 2554-2586, 2554-2587, 2554-2588, 2554-2589, 2554-2590, 2554-2591, 2554-2592, 2554-2593, 2554-2594, 2554-2595, 2554-2596, 2554-2597, 2554-2598, 2554-2599, 2554-2600, 2554-2601, 2554-2602, 2554-2603, 2554-2604, 2554-2605, 2554-2606, 2554-2607, 2554-2608, 2554-2609, 2554-2610, 2554-2611, 2554-2612, 2554-2613, 2554-2614, 2554-2615, 2554-2616, 2554-2617, 2554-2618, 2554-2619, 2554-2620, 2554-2621, 2554-2622, 2554-2623, 2554-2624, 2554-2625, 2554-2626, 2554-2627, 2554-2628, 2554-2629, 2554-2630, 2554-2631, 2555-2572, 2555-2573, 2555-2574, 2555-2575, 2555-2576, 2555-2577, 2555-2578, 2555-2579, 2555-2580, 2555-2581, 2555-2582, 2555-2583, 2555-2584, 2555-2585, 2555-2586, 2555-2587, 2555-2588, 2555-2589, 2555-2590, 2555-2591, 2555-2592, 2555-2593, 2555-2594, 2555-2595, 2555-2596, 2555-2597, 2555-2598, 2555-2599, 2555-2600, 2555-2601, 2555-2602, 2555-2603, 2555-2604, 2555-2605, 2555-2606, 2555-2607, 2555-2608, 2555-2609, 2555-2610, 2555-2611, 2555-2612, 2555-2613, 2555-2614, 2555-2615, 2555-2616, 2555-2617, 2555-2618, 2555-2619, 2555-2620, 2555-2621, 2555-2622, 2555-2623, 2555-2624, 2555-2625, 2555-2626, 2555-2627, 2555-2628, 2555-2629, 2555-2630, 2555-2631, 2556-2573, 2556-2574, 2556-2575, 2556-2576, 2556-2577, 2556-2578, 2556-2579, 2556-2580, 2556-2581, 2556-2582, 2556-2583, 2556-2584, 2556-2585, 2556-2586, 2556-2587, 2556-2588, 2556-2589, 2556-2590, 2556-2591, 2556-2592, 2556-2593, 2556-2594, 2556-2595, 2556-2596, 2556-2597, 2556-2598, 2556-2599, 2556-2600, 2556-2601, 2556-2602, 2556-2603, 2556-2604, 2556-2605, 2556-2606, 2556-2607, 2556-2608, 2556-2609, 2556-2610, 2556-2611, 2556-2612, 2556-2613, 2556-2614, 2556-2615, 2556-2616, 2556-2617, 2556-2618, 2556-2619, 2556-2620, 2556-2621, 2556-2622, 2556-2623, 2556-2624, 2556-2625, 2556-2626, 2556-2627, 2556-2628, 2556-2629, 2556-2630, 2556-2631, 2557-2574, 2557-2575, 2557-2576, 2557-2577, 2557-2578, 2557-2579, 2557-2580, 2557-2581, 2557-2582, 2557-2583, 2557-2584, 2557-2585, 2557-2586, 2557-2587, 2557-2588, 2557-2589, 2557-2590, 2557-2591, 2557-2592, 2557-2593, 2557-2594, 2557-2595, 2557-2596, 2557-2597, 2557-2598, 2557-2599, 2557-2600, 2557-2601, 2557-2602, 2557-2603, 2557-2604, 2557-2605, 2557-2606, 2557-2607, 2557-2608, 2557-2609, 2557-2610, 2557-2611, 2557-2612, 2557-2613, 2557-2614, 2557-2615, 2557-2616, 2557-2617, 2557-2618, 2557-2619, 2557-2620, 2557-2621, 2557-2622, 2557-2623, 2557-2624, 2557-2625, 2557-2626, 2557-2627, 2557-2628, 2557-2629, 2557-2630, 2557-2631, 2558-2575, 2558-2576, 2558-2577, 2558-2578, 2558-2579, 2558-2580, 2558-2581, 2558-2582, 2558-2583, 2558-2584, 2558-2585, 2558-2586, 2558-2587, 2558-2588, 2558-2589, 2558-2590, 2558-2591, 2558-2592, 2558-2593, 2558-2594, 2558-2595, 2558-2596, 2558-2597, 2558-2598, 2558-2599, 2558-2600, 2558-2601, 2558-2602, 2558-2603, 2558-2604, 2558-2605, 2558-2606, 2558-2607, 2558-2608, 2558-2609, 2558-2610, 2558-2611, 2558-2612, 2558-2613, 2558-2614, 2558-2615, 2558-2616, 2558-2617, 2558-2618, 2558-2619, 2558-2620, 2558-2621, 2558-2622, 2558-2623, 2558-2624, 2558-2625, 2558-2626, 2558-2627, 2558-2628, 2558-2629, 2558-2630, 2558-2631, 2559-2576, 2559-2577, 2559-2578, 2559-2579, 2559-2580, 2559-2581, 2559-2582, 2559-2583, 2559-2584, 2559-2585, 2559-2586, 2559-2587, 2559-2588, 2559-2589, 2559-2590, 2559-2591, 2559-2592, 2559-2593, 2559-2594, 2559-2595, 2559-2596, 2559-2597, 2559-2598, 2559-2599. 2559-2600, 2559-2601, 2559-2602, 2559-2603, 2559-2604, 2559-2605, 2559-2606, 2559-2607, 2559-2608, 2559-2609, 2559-2610, 2559-2611, 2559-2612, 2559-2613, 2559-2614, 2559-2615, 2559-2616, 2559-2617, 2559-2618, 2559-2619, 2559-2620, 2559-2621, 2559-2622, 2559-2623, 2559-2624, 2559-2625, 2559-2626, 2559-2627, 2559-2628, 2559-2629, 2559-2630, 2559-2631, 2560-2577, 2560-2578, 2560-2579, 2560-2580, 2560-2581, 2560-2582, 2560-2583, 2560-2584, 2560-2585, 2560-2586, 2560-2587, 2560-2588, 2560-2589, 2560-2590, 2560-2591, 2560-2592, 2560-2593, 2560-2594, 2560-2595, 2560-2596, 2560-2597, 2560-2598, 2560-2599, 2560-2600, 2560-2601, 2560-2602, 2560-2603, 2560-2604, 2560-2605, 2560-2606, 2560-2607, 2560-2608, 2560-2609, 2560-2610, 2560-2611, 2560-2612, 2560-2613, 2560-2614, 2560-2615, 2560-2616, 2560-2617, 2560-2618, 2560-2619. 2560-2620, 2560-2621, 2560-2622, 2560-2623, 2560-2624, 2560-2625, 2560-2626, 2560-2627, 2560-2628, 2560-2629, 2560-2630, 2560-2631, 2561-2578, 2561-2579, 2561-2580, 2561-2581, 2561-2582, 2561-2583, 2561-2584, 2561-2585, 2561-2586, 2561-2587, 2561-2588, 2561-2589, 2561-2590, 2561-2591, 2561-2592, 2561-2593, 2561-2594, 2561-2595, 2561-2596, 2561-2597, 2561-2598, 2561-2599, 2561-2600, 2561-2601, 2561-2602, 2561-2603, 2561-2604, 2561-2605, 2561-2606, 2561-2607, 2561-2608, 2561-2609, 2561-2610, 2561-2611, 2561-2612, 2561-2613, 2561-2614, 2561-2615, 2561-2616, 2561-2617, 2561-2618, 2561-2619, 2561-2620, 2561-2621, 2561-2622, 2561-2623, 2561-2624, 2561-2625, 2561-2626, 2561-2627, 2561-2628, 2561-2629, 2561-2630, 2561-2631, 2562-2577, 2562-2578, 2562-2579, 2562-2580, 2562-2581, 2562-2582, 2562-2583, 2562-2584, 2562-2585, 2562-2586, 2562-2587, 2562-2588, 2562-2589, 2562-2590, 2562-2591, 2562-2592, 2562-2593, 2562-2594, 2562-2595, 2562-2596, 2562-2597, 2562-2598, 2562-2599, 2562-2600, 2562-2601, 2562-2602, 2562-2603, 2562-2604, 2562-2605, 2562-2606, 2562-2607, 2562-2608, 2562-2609, 2562-2610, 2562-2611, 2562-2612, 2562-2613, 2562-2614, 2562-2615, 2562-2616, 2562-2617, 2562-2618, 2562-2619, 2562-2620, 2562-2621, 2562-2622, 2562-2623, 2562-2624, 2562-2625, 2562-2626, 2562-2627, 2562-2628, 2562-2629, 2562-2630, 2562-2631, 2563-2580, 2563-2581, 2563-2582, 2563-2583, 2563-2584, 2563-2585, 2563-2586, 2563-2587, 2563-2588, 2563-2589, 2563-2590, 2563-2591, 2563-2592, 2563-2593, 2563-2594, 2563-2595, 2563-2596, 2563-2597, 2563-2598, 2563-2599, 2563-2600, 2563-2601, 2563-2602, 2563-2603, 2563-2604, 2563-2605, 2563-2606, 2563-2607, 2563-2608, 2563-2609, 2563-2610, 2563-2611, 2563-2612, 2563-2613, 2563-2614, 2563-2615, 2563-2616, 2563-2617, 2563-2618, 2563-2619, 2563-2620, 2563-2621, 2563-2622, 2563-2623, 2563-2624, 2563-2625, 2563-2626, 2563-2627, 2563-2628, 2563-2629, 2563-2630, 2563-2631, 2564-2581, 2564-2582, 2564-2583, 2564-2584, 2564-2585, 2564-2586, 2564-2587, 2564-2588, 2564-2589, 2564-2590, 2564-2591, 2564-2592, 2564-2593, 2564-2594, 2564-2595, 2564-2596, 2564-2597, 2564-2598, 2564-2599, 2564-2600, 2564-2601, 2564-2602, 2564-2603, 2564-2604, 2564-2605, 2564-2606, 2564-2607, 2564-2608, 2564-2609, 2564-2610, 2564-2611, 2564-2612, 2564-2613, 2564-2614, 2564-2615, 2564-2616, 2564-2617, 2564-2618, 2564-2619, 2564-2620, 2564-2621, 2564-2622, 2564-2623, 2564-2624, 2564-2625, 2564-2626, 2564-2627, 2564-2628, 2564-2629, 2564-2630, 2564-2631, 2565-2584, 2565-2585, 2565-2586, 2565-2587, 2565-2588, 2565-2589, 2565-2590, 2565-2591, 2565-2592, 2565-2593, 2565-2594, 2565-2595, 2565-2596, 2565-2597, 2565-2598, 2565-2599, 2565-2600, 2565-2601, 2565-2602, 2565-2603, 2565-2604, 2565-2605, 2565-2606, 2565-2607, 2565-2608, 2565-2609, 2565-2610, 2565-2611, 2565-2612, 2565-2613, 2565-2614, 2565-2615, 2565-2616, 2565-2617, 2565-2618, 2565-2619, 2565-2620, 2565-2621, 2565-2622, 2565-2623, 2565-2624, 2565-2625, 2565-2626, 2565-2627, 2565-2628, 2565-2629, 2565-2630, 2565-2631, 2566-2583, 2566-2584, 2566-2585, 2566-2586, 2566-2587, 2566-2588, 2566-2589, 2566-2590, 2566-2591, 2566-2592, 2566-2593, 2566-2594, 2566-2595, 2566-2596, 2566-2597, 2566-2598, 2566-2599, 2566-2600, 2566-2601, 2566-2602, 2566-2603, 2566-2604, 2566-2605, 2566-2606, 2566-2607, 2566-2608, 2566-2609, 2566-2610, 2566-2611, 2566-2612, 2566-2613, 2566-2614, 2566-2615, 2566-2616, 2566-2617, 2566-2618, 2566-2619, 2566-2620, 2566-2621, 2566-2622, 2566-2623, 2566-2624, 2566-2625, 2566-2626, 2566-2627, 2566-2628, 2566-2629, 2566-2630, 2566-2631, 2567-2584, 2567-2585, 2567-2586, 2567-2587, 2567-2588, 2567-2589, 2567-2590, 2567-2591, 2567-2592, 2567-2593, 2567-2594, 2567-2595, 2567-2596, 2567-2597, 2567-2598, 2567-2599, 2567-2600, 2567-2601, 2567-2602, 2567-2603, 2567-2604, 2567-2605, 2567-2606, 2567-2607, 2567-2608, 2567-2609, 2567-2610, 2567-2611, 2567-2612, 2567-2613, 2567-2614, 2567-2615, 2567-2616, 2567-2617, 2567-2618, 2567-2619, 2567-2620, 2567-2621, 2567-2622, 2567-2623, 2567-2624, 2567-2625, 2567-2626, 2567-2627, 2567-2628, 2567-2629, 2567-2630, 2567-2631, 2568-2585, 2568-2586, 2568-2587, 2568-2588, 2568-2589, 2568-2590, 2568-2591, 2568-2592, 2568-2593, 2568-2594, 2568-2595, 2568-2596, 2568-2597, 2568-2598. 2568-2599, 2568-2600, 2568-2601, 2568-2602, 2568-2603, 2568-2604, 2568-2605, 2568-2606, 2568-2607, 2568-2608, 2568-2609, 2568-2610, 2568-2611, 2568-2612, 2568-2613, 2568-2614, 2568-2615, 2568-2616, 2568-2617, 2568-2618, 2568-2619, 2568-2620, 2568-2621, 2568-2622, 2568-2623, 2568-2624, 2568-2625, 2568-2626, 2568-2627. 2568-2628, 2568-2629, 2568-2630, 2568-2631, 2569-2586, 2569-2587, 2569-2588, 2569-2589, 2569-2590, 2569-2591, 2569-2592, 2569-2593, 2569-2594, 2569-2595, 2569-2596, 2569-2597, 2569-2598, 2569-2599, 2569-2600, 2569-2601, 2569-2602, 2569-2603, 2569-2604, 2569-2605, 2569-2606, 2569-2607, 2569-2608, 2569-2609, 2569-2610, 2569-2611, 2569-2612, 2569-2613, 2569-2614, 2569-2615, 2569-2616, 2569-2617, 2569-2618, 2569-2619, 2569-2620, 2569-2621, 2569-2622, 2569-2623, 2569-2624, 2569-2625, 2569-2626, 2569-2627, 2569-2628, 2569-2629, 2569-2630, 2569-2631, 2569-2586, 2569-2587, 2569-2588, 2569-2589, 2569-2590, 2569-2591, 2569-2592, 2569-2593, 2569-2594, 2569-2595, 2569-2596, 2569-2597, 2569-2598, 2569-2599, 2569-2600, 2569-2601, 2569-2602, 2569-2603, 2569-2604, 2569-2605, 2569-2606, 2569-2607, 2569-2608, 2569-2609, 2569-2610, 2569-2611, 2569-2612, 2569-2613, 2569-2614, 2569-2615, 2569-2616, 2569-2617, 2569-2618, 2569-2619, 2569-2620, 2569-2621, 2569-2622, 2569-2623, 2569-2624, 2569-2625, 2569-2626, 2569-2627, 2569-2628, 2569-2629, 2569-2630, 2569-2631, 2571-2588, 2571-2589, 2571-2590, 2571-2591, 2571-2592, 2571-2593, 2571-2594, 2571-2595, 2571-2596, 2571-2597, 2571-2598, 2571-2599, 2571-2600, 2571-2601, 2571-2602, 2571-2603, 2571-2604, 2571-2605, 2571-2606, 2571-2607, 2571-2608, 2571-2609, 2571-2610, 2571-2611, 2571-2612, 2571-2613, 2571-2614, 2571-2615, 2571-2616, 2571-2617, 2571-2618, 2571-2619, 2571-2620, 2571-2621, 2571-2622, 2571-2623, 2571-2624, 2571-2625, 2571-2626, 2571-2627, 2571-2628, 2571-2629, 2571-2630, 2571-2631, 2572-2589, 2572-2590, 2572-2591, 2572-2592, 2572-2593, 2572-2594, 2572-2595, 2572-2596, 2572-2597, 2572-2598, 2572-2599, 2572-2600, 2572-2601, 2572-2602, 2572-2603, 2572-2604, 2572-2605, 2572-2606, 2572-2607, 2572-2608, 2572-2609. 2572-2610, 2572-2611, 2572-2612, 2572-2613, 2572-2614, 2572-2615, 2572-2616, 2572-2617, 2572-2618, 2572-2619, 2572-2620, 2572-2621, 2572-2622, 2572-2623, 2572-2624, 2572-2625, 2572-2626, 2572-2627, 2572-2628, 2572-2629, 2572-2630, 2572-2631, 2573-2590, 2573-2591, 2573-2592, 2573-2593, 2573-2594, 2573-2595, 2573-2596, 2573-2597, 2573-2598, 2573-2599, 2573-2600, 2573-2601, 2573-2602, 2573-2603, 2573-2604, 2573-2605, 2573-2606, 2573-2607, 2573-2608, 2573-2609, 2573-2610, 2573-2611, 2573-2612, 2573-2613, 2573-2614, 2573-2615, 2573-2616, 2573-2617, 2573-2618, 2573-2619, 2573-2620, 2573-2621, 2573-2622, 2573-2623, 2573-2624, 2573-2625, 2573-2626, 2573-2627, 2573-2628, 2573-2629, 2573-2630, 2573-2631, 2574-2591, 2574-2592, 2574-2593, 2574-2594, 2574-2595, 2574-2596, 2574-2597, 2574-2598, 2574-2599, 2574-2600, 2574-2601, 2574-2602, 2574-2603, 2574-2604, 2574-2605, 2574-2606, 2574-2607, 2574-2608, 2574-2609, 2574-2610, 2574-2611, 2574-2612, 2574-2613, 2574-2614, 2574-2615, 2574-2616, 2574-2617, 2574-2618, 2574-2619, 2574-2620, 2574-2621, 2574-2622, 2574-2623, 2574-2624, 2574-2625, 2574-2626, 2574-2627, 2574-2628, 2574-2629, 2574-2630, 2574-2631, 2575-2592, 2575-2593, 2575-2594, 2575-2595, 2575-2596, 2575-2597, 2575-2598, 2575-2599, 2575-2600, 2575-2601, 2575-2602, 2575-2603, 2575-2604, 2575-2605, 2575-2606, 2575-2607, 2575-2608, 2575-2609, 2575-2610, 2575-2611, 2575-2612, 2575-2613, 2575-2614, 2575-2615, 2575-2616, 2575-2617, 2575-2618, 2575-2619, 2575-2620, 2575-2621. 2575-2622, 2575-2623, 2575-2624, 2575-2625, 2575-2626, 2575-2627, 2575-2628, 2575-2629, 2575-2630, 2575-2631, 2576-2593, 2576-2594, 2576-2595, 2576-2596, 2576-2597, 2576-2598, 2576-2599, 2576-2600, 2576-2601, 2576-2602, 2576-2603, 2576-2604, 2576-2605, 2576-2606, 2576-2607, 2576-2608, 2576-2609, 2576-2610, 2576-2611, 2576-2612, 2576-2613, 2576-2614, 2576-2615, 2576-2616, 2576-2617, 2576-2618, 2576-2619, 2576-2620, 2576-2621, 2576-2622, 2576-2623, 2576-2624, 2576-2625, 2576-2626, 2576-2627, 2576-2628, 2576-2629, 2576-2630, 2576-2631, 2577-2594, 2577-2595, 2577-2596, 2577-2597, 2577-2598, 2577-2599, 2577-2600, 2577-2601, 2577-2602, 2577-2603, 2577-2604, 2577-2605, 2577-2606, 2577-2607, 2577-2608, 2577-2609, 2577-2610, 2577-2611, 2577-2612, 2577-2613, 2577-2614, 2577-2615, 2577-2616, 2577-2617, 2577-2618, 2577-2619, 2577-2620, 2577-2621, 2577-2622, 2577-2623, 2577-2624, 2577-2625, 2577-2626, 2577-2627, 2577-2628, 2577-2629, 2577-2630, 2577-2631, 2578-2597, 2578-2598, 2578-2599, 2578-2600, 2578-2601, 2578-2602, 2578-2603, 2578-2604, 2578-2605, 2578-2606, 2578-2607, 2578-2608, 2578-2609, 2578-2610, 2578-2611, 2578-2612, 2578-2613, 2578-2614, 2578-2615, 2578-2616, 2578-2617, 2578-2618, 2578-2619, 2578-2620, 2578-2621, 2578-2622, 2578-2623, 2578-2624, 2578-2625, 2578-2626, 2578-2627, 2578-2628, 2578-2629, 2578-2630, 2578-2631, 2579-2598, 2579-2599, 2579-2600, 2579-2601, 2579-2602, 2579-2603, 2579-2604, 2579-2605, 2579-2606, 2579-2607, 2579-2608, 2579-2609, 2579-2610, 2579-2611, 2579-2612, 2579-2613, 2579-2614, 2579-2615, 2579-2616, 2579-2617, 2579-2618, 2579-2619, 2579-2620, 2579-2621, 2579-2622, 2579-2623, 2579-2624, 2579-2625, 2579-2626, 2579-2627, 2579-2628, 2579-2629, 2579-2630, 2579-2631, 2580-2598, 2580-2599, 2580-2600, 2580-2601, 2580-2602, 2580-2603. 2580-2604, 2580-2605, 2580-2606, 2580-2607, 2580-2608, 2580-2609, 2580-2610, 2580-2611, 2580-2612, 2580-2613. 2580-2614, 2580-2615, 2580-2616, 2580-2617, 2580-2618, 2580-2619, 2580-2620, 2580-2621, 2580-2622, 2580-2623, 2580-2624, 2580-2625, 2580-2626, 2580-2627, 2580-2628, 2580-2629, 2580-2630, 2580-2631, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2581-2601, 2581-2602, 2581-2603, 2581-2604, 2581-2605, 2581-2606, 2581-2607, 2581-2608, 2581-2609, 2581-2610, 2581-2611, 2581-2612, 2581-2613, 2581-2614, 2581-2615, 2581-2616, 2581-2617, 2581-2618, 2581-2619, 2581-2620, 2581-2621, 2581-2622, 2581-2623, 2581-2624, 2581-2625, 2581-2626, 2581-2627, 2581-2628, 2581-2629, 2581-2630, 2581-2631, 2582-2600, 2582-2601, 2582-2602, 2582-2603, 2582-2604, 2582-2605, 2582-2606, 2582-2607, 2582-2608, 2582-2609, 2582-2610, 2582-2611, 2582-2612, 2582-2613, 2582-2614, 2582-2615, 2582-2616, 2582-2617, 2582-2618, 2582-2619, 2582-2620, 2582-2621, 2582-2622, 2582-2623, 2582-2624, 2582-2625, 2582-2626, 2582-2627, 2582-2628, 2582-2629, 2582-2630, 2582-2631, 2583-2601, 2583-2602, 2583-2603, 2583-2604, 2583-2605, 2583-2606, 2583-2607, 2583-2608, 2583-2609, 2583-2610, 2583-2611, 2583-2612, 2583-2613, 2583-2614, 2583-2615, 2583-2616, 2583-2617, 2583-2618, 2583-2619, 2583-2620, 2583-2621, 2583-2622, 2583-2623, 2583-2624, 2583-2625, 2583-2626, 2583-2627, 2583-2628, 2583-2629, 2583-2630, 2583-2631, 2585-2603, 2585-2604, 2585-2605, 2585-2606, 2585-2607, 2585-2608, 2585-2609, 2585-2610, 2585-2611, 2585-2612, 2585-2613, 2585-2614, 2585-2615, 2585-2616, 2585-2617, 2585-2618, 2585-2619, 2585-2620, 2585-2621, 2585-2622, 2585-2623, 2585-2624, 2585-2625, 2585-2626, 2585-2627, 2585-2628, 2585-2629, 2585-2630, 2585-2631, 2586-2604, 2586-2605, 2586-2606, 2586-2607, 2586-2608, 2586-2609, 2586-2610, 2586-2611, 2586-2612, 2586-2613, 2586-2614, 2586-2615, 2586-2616, 2586-2617, 2586-2618, 2586-2619, 2586-2620, 2586-2621, 2586-2622, 2586-2623, 2586-2624, 2586-2625, 2586-2626, 2586-2627, 2586-2628, 2586-2629, 2586-2630, 2586-2631, 2587-2605, 2587-2606, 2587-2607, 2587-2608, 2587-2609, 2587-2610, 2587-2611, 2587-2612, 2587-2613, 2587-2614, 2587-2615, 2587-2616, 2587-2617, 2587-2618, 2587-2619, 2587-2620, 2587-2621, 2587-2622, 2587-2623, 2587-2624, 2587-2625, 2587-2626, 2587-2627, 2587-2628, 2587-2629, 2587-2630, 2587-2631, 2588-2606, 2588-2607, 2588-2608, 2588-2609, 2588-2610, 2588-2611, 2588-2612, 2588-2613, 2588-2614, 2588-2615, 2588-2616, 2588-2617, 2588-2618, 2588-2619, 2588-2620, 2588-2621, 2588-2622, 2588-2623, 2588-2624, 2588-2625, 2588-2626, 2588-2627, 2588-2628, 2588-2629, 2588-2630, 2588-2631, 2589-2607, 2589-2608, 2589-2609, 2589-2610, 2589-2611, 2589-2612, 2589-2613, 2589-2614, 2589-2615, 2589-2616, 2589-2617, 2589-2618, 2589-2619, 2589-2620, 2589-2621, 2589-2622, 2589-2623, 2589-2624, 2589-2625, 2589-2626, 2589-2627, 2589-2628, 2589-2629, 2589-2630, 2589-2631, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2590-2610, 2590-2611, 2590-2612, 2590-2613, 2590-2614, 2590-2615, 2590-2616, 2590-2617, 2590-2618, 2590-2619, 2590-2620, 2590-2621, 2590-2622, 2590-2623, 2590-2624, 2590-2625, 2590-2626. 2590-2627, 2590-2628, 2590-2629, 2590-2630, 2590-2631, 2591-2610, 2591-2611, 2591-2612, 2591-2613, 2591-2614, 2591-2615, 2591-2616, 2591-2617, 2591-2618, 2591-2619, 2591-2620, 2591-2621, 2591-2622, 2591-2623, 2591-2624, 2591-2625, 2591-2626, 2591-2627, 2591-2628, 2591-2629, 2591-2630, 2591-2631, 2592-2611, 2592-2612, 2592-2613, 2592-2614, 2592-2615, 2592-2616, 2592-2617, 2592-2618, 2592-2619, 2592-2620, 2592-2621, 2592-2622, 2592-2623, 2592-2624, 2592-2625, 2592-2626, 2592-2627, 2592-2628, 2592-2629, 2592-2630, 2592-2631, 2593-2608, 2593-2612, 2593-2613, 2593-2614, 2593-2615, 2593-2616, 2593-2617, 2593-2618, 2593-2619, 2593-2620, 2593-2621, 2593-2622, 2593-2623, 2593-2624, 2593-2625, 2593-2626, 2593-2627, 2593-2628, 2593-2629, 2593-2630, 2593-2631, 2594-2612, 2594-2613, 2594-2614, 2594-2615, 2594-2616, 2594-2617, 2594-2618, 2594-2619, 2594-2620, 2594-2621, 2594-2622, 2594-2623, 2594-2624, 2594-2625, 2594-2626, 2594-2627, 2594-2628, 2594-2629, 2594-2630, 2594-2631, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2595-2615, 2595-2616, 2595-2617, 2595-2618, 2595-2619, 2595-2620, 2595-2621, 2595-2622, 2595-2623, 2595-2624, 2595-2625, 2595-2626, 2595-2627, 2595-2628, 2595-2629, 2595-2630, 2595-2631, 2596-2614, 2596-2615, 2596-2616, 2596-2617, 2596-2618, 2596-2619, 2596-2620, 2596-2621, 2596-2622, 2596-2623, 2596-2624, 2596-2625, 2596-2626, 2596-2627, 2596-2628, 2596-2629, 2596-2630, 2596-2631, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2597-2617, 2597-2618, 2597-2619, 2597-2620, 2597-2621, 2597-2622, 2597-2623, 2597-2624, 2597-2625, 2597-2626, 2597-2627, 2597-2628, 2597-2629, 2597-2630, 2597-2631, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2598-2618, 2598-2619, 2598-2620, 2598-2621, 2598-2622, 2598-2623, 2598-2624, 2598-2625, 2598-2626, 2598-2627, 2598-2628, 2598-2629, 2598-2630, 2598-2631, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2599-2619, 2599-2620, 2599-2621, 2599-2622, 2599-2623, 2599-2624, 2599-2625, 2599-2626, 2599-2627, 2599-2628, 2599-2629, 2599-2630, 2599-2631, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2600-2620, 2600-2621, 2600-2622, 2600-2623, 2600-2624, 2600-2625, 2600-2626, 2600-2627, 2600-2628, 2600-2629, 2600-2630, 2600-2631, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2601-2621, 2601-2622, 2601-2623, 2601-2624, 2601-2625, 2601-2626, 2601-2627, 2601-2628, 2601-2629, 2601-2630, 2601-2631, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2602-2622, 2602-2623, 2602-2624, 2602-2625, 2602-2626, 2602-2627, 2602-2628, 2602-2629, 2602-2630, 2602-2631, 2603-2620, 2603-2621, 2603-2622, 2603-2623, 2603-2624, 2603-2625, 2603-2626, 2603-2627, 2603-2628, 2603-2629, 2603-2630, 2603-2631, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2604-2624, 2604-2625, 2604-2626, 2604-2627, 2604-2628, 2604-2629, 2604-2630, 2604-2631, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2605-2625, 2605-2626, 2605-2627, 2605-2628, 2605-2629, 2605-2630, 2605-2631, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2606-2626, 2606-2627, 2606-2628, 2606-2629, 2606-2630, 2606-2631, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2607-2627, 2607-2628, 2607-2629, 2607-2630, 2607-2631, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2608-2628, 2608-2629, 2608-2630, 2608-2631, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2609-2629, 2609-2630, 2609-2631, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2610-2630, 2610-2631, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2611-2631, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2631 или 2616-2631. В некоторых аспектах антисмысловые соединения или олигонуклеотиды направлены на по меньшей мере 8, 9, 10, 11, 12, 13, 14, 15 или 16 смежных азотистых оснований в пределах вышеуказанных областей азотистых оснований.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 1, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 50% ингибирование: 30-49, 48-63, 150-169, 151-170, 152-171, 154-169, 154-173, 156-171, 156-175, 157-176, 158-173, 158-177, 480-499, 600-619, 638-657, 644-663, 738-757, 1089-1108, 1135-1154, 1141-1160,1147-1166, 1150-1169, 1153-1172, 1159-1178, 1162-1181, 1165-1184, 1171-1186, 1171-1190, 1173-1188, 1173-1192, 1175-1190, 1175-1194, 1177-1196, 1183-1202, 1208-1227, 1235-1254, 1298-1317, 1304-1323, 1310-1329, 1316-1335, 1319-1338, 1322-1341, 1328-1347, 1349-1368, 1355-1374, 1393-1412, 1396-1415, 1399-1418, 1405-1424, 1421-1440, 1621-1640, 1646-1665, 1646-1665, 1647-1666, 1689-1708, 1749-1768, 1763-1782, 1912-1931, 2073-2092, 2085-2104, 2166-2185, 2172-2191. 2189-2208, 2191-2210, 2193-2212, 2195-2210, 2195-2214, 2196-2215, 2197-2212, 2197-2216, 2202-2221, 2223-2238, 2223-2242, 2225-2240, 2226-2245, 2227-2242, 2227-2246, 2238-2257, 2241-2260, 2267-2286, 2361-2380, 2388-2407, 2397-2416, 2448-2467, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2459-2478, 2461-2476, 2461-2480, 2532-2551, 2550-2569, 2551-2566, 2551-2570, 2552-2568, 2552-2570, 2552-2571, 2553-2568, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2555-2570, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2573, 2557-2574, 2557-2575, 2557-2576, 2558-2575, 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2576, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2583, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2585, 2570-2587, 2570-2589, 2571-2586, 2571-2588, 2571-2590, 2572-2589, 2572-2590, 2572-2591, 2573-2590, 2573-2592, 2574-2590, 2574-2591, 2574-2593, 2575-2590, 2575-2591, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2595, 2577-2596, 2578-2594, 2578-2596, 2578-2597, 2579-2598, 2580-2596, 2580-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2582-2598, 2582-2599, 2582-2600, 2582-2601, 2583-2599, 2583-2600, 2583-2601, 2583-2602, 2584-2600, 2584-2601, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2601, 2586-2602, 2586-2604, 2586-2605, 2587-2602, 2587-2603, 2587-2605, 2587-2606, 2588-2603, 2588-2604, 2588-2605, 2588-2606, 2588-2607, 2589-2604, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2590-2609, 2591-2607, 2591-2608, 2591-2609, 2591-2610, 2592-2607, 2592-2608, 2592-2609, 2592-2610, 2592-2611, 2593-2608, 2593-2609, 2593-2610, 2593-2612, 2594-2609, 2594-2610, 2594-2611, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2612, 2596-2613, 2596-2614, 2596-2615, 2597-2612, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2618, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2631 и 2616-2631.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 2, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 50% ингибирование: 1608-1627, 1685-1704, 1686-1705, 1751-1770, 1769-1784, 1871-1890, 1872-1891, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1878-1897, 1879-1894, 1879-1898, 2288-2307, 2808-2827, 2846-2865, 2852-2871, 2946-2965, 3773-3792, 3819-3838, 3825-3844, 3831-3850, 3834-3853, 3837-3856, 3843-3862, 4151-4166, 4151-4170, 4153-4172, 4159-4178, 4184-4203, 4211-4230, 4609-4628, 4612-4631, 4615-4634, 4621-4640, 4642-4661, 4648-4667, 4686-4705, 4689-4708, 4692-4711, 4698-4717, 4714-4733, 5270-5289, 5295-5314, 5296-5315, 5830-5849, 5890-5909, 5904-5923, 6406-6425, 6662-6681, 6674-6693, 6954-6973, 6960-6979, 6977-6996, 6979-6998, 6981-7000, 6983-6998, 6983-7002, 6984-7003, 6985-7000, 6985-7004, 6990-7009, 7122-7141, 7125-7144, 7151-7170, 7353-7372, 7362-7381, 7683-7702, 7688-7707, 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7694-7713, 7696-7711, 7696-7715, 7767-7786, 7785-7804, 7786-7801, 7787-7803, 7787-7805, 7787-7806, 7788-7803, 7788-7805. 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7805, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7808, 7792-7809, 7792-7810, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7811, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7818, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7820, 7805-7822, 7805-7824, 7806-7821, 7806-7823, 7806-7825, 7807-7824, 7807-7825, 7807-7826, 7808-7825, 7808-7827, 7809-7825, 7809-7826, 7809-7828, 7810-7825, 7810-7826, 7810-7827, 7810-7829, 7811-7828, 7811-7830, 7812-7829, 7812-7830, 7812-7831, 7813-7829, 7813-7831, 7813-7832, 7814-7833, 7815-7831, 7815-7832, 7815-7833, 7815-7834, 7816-7832, 7816-7833, 7816-7834, 7816-7835, 7817-7833, 7817-7834, 7817-7835, 7817-7836, 7818-7834, 7818-7835, 7818-7836, 7818-7837, 7819-7835, 7819-7836, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7836, 7821-7837, 7821-7839, 7821-7840, 7822-7837, 7822-7838, 7822-7840, 7822-7841, 7823-7838, 7823-7839, 7823-7839, 7823-7840, 7823-7841, 7823-7842, 7824-7839, 7824-7840, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7843, 7825-7844, 7826-7842, 7826-7843, 7826-7844, 7826-7845, 7827-7842, 7827-7843, 7827-7844, 7827-7845, 7827-7846, 7828-7843, 7828-7844, 7828-7845, 7828-7847, 7829-7844, 7829-7845, 7829-7846, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7847, 7831-7848, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7853, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861 и 7846-7862.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 1, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 60% ингибирование: 48-63, 150-169, 152-171, 154-169, 154-173, 156-171, 156-175, 158-173, 158-177, 600-619, 1135-1154, 1141-1160, 1147-1166, 1153-1172, 1171-1186, 1173-1188, 1175-1190, 1749-1768, 1763-1782, 1763-1782, 1912-1931, 2189-2208, 2191-2210, 2193-2212, 2195-2210, 2195-2214, 2197-2212, 2197-2216, 2223-2238, 2225-2240, 2227-2242, 2238-2257, 2448-2467, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2459-2478, 2461-2476, 2461-2480, 2550-2569, 2551-2566, 2552-2571, 2553-2568, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2574, 2557-2575, 2557-2576, 2558-2575, 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2583, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2587, 2570-2589, 2571-2588, 2572-2590, 2572-2591, 2573-2590, 2573-2592, 2574-2591, 2574-2593, 2575-2590, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2595, 2577-2596, 2578-2594, 2578-2597, 2579-2598, 2580-2596, 2580-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2598, 2581-2599, 2581-2600, 2582-2598, 2582-2599, 2582-2600, 2582-2601, 2583-2599, 2583-2600, 2583-2601, 2583-2602, 2584-2600, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2602, 2586-2604, 2586-2605, 2587-2603, 2587-2605, 2587-2606, 2588-2603, 2588-2604, 2588-2606, 2588-2607, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2608, 2590-2609, 2591-2607, 2591-2609, 2591-2610, 2592-2608, 2592-2609, 2592-2611, 2593-2608, 2593-2609, 2593-2612, 2594-2609, 2594-2610, 2594-2611, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2612, 2596-2613, 2596-2614, 2596-2615, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2618, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2626, 2611-2627, 2611-2628, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2630, 2615-2631, 2615-2631 и 2616-2631. В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 2, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 60% ингибирование: 1685-1704, 1686-1705, 1769-1784, 1871-1890, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1879-1894, 1879-1898, 2808-2827, 3819-3838, 3825-3844, 3831-3850, 3837-3856, 4151-4166, 5890-5909, 5904-5923, 5904-5923, 6406-6425, 6977-6996, 6979-6998, 6981-7000, 6983-6998, 6983-7002, 6985-7000, 6985-7004, 7122-7141, 7683-7702, 7688-7707, 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7696-7711, 7696-7715, 7786-7801, 7787-7806, 7788-7803, 7788-7805, 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7809, 7792-7810, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7818, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7822, 7805-7824, 7806-7823, 7806-7825, 7807-7824, 7807-7825, 7807-7826, 7808-7825, 7808-7827, 7809-7826, 7809-7828, 7810-7825, 7810-7827, 7810-7829, 7811-7828, 7811-7830, 7812-7829, 7812-7830, 7812-7831, 7813-7829, 7813-7832, 7814-7833, 7815-7831, 7815-7832, 7815-7833, 7815-7834, 7816-7832, 7816-7833, 7816-7834, 7816-7835, 7817-7833, 7817-7834, 7817-7835, 7817-7836, 7818-7834, 7818-7835, 7818-7836, 7818-7837, 7819-7835, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7837, 7821-7839, 7821-7840, 7822-7838, 7822-7840, 7822-7841, 7823-7838, 7823-7839, 7823-7841, 7823-7842, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7843, 7825-7844, 7826-7842, 7826-7844, 7826-7845, 7827-7843, 7827-7844, 7827-7846, 7828-7843, 7828-7844, 7828-7847, 7829-7844, 7829-7845, 7829-7846, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7847, 7831-7848, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7853, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861, 7846-7862 и 7847-7862.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 1, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 70% ингибирование: 48-63, 150-169, 152-171, 154-169, 154-173, 156-171, 156-175, 158-173, 158-177, 1135-1154, 1141-1160, 1147-1166, 1171-1186, 1173-1188, 1175-1190, 1749-1768, 1763-1782, 1912-1931, 2193-2212, 2195-2210, 2195-2214, 2197-2212, 2197-2216, 2223-2238, 2225-2240, 2227-2242, 2453-2472, 2455-2474, 2457-2472, 2457-2476, 2459-2474, 2461-2476, 2461-2480, 2550-2569, 2551-2566, 2552-2571, 2553-2570, 2553-2571, 2553-2572, 2554-2571, 2554-2572, 2554-2573, 2554-2573, 2555-2572, 2555-2574, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2574, 2557-2576, 2558-2575, 2558-2576, 2558-2577, 2559-2576, 2559-2577, 2559-2578. 2560-2577, 2560-2578, 2560-2579, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2578, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2566-2585, 2567-2582, 2567-2584, 2567-2586, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2587, 2570-2589, 2571-2588, 2571-2590, 2572-2589, 2572-2591, 2573-2590, 2573-2592, 2574-2591, 2574-2593, 2575-2592, 2575-2594, 2576-2593, 2576-2595, 2577-2594, 2577-2596, 2578-2597, 2579-2598, 2580-2596, 2580-2598, 2580-2599, 2581-2597, 2581-2600, 2582-2598, 2582-2600, 2582-2601, 2583-2599, 2583-2601, 2583-2602, 2584-2600, 2584-2602, 2584-2603, 2585-2601, 2585-2603, 2585-2604, 2586-2605, 2587-2606, 2588-2604, 2588-2606, 2588-2607, 2589-2605, 2589-2606, 2589-2607, 2589-2608, 2590-2605, 2590-2606, 2590-2607, 2590-2609, 2591-2607, 2591-2610, 2592-2611, 2593-2608, 2593-2612, 2594-2609, 2594-2610, 2594-2612, 2594-2613, 2595-2610, 2595-2611, 2595-2612, 2595-2613, 2595-2614, 2596-2611, 2596-2614, 2596-2615, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2615, 2599-2616, 2599-2617, 2599-2618, 2600-2615, 2600-2616, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2618, 2601-2619, 2601-2620, 2602-2617, 2602-2618, 2602-2619, 2602-2620, 2602-2621, 2603-2619, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2626, 2608-2627, 2609-2624, 2609-2625, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2627, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2629, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2630, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630, 2615-2630, 2615-2631 и 2616-2631.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 2, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 70% ингибирование: 1685-1704, 1686-1705, 1769-1784, 1871-1890, 1873-1892, 1875-1890, 1875-1894, 1877-1892, 1877-1896, 1879-1894, 1879-1898, 3819-3838, 3825-3844, 3831-3850, 4151-4166, 5890-5909, 5904-5923, 5904-5923, 6406-6425, 6983-6998, 6983-7002, 6985-7000, 6985-7004, 7688-7707. 7690-7709, 7692-7707, 7692-7711, 7694-7709, 7696-7711, 7696-7715, 7786-7801, 7787-7806, 7788-7805, 7788-7806, 7788-7807, 7789-7806, 7789-7807, 7789-7808, 7790-7807, 7790-7809. 7791-7808, 7791-7809, 7791-7810, 7792-7809, 7792-7811, 7793-7810, 7793-7811, 7793-7812, 7794-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7813, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7801-7820, 7802-7817, 7802-7819, 7802-7821, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7822, 7805-7824, 7806-7823, 7806-7825, 7807-7824, 7807-7826, 7808-7825, 7808-7827, 7809-7826, 7809-7828, 7810-7827, 7811-7828, 7811-7830, 7812-7829, 7812-7831, 7813-7832, 7814-7833, 7815-7831, 7815-7833, 7815-7834, 7816-7832, 7816-7835, 7817-7833, 7817-7835, 7817-7836, 7818-7834, 7818-7836, 7818-7837, 7819-7835, 7819-7837, 7819-7838, 7820-7836, 7820-7838, 7820-7839, 7821-7840, 7822-7841, 7823-7839, 7823-7841, 7823-7842, 7824-7840, 7824-7841, 7824-7842, 7824-7843, 7825-7840, 7825-7841, 7825-7842, 7825-7844, 7826-7842, 7826-7845, 7827-7846, 7828-7843, 7828-7847, 7829-7844, 7829-7845, 7829-7847, 7829-7848, 7830-7845, 7830-7846, 7830-7847, 7830-7848, 7830-7849, 7831-7846, 7831-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7850, 7834-7851, 7834-7852, 7834-7853, 7835-7850, 7835-7851, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7853, 7836-7854, 7836-7855, 7837-7852, 7837-7853, 7837-7854, 7837-7855, 7837-7856, 7838-7854, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7861, 7843-7862, 7844-7859, 7844-7860, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7845-7862, 7846-7861, 7846-7862 и 7847-7862.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 1, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 80% ингибирование: 152-171, 154-169, 156-171, 158-173, 1135-1154, 1171-1186, 1173-1188, 1175-1190, 1763-1782, 1912-1931, 2197-2212, 2223-2238, 2225-2240, 2227-2242, 2457-2472, 2459-2474, 2461-2476, 2551-2566, 2553-2570, 2553-2571, 2553-2572, 2554-2573, 2555-2572, 2555-2574, 2556-2573, 2556-2574, 2556-2575, 2557-2574, 2557-2576, 2558-2575, 2558-2576, 2559-2577, 2559-2578, 2560-2577, 2560-2578, 2560-2579, 2561-2578, 2561-2579, 2561-2580, 2562-2577, 2562-2579, 2562-2581, 2563-2580, 2563-2582, 2564-2581, 2564-2583, 2565-2584, 2566-2583, 2567-2584, 2567-2586, 2568-2585, 2568-2587, 2569-2586, 2569-2588, 2570-2587, 2571-2588, 2571-2590, 2572-2589, 2572-2591, 2573-2590, 2573-2592, 2574-2591, 2574-2593, 2575-2592, 2576-2593, 2576-2595, 2577-2594, 2577-2596, 2578-2597, 2580-2598, 2580-2599, 2581-2597, 2581-2600, 2582-2601, 2583-2602, 2584-2603, 2585-2604, 2586-2605, 2587-2606, 2588-2607, 2589-2608, 2590-2606, 2590-2607, 2590-2609, 2591-2610, 2592-2611, 2593-2608, 2593-2612, 2594-2613, 2595-2611, 2595-2614, 2596-2615, 2597-2612, 2597-2613, 2597-2614, 2597-2615, 2597-2616, 2598-2613, 2598-2613, 2598-2614, 2598-2615, 2598-2616, 2598-2617, 2599-2614, 2599-2617, 2599-2618, 2600-2615, 2600-2617, 2600-2618, 2600-2619, 2601-2616, 2601-2617, 2601-2619, 2601-2620, 2602-2618, 2602-2621, 2603-2620, 2603-2621, 2603-2622, 2604-2619, 2604-2620, 2604-2621, 2604-2622, 2604-2623, 2605-2620, 2605-2621, 2605-2622, 2605-2623, 2605-2624, 2606-2621, 2606-2622, 2606-2623, 2606-2624, 2606-2625, 2607-2622, 2607-2623, 2607-2624, 2607-2625, 2607-2626, 2608-2623, 2608-2624, 2608-2625, 2608-2627, 2609-2624, 2609-2626, 2609-2627, 2609-2628, 2610-2625, 2610-2626, 2610-2628, 2610-2629, 2611-2626, 2611-2627, 2611-2629, 2611-2630, 2612-2627, 2612-2628, 2612-2630, 2612-2631, 2613-2628, 2613-2629, 2613-2631, 2614-2629, 2614-2630, 2614-2631, 2615-2630 и 2616-2631.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 2, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 80% ингибирование: 1685-1704, 1686-1705, 1873-1892, 1875-1890, 1877-1892, 1879-1894, 3819-3838, 4151-4166, 5904-5923, 6406-6425, 6985-7000, 7692-7707, 7694-7709, 7696-7711, 7786-7801, 7788-7805, 7788-7806, 7788-7807, 7789-7808, 7790-7807, 7790-7809, 7791-7808, 7791-7809, 7791-7810, 7792-7809, 7792-7811, 7793-7810, 7793-7811, 7794-7812, 7794-7813, 7795-7812, 7795-7813, 7795-7814, 7796-7813, 7796-7814, 7796-7815, 7797-7812, 7797-7814, 7797-7816, 7798-7815, 7798-7817, 7799-7816, 7799-7818, 7800-7819, 7801-7818, 7802-7819, 7802-7821, 7803-7820, 7803-7822, 7804-7821, 7804-7823, 7805-7822, 7806-7823, 7806-7825, 7807-7824, 7807-7826, 7808-7825, 7808-7827, 7809-7826, 7809-7828, 7810-7827, 7811-7828, 7812-7829, 7812-7831, 7813-7832, 7814-7833, 7815-7834, 7816-7832, 7816-7835, 7817-7836, 7818-7837, 7819-7838, 7820-7839, 7821-7840, 7822-7841, 7823-7842, 7824-7843, 7825-7841, 7825-7842, 7825-7844, 7826-7845, 7827-7846, 7828-7843, 7828-7847, 7829-7848, 7830-7846, 7830-7849, 7831-7850, 7832-7847, 7832-7848, 7832-7849, 7832-7850, 7832-7851, 7833-7848, 7833-7849, 7833-7850, 7833-7851, 7833-7852, 7834-7849, 7834-7852, 7834-7853, 7835-7850, 7835-7852, 7835-7853, 7835-7854, 7836-7851, 7836-7852, 7836-7854, 7836-7855, 7837-7853, 7837-7856, 7838-7855, 7838-7856, 7838-7857, 7839-7854, 7839-7855, 7839-7856, 7839-7857, 7839-7858, 7840-7855, 7840-7856, 7840-7857, 7840-7858, 7840-7859, 7841-7856, 7841-7857, 7841-7858, 7841-7859, 7841-7860, 7842-7857, 7842-7858, 7842-7859, 7842-7860, 7842-7861, 7843-7858, 7843-7859, 7843-7860, 7843-7862, 7844-7859, 7844-7861, 7844-7862, 7845-7860, 7845-7861, 7846-7862 и 7847-7862.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 1, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 90% ингибирование: 154-169, 156-171, 158-173, 1135-1154, 1171-1186, 1173-1188, 1763-1782, 1912-1931, 2223-2238, 2227-2242, 2459-2474, 2461-2476, 2554-2573, 2555-2574, 2560-2577, 2561-2578, 2561-2579, 2562-2581, 2563-2580, 2563-2582, 2564-2581, 2566-2583, 2567-2584, 2568-2585, 2568-2587, 2569-2586, 2570-2587, 2576-2593, 2577-2594, 2577-2596, 2578-2597, 2580-2599, 2581-2600, 2582-2601, 2583-2602, 2584-2603, 2586-2605, 2587-2605, 2587-2606, 2588-2607, 2589-2608, 2590-2607, 2590-2609, 2592-2611, 2595-2614, 2596-2615, 2597-2612, 2597-2613, 2597-2615, 2597-2616, 2598-2613, 2598-2613, 2598-2617, 2599-2614, 2599-2618, 2600-2615, 2600-2619, 2601-2617, 2601-2620, 2602-2621, 2603-2622, 2604-2623, 2605-2621, 2605-2622, 2605-2624, 2606-2625, 2607-2626, 2608-2623, 2608-2625, 2609-2628, 2611-2627, 2611-2630, 2612-2628, 2612-2631, 2613-2629, 2614-2629, 2615-2630 и 2616-2631.
В некоторых вариантах реализации следующие нуклеотидные области SEQ ID NO: 2, при направленном воздействии антисмысловых соединений или олигонуклеотидов, демонстрируют по меньшей мере 90% ингибирование: 1685-1704, 1686-1705, 1875-1890, 1877-1892, 1879-1894, 3819-3838, 5904-5923, 6406-6425, 7694-7709, 7696-7711, 7789-7808, 7790-7809, 7795-7812, 7795-7813, 7796-7813, 7796-7814, 7797-7814, 7797-7816, 7798-7815, 7798-7817, 7799-7816, 7801-7818, 7802-7819, 7803-7820, 7803-7822, 7804-7821, 7805-7822, 7811-7828, 7812-7829, 7812-7831, 7813-7832, 7815-7834, 7818-7837, 7819-7838, 7821-7840, 7822-7840, 7822-7841, 7825-7842, 7832-7847, 7832-7848, 7832-7850, 7833-7848, 7833-7852, 7834-7849, 7834-7853, 7835-7850, 7836-7852, 7836-7855, 7837-7856, 7838-7856, 7839-7857, 7839-7858, 7840-7856, 7840-7857, 7840-7859, 7843-7858, 7843-7860 и 7846-7862.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 50% ингибирование мРНК CFB, ISIS NO: 516350, 532614, 532632, 532635, 532638, 532639, 532686, 532687, 532688, 532689, 532690, 532691, 532692, 532692, 532693, 532694, 532695, 532696, 532697, 532698, 532699, 532700, 532701, 532702, 532703, 532704, 532705, 532706, 532707, 532770, 532775, 532778, 532780, 532791, 532800, 532809, 532810, 532811, 532917, 532952, 588509. 588510, 588511, 588512, 588513, 588514, 588515, 588516, 588517, 588518, 588519, 588520, 588522, 588523, 588524, 588525, 588527, 588528, 588529, 588530, 588531, 588532, 588533, 588534, 588535, 588536, 588537, 588538, 588539, 588540, 588541, 588542, 588543, 588544, 588545, 588546, 588547, 588548, 588549, 588550, 588551, 588552, 588553, 588554, 588555, 588556, 588557, 588558, 588559, 588560, 588561, 588562, 588563, 588564, 588565, 588566, 588567, 588568, 588569, 588570, 588571, 588572, 588573, 588574, 588575, 588576, 588577, 588580, 588581, 588585, 588586, 588589, 588590, 588599, 588603, 588606, 588608, 588610, 588614, 588616, 588628, 588631, 588632, 588634, 588636, 588638, 588640, 588645, 588646, 588654, 588656, 588658, 588660, 588662, 588664, 588670, 588672, 588676, 588682, 588688, 588696, 588698, 588807, 588808, 588809, 588813, 588814, 588815, 588819, 588820, 588822, 588823, 588838, 588839, 588840, 588841, 588842, 588846, 588847, 588848, 588849, 588850, 588851, 588852, 588853, 588854, 588855, 588856, 588857, 588858, 588859, 588860, 588861, 588862, 588863, 588864, 588865, 588866, 588867, 588868, 588870, 588871, 588872, 588873, 588874, 588875, 588876, 588877, 588878, 588879, 588880, 588881, 588882, 588883, 588884, 598999, 599000, 599001, 599002, 599003, 599004, 599005, 599006, 599007, 599008, 599009, 599010, 599011, 599012, 599013, 599014, 599015, 599018, 599019, 599023, 599024, 599025, 599026, 599027, 599028, 599029, 599030, 599031, 599032, 599033, 599034, 599035, 599058, 599062, 599063, 599064, 599065, 599070, 599071, 599072, 599073, 599074, 599076, 599077, 599078, 599079, 599080, 599081, 599082, 599083, 599084, 599085, 599086, 599087, 599088, 599089, 599090, 599091, 599092, 599093, 599094, 599095, 599096, 599097, 599098, 599102, 599119, 599123, 599124, 599125, 599126, 599127, 599128, 599132, 599133, 599134, 599135, 599136, 599137, 599138, 599139, 599140, 599141, 599142, 599143, 599144, 599145, 599147, 599148, 599149, 599150, 599151, 599152, 599153, 599154, 599155, 599156, 599157, 599158, 599159, 599178, 599179, 599180, 599181, 599182, 599186, 599187, 599188, 599189, 599190, 599191, 599192, 599193, 599194, 599195, 599196, 599197, 599198, 599199, 599200, 599201, 599202, 599203, 599204, 599205, 599206, 599207, 599208, 599209, 599210, 599211, 599212, 599213, 599214, 599215, 599216, 599217, 599218, 599219, 599220, 599221, 599221, 599222, 599223, 599224, 599225, 599226, 599227, 599228, 599229, 599230, 599231, 599232, 599233, 599234, 599235, 599236, 599241, 599247, 599248, 599249, 599255, 599256, 599257, 599258, 599260, 599261, 599262, 599263, 599264, 599265, 599266, 599267, 599268, 599269, 599270, 599271, 599272, 599273, 599274, 599275, 599276, 599277, 599278, 599279, 599280, 599297, 599299, 599306, 599307, 599308, 599309, 599311, 599312, 599313, 599314, 599315, 599316, 599317, 599318, 599319, 599320, 599321, 599322, 599323, 599324, 599325, 599326, 599327, 599328, 599329, 599330, 599338, 599349, 599353, 599354, 599355, 599356, 599357, 599358, 599359, 599360, 599361, 599362, 599363, 599364, 599369, 599371, 599372, 599373, 599376, 599378, 599379, 599382, 599383, 599384, 599385, 599386, 599387, 599388, 599389, 599390, 599391, 599392, 599393, 599394, 599395, 599396, 599397, 599398, 599399, 599400, 599401, 599402, 599403, 599404, 599405, 599406, 599407, 599408, 599409, 599410, 599412, 599413, 599414, 599415, 599416, 599417, 599418, 599419, 599420, 599421, 599422, 599423, 599424, 599425, 599426, 599433, 599434, 599435, 599436, 599437, 599438, 599439, 599440, 599441, 599442, 599443, 599444, 599445, 599446, 599447, 599448, 599450, 599454, 599455, 599456, 599467, 599468, 599469, 599471, 599472, 599473, 599474, 599475, 599476, 599477, 599478, 599479, 599480, 599481, 599482, 599483, 599484, 599485, 599486, 599487, 599488, 599489, 599490, 599491, 599492, 599493, 599494, 599495, 599496, 599497, 599498, 599499, 599500, 599501, 599502, 599503, 599504, 599505, 599506, 599507, 599508, 599509, 599512, 599515, 599518, 599531, 599541, 599541, 599546, 599547, 599548, 599549, 599550, 599552, 599553, 599554, 599555, 599557, 599558, 599561, 599562, 599563, 599564, 599565, 599566, 599567, 599568, 599569, 599570, 599577, 599578, 599579, 599580, 599581, 599581, 599582, 599584, 599585, 599586, 599587, 599588, 599589, 599590, 599591, 599592, 599593, 599594, 599595, 601321, 601322, 601323, 601325, 601327, 601328, 601329, 601330, 601332, 601333, 601334, 601335, 601336, 601337, 601338, 601339, 601341, 601342, 601343, 601344, 601345, 601346, 601347. 601348, 601349, 601362, 601367, 601368, 601369, 601371, 601372, 601373, 601374, 601375, 601377, 601378, 601380, 601381, 601382, 601383, 601384, 601385, 601386, 601387 и 601388.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 50% ингибирование мРНК CFB, SEQ ID NO: 12, 30, 33, 36, 37, 84, 85, 86, 87, 88, 89, 90, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 198, 203, 206, 208, 219, 228, 237, 238, 239, 317. 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 434, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 468, 472, 473, 475, 478, 479, 488, 492, 494, 495, 498, 499, 500, 502, 503, 509, 510, 511, 512, 513, 514, 515, 517, 518, 522, 523, 524, 525, 529, 530, 531, 534, 535, 537, 540, 541, 542, 543, 544, 545, 546, 547, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 559, 563, 564, 565, 569, 570, 572, 573, 577, 588, 589, 590, 591, 592, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 623, 640, 641, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 700, 704, 705, 706, 707, 708, 709, 711, 712, 713, 714, 715, 716, 717, 718, 720, 721, 722, 723, 724, 725, 726, 727, 728, 729, 730, 731, 732, 733, 734, 735, 736, 737, 738, 739, 740, 741, 742, 743, 744, 745, 745, 746, 747, 748, 749, 750, 751, 752, 753, 754, 755, 756, 758, 759, 760, 761, 762, 766, 767, 768, 769, 770, 771, 772, 773, 774, 775, 776, 777, 778, 779, 780, 781, 782, 783, 784, 785, 786, 787, 788, 789, 790, 791, 792, 793, 794, 795, 796, 797, 798, 799, 813, 833, 834, 841, 846, 849, 850, 867 и 873.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 60% ингибирование мРНК CFB, ISIS NO: 516350, 532614, 532635, 532686, 532687, 532688, 532689, 532770, 532800, 532809, 532810, 532811, 532917, 532952, 588512, 588513, 588514, 588515, 588516, 588517, 588518, 588519. 588522, 588523, 588524, 588525, 588527, 588528, 588529, 588530, 588531, 588532, 588533, 588534, 588535, 588536, 588537, 588538, 588539, 588540, 588541, 588542, 588543, 588544, 588545, 588546, 588547, 588548, 588549, 588550, 588551, 588552, 588553, 588554, 588555, 588556, 588557, 588558, 588559, 588560, 588561, 588562, 588563, 588564, 588565, 588566, 588567, 588568, 588569, 588570, 588571, 588572, 588573, 588574, 588575, 588576, 588577, 588636, 588638, 588640, 588664, 588676, 588696, 588698, 588807, 588808, 588814, 588815, 588819, 588820, 588840, 588842, 588846, 588847, 588848, 588849, 588850, 588851, 588852, 588853, 588854, 588855, 588856, 588857, 588858, 588859, 588860, 588861, 588862, 588863, 588864, 588866, 588867, 588868, 588870, 588871, 588872, 588873, 588874, 588875, 588876, 588877, 588878, 588879, 588880, 588881, 588882, 588883, 588884, 598999, 599000, 599001, 599002, 599003, 599004, 599005, 599006, 599007, 599008, 599009, 599010, 599011, 599012, 599013, 599014, 599015, 599019, 599024, 599025, 599026, 599027, 599028, 599029, 599030, 599031, 599032, 599033, 599034, 599035, 599064, 599065, 599071, 599072, 599077, 599078, 599079, 599080, 599083, 599084, 599085, 599086, 599087, 599088, 599089, 599090, 599091, 599092, 599093, 599094, 599095, 599096, 599097, 599125, 599126, 599127, 599133, 599134, 599135, 599136, 599138, 599139, 599140, 599141, 599142, 599148, 599149, 599150, 599151, 599152, 599154, 599155, 599156, 599157, 599158, 599159, 599178, 599179, 599180, 599181, 599187, 599188, 599190, 599192, 599193, 599194, 599195, 599196, 599197, 599198, 599199, 599200, 599201, 599202, 599203, 599204, 599205, 599206, 599207, 599208, 599209, 599210, 599211, 599212, 599213, 599214, 599215, 599216, 599217, 599218, 599219, 599220, 599221, 599222, 599223, 599224, 599225, 599226, 599227, 599228, 599229, 599230, 599231, 599232, 599233, 599234, 599235, 599236, 599247, 599255, 599256, 599257, 599263, 599264, 599265, 599266, 599270, 599271, 599272, 599273, 599274, 599275, 599276, 599277, 599278, 599279, 599280, 599306, 599307, 599308, 599311, 599312, 599313, 599314, 599315, 599316, 599317, 599318, 599319, 599320, 599321, 599322, 599323, 599324, 599325, 599327, 599328, 599329, 599330, 599349, 599353, 599355, 599356, 599357, 599358, 599359, 599360, 599361, 599362, 599363, 599364, 599369, 599371, 599372, 599373, 599376, 599378, 599379, 599382, 599384, 599386, 599387, 599388, 599389, 599390, 599391, 599392, 599393, 599394, 599395, 599396, 599397, 599398, 599399, 599400, 599401, 599402, 599403, 599404, 599405, 599406, 599407, 599408, 599409, 599410, 599412, 599413, 599414, 599415, 599416, 599417, 599418, 599419, 599420, 599421, 599422, 599423, 599424, 599425, 599433, 599434, 599435, 599436, 599437, 599438, 599439, 599440, 599441, 599442, 599443, 599444, 599445, 599446, 599447, 599448, 599456, 599467, 599468, 599471, 599472, 599473, 599474, 599475, 599476, 599477, 599478, 599479, 599480, 599481, 599482, 599483, 599484, 599485, 599486, 599487, 599488, 599489, 599490, 599491, 599492, 599493, 599494, 599495, 599496, 599497, 599498, 599499, 599500, 599501, 599502, 599503, 599504, 599505, 599506, 599507, 599508, 599512, 599531, 599547, 599548, 599549, 599552, 599553, 599554, 599555, 599557, 599558, 599562, 599563, 599564, 599565, 599566, 599567, 599568, 599569, 599570, 599577, 599578, 599579, 599580, 599581, 599582, 599584, 599585, 599586, 599587, 599588, 599589, 599590, 599591, 599592, 599593, 599594, 599595, 601323, 601327, 601329, 601332, 601333, 601333, 601334, 601335, 601336, 601338, 601339, 601341, 601342, 601343, 601344, 601345, 601346, 601347, 601348, 601349, 601368, 601369, 601371, 601372, 601374, 601375, 601377, 601378, 601380, 601381, 601382, 601383, 601384, 601385, 601386, 601387 и 601388.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 60% ингибирование мРНК CFB, SEQ ID NO: 12, 33, 84, 85, 86, 87, 198, 228, 237, 238, 239, 317, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 472, 473, 513, 514, 515, 531, 537, 541, 542, 543, 544, 545, 546, 547, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 564, 565, 569, 570, 577, 590, 592, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 682, 683, 684, 685, 686, 687, 688, 689, 700, 704, 706, 707, 708, 709, 711, 712, 713, 714, 715, 716, 717, 720, 721, 722, 723, 724, 725, 726, 727, 727, 728, 729, 730, 731, 732, 733, 734, 736, 737, 738, 739, 740, 741, 742, 743, 744. 745, 745, 746, 747, 748, 749, 750, 751, 752, 753, 754, 755, 756, 758, 759, 760, 761, 767, 768, 770, 772, 773, 774, 775, 775, 776, 776, 777, 777, 778, 779, 780, 781, 782, 783, 783, 784, 784, 785, 786, 787, 788, 789, 790, 791, 792, 793, 794, 795, 796, 797, 798, 799, 813, 833, 834, 841, 846, 849 и 850.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 70% ингибирование мРНК CFB, ISIS NO: 516350, 532614, 532686, 532687, 532688, 532770, 532800, 532809, 532810, 532811, 532917, 532952, 588512, 588513, 588514, 588515, 588516, 588517, 588518, 588524, 588529, 588530, 588531, 588532, 588533, 588534, 588535, 588536, 588537, 588538, 588539, 588540, 588541, 588542, 588543, 588544, 588545, 588546, 588547, 588548, 588549, 588550, 588551, 588552, 588553, 588554, 588555, 588556, 588557, 588558, 588559, 588560, 588561, 588562, 588563, 588564, 588565, 588568, 588569, 588570, 588571, 588572, 588573, 588574, 588575, 588577, 588636, 588638, 588640, 588696, 588698, 588807. 588814, 588815, 588819, 588842, 588847, 588848, 588849, 588850, 588851, 588852, 588853, 588856, 588857, 588858, 588859, 588860, 588861, 588862, 588863, 588866, 588867, 588870, 588871, 588872, 588873, 588874, 588875, 588876, 588877, 588878, 588879, 588880, 588881, 588882, 588883, 588884, 599000, 599001, 599003, 599004, 599005, 599008, 599009, 599010, 599011, 599014, 599015, 599024, 599025, 599027, 599028, 599029, 599030, 599031, 599032, 599033, 599034, 599072, 599077, 599080, 599085, 599086, 599087, 599088, 599089, 599090, 599091, 599093, 599094, 599095, 599096, 599097, 599125, 599126, 599134, 599138, 599139, 599148, 599149, 599150, 599151, 599152, 599154, 599155, 599156, 599157, 599158, 599187, 599188, 599193, 599195, 599196, 599197, 599198, 599199, 599200, 599201, 599202, 599203, 599204, 599205, 599206, 599207, 599208, 599210, 599211, 599212, 599213, 599214, 599215, 599216, 599217, 599218, 599219, 599220, 599221, 599222, 599223, 599224, 599225, 599226, 599227, 599228, 599229, 599230, 599231, 599232, 599233, 599234, 599235, 599236, 599266, 599272, 599272, 599273, 599274, 599275, 599277, 599278, 599279, 599280, 599280, 599306, 599311, 599312, 599313, 599314, 599315, 599316, 599317, 599318, 599319, 599320, 599321, 599322, 599323, 599325, 599327, 599328, 599329, 599330, 599355, 599357, 599358, 599359, 599360, 599361, 599362, 599363, 599364, 599369, 599371, 599372, 599373, 599378, 599379, 599382, 599384, 599386, 599387, 599388, 599389, 599390, 599391, 599392, 599393, 599394, 599395, 599396, 599397, 599398, 599399, 599400, 599401, 599402, 599403, 599404, 599405, 599406, 599407, 599408, 599409, 599410, 599413, 599414, 599415, 599416, 599417, 599418, 599419, 599420, 599421, 599422, 599423, 599424, 599433, 599434, 599435, 599436, 599437, 599438, 599439, 599440, 599441, 599442, 599443, 599445, 599446, 599447, 599448, 599472, 599473, 599474, 599475, 599476, 599477, 599478, 599479, 599480, 599481, 599482, 599483, 599484, 599485, 599486, 599487, 599488, 599489, 599490, 599491, 599492, 599493, 599494, 599495, 599496, 599497, 599498, 599499, 599500, 599501, 599502, 599503, 599504, 599505, 599506, 599507, 599508, 599512, 599547, 599548, 599552, 599553, 599554, 599555, 599558, 599562, 599563, 599564, 599566, 599567, 599568, 599569, 599570, 599577, 599578, 599579, 599580, 599581, 599582, 599585, 599586, 599587, 599588, 599589, 599590, 599591, 599592, 599593, 599594, 599595, 601332, 601335, 601341, 601343, 601344, 601345, 601346, 601347, 601348, 601349, 601371, 601372, 601380, 601382, 601383. 601384, 601385, 601386 и 601387.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 70% ингибирование мРНК CFB, SEQ ID NO: 12, 84, 85, 86, 198, 228, 237, 238, 239, 317, 395, 396, 397, 398, 399, 402, 403, 404, 405, 407, 408, 410, 411, 412, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463. 464, 464, 465, 472, 473, 513, 514, 515, 541, 542, 543, 544, 545, 546, 547, 549, 550, 551, 552, 553, 554, 555, 556, 557, 564, 565, 569, 592, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 645, 646, 647, 648, 649, 650, 653, 654, 655, 656, 659, 660, 662, 663, 664, 665, 666, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 677, 678, 679, 680, 682, 683, 684, 686, 687, 688, 689, 706, 708, 709, 711, 712, 713, 714, 715, 720, 721, 722, 723, 724, 725, 726, 727, 728, 729, 730, 731, 732, 733, 734, 736, 737, 738, 739, 740, 741, 742, 743, 744, 745, 746, 747, 748, 749, 750, 751, 752, 753, 754, 755, 756, 767, 768, 773, 775, 776, 777, 778, 779, 780, 781, 782, 783, 784, 785, 786, 787, 788, 789, 790, 791, 792, 793, 793, 794, 795, 797, 798, 799, 813, 833, 834, 841, 846, 849, 867 и 873.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 80% ингибирование мРНК CFB, ISIS NO: 532686, 532809, 532810, 532811, 532917, 532952, 588512, 588517, 588518, 588533, 588534, 588535, 588536, 588537, 588538, 588539, 588540, 588542, 588543, 588544, 588545, 588546, 588547, 588548, 588549, 588550, 588551, 588552, 588553, 588554, 588555, 588556, 588557, 588558, 588559, 588560, 588561, 588562, 588563, 588564, 588565, 588571, 588638, 588640, 588696, 588698, 588807, 588814, 588849, 588850, 588851, 588853, 588857, 588858, 588859, 588860, 588861, 588862, 588863, 588866, 588867, 588871, 588872, 588873, 588874, 588875, 588876, 588877, 588878, 588879, 588880, 588881, 588882, 588883, 599001, 599024, 599025, 599033, 599086, 599087, 599088, 599089, 599093, 599094, 599095, 599096, 599134. 599139, 599148, 599149, 599151, 599154, 599155, 599156, 599158, 599188, 599195, 599196, 599198, 599201, 599202, 599203, 599204, 599205, 599206, 599207, 599212, 599213, 599215, 599216, 599217, 599218, 599219, 599220, 599221, 599222, 599223, 599224, 599225, 599226, 599227, 599228, 599229, 599230, 599231, 599232, 599233, 599234, 599235, 599236, 599272, 599273, 599275, 599277, 599278, 599279, 599280, 599311, 599313, 599314, 599316, 599317, 599318, 599320, 599321, 599322, 599323, 599327, 599328, 599329, 599330, 599355, 599357, 599358, 599359, 599360, 599361, 599362, 599363, 599364, 599371, 599372, 599373, 599378, 599379, 599382, 599384, 599386, 599387, 599388, 599389, 599390, 599391, 599392, 599393, 599397, 599398, 599399, 599400, 599401, 599403, 599404, 599405, 599407, 599408, 599409, 599410, 599413, 599414, 599415, 599416, 599417, 599418, 599419, 599420, 599421, 599422, 599423, 599424, 599433, 599434, 599435, 599436, 599437, 599438, 599439, 599440, 599441, 599445, 599446, 599447, 599448, 599474, 599476, 599477, 599479, 599481, 599482, 599483, 599485, 599486, 599487, 599488, 599489, 599490, 599491, 599492, 599494, 599495, 599496, 599497, 599498, 599499, 599500, 599502, 599503, 599504, 599505, 599506, 599507. 599508, 599547, 599552, 599553, 599554, 599558, 599563, 599567, 599568, 599569, 599570, 599577, 599578, 599581, 599582, 599585, 599587, 599588, 599590, 599591, 599592, 599593, 599594, 601332, 601344, 601345, 601382, 601383 и 601385.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 80% ингибирование мРНК CFB, SEQ ID NO: 84, 237, 238, 239, 317, 395, 397, 411, 412, 413, 414, 415, 417, 418, 419, 420, 421, 422, 423, 425, 426, 427, 429, 430, 431, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 472, 473, 514, 515, 542, 543, 544, 545, 546, 547, 550, 551, 552, 553, 554, 555, 556, 557, 564, 595, 599, 600, 601, 602, 603, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 646, 655, 660, 662, 663, 666, 669, 670, 671, 672, 673, 675, 676, 677, 678, 679, 682, 684, 686, 687, 688, 689, 706, 708, 709, 711, 712, 713, 714, 715, 720, 722, 723, 724, 725, 726, 727, 729, 730, 731, 732, 733, 736, 737, 738, 739, 740, 741, 742, 743, 744, 745, 746, 747, 748, 749, 750, 751, 752, 753, 754, 755, 756, 768, 775, 776, 778, 781, 782, 783, 784, 785, 787, 788, 789, 790, 791, 792, 793, 794, 799, 813, 833, 834, 841, 849, 867 и 873.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 90% ингибирование мРНК CFB, ISIS NO: 532686, 532811, 532917, 588536, 588537, 588538, 588539, 588544, 588545, 588546, 588548, 588551, 588552, 588553, 588554, 588555, 588556, 588557, 588558, 588559, 588560, 588561, 588562, 588564, 588638, 588640, 588696, 588698, 588849, 588850, 588851, 588860, 588866, 588867, 588872, 588873, 588874, 588876, 588877, 588878, 588879, 588881, 588883, 599149, 599188, 599203, 599206, 599220, 599221, 599222, 599223, 599224, 599225, 599226, 599227, 599228, 599229, 599235, 599236, 599279, 599280, 599314, 599321, 599362, 599378, 599390, 599391, 599398, 599399, 599404, 599413, 599414, 599416, 599419, 599420, 599422, 599435, 599437, 599438, 599441, 599483, 599494, 599508, 599552, 599553, 599554, 599568, 599570, 599577, 599581, 599591, 599592 и 599593.
В некоторых вариантах реализации следующие антисмысловые соединения или олигонуклеотиды направлены на область нуклеиновой кислоты CFB и вызывают по меньшей мере 90% ингибирование мРНК CFB, SEQ ID NO: 84, 238, 239, 317, 412, 413,420, 421, 426, 434, 436, 437, 438, 439, 440, 442, 443, 444, 445, 446, 448, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 464, 465, 472, 473, 514, 515, 542, 543, 544, 545, 546, 551, 553, 555, 556, 599, 600, 601, 602, 610, 616, 617, 618, 662, 666, 670, 676, 677, 678, 688, 689, 713, 723, 729, 730, 740, 741, 742, 743, 744, 745, 746, 747, 748, 749, 755, 756, 768, 783, 793, 833 и 867.
В некоторых вариантах реализации соединение может содержать или состоять из любого олигонуклеотида, направленного на CFB, описанного в настоящем документе, и группы конъюгата.
В некоторых вариантах реализации соединение содержит модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, комплементарных в диапазоне нуклеотидов 2193-2212, 2195-2210, 2457-2476, 2571-2590, 2584-2603, 2588-2607, 2592-2611, 2594-2613, 2597-2616, 2600-2619 или 2596-2611 SEQ ID NO: 1.
В некоторых вариантах реализации соединение содержит модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598.
В некоторых вариантах реализации соединение содержит модифицированный олигонуклеотид и группу конъюгата, где модифицированный олигонуклеотид имеет последовательность азотистых оснований, состоящую из любой из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598.
В некоторых вариантах реализации любое из предыдущих соединений или олигонуклеотидов может содержать по меньшей мере одну модифицированную межнуклеозидную связь, по меньшей мере один модифицированный сахар и/или по меньшей мере одно модифицированное азотистое основание.
В некоторых аспектах любое из предыдущих соединений или олигонуклеотидов может содержать по меньшей мере один модифицированный сахар. В некоторых аспектах по меньшей мере один модифицированный сахар содержит 2'-O-метоксиэтильную группу. В некоторых аспектах по меньшей мере один модифицированный сахар представляет собой бициклический сахар, такой как группа 4'-СН(CH3)-O-2', группа 4'-CH2-O-2' или группа 4'-(CH2)2-O-2'.
В некоторых аспектах модифицированный олигонуклеотид содержит по меньшей мере одну модифицированную межнуклеозидную связь, такую как тиофосфатная межнуклеозидная связь.
В некоторых вариантах реализации модифицированный олигонуклеотид содержит по меньшей мере 1, 2, 3, 4, 5, 6 или 7 фосфодиэфирных межнуклеозидных связей.
В некоторых вариантах реализации каждая межнуклеозидная связь модифицированного олигонуклеотида выбрана из фосфодиэфирной межнуклеозидной связи и тиофосфатной межнуклеозидной связи.
В некоторых вариантах реализации каждая межнуклеозидная связь модифицированного олигонуклеотида представляет собой тиофосфатную связь.
В некоторых вариантах реализации любые предыдущие соединения или олигонуклеотиды содержат по меньшей мере одно модифицированное азотистое основание, такое как 5-метилцитозин.
В некоторых вариантах реализации соединение содержит группу конъюгата и модифицированный олигонуклеотид, содержащий:
сегмент гэп, состоящий из связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из связанных нуклеозидов;
причем сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла и, при этом каждый нуклеозид каждого сегмента крыла содержит модифицированный сахар. В некоторых вариантах реализации олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую последовательность, указанную в SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 или 598.
В некоторых вариантах реализации модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую или состоящую из последовательности, указанной в SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453 или 455, причем модифицированный олигонуклеотид содержит:
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов;
где каждый сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла, причем каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтильный сахар; где каждая межнуклеозидная связь представляет собой тиофосфатную связь, и где каждый цитозин представляет собой 5-метилцитозин.
В некоторых вариантах реализации соединение содержит или состоит из одноцепочечного модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов, имеющих последовательность азотистых оснований, состоящую из последовательности, указанной в SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453 или 455, причем олигонуклеотид содержит:
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов;
где сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла, где каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтильный сахар; причем каждая межнуклеозидная связь представляет собой тиофосфатную связь; и где каждый цитозин представляет собой 5-метилцитозин.
В некоторых вариантах реализации соединение содержит или состоит из ISIS 588540 и группы конъюгата. В некоторых вариантах реализации ISIS 588540 имеет следующую химическую структуру:
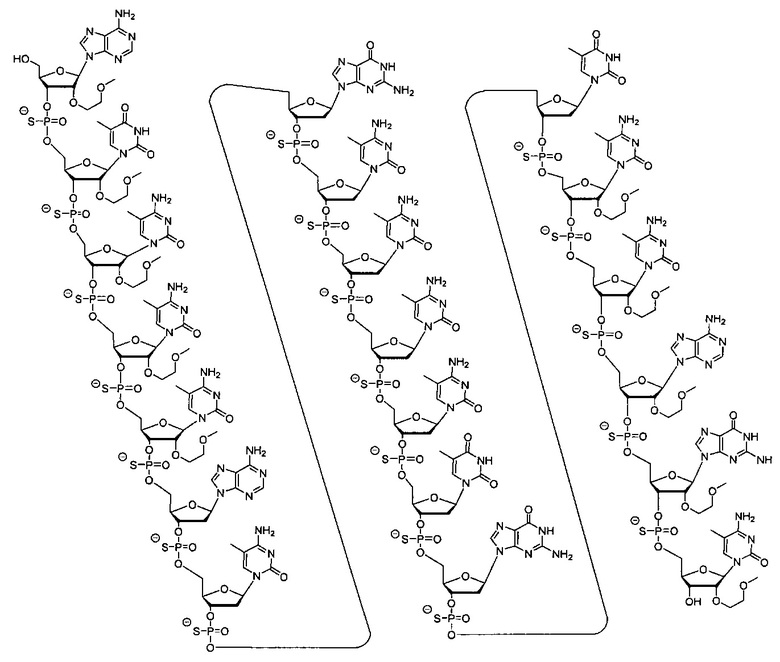
В некоторых вариантах реализации модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую или состоящую из последовательности, указанной в SEQ ID NO: 549, где модифицированный олигонуклеотид содержит
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из трех связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из трех связанных нуклеозидов;
где сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла; причем каждый нуклеозид каждого сегмента крыла содержит cEt сахар; где каждая межнуклеозидная связь представляет собой тиофосфатную связь; и где каждый цитозин представляет собой 5-метилцитозин.
В некоторых аспектах модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую или состоящую из последовательности, указанной в SEQ ID NO: 598, где модифицированный олигонуклеотид содержит
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из трех связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из трех связанных нуклеозидов;
где сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла; где сегмент 5'-крыла содержит 2'-O-метоксиэтильный сахар, 2'-O-метоксиэтильный сахар и cEt сахар в направлении от 5' к 3'; где сегмент 3'-крыла содержит cEt сахар, cEt сахар и 2'-O-метоксиэтильный сахар в направлении от 5' к 3'; где каждая межнуклеозидная связь представляет собой тиофосфатную связь; и где каждый цитозин представляет собой 5-метилцитозин.
В некоторых предыдущих вариантах реализации соединение или олигонуклеотид может быть по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% комплементарен нуклеиновой кислоте, кодирующей CFB.
В любых предыдущих вариантах реализации соединение или олигонуклеотид может быть одноцепочечным.
В некоторых вариантах реализации группа конъюгата связана с модифицированный олигонуклеотидом на 5'-конце модифицированного олигонуклеотида. В некоторых вариантах реализации группа конъюгата связана с модифицированным олигонуклеотидом на 3'-конце модифицированного олигонуклеотида. В некоторых вариантах реализации группа конъюгата содержит по меньшей мере один N-ацетилгалактозамин (GalNAc), по меньшей мере два N-ацетилгалактозамина (GalNAc) или по меньшей мере три N-ацетилгалактозамина (GalNAc).
В некоторых вариантах реализации соединение, имеющее следующую химическую структуру, содержит или состоит из ISIS 588540 с 5'-Х, где Х представляет собой группу конъюгата, содержащую GalNAc, как описано в настоящем документе:
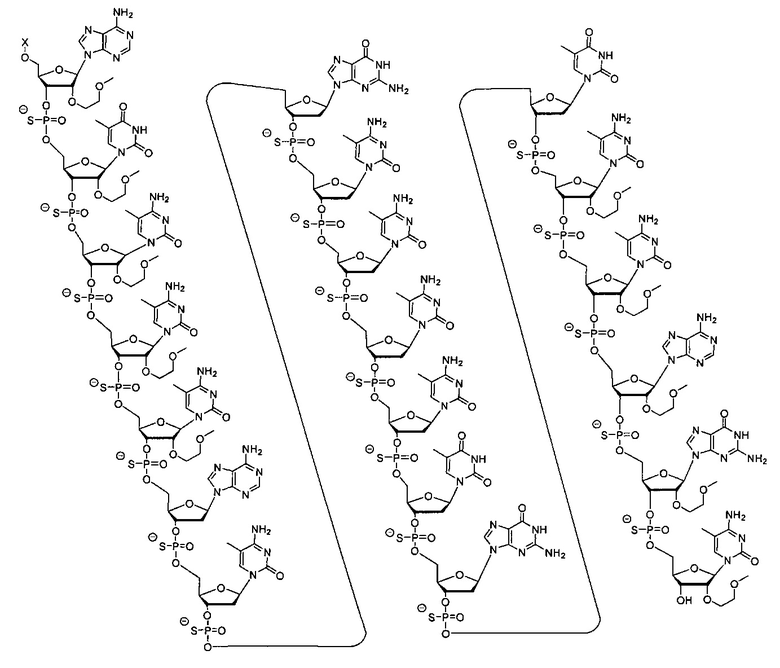
В некоторых вариантах реализации соединение содержит или состоит из SEQ ID NO: 440, 5'-GalNAc и химических модификаций, как показано следующей химической структурой:
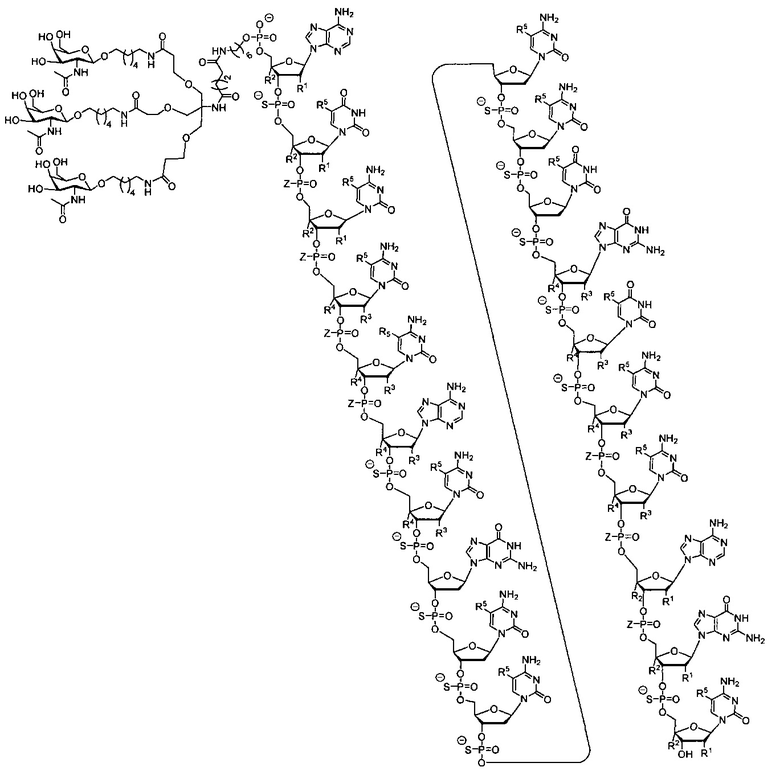
где любой R1 представляет собой -OCH2CH2OCH3 (МОЕ), и R2 представляет собой Н; или R1 и R2 вместе образуют мостик, где R1 представляет собой -O-, и R2 представляет собой -CH2-, -СН(CH3)- или -CH2CH2-, и R1 и R2 напрямую связаны так, что полученный мостик выбран из: -O-CH2-, -О-СН(CH3)- и -O-CH2CH2-;
И для каждой пары R3 и R4 в одном кольце, независимо для каждого кольца: каждый R3 выбран из Н и -OCH2CH2OCH3, и R4 представляет собой Н; или R3 и R4 вместе образуют мостик, где R3 представляет собой -O-, и R4 представляет собой -CH2-, -СН(CH3)- или -CH2CH2-, и R3 и R4 напрямую соединены так, что полученный мостик выбран из: -O-CH2-, -О-СН(CH3)- и -O-CH2CH2-;
И R5 выбран из Н и -CH3;
И Z выбран из S- и О-.
В некоторых вариантах реализации соединение содержит ISIS 696844. В некоторых вариантах реализации соединение состоит из ISIS 696844. В некоторых вариантах реализации ISIS 696844 имеет следующую химическую структуру:
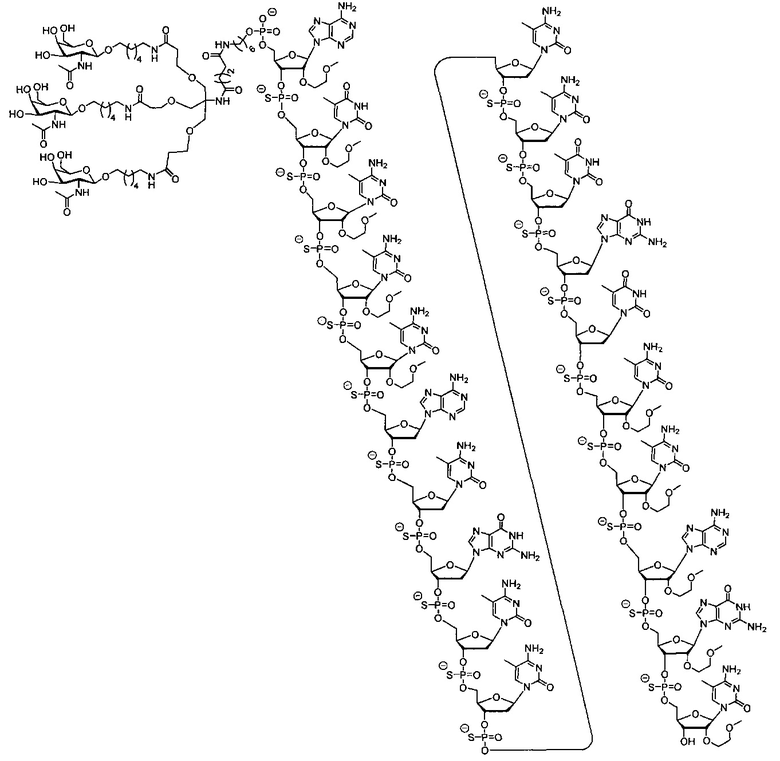
В некоторых вариантах реализации соединение содержит ISIS 696845. В некоторых вариантах реализации соединение состоит из ISIS 696845. В некоторых вариантах реализации ISIS 696845 имеет следующую химическую структуру:
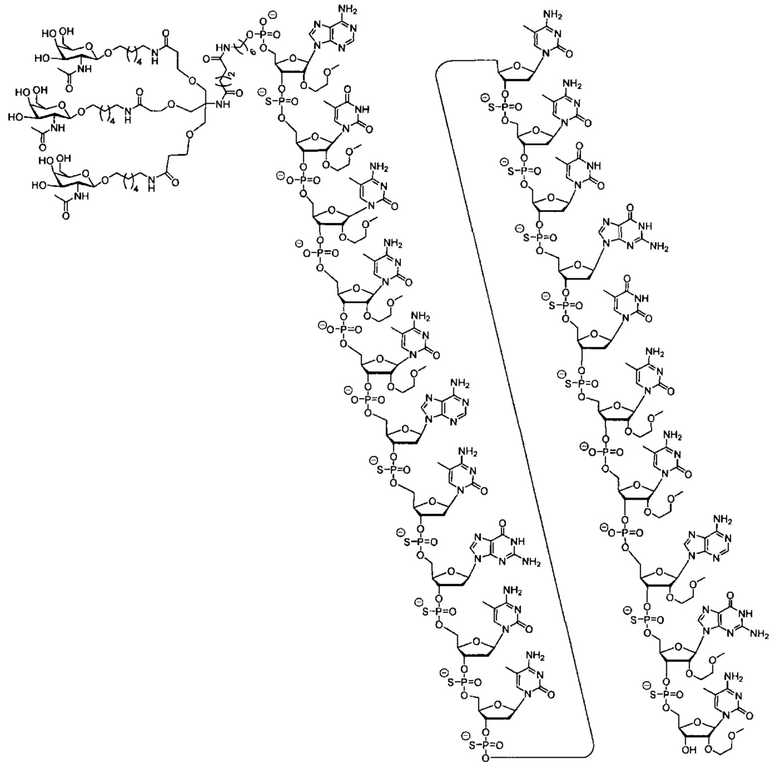
В некоторых вариантах реализации соединение содержит ISIS 698969. В некоторых вариантах реализации соединение состоит из ISIS 698969. В некоторых вариантах реализации ISIS 698969 имеет следующую химическую структуру:
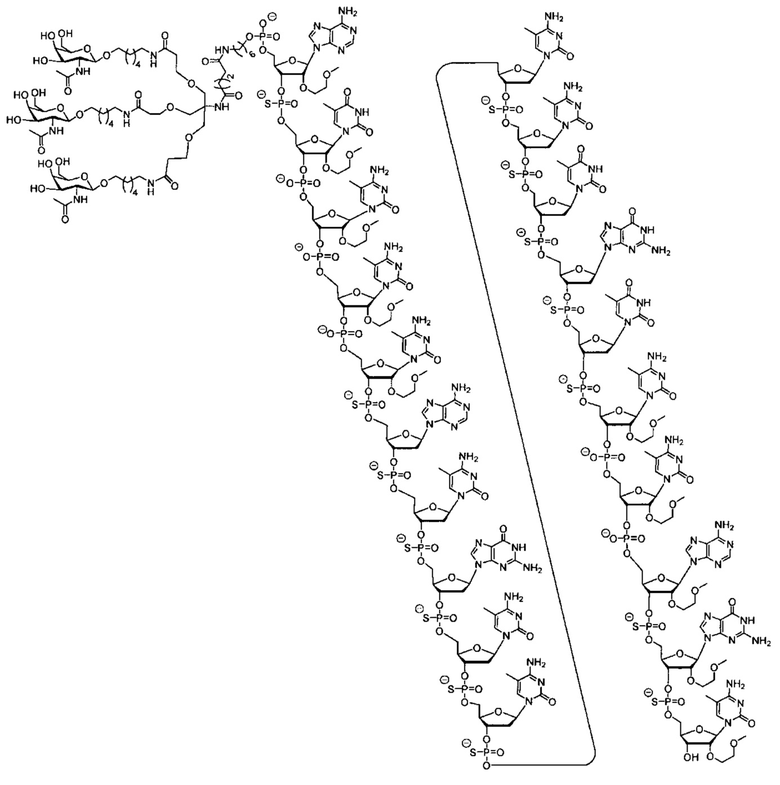
В некоторых вариантах реализации соединение содержит ISIS 698970. В некоторых вариантах реализации соединение состоит из ISIS 698970. В некоторых вариантах реализации ISIS 698970 имеет следующую химическую структуру:
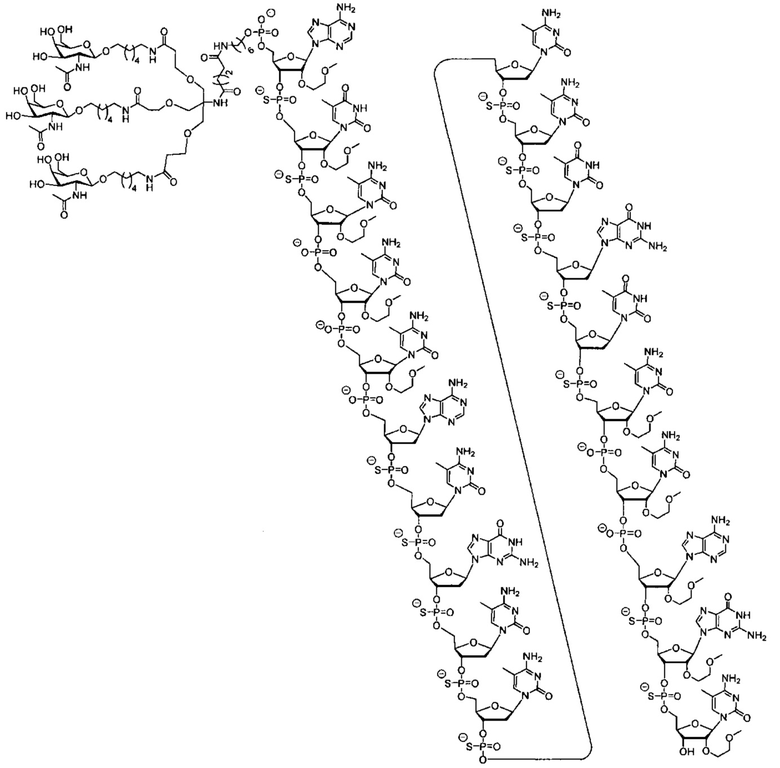
В некоторых вариантах реализации изобретения предложены композиции, содержащие любое соединение, содержащее или состоящее из модифицированного олигонуклеотида, направленного на CFB, или его соль, и группу конъюгата, и по меньшей мере один фармацевтически приемлемый носитель или разбавитель.
В некоторых вариантах реализации соединения или композиции, описанные в настоящем документе, эффективны в том отношении, что они имеют по меньшей мере одну in vitro IC50 менее 250 нм, менее 200 нМ, менее 150 нМ, менее 100 нМ, менее 90 нМ, менее 80 нМ, менее 70 нМ, менее 65 нМ, менее 60 нМ, менее 55 нМ, менее 50 нМ, менее 45 нМ, менее 40 нМ, менее 35 нМ, менее 30 нМ, менее 25 нМ или менее 20 нМ.
В некоторых вариантах реализации соединения или композиции, описанные в настоящем документе, являются хорошо переносимыми, что демонстрируется наличием по меньшей мере одного из показателей: повышения значения ALT или AST не более чем в 4 раза, 3 раза или 2 раза по сравнению с животными, обработанными солевым раствором, или увеличения массы печени, селезенки или почек не более чем на 30%, 20%, 15%, 12%, 10%, 5% или 2%. В некоторых вариантах реализации соединения или композиции, описанные в настоящем документе, являются хорошо переносимыми, что демонстрируется отсутствием увеличения ALT или AST по сравнению с животными, обработанными солевым раствором. В некоторых вариантах реализации соединения или композиции, описанные в настоящем документе, являются хорошо переносимыми, что демонстрируется отсутствием увеличения массы печени, селезенки или почек по сравнению с животными, обработанными солевым раствором.
В некоторых вариантах реализации предложена композиция, содержащая соединение по любому из предыдущих вариантов реализации или его соль и по меньшей мере один из фармацевтически приемлемого носителя или разбавителя. В некоторых аспектах композиция имеет вязкость менее около 40 сантипуаз (сП), менее около 30 сантипуаз (сП), менее около 20 сантипуаз (сП), менее около 15 сантипуаз (сП) или мене около 10 сантипуаз (сП). В некоторых аспектах композиция, имеющая любую вышеуказанную вязкость, содержит соединение, предложенное в настоящем документе, в концентрации около 100 мг/мл, около 125 мг/мл, около 150 мг/мл, около 175 мг/мл, около 200 мг/мл, около 225 мг/мл, около 250 мг/мл, около 275 мг/мл или около 300 мг/мл. В некоторых аспектах композиция, имеющая любую вышеуказанную вязкость и/или концентрацию соединения, имеет температуру комнатной температуры или около 20°С, около 21°C, около 22°С, около 23°С, около 24°С, около 25°С, около 26°С, около 27°С, около 28°С, около 29°С или около 30°С.
В некоторых вариантах реализации способ лечения, предупреждения или ослабления заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения или композиции, описанной в настоящем документе, тем самым обеспечивая лечение, предупреждение или облегчение заболевания. В некоторых аспектах альтернативный путь комплемента активирован выше нормального уровня. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970.
В некоторых вариантах реализации способ лечения, предупреждения или облегчения дегенерации желтого пятна, такой как возрастная дегенерация желтого пятна (AMD), у субъекта включает введение субъекту соединения или композиции, описанной в настоящем документе, тем самым обеспечивая лечение, предупреждение или облегчение AMD. В некоторых аспектах альтернативный путь комплемента активирован выше нормального уровня. В некоторых аспектах AMD представляет собой влажную AMD. В некоторых вариантах реализации AMD представляет собой сухую AMD или географическую атрофию. В некоторых вариантах реализации способ лечения, предупреждения или облегчения дегенерации желтого пятна у субъекта, такой как возрастная дегенерация желтого пятна (AMD), влажная AMD, сухая AMD или географическая атрофия, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ лечения, предупреждения или облегчения дегенерации желтого пятна, такой как возрастная дегенерация желтого пятна (AMD), влажная AMD, сухая AMD или географическая атрофия у субъекта, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ лечения, предупреждения или облегчения дегенерации желтого пятна, такой как возрастная дегенерация желтого пятна (AMD), влажная AMD, сухая AMD или географическая атрофия у субъекта, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970. В некоторых аспектах соединение или композицию вводят субъекту парентерально.
В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания почек, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения или композиции, описанной в настоящем документе, обеспечивая тем самым лечение, предупреждение или облегчение заболевания почек. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания почек, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания почек, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любУю из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ лечения, предупреждения или облегчения заболевания почек, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970. В некоторых аспектах альтернативный путь комплемента активирован выше нормального уровня. В некоторых аспектах заболевание почек представляет собой волчаночный нефрит, системную красную волчанку (SLE), болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипичный гемолитико-уремический синдром (aHUS), или любую их комбинаци. В некоторых аспектах заболевание почек связано с отложением С3, например, отложением С3 в гломеруле. В некоторых аспектах заболевание почек связано с более низкими по сравнению с нормальными уровнями циркулирующего С3, например, уровнями С3 в сыворотке или плазме. В некоторых аспектах введение соединение или композиции снижает или ингибирует накопление содержания С3 в глазах, например, содержания белка С3. В некоторых аспектах введение соединения или композиции снижает уровень отложений С3 в глазах или ингибирует накопление содержания С3 в глазах. В некоторых аспектах соединение или композицию вводят субъекту парентерально. В некоторых аспектах введение соединения или композиции снижает или ингибирует накопление содержания С3 в почках, например, содержания белка С3. В некоторых аспектах введение соединения или композиции снижает уровни отложений С3 в почках или ингибирует накопление отложений С3 в почках, например, уровней С3 в гломеруле. В некоторых аспектах субъекта идентифицируют как страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, например, путем определения уровней комплемента или уровней мембраноатакующего комплекса в крови субъекта и/или путем генетического теста на генетические мутации факторов комплемента, связанные с заболеванием.
В некоторых вариантах реализации способ ингибирования экспрессии фактора комплемента В (CFB) у субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения или композиции, описанной в настоящем документе, обеспечивая тем самым ингибирование экспрессии CFB у субъекта. В некоторых вариантах реализации способ ингибирования экспрессии фактора комплемента В (CFB) у субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ ингибирования экспрессии фактора комплемента В (CFB) у субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ ингибирования экспрессии фактора комплемента В (CFB) у субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970. В некоторых аспектах введение соединения или композиции ингибирует экспрессию CFB в глазах. В некоторых аспектах субъект страдает или имеет риск возникновения возрастной дегенерации желтого пятна (AMD), такой как влажная AMD или сухая AMD. В некоторых аспектах сухая AMD может представлять собой географическую атрофию. Географическую атрофию считают прогрессирующей формой сухой AMD, затрагивающей дегенерацию сетчатки. В некоторых аспектах введение соединения или композиции ингибирует экспрессию CFB в почках, например, в гломеруле. В некоторых аспектах субъект страдает или имеет риск возникновения волчаночного нефрита, системной красной волчанки (SLE), болезни плотного осадка (DDD), С3 гломерулонефрита C3GN), CFHR5 нефропатии или атипического гемолитико-уремического синдрома (aHUS), или любой их комбинации.
В некоторых вариантах реализации способ снижения или ингибирования накопления отложения С3 в глазу субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения или композиции, описанной в настоящем документе, тем самым снижая или ингибируя накопление отложений С3 в глазу субъекта. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в глазу субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в глазу субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в глазу субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970. В некоторых аспектах субъект страдает или имеет риск возникновения возрастной дегенерации желтого пятна (AMD), такой как влажная AMD или сухая AMD. В некоторых аспектах сухая AMD может представлять собой географическую атрофию. В некоторых аспектах соединение или композицию вводят субъекту парентерально.
В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в почках субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения или композиции, описанной в настоящем документе, тем самым снижая или ингибируя накопление отложений С3 в почках субъекта. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в почках субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в почках субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований любой из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598. В некоторых вариантах реализации способ снижения или ингибирования накопления отложений С3 в почках субъекта, страдающего или имеющего риск возникновения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, включает введение субъекту соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970. В некоторых аспектах субъект страдает или имеет риск возникновения волчаночного нефрита, системной красной волчанки (SLE), болезни плотного осадка (DDD), С3 гломерулонефрита C3GN), CFHR5 нефропатии или атипического гемолитико-уремического синдрома (aHUS), или любой их комбинации. В некоторых аспектах соединение или композицию вводят субъекту парентерально.
Некоторые варианты реализации изобретения относятся к применению соединения или композиции, описанной в настоящем документе, для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента. Некоторые варианты реализации относятся к применению соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808, для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента. Некоторые варианты реализации изобретения относятся к применению соединения, содержащего или состоящего из модифицированного олигонуклеотида и группы конъюгата, где модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов, имеющих последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598, для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента. Некоторые варианты реализации относятся к применению соединения, содержащего или состоящего из ISIS 696844, ISIS 696845, ISIS 698969 или ISIS 698970, для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента. В некоторых аспектах альтернативный путь комплемента активирован выше нормального уровня. В некоторых аспектах заболевание представляет собой дегенерацию желтого пятна, такую как возрастная дегенерация желтого пятна (AMD), которая может быть влажной AMD или сухой AMD. В некоторых аспектах сухая AMD может представлять собой географическую атрофию. В некоторых аспектах заболевание представляет собой болезнь почек, такую как волчаночный нефрит, системная красная волчанка (SLE), болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатия или атипичный гемолитико-уремический синдром (aHUS), или любая их комбинация. В некоторых аспектах соединение или композицию вводят субъекту парентерально.
В некоторых вариантах реализации соединение или композицию, описанную в настоящем документе, вводят парентерально. Например, в некоторых вариантах реализации соединение или композиция может быть введена через инъекцию или инфузию. Парентеральное введение включает подкожное введение, внутривенное введение, внутримышечное введение, внутриартериальное введение, внутрибрюшинное введение или внутричерепное введение, например, интратекальное или интрацеребровентрикулярное введение.
Антисмысловые соединения
Олигомерные соединения включают, но не ограничиваются ими, олигонуклеотиды, олигонуклеозиды, аналоги олигонуклеотидов, миметики олигонуклеотидов, антисмысловые соединения, антисмысловые олигонуклеотиды и миРНК. Олигомерное соединение может быть «антисмысловым» к нуклеиновой кислоте-мишени, что означает, что оно способно подвергаться гибридизации с нуклеиновой кислотой-мишенью посредством водородного связывания.
В некоторых вариантах реализации антисмысловое соединение содержит последовательность азотистых оснований, которая при написании в 5'-3' направлении содержит обратный комплемент целевого сегмента нуклеиновой кислоты-мишени, на которую она нацелена.
В некоторых вариантах реализации антисмысловое соединение имеет 10-30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 12 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 12 до 22 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение содержит от 14 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 14 до 20 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 15 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 15 до 20 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 16 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 16 до 20 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 17 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 17 до 20 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 18 до 30 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 18 до 21 субъединицы в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 18 до 20 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет от 20 до 30 субъединиц в длину. Другими словами, такие антисмысловые соединения имеет от 12 до 30 связанных субъединиц, от 14 до 30 связанных субъединиц, от 14 до 20 субъединиц, от 15 до 30 субъединиц, от 15 до 20 субъединиц, от 16 до 30 субъединиц, от 16 до 20 субъединиц, от 17 до 30 субъединиц, от 17 до 20 субъединиц, от 18 до 30 субъединиц, от 18 до 20 субъединиц, от 18 до 21 субъединицы, от 20 до 30 субъединиц или от 12 до 22 связанных субъединиц, соответственно. В некоторых вариантах реализации антисмысловое соединение имеет 14 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет 16 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет 17 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет 18 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет 19 субъединиц в длину. В некоторых вариантах реализации антисмысловое соединение имеет 20 субъединиц в длину. В других вариантах реализации антисмысловое соединение имеет 8-80, 12-50, 13-30, 13-50, 14-30, 14-50, 15-30, 15-50, 16-30, 16-50, 17-30, 17-50, 18-22, 18-24, 18-30, 18-50, 19-22, 19-30, 19-50 или 20-30 связанных субъединиц. В некоторых таких вариантах реализации антисмысловые соединения содержат 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79 или 80 связанных субъединиц в длину или диапазон, определяемый любыми двумя из указанных выше значений. В некоторых вариантах реализации антисмысловое соединение представляет собой антисмысловый олигонуклеотид, а связанные субъединицы представляют собой нуклеотиды.
В некоторых вариантах реализации антисмысловые олигонуклеотиды могут быть укороченными или усеченными. Например, одна субъединица может быть удалена с 5' конца (5' усечение), или же с 3' конца (3' усечение). Укороченное или усеченное антисмысловое соединение, направленное на нуклеиновую кислоту CFB, может иметь две субъединицы удаленные с 5' конца, или же может иметь две субъединицы удаленные с 3' конца антисмыслового соединения. В альтернативном варианте, удаленные нуклеозиды могут быть рассеяны по всему антисмысловому соединению, например, в антисмысловом соединении с одним нуклеозидом, удаленным с 5' конца, и одним нуклеозидом, удаленным с 3'конца.
Если одна дополнительная субъединица присутствует в удлиненном антисмысловом соединении, дополнительная субъединица может быть расположена на 5' или 3' конце антисмыслового соединения. Если присутствуют две или более дополнительных субъединиц, присоединенные субъединицы могут быть смежными друг с другом, например, в антисмысловом соединении, имеющем две субъединицы, присоединенные к 5' концу (5' присоединение) или же к 3' концу (3' присоединение) антисмыслового соединения. В альтернативном варианте присоединенные субъединицы могут быть рассеяны по всему антисмысловому соединению, например, в антисмысловом соединении, имеющем одну субъединицу, присоединенную к 5' концу, и одну субъединицу, присоединенную к 3' концу.
Возможно увеличение или уменьшение длины антисмыслового соединения, такого как антисмысловой олигонуклеотид, и/или введение некомплементарного азотистого основания без устранения активности. Например, Woolf et al. (Proc. Natl. Acad. Sci. USA 89: 7305-7309, 1992), описывают ряд антисмысловых олигонуклеотидов длиной 13-25 азотистых оснований, которые были испытаны на их способность индуцировать расщепление РНК-мишени в модели инъекции в ооцит. Антисмысловые олигонуклеотиды длиной 25 азотистых оснований с 8 или 11 некомплементарными основаниями вблизи концов антисмысловых олигонуклеотидов были в состоянии управлять прямым специфическим расщеплением мРНК-мишени, хотя и в меньшей степени, чем антисмысловые олигонуклеотиды, которые не содержали никаких несоответствий. Аналогичным образом, целевое специфическое расщепление было получено с применением антисмысловых олигонуклеотидов из 13 азотистых оснований, включая такие, что имели 1 или 3 несоответствия.
Gautschi et al. (J. Natl. Cancer Inst. 93: 463-471, март, 2001) продемонстрировали способность олигонуклеотида, обладающего 100% комплементарностью к мРНК bcl-2 и содержащего 3 рассогласованных основания по отношению к мРНК bcl-xL, уменьшать экспрессию как bcl-2, так и bcl-xL in vitro и in vivo. Кроме того, данный олигонуклеотид продемонстрировал высокую противоопухолевую активность in vivo.
Maher and Dolnick (Nuc. Acid. Res. 16: 3341-3358, 1988) испытания серии тандемов антисмысловых олигонуклеотидов из 14 азотистых оснований и антисмысловых олигонуклеотидов из 28 и 42 азотистых оснований, состоящий из последовательности двух или трех тандемов антисмысловых олигонуклеотидов, соответственно, на их способность к блокированию трансляции ДГФР человека в анализе на ретикулоцитах кролика. Каждый из трех антисмысловых олигонуклеотидов из 14 азотистых оснований в одиночку был способен ингибировать трансляцию, хотя и на более низком уровне, чем антисмысловые олигонуклеотиды из 28 или 42 азотистых оснований.
Некоторые мотивы и механизмы антисмысловых соединений
В некоторых вариантах реализации изобретения антисмысловые соединения содержат химически модифицированные субъединицы, организованные в паттерны или мотивы, для придания антисмысловым соединениям таких свойств, как усиленная ингибирующая активность, повышенная аффинность связывания с нуклеиновой кислотой-мишенью или сопротивление разложению нуклеазами in vivo
Химерные антисмысловые соединения обычно содержат по меньшей мере один участок, измененный таким образом, чтобы придать повышенную устойчивость к деградации под действием нуклеаз, усиление клеточного поглощения, повышенную аффинность связывания с нуклеиновой кислотой-мишенью и/или повышенную ингибирующую активность. Второй участок химерного антисмыслового соединения может обеспечивать другое требуемое свойство, например, служить в качестве субстрата для клеточной эндонуклеазы РНКазы Н, которая расщепляет спираль РНК в дуплексе РНК : ДНК.
Антисмысловая активность может быть результатом любого механизма, затрагивающего гибридизацию антисмыслового соединения (например, олигонуклеотида) с нуклеиновой кислотой-мишенью, при этом гибридизация в конечном итоге приводит к биологическому эффекту. В некоторых вариантах реализации модулируют количество и/или активность нуклеиновой кислоты-мишени. В некоторых вариантах реализации снижают количество и/или активность нуклеиновой кислоты-мишени. В некоторых вариантах реализации гибридизация антисмыслового соединения с нуклеиновой кислотой-мишенью в конечном итоге приводит к разрушению нуклеиновой кислоты-мишени. В некоторых вариантах реализации гибридизация антисмыслового соединения с нуклеиновой кислотой-мишенью не приводит к разрушению нуклеиновой кислоты-мишени. В некоторых вариантах реализации наличие антисмыслового соединения, гибридизованного с нуклеиновой кислотой-мишенью (занятость), приводит к модулированию антисмысловой активности. В некоторых вариантах реализации антисмысловые соединения, имеющие определенный химический мотив или паттерн химических модификаций, особенно подходят для функционирования одного или более механизмов. В некоторых вариантах реализации антисмысловые соединения функционируют более чем по одному механизму и/или по механизмам, которые не были выяснены. Соответственно, антисмысловые соединения, описанные в настоящем документе, не ограничены конкретным механизмом.
Антисмысловые механизмы включают, без ограничения, антисенс, опосредованный РНКазой Н; механизмы РНКи, в которых используется путь RISC и которые включают, без ограничения, механизмы миРНК, оцРНК и микроРНК; и механизмы на основании занятости. Некоторые антисмысловые соединения могут действовать более чем по одному такому механизму и/или по дополнительным механизмам.
Антисенс, опосредованный РНКазой Н
В некоторых вариантах реализации антисмысловая активность по меньшей мере частично обусловлена разрушением РНК-мишени РНКазой Н. РНКаза Н представляет собой клеточную эндонуклеазу, которая расщепляет спираль РНК дуплекса РНК : ДНК. В данной области техники известно, что одноцепочечные антисмысловые соединения, которые являются «ДНК-подобными», вызывают активность РНКазы Н в клетках млекопитающих. Соответственно, антисмысловые соединения, содержащие по меньшей мере часть ДНК или ДНК-подобных нуклеозидов, могут активировать РНКазу Н, приводя к расщеплению нуклеиновой кислоты-мишени. В некоторых вариантах реализации антисмысловые соединения, использующие РНКазу Н, содержат один или более модифицированных нуклеозидов. В некоторых вариантах реализации такие антисмысловые соединения содержат по меньшей мере один блок из 1-8 модифицированных нуклеозидов. В некоторых вариантах реализации модифицированные нуклеозиды не поддерживают активность РНКазы Н. В некоторых вариантах реализации такие антисмысловые соединения представляют собой гэпмеры, как описано в настоящем документе. В некоторых таких вариантах реализации гэп гэпмера содержит ДНК нуклеозиды. В некоторых таких вариантах реализации гэп гэпмера содержит ДНК-подобные нуклеозиды. В некоторых таких вариантах реализации гэп гэпмера содержит ДНК нуклеозиды и ДНК-подобные нуклеозиды.
Некоторые антисмысловые соединения, имеющие гэмперный мотив, считаются химерными антисмысловыми соединениями. В гэпмере внутренний участок имеет множество нуклеотидов, которые поддерживают расщепление РНКазой Н, расположенных между внешними областями, имеющими множество нуклеотидов, химически отличных от нуклеозидов внутренней области. В случае, когда антисмысловой олигонуклеотид имеет гэпмерный мотив, сегмент гэп, как правило, служит в качестве субстрата для расщепления эндонуклеазой, в то время, как сегменты крыльев содержат модифицированные нуклеозиды. В некоторых вариантах реализации участки гэпмера различаются по типам сахарных фрагментов в составе каждого отдельного участка. Типы сахарных фрагментов, используемых для дифференциации участков гэпмера, в некоторых вариантах реализации могут включать β-D-рибонуклеозиды, β-D-дезоксирибонуклеозиды, 2'-модифицированные нуклеозиды (такие 2'-модифицированные нуклеозиды могут включать, среди прочих, 2'-МОЕ и 2'-O-CH3) и модифицированные нуклеозиды с бициклическим сахаром (такие модифицированные нуклеозиды с бициклическим сахаром могут включать те, которые содержат стерически затрудненный этил). В некоторых вариантах реализации нуклеозиды в крыльях могут содержать несколько модифицированных сахарных фрагментов, включая, например, 2'-МОЕ и бициклические сахарные фрагменты, такие как стерически затрудненный этил или LNA. В некоторых вариантах реализации крылья могут содержать несколько модифицированных и немодифицированных сахарных фрагментов. В некоторых вариантах реализации крылья могут содержать различные комбинации 2'-МОЕ нуклеозидов, бициклических сахарных фрагментов, таких как нуклеозиды со стерически затрудненным этилом или LNA нуклеозиды, и 2'-дезоксинуклеозиды.
Каждый отдельный участок может содержать одинаковые сахарные фрагменты, отличные или чередующиеся сахарные фрагменты. Мотив крыло-гэп-крыло часто описывают как «X-Y-Z», где «X» обозначает длину 5' крыла, «Y» обозначает длину гэпа, а «Z» обозначает длину 3' крыла. «X» и «Z» могут содержать одинаковые, отличные или чередующиеся сахарные фрагменты. В некоторых вариантах реализации «X» и «Y» могут содержать один или более 2'-дезоксинуклеозидов. «Y» может содержать 2'-дезоксинуклеозиды. В данном контексте гэпмер, описанный как «X-Y-Z», имеет конфигурацию, в которой гэп расположен непосредственно прилегая к 5' крылу и 3' крылу. Таким образом, между 5' крылом и гэпом или гэпом и 3' крылом не существует промежуточных нуклеотидов. Любые антисмысловые соединения, описанные в настоящем документе, могут иметь гэпмерный мотив. В некоторых вариантах реализации «X» и «Z» являются одинаковыми; в других вариантах реализации они различны. В некоторых вариантах реализации «Y» содержит от 8 до 15 нуклеозидов. X, Y или Z могут содержать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30 или более нуклеозидов.
В некоторых вариантах реализации антисмысловое соединение, направленное на нуклеиновую кислоту CFB, имеет гэпмерный мотив, в котором гэп состоит из 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 связанных нуклеозидов.
В некоторых вариантах реализации антисмысловый олигонуклеотид имеет сахарный мотив, описанный Формулой А, представленной ниже: (J)m-(B)n-(J)p-(B)r-(A)t-(D)g-(A)v-(B)w-(J)x-(B)y-(J)z
где
каждый А независимо представляет собой 2'-замещенный нуклеозид;
каждый В независимо представляет собой бициклический нуклеозид;
каждый J независимо представляет собой либо 2'-замещенный нуклеозид, либо 2'-дезоксинуклеозид;
каждый D представляет собой 2'-дезоксинуклеозид;
m равен 0-4; n равен 0-2; р равен 0-2; r равен 0-2; t равен 0-2; v равен 0-2; w равен 0-4; х равен 0-2; y равен 0-2; z равен 0-4; g равен 6-14;
при условии, что:
по меньшей мере один из m, n и r отличен от 0;
по меньшей мере один из w и y отличен от 0;
сумма m, n, р, r и t равна от 2 до 5; и
сумма v, w, х, y и z равна от 2 до 5.
Соединения РНКи
В некоторых вариантах реализации антисмысловые соединения представляют собой соединения интерферирующей РНК (РНКи), которые включают двухцепочечные соединения РНК (также называемые малой интерферирующей РНК или миРНК) и одноцепочечные соединения РНКи (или оцРНК). Такие соединения по меньшей мере частично действуют по пути RISC для разрушения и/или изолирования нуклеиновой кислоты-мишени (следовательно, включают соединения микроРНК/микроРНК-миметики). В некоторых вариантах реализации антисмысловые соединения содержат модификации, которые делают их особенно подходящими для таких механизмов.
i. Соединения оцРНК
В некоторых вариантах реализации антисмысловые соединения, включая соединения, особенно подходящие для применения в качестве одноцепочечных РНКи соединений (оцРНК), содержат модифицированный 5'-терминальный конец. В некоторых таких вариантах реализации 5'-теримнальный конец содержит модифицированный фосфатный фрагмент. В некоторых вариантах реализации такой модифицированный фосфат является стабилизированным (например, усттойчивым к разложению/расщеплению по сравнению с немодифицированным 5'-фосфатом). В некоторых вариантах реализации такие 5'-концевые нуклеозиды стабилизируют 5'-фосфорный фрагмент. Некоторые модифицированные 5'-концевые нуклеозиды описаны в известном уровне техники, например, в WO/2011/139702.
В некоторых вариантах реализации 5'-нуклеозид соединения оцРНК имеет формулу IIc:
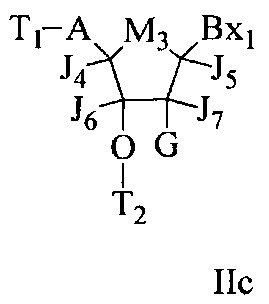
где
T1 представляет собой необязательно защищенный фосфорный фрагмент;
Т2 представляет собой межнуклеозидную линкерную группу, связывающую соединение Формулы IIc с олигомерным соединением;
А имеет одну из формул:
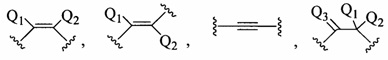 или
или 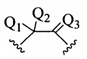
Q1 и Q2, каждый независимо, представляют собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил, замещенный С2-С6 алкинил или N(R3)(R4);
Q3 представляет собой О, S, N(R5) или С(R6)(R7);
каждый R3, R4 R5, R6 и R7 независимо представляет собой Н, C1-C6 алкил, замещенный C1-C6 алкил или C1-C6 алкокси;
М3 представляет собой О, S, NR14, C(R15)(R16), C(R15)(R16)C(R17)(R18), C(R15)=C(R17), OC(R15)(R16) или OC(R15)(Bx2);
R14 представляет собой Н, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
R15, R16, R17 и R18, каждый независимо, представляют собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
Bx1 представляет собой фрагмент гетероциклического основания;
или если присутствует Вх2, то Вх2 представляет собой фрагмент гетероциклического основания, а Bx1 представляет собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
J4, J5, J6 и J7, каждый независимо, представляют собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
или J4 образует мостик с одним из J5 или J7, где указанный мостик состоит из 1-3 связанных бирадикальных групп, выбранных из О, S, NR19, C(R20)(R21), C(R20)=C(R21), C[=C(R20)(R21)] и С(=O), а другие два из J5, J6 и J7, каждый независимо, представляют собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
каждый R19, R20 и R21 независимо представляет собой Н, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил или замещенный С2-С6 алкинил;
G представляет собой Н, ОН, галоген или O-[C(R8)(R9)]n-[(C=O)m-X1]j-Z;
каждый R8 и R9 независимо представляет собой Н, галоген, C1-C6 алкил или замещенный C1-C6 алкил;
X1 представляет собой О, S или N(E1);
Z представляет собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, С2-С6 алкенил, замещенный С2-С6 алкенил, С2-С6 алкинил, замещенный С2-С6 алкинил или N(E2)(E3);
E1, E2 и Е3, каждый независимо, представляют собой Н, C1-C6 алкил или замещенный C1-C6 алкил;
n равен от 1 до около 6;
m равен 0 или 1;
j равен 0 или 1;
каждая замещенная группа содержит одну или более необязательно защищенных групп заместителей, независимо выбранных из галогена, OJ1, N(J1)(J2), =NJ1, SJ1, N3, CN, OC(=X2)J1, OC(=X2)N(J1)(J2) и C(=X2)N(J1)(J2);
X2 представляет собой О, S или NJ3;
каждый J1, J2 и J3 независимо представляет собой Н или C1-C6 алкил;
если j равен 1, то Z отличен от галогена или N(Е2)(Е3); и
где указанное олигомерное соединение содержит от 8 до 40 мономерных субъединиц и может подвергаться гибридизации с по меньшей мере частью нуклеиновой кислоты-мишени.
В некоторых вариантах реализации М3 представляет собой О, СН=СН, OCH2 или ОС(Н)(Вх2). В некоторых вариантах реализации М3 представляет собой О.
В некоторых вариантах реализации J4, J5, J6 и J7 представляют собой Н. В некоторых вариантах реализации J4 образует мостик с одним из J5 или J7.
В некоторых вариантах реализации А имеет одну из формул:
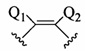 или
или 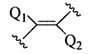
где
Q1 и Q2, каждый независимо, представляют собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси или замещенный C1-C6 алкокси. В некоторых вариантах реализации Q1 и Q2 представляют собой Н. В некоторых вариантах реализации Q1 и Q2, каждый независимо, представляют собой Н или галоген. В некоторых вариантах реализации Q1 и Q2 представляет собой Н, а другой из Q1 и Q2 представляет собой F, CH3 или OCH3.
В некоторых вариантах реализации T1 имеет формулу:
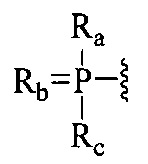
где
Ra и Rc, каждый независимо, представляют собой защищенный гидроксил, защищенный тиол, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, защищенный амино или замещенный амино; и
Rb iпредставляет собой О или S. В некоторых вариантах реализации Rb представляет собой О, а Ra и Rc, каждый независимо, представляют собой OCH3, OCH2CH3 или СН(CH3)2.
В некоторых вариантах реализации G представляет собой галоген, OCH3, OCH2F, OCHF2, OCF3, OCH2CH3, O(CH2)2F, OCH2CHF2, OCH2CF3, OCH2-СН-CH2, O(CH2)2-OCH3, O(CH2)2-SCH3, O(CH2)2-OCF3, O(CH2)3-N(R10)(R11), O(CH2)2-ON(R10)(R11), O(CH2)2-O(CH2)2-N(R10)(R11), OCH2C(=O)-N(R10)(R11), OCH2C(=O)-N(R12)-(CH2)2-N(R10)(R11) или O(CH2)2-N(R12)-C(=NR13)[N(R10)(R11)], где R10, R11, R12 и R13, каждый независимо, представляют собой Н или C1-C6 алкил. В некоторых вариантах реализации G представляет собой галоген, OCH3, OCF3, OCH2CH3, OCH2CF3, OCH2-СН-CH2, O(CH2)2-OCH3, O(CH2)2-O(CH2)2-N(CH3)2, OCH2C(=O)-N(H)CH3, OCH2C(-O)-N(Н)-(CH2)2-N(CH3)2 или OCH2-N(H)-C(=NH)NH2. В некоторых вариантах реализации G представляет собой F, OCH3 или O(CH2)2-OCH3. В некоторых вариантах реализации G представляет собой O(CH2)2-OCH3.
В некоторых вариантах реализации 5'-концевой нуклеозид имеет Формулу IIe:
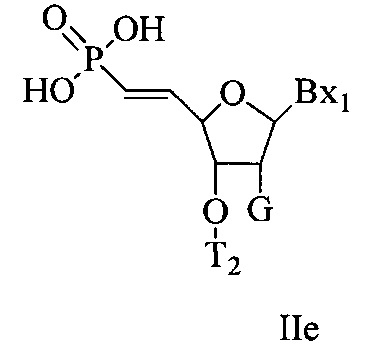
В некоторых вариантах реализации изобретения антисмысловые соединения, включая соединения, которые особенно подходят для оцРНК, содержат один или более типов модифицированных сахарных фрагментов и/или природных сахарных фрагментов, расположенных вдоль олигонуклеотида или его области в определенном паттерне или мотиве сахарной модификации. Такие мотивы могут содержать любые сахарные модификации, рассмотренные в настоящем документе, и/или другие известные модификации сахара.
В некоторых вариантах реализации олигонуклеотиды содержат или состоят из области, имеющей одинаковые сахарные модификации. В некоторых вариантах реализации каждый нуклеозид области содержит одинаковую РНК-подобную сахарную модификацию. В некоторых вариантах реализации каждый нуклеозид области представляет собой 2'-F нуклеозид. В некоторых вариантах реализации каждый нуклеозид области представляет собой 2'-ОМе нуклеозид. В некоторых вариантах реализации каждый нуклеозид области представляет собой 2'-МОЕ нуклеозид. В некоторых вариантах реализации каждый нуклеозид области представляет собой cEt нуклеозид. В некоторых вариантах реализации каждый нуклеозид области представляет собой LNA нуклеозид. В некоторых вариантах реализации однородная область образует весь или по существу весь олигонуклеотид. В некоторых вариантах реализации область образует весь нуклеотид, за исключением 1-4 концевых нуклеозидов.
В некоторых вариантах реализации олигонуклеотиды содержат одну или более областей чередующихся сахарных модификаций, где нуклеозиды чередуются между нуклеотидами, имеющими сахарную модификацию первого типа, и нуклеотидами, имеющими сахарную модификацию второго типа. В некоторых вариантах реализации нуклеозиды обоих типов представляют собой РНК-подобные нуклеозиды. В некоторых вариантах реализации чередующиеся нуклеозиды выбраны из: 2'-ОМе, 2'-F, 2'-МОЕ, LNA и cEt. В некоторых вариантах реализации чередующиеся модификации представляют собой 2'-F и 2'-ОМе. Такие области могут быть смежными или могут быть прерваны по-другому модифицированными нуклеозидами или конъюгированными нуклеозидами.
В некоторых вариантах реализации каждая чередующаяся область чередующихся модификаций состоит из одного нуклеозида (т.е. паттерн представляет собой (АВ)xAy, где А представляет собой нуклеозид, имеющий сахарную модификацию первого типа, и В представляет собой нуклеозид, имеющий сахарную модификацию второго типа; x равен 1-20, и y равен 0 или 1). В некоторых вариантах реализации одна или более чередующихся областей в чередующемся мотиве содержит более одного нуклеозида некоторого типа. Например, олигонуклеотиды могут содержать одну или более областей любого из следующих нуклеозидных мотивов:
ААВВАА;
АВВАВВ;
ААВААВ;
АВВАВААВВ;
АВАВАА;
ААВАВАВ;
АВАВАА;
АВВААВВАВАВАА;
ВАВВААВВАВАВАА; или
АВАВВААВВАВАВАА;
где А представляет собой нуклеозид первого типа, и В представляет собой нуклеозид второго типа. В некоторых вариантах реализации каждый А и В выбран из 2'-F, 2'-ОМе, БНК и МОЕ.
В некоторых вариантах реализации олигонуклеотиды, имеющие такой чередующийся мотив, содержат также модифицированный 5'-концевой нуклеозид, такой как нуклеозид формулы IIc или IIe.
В некоторых вариантах реализации олигонуклеотиды содержат область, имеющую мотив 2-2-3. Такие области содержат следующий мотив:
-(А)2-(В)х-(А)2-(С)y-(А)3-
где А представляет собой первый тип модифицированного нуклеозида;
В и С представляют собой нуклеозиды, модифицированные иначе, чем А, однако В и С могут иметь одинаковые или разные модификации относительно друг друга;
x и y равны от 1 до 15.
В некоторых вариантах реализации А представляет собой 2'-ОМе модифицированный нуклеозид. В некоторых вариантах реализации В и С представляют собой 2'-F модифицированные нуклеозиды. В некоторых вариантах реализации А представляет собой 2'-ОМе модифицированный нуклеозид, а В и С представляют собой 2'-F модифицированные нуклеозиды.
В некоторых вариантах реализации олигонуклеозиды имеют следующий сахарный мотив:
5'-(Q)-(AB)xAy-(D)z
где
Q представляет собой нуклеозид, содержащий стабилизированный фосфатный фрагмент. В некоторых вариантах реализации Q представляет собой нуклеозид, имеющий Формулы IIc или IIe;
А представляет собой первый тип модифицированного нуклеозида;
В представляет собой второй тип модиицированного нуклеозида;
D представляет собой модифицированный нуклеозид, содержащий модификацию, отличную от нуклеозида, смежного с ним. Так, если y равен 0, то D должен быть модифицирован иначе, чем В, а если y равен 1, то D должен быть модифицирован иначе, чем А. В некоторых вариантах реализации D отличен и от А, и от В.
Х равен 5-15;
Y равен 0 или 1;
Z равен 0-4.
В некоторых вариантах реализации олигонуклеозиды имеют следующий сахарный мотив:
5'-(Q)-(A)x-(D)z
где
Q представляет собой нуклеозид, содержащий стабилизированный фосфатный фрагмент. В некоторых вариантах реализации Q представляет собой нуклеозид, имеющий Формулы IIc или IIe;
А представляет собой первый тип модифицированного нуклеозида;
D представляет собой модифицированный нуклеозид, содержащий модификацию, отличную от А.
Х равен 11-30;
Z равен 0-4.
В некоторых вариантах реализации А, В, С и D В представленных выше мотивах выбраны из: 2'-ОМе, 2'-F, 2'-МОЕ, LNA и cEt. В некоторых вариантах реализации D представляет собой концевые нуклеозиды. В некоторых вариантах реализации такие концевые нуклеозиды не предназначены для гибридизации с нуклеиновой кислотой-мишенью (хотя может происходить случайная гибридизация одного или более из них). В некоторых вариантах реализации азотистое основание каждого нуклеозида D представляет собой аденин, независимо от идентичности азотистого основания в соответствующем положении нуклеиновой кислоты-мишени. В некоторых вариантах реализации азотистое основание каждого нуклеозида D представляет собой тимин.
В некоторых вариантах реализации антисмысловые соединения, включая соединения, которые особенно подходят для применения в качестве оцРНК, содержат модифицированные межнуклеозидные связи, расположенные вдоль олигонуклеотида или его области в определенном порядке или в мотиве модифицированной межнуклеозидной связи. В некоторых вариантах реализации олигонуклеотиды содержат область, имеющую мотив чередующихся межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотиды содержат область одинаково модифицированных межнуклеозидных связей. В некоторых таких вариантах реализации олигонуклеотид содержит область, которая равномерна связана тиофосфатными межнуклеозидными связями. В некоторых вариантах реализации олигонуклеотид равномерно связан тиофосфатными межнуклеозидными связями. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбрана из фосфодиэфира и тиофосфата. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбрана из фосфодиэфира и тиофосфата, и по меньшей мере одна межнуклеозидная связь представляет собой тиофосфат.
В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 6 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 8 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 10 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 6 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 8 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 10 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 12 последовательных тиофосфатных межнуклеозидных связей. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен на 3' конце олигонуклеотида. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен в пределах 3 нуклеозидов от 3' конца олигонуклеотида.
Олигонуклеотиды, имеющие любые из различных сахарных мотивов, описанных в настоящем документе, могут иметь любой связывающий мотив. Например, олигонуклеотиды, включая, но не ограничиваясь ими, те, которые описаны выше, могут иметь связывающий мотив, выбранный из неограничивающей таблицы, представленной ниже:

ii. Соединения миРНК
В некоторых вариантах реализации антисмысловые соединения представляют собой двухцепочечные РНКи соединения (миРНК). В таких вариантах реализации одна или обе цепи могут содержать любой мотив модификации, описанный выше для оцРНК. В некоторых вариантах реализации оцРНК соединения могут представлять собой немодифицированные РНК. В некоторых вариантах реализации соединения миРНК могут содержать немодифицированные нуклеозиды РНК, но модифицированные межнуклеозидные связи.
Некоторые варианты реализации относятся к двухцепочечным композициям, в которых каждая цепь содержит мотив, определенный положением одного или более модифицированных или немодифицированных нуклеозидов. В некоторых вариантах реализации предложены композиции, содержащие первое и второе олигомерное соединение, которые полностью или по меньшей мере частично гибридизованы с образованием дуплексной области, и дополнительно содержащие область, которая комплементарна нуклеиновой кислоте-мишени и гибридизуется с ней. Удобно, что такая композиция содержит первое олигомерное соединение, которое представляет собой антисмысловую цепь, имеющую полную или частичную комплементарность нуклеиновой кислоте-мишени, и второе олигомерное соединение, которое представляет собой смысловую цепь, имеющую одну или более областей, комплементарных и образующих по меньшей мере одну дуплексную область с первым олигомерным соединением.
Композиции согласно некоторым вариантам реализации модулируют геннуюю экспрессию посредством гибридизации с нуклеиновой кислотой-мишенью, что приводит к потере ее нормальной функции. В некоторых вариантах реализации нуклеиновая кислота-мишень представляет собой CFB. В некоторых вариантах реализации разрушение CFB-мишени облегчается активированным комплексом RISC, который образуется с композициями согласно настоящему изобретению.
Некоторые варианты реализации относятся к двухцепочечным композициям, в которых одна из цепей подходит, например, для воздействия на предпочтительное включения противоположной цепи в RISC (или расщепляющий) комплекс. Указанные композиции подходят для направленного воздействия на выбранные молекулы нуклеиновых кислот и для модулирования экспрессии одного или более генов. В некоторых вариантах реализации композиции согласно настоящему изобретению гибридизуются с частью РНК-мишени, что приводит к потере нормальной функции РНК-мишени.
Некоторые варианты реализации относятся к двухцепочечным композициям, в которых обе цепи содержат гемимерный мотив, полностью модифицированный мотив, позиционно модифицированный мотив или чередующийся мотив. Каждая цепь композиций согласно настоящему изобретению может быть модифицирована для выполнения определенной роли, например, в каскаде миРНК. Используя различные мотивы в каждой цепи или одинаковый мотив с различными химическими модификациями в каждой цепи, может быть обеспечено направленное воздействие на антисмысловую цепь комплекса RISC при ингибировании внедрения смысловой цепи. В рамках такой модели каждая цепь может быть модифицирована независимо, так что она лучше выполняет свою конкретную роль. Антисмысловая цепь может быть модифицирована на 5'-конце для усиления его роли в одной области RISC, тогда как 3'-конец может быть модифицирован иначе для усиления его роли в другой области RISC.
Молекулы двухцепочечных олигонуклеотидов могут представлять собой молекулу двухцепочечного полинуклеотида, содержащую самокомплементарные смысловые и антисмысловые области, где антисмысловая область содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в молекуле нуклеиновой кислоты-мишени или ее части, а смысловая область имеет нуклеотидную последовательность, соответствующую последовательности нуклеиновой кислоты-мишени или ее части. Молекулы двухцепочечных олигонуклеотидов могут быть собраны из двух отдельных олигонуклеотидов, где одна цепь представляет собой смысловую цепь, а другая представляет собой антисмысловую цепь, при этом антисмысловая и смысловая цепи являются самокомплементарными (т.е. каждая цепь содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в другой цепи; например, если антисмысловая цепь и смысловая цепь образуют дуплекс или двухцепочечную структуру, например, если двухцепочечная область имеет от около 15 до около 30, например, около 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 пар оснований); антисмысловая цепь содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в молекуле нуклеиновой кислоты-мишени или ее части, а смысловая цепь содержит нуклеотидную последовательность, соответствующую последовательности нуклеиновой кислоты-мишени или ее части (например, от около 15 до около 25 или более нуклеотидов молекулы двухцепочечного олигонуклеотида комплементарны нуклеиновой кислоте-мишени или ее части). В альтернативном варианте, двухцепочечный олигонуклеотид собирается из одного олигонуклеотида, где самокомплементарные смысловые и антисмысловые области миРНК связаны посредством линкера(-ов) на основе нуклеиновой кислоты или не на основе нуклеиновой кислоты.
Двухцепочечный олигонуклеотид может представлять собой полинуклеотид с дуплексом, асимметричным дуплексом, шпилечной или асимметричной шпилечной вторичной структурой, имеющий самокомплементарные смысловые и антисмысловые области, при этом антисмысловая область содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в отдельной молекуле нуклеиновой кислоты-мишени или ее части, а смысловая область имеет нуклеотидную последовательность, соответствующую последовательности нуклеиновой кислоты-мишени или ее части. Двухцепочечный олигонуклеотид может представлять собой кольцевой одноцепочечный полинуклеотид, имеющий две или более петлевых структур и ствол, содержащий самокомплементарные смысловые и антисмысловые области, при этом антисмысловая область содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в молекуле нуклеиновой кислоты-мишени или ее части, а смысловая область имеет нуклеотидную последовательность, соответствующую последовательности нуклеиновой кислоты-мишени или ее части, и при этом кольцевой полинуклеотид может быть процессирован in vivo или in vitro с получением активной молекулы миРНК, способной опосредовать РНКи.
В некоторых вариантах реализации двухцепочечный олигонуклеотид содержит отдельные смысловые и антисмысловые последовательности или области, при этом смысловая и антисмысловая области ковалентно связаны нуклеотидными или ненуклеотидными линкерными молекулами, известными в данной области техники, или в альтернативном варианте реализации связаны нековалентно посредством ионных взаимодействий, водородного связывания, ван-дер-ваальсовских взаимодействий, гидрофобных взаимодействий и/или стэкинг-взаимодействий. В некоторых вариантах реализации двухцепочечный олигонуклеотид содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности гена-мишени. В другом варианте реализации двухцепочечный олигонуклеотид взаимодействует с нуклеотидной последовательностью гена-мишени таким образом, который вызывает ингибирование экспрессии гена-мишени.
В данном контексте двухцепочечные олигонуклеотиды не ограничены молекулами, содержащими только РНК, а дополнительно охватывают химически модифицированные нуклеотиды и ненуклеотиды. В некоторых вариантах реализации молекулы малой интерферирующей нуклеиновой кислоты не имеют нуклеотидов, содержащих 2'-гидрокси (2'-ОН). В некоторых вариантах реализации малые интерферирующие нуклеиновые кислоты необязательно не содержат рибонуклеотидов (например, нуклеотидов, имеющих группу 2'-ОН). Такие двухцепочечные олигонуклеотиды, которые не требуют наличия рибонуклеотидов в молекуле для поддержания РНКи, могут тем не менее иметь присоединенный линкер или линкеры или другие присоединенные или связанные группы, фрагменты или цепи, содержащие один или более нуклеотидов с группами 2'-ОН. Необязательно, двухцепочечный олигонуклеотиды могут содержать рибонуклеотиды в около 5, 10, 20, 30, 40 или 50% положений нуклеотидов. В контексте настоящего документа термин миРНК считают эквивалентным другим терминам, используемым для описания молекул нуклеиновых кислот, которые могут опосредовать последовательность-специфичную РНКи, например, малой интерферирующей РНК (миРНК), двухцепочечной РНК (дцРНК), микро-РНК (микроРНК), короткой шпилечной РНК (кшРНК), малого интерферирующего олигонуклеотида, малой интерферирующей нуклеиновой кислоты, малого интерферирующего модифицированного олигонуклеотида, химически модифицированной миРНК, РНК посттранскрипционного сайленсинга гена (ptgsPHK) и других. Кроме того, в данном контексте термин РНК считают эквивалентным другим терминам, используемым для описания последовательность-специфической интерференции РНК, такой как посттранскрипционный сайленсинг гена, трансляционное ингибирование или эпигенетика. Например, двухцепочечные олигонуклеотиды могут быть использованы для эпигенетического сайленсинга генов на посттранскрипционном уровне и на дотранскрипционном уровне. В неограничивающем примере эпигенетическое регулирование генной экспрессии молекулами миРНК согласно настоящему изобретению может быть результатом миРНК-опосредованной модификации структуры хроматина или паттерна метилирования для изменения генной экспрессии (см., например, Verdel et al., 2004, Science, 303, 672-676; Pal-Bhadra et al., 2004, Science, 303, 669-672; Allshire, 2002, Science, 297, 1818-1819; Volpe et al., 2002, Science, 297, 1833-1837; Jenuwein, 2002, Science, 297, 2215-2218; и Hall et al., 2002, Science, 297, 2232-2237).
Подразумевается, что соединения и композиции согласно некоторым вариантам реализации, предложенным в настоящем документе, могут направленно воздействовать на CFB посредством дцРНК-опосредованного сайленсинга гена или механизма РНКи, включая, например, эффекторные молекулы «шпилечной» или двухцепочечной РНК из ствола-петли, в которых одна цепь РНК с самокомплементарными последовательностями может принимать двухцепочечную конформацию, или эффекторные молекулы дуплексной дцРНК, содержащие две отдельные цепи РНК. В различных вариантах реализации дцРНК полностью состоит из рибонуклеотидов или состоит из смеси рибонуклеотидов и дезоксинуклеотидов, таких как гибриды РНК/ДНК, описанные, например, в WO 00/63364, поданной 19 апреля 2000 года, или в патенте США с серийным номером 60/130377, поданном 21 апреля 1999 года. дцРНК или эффекторная молекула дцРНК может представлять собой одну молекулу с областью самокомплементарности, так что нуклеотиды в одном сегменте молекулы участвуют в спаривании оснований с нуклеотидами в другом сегменте молекулы. В различных вариантах реализации дцРНК, которая состоит из одной молекулы, полностью состоит из рибонуклеотидов или содержит область рибонуклеотидов, которая комплементарна области дезоксирибонуклеотидов. В альтернативном варианте реализации дцРНК может содержать две разные цепи, которые имеют область комплементарности друг с другом.
В различных вариантах реализации обе цепи полностью состоят из рибонуклеотидов, одна цепь полностью состоит из рибонуклеотидов, и одна цепь полностью состоит из дезоксирибонуклеотидов, или одна или обе цепи содержат смесь рибонуклеотидов и дезоксирибонуклеотидов. В некоторых вариантах реализации области комплементарности по меньшей мере на 70, 80, 90, 95, 98 или 100% комплементарны друг другу и последовательности нуклеиновой кислоты-мишени. В некоторых вариантах реализации область дцРНК, которая находится в двухцепочечной конформации, содержит по меньшей мере 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 50, 75, 100, 200, 500, 1000, 2000 или 5000 нуклеотидов или содержит все нуклеотиды в кДНК или другой последовательности нуклеиновой кислоты-мишени, находящейся в дцРНК. В некоторых вариантах реализации дцРНК не содержит одноцепочечных областей, таких как одноцепочечные концы, или дцРНК представляет собой шпильку. В других вариантах реализации дцРНК имеет одну или более одноцепочечных областей или выступов. В некоторых вариантах реализации гибриды РНК/ДНК содержат цепь или область ДНК, которая представляет собой антисмысловую цепь или область (например, имеет по меньшей мере 70, 80, 90, 95, 98 или 100% комплементарность с нуклеиновой кислотой-мишенью), и цепь или область РНК, которая представляет собой смысловую цепь или область (например, имеет по меньшей мере 70, 80, 90, 95, 98 или 100% идентичность с нуклеиновой кислотой-мишенью) и наоборот.
В различных вариантах реализации гибрид РНК/ДНК получают in vitro с помощью методов ферментного или химического синтеза, таких как описаны в настоящем документе или в WO 00/63364, поданной 19 апреля 2000 года, или в патенте США с серийным номером 60/130377, поданном 21 апреля 1999 года. В других вариантах реализации цепь ДНК, синтезированная in vitro, связана в комплекс с цепью РНК, полученной in vivo или in vitro до, после или одновременно с трансформацией ДНК цепи в клетку. В других вариантах реализации дцРНК представляет собой одну кольцевую нуклеиновую кислоту, содержащую смысловую и антисмысловую область, или дцРНК содержит кольцевую нуклеиновую кислоту и вторую кольцевую нуклеиновую кислоту или линейную нуклеиновую кислоту (см., например, WO 00/63364, поданную 19 апреля 2000 года, или в патенте США с серийным номером 60/130377, поданном 21 апреля 1999 года). Иллюстративные кольцевые нуклеиновые кислоты включают лариатные структуры, в которых свободная 5' фосфорильная группа нуклеотида становится связанной с 2' гидроксильной группой другого нуклеотида путем закольцовывания.
В других вариантах реализации дцРНК содержит один или более модифицированных нуклеотидов, в которых 2' положение сахара содержит галоген (такой как группа фтора) или содержит алкокси-группу (такую как метокси-группа), что увеличивает период полувыведения дцРНК in vitro или in vivo по сравнению с соответствующей дцРНК, в которой соответствующее 2' положение содержит водород или гидроксильную группу. В других вариантах реализации дцРНК содержит одну или более связей между смежными нуклеотидами, отличных от природной фосфодиэфирной связи. Примеры таких связей включают фосфорамидные, тиофосфатные и дитиофосфатные связи. дцРНК также могут представлять собой химически модифицированные молекулы нуклеиновых кислот, как описано в патенте США №6673661. В других вариантах реализации дцРНК содержит одну или две кэпированных цепей, как описано, например, в WO 00/63364, поданной 19 апреля 2000 года, или в патенте США с серийным номером 60/130377, поданном 21 апреля 1999 года.
В других вариантах реализации дцРНК может представлять собой любую из по меньшей мере частично дцРНК молекул, описанных в WO 00/63364, а также любую из дцРНК молекул, описанных в предварительной заявке США 60/399998; и в предварительной заявке США 60/419532, и в PCT/US2003/033466, содержание которых включено в настоящий документ посредством ссылки. Любая из дцРНК может быть экспрессирована in vitro или in vivo с помощью способов, описанных в настоящем документе, или стандартных способов, таких как описаны в WO 00/63364.
Занятость
В некоторых вариантах реализации антисмысловые соединения предположительно не приводят к расщеплению нуклеиновой кислоты-мишени посредством РНКазы Н или не приводят к расщеплению или секвестрации по пути RISC. В некоторых таких вариантах реализации антисмысловая активность может быть результатом занятости, при этом наличие гибридизованного антисмыслового соединения нарушает активность нуклеиновой кислоты-мишени. В некоторых таких вариантах реализации антисмысловое соединение может быть равномерно модифицировано или может содержать смесь модификаций и/или модифицированных и немодифицированных нуклеозидов.
Нуклеиновые кислоты-мишени, области-мишени и нуклеотидные последовательности
Нуклеотидные последовательности, кодирующие фактор комплемента В (CFB), включают, без ограничения, следующие: с номером доступа GENBANK NM_001710.5 (включенную в настоящий документ как SEQ ID NO: 1), с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000 (включенную в настоящий документ как SEQ ID NO: 2), с номером доступа GENBANK NW_001116486.1, усеченную с нуклеотида 536000 по 545000 (включенную в настоящий документ как SEQ ID NO: 3), с номером доступа GENBANK XM_001113553.2 (включенную в настоящий документ как SEQ ID NO: 4) или с номером доступа GENBANK NM_008198.2 (включенную в настоящий документ как SEQ ID NO: 5).
Гибридизация
В некоторых вариантах реализации гибридизация происходит между антисмысловым соединением, описанным в настоящем документе, и нуклеиновой кислотой CFB. Наимболее распространенный механизм гибридизации включает водородное связывание (например, уотсон-криковское, хугстиновское или обратное хугстиновское водородное связывание) между комплементарными азотистыми основаниями молекул нуклеиновых кислот.
Гибридизация может происходить в различных условиях. Жесткие условия являются последовательность-зависимыми и определяются природой и составом гибридизируемых молекул нуклеиновых кислот.
Способ определения, является ли последовательность специфически гибридизируемой с целевой нуклеиновой кислотой, хорошо известны в данной области техники. В некоторых вариантах реализации антисмысловые соединения, представленные в настоящем документе, являются специфически гибридизируемыми с нуклеиновой кислотой CFB.
Комплементарность
Антисмысловое соединение и нуклеиновая кислота-мишень являются комплементарными друг к другу, если достаточное количество азотистых оснований антисмыслового соединения могут образовать водородные связи с соответствующими азотистыми основаниями нуклеиновой кислоты-мишени, таким образом, чтобы возникал желаемый эффект (например, антисмысловое ингибирование нуклеиновой кислоты-мишени, такой как нуклеиновая кислота CFB).
Некомплементарные азотистые основания между антисмысловым соединением и нуклеиновой кислотой CFB могут быть приемлемыми при условии, что антисмысловое соединение по-прежнему способно специфически гибридизироваться с нуклеиновой кислотой-мишенью. Кроме того, антисмысловое соединение может гибридизоваться более чем с одним или более сегментами нуклеиновой кислоты CFB так, чтобы промежуточные или соседние сегменты не участвовали в гибридизации (например, петлевая структура, некомплементарное основание или шпилька).
В некоторых вариантах реализации антисмысловые соединения, представленные в настоящем изобретении, или определенные их части, являются или по меньшей мере на 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% комплементарны к нуклеиновой кислоте CFB, области-мишени, сегменту-мишени или определенной ее части. Процент комплементарности антисмыслового соединения с целевой нуклеиновой кислотой может быть определен с использованием стандартных методов.
Например, антисмысловое соединение, в котором 18 из 20 азотистых оснований антисмыслового соединения являются комплементарными к области-мишени, и поэтому будут специфически гибридизоваться, имеет 90 процентов комплементарности. В данном примере оставшиеся некомплементарные азотистые основания могут быть расположены кластерно или вперемешку с комплементарных азотистыми основаниями и не обязаны быть смежными друг с другом или комплементарными азотистыми основаниям. Таким образом, антисмысловое соединение, длина которого составляет 18 азотистых оснований, содержащее четыре некомплементарных азотистых основания, фланкированных двумя участками полной комплементарности с нуклеиновой кислотой-мишенью, обладает общей комплементарностью с нуклеиновой кислотой-мишенью 77,8%, и таким образом, входит в пределы объема настоящего изобретения. Процент комплементарности антисмыслового соединения с областью нуклеиновой кислоты-мишени может быть определен с помощью программ BLAST (основное средство поиска локального выравнивания) и программ PowerBLAST, известных в данной области техники (Altschul et al., J. Mol. Biol., 1990, 215, 403 410; Zhang и Madden, Genome Res., 1997, 7, 649 656). Процент гомологии, идентичность или комплементарность последовательностей, могут быть определены, например, программой Gap (висконсинский пакет анализа последовательностей, версия 8 для Unix, Genetics Computer Group, Висконсинский Университет, Мэдисон, штат Висконсин), с использованием настроек по умолчанию, которые использует алгоритм Смита и Ватермана (Adv. Appl. Math., 1981, 2, 482 489).
В некоторых вариантах реализации антисмысловые соединения, предложенные в настоящем документе, или их определенные части полностью комплементарны (т.е. на 100% комплементарны) нуклеиновой кислоте-мишени или ее определенной части. Например, антисмысловое соединение может быть полностью комплементарно нуклеиновой кислоте CFB или ее области-мишени, или ее сегменту-мишени, или ее последовательности-мишени. В данном контексте «полностью комплементарный» означает, что каждое азотистое основание антисмыслового соединения способно точно спариваться с соответствующими азотистыми основаниями нуклеиновой кислоты-мишени. Например, антисмысловое соединение из 20 азотистых оснований полностью комплементарно целевой последовательности, имеющей 400 азотистых оснований, если существует соответствующий фрагмент из 20 азотистых оснований нуклеиновой кислоты-мишени, полностью комплементарный антисмысловому соединению. Полностью комплементарный может также использоваться в ссылке на определенный фрагмент первой и/или второй нуклеиновой кислоты. Например, фрагмент из 20 азотистых оснований антисмыслового соединения, состоящего из 30 азотистых оснований, может быть «полностью комплементарным» к последовательности-мишени, которая имеет 400 азотистых оснований в длину. Фрагмент из 20 азотистых оснований олигонуклеотида, состоящего из 30 азотистых оснований, полностью комплементарен целевой последовательности, если целевая последовательность имеет соответствующий фрагмент из 20 азотистых оснований, при этом каждое его азотистое основание комплементарно фрагменту из 20 азотистых оснований антисмыслового соединения. В то же время, все антисмысловое соединение из 30 азотистых оснований может быть или не быть полностью комплементарным целевой последовательности в зависимости от того, будут ли остальные 10 азотистых оснований антисмыслового соединения также комплементарны целевой последовательности.
Некомплементарное азотистое основание может располагаться на 5' конце или 3' конце антисмыслового соединения. В альтернативном варианте некомплементарное азотистое основание или азотистые основания могут быть внутри антисмыслового соединения. Если присутствуют два или более некомплементарных азотистых оснований, они могут быть смежными (т.е. связанными) или не смежными. В одном варианте реализации некомплементарное азотистое основание располагается в сегменте крыла гэпмера антисмыслового олигонуклеотида.
В некоторых вариантах реализации антисмысловые соединения, которые содержат точно или до 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 азотистых оснований в длину, содержат не более 4, не более 3, не более 2 или не более 1 некомплементарного азотистого основания(-ий) относительно нуклеиновой кислоты-мишени, такой как нуклеиновая кислота CFB, или ее определенной части.
В некоторых вариантах реализации антисмысловые соединения, которые содержат точно или до 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 азотистых оснований в длину, содержат не более 6, не более 5, не более 4, не более 3, не более 2 или не более 1 некомплементарного азотистого основания(-ий) относительно нуклеиновой кислоты-мишени, такой как нуклеиновая кислота CFB, или ее определенной части.
Предложенные антисмысловые соединения включают также соединения, которые комплементарны части нуклеиновой кислоты-мишени. В данном контексте «часть» относится к определенному количеству смежных (т.е. связанных) азотистых оснований в пределах области или сегмента нуклеиновой кислоты-мишени. «Часть» также может относиться к определенному количеству смежных азотистых оснований антисмыслового соединения. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 8 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 9 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 10 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 11 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 12 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 13 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 14 азотистых оснований. В некоторых вариантах реализации антисмысловые соединения комплементарны части целевого сегмента из по меньшей мере 15 азотистых оснований. Также рассматриваются антисмысловые соединения, которые являются комплементарными по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более азотистым основаниям части целевого сегмента, или диапазон, определяемый любыми двумя из указанных значений.
Идентичность
Антисмысловые соединения, представленные в настоящем документе, также могут иметь определенный процент идентичности конкретной нуклеотидной последовательности, SEQ ID NO, или соединению, представленному конкретным номером Isis, или его части. В данном контексте антисмысловое соединение идентично последовательности, описанной в настоящем документе, если оно имеет такую же способность к спариванию азотистых оснований. Например, РНК, которая содержит урацил вместо тимидина в описанной последовательности ДНК, считают идентичной последовательности ДНК, поскольку и урацил, и тимидин спариваются с аденином. Рассматриваются также укороченный и удлиненный варианты антисмысловых соединений, описанных в настоящем документе, а также соединений, обладающих неидентичными основаниями по отношению к антисмысловым соединениям, предложенным в настоящем документе. Неидентичные основания могут быть смежными друг с другом или рассеянными по всему антисмысловому соединению. Процент идентичности антисмыслового соединения рассчитывают по количеству оснований, которые имеют идентичное спаривание оснований, относительно последовательности, с которой идет сравнение.
В некоторых вариантах реализации антисмысловые соединения или их части по меньшей мере на 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентичны одному или более антисмысловым соединениям из SEQ ID NO, или их части, как описано в настоящем документе.
В некоторых вариантах реализации фрагмент антисмыслового соединения сравнивают с равной по длине части нуклеиновой кислоты-мишени. В некоторых вариантах реализации сравнивают часть из 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 азотистых оснований с равной по длине частью нуклеиновой кислоты-мишени.
В некоторых вариантах реализации часть антисмыслового олигонуклеотида сравнивают с равной по длине частью нуклеиновой кислоты-мишени. В некоторых вариантах реализации сравнивают часть из 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 азотистых оснований с равной по длине частью нуклеиновой кислоты-мишени.
Модификации
Нуклеозид представляет собой комбинацию азотистое основание-сахар. Азотистое основание (также известное как основание) - часть нуклеозида, обычно представляющая собой фрагмент гетероциклического основания. Нуклеотиды представляют собой нуклеозиды, которые дополнительно содержат фосфатную группу, ковалентно связанную с сахарной частью нуклеозида. Для тех нуклеозидов, которые содержат пентофуранозильный сахар, фосфатная группа может быть связана с 2', 3' или 5' гидроксильным фрагментом сахара. Олигонуклеотиды образуются посредством ковалентного связывания соседних нуклеозидов друг с другом с образованием линейного полимерного олигонуклеотида. В олигонуклеотидной структуре фосфатные группы обычно называют как образующие межнуклеозидные связи олигонуклеотида.
Модификации антисмысловых соединений охватывают замещения или изменения межнуклеозидных связей, сахарных фрагментов или азотистых оснований. Модифицированные антисмысловые соединения зачастую предпочтительны по сравнению с нативными формами за счет желаемых свойств, таких как, например, улучшенное клеточное поглощение, повышенная аффинность связывания с нуклеиновой кислотой-мишенью, повышенная стабильность в присутствии нуклеаз или повышенная ингибирующая активность.
Химически модифицированные нуклеозиды также могут быть использованы для повышения аффинности связывания укороченного или усеченного антисмыслового олигонуклеотида с его нуклеиновой кислотой-мишенью. Следовательно, сопоставимые результаты часто могут быть получены с помощью более коротких антисмысловых соединений, которые имеют такие химически модифицированные нуклеозиды.
Модифицированные межнуклеозидные связи
Природная межнуклеозидная связь РНК и ДНК представляет собой 3'-5' фосфодиэфирную связь. Антисмысловые соединения, имеющие одну или более модифицированных, т.е. неприродных межнуклеозидных связей, часто предпочтительны по сравнению с антисмысловыми соединениями, имеющими природные межнуклеозидные связи, благодаря желаемым свойствам, таким как, например, улучшенное клеточное поглощение, усиленная аффинность связывания с нуклеиновыми кислотами-мишенями и повышенная стабильность в присутствии нуклеаз.
Олигонуклеотиды, имеющие модифицированные межнуклеозидные связи, включают межнуклеозидные связи, которые сохраняют атом фосфора, а также межнуклеозидные связи, которые не имеют атома фосфора. Иллюстративные фосфорсодержащие межнуклеозидные связи включают, но не ограничиваются ими, фосфодиэфиры, фосфотриэфиры, метилфосфонаты, фосфорамидаты и тиофосфаты. Способы получения фосфорсодержащих и не содержащих фосфор связей хорошо известны.
В некоторых вариантах реализации антисмысловые соединения, направленные на нуклеиновую кислоту CFB, содержат одну или более модифицированных межнуклеозидных связей. В некоторых вариантах реализации модифицированные межнуклеозидные связи представляют собой тиофосфатные связи. В некоторых вариантах реализации каждая межнуклеозидная связь антисмыслового соединения представляет собой тиофосфатную межнуклеозидную связь.
В некоторых вариантах реализации олигонуклеотиды содержат модифицированные межнуклеозидные связи, расположенные вдоль олигонуклеотида или его области определенным образом в виде мотива модифицированной межнуклеозидной связи. В некоторых вариантах реализации межнуклеозидные связи расположены в разорванном мотиве. В таких вариантах реализации межнуклеозидные связи в каждой из двух областей крыльев отличны от межнуклеозидных связей в области гэп. В некоторых вариантах реализации межнуклеозидные связи в крыльях являются фосфодиэфирными, а межнуклеозидные связи в гэп являются тиофосфатными. Нуклеозидный мотив выбран независимо, так что олигонуклеотиды, имеющие разорванный мотив межнуклеозидных связей может иметь или не иметь разорванный нуклеозидный мотив, и если он имеет разорванный нуклеозидный мотив, то длина крыльев и гэп может быть или не быть одинаковой.
В некоторых вариантах реализации олигонуклеотиды содержат область, имеющую мотив чередующихся межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотиды согласно настоящему изобретению содержат область одинаково модифицированных межнуклеозидных связей. В некоторых таких вариантах реализации олигонуклеотид содержит область, которая равномерна связана тиофосфатными межнуклеозидными связями. В некоторых вариантах реализации олигонуклеотид равномерно связан тиофосфатными межнуклеозидными связями. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбрана из фосфодиэфира и тиофосфата. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбрана из фосфодиэфира и тиофосфата, и по меньшей мере одна межнуклеозидная связь представляет собой тиофосфат.
В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 6 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 8 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 10 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 6 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 8 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 10 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок из по меньшей мере 12 последовательных тиофосфатных межнуклеозидных связей. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен на 3' конце олигонуклеотида. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен в пределах 3 нуклеозидов от 3' конца олигонуклеотида.
В некоторых вариантах реализации олигонуклеотиды содержат одну или более метилфосфонатных связей. В некоторых вариантах реализации олигонуклеотиды, имеющие гэпмерный нуклеозидный мотив, содержат мотив связи, содержащий все тиофосфатные межнуклеозидные связи, за исключением одной или двух метилфосфонатных связей. В некоторых вариантах реализации одна метилфосфонатная связь находится в центральном гэп олигонуклеотида, имеющего гэпмерный нуклеозидный мотив.
В некоторых вариантах реализации желательно распределять количество тиофосфатных межнуклеозидных связей и фосфодиэфирных межнуклеозидных связей для сохранения устойчивости к действию нуклеаз. В некоторых вариантах реализации желательно распределять количество и положение тиофосфатных межнуклеозидных связей и количество и положение фосфодиэфирных межнуклеозидных связей для сохранения устойчивости к действию нуклеаз. В некоторых вариантах реализации количество тиофосфатных межнуклеозидных связей может быть уменьшено, а количество фосфодиэфирных межнуклеозидных связей может быть увеличено. В некоторых вариантах реализации количество тиофосфатных межнуклеозидных связей может быть уменьшено, а количество фосфодиэфирных межнуклеозидных связей может быть увеличено при сохранении устойчивости к действию нуклеаз. В некоторых вариантах реализации желательно уменьшить количество тиофосфатных межнуклеозидных связей при сохранении устойчивости к действию нуклеаз. В некоторых вариантах реализации желательно увеличить количество фосфодиэфирных межнуклеозидных связей при сохранении устойчивости к действию нуклеаз. Модифицированные сахарные фрагменты
Антисмысловые соединения могут необязательно содержать один или более нуклеозидов, в которых модифицирована сахарная группа. Указанные нуклеозиды с модифицированным сахаром могут обеспечивать повышенную устойчивость к действию нуклеаз, повышенную аффинность связывания или некоторые другие полезные биологические свойства антисмысловых соединений. В некоторых вариантах реализации нуклеозиды содержат химически модифицированные фрагменты рибофуранозного кольца. Примеры химически модифицированных рибофуранозных колец включают, без ограничения, добавление групп заместителей (включая 5' и 2' группы заместителей, соединение мостиком негеминальных кольцевых атомов с образованием бициклических нуклеиновых кислот (БНК), замену рибозильного кольцевого атома кислорода на S, N(R) или C(R1)(R2) (R, R1 и R2, каждый независимо, представляют собой Н, C1-C12 алкил или защитную группу) и их комбинации. Примеры химически модифицированных сахаров включают 2'-F-5'-метилзамещенный нуклеозид (см. международную заявку РСТ WO 2008/101157, опубликованную 8/21/08, где описаны другие 5',2'-бис-замещенные нуклеозиды) или замену рибозильного кольцевого атома кислорода на S с дополнительным замещением в 2'-положении (см. опубликованную заявку на патент США US 2005-0130923, опубликованную 16 июня 2005 года), или в альтернативном варианте 5'-замещение БНК (см. международную заявку РСТ WO 2007/134181, опубликованную 11/22/07, где LNA замещена, например, 5'-метильной или 5'-винильной группой).
Примеры нуклеозидов, имеющих модифицированные сахарные фрагменты, включают, без ограничения, нуклеозиды, содержащие 5'-винильные, 5'-метильные (R или S), 4'-S, 2'-F, 2'-OCH3, 2'-OCH2CH3, 2'-OCH2CH2F и 2'-O(CH2)2OCH3 группы заместителей. Заместитель в 2' положении также может быть выбран из аллила, амино, азидо, тио, O-аллила, O-C1-C10 алкила, OCF3, OCH2F, O(CH2)2SCH3, O(CH2)2-O-N(Rm)(Rn), O-CH2-C(=O)-N(Rm)(Rn) и O-CH2-C(=O)-N(Rl)-(CH2)2-N(Rm)(Rn), где каждый Rl, Rm и Rn независимо представляет собой Н или замещенный или незамещенный C1-C10 алкил.
В данном контексте «бициклические нуклеозиды» относятся к модифицированным нуклеозидам, содержащим бициклический сахарный фрагмент. Примеры бициклических нуклеозидов включают без ограничения нуклеозиды, содержащие мостик между 4' и 2' атомами рибозильного кольца. В некоторых вариантах реализации антисмысловые соединения, предложенные в настоящем документе, содержат один или более бициклических нуклеозидов, содержащих 4'-2' мостик. Примеры таких бициклических нуклеозидов с 4'-2' мостиками включают, но не ограничиваются одной из формул: 4'-(CH2)-O-2' (LNA); 4'-(CH2)-S-2'; 4'-(CH2)2-O-2' (ENA); 4'-СН(CH3)-O-2' (также называемая стеричиски затруденнным этилом или cEt) и 4'-СН(CH2OCH3)-O-2' (и их аналоги, см. патент США 7399845, выданный 15 июля 2008 года); 4'-С(CH3)(CH3)-O-2' (и их аналоги, см. опубликованную международную заявку WO 2009/006478, опубликованную 8 января 2009 года); 4'-CH2-N(OCH3)-2' (и их аналоги, см. опубликованную международную заявку WO/2008/150729, опубликованную 11 декабря 2008 года); 4'-CH2-O-N(CH3)-2' (см. опубликованную заявку на патент США US 2004-0171570, опубликованную 2 сентября 2004 года); 4'-CH2-N(R)-O-2', где R представляет собой Н, C1-C12 алкил или защитную группу (см. патент США 7427672, выданный 23 сентября 2008 года); 4'-CH2-С(Н)(CH3)-2' (см. Zhou et al., J. Org. Chem., 2009, 74, 118-134); и 4'-CH2-С(=CH2)-2' (и их аналоги, см. опубликованную международную заявку WO 2008/154401, опубликованную 8 декабря 2008 года).
Дальнейшие сообщения, связанные с бициклическими нуклеозидами могут также быть найдены в опубликованной литературе (см., например: Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Wahlestedt et al., Proc. Natl. Acad. Sci. U.S.A., 2000, 97, 5633-5638; Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; Srivastava et al., J. Am. Chem. Soc., 2007, 129(26) 8362-8379; Elayadi et al., Curr. Opinion Invest. Drugs, 2001, 2, 558-561; Braasch et al., Chem. Biol., 2001, 8, 1-7; и Orum et al., Curr. Opinion Mol. Ther., 2001, 3, 239-243; патенты США №6268490; 6525191; 6670461; 6770748; 6794499; 7034133; 7053207; 7399845; 7547684; 8530640; и 7696345; публикации патентов США № US 2008-0039618; US 2009-0012281; патенты США с серийными номерами 61/026995 и 61/097787; опубликованные международные заявки РСТ; WO 2009/067647; WO 2011/017521; WO 2010/036698 WO 1999/014226; WO 2004/106356; WO 2005/021570; WO 2007/134181; WO 2008/150729; WO 2008/154401; и WO 2009/006478. Каждый из указанных бициклических нуклеозидов можно получить, имея одну или более стереохимическую сахарную конфигурацию, включающие, например, α-L-рибофуранозу и β-D-рибофуранозу (см. международную заявку РСТ PCT/DK98/00393, опубликованную 25 марта 1999 как WO 99/14226).
В некоторых вариантах реализации бициклические сахарные фрагменты нуклеозидов БНК включают, но не ограничиваются ими, соединения, имеющие по меньшей мере один мостик между 4' и 2' положением пентофуранозильного сахарного фрагмента, где такие мостики независимо содержат 1 или от 2 до 4 связанных групп, независимо выбранных из -[C(Ra)(Rb)]n-, -C(Ra)=C(Rb)-, -C(Ra)=N-, -C(=O)-, -C(=NRa)-, -C(=S)-, -O-, -Si(Ra)2-, -S(=O)x- и -N(Ra)-;
где
x равен 0, 1 или 2;
n равен 1, 2, 3 или 4;
каждый Ra и Rb независимо представляет собой Н, защитную группу, гидроксил, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, C5-C20 арил, замещенный C5-C20 арил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, C5-C7 алициклический радикал, замещенный C5-C7 алициклический радикал, галоген, OJ1, NJ1J2, SJ1, N3, COOJ1, ацил (С(=O)-Н), замещенный ацил, CN, сульфонил (S(=O)2-J1) или сульфоксил (S(=O)-J1); и каждый J1 и J2 независимо представляет собой Н, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, C5-C20 арил, замещенный C5-C20 арил, ацил (С(=O)-Н), замещенный ацил, гетероциклический радикал, замещенный гетероциклический радикал, C1-C12 аминоалкил, замещенный C1-C12 аминоалкил или защитную группу.
В некоторых вариантах реализации мостик бициклического сахарного фрагмента представляет собой -[C(Ra)(Rb)]n-, -[C(Ra)(Rb)]n-O-, -C(RaRb)-N(R)-O- или -C(RaRb)-O-N(R)-. В некоторых вариантах реализации мостик представляет собой 4'-CH2-2', 4'-(CH2)2-2', 4'-(CH2)3-2', 4'-CH2-O-2', 4'-(CH2)2-O-2', 4'-CH2-O-N(R)-2' и 4'-CH2-N(R)-O-2'-, где каждый R независимо представляет собой Н, защитную группу или C1-C12 алкил.
В некоторых вариантах реализации бициклические нуклеозиды дополнительно определяют по изомерной конфигурации. Например, нуклеозид, содержащий мостик 4'-2'-метиленокси, может быть в α-L конфигурации или в β-D конфигурации. Ранее α-L-метиленокси (4'-CH2-O-2') БНК были внедрены в антисмысловые олигонуклеотиды, которые демонстрировали антисмысловую активность (Frieden et al., Nucleic Acids Research, 2003, 21, 6365-6372).
В некоторых вариантах реализации бициклические нуклеозиды включают, но не ограничиваются ими, (А) α-L-метиленокси (4'-CH2-O-2') БНК, (В) β-D-метиленокси (4'-CH2-O-2') БНК, (С) этиленокси (4'-(CH2)2-O-2') БНК, (D) аминоокси (4'-CH2-O-N(R)-2') БНК, (Е) оксиамино (4'-CH2-N(R)-O-2') БНК и (F) метил(метиленокси) (4'-СН(CH3)-O-2') БНК, (G) метилентио (4'-CH2-S-2') БНК, (Н) метиленамино (4'-CH2-N(R)-2') БНК, (I) метилкарбоциклические (4'-CH2-СН(CH3)-2') БНК, (J) пропиленкарбоциклические (4'-(CH2)3-2') БНК и (K) винил БНК, как показано ниже:
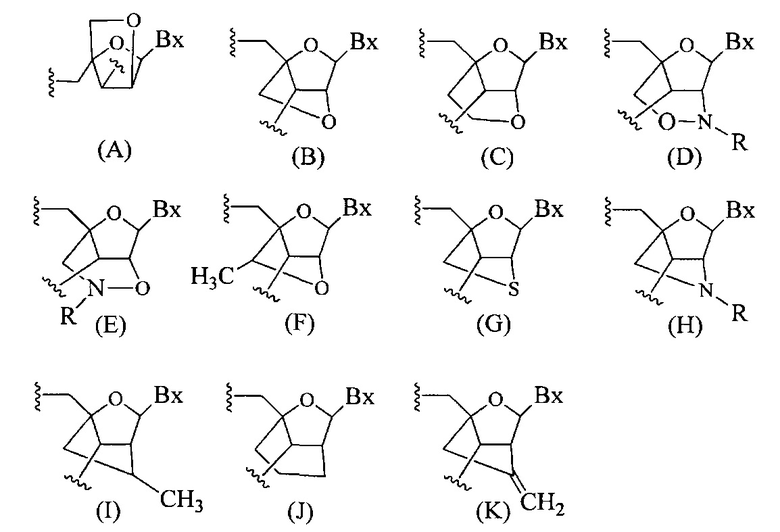
где Вх представляет собой фрагмент основания, а R независимо представляет собой Н, защитную группу, C1-C12 алкил или C1-C12 алкокси.
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу I:
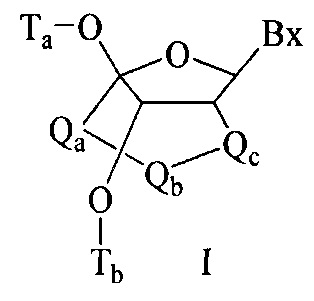
где
Вх представляет собой фрагмент гетероциклического основания;
-Qa-Qb-Qc- представляет собой -CH2-N(Rc)-CH2-, -C(=O)-N(Rc)-CH2-, -CH2-O-N(Rc)-, -CH2-N(Rc)-O- или -N(Rc)-O-CH2;
Rc представляет собой C1-C12 алкил или аминозащитную группу; и
Та и Tb, каждый независимо, представляют собой Н, гидроксил-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки.
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу II:
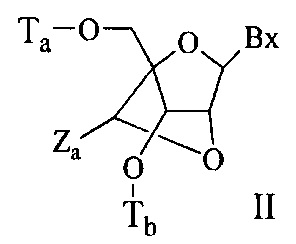
где
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой Н, гидрокси-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки;
Za представляет собой C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, замещенный C1-C6 алкил, замещенный C2-C6 алкенил, замещенный C2-C6 алкинил, ацил, замещенный ацил, замещенный амид, тиол или замещенный тио.
В одном из вариантов реализации каждая из замещенных групп независимо является моно или полизамещенной группами заместителей, выбранными из галогена, оксо, гидроксила, OJc, NJcJd, SJc, N3, OC(=X)Jc и NJeC(=X)NJcJd, где каждый Jc, Jd и Je независимо представляет собой Н, C1-C6 алкил ил изамещенный C1-C6 алкил, и Х представляет собой О или NJc.
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу III:
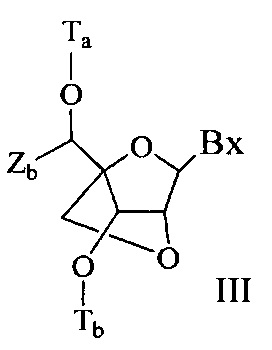
где
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой Н, гидрокси-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки;
Zb представляет собой C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, замещенный C1-C6 алкил, замещенный C2-C6 алкенил, замещенный C2-C6 алкинил или замещенный ацил (С(=O)-).
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу IV:
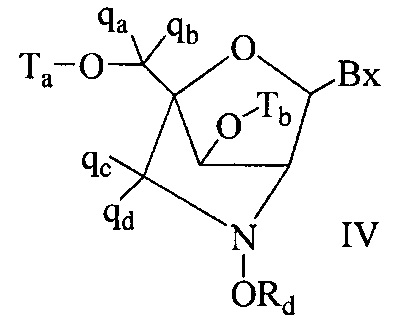
где
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой Н, гидрокси-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки;
Rd представляет собой C1-C6 алкил, замещенный C1-C6 алкил, C2-C6 алкенил, замещенный C2-C6 алкенил, C2-C6 алкинил ил изамещенный C2-C6 алкинил;
каждый qa, qb, qc и qd независимо представляет собой Н, галоген, C1-C6 алкил, замещенный C1-C6 алкил, C2-C6 алкенил, замещенный C2-C6 алкенил, C2-C6 алкинил или замещенный C2-C6 алкинил, C1-C6 алкоксил, замещенный C1-C6 алкоксил, ацил, замещенный ацил, C1-C6 аминоалкил или замещенный C1-C6 аминоалкил;
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу V:
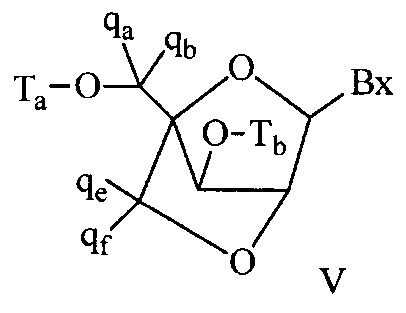
где
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой Н, гидрокси-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки;
qa, qb, qe и qf, каждый независимо, представляют собой водород, галоген, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, C1-C12 алкокси, замещенный C1-C12 алкокси, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk или N(H)C(=S)NJjJk;
или qe и qf вместе представляют собой =C(qg)(qh);
qg и qh, каждый независимо, представляют собой Н, галоген, C1-C12 алкил или замещенный C1-C12 алкил.
Описаны синтез и получение метиленокси (4'-CH2-O-2') мономеров БНК: аденина, цитозина, гуанина, 5-метилцитозина, тимина и урацила, а также их олигомеризация и свойства распознавания нуклеиновых кислот (Koshkin et al., Tetrahedron, 1998, 54, 3607-3630). БНК и их получение также описаны в WO 98/39352 и WO 99/14226.
Были также получены аналоги метиленокси (4'-CH2-O-2') БНК и 2'-тио-БНК (Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222). Описано также получение аналогов запертых нуклеозидов, содержащих олигодезоксирибонуклеотидные дуплексы в качестве субстратов полимераз нуклеиновых кислот (Wengel et al., WO 99/14226). Кроме того, в данной области техники описан синтез 2'-амино-БНК, нового конформационно ограниченного высокоаффинного аналоге олигонуклеотида (Singh et al., J. Org. Chem., 1998, 63, 10035-10039). Кроме того, ранее были получены 2'-амино- и 2'-метиленамино БНК, и была описана термостабильность их дуплексов с комплементарными нитями РНК и ДНК.
В некоторых вариантах реализации представлены бициклические нуклеозиды, имеющие формулу VI:
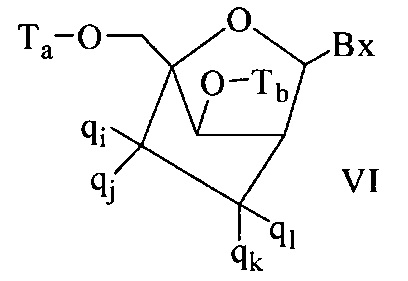
где
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой Н, гидрокси-защитную группу, группу конъюгата, реакционноспособную фосфорную группу, фосфорный фрагмент или ковалентное присоединение к среде подложки;
каждый qi, qj, qk и ql независимо представляет собой Н, галоген, C1-C12 алкил, замещенный C1-C12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, C1-C12 алкоксил, замещенный C1-C12 алкоксил, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk или N(H)C(=S)NJjJk; и
qi и qj или ql и qk вместе представляют собой =C(qg)(qh), где qg и qh, каждый независимо, представляют собой Н, галоген, C1-C12 алкил или замещенный C1-C12 алкил.
Описан один карбоциклический бициклический нуклеозид, имеющий мостик 4'-(CH2)3-2', и мостик из аналога алкенила 4'-СН=СН-CH2-2' (Freier et al., Nucleic Acids Research, 1997, 25(22), 4429-4443 и Albaek et al., J. Org. Chern., 2006, 77, 7731-7740). Описан также синтез и получение карбоциклических бициклических нуклеозидов вместе с их олигомеризацией и биохимическими исследованиями (Srivastava et al., J. Am. Chem. Soc., 2007, 129(26), 8362-8379).
В данном контексте «4'-2' бициклический нуклеозид» или «4' к 2' бициклический нуклеозид» относится к бициклическому нуклеозиду, содержащему фуранозное кольцо, содержащее мостик, соединяющий два атома углерода фуранозного кольца, соединяющий 2' атом углерода и 4' атом углерода сахарного кольца.
В данном контексте «моноциклические нуклеозиды» относятся к нуклеозидам, содержащим модифицированные сахарные фрагменты, которые не являются бициклическими сахарными фрагментами. В некоторых вариантах реализации сахарный фрагмент или аналог сахарного фрагмента нуклеозида может быть модифицирован или замещен в любом положении.
В данном контексте «2'-модифицированный сахар» означает фуранозильный сахар, модифицированный в 2' положении. В некоторых вариантах реализации такие модификации включают заместители, выбранные из: галогенидов, включая, но не ограничиваясь ими, замещенный и незамещенный алкокси, замещенный и незамещенный тиоалкил, замещенный и незамещенный аминоалкил, замещенный и незамещенный алкил, замещенный и незамещенный аллил и замещенный и незамещенный алкинил. В некоторых вариантах реализации 2' модификации выбраны из заместителей, включающих, но не ограничиваясь ими: O[(CH2)nO]mCH3, O(CH2)nNH2, O(CH2)nCH3, O(CH2)nF, O(CH2)nONH2, OCH2C(=O)N(Н)CH3 и О(CH2)nON[(CH2)nCH3]2, где n и m равны от 1 до около 10. Другие 2' группы заместителей также могут быть выбраны из: C1-C12 алкила, замещенного алкила, алкенила, алкинила, алкарила, аралкила, O-алкарила или O-аралкила, SH, SCH3, OCN, Cl, Br, CN, F, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, гетероциклоалкила, гетероциклоалкарила, аминоалкиламино, полиалкиламино, замещенного силила, РНК расщепляющей группы, репортерной группы, интеркалятора, группы для улучшения фармакокинетических свойств или группы для улучшения фармакодинамических свойств антисмыслового соединения, и других заместителей с подобными свойствами. В некоторых вариантах реализации модифицированные нуклеозиды содержат 2'-МОЕ боковую цепь (Baker et al., J. Biol. Chem., 1997, 272, 11944-12000). Такие 2'-МОЕ замещения описаны как улучшающие аффинность связывания по сравнению с немодифицированными нуклеозидами и с другими модифицированными нуклеозидами, такими как 2'-O-метил, O-пропил и O-аминопропил. Было показано, что олигонуклеотиды, имеющие 2'-МОЕ заместитель, являются антисмысловыми ингибиторами экспрессии генов с перспективными возможностями для применения in vivo (Martin, Helv. Chim. Acta, 1995, 78, 486-504; Altmann et al., Chimia, 1996, 50, 168-176; Altmann et al., Biochem. Soc. Trans., 1996, 24, 630-637; и Altmann et al., Nucleosides Nucleotides, 1997, 16, 917-926).
В данном контексте «модифицированный тетрагидропирановый нуклеозид» или «модифицированный ТГП нуклеозид» означает нуклеозид, имеющий шестичленный тетрагидропирановый «сахар», заменивший пентофуранозильный остаток в обычных нуклеозидах (заменитель сахара). ТГП-модифицированные нуклеозиды включают, но не ограничиваются ими, те, которые в данной области техники называют гекситоловой нуклеиновой кислотой (ГНК), анитоловой нуклеиновой кислотой (АНК), манитоловой нуклеиновой кислотой (МНК) (см. Leumann, Bioorg. Med. Chem., 2002, 10, 841-854) или фтор-ГНК (F-ГНК), имеющие тетрагидропирановую кольцевую систему, представленную ниже:
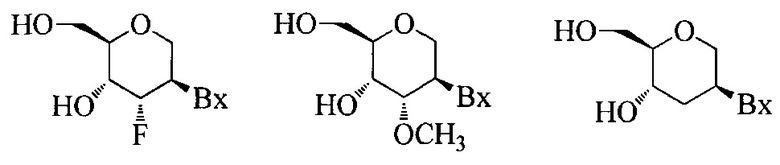
В некоторых вариантах реализации выбраны заменители сахара, имеющие формулу VII:
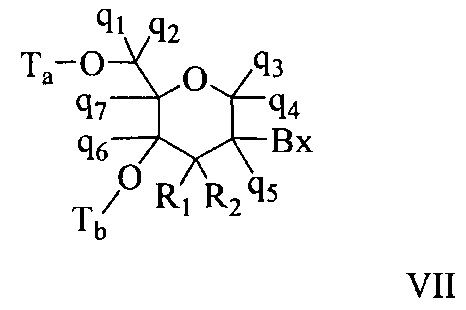
где независимо для каждого из указанного по меньшей мере одного тетрагидропиранового нуклеозидного аналога формулы VII:
Вх представляет собой фрагмент гетероциклического основания;
Та и Tb, каждый независимо, представляют собой межнуклеозидную линкерную группу, которая связывает тетрагидропирановый нуклеозидный аналог с антисмысловым соединением, или один из Ta и Tb представляет собой межнуклеозидную линкерную группу, которая связывает тетрагидропирановый нуклеозидный аналог с антисмысловым соединением, а другой из Та и Tb представляет собой Н, гидроксил-защитную группу, связанную группу конъюгата или 5' или 3'-концевую группу;
q1, q2, q3, q4, q5, q6 и q7, каждый независимо, представляют собой Н, C1-C6 алкил, замещенный C1-C6 алкил, C2-C6 алкенил, замещенный C2-C6 алкенил, C2-C6 алкинил или замещенный C2-C6 алкинил; и каждый из R1 и R2 выбран из водорода, гидроксила, галогена, замещенного или незамещенного алкокси, NJ1J2, SJ1, N3, OC(=X)J1, OC(=X)NJ1J2, NJ3C(=X)NJ1J2 и CN, где X представляет собой О, S или NJ1, и каждый J1, J2 и J3 независимо представляет собой Н или C1-C6 алкил.
В некоторых вариантах реализации предложены модифицированные ТГП нуклеозиды формулы VII, где q1, q2, q3, q4, q5, q6 и q7 представляют собой Н. В некоторых вариантах реализации по меньшей мере один из q1, q2, q3, q4, q5, q6 и q7 является отличным от Н. В некоторых вариантах реализации по меньшей мере один из q1, q2, q3, q4, q5, q6 и q7 представляет собой метил. В некоторых вариантах реализации предложены ТГП нуклеозиды формулы VII, где один из R1 и R2 представляет собой фтор. В некоторых вариантах реализации R1 представляет собой фтор, а R2 представляет собой Н; R1 представляет собой метокси, а R2 представляет собой Н, и R1 представляет собой метоксиэтокси, а R2 представляет собой Н.
в некоторых вариантах реализации заменители сахара содержат кольца, имеющие более 5 атомов и более одного гетероатома. Например, описаны нуклеозиды, содержащие морфолиносахарные фрагменты, и их применение в олигомерных соединениях (см., например: Braasch et al., Biochemistry, 2002, 41, 4503-4510; и патенты США 5698685; 5166315; 5185444; и 5034506). В данном контексте термин «морфолино» означает заменитель сахара, имеющий следующую формулу:
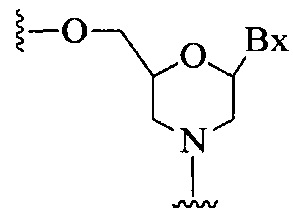 .
.
В некоторых вариантах реализации морфолино могут быть модифицированными, например, добавлением или изменением различных групп заместителей относительно представленной выше структуры морфолино. Такие заменители сахара в данном контексте называют «модифицированными морфолино».
Предложены также комбинации модификаций, без ограничения, такие как 2'-F-5'-метил-замещенные нуклеозиды (см. международную заявку РСТ WO 2008/101157, опубликованную 8/21/08, где описаны другие 5', 2'-бис-замещенные нуклеозиды) и замену рибозильного кольцевого атома кислорода на S с дополнительным замещением в 2'-положении (см. опубликованную заявку на патент США US 2005-0130923, опубликованную 16 июня 2005 года) или в альтернативном варианте с 5'-замещением бициклической нуклеиновой кислоты (см. международную заявку РСТ WO 2007/134181, опубликованную 11/22/07, где 4'-CH2-O-2' бициклический нуклеозид дополнительно замещен в 5' положении 5'-метальной или 5'-винильной группой). Описан также синтез и получение карбоциклических бициклических нуклеозидов вместе с их олигомеризацией и биохимическими исследованиями (см., например, Srivastava et al., J. Am. Chem. Soc. 2007, 129(26), 8362-8379).
В некоторых вариантах реализации антисмысловые соединения содержат один или более модифицированных циклогексенильных нуклеозидов, которые представляют собой нуклеозиды, имеющие шестичленный циклогексенил вместо пентофуранозильного остатка в природных нуклеозидах. Модифицированные циклогексенильные нуклеозиды включают, но не ограничиваются ими, нуклеозиды, описанные в данной области техники (см., например, параллельную опубликованную заявку РСТ WO 2010/036696, опубликованную 10 апреля, 2010, Robeyns et al., J. Am. Chem. Soc., 2008, 130(6), 1979-1984; 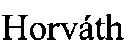 et al., Tetrahedron Letters, 2007, 48, 3621-3623; Nauwelaerts et al., J. Am. Chem. Soc., 2007, 129(30), 9340-9348; Gu et al., Nucleosides, Nucleotides & Nucleic Acids, 2005, 24(5-7), 993-998; Nauwelaerts et al., Nucleic Acids Research, 2005, 33(8), 2452-2463; Robeyns et al., Acta Crystallographica, Section F: Structural Biology and Crystallization Communications, 2005, F61(6), 585-586; Gu et al., Tetrahedron, 2004, 60(9), 2111-2123; Gu et al., Oligonucleotides, 2003, 13(6), 479-489; Wang et al., J. Org. Chem., 2003, 68, 4499-4505; Verbeure et al., Nucleic Acids Research, 2001, 29(24), 4941-4947; Wang et al., J. Org. Chem., 2001, 66, 8478-82; Wang et al., Nucleosides, Nucleotides & Nucleic Acids, 2001, 20(4-7), 785-788; Wang et al., J. Am. Chem., 2000, 722, 8595-8602; опубликованную заявку РСТ WO 06/047842; и опубликованную заявку РСТ WO 01/049687; полное содержание каждой из которых включено в настоящий документ посредством ссылки). Некоторые модифицированные циклогексенильные нуклеозиды имеют формулу X.
et al., Tetrahedron Letters, 2007, 48, 3621-3623; Nauwelaerts et al., J. Am. Chem. Soc., 2007, 129(30), 9340-9348; Gu et al., Nucleosides, Nucleotides & Nucleic Acids, 2005, 24(5-7), 993-998; Nauwelaerts et al., Nucleic Acids Research, 2005, 33(8), 2452-2463; Robeyns et al., Acta Crystallographica, Section F: Structural Biology and Crystallization Communications, 2005, F61(6), 585-586; Gu et al., Tetrahedron, 2004, 60(9), 2111-2123; Gu et al., Oligonucleotides, 2003, 13(6), 479-489; Wang et al., J. Org. Chem., 2003, 68, 4499-4505; Verbeure et al., Nucleic Acids Research, 2001, 29(24), 4941-4947; Wang et al., J. Org. Chem., 2001, 66, 8478-82; Wang et al., Nucleosides, Nucleotides & Nucleic Acids, 2001, 20(4-7), 785-788; Wang et al., J. Am. Chem., 2000, 722, 8595-8602; опубликованную заявку РСТ WO 06/047842; и опубликованную заявку РСТ WO 01/049687; полное содержание каждой из которых включено в настоящий документ посредством ссылки). Некоторые модифицированные циклогексенильные нуклеозиды имеют формулу X.
где независимо для каждого указанного по меньшей мере одного циклогексенильного нуклеозидного аналога формулы X:
Вх представляет собой фрагмент гетероциклического основания;
Т3 и Т4, каждый независимо, представляют собой межнуклеозидную линкерную группу, которая связывает циклогексенильный нуклеозидный аналог с антисмысловым соединением, или один из Т3 и Т4 представляет собой межнуклеозидную линкерную группу, которая связывает тетрагидропирановый нуклеозидный аналог с антисмысловым соединением, а другой из Т3 и Т4 представляет собой Н, гидроксил-защитную группу, связанную группу конъюгата или 5'-или 3'-концевую группу; и
q1, q2, q3, q4, q5, q6, q7, q8 и q9, каждый независимо, представляют собой Н, C1-C6 алкил, замещенный C1-C6 алкил, C2-C6 алкенил, замещенный C2-C6 алкенил, C2-C6 алкинил, замещенный C2-C6 алкинил или другие группы-заместители сахара.
В данном контексте «2'-модифицированный» или «2'-замещенный» относится к нуклеозиду, содержащему сахар, содержащий заместитель в 2' положении, отличный от Н или ОН. 2'-модифицированные нуклеозиды включают, но не ограничиваются ими, бициклические нуклеозиды, в которых мостик, соединяющий два атом углерода сахарного кольца, соединяет 2' атом углерода и другой атом углерода сахарного кольца; и нуклеозиды с немостиковыми 2' заместителями, такими как аллил, амино, азидо, тио, O-аллил, O-C1-С10 алкил, -OCF3, O-(CH2)2-O-CH3, 2'-O(CH2)2SCH3, O-(CH2)2-O-N(Rm)(Rn), or O-CH2-С(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой Н или замещенный или незамещенный C1-C10 алкил. 2'-модифицированные нуклеозиды могут также содержать другие модификации, например, в других положениях сахара и/или азотистого основания.
В данном контексте «2'-F» относится к нуклеозиду, содержащему сахар, содержащий группу фтора в 2' положении сахарного кольца.
В данном контексте «2'-ОМе» или «2'-OCH3», или «2'-O-метил» относится к нуклеозиду, содержащему сахар, содержащий группу -OCH3 в 2' положении сахарного кольца.
В данном контексте «МОЕ» или «2'-МОЕ», или «2'-OCH2CH2OCH3», или «2'-O-метоксиэтил» относится к нуклеозиду, содержащему сахар, содержащий группу -OCH2CH2OCH3 в 2' положении сахарного кольца.
В данном контексте «олигонуклеотид» относится к соединению, содержащему множество связанных нуклеозидов. В некоторых вариантах реализации один или более из множества нуклеозидов являются модифицированными. В некоторых вариантах реализации олигонуклеотид содержит один или более рибонуклеозидов (РНК) и/или дезоксирибонуклеозидов (ДНК).
В данной области техники известны также многие другие бициклические и трициклические кольцевые системы заменителей сахара, которые могут быть использованы для модификации нуклеозидов для внедрения в антисмысловые соединения (см., например, обзорную статью: Leumann, Bioorg. Med. Chem., 2002, 10, 841-854). Такие кольцевые системы могут подвергаться различным дополнительным замещениям для повышения активности.
Способы получения модифицированных сахаров хорошо известны специалистам в данной области техники. Некоторые иллюстративные патенты США, которые описывают получение таких модифицированных сахаров, включают, без ограничения, патенты США: 4981957; 5118800; 5319080; 5359044; 5393878; 5446137; 5466786; 5514785; 5519134; 5567811; 5576427; 5591722; 5597909; 5610300; 5627053; 5639873; 5646265; 5670633; 5700920; 5792847 и 6600032, а также международную заявку PCT/US2005/019219, поданную 2 июня 2005 года и опубликованную как WO 2005/121371 12 декабря 2005 года, полное содержание каждого из которых включено в настоящий документ посредством ссылки.
В нуклеотидах, имеющих модифицированные сахарные фрагменты, фрагменты азотистых оснований (природные, модифицированные или их комбинации) сохраняются для гибридизации с соответствующей нуклеиновой кислотой-мишенью.
В некоторых вариантах реализации антисмысловые соединения содержат один или более нуклеозидов, имеющих модифицированные сахарные фрагменты. В некоторых вариантах реализации модифицированный сахарный фрагмент представляет собой 2'-МОЕ. В некоторых вариантах реализации 2'-МОЕ модифицированные нуклеозиды расположены в гэпмерном мотиве. В некоторых вариантах реализации модифицированный сахарный фрагмент представляет собой бициклический нуклеозид, имеющий мостиковую группу (4'-СН(CH3)-O-2'). В некоторых вариантах реализации (4'-СН(CH3)-O-2') модифицированные нуклеозиды расположены в крыльях гэпмерного мотива.
Модифицированные азотистые основания
Модификации или замещения азотистого основания (или основания) структурно отличаются и функционально взаимозаменимы с природными или синтетическими немодифицированными азотистыми основаниями. Природные и модифицированные азотистые основания могут участвовать в водородном связывании. Такие модификации азотистых оснований могут влиять на стабильность к действию нуклеаз, аффинность связывания или некоторые другие полезные биологические свойства антисмысловых соединений. Модифицированные азотистые основания включают синтетические и природные азотистые основания, такие как, например, 5-метилцитозин (5-me-С). Некоторые замещения азотистых оснований, включая 5-метилцитозиновые замещения, особенно подходят для повышения аффинности связывания антисмыслового соединения с нуклеиновой кислотой-мишенью. Например, было показано, что 5-метилцитозиновые замещения повышают стабильность дуплекса нуклеиновой кислоты на 0,6-1,2°С (Sanghvi, Y.S., Crooke, S.T. и Lebleu, В., ред., Antisense Research and Applications, CRC Press, Boca Raton, 1993, cc. 276-278).
Дополнительные модифицированные азотистые основания включают 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил и другие алкильные производные аденина и гуанина, 2-пропил и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галогенурацил и цитозин, 5-пропинил (-С≡С-CH3) урацил и цитозин и другие алкинильные производные пиримидиновых оснований, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген, 8-амино, 8-тиол, 8-тиоалкил, 8-гидроксил и другие 8-замещенные аденины и гуанины, 5-галоген, в частности, 5-бром, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 2-F-аденин, 2-аминоаденин, 8-азагуанин и 8-азааденин, 7-дезазагуанин и 7-дезазааденин, и 3-дезазагуанин и 3-дезазааденин.
Фрагменты гетероциклических оснований также могут включать те, в которых пуриновое или пиримидиновое основание заменено другими гетероциклами, например, 7-дезазааденин, 7-дезазагуанозин, 2-аминопиридин и 2-пиридон. Азотистые основания, которые особенно подходят для повышения аффинности связывания антисмысловых соединений, включают 5-замещенные пиримидины, 6-азапиримидины и N-2, N-6 и O-6 замещенные пурины, включая 2-аминопропиладенин, 5-пропинилурацил и 5-пропинилцитозин.
В некоторых вариантах реализации антисмысловые соединения, направленные на нуклеиновую кислоту CFB, содержат одно или более модифицированных азотистых оснований. В некоторых вариантах реализации укороченные или гэп-расширенные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту CFB, содержат одно или более модифицированных азотистых оснований. В некоторых вариантах реализации модифицированное азотистое основание представляет собой 5-метилцитозин. В некоторых вариантах реализации каждый цитозин представляет собой 5-метилцитозин.
Сопряженные антисмысловые соединения
В некоторых вариантах реализации настоящего описания предложены сопряженные антисмысловые соединения. В некоторых вариантах реализации настоящего описания предложены сопряженные антисмысловые соединения, содержащие антисмысловый олигонуклеотид, комплементарный транскрипту нуклеиновой кислоты. В некоторых вариантах реализации настоящего описания предложены способы, включающие приведение в контакт клетки с сопряженным антисмысловым соединением, содержащим антисмысловый олигонуклеотид, комплементарный транскрипту нуклеиновой кислоты. В некоторых вариантах реализации настоящего описания предложены способы, включающие приведение в контакт клетки с сопряженным антисмысловым соединением, содержащим антисмысловый олигонуклеотид, и уменьшение количества или активности транскрипта нуклеиновой кислоты в клетке.
Ранее был описан асиалогликопротеиновый рецептор (ASGP-R). См. например. Park et al., PNAS, том. 102, №47, сс. 17125-17129 (2005). Такие рецепторы экспрессируются на клетках печени, в частности, гепатоцитах. Кроме того, было показано, что соединения, содержащие кластеры трех N-ацетилгалактозаминовых (GalNAc) лигандов, способны связываться с ASGP-R, приводя к захвату указанного соединения в клетку. См. например, Khorev et al., Bioorganic and Medicinal Chemistry, 16, 9, сс. 5216-5231 (май, 2008). Соответственно, конъюгаты, содержащие такие кластеры GalNAc, использовали для облегчения захвата некоторых соединений в клетки печени, в частности, гепатоциты. Например, было показано, что некоторые GalNAc-содержащие конъюгаты увеличивают активность дуплексных миРНК соединений в клетках печени in vivo. В таких случаях GalNAc-содержащий конъюгат, как правило, прикрепляется к смысловой спирали дуплекса миРНК. Поскольку смысловая спираль отбрасывается перед окончательной гибридизацией антисмысловой спирали с нуклеиновой кислотой-мишенью, то маловероятно, что такой конъюгат будет влиять на активность. Как правило, конъюгат присоединяется к 3'-концу смысловой спирали миРНК. См. например, патент США 8106022. Некоторые группы конъюгата, описанные в настоящем документе, более активны и/или синтезируются легче, чем группы конъюгата, описанные ранее.
В некоторых вариантах реализации настоящего изобретения конъюгаты присоединяются к односпиральным антисмысловым соединениям, включая, но не ограничиваясь ими, антисмысловые соединения на основе РНКазы Н и антисмысловые соединения, которые изменяют сплайсинг целевой нуклеиновой кислоты пре-мРНК. В таких вариантах реализации конъюгат должен оставаться присоединенным к антисмысловому соединению достаточно долго для обеспечения преимущества (улучшенного захвата в клетки), но затем он должен либо расщепляться, либо иным образом не препятствовать последующим стадиям, необходимым для активности, таким как гибридизация с целевой нуклеиновой кислотой и взаимодействие с РНКазой Н или ферментами, связанными со сплайсингом или модулированием сплайсирования. Такой баланс свойств более важен при осаждении односпиральных антисмысловых соединений, чем соединений миРНК, где конъюгат может быть просто присоединен к смысловой спирали. В настоящем документе описаны односпиральные антисмысловые соединения, обладающие улучшенной активностью в клетках печени in vivo, по сравнению с таким же антисмысловым соединением, не имеющим конъюгата. Учитывая необходимый баланс свойств для этих соединений, такая улучшенная активность является неожиданной.
В некоторых вариантах реализации группы конъюгата по настоящему документу содержат расщепляемый фрагмент. Как было отмечено, не ограничиваясь каким-либо механизмом, логично, что конъюгат должен сохраняться у соединения достаточно долго для обеспечения усиления захвата, но после этого желательно, чтобы некоторая его часть или, в идеале, весь конъюгат расщеплялся, выделяя исходное соединение (например, антисмысловое соединение) в его наиболее активной форме. В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемый нуклеозид. Такие варианты реализации обладают преимуществом эндогенных нуклеаз в клетке за счет присоединения остальной части конъюгата (кластера) к антисмысловому олигонуклеотиду через нуклеозид при помощи одной или более расщепляемых связей, таких как фосфодиэфирная связь. В некоторых вариантах реализации кластер связан с расщепляемым нуклеозидом через фосфодиэфирную связь. В некоторых вариантах реализации расщепляемый нуклеозид присоединен к антисмысловому олигонуклеотиду (антисмысловому соединению) фосфодиэфирной связью. В некоторых вариантах реализации группа конъюгата может содержать два или три расщепляемых нуклеозида. В таких вариантах реализации указанные расщепляемые нуклеозиды связаны друг с другом, с антисмысловым соединением и/или с кластером посредством расщепляемых связей (таких как фосфодиэфирная связь). Некоторые конъюгаты по настоящему документу не содержат расщепляемый нуклеозид, а вместо этого содержат расщепляемую связь. Показано, что достаточное расщепление конъюгата из олигонуклеотида обеспечивается по меньшей мере за счет одной связи, которая легко поддается расщеплению в клетке (расщепляемая связь).
В некоторых вариантах реализации сопряженные антисмысловые соединения представляют собой пролекарства. Такие пролекарства вводят животному, и они в конечном итоге метаболизируются до более активной формы. Например, сопряженные антисмысловые соединения расщепляются с удалением всего или части конъюгата, приводя к активной (или более активной) форме антисмыслового соединения, не содержащего всего или части конъюгата.
В некоторых вариантах реализации конъюгаты присоединены у 5'-конца олигонуклеотида. Некоторые такие 5'-конъюгаты расщепляются более эффективно, чем аналоги, имеющие такую же группу конъюгата, присоединенную у 3'-конца. В некоторых вариантах реализации улучшенная активность может коррелировать с улучшенным расщеплением. В некоторых вариантах реализации олигонуклеотиды, содержащие конъюгат у 5'-конца, обладают более высокой эффективностью, чем олигонуклеотиды, содержащие конъюгат у 3'-конца (см., например. Примеры 56, 81, 83 и 84). Кроме того, 5'-присоединение обеспечивает более простой синтез олигонуклеотида. Как правило, олигонуклеотиды синтезируют на твердой подложке в направлении от 3' к 5'. Для получения 3'-сопряженного олигонуклеотида, как правило присоединяют предварительно сопряженный 3'-нуклеозид к твердой подложке, а затем обычным путем создают олигонуклеотид. Однако присоединение такого сопряженного нуклеозида к твердой подложке усложняет синтез. Кроме того, используя такой подход, конъюгат затем присутствует в ходе всего синтеза олигонуклеотида и может разрушаться во время последующих стадий или может ограничивать типы реакций и реагентов, которые можно использовать. Используя структуры и методики, описанные в настоящем документе для 5'-сопряженных олигонуклеотидов, можно синтезировать олигонуклеотид при помощи стандартных автоматизированных методик и внедрять в конъюгат последний (5'-крайний) нуклеозид или после отделения олигонуклеотида от твердой подложки.
С учетом известного уровня техники и настоящего описания, специалисты в данной области техники могут легко получить любые из конъюгатов и сопряженных олигонуклеотидов, описанных в настоящем документе. Кроме того, синтез некоторых таких конъюгатов и сопряженных олигонуклеотидов, описанных в настоящем документе, проще и/или требует меньше стадий и, следовательно, менее дорогой, чем синтез ранее описанных конъюгатов, что дает преимущество при производстве. Например, синтез некоторых групп конъюгата состоит из меньшего количества синтетических стадий, что приводит к увеличению выхода, по сравнению с ранее описанными группами конъюгата. Группы конъюгатов, такие как GalNAc3-10 в Примере 46 и GalNAc3-7 в Примере 48 гораздо проще, чем ранее описанные конъюгаты, такие как описаны в публикациях U.S. 8106022 или U.S. 7262177, для которых необходима сборка большего количества химических промежуточных соединений. Соответственно, эти и другие конъюгаты, описанные в настоящем документе, обладают преимуществом по сравнению с ранее описанными соединениями для применения с любым олигонуклеотидом, включая односпиральные олигонуклеотиды и любую спираль двухспиральных олигонуклеотидов (например, миРНК).
Точно так же, в настоящем документе описаны группы конъюгатов, имеющие только один или два лиганда GalNAc. Как показано, такие сопряженные группы усиливают активность антисмысловых соединений. Такие соединения гораздо проще получить, чем конъюгаты, содержащие три лиганда GalNAc. Группы конъюгатов, содержащие один или два лиганда GalNAc, могут быть присоединены к любым антисмысловым соединениям, включая односпиральные олигонуклеотиды и любую спираль двухспиральных олигонуклеотидов (например, миРНК).
В некоторых вариантах реализации конъюгаты, описанные в настоящем документе, существенно не изменяют некоторые показатели переносимости. Например, в настоящем документе показано, что сопряженные антисмысловые соединения являются не более иммуногенными, чем несопряженные исходные соединения. Поскольку активность улучшается, то варианты реализации, в которых переносимость остается такой же (или в действительности если даже переносимость ухудшается лишь незначительно, по сравнению с приростом активности), обладают улучшенными характеристиками для терапии.
В некоторых вариантах реализации сопряжение позволяет изменять антисмысловые соединения так, чтобы они обладали менее выраженными последствиями в отсутствие сопряжения. Например, в некоторых вариантах реализации замена одной или более тиофосфатных связей полностью тиофосфатного антисмыслового соединения на фосфодиэфирные связи приводит к улучшению некоторых показателей переносимости. Например, в некоторых случаях такие антисмысловые соединения, имеющие один или более фосфодиэфиров, являются менее иммуногенными, чем такие же соединения, в которых каждая связь представляет собой тиофосфат. Однако в некоторых случаях, как показано в Примере 26, такое же замещение одной или более тиофсофатных связей на фосфодиэфирные связи приводит также к снижению клеточного захвата и/или к снижению активности. В некоторых вариантах реализации сопряженные антисмысловые соединения, описанные в настоящем документе, допускают такое изменение связей с небольшим снижением или без снижения захвата и активности, по сравнению с сопряженным полностью тиофосфатным аналогом. В действительности, в некоторых вариантах реализации, например, в Примерах 44, 57, 59 и 86, олигонуклеотиды, содержащие конъюгат и по меньшей мере одну фосфодиэфирную межнуклеозидную связь, фактически демонстрируют повышенную активность in vivo даже по сравнению с полностью тиофосфатным аналогом, также содержащим такой же конъюгат. Более того, поскольку сопряжение приводит к значительному увеличению захвата /активности, то небольшое снижение такого существенного прироста может быть приемлемым для достижения улучшенной переносимости. Соответственно, в некоторых вариантах реализации сопряженные антисмысловые соединения содержат по меньшей мере одну фосфодиэфирную связь.
В некоторых вариантах реализации сопряжение антисмысловых соединений по настоящему документу приводит к улучшенной доставке, захвату и активности в гепатоцитах. Следовательно, в ткань печени доставляется большее количество соединения. Однако в некоторых вариантах реализации такая улучшенная доставка сама по себе не объясняет общего увеличения активности. В некоторых таких вариантах реализации в гепатоциты поступает большее количество соединения. В некоторых вариантах реализации даже такой улучшенный захват гепатоцитов сам по себе не объясняет общего увеличения активности. В таких вариантах реализации увеличивается продуктивный захват сопряженного соединения. Например, как показано в Примере 102, некоторые варианты реализации GalNAc-содержащих конъюгатов увеличивают обогащение антисмысловых олигонуклеотидов в гепатоцитах, по сравнению с не паренхимальными клетками. Такое обогащение преимущественно для олигонуклеотидов, которые направлены на гены, экспрессируемые в гепатоцитах.
В некоторых вариантах реализации сопряженные антисмысловые соединения по настоящему документу приводят к уменьшению воздействия на почки. Например, как показано в Примере 20, концентрации антисмысловых олигонуклеотидов, содержащих некоторые варианты реализации GalNAc-содержащих конъюгатов, в почках ниже, чем концентрации антисмысловых олигонуклеотидов, не имеющих GalNAc-содержащего конъюгата. Это имеет несколько преимущественных терапевтических применений. Для терапевтических показаний, в которых не требуется проявление активности в почках, воздействие на почки подвергает их риску токсичности без соответствующей пользы. Более того, высокая концентрация в почках обычно приводит к выводу соединения с мочой, обеспечивая более быстрое выведение. Соответственно, для внепочечных мишеней накопление в почках является нежелательным.
В некоторых вариантах реализации настоящего описания предложены сопряженные антисмысловые соединения, представленные формулой:
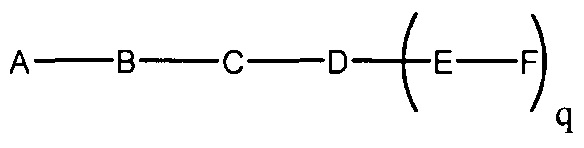
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
На представленной выше схеме и в аналогичных схемах в настоящем документе группа ветвления «D» разветвляется такое количество раз, которое необходимо для соответствия количеству групп (E-F), указанному количеством «q». Следовательно, если q=1, то формула представляет собой:

если q=2, то формула представляет собой:
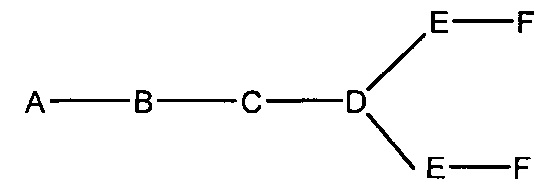
если q=3, то формула представляет собой:
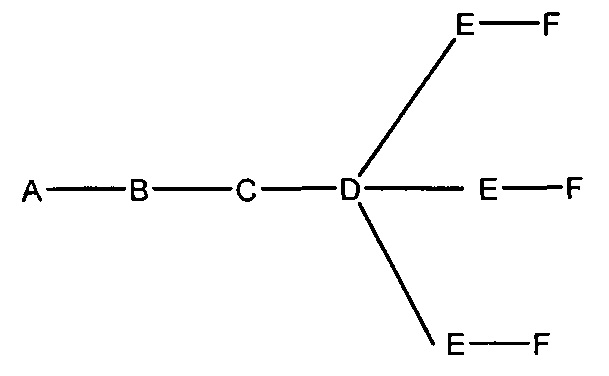
если q=4, то формула представляет собой:
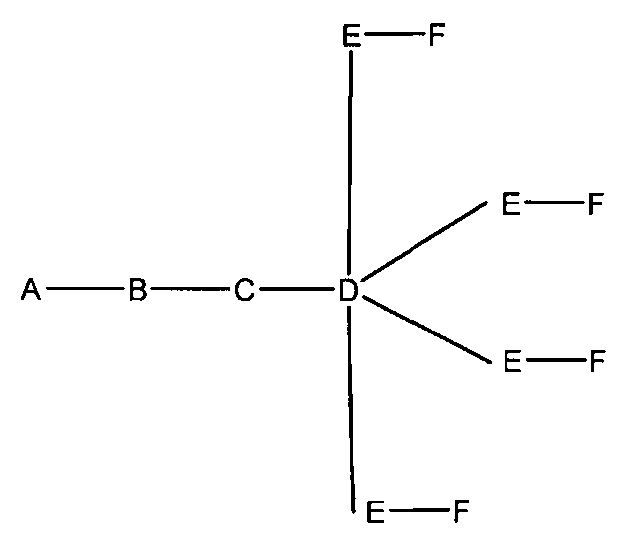
если q=5, то формула представляет собой:
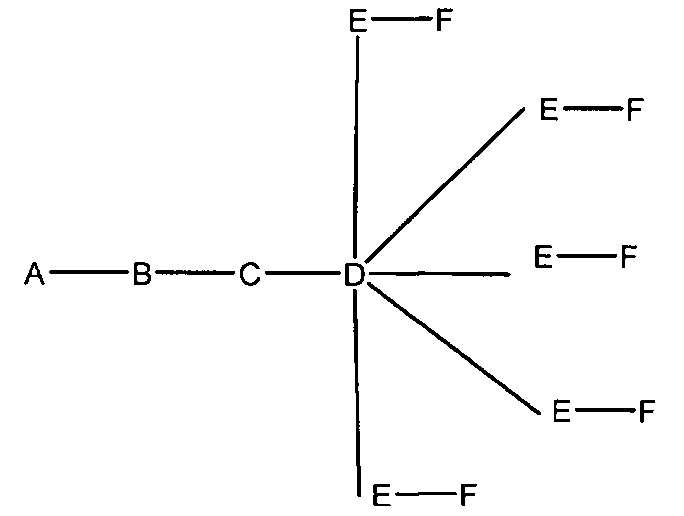
В некоторых вариантах реализации предложены сопряженные антисмысловые соединения, имеющие структуру:
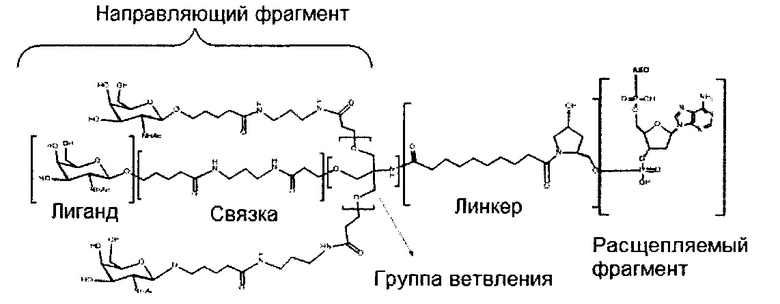 .
.
В некоторых вариантах реализации предложены сопряженные антисмысловые соединения, имеющие структуру:
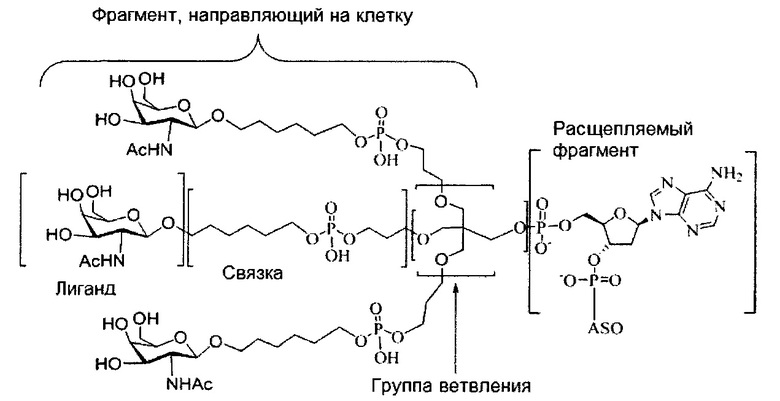 .
.
В некоторых вариантах реализации предложены сопряженные антисмысловые соединения, имеющие структуру:
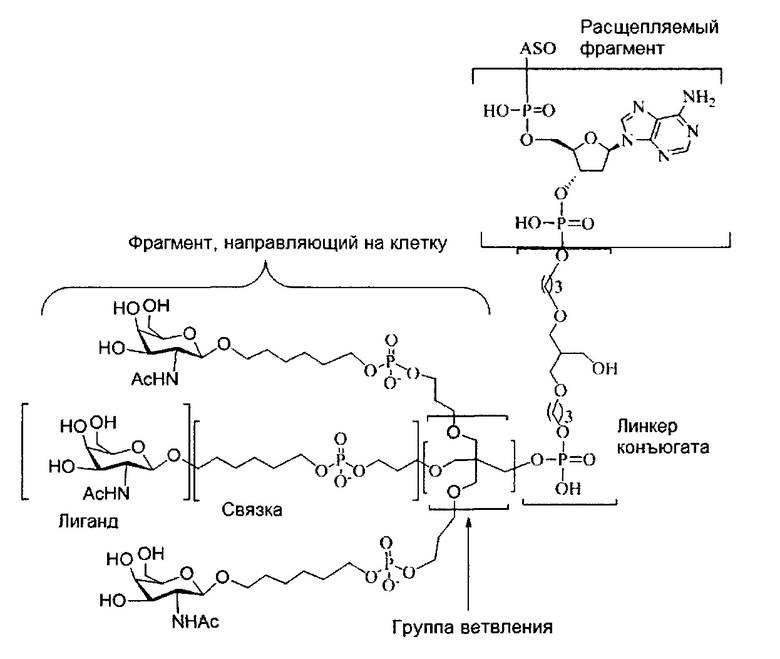
В некоторых вариантах реализации предложены сопряженные антисмысловые соединения, имеющие структуру:
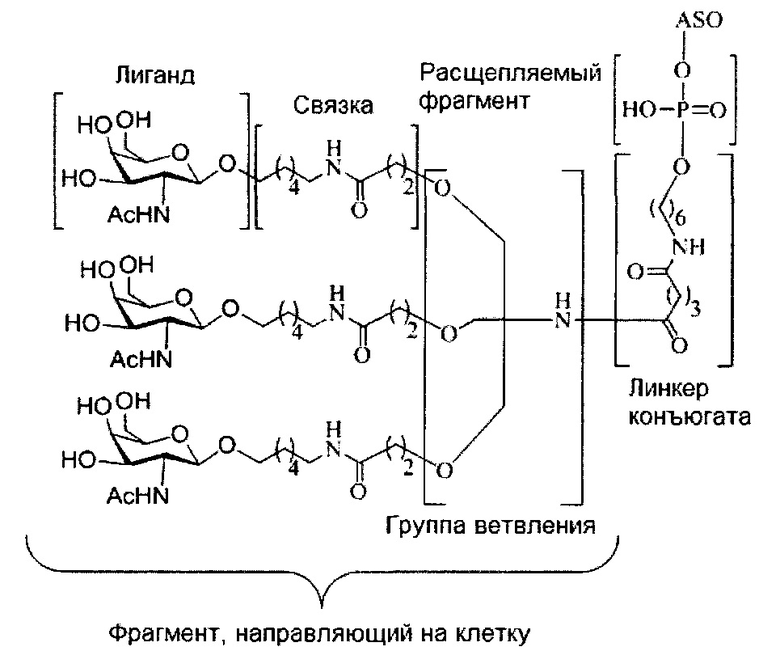
В настоящем описании предложены следующие неограничивающие нумерованные варианты реализации:
Вариант реализации 1. Сопряженное антисмысловое соединение по любому из вариантов реализации 1179-1182, в котором связка имеет структуру, выбранную из: 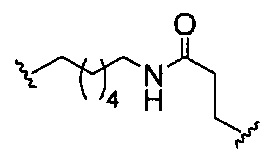 или
или 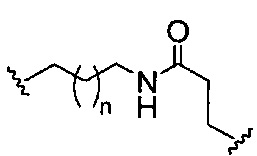 ; где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
; где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
Вариант реализации 2. Сопряженное антисмысловое соединение по любому из вариантов реализации 1179-1182, в котором связка имеет структуру:
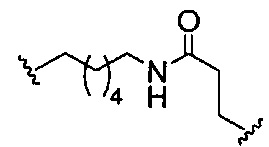 .
.
Вариант реализации 3. Сопряженное антисмысловое соединение по любому из вариантов реализации 1179-1182 или 1688-1689, в котором линкер имеет структуру, выбранную из:
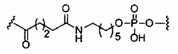 и
и 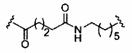 .
.
Вариант реализации 4. Сопряженное антисмысловое соединение по любому из вариантов реализации 1179-1182 или 1688-1689, в котором линкер имеет структуру, выбранную из:
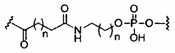 и
и 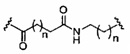 ;
;
где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
Вариант реализации 5. Сопряженное антисмысловое соединение по любому из вариантов реализации 1179-1182 или 1688-1689, в котором линкер имеет структуру:
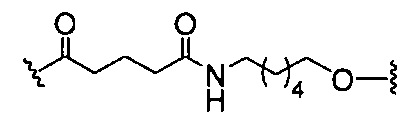 .
.
В вариантах реализации, имеющих более одной конкретной переменной (например, более одного «m» или «n»), если не указано иное, каждая такая конкретная переменная выбрана независимо. Следовательно, для структуры, имеющей более одного n, каждый n выбран независимо, так что они могут быть или не быть одинаковыми между собой.
i. Некоторые расщепляемые фрагменты
В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемую связь. В некоторых вариантах реализации расщепляемый фрагмент содержит расщепляемую связь. В некоторых вариантах реализации группа конъюгата содержит расщепляемый фрагмент. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется к антисмысловому олигонуклеотиду. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется непосредственно к фрагменту, направляющему на клетку. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется к линкеру конъюгата. В некоторых вариантах реализации расщепляемый фрагмент содержит фосфат или фосфодиэфир. В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемый нуклеозид или нуклеозидный аналог. В некоторых вариантах реализации нуклеозид или нуклеозидный аналог содержит необязательно защищенное гетероциклическое основание, выбранное из пурина, замещенного пурина, пиримидина или замещенного пиримидина. В некоторых вариантах реализации расщепляемый фрагмент представляет собой нуклеозид, содержащий необязательно защищенное гетероциклическое основание, выбранное из урацила, тимина, цитозина, 4-N-бензоилцитозина, 5-метилцитозина, 4-N-бензоил-5-метилцитозина, аденина, 6-N-бензоиладенина, гуанина и 2-N-изобутирилгуанина. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксинуклеозид, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной или тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксиаденозин, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной или тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксиаденозин, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной связью.
В некоторых вариантах реализации расщепляемый фрагмент присоединен к 3'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к 5'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к 2'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к антисмысловому олигонуклеотиду фосфодиэфирной связью. В некоторых вариантах реализации расщепляемый фрагмент присоединен к указанному линкеру либо фосфодиэфирной, либо тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент присоединен к указанному линкеру фосфодиэфирной связью. В некоторых вариантах реализации группа конъюгата не содержит расщепляемый фрагмент.
В некоторых вариантах реализации расщепляемый фрагмент расщепляется после введения указанного комплекса в организм животного только после его поглощения целевой клеткой. Внутри клетки расщепляемый фрагмент расщепляется, высвобождая таким образом активный антисмысловый олигонуклеотид. Не ограничиваясь теорией, предполагают, что расщепляемый фрагмент расщепляется под действием одной или более нуклеаз внутри клетки. В некоторых вариантах реализации одна или более нуклеаз расщепляют фосфодиэфирную связь между расщепляемым фрагментом и линкером. В некоторых вариантах реализации расщепляемый фрагмент имеет структуру, выбранную из следующих:
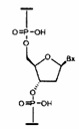 ;
; 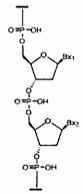 ; и
; и 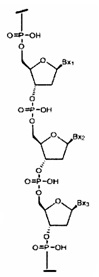
где каждый из Вх, Bx1, Bx2 и Вх3 независимо представляет собой фрагмент гетероциклического основания. В некоторых вариантах реализации расщепляемый фрагмент имеет структуру, выбранную из следующих:
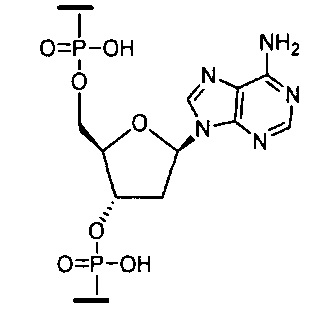
ii. Некоторые линкеры
В некоторых вариантах реализации группы конъюгата содержат линкер. В некоторых таких вариантах реализации линкер ковалентно связан с расщепляемым фрагментом. В некоторых таких вариантах реализации линкер ковалентно связан с антисмысловым олигонуклеотидом. В некоторых вариантах реализации линкер ковалентно связан с фрагментом, направляющим на клетку. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к твердой подложке. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к белковому связывающему фрагменту. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к твердой подложке и дополнительно содержит ковалентное присоединение к белковому связывающему фрагменту. В некоторых вариантах реализации линкер содержит несколько положений для присоединения связанных лигандов. В некоторых вариантах реализации линкер содержит несколько положений для присоединения связанных лигандов и не присоединен к группе ветвления. В некоторых вариантах реализации линкер дополнительно содержит одну или более расщепляемых связей. В некоторых вариантах реализации группа конъюгата не содержит линкер.
В некоторых вариантах реализации линкер содержит по меньшей мере одну линейную группу, содержащую группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, тиоэфирных (-S-) и гидроксиламино (-O-N(H)-) групп. В некоторых вариантах реализации линейная группа содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации линейная группа содержит группы, выбранные из алкильных и простых эфирных групп. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну фосфорную линкерную группу. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну фосфодиэфирную группу. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну нейтральную линкерную группу. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, направляющему на клетку, и к расщепляемому фрагменту. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, направляющему на клетку, и к антисмысловому олигонуклеотиду. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, направляющему на клетку, к расщепляемому фрагменту и к твердой подложке. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, направляющему на клетку, к расщепляемому фрагменту, к твердой подложке и к белковому связывающему фрагменту. В некоторых вариантах реализации линейная группа содержит одну или более расщепляемых связей.
В некоторых вариантах реализации линкер содержит линейную группу, ковалентно присоединенную к группе скелета. В некоторых вариантах реализации скелет содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, простых эфирных, тиоэфирных и гидроксиламино-групп. В некоторых вариантах реализации скелет содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации скелет содержит по меньшей мере одну моно- или полициклическую кольцевую систему. В некоторых вариантах реализации скелет содержит по меньшей мере две моно- или полициклические кольцевые системы. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту и линкеру. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру и твердой подложке. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру и белковому связывающему фрагменту. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру, белковому связывающему фрагменту и твердой подложке. В некоторых вариантах реализации группа скелета содержит одну или более расщепляемых связей.
В некоторых вариантах реализации линкер содержит белок связывающий фрагмент. В некоторых вариантах реализации белок связывающий фрагмент представляет собой липид, такой как, например, включая, но не ограничиваясь ими, холестерин, холевая кислота, адамантан-уксусная кислота, 1-пирен-масляная кислота, дигидротестостерон, 1,3-бис-O(гексадецил)глицерин, геранилоксигексиловая группа, гексадецилглицерин, борнеол, ментол, 1,3-пропандиол, гептадециловая группа, пальмитиновая кислота, миристиновая кислота, O3-(олеоил)литохолевая кислота, O3-(олеоил)холеновая кислота, диметокситритил или феноксазин, витамин (например, фолат, витамин А, витамин Е, биотин, пиридоксаль), пептид, углевод (например, моносахарид, дисахарид, трисахарид, тетрасахарид, олигосахарид, полисахарид), эндосомолитический компонент, стероид (например, уваол, гецигенин, диосгенин), терпен (например, тритерпен, например, сарсасапогенин, фриделин, литохолевая кислота, дериватизованная эпифриделанолом) или катионный липид. В некоторых вариантах реализации белок связывающий фрагмент представляет собой насыщенную или ненасыщенную жирную кислоту с длиной цепи от С16 до С22, холестерин, холевую кислоту, витамин Е, адамантан или 1-пентафторпропил.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
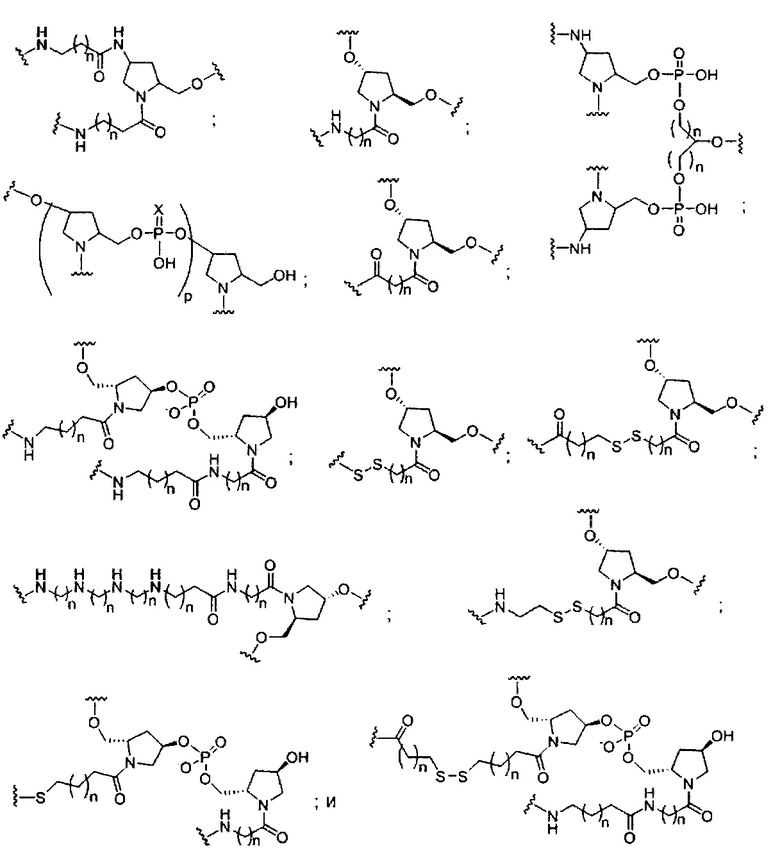
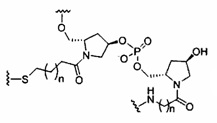 ; и
; и 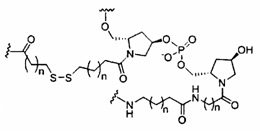
где каждый n независимо равен от 1 до 20; и р равен от 1 до 6.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
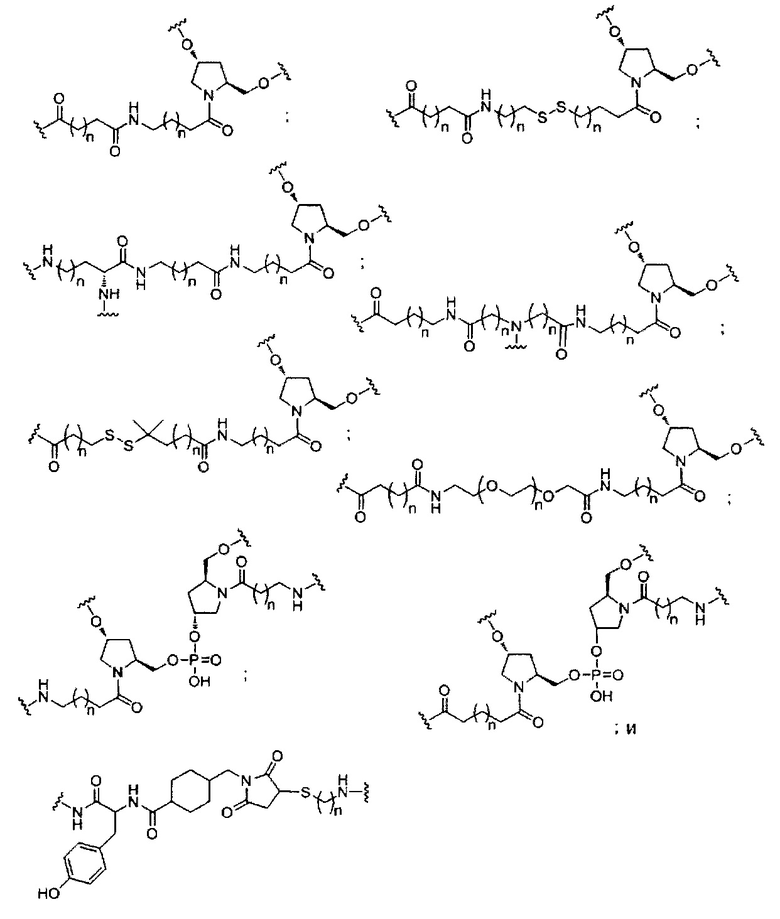
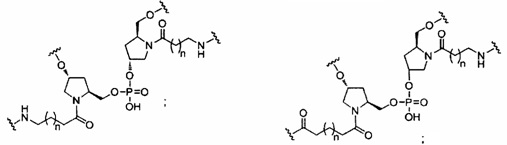 и
и
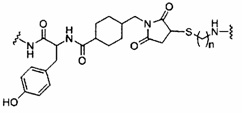
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
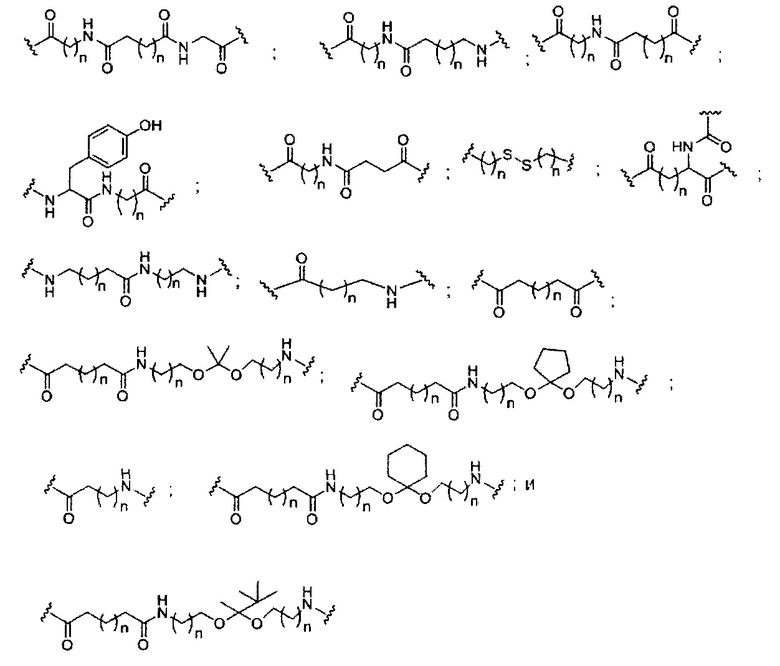
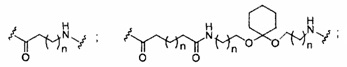 и
и
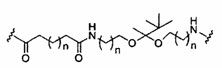
где n равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
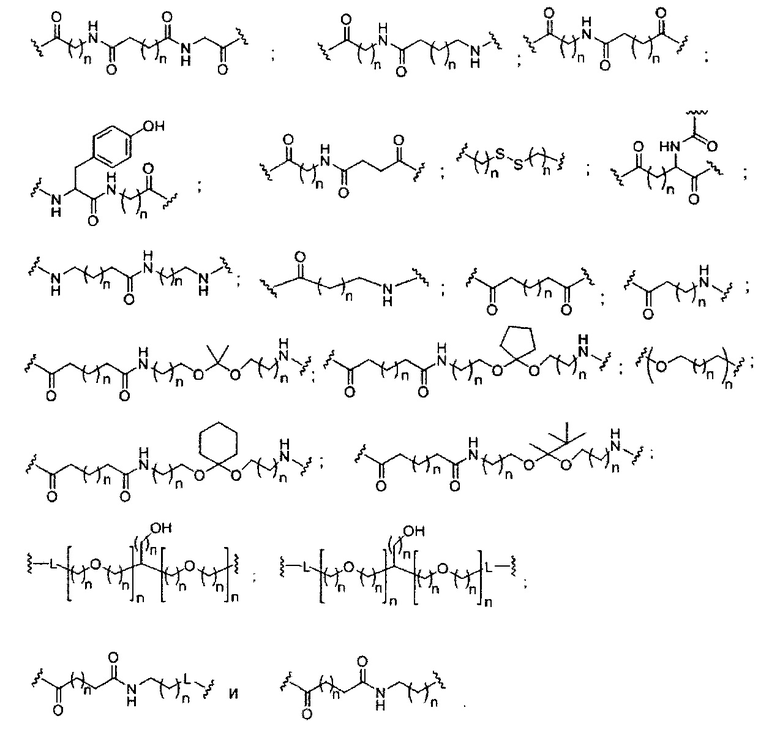
 и
и 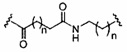 .
.
где каждый L независимо представляет собой фосфорную линкерную группу или нейтральную линкерную группу; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
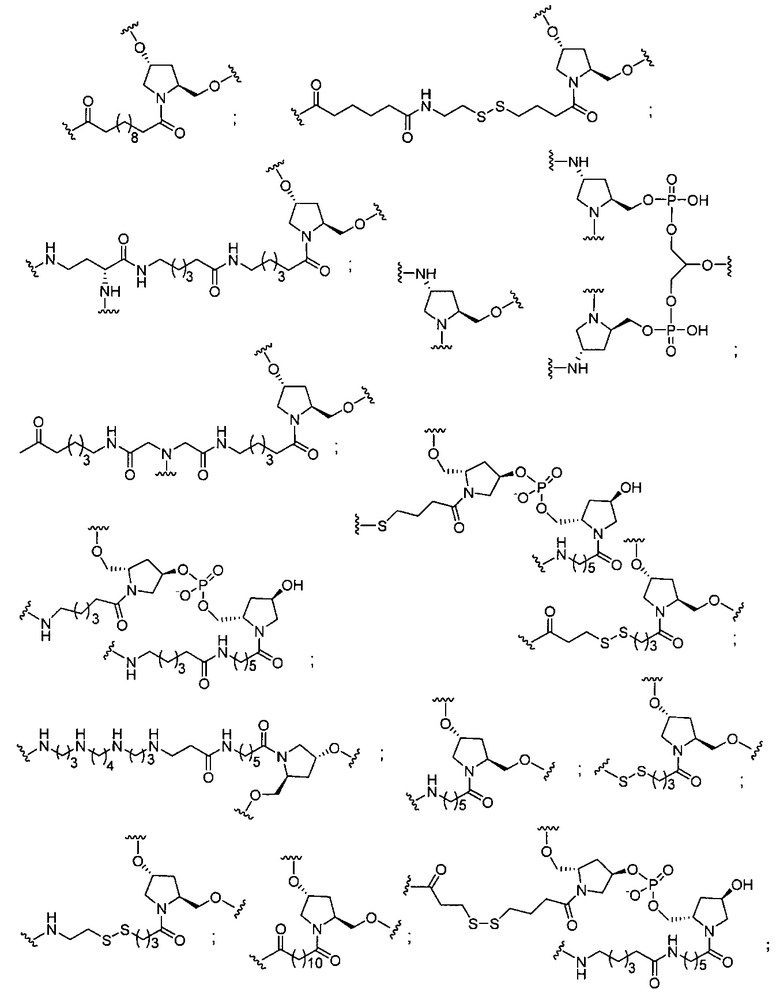
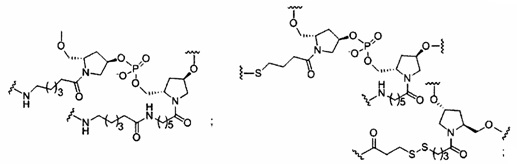 и
и
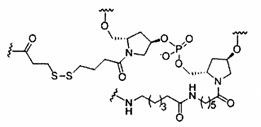 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
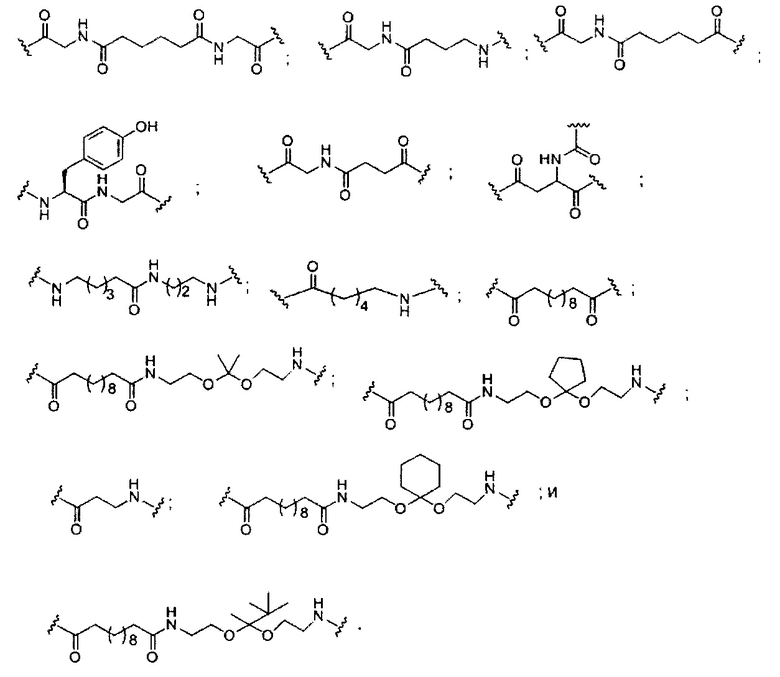
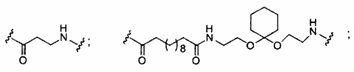 и
и
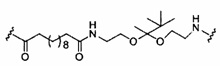 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
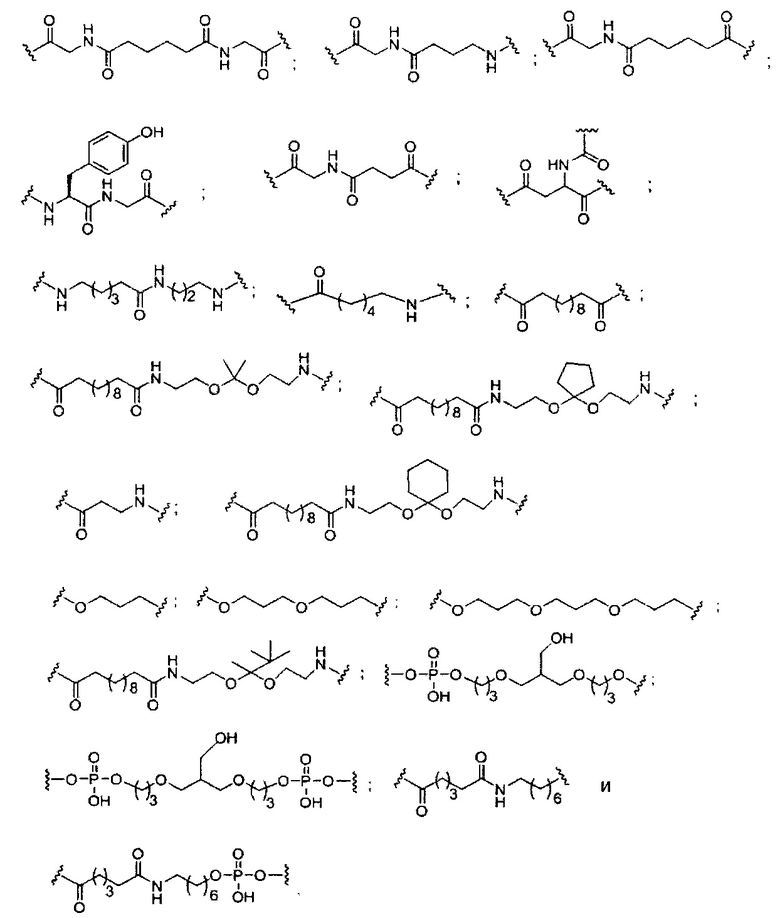
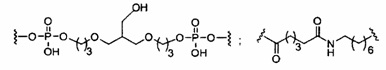 и
и
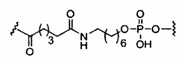 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
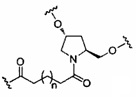 и
и 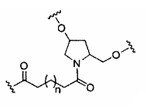
где n равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
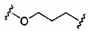 ;
;  ; и
; и  .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
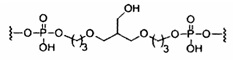 и
и 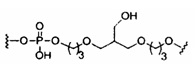 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
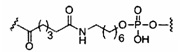 и
и 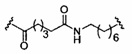 .
.
В некоторых вариантах реализации линкер конъюгата имеет структуру:
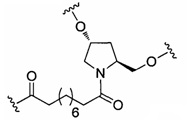 .
.
В некоторых вариантах реализации линкер конъюгата имеет структуру:
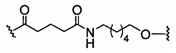 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
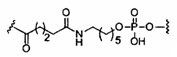 и
и 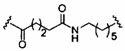 .
.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
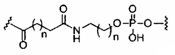 и
и 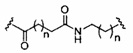 ;
;
где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
iii. Некоторые фрагменты, направляющие на клетку
В некоторых вариантах реализации группы конъюгата содержат фрагменты, направляющие на клетку. Некоторые такие фрагменты,- направляющие на клетку, увеличивают клеточный захват антисмысловых соединений. В некоторых вариантах реализации фрагменты, направляющие на клетку, содержат группу ветвления, одну или более связок и один или более лигандов. В некоторых вариантах реализации фрагменты, направляющие на клетку, содержат группу ветвления, одну или более связок, один или более лигандов и одну или более расщепляемых связей.
1. Некоторые группы ветвления
В некоторых вариантах реализации группы конъюгата содержат нацеливающий фрагмент, содержащий группу ветвления и по меньшей мере два связанных лиганда. В некоторых вариантах реализации группа ветвления присоединяет линкер конъюгата. В некоторых вариантах реализации группа ветвления присоединяет расщепляемый фрагмент. В некоторых вариантах реализации группа ветвления присоединяет антисмысловый олигонуклеотид. В некоторых вариантах реализации группа ветвления ковалентно присоединена к линкеру и каждому из связанных лигандов. В некоторых вариантах реализации группа ветвления содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, простых эфирных, тиоэфирных и гидроксиламино-групп. В некоторых вариантах реализации группа ветвления содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации группа ветвления содержит группы, выбранные из алкильных и простых эфирных групп. В некоторых вариантах реализации группа ветвления содержит моно- или полициклическую кольцевую систему. В некоторых вариантах реализации группа ветвления содержит одну или более расщепляемых связей. В некоторых вариантах реализации группа конъюгата не содержит группу ветвления.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
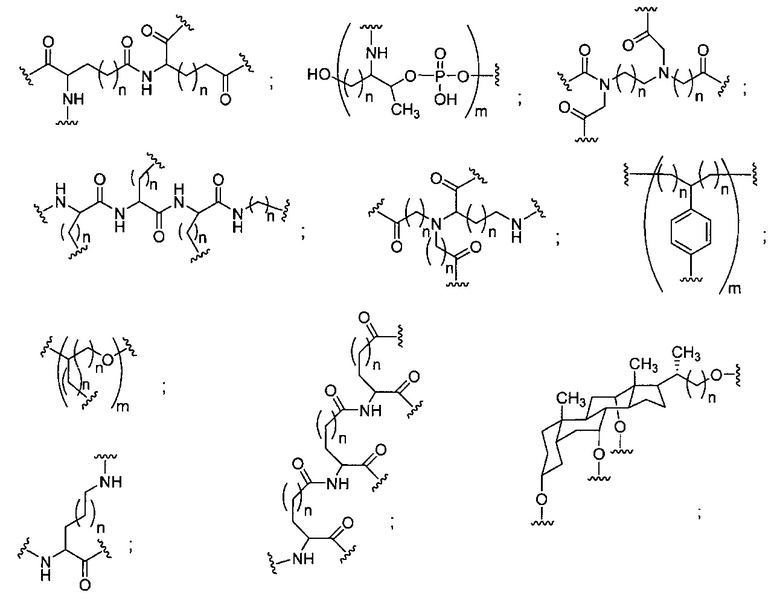
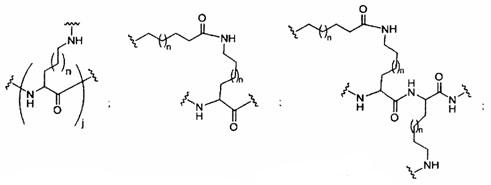
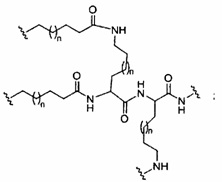 и
и 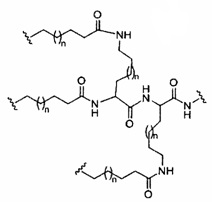 .
.
где каждый n независимо равен от 1 до 20;
j равен от 1 до 3; и
m равен от 2 до 6.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
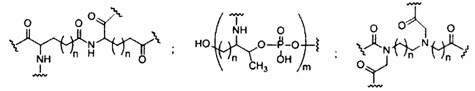
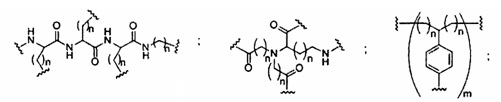
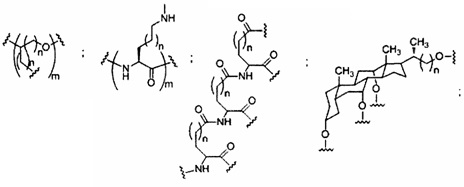 и
и
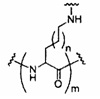
где каждый n независимо равен от 1 до 20; и
m равен от 2 до 6.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
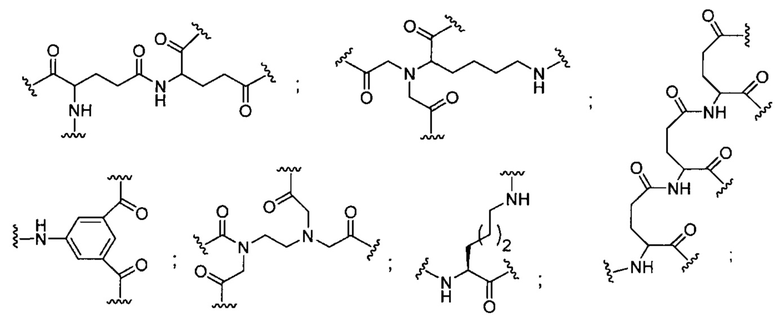
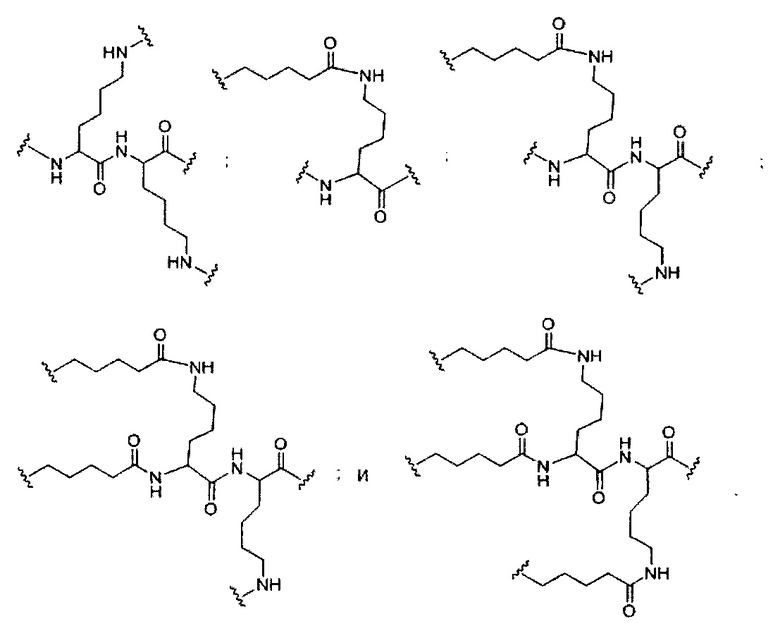
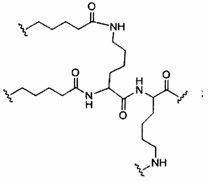 и
и 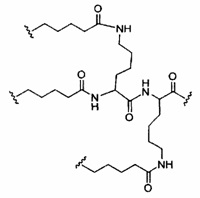 .
.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
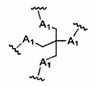 и
и 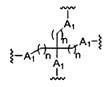
где каждый A1 независимо представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
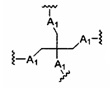 ;
; 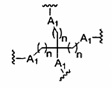 и
и 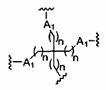
где каждый A1 независимо представляет собой О, S, С=O или NH; и каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
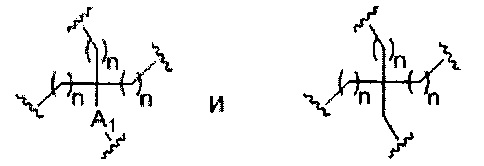
где A1 представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
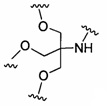 .
.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
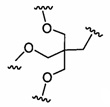 .
.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
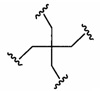 .
.
2. Некоторые связки
В некоторых вариантах реализации группы конъюгата содержат одну или более связок, ковалентно присоединенных к группе ветвления. В некоторых вариантах реализации группы конъюгата содержат одну или более связок, ковалентно присоединенных к линкерной группе. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, простых эфирных, тиоэфирных, дисульфидных, амидных и полиэтиленгликолевых групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, замещенных алкильных, простых эфирных, тиоэфирных, дисульфидных, амидных, фосфодиэфирных и полиэтиленгликолевых групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, простых эфирных и амидных групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, замещенных алкильных, фосфодиэфирных, простых эфирных и амидных групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкила и фосфодиэфира в любой комбинации. В некоторых вариантах реализации каждая связка содержит по меньшей мере одну фосфорную линкерную группу или нейтральную линкерную группу.
В некоторых вариантах реализации связка содержит одну или более расщепляемых связей. В некоторых вариантах реализации связка присоединена к группе ветвления либо через амидную, либо через простую эфирную группу. В некоторых вариантах реализации связка присоединена к группе ветвления через фосфордиэфирную группу. В некоторых вариантах реализации связка присоединена к группе ветвления через фосфорную линкерную группу или через нейтральную линкерную группу. В некоторых вариантах реализации связка присоединена к группе ветвления через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду либо через амидную, либо через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду либо через амидную, либо через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду через простую эфирную группу.
В некоторых вариантах реализации каждая связка имеет длину от около 8 до около 20 атомов в цепи между лигандом и группой ветвления. В некоторых вариантах реализации каждая связка имеет длину от около 10 до около 18 атомов в цепи между лигандом и группой ветвления. В некоторых вариантах реализации каждая связка имеет длину около 13 атомов в цепи.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
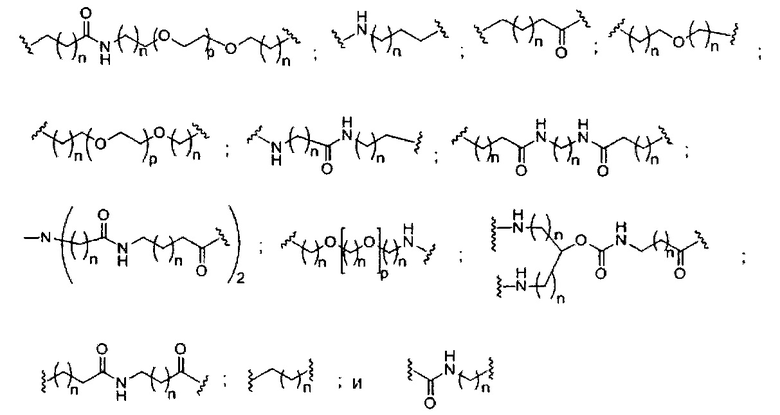
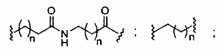 и
и 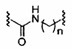
где каждый n независимо равен от 1 до 20; и
каждый р равен от 1 до около 6.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
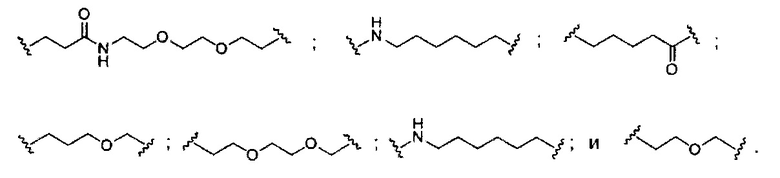
 и
и 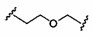 .
.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
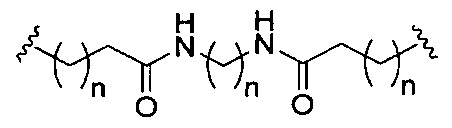
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
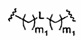 и
и 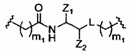
где L представляет собой либо фосфорную линкерную группу, либо нейтральную линкерную группу;
Z1 представляет собой C(=O)O-R2;
Z2 представляет собой Н, C1-C6 алкил или замещенный C1-C6 алкил;
R2 представляет собой Н, C1-C6 алкил или замещенный C1-C6 алкил; и
каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
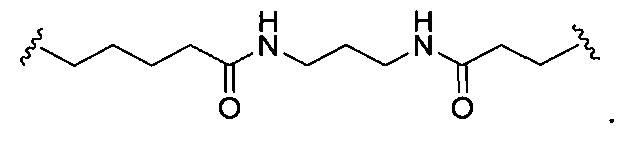
В некоторых вариантах реализации связка имеет структуру, выбранную из:
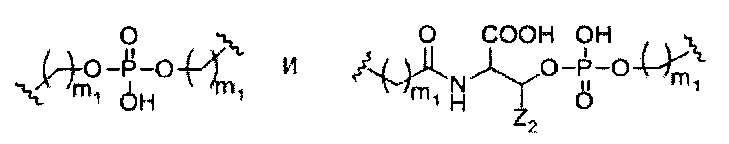 и
и 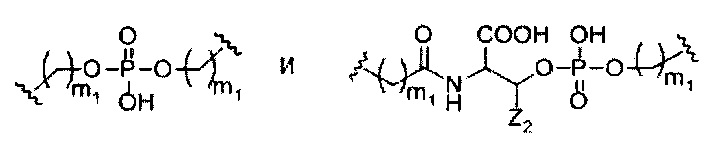
где Z2 представляет собой Н или CH3; и
каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации связка имеет структуру, выбранную из: 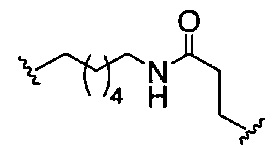 или
или 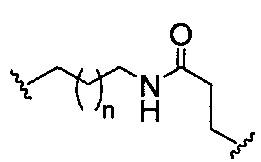 ; где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
; где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
В некоторых вариантах реализации связка содержит фосфорную линкерную группу. В некоторых вариантах реализации связка не содержит ни одной амидной связи. В некоторых вариантах реализации связка содержит фосфорную линкерную группу и не содержит ни одной амидной связи.
3. Некоторые лиганды
В некоторых вариантах реализации настоящего описания представлены лиганды, при этом каждый лиганд ковалентно присоединен к связке. В некоторых вариантах реализации каждый лиганд выбран так, чтобы он обладал аффинностью по меньшей мере к одному типу рецептора на клетке-мишени. В некоторых вариантах реализации лиганды выбраны так, чтобы они обладали аффинностью по меньшей мере к одному типу рецептора на поверхности клетки печени млекопитающего. В некоторых вариантах реализации лиганды выбраны так, чтобы они обладали аффинностью к печеночному асиалогликопротеиновому рецептору (ASGP-R). В некоторых вариантах реализации каждый лиганд представляет собой углевод. В некоторых вариантах реализации каждый лиганд независимо выбран из галактозы, N-ацетилгалактозамина, маннозы, глюкозы, глюкозамина и фукозы. В некоторых вариантах реализации каждый лиганд представляет собой N-ацетилгалактозамин (GalNAc). В некоторых вариантах реализации нацеливающий фрагмент содержит 2-6 лигандов. В некоторых вариантах реализации нацеливающий фрагмент содержит 3 лиганда. В некоторых вариантах реализации нацеливающий фрагмент содержит 3 N-ацетилгалактозаминовых лиганда.
В некоторых вариантах реализации лиганд представляет собой углевод, углеводное производное, модифицированный углевод, поливалентный углеводный кластер, полисахарид, модифицированный полисахарид или полисахаридное производное. В некоторых вариантах реализации лиганд представляет собой аминосахар или тиосахар. Например, аминосахара могут быть выбраны из любого количества соединений, известных в данной области техники, например, глюкозамина, сиаловой кислоты, α-D-галактозамина, N-ацетилгалактозамина, 2-ацетамидо-2-дезокси-D-галактопиранозы (GalNAc), 2-амино-3-O-[(R)-1-карбоксиэтил]-2-дезокси-β-D-глюкопиранозы (β-мурамовой кислоты), 2-дезокси-2-метиламино-L-глюкопиранозы, 4,6-дидезокси-4-формамидо-2,3-ди-О-метил-D-маннопиранозы, 2-дезокси-2-сульфоамино-D-глюкопиранозы и N-сульфо-D-глюкозамина, и N-гликолоил-α-нейраминовой кислоты. Например, тиосахара могут быть выбраны из группы, состоящей из 5-тио-β-D-глюкопиранозы, метил-2,3,4-три-O-ацетил-1-тио-6-О-тритил-α-D-глюкопиранозида, 4-тио-β-D-галактопиранозы и этил-3,4,6,7-тетра-O-ацетил-2-дезокси-1,5-дитио-α-D-gluco-гептопиранозида.
В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе, обычно упоминаемой в литературе как N-ацетилгалактозамин. В некоторых вариантах реализации «N-ацетилгалактозамин» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе. В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе. В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе, которая включает и β-форму: 2-(ацетиламино)-2-дезокси-β-D-галактопиранозу, и α-форму: 2-(ацетиламино)-2-дезокси-D-галактопиранозу. В некоторых вариантах реализации обе формы, β-форма: 2-(ацетиламино)-2-дезокси-β-D-галактопираноза, и α-форма: 2-(ацетиламино)-2-дезокси-D-галактопираноза, могут быть использованы взаимозаменяемо. Соответственно, в структурах, в которых изображена одна форма, подразумевается, что эти структуры включают также и другую форму. Например, если показана структура для α-формы: 2-(ацетиламино)-2-дезокси-D-галактопиранозы, то подразумевается, что эта структура включает также и другую форму. В некоторых предпочтительных вариантах реализации β-форма 2-(ацетиламино)-2-дезокси-D-галактопиранозы является предпочтительным вариантом реализации.
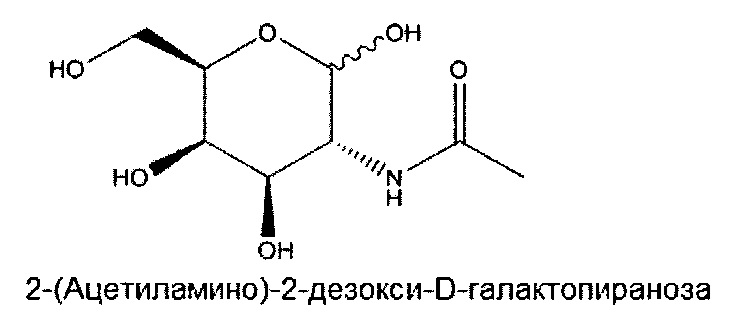
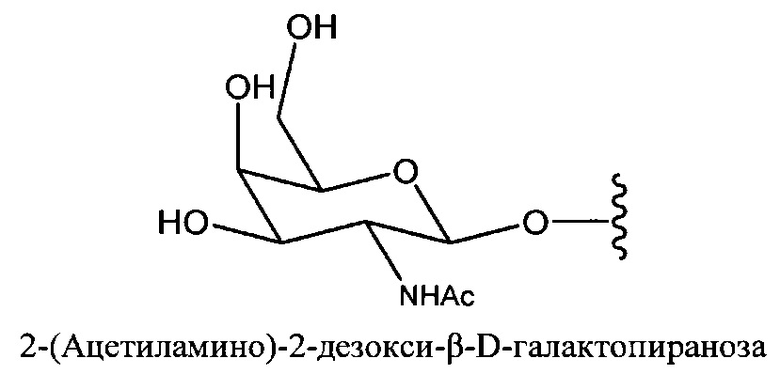
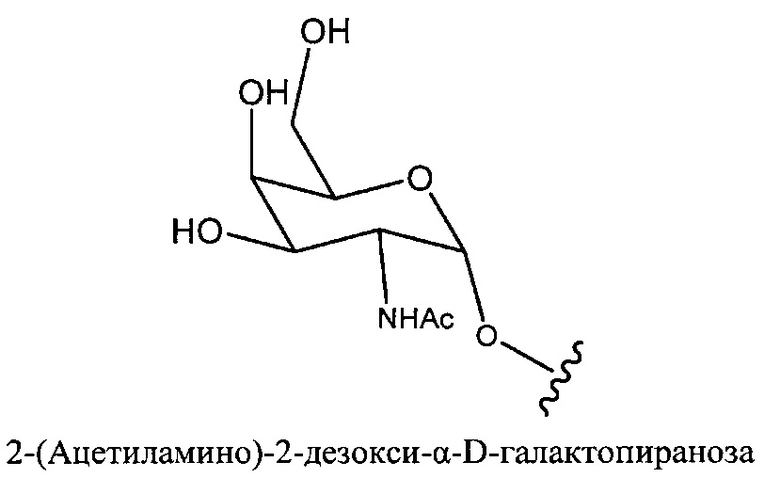
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
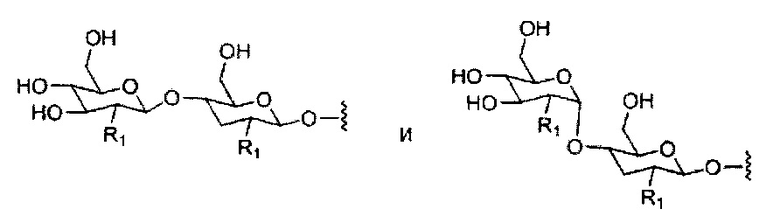 и
и 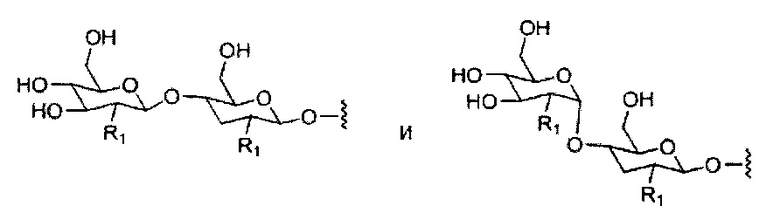
где каждый R1 выбран из ОН и NHCOOH.
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
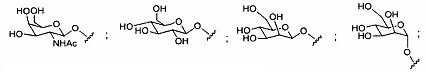
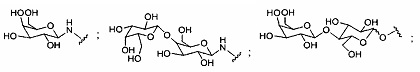 и
и
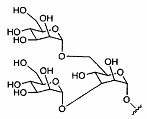 .
.
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
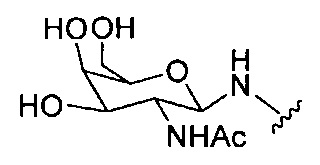 .
.
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
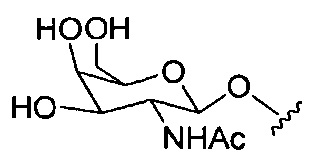 .
.
i. Некоторые конъюгаты
В некоторых вариантах реализации группы конъюгата содержат структурные особенности, представленные выше. В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
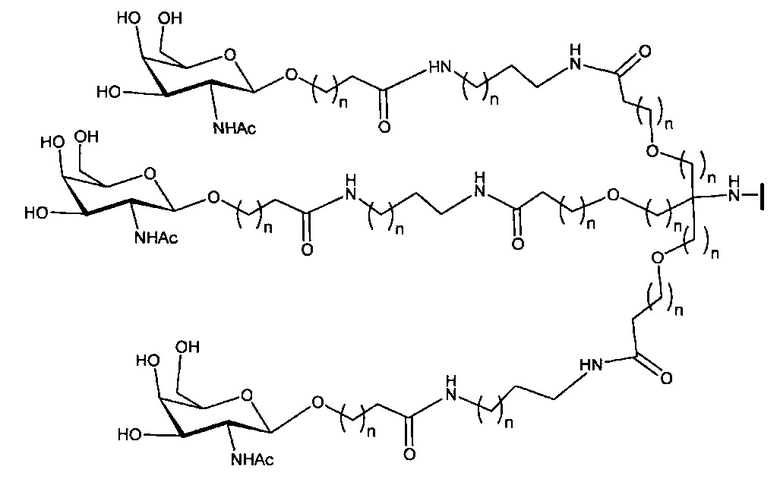 .
.
где каждый n независимо равен от 1 до 20.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
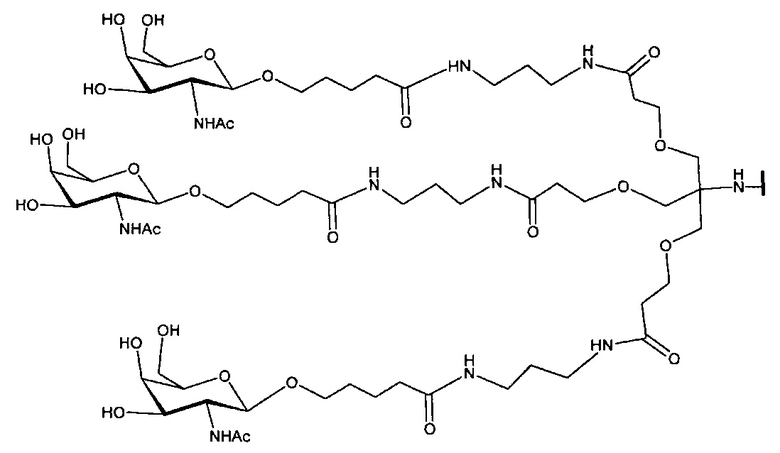 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
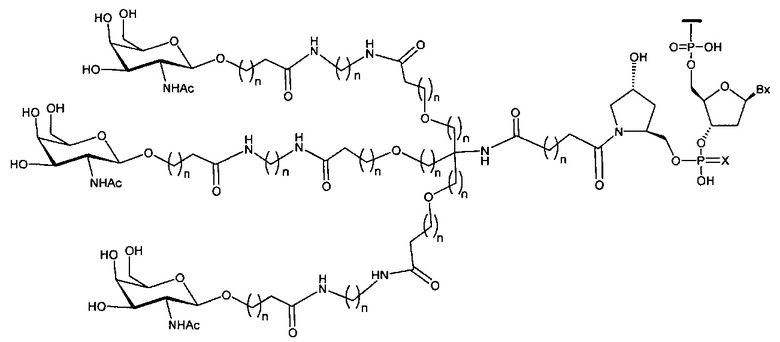
где каждый n независимо равен от 1 до 20;
Z представляет собой Н или связанную твердую подложку;
Q представляет собой антисмысловое соединение;
Х представляет собой О или S; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
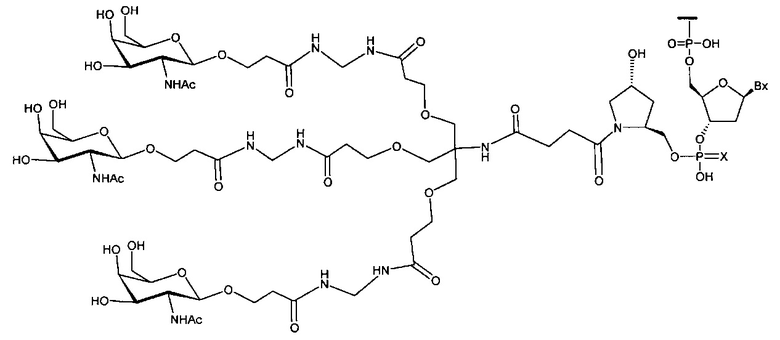
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
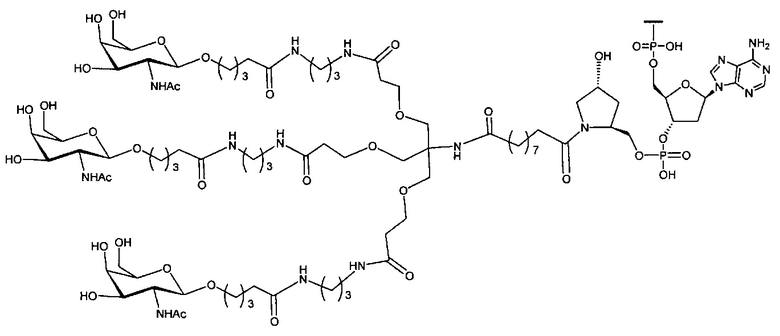
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
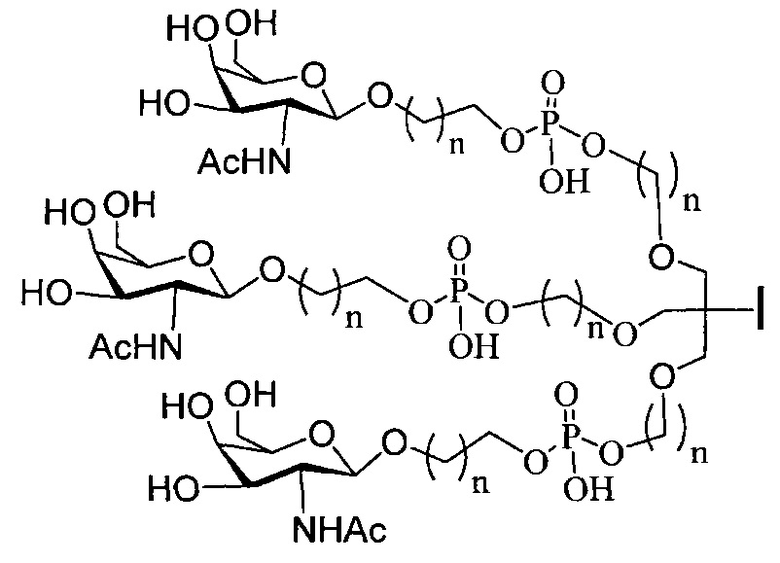 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
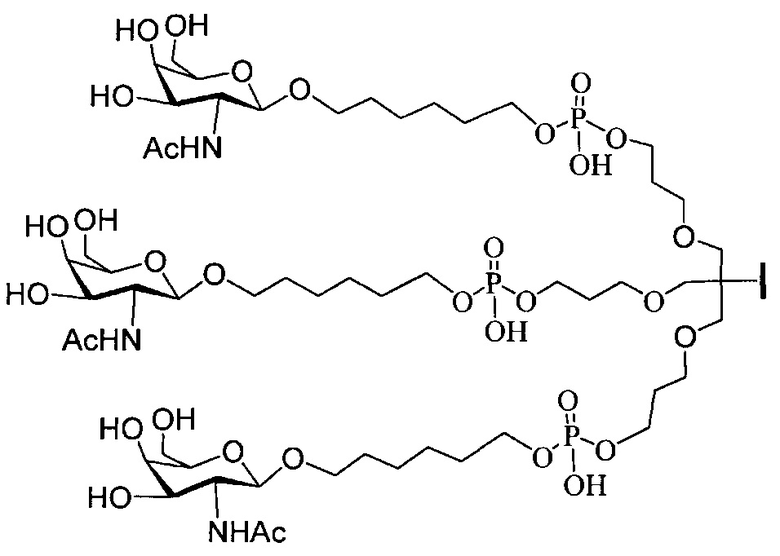 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
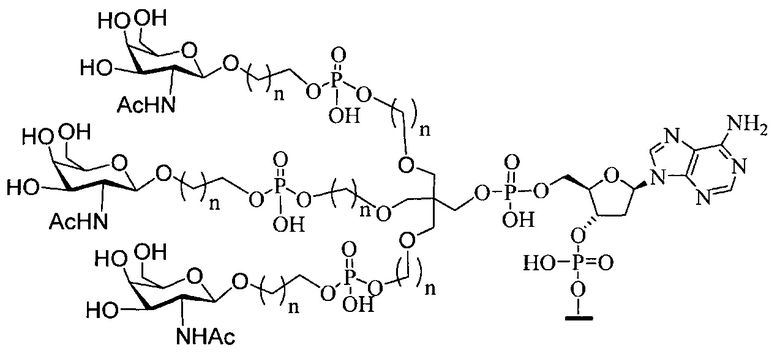 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
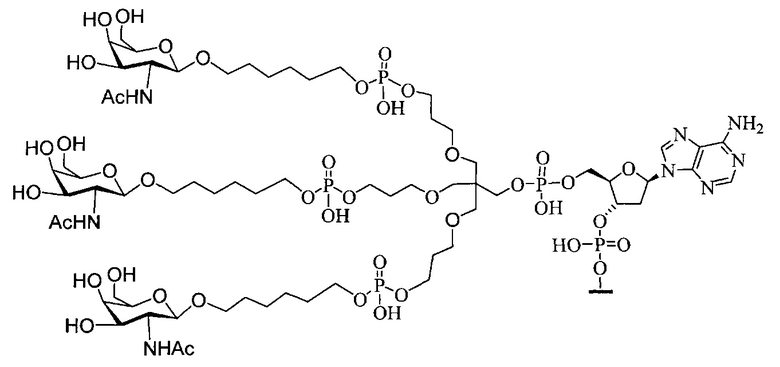
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
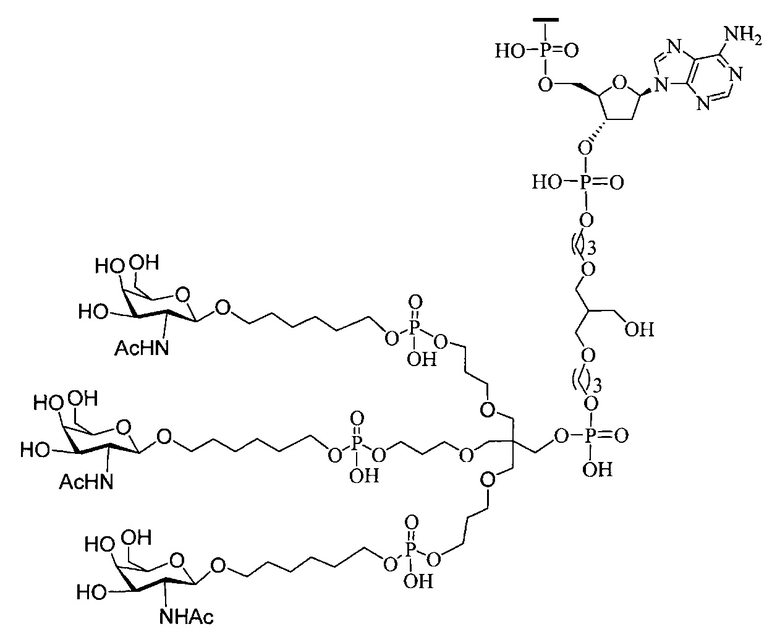 .
.
В некоторых вариантах реализации конъюгаты не содержат пирролидин.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
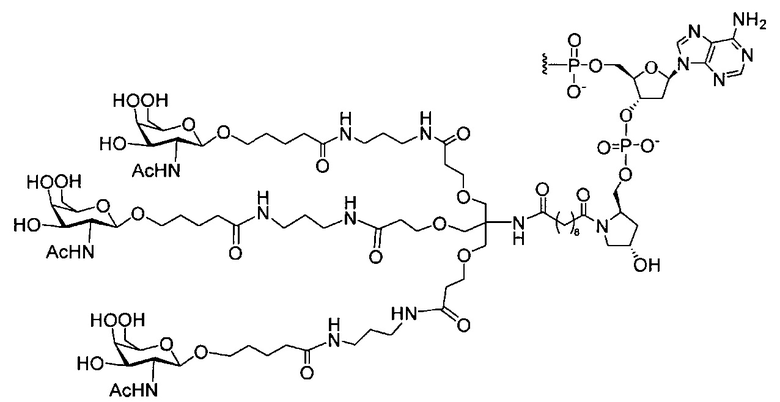 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
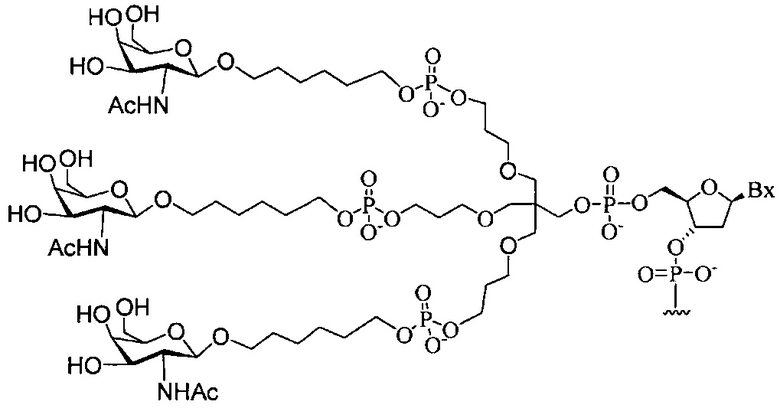 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
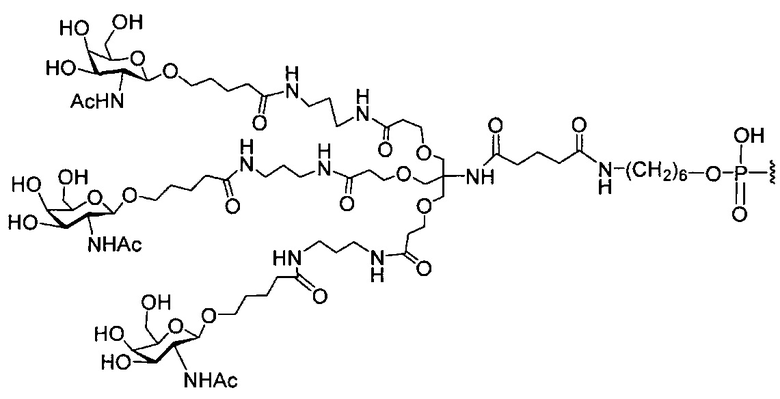 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
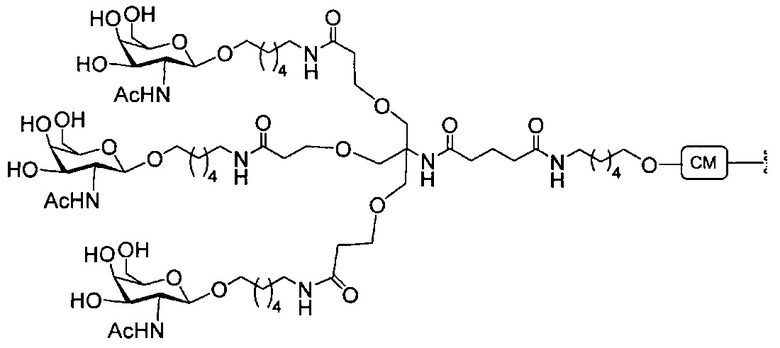 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
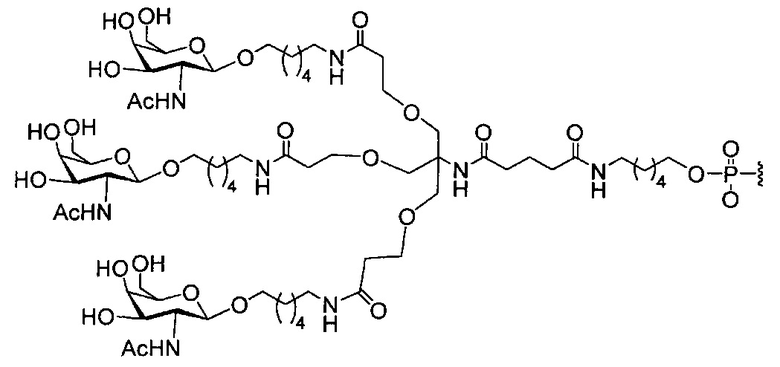 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
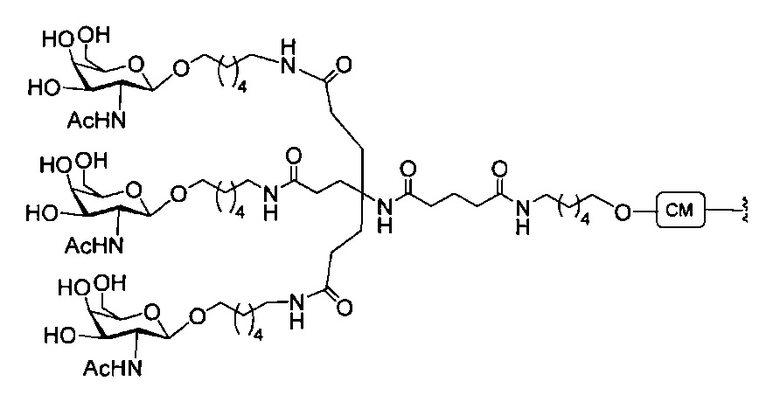 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
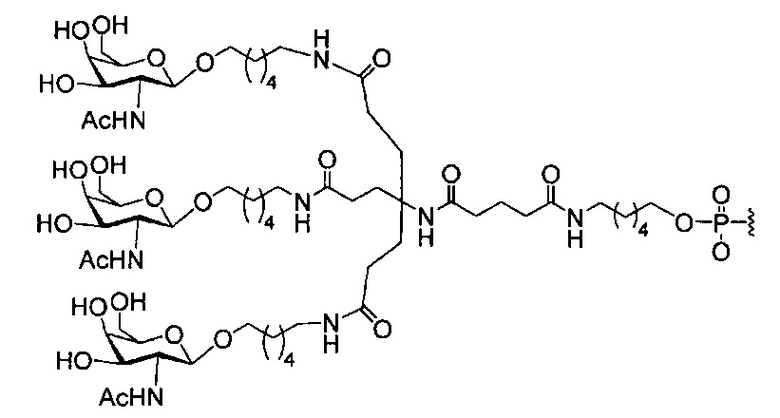 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
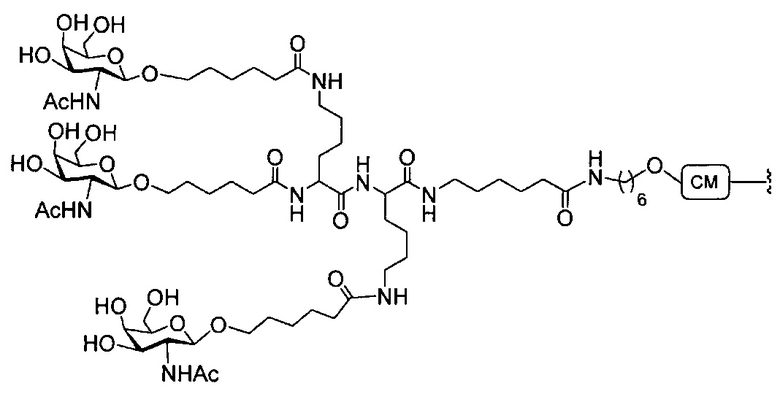 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
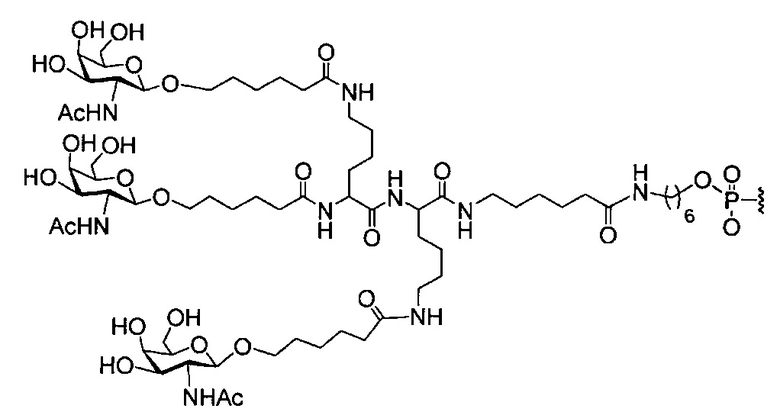 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
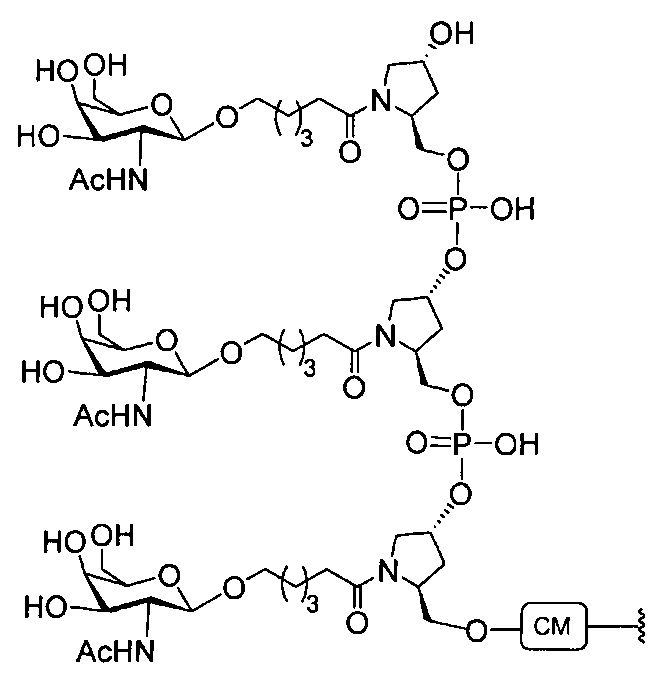 .
.
В некоторых таких вариантах реализации группы конъюгата имеют следующую структуру:
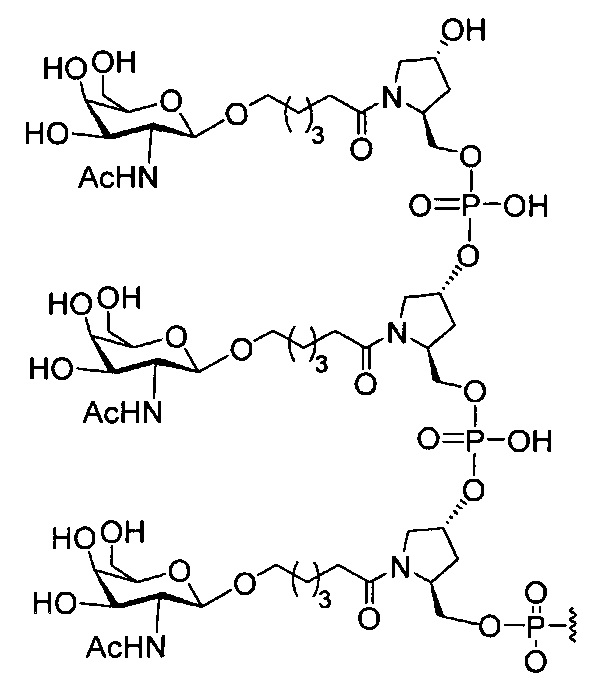 .
.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
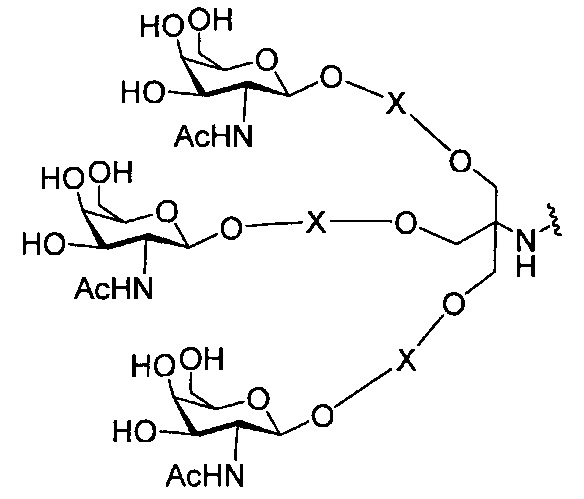
где Х представляет собой замещенную или незамещенную связку из шести-одиннадцати последовательно связанных атомов.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
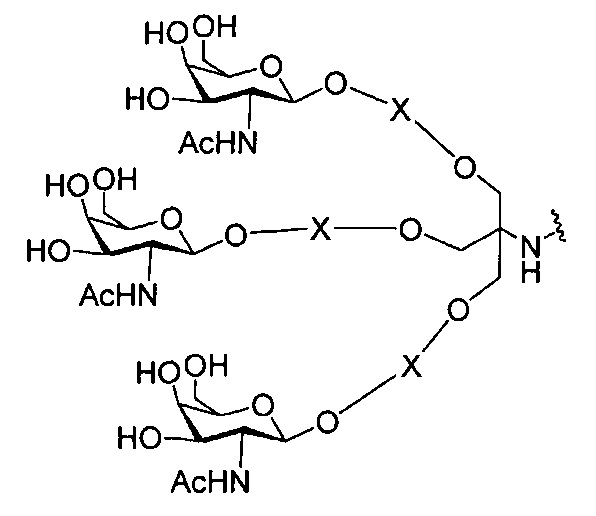
где X представляет собой замещенную или незамещенную связку из десяти последовательно связанных атомов.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
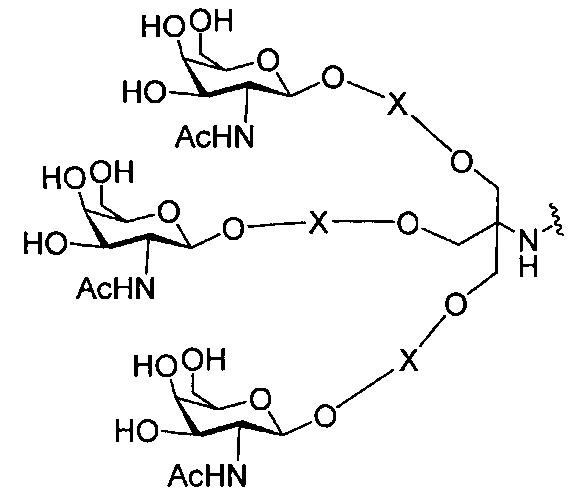
где Х представляет собой замещенную или незамещенную связку из четырех-одиннадцати последовательно связанных атомов, и при этом указанная связка содержит только одну амидную связь.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
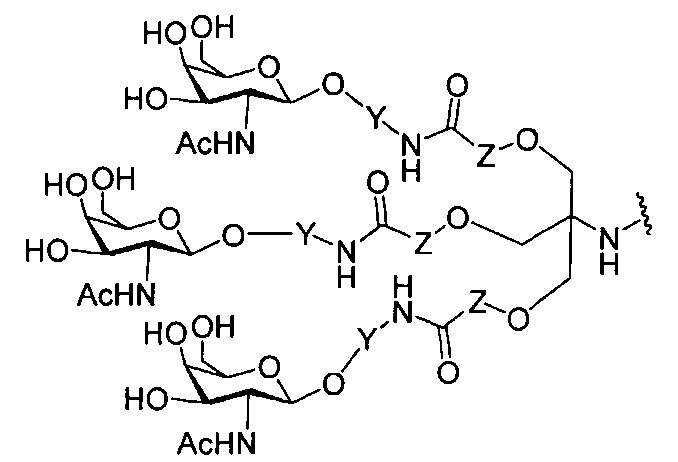
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной, алкенильной или алкинильной группы или группы, содержащей эфир, кетон, амид, сложный эфир, карбамат, амин, пиперидин, фосфат, фосфодиэфир, тиофосфат, триазол, пирролидин, дисульфид или тиоэфир.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
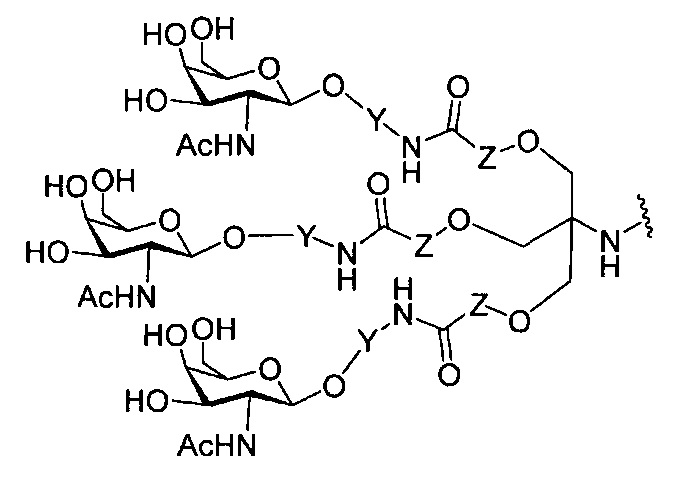
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной группы или группы, содержащей только один эфир или только два эфира, амид, амин, пиперидин, фосфат, фосфодиэфир или тиофосфат.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
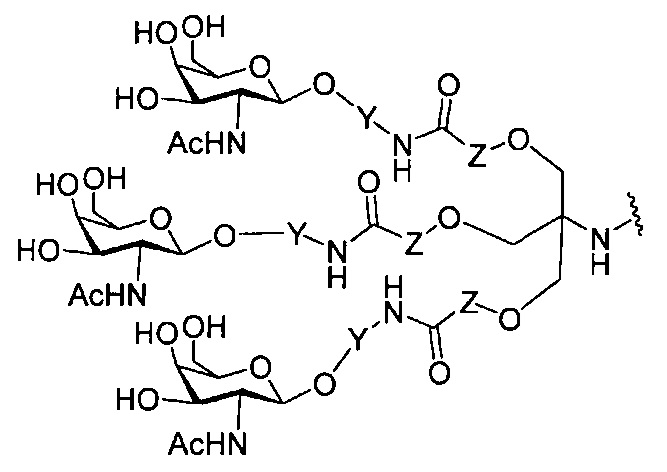
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной группы.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
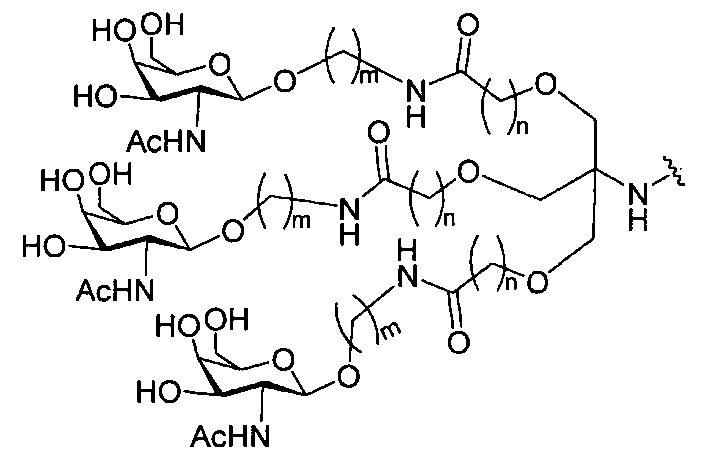
где m и n независимо выбраны из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
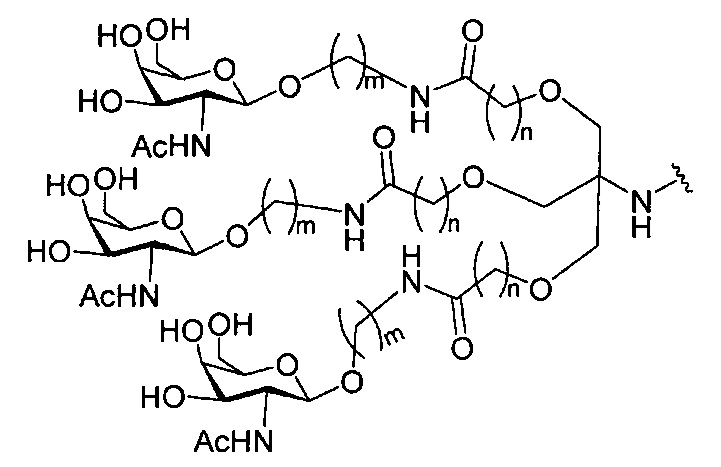
где m равен 4, 5, 6, 7 или 8, и n равен 1, 2, 3 или 4.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
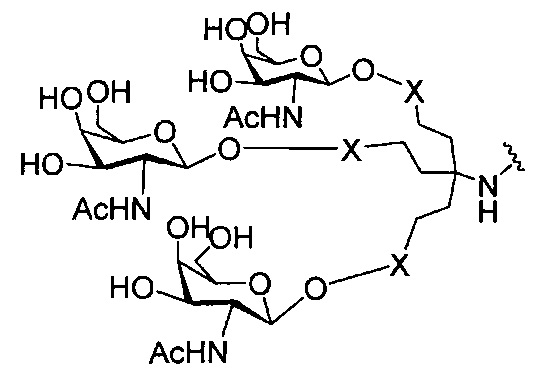
где Х представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом Х не содержит эфирную группу.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
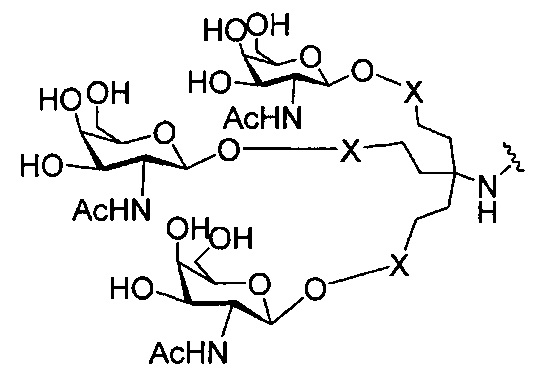
где Х представляет собой замещенную или незамещенную связку из восьми последовательно связанных атомов, и при этом Х не содержит эфирную группу.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
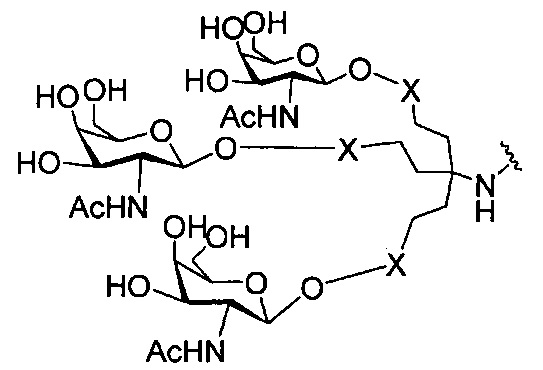
где Х представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом указанная связка содержит только одну амидную связь, а Х не содержит эфирную группу.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
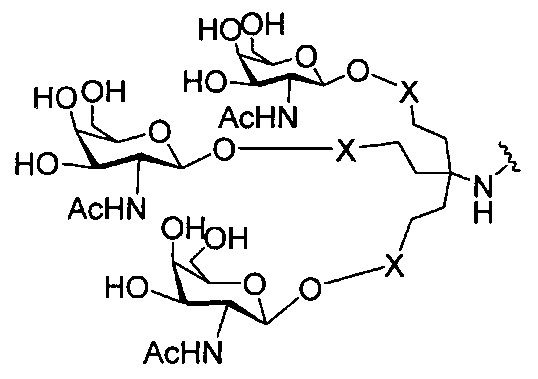
где Х представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом указанная связка состоит из амидной связи и замещенной или незамещенной С2-С11 алкильной группы.
В некоторых вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
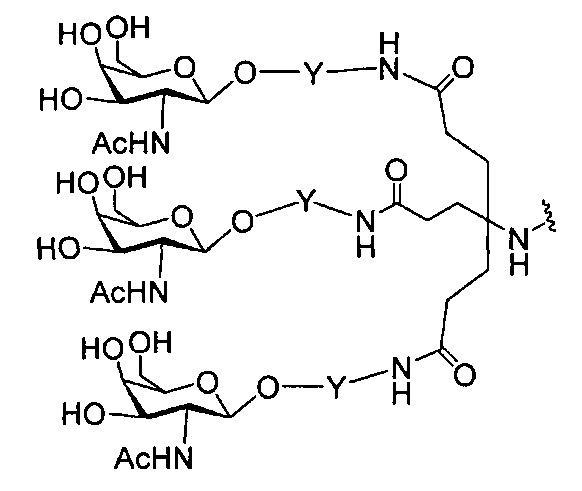
где Y выбран из C1-C12 замещенной или незамещенной алкильной, алкенильной или алкинильной группы или группы, содержащей эфир, кетон, амид, сложный эфир, карбамат, амин, пиперидин, фосфат, фосфодиэфир, тиофосфат, триазол, пирролидин, дисульфид или тиоэфир.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
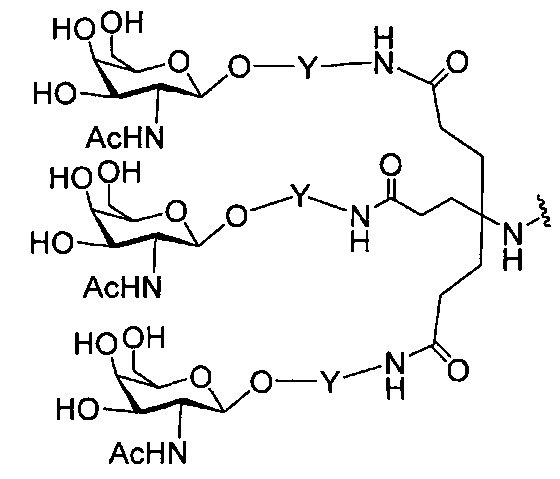
где Y выбран из C1-C12 замещенной или незамещенной алкильной группы или группы, содержащей эфир, амин, пиперидин, фосфат, фосфодиэфир или тиофосфат.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
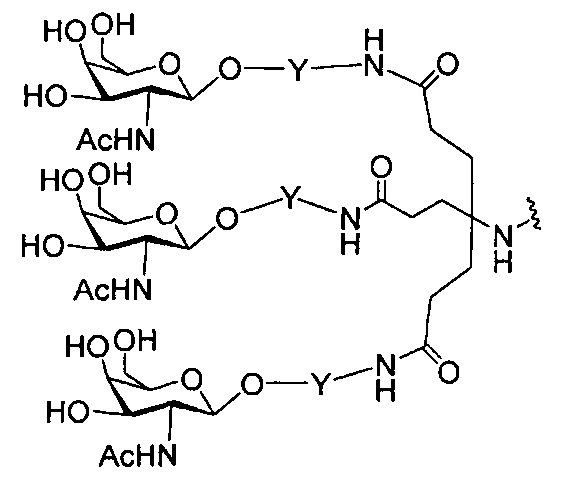
где Y выбран из C1-C12 замещенной или незамещенной алкильной группы.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
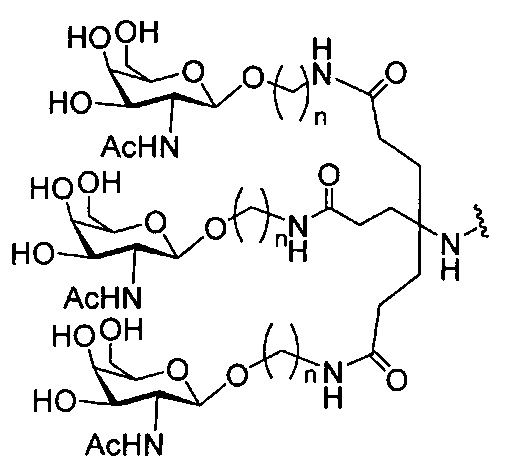
где n равен 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12.
В некоторых таких вариантах реализации фрагмент группы конъюгата, нацеливающий на клетку, имеет следующую структуру:
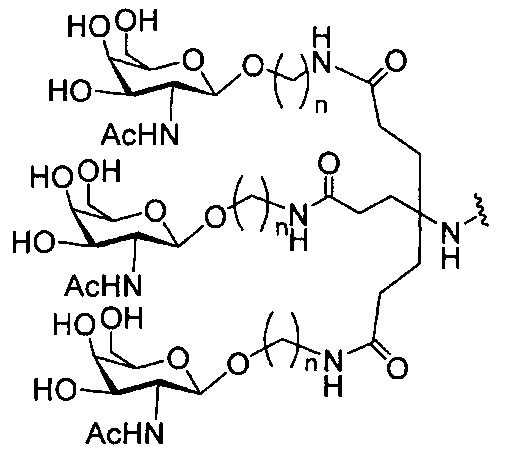
где n равен 4, 5, 6, 7 или 8.
В некоторых вариантах реализации конъюгаты не содержат нирролидин.
Некоторые сопряженные антисмысловые соединения
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида. В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
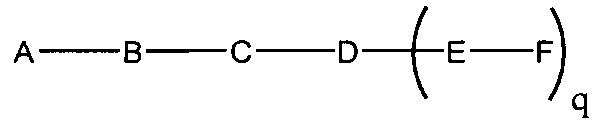
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
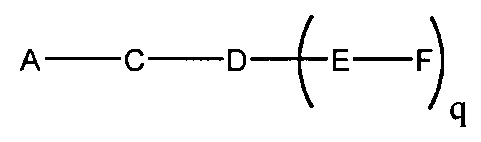
где
А представляет собой антисмысловый олигонуклеотид;
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых таких вариантах реализации линкер конъюгата содержит по меньшей мере одну расщепляемую связь.
В некоторых таких вариантах реализации группа ветвления содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации каждая связка содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
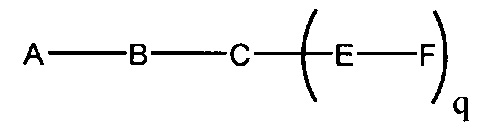
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида. В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
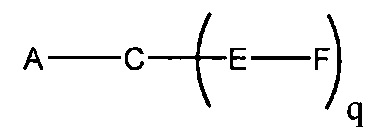
где
А представляет собой антисмысловый олигонуклеотид;
С представляет собой линкер конъюгата
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
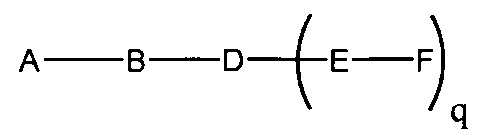
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет следующую структуру:
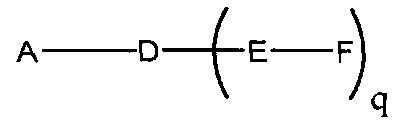
где
А представляет собой антисмысловый олигонуклеотид;
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых таких вариантах реализации линкер конъюгата содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации каждая связка содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет структуру, выбранную из следующих:
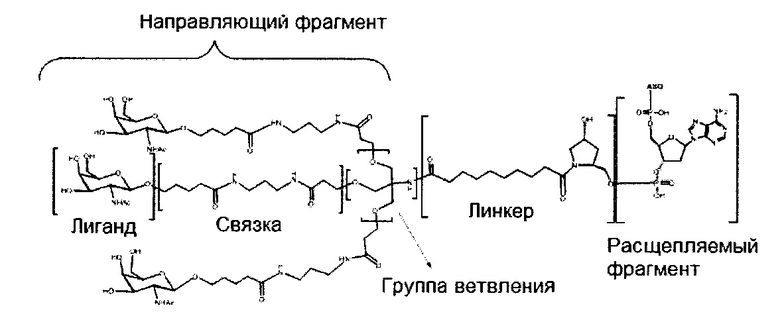 .
.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет структуру, выбранную из следующих:
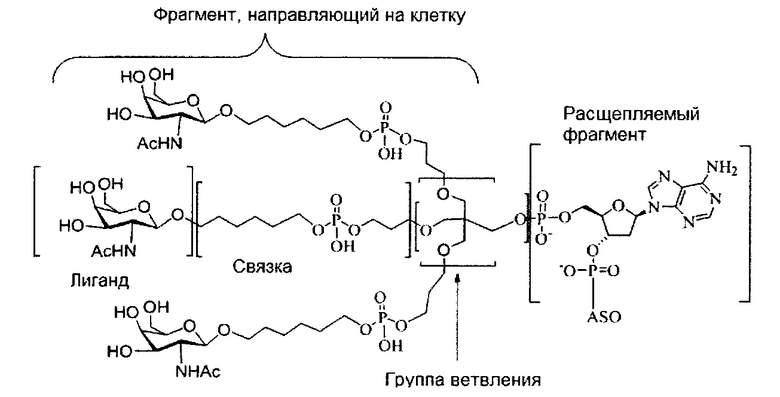 .
.
В некоторых вариантах реализации сопряженное антисмысловое соединение имеет структуру, выбранную из следующих:
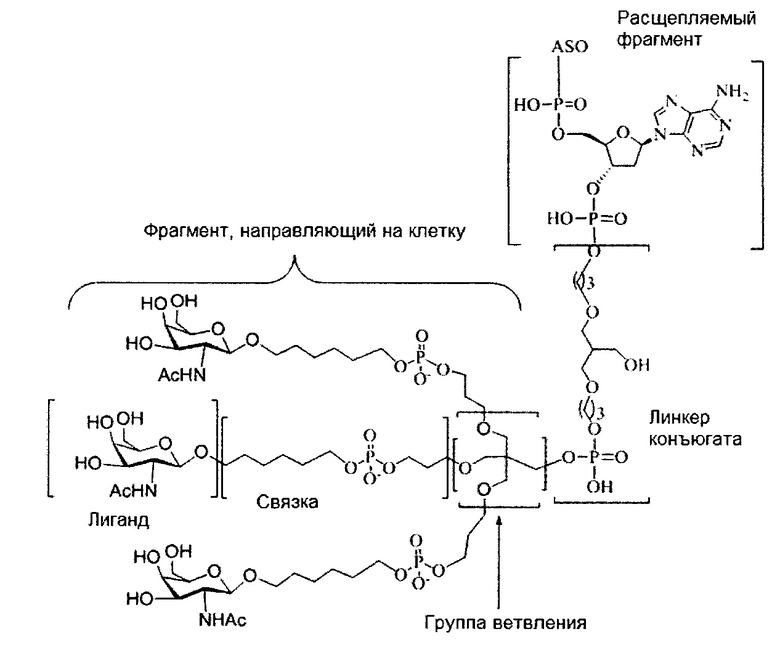 .
.
Иллюстративные патенты Соединенных штатов Америки, публикации патентных заявок Соединенных штатов Америки и публикации международных патентных заявок, в которых описано получение некоторых из указанных выше конъюгатов, сопряженных антисмысловых соединений, связок, линкеров, групп ветвления, лигандов, расщепляемых фрагментов, а также других модификаций, включают, без ограничения, US 5994517, US 6300319, US 6660720, US 6906182, US 7262177, US 7491805, US 8106022, US 7723509, US 2006/0148740, US 2011/0123520, WO 2013/033230 и WO 2012/037254, каждая из которых включена в настоящий документ посредством ссылки в полном объеме.
Иллюстративные публикации, в которых описано получение некоторых из указанных выше конъюгатов, сопряженных антисмысловых соединений, связок, линкеров, групп ветвления, лигандов, расщепляемых фрагментов, а также других модификаций, включают, без ограничения, BIESSEN et al., «The Cholesterol Derivative of a Triantennary Galactoside with High Affinity for the Hepatic Asialoglycoprotein Receptor: a Potent Cholesterol Lowering Agent» J. Med. Chem. (1995) 38: 1846-1852, BIESSEN et al., «Synthesis of Cluster Galactosides with High Affinity for the Hepatic Asialoglycoprotein Receptor» J. Med. Chem. (1995) 38: 1538-1546, LEE et al., «New and more efficient multivalent glyco-ligands for asialoglycoprotein receptor of mammalian hepatocytes» Bioorganic & Medicinal Chemistry (2011) 19: 2494-2500, RENSEN et al., «Determination of the Upper Size Limit for Uptake and Processing of Ligands by the Asialoglycoprotein Receptor on Hepatocytes in Vitro and in Vivo» J. Biol. Chem. (2001) 276(40): 37577-37584, RENSEN et al., «Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asialoglycoprotein Receptor» J. Med. Chem. (2004) 47: 5798-5808, SLIEDREGT et al., «Design and Synthesis of Novel Amphiphilic Dendritic Galactosides for Selective Targeting of Liposomes to the Hepatic Asialoglycoprotein Receptor» J. Med. Chem. (1999) 42: 609-618, и Valentijn et al., «Solid-phase synthesis of lysine-based cluster galactosides with high affinity for the Asialoglycoprotein Receptor» Tetrahedron, 1997, 53 (2), 759-770, каждый из которых включен в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах реализации сопряженные антисмысловые соединения содержат олигонуклеотид на основе РНКазы Н (такой как гэпмер) или сплайс-модулирующий олигонуклеотид (такой как полностью модифицированный олигонуклеотид) и любую группу конъюгата, содержащую по меньшей мере одну, две или три группы GalNAc. В некоторых вариантах реализации сопряженное антисмысловое соединение содержит любую группу конъюгата, описанную в любой из следующих ссылок: Lee, Carbohydr Res, 1978, 67, 509-514; Connolly et al., J Biol Chem, 1982, 257, 939-945; Pavia et al., Int J Pep Protein Res, 1983, 22, 539-548; Lee et al., Biochem, 1984, 23, 4255-4261; Lee et al., Glycoconjugate J, 1987, 4, 317-328; Toyokuni et al., Tetrahedron Lett, 1990, 31, 2673-2676; Biessen et al., J Med Chem, 1995, 38, 1538-1546; Valentijn et al., Tetrahedron, 1997, 53, 759-770; Kim et al., Tetrahedron Lett, 1997, 38, 3487-3490; Lee et al., Bioconjug Chem, 1997, 8, 762-765; Kato et al., Glycobiol, 2001, 11, 821-829; Rensen et al, J Biol Chem, 2001, 276, 37577-37584; Lee et al., Methods Enzymol, 2003, 362, 38-43; Westerlind et al., Glycoconj J, 2004, 21, 227-241; Lee et al., Bioorg Med Chem Lett, 2006, 16(19), 5132-5135; Maierhofer et al., Bioorg Med Chem, 2007, 15, 7661-7676; Khorev et al., Bioorg Med Chem, 2008, 16, 5216-5231; Lee et al., Bioorg Med Chem, 2011, 19, 2494-2500; Komilova et al., Analyt Biochem, 2012, 425, 43-46; Pujol et al., Angew Chemie Int Ed Engl, 2012, 51, 7445-7448; Biessen et al., J Med Chem, 1995, 38, 1846-1852; Sliedregt et al., J Med Chem, 1999, 42, 609-618; Rensen et al., J Med Chem, 2004, 47, 5798-5808; Rensen et al., Arterioscler Thromb Vasc Biol, 2006, 26, 169-175; van Rossenberg et al., Gene Ther, 2004, 11, 457-464; Sato et al., J Am Chem Soc, 2004, 126, 14013-14022; Lee et al., J Org Chem, 2012, 77, 7564-7571; Biessen et al., FASEB J, 2000, 14, 1784-1792; Rajur et al., Bioconjug Chem, 1997, 8, 935-940; Duff et al., Methods Enzymol, 2000, 313, 297-321; Maier et al., Bioconjug Chem, 2003, 14, 18-29; Jayaprakash et al., Org Lett, 2010, 12, 5410-5413; Manoharan, Antisense Nucleic Acid Drug Dev, 2002, 12, 103-128; Merwin et al., Bioconjug Chem, 1994, 5, 612-620; Tomiya et al., Bioorg Med Chem, 2013, 21, 5275-5281; в международных заявках WO 1998/013381; WO 2011/038356; WO 1997/046098; WO 2008/098788; WO 2004/101619; WO 2012/037254; WO 2011/120053; WO 2011/100131; WO 2011/163121; WO 2012/177947; WO 2013/033230; WO 2013/075035; WO 2012/083185; WO 2012/083046; WO 2009/082607; WO 2009/134487; WO 2010/144740; WO 2010/148013; WO 1997/020563; WO 2010/088537; WO 2002/043771; WO 2010/129709; WO 2012/068187; WO 2009/126933; WO 2004/024757; WO 2010/054406; WO 2012/089352; WO 2012/089602; WO 2013/166121; WO 2013/165816; в патентах США 4751219; 8552163; 6908903; 7262177; 5994517; 6300319; 8106022; 7491805; 7491805; 7582744; 8137695; 6383812; 6525031; 6660720; 7723509; 8541548; 8344125; 8313772; 8349308; 8450467; 8501930; 8158601; 7262177; 6906182; 6620916; 8435491; 8404862; 7851615; в опубликованных заявках на патент США US 2011/0097264; US 2011/0097265; US 2013/0004427; US 2005/0164235; US 2006/0148740; US 2008/0281044; US 2010/0240730; US 2003/0119724; US 2006/0183886; US 2008/0206869; US 2011/0269814; US 2009/0286973; US 2011/0207799; US 2012/0136042; US 2012/0165393; US 2008/0281041; US 2009/0203135; US 2012/0035115; US 2012/0095075; US 2012/0101148; US 2012/0128760; US 2012/0157509; US 2012/0230938; US 2013/0109817; US 2013/0121954; US 2013/0178512; US 2013/0236968; US 2011/0123520; US 2003/0077829; US 2008/0108801; и US 2009/0203132; полное содержание которых включено в настоящий документ посредством ссылки.
Тестирование антисмысловых олигонуклеотидов in vitro
Описываемые в настоящем документе способы лечения клеток с помощью антисмысловых олигонуклеотидов могут быть изменены соответствующим образом для лечения другими антисмысловыми соединениями.
Клетки могут быть обработаны антисмысловыми олигонуклеотидами при 60-80% уровне конфлюентности в культуре.
Реагент, используемый для введения антисмысловых олигонуклеотидов в культивируемые клетки, включает катионный липидный трансфекционный реагент Липофектин (Invitrogen, Карлсбад, штат Калифорния). Антисмысловые олигонуклеотиды могут быть смешаны с Липофектином в OPTI-MEM 1 (Invitrogen, Карлсбад, штат Калифорния) для достижения желаемой конечной концентрации антисмысловых олигонуклеотидов и концентрации Липофектина в пределах от 2 до 12 мкг/мл при 100 нМ антисмыслового олигонуклеотида.
Другой реагент, используемый для введения антисмысловых олигонуклеотидов в культивируемые клетки, включает Липофектамин (Invitrogen, Карлсбад, штат Калифорния). Антисмысловой олигонуклеотид смешивают с Липофектамином в среде OPTI-MEM 1 со сниженным содержанием сыворотки (Invitrogen, Карлсбад, штат Калифорния) для достижения желаемой концентрации антисмысловых олигонуклеотидов и концентрации Липофектамина в пределах от 2 до 12 мкг/мл при 100 нМ антисмыслового олигонуклеотида.
Еще одна методика, используемая для введения антисмысловых олигонуклеотидов в культивируемые клетки, включает электропорацию.
Другая методика, используемая для введения антисмысловых олигонуклеотидов в культивируемые клетки, включает свободный захват олигонуклеотидов клетками.
Клетки обрабатывают антисмысловыми олигонуклеотидами с помощью стандартных способов. Клетки могут быть отобраны через 16-24 часов после обработки антисмысловым олигонуклеотидом, после чего уровни РНК или белков нуклеиновых кислот-мишеней измеряют методами, известными в данной области техники и описанными в настоящем документе. Как правило, если обработку проводят в нескольких повторениях, данные представляются как среднее значение для многократных обработок.
Концентрация используемого антисмыслового олигонуклеотида варьируется в зависимости от линии клеток. Способы определения оптимальной концентрации антисмыслового олигонуклеотидна для конкретной линии клеток хорошо известны в данной области техники. Антисмысловые олигонуклеотиды обычно используют в концентрациях от 1 нМ до 300 нМ, при трансфецировании с использованием Липофектамина. Антисмысловые олигонуклеотиды используют в более высоких концентрациях в диапазоне от 625 до 20000 нМ при трансфецировании с использованием электропорации.
Изоляция РНК
Анализ РНК может быть проведен на общей клеточной РНК или поли(А)+ мРНК. Способы изоляции РНК хорошо известны в данной области техники. РНК получают с использованием способов, хорошо известных в данной области техники, например, с использованием реагента Тризол (Invitrogen, Карлсбад, штат Калифорния) по рекомендуемым протоколам производителя.
Некоторые показания
Некоторые варианты реализации, предложенные в настоящем документе, относятся к способам лечения, предупреждения или облегчения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, у субъекта посредством введения специфического ингибитора CFB, такого как антисмысловое соединение, направленное на CFB.
Примеры почечных заболеваний, связанных с дисрегуляцией альтернативного пути комплемента, которые можно лечить, предупреждать и/или облегчать по способам, предложенным в настоящем документе, включают С3 гломерулопатию, атипичный геполитико-уремический синдром (aHUS), болезнь плотного осадка (DDD; также известную как MPGN типа II или C3Neph) и CFHR5 нефропатию.
Дополнительные почечные заболевания, связанные с дисрегуляцией альтернативного пути комплемента, которые можно лечить, предупреждать и/или облегчать по способам, предложенным в настоящем документе, включают IgA нефропатию; мезангиокапиллярный (мембранопролиферативный) гломерулонефрит (MPGN); аутоиммунные расстройства, включая волчаночный нефрит и системную красную волчанку (SLE); инфекционный гломерулонефрит (также известный как постинфекционный гломерулонефрит) и ишемически-реперфузионное повреждение почек, например, ишемически-реперфузионное повреждение почек после пересадки органа.
Примеры внепочечных расстройств, связанных с дисрегуляцией альтернативного пути комплемента, которые можно лечить и/или предупреждать по способам, предложенным в настоящем документе, включают глазные заболевания, такие как дегенерация желтого пятна, например, возрастная дегенерация желтого пятна (AMD), включая влажную AMD и сухую AMD, такую как географическая атрофия; нейромиелит зрительного нерва; болезнь роговицы, такую как воспаление роговицы; аутоиммунные увеиты; и диабетическую ретинопатию. Описано, что система комплемента участвует в глазных заболеваниях. Jha P, et al., Mol Immunol (2007) 44(16): 3901-3908. Дополнительные примеры внепочечных расстройств, связанных с дисрегуляцией альтернативного пути комплемента, которые можно лечить и/или предупреждать по способам, предложенным в настоящем документе, включают ANCA-связанные васкулиты, антифосфолипидный синдром (также известный как синдром антифосфолипидных антител (APS)), астму, ревматоидный артрит, миастению гравис и рассеянный склероз.
Некоторые варианты реализации, предложенные в настоящем документе, относятся к способам лечения, предупреждения или облегчения почечного заболевания, связанного с дисрегуляцией альтернативного пути комплемента, у субъекта посредством введения специфического ингибитора CFB, такого как антисмысловое соединение, направленное на CFB. В некоторых аспектах почечное заболевание представляет собой волчаночный нефрит, системную красную волчанку (SLE), болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипичный гемолитико-уремический синдром), или любую их комбинацию.
Некоторые варианты реализации, предложенные в настоящем документе, относятся к способам лечения, предупреждения или облегчения дегенерации желтого пятна, такой как возрастная дегенерация желтого пятна (AMD), у субъекта посредством введения специфического ингибитора CFB, такого как антисмысловое соединение, направленное на CFB. В некоторых аспектах AMD представляет собой влажную AMD или сухую AMD. В некоторых аспектах сухая AMD может представлять собой географическую атрофию. В исследованиях показана связь дисрегуляции альтернативного пути комплемента с AMD. Компоненты комплемента представляют собой обычные составляющие глазной друзы, внеклеточного материала, который накапливается в желтом пятне пациентов с AMD. Кроме того, было описано, что CFH и CFB варианты составляют около 75% случаев AMD в Северной Европе и Северной Америке. <skj также обнаружено, что специфический полиморфизм CFB обеспечивает защиту от AMD. Patel, N. et al., Eye (2008) 22(6): 768-76. Кроме того, гомозиготные по нулевому CFB мыши обладают более низкой активностью пути комплемента, демонстрируют более слабые глазные повреждения и хориоидальную неоваскуляризацию (CNV) после лазерной фотокоагуляции. Rohrer, В. et al., Invest Ophthalmol Vis Sci. (2009) 50(7): 3056-64. Кроме того, лечение с применением миРНК CFB защищает мышей от CNV, индуцированной лазером. Bora, NS et al., J Immunol. (2006) 177(3): 1872-8. В исследованиях показано также, что почки и глаза имеют общие пути развития и структурные особенности, включая состав промотора коллагена базальной мембраны IV и васкулярность. Savige et al., J Am Soc Nephrol. (2011) 22(8): 1403-15. Существуют данные, что путь комплемента участвует в почечных и глазных заболеваниях. Например, наследственный дефицит регуляторного белка системы комплемента вызывает предрасположенность к атипическому гемолитико-уремическому синдрому и AMD. Richards A et al., Adv Immunol. (2007) 96: 141-77. Кроме того, хроническая болезнь почек связана с AMD. Nitsch, D. et al., Ophthalmic Epidemiol. (2009) 16(3): 181-6; Choi, J. et al, Ophthalmic Epidemiol. (2011) 18(6): 259-63. Болезнь плотного осадка (DDD), заболевание почек, связанное с дисрегуляцией альтернативного пути комплемента, характеризуется острым нефритическим синдромом и глазными друзами. Cruz and Smith, GeneReviews (2007) Jul 20. Кроме того, мыши, несущие генетическую делецию компонента альтернативного пути комплемента, одновременно демонстрируют фенотипы почечной и глазной болезни. Описано, что у гомозиготных по нулевому CFH мышей развивается DDD и присутствуют патологии сетчатки, а также зрительная дисфункция. Pickering et al., Nat Genet. (2002) 31(4): 424-8. Мышиные модели почечных заболеваний, связанных с дисрегуляцией альтернативного пути комплемента, также являются общепринятыми моделями AMD. Pennesi ME et al., Mol Aspects Med (2012) 33: 487-509. Нулевые по CFH мыши, например, представляют собой общепринятую модель почечных заболеваний, таких как DDD, и AMD. Кроме того, описано, что AMD связана с системным источником факторов комплемента, которые локально накапливаются в глазах, приводя в действие альтернативный путь активации комплемента. Loyet et al., Invest Ophthalmol Vis Sci. (2012) 53(10): 6628-37.
Примеры
Следующие примеры иллюстрируют некоторые варианты реализации настоящего описания и не являются ограничивающими. Более того, если представлены конкретные варианты реализации, авторы изобретения подразумевают общее применение указанных конкретных вариантов реализации. Например, описание олигонуклеотида, содержащего конкретный мотив, дает обоснованное основание для дополнительных олигонуклеотидов, содержащих такой же или похожий мотив. И, например, если конкретная высокоаффинная модификация возникает в определенном положении, то в этом же положении считаются подходящими другие высокоаффинные модификации, если не указано иное.
Пример 1: Общий способ получения фосфорамидитов. Соединений 1, 1а и 2
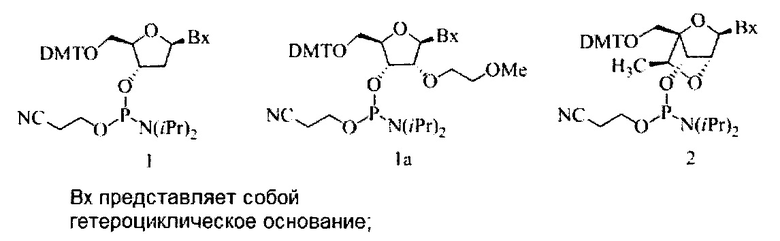
Соединения 1, 1a и 2 были получены по способам, общеизвестным в данной области техники, как описано в настоящем документе (см. Seth et al., Bioorg. Med. Chem., 2011, 21(4), 1122-1125, J. Org. Chem., 2010, 75(5), 1569-1581, Nucleic Acids Symposium Series, 2008, 52(1), 553-554); и см. также опубликованные Международные заявки РСТ (WO 2011/115818, WO 2010/077578, WO 2010/03 6698, WO 2009/143369, WO 2009/006478 и WO 2007/090071) и патент США 7569686).
Пример 2: Получение Соединения 7
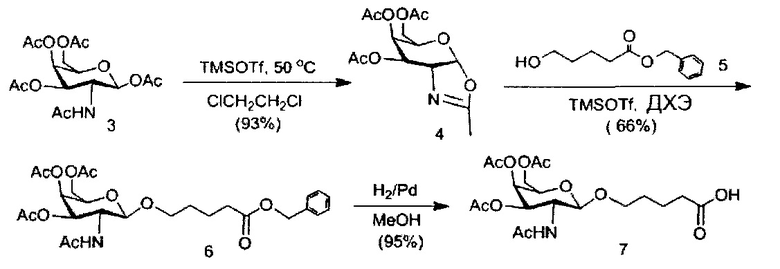
Соединение 3 (2-ацетамидо-1,3,4,6-тетра-(O-ацетил-2-дезокси-β-D-галактопираноза или галактозамина пентаацетат) имеется в продаже. Соединение 5 получили по опубликованным методикам (Weber et al., J. Med. Chem., 1991, 34, 2692).
Пример 3: Получение Соединения 11
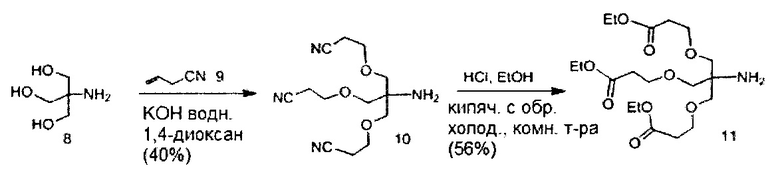
Соединения 8 и 9 имеются в продаже.
Пример 4: Получение Соединения 18
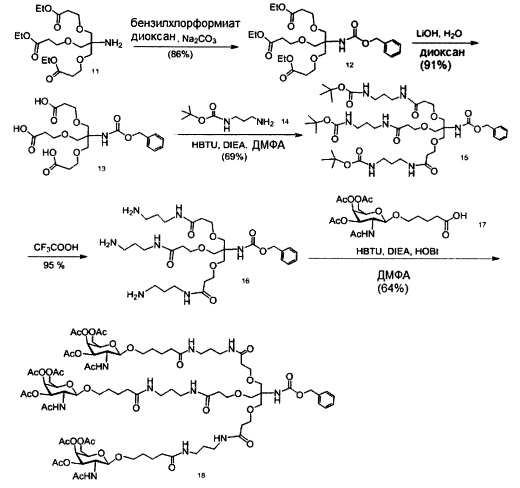
Соединение 11 получили по способам, описанным в Примере 3. Соединение 14 имеется в продаже. Соединение 17 получили по такому же способу, как описан в публикации Rensen et al., J. Med. Chem., 2004, 47, 5798-5808.
Пример 5: Получение Соединения 23
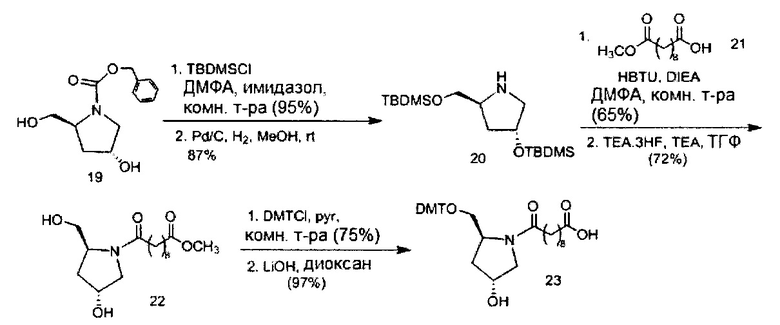
Соединения 19 и 21 имеются в продаже. Пример 6: Получение Соединения 24
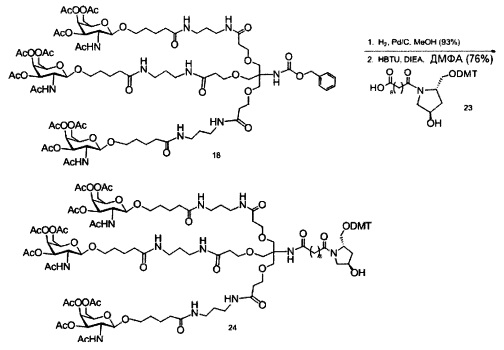
Соединения 18 и 23 получили так, как описано в способах в Примерах 4 и 5.
Пример 7: Получение Соединения 25
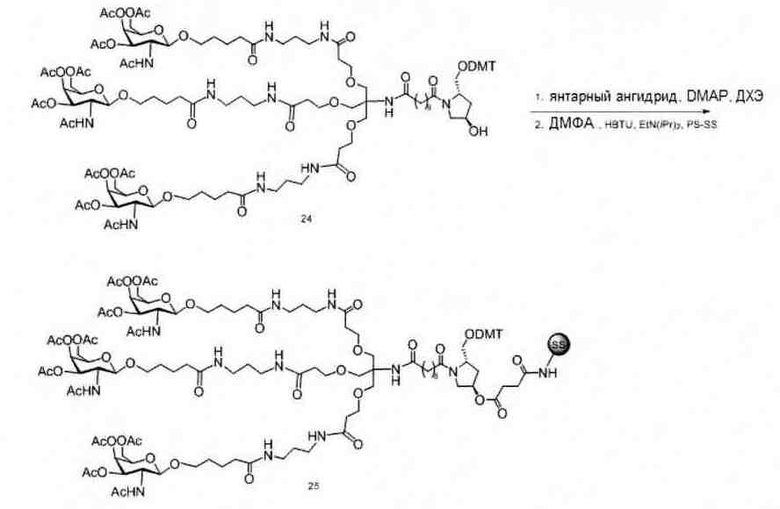
Соединение 24 получили по способам, представленным в Примере 6.
Пример 8: Получение Соединения 26
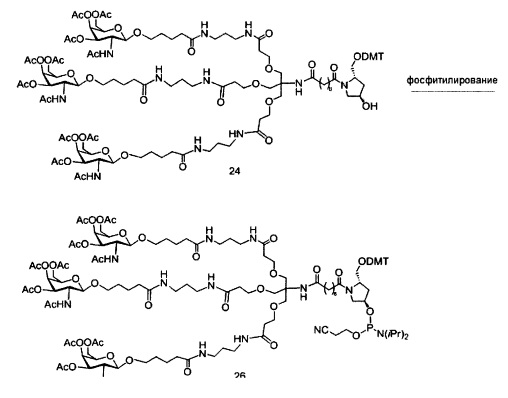
Соединение 24 получили по способам, представленным в Примере 6.
Пример 9: Общее получение сопряженных ASO, содержащих GalNAc3-1 у 3'-конца, Соединения 29
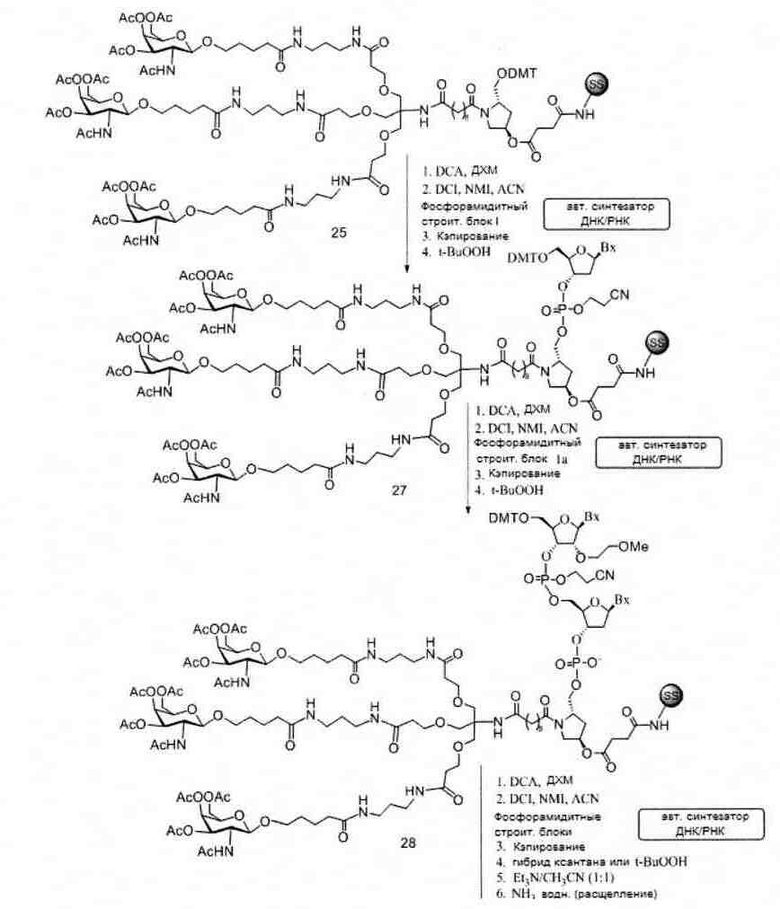
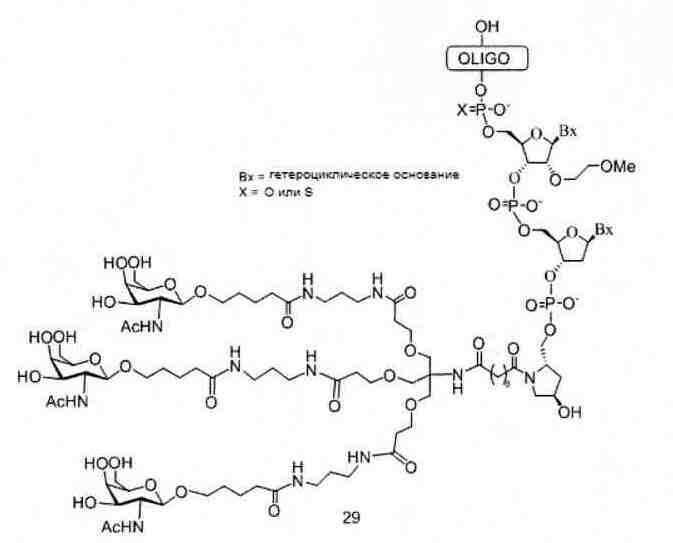
где защищенный GalNAc3-1 имеет структуру:
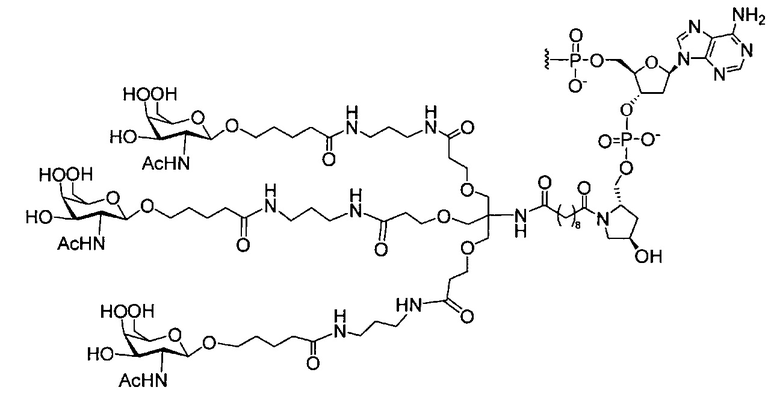
Кластерная часть GalNAc3 группы конъюгата GalNAc3-1 (GalNAc3-1a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Где GalNAc3-1a имеет формулу:
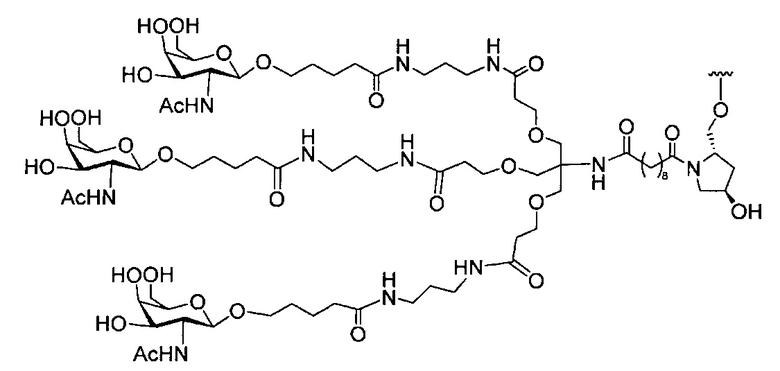
Защищенный GalNAc3-1, связанный с твердой подложкой. Соединение 25, получили по способам, представленным в Примере 7. Олигомерное соединение 29, содержащее GalNAc3-1 у 3'-конца, получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). Фосфорамидитные строительные блоки, Соединения 1 и 1а, получили так, как описано в способах в примере 1. Изображенные фосфорамидиты являются иллюстративными и не предназначены для ограничения, поскольку могут быть использованы другие фосфорамидитные строительные блоки для получения олигомерных соединений, имеющих заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения разорванных олигомерных соединений, описанных в настоящем документе. Такие разорванные олигомерные соединения могут иметь заданный состав и последовательность оснований, продиктованную любой данной мишенью.
Пример 10: Общее получение сопряженных ASO, содержащих GalNAc3-1 у 5'-конца, Соединения 34
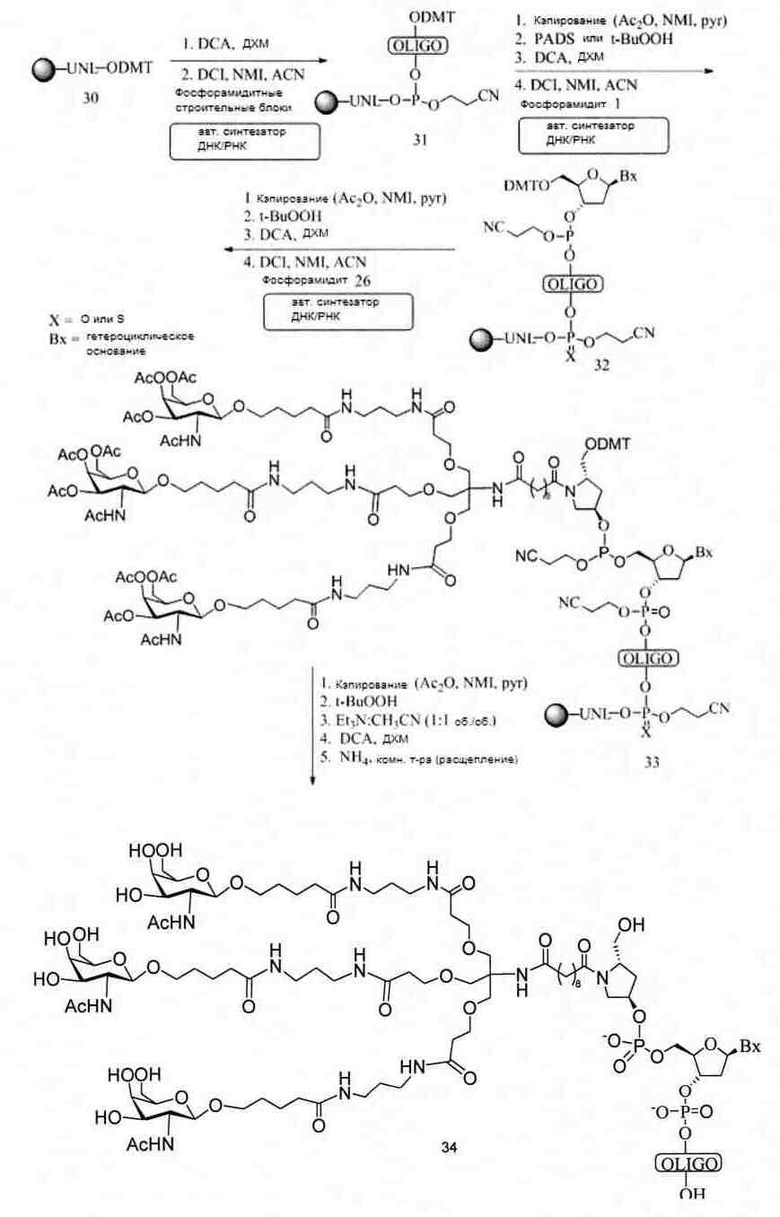
Unylinker™ 30 имеется в продаже. Олигомерное соединение 34, содержащее кластер GalNAc3-1 у 5'-конца, получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). Фосфорамидитные строительные блоки, Соединения 1 и 1а, получили так, как описано в способах в примере 1. Изображенные фосфорамидиты являются иллюстративными и не предназначены для ограничения, поскольку могут быть использованы другие фосфорамидитные строительные блоки для получения олигомерных соединений, имеющих заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения разорванных олигомерных соединений, описанных в настоящем документе. Такие разорванные олигомерные соединения могут иметь заданный состав и последовательность оснований, продиктованную любой данной мишенью.
Пример 11: Получение Соединения 39
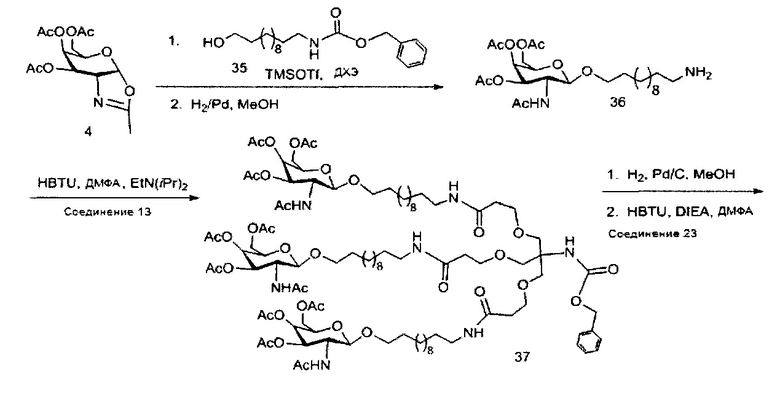
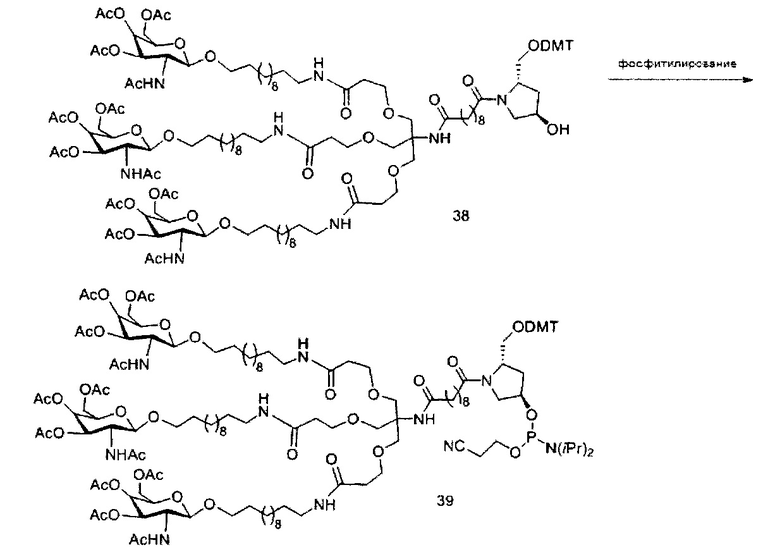
Соединения 4, 13 и 23 получили так, как описано в способах в Примерах 2, 4 и 5. Соединение 35 получили по такому же способу, как описан в публикации Rouchaud et al., Eur. J. Org. Chem., 2011, 72, 2346-2353.
Пример 12: Получение Соединения 40
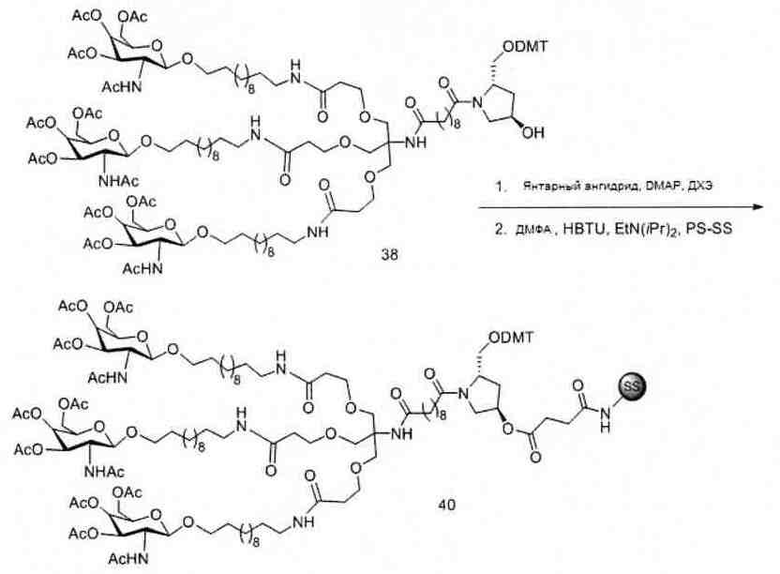
Соединение 38 получили по способам, представленным в Примере 11.
Пример 13: Получение Соединения 44
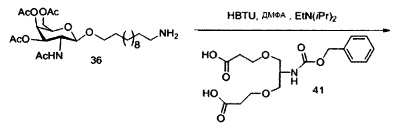
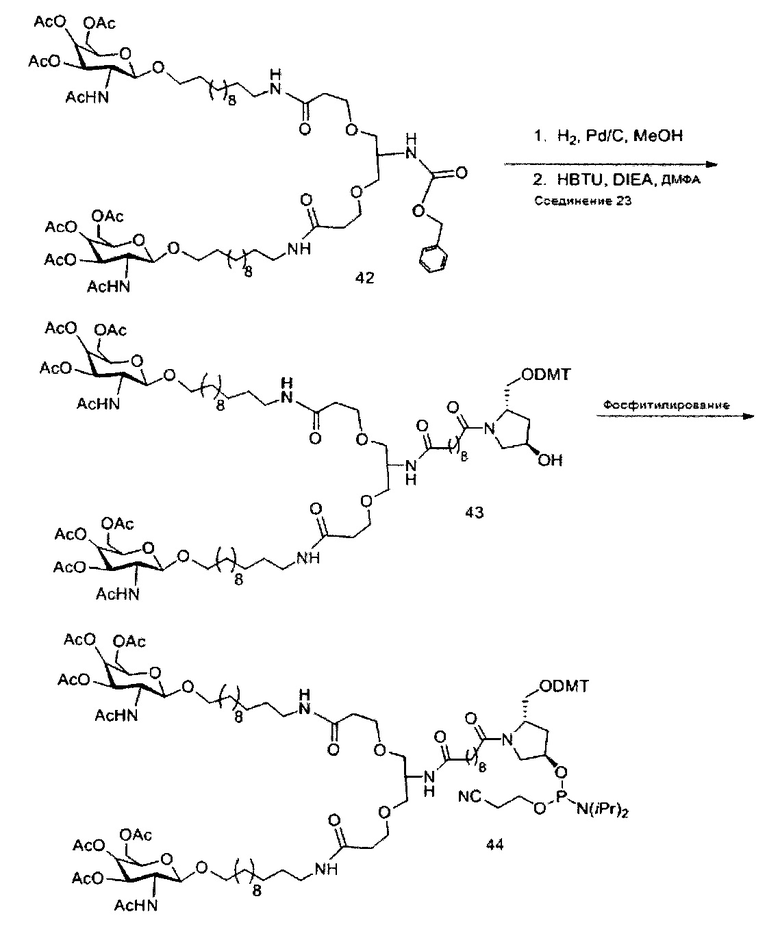
Соединения 23 и 36 получили так, как описано в способах в Примерах 5 и 11. Соединение 41 получили по такому же способу, как описан в публикации WO 2009082607.
Пример 14: Получение Соединения 45
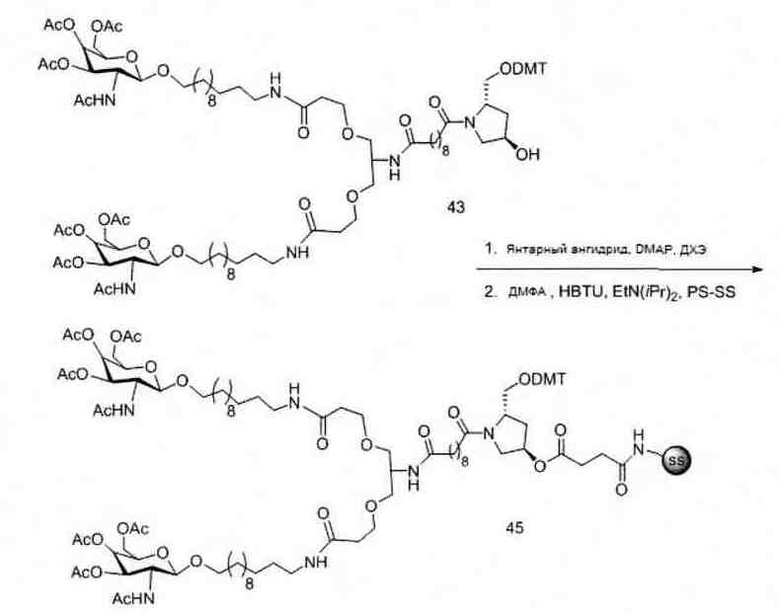
Соединение 43 получили по способам, представленным в Примере 13.
Пример 15: Получение Соединения 47
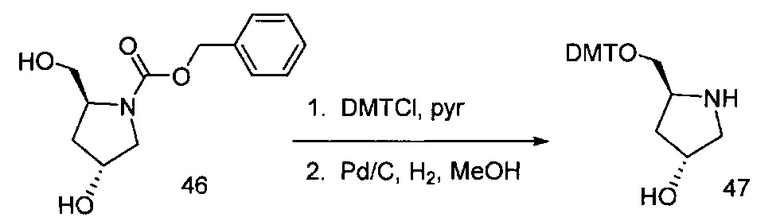
Соединение 46 имеется в продаже.
Пример 16: Получение Соединения 53
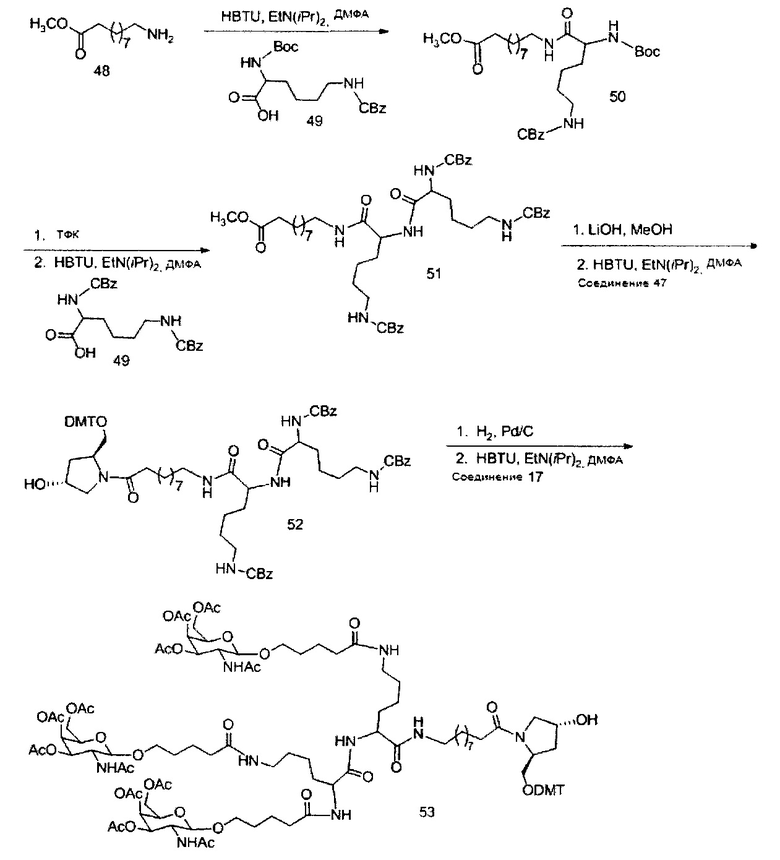
Соединения 48 и 49 имеются в продаже. Соединения 17 и 47 получили так, как описано в способах в Примерах 4 и 15.
Пример 17: Получение Соединения 54
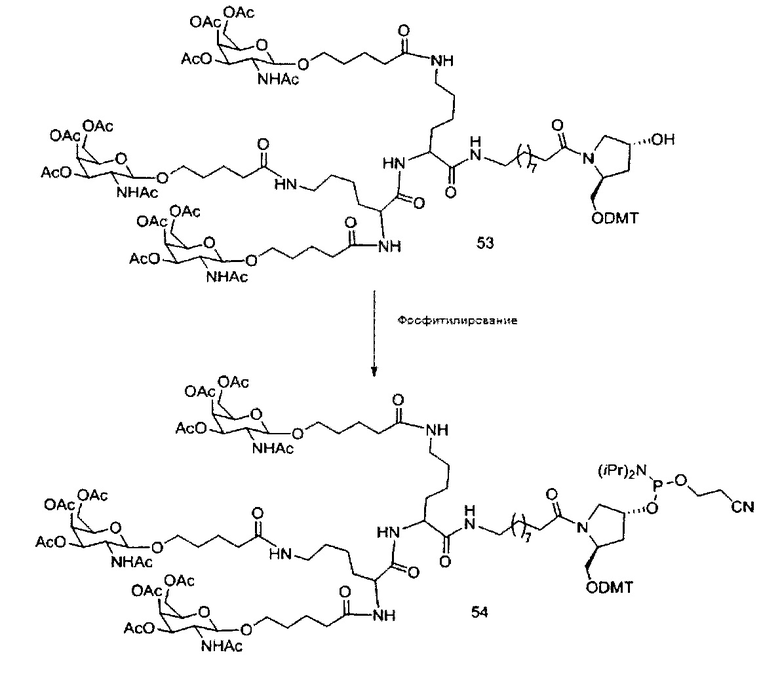
Соединение 53 получили по способам, представленным в Примере 16.
Пример 18: Получение Соединения 55
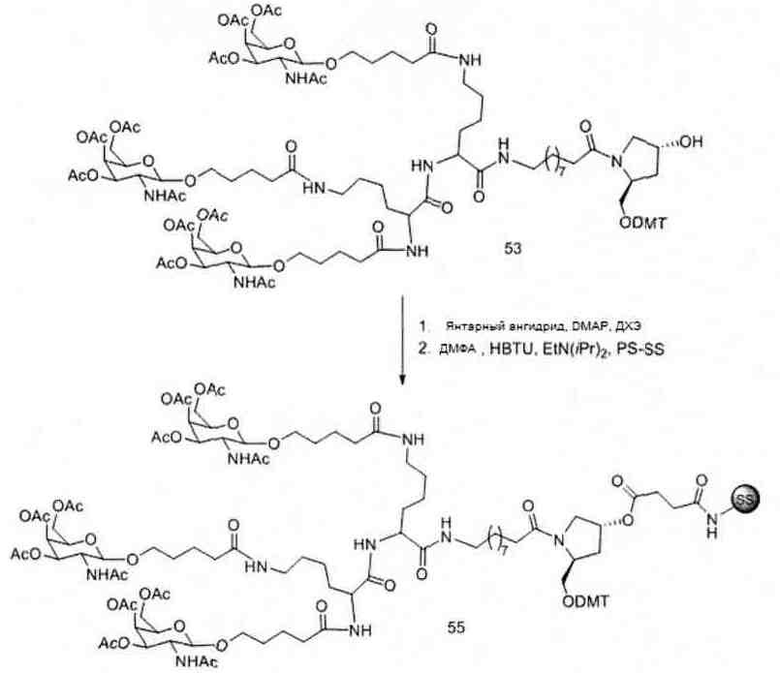
Соединение 53 получили по способам, представленным в Примере 16.
Пример 19: Общий способ получения сопряженных ASO, содержащих GalNAc3-1 в 3'-положении, при помощи твердофазных методик (получение ISIS 647535, 647536 и 651900)
Если не указано иное, все реагенты и растворы, использованные для синтеза олигомерных соединений, приобретены у коммерческих поставщиков. Стандартные фосфорамидитные строительные блоки и твердую подложку использовали для внедрения нуклеозидных остатков, которые включают, например, остатки Т, A, G и mC. 0,1 М раствор фосфорамидита в безводном ацетонитриле использовали для β-D-2'-дезоксирибонуклеозида и 2'-МОЕ.
Синтез антисмысловых олигонуклеотидов (ASO) выполнили на синтезаторе ABI 394 (в масштабе 1-2 мкмоль) или на синтезаторе  Oligopilot производства GE Healthcare Bioscience (в масштабе 40-200 мкмоль) по способу фосфорамидитного связывания на твердой подложке VIMAD, наполненной GalNAc3-1 (110 мкмоль/г, Guzaev et al., 2003), упакованной в колонку. Для стадии связывания фосфорамидиты вводили в 4-кратном избытке по сравнению с загрузкой на твердой подложке, а конденсацию фосфорамидита выполняли в течение 10 минут. Все остальные стадии выполняли по стандартным протоколам, предоставленным производителем. Для удаления диметокситритильной (DMT) группы с 5'-гидроксильной группы нуклеотида использовали 6% раствор дихлоруксусной кислоты в толуоле. На стадии связывания в качестве активатора использовали 4,5-дицианоимидазол (0,7 М) в безводном CH3CN. Тиофосфатные связи внедряли сульфированием при помощи 0,1 М раствора гидрида ксантана в 1:1 смеси пиридина/CH3CN в течение 3 минут времени контакта. В качестве окислительного агента для получения фосфодиэфирных межнуклеозидных связей использовали 20% раствор трет-бутилгидропероксида в CH3CN, содержащий 6% воды, в течение 12 минут времени контакта.
Oligopilot производства GE Healthcare Bioscience (в масштабе 40-200 мкмоль) по способу фосфорамидитного связывания на твердой подложке VIMAD, наполненной GalNAc3-1 (110 мкмоль/г, Guzaev et al., 2003), упакованной в колонку. Для стадии связывания фосфорамидиты вводили в 4-кратном избытке по сравнению с загрузкой на твердой подложке, а конденсацию фосфорамидита выполняли в течение 10 минут. Все остальные стадии выполняли по стандартным протоколам, предоставленным производителем. Для удаления диметокситритильной (DMT) группы с 5'-гидроксильной группы нуклеотида использовали 6% раствор дихлоруксусной кислоты в толуоле. На стадии связывания в качестве активатора использовали 4,5-дицианоимидазол (0,7 М) в безводном CH3CN. Тиофосфатные связи внедряли сульфированием при помощи 0,1 М раствора гидрида ксантана в 1:1 смеси пиридина/CH3CN в течение 3 минут времени контакта. В качестве окислительного агента для получения фосфодиэфирных межнуклеозидных связей использовали 20% раствор трет-бутилгидропероксида в CH3CN, содержащий 6% воды, в течение 12 минут времени контакта.
После сборки требуемой последовательности цианоэтил-фосфатные защитные группы снимали при помощи 1:1 (об./об.) смеси триэтиламина и ацетонитрила в течение 45 минут времени контакта. Связанные с твердой подложкой ASО суспендировали в водном растворе аммиака (28-30 масс. %) и нагревали при 55°С в течение 6 часов.
Затем отфильтровывали не связанные ASO и выпаривали аммиак кипячением. Остаток очищали жидкостной хроматографией высокого давления на сильной анионообменной колонке (GE Healthcare Bioscience, Source 30Q, 30 мкм, 2,54×8 см, А=100 мМ ацетата аммония в 30% водном CH3CN, В=1,5 М NaBr в А, 0-40% В за 60 мин., скорость потока 14 мл.мин-1, λ=260 нм). Остаток обессоливали при помощи ВЭЖХ на обращенно-фазовой колонке с получением заданных ASO с выделенным выходом 15-30% относительно первоначальной загрузки на твердую подложку. ASO характеризовали при помощи ион-парной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.
Антисмысловые олигонуклеотиды, не содержащие конъюгат, синтезировали по стандартным способам синтеза олигонуклеотидов, общеизвестным в данной области техники.
Применяя эти способы, получили три отдельных антисмысловых соединения, направленных на АроС III. Как показано ниже в Таблице 17, каждое из трех антисмысловых соединений, направленных на АроС III, имеет одну и ту же последовательность нуклеооснований. ISIS 304801 представляет собой 5-10-5 МОЕ гэпмер, содержащий только тиофосфатные связи; ISIS 647535 является таким же, как ISIS 304801, за исключением того, что он содержит GalNAc3-1, сопряженный у его 3'-конца; и ISIS 647536 является таким же, как ISIS 647535, за исключением того, что некоторые межнуклеозидные связи этого соединения представляют собой фосфодиэфирные связи. Как дополнительно показано в Таблице 17, были синтезированы два отдельных антисмысловых соединения, направленных на SRB-1. ISIS 440762 представляет собой 2-10-2 cEt гэпмер, содержащий только тиофосфатные межнуклеозидные связи; ISIS 651900 является таким же, как ISIS 440762, за исключением того, что он содержит GalNAc3-1 у его 3'-конца.
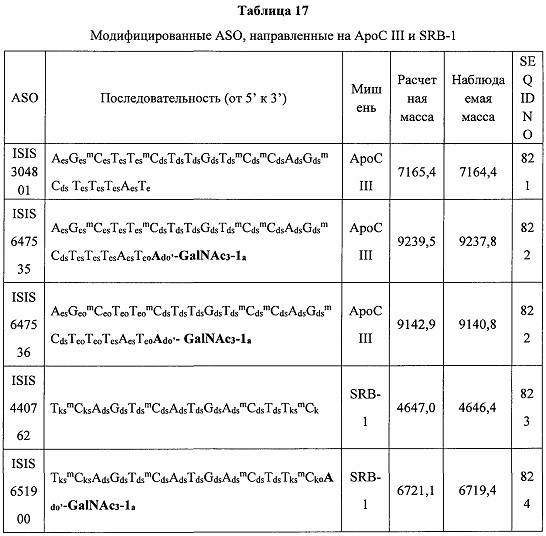
Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «о'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. «GalNAc3-1» означает группу конъюгата, имеющую структуру, показанную ранее в Примере 9. Следует отметить, что GalNAc3-1 содержит расщепляемый аденозин, которые связывает ASO с остальной частью конъюгата, обозначенной «GalNAc3-1a.» Номенклатура, используемая в представленной выше таблице, показывает полную последовательность азотистых оснований, включая аденозин, который является частью конъюгата. Следовательно, в представленной выше таблице последовательности также могут быть перечислены с окончание «GalNAc3-1», без «Ado». Такое условное применение нижнего индекса «а» для обозначения части группы конъюгата, не содержащей расщепляемого нуклеозида или расщепляемого фрагмента, используется во всех представленных Примерах. Эта часть группы конъюгата, не содержащая расщепляемого фрагмента, упоминается в настоящем документе как «кластер» или «кластер конъюгата» или «кластер GalNAc3». В некоторых случаях группа конъюгата для удобства описана путем отдельного представления ее кластера и ее расщепляемого фрагмента.
Пример 20: Дозозависимое антисмысловое ингибирование человеческого АроС III у huApoC III трансгенных мышей
ISIS 304801 и ISIS 647535, каждый из которых направлен на человеческий АроС III и описан выше, отдельно испытывали и оценивали в дозозависимом исследовании на их способность ингибировать человеческий АроС III у трансгенных мышей с человеческим АроС III. Лечение
Трансгенных мышей с человеческим ApoCIII выдерживали при 12-часовом цикле освещения/темноты и обеспечивали ad libitum доступ к пище Teklad lab. До начала эксперимента животных акклиматизировали по меньшей мере в течение 7 дней в исследовательской лаборатории. Получили ASO в PBS и стерилизовали фильтрованием через фильтр 0,2 микрона. ASO растворили в 0,9% PBS для инъекций.
Трансгенным мышам с человеческим АроС III один раз в неделю в течение двух недель внутрибрюшинно вводили инъекции ISIS 304801 или 647535 при 0,08, 0,25, 0,75, 2,25 или 6,75 мкмоль/кг или PBS в качестве контроля. Каждая экспериментальная группа состояла из 4 животных. Через сорок восемь часов после введения последней дозы каждую мышь обескровили и усыпили, и собрали ткани.
Анализ мРНК АроС III
Уровни мРНК АроС-III в печени мышей определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК АроС III определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, представлены как средний процент уровней мРНК АроС III для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». Полумаксимальная эффективная доза (ED50) каждого ASO представлена также ниже в Таблице 18.
Показано, что оба антисмысловых соединения снижают РНК АроС III, по сравнению с контрольным образцом, обработанным PBS. Кроме того, антисмысловое соединение, сопряженное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).

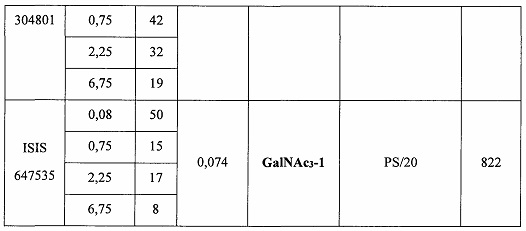
Анализ белка АроС III (турбидиметрический анализ)
Анализ белка АроС III в плазме выполнили по способам, описанным в работе Graham et al, Circulation Research, до печати опубликованной онлайн 29 марта 2013 года.
Приблизительно 100 мкл плазмы, выделенной из мышей, анализировали без разбавления, используя клинический анализатор Olympus и имеющийся в продаже турбидиметрический аналитический набор АроС III (Kamiya, кат. № KAI-006, Kamiya Biomedical, Сиэтл, штат Вашингтон). Протокол анализа выполняли по описанию поставщика.
Как показано ниже в Таблице 19, оба антисмысловых соединения снижают белок АроС III, по сравнению с PBS контрольным образцом. Кроме того, антисмысловое соединение, сопряженное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).

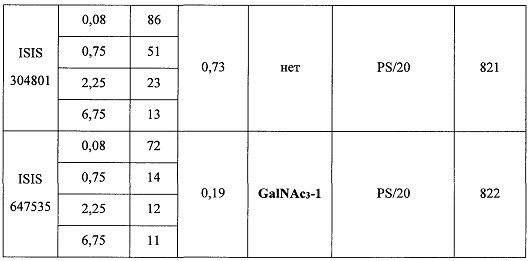
Триглицериды и холестерин плазмы выделили по способу Bligh и Dyer (Bligh, E.G. и Dyer, W.J. Can. J. Biochem. Physiol. 37: 911-917, 1959)(Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959) (Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959) и измерили при помощи клинического анализатора Beckmann Coulter и имеющихся в продаже реагентов.
Уровни триглицеридов измерили относительно мышей, инъецированных PBS, и выразили как «% PBS». Результаты представлены в Таблице 20. Показано, что оба антисмысловых соединения снижают уровни триглицеридов. Кроме того, антисмысловое соединение, сопряженное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).
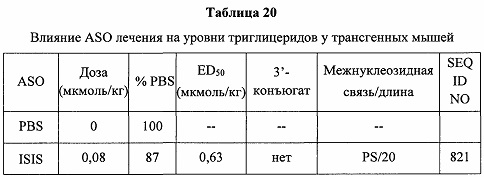
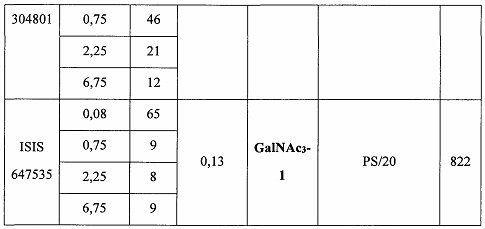
Образцы плазмы анализировали при помощи ВЭЖХ для определения количества общего холестерина и различных фракций холестерина (HDL и LDL). Результаты представлены в таблицах 21 и 22. Показано, что оба антисмысловых соединения снижают общие уровни холестерина; оба снижают LDL; и оба повышают HDL. Кроме того, антисмысловое соединение, сопряженное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801). Увеличение уровней HDL и снижение уровней LDL представляет собой преимущественный сердечно-сосудистый эффект антисмыслового ингибирования АроС III.
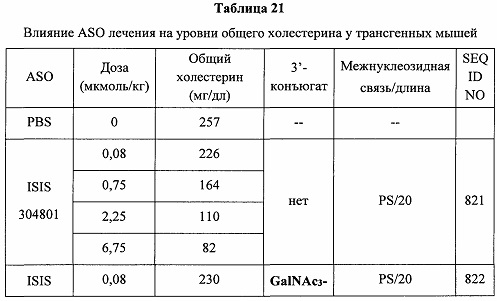
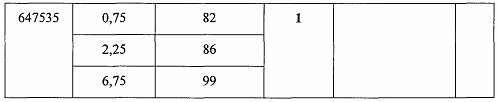
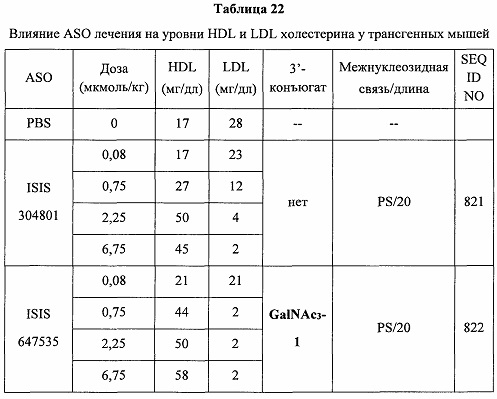
Фармакокинетический анализ (ФК)
Исследовали также ФК ASO. Образцы печени и почек измельчали и экстрагировали по стандартным протоколам. Образцы анализировали на MSD1, используя ИП-ВЭЖХ-МС. Определили содержание (мкг/г) в ткани ISIS 304801 и 647535 полной длины, и результаты представлены в Таблице 23. Показано, что концентрации в печени антисмысловых соединений полной длины были одинаковыми для двух антисмысловых соединений. Следовательно, даже несмотря на то, что GalNAc3-1-сопряженное антисмысловое соединение является более активным в печени (как показано по данным РНК и белка, представленным выше), его содержание в печени не намного выше. Действительно, рассчитанное значение ЕС50 (представленное в Таблице 23) подтверждает, что наблюдаемое увеличение эффективности сопряженного соединения не может быть приписано исключительно повышенному накоплению. Такой результат позволяет предположить, что конъюгат улучшает эффективность по другому механизму, чем простое накопление в печени, возможно за счет увеличения продуктивного захвата антисмыслового соединения в клетки.
Эти результаты показывают также, что концентрация GalNAc3-1-сопряженного антисмыслового соединения почках ниже, чем концентрация антисмыслового соединения, не содержащего конъюгата GalNAc. Это имеет несколько преимущественных терапевтических применений. Для терапевтических показаний, в которых не требуется проявление активности в почках, воздействие на почки подвергает их риску токсичности без соответствующей пользы. Более того, высокая концентрация в почках обычно приводит к выводу соединения с мочой, обеспечивая более быстрое выведение. Соответственно, для внепочечных мишеней накопление в почках является нежелательным. Эти данные позволяют предположить, что сопряжение с GalNAc3-1 снижает накопление в почках.
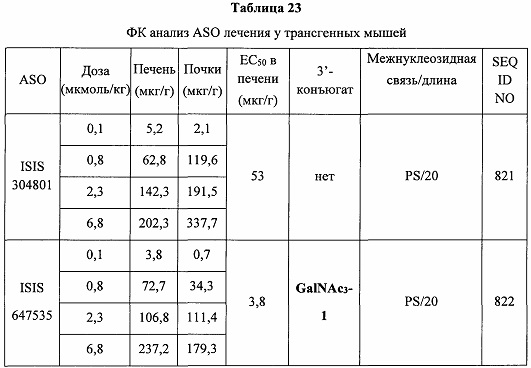
Идентифицировали также метаболиты ISIS 647535 и подтвердили их массы при помощи масс-спектрометрического анализа высокого разрешения. Сайты расщепления и структуры наблюдаемых метаболитов представлены ниже. Относительный % от общей длины ASO рассчитали по стандартным технологиям, а результаты представлены в Таблице 23а. Основной метаболит ISIS 647535 представляет собой ASO полной длины без всего конъюгата (то есть ISIS 304801), который образуется в результате расщепления по сайту расщепления А, представленному ниже. Кроме того, наблюдали также дополнительные метаболиты, образующиеся из других сайтов расщепления. Эти результаты позволяют предположить, что может быть пригодным также внедрение других расщепляемых связей, таких как сложные эфиры, пептиды, дисульфиды, фосфорамидаты или ацил-гидразоны, между сахаром GalNAc3-1 и ASO, которые могут расщепляться под действием ферментов внутри клетки или которые могут расщепляться в восстановительной среде цитозоля, или которые лабильны в кислотном рН внутри эндосом и лизосом.
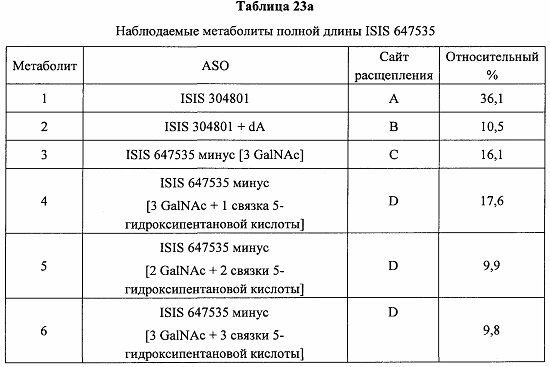
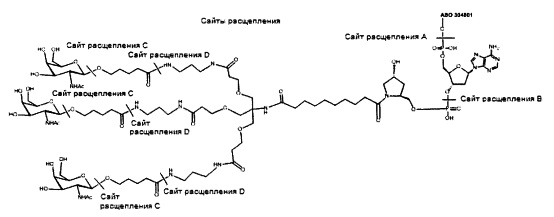

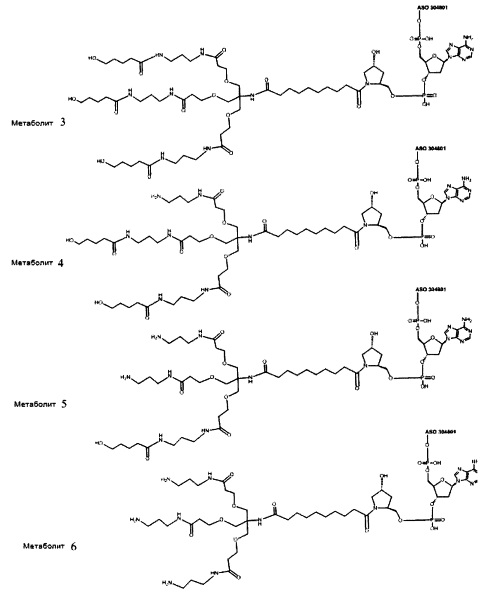
Пример 21: Антисмысловое ингибирование человеческого АроС III у трансгенных мышей с АроС III в исследовании одного введения
ISIS 304801, 647535 и 647536, каждый из которых направлен на человеческий АроС III и описан в Таблице 17, дополнительно оценивали в исследовании однокраного введения на их способность ингибировать человеческий АроС III у трансгенных мышей с человеческим АроС III.
Лечение
Трансгенных мышей с человеческим ApoCIII выдерживали при 12-часовом цикле освещения/темноты и обеспечивали ad libitum доступ к пище Teklad lab. До начала эксперимента животных акклиматизировали по меньшей мере в течение 7 дней в исследовательской лаборатории. Получили ASO в PBS и стерилизовали фильтрованием через фильтр 0,2 микрона. ASO растворили в 0,9% PBS для инъекций.
Трансгенным мышам с человеческим АроС III внутрибрюшинно ввели однократную инъекцию дозы, представленной ниже, соединения ISIS 304801, 647535 или 647536 (описанных выше), или PBS в качестве контрольного образца. Экспериментальная группа состояла из 3 животных, а контрольная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей усыпили через 72 часа после последнего введения.
Образцы собрали и анализировали для определения уровней мРНК АроС III и белка в печени; триглицеридов в плазме; и холестерина, включая фракции HDL и LDL, которые анализировали так, как описано выше (Пример 20). Данные этих анализов представлены ниже в Таблицах 24-28. Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Уровни ALT и AST показали, что антисмысловые соединения хорошо переносятся при всех введенных дозах.
Эти результаты демонстрируют усиление эффективности антисмысловых соединений, содержащих конъюгат GalNAc3-1 у 3'-конца (ISIS 647535 и 647536), по сравнению с антисмысловым соединением, не содержащим конъюгат GalNAc3-1 (ISIS 304801). Кроме того, ISIS 647536, который содержит конъюгат GalNAc3-1 и несколько фосфодиэфирных связей, был таким же эффективным, как ISIS 647535, который содержит тот же конъюгат, и все межнуклеозидные связи в этом ASO являются тиофосфатными.
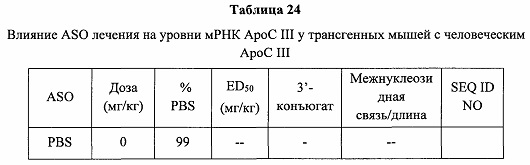
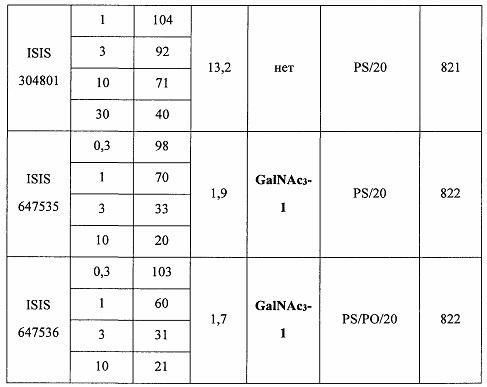
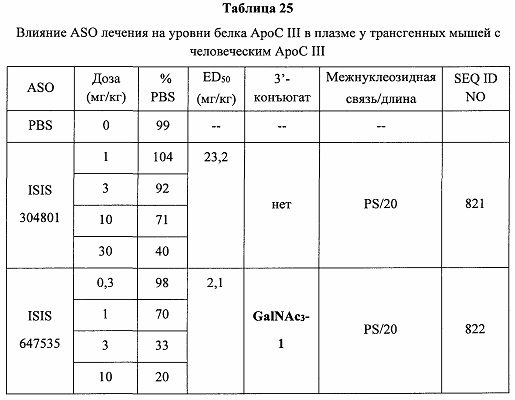
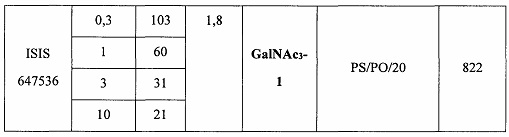
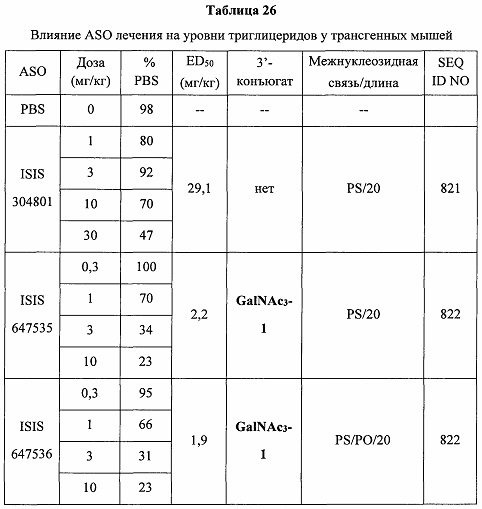

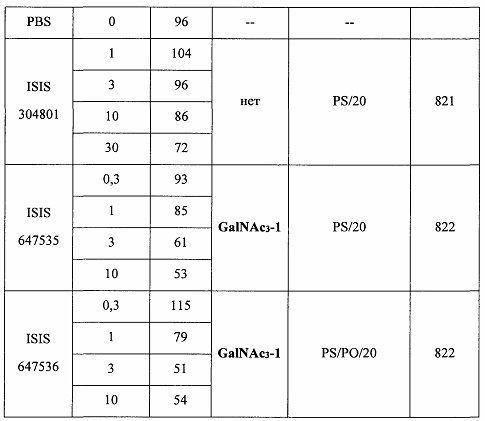
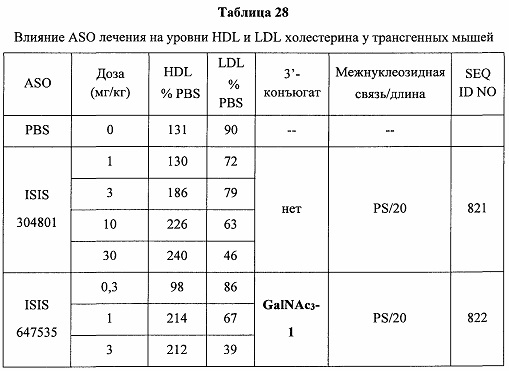
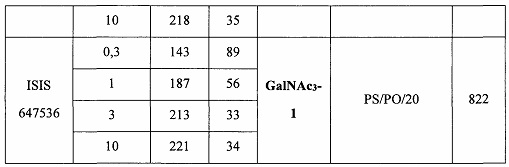
Эти результаты подтверждают, что конъюгат GalNAc3-1 улучшает эффективность антисмыслового соединения. Эти результаты показывают также равную эффективность GalNAc3-1-сопряженных антисмысловых соединений, в которых антисмысловые олигонуклеотиды имеют смешанные связи (ISIS 647536, который имеет шесть фосфодиэфирных связей), и полностью тиофосфатной версии того же антисмыслового соединения (ISIS 647535).
Тиофосфатные связи обеспечивают несколько свойств антисмысловых соединений. Например, они устойчивы к нуклеазному расщеплению и связываются с белками, что приводит к накоплению соединения в печени, а не в почках/моче. Эти свойства являются желательными, особенно при лечении показаний в печени. Однако тиофосфатные связи связаны также с воспалительной реакцией. Соответственно, уменьшение количества - тиофосфатных связей в соединении предположительно снижает риск воспаления, но снижает также концентрацию соединения в печени, повышает концентрацию в почках и моче, снижает стабильность в присутствии нуклеаз и уменьшает общую эффективность. Представленные результаты демонстрируют, что GalNAc3-1-сопряженное антисмысловое соединение, в котором некоторые тиофосфатные связи заменены фосфодиэфирными связи, настолько же эффективно против мишени в печени, как и аналог, содержащий только -тиофосфатные связи. Такие соединения предположительно являются менее провоспалительными (см. Пример 24, в котором описан эксперимент, демонстрирующий, что уменьшение тиофосфатов (PS) приводит к снижению воспалительного действия).
Пример 22: Влияние модифицированного GalNAc3-1-сопряженного ASO, направленного на SRB-1, in vivo
ISIS 440762 и 651900, каждый из которых направлен на SRB-1 и описан в Таблице 17, оценили в дозозависимом исследовании на их способность ингибировать SRB-1 у Balb/c мышей.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 440762, 651900 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 48 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS».
Как показано в Таблице 29, оба антисмысловых соединения снижают уровни мРНК SRB-1. Кроме того, антисмысловое соединение, содержащее конъюгат GalNAc3-1 (ISIS 651900), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 440762). Эти результаты демонстрируют, что преимущество эффективности конъюгатов GalNAc3-1 наблюдается при использовании антисмысловых олигонуклеотидов, комплементарных различным мишеням и имеющих различные химически модифицированные нуклеозиды, в этом случае модифицированные нуклеозиды содержат стерически затрудненные этил-сахарные фрагменты (бициклический сахарный фрагмент).
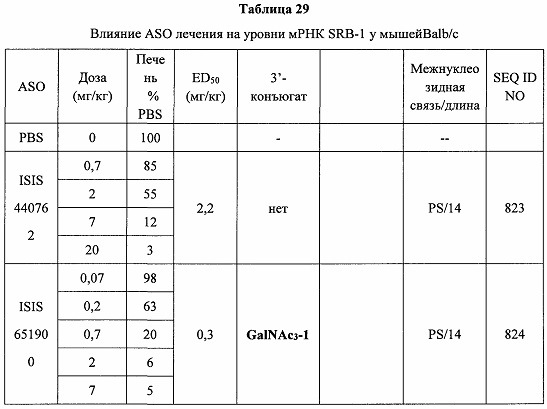
Пример 23: Протокол анализа человеческих мононуклеарных клеток периферической крови (hPBMC)
Анализ hPBMC выполнили при помощи пробирочного способа BD Vautainer CPT. Получили образец цельной крови, полученной от доноров-добровольцев, давших информированное согласие в Медицинской клинике США (Faraday & El Camino Real, Карлсбад), и собрали его в 4-15 пробирки BD Vacutainer CPT по 8 мл (VWR, кат. № BD362753). Приблизительный исходный общий объем цельной крови в пробирке CPT для каждого донора записали в формуляре анализа РВМС.
Непосредственно перед центрифугированием образец крови повторно перемешали, осторожно переворачивая пробирки 8-10 раз. Пробирки CPT центрифугировали при комнатной температуре (18-25°С) в горизонтальном (с избыточной поворачиваемостью) роторе в течение 30 минут с фактором разделения (RCF) 1500-1800 с затормаживанием (2700 об./мин. Beckman Allegra 6R). Клетки сняли с лейкоцитарной поверхности раздела (между слоями фиколла и полимерного геля); перенесли в стерильную 50 мл коническую пробирку и сгруппировали по 5 СРТ пробирок/50 мл коническая пробирка/донор. Затем клетки дважды промыли PBS (без Са++, Mg++; GIBCO). Пробирки пополнили до 50 мл и перемешали, переворачивая несколько раз. Затем образец центрифугировали при 330 × g в течение 15 минут при комнатной температуре (1215 об./мин. в Beckman Allegra 6R) и аспирировали максимальное количество надосадочной жидкости, не нарушая осадок. Клеточный осадок сняли, осторожно поворачивая пробирку, и повторно суспендировали клетки в RPMI + 10% FBS + пенициллин/стрептомицин (~1 мл / 10 мл исходного объема цельной крови). Пипеткой взяли 60 мкл образца и поместили во флакон с пробой (Beckman Coulter), содержащий 600 мкл реагента VersaLyse (Beckman Coulter, кат. № А09777), и осторожно перемешивали на вортексе в течение 10-15 секунд. Образец оставили инкубироваться в течение 10 минут при комнатной температуре, и снова перемешали перед подсчетом. Суспензию клеток считывали на анализаторе жизнеспособности клеток Vicell XR (Beckman Coulter), используя клетки типа РВМС (сохранили фактор разбавления 1:11 с другими параметрами). Записали количество живых клеток/мл и жизнеспособность. Клеточную суспензию разбавили до 1×107 живых РВМС/мл в RPMI + 10% FBS + пенициллин/стрептомицин.
Клетки поместили на планшет при 5×105 в 50 мкл/лунку 96-луночного тканевого культурального планшета (Falcon Microtest). 50 мкл/лунку 2× концентрации олигомеров/контроля, разбавленных в RPMI + 10% FBS + пенициллин/стрептомицин, добавили в соответствии с экспериментальной матрицей (в целом 100 мкл/лунку). Планшеты установили на шейкер и оставили перемешиваться в течение около 1 мин. После инкубации в течение 24 часов при 37°С; 5% CO2, планшеты центрифугировали при 400 × g в течение 10 минут, затем удалили надосадочную жидкость для анализа цитокинов MSD (то есть человеческих IL-6, IL-10, IL-8 и МСР-1).
Пример 24: Оценка провоспалительных эффектов в анализе hPBMC для GalNAc3-1-сопряженных ASO
Антисмысловые олигонуклеотиды (ASO), перечисленные в Таблице 30, оценили на провоспалительное действие в анализе hPBMC, используя протокол, описанный в Примере 23. ISIS 353512 представляет собой внутренний стандарт, который, как известно, обладает высоким ответом на высвобождение IL-6 в этом анализе. hPBMC выделили из свежих образцов, полученных от доноров-добровольцев, и обработали ASO в концентрациях 0, 0,0128, 0,064, 0,32, 1,6, 8, 40 и 200 мкМ. Через 24 часа обработки измерили уровни цитокинов.
Уровни IL-6 использовали в качестве первичного значения. ЕС50 и Emax расчитывали по стандарным способам. Результаты выразили как среднее отношение Emax/ЕС50 для двух доноров и обозначили как «Emax/ЕС50». Более низкое соотношение означает относительное снижение провоспалительного ответа, а более высокое соотношение означает относительное увеличение провоспалительного ответа.
В отношении исследуемых соединений, наименее провоспалительным соединением было ASO, соединенное при помощи PS/PO (ISIS 616468). GalNAc3-1-сопряженное ASO, ISIS 647535, было немного менее провоспалительным, чем его несопряженный аналог, ISIS 304801. Эти результаты показывают, что внедрение нескольких РО связей снижает провоспалительную реакцию, а добавление конъюгата GalNAc3-1 не делает соединение более провоспалительным, и может снижать провоспалительную реакцию. Соответственно, можно ожидать, что антисмысловое соединение, содержащее смешанные PS/PO связи и конъюгат GalNAc3-1, может вызывать более слабые провоспалительные реакции, по сравнению с антисмысловым соединением, связанным только посредством PS, с конъюгатом GalNAc3-1 или без него. Эти результаты показывают, что GalNAc3-1-сопряженные антисмысловые соединения, в частности, соединения, имеющие меньшее содержание PS, являются менее провоспалительными.
В целом, эти результаты позволяют предположить, что GalNAc3-1-сопряженное соединение, в частности, соединение со сниженным содержанием PS, может быть введено в более высокой дозе, чем аналогичное полностью PS антисмысловое соединение без конъюгата GalNAc3-1. Поскольку не ожидается, что период полувыведения для этих соединений будет существенно различаться, то такое введение в более высокой дозе обусловит менее частое введение доз. В действительности, такое введение может быть еще более редким, поскольку GalNAc3-1-сопряженные соединения являются более эффективными (см. Примеры 20-22), а повторное введение дозы необходимо только при снижении концентрации соединения ниже заданного уровня, при этом такой заданный уровень обусловлен эффективностью.
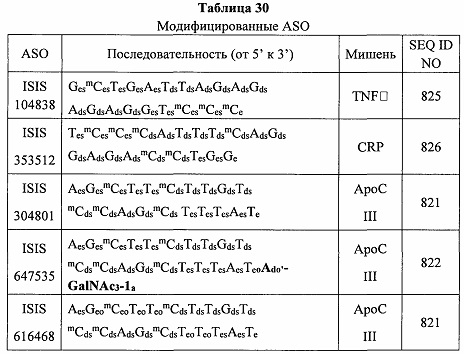
Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «о'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. «Ado'-GalNAc3-1a» означает конъюгат, имеющий структуру GalNAc3-1, показанную в Примере 9, присоединенную к 3'-концу антисмыслового олигонуклеотида, как показано.
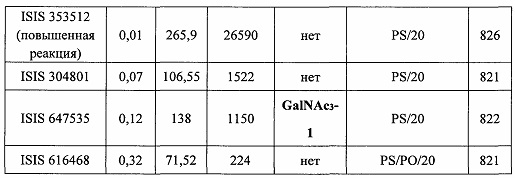
Пример 25: Влияние модифицированного GalNAc3-1-сопряженного ASO, направленного на человеческий АроС III, in vitro
ISIS 304801 и 647535, описанные выше, испытали in vitro. Первичные гепатоцитарные клетки трансгенных мышей при плотности 25000 клеток на лунку обработали концентрациями 0,03, 0,08, 0,24, 0,74, 2,22, 6,67 и 20 мкМ модифицированных олигонуклеотидов. После обработки в течение приблизительно 16 часов, из клеток выделили РНК и измерили уровни мРНК при помощи количественной ПЦР в реальном времен, а уровни мРНК hApoC III скорректировали в соответствии с общим содержанием РНК, измеренным при помощи RIBOGREEN.
IC50 рассчитали по стандартным способам, а результаты представлены в Таблице 32. Показано, что наблюдали сравнимую эффективность в клетках, обработанных ISIS 647535, по сравнению с контрольным образцом, ISIS 304801.

В этом эксперименте in vitro не наблюдали такого большого преимущества эффективности сопряжения с GalNAc3-1, как наблюдали in vivo. Последующие эксперименты свободного захвата в первичных гепатоцитах in vitro не показали повышенной эффективности олигонуклеотидов, содержащих различные конъюгаты GalNAc, по сравнению с олигонуклеотидами, не содержащими конъюгаты GalNAc (см. Примеры 60, 82 и 92).
Пример 26: Влияние линкеров PO/PS на кативность ASO в отношении АроС III
Трансгенным мышам с человеческим АроС III внутрибрюшинной инъекцией вводили 25 мг/кг ISIS 304801 или ISIS 616468 (оба описаны выше) или PBS в качестве контрольного образца, один раз в неделю в течение двух недель. Экспериментальная группа состояла из 3 животных, а контрольная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей усыпили через 72 часа после последнего введения.
Образцы собрали и анализировали для определения уровней белка АроС III в печени, как описано выше (Пример 20). Данные этих анализов представлены ниже в Таблице 33.
Эти результаты демонстрируют снижение эффективности антисмысловых соединений с PO/PS (ISIS 616468) в крыльях, по сравнению с соединениями, содержащими только PS (ISIS 304801).
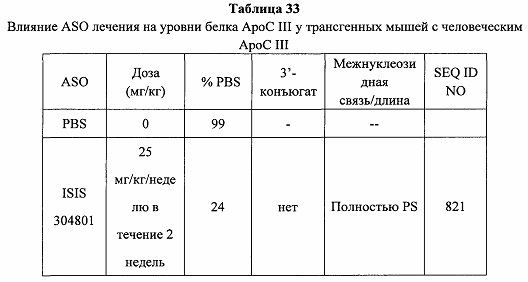
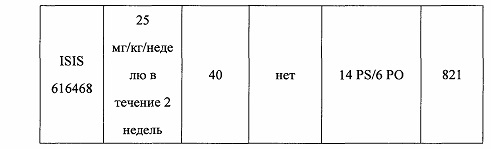
Пример 27: Соединение 56
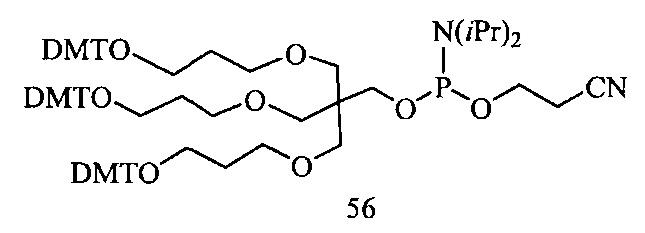
Соединение 56 имеется в продаже у компании Glen Research или может быть получено по опубликованным методикам, описанным авторами Shchepinov et al.. Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 28: Получение Соединения 60
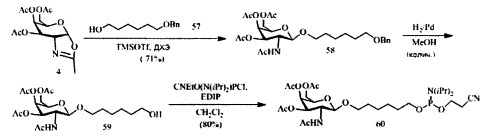
Соединение 4 получили по способам, представленным в Примере 2. Соединение 57 имеется в продаже. Соединение 60 подтвердили структурным анализом.
Соединение 57 является иллюстративным, и его не следует считать ограничивающим, поскольку могут быть использованы другие монозащищенные замещенные или незамещенные алкилдиолы, включая, но не ограничиваясь ими, те, которые представлены в данном описании, для получения фосфорамидитов, имеющих заданный состав.
Пример 29: Получение Соединения 63
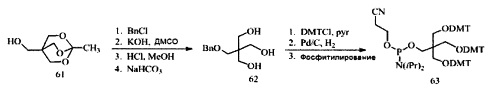
Соединения 61 и 62 получили по такому же способу, как описан в публикации Tober et al., Eur. J. Org. Chem., 2013, 3, 566-577; и Jiang et al., Tetrahedron, 2007, 63(19), 3982-3988.
Альтернативно, Соединение 63 получили по таким же способам, как описаны в научной и патентной литературе авторами Kim et al., Synlett, 2003, 12, 1838-1840; и Kim et al., в опубликованной международной заявке РСТ WO 2004063208.
Пример 30: Получение Соединения 63b
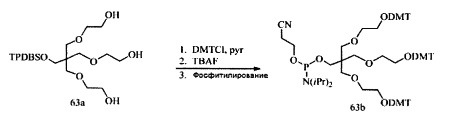
Соединение 63 а получили по таким же способам, как описаны авторами Hanessian et al., Canadian Journal of Chemistry, 1996, 74(9), 1731-1737.
Пример 31: Получение Соединения 63d
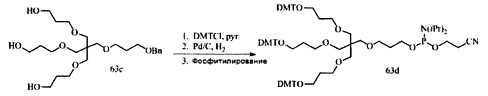
Соединение 63 с получили по таким же способам, как описаны авторами Chenet al., Chinese Chemical Letters, 1998, 9(5), 451-453.
Пример 32: Получение Соединения 67
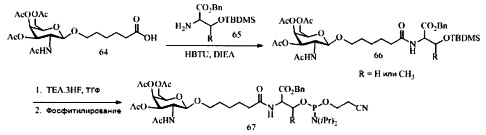
Соединение 64 получили по способам, представленным в Примере 2. Соединение 65 получили по таким же способам, как описаны авторами Or et al., в опубликованной международной заявке РСТ WO 2009003009. Защитные группы, использованные для Соединения 65, являются иллюстративным, и их не следует считать ограничением, поскольку могут быть использованы другие защитные группы, включая, но не ограничиваясь ими, те, которые представлены в данном описании.
Пример 33: Получение Соединения 70
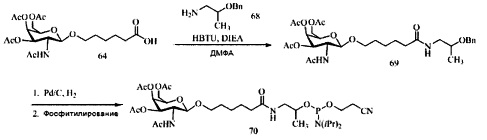
Соединение 64 получили по способам, представленным в Примере 2. Соединение 68 имеется в продаже. Защитная группа, использованная для Соединения 68, является иллюстративной, и ее не следует считать ограничением, поскольку могут быть использованы другие защитные группы, включая, но не ограничиваясь ими, те, которые представлены в данном описании.
Пример 34: Получение Соединения 75а
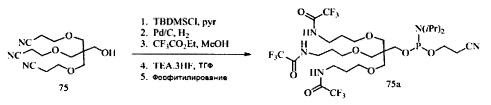
Соединение 75 получили по опубликованным способам, описанным авторами Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 35: Получение Соединения 79
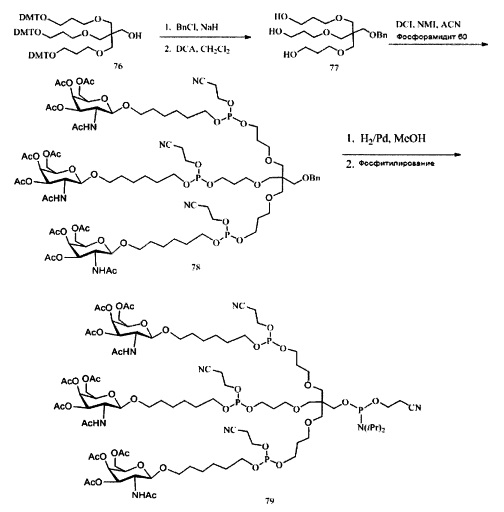
Соединение 76 получили по опубликованным способам, описанным авторами Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 36: Получение Соединения 79а
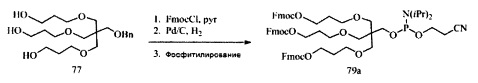
Соединение 77 получили по способам, представленным в Примере 35.
Пример 37: Общий способ получения сопряженного олигомерного соединения 82, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца, via твердой подложки (Способ I),
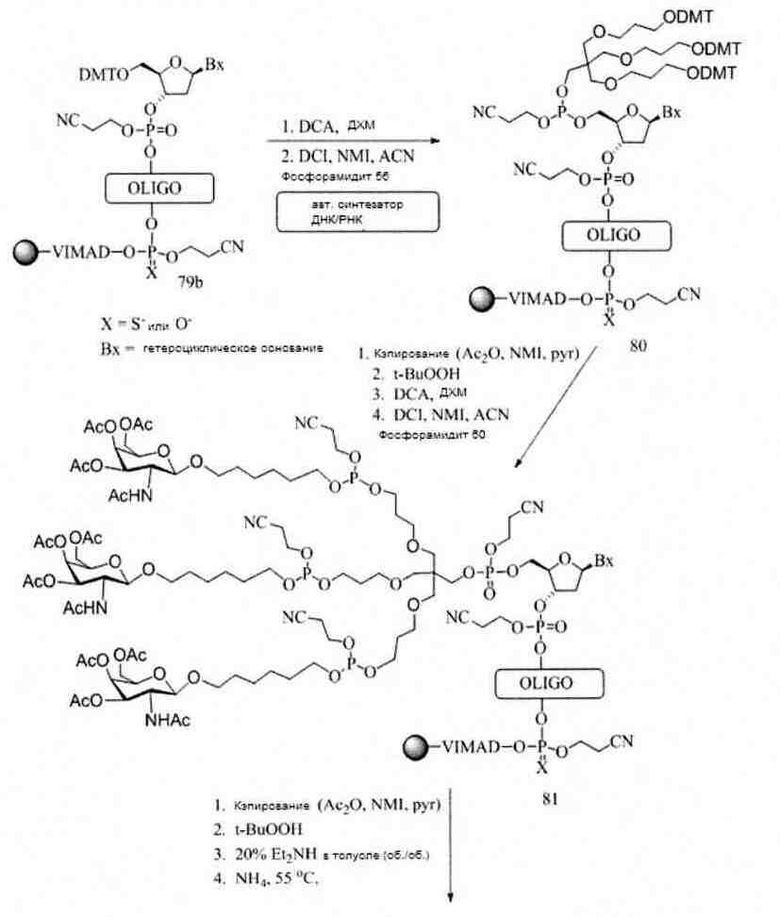
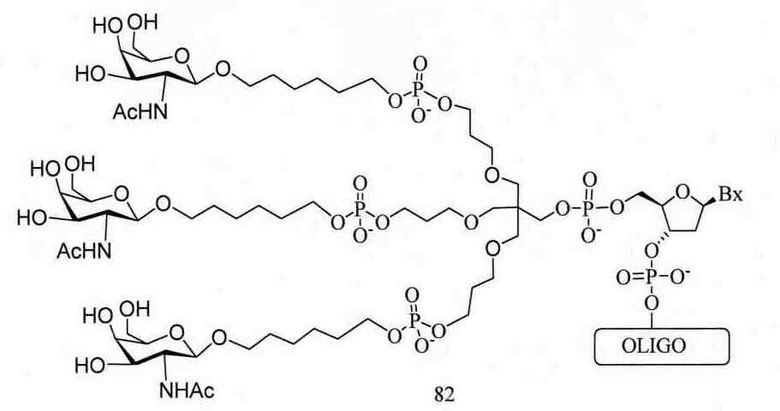
где GalNAc3-2 имеет структуру:
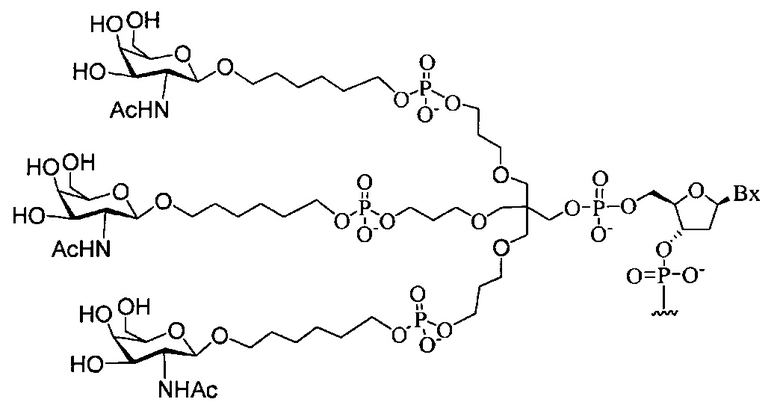
Кластерная часть GalNAc3 группы конъюгата GalNAc3-2 (GalNAc3-2a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Где GalNAc3-2a имеет формулу:
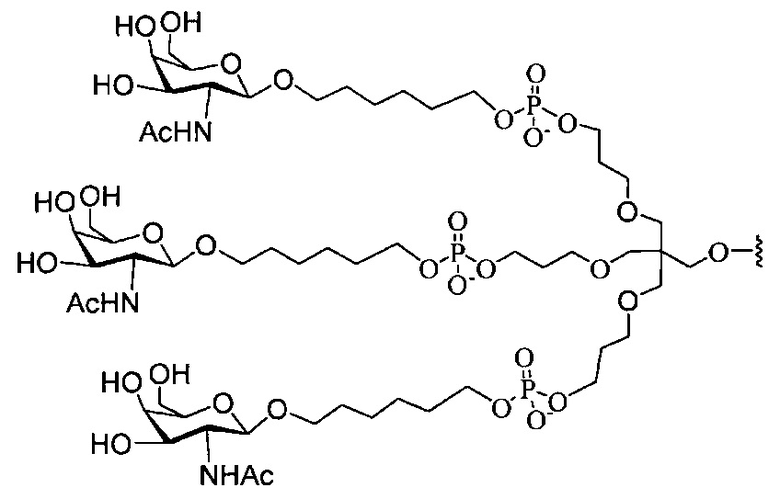
VIMAD-связанное олигомерное соединение 79b получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). Фосфорамидитные Соединения 56 и 60 получили так, как описано в способах в Примерах 27 и 28, соответственно. Изображенные фософорамидиты являются иллюстративными, и их не следует считать ограничением, поскольку могут быть использованы другие фосфорамидитные строительные блоки, включая, но не ограничиваясь ими, те, которые представлены в данном описании, для получения олигомерного соединения, содержащего фосфодиэфир-связанную группу конъюгата у 5'-конца. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 38: Альтернативный способ получения олигомерного соединения 82, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца (Способ II)
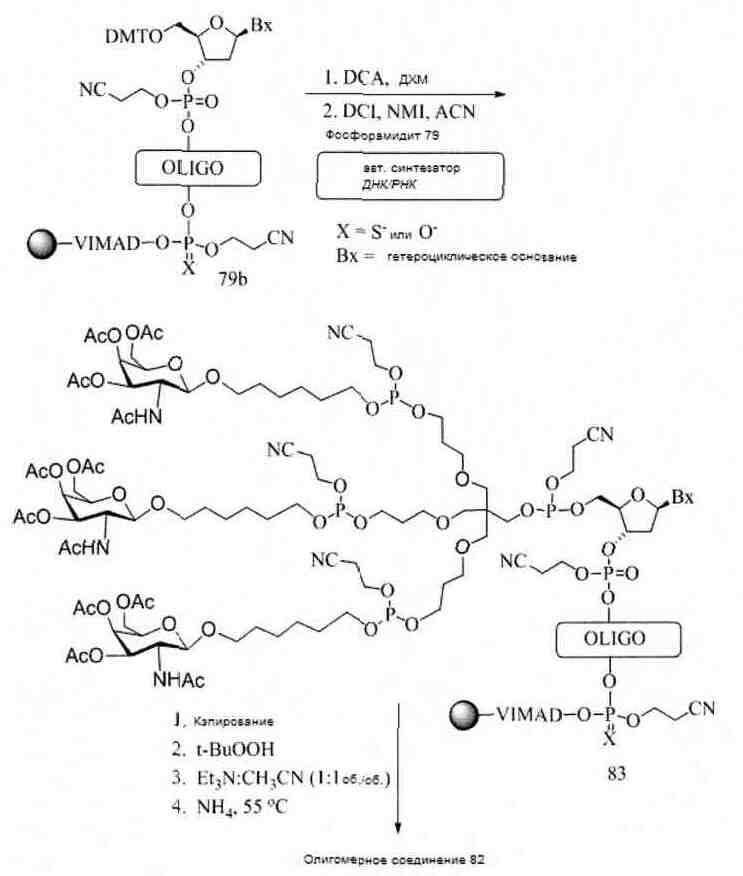
VIMAD-связанное олигомерное соединение 79b получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). GalNAc3-2-кластерный фосфорамидит, Соединение 79 получили по способам, представленным в Примере 35. Альтернативный способ обеспечивает возможность одностадийной установки фосфодиэфир-связанного GalNAc3-2 конъюгата на олигомерное соединение на последней стадии синтеза. Изображенные фософорамидиты являются иллюстративными, и их не следует считать ограничением, поскольку могут быть использованы другие фосфорамидитные строительные блоки, включая, но не ограничиваясь ими, те, которые представлены в данном описании, для получения олигомерных соединений, содержащих фосфодиэфирный конъюгат у 5'-конца. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 39: Общий способ получения олигомерного соединения 83h, содержащего конъюгат GalNAc3-3 у 5'-конца (GalNAc3-1, модифицированный для 5'-концевого присоединения), via твердой подложки.
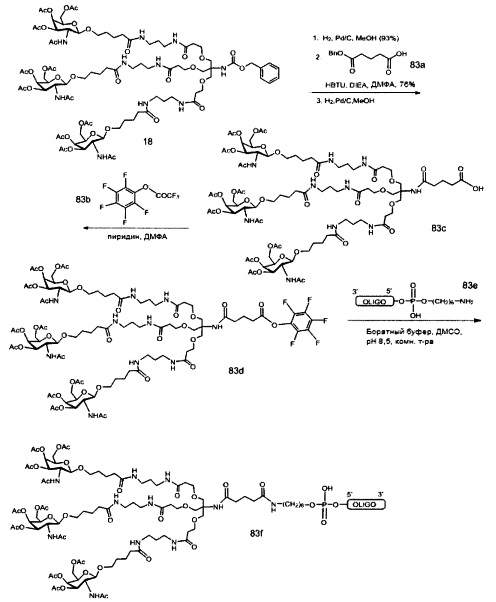
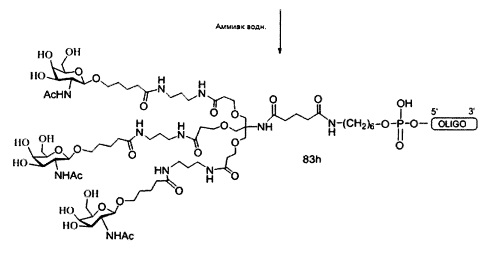
Соединение 18 получили по способам, представленным в Примере 4. Соединения 83а и 83b имеются в продаже. Олигомерное Соединение 83е, содержащее связанный через фосфодиэфир гексиламин, получили по стандартным способам синтеза олигонуклеотидов. В результате обработки защищенного олигомерного соединения водным раствором аммиака получили 5'-GalNAc3-3 сопряженное олигомерное соединение (83h).
Где GalNAc3-3 имеет структуру:
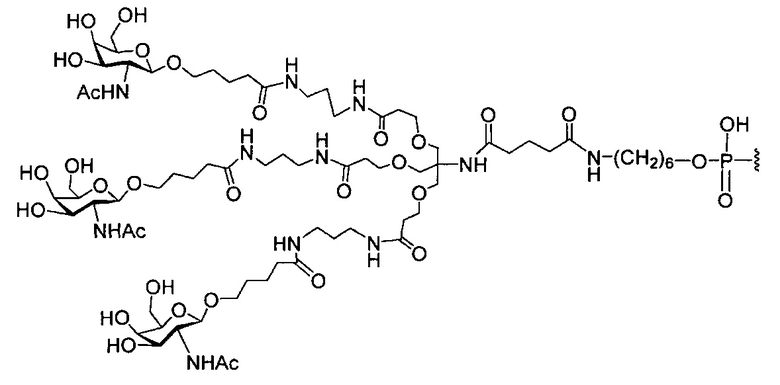 .
.
Кластерная часть GalNAc3 группы конъюгата GalNAc3-3 (GalNAc3-3a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Где GalNAc3-3a имеет формулу:
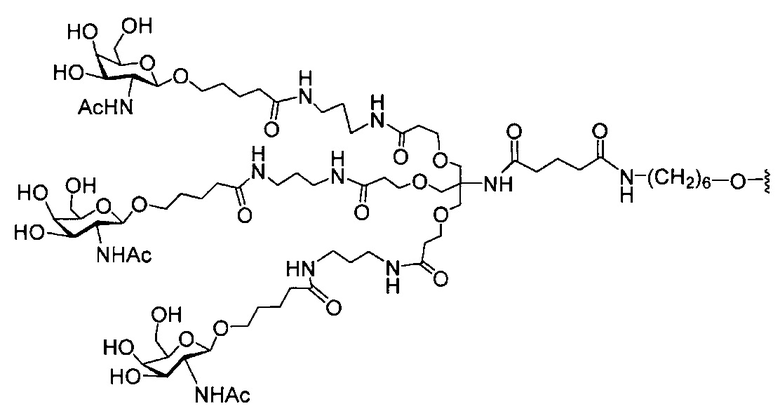 .
.
Пример 40: Общий способ получения олигомерного соединения 89, содержащего связанный фосфодиэфирным линкером GalNAc3-4 конъюгат у 3'-конца via твердой подложки
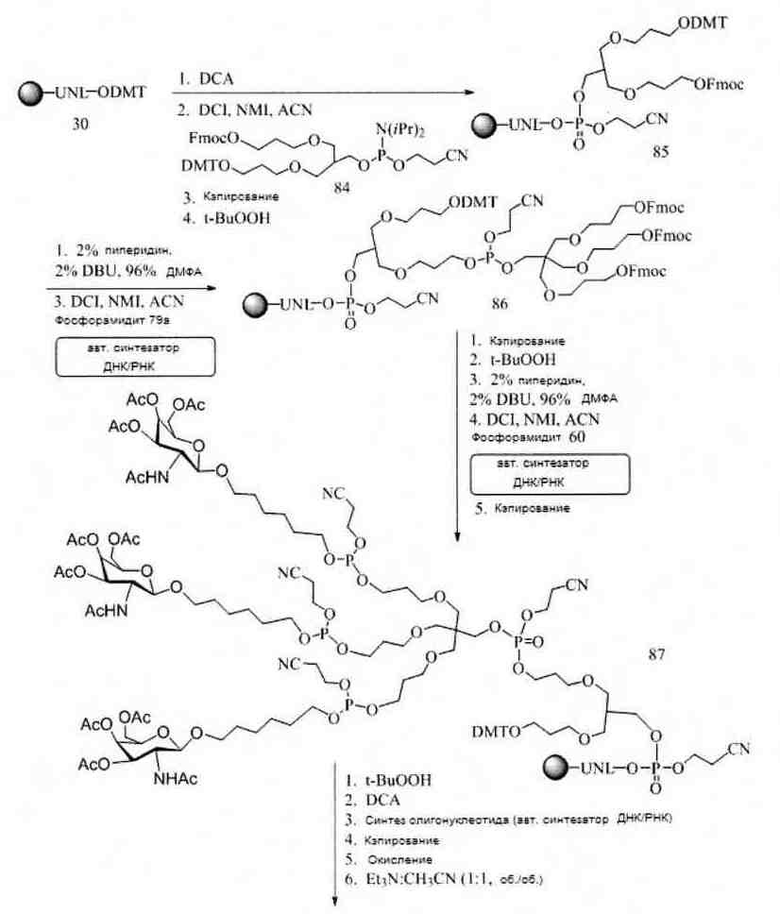
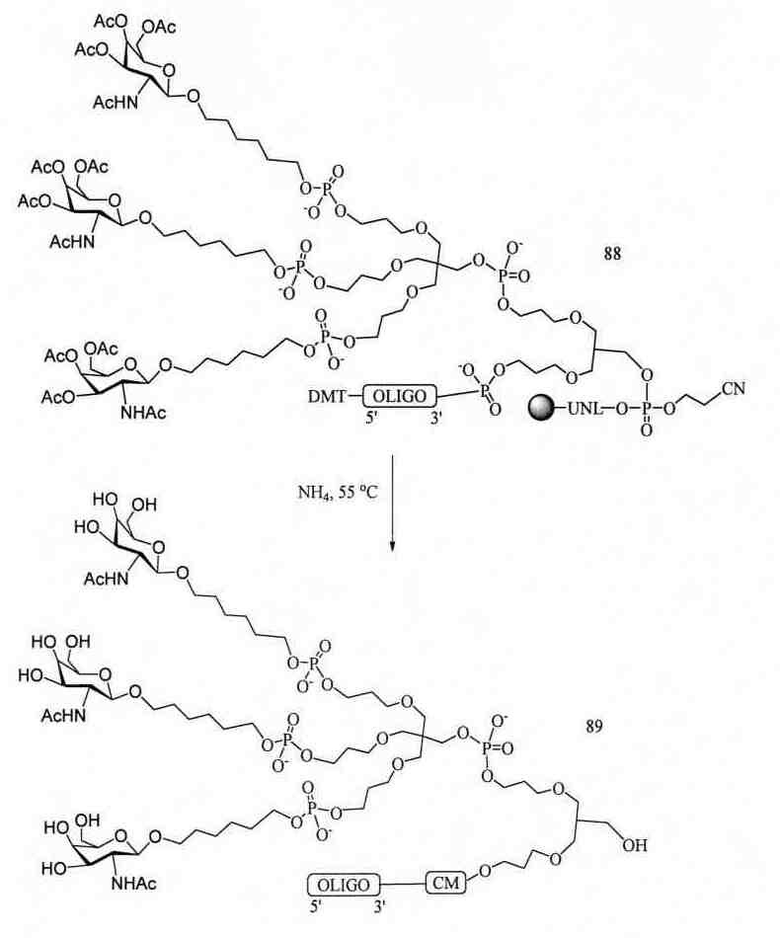
Где GalNAc3-4 имеет структуру:
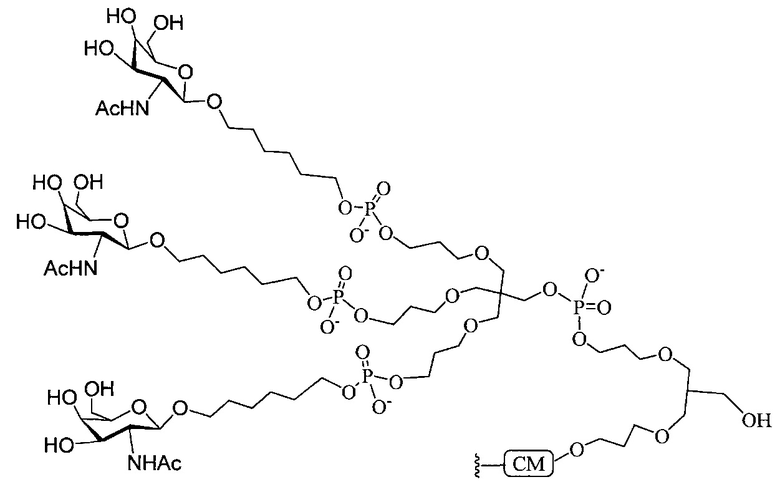
Где СМ представляет собой расщепляемый фрагмент. В некоторых вариантах реализации расщепляемый фрагмент представляет собой:
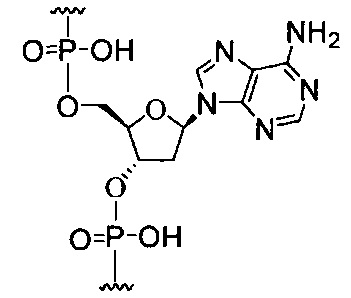
Кластерная часть GalNAc3 группы конъюгата GalNAc3-4 (GalNAc3-4a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Где GalNAc3-4a имеет формулу:
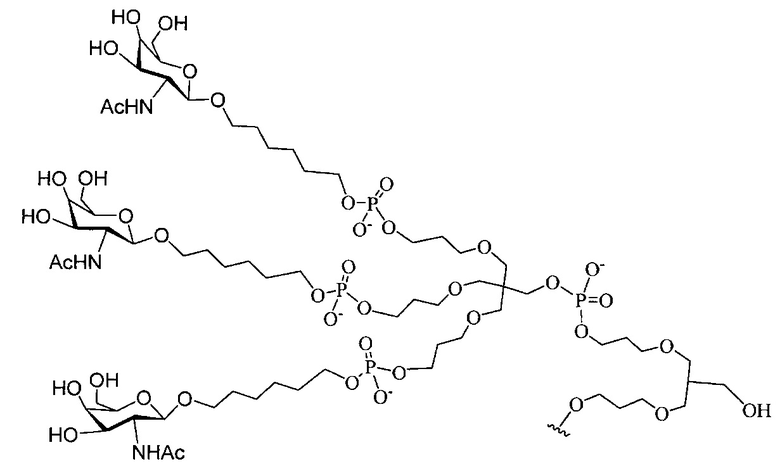
Защищенное Соединение 30 на функционализированной твердой подложке Unylinker имеется в продаже. Соединение 84 получили по таким же способам, как описаны в литературе (см. Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454; Shchepinov et al., Nucleic Acids Research, 1999, 27, 3035-3041; и Hornet et al., Nucleic Acids Research, 1997, 25, 4842-4849).
Фосфорамидитные строительные блоки, Соединения 60 и 79а, получили так, как описано в способах в примерах 28 и 36. Изображенные фосфорамидиты являются иллюстративными и не предназначены для ограничения, поскольку могут быть использованы другие фосфорамидитные строительные блоки для получения олигомерного соединения, имеющего фосфодиэфир-связанный конъюгат у 3'-конца и заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 41: Общий способ получения ASO, содержащих фосфодиэфир-связанный конъюгат GalNAc3-2 (см. Пример 37, Вх представляет собой аденин) в 5'-положении via твердофазному способу (получение ISIS 661134)
Если не указано иное, все реагенты и растворы, использованные для синтеза олигомерных соединений, приобретены у коммерческих поставщиков. Стандартные фосфорамидитные строительные блоки и твердую подложку использовали для внедрения нуклеозидных остатков, которые включают, например, остатки Т, A, G и mC. Фосфорамидитные соединения 56 и 60 использовали для синтеза фосфодиэфир-связанного конъюгата GalNAc3-2 у 5'-конца. 0,1 М раствор фосфорамидита в безводном ацетонитриле использовали для β-D-2'-дезоксирибонуклеозида и 2'-МОЕ.
Синтез антисмысловых олигонуклеотидов (ASO) выполнили на синтезаторе ABI 394 (в масштабе 1-2 мкмоль) или на синтезаторе АКТА Oligopilot производства GE Healthcare Bioscience (в масштабе 40-200 мкмоль) по способу фосфорамидитного связывания на твердой подложке VIMAD (110 мкмоль/г, Guzaev et al., 2003), упакованной в колонку. Для стадии связывания фосфорамидиты вводили в 4-кратном избытке по сравнению с исходной загрузкой на твердой подложке, а конденсацию фосфорамидита выполняли в течение 10 минут. Все остальные стадии выполняли по стандартным протоколам, предоставленным производителем. Для удаления диметокситритильных (DMT) групп с 5'-гидроксильных групп нуклеотида использовали 6 % раствор дихлоруксусной кислоты в толуоле. На стадии связывания в качестве активатора использовали 4,5-дицианоимидазол (0,7 М) в безводном CH3CN. Тиофосфатные связи внедряли сульфированием при помощи 0,1 М раствора гидрида ксантана в 1:1 смеси пиридина/CH3CN в течение 3 минут времени контакта. В качестве окислительного агента для получения фосфодиэфирных межнуклеозидных связей использовали 20% раствор трет-бутилгидропероксида в CH3CN, содержащий 6% воды, в течение 12 минут времени контакта.
После сборки требуемой последовательности цианоэтил-фосфатные защитные группы снимали при помощи 20% диэтиламина в толуоле (об./об.) в течение 45 минут времени контакта. Связанные с твердой подложкой ASO суспендировали в водном растворе аммиака (28-30 масс. %) и нагревали при 55°С в течение 6 часов.
Затем отфильтровывали не связанные ASO и выпаривали аммиак кипячением. Остаток очищали жидкостной хроматографией высокого давления на сильной анионообменной колонке (GE Healthcare Bioscience, Source 30Q, 30 мкм, 2,54×8 см, А=100 мМ ацетата аммония в 30% водном CH3CN, В=1,5 М NaBr в А, 0-40% В за 60 мин., скорость потока 14 мл.мин-1, λ=260 нм). Остаток обессоливали при помощи ВЭЖХ на обращенно-фазовой колонке с получением заданных ASO с выделенным выходом 15-30% относительно первоначальной загрузки на твердую подложку. ASO характеризовали при помощи ион-парной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «о'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура GalNAc3-2a показана в Примере 37.
Пример 42: Общий способ получения ASO, содержащих конъюгат GalNAc3-3 в 5'-положении, via твердофазным методикам (получение ISIS 661166)
Синтез ISIS 661166 выполнили по таким же способам, как представлены в Примерах 39 и 41.
ISIS 661166 представляет собой 5-10-5 МОЕ гэпмер, в котором 5'-положение содержит конъюгат GalNAc3-3. Это ASO характеризовали при помощи ион-парной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатные межнуклеозидные линкеры (PS); «о» означает фосфодиэфирные межнуклеозидные линкеры (РО); и «о'» означает ОР(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура «5'-GalNAc3-3a» показана в Примере 39.
Пример 43: Дозозависимое исследование фосфодиэфир-связанного GalNAc3-2 (см. Примеры 37 и 41, Вх представляет собой аденин) у 5'-конца, направленного на SRB-1, in vivo
ISIS 661134 (см. Пример 41), содержащий фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца, испытывали в дозозависимом исследовании на антисмысловое ингибирование SRB-1 у мышей. Несопряженные ISIS 440762 и 651900 (конъюгат (GalNAc3-1 у 3'-конца, см. Пример 9) включены в исследование для сравнения и описаны ранее в Таблице 17.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 440762, 651900, 661134 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». ED50 измеряли по таким же способам, как описаны ранее, и указанные значения представлены ниже.
Как показано в Таблице 35, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца (ISIS 661134) или конъюгат GalNAc3-1, связанный у 3'-конца (ISIS 651900), демонстрируют значительное улучшение эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 440762). Кроме того, ISIS 661134, который содержит фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца, был настолько же эффективным, как ISIS 651900, который содержит конъюгат GalNAc3-1 у 3'-конца.
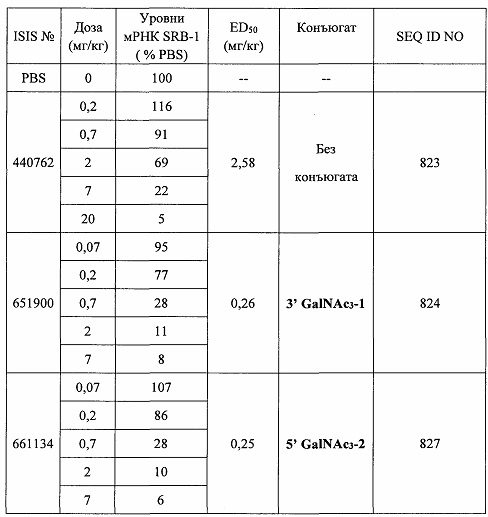
Структуры 3' GalNAc3-1 и 5' GalNAc3-2 описаны ранее в Примерах 9 и 37.
Фармакокинетический анализ (ФК)
ФК для ASO из группы высокой дозы (7 мг/кг) исследовали и оценили таким же образом, как описано в Примере 20. Образцы печени измельчили и экстрагировали по стандартным протоколам. Идентифицировали метаболиты полной длины 661134 (5' GalNAc3-2) и ISIS 651900 (3' GalNAc3-1) и подтвердили их массы при помощи масс-спектрометрического анализа высокого разрешения. Результаты показали, что основной метаболит, обнаруженный для ASO, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 у 5'-конца (ISIS 661134), представлял собой ISIS 440762 (данные не показаны). Не наблюдали никаких дополнительных метаболитов в обнаруживаемом количестве. В отличие от него, для ASO, содержащего конъюгат GalNAc3-1 у 3'-конца (ISIS 651900), наблюдали дополнительные метаболиты, аналогичные тем, которые описаны ранее в Таблице 23а. Эти результаты позволяют предположить, что наличие фосфодиэфир-связанного конъюгата GalNAc3-1 или GalNAc3-2 может улучшать ФК профиль ASO без ухудшения их эффективности.
Пример 44: Влияние PO/PS линкеров на антисмысловое ингибирование ASO, содержащих конъюгат GalNAc3-1 (см. Пример 9) у 3'-конца, направленных на SRB-1
ISIS 655861 и 655862, содержащие конъюгат GalNAc3-1 у 3'-конца, каждый из которых направлен на SRB-1, испытали в исследовании однократного введения на их способность ингибировать SRB-1 у мышей. Исходное несопряженное соединение, ISIS 353382, включили в исследование для сравнения.
Эти ASO представляют собой 5-10-5 МОЕ гэпмеры, в которых гэп-область содержит десять 2'-дезоксирибонуклеозидов, и каждая область крыльев содержит пять 2'-МОЕ модифицированных нуклеозидов. Эти ASO получили по таким же способам, как показаны ранее в Примере 19, и они описаны ниже в Таблице 36.


Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатные межнуклеозидные линкеры (PS); «о» означает фосфодиэфирные межнуклеозидные линкеры (РО); и «о'» означает ОР(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура «GalNAc3-1» показана в Примере 9.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 353382, 655861, 655862 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». ED50 измеряли по таким же способам, как описаны ранее, и указанные значения представлены ниже.
Как показано в Таблице 37, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом, по сравнению с контрольным образцом, обработанным PBS. Действительно, антисмысловые олигонуклеотиды, содержащие конъюгат GalNAc3-1 у 3'-конца (ISIS 655861 и 655862), демонстрируют значительное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 353382). Кроме того, ISIS 655862 со смешанными PS/PO линкерами демонстрирует усиление эффективности, по сравнению с соединением, содержащим только PS (ISIS 655861).

Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также массу органов. Результаты показывают, что не наблюдали какого-либо увеличения уровней трансаминазы (Таблица 38) или массы органов (данные не показаны) у мышей, обработанных ASO, по сравнению с PBS контролем. Кроме того, ASO со смешанными PS/PO линкерами (ISIS 655862) демонстрирует схожие уровни трансаминазы, по сравнению с соединением, содержащим только PS (ISIS 655861).
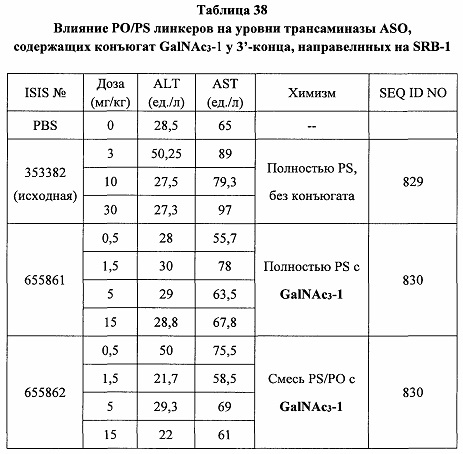
Пример 45: Получение PFP эфира, Соединения 110а
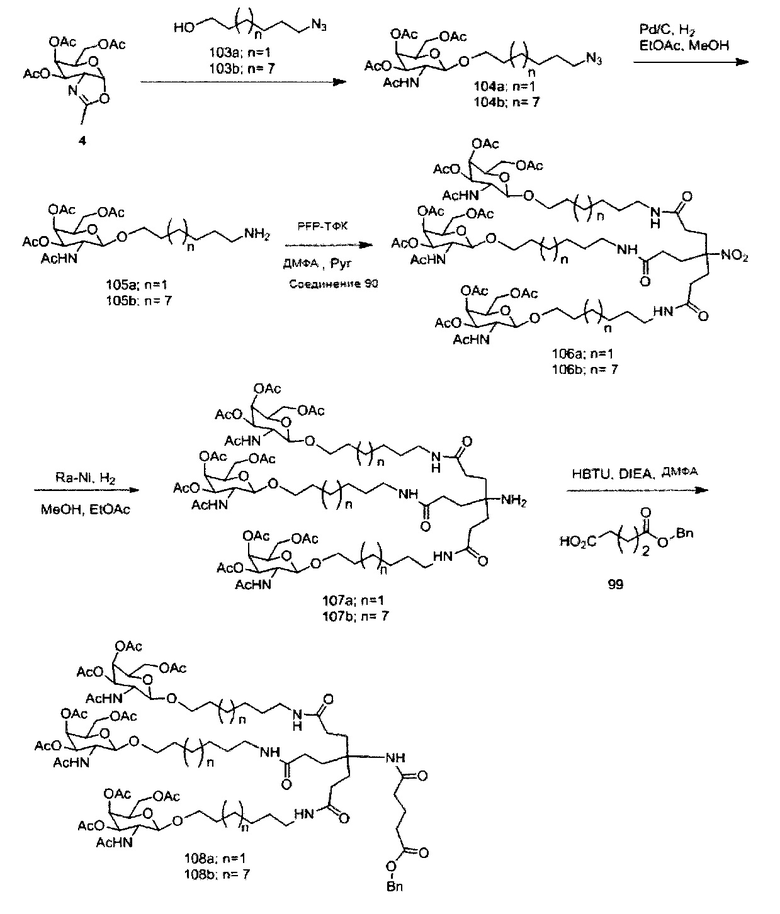
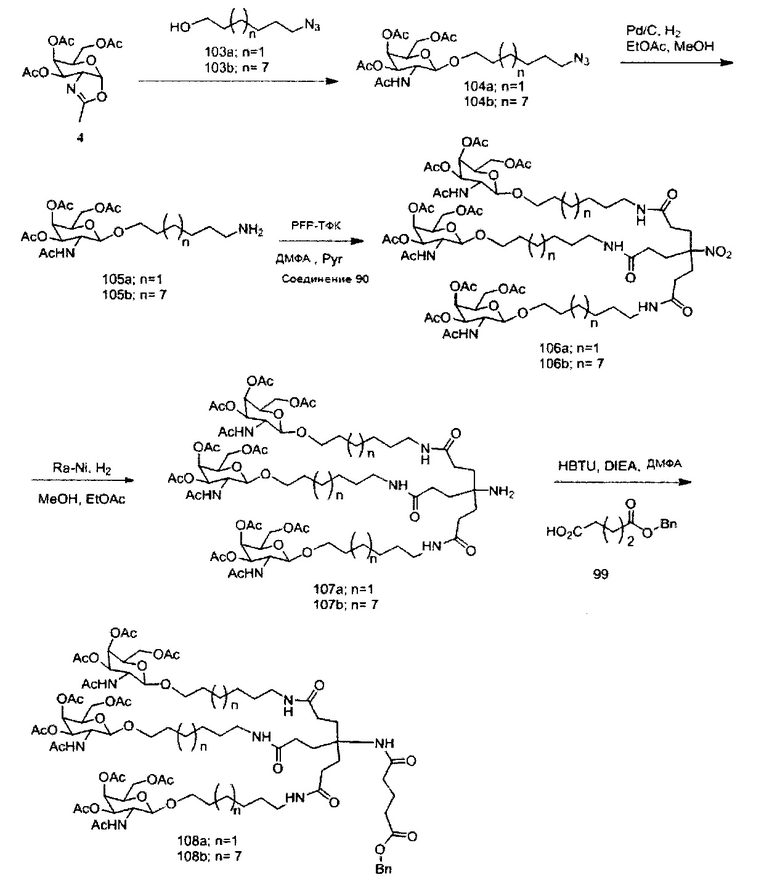
Соединение 4 (9,5 г, 28,8 ммоль) обработали по отдельности соединением 103а или 103b (38 ммоль) и TMSOTf (0,5 экв.), и молекулярными ситами в дихлорметане (200 мл), и перемешивали в течение 16 часов при комнатной температуре. Затем органический слой отфильтровали через целит, затем промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->10% метанол/дихлорметан) с получением соединений 104а и 104b с выходом >80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 104а и 104b обработали в тех же условиях, что и соединения 100a-d (Пример 47), с получением соединений 105а и 105b с выходом >90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 105а и 105b по отдельности обработали соединением 90 при тех же условиях, что и соединения 901a-d, с получением соединений 106а (80%) и 106b (20%). Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 106а и 106b обработали в тех же условиях, что и соединения 96a-d (Пример 47), с получением соединения 107а (60%) и 107b (20%). Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 107а и 107b обработали в тех же условиях, что и соединения 97a-d (Пример 47), с получением соединений 108а and 108b с выходом 40-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 108а (60%) и 108b (40%) обработали в тех же условиях, что и соединения 100a-d (Пример 47), с получением соединений 109а и 109b с выходом >80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 109а обработали в тех же условиях, что и соединения 101a-d (Пример 47), с получением соединения 110а с выходом 30-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой. Альтернативно, Соединение 110b может быть получено таким же образом, исходя из Соединения 109b.
Пример 46: Общий способ сопряжения с PFP эфирами (олигонуклеотид 111); получение ISIS 666881 (GalNAc3-10)
Синтезировали и очистили 5'-гексиламино-модифицированный олигонуклеотид по стандартным способам твердофазного получения олигонуклеотидов. 5'-Гексиламино-модифицированный олигонуклеотид растворили в 0,1 М растворе тетрабората натрия, рН 8,5 (200 мкл) и добавили 3 эквивалента выбранного PFP-эстерифицированного кластера GalNAc3, растворенного в ДМСО (50 мкл). Если при добавлении раствора ASO эфир PFP выпадал в осадок, то добавляли ДМСО до перехода всего эфира PFP в раствор. Реакция была завершена примерно через 16 часов перемешивания при комнатной температуре. Полученный раствор разбавили водой до 12 мл, а затем центрифугировали при 3000 об./мин. в центробежном фильтре с отсечением по массе 3000 Да. Этот прием повторили два раза для удаления низкомолекулярных примесей. Затем раствор лиофилизировали досуха и повторно растворили в концентрированном водном растворе аммиака, и перемешивали при комнатной температуре в течение 2,5 часов, затем концентрировали in vacua для удаления большей части аммиака. Сопряженный олигонуклеотид очистили и обессолили при помощи ОФ-ВЭЖХ, и лиофилизировали с получением GalNAc3 сопряженного олигонуклеотида.
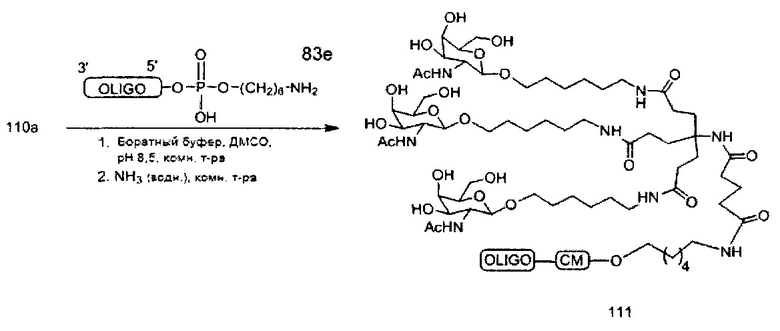
Олигонуклеотид 111 сопряжен с GalNAc3-10. Кластерная часть GalNAc3 группы конъюгата GalNAc3-10 (GalNAc3-10a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-, как показано ниже в олигонуклеотиде (ISIS 666881), синтезированном с GalNAc3-10. Структура GalNAc3-10 (GalNAc3-10a-CM-) представлена ниже:
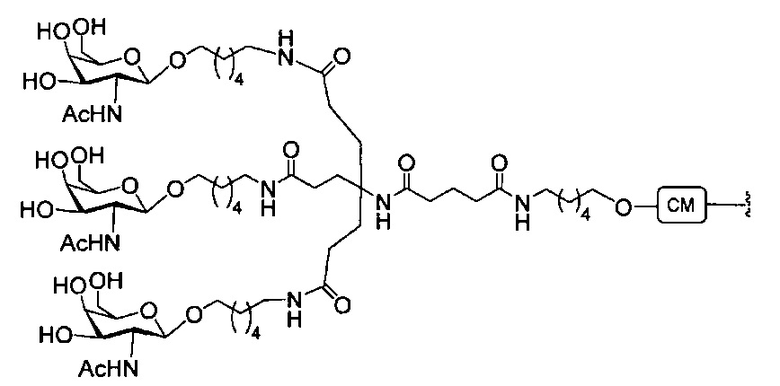
По указанному общему способу получили ISIS 666881. Синтезировали и очистили 5'-гексиламино-модифицированный олигонуклеотид, ISIS 660254, по стандартным способам твердофазного получения олигонуклеотидов. ISIS 660254 (40 мг, 5,2 мкмоль) растворили в 0,1 М растворе тетрабората натрия, рН 8,5 (200 мкл) и добавили 3 эквивалента PFP эфира (Соединения 110а), растворенного в ДМСО (50 мкл). Эфир PFP выпал в осадок при добавлении раствора ASO, поэтому потребовалось добавление дополнительного количества ДМСО (600 мкл) для полного растворения PFP эфира. Реакция была завершена через 16 часов перемешивания при комнатной температуре. Раствор разбавили водой до общего объема 12 мл, а затем центрифугировали при 3000 об./мин. в центробежном фильтре с отсечением по массе 3000 Да. Этот прием повторили два раза для удаления низкомолекулярных примесей. Раствор лиофилизировали досуха и повторно растворили в концентрированном водном растворе аммиака, перемешивая при комнатной температуре в течение 2,5 часов, затем концентрировали in vacuo для удаления большей части аммиака. Сопряженный олигонуклеотид очистили и обессолили при помощи ОФ-ВЭЖХ, и лиофилизировали с получением ISIS 666881 с выходом 90% по массе (42 мг, 4,7 мкмоль).
GalNAc3-10-сопряженный олигонуклеотид
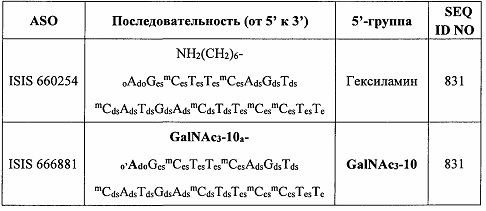
Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а "С означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Пример 47: Получение олигонуклеотида 102, содержащего GalNAc3-8
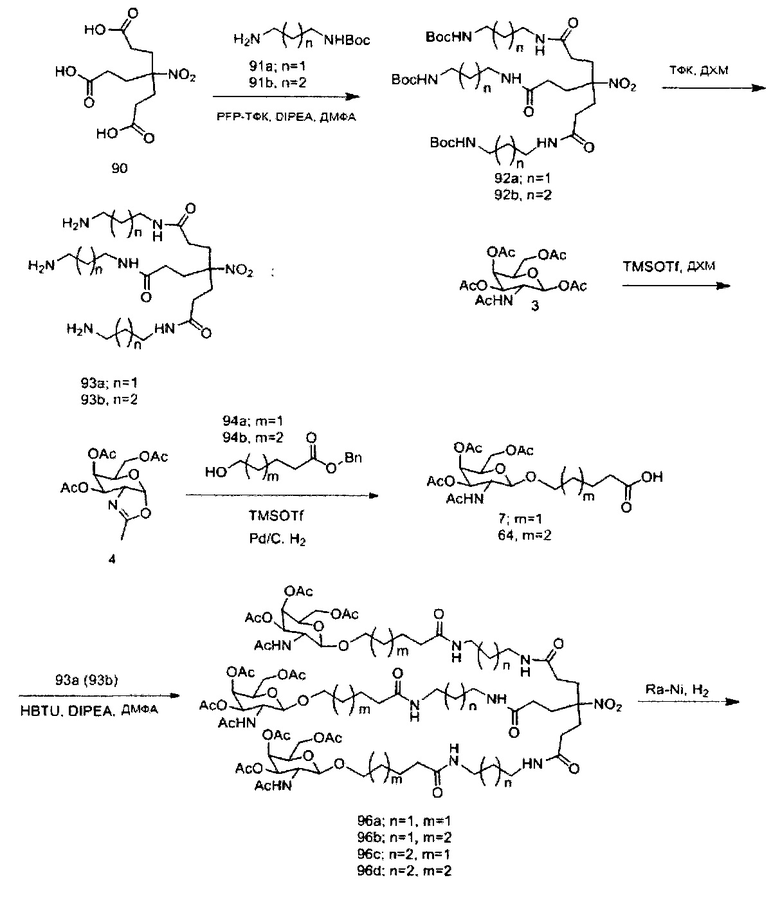
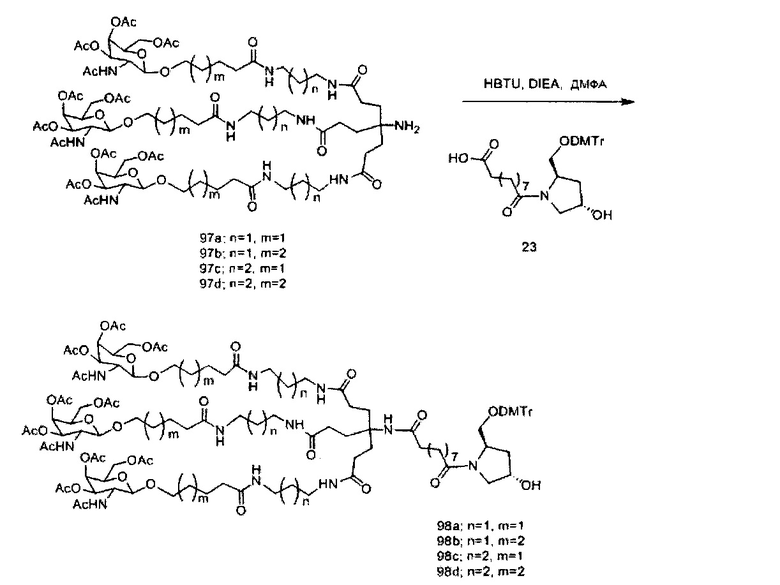
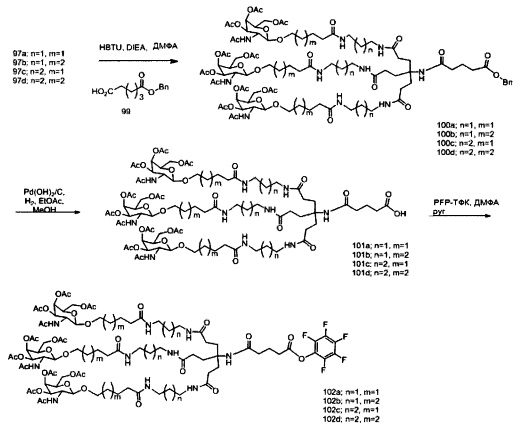
Трехкислотное соединение 90 (4 г, 14,43 ммоль) растворили в ДМФА (120 мл) и N,N-диизопропилэтиламине (12,35 мл, 72 ммоль). По каплям добавили пентафторфенила трифторацетат (8,9 мл, 52 ммоль) в атмосфере аргона и оставили реакционную смесь перемешиваться при комнатной температуре в течение 30 минут. Добавили Вос-диамин 91 а или 91b (68,87 ммоль) вместе с N,N-диизопропилэтиламином (12,35 мл, 72 ммоль) и оставили реакционную смесь перемешиваться при комнатной температуре в течение 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->10% метанол/дихлорметан) с получением соединений 92а и 92b с приблизительным выходом 80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 92а или 92b (6,7 ммоль) обрабатывали 20 мл дихлорметана и 20 мл трифторуксусной кислоты при комнатной температуре в течение 16 часов. Полученный раствор выпарили, а затем растворили в метаноле и обрабатывали смолой DOWEX-OH в течение 30 минут. Полученный раствор отфильтровали и упарили до маслянистого вещества при пониженном давлении с получением 85-90% выхода соединений 93а и 93b.
Соединения 7 или 64 (9,6 ммоль) обрабатывали HBTU (3,7 г, 9,6 ммоль) и N,N-диизопропилэтиламином (5 мл) в ДМФА (20 мл) в течение 15 минут. К смеси добавили либо соединение 93а, либо 93b (3 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (5%-->20% метанол/дихлорметан) с получением соединений 96a-d с выходом 20-40%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 96a-d (0,75 ммоль) по отдельности гидрировали на никеле Ренея в течение 3 часов в этаноле (75 мл). Затем катализатор удалили фильтрованием через целит, а этанол удалили при пониженном давлении с получением соединений 97a-d с выходом 80-90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 23 (0,32 г, 0,53 ммоль) обрабатывали HBTU (0,2 г, 0,53 ммоль) и N,N-диизопропилэтиламином (0,19 мл, 1,14 ммоль) в ДМФА (30 мл) в течение 15 минут. К смеси по отдельности добавили соединения 97a-d (0,38 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->20% метанол/дихлорметан) с получением соединений 98a-d с выходом 30-40%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 99 (0,17 г, 0,76 ммоль) обрабатывали HBTU (0,29 г, 0,76 ммоль) и N,N-диизопропилэтиламином (0,35 мл, 2,0 ммоль) в ДМФА (50 мл) в течение 15 минут. К смеси по отдельности добавили соединения 97a-d (0,38 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (5%-->20% метанол/дихлорметан) с получением соединений 100a-d с выходом 40-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 100a-d (0,16 ммоль) по отдельности гидрировали на 10% Pd(OH)2/C в течение 3 часов в метаноле/этилацетате (1:1, 50 мл). Затем катализатор удалили фильтрованием через целит, а органические растворители удалили при пониженном давлении с получением соединений 101a-d с выходом 80-90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 101a-d (0,15 ммоль) по отдельности растворили в ДМФА (15 мл) и пиридине (0,016 мл, 0,2 ммоль). По каплям добавили пентафторфенила трифторацетат (0,034 мл, 0,2 ммоль) в атмосфере аргона и оставили реакционную смесь перемешиваться при комнатной температуре в течение 30 минут. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->5% метанол/дихлорметан) с получением соединений 102a-d с приблизительным выходом 80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
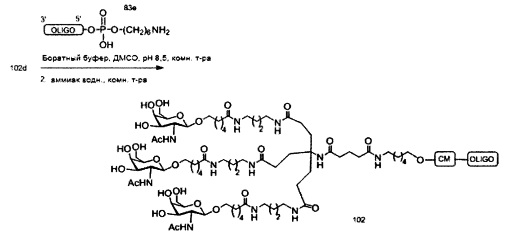
Олигомерное соединение 160, содержащее группу конъюгата GalNAc3-8, получили по стандартным способам синтеза олигонуклеотидов. Кластерная часть GalNAc3 группы конъюгата GalNAc3-8 (GalNAc3-8a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В предпочтительном варианте реализации расщепляемый фрагмент представляет собой-Р(=O)(ОН)-Ad-Р(=O)(ОН)-.
Структура GalNAc3-8 (GalNAc3-8a-CM-) представлена ниже:
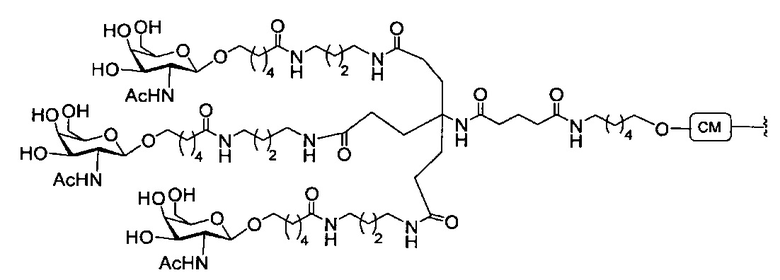 .
.
Пример 48: Получение олигонуклеотида 119, содержащего GalNAc3-7
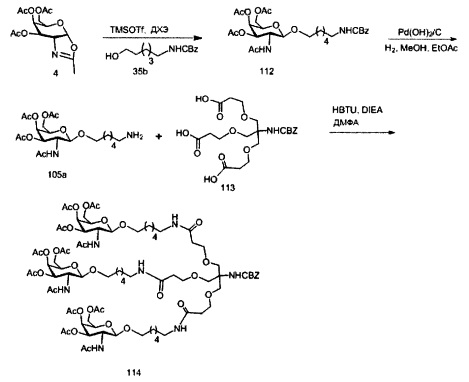
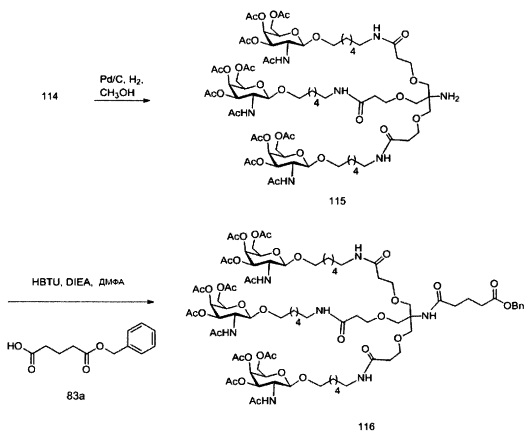
Соединение 112 синтезировали по способу, описанному в литературе (J. Med. Chem. 2004, 47, 5798-5808).
Соединение 112 (5 г, 8,6 ммоль) растворили в 1:1 смеси метанола/этилацетата (22 мл/22 мл). Добавили гидроксид палладия на углероде (0,5 г). Реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь отфильтровали через слой целита и промыли этот слой 1:1 смесью метанола/этилацетата. Фильтрат и промывочные растворы объединили и концентрировали досуха с получением Соединения 105а (количественно). Структуру подтвердили по ЖХМС.
Соединение 113 (1,25 г, 2,7 ммоль), HBTU (3,2 г, 8,4 ммоль) и DIEA (2,8 мл, 16,2 ммоль) растворили в безводном ДМФА (17 мл) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К этой смеси добавили раствор Соединения 105а (3,77 г, 8,4 ммоль) в безводном ДМФА (20 мл). Реакционную смесь перемешивали при комнатной температуре в течение 6 часов. Растворитель удалили при пониженном давлении с получением маслянистого вещества. Остаток растворили в CH2Cl2 (100 мл) и промыли насыщенным водным раствором NaHCO3 (100 мл) и насыщенным солевым раствором (100 мл). Органическую фазу отделили, высушили (Na2SO4), отфильтровали и выпарили. Остаток очистили силикагелевой колоночной хроматографией и элюировали от 10 до 20% МеОН в дихлорметане с получением Соединения 114 (1,45 г, 30%). Структуру подтвердили анализом ЖХМС и 1Н ЯМР.
Соединение 114 (1,43 г, 0,8 ммоль) растворили в 1:1 смеси метанола/этилацетата (4 мл/4 мл). Добавили палладий на углероде (влажный, 0,14 г). Реакционную смесь продували водородом и перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь фильтровали через слой целита. Слой целита промыли метанолом/этилацетатом (1:1). Фильтрат и промывочные растворы объединили и выпарили при пониженном давлении с получением Соединения 115 (количественно). Структуру подтвердили анализом ЖХМС и 1H ЯМР.
Соединение 83а (0,17 г, 0,75 ммоль), HBTU (0,31 г, 0,83 ммоль) и DIEA (0,26 мл, 1,5 ммоль) растворили в безводном ДМФА (5 мл) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К этой смеси добавили раствор Соединения 115 (1,22 г, 0,75 ммоль) в безводном ДМФА и перемешивали реакционную смесь при комнатной температуре в течение 6 часов. Растворитель удалили при пониженном давлении, а остаток растворили в CH2Cl2. Органический слой промыли насыщенным водным раствором NaHCO3 и насыщенным солевым раствором, и высушили над безводным Na2SO4, и отфильтровали. Органический слой концентрировали досуха, а полученный остаток очистили силикагелевой колоночной хроматографией и элюировали от 3 до 15% МеОН в дихлорметане с получением Соединения 116 (0,84 г, 61%). Структуру подтвердили анализом ЖХМС и 1Н ЯМР.
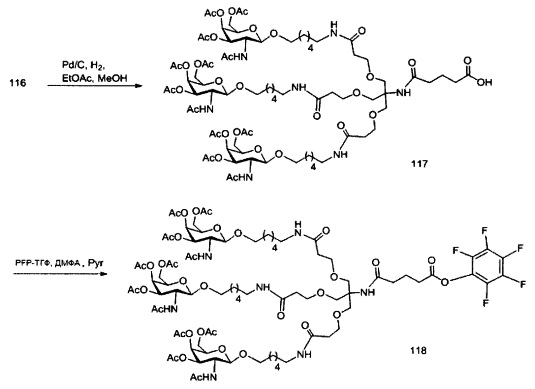
Соединение 116 (0,74 г, 0,4 ммоль) растворили в 1:1 смеси метанола/этилацетата (5 мл/5 мл). Добавили палладий на углероде (влажный, 0,074 г). Реакционную смесь продували водородом и перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь фильтровали через слой целита. Слой целита промыли метанолом/этилацетатом (1:1). Фильтрат и промывочные растворы объединили и выпарили при пониженном давлении с получением соединения 117 (0,73 г, 98%). Структуру подтвердили анализом ЖХМС и 1H ЯМР.
Соединение 117 (0,63 г, 0,36 ммоль) растворили в безводном ДМФА (3 мл). К этому раствору добавили N,N-диизопропилэтиламин (70 мкл, 0,4 ммоль) и пентафторфенила трифторацетат (72 мкл, 0,42 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 12 часов и вылили в насыщенный водный раствор NaHCO3. Смесь экстрагировали дихлорметаном, промыли насыщенным солевым раствором и высушили над безводным Na2SO4. Дихлорметановый раствор концентрировали досуха и очистили силикагелевой колоночной хроматографией, и элюировали от 5 до 10% МеОН в дихлорметане с получением соединения 118 (0,51 г, 79%). Структуру подтвердили анализом ЖХМС и 1Н и 1Н и 19F ЯМР.
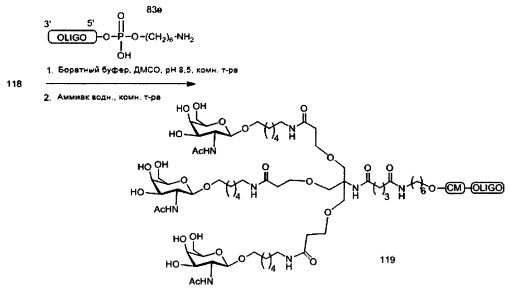
Олигомерное соединение 119, содержащее группу конъюгата GalNAc3-7, получили по общим способам, представленным в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-7 (GalNAc3-7a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc3-7 (GalNAc3-7a-CM-) представлена ниже:
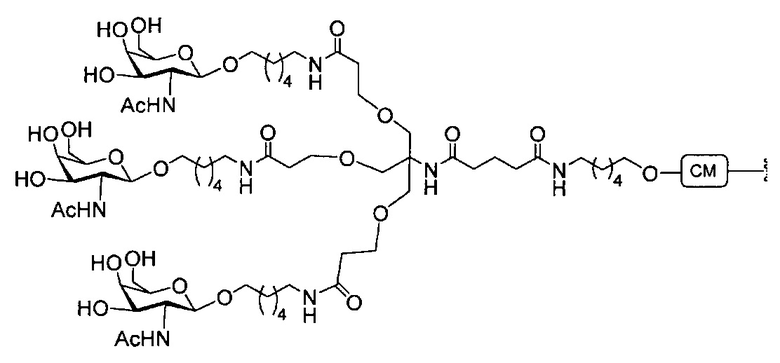 .
.
Пример 49: Получение олигонуклеотида 132, содержащего GalNAc3-5
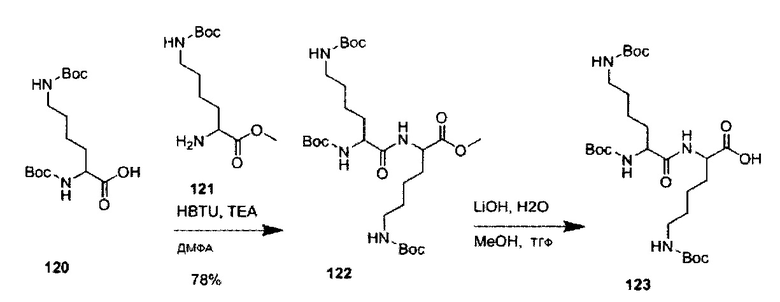
Соединение 120 (14,01 г, 40 ммоль) и HBTU (14,06 г, 37 ммоль) растворили в безводном ДМФА (80 мл). Добавили триэтиламин (11,2 мл, 80,35 ммоль) и перемешивали в течение 5 минут. Реакционную смесь охладили на ледяной бане и добавили раствор соединения 121 (10 г, ммоль) в безводном ДМФА (20 мл). Добавили дополнительное количество триэтиламина (4,5 мл, 32,28 ммоль) и перемешивали реакционную смесь в течение 18 часов в атмосфере аргона. Реакцию контролировали по ТСХ (этилацетат : гексан; 1:1; Rf=0,47). Растворитель удалили при пониженном давлении. Остаток растворили в EtOAc (300 мл) и промыли 1 М раствором NaHSO4 (3×150 мл), насыщенным водным раствором NaHCO3 (3×150 мл) и насыщенным солевым раствором (2×100 мл). Органический слой высушили над Na2SO4. Высушивающий агент удалили фильтрованием, а органический слой концентрировали на ротационном испарителе. Неочищенную смесь очистили силикагелевой колоночной хроматографией и элюировали при помощи 35-50% EtOAc в гексане с получением соединения 122 (15,50 г, 78,13%). Структуру подтвердили анализом ЖХМС и 1Н ЯМР. Масса m/z 589,3 [М+Н]+.
К охлажденному раствору соединения 122 (7,75 г, 13,16 ммоль), растворенного в метаноле (15 мл), добавили раствор LiOH (92,15 ммоль) в воде (20 мл) и ТГФ (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 45 минут и контролировали по ТСХ (EtOAc : гексан; 1:1). Реакционную смесь концентрировали до половины объема при пониженном давлении. Оставшийся раствор охладили на ледяной бане и нейтрализовали добавлением концентрированной HCl. Реакционную смесь разбавили, экстрагировали EtOAc (120 мл) и промыли насыщенным солевым раствором (100 мл). При стоянии в течение ночи образовалась и осветлилась эмульсия. Органический слой отделили, высушили (Na2SO4), отфильтровали и выпарили с получением Соединения 123 (8,42 г). Избыточную массу вероятно обусловливает остаточная соль. ЖХМС согласовался со структурой. Продукт использовали без какой-либо дополнительной очистки. Мол. масса, расчетная: 574,36; мол. масса, найденная: 575,3 [М+Н]+.
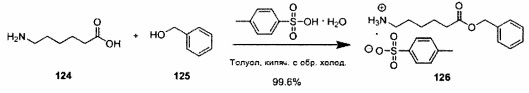
Соединение 126 синтезировали по способу, описанному в литературе (J. Am. Chem. Soc. 2011, 133, 958-963).
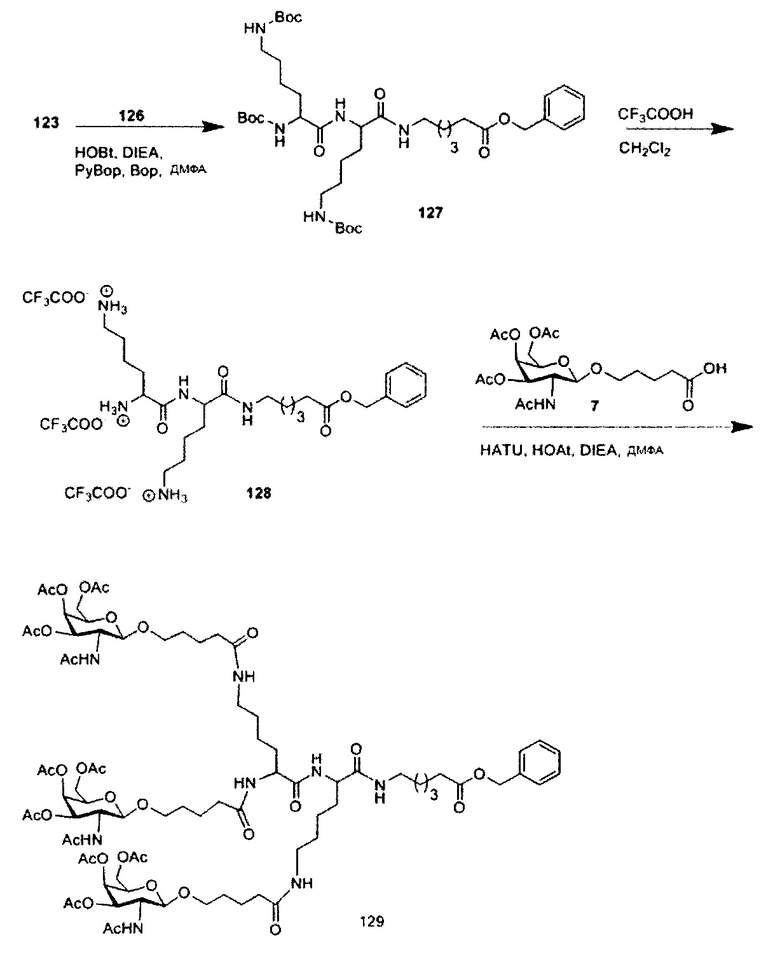
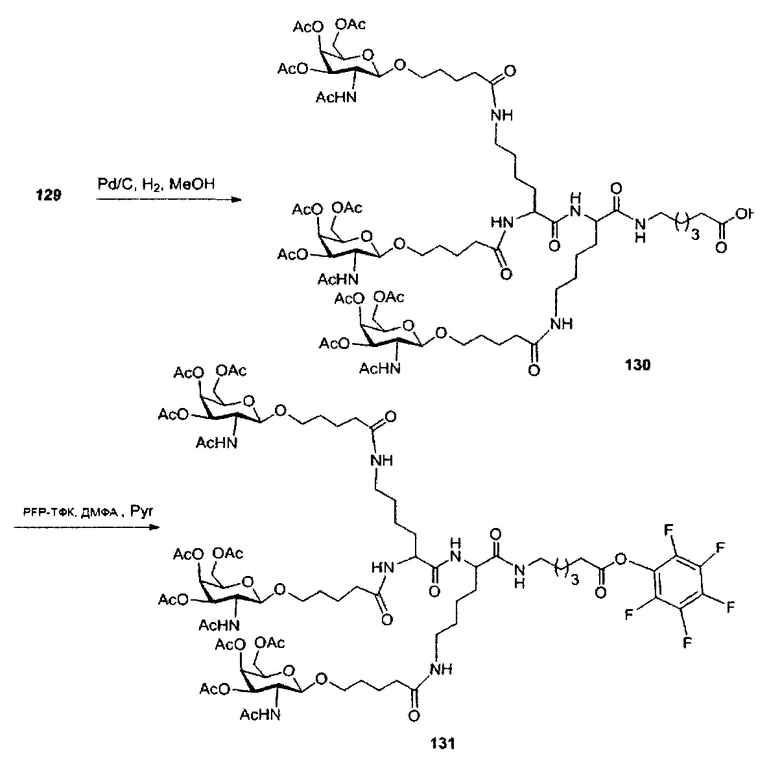
Соединение 123 (7,419 г, 12,91 ммоль), HOBt (3,49 г, 25,82 ммоль) и соединение 126 (6,33 г, 16,14 ммоль) растворили в ДМФА (40 мл), а полученную реакционную смесь охладили на ледяной бане. К смеси добавили N,N-диизопропилэтиламин (4,42 мл, 25,82 ммоль), PyBop (8,7 г, 16,7 ммоль), затем Bop-связывающий агент (1,17 г, 2,66 ммоль) в атмосфере аргона. Ледяную баню убрали и оставили раствор нагреваться до комнатной температуры. Реакция была завершена через 1 час, по результатам ТСХ (ДХМ : МеОН : АА; 89:10:1). Реакционную смесь концентрировали при пониженном давлении. Остаток растворили в EtOAc (200 мл) и промыли 1 М NaHSO4 (3×100 мл), насыщенным водным раствором NaHCO3 (3×100 мл) и насыщенным солевым раствором (2×100 мл). Отделенную органическую фазу высушили (Na2SO4), отфильтровали и концентрировали. Остаток очистили хроматографией на силикагелевой колонке с градиентом от 50% гексанов/EtOAc до 100% EtOAc с получением Соединения 127 (9,4 г) в виде белого пенистого вещества. Данные ЖХМС и 1Н ЯМР согласовались со структурой. Масса m/z 778,4 [М+Н]+.
Трифторуксусную кислоту (12 мл) добавили к раствору соединения 127 (1,57 г, 2,02 ммоль) в дихлорметане (12 мл) и перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь выпарили совместно с толуолом (30 мл) при пониженном давлении досуха. Полученный остаток два раза совместно выпарили с ацетонитрилом (30 мл) и толуолом (40 мл) с получением Соединения 129 (1,67 г) в виде трифторацетатной соли и использовали для следующей стадии без дополнительной очистки. Данные ЖХМС и 1Н ЯМР согласовались с указанной структурой. Масса m/z 478,2 [М+Н]+.
Соединение 7 (0,43 г, 0,963 ммоль), HATU (0,35 г, 0,91 ммоль) и HOAt (0,035 г, 0,26 ммоль) объединили и высушивали в течение 4 часов над P2O5 при пониженном давлении в круглодонной колбе, а затем растворили в безводном ДМФА (1 мл) и перемешивали в течение 5 минут. К полученной смеси добавили раствор соединения 128 (0,20 г, 0,26 ммоль) в безводном ДМФА (0,2 мл) и N,N-диизопропилэтиламине (0,2 мл). Реакционную смесь перемешивали при комнатной температуре в атмосфере аргона. Реакция была завершена через 30 минут, по данным ЖХМС и ТСХ (7% МеОН/ДХМ). Реакционную смесь концентрировали при пониженном давлении. Остаток растворили в ДХМ (30 мл) и промыли 1 М NaHSO4 (3×20 мл), насыщенным водным раствором NaHCO3 (3×20 мл) и насыщенным солевым раствором (3×20 мл). Органическую фазу отделили, высушили над Na2SO4, отфильтровали и концентрировали. Остаток очистили колоночной хроматографией на силикагеле, используя 5-15% МеОН в дихлорметане, с получением Соединения 129 (96,6 мг). Данные ЖХМС и 1Н ЯМР согласовались со структурой. Масса m/z 883,4 [М+2Н]+.
Соединение 129 (0,09 г, 0,051 ммоль) растворили в метаноле (5 мл) в сцинтилляционной пробирке объемом 20 мл. К смеси добавили небольшое количество 10% Pd/C (0,015 мг) и продували реакционный сосуд газообразным H2. Реакционную смесь перемешивали при комнатной температуре в атмосере H2 в течение 18 часов. Реакционную смесь отфильтровали через слой целита и промыли слой целита метанолом. Фильтрат и промывочные растворы слили вместе и концентрировали при пониженном давлении с получением Соединения 130 (0,08 г). Данные ЖХМС и 1Н ЯМР согласовались с указанной структурой. Продукт использовали без дополнительной очистки. Масса m/z 838,3 [М+2H]+.
В коническую кругло донную колбу объемом 10 мл добавили соединение 130 (75,8 мг, 0,046 ммоль), 0,37 М пиридин/ДМФА (200 мкл) и мешалку. К этому раствору по каплям добавили 0,7 М пентафторфенилтрифторацетат/ДМФА (100 мкл) при перемешивании. По данным ЖХМС реакция была завершена через 1 час. Растворитель удалили при пониженном давлении и растворили остаток в CHCl3 (~ 10 мл). Органический слой разделили между NaHSO4 (1 М, 10 мл), насыщенным водным раствором NaHCO3 (10 ил) и насыщенным солевым раствором (10 мл), с каждым раствором по три раза. Органическую фазу отделили и высушили над Na2SO4, отфильтровали и концентрировали с получением Соединения 131 (77,7 мг). ЖХМС согласовался со структурой. Использовали без дополнительной очистки. Масса m/z 921,3 [М+2H]+.
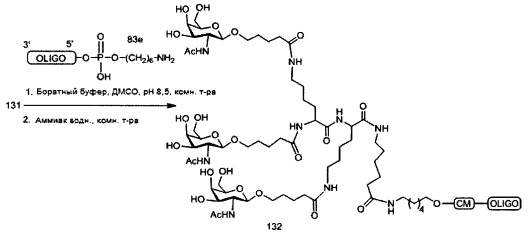
Олигомерное Соединение 132, содержащее группу конъюгата GalNAc3-5, получили по общим способам, представленным в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-5 (GalNAc3-5a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc3-5 (GalNAc3-5a-CM-) представлена ниже:
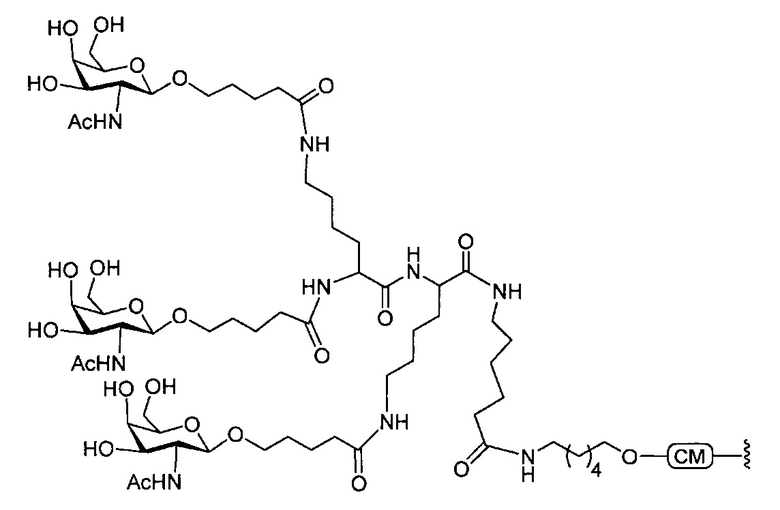 .
.
Пример 50: Получение олигонуклеотида 144, содержащего GalNAc4-11
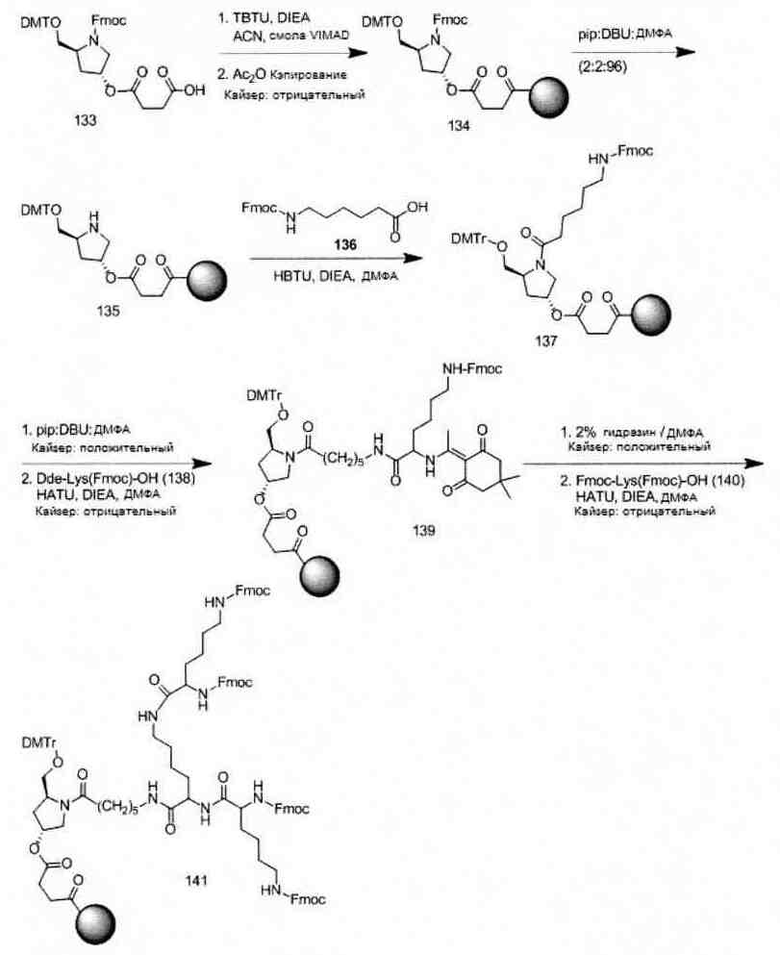
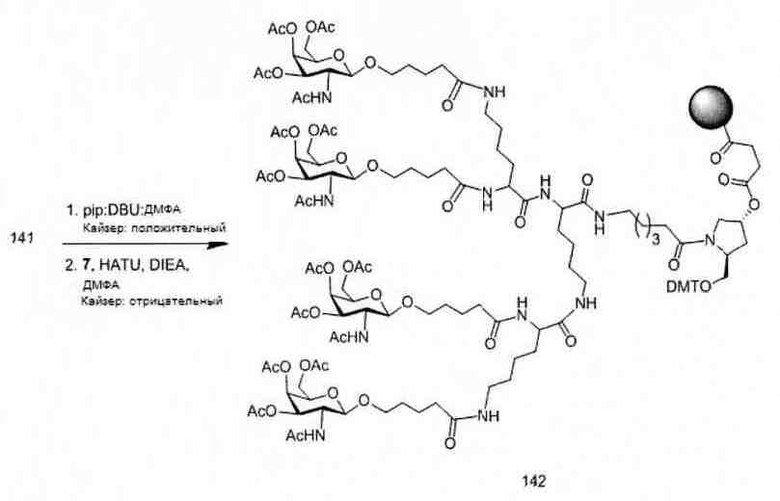
Синтез Соединения 134. В колбу Меррифилда добавили аминометиловую смолу VIMAD (2,5 г, 450 мкмоль/г), которую промыли ацетонитрилом, диметилформамидом, дихлорметаном и ацетонитрилом. Смолу оставили набухать в ацетонитриле (4 мл). Соединение 133 предварительно активировали в 100 мл кругло донной колбе путем добавления 20 (1,0 ммоль, 0,747 г), TBTU (1,0 ммоль, 0,321 г), ацетонитрила (5 мл) и DIEA (3,0 ммоль, 0,5 мл). Этот раствор оставили перемешиваться на 5 минут, а затем добавили в колбу Меррифилда при встряхивании. Суспензию оставили встряхиваться на 3 часа. Реакционную смесь слили, а смолу промыли ацетонитрилом, ДМФА и ДХМ. Заполнение новой смолы количественно определили по измерению абсорбции DMT катиона при 500 нм (коэффициент экстинкции = 76000) в ДХМ, которое составило 238 мкмоль/г. Смолу кэпировали трехкратным суспендированием в растворе уксусного ангидрида в течение десяти минут.
Соединение 141, связанное с твердой подложкой, синтезировали многократным повторением способов твердофазного синтеза пептидов при помощи Fmoc. Взяли небольшое количество твердой подложки и суспендировали в водном растворе аммиака (28-30 масс. %) в течение 6 часов. Расщепленное соединение анализировали по ЖХ-МС и наблюдали, что масса согласуется со структурой. Масса m/z 1063,8 [М+2H]+.
Соединение 142, связанное с твердой подложкой, синтезировали по способам твердофазного синтеза пептидов.
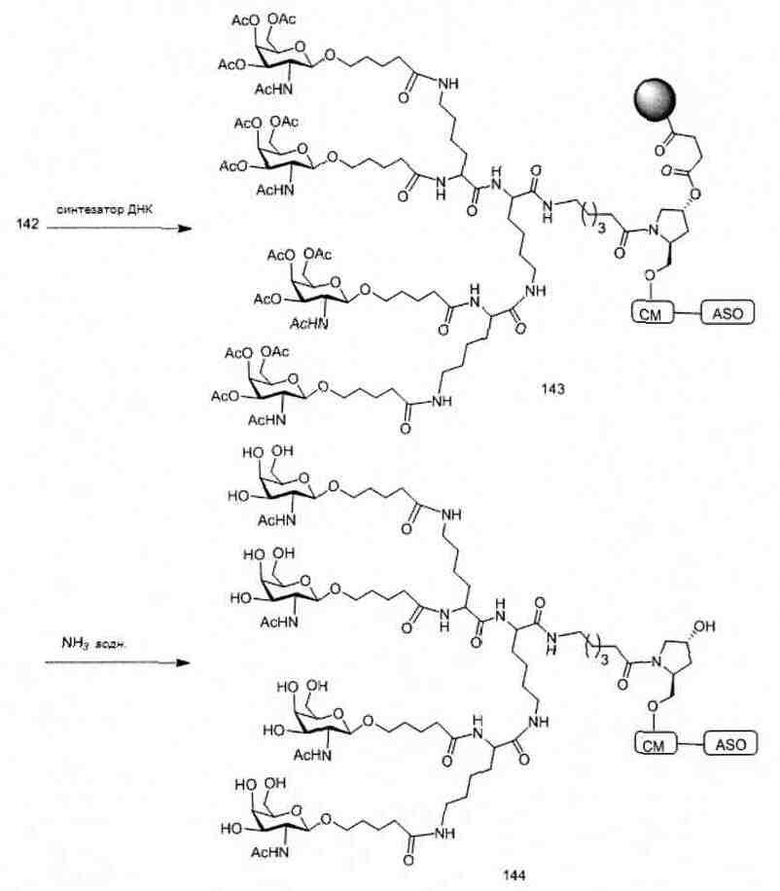
Соединение 143, связанное с твердой подложкой, синтезировали при помощи стандартного твердофазного синтеза на ДНК синтезаторе.
Соединение 143, связанное с твердой подложкой, суспендировали в водном аммиаке (28-30 масс. %) и нагревали при 55°C С в течение 16 часов. Раствор охладили, а твердую подложку отфильтровали. Фильтрат концентрировали, а остаток растворили в воде и очистили при помощи ВЭЖХ на сильной анионообменной колонке. Фракции, содержащие соединение 144 полной длины, слили вместе и обессолили. Полученное GalNAc4-11-сопряженное олигомерное соединение анализировали при помощи ЖХ-МС и наблюдали, что масса согласуется со структурой.
Кластерная часть GalNAc4 группы конъюгата GalNAc4-11 (GalNAc4-11а) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc4-11 (GalNAc4-11a-CM) представлена ниже:
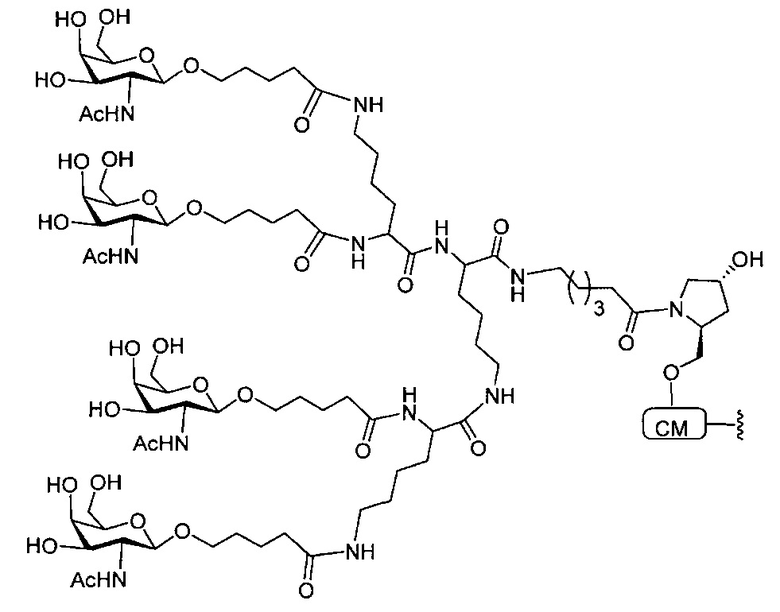 .
.
Пример 51: Получение олигонуклеотида 155, содержащего GalNAc3-6
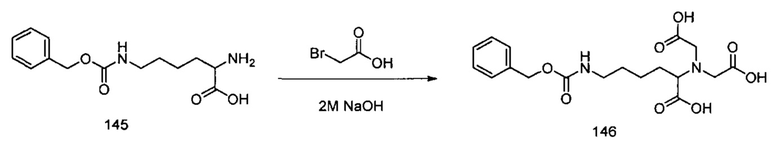
Соединение 146 синтезировали так, как описано в литературе (Analytical Biochemistry 1995, 229, 54-60).
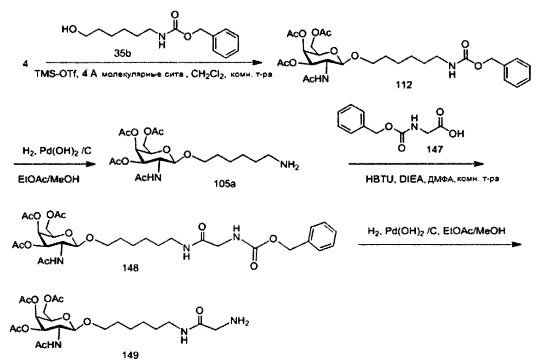
Соединение 4 (15 г, 45,55 ммоль) и соединение 35b (14,3 грамм, 57 ммоль) растворили в CH2Cl2 (200 мл). Добавили активированные молекулярные сита (4  , 2 г, порошкообразные) и оставили реакционную смесь перемешиваться в течение 30 минут в атмосфере азота. Добавили TMS-OTf (4,1 мл, 22,77 ммоль) и оставили реакционную смесь перемешиваться при комнатной температуре в течение ночи. После завершения реакции смесь погасили, вылив в насыщенный водный раствор NaHCO3 (500 мл) с дробленым льдом (~ 150 г). Органический слой отделили, промыли насыщенным солевым раствором, высушили над MgSO4, отфильтровали и концентрировали до оранжевого маслянистого вещества при пониженном давлении. Неочищенный материал очистили силикагелевой колоночной хроматографией и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 112 (16,53 г, 63%). ЖХМС и 1Н ЯМР согласовались с ожидаемым соединением.
, 2 г, порошкообразные) и оставили реакционную смесь перемешиваться в течение 30 минут в атмосфере азота. Добавили TMS-OTf (4,1 мл, 22,77 ммоль) и оставили реакционную смесь перемешиваться при комнатной температуре в течение ночи. После завершения реакции смесь погасили, вылив в насыщенный водный раствор NaHCO3 (500 мл) с дробленым льдом (~ 150 г). Органический слой отделили, промыли насыщенным солевым раствором, высушили над MgSO4, отфильтровали и концентрировали до оранжевого маслянистого вещества при пониженном давлении. Неочищенный материал очистили силикагелевой колоночной хроматографией и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 112 (16,53 г, 63%). ЖХМС и 1Н ЯМР согласовались с ожидаемым соединением.
Соединение 112 (4,27 г, 7,35 ммоль) растворили в 1:1 МеОН/EtOAc (40 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде, 400 мг) и пропускали через раствор газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в CH2Cl2, и ЖХМС), катализатор удалили фильтрованием через слой целита. Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 105а (3,28 г). Данные ЖХМС и 1Н ЯМР согласовались с заданным продуктом.
Соединение 147 (2,31 г, 11 ммоль) растворили в безводном ДМФА (100 мл). Добавили N,N-диизопропилэтиламин (DIEA, 3,9 мл, 22 ммоль), затем HBTU (4 г, 10,5 ммоль). Реакционную смесь оставили перемешиваться в течение ~15 минут в атмосфере азота. К этой смеси добавили раствор соединения 105а (3,3 г, 7,4 ммоль) в сухом ДМФА и перемешивали в течение 2 часов в атмосфере азота. Реакционную смесь разбавили EtOAc и промыли насыщенным водным раствором NaHCO3 и насыщенным солевым раствором. Органическую фазу отделили, высушили (MgSO4), отфильтровали и концентрировали до оранжевого сиропообразного вещества. Неочищенный материал очистили колоночной хроматографией и элюировали 2-5% МеОН в CH2Cl2 с получением Соединения 148 (3,44 г, 73%). ЖХМС и 1H ЯМР согласовались с ожидаемым продуктом.
Соединение 148 (3,3 г, 5,2 ммоль) растворили в 1:1 МеОН/ЕtOАс (75 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде) (350 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием через слой целита. Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 149 (2,6 г). Данные ЖХМС согласовались с заданным продуктом. Остаток растворили в сухом ДМФА (10 мл) и сразу использовали на следующей стадии.
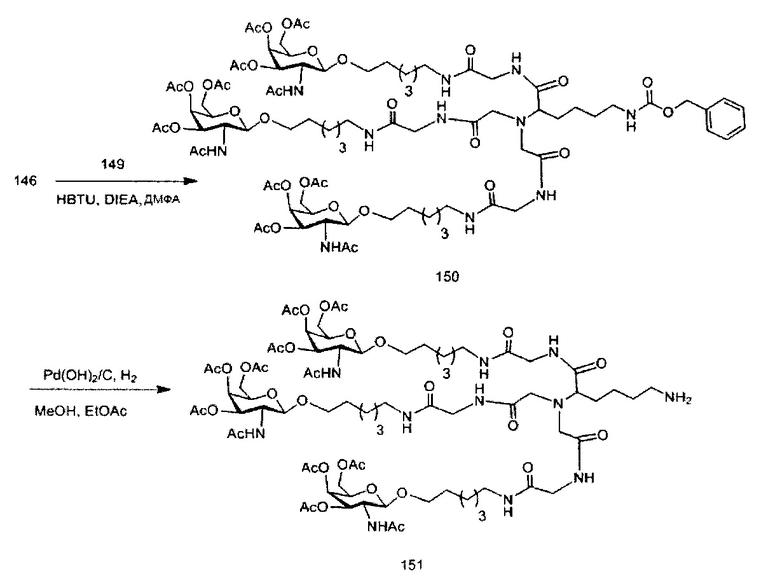
Соединение 146 (0,68 г, 1,73 ммоль) растворили в сухом ДМФА (20 мл). К нему добавили DIEA (450 мкл, 2,6 ммоль, 1,5 экв.) и HBTU (1,96 г, 0,52 ммоль). Реакционную смесь оставили перемешиваться в течение 15 минут при комнатной температуре в атмосфере азота. Добавили раствор соединения 149 (2,6 г) в безводном ДМФА (10 мл). рН реакционной смеси довели до рН=9-10 добавлением DIEA (при необходимости). Реакционную смесь оставили перемешиваться в течение 2 часов при комнатной температуре в атмосфере азота. После завершения реакции смесь разбавили EtOAc (100 мл) и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органическую фазу отделили, высушили над MgSO4, отфильтровали и концентрировали. Остаток очистили силикагелевой колоночной хроматографией и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 150 (0,62 г, 20%). ЖХМС и 1H ЯМР согласовались с заданным продуктом.
Соединение 150 (0,62 г) растворили в 1:1 МеОН/EtOAc (5 л). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде) (60 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием (тефлоновый фильтр с переходной канюлей шприца, 0,45 мкм). Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 151 (0,57 г). Данные ЖХМС согласовались с заданным продуктом. Продукт растворили в 4 мл сухого ДМФА и сразу использовали на следующей стадии.
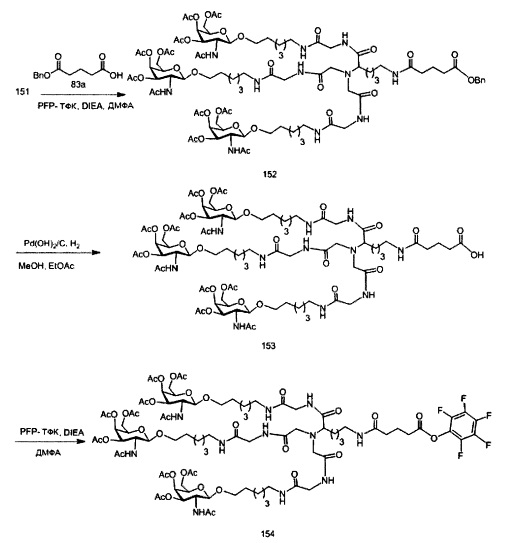
Соединение 83а (0,11 г, 0,33 ммоль) растворили в безводном ДМФА (5 мл) и добавили N,N-диизопропилэтиламин (75 мкл, 1 ммоль) и PFP-ТФК (90 мкл, 0,76 ммоль). При соприкосновении реакционная смесь стала пурпурной и постепенно изменила цвет на оранжевый в течение следующих 30 минут. Ход реакции контролировали по ТСХ и ЖХМС. После завершения (образования эфира PFP) добавили раствор соединения 151 (0,57 г, 0,33 ммоль) в ДМФА. рН реакционной смеси довели до рН=9-10 добавлением N,N-диизопропилэтиламина (при необходимости). Реакционную смесь перемешивали в атмосфере азота в течение ~30 минут. После завершения реакции большую часть растворителя удалили при пониженном давлении. Остаток разбавили CH2Cl2 и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органическую фазу отделили, высушили над MgSO4, отфильтровали и концентрировали до оранжевого сиропообразного вещества. Остаток очистили колоночной хроматографией на силикагеле (2-10% МеОН в CH2Cl2) с получением Соединения 152 (0,35 г, 55%). ЖХМС и 1Н ЯМР согласовались с заданным продуктом.
Соединение 152 (0,35 г, 0,182 ммоль) растворили в 1:1 MeOH/EtOAc (10 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде) (35 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием (тефлоновый фильтр с переходной канюлей шприца, 0,45 мкм). Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 153 (0,33 г, количественно). Данные ЖХМС согласовались с заданным продуктом.
Соединение 153 (0,33 г, 0,18 ммоль) растворили в безводном ДМФА (5 мл) при перемешивании в атмосфере азота. К нему добавили добавили N,N-диизопропилэтиламин (65 мкл, 0,37 ммоль) и PFP-ТФК (35 мкл, 0,28 ммоль). Реакционную смесь перемешивали в атмосфере азота в течение ~30 минут. При соприкосновении реакционная смесь стала пурпурной и постепенно изменила цвет на оранжевый. рН реакционной смеси поддерживали при рН=9-10 добавлением дополнительного количества N,N-диизопропилэтиламина. Ход реакции контролировали по ТСХ и ЖХМС. После завершения реакции большую часть растворителя удалили при пониженном давлении. Остаток разбавили CH2Cl2 (50 мл) и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органический слой высушили над MgSO4, отфильтровали и концентрировали до оранжевого сиропообразного вещества. Остаток очистили колоночной хроматографией и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 154 (0,29 г, 79%). ЖХМС и 1H ЯМР согласовались с заданным продуктом.
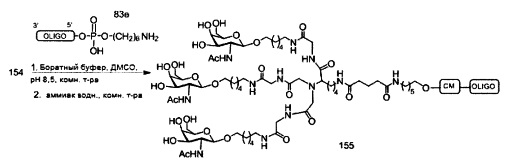
Олигомерное Соединение 155, содержащее группу конъюгата GalNAc3-6, получили по общим способам, представленным в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-6 (GalNAc3-6a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc3-6 (GalNAc3-6a-CM-) представлена ниже:
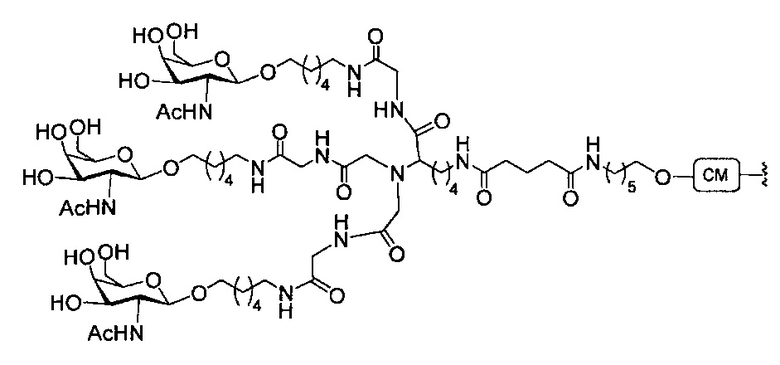 .
.
Пример 52: Получение олигонуклеотида 160, содержащего GalNAc3-9
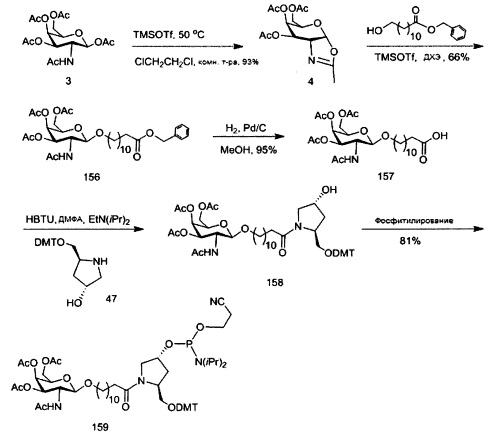
Соединение 112 синтезировали по способу, описанному в литературе (J. Med. Chem. 2004, 47, 5798-5808).
Соединение 156 (18,60 г, 29,28 ммоль) растворили в метаноле (200 мл). Добавили палладий на углероде (6,15 г, загрузка 10 масс. % (в пересчете на сухое вещество), матрица из порошкообразного углерода, влажный). Реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 18 часов. Реакционную смесь отфильтровали через слой целита и тщательно промыли слой целита метанолом. Объединенный фильтрат промыли и концентрировали досуха. Остаток очистили силикагелевой колоночной хроматографией и элюировали 5-10% метанола в дихлорметане с получением Соединения 157 (14,26 г, 89%). Масса m/z 544,1 [М-Н]-.
Соединение 157 (5 г, 9,17 ммоль) растворили в безводном ДМФА (30 мл). Добавили HBTU (3,65 г, 9,61 ммоль) и N,N-диизопропилэтиламин (13,73 мл, 78,81 ммоль) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К нему добавили раствор соединения 47 (2,96 г, 7,04 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 8 часов. Реакционную смесь вылили в насыщенный водный раствор NaHCO3. Смесь экстрагировали этилацетатом, а органический слой промыли насыщенным солевым раствором и высушили (Na2SO4), отфильтровали и выпарили. Полученный остаток очистили силикагелевой колоночной хроматографией и элюировали 50% этилацетатом в гексане с получением Соединения 158 (8,25 г, 73,3%). Структуру подтвердили анализом МС и 1H ЯМР.
Соединение 158 (7,2 г, 7,61 ммоль) высушили над P2O5 при пониженном давлении. Высушенное соединение растворили в безводном ДМФА (50 мл). К нему добавили 1Н-тетразол (0,43 г, 6,09 ммоль) и N-метилимидазол (0,3 мл, 3,81 ммоль), и цианоэтил-N,N,N',N'-тетраизопропил-фосфородиамидит (3,65 мл, 11,50 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 4 часов. Реакционную смесь разбавили этилацетатом (200 мл). Реакционную смесь промыли насыщенным раствором NaHCO3 и насыщенным солевым раствором. Органическую фазу отделили, высушили (Na2SO4), отфильтровали и выпарили. Остаток очистили силикагелевой колоночной хроматографией и элюировали 50-90% этилацетатом в гексане с получением Соединения 159 (7,82 г, 80,5%). Структуру подтвердили анализом ЖХМС и 31P ЯМР.
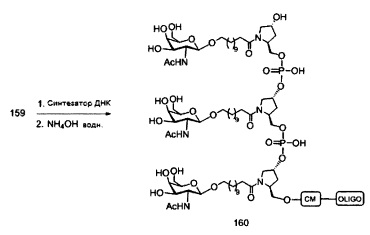
Олигомерное соединение 160, содержащее группу конъюгата GalNAc3-9, получили по стандартным способам синтеза олигонуклеотидов. Три единицы соединения 159 связали с твердой подложкой, затем с фосфорамидитами нуклеотидов. В результате обработки защищенного олигомерного соединения водным раствором аммиака получили соединение 160. Кластерная часть GalNAc3 группы конъюгата GalNAc3-9 (GalNAc3-9a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-9 (GalNAc3-9a-CM) представлена ниже:
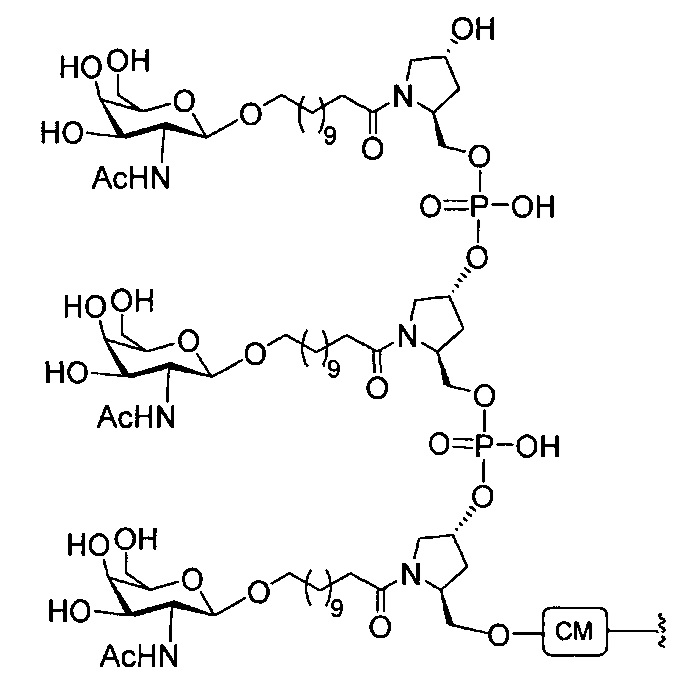 .
.
Пример 53: Альтернативный способ получения Соединения 18 (GalNAc3-1a и GalNAc3-3a)
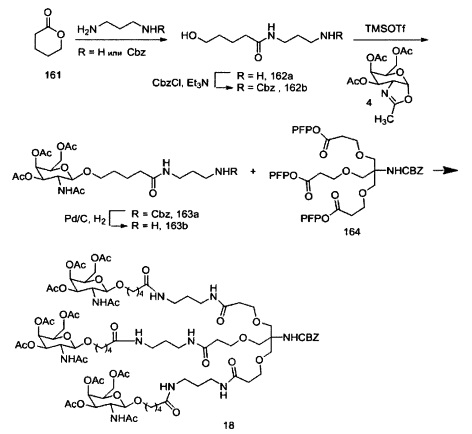
Выполнили реакцию лактона 161 с диаминопропаном (3-5 экв.) или моно-Вос-защищинным диаминопропаном (1 экв.) с получением спирта 162а или 162b. При использовании для описанной выше реакции незащищенного пропандиамина, избыток диамина удалили выпариванием под высоким вакуумом, а свободную аминогруппу в 162а защитили при помощи CbzCl с получением 162b в виде белого твердого вещества после очистки колоночной хроматографией. Спирт 162b затем взаимодействовал с соединением 4 в присутствии TMSOTf c получением 163а, которое преобразовали в 163b путем снятия Cbz группы при помощи каталитического гидрирования. Пентафторфениловый (PFP) эфир 164 получили взаимодействием трехкислотного соединения 113 (см. Пример 48) с PFP-ТФК (3,5 экв.) и пиридином (3,5 экв.) в ДМФА (от 0,1 до 0,5 М). Триэфир 164 непосредственно взаимодействовал с амином 163b (3-4 экв.) и DIPEA (3-4 экв.) с получением Соединения 18. Представленный выше способ значительно облегчает очистку промежуточных соединений и минимизирует образование побочных продуктов, которые образуются при использовании способа, описанного в Примере 4.
Пример 54: Альтернативный способ получения Соединения 18 (GalNAc3-1a и GalNAc3-3а)
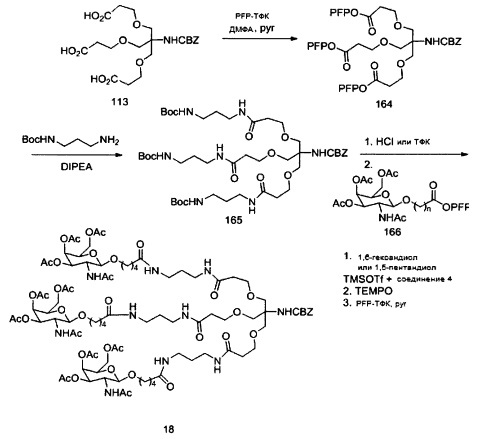
Три-PFP эфир 164 получили из кислоты 113 по способу, представленному выше в Примере 53, выполнили реакцию этого эфира с моно-Вос-защищенным диамином с получением 165 практически с количественным выходом. Вое группы сняли хлористоводородной кислотой или трифторуксусной кислотой с получением триамина, который взаимодействовал с активированной кислотой PFP 166 в присутствии подходящего основания, такого как DIPEA, с получением Соединения 18.
PFP-защищенную кислоту Gal-NAc 166 получили из соответствующей кислоты обработкой PFP-ТФК (1-1,2 экв.) и пиридином (1-1,2 экв.) в ДМФА. Кислоту-предшественник, в свою очередь, получили из соответствующего спирта окислением с использованием TEMPO (0,2 экв.) и BAIB в ацетонитриле и воде. Спирт-предшественник получили из сахарного промежуточного соединения 4 взаимодействием с 1,6-гександиолом (или 1,5-гександиолом или другим диолом для других значений n) (2-4 экв.) и TMSOTf, используя условия, описанные ранее в Примере 47.
Пример 55: Дозозависимое исследование олигонуклеотидов, содержащих либо 3', либо 5'-группу конъюгата (сравнение GalNAc3-1, 3, 8 и 9), направленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Несопряженный ISIS 353382 включили в качестве стандарта. Каждая из различных групп конъюгата GalNAc3 была присоединена либо к 3', либо к 5'-концу соответствующего олигонуклеотида при помощи фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида (расщепляемый фрагмент).

Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-9 показана ранее в Примере 52. Структура GalNAc3-3 показана ранее в Примере 39. Структура GalNAc3-8 показана ранее в Примере 47.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 353382, 655861, 664078, 661161, 665001 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 40, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-1 и GalNAc3-9 у 3'-конца (ISIS 655861 и ISIS 664078), а также конъюгаты GalNAc3-3 и GalNAc3-8, связанные у 5'-конца (ISIS 661161 и ISIS 665001) демонстрируют существенное улучшение эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 353382). Кроме того, ISIS 664078, содержащий конъюгат GalNAc3-9 у 3'-конца, был по существу настолько же эффективным, как ISIS 655861, который содержит конъюгат GalNAc3-1 у 3'-конца. 5'-сопряженные антисмысловые олигонуклеотиды, ISIS 661161 и ISIS 665001, содержащие GalNAc3-3 или GalNAc3-9, соответственно, обладают повышенной эффективностью, по сравнению с 3'-сопряженными антисмысловыми соединениями (ISIS 655861 и ISIS 664078).
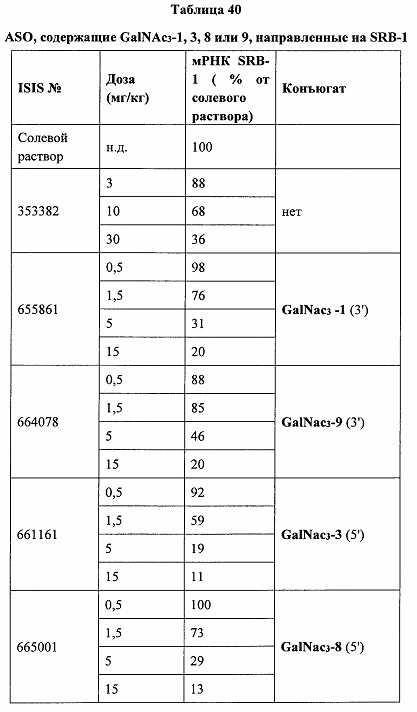
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК представлены ниже в таблице.
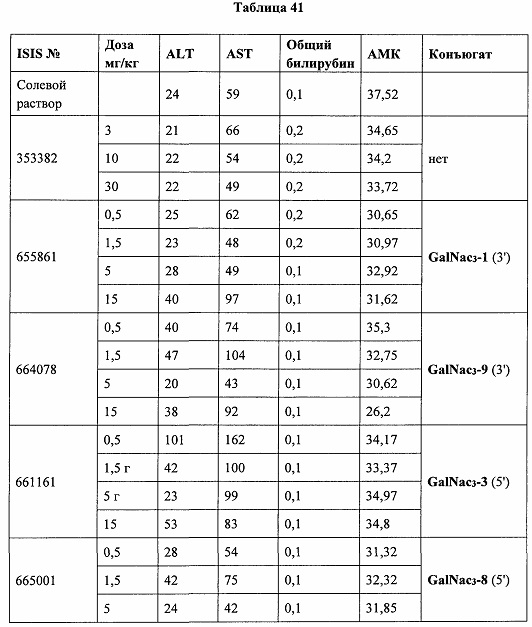

Пример 56: Дозозависимое исследование олигонуклеотидов, содержащих либо 3', либо 5'-группу конъюгата (сравнение GalNAc3-1, 2, 3, 5, 6, 7 и 10), направленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Несопряженный ISIS 353382 включили в качестве стандарта. Каждая из различных групп конъюгата GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида фосфодиэфир-связанным 2'-дезоксиаденозиновым нуклеозидом (расщепляемый фрагмент), за исключением ISIS 655861, в котором группа конъюгата GalNAc3 присоединена к 3'-концу.
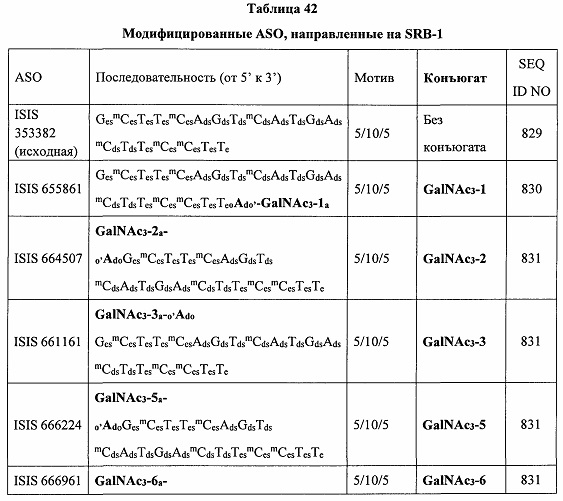
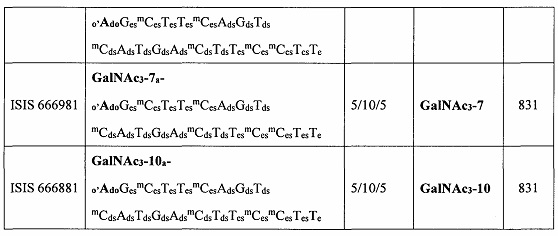
Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-2a показана ранее в Примере 37. Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-5a показана ранее в Примере 49. Структура GalNAc3-6a показана ранее в Примере 51. Структура GalNAc3-7a показана ранее в Примере 48. Структура GalNAc3-10a показана ранее в Примере 46.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 353382, 655861, 664507, 661161, 666224, 666961, 666981, 666881 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 43, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, сопряженные антисмысловые олигонуклеотиды демонстрируют значительное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 353382). 5'-сопряженные антисмысловые олигонуклеотиды демонстрируют небольшое усиление эффективности, по сравнению с 3'-сопряженным антисмысловым олигонуклеотидом.
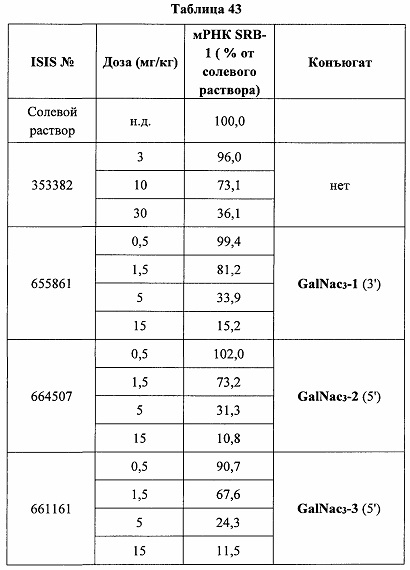
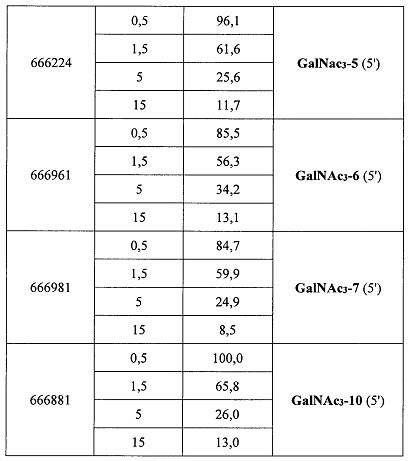
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 44.
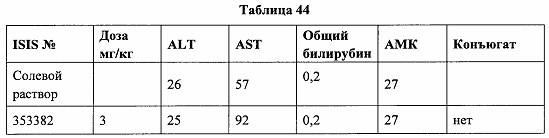
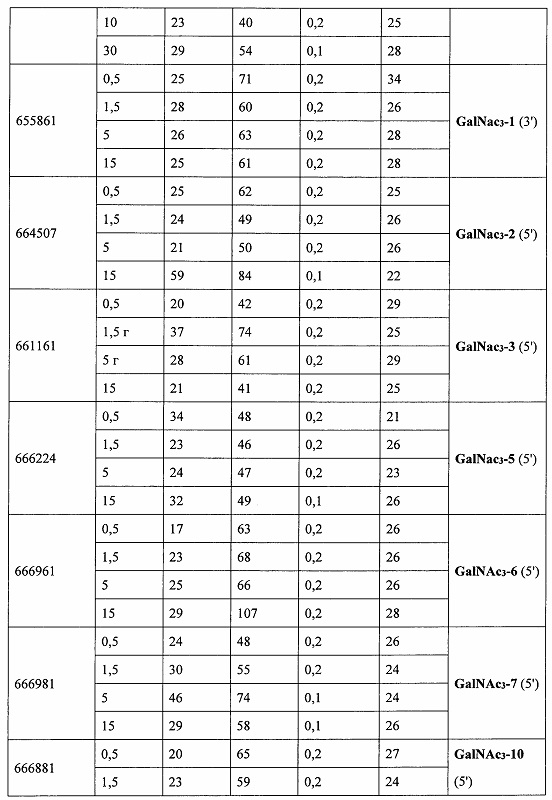
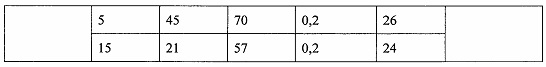
Пример 57: Исследование продолжительности действия олигонуклеотидов, содержащих 3'-группу конъюгата, направленных на АроС III, in vivo
Мышам однократно ввели инъекцию дозы, указанной ниже, и в течение 42 дней наблюдали уровни АроС-III и триглицеридов в плазме (TG в плазме). Исследование выполнили, используя в каждой группе 3 трансгенных мышей, которые экспрессируют человеческий APOC-III.

Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-1a показана ранее в Примере 9.
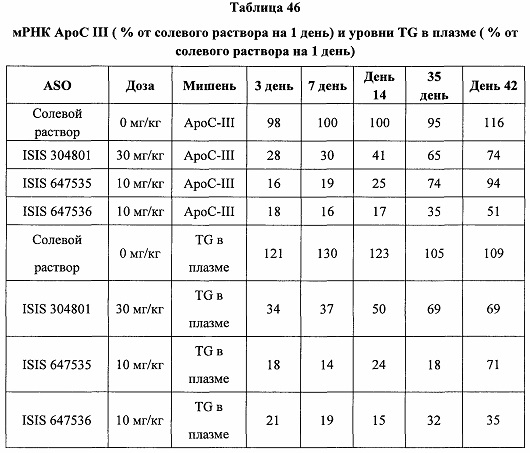
Как можно видеть в представленной выше таблице, продолжительность действия увеличивается при добавлении 3'-группы конъюгата, по сравнению с несопряженным олигонуклеотидом. Дополнительное увеличение продолжительности действия наблюдали для смешанного сопряженного PO/PS олигонуклеотида 647536, по сравнению с сопряженным олигонуклеотидом 647535, содержащим только PS.
Пример 58: Дозозависимое исследование олигонуклеотидов, содержащих 3'-группу конъюгата (сравнение GalNAc3-1 и GalNAc4-11), направленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Несопряженный ISIS 440762 включили в качестве несопряженного стандарта. Каждая из групп конъюгата была присоединена к 3'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-11a показана ранее в Примере 50.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 440762, 651900, 663748 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 47, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-1 и GalNAc4-11 у 3'-конца (ISIS 651900 и ISIS 663748), демонстрируют значительное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 440762). Эти два сопряженных олигонуклеотида, GalNAc3-1 и GalNAc4-11, были одинаково эффективными.


Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь (PS); «о» означает фосфодиэфирную межнуклеозидную связь (РО); и «о'» означает -O-Р(=O)(ОН)-. Группы конъюгата выделены жирным.
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 48.
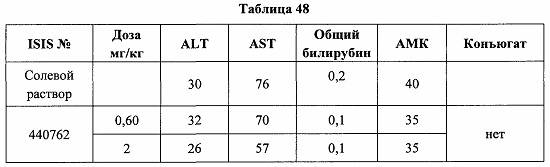
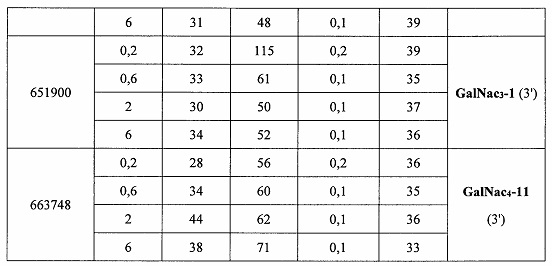
Пример 59: Действие GalNAc3-1-сопряженных ASO, направленных на FXI, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в исследовании действия многократных нарастающих доз на антисмысловое ингибирование FXI у мышей. ISIS 404071 включили в качестве несопряженного стандарта. Каждая из групп конъюгата была присоединена к 3'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.
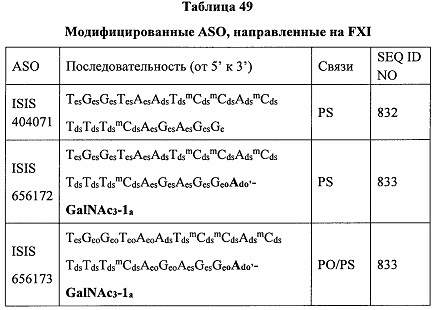
Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-1a показана ранее в Примере 9.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) дважды в неделю в течение 3 недель вводили подкожную инъекцию дозы, представленной ниже, соединения ISIS 404071, 656172, 656173 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК FXI в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Измерили также уровни белка FXI в плазме при помощи твердофазного иммуноферментного анализа. Уровни мРНК FXI определяли относительно общей РНК (при помощи RIBOGREEN®), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, представлены как средний процент уровней мРНК FXI для каждой экспериментальной группы. Данные нормализовали к контрольному образцу, обработанному PBS, и обозначили как «% PBS». ED50 измеряли по таким же способам, как описаны ранее, и указанные значения представлены ниже.

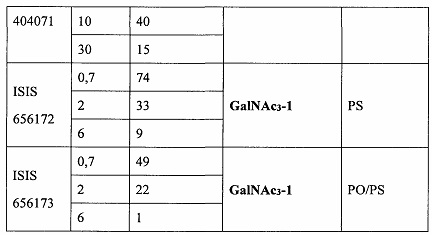
Как показано в Таблице 50, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК FXI дозозависимым образом. Олигонуклеотиды, содержащие группу конъюгата 3'-GalNAc3-1, демонстрируют значительное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 404071). Между эти двумя сопряженными олигонуклеотидами дополнительное усиление эффективности было обеспечено за счет замены некоторых PS линкеров на РО (ISIS 656173).
Как показано в Таблице 50а, лечение антисмысловыми олигонуклеотидами снижает уровни белка FXI дозозависимым образом. Олигонуклеотиды, содержащие группу конъюгата 3'-GalNAc3-1, демонстрируют значительное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 404071). Между эти двумя сопряженными олигонуклеотидами дополнительное усиление эффективности было обеспечено за счет замены некоторых PS линкеров на РО (ISIS 656173).

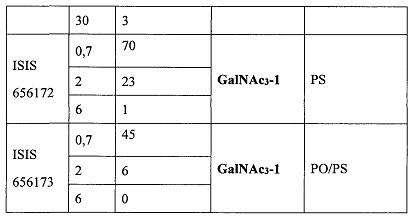
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин, общий альбумин, CRE и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК представлены ниже в таблице.
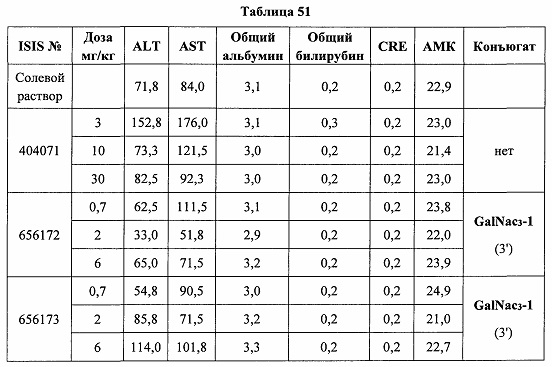
Пример 60: Действие сопряженных ASO, направленных на SRB-1, in vitro
Олигонуклеотиды, перечисленные ниже, испытали в исследовании действия многократных нарастающих доз на антисмысловое ингибирование SRB-1 в первичных гепатоцитах мышей. ISIS 353382 включили в качестве несопряженного стандарта. Каждая из групп конъюгата была присоединена к 3' или 5'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.
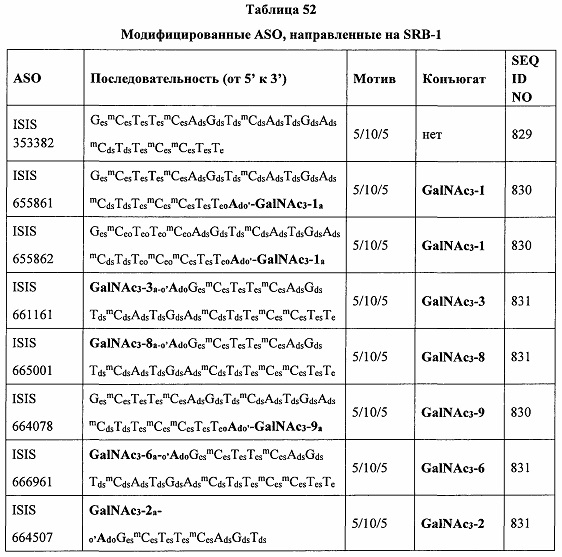
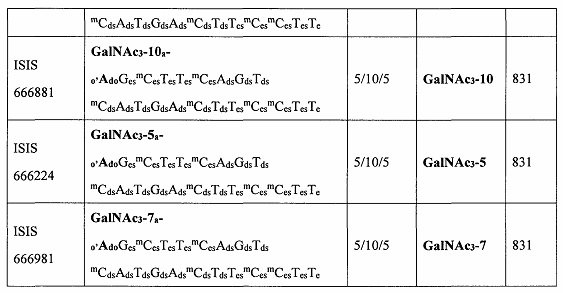
Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-8a показана ранее в Примере 47. Структура GalNAc3-9a показана ранее в Примере 52. Структура GalNAc3-6a показана ранее в Примере 51. Структура GalNAc3-2a показана ранее в Примере 37. Структура GalNAc3-10a показана ранее в Примере 46. Структура GalNAc3-5a показана ранее в Примере 49. Структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Олигонуклеотиды, перечисленный выше, испытывали in vitro в первичных гепатоцитах мышей, помещенных на планшет при плотности 25000 клеток на лунку, и обрабатывали 0,03, 0,08, 0,24, 0,74, 2,22, 6,67 или 20 нМ модифицированного олигонуклеотида. После обработки в течение приблизительно 16 часов, из клеток выделили РНК и измерили уровни мРНК при помощи количественной ПЦР в реальном времени, а уровни мРНК SRB-1 III скорректировали в соответствии с общим содержанием РНК, измеренным при помощи RIBOGREEN®.
IC50 рассчитали по стандартным способам, а результаты представлены в Таблице 53. Результаты показывают, что при условиях свободного поглощения, в которых не использованы никакие реагенты или электроимпульсные приемы для искусственного ускорения входа олигонуклеотидов в клетки, олигонуклеотиды, содержащие конъюгат GalNAc, были существенно более эффективными в гепатоцитах, чем исходный олигонуклеотид (ISIS 353382), который не содержит конъюгат GalNAc.
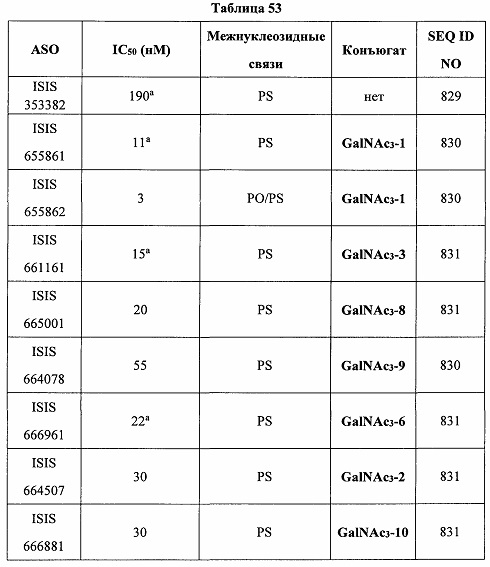
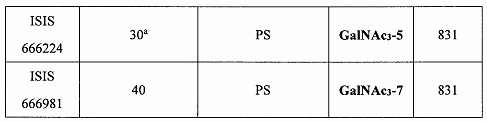
aСреднее для нескольких повторов.
Пример 61: Получение олигомерного соединения 175, содержащего GalNAc3-12
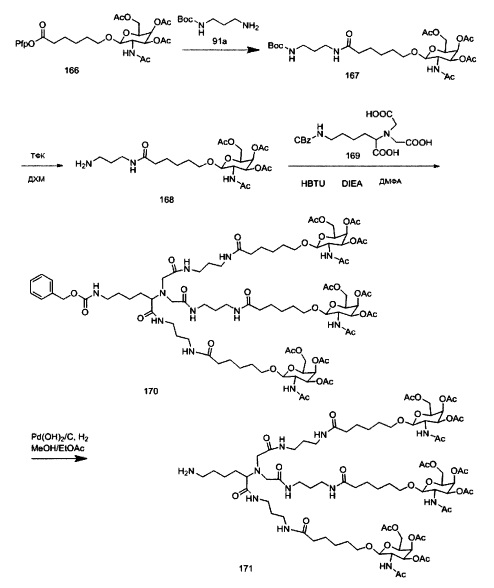
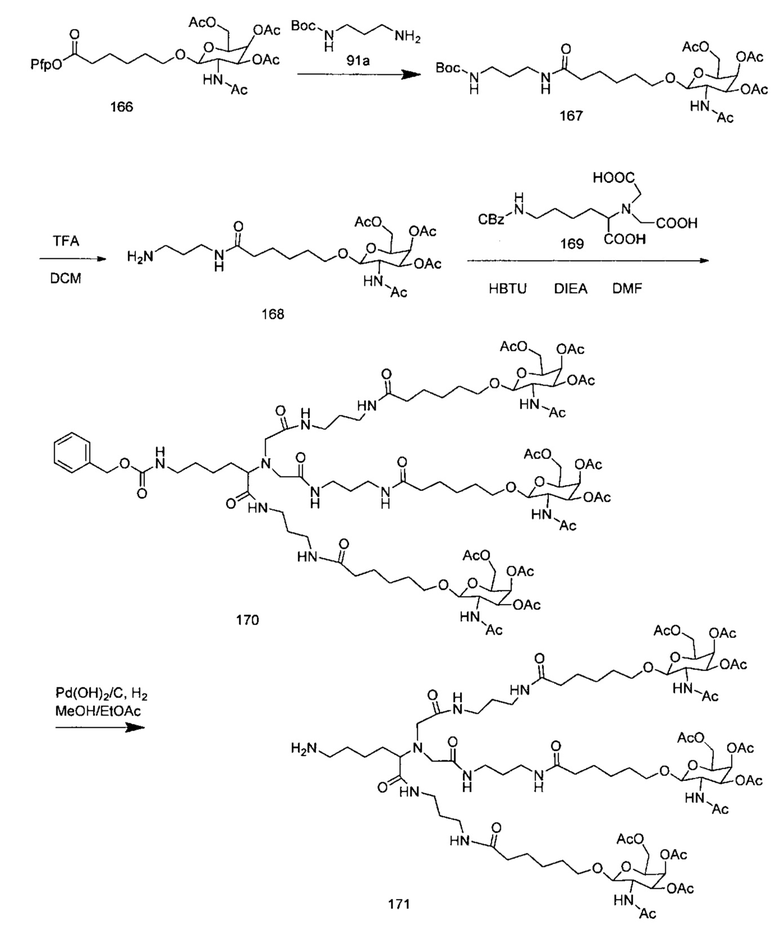
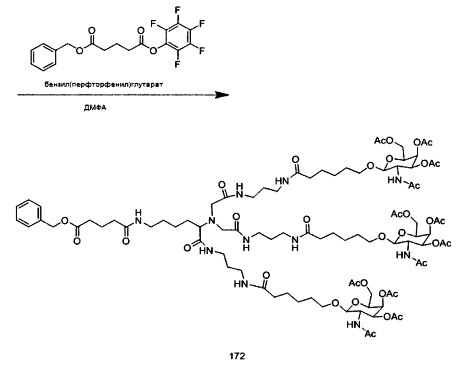
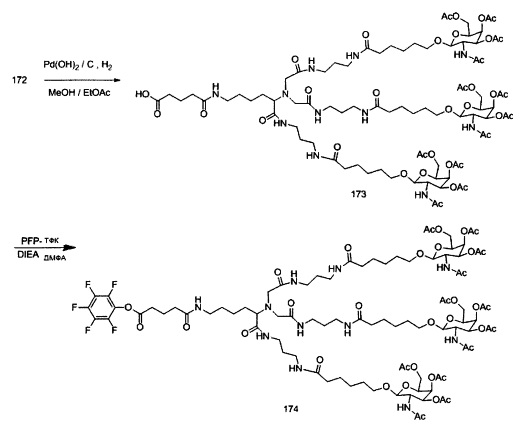
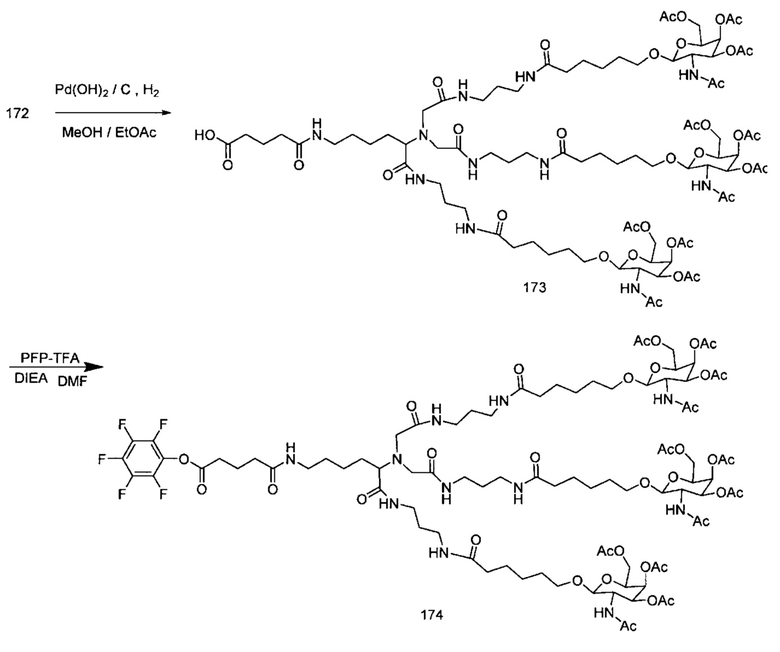
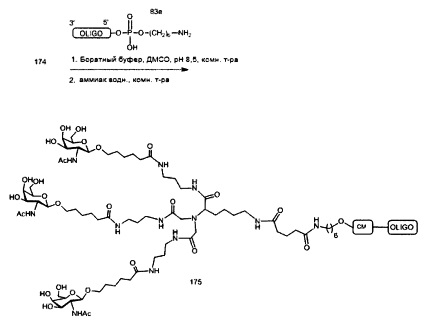
Соединение 169 имеется в продаже. Соединение 172 получили добавлением бензил(перфторфенил)глутарата к соединению 171. Бензил(перфторфенил)глутарат получили добавлением PFP-ТФК и DIEA к 5-(бензилокси)-5-оксопентановой кислоте в ДМФА. Олигомерное соединение 175, содержащее группу конъюгата GalNAc3-12, получили из соединения 174, используя общие способы, описанные в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-12 (GalNAc3-12a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-. Структура GalNAc3-12 (GalNAc3-12a-CM-) представлена ниже:
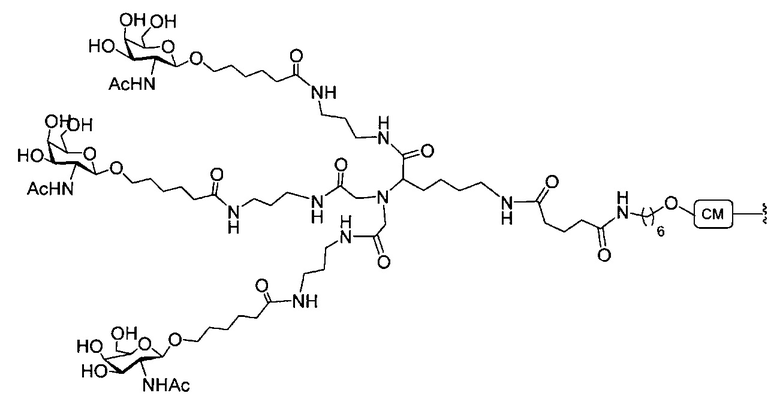
Пример 62: Получение олигомерного соединения 180, содержащего GalNAc3-13
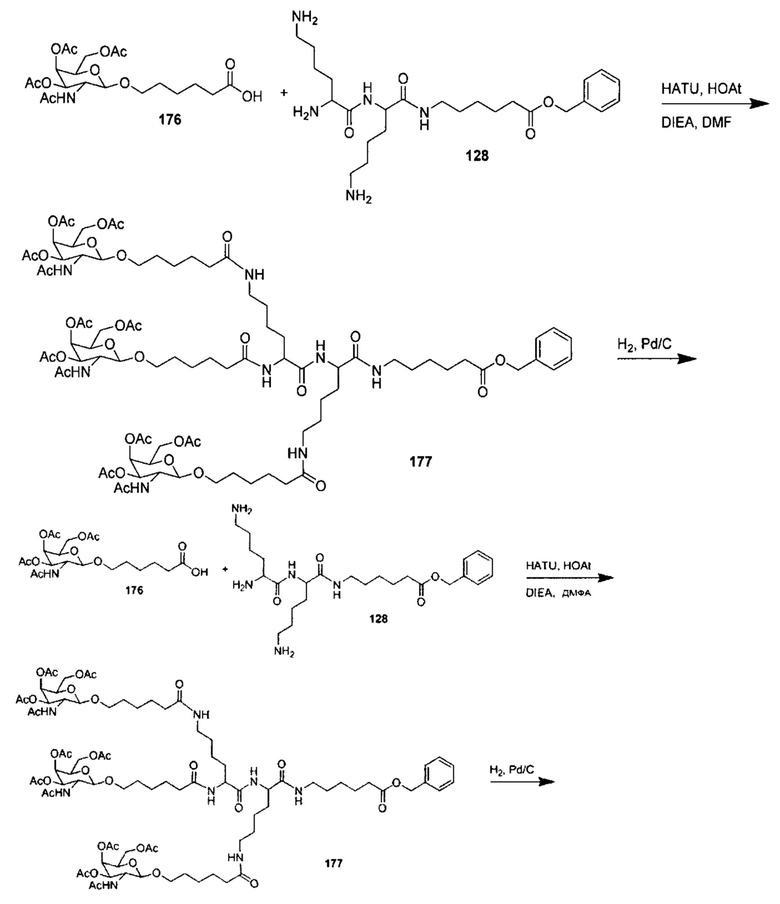
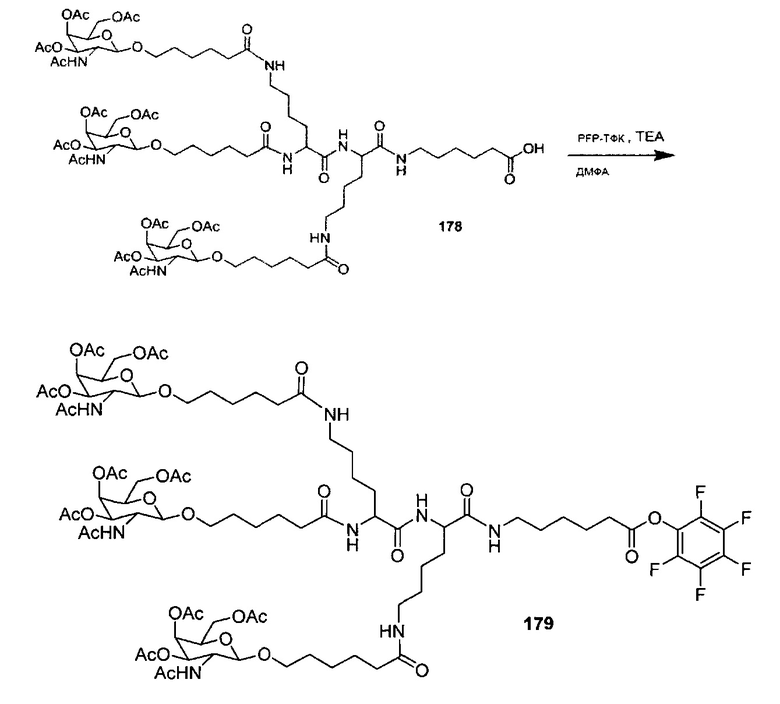
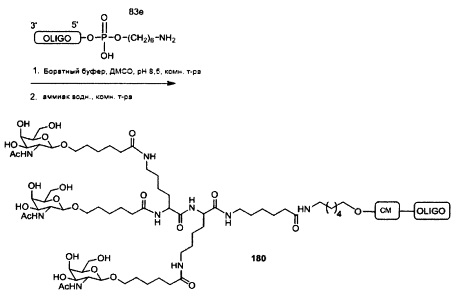
Соединение 176 получили по общему способу, представленному в Примере 2. Олигомерное соединение 180, содержащее группу конъюгата GalNAc3-13, получили из соединения 177, используя общие способы, описанные в Примере 49. Кластерная часть GalNAc3 группы конъюгата GalNAc3-13 (GalNAc3-13а) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-13 (GalNAc3-13а-СМ-) представлена ниже:
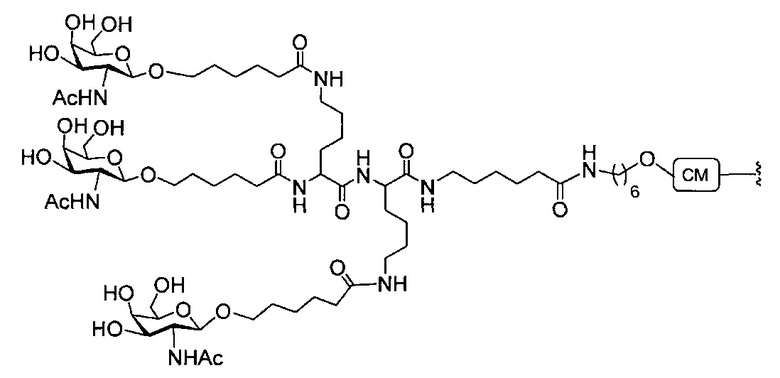
Пример 63: Получение олигомерного соединения 188, содержащего GalNAc3-14
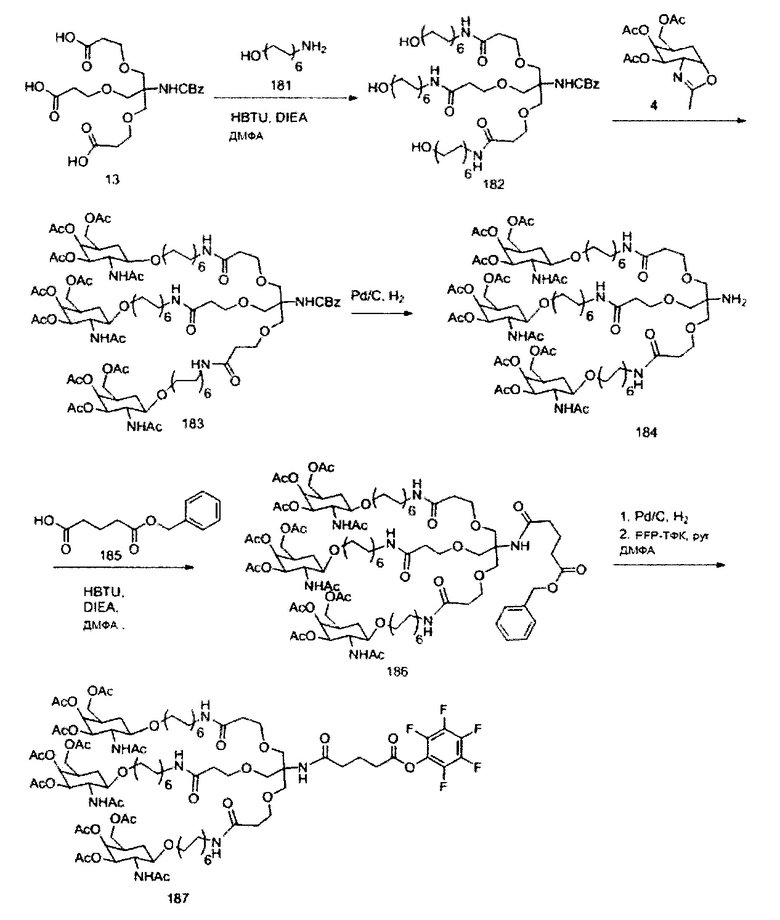
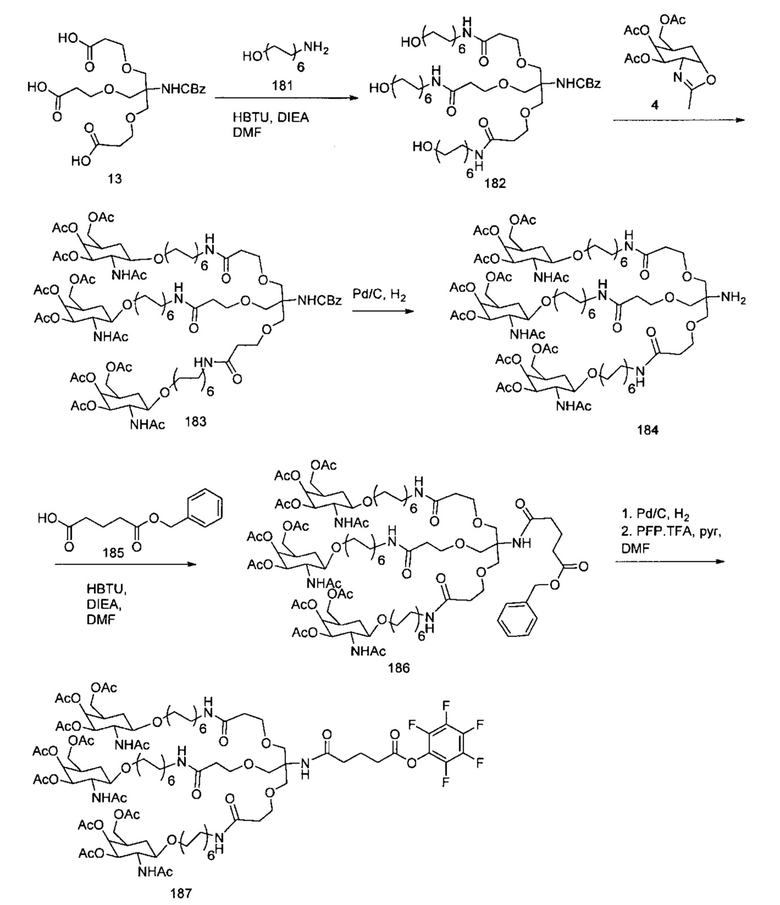
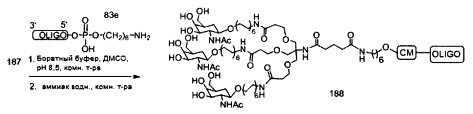
Соединения 181 и 185 имеются в продаже. Олигомерное соединение 188, содержащее группу конъюгата GalNAc3-14, получили из соединения 187, используя общие способы, описанные в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-14 (GalNAc3-14a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-14 (GalNAc3-14a-CM-) представлена ниже:
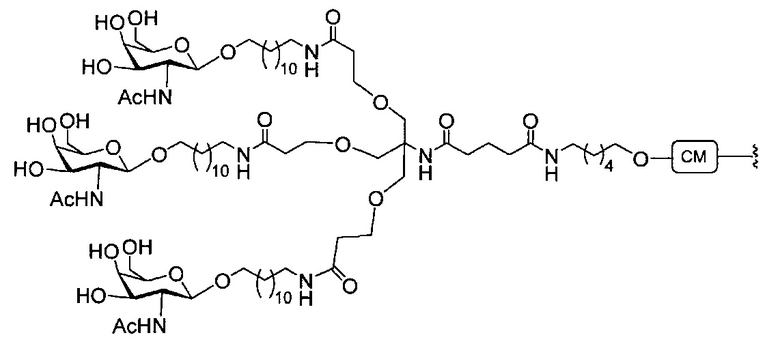
Пример 64: Получение олигомерного соединения 188, содержащего GalNAc3-15
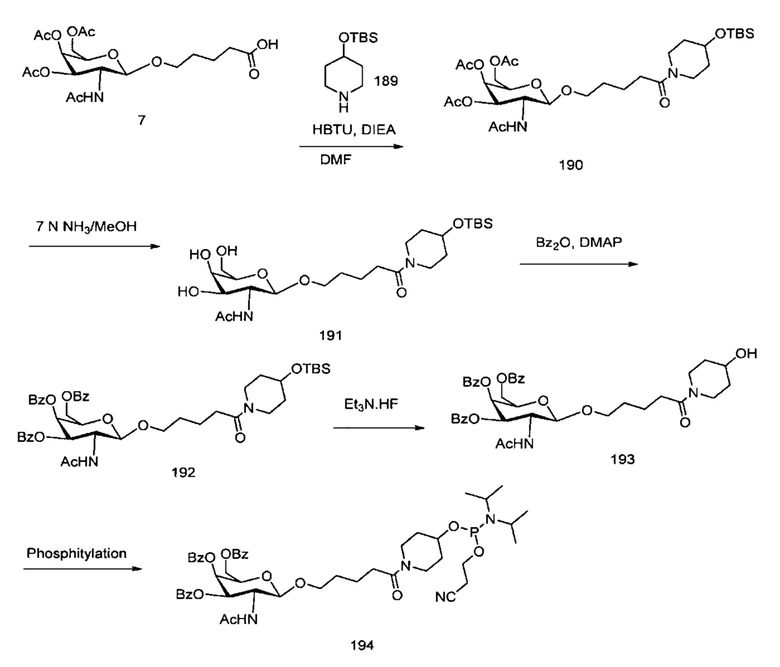
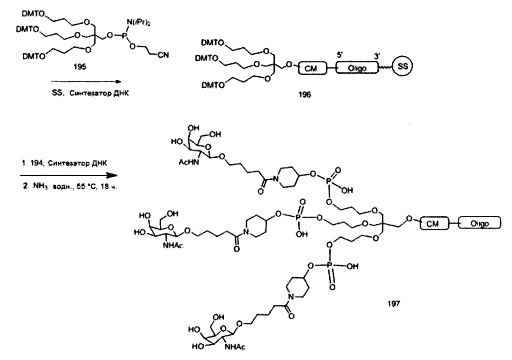
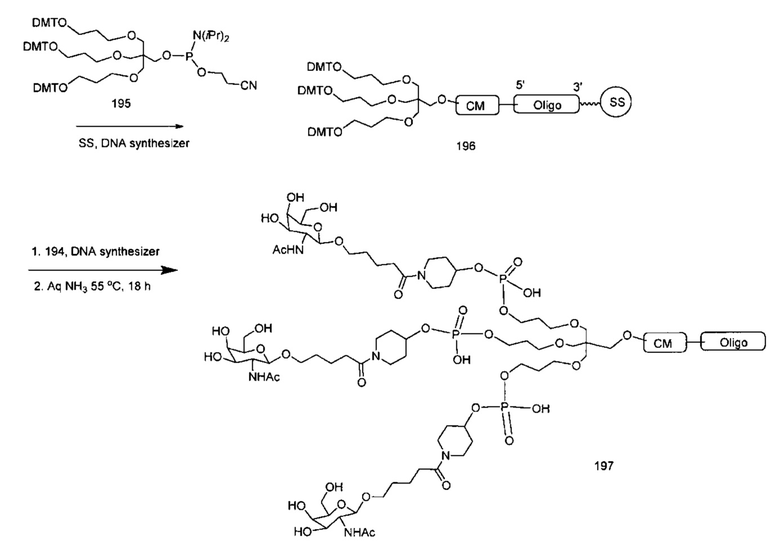
Соединение 189 имеется в продаже. Соединение 195 получили по общему способу, представленному в Примере 31. Олигомерное соединение 197, содержащее группу конъюгата GalNAc3-15, получили из соединений 194 и 195 по стандартным способам синтеза олигонуклеотидов. Кластерная часть GalNAc3 группы конъюгата GalNAc3-15 (GalNAc3-15a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(ОН)-Ad-Р(=O)(ОН)-. Структура GalNAc3-15 (GalNAc3-15а-СМ-) представлена ниже:
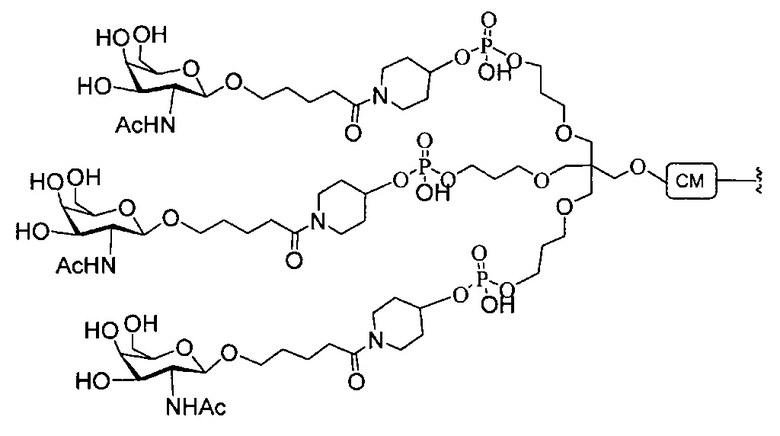
Пример 65: Дозозависимое исследование олигонуклеотидов, содержащих 5'-группу конъюгата (сравнение GalNAc3-3, 12, 13, 14 и 15), направленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Несопряженный ISIS 353382 включили в качестве стандарта. Каждая из групп конъюгата GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.


Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-12а показана ранее в Примере 61. Структура GalNAc3-13a показана ранее в Примере 62. Структура GalNAc3-14a показана ранее в Примере 63. Структура GalNAc3-15a показана ранее в Примере 64.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один или два раза ввели подкожную инъекцию дозы, представленной ниже, соединения ISIS 353382, 661161, 671144, 670061, 671261, 671262 или солевого раствора. Мыши, которым вводили дозу два раза, вторую дозу вводили через три дня после первой дозы. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 55, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Не наблюдали значительной разницы нокдауна мишени между животными, получавшими одну дозу, и животными, получавшими две дозы (см. ISIS 353382 в дозах 30 и 2×15 мг/кг; и ISIS 661161 в дозах 5 и 2×2,5 мг/кг). Антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-3, 12, 13, 14 и 15, демонстрируют существенное усиление эффективности, по сравнению с несопряженным антисмысловым олигонуклеотидом (ISIS 335382).
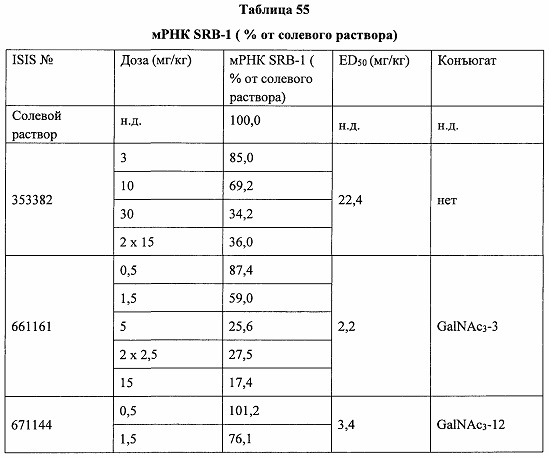
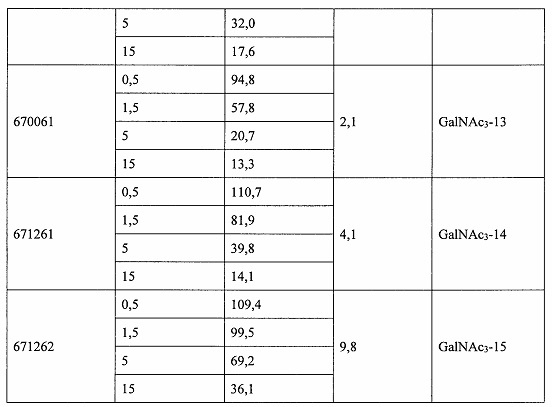
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 56.
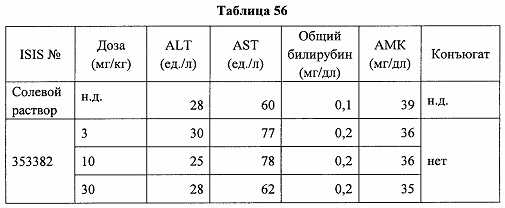
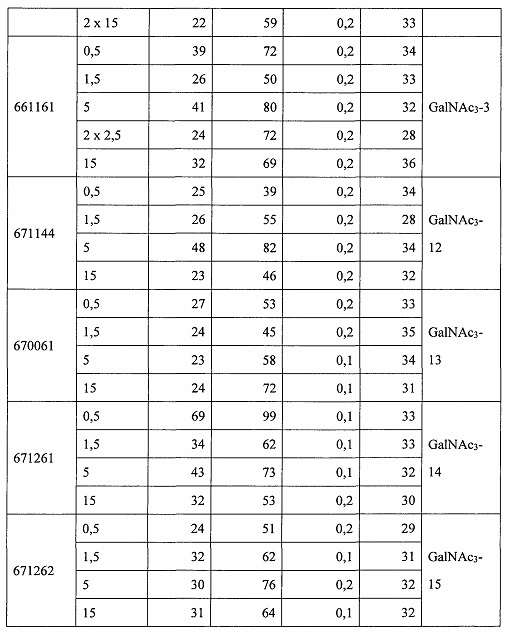
Пример 66: Влияние различных расщепляемых фрагментов на антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих кластер 5'-GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Каждая из групп конъюгата GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида при помощи фосфодиэфир-связанного нуклеозида (расщепляемый фрагмент (СМ)).
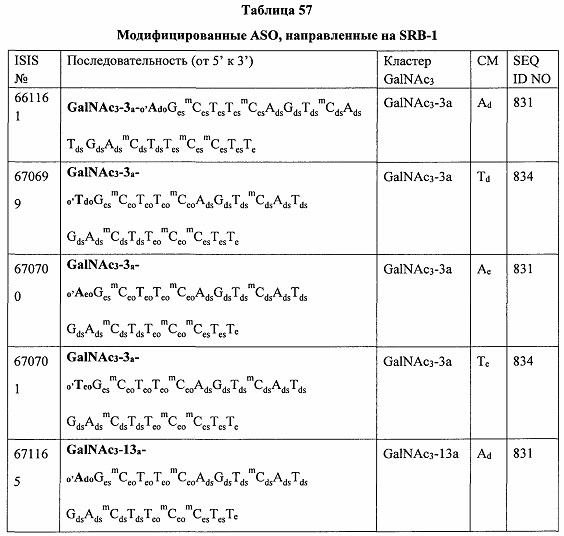
Заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-13a показана ранее в Примере 62.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, соединения ISIS 661161, 670699, 670700, 670701, 671165 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 58, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Все антисмысловые олигонуклеотиды, содержащие различные расщепляемые фрагменты, демонстрируют одинаковую эффективность.
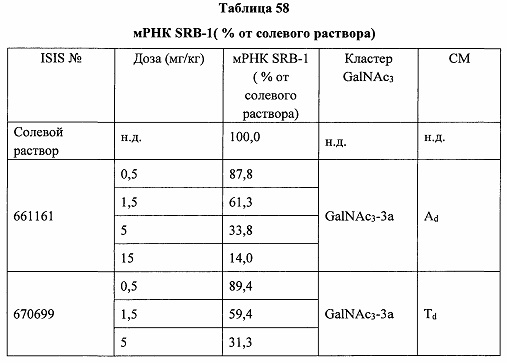
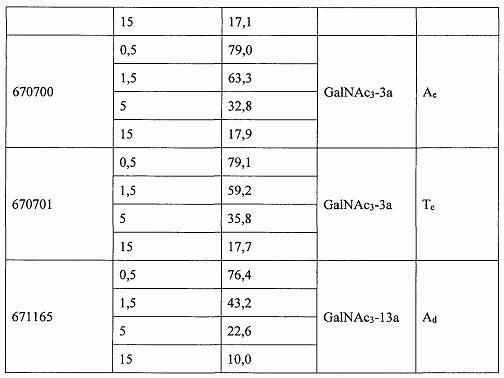
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 56.
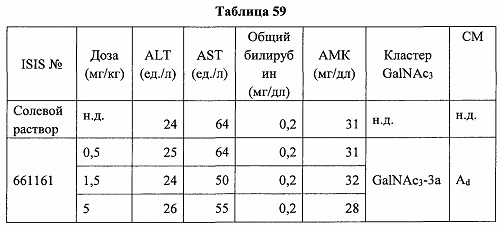
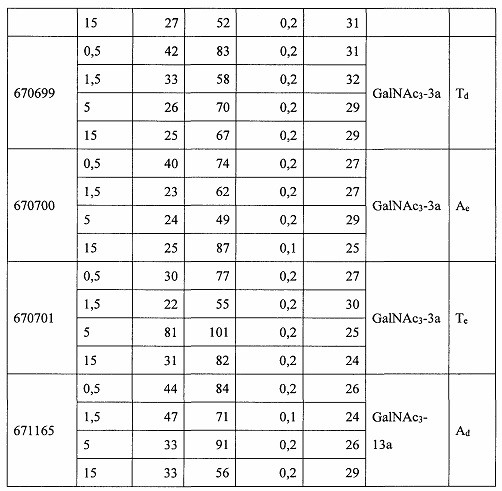
Пример 67: Получение олигомерного соединения 199, содержащего GalNAc3-16
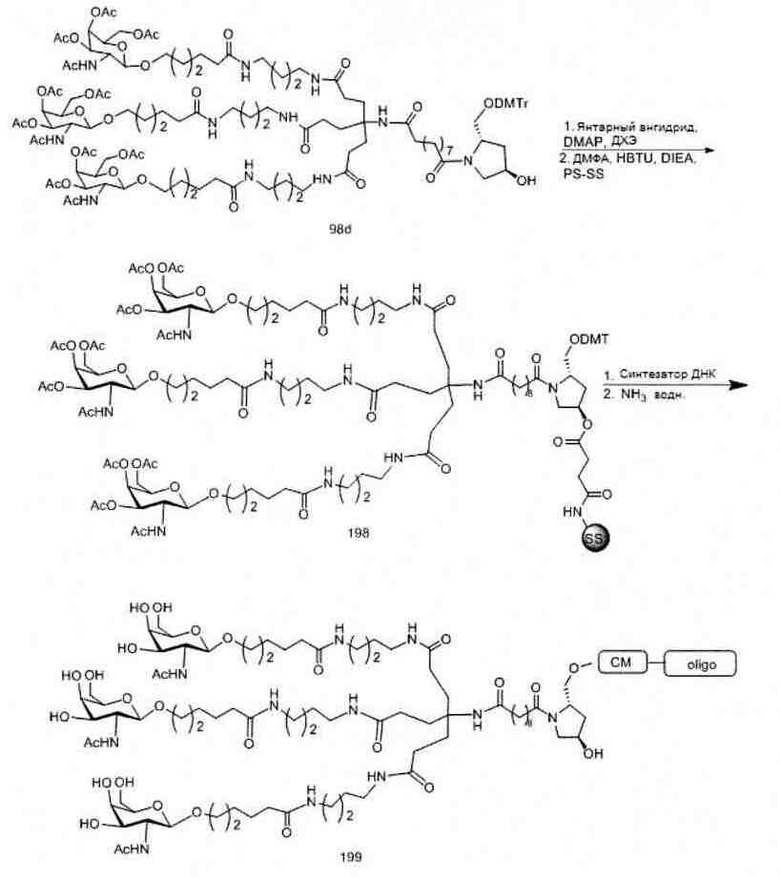
Олигомерное соединение 199, содержащее группу конъюгата GalNAc3-16, получили с помощью общих способов, описанных в Примерах 7 и 9. Кластерная часть GalNAc3 группы конъюгата GalNAc3-16 (GalNAc3-16a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-16 (GalNAc3-16a-СМ-) представлена ниже:
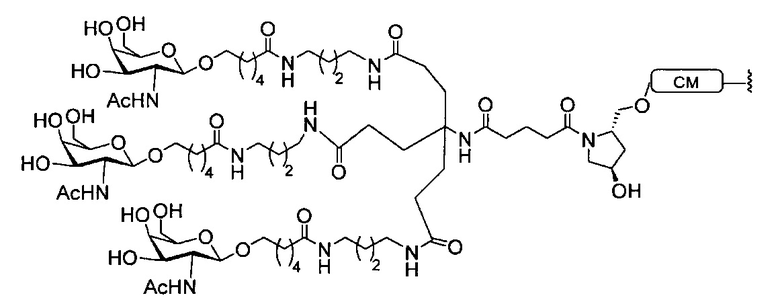
Пример 68: Получение олигомерного соединения 200, содержащего GalNAc3-17
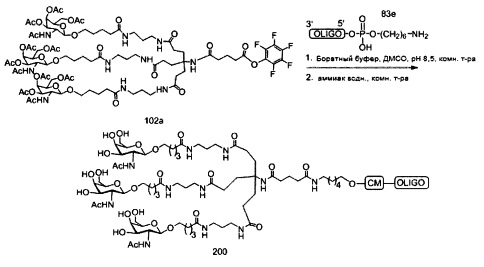
Олигомерное Соединение 200, содержащее группу конъюгата GalNAc3-17, получили по общим способам, представленным в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-17 (GalNAc3-17a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-17 (GalNAc3-17a-CM-) представлена ниже:
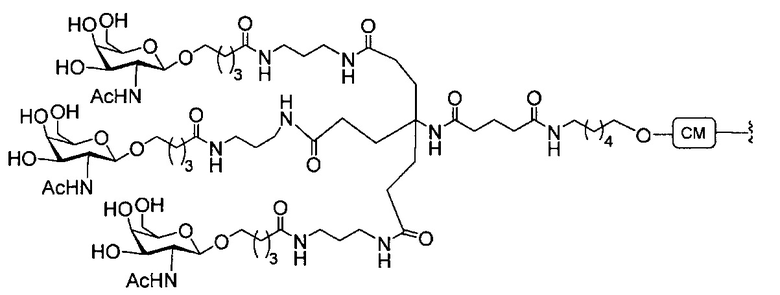
Пример 69: Получение олигомерного соединения 201, содержащего GalNAc3-18
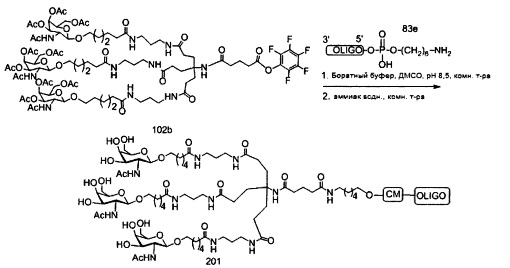
Олигомерное Соединение 201, содержащее группу конъюгата GalNAc3-18, получили по общим способам, представленным в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-18 (GalNAc3-18a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-18 (GalNAc3-18a-СМ-) представлена ниже:
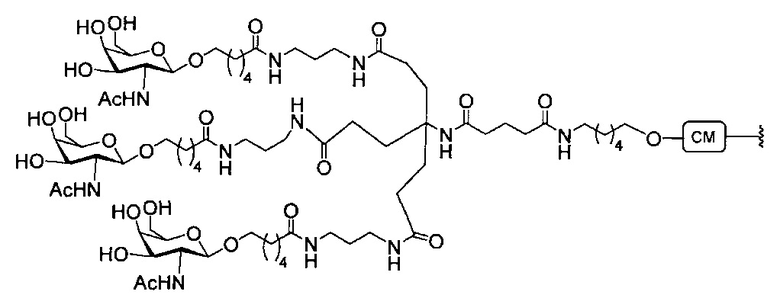
Пример 70: Получение олигомерного соединения 204, содержащего GalNAc3-19
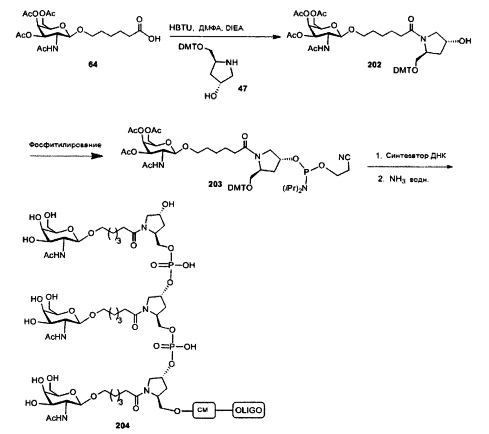
Олигомерное соединение 204, содержащее группу конъюгата GalNAc3-19, получили из соединения 64, используя общие способы, описанные в Примере 52.. Кластерная часть GalNAc3 группы конъюгата GalNAc3-19 (GalNAc3-19a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-. Структура GalNAc3-19 (GalNAc3-19a-СМ-) представлена ниже:
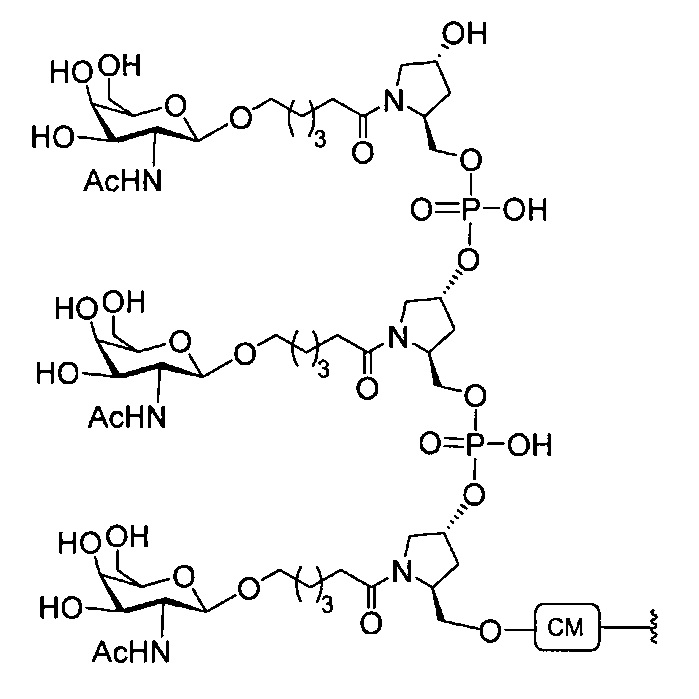
Пример 71: Получение олигомерного соединения 210, содержащего GalNAc3-20
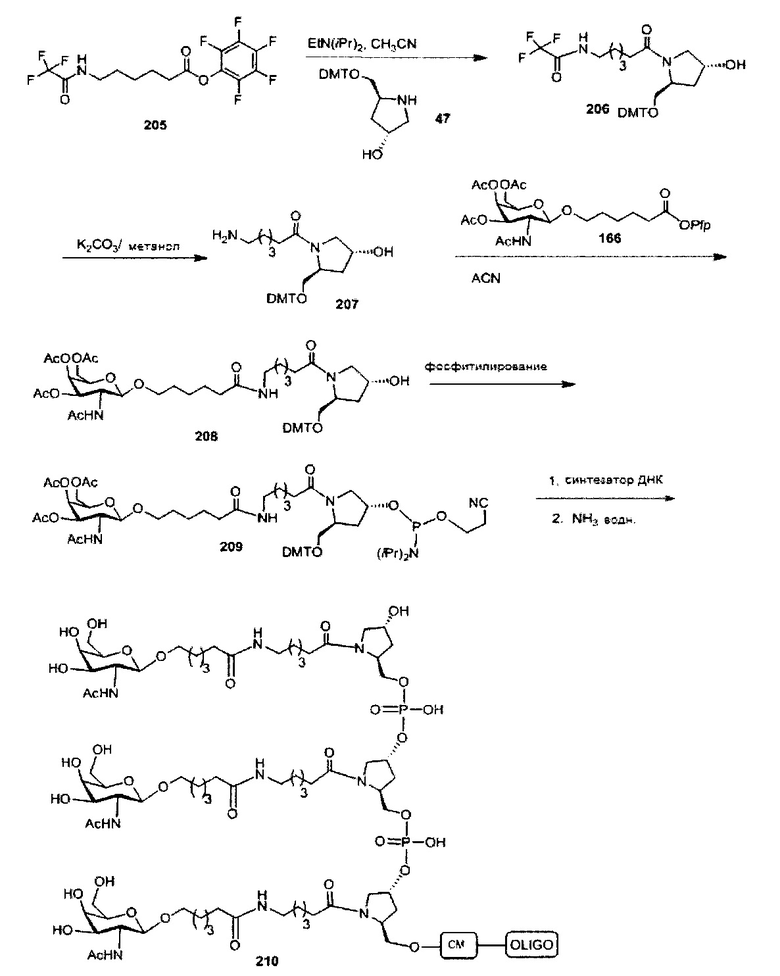
Соединение 205 получили добавлением PFP-ТФК и DIEA к 6-(2,2,2-трифторацетамидо)гексановой кислоте в ацетонитриле, которую получили добавлением трифторуксусного ангидрида к 6-аминогексановой кислоте. Реакционную смесь нагрели до 80°С, затем охладили до комнатной температуры. Олигомерное соединение 210, содержащее группу конъюгата GalNAc3-20, получили из соединения 208, используя общие способы, представленные в Примере 52. Кластерная часть GalNAc3 группы конъюгата GalNAc3-20 (GalNAc3-20a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-. Структура GalNAc3-20 (GalNAc3-20a-CM-) представлена ниже:
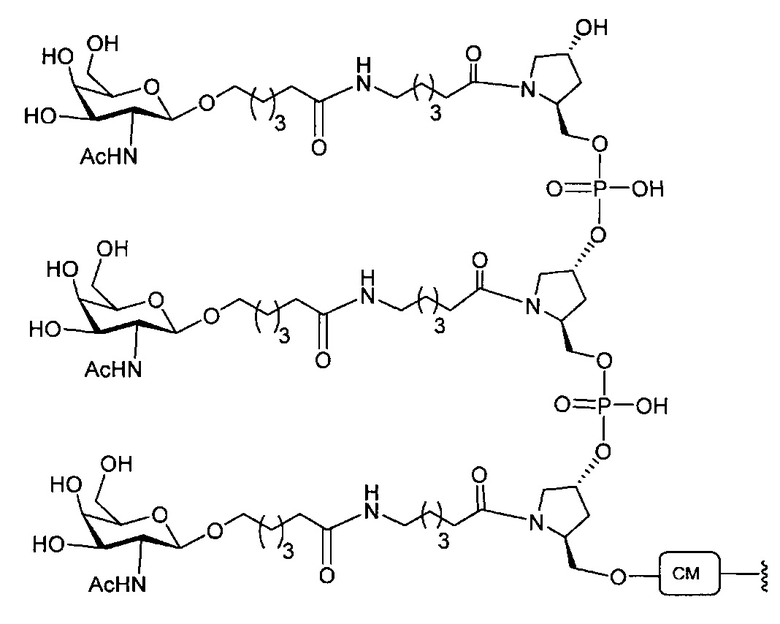
Пример 72: Получение олигомерного соединения 215, содержащего GalNAc3-21
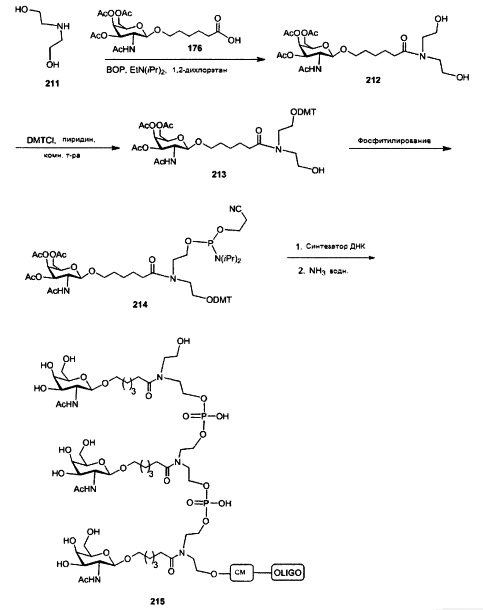
Соединение 211 имеется в продаже. Олигомерное соединение 215, содержащее группу конъюгата GalNAc3-21, получили из соединения 213, используя общие способы, представленные в Примере 52. Кластерная часть GalNAc3 группы конъюгата GalNAc3-21 (GalNAc3-21a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-21 (GalNAc3-21a-CM-) представлена ниже:
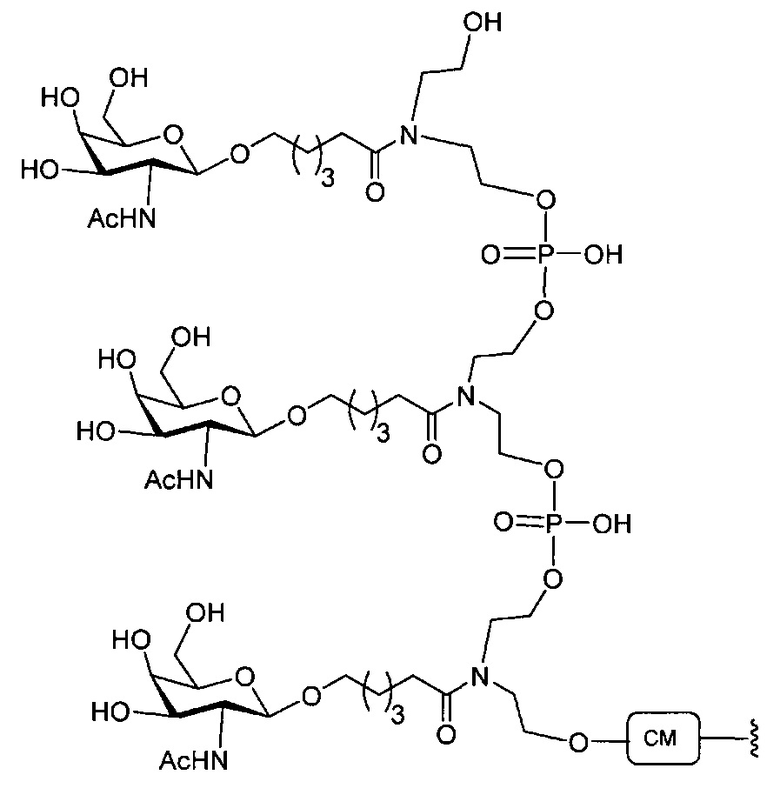
Пример 73: Получение олигомерного соединения 188, содержащего GalNAc3-22
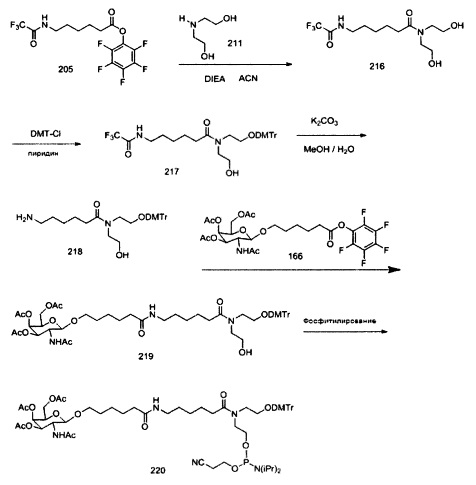
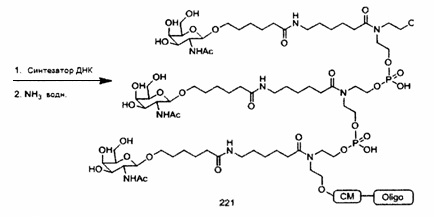
Соединение 220 получили из соединения 219, используя тетразолид диизопропиламмония. Олигомерное соединение 221, содержащее группу конъюгата GalNAc3-21, получили из соединения 220, используя общий способ, описанный в Примере 52. Кластерная часть GalNAc3 группы конъюгата GalNAc3-22 (GalNAc3-22a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-. Структура GalNAc3-22 (GalNAc3-22a-CM-) представлена ниже:
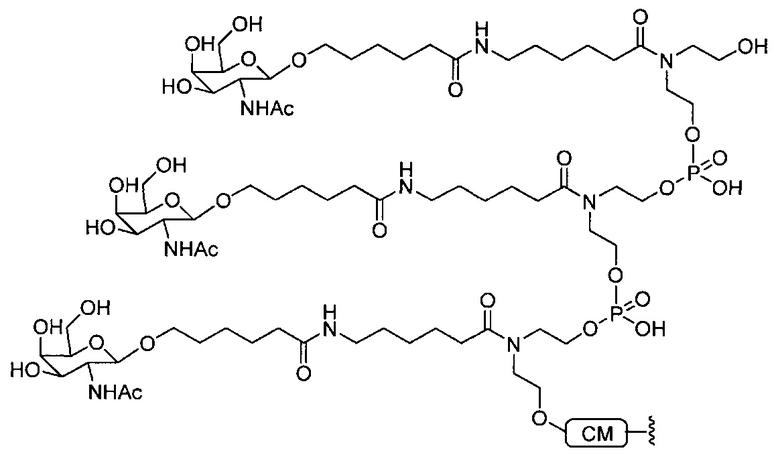
Пример 74: Влияние различных расщепляемых фрагментов на антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих конъюгат 5'-GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Каждая из групп конъюгата GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида.

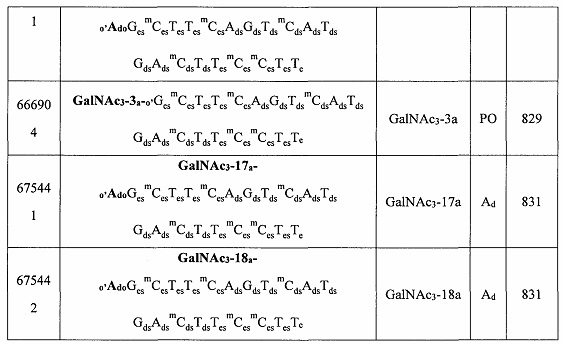
Во всех таблицах заглавные буквы указывают нуклеооснование для каждого нуклеозида, а mC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатный межнуклеозидный линкер (PS); «о» означает фосфодиэфирный межнуклеозидный линкер (РО); и «о'» означает ОР(=O)(ОН)-. Группы конъюгата выделены жирным.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-17a показана ранее в Примере 68, а структура GalNAc3-18a показана ранее в Примере 69.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, олигонуклеотида, перечисленного в Таблице 60, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 61, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Антисмысловые олигонуклеотиды, содержащие конъюгат GalNAc, демонстрируют равные эффективности и являются значительно более эффективными, чем исходный олигонуклеотид, не имеющий конъюгата GalNAc.
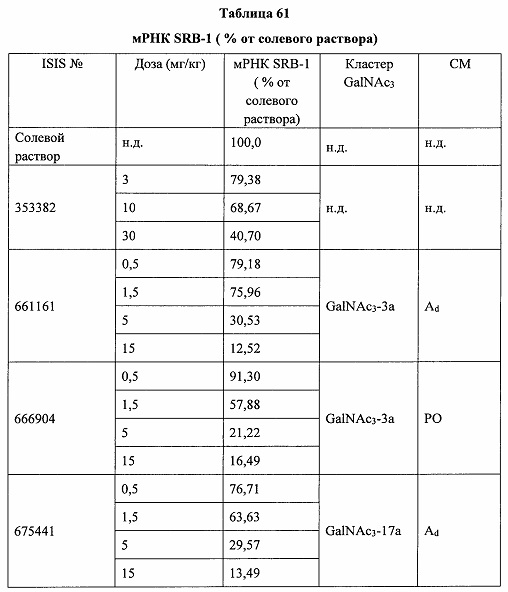
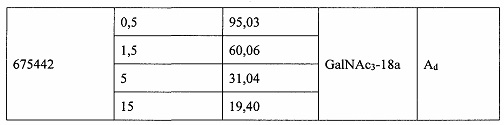
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 62.
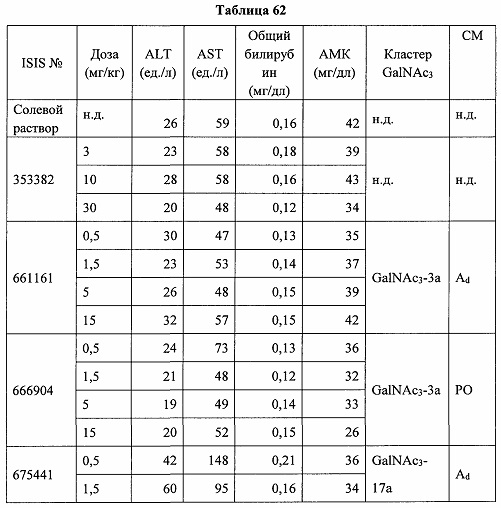
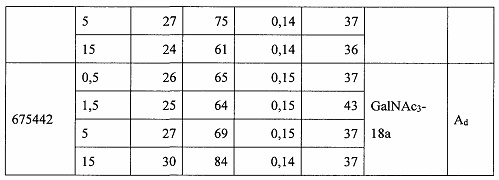
Пример 75: Фармакокинетический анализ олигонуклеотидов, содержащих 5'-группу конъюгата
ФК ASO, представленных выше в Таблицах 54, 57 и 60, оценили с использованием образцов печени, которые получили после выполнения способов лечения, описанных в Примерах 65, 66 и 74. Образцы печени измельчили и экстрагировали по стандартным протоколам, и анализировали при помощи ИП-ВЭЖХ-МС вместе с внутренним стандартом. Суммарный уровень (мкг/г) всех метаболитов в ткани измерили интегрированием соответствующих УФ пиков, а уровни в ткани ASO полной длины, не содержащих конъюгата («исходное», в данном случае Isis №353382), измерили с использованием подходящих ион-экстракционных хроматограмм (EIC).
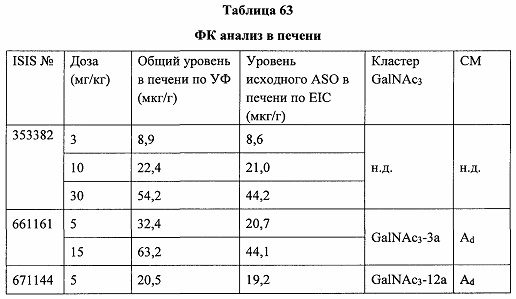
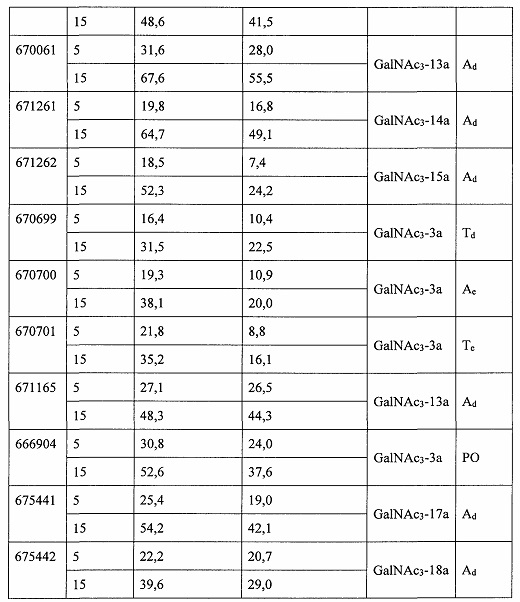
Результаты, представленные выше в Таблице 63, демонстрируют, что наблюдали более высокие уровни в печени олигонуклеотидов, содержащих группу конъюгата GalNAc3, чем исходного олигонуклеотида, не содержащего группу GalNAc3 (ISIS 353382) через 72 часа после введения олигонуклеотида, особенно с учетом введения различных доз для олигонуклеотидов с группой конъюгата GalNAc3 и без нее. Кроме того, через 72 часа 40-98% каждого олигонуклеотида, содержащего группу конъюгата GalNAc3, было метаболизировано до исходного соединения, что указывает на то, что группы конъюгата GalNAc3 расщепляются в указанных олигонуклеотидах.
Пример 76: Получение олигомерного соединения 230, содержащего GalNAc3-23
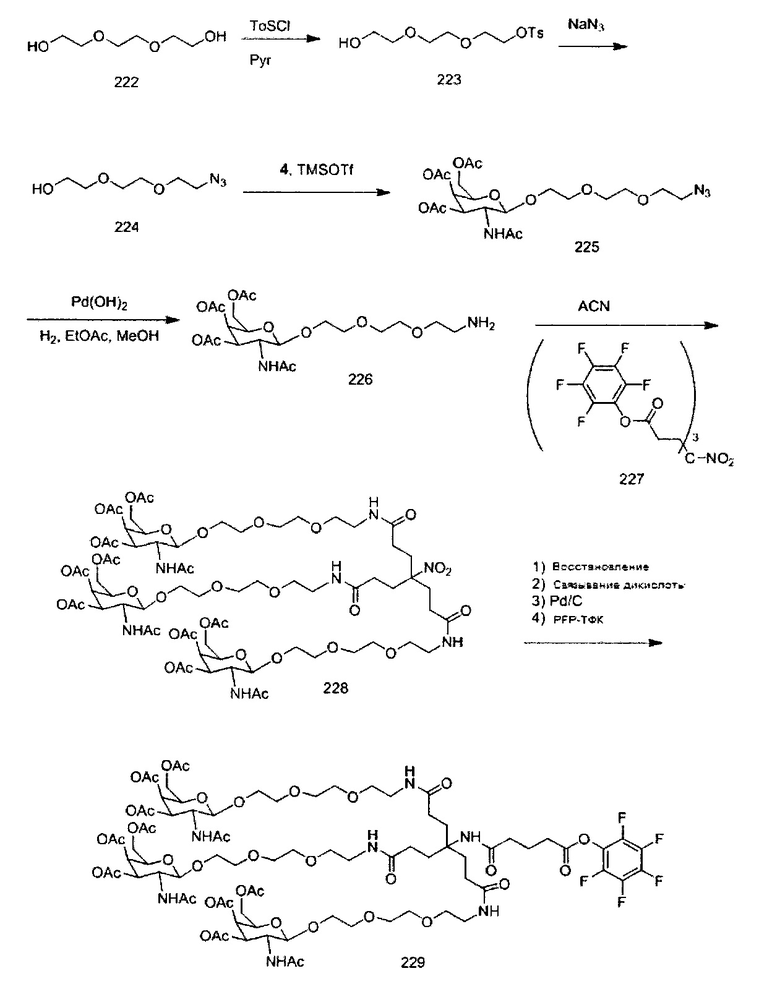
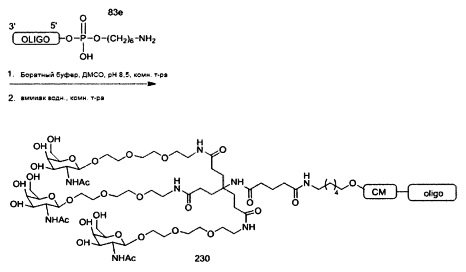
Соединение 222 имеется в продаже. 44,48 мл (0,33 моль) соединения 222 обрабатывали тозилхлоридом (25,39 г, 0,13 моль) в пиридине (500 мл) в течение 16 часов. Затем реакционную смесь выпарили до маслянистого вещества, растворили в EtOAc и промыли водой, насыщенным раствором NaHCO3, насыщенным солевым раствором и высушили над Na2SO4. Этилацетат концентрировали досуха и очистили колоночной хроматографией, элюировали EtOAc в гексанах (1:1), затем 10% метанола в CH2Cl2 с получением соединения 223 в виде бесцветного маслянистого вещества. Данные ЖХМС и ЯМР согласовались с указанной структурой. 10 г (32,86 ммоль) 1-тозилтриэтиленгликоля (соединение 223) обрабатывали азидом натрия (10,68 г, 164,28 ммоль) в ДМСО (100 мл) при комнатной температуре в течение 17 часов. Затем реакционную смесь вылили в воду и экстрагировали EtOAc. Органический слой три раза промыли водой и высушили над Na2SO4. Органический слой концентрировали досуха с получением 5,3 г соединения 224 (92%). Данные ЖХМС и ЯМР согласовались с указанной структурой. 1-Азидотриэтиленгликоль (соединение 224, 5,53 г, 23,69 ммоль) и соединение 4 (6 г, 18,22 ммоль) обработали 4А молекулярными ситами (5 г) и TMSOTf (1,65 мл, 9,11 ммоль) в дихлорметане (100 мл) под инертной атмосферой. Через 14 часов реакционную смесь отфильтровали для удаления сит, а органический слой промыли насыщенным раствором NaHCO3, водой, насыщенным солевым раствором и высушили над Na2SO4. Органический слой концентрировали досуха и очистили колоночной хроматографией, элюировали градиентом от 2 до 4% метанола в дихлорметане с получением соединения 225. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 225 (11,9 г, 23,59 ммоль) гидрировали в EtOAc/метаноле (4:1, 250 мл) на катализаторе Перлмана. Через 8 часов катализатор удалили фильтрованием, а растворители удалили досуха с получением соединения 226. Данные ЖХМС и ЯМР согласовались с указанной структурой.
Для получения соединения 227 раствор нитрометантриспропионовой кислоты (4,17 г, 15,04 ммоль) и основание Хюнига (10,3 мл, 60,17 ммоль) в ДМФА (100 мл) по каплям обработали пентафтортрифторацетатом (9,05 мл, 52,65 ммоль). Через 30 минут реакционную смесь вылили в ледяную воду и экстрагировали EtOAc. Органический слой промыли водой, насыщенным солевым раствором и высушили над Na2SO4. Органический слой концентрировали досуха, а затем перекристаллизовали из гептана с получением соединения 227 в виде белого твердого вещества. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 227 (1,5 г, 1,93 ммоль) и соединение 226 (3,7 г, 7,74 ммоль) перемешивали при комнатной температуре в ацетонитриле (15 мл) в течение 2 часов. Затем реакционную смесь выпарили досуха и очистили колоночной хроматографией, элюируя градиентом от 2 до 10% метанола в дихлорметане, с получением соединения 228. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 228 (1,7 г, 1,02 ммоль) обработали никелем Ренея (около 2 г, влажный) в этаноле (100 мл) в атмосфере водорода. Через 12 часов катализатор удалили фильтрованием, а органический слой выпарили до твердого вещества, которое использовали непосредственно на следующей стадии. Данные ЖХМС и ЯМР согласовались с указанной структурой. Это твердое вещество (0,87 г, 0,53 ммоль) обработали бензилглутаровой кислотой (0,18 г, 0,8 ммоль), HBTU (0,3 г, 0,8 ммоль) и DIEA (273,7 мкл, 1,6 ммоль) в ДМФА (5 мл). Через 16 часов ДМФА удалили при пониженном давлении при 65°С до маслянистого вещества, и это маслянистое вещество растворили в дихлорметане. Органический слой промыли насыщенным раствором NaHCO3, насыщенным солеым раствором и высушили над Na2SO4. После выпаривания органического слоя соединение очистили колоночной хроматографией и элюировали градиентом от 2 до 20% метанола в дихлорметане с получением связанного продукта. Данные ЖХМС и ЯМР согласовались с указанной структурой. С бензилового эфира сняли защиту на катализаторе Перлмана в атмосфере водорода в течение 1 часа. Затем катализатор удалили фильтрованием, а растворители удалили досуха с получением кислоты. Данные ЖХМС и ЯМР согласовались с указанной структурой. Эту кислоту (486 мг, 0,27 ммоль) растворили в сухом ДМФА (3 мл). Добавили пиридин (53,61 мкл, 0,66 ммоль) и продули реакционную смесь аргоном. К реакционной смеси медленно добавили пентафтортрифторацетат (46,39 мкл, 0,4 ммоль). Цвет реакционной смеси изменился с бледно-желтого на винный, и появился легкий дымок, который улетучился с потоком аргона. Реакционную смесь оставили перемешиваться при комнатной температуре на один час (завершение реакции подтвердили по ЖХМС). Растворитель удалили при пониженном давлении (ротационный испаритель) при 70°С. Остаток разбавили ДХМ и промыли 1 н. NaHSO4, насыщенным солевым раствором, насыщенным раствором бикарбоната натрия и снова насыщенным солевым раствором. Органический слой высушили над Na2SO4, отфильтровали и концентрировали досуха с получением 225 мг соединения 229 в виде хрупкой желтой пены. Данные ЖХМС и ЯМР согласовались с указанной структурой.
Олигомерное соединение 230, содержащее группу конъюгата GalNAc3-23, получили из соединения 229, используя общий способ, описанный в Примере 46. Кластерная часть GalNAc3 группы конъюгата GalNAc3-23 (GalNAc3-23a) может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Структура GalNAc3-23 (GalNAc3-23a-CM) представлена ниже:
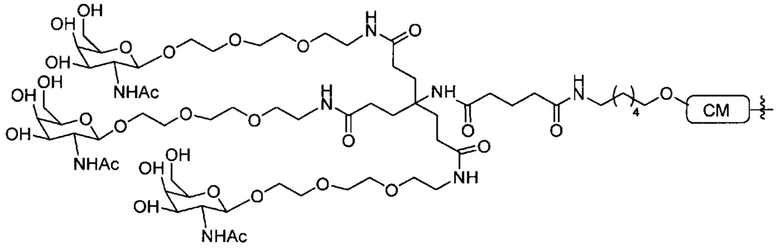
Пример 77: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
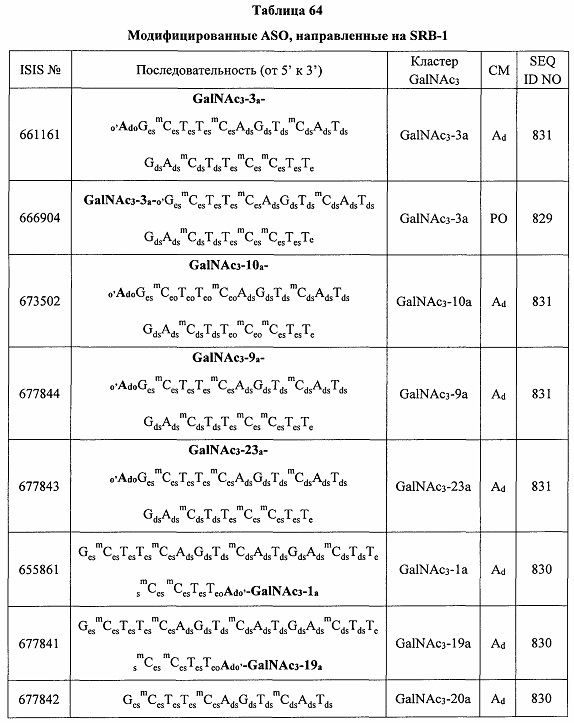
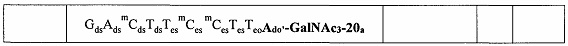
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3а показана в Примере 39, GalNAc3-9a показана в Примере 52, GalNAc3-10a показана в Примере 46, GalNAc3-19a показана в Примере 70, GalNAc3-20a показана в Примере 71 и GalNAc3-23a показана в Примере 76.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) вели однократную подкожную инъекцию дозы, представленной ниже, олигонуклеотида, перечисленного в Таблице 64, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения для определения уровней мРНК SRB-1 при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 65, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом.
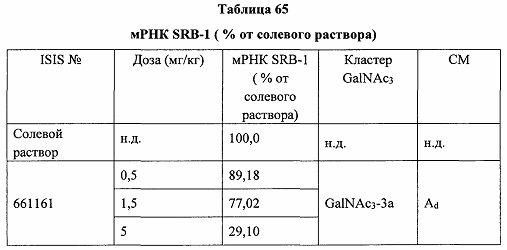
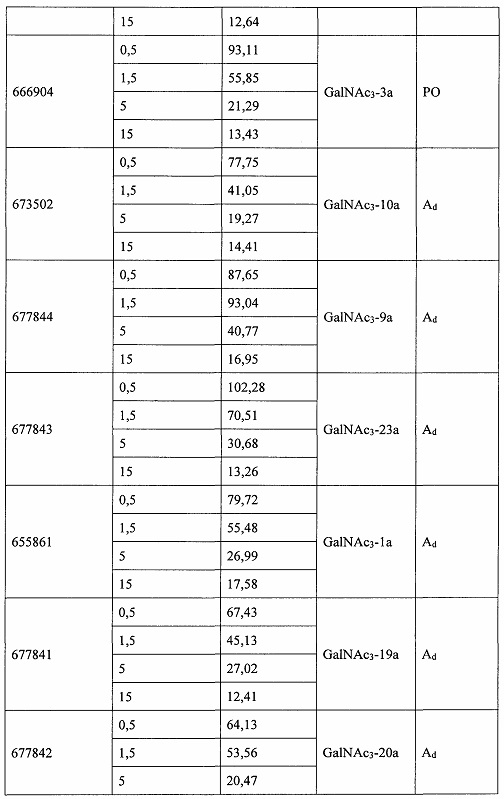
Измерили также уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке, используя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК представлены ниже в Таблице 66.
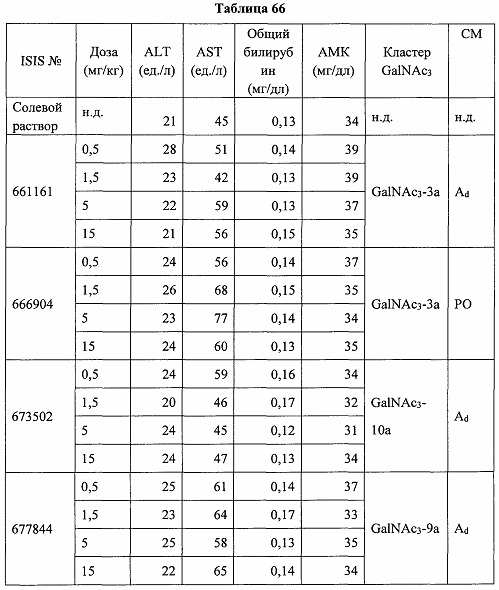
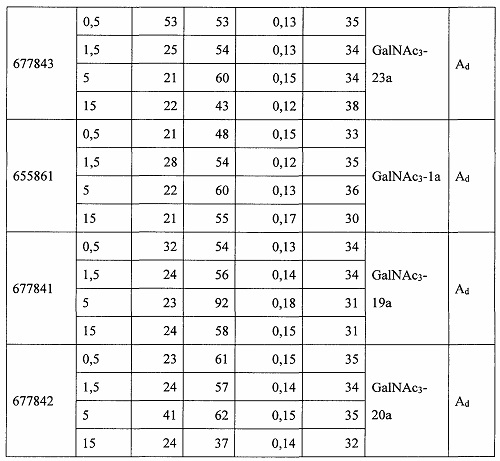
Пример 78: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на ангиотензиноген, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования ангиотензиногена (AGT) у нормотензивных мышей Спрага-Доули.

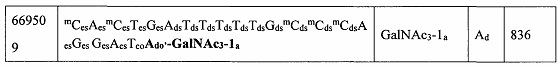
Структура GalNAc3-1a показана ранее в Примере 9.
Лечение
Шестинедельным самцам крыс Спрага-Доули один раз в неделю вводили подкожную инъекцию дозы, представленной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 67, или PBS. Каждая экспериментальная группа состояла из 4 животных. Крыс усыпили через 72 часа после последней дозы. Уровни мРНК AGT в печени измерили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка AGT в плазме измерили при помощи твердофазного иммуноферментного анализа для определения общего ангиотензиногена (кат. № JP27412, IBL International, Торонто, штат Онтарио) с разбавлением плазмы 1:20000. Результаты, показанные ниже, представлены как средний процент от уровней мРНК AGT в печени или от уровней белка AGT в плазме для каждой экспериментальной группы, нормализованных к контрольному образцу с PBS.
Как показано в Таблице 68, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК AGT в печени и уровни белка в плазме дозозависимым образом, и олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным, чем исходный олигонуклеотид, не содержащий конъюгата GalNAc.
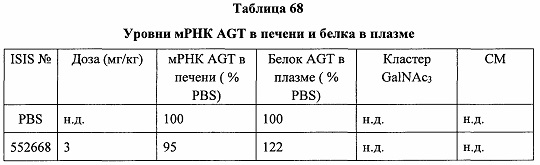
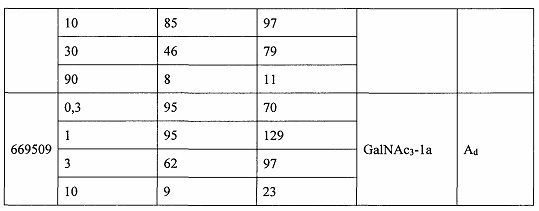
Измерили также уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в плазме, а также массу тела в момент умерщвления, используя стандартные протоколы. Результаты представлены ниже в Таблице 69.
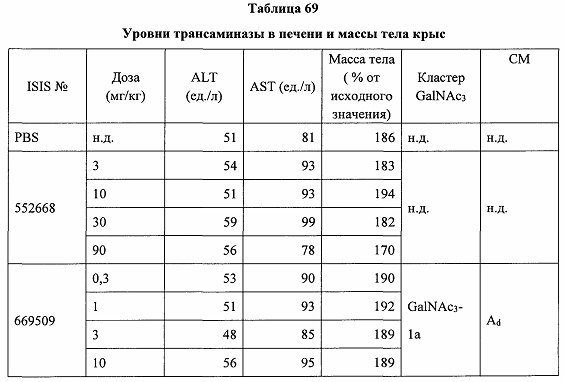
Пример 79: Продолжительность действия in vivo олигонуклеотидов, направленных на APOC-III, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 70, испытали в исследовании однократной дозы на продолжительность действия у мышей.
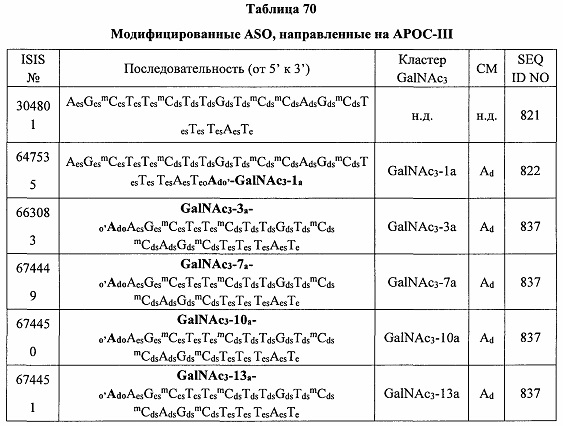
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46 и GalNAc3-13a показана в Примере 62.
Лечение
Шести-восьминедельным трансгенным мышам, экспрессирующим человеческий APOC-III, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 70, или PBS. Каждая экспериментальная группа состояла из 3 животных. Образцы крови брали до введения дозы для определения исходного значения, а также через 72 часа, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель и 6 недель после введения дозы. Уровни триглицеридов и белка APOC-III в плазме измеряли так, как описано в Примере 20. Результаты, показанные ниже, представлены как средний процент от уровней триглицеридов и APOC-III в плазме для каждой экспериментальной группы, нормализованных и исходным значениям, и они демонстрируют, что олигонуклеотиды, содержащие группу конъюгата GalNAc, обладают более продолжительным действием, чем исходный олигонуклеотид, не содержащий группу конъюгата (ISIS 304801) даже несмотря на то, что доза исходного соединения была в три раза выше, чем доза олигонуклеотидов, содержащих группу конъюгата GalNAc.
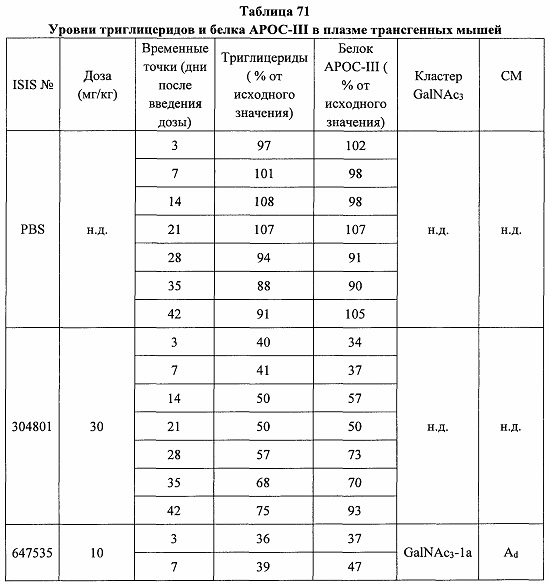
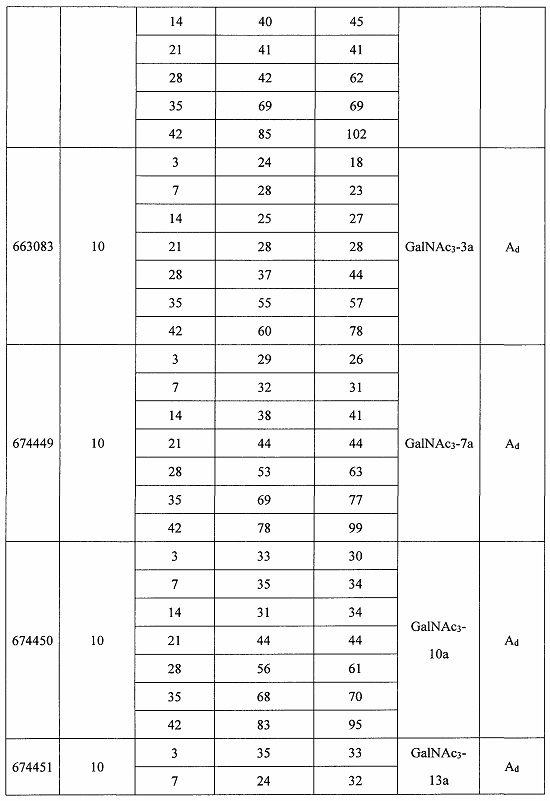
Пример 80: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на альфа-1 антитрипсин (А1АТ), содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 72, испытали в исследовании дозозависимого ингибирования А1АТ у мышей.

Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46 и GalNAc3-13a показана в Примере 62.
Лечение
Шестинедельным самцам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один раз в неделю вводили подкожную инъекцию дозы, представленной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 72, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения. Уровни мРНК А1АТ в печени определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка А1АТ в плазме определили при помощи твердофазного иммуноферментного анализа для определения мышиного альфа 1-антитрипсина (кат. №41-A1AMS-E01, Alpco, Салем, штат Нью-Гэмпшир). Результаты, показанные ниже, представлены как средний процент уровней мРНК А1АТ в печени и белка в плазме для каждой экспериментальной группы, нормализованных к контрольному образцу с PBS.
Как показано в Таблице 73, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК А1АТ в печени и уровни белка А1АТ в плазме дозозависимым образом. Олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем исходное соединение (ISIS 476366).
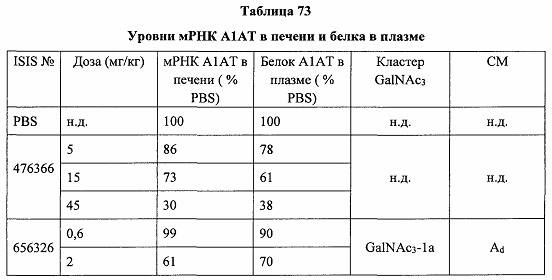
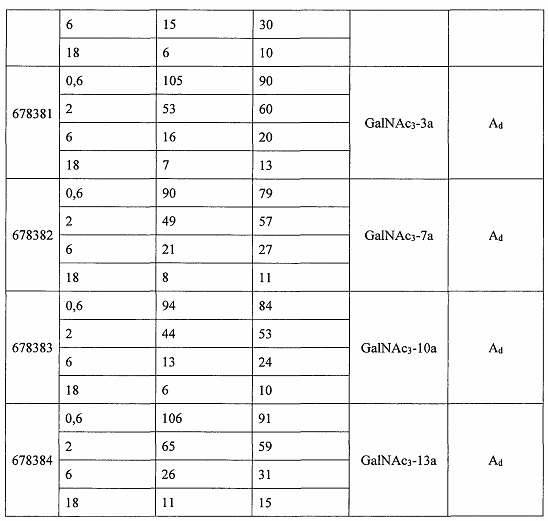
Во время умерщвления измерили уровни трансаминазы в печени и АМК в плазме по стандартным протоколам. Измерили также массы тела и массы органов. Результаты представлены ниже в Таблице 74. Масса тела представлена как % относительно исходного значения. Массы органов представлены как % от массы тела относительно контрольной группы с PBS.
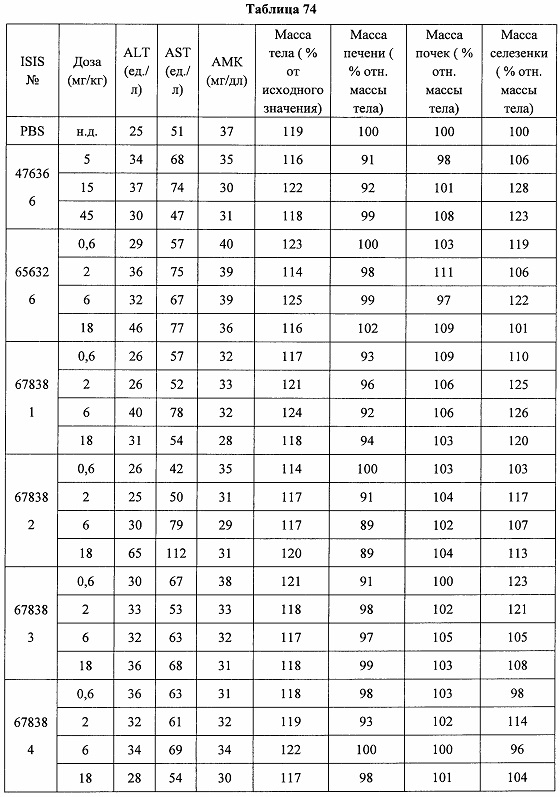
Пример 81: Продолжительность действия in vivo олигонуклеотидов, направленных на А1АТ, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные в Таблице 72, испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Шестинедельным самцам мышей C57BL/6 ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 72, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали за день до введения дозы для определения исходного значения, а также на 5, 12, 19 и 25 день после введения дозы. Уровни белка А1АТ в плазме измерили при помощи твердофазного иммуноферментного анализа (см. Пример 80). Результаты, показанные ниже, представлены как средний процент уровней белка А1АТ в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Результаты демонстрируют, что Олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными и имели более продолжительное действие, чем исходное соединение без конъюгата GalNAc (ISIS 476366). Кроме того, Олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 678381, 678382, 678383 и 678384), были, в целом, еще более эффективными с еще более продолжительным действием, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656326).
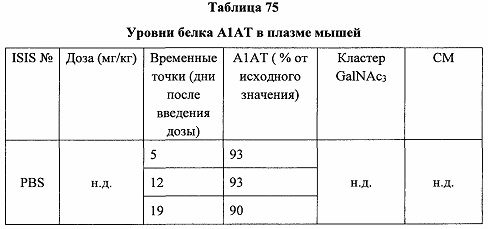
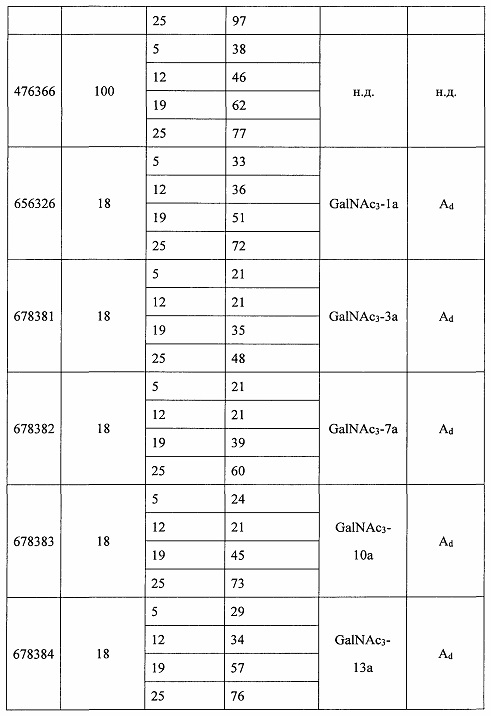
Пример 82: Антисмысловое ингибирование in vitro под действием олигонуклеотидов, направленных на SRB-1, содержащих конъюгат GalNAc3
Первичные гепатоциты печени мышей высеивали в 96-луночные планшеты при 15000 клеток на лунку за 2 часа до обработки. Олигонуклеотиды, перечисленные в Таблице 76, добавили в концентрации 2, 10, 50 или 250 нМ в среде Уильяма Е, и инкубировали клетки в течение ночи при 37°С в 5% CO2. Клетки лизировали через 16 часов после добавления олигонуклеотида, а общую РНК очистили при помощи RNease 3000 BioRobot (Qiagen). Уровни мРНК SRB-1 определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Значения IC50 определили при помощи программы Prism 4 (GraphPad). Результаты демонстрируют, что олигонуклеотиды, содержащие множество различных групп конъюгата GalNAc и множество различных расщепляемых фрагментов, являются значительно более эффективными в т vitro эксперименте свободного поглощения, чем исходные олигонуклеотиды, не содержащие группу конъюгата GalNAc (ISIS 353382 и 666841).

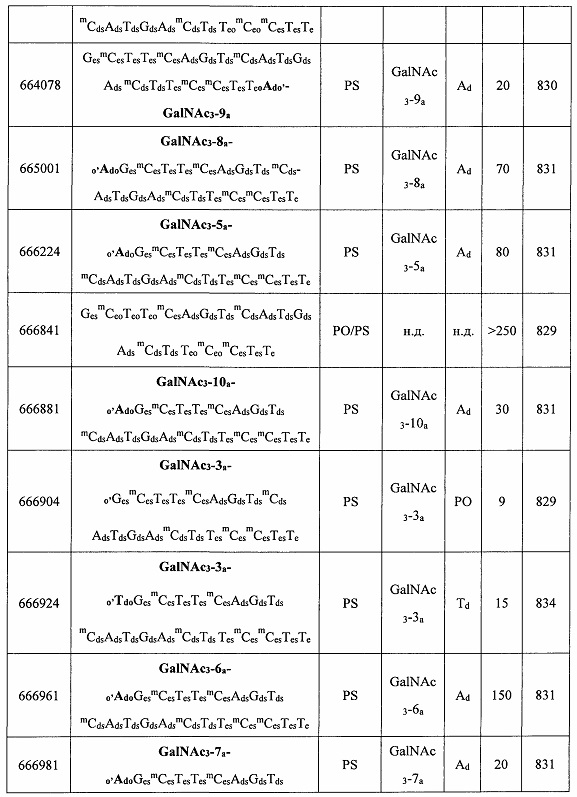
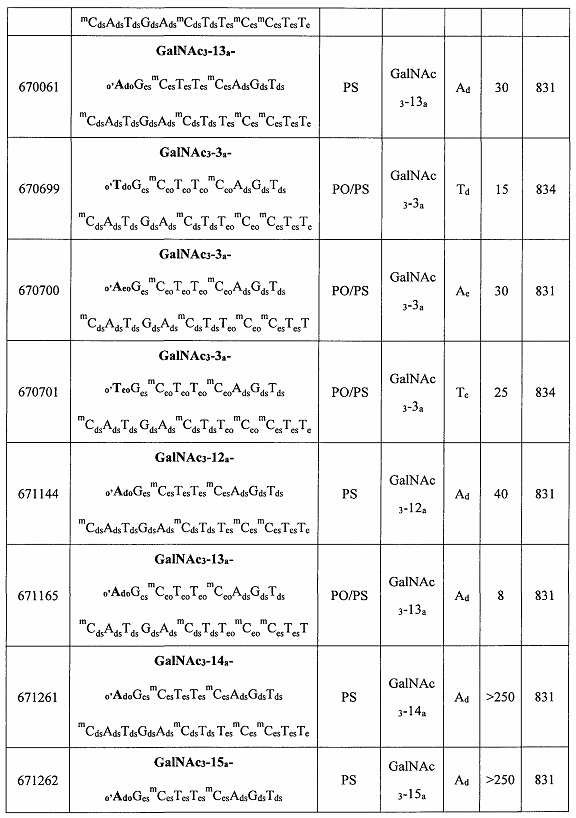
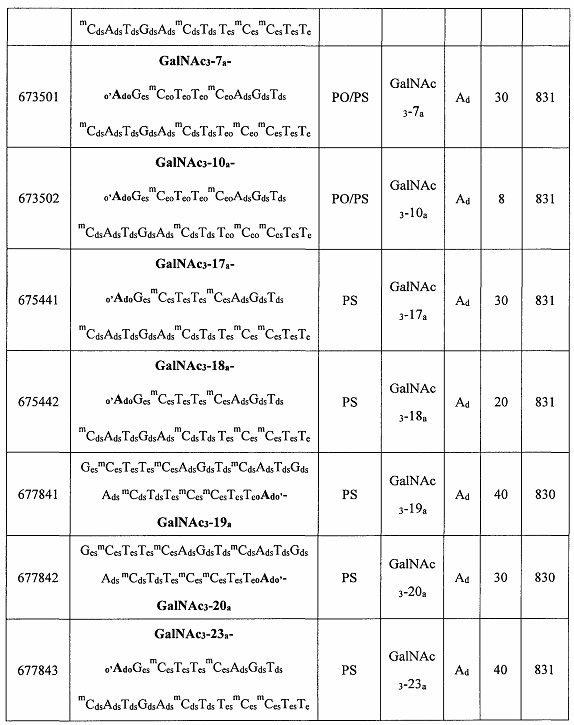
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3а показана в Примере 39, GalNAc3-5a показана в Примере 49, GalNAc3-6a показана в Примере 51, GalNAc3-7a показана в Примере 48, GalNAc3-8a показана в Примере 47, GalNAc3-9a показана в Примере 52, GalNAc3-10a показана в Примере 46, GalNAc3-12a показана в Примере 61, GalNAc3-13a показана в Примере 62, GalNAc3-14a показана в Примере 63, GalNAc3-15a показана в Примере 64, GalNAc3-17a показана в Примере 68, GalNAc3-18a показана в Примере 69, GalNAc3-19a показана в Примере 70, GalNAc3-20a показана в Примере 71 и GalNAc3-23a показана в Примере 76.
Пример 83: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на фактор XI, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 77, испытали в исследовании дозозависимого ингибирования фактора XI у мышей.
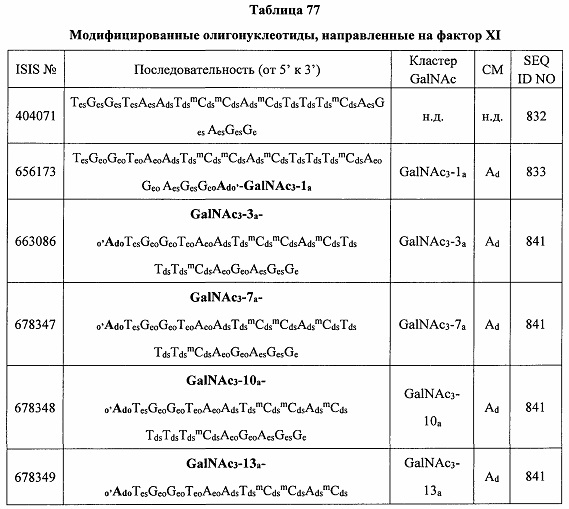
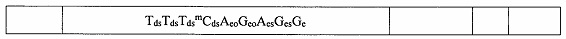
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3а показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46 и GalNAc3-13a показана в Примере 62.
Лечение
Шести-восьминедельным мышам один раз в неделю вводили подкожную инъекцию дозы, представленной ниже, в целом три дозы олигонуклеотида, перечисленного ниже, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последней дозы. Уровни мРНК фактора XI в печени измерили при помощи ПЦР в реальном времени и нормализовали к циклофилину по стандартным протоколам. Измерили также трансаминазы в печени, АМК и билирубин. Результаты, показанные ниже, представлены как средний процент для каждой экспериментальной группы, нормализованный к контролю с PBS.
Как показано в Таблице 78, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК фактора XI в печени дозозависимым образом. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными, чем исходное соединение без конъюгата GalNAc (ISIS 404071). Кроме того, олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 663086, 678347, 678348 и 678349), были еще более эффективными, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656173).
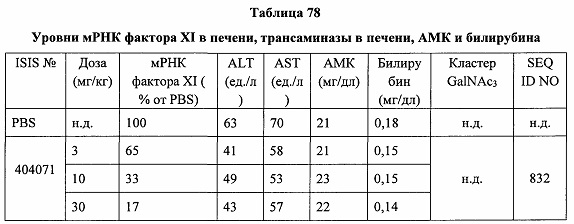
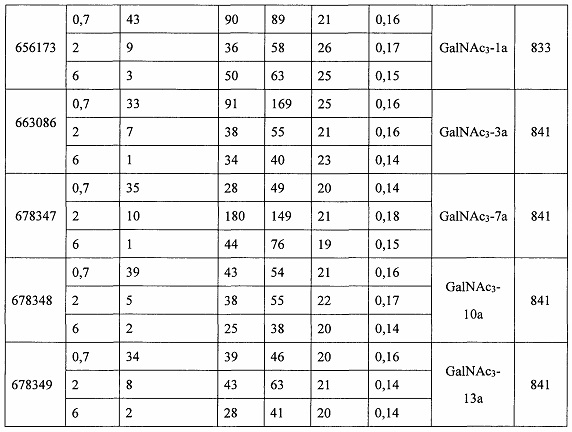
Пример 84: Продолжительность действия in vivo олигонуклеотидов, направленных на фактор XI, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 77, испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Шести-восьминедельным мышам ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 77, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали из хвостовой вены за день до введения дозы для определения исходного значения, а также на 3, 10 и 17 день после введения дозы. Уровни белка фактора XI в плазме определяли твердофазным иммуноферментным анализом, используя иммобилизованные и биотинилированные детекторные антитела для фактора XI производства R & D Systems, Миннеаполис, штат Миннесота (кат. № AF2460 и № BAF2460, соответственно), а также реагент OptEIA, набор В (кат. №550534, BD Biosciences, Сан-Хосе, штат Калифорния). Результаты, показанные ниже, представлены как средний процент уровней белка фактора XI в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными и имели более продолжительное действие, чем исходное соединение без конъюгата GalNAc (ISIS 404071). Кроме того, олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 663086, 678347, 678348 и 678349), были еще более эффективными с еще более продолжительным действием, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656173).
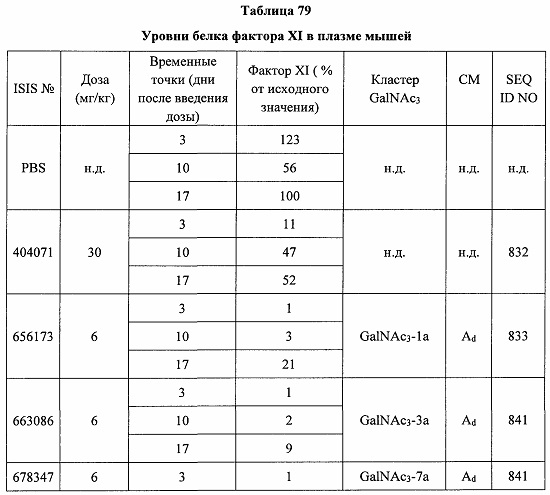
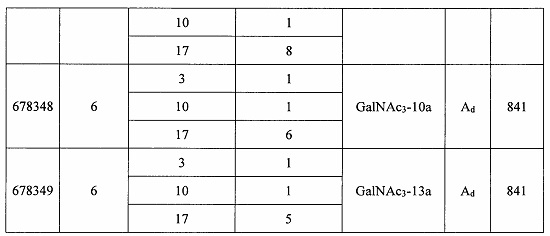
Пример 85: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 76, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
Лечение
Шести-восьминедельным мышам C57BL/6 один раз в неделю вводили подкожную инъекцию дозы, представленной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 76, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 48 часов после последнего введения для определения уровней мРНК SRB-1 при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 в печени для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблицах 80 и 81, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом.

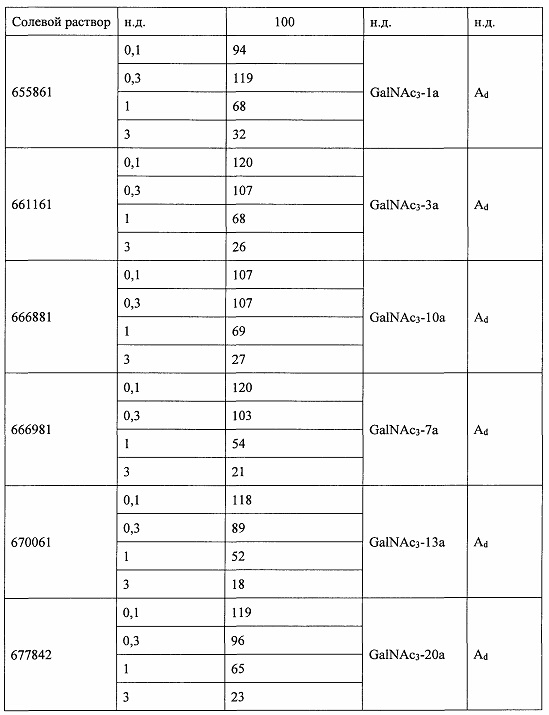

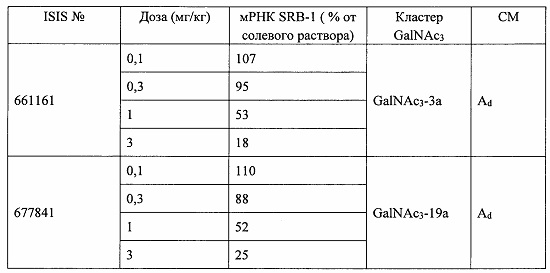
Измерили также уровни трансаминазы в печени, общего билирубина, АМК и массы тела по стандартным протоколам. Средние значения для каждой экспериментальной группы представлены ниже в Таблице 82.
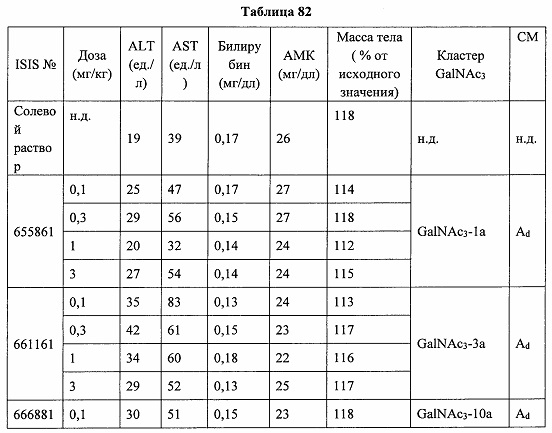
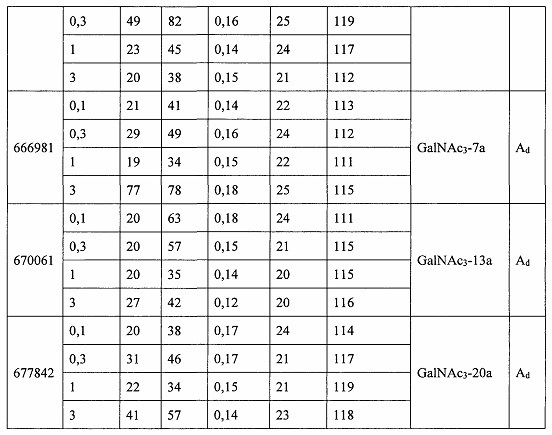
Пример 86: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на TTR, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 83, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого транстиретина (TTR) у трансгенных мышей, экспрессирующих человеческий TTR ген.
Лечение
Восьминедельным TTR трансгенным мышам один раз в неделю в течение трех недель, в целом три дозы, вводили подкожную инъекцию олигонуклеотида и дозы, перечисленных в представленных ниже таблицах, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения. В течение эксперимента в различных временных точках брали образцы крови из хвостовой вены и измеряли уровни белка TTR в плазме, ALT и AST, которые представлены в Таблицах 85-87. После усыпления животных измерили уровни ALT, AST и человеческого TTR в плазме, а также массы тела, массы органов и уровни мРНК человеческого TTR в печени. Уровни белка TTR измерили при помощи клинического анализатора (AU480, Beckman Coulter, штат Калифорния). ПЦР в реальном времени и реагент для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) использовали по стандартным протоколам для определения уровней мРНК человеческого TTR в печени. Результаты, показанные в Таблицах 84-87, представляют собой средние значения для каждой экспериментальной группы. Уровни мРНК представляют собой средние значения относительно среднего значения для PBS группы. Уровни белка в плазме представляют собой средние значения относительно среднего значения для PBS группы в исходном состоянии. Массы тела представляют собой среднее процентное изменение массы от исходного значения до умерщвления для каждой отдельной экспериментальной группы. Представленные массы органов нормализованы к массе тела животного, а затем представлена средняя нормализованная масса органов для каждой экспериментальной группы относительно средней нормализованной массы органов для PBS группы.
В Таблицах 84-87 «BL» означает исходное значения измерений, выполненных непосредственно перед введением первой дозы. Как показано в Таблицах 84 и 85, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии TTR дозозависимым образом. Олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными, чем исходное соединение без конъюгата GalNAc (ISIS 420915). Кроме того, олигонуклеотиды, содержащие конъюгат GalNAc и смешанные PS/PO межнуклеозидные линкеры, были еще более эффективными, чем олигонуклеотид, содержащий конъюгат GalNAc и только PS линкеры.

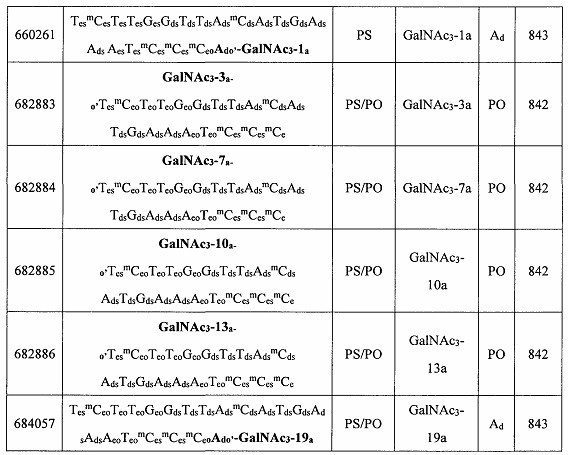
Легенда для Таблицы 85 представлена в Примере 74. Структура GalNAc3-1 показана в Примере 9. Структура GalNAc3-3а показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10а показана в Примере 46. Структура GalNAc3-13a показана в Примере 62. Структура GalNAc3-19a показана в Примере 70.
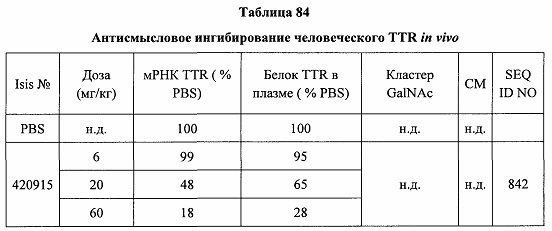
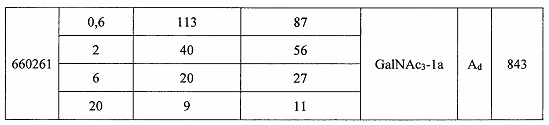
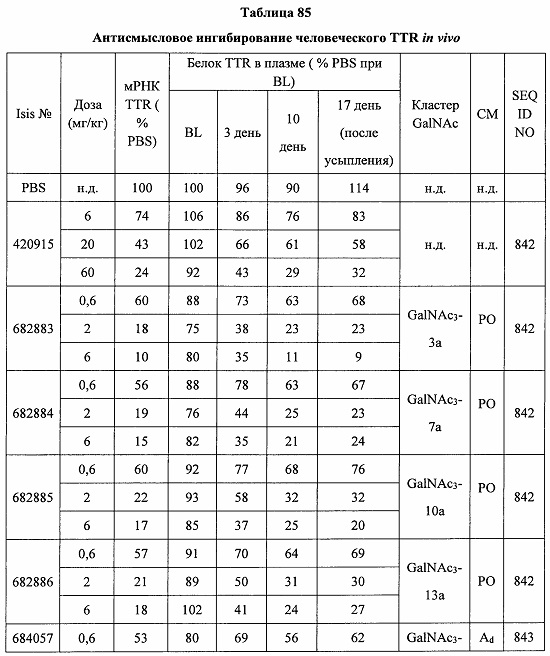
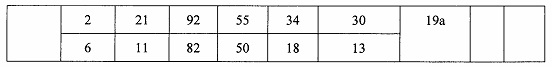
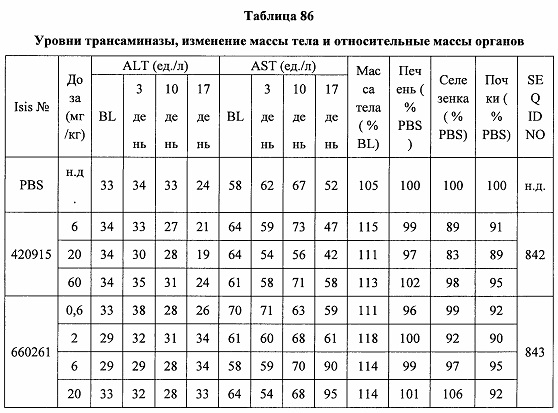
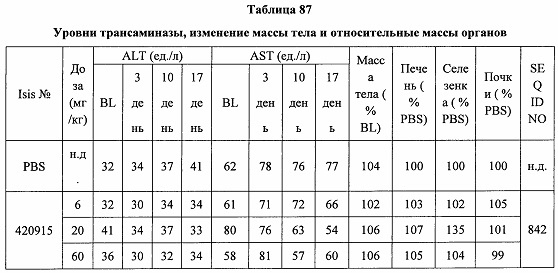
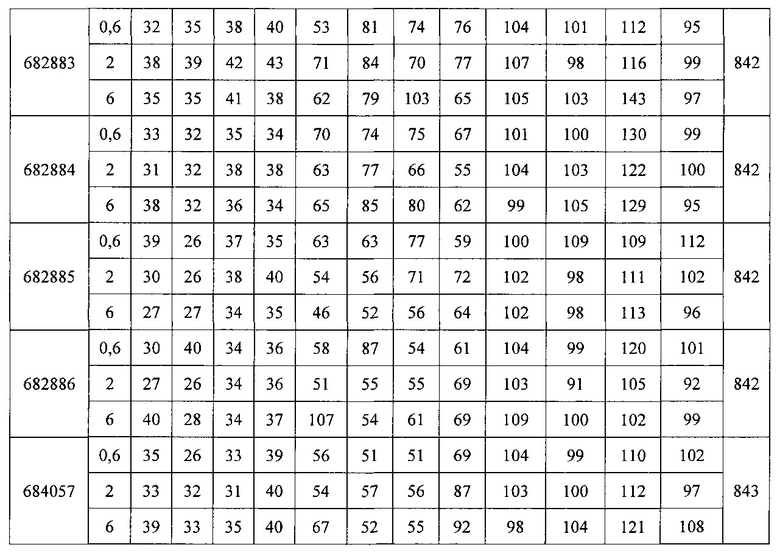
Пример 87: Продолжительность действия in vivo однократных доз олигонуклеотидов, направленных на TTR, содержащих кластер GalNAc3
ISIS №420915 и 660261 (см. Таблицу 83), испытали в исследовании однократной дозы на продолжительность действия у мышей. ISIS №420915, 682883 и 682885 (см. Таблицу 83) также испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Восьминедельным самцам трансгенных мышей, которые экспрессируют человеческий TTR, ввели однократную подкожную инъекцию 100 мг/кг ISIS №420915 или 13,5 мг/кг ISIS №660261. Каждая экспериментальная группа состояла из 4 животных. Образцы крови из хвостовой вены брали до введения дозы для определения исходных показателей и на 3, 7, 10, 17, 24 и 39 день после введения дозы. Уровни белка TTR в плазме измерили так, как описано в Примере 86. Результаты, показанные ниже, представлены как средний процент уровней TTR в плазме для каждой экспериментальной группы, нормализованных к исходным уровням.
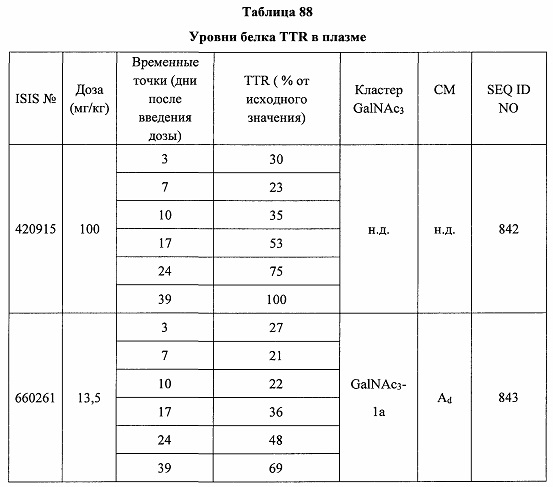
Лечение
Восьминедельным самкам трансгенных мышей, которые экспрессируют человеческий TTR, ввели однократную подкожную инъекцию 100 мг/кг ISIS №420915,10,0 мг/кг ISIS №682883 или 10,0 мг/кг 682885. Каждая экспериментальная группа состояла из 4 животных. Образцы крови из хвостовой вены брали до введения дозы для определения исходных показателей и на 3, 7, 10, 17, 24 и 39 день после введения дозы. Уровни белка TTR в плазме измерили так, как описано в Примере 86. Результаты, показанные ниже, представлены как средний процент уровней TTR в плазме для каждой экспериментальной группы, нормализованных к исходным уровням.
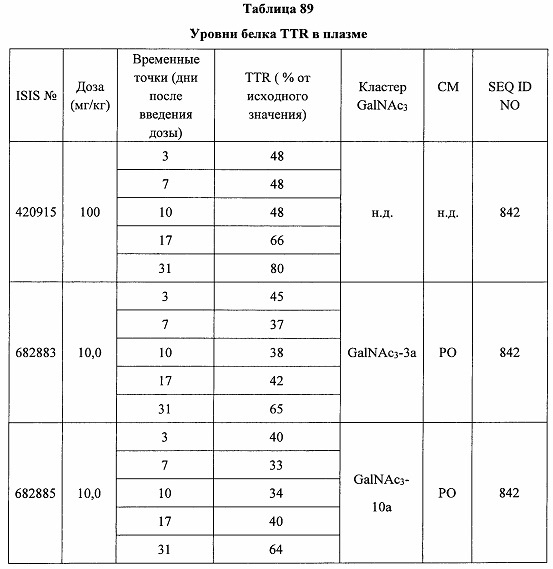
Результаты в Таблицах 88 и 89 демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, являются более эффективными и имеют более продолжительное действие, чем исходный олигонуклеотид без конъюгата (ISIS 420915).
Пример 88: Сплайсинг-модулирование in vivo под действием олигонуклеотидов, направленных на SMN, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 90, испытали на сплайсинг-модулирование человеческих генов выживаемости мотонейронов (SMN) у мышей.
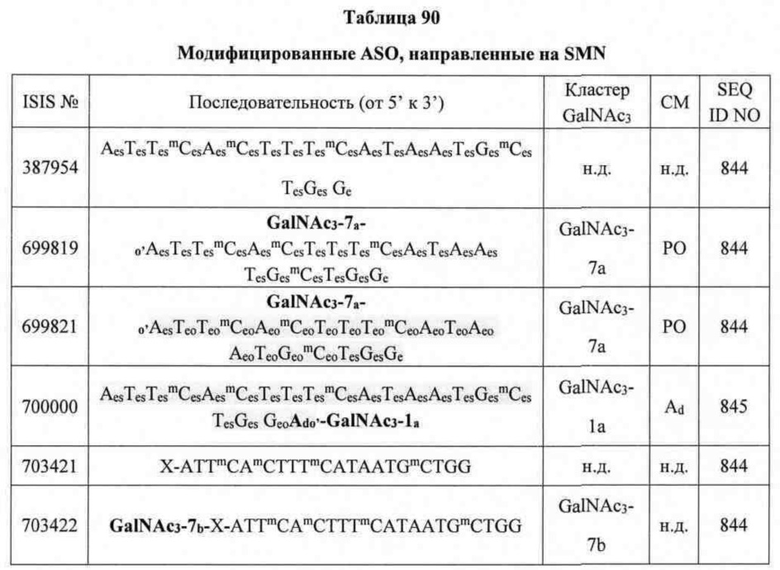
Структура GalNAc3-7a показана ранее в Примере 48. «X» означает 5'-первичный амин, полученный компанией Gene Tools (Филомат, штат Орегон), a GalNAc3-7b означает структуру GalNAc3-7a, не содержащую часть -NH-С6-О линкера, как показано ниже:
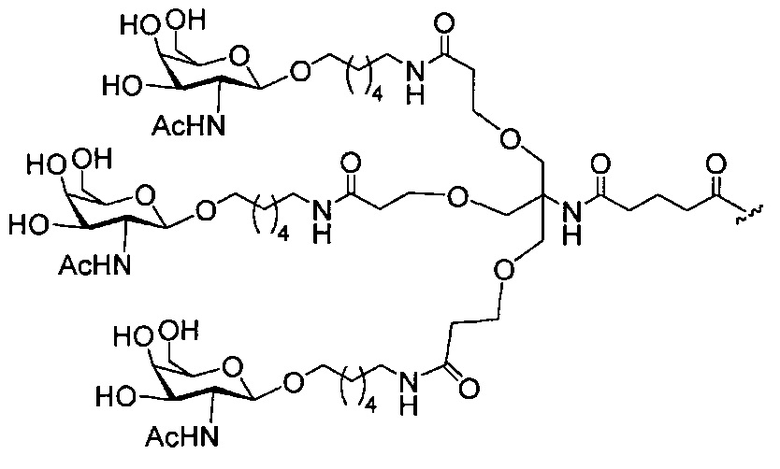 .
.
ISIS №703421 и 703422 представляют собой морфолино-олигонуклеотиды, при этом каждый нуклеотид из двух олигонуклеотидов представляет собой морфолино-нуклеотид.
Лечение
Шестинедельным трансгенным мышам, экспрессирующим человеческий SMN, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 91, или солевого раствора. Каждая экспериментальная группа состояла из 2 самцов и 2 самок. Мышей усыпили через 3 дня после введения дозы для определения уровней мРНК человеческого SMN в печени с экзоном 7 и без него, используя ПЦР в реальном времени по стандартным протоколам. Общую РНК измерили при помощи реагента Ribogreen. Уровни мРНК SMN нормализовали к общей мРНК, а затем нормализовали к средним значениям в группе, обработанной солевым раствором. Полученные средние отношения мРНК SMN, содержащей экзон 7, к мРНК SMN, не содержащей экзон 7, представлены в Таблице 91. Результаты демонстрируют, что полностью модифицированные олигонуклеотиды, которые модулируют сплайсинг и содержат конъюгат GalNAc, являются значительно более эффективными для изменения сплайсинга в печени, чем исходные олигонуклеотиды, не содержащие конъюгат GalNAc. Кроме того, эта тенденция сохраняется для химизма многократных модификаций, включая 2'-МОЕ и морфолино-модифицированные олигонуклеотиды.
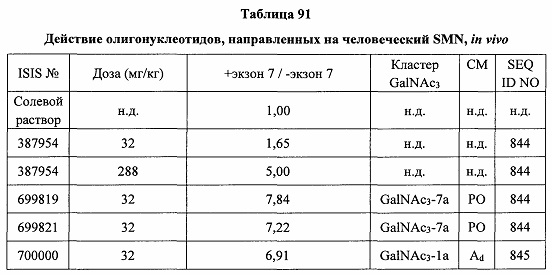

Пример 89: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на аполипопротеин А (Аро(а)), содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 92, испытали в исследовании дозозависимого ингибирования Аро(а) у трансгенных мышей.

Структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Восьминедельным самкам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один раз в неделю вводили подкожную инъекцию дозы, представленной ниже, в целом шесть доз олигонуклеотида, перечисленного в Таблице 92, или PBS. Каждая экспериментальная группа состояла из 3-4 животных. Образцы крови из хвостовой вены брали за день до введения первой дозы и еженедельно после введения каждой дозы для определения уровней белка Аро(а) в плазме. Мышей усыпили через два дня после последнего введения. Уровни мРНК Аро(а) в печени определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка Аро(а) в плазме определили при помощи твердофазного иммуноферментного анализа, и определили уровни трансаминазы в печени. Результаты анализа мРНК и белка в плазме в Таблице 93 представлены как среднее процентное значение для экспериментальной группы относительно группы, обработанной PBS. Уровни белка в плазме дополнительно нормализовали к исходному значению (BL) для группы с PBS. Средние абсолютные уровни трансаминазы и массы тела (% относительно среднего исходного значения) представлены в Таблице 94.
Как показано в Таблице 93, лечение олигонуклеотидами снижает уровни мРНК Аро(а) в печени и уровни белка в плазме дозозависимым образом. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным с более продолжительным действием, чем исходный олигонуклеотид, не содержащий конъюгат GalNAc. Как показано в Таблице 94, представленные олигонуклеотиды не влияют на уровни трансаминазы и массы тела, что указывает на хорошую переносимость олигонуклеотидов.
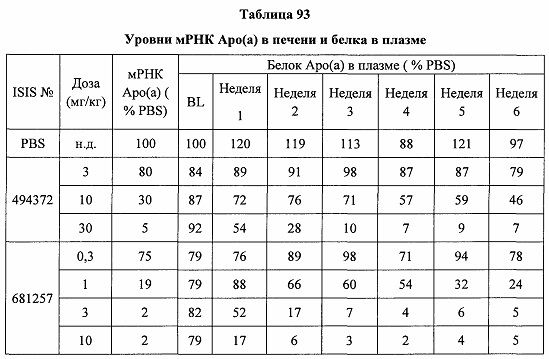

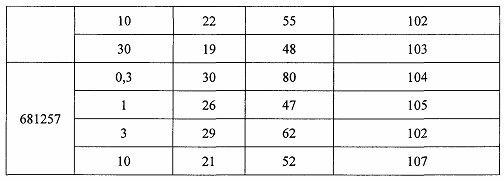
Пример 90: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на TTR, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 95, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого транстиретина (TTR) у трансгенных мышей, экспрессирующих человеческий TTR ген.
Лечение
TTR трансгенным мышам один раз в неделю в течение трех недель, в целом три дозы, вводили подкожную инъекцию олигонуклеотида и дозы, перечисленных в Таблице 96, или PBS. Каждая экспериментальная группа состояла из 4 животных. Перед введением первой дозы взяли образец крови из хвостовой вены для определения уровней белка TTR в плазме в исходном состоянии (BL). Мышей усыпили через 72 часа после последнего введения. Уровни белка TTR измерили при помощи клинического анализатора (AU480, Beckman Coulter, штат Калифорния). При помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) использовали по стандартным протоколам для определения уровней мРНК человеческого TTR в печени. Результаты, показанные в Таблице 96, представляют собой средние значения для каждой экспериментальной группы. Уровни мРНК представляют собой средние значения относительно среднего значения для PBS группы. Уровни белка в плазме представляют собой средние значения относительно среднего значения для PBS группы в исходном состоянии. «BL» означает исходное значения измерений, выполненных непосредственно перед введением первой дозы. Как показано в Таблице 96, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии TTR дозозависимым образом. Олигонуклеотид, содержащий конъюгат GalNAc, был более эффективным, чем исходное соединение без конъюгата GalNAc (ISIS 420915), а олигонуклеотиды, содержащие фосфодиэфирный или дезоксиаденозиновый расщепляемый фрагмент, демонстрировали значительное усиление эффективности, по сравнению с исходным соединением, не содержащим конъюгат (см. ISIS №682883 и 666943 по сравнению с 420915, а также см. Примеры 86 и 87).
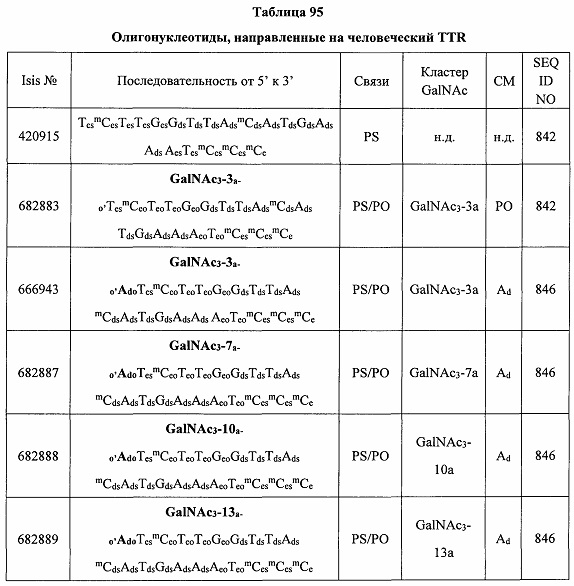
Легенда для Таблицы 95 представлена в Примере 74. Структура GalNAc3-3а показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10a показана в Примере 46. Структура GalNAc3-13a показана в Примере 62.
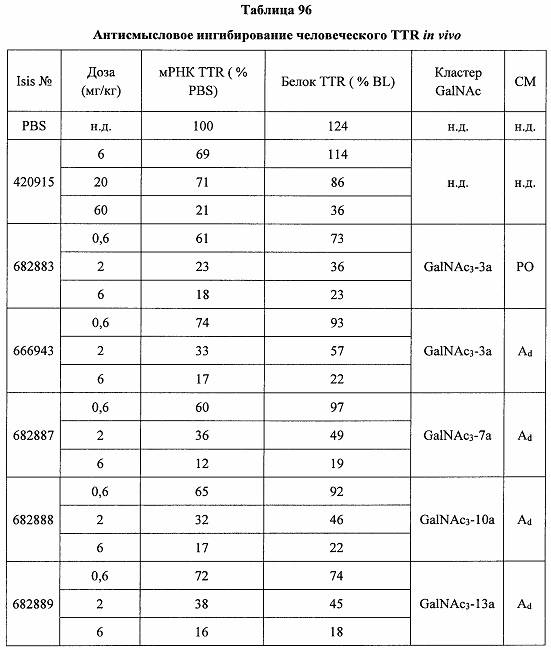
Пример 91: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на фактор VII, содержащих конъюгат GalNAc3, у приматов, не являющихся человеком
Олигонуклеотиды, перечисленные ниже в Таблице 97, испытали в нетерминальном исследовании повышения дозы на антисмысловое ингибирование фактора VII у обезьян.
Лечение
Обезьянам, ранее не подверженным экспериментам, на 0, 15 и 29 день вводили подкожные инъекции повышающихся доз олигонуклеотидов, перечисленных в Таблице 97, или PBS. Каждая экспериментальная группа состояла из 4 самцов и 1 самки. Перед введением первой дозы и в различные временные точки после нее брали образцы крови для определения уровней белка фактора VII в плазме. Уровни белка фактора VII определяли с помощью твердофазного иммуноферментного анализа. Результаты, показанные в Таблице 98, представляют собой средние значения для каждой экспериментальной группы относительно среднего значения для группы PBS в исходном состоянии (BL), измерения выполнены непосредственно перед введением первой дозы. Как показано в Таблице 98, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии фактора VII дозозависимым образом, и олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным у обезьян, чем олигонуклеотид, не содержащий конъюгата GalNAc.

Легенда для Таблицы 97 представлена в Примере 74. Структура GalNAc3-10a показана в Примере 46.
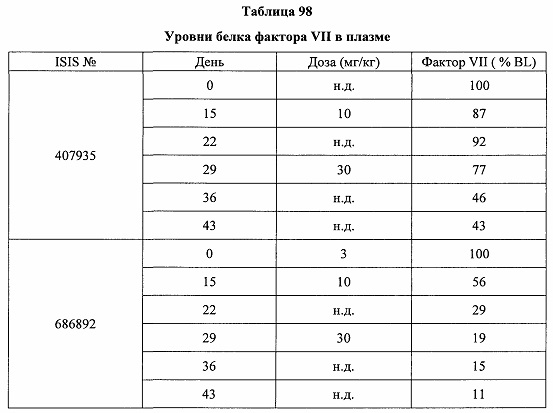
Пример 92: Антисмысловое ингибирование в первичных гепатоцитах под действием олигонуклеотидов, направленных на Аро-CIII, содержащих конъюгат GalNAc3
Первичные мышиные гепатоциты высеивали в 96-луночные планшеты при 15000 клеток на лунку и добавляли олигонуклеотиды, перечисленные в Таблице 99, направленные на мышиный АроС-III в концентрации 0,46, 1,37, 4,12 или 12,35, 37,04, 111,11 или 333,33 нМ, или 1,00 мкМ. После инкубации с олигонуклеотидами в течение 24 часов клеки лизировали и очистили общую РНК при помощи RNeasy (Qiagen). Уровни мРНК АроС-III определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc.) по стандартным протоколам. Значения IC50 определили при помощи программы Prism 4 (GraphPad). Результаты демонстрируют, что независимо от того, является ли расщепляемый фрагмент фосфодиэфиром или фосфодиэфир-связанным дезоксиаденозином, олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата.
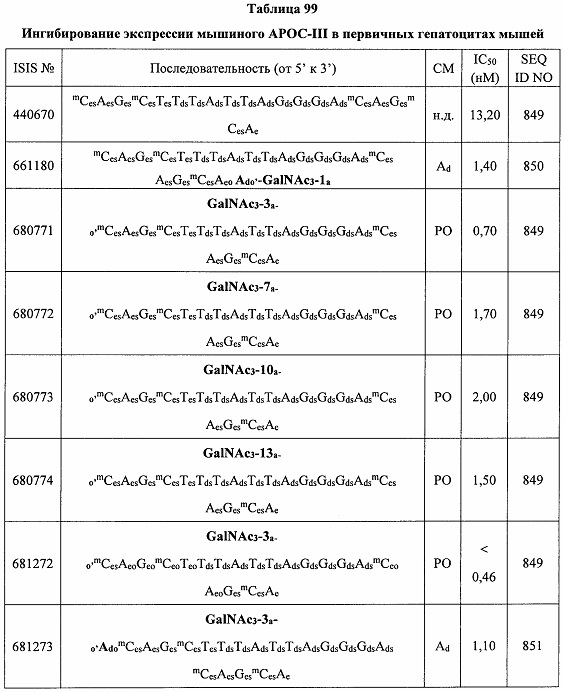
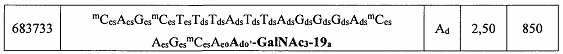
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46, GalNAc3-13a показана в Примере 62 и GalNAc3-19a показана в Примере 70.
Пример 93: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих смешанные крылья и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 100, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
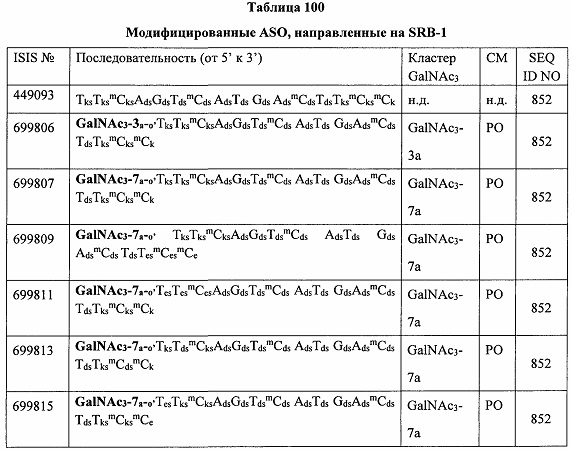
Структура GalNAc3-3a показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (cEt); «s» означает тиофосфатные межнуклеозидные линкеры (PS); «о» означает фосфодиэфирные межнуклеозидные линкеры (РО). Верхний индекс «m» означает 5-метилцитозины.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, представленной ниже, олигонуклеотида, перечисленного в Таблице 100, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения. Уровни мРНК SRB-1 в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК SRB-1 нормализовали к уровням мРНК циклофилина по стандартным протоколам. Результаты, показанные ниже, представлены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, по сравнению с контрольной группой, обработанной солевым раствором. Как показано в Таблице 101, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом, а гэпмерные олигонуклеотиды, содержащие конъюгат GalNAc и имеющие крылья, которые представляют собой либо полностью cEt, либо смешанные сахарные модификации, были существенно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата и содержащий полностью cEt модифицированные крылья.
Измерили также массы тела, уровни трансаминазы в печени, общий билирубин и АМК, а средние значения для каждой экспериментальной группы представлены в Таблице 101. Масса тела показана как средний процент массы тела относительно исходной массы тела (% BL), измеренный непосредственно перед введением дозы олигонуклеотида.
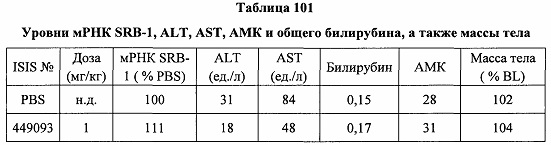
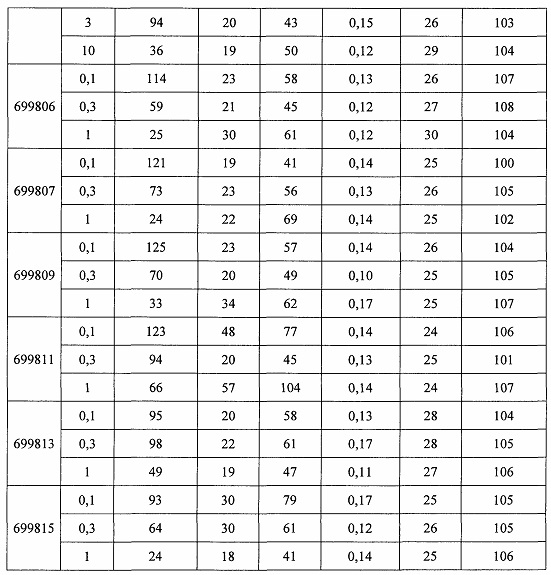
Пример 94: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих 2'-сахарные модификации и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 102, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.


Верхний индекс «m» означает 2'-O-метил-модифицированный нуклеозид. Полная легенда к таблице представлена в Примере 74. Структура GalNAc3-3а показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Исследование проводили по протоколу, описанному в Примере 93. Результаты представлены ниже в Таблице 103 и демонстрируют, что и 2'-МОЕ, и 2'-ОМе-модифицированные олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем соответствующие исходные олигонуклеотиды, не содержащие конъюгата. Результаты измерений массы тела, трансаминазы в печени, общего билирубина и АМК демонстрируют, что эти соединения хорошо переносятся.
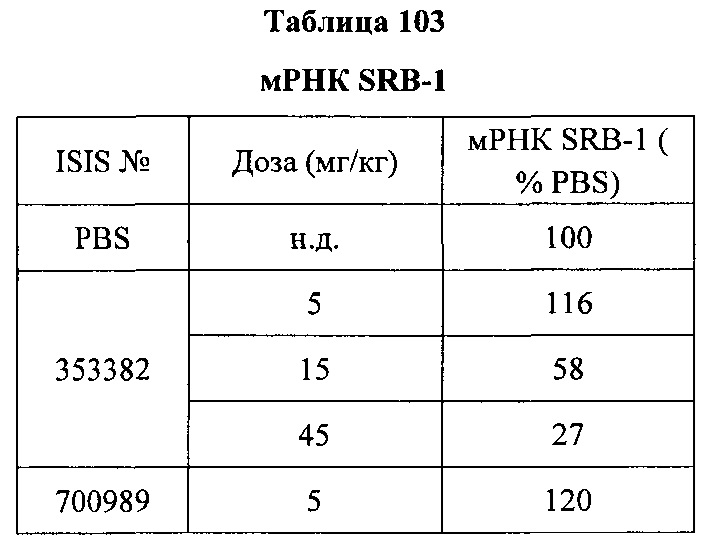
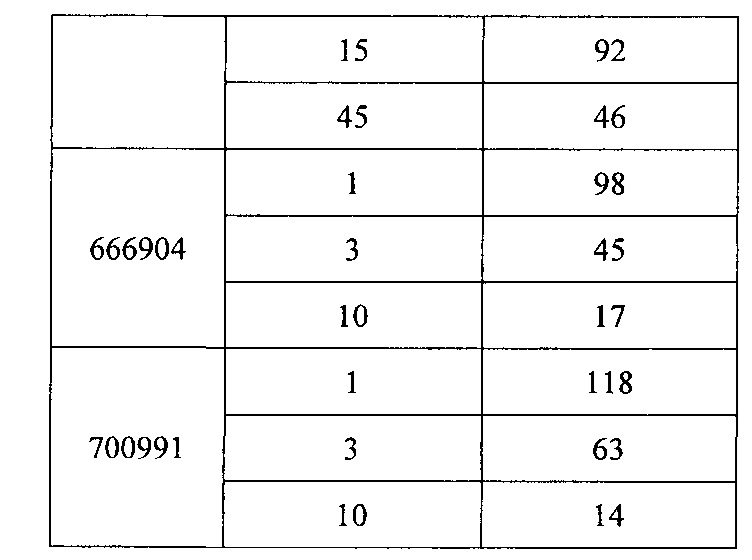
Пример 95: Анти смысловое ингибирование in vivo под действием олигонуклеотидов, направленных на SRB-1, содержащих бициклические нуклеозиды и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 104, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.

Нижний индекс «g» означает фтор-ГНК нуклеозид, нижний индекс «l» означает закрытый нуклеозид, содержащий мостик 2'-O-СН2-4'. Другие сокращения представлены в легенде таблицы Примера 74. Структура GalNAc3-1a показана ранее в Примере 9, структура GalNAc3-3a показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Исследование проводили по протоколу, описанному в Примере 93. Результаты представлены ниже в Таблице 105 и демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc и различные бициклические нуклеозидные модификации, были значительно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата и содержащий бициклические нуклеозидные модификации. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc и фтор-ГНК модификации, был существенно более эффективным, чем исходное соединение, не содержащее конъюгата и содержащее фтор-ГНК модификации. Результаты измерений массы тела, трансаминазы в печени, общего билирубина и АМК демонстрируют, что эти соединения хорошо переносятся.
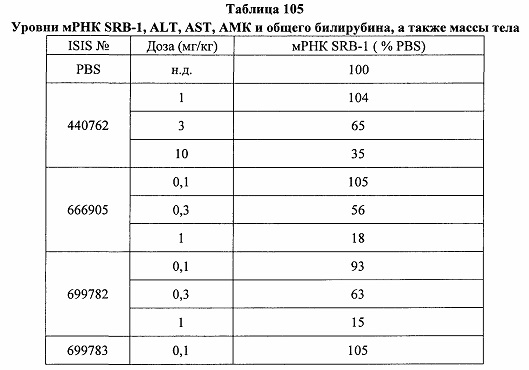
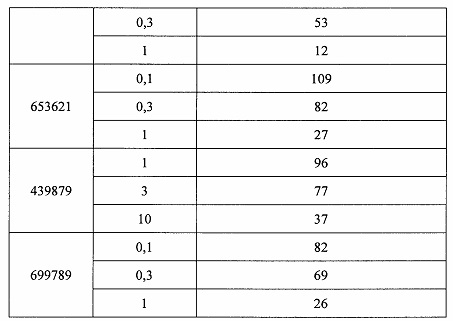
Пример 96: Связывание белка плазмы антисмысловыми олигонуклеотидами, содержащими группу конъюгата GalNAc3
Олигонуклеотиды, перечисленные в Таблице 70, направленные на АроС-III, и олигонуклеотиды в Таблице 106, направленные на Аро(а), испытали в анализе ультрафильтрации для оценки связывания белка в плазме.

Легенда таблицы представлена в Примере 74. Структура GalNAc3-7a показана ранее в Примере 48.
Элементы для ультрафильтрации Ultrafree-MC (номинальное ограничение молекулярной массы 30000, слабосвязывающая регенерированная целлюлозная мембрана, Millipore, Бедфорд, штат Массачусетс) предварительно кондиционировали с 300 мкл 0,5% Tween 80 и центрифугировали при 2000 g в течение 10 минут, затем с 300 мкл 300 мкг/мл раствора контрольного олигонуклеотида в H2O и центрифугировали при 2000 g в течение 16 минут. Для оценки неспецифического связывания с фильтрами каждого исследуемого олигонуклеотида из Таблиц 70 и 106, используемых в испытаниях, 300 мкл 250 нг/мл раствора олигонуклеотида в H2O при рН 7,4 поместили в предварительно кондиционированные фильтры и центрифугировали при 2000 г в течение 16 минут. Нефильтрованные и фильтрованные образцы анализировали твердофазным иммуноферментным анализом для определения концентраций олигонуклеотидов. Для получения средней концентрации для каждого образца использовали три экземпляра. Среднюю концентрацию фильтрованного образца относительно нефильтрованного образца использовали для определения процента олигонуклеотида, прошедшего через фильтр без плазмы (% выделения).
Замороженные образцы цельной плазмы, собранные в K3-ЭДТК и полученные от здоровых, не принимающих лекарства людей-добровольцев, яванских макак и мышей CD-1, приобрели у компании Bioreclamation LLC (Вестбери, штат Нью-Йорк). Исследуемые олигонуклеотиды добавляли к 1,2 мл аликвотам плазмы в двух концентрациях (5 и 150 мкг/мл). Аликвоту (300 мкл) каждого маркированного образца плазмы поместили на предварительно кондиционированный фильтровальный элемент и инкубировали при 37°С в течение 30 минут, затем сразу выполнили центрифугирование при 2000 g в течение 16 минут. Аликвоты фильтрованных и нефильтрованных маркированных образцов плазмы анализировали твердофазным иммуноферментным анализом для определения концентрации олигонуклеотида в каждом образце. Использовали три экземпляра каждой концентрации для определения среднего процента связанного и несвязанного олигонуклеотида в каждом образце. Среднюю концентрацию фильтрованного образца относительно концентрации нефильтрованного образца использовали для определения процента олигонуклеотида в плазме, не связанного с белками плазмы (% несвязанного). Окончательные значения несвязанного олигонуклеотида корректировали на неспецифическое связывание путем деления % несвязанного на % выделения для каждого олигонуклеотида. Окончательные значения % связанного олигонуклеотида определили вычитанием окончательных значений % несвязанного из 100. Результаты показаны в Таблице 107 для двух концентраций испытанного олигонуклеотида (5 и 150 мкг/мл) в плазме каждого вида. Результаты демонстрируют, что группы конъюгата GalNAc не оказывают существенного влияния на связывание белка плазмы. Кроме того, олигонуклеотиды, содержащие только PS межнуклеозидные линкеры и смешанные PO/PS линкеры, - оба варианта связывают белки плазмы, при этом олигонуклеотиды, содержащие только PS линкеры, связывают белки плазмы в несколько большей степени, чем олигонуклеотиды, содержащие смешанные PO/PS линкеры.
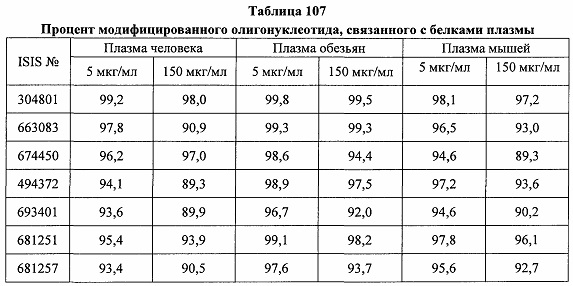
Пример 97: Модифицированные олигонуклеотиды, направленные на TTR, содержащие группу конъюгата GalNAc3
Олигонуклеотиды, представленные в Таблице 108, содержащие конъюгат GalNAc, предназначены для воздействия на TTR.
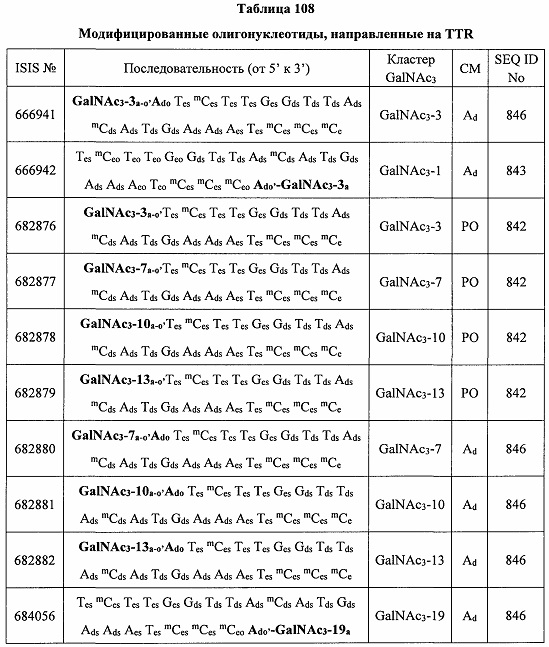
Легенда для Таблицы 108 представлена в Примере 74. Структура GalNAc3-1 показана в Примере 9. Структура GalNAc3-3a показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10a показана в Примере 46. Структура GalNAc3-13a показана в Примере 62. Структура GalNAc3-19a показана в Примере 70.
Пример 98: Оценка провоспалительного действия олигонуклеотидов, содержащих конъюгат GalNAc, в анализе hPMBC
Олигонуклеотиды, перечисленные в Таблице 109, исследовали на провоспалительное действие в анализе hPMBC, описанном в Примерах 23 и 24. (См. Таблицы 30, 83, 95 и 108, где представлено описание олигонуклеотидов). ISIS 353512 обладает высоким ответом, и его использовали в качестве положительного контроля, а другие олигонуклеотиды описаны в Таблицах 83, 95 и 108. Результаты, представленные в Таблице 109, получены с использованием крови, полученной от одного донора-добровольца. Результаты демонстрируют, что олигонуклеотиды, содержащие смешанные PO/PS межнуклеозидные линкеры, вызывают значительно более слабые провоспалительные реакции, по сравнению с теми же олигонуклеотидами, содержащими только PS линкеры. Кроме того, в этом анализе группа конъюгата GalNAc не оказывает существенного влияния.
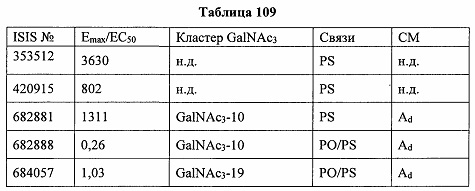
Пример 99: Связывающие аффинности олигонуклеотидов, содержащих конъюгат GalNAc, в отношении асиалогликопротеинового рецептора
Связывающие аффинности олигонуклеотидов, перечисленных в Таблице 110 (см. Таблицу 76, в которой представлено описание олигонуклеотидов), в отношении асиалогликопротеинового рецептора испытали в анализе конкурентного связывания рецепторов. Конкурирующий лиганд, α1-кислый гликопротеин (AGP), инкубировали в 50 мМ ацетатно-натриевом буфере (рН 5) с 1 ед. нейраминидазы-агарозы в течение 16 часов при 37°С, а >90% дезалилирование подтвердили анализом с сиаловой кислотой или эксклюзионной хроматографией (SEC). Для йодирования АГФ использовали монохлорид йода по способу, описанному авторами Atsma et al. (см. J Lipid Res. январь 1991 г.; 32(1): 173-81.) В этом способе дезалилированный α1-кислый гликопротеин (de-AGP) добавляли к 10 мМ хлориду йода, Na125I и 1 М глицина в 0,25 М NaOH. После инкубации в течение 10 минут при комнатной температуре, 125I -меченный de-AGP отделили от свободного 125I двукратным концентрированием смеси с использованием спин-колонки с номинальным отсечением по молекулярной массе 3 кДа. Белок испытали на эффективность мечения и чистоту на системе ВЭЖХ, оснащенной колонкой Agilent SEC-3 (7,8×300 мм) и счетчиком β-RAM. Конкуретные исследования с использованием 125I -меченного de-AGP и ASO, содержащих различные GalNAc-кластеры, выполнили следующим образом. Человеческие клетки HepG2 (106 клеток/мл) поместили на 6-луночные планшеты в 2 мл соответствующей питательной среды. Использовали среду MEM с добавлением 10% фетальной бычьей сыворотки (FBS), 2 мМ L-глутамина и 10 мМ HEPES. Клетки выращивали в течение 16-20 часов при 37°C с 5% и 10% CO2, соответственно. Перед экспериментом клетки промыли средой без FBS. Клетки выращивали в течение 30 минут при 37°C с 1 мл конкурентной смеси, содержащей соответствующую питательную среду с 2% FBS, 10-8 М 125I -меченным de-AGP и ASO, содержащим GalNAc-кластер в концентрациях в диапазоне от 10-11 до 10-5 М. Неспецифическое связывание определили в присутствии 10-2 М GalNAc сахара. Клетки дважды промыли средой без FBS для удаления несвязанного 125I -меченного de-AGP и конкурирующего GalNAc ASO. Клетки лизировали с использованием буфера RLT производства компании Qiagen, содержащего 1% β-меркаптоэтанола. Лизаты перенесли в круглодонные аналитические пробирки после быстрого 10-минутного цикла замораживания/оттаивания, и анализировали на γ-счетчике. Неспецифическое связывание вычли, а затем разделили импульсы белка 125I на значение импульсов при самой низкой концентрации GalNAc-ASO. Кривые ингибирования построили по уравнению моносайтового конкурентного связывания, используя алгоритм нелинейной регрессии для расчета связывающей аффиности (KD).
Результаты в Таблице 110 были получены в экспериментах, выполненных в пять разных дней. Результаты для олигонуклеотидов, отмеченных верхним индексом «а», представляют собой средние значения экспериментов, выполненных в два разных дня. Результаты демонстрируют, что олигонуклеотиды, содержащие группу конъюгата GalNAc у 5'-конца, связывают асиалогликопротеиновый рецептор человеческих клеток HepG2 с аффинностью, которая в 1,5-16 раз больше, чем для олигонуклеотидов, содержащих группу конъюгата GalNAc у 3'-конца.
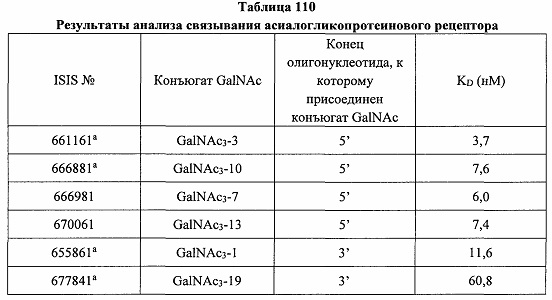
Пример 100: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, содержащих группу конъюгата GalNAc, направленных на Аро(а), in vivo
Олигонуклеотиды, перечисленные ниже в Таблице 111a, испытали в исследовании однократной дозы на продолжительность действия у мышей.

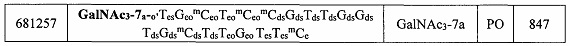
Структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Каждой самке трансгенных мышей, экспрессирующих человеческий Аро(а), один раз в неделю, в целом 6 доз, вводили подкожную инъъекцию олигонуклеотида и дозы, перечисленной в Таблице 111b, или PBS. Каждая экспериментальная группа состояла из 3 животных. Образцы крови брали за день до введения дозы для определения исходных уровней белка Аро(а) в плазме, а также через 72 часа, 1 неделю и 2 недели после введения первой дозы. Дополнительные пробы крови брали через 3 недели, 4 недели, 5 недель и 6 недель после введения первой дозы. Уровни белка Аро(а) в плазме измеряли при помощи твердофазного иммуноферментного анализа. Результаты в Таблице 111b представлены как средний процент от уровней белка Аро(а) в плазме для каждой экспериментальной группы, нормализованных к исходным уровням (% BL). Результаты показывают, что олигонуклеотиды, содержащие группу конъюгата GalNAc, демонстрируют эффективное снижение экспрессии Аро(а). Этот мощный эффект наблюдали для олигонуклеотида, содержащего только PS межнуклеозидные линкеры, и для олигонуклеотида, содержащего смешанные РО и PS линкеры.

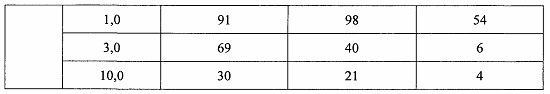
Пример 101: Анти смысловое ингибирование олигонуклеотидами, содержащими кластер GalNAc, связанный через стабильный фрагмент
Олигонуклеотиды, перечисленные в Таблице 112, испытали на ингибирование экспрессии мышиного APOC-III in vivo. Мышам C57Bl/6 ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 112, или PBS. Каждая экспериментальная группа состояла из 4 животных. Каждой мыши, обработанной ISIS 440670, вводили дозу 2,6,20 или 60 мг/кг. Каждой мыши, обработанной 680772 или 696847, вводили 0,6, 2, 6 или 20 мг/кг. Группа конъюгата GalNAc в ISIS 696847 связана через стабильный фрагмент, тиофосфатную связь, вместо легко расщепляемой фосфодиэфир-содержащей связи. Животных усыпили через 72 часа после введения дозы. Уровни мРНК APOC-III в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК APOC-III нормализовали к уровням мРНК циклофилина по стандартным протоколам. Результаты представлены в Таблице 112 как средний процент уровней мРНК APOC-III для каждой экспериментальной группы, по сравнению с контрольной группой, обработанной солевым раствором. Результаты демонстрируют, что олигонуклеотиды, содержащие группу конъюгата GalNAc, были существенно более эффективными, чем олигонуклеотид, не содержащий группу конъюгата. Кроме того, олигонуклеотид, содержащий группу конъюгата GalNAc, связанную с олигонуклеотидом через расщепляемый фрагмент (ISIS 680772), был еще более эффективным, чем олигонуклеотид, содержащий группу конъюгата GalNAc, связанную с олигонуклеотидом через стабильный фрагмент (ISIS 696847).

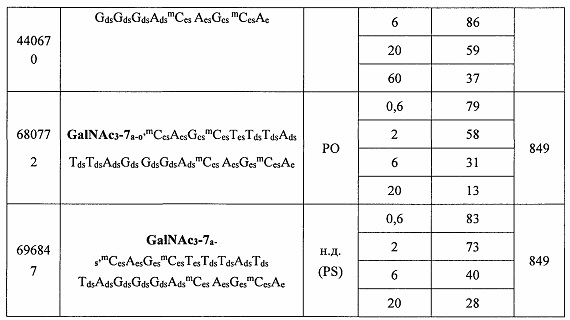
Структура GalNAc3-7a показана ранее в Примере 48.
Пример 102: Распределение в печени антисмысловых олигонуклеотидов, содержащих конъюгат GalNAc
Оценили распределение в печени ISIS 353382 (см. Таблицу 36), который не содержит конъюгата GalNAc, и ISIS 655861 (см. Таблицу 36), который содержит конъюгат GalNAc. Самцам мышей balb/c ввели однократную подкожную инъекцию ISIS 353382 или 655861 в дозе, перечисленной в Таблице 113. Каждая экспериментальная группа состояла из 3 животных, за исключением группы с дозой 18 мг/кг для ISIS 655861, которая состояла из 2 животных. Животных усыпили через 48 часов после введения дозы для определения распределения олигонуклеотидов в печени. Для измерения количества молекул антисмыслового олигонуклеотида на клетку, метку трис-бипиридина рутения(II) (MSD TAG, Meso Scale Discovery) конъюгировали с олигонуклеотидным образцом, используемым для обнаружения антисмысловых олигонуклеотидов. Результаты, представленные в Таблице 113, представляют собой средние концентрации олигонуклеотида для каждой экспериментальной группы в единицах измерения миллионов молекул олигонуклеотида на клетку. Результаты демонстрируют, что при равных дозах олигонуклеотид, содержащий конъюгат GalNAc, содержался в более высоких концентрациях в целом в печени и в гепатоцитах, чем олигонуклеотид, не содержащий конъюгата GalNAc. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc, содержался в более низких концентрациях в непаренхиматозных клетках печени, чем олигонуклеотид, не содержащий конъюгата GalNAc. И тогда как концентрации ISIS 655861 в гепатоцитах и непаренхиматозных клетках печени были одинаковыми в расчете на одну клетку, содержание гепатоцитов в печени составляет приблизительно 80% по объему. Следовательно, основная часть олигонуклеотида ISIS 655861, содержащегося в печени, находилась в гепатоцитах, тогда как основная часть олигонуклеотида ISIS 353382, содержащегося в печени, находилась в непаренхиматозных клетках печени.
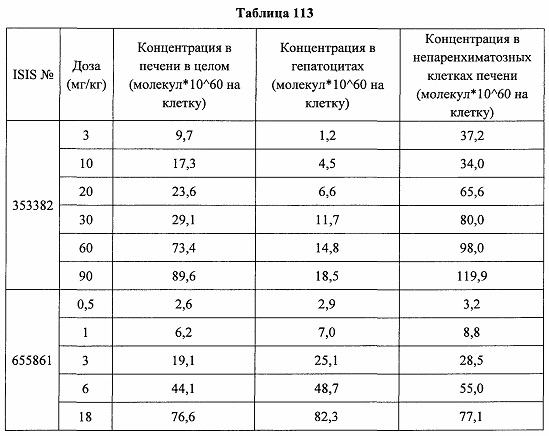
Пример 103: Продолжительность действия in vivo олигонуклеотидов, направленных на АРОС-III, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 114, испытали в исследовании однократной дозы на продолжительность действия у мышей.

Структура GalNAc3-3a показана в примере 39, a GalNAc3-19a показана в Примере 70.
Лечение
Самкам трансгенных мышей, экспрессирующим человеческий APOC-III, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 114, или PBS. Каждая экспериментальная группа состояла из 3 животных. Образцы крови из брали до введения дозы для определения исходных показателей и на 3, 7, 14, 21, 28, 35 и 42 день после введения дозы. Уровни триглицеридов и белка APOC-III в плазме измеряли так, как описано в Примере 20. Результаты в Таблице 115 представлены как средний процент уровней триглицеридов и APOC-III в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Сравнение результатов в Таблице 71 примера 79 с результатами, представленными ниже в таблице 115, демонстрирует, что олигонуклеотиды, содержащие смесь фосфодиэфирных и тиофосфатных межнуклеозидных линкеров, обладают увеличенной продолжительностью действия, чем эквивалентные олигонуклеотиды, содержащие только тиофосфатные межнуклеозидные линкеры.
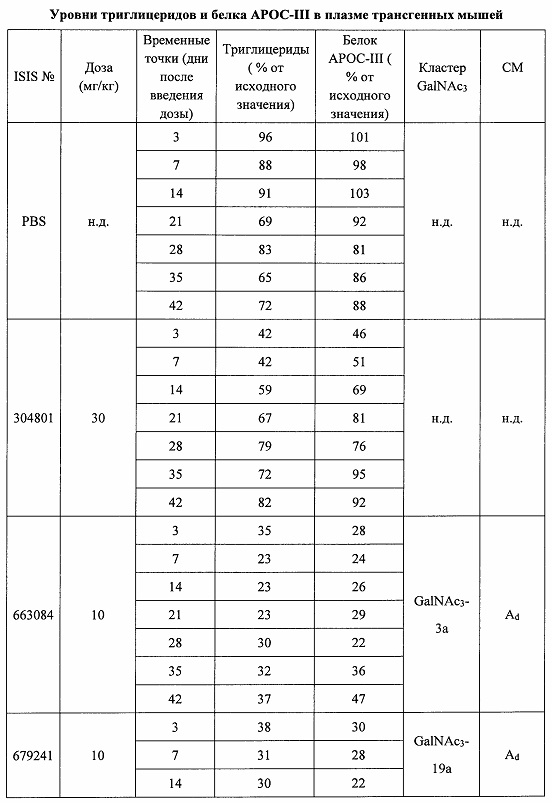
Пример 104: Синтез олигонуклеотидов, содержащих конъюгат 5'-GalNAc2
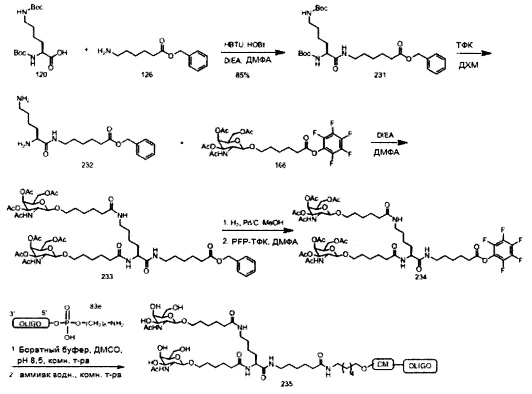
Соединение 120 имеется в продаже, а синтез соединения 126 описан в Примере 49. Соединение 120 (1 г, 2,89 ммоль), HBTU (0,39 г, 2,89 ммоль) и HOBt (1,64 г, 4,33 ммоль) растворили в ДМФА (10 мл) и добавили N,N-диизопропилэтиламин (1,75 мл, 10,1 ммоль). Примерно через 5 минут в реакционную смесь добавили бензиловый эфир аминогексановой кислоты (1,36 г, 3,46 ммоль). Через 3 часа реакционную смесь вылили в 100 мл 1 М раствора NaHSO4 и экстрагировали 2×50 мл этилацетата. Органические слои объединили и промыли 3×40 мл насыщенного раствора NaHCO3 и 2 × насыщенным солевым раствором, высушили при помощи Na2SO4, отфильтровали и концентрировали. Продукт очистили силикагелевой колоночной хроматографией (ДХМ : ЕА : гексаны, 1:1:1) с получением соединения 231. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 231 (1,34 г, 2,438 ммоль) растворили в дихлорметане (10 мл) и добавили трифторуксусную кислоту (10 мл). После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь концентрировали при пониженном давлении и выпарили вместе с толуолом (3×10 мл). Остаток высушили при пониженном давлении с получением соединения 232 в виде трифторацетатной соли. Синтез соединения 166 описан в Примере 54. Соединение 166 (3,39 г, 5,40 ммоль) растворили в ДМФА (3 мл). Раствор соединения 232 (1,3 г, 2,25 ммоль) растворили в ДМФА (3 мл) и добавили N,N-иизопропилэтиламин (1,55 мл). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут, затем вылили в воду (80 мл), а водный слой экстрагировали EtOAc (2×100 мл). Органическую фазу отделили и промыли насыщенным водным раствором NaHCO3 (3×80 mL), 1 M NaHSO4 (3×80 мл) и насыщенным солевым раствором (2×80 мл), затем высушили (Na2SO4), отфильтровали и концентрировали. Остаток очистили силикагелевой колоночной хроматографией с получением соединения 233. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 233 (0,59 г, 0,48 ммоль) растворили в метаноле (2,2 мл) и этилацетате (2,2 мл). Добавили палладий на углероде (10 масс. % Pd/C, влажный, 0,07 г) и перемешивали реакционную смесь в атмосфере водорода в течение 3 часов. Реакционную смесь отфильтровали через слой целита и концентрировали с получением карбоновой кислоты. Карбоновую кислоту (1,32 г, 1,15 ммоль, не содержащая кластера кислота) растворили в ДМФА (3,2 мл). К ней добавили N,N-диизопропилэтиламин (0,3 мл, 1,73 ммоль) и PFP-ТФК (0,30 мл, 1,73 ммоль). Через 30 минут перемешивания при комнатной температуре реакционную смесь вылили в воду (40 мл) и экстрагировали EtOAc (2×50 мл). Выполнили стандартную процедуру выделения продукта, как описано выше, с получением соединения 234. Данные ЖХМС и ЯМР согласовались с указанной структурой. Олигонуклеотид 235 получили по общему способу, описанному в Примере 46. Кластерная часть GalNAc2 (GalNAc2-24a) группы конъюгата GalNAc2-24 может быть комбинирована с любым расщепляемым фрагментом с получением различных групп конъюгата. Структура GalNAc2-24 (GalNAc2-24a-CM) представлена ниже:
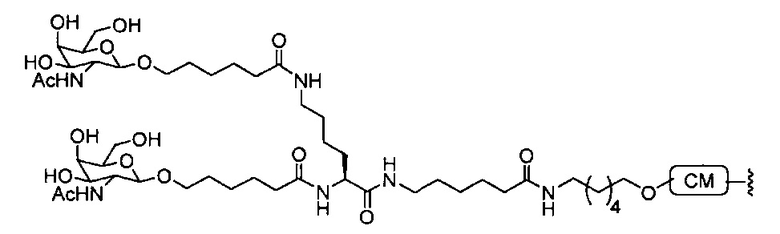
Пример 105: Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-25
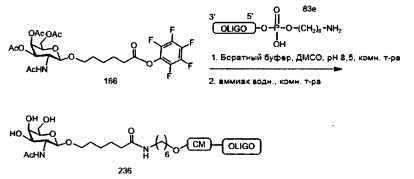
Синтез соединения 166 описан в Примере 54. Олигонуклеотид 236 получили по общему способу, описанному в Примере 46.
Альтернативно, олигонуклеотид 236 синтезировали по схеме, изображенной ниже, а соединение 238 использовали для получения олигонуклеотида 236 по способам, описанным в Примере 10.
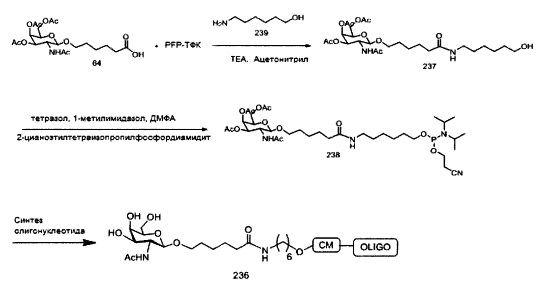
Кластерная часть GalNAc1 (GalNAc1-25a) группы конъюгата GalNAc1-25 может быть комбинирована с любым расщепляемым фрагментом, присутствующим в олигонуклеотиде, с получением различных групп конъюгата. Структура GalNAc1-25 (GalNAc1-25a-CM) представлена ниже:
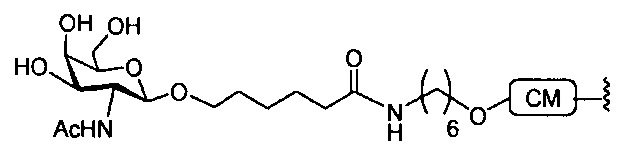
Пример 106: Антисмысловое ингибирование in vivo олигонуклеотидами, направленными на SRB-1, содержащими конъюгат 5'-GalNAc2 или 5'-GalNAc3
Олигонуклеотиды, перечисленные в Таблицах 116 и 117, испытали в дозозависимых исследованиях антисмыслового ингибирования SRB-1 у мышей.
Лечение
Шестинедельным самцам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию 2, 7 или 20 мг/кг ISIS №440762; или 0,2, 0,6, 2, 6 или 20 мг/кг ISIS №686221, 686222 или 708561; или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 72 часа после последнего введения. Уровни мРНК SRB-1 в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК SRB-1 нормализовали к уровням мРНК циклофилина по стандартным протоколам. Антисмысловые олигонуклеотиды, снижающие уровни мРНК SRB-1 дозозависимым образом, а также результаты ED50 представлены в Таблицах 116 и 117. Хотя в предыдущих исследованиях показано, что трехвалентные GalNAc-сопряженные олигонуклеотиды существенно более эффективны, чем двухвалентные GalNAc-сопряженные олигонуклеотиды, которые в свою очередь существенно более эффективны, чем одновалентные GalNAc-сопряженные олигонуклеотиды (см., например, Khorev et al., Bioorg. & Med. Chem., т. 16, 5216-5231 (2008)), обработка антисмысловыми олигонуклеотидами, содержащими одновалентные, двухвалентные и трехвалентные кластеры GalNAc, приводит к снижению уровней мРНК SRB-1 с одинаковой эффективностью, как показано в Таблицах 116 и 117.

Легенда к таблице представлена в Примере 93. Структура GalNAc3-13a показана в примере 62, а структура GalNAc2-24 показана в Примере 104.

Легенда к таблице представлена в Примере 93. Структура GalNAc1-25a показана в Примере 105.
Оценили также концентрации олигонуклеотидов, представленных в Таблицах 116 и 117, в печени, используя способы, описанные в Примере 75. Результаты, показанные ниже в Таблицах 117а и 117b, представляют собой средние значения общего содержания антисмысловых олигонуклеотидов в тканях для каждой экспериментальной группы, измеренные по УФ, в единицах измерения мкг олигонуклеотида на грамм ткани печени. Результаты демонстрируют, что олигонуклеотиды, содержащие группу конъюагата GalNAc, накапливаются в печени в существенно более высоких количествах, чем при той же дозе олигонуклеотида, не содержащего группу конъюгата GalNAc. Кроме того, антисмысловые олигонуклеотиды, содержащие один, два или три лиганда GalNAc в своих соответствующих группах конъюгата, накапливаются в печени в равных количествах. Этот результат является неожиданным с учетом данных, представленных выше в литературном источнике Khorev et al., и он согласуется с данными активности, представленными выше в Таблицах 116 и 117.
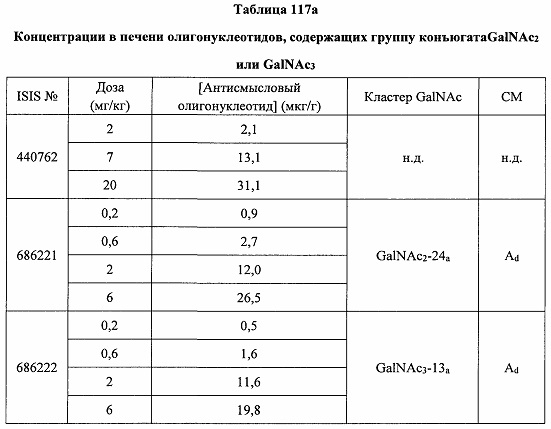


Пример 107: Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-26 или GalNAc1-27
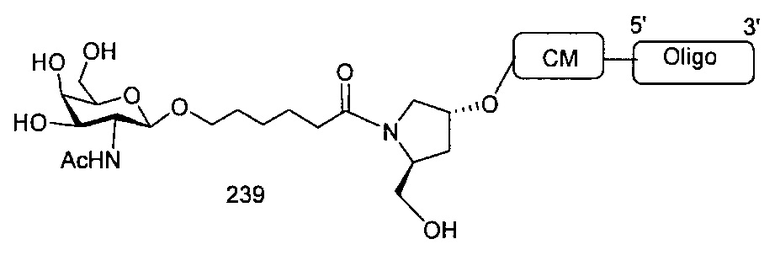
Олигонуклеотид 239 синтезировали связыванием соединения 47 (см. Пример 15) с кислотой 64 (см. Пример 32), используя HBTU и DIEA в ДМФА. Полученное амид-содержащее соединение фосфитилировали, затем присоединили к 5'-концу олигонуклеотида по способам, описанным в Примере 10. Кластерная часть GalNAc1 (GalNAc1-26a) группы конъюгата GalNAc1-26 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. Структура GalNAc1-26 (GalNAc1-26a-CM) представлена ниже:
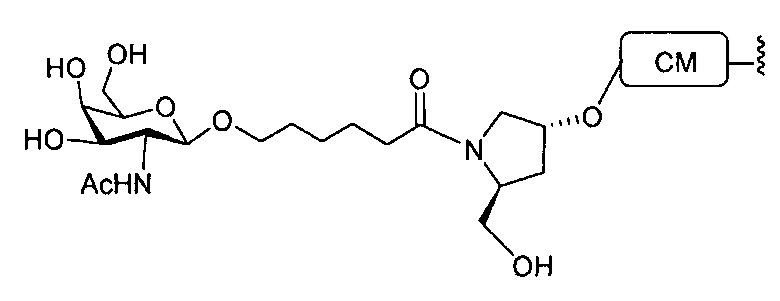 .
.
Для присоединения группы конъюгата GalNAc1 к 3'-концу олигонуклеотида амид, образованный по реакции соединений 47 и 64, присоединили к твердой подложке по способам, описанным в Примере 7. Затем выполнили синтез олигонуклеотида по способам, описанным в Примере 9, с получением олигонуклеотида 240.
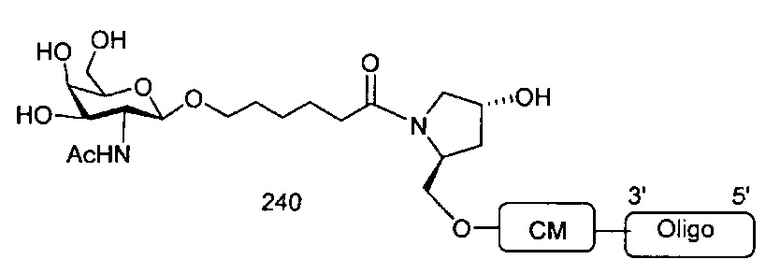
Кластерная часть GalNAc1 (GalNAc1-27a) группы конъюгата GalNAc1-27 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. Структура GalNAc1-27 (GalNAc1-27a-CM) представлена ниже:
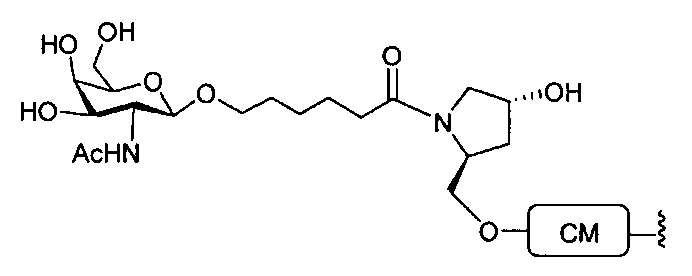
Пример 108: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, содержащих группу конъюгата GalNAc, направленных на Аро(а), in vivo
Олигонуклеотиды, перечисленные ниже в Таблице 118, испытали в исследовании однократной дозы на мышах.

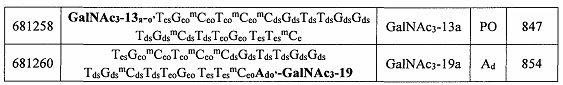
Структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Самцам трансгенных мышей, экспрессирующим человеческий Аро(а), ввели однократную подкожную инъекцию олигонуклеотида и дозы, перечисленных в Таблице 119, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали за день до введения дозы для определения исходных уровней белка Аро(а) в плазме, а также через 1 неделю после введения первой дозы. Образцы крови брали дополнительно еженедельно в течение около 8 недель. Уровни белка Аро(а) в плазме измеряли при помощи твердофазного иммуноферментного анализа. Результаты в Таблице 119 представлены как средний процент от уровней белка Аро(а) в плазме для каждой экспериментальной группы, нормализованных к исходным уровням (% BL). Результаты показывают, что антисмысловые олигонуклеотиды снижают экспрессию белка Аро(а). Кроме того, олигонуклеотиды, содержащие группу конъюгата GalNAc, демонстрируют еще более эффективное снижение экспрессии Аро(а), чем олигонуклеотид не содержащий группу конъюгата.
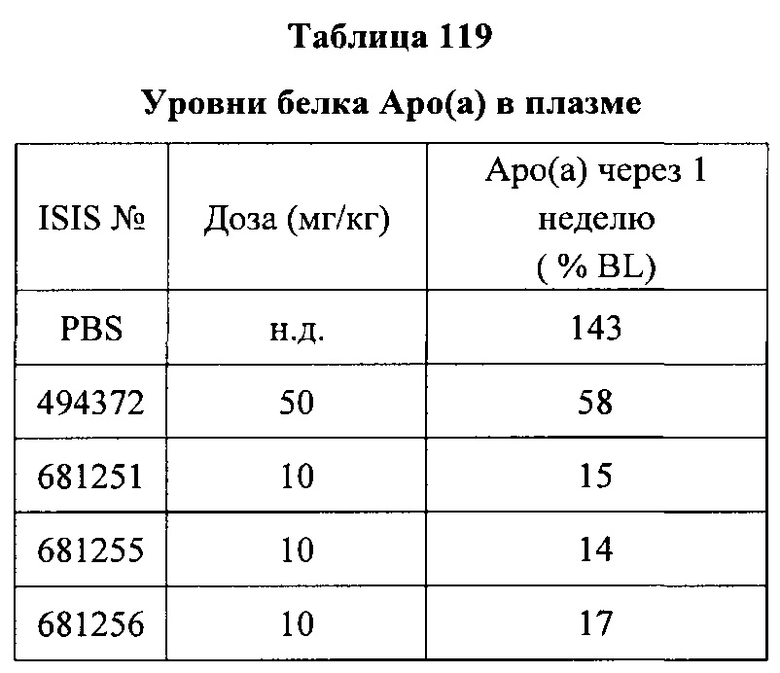
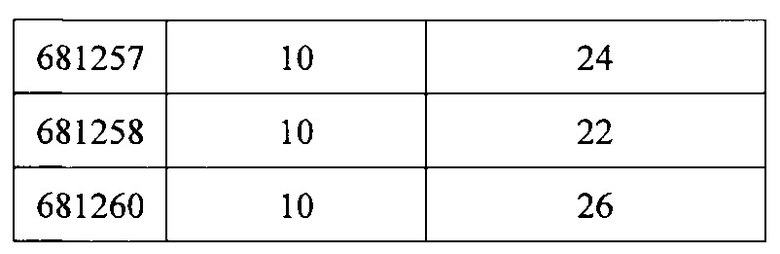
Пример 109: Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-28 или GalNAc1-29
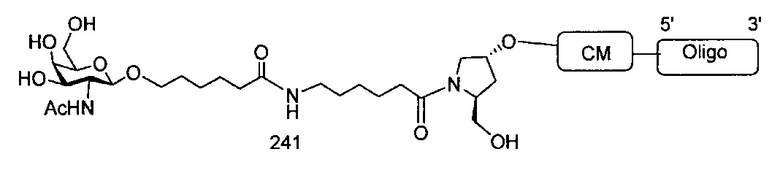
Олигонуклеотид 241 синтезировали по таким же способам, как описаны в Примере 71, с получением фосфорамидитного промежуточного соединения, после чего выполнили приемы, описанные в Примере 10, для синтеза олигонуклеотида. Кластерная часть GalNAc1 (GalNAc1-28a) группы конъюгата GalNAc1-28 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. Структура GalNAc1-28 (GalNAc1-28a-CM) представлена ниже:
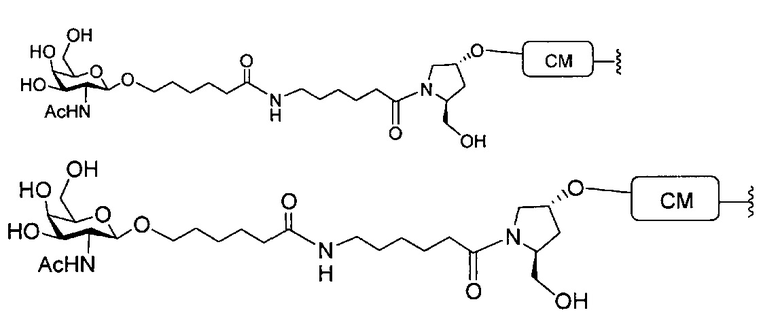
Для присоединения группы конъюгата GalNAc1 к 3'-концу олигонуклеотида использовали такие же способы, как описаны в Примере 71, с получение гидроксильного промежуточного соединения, которое затем присоединили к твердой подложке по способам, описанным в Примере 7. Затем выполнили синтез олигонуклеотида по способам, описанным в Примере 9, с получением олигонуклеотида 242.
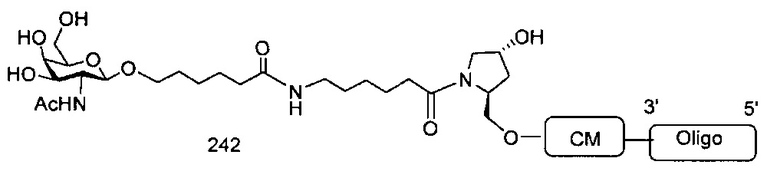
Кластерная часть GalNAc1 (GalNAc1-29a) группы конъюгата GalNAc1-29 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. Структура GalNAc1-29 (GalNAc1-29a-CM) представлена ниже:
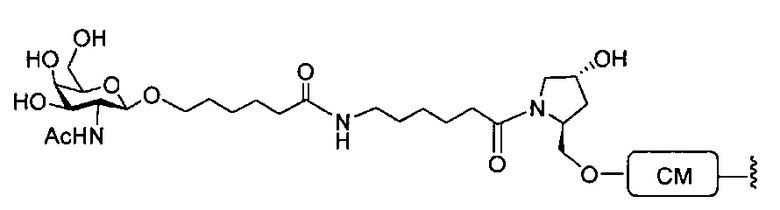 .
.
Пример 110: Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-30
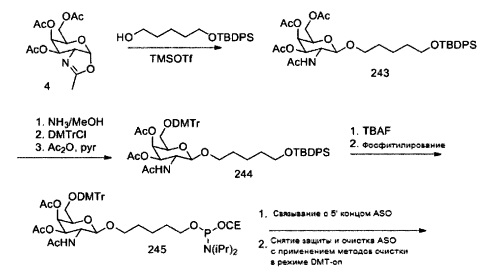
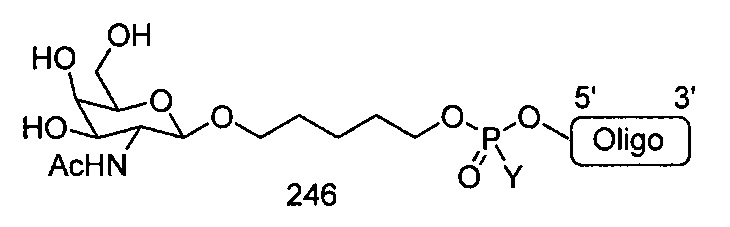
Олигонуклеотид 246, содержащий группу конъюгата GalNAc1-30, где Y выбран из О, S, замещенного или незамещенного C1-C10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GalNAc1 (GalNAc1-30а) группы конъюгата GalNAc1-30 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. В некоторых вариантах реализации Y представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc1-30а представлена ниже:
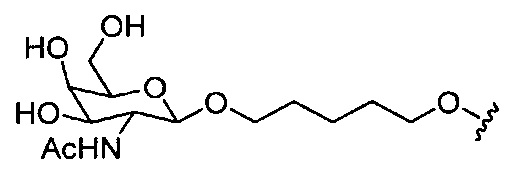
Пример 111: Синтез олигонуклеотидов, содержащих конъюгат GalNAc2-31 или GalNAc2-32
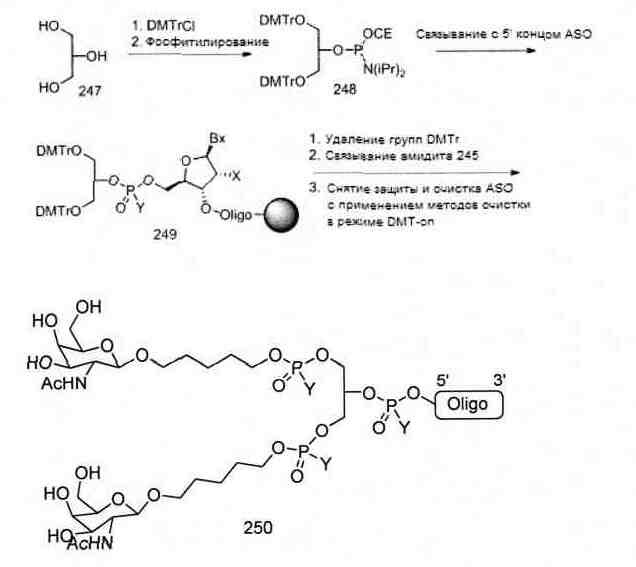
Олигонуклеотид 250, содержащий группу конъюгата GalNAc2-31, где Y выбран из О, S, замещенного или незамещенного C1-C10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GalNAc2 (GalNAc2-31а) группы конъюгата GalNAc2-31 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc2-31а представлена ниже:
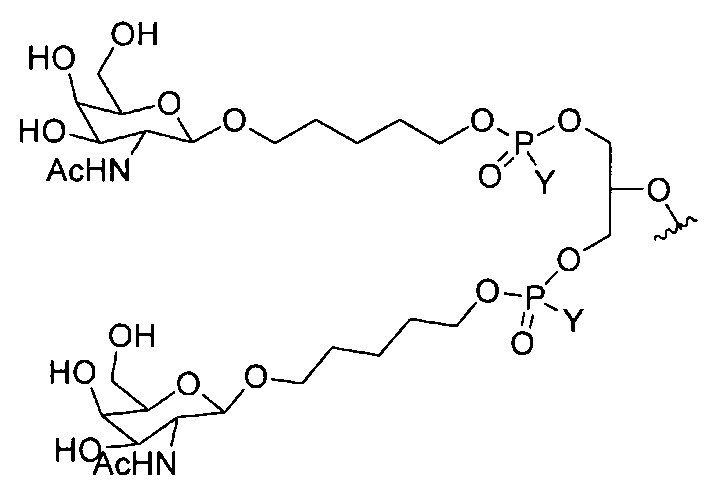
Синтез олигонуклеотида, содержащего конъюгат GalNAc2-32, представлен ниже.
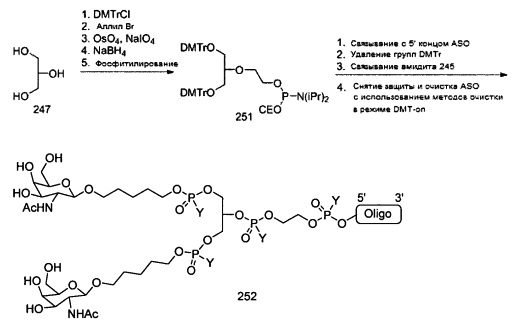
Олигонуклеотид 252, содержащий группу конъюгата GalNAc2-32, где Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GalNAc2 (GalNAc2-32a) группы конъюгата GalNAc2-32 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных групп конъюгата. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc2-32a представлена ниже:
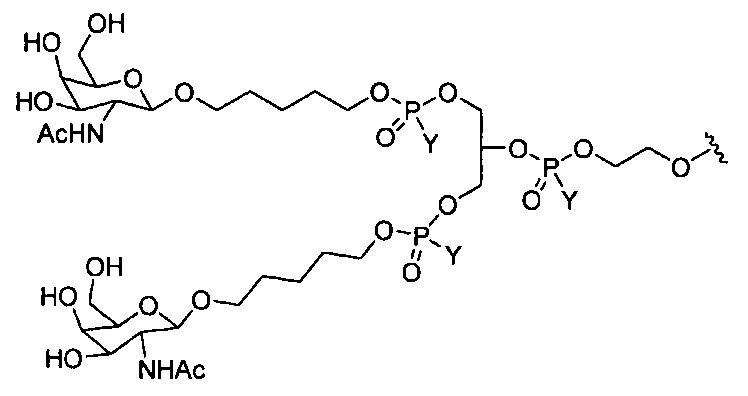
Пример 112: Модифицированные олигонуклеотиды, содержащие конъюгат GalNAc1
Олигонуклеотиды в Таблице 120, направленные на SRB-1, были синтезированы с группой конъюгата GalNAc1 для дополнительной проверки эффективности олигонуклеотидов, содержащих группы конъюгата, которые содержат один лиганд GalNAc.
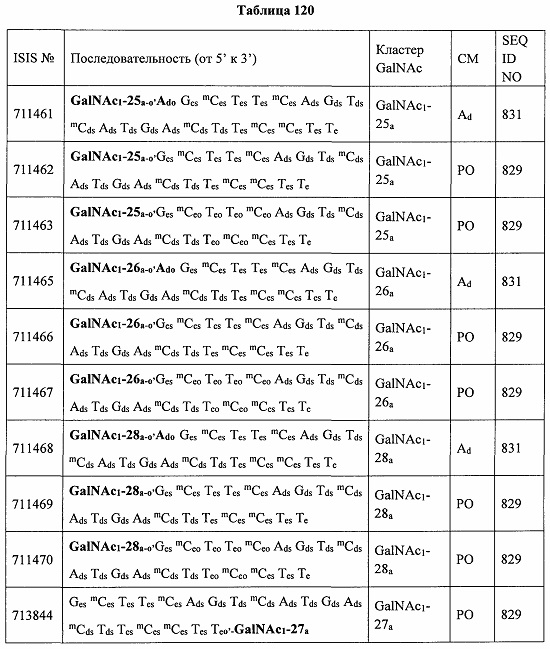

Пример 113: Анти смысловое ингибирование in vivo под действием олигонуклеотидов, направленных на CFB
Олигонуклеотиды, перечисленные в Таблице 121, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого фактора комплемента В (CFB) у мышей.

Структура GalNAc3-3a показана ранее в Примере 39.
Лечение
Каждой трансгенной мыши, экспрессирующей человеческий CFB (Jackson Laboratory, Бар-Харбор, штат Мэн), один раз в неделю в течение 3 недель (в целом 4 дозы) вводили подкожную инъъекцию олигонуклеотида, перечисленного в Таблице 122, или солевого раствора. Четырем экспериментальным группам, которым вводили ISIS №588540, вводили 6, 12, 25 или 50 мг/кг на дозу. Четырем экспериментальным группам, которым вводили ISIS №687301, вводили 0,25, 0,5, 2 или 6 мг/кг на дозу. Каждая экспериментальная группа состояла из 4 животных. Мышей усыпили через 2 дня после последнего введения дозы для определения уровней человеческого CFB и мРНК циклофилина в печени и почках, используя ПЦР в реальном времени по стандартным протоколам. Уровни мРНК CFB нормализовали к уровням циклофилина, а средние значения для каждой экспериментальной группы использовали для определения дозы, которая обеспечивает достижение 50% ингибирования экспрессии транскрипта человеческого CFB (ED50). Результаты представляют собой средине значения для четырех экспериментов, проведенных с двумя разными наборами праймерных зондов, и представлены в Таблице 122.
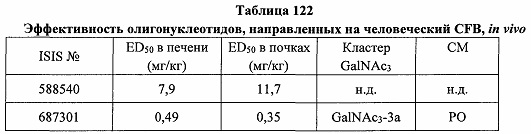
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, используя стандартные протоколы. Оценили также общий билирубин, азот мочевины крови (АМК) и массу тела. Результаты демонстрируют, что экспериментальные группы не демонстрируют существенных отличий от группы, обработанной солевым раствором (данные не показаны), что указывает на хорошую переносимость обоих олигонуклеотидов.
Пример 114: Антисмысловое ингибирование in vivo под действием олигонуклеотидов, направленных на CFB
Олигонуклеотиды, перечисленные в Таблице 123, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого CFB у мышей.
Лечение
Каждой трансгенной мыши, экспрессирующей человеческий CFB (Jackson Laboratory, Бар-Харбор, штат Мэн), ввели однократную подкожную инъекцию 0,6, 1, 6 или 18 мг/кг олигонуклеотида, перечисленного в Таблице 123, или солевого раствора. Каждая экспериментальная группа состояла из 4 или 5 животных. Мышей усыпили через 72 часа после введения дозы для определения уровней человеческого CFB и мРНК циклофилина в печени, используя ПЦР в реальном времени по стандартным протоколам. Уровни мРНК CFB нормализовали к уровням циклофилина, а средние значения для каждой экспериментальной группы использовали для определения дозы, которая обеспечивает достижение 50% ингибирования экспрессии транскрипта человеческого CFB (ED50). Результаты представлены в Таблице 123.

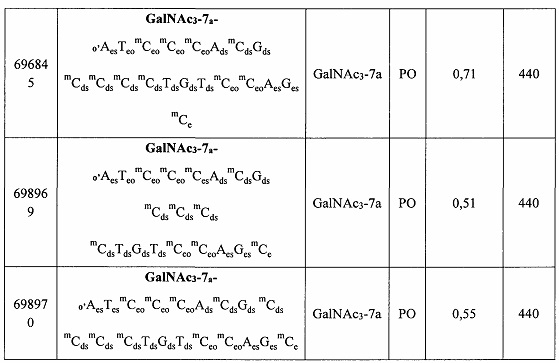
Структура GalNAc3-7a показана ранее в Примере 48.
Пример 115: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов, которые имели аналогичные условия культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку трансфицировали с использованием электропорации с 4500 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймерных зондов RTS3459 (прямая последовательность AGTCTCTGTGGCATGGTTTGG, обозначенная в настоящем документе как SEQ ID NO: 810; обратная последовательность GGGCGAATGACTGAGATCTTG, обозначенная в настоящем документе как SEQ ID NO: 811; последовательность зонда TACCGATTACCACAAGCAACCATGGCA, обозначенная в настоящем документе как SEQ ID NO: 812) был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды, указанные в представленных ниже таблицах, были сконструированы как 5-10-5 МОЕ гэпмеры. Гэпмеры 5-10-5 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины. «Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.

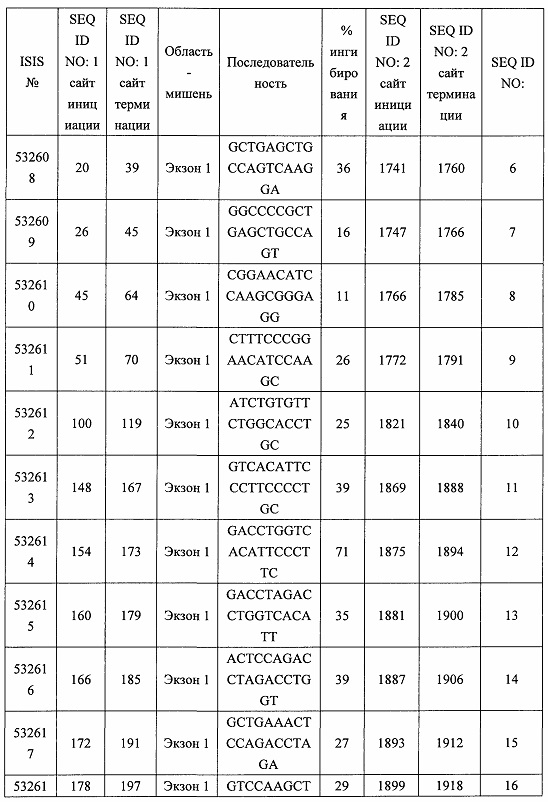
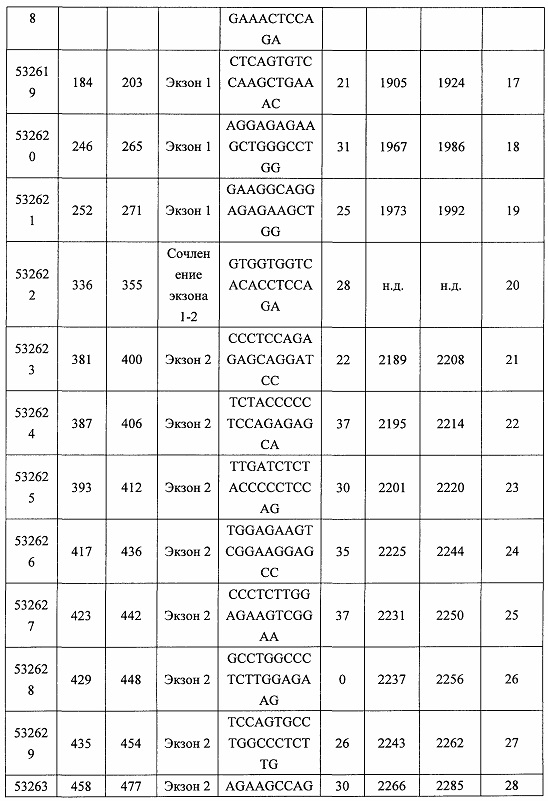
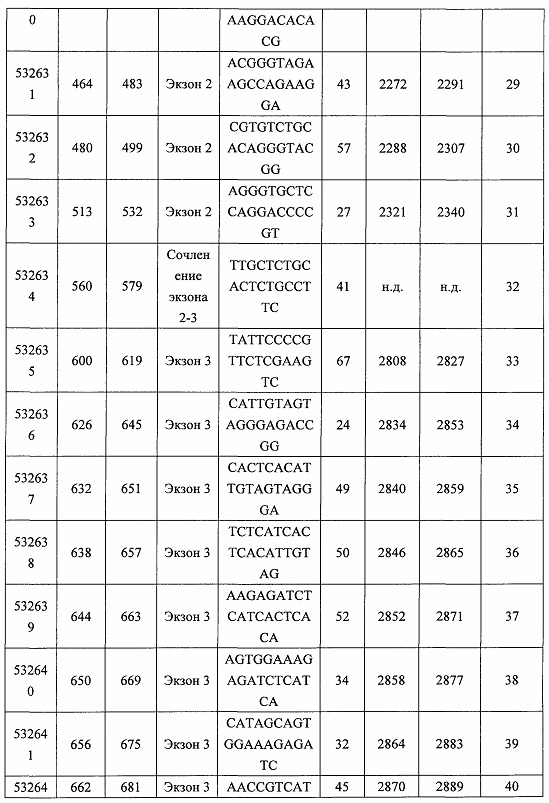
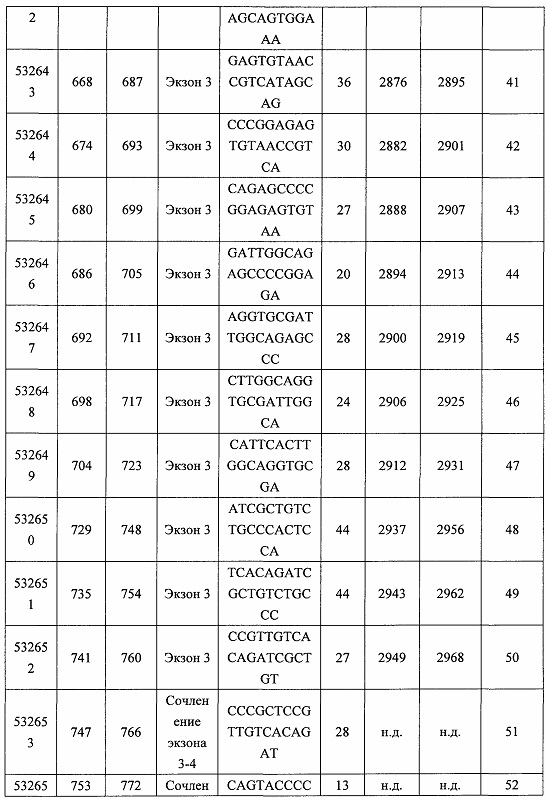
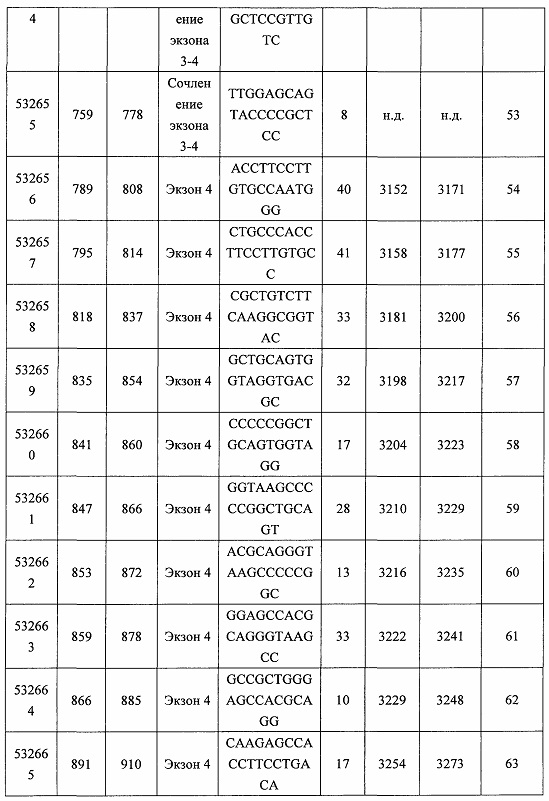
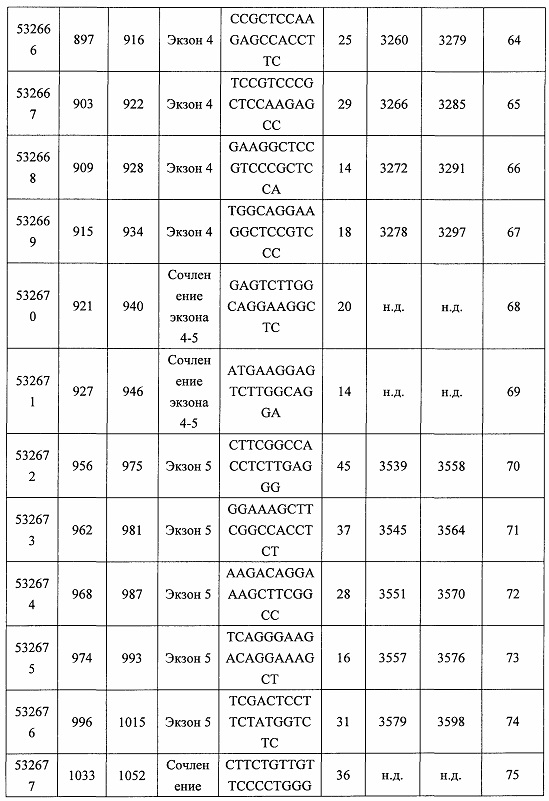
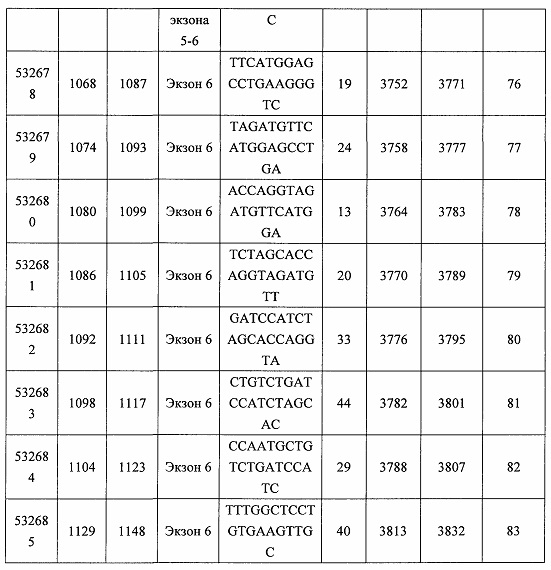
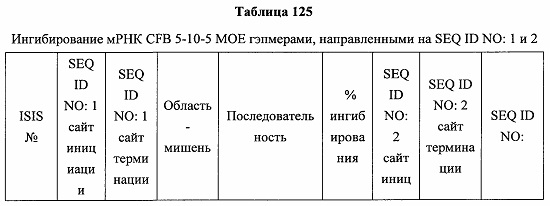
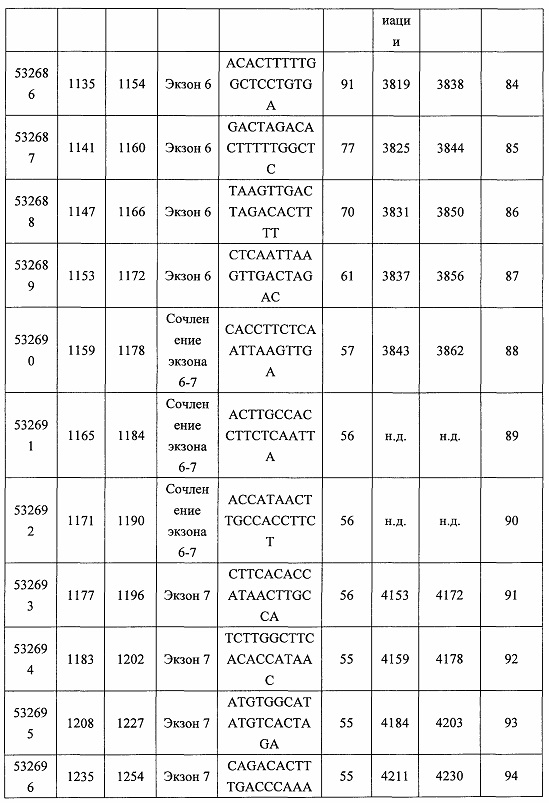
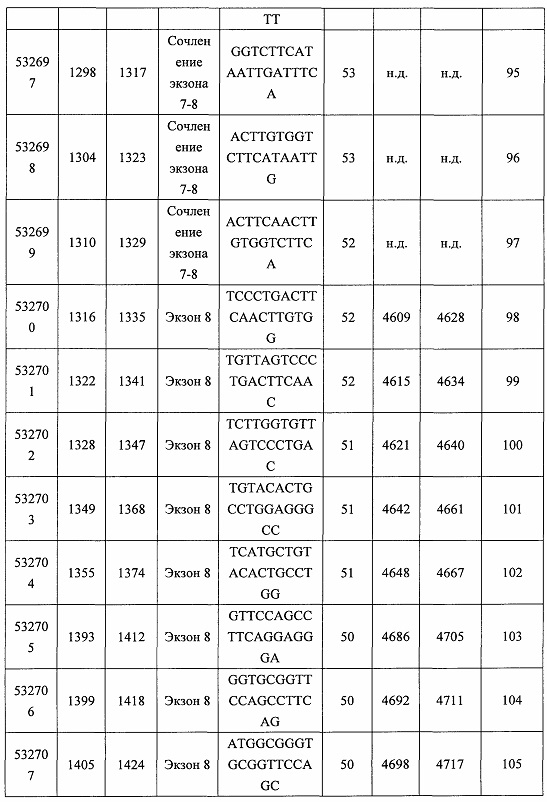

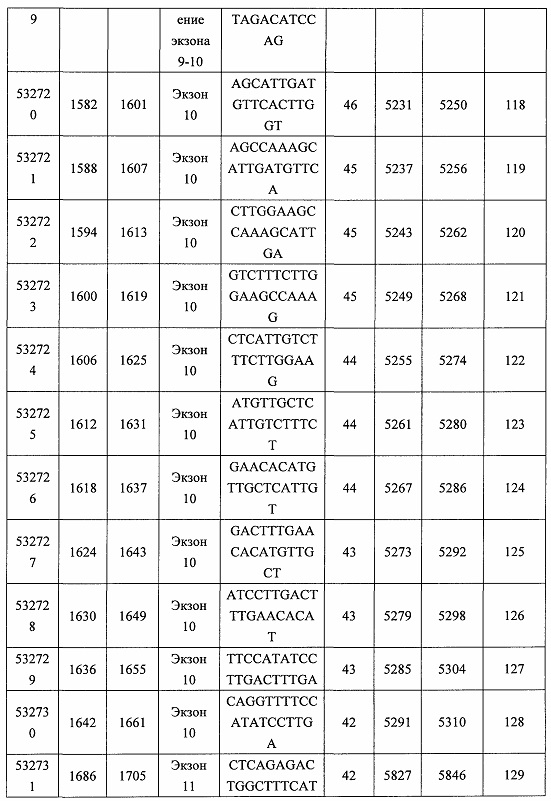
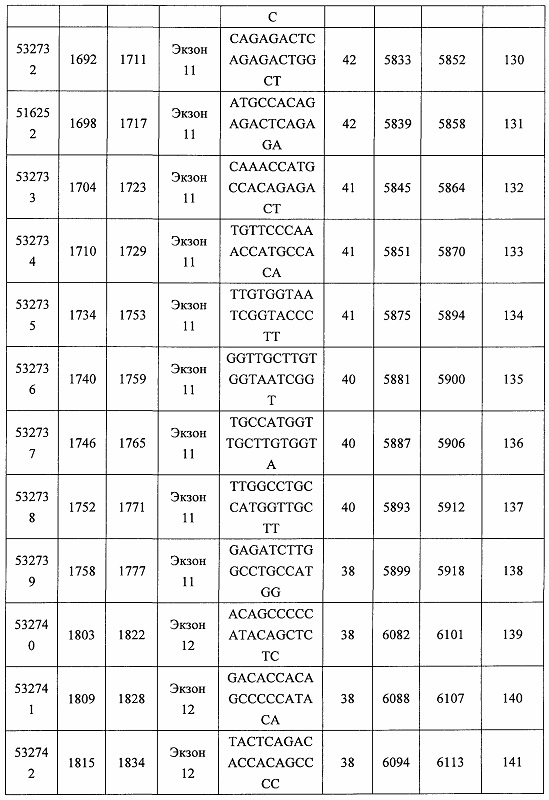
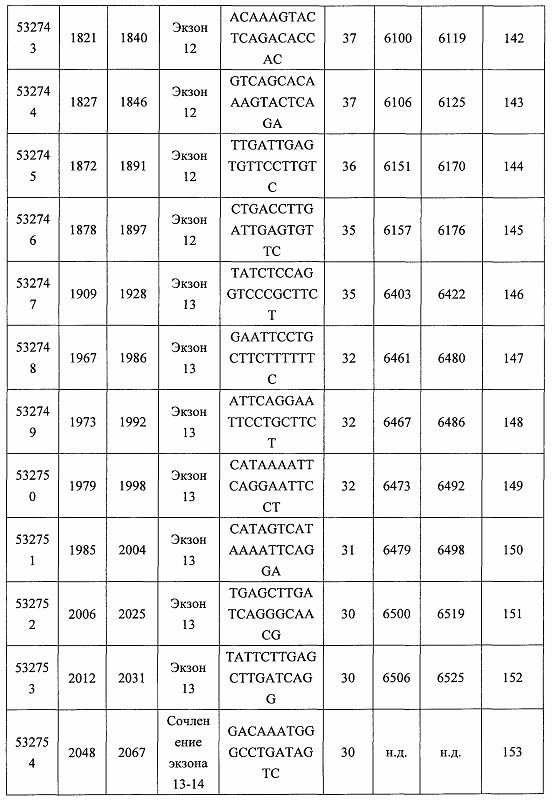
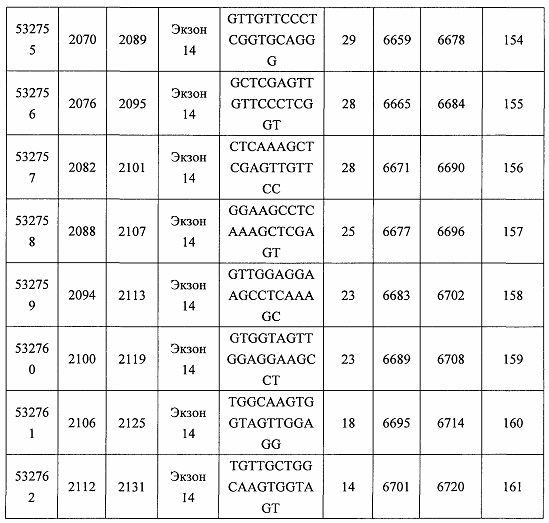
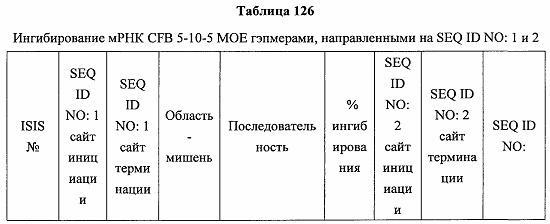
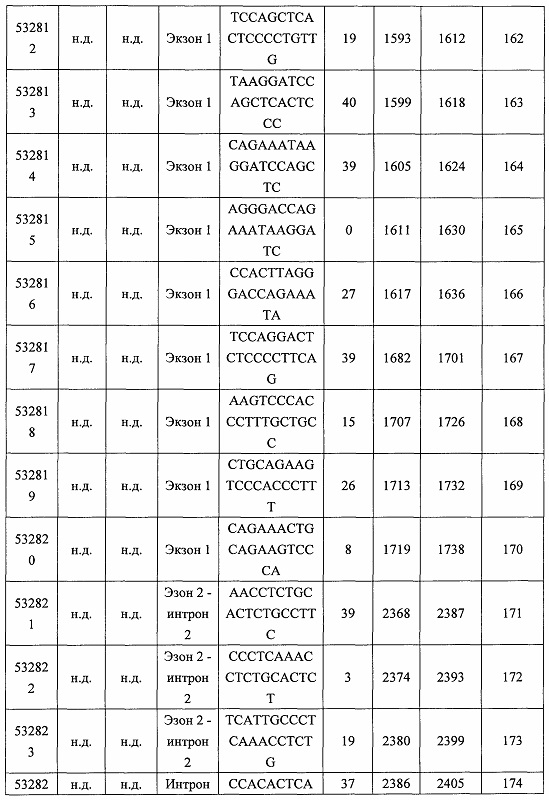
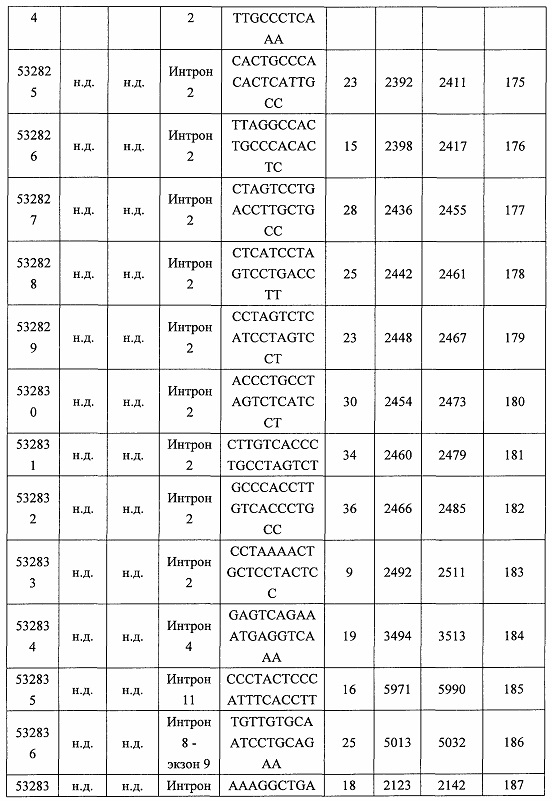
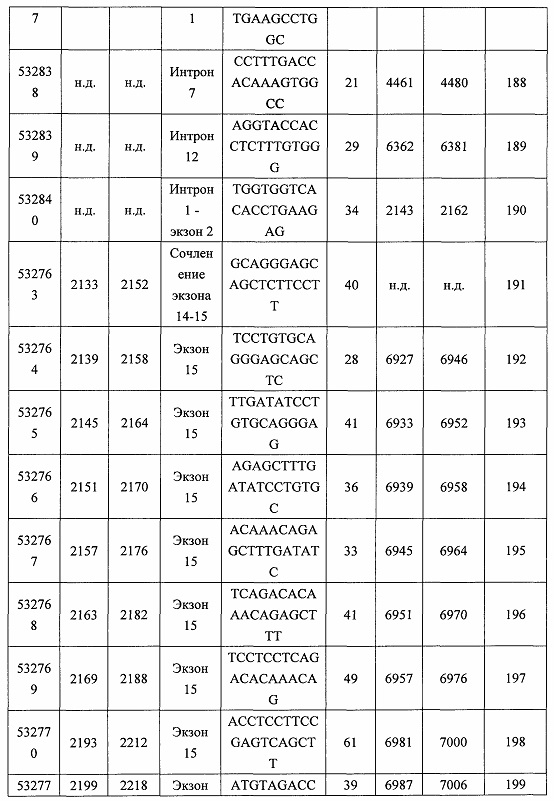
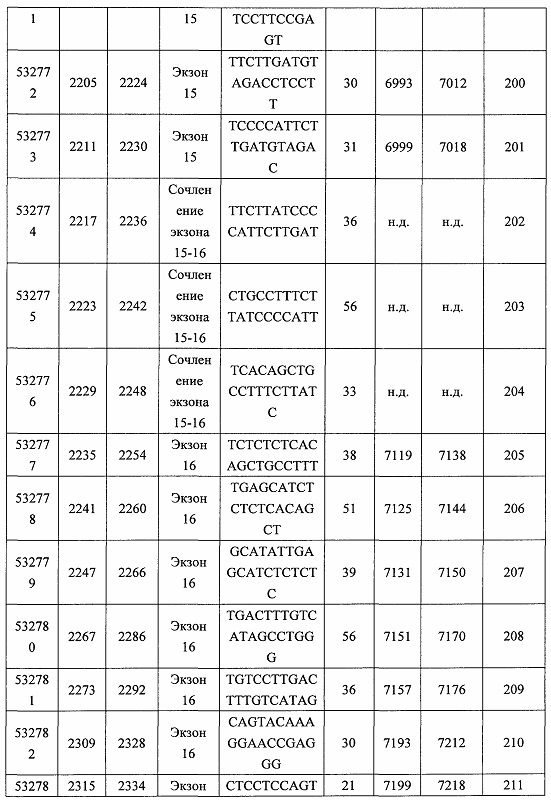
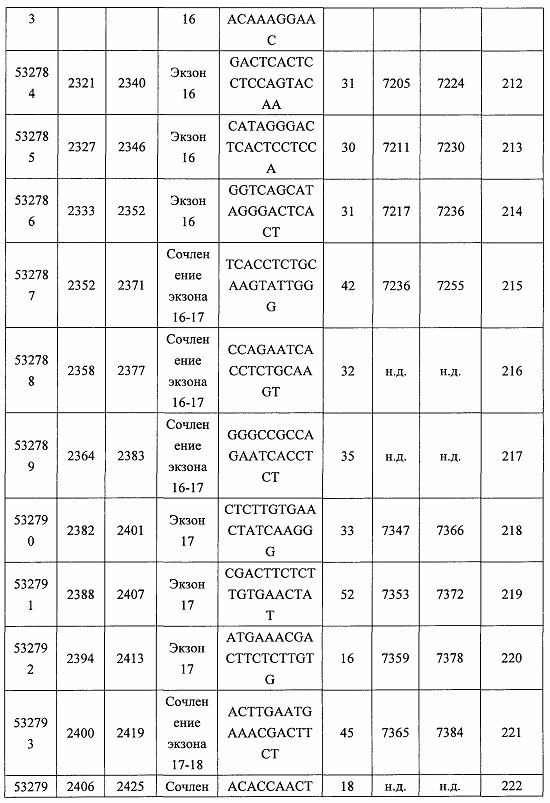
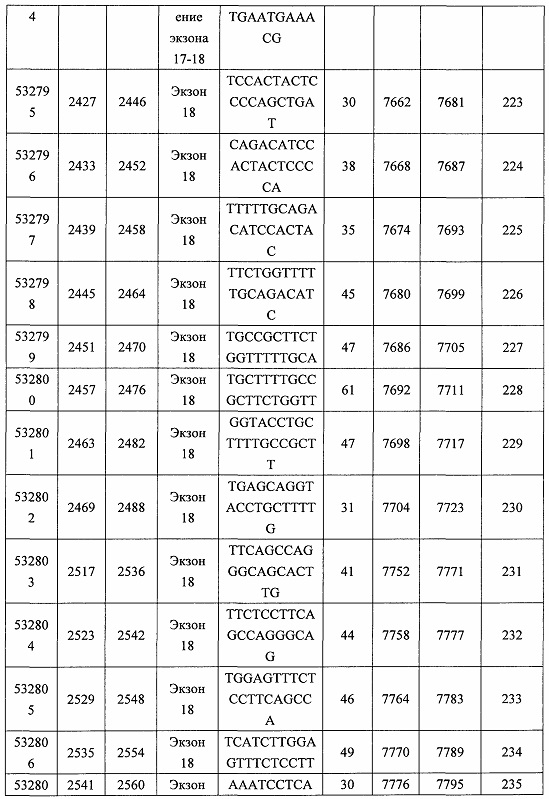

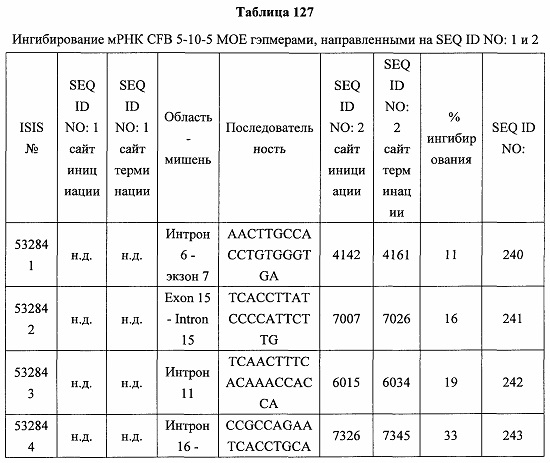
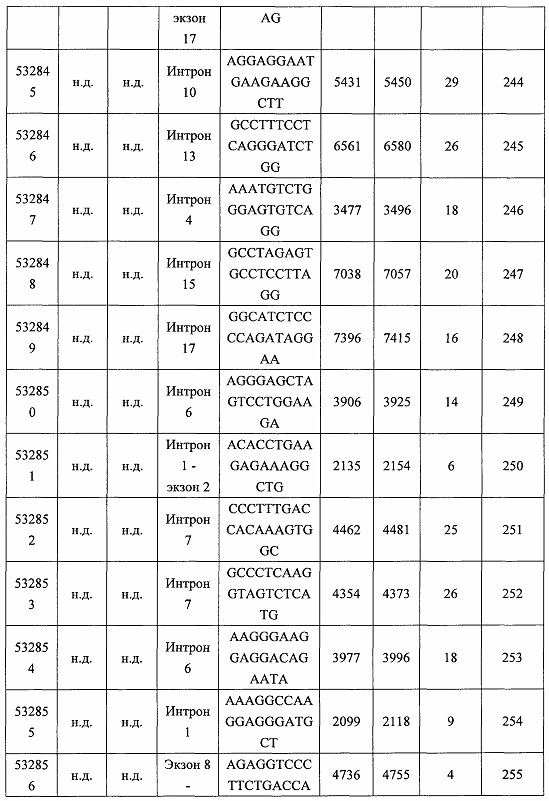
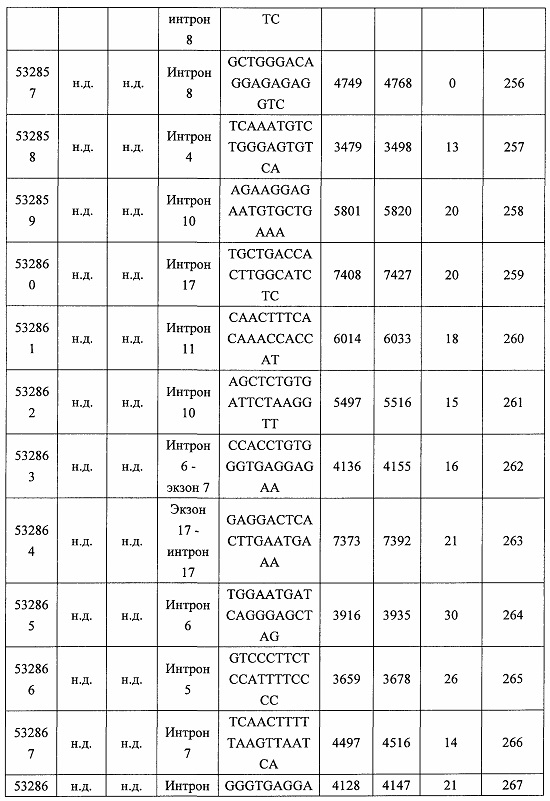
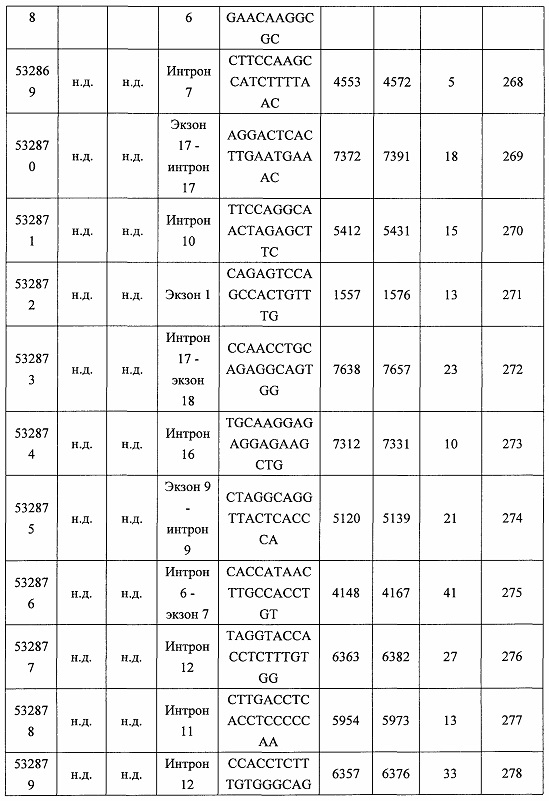
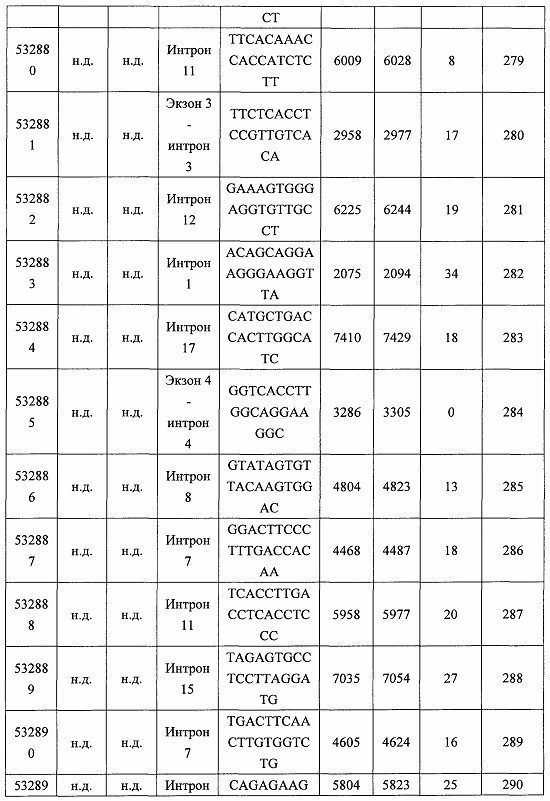
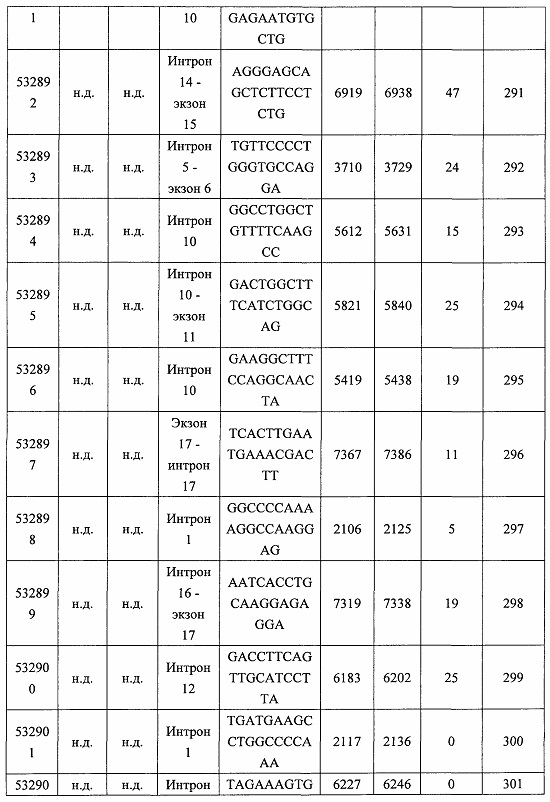


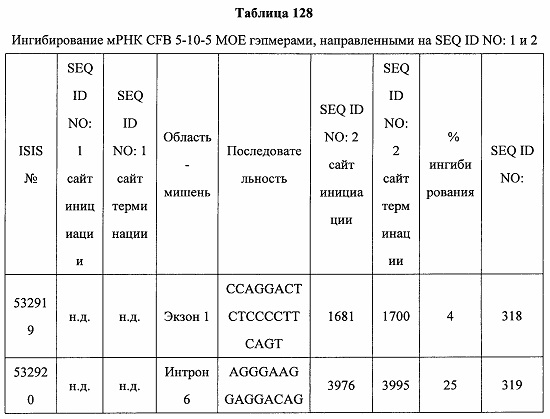
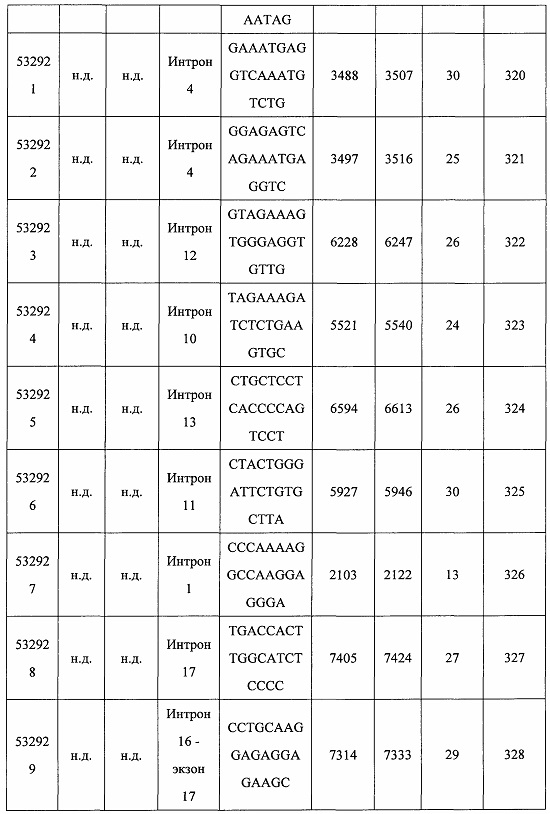
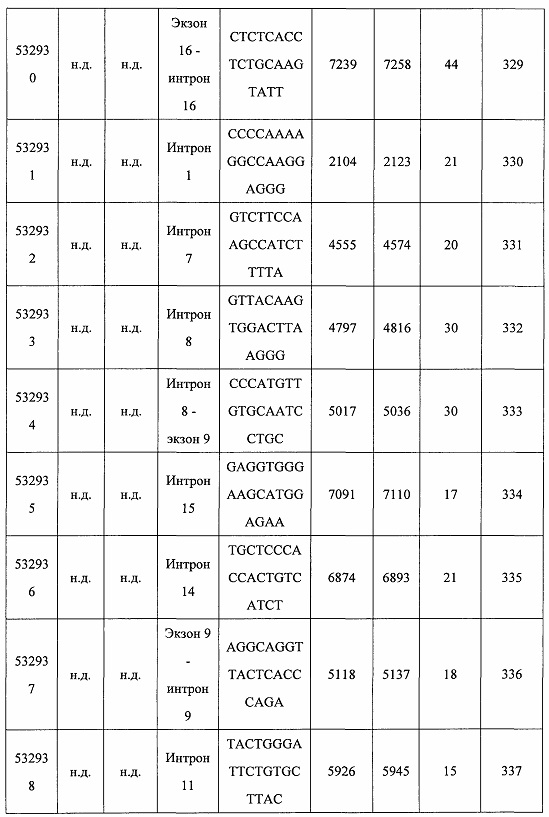
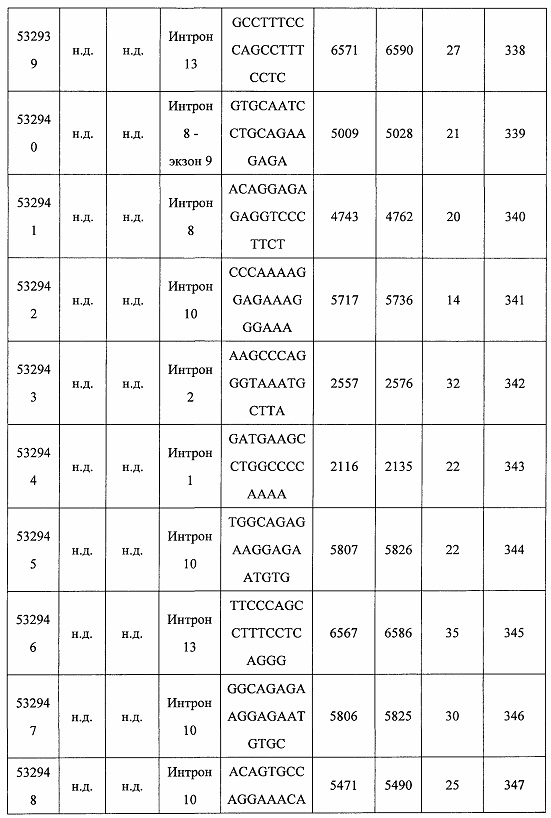
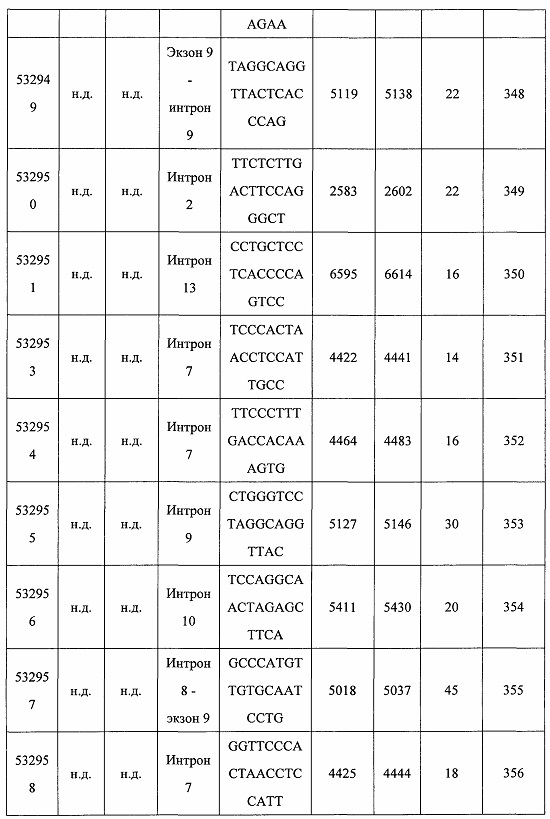
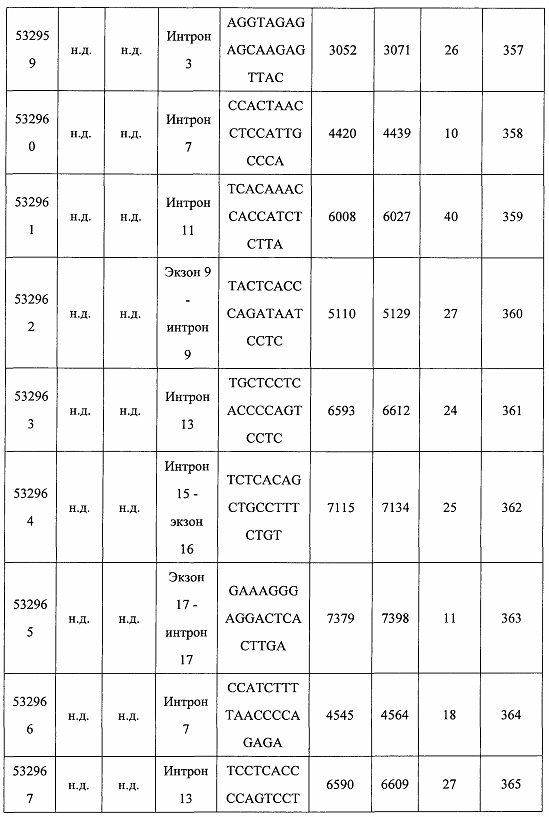
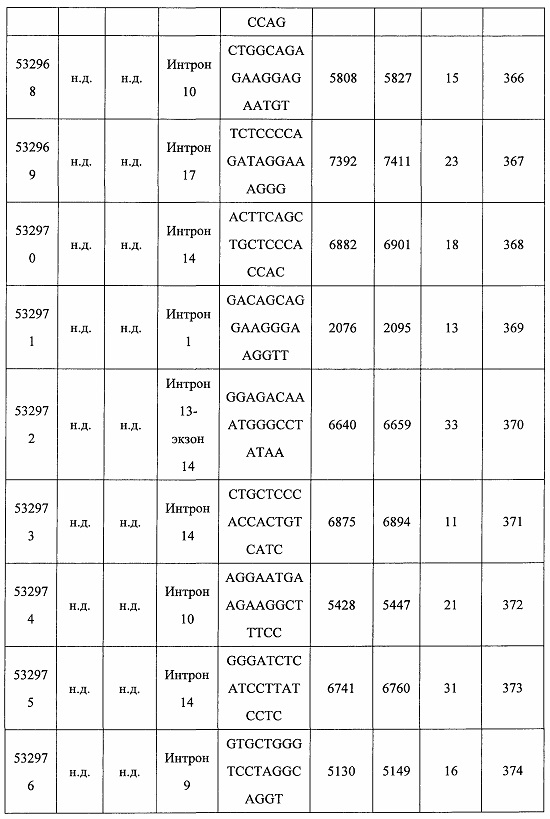
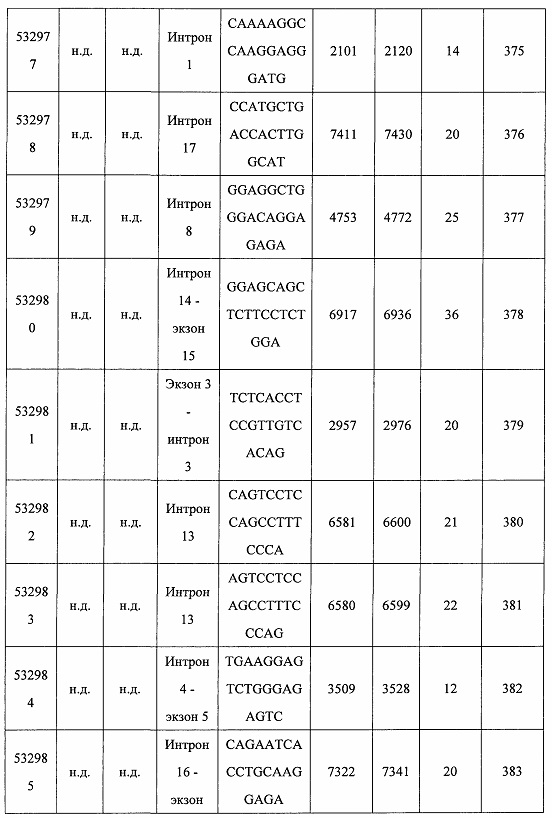
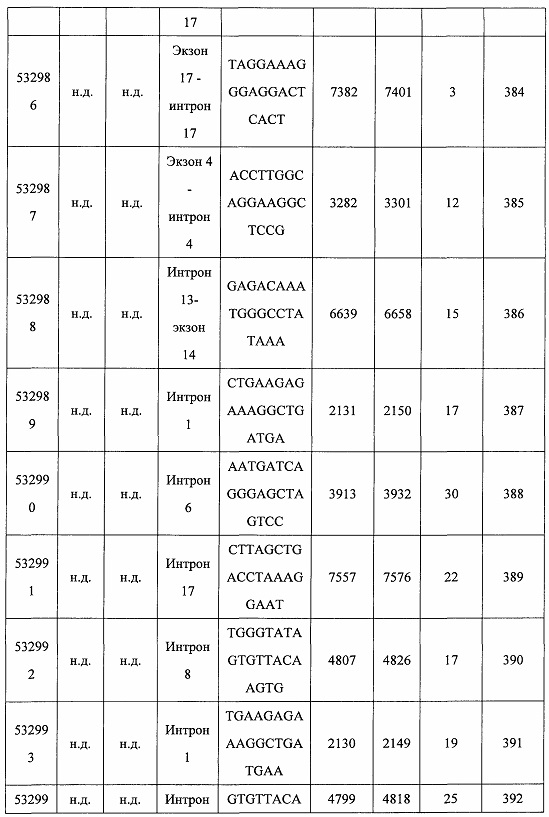
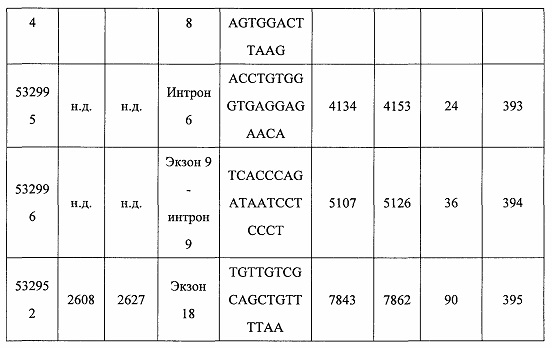
Пример 116: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы дополнительные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку трансфицировали с использованием электропорации с 4500 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймерных зондов RTS3460_MGB (прямая последовательность CGAAGCAGCTCAATGAAATCAA, обозначенная в настоящем документе как SEQ ID NO: 813; обратная последовательность TGCCTGGAGGGCCTTCTT, обозначенная в настоящем документе как SEQ ID NO: 814; последовательность зонда AGACCACAAGTTGAAGTC, обозначенная в настоящем документе как SEQ ID NO: 815) был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды, указанные в представленных ниже таблицах, были сконструированы как 5-10-5 МОЕ гэпмеры. Гэпмеры 5-10-5 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины. «Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.

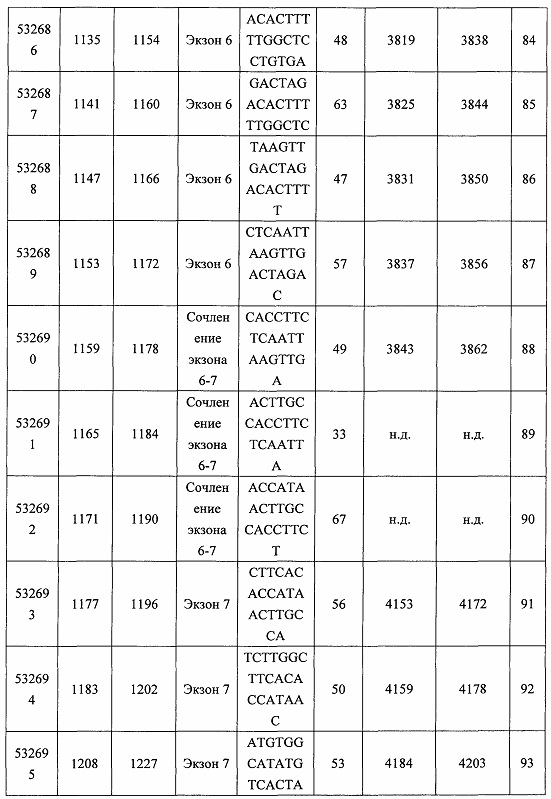
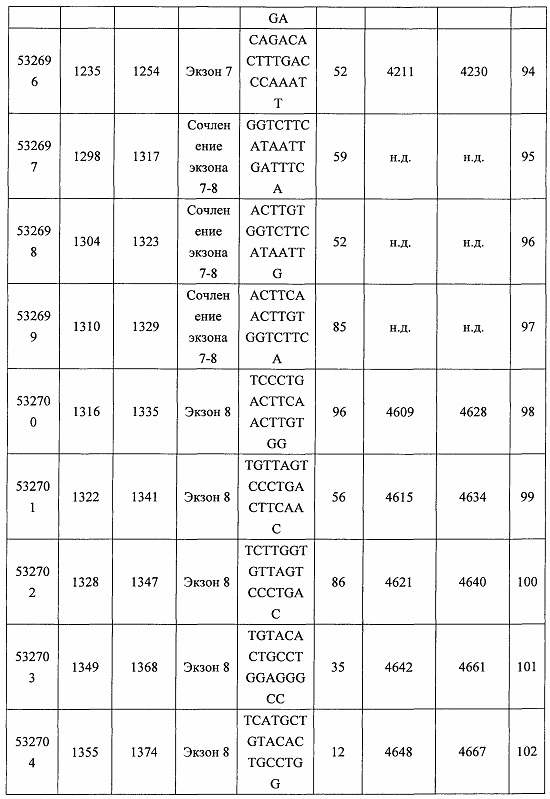
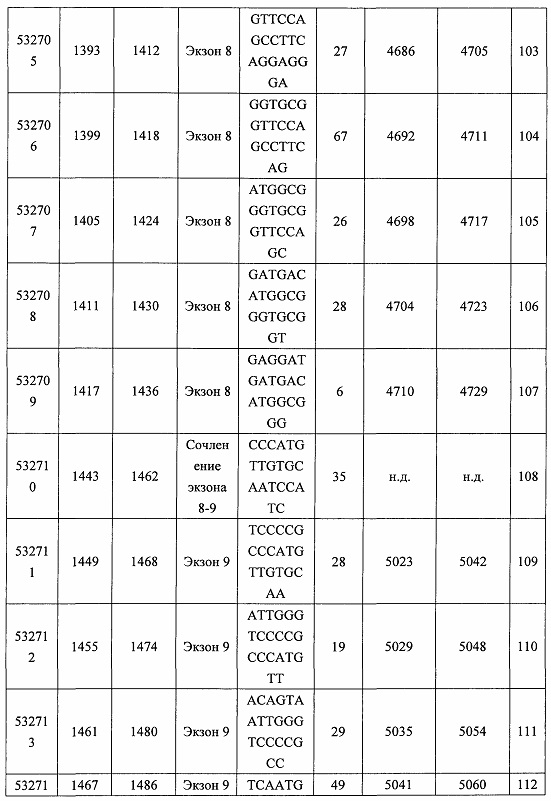
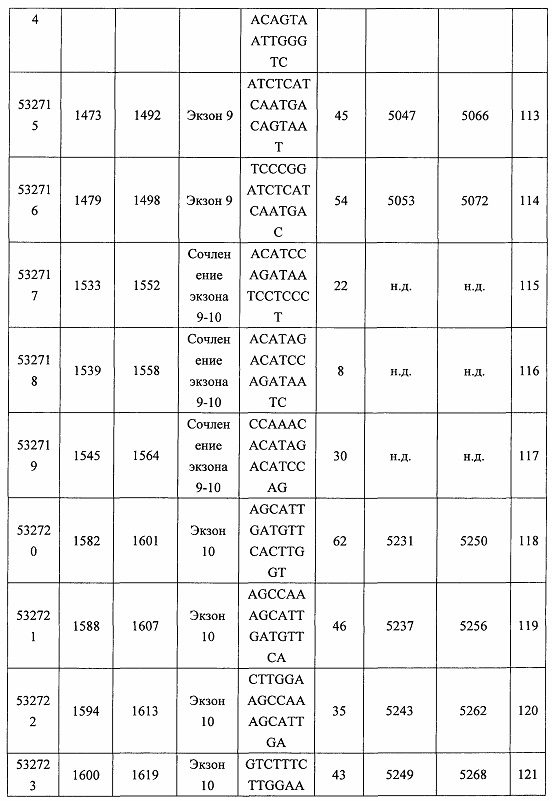
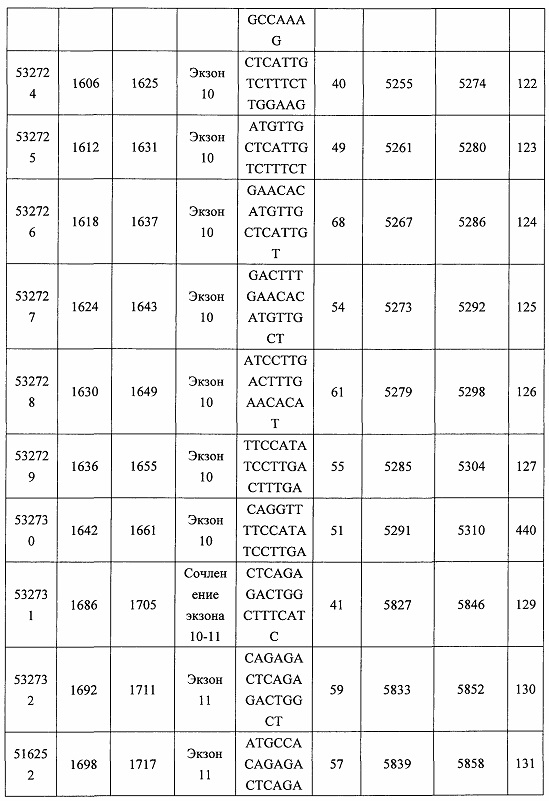
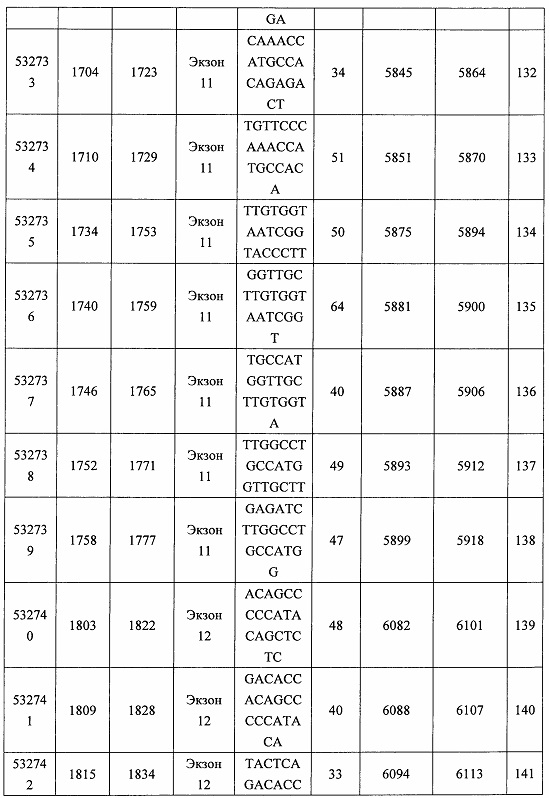

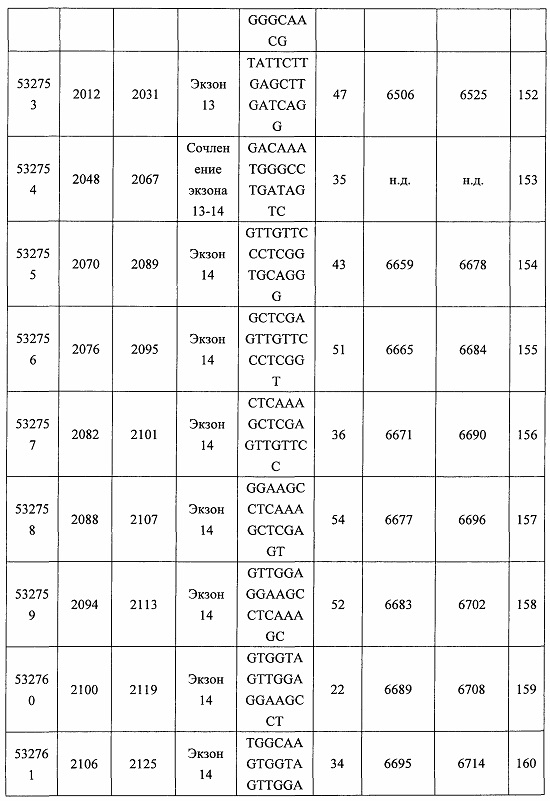
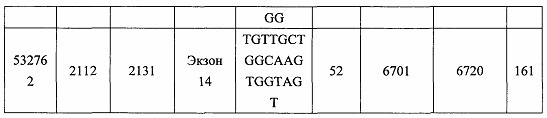
Пример 117: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы дополнительные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов, которые имели аналогичные условия культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку были трансфицированны с использованием электропорации с 5000 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды, указанные в представленных ниже таблицах, были сконструированы как 5-10-5 МОЕ гэпмеры. Гэпмеры имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины. «Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью. Если в определенной таблице не показано выравнивание последовательности к гену-мишени, то следует понимать, что ни один из олигонуклеотидов, представленных в указанной таблице, не выравнивается со 100% комплементарностью с указанным геном-мишенью.
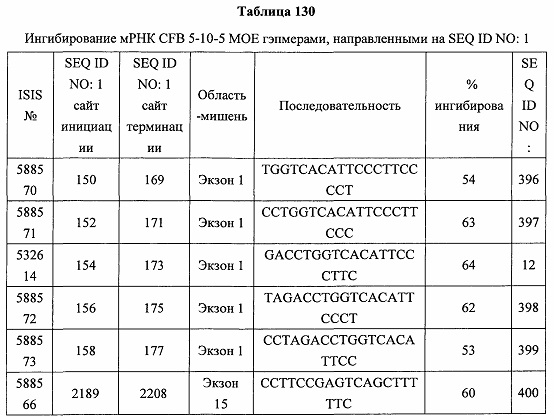
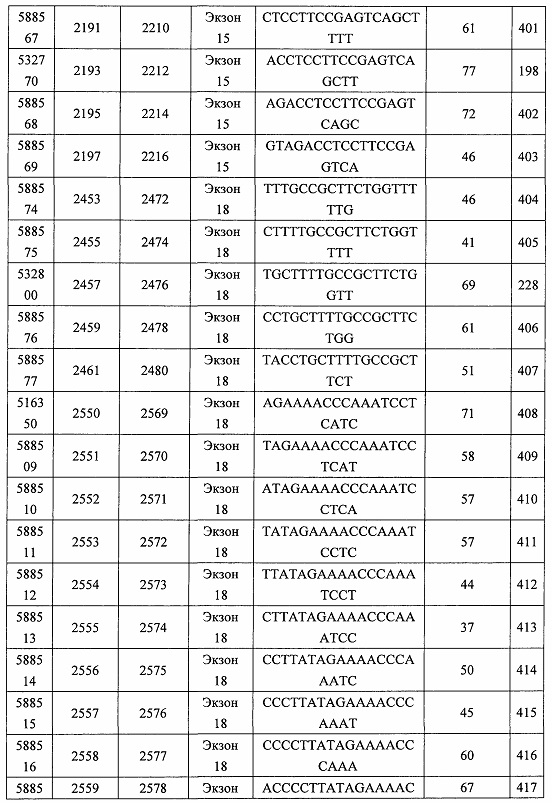
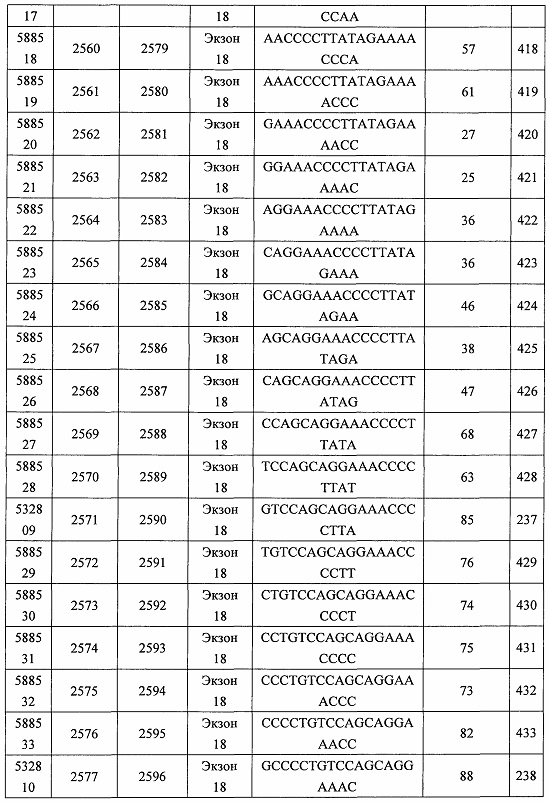
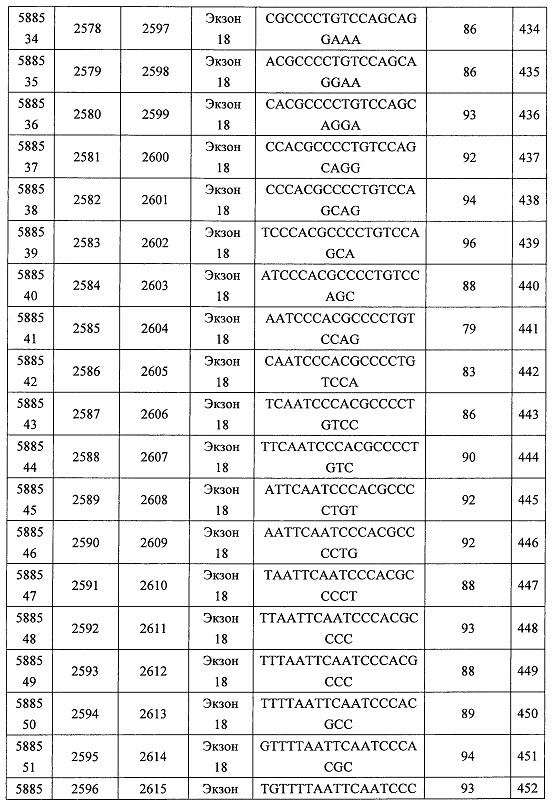
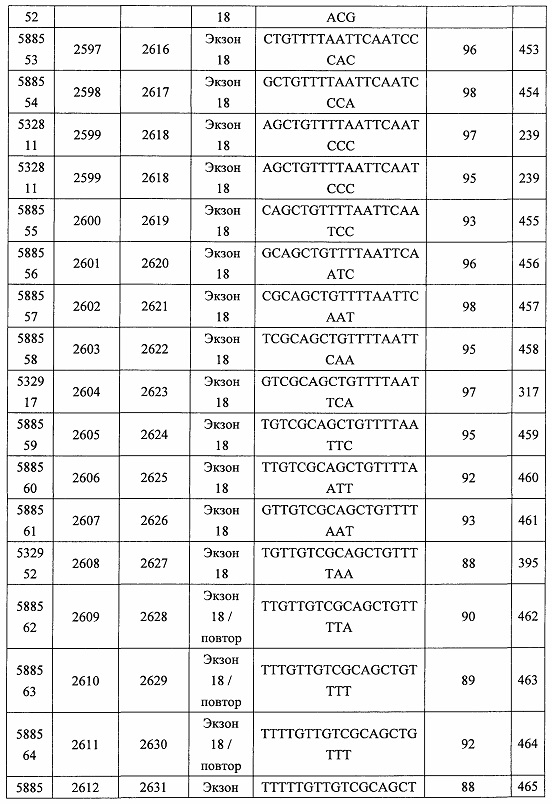
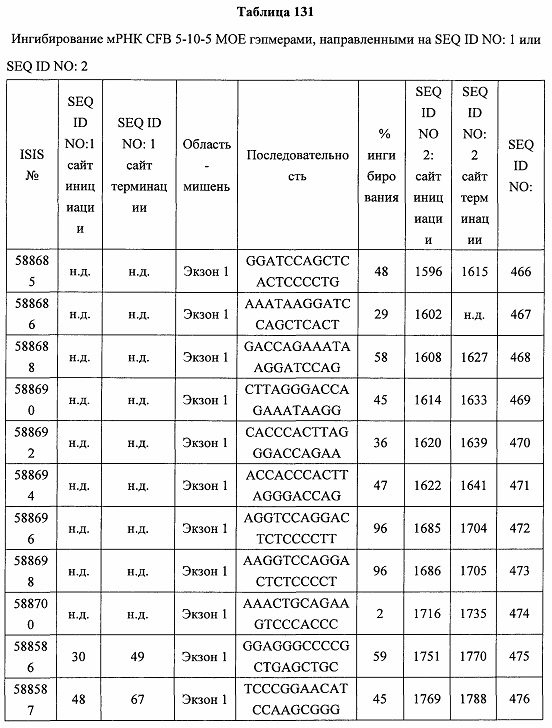
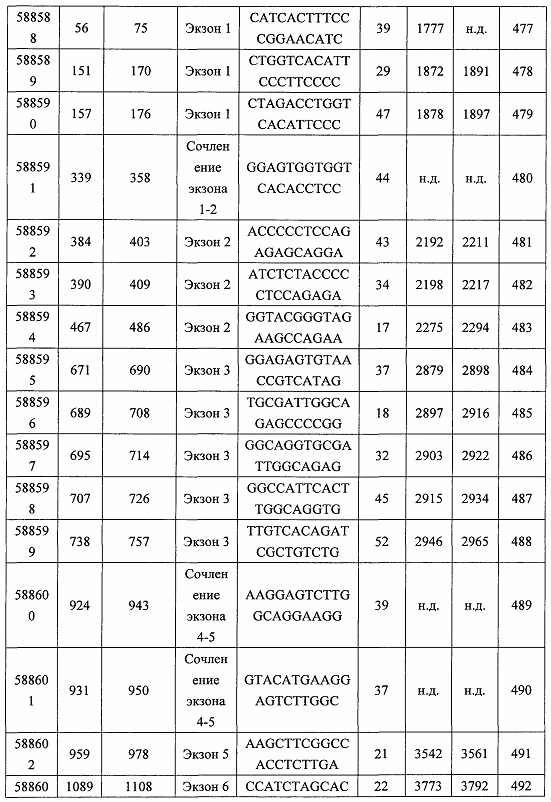
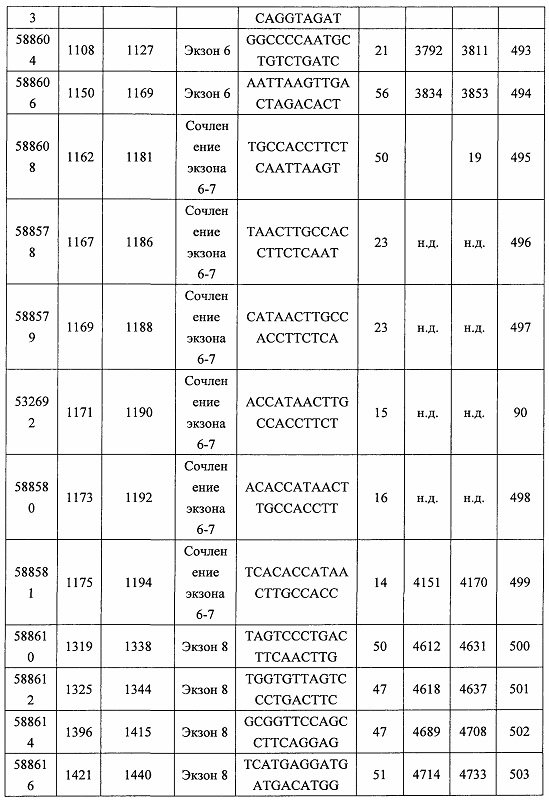
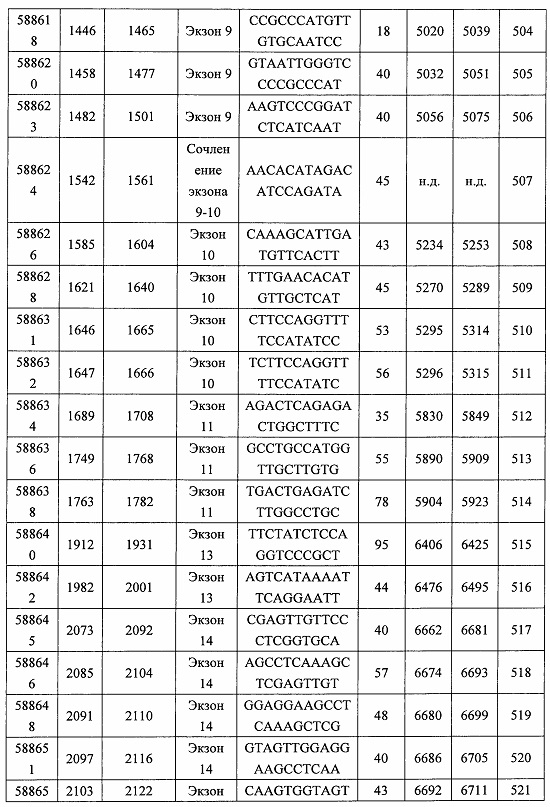
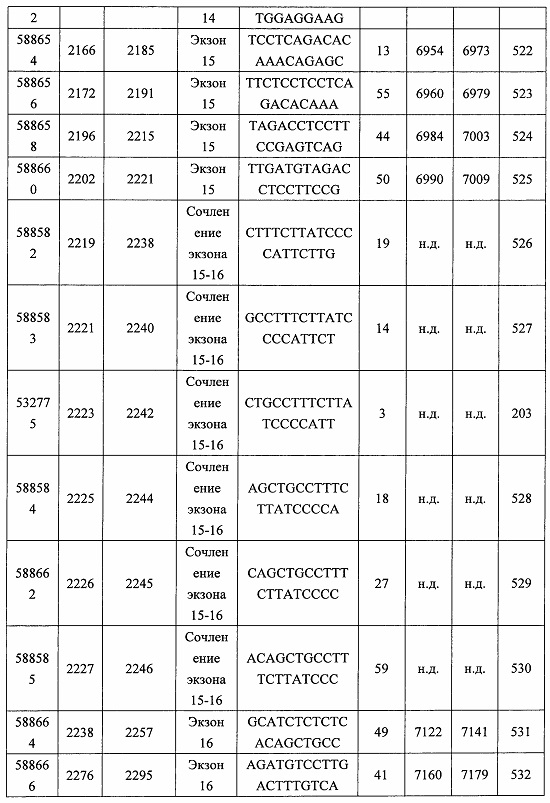
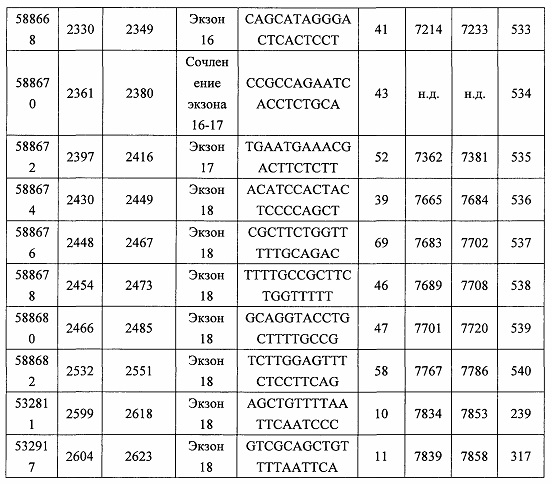
Пример 118: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов, которые имели аналогичные условия культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку были трансфицированны с использованием электропорации с 3000 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды в представленных ниже таблицах были сконструированы как 4-8-5 МОЕ, 5-9-5 МОЕ, 5-10-5 МОЕ, 3-10-4 МОЕ, 3-10-7 МОЕ, 6-7-6- МОЕ, 6-8-6 МОЕ или 5-7-5 МОЕ гэпмеры, или как дезокси, МОЕ и (S)-cEt олигонуклеотиды.
Гэпмеры 4-8-5 МОЕ имеют 17 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими четыре и пять нуклеозидов соответственно. Гэпмеры 5-9-5 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из девяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-10-5 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-7-5 МОЕ имеют 17 нуклеозидов в длину, причем центральный гэп состоит из семи 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 3-10-4 МОЕ имеют 17 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими три и четыре нуклеозида соответственно. Гэпмеры 3-10-7 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими три и семь нуклеозидов соответственно. Гэпмеры 6-7-6 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из семи 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Гэпмеры 6-8-6 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины.
Дезокси, МОЕ и (S)-cEt олигонуклеотиды имеют 16 нуклеозидов в длину, причем нуклеозид содержит либо модификацию сахара МОЕ, либо модификацию сахара (S)-cEt, либо дезокси модификацию. В колонке «Химизм» описаны модификации сахара для каждого олигонуклеотида. «k» означает (S)-cEt модификацию сахара; «d» означает дезоксирибозу; и «е» означает модификацию МОЕ.
«Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.

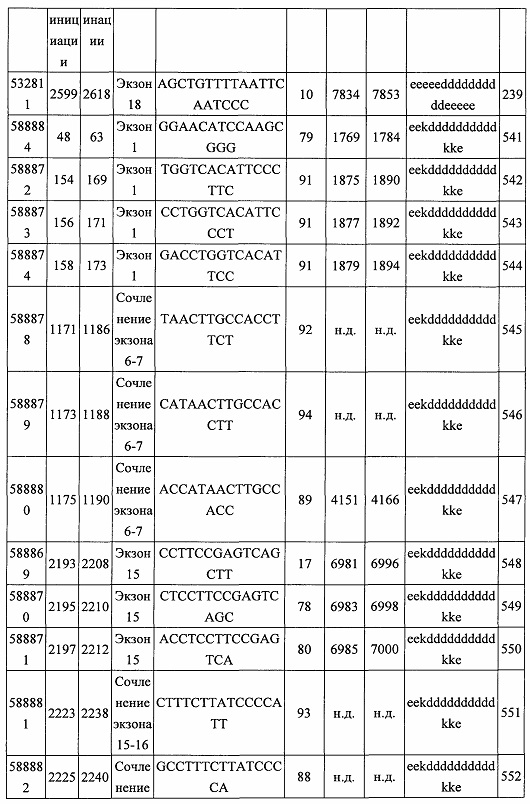
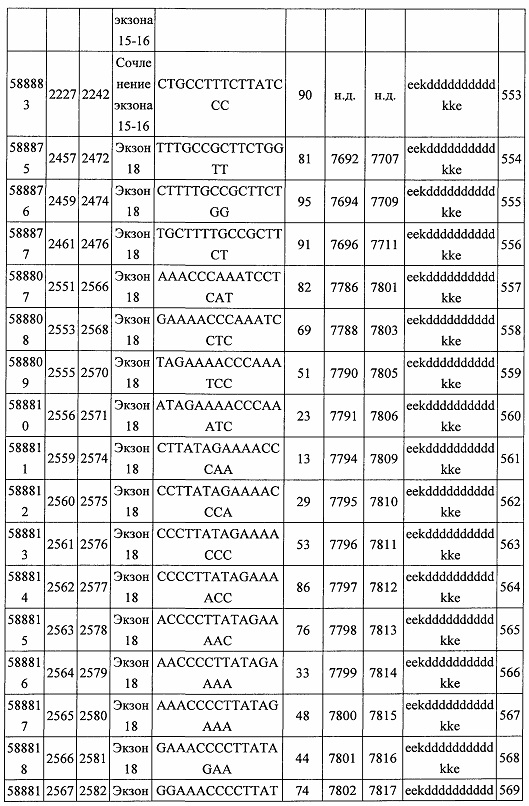
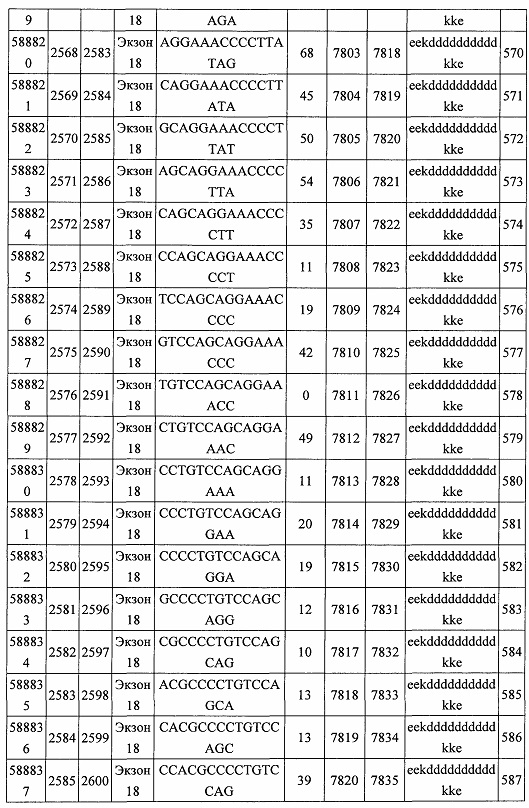
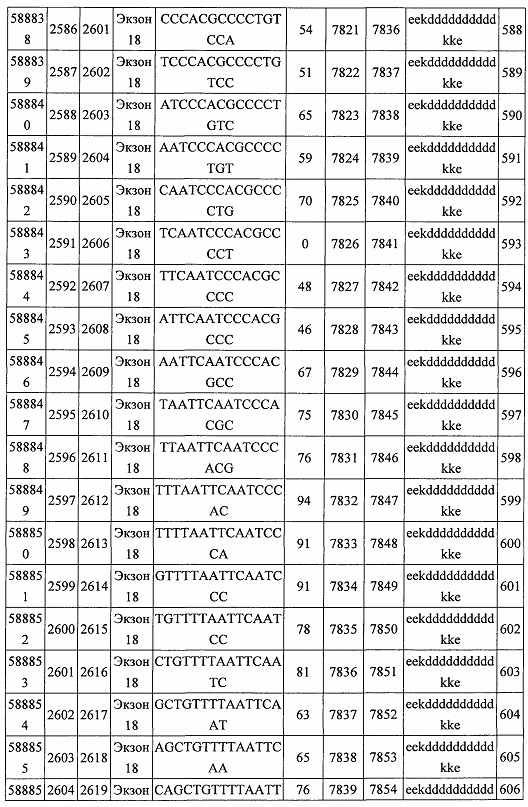
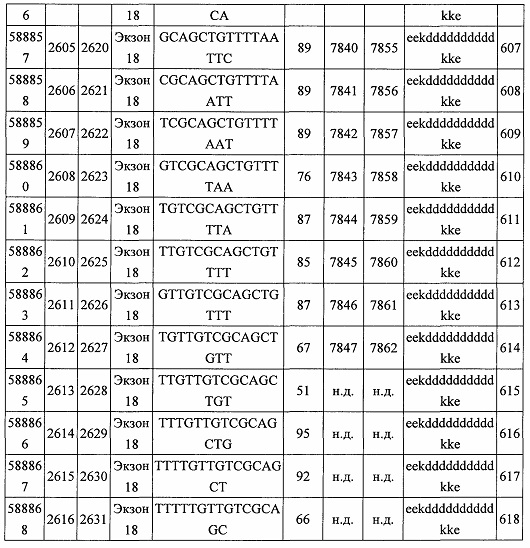

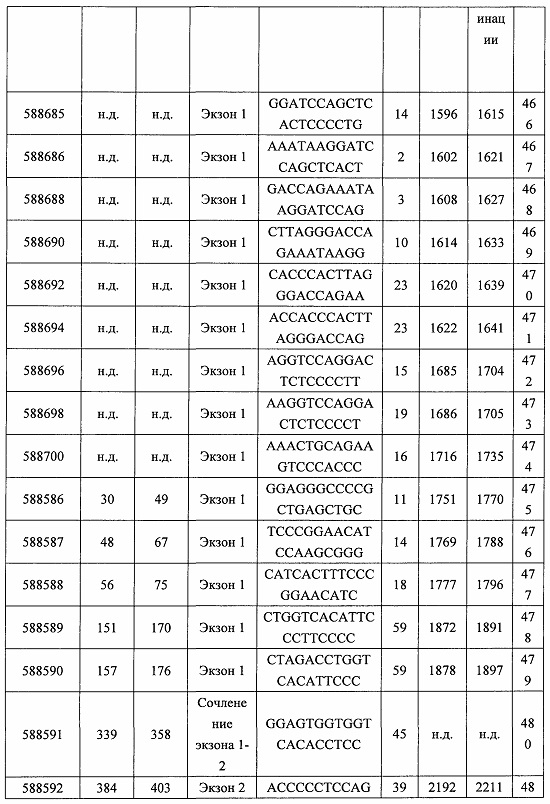
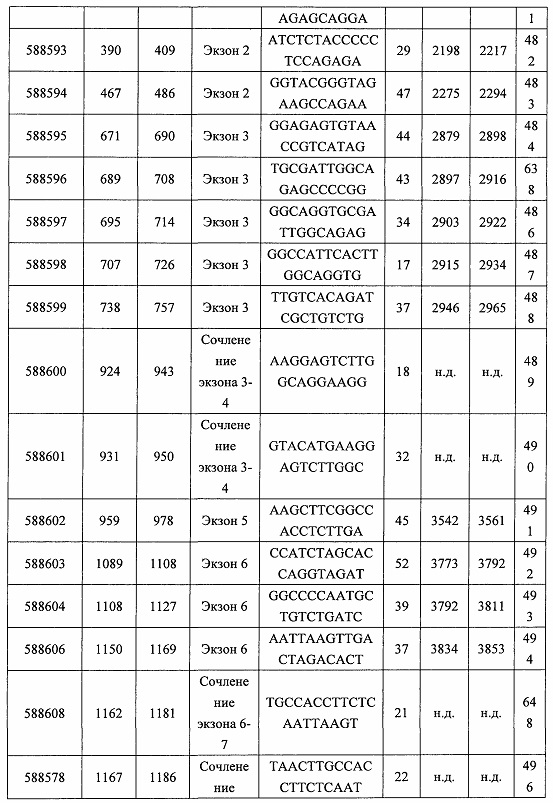
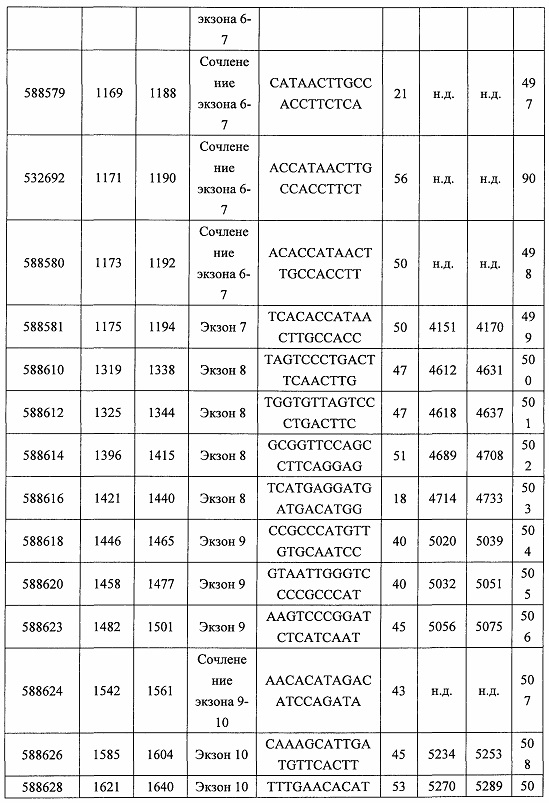
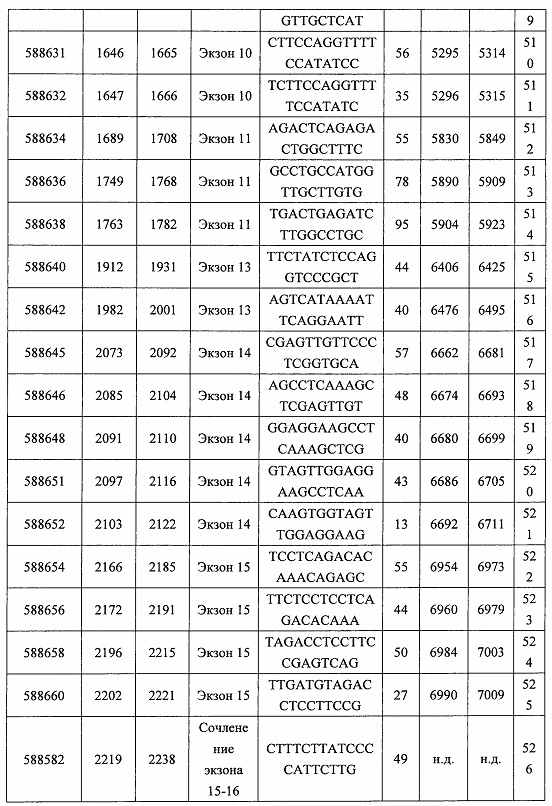
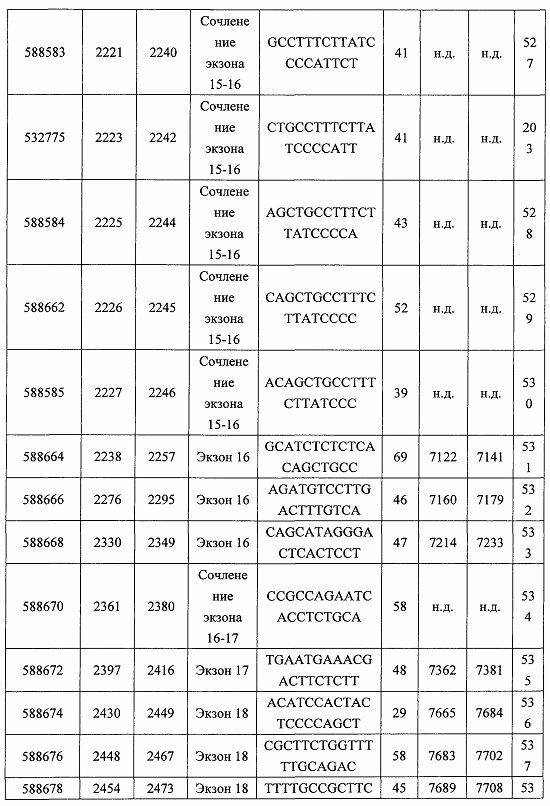

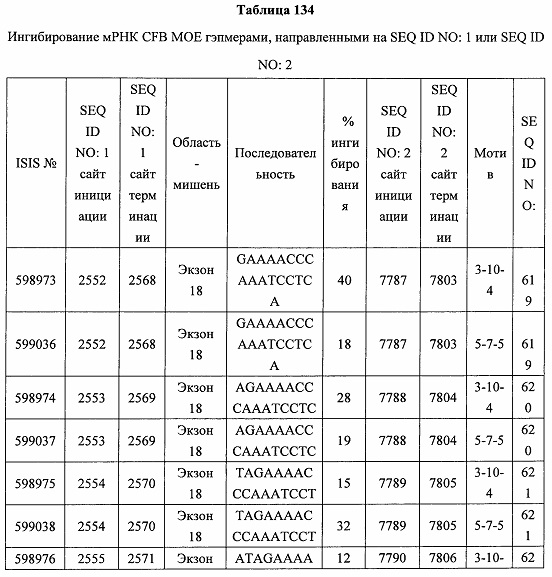
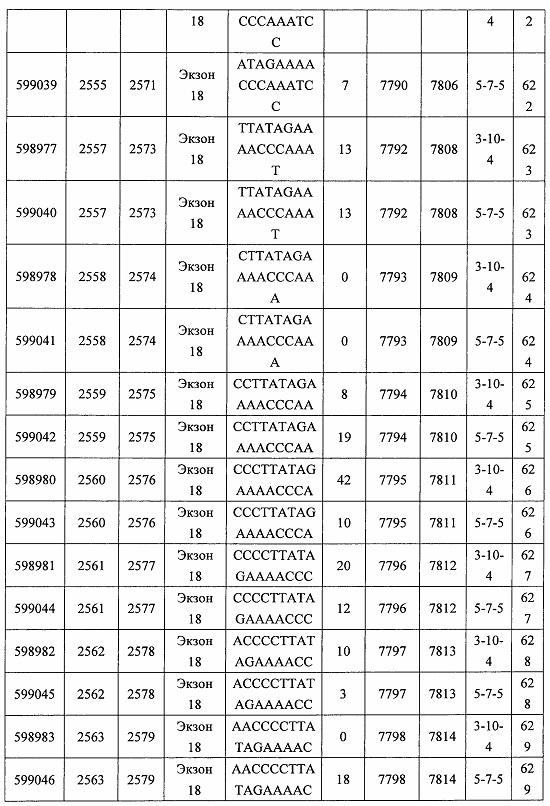
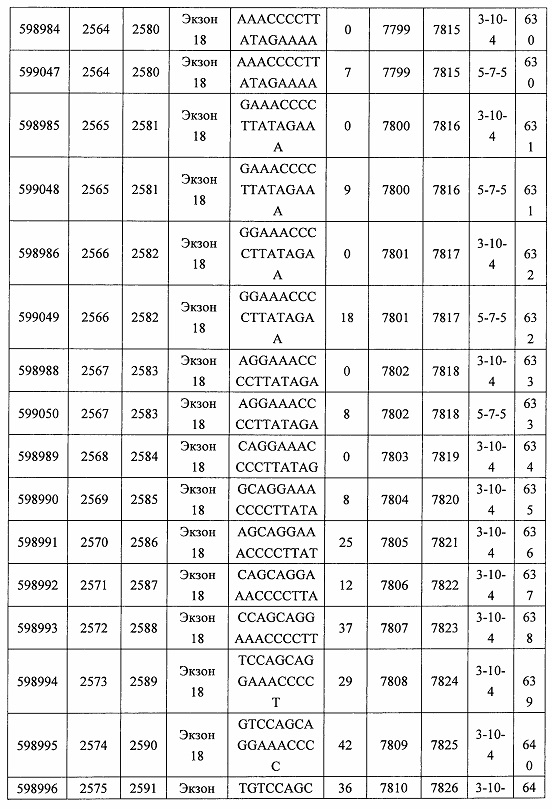
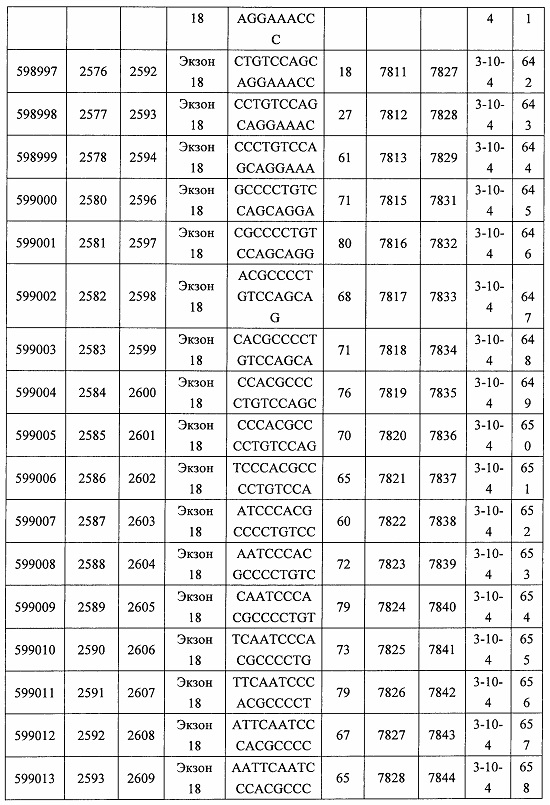
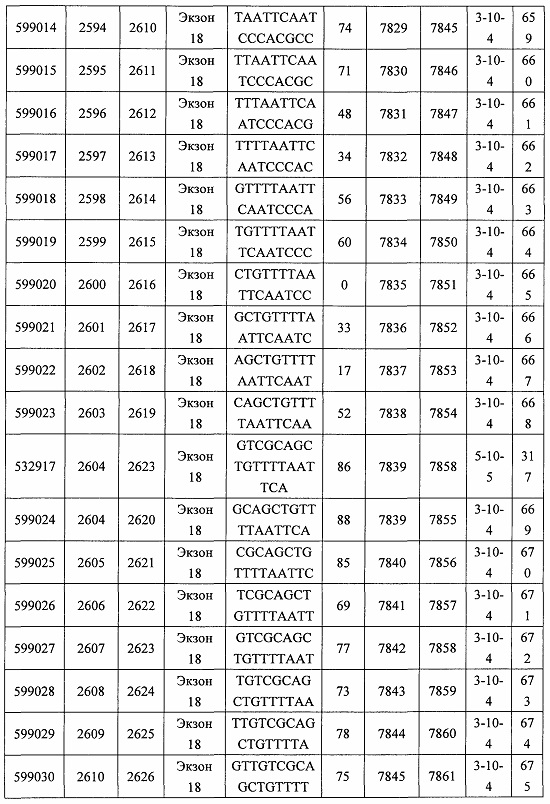
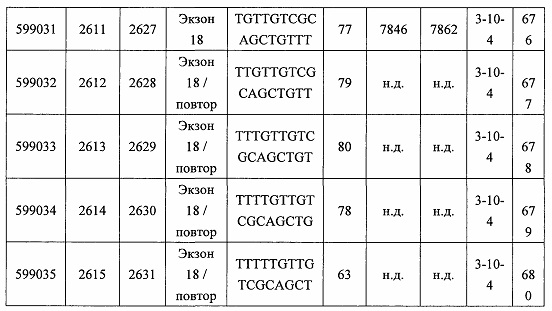
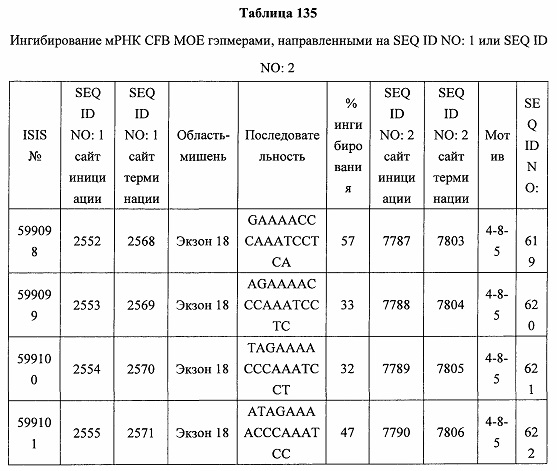
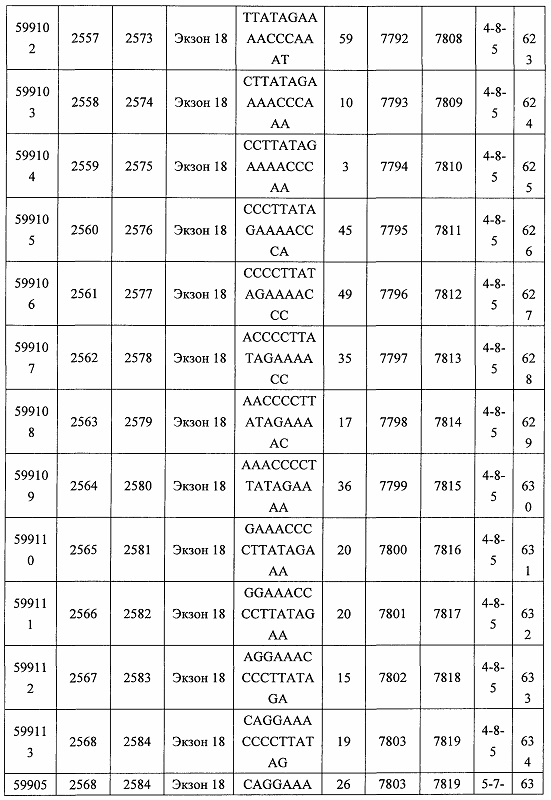
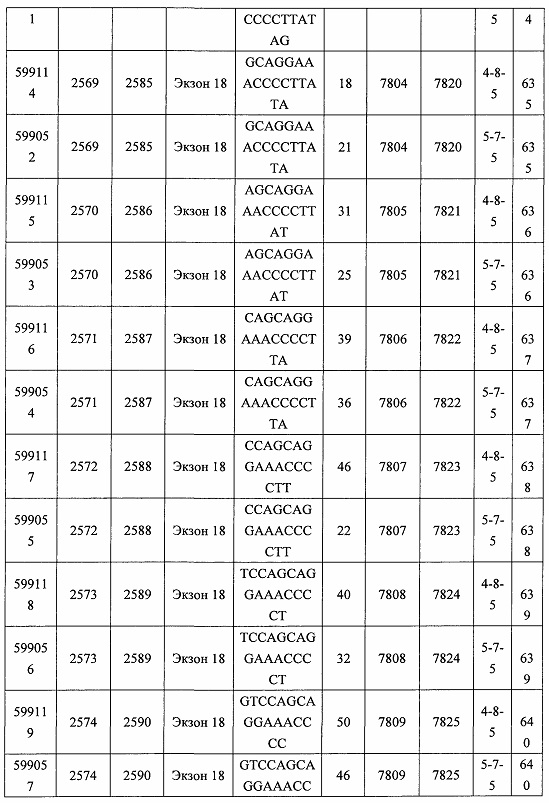
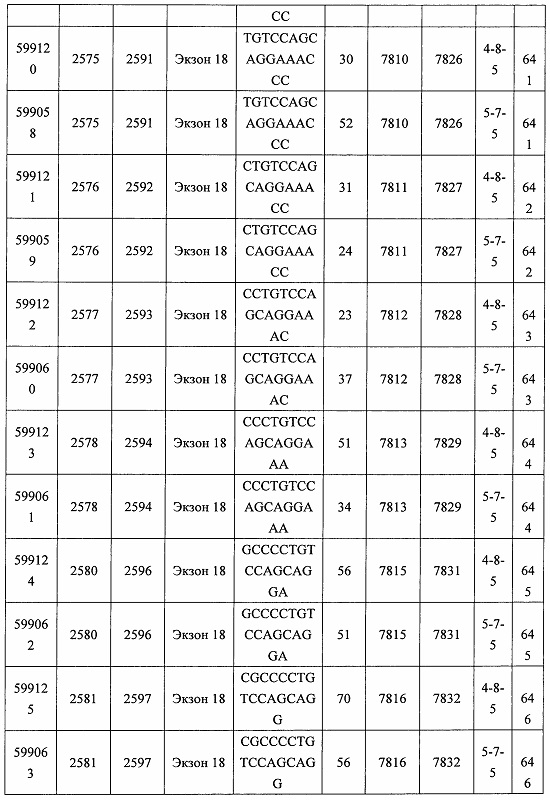
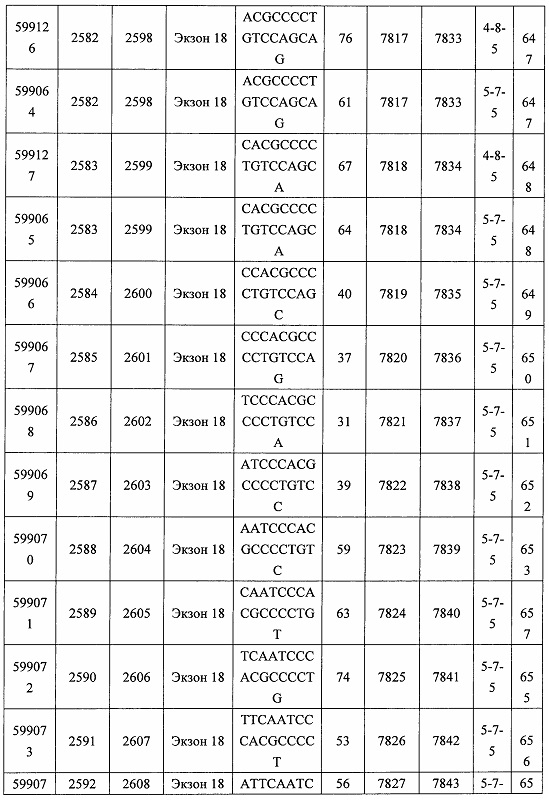
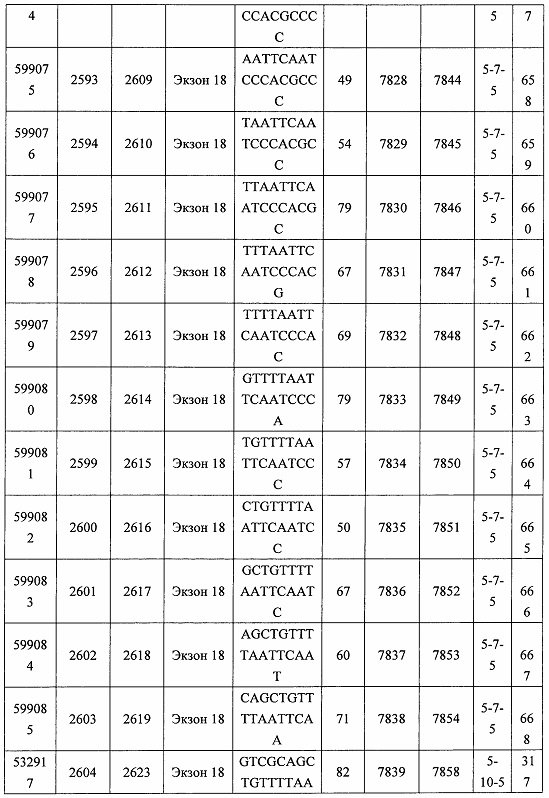
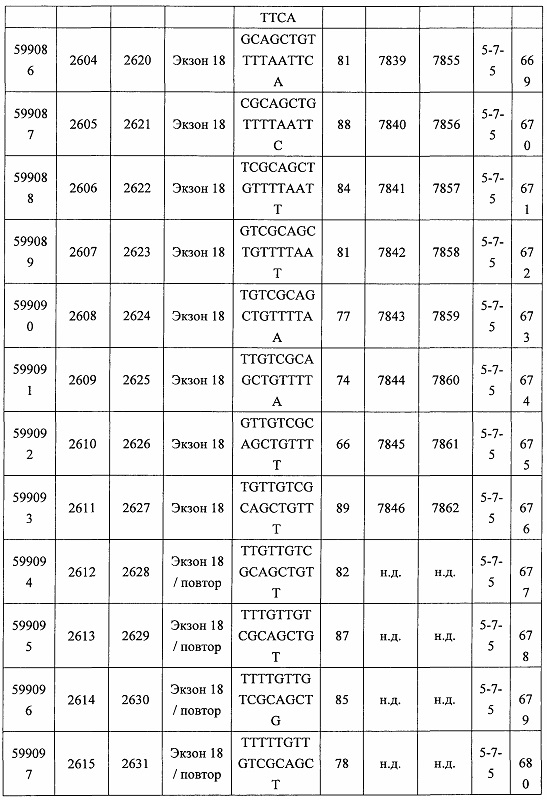
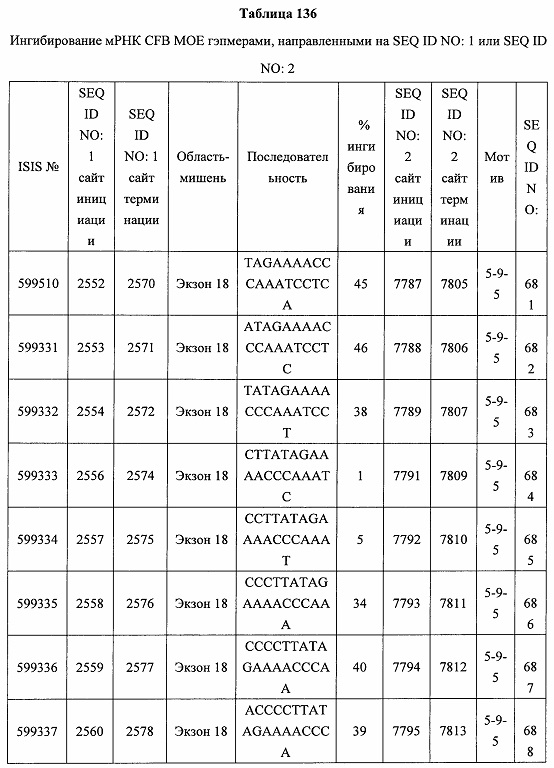
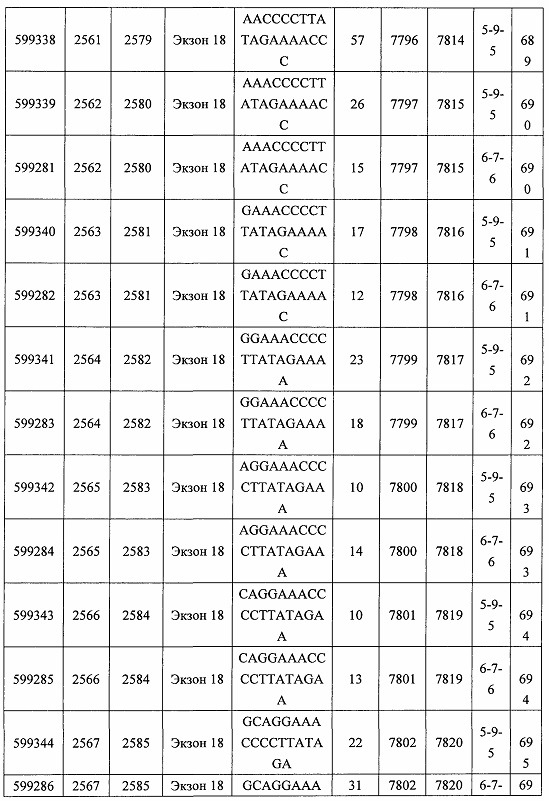
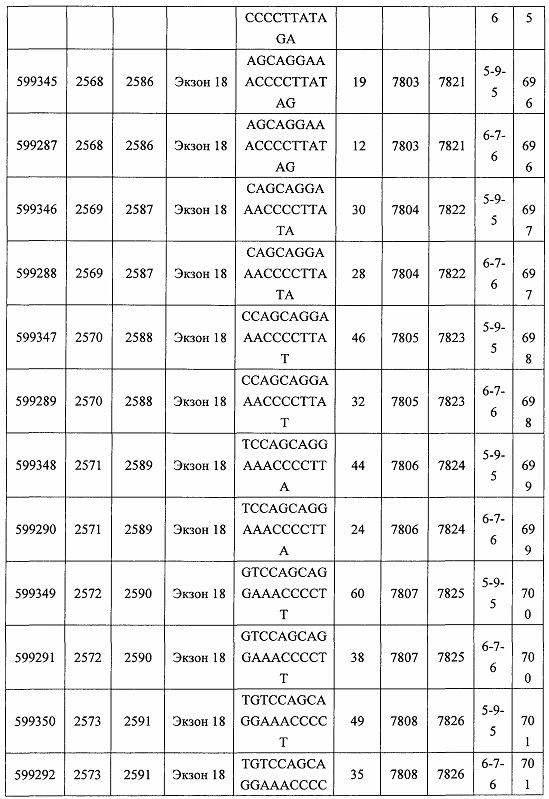
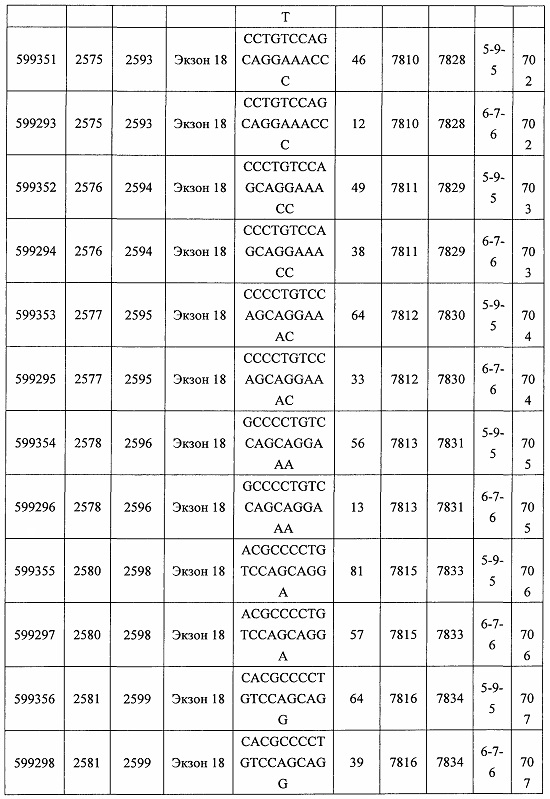
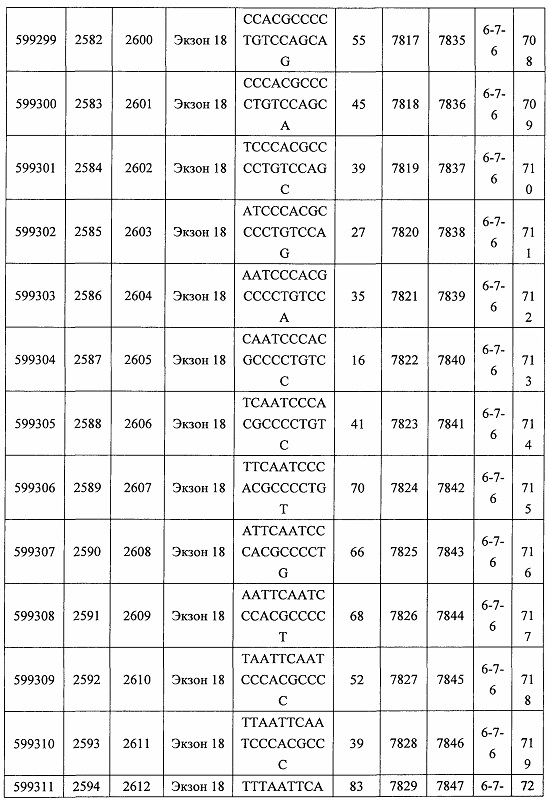
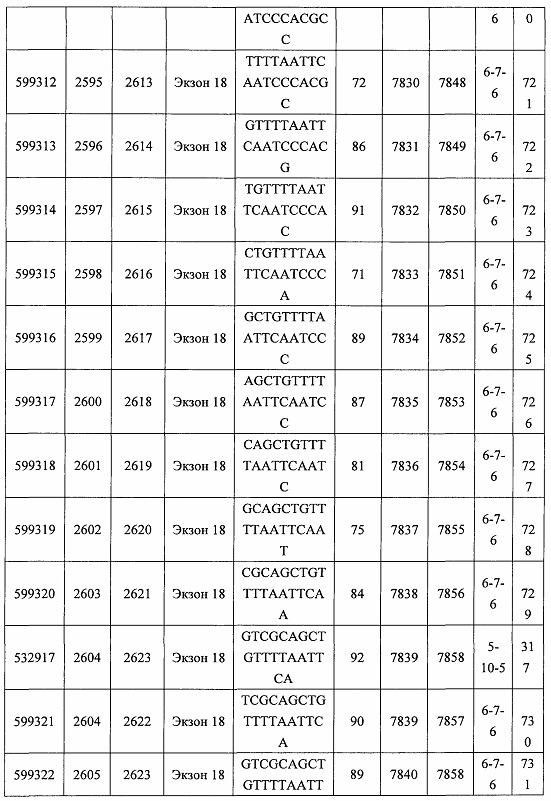
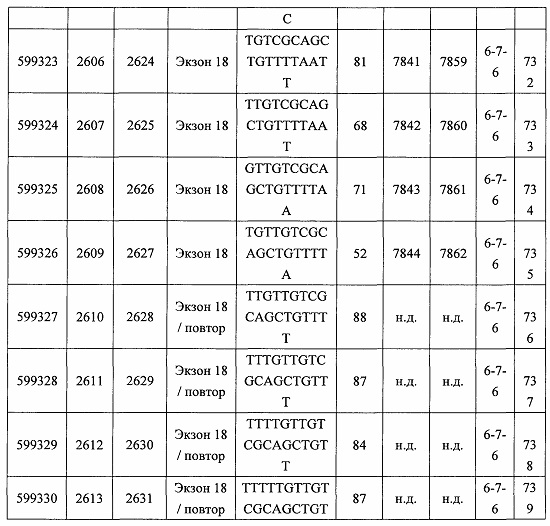

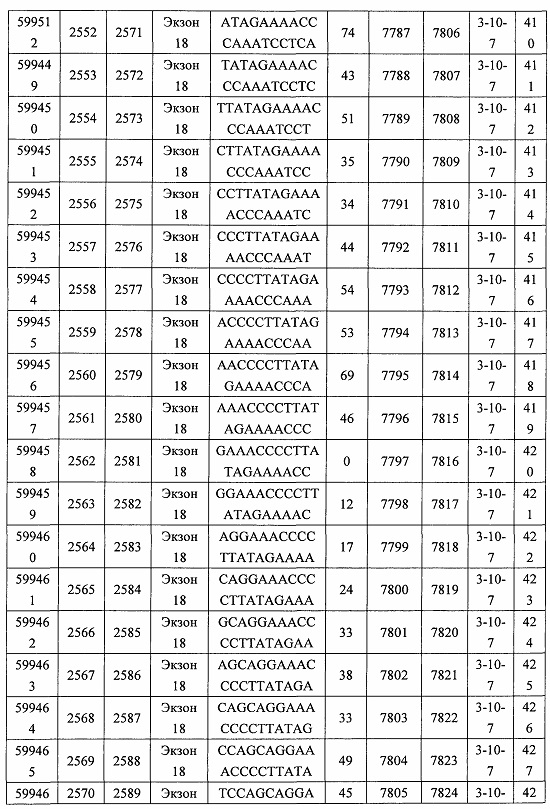
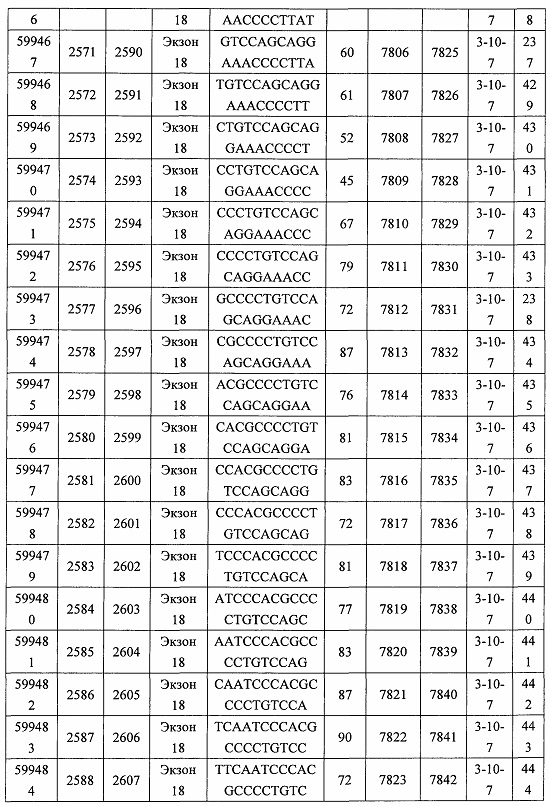
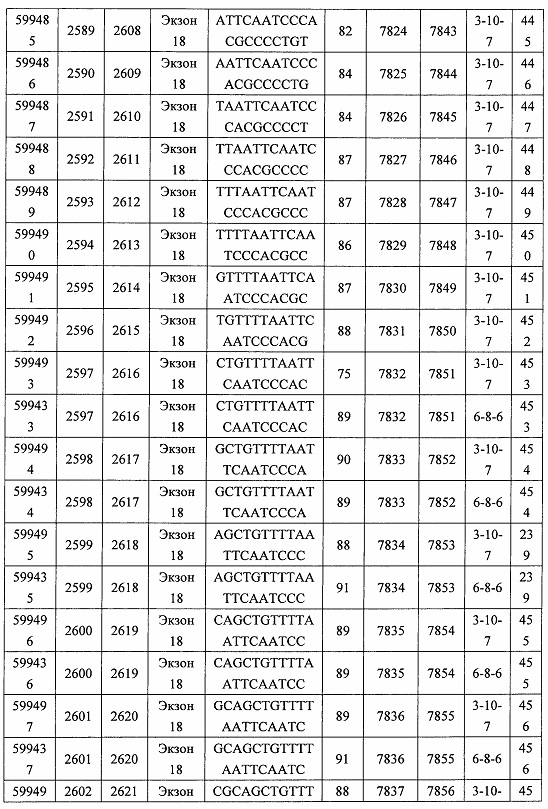
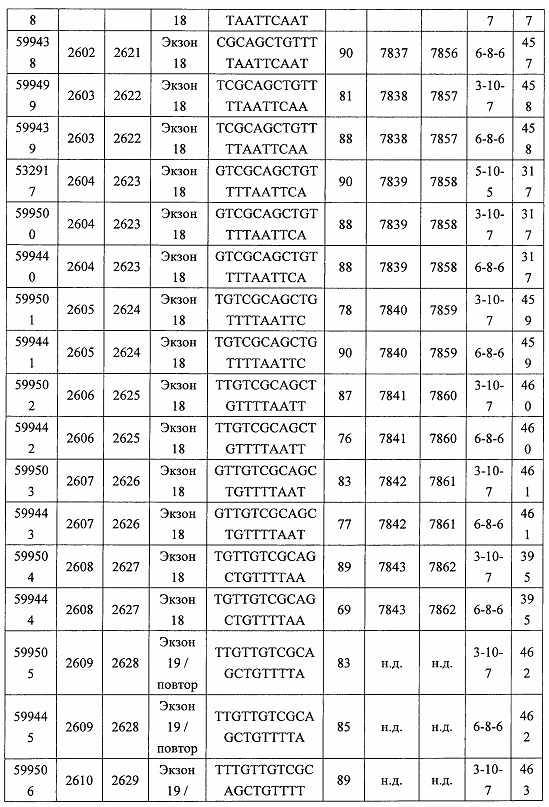
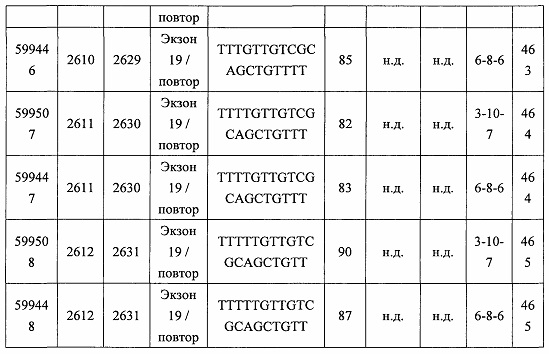
Пример 119: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы дополнительные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов, которые имели аналогичные условия культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку были трансфицированны с использованием электропорации с 2000 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды в представленных ниже таблицах были сконструированы как 4-8-5 МОЕ, 5-8-5 МОЕ, 5-9-5 МОЕ, 5-10-5 МОЕ, 6-7-6- МОЕ, 3-10-5 МОЕ или 6-8-6 МОЕ гэпмеры.
Гэпмеры 4-8-5 МОЕ имеют 17 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими четыре и пять нуклеозидов соответственно. Гэпмеры 5-8-5 МОЕ имеют 18 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-9-5 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из девяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-10-5 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 3-10-5 МОЕ имеют 18 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими три и пять нуклеозидов соответственно. Гэпмеры 6-7-6 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из семи 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Гэпмеры 6-8-6 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины.
«Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.
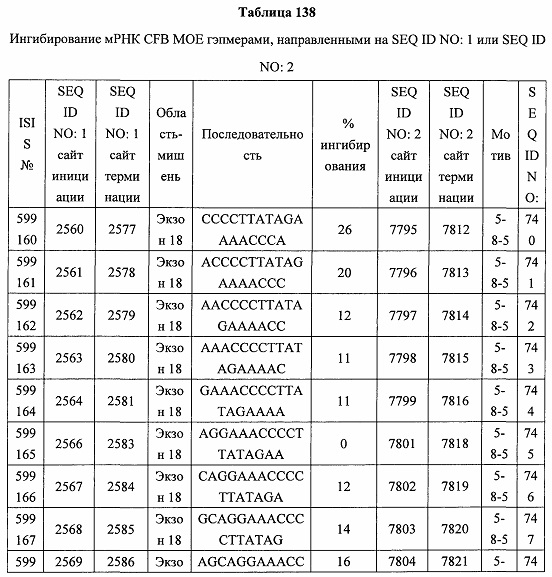
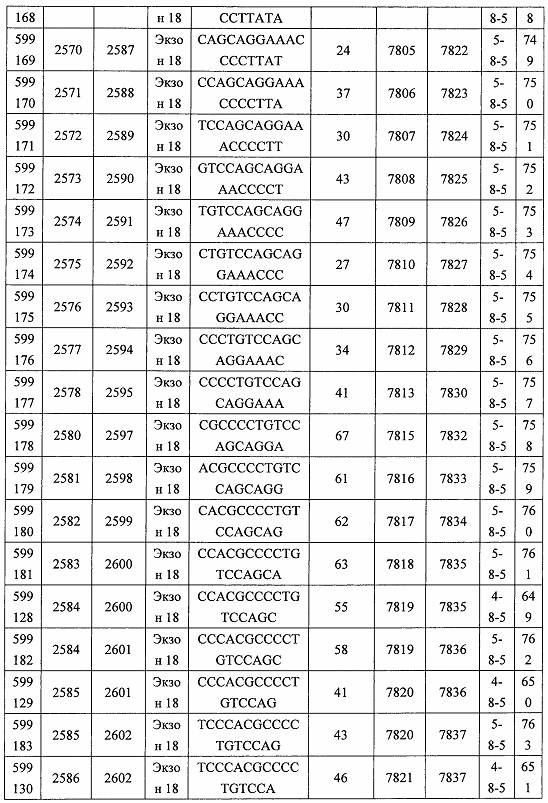
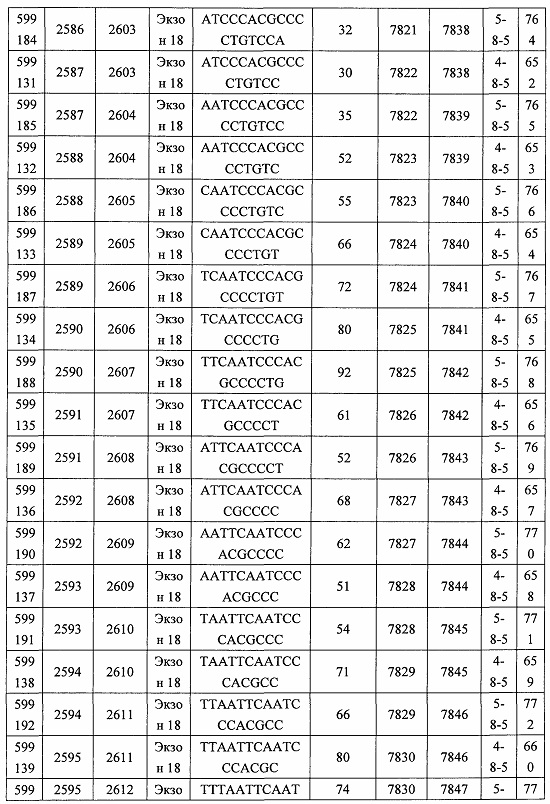
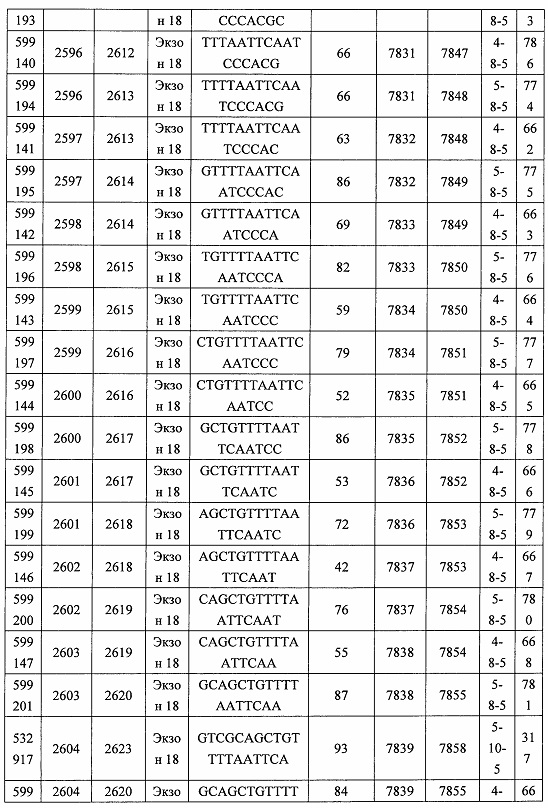
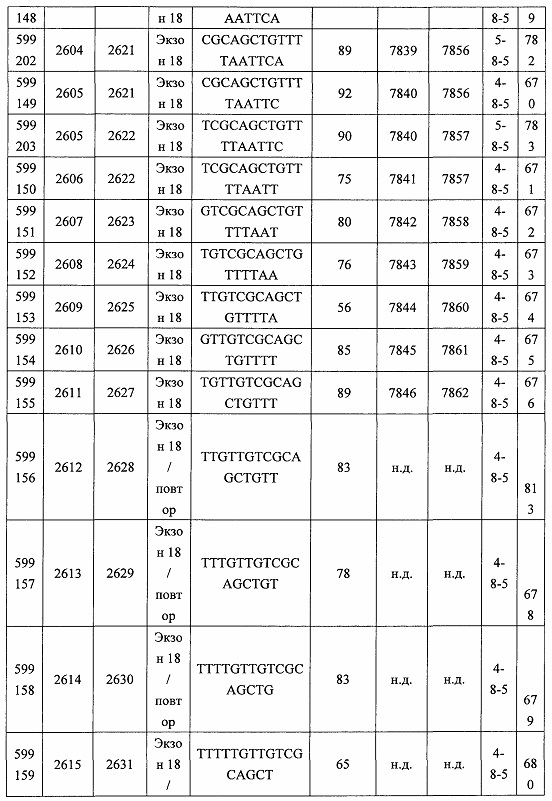

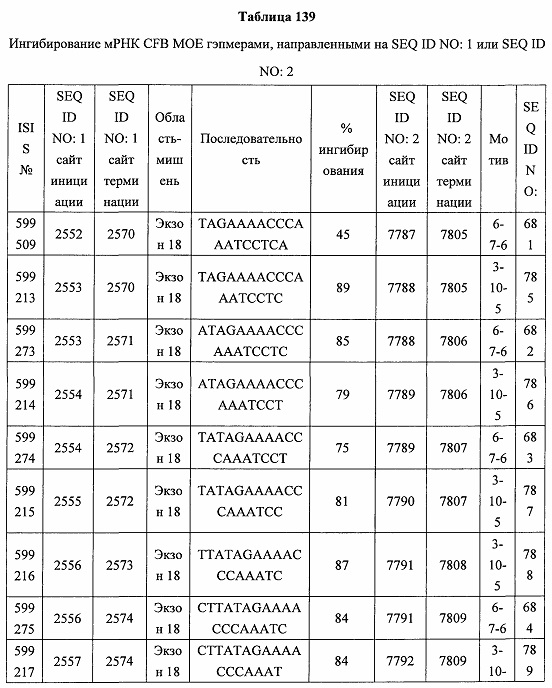
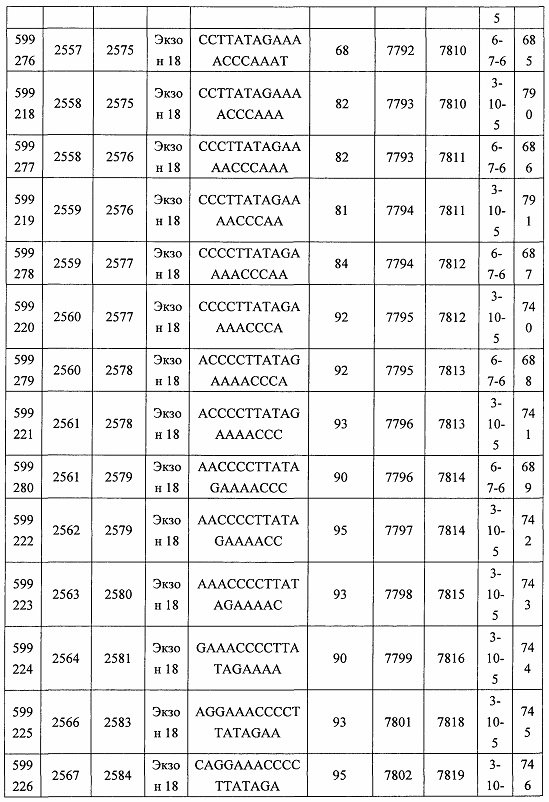
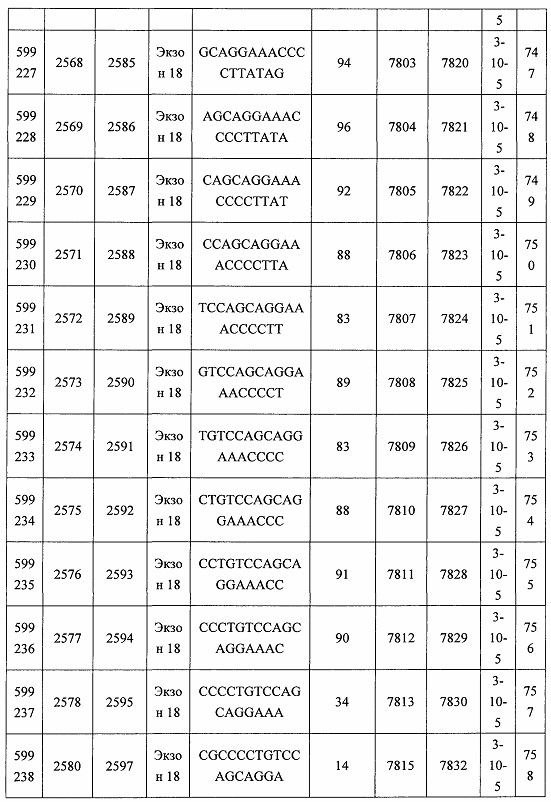
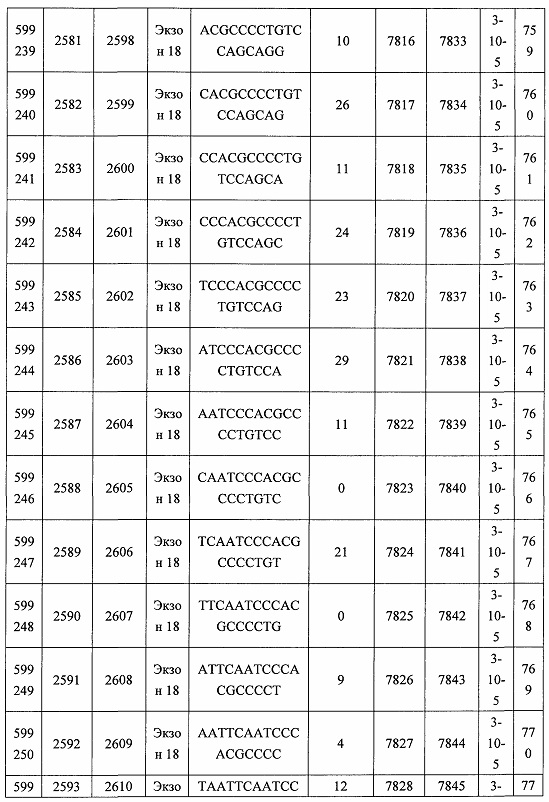
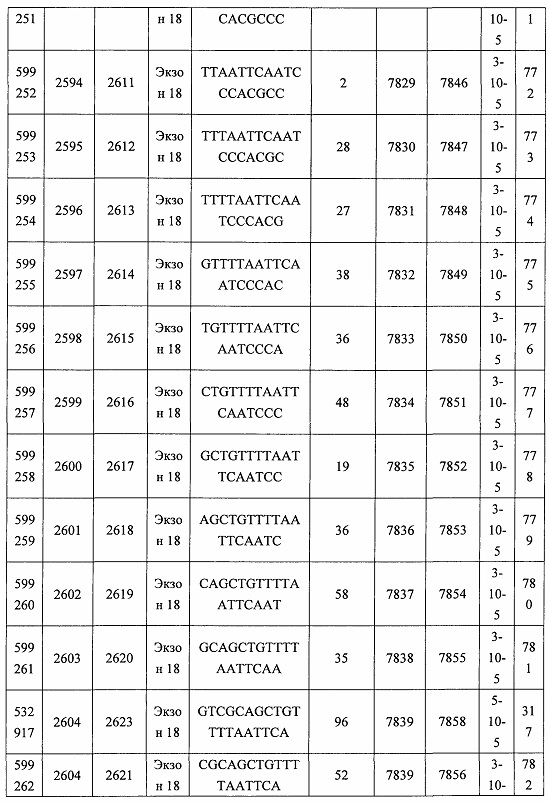
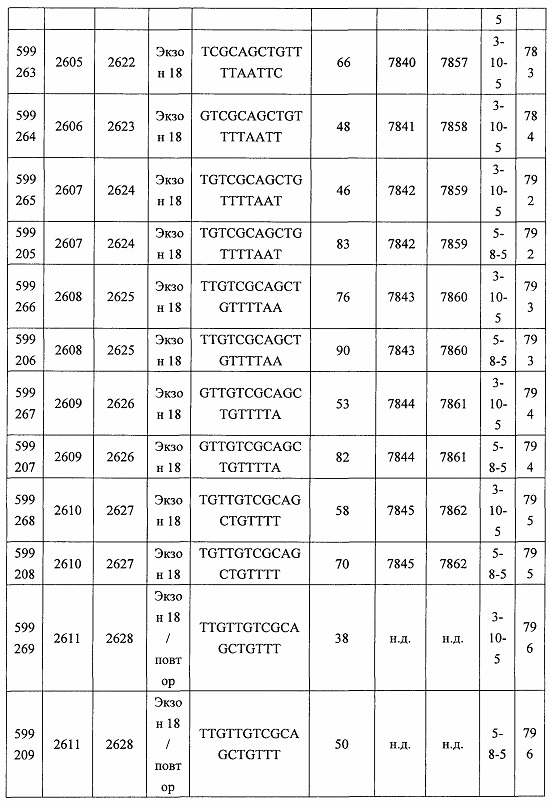
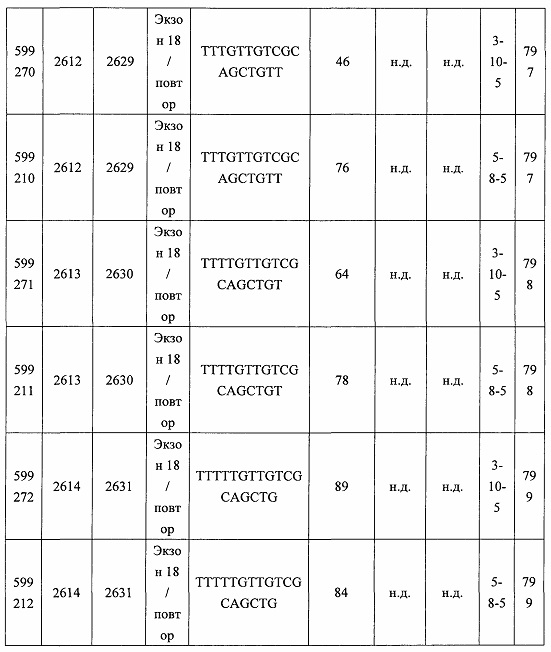

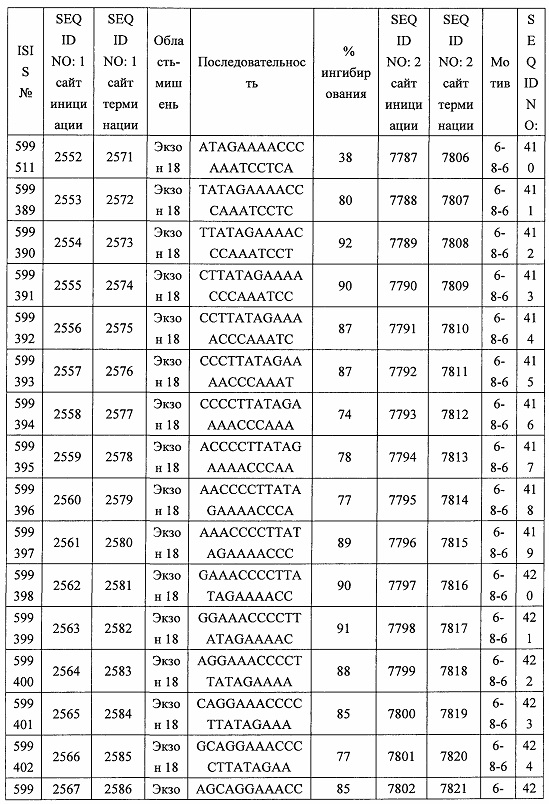
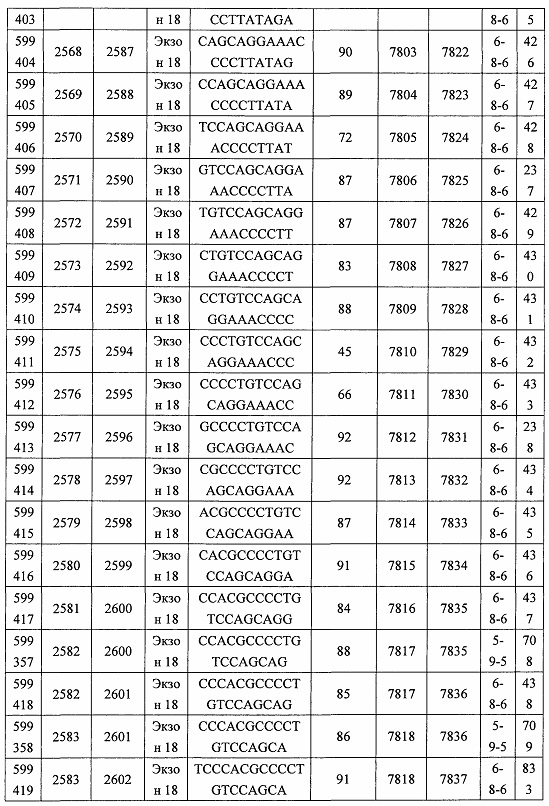
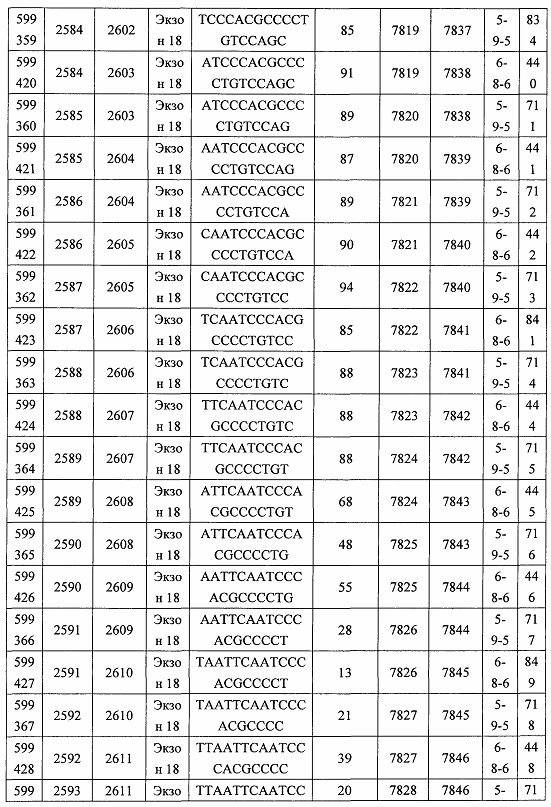
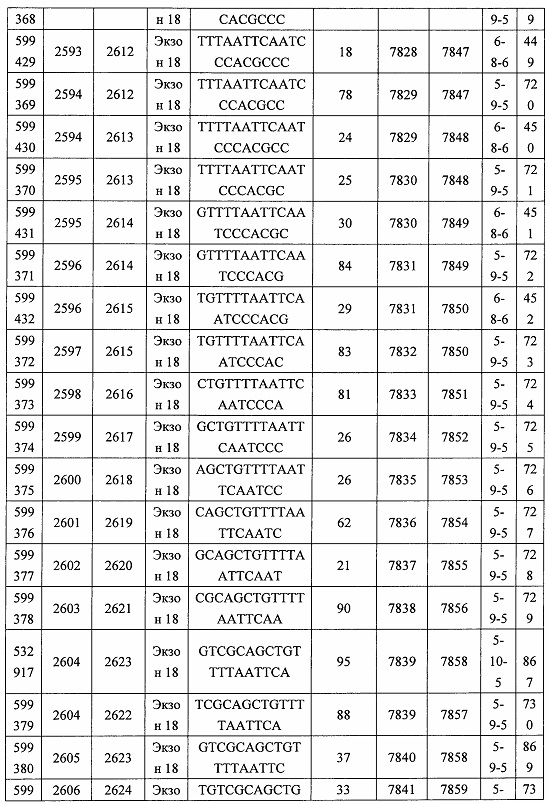
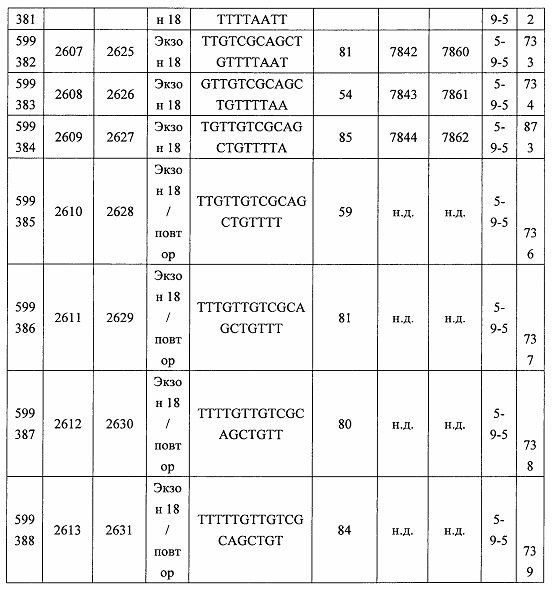
Пример 120: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы дополнительные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку были трансфицированны с использованием электропорации с 1000 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды в представленных ниже таблицах были сконструированы как дезокси, МОЕ и (S)-cEt олигонуклеотиды. Дезокси, МОЕ и (S)-cEt олигонуклеотиды имеют 16 нуклеозидов в длину, причем нуклеозид содержит либо модификацию сахара МОЕ, либо модификацию сахара (S)-cEt, либо дезокси модификацию. В колонке «Химизм» описаны модификации сахара для каждого олигонуклеотида. «k» означает (S)-cEt модификацию сахара; «d» означает дезоксирибозу; и «е» означает модификацию МОЕ.
«Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.

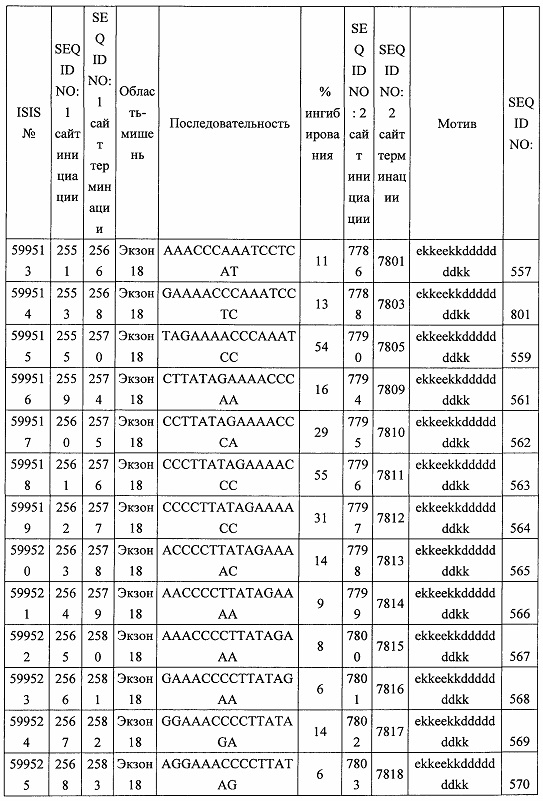
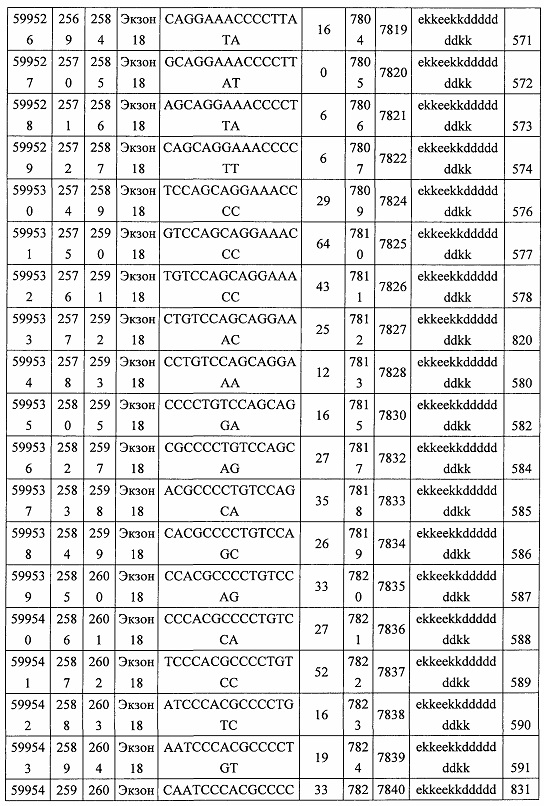
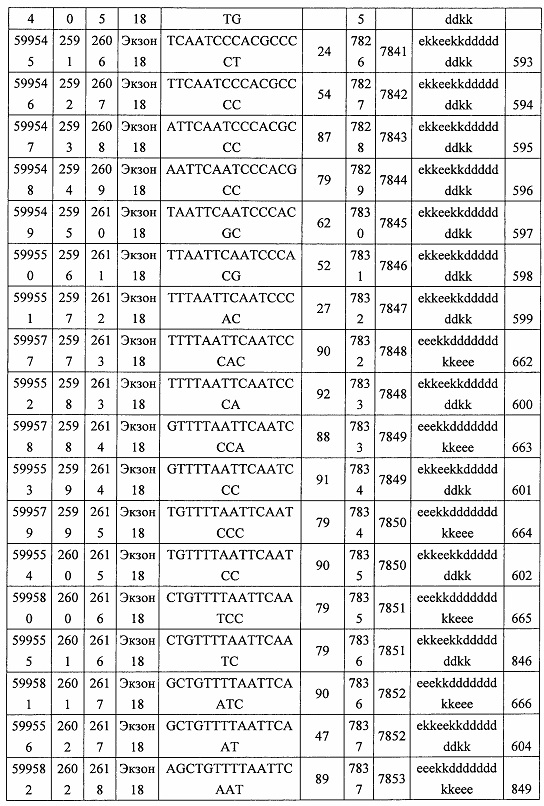
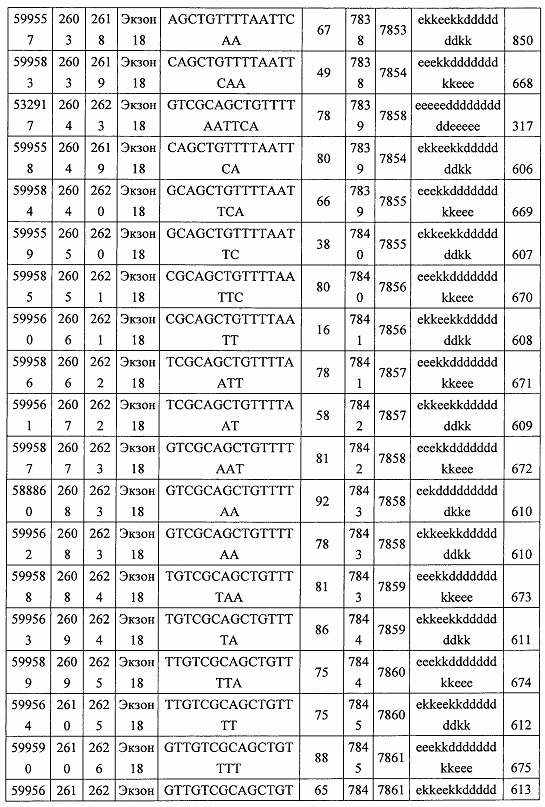
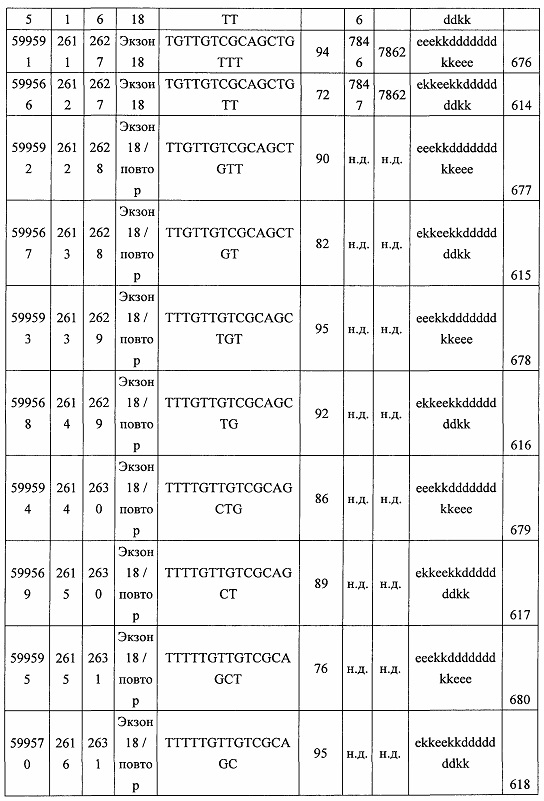
Пример 121: Антисмысловое ингибирование человеческого фактора комплемента В (CFB) в HepG2 клетках МОЕ гэпмерами
Были сконструированы дополнительные антисмысловые олигонуклеотиды, направленные на нуклеиновую кислоту человеческого фактора комплемента В (CFB), и были протестированы на их воздействие in vitro на мРНК CFB. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов, которые имели аналогичные условия культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Культивированные клетки HepG2 с плотностью 20000 клеток на лунку трансфицировали с использованием электропорации с 500 нМ антисмыслового олигонуклеотида. После периода обработки в течение около 24 часов, РНК выделяли из клеток и уровни мРНК CFB измеряли методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Впервые сконструированные химерные антисмысловые олигонуклеотиды в представленных ниже таблицах были сконструированы как дезокси, МОЕ и (S)-cEt олигонуклеотиды или как 5-8-5 МОЕ, 5-9-5 МОЕ, 5-10-5 МОЕ, 6-7-6- МОЕ, 3-10-5 МОЕ или 6-8-6 МОЕ гэпмеры.
Дезокси, МОЕ и (S)-cEt олигонуклеотиды имеют 16 нуклеозидов в длину, причем нуклеозид содержит либо модификацию сахара МОЕ, либо модификацию сахара (S)-cEt, либо дезокси модификацию. В колонке «Химизм» описаны модификации сахара для каждого олигонуклеотида. «k» означает (S)-cEt модификацию сахара; «d» означает дезоксирибозу; и «е» означает модификацию МОЕ.
Гэпмеры 5-8-5 МОЕ имеют 18 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-9-5 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из девяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 5-10-5 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по пять нуклеозидов каждое. Гэпмеры 3-10-5 МОЕ имеют 18 нуклеозидов в длину, причем центральный гэп состоит из десяти 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими три и пять нуклеозидов соответственно. Гэпмеры 6-7-6 МОЕ имеют 19 нуклеозидов в длину, причем центральный гэп состоит из семи 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Гэпмеры 6-8-6 МОЕ имеют 20 нуклеозидов в длину, причем центральный гэп состоит из восьми 2'-дезоксинуклеозидов и окружен крыльями с 5' конца и в 3' конца, содержащими по шесть нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины.
«Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена человека. «Сайт терминации» обозначает самый крайний 3' нуклеозид, на который направлен гэпмер в последовательности гена человека. Каждый гэпмер, перечисленный в представленных ниже таблицах, направлен на мРНК CFB человека, обозначенную в данном описании как SEQ ID NO: 1 (с номером доступа GENBANK NM_001710.5) или на геномную последовательность CFB человека, обозначенную в настоящем документе как SEQ ID NO: 2 (с номером доступа GENBANK NT_007592.15, усеченную с нуклеотида 31852000 по 31861000), или на обе последовательности, «н/д» означает, что антисмысловый олигонуклеотид не направлен на указанную конкретную последовательность гена с 100% комплементарностью.

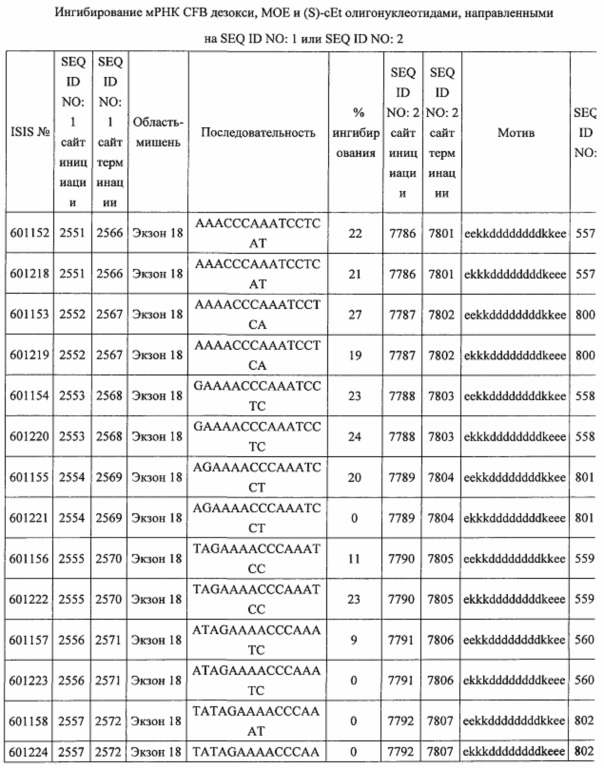
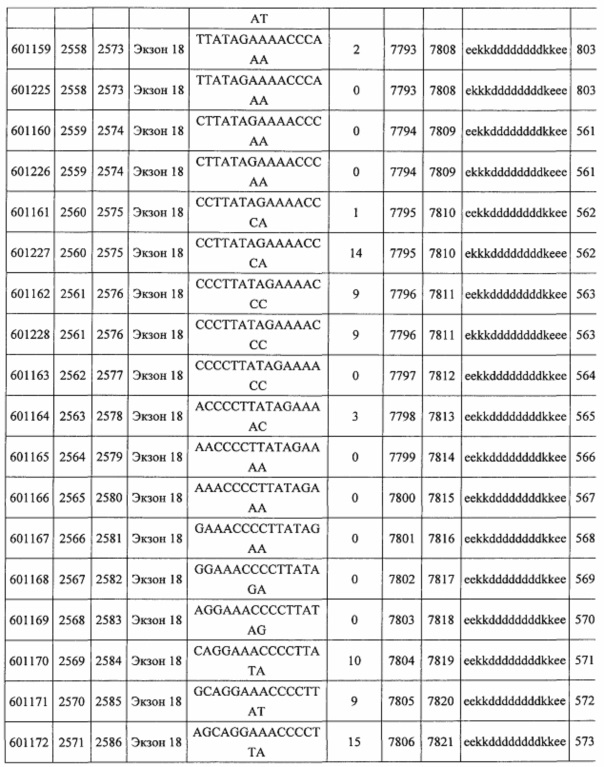
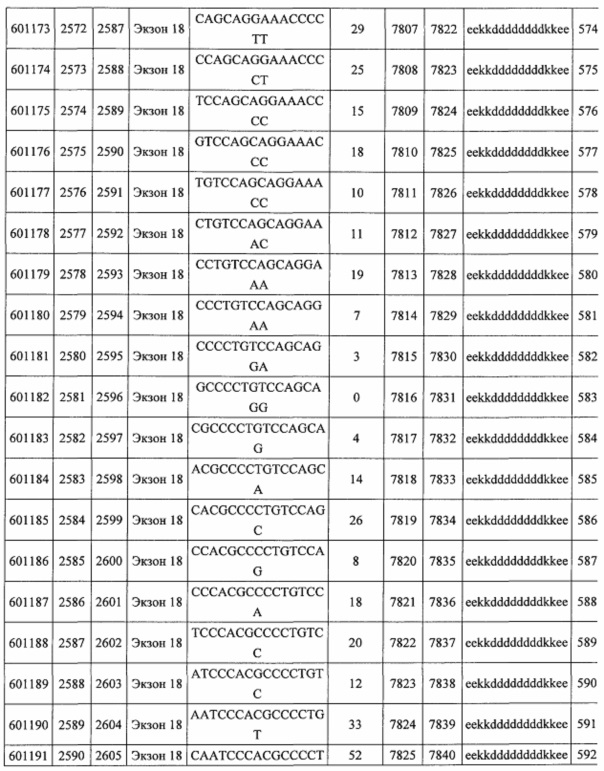
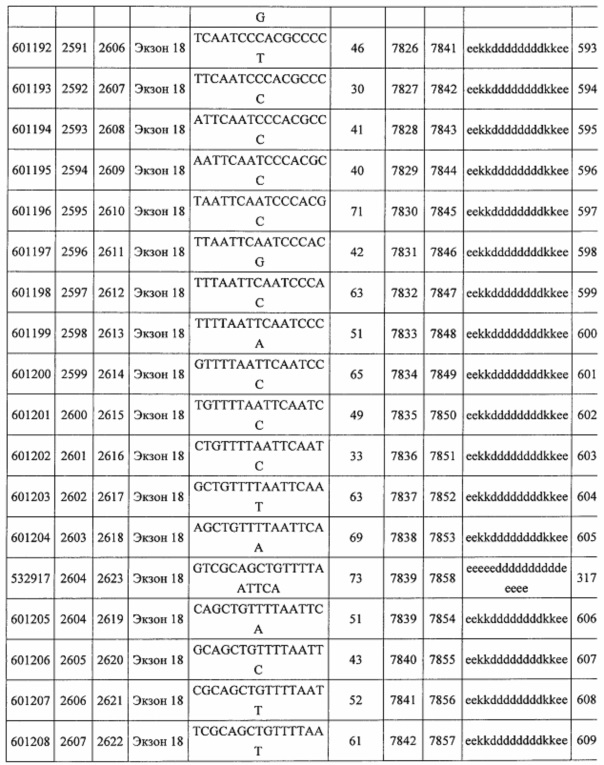
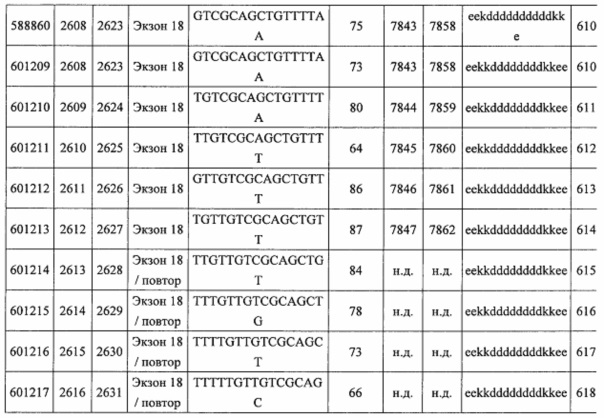
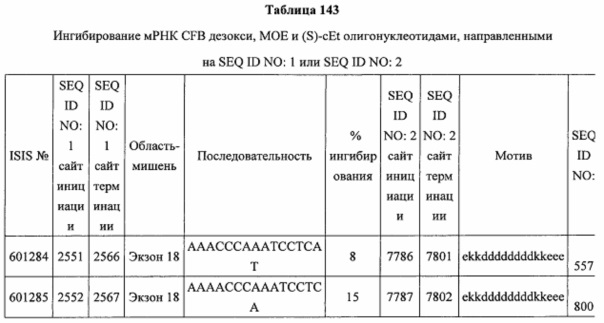
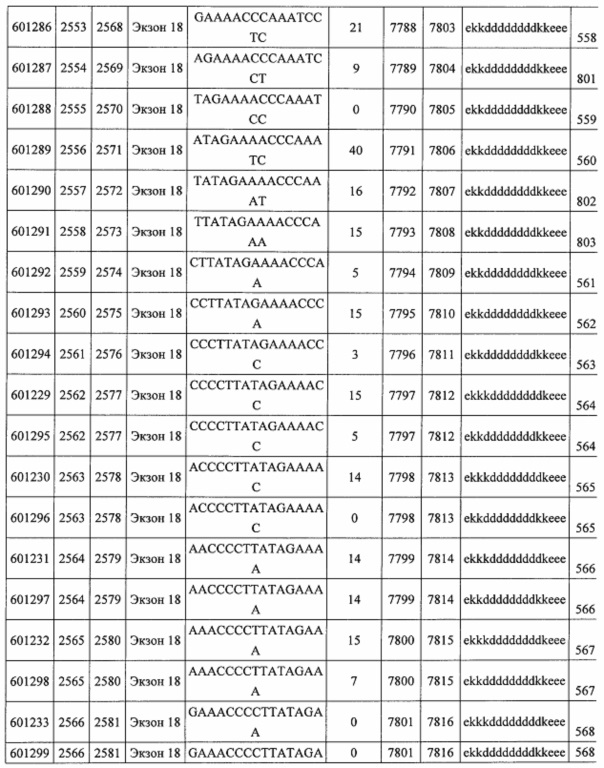
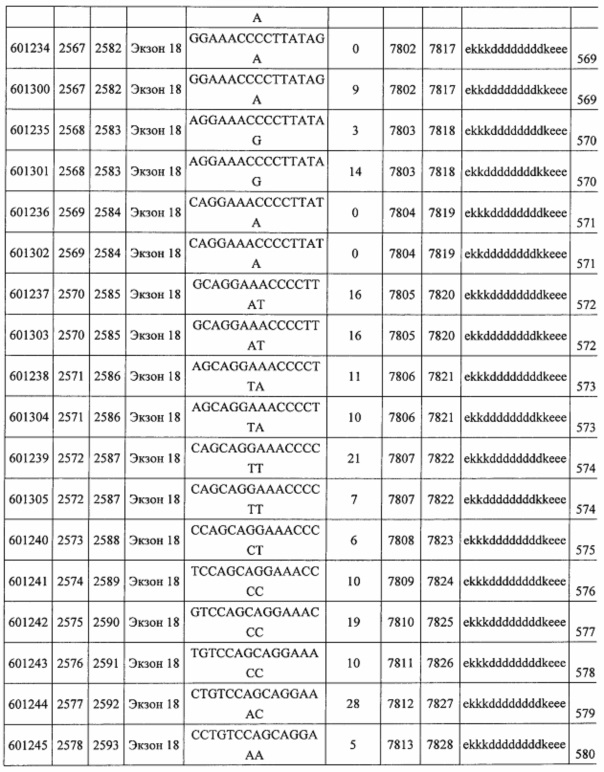
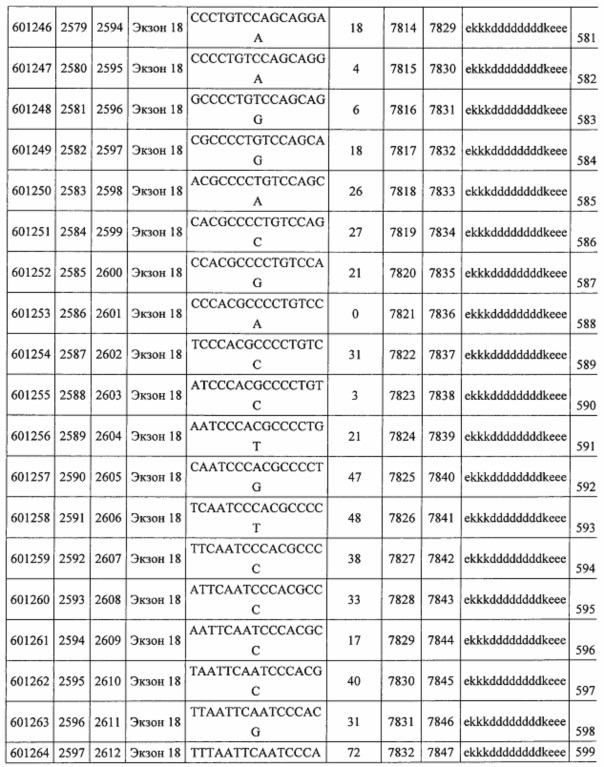
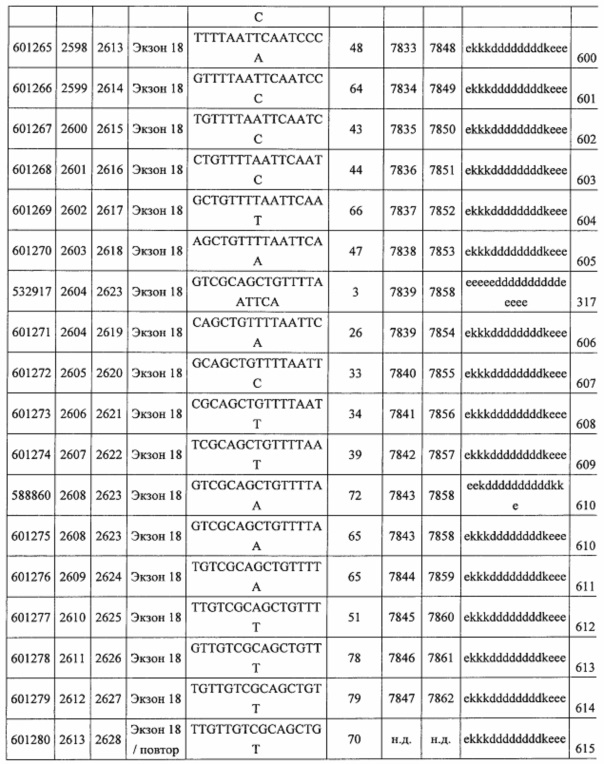

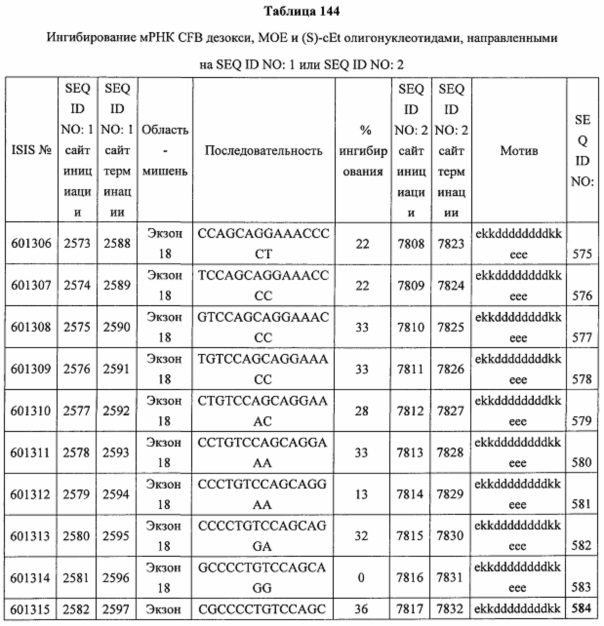
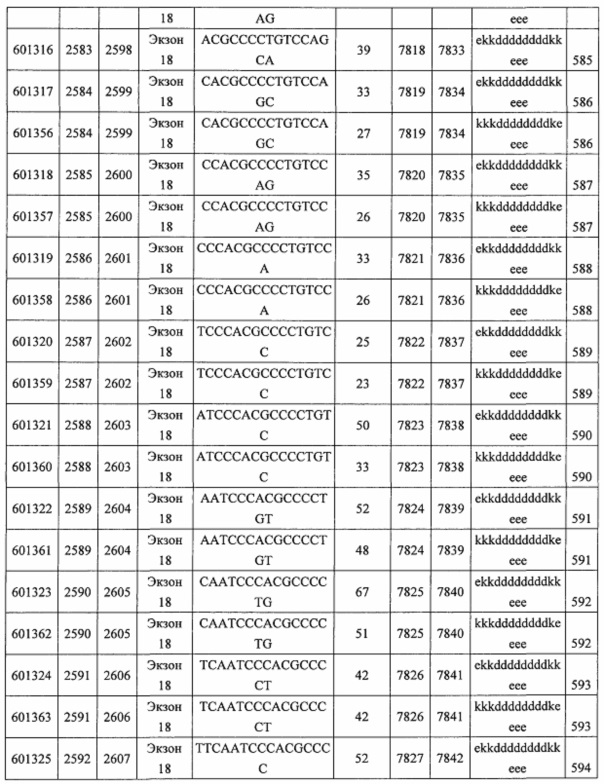
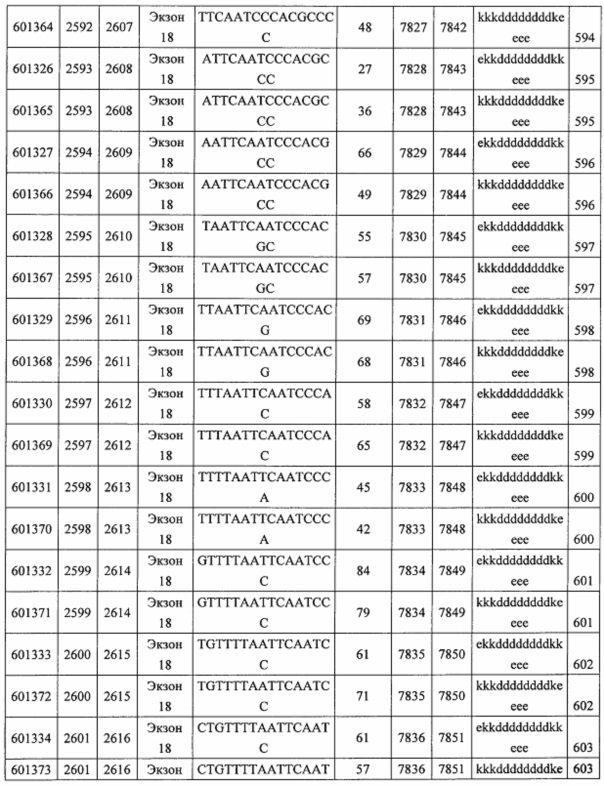
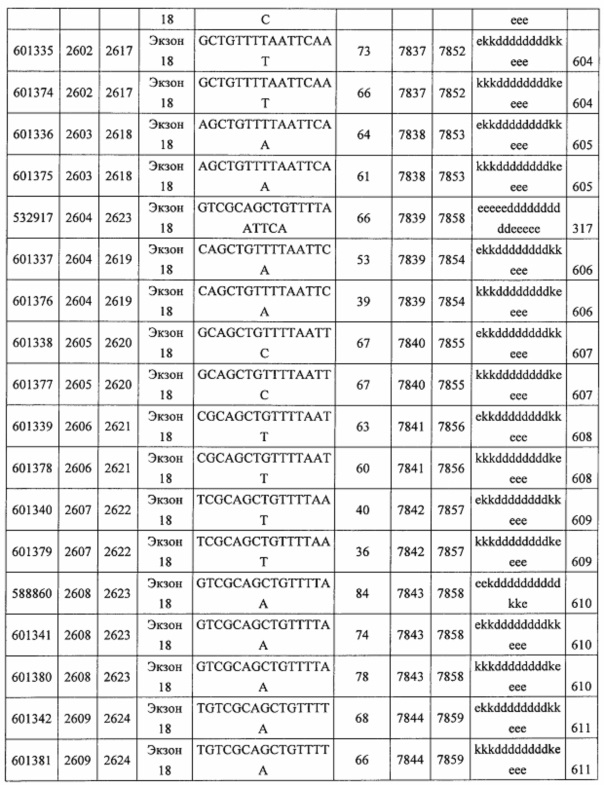
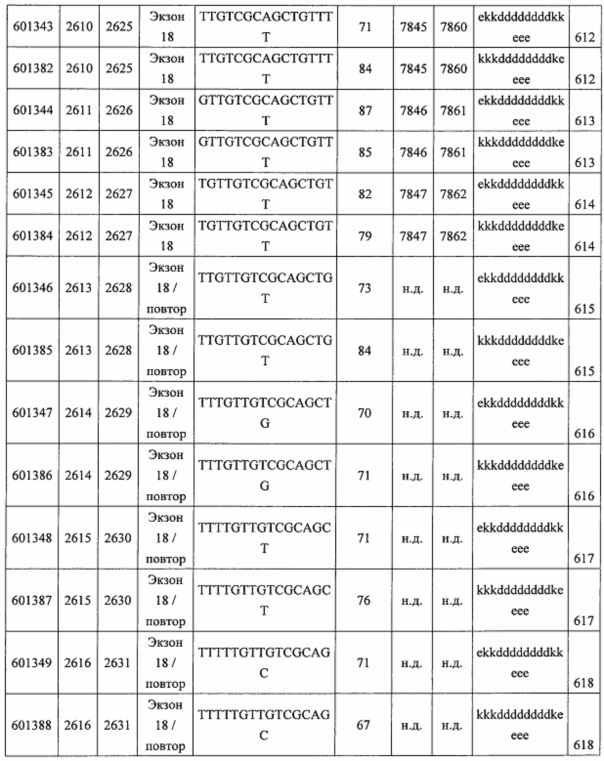
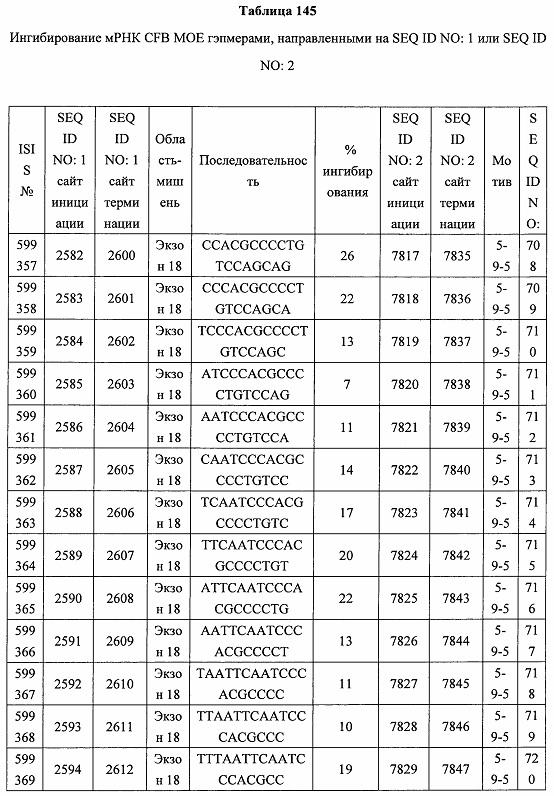
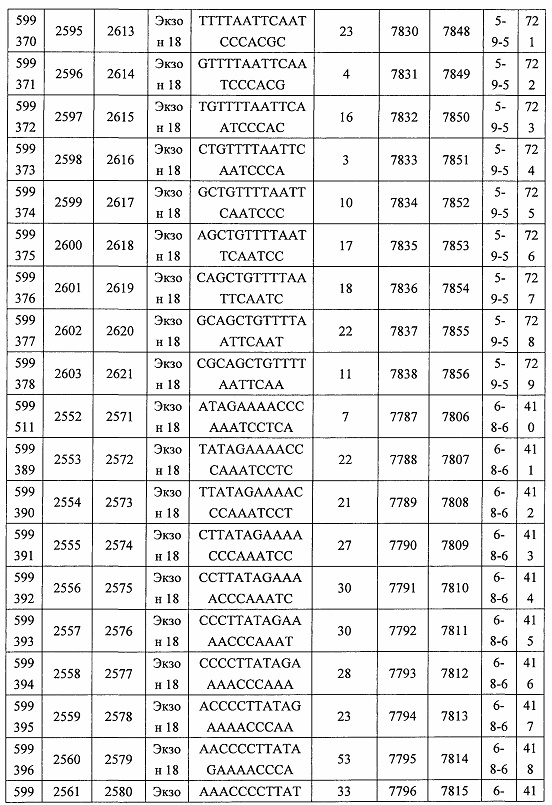
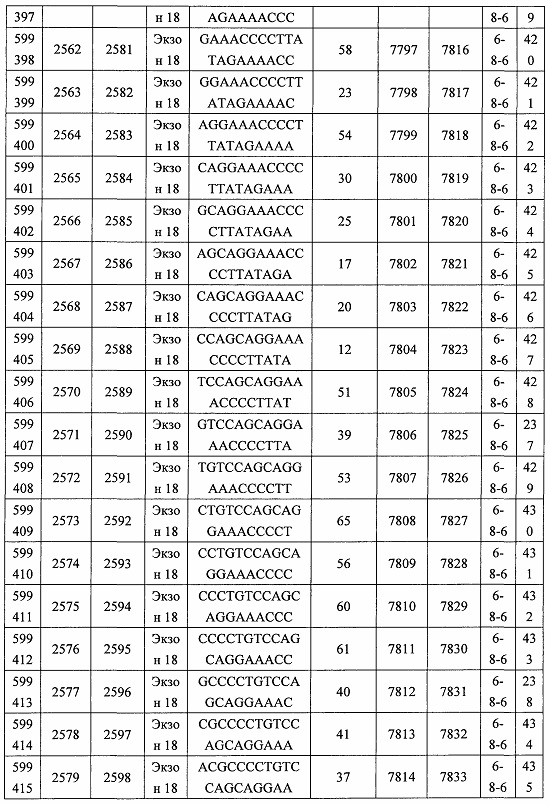
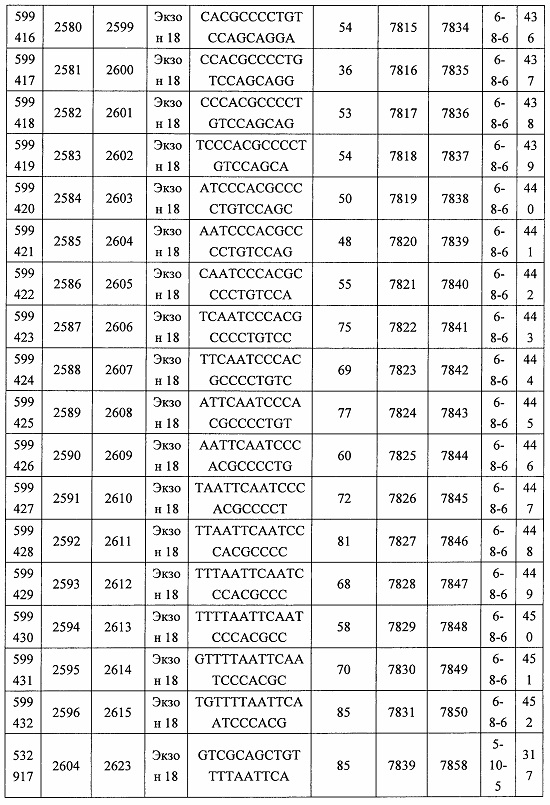
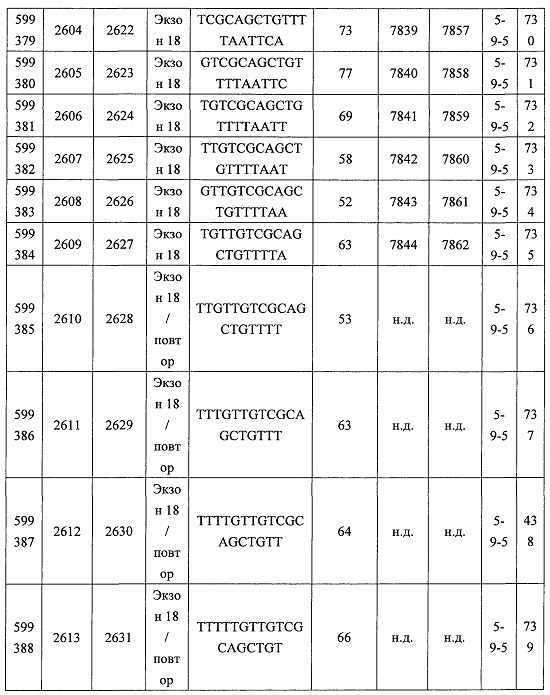

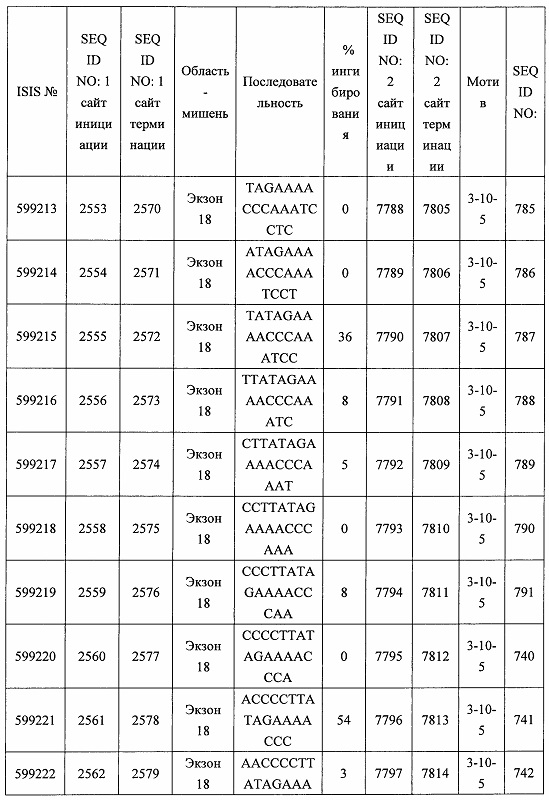
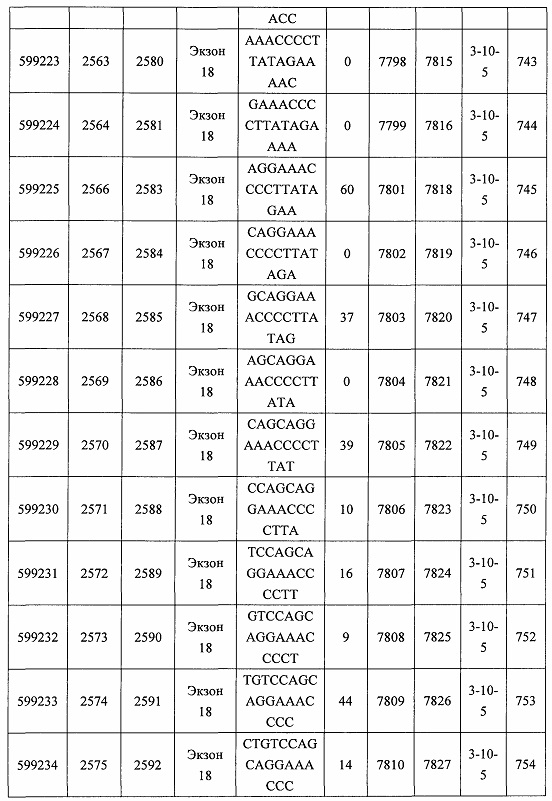
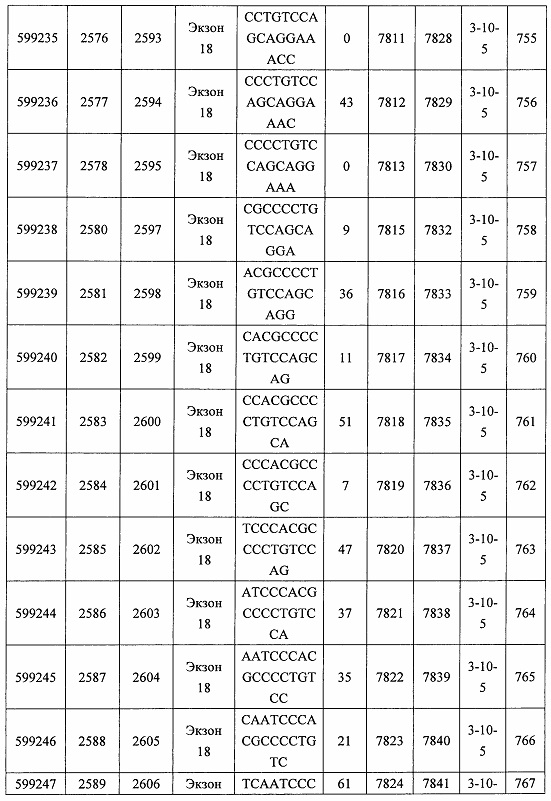
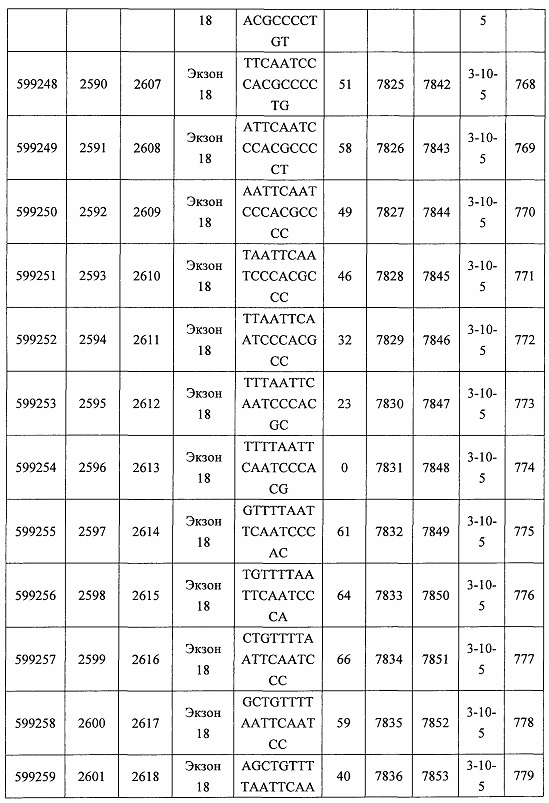
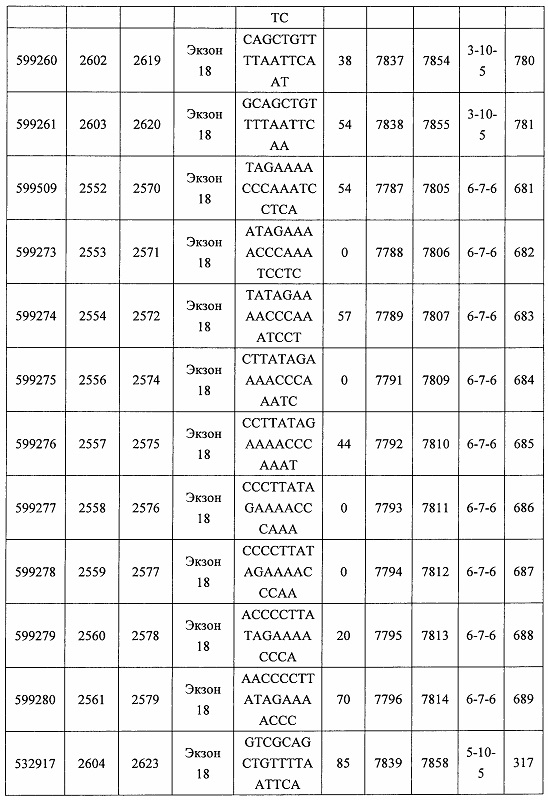
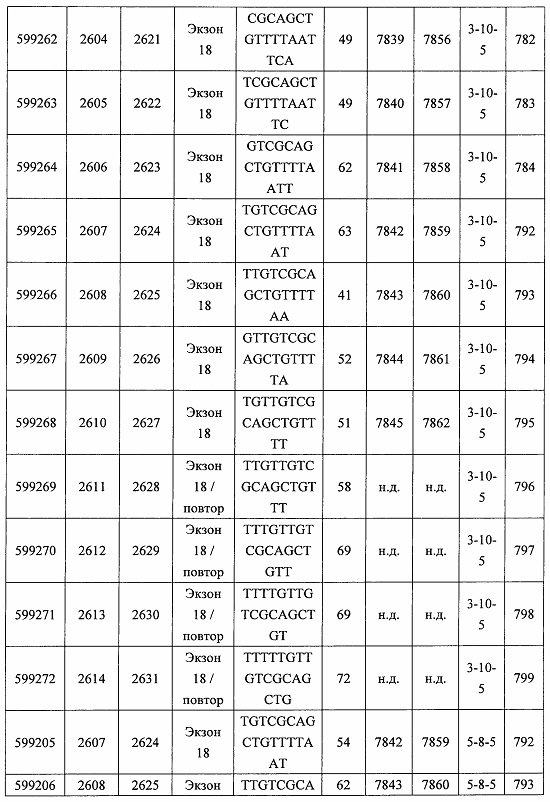
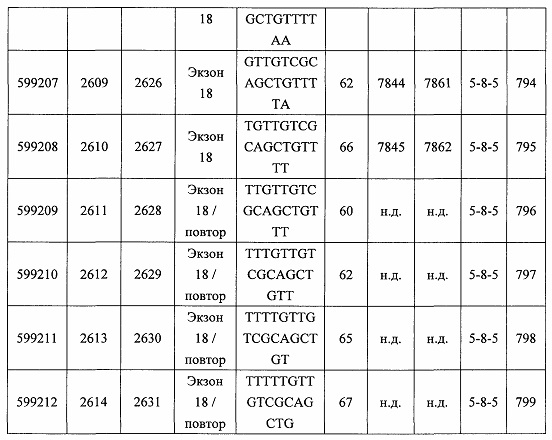
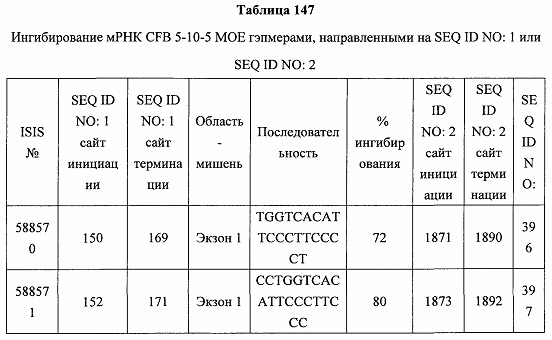
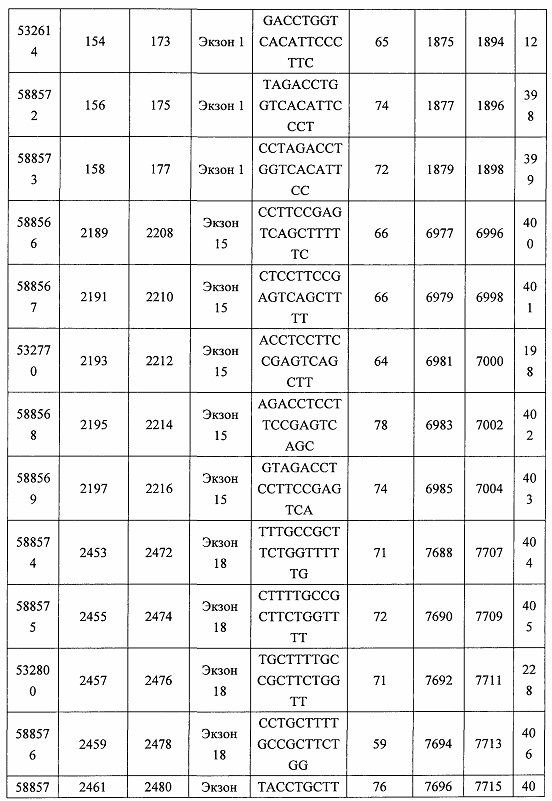
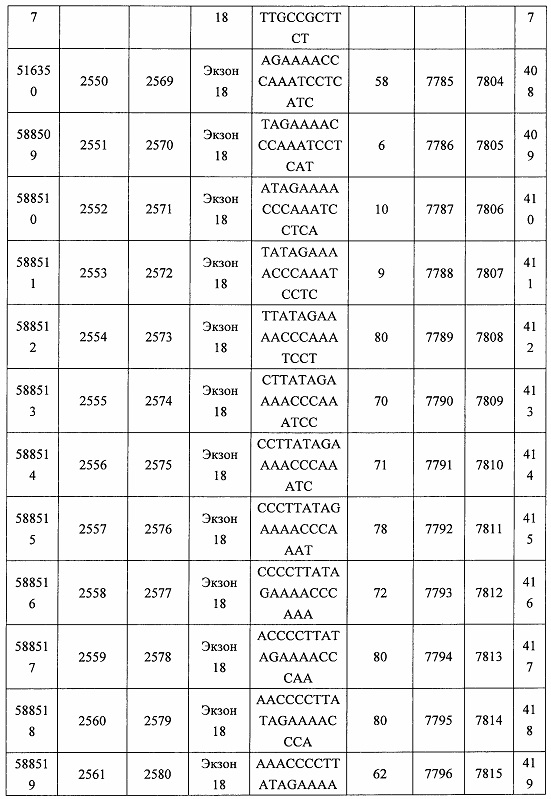
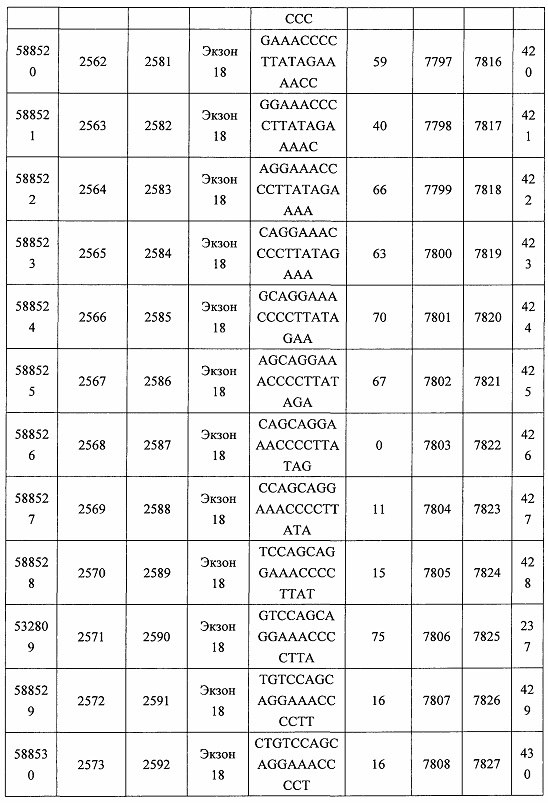
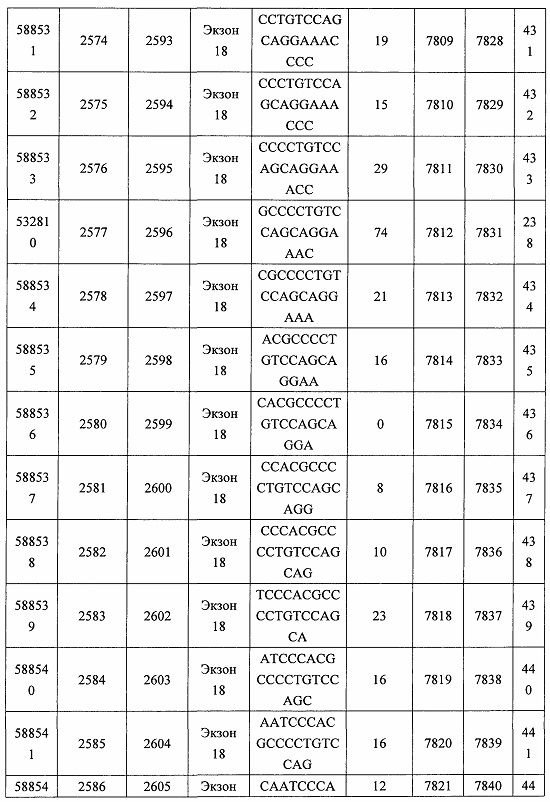
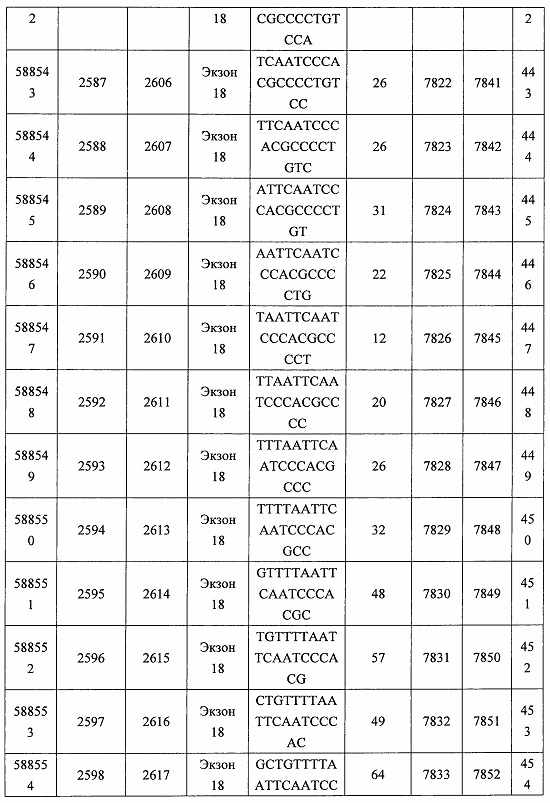
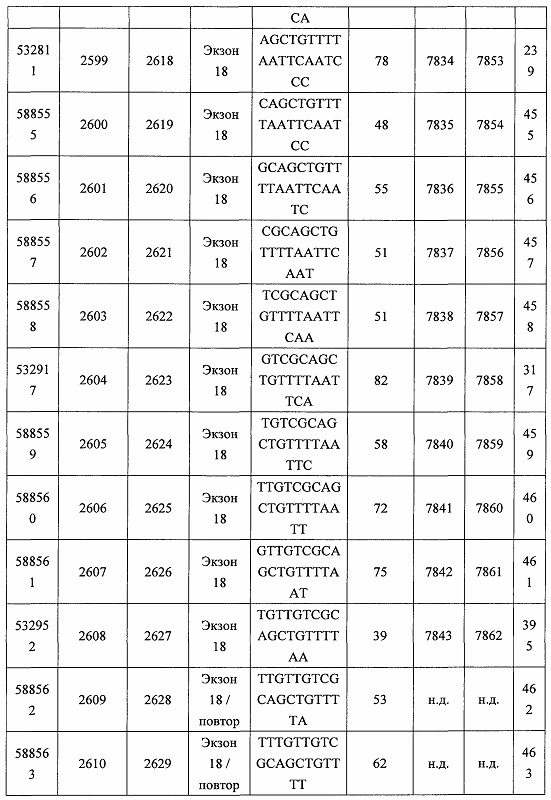

Пример 122: Дозозависимое антисмысловое ингибирование человеческого CFB в клетках HepG2 5-10-5 МОЕ гэпмерами
Гэпмеры из исследований, описанных выше, демонстрирующие значительное in vitro ингибирование мРНК CFB, были выбраны и испытаны в различных дозах в клетках HepG2. Клетки были высеяны с плотностью 20000 клеток на лунку и трансфицированны с использованием электропорации с концентрациями антисмыслового олигонуклеотида, равными 0,313 мкМ, 0,625 мкМ, 1,25 мкМ, 2,50 мкМ, 5,00 мкМ или 10,00 мкМ, как указано в представленной ниже таблице. После периода обработки в течение около 16 часов, РНК выделяли из клеток и измеряли уровни мРНК CFB методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Указана также полумаксимальная ингибирующая концентрация (IC50) каждого олигонуклеотида. Обработка антисмысловыми олигонуклеотидами снижает уровни мРНК CFB в клетках дозозависимым образом.
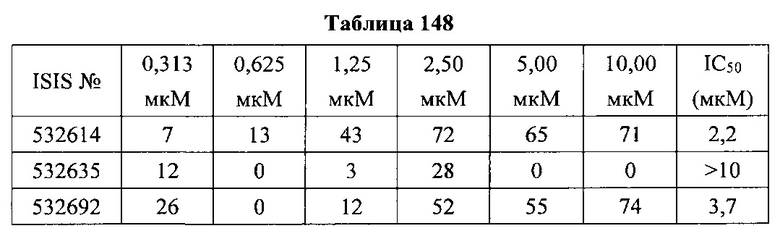
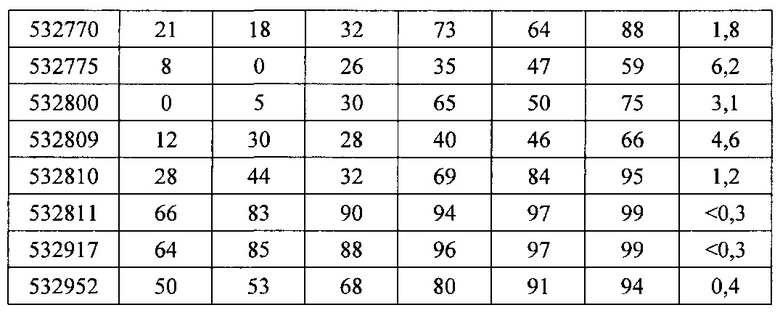
Пример 123: Дозозависимое антисмысловое ингибирование человеческого CFB в клетках HepG2
Гэпмеры из исследований, описанных выше, демонстрирующие значительное in vitro ингибирование мРНК CFB, были выбраны и испытаны в различных дозах в клетках HepG2. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов с аналогичными условиями культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Клетки были высеяны с плотностью 20000 клеток на лунку и трансфицированы с использованием электропорации с концентрациями антисмыслового олигонуклеотида, равными 0,08 мкМ, 0,25 мкМ, 0,74 мкМ, 2,22 мкМ, 6,67 мкМ и 20,00 мкМ, как указано в представленной ниже таблице. После периода обработки в течение около 16 часов, РНК выделяли из клеток и измеряли уровни мРНК CFB методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Указана также полумаксимальная ингибирующая концентрация (IC50) каждого олигонуклеотида. Обработка антисмысловыми олигонуклеотидами снижает уровни мРНК CFB в клетках дозозависимым образом.
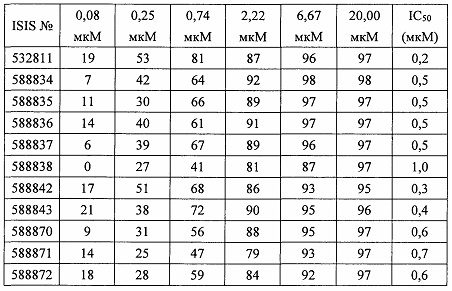
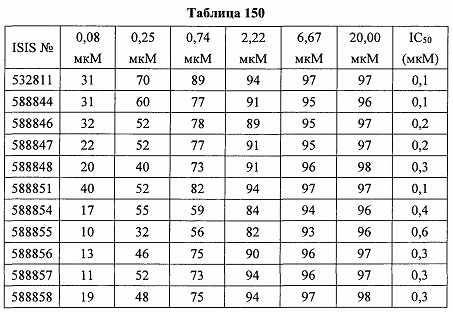
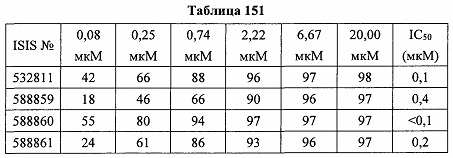
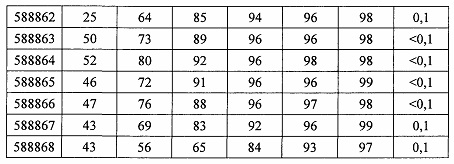
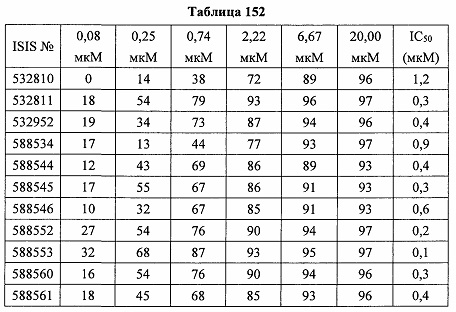
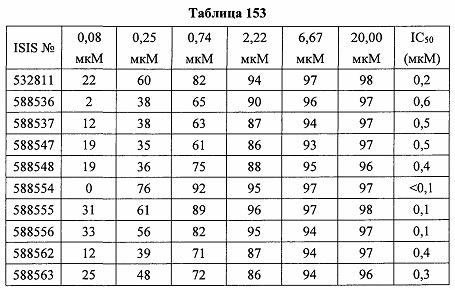

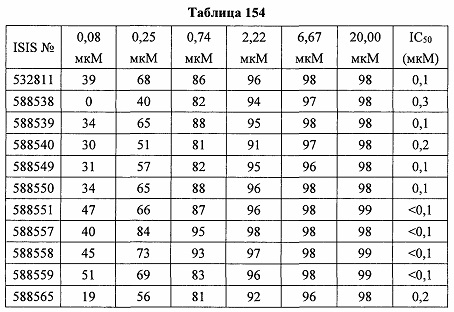
Пример 124: Дозозависимое антисмысловое ингибирование человеческого CFB в клетках HepG2
Гэпмеры из исследований, описанных выше, демонстрирующие значительное in vitro ингибирование мРНК CFB, были выбраны и испытаны в различных дозах в клетках HepG2. Антисмысловые олигонуклеотиды были протестированы в серии экспериментов с аналогичными условиями культивирования. Результаты для каждого эксперимента представлены в отдельных таблицах, показанных ниже. Клетки были высеяны с плотностью 20000 клеток на лунку и трансфицированы с использованием электропорации с концентрациями антисмыслового олигонуклеотида, равными 0,06 мкМ, 0,25 мкМ, 1,00 и 4,00 мкМ, как указано в представленной ниже таблице. После периода обработки в течение около 16 часов, РНК выделяли из клеток и измеряли уровни мРНК CFB методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Указана также полумаксимальная ингибирующая концентрация (IC50) каждого олигонуклеотида. Обработка антисмысловыми олигонуклеотидами снижает уровни мРНК CFB в клетках дозозависимым образом.
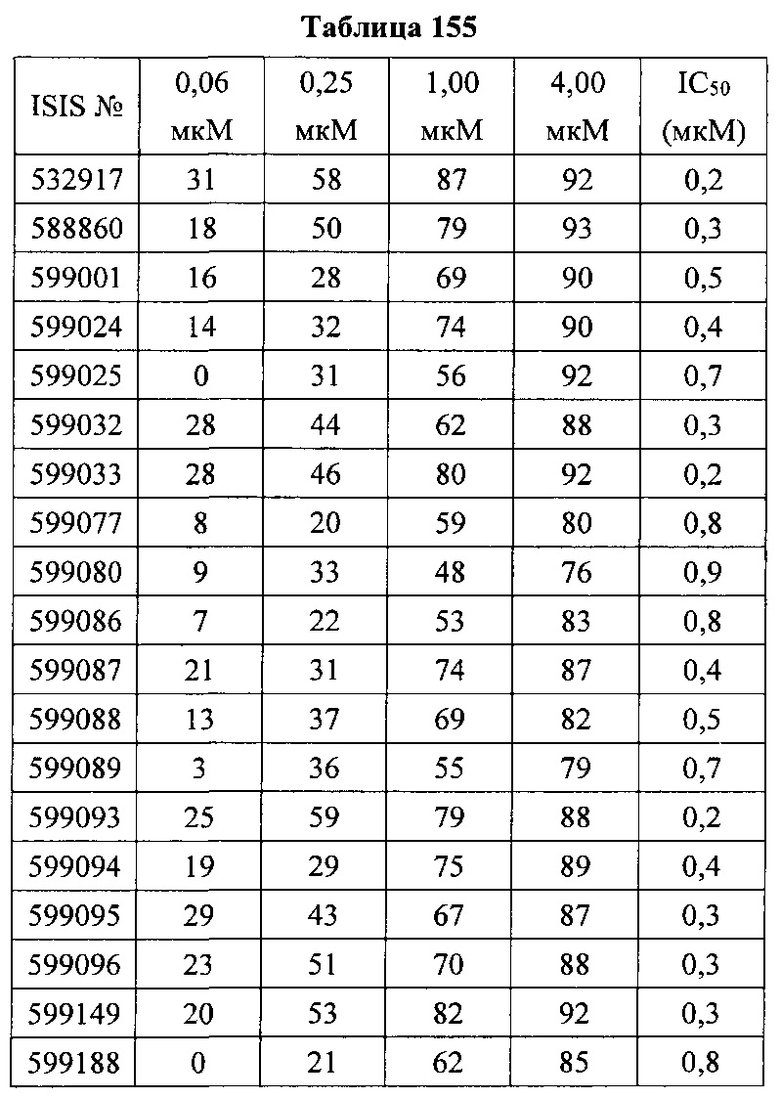
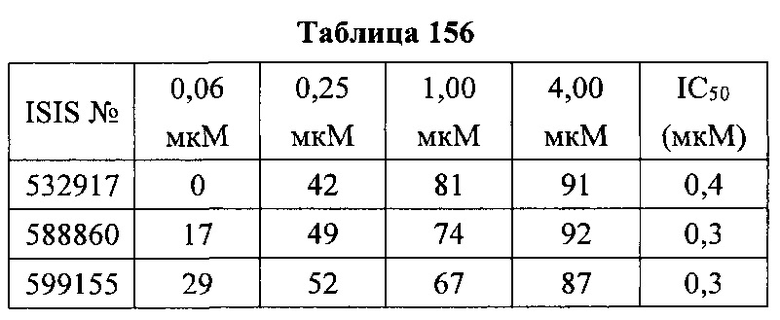
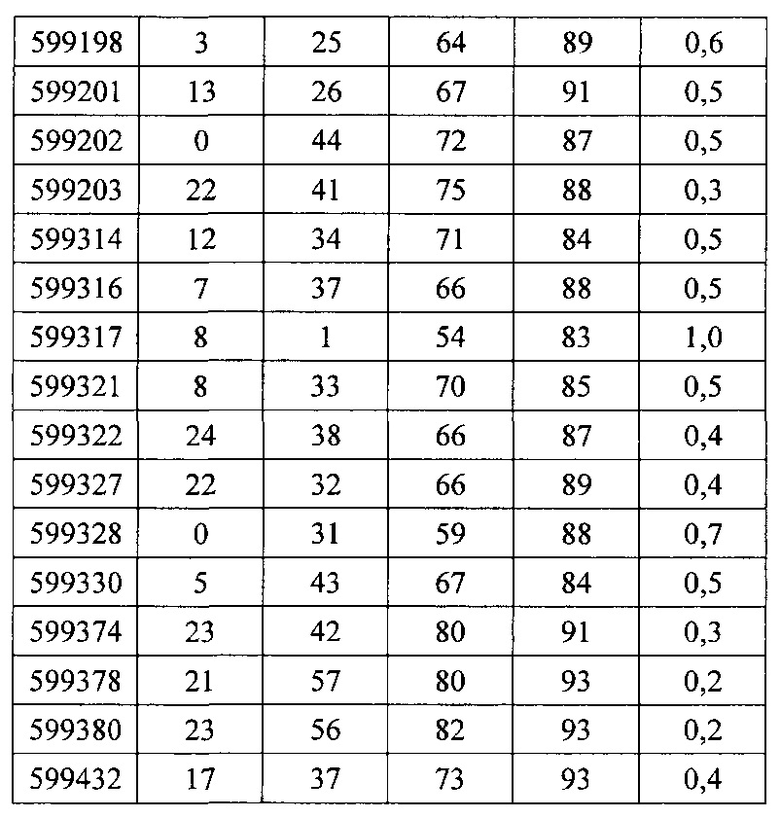
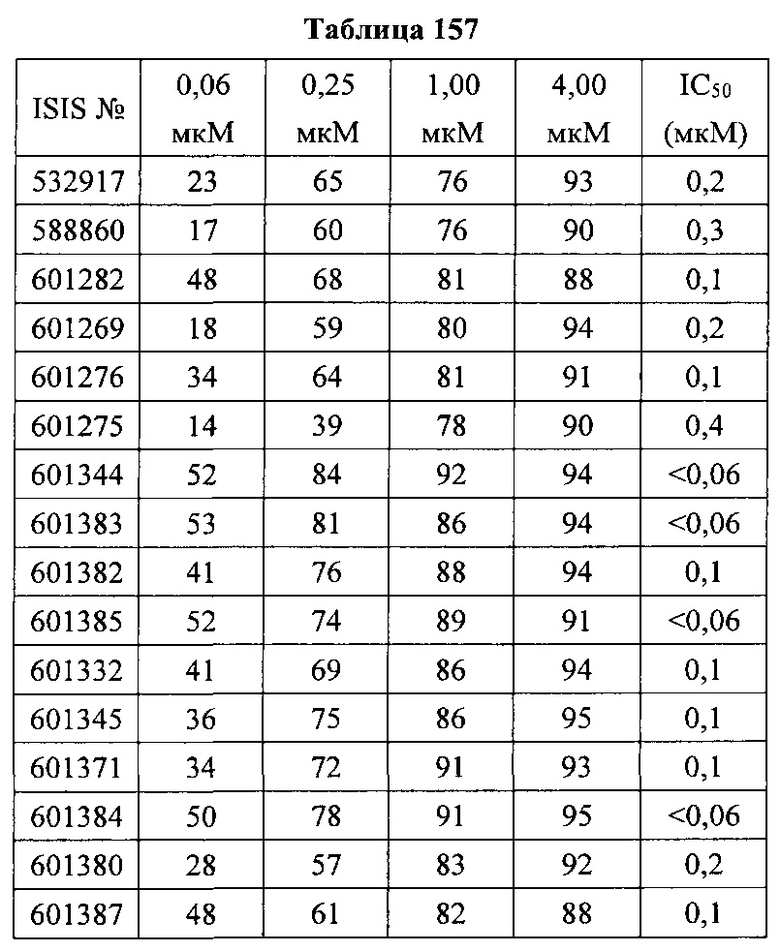
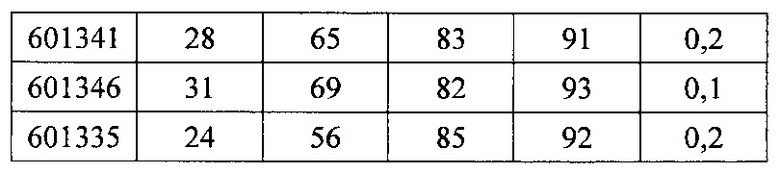
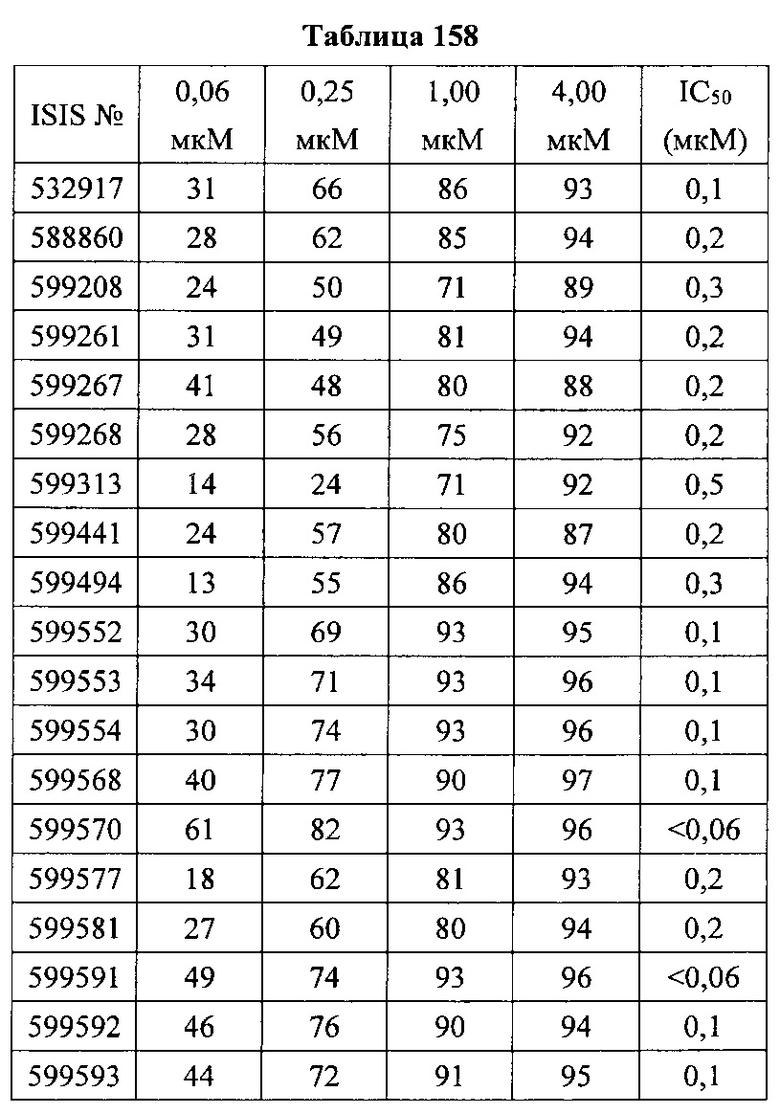
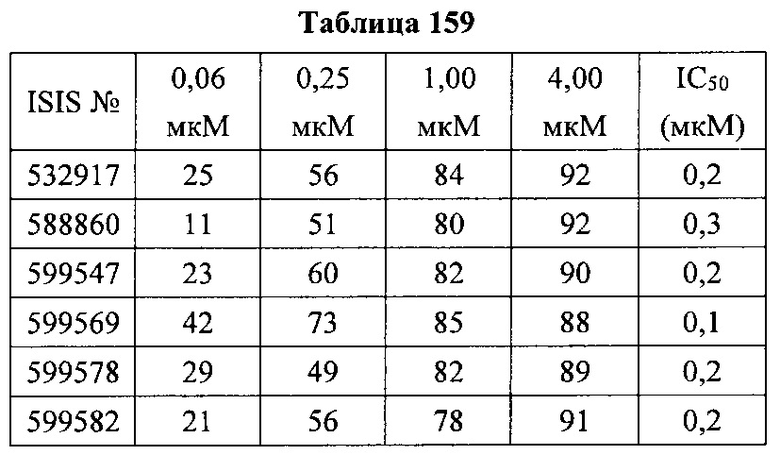
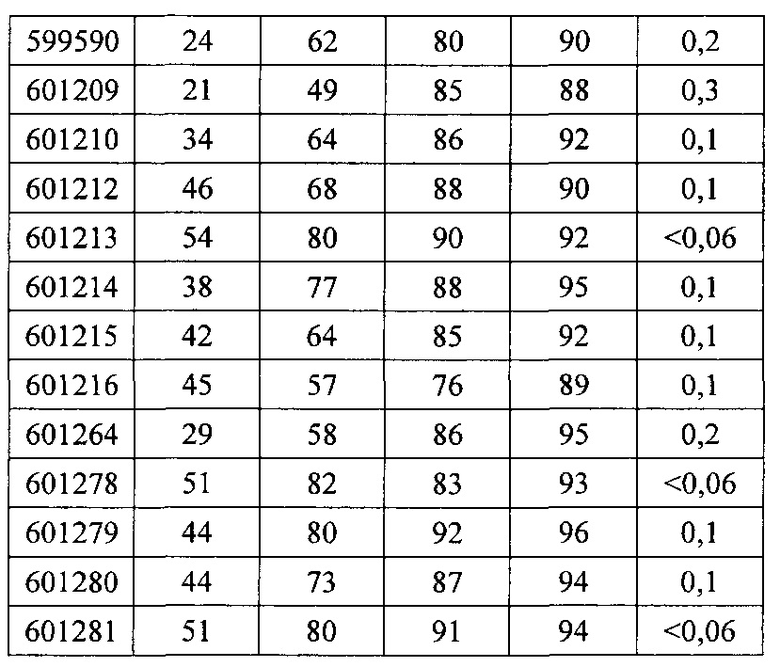
Пример 125: Дозозависимое антисмысловое ингибирование человеческого CFB в клетках HepG2
Гэпмеры из исследований, описанных выше, демонстрирующие значительное in vitro ингибирование мРНК CFB, были выбраны и испытаны в различных дозах в клетках HepG2. Дополнительно был сконструирован дезокси, МОЕ и (S)-cEt олигонуклеотид, ISIS 594430, имеющий такую же последовательность (CTCCTTCCGAGTCAGC, SEQ ID NO: 549) и область-мишень (целевой сайт инициации 2195 в SEQ ID NO: 1 и целевой сайт инициации 6983 в SED ID NO: 2), как ISIS 588870, другой дезокси, МОЕ и (S)-cEt олигонуклеотид. ISIS 594430 представляет собой 3-10-3 (S)-cEt гэпмер.
Клетки были высеяны с плотностью 20000 клеток на лунку и трансфицированны с использованием электропорации с концентрациями антисмыслового олигонуклеотида, равными 0,01 мкМ, 0,04 мкМ, 0,12 мкМ, 0,37 мкМ, 1,11 мкМ, 3,33 мкМ и 10,00 мкМ, как указано в представленной ниже таблице. После периода обработки в течение около 16 часов, РНК выделяли из клеток и измеряли уровни мРНК CFB методом количественной ПЦР в реальном времени. Набор человеческих праймеров RTS3459 был использован для измерения уровней мРНК. Уровни мРНК CFB были скорректированы в соответствии с содержанием суммарной РНК, измеренным с помощью RIBOGREEN®. Результаты представлены как процентное ингибирование CFB относительно необработанных контрольных клеток.
Указана также полумаксимальная ингибирующая концентрация (IC50) каждого олигонуклеотида. Обработка антисмысловыми олигонуклеотидами снижает уровни мРНК CFB в клетках дозозависимым образом.
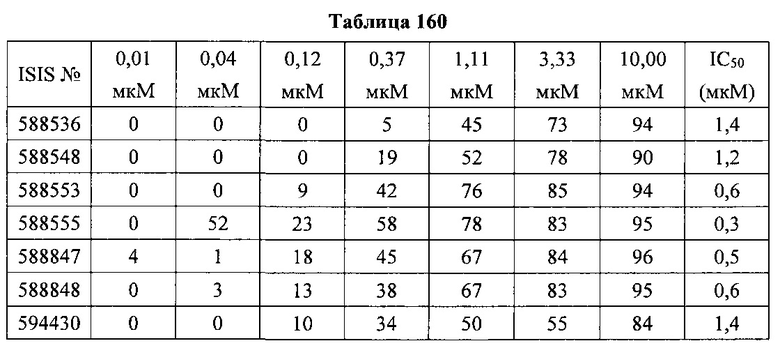
Пример 126: Переносимость МОЕ гэпмеров, направленных на человеческий CFB, у мышей CD1
Мыши CD1® (Чарльз Ривер, штат Массачусетс) представляют собой многоцелевую мышиную модель, часто используемую для испытаний безопасности и эффективности. Мышей лечили антисмысловыми олигонуклеотидами ISIS, выбранными из описанных выше исследований, и оценивали изменения уровней различных химических маркеров в плазме.
Испытание 1 (с 5-10-5 МОЕ гэпмерами)
Группам семинедельных мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг олигонуклеотида ISIS. Одной группе самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Одной группе мышей один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг контрольного олигонуклеотида ISIS 141923 (CCTTCCCTGAAGGTTCCTCC, в настоящем документе обозначена как SEQ ID NO: 809, 5-10-5 МОЕ гэпмер, не имеющий известной мышиной мишени). Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотида ISIS на функцию печени и почек измеряли уровни трансаминаз и АМК в плазме с использованием автоматического клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
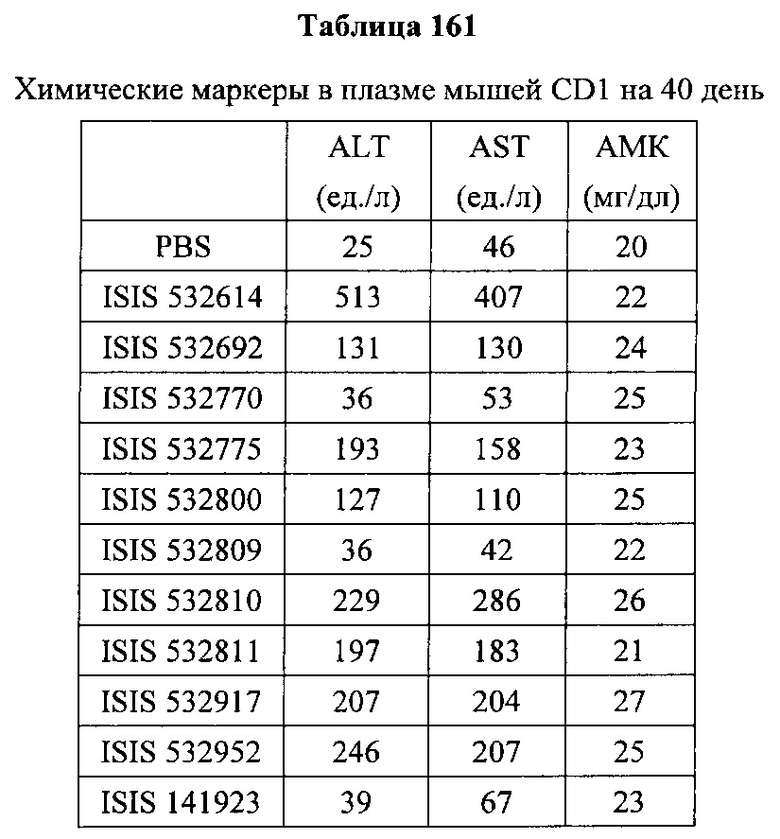
Масса
Перед усыплением мышей на 40 день измерили также массу тела мышей. После усыпления мышей измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
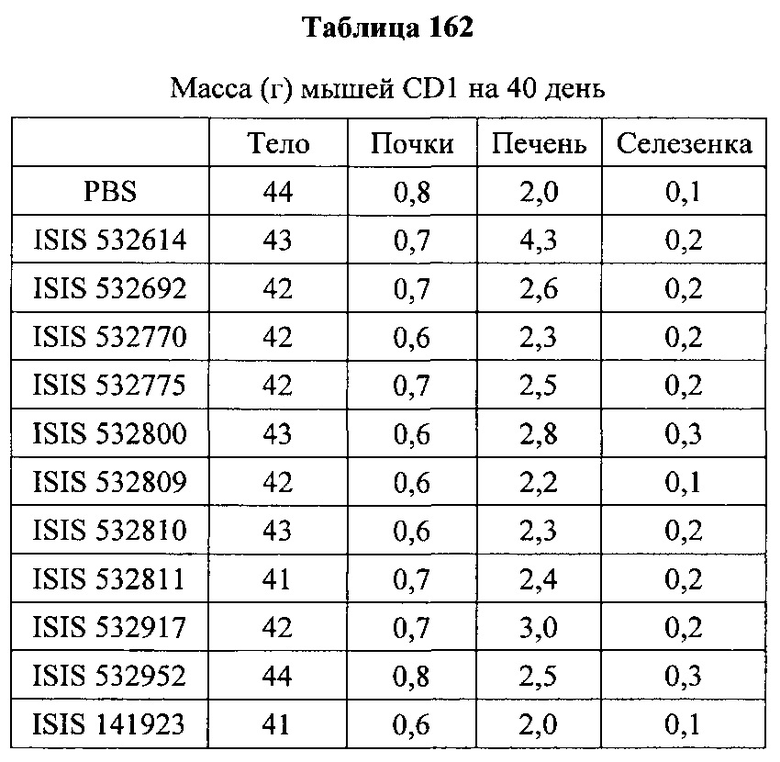
Испытание 2 (с 5-10-5 МОЕ гэпмерами)
Группам шести-восьминедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг олигонуклеотида ISIS. Двум группам самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS Одной группе мышей один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг контрольного олигонуклеотида ISIS 141923. Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина и АМК в плазме, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
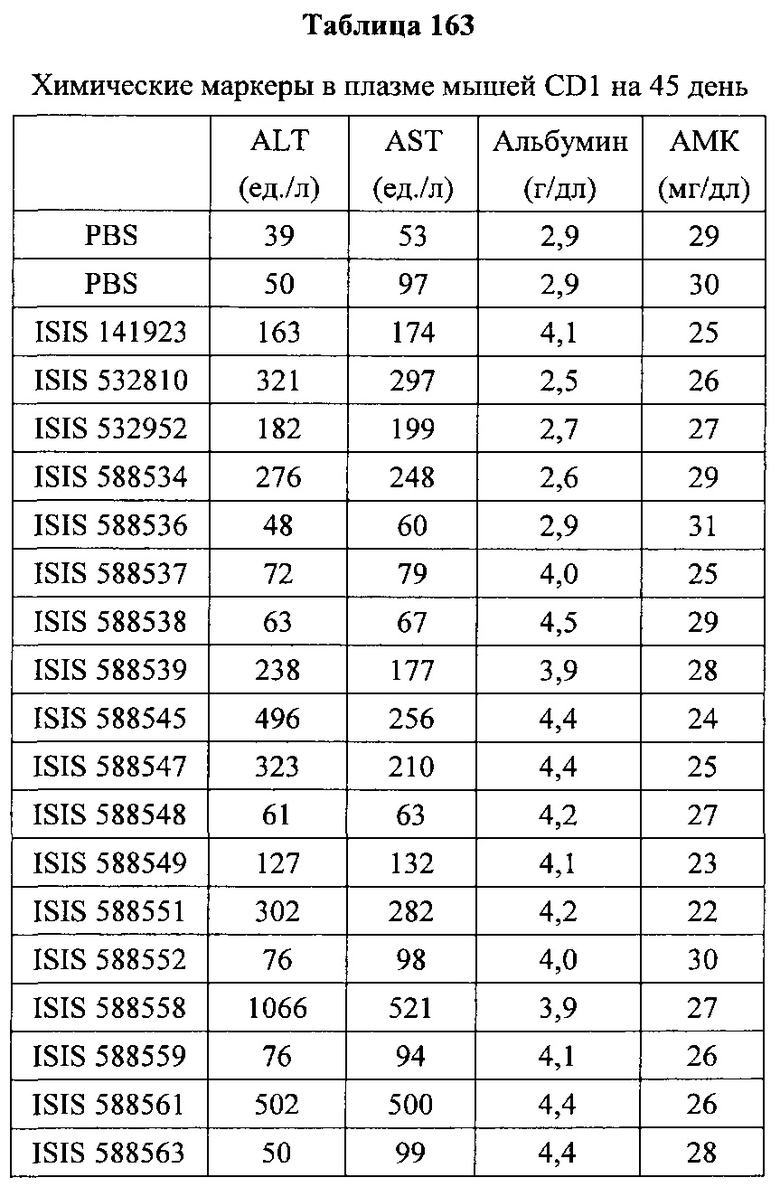
Масса
Массу тела мышей измерили на 42 день. После усыпления мышей на 45 день измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
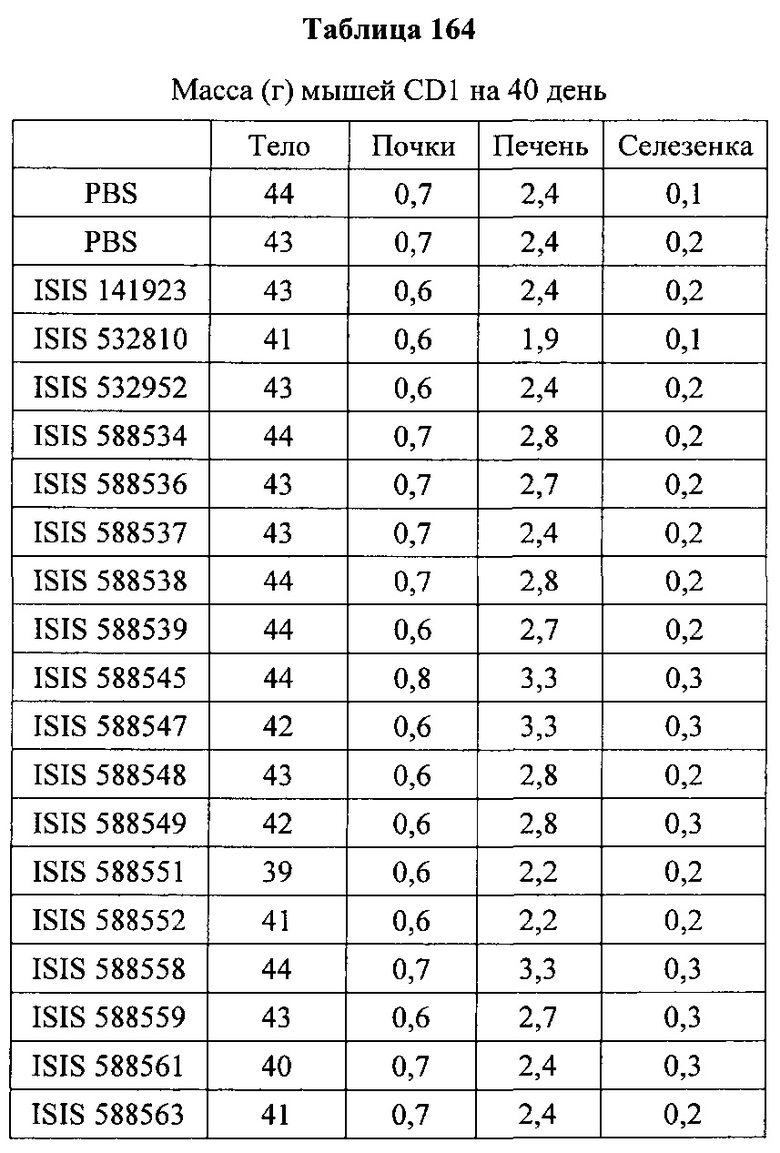
Испытание 3 (с 5-10-5 МОЕ гэпмерами)
Группам шести-восьминедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг олигонуклеотида ISIS. Двум группам самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина и АМК в плазме, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
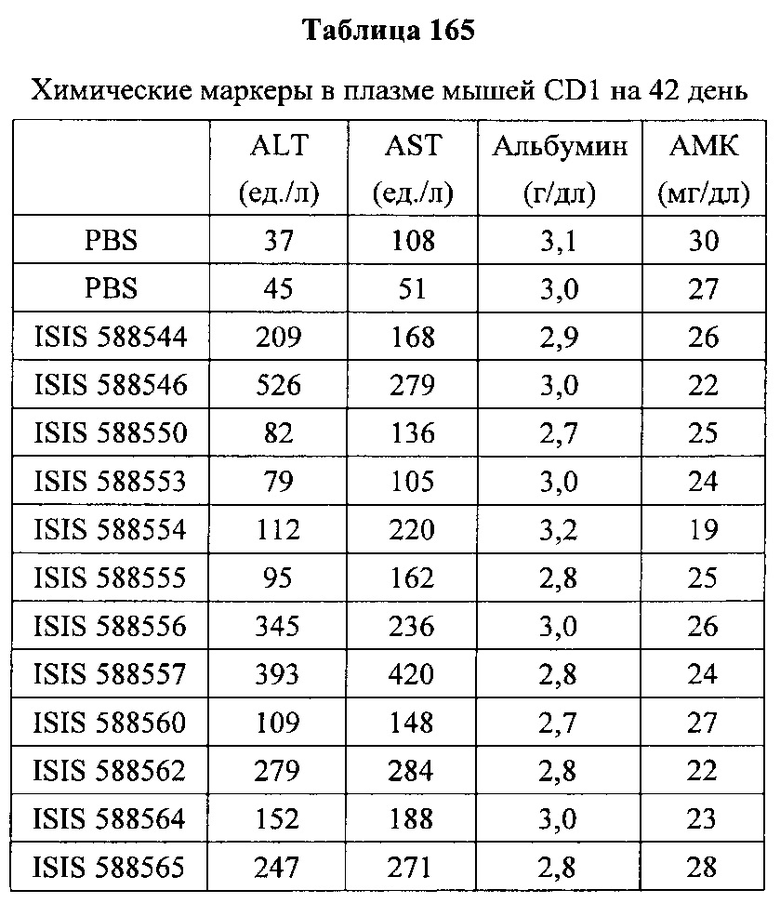
Масса
Массу тела мышей измерили на 42 день. После усыпления мышей на 42 день измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
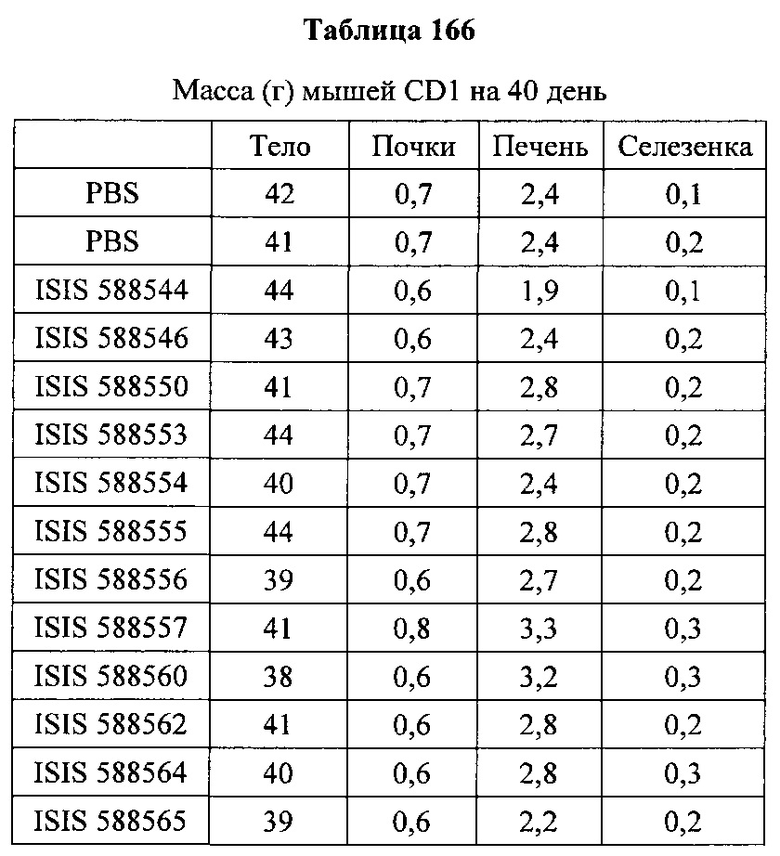
Испытание 4 (с (S)-cEt гэпмерами и дезокси, МОЕ и (S)-cEt олигонуклеотидами)
Группам десятинедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 50 мг/кг олигонуклеотида ISIS из исследований, описанных выше. Кроме того, были сконструированы два олигонуклеотида, ISIS 594431 и ISIS 594432, сконструированные как 3-10-3 (S)-cEt гэпмеры, и они также были испытаны в данном исследовании. ISIS 594431 (ACCTCCTTCCGAGTCA, SEQ ID NO: 550) направлен на ту же область, что и ISIS 588871, дезокси, МОЕ и (S)-cEt гэпмер (целевой сайт инициации 2197 в SEQ ID NO: 1 и целевой сайт инициации 6985 в SEQ ID NO: 2). ISIS 594432 (TGGTCACATTCCCTTC, SEQ ID NO: 542) направлен на ту же область, что и ISIS 588872, дезокси, МОЕ и (S)-cEt гэпмер (целевой сайт инициации 154 в SEQ ID NO: 1 и целевой сайт инициации 1875 в SEQ ID NO: 2).
Двум группам самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина, креатинина и АМК в плазме с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
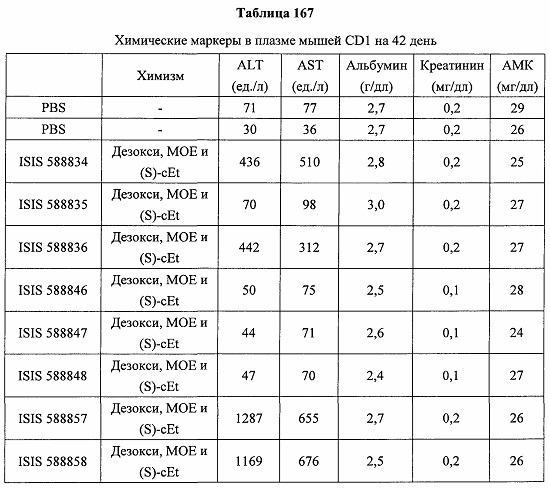
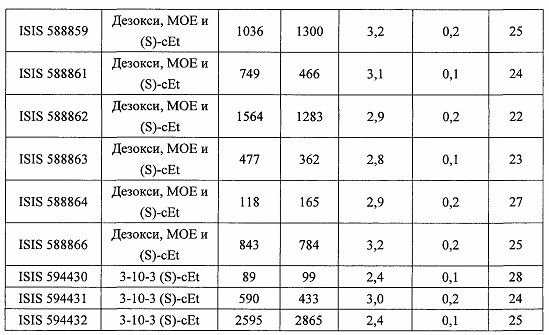
Масса
На 39 день измерили массу тела мышей. После усыпления мышей на 42 день измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
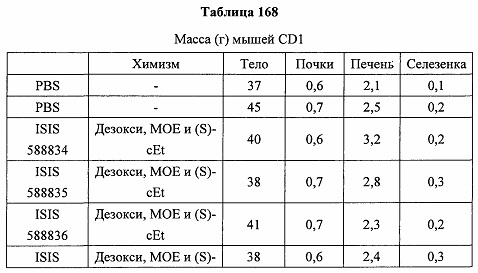
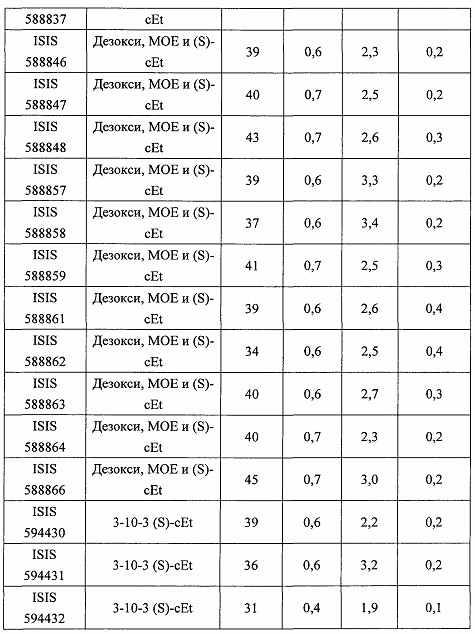
Испытание 5 (с МОЕ гэпмерами, (S)-cEt гэпмерами и дезокси. МОЕ и (S)-cEt олигонуклеотидами)
Группам восьми-девятинедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 50 мг/кг олигонуклеотида ISIS. Двум группам самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина, креатинина и АМК в плазме с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
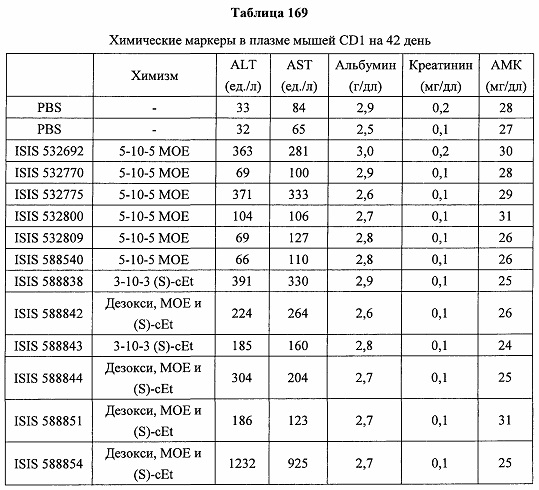
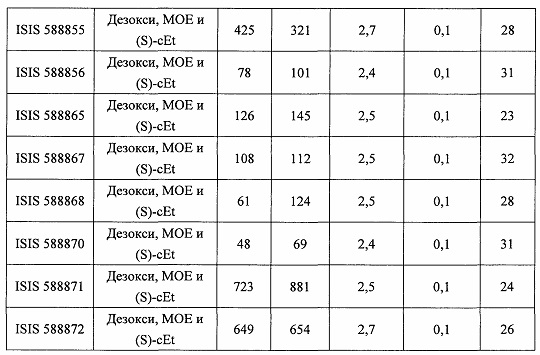
Масса
На 40 день измерили массу тела мышей. После усыпления мышей на 42 день измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
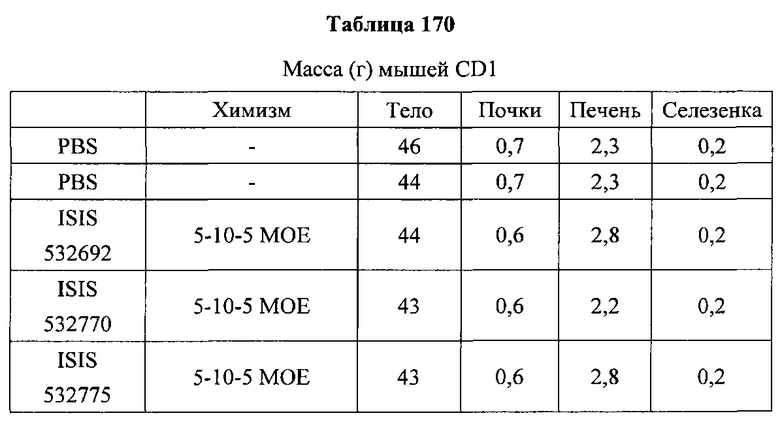
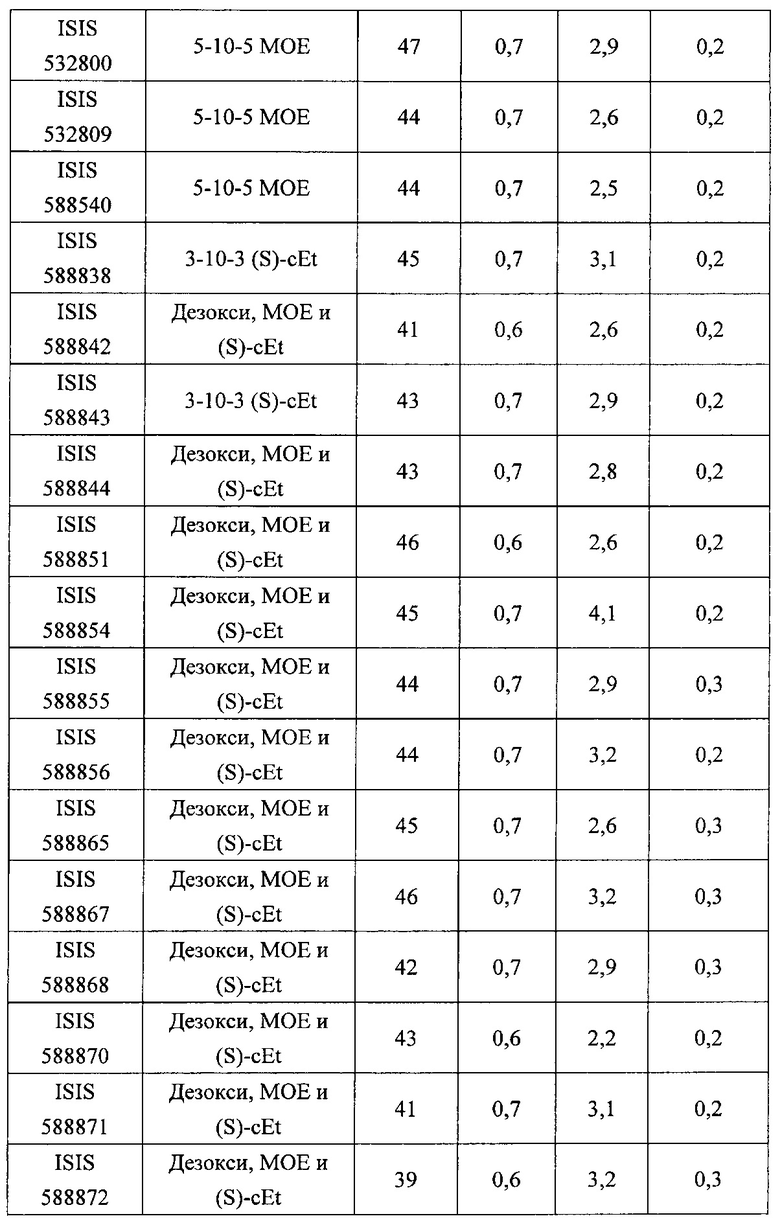
Испытание 6 (с дезокси, МОЕ и (S)-cEt олигонуклеотидами)
Группам восьми-девятинедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 50 мг/кг дезокси, МОЕ и (S)-cEt олигонуклеотидов. Двум группам самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина, креатинина, билирубина и АМК в плазме, используя автоматический клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
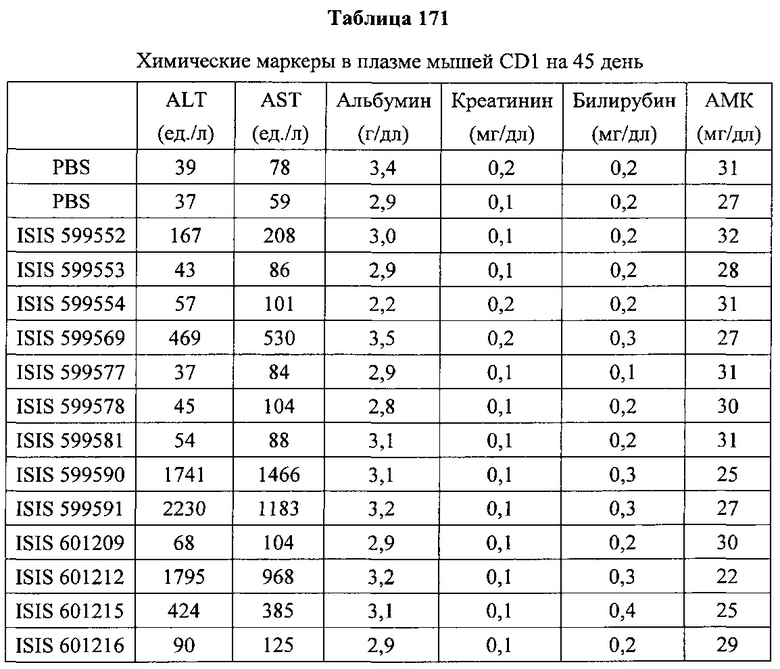

Масса
На 40 день измерили массу тела мышей. После усыпления мышей на 45 день измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
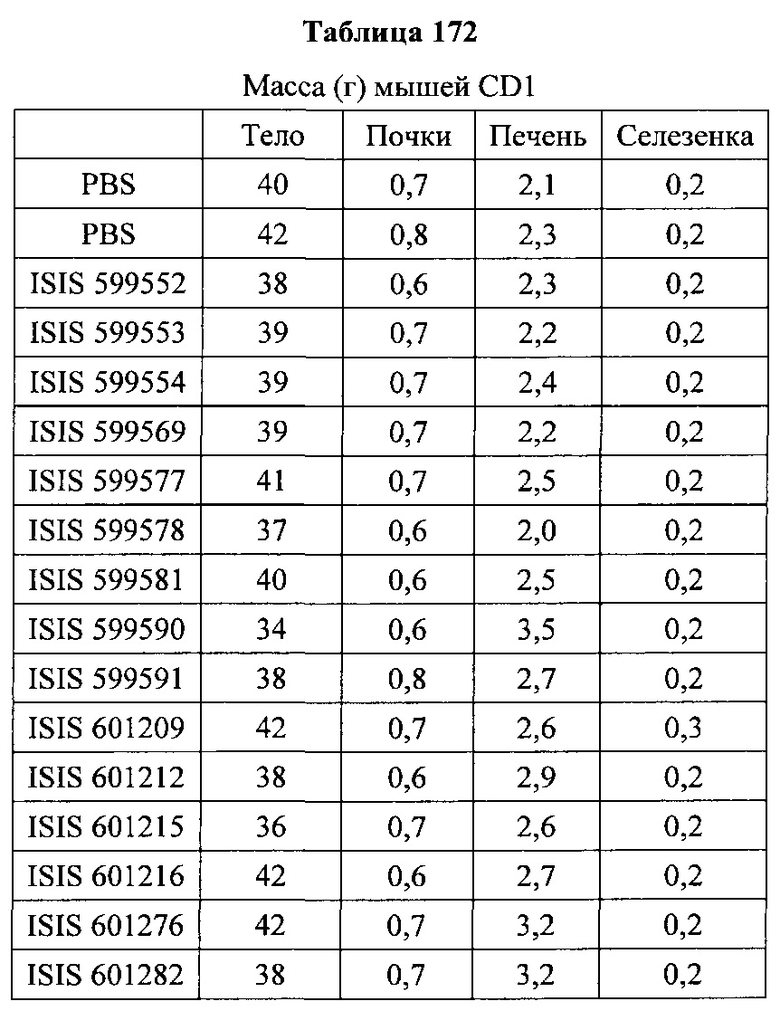
Испытание 7 (с МОЕ гэпмерами и дезокси. МОЕ и (S)-cEt олигонуклеотидами)
Группами восьми-девятинедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг олигонуклеотидов ISIS. Одной группе самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина, креатинина и АМК в плазме с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции печени или почек за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали для дальнейших исследований.
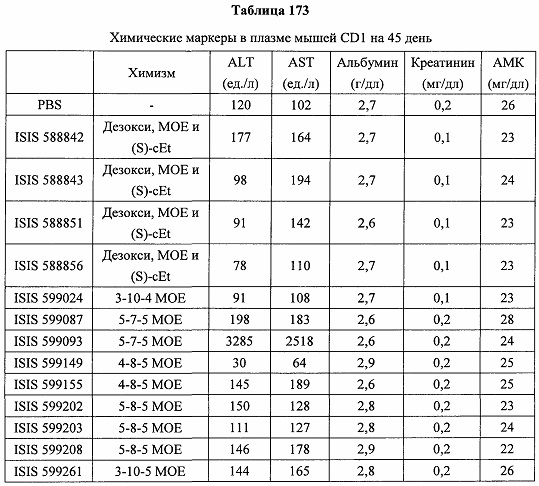
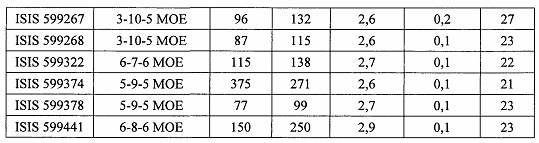
Масса
На 44 день измерили массу тела мышей. На 49 день, после усыпления мышей измерили также массу органов, печени, почек и селезенки. Результаты представлены ниже в таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
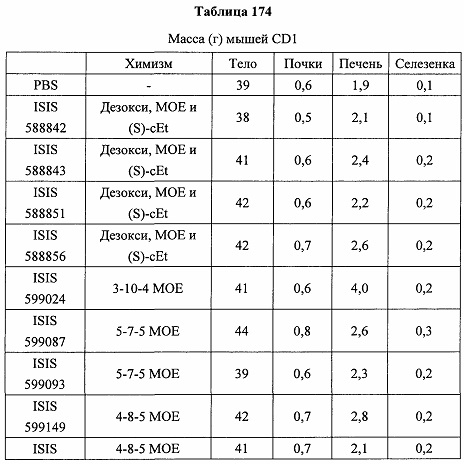
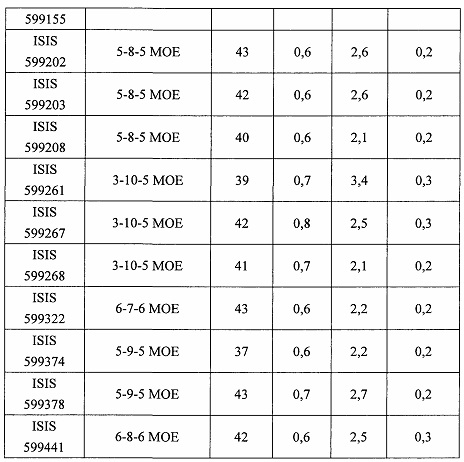
Испытания 8 (с МОЕ гэпмерами. дезокси, МОЕ и (S)-cEt олигонуклеотидами и (S)-cEt гэпмерами)
Группам восьми-девятинедельных самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции 10 мг/кг МОЕ гэпмеров или 50 мг/кг дезокси и (S)-cEt олигонуклеотидов, или (S)-cEt гэпмеров. Одной группе самцов мышей CD1 один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Мышей усыпляли через 48 часов после введения последней дозы и собирали органы и плазму для дальнейших анализов.
Химические маркеры в плазме
Для оценки влияния олигонуклеотидов ISIS на функцию печени и почек измеряли уровни трансаминаз, альбумина, креатинина и АМК в плазме с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в таблице.
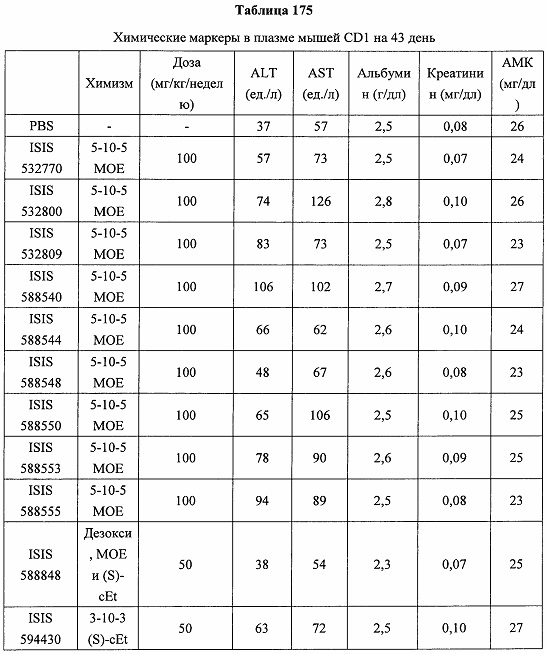
Масса
Массу тела мышей измеряли на 36 день. После усыпления мышей, на 43 день измеряли также массу органов, печени, почек и селезенки. Результаты измерений массы органов выражены как соотношение к массе тела и нормализованы к соотношению контрольной группы с PBS.
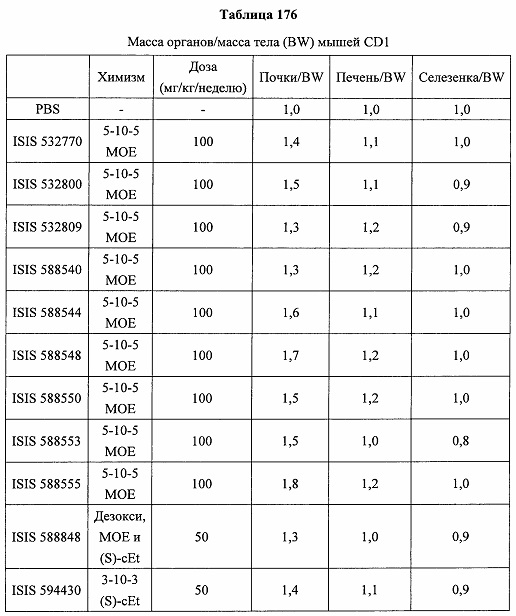
Анализ цитокинов
Кровь, собранную во всех группах мышей, направили в компанию Antech Diagnostics для измерения уровней различных цитокинов, таких как IL-6, MDC, MIP1β, IP-10, МСР1, MIP-1α и RANTES. Результаты представлены в Таблице 54.

Гематологический анализ
Кровь, собранную во всех группах мышей, направили в компанию Antech Diagnostics для измерения гематокрита (НСТ), а также различных кровяных клеток, таких как белые кровяные тельца, красные кровяные тельца и тромбоциты, а также общего содержания гемоглобина (Hb). Результаты представлены в Таблице 55.
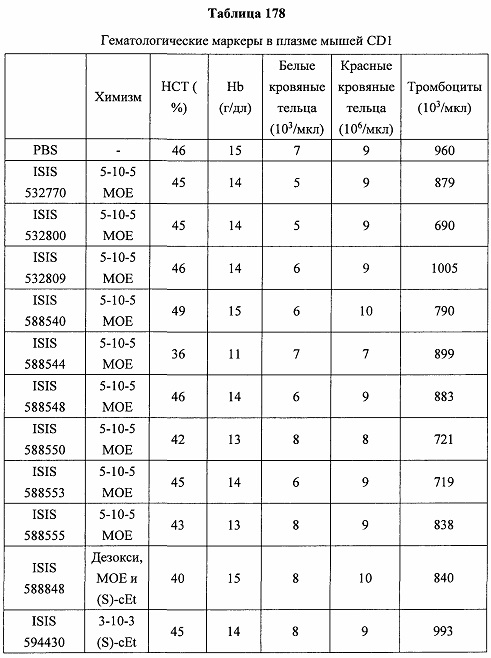
Пример 127: Переносимость антисмысловых олигонуклеотидов, направленных на человеческий CFB, у крыс Спрага-Доули
Крысы Спрага-Доули представляют собой многоцелевую модель, используемую для оценки безопасности и эффективности. Крыс лечили антисмысловыми олигонуклеотидами ISIS из исследований, описанных выше в Примерах, и оценивали на изменения уровней различных химических маркеров в крови.
Испытание 1 (с 5-10-5 МОЕ гэпмерами)
Самцов крыс Спрага-Доули возрастом от семи до восьми недель выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг 5-10-5 МОЕ гэпмеров. Одной контрольной группе из 6 крыс один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы) и представили результаты в следующей Таблице, выраженные в МЕ/л. Олигонуклеотиды ISIS, которые вызывали в печени изменения любых маркеров функции печени за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.

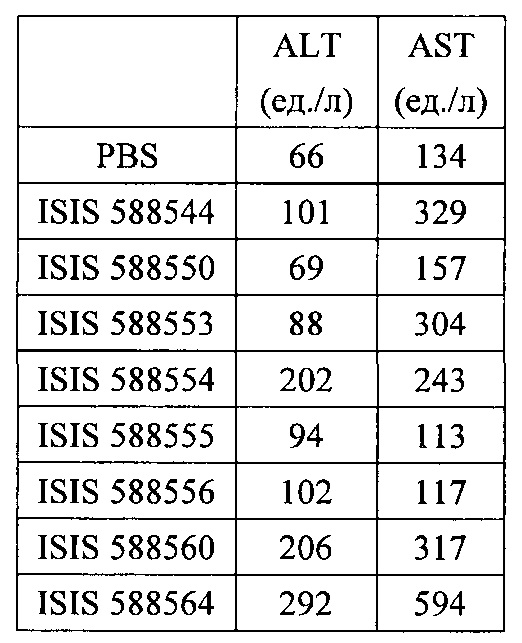
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни азота мочевины крови (АМК) и креатинина с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты, выраженные в мг/дл, представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.
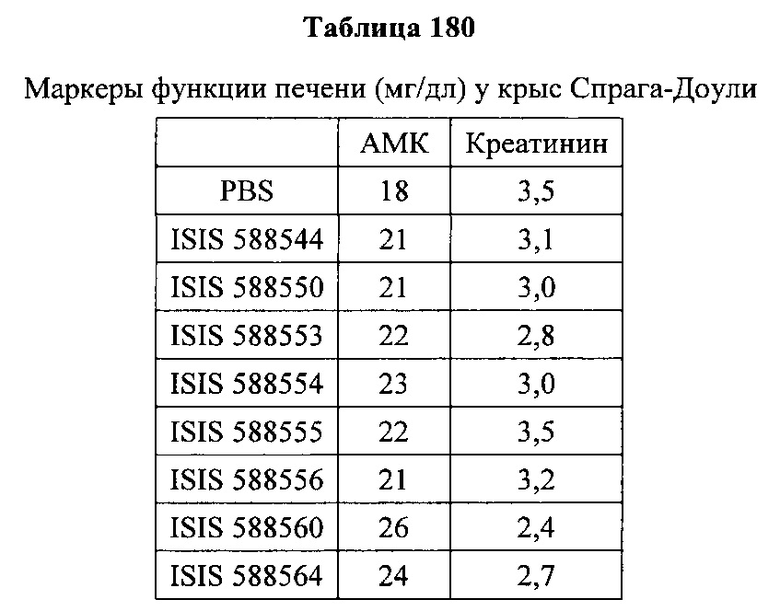
Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы органов за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
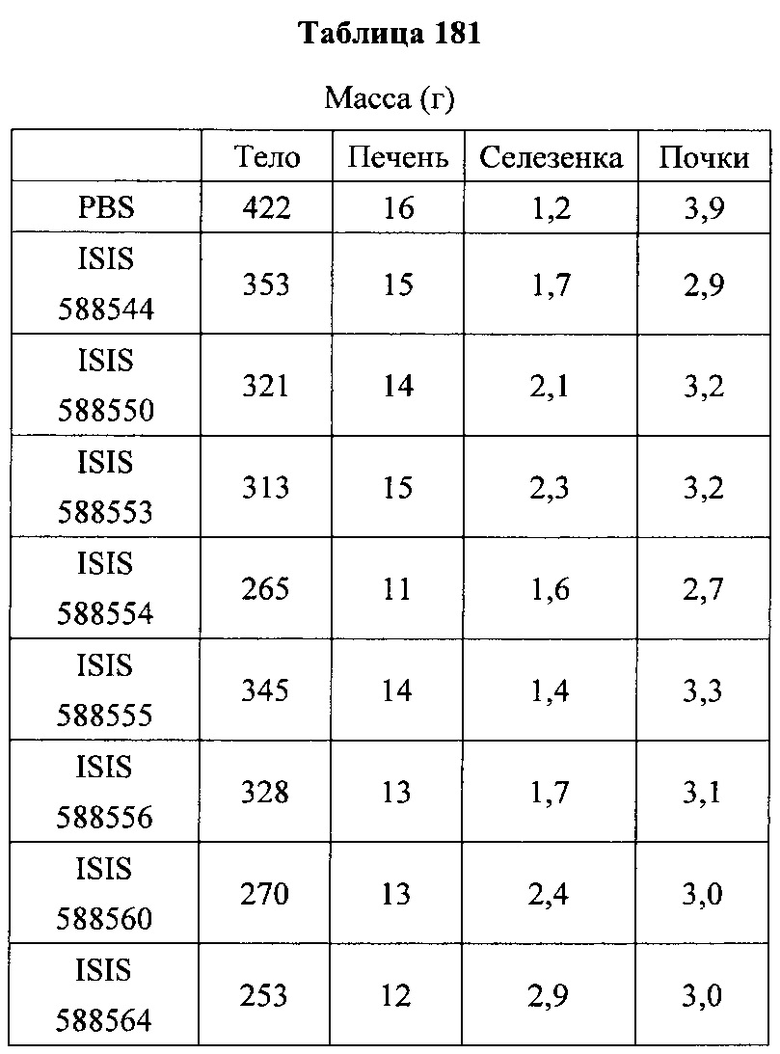
Испытание 2 (с дезокси, МОЕ и (S)-cEt олигонуклеотидами)
Самцов крыс Спрага-Доули возрастом от девяти до десяти недель выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг дезокси, МОЕ и (S)-cEt олигонуклеотидов. Двум контрольным группам по 3 крысы один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме на 42 день, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы), и альбумина в сыворотке, и результаты представлены ниже в Таблице. Олигонуклеотиды ISIS, которые вызывали в печени изменения любых маркеров функции печени за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
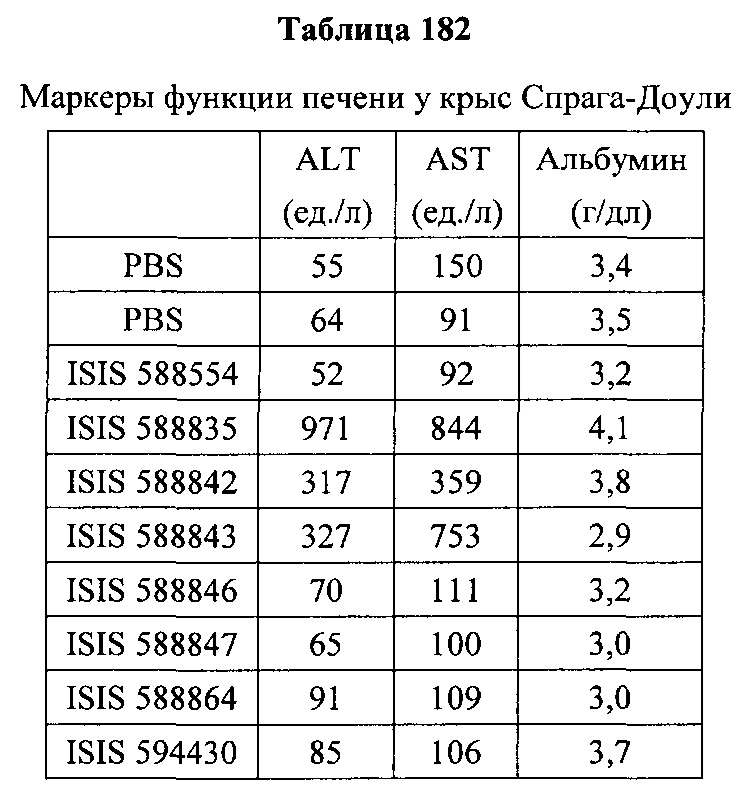
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни азота мочевины крови (АМК) и креатинина с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты, выраженные в мг/дл, представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.
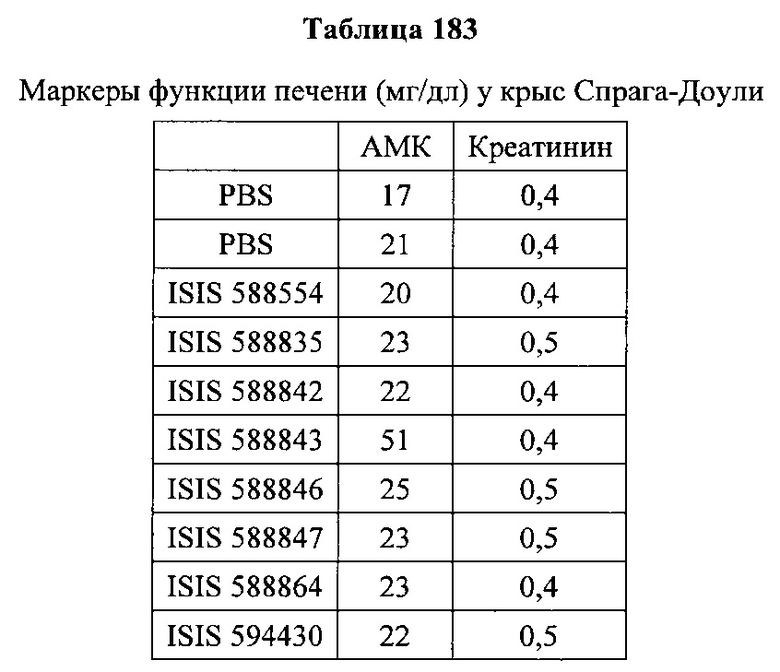
Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы органов за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
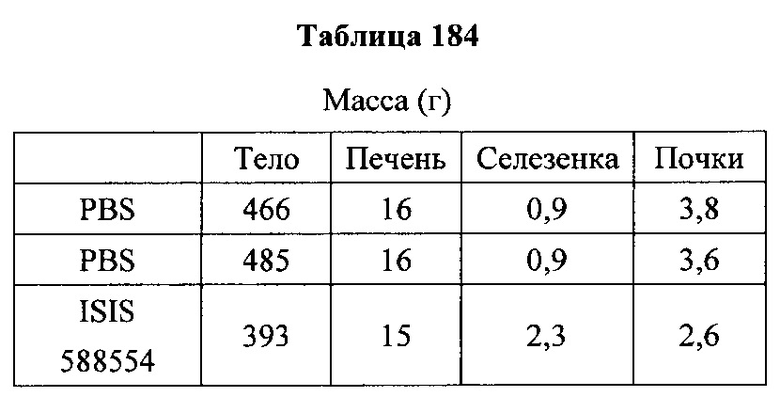
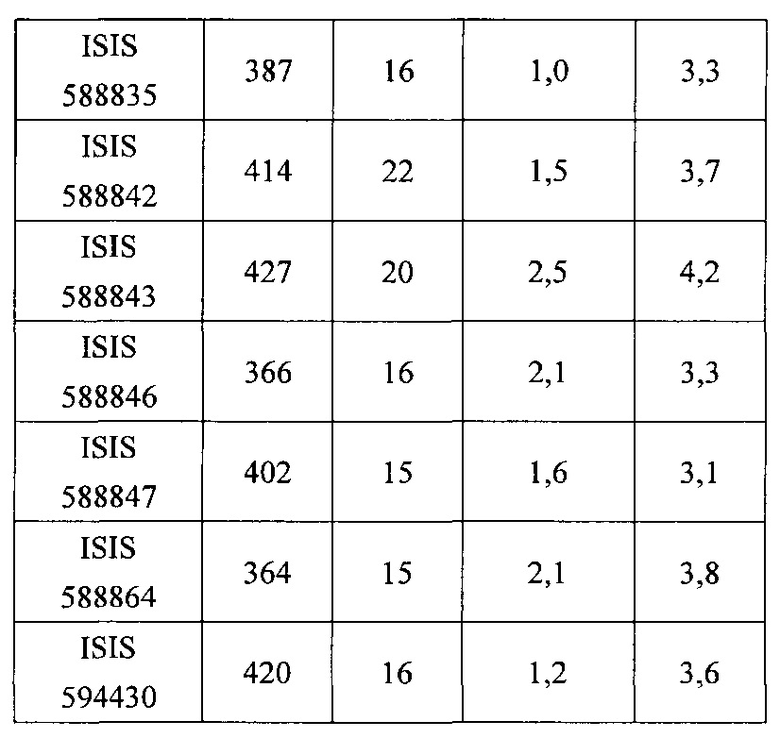
Испытание 3 (с МОЕ гэпмерами)
Самцов крыс Спрага-Доули возрастом от девяти до десяти недель выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг МОЕ гэпмеров. Одной контрольной группе из 6 крыс один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме на 43 день, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы) и представили результаты в следующей Таблице, выраженные в МЕ/л. Олигонуклеотиды ISIS, которые вызывали в печени изменения любых маркеров функции печени за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
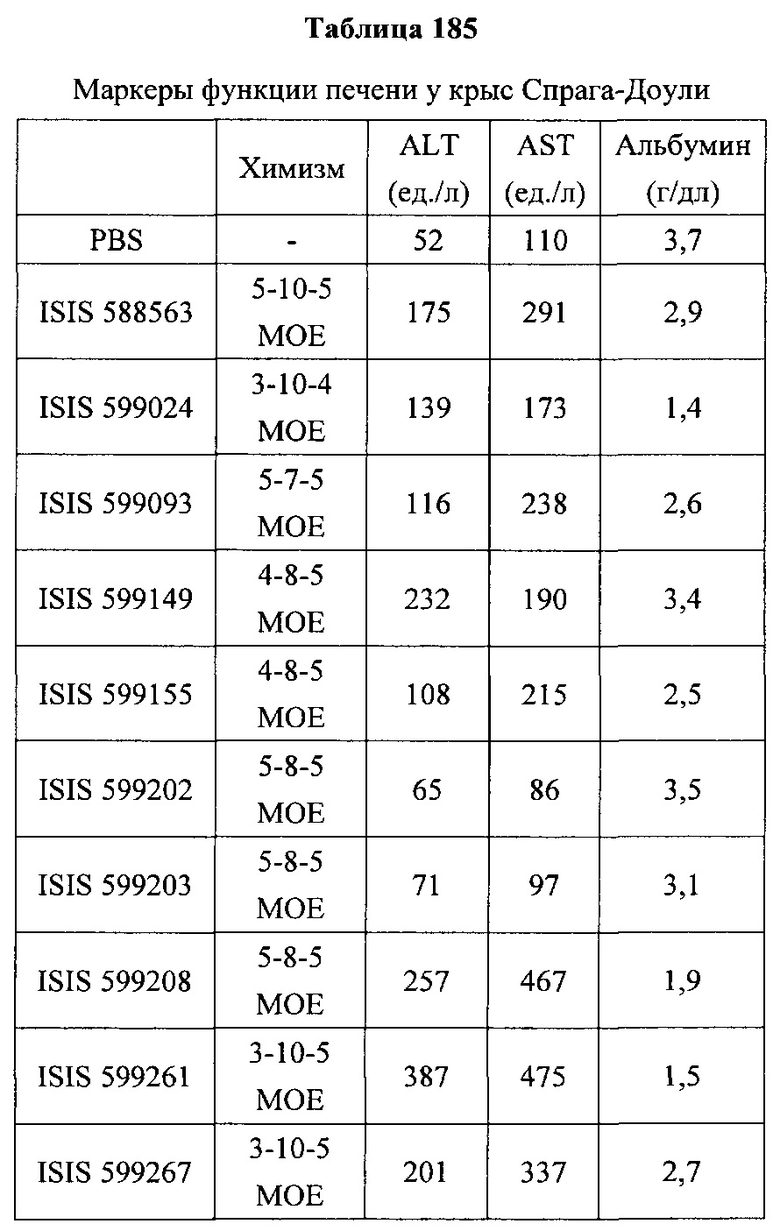
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни азота мочевины крови (АМК) и креатинина с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты, выраженные в мг/дл, представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.
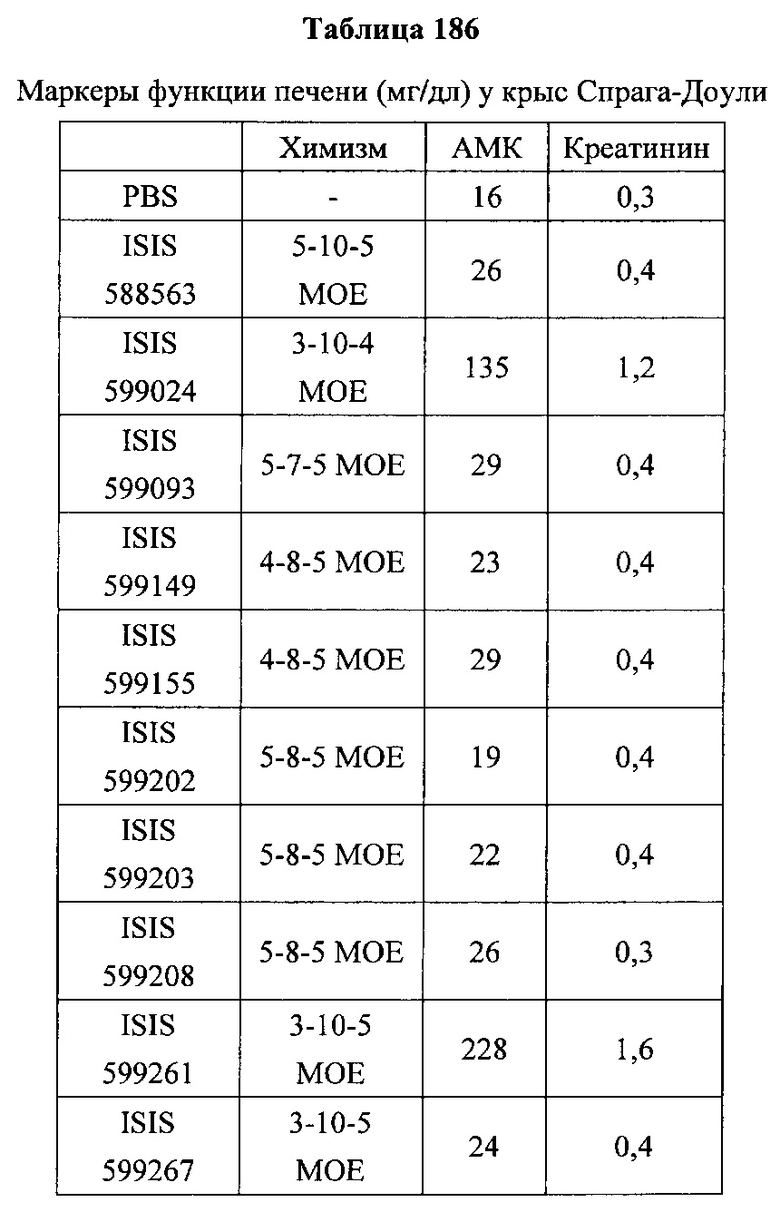
Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы органов за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
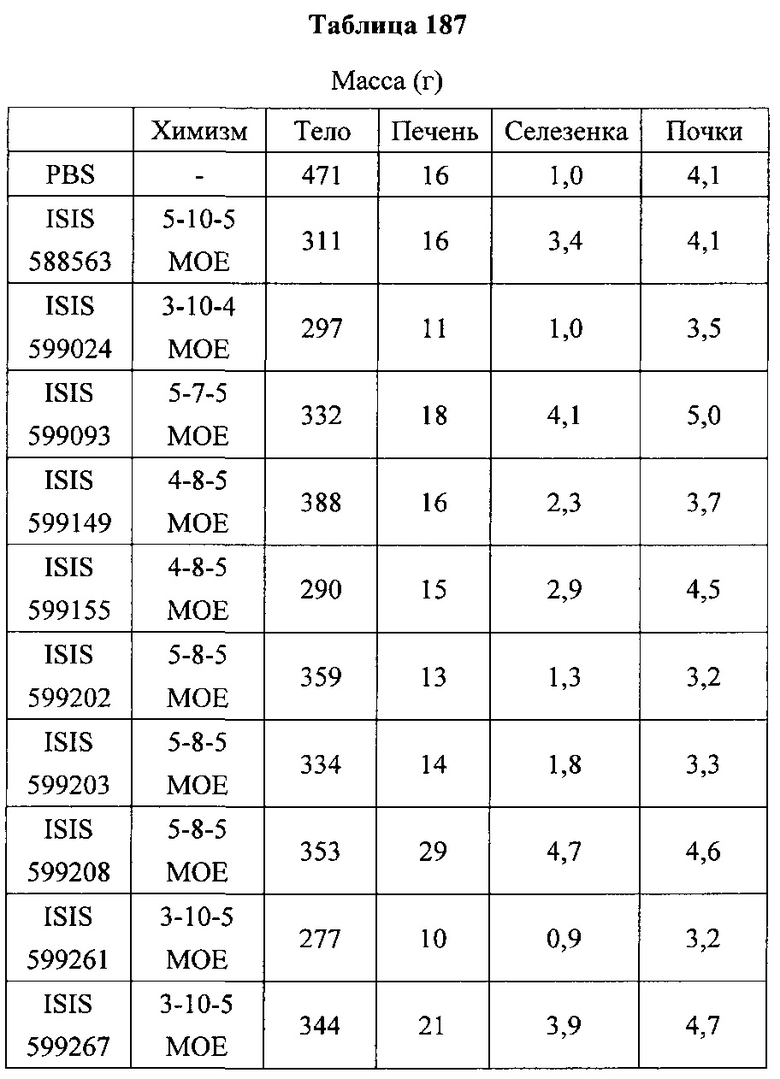
Испытание 4 (с МОЕ гэпмерами)
Самцов крыс Спрага-Доули возрастом от девяти до десяти недель выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг МОЕ гэпмеров. Одной контрольной группе из 6 крыс один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме на 42 день, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы) и представили результаты в следующей Таблице, выраженные в МЕ/л. Олигонуклеотиды ISIS, которые вызывали в печени изменения любых маркеров функции печени за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
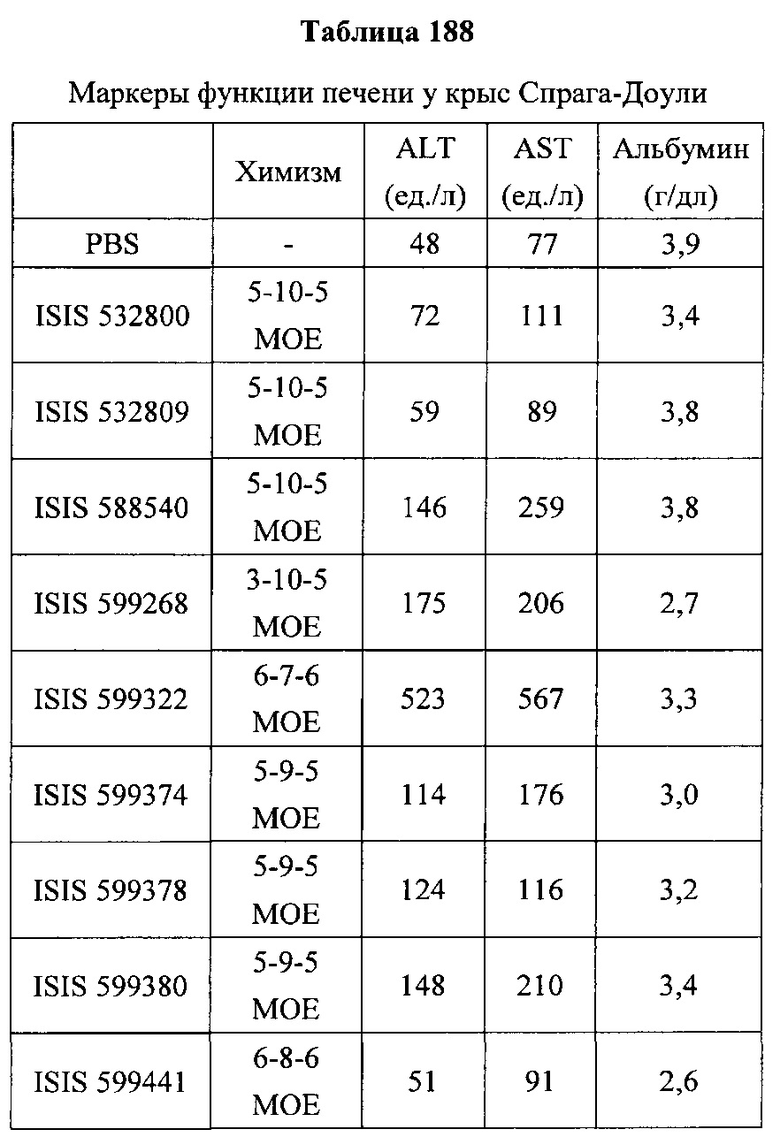
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни азота мочевины крови (АМК) и креатинина с помощью автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты, выраженные в мг/дл, представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.
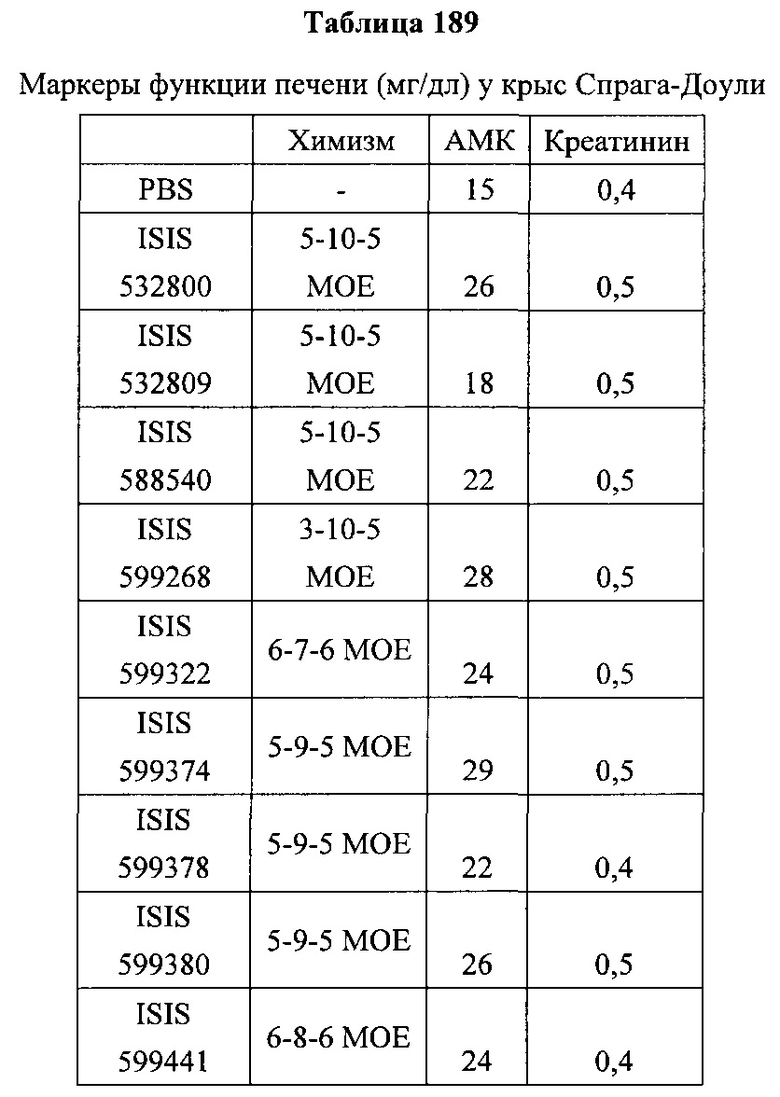
Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы органов за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
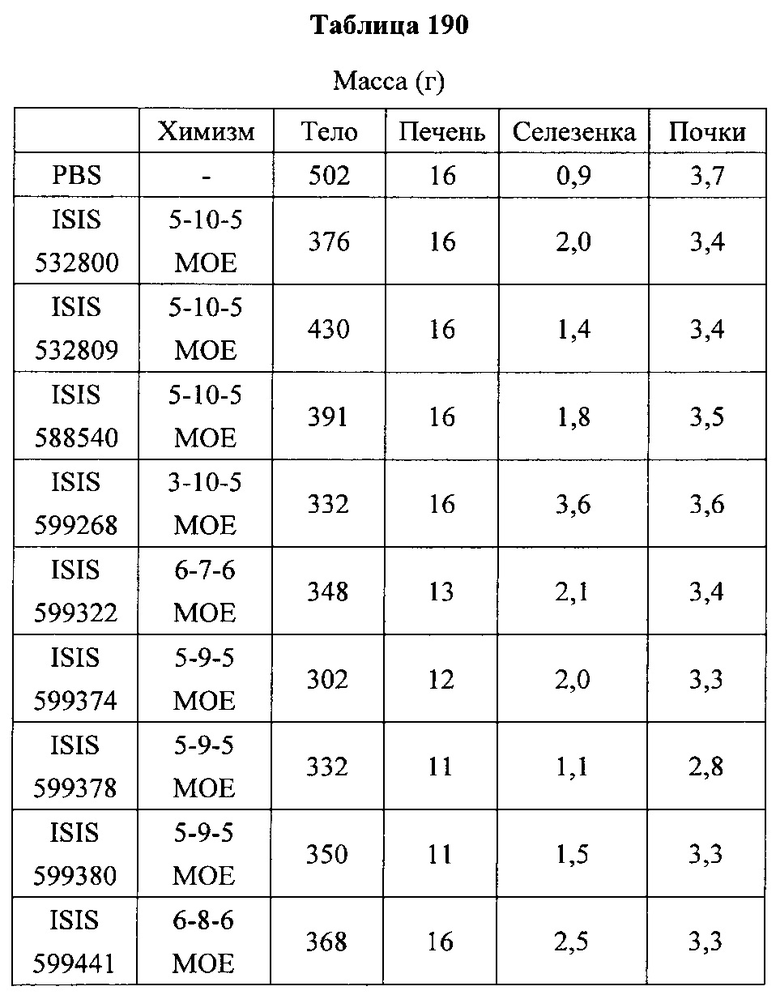
Испытание 5 (с МОЕ гэпмерами и дезокси, МОЕ и (S)-cEt олигонуклеотидами)
Самцов крыс Спрага-Доули возрастом от девяти до десяти недель выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг МОЕ гэпмера или 50 мг/кг дезокси, МОЕ и (S)-cEt олигонуклеотидов. Одной контрольной группе из 4 крыс один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме на 42 день, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы) и представили результаты в следующей Таблице, выраженные в МЕ/л. Олигонуклеотиды ISIS, которые вызывали в печени изменения любых маркеров функции печени за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
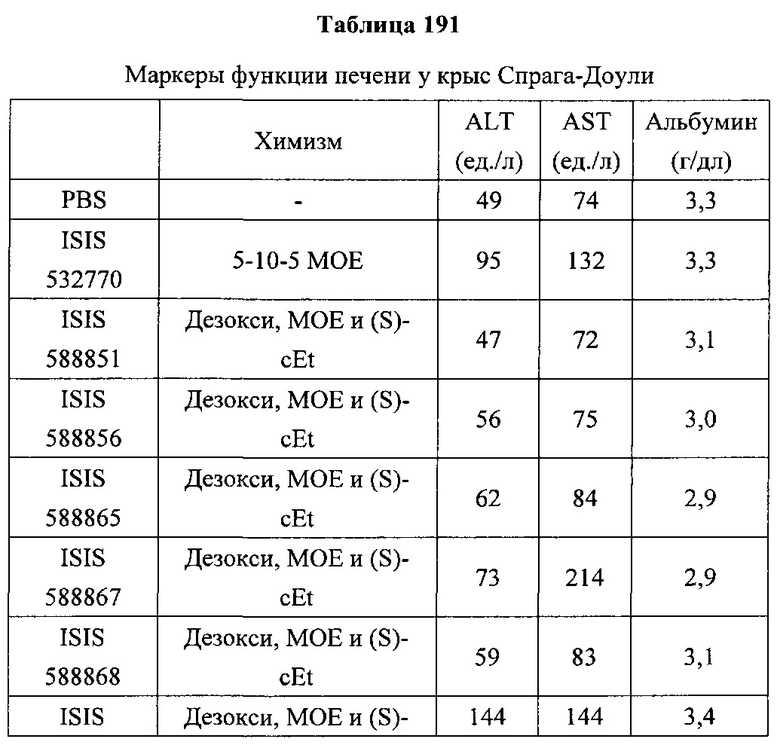

Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни азота мочевины крови (АМК) и креатинина в плазме и моче при помощи автоматизированного клинического анализатора химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты, выраженные в мг/дл, представлены ниже в Таблицах. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.



Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Олигонуклеотиды ISIS, которые вызывали изменения массы органов за пределами ожидаемого диапазона для антисмысловых олигонуклеотидов, не использовали в дальнейших исследованиях.
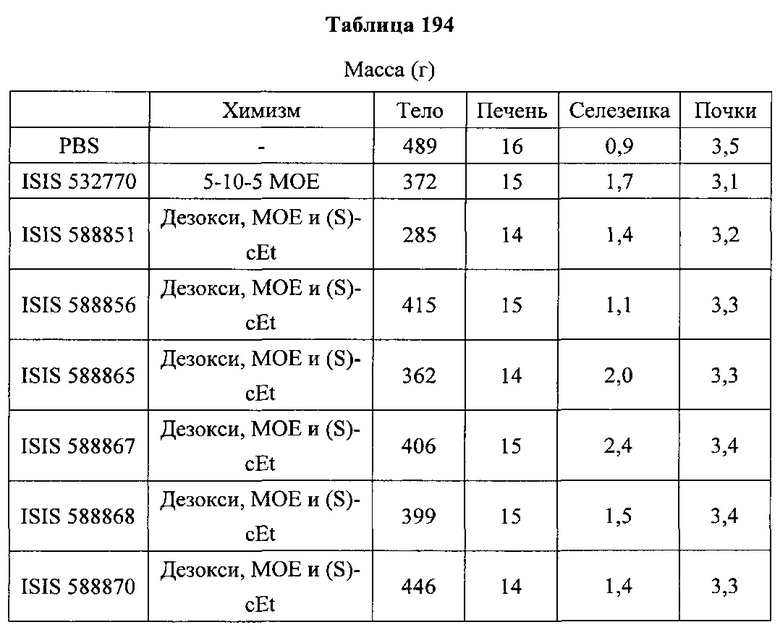
Испытание 6 (с МОЕ гэпмерами. дезокси, МОЕ и (S)-cEt олигонуклеотидами и (S)-cEt гэпмерами)
Самцов крыс выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к нормальному корму для крыс Purina, рацион 5001. Группам по 4 крысы Спрага-Доули один раз в неделю в течение 6 недель вводили подкожные инъекции 100 мг/кг МОЕ гэпмеров или 50 мг/кг дезокси, МОЕ и (S)-cEt олигонуклеотида, или (S)-cEt гэпмера. Одной контрольной группе из 4 крыс один раз в неделю в течение 6 недель вводили подкожные инъекции PBS. Через сорок восемь часов после введения последней дозы крыс усыпили и собрали органы и плазму для дальнейших анализов.
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени измеряли уровни трансаминаз в плазме на 42 день, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Измерили уровни ALT (аланинтрансаминазы) и AST (аспартаттрансаминазы) и представили результаты в следующей Таблице, выраженные в МЕ/л.
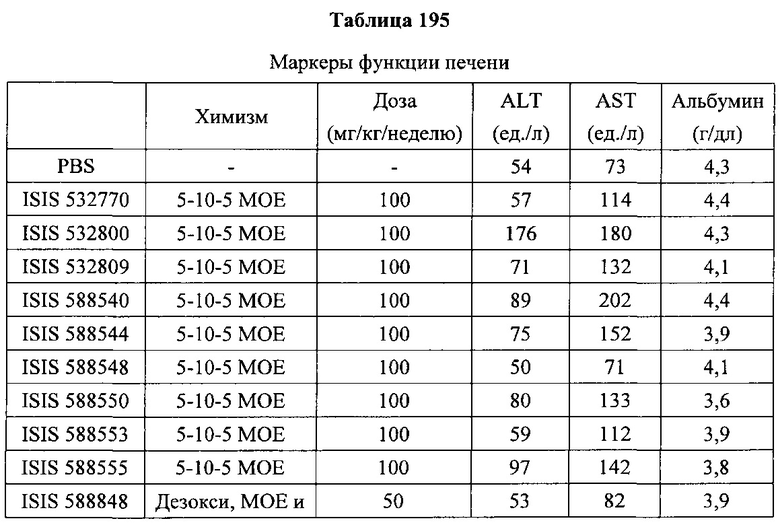
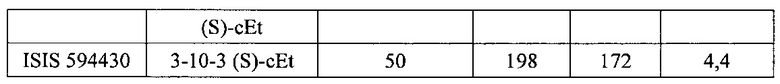
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек измеряли уровни общего белка и креатинина в моче, используя автоматизированный клинический анализатор химического состава (Hitachi Olympus AU400e, Мелвилл, штат Нью-Йорк). Результаты представлены ниже в Таблице. Олигонуклеотиды ISIS, которые вызывали изменения уровней любых маркеров функции почек за пределами ожидаемого диапазона для антисмыслоых олигонуклеотидов, не использовали в дальнейших исследованиях.
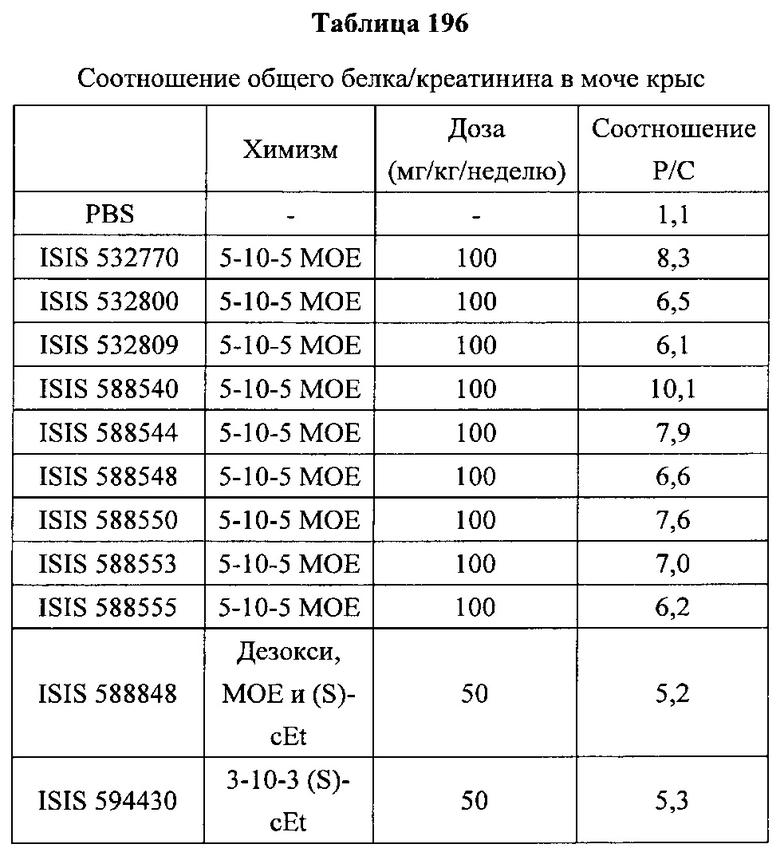
Масса
На 39 день измеряли массу тела. Массу печени, сердца, селезенки и почек измеряли по окончании исследования на 42 день, и результаты представлены в следующей таблице. Результаты измерений массы органов выражены как соотношение к массе тела и нормализованы к соотношению контрольной группы с PBS.
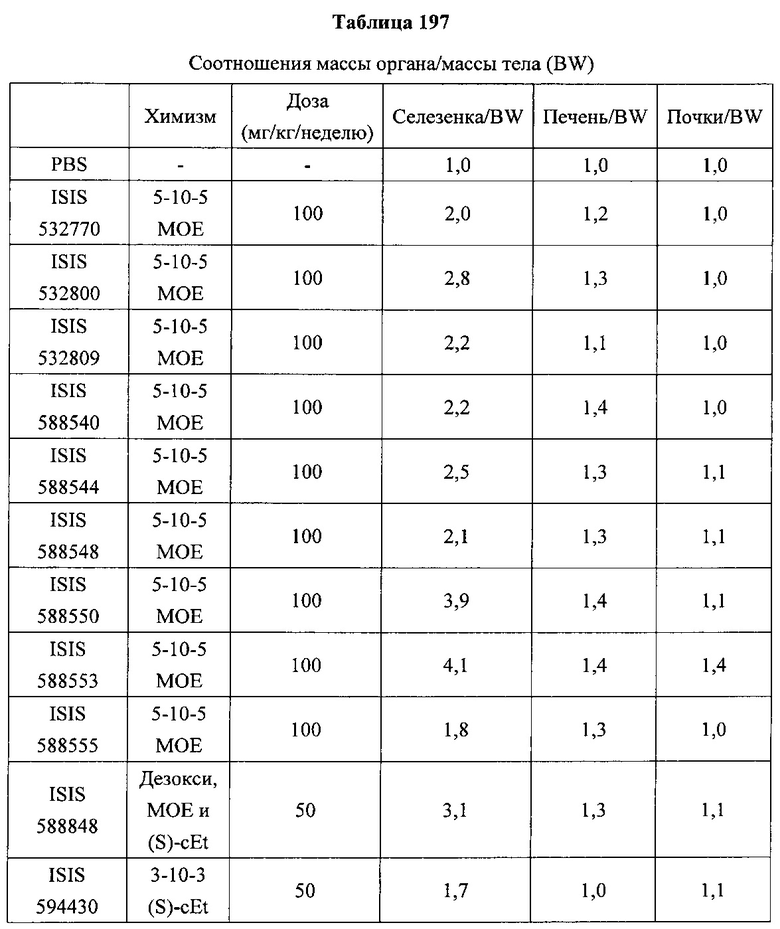
Пример 128: Эффективность антисмысловых олигонуклеотидов против мРНК CFB у мышей hCFB
Выбранные соединения были протестированы на эффективность у трансгенных мышей с человеческим CFB, линия-основатель №6. Ген человеческого CFB расположен на хромосоме 6: положение 31913721-31919861. Выбрали фосмиду (АВС14-50933200С23), содержащую последовательность CFB, для получения трансгенных мышей, экспрессирующих ген человеческого CFB. Использовали рестрикционные ферменты Cla I (31926612) и Age I (31926815) для получения фрагмента размером 22127 п.о., содержащего ген CFB, для пронуклеарной инъекции. ДНК подтвердили анализом рестрикционного фермента, используя Pvu I. Фрагмент ДНК размером 22127 п.о. инъецировали в эмбрионы C57BL/6NTac. Вывели 6 положительных основателей. Основатель №6 экспрессировали в мРНК CFB печени человека и скрестили с 3им поколением. Потомство 3его поколения мышей использовали для оценки влияния ASO человеческого CFB на восстановлением мРНК человеческого CFB.
Лечение
Группам по 3 крысы два раза в неделю в течение первой недели вводили подкожные инъекции 50 мг/кг олигонуклеотидов ISIS, затем один раз в неделю дозу 50 мг/кг олигонуклеотидов ISIS в течение еще трех недель. Одной контрольной группе из 4 мышей два раза в неделю в течение первой недели вводили подкожные инъекции PBS, затем один раз в неделю в течение дополнительных трех недель. Через сорок восемь часов после введения последней дозы мышей усыпили и собрали органы и плазму для дальнейших анализов.
Анализ РНК
По окончании периода введения доз выделили РНК из печени и почек для анализа ПЦР в реальном времени для определения уровней мРНК CFB. Уровни мРНК человеческого CFB измеряли с помощью набора человеческих праймерных зондов RTS3459. Уровни мРНК CFB нормализовали к RIBOGREEN®, а также к конститутивному гену, циклофилину. Результаты рассчитывали как процентное ингибирование экспрессии мРНК CFB по сравнению с контролем. Все антисмысловые олигонуклеотиды вызывали ингибирование уровней мРНК человеческого CFB в печени.
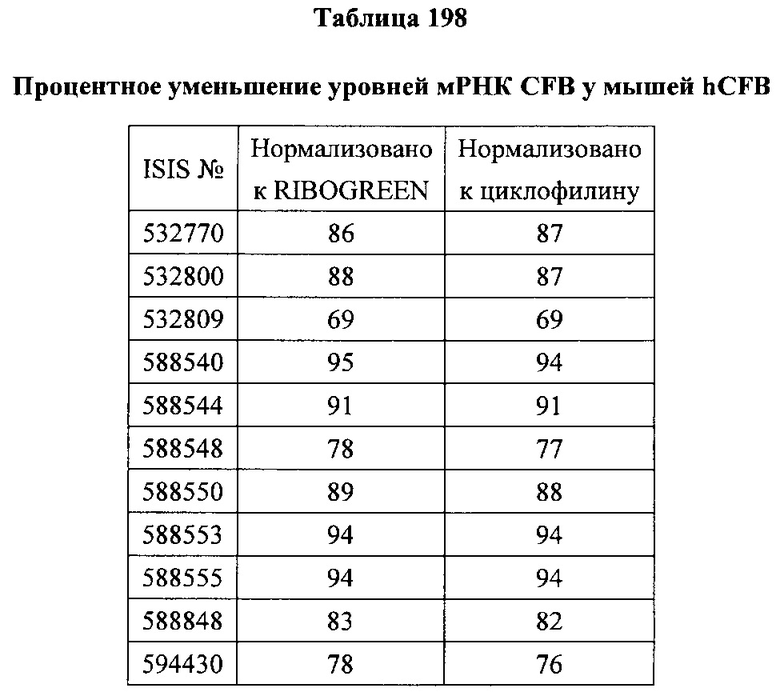
Пример 129: In vivo антисмысловое ингибирование мышиного CFB
Сконструировали несколько антисмысловых олигонуклеотидов, направленных на мРНК мышиного CFB (номер доступа GENBANK NM_008198.2, включенная в настоящий документ как SEQ ID NO: 5). Целевые сайты инициации и последовательности каждого олигонуклеотида описаны в представленных ниже таблицах. Химерные антисмысловые олигонуклеотиды в представленной ниже таблице сконструированы как 5-10-5 МОЕ гэпмеры. Гэпмеры имеют 20 нуклеозидов в длину, причем центральный гэп состоит из 10 2'-дезоксинуклеозидов и с обеих сторон (в направлениях 5' и 3') окружен крыльями, содержащими по 5 нуклеозидов каждое. Каждый нуклеозид 5' крыла и нуклеозид 3' крыла имеет 2'-МОЕ модификации. Межнуклеозидные связи в каждом гэпмере представляют собой тиофосфатные (P=S) связи. Все остатки цитозина в каждом гэпмере представляют собой 5-метилцитозины.

Лечение
Группам по четыре мыши C57BL/6 вводили подкожные инъекции 50 мг/кг ISIS 516269, ISIS 516272, ISIS 516323, ISIS 516330 или ISIS 516341, один раз в неделю в течение 3 недель. Контрольной группе мышей вводили инъекцию с фосфатно-солевым буферным раствором (PBS) один раз в неделю в течение 3 недель.
Анализ РНК CFB
По окончании исследования из печеночной ткани выделили РНК для анализа CFB с помощью ПЦР в реальном времени, используя набор праймерных зондов RTS3430 (прямая последовательность GGGCAAACAGCAATTTGTGA, обозначенная в настоящем документе как SEQ ID NO: 816; обратная последовательность TGGCTACCCACCTTCCTTGT, обозначенная в настоящем документе как SEQ ID NO: 817; последовательность зонда CTGGATACTGTCCCAATCCCGGTATTCCX, обозначенная в настоящем документе как SEQ ID NO: 818). Уровни мРНК нормализовали с помощью RIBOGREEN®. Как показано в представленной ниже таблице, некоторые антисмысловые олигонуклеотиды обеспечивали снижение мышиного CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
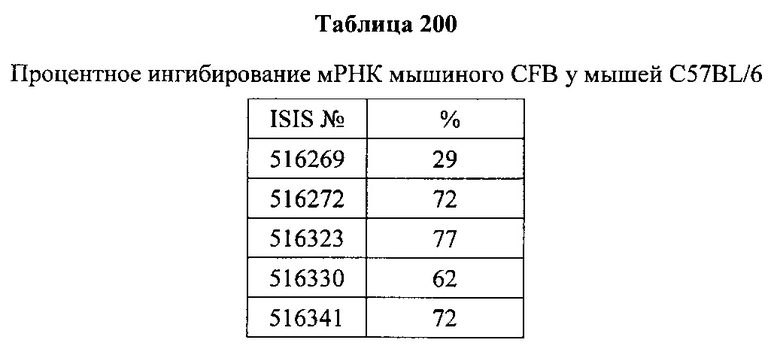
Анализ белка
Уровни белка CFB измеряли в почках, печени, плазме и глазах с помощью вестерн-блоттинга, используя козье анти-CFB антитело (Sigma-Aldrich). Результаты представлены как процент ингибирования CFB относительно контрольного образца с PBS. «н.д.» означает, что для указанного образца измерения не проводили. Как показано в представленной ниже таблице, антисмысловое ингибирование CFB олигонуклеотидами ISIS приводит к снижению белка CFB в различных тканях. Как показано в представленной ниже таблице, системное введение олигонуклеотидов ISIS эффективно для снижения уровней CFB в глазах.
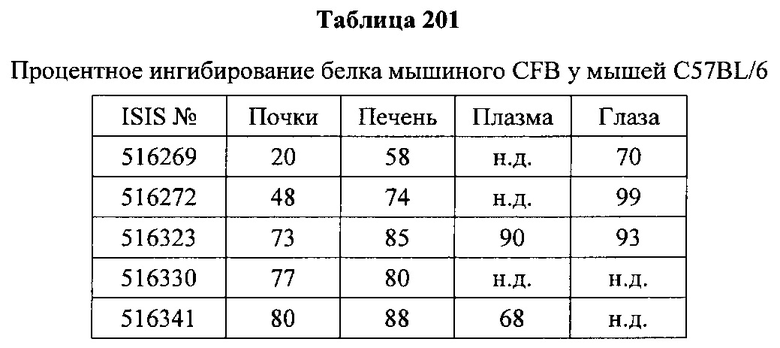
Пример 130: Дозозависимое антисмысловое ингибирование мышиного CFB
Группам по четыре крысы C57BL/6 один раз в неделю в течение 6 недель вводили инъекции 25 мг/кг, 50 мг/кг или 100 мг/кг ISIS 516272 и ISIS 516323. Другим двум группам мышей один раз в неделю в течение 6 недель вводили инъекции 100 мг/кг ISIS 516330 или ISIS 516341. Двум контрольным группам мышей один раз в неделю в течение 6 недель вводили инъекции фосфатно-солевого буферного раствора (PBS).
Анализ РНК CFB
Выделили РНК из тканей печени и почек для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Уровни мРНК нормализовали с помощью RIBOGREEN®. Как показано в представленной ниже таблице, антисмысловые олигонуклеотиды обеспечивали дозозависимое снижение мышиного CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
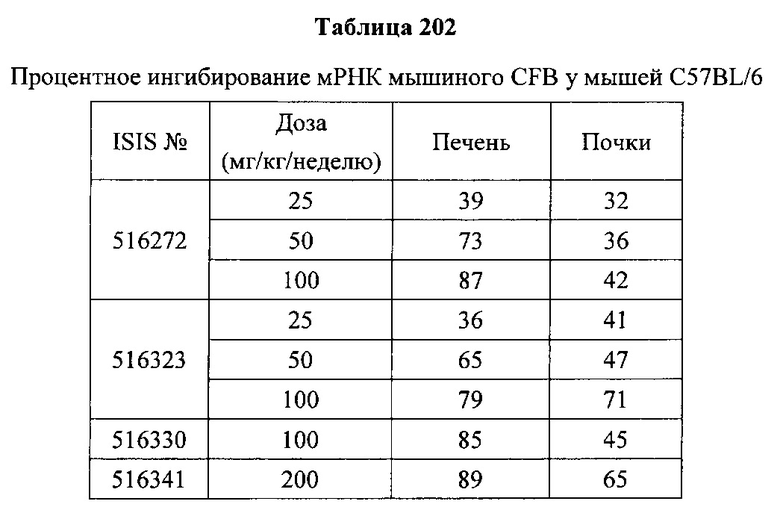
Анализ белка
Уровни белка CFB измеряли в плазме с помощью вестерн-блоттинга, используя козье анти-CFB антитело (Sigma-Aldrich). Как показано в представленной ниже таблице, антисмысловое ингибирование CFB олигонуклеотидами ISIS приводит к снижению белка CFB. Результаты представлены как процент ингибирования CFB относительно контрольного образца с PBS. «н.д.» означает, что для указанного образца измерения не проводили.
Уровни белка CFB в глазах также измеряли с помощью вестерн-блоттинга. Все экспериментальные группы демонстрировали ингибирование CFB на 95%, при этом значения некоторых образцов были ниже предела обнаружения анализа.
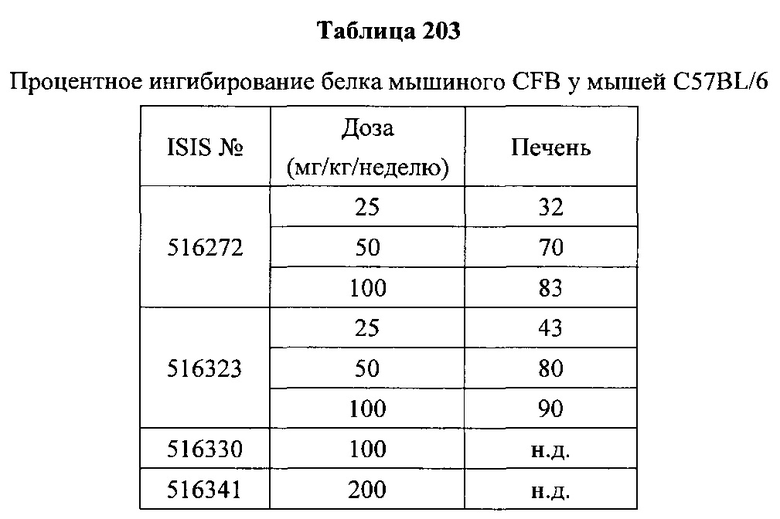
Пример 131: Влияние антисмыслового ингибирования CFB в мышиной модели NZB/W F1
NZB/W F1 представляет собой старейшую классическую модель волчанки, в которой у мышей развивается тяжелый волчаночный фенотип, сравнимый с фенотипом пациентов с волчанкой (Theofilopoulos, A.N. и Dixon, F.J. Advances in Immunology, т. 37, сс. 269-390, 1985). Такой волчаночный фенотип включает лимфаденопатию, спленомегалию, повышенное содержание антинуклеарных аутоантител в сыворотке (ANA), включая анти-дпДНК IgG, большинство из которых представляют собой IgG2a и IgG3, и иммунокомплексный гломерулонефрит (GN), который становится очевидным в возрасте 5-6 месяцев, что приводит к почечной недостаточности и гибели в возрасте 10-12 месяцев.
Испытание 1
Испытание проводили для демонстрации того, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, облегчает почечную патологию в мышиной модели. Самок мышей NZB/W F1 возрастом 17 недель приобрели у компании Jackson Laboratories. Группам из 16 мышей вводили дозы 100 мкг/кг/неделю ISIS 516272 или ISIS 516323 в течение 20 недель. Другой группе из 16 мышей вводили дозы 100 мкг/кг/неделю контрольного олигонуклеотида ISIS 141923 в течение 20 недель. Другой группе из 10 мышей вводили дозы PBS в течение 20 недель и использовали в качестве контрольной группы, с которой сравнивали все остальные группы. Конечные значения получили через 48 часов после инъекции последней дозы.
Анализ РНК CFB
Выделили РНК из тканей печени и почек для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Уровни мРНК нормализовали с помощью RIBOGREEN®. Как показано в представленной ниже таблице, некоторые антисмысловые олигонуклеотиды обеспечивали снижение мышиного CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
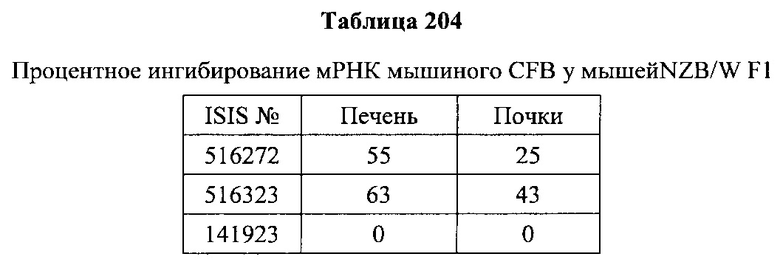
Протеинурия
Протеинурия ожидается у 60% животных в указанной мышиной модели. Кумулятивную частоту случаев возникновения тяжелой протеинурии измеряли расчетом соотношения общего белка к креатинину, используя клинический анализатор. Результаты представлены в следующей таблице и демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, обеспечивает снижение протеинурии у мышей, по сравнению с контрольной группой с PBS и мышами, обработанными контрольным олигонуклеотидом.
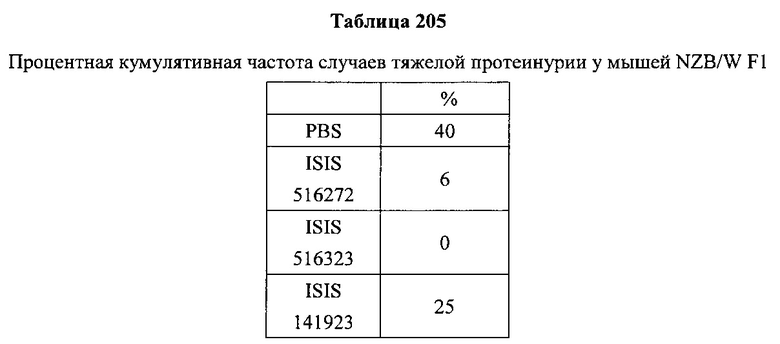
Выживаемость
Выживаемость мышей контролировали, подсчитывая количество мышей в начале лечения, затем на 20 неделе. Результаты представлены в следующей таблице и демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, увеличивает выживаемость мышей, по сравнению с контрольной группой с PBS и мышами, обработанными контрольным олигонуклеотидом.
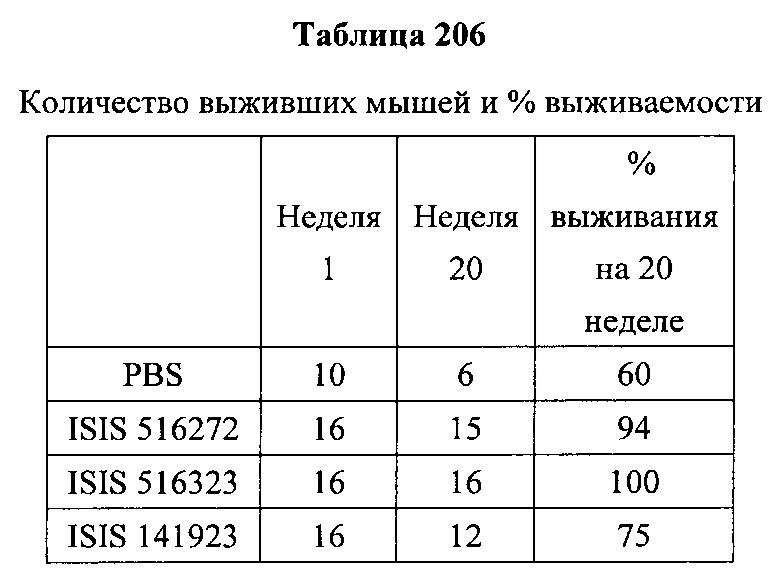
Гломерулярное отложение
Количество отложения С3, а также отложения IgG в гломерулах почек измеряли посредством иммуногистохимии с анти-С3 антителом. Результаты представлены в следующей таблице и демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, обеспечивает снижение отложений С3 и IgG в гломерулах почек, по сравнению с контрольным образцом с PBS и мышами, обработанными контрольным олигонуклеотидом.
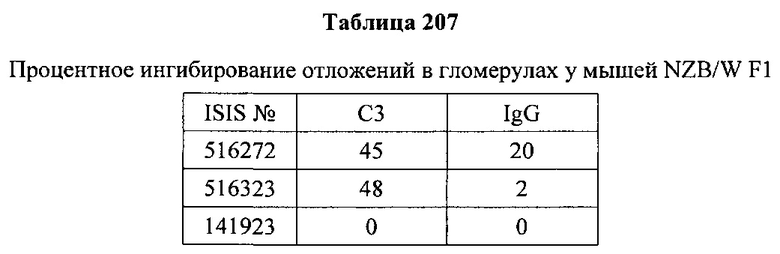
Испытание 2
Самок мышей NZB/W F1 возрастом 16 недель приобрели у компании Jackson Laboratories. Группе из 10 мышей вводили дозы 100 мкг/кг/неделю ISIS 516323 в течение 12 недель. Другой группе из 10 мышей вводили дозы 100 мкг/кг/неделю контрольного олигонуклеотида ISIS 141923 в течение 12 недель. Другой группе из 10 мышей вводили дозы PBS в течение 12 недель и использовали в качестве контрольной группы, с которой сравнивали все остальные группы. Конечные значения получили через 48 часов после инъекции последней дозы.
Анализ РНК CFB
Выделили РНК из тканей печени и почек для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Как показано в представленной ниже таблице, лечение с ISIS 516323 обеспечивает снижение мышиного CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.


Протеинурия
Кумулятивную частоту возникновения тяжелой протеинурии оценивали путем измерения соотношения общего белка в моче к креатинину, а также путем измерения общего уровня микроальбумина. Результаты представлены в следующих таблицах и демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, снижает протеинурии у мышей, по сравнению с контрольным образцом с PBS и мышами, обработанными контрольным олигонуклеотидом.
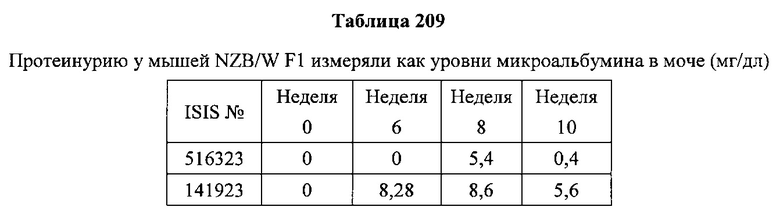
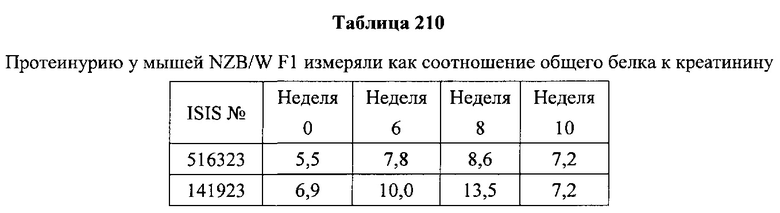
Выживаемость
Выживаемость мышей контролировали путем подсчета количества мышей в начале лечения, а затем на 12 неделе. Результаты представлены в следующей таблице и демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, увеличивает выживаемость мышей, по сравнению с контрольной группой с PBS и мышами, обработанными контрольным олигонуклеотидом.
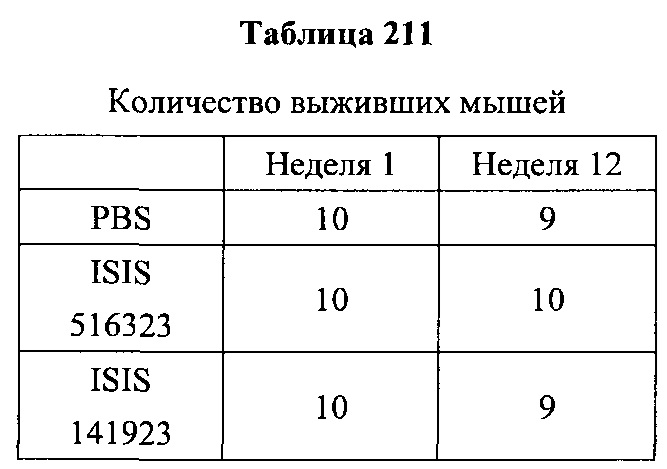
Пример 132: Влияние антисмыслового ингибирования CFB в мышиной модели MRL
В мышиной модели волчаночного нефрита MRL/lpr развивается волчаночный фенотип, характеризующийся лимфаденопатией в результате накопления двойных отрицательных (CD4- CD8-) и B220+ Т-клеток. Указанные мыши демонстрируют ускоренную смертность. Кроме того, мыши имеют более высокие концентрации циркулирующих иммуноглобулинов, включая повышенные уровни аутоантител, таких как ANA, анти-оцДНК, анти-дцДНК, анти-Sm и ревматоидные факторы, что приводит к большому количеству иммунных комплексов (Andrews, В. et al., J. Exp. Med. 148: 1198-1215, 1978).
Лечение
Проводили испытание для изучения того, вызывает ли лечение антисмысловыми олигонуклеотидами, направленными на CFB, регресс почечной патологии в мышиной модели. Самок мышей MRL/lpr возрастом 14 недель приобрели у компании Jackson Laboratories. Группе из 10 мышей вводили дозы 50 мкг/кг/неделю ISIS 516323 в течение 7 недель. Другой группе из 10 мышей вводили дозы 50 мкг/кг/неделю контрольного олигонуклеотида ISIS 141923 в течение 7 недель. Другой группе из 10 мышей вводили дозы PBS в течение 7 недель и использовали в качестве контрольной группы, с которой сравнивали все остальные группы. Конечные значения получили через 48 часов после инъекции последней дозы.
Анализ РНК CFB
Выделили РНК из тканей печени для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Как показано в представленной ниже таблице, ISIS 516323 обеспечивает снижение CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
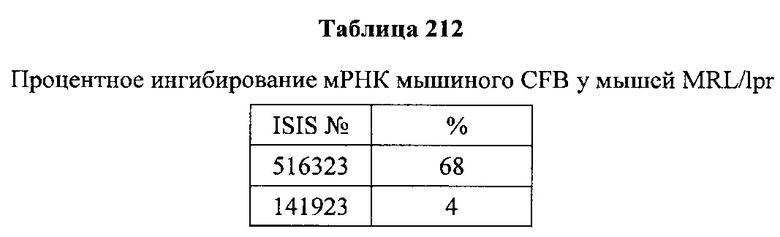
Почечная патология
Почечную патологию оценивали двумя способами. Гистологические срезы почек окрашивали гематоксилином и эозином. Контрольный образец с PBS демонстрировал наличие мультигломерулярных серповидных трубчатых цилиндров, что является симптомом гломерулосклероза. Напротив, срезы от мышей, обработанных ISIS 516323, демонстрировали отсутствие серповидных трубчатых цилиндров с минимальными фибротическими изменениями боуменовой капсулы, от умеренного до сильного расширение сегментарных мезангиальных клеток и утолщение гломерулярной базальной мембраны.
Накопление C3 в почках также оценивали с помощью иммуногистохимии с анти-C3 антителами. Иммуногистохимическую оценку интенсивности C3 в целой почке рассчитывали по балльной системе интенсивности, которую рассчитывали отбором 10 гломерул на почку и подсчетом интенсивности положительного окрашивания C3. Результаты представлены в следующей таблице и демонстрируют, что лечение с ISIS 516323 снижает накопление C3 в почках, по сравнению с контрольными группами.

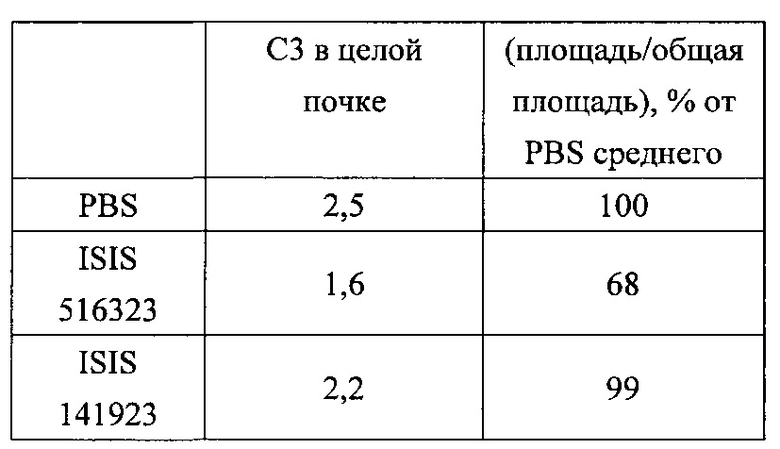
Уровни С3 в плазме
Снижение CFB ингибирует активацию альтернативного пути комплемента, препятствуя поглощению C3 и приводя к заметному повышению уровней C3 в плазме. Уровни C3 в плазме терминальной крови измеряли с помощью клинического анализатора. Результаты представлены в следующей таблице и демонстрируют, что лечение с ISIS 516323 повышает уровни C3 (р<0,001) в плазме, по сравнению с контрольными группами.
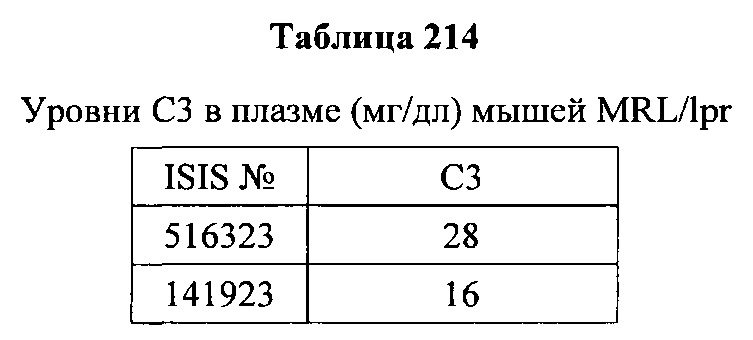
Результаты демонстрируют, что лечение антисмысловыми олигонуклеотидами, направленными на CFB, реверсирует почечную патологию в мышиной модели волчанки.
Пример 133: Влияние антисмыслового ингибирования CFB в мышиной модели CFH Het
CFH гетерозиготная (CFH Het, CFH+/-) мышиная модель экспрессирует мутантный белок фактора Н в комбинации с мышиным белком полной длины (Pickering, M.C. et al., J. Exp. Med. 2007. 204: 1249-56). Почечная гистология у этих мышей остается нормальной до шестимесячного возраста.
Испытание 1
Группам по 8 мышей CFH+/- возрастом 6 недель вводили дозы 75 мг/кг/неделю ISIS 516323 или ISIS 516341 в течение 6 недель. Другой группе из 8 мышей вводили дозы 75 мг/кг/неделю контрольного олигонуклеотида ISIS 141923 в течение 6 недель. Другой группе из 8 мышей вводили дозы PBS в течение 6 недель и использовали в качестве контрольной группы, с которой сравнивали все остальные группы. Конечные значения получили через 48 часов после инъекции последней дозы.
Анализ РНК CFB
Выделили РНК из тканей печени и почек для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Как показано в представленной ниже таблице, антисмысловые олигонуклеотиды обеспечивают снижение CFB по сравнению с контрольным образцом с PBS. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
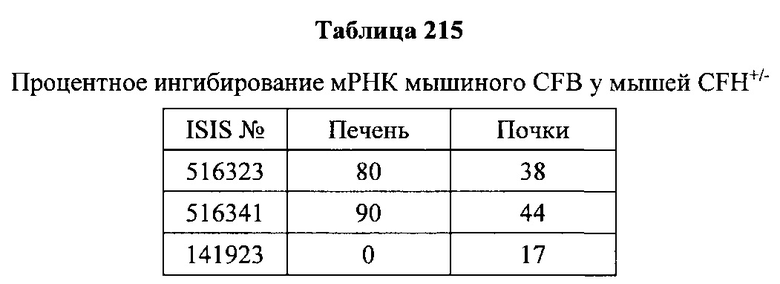
Уровни C3 в плазме
Снижение CFB ингибирует активацию альтернативного пути комплемента, препятствуя поглощению C3 и приводя к заметному повышению уровней C3 в плазме. Уровни C3 в плазме терминальной крови измеряли с помощью клинического анализатора. Результаты представлены в следующей таблице и демонстрируют, что лечение с ISIS 516323 повышает уровни C3 в плазме до нормальных уровней.


Испытание 2
Группам по 5 мышей CFH+/- вводили дозы 12,5 мг/кг/неделю, 25 мг/кг/неделю, 50 мг/кг/неделю, 75 мг/кг/неделю или 100 мг/кг/неделю ISIS 516323 или ISIS 516341 в течение 6 недель. Другой группе из 5 мышей вводили дозы 75 мкг/кг/неделю контрольного олигонуклеотида ISIS 141923 в течение 6 недель. Другой группе из 5 мышей вводили дозы PBS в течение 6 недель и использовали в качестве контрольной группы, с которой сравнивали все остальные группы. Конечные значения получили через 48 часов после инъекции последней дозы.
Анализ РНК CFB
Выделили РНК из тканей печени и почек для анализа CFB с помощью ПЦР в реальном времени с использованием набора праймерных зондов RTS3430. Как показано в представленной ниже таблице, антисмысловые олигонуклеотиды обеспечивают снижение CFB по сравнению с контрольным образцом с PBS дозозависимым образом. Результаты представлены как процент ингибирования CFB относительно контрольного образца.
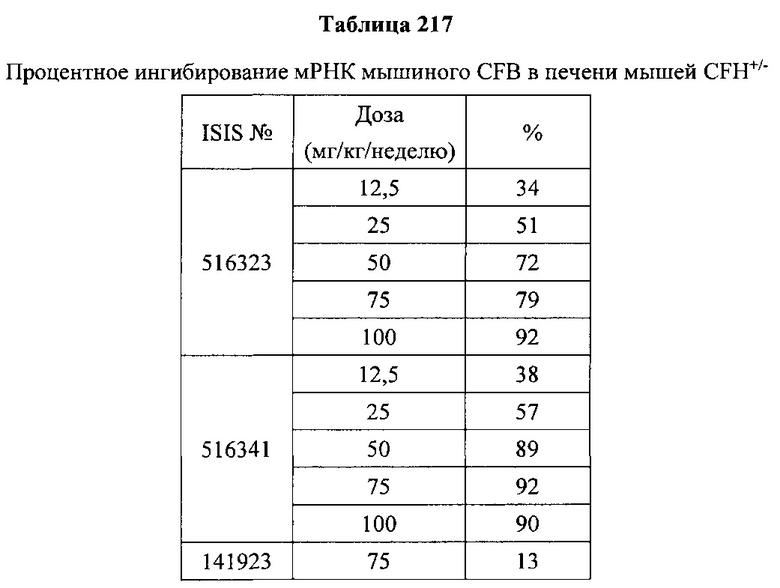
Уровни C3 в плазме
Снижение CFB ингибирует активацию альтернативного пути комплемента, препятствуя поглощению C3 и приводя к заметному повышению уровней C3 в плазме. Уровни C3 в плазме терминальной крови измеряли с помощью клинического анализатора. Результаты представлены в следующей таблице и демонстрируют, что лечение олигонуклеотидами ISIS, направленными на CFB, повышает уровни C3 в плазме.
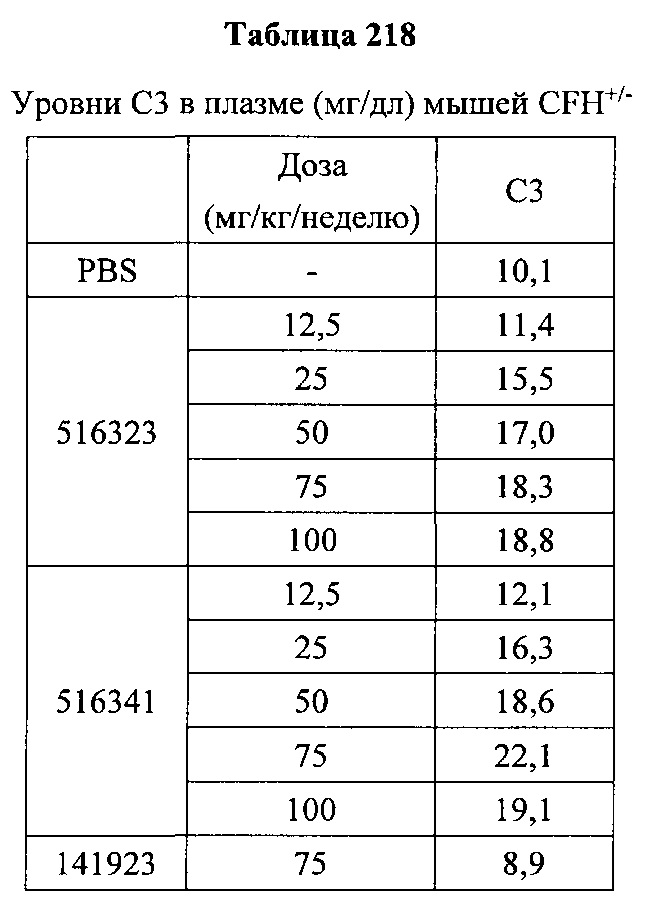
Пример 134: Влияние антисмысловых олигонуклеотидов ISIS, нпаравленных на CFB человека, у яванских макак
Яванских макак лечили антисмысловыми олигонуклеотидами ISIS, отобранными в исследованиях, описанных в представленных выше примерах. Оценивали эффективность и переносимость антисмысловых олигонуклеотидов, а также их фармакокинетический профиль в печени и почках.
Во время проведения испытаний геномная последовательность яванских макак отсутствовала в базе данных Национального центра биотехнологической информации (NCBI); поэтому перекрестная реактивность с последовательностью гена яванских макак не может быть подтверждена. Вместо этого последовательности антисмысловых олигонуклеотидов ISIS, использованные на яванских макаках, сравнивали с последовательностью резус-макак на предмет гомологии. Предполагается, что олигонуклеотиды ISIS с гомологией к последовательности резус-макак, являются также полностью перекрестно реактивными с последовательностью яванских макак. Испытанные человеческие антисмысловые олигонуклеотиды являются перекрестно реактивными с геномной последовательностью резуса (номер доступа GENBANK NW_001116486.1, усеченной по нуклеотидам с 536000 по 545000, обозначенной в настоящем документе как SEQ ID NO: 3). Чем выше комплементарность между человеческим олигонуклеотидом и последовательностью макаки резус, тем вероятнее, что человеческий олигонуклеотид может перекрестно реагировать с последовательностью макак резус. Сайты инициации и терминации каждого олигонуклеотида, направленного на SEQ ID NO: 3, представлены в следующей таблице. «Сайт инициации» обозначает самый крайний 5' нуклеозид, на который направлен гэпмер в последовательности гена резус-макаки. «Рассогласование» указывает на количество азотистых оснований в человеческом олигонуклеотиде, которые не соответствуют геномной последовательности резуса.
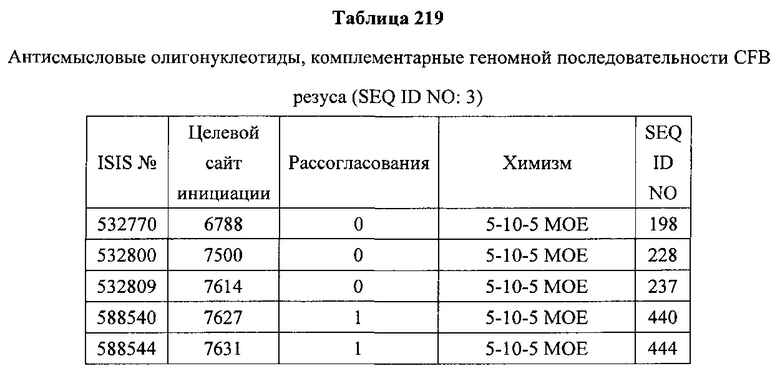

Лечение
Перед началом исследования обезьян выдерживали на карантине в течение по меньшей мере 30 дней, в течение которых ежедневно следили за общим состоянием здоровья животных. Возраст обезьян составлял 2-4 года, а масса от 2 до 4 кг. Одиннадцати группам по 4-6 случайным образом распределенных самцов яванских макак вводили подкожные инъекции олигонуклеотида ISIS или PBS в четырех местах на спине по часовой стрелке (т.е. слева, сверху, справа и снизу), по одному месту на дозу. Обезьянам вводили четыре насыщающие дозы PBS или 40 мг/кг ISIS 532800, ISIS 532809, ISIS 588540, ISIS 588544, ISIS 588548, ISIS 588550, ISIS 588553, ISIS 588555, ISIS 588848 или ISIS 594430 в течение первой недели (1, 3, 5 и 7 день), а затем вводили дозы один раз в неделю в течение 12 недель (14, 21, 28, 35, 42, 49, 56, 63, 70, 77 и 84 день) PBS или 40 мг/кг олигонуклеотидов ISIS. ISIS 532770 испытали в отдельном исследовании с аналогичными условиями на двух самцах и двух самках яванских макак в одной группе.
Снижение печеночной мишени
Анализ РНК
На 86 день собрали образцы печени и почек в двух экземплярах (примерно по 250 мг каждый) для анализа мРНК CFB. После вскрытия образцы быстро заморозили в жидком азоте в течение около 10 минут после усыпления.
Выделили РНК из тканей печени и почек для анализа экспрессии мРНК CFB с помощью ПЦР в реальном времени. Результаты представлены как процентное изменение мРНК относительно контрольного образца с PBS, нормализованное по RIBOGREEN®. Уровни РНК нормализовали также по конститутивному гену, циклофилину А. Уровни РНК измеряли с помощью наборов праймерных зондов RTS3459, описанных выше, или RTS4445_MGB (прямая последовательность CGAAGAAGCTCAGTGAAATCAA, обозначенная в настоящем документе как SEQ ID NO: 819; обратная последовательность TGCCTGGAGGGCCCTCTT, обозначенная в настоящем документе как SEQ ID NO: 820; последовательность зонда AGACCACAAGTTGAAGTC, обозначенная в настоящем документе как SEQ ID NO: 815).
Как показано в представленных ниже таблицах, лечение антисмысловыми олигонуклеотидами ISIS приводит к снижению мРНК CFB по сравнению с контрольным образцом с PBS. Анализ уровней мРНК CFB показал, что некоторые олигонуклеотиды ISIS снижают уровни CFB в печени и/или почках. «0» означает, что уровни экспрессии не были ингибированы. «*» означает, что олигонуклеотид испытывали в отдельном исследовании с аналогичными условиями.
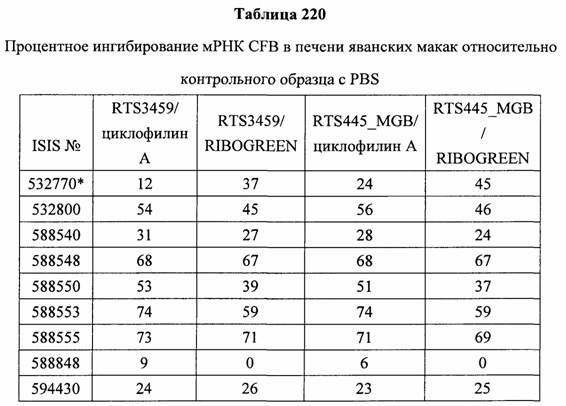

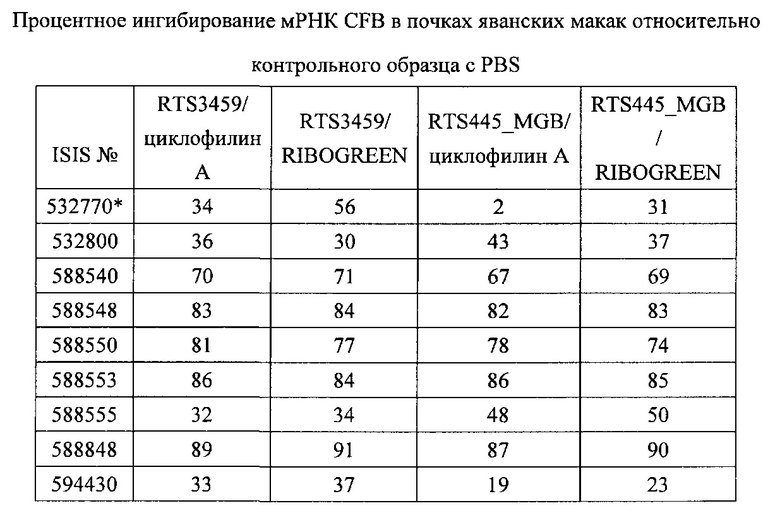
Анализ белка
Около 1 мл крови взяли у всех доступных животных на 85 день и поместили в пробирки, содержащие калиевую соль ЭДТК. Образцы крови сразу поместили на влажный лед или Kryorack и центрифугировали (3000 об./мин. в течение 10 минут при 4°С) с получением плазмы (0,4 мл) в течение 60 минут после сбора. Уровни CFB в плазме измеряли в плазме радиальной иммунодиффузией (RID), используя поликлональное антитело анти-фактор В. Результаты представлены ниже в таблице. ISIS 532770 испытали в отдельном исследовании, и в этой группе уровни белка в плазме измеряли на 91 или 92 день.
Анализ CFB в плазме показал, что некоторые олигонуклеотиды ISIS устойчиво снижают уровни белка. ISIS 532770, который испытывали в отдельном исследовании, обеспечил снижение белка CFB на 91/92 день на 50% относительно исходных значений. Снижение уровней белка CFB в плазме хорошо коррелирует со снижением уровней мРНК CFB в печени в соответствующих группах животных.

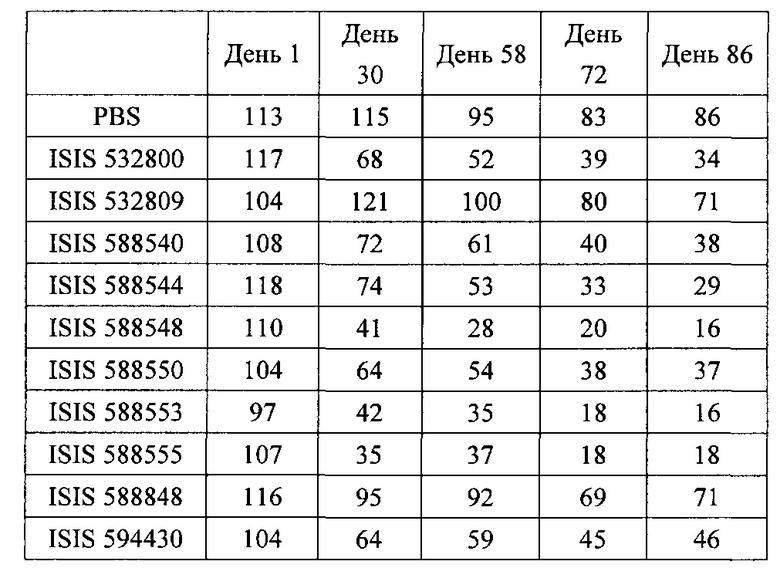
Исследования переносимости
Измерения массы тела
Для оценки влияния олигонуклеотидов ISIS на общее состояние здоровья животных измеряли массу тела и органов, и результаты представлены в следующей таблице. «*» означает, что олигонуклеотид испытывали в отдельном исследовании с аналогичными условиями, и значение является средним для измерений у самцов и самок обезьян. Результаты демонстрируют, что влияние лечения антисмысловыми олигонуклеотидами на массу тела и органов находится в пределах ожидаемого диапазона для антисмысловых олигонуклеотидов.
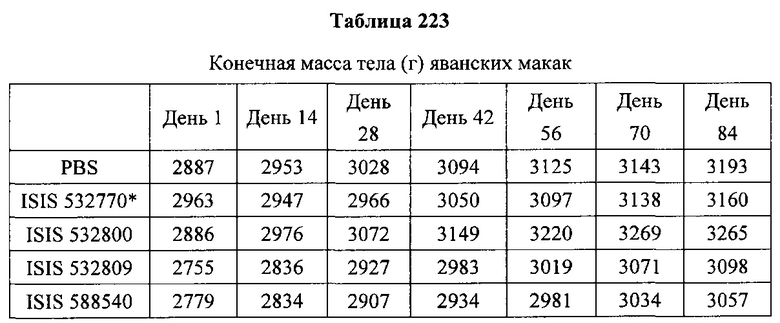
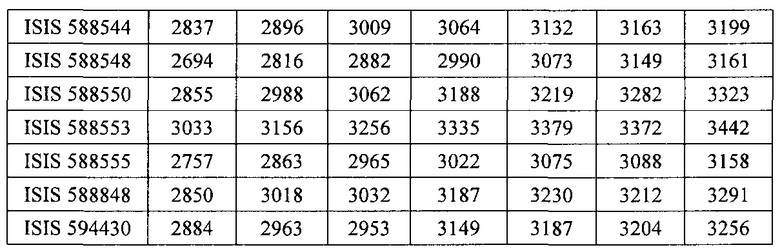
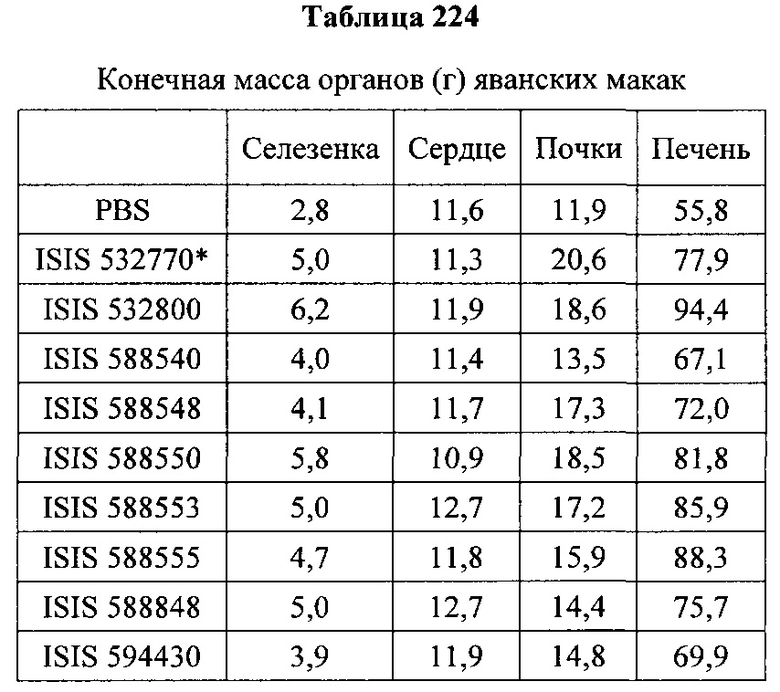
Функция печени
Для оценки влияния олигонуклеотидов ISIS на функцию печени из всех экспериментальных групп взяли образцы крови. Образцы крови брали из головной, подкожной или бедренной вены через 48 часов после введения дозы. Обезьяны не принимали пищу в течение ночи до сбора крови. Кровь (1,5 мл) собирали в пробирки без антикоагулянта для отделения сыворотки. Пробирки выдерживали при комнатной температуре в течение не менее 90 минут, а затем центрифугировали (около 3000 об./мин. в течение 10 минут) для получения сыворотки. Уровни различных маркеров функции печени измеряли с помощью анализатора химического состава Toshiba 200FR NEO (Toshiba Co., Япония).
Измеряли уровни ALT и AST в плазме, и результаты, выраженные в МЕ/л, представлены в следующей таблице. Таким же образом измеряли билирубин, маркер функции печени, и результаты, выраженные в мг/дл, представлены в следующей таблице. «*» означает, что олигонуклеотид испытывали в отдельном исследовании с аналогичными условиями, и значение является средним для измерений у самцов и самок обезьян. Результаты демонстрируют, что большинство антисмысловых олигонуклеотидов не оказывают воздействия на функцию печени, выходящего за пределы ожидаемого диапазона для антисмысловых олигонуклеотидов.
Функция почек
Для оценки влияния олигонуклеотидов ISIS на функцию почек из всех экспериментальных групп взяли образцы крови. Образцы крови брали из головной, подкожной или бедренной вены через 48 часов после введения дозы. Обезьяны не принимали пищу в течение ночи до сбора крови. Кровь собирали в пробирки без антикоагулянта для отделения сыворотки. Пробирки выдерживали при комнатной температуре в течение не менее 90 минут, а затем центрифугировали (около 3000 об./мин. в течение 10 минут) для получения сыворотки. Уровни АМК и креатинина измеряли с помощью анализатора химического состава Toshiba 200FR NEO (Toshiba Co., Япония). Результаты, выраженные в мг/дл, представлены в следующей таблице. «*» означает, что олигонуклеотид испытывали в отдельном исследовании с аналогичными условиями, и значение является средним для измерений у самцов и самок обезьян.
Для анализа мочи свежую мочу всех животных собирали утром, используя чистый лоток для клетки на мокром льду. За день до сбора мочи животным в течение ночи не давали пищу, оставив только воду. Образцы мочи (около 1 мл) анализировали на соотношение белка к креатинину (Р/С) с помощью автоматизированного анализатора химического состава Toshiba 200FR NEO (Toshiba Co., Япония), «н.д.» означает, что уровень белка в моче ниже предела обнаружения анализатора.
Данные химического анализа плазмы и мочи показывают, что большинство олигонуклеотидов ISIS не оказывало какого-либо влияния на почечную функцию за пределами ожидаемого для антисмысловых олигонуклеотидов диапазона.
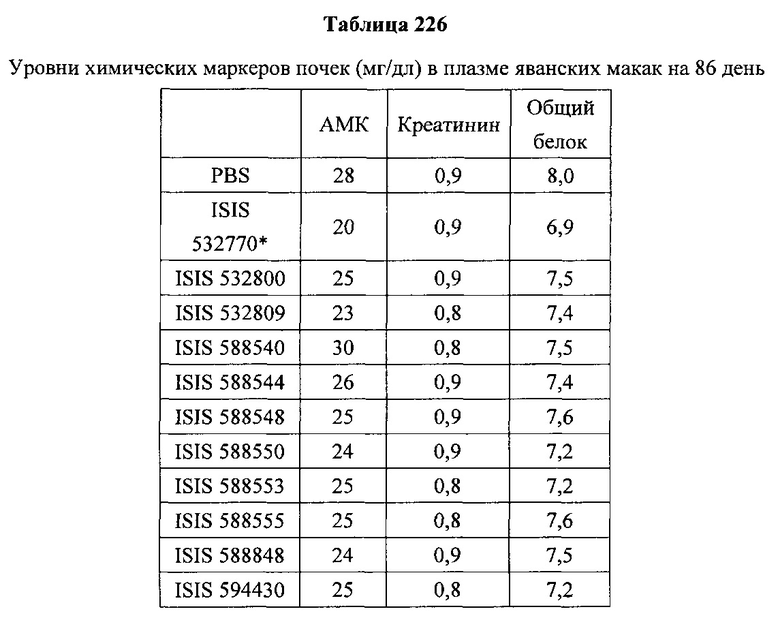
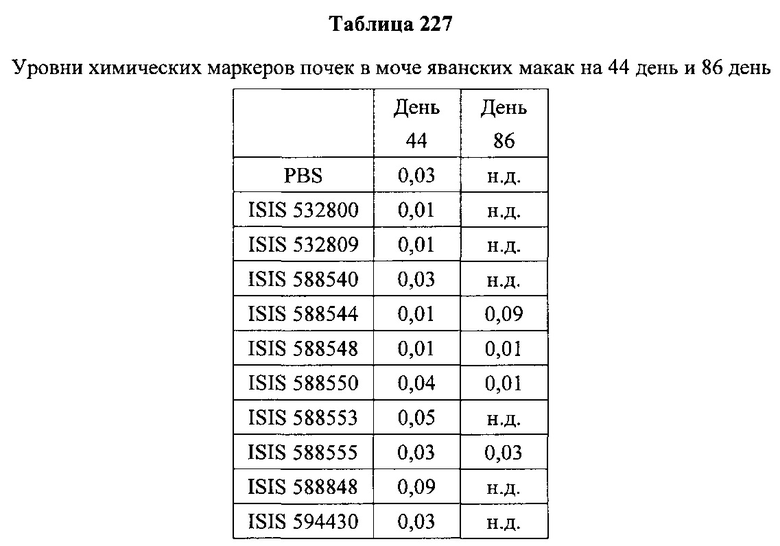
Гематология
Чтобы оценить влияние олигонуклеотидов ISIS на гематологические параметры яванских макак, образцы крови объемом около 0,5 мл крови отбирали у каждого из доступных экспериментальных животных в пробирки, содержащие K2-ЭДТА. Образцы анализировали на содержание красных кровяных телец (RBC), содержание белых кровяных телец (WBC), количество отдельных белых кровяных телец, таких как моноциты, нейтрофилы, лимфоциты, а также на количество тромбоцитов, содержание гемоглобина и гематокрита, используя анализатор гематологии ADVIA120 (Вауеr, США). Данные представлены в следующих таблицах. «*» означает, что олигонуклеотид испытывали в отдельном исследовании с аналогичными условиями, и значение является средним для измерений у самцов и самок обезьян.
Данные показывают, что олигонуклеотиды не вызывали каких-либо изменений гематологических параметров за пределами ожидаемого для антисмысловых олигонуклеотидов диапазона.

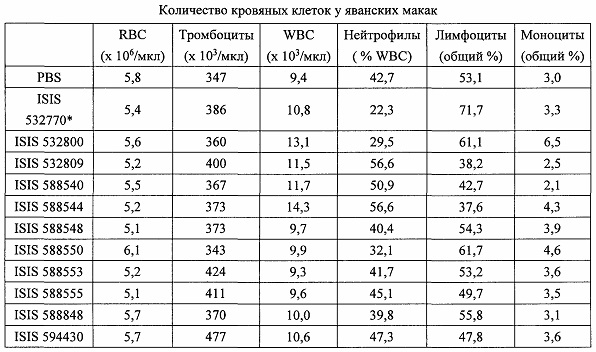
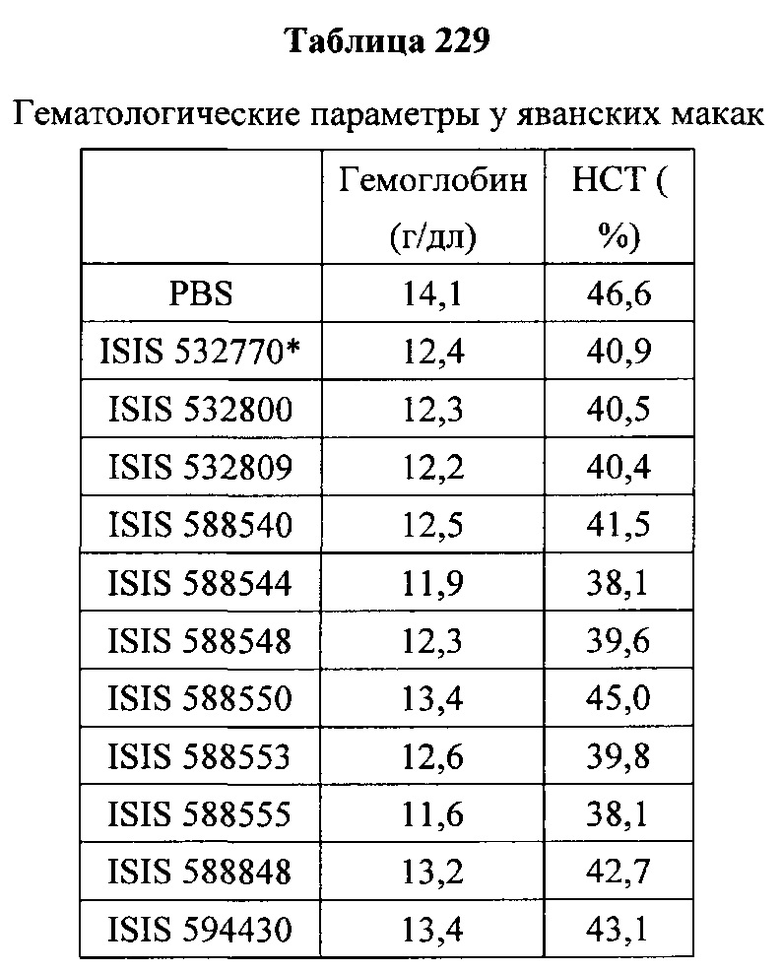
Измерение концентрации олигонуклеотида
Концентрацию олигонуклеотида полной длины измеряли в тканях почек и печени. Использованные способы представляют собой модификацию ранее опубликованных способов (Leeds et al., 1996; Geary et al., 1999), которые состоят из экстракции фенолом-хлороформом (жидкость-жидкость) с последующей твердофазной экстракцией. Концентрации в образце ткани рассчитывали с помощью калибровочных кривых, где нижний предел количественного обнаружения (LLOQ) составляет около 1,14 мкг/г. Результаты, выраженные в мкг/г ткани печени или почек, представлены в следующей таблице.
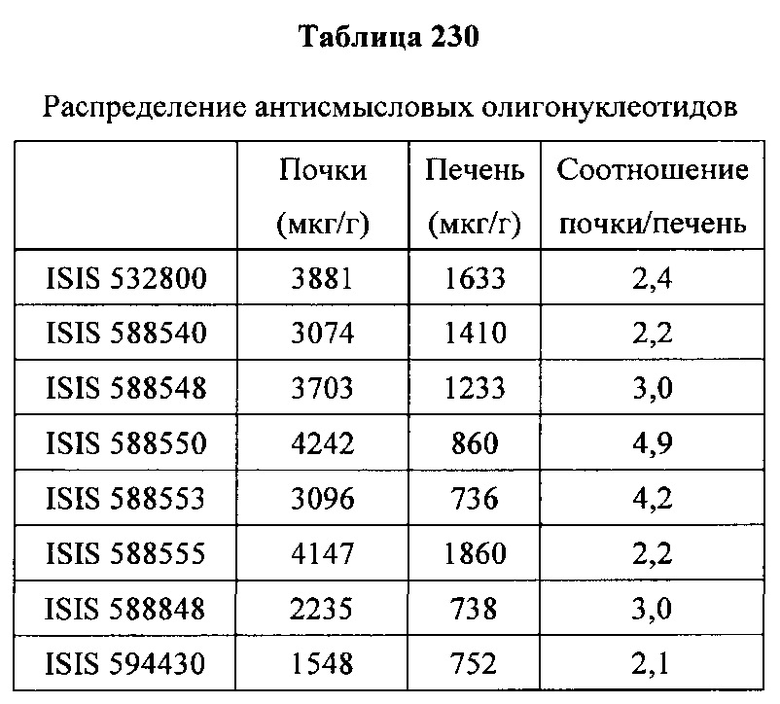
Пример 135: 6-Недельное испытание эффективности несопряженных и 5'-THA-GalNAc3 сопряженных антисмысловых олигонуклеотидов, направленных на человеческий CFB, у трансгенных мышей
Два антисмысловых олигонуклеотида, имеющих одинаковую последовательность азотистых оснований: несопряженный антисмысловый олигонуклеотид ISIS 588540 и 5'-THA-GalNAc3-сопряженный антисмысловый олигонуклеотид ISIS 696844, испытывали у трансгенных мышей с человеческим CFB (hCFB-Tg мыши).
Мышам подкожно вводили ISIS 696844 в дозах 0,1, 1,25, 0,5, 2,0, 6,0 или 12,0 мг/кг/неделю или ISIS 588540 в дозах 2, 6, 12, 25 или 50 мг/кг/неделю в течение 6 недель. Контрольной группе мышей подкожно вводили PBS в течение 6 недель. Мышей усыпили через 48 часов после введения последней дозы. Уровни мРНК в печени анализировали с помощью количественной ПЦР в реальном времени.
Испытание 1
Результаты представлены в следующей таблице и демонстрируют, что 5'-THA-GalNAc3-сопряженный антисмысловый олигонуклеотид, направленный на CFB, более эффективен, чем несопряженный антисмысловый олигонуклеотид с такой же последовательностью.

Испытание 2
Уровни мРНК в печени измеряли с двумя различными наборами праймерных зондов, направленными на разные области мРНК, и нормализовали по RIBOGREEN® (RGB) или циклофилину. Наборы праймерных зондов представляли собой RTS3459, описанный выше, и RTS3460 (прямая последовательность CGAAGCAGCTCAATGAAATCAA, обозначенная в настоящем документе как SEQ ID NO: 813; обратная последовательность TGCCTGGAGGGCCTTCTT, обозначенная в настоящем документе как SEQ ID NO: 814; последовательность зонда AGACCACAAGTTGAAGTC, обозначенная в настоящем документе как SEQ ID NO: 815). Результаты представлены в следующей таблице и демонстрируют, что 5'-ТНА-GalNAc3-сопряженный антиемысловый олигонуклеотид, направленный на CFB, более эффективен, чем несопряженный антисмысловый олигонуклеотид с такой же последовательностью, независимо от используемого набора праймерных зондов.
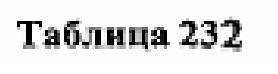
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯТОРЫ ФАКТОРА В КОМПЛЕМЕНТА | 2014 |
|
RU2662967C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ HBV И TTR | 2014 |
|
RU2670614C9 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ ПКП | 2015 |
|
RU2703411C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ HBV И TTR | 2014 |
|
RU2782034C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА (A) | 2014 |
|
RU2824214C1 |
| КОМПОЗИЦИИ И СПОСОБЫ | 2014 |
|
RU2686080C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА C-III | 2014 |
|
RU2650510C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА (А) | 2014 |
|
RU2699985C2 |
| СОПРЯЖЕННЫЕ АНТИСМЫСЛОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2697152C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АНГИОПОЭТИН-ПОДОБНОГО БЕЛКА 3 | 2015 |
|
RU2734658C2 |
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая соединение для ингибирования экспрессии фактора комплемента В (CFB) (варианты), фармацевтическую композицию для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, способ лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, применение вышеуказанного соединения или композиции для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента, применение вышеуказанного соединения или композиции при изготовлении лекарственного средства для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента. В одном из вариантов реализации соединение содержит модифицированный олигонуклеотид и группу конъюгата. Изобретение расширяет арсенал средств для ингибирования экспрессии фактора комплемента В (CFB). 10 н. и 32 з.п. ф-лы, 232 табл., 135 пр.
1. Соединение для ингибирования экспрессии фактора комплемента В (CFB), содержащее модифицированный олигонуклеотид и группу конъюгата, причем модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 440, 198, 228, 237, 444, 448, 450, 453, 455, 549, 598, 6-197, 199-227, 229-236, 238-439, 441-443, 445-447, 449, 451, 452, 454, 456-548, 550-597 или 599-808, и где группа конъюгата включает:
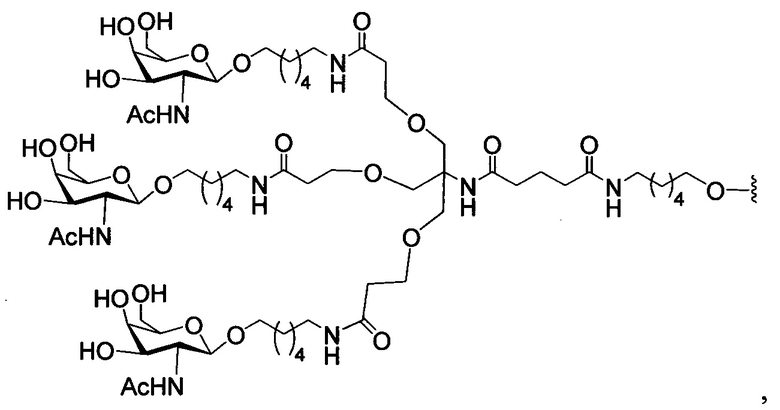
при этом модифицированный олигонуклеотид содержит модифицированный сахар, модифицированное азотистое основание и/или модифицированную межнуклеозидную связь,
при этом группа конъюгата связана с модифицированным олигонуклеотидом:
a) на 5' конце модифицированного олигонуклеотида; или
b) на 3' конце модифицированного олигонуклеотида.
2. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую:
a) по меньшей мере 9 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808;
b) по меньшей мере 10 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808;
c) по меньшей мере 11 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808; или
d) по меньшей мере 12 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 6-808.
3. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую последовательность азотистых оснований любой из SEQ ID NO: 6-808.
4. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из последовательности азотистых оснований любой из SEQ ID NO: 6-808.
5. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую часть из по меньшей мере 8 азотистых оснований любой из SEQ ID NO: 84, 238, 239, 317, 412, 413, 420, 421, 426, 434, 436, 437, 438, 439, 440, 442, 443, 444, 445, 446, 448, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 464, 465, 472, 473, 514, 515, 542, 543, 544, 545, 546, 551, 553, 555, 556, 599, 600, 601, 602, 610, 616, 617, 618, 662, 666, 670, 676, 677, 678, 688, 689, 713, 723, 729, 730, 740, 741, 742, 743, 744, 745, 746, 747, 748, 749, 755, 756, 768, 783, 793, 833 и 867.
6. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 10-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую любую из SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453, 455, 549 и 598, причем модифицированный олигонуклеотид имеет:
сегмент гэп, состоящий из связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из связанных нуклеозидов;
при этом сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла и, при этом каждый нуклеозид каждого сегмента крыла содержит модифицированный сахар.
7. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов и имеет последовательность азотистых оснований, состоящую из последовательности, указанной в SEQ ID NO: 198, 228, 237, 440, 444, 448, 450, 453 или 455, причем модифицированный олигонуклеотид имеет:
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов;
при этом сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла, причем каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтильный сахар; где каждая межнуклеозидная связь модифицированного олигонуклеотида представляет собой тиофосфатную связь, и где каждый цитозин представляет собой 5-метилцитозин.
8. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 16 связанных нуклеозидов и имеет последовательность азотистых оснований, состоящую из последовательности, указанной в SEQ ID NO: 598, причем модифицированный олигонуклеотид имеет:
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из трех связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из трех связанных нуклеозидов;
при этом сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла; где сегмент 5'-крыла содержит 2'-O-метоксиэтильный сахар, 2'-O-метоксиэтильный сахар и cEt сахар в направлении от 5' к 3'; где сегмент 3'-крыла содержит cEt сахар, cEt сахар и 2'-O-метоксиэтильный сахар в направлении от 5' к 3'; где каждая межнуклеозидная связь модифицированного олигонуклеотида представляет собой тиофосфатную связь; и где каждый цитозин представляет собой 5-метилцитозин.
9. Соединение по п. 1, отличающееся тем, что модифицированный олигонуклеотид состоит из 16 связанных нуклеозидов и имеет последовательность азотистых оснований, состоящую из последовательности, указанной в SEQ ID NO: 549, причем модифицированный олигонуклеотид имеет:
сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов;
сегмент 5'-крыла, состоящий из трех связанных нуклеозидов; и
сегмент 3'-крыла, состоящий из трех связанных нуклеозидов;
при этом сегмент гэп расположен между сегментом 5'-крыла и сегментом 3'-крыла; причем каждый нуклеозид каждого сегмента крыла содержит cEt сахар; где каждая межнуклеозидная связь модифицированного олигонуклеотида представляет собой тиофосфатную связь; и где каждый цитозин представляет собой 5-метилцитозин.
10. Соединение по любому из пп. 1-9, отличающееся тем, что олигонуклеотид по меньшей мере на 80%, 85%, 90%, 95% или 100% комплементарен SEQ ID NO: 1 или 2.
11. Соединение по пп. 1-10, отличающееся тем, что модифицированная межнуклеозидная связь представляет собой тиофосфатную межнуклеозидную связь.
12. Соединение по п. 11, отличающееся тем, что модифицированный олигонуклеотид содержит:
a) по меньшей мере 1 фосфодиэфирную межнуклеозидную связь;
b) по меньшей мере 2 фосфодиэфирные межнуклеозидные связи;
c) по меньшей мере 3 фосфодиэфирные межнуклеозидные связи;
d) по меньшей мере 4 фосфодиэфирные межнуклеозидные связи;
e) по меньшей мере 5 фосфодиэфирных межнуклеозидных связей;
f) по меньшей мере 6 фосфодиэфирных межнуклеозидных связей; или
g) по меньшей мере 7 фосфодиэфирных межнуклеозидных связей.
13. Соединение по п. 12, отличающееся тем, что каждая межнуклеозидная связь модифицированного олигонуклеотида выбрана из фосфодиэфирной межнуклеозидной связи и тиофосфатной межнуклеозидной связи.
14. Соединение по п. 11, отличающееся тем, что каждая межнуклеозидная связь модифицированного олигонуклеотида содержит тиофосфатную межнуклеозидную связь.
15. Соединение по любому из пп. 1-14, отличающееся тем, что модифицированный сахар представляет собой:
a) бициклический сахар, при этом необязательно бициклический сахар выбран из группы, состоящей из: 4'-(СН2)-O-2' (LNA); 4'-(СН2)2-O-2' (ENA) и 4'-СН(СН3)-O-2' (cEt); или
b) модифицированный сахар, который представляет собой 2'-O-метоксиэтил.
16. Соединение по любому из пп. 1-15, отличающееся тем, что модифицированное азотистое основание представляет собой 5-метилцитозин.
17. Соединение по любому из пп. 1-16, отличающееся тем, что модифицированный олигонуклеотид имеет:
(a) сегмент гэп, состоящий из связанных дезоксинуклеозидов;
(b) сегмент 5'-крыла, состоящий из связанных нуклеозидов; и
(c) сегмент 3'-крыла, состоящий из связанных нуклеозидов;
при этом сегмент гэп расположен непосредственно рядом и между сегментом 5' крыла и сегментом 3' крыла, и при этом каждый нуклеозид каждого сегмента крыла содержит модифицированный сахар.
18. Соединение по любому из пп. 1-17, отличающееся тем, что соединение является:
a) одноцепочечным; или
b) двухцепочечным.
19. Соединение по любому из пп. 1-18, отличающееся тем, что соединение содержит:
a) рибонуклеотиды; или
b) дезоксирибонуклеотиды.
20. Соединение по любому из пп. 1-19, отличающееся тем, что модифицированный олигонуклеотид:
a) состоит из 15-20 связанных нуклеозидов;
b) состоит из 12-30 связанных нуклеозидов; или
c) состоит из 15-30 связанных нуклеозидов.
21. Соединение для ингибирования экспрессии фактора комплемента В (CFB), характеризующееся формулой:
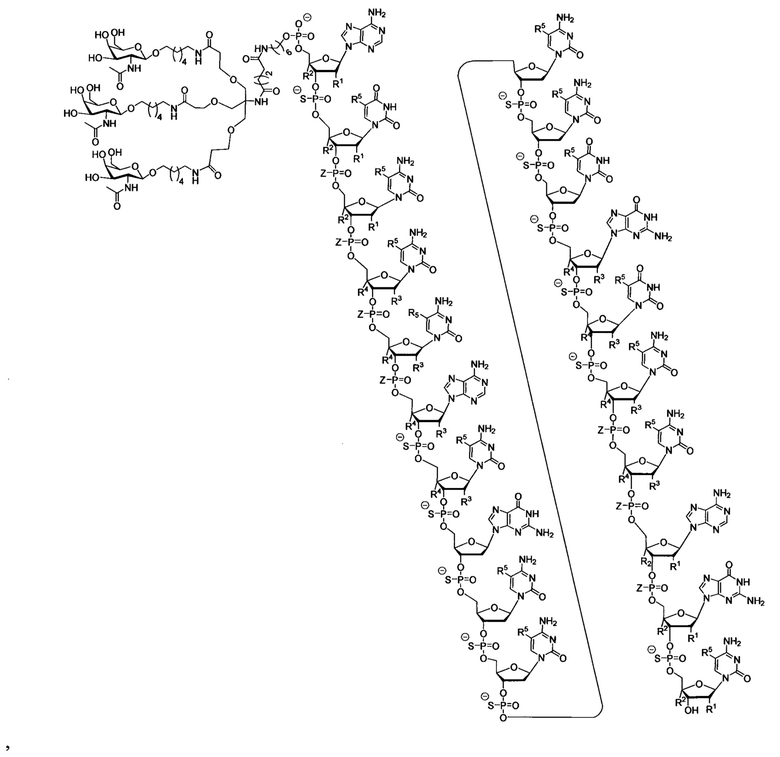
где каждый R1 представляет собой -ОСН2СН2ОСН3, и R2 представляет собой Н; или R1 и R2 вместе образуют мостик, где R1 представляет собой -О- и R2 представляет собой -CH2-, -СН(СН3)- или -СН2СН2-, и R1 и R2 напрямую связаны так, что полученный мостик выбран из: -O-СН2-, -О-СН(СН3)- и -О-СН2СН2-;
и для каждой пары R3 и R4 в одном кольце, независимо для каждого кольца: каждый R3 выбран из Н и -ОСН2СН2ОСН3 и R4 представляет собой Н; или R3 и R4 вместе образуют мостик, где R3 представляет собой -О-, и R4 представляет собой -СН2-, -СН(СН3)- или -СН2СН2-, и R3 и R4 напрямую соединены так, что полученный мостик выбран из: -О-СН2-, -О-СН(СН3)- и -О-СН2СН2-;
и R5 выбран из Н и -СН3;
и Z выбран из S- и О-.
22. Соединение для ингибирования экспрессии фактора комплемента В (CFB), характеризующееся формулой:
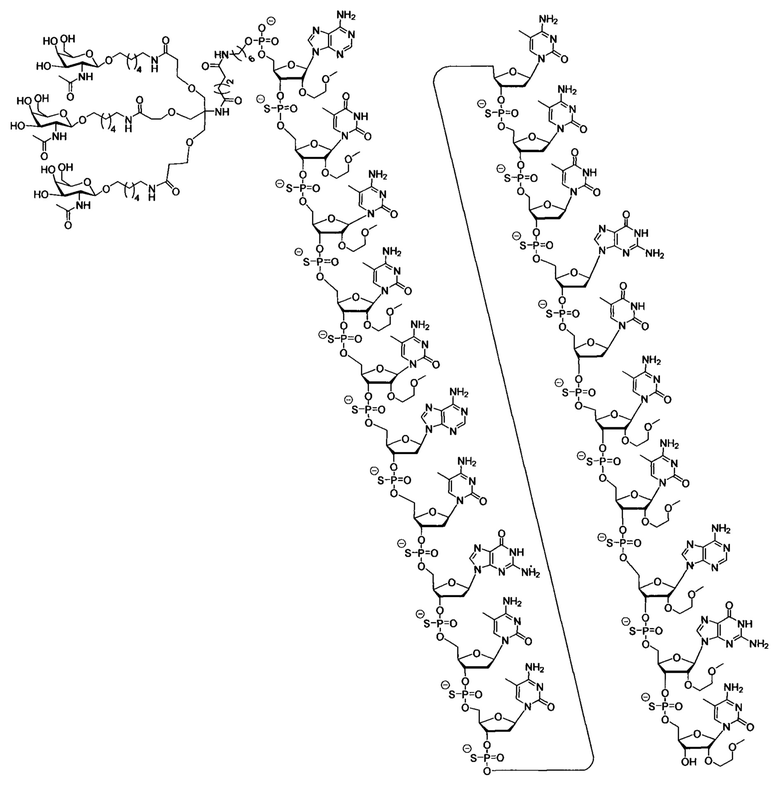
23. Соединение для ингибирования экспрессии фактора комплемента В (CFB), характеризующееся формулой:
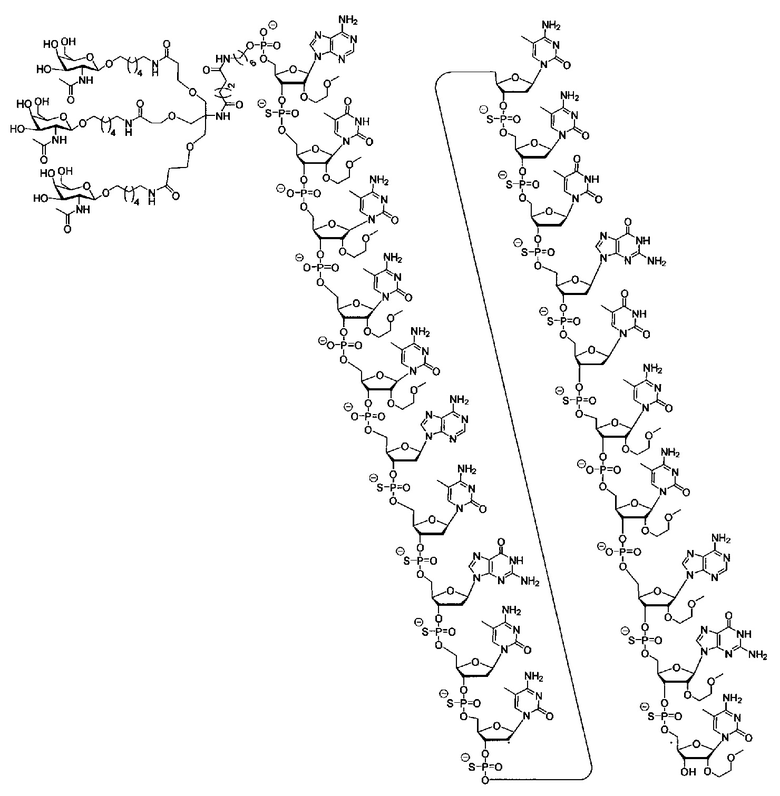
24. Соединение для ингибирования экспрессии фактора комплемента В (CFB), характеризующееся формулой:
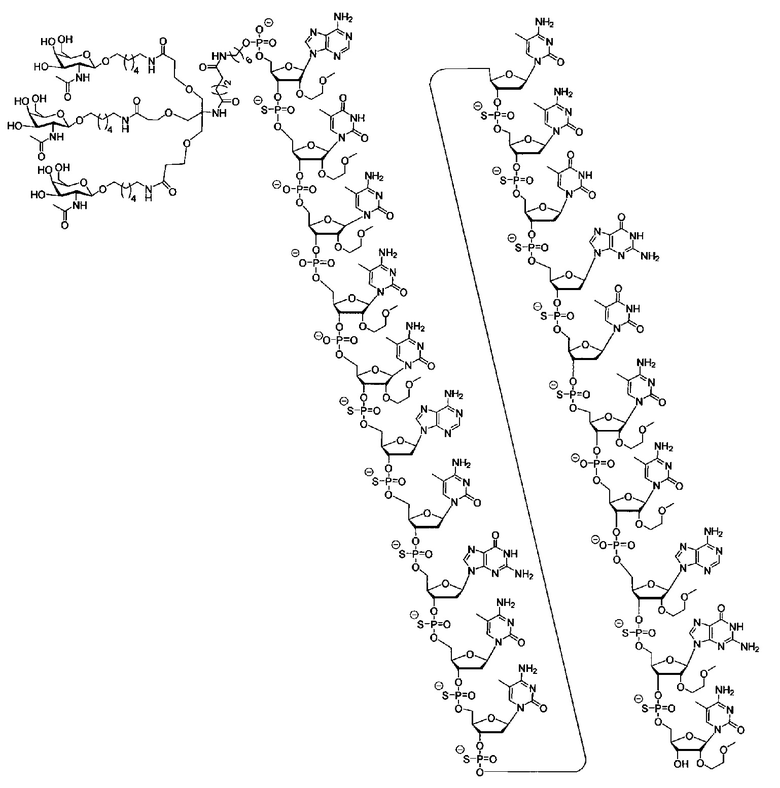
25. Соединение для ингибирования экспрессии фактора комплемента В (CFB), характеризующееся формулой:
26. Фармацевтическая композиция для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, содержащая терапевтически эффективное количество соединения по любому из пп. 1-25 или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель или разбавитель.
27. Способ лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента у субъекта, причем способ предусматривает введение субъекту соединения по любому из пп. 1-25 или композиции по п. 26, тем самым обеспечивая лечение заболевания.
28. Способ по п. 27, отличающийся тем, что заболевание представляет собой дегенерацию желтого пятна, возрастную дегенерацию желтого пятна (AMD), влажную AMD, сухую AMD или географическую атрофию.
29. Способ по п. 27, отличающийся тем, что заболевание представляет собой болезнь почек.
30. Способ по п. 29, отличающийся тем, что болезнь почек представляет собой волчаночный нефрит, системную красную волчанку (SLE), болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипичный гемолитико-уремический синдром (aHUS).
31. Применение соединения по любому из пп. 1-25 или композиции по п. 26 для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента.
32. Применение по п. 31, отличающееся тем, что заболевание представляет собой дегенерацию желтого пятна, возрастную дегенерацию желтого пятна (AMD), влажную AMD, сухую AMD или географическую атрофию.
33. Применение по п. 31, отличающееся тем, что заболевание представляет собой болезнь почек.
34. Применение по п. 33, отличающееся тем, что болезнь почек представляет собой волчаночный нефрит, болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипический гемолитико-уремический синдром (aHUS).
35. Соединение по любому из пп. 1-25 или композиция по п. 26 для применения в способе лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента.
36. Соединение или композиция для применения по п. 35, отличающиеся тем, что заболевание представляет собой дегенерацию желтого пятна, возрастную дегенерацию желтого пятна (AMD), влажную AMD, сухую AMD или географическую атрофию.
37. Соединение или композиция для применения по п. 35, отличающиеся тем, что заболевание представляет собой болезнь почек.
38. Соединение или композиция для применения по п. 37, отличающиеся тем, что болезнь почек представляет собой волчаночный нефрит, болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипический гемолитико-уремический синдром (aHUS).
39. Применение соединения по любому из пп. 1-25 или композиции по п. 26 при изготовлении лекарственного средства для лечения заболевания, связанного с дисрегуляцией альтернативного пути комплемента.
40. Применение соединения или композиции при изготовлении лекарственного средства по п. 39, отличающееся тем, что заболевание представляет собой дегенерацию желтого пятна, возрастную дегенерацию желтого пятна (AMD), влажную AMD, сухую AMD или географическую атрофию.
41. Применение соединения или композиции при изготовлении лекарственного средства по п. 39, отличающееся тем, что заболевание представляет собой болезнь почек.
42. Применение соединения или композиции при изготовлении лекарственного средства по п. 41, отличающееся тем, что болезнь почек представляет собой волчаночный нефрит, болезнь плотного осадка (DDD), С3 гломерулонефрит (C3GN), CFHR5 нефропатию или атипический гемолитико-уремический синдром (aHUS).
| US 20100093085 A1, 15.04.2010 | |||
| US 20020082227 A1, 27.06.2002 | |||
| НУКЛЕОЗИДЫ С МОДИФИЦИРОВАННЫМИ САХАРАМИ И ОЛИГОНУКЛЕОТИДЫ | 1995 |
|
RU2145964C1 |
| ОЛИГОНУКЛЕОТИДЫ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ EG5 ЧЕЛОВЕКА | 2000 |
|
RU2249458C2 |
| US 20040038274 A1, 26.02.2004. | |||
Авторы
Даты
2019-09-30—Публикация
2015-05-01—Подача