Изобретение относится к области иммунологии, биотехнологии и клинической лабораторной диагностики и может найти применение для определения индивидуальных рисков возникновения заболеваний, связанных с воздействием химических канцерогенов окружающей среды: злокачественных опухолей, врожденных пороков развития, аутоиммунных и других.
Известно достаточно много аналогичных решений, но все они на наш взгляд имеют те или иные недостатки. Все найденые нами аналоги разбираются ниже. В литературе и базах данных не описан количественный мультплексный способ определения антител к полициклическим ароматическим углеводоролам в биологических жидкостях с использованием рекомбинантных идиотипичеких и антиидиотипичеких человеческих антител, предлагаемый нами.
Одним из известных подходов к решению определения индивидуальных онкорисков является анализ антител, специфических к химическим канцерогенам, в биологических жидкостях человека. Ранее были обнаружены ассоциации антител к химическим канцерогенам с канцерогенной нагрузкой окружающей среды и с онкологическими заболеваниями (Galati R. et al., 2001; Pauk N. et al, 2013; Glushkov A. et al, 2016).
Однако эти известные исследования были выполнены с помощью качественных, либо полуколичественных методов иммуноферментного анализа антител с использованием конъюгатов химических канцерогенов и их метаболитов с ДНК или белком. Качественные методы не дают точной оценки специфической иммунной реакции организма на химические канцерогены, которая необходима для дальнейшей разработки перспективной стратегии иммунопрофилактики рака у человека с помощью антиканцерогенных вакцин (Silbart L. et al, 1999; De Buck S. and Mullerc C., 2005; Schellenberger M. et al, 2011). Кроме того, наличие канцерогенов или их метаболитов в составе аналитических тест-систем представляет собой угрозу здоровью для пользователей и исследователей.
Аналогами заявляемого изобретения являются способы количественного определения антител в биологических жидкостях человека (например, патенты РФ: G01N33/531, G01N33/68, G01N33/577, G01N33/53, CN108196061 (A), CN108226460 (A), CN107677810 (A); другие патенты: US8383350 (B1), WO2005108989 (A2), US5219730 (A), US4910131 (A), WO9901477 (A1), WO9006515 (A1), CN105785030 (A), CN105203750 (A), UA78419 (U)), основанных на использовании твердофазного иммуноферментного анализа, который является аналогом изобретения. Традиционный твердофазный иммуноферментный анализ включает связывание антигена с поверхностью микропланшета с последующим помещением биологической жидкости, содержащей антитела, на микропланшет, инкубирование, проведение цветной реакции и спектрофотометрическую оценку показателей цветной реакции. Для определения концентраций антител в биологических жидкостях используется калибровочная кривая – стандартный препарат антител соответствующей специфичности с известной концентрацией. Другой пример, использование твердофазного носителя – гранулированный аэросил (патент РФ SU1513403, дата публикации 07.10.1989, класс МПК G01N33/53), который обрабатывают эритроцитами барана, инкубируют с исследуемой сывороткой и затем десорбируют белок с поверхности аэросила. Затем определяют концентрацию белка, а количество специфических антител определяют по разнице между количеством белка в комплексе антиген-антитело и количеством белка сорбированных на эритроцитах барана.
Однако аналог (твердофазный иммуноферментный анализ) имеет свои недостатки, препятствующие его использованию в качестве количественного метода определения антител в биологических жидкостях:
1) воспроизводимость метода составляет около 30%;
2) невысокая чувствительность метода;
3) трудоемкость проведения анализа;
4) невозможность проведения мультиплексного анализа антител в одном образце исследуемой биологической жидкости.
Используя иммуноферментный анализ в патентах: US8383350 (B1), WO2005108989 (A2), US5219730 (A), US4910131 (A), WO9901477 (A1), WO9006515 (A1) было предложено использовать антиидиотипичекие антитела для детекции идиотипических антител в биологических жидкостях человека.
Признаками известного технического решения, совпадающего с существенными признаками заявляемого изобретения являются: 1) определение антител в биологических жидкостях человека (в сыворотке крови человека); 2) использование адсорбированного антиидиотипичекого антитела в лунках иммунологического планшета или в представляемом патенте – иммобилизованного на поверхность магнитных микросфер; 3) инкубация разведенной исследуемой биологической жидкости человека в лунках планшета или, в представляемом патенте – с магнитными микросферами; 4) определение связавшихся антител из биологической жидкости человека по интенсивности цветной ферментативной реакции или в представляемом патенте – по интенсивности флюоресцентности биотин-стрептавидинового комплекса.
При помощи этих ранее предложенных методов: 1) определяют качественное, но не количественные уровни антител в биологических жидкостях человека; 2) было предложено использовать моноклональные антитела. Кроме того, из-за сложности их получения эти запатентованные методы очень трудоемки; 3) моноклональные антитела производятся мышиными клетками, т.е. они являются мышиными, а не человеческими антителами; 4) не было предложено использовать антиидиотипичекие антитела против полициклических ароматических углеводородов.
Еще одним аналогом заявляемого изобретения является метод, запатентованный ранее с использованием липосом в качестве иммуносорбента антиидиотипических антител для определения идиотипических антител в биологических жидкостях человека (WO8806293 (A2)).
Другим аналогом заявляемого изобретения является метод, запатентованный ранее (патент RU 2124731 G01N33/573, дата п убликации 10.01.1999). Согласно этому методу предлагается использовать твердофазный иммуноферментный анализ, где конъюгат фторметилбензантрила уксусной кислоты с человеческим сывороточным альбумином адсорбирован на стенках лунок иммунологического планшета. Затем инкубируют исследуемую биологическую жидкость с адсорбированным антигеном. Проявляют связавшиеся с антигеном антитела с помощью анти-антител, меченых ферментом.
Недостатками известного способа являются: 1) качественное, но не количественное определение антител против полициклических ароматических углеводородов в биологических жидкостях человека; 2) низкая чувствительность метода; 3) низкая воспроизводимость; 4) использование конъюгата модифицированных полициклических ароматических углеводородов для определения идиотипических антител против полициклических ароматических углеводородов, что может привести неточному определению идиотипических антител в биологической жидкости человека; 5) использование конъюгата фторметилбензантрила уксусной кислоты с человеческим сывороточным альбумином в качестве антигена может сопровождаться в ряде случаев высоким неспецифическим связыванием антител исследуемой биологической жидкости человека не с антигеном, а с белком-носителем, что существенно ограничивает возможность метода; 6) невозможность проведения комплексного (мультиплексного) анализа антител в одном образце биологической жидкости человека.
Известным аналогом заявляемого изобретения является метод, запатентованный ранее, с использованием микрочипов (патенты: KR20180006092 (A), CN107064493 (A)), когда на микрочип иммобилизуют антитела для количественного определения антигенов в биологических жидкостях человека.
Недостатками запатентованного способа являются: 1) было предложено использовать моноклональные антитела. Из-за сложности и дороговизны их получения эти запатентованные методы очень трудоемки и нерентабельны; 2) моноклональные антитела производятся мышиными клетками, т.е. они являются мышиными, а не человеческими антителами; 3) определение антигенов, а не антител в образцах биологической жидкости человека.
Также было предложено использовать биологические микрочипы (еще один аналог, предлагаемого изобретения), содержащие гидрогелевые элементы с иммобилизованными антителами к белковым онкомаркерам, гидрогелевые элементы с иммобилизованными гликанами, гидрогелевые элементы с иммобилизованными антителами против иммуноглобулинов человека классов А, G и М, где изменение концентрации анализируемых маркеров по сравнению с контрольным образцом, полученным от здорового человека, свидетельствует о колоректальном раке (патент RU 2625018). Таким образом, способ, предлагаемый в настоящем изобретении, позволяет проводить диагностику колоректального рака, основанную на одновременном количественном определении онкомаркеров белковой природы, антител к гликанам, иммуноглобулинов А, G и M в крови человека.
Недостатками этого способа являются:
1) было предложено использовать моноклональные антитела. Из-за сложности и дороговизны их получения эти запатентованные методы очень трудоемки и нерентабельны;
2) моноклональные антитела производятся мышиными клетками, т.е. они являются мышиными, а не человеческими антителами;
3) определение антигенов, а не антител в образцах биологической жидкости человека;
4) невозможность мультиплексного анализа в одном образце исследуемой биологической жидкости человека, т.е. для мультиплексирования используется весь гидрогелиевый чип через который пропускается один образец биологической жидкости, в отличие от предлагаемого метода с использованием магнитных микросфер, где в один образец биологической жидкости добавляется целый набор магнитных микросфер с одновременной и отдельной детекцией каждого вида микросфер.
Известен запатентованный ранее метод (аналог данного изобретения), с использованием стрипов с иммобилизованными на них антителами для детекции антигенов в биологических жидкостях человека (CN108020666 (A)).
Недостатками этого метода являются:
1) было предложено использовать моноклональные антитела. Из-за сложности и дороговизны их получения эти запатентованные методы очень трудоемки и нерентабельны;
2) моноклональные антитела производятся мышиными клетками, т.е. они являются мышиными, а не человеческими антителами;
3) определение антигенов, а не антител в образцах биологической жидкости человека;
4) невозможность мультиплексного анализа в одном образце исследуемой биологической жидкости человека, в отличие от предлагаемого метода с использованием магнитных микросфер, где в один образец биологической жидкости добавляется целый набор магнитных микросфер с одновременной и отдельной детекцией каждого вида микросфер;
5) качественное, но не количественное определение аналитов в биологической жидкости;
6) низкая чувствительность метода.
Аналогом заявляемого изобретения также является метод, запатентованный ранее количественный метод определения антител и антигенов в биологических жидкостях человека с использованием магнитных микросфер, на которые иммобилизуют идиотипические антитела для определения антигенов в биологических жидкостях человека: KR101807871 (B1), CN105259344 (A), US2014170767 (A1), CN106290867 (A), CN106366197 (A), CN103278521 (A); иммобилизованные анти-IgE для определения IgE в сыворотке крови человека: CN101696973 (A); иммобилизованный антиген для определения IgE в сыворотке крови человека: CN105785030 (A); комбинация из стрипов и магнитных микросфер с комбинацией иммобилизованных антител и антигенов для полуколичественного определения пневмонии: CN107748252 (A) и простатита CN107271666 (A).
За прототип принято изобретение CN107271666 (дата публикации 20.10.2017, класс МПК G01N33/558).
Признаками прототипа, совпадающего с существенными признаками заявляемого изобретения являются: 1) определение аналитов в биологических жидкостях человека (в сыворотке крови человека); 2) использование иммобилизованного антигена или антитела на поверхность магнитных микросфер; 3) инкубация разведенной исследуемой биологической жидкости с магнитными микросферами; 4) определение связавшихся аналитов из биологической жидкости человека по интенсивности флюоресцентности биотин-стрептавидинового комплекса. 4) количественный анализ аналитов в биологических жидкостях человека (в сыворотке крови человека); 5) высокая чувствительность, точность и воспроизводимость методов.
Недостатками прототипа являются:
1) было предложено использовать моноклональные антитела. Из-за сложности и дороговизны их получения эти запатентованные методы очень трудоемки и нерентабельны;
2) моноклональные антитела производятся мышиными клетками, т.е. они являются мышиными, а не человеческими антителами;
3) не было предложено использовать идиотипические и антиидиотипичекие антитела против полициклических ароматических углеводородов.
Техническим результатом предлагаемого изобретения является повышение точности, чувствительности и воспроизводимости метода по сравнению с иммуноферментным анализом за счет проведения мультиплексного анализа (множественного определения) антител в одном образце биологической жидкости человека, и при этом снижение канцерогенной опасности для здоровья исследователя и изготовителя тест-систем, снижение неспецифического связывания антител исследуемой биологической жидкости человека.
Предлагается способ количественного определения антител к химическим канцерогенам группы полициклических ароматических углеводородов, включающий забор и подготовку донорской крови, иммобилизацию человеческих рекомбинантных антиидиотипических антител к бензо[а]пирену на магнитные микросферы.
Отличием является то, что подают разведенную сыворотку крови человека, разбавленную фосфатным буферным раствором PBS в соотношении 1:100, инкубацию проводят с биотинилированными идиотипическими антителами (в количестве 20 нг/мкл) в качестве конкурента с сывороткой крови человека за связывание с магнитными микросферами, инкубацию микросфер 1 час осуществляют при комнатной температуре, детекцию связывания антител с микросферами и анализ количества связанных антител с микросферами определяют по калибровочной кривой.
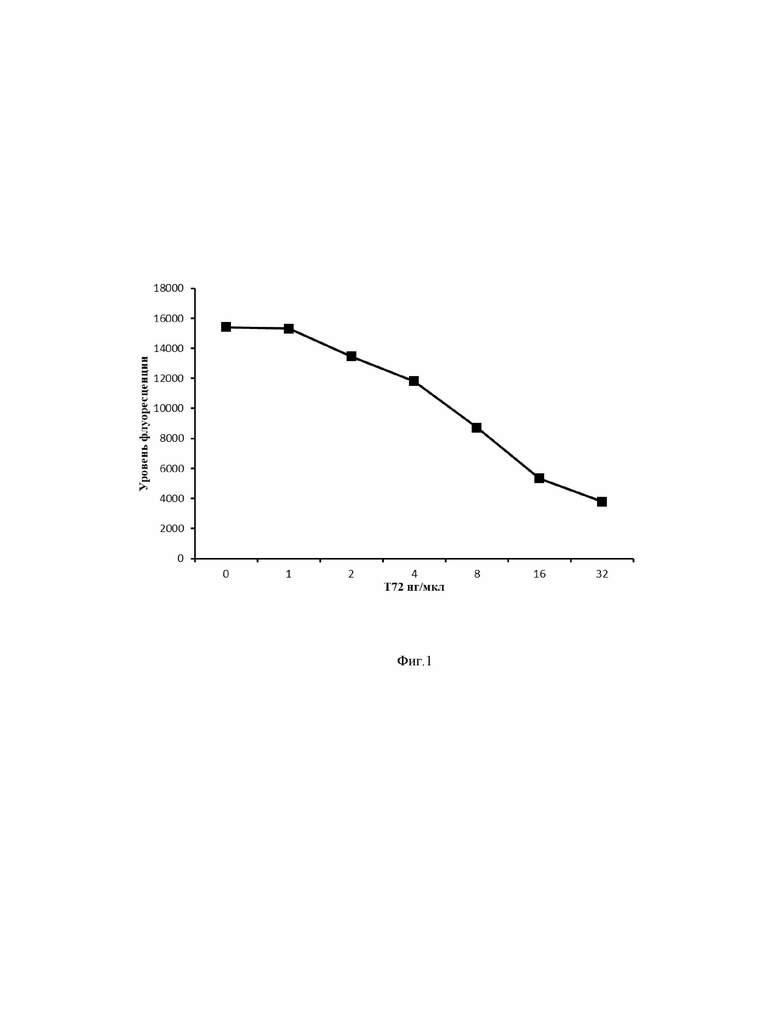
Сущность предлагаемого изобретения показана на фиг.1 и фиг.2, где на фиг.1 показана калибровочная кривая конкурентного связывания БТ72 (10 нг/мкл) и Т72 (от 1 нг/мкл до 32 нг/мкл) с МВ5, а на фиг.2 – концентрации антител против бензо[a]пирена в сыворотке крови человека.
Предлагаемый способ осуществляется следующим образом:
1. Для осуществления способа использовались сыворотки крови 10 доноров. Все исследования были проведены с согласия доноров крови.
2. Антитела по изобретению известны и подробно описаны в Ustinov et al, 2015 и Arnst et al, 2017. Использовались: человеческое рекомбинантное идиотипическое антитело против бензо[a]пирена – Т72, и человеческое рекомбинантное антиидиотипическое антитело против бензо[a]пирена – В5. Все антитела были экспрессированы и выделены из E.coli.
3. Иммобилизация В5 на магнитные микросферы проводилась по аминогруппам с использованием набора для иммобилизации Bio-Plex фирмы Bio-Rad (США).
4. Биотинилирование T72 было проводилось набором Силекс (Россия).
5. Для анализа количественного антител против бензо[a]пирена в сыворотке крови человека 100 мкл фосфатного буферного раствора of PBS с 0,5% БСА были добавлены в лунки непрозрачного иммунологического планшета для уменьшения неспецифичного связывания. Затем в каждую лунку были добавлены сначала по 6000 магнитных микросфер с иммобилизованными на них В5 (МВ5), затем по 50 мкл биотинилированного Т72 (БТ72) с концентрациями от 34,827 пг/мкл до 16 пг/мкл. Стрептовидин-фикоэритрин фирмы Bio-Rad (США) использовался для детекции МВ5-БТ72 комплекса. В качестве контроля фонового связывания использовались 6000 магнитных микросфер без добавления к ним БТ72. Значения фонового связывания использовались вычитались из значения всех остальных точек связывания. Половинная концентрация БТ72 от максимального связывания БТ72 с МВ5 составляла 10 нг/мкл. Эта концентрация использовалась в дальнейшем.
6. Калибровочная кривая строилась на основе конкуренции БТ72 и Т72 за связывание с МВ5 следующим образом: БТ72 в концентрации 10 нг/мкл добавлялся во все лунки непрозрачного иммунологического планшета. Затем в те же лунки добавлялся Т72 с двойным шагом разведения от концентрации 1 до 32 нг/мкл. Максимальная флюоресценция составляла 15410. Чувствительность калибровочной кривой (минимальное связывание и, как следствие, чувствительность определения антител в сыворотке крови человека) находилась в диапазоне меньше чем от 1 нг/мкл. Калибровочная кривая представлена на фиг.1.
7. Для количественного определения антитела против бензо[a]пирена в сыворотке крови человека образцы сывороток были разбавлены фосфатным буферным раствором PBS в соотношении 1:100. Затем разбавленная сыворотка человека была добавлена в реакцию связывания (см. п. 5 данного раздела) вместо Т72 в качестве конкурента с БТ72 (20 нг/мкл) за связывание с МВ5. Конечный объем реакционной смеси составлял 50 мкл в каждой лунке иммунологического непрозрачного планшета (половина на половину от объема разбавленной сыворотки человека и БТ72). Затем иммунологический планшет инкубировался 1 час при комнатной температуре. В качестве отрицательного контроля на неспецифическое связывание использовалась инкубационная смесь MB5 с сывороткой человека, но без БТ72. Этот контроль проходил все стадии данной методики. Неспецифическое связывание составляло 120 единиц флюоресценции, которое вычиталось как фон из всех остальных значений флюоресценции. Концентрации антител против бензо[a]пирена в сыворотке крови человека составляли от 8620 пг/мкл до 17768 пг/мкл (среднее значение 12946,5 (9671.0:15469,0) пг/мкл) (фиг.2). Причем нижняя граница концентрации находилась в центре калибровочной кривой (фиг.1).
Изобретение предлагается использовать для осуществления количественного метода иммуноанализа антител против полициклических ароматических углеводородов в биологических жидкостях человека конкурентным методом иммуноанализа, в котором в качестве антигена – человеческие рекомбинантные антиидиотипические антитела к полициклическим ароматическим углеводородам, иммобилизованные на магнитах микросферах, а в качестве стандартных антител – человеческие рекомбинантные идиотипические антитела против полициклических ароматических углеводородов.
К подготовленным микросферам добавляется биотинилированные идиотипические антитела в постоянной концентрации и небиотинилированные идиотипические антитела в возрастающих концентрациях, которые конкурируют с биотинилированными идиотипическими антителами за связывание с иммобилизованными антиидиотипическими. К связавшимся биотинилированным идиотипическим антителам добавляется конъюгат стрептовидин-фикоэритрин. Степень конкуренции оценивается по степени флюоресценции фикоэритрина в комплексе стрептовидин-биотин на приборе Bio-Plex 200 или на других аналитических приборах. В отдельных пробах к микросферам вместе с биотинилированными идиотипическими антителами добавляется образец биологической жидкости человека и содержащиеся в ней антитела против полициклических ароматических углеводородов конкурируют с биотинилированными идиотипическими антителами за связывание с иммобилизованными антиидиотипическими антителами, после чего в пробу добавляется комплекс стрептовидин-фикоэритрин. Степень подавления флуоресценции под действием искомых антител в биологической жидкости человека сопоставляется с таковой под действием небиотинилированных идиотипических антител и количество искомых антител в биологической жидкости человека приравнивается к количеству небиотинилированных идиотипических антител с таким же уровнем флуоресценции.
В то же время, нами получены рекомбинантные антитела человека, специфичные к наиболее распространенным канцерогенам окружающей среды – полициклическим ароматическим углеводородам (в частности, к бензо[а]пирену), которые можно использовать в качестве стандарта, а также соответствующие антиидиотипические рекомбинантные антитела человека (в частности, к бензо[а]пирену), которые можно использовать в качестве антигена при разработке безопасного для здоровья количественного метода иммуноанализа антител против химических канцерогенов в биологических жидкостях человека.
Таким образом, значимость и причинно-следственная связь с заявленным техническим результатом разработки предлагаемого способа количественного определения антител к полициклическим ароматическим углеводородам в биологических жидкостях человека обусловлена следующим:
– доказанным канцерогенным эффектом полициклических ароматических углеводородов окружающей среды;
– возможностью выявления неизвестных ранее иммунологических механизмов адаптации человека к полициклическим ароматическим углеводородам и особенностей их нарушения при онкологических заболеваниях;
– практической важностью создания информативного и безопасного для здоровья метода оценки индивидуальных онкологических рисков для последующей профилактики рака.
Причинно-следственная связь с заявленным техническим результатом достигается за счет:
1. Использования в качестве антигена не конъюгаты нативных полициклических ароматических углеводородов с белком, а антиидиотипические антитела, несущие иммунологический слепок антигена.
2. Использования конкурентный метод анализа, при котором для калибровочной кривой применяется конкуренция между биотинилированным и небиотинилированным идиотипическими антителами, а для определения концентрации идиотипических антител в биологичекой жидкости человека конкуренция между биотинилированным идиотипическими антителами и самой биологической жидкостью.
3. Для повышения точности, чувствительности и воспроизводимости метода, множественного определения антител в одном образце биологической жидкости человека, уменьшения количества образца биологической жидкости человека, способности обрабатывать сразу большое количество образцов биологической жидкости человека и более легкому в исполнении количественному методу определения антител используется мультиплексная система с использованием флуоресцентных магнитных микросфер.
Предлагаемый способ актуален, осуществим и позволяет достигать заявленный технический результат, отличается от известных аналогов и имеет явные преимущества перед ними.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИММУНОФЕРМЕНТНОГО АНАЛИЗА ИДИОТИПИЧЕСКИХ И АНТИИДИОТИПИЧЕСКИХ АНТИТЕЛ К БЕНЗО[А]ПИРЕНУ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЧЕЛОВЕКА | 2019 |
|
RU2741382C1 |
| СПОСОБ ИММУНОФЕРМЕНТНОГО АНАЛИЗА АНТИТЕЛ К ХИМИЧЕСКИМ КАНЦЕРОГЕНАМ ГРУППЫ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1994 |
|
RU2124731C1 |
| ПЕПТИД-ИММУНОМИМЕТИК ХИМИЧЕСКИХ КАНЦЕРОГЕНОВ, ОБЛАДАЮЩИЙ СПОСОБНОСТЬЮ СПЕЦИФИЧЕСКИ ВЗАИМОДЕЙСТВОВАТЬ С АНТИТЕЛАМИ ПРОТИВ БЕНЗО[α]ПИРЕНА И БЕНЗ[α]АНТРАЦЕНА | 2007 |
|
RU2357975C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ УРОВНЯ ЕСТЕСТВЕННЫХ АУТОАНТИТЕЛ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЧЕЛОВЕКА | 2010 |
|
RU2465601C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СПЕЦИФИЧЕСКИХ ИММУНОГЛОБУЛИНОВ G К КОНЪЮГАТУ ФОРМАЛЬДЕГИД - СЫВОРОТОЧНЫЙ ЧЕЛОВЕЧЕСКИЙ АЛЬБУМИН В СЫВОРОТКЕ КРОВИ | 2010 |
|
RU2473908C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ УРОВНЯ ЕСТЕСТВЕННЫХ АУТОАНТИТЕЛ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЧЕЛОВЕКА ПУТЕМ ИММУНОФЕРМЕНТНОГО АНАЛИЗА | 2010 |
|
RU2465600C2 |
| АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА, КОТОРЫЕ ИНДУЦИРУЮТ ИММУННЫЙ ОТВЕТ ПРОТИВ РЕЦЕПТОРА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА | 1996 |
|
RU2172636C2 |
| МОНОКЛОНАЛЬНОЕ АНТИИДИОТИПИЧЕСКОЕ АНТИТЕЛО Ab2, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ИСПОЛЬЗОВАНИЯ ПРОТИВ БОЛЕЗНЕЙ, СОПРОВОЖДАЮЩИХСЯ ЭКСПРЕССИЕЙ Lewis Y6 АНТИГЕНА, И ДЛЯ ОЧИСТКИ ВАРИАНТА BR55-2 АНТИТЕЛА, ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЙ СОСТАВ | 1993 |
|
RU2208642C2 |
| СПОСОБ ОБНАРУЖЕНИЯ МУЛЬТИСПЕЦИФИЧЕСКОГО СВЯЗЫВАЮЩЕГО АГЕНТА | 2013 |
|
RU2636822C2 |
| СПОСОБ ИММУНОФЛУОРЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ ПРОТЕКТИВНОГО АНТИГЕНА ВОЗБУДИТЕЛЯ СИБИРСКОЙ ЯЗВЫ | 2011 |
|
RU2478970C1 |

Изобретение относится к области иммунологии, биотехнологии и клинической лабораторной диагностики и может найти применение для определения индивидуальных рисков возникновения заболеваний, связанных с воздействием химических канцерогенов окружающей среды. Раскрыт способ количественного определения антител к бензо[а]пирену в биологических жидкостях человека, включающий забор и подготовку донорской крови; иммобилизацию человеческих рекомбинантных антиидиотипических антител к бензо[а]пирену на магнитные микросферы; при этом в реакционную смесь подают разведенную сыворотку крови человека, разбавленную фосфатным буферным раствором PBS в соотношении 1:100; инкубацию с биотинилированными идиотипическими антителами к бензо[а]пирену в конечной концентрации 20 нг/мкл в качестве конкурента с сывороткой крови человека за связывание с магнитными микросферами; инкубацию микросфер 1 час осуществляют при комнатной температуре; детекцию связывания антител с микросферами определяют с помощи конъюгата стрептавидин-фикоэритрин и анализ количества связанных антител с микросферами - по калибровочной кривой. Изобретение обеспечивает повышение точности, чувствительности и воспроизводимости метода по сравнению с иммуноферментным анализом, а также снижение канцерогенной опасности для здоровья исследователя и изготовителя тест-систем и снижение неспецифического связывания антител исследуемой биологической жидкости человека. 2 ил.
Способ количественного определения антител к бензо[а]пирену в биологических жидкостях человека, включающий забор и подготовку донорской крови; иммобилизацию человеческих рекомбинантных антиидиотипических антител к бензо[а]пирену на магнитные микросферы; отличающийся тем, что для количественного анализа антител против бензо[a]пирена в реакционную смесь подают разведенную сыворотку крови человека, разбавленную фосфатным буферным раствором PBS в соотношении 1:100; инкубацию с биотинилированными идиотипическими антителами к бензо[а]пирену, в конечной концентрации 20 нг/мкл, в качестве конкурента с сывороткой крови человека за связывание с магнитными микросферами; инкубацию микросфер 1 час осуществляют при комнатной температуре; детекцию связывания антител с микросферами определяют с помощью конъюгата стрептавидин-фикоэритрин и анализ количества связанных антител с микросферами - по калибровочной кривой.
| СПОСОБ ИММУНОФЕРМЕНТНОГО АНАЛИЗА АНТИТЕЛ К ХИМИЧЕСКИМ КАНЦЕРОГЕНАМ ГРУППЫ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1994 |
|
RU2124731C1 |
| CN 107271666 A, 20.10.2017 | |||
| KIM J.S | |||
| et al | |||
| Multiplexed magnetic microsphere immunoassays for detection of pathogens in foods // Sens | |||
| Instrum | |||
| Food Qual | |||
| Saf., 2010, v.4, pp.73-81 | |||
| МАЗУНИНА Е.П | |||
| ПРОТОКОЛ РАЗРАБОТКИ СКРИНИНГОВОЙ ТЕСТ-СИСТЕМЫ ДЛЯ ОЦЕНКИ ИММУНОЛОГИЧЕСКОЙ ПАМЯТИ К ВАКЦИНОУПРАВЛЯЕМЫМ ИНФЕКЦИЯМ: ОДНОВРЕМЕННОЕ ОПРЕДЕЛЕНИЕ ТИТРА АНТИТЕЛ К КОРИ, ПАРОТИТУ, КРАСНУХЕ И ГЕПАТИТУ В // Вестник РГМУ, 2017, т.5, стр.45-57. | |||
Авторы
Даты
2019-10-14—Публикация
2018-12-03—Подача