Изобретение относится к области медицины, в частности к лабораторной диагностике, и может быть использовано для повышения эффективности и достоверности количественного определения концентрации естественных аутоантител в биологических жидкостях человека.
Из уровня техники известен способ количественного определения уровня аутоантител к эндогенным белкам в биологических жидкостях человека путем твердофазного иммуноферментного анализа (ИФА) (RU 2137134 C1, G01N 33/53, 1999). Однако данный способ мало пригоден для количественного определения уровня естественных аутоантител в биологических жидкостях человека.
Известен также способ проведения иммуноферментного анализа, включающий адсорбцию антигенов на твердой фазе физической сорбции, инкубацию тестируемых биологических образцов, инкубацию конъюгатсодержащего раствора, спектрофотометрический анализ реакции по экстинции раствора хромагента (RU 2014610 C1, G01N 33/535, 1994).
Кроме того, также известен способ проведения иммуноферментного анализа для определения уровня естественных аутоантител, включающий адсорбцию антигенов на твердой фазе физической сорбции, инкубацию тестируемых биологических образцов, инкубацию конъюгатсодержащего раствора и спектрофотометрический анализ реакции по экстинции раствора хромагента (BMS217TEN Human anti-IFN-alpha ELISA, Bender MedSystems GmbH, Австрия). Несмотря на достаточную простоту, чувствительность и специфичность данного решения полученные результаты могут быть ложноположительными, из-за неспецифического и низкоаффинного связывания различных иммуноглобулинов сыворотки или плазмы с антигеном, адсорбированным на ИФА планшете. Кроме того, присутствие в крови полиреактивных иммуноглобулинов, не являющихся естественными антителами, также приводит к получению ложноположительных результатов из-за неспецифического связывания полиреактивных иммуноглобулинов с компонентами ИФА планшета. Боле того, в ИФА детектируется только фракция свободных естественных аутоантител, в то время как большая часть естественных аутоантител присутствуют в крови в связанном со своим антигеном комплексе.
Изобретение направлено на создание технологически простого, чувствительного и специфического способа количественного определения уровня естественных аутоантител в биологических жидкостях человека ИФА методом.
Решение поставленной задачи обеспечивается тем, что в способе количественного определения уровня естественных аутоантител в биологических жидкостях человека путем иммуноферментного анализа, включающем обработку твердой фазы физической сорбции антигеном, внесение тестируемых биологических образцов, обработку твердой фазы конъюгатсодержащим раствором, разделение твердой и жидкой фаз и спектрофотометрический анализ реакции по экстинции раствора хромагента, согласно изобретению, в качестве твердой фазы физической сорбции используют твердую фазу физической сорбции, покрытую стрептавидином, а обработку твердой фазы физической сорбции производят предварительно биотинилированным антигеном и блокирующим агентом для закрытия на твердой фазе физической сорбции мест неспецифического связывания, в качестве которого используют биотинилированные по стандартной процедуре белки, в качестве конъюгатсодержащего раствора используют моноклональные или поликлональные антитела, меченные ферментом, реагирующие с одним или всеми изотипами человеческих иммуноглобулинов, при этом тестируемую биологическую жидкость предварительно разводят в буфере, содержащем белки, используемые для закрытия на твердой фазе физической сорбции мест неспецифического связывания, а также вещества, защищающие естественные аутоантитела от разрушения при термической обработке, подвергают биологическую жидкость воздействию железосодержащим окислителем и производят термическую обработку, для каждого тестируемого образца биологической жидкости применяют биотинирилованный контрольный белок (идентичные белку, используемому для закрытия на твердой фазе физической сорбции мест неспецифического связывания) для связывания со стрептавидином твердой фазы, а количество естественных аутоантител определяют с использованием калибровочной кривой, которая стандартизуется по моноклональным или поликлональным антителам к антигену.
Благодаря сочетанию использования в качестве твердой фазы физической сорбции твердой фазы физической сорбции, покрытой стрептавидином, и биотинилированных антигенов, у иммобилизированного антигена все эпитопы остаются свободными для связывания с ними естественных аутоантител, и тем самым повышается чувствительность заявленного способа, в то время как прямая иммобилизация антигена приводит к конформационным изменениям и разрушению эпитопов антигена, что снижает чувствительность ИФА метода. Кроме того, использование антител, меченных ферментом и реагирующих с одним или всеми изотипами человеческих иммуноглобулинов, позволяет определить уровень определенного изотипа или всех изотипов естественных аутоантител, и соответственно, расширяет функциональные возможности заявленного способа. Предварительное разведение исследуемого образца в буфере, содержащем белки, присутствующие в блокирующем буфере и используемые для закрытия на твердой фазе физической сорбции мест неспецифического связывания, минимизирует возможность неспецифического связывания антител исследуемого образца с твердой фазой, на которой иммобилизированы белки, что также повышает специфичность заявленного способа. Добавление железосодержащего окислителя и проведение термической обработки исследуемого образца позволяет разрушить комплекс естественных аутоантител с антигенами и анти-идиотипическими антителами, или обеспечивать доступность паратопов антител эпитопам антигенов за счет различных демаскирующих эффектов, а предварительное разведение исследуемого образца в буфере защищает естественные аутоантитела от разрушения при термической обработке, что позволяет определить общий уровень естественных аутоантител (то есть как свободную и связанную с антигеном формы естественных аутоантител или естественных аутоантител с закрытыми паратопами), и тем самым снижает возможность получения ложноотрицательных результатов, повышает чувствительность, эффективность и функциональные возможности заявленного способа. Использование для каждого из исследуемых образцов биологической жидкости индивидуальной контрольной твердой фазы физической сорбции, на которой иммобилизирован биотинилированный блокирующий белок, позволяет измерить специфический для естественных аутоантител спектрофотометрический сигнал и не специфический спектрофотометрический сигнал, что также снижает возможность получения ложноположительных результатов и повышает чувствительность заявленного способа.
Кроме того, заявленная совокупность существенных признаков, которая обеспечивает возможность количественного определения уровня естественных аутоантител, расширяет арсенал технических средств для решения поставленной задачи.
Заявленный способ количественного определения уровня естественных аутоантител в биологических жидкостях человека реализуют следующим образом.
Твердую фазу физической сорбции (лунки) стандартного луночного планшета покрывают стрептавидином или его аналогами (например, авидином и др.), блокируют твердую фазу физической сорбции блокирующим агентом и инкубируют с биотинилированным антигеном (для определения антиген специфических антител), к которому необходимо определить уровень естественных аутоантител, или (для контрольных лунок) с биотинилированным блокирующим белком (например, бычьим сывороточным альбумином, овальбумином, человеческим сывороточным альбумином, кроличьим сывороточным альбумином, желатином и др.), являющимся контролем неспецифического связывания. Антиген биотинилируется минимальным количеством биотина (молярное отношение антиген: биотин составляет 1:2) для минимизации разрушения эпитопов.
Подготавливают для анализа исследуемую биологическую жидкость (например, сыворотка крови, плазма крови и др.), при этом тестируемые образцы разводят (в диапазоне от 50 до 200000 раз) в буферном растворе, содержащем белки, входящие в состав блокирующего буфера (например, бычий сывороточный альбумин, овальбумин, человеческий сывороточный альбумин, кроличий сывороточный альбумин, желатин и др.), консерванты (например, тимерозал и др.) и поверхностно-активные вещества (например, Triton-X100 и др.), которые защищают естественные аутоантитела от разрушения при термической обработке, обрабатывают железосодержащим окислителем (например, хлорид железа (III) [FeCl3] и производят термическую обработку полученного раствора биологической жидкости путем инкубации в температурном диапазоне от 50°С до 80°С. Затем обработанный железосодержащим окислителем и термически обработанный раствор исследуемой биологической жидкости вносят в лунки также, как и антиген - специфические антитела, используемые для построения калибровочной кривой, в качестве которых используют моноклональные или поликлональные антитела к антигену с известной концентрацией. Для проявления образовавшегося иммунного комплекса (антиген - естественные аутоантитела) используют конъюгат поликлональных или моноклональных антител (например, козьи поликлональные антитела, овечьи поликлональные антитела, мышиные моноклональные антитела и др.) к легким цепям определенного или всех иммуноглобулинов человека с ферментом (например, щелочной фосфатазой, пероксидазой хрена и др.). Определяют количество естественных аутоантител, учитывая реакцию по экстинции раствора хромагента, изменяющего свою окраску в зависимости от количества хромагента, выделенного из субстрата при разложении его ферментом (например, щелочной фосфатазой и др.) - субстрат продуцирует растворимый продукт, цветовые характеристики которого могут быть измерены спектрофотометрически при определенной длине волны.
Пример 1.
Для подтверждения возможности получения технического результата при осуществлении заявленного способа количественного определения уровня естественных аутоантител к интерферону гамма человека были взяты образцы сыворотки двадцати здоровых доноров, у которых не проводилась интерферонотерапия, и следовательно, в сыворотке отсутствуют аутоантитела к интерферону гамма человека, но присутствуют естественные аутоантитела к интерферону гамма человека,
В часть лунок 96 луночного планшета, покрытого стрептавидином, компании Greiner bio-one GmbH (кат. №655990) вносили рекомбинантный интерферон гамма человека производства eBiosciences (кат. №.34-8319-85) и в другую часть (контрольные лунки для исследуемых образцов) - бычий сывороточный альбумин производства Sigma Aldrich (кат. №. А-3803), биотинилированные по стандартной процедуре компании U-CyTech bioscience (СОП № UCT-127) из расчета 100 мкл/лунка и инкубировали в течение 2 часов при температуре 37°С и при 100% влажности.
Образцы сыворотки крови разводили в 10 раз (10 мкл сыворотки разводили в 90 мкл фосфатно-солевого буфера, содержащего 1% Triton-Х100 и 0,002% тимерозал), обрабатывали 2 мМ FeCl3 и инкубировали в течение 40 минут при температуре 56°С.
Затем проинкубированный раствор еще разводили в 5 раз (100 мкл проинкубированного раствора разводили в 400 мкл фосфатно-солевого буфера, содержащего 1% бычий сывороточный альбумин (БСА), 1% Triton-X100 и 0,002% тимерозал) и в дальнейшем использовали для внесения в лунки планшета (по 100 мкл в лунку).
Для построения калибровочной кривой приготавливали растворы стандартных антител (мышиные моноклональные антитела к интерферону гамма человека, клон MD-2) в диапазоне концентраций от 16 Ед/мл до 0,5 Ед/мл. За 1 Ед/мл принимали 100 пкг/мл мышиных моноклональных антител.
Подготовленные стандартные антитела, раствор, используемый в качестве отрицательного контроля (фосфотно-солевой буфер, содержащий 1% БСА, 1% Triton-X100 и 0,002% тимерозал) и растворы исследуемых образцов вносили в лунки планшета, как указано в таблице 1, и инкубировали при температуре 37°С в течение 2 часов. По завершению инкубации жидкость удаляли из планшета декантированием и 5 раз планшет промывали стандартным моющим раствором (фосфатно-солевой буфер, содержащий 0,05% Твин-20 и 0,01% тимерозал).
В таблице 1 приведена схема внесения образцов в лунки планшета.

N: Отрицательный контроль - фосфотно-солевой буфер, содержащий 1% БСА, 1% Triton-X100 и 0,002% тимерозал
S1-S20: Исследуемые образцы 1-20
ИФН-γ - рекомбинантный интерферон гамма человека
БСА - бычий сыворотчный альбумин
Затем во все лунки планшета вносили по 100 мкл раствора, содержащего смесь конъюгированых с щелочной фосфатазой козьих антител к IgA, IgM, IgG человека (Sigma Aldrich; кат. № A-3313), что позволяет определить уровень всех изотипов естественных аутоантител к интерферону гамма человека, или козьи антитела к IgG мыши (Sigma Aldrich; кат. № А-3562), конъюгированные с щелочной фосфатазой, для определения уровня моноклональных антител к интерферону гамма человека (MD-2), используемых для построения калибровочной кривой. Затем планшет инкубировали в течение 1 часа при температуре 37°С. По завершении инкубации жидкость удаляли из лунок планшета декантированием и 5 раз планшет промывали стандартным моющим раствором (фосфатно-солевой буфер, содержащий 0,05% Твин-20 и 0,01% тимерозал).
За 15 минут до окончания инкубации с конъюгатсодержащим раствором готовили раствор хромагента, растворяя 1 таблетку субстратного буфера и 1 таблетку субстрата (пара-нитрофенилфосфат), производства фирмы Sigma (кат. № N-2770) в 20 мл дистиллированной воды.
По 100 мкл приготовленного раствора хромагента вносили в каждую из лунок планшета и инкубировали планшет в течение 30 минут при температуре 37°С.
По окончании инкубации во все лунки планшета вносили останавливающий раствор (3N гидроксид натрия) производства фирмы Merck KgaA (кат. №.1.06495) и измеряли экстинцию при длине волны 405 нм с использованием стандартного фотометра.
По полученным результатам измерений рассчитывали уровень естественных аутоантител к интерферону гамма. Для этого определяли истинное значение оптической плотности (ОП) стандартных антител и истинное значение ОП исследуемых образцов следующим образом:
1. Рассчитывали среднюю ОП для отрицательного контроля (среднее арифметическое значение ОП в лунках 1G, 1Н, 2G, 2Н).
2. Рассчитывали среднюю ОП для стандартных антител (среднее арифметическое значение ОП в лунках соответствующего стандарта Р1-Р6).
3. Рассчитывали истинное значения ОП стандартных антител как разность среднего значения ОП стандартных антител и среднего значения ОП отрицательного контроля.
Результаты расчетов приведены в таблице 2.
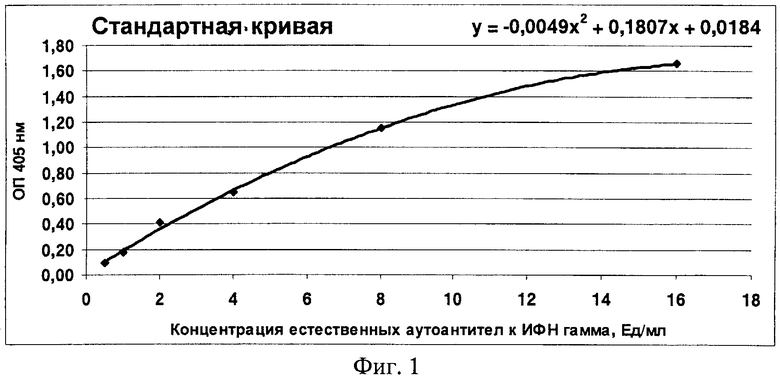
4. По полученным значениям истинной ОП стандартных антител построили калибровочную кривую (см. фиг.1), где по оси ординат (y) расположены значения ОП, по оси абсцисс (x) - концентрация антител к интерферону гамма. Построенная калибровочная кривая может быть описана следующим уравнением: y=-0,0049x2+0,1807x+0,0184
5. Рассчитывали среднее ОП для исследуемых образцов в лунках планшета, в которых иммобилизирован биотинилированный ИФН-γ (ряды 3, 5, 7, 9, 11 в таблице 1) и в которых иммобилизирован биотинилированный БСА (ряды 4, 6, 8, 10, 12 в таблице 1). Например, для исследуемого образца S1 среднее значение ОП в лунках A3, В3 и А4, В4, соответственно.
6. Рассчитывали истинное значения ОП для исследуемых образцов как разность среднего значения ОП для исследуемых образцов, измеренной в лунках планшета, в которых иммобилизирован биотинилированный ИФН-γ, и среднего значение ОП для исследуемых образцов, измеренной в лунках планшета, в которых иммобилизирован биотинилированный БСА. Например, для исследуемого образца S1 вычитаем из среднего значения ОП, измеренного в лунках планшета A3, В3, среднее значение ОП, измеренное в лунках планшета А4, В4.
7. Используя калибровочную кривую (фиг.1), определяли концентрацию разведенных естественных аутоантител к интерферону гамма человека в исследуемых образцах. Для получения истинного значения концентрации естественных аутоантител к интерферону гамма человека в исследуемых образцах полученный результат умножали на степень разведения образцов (на 100).
8. Результаты представлены в таблице 3.
Таким образом, приведенные примеры с использования сыворотки крови, в которой присутствуют естественные аутоантитела к интерферону гамма человека, подтверждают эффективность и надежность количественного определение уровня естественных аутоантител к интерферону гамма человека при реализации заявленной совокупности признаков
Изобретение относится к области медицины, в частности к лабораторной диагностике, и может быть использовано для определения концентрации естественных аутоантител в биологических жидкостях человека иммуноферментным анализом. Для этого используют твердую фазу физической сорбции, покрытую стрептавидином. Предварительно производят обработку твердой фазы физической сорбции биотинилированным антигеном и блокирующим агентом для закрытия мест неспецифического связывания. Для этого используют биотинилированные по стандартной процедуре белки, в качестве конъюгатсодержащего раствора используют моноклональные или поликлональные антитела, меченные ферментом, реагирующие с одним или всеми изотопами человеческих иммуноглобулинов. Тестируемый образец предварительно разводят в буфере, содержащем белки, используемые для закрытия на твердой фазе физической сорбции мест неспецифического связывания, тимерозал и Triton-X100. Подвергают воздействию хлоридом железа (III) и производят термическую обработку. Для тестируемого образца применяют контрольную твердую фазу физической сорбции, на которой не иммобилизирован биотинилированный антиген. Количество естественных аутоантител определяют по калибровочной кривой. Изобретение обеспечивает надежность и эффективность количественного определения уровня естественных аутоантител в биологических жидкостях человека. 3 табл., 1 ил., 1 пр.
Способ количественного определения уровня естественных аутоантител в биологических жидкостях человека путем иммуноферментного анализа, включающий обработку твердой фазы физической сорбции антигеном, внесение тестируемых биологических образцов, обработку твердой фазы конъюгатсодержащим раствором, разделение твердой и жидкой фаз и анализ реакции по экстинции раствора хромагента, отличающийся тем, что в качестве твердой фазы физической сорбции используют твердую фазу физической сорбции, покрытую стрептавидином, а обработку твердой фазы физической сорбции производят предварительно биотинилированным антигеном и блокирующим агентом для закрытия на твердой фазе физической сорбции мест неспецифического связывания, в качестве которого используют биотинилированные по стандартной процедуре белки, в качестве конъюгатсодержащего раствора используют моноклональные или поликлональные антитела, меченные ферментом, реагирующие с одним или всеми изотипами человеческих иммуноглобулинов, при этом тестируемую биологическую жидкость предварительно разводят в буфере, содержащем белки, используемые для закрытия на твердой фазе физической сорбции мест неспецифического связывания, в сочетании с консервантами, преимущественно тимерозалом и поверхностно-активными веществами, преимущественно Triton-X100, которые защищают естественные аутоантитела от разрушения при термической обработке, подвергают биологическую жидкость воздействию железосодержащим окислителем - хлоридом железа (III) FeCl3 и производят термическую обработку, для каждого тестируемого образца биологической жидкости применяют биотинилированный контрольный белок, идентичный белку, используемому для закрытия на твердой фазе физической сорбции мест неспецифического связывания, для связывания со стрептавидином твердой фазы, а количество естественных аутоантител определяют с использованием калибровочной кривой, которая стандартизуется по моноклональным или поликлональным антителам к антигену.
| HYLKEMA MN et al | |||
| Clinical evaluation of a modified ELISA, using photobiotinylated DNA, for the detection of anti-DNA antibodies.J Immunol Methods | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| (ref.) | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ РИСКА РАЗВИТИЯ НЕРВНО-ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1997 |
|
RU2147128C1 |
| Набор для иммуноферментного определения аллергенспецифического иммуноглобулина Е в сыворотке и плазме крови | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| найдено из Интернет, | |||
Авторы
Даты
2012-10-27—Публикация
2010-05-05—Подача