Область техники
Изобретение относится к области получения сверхтвердых материалов, а именно, к разработке нового способа синтеза поли[(R)карбинов] (R=Н, алкил, арил), используемых для получения алмазных материалов.
Уровень техники
Известен способ получения поли[(R)карбинов] (R=Н, алкил, арил) путем электролиза, содержащего трихлорметильную группу органического соединения RCCl3 (R=Н, алкил, арил) или гексахлорэтана C2Cl6 [J. Mater. Sci. 2009. V. 44 Р. 2774]. К недостаткам этого способа относятся: выделение в ходе реакции ядовитого хлора (Cl2), который необходимо дегазировать, использование двух растворителей (ацетонитрил и тетрагидрофуран), большая продолжительность реакции (4 ч), и необходимость длительной (более 12 ч) очистки продукта с помощью дорогого и пожароопасного LiAlH4.
Известен способ получения поли[(R)карбинов] (R=Н, алкил, арил) путем реакции содержащего тригалоидметильную группу органического соединения CX3R (где X=Cl, Br; R=Н, арил, алкил) со сплавом KNa в мощном ультразвуке [Патент US N20060106184, 2006, МКИ C08G 077/00]. Недостатками этого способа являются: использование крайне пожаро- и взрывоопасного сплава KNa, необходимость использования источника мощного ультразвука и зависимость свойств продукта от его параметров, плохая воспроизводимость реакции и низкий выход целевого продукта.
Известен способ получения поли[(R)карбинов] (R=Н, алкил, арил) путем реакции содержащего тригалоидметильную группу органического соединения CX3R (где X=Cl, Br; R=Н, арил, алкил) в механическом планетарном активаторе с магнием (Mg) без катализатора [Патент RU №2466150, 2012, МКИ C08G 077/00, G 061/00, G 061/02] и в присутствии катализатора (соли Со, Ni, Fe, Cu и др.) [Патент RU №2573568, 2016, МКИ C08G 61/02, C08G 85/00]. Недостатками этих способов являются: необходимость использования механического планетарного активатора, зависимость свойств целевого продукта от материала и состояния соприкасающихся с реакционной смесью поверхностей активатора, а также от таких факторов, как скорость вращения активатора, соотношение геометрических и весовых параметров активатора и исходных реагентов.
Наиболее близким к заявляемому является способ получения поли[(R)карбинов] путем реакции органического соединения, содержащего тригалоидметильную группу CX3R (X=Cl, Br; R=Н, алкил, арил), с солями М+(Ar-) (где M=Li, Na, K, a Ar = нафталин, антрацен и т.д.) [Известия РАН, сер.хим., 2010, №9, с. 1678-1682]. К недостаткам способа относится большая продолжительность предварительного получения солей M+(Ar-) (M=Li, Na, K; Ar = нафталин, антрацен и т.д.) (12 часов), низкая стабильность этих солей, необходимость использования щелочных металлов, загрязнение целевого продукта ареном (Ar), невысокий выход продукта (менее 70%).
Раскрытие изобретения
Технической проблемой, решаемой посредством заявляемого изобретения, является разработка безопасного и простого способа получения поли[(R)карбинов] (R=Н, алкил, арил), обеспечивающего получение продуктов со стабильным высоким выходом.
Поставленная проблема решается способом получения поли[(R)карбинов], где R=Н, алкил, арил, заключающийся в том, что к охлажденному раствору дииодида лантанида LnI2, где Ln = неодим, диспрозий, с концентрацией от 0.1М до 0.5М в органическом растворителе эфирного типа при перемешивании добавляют раствор органического соединения, содержащего тригалоидметильную группу формулы CX3R, где X=Cl, Br; R=Н, алкил или арил с концентрацией от 0.5 М до 1.5 М в том же органическом растворителе. Растворы берут в мольном соотношении 3:1, реакционной смеси дают нагреться до комнатной температуры, затем приливают воду до выпадения осадка, полученный осадок отфильтровывают, фильтрат упаривают досуха, затем растворяют в органическом растворителе эфирного типа, полученный поликарбин выделяют путем замены растворителя на галогензамещенный углеводород, с последующим высаживанием из раствора углеводородом общей формулы CnH2n+2, где n≥6. При этом в качестве органического растворителя эфирного типа используют тетрагидрофуран, диэтиловый эфир, диоксан, а в качестве галогензамещенного углеводорода используют хлористый метилен, хлороформ. Раствор дииодида лантанида LnI2 охлаждают до температуры от 263 до 195 К.
Технический результат, достигаемый при использовании заявляемого изобретения, заключается в упрощении способа синтеза поли[(R)карбинов] (R=Н, алкил, арил) за счет исключения использования специального оборудования (ультразвуковой излучатель, механический активатор), что позволяет проводить синтез в обычной химической посуде (аппаратуре) с использованием больших загрузок исходных веществ и получать значительные количества продукта из одной реакции. Преимуществом предлагаемого способа также является получение продуктов со стабильным высоким выходом (не менее 70%) по сравнению с известными из уровня техники способами. Исходные вещества, используемые в данном методе, не токсичны, их применение не требует соблюдения специальных мер безопасности.
Осуществление изобретения
Ниже представлено более подробное описание заявляемого изобретения. Настоящее изобретение может подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания. Такие изменения не ограничивают объем притязаний. Все используемые реагенты являются коммерчески доступными, все процедуры, если не оговорено особо, осуществляли при комнатной температуре (от 18 до 25°С).
Для проведения реакции предварительно синтезируют LnI2 сплавлением Ln и I2 по известному методу [J. Organomet. Chem. 2003. V. 682 Р. 218]. К охлажденному до температуры от 263 до 195 К раствору с концентрацией от 0.1М до 0.5М дииодида лантанида LnI2 (где Ln=Nd (неодим), Dy (диспрозий)) в органическом растворителе эфирного типа, в качестве которого могут быть использованы тетрагидрофуран, диэтиловый эфир, диокеан, при перемешивании добавляют в течение 10-15 минут раствор CX3R (X=Cl, Br; R=Н, арил, алкил) в том же органическом растворителе с концентрацией от 0.5 М до 1.5 М. Растворы берут в мольном соотношении 3:1. Полученной реакционной смеси дают нагреться до комнатной температуры, затем добавляют дистиллированную воду в количестве, обеспечивающем выпадение осадка, осадок фильтруют, фильтрат упаривают досуха в вакууме, затем растворяют в органическом растворителе эфирного типа, а полученный поликарбин выделяют путем замены растворителя на галогензамещенный углеводород, например, хлористый метилен или хлороформ, с последующим высаживанием из раствора углеводородом общей формулы CnH2n+2, где n≥6.
Примеры получения поли[(R)карбинов] (R=Н, алкил, арил)
Пример 1.
К охлажденному до температуры 263 К раствору 15.62 г дииодида диспрозия (DyI2) в 80 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 10-15 минут раствор 3.01 г бромоформа (CHBr3) в 10 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли дистиллированную воду (5 мл), фильтровали (стеклянный фильтр №4), упаривали досуха на роторном испарителе. Сухой остаток растворяли в 20 мл хлористого метилена (CH2Cl2) Из раствора в хлористом метилене продукт выделяли осаждением гексаном (С6Н14) (соотношение CH2Cl2: С6Н12=1:3).. Масса продукта коричневого цвета - поли(гидридокарбина) - 128 мг, что составляет 83% от теоретического.
Пример 2.
Пример 2 отличается от примера 1 тем, что реакцию проводили при температуре 195 К. Масса продукта коричневого цвета - поли(гидридокарбина) - 139 мг, что составляет 90% от теоретического.
Пример 3.
К охлажденному до температуры 195 К раствору 14.93 г дииодида неодима (NdI2) в 80 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 10-15 минут раствор 3.01 г бромоформа (CHBr3) в 10 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли воду (5 мл), фильтровали (фильтр №4), упаривали досуха. Сухой остаток растворяли в 20 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(гидридокарбина) - 142 мг, что составляет 92% от теоретического.
Пример 4.
Пример 4 отличается от примера 3 концентрацией реагирующих веществ. К раствору 6.20 г дииодида неодима (NdI2) в 160 мл тетрагидрофурана добавляли раствор 1.25 г бромоформа (CHBr3) в 10 мл сухого перегнанного тетрагидрофурана. Масса продукта коричневого цвета - поли(гидридокарбина) - 58.5 мг, что составляет 91% от теоретического.
Пример 5.
К охлажденному до температуры 195 К раствору 13.78 г дииодида диспрозия (DyI2) в 100 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 10-15 минут раствор 1.55 г 1,1,1-трихлорпропана (C2H5CCl3) в 10 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли воду (5 мл), фильтровали (стеклянный фильтр №4), упаривали досуха. Сухой остаток растворяли в 25 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(этилкарбина) - 345 мг, что составляет 80% от теоретического.
Пример 6.
Пример 6 отличается от примера 5 тем, что реакцию проводили при температуре 223 К. Масса продукта коричневого цвета - поли(этилкарбина) -365 мг, что составляет 75% от теоретического.
Пример 7.
Пример 7 отличается от примера 6 тем, что в качестве восстановителя вместо дииодида диспрозия (DyI2) использовали дииодид неодима (NdI2). К охлажденному до температуры 223 К раствору 14.87 г дииодида неодима (NdI2) в 120 мл тетрагидрофурана добавляли раствор 1.75 г 1,1,1-трихлорпропана (C2H5CCl3). Масса продукта коричневого цвета - поли(этилкарбина) - 370 мг, что составляет 76% от теоретического.
Пример 8.
К охлажденному до температуры 263 К раствору 15.74 г дииодида диспрозия (DyI2) в 100 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 10-15 минут раствор 2.34 г α,α,α,- трихлортолуола (CCl3C6H5) в 10 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли воду, фильтровали, упаривали досуха. Сухой остаток растворяли в 20 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(фенилкарбина) - 950 мг, что составляет 89% от теоретического.
Пример 9.
Пример 9 отличается от примера 8 тем, что реакцию проводили при температуре 223 К. Масса продукта коричневого цвета - поли(фенилкарбина) - 982 мг, что составляет 92% от теоретического.
Пример 10.
Пример 10 отличается от примера 9 тем, что реакцию проводили при температуре 195 К. Масса продукта коричневого цвета - поли(фенилкарбина) - 673 мг, что составляет 97% от теоретического.
Пример 11.
К охлажденному до температуры 195 К раствору 9.71 г дииодида неодима (NdI2) в 80 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 10-15 минут раствор 1.51 г α,α,α,- трихлортолуола (CCl3C6H5) в 10 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли дистиллированную воду (5 мл), фильтровали (стеклянный фильтр №4), упаривали досуха. Сухой остаток растворяли в 15 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(фенилкарбина) - 661 мг, что составляет 96% от теоретического.
Пример 12.
К охлажденному до температуры 195 К раствору 132.50 г дииодида неодима (NdI2) в 600 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 20-30 минут раствор 25.05 г бромоформа (CHBr3) в 75 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли воду (5 мл), фильтровали (стеклянный фильтр №4), упаривали досуха. Сухой остаток растворяли в 150 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(гидридокарбина) - 1.17 г, что составляет 91% от теоретического.
Пример 13.
К охлажденному до температуры 195 К раствору 170.40 г дииодида диспрозия (DyI2) в 800 мл сухого перегнанного тетрагидрофурана при перемешивании добавляли в течение 20-30 минут раствор 23.40 г α,α,α,- трихлортолуола (CCl3C6H5) в 80 мл сухого перегнанного тетрагидрофурана, реакционной смеси давали нагреться до комнатной температуры, добавляли воду (5 мл), фильтровали (стеклянный фильтр №4), упаривали досуха. Сухой остаток растворяли в 200 мл хлористого метилена (CH2Cl2) Продукт выделяли из органического слоя упариванием и очищали осаждением гексаном (С6Н14) из раствора в хлористом метилене (соотношение CH2Cl2:С6Н12=1:3). Масса продукта коричневого цвета - поли(фенилкарбина) - 9.60 г, что составляет 90% от теоретического.
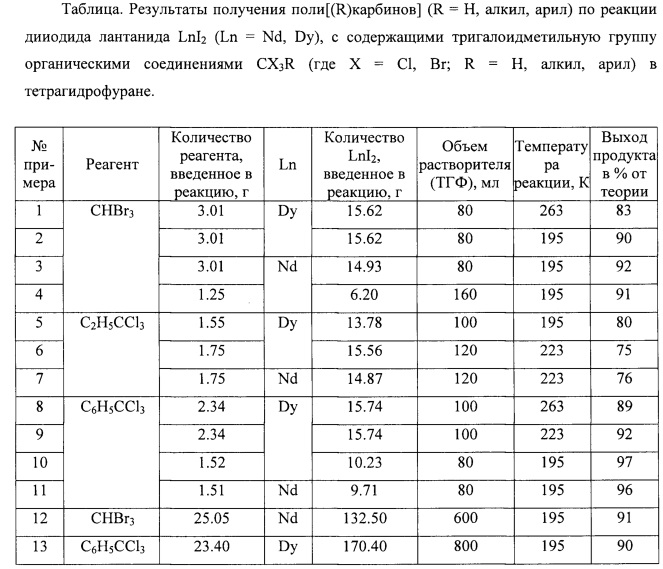
В таблице приведены данные примеров 1-13 получения поли[(R)карбинов] (R=Н, алкил, арил) по реакции дииодида лантанида LnI2 (Ln=Nd (неодим), Dy (диспрозий)) с содержащими тригалоидметильную группу органическими соединениями CX3R (где X=Cl, Br; R=Н, алкил, арил) в тетрагидрофуране.
Как видно из приведенных в таблице данных, изобретение позволяет получать поли[(R)карбины] (R=Н, алкил, арил) в одну стадию реакцией дииодида лантанида LnI2 (Ln=Nd, Dy) с содержащими тригалоидметильную группу органическими соединениями CX3R (где X=Cl, Br; R=Н, алкил, арил) в тетрагидрофуране за незначительный интервал времени (10-15 минут) (примеры 1-11), что значительно упрощает способ, причем выходы поликарбинов составляют от 75 до 80% для C2H5CCl3 (примеры 5-7), от 83 до 92% для CHBr3 (примеры 1-4), от 89 до 97% для C6H5CCl3 (примеры 8-11). Отсутствие необходимости использования специального оборудования делает возможным масштабирование эксперимента путем изменения концентраций реагирующих веществ (пример 4) или увеличением количества реагентов (примеры 12, 13) что позволяет получать необходимое количество продукта из одного синтеза, независимо от возможностей аппаратуры.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИ[(R)КАРБИНОВ] (R=H, АЛКИЛ, АРИЛ) | 2011 |
|
RU2466150C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИ[(R)КАРБИНОВ] (R=H, АЛКИЛ, АРИЛ) И КАТАЛИЗАТОР ДЛЯ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2573568C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕГИРОВАННЫХ ПОЛИ[(R)КАРБИНОВ] (R=H, АЛКИЛ, АРИЛ) | 2014 |
|
RU2575711C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ, ПРЕКАТАЛИЗАТОР ДЛЯ КАТАЛИТИЧЕСКОЙ СИСТЕМЫ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИТИЧЕСКОЙ СИСТЕМЫ | 2017 |
|
RU2676764C1 |
| 6-(ЗАМЕЩЕННЫЕ МЕТИЛЕН)ПЕНЕМЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2133750C1 |
| ПИГМЕНТ ДЛЯ ЗАЩИТНЫХ ЭЛЕМЕНТОВ МНОГОСЛОЙНЫХ ИЗДЕЛИЙ НА ОСНОВЕ ЗАМЕЩЕННЫХ ДИТИОЛЕНОВЫХ КОМПЛЕКСОВ НИКЕЛЯ С НЕСИММЕТРИЧНЫМИ ЛИГАНДАМИ | 2019 |
|
RU2703168C1 |
| Способ получения производных гексагидроазепина или пиперидина, или пирролидина (его варианты) | 1978 |
|
SU1301311A3 |
| ИНГИБИТОРЫ ДИПЕПТИДИЛПЕПТИДАЗЫ IV НА ОСНОВЕ КОНДЕНСИРОВАННЫХ ЦИКЛОПРОПИЛПИРРОЛИДИНОВ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2001 |
|
RU2286986C2 |
| 6-ГЕТЕРОЦИКЛИЧЕСКИЗАМЕЩЕННЫЕ 4-АМИНО-1,2,2А,3,4,5-ГЕКСАГИДРОБЕНЗ-(CD)-ИНДОЛЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2062775C1 |
| ЧЕТЫРЕХЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2174513C2 |
Изобретение относится к способу получения поли[(R)карбинов], где R=Н, алкил, арил, заключающийся в проведении реакции органического соединения, содержащего тригалоидметильную группу формулы CX3R, где X=Cl, Br; R=Н, алкил, арил с дииодидом лантанида LnI2, где Ln = неодим, диспрозий. Способ характеризуется тем, что к охлажденному до температуры от 263 до 195 К раствору дииодида лантанида LnI2 с концентрацией от 0.1М до 0.5М в органическом растворителе эфирного типа, при перемешивании добавляют раствор CX3R концентрации от 0.5 М до 1.5 М в том же органическом растворителе, взятые в мольном соотношении 3:1, реакционной смеси дают нагреться до комнатной температуры, затем приливают воду до выпадения осадка, полученный осадок отфильтровывают, фильтрат упаривают досуха, затем растворяют в органическом растворителе эфирного типа, полученный поликарбин выделяют путем замены растворителя на галогензамещенный углеводород с последующим высаживанием из раствора углеводородом общей формулы СnН2n+2, где n≥6. Использование предлагаемого способа позволяет получать поли[(R)карбины] (R=Н, алкил, арил) с высоким выходом без использования пожаро- и взрывоопасных или агрессивных реагентов. Помимо этого преимуществом данного способа является то, что он не требует использования специального оборудования (ультразвуковой излучатель, механический активатор), что дает возможность проводить синтез с большими загрузками исходных веществ в обычной химической посуде и, таким образом, получать значительные количества продукта из одной реакции. 2 з.п. ф-лы, 1 табл., 13 пр.
1. Способ получения поли[(R)карбинов], где R=Н, алкил, арил, заключающийся в проведении реакции органического соединения, содержащего тригалоидметильную группу формулы CX3R, где X=Cl, Br; R=Н, алкил, арил с дииодидом лантанида LnI2, где Ln = неодим, диспрозий, отличающуюся тем, что к охлажденному до температуры от 263 до 195 К раствору дииодида лантанида LnI2 с концентрацией от 0.1М до 0.5М в органическом растворителе эфирного типа при перемешивании добавляют раствор CX3R концентрации от 0.5 М до 1.5 М в том же органическом растворителе, взятые в мольном соотношении 3:1, реакционной смеси дают нагреться до комнатной температуры, затем приливают воду до выпадения осадка, полученный осадок отфильтровывают, фильтрат упаривают досуха, затем растворяют в органическом растворителе эфирного типа, полученный поликарбин выделяют путем замены растворителя на галогензамещенный углеводород, с последующим высаживанием из раствора углеводородом общей формулы СnН2n+2, где n≥6.
2. Способ по п. 1, отличающийся тем, что в качестве органического растворителя эфирного типа используют тетрагидрофуран, диэтиловый эфир, диоксан.
3. Способ по п. 1, отличающийся тем, что в качестве галогензамещенного углеводорода используют хлористый метилен, хлороформ.
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИ[(R)КАРБИНОВ] (R=H, АЛКИЛ, АРИЛ) | 2011 |
|
RU2466150C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИ[(R)КАРБИНОВ] (R=H, АЛКИЛ, АРИЛ) И КАТАЛИЗАТОР ДЛЯ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2573568C2 |
| RU 2011101298 A, 27.07.2012 | |||
| WO 2008010781 A2, 24.01.2008. | |||
Авторы
Даты
2019-10-17—Публикация
2018-11-08—Подача