Заявляемое изобретение относится к химико-фармацевтической промышленности, а именно к противовирусным фармацевтическим комбинациям, предназначенным для лечения вирусной гриппозной пневмонии.
Одним из подходов повышения эффективности действия химиопрепарата против вирусной инфекции является его использование в комбинации с другим препаратом. Преимущества комбинированной терапии заключаются в приеме более низких доз препаратов, что, в свою очередь, позволяет повысить эффективность их применения, а также снизить побочные эффекты (Govorkova Е.A., Webster R.G. Combination chemotherapy for influenza. Viruses. 2010 Aug;2(8): 1510-29 - [1]).
Кроме того, использование комбинированной терапии - это один из возможных путей предотвращения возникновения резистентных к препарату штаммов вируса.
Из уровня техники известна комбинация осельтамивира ((3R,4R,5S)-4-(Ацетиламино)-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир), римантадина (альфа-Метилтрицикло[3.3.1.13,7]декан-1-метанамин (в виде гидрохлорида) и рибавирина (1-(3-0-рибофуранозил-1 Н-1,2,4-триазол-3-карбоксамид) в культуре клеток, эффективная в отношении штаммов вируса гриппа, резистентных к римантадину и осельтамивиру (Nguyen J.T., Hoopes J.D., Le М.Н. et al.Triple combination of amantadine, ribavirin, and oseltamivir is highly active and synergistic against drug resistant influenza virus strains in vitro. PLoS One 2010; 5 (2): e9332 - [2]). Данная комбинация была успешно применена при лечении тяжелого случая гриппа, вызванного пандемическим штаммов вируса гриппа H1.
Синергидный эффект комбинации умифеновира (этиловый эфир 6-бром-5-гидрокси-1-метил-4-диметиламинометил-2-фенилтиометилиндол-3-карбоновой кислоты (в виде гидрохлорида моногидрата) с римантадином и осельтамивиром был показан в культуре клеток, при этом эффективность такой комбинации подтвердилась в клинических исследованиях (Leneva I.A. Medical agent for treating viral infections. Patentlnternational Pub. No. WO/2007/075102: International Application No.: PCT/RU2005/000677, 2007 - [3]; Ленева И.А., Федякина И.Т., Гусъкова T.A., Глушков Р.Г. Чувствительность различных штаммов вируса гриппа к арбидолу. Изучение эффекта арбидола на репродукцию вируса гриппа А в комбинации с различными противовирусными препаратами. Терапевтический архив, 2005, №8. С. 84-88 - [4]).
Показано, что наилучшие результаты дает сочетание препаратов, имеющих различный механизм действия [1].
Мишенью для применяемых в химиотерапии вируса гриппа препаратов занамивира и осельтамивира является поверхностный гликопротеид нейраминидаза, функцию которого эти препараты ингибируют.
Известен риамиловир (метилтионитрооксодигидротриазолотриазинид натрия, «Триазавирин®») - препарат семейства азолоазинов, аналог пуринового нуклеозида (гуанозина), который относится к ингибиторам синтеза вирусных РНК и репликации геномных фрагментов (Чупахин О.К, Киселев О.К, редакторы. Триазавирин - противовирусный препарат нового поколения. Монография, 2016 - [5]), который обладает широким спектром противовирусной активности и эффективен для ряда острых респираторных вирусных инфекций (Тихонова Е.П., Кузьмина Т.Ю., Андронова Н.В., Тюшевская О.А., Елисшратова Т.А., Кузьмин А.Е. Изучение эффективности противовирусных препаратов (умифеновира, триазавирина) в отношении острых респираторных вирусных инфекций (Казанский медицинский журнал, 2018 г., том 99, №2 - [6]), в том числе гриппа А и В, как в культуре клеток (Логинова С.Я., Борисевич С.В., Максимов В.А. и др. Изучение противовирусной активности триазавирина в отношении возбудителя гриппа A (H5N1). Антибиотики и химиотерапия. 2007. Т. 52. No11-12. С. 18-20 - [7], так и на модели вторичной пневмонии мышей после гриппозной инфекции (Leneva I. А., Falynskova I. N, Makhmudova N. R., Glubokova E. A., Kartasheva N. P., Leonova E. I., Mikhailova N. A., Shestakova I. V. Effect of triazavirine on the outcome of a lethal influenza infection and secondary bacterial pneumonia following influenza in mice. Microbiology Independent Research (MIR) journal. Volume 4, Number 1, 2017. P. 52-57 - [8]).
Триазавирин включен в клинические рекомендации для лечения гриппа у взрослых (Федеральные клинические рекомендации под редакцией Международной ассоциации специалистов в области инфекций (МАСОИ) «Грипп у взрослых», 2017 г. С. 32 - [9]; Клинические рекомендации ассоциаций «Национальное научное общество инфекционистов» и «Общероссийская общественная организация Российское научное медицинское общество терапевтов», 2017 г., с. 29 - [10].
Установлено, что использование риамиловира в этиотропной терапии гриппа способствует сокращению продолжительности основных симптомов заболевания, таких как интоксикация лихорадка, катаральные симптомы, а также значительно снижает частоту развития осложнений и объем симптоматической терапии.
Существующие в настоящее время данные указывают на его плейотропность. Однако, основным механизмом риамиловира, по всей вероятности, является ингибирование синтеза вирусных РНК и репликации геномных фрагментов (Триазавирин (Triazavirin) Инструкция по применению, регистрационный номер ЛП-002604 - [11]).
Техническим результатом, на достижение которого направлена предлагаемое к защите изобретение, является повышение эффективности лечения противогриппозными препаратами риамиловиром и осельтамивиром вирусной гриппозной пневмонии, сокращение продолжительности основных симптомов заболевания.
Указанный технический результат достигается тем, что комбинация противовирусных средств для лечения вирусной гриппозной пневмонии, согласно изобретению состоит из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), взятых в следующих соотношениях, мг/кг/день:
Риамиловир - 12,5 или 25,0
Осельтамивир - 5,0
Применение комбинации противовирусных средств, состоящей из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), для лечения вирусной гриппозной пневмонии по первому варианту, при котором суточная доза риаломивира составляет 12,5 мг/кг/день, а осельтамивира - 5,0 мг/кг/день.
Применение комбинации противовирусных средств, состоящей из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), для лечения вирусной гриппозной пневмонии по второму варианту, при котором суточная риаломивира составляет 25,0 мг/кг/день, а осельтамивира - 5,0 мг/кг/день.
Заявляемое изобретение поясняется чертежами, где
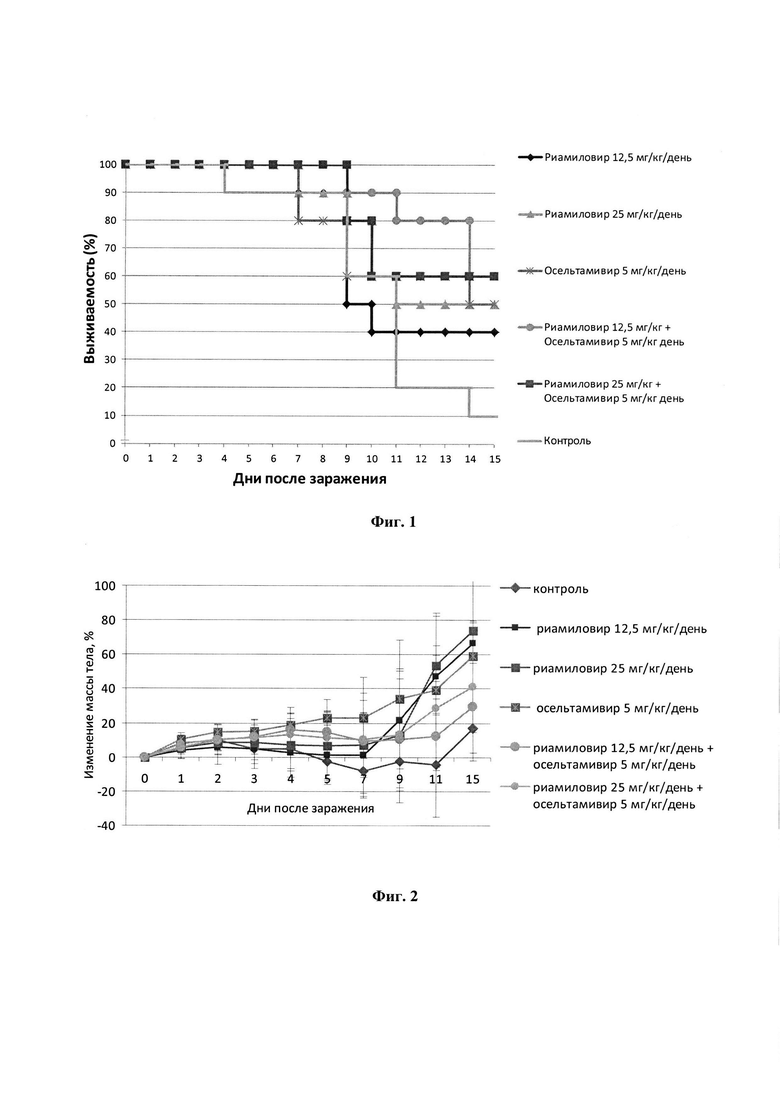
Фиг. 1 - график выживаемости мышей при лечении препаратами риамиловир, осельтамивир и их комбинациями на модели гриппозной пневмонии мышей, инфицированных низкой дозой (МЛД90) вируса гриппа (опыт I);
Фиг. 2 - график изменения массы тела мышей при лечении препаратами риамиловир, осельтамивир и их комбинациями на модели гриппозной пневмонии мышей, инфицированных низкой дозой (МЛД90) вируса гриппа (опыт I);
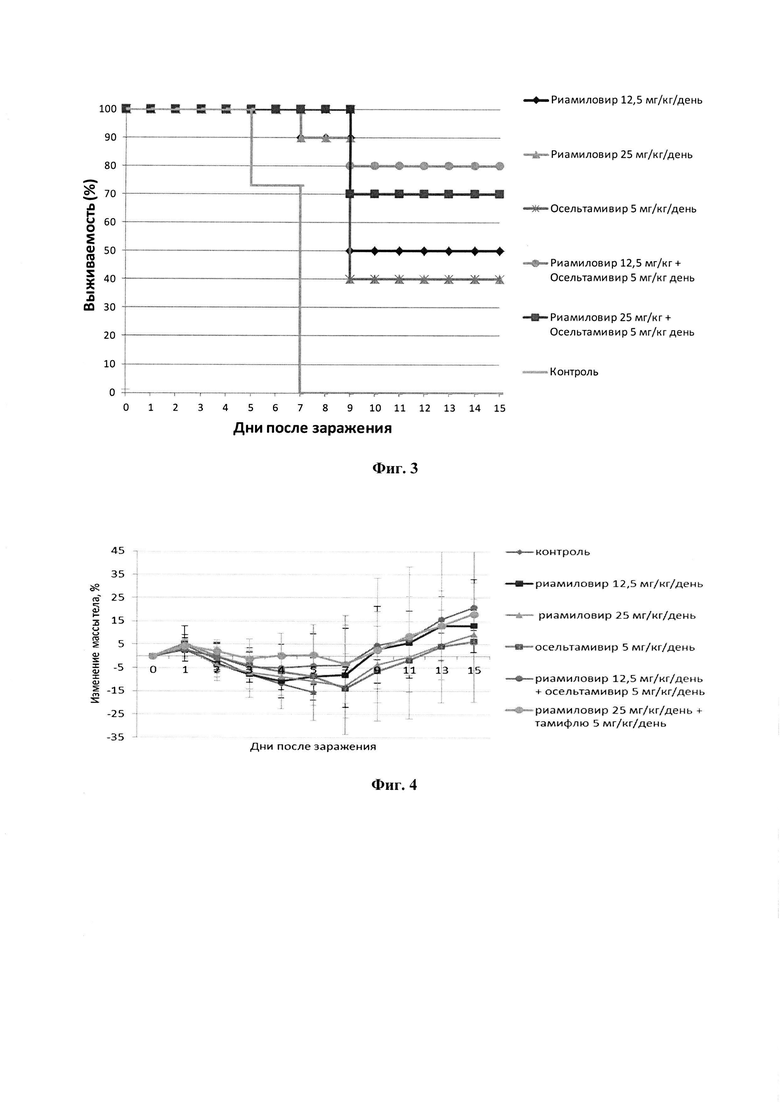
Фиг.3 - график выживаемости мышей при лечении препаратами риамиловир, осельтамивир и их комбинациями на модели гриппозной пневмонии мышей, инфицированных высокой (10МЛД50) дозой вируса гриппа (опыт II);
Фиг. 4 - график изменения массы тела мышей при лечении препаратами риамиловир, осельтамивир и их комбинациями на модели гриппозной пневмонии мышей, инфицированных высокой (10МЛД50) дозой вируса гриппа (опыт И);
Фиг. 5 - распределение очагов пневмонии на тотальных срезах легких мышей экспериментальных групп, где Гр. 1 - контрольная группа; Гр. 2 - группа, получавшая 12,5 мг/кг риамиловира; Гр. 3 - группа, получавшая 25,0 мг/кг риамиловира; Гр. 4 - группа, получавшая 5 мг/кг осельтамивира; Гр. 5 - группа, получавшая композицию, содержащую осельтамивир 5 мг/кг и риамиловир 12,5 мг/кг;
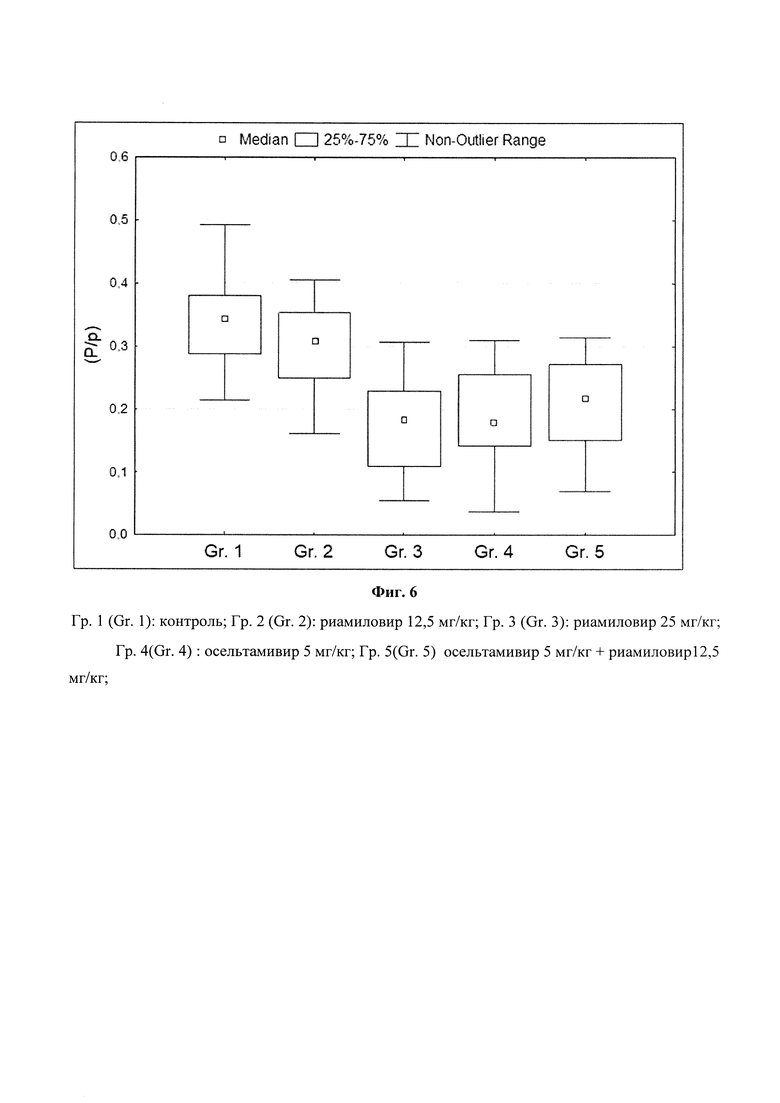
Фиг. 6 - гистограмма размаха - зависимость объемной доли воспалительного инфильтрата от примененного препарата и его дозы.
Осуществление изобретения подтверждается примерами конкретного выполнения.
Проведено изучение комбинированного действия риамиловира с противогриппозным препаратом ингибитором нейраминидазы осельтамивиром в двух сериях независимых экспериментов с использованием различных доз заражения вирусом - низкой МЛД90 (МЛД - мышиные летальные дозы) и высокой 10МЛД50. Для определения дозы вируса, содержащей МЛД90 и 10МЛД50, группы животных заражали полученным цельным аллантоисным вирусом с последовательными 10-кратными его разведениями. По данным, свидетельствующих о гибели мышей, вычислялись необходимые дозы вируса.
Для моделирования гриппозной пневмонии мышей был использован штамм вируса гриппа А/Калифорния/04/2009 (пндм H1N1 2009), полученный из Всемирной организации здравоохранения (ВОЗ) и адаптированный к мышам. Для подготовки инфицирующего материала мышей заражали интраназально аллантоисным вирусом. После проявления признаков болезни в стерильных условиях получали гомогенат легочной ткани, который затем использовали для заражения 10-дневных куриных эмбрионов, предназначенных для культивирования аллантоисного вируса. После определения инфекционной активности вируса его использовали для инфицирования животных. В обоих опытах, один из которых предусматривал инфицирование низкой дозой (МЛД90) вируса гриппа, другой -инфицирование высокой дозой (10МЛД50) вируса, использовали аликвоты одного пула вируса, который замораживали и хранили при температуре - 70°С.
В качестве лекарственных препаратов применяли субстацию риамиловира (метилтионитрооксодигидротриазоло-триазинид натрия, Триазавирин), предоставленную производителем, ООО «Завод Медсинтез», и лекарственную форму осельтамивира в виде капсул «Тамифлю», производства «Хоффманн-Ля Рош Лтд».
Перед проведением эксперимента препараты растворяли в дистиллированной воде с целью приготовления растворов для последующего их введения животным.
Дозы осельтамивира изготавливали и в дальнейшем указывали из расчета содержания чистой субстанции в лекарственной форме.
Вещества взвешивали с точностью до 0,1 мг на аналитических весах. Дозы препаратов рассчитывали в относительных весовых единицах - мг/кг массы тела животных (мышей) в сутки.
Растворы каждого из препаратов, а также их комбинации вводили животным перорально в общем объеме 200 мкл.
В качестве исследуемых доз препаратов были приняты: риамиловир - 12,5 и 25,0 мг/кг/день; осельтамивир - 5,0 мг/кг/день; а также их комбинации, содержащие риамиловира 12,5 или 25,0 мг/кг/день и осельтамивир 5,0 мг/кг/день.
Нелинейных мышей - самок весом 12-14 г, содержали на стандартном рационе в виварии. Содержание животных соответствовало правилам по устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев). Кормили животных брикетированными кормами в соответствии с утвержденными нормами. У животных был свободный доступ к воде. Маркировка животных по экспериментальным группам производилась с помощью окраски поверхности тела различными красителями.
Все эксперименты были проведены в соответствии с правилами гуманного обращения с животными и утверждены Этическим комитетом ФГНБУ НИИ вакцин и сывороток им. И.И. Мечникова, Москва.
Опыт I.
Изучение действия комбинации, состоящей из риамиловира и осельтамивира, на модели гриппозной пневмонии мышей, индуцированной низкой (МЛД90) дозой вируса гриппа, по сравнению с отдельным применением риамиловира или осельтамивира.
При определении эффективности лечения риамиловиром была использована следующая схема лечения: препарат вводили за 24 часа до инфицирования, за 4 часа до и через 4 часа после инфицирования, а далее препарат вводили 2 раза в день в течение 5 дней.
При лечении животных только осельтамивиром использовали следующую схему: препарат вводили за 1 час до инфицирования, далее - через 8 часов после инфицирования, а затем два раза в день в течение 5 дней.
Комбинацию из риамиловира и осельтамивира использовали по схеме лечения осельтамивиром.
Для перорального введения препаратов использовали одноразовый инсулиновый шприц с зондом для кормления животных.
Все животные были разделены на пять групп, каждая из которых включала по 18 особей.
Предварительно взвешенных мышей инфицировали интраназально под наркозом вирусом гриппа А/Калифорния/04/09 в дозе МЛД90.
При этом животные контрольной группы, инфицированные вирусом гриппа, не получали никакого лечения, кроме перорально вводимой дистиллированной воды в объеме 200 мкл - по схеме применения комбинации противовирусных средств.
За всеми животными, получающими и не получающими лечение, велось ежедневное наблюдение. Первые пять дней после инфицирования вирусом гриппа низкой дозы мышей взвешивали каждый день, далее взвешивания проводили через один-два дня.
Химиотерапевтическую активность лекарственных соединений на модели вирусной гриппозной пневмонии мышей оценивали по следующим критериям: выживаемость животных, увеличение средней продолжительности жизни и уменьшение снижения веса в группах животных, леченных препаратами по сравнению с контрольной группой, не получавшей лечение. Средняя продолжительность жизни мышей высчитывалась по формуле: MSD=Σf(d-1)/n, где f-количество мышей умерших на день d, выжившие мыши также включены в f и d в этом случае равно 16, n-количество мышей в группе. Уменьшение или увеличение веса рассчитывалось отдельно для каждой мыши и выражалось в процентах, при этом за 100% принимался вес животного перед инфицированием. Для всех мышей одной группы определялось среднее значение процента потери или увеличения веса.
На четвертый день после инфицирования низкой дозой вируса гриппа для определения титра вируса в легких забивали 3 животных, а на морфологическое изучение - 5. Таким образом, в каждой группе оставалось по 10 животных.
После умерщвления в каждой группе по 3 мыши у них в стерильных условиях извлекали легкие. После промывки в фосфатно-солевом буфере (ФСБ), легкие гомогенизировали и ресуспендировали в 1 мл холодного стерильного раствора ФСБ. Суспензию осветляли от клеточного дебриса центрифугированием при 2000 g в течение 10 мин. и затем супернатант использовали для определения инфекционного титра вируса в культуре клеток MDCK (Madin-Darby Canine Kidney - культура клеток почки собаки).
После умерщвления в каждой группе по 5 мышей каждому животному через трахею, используя шприц, вводили по 1 мл 10% забуференного формалина. После раздувания трахеи с помощью хирургического инструмента вскрывали грудину, извлекали легкие и помещали их в стеклянную емкость с формалином.
Легкие мышей проводили по спиртовым растворам восходящей концентрации и ксилолам в аппарате Tissue-Tek VIP5Jr. Обезвоженные образцы заливали в гистомикс на аппарате Tissue-Tek ТЕС. Тотальные ступенчатые срезы легких толщиной 4-6 мкм изготавливали на микротоме модели Microm НМ340Е, депарафинировали и окрашивали гематоксилином и эозином.
Для количественной оценки распространенности воспалительных изменений в легких, ступенчатые тотальные срезы (3 уровня) были отсканированы и объединены в единое изображение на микроскопе Axioplan 2 Imaging Carl Zeiss. Затем с помощью компьютерной программы Adobe Photoshop зоны воспалительной инфильтрации на полученных изображениях были обведены световым пером и окрашены в красный цвет. Остальные зоны срезов, без признаков воспалительного процесса обводили и окрашивали в голубой цвет. Измерение площадей проводили в морфометрической программе Image-Pro Premier 3D 9.1 Media Cibernetics Inc. Вычисляли объемную плотность (Р/р) - долю площади инфильтрата от суммарной площади среза.
Полученные цифровые данные были подвергнуты статистической обработке с использованием компьютерной программы, например, «Statistica 8.0». Поскольку количество животных в группах было небольшим и распределение не подчинялось нормальному закону распределения, были применены методы непараметрической статистики. При этом центральные тенденции были вычислены в виде медианы и нижних (25%), и верхних (75%) квартилей, а сравнение полученных данных всех групп было проведено с использованием метода множественных сравнений Kruskal-Wallis test.
Сравнение показателей выживаемости в группах животных проводили посредством однофакторного дисперсионного анализа (ANOVA) в компьютерной программе «Statistica 8.0».
Для графического представления полученных данных использован метод Каплана-Мейера.
При сравнении изменений веса мышей использовался однофакторный дисперсионный анализ для нелинейных моделей, а также четырехпараметрическая log-логистическая модель. Анализ данных выполнен в приложении R-Studio (Version 1.0.136), пакет 'drc' (С. Ritz, 2016).
В контрольной группе животных, зараженных низкой дозой вируса гриппа и не получавшей никакого лечения, начиная с четвертого дня, наблюдалась гибель мышей, при этом к 16 дню наблюдения выжила всего 1 мышь из 10 (фиг. 1).
Средняя продолжительность жизни в этой группе составила 9,5 дней (Таблица 1).
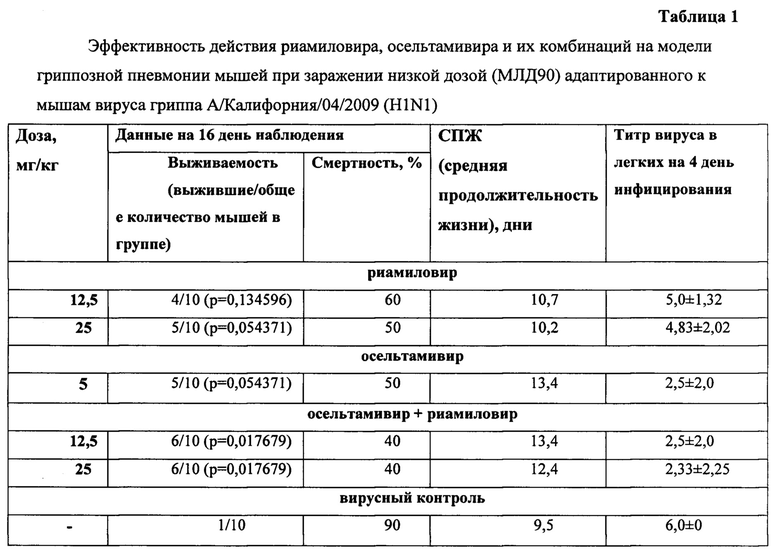
Анализ изменения массы тела животных показал, что в контрольной группе мышей, не получавших лечение, наблюдалось максимальное снижение массы тела, достигшее к 7 дню наблюдения около 15% (фиг. 2).
Лечение только риамиловиром снижало смертность животных и повышало среднюю продолжительность их жизни в дозах 12,5 и 25,0 мг/кг/день, однако эти эффекты не были статистически значимы. В этих группах также было отмечено меньшее снижение веса по сравнению с контрольной группой (фиг. 2).
Лечение только осельтамивиром в дозе 5,0 мг/кг/день было приближено по эффективности действия с лечением риамиловиром в дозах 12,5 и 25,0 мг/кг/день, защищая 40% инфицированных животных, увеличивая среднюю продолжительность их жизни (фиг. 1, 2), при этом потери веса в данной группе не наблюдалось.
Применение комбинаций риамиловира в двух дозах 12,5 и 25,0 мг/кг/день с осельтамивиром в дозе 5,0 мг/кг/день было более эффективно, чем лечение каждым из препаратов в отдельности, статистически значимо снижая гибель мышей, предотвращая потерю веса и увеличивая среднюю продолжительность жизни инфицированных и леченных животных. При комбинации риамиловира с осельтамивиром повышение дозы риамиловира с 12,5 до 25 мг/кг/день не приводило к увеличению эффективности лечения по всем параметрам.
Результаты вирусологического исследования легких исследуемых животных подтвердили данные клинической эффективности. Лечение отдельно риамиловиром во всех изученных дозах, а также только осельтамивиром в дозе 5,0 мг/кг/день, примерно одинаково, на 1,0-1,33 lg ТЦИД50 (тканевая цитопатическая инфекционная доза 50) ингибировало титр вируса, однако это ингибирование не было статистически значимым. При комбинированном использовании препаратов риаломивира и осельтамивира подавление размножения вируса в легких животных статистически значимо и составляет 3,5-3,67lg ТЦИД50 (Таблица 1).
Опыт II
Изучение комбинированного действия риамиловира с осельтамивиром на модели гриппозной пневмонии мышей индуцированной высокой (10МЛД50) дозой вируса гриппа по сравнению с отдельным применением риамиловира или осельтамивира
Во второй серии опытов была использована высокая доза заражения 10МЛД50 мышей, вызывающая более острое течение инфекции и гибель всех животных в группе вирусного контроля.
В контрольной группе животных, зараженных вирусом гриппа в дозе 10МЛД50 и не получавшей лечения, в соответствии с дозой заражения, начиная с 5 дня наблюдалась гибель, которая за два дня, т.е. к 7 дню наблюдения достигла 100% (фиг. 3). Средняя продолжительность жизни в этой группе составила 5,5 дней.
Ко дню полной гибели мышей контрольной группы лечение, как отдельно риамиловиром в двух изученных дозах 12,5 и 25,0 мг/кг/день и отдельно осельтамивиром в дозе 5,0 мг/кг/день, а также их комбинациями практически полностью предотвращало гибель животных. Лечение наиболее высокой из изученных доз риамиловира защищало от смертности треть животных, при этом потеря веса животных от вирусной гриппозной пневмонии была сравнима с группой вирусного контроля (Таблица 2, фиг. 4).

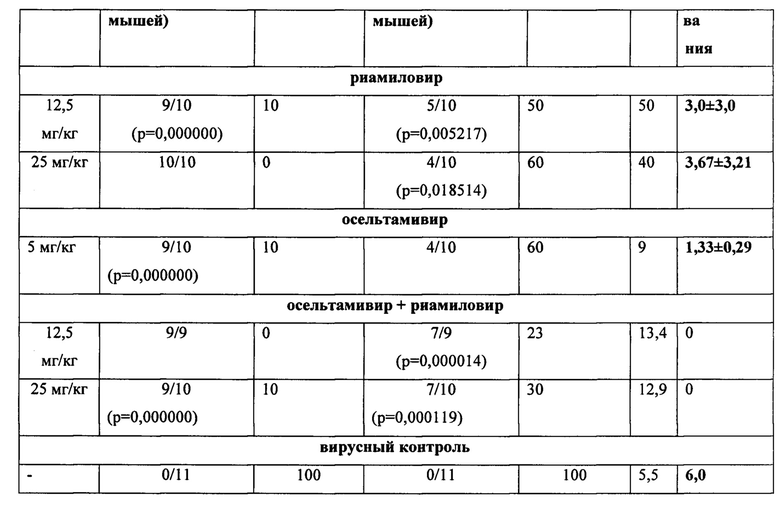
При дальнейшем наблюдении за животными было отмечено, что во всех группах леченных животных наблюдалась гибель. К концу срока наблюдения оказалось, что лечение только риамиловиром в дозах 12,5 и 25,0 мг/кг/день было сходно по эффективности с лечением осельтамивиром в дозе 5,0 мг/кг/день и защищало от смертности 40-50% животных, увеличивая продолжительность их жизни в 1,6-2 раза и снижая потерю веса.
Лечение комбинацией риамиловира в дозах 12,5 и 25,0 мг/кг/день с осельтамивиром в дозе 5,0 мг/кг/день было наиболее эффективно, чем лечение каждым из препаратов в соответствующих дозах по отдельности. Данное лечение приводило к защите от смертности 70-77% животных, увеличению их продолжительности жизни более, чем в 2 раза, и к практически полному предотвращению потери веса (фиг. 3, 4).
Лечение всеми препаратами по отдельности ингибировало размножение вируса в легких животных (Таблица 1).
Наиболее эффективное по клиническим признакам лечение комбинациями препаратов полностью подавляло размножение вируса в легких: вирус в легких таких животных не определялся.
Во всех группах в легких мышей, зараженных вирусом гриппа, выявлялись обширные очаги бронхопневмонии, просветы альвеол были заполнены лимфоцитами, макрофагами, эритроцитами и нейтрофилами. В бронхах разных порядков определялся экссудат из нейтрофилов, лимфоцитов, макрофагов, эпителий был очагово десквамирован (фиг. 5). В легких мышей, леченных только препаратом риамиловир в дозе 12,5 мг/кг/день, отличий от контрольной группы не обнаружено.
В группах мышей, леченных препаратом риамиловир в дозе 25,0 мг/кг/день, осельтамивир в дозе 5 мг/кг/день, комбинацией риамиловира в дозе 12,5 мг/кг/день и осельтамивира в дозе 5 мг/кг/день, очаги пневмонии были четко очерченными и располагались преимущественно перибронхиально, при этом в них был менее выражен геморрагический компонент.
В дополнении к качественному гистологическому изучению легких животных был проведен количественный морфометрический анализ. Данные, по количественной оценке, распространенности воспалительного процесса в легких мышей после заражения вирусами гриппа и лечения антивирусными препаратами представлены на гистограмме (фиг. 6).
В Таблице №3 представлена доверительная вероятность результатов сравнения цифровых данных.
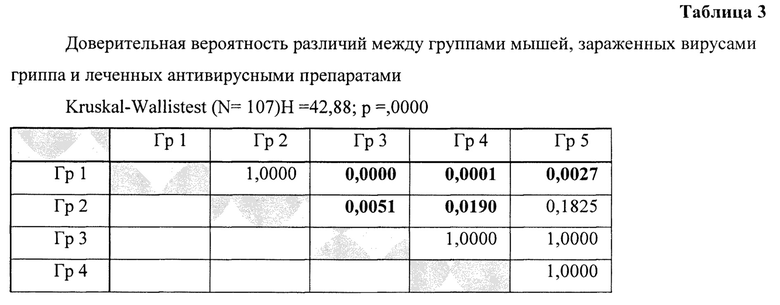
Гр. 1: - контрольная; Гр. 2: риамиловир -12,5 мг/кг; Гр. 3: риамиловир - 25,0 мг/кг;
Гр. 4: осельтамивир - 5,0 мг/кг; Гр. 5: осельтамивир 5,0 мг/кг + риамиловир 12,5 мг/кг;
По данным морфометрической оценки риамиловир в дозах 12,5 и 25,0 мг/кг не оказал терапевтического эффекта. Введение препарата осельтамивир в дозе 5,0 мг/кг оказывало терапевтический эффект - объемная плотность Р/р очагов воспалительной инфильтрации был снижен на 53% по сравнению с мышами контрольной группы.
Комбинация препаратов осельтамивира в дозе 5,0 мг/кг и риамиловира в дозе 12,5 мг/кг оказывали заметный терапевтический эффект, при этом объемная плотность Р/р воспалительного инфильтрата снижалась на 60%, по сравнению с легкими нелеченных мышей, а также по сравнению с группой животных, леченных только риамиловиром в дозе 12,5 мг/кг. Таким образом, гистологическое изучение легких полностью подтвердило данные, полученные по клиническим признакам и при вирусологическом изучении легких мышей.
В проведенных исследованиях на модели гриппозной пневмонии мышей показано, что комбинация риамиловира в дозах 12,5 или 25,0 мг/кг/день с осельтамивиром в дозе 5,0 мг/кг/день позволяет повысить эффективность лечения по сравнению с эффективностью лечения отдельно каждым из препаратов, взятых в соответствующей дозе и принимаемых по соответствующей схеме. Данное лечение на модели гриппозной пневмонии мышей статистически значимо снижало гибель животных, предотвращало потерю ими массы тела и увеличивало продолжительность жизни по сравнению с контрольной группой нелеченных животных.
Указанные комбинации препаратов при заражении низкой дозой вируса снижали размножение вируса в легких животных, а при высокой дозе заражения подавляли размножение вируса полностью. Кроме того, лечение комбинацией риамиловира в дозе 12,5 мг/кг/день с осельтамивиром оказывало влияние на состояние легких животных, уменьшая площадь очагов пневмонии. Данное исследование подтвердило, что комбинированное действие препаратов более эффективно, чем действие каждого из препаратов по отдельности. Осуществленные ранее исследования выявили, что риамиловир в модели гриппозной пневмонии мышей имеет узкое терапевтическое окно, то есть диапазон концентраций, при котором он является эффективным.
В проведенных исследованиях комбинация риамиловира с осельтамивиром позволила снизить концентрацию риамиловира без снижения эффективности его действия. В настоящее время штаммы, резистентные к риамиловиру, не выявлены ни в экспериментальной, ни в клинической практике. Резистентность к осельтамивиру при его клиническом использовании выявляется у 1,5-2,5% взрослых пациентов и достигает более высокого процента у детей (18%), а также пациентов, страдающих нарушениями иммунной системы [Hurt А.С. The epidemiology and spread of drug resistant human influenza viruses. Curr Opin Virol. 2014;8:22-29. - [12].
Применение комбинации риамиловира с осельтамивиром для лечения вирусной гриппозной пневмонии позволяет также снизить и риск возникновения резистентности к осельтамивиру. Полученные данные являются основанием для оптимизации схем и доз лечения противогриппозными препаратами риамиловиром и осельтамивиром вирусной гриппозной пневмонии.

Изобретение относится к медицине, в частности к комбинации противовирусных средств для лечения вирусной гриппозной пневмонии, а также к применению комбинации риамиловира и осельтамивира. Комбинация противовирусных средств состоит из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), взятых в следующих соотношениях, мг/кг/день: риамиловир - 12,5 или 25,0, осельтамивир - 5,0. Осуществление изобретения позволит повысить эффективность лечения противогриппозными препаратами риамиловиром и осельтамивиром вирусной гриппозной пневмонии, а также сократить продолжительность основных симптомов заболевания. 3 н.п. ф-лы, 6 ил., 3 табл.
1. Комбинация противовирусных средств для лечения вирусной гриппозной пневмонии, согласно изобретению состоит из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), взятых в следующих соотношениях, мг/кг/день:
2. Применение комбинации противовирусных средств, состоящей из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), для лечения вирусной гриппозной пневмонии, при котором суточная доза риаломивира составляет 12,5 мг/кг/день, а осельтамивира - 5,0 мг/кг/день.
3. Применение комбинации противовирусных средств, состоящей из риамиловира (метилтионитрооксодигидротриазолотриазинид натрия) и осельтамивира ((3R,4R,5S)-4-ацетиламино-5-амино-3-(1-этилпропокси)-1-циклогексен-1-карбоновой кислоты этиловый эфир, фосфат), для лечения вирусной гриппозной пневмонии, при котором суточная доза риаломивира составляет 25,0 мг/кг/день, а осельтамивира - 5,0 мг/кг/день.
| RU 2013146452 A, 27.04.2015 | |||
| (3R,4R,5S)-5-АМИНО-4-АЦИЛАМИНО-3-(1-ЭТИЛ-ПРОПОКСИ)-ЦИКЛОГЕКС-1-ЕН-КАРБОНОВЫЕ КИСЛОТЫ, ИХ ЭФИРЫ И СПОСОБ ПРИМЕНЕНИЯ | 2011 |
|
RU2469020C1 |
Авторы
Даты
2019-10-21—Публикация
2018-07-25—Подача