Изобретение относится к области медицины, а именно к хирургии и может быть использовано для предварительной диагностики стафилококковой абдоминальной хирургической инфекции.
Анализ структуры летальности у больных с абдоминальной хирургической патологией показывает, что основной причиной смерти у этих больных был и остается перитонит (Абдоминальная хирургическая инфекция: клиника, диагностика, антимикробная терапия. Практическое руководство / Под ред. B.C. Савельева, Б.Р. Гельфанда. - М.: Литтерра, 2006. - 168 с), а летальность при перитоните колеблется в пределах 18-20%, а при распространенной форме она повышается до 60%. Такой большой процент летальности у этой категории больных связан с клинически важной особенностью интраабдоминальных инфекций, во многом определяющей неудовлетворительный прогноз, заключающейся в быстром развитии генерализованной реакции макроорганизма в ответ на инфекционный процесс, обусловленной действием бактериальных эндо- и экзотоксинов и различных медиаторов воспаления.
Исследования, проведенные в клиниках России, подтверждают полимикробный характер интраабдоминальных инфекций с участием широкого спектра аэробных и анаэробных грамотрицательных и грамположительных бактерий (Гельфанд Б.Р., Гологорский В.А., Бурневич С.З. Антибактериальная терапия при отдельных формах абдоминальной хирургической инфекции. // Consilium medicum. - 2000. - №4. С. 21-26; Савельев B.C., Гельфанд Б.Р. Абдоминальная хирургическая инфекция: клиника, диагностика. Антимикробная терапия: практическое руководство 2006. - 168 с; Чернов В.Н. Неотложная хирургия: диагностика и лечение острой хирургической патологии. М., 2007. - 350 с).
Однако, в 43,62% случаев при абдоминальной хирургической инфекции из перитонеального экссудата высеивается монокультуры патогенных бактерий (Волков А.Г., Заривчацкий М.Ф. Микробный пейзаж абдоминальных хирургических инфекций у больных многопрофильного стационара // Пермский медицинский журнал. - 2014. - Том XXXI, №1. - С. 53-57).
По данным многих исследователей, в этиологии перитонита доминирующая роль принадлежит группе кишечной палочки. Доля в структуре абдоминальных микроорганизмов Escherichia coli составляет не менее 40% (Абдоминальная хирургическая инфекция. Российские национальные рекомендации. / Под ред. B.C. Савельева, Б.Р. Гельфанда. - М.: Компания БОРГЕС, 2011. - 99 с).
Однако, значимыми в этиологическом плане являются также микроорганизмы родов Staphylococcus (от 8,33 до 42,86%) (Волков А.Г., Заривчацкий М.Ф. Микробный пейзаж абдоминальных хирургических, инфекций у больных многопрофильного стационара // Пермский медицинский журнал. - 2014. - Том XXXI, №1. - С. 53-57.).
Оперирующему хирургу на участие тех или иных бактерий в развитии внутрибрюшных инфекционных процессов иногда может указать ряд клинических признаков: некроз тканей в воспалительных очагах; окрашивание экссудата в черный цвет; зловонный запах экссудата, содержимого абсцесса или раневого отделяемого, связанный с образованием кислых продуктов метаболизма при участии анаэробов. Газообразование наиболее выражено в присутствии Clostridium spp., или может быть результатом влияния некоторых факультативных аэробов; сопутствующий септический тромбофлебит и септическая эмболия сосудов печени характерны для участия в патологическом процессе бактероидов.
Однако, такая быстро получаемая информация необъективна и напрямую связана с опытом и другими субъективными качествами хирурга (Абдоминальная хирургическая инфекция. Российские национальные рекомендации. / Под ред. B.C. Савельева, Б.Р. Гельфанда. - М.: Компания БОРГЕС, 2011. - 99 с).
Поэтому единственным объективным и достоверным методом диагностики стафилококковой абдоминальной хирургической инфекции является бактериологическое исследование, регламентированное на всех этапах официальными инструкциями. Данные микробиологических исследований играют решающую роль для рациональной антибиотикотерапии абдоминальной инфекции в хирургии. Окончательную идентификацию возбудителей и определение их чувствительности к антибактериальным препаратам проводят после получения чистой культуры. Результаты нативной бактериоскопии помогают в назначении первичной эмпирической антибактериальной терапии (Ерюхин И.А., Хрупкий В.А., Бадиков В.М. http://medbe.ru/materials/infektsii-v-khirurgii/bakteriologicheskava-mikrobiologicheskaya-diagnostika-ranevoy-infektsii).
Однако, специфическая бактериологическая диагностика инфекции трудоемка, длительна и доступна немногим лечебным учреждениям: через 24-48 часов после посева культуральные и морфологические свойства выросших колоний оценивают визуально и, как правило, осуществляется пересев отдельных колоний на специализированные среды. Затем проводится идентификация штаммов на основе биохимического обнаружения специфических маркеров-ферментов или типовых метаболитов.
В крупных лечебных центрах могут использоваться ускоренные методы микрообъемной биохимической идентификации бактерий с помощью автоматических бактериологических анализаторов компаний "Bio Merieux" (Франция) или "Dade AG" (США), позволяющих сократить сроки бактериологических исследований до 4-6 ч. Указанные приборы и расходные материалы к ним имеют высокую стоимость, что ограничивает их применение (Сиволодский Е.П. Систематика и идентификация энтеробактерий. // ФБУН НИИ эпидемиологии и микробиологии имени Пастера. Отдел новых технологий / Издание третье, переработанное и дополненное. СПб, 2011. - 21 с.),
В стадии изучения клинической эффективности находятся высокотехнологичные способы диагностики доминирующих в микробной ассоциации возбудителей, независимо от их количественного содержания. К таким методам относится, к примеру, газовая хроматография, позволяющая распознать характерные метаболиты отдельных микробиотов, которые по своим микробиологическим свойствам способны выступить в качестве доминирующих патогенов (Патент РФ №2235325 от 26.08.2002 «Способ определения инфицированного выпота брюшной полости и способ лечения заболеваний, сопровождающихся выпотом в брюшную полость»).
Сюда же следует отнести современные методы генетического анализа с использованием искусственной полимеразной цепной реакции (ПЦР) (Патент РФ №2509804 от 20.03.2014 «Набор дифференцирующих и специфических олигонуклеотидов для идентификации ДНК возбудителей острых кишечных инфекций, способ идентификации ОКИ, микрочип и диагностическая система для осуществления способа»).
Недостатками всех перечисленных специфических бактериологических методов идентификации возбудителя хирургической абдоминальной инфекции являются:
- недоступность в обозримом будущем для большинства хирургических отделений из-за высокой стоимости аппаратуры, реагентов и квалифицированного персонала для обслуживания соответствующего оборудования.
- длительность и сложность исследования;
- необходимость в предварительной наработке достаточного биоматериала для исследования;
- клиницистами подвергается сомнению целесообразность всеобъемлющего микробиологического мониторинга при ведении больных с абдоминальными инфекционными процессами.
Существуют способы серодиагностики возбудителя инфекции, основанные на выявлении в крови пациентов специфических антител к различным антигенам бактерий реакциями прямой (РПГА) и непрямой гемагглютинации (РНГА), связывания комплемента (РСК) и их многочисленными модификациями (Катханов A.M., Климова Л.И., Бойко Н.А., Тлиш М.М. Способ диагностики стафилококковой инфекции // Патент РФ №2144190 от 13.01.1998; Кузнецов А.А., Кузнецов О.А., Билецкий С.Ф., Билецкая Н.И. Способ выделения и идентификации бактериальных клеток // Патент РФ №2330292 от 27.07.2008).
Основными недостатками этих способов являются:
- неэффективность серодиагностики в отношении быстроразвивающейся абдоминальной инфекции, поскольку титр специфических антител в крови нарастает в ответ на уже перенесенную инфекцию;
- невозможность применения методов серодиагностики в условиях ургентной лабораторной службы;
- серодиагностика ненадежна, поскольку уровень специфических антител к возбудителю колеблется в широких пределах в зависимости от состояния иммунной системы больного и наличия перенесенных инфекций в анамнезе.
Среди способов небактериологической диагностики инфекции существуют способы биохимической диагностики бактериальной инфекции или сепсиса, заключающиеся в исследовании крови и определении в сыворотке крови больных повышенных уровней маркерных белков (Бельков В.В. Комплексная лабораторная диагностика системных инфекций и сепсиса: С-реактивный белок, прокальцитонин, пресепсин. 2015. - 117 с; Чернов В.Н., Таранов И. И., Бабиев В. Ф. Способ диагностики анаэробной хирургической инфекции мягких тканей // Патент РФ №2073245 от 10.02.1997).
Недостатками этих способов являются:
- неэффективность в отношении диагностики микробиологической структуры абдоминальной хирургической инфекции;
- диагностика основывается на определении в крови определенной пороговой величины биохимического аналита и не свободна от различного рода ошибок измерения (в том числе, связанных с гемодилюцией).
- для установления диагноза необходимо неоднократное исследование крови у одного и того же пациента ввиду чрезвычайно широкого интервала индивидуальных значений биохимических маркерных белков.
Наиболее близким к предлагаемому нами способу является способ диагностирования бактериальной инфекции у пациента с неспецифическими жалобами, включающего следующие этапы: (i) обеспечение образца из организма пациента, поступившего с неспецифическими жалобами; (ii) определение уровня прокальцитонина (РСТ) или его фрагмента длиной как минимум 12 аминокислот в вышеупомянутом образце и (iii) определение у вышеупомянутого пациента наличия или отсутствия бактериальной инфекции путем сравнения вышеупомянутого определенного уровня РСТ с заданным пороговым уровнем (Штрук Й., Никель К., Бингиссер Р., Гирсдорф С., Хартманн О. Прокальцитонин для диагностики бактериальных инфекций и контроля лечения антибиотиками для пациентов с неспецифическими жалобами // Патент РФ №2580278 от 10.04.2016).
Недостатками прототипа являются:
- неэффективность способа для дифференциальной диагностики грамположительной и грамотрицательной абдоминальной хирургической инфекции, требующих каждая своей антибактериальной терапии;
- ограниченность способа - использование единственного параметра (уровня прокальцитонина) дает минимум диагностической информации (позволяет различать только вирусную и бактериальную инфекцию);
- высокая стоимость аппаратуры и реагентов - определение концентрации прокальцитонина на хемилюминометре в формате РСТ-теста (BRAHMS РСТ LIA sensitive) с чувствительностью 0,007 нг/мл недоступно для большинства клинических лабораторий;
- трудоемкость способа - диагностика основывается на сложных предварительных расчетах пороговых уровней прокальцитонина для каждого варианта иммуноанализа;
- неэффективность способа для обоснования этиотропной антибактериальной химиотерапии.
Изобретение направлено на повышение эффективности диагностики стафилококковой абдоминальной хирургической инфекции.
Указанный технический результат достигается тем, что у хирургических больных с послеоперационным перитонитом одновременно в сыворотке крови и перитонеальной жидкости определяют концентрации иммуноглобулина G и продуктов деградации фибриногена и вычисляют диагностический коэффициент ДК по формуле:
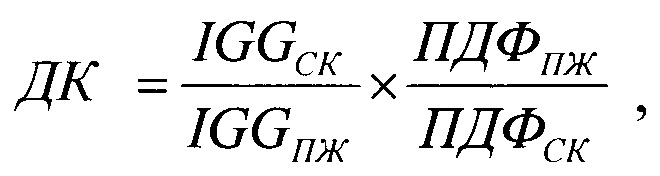
где:
ДК - диагностический коэффициент наличия стафилококковой абдоминальной хирургической инфекции;
IGGСК - концентрация иммуноглобулина G в сыворотке крови (г/л);
IGGПЖ - концентрация иммуноглобулина G в перитонеальной жидкости (г/л);
ПДФПЖ - концентрация продуктов деградации фибриногена в перитонеальной жидкости (мг/л);
ПДФСК - концентрация продуктов деградации фибриногена в сыворотке крови (мг/л);
и при значениях коэффициента ДК равных или выше 2,4 диагностируют наличие стафилококковой абдоминальной инфекции.
В предлагаемом способе предварительной диагностики стафилококковой абдоминальной хирургической инфекции, способного прогнозировать развивающуюся инфекцию у пациентов с послеоперационным перитонитом, проводится одновременное количественное определение в сыворотке крови и перитонеальной жидкости двух белков - иммуноглобулина G (IGG) и продуктов деградации фибриногена (ПДФ).
Изобретение основано на выявленном нами техническом результате, заключающемся в том, что при инфицированности перитонеальной жидкости (ПЖ) в ней обнаруживаются более высокие концентрации ПДФ, чем в сыворотке крови (СК), и наоборот, более высокие концентрации IGG в крови, чем в перитонеальной жидкости.
Получение перитонеальной жидкости посредством лаважа физиологическим раствором приводит к ее разведению и снижению истинных концентраций IGG и ПДФ, а также общего белка в ней. То есть в клинической практике абдоминального хирурга для биохимического анализа перитонеальной жидкости забирается разведенная жидкость, оттекающая по дренажам, искажающая результаты исследования.
Способ не зависит от степени разведения перитонеальной жидкости.
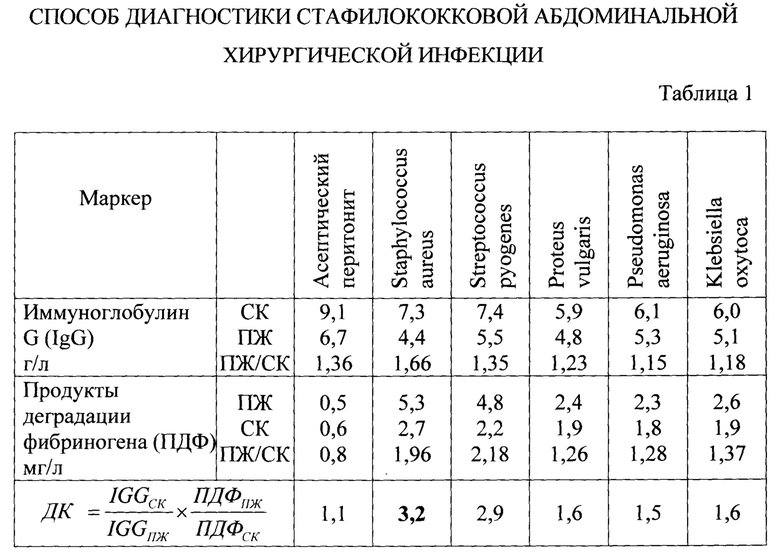
Параллельное измерение концентрации IGG и ПДФ одновременно в двух биологических жидкостях - сыворотке крови и перитонеальной жидкости позволяет рассчитать не только отношения, но и вычислить их произведение, названное нами диагностическим коэффициентом ДК. Выбор конкретных двух белков (IGG и ПДФ) для диагностики стафилококковой абдоминальной хирургической инфекции у пациентов с перитонитом объясняется не столько тем, что оба белка обладают аффинитетом к стафиллококку, сколько результатами, полученными в экспериментах на животных и в условиях хирургической клиники (Таблицы 1 и 2).
Предварительно, в экспериментах по моделированию бактериального перитонита на лабораторных крысах путем внутрибрюшинного введения монокультуры патогенных бактерий нами установлено, что в зависимости от вида возбудителя абдоминальной хирургической инфекции изменения отношение специфического белка в ПЖ и СК касаются не всех исследованных белков, а только строго определенной группы белков (Таблица 1).
Эксперименты на крысах по моделированию внутрибрюшинной инфекции монокультурой патогенных бактерий, образцы сыворотки крови и перитонеального экссудата которых были протестированы в динамике на уровни С-реактивный белок (СРБ), лактоферрин (ЛФ), продукты деградации фибриногена (ПДФ), иммуноглобулины трех классов (IgG, IgM, IgA) и лизоцим (ЛЗЦ), и их многофакторный анализ показали, что минимальным и достаточным для дифференциальной диагностики стафилококковой абдоминальной инфекции от грамотрицательной и стрептококковой является определение ДК всего для двух белков: IGG и ПДФ (Таблица 1).
То есть, перитонит у крыс, вызванный стафилококковой бактериями в дозах, равных 0,5 LD50 приводил к значительному увеличению отношений только для IGGСК / IGGПЖ до 1,66 и ПДФПЖ / ПДФСК до 1,96 (Таблица 1).
Еще более показательным и чувствительным индикатором для диагностики стафилококковой абдоминальной инфекции (Таблица 1) является произведение отношений IGGСК / IGGПЖ и ПДФПЖ /ПДФСК, названное нами диагностическим коэффициентом ДК (ДК=IGGПЖ / IGGСК×ПДФПЖ / ПДФСК).
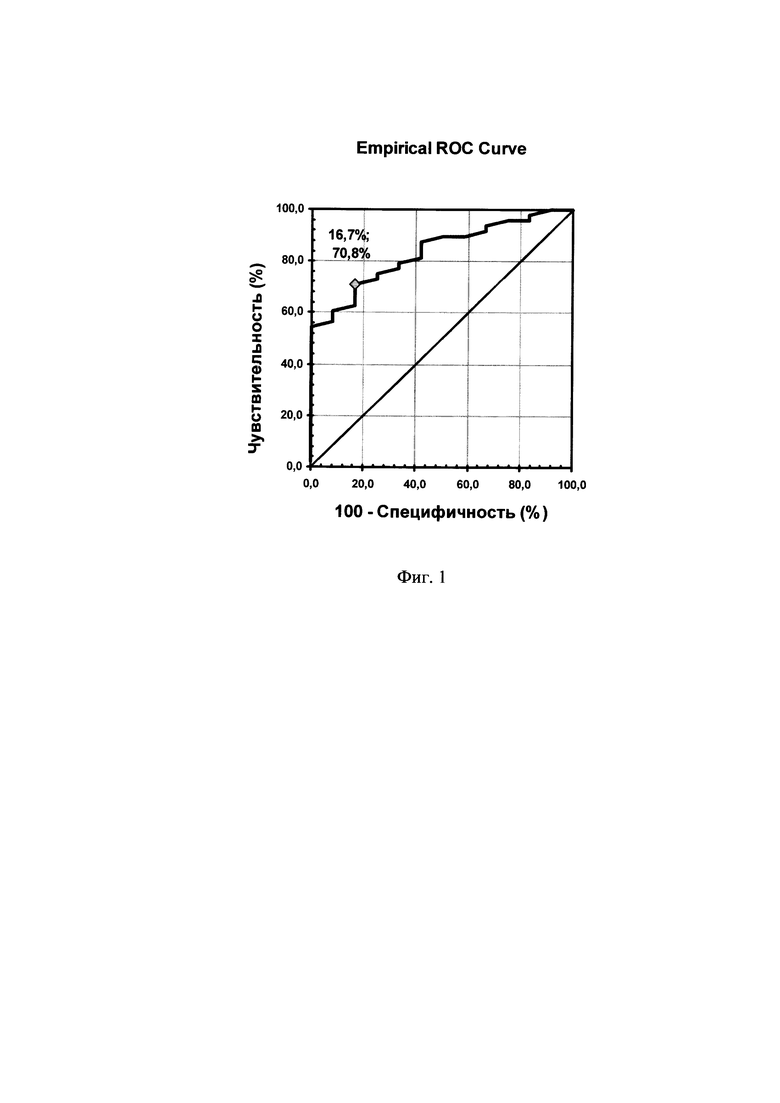
По данным ROC-анализа пороговым значением ДК, отсекающим (cut-off) наличие перитонита, вызванного грамотрицательной абдоминальной инфекцией, от перитонита с грамположительной абдоминальной инфекцией с помощью вычисления отношений IGGСК / IGGПЖ и ПДФПЖ / ПДФСК является значение ДК, равное или выше 2,4 (Фиг. 1).
ROC-кривая, объясняющая выбор порогового значения (cut-off) для диагностического коэффициента ДК, обеспечивающего максимальную диагностическую чувствительность, диагностическую специфичность и диагностическую эффективность способа диагностики стафилококковой абдоминальной хирургической инфекции, представлена на Фиг. 1.
Аналогичные результаты были получены в случаях диагностики стафилококковой инфекции у больных с распространенным гнойным перитонитом на фоне панкреонекроза, флегмонозного аппендицита или доказанного ее отсутствия у пациентов с острым деструктивным панкреатитом, осложненным разлитым ферментативным перитонитом без инфицирования перитонеального выпота.
Изложенная сущность изобретения поясняется таблицами 1 и 2 и фигурой 1.
Предлагаемый способ прошел успешную апробацию в хирургических отделениях НУЗ «Отделенческой больницы на ст. Астрахань-1» ОАО РЖД, ГБУЗ АО «Александро-Мариинской областной клинической больницы», ГБУЗ АО «Городской клинической больницы №3 им. СМ. Кирова», на кафедрах патологической физиологии, и хирургических болезней педиатрического факультета Астраханского государственного медицинского университета в течение 2016-2018 гг.
Ниже приводятся результаты апробации:
Пример 1
Исследовались отношения уровней белков и их соотношения ПЖ и СК для группы диагностически значимых белков в экспериментах на белых лабораторных крысах. Животные были распределены на 5 групп по 12 крыс, которым однократно внутрибрюшинно вводились пять различных культур условно патогенных бактерий. В 6-й группе сравнения из 30 животных воспроизводили асептический перитонит однократным внутрибрюшинным введением каррагинана в 1 мл физиологического раствора, который готовили, растворяя каррагинан (ООО Тинокс-Хим, Москва) в стерильном изотоническом растворе хлорида натрия из расчета 50 мг сухого порошка на ампулу (10 мл).
Для заражения животных использовали суточные агаровые культуры аэробных грамположительных бактерий: Staphylococcus aureus, Streptococcus pyogenes (серовар А) и аэробных грамотрицательных бактерий: Proteus vulgaris, Pseudomonas aeruginosa, Klebsiella oxytoca, приготовленные на 0,9% растворе натрия хлорида. Внутрибрюшинное заражение животного проводили инъекцией предварительно оттитрованных доз, содержащих в объеме 0,5 мл 1×108 микробных тел стафилококка и стрептококка и 1×107 микробных тел протея, клебсиеллы и синегнойнои палочки. Выбор этих 5 штаммов бактерий объясняется наиболее частым обнаружением именно их в перитонеальном экссудате при разлитом гнойном перитоните. Выбор дозы каждой бактериальной культуры обеспечивал 0,5 LD50 и обеспечивал выживание всех лабораторных животных более 3-х суток. Для замедления резорбции бактерий в кровь и профилактики летального сепсиса всем животным одномоментно с заражением внутрибрюшинно вводился раствор каррагинана по схеме и в дозах животных 6-й группы сравнения. Через 48 часов после внутрибрюшинных инъекций под эфирным наркозом путем декапитации осуществляли эвтаназию животных с последующим забором материала.
Материалом для исследования служила сыворотка крови лабораторных животных, полученной из яремной вены, и цельный перитонеальный экссудат, полученный аспирацией брюшной полости пастеровской пипеткой.
Количественное определение продуктов деградации фибриногена (ПДФ) проводились методом иммунодиффузионного анализа (ИДА) в агаре по O.Ouchterlony в модификации Н.И. Храмковой и Г.И. Абелева с помощью иммунохимических тест-систем, разработанных на кафедре биологической химии ФГБОУ ВО «Астраханский ГМУ» Минздрава России, чувствительность метода 3,5 мг/л. Концентрации иммуноглобулинов IgG, IgM и IgA определяли методом радиальной иммунодиффузии (РИД) в агаре по методу Манчини по инструкциям фирм-производителей. Содержание общего белка в образцах перитонеальной жидкости и сыворотках крови крыс определяли спектрофотометрически при 280 и 260 нм по Варбургу.
Так как концентрация общего белка в перитонеальной жидкости крыс соответствовала ее концентрации в сыворотке крови, то фактор F=1.
Средние концентрации IGG и ПДФ в перитонеальной жидкости (ПЖ) и сыворотке крови (СК), их отношение (ПЖ/СК) и диагностический коэффициент ДК после моделирования у крыс перитонита различными штаммами грамположительных и грамотрицательных бактерий показаны в таблице 1.
Особенностью иммуноглобулина G (IgG), в отличие от других исследованных белков, является то, что его концентрация при перитонитах в перитонеальной жидкости всегда ниже, чем в сыворотке крови, независимо от причины перитонита. После внутрибрюшинной инъекции всех трех штаммов грамотрицательных бактерий: Proteus vulgaris, Pseudomonas aeruginosa, Klebsiella oxytoca, грамположительного Streptococcus pyogenes и при асептическом перитоните, вызванном внутрибрюшинной инъекцией каррагинана, концентрация IgG в перитонеальной жидкости крыс была достоверно (P(U)<0,01) на 15-35% ниже, чем концентрация IgG в сыворотке крови этих же крыс. И только при перитоните, вызванном внутрибрюшинной инъекцией Staphylococcus aureus, концентрация IgG в перитонеальной жидкости крыс статистически достоверно снижалась более, чем в 1,5 раза от концентрации IgG в крови (IgGСК / IgGПЖ=1,66) (Таблица 1).
Средняя концентрация ПДФ в перитонеальной жидкости крыс достоверно (P(U)<0,01) выше, чем уровень ПДФ в сыворотке крови этих же крыс только после внутрибрюшинной инъекции грамположительных бактерий Staphylococcus aureus и Streptococcus pyogenes и достоверно не отличалась от уровня ПДФ в крови при асептическом перитоните и перитоните, вызванном внутрибрюшинной инъекцией штаммов грамотрицательных бактерий: Proteus vulgaris, Pseudomonas aeruginosa, Klebsiella oxytoca (Таблица 1).
Диагностический коэффициент ДК у крыс с перитонитом после внутрибрюшинного заражения стафилококковой абдоминальной инфекцией составил:
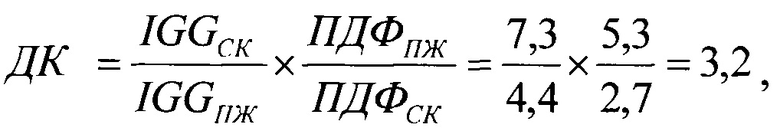
а при внутрибрюшинном заражении стрептококком - ДК=2,9 (Таблица 1).
Аналогичные значения ДК после внутрибрюшинного заражения крыс грамотрицательными бактериями: для Proteus vulgaris и для Klebsiella oxytoca ДК=1,6, для Pseudomonas aeruginosa ДК=1,5 (Таблица 1).
Таким образом, при ДК, равном или выше 2,4, с высокой степенью достоверности диагностируют наличие именно стафилококковой абдоминальной инфекции.
Пример 2
Пациент И., 69 лет, поступил в отделение экстренной хирургии ГКБ №3 27.09.2016 г. с диагнозом: острый панкреатит. По результатам физикального осмотра больной был помещен в палату интенсивной терапии. Назначено консервативное лечение. В течение суток состояние больного не улучшилось, несмотря на проводимое лечение, ЧСС - 114 в мин, ЧДД - 35 в мин, увеличился лейкоцитоз, температура тела поднялась до 38°С, нарастала амилазная активность. Общий анализ крови: эритроциты 4,05×1012/л; Hb - 113 г/л; Le - 11,2×109/л, ЛИИ=8,1, СОЭ - 10 мм/час, биохимический анализ крови: общий белок - 41 г/л, креатинин - 178 ммоль/л, мочевина - 21,5 ммоль/л, глюкоза крови - 5,7 ммоль/л, α-амилаза - 49 г/л*ч, липаза - 505 г/л*ч, диастаза мочи - 658 г/л*ч. Сывороточный уровень иммуноглобулина G (IGG) - 6,5 г/л, продуктов деградации фибриногена (ПДФ) - 2,3 мг/л.
УЗ-заключение: «Эхографические признаки увеличения панкреатогенного инфильтрата, неоднородность структуры инфильтрата с множеством мелких анэхогенных образований правильной округлой формы до 0,5-1 мм в диаметре (пузырьки газа), по контуру образования, в левом и правом забрюшинном коллекторах визуализируется жидкость с небольшим количеством гиперэхогенной взвеси. Гепатомегалия. Эхографические признаки диффузных изменений в печени, конкрементов в желчном пузыре». МСКТ-заключение: «Увеличение размеров ПЖ, неоднородность изображения паренхимы, определяются ограниченные жидкостные образования в забрюшинной клетчатке». Вечером того же дня пациенту была выполнена диагностическая видеолапароскопия с дренированием и санацией брюшной полости. Под контролем УЗИ проведен забор экссудата (1,5 мл) из брюшной полости. Диагностирован парез кишечника тяжелой степени.
В перитонеальном экссудате определена концентрации иммуноглобулина G (IGG) - 4,2 г/л и продуктов деградации фибриногена (ПДФ) - 5,1 мг/л, необходимых для способа диагностики.
Согласно способу диагностики проведено определение ДК по формуле:
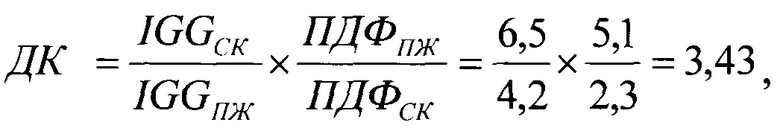
что свидетельствовало о наличии у пациента стафиллококковой абдоминальной инфекции и высоком риске перехода стерильного панкреонекроза в панкреонекроз, инфицированный стафиллококком. Больному назначена мощная антибактериальная, иммуномодулирующая и дезинтоксикационная терапия.
В течение следующих суток состояние пациента продолжало ухудшаться. 28.09.2016 г. больному была выполнена лапаротомия. Вскрытие, санация и дренирование сальниковой сумки, брюшной полости, забрюшинного пространства. Холецистэктомия. Проведено дренирование холедоха по Пиковкому.
Полученные результаты бактериологического посева перитонеального выпота брюшной полости выявили рост колоний Staphylococcus aureus и подтвердили результат диагностики по предложенному нами способу.
После оперативного лечения и коррекции лекарственной терапии отмечалась медленное улучшение лабораторных и биохимических показателей. Клинически у пациента в послеоперационном периоде достаточно длительное время сохранялась гипертермия. Постепенно купировались признаки эндогенной интоксикации, пришли в норму лабораторные показатели. На контрольных УЗИ и МСКТ отмечалась положительная диамика. Пациент выписан на 24 сутки в удовлетворительном состоянии.
При осмотре через 1 месяц - жалоб не предъявляет.
Основной диагноз: Острый некротизирующий панкреатит.
Осложнение основного диагноза: Оментобурсит. Абсцессы сальниковой сумки. Флегмона забрюшинного пространства. Разлитой гнойный перитонит.
Концентрации IGG и ПДФ в перитонеальной жидкости (ПЖ) и сыворотке крови (СК), их отношение (ПЖ/СК) и диагностические коэффициенты ДК у пациентов с перитонитами из примеров 2, 3 и 4 представлены в таблице 2.
Пример 3
Пациентка К., 57 лет. Поступила в отделение интенсивной терапии и реанимации ГКБ №3 11.12.2017 г. с направительным диагнозом: острый деструктивный панкреатит. УЗИ-заключение: «Эхоструктурные признаки диффузного увеличения поджелудочной железы, острого панкреатита, оментобурсита, инфильтрации забрюшинной клетчатки. Гепатомегалия, диффузные изменения в печени». Операция - лапароскопическое дренирование брюшной полости, сальниковой сумки. Длительность заболевания - трое суток, температура - 38° С, ЧСС - 88 в мин, ЧДД - 18 в мин. Общий анализ крови: эритроциты 4,37×1012/л; Hb - 121 г/л; Le - 9,8×109/л, ЛИИ=7, СОЭ - 12 мм/час, биохимический анализ крови: общий белок - 56 г/л, креатинин - 256 ммоль/л, мочевина - 9,3 ммоль/л, глюкоза крови - 5,8 ммоль/л, α-амилаза - 43 г/л*ч, липаза - 402 г/л*ч, диастаза мочи - 256 г/л*ч. Сывороточный уровень иммуноглобулина G (IGG) - 7,4 г/л, продуктов деградации фибриногена (ПДФ) - 3,6 мг/л
Согласно способу диагностики в перитонеальной жидкости определена концентрация иммуноглобулина G (IGG) - 6,2 г/л, продуктов деградации фибриногена (ПДФ) - 4,7 мг/л.
Определение ДК по формуле согласно способу диагностики:
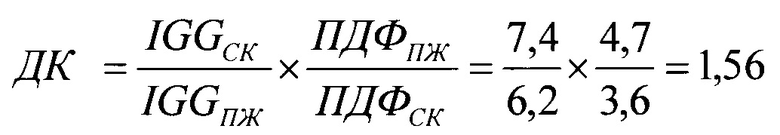
свидетельствует об отсутствии стафилококковой абдоминальной инфекции.
Для данной пациентки была определена возможность консервативного лечения; на третьи сутки у пациентки постепенно нормализовалась температура тела, купировались признаки эндогенной интоксикации, нормализовались лабораторные показатели, данные УЗИ. На 12 сутки удален дренаж из сальниковой сумки. Больная выписана на амбулаторное долечивание в удовлетворительном состоянии на 18 сутки.
Основной диагноз: Острый некротизирующий панкреатит. Осложнение основного диагноза: Оментобурсит. Разлитой ферментативный перитонит.
Таким образом, ДК подтвердил отсутствие панкреонекроза, инфицированного стафилококковой микрофлорой. Разлитой ферментативный перитонит не перешел в инфицированный, что на ранних стадиях лечения было спрогнозировано результатом диагностики по предложенному нами способу.
Пример 4
Больной С. заболел 07.01.16 года, за медицинской помощью не обращался. Больной доставлен машиной скорой медицинской помощи 10.01.16 года в тяжелом состоянии, в сознании, вялый, температура кожных покровов 39,4°С. Кожные покровы бледного цвета сухие на ощупь, выражен спазм периферических сосудов. ЧСС 108 уд. в 1 минуту, ЧДД 24 в 1 минуту. Живот вздут, болезнен при пальпации. Положителен симптом Щеткина-Блюмберга. Перистальтика вялая единичными волнами. Общий анализ крови: эритроциты 3,37×1012/л; Hb - 118 г/л; Le - 15,4×109/л. СОЭ - 8 мм/час. Д-з: Перитонит. На операции: острый гангренозно-перфоративный аппендицит. Разлитой гнойный перитонит.
Для лечения в послеоперационном периоде больной был переведен в реанимационное отделение. Состояние больного продолжало оставаться тяжелым. Температура кожных покровов держалась на фибрильных цифрах: 38,0-38,9°С. ЧСС 100-108 уд./мин.; ЧДД 28-30 дыханий в 1 минуту. Живот вздут, перистальтика вялая, неравномерная по всему животу. Общий анализ крови: эритроциты 3,37×10/л; Hb - 99 г/л; Le - 10,6×109/л. СОЭ - 11 мм/час, биохимический анализ крови: общий белок - 48 г/л, креатинин - 154 ммоль/л, мочевина - 12,6 ммоль/л, глюкоза - 6,4 ммоль/л, ЛИИ - 5,7 у.е., иммуноглобулина G (IGG) - 6,1 г/л, продуктов деградации фибриногена (ПДФ) - 2,4 мг/л. Биохимический анализ перитонеальной жидкости: общий белок: 39 г/л, иммуноглобулина G (IGG) - 5,6 г/л, продуктов деградации фибриногена (ПДФ) - 5,3 мг/л.
Согласно способу диагностики проведено определение ДК по формуле
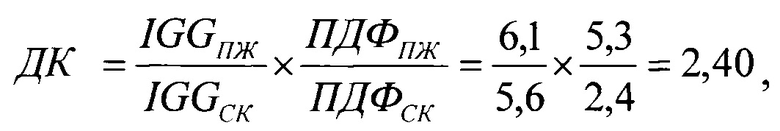
что свидетельствовало о наличии у пациента стафилококковой абдоминальной инфекции.
Результаты бактериологического исследования перитонеального экссудата, полученные спустя три дня после операции, выявили как грамотрицательные штаммы Proteus vulgaris, Pseudomonas aeruginosa, так и наличие в экссудате грамположительной кокковой микрофлоры (Staphylococcus aureus, Streptococcus pyogenes), что соответствовало результатам диагностики по предложенному способу.
Больному проводилась инфузионная терапия, включающая в себя растворы кристаллоидов, коллоиды, 10% раствор глюкозы, антибактериальное лечение, сердечные препараты и витамины.
13 и 14 января 2016 года состояние больного оставалось стабильно среднетяжелым. Температура кожных покровов держалась на субфебрильных и низких фебрильных цифрах: 37,2-38,0°С. ЧСС 90-92 уд./мин., ЧДД 24-26 дыханий в 1 минуту.
19 января 2016 года больной был взят в операционную и оперирован. На операции обнаружены межпетлевые абсцессы. Абсцессы вскрыты, брюшная полость промыта и ушита наглухо. В первые послеоперационные сутки у больного сохранялась интоксикация тяжелой степени. В последующем послеоперационный период протекал гладко и изучаемые показатели постепенно пришли к норме. 9 февраля 2016 года больной был выписан из больницы.
Данный пример показывает, что способ диагностики позволяет заблаговременно на начальных стадиях перитонита прогнозировать возможное развитие стафилококковой абдоминальной инфекции.
Предлагаемым способом достигается повышение эффективности диагностики наличия стафилококковой абдоминальной инфекции у хирургических больных с подозрением на послеоперационный перитонит, а именно:
- повышение диагностической специфичности до 83% и диагностической чувствительности до 71% (для порогового значения ДК=2,4). Площадь под кривой (AUC), отражающая диагностическую эффективность способа, составила 0,844 (в прототипе - 0,721).
- высокая скорость иммуноферментного анализа белков, входящих в данный способ обеспечивает быстрое получения результата исследования;
- доказательное назначение антибактериальных средств;
- раннее начало целенаправленной антибактериальной химиотерапии;
- техническая простота, незначительные трудозатраты (для практического исполнения способа достаточно 1 лаборанта);
- доступность способа для хирургического отделения любого звена здравоохранения;
- экономичность (способ не требует эксклюзивного и дорогостоящего оборудования и реактивов, вспомогательной аппаратуры и высококвалифицированного медперсонала), выполняемые анализы имеют низкая стоимость;
Предлагаемый способ дает возможность прогнозировать развитие послеоперационных инфекционных осложнений в брюшной полости.
Предлагаемый способ может быть внедрен в любом хирургическом отделении для экспресс-диагностики наличия стафилококковой абдоминальной хирургической инфекции, опережающей результаты бактериологического исследования, и своевременного начала этиотропной антибактериальной терапии.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики стрептококковой абдоминальной хирургической инфекции | 2019 |
|
RU2705385C1 |
| Способ диагностики грамотрицательной абдоминальной хирургической инфекции | 2019 |
|
RU2705384C1 |
| СПОСОБ ВЫБОРА ЭНТЕРАЛЬНОЙ ДЕТОКСИКАЦИИ ПРИ РАСПРОСТРАНЕННОМ ПЕРИТОНИТЕ | 2003 |
|
RU2241227C1 |
| Способ диагностики бактериальной абдоминальной хирургической инфекции при аппендиците | 2023 |
|
RU2823995C1 |
| СПОСОБ ДИАГНОСТИКИ ПОСЛЕОПЕРАЦИОННОГО ПЕРИТОНИТА | 2011 |
|
RU2456621C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ЭНТЕРАЛЬНОЙ ДЕТОКСИКАЦИИ ПРИ РАСПРОСТРАНЕННОМ ПЕРИТОНИТЕ | 2003 |
|
RU2247392C1 |
| СПОСОБ ДИАГНОСТИКИ ГНОЙНО-НЕКРОТИЧЕСКОЙ ДЕСТРУКЦИИ В ПРИДАТКАХ МАТКИ ПРИ ОТГРАНИЧЕННОМ ПЕРИТОНИТЕ | 2009 |
|
RU2402778C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА У БОЛЬНЫХ С ВОСПАЛИТЕЛЬНЫМИ ЗАБОЛЕВАНИЯМИ В ПРИДАТКАХ МАТКИ ПОСЛЕ ОРГАНОСОХРАНЯЮЩИХ ВМЕШАТЕЛЬСТВ ЛАПАРОСКОПИЧЕСКИМ ДОСТУПОМ | 2008 |
|
RU2389437C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭКСТРАПЕРИТОНЕАЛЬНЫХ ОСЛОЖНЕНИЙ ПРИ РАСПРОСТРАНЕННОМ ПЕРИТОНИТЕ | 2003 |
|
RU2242010C1 |
| Способ моделирования интраперитонеального стафилококкового инфекционного процесса | 2019 |
|
RU2723745C1 |
Изобретение относится к медицине, а именно к хирургии, и может быть использовано для диагностики стафилококковой абдоминальной хирургической инфекции. Проводят исследование биологических жидкостей. У хирургических больных с послеоперационным перитонитом одновременно в сыворотке крови и перитонеальной жидкости определяют концентрации иммуноглобулина G и продуктов деградации фибриногена. Вычисляют диагностический коэффициент ДК по формуле:
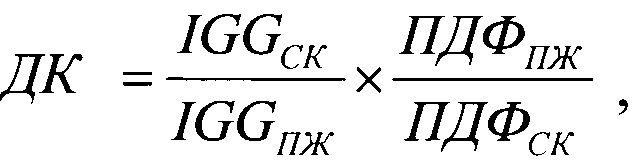
где: ДК - диагностический коэффициент наличия стафилококковой абдоминальной хирургической инфекции; IGGСК - концентрация иммуноглобулина G в сыворотке крови (г/л); IGGПЖ - концентрация иммуноглобулина G в перитонеальной жидкости (г/л); ПДФПЖ - концентрация продуктов деградации фибриногена в перитонеальной жидкости (мг/л); ПДФСК - концентрация продуктов деградации фибриногена в сыворотке крови (мг/л). При значениях коэффициента ДК равных или выше 2,4 диагностируют наличие стафилококковой абдоминальной инфекции. Способ обеспечивает повышение эффективности диагностики стафилококковой абдоминальной хирургической инфекции за счет одновременного количественного определения в сыворотке крови и перитонеальной жидкости двух белков – иммуноглобулина G и продуктов деградации фибриногена. 1 ил., 2 табл., 4 пр.
Способ диагностики стафилококковой абдоминальной хирургической инфекции, заключающийся в исследовании биологических жидкостей, отличающийся тем, что у хирургических больных с послеоперационным перитонитом одновременно в сыворотке крови и перитонеальной жидкости определяют концентрации иммуноглобулина G и продуктов деградации фибриногена и вычисляют диагностический коэффициент ДК по формуле:
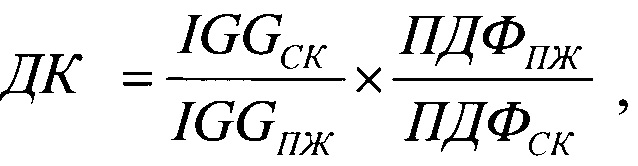
где:
ДК - диагностический коэффициент наличия стафилококковой абдоминальной хирургической инфекции;
IGGСК - концентрация иммуноглобулина G в сыворотке крови (г/л);
IGGПЖ - концентрация иммуноглобулина G в перитонеальной жидкости (г/л);
ПДФПЖ - концентрация продуктов деградации фибриногена в перитонеальной жидкости (мг/л);
ПДФСК - концентрация продуктов деградации фибриногена в сыворотке крови (мг/л);
и при значениях коэффициента ДК равных или выше 2,4 диагностируют наличие стафилококковой абдоминальной инфекции.
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНФИЦИРОВАННОГО ВЫПОТА БРЮШНОЙ ПОЛОСТИ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ ВЫПОТОМ В БРЮШНУЮ ПОЛОСТЬ | 2002 |
|
RU2235325C2 |
| НАБОР ДИФФЕРЕНЦИРУЮЩИХ И СПЕЦИФИЧЕСКИХ ОЛИГОНУКЛЕОТИДОВ ДЛЯ ИДЕНТИФИКАЦИИ ДНК ВОЗБУДИТЕЛЕЙ ОСТРЫХ КИШЕЧНЫХ ИНФЕКЦИЙ, СПОСОБ ИДЕНТИФИКАЦИИ ОКИ, МИКРОЧИП И ДИАГНОСТИЧЕСКАЯ СИСТЕМА ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2010 |
|
RU2509804C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕЦИДИВИРУЮЩЕГО И ПОВТОРНОГО ДИАЛИЗНОГО ПЕРИТОНИТА СТАФИЛОКОККОВОЙ ЭТИОЛОГИИ | 2011 |
|
RU2449273C1 |
| RU 2007128172 A, 27.11.2009 | |||
| СПОСОБ ВЫДЕЛЕНИЯ И ИДЕНТИФИКАЦИИ БАКТЕРИАЛЬНЫХ КЛЕТОК | 2003 |
|
RU2330292C2 |
| US 20160244511 A1, 25.08.2016 | |||
| WO 2012059556 A1, 10.05.2012. | |||
Авторы
Даты
2019-11-07—Публикация
2019-01-10—Подача