ОБЛАСТЬ И УРОВЕНЬ ТЕХНИКИ
Настоящее изобретение относится к способам лечения болезней с использованием адгезивных клеток жировой ткани или плаценты - а именно, к способам лечения ишемии и/или заболеваний, при которых требуется регенерация и/или восстановление соединительной ткани, с помощью адгезивных клеток.
Во всем мире медицина испытывает растущую потребность в больших количествах зрелых стволовых клеток для их использования в целях вживления клеток и тканевой инженерии. Кроме того, непрерывно развиваются методы терапевтического применения зрелых стволовых клеток с целью лечения и заживления поражений при таких патологических состояниях как расстройства гемопоэза, заболевания сердца, болезнь Паркинсона, болезнь Альцгеймера, инсульт, ожоги, мышечная дистрофия, аутоиммунные расстройства, сахарный диабет и артрит.
В последние годы внимание исследователей было в значительной степени сконцентрировано на терапевтическом потенциале мезенхимальных стромальных клеток (МСК; MSCs) при их использовании в связи с различными медицинскими показаниями, включая восстановление тканей поврежденных органов (например, головного мозга, сердца, костей и печени), а также с целью поддержки трансплантации костного мозга (ТКМ; ВМТ). МСК - это разнородная популяция клеток, получаемых, например, из костного мозга, жировой ткани, плаценты и крови, способная дифференцироваться в различные типы зрелых мезенхимальных клеток (например, ретикулоэндотелиальные клетки, фибробласты, адипоциты, остеогенные клетки-предшественники) в зависимости от воздействий, оказываемых разнообразными биологически активными факторами. Соответственно, МСК широко исследуются специалистами в области регенеративной медицины с целью их использования в качестве основы для формирования новых тканей (например, костной, хрящевой и жировой ткани), необходимых для восстановления повреждений или замены патологически измененных тканей, а также в качестве средства лечения наследственных и приобретенных заболеваний [Fibbe и Noort, Ann Ν Y Acad Sci (2003) 996: 235-44; Horwitz с соавт., Cytotherapy (2005) 7(5): 393-5; Zimmet и Hare, Basic Res Cardiol (2005) 100(6): 471-81]. Кроме того, МСК, благодаря их полипотентности простоте выделения и культивирования, а также высокому потенциалу экспансии ex vivo, являются привлекательным материалом для изучения в качестве возможного терапевтического средства [Fibbe и Noort, см. выше; Minguell с соавт. Exp Biol Med (Maywood) (2001) 226(6): 507- 20].
Плацентарные МСК имеют большое количество общих маркеров с МСК, выделяемыми из других тканей (например, CD105, CD73, CD90 и CD29), и демонстрируют отсутствие экспрессии клеточных маркеров, специфичных для гемопоэтических, эндотелиальных и трофобластных клеток. При культивировании плацентарных МСК в соответствующих условиях достигалась адипогенная, остеогенная и нейрогенная дифференцировка клеток [Yen с соавт., Stem cells (2005) 23(1):3-9]. Кроме того, было показано, что МСК, выделенные из плаценты и культивированные in vitro, характеризуются наличием той же иммунологической привилегированности, которая свойственна МСК. Таким образом, плацента является этически непротиворечивым и легкодоступным источником МСК для экспериментального и клинического применения [Zhang с соавт., Exp Hematol (2004) 32(7): 657- 64].
Данные изобретатели ранее разработали условия трехмерного культивирования (3D), пригодные для экспансии плацентарных МСК (заявка РСТ №IL2007/000380), полностью включенная в данный документ посредством ссылки на нее.
Ниже суммированы основные виды клинического применения МСК.
Ишемия
Заболевание периферических артерий (ЗПА; PAD)
Заболевание периферических артерий (ЗПА) - это хроническое заболевание, постепенно уменьшающее кровоток в конечностях и способное привести к серьезным медицинским осложнениям. Это заболевание часто сочетается с другими заболеваниями и патологическими состояниями, включая гипертонию, сердечно-сосудистые заболевания, гиперлипидемию, сахарный диабет, ожирение и инсульт. Случаи наличия болей, язв, потери ткани или гангрены конечности, вызванные хронической ишемией, охватываются термином "критическая ишемия конечности" (КИК; CLI). КИК является конечной стадией ЗПА, требующей проведения всестороннего лечения сосудистым хирургом или сосудистым терапевтом. В отличие от заболевания коронарных артерий или артерий головного мозга, заболевание периферических артерий (ЗПА) остается недооцененным и редко диагностируется, и еще реже подвергается лечебным воздействиям, несмотря на свою серьезность и чрезвычайно высокую распространенность. В связи с этим, КИК часто приводит к ампутации конечности или смерти, и смертность пациентов с ЗПА превышает смертность пациентов с инфарктом миокарда и инсультом.
Осуществляются попытки лечения ишемических расстройств с помощью различных зрелых стволовых клеток. Было показано, что совместное культивирование стромальных клеток жировой ткани (СКЖТ; ADSC), и эндотелиальных клеток (ЭК; ЕС) приводило к значительному повышению жизнеспособности и миграции ЭК, а также увеличению активности формирования ими трубок (в основном, за счет секреции сосудистого эндотелиального фактора роста (СЭФР; VEGF) и гепатоцитарного фактора роста (ГФР; HGF)). Через 4 недели после трансплантации стромальных клеток в ишемизированную заднюю конечность мыши отмечалось улучшение ангиогенных баллов [Nakagami с соавт., J Atheroscler Thromb (2006) 13(2): 77-81]. Moon с соавт. [Cell Physiol Biochem. (2006) 17: 279-90] в исследовании терапевтического воздействия клеток- предшественников жировой ткани (СКЖТ) на ишемизированную конечность иммунодефицитных мышей продемонстрировали значительное возрастание индекса перфузии, оцениваемого с помощью лазерной допплерографии, в группе животных с трансплантированными СКЖТ.
Кроме того, в исследовании Kim с соавт. [Stem Cells (2006) 24(6): 1620-6] трансплантация мезенхимальных стволовых клеток пуповинной крови (ПК; UCB) четырем мужчинам, страдавшим болезнью Бюргера и ранее уже получавшим терапевтическое и хирургическое лечение, привела к внезапному исчезновению ишемических болей в покое, присутствовавших в пораженных конечностях. В исследовании Ventura с соавт. [J. Biol. Chem. (2007) 282: 14243-52] было также показано, что трансплантация мезенхимальных стволовых клеток человека, выделенных из плодных оболочек доношенной плаценты (МСКЧВПО; FMhMSC), в сердце крысы, пораженное инфарктом, приводит к увеличению плотности расположения капилляров, нормализации функции левого желудочка и значительному уменьшению рубцовой ткани; данный эффект усиливался в случае прекондиционирования стволовых клеток со смешанным эфиром гиалуронана с масляной и ретиноевой кислотами.
Инсульт
Инсульт является одной из ведущих причин смертности во всем мире; он является причиной примерно 9% всех случаев смерти, и на его долю приходятся примерно 2-4% общих расходов здравоохранения. Несмотря на постоянное снижение смертности от инсульта в развитых странах, связанное, вероятно, с улучшением контроля факторов риска возникновения инсульта (особенно высокого артериального давления, сахарного диабета и курения сигарет), инсульт продолжает вызывать стойкие поражения (например, повреждения ткани, неврологические расстройства).
К числу новых способов лечения инсульта принадлежит терапия стволовыми клетками. Трансплантация стволовых клеток или клеток-предшественников в поврежденную ткань (как местно, так и внутривенным путем), рассматриваемая как средство замещения нефункционирующих клеток, усиления пролиферации и/или дифференцировки эндогенных стволовых клеток или клеток-предшественников и обеспечения восстановительного процесса необходимыми иммуномодуляторами, составляет основу клеточной лечебной стратегии. Возможные источники стволовых клеток/клеток-предшественников для использования при инсульте включают в себя нервные стволовые клетки плода, эмбриональные стволовые клетки, клетки нейротератокарциномы, негемопоэтические стволовые клетки пуповинной крови, стволовые клетки костного мозга и плацентарные мезенхимальные стволовые клетки [Andres с соавт., Neurosurg Focus (2008) 24(3-4): Ε 16].
В недавно проведенном исследовании с использованием крысиной модели ишемического инсульта Koh с соавт. [Koh с соавт., Brain Res. (2008)] оценили нейропротекторные эффекты и механизмы действия имплантированных человеческих пуповинных мезенхимальных стволовых клеток (ЧПМСК; hUC-MSCs). Через 20 дней после индукции нейрональной дифференцировки in vitro ЧПМСК демонстрировали наличие морфологических признаков нейронов и экспрессировали нейрональные клеточные маркеры и нейрональные факторы (например, глиальный нейротрофический фактор и мозговой нейротрофический фактор). Кроме того, имплантация ЧПМСК in vivo в поврежденное полушарие крыс с подавленным иммунитетом, имевших ишемический инсульт, привела к улучшению нейроповеденческих функций и уменьшению объема инфаркта по сравнению с контрольными крысами. Через три недели после имплантации ЧПМСК присутствовали в поврежденном полушарии и демонстрировали экспрессию нейроноспецифичных маркеров, однако они не стали функционально активными нейронами.
Применение в ортопедии
При различных патологических состояниях и заболеваниях возникает потребность в регенерации и/или восстановлении соединительной ткани (например, костей, сухожилий и связок). Эти патологические состояния/заболевания включают в себя, например, переломы костей, ожоги, ожоговые раны, глубокие раны, дегенеративные изменения костей, различные раковые опухоли, сопровождающиеся потерей соединительной ткани (например, рак кости, остеосаркома, костные метастазы), и дефекты суставного хряща.
Использование аутологичных костномозговых МСК с целью стимуляции заживления кости описано в ветеринарной и медицинской ортопедической практике. Оно включает в себя чрескожные инъекции костного мозга с целью заживления связок (Carstanjen с соавт., 2006); лечение костных дефектов ауто- или аллотрансплантатами костного мозга в ортопедической клинике (Horwitz с соавт., 1999, Horwitz с соавт., 2002); регенерацию костного дефекта критических размеров у собак с использованием аллогенных [Arinzeh TL с соавт., J Bone Joint Surg Am. 2003, 85-A(IO): 1927-35] или аутологичных [Bruder SP, с соавт., J Bone Joint Surg Am. 1998 Jul; 80(7):985-96] костномозговых МСК, нанесенных на керамический цилиндр, состоящий из гидроксиапатита-трикальцийфосфата, и у кроликов с использованием аллогенных МСК периферической крови (Chao с соавт., 2006.); и имплантацию МСК бабуинам с целью обеспечения обширного костеобразования (Livingston с соавт., 2003). В области ортопедического лечения лошадей мезенхимальные стволовые клетки костного мозга и жировой ткани экспериментально используются при хирургическом лечении субхондральных костных кист, с целью заживления переломов костей [Kraus и Kirker-Head, Vet Surg (2006) 35(3): 232-42] и восстановления хряща [Brehm с соавт., Osteoarthritis Cartilage (2006) 14(12): 1214-26; Wilke с соавт., J Orthop Res (2007) 25(7): 913-25], а также с целью лечения повреждений сухожилий, связанных с их перенапряжением. Кроме того, различные терапевтические методы используются для стимуляции заживления подвешивающей связки у лошадей (Herthel, 2001). Herthel (2001) продемонстрировал новый биологической подход к ускорению заживления подвешивающей связки, включающий в себя инъекции аутологичных стволовых клеток и сопутствующих компонентов костного мозга в участки поражений с целью стимуляции естественной регенерации связки.
В исследованиях на кроликах с экспериментальным повреждением сухожилий было показано, что ткани, обработанные МСК, прочнее и жестче тканей, восстановленных естественным путем (Gordon с соавт., 2005). Кроме того, введение культивированных МСК в область разрыва сухожилия приводило к значительному улучшению биомеханики восстановления (Young с соавт., 1998, Осирис Терэпьютикс, www.osiris.com).
В настоящее время в исследованиях на пациентах оценивается безопасность и эффективность препарата "Осирис Хондроген" (взрослых мезенхимальных стволовых клеток). У животных, получавших лечение МСК, отмечалась регенерация хирургически удаленной ткани мениска, защищенность поверхности хряща и меньшая степень повреждения сустава по сравнению с контрольными животными. Эти преимущества сохранялись у экспериментальных животных в течение, как минимум, одного года (Осирис Терэпьютикс, www.osiris.com).
КРАТКОЕ ОПИСАНИЕ И3ОБРЕТЕНИЯ
Один из признаков некоторых вариантов осуществления настоящего изобретения связан со способом лечения ишемии у пациентов, нуждающихся в данном лечении, заключающимся во введении пациентам терапевтически эффективного количества адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань, и лечении, благодаря этому введению, имеющейся у пациента ишемии.
Другой признак некоторых вариантов осуществления настоящего изобретения связан со способом лечения заболевания, при котором требуется регенерация и/или восстановление соединительной ткани у пациентов, нуждающихся в данном лечении, заключающимся во введении пациентам терапевтически эффективного количества адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань, и лечении, благодаря этому введению, имеющегося у пациента заболевания, при котором требуется регенерация и/или восстановление соединительной ткани.
Другой признак некоторых вариантов осуществления настоящего изобретения связан с использованием адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань, с целью производства лекарственного препарата, предназначенного для лечения ишемии.
Другой признак некоторых вариантов осуществления настоящего изобретения связан с использованием адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань, с целью производства лекарственного препарата, предназначенного для лечения заболевания, при котором требуется регенерация и/или восстановление соединительной ткани.
Другой признак некоторых вариантов осуществления настоящего изобретения связан с производимым изделием, представляющим собой упаковочный материал, включая этикетку для использования при лечении ишемии, и содержащееся в упаковочном материале фармацевтически эффективное количество адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань.
Другой признак некоторых вариантов осуществления настоящего изобретения связан с производимым изделием, представляющим собой упаковочный материал, включая этикетку для использования при лечении заболевания, при котором требуется регенерация и/или восстановление соединительной ткани, и содержащееся в упаковочном материале фармацевтически эффективное количество адгезивных клеток ткани, выбранной из группы тканей, включающей в себя плаценту и жировую ткань.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки способны подавлять иммунную реакцию пациента.
Некоторые варианты осуществления настоящего изобретения: не менее 10% адгезивных клеток находятся в фазе пролиферации.
Некоторые варианты осуществления настоящего изобретения: ишемия представляет собой заболевание периферических артерий (ЗПА).
Некоторые варианты осуществления настоящего изобретения: заболевание периферических артерий (ЗПА) представляет собой критическую ишемию конечности (КИК).
Некоторые варианты осуществления настоящего изобретения: ишемия представляет собой ишемию центральной нервной системы (ЦНС).
Некоторые варианты осуществления настоящего изобретения: ишемия выбирается из группы, состоящей из заболевания периферических артерий, ишемического сосудистого заболевания, ишемического заболевания сердца, ишемического заболевания головного мозга, ишемического заболевания почек и ишемии плаценты.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки получают с помощью трехмерного (3D) культивирования.
Некоторые варианты осуществления настоящего изобретения: трехмерное (3D) культивирование осуществляется с использованием трехмерного (3D-) биореактора.
Некоторые варианты осуществления настоящего изобретения: трехмерное культивирование клеток осуществляется в условиях перфузии.
Некоторые варианты осуществления настоящего изобретения: условия трехмерного культивирования включают в себя наличие адгезивного материала, выбранного из группы, состоящей из полиэфира и полипропилена.
Некоторые варианты осуществления настоящего изобретения: культивирование клеток осуществляется в течение не менее 3 дней.
Некоторые варианты осуществления настоящего изобретения: культивирование клеток осуществляется до тех пор, пока количество пролиферирующих клеток не достигнет не менее чем 10% уровня.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки демонстрируют экспрессию позитивного маркера, выбранного из группы, состоящей из CD73, CD90, CD29 и CD105.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки демонстрируют экспрессию негативного маркера, выбранного из группы, состоящей из CD3, CD4, CD45, CD80, HLA-DR, CD11b, CD14, CD19, CD34 и CD79.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки демонстрируют профиль экспрессии, соответствующий, в целом, профилю экспрессии, описанному в данном документе.
Некоторые варианты осуществления настоящего изобретения: адгезивные клетки являются клетками, имеющими фенотип стромальных стволовых клеток.
Некоторые варианты осуществления настоящего изобретения: фенотип стромальных стволовых клеток включает в себя подавляющее воздействие на Т-клетки.
Некоторые варианты осуществления настоящего изобретения: соединительная ткань представляет собой сухожилия, кости и/или связки.
Некоторые варианты осуществления настоящего изобретения: заболевание, при котором требуется регенерация и/или восстановление соединительной ткани, выбирается из группы, включающей в себя перелом кости, рак кости, ожоговую рану, дефект суставного хряща и глубокую рану.
Некоторые варианты осуществления настоящего изобретения: данное заболевание выбирается из группы, включающей в себя субхондральную костную кисту, перелом кости, остеопороз, остеоартрит, дегенерацию кости, рак кости, повреждение хряща, дефект суставного хряща, дегенеративное заболевание межпозвонковых дисков, несовершенный остеогенез (osteogenesis imperfecta) (OI), ожог, ожоговую рану, глубокую рану, замедленное заживление раны, повреждение сухожилия и повреждение связки.
Смысл всех технических и научных терминов, используемых в данном документе, совпадает со смыслом этих терминов, понимаемым обычными специалистами в той области, к которой относится данное изобретение, если в данном документе отсутствуют иные определения данных терминов. Хотя методы и материалы, подходящие для практического применения или испытаний данного изобретения, описаны ниже, в этих целях могут быть использованы и аналогичные или эквивалентные методы и материалы. В случае выявления каких-либо несоответствий, в качестве контроля следует использовать описание изобретения к патенту, содержащее определения. Кроме того, материалы, методы и примеры представлены только лишь в качестве иллюстрации и не должны рассматриваться как указание границ применимости данного изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Данное изобретение описано ниже с помощью одних лишь примеров, иллюстрируемых прилагаемыми чертежами. В отношении этих детальных чертежей следует подчеркнуть, что представленные на них подробности являются всего лишь примерами, предназначенными для иллюстрации обсуждения вариантов осуществления настоящего изобретения; эти чертежи представлены с целью обеспечения предполагаемого наиболее удобного и понятного описания принципов и концептуальных признаков данного изобретения. В связи с этим, не было предпринято каких-либо попыток представить структурные детали данного изобретения более подробно, чем это необходимо для понимания основ изобретения; для специалистов в данной области это описание в сочетании с данными чертежами дает четкое представление о том, каким образом различные формы этого изобретения могут быть осуществлены на практике.
На данных чертежах представлено следующее:
На Фиг. 1A-G представлена микросреда, напоминающая кость, созданная в биореакторной системе, содержащей трехмерные носители. На Фиг. 1А-В представлены сравнительные электронные микрофотографии естественной кости (Фиг. 1А) и структуры носителя PluriX™ 3D через 7 дней после высевания адгезивных клеток, имитирующих костную микросреду (Фиг. 1В). На Фиг. 1C-F представлены электронные микрофотографии матрикса PluriX™ 3D, засеянного адгезивными клетками, полученными из костного мозга, через 20 дней (Фиг. 1C-D, увеличение х150 и х250 соответственно) и 40 дней (Фиг. 1E-F, увеличение х350 и х500 соответственно) после высева. На Фиг. 1G представлена схема биореактора идеального вытеснения Plurix 3D, отдельные элементы которого обозначены номерами: резервуар питательной среды (1), система подачи газовой смеси (2), фильтр (3), точка инъекций (4), колонка, в которую помещены трехмерные носители (5), монитор потока (6), клапан потока (6а), разделительная емкость (7), анализаторы роста клеток (8); перистальтический насос (9), точка отбора проб (10), электрод для измерения растворенного О2 (11), электрод для измерения рН (12), система управления (13), свежая питательная среда (14), использованная питательная среда (15).
На Фиг. 2 представлен график, характеризующий разные производственные партии (партии №№5-8) адгезивных клеток плацентарного происхождения, выращенных в биореакторных системах в условиях трехмерного культивирования. Адгезивные клетки (2×106) высевали в биореактор; плотность высева составляла 10000-15000 клеток на один носитель. После 12 дней культивирования плотность пространственно располагающихся адгезивных клеток достигала уровня 150000-250000 клеток на один носитель или 22,5-37,5×106 клеток на один биореактор, содержащий 150 носителей.
На Фиг. 3А-В представлены столбиковые диаграммы, демонстрирующие отличие уровней экспрессии экспрессируемых мембранных маркеров пространственно располагающихся адгезивных клеток плацентарного происхождения (темно-фиолетовый цвет) от уровней экспрессии мембранных маркеров клеток плаценты, культивирумых в условиях обычной двухмерной питательной среды (светло-фиолетовый цвет). Адгезивные клетки выращивали в течение 4-6 недель в колбах (2D) или в течение 2-3 недель в биореакторной системе на полистироловых носителях (3D). Клетки, собранные из колб или с носителей, инкубировали и обрабатывали набором моноклональных антител (МАb), распознающих мембранные маркеры, характерные для адгезивных (Фиг. 3А) или гемопоэтических клеток (Фиг. 3В). Обратите внимание на значительно более высокую экспрессию мембранных маркеров МСК CD90, CD105, CD73 и CD29 на клетках, культивирумых в условиях двухмерной питательной среды, по сравнению мембранными маркерами МСК на трехмерно культивируемых адгезивных клетках; это в особенности относится к маркеру CD105, демонстрирующему 56% экспрессию на трехмерно культивируемых клетках и 87% экспрессию на двухмерно культивируемых клетках (Фиг. 3А). Адгезивные клетки как в двухмерных, так и в трехмерных культурах не экспрессировали каких-либо гемопоэтических мембранных маркеров (Фиг. 3В).
На Фиг. 4A-D представлены столбиковые диаграммы, сравнивающие уровни белка в адгезивных клетках, полученных из плаценты, культивированных в двухмерных и трехмерных условиях, а также уровни белка в кондиционированных питательных средах этих клеток. На Фиг.4А-С представлены уровни лиганда Flt-3 (Фиг. 4А), IL-6 (Фиг. 4 В) и фактора стволовых клеток (ФСК; SCF) (Фиг. 4С) в пг/мл, нормализованные к 1×106 клеток/мл, выявленные с помощью иммуноферментного анализа (ИФА; ELISA) в кондиционированных средах адгезивных клеток при их культивировании в двухмерных и трехмерных условиях. Представлены результаты одного из трех отдельных экспериментов. На Фиг. 4D представлено сравнение уровней экспрессии различных клеточных белков, определенных с помощью масс-спектрометрии с использованием мечения проб белка реактивами iTRAQ. Пробы белка были получены из адгезивных клеток, выращенных в двухмерных (2D, белые столбики) и трехмерных (3D, серые столбики) условиях. На данном чертеже представлена одна из двух повторностей экспериментов. Обратите внимание на различие уровней экспрессии некоторых белков в клетках и кондиционированных средах при культивировании в двухмерных и трехмерных условиях.
На Фиг. 5A-D представлены микрофотографии, демонстрирующие способность адгезивных клеток плацентарного происхождения, выращенных в условиях трехмерного культивирования, дифференцироваться в остеобласты in vitro. Человеческие адгезивные клетки плацентарного происхождения культивировали в питательной среде, вызывающей остеогенную дифференцировку (среде Игла, модифицированной по способу Дульбекко (DMEM), содержащей 10% фетальную телячью сыворотку (ФТС; FCS), 100 нМ дексаметазона, 0,05 мМ 2-фосфата аскорбиновой кислоты, 10 мМ В-глицерофосфата), в течение 3 недель. На Фиг. 5А-В показаны клетки, экспрессирующие кальцифицированный матрикс, выявляемый с помощью окрашивания Ализарином Красным S. На Фиг. 5C-D показаны контрольные клетки, которые не были обработаны средой, вызывающей остеогенную дифференцировку; эти клетки сохраняли фибробластоподобный фенотип и демонстрировали отсутствие минерализации.
На Фиг. 6 представлен график, показывающий процент человеческих клеток CD45+, выявленный в костном мозге (КМ; ВМ) мышей NOD-SCID, получавших химиотерапию (интраперитонеальные инъекции бисульфана в дозе 25 мг/кг в течение двух последующих недель) через 3,5 недели после трансплантации. Клетки CD34+ (100 000), выделенные из мононуклеарных клеток пуповинной крови, трансплантировали в отдельности (5 мышей, а), в сочетании с 0,5×106 адгезивных клеток плаценты, культивированных в двумерных условиях (2D-адгезивные клетки; 2 мыши, b), а также в сочетании с адгезивными клетками плаценты, культивированными в трехмерных условиях в биореакторе pluriX™ (3D-адгезивные клетки; 5 мышей, с). Затем получали пробы КМ из бедренных и большеберцовых костей мышей. Человеческие клетки в КМ выявляли с помощью проточной цитометрии. Процент человеческих клеток, экспрессирующих CD45, определяли с помощью инкубирования клеток с антителами против человеческих CD45, мечеными ФИТЦ (FITC). Обратите внимание на более высокий процент человеческих клеток CD45+ (hCD45+) в костном мозге мышей, которым трансплантация осуществлялась в сочетании с 20-адгезивными клетками (b), а также мышей, которым трансплантация осуществлялась в сочетании с 3D-адгезивными клетками (с), по сравнению с процентом человеческих клеток у мышей, получавших гемопоэтические стволовые клетки (ГСК; HSCs) в отдельности (а). Более высокий уровень вживления, выявленный у мышей, получавших культивированные 3D-адгезивные клетки, по сравнению с мышами, получавшими культивированные 2D-адгезивные клетки, свидетельствует о наличии терапевтических преимуществ у культивированных 3D-адгезивных клеток.
На Фиг. 7А-В представлены данные определения количества трансплантированных человеческих клеток CD45+ у мышей, которым была осуществлена пересадка только клеток CD34+ (Фиг. 7А), в сравнении с мышами, которым клетки CD34+ были пересажены в сочетании с адгезивными клетками жировой ткани (Фиг. 7В); эти данные были получены с помощью метода флюоресцентно-активированной сортировки клеток (ФАСК; FACS). Обратите внимание на значительно более высокий процент человеческой гемопоэтической популяции (hCD45+) (7А - 29%) у мыши, которой клетки CD34+ были пересажены в сочетании с адгезивными клетками жировой ткани, по сравнению с мышью, которой были пересажены только человеческие клетки CD34+ (7В - 12%).
На Фиг. 8А представлена столбиковая диаграмма, демонстрирующая реакцию смешанных лимфоцитов, проведенную между человеческими мононуклеарными клетками пуповинной крови (ПК; СВ) и, соответственно, равными количествами облученных клеток пуповинной крови (3000 рад; ОКПК; iCB); человеческих моноцитов периферической крови (МПК; РВМС); плацентарных адгезивных клеток, культивированных в двухмерных (2D) или трехмерных (3D) условиях; и сочетания МПК и 2D- и 3D-культивированных плацентарных адгезивных клеток (МПК+20 и ΜΠΚ+3D). Величину популяции клеток ПК отражал уровень захвата 3Н-тимидина (измеряемый количеством импульсов в минуту (КИМ; СРМ)); этот показатель оценивали в последние 18 часов культивирования. Повышенная пролиферация стимулированных клеток ПК свидетельствует о более высоком уровне иммунной реакции. Обратите внимание на менее высокий уровень иммунной реакции, демонстрируемый клетками, инкубированными с адгезивными клетками, и, в частности, на пониженную иммунную реакцию клеток ПК на МПК при совместном инкубировании с адгезивными клетками. Каждую реакцию проводили в трех повторностях.
На Фиг. 8В представлена схема процесса получения 3D-адгезивных клеток из плаценты с помощью биореактора Celligen™ (наименование клеток - "клетки PLX-C").
На Фиг. 8С представлена схема резервуара и отверстий биореактора Celligen™ (заимствовано с сайта The New Brunswick Scientific с внесением соответствующих изменений).
На Фиг. 9А-В представлен анализ клеточного цикла 3D-адгезивных клеток, производимых с помощью биореактора Plurix (наименование клеток - "клетки PLX"; Фиг. 9В) и с помощью биореактора Celligen (наименование клеток - "клетки PLX-C"; Фиг. 9А). Клетки фиксировали в 70% EtOH O.N, центрифугировали и ресуспендировали в растворе пропидия йодида (ПЙ; PI), а затем анализировали с помощью ФАСК.
Фиг. 10А-С демонстрирует экспрессию маркеров, типичных для фибробластов, но не экспрессию маркеров, типичных для эндотелиальных клеток, на клетках PLX-C. На Фиг. 10А показана негативная экспрессия эндотелиального маркера CD31, на Фиг. 10В - негативная экспрессия эндотелиального маркера KDR и на Фиг. 10С - позитивная экспрессия маркера фибробластов человека (D7-FIB). Гистограммы красного цвета для изотипа IgG1 (ФИТЦ) представляют негативный контроль, а гистограммы синего цвета - положительно окрашенные клетки.
Фиг. 11A-D демонстрирует экспрессию стимулирующих и ко-стимулирующих молекул на клетках PLX-C. На Фиг. 11А показана экспрессия CD80 на клетках PLX-C, на Фиг. 11В - экспрессия CD86 на клетках PLX-C, на Фиг. 11С - экспрессия CD40 на клетках PLX-C и на Фиг. 11D - экспрессия HLA-А/В/С на клетках PLX-C. Были приготовлены негативные контроли с флюоресцентными молекулами соответствующего изотипа. Гистограммы красного цвета представляют популяцию клеток PLX-C, экспрессирующую маркер, гистограммы синего цвета - популяцию клеток костного мозга (КМ; ВМ), экспрессирующую маркер, а гистограммы зеленого цвета - популяцию мононуклеарных клеток (МНК; MNC), экспрессирующую маркер.
На Фиг. 12А-В показано ингибирование пролиферации лимфоцитов клетками PLX-C. На Фиг. 12А представлены результаты тестов реакции смешанных лимфоцитов (РСЛ; MLR), проведенных с использованием 2×105 МНК периферической крови (ПК; PB) (донор А), стимулированных равным количеством облученных МНК ПК (3000 рад; донор В), с последующим добавлением к культурам возрастающих количеств клеток PLX-C. Каждую группу высевали на 96-луночные планшеты в трех повторностях. На основании данных о включении [3Н]тимидина оценивали скорость пролиферации клеток; на Фиг. 12В представлены данные в отношении МНК периферической крови (ПК; PB), стимулированных СоnА (1,5 мг/мл). К культурам добавляли возрастающие количества клеток PLX-C. Каждую группу высевали на 96-луночные планшеты в трех повторностях. На основании данных о включении [3Н]тимидина оценивали скорость пролиферации клеток;
На Фиг. 13А-С показано регулирование клетками PLX-C секреции провоспалительных и противовоспалительных цитокинов клетками периферической крови при их совместном культивировании. На Фиг. 13А-В показана секреция IFNγ (Фиг. 13А) и TNFα (Фиг. 13В) при совместном культивировании человеческих МНК (выделенных из периферической крови), стимулированных СоnА, с клетками PLX-C; на Фиг. 13С показана секреция IFNγ, TNFα и IL-10 при совместном культивировании человеческих МНК (выделенных из периферической крови), стимулированных липополисахаридом (ЛПС; LPS), с клетками PLX-C. Осуществляли сбор надосадочной жидкости и анализ цитокинов с помощью ИФА.
На Фиг. 14 представлен вектор экспрессии люциферазы, использованный для инфицирования клеток PLX-C. В данном случае был использован вектор экспрессии Lv33 OmicsLink. Ген люциферазы был клонирован в открытую рамку считывания (ОРС; ORF).
На Фиг. 15 показана высокая экспрессия люциферазы, демонстрируемая инфицированными клетками PLX-C. Данные клетки были инфицированы вектором экспрессии люциферазы и визуализированы с помощью системы IVIS через 48 часов после инфицирования. Следует отметить, что клетки демонстрировали высокий уровень экспрессии люциферазы.
На Фиг. 16A-D представлена инъекция 2×106 клеток PLX-C, экспрессирующих люциферазу, мышам линии SCID/Beige. Одной мыши была осуществлена внутримышечная инъекция, и одной мыши - внутривенная инъекция. Осуществлялся мониторинг мышей, которым были введены данные клетки, с помощью системы IVIS с целью оценки биораспределения клеток PLX-C in vivo. Представлены результаты оценки с помощью системы IVIS в 1-й день (Фиг. 16А), а также на 4-й (Фиг. 16В), 6-й (Фиг. 16С) и 22-й (Фиг. 16D) дни.
На Фиг. 17 представлен график, демонстрирующий повышение перфузии в бедре и стопе мышей, которым были введены адгезивные клетки по настоящему изобретению (клетки "PLX-С"). На этом чертеже указана медиана процента перфузии в бедре и стопе мыши. Кровоток в бедре и стопе определяли с помощью бесконтактного лазерного допплерографического исследования на обеих конечностях на 0, 6, 9, 14 и 21-й день после операции (показаны результаты измерений, выполненных на 21-й день). Результаты выражены как отношение кровотока в ишемизированной конечности к кровотоку в нормальной конечности во время эксперимента.
На Фиг. 18 представлен график, демонстрирующий результаты оценки функции и ишемического поражения конечности in vivo. Была осуществлена последовательная полуколичественная оценка нарушения функции ишемизированной конечности с использованием следующей балльной системы: 3 = волочение конечности, 2 = волочение отсутствует, однако отсутствует и подошвенное сгибание, 1 = имеется подошвенное сгибание и 0 = имеется сгибание пальцев стопы как реакции сопротивления при легком потягивании за хвост.
На Фиг. 19А-С показано повышение плотности расположения капилляров при применении клеток PLX-C. На Фиг. 19А показана плотность расположения капилляров у мышей, которым вводили физраствор, забуференный фосфатом (ФЗФ; PBS); на Фиг. 19В - плотность расположения капилляров у мышей, которым вводили клетки PLX-C; на Фиг. 19С - столбиковая диаграмма количества капилляров, приходящегося на мышечные клетки. Следует отметить, что у мышей, которым вводили клетки PLX-C, отмечалось увеличение плотности расположения капилляров после индуцированной ишемии конечности, продемонстрированное с помощью специфического окрашивания капилляров; у контрольных животных увеличения плотности расположения капилляров выявлено не было.
На Фиг. 20А-В продемонстрировано уменьшение окислительного стресса и воспаления эндотелия после введения клеток PLX-C. На Фиг. 20А показана столбиковая диаграмма окислительного стресса (окрашивание нитротирозином); а на Фиг. 20В показана столбиковая диаграмма воспаления эндотелия (оценка VCAM). Следует отметить, что у мышей, которым вводили клетки PLX-C, окислительный стресс и воспаление эндотелия уменьшались.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Данное изобретение связано со способами увеличения ангиогенеза в тканях и лечения ишемии или заболеваний, при которых требуется регенерация и/или восстановление соединительной ткани с помощью адгезивных клеток плаценты или жировой ткани; ниже представлены некоторые соответствующие варианты осуществления данного изобретения.
Чертежи и сопровождающие их описания способствуют лучшему пониманию принципов и осуществления настоящего изобретения.
Перед началом подробного рассмотрения вариантов осуществления настоящего изобретения необходимо уточнить, что применение данного изобретения не ограничивается деталями, представленными ниже в описании или в разделе "Примеры". Возможны и другие варианты осуществления данного изобретения, а также различные пути его реализации или выполнения. Кроме того, следует иметь в виду, что используемые в данном документе фразы и термины используются лишь в целях описания и не должны рассматриваться как ограничители объема данного изобретения.
В процессе разработки способов практического применения изобретения, данные изобретатели установили, что адгезивные клетки плаценты или жировой ткани высокоэффективны в отношении увеличения ангиогенеза в тканях, а также в отношении лечения ишемии и заболеваний, при которых требуется регенерация и/или восстановление соединительной ткани.
Как показано в представленных ниже иллюстрациях и в Примерах 1-8 (раздел "Примеры"), данным изобретателям удалось обеспечить экспансию адгезивных клеток жировой ткани и плаценты, обладающих свойствами стромальных стволовых клеток. Анализ адгезии и анализ репопуляционного потенциала (см. Пример 1) показал, что клетки, продуцированные в результате такой экспансии, сохраняют жизнеспособность после криоконсервации. Анализ адгезивных клеток плаценты методом проточной цитометрии продемонстрировал их отчетливый профиль экспрессии маркеров (см. Фиг. 3А-В). Как будет показано ниже в Примере 6 раздела "Примеры", имплантация плацентарных адгезивных клеток значительно увеличивала кровоток в бедре и стопе (Фиг. 17) мышей с перевязанной артерией (модель ишемии задней конечности), значительно улучшала функцию конечности (Фиг. 18), увеличивала плотность расположения капилляров (Фиг. 19А-С), а также уменьшала окислительный стресс и воспаление эндотелия (Фиг. 20А-В).
Таким образом, один из признаков настоящего изобретения связан со способом увеличения ангиогенеза в тканях. Данный способ осуществляется путем обеспечения контакта ткани с адгезивными клетками ткани, выбранной из группы, включающей в себя плаценту и жировую ткань, и увеличения за счет этого ангиогенеза в тканях.
В рамках данного документа выражение "увеличение ангиогенеза в ткани" означает нарастание (индуцирование, повышающую регуляцию) процесса формирования новых кровеносных капилляров в ткани.
В рамках данного документа выражение "адгезивные клетки" означает однородную или неоднородную популяцию субстратзависимых клеток (то есть, клеток, нуждающихся в прикреплении к поверхности для роста in vitro).
В рамках данного документа термин "жировая ткань" означает соединительную ткань, содержащую жировые клетки (адипоциты).
В рамках данного документа термин "ткань плаценты" означает любую часть женского органа млекопитающего, выстилающего стенку матки и при беременности окружающего плод, прикрепляющийся к нему с помощью пупочного канатика. После родов плацента изгоняется из матки (плацента, изгнанная из матки, называется "послеродовой плацентой"). В варианте осуществления, приводимом в качестве примера, термин "плацента" означает целую плаценту. Размножение адгезивных клеток плаценты или жировой ткани может обеспечиваться в условиях двухмерного или трехмерного культивирования.
Условия размножения адгезивных клеток в двухмерной культуре дополнительно описаны ниже, а также следующем далее разделе "Примеры".
В рамках данного документа выражение "трехмерная культура" означает культуру, условия которой обеспечивают возможность роста клеток более чем в один слой. Следует иметь в виду, что в живом организме (или живой ткани) среда существования клетки in situ имеет трехмерную архитектуру. Клетки окружены другими клетками. Они удерживаются в сложной сети наноскопических волокон внеклеточного матрикса, обеспечивающей возможность создания различных местных микросред. Их внеклеточные лиганды обусловливают не только прикрепление клеток к базальной мембране, но и доступ к различным кровеносным и лимфатическим сосудам. К клеткам доставляются кислород, гормоны и питательные вещества, а удаляются продукты их жизнедеятельности. Как будет показано в нижеприведенных примерах, в трехмерной культуре по данному изобретению создаются условия, имитирующие условия естественной среды.
Следует иметь в виду, что условия трехмерной культуры обеспечивают возможность экспансии адгезивных клеток.
В рамках данного документа термины "демонстрирующие экспансию" и "экспансия" относятся к поддерживаемым клеткам, демонстрирующим, в конечном счете, размножение без существенной дифференцировки, то есть, означают увеличение клеточной популяции (например, не менее чем двухкратное) без сопровождающей это увеличение дифференцировки.
В рамках данного документа термины "поддерживающий" и "поддержание" относятся к обновлению клеток без их существенной дифференцировки, то есть, к стационарной, в значительной мере, клеточной популяции, не демонстрирующей какой-либо сопровождающей данную стационарность дифференцировки.
Как было указано выше, адгезивные клетки по данному признаку изобретения извлекают из жировой ткани или ткани плаценты.
Плацентарные клетки могут быть получены из доношенной или недоношенной плаценты. Взятие клеток плаценты предпочтительно осуществлять сразу же после удаления из нее крови. Перфузию плаценты предпочтительно осуществлять в течение периода времени, достаточного для удаления остаточных клеток. В рамках данного документа термины "перфузировать" и "перфузия" относятся к подаче жидкости на поверхность органа или ткани или пропусканию жидкости через орган или ткань. Ткань плаценты может принадлежать любому млекопитающему - например, человеку. Удобным источником ткани плаценты является послеродовая плацента (например, через 1-6 часов после родов); однако по настоящему изобретению источник ткани или клеток плаценты, а также способ выделения ткани плаценты, не играет важной роли.
Адгезивные клетки плаценты могут быть получены как из плодных (то есть, амниона или внутренних частей плаценты, см. Пример 1), так и материнских (то есть, decidua basalis и decidua parietalis) частей плаценты. Образцы ткани промывают в забуференном физиологическом растворе [например, в физиологическом растворе, забуференном фосфатом (ФЗФ) или буферном растворе Хэнкса]. Одноклеточные суспензии получают с помощью обработки ткани пищеварительным ферментом (см. ниже) и/или измельчения и вымывания частиц ткани через нейлоновый фильтр или осторожного пипетирования (Falcon, Becton, Dickinson, Сан Хосе, Калифорния) с промывочной средой.
Адгезивные клетки жировой ткани могут быть выделены с помощью различных способов, известных специалистам в данной области. Эти способы описаны, например, в патенте США №6,153,432. Жировая ткань может быть получена из сальниковой/внутренностной области, области расположения молочных желез, области расположения половых желез, а также других областей, богатых жировой тканью. Одним из источников жировой ткани является сальниковый жир. Как правило, жировую ткань человека получают с помощью липосакции. Адгезивные клетки жировой ткани могут быть выделены с помощью обработки ткани пищеварительным ферментом (например, коллагеназой, трипсином и/или диспазой) и/или эффективными концентрациями гиалуронидазы или ДНКазы и этилендиаминтетрауксусной кислотой (ЭДТК) при температурах от 25 до 50°С в течение 10 минут - 3 часов. Затем клетки могут быть профильтрованы через нейлоновую или марлевую сетку с размером отверстий от 20 мкм до 1 мм. Затем клетки подвергают дифференцированному центрифугированию непосредственно в среде, либо над фиколлом или перколлом, либо в другом градиенте для разделения частиц. Клетки центрифугируют со скоростью от 100 до 3000 g в течение периодов времени от 1 минуты до 1 часа при температуре от 4 до 50°С (см. патент США №7,078,230).
Помимо адгезивных клеток плаценты или жировой ткани, данное изобретение предусматривает использование адгезивных клеток с фенотипом стромальных стволовых клеток, полученных из других источников (см. описание ниже). Тканевые источники, из которых могут быть получены адгезивные клетки, включают в себя, помимо прочего, пуповинную кровь, волосистую часть кожи головы, волосяные фолликулы [например, согласно описанию в заявке на патент США 20060172304], яички [например, согласно описанию в работе Guan К. с соавт., Nature. 2006 Apr 27; 440(7088): 1 199-203], слизистая обонятельной области носовой полости человека [например, согласно описанию в работе Marshall, СТ. с соавт., Histol Histopathol. 2006 Jun; 21(6):633-43], эмбриональный желточный мешок [например, согласно описанию в работе Geijsen Ν, Nature. 2004 Jan 8; 427(6970): 148-54] и амниотическая жидкость [Pieternella с соавт. (2004) Stem Cells 22:1338-1345];
известно, что все эти источники содержат мезенхимальные стволовые клетки. Адгезивные клетки могут быть выделены из этих тканевых источников с помощью культивирования клеток на адгезивной поверхности, обеспечивающего отделение адгезивных клеток от других клеток, присутствующих в исходной популяции.
Извлечение клеток, независимо от их происхождения (например, клеток плаценты или жировой ткани), предпочтительно осуществлять в стерильных условиях. Выделенным клеткам дают возможность прикрепиться к адгезивному материалу (например, сконфигурированному в форме поверхности), чтобы, таким образом, выделить адгезивные клетки. Культивирование может продолжаться в двухмерных условиях как описано в Примере 4 раздела "Примеры", а затем клетки могут быть перемещены в трехмерные условия культивирования.
В рамках данного документа термин "адгезивный материал" означает синтетический, натуральный или комбинированный синтетически-натуральный нецитотоксичный (то есть, биологически совместимый) материал, обладающий химической структурой, способной удерживать клетки на поверхности (например, открытыми поверхностными заряженными группами).
Примерами адгезивных материалов, которые могут быть использованы в соответствии с данным признаком изобретения, являются, помимо прочего, полиэфир, полипропилен, полиалкилен, полифторхлорэтилен, поливинилхлорид, полистирол, полисульфон, ацетат целлюлозы, слекловолокно, керамические частицы, матригель, компонент внеклеточного матрикса (например, фибронектин, хондронектин, ламинин), коллаген, поли-L-молочная кислота и инертное металлическое волокно.
С помощью способов, хорошо известных специалистам в данной отрасли (например, нижеописанной ФАСК с использованием экспрессии маркеров стромальных стволовых клеток), могут быть осуществлены дополнительные этапы очистки или обогащения стромальных стволовых клеток.
Примерами базовых питательных сред, пригодных для культивирования в соответствии с настоящим изобретением, не ограничивающими объема данного изобретения, являются Минимальная эссенциальная среда Игла, ADC-I, LPM (не содержащая бычьего сывороточного альбумина), F10(HAM), F12(НАМ), DCCM1, DCCM2, RPMI 1640, Среда BGJ (в модификации Фиттона-Джексона и без нее), Базальная среда Игла (ВМЕ, с добавлением солевой основы Эрла), Среда Игла в модификации Дульбекко (DMEM, без сыворотки), Yamane, IMEM-20, Среда Игла в модификации Глазго (GMEM), Среда Лейбовитца L-15, Среда МакКоя 5А, Среда M199 (М199Е, с солевой основой Эрла), Среда M199 (М199Н, с солевой основой Хэнка), Минимальная эссенциальная среда Игла (МЕМ-Е, с солевой основой Эрла), Минимальная эссенциальная среда Игла (МЕМ-Н, с солевой основой Хэнка) и Минимальная эссенциальная среда Игла (MEM-NAA с заменимыми аминокислотами), а также многочисленные другие среды, включая среду 199, CMRL 1415, CMRL 1969, CMRL 1066, NCTC 135, MB 75261, МАВ 8713, DM 145, среду Уильямса G, среду Неймана и Тителла, среду Хигучи, MCDB 301, MCDB 202, MCDB 501, MCDB 401, MCDB 411, MDBC 153. Предпочтительной средой для использования в соответствии с данным изобретением является DMEM. Эти и другие применимые питательные среды могут быть приобретены у компании GIBCO, Grand Island, Нью Йорк, США и компании Biological Industries, Bet HaEmek, Израиль, а также у других компаний. Краткий обзор ряда этих сред представлен в книге Methods in Enzymology, Volume LVIII, "Cell Culture", pp.62-72, под редакцией William В. Jakoby и Ira H. Pastan, опубликованной Academic Press, Inc.
Питательная среда может быть дополнена, например, сывороткой (такой как фетальная сыворотка быка или другого вида животного, а также, по выбору или в качестве альтернативы, факторами роста, витаминами (например, аскорбиновой кислотой), цитокинами, солями (например, В-глицерофосфатом), стероидами (например, дексаметазоном) и гормонами - например, гормоном роста, эритропоэтином, тромбопоэтином, интерлейкином 3, интерлейкином 6, интерлейкином 7, макрофагальным колониестимулирующим фактором, лигандом c-kit/фактором стволовых клеток, лигандом остеопротегерина, инсулином, инсулиноподобными факторами роста, эпидермальным фактором роста, фактором роста фибробластов, фактором роста нервов, цилиарным нейротрофическим фактором, тромбоцитарным фактором роста и костным морфогенетическим белком - в концентрациях, варьирующих от пикограммов на миллилитр до миллиграммов на миллилитр.
Кроме того, следует иметь в виду, что к питательной среде могут быть добавлены дополнительные ингредиенты. Такими ингредиентами могут быть антибиотики, противогрибковые препараты, альбумин, аминокислоты и другие ингредиенты, известные специалистам в области культивирования клеток. Помимо этого, в случае необходимости могут быть добавлены ингредиенты, ускоряющие процесс дифференцировки клеток (см. ниже).
Следует иметь в виду, что, в случае введения адгезивных клеток, описываемых в настоящем изобретении, человеку, данные клетки и питательная среда (например, среда, содержащая вышеописанные добавки) должны быть в значительной мере свободны от инородных агентов, то есть, не должны содержать каких-либо загрязняющих примесей животного происхождения - например, микоплазм. В питательную среду могут быть добавлены, например, заменитель сыворотки, человеческая сыворотка и/или синтетические или рекомбинантные факторы.
Как было отмечено выше, полученные адгезивные клетки могут быть перемещены в условия последующего двухмерного или трехмерного культивирования (см. Примеры 1 и 4 в разделе "Примеры" ниже). Однако следует иметь в виду, что перемещение клеток на трехмерный матрикс может быть осуществлено либо сразу же после их выделения, либо после их культивирования в двухмерных условиях (как уже было указано выше).
Таким образом, адгезивный материал по данному признаку изобретения имеет конфигурацию, предназначенную для трехмерного культивирования, и представляет собой ростовой матрикс, существенно увеличивающий доступную площадь адгезии клеток и имитирующий инфраструктуру ткани (например, ткани плаценты).
При крупносерийном производстве культивирование может осуществляться в трехмерном биореакторе.
Примерами таких биореакторов являются, помимо прочего, биореактор идеального вытеснения, биореактор непрерывного перемешивания, стационарный биореактор, биореакторная система CelliGen Plus® (New Brunswick Scientific (NBS)) или биореакторная система BIOFLO 310 (New Brunswick Scientific (NBS).
Как показано в Примере 4 раздела "Примеры", биореактор Celligen способен обеспечивать трехмерную экспансию адгезивных клеток в контролируемых условиях (например, рН, температуры и уровня кислорода) и при постоянной перфузии среды размножения клеток. Кроме того, может осуществляться непосредственный динамический контроль культур клеток в отношении концентраций глюкозы, лактата, глютамата и аммония. Определение уровня потребления глюкозы и скорости продукции лактата адгезивными клетками дает возможность оценивать скорость роста клеток и устанавливать время сбора клеток.
Другими трехмерными биореакторами, которые могут быть использованы в соответствии с данным изобретением помимо прочих биореакторов, являются биореактор непрерывного перемешивания, характеризующийся непрерывной подачей питательной среды в биореактор и непрерывным извлечением продукта, а также поддержанием постоянного равновесного состояния в реакторе (биореактор непрерывного перемешивания с волоконной корзиной может быть приобретен, например, у компании New Brunswick Scientific Co., Edison, NJ); стационарный биореактор; биореактор подъема воздуха, в котором воздух, как правило, подается снизу в центральную трубку, поднимается пузырьками вверх и удаляется через отдушину в верхней части колонны; перфузионный биореактор высева клеток с полиактивными пенами [согласно описанию в работе Wendt, D. с соавт., Biotechnol Bioeng 84: 205-214, (2003)]; перфузионный биореактор радиального потока с трубчатыми поли-L-лактацидными (PLLA) пористыми опорными конструкциями [согласно описанию в работе Kitagawa с соавт., Biotechnology and Bioengineering 93(5): 947-954 (2006). Другие биореакторы, которые могут быть использованы в соответствии с данным изобретением, описаны в патентах США №№6,277,151, 6,197,575, 6,139,578, 6,132,463, 5,902,741 и 5,629,186.
Высев клеток предпочтительно осуществлять в количестве 100000-1500000 клеток на миллиметр при высеве. В варианте осуществления, приводимом в качестве примера, осуществляется высев, в целом, 150±30×106 клеток, по 3-5×106 клеток на 1 г носителя или 0,015-0,1×106 клеток на миллилитр.
Сбор клеток можно осуществлять при наличии пролиферации примерно не менее 10% клеток и отсутствии неконтролиуремой дифференцировки и старения.
Культивирование осуществляют в течение примерно не менее 2 дней, 3 дней, 4 дней, 5 дней, 10 дней, 20 дней, одного месяца или даже в течение более длительного периода времени. Следует иметь в виду, что культивирование в биореакторе может продлевать этот период. Культивирование адгезивных клеток в трехмерной культуре может осуществляться в условиях непрерывного потока питательной среды. С целью увеличения количества клеток может применяться пассирование. Следует иметь в виду, что питательная среда может быть изменена с целью увеличения продолжительности культивирования и улучшения его условий.
Согласно некоторым вариантам осуществления настоящего изобретения, примерное количество пролиферирующих адгезивных клеток (которое может быть определено посредством контроля фаз S и G2/M с помощью ФАСК) равно не менее 10%, 28%, 30%, 50%, 80% или большего количества процентов.
Согласно некоторым вариантам осуществления настоящего изобретения, адгезивные клетки могут содержать по крайней мере один "фенотип стромальной стволовой клетки".
В рамках данного документа термин "фенотип стромальной стволовой клетки" обозначает структурный или функциональный фенотип, типичный для стромальных (то есть, мезенхимальных) стволовых клеток костного мозга.
В рамках данного документа термин "стволовая клетка" обозначает клетку, не являющуюся конечно дифференцированной клеткой.
Таким образом, эти клетки, например, могут иметь веретенообразную форму. В качестве альтернативы или дополнения данные клетки могут экспрессировать маркер или набор маркеров (например, поверхностный маркер), типичный для стромальных стволовых клеток. Примерами поверхностных маркеров стромальных стволовых клеток (позитивных и негативных) являются, помимо прочего, CD105+, CD29+, CD44+, CD73+, CD90+, CD3-, CD4-, CD34-, CD45-, CD80-, CD19-, CD5-, CD20-, CDI1В-, CD14-, CD19-, CD79-, HLA-DR- и FMC7-. Другими маркерами стромальных стволовых клеток являются, помимо прочего, тирозингидроксилаза, нестин и H-NF.
Адгезивные клетки ткани плаценты, вырабатываемые в соответствии с настоящим изобретением, имеют профиль экспрессии генов, соответствующий, в целом, профилю, описанному в Примере 4 раздела "Примеры", представленного ниже.
Примерами функциональных фенотипов, типичных для стромальных стволовых клеток, являются, помимо прочего, супрессирующее воздействие на Т-клетки (не стимулирование, а, наоборот, подавление Т-клеток), поддерживающее воздействие на гемопоэтические стволовые клетки, а также наличие любого из следующих направлений дифференцировки - адипогенного, гепатогенного, остеогенного и неврогенного.
Любая из этих структурных или функциональных черт может быть использована для идентификации клеток, соответствующих настоящему изобретению (см. Пример 4 раздела "Примеры", представленного ниже).
Популяции клеток, выработанные в соответствии с настоящим изобретением, характеризуются наличием уникального профиля экспрессии белков (см. Пример 1 в разделе "Примеры"). Так, например, адгезивные клетки плаценты или жировой ткани, выработанные в соответствии с настоящим изобретением, способны экспрессировать и/или секретировать высокие уровни определенных факторов. Эти клетки, например, экспрессируют или секретируют ФСК, Flt-3, семейство гистонов Н2А (H2AF) или альдегиддегидрогеназу X (АЛДГ X) не менее чем в 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или даже 12 раз сильнее, чем адгезивные клетки плаценты или жировой ткани, выращенные с помощью двухмерного культивирования. В качестве альтернативы или дополнения, популяция клеток по данному изобретению секретирует или экспрессирует IL-6, эукариотический фактор элонгации трансляции 2 (EEEF2), ретикулокарбин 3, домен ветви EF, связывающий кальций (RCN2), или основной гладкомышечный кальпонин 1 (CNN1) не менее чем в 2, 3 или 5 раз сильнее, чем адгезивные клетки плаценты или жировой ткани, выращенные с помощью двухмерного культивирования. В качестве альтернативы или дополнения, популяция клеток по данному изобретению характеризуется менее высоким уровнем экспрессии различных других белков по сравнению с клетками, выращенными с помощью двухмерного культивирования. Так, например, секреция или экспрессия популяцией клеток по данному изобретению гетерогенного ядерного рибонуклеопротеина H1 (Hnrphl), предшественника изоформы 2 антигена CD44, изоформы а синтазы 3-фосфоаденозина 5-фосфосульфата 2 (Papss2) или рибосомального белка L7a (rpL7a) составляет менее 0,6, 0,5, 0,25 или 0,125 от уровня секреции или экспрессии данных белков адгезивными клетками плаценты или жировой ткани, выращенными с помощью двухмерного культивирования.
Как показано в Примерах 3-4 в разделе "Примеры", приведенном ниже, адгезивные клетки и, в частности, 3D-адгезивные клетки подавляют иммунную реакцию мононуклеарных клеток пуповинной крови человека в анализе реакции смешанных лимфоцитов (РСЛ), демонстрируя, таким образом, биологическую активность (например, эффект подавления Т-клеток и эффект поддержания гемопоэтических стволовых клеток), которая может найти применение в клинике.
Вариант осуществления настоящего изобретения: адгезивные клетки по настоящему изобретению способны подавлять иммунную реакцию пациента.
В рамках данного документа выражение "подавление иммунной реакции пациента" означает уменьшение или ингибирование иммунной реакции на антиген, возникающей у пациента, например, на инородную клетку или ее часть. Иммунные реакции, которые могут быть подавлены адгезивными клетками, включают в себя гуморальные иммунные реакции и клеточные иммунные реакции, включающие в себя специфичное распознавание антигенов патогенного микроорганизма соответственно антителами и Т-лимфоцитами (пролиферацию Т-клеток).
Вариант осуществления настоящего изобретения: адгезивные клетки по настоящему изобретению характеризуются более высокой иммуносупрессорной активностью по сравнению с адгезивными клетками плаценты или жировой ткани, выращенными с помощью двухмерного культивирования.
Вариант осуществления настоящего изобретения: иммуносупрессорная активность включает в себя снижение пролиферации Т-клеток.
Как было упомянуто выше и описано в Примере 6 раздела "Примеры", представленного ниже, адгезивные клетки по настоящему изобретению индуцировали ангиогенез in vivo (например, улучшали кровоток в бедре и нижней конечности), значительно улучшали функцию конечностей у животных, которым была осуществлена перевязка артерии, увеличивали плотность расположения капилляров и уменьшали окислительный стресс и воспаление эндотелия. Кроме того, как подробно описано в Примере 7 раздела "Примеры", представленного ниже, адгезивные клетки по настоящему изобретению значительно улучшали процесс восстановления после инсульта в экспериментах на крысах.
Таким образом, другой признак настоящего изобретения связан со способом лечения ишемии у пациентов, нуждающихся в данном лечении. Данный способ осуществляется посредством введения пациенту терапевтически эффективного количества адгезивных клеток по настоящему изобретению и обеспечения, таким образом, лечения присутствующей у пациента ишемии.
В рамках данного документа термин "ишемия" обозначает любую патологию (заболевание, патологическое состояние, синдром или расстройство), характеризующуюся недостаточностью ангиогенеза или связанную с недостаточностью ангиогенеза. Примерами ишемии являются, помимо прочего, заболевание периферических артерий (ЗПА) (например, ишемия конечности и критическая ишемия конечности (КИК), ишемическая болезнь сердца, ишемическая болезнь головного мозга (например, инсульт), замедленное заживление ран, замедленное заживление язв, нарушения репродуктивной функции, артериосклероз, ишемическое сосудистое заболевание, ишемическая болезнь сердца, ишемия миокарда, заболевание коронарных артерий (ЗКА; CAD), атеросклеротическое сердечно-сосудистое заболевание, заболевание главного ствола левой коронарной артерии, облитерирующее заболевание артерий, периферическая ишемия, заболевание периферических сосудов, сосудистое заболевание почки, заболевание периферических артерий, ишемия конечностей, ишемия нижних конечностей, ишемия головного мозга, цереброваскулярное заболевание, ретинопатия, нарушение восстановления и ремоделирования сетчатки, синдром фон Хиппеля-Линдау, наследственная геморрагическая телеангиэктазия, ишемическое сосудистое заболевание, болезнь Бюргера, ишемическое заболевание почек и ишемия плаценты.
В рамках данного документа термин "лечение" обозначает ингибирование или остановку развития патологии (например, ишемии) и/или индуцирование уменьшения выраженности, ремиссии или регрессии патологии. Специалистам в данной области известны различные способы и анализы, используемые с целью оценки развития патологии, а также различные способы и анализы, используемые для оценки уменьшения выраженности, ремиссии или регрессии патологии. Кроме того, термин "лечение" может обозначать облегчение или ослабление симптомов, связанных с патологией.
В рамках данного документа выражение "пациенты, нуждающиеся в данном лечении" обозначает любого пациента (например, млекопитающего), включая, например, человека, у которого выявлена соответствующая патология или человека, страдающего соответствующей патологией. Как уже было отмечено выше и описано в Примере 8 раздела "Примеры", представленного ниже, данные изобретатели установили, что адгезивные клетки по настоящему изобретению способны регенерировать и/или восстанавливать соединительную ткань.
Таким образом, другой признак настоящего изобретения связан со способом лечения заболевания, при котором необходима регенерация и/или восстановление соединительной ткани, у пациента, нуждающегося в данном лечении. Данный способ осуществляют путем введения пациенту терапевтически эффективного количества адгезивных клеток по настоящему изобретению.
Термин "соединительная ткань" обозначает поддерживающую каркасную ткань, состоящую из пучков коллагеновых и эластических волокон (расположенную, например, между мышцами и кровеносными сосудами и вокруг них) и простых клеток. Примерами соединительной ткани являются, помимо прочего, плотная соединительная ткань (например, связки, сухожилия, периодонтальная связка); ареолярная соединительная ткань (например, содержащая волокна, состоящие из белка - например, коллагена и эластина); ретикулярная соединительная ткань; жировая ткань; кровь; кость; хрящ; кожа; межпозвонковый диск; пульпа зуба; дентин; десна; клетки, образующие внеклеточный матрикс (ВКМ; ЕСМ); рыхлая соединительная ткань; и гладкомышечные клетки.
В рамках данного документа выражение "заболевание, при котором необходима регенерация и/или восстановление соединительной ткани" обозначает любую патологию, характеризующуюся наличием повреждения (то есть, наличием нефункционирующей ткани, раковой или предраковой ткани, разрыва ткани, перелома ткани, фиброзной ткани или ишемизированной ткани) или потери (например, после травмы, инфекционного заболевания, при наследственном заболевании и т.п.) соединительной ткани. Примерами таких патологий, не ограничивающими объема данного изобретения, являются перелом кости, рак кости (например, остеосаркома, костные метастазы), ожоговая рана, дефект суставного хряща и глубокая рана.
Выражение "ведение пациенту" обозначает введение клеток по настоящему изобретению в ткань-мишень. Клетки могут быть получены от реципиента или от аллогенного или ксеногенного донора. Это выражение также охватывает понятия "трансплантации", "замещения клеток" или "пересадки" пациенту клеток по настоящему изобретению.
Пациент может быть любым млекопитающим, нуждающимся в регенерации и/или восстановлении соединительной ткани, включая, например, человека или одомашненных животных - в том числе, помимо прочего, лошадей, крупный рогатый скот, коз, овец, свиней, собак, кошек, верблюдов, альпак, лам и яков.
Вариант осуществления настоящего изобретения: адгезивные клетки по настоящему изобретению могут быть использованы с целью лечения заболеваний, включающих в себя субхондральные костные кисты, переломы кости, остеопороз, остеоартрит, дегенерацию кости, различные раковые опухоли, сопровождающиеся потерей соединительной ткани (например, рак кости, остеосаркома, костные метастазы), повреждение хряща, дефект суставного хряща, дегенеративное заболевание межпозвонкового диска, osteogenesis imperfecta (OI), ожоги, ожоговые раны, глубокие раны, замедленное заживление раны, повреждения связок и повреждения сухожилий (например, повреждения сухожилий, связанные с их перенапряжением, у лошадей) у пациентов, нуждающихся в данном лечении (см. выше).
Клетки, которые можно вводить пациенту в соответствии с этим признаком настоящего изобретения, включают в себя вышеописанные адгезивные клетки, которые могут быть выращены в трехмерной или двухмерной культуре, а также мезенхимальные и немезенхимальные частично или окончательно дифференцированные производные этих клеток.
Способы получения клеток определенной линии дифференцировки из стромальных стволовых клеток по настоящему изобретению хорошо известных специалистам в данной отрасли (см., например, патенты США №№5,486,359, 5,942,225, 5,736,396, 5,908,784 and 5,902,741).
Клетки могут быть интактными или генетически модифицированными с целью получения клеток интересующей линии дифференцировки (см. Заявку на патент США №20030219423).
Клетки могут быть получены из аутологичного или неаутологичного (то есть, аллогенного или ксеногенного) источника, из свежих или замороженных (например, криоконсервированных) препаратов.
В зависимости от конкретного заболевания, пациенту могут вводить дополнительные химические препараты (например, иммуномодулирующие, химиотерапевтические и др. препараты) или клетки.
Поскольку введение в организм неаутологичных клеток может вызывать иммунную реакцию, было разработано несколько подходов, позволяющих снизить вероятность отторжения неаутологичных клеток. Эти подходы включают в себя либо подавление иммунной системы реципиента, либо инкапсулирование неаутологичных клеток перед трансплантацией с помощью ииммуноизолирующих полупроницаемых мембран.
Методики инкапсулирования, в целом, делятся на методики микроинкапсулирования (осуществляемые с использованием мелких сферических носителей) и методики макроинкапсулирования (осуществляемые с использованием более крупных мембран в форме плоских листов и полых волокон (Uludag, H. с соавт.Technology of mammalian cell encapsulation. Adv Drug Deliv Rev. 2000; 42: 29-64).
Способы приготовления микрокапсул известны специалистам в данной отрасли; они включают в себя, например, способы, описанные Lu MZ с соавт. в работе Cell encapsulation with alginate and alpha- phenoxycinnamylidene-acetylated poly(allylamine). Biotechnol Bioeng. 2000, 70: 479-83; Chang TM и Prakash S. в работе Procedures for microencapsulation of enzymes, cells and genetically engineered microorganisms. Mol Biotechnol. 2001, 17: 249-60; и Lu MZ, с соавт. в работе A novel cell encapsulation method using photosensitive poly(allylamine alpha-cyanocinnamylideneacetate). J Microencapsul. 2000, 17: 245-51.
Так, например, микрокапсулы приготавливают путем формирования комплекса модифицированного коллагена с третичной полимерной оболочкой 2-гидроксиэтилметилакрилата (ГЭМА; НЕМА), метакриловой кислоты (МАК; МАА) и метилметакрилата (ММА); толщина получаемой капсулы составляет 2-5 мкм. Такие микрокапсулы могут быть покрыты дополнительными оболочками из третичного полимера, каждая толщиной по 2-5 мкм, чтобы обеспечить получение гладкой поверхности, несущей отрицательный заряд, и снизить до минимума абсорбцию белков плазмы (Chia, S.М. с соавт., Multi-layered microcapsules for cell encapsulation Biomaterials. 2002 23: 849-56).
Другие микрокапсулы получают на основе морского полисахарида альгината (Sambanis, А. Encapsulated islets in diabetes treatment. Diabetes Technol. Ther. 2003, 5: 665-8) или его производных. Так, например, микрокапсулы могут быть приготовлены путем формирования полиэлектролитного комплекса полианионов альгината натрия и целлюлозы натрия сульфата с поликатионом поли(метилен-ко-гуанидином) гидрохлоридом в присутствии хлорида кальция. Следует иметь в виду, что инкапсулирование клеток осуществляется более эффективно в случае использования капсул меньших размеров. Так, показатели контроля качества, механической стабильности, диффузионных свойств и активности in vitro инкапсулированных клеток улучшались при уменьшении размера капсул с 1 мм до 400 мкм (Canaple L. с соавт., Improving cell encapsulation through size control. J Biomater Sci Polym Ed. 2002; 13:783-96). Кроме того, было показано, что нанопорозные биокапсулы с адекватным контролем размера пор, равного всего лишь 7 нм, правильно подобранными химическими свойствами поверхности и прецизионной микроархитектоникой обеспечивают эффективную иммуноизоляцию микросреды клеток (Williams D. Small is beautiful: microparticle and nanoparticle technology in medical devices. Med Device Technol. 1999, 10: 6-9; Desai, T.A. Microfabrication technology for pancreatic cell encapsulation. Expert Opin Biol Ther. 2002, 2: 633-46).
Примерами иммуносупрессорных агентов являются, помимо прочего, метотрексат, циклофосфамид, циклоспорин, циклоспорин А, хлорохин, гидроксихлорохин, сульфасалазин (сульфасалазопирин), соли золота, D-пеницилламин, лефлюномид, азатиоприн, анакинра, инфликсимаб (РЕМИКЭЙД), этанерцепт, блокаторы TNF-альфа, биологический агент, нацеливающий воспалительный цитокин, и нестероидные противовоспалительные препараты (НСПВП). Примерами НСПВП являются, помимо прочего, ацетилсалициловая кислота, салицилат холина и салицилат магния, дифлюнизал, магния салицилат, сальсалат, салицилат натрия, диклофенак, этодолак, фенопрофен, флюрбипрофен, индометацин, кетопрофен, кеторолак, меклофенамат, напроксен, набуметон, фенилбутазон, пироксикам, сулиндак, толметин, ацетаминофен, ибупрофен, ингибиторы ЦОГ-2 и трамадол.
При использовании любого из способов, описанных в данном документе, клетки можно вводить либо в изолированном виде, либо, предпочтительно, в составе фармацевтической композиции, которая дополнительно включает в себя фармацевтически приемлемый носитель. В рамках данного документа выражение "фармацевтическая композиция" обозначает препарат адгезивных клеток по настоящему изобретению (то есть, адгезивных клеток ткани, выбранной из группы, состоящей из плаценты и жировой ткани, полученных в результате трехмерного культивирования), дополнительно содержащий другие химические компоненты - например, фармацевтически пригодные носители и неактивные вещества. Фармацевтическая композиция предназначена для облегчения введения клеток пациенту.
В рамках данного документа термин "фармацевтически приемлемый носитель" обозначает носитель или разбавитель, не вызывающий у пациента значительного раздражения и не отменяющий биологической активности и свойств вводимого соединения. Примерами носителя, не ограничивающими объема настоящего изобретения, являются пропиленгликоль, физраствор, эмульсии и смеси органических растворителей с водой.
В рамках данного документа термин "неактивное вещество" обозначает инертное вещество, добавленное в фармацевтическую композицию с целью дополнительного облегчения введения действующего агента. Примерами неактивных веществ, не ограничивающими объема настоящего изобретения, являются карбонат кальция, фосфат кальция, различные сахара и виды крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли. Предпочтительный вариант осуществления настоящего изобретения: фармацевтический носитель является физиологическим раствором.
Методики приготовления состава и введения препаратов представлены в последнем издании "Remington's Pharmaceutical Sciences" Mack Publishing Co., Easton, PA, включенном в данный документ посредством ссылки на него.
Возможно системное введение данной фармацевтической композиции (как описано выше). Как альтернативный вариант, эту фармацевтическую композицию можно вводить местно - например, с помощью инъекции данной фармацевтической композиции непосредственно в ткань пациента.
Производство фармацевтических композиций по настоящему изобретению может осуществляться с использованием технологических процессов, хорошо известных специалистам в данной отрасли - например, с помощью обычных процессов смешивания, растворения, гранулирования, формирования драже, отмучивания, эмульгирования, инкапсулирования, улавливания или лиофилизации.
Таким образом, производство фармацевтических композиций, предназначенных для использования в соответствии с данным изобретением, может осуществляться обычными способами, с использованием одного или нескольких физиологически приемлемых носителей, включающих в себя неактивные и вспомогательные вещества, дающие возможность получить препараты с данными активными ингредиентами, пригодные для фармацевтического применения. Состав препарата зависит от способа введения, для которого он предназначен. Активные ингредиенты фармацевтических композиций, предназначенных для инъекций, могут быть представлены в форме водных растворов - предпочтительно в физиологически совместимых буферных растворах (например, в растворе Хэнка, растворе Рингера, забуференном физрастворе) или в замораживаемой среде, содержащей криоконсерванты. В составе препаратов, предназначенных для трансмукозального введения, должны присутствовать проникающие вещества, соответствующие преодолеваемому слизистому барьеру. Такие проникающие вещества, в целом, известны специалистам в данной отрасли.
Терапевтически эффективное количество или доза любого препарата, используемого в соответствии со способами, описанными в настоящем изобретении, может быть рассчитано предварительно на основании результатов анализов in vitro и анализов клеточных культур. Предпочтительным способом определения дозы является оценка достижения желаемой концентрации или титра препарата в исследовании на животных. Данная информация может быть использована с целью более точного определения доз, пригодных для применения у человека.
Токсичность и терапевтическая эффективность активных ингредиентов, описанных в данном документе, может быть определена с помощью стандартных фармацевтических методик in vitro, а также в исследованиях культур клеток и экспериментальных животных.
Данные, полученные в этих исследованиях in vitro, а также в исследованиях культур клеток и экспериментальных животных, могут быть использованы для определения диапазона доз, применимого при лечении людей. Дозы могут варьировать в зависимости от используемой фармацевтической формы и способа введения препарата. Конкретный состав, способ введения и доза могут быть выбраны врачом с учетом состояния пациента (см., например, данные Fingl с соавт. в кн. "The Pharmacological Basis of Therapeutics", глава 1, часть 1 (1975)). Так, например, динамическое наблюдение пациента с болезнью Паркинсона, оценивающее ослабление симтоматики двигательных нарушений, дает возможность определить положительную реакцию на лечение.
Активные ингредиенты фармацевтических композиций, предназначенных для инъекций, могут быть представлены в форме водных растворов - предпочтительно в физиологически совместимых буферных растворах (например, в растворе Хэнка, растворе Рингера, забуференном физрастворе).
Величину дозы и интервал между введениями можно устанавливать индивидуально, обеспечивая достижение уровней активного ингредиента, достаточных для эффективного регулирования синтеза нейромедиаторов имплантированными клетками. Дозы, необходимые для достижения желаемого эффекта, зависят от индивидуальных характеристик пациента и способа введения препарата. С целью определения концентраций препарата в плазме могут быть использованы соответствующие анализы.
В зависимости от тяжести заболевания и степени его резистентности к лечению, можно использовать однократное или многократное введение доз и продолжительность курса лечения, варьирующую от нескольких дней до нескольких недель или до достижения определенного улучшения состояния пациента.
Конечно, количество вводимого состава зависит от индивидуальных характеристик пациента, тяжести заболевания, способа введения препарата, мнения врача, назначающего препарат, и т.д. Дозы и интервалы между их введениями необходимо корректировать в зависимости от результатов тщательного непрерывного контроля динамики заболевания у данного пациента. Так, например, при лечении пациента с болезнью Паркинсона следует использовать такое количество клеток, которое достаточно для облегчения симптомов данного заболевания, обнаруживаемого с помощью контроля динамики состояния больного.
Модели повреждения связки включают в себя, помимо прочего, кроличью модель реконструкции передней крестообразной связки с использованием мезенхимальных стволовых клеток [Jit-Kheng с соавт., Arthroscopy (2004) 20(9): 899-910] и модель восстановления передней крестообразной связки с помощью длительно сохраняющейся биорезорбируемой опорной конструкции у коз [Altaian с соавт., J Am Acad Orthop Surg. (2008) 16(4): 177-187]. Модели восстановления сухожилия включают в себя, помимо прочего, модель восстановления сухожилия с использованием аутологичных мезенхимальных стволовых клеток у взрослых новозеландских белых кроликов [Awad с соавт., Tissue Eng. (1999) 5(3):267-77]. Модели восстановления кости описаны, например, в книге "Stem Cells in Endocrinology", Humana Press (2005) стр. 183-206; в этой книге описаны методики применения мезенхимальных стволовых клеток с целью восстановления кости.
После трансплантации клетки по настоящему изобретению предпочтительно выживают в пораженной области в течение некоторого периода времени (например, примерно одного месяца), достаточного для появления наблюдаемого терапевтического эффекта. Составы, в том числе, препарат по настоящему изобретению, содержащие совместимый фармацевтический носитель, могут быть приготовлены, помещены в соответствующую емкость и снабжены этикеткой с целью их последующего использования для лечения заболеваний, присутствующих в составе показаний.
Составы по настоящему изобретению можно, по желанию, выпускать в упаковке или диспенсерном устройстве (таком как, например, набор, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA)), в которых может присутствовать одна или более чем одна единичная доза препарата, содержащая активный ингредиент. Упаковка может быть изготовлена, например, из металлической или пластиковой фольги (как, например, блистерная упаковка). К упаковке или диспенсерному устройству могут прилагаться инструкции по применению препарата. Кроме того, в упаковке или диспенсере может присутствовать прилагаемое к емкости уведомление, свидетельствующее об одобрении органом, регулирующим производство, использование или продажу фармацевтических препаратов, данной формы выпуска и состава препарата для применения в медицине или ветеринарии; форма такого уведомления устанавливается данным государственным органом. Такое уведомление, например, может иметь форму этикетки, одобренной FDA для препаратов, отпускаемых по рецепту, или форму одобренного вкладыша в упаковку продукта.
Адгезивные клетки по настоящему изобретению могут иметь форму удобных фармацевтических композиций, удобно упакованных как фармацевтический продукт. Такой продукт включает в себя упаковочный материал, содержащий этикетку, указывающую, что данный препарат предназначен для использования с целью увеличения ангиогенеза в тканях и лечения ишемии и/или патологии, при которой необходима регенерация и/или восстановление соединительной ткани; при этом данный упаковочный материал отличается тем, что в нем упакованы адгезивные клетки по настоящему изобретению.
Следует иметь в виду, что адгезивные клетки по настоящему изобретению способны вызывать у пациента иммуносупрессию и/или толерантность. Таким образом, данные адгезивные клетки могут быть использованы с целью лечения любого заболевания, при котором необходима иммуносупрессия и/или толерантность. Такими заболеваниями являются, помимо прочего, аутоиммунные и воспалительные заболевания (включая острые и хронические воспалительные заболевания) - в том числе, помимо прочего, сердечно-сосудистые заболевания, ревматические заболевания, заболевания желез, заболевания желудочно-кишечного тракта, кожные заболевания, заболевания печени, неврологические заболевания, заболевания мышц, заболевания почек, заболевания половой системы, заболевания соединительной ткани и системные заболевания.
Примерами аутоиммунных сердечно-сосудистых заболеваний являются, помимо прочего, атеросклероз (Matsuura Ε. с соавт., Lupus. 1998;7 Suppl 2:S135), инфаркт миокарда (Vaarala О. Lupus. 1998;7 Suppl 2:S132), тромбоз (Tincani А. С соавт. Lupus 1998;7 Suppl 2:S 107-9), грануломатоз Вегенера, артериит Такаясу, синдром Кавасаки (Praprotnik S. С соавт., Wien Klin Wochenschr 2000 Aug 25; 1 12 (15-16):660), аутоиммунное заболевание с выработкой антител против фактора VIII (Lacroix-Desmazes S. С соавт., Semin Thromb Hemost.2000;26 (2): 157), некротизирующий васкулит мелких сосудов, микроскопический полиангиит, синдром Черджа и Штраусса, малоиммунный очаговый некротизирующий и полулунный гломерулонефрит (Noel LH. Ann Med Interne (Paris). 2000 May; 151 (3): 178), антифосфолипидный синдром (Flamholz R. С соавт, J Clin Apheresis 1999; 14 (4): 171), сердечная недостаточность, индуцированная антителами (Wallukat G. С соавт., Am J Cardiol. 1999 Jun 17;83 (12A):75H), тромбоцитопеническая пурпура (Moccia F. Ann Ital Med Int. 1999 Apr-Jun;14 (2): 114; Semple JW. С соавт. Blood 1996 May 15; 87 (10):4245), аутоиммунная гемолитическая анемия (Efremov DG. С соавт., Leuk Lymphoma 1998 Jan;28 (3-4):285; Sallah S. С соавт., Ann Hematol 1997 Mar;74 (3): 139), аутоиммунное поражение сердца при болезни Чагаса (Cunha-Neto Ε. С соавт., J Clin Invest 1996 Oct 15;98 (8): 1709) и аутоиммунное состояние, характеризующееся выработкой антител против Т-хелперов (Caporossi АР. С соавт., Viral Immunol 1998; 11 (1):9). Примерами аутоиммунных ревматических заболеваний являются, помимо прочего, ревматоидный артрит (Krenn V. С соавт., Histol Histopathol 2000 Jul; 15 (3): 791; Tisch R, McDevitt HO. Proc Natl Acad Sci units S A 1994 Jan 18;91 (2):437) и анкилозирующий спондилит (Jan Voswinkel с соавт., Arthritis Res 2001; 3 (3): 189).
Примерами аутоиммунных заболеваний желез являются, помимо прочего, заболевание поджелудочной железы, сахарный диабет I типа, заболевание щитовидной железы, болезнь Грейвса, тиреоидит, спонтанный аутоиммунный тиреоидит, тиреоидит Хашимото, идиопатическая микседема, аутоиммунное заболевание яичников, аутоиммунное бесплодие, связанное с выработкой антител против сперматозоидов, аутоиммунный простатит и аутоиммунный полигландулярный синдром I типа. Эти заболевания включают в себя, помимо прочего, аутоиммунные заболевания поджелудочной железы, сахарный диабет I типа (Castano L. и Eisenbarth GS. Ann. Rev. Immunol. 8:647; Zimmet P. Diabetes Res Clin Pract 1996 Oct; 34 Suppl:S125), аутоиммунные заболевания щитовидной железы, болезнь Грейвса (Orgiazzi J. Endocrinol Metab Clin North Am 2000 Jun; 29 (2):339; Sakata S. С соавт., Mol Cell Endocrinol 1993 Mar; 92 (1):77), спонтанный аутоиммунный тиреоидит (Braley-Mullen H. и Yu S, J Immunol 2000 Dec 15; 165 (12):7262), тиреоидит Хашимото (Toyoda N. с соавт., Nippon Rinsho 1999 Aug; 57 (8): 1810), идиопатическую микседему (Mitsuma T. Nippon Rinsho. 1999 Aug; 57 (8): 1759), аутоиммунное заболевание яичников (Garza KM. С соавт., J Reprod Immunol 1998 Feb; 37 (2):87), аутоиммунное бесплодие, связанное с выработкой антител против сперматозоидов (Diekman АВ. С соавт., Am J Reprod Immunol. 2000 Mar; 43 (3): 134), аутоиммунный простатит (Alexander RB. С соавт., Urology 1997 Dec; 50 (6):893) и аутоиммунный полигландулярный синдром 1 типа (Наrа Т. С соавт., Blood. 1991 Mar 1; 77 (5): 1127).
Примерами аутоиммунных желудочно-кишечных заболеваний являются, помимо прочего, хронические воспалительные заболевания кишечника (Garcia Herola А. С соавт., Gastroenterol Hepatol. 2000 Jan; 23 (1): 16), глютеиновая болезнь (Landau YE. И Shoenfeld Y. Harefuah 2000 Jan 16; 138 (2): 122), колит, илеит и болезнь Крона.
Примерами аутоиммунных кожных заболеваний являются, помимо прочего, аутоиммунные буллезные заболевания кожи, включая, помимо прочего, обыкновенная пузырчатка, буллезный пемфигоид и листовидная пузырчатка.
Примерами аутоиммунных заболеваний печени являются, помимо прочего, гепатит, аутоиммунный хронический активный гепатит (Franco А. С соавт., Clin Immunol Immunopathol 1990 Mar; 54 (3):382), первичный билиарный цирроз (Jones DE. Clin Sci (Colch) 1996 Nov; 91 (5):551; Strassburg СР. с соавт., Eur J Gastroenterol Hepatol. 1999 Jun; 11 (6):595) и аутоиммунный гепатит (Manns MP. J Hepatol 2000 Aug; 33 (2):326).
Примерами аутоиммунных неврологических заболеваний являются, помимо прочего, рассеянный склероз (Cross АН. С соавт., J Neuroimmunol 2001 Jan 1; 112 (1-2):1), болезнь Альцгеймера (Oron L. С соавт., J Neural Transm Suppl. 1997; 49:77), myasthenia gravis (Infante AJ. и Kraig E, Int Rev Immunol 1999; 18 (1-2): 83; Oshima M. с соавт., Eur J Immunol 1990 Dec; 20 (12):2563), нейропатии, двигательные нейропатии (Kornberg AJ. J Clin Neurosci. 2000 May; 7 (3): 191); синдром Гийена-Барре и аутоиммунные нейропатии (Kusunoki S. Am J Med Sci. 2000 Apr; 319 (4):234), миастения, миастенический синдром Ламбера-Итона (Takamori M. Am J Med Sci. 2000 Apr; 319 (4):204); паранеопластические неврологические заболевания, атрофия мозжечка, паранеопластическая атрофия мозжечка и синдром мышечной скованности (Hiemstra HS. С соавт., Proc Natl Acad Sci units S A 2001 Mar 27; 98 (7):3988); не-паранеопластический синдром мышечной скованности, прогрессирующие атрофии мозжечка, энцефалит, энцефалит Расмуссена, амиотрофический латеральный склероз, хорея Сиденгама, синдром Жиля де ля Туретта и аутоиммунные полиэндокринопатии (Antoine JC. и Honnorat J. Rev Neurol (Paris) 2000 Jan; 156 (1):23); нейропатии, связанные с расстройством иммунитета (Nobile-Orazio Ε. С соавт., Electroencephalogr Clin Neurophysiol Suppl 1999; 50:419); приобретенная нейромиотония, множественный врожденный артрогрипоз (Vincent А. С соавт., Ann Ν Y Acad Sci. 1998 May 13; 841:482), неврит, неврит зрительного нерва (Soderstrom M. с соавт., J Neurol Neurosurg Psychiatry 1994 May; 57 (5):544) и нейродегенеративные заболевания.
Примерами аутоиммунных заболеваний мышц являются, помимо прочего, миозит, аутоиммунный миозит и первичный синдром Шегрена (Feist Ε. с соавт., Int Arch Allergy Immunol 2000 Sep; 123 (1):92) и аутоиммунное заболевание гладких мышц (Zauli D. С соавт., Biomed Pharmacother 1999 Jun; 53 (5-6):234).
Примерами аутоиммунных заболеваний почек являются, помимо прочего, нефрит и аутоиммунный интерстициальный нефрит (Kelly CJ. J Am Soc Nephrol 1990 Aug; 1(2): 140). Примерами аутоиммунных заболеваний, связанных с половыми органами, являются, помимо прочего, повторные потери плода (Tincani А. с соавт., Lupus 1998; 7 Suppl 2:S107-9).
Примерами аутоиммунных заболеваний соединительной ткани являются, помимо прочего, ушные заболевания, аутоиммунные ушные заболевания (Yoo TJ. С соавт., Cell Immunol 1994 Aug; 157 (1):249) и аутоиммунные заболевания внутреннего уха (Gloddek В. С соавт., Ann Ν Y Acad Sci 1997 Dec 29; 830:266).
Примерами аутоиммунных системных заболеваний являются, помимо прочего, системная красная волчанка (Erikson J. С соавт., Immunol Res 1998; 17 (1-2):49) и системный склероз (Renaudineau Y. С соавт., Clin Diagn Lab Immunol. 1999 Mar; 6 (2): 156); Chan ОТ. С соавт., Immunol Rev 1999 Jim; 169: 107).
Кроме того, адгезивные клетки могут быть использованы с целью лечения заболеваний, связанных с пересадкой трансплантата, включая, помимо прочего, отторжение трансплантата, хроническое отторжение трансплантата, подострое отторжение трансплантата, сверхострое отторжение трансплантата, острое отторжение трансплантата и реакцию "трансплантат против хозяина".
В рамках данного документа термин "примерно" обозначает отклонение ±10%.
Изучение представленных ниже примеров, не налагающих каких-либо ограничений на объем данного изобретения, позволит обычным специалистам в данной отрасли ясно оценить дополнительные объекты, преимущества и новые признаки настоящего изобретения. Кроме того, приведенные ниже примеры подкрепляют экспериментальными данными каждый из различных вариантов осуществления и признаков настоящего изобретения, указанных выше и заявленных в разделе "Формула изобретения" ниже.
ПРИМЕРЫ
Ниже приведены ссылки на примеры, которые, в совокупности с вышеприведенными описаниями, иллюстрируют данное изобретение, никоим образом не ограничивая его объема. В целом, используемая в этом документе номенклатура, а также используемые в настоящем изобретении лабораторные методики, относятся к молекулярным, биохимическим и микробиологическим методикам, а также к методикам применения рекомбинантой ДНК. Эти методики подробно разъяснены в литературе - например, в таких работах как "Molecular Cloning: A laboratory Manual" Sambrook с соавт., (1989); "Current Protocols in Molecular Biology" том I-III, под ред. Ausubel, R.M. (1994); Ausubel с соавт. "Current Protocols in Molecular Biology", John Wiley and Sons, Baltimore, Maryland (1989); Perbal, "A Practical Guide to Molecular Cloning", John Wiley & Sons, New York (1988); Watson с соавт., "Recombinant DNA", Scientific American Books, New York; "Genome Analysis: A Laboratory Manual Series" под ред. Birren с соавт., том 1-4, Cold Spring Harbor Laboratory Press, New York (1998); методики в патентах США №№4,666,828; 4,683,202; 4,801,531; 5,192,659 и 5,272,057; "Cell Biology: A Laboratory Handbook", том I-III, под ред. Cellis, J.Ε., (1994); "Current Protocols in Immunology", том I-III, под ред. Coligan J. Ε. (1994); "Basic and Clinical Immunology" (8-e издание), под ред. Stites с соавт., Appleton & Lange, Norwalk, CT (1994); "Selected Methods in Cellular Immunology", под ред. Mishell и Shiigi, W. H. Freeman and Co., New York (1980); существующие иммунологические анализы подробно описаны в патенте и научной литературе: см., например, патенты США №№3,791,932; 3,839,153; 3,850,752; 3,850,578; 3,853,987; 3,867,517; 3,879,262; 3,901,654; 3,935,074; 3,984,533; 3,996,345; 4,034,074; 4,098,876; 4,879,219; 5,011,771 и 5,281,521; ''Oligonucleotide Synthesis'' ред. Gait, M.J. (1984); "Nucleic Acid Hybridization" под ред. Hames, В.D., и Higgins S.J. (1985); "Transcription and Translation" под ред. Hames, В.D. и Higgins S.J. (1984); "Animal Cell Culture" под ред. Freshney, R.L (1986); "Immobilized Cells and Enzymes" IRL Press, (1986); "A Practical Guide to Molecular Cloning" Perbal, В., (1984) и "Methods in Enzymology" Vol. 1-317, Academic Press; "PCR Protocols: A Guide To Methods And Applications", Academic Press, San Diego, CA (1990); Marshak с соавт., "Strategies for Protein Purification and Characterization - A Laboratory Course Manual" CSHL Press (1996); все эти работы включены в данный документ посредством ссылки на них точно так же, как было бы в случае их полного изложения в нем. В разных разделах этого документа приведены другие общие ссылки. Методики, описанные в работах, на которые даны ссылки, считаются хорошо известными в данной отрасли знаний и представлены для удобства читателя. Вся информация, содержащаяся в этих работах, включена в данный документ посредством ссылок на эти работы.
ПРИМЕР 1
ПРОИЗВОДСТВО И КУЛЬТИВИРОВАНИЕ АДГЕЗИВНЫХ КЛЕТОК КОСТНОГО МОЗГА, ПЛАЦЕНТЫ И ЖИРОВОЙ ТКАНИ
Адгезивные клетки культивировали в биореакторной системе, содержавшей трехмерные носители, с целью производства 3D-адгезивных клеток, характеризующихся специфическим профилем экспрессии клеточных маркеров. Эффективность выращивания клеток проверяли с помощью их подсчета. Способность этих клеток к дифференцировке проверяли с помощью культивирования в дифференцировочной среде.
Материалы и методики экспериментов
Адгезивные клетки костного мозга - Адгезивные клетки костного мозга (КМ; ВМ) получали из грудинного аспирата костного мозга гематологически здоровых доноров, которым проводилась открытая операция на сердце или биопсия костного мозга. Аспираты костного мозга разбавляли в 3 раза в сбалансированном солевом растворе Хэнка (HBSS; GIBCO BRL/Invitrogen, Гейтерсбург, Мэриленд) и центрифугировали в градиенте плотности Фиколл-Гипака (Robbins Scientific Corp. Саннивэйл, Калифорния). Затем осуществляли сбор мононуклеарных клеток костного мозга (<1,077 г/см3), их трехкратную промывку в HBSS и ресуспендирование в питательной среде [DMEM (Biological Industries, Бейт Ха'Эмек, Израиль) с добавлением 10% раствора ФТС (GIBCO BRL), 10-4 M раствора меркаптоэтанола (Merck, Уайт Хаус Стэйшн, Нью Джерси), смеси пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл; Бейт Ха'Эмек) и 2 мМ раствора L-глютамина (Бейт Ха'Эмек)]. Клетки, полученные от разных доноров, инкубировали раздельно в колбах для тканевых культур (Corning, Эктон, Массачусетс) при 37°С (5% СО2) с еженедельными сменами питательной среды. Каждые 3-4 дня клетки разъединяли с помощью 0,25% раствора трипсина-ЭДТК (Бейт Ха'Эмек). После 2-40 пассажей, при достижении 60-80% слияния, осуществляли сбор клеток для анализа или культивирования в биореакторах.
Адгезивные клетки плаценты - В стерильных условиях отсекали внутренние части родившейся доношенной плаценты (медицинский центр Бней Цион, Хайфа, Израиль), промывали их 3 раза буферным раствором Хэнка и инкубировали в течение 3 часов при 37°С с 0,1% раствором коллагеназы (1 мг/мл ткани; Sigma-Aldrich, Сент Луис, Монтана). С помощью осторожного пипетирования суспендированные клетки затем промывали DMEM, содержащей добавку 10% ФТС, смеси пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл) и 2 мМ раствора L-глютамина, высевали в колбы объемом 75 см2 и инкубировали при 37°С в инкубаторе культур тканей в условиях увлажнения, в атмосфере 5% СО2. Затем в течение 72 часов клетки прикреплялись к пластиковой поверхности, после чего каждые 3-4 дня осуществлялась смена питательной среды. При достижении 60-80% слияния (обычно через 10-12 дней) клетки отделяли от ростовой колбы с помощью 0,25% раствора трипсина-ЭДТК и высевали в новые колбы. Культивированные клетки затем собирали с целью проведения анализа или культивирования в биореакторах.
Адгезивные клетки жировой ткани - Адгезивные клетки были выделены из жировой ткани человека, полученной при проведении операций липосакции (Рамбам Хайфа, Израиль). Жировую ткань тщательно промывали равным объемом ФЗФ и переваривали при 37°С в течение 30 минут с помощью раствора коллагеназы в концентрации 20 мг/мл. Затем клетки промывали DMEM, содержащей добавку 10% ФТС, смеси пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл) и L-глютамина, центрифугировали со скоростью 1200 об./мин в течение 10 минут при комнатной температуре (КТ), ресуспендировали лизирующим раствором (1:10; Biological Industries, Бейт Ха'Эмек, Израиль, с целью удаления эритроцитов), центрифугировали и ресуспендировали в DMEM, содержащей добавку 10% ФТС, смеси пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл) и L-глютамина. Затем промытые клетки высевали в колбу со стерильной питательной средой для культуры ткани в количестве 3-10×107 клеток на одну колбу. На следующий день клетки промывали ФЗФ с целью удаления остаточных эритроцитов и мертвых клеток. Клетки хранили при 37°С в инкубаторе культур тканей в условиях увлажнения, в атмосфере 5% СО2. Каждые 3-4 дня осуществлялась смена питательной среды. При достижении 60-80% слияния клетки отделяли от ростовой колбы с помощью 0,25% раствора трипсина-ЭДТК и высевали в новые колбы. После 2-40 пассажей, при достижении 60-80% слияния клеток, осуществляли сбор клеток для анализа или культивирования в биореакторах.
Биореактор идеального вытеснения PluriX™ - В биореактор идеального вытеснения PluriX™ (Pluristem, Хайфа, Израиль; см. иллюстрации на Фиг. IG; см. также патент США №6,911,201) загружали 1-100 мл уплотненного трехмерного порозного носителя (диаметром 4 мм), изготовленного из полиэфирного неплетеного тканевого матрикса. Такой носитель обеспечивает возможность размножения большого количества клеток в относительно небольшом объеме. Разработка и производство стеклянной посуды были осуществлены компанией Pluristem (Pluristem, Хайфа, Израиль). Биореактор находился в инкубаторе, поддерживавшем температуру 37°С; скорость потока регулировали и контролировали с помощью клапана (6а на Фиг. IG) и перистальтического насоса (9 на Фиг. IG). Биореактор имеет порт для отбора проб и инъекций (4 на Фиг. IG), дающий возможность осуществлять последовательные высевы клеток. Питательную среду подавали при рН 6,7-7,4 из резервуара (1 на Фиг. IG). В резервуар подавали профильтрованную газовую смесь (2, 3 на Фиг. IG), содержавшую воздух/СО2/О2 в пропорциях, изменяемых в зависимости от плотности расположения клеток в биореакторе. Пропорцию О2 регулировали в зависимости от уровня растворенного О2 на выходе из биореактора, определяемого монитором (6 на Фиг. IG). Газовую смесь подавали в резервуар по силиконовым трубкам или с помощью диффузора (Degania Bet, Эмек Хайярден, Израиль). Питательную среду пропускали через сепараторную емкость (7 на Фиг. IG), позволяющую осуществлять сбор циркулирующих неадгезивных клеток. Циркуляция питательной среды обеспечивалась перистальтическим насосом (9 на Фиг. IG). Биореактор был дополнительно снабжен добавочным портом для отбора проб (10 на Фиг. IG) и емкостями для непрерывного обмена питательной среды.
Производство 3D-адгезивных клеток - Несливающиеся первичные 2D-культуры адгезивных клеток человека, выращенные в соответствии с описанием, представленным выше, были трипсинизированы, промыты, ресуспендированы в DMEM, дополненной 10% ФТС, смесью пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл) и 2 мМ раствором L-глютамина, и высеяны (103-105 клеток/мл) через инъекционный порт на 3D- носитель в стерильный биореактор идеального вытеснения (см. Фиг. IG). Перед высевом биореактор заполняли PBS-Ca-Mg (Biological Industries, Бейт Ха'Эмек, Израиль), автоклавировали (120°С, 30 мин) и промывали питательной средой Дульбекко, содержавшей 10% фетальную телячью сыворотку, инактивированную нагреванием, и смесь пенициллина-стрептомицина-нистатина (100 Ед/мл: 100 мкг/мл: 1,25 ед/мл). Расход поддерживали на уровне 0,1-5 мл/мин. Процесс высева осуществлялся в условиях 2-48-часовой остановки циркуляции, обеспечивавшей возможность заселения клетками носителей. С помощью инкубатора, в который, в соответствии с необходимостью, подавали стерильный воздух и СО2, обеспечивалось пребывание биореактора в условиях контролируемой температуры (37°С) и рН (рН=6,7-7,4).
Смена питательной среды осуществлялась 2-3 раза в неделю. Циркуляционную среду заменяли свежей средой DMEM с периодичностью, варьировавшей от 4 часов до 7 дней. После 12-40 дней роста, когда плотность клеток достигала 1×106-1×107 клеток/мл, из биореактора извлекали весь объем питательной среды, после чего биореактор и носитель 3-5 раз промывали ФЗФ. Затем 3D-адгезивные клетки отделяли от носителя с помощью трипсина-ЭДТК (Biological Industries, Beit Ha'Emek, Израиль; 3-15 минут осторожного перемешивания, 1-5 раз), после чего ресуспендировали в DMEM и криоконсервировали.
Качественные биологические анализы 3D-адгезивных клеток - Осуществляли оттаивание и подсчет криоконсервированных 3D-адгезивных клеток. С целью оценки жизнеспособности клеток, 2×105 клеток высевали в 150-см2 колбу для культур ткани и в течение 7 дней после высева оценивали способность клеток к приклеиванию и повторному заселению. После этого анализировали фенотип мембранных маркеров 3D-адгезивных клеток с помощью флоуцитометра с использованием флюоресцентных моноклональных антител (Beckman Coulter, Фуллертон, Калифорния).
Сравнение профилей маркеров клеточных мембран культивированных 3D- и 2D-адгезивных клеток, выявленных с помощью проточной цитометрии Было осуществлено суспендирование 100000-200000 адгезивных клеток двухмерных и трехмерных (в системе потока) культур в 0,1 мл питательной среды в 5-мл пробирке и инкубирование (4°С, 30 минут, в темноте) с насыщающими концентрациями каждого из следующих моноклональных антител (МКА; Mabs): антителом против CD90 человека, конъюгированным с ФИТЦ (Chemicon International Inc. Темекула, Калифорния), антителом против CD73 человека, конъюгированным с фикоэритрином (ФЭ; РЕ) (Bactlab Diagnostic, Ceasarea, Израиль), антителом против CD 105 человека, конъюгированным с ФЭ (eBioscience, Сан Диего, Калифорния), антителом против CD29 человека, конъюгированным с ФИТЦ (eBioscience, Сан Диего, Калифорния), антителом против CD45 человека, конъюгированным с Су7-ФЭ (eBiosience), антителом против CD 19 человека, конъюгированным с ФЭ (IQProducts, Гронинген, Голландия), антителом против CD 14 человека, конъюгированным с ФЭ (IQProducts), антителом против CD11b человека, конъюгированным с ФИТЦ (IQProducts), антителом против CD34 человека, конъюгированным с ФЭ (IQProducts) и антителом против HLA-DR человека, конъюгированным с ФИТЦ (IQProducts). После инкубирования клетки дважды промывали в ледяном ФЗФ, содержавшем 1% ФТС, инактивированную нагреванием, ресуспендировали в 500 мкл 0,5% формальдегида и анализировали с помощью флоуцитометра FC-500 (Beckman Coulter, Фуллертон, Калифорния).
Сравнение профилей белков культивированных 3D- и 2D-адгезивных клеток, выявленных с помощью масс-спектрометрического анализа. Культивированные 2D- и 3D-адгезивные клетки были получены из плаценты в соответствии с описанием, представленным выше. Вкратце, двухмерные культуры были получены с помощью четырехдневного культивирования 0,3-0,75×106 клеток в 175-см2 колбах в увлажненной атмосфере 5% СО2 при 37°С до достижения 60-80% слияния. Трехмерные культуры были получены с помощью высевания 2-10×10 клеток/грамм в биореактор, содержащий 2000 единичных носителей, и культивирования в течение 18 дней. Собранные клетки промывали три раза, чтобы удалить всю сыворотку, осаждали центрифугированием и замораживали. Из осажденных клеток выделяли белки с помощью набора Tri Reagent (Sigma, Saint Louis, США); затем эти белки переваривали трипсином и метили реактивом iTRAQ (Applied Biosciences, Фостер Сити, Калифорния)] в соответствии с методикой, описанной производителем. Вкратце iTRAQ можно охарактеризовать как неполимерные изобарные маркерные реактивы. Пептиды каждой пробы метятся одной из четырех изобарных меток, кодированных изотопом, в области N-конца и/или в области боковых цепей, содержащих лизин. Смешивают четыре меченые пробы и анализируют пептиды с помощью масс-спектрометрии. При фрагментировании пептидов каждая метка высвобождает особый масс-репортерный ион; таким образом, соотношение четырех репортеров указывает относительное количество данного пептида в пробе (см. информацию, представленную на сайте www.docs.appliedbiosystems.com/pebiodocs/00113379.pdf).
Сравнительный протеомный анализ двухмерной и трехмерной культур адгезивных клеток плаценты был выполнен в протеомном центре Смолера (Отделение биологии, Technion, Хайфа, Израиль) с использованием LC-MS/MS на QTOF-Premier (Waters, Сан Франциско, Калифорния); идентификация и анализ были выполнены с помощью программного обеспечения Pep-Miner [Beer, I., с соавт., Proteomics, 4, 950-60 (2004)] путем сопоставления с человеческой частью базы данных nr. Были проанализированы следующие белки: гетерогенный ядерный рибонуклеопротеин HI (Hnrphl, номер доступа GenBank: NP 005511), семейство гистонов Н2А (H2AF, номер доступа GenBank: NP 034566.1), эукариотический фактор элонгации трансляции 2 (EEEF2, номер доступа GenBank: NP 031933.1), ретикулокальбин 3, домен ветви EF, связывающий кальций (RCN2, номер доступа GenBank: NP 065701), предшественник изоформы 2 антигена CD44 (номер доступа GenBank: NP 001001389), основной гладкомышечный кальпонин 1 (CNN1, GenBank Accession No. NP 001290), изоформа а синтазы 3-фосфоаденозина 5-фосфосульфата 2 (Papss2, номер доступа GenBank: NP 004661), рибосомальный белок L7a (rpL7a, номер доступа GenBank: NP 000963) и альдегиддегидрогеназа X (ALDH X, номер доступа GenBank: Р47738). Каждый эксперимент проводили в двух повторностях. С учетом особенностей данного анализа, каждый белок был проанализирован в соответствии с количеством обнаружений его пептидов в пробе (2-20 обнаружений белка в каждом анализе).
Сравнение белков, секретируемых адгезивными клетками, полученными в результате двухмерного и трехмерного культивирования, с помощью ИФА - С помощью методик, описанных выше, получали 2D- и 3D-адгезивные клетки плаценты (3D-культуры - в течение 24 дней). Затем осуществляли сбор кондиционированных сред и их анализ с целью определения лиганда Flt-3, IL-6, тромбопоэтина (ТП; ТРО) и фактора стволовых клеток (ФСК) с помощью ИФА ELISA (R&D Systems, Миннеаполис, Миннесота) в трех независимых экспериментах. Результаты были нормализованы к 1×106 клеткам/мл.
Дифференцировочная среда остеобластов- Остеогенную дифференцировку оценивали с помощью культивирования клеток в дифференцировочной среде остеобластов, представлявшей собой DMEM, дополненную 10% ФТС, 100 нМ дексаметазона, 0,05 мМ 2-фосфата аскорбиновой кислоты, 10 мМ В-глицерофосфата, в течение 3 недель. Окрашивали кальцифицированный матрикс ализарином красным S, а также обнаруживали щелочную фосфатазу с помощью набора для определения щелочной фосфатазы (все реактивы были приобретены у компании Sigma-Aldrich, Сент Луис, Монтана).
Результаты экспериментов
Биореакторная система PluriX™ создает физиологичную микросреду
С целью обеспечения условий для эффективного культивирования адгезивных клеток, был использован биореактор PluriX (Pluristem, Хайфа, Израиль; носитель показан на Фиг. IG, а также, перед высевом клеток, на Фиг. IB), обеспечивающий создание физиологичной среды, показанной на Фиг. IA. Как показано на Фиг. IC-F, были обеспечены успешные культивирование и эфкспансия 3D-адгезивных клеток костного мозга на трехмерном матриксе через 20 дней (Фиг. IB-C, увеличение соответственно x150 и х250) и 40 дней (Фиг. IC-D, увеличение соответственно х350 и х500) после высева.
Биореакторная система PluriX обеспечивала значительную экспансию клеток - В биореакторных системах PluriX выращивали различные производственные партии 3D-адгезивных клеток плаценты. Плотность высева составляла 13300 клеток/носитель (общее количество - 2×10 клеток). Через 14 дней после высева плотность расположения клеток увеличивалась в 15 раз, достигая примерного уровня 200000 клеток/носитель (Фиг. 2) или 30×106 клеток в одном биореакторе, содержащем 150 единичных носителей. В другом эксперименте клетки высевали в биореактор в концентрации 1,5×104 клеток/мл, и через 30 дней после высева носитель содержал уже более чем в 50 раз большее количество клеток - то есть, примерно 0,5×106 клеток/носитель или 0,5×107 клеток/мл. Плотность расположения клеток равномерно распределялась между носителями на разных уровнях колонки роста, что свидетельствовало о равномерности доставки кислорода и питательных веществ к клеткам. Таким образом, было доказано, что данная система трехмерного культивирования обеспечивает условия, поддерживающие рост и длительное существование культур мезенхимальных клеток с высокой плотностью расположения клеток, и данные культуры можно эффективно выращивать в количествах, достаточных для использования в целях поддержки вживления клеток и успешной трансплантации.
3D-адгезивные клетки демонстрируют уникальные характеристики мембранных маркеров - С целью определения особенностей профилей секреции растворимых молекул и продукции белков, обусловленных процедурой трехмерного культивирования, моделирующей условия костной среды, был проведен анализ методом ФАСК. Как показано на Фиг. 3А, с помощью анализа маркеров клеток методом ФАСК было установлено, что 3D-адгезивные клетки отличаются от адгезивных клеток, выращенных в двухмерных условиях, в отношении профиля экспрессии маркеров. Клетки, выращенные в двухмерных условиях, экспрессировали значительно более высокие уровни положительных мембранных маркеров CD90, CD105, CD73 и CD29 по сравнению с клетками, выращенными в трехмерных условиях. Так, например, 3D-клетки демонстрировали 56%-ную, а 2D-клетки - 87%-ную экспрессию CD105. Как 2D-, так и 3D-адгезивные клетки плаценты не экспрессировали каких-либо гемопоэтических мембранных маркеров (Фиг. 3В).
3D-адгезивные клетки демонстрируют уникальный профиль растворимых факторов - Гемопоэтическая ниша включает в себя поддерживающие клетки, продуцирующие разнообразные цитокины, хемокины и факторы роста. С целью дополнительной оценки различий между 2D- и 3D-адгезивными клетками, с помощью ИФА был исследован профиль четырех основных секретируемых гемопоэтических белков в кондиционированных средах двухмерных и трехмерных культур адгезивных клеток. На Фиг. 4А-С показано, что клетки, выращенные в трехмерных условиях, продуцировали кондиционированную среду с более высокими уровнями лиганда Flt-3 (Фиг. 4А), IL-60 (Фиг. 4 В) и ФСК (Фиг. 4С); в кондиционированной среде двухмерных культур отмечались низкие уровни IL-6, а уровни лиганда Flt-3 и ФСК приближались к нулю. Продукция тромбопоэтина (ТРО) была очень низкой и одинаковой в обоих этих видах культур.
3D-адгезивные клетки демонстрируют уникальный профиль белков, оцениваемый с помощью масс-спектрометрического анализа - С целью дополнительной оценки различий между 2D- и 3D-адгезивными клетками, с помощью масс-спектрометрии был исследован белковый профиль этих клеток. Фиг. 4D показывает, что профили экспрессии белков 2D- и 3D-адгезивных клеток существенно различаются. Согласно данным, приведенным в таблице 1 ниже, трехмерно культивированные клетки демонстрировали гораздо более высокий уровень экспрессии H2AF и ALDH X (соответственно более чем в 9 и 12 раз выше) и более высокий уровень экспрессии белков EEEF2, RCN2 и CNN1 (соответственно примерно в 3, 2,5 и 2 раза выше), чем двухмерно культивированные клетки. Кроме того, трехмерно культивированные клетки демонстрировали примерно половину от уровня экспрессии белков Hnrphl и предшественника изоформы 2 антигена CD44, а также примерно треть от уровня экспрессии белков Papss2 и rpL7a, обнаруживаемого у двухмерно культивированных клеток.
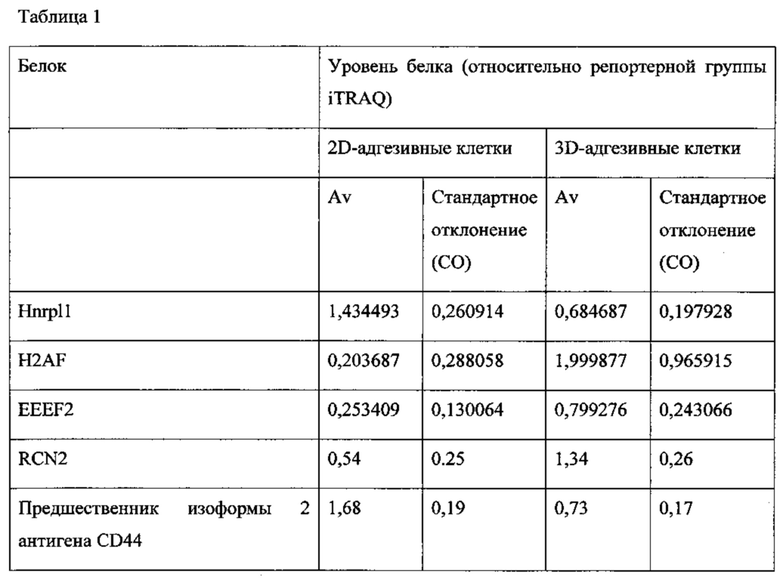
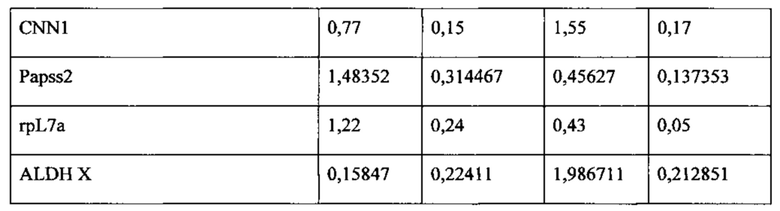
3D-адгезивные клетки обладают способностью дифференцировки в остеобласты - С целью оценки дополнительных характеристик 3D-адгезивных клеток, данные клетки культивировали в остеобластной дифференцировочной среде в течение 3 недель. Затем осуществлялось осаждение кальция. Было показано, что дифференцированные клетки вырабатывали кальций (кальцию соответствует красный цвет на Фиг. 5А-В), тогда как контрольные клетки сохраняли фибробластоподобный фенотип и демонстрировали отсутствие минерализации (Фиг. 5C-D). Эти результаты показывают, что 3D-адгезивные клетки плаценты способны дифференцироваться в остеобласты in vitro.
ПРИМЕР 2
ОЦЕНКА СПОСОБНОСТИ 3D-АДГЕЗИВНЫХ КЛЕТОК ПЛАЦЕНТЫ УЛУЧШАТЬ ВЖИВЛЕНИЕ ГСК
Поддержка 3D-адгезивными клетками вживления ГСК была оценена на основании данных об уровне гемопоэтических клеток человека (hCD45+), выявляемом у иммунодефицитных мышей NOD-SCID, подвергнутых сублетальному облучению или предварительной химиотерапии.
Материалы и методики экспериментов
Выделение клеток CD34+ - Во время родов в стерильных условиях получали пробы пуповинной крови (Медицинский центр Бней Цион, Хайфа, Израиль) и осуществляли фракционирование мононуклеарных клеток с помощью центрифугирования в градиенте плотности на приборе Lymphoprep (Axis-Shield РоС As, Осло, Норвегия) с последующим криоконсервированием клеток. Оттаянные мононуклеарные клетки промывали и инкубировали с антителами против CD34, а затем выделяли с помощью midi MACS (Miltenyl Biotech, Бергиш Гладбах, Германия). С целью получения желаемого количества клеток (50000-100000 клеток) объединяли нескольких проб. Выявление трансплантированных клеток у облученных мышей - Семинедельных самцов и самок мышей NOD-SCID (NOD-CB 17-Prkdcscid/J; Harlan/ Weizmann Inst., Реховот, Израиль) содержали в стерильных клетках открытого типа; мыши получали стерильную пищу и автоклавированную кислую воду. Мышей подвергали сублетальному облучению (350 сГр), а затем (через 48 часов после облучения) трансплантировали им 50000-100000 клеток hCD34+ в сочетании с дополнительным внутривенным введением в латеральную вену хвоста адгезивных клеток (0,5×106-1×106), полученных из плаценты или жировой ткани (3-7 мышей в каждой группе) или без введения адгезивных клеток. Через 4-6 недель после трансплантации мышей умерщвляли дислокацией шейных позвонков и осуществляли сбор костного КМ с помощью промывания обеих бедренных и большеберцовых костей ФАСК-буфером (50 мл ФЗФ, 5 мл фетальной бычьей сыворотки (ФБС; FBS), 0,5 мл 5% азида натрия). В КМ мышей с помощью проточной цитометрии выявляли клетки человека, и с помощью инкубирования клеток с антителами против CD45 человека, мечеными ФИТЦ (IQ Products, Гронинген, Голландия), у данных мышей NOD-SCID, подвергнутых воздействию, определяли процент человеческих и мышиных клеток, экспрессирующих гемопоэтический клеточный маркер CD45. Нижний порог несомненного вживления клеток человека был установлен на уровне 0,5%.
Выявление трансплантированных клеток у мышей, получавших химиотерапию - Самцам мышей NOD-SCID (NOD.CB17/JhkiHsd-scid; Harlan, Реховот, Израиль) в возрасте 6,5 недель, которых содержали в соответствии с условиями, описанными выше для облученных мышей, осуществляли внутрибрюшинное введение Бусульфана (25 мг/кг в течение двух последовательных дней). Через два дня после второй инъекции Бусульфана мышам вводили CD34+ клетки в сочетании с 0,5×106 адгезивных клеток, полученных из плаценты, или без введения адгезивных клеток. Через 3,5 недели после трансплантации мышей умерщвляли и оценивали присутствие человеческих гемопоэтических клеток в соответствии с методикой, описанной выше для облученных мышей.
Результаты экспериментов
3D-адгезивные клетки улучшали вживление ГСК у облученных мышей - Облученным мышам NOD-SCID трансплантировали сочетание человеческих гемопоэтических клеток CD34+ и 3D-адгезивных клеток, полученных из плаценты или жировой ткани. Эффективность вживления оценивали через 4 недели после данной сочетанной трансплантации; сравнивали полученные результаты с данными для мышей, которым трансплантировали только ГСК. В таблице 2 показано, что сочетанная трансплантация 3D-адгезивных клеток и клеток CD34+ пуповинной крови характеризовалась существенно более высокой частотой случаев вживления и более высокими уровнями человеческих клеток в костном мозге мышей-реципиентов по сравнению с мышами, получавшими только клетки CD34+ пуповинной крови.


3D-адгезивные клетки улучшали вживление ГСК у мышей, получавших химиотерапию - Мышам NOD-SCID, предварительно получавшим химиотерапию, трансплантировали сочетание человеческих гемопоэтических клеток CD34+ и 500000 2D-адгезивных клеток или 3D-адгезивных клеток, полученных из плаценты. Эффективность вживления оценивали через 3,5 недели после данной сочетанной трансплантации; сравнивали полученные результаты с данными для мышей, которым трансплантировали только ГСК. Как показывают таблица 3 и Фиг. 6, сочетанная трансплантация адгезивных клеток и клеток CD34+ пуповинной крови обеспечила более высокий уровень вживления в КМ мышей-реципиентов по сравнению с трансплантацией только лишь клеток CD34+ пуповинной крови. Кроме того, таблица 3 показывает, что средний уровень вживления был выше у мышей, которым были сочетанно трансплантированы адгезивные клетки плаценты, выращенные в биореакторной системе PluriX (3D-адгезивные клетки), чем у мышей, которым были сочетанно трансплантированы клетки того же донора, выращенные в обычной статичной двухмерной культуре (в колбе).
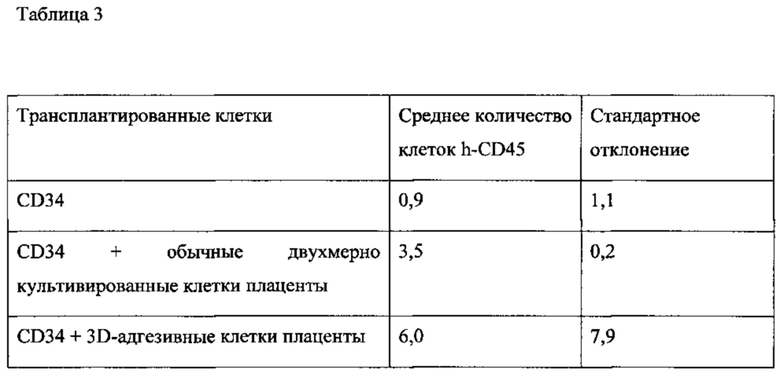
Результаты анализа методом ФАСК, представленные на Фиг. 7А-В, свидетельствуют о преимуществе сочетанной трансплантации адгезивных клеток и человеческих ГСК (Фиг. 7В), а также о способности адгезивных клеток улучшать процесс восстановления гемопоэтической системы после трансплантации ГСК.
Совокупность этих результатов показывает, что адгезивные клетки могут выполнять функцию поддерживающих клеток, улучшающих процесс восстановления гемопоэза после трансплантации ГСК (аутологичных или аллогенных). Способность 3D-адгезивных клеток повышать эффективность вживления стволовых гемопоэтических клеток и/или клеток-предшественников гемопоэза после трансплантации ГСК может быть следствием способности 3D-адгезивных клеток секретировать цитокины, поддерживающие ГСК и улучшающие процессы заселения и самообновления трансплантированных клеток, а также повышающие их способность к пролиферации; с другой стороны, она может быть следствием способности этих клеток восстанавливать нарушенную гемопоэтическую микросреду, необходимую для присутствия и пролиферации трансплантированных клеток ГСК.
ПРИМЕР 3
ПОДАВЛЕНИЕ РЕАКЦИИ ЛИМФОЦИТОВ 2D- И 3D-АДГЕЗИВНЫМИ КЛЕТКАМИ
Анализ PCЛ показал, что адгезивные клетки, особенно 3D-адгезивные клетки, подавляют иммунную реакцию мононуклеарных клеток пуповинной крови человека.
Материалы и методики экспериментов
Анализ реакции смешанных лимфоцитов (РСЛ) - Иммуносупрессорное действие и иммунологическая привилегированность 2D- и 3D-адгезивных клеток, полученных из плаценты, были продемонстрированы с помощью анализа РСЛ, оценивающего гистосовместимость по локусу HLA на основании данных о скорости пролиферации несовместимых лимфоцитов в смешанных культурах реагирующих (пролиферирующих) и стимулирующих (непролиферирующих) клеток. В качестве реагирующих клеток были использованы мононуклеарные клетки пуповинной крови человека (2×105); стимуляция этих клеток осуществлялась равными количествами (105) совместно культивируемых облученных (3000 Рад) моноцитов периферической крови (МПК; РВМС) человека, либо 2D- или 3D-адгезивных клеток, полученных из плаценты, либо сочетания адгезивных клеток и МПК. Каждый анализ выполняли в трех повторностях. Клетки совместно культивировали на 96-луночном планшете в течение 4 дней в среде RPMI 1640, содержащей 20% ФБС, в увлажненной атмосфере 5% СО2 при 37°С. В последние 18 часов культивирования осуществлялась обработка планшетов 1 мкКи 3Н-тимидина. Затем осуществлялись сбор клеток над стекловолоконным фильтром и количественное определение захвата тимидина с помощью сцинтилляционного счетчика.
Результаты экспериментов
На Фиг. 8А показана иммунная реакция клеток пуповинной крови, проявляющаяся повышенной пролиферацией этих клеток под влиянием стимуляции МПК; без каких-либо теоретических объяснений можно высказать предположение о том, что данная пролиферация, вероятно, связана с пролиферацией Т-клеток в ответ на несовместимость HLA. Вместе с тем, эти клетки демонстрировали существенно менее высокий уровень иммунной реакции при инкубировании с адгезивными клетками по настоящему изобретению. Более того, иммунная реакция клеток пуповинной крови на МПК была существенно уменьшена при совместном инкубировании с этими адгезивными клетками. Таким образом, было показано, что адгезивные клетки, как и МСК, способны уменьшать Т-клеточную пролиферацию донорских клеток, типичную для реакции "трансплантат против хозяина". Хотя иммунную реакцию лимфоцитов уменьшали обе культуры (как двухмерная, так и трехмерная), 3D-адгезивные клетки обладали более выраженным иммуносупрессорным эффектом; эта особенность хорошо согласуется с другими преимуществами 3D-адгезивных клеток, описанными выше.
ПРИМЕР 4
СРАВНЕНИЕ 3D-АДГЕЗИВНЫХ КЛЕТОК, ПРОИЗВОДИМЫХ PLURIX, С 3D-АДГЕЗИВНЫМИ КЛЕТКАМИ, ПРОИЗВОДИМЫМИ CELLIGEN
С целью получения больших количеств 3D-адгезивных клеток, была использована новая производственная система, называемая в этом документе "Celligen".
Материалы и методы экспериментов
Биореактор идеального вытеснения PluriX™ - Согласно описанию в Примере 1 выше.
Производство 3D-адгезивных клеток (клеток PLX) с помощью Plurix - Согласно описанию в Примере 1 выше.
Биореактор идеального вытеснения Celligen™- Производство адгезивных клеток (клеток PLX-С) с помощью Celligen состоит из нескольких основных этапов, проиллюстрированных на Фиг. 8В. Этот процесс начинается с получения плаценты во время плановой операции кесарева сечения при доношенной беременности.
Затем из целых плацент выделяют адгезивные клетки, выращивают их в колбах для культур тканей (двухмерные культуры), собирают и хранят в жидком азоте в качестве исходного запаса 2D-клеток (ИЗ2D; 2DCS). В последующем оттаивают необходимое количество ИЗ2D, промывают клетки и высевают их на носитель в биореакторах с целью экспансии в трехмерной культуре. После 1-3 недельного выращивания клеток в биореакторах осуществляют сбор клеток и их криоконсервирование в газовой фазе жидкого азота (наименование клеток - "клетки PLX-C").
Получение ткани человека
Все плаценты были получены в родильном отделении после получения соответствующего одобрения комитета по этике медицинского учреждения. Все доноры плаценты подписали информированное согласие. Были проведены скрининг доноров и тестирование доноров (IPCl). Сразу же после получения плаценты от донора во время операции кесарева сечения ее помещали в стерильный пластиковый мешок, а затем - в коробку Styrofoam с пакетами льда. Доставляемые плаценты немедленно помещали в карантинную зону, в которой специалистами отдела контроля качества (ОКК; QC) и отдела обеспечения качества (ООК; QA) осуществлялся выпуск плацент для последующего использования. Все последующие этапы производства выполнялись в карантине, в чистом помещении, до одобрения отделом контроля качества полученных результатов теста на микоплазмы и выпуска клеток для двухмерного культивирования.
Извлечение и обработка адгезивных клеток.
Производственный процесс начинался с разрезания целой плаценты на кусочки в условиях асептики в вытяжном шкафу с ламинарным потоком воздуха, промывания кусочков забуференным раствором Хэнка и их инкубирования с 0,1% раствором коллагеназы (1 мг коллагеназы на 1 миллилитр ткани) в течение 3 часов при 37°С. Добавляли питательную среду для двухмерного культивирования клеток (2D-Medium; эта среда представляла собой среду DMEM с добавлением 10% ФБС, 0,25 мкг/мл фунгизона и 50 мкг/мл гентамицина) и переваренную ткань грубо профильтровывали через стерильное металлическое сито, собирали в стерильный химический стакан и центрифугировали (10 минут, 1200 об./мин, 4°С). Затем с помощью осторожного пипетирования суспендированные клетки промывали средой 2D-Medium с добавлением антибиотиков, высевали в 80-см2 колбы и инкубировали при 37°С в инкубаторе для культур тканей в условиях увлажнения в атмосфере 5% СО2. По прошествии 2-3 дней, в течение которых клетки приклеивались к поверхности колбы, клетки промывали ФЗФ и добавляли 2D-Medium.
Двухмерное (2D) культивирование клеток
Перед первым пассированием объединяли пробы питательной среды 10% общего количества колб, находившихся в карантине, и проводили их анализ на микоплазмы (IPC2). В случае получения отрицательного результата анализа клеток на микоплазмы (набор EZ-PCR Mycoplasma, Biological Industries, Израиль), клетки выпускали из карантина. После 1-2 дополнительных пассажей клетки переносили в чистое помещение для 20-производства (2D-П; 2DP). После переноса клеток в помещение 2DP культивирование продолжали в течение еще 3-5 пассажей. После 4-го пассажа брали пробу IPC-3 с целью определения иммунологического фенотипа. В течение всего производственного процесса культивирование осуществлялось на среде 2D-Medium без антибиотиков, в инкубаторе для культур тканей, в увлажненной атмосфере 5% СО2, при температуре 37°С. После 6-8 пассажей (9-16 удвоений количества клеток) осуществляли сбор и криоконсервирование клеток с целью их использования в качестве исходного запаса 2D-клеток (ИЗ2D; 2DCS).
Первое пассирование обычно осуществляли по прошествии 10-15 дней. Начиная со 2-го пассажа и заканчивая 6-8-м пассажем, клетки пассировали по достижении 70-80% слияния - обычно через 3-5 дней (1,5-2 удвоения клеток). Клетки отделяли от колб с помощью 0,25% раствора трипсина-ЭДТК (в течение 4 минут при 37°С) и высевали исходя из расчетной плотности культуры 3±0,2×103 клеток/см2. Размеры используемых колб для культур тканей увеличивались по мере осуществления последовательных перевиваний клеток. Процесс культивирования начинали в 80-см2 колбе для культур тканей и продолжали последовательно в 175-см2 и 500-см2 (тройной) колбе, после чего клетки высевали на лоток Cell Factory 10 (6320 см2).
Перед криоконсервированием (в конце периода производства ИЗ2D) осуществляли сбор питательной среды и брали пробу для отправки в одобренную лабораторию, соответствующую требованиям Надлежащей лабораторной практики (GLP), для проведения теста на микоплазмы (IPC 4).
Методика криоконсервирования произведенного исходного запаса 2D-клеток
С целью криоконсервирования ИЗ2D, осуществляли сбор двухмерно культивированных клеток в асептических условиях с использованием 0,25% раствора трипсина-ЭДТК. Клетки центрифугировали (1200 об./мин, 10 минут, 4°С), подсчитывали и ресуспендировали в среде 2D-Medium.
С целью замораживания, суспензии клеток разбавляли смесью для замораживания 2D-клеток в соотношении 1:1 (окончательные концентрации составляли 10% DMSO, 40% ФБС и 50% 2D-Medium). На основе материала одной плаценты производили примерно 1,5-2,5×109 клеток. Клетки хранили в 5-мл полипропиленовых флаконах для криоконсервирования, по 4 мл в каждом флаконе, в конечной концентрации 10×106/мл. Флаконы, снабженные этикетками, переносили в морозильник с регулируемой температурой с целью постепенного замораживания (со скоростью 1°С/мин); после замораживания флаконы переносили в газовую фазу морозильника с жидким азотом, расположенного в помещении холодильного хранения, с целью последующего хранения. Данный материал называли "партией исходного запаса 2D-клеток (ИЗ2D)".
Начало процедур трехмерного (3D) культивирования С целью начала процедур трехмерного культивирования, оттаивали соответствующее количество клеток (150±30×106) из ИЗ2D в помещении 2D-Π и промывали средой 3D-Medium (DMEM с 10% ФБС и 20 мМ Hepes) с целью удаления DMSO перед высевом в предварительно подготовленные биореакторные системы. Содержимое каждого флакона ИЗ2D пипетировали и разбавляли в соотношении 1:9 средой 3D-Medium, предварительно подогретой до температуры 37°С. Клетки центрифугировали (1200 об./мин, 10 минут, 4°С) и ресуспендировали в 50-100 мл среды 3D-Medium, предварительно подогретой до температуры 37°С, в стерильном флаконе объемом 250 мл. Брали пробу и подсчитывали клетки с помощью окрашивания трипановым синим с целью определения количества и жизнеспособности клеток. Суспензию клеток переносили в посевной флакон объемом 0,5 Л в вытяжном шкафу с ламинарным потоком воздуха. Из посевного флакона суспензия клеток перемещалась по стерильной трубке в биореактор под действием силы тяжести.
Производство 3D-адгезивных клеток в биореакторе Celligen (PLX-C)
Описание биореактора
Этап трехмерного культивирования осуществляли с помощью автоматической биореакторной системы CelliGen Plus® или BIOFLO 310 [(New Brunswick Scientific (NBS)], описанной на Фиг. 8С. Эта биореакторная система была использована с целью культивирования клеток в условиях, подходящих для высоких концентраций клеток. Процесс культивирования клеток осуществлялся в перфузионном режиме работы биореактора. Лабораторный биореактор состоял из двух основных систем - системы управления и самого биореактора (резервуара и принадлежностей). Контроль параметров процесса и управление ими осуществлялись с помощью пульта управления, включавшего в себя соединители для зондов, электродвигателя и насосов; контуры управления для растворенного кислорода (РК; DO), рН, перфузии и перемешивания (с помощью электродвигателя); систему управления газами; систему циркуляции и нагрева воды; управление температурой; и интерфейс оператора. Контролируемые параметры производственного процесса (например, температуру, рН, РК и т.д.) можно выводить на дисплей интерфейса оператора и контролировать с помощью соответствующего контроллера.
Процедура выращивания культур клеток в биореакторах
Как уже было указано выше, осуществлялось оттаивание, промывание и высев в стерильный биореактор 150±30×106 клеток из криоконсервированного ИЗ2D. Биореактор содержал 30-50 г носителя (диски FibraCel®, NBS), изготовленного из полиэфира и полипропилена, и 1,5±0,1 Л среды 3D-Medium. В биореакторе поддерживались следующие условия питательной среды: 37°С, 70% растворенного кислорода (РК) и рН 7,3. Система управления осуществляла регулируемую подачу профильтрованных газов (воздуха, СО2, N2 и О2), обеспечивающую поддержание РК на уровне 70% и рН на уровне 7,3. В течение первых 24 часов осуществлялось перемешивание среды со скоростью 50 оборотов в минуту (об./мин); в течение следующих 24 часов скорость перемешивания постепенно увеличивалась до уровня 200 об./мин. В течение первых 2-3 дней культивирование клеток осуществлялось по партиям. Перфузию начинали при снижении глюкозы в питательной среде до уровня менее 550 мг/литр. Питательную среду перекачивали из питающей емкости в биореактор по стерильной силиконовой трубке. Все подсоедининения этой трубки были выполнены в условиях ламинарного потока воздуха с использованием стерильных соединителей. Перфузию ежедневно корректировали с целью поддержания концентрации глюкозы на постоянном уровне, равном примерно 550±50 мг/литр. Каждые 1-2 дня брали пробу питательной среды с целью определения уровней глюкозы, лактата, глютамина, глютамата и аммония (анализатор BioProfile 400, Nova Biomedical). Данные об уровне потребления глюкозы и скорости образования лактата культурой клеток давали возможность оценить скорость размножения клеток. Эти параметры были использованы для определения времени сбора клеток с учетом накопленных экспериментальных данных.
Извлечение 3D-клеток PLX-X из биореактора
Процесс сбора клеток начинали в конце фазы роста (4-10 дней). Получали 2 пробы питательной среды. Одну пробу подготавливали к отправке в одобренную лабораторию, отвечающую требованиям GLP, для проведения анализа на микоплазмы в соответствии со стандартами Фармакопеи США (USP) и Европейского Союза, а другую пробу переносили в морозильник с управляемой скоростью охлаждения с целью постепенного замораживания (1°С/мин), после которого эту пробу переносили в газовую фазу морозильника с жидким азотом, расположенного в Помещении холодильного хранения, для хранения на случай проведения повторного теста на микоплазмы. Эти пробы питательной среды рассматривались как часть теста конечного продукта на микоплазмы, и результаты их исследований считались частью выпускных критериев продукта.
Сбор клеток трехмерной культуры осуществлялся в зоне ламинарного потока воздуха класса 100 помещения 3DP следующим образом:
Резервуар биореактора опорожняли под действием силы тяжести через трубку в емкость для отходов. Резервуар открывали, снимая верхнюю стенку, и носители асептически переносили с помощью стерильного пинцета из корзины в верхнюю сетку корзины (см. Фиг. 8С). Затем резервуар биореактора закрывали и снова заполняли 1,5 литрами предварительно подогретого ФЗФ (37°С). Скорость перемешивания повышали до 150 об./мин и осуществляли перемешивание с этой скоростью в течение 2 минут. Затем ФЗФ сливали через трубку под давлением или под действием силы тяжести в бутыль для отходов. Данную процедуру промывания выполняли два раза.
С целью отделения клеток от носителя в резервуар биореактора заливали 1,5 Л предварительно подогретого до 37°С трипсина-ЭДТК (трипсин 0,25%, ЭДТК 1 мМ), и носитель перемешивали в течение 5 минут со скоростью 150 об/мин при 37°С. Суспензию клеток собирали в стерильную емкость объемом 5 литров, содержавшую 250 мл ФБС. Суспензию клеток разливали в четыре 500-мл стерильные центрифужные пробирки и брали пробу для анализа на микоплазмы. Закрытые центрифужные пробирки передавали через активное передаточное окно 3DP в помещение фасования класса 10000 (FR1), в котором осуществлялось асептическое фасование и криоконсервирование клеток ("клетки PLX-C"). Анализ клеточного цикла - Клетки PLX-C, полученные с помощью Celligen, и клетки PLX, олученные с помощью Plurix, фиксировали с помощью 70% EtOH O.N, центрифугировали и ресуспендировали в растворе йодида пропидия (ЙП; PI), содержавшем 2 мкг/мл ЙП (Sigma), 0,2 мг/мл РНКазы A (Sigma) и 0,1% (в объемном отношении) Тритона (Sigma) в течение 30 минут. Анализ клеточного цикла осуществляли с помощью ФАСК.
Массив экспрессии генов (Микромассив) - Адгезивные клетки получали из доношенных плацент человека; экспансию адгезивных клеток осуществляли в Plurix или Celligen. Для дальнейших исследований каждым из способов экспансии было получено по три разных партии клеток.
Из клеток экстрагировали РНК (микронабор Qiagen-Rneasy) и исследовали ее с помощью технологии Affymetrix для оценки массива экспрессии целого генома. Был использован набор для оценки чипов GeneChip® Human Exon 1.0 ST Array (Affymetrix, Santa Clara, Калифорния, США).
Анализ мембранных маркеров с помощью ФАСК - Клетки окрашивали моноклональными антителами как описано выше. Вкратце, 400000-600000 клеток суспендировали в 0,1 мл флоуцитометрического буфера в 5-мл пробирке и инкубировали в течение 15 минут при комнатной температуре (КТ; RT), в темноте, с каждым из следующих моноклональных антител (МАА; MAbs): МАА против CD29 человека, конъюгированным с ФИТЦ (eBioscience), МАА против CD73 человека, конъюгированным с фикоэритрином (ФЭ; РЕ) (Бектон Диккинсон), МАА против CD 105 человека, конъюгированным с ФЭ (eBioscience), МАА против CD90 человека, конъюгированным с ФЭ (Бектон Диккинсон), МАА против CD45 человека, конъюгированным с ФИТЦ (IQProducts), МАА против CD 19 человека, конъюгированным с ФЭ (IQProducts), МАА против CD 14 человека, конъюгированным с ФЭ (IQProducts), МАА против HLA-DR человека, конъюгированным с ФИТЦ (IQProducts), МАА против CD34 человека, конъюгированным с ФЭ (IQProducts), МАА против CD31 человека, конъюгированным с ФИТЦ (eBioscience), МАА против KDR человека, конъюгированным с ФИТЦ (R&D systems), МАА против маркера фибробластов человека (D 7-FIB) (ACRIS), МАА против CD80 человека, конъюгированным с ФИТЦ (BD), МАА против CD86 человека, конъюгированным с ФИТЦ (BD), МАА против CD40 человека, конъюгированным с ФИТЦ (BD), МАА против HLA-ABC человека, конъюгированным с ФИТЦ (BD), изотипом IgGl, конъюгированным с ФИТЦ (IQ Products), и изотипом IgGl, конъюгированным с ФЭ (IQ Products).
Клетки дважды промывали во флоуцитометрическом буфере, ресуспендировали в 500 мкл флоуцитометрического буфера и анализировали с помощью проточной цитометрии с использованием флоуцитометра FC-500 (Beckman Coulter). Отрицательные контроли были приготовлены с использованием флюоресцентных молекул соответствующего изотипа.
Реакция смешанных лимфоцитов (РСЛ)
2×105 МНК периферической крови (ПК; PB), полученных от донора А, были подвергнуты стимулирующему воздействию равного количества облученных (3000 Рад) МНК ПК, полученных от донора В. К этим культурам добавляли возрастающие количества клеток PLX-С. Осуществляли высев каждой группы на 96-луночные планшеты в трех повторностях. Клетки культивировали на среде RPMI 1640, содержавшей 20% ФБС. В последние 18 часов пятидневного культивирования осуществлялась обработка планшетов 1 мкКи 3Н-тимидина. Затем осуществлялись сбор клеток над стекловолоконным фильтром и количественное определение захвата тимидина с помощью сцинтилляционного счетчика.
С целью оценки пролиферации МНК ПК перед культивированием окрашивали CFSE (Molecular Probes). Через пять дней осуществляли сбор клеток и оценивали интенсивность окрашивания CFSE с помощью проточной цитометрии.
ИФА
ИФА осуществляли в соответствии с описаниями, представленными ранее. Вкратце, МНК, выделенные из периферической крови, стимулировали 5 мкг/мл ConA (Sigma), 0,5 мкг/мл LPS (SIGMA) или 10 мкг/мл РНА (SIGMA) в присутствии PLX-C в увлажненной атмосфере 5% СО2 при 37°С. Собирали надосадочную жидкость и подвергали ее анализу на цитокины с помощью наборов ИФА для IFNγ (DIACLONE), TNFα (DIACLONE) и IL-10 (DIACLONE).
Результаты экспериментов
Было выявлено несколько важных различий производственных показателей при использовании Celligen в сравнении с Plurix; эти различия суммированы ниже в таблице 4.


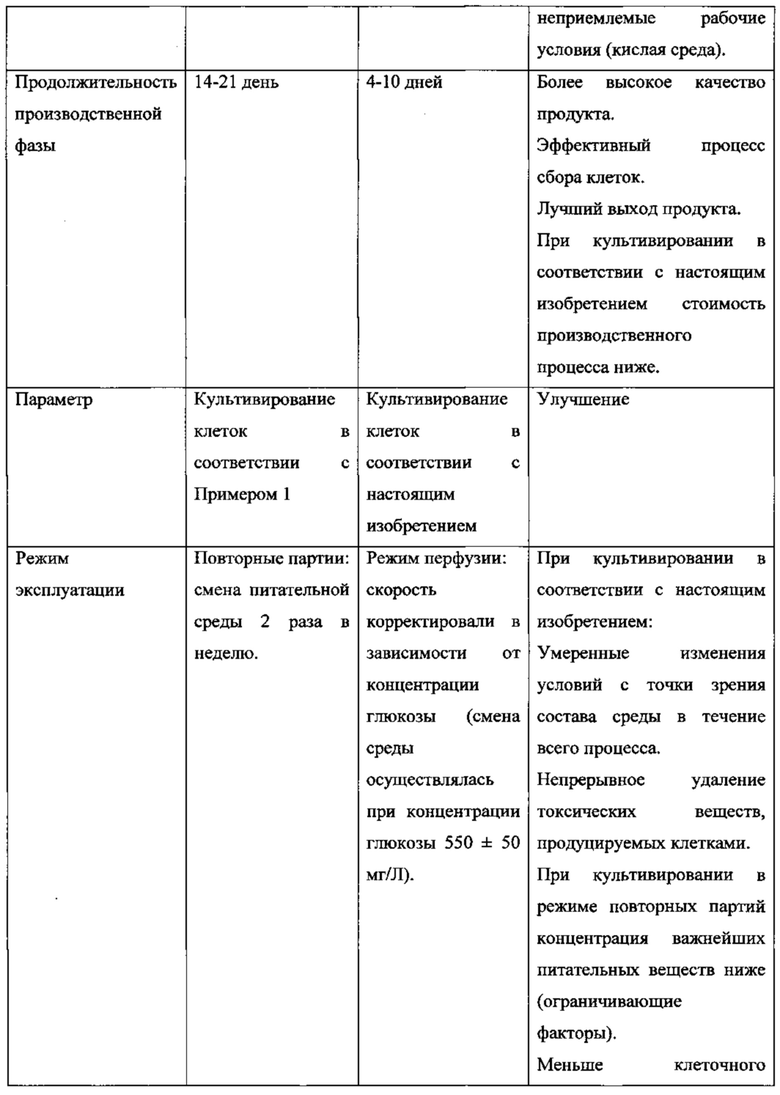
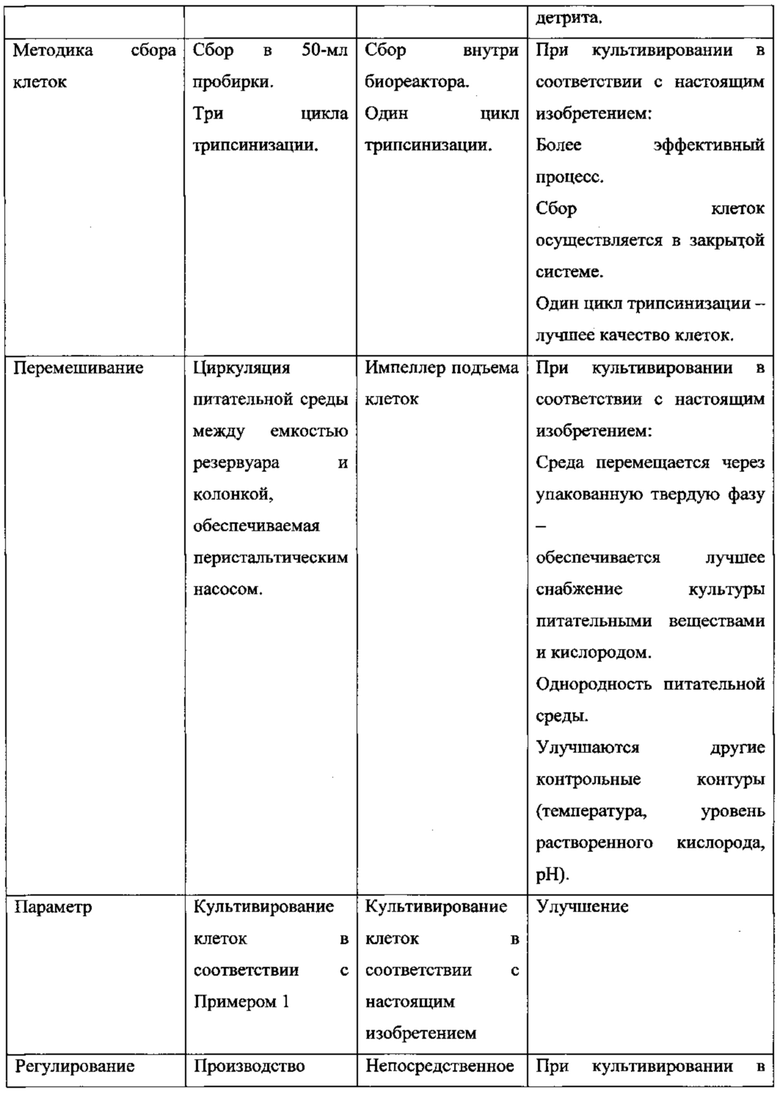
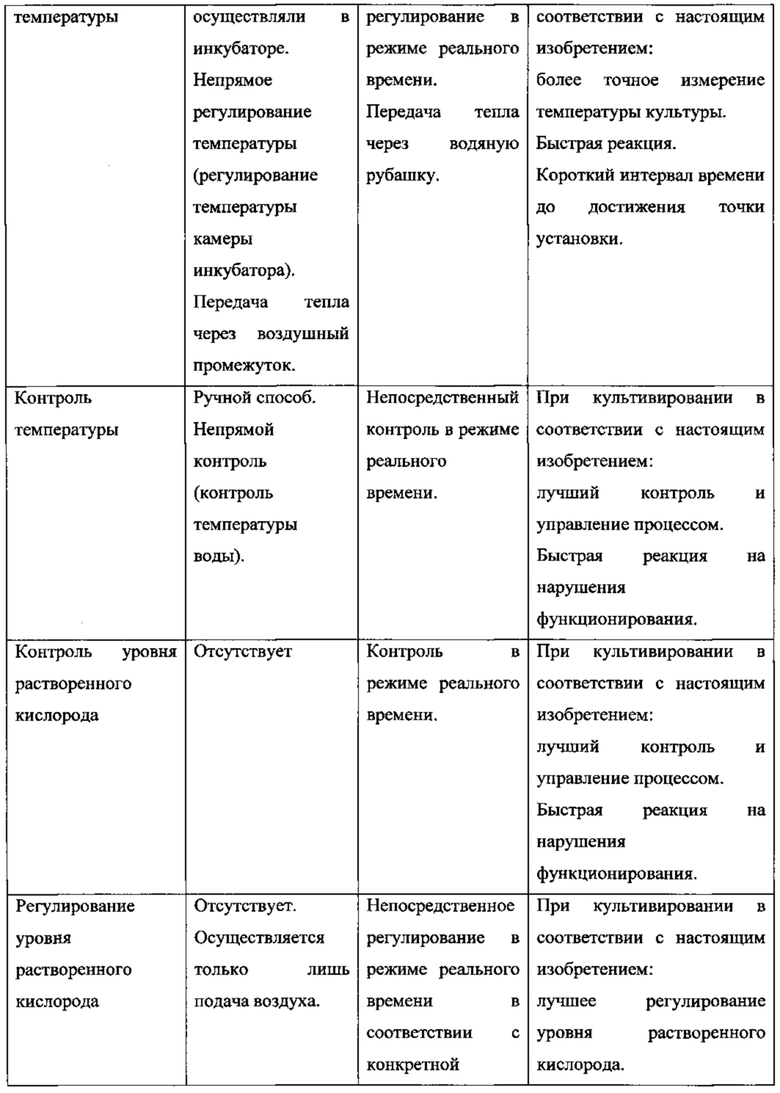

Различия производственных процессов привели к различиям характеристик получаемых 3D-адгезивных клеток. Эти различия суммированы ниже.
Анализ клеточного цикла PLX, производимых Plurix, в сравнении с клеточным циклом PLX-C, производимыми Celligen - С целью оценки распределения клеток между различными фазами клеточного цикла, было осуществлено сравнение клеток PLX-C, получаемых с помощью Celligen, с клетками PLX, получаемыми с помощью Plurix. Как показано на Фиг. 9А-В, клетки PLX-C, размножаемые с помощью Celligen, демонстрировали типичный профиль пролиферации (распределение клеток между разными фазами клеточного цикла) - а именно, 28% клеток находились в фазах S и G2/M (Фиг. 9А). Эти результаты показали, что сбор клеток осуществлялся во время пролиферации, и условия, создаваемые в биореакторе Celligen, поддерживали размножение клеток.
Сравнение микромассивов экспрессии генов клеток, полученных с помощью Plurix, и клеток, полученных с помощью Celligen - Оценка массивов экспрессии генов давала возможность одновременно контролировать профили экспрессии генов в пределах целого генома адгезивных клеток, получаемых из доношенных плацент человека и размножаемых с помощью Plurix (PLX) или Celligen (PLX-C). Полученные результаты позволили оценить молекулярный механизм, лежащий в основе фенотипических различий между клетками, получаемыми с помощью этих разных способов культивирования (см. таблицу 5 ниже).
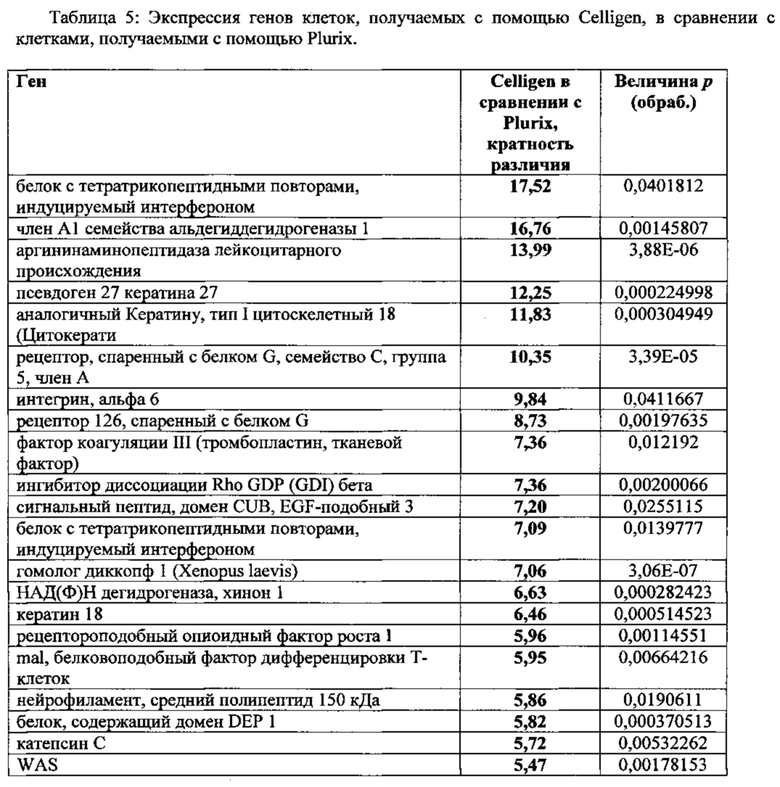
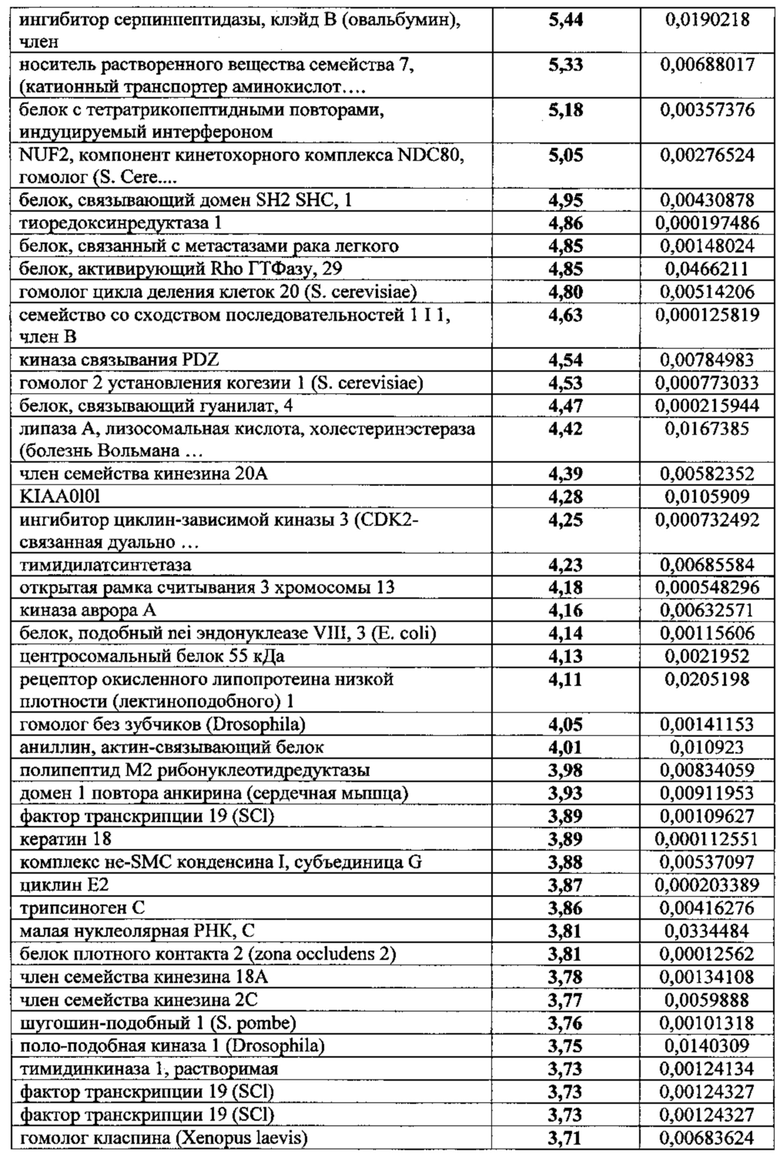
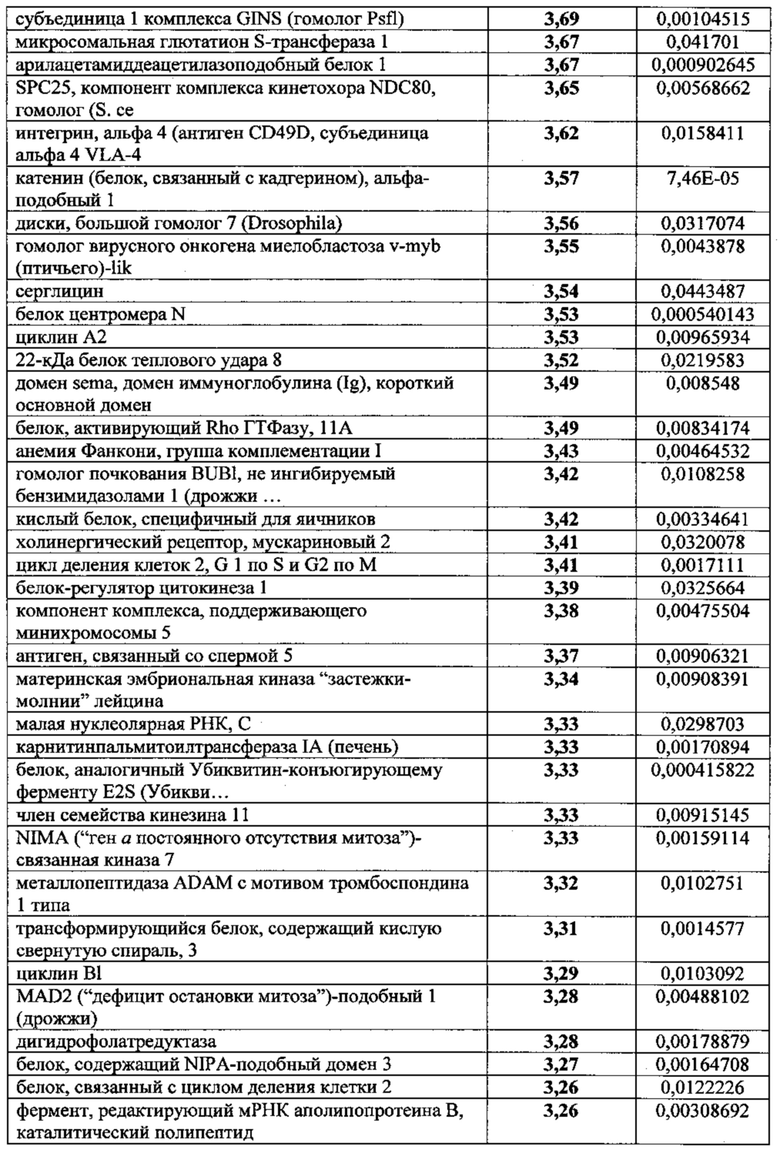
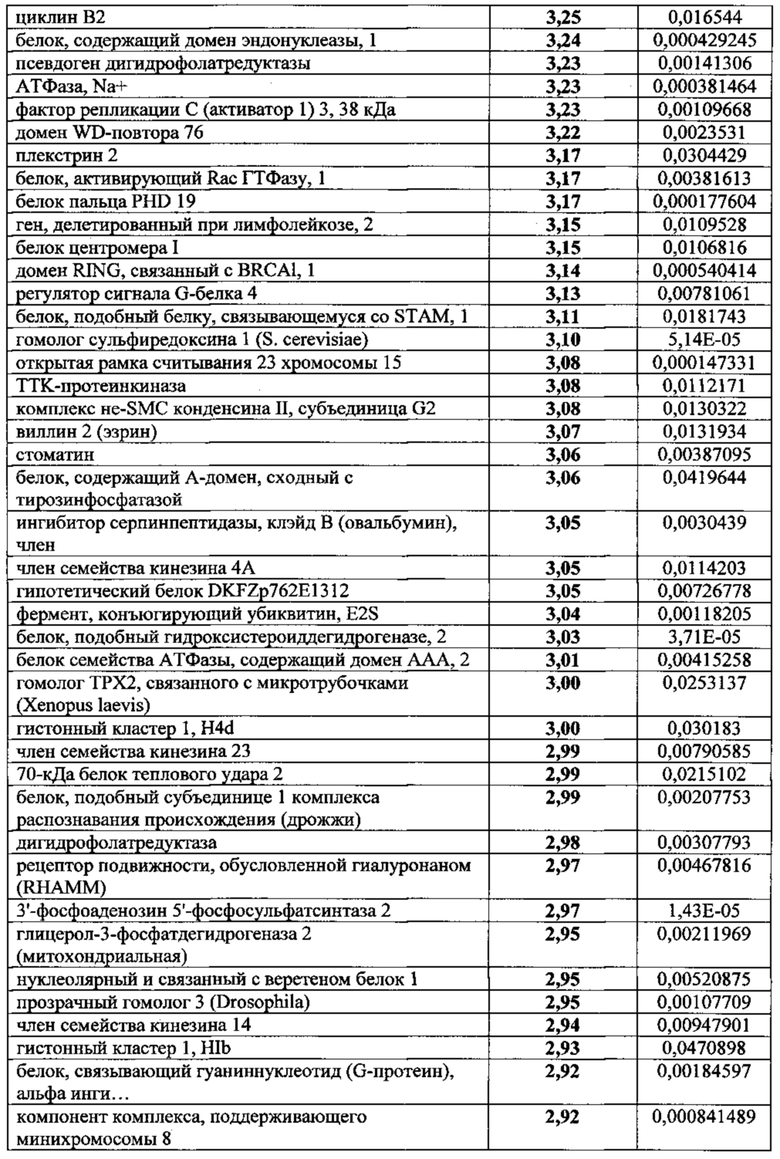
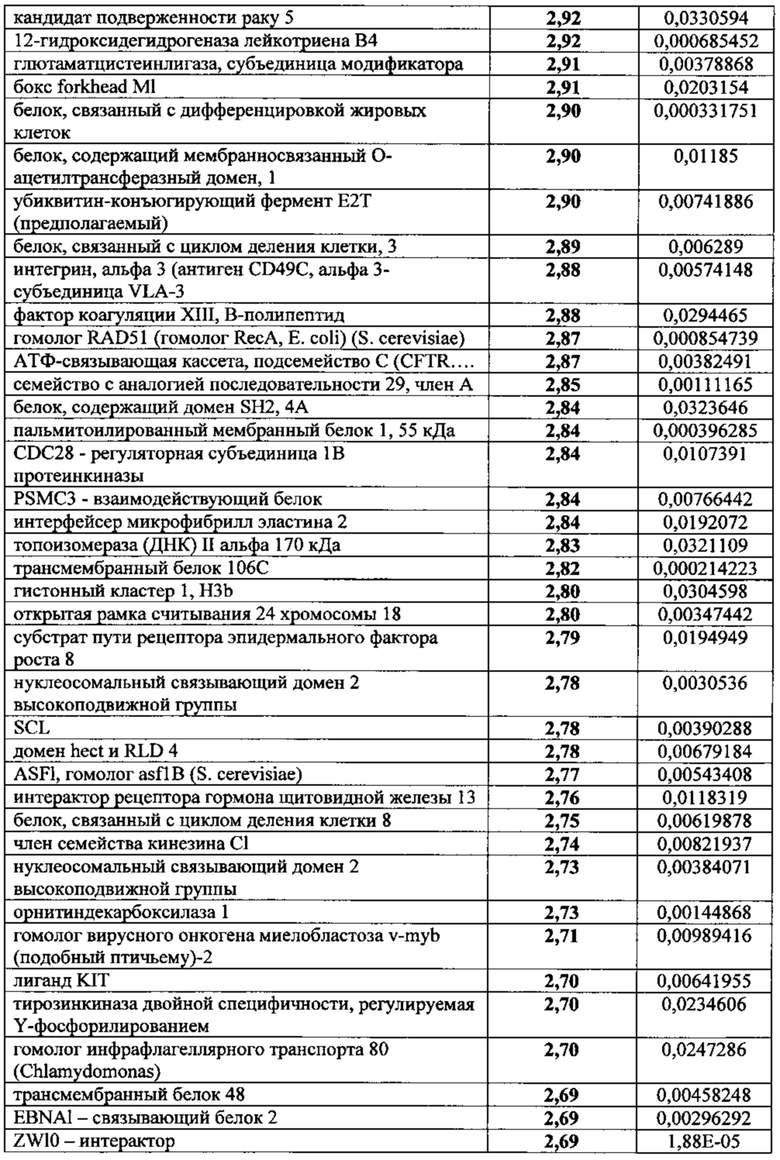
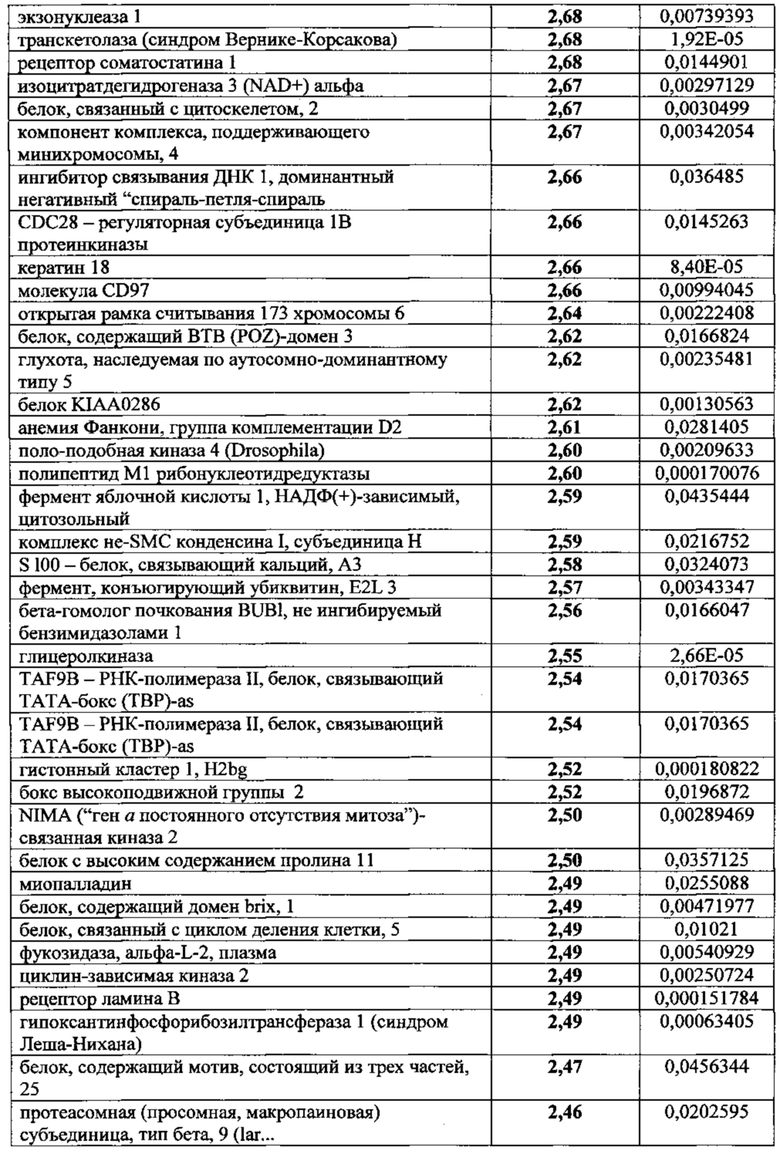
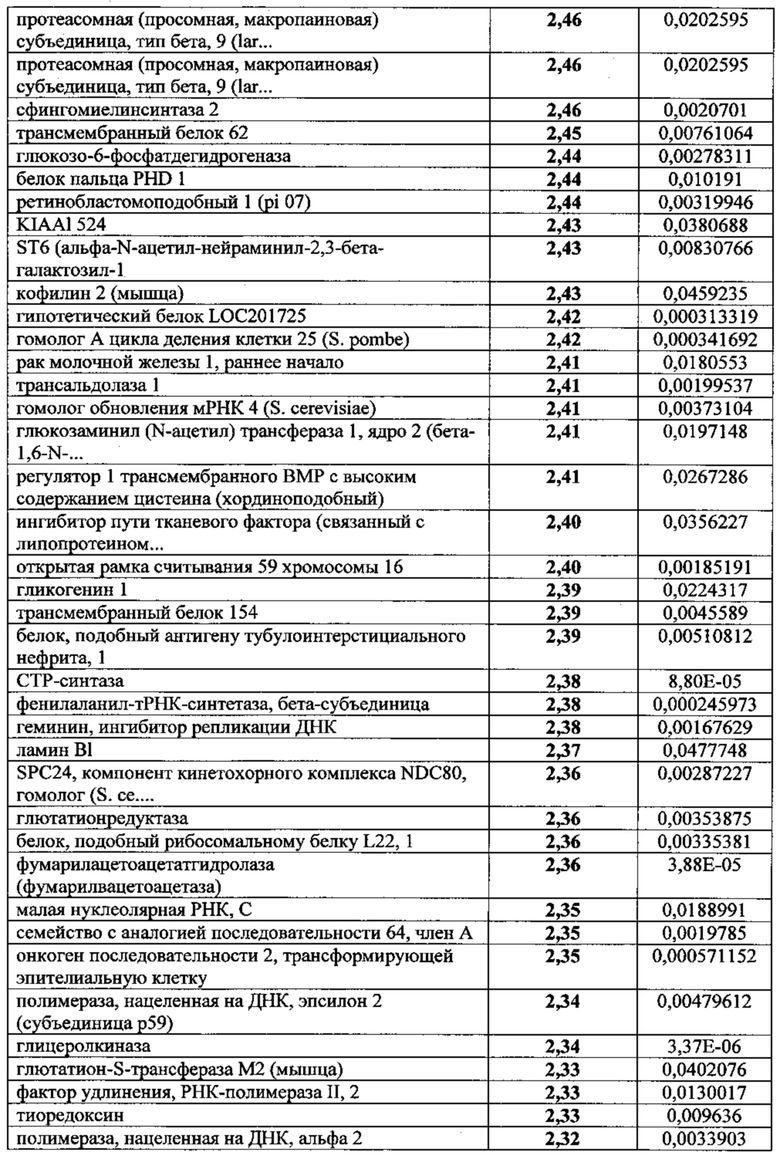
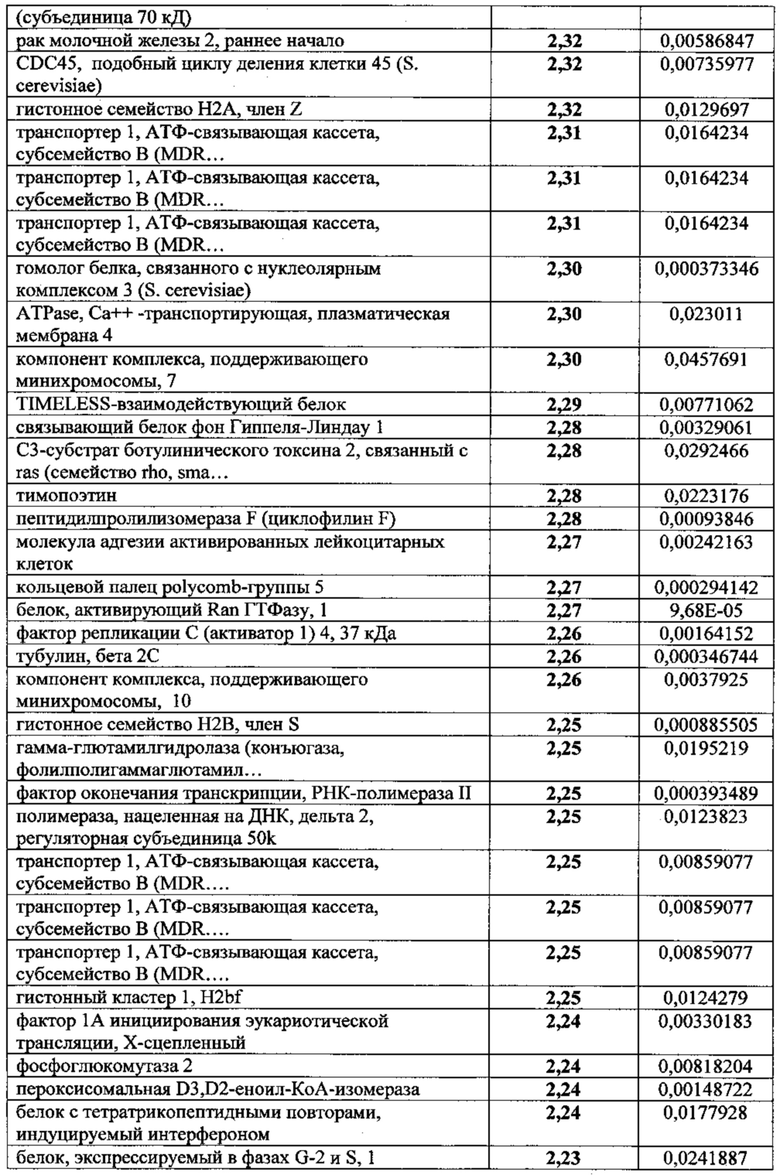
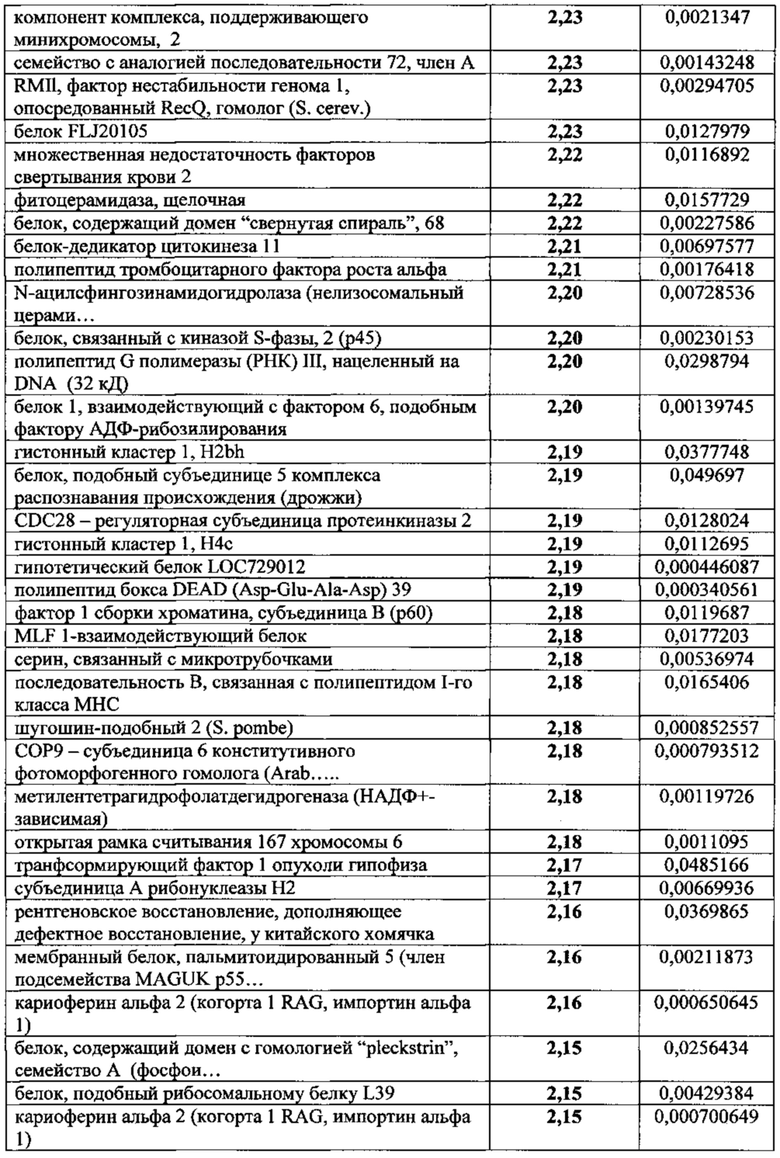
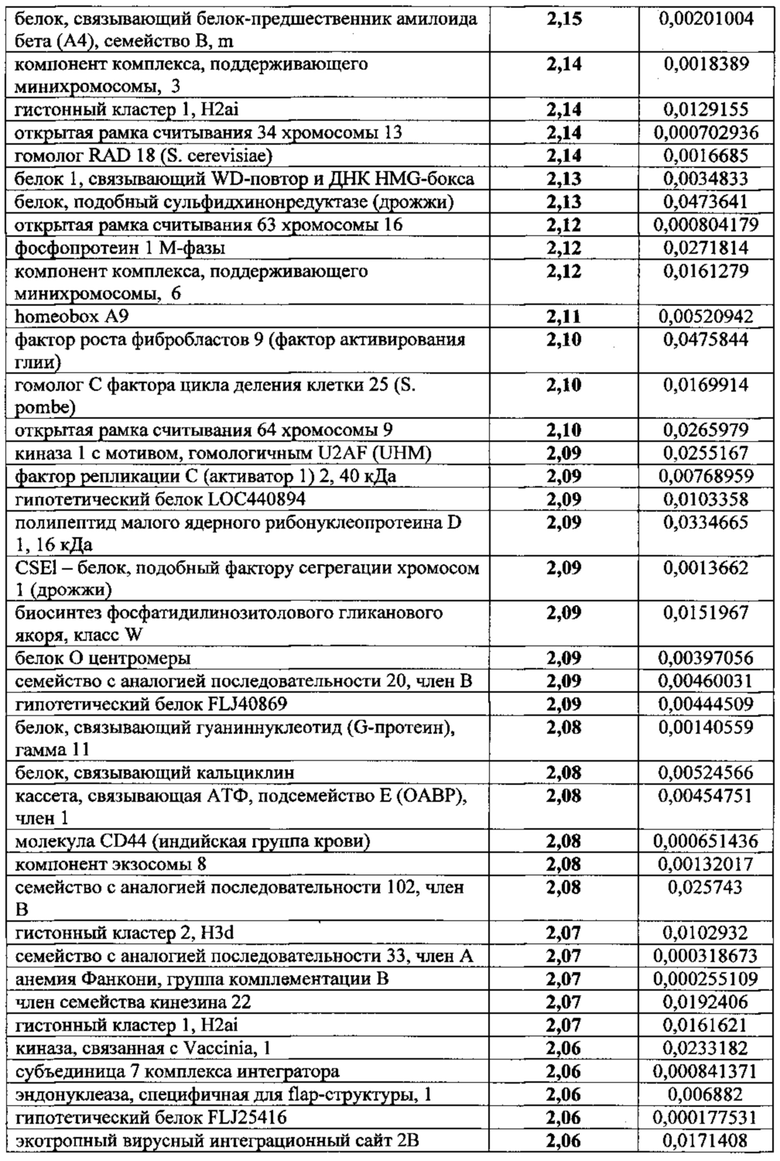
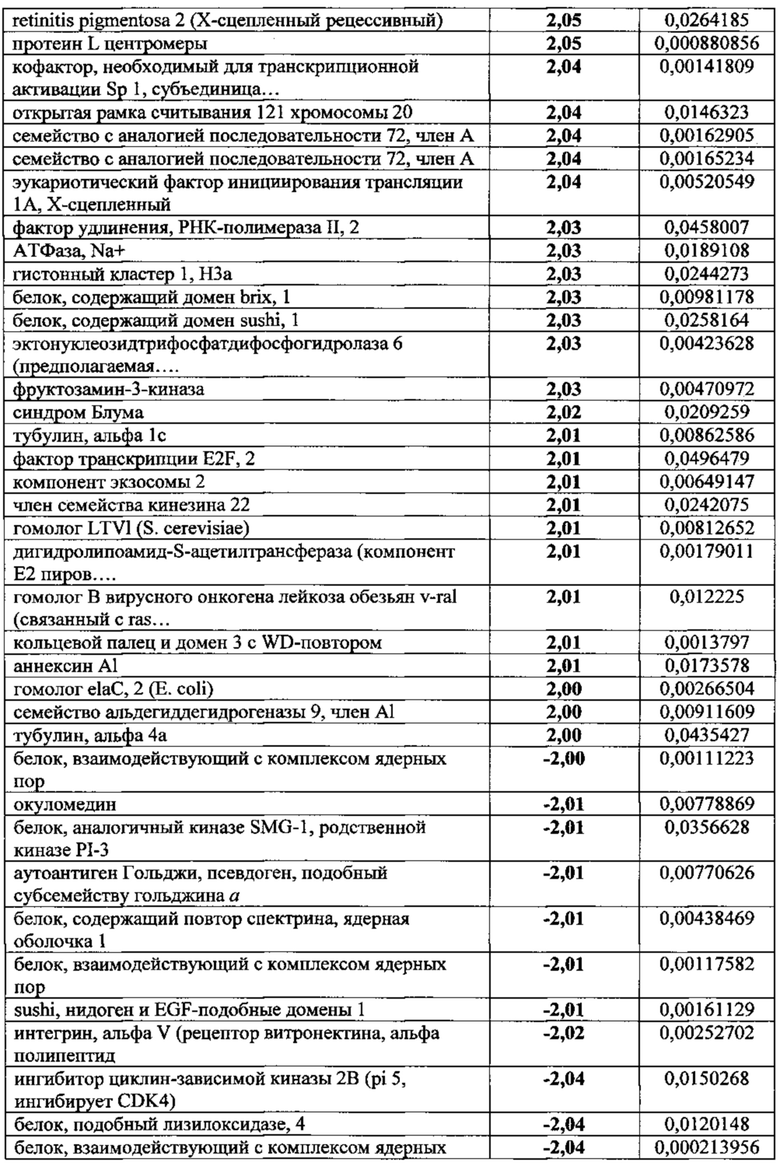
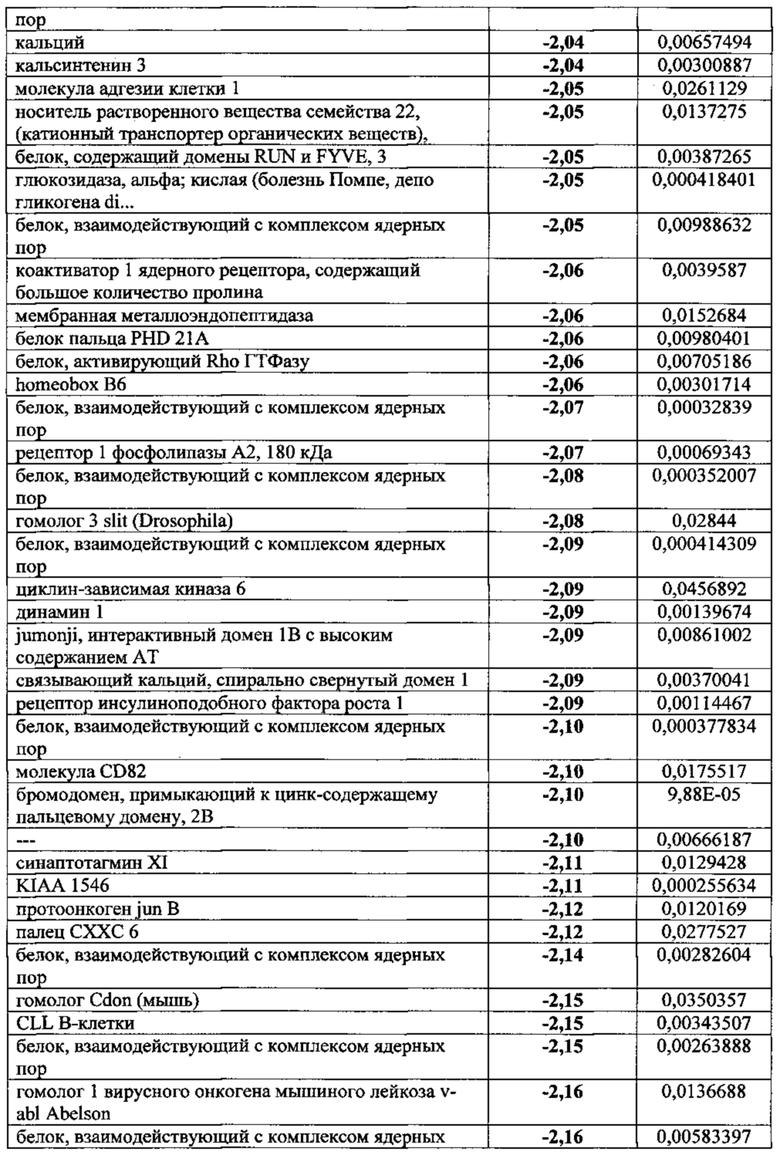
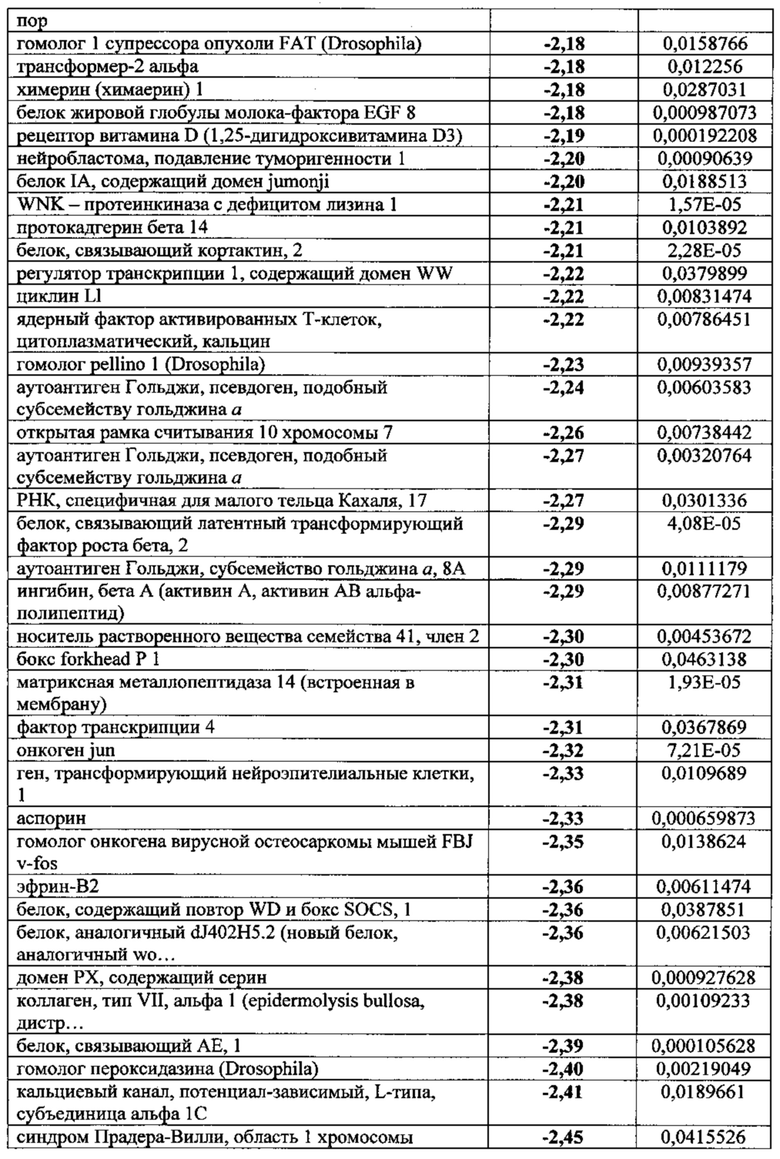
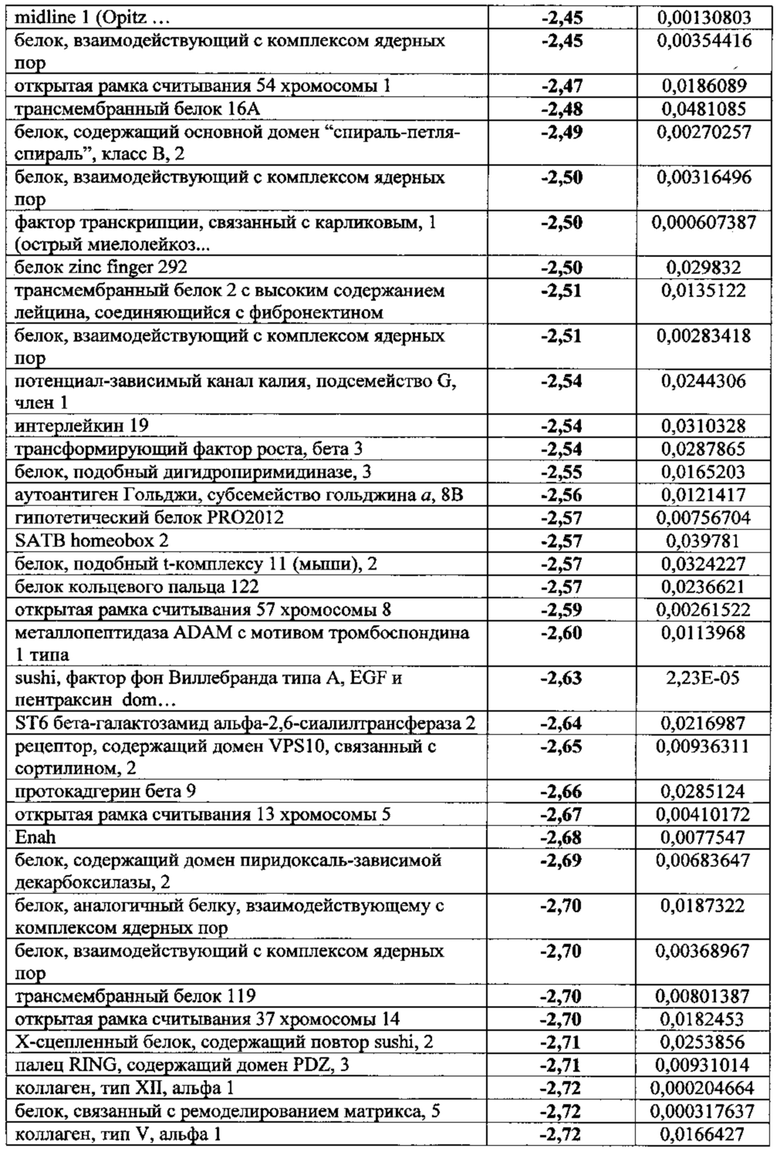
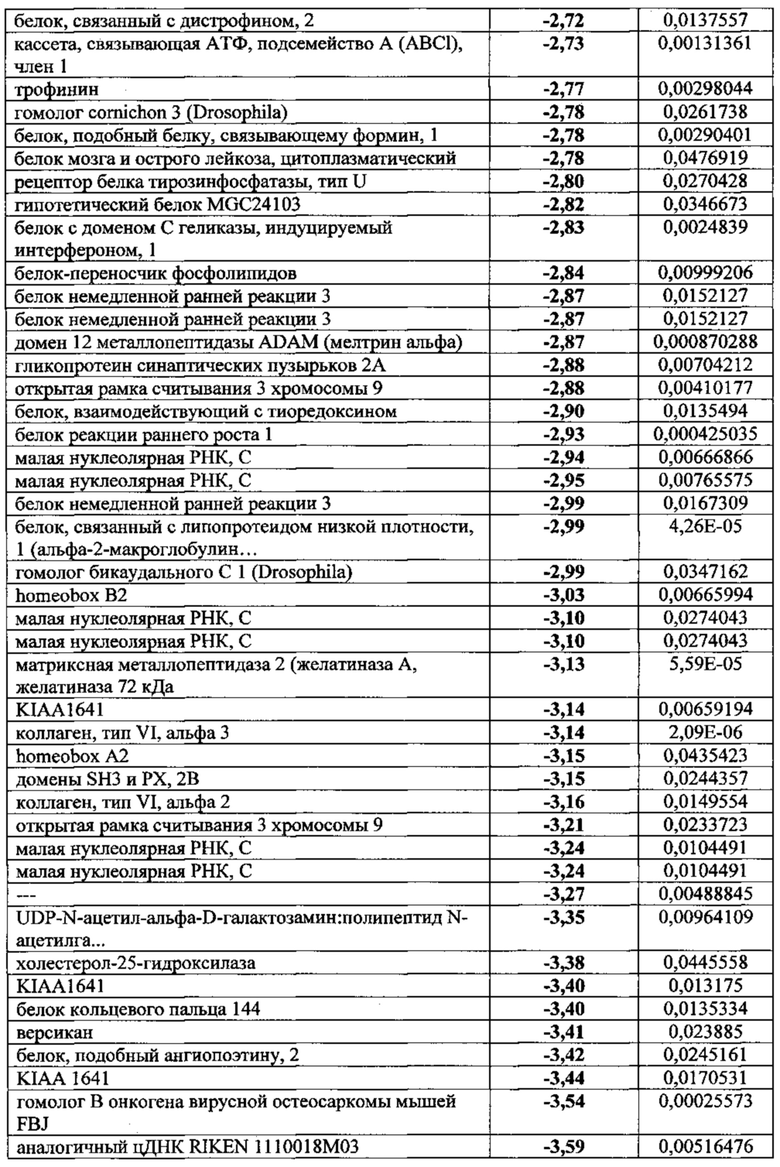

Экспрессия клеточных маркеров на клетках PLX-C - С помощью моноклональных антител были исследованы поверхностные антигены, экспрессируемые клетками PLX-C. Полученные результаты показали, что клетки PLX-C характеризуются наличием позитивных маркеров CD73, CD29 и CD105 и негативных маркеров CD34, CD45, CD 19, CD 14 и HLA-DR (данные не представлены). Были установлены следующие спецификации теста иммунного фенотипа:≥90% для всех позитивных маркеров и ≤3% для всех негативных маркеров.
Кроме того, как показано на Фиг. 10А-В, культуры клеток PLX-C не экспрессировали эндотелиальных маркеров, о чем свидетельствуют отрицательные результаты окрашивания двух эндотелиальных маркеров - CD31 и KDR. Вместе с тем, присутствовала явная экспрессия клетками PLX-C маркера, типичного для фибробластов (экспрессия D7-fib, Фиг. 10С).
Иммуногенность и иммуномодулирующие свойства клеток PLX-C - Поскольку клетки PLX-C являются адгезивными клетками, получаемыми из плаценты, они, предположительно, должны экспрессировать HLA I типа, экспрессируемый всеми клетками тела и известный своей способностью индуцировать аллореактивный иммунный ответ. HLA II типа и другие ко-стимулирующие молекулы экспрессируются, как правило, только на поверхности антигенпрезентирующих клеток (АПК; АРС).
С целью оценки иммуногенности получаемых клеток PLX-C, была исследована экспрессия ко-стимулирующих молекул на поверхности мембран этих клеток. ФАСК-анализ продемонстрировал отсутствие CD80, CD86 и CD40 на мембранах клеток PLX-C (Фиг. 1 IA-С). Кроме того, клетки PLX-C демонстрировали низкий уровень экспрессии HLA I класса при ее выявлении методом окрашивания на HLA А/В/С (Фиг. HD). Экспрессия стимулирующих и ко-стимулирующих молекул была такой же, как и у МСК, полученных из костного мозга (КМ; ВМ)(см. Фиг. 11A-D).
С целью дополнительного исследования иммуногенных и иммуномодулирующих свойств клеток PLX-C, были выполнены тесты реакции смешанных лимфоцитов (РСЛ). Как показано на Фиг. 12А-В, клетки PLX-C избегают аллораспознавания и уменьшают реакцию Т-клеток, оцениваемую по включению тимидина. Кроме того, уменьшение пролиферации лимфоцитов (оцениваемой по КИМ) становилось более выраженным по мере увеличения количества клеток PLX-C (имело дозозависимый характер). К тому же, клетки PLX-C уменьшали пролиферацию лимфоцитов в условиях митогенной стимуляции, обеспечиваемой, например, Конкавалином A (Con А, Фиг. 12В) и Фитогемагглютинином (ФГА; РНА), и неспецифической стимуляции антителами против CD3 и CD28 (данные не представлены).
С целью оценки механизма иммуномодулирующего воздействия клеток PLX-C на пролиферацию лимфоцитов, а также с целью выяснения вопроса о том, обеспечивается ли это воздействие межклеточным взаимодействием или секрецией цитокинов, осуществлялась стимуляция мононуклеарных клеток (МНК) периферической крови РНА с помощью метода разделения полупроницаемой мембраной (Transwell); этот метод предотвращает контакт между клетками, но обеспечивает диффузию цитокинов между двумя компартментами). Полученные результаты показали, что ингибирование пролиферации сохранялось даже в условиях предотвращения контакта между клетками (данные не представлены).
Секреция цитокинов - Как было описано выше, клетки PLX-C уменьшают скорость пролиферации лимфоцитов - вероятно, посредством растворимых факторов. С целью выяснения механизма действия клеток PLX-C, было проведено дополнительное исследование цитокинов, секретеруемых лимфоцитами в ответ на воздействие PLX-C. Как показано на Фиг. 13А-В, культивирование мононуклеарных клеток с клетками PLX-C немного уменьшает секрецию провоспалительного цитокина INFγ и резко уменьшает секрецию TNFα (даже в присутствии малых количеств клеток PLX-C). Кроме того, после стимуляции липополисахаридом (ЛПС; LPS), в присутствии клеток PLX-C отмечалось дозозависимое увеличение секреции IL-10 и уменьшение секреции TNFα мононуклеарными клетками периферической крови (Фиг. 13С).
ПРИМЕР 5
БИОРАСПРЕДЕЛЕНИЕ КЛЕТОК PLX-C
Материалы и методы экспериментов
Трансфицирование клеток PLX-C вектором экспрессии люциферазы
Клетки PLX-C были стабильно инфицированы лентивирусным конструктом, экспрессирующим ген люциферазы под контролем промотора CMV (Фиг. 14).
Производство инфицирующего вируса
Клетки-продуценты линии 293TN выращивали в питательной среде DMEM (Gibco) с добавлением сыворотки и антибиотиков в течение 2-3 дней (до достижения 50-70% слияния) перед трансфицированием. К 400 мкл DMEM, не содержавшей добавок, добавляли смесь, содержавшую 10 мкг упаковочной плазмиды, 2 мкг экспрессионного конструкта и 20 мкл Plus™ Reagent (Invitrogen). Эту смесь инкубировали в течение 15 минут при комнатной температуре (КТ; RT) и добавляли Липофектамин™ (30 мкл Липофектамина™ разбавляли в 400 мкл DMEM). Эту смесь инкубировали при КТ в течение 15 минут. Клетки линии 293TN промывали и переносили в 2%-ную сывороточную среду и добавляли трансфекционную смесь. Клетки инкубировали в инкубаторе в атмосфере СО2 при 37°С с вечера до утра, и через 24-60 часов после инфицирования осуществляли сбор среды. Максимальная продукция вируса достигалась через 48 часов. Питательную среду собирали и центрифугировали со скоростью 3000 об./мин при комнатной температуре в течение 5 минут, чтобы осадить клеточный детрит. После центрифугирования надосадочную жидкость профильтровывали через PVDF-фильтры Millex-HV с размером пор 0,45 мкм (Millipore, номер в каталоге - SLHVR25LS).
Инфицирование клеток PLX-C
Клетки PLX-C высевали на 24-луночный планшет из расчета 0,6-1×103 клеток на одну лунку, в полную среду, за 24 часа до инфицирования вирусами. Через 24 часа добавляли 0,5 мл вирусной суспензии (разбавленной в полной среде с полибреном в конечной концентрации 5-8 мкг/мл). Клетки инкубировали в течение 24 часов, после чего среду заменяли полной средой DMEM и инкубировали клетки при 37°С в атмосфере 5% СО2 с вечера до утра. На 4-й день достигалось слияние культуры, и ее делили на 3-5 частей; далее клетки выращивали в течение 48 часов в полной среде DMEM, после чего осуществляли анализ клеток в отношении экспрессии люциферазы.
Уровень эффективности инфицирования приближался к 100%. Оценка люминесценции живых клеток и живых мышей осуществлялась с помощью системы IVIS Lumina Imaging, включавшей в себя высокочувствительную CCD-камеру для регистрации люминесцентного сигнала люциферазы.
Через 2 недели после инфицирования 2×106 клеток вводили внутримышечно или внутривенно мышам линий SCID/Beige, NOD/SCID, SCID и Balb/C. Клетки, введенные животным, контролировали с помощью вышеописанной системы IVIS.
Результаты экспериментов
Как показали результаты экспериментов, после инфицирования клетки CXL продолжали делиться, а уровни экспрессии люциферазы в размножающихся клетках оставались стабильно высокими (Фиг. 15).
Был оценен характер биораспределения клеток PLX-C, введенных мышам линии Balb/C. Согласно полученным данным, клетки исчезали через 72 часа после внутримышечной инъекции (данные не представлены). Однако, в условиях in vitro клетки PLX-C сохраняли постоянно высокие уровни экспрессии люциферазы в течение более трех недель (данные не представлены).
Как показано на Фиг. 16A-D, клетки, введенные внутримышечно иммунодефицитным мышам линии SCID/Beige, оставались в месте инъекции в течение периода до 5 дней и в дальнейшем не обнаруживались. Клетки CXL, введенные внутривенно мышам линии SCID/Beige, мигрировали в легкие спустя 24 часа, а затем возвращались к месту инъекции (предположительно, к месту травмы). В дальнейшем клетки постепенно исчезали, и спустя 3-4 недели уже не обнаруживались.
ПРИМЕР 6
АДГЕЗИВНЫЕ КЛЕТКИ СПОСОБНЫ ОКАЗЫВАТЬ ЛЕЧЕБНОЕ ВОЗДЕЙСТВИЕ НА ИШЕМИЮ КОНЕЧНОСТИ IN VIVO
С целью оценки способности имплантированных плацентарных адгезивных клеток уменьшать выраженность ишемических поражений и улучшать клиническое состояние и двигательную функцию конечностей, была использована описанная ниже модель ишемии задней конечности.
Материалы и методы экспериментов
Модель ишемии задней конечности - Ишемия задней конечности была индуцирована у 20 самцов мыши линии Balb/c, не имевших иммунодефицита, в возрасте 8-10 недель, при весе тела, равном примерно 25 г±20%. С животными обращались в соответствии с требованиями Национального института здоровья (NIH) и Ассоциации по оценке и аккредитации ухода за лабораторными животными (AAALAC). Животных содержали в стандартных лабораторных условиях и использованием климат-контроля. Температура колебалась в пределах от 20 до 24°С, а относительная влажность (OB; RH) - от 30 до 70%. Поддерживали цикл, состоявший из 12 часов светлого времени и 12 часов темного времени.
Мышей рандомизировали в две группы по 10 животных с помощью программы рандомизации "Исследовательский рандомизатор", сгенерированной компьютером. Одна группа получала внутримышечную инъекцию 1×106 плацентарных адгезивных клеток (PLX-C), а другая группа служила контролем (получала инъекцию ФЗФ).
Хирургические процедуры - Проводили хирургический разрез кожи длиной 1-1,5 см в паховой области. Дважды перевязывали бедренную артерию шелковой нитью (размер 6-0) и пересекали ее дистальнее лигатуры. Рану ушивали шелковым швом (3-0) и дожидались выздоровления животного. Через 5 часов после оперативного пересечения одной бедренной артерии мышам в два места внутримышечно вводили 1×106 плацентарных адгезивных клеток (PLX-C) в общем объеме 50 мкл. В контрольной группе осуществлялось аналогичное введение ФЗФ (Gibco) (см. таблицу 6 ниже).
Таблица 6: Экспериментальное исследование применения клеток PLX-C в условиях моделирования ишемии задней конечности у мышей.

Последующее наблюдение животных - Осуществляли трехкратные измерения кровотока на обеих задних конечностях с помощью бесконтактной лазерной допплерографии непосредственно после операции, а также на 6, 9, 14 и 21-й день после операции; полученные данные выражали как отношение кровотока в ишемизированной конечности к кровотоку в нормальной конечности [Tokai. J. С соавт.].
Макроскопическая оценка тяжести ишемии - Ишемизированную конечность оценивали макроскопически в 1, 6, 9, 14 и 21 день и далее до конца исследования, используя шкалу степеней морфологических изменений зоны некроза; 0-я степень: отсутствие некроза, I-я степень: некроз, захватывающий только пальцы (утрата пальцев), II-я степень: некроз, распространяющийся на тыльную сторону стопы (утрата стопы), III-я степень: некроз, распространяющийся на голень (потеря коленного сустава), IV-я степень: некроз, распространяющийся на бедро (потеря всей задней конечности) [Tokai. J. с соавт.].
Оценка функции конечности и ишемических повреждений in vivo - Была осуществлена следующая последовательная полуколичественная оценка нарушений функции ишемизированной конечности: 3 балла = волочение конечности, 2 балла = волочение отсутствует, однако отсутствует и подошвенное сгибание, 1 балл = имеется подошвенное сгибание и 0 баллов = имеется сгибание пальцев стопы как реакции сопротивления при легком потягивании за хвост (Rutherford с соавт., 1997).
Молекулярный и биохимический анализ - Помимо клинической оценки, на 21-й день были взяты пробы для выполнения молекулярных и биохимических анализов; в настоящее время выполняются анализы этих проб с целью углубления представлений о молекулярных механизмах, лежащих в основе улучшения процессов заживления в группе введения плацентарных адгезивных клеток (PLX-C).
Результаты экспериментов
Имплантация плацентарных адгезивных клеток значительно увеличивала кровоток в бедре и стопе в условиях моделирования ишемии задней конечности - С целью проверки эффективности адгезивных клеток in vivo, мышам осуществляли перевязку артерии и последующие внутримышечные инъекции плацентарных адгезивных клеток; в определенных точках времени после инъекций с помощью бесконтактной лазерной допплерографии измеряли кровоток в бедрах и стопах (правых и левых). Как показано на Фиг. 17, инъекция клеток PLX-C заметно улучшала кровоток (К; BF) в пораженной конечности; об этом свидетельствовали результаты измерений кровотока, улучшение функционирования конечности, повышение плотности расположения капилляров, а также уменьшение окислительного стресса и поражения эндотелия. Положительное воздействие на кровоток отмечалось через 9 дней после инъекции и присутствовало на протяжении всего исследования. Оценка бедра в зоне имплантации в 0-й и на 21-й дни показала, что в группе введения клеток PLX-C кровоток увеличился с 24±2,3 до 80±4,7%, а в контрольной группе, которой вводили носитель - с 35±2 до 54±4,5%. Аналогичное, но менее выраженное, увеличение кровотока было выявлено и в дистальном отделе конечности мыши после введения клеток PLX-C. Так, в группе введения носителя кровоток увеличился с 12±0,6 до 46±4,9%, а в группе PLX-C - с 10±0,7 до 52±5,5% (соответственно с 0-го по 21-й день) (см. Фиг. 17).
Адгезивные клетки способны улучшать функцию конечности in vivo - С целью дополнительной оценки эффектов плацентарных адгезивных клеток in vivo, с помощью балльной системы, описанной выше в разделе "Материалы и методы экспериментов", было исследовано функционирование конечности мышей, подвергнутых данному экспериментальному воздействию. Как показано на Фиг. 18, мыши, которым были введены адгезивные клетки, демонстрировали значительное улучшение функционирования конечности (2,5±0,2 (контрольная группа) против 2,1±0,2 (группа PLX-C); обратите внимание на значительный эффект на 21-й день после лечения). Вместе с тем, степень улучшения функции конечности в период наблюдения продолжительностью 21 день была сопоставимой в обеих группах; эти результаты свидетельствуют о том, что в условиях данного эксперимента применение клеток PLX-C не оказывало выраженного воздействия на процесс восстановления функций конечности.
Макроскопическая оценка тяжести ишемии показала, что в контрольной группе, получавшей носитель, на 6-й день у двух животных присутствовал некроз, захватывавший только пальцы стопы. В группе введения PLX-C некроз, захватывавший только пальцы стопы, был выявлен лишь у одного животного и только через 14 дней.
Посмертные иммуногистохимические исследования конечностей, в которые были введены клетки PLX-C, продемонстрировали значительное увеличение количества новообразованных капилляров (сосудов), обеспечивающих кровоснабжение конечности; эти данные свидетельствуют о способности клеток PLX-C активизировать ангиогенез (Фиг. 19). Наконец, у мышей, получивших клетки PLX-C, было выявлено уменьшение окислительного стресса и воспаления эндотелия (косвенно свидетельствовавшее об улучшении функции эндотелия) (Фиг. 20А-В). По-видимому, данное улучшение было связано с повышением уровня снабжения тканей кислородом у мышей, получивших клетки PLX-C; аналогичного улучшения у контрольных мышей, которым вводили ФЗФ, выявлено не было.
В заключение следует отметить, что ни у одной из мышей, получившей клетки PLX-C, в сравнении с контрольными мышами, получившими ФЗФ, не было выявлено каких-либо неблагоприятных клинических признаков или симптомов, вызванных внутримышечным введением клеток. Таким образом, клетки PLX-C вызывают увеличение кровотока, которое, по-видимому, является следствием ангиогенеза; это подтверждается результатами гистологического исследования пораженной конечности. Кроме того, замедление развития некроза и разница количеств пораженных животных свидетельствуют о наличии клинической реакции.
Имплантация плацентарных адгезивных клеток
Другое исследование эффективности было проведено на мышах линии Balb/C и включало в себя оценку показателей безопасности (то есть, вскрытие животных и патогистологическое исследование определенных органов) (см. описание в разделе "Материалы и методы" выше). В этом исследовании были использованы 7 групп мышей; каждая группа состояла из 10 самцов мышей линии Balb/c с ишемией задней конечности (см. таблицу 7 ниже). В одной группе, состоявшей из 10 мышей, индукция ишемии отсутствовала (в этой группе оценивалась общая безопасность и переносимость клеток PLX-C у нормальных, здоровых животных). После индукции ишемии в пораженную конечность внутримышечно вводили контрольный буферный раствор или клетки PLX-C и наблюдали мышей в течение периода продолжительностью до 1 месяца после введения дозы. В одной группе мышей осуществляли две инъекции в пораженную конечность с интервалом, равным одной неделе (в 1-й день и на 8-й день). Контроль кровотока осуществляли с помощью лазерного доплеровского исследования, а тяжесть ишемии оценивали макроскопически и исходя из поведения животного, до 30-го дня после введения дозы. На 30-й день мышей умерщвляли и осуществляли забор тканей для гистологического анализа.

В этом исследовании были использованы клетки PLX-C разных партий в трех концентрациях. Полученные результаты показали, что дозы, равные 0,1×106 и 0,5×106 клеткам PLX-C, обладают слабым терапевтическим эффектом. Заметное улучшение кровотока появлялось к 29 дню (конец эксперимента) у животных, получивших дозу 1×106 клеток. Это улучшение кровотока было значительным (р<0,05) в группе 2М (партия G.C25) по сравнению с контролем (т.е., мышами, которым был введен носитель). Кроме того, вторая инъекция клеток той же партии значительно улучшила кровоток на 15-й день по сравнению с однократной инъекцией (55±24 против 31±12,9 и 27±12,5% соответственно). Макроскопическая оценка тяжести ишемии выявила тенденцию к улучшению в группах, получавших 1×106 клеток (1М и 2М), по сравнению с контрольной группой введения носителя (6М).
В целом, эти результаты продемонстрировали эффективность адгезивных клеток в отношении индуцирования васкуляризации (например, в отношении улучшения кровотока) и улучшения функций конечности в условиях моделирования ишемии задней конечности у мышей, и показали возможность использования этих клеток (например, плацентарных адгезивных клеток) с целью лечения ишемических заболеваний конечностей.
ПРИМЕР 7
ПРИМЕНЕНИЕ КЛЕТОК PLX-C С ЦЕЛЬЮ ЛЕЧЕНИЯ ИНСУЛЬТА
Целью этого исследования была оценка терапевтической эффективности системной (внутривенной) трансплантации адгезивных клеток PLX-C плаценты человека при лечении инсульта.
Материалы и методы экспериментов
Исследуемые животные, операции и трансплантация
Были использованы самцы крыс со спонтанной гипертензией, имевшие гипертензию, гиперхолестеринемию, сахарный диабет и микроангиопатию. Животных содержали в условиях постоянства температуры, влажности воздуха и цикла светлого и темного времени суток. Была осуществлена рандомизация животных в исследуемые группы (см. таблицу 8 ниже).

Животные получали однократную или двухкратную инъекцию дозы 1×106 клеток PLX-C разных партий. Все процедуры трансплантации осуществлялись внутривенно. В группе двухкратной инъекции трансплантация осуществлялась через 10 и 24 часа после возникновения ишемии мозга; в группе однократной инъекции трансплантация осуществлялась через 24 часа после инсульта. Все трансплантированные клетки были предварительно помечены флюоресцентным красителем РКН26.
Экспериментальную ишемию головного мозга индуцировали посредством постоянной окклюзии правой церебральной артерии. Следует отметить, что одно животное погибло после применения анестезии.
Магнитно-резонансное исследование (МРИ)
Было осуществлено МРИ развития поражения в 1, 8, 29 и 60 дни с использованием сканера 1,5Т (Philips). Измерение и расчет объема инфаркта и атрофии головного мозга осуществляли с помощью усреднения величин, полученных тремя "ослепленными" исследователями с использованием корональных Т2-последовательностей.
Поведенческие тесты
Функциональные изменения оценивали с помощью двух дополняющих поведенческих тестов. Тест "сужающаяся дорожка" - обычный тест, используемый с целью количественной оценки сенсо-моторной недостаточности. Создавали условия для пробега крысы по горизонтально установленному бруску, на конце которого находилась клетка крысы. Время пробега регистрировали пять раз и документировали его среднесуточную величину. Повисание на бруске засчитывали как 20 секунд, а падение - как 30 секунд. В течение первой недели измерения осуществляли ежедневно, а затем - каждый седьмой день до конца периода наблюдения.
Второй тест - модифицированная балльная оценка тяжести неврологических нарушений (mNSS) - включал в себя дополнительные пункты, охватывающие чувствительность, двигательные функции и рефлексы. Результатом оценки с помощью теста mNSS являлось определение баллов, варьировавших в пределах от 1 до 18, причем, баллы от 1 до 6 свидетельствовали о легком, от 7 до 12 - умеренном и от 13 до 18 - тяжелом поражении. Баллы mNSS определяли в 1, 4, 7, 14, 21, 28, 35, 42, 49 и 56 день после индуцирования ишемии головного мозга.
Гистология
По завершении периода эксперимента всех крыс умерщвляли и осуществляли транскардиальную перфузию 4% раствора формалина. Осуществляли криоконсервацию извлеченного головного мозга, после чего получали срезы головного мозга толщиной 30 мкм. С целью оценки реакции глии, проводили иммуногистохимическое исследование с использованием первичного антитела против глиального фибриллярного кислого белка (ГФКБ; GFAP). Осуществляли полуколичественную оценку плотности расположения клеток GFAP+ в зоне шириной 750 мкм, примыкающей к границе инфаркта. С целью оценки реакции астроглии исследовали 15 участков, разделенных интервалами, равными, в среднем, 0,6 мм.
Статистика
Все данные, касающиеся веса, результатов анализа МРИ и гистологических исследований были оценены в отношении наличия Гауссова распределения и проанализированы с целью выявления статистически значимых различий с помощью вариационного анализа и, соответственно, рангового вариационного анализа.
Данные, полученные с помощью теста "сужающаяся дорожка" и теста mNSS, были подвергнуты подробному статистическому анализу с внесением поправки на повторные измерения, выполняемые на испытываемых животных, а также на индивидувальную динамику их данных (стратифицированному анализу). С целью компенсирования межиндивидуальных различий в отношении степени повреждения головного мозга, была использована модель случайных отрезков. Таким образом, данные, полученные в тесте "сужающаяся дорожка", было необходимо перевести в категориальную систему; при этом, величины времени, равные менее 5 секунд, были отнесены к категории "0", от 5 до 10 секунд - к категории "1", от 10 до 15 секунд - к категории "2", от 15 до 20 секунд - к категории "3", повисание - к категории "4", и падение - к категории "5".
Результаты экспериментов
Вес
Периодическое взвешивание давало возможность адекватно оценить общее состояние здоровья животных. Во всех группах отмечалось первоначальное уменьшение веса тела в связи с анестезией и хирургическим вмешательством (данные не приведены). Затем отмечалась быстрая нормализация веса и сохранение стабильного веса до конца эксперимента (т.е., до 60-го дня) (данные не приведены). Экспериментальные группы демонстрировали сходную динамику веса тела.
Тест "сужающаяся дорожка"
Во всех экспериментальных группах в течение периода эксперимента отмечалось значительное понижение категории, выявляемой в тесте "сужающаяся дорожка" (данные не представлены). В экспериментальной группе №1 (клетки PLX-C, партия 1, однократное введение) отмечалось значительно более выраженное понижение категории, выявляемой в тесте "сужающаяся дорожка", чем в контрольной группе (-0,01247 против -0.02931 соответственно). Какие-либо свидетельства статистически значимых различий между экспериментальной группой №3 (клетки PLX-C, партия 2, однократное введение) и контрольной группой отсутствовали (данные не представлены).
Модифицированная балльная оценка тяжести неврологических нарушений (mNss)
Все экспериментальные группы демонстрировали значительное снижение баллов неврологических нарушений (данные не представлены). Результаты оценки mNSS в группе PLX-2 (двухкратное введение клеток PLX-C) имели достоверное превосходство над результатами оценки mNSS в контрольной группе. Результаты оценки mNSS в группе двухкратной трансплантации клеток партии 2 (группа №3) имели достоверное превосходство над результатами оценки mNSS в группе однократной инъекции клеток той же партии (данные не представлены).
Определение объема инфаркта
Магнитно-резонансное исследование - высокотехнологичный способ оценки степени повреждения головного мозга и потери ткани in vivo. Учитывая межиндивидуальную изменчивость, индивидуальную оценку динамики объема инфаркта выражали как процент от объема инфаркта, присутствовавшего в 1-й день у данного животного. Экспериментальные группы не имели значительных различий в отношении объема инфаркта, присутствовавшего в 1-й день. В целом, за период с 1-го по 8-й день объем инфаркта уменьшился примерно на 50%. Это уменьшение было связано, в основном, с обратным развитием первоначально возникшего отека головного мозга. Исследование динамики поражения in vivo с помощью МРИ показало, что группа №4 (клетки PLX-C, партия 2, двухкратное введение) имела значительно меньший показатель инфаркта на 60-й день (0,48±0,02 против 0,60±0,03, соответственно, результаты не представлены).
Совокупность данных, полученных с помощью обоих поведенческих тестов, показывает, что внутрисосудистое введение клеток PLX-C с целью лечения инсульта значительно улучшает процесс восстановления функций. Кроме того, наблюдалось существенное и достоверное превосходство двухкратного введения клеток PLX-C по сравнению с однократным введением аналогичных клеток.
У животных, дважды получавших клетки PLX-C, отмечалось очевидное взаимное соответствие данных о динамике улучшения состояния, получаемых с помощью поведенческих тестов и с помощью МРИ. Кроме того, в конце эксперимента наблюдалось значительное уменьшение объема инфаркта и атрофии головного мозга. Более того, оба функциональных теста продемонстрировали стабильно более активное функциональное восстановление после двухкратного введения дозы трансплантируемых клеток PLX-C, чем в контрольной группе, и неопределенные эффекты при однократном введении дозы этих клеток.
ПРИМЕР 8
ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, ПРИ КОТОРЫХ ТРЕБУЕТСЯ РЕГЕНЕРАЦИЯ И/ИЛИ ВОССТАНОВЛЕНИЕ СОЕДИНИТЕЛЬНОЙ ТКАНИ
Лечение заболеваний, при которых требуется регенерация и/или восстановление кости с помощью адгезивных клеток по настоящему изобретению
С целью оценки воздействия адгезивных клеток плаценты или жировой ткани по настоящему изобретению, получаемых с помощью трехмерного культивирования (например, клеток PLX-С), на заживление сегментных дефектов бедренных костей критических размеров было использовано моделирование данного процесса на животных (например, зрелых новозеландских белых кроликах). Животные были рандомизированы в три группы. Животным группы А в зону дефекта вводили 1-10×106 адгезивных клеток (клеток PLX-C). Животным группы В вводили ФЗФ. Животным группы С никакого лечения дефекта не осуществлялось. Непосредственно после операции и с недельными интервалами получали рентгеновские снимки. На этапе 12 недель животных умерщвляли и извлекали поврежденные бедренные кости; затем приготавливали недекальцинированные гистологические срезы дефектов и примыкающих участков кости. С целью оценки заживления дефектов и образования костной ткани в зоне дефекта и вокруг него, проводили механические, гистологические и гистоморфометрические исследования. Кроме того, с целью выявления мРНК коллагена I-го и II-го типов, проводили исследование методом полимеразной цепной реакции с обратной транскрипцией (RT-PCR).
Лечение заболеваний, при которых требуется регенерация и/или восстановление сухожилия с помощью адгезивных клеток по настоящему изобретению
С целью оценки воздействия адгезивных клеток по настоящему изобретению (например, клеток PLX-C) на заживление сухожилий было использовано моделирование данного процесса на животных (например, новозеландских белых кроликах, зрелых согласно данным исследования скелета). Сухожилие длинного сгибателя большого пальца перемещали в туннель пяточной кости диаметром 2,5 мм. Осуществляли лечение костного туннеля с использованием клеток PLX-C или без них. Животных рандомизировали в три группы. Животным группы А в зону дефекта или внутривенно вводили 1-10×106 клеток PLX-C. Животным группы В вводили ФЗФ. Животным группы С никакого лечения дефекта не осуществлялось. На этапах 2, 4 и 6 недель после операции осуществляли сбор трех образцов в каждой группе и оценивали морфологические характеристики заживления контактирующих поверхностей сухожилия и кости с помощью обычных гистологических методик, а также с использованием иммуногистохимического выявления коллагенов I, II и III типов.
Лечение заболеваний, при которых требуется регенерация и/или восстановление хряща с помощью адгезивных клеток по настоящему изобретению
С целью оценки воздействия адгезивных клеток по настоящему изобретению (например, клеток PLX-C) на заживление хряща было использовано моделирование данного процесса на животных (например, новозеландских белых кроликах, зрелых согласно данным исследования скелета). Создавали дефект, распространявшийся на всю толщу суставного хряща в области надколенниковой борозды на дистальном конце левой бедренной кости. Из фасции, покрывающей четырехглавую мышцу бедра, вырезали лоскут размером примерно 6 мм и пришивали его к периферическому краю искусственного дефекта с помощью кетгутовой нити размером 6-0. Животных рандомизировали в три группы. Животным группы А в зону дефекта или внутривенно вводили 1-10×106 клеток PLX-C. Животным группы В вводили ФЗФ. Животным группы С никакого лечения дефекта не осуществлялось. Животных умерщвляли. Через 14 недель после имплантации клеток PLX-C в область костно-хрящевого дефекта резецировали дистальные отделы бедренных костей и проводили гистологическое исследование; образцы классифицировали на основании результатов полуколичественной оценки, учитывающей преобладающий характер тканевого регенерата, окрашивание матрикса, ровность поверхности, целостность структуры, толщину восстановления, сопоставление восстановленного хряща и окружающего нормального хряща, отсутствие признаков дегенеративных изменений восстановленной ткани и отсутствие дегенеративных изменений окружающего нормального хряща.
Лечение заболеваний, при которых требуется регенерация и/или восстановление связки с помощью адгезивных клеток по настоящему изобретению
С целью оценки воздействия адгезивных клеток по настоящему изобретению (например, клеток PLX-C) на заживление связки было использовано моделирование данного процесса на животных (например, новозеландских белых кроликах, зрелых согласно данным исследования скелета). Создавали уникортикальные циркулярные дефекты диаметром 8 мм. Животных рандомизировали в три группы. Животным группы А в зону дефекта или внутривенно вводили 1-10×106 клеток PLX-C. Животным группы В вводили ФЗФ. Животным группы С никакого лечения дефекта не осуществлялось. Через 14 недель после имплантации клеток PLX-C в область дефекта связки животных умерщвляли. Проводили гистологическое исследование и образцы классифицировали на основании результатов полуколичественной оценки, учитывающей преобладающий характер тканевого регенерата.
Следует подчеркнуть, что определенные признаки данного изобретения, описанные, в целях облегчения понимания, в контексте отдельных вариантов осуществления, могут быть также представлены в сочетании друг с другом в одном варианте осуществления. Наоборот, различные признаки данного изобретения, описанные, в целях обеспечения краткости изложения, в контексте одного варианта осуществления, могут быть также представлены в отдельности или в любом подходящем сочетании меньшего количества этих признаков. Хотя данное изобретение описано в связи с конкретными вариантами его осуществления, ясно, что многие альтернативы, модификации и варианты станут очевидными для специалистов в данной отрасли знаний. Соответственно, целью данного изобретения является охват всех таких альтернатив, модификаций и вариантов, соответствующих сущности и широкому объему прилагаемой формулы изобретения. Все публикации, патенты и заявки на изобретение, а также каталожные номера GenBank, упомянутые в этой спецификации, включены в данный документ во всей их полноте посредством ссылки - точно так же, как было бы в том случае, если бы каждая отдельная публикация, патент или заявка на изобретение или каталожный номер GenBank были бы конкретно и индивидуально включены в данный документ посредством ссылки на них. Кроме того, цитирование или указание в этой заявке какой-либо ссылки не должно рассматриваться как признание доступности информации, на которую дана эта ссылка, в виду ее принадлежности к известному уровню техники.
СПИСОК ЛИТЕРАТУРЫ
(Дополнительные ссылки приведены в тексте)
Bauer, Thomas W., Muschler, George F., Bone Graft Materials: An Overview of the Basic Science. Clinical Orthopaedics & Related Research. 371:10-27, February 2000.
Carstanjen B, Desbois C, Hekmati M, and Behr L. Successful engraftment of cultured autologous mesenchymal stem cells in a surgically repaired soft palate defect in an adult horse. Can J Vet Res. 2006 April; 70(2): 143-147.
Brader SP, et al. 1998 The effect of implants loaded with autologous mesenchymal stem cells on the healing of canine segmental bone defects. J Bone Joint Surg Am. 80(7):985-96.
Chao Wan, Qiling He, Gang Li, 2006. Allogenic peripheral blood derived mesenchymal stem cells (MSCs) enhance bone regeneration in rabbit ulna critical-sized bone defect model. Journal of Orthopaedic Research 24 (4) 610-618.
Herthel D.J. 2001, Enhanced Suspensory Ligament Healing in 100 Horses by Stem Cells and Other Bone Marrow Components. AAEP PROCEEDINGS / Vol. 47.
Gordon с соавт., Tendon Regeneration Using Mesenchymal Stem cells, p 313-320 in Tendo Injuries. Springer London. 2005.
Horwitz с соавт., 1999. Transplantability and therapeutic effects of bone marrow derived mesenchymal cells in children with osteogenesis imperfecta. Nat. Med. 5:309-313.
Horwitz с соавт., 2002. Isolated allogeneic bone marrow-derived mesenchymal cells engraft and stimulate growth in children with osteogenesis imperfecta: Implications for cell therapy of bone. PNAS 99(13)8932-8937.
Livingston, T.L. 2003 Mesenchymal stem cells combined with biphasic calcium phosphate ceramics promote bone regeneration. Journal of Materials Science: Volume 14 (3):211-218.
Young et al. 1998. Use of mesenchymal stem cells in a collagen matrix for Achilles tendon repair. J Orthop Res. 16(4):406-13.

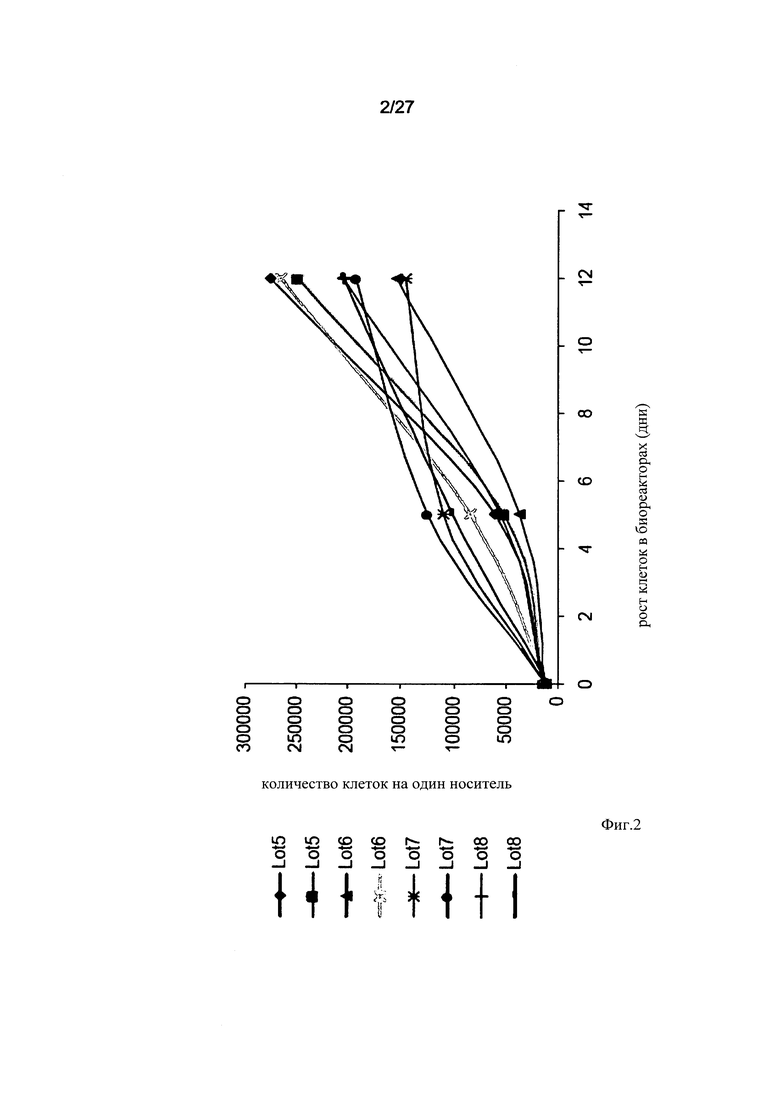
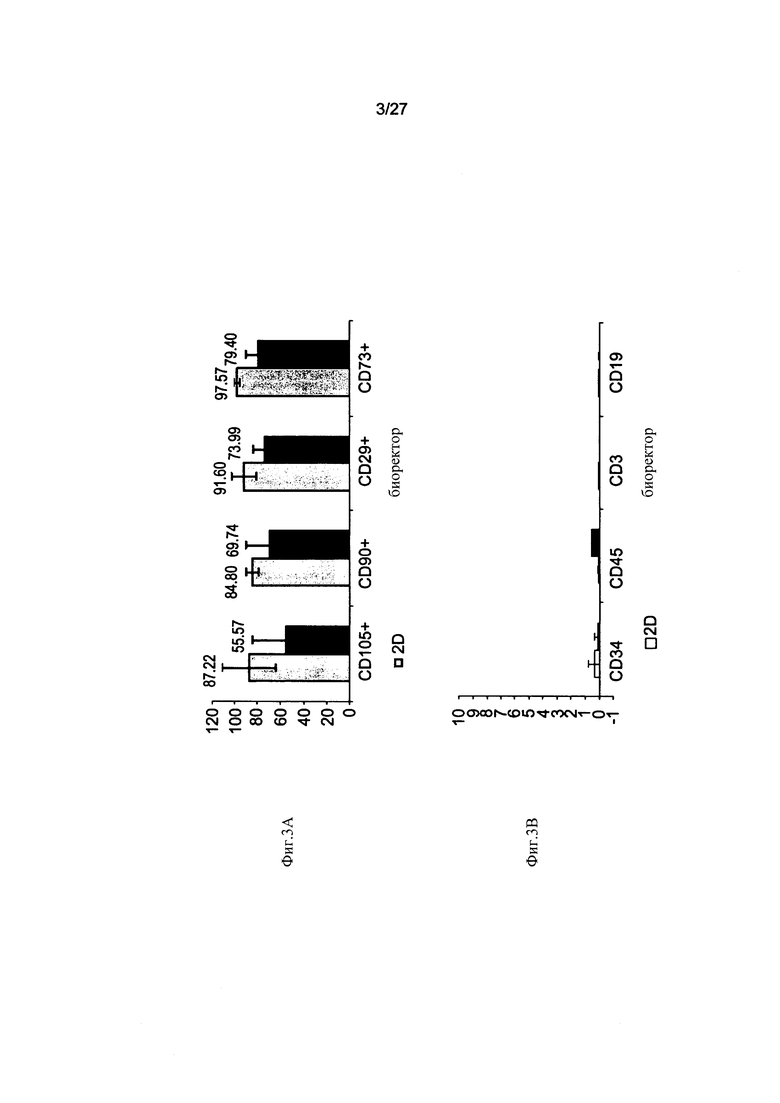
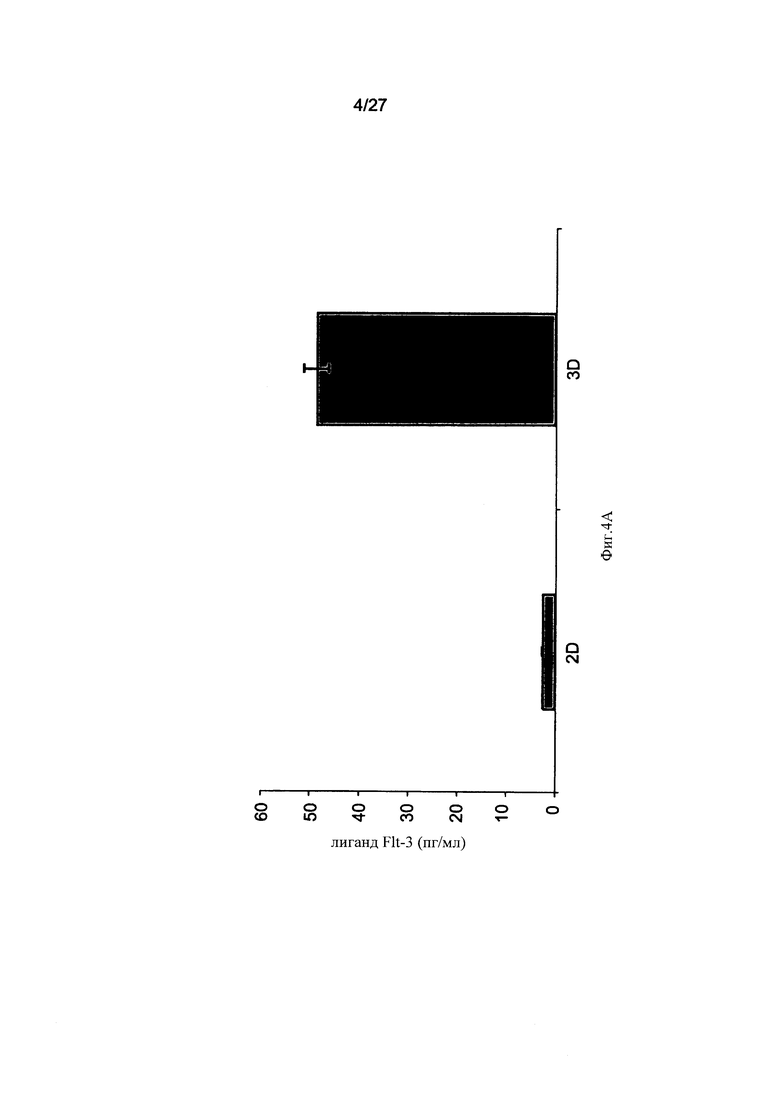
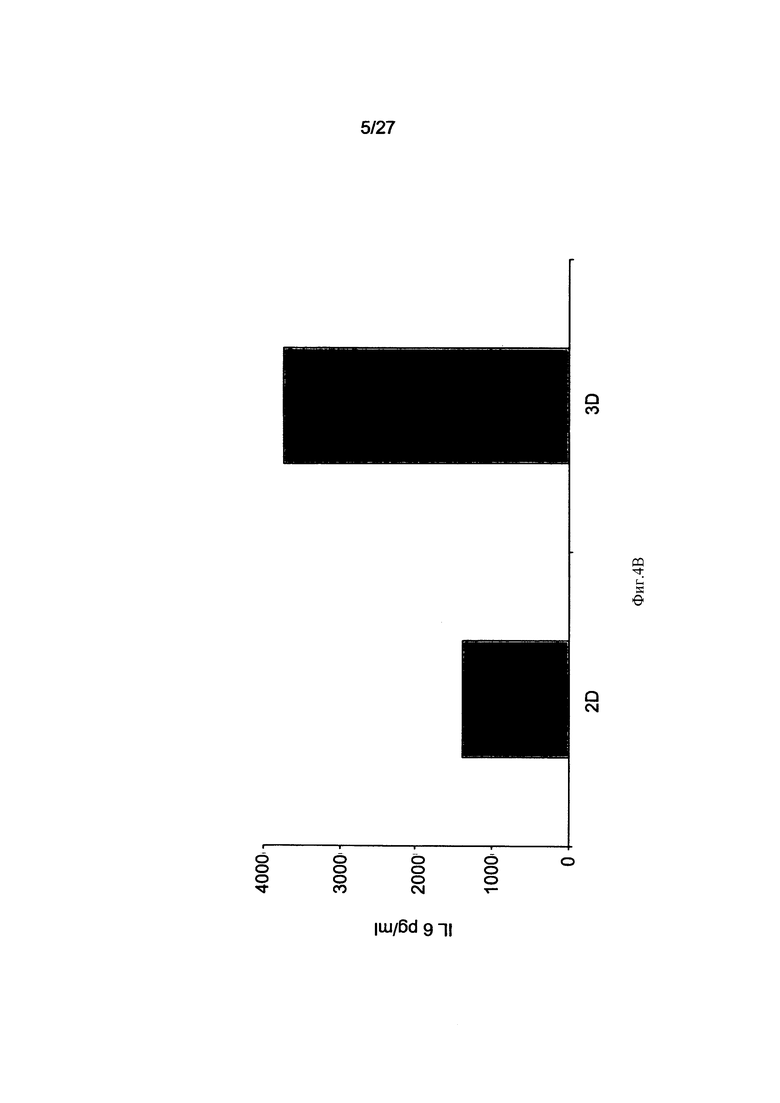
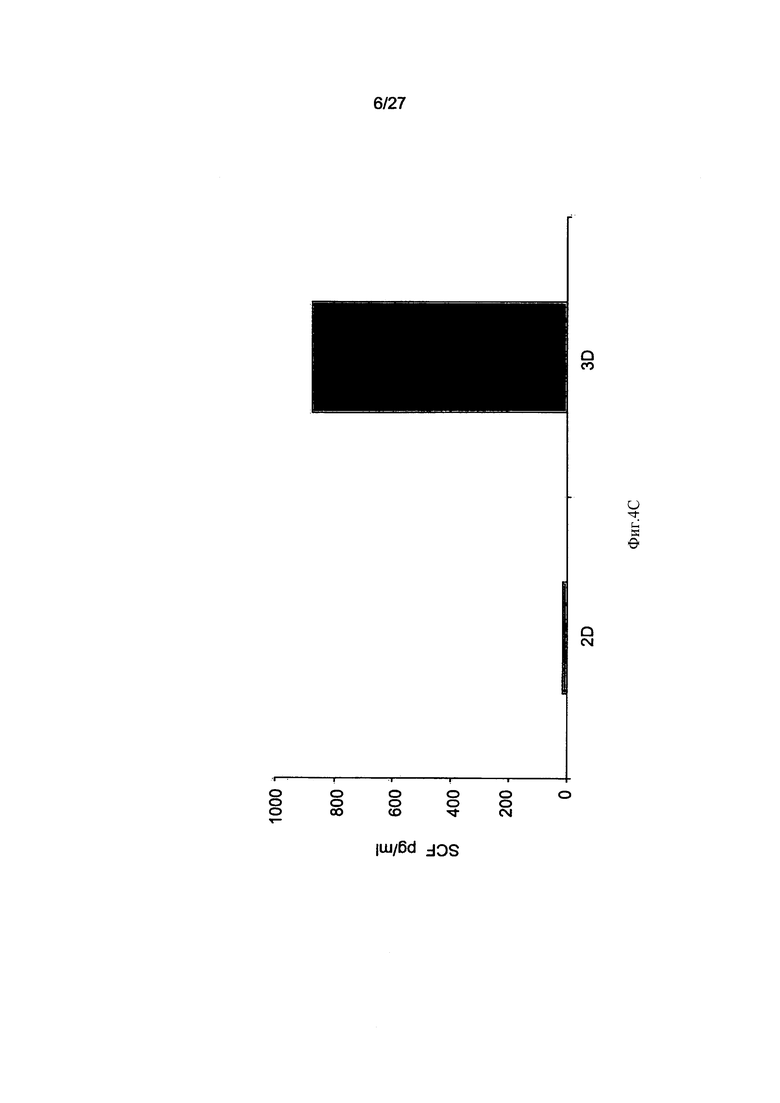
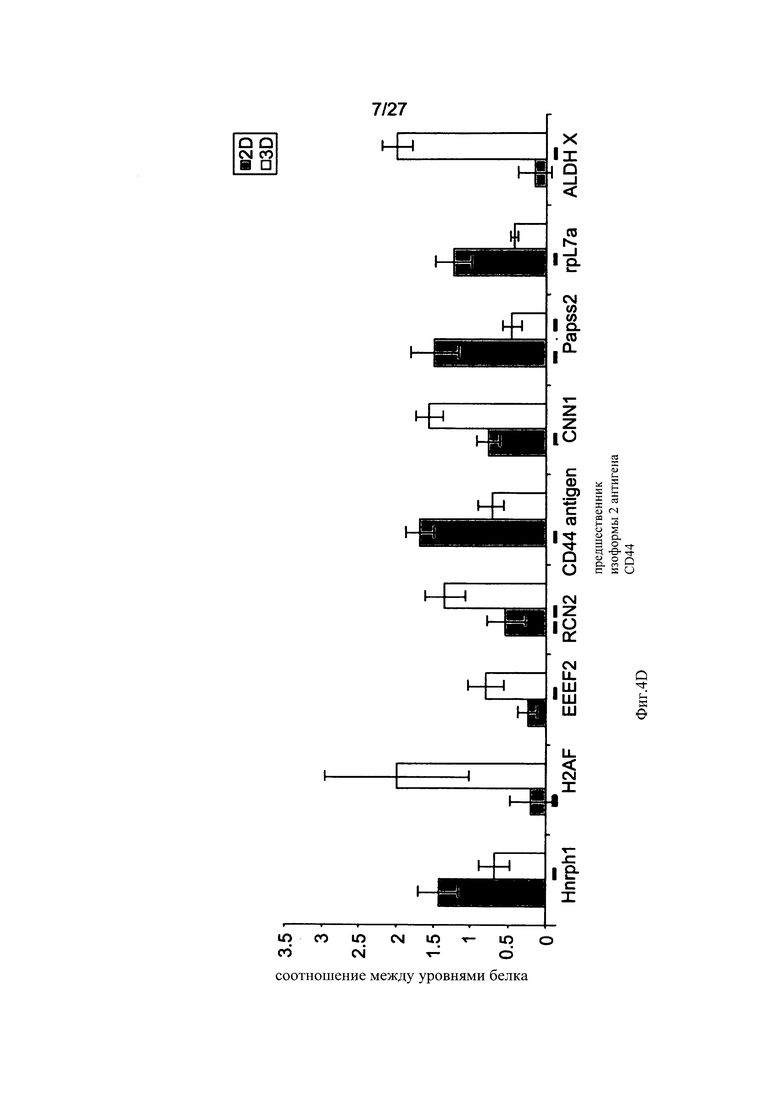

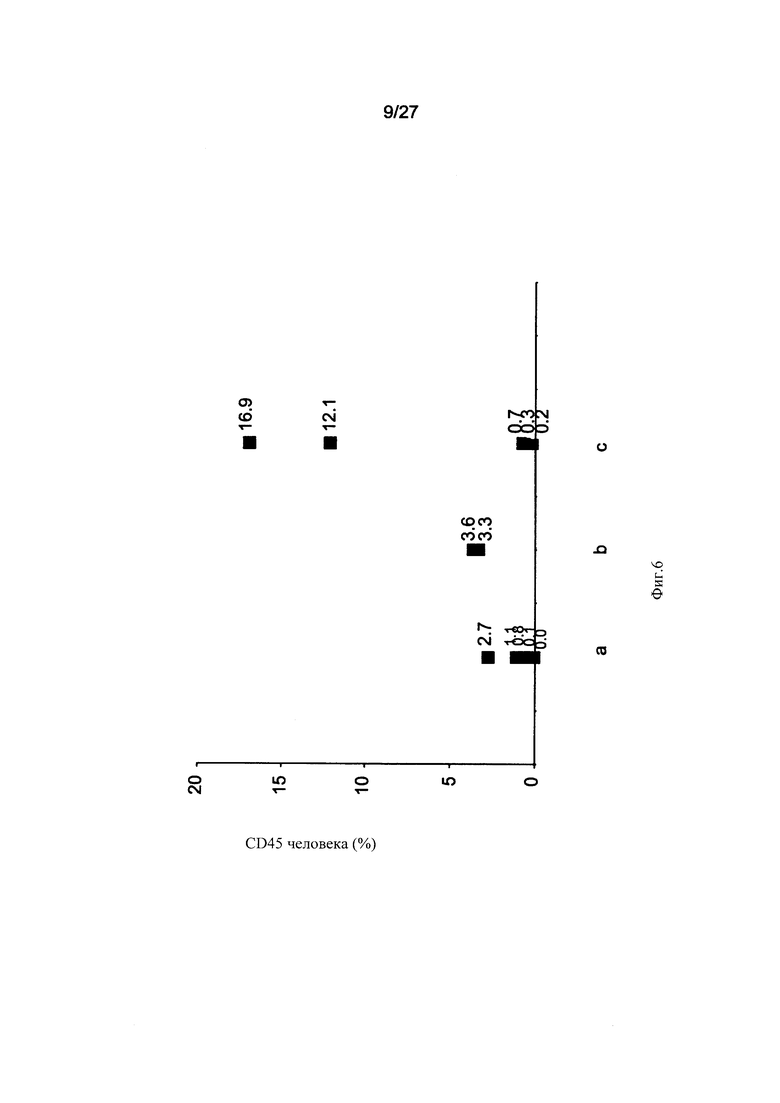
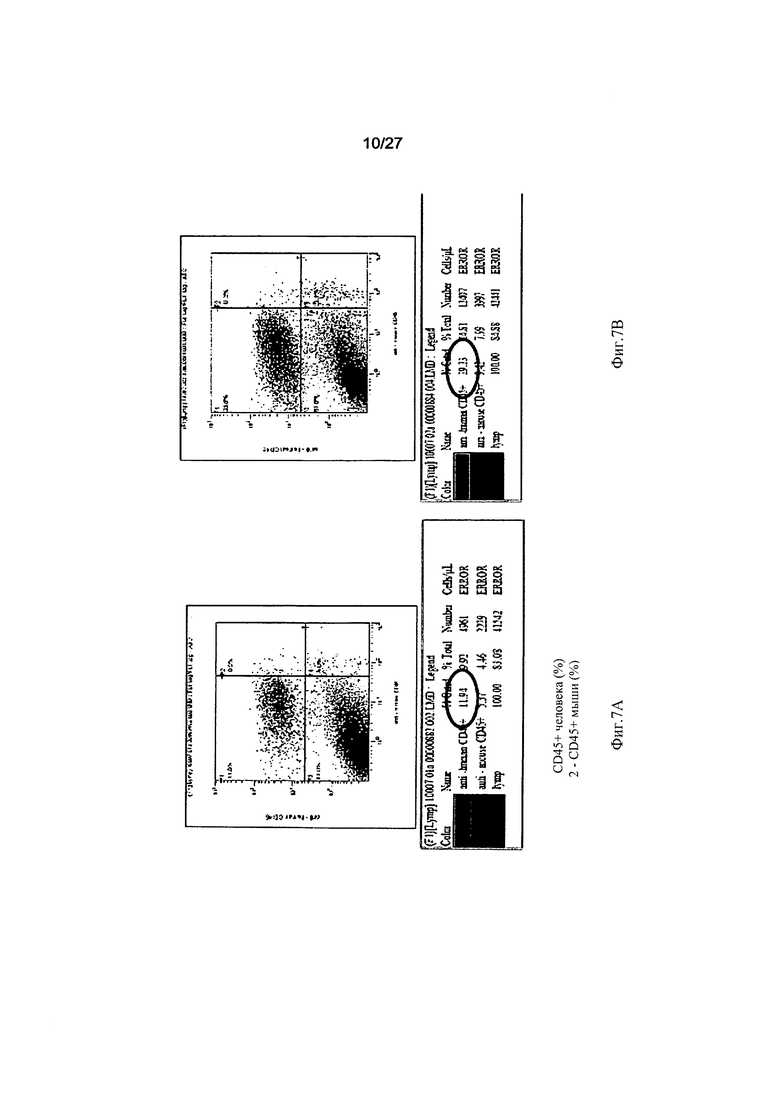

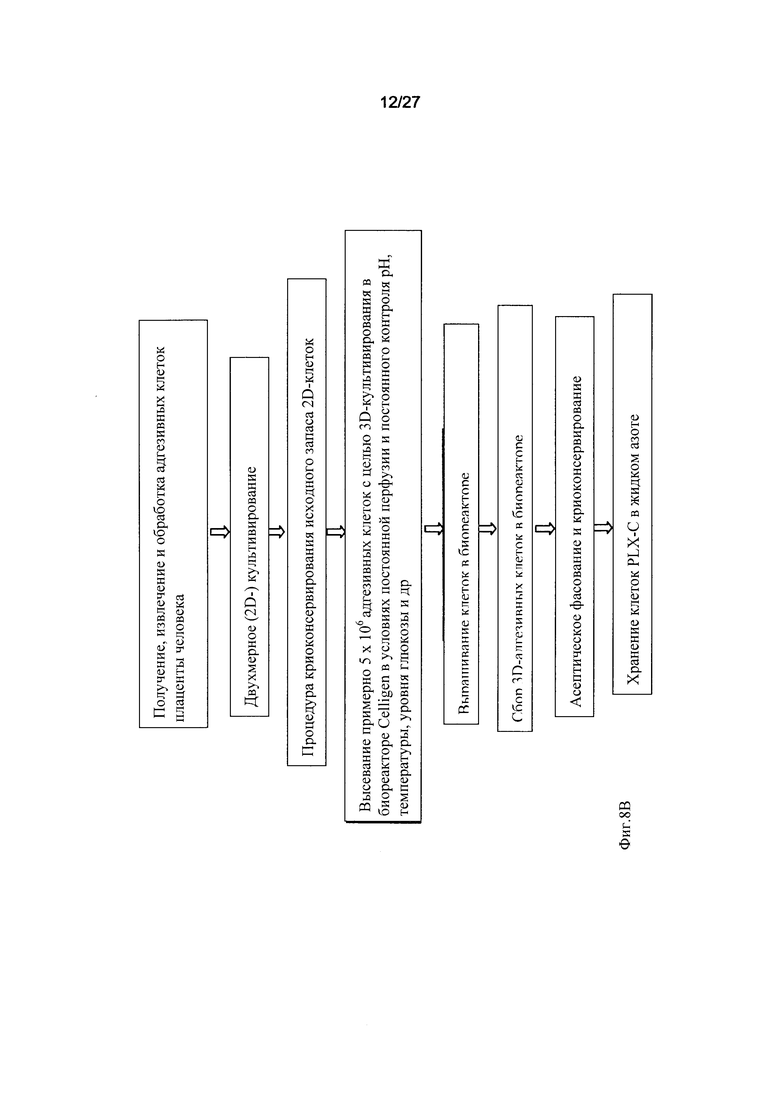
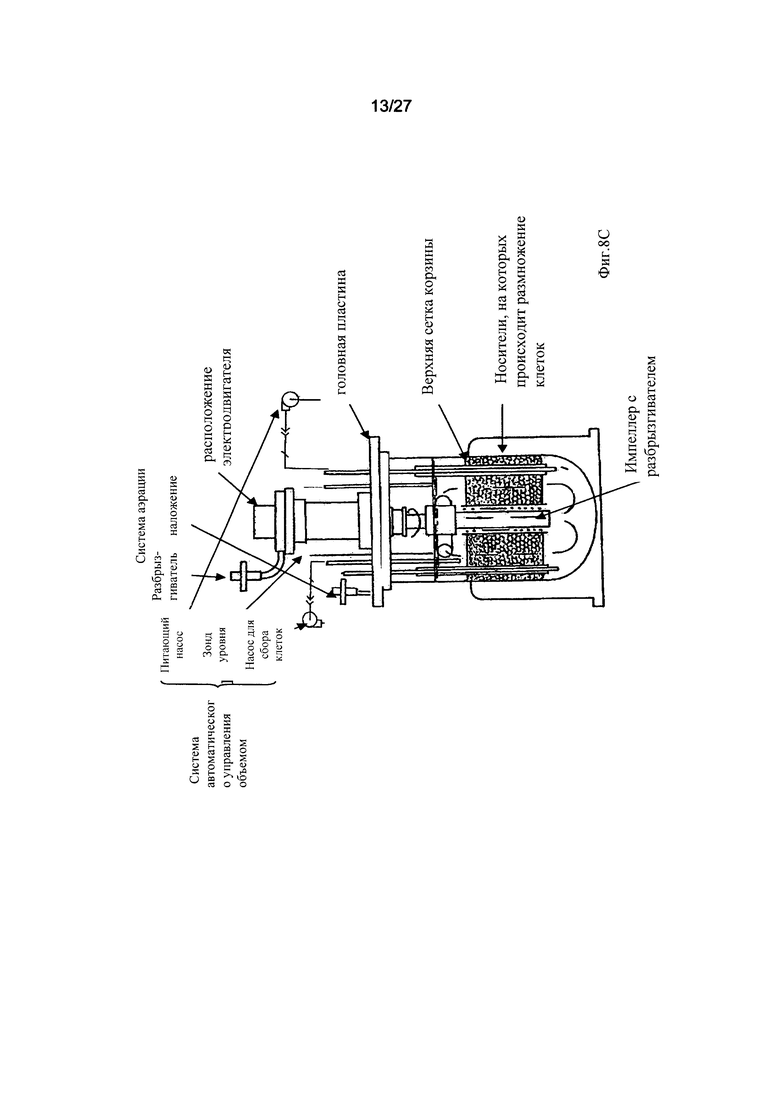
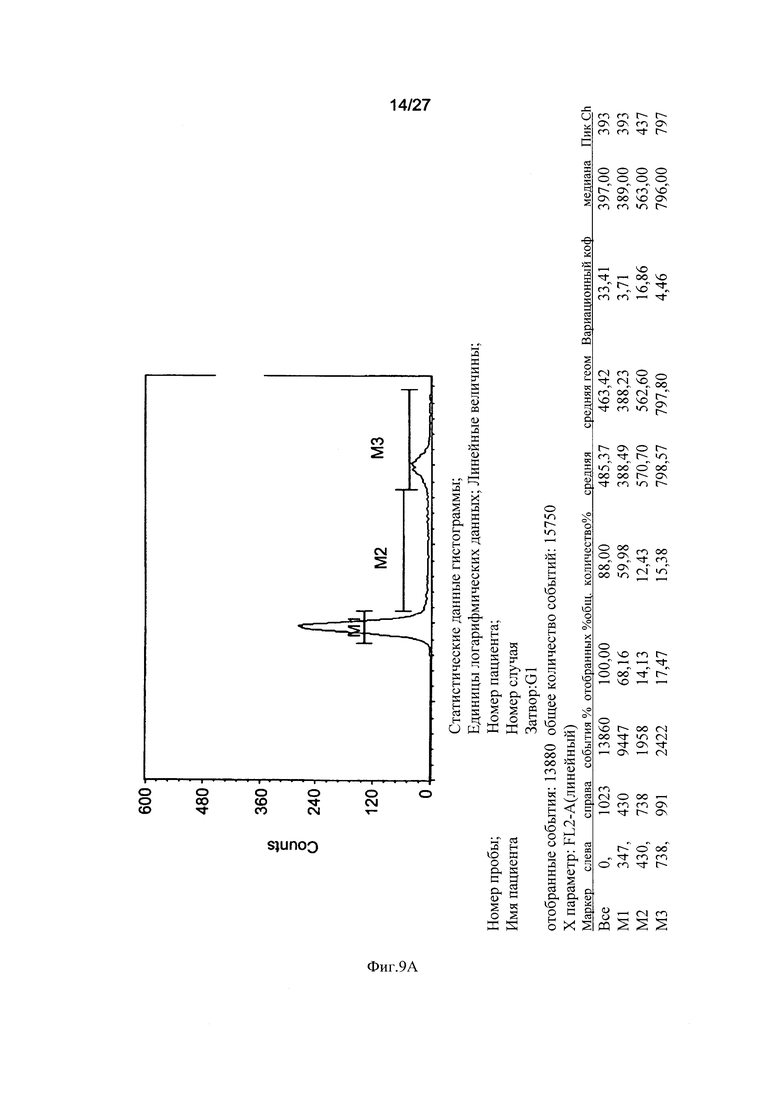
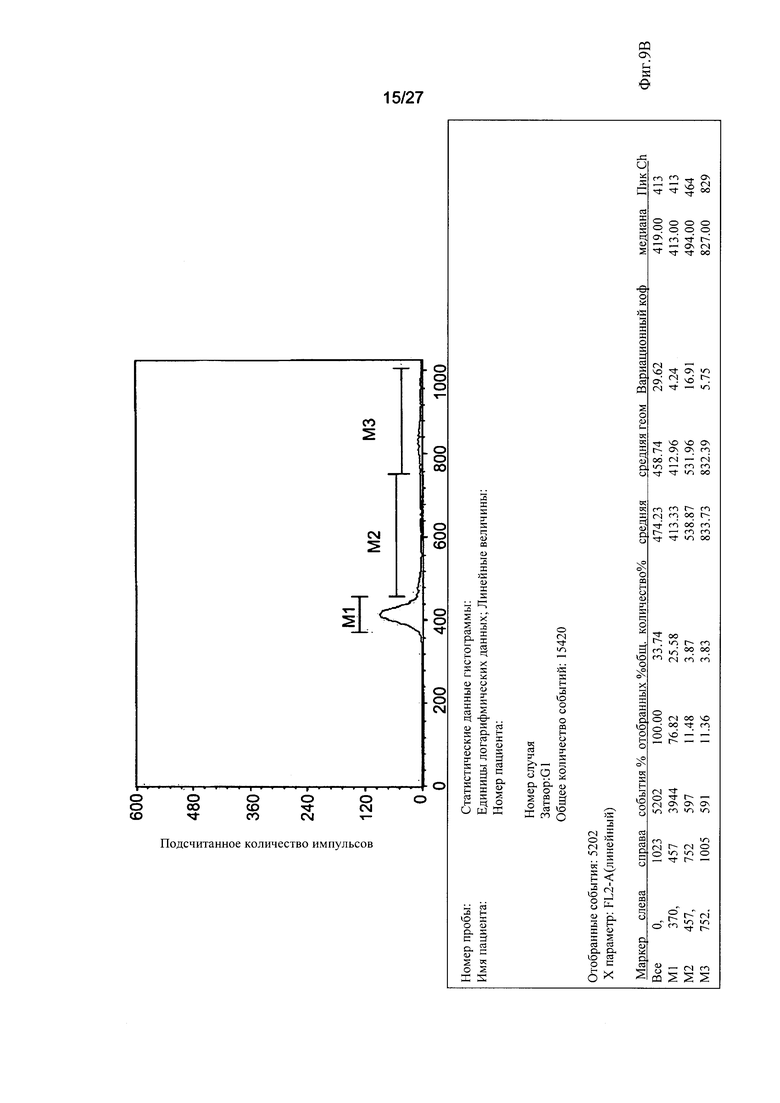
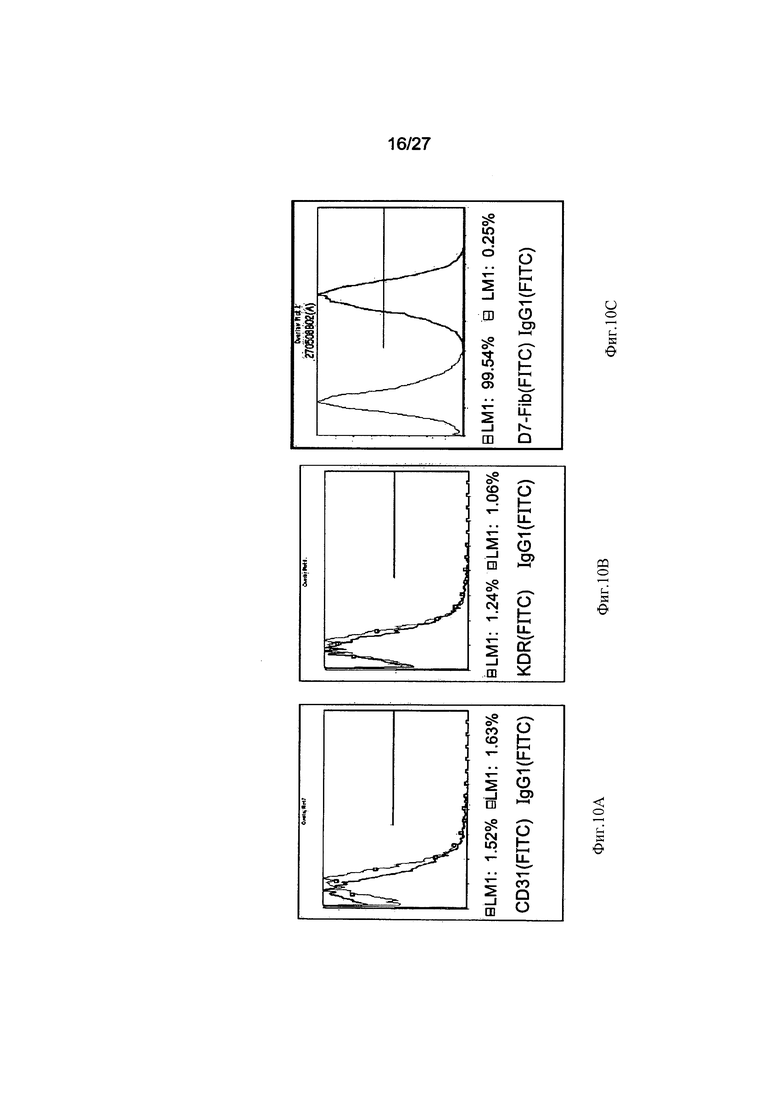
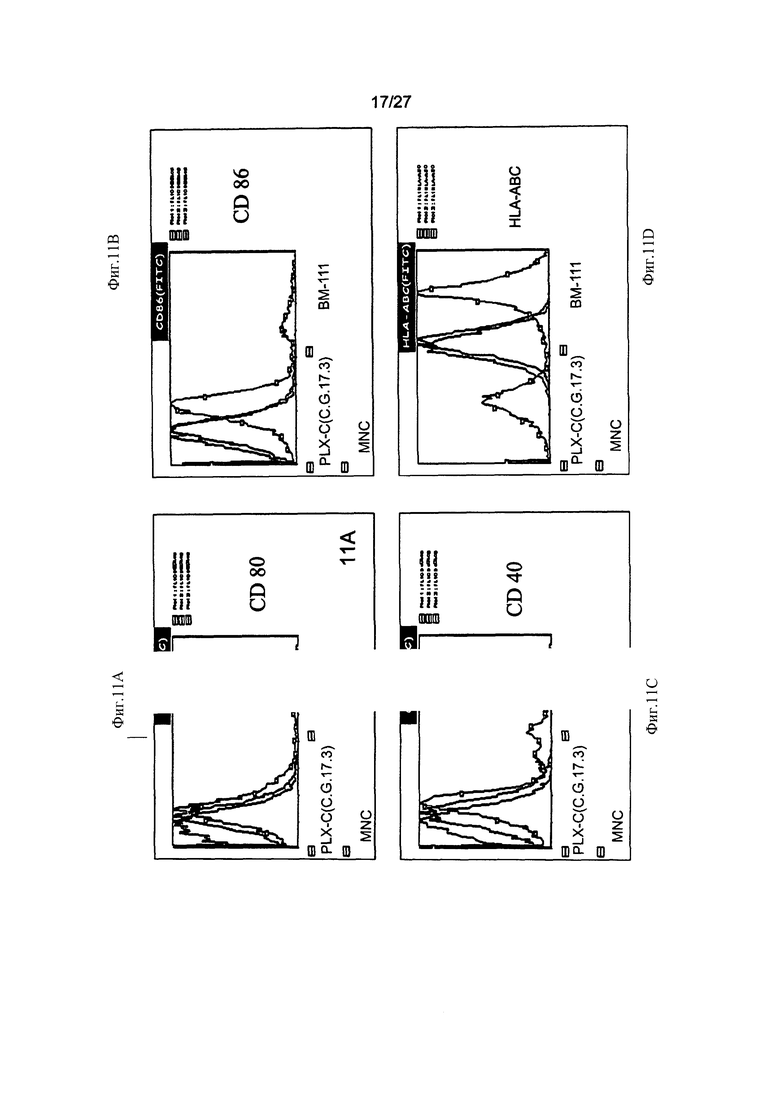
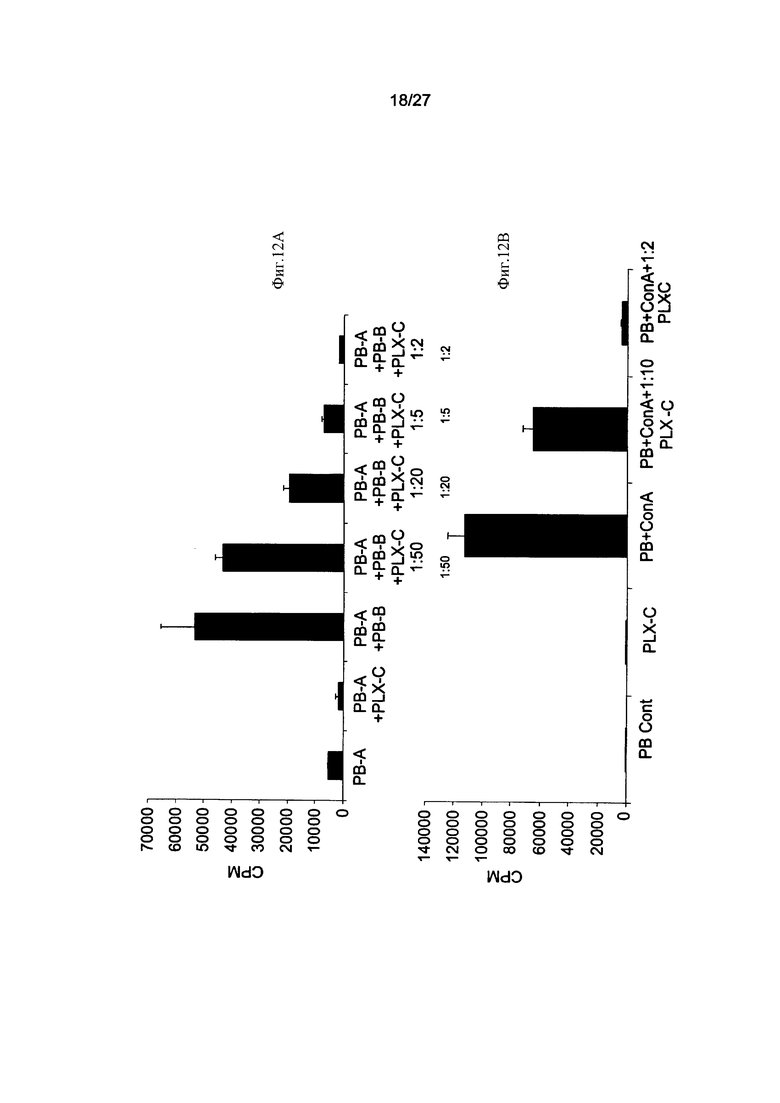

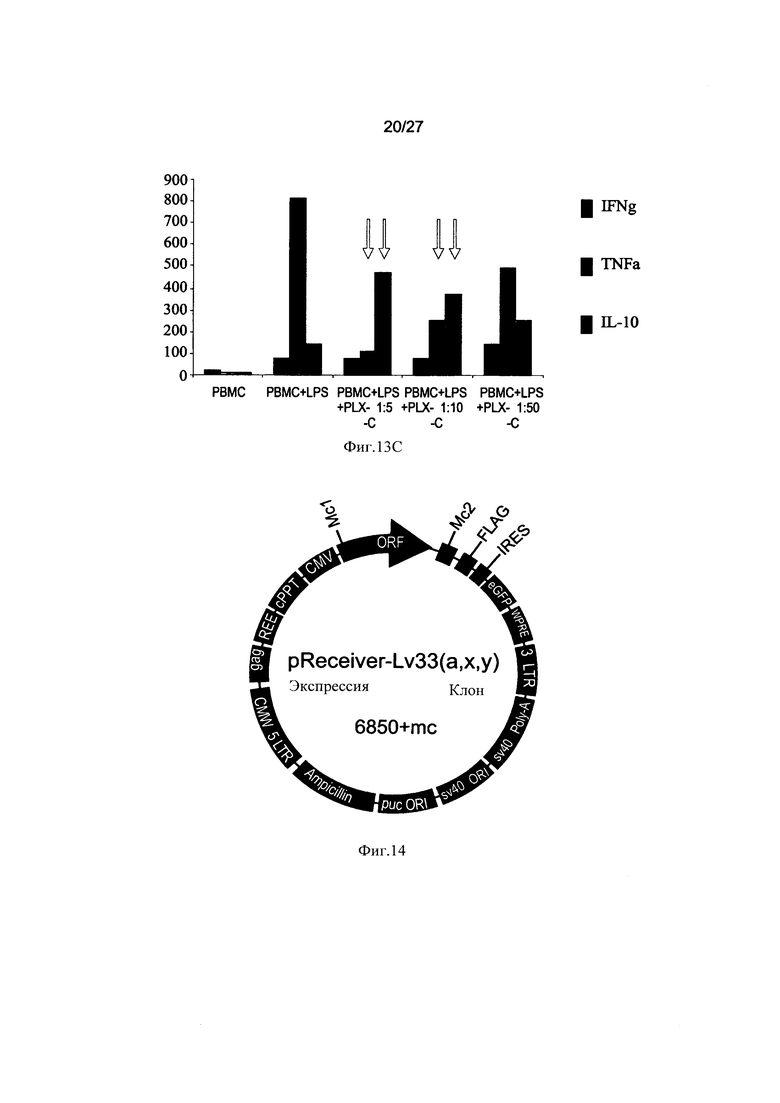


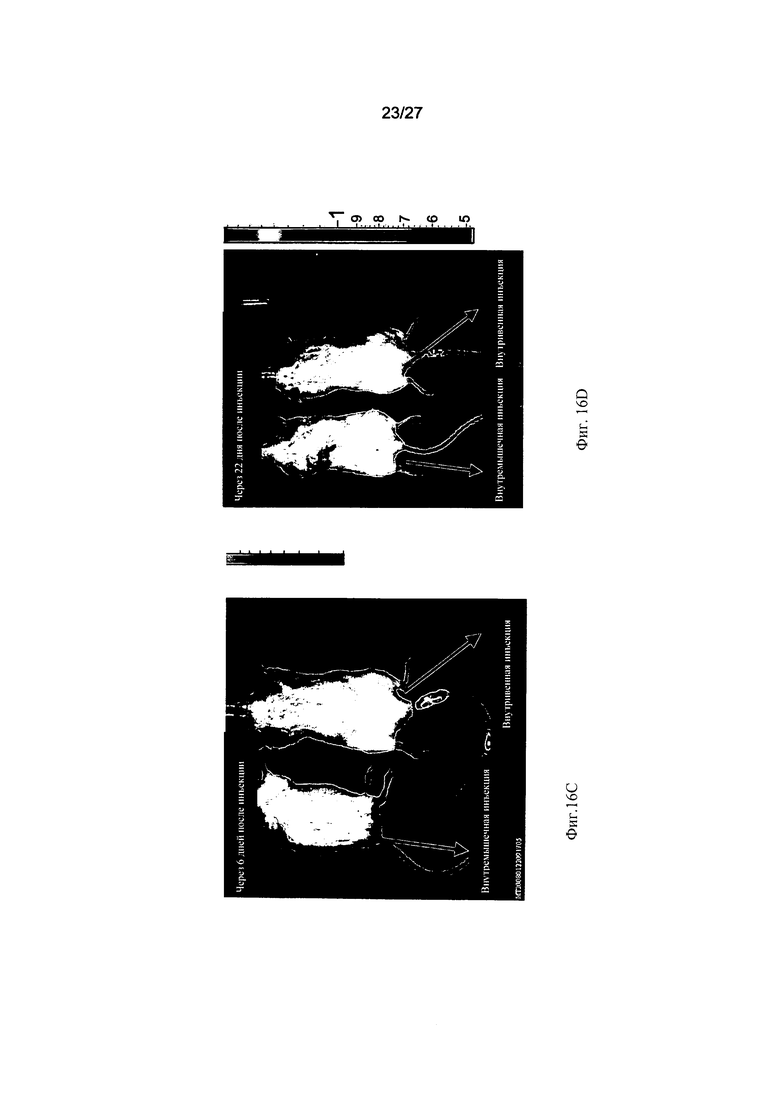
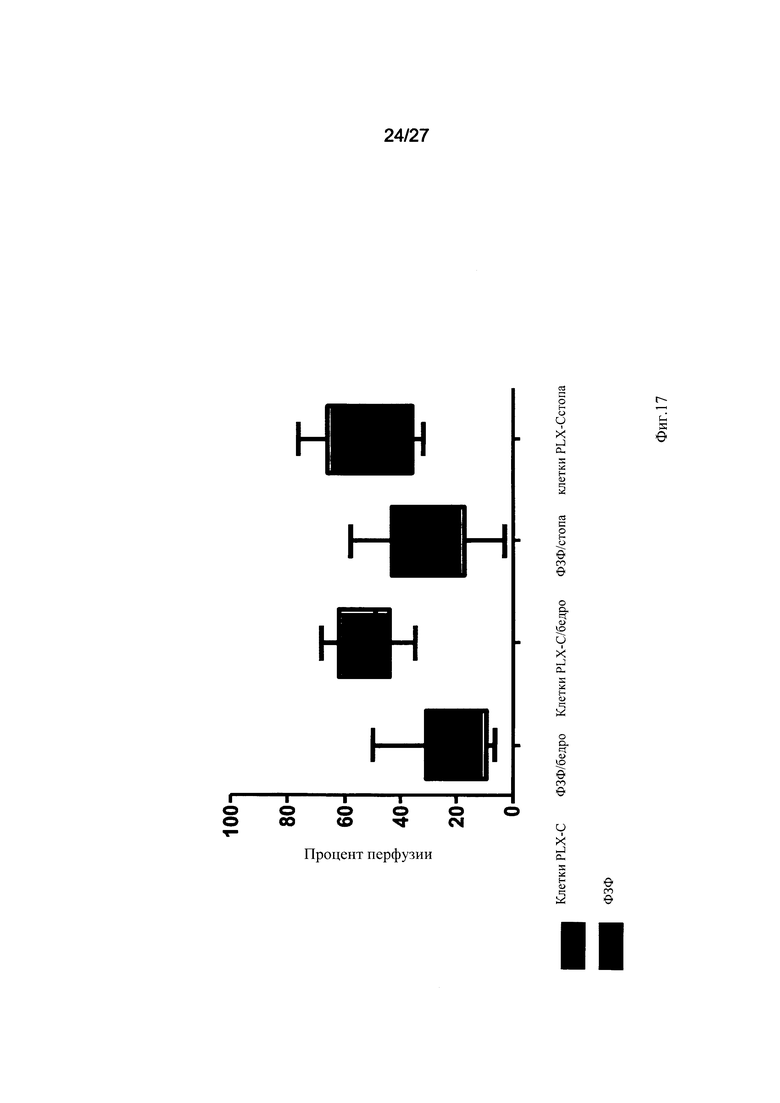
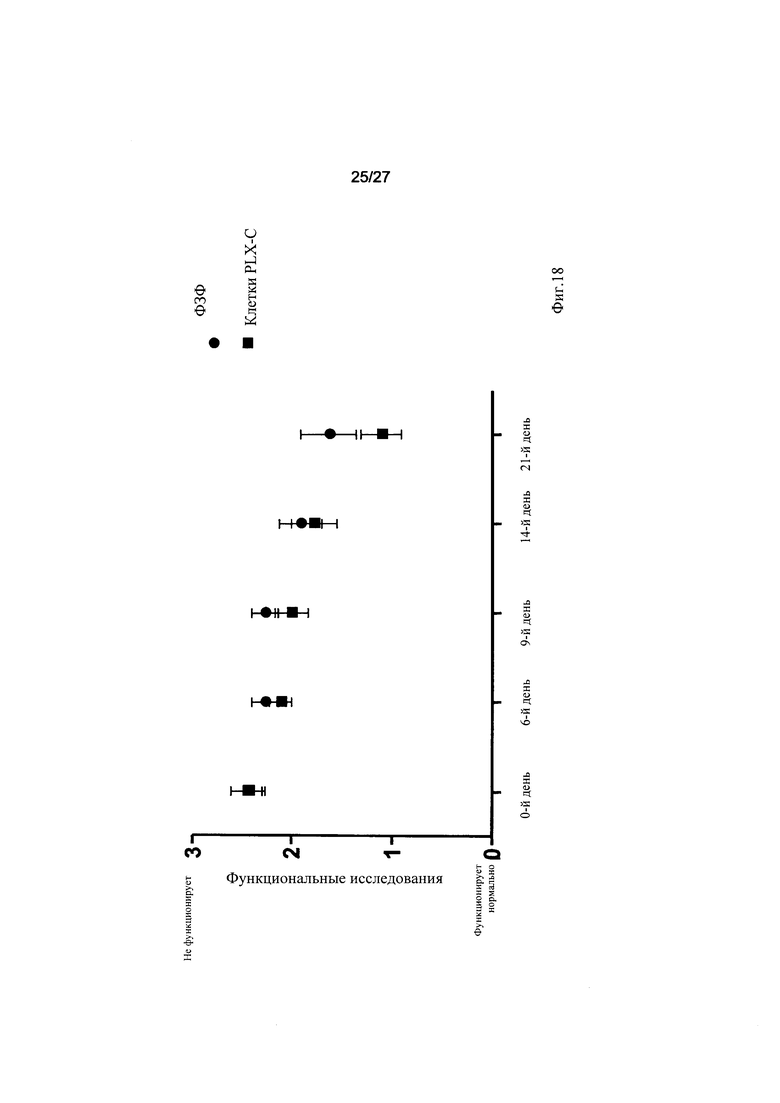
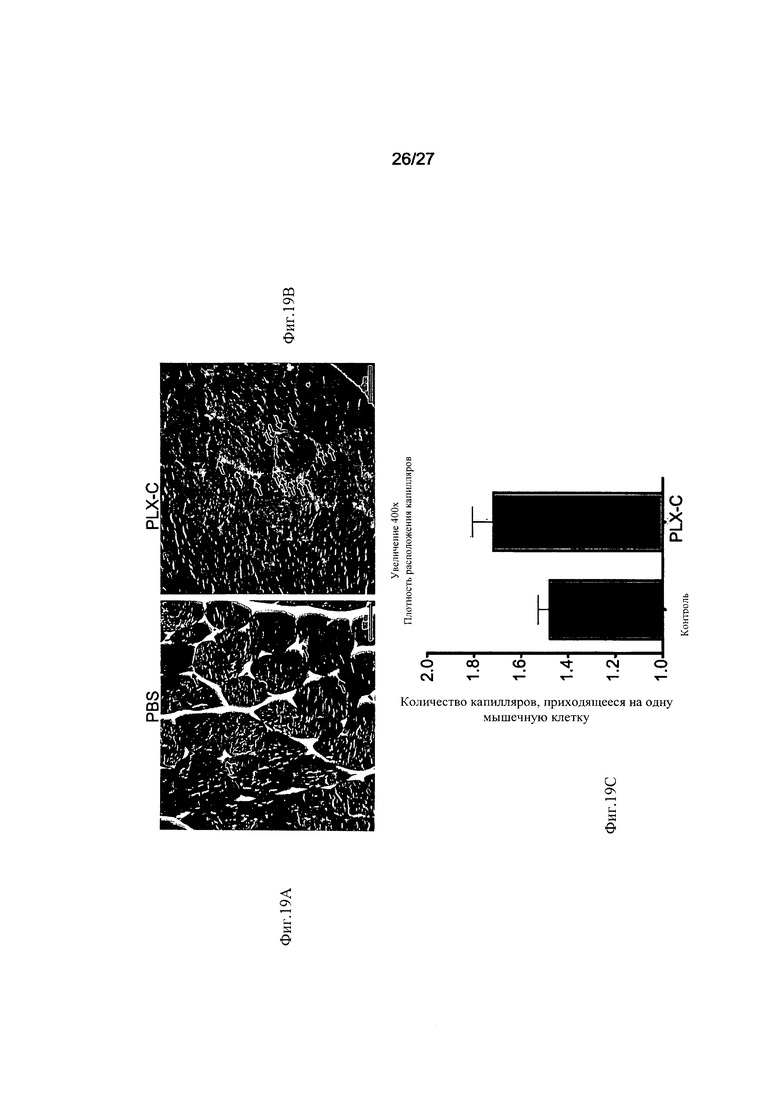
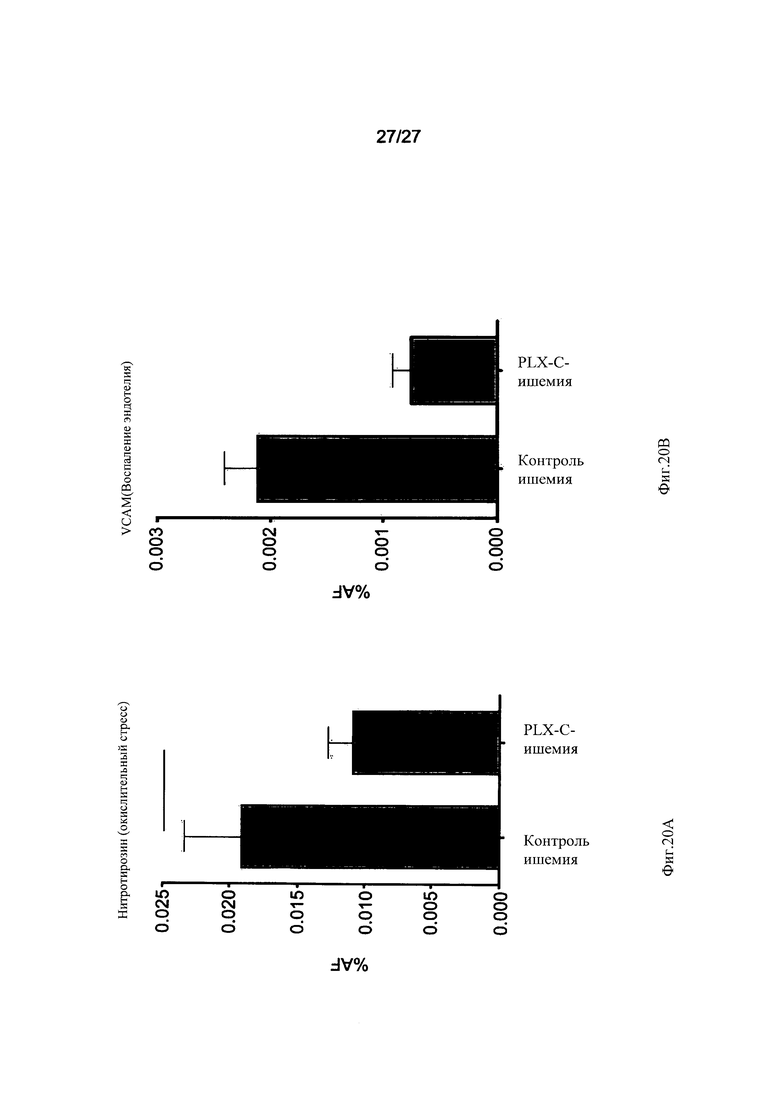
Изобретение относится к медицине и может быть использовано для получения фармацевтической суспензии при лечении ишемии у пациента. Для этого осуществляют размножение адгезивных клеток плаценты из базальной отпадающей оболочки матки (decidua basalis) и париетальной отпадающей оболочки матки (decidua parietalis), имеющих фенотип стромальных стволовых клеток. При этом используют двухмерное (2D) культивирование указанных клеток. Затем их культивируют на трехмерной (3D) подложке. После чего удаляют упомянутые адгезивные клетки плаценты из 3D-подложки и вводят их в фармацевтическую суспензию. Изобретение обеспечивает получение фармацевтической суспензии адгезивных клеток плаценты из базальной отпадающей оболочки матки (decidua basalis) и париетальной отпадающей оболочки матки (decidua parietalis), имеющих фенотип стромальных стволовых клеток, для лечения ишемии у пациента. 10 з.п. ф-лы, 8 табл., 20 ил., 8 пр.
1. Способ получения фармацевтической суспензии для использования при лечении ишемии, включающий размножение адгезивных клеток плаценты из базальной отпадающей оболочки матки (decidua basalis) и париетальной отпадающей оболочки матки (decidua parietalis), имеющих фенотип стромальных стволовых клеток, с использованием двухмерного (2D) культивирования, затем культивирования на трехмерной (3D) подложке, затем удаления упомянутых адгезивных клеток плаценты, имеющих фенотип стромальных стволовых клеток, из упомянутой 3D-подложки и введения упомянутых адгезивных клеток плаценты, имеющих фенотип стромальных стволовых клеток, в упомянутую фармацевтическую суспензию.
2. Способ по п. 1, отличающийся тем, что упомянутые клетки способны подавлять иммунный ответ пациента.
3. Способ по п. 1, отличающийся тем, что по меньшей мере 10% из упомянутых адгезивных клеток находятся на стадии пролиферации.
4. Способ по п. 1, отличающийся тем, что упомянутое культивирование на трехмерной (3D) подложке включает 3D-биореактор.
5. Способ по п. 1 или 4, отличающийся тем, что культивирование упомянутых клеток в упомянутой культуре на 3D-подложке осуществляют с перфузией.
6. Способ по любому одному из пп. 1, 4 и 5, отличающийся тем, что упомянутая трехмерная подложка включает адгезивный материал, выбираемый из группы, состоящей из полиэфира и полипропилена.
7. Способ по п. 1, отличающийся тем, что упомянутые клетки экспрессируют маркер, выбираемый из группы, состоящей из CD73, CD90, CD29 и CD105.
8. Способ по п. 1, отличающийся тем, что упомянутые клетки не экспрессируют маркер, выбираемый из группы, состоящей из CD3, CD4, CD45, CD80, HLA-DR, CD11b, CD14, CD19, CD34 и CD79.
9. Способ по п. 1, отличающийся тем, что упомянутые адгезивные клетки включают фенотип стромальных стволовых клеток.
10. Способ по п. 1, отличающийся тем, что упомянутая ишемия является заболеванием периферических артерий (ЗПА).
11. Способ по п. 1, отличающийся тем, что упомянутая ишемия является ишемией центральной нервной системы (ЦНС).
| US 20070160588 A1, 12.07.2007 | |||
| WO 2006121532 A2, 16.11.2006 | |||
| MAURICE S | |||
| et al., Isolation of progenitor cells from cord blood using adhesion matrices | |||
| Cytotechnology | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| ZHAO F | |||
| et al., Perfusion bioreactor system for human mesenchymal stem cell tissue engineering: dynamic cell seeding and | |||
Авторы
Даты
2019-12-20—Публикация
2008-09-02—Подача