Изобретение относится к медицине, а именно к инфекционным болезням, фтизиатрии и терапии, и может быть использовано для прогнозирования летального исхода при клиническом течении коинфекции ВИЧ и туберкулез, сопровождающемся множественной лекарственной устойчивостью Mycobacterium tuberculosis.
ВИЧ-инфекция остается одной из основных проблем глобального общественного здравоохранения: на сегодняшний день она унесла более 35,4 млн. жизней. В 2017 году около миллиона людей в мире умерли от причин, связанных с ВИЧ. Напряженность эпидемиологической ситуации по ВИЧ-инфекции проявляется и в увеличении числа инфицированных ВИЧ и в росте летальности среди больных ВИЧ-инфекцией. Прогрессия ВИЧ-ассоциированного иммунодефицита наиболее часто (в 60% случаев) приводит к развитию туберкулеза (ТБ), занимающего лидирующую позицию (в 50% случаев) среди причин смерти больных ВИЧ-инфекцией. Известно, что при туберкулезе у больных ВИЧ-инфекцией (коинфекция ВИЧ/ТБ) часто выявляется множественная лекарственная устойчивость микобактерий туберкулеза (МЛУ МБТ), наличие которой ассоциировано с низкими показателями излечения ТБ и более высокими показателями летальности в сравнении с пациентами с сохраненной лекарственной чувствительностью Mycobacterium tuberculosis.
Поиск прогностических маркеров ВИЧ/ТБ при МЛУ МБТ является актуальным в связи с проблемой выбора адекватных противотуберкулезных мероприятий, способных снизить уровень летальности. Некоторые из предложенных предикторов, связанные с успешными результатами лечения, включают высокий индекс массы тела, использование более четырех эффективных препаратов, отрицательный исходный мазок мокроты, проведение хирургической резекции, использование фторхинолонов или линезолида в схеме лечения туберкулеза, применение персонализированного лечения (Y. Kwon, Y. Kim, G. Suh et al. Treatment outcomes for HIV-uninfected patients with multidrug-resistant and extensively drug-resistant tuberculosis. Clinical Infectious Diseases. 2008; 47(4):496-502; N. Kwak, H. Kim, C. Yoo, Y. W. Kim, S. K. Han, and J. Yim. Changes in treatment outcomes of multidrug-resistant tuberculosis. The International Journal of Tuberculosis and Lung Disease. 2015; 19(5): 525-530. doi:10.5588/ijtld.14.0739; K.T. Kibret, Y. Moges, P. Memiah, and S. Biadgilign. Treatment outcomes for multidrug-resistant tuberculosis under DOTS-Plus: a systematic review and meta-analysis of published studies. Infectious Diseases of Poverty. 2017; 6(1): 7. doi:10.1186/s40249-016-0214-х).
К предикторам неблагоприятного прогноза и неудовлетворительных результатов лечения, кроме МЛУ МБТ (S. Tang, S. Tan, L. Yao et al. Risk factors for poor treatment outcomes in patients with MDR-TB and XDR-TB in China: retrospective multi-center investigation. PLoS ONE. 2013; 8(12): 1-8. doi:10.1371/journal.pone.0082943; K. Schnippel, K. Shearer, D. Evans, R. Berhanu, S. Dlamini, and N. Ndjeka. Predictors of mortality and treatment success during treatment for rifampicin-resistant tuberculosis within the South African National ТВ Programme, 2009 to 2011: a cohort analysis of the national case register. International Journal of Infectious Diseases. 2015; 39:89-94), относят низкий индекс массы тела (М.A. Khan, S. Mehreen, A. Basit et al. Predictors of poor outcomes among patients treated for multidrug- resistant tuberculosis at tertiary care hospital in Pakistan. American-Eurasian Journal of Toxicological Sciences. 2015; 7(3): 162-172), наличие множественных локализаций туберкулеза и выраженную иммуносупрессию (Brust J.C.M., Shah N.S., Mlisana K, et al. Improved Survival and Cure Rates With Concurrent Treatment for Multidrug-Resistant Tuberculosis-Human Immunodeficiency Virus Coinfection in South Africa. Clin Infect Dis. 2018; 66(8):1246-1253. doi:10.1093/cid/cix1125; Mollel E.W., Chilongola J.O. Predictors for Mortality among Multidrug-Resistant Tuberculosis Patients in Tanzania. J Trop Med. 2017; 2017:9241238. doi:10.1155/2017/9241238; Bei C., Fu M., Zhang Y. et al. Mortality and associated factors of patients with extensive drug-resistant tuberculosis: an emerging public health crisis in China. BMC Infect Dis. 2018; 18(1):261. doi:10.1186/s12879-018-3169; Gandhi N.R., Andrews J.R., Brust J.C. et al. Risk factors for mortality among MDR- and XDR-TB patients in a high HIV prevalence setting. Int J Tuberc Lung Dis. 2012; 16(1):90-97. doi:10.5588/ijt1d.11.0153). Низкий иммунный статус, определяемый по количеству CD4-лимфоцитов в крови и неподавленная вирусная нагрузка (ВН), в том числе на фоне анти-ретровирусной терапии (APT), считаются основными предикторами летального исхода при коинфекции ВИЧ/ТБ (Kwan С.K., Ernst J.D. HIV and tuberculosis: a deadly human syndemic. Clin Microbiol Rev. 2011; 24(2):351-376. doi:10.1128/CMR.00042-10; Vijay S., Kumar P., Chauhan L.S., Rao S.V., Vaidyanathan P. Treatment outcome and mortality at one and half year follow-up of HIV infected ТВ patients under ТВ control programme in a district of South India. PLoS One. 2011; 6(7): e21008. doi:10.1371/journal.pone.0021008; Sharma S.K., Soneja M., Prasad K.T., Ranjan S. Clinical profile & predictors of poor outcome of adult HIV-tuberculosis patients in a tertiary care centre in north India. Indian J Med Res. 2014; 139(1):154-160; Zhang G., Gong Y., Wang Q. et al. Outcomes and factors associated with survival of patients with HIV/AIDS initiating antiretroviral treatment in Liangshan Prefecture, southwest of China: A retrospective cohort study from 2005 to 2013. Medicine (Baltimore). 2016; 95(27):e3969. doi:10.1097/MD.0000000000003969; Pathmanathan I., Dokubo E.K., Shiraishi R.W., Agolory S.G., Auld A.F., Onotu D. et al. Incidence and predictors of tuberculosis among HIV-infected adults after initiation of antiretroviral therapy in Nigeria, 2004-2012. PLoS ONE. 2017;12(3): e0173309. https://doi.org/10.1371/journal.pone.0173309). Однако среди умерших пациентов нередко встречаются лица, относящиеся к группе с плохо прогнозируемым летальным исходом, т.е. у них не наблюдается выраженной иммуносупрессии и отмечается снижение вирусной нагрузки при адекватной APT. С другой стороны, нередко среди долгоживущих обнаруживаются лица с выраженным иммунодефицитом, у которых количество CD4-лимфоцитов меньше 100 клеток в 1 мкл крови. Проблема предикции неблагоприятных исходов среди этой категории пациентов, особенно, при МЛУ МБТ, является крайне важной и требует выявления дополнительных прогностических факторов/маркеров ВИЧ/ТБ, использование которых позволит оптимизировать лечебно-диагностическую тактику и программу диспансерного наблюдения больных.
Назначением настоящего изобретения является разработка способа прогнозирования летального исхода при клиническом течении коинфекции ВИЧ и туберкулез, сопровождающемся множественной лекарственной устойчивостью Mycobacterium tuberculosis.
Назначение изобретения достигается способом прогнозирования летального исхода при клиническом течении коинфекции ВИЧ и туберкулез. У пациентов с выявленной множественной лекарственной устойчивостью Mycobacterium tuberculosis и известным количеством CD4-лимфоцитов проводят забор образцов венозной крови, выделение плазмы крови и иммуно-ферментный анализ с целью определения концентрации неспецифических (общих) иммуноглобулинов IgE (в МЕ/мл), IgM (в мг/мл), IgA (в мг/мл) и секреторного IgA (в мг/л) в плазме крови, вычисляют коэффициент предикции летального исхода, равный отношению произведения их концентраций к количеству CD4-лимфоцитов в 1 мкл крови (КП= IgE×IgM×IgA×sIgA / CD4) и при превышении этим коэффициентом значения 200 прогнозируют летальный исход с 56,7-кратным относительным риском.
Новизна изобретения:
1. В плазме крови больных коинфекцией ВИЧ/ТБ с МЛУ МБТ содержание неспецифических (общих) иммуноглобулинов IgE, IgM, IgA и секреторного IgA повышено в сравнении с практически здоровыми лицами.
2. У умерших больных коинфекцией ВИЧ/ТБ с МЛУ МБТ содержание общего IgE и секреторного IgA повышено в сравнении с живущими.
3. Между содержанием общего IgE, а также секреторного IgA, и летальным исходом при ВИЧ/ТБ с МЛУ МБТ наблюдается средняя положительная корреляционная связь (R=15% r=0,3929 Р=0,0052 n=49 и R=11% r=0,3258 Р=0,0223 n=49 соответственно).
4. Между содержанием общего IgE и количеством CD4-лимфоцитов наблюдается средняя отрицательная корреляционная связь (R=12% r= -0,3490 Р=0,0140 n=49).
5. Предложен коэффициент предикции летального исхода (КП) у больных ВИЧ/ТБ с МЛУ МБТ, равный отношению произведения концентраций общих IgE (в МЕ/мл), IgM (в мг/мл), IgA (в мг/мл) и секреторного IgA (в мг/л) в плазме крови к количеству CD4-лимфоцитов в 1 мкл крови (КП= IgE×IgM×IgA×sIgA / CD4).
6. Между КП и вирусной нагрузкой (ВН) при коинфекции ВИЧ/ТБ с МЛУ МБТ выявлена средняя положительная корреляционная связь (R=21%, r=0,462 p=0,046 n=19).
7. Между КП и летальным исходом при коинфекции ВИЧ/ТБ с МЛУ/МБТ выявлена сильная положительная корреляционная связь (R=50% r=0,7090 Р<0,0001 n=31).
8. КП более 200 выявляется у 77% умерших и 6% живущих больных ВИЧ/ТБ с МЛУ МБТ.
9. При превышении КП значения 200 прогнозируется летальный исход с 56,7-кратным относительным риском.
Новый технический результат изобретения позволяет выявлять больных коинфекцией ВИЧ/ТБ с МЛУ МБТ, получающих противотуберкулезную терапию, с предрасположенностью к летальному исходу заболевания, определенной по показателю КП= IgE×IgM×IgA×sIgA/ CD4, превышающему значение 200, т.е. прогнозировать неблагоприятный исход заболевания с высокой вероятностью и корректировать лечебную тактику ведения данной когорты больных, способствующую снижению летальности.
В патентной и научной литературе отсутствуют сведения об аналогичном способе прогнозирования летального исхода при клиническом течении коинфекции ВИЧ-туберкулез, сопровождающемся множественной лекарственной устойчивостью Mycobacterium tuberculosis. Совокупность существенных признаков позволяет прогнозировать летальный исход больных коинфекцией ВИЧ/ТБ с МЛУ МБТ при коэффициенте предикции, равном отношению произведения установленных концентраций неспецифических (общих) IgE (в МЕ/мл), IgM (в мг/мл), IgA (в мг/мл) и секреторного IgA (в мг/л) в плазме крови к количеству CD4-лифоцитов в 1 мкл крови, превышающем значение 200.
Более двух десятков лет назад выявлено, что развитие ВИЧ-инфекции сопровождается существенным повышением уровня сывороточного IgE ( D., Labrousse F., Tourani J.-M., Sors H., Andrieu J.-M. et al. Elevation of IgE in HIV-infected subjects: a marker of poor prognosis. Allergy Clin. Immunol. 1992; 89(1): 68-75. doi:10.1016/s0091-6749(05)80042-9), которое ассоциировано с плохим прогнозом заболевания (переход в СПИД, смерть) (Klein S.A., Dobmeyer J.M., Dobmeyer T.S., Раре М., Ottmann O.G., Helm Е.В., Hoelzer D. and Rossol R. Demonstration of the Th1 to Th2 cytokine shift during the course of HIV-1 infection using cytoplasmic cytokine detection on single cell level by flow cytometry. Medical Clinic III. 1997; 11(9): 1111-1118. doi:10.1097/00002030-199709000-00005; Wasik T.J., Jagodzinski P.P., Hyjek E.M., Wustner J., Trinchieri G., Lischner H.W., Kozbor D. Diminished HIV-specific CTL activity is associated with lower type 1 and enhanced type 2 responses to HIV-specific peptides during perinatal HIV infection. Immunol. 1997; 158(12): 6029-6036). Несмотря на давность установленного факта и выдвинутые гипотезы о механизме развития ВИЧ-инфекции по типу аллергических заболеваний (Becker Y. The changes in the T helper 1 (th1) and T helper 2 (th2) cytokine balance during HIV-1 infection are indicative of an allergic response to viral proteins that may be reversed by th2 cytokine inhibitors and immune response modifiers - a review and hypothesis. Virus genes. 2004; 28(1): 5-18. doi:10.1023/b:viru.0000012260.32578.72), прошедший временной срок характеризуется немногочисленными исследованиями Th2-звена иммунитета, ответственного за синтез антител, в то числе IgE-класса, у ВИЧ-инфицированных больных. В настоящее время во всем мире у значительного числа больных ВИЧ-инфекцией регистрируется туберкулез, являющийся самым частым вторичным заболеванием. Повышенный уровень сывороточного IgE при ТБ у больных ВИЧ-инфекцией некоторые исследователи связывают с асимптоматическим инфицированием гельминтами (Abate Е., Belayneh М., Gelaw A., Idh J., Getachew A., Alemu S., Diro E., Fikre N., Britton S., Elias D., Aseffa A., Stendahl О.,
D., Labrousse F., Tourani J.-M., Sors H., Andrieu J.-M. et al. Elevation of IgE in HIV-infected subjects: a marker of poor prognosis. Allergy Clin. Immunol. 1992; 89(1): 68-75. doi:10.1016/s0091-6749(05)80042-9), которое ассоциировано с плохим прогнозом заболевания (переход в СПИД, смерть) (Klein S.A., Dobmeyer J.M., Dobmeyer T.S., Раре М., Ottmann O.G., Helm Е.В., Hoelzer D. and Rossol R. Demonstration of the Th1 to Th2 cytokine shift during the course of HIV-1 infection using cytoplasmic cytokine detection on single cell level by flow cytometry. Medical Clinic III. 1997; 11(9): 1111-1118. doi:10.1097/00002030-199709000-00005; Wasik T.J., Jagodzinski P.P., Hyjek E.M., Wustner J., Trinchieri G., Lischner H.W., Kozbor D. Diminished HIV-specific CTL activity is associated with lower type 1 and enhanced type 2 responses to HIV-specific peptides during perinatal HIV infection. Immunol. 1997; 158(12): 6029-6036). Несмотря на давность установленного факта и выдвинутые гипотезы о механизме развития ВИЧ-инфекции по типу аллергических заболеваний (Becker Y. The changes in the T helper 1 (th1) and T helper 2 (th2) cytokine balance during HIV-1 infection are indicative of an allergic response to viral proteins that may be reversed by th2 cytokine inhibitors and immune response modifiers - a review and hypothesis. Virus genes. 2004; 28(1): 5-18. doi:10.1023/b:viru.0000012260.32578.72), прошедший временной срок характеризуется немногочисленными исследованиями Th2-звена иммунитета, ответственного за синтез антител, в то числе IgE-класса, у ВИЧ-инфицированных больных. В настоящее время во всем мире у значительного числа больных ВИЧ-инфекцией регистрируется туберкулез, являющийся самым частым вторичным заболеванием. Повышенный уровень сывороточного IgE при ТБ у больных ВИЧ-инфекцией некоторые исследователи связывают с асимптоматическим инфицированием гельминтами (Abate Е., Belayneh М., Gelaw A., Idh J., Getachew A., Alemu S., Diro E., Fikre N., Britton S., Elias D., Aseffa A., Stendahl О.,  T. The Impact of asymptomatic helminth coinfection in patients with newly diagnosed tuberculosis in North-West Ethiopia. Plos one. 2012; 7(8): e42901.published online 2012 aug 29. doi: 10.1371/journal.pone.0042901 pmcid: pmc3430660 pmid: 22952620). Однако антитела класса IgE, как общие, так и антиген-специфические, определены в повышенной концентрации в крови не только при атопических и паразитарных заболеваниях, но и при бактериальных и вирусных инфекциях, и уже давно не подвергается сомнению участие IgE в иммунном ответе на инфицирование патогенами различного происхождения.
T. The Impact of asymptomatic helminth coinfection in patients with newly diagnosed tuberculosis in North-West Ethiopia. Plos one. 2012; 7(8): e42901.published online 2012 aug 29. doi: 10.1371/journal.pone.0042901 pmcid: pmc3430660 pmid: 22952620). Однако антитела класса IgE, как общие, так и антиген-специфические, определены в повышенной концентрации в крови не только при атопических и паразитарных заболеваниях, но и при бактериальных и вирусных инфекциях, и уже давно не подвергается сомнению участие IgE в иммунном ответе на инфицирование патогенами различного происхождения.
Целью настоящей работы явилось исследование эффективности показателей неспецифических сывороточных иммуноглобулинов различных классов в качестве предикторов летального исхода у пациентов с коинфекцией ВИЧ/ТБ и МЛУ МБТ, получающих противотуберкулезную терапию. В исследование были включены 50 больных коинфекцией ВИЧ и туберкулез с множественной лекарственной устойчивостью Mycobacterium tuberculosis (коинфекция ВИЧ/ТБ с МЛУ МБТ) в возрасте от 24 до 54 (36,08±0,94) лет, находившихся на стационарном лечении в ГКУЗ Кемеровской области «Новокузнецком клиническом противотуберкулезном диспансере» г. Новокузнецка в период 2017-2018 гг. Из них мужчин - 31 человек (62%), женщин - 19 (38%). Работающих было 14 (28%) человек, не работали 34 (68%) человека, инвалидами являлись 2 человека (4%). Злоупотребляли алкоголем 18 (36%) пациентов, 34 (68%) человека указали на инъекционное употребление психоактивных веществ в течение 2-23 лет.
Критериями включения в исследование были:
1. установленный диагноз коинфекции ВИЧ/ТБ;
2. МЛУ МБТ (резистентность одновременно к изониазиду и рифампицину), обнаруженная методом абсолютных концентраций на плотных питательных средах и/или выявлением мутации в гене rpoB, ответственной за резистентность к рифампицину (маркер МЛУ) методом GeneXpert MTB/RIF; в том числе у 12 больных с МЛУ имелась дополнительная резистентность к фторхинолонам.
3. сведения о количестве CD4-лимфоцитов в 1 мкл крови (получены в ГБУЗ КО «Новокузнецкий Центр-СПИД»);
4. проведение противотуберкулезной терапии согласно действующим Федеральным клиническим рекомендациям: больные с МЛУ МБТ - по IV режиму, а при дополнительной устойчивости к фторхинолонам - по V режиму лечения ТБ (Федеральные клинические рекомендации по диагностике и лечению туберкулеза у больных ВИЧ-инфекцией / Васильева И.А., Покровский В.В., Аксенова В.А., Марьяндышев А.О., Эргешов А.Э., Черноусова Л.Н., Пантелеев A.M., Зимина В.Н., Юрин О.Г., Кравченко А.В., Скорняков С.Н., Стаханов В.А., Викторова И.Б., Самойлова А.Г., Загдын З.М., Охтяркина В.В., Корнилова З.Х., Карпина Н.Л., Морозова Т.И., Валиев Р.Ш., Казимирова Н.Е. Клевно Н.И., Багдасарян Т.Р., Каюкова С.И., Барышникова Л.А., Ларионова Е.Е., Севастьянова Э.В., Михайловский A.M., Конончук О.Н., 2015 г.);
5. согласие пациентов на участие в исследовании.
Гельминтозы не были диагностированы ни у одного больного по результатам рутинного обследования пациентов в противотуберкулезном учреждении (анализ кала на яйца глистов).
Вирусная нагрузка (ВН, количество копий РНК ВИЧ в 1 мл плазмы крови) определена методом ПЦР у 33 из 50 больных с МЛУ МБТ (66,0%) в ГБУЗ КО «Новокузнецкий Центр-СПИД».
Летальный исход. Смертельные исходы на протяжении от 2017 до начала 2019 гг. зарегистрированы у 14 (28,0%) больных коинфекцией ВИЧ/ТБ с МЛУ/МБТ. Результаты аутопсии известны для 13 больных (92,9%): во всех случаях причиной смерти стало прогрессирование туберкулеза с полиорганным поражением. Сроки смерти больных составили от 40 дней до 1,5 лет с момента утверждения диагноза туберкулеза и взятия на диспансерный фтизиатрический учет. У четверых человек смертельный исход наступил в течение первых 3 месяцев с момента утверждения диагноза, у 4-х - в сроки 3-11 месяцев, и еще у 4-х - в сроки 1-1,5 года.
В группу контроля включено 49 практически здоровых лиц в возрасте от 27 до 72 лет (26 женщин и 23 мужчины), не имеющих признаков очаговой и системной инфекции с умеренно выраженными возрастными изменениями (у лиц старше 60 лет).
Иммуноферментный анализ. В образцах плазмы крови определяли концентрацию неспецифических (общих) иммуноглобулинов Е (IgE), А (IgA), М (IgM) и секреторного A (sIgA) с использованием стандартных наборов реагентов IgE общий-ИФА-БЕСТ-8660 (ВЕКТОР БЕСТ, Новосибирск), IgA общий-ИФА-БЕСТ-8666 (ВЕКТОР БЕСТ, Новосибирск), IgM общий-ИФА-БЕСТ-8664 (ВЕКТОР БЕСТ, Новосибирск) и IgA секреторный-ИФА-БЕСТ (набор реагентов А-8668, ВЕКТОР БЕСТ, Новосибирск) методом твердофазного иммуноферментного анализа на иммуноферментном автоматическом анализаторе Лазурит (Dynex Technol., США).
Статистический анализ. Статистическая обработка результатов исследования проводилась с использованием программ Microsoft® Excel® версия 14.4.6 (141106), Statistica 6.0, InStatII, SPSS. Стандартная обработка включала подсчет выборки (n - количество обследованных лиц), средних арифметических величин (М), ошибки средней (m), медианы (Me), а также диапазон разброса данных от минимального до максимального значения (Min-Max) в каждой исследуемой выборке. Значимость различий показателей между группами оценивали с помощью непараметрического критерия Манна-Уитни (Р). Относительный риск по конкретному признаку вычисляли как соотношение шансов (OR= odds ratio). Корреляционную связь (согласованное изменение двух признаков) между показателями оценивали с помощью непараметрического критерия Спирмена (r). Влияние одного показателя на степень изменчивости другого оценивали по коэффициенту детерминации в % (R= r2×100). Критический уровень значимости (Р) при проверке статистических гипотез принимался равным 0,05.
Способ осуществляется следующим образом.
В момент забора крови на исследование пациенты с коинфекцией ВИЧ/ТБ и МЛУ МБТ находились на интенсивной фазе лечения ТБ. У каждого из них забирают около 3 мл крови из локтевой вены в коммерческие стерильные вакуумные одноразовые пластиковые пробирки, содержащие антикоагулянт ЭДТА-K3 (IMPROVE, China). Выделение плазмы крови проводят стандартно после осаждения клеток центрифугированием при 3000 об/мин в течение 5 минут. В образцах плазмы крови определяют концентрацию неспецифических (общих) IgE (в МЕ/мл), IgM (в мг/мл), IgA (в мг/мл) и секреторного IgA (в мг/л), вычисляют коэффициент предикции летального исхода (КП), равный отношению произведения их концентраций к количеству CD4-лимфоцитов в 1 мкл крови (КП= IgE×IgM×IgA×sIgA / CD4). При значениях КП более 200 прогнозируют летальный исход с 56,7-кратной вероятностью.
Результаты.
1. Количество CD4-лимфоцитов у обследованных больных коинфекцией ВИЧ/ТБ с МЛУ МБТ
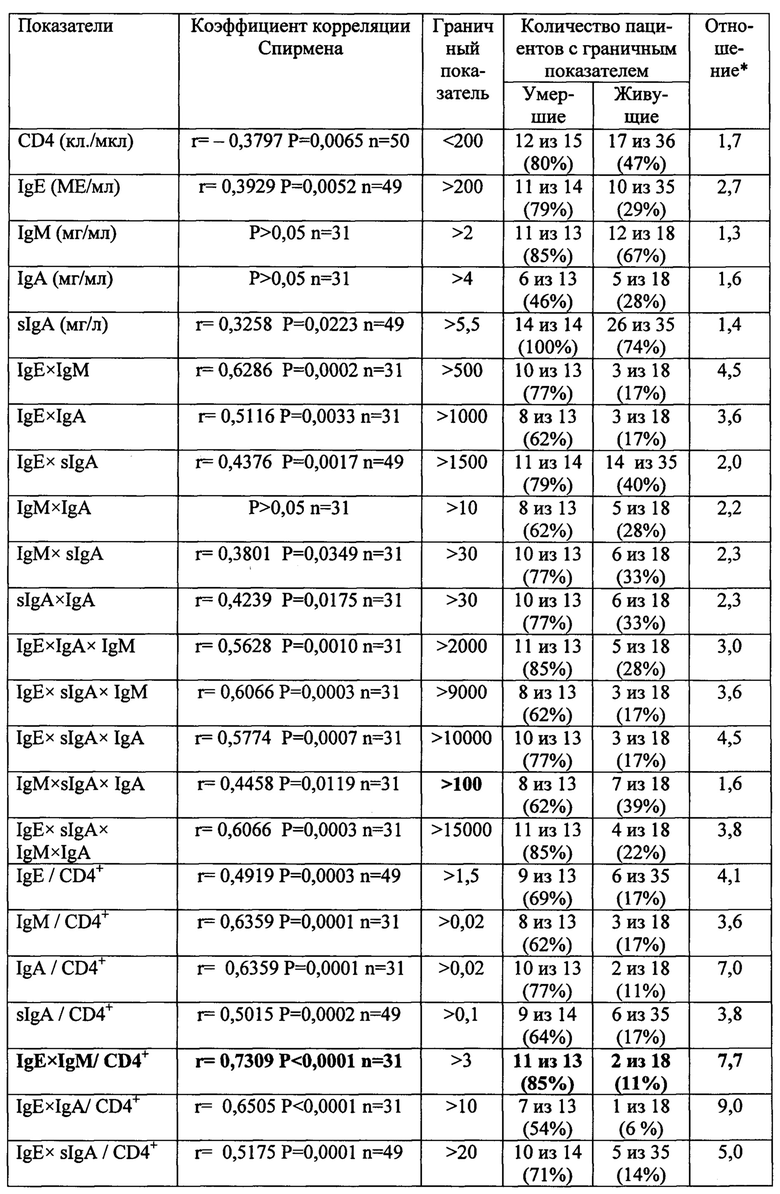
Сведения о количестве CD4-лимфоцитов имелись у всех больных коинфекцией ВИЧ/ТБ с МЛУ МБТ (Ме=181,5 Min-Max=26-1624 n=50). Обнаружен большой интервал индивидуальной вариабельности количества CD4-лимфоцитов как среди умерших, так и среди живущих обследованных пациентов. Так, диапазон значений количества CD4-лимфоцитов в 1 мкл крови среди умерших больных варьировал от 50 до 683 (М±m=159,7±43,7; Ме=112,0; n=14), а у живущих - от 26 до 1624 (М±m=359,5±58,4; Ме=233,5; n=36). В среднем меньшее значение количества CD4-лимфоцитов среди умерших пациентов в сравнении с живущими (р=0,0081) обусловлено различным распределением пациентов с отличающимся иммунным статусом в этих когортах. В таблице 1 показано, что пациентов с числом CD4-лимфоцитов ≤ 200/мкл среди умерших лиц относительно больше (12 умерших, 86%), чем среди живущих (17 человек, 47%, Р=0,0237). Тем не менее, как среди умерших, так и среди живущих обнаружены лица, как с низкими, так и с высокими значениями количества CD4-лимфоцитов. Выраженная вариабельность показателей CD4-лимфоцитов в обеих когортах обусловила низкий коэффициент детерминации и среднюю по выраженности отрицательную корреляционную связь между количеством CD4-лимфоцитов и летальным исходом (R=14% r= -0,3797 Р=0,0065 n=50).
ВН, определенная у 31 больного (62%), также широко варьировала, составив диапазон от 500 до 4708296 копий/мл (М=656 042 коп./мл, Me=471 408 коп./мл). Подавленная ВН (<500 копий/мл) обнаружена только у 2 из 33 обследованных больных (6,1%). Вариабельность обоих показателей (количества CD4-лимфоцитов и ВН) обусловила низкий коэффициент детерминации (R=13% Р=0,043 n=33) между ними, означающий слабое влияние ВН на показатель CD4-лимфоцитов, и среднюю отрицательную корреляционную связь (r= -0,355 Р=0,043 n=33).


Таким образом, большая индивидуальная вариабельность показателя количества CD4-лимфоцитов как у умерших, так и у живущих обследованных нами пациентов с коинфекцией ВИЧ/ТБ и МЛУ МБТ является недостатком использования показателя количества CD4-лимфоцитов для предикции летальности.
У обследованных нами пациентов была обнаружена отрицательная связь уровня CD4-лимфоцитов с количеством IgE (R=12% r=- 0, 3490 р=0,0140 n=49), что послужило поводом для исследования связи уровня иммуноглобулинов в плазме крови с летальным исходом.
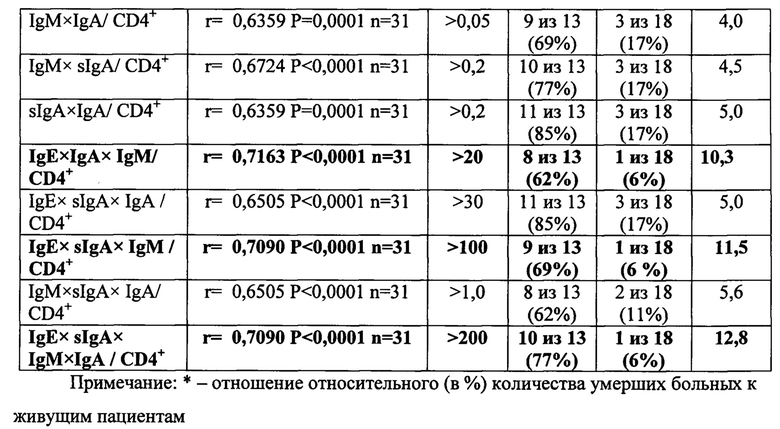
2. Исследование связи уровня IgE, IgM, IgA и sIgA в плазме крови с летальным исходом у обследованных пациентов с коинфекцией ВИЧ/ТБ и МЛУ МБТ
У больных коинфекцией ВИЧ/ТБ с МЛУ МБТ выявлено повышенное количество четырех классов неспецифических (общих) иммуноглобулинов в плазме крови в сравнении с контролем (табл. 2). У умерших больных содержание IgE, также как и sIgA, достоверно превышало соответствующее их количество у живущих и поэтому данные показатели могут быть связаны с летальным исходом. Выявлена корреляционная связь количества IgE и sIgA, а также коэффициентов, рассчитанных с использованием значений концентраций всех тестируемых иммуноглобулинов, с летальным исходом (табл. 3). Сильная корреляционная связь с летальным исходом (R>50% r ≥ 0,7) обнаружена для четырех показателей. В качестве коэффициента предикции летального исхода (КП) у больных коинфекцией ВИЧ/ТБ с МЛУ МБТ выбран коэффициент, равный отношению произведения концентраций IgE, IgM, IgA и секреторного IgA в плазме крови на количество CD4-лимфоцитов (КП= IgE×IgM×IgA×sIgA / CD4). КП более 200 выявлен у 77% умерших и 6% живущих пациентов, т.е. количество умерших больных с КП >200 превысило количество живущих с КП >200 в 12,8 раз. КП положительно и сильно коррелировал с летальным исходом (R=50% r=0,7090 Р<0,0001 n=31) и вирусной нагрузкой (R=21% r=0,462 р=0,046 n=19). Относительный риск летального исхода при КП >200 оказался очень высоким (OR=56,7 р<0,0001).


Клинические примеры.
Клинический пример №1.
Пациентка Ф., 1977 г.р., с ВИЧ-инфекцией, выявленной 3 года назад во время беременности, APT ранее не принимала. Считает себя больной в течение 6 мес., когда появились лихорадка до 38-39°С, неврологические симптомы в виде нарушения мнестических функций, диарея до 3-4 раз в сутки и снижение веса. Из общелечебной сети была переведена в ГКУЗ КО «Новокузнецкий клинический противотуберкулезный диспансер», где было подтверждено наличие туберкулеза (ТБ) множественных локализаций (кислотоустойчивые микобактерии, КУМ) при микроскопии мазка мокроты и кала, а так же выявление ДНК МБТ молекулярно-генетическим методом (МГМ) при исследовании мокроты. Диагноз генерализованного туберкулеза у больной ВИЧ-инфекцией в стадии вторичных заболеваний был утвержден Центральной врачебной контрольной комиссией (ЦВКК) 03.10.2018 г.: диссеминированный ТБ легких, ТБ внутригрудных, внутрибрюшных лимфатических узлов, ТБ кишечника, МБТ (+), резистентность к рифампицину МГМ, IA(+) диспансерного учета. Учитывая, что по результатам молекулярно-генетического исследования мокроты (GeneXpert MTB/RIF) была выявлена мутация в гене rpoB, ответственная за лекарственную устойчивость к рифампицину (т.е. маркер МЛУ), пациентке был назначен стандартный IV режим химиотерапии туберкулеза (левофлоксацин, капреомицин, пиразинамид, циклосерин, протионамид и ПАСК) с планируемой длительностью лечения не менее 24 мес.
Количество CD4-лимфоцитов - 126 клеток/мкл, вирусная нагрузка (ВН) - 2 035 632 коп./мл от 02.11.2018 г., APT была начата с 07.11.2018 г. (ламивудин, тенофовир и невирапин). Иммуноглобулины: общий IgA 4,7 мг/мл, общий IgM 3,2 мг/мл, общий IgE 975,7 МЕ/мл, секреторный IgA 15,5 мг/л. КП= IgE×IgM×IgA×sIgA / CD4=1819 (>200), что указывает на высокую вероятность неблагоприятного прогноза заболевания (относительный риск равен 56,7).
В период госпитализации были получены сведения о росте МБТ из мокроты (на плотных питательных средах) и МЛУ МБТ (устойчивость к рифампицину, изониазиду, этамбутолу), чувствительность к препаратам второго ряда была сохранена.
При дообследовании было верифицировано наличие менингоэнцефалита, а в крови и ликворе методом ПЦР была выявлена ДНК цитомегаловируса (ЦМВ).
Пациентке была продолжена химиотерапия ТБ по IV режиму, проводилось переливание крови дважды в связи с развитием тяжелой анемии (снижение гемоглобина до 51 г/л) без клинических признаков кровотечения; инфузионная терапия. В связи с верификацией манифестной ЦМВ-инфекции планировалось назначение ганцикловира, однако его назначить не удалось по объективным причинам.
На фоне проводимой терапии состояние пациентки оставалось крайне тяжелым: сохранялись лихорадка, неврологические симптомы, кахексия, пролежни. Несмотря на проводимое лечение, 01.12.2018 г. была констатирована смерть больной.
Диагноз: ВИЧ-инфекция в стадии вторичных заболеваний (4В), фаза прогрессирования на фоне начатой APT. Диссеминированный ТБ легких, ТБ внутригрудных, внутрибрюшных лимфатических узлов, ТБ кишечника, МБТ (+), МЛУ (рифампицин, изониазид, этамбутол). Манифестная ЦМВ-инфекция (ЦМВ-энцефалит, ЦМВ-колит). Осложнение: кахексия 3 ст., пролежни 1 ст.
Клинический пример №2.
Пациент 3., 1973 г.р., обратился в общелечебную сеть в связи с лихорадкой до 38°С в течение 2 мес., где при микроскопии мокроты были выявлены КУМ. Пациент был направлен в ГКУЗ КО «Новокузнецкий клинический противотуберкулезный диспансер», где диагноз туберкулеза был подтвержден и утвержден на ЦВКК 22.01.2018 г. (диссеминированный ТБ легких, фаза распада, МБТ (+), IA группа диспансерного учета). Молекулярно-генетическое исследование мокроты не проводилось. При поступлении в диспансер был назначен I режим химиотерапии ТБ (изониазид, рифампицин, пиразинамид и этамбутол), который больной принимал в течение 2 месяцев до получения результатов посевов мокроты (рост МБТ 2+) и сведений о МЛУ МБТ (устойчивость к рифампицину, изониазиду и этамбутолу), чувствительность к препаратам второго ряда была сохранена. В связи с выявлением МЛУ МБТ 28.03.2018 г. был назначен IV режим лечения ТБ (спарфлоксацин, канамицин, пиразинамид, циклосерин, протионамид и ПАСК) с планируемой длительностью не менее 24 мес.
ВИЧ-инфекция была впервые выявлена в противотуберкулезном диспансере вместе с верификацией ТБ (количество CD4-лимфоцитов - 943 клеток/мкл от 14.02.2018 г., сведений о вирусной нагрузке не было). Тогда же был впервые диагностирован декомпенсированный осложненный сахарный диабет (гликемия до 19,2-23,4 ммоль/л, явления полинейропатии нижних конечностей). Иммуноглобулины: общий IgA 1,4 мг/мл, общий IgM 1,8 мг/мл, общий IgE 26,2 МЕ/мл, секреторный IgA 7,9 мг/л. КП= IgE×IgM×IgA×sIgA / CD4= 0,55 (<200), что указывает на благоприятный прогноз заболевания.
Пациент отрицал наличие у себя ВИЧ-инфекции и сахарного диабета, категорически отказался от осмотра инфекциониста и приема APT, от соблюдения режима питания, осмотра эндокринолога и инсулинотерапии. С недоверием воспринимал информацию о наличии у него ТБ с бактериовыделением. Противотуберкулезные препараты принимал нерегулярно, пропускал лечение, алкоголизировался, из стационара был выписан досрочно за нарушение режима.
За время лечения получена некоторая положительная рентгенологическая динамика в виде частичного рассасывания диссеминации и уменьшения размеров полостей распада, был условно абациллирован (прекращение бактериовыделения по мазкам мокроты).
Диагноз: ВИЧ-инфекция в стадии вторичных заболеваний (4Б), фаза прогрессирования без APT. Диссеминированный ТБ легких, фаза распада, МБТ (+), МЛУ (изониазид, рифампицин, этамбутол), IA группа диспансерного учета. Сахарный диабет II типа, впервые выявленный, средней степени тяжести, декомпенсированный, осложненный полинейропатией нижних конечностей. Бытовое пьянство.
В настоящее время находится на амбулаторном лечении по IV режиму.
Клинический пример №3.
Пациентка С., 1993 г.р., выявлена в июне 2018 г. при обращении в общелечебную сеть с жалобами на лихорадку до 38°С в течение 2 недель, слабость. После курса неспецифической антимикробной терапии была направлена в ГКУЗ КО «Новокузнецкий клинический противотуберкулезный диспансер» с связи с высоковероятным туберкулезом.
Бактериовыделения на момент установления диагноза туберкулеза не было (микроскопия мокроты не выявила КУМ), при молекулярно-генетическом исследовании мокроты ДНК МБТ не выявлена. КУМ были выявлены в кале, а при ультразвуковом исследовании - признаки внутрибрюшной лимфаденопатии с размерами лимфатических узлов до 2,5 см. Не работает, проживает с двумя детьми (3 и 8 лет). Диагноз ВИЧ-инфекции подтвержден в 2014 году, употребление психоактивных веществ, как в прошлом, так и в настоящее время категорически отрицает; антиретровирусные препараты получала ранее только во время беременности (профилактика вертикальной передачи ВИЧ). Количество CD4-лимфцитов в период верификации ТБ (07.2018 г.) - 97 кл./мкл, вирусная нагрузка (ВН) - 199 841 коп./мл.
Диагноз туберкулеза множественных локализаций у пациентки с ВИЧ-ассоциированной иммуносупрессией был утвержден на ЦВКК 02.07.2018 г.: ТБ внутригрудных лимфатических узлов с бронхолегочным поражением: инфильтративный ТБ I-II сегментов слева, ТБ периферических лимфатических узлов, ТБ внутрибрюшных лимфатических узлов, ТБ кишечника, МБТ (-), IA группа диспансерного учета. В стационаре был назначен III режим химиотерапии ТБ (комбинация изониазида, рифампицина, пиразинамида и этамбутола), который пациентка принимала в течение 7 месяцев. Была осмотрена инфекционистом, с сентября 2018 г. начата антиретровирусная терапия (APT) комбинацией ламивудина, тенофовира и эфавиренза (впоследствии было уточнено, что эфавиренз принимала нерегулярно из-за побочных реакций, о которых не сообщала врачу).
На фоне терапии по III режиму и положительной рентгенологической динамики туберкулеза в виде частичного рассасывания инфильтрации и очагов, а так же уменьшения размеров всех групп лимфатических узлов, с ноября 2018 г. появилось бактериовыделение по посевам мокроты (рост МБТ 3+). К февралю 2019 г. были получены сведения о наличии МЛУ МБТ (устойчивость к рифампицину, изониазиду и этамбутолу), чувствительность к препаратам второго ряда была сохранена. В связи с выявлением МЛУ с 18.02.2019 г. была назначена терапия по IV режиму (спарфлоксацин, канамицин, пиразинамид, циклосерин, протионамид и ПАСК) с планируемой длительностью не менее 24 мес.
В дальнейшем на фоне лечения по IV режиму бактериовыделения по мазкам мокроты не было, а с февраля 2019 г. было зафиксировано прекращение бактериовыделения по посевам; при контрольном рентгено-томографическом исследовании органов грудной клетки определяется дальнейшее рассасывание и уплотнение инфильтративных и очаговых изменений в I-II сегментах левого легкого.
Динамическое исследование иммунного статуса и вирусной нагрузки на фоне APT показало сохраняющуюся иммуносупрессию (количество CD4-лимфоцитов - 99 клеток/мкл) при снижении ВН (<500 коп./мл). Иммуноглобулины: общий IgA 1,41 мг/мл, общий IgM 2,62 мг/мл, общий IgE 154,15 МЕ/мл, секреторный IgA 10,2 мг/л. КП= IgE×IgM×IgA×sIgA / CD4= 58,7 (<200), что указывает на благоприятный прогноз заболевания.
Диагноз: ВИЧ-инфекция в стадии вторичных заболеваний (4В), фаза стабилизации на APT. ТБ внутригрудных лимфатических узлов с бронхолегочным поражением: инфильтративный ТБ I-II сегментах слева, ТБ периферических лимфатических узлов, ТБ внутрибрюшных лимфатических узлов, ТБ кишечника, МБТ (+), фаза частичного рассасывания и уплотнения, IA группа диспансерного учета.
В настоящее находится на амбулаторном лечении туберкулеза с МЛУ МБТ, проводится интенсивная фаза лечения, прием препаратов нерегулярный (пропуски в лечении составляют до 13 дней подряд), продолжает APT и профилактический прием триметоприма/сульфометоксазола.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗА СРОКА ДОЖИТИЯ ПАЦИЕНТОВ ПРИ КЛИНИЧЕСКОМ ТЕЧЕНИИ КОИНФЕКЦИИ ВИЧ И ТУБЕРКУЛЕЗ, СОПРОВОЖДАЮЩЕМСЯ МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ MYCOBACTERIUM TUBERCULOSIS | 2021 |
|
RU2764830C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТИ К РАЗВИТИЮ ТУБЕРКУЛЕЗА С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ MYCOBACTERIUM TUBERCULOSIS ПРИ ВИЧ-ИНФЕКЦИИ | 2020 |
|
RU2750715C1 |
| Способ прогнозирования летального исхода у больных с ко-инфекцией туберкулез и COVID-19 | 2022 |
|
RU2797141C1 |
| Способ определения вероятности летального исхода у больного туберкулезом с ВИЧ-инфекцией при поступлении в стационар Федеральной службы исполнения наказаний РФ по двум лабораторным показателям | 2020 |
|
RU2742802C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТУБЕРКУЛЕЗА ЛЕГКИХ С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ | 2012 |
|
RU2504787C1 |
| Способ определения вероятности летального исхода на основании жалоб у больного туберкулезом с ВИЧ-инфекцией при поступлении в стационар Федеральной службы исполнения наказаний РФ | 2020 |
|
RU2765744C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОСТРОГО И ПОДОСТРОГО ИНФЕКЦИОННОГО ЭНДОКАРДИТА ПО ИММУННОМУ ПОКАЗАТЕЛЮ | 2017 |
|
RU2675264C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЫЖИВАЕМОСТИ В ПЕРВЫЕ 21 ДЕНЬ ГОСПИТАЛИЗАЦИИ С ЖЕЛУДОЧНО-КИШЕЧНЫМИ КРОВОТЕЧЕНИЯМИ ПРИ ВИЧ-ИНФЕКЦИИ И КО-ИНФЕКЦИИ ВИЧ/ТБ | 2024 |
|
RU2830137C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ АНТИРЕТРОВИРУСНОЙ ТЕРАПИИ ПРИ ВИЧ-ИНФЕКЦИИ | 2009 |
|
RU2414858C1 |
| СПОСОБ КОМПЛЕКСНОЙ ДИАГНОСТИКИ АКТИВНОГО ГЕНИТАЛЬНОГО ТУБЕРКУЛЕЗА У ЖЕНЩИН | 2011 |
|
RU2473089C1 |
Изобретение относится к медицине, а именно к инфекционным болезням, фтизиатрии и терапии. Раскрыт способ прогнозирования летального исхода при клиническом течении коинфекции ВИЧ-туберкулез, при котором у пациентов с выявленной множественной лекарственной устойчивостью Mycobacterium tuberculosis и известным количеством CD4-лимфоцитов проводят забор образцов венозной крови, выделение плазмы крови и иммуноферментный анализ с целью определения концентрации неспецифических общих иммуноглобулинов IgE в МЕ/мл, IgM в мг/мл, IgA в мг/мл и секреторного IgA в мг/л в плазме крови, вычисляют коэффициент предикции летального исхода (КП), равный отношению произведения их концентраций к количеству CD4-лимфоцитов в 1 мкл крови и при превышении этим коэффициентом значения 200 прогнозируют летальный исход с 56,7-кратным относительным риском. Изобретение позволяет прогнозировать неблагоприятный исход заболевания с высокой вероятностью и корректировать лечебную тактику ведения данной когорты больных, способствующую снижению летальности. 3 табл., 3 пр.
Способ прогнозирования летального исхода при клиническом течении коинфекции ВИЧ-туберкулез, характеризующийся тем, что у пациентов с выявленной множественной лекарственной устойчивостью Mycobacterium tuberculosis и известным количеством CD4-лимфоцитов проводят забор образцов венозной крови, выделение плазмы крови и иммуноферментный анализ с целью определения концентрации неспецифических общих иммуноглобулинов IgE в МЕ/мл, IgM в мг/мл, IgA в мг/мл и секреторного IgA в мг/л в плазме крови, вычисляют коэффициент предикции летального исхода (КП), равный отношению произведения их концентраций к количеству CD4-лимфоцитов в 1 мкл крови, и при превышении этим коэффициентом значения 200 прогнозируют летальный исход с 56,7-кратным относительным риском.
| ЗИМИНА В.Н | |||
| СОВЕРШЕНСТВОВАНИЕ ДИАГНОСТИКИ И ЭФФЕКТИВНОСТЬ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА У БОЛЬНЫХ ВИЧ-ИНФЕКЦИЕЙ ПРИ РАЗЛИЧНОЙ СТЕПЕНИ ИММУНОСУПРЕССИИ | |||
| Автореферат диссертации на соискание ученой степени доктора медицинских наук, Москва, 2012, стр.1-45 | |||
| Способ оценки тяжести состояния больного при ВИЧ-инфекции | 2017 |
|
RU2670652C2 |
| WO 2017207825 A1, 07.12.2017 | |||
| БАБАЕВА И.Ю | |||
| и др | |||
| Случай смерти от цирроза | |||
Авторы
Даты
2019-12-25—Публикация
2019-09-26—Подача