Область техники
Изобретение относится к медицине, а именно к производству биологических протезов клапанов сердца, предпочтительно на основе бычьего перикарда для сердечнососудистой хирургии с улучшенными механическими свойствами.
Уровень техники
Ксеногенные биологические протезы клапанов сердца на основе бычьего перикарда широко используются в мировой кардиохирургии (Zilla, P., Brink, J., Human, P., & Bezuidenhout, D. (2008). Prosthetic heart valves: Catering for the few. Biomaterials, 29(4), 385-406). Для предотвращения выраженного иммунного ответа и увеличения механической прочности биоткани, коллагеновую матрицу биопротеза стабилизируют глутаровым альдегидом (Manji, R.A., Zhu, L.F., Nijjar, N.К., Rayner, D.С, Korbutt, G.S., Churchill, T.A., Ross, D.B. (2006). Glutaraldehyde-Fixed Bioprosthetic Heart Valve Conduits Calcify and Fail From Xenograft Rejection. Circulation, 114(4), 318-327), но именно свободные альдегидные группы глутарового альдегида, не связавшиеся с белковой структурой коллагеновой матрицы, являются центрами инициации кальциноза (Sinha, P., Zurakowski, D., Susheel Kumar, Т.К., Не, D., Rossi, С, & Jonas, R.А. (2012). Effects of glutaraldehyde concentration, pretreatment time, and type of tissue (porcine versus bovine) on postimplantation calcification. The Journal of Thoracic and Cardiovascular Surgery, 143(1), 224-227). Для связывания свободных альдегидных групп предложено использовать хитозановые покрытия (Gallyamov, М.О., Chaschin, I.S., Khokhlova, М.A., Grigorev, Т.Е., Bakuleva, N.P., Lyutova, I G., Khokhlov, A.R. (2014). Collagen tissue treated with chitosan solutions in carbonic acid for improved biological prosthetic heart valves. Materials Science and Engineering: C, 37(1), 127-140).
В частности, из уровня техники известен способ модифицирования поверхности бычьего перикарда хитозаном из воды, насыщенной углекислым газом при высоком давлении (Патент RU 2519219). Способ позволяет повысить эффективность и сроки функционирования в организме биологического протеза клапана сердца за счет исключения возможности образования на его поверхности осадка кальция, улучшить эластичность, усилить антимикробные свойства. Однако, материал, описанный в прототипе характеризуется низкой прочностью.
Проблема создания биологических протезов нового поколения с существенно увеличенным сроком службы (порядка нескольких десятков лет) является нетривиальной задачей, решение которой позволит устанавливать протезы клапанов сердца, которые, с одной стороны, наилучшим образом будут воспроизводить работу собственного человеческого клапана и не будут требовать пожизненной антикоагулянтной терапии, в отличие от механических протезов, а с другой стороны, позволят снизить риск необходимости повторных операций по их замене, что важно для пациентов всех возрастных групп, а особенно, для лиц пожилого возраста, для которых существует высокий риск осложнений при повторных операциях.
Из уровня техники известны биологическая ткань из бычьего перикарда для изготовления биологических клапанов сердца и способ обработки бычьего перикарда, обеспечивающий увеличение биосовместимости биологической ткани и продолжительности ее срока службы (RU 2456023), при этом упомянутые преимущества обеспечиваются за счет физической плазменной обработки ткани с помощью плазменного газового метода, в котором в качестве ионизированного газа применяют азот, водород, аргон или, предпочтительно, кислород. Перед обработкой плазменным газовым методом ткань сушат, на ткань, подвергнутую плазменной обработке, наносят биосовместимое металлсодержащее покрытие, после плазменной обработки высушенный имплантат подвергают действию влаги. Металлсодержащее покрытие наносят посредством химического осаждения паров или газов в плазменной среде. Металлсодержащее покрытие выбирают из группы, состоящей из Ti, Та, Nb, Zr, Hf, Ir, Au, Pd, Pt, Ag и Cu.
Нанесение металлических покрытий на биологические ткани с помощью импульсного лазерного напыления описано в US 2012/0221099 Аl (прототип). Там же описана возможность нанесения покрытий из аморфного и алмазоподобного углерода на биологическую ткань при использовании соответствующей среды. При использовании данного подхода биологическая ткань помещается в специальную вакуумную камеру для импульсного лазерного напыления, где находится металлическая мишень, которую облучают лазерным пучком. В случае нанесения углеродных покрытий процесс двухстадийный и включает дополнительную стадию нанесения углеводородного слоя с использованием плазменного процесса. По мере продолжения процесса содержание водорода в плазменном полимере снижается до тех пор, пока углерод не будет присутствовать в форме алмаза. Данный способ нанесения металлических покрытий на биологические ткани достаточно сложный и требует специального оборудования. В тексте заявки отсутствуют данные о толщине наносимого покрытия, которые имеют значения при определении механических свойств материала и устойчивости покрытия на поверхности биоткани.
Раскрытие изобретения
Технической проблемой, решаемой изобретением, является создание биоматериала для изготовления протезов клапанов сердца на основе бычьего перикарда и способа получения биоматериала, лишенного недостатков перечисленных выше аналогов, и характеризующегося высокой прочностью и износостойкостью.
Техническим результатом, на достижение которого направлено заявленное изобретение, является получение биоматериала с контролируемыми механическими свойствами с сохранением эластичности, биосовместимости и антимикробных свойств при упрощении способа его получения.
Технический результат достигается нанесением на поверхность бычьего перикарда (перикарда биологического протеза клапана сердца) наноалмазного покрытия (пленки) от 1.5 до 4 мг наноалмазов на грамм ткани бычьего перикарда, со средним размером агрегатов наноалмазов от 17 до 28 нм, тем самым приводя к увеличению прочности материала, по сравнению с немодифицированным образцом. Нанесение наноалмазной пленки проводят из водной суспензии с концентрацией наноалмазов 1-1,5 г/л и размером наноалмазных агрегатов от 50 до 100 нм на поверхность перикарда биологического протеза клапана сердца. Используют наноалмазы детонационного синтеза (см. например, Ultrananocrystalline Diamond. Synthesis, Properties, and Applications. 2006. Ed. O.A. Shenderova, D.M. Gruen), обладающие положительным значением электрокинетического потенциала в воде. Полученный, таким образом материал обладает прочностью на разрыв 9-10 МПа, начальным модулем Юнга около 1 МПа и конечным модулем Юнга около 30 Мпа.
В одном из вариантов осуществления изобретения на поверхность наноалмаза может быть нанесен слой хитозана в количестве 20 мг/г.
Технический результат достигается также посредством реализации способа получения биометериала, включающего:
- приготовление водной суспензии наноалмазов детонационного синтеза с концентрацией наноалмазов 1-1,5 г/л из порошка наноалмазов посредством ее ультразвуковой обработки, с последующим испарением суспензии до сухого остатка и повторным ресуспендированием в воде с концентрацией наноалмазов 1-1.5 г/л с помощью ультразвуковой обработки;
- размещение бычьего перикарда в суспензии, перемешивание в течение 7-8 часов, выдерживание при 4°С в течение 10-12 часов;
- извлечение бычьего перикарда из суспензии, промывка его физиологическим раствором;
- хранение в физиологическом растворе при 4°С.
Ультразвуковую обработку осуществляют в течение 2-3 часов при мощности ультразвука 110 Вт и рабочей частоте 35 кГц. Перемешивание суспензии наноалмазов с размещенным в нем бычьим перикардом проводят на орбитальном шейкере со скоростью 190 оборотов/мин при комнатной температуре 20-25°С. При необходимости получения биоматериала с хитозановым покрытием, последний наносят на наноалмаз из раствора 1 г/л в 0,01 н соляной кислоте, для чего суспензию наноалмазов смешивают с раствором хитозана, полученную суспензию инкубируют в течение 48 часов при комнатной температуре (20-25°С), затем центрифугируют 30 минут при 13400 об/мин, декантируют осадок, промывают его водой и суспензируют в воде до концентрации 1-1,5 г/л.
Толщина нанесенной пленки наноалмаза определялась с помощью метода радиоактивных индикаторов. Полученная величина является оптимальной для получения заявленных механических свойств поскольку обеспечивается полное равномерное устойчивое покрытие поверхности биоткани.
Указанные в заявляемом способе точечные значения параметров при реализации изобретения могут иметь допустимое отклонение на величину не более 10%.
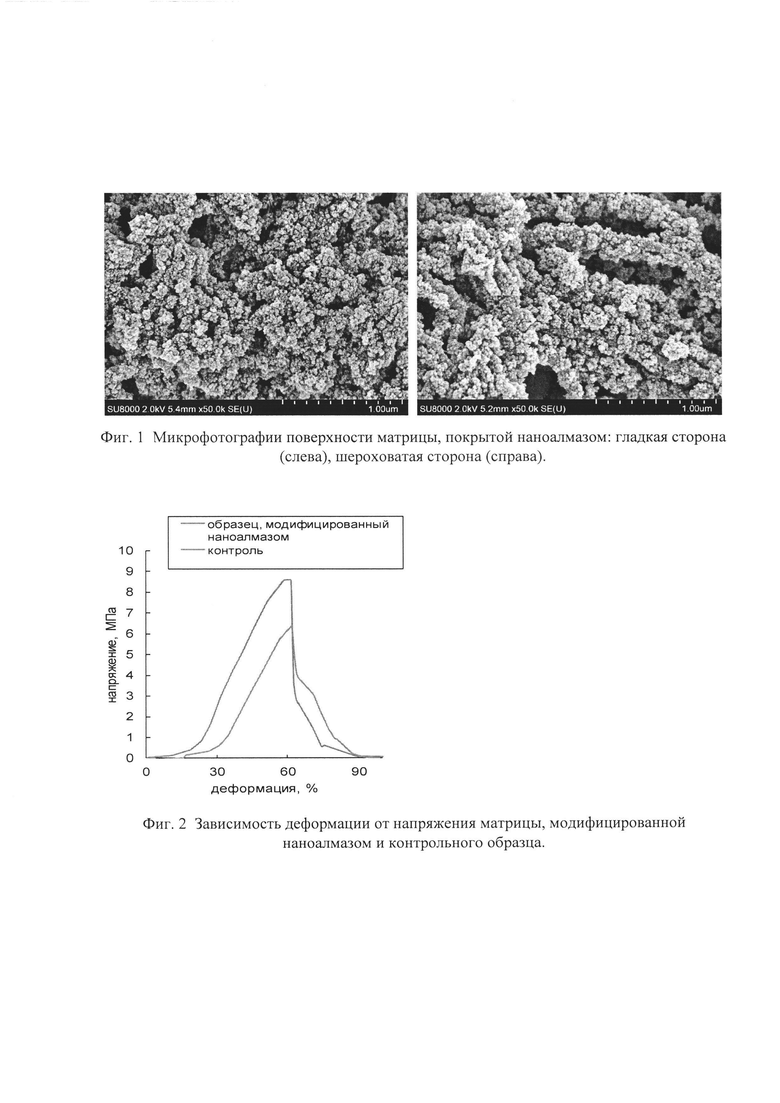
Краткое описание чертежей
Изобретение поясняется чертежами, где на фиг. 1 представлены микрофотографии поверхности матрицы, покрытой наноалмазом: гладкая сторона (слева), шероховатая сторона (справа); на фиг. 2 - зависимость деформации от напряжения матрицы, модифицированной наноалмазом и контрольного образца; на фиг. 3 - микрофотографии поверхности матрицы, покрытой наноалмазом, модифицированным хитозаном: гладкая сторона (слева), шероховатая сторона (справа); на фиг. 4 - зависимость деформации от напряжения матрицы, модифицированной наноалмазом с адсорбированным хитозаном и контрольного образца.
Осуществление изобретения
Настоящее изобретение поясняется примерами выполнения, которые не ограничивают сущность заявляемого решения, при этом наглядно демонстрируют возможность достижения заявляемого технического результата. В частности, возможность реализации изобретения продемонстрирована при использовании в качестве коллагеновой матрицы бычьего перикарда, при этом также возможно применение и тканей других животных, используемых для изготовления клапанов.
Подготовку наноалмазов проводят следующим образом. Готовят суспензию наноалмазов, для чего порошок наноалмазов суспендируют в воде (концентрация наноалмазов суспензии 5 г/л для достижения наилучшего разбиения агрегатов) с помощью ультразвуковой обработки, в течение 2-3 часов при мощности ультразвука 110 Вт (рабочая частота 35 кГц). Затем суспензию выдерживают при 4°С в течение 12-24 часов для осаждения крупных агрегатов. После этого надосадочную суспензию отбирают, высушивают с помощью роторного испарителя, определяют гравиметрически количество твердой фазы и повторно суспендируют в деионизированной воде до конечной концентрации 1-1,5 г/л с помощью ультразвуковой обработки при аналогичных режимах (в течение 2-3 часов, мощности ультразвука 110 Вт, рабочей частоте 35 кГц). Полученная суспензия характеризуется средним размером агрегатов, не превышающим 100 нм, по данным динамического рассеивания света и электрокинетическим потенциалом от +20 до 40 мВ. Двухстадийная ультразвуковая обработка позволяет получить суспензию наноалмазов воде с приведенными выше характеристиками без использования погружного источника ультразвука, который, во-первых, портится при контакте с наноалмазом и, во-вторых, его частички загрязняют получаемую суспензию.
Для дополнительного улучшения механических свойств полученного биоматериала на наноалмаз наносят слой хитозана из раствора 1 г/л в 0,01 н соляной кислоте. Суспензию наноалмазов смешивают с раствором хитозана. Полученную таким образом суспензию инкубируют в течение 48-72 часов при комнатной температуре (20-25°С), затем центрифугируют до полного осаждения наноалмазной фазы (30 минут при 13400 об/мин), декантируют осадок, промывают его водой и суспендируют в воде до концентрации твердой фазы 1-1,5 г/л. Полученная суспензия характеризуется средним размером агрегатов, не превышающим 100 нм, по данным динамического рассеивания света и электрокинетическим потенциалом от +35 до +45 мВ.
В водную суспензию наноалмазов или наноалмазов с хитозановым покрытием помещают перикард биологического протеза клапана сердца, перемешивают на орбитальном шейкере со скоростью 190 об./мин при комнатной температуре (20-25°С) в течение 7-8 часов, после этого выдерживают при 4°С в течение 10-12 часов. Затем биоматериал изымают из суспензии и промывают физиологическим раствором. Полученный продукт хранят в физиологическом растворе. Поскольку наноалмаз и наноалмаз с хитозановым покрытием обладает положительным электрокинетическим потенциалом, то полученная пленка равномерно покрывает и гладкую, и шероховатую поверхности перикарда биологического протеза клапана сердца и удерживается на его поверхности за счет электростатического взаимодействия. Полученный биоматериал характеризуется начальным модулем Юнга около 1 МПа и конечным модулем Юнга около 30 МПа, как и исходный материал, при этом прочность на разрыв увеличивается до 9-10 МПа по сравнению с 6 для исходного материала.
Пример 1. Перикард биологического протеза клапана сердца в виде матрицы площадью 30 см2 и толщиной 0,4-0,5 мм, предварительно обработанной 0,625% раствором глутарового альдегида и несколько раз тщательно промытой стерильным физиологическим раствором с 6-кратной сменой раствора из расчета 500-550 мл на 100 г перикарда, поместили в водную суспензию наноалмазов с концентрацией 1 мг/мл. Для определения количества наноалмаза на поверхности использовали меченный тритием наноалмаз. Суспензии перемешивали на орбитальном шейкере при комнатной температуре (20-25°С) в течение 7 часов, затем выдерживали суспензию с матрицей при 4°С в течение 12 часов. Затем матрицы изымали из суспензии и промывали физиологическим раствором. Полученный продукт хранили в физиологическом растворе. На фиг. 1 приведена микрофотография матрицы с нанесенным наноалмазом.
Размер агрегатов на поверхности матрицы составлял в среднем 17 нм. Для определения количества наноалмазов на поверхности матрицы ее разлагали азотной кислотой и измеряли радиоактивность. Получено, что общее количество наноаноалмазов на поверхности матрицы составляет 4 мг на грамм матрицы.
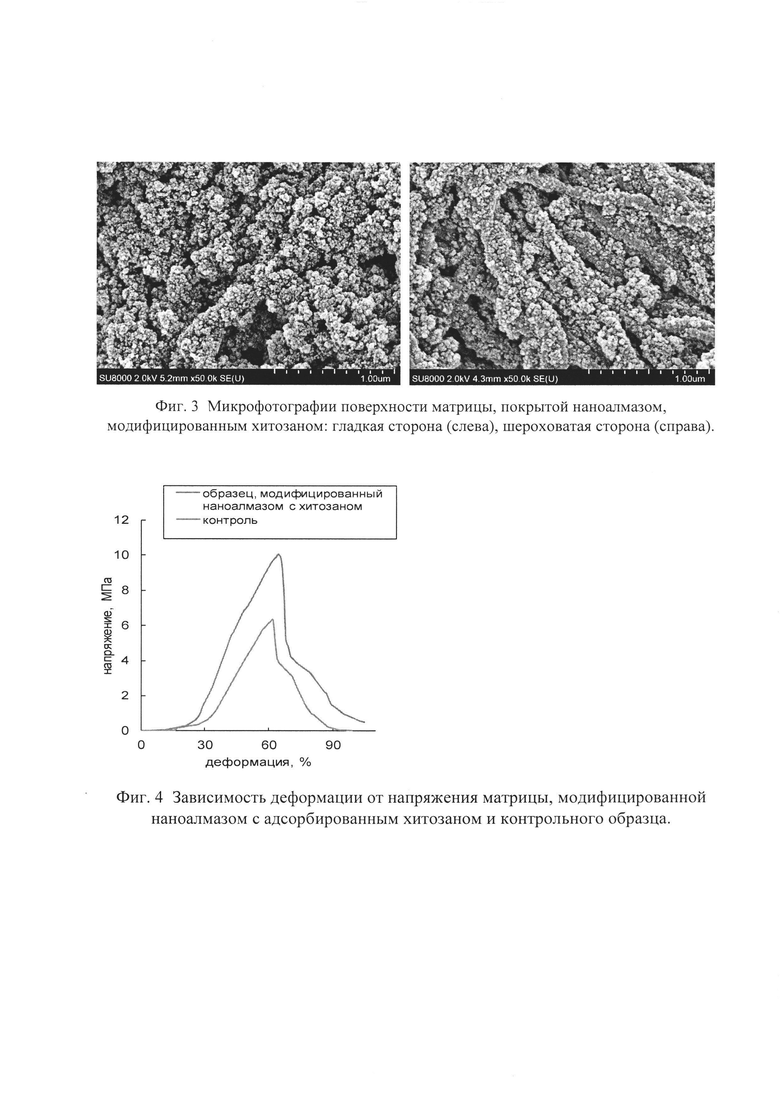
На фиг. 2 приведена зависимость деформации от напряжения для материала, модифицированного наноалмазом по сравнению с контрольным образцом - коллагеновой матрицей, модифицированной глутаровым альдегидом.
Как следует из фиг. 2 наноалмазное покрытие придает коллагеновой матрице дополнительную прочность. Если значения начального и конечного модуля Юнга одинаковы для обоих образцов и составляют 1 МПа и 20 МПа, соответственно, то прочность на разрыв образца с наноамалзным покрытием увеличивается до 9 МПа по сравнению с 6 МПа для необработанного образца.
Пример 2. В водную суспензию наноалмазов с нанесенным хитозановым покрытием с концентрацией наночастиц 1 мг/мл поместили коллагеновые матрицы, обработанные как описано в примере 1. Для определения количества наноалмаза на поверхности использовали меченный тритием наноалмаз. Суспензии перемешивали на орбитальном шейкере при комнатной температуре (20-25°С) в течение 7 часов, затем выдерживают суспензию с матрицей при 4°С в течение 12 часов. Затем матрицы изымали из суспензии и промывали физиологическим раствором. Полученный продукт хранили в физиологическом растворе. На фиг. 3 приведена микрофотография матрицы с нанесенным наноалмазом.
Размер агрегатов на поверхности матриц составлял в среднем 28 нм. Для определения количества наноалмазов на поверхности матрицы ее разлагали азотной кислотой и измеряли радиоактивность. Получено, что общее количество наноаноалмазов на поверхности матрицы составляет 1.5 мг на грамм матрицы.
На фиг. 4 приведена зависимость деформации от напряжения для материала, модифицированного наноалмазом, модифицированным хитозаном, по сравнению с контрольным образцом - коллагеновой матрицей, модифицированной глутаровым альдегидом.
Как следует из фиг. 4 наноалмазное покрытие придает коллагеновой матрице дополнительную прочность. Если значения начального и конечного модуля Юнга одинаковы для обоих образцов и составляют 1 МПа и 20 МПа соответственно, то прочность на разрыв образца с наноамалзным покрытием увеличивается до 10 МПа по сравнению с 6 МПа для необработанного образца.
Варьирование времени перемешивания суспензии наноалмазов и бычьего перикарда и инкубирования суспензии при 4°С в диапазоне параметров, приведенных в части «Осуществление изобретения», приводит к получению аналогичных результатов с точки зрения механических свойств продукта.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ обработки трансплантатов для сердечно-сосудистой хирургии с использованием суб- и сверхкритического диоксида углерода | 2022 |
|
RU2796364C1 |
| БИОЛОГИЧЕСКИЙ ПЕРИКАРДИАЛЬНЫЙ ПРОТЕЗ КЛАПАНА СЕРДЦА С ХИТОЗАНОВЫМ ПОКРЫТИЕМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2519219C1 |
| Способ стерилизации | 2012 |
|
RU2630979C2 |
| БИОМАТЕРИАЛ ДЛЯ ХИРУРГИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2780831C1 |
| ОРГАНОСПЕЦИФИЧЕСКИЙ БИОПЛАСТИЧЕСКИЙ МАТЕРИАЛ НА ОСНОВЕ РАСТВОРИМОЙ ФОРМЫ СТАБИЛИЗИРОВАННОГО ВНЕКЛЕТОЧНОГО МАТРИКСА | 2019 |
|
RU2722744C1 |
| БИОРЕЗОРБИРУЕМАЯ ГИДРОГЕЛЕВАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ С БИОЛОГИЧЕСКИ АКТИВНЫМИ ВЕЩЕСТВАМИ (ВАРИАНТЫ) | 2012 |
|
RU2519103C2 |
| СПОСОБ ОБРАБОТКИ БИОЛОГИЧЕСКОЙ ТКАНИ ЖИВОТНОГО ИЛИ ЧЕЛОВЕЧЕСКОГО ПРОИСХОЖДЕНИЯ, КАК, НАПРИМЕР, СВИНОГО ИЛИ БЫЧЬЕГО ПЕРИКАРДА ИЛИ СЕРДЕЧНЫХ КЛАПАНОВ ТРУПА ЧЕЛОВЕКА, И СООТВЕТСТВУЮЩИМ ОБРАЗОМ ОБРАБОТАННАЯ БИОЛОГИЧЕСКАЯ ТКАНЬ | 2008 |
|
RU2456023C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАТЕРИАЛА ДЛЯ ИСПОЛЬЗОВАНИЯ В ОФТАЛЬМОЛОГИИ "СКЛЕРОПЛАНТ" | 2005 |
|
RU2290899C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2014 |
|
RU2558089C1 |
| Способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии | 2023 |
|
RU2827028C1 |
Изобретение относится к медицине и раскрывает биоматериал для изготовления протезов клапанов сердца и способ его получения. Биоматериал включает бычий перикард, покрытый наноалмазами детонационного синтеза, обладающими положительным электрокинетическим потенциалом в воде, с содержанием наноалмаза от 1.5 до 4 мг на грамм биологической ткани, со средним размером агрегатов от 17 до 28 нм на поверхности биоматериала. Биоматериал характеризуется высокой прочностью и износостойкостью и предназначен для улучшения механических свойств материалов для изготовления искусственных клапанов сердца. 2 н. и 5 з.п. ф-лы, 4 ил., 2 пр.
1. Биоматериал для изготовления протезов клапанов сердца, включающий бычий перикард, покрытый наноалмазами детонационного синтеза, обладающими положительным электрокинетическим потенциалом в воде, с содержанием наноалмаза от 1,5 до 4 мг на грамм биологической ткани, со средним размером агрегатов от 17 до 28 нм на поверхности биоматериала.
2. Биоматериал по п. 1, характеризующийся тем, что он обладает прочностью на разрыв 9-10 МПа, начальным модулем Юнга около 1 МПа и конечным модулем Юнга около 30 МПа.
3. Биоматериал по п. 1, характеризующийся тем, что на поверхность наноалмаза нанесен слой хитозана в количестве 20 мг/г.
4. Способ получения биоматериала по п. 1, включающий
- приготовление водной суспензии наноалмазов детонационного синтеза с концентрацией наноалмазов 1-1,5 г/л из порошка наноалмазов посредством ее ультразвуковой обработки, с последующим испарением суспензии до сухого остатка и повторным ресуспендированием в воде с концентрацией наноалмазов 1-1,5 г/л с помощью ультразвуковой обработки;
- размещение бычьего перикарда в суспензии, перемешивание в течение 7-8 часов, выдерживание при 4°С в течение 10-12 часов;
- извлечение бычьего перикарда из суспензии, промывка его физиологическим раствором с последующим хранением в физиологическом растворе.
5. Способ по п. 4, характеризующийся тем, что ультразвуковую обработку осуществляют в течение 2-3 часов при мощности ультразвука 110 Вт и рабочей частоте 35 кГц.
6. Способ по п. 4, характеризующийся тем, что перемешивание суспензии наноалмазов с размещенным в нем бычьим перикардом проводят на орбитальном шейкере со скоростью 190 оборотов/мин при комнатной температуре 20-25°С.
7. Способ по п. 4, характеризующийся тем, что на наноалмаз наносят хитозан из раствора 1 г/л в 0,01 н соляной кислоте для чего суспензию наноалмазов смешивают с раствором хитозана, полученную суспензию инкубируют в течение 48 часов при комнатной температуре (20-25°С), затем центрифугируют 30 минут при 13400 об/мин, декантируют осадок, промывают его водой и суспензируют в воде до концентрации 1-1,5 г/л.
| US 20120221099 A1, 30.08.2012 | |||
| БИОЛОГИЧЕСКИЙ ПЕРИКАРДИАЛЬНЫЙ ПРОТЕЗ КЛАПАНА СЕРДЦА С ХИТОЗАНОВЫМ ПОКРЫТИЕМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2519219C1 |
| US 9248015 B2, 02.02.2016 | |||
| КАРПУХИН А.В | |||
| Наноалмаз детонационного синтеза: химическое модифицирование, свойства и возможные применения | |||
| Автореферат диссертации на соскание ученой сепени кандидата химических наук, 2012, Москва, 26 с. | |||
Авторы
Даты
2020-01-17—Публикация
2018-12-29—Подача