ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет на предварительно поданную заявку на патент США № 62/068181, поданную 24 октября 2014 г., полное содержание которой включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам биотехнологии и биологического производства рекомбинантных белков.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Клетки млекопитающих, содержащие нуклеиновую кислоту, которая кодирует рекомбинантный белок, часто применяют для получения белков, важных с терапевтической или коммерческой точки зрения. В сложившихся условиях процессов производства различных продуктов биотехнологическим компаниям все в большей степени приходится разрабатывать инновационные решения для очень гибкого и экономически эффективного производства терапевтических средств (например, лекарственных веществ на основе терапевтического белка).
В непрерывном процессе биологического производства зачастую необходимо удалять текучие среды из стерильного технологического сосуда. Удаление такой текучей среды может представлять собой либо непрерывный поток, либо прерывистый поток на основе некоторого предварительно заданного сигнала. Удаление необходимо осуществлять таким образом, чтобы защитить стерильность сосуда, из которого удаляется текучая среда. Это может представлять собой особую сложность в биологическом производстве, когда поток текучей среды обладает возможностью активировать биологический рост, который может, в конечном счете, постепенно разрастаться в стерильном технологическом сосуде. Основной способ, применяемый в настоящее время, представляет собой периодический способ передачи, в котором потоки отходов собираются во втором стерильном сосуде, и при полной вместимости данного сосуда он затем отсоединяется от стерильного технологического сосуда, и далее отходы выводятся. Данный процесс не является идеальным, поскольку он является периодическим (не непрерывным) и требуется большое количество времени для обработки и стерилизации сосудов. Такие манипуляции также могут приводить к возникновению факторов риска в процессе, если какая-либо стадия не будет выполнена. В качестве альтернативы, такой же процесс может быть осуществлен с предварительно простерилизованными мешками, однако, стоимость мешков может быть недопустимой для непрерывного процесса, и применение мешков не исключает возникновение факторов риска в процессе.
КРАТКОЕ ОПИСАНИЕ
Настоящее изобретение основано частично на разработке процесса выделения и связанного с ним аппаратного оборудования для обеспечения возможности периодического или непрерывного выделения потоков текучей среды (например, удаления) из стерилизованной системы (например, стерильного технологического сосуда), которая содержит стерильный технологический поток. В способе выделения применяют отделяющий сосуд для отделения стерильного технологического потока от окружающей среды и потоков отходов. Отделяющий сосуд является лишь частично заполненным и поддерживает свободное пространство в сосуде, при этом свободное пространство содержит стерилизующее средство. Стерилизующее средство (например, стерилизующий газ (например, газ, содержащий озон, этиленоксид, диоксид азота или выпаренный пероксид водорода)) может быть барботировано в сосуд или введено непосредственно в свободное пространство сосуда. Стерилизующее средство поддерживает стерилизующую атмосферу внутри свободного пространства сосуда, что обеспечивает выделение между входящим стерильным технологическим потоком и выходящим потоком текучей среды (например, потоком отходов). Концентрацию стерилизующего средства (например, стерилизующего газа) контролируют внутри свободного пространства сосуда для обеспечения необходимой стерилизующей атмосферы.
В одном аспекте согласно изобретению предложен способ предотвращения контаминации стерилизованной системы, при этом способ включает обеспечение системы, содержащей первый сосуд, при этом первый сосуд содержит жидкость, обеспечение течения первого объема жидкости из первого сосуда, причем через объем стерилизующего газа, во второй сосуд. Рассматриваемые в данном документе стерилизованные системы включают без ограничения системы биологического производства и системы фармацевтического производства. Первый сосуд представляет собой стерилизованный сосуд. В иллюстративных вариантах осуществления первый сосуд содержит компонент системы биологического производства. Например, первый сосуд может представлять собой (например, любой из иллюстративных биореакторов, описанных в данном документе или известных из уровня техники) один или несколько компонентов систем для хроматографии (например, хроматографическую колонку), один или несколько компонентов системы для микрофильтрации или один или несколько компонентов системы для ультрафильтрации/диафильтрации (UF/DF). Для системы биологического производства жидкость первого сосуда может представлять собой жидкую культуральную среду и/или жидкость, содержащую рекомбинантный терапевтический белок. В некоторых вариантах осуществления жидкость первого сосуда содержит клетку, содержащую рекомбинантный терапевтический белок. Рекомбинантный терапевтический белок может представлять собой белок, секретируемый из клетки или не секретируемый из клетки.
В некоторых аспектах стерилизующий газ выбирают из группы, состоящей из озона, этиленоксида, диоксида азота, выпаренного пероксида водорода (например, газа, содержащего озон, газа, содержащего этиленоксид, газа, содержащего оксид азота, и газа, содержащего перекись водорода).
Первый объем жидкости, протекающей из первого сосуда во второй сосуд, может представлять собой поток отходов. В другом аспекте первый объем жидкости, протекающей из первого сосуда во второй сосуд, содержит рекомбинантный терапевтический белок. В качестве альтернативы, первый объем жидкости, протекающей из первого сосуда во второй сосуд, не содержит рекомбинантный терапевтический белок (т. е. первый объем жидкости представляет собой поток отходов или содержит культуральную среду перед инициацией клеточной культуры). Первый объем жидкости может содержать побочные продукты ферментации.
В одном аспекте способы, раскрытые в данном документе, дополнительно включают обеспечение течения второго объема жидкости из второго сосуда в установку для очистки и доочистки рекомбинантного белка. Например, способ, раскрытый в данном документе, может дополнительно включать обеспечение течения второго объема жидкости из второго сосуда в первую систему для многоколоночной хроматографии (MCCS1), сбор указанного рекомбинантного терапевтического белка из жидкой культуральной среды с применением MCCS1, при этом элюат MCCS1, содержащий рекомбинантный терапевтический белок, непрерывно подают во вторую систему для многоколоночной хроматографии (MCCS2), и очистку и доочистку рекомбинантного терапевтического белка с применением MCCS2, при этом элюат из MCCS2 представляет собой рекомбинантный терапевтический белок; и при этом технологический процесс является совмещенным и осуществляется непрерывно от указанной жидкости в первом сосуде к элюату из MCCS2, который представляет собой рекомбинантный терапевтический белок. В некоторых вариантах осуществления второй объем жидкости содержит рекомбинантный белок.
В одном аспекте способы, раскрытые в данном документе, дополнительно включают обеспечение течения второго объема жидкости из второго сосуда в резервуар для размещения потока биологических отходов. Резервуар может представлять собой, например, приемник для размещения отходов, или химический стакан, или другой контейнер для хранения и/или удаления жидких отходов.
В раскрытии также предусмотрена система для выделения стерильных технологических потоков из нестерильных сред. В одном аспекте система содержит первый сосуд, содержащий выпускное отверстие для текучей среды; и по меньшей мере один второй сосуд, содержащий впускное отверстие для текучей среды, находящееся в сообщении по текучей среде с выпускным отверстием для текучей среды первого сосуда и выполненное таким образом, что текучая среда, входящая во второй сосуд, проходит через заполненное стерилизующим газом свободное пространство внутри второго сосуда, выпускное отверстие для текучей среды, выполненное таким образом, что текучая среда, выходящая из второго сосуда, удаляется ниже заполненного стерилизующим газом свободного пространства внутри второго сосуда, по меньшей мере одно впускное отверстие для газа и по меньшей мере одно выпускное отверстие для газа. В некоторых примерах первый сосуд представляет собой стерилизованный сосуд. В иллюстративном варианте осуществления первый сосуд представляет собой компонент системы биологического производства. Например, первый сосуд представляет собой трубку для текучей среды (например, любой из иллюстративных биореакторов, описанных в данном документе или известных из уровня техники), один или несколько компонентов систем для хроматографии (например, хроматографическую колонку), один или несколько компонентов системы для микрофильтрации или один или несколько компонентов системы для ультрафильтрации/диафильтрации. Биореактор представляет собой, например, перфузионный биореактор, биореактор периодического действия с подпиткой, производственный биореактор или биореактор для выращивания посевного материла. В некоторых вариантах осуществления выпускное отверстие для текучей среды второго сосуда находится в сообщении по текучей среде с установкой для очистки и доочистки рекомбинантного белка. В иллюстративном варианте осуществления первый сосуд и второй сосуд размещены на подставке.
В некоторых аспектах системы, раскрытые в данном документе, дополнительно содержат трубку для текучей среды, размещенную между первым сосудом и вторым сосудом, и, необязательно, дополнительно содержат фильтр, размещенный в трубке для текучей среды между первым сосудом и вторым сосудом и выполненный с возможностью удаления твердых частиц из текучей среды в трубке для текучей среды. Системы, раскрытые в данном документе, могут также содержать насосную систему (например, насос), при этом насосная система размещена в трубке для текучей среды. В некоторых примерах системы, раскрытые в данном документе, содержат насос в сообщении по текучей среде с выпускным отверстием для текучей среды первого сосуда, насос в сообщении по текучей среде с выпускным отверстием для текучей среды составного сосуда, или оба. В одном варианте осуществления насосная система выполнена с возможностью удаления объема текучей среды из выпускного отверстия сосуда и обеспечения течения объема во впускное отверстие для текучей среды второго сосуда.
В одном аспекте системы, раскрытые в данном документе, содержат заполненное стерилизующим газом свободное пространство внутри второго сосуда. Стерилизующий газ может представлять собой, например, газ, выбранный из группы, состоящей из озона, этиленоксида, диоксида азота или выпаренного пероксида водорода. В некоторых вариантах осуществления по меньшей мере одно впускное отверстие для газа присоединено к одному или нескольким барботирующим газ элементам, которые обеспечивают возможность выделения газа во второй сосуд и подачи в свободное пространство. Термин «барботирующий элемент» относится к пористому элементу (например, фильтру, открытой трубке или фритте) для барботирования газа через жидкость. С целью заполнения свободного пространства второй сосуд содержит по меньшей мере одно впускное отверстие для газа в сообщении по газовой фазе с системой для генерирования или доставки стерилизующего газа или для генерирования и доставки стерилизующего газа. В некоторых вариантах осуществления система для генерирования или доставки стерилизующего газа представляет собой систему генерирования или доставки озона или систему генерирования и доставки озона. В некоторых вариантах осуществления система для доставки стерилизующего газа представляет собой баллонный газ. Кроме того, в некоторых вариантах осуществления второй сосуд содержит по меньшей мере одно выпускное отверстие для газа, выполненное с возможностью непрерывного или периодического отведения газа из второго сосуда. Для систем с применением озона выпускное отверстие для газа находится в сообщении по газовой фазе с блоком разрушения озона. Для контроля концентрации или количества стерилизующего газа, содержащегося во втором сосуде, система может содержать, например, зонд или датчик для растворенного газа для отслеживания концентрации стерилизующего газа в свободном пространстве второго сосуда.
В одном аспекте первый сосуд содержит выпускное отверстие для текучей среды в сообщении по текучей среде с впускным отверстием для текучей среды второго сосуда. В иллюстративном варианте осуществления второй сосуд содержит впускное отверстие для текучей среды, выполненное таким образом, что объем жидкости, входящей во второй сосуд, проходит через свободное пространство (например, впускное отверстие для текучей среды, расположенное на втором сосуде в положении выше уровня жидкости), выпускное отверстие для текучей среды, выполненное таким образом, что жидкость, выходящая из второго сосуда, течет ниже заполненного стерилизующим газом свободного пространства (например, выпускного отверстия для текучей среды, расположенного на втором сосуде в положении ниже уровня жидкости), по меньшей мере одно впускное отверстие для газа и по меньшей мере одно выпускное отверстие для газа, при этом впускное отверстие для текучей среды находится в сообщении по текучей среде с первым сосудом. Преимущественно, объем стерилизующего газа размещен внутри свободного пространства второго сосуда. С целью заполнения свободного пространства стерилизующий газ может быть барботирован во второй сосуд или введен непосредственно в свободное пространство второго сосуда. В некоторых примерах второй сосуд по меньшей мере частично заполнен жидкостью.
В некоторых вариантах осуществления жидкость в первом сосуде содержит рекомбинантный терапевтический белок.
В контексте данного документа форма единственного числа существительного обозначает одно или несколько конкретных существительных. Например, выражение «рекомбинантная клетка млекопитающего» обозначает «одну или несколько рекомбинантных клеток млекопитающих».
Термин «сосуд» хорошо известен из уровня техники и означает устройство (например, контейнер) любой формы или размера с внутренним объемом, пригодным для удержания объема жидкости или газа. Сосуд может быть открытым (т. е. устройство, которое взаимодействует непосредственно с его окружающей средой) или закрытым (т. е. изолированное устройство, которое никак не взаимодействует с его окружающей средой). Термин «сосуд» включает, например, устройство с внутренним объемом, пригодным для культивирования ряда клеток (например, рекомбинантных клеток млекопитающих) в жидкой культуральной среде при контролируемой совокупности физических условий, которые обеспечивают возможность поддержания или пролиферации клеток. Неограничивающие примеры сосудов представляют собой трубки для текучей среды, биореакторы (например, любой из иллюстративных биореакторов, описанных в данном документе или известных из уровня техники), один или несколько компонентов систем для хроматографии (например, хроматографическую колонку), один или несколько компонентов системы для микрофильтрации, один или несколько компонентов системы для ультрафильтрации/диафильтрации, химические стаканы, приемники или пробирки.
Термин «стерилизация» известен из уровня техники и относится к любому утвержденному процессу, применяемому для получения стерильной композиции, например, процессу, который устраняет (удаляет) или уничтожает все формы жизни, включая возбудителей болезней, передающихся различным путем (таких как грибы, бактерии, вирусы, формы спор, т. д.), присутствующих на поверхности, содержащихся в текучей среде, в лекарственном препарате или в соединении, таком как биологическая культуральная среда. Стерилизации можно достигать путем применения тепла, химических соединений (например, газа), излучения, высокого давления или фильтрации или их комбинаций.
Термин «стерилизующий газ» в контексте данного документа относится к газу или газообразной композиции, обеспечивающим возможность получения стерильной композиции, например, в процессе, с помощью которого устраняют (удаляют) или уничтожают все формы жизни, включая возбудителей болезней, передающихся различным путем (таких как грибы, бактерии, вирусы, формы спор, т. д.), присутствующих на поверхности, содержащихся в текучей среде, в лекарственном препарате или в соединении, таком как биологическая культуральная среда.
«Абсолютная стерильность» или «абсолютно стерильный» являются терминами, применяемыми для описания композиции или процесса, который/которые полностью не включает/не включают самореплицирующиеся биологические контаминанты. Например, термин можно применять к гамма-облученным сосуду, внутренней поверхности и содержимому сосуда и/или буферу. Абсолютно стерильные композиция или процесс могут быть чистыми (как известен термин из уровня техники).
«Стерильный» или «стерильность» являются терминами, применяемыми для описания композиции или процесса, которые имеют гарантированный уровень стерильности приблизительно или менее 1,0×10-6 (например, приблизительно или менее 1,0×10-7, приблизительно или менее 1,0×10-8, приблизительно или менее 1,0×10-9 или 1×10-10). Определение того, являются ли композиция или процесс стерильными, можно исследовать с применением ряда утвержденных производственных процессов, известных из уровня техники. Например, стерильные композиция или процесс могут полностью не включать жизнеспособных самореплицирующихся биологических контаминантов (например, какого-либо из самореплицирующихся биологических контаминантов, описанных в данном документе). Стерильные композиция или процесс могут также быть чистыми (как известен термин из уровня техники). В стерильной клеточной культуре отсутствует контаминация.
Термин « гарантированный уровень стерильности» или «SAL» известен из уровня техники и означает уровень достоверности достижения абсолютной стерильности внутри партии обработанных единиц. Вероятность, как правило, рассчитывают на основе результатов исследований инактивации, осуществляемых во время проверки на достоверность и выражаемых в форме 1×10-n.
Термины «стерилизованный сосуд» и «стерильный технологический сосуд» являются взаимозаменяемыми и относятся к сосуду, который был подвержен процессу стерилизации. В контексте данного документа термины «стерилизованный сосуд» или «стерильный технологический сосуд» включают, например, сосуд, содержащий контролируемую монокультуру с биологической нагрузкой (например, контролируемую монокультуру с биологической нагрузкой рекомбинантных клеток млекопитающих). В контексте данного документа термин «стерильная система» относится к системе, содержащей набор одного или нескольких (например, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти или более) стерильных технологических сосудов, которые функционируют совместно для достижения конкретного результата (например, экспрессии и очистки рекомбинантного белка из жидкой культуральной среды). «Стерильная система» относится к системе из суммарно двух или более взаимосвязанных или переключающихся сосудов, при этом по меньшей мере один или несколько сосудов системы представляют собой стерилизованный сосуд.
В контексте данного документа термин «система биологического производства» или «система биопроизводства» относится к системе для получения биологического лекарственного средства. Термин «система фармацевтического производства» относится к системе для получения низкомолекулярного лекарственного средства (например, лекарственного средства, пролекарства или лекарственного продукта). Компоненты систем биологического производства и фармацевтических систем, рассматриваемые в данном документе, включают, например, один или несколько биореакторов для инициации культивирования и выращивания культур, колбы, трубки для текучей среды, сосуды, один или несколько компонентов систем для хроматографии (например, хроматографическую колонку, насосы, технологические сосуды), один или несколько компонентов системы для фильтрации (например, один или несколько компонентов системы для микрофильтрации или один или несколько компонентов системы для ультрафильтрации/диафильтрации) и другие устройства, применяемые для выделения и очистки лекарственного средства. Системы могут быть открытыми, закрытыми, совмещенными или непрерывными, как определено в данном документе, или как иным образом в целом понятны специалисту в данной области.
Термин «биологическое лекарственное средство» в контексте данного документа относится к любому терапевтическому веществу, произведенному или полученному из живого организма или его продуктов, которое применяют в предупреждении, диагностике или лечении патологии. Таким образом, биологическое лекарственное средство или биологический фармацевтический препарат представляет собой медицинское лекарственное средство, полученное с применением биотехнологии, например, белка (например, рекомбинантного терапевтического белка), или нуклеиновый кислоты (ДНК, РНК или антисмысловых олигонуклеотидов), применяемых для терапевтических или in vivo диагностических целей.
Термин «низкомолекулярное лекарственное средство» в контексте данного документа относится к терапевтическому средству с низкомолекулярной массой, которое применяют в предупреждении, диагностике или лечении патологии. Терапевтическое средство, как правило, синтезируют путем органической химии, но может также быть выделено из природных источников, таких как растения, грибы и микроорганизмы.
В контексте данного документа первый сосуд находится в «сообщении по газовой фазе» со вторым сосудом при соединении первого и второго сосудов посредством устройства или трубки, обеспечивающих возможность потока или сообщения по газовой фазе между сосудами. Подобным образом, первый сосуд находится в «сообщении по текучей среде» со вторым сосудом при соединении первого и второго сосудов посредством устройства или трубки, обеспечивающих возможность потока или сообщения по текучей среде между сосудами. В соответствии с идеями настоящего изобретения предполагается, что термины «сообщение по текучей среде» и «сообщение по газовой фазе» представляют собой синонимические термины. В этом отношении текучая среда предназначена включать вещество, либо жидкость, либо газ, выполненное с возможностью течения или прилегания к внешней границе его контейнера. В этом отношении не только жидкость подпадает под определение текучей среды, но также и газ, поскольку газ может течь и прилегать к внешней границе контейнера, внутри которого он присутствует.
Термин «перфузионный биореактор» известен из уровня техники и означает биореактор с внутренним объемом для культивирования ряда клеток (например, рекомбинантных клеток млекопитающих) в жидкой культуральной среде, и имеющий средство (например, выпускное отверстие, впускное отверстие, насос или другое такое устройство) для периодического или непрерывного удаления жидкой культуральной среды из биореактора, и имеющий средство (например, выпускное отверстие, впускное отверстие, насос или другое такое устройство) для добавления по существу такого же объема замещающей жидкой культуральной среды в биореактор. Добавление замещающей жидкой культуральной среды можно осуществлять по существу одновременно или вскоре после удаления жидкой культуральной среды из биореактора. Средство для удаления жидкой культуральной среды из биореактора и средство для добавления замещающей жидкой культуральной среды могут представлять собой одно устройство или систему.
Термин «производственный биореактор» является термином из области техники и означает биореактор большого масштаба (например, с внутренним объемом более 500 л, 1000 л, 5000 л, 10000 л, 20000 л, 50000 л или 100000 л). Например, производственный биореактор может представлять собой перфузионный биореактор.
Термин «биореактор периодического действия с подпиткой» является термином из области техники и означает биореактор, содержащий ряд клеток (например, рекомбинантных клеток млекопитающих) в первой жидкой культуральной среде, где культивирование клеток, присутствующих в биореакторе, включает периодическое или непрерывное добавление второй жидкой культуральной среды в первую жидкую культуральную среду без существенного или значительного удаления первой жидкой культуральной среды или второй жидкой культуральной среды из культуры клеток. Вторая жидкая культуральная среда может быть такой же, как и первая жидкая культуральная среда. В некоторых примерах культуры с периодической подпиткой вторая жидкая культуральная среда представляет собой концентрированную форму первой жидкой культуральной среды. В некоторых примерах культуры с периодической подпиткой вторую жидкую культуральную среду добавляют в виде сухого порошка.
Термин «система для многоколоночной хроматографии» или «MCCS» означает систему из суммарно двух или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Неограничивающим примером системы для многоколоночной хроматографии является система для периодической противоточной хроматографии (PCC), содержащая суммарно две или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Дополнительные примеры систем для многоколоночной хроматографии описаны в данном документе и известны из уровня техники.
Термин «клетка млекопитающего» означает любую клетку любого млекопитающего или любую клетку, полученную из любого млекопитающего (например, человека, хомячка, мыши, зеленой мартышки, крысы, свиньи, коровы или кролика). Например, клетка млекопитающего может представлять собой иммортализованную клетку. В некоторых вариантах осуществления клетка млекопитающего представляет собой дифференцированную клетку. В некоторых вариантах осуществления клетка млекопитающего представляет собой недифференцированную клетку. Неограничивающие примеры клеток млекопитающих описаны в данном документе. Дополнительные примеры клеток млекопитающих известны из уровня техники.
Термин «культивирование» или «культивирование клетки» означает поддержание или пролиферацию клетки млекопитающего (например, рекомбинантной клетки млекопитающего) при контролируемой совокупности физических условий.
Термин «культура клеток млекопитающих» или «культура клеток» означает жидкую культуральную среду, содержащую ряд клеток млекопитающих, которые поддерживают или пролиферируют при контролируемой совокупности физических условий.
Термин «жидкая культуральная среда» или «культуральная среда» означает текучую среду, которая содержит достаточно питательных веществ для обеспечения возможности роста или пролиферации клетки (например, клетки млекопитающего) in vitro. Например, жидкая культуральная среда может содержать одно или несколько из аминокислот (например, 20 аминокислот), пурина (например, гипоксантина), пиримидина (например, тимидина), холина, инозитола, тиамина, фолиевой кислоты, биотина, кальция, никотинамида, пиридоксина, рибофлавина, тимидина, цианокобаламина, пирувата, липоевой кислоты, магния, глюкозы, натрия, калия, железа, меди, цинка и бикарбоната натрия. В некоторых вариантах осуществления жидкая культуральная среда может содержать сыворотку от млекопитающего. В некоторых вариантах осуществления жидкая культуральная среда не содержит сыворотку или другой экстракт от млекопитающего (жидкая культуральная среда с определенным составом). В некоторых вариантах осуществления жидкая культуральная среда может содержать следы металлов, гормон роста млекопитающих и/или фактор роста млекопитающих. Другим примером жидкой культуральной среды является минимальная среда (например, среда, содержащая только неорганические соли, источник углерода и воду). Неограничивающие примеры жидкой культуральной среды описаны в данном документе. Дополнительные примеры жидкой культуральной среды известны из уровня техники и являются коммерчески доступными. Жидкая культуральная среда может содержать клетки млекопитающих при любой плотности. Например, в контексте данного документа некоторый объем жидкой культуральной среды, удаляемой из производственного биореактора, может по существу не содержать клеток млекопитающих.
Термины «рекомбинантный терапевтический белок» или «рекомбинантный белок» известен из уровня техники и означает любой терапевтический белок, полученный посредством технологии с применением рекомбинантной ДНК. В контексте данного документа «рекомбинантный терапевтический белок» включает, например, антитело или фрагмент антитела, фермент, сконструированный белок или иммуногенный белок или фрагмент белка.
Термин «фрагмент белка» или «фрагмент полипептида» означает часть полипептидной последовательности длиной по меньшей мере или приблизительно 4 аминокислоты, по меньшей мере или приблизительно 5 аминокислот, по меньшей мере или приблизительно 6 аминокислот, по меньшей мере или приблизительно 7 аминокислот, по меньшей мере или приблизительно 8 аминокислот, по меньшей мере или приблизительно 9 аминокислот, по меньшей мере или приблизительно 10 аминокислот, по меньшей мере или приблизительно 11 аминокислот, по меньшей мере или приблизительно 12 аминокислот, по меньшей мере или приблизительно 13 аминокислот, по меньшей мере или приблизительно 14 аминокислот, по меньшей мере или приблизительно 15 аминокислот, по меньшей мере или приблизительно 16 аминокислот, по меньшей мере или приблизительно 17 аминокислот, по меньшей мере или приблизительно 18 аминокислот, по меньшей мере или приблизительно 19 аминокислот или по меньшей мере или приблизительно 20 аминокислот или длиной более 20 аминокислот. Фрагмент рекомбинантного белка можно получить с применением каких-либо из процессов, описанных в данном документе.
Термин «сконструированный белок» означает полипептид, который в естественных условиях не кодируется эндогенной нуклеиновой кислотой, присутствующей в организме (например, млекопитающем). Примеры сконструированных белков включают ферменты (например, с одной или несколькими аминокислотными заменами, делециями, вставками или добавлениями, которые приводят к повышенной стабильности и/или каталитической активности сконструированного фермента), гибридные белки, антитела (например, бивалентные антитела, тривалентные антитела или диатело) и антигенсвязывающие белки, которые содержат по меньшей мере одну рекомбинантную каркасную последовательность.
Термин «совмещенный процесс» означает процесс, который осуществляют с применением структурных элементов, которые функционируют совместно для обеспечения определенного результата (например, получения выделенного рекомбинантного белка из жидкой культуральной среды).
Термин «непрерывный процесс» означает процесс, с помощью которого текучая среда непрерывно транспортируется по меньшей мере через часть системы.
Термин «фильтрация» означает удаление по меньшей мере части (например, по меньшей мере 80%, 90%, 95%, 96%, 97%, 98% или 99%) нежелательных биологических контаминантов (например, клетки млекопитающего, бактерий, дрожжевых клеток, вирусов или микобактерий) и/или твердых частиц (например, осажденных белков) из жидкости (например, жидкой культуральной среды или текучей среды, присутствующих в любой из систем или процессов, описанных в данном документе).
Термин «перфузионное культивирование» является термином из области техники и означает культивирование культуры клеток в сосуде (например, биореакторе), где культивирование культуры клеток в сосуде включает периодическое или постоянное удаление жидкой культуральной среды, присутствующей в сосуде (например, жидкой культуральной среды, которая по существу не содержит клетки), и одновременное или вскоре после этого добавление по существу такого же объема замещающей жидкой культуральной среды в сосуд. В некоторых примерах постепенно изменяют (например, повышают или снижают) объем жидкой культуральной среды, который удаляют, и объем замещающей культуральной среды, который и добавляют, в течение дискретных периодов (например, приблизительно 24-часового периода, периода, составляющего от приблизительно 1 минуты до приблизительно 24 часов, или периода, превышающего 24 часа) во время периода культивирования (например, скорость повторной подпитки культуральной средой ежесуточно). Фракция среды, которую удаляют и заменяют каждый день, может изменяться в зависимости от конкретных подлежащих культивированию клеток, исходной плотности посева и плотности клеток в конкретный момент времени. «RV» или «объем реактора» означает объем культуральной среды, имеющийся в начале процесса культивирования (например, общий объем культуральной среды, имеющийся после посева).
Термин «периодическое культивирование с подпиткой» является термином из области техники и означает сосуд (например, производственный биореактор), включающий ряд клеток (например, клеток млекопитающих) в жидкой культуральной среде, где культивирование клеток, присутствующих в сосуде (например, производственном биореакторе), включает периодическое или постоянное добавление свежей жидкой культуральной среды в сосуд без существенного или значительного удаления жидкой культуральной среды из сосуда во время культивирования. Свежая жидкая культуральная среда может быть такой же, как жидкая культуральная среда, присутствующая в сосуде в момент начала культивирования. В некоторых примерах периодического культивирования с подпиткой свежая жидкая культуральная среда представляет собой концентрированную форму жидкой культуральной среды, присутствующей в сосуде в момент начала культивирования. В некоторых примерах периодической культуры с подпиткой свежую культуральную среду добавляют в виде сухого порошка.
«Подставка» является термином из области техники и в контексте данного документа относится к трехмерной твердой структуре, которая может функционировать в качестве платформы или опоры для системы, описанной в данном документе. Если подставка содержит одну или несколько структур, которые обеспечивают движение (например, колесики, ролики и т. п.), она может придавать подвижность системе или ее части. Неограничивающие примеры подставок описаны в данном документе. Дополнительные примеры подставок известны из уровня техники.
Если не указано иное, все технические и научные термины, применяемые в данном документе, имеют такое же значение, которое обычно понятно специалисту в данной области, к которой относится настоящее изобретение. Способы и материалы описаны в данном документе для применения в настоящем изобретении; при этом также можно применять и другие подходящие способы и материалы, известные из уровня техники. Материалы, способы и примеры являются только иллюстративными и не предназначены для ограничения. Все публикации, патентные заявки, патенты, последовательности, записи в базах данных и другие ссылки, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. В случае противоречий настоящее описание, включая определения, будет иметь преимущественную силу.
Другие признаки и преимущества изобретения станут очевидными из нижеследующих подробного описания и фигур, а также из формулы изобретения.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фиг. 1 представлена схематическая диаграмма, иллюстрирующая типовую систему для выделения стерильных технологических потоков из нестерильных сред согласно настоящему изобретению.
На фиг. 2 представлена схематическая диаграмма, иллюстрирующая типовую систему для выделения стерильных технологических потоков из нестерильных сред согласно настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ
В данном документе предусмотрены процессы выделения и связанное с ними аппаратное оборудование для обеспечения возможности выделения потоков текучей среды из стерилизованной системы (например, стерильного технологического сосуда), которая содержит стерильный технологический поток. Процессы выделения, описанные в данном документе, обеспечивают множество преимуществ. Например, процессы выделения обеспечивают возможность периодического или непрерывного удаления потоков текучей среды из стерилизованной системы, что обеспечивает меньшее количество ручных манипуляций со стерилизованной системой и пониженный риск загрязнения стерилизованной системы. Например, процессы выделения, описанные в данном документе, обеспечивают периодическое или непрерывное удаление жидкости (например, потоков отходов, жидкости, содержащей рекомбинантные терапевтические белки) из биореактора, который, в свою очередь, обеспечивает меньшее количество ручных манипуляций с культурой клеток и пониженный риск загрязнения культуры клеток. Неограничивающие аспекты данных процессов выделения описаны в данном документе, и их можно применять в любой комбинации.
Способы, описанные в данном документе, включают обеспечение течения объемов текучей среды из первого сосуда во второй сосуд, обеспечение течения объемов текучей среды из третьего сосуда в четвертый сосуд или обеспечение течения объемов текучей среды из пятого сосуда в шестой сосуд. Как можно понять из уровня техники, имеется множество путей течения объема жидкости из первого сосуда во второй сосуд, таких как гравитационное течение или течение при помощи насоса. Таким образом, в некоторых аспектах системы, описанные в данном документе, могут также содержать один или несколько (например, два, три, четыре или пять) насосов (например, автоматических, например, автоматических перистальтических насосов). Один или несколько насосов могут быть размещены в трубке для текучей среды, размещенной между первым сосудом и вторым сосудом. Например, системы, описанные в данном документе, могут также содержать один или несколько насосов, выполненных с возможностью удаления объема текучей среды из выпускного отверстия первого сосуда и обеспечения течения объема во второй сосуд. В некоторых примерах один или несколько насосов выполнены с возможностью удаления объема текучей среды из выпускного отверстия стерильного технологического сосуда и обеспечения течения объема во впускное отверстие для текучей среды отделяющего сосуда, как описано в данном документе. В некоторых примерах один или несколько насосов находятся в сообщении по текучей среде по меньшей мере с одним выпускным отверстием для текучей среды отделяющего сосуда. Текучая среда может быть удалена из стерильного технологического сосуда при помощи насосной системы (например, системы фильтрации с переменным тангенциальным потоком (ATF) или фильтрации текучей среды с тангенциальным потоком (TFF)).
В некоторых примерах системы, описанные в данном документе, могут также содержать один или несколько (например, два, три, четыре или пять) фильтров для удаления нежелательных биологических контаминантов (например, клетки млекопитающего, бактерий, дрожжевых клеток, вирусов или микобактерий) и/или твердых частиц (например, осажденных белков) из жидкости (например, жидкой культуральной среды или текучей среды, присутствующих в любых из систем или процессов, описанных в данном документе).
В некоторых аспектах согласно изобретению предложены способы предотвращения контаминации стерилизованной системы, включающие обеспечение системы, содержащей первый сосуд, при этом первый сосуд содержит жидкость, обеспечение течения первого объема жидкости из первого сосуда, причем через объем стерилизующего газа, во второй сосуд.
В некоторых аспектах согласно изобретению предложены способы предотвращения контаминации стерилизованной системы, включающие обеспечение системы, содержащей первый сосуд, при этом первый сосуд содержит жидкость, обеспечение течения первого объема жидкости из первого сосуда, причем через объем стерилизующего газа, во второй сосуд. В некоторых примерах первый сосуд представляет собой стерильный технологический сосуд, при этом стерильный технологический сосуд содержит выпускное отверстие для текучей среды в сообщении по текучей среде с впускным отверстием для текучей среды второго сосуда. В некоторых примерах второй сосуд представляет собой отделяющий сосуд, как описано в данном документе, и объем стерилизующего газа размещен внутри свободного пространства отделяющего сосуда.
В некоторых аспектах согласно изобретению предложены системы для выделения стерильных технологических потоков от нестерильных сред. Для некоторых примеров система содержит стерильный технологический сосуд (например, первый сосуд), содержащий выпускное отверстие для текучей среды, и по меньшей мере один отделяющий сосуд (например, второй сосуд), при этом по меньшей мере один отделяющий сосуд содержит (i) впускное отверстие для текучей среды, находящееся в сообщении по текучей среде с выпускным отверстием для текучей среды первого сосуда и выполненное таким образом, что текучая среда, входящая во второй сосуд, проходит через заполненное стерилизующим газом свободное пространство внутри второго сосуда, (ii) выпускное отверстие для текучей среды, выполненное таким образом, что текучая среда, выходящая из второго сосуда, удаляется ниже заполненного стерилизующим газом свободного пространства внутри второго сосуда, (iii) по меньшей мере одно впускное отверстие для газа, и (iv) по меньшей мере одно выпускное отверстие для газа. В некоторых примерах системы, раскрытые в данном документе, дополнительно содержат трубку для текучей среды, размещенную между первым сосудом и вторым сосудом.
В процессах выделения, раскрытых в данном документе, применяют сосуд (т. е. «отделяющий сосуд») для выделения стерильного технологического потока из окружающей среды и потоков отходов. В некоторых примерах отделяющий сосуд содержит (i) впускное отверстие для текучей среды, находящееся в сообщении по текучей среде с выпускным отверстием для текучей среды стерильного технологического сосуда и выполненное таким образом, что текучая среда, входящая в отделяющий сосуд, проходит через заполненное стерилизующим газом свободное пространство внутри отделяющего сосуда, (ii) выпускное отверстие для текучей среды, выполненное таким образом, что текучая среда, выходящая из отделяющего сосуда, удаляется ниже заполненного стерилизующим газом свободного пространства внутри отделяющего сосуда, (iii) по меньшей мере одно впускное отверстие для газа, и (iv) по меньшей мере одно выпускное отверстие для газа.
Как можно понять из уровня техники, отделяющий сосуд может иметь целый ряд различных объемов. Например, отделяющий сосуд может иметь внутренний объем
от приблизительно 0,20 л до приблизительно 20 л (например, от приблизительно 0,20 л до приблизительно 18 л, от приблизительно 0,20 л до приблизительно 16 л, от приблизительно 0,20 л до приблизительно 14 л, от приблизительно 0,20 л до приблизительно 12 л, от приблизительно 0,20 л до приблизительно 10 л, от приблизительно 0,20 л до приблизительно 9,0 л, от приблизительно 0,20 л до приблизительно 8,0 л, от приблизительно 0,20 л до приблизительно 7,0 л, от приблизительно 0,20 л до приблизительно 6,0 л, от приблизительно 0,20 л до приблизительно 5,0 л, от приблизительно 0,20 л до приблизительно 4,0 л, от приблизительно 0,20 л до приблизительно 3,0 л, от приблизительно 0,20 л до приблизительно 2,0 л, от приблизительно 0,20 л до приблизительно 1,0 л, от приблизительно 0,50 л до приблизительно 18 л, от приблизительно 0,50 л до приблизительно 16 л, от приблизительно 0,50 л до приблизительно 14 л, от приблизительно 0,50 л до приблизительно 12 л, от приблизительно 0,50 л до приблизительно 10 л, от приблизительно 0,50 л до приблизительно 9,0 л, от приблизительно 0,50 л до приблизительно 8,0 л, от приблизительно 0,50 л до приблизительно 7,0 л, от приблизительно 0,50 л до приблизительно 6,0 л, от приблизительно 0,50 л до приблизительно 5,0 л, от приблизительно 0,50 л до приблизительно 4,0 л, от приблизительно 0,50 л до приблизительно 3,0 л, от приблизительно 0,50 л до приблизительно 2,0 л, от приблизительно 0,50 л до приблизительно 1,0 л, от приблизительно 1,0 л до приблизительно 20 л, от приблизительно 1,0 л до приблизительно 18 л, от приблизительно 1,0 л до приблизительно 16 л, от приблизительно 1,0 л до приблизительно 14 л, от приблизительно 1,0 л до приблизительно 12 л, от приблизительно 1,0 л до приблизительно 10 л, от приблизительно 1,0 л до приблизительно 9,0 л, от приблизительно 1,0 л до приблизительно 8,0 л, от приблизительно 1,0 л до приблизительно 7,0 л, от приблизительно 1,0 л до приблизительно 6,0 л, от приблизительно 1,0 л до приблизительно 5,0 л, от приблизительно 1,0 л до приблизительно 4,0 л, от приблизительно 1,0 л до приблизительно 3,0 л, от приблизительно 1,0 л до приблизительно 2,0 л, от приблизительно 1,0 л до приблизительно 1,0 л), или приблизительно 0,20 л, приблизительно 0,50 л, приблизительно 1,0 л, приблизительно 2,0 л, приблизительно 3,0 л, приблизительно 4,0 л, приблизительно 5,0 л, приблизительно 6,0 л, приблизительно 7,0 л, приблизительно 8,0 л, приблизительно 9,0 л, приблизительно 10,0 л, приблизительно 12,0 л, приблизительно 14,0 л, приблизительно 16,0 л, приблизительно 18,0 л или приблизительно 20,0 л.
Отделяющий сосуд является лишь частично заполненным и поддерживает свободное пространство в сосуде. Свободное пространство может содержать стерилизующее средство (например, стерилизующий газ). В некоторых примерах заполненное стерилизующим газом свободное пространство, содержащееся внутри отделяющего сосуда, охватывает от приблизительно 3% до приблизительно 97% общего внутреннего объема отделяющего сосуда; от приблизительно 5% до приблизительно 95% общего внутреннего объема отделяющего сосуда, например, от приблизительно 10% до приблизительно 90% общего внутреннего объема отделяющего сосуда; от приблизительно 15% до приблизительно 85% общего внутреннего объема отделяющего сосуда; от приблизительно 20% до приблизительно 80% общего внутреннего объема отделяющего сосуда; от приблизительно 25% до приблизительно 75% общего внутреннего объема отделяющего сосуда; от приблизительно 30% до приблизительно 70% общего внутреннего объема отделяющего сосуда; от приблизительно 35% до приблизительно 65% общего внутреннего объема отделяющего сосуда; от приблизительно 40% до приблизительно 60% общего внутреннего объема отделяющего сосуда; от приблизительно 45% до приблизительно 55% общего внутреннего объема отделяющего сосуда; или приблизительно 5% общего внутреннего объема отделяющего сосуда; приблизительно 10% общего внутреннего объема отделяющего сосуда; приблизительно 15% общего внутреннего объема отделяющего сосуда, приблизительно 20% общего внутреннего объема отделяющего сосуда; приблизительно 25% общего внутреннего объема отделяющего сосуда; приблизительно 30% общего внутреннего объема отделяющего сосуда; приблизительно 35% общего внутреннего объема отделяющего сосуда; приблизительно 40% общего внутреннего объема отделяющего сосуда; приблизительно 45% общего внутреннего объема отделяющего сосуда; приблизительно 50% общего внутреннего объема отделяющего сосуда; приблизительно 55% общего внутреннего объема отделяющего сосуда; приблизительно 60% общего внутреннего объема отделяющего сосуда; приблизительно 65% общего внутреннего объема отделяющего сосуда; приблизительно 75% общего внутреннего объема отделяющего сосуда; приблизительно 80% общего внутреннего объема отделяющего сосуда; приблизительно 85% общего внутреннего объема отделяющего сосуда; приблизительно 90% общего внутреннего объема отделяющего сосуда; или приблизительно 95% общего внутреннего объема отделяющего сосуда.
Иллюстративные стерилизующие газы для применения в системах и способах, раскрытых в данном документе, включают, например, газ озона, газ этиленоксида, газ диоксида азота и выпаренный пероксид водорода (например, газ, содержащий озон, газ, содержащий этиленоксид, газ, содержащий оксид азота, и газ, содержащий перекись водорода), или любую приемлемую смесь таких газов. В некоторых примерах стерилизующий газ, содержащийся внутри свободного пространства отделяющего сосуда, может поддерживаться, например, при температуре от приблизительно 15°C до приблизительно 70°C, от приблизительно 20°C до приблизительно 65°C, от приблизительно 25°C до приблизительно 60°C, от приблизительно 30°C до приблизительно 55°C, от приблизительно 35°C до приблизительно 50°C или от приблизительно 40°C до приблизительно 45°C.
Озон предоставляет много преимуществ в качестве стерилизующего газа. Озон представляет собой очень эффективное стерилизующее средство вследствие своих сильных окисляющих свойств, которые способны разрушать широкий диапазон патогенов, включая прионы. Высокая реактивность средств на основе озона, которые расходуют озон, может быть разрушена путем прохождения озона над простым катализатором, который обращает озон в кислород. Это также означает, что время цикла является относительно коротким. В некоторых примерах свободное пространство содержит озон, например, газ, содержащий озон, с концентрацией озона по меньшей мере приблизительно 3000 ppm, например, по меньшей мере приблизительно 4000 ppm, по меньшей мере приблизительно 5000 ppm, по меньшей мере приблизительно 6000 ppm, по меньшей мере приблизительно 7000 ppm, по меньшей мере приблизительно 8000 ppm, по меньшей мере приблизительно 9000 ppm, по меньшей мере приблизительно 10000 ppm, по меньшей мере приблизительно 15000 ppm, по меньшей мере приблизительно 20000 ppm, по меньшей мере приблизительно 50000 ppm, по меньшей мере приблизительно 100000 ppm, по меньшей мере приблизительно 500000 ppm или по меньшей мере приблизительно 1000000 ppm.
Этиленоксид обладает микробиоцидными свойствами и может уничтожать все известные вирусы, бактерии и грибы, включая бактериальные споры, и совместим с большей частью материалов (например, стерильными технологическими сосудами, применяемыми в процессах биологического производства). В некоторых примерах свободное пространство содержит этиленоксид, например, газ, содержащий этиленоксид, с концентрацией этиленоксида по меньшей мере приблизительно 500 ppm, например, по меньшей мере приблизительно 850 ppm, по меньшей мере приблизительно 1000 ppm, по меньшей мере приблизительно 2000 ppm, по меньшей мере приблизительно 3000 ppm, по меньшей мере приблизительно 4000 ppm, по меньшей мере приблизительно 5000 ppm, по меньшей мере приблизительно 6000 ppm, по меньшей мере приблизительно 7000 ppm, по меньшей мере приблизительно 8000 ppm, по меньшей мере приблизительно 9000 ppm, по меньшей мере приблизительно 10000 ppm, по меньшей мере приблизительно 15000 ppm, по меньшей мере приблизительно 20000 ppm, по меньшей мере приблизительно 50000 ppm, по меньшей мере приблизительно 100000 ppm, по меньшей мере приблизительно 500000 ppm или по меньшей мере приблизительно 1000000 ppm.
Газ диоксида азота (NO2) является эффективным в качестве стерилизатора, направленного против широкого диапазона микроорганизмов, включая известные бактерии, вирусы и споры. В некоторых примерах свободное пространство содержит диоксид азота, например, газ, содержащий диоксид азота, с концентрацией этиленоксида по меньшей мере приблизительно 500 ppm, по меньшей мере приблизительно 850 ppm, по меньшей мере приблизительно 1000 ppm, по меньшей мере приблизительно 2000 ppm, по меньшей мере приблизительно 3000 ppm, по меньшей мере приблизительно 4000 ppm, по меньшей мере приблизительно 5000 ppm, по меньшей мере приблизительно 6000 ppm, по меньшей мере приблизительно 7000 ppm, по меньшей мере приблизительно 8000 ppm, по меньшей мере приблизительно 9000 ppm, по меньшей мере приблизительно 10000 ppm, по меньшей мере приблизительно 15000 ppm, по меньшей мере приблизительно 20000 ppm, по меньшей мере приблизительно 50000 ppm, по меньшей мере приблизительно 100000 ppm, по меньшей мере приблизительно 500000 ppm или по меньшей мере приблизительно 1000000 ppm.
Перекись водорода (H2O2) обладает хорошими стерилизующими свойствами и может быть расщеплена на воду и кислород. В некоторых примерах свободное пространство содержит пероксид водорода, например, газ, содержащий пероксид водорода, с концентрацией этиленоксида по меньшей мере приблизительно 5 ppm, по меньшей мере приблизительно 5 ppm, по меньшей мере приблизительно 10 ppm, по меньшей мере приблизительно 50 ppm, по меньшей мере приблизительно 100 ppm, по меньшей мере приблизительно 250 ppm, по меньшей мере приблизительно 500 ppm, по меньшей мере приблизительно 850 ppm, по меньшей мере приблизительно 1000 ppm, по меньшей мере приблизительно 2000 ppm, по меньшей мере приблизительно 3000 ppm, по меньшей мере приблизительно 4000 ppm, по меньшей мере приблизительно 5000 ppm, по меньшей мере приблизительно 6000 ppm, по меньшей мере приблизительно 7000 ppm, по меньшей мере приблизительно 8000 ppm, по меньшей мере приблизительно 9000 ppm, по меньшей мере приблизительно 10000 ppm, по меньшей мере приблизительно 15000 ppm, по меньшей мере приблизительно 20000 ppm, по меньшей мере приблизительно 50000 ppm, по меньшей мере приблизительно 100000 ppm, по меньшей мере приблизительно 500000 ppm или по меньшей мере приблизительно 1000000 ppm.
Отделяющий сосуд может дополнительно содержать компонент для отслеживания концентрации стерилизующего средства (например, стерилизующего газа) внутри свободного пространства камеры с целью отслеживания стерилизующей атмосферы. Например, отделяющий сосуд может содержать датчик для отслеживания концентрации стерилизующего газа внутри свободного пространства или датчик (например, зонд для растворенного газа) для отслеживания концентрации растворенного газа жидкости, содержащейся в отделяющем сосуде.
В некоторых примерах заполненное жидкостью пространство внутри отделяющего сосуда представляет от приблизительно 3% до приблизительно 97% общего объема отделяющего сосуда; от приблизительно 5% до приблизительно 95% общего объема отделяющего сосуда; от приблизительно 10% до приблизительно 90% общего объема отделяющего сосуда; от приблизительно 15% до приблизительно 85% общего объема отделяющего сосуда; от приблизительно 20% до приблизительно 80% общего объема отделяющего сосуда; от приблизительно 25% до приблизительно 75% общего объема отделяющего сосуда; от приблизительно 30% до приблизительно 70% общего объема отделяющего сосуда; от приблизительно 35% до приблизительно 65% общего объема отделяющего сосуда; от приблизительно 40% до приблизительно 60% общего объема отделяющего сосуда; от приблизительно 45% до приблизительно 55% общего объема отделяющего сосуда; или приблизительно 5% общего объема отделяющего сосуда; приблизительно 10% общего объема отделяющего сосуда; приблизительно 15% общего объема отделяющего сосуда; приблизительно 20% общего объема отделяющего сосуда; приблизительно 25% общего объема отделяющего сосуда; приблизительно 30% общего объема отделяющего сосуда; приблизительно 35% общего объема отделяющего сосуда; приблизительно 40% общего объема отделяющего сосуда; приблизительно 45% общего объема отделяющего сосуда; приблизительно 50% общего объема отделяющего сосуда; приблизительно 55% общего объема отделяющего сосуда; приблизительно 60% общего объема отделяющего сосуда; приблизительно 65% общего объема отделяющего сосуда; приблизительно 75% общего объема отделяющего сосуда; приблизительно 80% общего объема отделяющего сосуда; приблизительно 85% общего объема отделяющего сосуда; приблизительно 90% общего объема отделяющего сосуда; или приблизительно 95% общего объема отделяющего сосуда.
Отделяющий сосуд может содержать по меньшей мере одно впускное отверстие для газа с целью введения стерилизующего газа в свободное пространство отделяющего сосуда. Как можно понять из уровня техники, имеется множество путей, при помощи которых газ может быть введен в свободное пространство сосуда. Например, газ может быть барботирован в сосуд или введен непосредственно в свободное пространство сосуда. Таким образом, по меньшей мере одно впускное отверстие для газа может быть присоединено к одному или нескольким барботирующим газ элементам, которые обеспечивают возможность выделения газа в отделяющий сосуд. Впускное отверстие для газа может находиться в сообщении по газовой фазе посредством трубки с системой для генерирования или доставки стерилизующего газа или для генерирования и доставки стерилизующего газа (например, озона, этиленоксида, диоксида азота, или выпаренного пероксида водорода). Например, впускное отверстие для газа может находиться в сообщении по газовой фазе с системой для генерирования озона, как хорошо известно из уровня техники.
Отделяющий сосуд может содержать по меньшей мере одно выпускное отверстие для газа, выполненное с возможностью непрерывного или периодического отведения газа из свободного пространства отделяющего сосуда. Как можно понять из уровня техники, выпускное отверстие для газа может быть выполнено с возможностью автоматического отведения газа, давление газа в свободном пространстве должно быть излишним. Выпускное отверстие для газа может находиться в сообщении по газовой фазе с блоком, выполненным с возможностью вмещения, разрушения или уменьшения количества стерилизующего газа. Например, выпускное отверстие для газа может находиться в сообщении по газовой фазе с блоком разрушения озона. Блоки разрушения озона известны из уровня техники и могут быть каталитическими, термическими, термокаталитическими или представлять собой активированный уголь. Каталитические блоки могут применять либо диоксид магния, либо быть покрыты алюминием с палладием и разрушать озон при температуре приблизительно 50°C. Термические блоки разрушения, как правило, работают при температуре приблизительно 120°C.
В некоторых примерах отделяющий сосуд, описанный в данном документе, содержит по меньшей мере одно впускное отверстие для текучей среды, находящееся в сообщении по текучей среде по меньшей мере с одним выпускным отверстием для текучей среды стерильного технологического сосуда и выполненное таким образом, что текучая среда, входящая в отделяющий сосуд, проходит через заполненное стерилизующим газом свободное пространство внутри отделяющего сосуда. В некоторых аспектах по меньшей мере одно впускное отверстие для текучей среды отделяющего сосуда находится в сообщении по текучей среде по меньшей мере с одним выпускным отверстием для текучей среды стерильного технологического сосуда посредством трубки для текучей среды.
В некоторых примерах отделяющий сосуд, описанный в данном документе, содержит по меньшей мере одно выпускное отверстие для текучей среды. Для некоторых иллюстративных конфигураций системы по меньшей мере одно выпускное отверстие для текучей среды отделяющего сосуда находится в сообщении по текучей среде с установкой для очистки и доочистки рекомбинантного белка. Таким образом, в некоторых аспектах способы, раскрытые в данном документе, включают обеспечение течения объема жидкости из отделяющего сосуда (например, второго сосуда) в установку для очистки и доочистки рекомбинантного белка.
Термин «очистка» означает стадию, осуществляемую для выделения рекомбинантного белка (например, рекомбинантного терапевтического белка) из одной или нескольких других примесей (например, объемных примесей) или компонентов, присутствующих в текучей среде, содержащей рекомбинантный белок (например, белков жидкой культуральной среды или одного или нескольких других компонентов (например, ДНК, РНК, других белков, эндотоксинов, вирусов и т. д.), присутствующих в клетке млекопитающего или секретируемых ею). Например, очистку можно осуществлять во время или после стадии первичного сбора. Очистку можно осуществлять с применением любого способа, известного из уровня техники, например, с применением смолы, мембраны или любой другой твердой подложки, которая связывает либо рекомбинантный белок, либо контаминанты (например, путем применения аффинной хроматографии, хроматографии гидрофобного взаимодействия, анионо- или катионообменной хроматографии или хроматографии на молекулярных ситах). Рекомбинантный белок можно очищать из текучей среды, содержащей рекомбинантный белок, с применением по меньшей мере одной хроматографической колонки и/или хроматографической мембраны (например, любой из хроматографических колонок или хроматографических мембран, описанных в данном документе).
Термин «доочистка» является термином из области техники и означает стадию, осуществляемую для удаления оставшихся следовых или небольших количеств контаминантов или примесей из текучей среды, содержащей рекомбинантный терапевтический белок, приближающий ее к окончательной необходимой чистоте. Например, доочистку можно осуществлять пропусканием текучей среды, содержащей рекомбинантный терапевтический белок, через хроматографическую(-ие) колонку(-и) или мембранный(-ые) поглотитель(-и), которые выборочно связываются либо с целевым рекомбинантным терапевтическим белком, либо с небольшими количествами контаминантов или примесей, присутствующих в текучей среде, содержащей рекомбинантный терапевтический белок. В таком примере элюат/фильтрат хроматографической(-их) колонки(-ок) или мембранного(-ых) поглотителя(-ей) содержит рекомбинантный терапевтический белок.
Например, согласно изобретению предложены способы, включающие обеспечение течения объема жидкости, содержащей рекомбинантный белок, из отделяющего сосуда (например, второго сосуда) в первую систему для многоколоночной хроматографии (MCCS1), сбор указанного рекомбинантного терапевтического белка из жидкой культуральной среды с применением MCCS1, при этом элюат MCCS1, содержащий рекомбинантный терапевтический белок, непрерывно подают во вторую систему для многоколоночной хроматографии (MCCS2); и очистку и доочистку рекомбинантного терапевтического белка с применением MCCS2, при этом элюат из MCCS2 представляет собой рекомбинантный терапевтический белок; и при этом технологический процесс является совмещенным и осуществляется непрерывно от указанного первого сосуда к элюату из MCCS2, который представляет собой рекомбинантный терапевтический белок.
Термин «система для многоколоночной хроматографии» или «MCCS» означает систему из суммарно двух или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Неограничивающим примером системы для многоколоночной хроматографии является система для периодической противоточной хроматографии (PCC), содержащая суммарно две или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Дополнительные примеры систем для многоколоночной хроматографии описаны в данном документе и известны из уровня техники.
Термин «сбор» означает стадию, осуществляемую для частичной очистки или выделения (например, обеспечения по меньшей мере или приблизительно 5%, например, по меньшей мере или приблизительно 10%, 15%, 20%, 25%, 30%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или по меньшей мере или приблизительно 95% чистоты по весу), концентрирования и стабилизации рекомбинантного белка (например, рекомбинантного терапевтического белка) от одного или нескольких других компонентов, присутствующих в жидкой культуральной среде или разбавленной жидкой культуральной среде (например, белков культуральной среды или одного или нескольких других компонентов (например, ДНК, РНК или других белков), присутствующих в клетке млекопитающего или секретируемых ею). Как правило, сбор осуществляют с применением смолы, которая связывает рекомбинантный белок (например, путем применения аффинной хроматографии). Неограничивающие способы сбора рекомбинантного белка из жидкой культуральной среды или разбавленной жидкой культуральной среды описаны в данном документе, а другие известны из уровня техники. Рекомбинантный белок можно собирать из жидкой культуральной среды с применением по меньшей мере одной хроматографической колонки и/или хроматографической мембраны (например, любой из хроматографических колонок и/или хроматографических мембран, описанных в данном документе).
Термин «элюат/фильтрат» является термином из области техники и означает текучую среду, которая выходит из хроматографической колонки или хроматографической мембраны, которая содержит выявляемое количество рекомбинантного белка (например, рекомбинантного терапевтического белка).
Термин «фильтрация» означает удаление по меньшей мере части (например, по меньшей мере 80%, 90%, 95%, 96%, 97%, 98% или 99%) нежелательных биологических контаминантов (например, клетки млекопитающего, бактерий, дрожжевых клеток, вирусов или микобактерий) и/или твердых частиц (например, осажденных белков) из жидкости (например, жидкой культуральной среды или текучей среды, присутствующих в любой из систем или процессов, описанных в данном документе).
Термины «секретируемый белок» или «секретируемый рекомбинантный белок» означают белок (например, рекомбинантный белок), который изначально содержит по меньшей мере одну сигнальную последовательность секреции при своей трансляции внутри клетки млекопитающего, и в результате по меньшей мере частичного ферментативного отщепления сигнальной последовательности секреции в клетке млекопитающего он секретируется по меньшей мере частично во внеклеточное пространство (например, жидкую культуральную среду). Квалифицированным специалистам-практикам будет понятно, что «секретированный» белок не должен быть полностью выделен из клетки, чтобы считаться секретированным белком.
Для некоторых иллюстративных конфигураций системы по меньшей мере одно выпускное отверстие для текучей среды отделяющего сосуда находится в сообщении по текучей среде с резервуаром для приема и/или размещения материала отходов (например, сосудом, приемником или блоком для размещения биологического технологического текучего материала, известного специалистам в данной области техники).
Процессы и системы выделения обеспечивают возможность выделения потоков текучей среды из сосуда стерилизованной системы (например, стерильного технологического сосуда), который содержит стерильный технологический поток. В некоторых примерах стерильный технологический сосуд содержит стерильный технологический поток и содержит по меньшей мере одно выпускное отверстие для текучей среды с целью удаления текучей среды из сосуда. Для процессов и систем, описанных в данном документе, по меньшей мере одно выпускное отверстие для текучей среды находится в сообщении по текучей среде по меньшей мере с одним впускным отверстием для текучей среды отделяющего сосуда, при этом впускное отверстие для текучей среды отделяющего сосуда выполнено таким образом, что текучая среда, входящая в отделяющий сосуд, проходит через заполненное стерилизующим газом свободное пространство внутри отделяющего сосуда.
Как можно понять из уровня техники, стерильный технологический сосуд может иметь целый ряд различных объемов. Например, стерильный технологический сосуд на стадии может иметь внутренний объем от приблизительно 0,50 л до приблизительно 200 л (например, от приблизительно 0,50 л до приблизительно 180 л, от приблизительно 0,50 л до приблизительно 160 л, от приблизительно 0,50 л до приблизительно 140 л, от приблизительно 0,50 л до приблизительно 120 л, от приблизительно 0,50 л до приблизительно 100 л, от приблизительно 0,50 л до приблизительно 90 л, от приблизительно 0,50 л до приблизительно 80 л, от приблизительно 0,50 л до приблизительно 70 л, от приблизительно 0,50 л до приблизительно 60 л, от приблизительно 0,50 л до приблизительно 50 л, от приблизительно 0,50 л до приблизительно 40 л, от приблизительно 0,50 л до приблизительно 30 л, от приблизительно 0,50 л до приблизительно 20 л, от приблизительно 0,50 л до приблизительно 10 л, от приблизительно 0,50 л до приблизительно 5,0 л, от приблизительно 1,0 л до приблизительно 200 л, от приблизительно 1,0 л до приблизительно 180 л, от приблизительно 1,0 л до приблизительно 160 л, от приблизительно 1,0 л до приблизительно 140 л, от приблизительно 1,0 л до приблизительно 120 л, от приблизительно 1,0 л до приблизительно 100 л, от приблизительно 1,0 л до приблизительно 90 л, от приблизительно 1,0 л до приблизительно 80 л, от приблизительно 1,0 л до приблизительно 70 л, от приблизительно 1,0 л до приблизительно 60 л, от приблизительно 1,0 л до приблизительно 50 л, от приблизительно 1,0 л до приблизительно 40 л, от приблизительно 1,0 л до приблизительно 30 л, от приблизительно 1,0 л до приблизительно 20 л, от приблизительно 1,0 л до приблизительно 10 л, от приблизительно 1,0 л до приблизительно 5,0 л, от приблизительно 1,5 л до приблизительно 200 л, от приблизительно 1,5 л до приблизительно 180 л, от приблизительно 1,5 л до приблизительно 160 л, от приблизительно 1,5 л до приблизительно 140 л, от приблизительно 1,5 л до приблизительно 120 л, от приблизительно 1,5 л до приблизительно 100 л, от приблизительно 1,5 л до приблизительно 90 л, от приблизительно 1,5 л до приблизительно 80 л, от приблизительно 1,5 л до приблизительно 70 л, от приблизительно 1,5 л до приблизительно 60 л, от приблизительно 1,5 л до приблизительно 50 л, от приблизительно 1,5 л до приблизительно 40 л, от приблизительно 1,5 л до приблизительно 30 л, от приблизительно 1,5 л до приблизительно 20 л, от приблизительно 1,5 л до приблизительно 10 л, от приблизительно 1,5 л до приблизительно 5,0 л, от приблизительно 2,0 л до приблизительно 200 л, от приблизительно 2,0 л до приблизительно 180 л, от приблизительно 2,0 л до приблизительно 160 л, от приблизительно 2,0 л до приблизительно 140 л, от приблизительно 2,0 л до приблизительно 120 л, от приблизительно 2,0 л до приблизительно 100 л, от приблизительно 2,0 л до приблизительно 90 л, от приблизительно 2,0 л до приблизительно 80 л, от приблизительно 2,0 л до приблизительно 70 л, от приблизительно 2,0 л до приблизительно 60 л, от приблизительно 2,0 л до приблизительно 50 л, от приблизительно 2,0 л до приблизительно 40 л, от приблизительно 2,0 л до приблизительно 30 л, от приблизительно 2,0 л до приблизительно 20 л, от приблизительно 2,0 л до приблизительно 10 л, от приблизительно 2,0 л до приблизительно 5,0 л, от приблизительно 2,5 л до приблизительно 200 л, от приблизительно 2,5 л до приблизительно 180 л, от приблизительно 2,5 л до приблизительно 160 л, от приблизительно 2,5 л до приблизительно 140 л, от приблизительно 2,5 л до приблизительно 120 л, от приблизительно 2,5 л до приблизительно 100 л, от приблизительно 2,5 л до приблизительно 90 л, от приблизительно 2,5 л до приблизительно 80 л, от приблизительно 2,5 л до приблизительно 70 л, от приблизительно 2,5 л до приблизительно 60 л, от приблизительно 2,5 л до приблизительно 50 л, от приблизительно 2,5 л до приблизительно 50 л, от приблизительно 2,5 л до приблизительно 40 л, от приблизительно 2,5 л до приблизительно 30 л, от приблизительно 2,5 л до приблизительно 20 л, от приблизительно 2,5 л до приблизительно 10 л, от приблизительно 2,5 л до приблизительно 5,0 л, от приблизительно 5,0 л до приблизительно 200 л, от приблизительно 5,0 л до приблизительно 180 л, от приблизительно 5,0 л до приблизительно 160 л, от приблизительно 5,0 л до приблизительно 140 л, от приблизительно 5,0 л до приблизительно 120 л, от приблизительно 5,0 л до приблизительно 100 л, от приблизительно 5,0 л до приблизительно 90 л, от приблизительно 5,0 л до приблизительно 80 л, от приблизительно 5,0 л до приблизительно 70 л, от приблизительно 5,0 л до приблизительно 60 л, от приблизительно 5,0 л до приблизительно 50 л, от приблизительно 5,0 л до приблизительно 40 л, от приблизительно 5,0 л до приблизительно 30 л, от приблизительно 5,0 л до приблизительно 20 л или от приблизительно 5,0 л до приблизительно 10 л).
В некоторых примерах сосуд, который содержит стерильный технологический поток, представляет собой компонент системы биологического производства. Компоненты систем биологического производства, рассматриваемые в данном документе, включают, например, колбу, трубку для текучей среды, биореактор, один или несколько компонентов систем для хроматографии (например, хроматографическую колонку), один или несколько компонентов системы для микрофильтрации или один или несколько компонентов системы для ультрафильтрации/диафильтрации.
В некоторых вариантах осуществления биореактор представляет собой перфузионный биореактор, биореактор периодического действия с подпиткой или производственный биореактор. Перфузионный биореактор может быть любым из иллюстративных перфузионных биореакторов, описанных в данном документе или известных из уровня техники. Например, перфузионный биореактор может быть изготовлен из нержавеющей стали или пластика (например, пластиковый стерильный мешок). Внутренняя поверхность перфузионного биореактора может иметь по меньшей мере одно покрытие (например, по меньшей мере одно покрытие из желатина, коллагена, поли-L-орнитина, полистирола и ламинина) и, как известно из уровня техники, одно или несколько отверстий для барботирования O2, CO2 и N2 в жидкую культуральную среду и устройство для перемешивания жидкой культуральной среды. Перфузионный биореактор также может быть оснащен механическим устройством, которое обеспечивает возможность удаления объема текучей среды (например, жидкой культуральной среды) из биореактора, и, необязательно, фильтром внутри механического устройства, который удаляет клетки из текучей среды во время процесса выведения текучей среды из биореактора (например, системой переменного тангенциального потока (ATF), системой для фильтрации в тангенциальном потоке (TFF) или системой фильтрации, описанной в предварительной заявке на патент США № 61/878502). Биореактор может быть оснащен одним или несколькими насосами и одним или несколькими резервуарами для удерживания удаленной текучей среды.
Объем жидкости можно удалять, например, с применением механической системы и/или путем пропускания или гравитационного течения объема через стерильную мембрану с отсечением по молекулярной массе, что исключает клетки млекопитающих, присутствующие в объеме.
Как можно понять из уровня техники, сосуд, который содержит стерильный технологический поток, может представлять собой любую установку, применяемую в уровне техники с целью культивирования клеток млекопитающих (например, колбу (например, колбу с мешалкой), вращающуюся пробирку или биореактор). Например, сосуд, который содержит стерильный технологический поток, может представлять собой любую установку, применяемую в области техники с целью культивирования рекомбинантных клеток млекопитающих. Сосуд может содержать внутреннее средство для перемешивания (например, мешалку), или сосуд можно встряхивать внешним образом (например, путем применения вращающей и/или качающей платформы). Сосуд может быть изготовлен из нержавеющей стали или пластика (например, пластиковый стерильный мешок). В некоторых вариантах осуществления сосуд может представлять собой биореактор одноразового применения (например, одноразовый биореактор MilliporeTM Mobius® Cellready объемом 3 л, одноразовый биореактор Pierre Guerin ATM1 NucleoTM объемом 20 л, одноразовый биореактор Sartorius Cultibag STRTM объемом 50 л, биореактор Sartorius Cultibag RMTM объемом 20 л, биореактор Sartorius Cultibag OrbitalTM объемом 50 л, биореактор GE Wave Bioreactor 2/10 System объемом 5 л, биореактор GE Wave Bioreactor 20/50 System объемом 25 л, биореактор GE Wave Bioreactor 200 System объемом 200 л или биореактор GE Wave Bioreactor 500/1000 System объемом 500 л). Внутренняя поверхность сосуда может иметь по меньшей мере одно покрытие (например, по меньшей мере одно покрытие из желатина, коллагена, поли-L-орнитина, полистирола и ламинина) и, как известно из уровня техники, одно или несколько отверстий для барботирования O2, CO2 и N2 в первую жидкую культуральную среду. Сосуд может быть оснащен одним или несколькими сенсорными датчиками. Если сосуд состоит из нежесткого пластического материала (например, пластиковый стерильный мешок), сосуд может быть связан с наружной опорой, которая окружает и поддерживает сосуд.
Рекомбинантная клетка млекопитающего может представлять собой клетку человека, мыши, хомячка или обезьяны. Например, рекомбинантная клетка млекопитающего может относиться к линии клеток, например, клеток яичника китайского хомячка (CHO) (например, клеток CHO DG44, клеток CHO-K1, клональных клеток C02.31, клональных клеток A14.13, клональных клеток C02.57 и клональных клеток F05.43), Sp2.0, клеток миеломы (например, NS/0), B-клеток, клеток гибридомы, T-клеток, эмбриональных клеток почки человека (HEK) (например, HEK 293E и HEK 293F), клеток почечного эпителия африканской зеленой мартышки (Vero) или клеток почечного эпителия собаки (коккер-спаниеля) Madin-Darby (MDCK).
Нуклеиновую кислоту, кодирующую рекомбинантный белок, можно вводить в клетку млекопитающего с получением рекомбинантной клетки млекопитающего с применением целого ряда способов, известных в области молекулярной биологии и молекулярной генетики. Неограничивающие примеры включают трансфекцию (например, липофекцию), трансдукцию (например, инфекцию лентивирусом, аденовирусом или ретровирусом) и электропорацию. В некоторых случаях нуклеиновая кислота, которая кодирует рекомбинантный белок, не интегрирована стабильно в хромосому рекомбинантной клетки млекопитающего (транзиентная трансфекция), в то время как в других рекомбинантных клетках млекопитающих нуклеиновая кислота интегрирована в хромосому. В качестве альтернативы или дополнения, нуклеиновая кислота, кодирующая рекомбинантный белок, может присутствовать в плазмиде и/или в искусственной хромосоме млекопитающего (например, человеческой искусственной хромосоме). В качестве альтернативы или дополнения, нуклеиновую кислоту можно вводить в клетку млекопитающего с помощью вирусного вектора (например, лентивирусного, ретровирусного или аденовирусного вектора). Нуклеиновая кислота может быть функционально связана с промоторной последовательностью (например, сильным промотором, таким как промотор β-актина и промотор CMV, или индуцируемым промотором). Вектор, содержащий нуклеиновую кислоту, может при необходимости также содержать селектируемый маркер (например ген, который придает клетке млекопитающего устойчивость к гигромицину, пуромицину или неомицину).
Жидкие культуральные среды (культуральные среды) известны из уровня техники. Жидкие культуральные среды могут быть дополнены сывороткой млекопитающего (например, эмбриональной телячьей сывороткой и бычьей сывороткой) и/или гормоном роста или фактором роста (например, инсулином, трансферрином и эпидермальным фактором роста). Любая из жидких культуральных сред, описанных в данном документе, может быть выбрана из группы, состоящей из жидкой культуральной среды, не содержащей компонентов животного происхождения, жидкой культуральной среды, не содержащей сыворотку, жидкой культуральной среды, содержащей сыворотку, жидкой культуральной среды с определенным химическим составом и жидкой культуральной среды, не содержащей белков. Неограничивающие примеры жидких культуральных сред с определенным химическим составом, жидких культуральных сред, не содержащих компонентов животного происхождения, жидких культуральных сред, не содержащих сыворотку, и жидких культуральных сред, содержащих сыворотку, являются коммерчески доступными.
Жидкая культуральная среда обычно содержит источник энергии (например углевод, такой как глюкоза), незаменимые аминокислоты (например, набор из двадцати основных аминокислот плюс цистеин), витамины и/или другие органические соединения, требуемые в низких концентрациях, свободные жирные кислоты и/или микроэлементы. Жидкие культуральные среды (например, первую и/или вторую жидкую культуральную среду) можно при необходимости дополнить, например, гормоном или фактором роста млекопитающих (например, инсулином, трансферрином или эпидермальным фактором роста), солями и буферами (например, солями кальция, магния и фосфатами), нуклеозидами и основаниями (например, аденозином, тимидином и гипоксантином), белком и тканевыми гидролизатами и/или любой комбинацией таких добавок.
Из уровня техники известны множество различных жидких культуральных сред, которые можно применять для культивирования клеток (например, клеток млекопитающих) в любой стадии любого из способов, описанных в данном документе. Компоненты среды, которые также можно применять в процессах по настоящему изобретению, включают без ограничения гидролизаты с известным химическим составом (CD), например, CD-пептон, CD-полипептиды (две или более аминокислоты) и CD-факторы роста. Дополнительные примеры жидкой культуральной среды для культуры тканей и компонентов среды известны из уровня техники.
Жидкую культуральную среду, полученную из культуры рекомбинантных клеток млекопитающих, можно фильтровать или очищать с получением жидкой культуральной среды, которая по существу не содержит клетки и/или вирусы. Способы фильтрации или очистки жидкой культуральной среды с целью удаления клеток известны из уровня техники (например, 0,2 мкм фильтрация, фильтрация с применением системы переменного тангенциального потока (ATFTM), системы фильтрации в тангенциальном потоке (TFF) или любой из систем, описанных в предварительной заявке на патент США № 61/878502). Рекомбинантные клетки также можно удалять из жидкой культуральной среды с применением центрифугирования и удаления отстоявшейся жидкости, которая представляет собой жидкую культуральную среду, которая по существу не содержит клетки, или путем обеспечения возможности оседания клеток на гравитационное дно контейнера (например, сосуда), содержащего жидкую культуральную среду, и удаления жидкой культуральной среды (жидкой культуральной среды, которая по существу не содержит клетки), которая расположена на некотором расстоянии от отстоявшихся рекомбинантных клеток млекопитающих. В некоторых вариантах осуществления одна или несколько (например, две, три или все) из первой культуральной среды, второй культуральной среды, третьей культуральной среды и четвертой культуральной среды идентичны.
Жидкая культуральная среда, применяемая на любой из стадий в любом из способов, описанных в данном документе, может представлять собой любой из типов жидкой культуральной среды, описанных в данном документе или известных из уровня техники. В любом из иллюстративных способов выделения рекомбинантного белка, описанных в данном документе, жидкую культуральную среду, полученную из культуры клеток-продуцентов, можно разводить путем добавления второй текучей среды (например, буфера).
Жидкую культуральную среду, содержащую рекомбинантный белок (например, рекомбинантный терапевтический белок), которая по существу не содержит клетки, можно хранить (например, при температуре ниже приблизительно 15°C (например, ниже приблизительно 10°C, ниже приблизительно 4°C, ниже приблизительно 0°C, ниже приблизительно -20°C, ниже приблизительно -50°C, ниже приблизительно -70°C или ниже приблизительно -80°C) в течение по меньшей мере 1 дня (например, по меньшей мере приблизительно 2 дней, по меньшей мере приблизительно 5 дней, по меньшей мере приблизительно 10 дней, по меньшей мере приблизительно 15 дней, по меньшей мере приблизительно 20 дней или по меньшей мере приблизительно 30 дней) перед выделением рекомбинантного белка (например, перед загрузкой жидкой культуральной среды в первую MCCS (например, первую PCCS)). В качестве альтернативы, в некоторых примерах жидкую культуральную среду, содержащую рекомбинантный белок, которая по существу не содержит клетки, подают в систему, применяемую для выделения рекомбинантного белка.
Рекомбинантный белок может представлять собой рекомбинантный терапевтический белок. Неограничивающие примеры рекомбинантных терапевтических белков, которые можно получить с помощью способов, представленных в данном документе, включают иммуноглобулины (в том числе легкие и тяжелые цепи иммуноглобулинов, антитела или фрагменты антител (например, любой из фрагментов антител, описанных в данном документе), ферменты (например, галактозидаза (например, альфа-галактозидаза), Myozyme® или Cerezyme®), белки (например, эритропоэтин человека, фактор некроза опухоли (TNF) или интерферон альфа или бета), или иммуногенные или антигенные белки или фрагменты белков (например, белки для применения в вакцине). Рекомбинантный терапевтический белок может представлять собой сконструированный антигенсвязывающий полипептид, который содержит каркас по меньшей мере одного многофункционального рекомбинантного белка (см., например, рекомбинантные антигенсвязывающие белки, описанные в Gebauer et al., Current Opin. Chem. Biol. 13:245-255, 2009; и публикацию заявки на патент США № 2012/0164066 (включенную в данный документ посредством ссылки во всей полноте)). Неограничивающие примеры рекомбинантных терапевтических белков, которые представляют собой антитела, включают: панитумумаб, омализумаб, абаговомаб, абциксимаб, актоксумаб, адалимумаб, адекатумумаб, афелимомаб, афутузумаб, алацизумаб, алацизумаб, алемтузумаб, алирокумаб, альтумомаб, аматуксимаб, аматуксимаб, анатумомаб, анрукинзумаб, аполизумаб, арцитумомаб, атинумаб, тоцилизумаб, базилизимаб, бектумомаб, белимумаб, бевацизумаб, безилезомаб, безлотоксумаб, бициромаб, канакинумаб, цертолизумаб, цетукцимаб, циксутумумаб, даклизумаб, деносумаб, денсумаб, экулизумаб, эдреколомаб, эфализумаб, эфунгумаб, эпратузумаб, эртумаксомаб, этарацизумаб, фигитумумаб, голимумаб, ибритутомаб тиуксетан, иговомаб, имгатузумаб, инфликсимаб, инолимомаб, инотузумаб, лабетузумаб, лебрикизумаб, моксетумомаб, натализумаб, обинутузумаб, ореговомаб, паливизумаб, панитумумаб, пертузумаб, ранибизумаб, ритуксимаб, тоцилизумаб, тозитумомаб, тралокинумаб, тукотузумаб, трастузумаб, велтузумаб, залутумумаб и затуксимаб. Дополнительные примеры рекомбинантных терапевтических антител, которые можно получить с помощью способов, описанных в данном документе, известны из уровня техники. Дополнительные неограничивающие примеры рекомбинантных терапевтических белков, которые можно получать с помощью способов по настоящему изобретению, включают: алглюкозидазу альфа, ларонидазу, абатацепт, галсульфазу, лютропин альфа, антигемофилический фактор, агалзидазу бета, интерферон бета-1a, дарбэпоэтин альфа, тенектеплазу, этанерцепт, фактор свертывания крови IX, фолликулостимулирующий гормон, интерферон бета-1a, имиглюцеразу, дорназу альфа, эпоэтин альфа, инсулин или аналоги инсулина, мекасермин, фактор VIII, фактор VIIa, антитромбин III, белок C, человеческий альбумин, эритропоэтин, гранулоцитарный колониестимулирующий фактор, гранулоцитарно-макрофагальный колониестимулирующий фактор, интерлейкин-11, ларонидазу, идурсульфазу, галсульфазу, ингибитор α-1-протеиназы, лактазу, аденозиндезаминазу, тканевой активатор плазминогена, тиреотропин альфа (например, Thyrogen®) и альтеплазу. Дополнительные примеры рекомбинантных белков, которые можно получать с помощью способов по настоящему изобретению, включают кислую α-глюкозидазу, залглюкозидазу альфа (например, Myozyme® и Lumizyme®), α-L-идуронидазу (например, Aldurazyme®), идуронат-сульфатазу, гепаран-N-сульфатазу, галактоза-6-сульфатазу, кислую β-галактозидазу, β-глюкоронидазу, N-ацетилглюкозамин-1-фосфотрансферазу, α-N-ацетилгалактозаминидазу, кислую липазу, лизосомальную кислую церамидазу, кислую сфингомиелиназу, β-глюкозидазу (например, Cerezyme® и Ceredase®), галактозилцерамидазу, α-галактозидазу-A (например, Fabrazyme®), кислую β-галактозидазу, β-галактозидазу, нейраминидазу, гексозаминидазу A и гексозаминидазу B.
Секретированный растворимый рекомбинантный белок можно извлекать из жидкой культуральной среды путем удаления или иного физического выделения жидкой культуральной среды из клеток (например, клеток млекопитающих). Множество различных способов удаления жидкой культуральной среды от клеток (например, клеток млекопитающих) известны из уровня техники, включая, например, центрифугирование, фильтрацию, перенесение с помощью пипетки и/или аспирацию. Затем секретированный рекомбинантный терапевтический белок можно извлекать и выделять из жидкой культуральной среды с применением различных биохимических методик, включая различные типы хроматографии (например, афинную хроматографию, хроматографию на молекулярных ситах, катионообменную хроматографию, хроматографию гидрофобного взаимодействия или анионообменную хроматографию) и/или фильтрацию (например, фильтрацию с отсечением по молекулярной массе).
Текучая среда может быть удалена из стерильного технологического сосуда путем непрерывного или периодического удаления. В некоторых примерах текучая среда, удаленная из стерильного технологического сосуда, содержит рекомбинантный белок. В некоторых примерах текучая среда, удаленная из стерильного технологического сосуда, содержит культуральную среду. В некоторых примерах текучая среда, удаленная из стерильного технологического сосуда, не содержит рекомбинантный белок.
ПРИМЕРЫ
Настоящее изобретение далее описывается в следующих примерах, которые не ограничивают объем изобретения, описанный в формуле изобретения.
Пример 1
На фиг. 2 описана типовая система для выделения стерильных технологических потоков из нестерильных сред согласно настоящему изобретению. Система может быть любым стерильным процессом, включая, например компонент технологического потока биологического производства. Как продемонстрировано на фиг. 2, система содержит стерильный технологический сосуд (110) (например, первый сосуд), содержащий выпускное отверстие (130) для текучей среды. Для технологического потока биологического производства первый сосуд может представлять собой, например, трубку для текучей среды для обеспечения течения жидкой среды, биореактор (например, любой из иллюстративных биореакторов, описанных в данном документе или известных из уровня техники), один или несколько компонентов систем для хроматографии (например, хроматографическую колонку), один или несколько компонентов системы для микрофильтрации или один или несколько компонентов системы для ультрафильтрации/диафильтрации. Система, описанная на фиг. 2, дополнительно содержит отделяющий сосуд (120) (например, второй сосуд), содержащий впускное отверстие (140) для текучей среды, находящееся в сообщении по текучей среде посредством трубки (210) для текучей среды с выпускным отверстием (130) для текучей среды первого сосуда (110) и выполненное таким образом, что текучая среда, входящая во второй сосуд, проходит через заполненное стерилизующим газом свободное пространство (150) внутри второго сосуда (120), выпускное отверстие (170) для текучей среды, выполненное таким образом, что текучая среда, выходящая из второго сосуда, удаляется ниже заполненного стерилизующим газом свободного пространства (150) внутри второго сосуда (120). Второй сосуд содержит по меньшей мере одно впускное отверстие (180) для газа для подачи стерилизующего газа посредством трубки (220) для газа с целью заполнения свободного пространства второго сосуда. Второй сосуд также содержит по меньшей мере одно выпускное отверстие (160) для газа, выполненное с возможностью непрерывного или периодического отведения газа из выделения.
На фиг. 1 предусмотрен иллюстративный вариант осуществления для выделения стерильных технологических потоков из нестерильных сред согласно настоящему изобретению. Для системы, описанной на фиг. 1, потоки отходов из стерильного технологического сосуда (например, первого сосуда, не показанного) находятся в сообщении по текучей среде с отделяющим сосудом (например, вторым сосудом), при этом отделяющий сосуд выполнен таким образом, что текучая среда входит в верхнюю часть второго сосуда и проходит через заполненное стерилизующим газом свободное пространство внутри второго сосуда. Второй сосуд дополнительно содержит выпускное отверстие для текучей среды, выполненное таким образом, что текучая среда, выходящая из второго сосуда, удаляется ниже заполненного стерилизующим газом свободного пространства (т. е. внизу заполненной текучей средой части второго сосуда) внутри второго сосуда. На фиг. 2 дополнительно продемонстрирована насосная система, содержащая насос, выполненный с возможностью удаления объема текучей среды через выпускное отверстие второго сосуда и обеспечения течения объема через резервуар для размещения потока биологических отходов. Второй сосуд содержит по меньшей мере одно впускное отверстие для газа в сообщении по газовой фазе с системой для генерирования или доставки стерилизующего газа или для генерирования и доставки стерилизующего газа (например, системой для генерирования озона) с целью заполнения свободного пространства второго сосуда. Согласно данному варианту осуществления стерилизующий газ барботируется во второй сосуд. Второй сосуд также содержит по меньшей мере одно выпускное отверстие для газа, выполненное с возможностью непрерывного или периодического отведения газа из выделения.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Следует понимать, что, хотя настоящее изобретение было описано во взаимосвязи с его подробным описанием, вышеупомянутое описание предназначено для иллюстрации и не ограничивает объем изобретения, который определен объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации находятся в пределах объема нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА РЕКОМБИНАНТНОГО ТЕРАПЕВТИЧЕСКОГО БЕЛКА | 2020 |
|
RU2790876C2 |
| ПРОЦЕССЫ КУЛЬТИВИРОВАНИЯ В СИСТЕМЕ ПОСЕВНЫХ ФЕРМЕНТЕРОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2786997C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ В СИСТЕМЕ ПОСЕВНЫХ ФЕРМЕНТЕРОВ (ВАРИАНТЫ) | 2015 |
|
RU2694327C2 |
| СТЕРИЛЬНАЯ СМОЛА ДЛЯ ХРОМАТОГРАФИИ И ЕЕ ПРИМЕНЕНИЕ В СПОСОБАХ ПРОИЗВОДСТВА | 2019 |
|
RU2809157C2 |
| ИЗМЕРЕНИЕ АТРИБУТА КАЧЕСТВА ПРОДУКТА | 2020 |
|
RU2825307C1 |
| КОНТРОЛИРОВАНИЕ ОБРАЗОВАНИЯ ДИСУЛЬФИДНЫХ СВЯЗЕЙ В БЕЛКОВЫХ РАСТВОРАХ С ПОМОЩЬЮ ДОБАВЛЕНИЯ ВОССТАНАВЛИВАЮЩИХ СРЕДСТВ | 2015 |
|
RU2721592C2 |
| СПОСОБЫ ПЕРФУЗИОННОГО КУЛЬТИВИРОВАНИЯ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2733539C2 |
| СПОСОБЫ ПЕРФУЗИОННОГО КУЛЬТИВИРОВАНИЯ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2708919C2 |
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ ЖИЗНЕСПОСОБНОСТИ КЛЕТОК | 2019 |
|
RU2786815C2 |
| ИНТЕГРИРОВАННОЕ НЕПРЕРЫВНОЕ ПРОИЗВОДСТВО ТЕРАПЕВТИЧЕСКИХ БЕЛКОВЫХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ | 2014 |
|
RU2662929C2 |
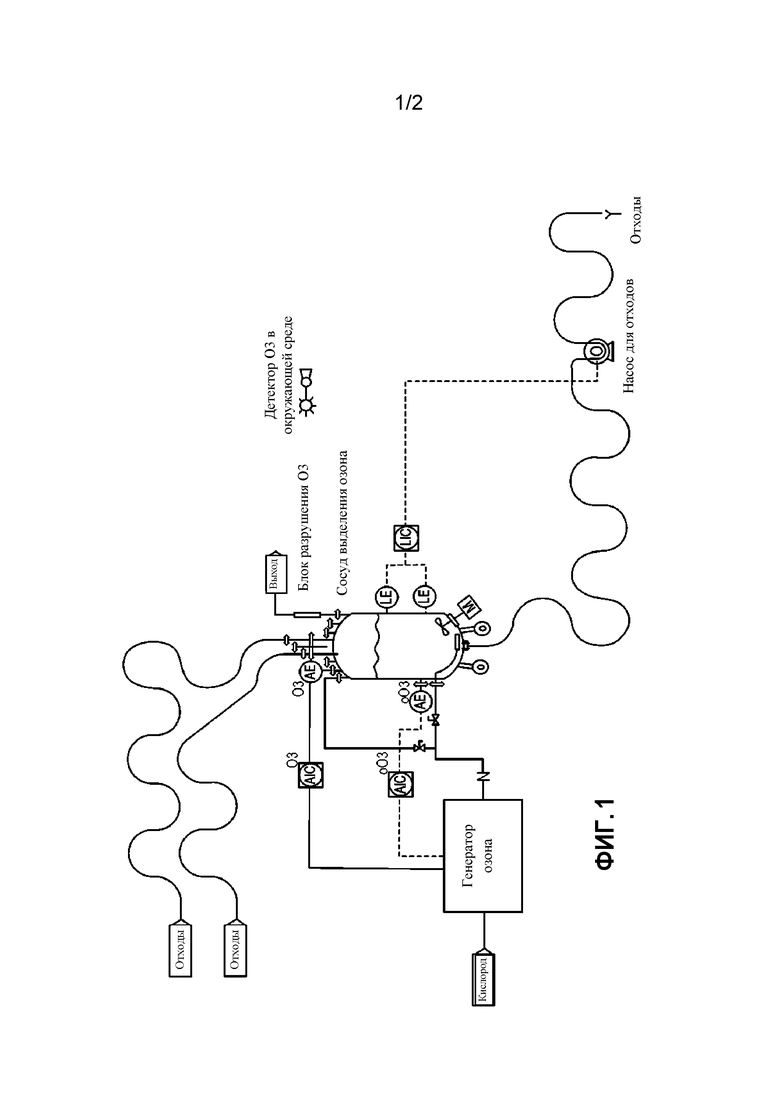
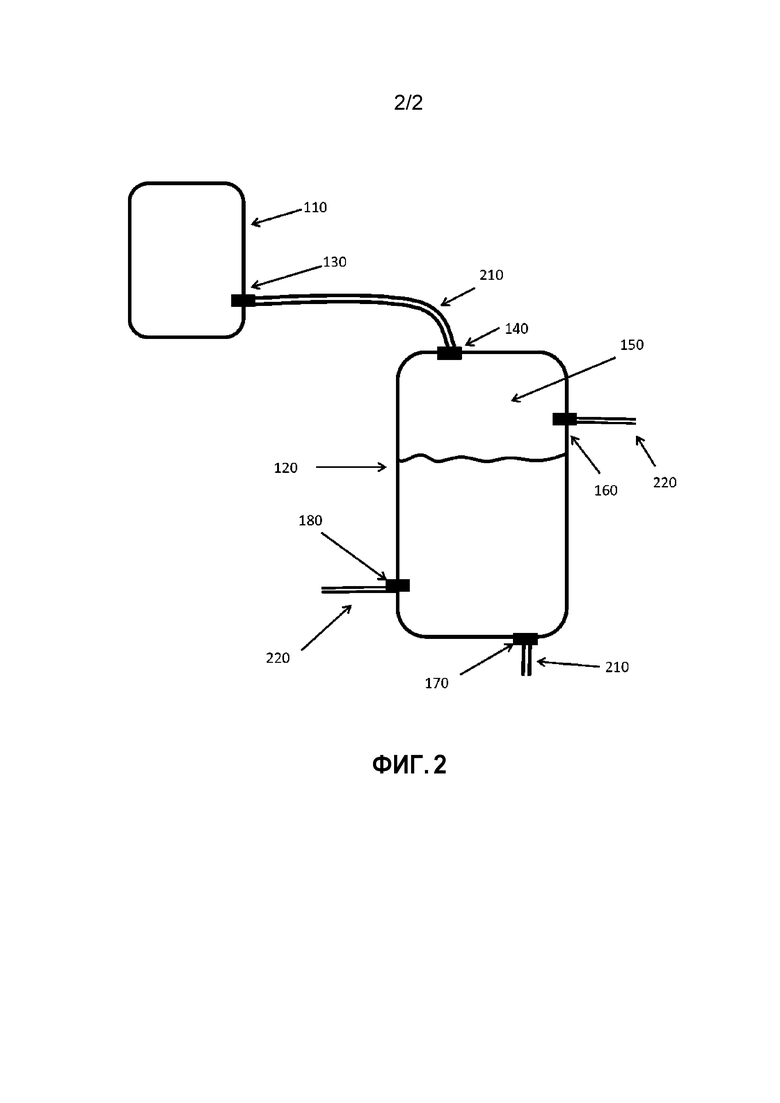
Изобретение относится к области биотехнологии, в частности к биотехнологическому производству рекомбинантных белков. Способ предотвращения контаминации системы предусматривает процессы выделения и связанное с ними аппаратное оборудование для обеспечения возможности выделения потоков текучей среды из системы, например стерильного технологического сосуда, которая содержит стерильный технологический поток. Способ включает обеспечение системы, содержащей первый сосуд и второй сосуд, при этом первой сосуд содержит жидкость, а второй сосуд содержит объем стерилизующего газа, обеспечение течения первого объема жидкости из первого сосуда во второй сосуд через объем стерилизующего газа, содержащийся в верхней части второго сосуда. Процессы выделения обеспечивают возможность непрерывного удаления потоков текучей среды, в частности потоков отходов, жидкости, содержащей рекомбинантные терапевтические белки из системы, например системы биологического производства, что обеспечивает меньшее количество ручных манипуляций со стерилизованной системой и пониженный риск загрязнения стерилизованной системы. Изобретение обеспечивает повышение эффективности и удобства предотвращения контаминации при одновременном сохранении требуемого качества стерильности сосудов и снижении материальных затрат. 17 з.п. ф-лы, 2 ил.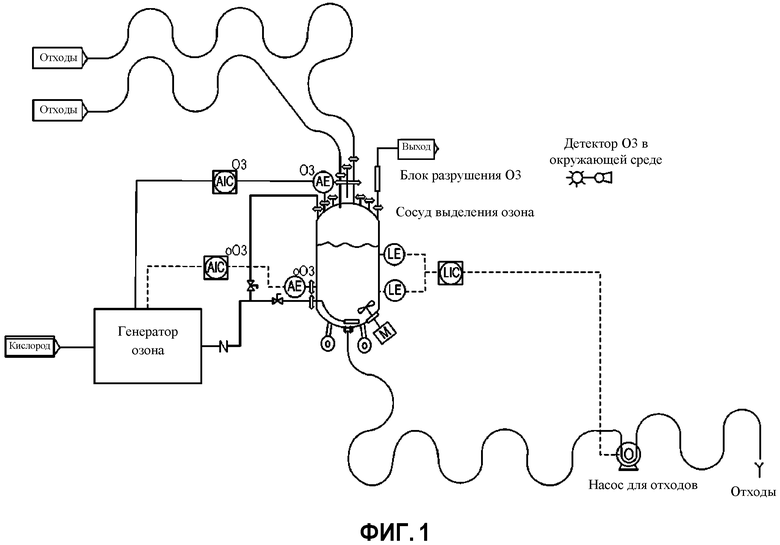
1. Способ предотвращения контаминации системы, при этом способ включает:
обеспечение системы, содержащей первый сосуд и второй сосуд, при этом первой сосуд содержит жидкость, а второй сосуд содержит объем стерилизующего газа;
обеспечение течения первого объема жидкости из первого сосуда во второй сосуд через объем стерилизующего газа, содержащийся в верхней части второго сосуда.
2. Способ по п. 1, отличающийся тем, что второй сосуд дополнительно содержит:
(i) впускное отверстие для текучей среды, выполненное таким образом, что объем жидкости, входящей во второй сосуд, проходит через верхнюю часть;
(ii) выпускное отверстие для текучей среды, выполненное таким образом, что жидкость, выходящая из второго сосуда, вытекает ниже заполненной стерилизующим газом верхней части;
(iii) по меньшей мере одно впускное отверстие для газа и
(iv) по меньшей мере одно выпускное отверстие для газа,
при этом впускное отверстие для текучей среды находится в сообщении по текучей среде с первым сосудом.
3. Способ по п. 2, отличающийся тем, что первый сосуд содержит
выпускное отверстие для текучей среды в сообщении по текучей среде с впускным отверстием для текучей среды второго сосуда.
4. Способ по п. 1, отличающийся тем, что стерилизующий газ барботируют во второй сосуд или вводят непосредственно в верхнюю часть второго сосуда.
5. Способ по п. 1, отличающийся тем, что первой сосуд представляет собой биореактор, систему для хроматографии, систему для микрофильтрации (MF) или систему для ультрафильтрации/диафильтрации (UF/DF).
6. Способ по п. 1, отличающийся тем, что первый объем жидкости содержит рекомбинантный терапевтический белок.
7. Способ по п. 6, дополнительно включающий:
(i) обеспечение течения второго объема жидкости из второго сосуда в первую систему для многоколоночной хроматографии (MCCS1);
(ii) сбор указанного рекомбинантного терапевтического белка из жидкой культуральной среды с применением MCCS1, при этом элюат MCCS1, содержащий рекомбинантный терапевтический белок, непрерывно подают во вторую систему для многоколоночной хроматографии (MCCS2); и
(iii) очистку и доочистку рекомбинантного терапевтического белка с применением MCCS2, при этом элюат из MCCS2 содержит рекомбинантный терапевтический белок; и
при этом технологический процесс является совмещенным и осуществляется непрерывно от указанного первого сосуда к элюату из MCCS2, который содержит рекомбинантный терапевтический белок.
8. Способ по п. 6, дополнительно включающий обеспечение течения второго объема жидкости из второго сосуда в установку для очистки и доочистки рекомбинантного терапевтического белка.
9. Способ по п. 7, отличающийся тем, что второй объем жидкости содержит рекомбинантный терапевтический белок.
10. Способ по п. 7, в котором рекомбинантный терапевтический белок представляет собой антитело или фрагмент антитела, фермент, сконструированный белок или иммуногенный белок или фрагмент белка.
11. Способ по п. 1, отличающийся тем, что стерилизующий газ выбирают из группы, состоящей из озона, этиленоксида, диоксида азота или выпаренного пероксида водорода.
12. Способ по п. 1, в котором первый сосуд представляет собой стерилизованный сосуд.
13. Способ по п. 1, в котором система представляет собой систему биологического производства или систему фармацевтического производства.
14. Способ по п. 1, в котором жидкость в первом сосуде содержит рекомбинантный терапевтический белок.
15. Способ по п. 14, в котором рекомбинантный терапевтический белок представляет собой антитело или фрагмент антитела, фермент, сконструированный белок или иммуногенный белок или фрагмент белка.
16. Способ по п. 14, в котором рекомбинантный терапевтический белок является секретированным из клетки.
17.Способ по п. 1, в котором жидкость в первом сосуде содержит побочные продукты ферментации.
18. Способ по п. 1, в котором первый объем жидкости представляет собой поток отходов.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Способ пластики связок коленного сустава | 1987 |
|
SU1498475A1 |
| Безредукторный привод буровой лебедки | 1954 |
|
SU109275A1 |
Авторы
Даты
2020-02-03—Публикация
2015-10-20—Подача