ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет предварительной заявки на патент США с регистрационным № 62/726043, поданной 31 августа 2018 года; полное содержание которой включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способам биотехнологии и биопроизводства рекомбинантных белков.
УРОВЕНЬ ТЕХНИКИ
Клетки млекопитающего, содержащие нуклеиновую кислоту, которая кодирует рекомбинантный белок, часто применяют для получения белков, важных с терапевтической или коммерческой точки зрения. В сложившихся условиях процессов производства различных продуктов биотехнологическим компаниям все в большей степени приходится разрабатывать инновационные решения для очень гибкого и экономически эффективного производства лекарственных веществ на основе терапевтического белка. Одна из стратегий эффективного выделения рекомбинантных белков заключается в способах, которые предусматривают непрерывную хроматографию (например, с применением закрытой системы). Одним известным ограничением непрерывной хроматографии является присутствие загрязняющих средств в системе (например, увеличенная бионагрузка), что приводит к загрязнению продукта, к уменьшению выхода продукта и к уменьшению расхода (или к увеличению давления) в системе. Например, увеличенная бионагрузка внутри системы может приводить к полной остановке системы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение основано, по меньшей мере частично, на открытии того, что подвергание смолы для хроматографии воздействию гамма-излучения уменьшает связывающую способность смолы для хроматографии, и что облучение в присутствии по меньшей мере одного спирта может способствовать предотвращению такого уменьшения связывающей способности смолы для хроматографии, обусловленного гамма-излучением. С учетом данного открытия, в данном документе предусмотрены способы уменьшения бионагрузки в смоле для хроматографии, которые предусматривают подвергание контейнера, включающего композицию, включающую (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после/во время воздействия дозы гамма-излучения. Также предусмотрены хроматографические колонки с уменьшенной бионагрузкой, содержащие смолу для хроматографии с уменьшенной бионагрузкой, полученную с помощью любого из способов, описанных в данном документе; композиции, включающие (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт; способы выполнения хроматографии на колонке с уменьшенной бионагрузкой с применением по меньшей мере одной из таких хроматографических колонок с уменьшенной бионагрузкой; и интегрированные закрытые или по сути закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают применение по меньшей мере одной из таких хроматографических колонок с уменьшенной бионагрузкой. Любая из смол для хроматографии, полученных с помощью любого из способов, описанных в данном документе, любая из заполненных хроматографических колонок, полученных с помощью любого из способов, описанных в данном документе, любой из способов выполнения колоночной хроматографии и любой из способов, описанных в данном документе, могут быть стерильными, абсолютно стерильными, асептическими или с уменьшенной бионагрузкой. Любая из смол для хроматографии, полученных с помощью любого из способов, описанных в данном документе, любая из хроматографических колонок, полученных с помощью любого из способов, описанных в данном документе, и любой из способов, описанных в данном документе, могут быть асептическими и стерильными, абсолютно стерильными, асептическими или с уменьшенной бионагрузкой.
В данном документе предусмотрены способы уменьшения бионагрузки в смоле для хроматографии, которые предусматривают подвергание контейнера, содержащего композицию, содержащую (i) смолу для хроматографии и (i) жидкость, содержащую по меньшей мере один спирт, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
В некоторых вариантах осуществления способ может дополнительно предусматривать перед воздействием помещение композиции в контейнер.
В некоторых вариантах осуществления контейнер представляет собой сосуд для хранения.
В некоторых вариантах осуществления контейнер представляет собой хроматографическую колонку.
В некоторых вариантах осуществления контейнер представляет собой заполненную хроматографическую колонку.
В некоторых вариантах осуществления композиция представляет собой взвесь осажденной смолы для хроматографии.
В некоторых вариантах осуществления композиция представляет собой смоченную твердую смесь.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, по меньшей мере один спирт выбран из группы, состоящей из бензилового спирта, циклогексанола, изобутилового спирта, 2-метил-2-бутанола, метанола, этанола, пропан-2-ола, пропан-1-ола, бутан-1-ола, пентан-1-ола, гексадекан-1-ола, 2-фенилэтанола, втор-фенилэтанола, 3-фенил-1-пропанола, 1-фенил-1-пропанола, 2-фенил-1-пропанола, 2-фенил-2-пропанола, 1-фенил-2-бутанола, 2-фенил-1-бутанола, 3-фенил-1-бутанола, 4-фенил-2-бутанола, DL-1-фенил-2-пентанола, 5-фенил-1-пентанола и 4-фенил-1-бутанола.
В некоторых вариантах осуществления по меньшей мере один спирт предусматривает бензиловый спирт.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, общая суммарная концентрация одного или нескольких спиртов в жидкости составляет от приблизительно 0,01% об./об. до приблизительно 10% об./об.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, жидкость может дополнительно включать по меньшей мере один антиоксидант и/или хелатор.
В некоторых вариантах осуществления жидкость включает по меньшей мере один антиоксидант и/или хелатор в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, жидкость включает по меньшей мере один антиоксидант, выбранный из группы, состоящей из восстановленного глутатиона, восстановленного тиоредоксина, восстановленного цистеина, каротиноида, мелатонина, ликопина, токоферола, восстановленного убихинона, аскорбата, билирубина, мочевой кислоты, липоевой кислоты, флавоноида, фенолпропановой кислоты, лидокаина, нарингина, фуллерена, глюкозы, маннита, 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила и диметилметоксихроманола.
В некоторых вариантах осуществления жидкость включает по меньшей мере один антиоксидант, выбранный из группы, состоящей из маннита, аскорбата натрия, гистидина и метионина.
В некоторых вариантах осуществления жидкость включает маннит, аскорбат натрия, гистидин и метионин.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, жидкость включает (i) от 75 мМ до приблизительно 125 мМ маннита; (ii) от 75 мМ до приблизительно 125 мМ метионина; (iii) от 75 мМ до приблизительно 125 мМ аскорбата натрия; (iv) от 75 мМ до приблизительно 125 мМ гистидина; (v) от 30 мМ до приблизительно 70 мМ метионина и от приблизительно 30 мМ до приблизительно 70 мМ гистидина; (vi) от приблизительно 10 мМ до приблизительно 50 мМ метионина, от приблизительно 10 мМ до приблизительно 50 мМ гистидина и от приблизительно 10 мМ до приблизительно 50 мМ аскорбата натрия или (vii) от приблизительно 5 мМ до приблизительно 45 мМ аскорбата натрия, от приблизительно 5 мМ до приблизительно 45 мМ метионина, от приблизительно 5 мМ до приблизительно 45 мМ маннита и от приблизительно 5 мМ до приблизительно 45 мМ гистидина.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, жидкость представляет собой буферный раствор.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, жидкость включает по меньшей мере один хелатор, выбранный из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), соли натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарной кислоты (DMSA), металлотионина и дефероксамина.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, смола для хроматографии выбрана из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
В некоторых вариантах осуществления композиция включает смолу для аффинной хроматографии, включающую белковый лиганд.
В некоторых вариантах осуществления белковый лиганд представляет собой белок A.
В некоторых вариантах осуществления композиция включает смолу для анионообменной хроматографии.
В некоторых вариантах осуществления смола для анионообменной хроматографии включает N-бензил-N-метилэтаноламинные группы.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, доза составляет от приблизительно 15 кГр до приблизительно 45 кГр.
В некоторых вариантах осуществления доза составляет от приблизительно 20 кГр до приблизительно 30 кГр.
В некоторых вариантах осуществления доза составляет от приблизительно 23 кГр до приблизительно 27 кГр.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, воздействие осуществляют при температуре, составляющей от приблизительно −25°C до приблизительно 0°C включительно.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, воздействие осуществляют при температуре, составляющей от приблизительно 0°C до приблизительно 25°C включительно.
В данном документе предусмотрены смолы для хроматографии с уменьшенной бионагрузкой, полученные с помощью любого из способов, описанных в данном документе.
В некоторых вариантах осуществления смола характеризуется уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−8 до приблизительно 1 × 10−5.
В некоторых вариантах осуществления смола характеризуется уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−7 до приблизительно 1 × 10−6.
В некоторых вариантах осуществления любой из смол, описанных в данном документе, смола для хроматографии предусматривает по меньшей мере одну смолу, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
В некоторых вариантах осуществления смола для хроматографии предусматривает смолу для аффинной хроматографии, включающую белковый лиганд.
В некоторых вариантах осуществления белковый лиганд представляет собой белок A.
В некоторых вариантах осуществления смола для хроматографии предусматривает смолу для анионообменной хроматографии.
В некоторых вариантах осуществления смола для анионообменной хроматографии включает N-бензил-N-метилэтаноламинные группы.
В данном документе предусмотрены способы получения заполненной хроматографической колонки с уменьшенной бионагрузкой, которые предусматривают обеспечение любой из смол для хроматографии с уменьшенной бионагрузкой, описанных в данном документе; и заполнение смолой для хроматографии колонки с уменьшенной бионагрузкой в асептических условиях.
В данном документе предусмотрены заполненные хроматографические колонки с уменьшенной бионагрузкой, полученные с помощью любого из способов, описанных в данном документе.
В данном документе предусмотрены заполненные хроматографические колонки с уменьшенной бионагрузкой, полученные с помощью любого из способов, описанных в данном документе.
В некоторых вариантах осуществления смола в заполненной колонке характеризуется уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−8 до приблизительно 1 × 10−5.
В некоторых вариантах осуществления смола характеризуется уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−7 до приблизительно 1 × 10−6.
В некоторых вариантах осуществления любой из смол, описанных в данном документе, смола в заполненной колонке включает по меньшей мере одну смолу, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
В некоторых вариантах осуществления смола предусматривает смолу для аффинной или псевдоаффинной хроматографии, включающую белковый лиганд.
В некоторых вариантах осуществления лиганд представляет собой белок A.
В некоторых вариантах осуществления смола предусматривает смолу для анионообменной хроматографии.
В некоторых вариантах осуществления смола для анионообменной хроматографии включает N-бензил-N-метилэтаноламинные группы.
В данном документе предусмотрены композиции, которые включают (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции.
В некоторых вариантах осуществления композиция представляет собой взвесь осажденной смолы для хроматографии.
В некоторых вариантах осуществления композиция представляет собой смоченную твердую смесь.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, по меньшей мере один спирт выбран из группы, состоящей из бензилового спирта, циклогексанола, изобутилового спирта, 2-метил-2-бутанола, метанола, этанола, пропан-2-ола, пропан-1-ола, бутан-1-ола, пентан-1-ола, гексадекан-1-ола, 2-фенилэтанола, втор-фенилэтанола, 3-фенил-1-пропанола, 1-фенил-1-пропанола, 2-фенил-1-пропанола, 2-фенил-2-пропанола, 1-фенил-2-бутанола, 2-фенил-1-бутанола, 3-фенил-1-бутанола, 4-фенил-2-бутанола, DL-1-фенил-2-пентанола, 5-фенил-1-пентанола и 4-фенил-1-бутанола.
В некоторых вариантах осуществления по меньшей мере один спирт предусматривает бензиловый спирт.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, общая суммарная концентрация одного или нескольких спиртов в жидкости составляет от приблизительно 0,01% об./об. до приблизительно 10% об./об.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, жидкость дополнительно включает по меньшей мере один антиоксидант и/или хелатор.
В некоторых вариантах осуществления жидкость дополнительно включает по меньшей мере один антиоксидант и/или хелатор в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, жидкость включает по меньшей мере один антиоксидант, выбранный из группы, состоящей из восстановленного глутатиона, восстановленного тиоредоксина, восстановленного цистеина, каротиноида, мелатонина, ликопина, токоферола, восстановленного убихинона, аскорбата, билирубина, мочевой кислоты, липоевой кислоты, флавоноида, фенолпропановой кислоты, лидокаина, нарингина, фуллерена, глюкозы, маннита, 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила и диметилметоксихроманола.
В некоторых вариантах осуществления жидкость включает по меньшей мере один антиоксидант, выбранный из группы, состоящей из маннита, аскорбата натрия, гистидина и метионина.
В некоторых вариантах осуществления жидкость включает маннит, аскорбат натрия, гистидин и метионин.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, жидкость включает (i) от 75 мМ до приблизительно 125 мМ маннита; (ii) от 75 мМ до приблизительно 125 мМ метионина; (iii) от 75 мМ до приблизительно 125 мМ аскорбата натрия; (iv) от 75 мМ до приблизительно 125 мМ гистидина; (v) от 30 мМ до приблизительно 70 мМ метионина и от приблизительно 30 мМ до приблизительно 70 мМ гистидина; (vi) от приблизительно 10 мМ до приблизительно 50 мМ метионина, от приблизительно 10 мМ до приблизительно 50 мМ гистидина и от приблизительно 10 мМ до приблизительно 50 мМ аскорбата натрия или (vii) от приблизительно 5 мМ до приблизительно 45 мМ аскорбата натрия, от приблизительно 5 мМ до приблизительно 45 мМ метионина, от приблизительно 5 мМ до приблизительно 45 мМ маннита и от приблизительно 5 мМ до приблизительно 45 мМ гистидина.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, жидкость представляет собой буферный раствор.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, композиция включает по меньшей мере один хелатор, выбранный из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), соли натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарной кислоты (DMSA), металлотионина и дефероксамина.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, смола для хроматографии предусматривает по меньшей мере одну смолу, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, смола предусматривает смолу для аффинной хроматографии, включающую белковый лиганд.
В некоторых вариантах осуществления белковый лиганд представляет собой белок A.
В данном документе предусмотрены способы выполнения хроматографии на колонке с уменьшенной бионагрузкой, которые предусматривают (a) обеспечение любой из заполненных хроматографических колонок с уменьшенной бионагрузкой, описанных в данном документе; и (b) выполнение колоночной хроматографии с применением заполненной хроматографической колонки с уменьшенной бионагрузкой и буфера с уменьшенной бионагрузкой в закрытой системе.
В некоторых вариантах осуществления хроматографию на колонке с уменьшенной бионагрузкой с применением заполненной хроматографической колонки с уменьшенной бионагрузкой проводят непрерывно в течение периода времени, составляющего по меньшей мере 4 дня.
В некоторых вариантах осуществления хроматографию на колонке с уменьшенной бионагрузкой с применением заполненной хроматографической колонки с уменьшенной бионагрузкой проводят непрерывно в течение периода времени, составляющего по меньшей мере 5 дней.
В некоторых вариантах осуществления хроматографию на колонке с уменьшенной бионагрузкой с применением заполненной хроматографической колонки с уменьшенной бионагрузкой проводят непрерывно в течение периода времени, составляющего по меньшей мере 7 дней.
В некоторых вариантах осуществления хроматографию на колонке с уменьшенной бионагрузкой с применением заполненной хроматографической колонки с уменьшенной бионагрузкой проводят непрерывно в течение периода времени, составляющего по меньшей мере 14 дней.
В некоторых вариантах осуществления хроматографию на колонке с уменьшенной бионагрузкой с применением заполненной хроматографической колонки с уменьшенной бионагрузкой проводят непрерывно в течение периода времени, составляющего по меньшей мере 28 дней.
В некоторых вариантах осуществления смола в заполненной хроматографической колонке с уменьшенной бионагрузкой в (a) характеризуется связывающей способностью в процентах, составляющей от приблизительно 75% до приблизительно 100% по сравнению с такой же смолой, не подвергнутой обработке с помощью гамма-излучения.
В некоторых вариантах осуществления смола в заполненной хроматографической колонке с уменьшенной бионагрузкой предусматривает по меньшей мере одну смолу, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
В некоторых вариантах осуществления смола предусматривает смолу для аффинной хроматографии, включающую белковый лиганд.
В некоторых вариантах осуществления белковый лиганд представляет собой белок A.
В некоторых вариантах осуществления смола предусматривает смолу для анионообменной хроматографии.
В данном документе предусмотрены интегрированные закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают (a) обеспечение жидкой культуральной среды, содержащей рекомбинантный белок, по сути не содержащей клеток; и (b) непрерывную подачу жидкой культуральной среды в систему для многоколоночной хроматографии (MCCS), содержащую по меньшей мере одну из любой из заполненных хроматографических колонок с уменьшенной бионагрузкой, описанных в данном документе; при этом в способе используют буфер с уменьшенной бионагрузкой, способ является интегрированным, и его осуществляют непрерывно от жидкой культуральной среды до элюата, выходящего из MCCS, который представляет собой очищенный рекомбинантный белок.
В некоторых вариантах осуществления в MCCS проводят по меньшей мере две различные отдельные операции.
В некоторых вариантах осуществления способ предусматривает переключение колонок.
В некоторых вариантах осуществления в MCCS проводят отдельные операции захвата рекомбинантного белка и инактивации вирусов.
В некоторых вариантах осуществления в MCCS проводят отдельные операции захвата и очистки рекомбинантного белка.
В некоторых вариантах осуществления MCCS содержит по меньшей мере две заполненные хроматографические колонки с уменьшенной бионагрузкой.
В некоторых вариантах осуществления MCCS представляет собой систему для периодической противоточной хроматографии.
В некоторых вариантах осуществления MCCS содержит ряд колонок для аффинной или псевдоаффинной хроматографии, катионообменной хроматографии, анионообменной хроматографии или эксклюзионной хроматографии или любую их комбинацию.
В некоторых вариантах осуществления MCCS содержит колонку для аффинной хроматографии, и при этом аффинную хроматографию проводят с помощью способа, предусматривающего механизм захвата, выбранный из группы, состоящей из механизма захвата посредством связывания с белком A, механизма захвата посредством связывания с субстратом, механизма захвата посредством связывания c антителом или фрагментом антитела, механизма захвата посредством связывания с аптамером и механизма захвата посредством связывания с кофактором.
В некоторых вариантах осуществления аффинную хроматографию проводят с помощью способа, предусматривающего механизм захвата посредством связывания с белком A, и при этом рекомбинантный белок представляет собой антитело или фрагмент антитела.
В данном документе предусмотрены интегрированные закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают (a) обеспечение жидкой культуральной среды, содержащей рекомбинантный белок, по сути не содержащей клеток; (b) непрерывную подачу жидкой культуральной среды в первую систему для многоколоночной хроматографии (MCCS1); (c) захват рекомбинантного белка в жидкой культуральной среде с применением MCCS1; (d) получение элюата, выходящего из MCCS1, который включает рекомбинантный белок, и непрерывную подачу элюата во вторую систему для многоколоночной хроматографии (MCCS2); (e) непрерывную подачу рекомбинантного белка из элюата в MCCS2 и последующее элюирование рекомбинантного белка с получением таким образом очищенного рекомбинантного белка, при этом в способе используют буфер с уменьшенной бионагрузкой, способ является интегрированным, и его осуществляют непрерывно от жидкой культуральной среды до очищенного рекомбинантного белка, и при этом по меньшей мере одна колонка в MCCS1 и/или MCCS2 содержит любую из заполненных хроматографических колонок с уменьшенной бионагрузкой, описанных в данном документе.
В некоторых вариантах осуществления в MCCS1 и/или MCCS2 проводят по меньшей мере две различные отдельные операции.
В некоторых вариантах осуществления способ предусматривает переключение колонок.
В некоторых вариантах осуществления в MCCS1 проводят отдельные операции захвата рекомбинантного терапевтического белка и инактивации вирусов.
В некоторых вариантах осуществления в MCCS2 проводят отдельные операции очистки и тонкой очистки рекомбинантного белка.
В некоторых вариантах осуществления MCCS1 и/или MCCS2 содержат по меньшей мере две хроматографические колонки.
В некоторых вариантах осуществления MCCS1 представляет собой первую систему для периодической противоточной хроматографии (PCCS1).
В некоторых вариантах осуществления захват проводят с применением аффинной хроматографии, катионообменной хроматографии, анионообменной хроматографии или эксклюзионной хроматографии или любой их комбинации.
В некоторых вариантах осуществления аффинную хроматографию проводят с помощью механизма захвата, выбранного из группы, состоящей из механизма захвата посредством связывания с белком A, механизма захвата посредством связывания с субстратом, механизма захвата посредством связывания c антителом или фрагментом антитела, механизма захвата посредством связывания с аптамером и механизма захвата посредством связывания с кофактором.
В некоторых вариантах осуществления аффинную хроматографию проводят с помощью механизма захвата посредством связывания с белком A, и при этом рекомбинантный белок представляет собой антитело или фрагмент антитела.
В некоторых вариантах осуществления MCCS2 представляет собой вторую систему для периодической противоточной хроматографии (PCCS2).
В некоторых вариантах осуществления любого из способов, описанных в данном документе, рекомбинантный белок представляет собой терапевтический рекомбинантный белок.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, способ дополнительно предусматривает составление очищенного терапевтического рекомбинантного белка в фармацевтическую композицию.
В некоторых вариантах осуществления любого из способов, описанных в данном документе, способ осуществляют непрерывно в течение периода времени, составляющего по меньшей мере 4 дня.
В некоторых вариантах осуществления способ осуществляют непрерывно в течение периода времени, составляющего по меньшей мере 5 дней.
В некоторых вариантах осуществления способ осуществляют непрерывно в течение периода времени, составляющего по меньшей мере 7 дней.
В некоторых вариантах осуществления способ осуществляют непрерывно в течение периода времени, составляющего по меньшей мере 14 дней.
В некоторых вариантах осуществления способ осуществляют непрерывно в течение периода времени, составляющего по меньшей мере 28 дней.
При использовании в данном документе форма единственного числа существительного означает одно или несколько объектов конкретного существительного. Например, выражение "хроматографическая колонка с уменьшенной бионагрузкой" представляет собой "одну или несколько хроматографических колонок с уменьшенной бионагрузкой".
Термин "бионагрузка" является известным в данной области техники и означает уровень самореплицирующихся биологических загрязнителей, присутствующих в композиции (например, в твердой или жидкой) и/или на поверхности (например, на внешней и/или внутренней поверхности) изделия(изделий). Например, бионагрузка может означать самореплицирующиеся биологические загрязнители, присутствующие в композиции, содержащей смолу для хроматографии, или в смоле для хроматографии в качестве насадки (например, самореплицирующиеся биологические загрязнители, присутствующие в смоле для хроматографии в качестве насадки в заполненной хроматографической колонке). В других примерах бионагрузка может означать самореплицирующиеся биологические загрязнители на внутренней поверхности хроматографической колонки и/или внутри смолы для хроматографии внутри хроматографической колонки (например, биологические загрязнители на внутренней поверхности хроматографической колонки и биологические загрязнители в смоле для хроматографии в качестве насадки внутри хроматографической колонки). Бионагрузка также может означать самореплицирующиеся биологические загрязнители, присутствующие внутри жидкости (например, буфера, применяемого в любом из способов или процессов, описанных в данном документе). Неограничивающими примерами самореплицирующихся биологических загрязнителей могут быть бактерии (например, грамположительные или грамотрицательные бактерии или бактериальные споры), микобактерии, вирусы (например, везивирус, вирус долины Кэш, парвовирус, вирус герпеса и буньявирус), паразиты, грибы, дрожжи и простейшие. Иллюстративные способы определения бионагрузки описаны в данном документе. Дополнительные способы определения бионагрузки известны из уровня техники.
Термин "уменьшение бионагрузки" является известным в данной области техники и означает снижение (например, выявляемое снижение) уровня самореплицирующихся биологических загрязнителей, присутствующих в композиции (например, в твердой или жидкой) и/или на поверхности (например, на внешней и/или внутренней поверхности) изделия(изделий). Неограничивающие примеры способов уменьшения бионагрузки в смоле для хроматографии (например, смолы для хроматографии в качестве насадки), буфера и/или хроматографической колонки (например, заполненной хроматографической колонки) описаны в данном документе. Дополнительные способы уменьшения бионагрузки в любой из композиций, описанных в данном документе, известны из уровня техники.
Термин "смола для хроматографии с уменьшенной бионагрузкой" означает смолу для хроматографии, которую подвергали обработке для снижения уровня самореплицирующихся биологических загрязнителей, присутствующих в смоле для хроматографии (например, выявляемого снижения уровня самореплицирующихся биологических загрязнителей, присутствующих в композиции, содержащей смолу для хроматографии, например, во взвеси). Например, смола для хроматографии с уменьшенной бионагрузкой может представлять собой смолу, подвергнутую воздействию гамма-излучения в дозе, достаточной для снижения уровня самореплицирующихся биологических загрязнителей в смоле для хроматографии (например, в композиции, содержащей смолу для хроматографии, подвергнутую воздействию гамма-излучения в дозе, достаточной для снижения уровня самореплицирующихся биологических загрязнителей в смоле для хроматографии). Например, смола для хроматографии с уменьшенной бионагрузкой может представлять собой смолу, которая была подвергнута воздействию излучения в дозе, составляющей от приблизительно 1 кГр до приблизительно 15 кГр, от приблизительно 1 кГр до приблизительно 20 кГр гамма-излучения, от приблизительно 1 кГр до приблизительно 25 кГр гамма-излучения, от приблизительно 1 кГр до приблизительно 30 кГр гамма-излучения или от приблизительно 1 кГр до приблизительно 35 кГр гамма-излучения. Иллюстративные способы уменьшения бионагрузки в смоле для хроматографии описаны в данном документе. Дополнительные способы уменьшения бионагрузки в смоле для хроматографии известны из уровня техники.
Термин "хроматографическая колонка с уменьшенной бионагрузкой" означает хроматографическую колонку (например, заполненную хроматографическую колонку), которая содержит подвергнутую обработке смолу для хроматографии (например, подвергнутую воздействию гамма-излучения смолу для хроматографии), которая характеризуется уровнем самореплицирующихся биологических загрязнителей, который меньше уровня самореплицирующихся биологических загрязнителей, присутствующих в идентичной хроматографической колонке, которая содержит не подвергнутую обработке смолу для хроматографии. Например, хроматографическая колонка с уменьшенной бионагрузкой может содержать подвергнутую обработке смолу для хроматографии, характеризующуюся уровнем обеспечения стерильности, составляющим по меньшей мере или приблизительно 1 × 10−6, 1 × 10−7, 1 × 10−8, 1 × 10−9 или 1 × 10−10.
Термин "буфер с уменьшенной бионагрузкой" является известным в данной области техники и означает подвергнутую обработке (например, подвергнутую фильтрованию, автоклавированию и/или воздействию гамма-излучения) жидкость (например, подвергнутый обработке буферный раствор), которая характеризуется уровнем самореплицирующегося(самореплицирующихся) загрязняющего(загрязняющих) средства(средств), который меньше уровня самореплицирующегося(самореплицирующихся) загрязняющего(загрязняющих) средства(средств), обнаруженного(обнаруженных) в идентичной не подвергнутой обработке жидкости. Например, буфер с уменьшенной бионагрузкой может характеризоваться уровнем обеспечения стерильности, составляющим по меньшей мере или приблизительно 1 × 10−6, 1 × 10−7, 1 × 10−8, 1 × 10−9 или 1 × 10−10.
"Абсолютная стерильность" или "абсолютно стерильный" представляют собой термины, используемые для описания композиции или способа, которые совсем не содержат/не предусматривают самореплицирующихся биологических загрязнителей. Например, термин может быть применимым к подвергнутой воздействию гамма-излучения смоле для хроматографии, к внутренней поверхности и содержимому (например, к смоле для хроматографии) хроматографической колонки и/или к буферу. Абсолютно стерильные композиция или способ могут быть чистыми (как данный термин известен в данной области техники).
"Стерильный" или "стерильность" представляют собой термины, используемые для описания композиции или способа, которые характеризуются уровнем обеспечения стерильности, составляющим приблизительно 1,0 × 10−6 или меньше (например, приблизительно 1,0 × 10−7 или меньше, приблизительно 1,0 × 10−8 или меньше, приблизительно 1,0 × 10−9 или меньше или 1 × 10−10). Определение того, являются ли композиция или способ стерильными, можно провести с применением ряда валидированных технологических процессов, известных из уровня техники. Например, стерильные композиция или способ могут совсем не содержать/не предусматривать жизнеспособных самореплицирующихся биологических загрязнителей (например, любого из самореплицирующихся биологических загрязнителей, описанных в данном документе). Стерильные композиция или способ также могут быть чистыми (как данный термин известен в данной области техники).
Термин "стерилизация" означает валидированный процесс, применяемый для придания композиции стерильности (определенной в данном документе). Можно измерять степень инактивации показательных устойчивых самореплицирующихся биологических загрязнителей (например, бактерий) во время способа обработки с целью определения того, была ли достигнута стерильность (определенная в данном документе) композиции.
Термин "уровень обеспечения стерильности" или "SAL" является известным в данной области техники и означает уровень достоверности достижения абсолютной стерильности внутри партии подвергнутых обработке единиц. Вероятность обычно рассчитывают на основе результатов исследований инактивации, проведенных во время валидации, и ее выражают в форме 1 × 10−n.
Термин "асептический" используют для описания композиции или способа, которые не содержат/не предусматривают обуславливающих заболевание или обуславливающих симптом самореплицирующихся биологических загрязнителей (например, любого из самореплицирующихся биологических загрязнителей, описанных в данном документе). Асептические композиция или способ также могут быть чистыми (как данный термин известен в данной области техники).
Термин "отдельная операция" является термином из данной области техники и означает функциональную стадию, которую можно проводить в способе очистки рекомбинантного белка из жидкой культуральной среды. Например, отдельной операцией может быть фильтрование (например, удаление загрязняющих бактерий, дрожжей, вирусов и/или микобактерий и/или твердых частиц из жидкости, включающей рекомбинантный белок), захват, удаление эпитопной метки, очистка, удерживание или хранение, тонкая очистка, инактивация вируса, регулирование концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок, и удаление нежелательных солей.
Термин "захват" означает стадию, которую проводят для частичной очистки или выделения (например, обеспечения по меньшей мере или приблизительно 5%, например, по меньшей мере или приблизительно 10%, 15%, 20%, 25%, 30%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или по меньшей мере или приблизительно 95% чистоты по весу) и концентрирования рекомбинантного белка (например, рекомбинантного терапевтического белка) от одного или нескольких других компонентов, присутствующих в жидкой культуральной среде или разбавленной жидкой культуральной среде (например, белков культуральной среды или одного или нескольких других компонентов (например, ДНК, РНК или других белков), присутствующих в клетке млекопитающего или секретируемых такой клеткой). Как правило, захват проводят с применением смолы для хроматографии, которая связывает рекомбинантный белок (например, путем применения аффинной хроматографии). Неограничивающие способы захвата рекомбинантного белка из жидкой культуральной среды или разбавленной жидкой культуральной среды описаны в данном документе, а другие известны из уровня техники. Рекомбинантный белок можно захватывать из жидкой культуральной среды с применением по меньшей мере одной хроматографической колонки и/или хроматографической мембраны (например, любой из хроматографических колонок и/или хроматографических мембран, описанных в данном документе).
Термин "очистка" означает стадию, которую проводят для отделения рекомбинантного белка (например, рекомбинантного терапевтического белка) от одной или нескольких других примесей (например, объемных примесей) или компонентов, присутствующих в текучей среде, включающей рекомбинантный белок (например, белков жидкой культуральной среды или одного или нескольких других компонентов (например, ДНК, РНК, других белков, эндотоксинов, вирусов и т. д.), присутствующих в клетке млекопитающего или секретируемых такой клеткой). Например, очистку можно проводить во время или после стадии первичного захвата. Очистку можно проводить с применением смолы для хроматографии, мембраны или любой другой твердой подложки, которая связывает либо рекомбинантный белок, либо загрязнители (например, путем применения аффинной хроматографии, хроматографии с гидрофобным взаимодействием, анионо- или катионообменной хроматографии или хроматография на молекулярных ситах). Рекомбинантный белок можно очищать из текучей среды, включающей рекомбинантный белок, с применением по меньшей мере одной хроматографической колонки и/или хроматографической мембраны (например, любой из хроматографических колонок или хроматографических мембран, описанных в данном документе).
Термин "тонкая очистка" является термином из данной области техники и означает стадию, которую проводят для удаления оставшихся следовых или небольших количеств загрязнителей или примесей из текучей среды, включающей рекомбинантный белок (например, рекомбинантный терапевтический белок), которая характеризуется чистотой, близкой к окончательной необходимой чистоте. Например, тонкую очистку можно проводить путем пропускания текучей среды, включающей рекомбинантный белок, через хроматографическую(хроматографические) колонку(колонки) или мембранный(мембранные) абсорбер(абсорберы), которые селективно связываются либо с целевым рекомбинантным белком, либо с небольшими количествами загрязнителей или примесей, присутствующих в текучей среде, включающей рекомбинантный белок. В таком примере элюат/фильтрат с хроматографической(хроматографических) колонки(колонок) или мембранного(мембранных) абсорбера(абсорберов) включает рекомбинантный белок.
Термин "фильтрование" означает удаление по меньшей мере части (например, по меньшей мере 80%, 90%, 95%, 96%, 97%, 98% или 99%) нежелательных биологических загрязнителей (например, клеток млекопитающего, бактерий, дрожжевых клеток, вирусов или микобактерий) и/или твердых частиц (например, осажденных белков) из жидкости (например, жидкой культуральной среды или текучей среды, представленных в любом из способов, описанных в данном документе).
Термин "элюат/фильтрат" является термином из данной области техники и означает текучую среду, которая выходит из хроматографической колонки или хроматографической мембраны, которая включает выявляемое количество рекомбинантного белка (например, рекомбинантного терапевтического белка).
Термин "интегрированный способ" означает способ, который проводят с применением структурных элементов, которые функционируют совместно для достижения конкретного результата (например, очистки рекомбинантного белка из жидкой культуральной среды).
Термин "непрерывный способ" означает способ, при котором текучую среду непрерывно подают через по меньшей мере часть системы. Например, непрерывный способ представляет собой способ, при котором непрерывно подают жидкую культуральную среду, включающую рекомбинантный белок, из биореактора через MCCS. Другим примером непрерывного способа является способ, при котором непрерывно подают жидкую культуральную среду, включающую рекомбинантный белок, из биореактора через первую и вторую MCCS (MCCS1 и MCCS2). Дополнительные примеры включают способ, при котором непрерывно подают жидкую культуральную среду, включающую рекомбинантный белок, через MCCS, способ, при котором непрерывно подают жидкую культуральную среду, включающую рекомбинантный белок, через MCCS1 и MCCS2, или способ, при котором непрерывно подают текучую среду, включающую рекомбинантный белок, через MCCS2.
Термин "закрытый способ" является термином из данной области техники и означает способ, который осуществляют так, чтобы компоненты способа (например, смолы для хроматографии и/или буферы), которые вступают в контакт с рекомбинантным белком или жидкостями, включающими рекомбинантный белок, не были намеренно подвергнуты воздействию загрязняющих средств в течение значительного периода времени (например, не были намеренно подвергнуты воздействию воздуха в течение значительного периода времени).
Термин "лекарственное вещество на основе терапевтического белка" означает рекомбинантный белок (например, иммуноглобулин, фрагмент белка, сконструированный белок или фермент), который был достаточно очищен или отделен от загрязняющих белков, липидов и нуклеиновых кислот (например, загрязняющих белков, липидов и нуклеиновых кислот, присутствующих в жидкой культуральной среде или полученных из клетки-хозяина (например, из клетки-хозяина, представляющего собой клетку млекопитающего, дрожжей или бактерии)), а также биологических загрязнителей (например, вирусных и бактериальных загрязнителей), и который можно составлять в фармацевтическое средство без каких-либо дополнительных значительных стадий очистки и/или очистки от загрязнений.
Термин "система для многоколоночной хроматографии" или "MCCS" означает систему из суммарно двух или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Неограничивающим примером системы для многоколоночной хроматографии является система для периодической противоточной хроматографии (PCC), включающая суммарно две или более взаимосвязанных или переключающихся хроматографических колонок и/или хроматографических мембран. Дополнительные примеры систем для многоколоночной хроматографии описаны в данном документе и известны из уровня техники.
Термин "по сути не содержит" означает композицию (например, жидкую культуральную среду), которая на по меньшей мере или приблизительно 90% очищена (например, на по меньшей мере или приблизительно 95%, 96%, 97%, 98%, или на по меньшей мере или приблизительно 99% очищена, или на приблизительно 100% очищена) от указанного вещества (например, клетки млекопитающего или загрязняющего белка, нуклеиновой кислоты, углевода или липида, образующих клетку млекопитающего).
Термин "клетка млекопитающего" означает любую клетку любого млекопитающего или любую клетку, полученную из любого млекопитающего (например, человека, хомяка, мыши, зеленой мартышки, крысы, свиньи, коровы или кролика). Например, клетка млекопитающего может представлять собой иммортализованную клетку. В некоторых вариантах осуществления клетка млекопитающего представляет собой дифференцированную клетку. В некоторых вариантах осуществления клетка млекопитающего представляет собой недифференцированную клетку. Неограничивающие примеры клеток млекопитающего описаны в данном документе. Дополнительные примеры клеток млекопитающего известны из уровня техники.
Термин "культивирование" или "культивирование клетки" означает поддержание или пролиферацию клетки млекопитающего при контролируемом наборе физических условий.
Термин "культура клеток млекопитающего" означает жидкую культуральную среду, включающую некоторое количество клеток млекопитающего, которые поддерживаются или пролиферируют при контролируемом наборе физических условий.
Термин "жидкая культуральная среда" означает текучую среду, которая включает достаточное количество питательных веществ для обеспечения роста и пролиферации клетки (например, клетки млекопитающего) in vitro. Например, жидкая культуральная среда может включать одно или несколько из аминокислот (например, 20 аминокислот), пурина (например, гипоксантина), пиримидина (например, тимидина), холина, инозита, тиамина, фолиевой кислоты, биотина, кальция, никотинамида, пиридоксина, рибофлавина, тимидина, цианокобаламина, пирувата, липоевой кислоты, магния, глюкозы, натрия, калия, железа, меди, цинка и бикарбоната натрия. В некоторых вариантах осуществления жидкая культуральная среда может включать сыворотку крови млекопитающего. В некоторых вариантах осуществления жидкая культуральная среда не включает сыворотки или другого продукта, извлеченного из организма млекопитающего (жидкая культуральная среда с определенным составом). В некоторых вариантах осуществления жидкая культуральная среда может включать следовые количества металлов, гормон роста млекопитающего и/или фактор роста млекопитающего. Другим примером жидкой культуральной среды является минимальная среда (например, среда, включающая только неорганические соли, источник углерода и воду). Неограничивающие примеры жидкой культуральной среды описаны в данном документе. Дополнительные примеры жидкой культуральной среды известны из уровня техники и являются коммерчески доступными. Жидкая культуральная среда может включать клетки млекопитающего при любой плотности. Например, в контексте данного документа объем жидкой культуральной среды, удаляемый из биореактора, может по сути не содержать клеток млекопитающего.
Термин "жидкая культуральная среда, не содержащая компонентов животного происхождения" означает жидкую культуральную среду, которая не включает каких-либо компонентов (например, белков или сыворотки), полученных из организма млекопитающего.
Термин "жидкая культуральная среда, не содержащая сыворотки" означает жидкую культуральную среду, которая не включает сыворотку крови млекопитающего.
Термин "жидкая культуральная среда, содержащая сыворотку" означает жидкую культуральную среду, которая включает сыворотку крови млекопитающего.
Термин "жидкая культуральная среда с определенным химическим составом" является термином из данной области техники и означает жидкую культуральную среду, в которой все химические компоненты являются известными. Например, жидкая культуральная среда с определенным химическим составом не включает фетальной бычьей сыворотки, альбумина бычьей сыворотки или сывороточного альбумина человека, поскольку такие препараты обычно включают сложную смесь альбуминов и липидов.
Термин "жидкая культуральная среда, не содержащая белков" означает жидкую культуральную среду, которая не включает какого-либо белка (например, какого-либо выявляемого белка).
Термин "иммуноглобулин" означает полипептид, включающий аминокислотную последовательность из по меньшей мере 15 аминокислот (например, из по меньшей мере 20, 30, 40, 50, 60, 70, 80, 90 или 100 аминокислот) белка-иммуноглобулина (например, последовательность вариабельного домена, последовательность каркаса и/или последовательность константного домена). Иммуноглобулин может включать, например, по меньшей мере 15 аминокислот из легкой цепи иммуноглобулина, например, по меньшей мере 15 аминокислот из тяжелой цепи иммуноглобулина. Иммуноглобулин может представлять собой выделенное антитело (например, IgG, IgE, IgD, IgA или IgM), например, подкласс IgG (например, IgG1, IgG2, IgG3 или IgG4). Иммуноглобулин может представлять собой фрагмент антитела, например, Fab-фрагмент, F(ab′)2-фрагмент или scFv-фрагмент. Иммуноглобулин может также представлять собой биспецифическое антитело, или триспецифическое антитело, или димерное, тримерное или мультимерное антитело, или диатело, Affibody®, или Nanobody®. Иммуноглобулин также может представлять собой сконструированный белок, включающий по меньшей мере один домен иммуноглобулина (например, слитый белок). Неограничивающие примеры иммуноглобулинов описаны в данном документе, а дополнительные примеры иммуноглобулинов известны из уровня техники.
Термин "фрагмент белка" или "фрагмент полипептида" означает часть полипептидной последовательности длиной по меньшей мере или приблизительно 4 аминокислоты, по меньшей мере или приблизительно 5 аминокислот, по меньшей мере или приблизительно 6 аминокислот, по меньшей мере или приблизительно 7 аминокислот, по меньшей мере или приблизительно 8 аминокислот, по меньшей мере или приблизительно 9 аминокислот, по меньшей мере или приблизительно 10 аминокислот, по меньшей мере или приблизительно 11 аминокислот, по меньшей мере или приблизительно 12 аминокислот, по меньшей мере или приблизительно 13 аминокислот, по меньшей мере или приблизительно 14 аминокислот, по меньшей мере или приблизительно 15 аминокислот, по меньшей мере или приблизительно 16 аминокислот, по меньшей мере или приблизительно 17 аминокислот, по меньшей мере или приблизительно 18 аминокислот, по меньшей мере или приблизительно 19 аминокислот или по меньшей мере или приблизительно 20 аминокислот или длиной более 20 аминокислот. Фрагмент рекомбинантного белка можно получать с применением любого из способов, описанных в данном документе.
Термин "сконструированный белок" означает полипептид, который в естественных условиях не кодируется эндогенной нуклеиновой кислотой, присутствующей в организме (например, млекопитающего). Примеры сконструированных белков включают ферменты (например, с одной или несколькими аминокислотными заменами, делециями, вставками или добавлениями, которые приводят к повышенной стабильности и/или каталитической активности сконструированного фермента), слитые белки, антитела (например, бивалентные антитела, тривалентные антитела или диатело) и антигенсвязывающие белки, которые включают по меньшей мере одну рекомбинантную последовательность остова.
Термин "секретируемый белок" или "секретируемый рекомбинантный белок" означает белок (например, рекомбинантный белок), который изначально включал по меньшей мере одну сигнальную последовательность секреции при его трансляции внутри клетки млекопитающего, и в результате по меньшей мере частичного ферментативного отщепления сигнальной последовательности секреции в клетке млекопитающего он секретируется по меньшей мере частично во внеклеточное пространство (например, жидкую культуральную среду). Квалифицированным специалистам-практикам будет понятно, что "секретируемый" белок не должен быть полностью отделен от клетки, чтобы считаться секретируемым белком.
Термин "перфузионный биореактор" означает биореактор, содержащий некоторое количество клеток (например, клеток млекопитающего) в первой жидкой культуральной среде, где культивирование клеток, присутствующих в биореакторе, включает периодическое или непрерывное удаление первой жидкой культуральной среды и, одновременно с этим или вскоре после этого, добавление в биореактор практически такого же объема второй жидкой культуральной среды. В некоторых примерах постепенно изменяют (например, увеличивают или уменьшают) объем первой жидкой культуральной среды, удаляемой и добавляемой в течение дискретных периодов времени (например, периода времени, составляющего приблизительно 24 часа, периода времени от приблизительно 1 минуты до приблизительно 24 часов или периода времени, составляющего более 24 часов) в ходе периода культивирования (например, скорость повторной подпитки культуральной среды ежесуточно). Доля среды, удаляемой и заменяемой каждый день, может меняться в зависимости от конкретных клеток, подлежащих культивированию, исходной плотности посева и плотности клеток в конкретный момент времени. "RV" или "объем реактора" означает объем культуральной среды, присутствующей в начале процесса культивирования (например, общий объем культуральной среды, присутствующей после посева).
Термин "биореактор периодического действия с подпиткой" является термином из данной области техники и означает биореактор, содержащий некоторое количество клеток (например, клеток млекопитающего) в первой жидкой культуральной среде, где культивирование клеток, присутствующих в биореакторе, предусматривает периодическое или непрерывное добавление второй жидкой культуральной среды к первой жидкой культуральной среде без существенного или значительного удаления первой жидкой культуральной среды или второй жидкой культуральной среды из культуры клеток. Вторая жидкая культуральная среда может быть такой же, как и первая жидкая культуральная среда. В некоторых примерах культуры с периодической подпиткой вторая жидкая культуральная среда представляет собой концентрированную форму первой жидкой культуральной среды. В некоторых примерах культуры с периодической подпиткой вторую жидкую культуральную среду добавляют в виде сухого порошка.
Термин "осветленная жидкая культуральная среда" означает жидкую культуральную среду, полученную при культивировании бактериальных или дрожжевых клеток, которая практически не содержит (например, очищена на по меньшей мере 80%, 85%, 90%, 92%, 94%, 96%, 98% или 99%) бактериальных или дрожжевых клеток.
Если не определено иное, все технические и научные термины, используемые в данном документе, имеют такое же значение, которое обычно понятно специалисту в той области техники, к которой относится настоящее изобретение. Способы и материалы описаны в данном документе для применения в настоящем изобретении; при этом также можно применять другие подходящие способы и материалы, известные из уровня техники. Материалы, способы и примеры являются лишь иллюстративными и не предназначены для ограничения. Все публикации, заявки на патент, патенты, последовательности, записи в базах данных и другие ссылочные материалы, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. В случае противоречий данное описание, в том числе определения, будут иметь преимущественную силу.
Другие признаки и преимущества настоящего изобретения станут очевидны из нижеследующих подробного описания и фигур, а также из формулы изобретения.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1 представляет собой график, на котором показана связывающая способность в процентах (по сравнению с не подвергнутой воздействию излучения смолой для хроматографии, загруженной тем же материалом) для MabSelectTM SuReTM (смола для хроматографии на основе связывания с белком A) в течение нескольких циклов хроматографии после воздействия 40-49 кГр излучения, в присутствии одного из следующих буферов: (i) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина и 25 мМ маннита в 50 мМ натрий-фосфатного буфера ("SMM'H"); (ii) 2% об./об. бензилового спирта ("2% BA") и (iii) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита и 2% об./об. бензилового спирта в 50 мМ натрий-фосфатного буфера ("SMM'H+2% BA").
Фиг. 2 представляет собой график, на котором показана связывающая способность в процентах (по сравнению с не подвергнутой воздействию излучения смолой для хроматографии, загруженной тем же материалом) для смолы для хроматографии Capto Adhere в течение нескольких циклов хроматографии после воздействия 28-34 кГр или 40-49 кГр излучения (описанного в примере 2), в присутствии одного из следующих буферов: (i) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина и 25 мМ маннита в 50 мМ натрий-фосфатного буфера ("SMM'H") или (ii) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита и 2% об./об. бензилового спирта в 50 мМ натрий-фосфатного буфера ("SMM'H+2% BA").
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе предусмотрены способы уменьшения бионагрузки в смоле для хроматографии, которые предусматривают подвергание контейнера, включающего композицию, включающую (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один (например, два, три, четыре или пять) спирт, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после/во время воздействия дозы гамма-излучения. Также предусмотрены хроматографические колонки с уменьшенной бионагрузкой, содержащие смолу для хроматографии с уменьшенной бионагрузкой, полученную с помощью любого из способов, описанных в данном документе; композиции, включающие (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один (например, два, три, четыре или пять) спирт; способы выполнения хроматографии на колонке с уменьшенной бионагрузкой с применением по меньшей мере одной из таких хроматографических колонок с уменьшенной бионагрузкой и интегрированные закрытые или по сути закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают применение по меньшей мере одной из таких хроматографических колонок с уменьшенной бионагрузкой. Неограничивающие аспекты таких способов и процессов описаны ниже. Как можно понять из уровня техники, различные аспекты, описанные ниже, можно применять в любой комбинации без ограничения.
Композиции, содержащие смолу для хроматографии и по меньшей мере один спирт
В данном документе предусмотрены композиции, включающие (i) смолу для хроматографии (например, любую из смол для хроматографии, описанных в данном документе или известных из уровня техники) и (ii) жидкость, включающую по меньшей мере один (например, два, три, четыре или пять) спирт (например, любой из иллюстративных спиртов, описанных в данном документе или известных из уровня техники), где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции. Например, смола для хроматографии может представлять собой по меньшей мере одну из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной или псевдоаффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии или любой их комбинации. В некоторых примерах смола для хроматографии представляет собой смолу, включающую белковый или пептидный лиганд (например, смолу для аффинной хроматографии с белковым или пептидным лигандом, например, смола для хроматографии на основе связывания с белком A или белком G).
Композиция, например, может представлять собой взвесь осажденной смолы для хроматографии. В некоторых примерах композиция может представлять собой смоченную или влажную твердую смесь. В некоторых примерах композиция представляет собой смолу для хроматографии, помещенную в жидкость.
В некоторых примерах любой из композиций по меньшей мере один (например, два, три, четыре или пять) спирт может быть выбран из группы, состоящей из бензилового спирта, циклогексанола, изобутилового спирта, 2-метил-2-бутанола, метанола, этанола, пропан-2-ола, пропан-1-ола, бутан-1-ола, пентан-1-ола, гексадекан-1-ола, 2-фенилэтанола, втор-фенилэтанола, 3-фенил-1-пропанола, 1-фенил-1-пропанола, 2-фенил-1-пропанола, 2-фенил-2-пропанола, 1-фенил-2-бутанола, 2-фенил-1-бутанола, 3-фенил-1-бутанола, 4-фенил-2-бутанола, DL-1-фенил-2-пентанола, 5-фенил-1-пентанола и 4-фенил-1-бутанола. В некоторых примерах по меньшей мере один спирт может представлять собой бензиловый спирт.
В некоторых примерах любой из композиций общая суммарная концентрация одного или нескольких спиртов в жидкости или композиции составляет от приблизительно 0,01% об./об. до приблизительно 20% об./об., от приблизительно 0,01% об./об. до приблизительно 19% об./об., от приблизительно 0,01% об./об. до приблизительно 18% об./об., от приблизительно 0,01% об./об. до приблизительно 17% об./об., от приблизительно 0,01% об./об. до приблизительно 16% об./об., от приблизительно 0,01% об./об. до приблизительно 15% об./об., от приблизительно 0,01% об./об. до приблизительно 14% об./об., от приблизительно 0,01% об./об. до приблизительно 13% об./об., от приблизительно 0,01% об./об. до приблизительно 12% об./об., от приблизительно 0,01% об./об. до приблизительно 11% об./об., от приблизительно 0,01% об./об. до приблизительно 10% об./об., от приблизительно 0,01% об./об. до приблизительно 9% об./об., от приблизительно 0,01% об./об. до приблизительно 8% об./об., от приблизительно 0,01% об./об. до приблизительно 7% об./об., от приблизительно 0,01% об./об. до приблизительно 6% об./об., от приблизительно 0,01% об./об. до приблизительно 5% об./об., от приблизительно 0,01% об./об. до приблизительно 4,5% об./об., от приблизительно 0,01% об./об. до приблизительно 4,0% об./об., от приблизительно 0,01% об./об. до приблизительно 3,5% об./об., от приблизительно 0,01% об./об. до приблизительно 3,0% об./об., от приблизительно 0,01% об./об. до приблизительно 2,5% об./об., от приблизительно 0,01% об./об. до приблизительно 2,2% об./об., от приблизительно 0,01% об./об. до приблизительно 2,0% об./об., от приблизительно 0,01% об./об. до приблизительно 1,8% об./об., от приблизительно 0,01% об./об. до приблизительно 1,6% об./об., от приблизительно 0,01% об./об. до приблизительно 1,4% об./об., от приблизительно 0,01% об./об. до приблизительно 1,2% об./об., от приблизительно 0,01% об./об. до приблизительно 1,0% об./об., от приблизительно 0,01% об./об. до приблизительно 0,8% об./об., от приблизительно 0,01% об./об. до приблизительно 0,6% об./об., от приблизительно 0,01% об./об. до приблизительно 0,4% об./об., от приблизительно 0,01% об./об. до приблизительно 0,2% об./об., от приблизительно 0,01% об./об. до приблизительно 0,1% об./об., от приблизительно 0,01% об./об. до приблизительно 0,05% об./об., от приблизительно 0,05% об./об. до приблизительно 20% об./об., от приблизительно 0,05% об./об. до приблизительно 19% об./об., от приблизительно 0,05% об./об. до приблизительно 18% об./об., от приблизительно 0,05% об./об. до приблизительно 17% об./об., от приблизительно 0,05% об./об. до приблизительно 16% об./об., от приблизительно 0,05% об./об. до приблизительно 15% об./об., от приблизительно 0,05% об./об. до приблизительно 14% об./об., от приблизительно 0,05% об./об. до приблизительно 13% об./об., от приблизительно 0,05% об./об. до приблизительно 12% об./об., от приблизительно 0,05% об./об. до приблизительно 11% об./об., от приблизительно 0,05% об./об. до приблизительно 10% об./об., от приблизительно 0,05% об./об. до приблизительно 9% об./об., от приблизительно 0,05% об./об. до приблизительно 8% об./об., от приблизительно 0,05% об./об. до приблизительно 7% об./об., от приблизительно 0,05% об./об. до приблизительно 6% об./об., от приблизительно 0,05% об./об. до приблизительно 5% об./об., от приблизительно 0,05% об./об. до приблизительно 4,5% об./об., от приблизительно 0,05% об./об. до приблизительно 4,0% об./об., от приблизительно 0,05% об./об. до приблизительно 3,5% об./об., от приблизительно 0,05% об./об. до приблизительно 3,0% об./об., от приблизительно 0,05% об./об. до приблизительно 2,5% об./об., от приблизительно 0,05% об./об. до приблизительно 2,2% об./об., от приблизительно 0,05% об./об. до приблизительно 2,0% об./об., от приблизительно 0,05% об./об. до приблизительно 1,8% об./об., от приблизительно 0,05% об./об. до приблизительно 1,6% об./об., от приблизительно 0,05% об./об. до приблизительно 1,4% об./об., от приблизительно 0,05% об./об. до приблизительно 1,2% об./об., от приблизительно 0,05% об./об. до приблизительно 1,0% об./об., от приблизительно 0,05% об./об. до приблизительно 0,8% об./об., от приблизительно 0,05% об./об. до приблизительно 0,6% об./об., от приблизительно 0,05% об./об. до приблизительно 0,4% об./об., от приблизительно 0,05% об./об. до приблизительно 0,2% об./об., от приблизительно 0,05% об./об. до приблизительно 0,1% об./об., от приблизительно 0,1% об./об. до приблизительно 20% об./об., от приблизительно 0,1% об./об. до приблизительно 19% об./об., от приблизительно 0,1% об./об. до приблизительно 18% об./об., от приблизительно 0,1% об./об. до приблизительно 17% об./об., от приблизительно 0,1% об./об. до приблизительно 16% об./об., от приблизительно 0,1% об./об. до приблизительно 15% об./об., от приблизительно 0,1% об./об. до приблизительно 14% об./об., от приблизительно 0,1% об./об. до приблизительно 13% об./об., от приблизительно 0,1% об./об. до приблизительно 12% об./об., от приблизительно 0,1% об./об. до приблизительно 11% об./об., от приблизительно 0,1% об./об. до приблизительно 10% об./об., от приблизительно 0,1% об./об. до приблизительно 9% об./об., от приблизительно 0,1% об./об. до приблизительно 8% об./об., от приблизительно 0,1% об./об. до приблизительно 7% об./об., от приблизительно 0,1% об./об. до приблизительно 6% об./об., от приблизительно 0,1% об./об. до приблизительно 5% об./об., от приблизительно 0,1% об./об. до приблизительно 4,5% об./об., от приблизительно 0,1% об./об. до приблизительно 4,0% об./об., от приблизительно 0,1% об./об. до приблизительно 3,5% об./об., от приблизительно 0,1% об./об. до приблизительно 3,0% об./об., от приблизительно 0,1% об./об. до приблизительно 2,5% об./об., от приблизительно 0,1% об./об. до приблизительно 2,2% об./об., от приблизительно 0,1% об./об. до приблизительно 2,0% об./об., от приблизительно 0,1% об./об. до приблизительно 1,8% об./об., от приблизительно 0,1% об./об. до приблизительно 1,6% об./об., от приблизительно 0,1% об./об. до приблизительно 1,4% об./об., от приблизительно 0,1% об./об. до приблизительно 1,2% об./об., от приблизительно 0,1% об./об. до приблизительно 1,0% об./об., от приблизительно 0,1% об./об. до приблизительно 0,8% об./об., от приблизительно 0,1% об./об. до приблизительно 0,6% об./об., от приблизительно 0,1% об./об. до приблизительно 0,4% об./об., от приблизительно 0,1% об./об. до приблизительно 0,2% об./об., от приблизительно 0,2% об./об. до приблизительно 20% об./об., от приблизительно 0,2% об./об. до приблизительно 19% об./об., от приблизительно 0,2% об./об. до приблизительно 18% об./об., от приблизительно 0,2% об./об. до приблизительно 17% об./об., от приблизительно 0,2% об./об. до приблизительно 16% об./об., от приблизительно 0,2% об./об. до приблизительно 15% об./об., от приблизительно 0,2% об./об. до приблизительно 14% об./об., от приблизительно 0,2% об./об. до приблизительно 13% об./об., от приблизительно 0,2% об./об. до приблизительно 12% об./об., от приблизительно 0,2% об./об. до приблизительно 11% об./об., от приблизительно 0,2% об./об. до приблизительно 10% об./об., от приблизительно 0,2% об./об. до приблизительно 9% об./об., от приблизительно 0,2% об./об. до приблизительно 8% об./об., от приблизительно 0,2% об./об. до приблизительно 7% об./об., от приблизительно 0,2% об./об. до приблизительно 6% об./об., от приблизительно 0,2% об./об. до приблизительно 5% об./об., от приблизительно 0,2% об./об. до приблизительно 4,5% об./об., от приблизительно 0,2% об./об. до приблизительно 4,0% об./об., от приблизительно 0,2% об./об. до приблизительно 3,5% об./об., от приблизительно 0,2% об./об. до приблизительно 3,0% об./об., от приблизительно 0,2% об./об. до приблизительно 2,5% об./об., от приблизительно 0,2% об./об. до приблизительно 2,2% об./об., от приблизительно 0,2% об./об. до приблизительно 2,0% об./об., от приблизительно 0,2% об./об. до приблизительно 1,8% об./об., от приблизительно 0,2% об./об. до приблизительно 1,6% об./об., от приблизительно 0,2% об./об. до приблизительно 1,4% об./об., от приблизительно 0,2% об./об. до приблизительно 1,2% об./об., от приблизительно 0,2% об./об. до приблизительно 1,0% об./об., от приблизительно 0,2% об./об. до приблизительно 0,8% об./об., от приблизительно 0,2% об./об. до приблизительно 0,6% об./об., от приблизительно 0,2% об./об. до приблизительно 0,4% об./об., от приблизительно 0,4% об./об. до приблизительно 20% об./об., от приблизительно 0,4% об./об. до приблизительно 19% об./об., от приблизительно 0,4% об./об. до приблизительно 18% об./об., от приблизительно 0,4% об./об. до приблизительно 17% об./об., от приблизительно 0,4% об./об. до приблизительно 16% об./об., от приблизительно 0,4% об./об. до приблизительно 15% об./об., от приблизительно 0,4% об./об. до приблизительно 14% об./об., от приблизительно 0,4% об./об. до приблизительно 13% об./об., от приблизительно 0,4% об./об. до приблизительно 12% об./об., от приблизительно 0,4% об./об. до приблизительно 11% об./об., от приблизительно 0,4% об./об. до приблизительно 10% об./об., от приблизительно 0,4% об./об. до приблизительно 9% об./об., от приблизительно 0,4% об./об. до приблизительно 8% об./об., от приблизительно 0,4% об./об. до приблизительно 7% об./об., от приблизительно 0,4% об./об. до приблизительно 6% об./об., от приблизительно 0,4% об./об. до приблизительно 5% об./об., от приблизительно 0,4% об./об. до приблизительно 4,5% об./об., от приблизительно 0,4% об./об. до приблизительно 4,0% об./об., от приблизительно 0,4% об./об. до приблизительно 3,5% об./об., от приблизительно 0,4% об./об. до приблизительно 3,0% об./об., от приблизительно 0,4% об./об. до приблизительно 2,5% об./об., от приблизительно 0,4% об./об. до приблизительно 2,2% об./об., от приблизительно 0,4% об./об. до приблизительно 2,0% об./об., от приблизительно 0,4% об./об. до приблизительно 1,8% об./об., от приблизительно 0,4% об./об. до приблизительно 1,6% об./об., от приблизительно 0,4% об./об. до приблизительно 1,4% об./об., от приблизительно 0,4% об./об. до приблизительно 1,2% об./об., от приблизительно 0,4% об./об. до приблизительно 1,0% об./об., от приблизительно 0,4% об./об. до приблизительно 0,8% об./об., от приблизительно 0,4% об./об. до приблизительно 0,6% об./об., от приблизительно 0,6% об./об. до приблизительно 20% об./об., от приблизительно 0,6% об./об. до приблизительно 19% об./об., от приблизительно 0,6% об./об. до приблизительно 18% об./об., от приблизительно 0,6% об./об. до приблизительно 17% об./об., от приблизительно 0,6% об./об. до приблизительно 16% об./об., от приблизительно 0,6% об./об. до приблизительно 15% об./об., от приблизительно 0,6% об./об. до приблизительно 14% об./об., от приблизительно 0,6% об./об. до приблизительно 13% об./об., от приблизительно 0,6% об./об. до приблизительно 12% об./об., от приблизительно 0,6% об./об. до приблизительно 11% об./об., от приблизительно 0,6% об./об. до приблизительно 10% об./об., от приблизительно 0,6% об./об. до приблизительно 9% об./об., от приблизительно 0,6% об./об. до приблизительно 8% об./об., от приблизительно 0,6% об./об. до приблизительно 7% об./об., от приблизительно 0,6% об./об. до приблизительно 6% об./об., от приблизительно 0,6% об./об. до приблизительно 5% об./об., от приблизительно 0,6% об./об. до приблизительно 4,5% об./об., от приблизительно 0,6% об./об. до приблизительно 4,0% об./об., от приблизительно 0,6% об./об. до приблизительно 3,5% об./об., от приблизительно 0,6% об./об. до приблизительно 3,0% об./об., от приблизительно 0,6% об./об. до приблизительно 2,5% об./об., от приблизительно 0,6% об./об. до приблизительно 2,2% об./об., от приблизительно 0,6% об./об. до приблизительно 2,0% об./об., от приблизительно 0,6% об./об. до приблизительно 1,8% об./об., от приблизительно 0,6% об./об. до приблизительно 1,6% об./об., от приблизительно 0,6% об./об. до приблизительно 1,4% об./об., от приблизительно 0,6% об./об. до приблизительно 1,2% об./об., от приблизительно 0,6% об./об. до приблизительно 1,0% об./об., от приблизительно 0,6% об./об. до приблизительно 0,8% об./об., от приблизительно 0,8% об./об. до приблизительно 20% об./об., от приблизительно 0,8% об./об. до приблизительно 19% об./об., от приблизительно 0,8% об./об. до приблизительно 18% об./об., от приблизительно 0,8% об./об. до приблизительно 17% об./об., от приблизительно 0,8% об./об. до приблизительно 16% об./об., от приблизительно 0,8% об./об. до приблизительно 15% об./об., от приблизительно 0,8% об./об. до приблизительно 14% об./об., от приблизительно 0,8% об./об. до приблизительно 13% об./об., от приблизительно 0,8% об./об. до приблизительно 12% об./об., от приблизительно 0,8% об./об. до приблизительно 11% об./об., от приблизительно 0,8% об./об. до приблизительно 10% об./об., от приблизительно 0,8% об./об. до приблизительно 9% об./об., от приблизительно 0,8% об./об. до приблизительно 8% об./об., от приблизительно 0,8% об./об. до приблизительно 7% об./об., от приблизительно 0,8% об./об. до приблизительно 6% об./об., от приблизительно 0,8% об./об. до приблизительно 5% об./об., от приблизительно 0,8% об./об. до приблизительно 4,5% об./об., от приблизительно 0,8% об./об. до приблизительно 4,0% об./об., от приблизительно 0,8% об./об. до приблизительно 3,5% об./об., от приблизительно 0,8% об./об. до приблизительно 3,0% об./об., от приблизительно 0,8% об./об. до приблизительно 2,5% об./об., от приблизительно 0,8% об./об. до приблизительно 2,2% об./об., от приблизительно 0,8% об./об. до приблизительно 2,0% об./об., от приблизительно 0,8% об./об. до приблизительно 1,8% об./об., от приблизительно 0,8% об./об. до приблизительно 1,6% об./об., от приблизительно 0,8% об./об. до приблизительно 1,4% об./об., от приблизительно 0,8% об./об. до приблизительно 1,2% об./об., от приблизительно 0,8% об./об. до приблизительно 1,0% об./об., от приблизительно 1,0% об./об. до приблизительно 20% об./об., от приблизительно 1,0% об./об. до приблизительно 19% об./об., от приблизительно 1,0% об./об. до приблизительно 18% об./об., от приблизительно 1,0% об./об. до приблизительно 17% об./об., от приблизительно 1,0% об./об. до приблизительно 16% об./об., от приблизительно 1,0% об./об. до приблизительно 15% об./об., от приблизительно 1,0% об./об. до приблизительно 14% об./об., от приблизительно 1,0% об./об. до приблизительно 13% об./об., от приблизительно 1,0% об./об. до приблизительно 12% об./об., от приблизительно 1,0% об./об. до приблизительно 11% об./об., от приблизительно 1,0% об./об. до приблизительно 10% об./об., от приблизительно 1,0% об./об. до приблизительно 9% об./об., от приблизительно 1,0% об./об. до приблизительно 8% об./об., от приблизительно 1,0% об./об. до приблизительно 7% об./об., от приблизительно 1,0% об./об. до приблизительно 6% об./об., от приблизительно 1,0% об./об. до приблизительно 5% об./об., от приблизительно 1,0% об./об. до приблизительно 4,5% об./об., от приблизительно 1,0% об./об. до приблизительно 4,0% об./об., от приблизительно 1,0% об./об. до приблизительно 3,5% об./об., от приблизительно 1,0% об./об. до приблизительно 3,0% об./об., от приблизительно 1,0% об./об. до приблизительно 2,5% об./об., от приблизительно 1,0% об./об. до приблизительно 2,2% об./об., от приблизительно 1,0% об./об. до приблизительно 2,0% об./об., от приблизительно 1,0% об./об. до приблизительно 1,8% об./об., от приблизительно 1,0% об./об. до приблизительно 1,6% об./об., от приблизительно 1,0% об./об. до приблизительно 1,4% об./об., от приблизительно 1,0% об./об. до приблизительно 1,2% об./об., от приблизительно 1,2% об./об. до приблизительно 20% об./об., от приблизительно 1,2% об./об. до приблизительно 19% об./об., от приблизительно 1,2% об./об. до приблизительно 18% об./об., от приблизительно 1,2% об./об. до приблизительно 17% об./об., от приблизительно 1,2% об./об. до приблизительно 16% об./об., от приблизительно 1,2% об./об. до приблизительно 15% об./об., от приблизительно 1,2% об./об. до приблизительно 14% об./об., от приблизительно 1,2% об./об. до приблизительно 13% об./об., от приблизительно 1,2% об./об. до приблизительно 12% об./об., от приблизительно 1,2% об./об. до приблизительно 11% об./об., от приблизительно 1,2% об./об. до приблизительно 10% об./об., от приблизительно 1,2% об./об. до приблизительно 9% об./об., от приблизительно 1,2% об./об. до приблизительно 8% об./об., от приблизительно 1,2% об./об. до приблизительно 7% об./об., от приблизительно 1,2% об./об. до приблизительно 6% об./об., от приблизительно 1,2% об./об. до приблизительно 5% об./об., от приблизительно 1,2% об./об. до приблизительно 4,5% об./об., от приблизительно 1,2% об./об. до приблизительно 4,0% об./об., от приблизительно 1,2% об./об. до приблизительно 3,5% об./об., от приблизительно 1,2% об./об. до приблизительно 3,0% об./об., от приблизительно 1,2% об./об. до приблизительно 2,5% об./об., от приблизительно 1,2% об./об. до приблизительно 2,2% об./об., от приблизительно 1,2% об./об. до приблизительно 2,0% об./об., от приблизительно 1,2% об./об. до приблизительно 1,8% об./об., от приблизительно 1,2% об./об. до приблизительно 1,6% об./об., от приблизительно 1,2% об./об. до приблизительно 1,4% об./об., от приблизительно 1,4% об./об. до приблизительно 20% об./об., от приблизительно 1,4% об./об. до приблизительно 19% об./об., от приблизительно 1,4% об./об. до приблизительно 18% об./об., от приблизительно 1,4% об./об. до приблизительно 17% об./об., от приблизительно 1,4% об./об. до приблизительно 16% об./об., от приблизительно 1,4% об./об. до приблизительно 15% об./об., от приблизительно 1,4% об./об. до приблизительно 14% об./об., от приблизительно 1,4% об./об. до приблизительно 13% об./об., от приблизительно 1,4% об./об. до приблизительно 12% об./об., от приблизительно 1,4% об./об. до приблизительно 11% об./об., от приблизительно 1,4% об./об. до приблизительно 10% об./об., от приблизительно 1,4% об./об. до приблизительно 9% об./об., от приблизительно 1,4% об./об. до приблизительно 8% об./об., от приблизительно 1,4% об./об. до приблизительно 7% об./об., от приблизительно 1,4% об./об. до приблизительно 6% об./об., от приблизительно 1,4% об./об. до приблизительно 5% об./об., от приблизительно 1,4% об./об. до приблизительно 4,5% об./об., от приблизительно 1,4% об./об. до приблизительно 4,0% об./об., от приблизительно 1,4% об./об. до приблизительно 3,5% об./об., от приблизительно 1,4% об./об. до приблизительно 3,0% об./об., от приблизительно 1,4% об./об. до приблизительно 2,5% об./об., от приблизительно 1,4% об./об. до приблизительно 2,2% об./об., от приблизительно 1,4% об./об. до приблизительно 2,0% об./об., от приблизительно 1,4% об./об. до приблизительно 1,8% об./об., от приблизительно 1,4% об./об. до приблизительно 1,6% об./об., от приблизительно 1,6% об./об. до приблизительно 20% об./об., от приблизительно 1,6% об./об. до приблизительно 19% об./об., от приблизительно 1,6% об./об. до приблизительно 18% об./об., от приблизительно 1,6% об./об. до приблизительно 17% об./об., от приблизительно 1,6% об./об. до приблизительно 16% об./об., от приблизительно 1,6% об./об. до приблизительно 15% об./об., от приблизительно 1,6% об./об. до приблизительно 14% об./об., от приблизительно 1,6% об./об. до приблизительно 13% об./об., от приблизительно 1,6% об./об. до приблизительно 12% об./об., от приблизительно 1,6% об./об. до приблизительно 11% об./об., от приблизительно 1,6% об./об. до приблизительно 10% об./об., от приблизительно 1,6% об./об. до приблизительно 9% об./об., от приблизительно 1,6% об./об. до приблизительно 8% об./об., от приблизительно 1,6% об./об. до приблизительно 7% об./об., от приблизительно 1,6% об./об. до приблизительно 6% об./об., от приблизительно 1,6% об./об. до приблизительно 5% об./об., от приблизительно 1,6% об./об. до приблизительно 4,5% об./об., от приблизительно 1,6% об./об. до приблизительно 4,0% об./об., от приблизительно 1,6% об./об. до приблизительно 3,5% об./об., от приблизительно 1,6% об./об. до приблизительно 3,0% об./об., от приблизительно 1,6% об./об. до приблизительно 2,5% об./об., от приблизительно 1,6% об./об. до приблизительно 2,2% об./об., от приблизительно 1,6% об./об. до приблизительно 2,0% об./об., от приблизительно 1,6% об./об. до приблизительно 1,8% об./об., от приблизительно 1,8% об./об. до приблизительно 20% об./об., от приблизительно 1,8% об./об. до приблизительно 19% об./об., от приблизительно 1,8% об./об. до приблизительно 18% об./об., от приблизительно 1,8% об./об. до приблизительно 17% об./об., от приблизительно 1,8% об./об. до приблизительно 16% об./об., от приблизительно 1,8% об./об. до приблизительно 15% об./об., от приблизительно 1,8% об./об. до приблизительно 14% об./об., от приблизительно 1,8% об./об. до приблизительно 13% об./об., от приблизительно 1,8% об./об. до приблизительно 12% об./об., от приблизительно 1,8% об./об. до приблизительно 11% об./об., от приблизительно 1,8% об./об. до приблизительно 10% об./об., от приблизительно 1,8% об./об. до приблизительно 9% об./об., от приблизительно 1,8% об./об. до приблизительно 8% об./об., от приблизительно 1,8% об./об. до приблизительно 7% об./об., от приблизительно 1,8% об./об. до приблизительно 6% об./об., от приблизительно 1,8% об./об. до приблизительно 5% об./об., от приблизительно 1,8% об./об. до приблизительно 4,5% об./об., от приблизительно 1,8% об./об. до приблизительно 4,0% об./об., от приблизительно 1,8% об./об. до приблизительно 3,5% об./об., от приблизительно 1,8% об./об. до приблизительно 3,0% об./об., от приблизительно 1,8% об./об. до приблизительно 2,5% об./об., от приблизительно 1,8% об./об. до приблизительно 2,2% об./об., от приблизительно 1,8% об./об. до приблизительно 2,0% об./об., от приблизительно 2,0% об./об. до приблизительно 20% об./об., от приблизительно 2,0% об./об. до приблизительно 19% об./об., от приблизительно 2,0% об./об. до приблизительно 18% об./об., от приблизительно 2,0% об./об. до приблизительно 17% об./об., от приблизительно 2,0% об./об. до приблизительно 16% об./об., от приблизительно 2,0% об./об. до приблизительно 15% об./об., от приблизительно 2,0% об./об. до приблизительно 14% об./об., от приблизительно 2,0% об./об. до приблизительно 13% об./об., от приблизительно 2,0% об./об. до приблизительно 12% об./об., от приблизительно 2,0% об./об. до приблизительно 11% об./об., от приблизительно 2,0% об./об. до приблизительно 10% об./об., от приблизительно 2,0% об./об. до приблизительно 9% об./об., от приблизительно 2,0% об./об. до приблизительно 8% об./об., от приблизительно 2,0% об./об. до приблизительно 7% об./об., от приблизительно 2,0% об./об. до приблизительно 6% об./об., от приблизительно 2,0% об./об. до приблизительно 5% об./об., от приблизительно 2,0% об./об. до приблизительно 4,5% об./об., от приблизительно 2,0% об./об. до приблизительно 4,0% об./об., от приблизительно 2,0% об./об. до приблизительно 3,5% об./об., от приблизительно 2,0% об./об. до приблизительно 3,0% об./об., от приблизительно 2,0% об./об. до приблизительно 2,5% об./об., от приблизительно 2,0% об./об. до приблизительно 2,2% об./об., от приблизительно 2,2% об./об. до приблизительно 20% об./об., от приблизительно 2,2% об./об. до приблизительно 19% об./об., от приблизительно 2,2% об./об. до приблизительно 18% об./об., от приблизительно 2,2% об./об. до приблизительно 17% об./об., от приблизительно 2,2% об./об. до приблизительно 16% об./об., от приблизительно 2,2% об./об. до приблизительно 15% об./об., от приблизительно 2,2% об./об. до приблизительно 14% об./об., от приблизительно 2,2% об./об. до приблизительно 13% об./об., от приблизительно 2,2% об./об. до приблизительно 12% об./об., от приблизительно 2,2% об./об. до приблизительно 11% об./об., от приблизительно 2,2% об./об. до приблизительно 10% об./об., от приблизительно 2,2% об./об. до приблизительно 9% об./об., от приблизительно 2,2% об./об. до приблизительно 8% об./об., от приблизительно 2,2% об./об. до приблизительно 7% об./об., от приблизительно 2,2% об./об. до приблизительно 6% об./об., от приблизительно 2,2% об./об. до приблизительно 5% об./об., от приблизительно 2,2% об./об. до приблизительно 4,5% об./об., от приблизительно 2,2% об./об. до приблизительно 4,0% об./об., от приблизительно 2,2% об./об. до приблизительно 3,5% об./об., от приблизительно 2,2% об./об. до приблизительно 3,0% об./об., от приблизительно 2,2% об./об. до приблизительно 2,5% об./об., от приблизительно 2,5% об./об. до приблизительно 20% об./об., от приблизительно 2,5% об./об. до приблизительно 19% об./об., от приблизительно 2,5% об./об. до приблизительно 18% об./об., от приблизительно 2,5% об./об. до приблизительно 17% об./об., от приблизительно 2,5% об./об. до приблизительно 16% об./об., от приблизительно 2,5% об./об. до приблизительно 15% об./об., от приблизительно 2,5% об./об. до приблизительно 14% об./об., от приблизительно 2,5% об./об. до приблизительно 13% об./об., от приблизительно 2,5% об./об. до приблизительно 12% об./об., от приблизительно 2,5% об./об. до приблизительно 11% об./об., от приблизительно 2,5% об./об. до приблизительно 10% об./об., от приблизительно 2,5% об./об. до приблизительно 9% об./об., от приблизительно 2,5% об./об. до приблизительно 8% об./об., от приблизительно 2,5% об./об. до приблизительно 7% об./об., от приблизительно 2,5% об./об. до приблизительно 6% об./об., от приблизительно 2,5% об./об. до приблизительно 5% об./об., от приблизительно 2,5% об./об. до приблизительно 4,5% об./об., от приблизительно 2,5% об./об. до приблизительно 4,0% об./об., от приблизительно 2,5% об./об. до приблизительно 3,5% об./об., от приблизительно 2,5% об./об. до приблизительно 3,0% об./об., от приблизительно 3,0% об./об. до приблизительно 20% об./об., от приблизительно 3,0% об./об. до приблизительно 19% об./об., от приблизительно 3,0% об./об. до приблизительно 18% об./об., от приблизительно 3,0% об./об. до приблизительно 17% об./об., от приблизительно 3,0% об./об. до приблизительно 16% об./об., от приблизительно 3,0% об./об. до приблизительно 15% об./об., от приблизительно 3,0% об./об. до приблизительно 14% об./об., от приблизительно 3,0% об./об. до приблизительно 13% об./об., от приблизительно 3,0% об./об. до приблизительно 12% об./об., от приблизительно 3,0% об./об. до приблизительно 11% об./об., от приблизительно 3,0% об./об. до приблизительно 10% об./об., от приблизительно 3,0% об./об. до приблизительно 9% об./об., от приблизительно 3,0% об./об. до приблизительно 8% об./об., от приблизительно 3,0% об./об. до приблизительно 7% об./об., от приблизительно 3,0% об./об. до приблизительно 6% об./об., от приблизительно 3,0% об./об. до приблизительно 5% об./об., от приблизительно 3,0% об./об. до приблизительно 4,5% об./об., от приблизительно 3,0% об./об. до приблизительно 4,0% об./об., от приблизительно 3,0% об./об. до приблизительно 3,5% об./об., от приблизительно 3,5% об./об. до приблизительно 20% об./об., от приблизительно 3,5% об./об. до приблизительно 19% об./об., от приблизительно 3,5% об./об. до приблизительно 18% об./об., от приблизительно 3,5% об./об. до приблизительно 17% об./об., от приблизительно 3,5% об./об. до приблизительно 16% об./об., от приблизительно 3,5% об./об. до приблизительно 15% об./об., от приблизительно 3,5% об./об. до приблизительно 14% об./об., от приблизительно 3,5% об./об. до приблизительно 13% об./об., от приблизительно 3,5% об./об. до приблизительно 12% об./об., от приблизительно 3,5% об./об. до приблизительно 11% об./об., от приблизительно 3,5% об./об. до приблизительно 10% об./об., от приблизительно 3,5% об./об. до приблизительно 9% об./об., от приблизительно 3,5% об./об. до приблизительно 8% об./об., от приблизительно 3,5% об./об. до приблизительно 7% об./об., от приблизительно 3,5% об./об. до приблизительно 6% об./об., от приблизительно 3,5% об./об. до приблизительно 5% об./об., от приблизительно 3,5% об./об. до приблизительно 4,5% об./об., от приблизительно 3,5% об./об. до приблизительно 4,0% об./об., от приблизительно 4,0% об./об. до приблизительно 20% об./об., от приблизительно 4,0% об./об. до приблизительно 19% об./об., от приблизительно 4,0% об./об. до приблизительно 18% об./об., от приблизительно 4,0% об./об. до приблизительно 17% об./об., от приблизительно 4,0% об./об. до приблизительно 16% об./об., от приблизительно 4,0% об./об. до приблизительно 15% об./об., от приблизительно 4,0% об./об. до приблизительно 14% об./об., от приблизительно 4,0% об./об. до приблизительно 13% об./об., от приблизительно 4,0% об./об. до приблизительно 12% об./об., от приблизительно 4,0% об./об. до приблизительно 11% об./об., от приблизительно 4,0% об./об. до приблизительно 10% об./об., от приблизительно 4,0% об./об. до приблизительно 9% об./об., от приблизительно 4,0% об./об. до приблизительно 8% об./об., от приблизительно 4,0% об./об. до приблизительно 7% об./об., от приблизительно 4,0% об./об. до приблизительно 6% об./об., от приблизительно 4,0% об./об. до приблизительно 5% об./об., от приблизительно 4,0% об./об. до приблизительно 4,5% об./об., от приблизительно 4,5% об./об. до приблизительно 20% об./об., от приблизительно 4,5% об./об. до приблизительно 19% об./об., от приблизительно 4,5% об./об. до приблизительно 18% об./об., от приблизительно 4,5% об./об. до приблизительно 17% об./об., от приблизительно 4,5% об./об. до приблизительно 16% об./об., от приблизительно 4,5% об./об. до приблизительно 15% об./об., от приблизительно 4,5% об./об. до приблизительно 14% об./об., от приблизительно 4,5% об./об. до приблизительно 13% об./об., от приблизительно 4,5% об./об. до приблизительно 12% об./об., от приблизительно 4,5% об./об. до приблизительно 11% об./об., от приблизительно 4,5% об./об. до приблизительно 10% об./об., от приблизительно 4,5% об./об. до приблизительно 9% об./об., от приблизительно 4,5% об./об. до приблизительно 8% об./об., от приблизительно 4,5% об./об. до приблизительно 7% об./об., от приблизительно 4,5% об./об. до приблизительно 6% об./об., от приблизительно 4,5% об./об. до приблизительно 5% об./об., от приблизительно 5% об./об. до приблизительно 20% об./об., от приблизительно 5% об./об. до приблизительно 19% об./об., от приблизительно 5% об./об. до приблизительно 18% об./об., от приблизительно 5% об./об. до приблизительно 17% об./об., от приблизительно 5% об./об. до приблизительно 16% об./об., от приблизительно 5% об./об. до приблизительно 15% об./об., от приблизительно 5% об./об. до приблизительно 14% об./об., от приблизительно 5% об./об. до приблизительно 13% об./об., от приблизительно 5% об./об. до приблизительно 12% об./об., от приблизительно 5% об./об. до приблизительно 11% об./об., от приблизительно 5% об./об. до приблизительно 10% об./об., от приблизительно 5% об./об. до приблизительно 9% об./об., от приблизительно 5% об./об. до приблизительно 8% об./об., от приблизительно 5% об./об. до приблизительно 7% об./об., от приблизительно 5% об./об. до приблизительно 6% об./об., от приблизительно 6% об./об. до приблизительно 20% об./об., от приблизительно 6% об./об. до приблизительно 19% об./об., от приблизительно 6% об./об. до приблизительно 18% об./об., от приблизительно 6% об./об. до приблизительно 17% об./об., от приблизительно 6% об./об. до приблизительно 16% об./об., от приблизительно 6% об./об. до приблизительно 15% об./об., от приблизительно 6% об./об. до приблизительно 14% об./об., от приблизительно 6% об./об. до приблизительно 13% об./об., от приблизительно 6% об./об. до приблизительно 12% об./об., от приблизительно 6% об./об. до приблизительно 11% об./об., от приблизительно 6% об./об. до приблизительно 10% об./об., от приблизительно 6% об./об. до приблизительно 9% об./об., от приблизительно 6% об./об. до приблизительно 8% об./об., от приблизительно 6% об./об. до приблизительно 7% об./об., от приблизительно 7% об./об. до приблизительно 20% об./об., от приблизительно 7% об./об. до приблизительно 19% об./об., от приблизительно 7% об./об. до приблизительно 18% об./об., от приблизительно 7% об./об. до приблизительно 17% об./об., от приблизительно 7% об./об. до приблизительно 16% об./об., от приблизительно 7% об./об. до приблизительно 15% об./об., от приблизительно 7% об./об. до приблизительно 14% об./об., от приблизительно 7% об./об. до приблизительно 13% об./об., от приблизительно 7% об./об. до приблизительно 12% об./об., от приблизительно 7% об./об. до приблизительно 11% об./об., от приблизительно 7% об./об. до приблизительно 10% об./об., от приблизительно 7% об./об. до приблизительно 9% об./об., от приблизительно 7% об./об. до приблизительно 8% об./об., от приблизительно 8% об./об. до приблизительно 20% об./об., от приблизительно 8% об./об. до приблизительно 19% об./об., от приблизительно 8% об./об. до приблизительно 18% об./об., от приблизительно 8% об./об. до приблизительно 17% об./об., от приблизительно 8% об./об. до приблизительно 16% об./об., от приблизительно 8% об./об. до приблизительно 15% об./об., от приблизительно 8% об./об. до приблизительно 14% об./об., от приблизительно 8% об./об. до приблизительно 13% об./об., от приблизительно 8% об./об. до приблизительно 12% об./об., от приблизительно 8% об./об. до приблизительно 11% об./об., от приблизительно 8% об./об. до приблизительно 10% об./об., от приблизительно 8% об./об. до приблизительно 9% об./об., от приблизительно 9% об./об. до приблизительно 20% об./об., от приблизительно 9% об./об. до приблизительно 19% об./об., от приблизительно 9% об./об. до приблизительно 18% об./об., от приблизительно 9% об./об. до приблизительно 17% об./об., от приблизительно 9% об./об. до приблизительно 16% об./об., от приблизительно 9% об./об. до приблизительно 15% об./об., от приблизительно 9% об./об. до приблизительно 14% об./об., от приблизительно 9% об./об. до приблизительно 13% об./об., от приблизительно 9% об./об. до приблизительно 12% об./об., от приблизительно 9% об./об. до приблизительно 11% об./об., от приблизительно 9% об./об. до приблизительно 10% об./об., от приблизительно 10% об./об. до приблизительно 20% об./об., от приблизительно 10% об./об. до приблизительно 19% об./об., от приблизительно 10% об./об. до приблизительно 18% об./об., от приблизительно 10% об./об. до приблизительно 17% об./об., от приблизительно 10% об./об. до приблизительно 16% об./об., от приблизительно 10% об./об. до приблизительно 15% об./об., от приблизительно 10% об./об. до приблизительно 14% об./об., от приблизительно 10% об./об. до приблизительно 13% об./об., от приблизительно 10% об./об. до приблизительно 12% об./об., от приблизительно 10% об./об. до приблизительно 11% об./об., от приблизительно 11% об./об. до приблизительно 20% об./об., от приблизительно 11% об./об. до приблизительно 19% об./об., от приблизительно 11% об./об. до приблизительно 18% об./об., от приблизительно 11% об./об. до приблизительно 17% об./об., от приблизительно 11% об./об. до приблизительно 16% об./об., от приблизительно 11% об./об. до приблизительно 15% об./об., от приблизительно 11% об./об. до приблизительно 14% об./об., от приблизительно 11% об./об. до приблизительно 13% об./об., от приблизительно 11% об./об. до приблизительно 12% об./об., от приблизительно 12% об./об. до приблизительно 20% об./об., от приблизительно 12% об./об. до приблизительно 19% об./об., от приблизительно 12% об./об. до приблизительно 18% об./об., от приблизительно 12% об./об. до приблизительно 17% об./об., от приблизительно 12% об./об. до приблизительно 16% об./об., от приблизительно 12% об./об. до приблизительно 15% об./об., от приблизительно 12% об./об. до приблизительно 14% об./об., от приблизительно 12% об./об. до приблизительно 13% об./об., от приблизительно 13% об./об. до приблизительно 20% об./об., от приблизительно 13% об./об. до приблизительно 19% об./об., от приблизительно 13% об./об. до приблизительно 18% об./об., от приблизительно 13% об./об. до приблизительно 17% об./об., от приблизительно 13% об./об. до приблизительно 16% об./об., от приблизительно 13% об./об. до приблизительно 15% об./об., от приблизительно 13% об./об. до приблизительно 14% об./об., от приблизительно 14% об./об. до приблизительно 20% об./об., от приблизительно 14% об./об. до приблизительно 19% об./об., от приблизительно 14% об./об. до приблизительно 18% об./об., от приблизительно 14% об./об. до приблизительно 17% об./об., от приблизительно 14% об./об. до приблизительно 16% об./об., от приблизительно 14% об./об. до приблизительно 15% об./об., от приблизительно 15% об./об. до приблизительно 20% об./об., от приблизительно 15% об./об. до приблизительно 19% об./об., от приблизительно 15% об./об. до приблизительно 18% об./об., от приблизительно 15% об./об. до приблизительно 17% об./об., от приблизительно 15% об./об. до приблизительно 16% об./об., от приблизительно 16% об./об. до приблизительно 20% об./об., от приблизительно 16% об./об. до приблизительно 19% об./об., от приблизительно 16% об./об. до приблизительно 18% об./об., от приблизительно 16% об./об. до приблизительно 17% об./об., от приблизительно 17% об./об. до приблизительно 20% об./об., от приблизительно 17% об./об. до приблизительно 19% об./об., от приблизительно 17% об./об. до приблизительно 18% об./об., от приблизительно 18% об./об. до приблизительно 20% об./об., от приблизительно 18% об./об. до приблизительно 19% об./об. или от приблизительно 19% об./об. до приблизительно 20% об./об.
В некоторых примерах любой из композиций, описанных в данном документе, жидкость может дополнительно включать по меньшей мере один (например, два, три, четыре или пять) антиоксидант и/или хелатор. В некоторых примерах любой из композиций, описанных в данном документе, жидкость может дополнительно включать по меньшей мере один (например, два, три, четыре или пять) антиоксидант и/или хелатор в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
В некоторых примерах любой из композиций, описанных в данном документе, жидкость может включать по меньшей мере один (например, два, три, четыре или пять) антиоксидант, выбранный из группы, состоящей из восстановленного глутатиона, восстановленного тиоредоксина, восстановленного цистеина, каротиноида, мелатонина, ликопина, токоферола, восстановленного убихинона, аскорбата, билирубина, мочевой кислоты, липоевой кислоты, флавоноида, фенолпропановой кислоты, лидокаина, нарингина, фуллерена, глюкозы, маннита, 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила и диметилметоксихроманола. В некоторых примерах любой из композиций, описанных в данном документе, жидкость может включать по меньшей мере один (например, два, три или четыре) антиоксидант, выбранный из группы, состоящей из маннита, аскорбата натрия, гистидина и метионина.
В некоторых примерах любой из композиций, описанных в данном документе, жидкость может содержать по меньшей мере одно (например, один, два, три или четыре) из метионина (или, в качестве альтернативы, цистеина или глутатиона), аскорбата натрия, гистидина и маннита. В некоторых примерах любой из композиций, описанных в данном документе, жидкость может содержать метионин (или, в качестве альтернативы, цистеин или глутатион), аскорбат натрия, гистидин и маннит. В некоторых примерах любой из композиций, описанных в данном документе, жидкость может включать (i) от 75 мМ до приблизительно 125 мМ (например, от 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) маннита; (ii) от 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона); (iii) от 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) аскорбата натрия; (iv) от 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) гистидина; (v) от приблизительно 30 мМ до приблизительно 70 мМ (например, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ или от приблизительно 45 мМ до приблизительно 55 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона) и от приблизительно 30 мМ до приблизительно 70 мМ (например, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ или от приблизительно 45 мМ до приблизительно 55 мМ) гистидина; (vi) от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ или от приблизительно 25 мМ до приблизительно 35 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона), от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ или от приблизительно 25 мМ до приблизительно 35 мМ) гистидина и от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ или от приблизительно 25 мМ до приблизительно 35 мМ) аскорбата натрия или (vii) от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ или от приблизительно 20 мМ до приблизительно 30 мМ) аскорбата натрия, от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ или от приблизительно 20 мМ до приблизительно 30 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона), от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ или от приблизительно 20 мМ до приблизительно 30 мМ) маннита и от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ или от приблизительно 20 мМ до приблизительно 30 мМ) гистидина. В некоторых примерах любой из композиций, описанных в данном документе, жидкость может представлять собой буферный раствор (например, фосфатно-буферный раствор, например, натрий-фосфатно-буферный раствор, такой как 50 мМ фосфата натрия, pH 6,0).
В некоторых вариантах осуществления любой из композиций, описанных в данном документе, жидкость может дополнительно включать по меньшей мере один (например, два, три, четыре или пять) хелатор (например, по меньшей мере один хелатор, выбранный из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), соли натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарной кислоты (DMSA), металлотионина и дефероксамина).
Также в данном документе предусмотрен контейнер (например, сосуд для хранения, например, пластиковый контейнер, или хроматографическая колонка), включающий композицию (например, любую из иллюстративных композиций, описанных в данном документе), включающую (i) смолу для хроматографии (например, любую из смол для хроматографии, описанных в данном документе или известных из уровня техники) и (ii) жидкость, включающую по меньшей мере один спирт (например, любой из иллюстративных спиртов, описанных в данном документе или известных из уровня техники), где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции. Например, контейнер (например, контейнер для хранения, например, пластиковый контейнер, или хроматографическая колонка) может характеризоваться внутренним объемом, составляющим, например, по меньшей мере приблизительно 1 мл, 5 мл, по меньшей мере приблизительно 10 мл, по меньшей мере приблизительно 20 мл, по меньшей мере приблизительно 30 мл, по меньшей мере приблизительно 40 мл, по меньшей мере приблизительно 50 мл, по меньшей мере приблизительно 60 мл, по меньшей мере приблизительно 70 мл, по меньшей мере приблизительно 80 мл, по меньшей мере приблизительно 90 мл, по меньшей мере приблизительно 100 мл, по меньшей мере приблизительно 110 мл, по меньшей мере приблизительно 120 мл, по меньшей мере приблизительно 130 мл, по меньшей мере приблизительно 140 мл, по меньшей мере приблизительно 150 мл, по меньшей мере приблизительно 160 мл, по меньшей мере приблизительно 170 мл, по меньшей мере приблизительно 180 мл, по меньшей мере приблизительно 190 мл, по меньшей мере приблизительно 200 мл, по меньшей мере приблизительно 210 мл, по меньшей мере приблизительно 220 мл, по меньшей мере приблизительно 230 мл, по меньшей мере приблизительно 240 мл, по меньшей мере приблизительно 250 мл, по меньшей мере 300 мл, по меньшей мере 350 мл, по меньшей мере 400 мл или по меньшей мере 500 мл. Например, контейнер может характеризоваться внутренним объемом, составляющим, например, от приблизительно 1 мл до приблизительно 500 мл, от приблизительно 1 мл до приблизительно 50 мл, от приблизительно 5 мл до приблизительно 500 мл, от приблизительно 5 мл до приблизительно 400 мл, от приблизительно 5 мл до приблизительно 350 мл, от приблизительно 5 мл до приблизительно 300 мл, от приблизительно 5 мл до приблизительно 250 мл, от приблизительно 5 мл до приблизительно 200 мл, от приблизительно 5 мл до приблизительно 150 мл, от приблизительно 5 мл до приблизительно 100 мл или от приблизительно 5 мл до приблизительно 50 мл. В некоторых примерах смола для хроматографии в контейнере представляет собой взвесь осажденной смолы для хроматографии в жидкости. В некоторых примерах контейнер включает смолу для хроматографии в качестве насадки (например, помещенную в жидкость).
В любой из композиций, предусмотренных в данном документе, жидкость может дополнительно содержать по меньшей мере один (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10) антиоксидант и/или по меньшей мере один (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10) хелатор. Любой из антиоксидантов, которые можно включать в любую из композиций, предусмотренных в данном документе, может обладать способностью гасить одну или несколько из следующих реактивных форм кислорода и/или азота: гидроксильный радикал, карбонатный радикал, супероксид-анион, пероксильный радикал, пероксинитрит, диоксид азота и оксид азота. Неограничивающие примеры антиоксидантов, которые можно включать в любую из композиций, предусмотренных в данном документе, включают восстановленный глутатион, восстановленный тиоредоксин, восстановленный цистеин, каротиноид, мелатонин, ликопин, токоферол, восстановленный убихинон, аскорбат, билирубин, мочевую кислоту, липоевую кислоту, флавоноид, фенолпропановую кислоту, лидокаин, нарингин, фуллерен, глюкозу, маннит, 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксил и диметилметоксихроманол. Дополнительные неограничивающие примеры антиоксидантов включают антиоксидантные ферменты (например, супероксиддисмутазу, глутатионпероксидазу, глутатионредуктазу, каталазу и тиоредоксинредуктазу). Дополнительные примеры антиоксидантов, которые можно включать в любую из композиций, предусмотренных в данном документе, включают маннит, аскорбат натрия, метионин и гистидин. Дополнительные примеры антиоксидантов включают цистеин, таурин, меркаптопропионилглицин, N-ацетилцистеин, масло чеснока, диаллилсульфид, дигидролипоевую кислоту и диаллилтрисульфид. Некоторые варианты осуществления, которые включают антиоксидантный фермент в качестве антиоксиданта, могут дополнительно включать один или несколько субстратов для фермента. Антиоксидант можно идентифицировать с применением ряда способов, известных из уровня техники, включающих, например, спиновую ловушку, редокс-чувствительные красители и хемолюминесцентные анализы.
Любой из хелаторов, которые могут быть включены в любую из композиций, предусмотренных в данном документе, может обладать способностью связывать редокс-активный металл (например, Cu2+ и Fe2+) с высокой аффинностью (например, приблизительно 1 мкМ или меньше, приблизительно 800 нМ или меньше, приблизительно 700 нМ или меньше, приблизительно 600 нМ или меньше, приблизительно 500 нМ или меньше, приблизительно 400 нМ или меньше, приблизительно 300 нМ или меньше, приблизительно 250 нМ или меньше, приблизительно 200 нМ или меньше, приблизительно 150 нМ или меньше, приблизительно 100 нМ или меньше, приблизительно 80 нМ или меньше, приблизительно 60 нМ или меньше, приблизительно 40 нМ или меньше, приблизительно 20 нМ или меньше или приблизительно 1 нМ или меньше). Неограничивающие примеры хелаторов, которые можно включать в любую из композиций, предусмотренных в данном документе, включают этилендиаминтетрауксусную кислоту (EDTA), соль натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарную кислоту (DMSA), металлотионин и дефероксамин.
Концентрация каждого из хелаторов и/или антиоксидантов, которые могут быть включены в любую из композиций, предусмотренных в данном документе, может составлять от приблизительно 0,1 мМ до приблизительно 150 мМ (например, от приблизительно 0,1 мМ до приблизительно 150 мМ, от приблизительно 0,1 мМ до приблизительно 125 мМ, от приблизительно 0,1 мМ до приблизительно 100 мМ, от приблизительно 0,1 мМ до приблизительно 80 мМ, от приблизительно 0,1 мМ до приблизительно 60 мМ, от приблизительно 0,1 мМ до приблизительно 50 мМ, от приблизительно 0,1 мМ до приблизительно 40 мМ, от приблизительно 0,1 мМ до приблизительно 30 мМ, от приблизительно 0,1 мМ до приблизительно 25 мМ, от приблизительно 0,1 мМ до приблизительно 20 мМ, от приблизительно 0,1 мМ до приблизительно 10 мМ, от приблизительно 0,1 мМ до приблизительно 5,0 мМ, от приблизительно 0,5 мМ до приблизительно 150 мМ, от приблизительно 0,5 мМ до приблизительно 100 мМ, от приблизительно 0,5 мМ до приблизительно 50 мМ, от приблизительно 0,5 мМ до приблизительно 25 мМ, от приблизительно 0,5 мМ до приблизительно 15 мМ, от приблизительно 0,5 мМ до приблизительно 10 мМ, от приблизительно 0,5 мМ до приблизительно 5 мМ, от приблизительно 1 мМ до приблизительно 125 мМ, от приблизительно 1 мМ до приблизительно 120 мМ, от приблизительно 1 мМ до приблизительно 100 мМ, от приблизительно 1 мМ до приблизительно 80 мМ, от приблизительно 1 мМ до приблизительно 60 мМ, от приблизительно 1 мМ до приблизительно 50 мМ, от приблизительно 1 мМ до приблизительно 40 мМ, от приблизительно 1 мМ до приблизительно 30 мМ, от приблизительно 1 мМ до приблизительно 25 мМ, от приблизительно 5 мМ до приблизительно 150 мМ, от приблизительно 5 мМ до приблизительно 125 мМ, от приблизительно 5 мМ до приблизительно 100 мМ, от приблизительно 5 мМ до приблизительно 80 мМ, от приблизительно 5 мМ до приблизительно 60 мМ, от приблизительно 5 мМ до приблизительно 50 мМ, от приблизительно 5 мМ до приблизительно 40 мМ, от приблизительно 5 мМ до приблизительно 30 мМ, от приблизительно 5 мМ до приблизительно 25 мМ, от приблизительно 10 мМ до приблизительно 150 мМ, от приблизительно 10 мМ до приблизительно 125 мМ, от приблизительно 1 мМ до приблизительно 100 мМ, от приблизительно 10 мМ до приблизительно 80 мМ, от приблизительно 10 мМ до приблизительно 60 мМ, от приблизительно 10 мМ до приблизительно 50 мМ, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 10 мМ до приблизительно 30 мМ, от приблизительно 10 мМ до приблизительно 25 мМ, от приблизительно 20 мМ до приблизительно 150 мМ, от приблизительно 20 мМ до приблизительно 125 мМ, от приблизительно 20 мМ до приблизительно 100 мМ, от приблизительно 20 мМ до приблизительно 80 мМ, от приблизительно 20 мМ до приблизительно 60 мМ, от приблизительно 20 мМ до приблизительно 50 мМ, от приблизительно 20 мМ до приблизительно 40 мМ, от приблизительно 20 мМ до приблизительно 30 мМ, от приблизительно 30 мМ до приблизительно 150 мМ, от приблизительно 30 мМ до приблизительно 125 мМ, от приблизительно 30 мМ до приблизительно 100 мМ, от приблизительно 30 мМ до приблизительно 80 мМ, от приблизительно 30 мМ до приблизительно 60 мМ, от приблизительно 30 мМ до приблизительно 50 мМ, от приблизительно 30 мМ до приблизительно 40 мМ, от приблизительно 40 мМ до приблизительно 150 мМ, от приблизительно 40 мМ до приблизительно 125 мМ, от приблизительно 40 мМ до приблизительно 100 мМ, от приблизительно 40 мМ до приблизительно 90 мМ, от приблизительно 40 мМ до приблизительно 80 мМ, от приблизительно 40 мМ до приблизительно 70 мМ, от приблизительно 40 мМ до приблизительно 60 мМ, от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 50 мМ до приблизительно 125 мМ, от приблизительно 50 мМ до приблизительно 100 мМ, от приблизительно 50 мМ до приблизительно 80 мМ, от приблизительно 50 мМ до приблизительно 60 мМ, от приблизительно 80 мМ до приблизительно 150 мМ, от приблизительно 80 мМ до приблизительно 125 мМ, от приблизительно 80 мМ до приблизительно 100 мМ, от приблизительно 100 мМ до приблизительно 150 мМ или от приблизительно 100 мМ до приблизительно 125 мМ).
В некоторых примерах композиции, предусмотренные в данном документе, могут содержать одно или несколько из маннита в количестве от 5 мМ до приблизительно 150 мМ (например, от приблизительно 10 мМ до приблизительно 150 мМ, от приблизительно 20 мМ до приблизительно 150 мМ, от приблизительно 30 мМ до приблизительно 150 мМ, от приблизительно 40 мМ до приблизительно 150 мМ, от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 60 мМ до приблизительно 140 мМ, от приблизительно 70 мМ до приблизительно 130 мМ, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 90 мМ до приблизительно 110 мМ, от приблизительно 95 мМ до приблизительно 105 мМ, от приблизительно 5 мМ до приблизительно 50 мМ, от приблизительно 5 мМ до приблизительно 45 мМ, от приблизительно 5 мМ до приблизительно 40 мМ, от приблизительно 5 мМ до приблизительно 35 мМ, от приблизительно 10 мМ до приблизительно 35 мМ, от приблизительно 15 мМ до приблизительно 35 мМ или от приблизительно 20 мМ до приблизительно 30 мМ маннита); метионина (или, в качестве альтернативы, цистеина или глутатиона) в количестве от 5 мМ до приблизительно 150 мМ (например, от приблизительно 10 мМ до приблизительно 150 мМ, от приблизительно 20 мМ до приблизительно 150 мМ, от приблизительно 30 мМ до приблизительно 150 мМ, от приблизительно 40 мМ до приблизительно 150 мМ, от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 60 мМ до приблизительно 140 мМ, от приблизительно 70 мМ до приблизительно 130 мМ, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 90 мМ до приблизительно 110 мМ, от приблизительно 95 мМ до приблизительно 105 мМ, от приблизительно 30 мМ до приблизительно 70 мМ, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ, от приблизительно 45 мМ до приблизительно 55 мМ, от приблизительно 20 мМ до приблизительно 50 мМ, от приблизительно 25 мМ до приблизительно 45 мМ, от приблизительно 30 мМ до приблизительно 40 мМ, от приблизительно 30 мМ до приблизительно 35 мМ, от приблизительно 5 мМ до приблизительно 45 мМ, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 20 мМ до приблизительно 25 мМ); аскорбата натрия в количестве от 5 мМ до 150 мМ (например, от приблизительно 10 мМ до приблизительно 150 мМ, от приблизительно 20 мМ до приблизительно 150 мМ, от приблизительно 30 мМ до приблизительно 150 мМ, от приблизительно 40 мМ до приблизительно 150 мМ, от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 60 мМ до приблизительно 140 мМ, от приблизительно 70 мМ до приблизительно 130 мМ, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 90 мМ до приблизительно 110 мМ, от приблизительно 95 мМ до приблизительно 105 мМ, от приблизительно 10 мМ до приблизительно 50 мМ, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ, от приблизительно 25 мМ до приблизительно 35 мМ, от приблизительно 30 мМ до приблизительно 35 мМ, от приблизительно 5 мМ до приблизительно 45 мМ, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ, от приблизительно 20 мМ до приблизительно 25 мМ аскорбата натрия) и гистидина в количестве от 5 мМ до приблизительно 150 мМ (например, от приблизительно 10 мМ до приблизительно 150 мМ, от приблизительно 20 мМ до приблизительно 150 мМ, от приблизительно 30 мМ до приблизительно 150 мМ, от приблизительно 40 мМ до приблизительно 150 мМ, от приблизительно 50 мМ до приблизительно 150 мМ, от приблизительно 60 мМ до приблизительно 140 мМ, от приблизительно 70 мМ до приблизительно 130 мМ, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 90 мМ до приблизительно 110 мМ, от приблизительно 95 мМ до приблизительно 105 мМ, от приблизительно 30 мМ до приблизительно 70 мМ, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ, от приблизительно 45 мМ до приблизительно 55 мМ, от приблизительно 20 мМ до приблизительно 50 мМ, от приблизительно 25 мМ до приблизительно 45 мМ, от приблизительно 30 мМ до приблизительно 40 мМ, от приблизительно 30 мМ до приблизительно 35 мМ, от приблизительно 5 мМ до приблизительно 45 мМ, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 20 мМ до приблизительно 25 мМ).
Неограничивающие примеры любой из композиций могут содержать (i) от приблизительно 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) маннита (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0); (ii) от приблизительно 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона) (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0); (iii) от приблизительно 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) аскорбата натрия (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0); (iv) от приблизительно 75 мМ до приблизительно 125 мМ (например, от приблизительно 80 мМ до приблизительно 120 мМ, от приблизительно 85 мМ до приблизительно 115 мМ, от приблизительно 90 мМ до приблизительно 110 мМ или от приблизительно 95 мМ до приблизительно 105 мМ) гистидина (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0); (v) от приблизительно 30 мМ до приблизительно 70 мМ (например, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ или от приблизительно 45 мМ до приблизительно 55 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона) и от приблизительно 30 мМ до приблизительно 70 мМ (например, от приблизительно 35 мМ до приблизительно 65 мМ, от приблизительно 40 мМ до приблизительно 60 мМ или от приблизительно 45 мМ до приблизительно 55 мМ) гистидина (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0); (vi) от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ, от приблизительно 25 мМ до приблизительно 35 мМ или от приблизительно 30 мМ до приблизительно 35 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона), от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ, от приблизительно 25 мМ до приблизительно 35 мМ или от приблизительно 30 мМ до приблизительно 35 мМ) гистидина и от приблизительно 10 мМ до приблизительно 50 мМ (например, от приблизительно 15 мМ до приблизительно 45 мМ, от приблизительно 20 мМ до приблизительно 40 мМ, от приблизительно 25 мМ до приблизительно 35 мМ или от приблизительно 30 мМ до приблизительно 35 мМ) аскорбата натрия (например, в буферном растворе, например, в фосфатном буфере, таком как 50 мМ фосфата натрия, pH 6,0) или (vii) от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 23 мМ до приблизительно 27 мМ) аскорбата натрия, от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 23 мМ до приблизительно 27 мМ) метионина (или, в качестве альтернативы, цистеина или глутатиона), от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 23 мМ до приблизительно 27 мМ) маннита и от приблизительно 5 мМ до приблизительно 45 мМ (например, от приблизительно 10 мМ до приблизительно 40 мМ, от приблизительно 15 мМ до приблизительно 35 мМ, от приблизительно 20 мМ до приблизительно 30 мМ или от приблизительно 23 мМ до приблизительно 27 мМ) гистидина (например, в буферном растворе, например, в фосфатном буфер, таком как 50 мМ фосфата натрия, pH 6,0).
Неограничивающие значения дозы гамма-излучения, достаточные для уменьшения бионагрузки в любой из композиций, предусмотренных в данном документе, описаны ниже. Дополнительные значения дозы гамма-излучения, достаточные для уменьшения бионагрузки в любой из композиций, предусмотренных в данном документе, известны из уровня техники. Например, любая из композиций, описанных в данном документе, может быть подвергнута воздействию гамма-излучения при любом из значений дозы, при любом из значений интенсивности гамма-излучения и/или при любом из значений температуры при подвергании воздействию гамма-излучения, описанных в данном документе (в любой комбинации). Бионагрузку в композиции можно определять, например, путем отбора образца из композиции, которая может содержать самореплицирующийся(самореплицирующиеся) биологический(биологические) загрязнитель(загрязнители), присутствующий(присутствующие) в композиции, например, путем гомогенизации на Stomacher, обработки ультразвуком, встряхивания, перемешивания на вортекс-мешалке, промывания, смешивания или отбора мазка, и качественного или количественного определения уровня самореплицирующегося(самореплицирующихся) биологического(биологических) загрязнителя(загрязнителей), присутствующего(присутствующих) в образце (например, путем помещения образца в среду для роста, которая будет обеспечивать возможность саморепликации биологического загрязнителя, например, посева образца на чашке Петри или пропускания образца через мембрану).
Количество по меньшей мере одного спирта, по меньшей мере одного антиоксиданта и/или по меньшей мере одного хелатора, достаточное для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции, может быть определено, например, с применением способов, описанных в примерах. Например, уровень уменьшения связывающей способности смолы для хроматографии, подвергнутой обработке с помощью гамма-излучения в присутствии некоторого количества по меньшей мере одного спирта (и необязательно дополнительно в присутствии по меньшей мере одного антиоксиданта и/или хелатора), можно сравнить с уровнем уменьшения связывающей способности смолы для хроматографии, подвергнутой обработке с помощью такой же дозы гамма-излучения при отсутствии по меньшей мере одного спирта (и необязательно по меньшей мере одного антиоксиданта и/или хелатора), где снижение уровня уменьшения связывающей способности смолы для хроматографии, подвергнутой воздействию гамма-излучения в присутствии по меньшей мере одного спирта (и необязательно дополнительно в присутствии по меньшей мере одного антиоксиданта и/или хелатора), по сравнению со смолой для хроматографии, подвергнутой воздействию гамма-излучения при отсутствии по меньшей мере одного спирта (и необязательно по меньшей мере одного антиоксиданта и/или хелатора), указывает на то, что по меньшей мере один спирт (и необязательно антиоксидант и/или хелатор) присутствовал в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии при обработке с помощью гамма-излучения. Иллюстративные способы определения связывающей способности смолы для хроматографии описаны в примерах. Дополнительные примеры способов определения связывающей способности смолы для хроматографии известны из уровня техники.
Способы уменьшения бионагрузки в смоле для хроматографии
В данном документе предусмотрены способы уменьшения бионагрузки в смоле для хроматографии. Такие способы предусматривают стадию подвергания контейнера, включающего композицию, включающую (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт (например, любую из иллюстративных композиций, включающих смолу для хроматографии и жидкость, включающую по меньшей мере один спирт, описанных в данном документе), воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения (или во время него).
Также предусмотрены способы уменьшения бионагрузки в смоле для хроматографии, которые предусматривают подвергание контейнера, включающего композицию, включающую (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после/во время воздействия гамма-излучения (например, любую из композиций, включающих смолу для хроматографии и жидкость, включающую по меньшей мере один спирт, описанный в данном документе), воздействию гамма-излучения с интенсивностью, составляющей от приблизительно 0,1 кГр/час до приблизительно 6 кГр/час (например, от приблизительно 0,1 кГр/час до приблизительно 5,5 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 5,0 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 4,5 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 4,0 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 3,5 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 3,0 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 2,5 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 2,0 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 1,5 кГр/час, от приблизительно 0,1 кГр/час до приблизительно 1,0 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 6 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 5,5 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 5,0 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 4,5 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 4,0 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 3,5 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 3,0 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 2,5 кГр/час, от приблизительно 0,5 кГр/час до приблизительно 2,0 кГр/час), и/или при температуре, составляющей от приблизительно 4°C до приблизительно 25°C (например, от приблизительно 4°C до приблизительно 20°C, от приблизительно 4°C до приблизительно 15°C, от приблизительно 4°C до приблизительно 10°C, от приблизительно 10°C до приблизительно 25°C, от приблизительно 10°C до приблизительно 20°C, от приблизительно 10°C до приблизительно 15°C или от приблизительно 15°C до приблизительно 25°C), с обеспечением дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии.
Некоторые варианты осуществления любого из таких способов могут включать, до и/или после стадии подвергания воздействию, хранение контейнера или композиции, включающей смолу для хроматографии и жидкость, включающую по меньшей мере один спирт (например, любого из контейнеров или любой из композиций, включающих смолу для хроматографии и жидкость, включающую по меньшей мере один спирт, описанных в данном документе) в течение периода времени, составляющего от приблизительно 1 часа до приблизительно 1 года, от приблизительно 1 часа до приблизительно 11 месяцев, от приблизительно 1 часа до приблизительно 10 месяцев, от приблизительно 1 часа до приблизительно 9 месяцев, от приблизительно 1 часа до приблизительно 8 месяцев, от приблизительно 1 часа до приблизительно 7 месяцев, от приблизительно 1 часа до приблизительно 6 месяцев, от приблизительно 1 часа до приблизительно 5 месяцев, от приблизительно 1 часа до приблизительно 4 месяцев, от приблизительно 1 часа до приблизительно 3 месяцев, от приблизительно 1 часа до приблизительно 2 месяцев, от приблизительно 1 часа до приблизительно 1 месяца, от приблизительно 1 часа до приблизительно 2 недель, от приблизительно 1 часа до приблизительно 1 недели, от приблизительно 1 часа до приблизительно 5 дней, от приблизительно 1 часа до приблизительно 2 дней, от приблизительно 1 часа до приблизительно 1 дня, от приблизительно 1 часа до приблизительно 12 часов, от приблизительно 1 часа до приблизительно 6 часов,
от приблизительно 6 часов до приблизительно 1 года, от приблизительно 6 часов до приблизительно 11 месяцев, от приблизительно 6 часов до приблизительно 10 месяцев, от приблизительно 6 часов до приблизительно 9 месяцев, от приблизительно 6 часов до приблизительно 8 месяцев, от приблизительно 6 часов до приблизительно 7 месяцев, от приблизительно 6 часов до приблизительно 6 месяцев, от приблизительно 6 часов до приблизительно 5 месяцев, от приблизительно 6 часов до приблизительно 4 месяцев, от приблизительно 6 часов до приблизительно 3 месяцев, от приблизительно 6 часов до приблизительно 2 месяцев, от приблизительно 6 часов до приблизительно 1 месяца, от приблизительно 6 часов до приблизительно 2 недель, от приблизительно 6 часов до приблизительно 1 недели, от приблизительно 6 часов до приблизительно 5 дней, от приблизительно 6 часов до приблизительно 2 дней, от приблизительно 6 часов до приблизительно 1 дня, от приблизительно 6 часов до приблизительно 12 часов, от приблизительно 12 часов до приблизительно 1 года, от приблизительно 12 часов до приблизительно 11 месяцев, от приблизительно 12 часов до приблизительно 10 месяцев, от приблизительно 12 часов до приблизительно 9 месяцев, от приблизительно 12 часов до приблизительно 8 месяцев, от приблизительно 12 часов до приблизительно 7 месяцев, от приблизительно 12 часов до приблизительно 6 месяцев, от приблизительно 12 часов до приблизительно 5 месяцев, от приблизительно 12 часов до приблизительно 4 месяцев, от приблизительно 12 часов до приблизительно 3 месяцев, от приблизительно 12 часов до приблизительно 2 месяцев, от приблизительно 12 часов до приблизительно 1 месяца, от приблизительно 12 часов до приблизительно 2 недель, от приблизительно 12 часов до приблизительно 1 недели, от приблизительно 12 часов до приблизительно 5 дней, от приблизительно 12 часов до приблизительно 2 дней, от приблизительно 12 часов до приблизительно 1 дня, от приблизительно 1 дня до приблизительно 1 года, от приблизительно 1 дня до приблизительно 11 месяцев, от приблизительно 1 дня до приблизительно 10 месяцев, от приблизительно 1 дня до приблизительно 9 месяцев, от приблизительно 1 дня до приблизительно 8 месяцев, от приблизительно 1 дня до приблизительно 7 месяцев, от приблизительно 1 дня до приблизительно 6 месяцев, от приблизительно 1 дня до приблизительно 5 месяцев, от приблизительно 1 дня до приблизительно 4 месяцев, от приблизительно 1 дня до приблизительно 3 месяцев, от приблизительно 1 дня до приблизительно 2 месяцев, от приблизительно 1 дня до приблизительно 1 месяца, от приблизительно 1 дня до приблизительно 2 недель, от приблизительно 1 дня до приблизительно 1 недели, от приблизительно 1 дня до приблизительно 5 дней, от приблизительно 1 дня до приблизительно 2 дней, от приблизительно 2 дней до приблизительно 1 года, от приблизительно 2 дней до приблизительно 11 месяцев, от приблизительно 2 дней до приблизительно 10 месяцев, от приблизительно 2 дней до приблизительно 9 месяцев, от приблизительно 2 дней до приблизительно 8 месяцев, от приблизительно 2 дней до приблизительно 7 месяцев, от приблизительно 2 дней до приблизительно 6 месяцев, от приблизительно 2 дней до приблизительно 5 месяцев, от приблизительно 2 дней до приблизительно 4 месяцев, от приблизительно 2 дней до приблизительно 3 месяцев, от приблизительно 2 дней до приблизительно 2 месяцев, от приблизительно 2 дней до приблизительно 1 месяца, от приблизительно 2 дней до приблизительно 2 недель, от приблизительно 2 дней до приблизительно 1 недели, от приблизительно 2 дней до приблизительно 5 дней, от приблизительно 5 дней до приблизительно 1 года, от приблизительно 5 дней до приблизительно 11 месяцев, от приблизительно 5 дней до приблизительно 10 месяцев, от приблизительно 5 дней до приблизительно 9 месяцев, от приблизительно 5 дней до приблизительно 8 месяцев, от приблизительно 5 дней до приблизительно 7 месяцев, от приблизительно 5 дней до приблизительно 6 месяцев, от приблизительно 5 дней до приблизительно 5 месяцев, от приблизительно 5 дней до приблизительно 4 месяцев, от приблизительно 5 дней до приблизительно 3 месяцев, от приблизительно 5 дней до приблизительно 2 месяцев, от приблизительно 5 дней до приблизительно 1 месяца, от приблизительно 5 дней до приблизительно 2 недель, от приблизительно 5 дней до приблизительно 1 недели, от приблизительно 1 недели до приблизительно 1 года, от приблизительно 1 недели до приблизительно 11 месяцев, от приблизительно 1 недели до приблизительно 10 месяцев, от приблизительно 1 недели до приблизительно 9 месяцев, от приблизительно 1 недели до приблизительно 8 месяцев, от приблизительно 1 недели до приблизительно 7 месяцев, от приблизительно 1 недели до приблизительно 6 месяцев, от приблизительно 1 недели до приблизительно 5 месяцев, от приблизительно 1 недели до приблизительно 4 месяцев, от приблизительно 1 недели до приблизительно 3 месяцев, от приблизительно 1 недели до приблизительно 2 месяцев, от приблизительно 1 недели до приблизительно 1 месяца, от приблизительно 1 недели до приблизительно 2 недель, от приблизительно 2 недель до приблизительно 1 года, от приблизительно 2 недель до приблизительно 11 месяцев, от приблизительно 2 недель до приблизительно 10 месяцев, от приблизительно 2 недель до приблизительно 9 месяцев, от приблизительно 2 недель до приблизительно 8 месяцев, от приблизительно 2 недель до приблизительно 7 месяцев, от приблизительно 2 недель до приблизительно 6 месяцев, от приблизительно 2 недель до приблизительно 5 месяцев, от приблизительно 2 недель до приблизительно 4 месяцев, от приблизительно 2 недель до приблизительно 3 месяцев, от приблизительно 2 недель до приблизительно 2 месяцев, от приблизительно 2 недель до приблизительно 1 месяца, от приблизительно 1 месяца до приблизительно 1 года, от приблизительно 1 месяца до приблизительно 11 месяцев, от приблизительно 1 месяца до приблизительно 10 месяцев, от приблизительно 1 месяца до приблизительно 9 месяцев, от приблизительно 1 месяца до приблизительно 8 месяцев, от приблизительно 1 месяца до приблизительно 7 месяцев, от приблизительно 1 месяца до приблизительно 6 месяцев, от приблизительно 1 месяца до приблизительно 5 месяцев, от приблизительно 1 месяца до приблизительно 4 месяцев, от приблизительно 1 месяца до приблизительно 3 месяцев, от приблизительно 1 месяца до приблизительно 2 месяцев, от приблизительно 2 месяцев до приблизительно 1 года, от приблизительно 2 месяцев до приблизительно 11 месяцев, от приблизительно 2 месяцев до приблизительно 10 месяцев, от приблизительно 2 месяцев до приблизительно 9 месяцев, от приблизительно 2 месяцев до приблизительно 8 месяцев, от приблизительно 2 месяцев до приблизительно 7 месяцев, от приблизительно 2 месяцев до приблизительно 6 месяцев, от приблизительно 2 месяцев до приблизительно 5 месяцев, от приблизительно 2 месяцев до приблизительно 4 месяцев, от приблизительно 2 месяцев до приблизительно 3 месяцев, от приблизительно 3 месяцев до приблизительно 1 года, от приблизительно 3 месяцев до приблизительно 11 месяцев, от приблизительно 3 месяцев до приблизительно 10 месяцев, от приблизительно 3 месяцев до приблизительно 9 месяцев, от приблизительно 3 месяцев до приблизительно 8 месяцев, от приблизительно 3 месяцев до приблизительно 7 месяцев, от приблизительно 3 месяцев до приблизительно 6 месяцев, от приблизительно 3 месяцев до приблизительно 5 месяцев, от приблизительно 3 месяцев до приблизительно 4 месяцев, от приблизительно 4 месяцев до приблизительно 1 года, от приблизительно 4 месяцев до приблизительно 11 месяцев, от приблизительно 4 месяцев до приблизительно 10 месяцев, от приблизительно 4 месяцев до приблизительно 9 месяцев, от приблизительно 4 месяцев до приблизительно 8 месяцев, от приблизительно 4 месяцев до приблизительно 7 месяцев, от приблизительно 4 месяцев до приблизительно 6 месяцев, от приблизительно 4 месяцев до приблизительно 5 месяцев, от приблизительно 5 месяцев до приблизительно 1 года, от приблизительно 5 месяцев до приблизительно 11 месяцев, от приблизительно 5 месяцев до приблизительно 10 месяцев, от приблизительно 5 месяцев до приблизительно 9 месяцев, от приблизительно 5 месяцев до приблизительно 8 месяцев, от приблизительно 5 месяцев до приблизительно 7 месяцев, от приблизительно 5 месяцев до приблизительно 6 месяцев, от приблизительно 6 месяцев до приблизительно 1 года, от приблизительно 6 месяцев до приблизительно 11 месяцев, от приблизительно 6 месяцев до приблизительно 10 месяцев, от приблизительно 6 месяцев до приблизительно 9 месяцев, от приблизительно 6 месяцев до приблизительно 8 месяцев, от приблизительно 6 месяцев до приблизительно 7 месяцев, от приблизительно 7 месяцев до приблизительно 1 года, от приблизительно 7 месяцев до приблизительно 11 месяцев, от приблизительно 7 месяцев до приблизительно 10 месяцев, от приблизительно 7 месяцев до приблизительно 9 месяцев, от приблизительно 7 месяцев до приблизительно 8 месяцев, от приблизительно 8 месяцев до приблизительно 1 года, от приблизительно 8 месяцев до приблизительно 11 месяцев, от приблизительно 8 месяцев до приблизительно 10 месяцев, от приблизительно 8 месяцев до приблизительно 9 месяцев, от приблизительно 9 месяцев до приблизительно 1 года, от приблизительно 9 месяцев до приблизительно 11 месяцев, от приблизительно 9 месяцев до приблизительно 10 месяцев, от приблизительно 10 месяцев до приблизительно 1 года, от приблизительно 10 месяцев до приблизительно 11 месяцев или от приблизительно 11 месяцев до приблизительно 1 года, например, при температуре от приблизительно 4°C до приблизительно 40°C, от приблизительно 4°C до приблизительно 35°C, от приблизительно 4°C до приблизительно 30°C, от приблизительно 4°C до приблизительно 28°C, от приблизительно 4°C до приблизительно 26°C, от приблизительно 4°C до приблизительно 24°C, от приблизительно 4°C до приблизительно 22°C, от приблизительно 4°C до приблизительно 20°C, от приблизительно 4°C до приблизительно 18°C, от приблизительно 4°C до приблизительно 16°C, от приблизительно 4°C до приблизительно 14°C, от приблизительно 4°C до приблизительно 12°C, от приблизительно 4°C до приблизительно 10°C, от приблизительно 4°C до приблизительно 8°C, от приблизительно 4°C до приблизительно 6°C, от приблизительно 6°C до приблизительно 40°C, от приблизительно 6°C до приблизительно 35°C, от приблизительно 6°C до приблизительно 30°C, от приблизительно 6°C до приблизительно 28°C, от приблизительно 6°C до приблизительно 26°C, от приблизительно 6°C до приблизительно 24°C, от приблизительно 6°C до приблизительно 22°C, от приблизительно 6°C до приблизительно 20°C, от приблизительно 6°C до приблизительно 18°C, от приблизительно 6°C до приблизительно 16°C, от приблизительно 6°C до приблизительно 14°C, от приблизительно 6°C до приблизительно 12°C, от приблизительно 6°C до приблизительно 10°C, от приблизительно 6°C до приблизительно 8°C, от приблизительно 8°C до приблизительно 40°C, от приблизительно 8°C до приблизительно 35°C, от приблизительно 8°C до приблизительно 30°C, от приблизительно 8°C до приблизительно 28°C, от приблизительно 8°C до приблизительно 26°C, от приблизительно 8°C до приблизительно 24°C, от приблизительно 8°C до приблизительно 22°C, от приблизительно 8°C до приблизительно 20°C, от приблизительно 8°C до приблизительно 18°C, от приблизительно 8°C до приблизительно 16°C, от приблизительно 8°C до приблизительно 14°C, от приблизительно 8°C до приблизительно 12°C, от приблизительно 8°C до приблизительно 10°C, от приблизительно 10°C до приблизительно 40°C, от приблизительно 10°C до приблизительно 35°C, от приблизительно 10°C до приблизительно 30°C, от приблизительно 10°C до приблизительно 28°C, от приблизительно 10°C до приблизительно 26°C, от приблизительно 10°C до приблизительно 24°C, от приблизительно 10°C до приблизительно 22°C, от приблизительно 10°C до приблизительно 20°C, от приблизительно 10°C до приблизительно 18°C, от приблизительно 10°C до приблизительно 16°C, от приблизительно 10°C до приблизительно 14°C, от приблизительно 10°C до приблизительно 12°C, от приблизительно 12°C до приблизительно 40°C, от приблизительно 12°C до приблизительно 35°C, от приблизительно 12°C до приблизительно 30°C, от приблизительно 12°C до приблизительно 28°C, от приблизительно 12°C до приблизительно 26°C, от приблизительно 12°C до приблизительно 24°C, от приблизительно 12°C до приблизительно 22°C, от приблизительно 12°C до приблизительно 20°C, от приблизительно 12°C до приблизительно 18°C, от приблизительно 12°C до приблизительно 16°C, от приблизительно 12°C до приблизительно 14°C, от приблизительно 14°C до приблизительно 40°C, от приблизительно 14°C до приблизительно 35°C, от приблизительно 14°C до приблизительно 30°C, от приблизительно 14°C до приблизительно 28°C, от приблизительно 14°C до приблизительно 26°C, от приблизительно 14°C до приблизительно 24°C, от приблизительно 14°C до приблизительно 22°C, от приблизительно 14°C до приблизительно 20°C, от приблизительно 14°C до приблизительно 18°C, от приблизительно 14°C до приблизительно 16°C, от приблизительно 16°C до приблизительно 40°C, от приблизительно 16°C до приблизительно 35°C, от приблизительно 16°C до приблизительно 30°C, от приблизительно 16°C до приблизительно 28°C, от приблизительно 16°C до приблизительно 26°C, от приблизительно 16°C до приблизительно 24°C, от приблизительно 16°C до приблизительно 22°C, от приблизительно 16°C до приблизительно 20°C, от приблизительно 16°C до приблизительно 18°C, от приблизительно 18°C до приблизительно 40°C, от приблизительно 18°C до приблизительно 35°C, от приблизительно 18°C до приблизительно 30°C, от приблизительно 18°C до приблизительно 28°C, от приблизительно 18°C до приблизительно 26°C, от приблизительно 18°C до приблизительно 24°C, от приблизительно 18°C до приблизительно 22°C, от приблизительно 18°C до приблизительно 20°C, от приблизительно 20°C до приблизительно 40°C, от приблизительно 20°C до приблизительно 35°C, от приблизительно 20°C до приблизительно 30°C, от приблизительно 20°C до приблизительно 28°C, от приблизительно 20°C до приблизительно 26°C, от приблизительно 20°C до приблизительно 24°C, от приблизительно 20°C до приблизительно 22°C, от приблизительно 22°C до приблизительно 40°C, от приблизительно 22°C до приблизительно 35°C, от приблизительно 22°C до приблизительно 30°C, от приблизительно 22°C до приблизительно 28°C, от приблизительно 22°C до приблизительно 26°C, от приблизительно 22°C до приблизительно 24°C, от приблизительно 24°C до приблизительно 40°C, от приблизительно 24°C до приблизительно 35°C, от приблизительно 24°C до приблизительно 30°C, от приблизительно 24°C до приблизительно 28°C, от приблизительно 24°C до приблизительно 26°C, от приблизительно 26°C до приблизительно 40°C, от приблизительно 26°C до приблизительно 35°C, от приблизительно 26°C до приблизительно 30°C, от приблизительно 26°C до приблизительно 28°C, от приблизительно 28°C до приблизительно 40°C, от приблизительно 28°C до приблизительно 35°C, от приблизительно 28°C до приблизительно 30°C, от приблизительно 30°C до приблизительно 40°C, от приблизительно 30°C до приблизительно 35°C или от приблизительно 35°C до приблизительно 40°C.
В способах, описанных в данном абзаце, уровень связывающей способности подвергнутой воздействию гамма-излучения смолы для хроматографии, полученной с помощью таких способов, больше уровня связывающей способности подвергнутой воздействию гамма-излучения смолы для хроматографии, которую подвергали воздействию гамма-излучения при интенсивности, составляющей более 6,1 кГр/час, и/или при температуре, составляющей более 25°C, или при обоих таких условиях.
Смола для хроматографии может быть подвергнута воздействию гамма-излучения с применением способов, известных из уровня техники. Например, в качестве источника гамма-лучей можно применять изотоп, такой как кобальт-60 или цезий-137. Смола для хроматографии может быть подвергнута воздействию гамма-излучения при температуре, приблизительно составляющей от приблизительно −25°C до приблизительно 0°C включительно или от приблизительно 0°C до приблизительно 25°C включительно. Смола для хроматографии может быть подвергнута воздействию гамма-излучения в дозе, составляющей от приблизительно 0,1 кГр до приблизительно 100 кГр, от приблизительно 1 кГр до приблизительно 100 кГр, от приблизительно 1 кГр до приблизительно 90 кГр, от приблизительно 1 кГр до приблизительно 80 кГр, от приблизительно 1 кГр до приблизительно 70 кГр, от приблизительно 1 кГр до приблизительно 65 кГр, от приблизительно 5 кГр до приблизительно 65 кГр, от приблизительно 10 кГр до приблизительно 60 кГр, от приблизительно 10 кГр до приблизительно 55 кГр, от приблизительно 10 кГр до приблизительно 50 кГр, от приблизительно 10 кГр до приблизительно 45 кГр, от приблизительно 10 кГр до приблизительно 40 кГр, от приблизительно 10 кГр до приблизительно 35 кГр, от приблизительно 10 кГр до приблизительно 30 кГр, от приблизительно 15 кГр до приблизительно 50 кГр, от приблизительно 15 кГр до приблизительно 45 кГр, от приблизительно 15 кГр до приблизительно 40 кГр, от приблизительно 15 кГр до приблизительно 35 кГр, от приблизительно 20 кГр до приблизительно 30 кГр или от приблизительно 23 кГр до приблизительно 27 кГр. Смола для хроматографии может быть подвергнута воздействию гамма-излучения в дозе, достаточной для обеспечения уровня обеспечения стерильности смолы для хроматографии, составляющего приблизительно 1 × 10−6 или меньше, приблизительно 1 × 10−7 или меньше, приблизительно 10 × 10−8 или меньше, приблизительно 1 × 10−11 или меньше или приблизительно 1 × 10−12 или меньше или от приблизительно 1 × 10−6 до приблизительно 1 × 10−12, от приблизительно 1 × 10−6 до приблизительно 1 × 10−11, от приблизительно 1 × 10−6 до приблизительно 1 × 10−10, от приблизительно 1 × 10−6 до приблизительно 1 × 10−9, от приблизительно 1 × 10−6 до приблизительно 1 × 10−8, от 1 × 10−6 до приблизительно 1 × 10−7, от приблизительно 1 × 10−7 до приблизительно 1 × 10−12, от приблизительно 1 × 10−7 до приблизительно 1 × 10−11, от приблизительно 1 × 10−7 до приблизительно 1 × 10−10, от приблизительно 1 × 10−7 до приблизительно 1 × 10−9, от приблизительно 1 × 10−7 до приблизительно 1 × 10−8, от приблизительно 1 × 10−8 до приблизительно 1 × 10−12, от приблизительно 1 × 10−8 до приблизительно 1 × 10−11, от приблизительно 1 × 10−8 до приблизительно 1 × 10−10 или от приблизительно 1 × 10−8 до приблизительно 1 × 10−9.
Дозу гамма-излучения, достаточную для уменьшения бионагрузки в смоле для хроматографии, можно определять с применением способов, известных из уровня техники. Например, уровень бионагрузки в смоле для хроматографии, подвергнутой обработке с помощью дозы гамма-излучения, можно сравнить с уровнем бионагрузки в не подвергнутой обработке смоле для хроматографии (например, контроля, не подвергнутого воздействию гамма-излучения), и снижение уровня бионагрузки в подвергнутой воздействию гамма-излучения смоле для хроматографии по сравнению с не подвергнутой обработке смолой для хроматографии указывает на то, что доза гамма-излучения является достаточной для уменьшения бионагрузки в смоле для хроматографии. Иллюстративные способы определения уровня бионагрузки в композиции (например, смоле для хроматографии) описаны в данном документе. Дополнительные способы определения уровня бионагрузки в композиции (например, смоле для хроматографии) известны из уровня техники.
Смола для хроматографии в любом из таких способов может представлять собой смолу для анионообменной хроматографии, смолу для катионообменной хроматографии, смолу для эксклюзионной хроматографии, смолу для хроматографии с гидрофобным взаимодействием или смолу для аффинной хроматографии или любую их комбинацию. Неограничивающие примеры смолы для аффинной хроматографии могут включать белковый или пептидный лиганд (например, длиной от приблизительно 5 аминокислот до приблизительно 100 аминокислот, от приблизительно 5 аминокислот до приблизительно 90 аминокислот, от приблизительно 5 аминокислот до приблизительно 80 аминокислот, от приблизительно 5 аминокислот до приблизительно 70 аминокислот, от приблизительно 5 аминокислот до приблизительно 60 аминокислот, от приблизительно 5 аминокислот до приблизительно 50 аминокислот, от приблизительно 5 аминокислот до приблизительно 40 аминокислот, от приблизительно 5 аминокислот до приблизительно 30 аминокислот, от приблизительно 5 аминокислот до приблизительно 25 аминокислот или от приблизительно 5 аминокислот до приблизительно 20 аминокислот), низкомолекулярный субстрат или кофактор фермента, аптамер, ингибитор (например, конкурентный ингибитор белка) или металл. В некоторых вариантах осуществления смола для аффинной хроматографии включает белковый лиганд (например, белок A). Дополнительные примеры смолы для аффинной хроматографии включают лиганд-кофактор, лиганд-субстрат, металлолиганд, лиганд-продукт или лиганд-аптамер. В некоторых примерах смола для хроматографии представляет собой бимодальную смолу для хроматографии (например, смолу для анионообменной хроматографии и смолу для хроматографии с гидрофобным взаимодействием). Смола для хроматографии может представлять собой смолу для анионообменной хроматографии (например, смолу для анионообменной хроматографии, включающую N-бензил-N-метилэтаноламинные группы).
Контейнер, который включает смолу для хроматографии, может представлять собой пластиковый контейнер (например, цилиндрическую трубку, герметичный ящик или ящик с зажимами, или герметичный пакет). Неограничивающие примеры контейнеров, применяемых в таких способах, включают сосуд для хранения или хроматографическую колонку. Например, композиция, включающая (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт (например, любая из иллюстративных композиций, описанных в данном документе), может быть представлена в герметичном контейнере (например, представлять собой взвесь в герметичном контейнере или смолу для хроматографии в качестве насадки в герметичном контейнере (например, в хроматографической колонке)). Контейнер, применяемый в способах, описанных в данном документе, может представлять собой одноразовую хроматографическую колонку. В некоторых вариантах осуществления контейнер, применяемый в способах, описанных в данном документе, представляет собой одноразовую хроматографическую колонку, помещенную в контурную ячейковую упаковку. Контейнер (например, сосуд для хранения или хроматографическая колонка) может характеризоваться общим внутренним объемом, составляющим от приблизительно 1 мл до приблизительно 1 л (например, от приблизительно 1 мл до приблизительно 900 мл, от приблизительно 1 мл до приблизительно 800 мл, от приблизительно 1 мл до приблизительно 700 мл, от приблизительно 1 мл до приблизительно 600 мл, от приблизительно 1 мл до приблизительно 500 мл, от приблизительно 1 мл до приблизительно 450 мл, от приблизительно 1 мл до приблизительно 400 мл, от приблизительно 1 мл до приблизительно 350 мл, от приблизительно 1 мл до приблизительно 300 мл, от приблизительно 1 мл до приблизительно 250 мл, от приблизительно 1 мл до приблизительно 200 мл, от приблизительно 1 мл до приблизительно 150 мл, от приблизительно 1 мл до приблизительно 100 мл, от приблизительно 1 мл до приблизительно 75 мл, от приблизительно 1 мл до приблизительно 50 мл, от приблизительно 1 мл до приблизительно 40 мл, от приблизительно 1 мл до приблизительно 30 мл или от приблизительно 1 мл до приблизительно 20 мл).
Композиция, содержащая (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт (например, любая из иллюстративных композиций, описанных в данном документе), включенная в контейнер, может быть представлена в виде смоченной или влажной твердой смеси. Например, контейнер может включать взвесь осажденной смолы для хроматографии в жидкости. В некоторых вариантах осуществления контейнер может включать смолу для хроматографии в качестве насадки. Например, контейнер, включающий композицию, включающую (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт (например, любую из композиций, описанных в данном документе), представляет собой заполненную хроматографическую колонку (например, где смола помещена в жидкость, включающую по меньшей мере один спирт). Некоторые варианты осуществления предусматривают перед воздействием помещение композиции, содержащей (i) смолу для хроматографии и (ii) жидкость, включающую по меньшей мере один спирт (например, любой из композиций, описанных в данном документе), в контейнер.
Любые спирты, антиоксиданты и/или хелаторы, описанные в данном документе, можно применять в любой комбинации, с применением любой комбинации иллюстративных значений концентрации, описанных в данном документе. Например, жидкость может включать по меньшей мере один спирт, выбранный из группы, состоящей из бензилового спирта, циклогексанола, изобутилового спирта, 2-метил-2-бутанола, метанола, этанола, пропан-2-ола, пропан-1-ола, бутан-1-ола, пентан-1-ола, гексадекан-1-ола, 2-фенилэтанола, втор-фенилэтанола, 3-фенил-1-пропанола, 1-фенил-1-пропанола, 2-фенил-1-пропанола, 2-фенил-2-пропанола, 1-фенил-2-бутанола, 2-фенил-1-бутанола, 3-фенил-1-бутанола, 4-фенил-2-бутанола, DL-1-фенил-2-пентанола, 5-фенил-1-пентанола и 4-фенил-1-бутанола. В некоторых примерах жидкость может дополнительно включать по меньшей мере один антиоксидант (например, по меньшей мере один антиоксидант, выбранный из группы, состоящей из восстановленного глутатиона, восстановленного тиоредоксина, восстановленного цистеина, каротиноида, мелатонина, ликопина, токоферола, восстановленного убихинона, аскорбата, билирубина, мочевой кислоты, липоевой кислоты, флавоноида, фенолпропановой кислоты, лидокаина, нарингина, фуллерена, глюкозы, маннита, 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила и диметилметоксихроманола), и/или по меньшей мере один хелатор (например, по меньшей мере один хелатор, выбранный из группы, состоящей из EDTA, DMPS, DMSA, металлотионина и дефероксамина).
Иллюстративные способы определения/идентификации количества(количеств) по меньшей мере одного спирта, по меньшей мере одного антиоксиданта и/или по меньшей мере одного хелатора, достаточного(достаточных) для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции, описаны в данном документе. Дополнительные способы определения/идентификации количества(количеств) по меньшей мере одного антиоксиданта и/или хелатора, достаточного(достаточных) для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции, известны из уровня техники.
Также в данном документе предусмотрена смола для хроматографии с уменьшенной бионагрузкой, полученная с помощью любого из способов, описанных в данном документе (например, смола для хроматографии с уменьшенной бионагрузкой, представленная в контейнере для хранения, например, в герметичном контейнере для хранения). Смола для хроматографии с уменьшенной бионагрузкой, полученная с применением любого из способов, описанных в данном документе, может характеризоваться уровнем обеспечения стерильности, составляющим приблизительно 1 × 10−6 или меньше, приблизительно 1 × 10−7 или меньше, приблизительно 10 × 10−8 или меньше, приблизительно 1 × 10−11 или меньше или приблизительно 1 × 10−12 или меньше или от приблизительно 1 × 10−6 до приблизительно 1 × 10−12, от приблизительно 1 × 10−6 до приблизительно 1 × 10−11, от приблизительно 1 × 10−6 до приблизительно 1 × 10−10, от приблизительно 1 × 10−6 до приблизительно 1 × 10−9, от приблизительно 1 × 10−6 до приблизительно 1 × 10−8, от 1 × 10−6 до приблизительно 1 × 10−7, от приблизительно 1 × 10−7 до приблизительно 1 × 10−12, от приблизительно 1 × 10−7 до приблизительно 1 × 10−11, от приблизительно 1 × 10−7 до приблизительно 1 × 10−10, от приблизительно 1 × 10−7 до приблизительно 1 × 10−9, от приблизительно 1 × 10−7 до приблизительно 1 × 10−8, от приблизительно 1 × 10−8 до приблизительно 1 × 10−12, от приблизительно 1 × 10−8 до приблизительно 1 × 10−11, от приблизительно 1 × 10−8 до приблизительно 1 × 10−10 или от приблизительно 1 × 10−8 до приблизительно 1 × 10−9. Смола для хроматографии с уменьшенной бионагрузкой, полученная с помощью любого из способов, описанных в данном документе, может характеризоваться связывающей способностью, составляющей по меньшей мере 74% (например, по меньшей мере 76%, по меньшей мере 78%, по меньшей мере 80%, по меньшей мере 82%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%) или от приблизительно 74% до 95%, от приблизительно 74% до приблизительно 95%, от приблизительно 76% до приблизительно 95%, по меньшей мере, от приблизительно 78% до приблизительно 95%, от приблизительно 80% до приблизительно 95% или от приблизительно 74% до приблизительно 90%, от приблизительно 76% до приблизительно 90%, от приблизительно 78% до приблизительно 90% или от приблизительно 80% до приблизительно 90% связывающей способности такой же смолы для хроматографии, которую не подвергали обработке с целью уменьшения ее бионагрузки (например, не подвергали воздействию гамма-излучения), при этом применяют один и тот же белок для тестирования связывающей способности как смолы для хроматографии, полученной с помощью способов, описанных в данном документе, так и контроля - не подвергнутой обработке смолы для хроматографии.
Способы получения заполненной хроматографической колонки с уменьшенной бионагрузкой
Также в данном документе предусмотрены способы получения уменьшенной заполненной хроматографической колонки, которые предусматривают обеспечение смолы для хроматографии с уменьшенной бионагрузкой, полученной с помощью любого из способов, описанных в данном документе, и заполнение смолой для хроматографии колонки с уменьшенной бионагрузкой в асептических условиях или в условиях с уменьшенной бионагрузкой. В некоторых вариантах осуществления заполненную хроматографическую колонку с уменьшенной бионагрузкой можно получать путем подвергания колонки, включающей смолу для хроматографии в качестве насадки и жидкость, включающую по меньшей мере один спирт (например, любую из иллюстративных жидкостей, описанных в данном документе, например, необязательно дополнительно включающую по меньшей мере один антиоксидант и/или хелатор) воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки колонки и смолы для хроматографии в качестве насадки, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии в качестве насадки после воздействия дозы гамма-излучения.
Также предусмотрена(предусмотрены) заполненная(заполненные) хроматографическая(хроматографические) колонка(колонки) с уменьшенной бионагрузкой, полученная(полученные) с помощью способов, описанных в данном документе. Любая из заполненных хроматографических колонок с уменьшенной бионагрузкой, полученных с помощью способов, описанных в данном документе, может характеризоваться уровнем обеспечения стерильности, составляющим приблизительно 1 × 10−6 или меньше, приблизительно 1 × 10−7 или меньше, приблизительно 10 × 10−8 или меньше, приблизительно 1 × 10−11 или меньше или приблизительно 1 × 10−12 или меньше или от приблизительно 1 × 10−6 до приблизительно 1 × 10−12, от приблизительно 1 × 10−6 до приблизительно 1 × 10−11, от приблизительно 1 × 10−6 до приблизительно 1 × 10−10, от приблизительно 1 × 10−6 до приблизительно 1 × 10−9, от приблизительно 1 × 10−6 до приблизительно 1 × 10−8, от 1 × 10−6 до приблизительно 1 × 10−7, от приблизительно 1 × 10−7 до приблизительно 1 × 10−12, от приблизительно 1 × 10−7 до приблизительно 1 × 10−11, от приблизительно 1 × 10−7 до приблизительно 1 × 10−10, от приблизительно 1 × 10−7 до приблизительно 1 × 10−9, от приблизительно 1 × 10−7 до приблизительно 1 × 10−8, от приблизительно 1 × 10−8 до приблизительно 1 × 10−12, от приблизительно 1 × 10−8 до приблизительно 1 × 10−11, от приблизительно 1 × 10−8 до приблизительно 1 × 10−10 или от приблизительно 1 × 10−8 до приблизительно 1 × 10−9. Любая из заполненных хроматографических колонок с уменьшенной бионагрузкой, полученных с помощью способов, описанных в данном документе, может содержать по меньшей мере одну смолу для хроматографии, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии (например, любой из смол для аффинной хроматографии, описанных в данном документе или известных из уровня техники), смолы для хроматографии с гидрофильным взаимодействием и смолы для эксклюзионной хроматографии. Например, любая из заполненных хроматографических колонок с уменьшенной бионагрузкой, описанных в данном документе, может содержать смолу для аффинной хроматографии, включающую белковый лиганд (например, белок A). Заполненная хроматографическая колонка с уменьшенной бионагрузкой, описанная в данном документе, может содержать смолу для анионообменной хроматографии (например, смолу для анионообменной хроматографии, включающую N-бензил-N-метилэтаноламинные группы).
Способы выполнения хроматографии с уменьшенной бионагрузкой
Способы, описанные в данном документе, предусматривают применение заполненной хроматографической колонки с уменьшенной бионагрузкой, предусмотренной в данном документе, и способы, описанные в данном документе, предусматривают применение одной или двух MCCS, которые включают по меньшей мере одну заполненную хроматографическую колонку с уменьшенной бионагрузкой, предусмотренную в данном документе. Подвергнутая воздействию гамма-излучения смола для хроматографии может представлять собой любой тип смолы, описанный в данном документе (или любой тип смолы для хроматографии, известный из уровня техники).
Заполненную хроматографическую колонку с уменьшенной бионагрузкой можно получать с применением любого из способов, описанных в данном документе. Например, заполненную хроматографическую колонку с уменьшенной бионагрузкой можно получать путем заполнения хроматографической колонки композицией, включающей смолу (смолы) для хроматографии и жидкость, включающую по меньшей мере один спирт (например, любой из таких композиций, описанных в данном документе), и подвергания заполненной колонки воздействию гамма-излучения (например, с применением любого из режимов воздействия и условий, описанных в данном документе). В других примерах заполненную хроматографическую колонку с уменьшенной бионагрузкой можно получать путем подвергания контейнера, включающего смолу для хроматографии и жидкость, включающую по меньшей мере один спирт (например, любую из иллюстративных жидкостей, описанных в данном документе, например, необязательно дополнительно включающую по меньшей мере один антиоксидант и/или по меньшей мере один хелатор), воздействию дозы гамма-излучения и заполнения хроматографической колонки полученной смолой для хроматографии с уменьшенной бионагрузкой. В таких способах смола для хроматографии (присутствующая в контейнере во время воздействия гамма-излучения) может быть представлена в виде взвеси в контейнере, и хроматографическую колонку заполняют в вытяжном шкафу с уменьшенной бионагрузкой. В других способах смолу для хроматографии, присутствующую в контейнере с жидкостью, включающей по меньшей мере спирт (например, с любой из жидкостей, описанных в данном документе, например, с необязательно дополнительно включающей по меньшей мере один антиоксидант и/или по меньшей мере один хелатор), можно подвергать воздействию гамма-излучения в виде смоченной или влажной твердой смеси в контейнере, и взвесь полученной смолы для хроматографии с уменьшенной бионагрузкой можно получать с применением буфера с уменьшенной бионагрузкой (например, получать в вытяжном шкафу с уменьшенной бионагрузкой), и применять полученную взвесь для заполнения хроматографической колонки в вытяжном шкафу с уменьшенной бионагрузкой. В некоторых таких примерах хроматографическую колонку перед заполнением можно подвергать обработке для уменьшения бионагрузки (например, подвергать автоклавированию, воздействию гамма-излучения или воздействию этиленоксида).
Заполненная хроматографическая колонка с уменьшенной бионагрузкой, применяемая в любом из способов, описанных в данном документе, может характеризоваться уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−3 до приблизительно 1 × 10−12, от приблизительно 1 × 10−4 до приблизительно 1 × 10−12, от 1 × 10−5 до приблизительно 1 × 10−11, от приблизительно 1 × 10−5 до приблизительно 1 × 10−10, от приблизительно 1 × 10−5 до приблизительно 1 × 10−9, от приблизительно 1 × 10−6 до приблизительно 1 × 10−9 или от приблизительно 1 × 10−6 до приблизительно 1 × 10−8 включительно.
Буферы с уменьшенной бионагрузкой
Способы и процессы, описанные в данном документе, можно осуществлять с применением одного или нескольких буферов с уменьшенной бионагрузкой. Как можно понять из уровня техники, буфер с уменьшенной бионагрузкой может представлять собой любой тип буфера, применяемого в цикле хроматографии (например, буфер, применяемый на любой из стадий в цикле хроматографии или в любой из отдельных операций, описанных в данном документе). Иллюстративные способы уменьшения бионагрузки в буфере включают фильтрацию (фильтрацию через поры размером 0,2 мкм), автоклавирование и воздействие гамма-излучения. Дополнительные способы уменьшения бионагрузки буфера известны из уровня техники. Буфер с уменьшенной бионагрузкой может характеризоваться уровнем обеспечения стерильности, составляющим от приблизительно 1 × 10−3 до приблизительно 1 × 10−12, от приблизительно 1 × 10−4 до приблизительно 1 × 10−12, от 1 × 10−5 до приблизительно 1 × 10−11, от приблизительно 1 × 10−5 до приблизительно 1 × 10−10, от приблизительно 1 × 10−5 до приблизительно 1 × 10−9, от приблизительно 1 × 10−6 до приблизительно 1 × 10−9 или от приблизительно 1 × 10−6 до приблизительно 1 × 10−8 включительно.
Рекомбинантные терапевтические белки
Рекомбинантный белок, описанный в данном документе, может представлять собой рекомбинантный терапевтический белок. Неограничивающие примеры рекомбинантных терапевтических белков, которые можно получать с помощью способов, предусмотренных в данном документе, включают иммуноглобулины (в том числе иммуноглобулины, содержащие легкую и тяжелую цепи, антитела или фрагменты антител (например, любой из фрагментов антител, описанных в данном документе), ферменты (например, галактозидазу (например, альфа-галактозидазу), Myozyme® или Cerezyme®), белки (например, эритропоэтин человека, фактор некроза опухоли (TNF) или интерферон альфа или бета) или иммуногенные или антигенные белки или фрагменты белков (например, белки для применения в вакцине). Рекомбинантный терапевтический белок может представлять собой сконструированный антигенсвязывающий полипептид, который включает остов по меньшей мере одного многофункционального рекомбинантного белка (см., например, рекомбинантные антигенсвязывающие белки, описанные в Gebauer et al., Current Opin. Chem. Biol. 13:245-255, 2009; и в публикации заявки на патент США № 2012/0164066 (включенной в данный документ посредством ссылки во всей своей полноте)). Неограничивающие примеры рекомбинантных терапевтических белков, которые являются антителами, включают панитумумаб, омализумаб, абаговомаб, абциксимаб, актоксумаб, адалимумаб, адекатумумаб, афелимомаб, афутузумаб, алацизумаб, алацизумаб, алемтузумаб, алирокумаб, альтумомаб, аматуксимаб, анатумомаб, аполизумаб, атинумаб, тоцилизумаб, базиликсимаб, бектумомаб, белимумаб, бевацизумаб, бициромаб, канакинумаб, цетуксимаб, даклизумаб, денсумаб, экулизумаб, эдреколомаб, эфализумаб, эфунгумаб, эртумаксомаб, этарацизумаб, голимумаб, инфликсимаб, натализумаб, паливизумаб, панитумумаб, пертузумаб, ранибизумаб, ритуксимаб, тоцилизумаб и трастузумаб. Дополнительные примеры рекомбинантных терапевтических антител, которые можно получать с помощью способов, описанных в данном документе, известны из уровня техники. Дополнительные неограничивающие примеры рекомбинантных терапевтических белков, которые можно получать/очищать с помощью способов по настоящему изобретению, включают алглюкозидазу альфа, ларонидазу, абатацепт, галсульфазу, лютропин альфа, антигемофилический фактор, агалзидазу бета, интерферон бета-1a, дарбепоэтин альфа, тенектеплазу, этанерцепт, фактор свертывания крови IX, фолликулостимулирующий гормон, интерферон бета-1a, имиглюцеразу, дорназу альфа, эпоэтин альфа и альтеплазу.
Секретированный растворимый рекомбинантный терапевтический белок можно получать из жидкой культуральной среды (например, первой и/или второй жидкой культуральной среды) путем удаления или иного физического отделения жидкой культуральной среды от клеток (например, клеток млекопитающего). Из уровня техники известно множество различных способов отделения жидкой культуральной среды от клеток (например, клеток млекопитающего), в том числе, например, центрифугирование, фильтрация, пипетирование и/или аспирация. Затем секретированный рекомбинантный терапевтический белок можно извлекать и дополнительно очищать из жидкой культуральной среды с применением ряда биохимических методик, в том числе различных типов хроматографии (например, аффинной хроматографии, хроматографии на молекулярных ситах, катионообменной хроматографии, анионообменной хроматографии или хроматография с гидрофобным взаимодействием, или любой их комбинации) и/или фильтрации (например, фильтрации с отсечением по молекулярной массе).
Цикл хроматографии
Как общеизвестно из уровня техники, стадии цикла хроматографии могут отличаться в зависимости от смолы для хроматографии, буферов, применяемых для проведения каждой стадии в цикле, и биофизических характеристик целевого рекомбинантного белка (например, рекомбинантного терапевтического белка). Например, колонка для аффинной хроматографии может предусматривать стадии загрузки колонки для аффинной хроматографии текучей средой, включающей целевой рекомбинантный белок, промывания колонки с удалением нежелательного биологического материала (например, загрязняющих белков и/или малых молекул), элюирования целевого рекомбинантного белка, связанного с колонкой, и повторного уравновешивания колонки. Цикл хроматографии с применением колонки для катионо- и/или анионообменной хроматографии, где целевой рекомбинантный белок связывается со смолой для хроматографии на стадии загрузки, может предусматривать стадии загрузки колонки текучей средой, включающей целевой белок, промывания колонки с удалением нежелательного биологического материала, элюирования целевого рекомбинантного белка, связанного с колонкой, и повторного уравновешивания колонки. В других примерах цикл хроматографии с применением колонки для катионо- и/или анионообменной хроматографии, где нежелательный биологический материал связывается со смолой для хроматографии во время стадии загрузки, тогда как целевой рекомбинантный белок не связывается, может предусматривать стадии загрузки колонки текучей средой, включающей целевой белок, сбора целевого рекомбинантного белка в непрерывном потоке и повторного уравновешивания колонки. Как общеизвестно из уровня техники, любая из отдельных стадий в цикле хроматографии может предусматривать один буфер или несколько буферов (например, два или более буферов), и одна или несколько из любых отдельных стадий в цикле хроматографии может предусматривать градиент буфера. В данных способах можно принимать любую из комбинаций различных общеизвестных аспектов отдельного цикла хроматографии в любой комбинации, например, различных смолы(смол) для хроматографии, значения(значений) расхода, буфера(буферов), значения(значений) "мертвого объема" колонки, значения(значений) объема слоя колонки, значения(значений) объема буфера, применяемого на каждой стадии, значения(значений) объема текучей среды, включающей целевой белок, и количества и типа буфера(буферов), применяемого(применяемых) на каждой стадии.
Способы выполнения хроматографии на колонке с уменьшенной бионагрузкой В данном документе предусмотрены способы выполнения хроматографии с уменьшенной бионагрузкой. Такие способы предусматривают обеспечение заполненной хроматографической колонки с уменьшенной бионагрузкой, полученной с применением любого из способов, описанных в данном документе, и выполнение колоночной хроматографии с применением заполненной хроматографической колонки с уменьшенной бионагрузкой. Заполненная хроматографическая колонка с уменьшенной бионагрузкой может содержать по меньшей мере одну из любых смол для хроматографии, описанных в данном документе, в любой комбинации. Например, смола для хроматографии, присутствующая в заполненной хроматографической колонке с уменьшенной бионагрузкой, может представлять собой смолу для аффинной хроматографии, включающую белковый лиганд (например, белок A), или может предусматривать смолу для анионообменной хроматографии. Заполненная хроматографическая колонка с уменьшенной бионагрузкой может характеризоваться любым из иллюстративных значений внутреннего объема, описанных в данном документе. Заполненная хроматографическая колонка с уменьшенной бионагрузкой может иметь любую форму (например, форму цилиндра, близкую к цилиндрической форму или эллиптическую форму), описанную в данном документе или известную из уровня техники. Колоночную хроматографию, проводимую с помощью таких способов, можно применять для очистки или выделения рекомбинантного белка (например, любого из рекомбинантных терапевтических белков, описанных в данном документе или известных из уровня техники). В некоторых примерах заполненная хроматографическая колонка с уменьшенной бионагрузкой является частью системы для многоколоночной хроматографии (MCCS), например, может являться частью системы для периодической противоточной хроматографии (PCCS).
Проводимая колоночная хроматография может предусматривать по меньшей мере один цикл хроматографии, описанный в данном документе или известный из уровня техники. Например, по меньшей мере один цикл хроматографии может предусматривать стадии захвата рекомбинантного белка путем приведения смолы для хроматографии в контакт с жидкостью, включающей рекомбинантный белок; промывания смолы для хроматографии путем приведения смолы для хроматографии в контакт с буфером для промывания, элюирования рекомбинантного белка путем приведения смолы для хроматографии в контакт с буфером для элюирования и восстановления смолы для хроматографии путем приведения смолы для хроматографии в контакт с буфером для регенерации. В некоторых примерах жидкость, включающая рекомбинантный белок, представляет собой жидкую культуральную среду (например, жидкую культуральную среду, собранную из перфузионной культуры или культуры с периодической подпиткой) или разбавленную жидкую культуральную среду (например, культуральную среду, разбавленную в буфере).
Колоночную хроматографию можно проводить с применением закрытой и интегрированной системы (например, любой из иллюстративных закрытых и интегрированных систем, описанных в данном документе или известных из уровня техники). Например, колоночную хроматографию можно проводить с применением закрытой и интегрированной системы, где буфер представляет собой буфер с уменьшенной бионагрузкой. Как общеизвестно из уровня техники, буфер с уменьшенной бионагрузкой можно получать с применением ряда различных способов (например, получать путем фильтрации, автоклавирования или термической обработки).
Колоночная хроматография может предусматривать два или больше (например, 3 или больше, 4 или больше, 5 или больше, 6 или больше, 7 или больше, 8 или больше, 9 или больше, 10 или больше, 11 или больше, 12 или больше, 13 или больше, 14 или больше, 15 или больше, 20 или больше, 25 или больше, 30 или больше, 35 или больше, 40 или больше, 45 или больше, 50 или больше, 55 или больше, 60 или больше, 65 или больше, 70 или больше, 75 или больше, 80 или больше, 85 или больше, 90 или больше, 95 или больше или 100 или больше) циклов хроматографии. В некоторых примерах колоночную хроматографию проводят непрерывно в течение периода времени, составляющего по меньшей мере 3 дня (например, по меньшей мере 4 дня, по меньшей мере 5 дней, по меньшей мере 6 дней, по меньшей мере 7 дней, по меньшей мере 8 дней, по меньшей мере 9 дней, по меньшей мере 10 дней, по меньшей мере 11 дней, по меньшей мере 12 дней, по меньшей мере 13 дней, по меньшей мере 14 дней, по меньшей мере 15 дней, по меньшей мере 16 дней, по меньшей мере 17 дней, по меньшей мере 18 дней, по меньшей мере 19 дней, по меньшей мере 20 дней, по меньшей мере 21 день, по меньшей мере 22 дня, по меньшей мере 23 дня, по меньшей мере 24 дня, по меньшей мере 25 дней, по меньшей мере 30 дней, по меньшей мере 35 дней, по меньшей мере 40 дней, по меньшей мере 45 дней, по меньшей мере 50 дней, по меньшей мере 55 дней, по меньшей мере 60 дней, по меньшей мере 65 дней, по меньшей мере 70 дней, по меньшей мере 75 дней, по меньшей мере 80 дней, по меньшей мере 85 дней, по меньшей мере 90 дней, по меньшей мере 95 дней или по меньшей мере 100 дней).
В некоторых вариантах осуществления смола для хроматографии в заполненной хроматографической колонке с уменьшенной бионагрузкой характеризуется связывающей способностью, составляющей от приблизительно 75% до приблизительно 100% (например, от приблизительно 76% до приблизительно 98%, от приблизительно 76% до приблизительно 96%, от приблизительно 76% до приблизительно 94%, от приблизительно 76% до приблизительно 92%, от приблизительно 76% до приблизительно 90%, от приблизительно 78% до приблизительно 100%, от приблизительно 78% до приблизительно 98%, от приблизительно 78% до приблизительно 96%, от приблизительно 78% до приблизительно 94%, от приблизительно 78% до приблизительно 92%, от приблизительно 78% до приблизительно 90%, от приблизительно 80% до приблизительно 100%, от приблизительно 80% до приблизительно 98%, от приблизительно 80% до приблизительно 96%, от приблизительно 80% до приблизительно 94%, от приблизительно 80% до приблизительно 92%, от приблизительно 80% до приблизительно 90%, от приблизительно 82% до приблизительно 100%, от приблизительно 82% до приблизительно 98%, от приблизительно 82% до приблизительно 96%, от приблизительно 82% до приблизительно 94%, от приблизительно 82% до приблизительно 92%, от приблизительно 82% до приблизительно 90%, от приблизительно 84% до приблизительно 100%, от приблизительно 84% до приблизительно 98%, от приблизительно 84% до приблизительно 96%, от приблизительно 84% до приблизительно 94%, от приблизительно 84% до приблизительно 92%, от приблизительно 84% до приблизительно 90%, от приблизительно 86% до приблизительно 100%, от приблизительно 86% до приблизительно 98%, от приблизительно 86% до приблизительно 96%, от приблизительно 86% до приблизительно 94%, от приблизительно 86% до приблизительно 92%, от приблизительно 88% до приблизительно 100%, от приблизительно 88% до приблизительно 98%, от приблизительно 88% до приблизительно 96%, от приблизительно 88% до приблизительно 94%, от приблизительно 90% до приблизительно 100%, от приблизительно 90% до приблизительно 98%, от приблизительно 90% до приблизительно 96%, от приблизительно 92% до приблизительно 100% или от приблизительно 92% до приблизительно 98%) по сравнению с такой же смолой, не подвергнутой обработке с помощью гамма-излучения (при этом применяют один и тот же белок для тестирования связывающей способности обеих смол) (например, при оценке непосредственно после воздействия гамма-излучения).
Интегрированные закрытые или по сути закрытые и непрерывные способы производства рекомбинантного белка
В данном документе предусмотрены интегрированные закрытые или по сути закрытые и непрерывные способы производства очищенного рекомбинантного белка (например, рекомбинантного терапевтического белка). Такие способы предусматривают обеспечение жидкой культуральной среды, включающей рекомбинантный белок (например, рекомбинантный терапевтический белок), по сути не содержащей клеток.
Некоторые способы предусматривают непрерывную подачу жидкой культуральной среды в систему для многоколоночной хроматографии (MCCS), которая включает по меньшей мере одну заполненную хроматографическую колонку с уменьшенной бионагрузкой, предусмотренную в данном документе, при этом в таких способах используют буфер с уменьшенной бионагрузкой, они являются интегрированными, и их осуществляют непрерывно от жидкой культуральной среды до элюата, выходящего из MCCS, который представляет собой очищенный рекомбинантный белок (например, лекарственное вещество на основе терапевтического белка).
Некоторые способы предусматривают непрерывную подачу жидкой культуральной среды в первую MCCS (MCCS1), захват рекомбинантного белка из жидкой культуральной среды с применением MCCS1, получение элюата, выходящего из MCCS1, который включает рекомбинантный белок, и непрерывную подачу элюата во вторую MCCS (MCCS2), и непрерывную подачу рекомбинантного белка из элюата в MCCS2, и последующее элюирование рекомбинантного белка с получением таким образом очищенного рекомбинантного белка, где по меньшей мере одна колонка в MCCS1 и/или MCCS2 представляет собой заполненную хроматографическую колонку с уменьшенной бионагрузкой, предусмотренную в данном документе, при этом в способах используют буфер с уменьшенной бионагрузкой, они являются интегрированными, и их осуществляют непрерывно от жидкой культуральной среды до очищенного рекомбинантного белка.
В некоторых примерах каждая из хроматографических колонок, применяемых в MCCS, MCCS1 и/или MCCS2, представляет собой заполненную хроматографическую колонку с уменьшенной бионагрузкой, предусмотренную в данном документе. Некоторые варианты осуществления дополнительно включают стадию составления очищенного рекомбинантного белка в фармацевтическую композицию.
Способы, описанные в данном документе, обеспечивают непрерывное и быстрое получение очищенного рекомбинантного белка из жидкой культуральной среды, включающей рекомбинантный белок. Например, время, которое проходит от подачи жидкой культуральной среды, включающей терапевтический белок, в MCCS или MCCS1, до элюирования рекомбинантного белка из MCCS или MCCS2 соответственно, может составлять, например, от приблизительно 4 часов до приблизительно 48 часов включительно, например, от приблизительно 4 часов до приблизительно 40 часов, от приблизительно 4 часов до приблизительно 35 часов, от приблизительно 4 часов до приблизительно 30 часов, от приблизительно 4 часов до приблизительно 28 часов, от приблизительно 4 часов до приблизительно 26 часов, от приблизительно 4 часов до приблизительно 24 часов, от приблизительно 4 часов до приблизительно 22 часов, от приблизительно 4 часов до приблизительно 20 часов, от приблизительно 4 часов до приблизительно 18 часов, от приблизительно 4 часов до приблизительно 16 часов, от приблизительно 4 часов до приблизительно 14 часов, от приблизительно 4 часов до приблизительно 12 часов, от приблизительно 6 часов до приблизительно 12 часов, от приблизительно 8 часов до приблизительно 12 часов, от приблизительно 6 часов до приблизительно 20 часов, от приблизительно 6 часов до приблизительно 18 часов, от приблизительно 6 часов до приблизительно 14 часов, от приблизительно 8 часов до приблизительно 16 часов, от приблизительно 8 часов до приблизительно 14 часов, от приблизительно 8 часов до приблизительно 12 часов, от приблизительно 10 часов до 20 часов, от приблизительно 10 часов до 18 часов, от приблизительно 10 часов до 16 часов, от приблизительно 10 часов до 14 часов, от приблизительно 12 часов до приблизительно 14 часов, от приблизительно 10 часов до приблизительно 40 часов, от приблизительно 10 часов до приблизительно 35 часов, от приблизительно 10 часов до приблизительно 30 часов, от приблизительно 10 часов до приблизительно 25 часов, от приблизительно 15 часов до приблизительно 40 часов, от приблизительно 15 часов до приблизительно 35 часов, от приблизительно 15 часов до приблизительно 30 часов, от приблизительно 20 часов до приблизительно 40 часов, от приблизительно 20 часов до приблизительно 35 часов или от приблизительно 20 часов до приблизительно 30 часов включительно. В других примерах, время, которое проходит от подачи жидкой культуральной среды, включающей рекомбинантный белок, в MCCS или MCCS1, до элюирования рекомбинантного белка из MCCS или MCCS2 соответственно, составляет, например, более чем приблизительно 4 часа и менее чем приблизительно 40 часов включительно, например, более чем приблизительно 4 часа и менее чем приблизительно 39 часов, приблизительно 38 часов, приблизительно 37 часов, приблизительно 36 часов, приблизительно 35 часов, приблизительно 34 часа, приблизительно 33 часа, приблизительно 32 часа, приблизительно 31 час, приблизительно 30 часов, приблизительно 29 часов, приблизительно 28 часов, приблизительно 27 часов, приблизительно 26 часов, приблизительно 25 часов, приблизительно 24 часа, приблизительно 23 часа, приблизительно 22 часа, приблизительно 21 час, приблизительно 20 часов, приблизительно 19 часов, приблизительно 18 часов, приблизительно 17 часов, приблизительно 16 часов, приблизительно 15 часов, приблизительно 14 часов, приблизительно 13 часов, приблизительно 12 часов, приблизительно 11 часов, приблизительно 10 часов, приблизительно 9 часов, приблизительно 8 часов, приблизительно 7 часов, приблизительно 6 часов, приблизительно 5 часов или приблизительно 4,5 часа включительно.
Неограничивающие аспекты MCCS, которые можно применять в любом из таких способов (MCCS, MCCS1 и/или MCCS2), описаны в предварительных заявках на патент США №№ 61/775060 и 61/856390 (каждая из которых включена в данный документ посредством ссылки).
В некоторых иллюстративных способах не используют стадию удерживания (например, не применяют резервуар (например, буферную емкость) во всем способе). В других случаях во всем способе могут применять максимально 1, 2, 3, 4 или 5 резервуаров (например, буферных емкостей). В любом из способов, описанных в данном документе, можно использовать максимально 1, 2, 3, 4 или 5 резервуаров (например, буферных емкостей) во всем способе, где в каждой буферной емкости рекомбинантный белок выдерживают только в течение общего периода времени, составляющего, например, от приблизительно 5 минут до менее чем приблизительно 6 часов включительно, например, от приблизительно 5 минут до приблизительно 5 часов, приблизительно 4 часов, приблизительно 3 часов, приблизительно 2 часов, приблизительно 1 часа или приблизительно 30 минут включительно.
В некоторых способах используют один, два, три, четыре, пять или шесть резервуаров (например, буферных емкостей), и они могут характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 300 мл включительно, например, от 1 мл до приблизительно 280 мл, приблизительно 260 мл, приблизительно 240 мл, приблизительно 220 мл, приблизительно 200 мл, приблизительно 180 мл, приблизительно 160 мл, приблизительно 140 мл, приблизительно 120 мл, приблизительно 100 мл, приблизительно 80 мл, приблизительно 60 мл, приблизительно 40 мл, приблизительно 20 мл или приблизительно 10 мл (включительно). Любой(любые) резервуар(резервуары) (например, буферная(буферные) емкость(емкости)), применяемый(применяемые) (в любом из способов, описанных в данном документе) для удерживания текучей среды перед ее подачей в MCCS или MCCS1, может(могут) характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 100% включительно, например, от 1 мл до приблизительно 90%, приблизительно 80%, приблизительно 70%, приблизительно 60%, приблизительно 50%, приблизительно 40%, приблизительно 30%, приблизительно 20%, приблизительно 10% или приблизительно 5% включительно относительно загрузочного объема первой колонки MCCS или MCCS1. Резервуар(резервуары) (например, буферную(буферные) емкость(емкости)) можно применять для удерживания элюата, выходящего из MCCS1, перед тем, как он входит в MCCS2, и он(они) характеризуется(характеризуются) емкостью, составляющей, например, от 1 мл до приблизительно 100% включительно, например, от 1 мл до приблизительно 90%, приблизительно 80%, приблизительно 70%, приблизительно 60%, приблизительно 50%, приблизительно 40%, приблизительно 30%, приблизительно 20%, приблизительно 10% или приблизительно 5% включительно относительно загрузочного объема первой колонки MCCS2.
Различные дополнительные аспекты данных способов подробно описаны ниже, и их можно применять без ограничения в любой комбинации в способах, предусмотренных в данном документе. Иллюстративные аспекты предусмотренных способов описаны ниже; тем не менее, специалисту в данной области техники будет понятно, что можно добавлять дополнительные стадии в способы, описанные в данном документе, и можно применять другие материалы для осуществления любой из стадий способов, описанных в данном документе.
Жидкая культуральная среда
Жидкая культуральная среда, которая включает рекомбинантный белок (например, рекомбинантный терапевтический белок), по сути не содержащая клеток, может быть получена из любого источника. Например, жидкая культуральная среда может быть получена из культуры рекомбинантных клеток (например, культуры рекомбинантных клеток бактерий, дрожжей или млекопитающего). Жидкая культуральная среда может быть получена из культуры клеток с периодической подпиткой (например, клеток млекопитающего) (например, из биореактора периодического действия с подпиткой, включающего культуру клеток млекопитающего, которые секретируют рекомбинантный белок) или перфузионной культуры клеток (например, клеток млекопитающего) (например, из перфузионного биореактора, включающего культуру клеток млекопитающего, которые секретируют рекомбинантный белок). Жидкая культуральная среда также может представлять собой осветленную жидкую культуральную среду из культуры клеток бактерий или дрожжей, которые секретируют рекомбинантный белок.
Жидкую культуральную среду, полученную из культуры рекомбинантных клеток, можно фильтровать или осветлять с получением жидкой культуральной среды, по сути не содержащей клеток и/или вирусов. Способы фильтрации или осветления жидкой культуральной среды для удаления клеток известны из уровня техники (например, фильтрация через поры размером 0,2 мкм или фильтрация с применением системы с переменным тангенциальным потоком (ATFTM)). Рекомбинантные клетки также можно удалять из жидкой культуральной среды с применением центрифугирования и удаления надосадочной жидкости, представляющей собой жидкую культуральную среду, по сути не содержащую клеток, или путем обеспечения возможности осаждения клеток на гравитационное дно контейнера (например, биореактора), включающего жидкую культуральную среду, и удаления жидкой культуральной среды (жидкой культуральной среды, по сути не содержащей клеток), которая расположена в отдалении от осажденных рекомбинантных клеток.
Жидкая культуральная среда может быть получена из культуры рекомбинантных клеток (например, рекомбинантных клеток бактерий, дрожжей или млекопитающего), продуцирующих любой из рекомбинантных белков (например, рекомбинантных терапевтических белков), описанных в данном документе или известных из уровня техники. Некоторые примеры любого из способов, описанных в данном документе, могут дополнительно предусматривать стадию культивирования рекомбинантных клеток (например, рекомбинантных клеток бактерий, дрожжей или млекопитающего), продуцирующих рекомбинантный белок (например, рекомбинантный терапевтический белок).
Жидкая культуральная среда может относиться к любому из типов жидкой культуральной среды, описанных в данном документе или известных из уровня техники. Например, жидкая культуральная среда может быть выбрана из группы, состоящей из жидкой культуральной среды, не содержащей компонентов животного происхождения, жидкой культуральной среды, не содержащей сыворотки крови, жидкой культуральной среды, содержащей сыворотку крови, жидкой культуральной среды с определенным химическим составом и жидкой культуральной среды, не содержащей белков. В любом из способов, описанных в данном документе, жидкую культуральную среду, полученную из культуры, можно разбавлять путем добавления второй текучей среды (например, буфера) перед ее подачей в MCCS или MCCS1.
Жидкую культуральную среду, включающую рекомбинантный белок, по сути не содержащую клеток, можно хранить (например, при температуре ниже чем приблизительно 15°C (например, ниже чем приблизительно 10°C, ниже чем приблизительно 4°C, ниже чем приблизительно 0°C, ниже чем приблизительно −20°C, ниже чем приблизительно −50°C, ниже чем приблизительно −70°C или ниже чем приблизительно −80°C) в течение по меньшей мере 1 дня (например, по меньшей мере приблизительно 2 дней, по меньшей мере приблизительно 5 дней, по меньшей мере приблизительно 10 дней, по меньшей мере приблизительно 15 дней, по меньшей мере приблизительно 20 дней или по меньшей мере приблизительно 30 дней) перед подачей жидкой культуральной среды в MCCS или MCCS1. В качестве альтернативы, в некоторых примерах жидкую культуральную среду подают в MCCS или MCCS1 непосредственно из биореактора (например, подают в MCCS или MCCS1 непосредственно из биореактора после стадии фильтрования или осветления).
Системы для многоколоночной хроматографии
Способы, описанные в данном документе, предусматривают применение MCCS или двух или более (например, двух, трех, четырех, пяти или шести) систем для многоколоночной хроматографии (MCCS) (например, MCCS1 и MCCS2). MCCS может содержать две или более хроматографических колонок, две или более хроматографических мембран или комбинацию по меньшей мере одной хроматографической колонки и по меньшей мере одной хроматографической мембраны. В неограничивающих примерах MCCS (например, MCCS, MCCS1 и/или MCCS2 в любом из способов в данном документе) может содержать четыре хроматографические колонки, три хроматографические колонки и хроматографическую мембрану, три хроматографические колонки, две хроматографические колонки, две хроматографические мембраны, а также две хроматографические колонки и одну хроматографическую мембрану. Специалист в данной области техники сможет без ограничения предположить дополнительные примеры комбинаций хроматографических колонок и/или хроматографических мембран для применения в MCCS (например, MCCS, MCCS1 и/или MCCS2 в любом из способов, описанных в данном документе). Отдельные хроматографические колонки и/или хроматографические мембраны, присутствующие в MCCS, могут быть идентичными (например, характеризоваться одинаковыми формой, объемом, смолой, механизмом захвата и отдельной операцией) или могут быть разными (например, характеризоваться одним или несколькими из различных формы, объема, смолы, механизма захвата и/или отдельной операции). В отдельной(отдельных) хроматографической(хроматографических) колонке(колонках) и/или хроматографической(хроматографических) мембране(мембранах), присутствующих в MCCS (например, MCCS, MCCS1 и/или MCCS2 в любом из способов, описанных в данном документе), можно проводить одну и ту же отдельную операцию (например, отдельную операцию захвата, очистки или тонкой очистки) или разные отдельные операции (например, разные отдельные операции, выбранные, например, из группы, включающей захват, очистку, тонкую очистку, инактивацию вирусов, регулирование концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок, и фильтрование). Например, в примерах способов, описанных в данном документе, в по меньшей мере одной хроматографической колонке и/или хроматографической мембране в MCCS или MCCS1 осуществляют отдельную операцию захвата рекомбинантного белка.
Одна или несколько хроматографических колонок, которые могут быть присутствовать в MCCS (например, присутствовать в MCCS, MCCS1 и/или MCCS2), могут характеризоваться объемом смолы, составляющим, например, от приблизительно 1 мл до приблизительно 2 мл, приблизительно 5 мл, приблизительно 10 мл, приблизительно 15 мл, приблизительно 20 мл, приблизительно 25 мл, приблизительно 30 мл, приблизительно 35 мл, приблизительно 40 мл, приблизительно 45 мл, приблизительно 50 мл, приблизительно 55 мл, приблизительно 60 мл, приблизительно 65 мл, приблизительно 70 мл, приблизительно 75 мл, приблизительно 80 мл, приблизительно 85 мл, приблизительно 90 мл, приблизительно 95 мл или приблизительно 100 мл включительно. Одна или несколько хроматографических колонок, которые могут присутствовать в MCCS (например, присутствовать в MCCS, MCCS1 и/или MCCS2), могут характеризоваться объемом смолы, составляющим от приблизительно 2 мл до приблизительно 100 мл, от приблизительно 2 мл до приблизительно 90 мл, от приблизительно 2 мл до приблизительно 80 мл, от приблизительно 2 мл до приблизительно 70 мл, от приблизительно 2 мл до приблизительно 60 мл, от приблизительно 2 мл до приблизительно 50 мл, от приблизительно 5 мл до приблизительно 50 мл, от приблизительно 2 мл до приблизительно 45 мл, от приблизительно 5 мл до приблизительно 45 мл, от приблизительно 2 мл до приблизительно 40 мл, от приблизительно 5 мл до приблизительно 40 мл, от приблизительно 2 мл до приблизительно 35 мл, от приблизительно 5 мл до приблизительно 35 мл, от приблизительно 2 мл до приблизительно 30 мл, от приблизительно 5 мл до приблизительно 30 мл, от приблизительно 2 мл до приблизительно 25 мл, от приблизительно 5 мл до приблизительно 25 мл, от приблизительно 15 мл до приблизительно 60 мл, от приблизительно 10 мл до приблизительно 60 мл, от приблизительно 10 мл до приблизительно 50 мл и от приблизительно 15 мл до приблизительно 50 мл. Одна или несколько хроматографических колонок в MCCS (например, MCCS, MCCS1 и/или MCCS2), применяемых в любом из способов, описанных в данном документе, могут характеризоваться по сути одинаковым объемом смолы или могут характеризоваться разными значениями объема смолы. Расход, применяемый для одной или нескольких хроматографических колонок в MCCS (например, в MCCS, MCCS1 и/или MCCS2), может составлять, например, от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута).
Одна или несколько хроматографических колонок в MCCS (например, в MCCS, MCCS1 и/или MCCS2) могут иметь по сути одинаковую форму или могут иметь по сути разные формы. Например, одна или несколько хроматографических колонок в MCCS (например, в MCCS, MCCS1 и/или MCCS2) могут иметь по сути форму кругового цилиндра или могут иметь по сути одинаковую форму овального цилиндра.
Одна или несколько хроматографических мембран, которые могут присутствовать в MCCS (например, присутствовать в MCCS, MCCS1 и/или MCCS2), могут характеризоваться объемом слоя, составляющим, например, от приблизительно 1 мл до приблизительно 500 мл (например, от приблизительно 1 мл до приблизительно 475 мл, от приблизительно 1 мл до приблизительно 450 мл, от приблизительно 1 мл до приблизительно 425 мл, от приблизительно 1 мл до приблизительно 400 мл, от приблизительно 1 мл до приблизительно 375 мл, от приблизительно 1 мл до приблизительно 350 мл, от приблизительно 1 мл до приблизительно 325 мл, от приблизительно 1 мл до приблизительно 300 мл, от приблизительно 1 мл до приблизительно 275 мл, от приблизительно 1 мл до приблизительно 250 мл, от приблизительно 1 мл до приблизительно 225 мл, от приблизительно 1 мл до приблизительно 200 мл, от приблизительно 1 мл до приблизительно 175 мл, от приблизительно 1 мл до приблизительно 150 мл, от приблизительно 1 мл до приблизительно 125 мл, от приблизительно 1 мл до приблизительно 100 мл, от приблизительно 2 мл до приблизительно 100 мл, от приблизительно 5 мл до приблизительно 100 мл, от приблизительно 1 мл до приблизительно 80 мл, от приблизительно 2 мл до приблизительно 80 мл, от приблизительно 5 мл до приблизительно 80 мл, от приблизительно 1 мл до приблизительно 60 мл, от приблизительно 2 мл до приблизительно 60 мл, от приблизительно 5 мл до приблизительно 60 мл, от приблизительно 1 мл до приблизительно 40 мл, от приблизительно 2 мл до приблизительно 40 мл, от приблизительно 5 мл до приблизительно 40 мл, от приблизительно 1 мл до приблизительно 30 мл, от приблизительно 2 мл до приблизительно 30 мл, от приблизительно 5 мл до приблизительно 30 мл, от приблизительно 1 мл до приблизительно 25 мл, от приблизительно 2 мл до приблизительно 25 мл, от приблизительно 1 мл до приблизительно 20 мл, от приблизительно 2 мл до приблизительно 20 мл, от приблизительно 1 мл до приблизительно 15 мл, от приблизительно 2 мл до приблизительно 15 мл, от приблизительно 1 мл до приблизительно 10 мл или от приблизительно 2 мл до приблизительно 10 мл).
Можно использовать один или несколько (например, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать, двадцать один, двадцать два, двадцать три или двадцать четыре) разных типов буфера с уменьшенной бионагрузкой во время применения MCCS, MCCS1 и/или MCCS2 в любом из способов, описанных в данном документе. Как известно из уровня техники, один или несколько типов буферов с уменьшенной бионагрузкой, применяемых в MCCS, MCCS1 и/или MCCS2 в способах, описанных в данном документе, будут зависеть от смолы, присутствующей в хроматографической(хроматографических) колонке(колонках) и/или в хроматографической(хроматографических) мембране(мембранах) в MCCS, MCCS1 и/или MCCS2, от биофизических свойств рекомбинантного белка и отдельной операции (например, от любой из иллюстративных отдельных операций, описанных в данном документе), которую проводят с помощью конкретной(конкретных) хроматографической(хроматографических) колонки(колонок) и/или хроматографических мембран в MCCS, MCCS1 и/или MCCS2. Специалист в данной области техники также сможет определить объем и тип буфера, используемого во время применения MCCS, MCCS1 и/или MCCS2 в любом из способов, описанных в данном документе (например, рассмотренных более подробно ниже). Например, объем и тип(типы) буфера, используемого во время применения MCCS, MCCS1 и/или MCCS2 в любом из способов, описанных в данном документе, можно выбирать с целью оптимизации одного или нескольких из следующего в очищенном рекомбинантном белке (например, в лекарственном препарате на основе рекомбинантного белка): общего выхода рекомбинантного белка, активности рекомбинантного белка, уровня чистоты рекомбинантного белка и удаления биологических загрязнителей из текучей среды, включающей рекомбинантный белок (например, жидкой культуральной среды) (например, с обеспечением отсутствия активных вирусов, микобактерий, дрожжей, бактерий или клеток млекопитающего).
MCCS, MCCS1 и/или MCCS2 могут представлять собой систему для периодической противоточной хроматографии (PCCS). PCCS может, например, содержать две или более хроматографических колонок (например, три колонки или четыре колонки), которые можно переключать для обеспечения непрерывного элюирования рекомбинантного белка из двух или более хроматографических колонок. PCCS может содержать две или более хроматографических колонок, две или более хроматографических мембран или по меньшей мере одну хроматографическую колонку и по меньшей мере одну хроматографическую мембрану. Операция в колонке (цикл) обычно состоит из стадий загрузки, промывания, элюирования и регенерации. В PCCS несколько колонок применяют для осуществления тех же стадий по отдельности и непрерывно циклическим образом. Поскольку колонки функционируют последовательно, вышедший поток и промывная жидкость из одной колонки захватываются другой колонкой. Этот уникальный признак PCCS обеспечивает возможность загрузки смолы до значений, близких к ее статической связывающей способности, а не значений динамической связывающей способности, типичных в ходе хроматографии в периодическом режиме. В результате непрерывного проведения циклов и элюирования текучая среда, входящая в PCCS, непрерывно обрабатывается, и непрерывно образуется элюат, содержащий рекомбинантный белок.
Стратегию переключения колонок применяют для продвижения от одной стадии к другой в цикле PCCS. Примеры переключения колонок, которые можно использовать в PCCS, описаны в предварительных заявках на патент США №№ 61/775060 и 61/856390. Например, в способе переключения колонок могут использоваться две автоматизированные операции переключения на колонку, первая из которых связана с проскоком исходного продукта, а вторая соответствует насыщению колонки. Определение того, когда должны происходить операции переключения колонок, может происходить путем отслеживания концентрации рекомбинантного белка (например, отслеживания, осуществляемого с помощью отслеживания по УФ-излучению) в элюате из каждой хроматографической колонки, присутствующей в PCCS. Например, переключение колонок может определяться с помощью любого средства PAT, обеспечивающего возможность измерения в потоке концентрации рекомбинантного белка с управлением с обратной связью. Средство PAT обеспечивает возможность измерения в потоке в реальном времени концентрации рекомбинантного белка с управлением с обратной связью. Как известно из уровня техники, переключения колонок также могут быть разработаны в зависимости от времени или количества текучей среды (например, буфера), проходящей через одну или несколько хроматографических колонок и/или хроматографических мембран в MCCS, MCCS1 и/или MCCS2.
В PCCS время удержания (RT) рекомбинантного белка в каждой хроматографической колонке и/или на хроматографической мембране, присутствующей в PCCS, можно снижать без увеличения размера колонки/мембраны, поскольку проскок из первой колонки/мембраны может захватываться на другой колонке/мембране в PCCS. Система для непрерывного способа может быть разработана с возможностью обработки жидкой культуральной среды при любой скорости перфузии (D) путем изменения объема колонки/мембраны (V) и RT с применением уравнения: V=D × RT.
Одна или несколько отдельных операций, которые можно проводить с помощью MCCS или MCC1 и/или MCCS2, применяемых в описанных в данном документе способах, включают, например, захват рекомбинантного белка, инактивацию вирусов, присутствующих в текучей среде, включающей рекомбинантный белок, очистку рекомбинантного белка, тонкую очистку рекомбинантного белка, удерживание текучей среды, включающей рекомбинантный белок (например, с применением любой из иллюстративных буферных емкостей, описанных в данном документе), фильтрование или удаление твердых частиц и/или клеток из текучей среды, включающей рекомбинантный белок, и регулирование концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок.
В некоторых вариантах осуществления MCCS или MCCS1 включает по меньшей мере одну хроматографическую колонку и/или хроматографическую мембрану, в которых проводят отдельную операцию захвата рекомбинантного белка. Отдельную операцию захвата можно проводить с применением по меньшей мере одной хроматографической колонки и/или смолы для хроматографии, например, в которой используется механизм захвата. Неограничивающие примеры механизмов захвата включают механизм захвата посредством связывания с белком A, механизм захвата посредством связывания c антителом или фрагментом антитела, механизм захвата посредством связывания с субстратом, механизм захвата посредством связывания с аптамером, механизм захвата посредством связывания с меткой (например, механизм захвата на основе метки поли-His) и механизм захвата посредством связывания с кофактором. Захват также можно проводить с применением смолы, которую можно применять для проведения катионообменной или анионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием. Неограничивающие смолы, которые можно применять для захвата рекомбинантного белка, описаны в данном документе. Дополнительные примеры смол, которые можно применять для захвата рекомбинантного белка, известны из уровня техники.
Отдельную операцию инактивации вирусов, присутствующих в текучей среде, включающей рекомбинантный белок, можно проводить с применением MCCS, MCCS1 и/или MCCS2 (например, которая(которые) включает(включают), например, хроматографическую колонку, хроматографическую мембрану или емкость для удерживания, пригодную для инкубирования текучей среды, включающей рекомбинантный белок, при pH, составляющем от приблизительно 3,0 до 5,0 (например, от приблизительно 3,5 до приблизительно 4,5, от приблизительно 3,5 до приблизительно 4,25, от приблизительно 3,5 до приблизительно 4,0, от приблизительно 3,5 до приблизительно 3,8 или приблизительно 3,75) в течение периода времени, составляющего по меньшей мере 30 минут (например, периода времени, составляющего от приблизительно 30 минут до 1,5 часа, периода времени, составляющего от приблизительно 30 минут до 1,25 часа, периода времени, составляющего от приблизительно 0,75 часа до 1,25 часа, или периода времени, составляющего приблизительно 1 час)).
Отдельную операцию очистки рекомбинантного белка можно проводить с применением одной или нескольких MCCS (например, MCCS, MCCS1 и/или MCCS2), которые включают, например, хроматографическую колонку или хроматографическую мембрану, которые содержат смолу, например, такую, в которой используется система захвата. Неограничивающие примеры механизмов захвата включают механизм захвата посредством связывания с белком A, механизм захвата посредством связывания c антителом или фрагментом антитела, механизм захвата посредством связывания с субстратом, механизм захвата посредством связывания с аптамером, механизм захвата посредством связывания с меткой (например, механизм захвата на основе метки поли-His) и механизм захвата посредством связывания с кофактором. Очистку также можно проводить с применением смолы, которую можно применять для проведения катионообменной или анионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием. Неограничивающие смолы, которые можно применять для очистки рекомбинантного белка, описаны в данном документе. Дополнительные примеры смол, которые можно применять для очистки рекомбинантного белка, известны из уровня техники.
Отдельную операцию тонкой очистки рекомбинантного белка можно проводить с применением одной или нескольких MCCS (например, MCCS, MCCS1 и/или MCCS), которые включают, например, хроматографическую колонку или хроматографическую мембрану, которые содержат смолу, например, такую, которую можно применять для проведения катионообменной, анионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием. Неограничивающие смолы, которые можно применять для тонкой очистки рекомбинантного белка, описаны в данном документе. Дополнительные примеры смол, которые можно применять для тонкой очистки рекомбинантного белка, известны из уровня техники.
Отдельную операцию удерживания текучей среды, включающей рекомбинантный белок, можно проводить с применением MCCS (например, MCCS, MCCS1 и/или MCCS2), которая включает по меньшей мере один резервуар (например, буферную емкость) или максимально 1, 2, 3, 4 или 5 резервуаров (например, буферных емкостей) в MCCS или в MCCS1 и MCCS2 в совокупности. Например, каждый из резервуаров (например, буферных емкостей), которые можно применять для осуществления данной отдельной операции, может характеризоваться объемом, составляющим от приблизительно 1 мл до приблизительно 1 л (например, от приблизительно 1 мл до приблизительно 800 мл, от приблизительно 1 мл до приблизительно 600 мл, от приблизительно 1 мл до приблизительно 500 мл, от приблизительно 1 мл до приблизительно 400 мл, от приблизительно 1 мл до приблизительно 350 мл, от приблизительно 1 мл до приблизительно 300 мл, от приблизительно 10 мл до приблизительно 250 мл, от приблизительно 10 мл до приблизительно 200 мл, от приблизительно 10 мл до приблизительно 150 мл или от приблизительно 10 мл до приблизительно 100 мл). Резервуар(резервуары) (например, буферная(буферные) емкость(емкости)), применяемый(применяемые) в способах, описанных в данном документе, может(могут) характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 300 мл включительно, например, от 1 мл до приблизительно 280 мл, приблизительно 260 мл, приблизительно 240 мл, приблизительно 220 мл, приблизительно 200 мл, приблизительно 180 мл, приблизительно 160 мл, приблизительно 140 мл, приблизительно 120 мл, приблизительно 100 мл, приблизительно 80 мл, приблизительно 60 мл, приблизительно 40 мл, приблизительно 20 мл или приблизительно 10 мл включительно. Любой из резервуаров (например, буферных емкостей), применяемых (в любом из способов, описанных в данном документе) для удерживания текучей среды перед тем, как она входит в MCCS или MCCS1, может характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 100% включительно, от приблизительно 1 мл до приблизительно 90%, приблизительно 80%, приблизительно 70%, приблизительно 60%, приблизительно 50%, приблизительно 40%, приблизительно 30%, приблизительно 20%, приблизительно 10% или приблизительно 5% включительно относительно загрузочного объема первой колонки MCCS или MCCS1. Любой из резервуаров (например, буферных емкостей), применяемых для удерживания элюата, выходящего из MCCS1 (включающего рекомбинантный белок), перед тем, как он входит в MCCS2, может характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 100% включительно, например, от приблизительно 1 мл до приблизительно 90%, приблизительно 80%, приблизительно 70%, приблизительно 60%, приблизительно 50%, приблизительно 40%, приблизительно 30%, приблизительно 20%, приблизительно 10% или приблизительно 5% включительно относительно загрузочного объема первой колонки MCCS2.
Каждый из резервуаров (например, буферных емкостей) может удерживать текучую среду, включающую рекомбинантный белок, в течение по меньшей мере 10 минут (например, по меньшей мере 20 минут, по меньшей мере 30 минут, по меньшей мере 1 часа, по меньшей мере 2 часов, по меньшей мере 4 часов или по меньшей мере 6 часов). В других примерах резервуар(резервуары) (например, буферная(буферные) емкость(емкости)) удерживает(удерживают) рекомбинантный белок только в течение общего периода времени, составляющего, например, от приблизительно 5 минут до менее чем приблизительно 6 часов включительно, например, от приблизительно 5 минут до приблизительно 5 часов, приблизительно 4 часов, приблизительно 3 часов, приблизительно 2 часов, приблизительно 1 часа или приблизительно 30 минут включительно. Резервуар(резервуары) (например, буферную(буферные) емкость(емкости)) можно применять как для удерживания, так и для охлаждения (например, при температуре, составляющей менее 25°C, менее 15°C или менее 10°C) текучей среды, включающей рекомбинантный белок. Резервуар может иметь любую форму, в том числе кругового цилиндра, овального цилиндра или примерно прямоугольной герметичной и непроницаемой камеры.
Отдельные операции фильтрования текучей среды, включающей рекомбинантный белок, можно проводить с применением MCCS (например, MCCS, MCCS1 и/или MCCS2), которая включает, например, фильтр, или хроматографическую колонку, или хроматографическую мембрану, которые содержат смолу для хроматографии на молекулярных ситах. Как известно из уровня техники, в данной области техники доступно большое разнообразие субмикронных фильтров (например, фильтр с размером пор, составляющим менее 1 мкм, менее 0,5 мкм, менее 0,3 мкм, приблизительно 0,2 мкм, менее 0,2 мкм, менее 100 нм, менее 80 нм, менее 60 нм, менее 40 нм, менее 20 нм или менее 10 нм), которые пригодны для удаления любого осажденного материала и/или клеток (например, осажденного несвернутого белка; осажденных нежелательных белков клетки-хозяина; осажденных липидов; бактерий; дрожжевых клеток; клеток грибов; микобактерий и/или клеток млекопитающего). Известно, что фильтры с размером пор, составляющим приблизительно 0,2 мкм или менее 0,2 мкм, эффективно удаляют бактерии из текучей среды, включающей рекомбинантный белок. Как известно из уровня техники, можно также применять хроматографическую колонку или хроматографическую мембрану, включающие смолу для хроматографии на молекулярных ситах, в MCCS (например, в MCCS, MCCS1 и/или MCCS2) для проведения отдельной операции фильтрования текучей среды, включающей рекомбинантный белок.
Отдельные операции регулирования концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок, можно проводить с применением MCCS (например, MCCS, MCCS1 и/или MCCS2), в которую включен и в которой используется резервуар для регулирования буфера (например, резервуар для регулирования буфера в потоке), который обеспечивает добавление нового буферного раствора в текучую среду, которая включает рекомбинантный белок (например, между колонками внутри MCCS, MCCS1 и/или MCCS2, или после последней колонки в предпоследней MCCS (например, MCCS1) и перед подачей текучей среды, включающей рекомбинантный белок, в первую колонку следующей MCCS (например, MCCS2)). Как можно понять из уровня техники, резервуар для регулирования буфера в потоке может иметь любой размер (например, более 100 мл) и может содержать любой буферный раствор (например, буферный раствор, который характеризуется одним или несколькими из повышенного или пониженного pH по сравнению с текучей средой, включающей рекомбинантный белок, повышенной или пониженной концентрации ионов (например, соли) по сравнению с текучей средой, включающей рекомбинантный белок, и/или повышенной или пониженной концентрации средства, конкурирующего с рекомбинантным белком за связывание со смолой, присутствующей в по меньшей мере одной хроматографической колонке или по меньшей мере одной хроматографической мембране в MCCS (например, в MCCS, MCCS1 и/или MCCS2)).
В MCCS, MCCS1 и/или MCCS2 можно проводить две или более отдельных операций. Например, в каждой из MCCS, MCCS1 и/или MCCS2 можно проводить по меньшей мере следующие отдельные операции: захват рекомбинантного белка и инактивацию вирусов, присутствующих в текучей среде, включающей рекомбинантный белок; захват рекомбинантного белка, инактивацию вирусов, присутствующих в текучей среде, включающей рекомбинантный белок, и регулирование концентрации ионов и/или pH жидкости, включающей рекомбинантный белок; очистку рекомбинантного белка и тонкую очистку рекомбинантного белка; очистку рекомбинантного белка, тонкую очистку рекомбинантного белка и фильтрование текучей среды, включающей рекомбинантный белок, или удаление осадков и/или твердых частиц из текучей среды, включающей рекомбинантный белок; и очистку рекомбинантного белка, тонкую очистку рекомбинантного белка, фильтрование текучей среды, включающей рекомбинантный белок, или удаление осадков и/или твердых частиц из текучей среды, включающей рекомбинантный белок, и регулирование концентрации ионов и/или pH жидкости, включающей рекомбинантный белок.
Захват рекомбинантного белка
Способы по настоящему изобретению предусматривают стадию захвата рекомбинантного белка с применением MCCS или MCCS1. Как можно понять из уровня техники, жидкую культуральную среду, включающую рекомбинантный белок, можно непрерывно подавать в MCCS или MCCS1 с применением ряда различных способов. Например, жидкую культуральную среду можно активно перекачивать в MCCS или MCCS1, или жидкую культуральную среду можно подавать в MCCS или MCCS1 с применением силы тяжести. Жидкую культуральную среду можно хранить в резервуаре (например, в емкости для удерживания) перед ее подачей в MCCS или MCCS1, или жидкую культуральную среду можно активно перекачивать из биореактора, включающего культуру клеток (например, клеток млекопитающего, которые секретируют рекомбинантный белок в культуральную среду), в MCCS или MCCS1.
Жидкую культуральную среду можно подавать (загружать) в MCCS или MCCS1 при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Жидкая культуральная среда, включающая рекомбинантный белок, может быть получена из любого из иллюстративных источников, описанных в данном документе или известных из уровня техники.
Некоторые примеры дополнительно предусматривают необязательную стадию фильтрования жидкой культуральной среды перед ее подачей в MCCS или MCCS1. Любой из иллюстративных способов фильтрования жидкой культуральной среды или текучей среды, включающей рекомбинантный белок, описанных в данном документе, или любые способы фильтрации, известные из уровня техники, можно применять для фильтрования жидкой культуральной среды, включающей рекомбинантный белок, перед ее подачей в MCCS или MCCS1.
В способах, описанных в данном документе, захват рекомбинантного белка из жидкой культуральной среды проводят с применением MCCS или MCCS1. Как можно понять из уровня техники, с целью осуществления захвата рекомбинантного белка по меньшей мере одна хроматографическая колонка или по меньшей мере одна хроматографическая мембрана в MCCS или MCCS1 должна содержать смолу, в которой используется механизм захвата (например, любой из иллюстративных механизмов захвата, описанных в данном документе), или содержать смолу, пригодную для выполнения катионообменной, анионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием. Например, если рекомбинантный белок представляет собой антитело или фрагмент антитела, то система захвата может представлять собой механизм захвата посредством связывания с белком A или механизм захвата посредством связывания с антигеном (при этом захватывающий антиген специфически распознается рекомбинантным антителом или фрагментом антитела). Если рекомбинантный белок представляет собой фермент, то в механизме захвата могут применяться антитело или фрагмент антитела, которые специфически связываются с ферментом для захвата рекомбинантного фермента, субстрат фермента для захвата рекомбинантного фермента, кофактор фермента для захвата рекомбинантного фермента или, если рекомбинантный фермент включает метку, то белок, хелат металла или антитело (или фрагмент антитела), которые специфически связываются с меткой, присутствующей в рекомбинантном ферменте. Неограничивающие смолы, которые можно применять для захвата рекомбинантного белка, описаны в данном документе, и дополнительные смолы, которые можно применять для захвата рекомбинантного белка, известны из уровня техники. Одним неограничивающим примером смолы, в которой используется механизм захвата посредством связывания с белком A, является смола Mab Select SuReTM (GE Healthcare, Пискатауэй, Нью-Джерси), JSR LifeSciences Amsphere ProA JWT203 (Саннивейл, Калифорния), и Kaneka KanCap A (Осака, Япония).
Иллюстративные неограничивающие размеры и формы хроматографической(хроматографических) колонки(колонок) или хроматографической(хроматографических) мембраны(мембран), присутствующей(присутствующих) в MCCS или MCCS1, которые можно применять для захвата рекомбинантного белка, описаны в данном документе. Жидкая культуральная среда, которую подают (загружают) в MCCS или MCCS1, может включать, например, от приблизительно 0,05 мг/мл до приблизительно 100 мг/мл рекомбинантного белка (например, от приблизительно 0,1 мг/мл до приблизительно 90 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 80 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 70 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 60 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 50 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 40 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 30 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 20 мг/мл, от 0,5 мг/мл до приблизительно 20 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,5 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 10 мг/мл или от приблизительно 0,5 мг/мл до приблизительно 10 мг/мл рекомбинантного белка). Среднее время, которое требуется для связывания рекомбинантного белка со смолой, применяемой для проведения отдельной операции захвата, может составлять, например, от приблизительно 5 секунд до приблизительно 10 минут (например, от приблизительно 10 секунд до приблизительно 8 минут, от приблизительно 10 секунд до приблизительно 7 минут, от приблизительно 10 секунд до приблизительно 6 минут, от приблизительно 10 секунд до приблизительно 5 минут, от приблизительно 30 секунд до приблизительно 5 минут, от приблизительно 1 минуты до приблизительно 5 минут, от приблизительно 10 секунд до приблизительно 4 минут, от приблизительно 30 секунд до приблизительно 4 минут или от приблизительно 1 минуты до приблизительно 4 минут).
Как можно понять из уровня техники, с целью захвата рекомбинантного белка с применением хроматографической(хроматографических) колонки(колонок) или хроматографической(хроматографических) мембраны(мембран), присутствующих в MCCS или MCCS1, необходимо проводить последовательные стадии хроматографии, представляющие собой загрузку, промывание, элюирование и регенерацию хроматографической(хроматографических) колонки(колонок) или хроматографической(хроматографических) мембраны(мембран), присутствующих в MCCS или MCCS1. Любое из иллюстративных значений расхода, объема буфера и/или продолжительности времени, отведенного на каждую последовательную стадию хроматографии, описанную в данном документе, можно применять в одной или нескольких из таких различных последовательных хроматографических стадий (например, одной или нескольких последовательных хроматографических стадиях загрузки, промывания, элюирования и регенерации хроматографической(хроматографических) колонки(колонок) или хроматографической(хроматографических) мембраны(мембран), присутствующих в MCCS или MCCS1, которые применяют для захвата рекомбинантного белка). Неограничивающие значения расхода, объема буфера и/или продолжительности времени, отведенного на каждую последовательную стадию хроматографии, которые можно применять для захвата в хроматографической(хроматографических) колонке(колонках) и/или в хроматографической(хроматографических) мембране(мембранах) в MCCS или MCCS1 (например, в PCCS или PCCS1), предусмотрены ниже. Кроме того, иллюстративные буферы, которые можно применять в MCCS и/или MCCS1, описаны ниже.
В MCCS или MCCS1, включающие по меньшей мере одну хроматографическую колонку и/или хроматографическую мембрану, включающие смолу, с помощью которой можно проводить отдельную операцию захвата (например, любую из иллюстративных смол, которые можно применять для захвата, описанных в данном документе), можно загружать жидкую культуральную среду, включающую рекомбинантный белок, с применением любого из значений расхода при загрузке (значений расхода при подаче), описанных выше. В некоторых примерах одну хроматографическую колонку или одну хроматографическую мембрану, включающие смолу, пригодную для выполнения отдельной операции захвата, загружают за время, составляющее, например, от приблизительно 10 минут до приблизительно 90 минут (например, от приблизительно 15 минут до приблизительно 90 минут, от приблизительно 20 минут до 80 минут, от приблизительно 30 минут до 80 минут, от приблизительно 40 минут до приблизительно 80 минут, от приблизительно 50 минут до приблизительно 80 минут и от приблизительно 60 минут до 80 минут). В некоторых примерах, где MCCS или MCCS1 включают по меньшей мере две соединенные последовательно хроматографические колонки, которые содержат смолу, пригодную для выполнения отдельной операции захвата, время, необходимое для загрузки двух соединенных последовательно хроматографических колонок, составляет, например, от приблизительно 50 минут до приблизительно 180 минут (например, от приблизительно 60 минут до приблизительно 180 минут, от приблизительно 70 минут до приблизительно 180 минут, от приблизительно 80 минут до приблизительно 180 минут, от приблизительно 90 минут до приблизительно 180 минут, от приблизительно 100 минут до приблизительно 180 минут, от приблизительно 110 минут до 150 минут и от приблизительно 125 минут до приблизительно 145 минут).
После загрузки рекомбинантного белка в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану в MCCS или MCCS1, которые содержат смолу, пригодную для выполнения отдельной операции захвата, по меньшей мере одну хроматографическую колонку или хроматографическую мембрану промывают с помощью по меньшей мере одного буфера для промывания. Как можно понять из уровня техники, по меньшей мере один (например, два, три или четыре) буфер для промывания предназначен для элюирования всех или большей части белков, отличных от рекомбинантного белка, из по меньшей мере одной хроматографической колонки или хроматографической мембраны без нарушения при этом взаимодействия рекомбинантного белка со смолой.
Буфер для промывания можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем применяемого буфера для промывания (например, совокупный общий объем применяемых буферов для промывания, если применяют более одного буфера для промывания) может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 15×CV (например, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Общее время промывания может составлять, например, от приблизительно 2 минут до приблизительно 3 часов (например, от приблизительно 2 минут до приблизительно 2,5 часа, от приблизительно 2 минут до приблизительно 2,0 часа, от приблизительно 5 минут до приблизительно 1,5 часа, от приблизительно 10 минут до приблизительно 1,5 часа, от приблизительно 10 минут до приблизительно 1,25 часа, от приблизительно 20 минут до приблизительно 1,25 часа или от приблизительно 30 минут до приблизительно 1 часа).
После промывания по меньшей мере одной хроматографической колонки или хроматографической мембраны в MCCS или MCCS1, которые содержат смолу, пригодную для выполнения отдельной операции захвата, рекомбинантный белок элюируют из по меньшей мере одной хроматографической колонки или хроматографической мембраны путем пропускания буфера для элюирования через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану в MCCS или MCCS1, которые содержат смолу, пригодную для выполнения отдельной операции захвата. Буфер для элюирования можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые содержат смолу, пригодную для выполнения отдельной операции захвата, при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 6,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 5,0 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем буфера для элюирования, применяемого для элюирования рекомбинантного белка из каждой из по меньшей мере одной хроматографической колонки или хроматографической мембраны, включающих смолу, пригодную для выполнения отдельной операции проведения очистки, может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 15×CV (например, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Общее время элюирования может составлять, например, от приблизительно 2 минут до приблизительно 3 часов (например, от приблизительно 2 минут до приблизительно 2,5 часа, от приблизительно 2 минут до приблизительно 2,0 часа, от приблизительно 2 минут до приблизительно 1,5 часа, от приблизительно 2 минут до приблизительно 1,5 часа, от приблизительно 2 минут до приблизительно 1,25 часа, от приблизительно 2 минут до приблизительно 1,25 часа, от приблизительно 2 минут до приблизительно 1 часа, от приблизительно 2 минут до приблизительно 40 минут, от приблизительно 10 минут до приблизительно 40 минут или от приблизительно 20 минут до приблизительно 40 минут). Неограничивающие примеры буферов для элюирования, которые можно применять в таких способах, будут зависеть от механизма захвата и/или рекомбинантного белка. Например, буфер для элюирования может предусматривать разную концентрацию соли (например, повышенную концентрацию соли), разный pH (например, повышенную или пониженную концентрацию соли) или молекулу, которая будет конкурировать с рекомбинантным белком за связывание со смолой, пригодной для выполнения отдельной операции захвата. Примеры таких буферов для элюирования для каждого иллюстративного механизма захвата, описанного в данном документе, являются общеизвестными из уровня техники.
После элюирования рекомбинантного белка из по меньшей мере одной хроматографической колонки или хроматографической мембраны в MCCS или MCCS1, которые содержат смолу, пригодную для выполнения отдельной операции захвата, и перед тем, как следующий объем жидкой культуральной среды может быть загружен в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, по меньшей мере одну хроматографическую колонку или хроматографическую мембрану необходимо уравновешивать с применением буфера для регенерации. Буфер для регенерации можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые содержат смолу, пригодную для выполнения отдельной операции захвата, при расходе, составляющем, например, от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 6,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 5,0 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута, от приблизительно 5,0 мл/минута до приблизительно 15,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем буфера для регенерации, применяемого для уравновешивания по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые содержат смолу, пригодную для выполнения отдельной операции захвата, может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 15×CV (например, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 5×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV).
В некоторых способах, описанных в данном документе, MCCS или MCCS1 включают резервуар, который обеспечивает удерживание текучей среды, включающей рекомбинантный белок, при низком pH (например, при pH ниже 4,6, ниже 4,4, ниже 4,2, ниже 4,0, ниже 3,8, ниже 3,6, ниже 3,4, ниже 3,2, или ниже 3,0) в течение периода времени, составляющего, например, от приблизительно 1 минуты до 1,5 часа (например, приблизительно 1 час) и инактивацию вирусов, присутствующих в текучей среде, включающей рекомбинантный белок. Примером резервуара, который можно применять для проведения отдельной операции инактивации вирусов, является колба с мешалкой (например, колба с мешалкой объемом 500 мл, например, колба с мешалкой объемом 500 мл с программируемой плитой мешалки), пригодная для удерживания текучей среды, включающей рекомбинантный белок, в течение периода времени, составляющего, например, от приблизительно 1 минуты до 1,5 часа, например, перед подачей текучей среды, включающей рекомбинантный белок, в MCCS2. Резервуар, который применяют для проведения отдельной операции инактивации вирусов, может представлять собой колбу с мешалкой объемом 500 мл с программируемой плитой мешалки (например, с плитой мешалки с установленной программой перемешивания (например, периодического перемешивания) текучей среды в резервуаре, например, каждые 4 часа). Другим примером резервуара, который можно применять для проведения отдельной операции инактивации вирусов, является пластиковый пакет (например, пластиковый пакет объемом 500 мл), пригодный для удерживания текучей среды, включающей рекомбинантный белок, в течение периода времени, составляющего, например, от приблизительно 1 минуты до 1,5 часа, например, перед подачей текучей среды, включающей рекомбинантный белок, в MCCS2. В некоторых примерах, текучая среда, включающая рекомбинантный белок, уже может характеризоваться низким pH (например, pH ниже 4,6, ниже 4,4, ниже 4,2, ниже 4,0, ниже 3,8, ниже 3,6, ниже 3,4, ниже 3,2 или ниже 3,0) при ее подаче в резервуар, который применяют для проведения отдельной операции инактивации вирусов. Как будет понятно специалисту в данной области техники, ряд других средств можно применять для осуществления отдельной операции инактивации вирусов. Например, УФ-облучение текучей среды, включающей рекомбинантный белок, можно также применять для осуществления отдельной операции инактивации вирусов. Неограничивающие примеры резервуаров, которые можно применять для осуществления отдельной операции инактивации вирусов, присутствующих в текучей среде, включающей рекомбинантный белок, описаны в данном документе.
MCCS или MCCS1 могут включать PCCS, содержащие четыре хроматографические колонки, при этом по меньшей мере в трех из четырех хроматографических колонок осуществляют отдельную операцию захвата рекомбинантного белка из жидкой культуральной среды (например, с применением MCCS, которая содержит любую из по меньшей мере одной хроматографической колонки, которая содержит смолу, пригодную для выполнения отдельной операции захвата (например, любую из описанных в данном документе)). В данных примерах в четвертой колонке PCC можно осуществлять отдельную операцию инактивации вирусов в текучей среде, включающей рекомбинантный белок (например, в любой из иллюстративных колонок, описанных в данном документе, которые можно применять для обеспечения инактивации вирусов в текучей среде, включающей рекомбинантный белок).
В некоторых примерах текучую среду, включающую рекомбинантный белок, непрерывно элюируют из MCCS1 (например, PCCS1) и непрерывно подают в MCCS2 (например, PCCS2). Процентная доля полученного рекомбинантного белка в элюате, выходящем из MCCS или MCCS1 (например, PCCS или PCCS1), может составлять, например, по меньшей мере 70%, по меньшей мере 72%, по меньшей мере 74%, по меньшей мере 76%, по меньшей мере 78%, по меньшей мере 80%, по меньшей мере 82%, по меньшей мере 84%, по меньшей мере 86%, по меньшей мере 88%, по меньшей мере 90%, по меньшей мере 92%, по меньшей мере 94%, по меньшей мере 96% или по меньшей мере 98%). Элюат, выходящий из MCCS1 (например, PCCS1), можно подавать в MCCS2 (например, PCCS2) с применением ряда средств, известных из уровня техники (например, трубки). Элюат, выходящий из MCCS1 (например, PCCS1), можно подавать в MCCS2 (например, PCCS2) при расходе, составляющем, например, от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 6,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 5,0 мг/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута, от приблизительно 5,0 мл/минута до приблизительно 15,0 мл/минута, от приблизительно 15 мл/минута до приблизительно 25 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута).
Некоторые описанные в данном документе способы могут дополнительно предусматривать стадию регулирования концентрации ионов и/или pH элюата, выходящего из MCCS1 (например, PCCS1), перед его подачей в MCCS2 (например, PCCS2). Как описано в данном документе, концентрацию ионов и/или pH элюата, выходящего из MCCS1 (например, PCCS1), можно регулировать (перед его подачей в MCCS2) путем добавления буфера к элюату (например, путем применения резервуара для регулирования буфера в потоке). Буфер можно добавлять к элюату, выходящему из MCCS1, при расходе, составляющем, например, от приблизительно 0,1 мл/минута до приблизительно 15 мл/минута (например, от приблизительно 0,1 мл/минута до приблизительно 12,5 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 10,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 8,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 6 мл/минута, от приблизительно 0,1 мл/минута до 4 мл/минута или от приблизительно 0,5 мл/минута до приблизительно 5 мл/минута).
Способы, описанные в данном документе, могут дополнительно предусматривать стадию удерживания или хранения (и необязательно также охлаждения) элюата, выходящего из MCCS1, до подачи элюата, выходящего из MCCS1, в MCCS2. Как описано в данном документе, данную стадию удерживания или хранения можно проводить с применением любого из резервуаров (например, резервных емкостей), описанных в данном документе.
Способы, описанные в данном документе, могут также предусматривать стадию фильтрования элюата, выходящего из MCCS1, перед подачей элюата в MCCS2. Любой из иллюстративных фильтров или способов фильтрования, описанных в данном документе, можно применять для фильтрования элюата, выходящего из MCCS1, перед подачей элюата в MCCS2.
Тонкая очистка и очистка рекомбинантного белка
MCCS, MCCS1 и/или MCCS2 можно применять для осуществления отдельной операции очистки и тонкой очистки рекомбинантного белка. Например, MCCS2 можно применять для осуществления операции очистки и тонкой очистки рекомбинантного белка и элюата, выходящего из MCCS2, который представляет собой лекарственное вещество на основе белка. MCCS, MCCS1 и/или MCCS2 могут содержать по меньшей мере одну (например, две, три или четыре) хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, и по меньшей мере одну (например, две, три или четыре) хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка.
По меньшей мере одна хроматографическая колонка или хроматографическая мембрана, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, могут содержать смолу, в которой используется механизм захвата (например, любой из механизмов захвата, описанных в данном документе или известных из уровня техники), или смолу, которую можно применять для осуществления анионообменной хроматографии, катионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием. По меньшей мере одна хроматографическая колонка или хроматографическая мембрана, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, могут содержать смолу, которую можно применять для осуществления анионообменной хроматографии, катионообменной хроматографии, хроматографии на молекулярных ситах или хроматография с гидрофобным взаимодействием (например, любую из иллюстративных смол для осуществления анионообменной хроматографии, катионообменной хроматографии, хроматографии на молекулярных ситах или хроматографии с гидрофобным взаимодействием, описанных в данном документе или известных из уровня техники).
Размер, форма и объем по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, и/или размер и форма по меньшей мере одной хроматографической мембраны, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, могут представлять собой любую из комбинации иллюстративных размеров, форм и объемов хроматографических колонок или хроматографических мембран, описанных в данном документе. Специалисту в данной области техники будет понятно, что стадия очистки или тонкой очистки рекомбинантного белка может, например, включать стадии загрузки, промывания, элюирования и уравновешивания по меньшей мере одной хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции очистки или тонкой очистки рекомбинантного белка. Как правило, буфер для элюирования, выходящий из хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции очистки, включает рекомбинантный белок. Как правило, буфер для загрузки и/или промывания, выходящий из хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции тонкой очистки, включает рекомбинантный белок.
Например, размер по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, может предусматривать объем, составляющий, например, от приблизительно 2,0 мл до приблизительно 200 мл (например, от приблизительно 2,0 мл до приблизительно 180 мл, от приблизительно 2,0 мл до приблизительно 160 мл, от приблизительно 2,0 мл до приблизительно 140 мл, от приблизительно 2,0 мл до приблизительно 120 мл, от приблизительно 2,0 мл до приблизительно 100 мл, от приблизительно 2,0 мл до приблизительно 80 мл, от приблизительно 2,0 мл до приблизительно 60 мл, от приблизительно 2,0 мл до приблизительно 40 мл, от приблизительно 5,0 мл до приблизительно 40 мл, от приблизительно 2,0 мл до приблизительно 30 мл, от приблизительно 5,0 мл до приблизительно 30 мл или от приблизительно 2,0 мл до приблизительно 25 мл). Расход текучей среды, включающей рекомбинантный белок, при ее загрузке в по меньшей мере одну хроматографическую колонку или по меньшей мере одну хроматографическую, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, может составлять, например, от приблизительно 0,1 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,1 мл/минута до приблизительно 12,5 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 10,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 8,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 6 мл/минута, от приблизительно 0,1 мл/минута до 4 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 3 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 2 мл/минута или приблизительно 0,2 мл/минута до приблизительно 4 мл/минута). Концентрация рекомбинантного белка в текучей среде, загружаемой в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, может составлять, например, от приблизительно 0,05 мг/мл до приблизительно 100 мг/мл рекомбинантного белка (например, от приблизительно 0,1 мг/мл до приблизительно 90 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 80 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 70 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 60 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 50 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 40 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 30 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 20 мг/мл, от 0,5 мг/мл до приблизительно 20 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,5 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 10 мг/мл или от приблизительно 0,5 мг/мл до приблизительно 10 мг/мл рекомбинантного белка). Смола в по меньшей мере одной хроматографической колонке или хроматографической мембране, применяемых для осуществления отдельной операции очистки, может представлять собой смолу, которую можно применять для осуществления анионообменной или катионообменной хроматографии. Смола в по меньшей мере одной хроматографической колонке или хроматографической мембране, которые применяют для осуществления отдельной операции очистки, может представлять собой катионообменную смолу (например, смолу Capto-S, GE Healthcare Life Sciences, Пискатауэй, Нью-Джерси).
После загрузки рекомбинантного белка в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции очистки рекомбинантного белка, по меньшей мере одну хроматографическую колонку или хроматографическую мембрану промывают с помощью по меньшей мере одного буфера для промывания. Как можно понять из уровня техники, по меньшей мере один (например, два, три или четыре) буфер для промывания предназначен для элюирования всех белков, отличных от рекомбинантного белка, из по меньшей мере одной хроматографической колонки или хроматографической мембраны без нарушения при этом взаимодействия рекомбинантного белка со смолой, или иным образом элюирования рекомбинантного белка.
Буфер для промывания можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем применяемого буфера для промывания (например, совокупный общий объем применяемых буферов для промывания, если применяют более одного буфера для промывания) может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 15×CV (например, от приблизительно 1×CV до приблизительно 14×CV, приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 2,5×CV до приблизительно 5,0×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Общее время промывания может составлять, например, от приблизительно 2 минут до приблизительно 3 часов (например, от приблизительно 2 минут до приблизительно 2,5 часа, от приблизительно 2 минут до приблизительно 2,0 часа, от приблизительно 5 минут до приблизительно 1,5 часа, от приблизительно 10 минут до приблизительно 1,5 часа, от приблизительно 10 минут до приблизительно 1,25 часа, от приблизительно 20 минут до приблизительно 1,25 часа, от приблизительно 30 минут до приблизительно 1 часа, от приблизительно 2 минут до 10 минут, от приблизительно 2 минут до 15 минут или от приблизительно 2 минут до 30 минут).
После промывания по меньшей мере одной хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции очистки рекомбинантного белка, рекомбинантный белок элюируют из по меньшей мере одной хроматографической колонки или хроматографической мембраны путем пропускания буфера для элюирования через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, применяемые для осуществления отдельной операции очистки рекомбинантного белка. Буфер для элюирования можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые могут применяться для осуществления отдельной операции очистки рекомбинантного белка, при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 6,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 5,0 мг/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем буфера для элюирования, применяемого для элюирования рекомбинантного белка из каждой из по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые могут применяться для осуществления отдельной операции очистки рекомбинантного белка, может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 25×CV (например, от приблизительно 1×CV до приблизительно 20×CV, от приблизительно 15×CV до приблизительно 25×CV, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Общее время элюирования может составлять, например, от приблизительно 2 минут до приблизительно 3 часов (например, от приблизительно 2 минут до приблизительно 2,5 часа, от приблизительно 2 минут до приблизительно 2,0 часа, от приблизительно 2 минут до приблизительно 1,5 часа, от приблизительно 2 минут до приблизительно 1,5 часа, от приблизительно 2 минут до приблизительно 1,25 часа, от приблизительно 2 минут до приблизительно 1,25 часа, от приблизительно 2 минут до приблизительно 1 часа, от приблизительно 2 минут до приблизительно 40 минут, от приблизительно 10 минут до приблизительно 40 минут, от приблизительно 20 минут до приблизительно 40 минут или от приблизительно 30 минут до 1,0 часа). Неограничивающие примеры буферов для элюирования, которые можно применять в таких способах, будут зависеть от смолы и/или биофизических свойств рекомбинантного белка. Например, буфер для элюирования может предусматривать разную концентрацию соли (например, повышенную концентрацию соли), разный pH (например, повышенную или пониженную концентрацию соли) или молекулу, которая будет конкурировать с рекомбинантным белком за связывание со смолой. Примеры таких буферов для элюирования для каждого из иллюстративных механизмов захвата, описанных в данном документе, хорошо известны из уровня техники.
После элюирования рекомбинантного белка из по меньшей мере одной хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции очистки рекомбинантного белка, и перед тем, как следующий объем текучей среды, включающей рекомбинантный белок, может быть загружен в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, по меньшей мере одну хроматографическую колонку или хроматографическую мембрану необходимо уравновешивать с применением буфера для регенерации. Буфер для регенерации можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, применяемые для осуществления отдельной операции очистки рекомбинантного белка, при расходе, составляющем, например, от приблизительно 0,2 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 6,0 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 5,0 мг/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута, от приблизительно 5,0 мл/минута до приблизительно 15,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем буфера для регенерации, применяемого для уравновешивания по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые содержат смолу, которая может использоваться для осуществления отдельной операции очистки рекомбинантного белка, может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 15×CV (например, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 5×CV, от приблизительно 2,5×CV до приблизительно 7,5×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Концентрация рекомбинантного белка в элюате, выходящего из по меньшей мере одной хроматографической колонки или хроматографической мембраны, применяемых для осуществления отдельной операции очистки рекомбинантного белка, может составлять, например, от приблизительно 0,05 мг/мл до приблизительно 100 мг/мл рекомбинантного белка (например, от приблизительно 0,1 мг/мл до приблизительно 90 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 80 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 70 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 60 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 50 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 40 мг/мл, от приблизительно 2,5 мг/мл до приблизительно 7,5 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 30 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 20 мг/мл, между 0,5 мг/мл до приблизительно 20 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,5 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 10 мг/мл или от приблизительно 0,5 мг/мл до приблизительно 10 мг/мл рекомбинантного белка).
По меньшей мере одна хроматографическая колонка или хроматографическая мембрана, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, могут содержать смолу, которую можно применять для осуществления катионообменной, анионообменной хроматографии или хроматографии на молекулярных ситах. Как можно понять из уровня техники, тонкая очистка рекомбинантного белка с применением по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, может предусматривать, например, стадии загрузки, прогонки и регенерации по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка. Например, если стадии загрузки, прогонки и регенерации применяют для осуществления тонкой очистки, рекомбинантный белок не связывается со смолой в по меньшей мере одной хроматографической колонке или хроматографической мембране, которые применяют для осуществления отдельной операции тонкой очистки рекомбинантного белка, и рекомбинантный белок элюируют из по меньшей мере одной хроматографической колонки или хроматографической мембраны на стадиях загрузки и прогонки, а стадию регенерации применяют для удаления любых примесей из по меньшей мере одной хроматографической колонки или хроматографической мембраны перед тем, как дополнительное количество текучей среды, включающей рекомбинантный белок, можно загружать в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану. Иллюстративные значения расхода и объема буфера, подлежащие применению в каждой из стадий загрузки, прогонки и регенерации, описаны ниже.
Размер, форма и объем по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, и/или размер и форма по меньшей мере одной хроматографической мембраны, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, могут представлять собой любую из комбинации иллюстративных размеров, форм и объемов хроматографических колонок или хроматографических мембран, описанных в данном документе. Например, размер по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, может предусматривать объем, составляющий, например, от приблизительно 0,5 мл до приблизительно 200 мл (например, от приблизительно 0,5 мл до приблизительно 180 мл, от приблизительно 0,5 мл до приблизительно 160 мл, от приблизительно 0,5 мл до приблизительно 140 мл, от приблизительно 0,5 мл до приблизительно 120 мл, от приблизительно 0,5 мл до приблизительно 100 мл, от приблизительно 0,5 мл до приблизительно 80 мл, от приблизительно 0,5 мл до приблизительно 60 мл, от приблизительно 0,5 мл до приблизительно 40 мл, от приблизительно 5,0 мл до приблизительно 40 мл, от приблизительно 0,5 мл до приблизительно 30 мл, от приблизительно 5,0 мл до приблизительно 30 мл, от приблизительно 0,5 мл до приблизительно 25 мл, от приблизительно 0,2 мл до приблизительно 10 мл или от приблизительно 0,2 мл до приблизительно 5 мл). Расход текучей среды, включающей рекомбинантный белок, при ее загрузке в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, может составлять, например, от приблизительно 0,1 мл/минута до приблизительно 25 мл/минута (например, от приблизительно 0,1 мл/минута до приблизительно 12,5 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 10,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 8,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 6 мл/минута, от приблизительно 0,1 мл/минута до 4 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 3 мл/минута, от приблизительно 2 мл/минута до приблизительно 6 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 2 мл/минута или приблизительно 0,2 мл/минута до приблизительно 4 мл/минута). Общий объем текучей среды, включающей рекомбинантный белок, загруженной в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, может составлять, например, от приблизительно 1,0 мл до приблизительно 250 мл (например, от приблизительно 1,0 мл до приблизительно 225 мл, от приблизительно 1,0 мл до приблизительно 200 мл, от приблизительно 1,0 мл до приблизительно 175 мл, от приблизительно 1,0 мл до приблизительно 150 мл, от приблизительно 100 мл до приблизительно 125 мл, от приблизительно 100 мл до приблизительно 150 мл, от приблизительно 1,0 мл до приблизительно 150 мл, от приблизительно 1,0 мл до приблизительно 125 мл, от приблизительно 1,0 мл до приблизительно 100 мл, от приблизительно 1,0 мл до приблизительно 75 мл, от приблизительно 1,0 мл до приблизительно 50 мл или от приблизительно 1,0 мл до приблизительно 25 мл). Смола в по меньшей мере одной хроматографической колонке или хроматографической мембране, применяемых для осуществления тонкой очистки, может представлять собой анионообменную или катионообменную смолу. Смола в по меньшей мере одной хроматографической колонке или хроматографической мембране, которые применяют для осуществления отдельной операции тонкой очистки, может представлять собой катионообменную смолу (например, смолу Sartobind® Q, Sartorius, Геттинген, Германия).
После стадии загрузки проводят стадию прогонки (например, буфер для прогонки пропускают через по меньшей мере одну хроматографическую мембрану или хроматографическую мембрану для сбора рекомбинантного белка, который по сути не связывается с по меньшей мере одной хроматографической колонкой или хроматографической мембраной). В данных примерах буфер для прогонки можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану при расходе, составляющем от приблизительно 0,2 мл/минута до приблизительно 50 мл/минута (например, от приблизительно 1 мл/минута до приблизительно 40 мл/минута, от приблизительно 1 мл/минута до приблизительно 30 мл/минута, от приблизительно 5 мл/минута до приблизительно 45 мл/минута, от приблизительно 10 мл/минута до приблизительно 40 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Применяемый объем буфера для прогонки может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 100×CV (например, от приблизительно 1×CV до приблизительно 90×CV, от приблизительно 1×CV до приблизительно 80×CV, от приблизительно 1×CV до приблизительно 70×CV, от приблизительно 1×CV до приблизительно 60×CV, от приблизительно 1× до приблизительно 50×CV, от приблизительно 1×CV до приблизительно 40×CV, от приблизительно 1×CV до приблизительно 30×CV, от приблизительно 1×CV до приблизительно 20×CV, от приблизительно 1×CV до приблизительно 15×CV, от приблизительно 5×CV до приблизительно 20×CV, от приблизительно 5×CV до приблизительно 30×CV, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 2,5×CV до приблизительно 5,0×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV). Общее время прогонки может составлять, например, от приблизительно 1 минуты до приблизительно 3 часов (например, от приблизительно 1 минуты до приблизительно 2,5 часа, от приблизительно 1 минуты до приблизительно 2,0 часа, от приблизительно 1 минуты до приблизительно 1,5 часа, от приблизительно 2 минут до приблизительно 1,5 часа, от приблизительно 1 минуты до приблизительно 1,25 часа, от приблизительно 2 минут до приблизительно 1,25 часа, от приблизительно 1 минуты до приблизительно 5 минут, от приблизительно 1 минуты до приблизительно 10 минут, от приблизительно 2 минут до приблизительно 4 минут, от приблизительно 30 минут до приблизительно 1 часа, от приблизительно 2 минут до приблизительно 10 минут, от приблизительно 2 минут до приблизительно 15 минут или от приблизительно 2 минут до приблизительно 30 минут). Совокупная концентрация рекомбинантного белка, присутствующего в элюате, выходящем из колонки, на стадии нагрузки и стадии прогонки, может составлять, например, от приблизительно 0,1 мг/мл до приблизительно 100 мг/мл рекомбинантного белка (например, от приблизительно 0,1 мг/мл до приблизительно 90 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 80 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 70 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 60 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 50 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 40 мг/мл, от приблизительно 2,5 мг/мл до приблизительно 7,5 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 30 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 20 мг/мл, от 0,5 мг/мл до приблизительно 20 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,5 мг/мл до приблизительно 15 мг/мл, от приблизительно 0,1 мг/мл до приблизительно 10 мг/мл, от приблизительно 0,5 мг/мл до приблизительно 10 мг/мл или от приблизительно 1 мг/мл до приблизительно 5 мг/мл рекомбинантного белка).
После стадии прогонки и перед тем, как следующий объем текучей среды, включающей рекомбинантный белок, может быть загружен в по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции тонкой очистки, по меньшей мере одну хроматографическую колонку или хроматографическую мембрану необходимо регенерировать с применением буфера для регенерации. Буфер для регенерации можно пропускать через по меньшей мере одну хроматографическую колонку или хроматографическую мембрану, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, при расходе, составляющем, например, от приблизительно 0,2 мл/минута до приблизительно 50 мл/минута (например, от приблизительно 1 мл/минута до приблизительно 40 мл/минута, от приблизительно 1 мл/минута до приблизительно 30 мл/минута, от приблизительно 5 мл/минута до приблизительно 45 мл/минута, от приблизительно 10 мл/минута до приблизительно 40 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 20 мл/минута, от приблизительно 0,2 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 15 мл/минута, от приблизительно 0,5 мл/минута до приблизительно 10 мл/минута, от приблизительно 0,5 мл минуты до приблизительно 14 мл/минута, от приблизительно 1,0 мл/минута до приблизительно 25,0 мл/минута или от приблизительно 1,0 мл/минута до приблизительно 15,0 мл/минута). Объем буфера для регенерации, применяемого для регенерации по меньшей мере одной хроматографической колонки или хроматографической мембраны, которые можно применять для осуществления отдельной операции тонкой очистки, может составлять, например, от приблизительно 1×объема колонки (CV) до приблизительно 500×CV (например, от приблизительно 1×CV до приблизительно 450×CV, от приблизительно 1×CV до приблизительно 400×CV, от приблизительно 1×CV до приблизительно 350×CV, от приблизительно 1×CV до приблизительно 300×CV, от приблизительно 1×CV до приблизительно 250×CV, от приблизительно 1×CV до приблизительно 200×CV, от приблизительно 1×CV до приблизительно 150×CV, от приблизительно 1×CV до приблизительно 100×CV, от приблизительно 1×CV до приблизительно 90×CV, от приблизительно 1×CV до приблизительно 80×CV, от приблизительно 1×CV до приблизительно 70×CV, от приблизительно 1×CV до приблизительно 60×CV, от приблизительно 1× до приблизительно 50×CV, от приблизительно 1×CV до приблизительно 40×CV, от приблизительно 1×CV до приблизительно 30×CV, от приблизительно 1×CV до приблизительно 20×CV, от приблизительно 1×CV до приблизительно 15×CV, от приблизительно 5×CV до приблизительно 20×CV, от приблизительно 5×CV до приблизительно 30×CV, от приблизительно 1×CV до приблизительно 14×CV, от приблизительно 1×CV до приблизительно 13×CV, от приблизительно 1×CV до приблизительно 12×CV, от приблизительно 1×CV до приблизительно 11×CV, от приблизительно 2×CV до приблизительно 11×CV, от приблизительно 3×CV до приблизительно 11×CV, от приблизительно 4×CV до приблизительно 11×CV, от приблизительно 2,5×CV до приблизительно 5,0×CV, от приблизительно 5×CV до приблизительно 11×CV или от приблизительно 5×CV до приблизительно 10×CV).
В других примерах одна или несколько хроматографических колонок и/или хроматографических мембран, применяемых для осуществления отдельной операции тонкой очистки, содержат смолу, которая селективно связывает или удерживает примеси, присутствующие в текучей среде, включающей рекомбинантный белок, и вместо регенерации одной или нескольких колонок и/или мембран, одну или несколько колонок и/или мембран заменяют (например, заменяют по сути аналогичными колонкой(колонками) и/или мембраной(мембранами)), как только связывающая способность смолы в одной или нескольких колонках и/или мембранах достигает предела или по сути приближается к достижению предела.
В некоторых примерах таких способов, описанных в данном документе, MCCS2 предусматривает PCCS, содержащую три хроматографические колонки и одну хроматографическую мембрану, например, при этом в трех хроматографических колонках в PCCS осуществляют отдельную операцию очистки рекомбинантного белка (например, с применением по меньшей мере одной хроматографической(хроматографических) колонки(колонок), которую(которые) можно применять для осуществления отдельной операции очистки белка), и в хроматографической мембране в PCCS осуществляют отдельную операцию тонкой очистки рекомбинантного белка. В данных примерах хроматографическая мембрана в PCCS, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка, может представлять собой любую из иллюстративных хроматографических мембран, описанных в данном документе, которые можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка. Любой из способов переключения колонок, описанных в данном документе, можно применять для определения того, когда можно переключать первые три хроматографические колонки и хроматографическую мембрану в PCCS в данном примере.
Некоторые варианты осуществления данного примера могут дополнительно предусматривать стадию регулирования концентрации ионов и/или pH элюата, выходящего из трех хроматографических колонок в PCCS, перед подачей элюата на хроматографическую мембрану в PCCS. Как описано в данном документе, концентрацию ионов и/или pH элюата, выходящего из трех хроматографических колонок в PCCS, можно регулировать (перед его подачей на хроматографическую мембрану в PCCS в данном примере) путем добавления буфера к элюату, выходящему из трех хроматографических колонок в PCCS (например, путем применения резервуара для регулирования буфера в потоке). Буфер можно добавлять к элюату при расходе, составляющем, например, от приблизительно 0,1 мл/минута до приблизительно 15 мл/минута (например, от приблизительно 0,1 мл/минута до приблизительно 12,5 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 10,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 8,0 мл/минута, от приблизительно 0,1 мл/минута до приблизительно 6 мл/минута, от приблизительно 0,1 мл/минута до 4 мл/минута или от приблизительно 0,5 мл/минута до приблизительно 5 мл/минута).
Такие примеры могут дополнительно предусматривать стадию удерживания или хранения элюата, выходящего из трех хроматографических колонок в PCCS, в данном примере перед подачей элюата на хроматографическую мембрану (хроматографическую мембрану, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка). Как описано в данном документе, данную стадию удерживания или хранения можно проводить с применением любого из резервуаров (например, резервных емкостей), описанных в данном документе.
Такие примеры также могут предусматривать стадию фильтрования элюата, выходящего из хроматографической мембраны в иллюстративной системе PCCS (элюата, выходящего из хроматографической мембраны, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка). Любой из иллюстративных фильтров или способов фильтрования, описанных в данном документе, можно применять для фильтрования элюата, выходящего из хроматографической мембраны в данной иллюстративной PCCS (элюата, выходящего из хроматографической мембраны, которую можно применять для осуществления отдельной операции тонкой очистки рекомбинантного белка).
Специалисту в данной области техники будет понятно, очищенный рекомбинантный белок можно периодически элюировать из MCCS или MCCS2 с применением любого из способов, описанных в данном документе. Например, любой из способов, описанных в данном документе, может обеспечивать элюирование очищенного рекомбинантного белка в течение периода, составляющего, например, от приблизительно 30 секунд до приблизительно 5 часов (например, от приблизительно 1 минуты до приблизительно 4 часов, от приблизительно 1 минуты до приблизительно 3 часов, от приблизительно 1 минуты до приблизительно 2 часов, от приблизительно 1 минуты или приблизительно 1,5 часа, от приблизительно 1 минуты до приблизительно 1 часа или от приблизительно 1 минуты до приблизительно 30 минут) при частоте, составляющей, например, от приблизительно 1 минуты до приблизительно 6 часов (например, от приблизительно 1 минуты до приблизительно 5 часов, от приблизительно 1 минуты до приблизительно 4 часов, от приблизительно 1 минуты до приблизительно 3 часов, от приблизительно 1 минуты до 2 часов, от приблизительно 1 минуты до 1 часа или от приблизительно 1 минуты до 30 минут), в зависимости от, например, хроматографической(хроматографических) колонки(колонок) и/или хроматографической(хроматографических) мембраны(мембран), применяемых в MCCS или MCCS1 и MCCS2.
Способы культивирования
Некоторые из способов, описанных в данном документе, дополнительно включают стадию культивирования клеток (например, рекомбинантных клеток млекопитающего), которые секретируют рекомбинантный белок в биореакторе (например, перфузионном биореакторе или биореакторе периодического действия с подпиткой), который содержит жидкую культуральную среду, где некоторый объем жидкой культуральной среды, которая по сути не содержит клеток (например, клеток млекопитающего), непрерывно или периодически удаляют из биореактора (например, перфузионного биореактора) и подают в MCCS или MCCS1. Биореактор может характеризоваться объемом, составляющим, например, от приблизительно 1 л до приблизительно 10000 л (например, от приблизительно 1 л до приблизительно 50 л, от приблизительно 50 л до приблизительно 500 л, от приблизительно 500 л до приблизительно 1000 л, от 500 л до приблизительно 5000 л, от приблизительно 500 л до приблизительно 10000 л, от приблизительно 5000 л до приблизительно 10000 л, от приблизительно 1 л до приблизительно 10000 л, от приблизительно 1 л до приблизительно 8000 л, от приблизительно 1 л до приблизительно 6000 л, от приблизительно 1 л до приблизительно 5000 л, от приблизительно 100 л до приблизительно 5000 л, от приблизительно 10 л до приблизительно 100 л, от приблизительно 10 л до приблизительно 4000 л, от приблизительно 10 л до приблизительно 3000 л, от приблизительно 10 л до приблизительно 2000 л или от приблизительно 10 л до приблизительно 1000 л). Количество жидкой культуральной среды, присутствующей в биореакторе, может составлять, например, от приблизительно 0,5 л до приблизительно 5000 л (например, от приблизительно 0,5 л до приблизительно 25 л, от приблизительно 25 л до приблизительно 250 л, от приблизительно 250 л до приблизительно 500 л, от 250 л до приблизительно 2500 л, от приблизительно 250 л до приблизительно 5000 л, от приблизительно 2500 л до приблизительно 5000 л, от приблизительно 0,5 л до приблизительно 5000 л, от приблизительно 0,5 л до приблизительно 4000 л, от приблизительно 0,5 л до приблизительно 3000 л, от приблизительно 0,5 л до приблизительно 2500 л, от приблизительно 50 л до приблизительно 2500 л, от приблизительно 5 л до приблизительно 50 л, от приблизительно 5 л до приблизительно 2000 л, от приблизительно 5 л до приблизительно 1500 л, от приблизительно 5 л до приблизительно 1000 л или от приблизительно 5 л до приблизительно 500 л). Культивирование клеток можно осуществлять, например, с применением биореактора периодического действия с подпиткой или перфузионного биореактора. Неограничивающие примеры и различные аспекты культивирования клеток (например, культивирования клеток млекопитающего) описаны ниже, и их можно применять в любой комбинации.
Клетки
Клетки, которые культивируют в некоторых из способов, описанных в данном документе, могут представлять собой клетки бактерий (например, грамотрицательных бактерий), дрожжей (например, Saccharomyces cerevisiae, Pichia pastoris, Hansenula polymorpha, Kluyveromyces lactis, Schizosaccharomyces pombe, Yarrowia lipolytica или Arxula adeninivorans) или клетки млекопитающего. Клетка млекопитающего может представлять собой клетку, которая растет в суспензии, или адгезивную клетку. Неограничивающие примеры клеток млекопитающего, которые можно культивировать в любом из способов, описанных в данном документе, включают клетки яичника китайского хомячка (СНО), (например, клетки СНО DG44 или клетки CHO-K1s), Sp2.0, клетки миеломы (например, NS/0), В-клетки, клетки гибридомы, Т-клетки, эмбриональные клетки почки человека (НЕК) (например, НЕК 293E и НЕК 293F), эпителиальные клетки почки африканской зеленой мартышки (клетки Vero) и эпителиальные клетки почки собаки (кокер-спаниель) Madin-Darby (клетки MDCK). В некоторых примерах, где культивируют адгезивную клетку, культура также может включать ряд микроносителей (например, микроносителей, которые содержат одну или несколько пор). Дополнительные клетки млекопитающего, которые можно культивировать в любом из способов, описанных в данном документе, известны из уровня техники.
Клетка млекопитающего может включать рекомбинантную нуклеиновую кислоту (например, нуклеиновую кислоту, стабильно интегрированную в геном клетки млекопитающего), которая кодирует рекомбинантный белок (например, рекомбинантный белок). Неограничивающие примеры рекомбинантных нуклеиновых кислот, которые кодируют иллюстративные рекомбинантные белки, описаны ниже, как и рекомбинантные белки, которые можно получить с применением способов, описанных в данном документе. В некоторых случаях клетку млекопитающего, которую культивируют в биореакторе (например, в любом из биореакторов, описанных в данном документе), получили из более крупной культуры.
Нуклеиновую кислоту, кодирующую рекомбинантный белок, можно вводить в клетку млекопитающего с применением целого ряда способов, известных в области молекулярной биологии и молекулярной генетики. Неограничивающие примеры включают трансфекцию (например, липофекцию), трансдукцию (например, инфекцию с помощью лентивируса, аденовируса или ретровируса) и электропорацию. В некоторых случаях нуклеиновая кислота, которая кодирует рекомбинантный белок, не интегрирована стабильно в хромосому клетки млекопитающего (транзиентная трансфекция), в то время как в других случаях эта нуклеиновая кислота интегрирована в хромосому. В качестве альтернативы или дополнения, нуклеиновая кислота, кодирующая рекомбинантный белок, может находиться в плазмиде и/или в искусственной хромосоме млекопитающего (например, человеческой искусственной хромосоме). В качестве альтернативы или в дополнение, нуклеиновую кислоту можно вводить в клетку с помощью вирусного вектора (например, лентивирусного, ретровирусного или аденовирусного векторов). Нуклеиновая кислота может быть функционально связана с последовательностью промотора (например, сильного промотора, такого как промотор β-актина и промотор CMV, или индуцируемого промотора). Вектор, включающий нуклеиновую кислоту, может при необходимости также включать селектируемый маркер (например ген, который придает клетке млекопитающего устойчивость к гигромицину, пуромицину или неомицину).
В некоторых случаях рекомбинантный белок представляет собой секретируемый белок и высвобождается клеткой млекопитающего во внеклеточную среду (например, первую и/или вторую жидкую культуральную среду). Например, последовательность нуклеиновой кислоты, кодирующая растворимый рекомбинантный белок, может включать последовательность, которая кодирует сигнальный пептид для секреции на N- или С-конце рекомбинантного белка, который отщепляется ферментом, присутствующим в клетке млекопитающего, и затем высвобождается во внеклеточную среду (например, первую и/или вторую жидкую культуральную среду).
Культуральные среды
Жидкие культуральные среды известны из уровня техники. Жидкие культуральные среды (например, первую и/или вторую среду для культуры тканей) можно дополнять сывороткой крови млекопитающих (например, эмбриональной телячьей сывороткой и бычьей сывороткой) и/или гормоном роста или фактором роста (например, инсулином, трансферрином и эпидермальным фактором роста). В качестве альтернативы или дополнения, жидкая культуральная среда (например, первая и/или вторая жидкая культуральная среда) может представлять собой жидкую культуральную среду с определенным химическим составом, жидкую культуральную среду, не содержащую компонентов животного происхождения, жидкую культуральную среду, не содержащую сыворотки крови, или жидкую культуральную среду, содержащую сыворотку крови. Неограничивающие примеры жидких культуральных сред с определенным химическим составом, жидких культуральных сред, не содержащих компонентов животного происхождения, жидких культуральных сред, не содержащих сыворотку крови, и жидких культуральных сред, содержащих сыворотку крови, являются коммерчески доступными.
Жидкая культуральная среда, как правило, включает источник энергии (например углевод, такой как глюкоза), незаменимые аминокислоты (например, набор из двадцати основных аминокислот плюс цистеин), витамины и/или другие органические соединения, требуемые в низких концентрациях, свободные жирные кислоты и/или микроэлементы. Жидкие культуральные среды (например, первую и/или вторую жидкую культуральную среду) можно при необходимости дополнять, например, гормоном или фактором роста млекопитающих (например, инсулином, трансферрином или эпидермальным фактором роста), солями и буферами (например, солями кальция, магния и фосфатами), нуклеозидами и основаниями (например, аденозином, тимидином и гипоксантином), белком и тканевыми гидролизатами, и/или любой комбинацией таких добавок.
Широкое разнообразие различных жидких культуральных сред, которые можно применять для культивирования клеток (например, клеток млекопитающего) в любом из способов, описанных в данном документе, известно из уровня техники. Компоненты среды, которые также можно применять в способах по настоящему изобретению, включают без ограничения гидролизаты с определенным химическим составом (CD), например, CD-пептон, CD-полипептиды (из двух или более аминокислот) и CD-факторы роста. Дополнительные примеры жидкой среды для культуры тканей и компонентов среды известны из уровня техники.
Квалифицированным специалистам-практикам будет понятно, что описанные в данном документе первая жидкая культуральная среда и вторая жидкая культуральная среда могут представлять собой один и тот же тип сред или разные среды.
Дополнительные свойства иллюстративных биореакторов
Внутренняя поверхность любого из биореакторов, описанных в данном документе, может иметь по меньшей мере одно покрытие (например, по меньшей мере одно покрытие из желатина, коллагена, поли-L-орнитина, полистирола и ламинина) и, как известно в данной области техники, одно или несколько отверстий для барботирования O2, CO2 и N2 в жидкую культуральную среду, а также устройство для перемешивания жидкой культуральной среды. В биореакторе можно инкубировать культуру клеток в контролируемой влажной атмосфере (например, при влажности более 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90% или 95% или при влажности 100%). Также биореактор может быть оснащен механическим устройством, которое выполнено с возможностью удаления некоторого объема жидкой культуральной среды из биореактора, и, необязательно, фильтром внутри механического устройства, который обеспечивает удаление клеток из жидкой культуральной среды в ходе процесса переноса жидкой культуральной среды из биореактора (например, ATF-система или система фильтрации клеток, описанная в предварительной заявке на патент США №61/878,502).
Температура
Стадию культивирования клеток млекопитающего можно выполнять при температуре от приблизительно 31ºC до приблизительно 40ºC. Квалифицированным специалистам-практикам будет понятно, что в ходе стадии культивирования температуру можно изменять в определенный(определенные) момент(моменты) времени, например, каждый час или каждые сутки. Например, температуру можно изменять или смещать (например, повышать или понижать) в течение приблизительно одного дня, двух дней, трех дней, четырех дней, пяти дней, шести дней, семи дней, восьми дней, девяти дней, десяти дней, одиннадцати дней, двенадцати дней, четырнадцати дней, пятнадцати дней, шестнадцати дней, семнадцати дней, восемнадцати дней, девятнадцати дней или приблизительно двадцати дней или более после исходного посева клетки в биореактор (например, клетки млекопитающего). Например, температуру можно смещать в сторону повышения (например, изменять на значение, не превышающее или равное приблизительно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5, 8,0, 8,5, 9,0, 9,5, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или на значение, не превышающее или равное приблизительно 20°C). Например, температуру можно регулировать в сторону понижения (например, изменять на значение, не превышающее или равное приблизительно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5, 8,0, 8,5, 9,0, 9,5, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или на значение, не превышающее или равное приблизительно 20ºC).
CO2
Стадия культивирования, описанная в данном документе, может дополнительно предусматривать подвергание жидкой культуральной среды в биореакторе воздействию атмосферы, включающей не более или приблизительно 15% CO2 (например, не более или приблизительно 14% CO2, 12% CO2, 10% CO2, 8% CO2, 6% CO2, 5% CO2, 4% CO2, 3% CO2, 2% CO2 или не более или приблизительно 1% CO2).
Перфузионный биореактор
Стадию культивирования, описанную в данном документе, можно проводить с применением перфузионного биореактора. Культивирование клетки (например, клетки млекопитающего) в перфузионном биореакторе предусматривает удаление из биореактора первого объема первой жидкой культуральной среды (например, характеризующейся любой концентрацией клеток млекопитающего, например, первого объема первой жидкой культуральной среды, которая практически не содержит клеток) и добавление к первой жидкой культуральной среде второго объема второй жидкой культуральной среды. Удаление и добавление можно проводить одновременно или последовательно, или путем их комбинирования. Кроме того, удаление и добавление можно осуществлять непрерывно (например, со скоростью, при которой удаляют или заменяют объем, составляющий от 0,1% до 800% (например, от 1% до 700%, от 1% до 600%, от 1% до 500%, от 1% до 400%, от 1% до 350%, от 1% до 300%, от 1% до 250%, от 1% до 100%, от 100% до 200%, от 5% до 150%, от 10% до 50%, от 15% до 40%, от 8% до 80% или от 4% до 30%) объема биореактора или объема первой жидкой культуральной среды в течение любого заданного периода времени (например, в течение периода времени, составляющего 24 часа, в течение дискретного периода времени от приблизительно 1 часа до приблизительно 24 часов или в течение дискретного периода времени, составляющего более 24 часов)) или периодически (например, один раз в три дня, один раз в два дня, один раз в день, два раза в день, три раза в день, четыре раза в день или пять раз в день), или в любой их комбинации. В случае периодического осуществления объем, который удаляют или заменяют (например, в течение периода времени, составляющего приблизительно 24 часа, в течение дискретного периода времени, составляющего от приблизительно 1 часа до приблизительно 24 часов, или в течение дискретного периода времени, составляющего более 24 часов), может составлять, например, от 0,1% до 800% (например, от 1% до 700%, от 1% до 600%, от 1% до 500%, от 1% до 400%, от 1% до 300%, от 1% до 200%, от 1% до 100%, от 100% до 200%, от 5% до 150%, от 10% до 50%, от 15% до 40%, от 8% до 80% или от 4% до 30%) объема биореактора или объема первой жидкой культуральной среды. Первый объем удаляемой первой жидкой культуральной среды и второй объем добавляемой второй жидкой культуральной среды в некоторых случаях можно поддерживать примерно одинаковыми в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от приблизительно 1 часа до приблизительно 24 часов, или дискретного периода времени, составляющего более 24 часов), в течение всего периода культивирования или его части. Как известно из уровня техники, скорость, с которой удаляют первый объем первой жидкой культуральной среды (объем/единица времени), и скорость, с которой добавляют второй объем второй жидкой культуральной среды (объем/единица времени), могут варьироваться. Скорость, с которой удаляют первый объем первой жидкой культуральной среды (объем/единица времени), и скорость, с которой добавляют второй объем второй жидкой культуральной среды (объем/единица времени), могут быть примерно одинаковыми или могут быть отличными.
В качестве альтернативы, удаляемый и добавляемый объемы можно изменять (например, постепенно увеличивать) в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от 1 часа до приблизительно 24 часов, или дискретного периода времени, составляющего более 24 часов), в ходе периода культивирования. Например, объем удаляемой первой жидкой культуральной среды и объем добавляемой второй жидкой культуральной среды в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от приблизительно 1 часа до более 24 часов, или дискретного периода времени, составляющего более 24 часов), в ходе периода культивирования можно увеличивать (например, постепенно или путем ступенчатых повышений) в ходе периода культивирования от значения объема, который составляет от 0,5% до приблизительно 20% объема биореактора или объема первой жидкой культуральной среды, до значения, составляющего от приблизительно 25% до приблизительно 150% объема биореактора или объема первой жидкой культуральной среды.
Квалифицированным специалистам-практикам будет понятно, что первая жидкая культуральная среда и вторая жидкая культуральная среда могут быть средами одного и того же типа. В иных случаях первая жидкая культуральная среда и вторая жидкая культуральная среда могут являться отличными.
Первый объем первой жидкой культуральной среды можно удалять, например, с помощью механической системы, которая может обеспечивать удаление первого объема первой жидкой культуральной среды из биореактора (например, первого объема первой жидкой культуральной среды, которая по сути не содержит клеток, из биореактора). В качестве альтернативы или дополнения, первый объем первой жидкой культуральной среды можно удалять путем обеспечения стекания или пропускания самотеком первого объема первой жидкой культуральной среды через стерильную мембрану с отсечением по молекулярной массе, которое исключает прохождение клетки (например, клетки млекопитающего).
Второй объем второй жидкой культуральной среды можно добавлять к первой жидкой культуральной среде в автоматическом режиме, например, с помощью перфузионного насоса.
В некоторых случаях удаление первого объема первой жидкой культуральной среды (например, первого объема первой жидкой культуральной среды, которая по сути не содержит клеток млекопитающего) и добавление к первой жидкой культуральной среде второго объема второй жидкой культуральной среды не осуществляют на протяжении по меньшей мере 1 часа (например, на протяжении 2 часов, на протяжении 3 часов, на протяжении 4 часов, на протяжении 5 часов, на протяжении 6 часов, на протяжении 7 часов, на протяжении 8 часов, на протяжении 9 часов, на протяжении 10 часов, на протяжении 12 часов, на протяжении 14 часов, на протяжении 16 часов, на протяжении 18 часов, на протяжении 24 часов, на протяжении 36 часов, на протяжении 48 часов, на протяжении 72 часов, на протяжении 96 часов или 96 часов спустя) после посева в биореактор клетки млекопитающего.
Биореактор периодического действия с подпиткой
Стадию культивирования, описанную в данном документе, можно осуществлять с применением биореактора периодического действия с подпиткой. Культивирование клетки в биореакторе периодического действия с подпиткой предусматривает, в течение большей части периода культивирования, добавление (например, периодическое или непрерывное добавление) к первой жидкой культуральной среде второго объема второй жидкой культуральной среды. Добавление второй жидкой культуральной среды можно осуществлять непрерывно (например, со скоростью, при которой объем увеличивается на величину, составляющую от 0,1% до 300% (например, от 1% до 250%, от 1% до 100%, от 100% до 200%, от 5% до 150%, от 10% до 50%, от 15% до 40%, от 8% до 80% или от 4% до 30%) объема биореактора или объема первой жидкой культуральной среды в течение любого заданного периода времени (например, в течение периода времени, составляющего 24 часа, в течение дискретного периода времени, составляющего от приблизительно 1 часа до приблизительно 24 часов, или в течение дискретного периода времени, составляющего более 24 часов)), или периодически (например, один раз в три дня, один раз в два дня, один раз в сутки, два раза в сутки, три раза в сутки, четыре раза в сутки или пять раз в сутки), или в любой их комбинации. В случае периодического осуществления объем, который добавляют (например, в течение периода времени, составляющего приблизительно 24 часа, в течение дискретного периода времени, составляющего от приблизительно 1 часа до приблизительно 24 часов, или в течение дискретного периода времени, составляющего более 24 часов), может составлять, например, от 0,1% до 300% (например, от 1% до 200%, от 1% до 100%, от 100% до 200%, от 5% до 150%, от 10% до 50%, от 15% до 40%, от 8% до 80% или от 4% до 30%) объема биореактора или объема первой жидкой культуральной среды. В некоторых случаях второй объем добавляемой второй жидкой культуральной среды можно поддерживать примерно на одинаковом уровне в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от приблизительно 1 часа до приблизительно 24 часов, или дискретного периода времени, составляющего более 24 часов), в ходе всего периода культивирования или его части. Как известно из уровня техники, скорость, с которой добавляют второй объем второй жидкой культуральной среды (объем/единица времени), может варьироваться в ходе всего периода культивирования или его части. Например, объем добавляемой второй жидкой культуральной среды можно изменять (например, постепенно увеличивать) в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от 1 часа до приблизительно 24 часов, или дискретного периода времени, составляющего более 24 часов), в ходе периода культивирования. Например, объем второй жидкой культуральной среды, добавляемый в течение каждого периода времени, составляющего 24 часа (или, в качестве альтернативы, дискретного периода времени, составляющего от приблизительно 1 часа до более 24 часов, или дискретного периода времени, составляющего более 24 часов), в ходе периода культивирования, можно увеличивать (например, постепенно или путем ступенчатых повышений) в ходе периода культивирования от значения объема, который составляет от 0,5% до приблизительно 20% объема биореактора или объема первой жидкой культуральной среды, до значения, составляющего от приблизительно 25% до приблизительно 150% объема биореактора или объема первой жидкой культуральной среды. Скорость, с которой добавляют второй объем второй жидкой культуральной среды (объем/единица времени), может быть приблизительно одинаковой на протяжение всего периода культивирования или его части.
Квалифицированным специалистам-практикам будет понятно, что первая жидкая культуральная среда и вторая жидкая культуральная среда могут быть средами одного и того же типа. В иных случаях первая жидкая культуральная среда и вторая жидкая культуральная среда могут являться отличными. Объем второй жидкой культуральной среды можно добавлять к первой жидкой культуральной среде в автоматическом режиме, например, с помощью перфузионного насоса.
В некоторых случаях добавление к первой жидкой культуральной среде второго объема второй жидкой культуральной среды не осуществляют на протяжении по меньшей мере 1 часа (например, на протяжении 2 часов, на протяжении 3 часов, на протяжении 4 часов, на протяжении 5 часов, на протяжении 6 часов, на протяжении 7 часов, на протяжении 8 часов, на протяжении 9 часов, на протяжении 10 часов, на протяжении 12 часов, на протяжении 14 часов, на протяжении 16 часов, на протяжении 18 часов, на протяжении 24 часов, на протяжении 36 часов, на протяжении 48 часов, на протяжении 72 часов, на протяжении 96 часов или более 96 часов) после посева в биореактор клетки млекопитающего. Среду, в которой культивируют клетки при периодическом культивировании с подпиткой, как правило, собирают в конце периода культивирования и применяют в любом из способов, описанных в данном документе, однако среду, в которой культивируют клетки при периодическом культивировании с подпиткой, также можно собирать в один или несколько моментов времени в ходе периода культивирования и применять в любом из способов, описанных в данном документе.
Квалифицированным специалистам-практикам будет понятно, что для осуществления данных способов любые из ряда параметров культивирования (например, контейнеры, значения объема, значения скорости или частоты замены объемов культуры, значения частоты перемешивания, значения температуры, среды и значения концентрации CO2) можно применять в любой комбинации. Кроме того, для получения рекомбинантного белка можно применять любые клетки млекопитающего, описанные в данном документе или известные из уровня техники.
Иллюстративные биологические производственные системы
Примеры биологических производственных систем, применяемых для выполнения способов, описанных в данном документе, и которые включают MCCS или MCCS1 и MCCS2 описаны в предварительной заявке на патент США №№61/775060 и 61/856390 (включены посредством ссылки). В таких иллюстративных системах по меньшей мере одна (например, по меньшей мере два, три, четыре, пять или шесть) заполненная хроматографическая колонка с уменьшенной бионагрузкой, предусмотренная в данном документе, присутствует в MCCS или в MCCS1 и/или MCCS2. Например, вся система может содержать в целом две, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать или двадцать заполненных хроматографических колонок с уменьшенной бионагрузкой, предусмотренных в данном документе. Например, MCCS, MCCS1 и/или MCCS2 могут содержать (или каждая может содержать) одну, две, три, четыре, пять, шесть, семь, восемь, девять или десять заполненных хроматографических колонок с уменьшенной бионагрузкой, предусмотренных в данном документе.
Например, применимые системы могут содержать MCCS1, которая включает впускное отверстие, и MCCS2, которая содержит выпускное отверстие, или MCCS, которая содержит впускное отверстие и выпускное отверстие. В некоторых вариантах осуществления MCCS1 и MCCS2 сообщаются по текучей среде друг с другом. Такие системы также могут быть выполнены таким образом, что текучая среда может поступать во впускное отверстие, проходить через MCCS1 и MCCS2 и выходить из производственной системы через выпускное отверстие. Такие системы обеспечивают непрерывное и эффективное в отношении затрачиваемого времени получение терапевтического лекарственного вещества из жидкой культуральной среды. Например, время, прошедшее между подачей текучей среды (например, жидкой культуральной среды), включающей терапевтический белок, в MCCS1 и элюированием очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка) из выпускного отверстия MCCS2, может составлять, например, от приблизительно 4 часов до приблизительно 48 часов включительно.
Некоторые иллюстративные системы не содержат буферной емкости. В других случаях система может содержать максимально 1, 2, 3, 4 или 5 буферных емкостей во всей системе (например, где каждая буферная емкость обеспечивает удерживание терапевтического белка в течение общего периода времени, составляющего, например, от приблизительно 5 минут до приблизительно 6 часов включительно). Буферная(буферные) емкость(емкости) может(могут) характеризоваться емкостью, составляющей от 1 мл до приблизительно 300 мл включительно. Любые буферные емкости, расположенные в системе так, чтобы текучая среда поступала в буферные емкости до поступления в MCCS1 или MCCS, могут характеризоваться емкостью, составляющей от 1 мл до приблизительно 100% включительно от загрузочного объема первой колонки MCCS1 или MCCS, соответственно. Любые буферные емкости, расположенные в системе так, чтобы текучая среда поступала в буферные емкости до поступления в MCCS2 (и после выхода из MCCS1), могут характеризоваться емкостью, составляющей, например, от 1 мл до приблизительно 100% включительно от загрузочного объема первой колонки MCCS2.
Структуры и свойства дополнительной иллюстративной системы
MCCS или MCCS1 могут содержать впускное отверстие, через которое жидкость (например, жидкая культуральная среда, которая по сути не содержит клеток) может поступать в MCCS или MCCS1, соответственно. Впускное отверстие может иметь любую структуру, известную из уровня техники для таких целей. Оно может включать, например, винтовую резьбу, ребристость или уплотнение, которые позволяют вставлять трубку для текучей среды, так что после вставки трубки для текучей среды во впускное отверстие текучая среда будет входить в MCCS или MCCS1 через впускное отверстие без значительной случайной утечки текучей среды из впускного отверстия. Неограничивающие впускные отверстия, которые можно применять в системах по настоящему изобретению, известны и будут понятны специалистам в данной области техники.
MCCS или MCCS1 могут содержать по меньшей мере две хроматографические колонки, по меньшей мере две хроматографические мембраны или по меньшей мере одну хроматографическую колонку и по меньшей мере одну хроматографическую мембрану и впускное отверстие. MCCS или MCCS1 могут представлять собой любую из иллюстративных MCCS, описанных в данном документе, или характеризоваться одним или несколькими из любых иллюстративных свойств MCCS (в любой комбинации), описанными в данном документе. Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны), присутствующие в MCCS или MCCS1, могут характеризоваться одной или несколькими из любых иллюстративных форм, размеров, объемов (объемов слоев) и/или отдельной(отдельных) операцией(операций), описанных в данном документе.
Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны), присутствующие в MCCS или MCCS1, могут содержать одну или несколько из любых иллюстративных смол, описанных в данном документе или известных из уровня техники. Например, смола, содержащаяся в одной или нескольких хроматографических колонках и/или хроматографических мембранах, присутствующих в MCCS или MCCS1, может представлять собой смолу, в которой используется механизм захвата (например, механизм захвата путем связывания с белком А, механизм захвата путем связывания с белком G, механизм захвата путем связывания с антителом или фрагментом антитела, механизм захвата путем связывания с субстратом, механизм захвата путем связывания с кофактором, механизм захвата путем связывания с аптамером и/или механизм захвата путем связывания с меткой). Смола, содержащаяся в одной или нескольких хроматографических колонках и/или хроматографических мембранах MCCS или MCCS1, может представлять собой катионообменную смолу, анионообменную смолу, смолу для хроматографии на молекулярных ситах или смолу для хроматографии с гидрофобным взаимодействием или любую их комбинацию. Дополнительные примеры смол, которые можно применять для очистки рекомбинантного белка, известны из уровня техники и могут содержаться в одной или нескольких хроматографических колонках и/или хроматографических мембранах, присутствующих в MCCS или MCCS1. Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны), присутствующие в MCCS или MCCS1, могут содержать одинаковую и/или разные смолы (например, любую из смол, описанных в данном документе или известных из уровня техники для применения в очистке рекомбинантного белка).
В двух или более хроматографических колонках и/или хроматографических мембранах, присутствующих в MCCS или MCCS1, можно осуществлять одну или несколько отдельных операций (например, захват рекомбинантного белка, очистку рекомбинантного белка, тонкую очистку рекомбинантного белка, инактивацию вирусов, регуляцию концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок, или фильтрование текучей среды, включающей рекомбинантный белок). В неограничивающих примерах в MCCS или MCCS1 можно осуществлять отдельные операции захвата рекомбинантного белка из текучей среды (например, жидкой культуральной среды) и инактивации вирусов, присутствующих в текучей среде, включающей рекомбинантный белок. В MCCS или MCCS1 можно осуществлять любые комбинации двух или более отдельных операций, описанных в данном документе или известных из уровня техники.
Хроматографическую(хроматографические) колонку(колонки) и/или хроматографическую(хроматографические) мембрану(мембраны), присутствующие в MCCS или MCCS1, можно соединять или перемещать относительно друг друга с помощью механизма переключения (например, механизма переключения колонок). MCCS или MCCS1 также могут содержать один или несколько (например, два, три, четыре или пять) насосов (например, автоматических, например, автоматических перистальтических насосов). События переключения колонок можно запускать при выявлении уровня рекомбинантного белка, выявленного с помощью поглощения УФ-излучения, соответствующего определенному уровню рекомбинантного белка в текучей среде, проходящей через MCCS или MCCS1 (например, входящем потоке и/или элюате, выходящем из одной или нескольких хроматографических колонок и/или хроматографических мембран в MCCS или MCCS1), конкретному объему жидкости (например, буфера) или конкретному прошедшему времени. Переключение колонок в основном означает механизм, с помощью которого по меньшей мере в двух разных хроматографических колонках и/или хроматографических мембранах в MCCS или MCCS1 (например, двух или более разных хроматографических колонках и/или хроматографических мембранах, присутствующих в MCCS1 или MCCS2) обеспечивается прохождение другой стадии (например, уравновешивания, загрузки, элюирования или промывания) практически в одно и то же время в ходе по меньшей мере части процесса.
MCCS или MCCS1 может представлять собой систему для периодической противоточной хроматографии (PCCS). Например, PCCS, которая представляет собой MCCS или MCCS1 (т. e., PCCS или PCCS1, соответственно), может содержать четыре хроматографические колонки, при этом в первых трех колонках осуществляется отдельная операция захвата рекомбинантного белка из текучей среды (например, жидкой культуральной среды), а в четвертой колонке PCCS осуществляется отдельная операция инактивации вирусов в текучей среде, включающей рекомбинантный белок. В PCCS, которая представляет собой MCCS или MCCS1, можно использовать механизм переключения колонок. В системе PCC можно использовать модифицированную систему ÄKTA (GE Healthcare, Пискатауэй, Нью-Джерси), в которой может функционировать, например, до четырех, пяти, шести, семи или восьми колонок или больше.
MCCS или MCCS1 могут быть оснащены одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) устройствами для отслеживания по УФ-излучению, одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) клапанами, одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) pH-метрами и/или одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) измерителями проводимости. MCCS или MCCS1 могут также оснащаться операционной системой, в которой используется программное обеспечение (например, программное обеспечение на основе Unicorn, GE Healthcare, Пискатауэй, Нью-Джерси) для определения того, когда должно произойти переключение колонок (например, на основе УФ-поглощения, объема жидкости или прошедшего времени), и которая влияет на (инициирует) события переключения колонок.
MCCS или MCCS1 могут дополнительно содержать один или несколько (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать, двадцать один, двадцать два, двадцать три или двадцать четыре) резервуаров для регулирования буфера в потоке и/или буферных резервуаров. В другом примере MCCS или MCCS1 могут содержать одну или несколько (например, две, три, четыре, пять или шесть) буферных емкостей, которые могут удерживать текучую среду, которая не может без промедления перемещаться в одну или несколько хроматографических колонок и/или хроматографических мембран в MCCS или MCCS1. Системы, описанные в данном документе, могут содержать одну или несколько буферных емкостей (например, буферную емкость, описанную в данном документе) в MCCS, MCCS1 и/или MCCS2. Другие примеры систем, описанных в данном документе, не содержат буферной емкости в MCCS, MCCS1 или MCCS2 или не содержат буферной емкости во всей системе. Другие примеры систем, описанных в данном документе, содержат максимум одну, две, три, четыре или пять буферных емкостей (например, любые буферные емкости, описанные в данном документе) во всей системе.
Вторая MCCS
Вторая MCCS (MCCS2) в иллюстративных системах содержит по меньшей мере две хроматографические колонки, по меньшей мере две хроматографические мембраны или по меньшей мере одну хроматографическую колонку и по меньшей мере одну хроматографическую мембрану и выпускное отверстие. MCCS2 может представлять собой любую из иллюстративных MCCS, описанных в данном документе, или может характеризоваться одним или несколькими из любых иллюстративных свойств MCCS (в любой комбинации), описанных в данном документе. Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны), присутствующие в MCCS2, могут характеризоваться одним или несколькими из любых иллюстративных форм, размеров, объемов (объемов слоев) и/или отдельных операций, описанных в данном документе. Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны) могут содержать любую из иллюстративных смол, описанных в данном документе или известных из уровня техники. Например, смола, содержащаяся в одной или нескольких хроматографических колонках и/или хроматографических мембранах, присутствующих в MCCS2, может представлять собой смолу, в которой используется механизм захвата (например, механизм захвата путем связывания с белком А, механизм захвата путем связывания с белком G, механизм захвата путем связывания с антителом или фрагментом антитела, механизм захвата путем связывания с субстратом, механизм захвата путем связывания с кофактором, механизм захвата путем связывания с меткой и/или механизм захвата путем связывания с аптамером). Применимые смолы включают, например, катионообменную смолу, анионообменную смолу, смолу для хроматографии на молекулярных ситах, смолу для хроматографии с гидрофобным взаимодействием. Дополнительные примеры смол известны из уровня техники. Хроматографическая(хроматографические) колонка(колонки) и/или хроматографическая(хроматографические) мембрана(мембраны), присутствующие в MCCS2, могут содержать одинаковые и/или разные смолы (например, любую из смол, описанных в данном документе или известных из уровня техники для применения в очистке рекомбинантного белка).
В хроматографической(хроматографических) колонке(колонках) и/или хроматографической(хроматографических) мембране(мембранах), присутствующих в MCCS2, можно осуществлять одну или несколько отдельных операций (например, любую из отдельных операций, описанных в данном документе, или любую комбинацию отдельных операций, описанных в данном документе). В неограничивающих примерах в MCCS2 можно осуществлять отдельные операции очистки рекомбинантного белка из текучей среды и тонкой очистки рекомбинантного белка, присутствующего в текучей среде, включающей рекомбинантный белок. В других неограничивающих примерах в MCCS2 можно осуществлять отдельные операции очистки рекомбинантного белка, присутствующего в текучей среде, тонкой очистки рекомбинантного белка, присутствующего в текучей среде, и фильтрования текучей среды, включающей рекомбинантный белок. В другом примере в MCCS2 можно осуществлять отдельные операции очистки рекомбинантного белка, присутствующего в текучей среде, тонкой очистки рекомбинантного белка, присутствующего в текучей среде, фильтровании текучей среды, включающей рекомбинантный белок, и регулирования концентрации ионов и/или pH текучей среды, включающей рекомбинантный белок. В MCCS2 можно осуществлять любую комбинацию двух или более отдельных операций, описанных в данном документе или известных из уровня техники.
Хроматографическую(хроматографические) колонку(колонки) и/или хроматографическую(хроматографические) мембрану(мембраны), присутствующие в MCCS2, можно соединять или перемещать относительно друг друга с помощью механизма переключения (например, механизма переключения колонок). MCCS2 может также содержать один или несколько (например, два, три, четыре или пять) насосов (например, автоматических, например, автоматических перистальтических насосов). События переключения колонок можно запускать при выявлении уровня рекомбинантного белка, выявленного с помощью поглощения УФ-излучения, соответствующего определенному уровню рекомбинантного белка в текучей среде, проходящей через MCCS2 (например, во входящем потоке и/или элюате, выходящем из одной или нескольких хроматографической(хроматографических) колонки(колонок) и/или хроматографических мембран в MCCS2), конкретному объему жидкой среды (например, буфера) или конкретному прошедшему времени.
MCCS2 может представлять собой систему для периодической противоточной хроматографии (т. e. PCCS2). Например, PCCS2 может содержать три колонки, в которых осуществляют отдельную операцию очистки рекомбинантного белка из текучей среды, и хроматографическую мембрану, в которой осуществляют отдельную операцию тонкой очистки рекомбинантного белка, присутствующего в текучей среде. Например, три колонки, в которых осуществляют отдельную операцию очистки рекомбинантного белка из текучей среды, могут содержать, например, катионообменную смолу, и хроматографическая мембрана, в которой осуществляют отдельную операцию тонкой очистки, может содержать катионообменную смолу. В PCCS2 можно использовать механизм переключения колонок. В PCCS2 можно использовать модифицированную систему ÄKTA (GE Healthcare, Пискатауэй, Нью-Джерси), в которой может функционировать, например, до четырех, пяти, шести, семи или восьми колонок или больше.
MCCS2 может быть оснащена одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) устройствами для отслеживания по УФ-излучению, одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) клапанами, одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) pH-метрами и/или одним или несколькими (например, двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью) измерителями проводимости. MCCS2 может также оснащаться операционной системой, в которой используется программное обеспечение (например, программное обеспечение на основе Unicorn, GE Healthcare, Пискатауэй, Нью-Джерси) для определения того, когда должно произойти событие переключение колонок (например, на основе УФ-поглощения, объема жидкости или прошедшего времени), и которая влияет на события переключения колонок.
MCCS2 может дополнительно содержать один или несколько (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать, восемнадцать, девятнадцать, двадцать, двадцать один, двадцать два, двадцать три или двадцать четыре) резервуаров для регулирования буфера в потоке и/или буферных резервуаров. В других примерах MCCS2 может содержать одну или несколько (например, две, три, четыре, пять или шесть) буферных емкостей (например, любую из буферных емкостей, описанных в данном документе), которые могут удерживать текучую среду, которая не может без промедления перемещаться в одну или несколько хроматографических колонок и/или хроматографических мембран в MCCS2.
MCCS2 содержит выпускное отверстие, через которое лекарственное вещество на основе терапевтического белка может выходить из системы. Выпускное отверстие может включать, например, винтовую резьбу, ребристость или уплотнение, которые позволяют вставлять трубку для текучей среды или флакон, выполненный с возможностью удерживания или хранения очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка). Выпускное отверстие может включать поверхность, которую можно применять для герметичной изоляции сосуда с уменьшенной бионагрузкой или другого такого контейнера для хранения на выпускном отверстии с целью обеспечения перемещения потока очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка) непосредственно в сосуд с уменьшенной бионагрузкой или контейнер для хранения. Неограничивающие выпускные отверстия, которые можно применять в системах по настоящему изобретению, известны и будут понятны специалистам в данной области техники.
Системы, описанные в данном документе, также могут содержать трубку для текучей среды, которая расположен между MCCS1 и MCCS2. Любая из трубок для текучей среды, описанных в данном документе, может представлять собой, например, трубу, которая выполнена, например, из полиэтилена, поликарбоната или пластмассы. Трубка для текучей среды, расположенная между MCCS1 и MCCS2, может дополнительно содержать одно или несколько из следующего в любой комбинации: один или несколько резервуаров для регулирования буфера в потоке, которые сообщаются по текучей среде с трубкой для текучей среды и расположены таким образом, что буфер, хранящийся внутри резервуара(резервуаров) для регулирования буфера в потоке, добавляется к текучей среде, присутствующей в трубке для текучей среды; буферную емкость (например, любую из буферных емкостей, описанных в данном документе), которая сообщается по текучей среде с трубкой для текучей среды и расположена таким образом, что она может удерживать любую избыточную текучую среду, присутствующую в трубке для текучей среды, которая не может без промедления подаваться в MCCS2; и один или несколько фильтров, которые расположены в трубке для текучей среды таким образом, что они способны фильтровать текучую среду (например, удалять бактерии), присутствующую в трубке для текучей среды. Любой из резервуаров для регулирования буфера в потоке может включать, например, объем от приблизительно 0,5 л до 50 л буфера (например, при температуре 25°C, 15°C или 10°C или ниже).
Системы, описанные в данном документе, могут необязательно содержать трубку для текучей среды, расположенную между конечной хроматографической колонкой или хроматографической мембраной в MCCS2 и выпускным отверстием. Системы, описанные в данном документе, могут дополнительно содержать один или несколько фильтров, находящихся в соединении по текучей среде с трубкой для текучей среды, расположенной между конечной хроматографической колонкой или хроматографической мембраной в MCCS2 и выпускным отверстием, вследствие чего фильтр может удалять, например, осажденный материал, твердые частицы или бактерии из текучей среды, присутствующей в трубке для текучей среды, расположенной между последней хроматографической колонкой или хроматографической мембраной в MCCS2 и выпускным отверстием.
Некоторые примеры систем, представленных в данном документе, также предусматривают биореактор, который находится в соединении по текучей среде с впускным отверстием MCCS или MCCS1. Любой из иллюстративных биореакторов, описанных в данном документе или известных из уровня техники, может использоваться в системах по настоящему изобретению.
Некоторые примеры систем, представленных в данном документе, также включают насосную систему. Насосная система может содержать одно или несколько из следующего: один или несколько (например, два, три, четыре, пять, шесть, семь, восемь, девять или десять) насосов (например, любых насосов, описанных в данном документе или известных в данной области техники), один или несколько (например, два, три, четыре или пять) фильтров (например, любых фильтров, описанных в данном документе или известных в данной области техники), один или несколько (например, два, три, четыре, пять, шесть, семь, восемь, девять или десять) УФ-детекторов и одну или несколько (например, две, три, четыре или пять) буферных емкостей (например, любых буферных емкостей, описанных в данном документе). Некоторые примеры систем, представленных в данном документе, дополнительно включают трубку для текучей среды, расположенную между насосом и впускным отверстием MCCS или MCCS1 (например, любую из иллюстративных трубок для текучей среды, описанных в данном документе или известных в данной области техники). В некоторых примерах такая конкретная трубка для текучей среды может включать один или несколько (например, два, три или четыре) насосов (например, любых насосов, описанных в данном документе или известных в данной области техники) и/или одну или несколько (например, две, три или четыре) буферных емкостей (например, любых иллюстративных буферных емкостей, описанных в данном документе), где такой(такие) насос(насосы) и/или буферная(буферные) емкость(емкости) находятся в соединении по текучей среде с текучей средой, присутствующей в трубке для текучей среды.
Некоторые примеры систем, описанных в данном документе, дополнительно включают дополнительную трубку для текучей среды, соединенную с трубкой для текучей среды, расположенной между насосом и впускным отверстием, где один конец дополнительной трубки для текучей среды находится в соединении по текучей среде с биореактором, а другой конец находится в соединении по текучей среде с трубкой для текучей среды, расположенной между насосом и впускным отверстием. Такая дополнительная трубка для текучей среды может содержать фильтр, который способен удалять клетки из жидкой культуральной среды, удаляемой из биореактора (например, систему удержания клеток ATF).
Системы, предусмотренные в данном документе, обеспечивают непрерывное производство очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка). Как известно из уровня техники, системы могут обеспечить периодическое элюирование очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка). Системы, описанные в данном документе, могут также приводить к обеспечению общего выхода очищенного рекомбинантного белка (например, лекарственного вещества на основе терапевтического белка), составляющего по меньшей мере приблизительно 5 г/день, по меньшей мере приблизительно 10 г/день, по меньшей мере приблизительно 15 г/день, по меньшей мере приблизительно 20 г/день, по меньшей мере приблизительно 30 г/день или по меньшей мере приблизительно 40 г/день, в течение непрерывного периода времени, составляющего по меньшей мере приблизительно 5 дней, по меньшей мере приблизительно 10 дней, по меньшей мере приблизительно 15 дней, по меньшей мере приблизительно 20 дней, по меньшей мере приблизительно 25 дней, по меньшей мере приблизительно 30 дней, по меньшей мере приблизительно 40 дней, по меньшей мере приблизительно 50 дней, по меньшей мере приблизительно 60 дней, по меньшей мере приблизительно 70 дней, по меньшей мере приблизительно 80 дней, по меньшей мере приблизительно 90 дней или по меньшей мере приблизительно 100 дней.
Способы уменьшения бионагрузки в смоле для хроматографии, которые предусматривают применение по сути сухой смолы для хроматографии
Также в данном документе предусмотрены способы уменьшения бионагрузки в смоле для хроматографии, предусматривающие (a) подвергание контейнера, содержащего по сути сухую смолу для хроматографии, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по сути сухая смола для хроматографии предусматривает жидкость, включающую по меньшей мере один спирт, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения. Некоторые варианты осуществления таких способов дополнительно включают перед стадией (a) высушивание смолы для хроматографии для по сути удаления жидкости (но не всей жидкости) из смолы для хроматографии. Высушивание смолы для хроматографии можно проводить с применением термической обработки (например, в печи) или осушителя. Дополнительные способы высушивания смолы для хроматографии известны из уровня техники.
В таких способах могут использоваться любые из условий и значений дозы гамма-излучения, описанных в данном документе. Например, доза гамма-излучения может составлять от приблизительно 15 кГр до приблизительно 45 кГр (например, от приблизительно 20 кГр до приблизительно 30 кГр). В таких способах могут использоваться любые из контейнеров, смол для хроматографии и жидкостей, включающих по меньшей мере один спирт, описанных в данном документе. Например, контейнер может представлять собой сосуд для хранения или хроматографическую колонку. Смола для хроматографии в таких способах может включать белковый лиганд (например, белок A или белок G). В некоторых примерах смола для хроматографии может предусматривать смолу для анионообменной хроматографии (например, смолу для хроматографии, содержащую N-бензил-N-метилэтаноламинные группы). В некоторых примерах смола для хроматографии ковалентно присоединена к поверхности изделия (например, чипу, мембране или кассете). В некоторых вариантах осуществления по сути сухая смола для хроматографии не содержит значительного количества антиоксиданта или значительного количества хелатора. Также предусмотрены смолы для хроматографии с уменьшенной бионагрузкой, полученные с помощью любого из способов, описанных в данном документе.
В некоторых примерах полученная смола для хроматографии с уменьшенной бионагрузкой характеризуется уровнем обеспечения стерильности (SAL), составляющим от приблизительно 1 × 10−8 до приблизительно 1 × 10−5 (например, SAL, составляющим от приблизительно 1 × 10−7 до приблизительно 1 × 10−6). Полученная смола для уменьшенной хроматографии может предусматривать по меньшей мере одну смолу, выбранную из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии. В некоторых примерах полученная смола для уменьшенной хроматографии предусматривает смолу для аффинной хроматографии, содержащую белковый лиганд (например, белок A). В некоторых примерах полученная смола для уменьшенной хроматографии предусматривает смолу для анионообменной хроматографии (например, смолу для анионообменной хроматографии, содержащую N-бензил-N-метилэтаноламинные группы). Также предусмотрены способы получения заполненной хроматографической колонки с уменьшенной бионагрузкой, которые предусматривают обеспечение смолы для хроматографии с уменьшенной бионагрузкой, полученной с помощью любого из способов, описанных в данном документе, и заполнение смолой для хроматографии колонки с уменьшенной бионагрузкой в асептических условиях. Также предусмотрены заполненные хроматографические колонки с уменьшенной бионагрузкой, полученные с помощью любого из способов, описанных в данном документе.
Также предусмотрены интегрированные закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают (a) обеспечение жидкой культуральной среды, включающей рекомбинантный белок, по сути не содержащей клеток; и (b) непрерывную подачу жидкой культуральной среды в систему для многоколоночной хроматографии (MCCS), содержащую по меньшей мере одну заполненную хроматографическую колонку с уменьшенной бионагрузкой, полученную с помощью любого из способов, предусмотренных в данном документе; где в способе используют буфер с уменьшенной бионагрузкой, способ является интегрированным, и его осуществляют непрерывно от жидкой культуральной среды до элюата, выходящего из MCCS, который представляет собой очищенный рекомбинантный белок. Также предусмотрены интегрированные закрытые и непрерывные способы производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, которые предусматривают (a) обеспечение жидкой культуральной среды, включающей рекомбинантный белок, по сути не содержащей клеток; (b) непрерывную подачу жидкой культуральной среды в первую систему для многоколоночной хроматографии (MCCS1); (c) захват рекомбинантного белка в жидкой культуральной среде с применением MCCS1; (d) получение элюата, выходящего из MCCS1, который включает рекомбинантный белок, и непрерывную подачу элюата во вторую систему для многоколоночной хроматографии (MCCS2); (e) непрерывную подачу рекомбинантного белка из элюата в MCCS2 и последующее элюирование рекомбинантного белка с получением таким образом очищенного рекомбинантного белка, при этом в способе используют буфер с уменьшенной бионагрузкой, способ является интегрированным, и его осуществляют непрерывно от жидкой культуральной среды до очищенного рекомбинантного белка, и при этом по меньшей мере одна колонка в MCCS1 и/или MCCS2 содержит заполненную хроматографическую колонку с уменьшенной бионагрузкой, полученную с помощью любого из способов, предусмотренных в данном документе. В таких способах могут использоваться любые из иллюстративных аспектов интегрированных закрытых и непрерывных способов для производства очищенного рекомбинантного белка с уменьшенной бионагрузкой, описанных в данном документе.
Способы получения мембран, смол, материалов с покрытием, чипов и кассет с уменьшенной бионагрузкой
Также в данном документе предусмотрены способы получения мембраны, смолы, материала с покрытием, чипа или кассеты с уменьшенной бионагрузкой, которые включают подвергание контейнера, включающего композицию, включающую (i) мембрану, смолу, материал с покрытием, чип или кассету (например, мембрану на основе целлюлозы, агарозы или сахара, смолу, материал с покрытием, чип или кассету) и (ii) жидкость, включающую по меньшей мере один спирт (например, и необязательно по меньшей мере один антиоксидант и/или хелатор), воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и в мембране, смоле, материале с покрытием, чипе или кассете, где по меньшей мере один спирт присутствует в количестве, достаточном для снижения повреждения мембраны, смолы, материала с покрытием, чипа и кассеты после воздействия дозы гамма-излучения. В некоторых примерах кассета представляет собой кассету, содержащую смолу (например, любую из иллюстративных смол, описанных в данном документе, или известных из уровня техники). В некоторых вариантах осуществления мембрана, смола, материал с покрытием, чип или кассета включают лиганд, представляющий собой белок A или белок G, ковалентно присоединенный к по меньшей мере одной из их поверхностей или их части. В некоторых вариантах осуществления композиция включает мембрану, смолу, материал с покрытием, чип или кассету и жидкость, включающую по меньшей мере спирт (например, и необязательно по меньшей мере один антиоксидант и/или по меньшей мере один хелатор). Любая из иллюстративных комбинаций и концентраций спиртов, антиоксиданта(антиоксидантов) и/или хелатора(хелаторов), описанных в данном документе, может использоваться в любом из таких способов. Любая из иллюстративных жидкостей, описанных в данном документе, может использоваться в любом из таких способах. В некоторых вариантах осуществления композиция представляет собой смоченный или увлажненный сухой материал. Также в данном документе предусмотрены мембрана, смола, материал с покрытием, чип или кассета с уменьшенной бионагрузкой, полученные с применением любого из способов, описанных в данном документе. В некоторых примерах контейнер представляет собой герметичный контейнер или сосуд для хранения.
Также в данном документе предусмотрены способы получения мембраны, смолы, материала с покрытием, чипа и кассеты с уменьшенной бионагрузкой, которые включают подвергание контейнера, включающего по сути сухую мембрану, смолу, материал с покрытием, чип или кассету (например, мембрану на основе целлюлозы, агарозы или сахара, смолу, материал с покрытием, чип или кассету) воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и в мембране, смоле, материале с покрытием, чипе или кассете. Некоторые примеры дополнительно включают стадию высушивания мембраны, смолы, материала с покрытием, чипа, или кассеты перед стадией подвергания воздействию. В некоторых вариантах осуществления мембрана, смола, материал с покрытием, чип или кассета включают лиганд, представляющий собой белок A или белок G, ковалентно присоединенный к их поверхности. В некоторых примерах кассета представляет собой кассету, содержащую смолу (например, любую из иллюстративных смол, описанных в данном документе, или известных из уровня техники). Также в данном документе предусмотрены мембрана, смола, материал с покрытием, чип или кассета с уменьшенной бионагрузкой, полученные с применением любого из способов, описанных в данном документе.
Настоящее изобретение дополнительно описано в нижеследующих примерах, которые не ограничивают объем настоящего изобретения, описанный в формуле изобретения.
ПРИМЕРЫ
Пример 1. Защитный эффект спирта в отношении подвергнутой воздействию гамма-излучения смолы для аффинной хроматографии
В первом наборе экспериментов MabSelectTM SuReTM (смола для хроматографии на основе связывания с белком A) облучали в трех разных буферах при дозе, составляющей 40-49 кГр, со стандартной интенсивностью дозы:
(1) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита в 50 мМ натрий-фосфатного буфера (излучение 40-49 кГр при интенсивности дозы >7,5 кГр/час);
(2) 2% об./об. бензилового спирта (40-49 кГр при интенсивности дозы >7,5 кГр/час) и
(3) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита, 2% бензилового спирта в 50 мМ натрий-фосфатного буфера - при более высокой дозе излучения (40-49 кГр и более высокой интенсивности дозы >7,5 кГр/час)
После облучения смолами для хроматографии заполняли отдельные хроматографические колонки и проводили несколько циклов с применением материала сбора клеточной культуры и временем удержания, составляющим шесть минут. Значения связывающей способности в отношении проскока записывали для подвергнутых воздействию излучения смол и сравнивали с таковыми для не подвергавшейся воздействию (не подвергавшейся облучению) смолы MabSelectTM SuReTM (хроматография на основе связывания с белком A).
Полученные в данном эксперименте данные показаны на фигуре 1.
Данные на фигуре 1 демонстрируют, что буфер (3) обеспечивает аддитивный эффект комбинации обоих буферов (1) и (2) в отношении сохранения связывающей способности. В данном случае 2% об./об. бензилового спирта в буфере выступают в качестве консерванта и при объединении с буфером (1) также обеспечивает некоторые защитные свойства.
В таблице 1 показано, что все измеренные данные по качеству продукта не отличались в значительной степени в зависимости от применения буферов (1)-(3), и являются подобными ожидаемым значениям, наблюдаемым для не подвергавшейся воздействию (не подвергавшейся облучению) MabSelectTM SuReTM (смолы для хроматографии на основе связывания с белком A).
Таблица 1.
SMM'H+2% BA
SMM'H
2% BA
Эти данные демонстрируют, что облучение смолы для хроматографии в жидкости, включающей спирт (например, бензиловый спирт), обеспечивает защиту смолы от последующей потери связывающей способности в течение множества циклов хроматографии.
Пример 2. Защитный эффект спирта в отношении подвергнутой воздействию гамма-излучения смолы для хроматографии CaptoTM Adhere
Гамма-облучение GE CaptoTM adhere (смола для анионообменной хроматографии с функциональными группами, обеспечивающими мультимодальность) предусматривало облучение в трех разных буферах при дозе, составляющей 28-49 кГр, со стандартной интенсивностью дозы:
(A) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина и 25 мМ маннита в 50 мМ натрий-фосфатного буфера (28-34 кГр, при интенсивности дозы 2-3 кГр/час);
(B) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита в 50 мМ натрий-фосфатного буфера (40-49 кГр, при интенсивности дозы >7,5 кГр/час) и
(C) 25 мМ аскорбата натрия, 25 мМ метионина, 25 мМ гистидина, 25 мМ маннита, 2% об./об. бензилового спирта в 50 мМ натрий-фосфатного буфера (40-49 кГр и более высокой интенсивности дозы >7,5 кГр/час).
После облучения смолами для хроматографии заполняли отдельные хроматографические колонки и проводили несколько циклов с применением материала сбора клеточной культуры и временем удержания, составляющим шесть минут. Значения связывающей способности для проскока записывали для подвергнутых воздействию излучения смол и сравнивали с таковыми для не подвергавшейся воздействию (не подвергавшейся облучению) смолы GE CaptoTM adhere (смола для анионообменной хроматографии с функциональными группами, обеспечивающими мультимодальность).
Данные из данного эксперимента показаны на фигуре 2. Данные на фигуре 2 демонстрируют, что не наблюдалось существенного изменения связывающей способности при облучении смолы в присутствии бензилового спирта, и присутствие бензилового спирта обеспечивает преимущественный эффект в виде повышенного времени хранения перед воздействием гамма-излучения.
В таблице 2 ниже показано, что облучение смолы в присутствии бензилового спирта не приводит к какому-либо значимому влиянию на другие данные по качеству в отношении эффективности смолы при очистке белка.
Таблица 2.
SMM'H с низкой дозой (28-34 кГр)
SMM'H с высокой дозой (40-49 кГр)
SMM'H+2% BA (40-49 кГр)
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Следует понимать, что хотя настоящее изобретение описано в сочетании с его подробным описанием, вышеизложенное описание предназначено для иллюстрации и не ограничивает объем настоящего изобретения, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации находятся в пределах объема нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТЕРИЛЬНАЯ ХРОМАТОГРАФИЧЕСКАЯ СМОЛА И ЕЕ ПРИМЕНЕНИЕ В СПОСОБАХ ПРОИЗВОДСТВА | 2015 |
|
RU2679134C2 |
| СТЕРИЛЬНАЯ ХРОМАТОГРАФИЧЕСКАЯ СМОЛА И ЕЕ ПРИМЕНЕНИЕ В СПОСОБАХ ПРОИЗВОДСТВА | 2015 |
|
RU2805607C2 |
| СПОСОБЫ СТЕРИЛЬНОЙ ХРОМАТОГРАФИИ И ПРОИЗВОДСТВА | 2015 |
|
RU2786078C2 |
| Способы стерильной хроматографии и производства | 2015 |
|
RU2679133C2 |
| ИНТЕГРИРОВАННОЕ НЕПРЕРЫВНОЕ ПРОИЗВОДСТВО ТЕРАПЕВТИЧЕСКИХ БЕЛКОВЫХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ | 2014 |
|
RU2768003C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ В СИСТЕМЕ ПОСЕВНЫХ ФЕРМЕНТЕРОВ (ВАРИАНТЫ) | 2015 |
|
RU2694327C2 |
| ПРОЦЕССЫ КУЛЬТИВИРОВАНИЯ В СИСТЕМЕ ПОСЕВНЫХ ФЕРМЕНТЕРОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2786997C2 |
| ИНТЕГРИРОВАННОЕ НЕПРЕРЫВНОЕ ПРОИЗВОДСТВО ТЕРАПЕВТИЧЕСКИХ БЕЛКОВЫХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ | 2014 |
|
RU2662929C2 |
| ИЗМЕРЕНИЕ АТРИБУТА КАЧЕСТВА ПРОДУКТА | 2020 |
|
RU2825307C1 |
| СПОСОБ ПРОИЗВОДСТВА РЕКОМБИНАНТНОГО ТЕРАПЕВТИЧЕСКОГО БЕЛКА | 2020 |
|
RU2790876C2 |
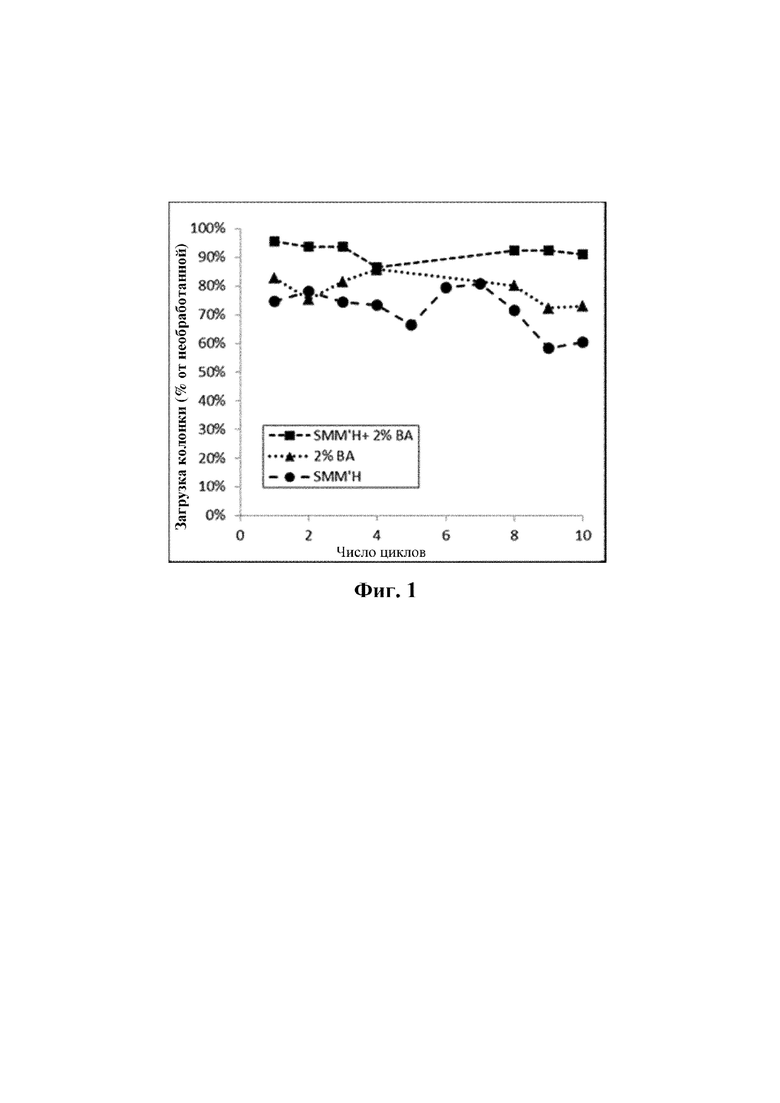
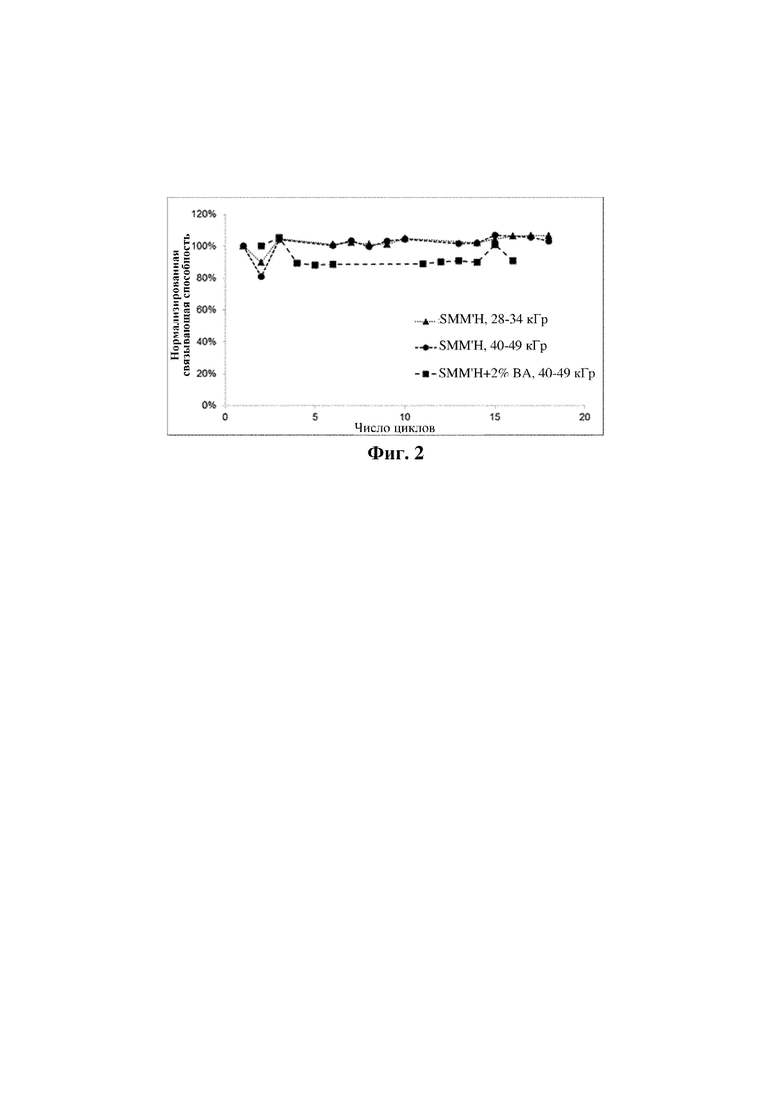
Настоящее изобретение относится к способу уменьшения бионагрузки в смоле для хроматографии, предусматривающему подвергание контейнера, содержащего композицию, содержащую (i) смолу для хроматографии и (ii) жидкость, содержащую бензиловый спирт и по меньшей мере два антиоксиданта, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии, где по меньшей мере два антиоксиданта выбирают из группы, состоящей из: маннита, аскорбата натрия, гистидина и метионина; и бензиловый спирт и по меньшей мере два антиоксиданта присутствуют в количествах, достаточных для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения. Также описана композиция для контейнера подвергающегося воздействию дозы гамма-облучения, содержащая (i) смолу для хроматографии и (ii) жидкость, содержащую бензиловый спирт и по меньшей мере два антиоксиданта, где по меньшей мере два антиоксиданта выбраны из группы, состоящей из: маннита, аскорбата натрия, гистидина и метионина, и бензиловый спирт и по меньшей мере два антиоксиданта присутствуют в количествах, достаточных для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции. Технический результат – предотвращение снижения связывающей способности смолы для хроматографии после воздействия дозы гамма – облучения. 2 н. и 27 з.п. ф-лы, 2 ил., 2 табл., 2 пр.
1. Способ уменьшения бионагрузки в смоле для хроматографии, предусматривающий
подвергание контейнера, содержащего композицию, содержащую (i) смолу для хроматографии и (ii) жидкость, содержащую бензиловый спирт и по меньшей мере два антиоксиданта, воздействию дозы гамма-излучения, достаточной для уменьшения бионагрузки в контейнере и смоле для хроматографии,
где
по меньшей мере два антиоксиданта выбирают из группы, состоящей из: маннита, аскорбата натрия, гистидина и метионина; и
бензиловый спирт и по меньшей мере два антиоксиданта присутствуют в количествах, достаточных для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
2. Способ по п. 1, где контейнер представляет собой сосуд для хранения.
3. Способ по п. 1, где контейнер представляет собой хроматографическую колонку.
4. Способ по п. 1, где контейнер представляет собой заполненную хроматографическую колонку.
5. Способ по п. 1, где композиция представляет собой взвесь осажденной смолы для хроматографии.
6. Способ по любому из пп. 1-5, где концентрация бензилового спирта в жидкости составляет от 0,01% об./об. до 10% об./об.
7. Способ по любому из пп. 1-6, где жидкость дополнительно содержит по меньшей мере один хелатор.
8. Способ по п. 7, где жидкость содержит по меньшей мере один хелатор в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
9. Способ по п. 1, где жидкость содержит маннит, аскорбат натрия, гистидин и метионин.
10. Способ по п. 1, где жидкость содержит
(i) от 30 мМ до 70 мМ метионина и от 30 мМ до 70 мМ гистидина;
(ii) от 10 мМ до 50 мМ метионина, от 10 мМ до 50 мМ гистидина и от 10 мМ до 50 мМ аскорбата натрия; или
(iii) от 5 мМ до 45 мМ аскорбата натрия, от 5 мМ до 45 мМ метионина, от 5 мМ до 45 мМ маннита и от 5 мМ до 45 мМ гистидина.
11. Способ по п. 7, где жидкость содержит по меньшей мере один хелатор, выбранный из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), соли натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарной кислоты (DMSA), металлотионина и дефероксамина.
12. Способ по п. 1, где смола для хроматографии выбрана из группы, состоящей из смолы для анионообменной хроматографии, смолы для катионообменной хроматографии, смолы для аффинной хроматографии, смолы для хроматографии с гидрофобным взаимодействием и смолы для эксклюзионной хроматографии.
13. Способ по п. 12, где композиция содержит смолу для аффинной хроматографии, содержащую белковый лиганд.
14. Способ по п. 13, где белковый лиганд представляет собой белок A.
15. Способ по п. 12, где композиция содержит смолу для анионообменной хроматографии.
16. Способ по п. 15, где смола для анионообменной хроматографии содержит N-бензил-N-метилэтаноламинные группы.
17. Способ по любому из пп. 1-16, где доза составляет от 15 кГр до 45 кГр.
18. Способ по п. 17, где доза составляет от 20 кГр до 30 кГр.
19. Способ по п. 18, где доза составляет от 23 кГр до 27 кГр.
20. Способ по любому из пп. 1-19, где подвергание воздействию проводят при температуре, составляющей от -25°C до 0°C включительно.
21. Способ по любому из пп. 1-19, где подвергание воздействию проводят при температуре, составляющей от 0°C до 25°C включительно.
22. Композиция для контейнера подвергающегося воздействию дозы гамма-облучения, содержащая (i) смолу для хроматографии и (ii) жидкость, содержащую бензиловый спирт и по меньшей мере два антиоксиданта, где по меньшей мере два антиоксиданта выбраны из группы, состоящей из: маннита, аскорбата натрия, гистидина и метионина, и бензиловый спирт и по меньшей мере два антиоксиданта присутствуют в количествах, достаточных для снижения потери связывающей способности смолы для хроматографии при обработке с помощью дозы гамма-излучения, достаточной для уменьшения бионагрузки в композиции.
23. Композиция по п. 22, где композиция представляет собой взвесь осажденной смолы для хроматографии.
24. Композиция по п. 22 или 23, где концентрация бензилового спирта в жидкости составляет от 0,01% об./об. до 10% об./об.
25. Композиция по любому из пп. 22-24, где жидкость дополнительно содержит по меньшей мере один хелатор.
26. Композиция по п. 25, где жидкость дополнительно содержит по меньшей мере один хелатор в количестве, достаточном для снижения потери связывающей способности смолы для хроматографии после воздействия дозы гамма-излучения.
27. Композиция по п. 22, где жидкость содержит маннит, аскорбат натрия, гистидин и метионин.
28. Композиция по п.25 или 26, где жидкость содержит
(i) от 30 мМ до 70 мМ метионина и от 30 мМ до 70 мМ гистидина;
(ii) от 10 мМ до 50 мМ метионина, от 10 мМ до 50 мМ гистидина и от 10 мМ до 50 мМ аскорбата натрия; или
(iii) от 5 мМ до 45 мМ аскорбата натрия, от 5 мМ до 45 мМ метионина, от 5 мМ до 45 мМ маннита и от 5 мМ до 45 мМ гистидина.
29. Композиция по п. 25, где композиция содержит по меньшей мере один хелатор, выбранный из группы, состоящей из этилендиаминтетрауксусной кислоты (EDTA), соли натрия и 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS), димеркаптоянтарной кислоты (DMSA), металлотионина и дефероксамина.
| WO 2015109246 A1, 23.07.2015 | |||
| WO 2015109246 A1, 23.07.2015 | |||
| US 20180154280 A1, 07.06.2018 | |||
| US 20180154280 A1, 07.06.2018 | |||
| WO 2018140887 A1, 02.08.2018 | |||
| WO 2018140887 A1, 02.08.2018 | |||
| WO 2015109151 A1, 23.07.2015 | |||
| WO 2015109151 A1, 23.07.2015 | |||
| WO 2008094237 A1, 07.08.2008 | |||
| Способ обработки полимерного сорбента для хроматографии | 1982 |
|
SU1033181A1 |
Авторы
Даты
2023-12-07—Публикация
2019-08-16—Подача