ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к полимерному конъюгату гексакоординированного комплекса платины, обладающему противоопухолевой активностью, и к лекарственному препарату, содержащему указанный полимерный конъюгат в качестве активного ингредиента.
УРОВЕНЬ ТЕХНИКИ
[0002] Комплексы платины, такие как цисплатин и оксалиплатин, используют в различных онкологических областях в качестве основных лекарств для комбинированной лекарственной противораковой химиотерапии. Однако известно, что комплексы платины вызывают почечные нарушения, тошноту и рвоту, расстройства периферических нервов, угнетение костного мозга и подобные побочные эффекты, и это является проблемой для клинического применения.
[0003] Для уменьшения указанных побочных эффектов и усиления терапевтического эффекта продолжается разработка комплексов платины с применением технологий доставки лекарств (DDS). Примеры DDS препаратов комплексов платины, которые до настоящего времени перешли на стадии клинических испытаний, могут включать, но не ограничиваются ими, координационное соединение диаминоциклогексан-платины (II) с блок-сополимером (NC-4016) (см. патентный документ 1), прицельные липосомы (MBP-426) с инкапсулированным оксалиплатином (см. патентный документ 2), диаминный комплекс N,O-амидомалоната платины (АР5346) (см. патентный документ 3), координационное соединение цисплатина с блок-сополимером (см. патентный документ 4) и липосомный препарат цисплатина (липоплатин) (см. непатентный документ 1). Однако DDS препараты комплексов платины, доступные на рынке, до сих пор отсутствуют.
[0004] В вышеупомянутых DDS препаратах комплексов платины, которые перешли на стадии клинических испытаний, в качестве комплекса платины использованы тетракоординированные комплексы платины; однако описаны также DDS препараты с применением гексакоординированных комплексов платины. Конкретные примеры DDS препарата с применением гексакоординированного комплекса платины могут включать соединение, содержащее наностержни золота в качестве носителя (см. непатентный документ 2), соединение, полученное посредством конъюгирования ингибитора серин/треонинфосфатазы-2А между носителем и гексакоординированным комплексом платины (см. непатентный документ 3), соединение, полученное сшиванием полимера в качестве носителя с использованием гексакоординированного комплекса платины (см. непатентный документ 4), соединение, полученное модификацией мицелл, которые содержат гексакоординированный комплекс платины, фолиевой кислотой (см. непатентный документ 5), соединение, содержащее фоточувствительный гексакоординированный комплекс платины, конъюгированный с носителем (см. непатентный документ 6), соединение, способное образовывать мицеллы посредством конъюгирования гексакоординированного комплекса платины и дауномицина, соответственно, с полимером (см. непатентный документ 7), соединение, способное образовывать мицеллы посредством конъюгирования гексакоординированного комплекса платины и паклитаксела, соответственно, с полимером (см. непатентный документ 8), и соединение, содержащее прицельный противораковый пептид, конъюгированный с гексакоординированным комплексом платины (см. непатентный документ 9).
[0005] Преимущество использования гексакоординированного комплекса платины может заключаться в том, что гексакоординированный комплекс платины можно конъюгировать с носителем DDS способом, отличным от способа с использованием тетракоординированного комплекса платины, с помощью лигандов в аксиальных положениях. Кроме того, известно, что гексакоординированный комплекс платины обычно менее активен по сравнению с тетракоординированным комплексом платины и восстанавливается до тетракоординированного комплекса под действием вещества, обладающего восстановительной активностью в клетках, проявляя противоопухолевую активность. Таким образом, можно ожидать, что побочные эффекты будут снижены при использовании гексакоординированного комплекса (см. непатентный документ 10). Примеры соединения, обладающего восстановительной активностью в клетках, могут включать глутатион и аскорбиновую кислоту, и известно, что концентрации указанных соединений в клетках (включая раковые клетки) выше, чем концентрации таких соединений в крови. Таким образом, полагают, что гексакоординированный комплекс платины селективно превращается в высокоактивный тетракоординированный комплекс платины в восстановительной среде в клетках. В то же время, хотя значения могут варьироваться в зависимости от цитированного документе, внутриклеточная концентрация аскорбиновой кислоты составляет от 300 до 10000 мкМ, а концентрация в крови составляет от 30 до 51 мкМ (см. непатентные документы 4 и 11). Способность комплекса платины высвобождаться из носителя при добавлении аскорбиновой кислоты показана в непатентных документах 4 и 7.
[0006] В отношении восстановительной способности низкомолекулярных гексакоординированных комплексов платины, известно, что восстановительная способность варьируется в зависимости от лигандов в аксиальных положениях. Однако все гексакоординированные комплексы платины, использованные в непатентных документах 2-9, упомянутых выше, представляют собой соединения, в которых любая или обе гидроксильные группы гексакоординированного комплекса платины, который содержит две гидрокисльные группы в качестве лигандов в аксиальных положениях, связаны с носителем сложноэфирной связью, и в этом отношении нет дальнейших разработок.
ДОКУМЕНТЫ ИЗВЕСТНОГО УРОВНЯ ТЕХНИКИ
ПАТЕНТНЫЕ ДОКУМЕНТЫ
[0007] Патентный документ 1: JP 3955992 В2
Патентный документ 2: JP 2008-538105 W
Патентный документ 3: JP 2011-137046 A
Патентный документ 4; JP 5458255 В2
НЕПАТЕНТНЫЕ ДОКУМЕНТЫ
[0008] Непатентный документ 1: ANTICANCER RESEARCH, 2007, 27, 471-476
Непатентный документ 2; ACS Appl. Mater. Interfaces, 2014, 6, 4382-4393
Непатентный документ 3: Macromol. Biosci., 2014, 14, 588-596
Непатентный документ 4: Macromol. Biosci., 2013, 13, 954-965
Непатентный документ 5: Biomacromolecules, 2013, 14, 962-975
Непатентный документ 6: Colloids and Surfaces B: Biointerfaces, 2014, 123, 734-741
Непатентный документ 7: Journal of Controlled Release, 2012, 163, 304-314
Непатентный документ 8: Biomaterials, 2012, 33, 6507-6519
Непатентный документ 9: Journal of Inorganic Biochemistry, 2012, 110, 58-63
Непатентный документ 10: J. Med. Chem., 2007, 50, 3403-3411
Непатентный документ 11; J. Am. Chem. Soc., 2014, 136, 8790-8798
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
ПОСТАВЛЕННАЯ ЗАДАЧА
[0009] DDS препарат комплекса платины, который селективно высвобождает высокоактивный комплекс платины в клетках, имеющих восстановительные условия, как описано выше, и демонстрирует высокую противоопухолевую активность, необходимую для его применения в качестве лекарства, до сих пор не может быть получен, и необходим новый DDS препарат комплекса платины, который можно использовать в клинических сферах. То есть в отношении DDS препаратов, в которых используют гексакоординированные комплексы платины, включая соединения, описанные выше, поскольку отсутствует соединение, используемое клинически, как в случае DDS препаратов тетракоординированных комплексов платины, существует потребность в клинически пригодном DDS препарате гексакоординированного комплекса платины, который высвобождает высокоактивный тетракоординированный комплекс платины в восстановительных условиях в клетках, с помощью особого гексакоординированного комплекса платины и носителя DDS.
РЕШЕНИЕ ЗАДАЧИ
[0010] Авторами настоящего изобретения проведены всесторонние исследования для решения проблем, описанных выше, и в результате ими обнаружено, что полимерное производное гексакоординированного комплекса платины, полученное посредством сложноэфирного связывания, напрямую или через линкер, гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, с карбоксильной группой боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, эффективно высвобождает комплекс платины в восстановительных условиях в клетках и демонстрирует противоопухолевую активность. Таким образом, авторами сделано настоящее изобретение.
[0011] То есть настоящее изобретение относится к следующим пунктам (1)-(16).
[0012] (1) Полимерный конъюгат гексакоординированного комплекса платины, содержащий блок-сополимер, который содержит полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты; и гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, где гексакоординированный комплекс платины прямо или через спейсер связан с карбоксильной группой боковой цепи указанного блок-сополимера.
[0013] (2) Полимерный конъюгат гексакоординированного комплекса платины по п. (1), отличающийся тем, что полимерный конъюгат представлен следующей формулой (I):
[Химическая формула 1]
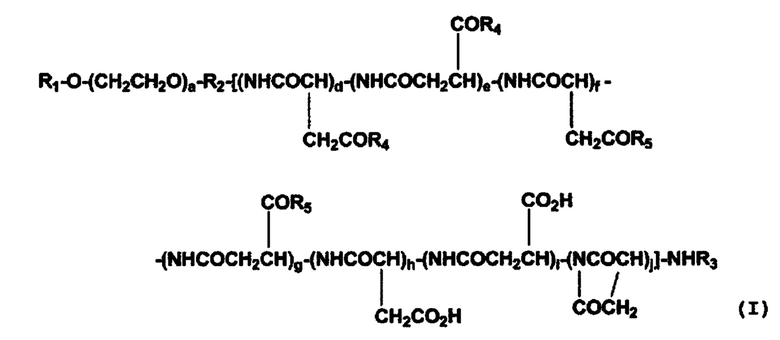
где R1 представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; R2 представляет собой связывающую группу; R3 представляет собой атом водорода или (С1-С6) ацильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, представленной следующей формулой (II);
[Химическая формула 2]

[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, гидроксильной группы, аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR6CONHR7; R6 и R7 могут быть одинаковыми или различными и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; и R8 представляет собой (С1-С10) алкильную группу, которая может содержать заместитель, бензильную группу или остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, заместителя, представленного следующей формулой (III), полученного отщеплением Н от α-аминогруппы производного α-аминокислоты:
[Химическая формула 3]
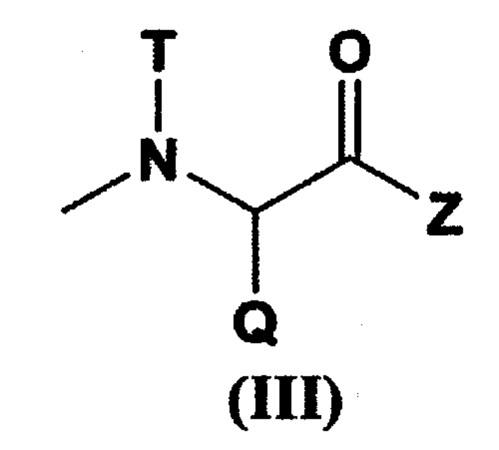
[где Q представляет собой α-аминокислотный остаток боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR12CONHR13; и R12 и R13 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой],
и -NR9CONHR10; R9 и R10 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; а представляет собой целое число от 5 до 11500; каждый d, e, f, g, h, i и j представляет собой целое число от 0 до 200; d+e представляет собой целое число от 1 до 200; d+e+f+g+h+i+j представляет собой целое число от 2 до 200; и порядок связывания различных составных звеньев полиаспарагиновой кислоты является произвольным.
[0014] (3) Полимерный конъюгат гексакоординированного комплекса платины по п. (2), отличающийся тем, что R1 представляет собой (С1-С3) алкильную группу, которая может содержать заместитель; R2 представляет собой (С2-С6) алкиленовую группу; R3 представляет собой (С1-С3) ацильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, состоящей из следующей формулы (IV):
[Химическая формула 4]
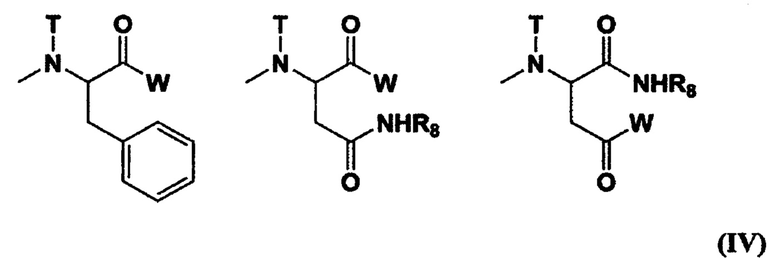
[где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (II), соответственно],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; а представляет собой целое число от 10 до 2000; каждый d, e, f, g, h, i и j представляет собой целое число от 0 до 100;
d+e представляет собой целое число от 1 до 100; и d+e+f+g+h+i+j представляет собой целое число от 4 до 100.
[0015] (4) Полимерный конъюгат гексакоординированного комплекса платины по п. (2) или (3), отличающийся тем, что R1 представляет собой метильную группу; R2 представляет собой гриметиленовую группу; R3 представляет собой ацетильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой заместитель, выбранный из группы, состоящей из остатка, полученного отщеплением Н от аминогруппы бензилового эфира фенилаланина, и -NR9CONHR10; и оба R9 и R10 представляют собой циклогексильную группу или изопропильную группу.
[0016] (5) Полимерный конъюгат гексакоординированного комплекса платины по п. (2) или (3), отличающийся тем, что R1 представляет собой метильную группу; R2 представляет собой триметиленовую группу; R3 представляет собой ацетильную группу; R4 представляет собой заместитель, выбранный из группы, представленной следующей формулой (V):
[Химическая формула 5]

[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и -NR6CONHR7; оба R6 и R7 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой -NR9CONHR10; и оба R9 и R10 представляют собой циклогексильную группу или изопропильную группу.
[0017] (6) Полимерный конъюгат гексакоординированного комплекса платины по п. (1), отличающийся тем, что полимерный конъюгат представлен следующей формулой (VI):
[Химическая формула 6]
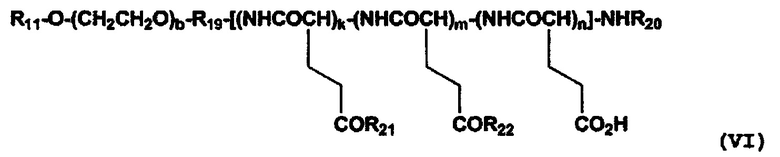
где R11 представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; R19 представляет собой связывающую группу; R20 представляет собой атом водорода или (С1-С6) ацильную группу; R21 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, представленной следующей формулой (VII):
[Химическая формула 7]
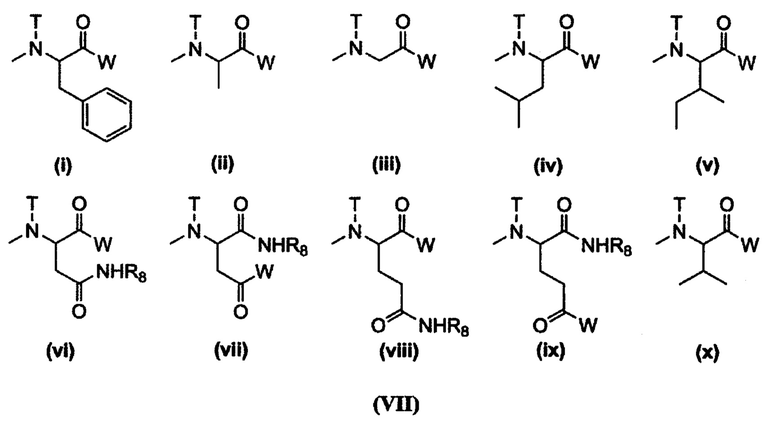
[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, гидроксильной группы, аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR16CONHR17; R16 и R17 могут быть одинаковыми или различными и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; R8 представляет собой (С1-С10) алкильную группу, которая может содержать заместитель, бензильную группу или остаток α-аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, остатка, представленного следующей формулой (VIII), полученного отщеплением Н от α-аминогруппы производного α-аминокислоты:
[Химическая формула 8]
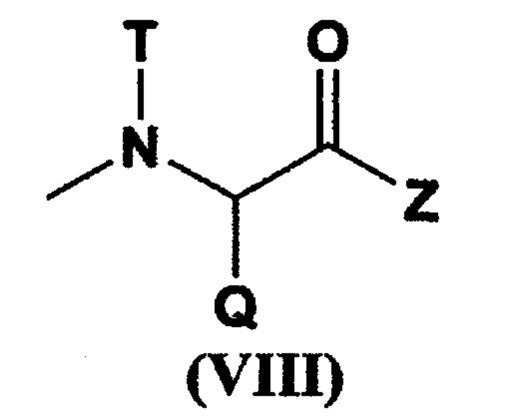
[где Q представляет собой α-аминокислотный остаток боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR24CONHR25; R24 и R25 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой],
и -NR14CONHR15; R14 и R15 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; b представляет собой целое число от 5 до 11500; k представляет собой целое число от 1 до 200; каждый m и n представляет собой целое число от 0 до 200; k+m+n представляет собой целое число от 2 до 200; и порядок связывания различных составных звеньев полиглутаминовой кислоты является произвольным.
[0018] (7) Полимерный конъюгат гексакоординированного комплекса платины по п. (6), отличающийся тем, что R11 представляет собой (С1-С3) алкильную группу, которая может содержать заместитель; R19 представляет собой (С2-С6) алкиленовую группу; R20 представляет собой (С1-С3) ацильную группу; R21 представляет собой остаток гексакоординированного комплекса, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, состоящей из следующей формулы (IX):
[Химическая формула 9]
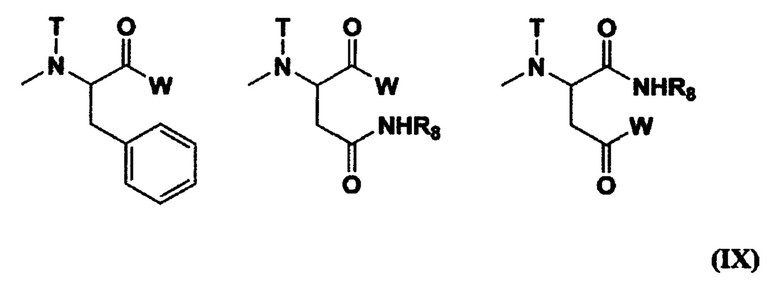
[где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (VII), соответственно],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; b представляет собой целое число от 10 до 2000; k представляет собой целое число от 1 до 100; каждый m и n представляет собой целое число от 0 до 100; и k+m+n представляет собой целое число от 3 до 100.
[0019] (8) Полимерный конъюгат гексакоординированного комплекса платины по п. (6) или (7), отличающийся тем, что R11 представляет собой метильную группу; R19 представляет собой триметиленовую группу; R20 представляет собой ацетильную группу; R21 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой заместитель, выбранный из группы, состоящей из остатка, полученного отщеплением Н от аминогруппы бензилового эфира фенилаланина, и -NR14CONHR15; и оба R14 и R15 представляют собой циклогексильную группу или изопропильную группу.
[0020] (9) Полимерный конъюгат гексакоординированного комплекса платины по п. (6) или (7), отличающийся тем, что R11 представляет собой метильную группу; R19 представляет собой триметиленовую группу; R20 представляет собой ацетильную группу; R21 представляет собой заместитель, выбранный из группы, представленной следующей формулой (X):
[Химическая формула 10]
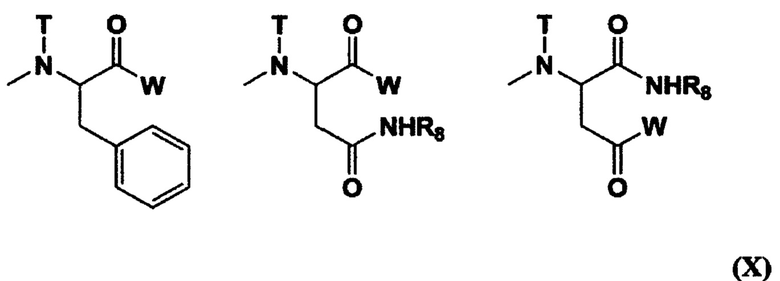
[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и -NR16CONHR17; оба R16 и R17 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой -NR14CONHR15; и оба R14 и R15 представляют собой циклогексильную группу или изопропильную группу.
[0021] (1) Полимерный конъюгат гексакоординированного комплекса платины по любому из пп. (1)-(9), отличающийся тем, что гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, представляет собой гексакоординированный комплекс платины, представленный следующей формулой (XI):
[Химическая формула 11]
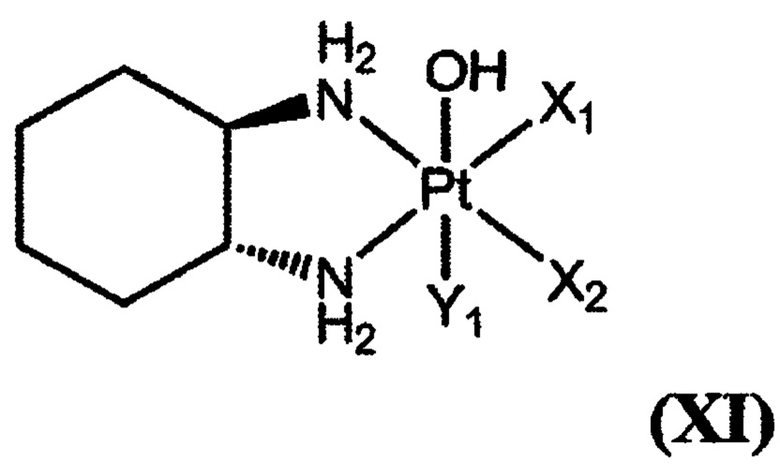
где оба X1 и Х2 представляют собой атом галогена, или они связаны друг с другом с образованием дикарбоксилата, выбранного из группы, состоящей из оксалата, малоната, сукцината и о-фталата; и Y1 представляет собой атом галогена.
[0022] (11) Полимерный конъюгат гексакоординированного комплекса платины по п. (10), отличающийся тем, что Y1 в гексакоординированном комплексе платины представляет собой атом хлора или атом брома; оба X1 и Х2 представляют собой атом хлора или атом брома, или они связаны друг с другом с образованием оксалата.
[0023] (12) Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. (1), в котором карбоксильную группу в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связывают сложноэфирной связью с помощью дегидратирующего конденсирующего агента.
[0024] (13) Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. (1), в котором линкер, с которым посредством сложноэфирной связи связывают гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связан с карбоксильной группой в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты.
[0025] (14) Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. (1), в котором линкер, связанный с карбоксильной группой в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связывают сложноэфирной связью.
[0026] (15) Лекарственное средство, содержащее полимерный конъюгат гексакоординированного комплекса платины по любому из пп. (1)-(11) в качестве активного ингредиента.
[0027]
(16) Противоопухолевый агент, содержащий полимерный конъюгат гексакоординированного комплекса платины по любому из пп. (1)-(11) в качестве активного ингредиента.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
[0028] Предложенный полимерный конъюгат гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, эффективно высвобождает указанный комплекс платины в восстановительных условиях в раковых клетках, а лекарственное средство, содержащее указанный полимерный конъюгат в качестве активного ингредиента, действует как лекарство, которое демонстрирует эффективную противоопухолевую активность с меньшими побочными эффектами, такими как расстройства периферического нерва, при клиническом лечении.
ОПИСАНИЕ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
[0029] Ниже представлено подробное описание настоящего изобретения.
[0030] Предложенный полимерный конъюгат гексакоординированного комплекса платины является таким, что гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, связан сложноэфирной связью, напрямую или через спейсер, с карбоксильной группой боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты, или блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиглутаминовой кислоты.
[0031] Полиэтиленгликолевый структурный фрагмент согласно настоящему изобретению включает полиэтиленгликоль, содержащий два модифицированных конца или один модифицированный конец, и модифицирующие группы на двух концах могут быть одинаковыми или различными. Примеры концевых модифицирующих групп могут включать метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, втор-бутильную группу, трет-бутильную группу, бензильную группу, 4-фенилбутильную группу, диметоксиэтильную группу, диэтоксиэтильную группу, аминоэтильную группу, аминопропильную группу и аминобутильную группу. Среди них предпочтительные примеры могут включать (С1-С3) алкильную группу, которая может содержать заместитель, аминоэтильную группу и аминопропильную группу.
[0032] Молекулярная масса полиэтиленгликолевого структурного фрагмента обычно составляет примерно 200-500000, предпочтительно примерно 300-100000, и более предпочтительно примерно 1000-50000.
[0033] Количество связей фрагмента полиаспарагиновой кислоты или фрагмента полиглутаминовой кислоты в блок-сополимере составляет в среднем от 1 до 300 связей, предпочтительно от 2 до 200 связей и более предпочтительно от 3 до 100 связей на одну молекулу. Количество связей можно определить нейтрализующим титрованием исходного блок-сополимера щелочью.
[0034] Гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, согласно настоящему изобретению не имеет специального ограничения, при условии, что центральный атом металла представляет собой платину (IV), а лиганды в аксиальных положениях представляют собой атом галогена и гидроксильную группу.
[0035] Предложенный полимерный конъюгат гексакоординированного комплекса платины представляет собой соединение, в котором указанная гидроксильная группа связана сложноэфирной связью с карбоксильной группой боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или полиэтиленгликолевый структурный фрагмент и фрагмент полиглутаминовой кислоты, или с карбоксильной группой линкера, который связан с казанной карбоксильной группой.
[0036] Фрагмент полиаспарагиновой кислоты согласно настоящему изобретению может представлять собой полимер α-формы или β-формы, или может представлять собой полимер, в котором смешана α-форма и β-форма, и предпочтительно фрагмент полиаспарагиновой кислоты представляет собой полимер, в котором смешана α-форма и β-форма.
[0037] Фрагмент полиглутаминовой кислоты согласно настоящему изобретению может представлять собой полимер α-формы или γ-формы, или может представлять собой полимер, в котором смешана α-форма и γ-форма, и предпочтительно фрагмент полиглутаминовой кислоты представляет собой полимер α-формы.
[0038] Фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты согласно настоящему изобретению может содержать только D-аминокислоты или только L-аминокислоты, или также допустимо, что D-аминокислоты и L-аминокислоты существуют в произвольной смеси.
[0039] В отношении предложенного блок-сополимера, степень связывания полимерного конъюгата гексакоординированного комплекса платины и блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, не имеет специального ограничения, при условии, что степень связывания является степенью, демонстрирующей эффективность. Однако обычно степень связывания составляет от 1% до 100% и предпочтительно от 5% до 80% от общего количества карбоксильных групп в полимере.
[0040] Атом галогена согласно настоящему изобретению означает атом фтора, атом хлора, атом брома или атом йода.
[0041] (С1-С10) алкильная группа, которая может содержать заместитель, согласно настоящему изобретению представляет собой линейную, разветвленную или циклическую (С1-С10) алкильную группу, и примеры могут включать метильную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, н-гексильную группу, н-октильную группу, н-децильную группу, изопропильную группу, втор-бутильную группу, трет-бутильную группу, 2,2-диметилпропильную группу, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, адамантильную группу, бензильную группу, фенетильную группу, 4-фенилбутильную группу, диметоксиэтильную группу, диэтоксиэтильную группу, диметоксипропильную группу, диэтоксипропильную группу, аминоэтильную группу, диаминоэтильную группу, аминопропильную группу и аминобутильную группу.
[0042] Примеры (С6-С10) арильной группы согласно настоящему изобретению могут включать фенильную группу и нафтильную группу.
[0043] Предложенный полимерный конъюгат гексакоординированного комплекса платины, в котором карбоксильная группа боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты, напрямую или через спейсер связана с гексакоординированным комплексом платины, содержащим атом галогена и гидроксильную группу в аксиальных положениях, представлен, например, формулой (I), изображенной выше.
[0044] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, для R1 в формуле (I), могут включать заместители, примеры которых приведены выше, и среди них предпочтительна (С1-С3) алкильная группа, которая может иметь заместитель, и особенно предпочтительна метильная группа.
Примеры (С6-С10) арильной группы для R1 в формуле (I) могут включать заместители, упомянутые выше в качестве примеров.
[0045] Связывающая группа, представленная как R2 в формуле (I), может представлять собой, например, линейную или разветвленную (С2-С6) алкиленовую группу. Среди всех групп предпочтительной является линейная (С2-С4) алкиленовая группа, и примеры могут включать этиленовую группу, триметиленовую группу и тетраметиленовую группу, и особенно предпочтительна триметиленовая группа.
[0046] Примеры (С1-С6) ацильной группы для R3 в формуле (I) могут включать формильную группу, ацетильную группу, пропионильную группу и пивалоильную группу, и предпочтительна (С1-С3) ацильная группа, и особенно предпочтительна ацетильная группа.
[0047] R4 в формуле (I) представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, как описано выше, или заместитель формулы (II).
[0048] Остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, представляет собой группу, полученную отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, описанного выше.
[0049] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, для W в формуле (II) могут включать заместители, упомянутые выше в качестве примеров, и среди них предпочтительна этильная группа и трет-бутильная группа.
[0050] Примеры (С1-С10) алкокси-группы, которая может содержать фенильную группу, для W в формуле (II) могут включать метокси-группу, этокси-группу, н-пропокси-группу, изопропокси-группу, трет-бутокси-группу, бензилокси-группу, фенетилокси-группу и 4-фенил-1-бутокси-группу.
Примеры (С6-С10) арилокси-группы для W в формуле (II) могут включать фенокси-группу и нафтокси-группу.
[0051] Примеры (С3-С6) циклической алкильной группы для R6 и R7 в -NR6CONHR7 для W в формуле (II) могут включать циклопропильную группу, циклобутильную группу, циклопентильную группу и циклогексильную группу, и среди них предпочтительна циклогексильная группа. Кроме того, примеры (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, могут включать метильную группу, этильную группу, н-пропильную группу, н-бутильную группу, н-пентильную группу, изопропильную группу, диметиламинопропильную группу и 2-морфолиноэтильную группу, и среди них предпочтительна изопропильная группа и диметиламинопропильная группа.
[0052] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, для Т в формуле (II) могут включать заместители, упомянутые выше в качестве примеров, и предпочтительные примеры могут включать метильную группу, этильную группу, н-пропильную группу и бензильную группу.
Примеры (С6-С10) арильной группы для Т в формуле (II) могут включать заместители, упомянутые выше в качестве примеров.
Особенно предпочтительные примеры для Т в формуле (II) могут включать атом водорода, метильную группу, этильную группу и бензильную группу.
[0053] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, для R8 в формуле (II) могут включать заместители, упомянутые выше в качестве примеров, и среди них предпочтительна этильная группа, фенильная группа, бензильная группа и 4-фенил-1-бутильная группа. Аминокислотный остаток, содержащий защищенную карбоксильную группу, не имеет специального ограничения; однако предпочтительные примеры могут включать (С1-С3) алкиловые сложные эфиры, незамещенные амиды, диметиламиды, диэтиламиды и дибензиламиды глицина, аланина, лейцина, изолейцина, валина и фенилаланина.
[0054] Заместитель, представленный формулой (II), для R4 в формуле (I) предпочтительно представляет собой заместитель, представленный формулой (IV) [где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (II), соответственно], и заместитель, представленный формулой (V) [где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и -NR6CONHR7; оба R6 и R7 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащей защищенную карбоновую кислоту], является особенно предпочтительным.
[0055] R5 формулы (I) представляет собой группу, выбранную из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, производного α-аминокислоты, представленного формулой (III) [где Q представляет собой остаток α-аминокислоты в боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу, или (С1-С10) алкильной группы, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR12CONHR13; и R12 и R13 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой], и -NR9CONHR10, и R9 и R10 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой.
[0056] Примеры (С1-С30) алкокси-группы могут включать метокси-группу, этокси-группу, н-бутокси-группу, трет-бутокси-группу, циклопропокси-группу, циклогексилокси-группу и адамантилокси-группу, и среди них предпочтительна этокси-группа и трет-бутокси-группа.
Примеры (С1-С30) аралкилокси-группы могут включать бензилокси-группу, 2-фенилэтокси-группу, 3-фенилпропокси-группу и 4-фенилбутокси-группу, и среди них предпочтительна бензилокси-группа и 4-фенил-1-бутоксигруппа.
Примеры (С6-С10) арилокси-группы могут включать фенокси-группу и нафтокси-группу.
[0057] Примеры (С1-С30) алкиламино-группы, которая может содержать заместитель, и ди(С1-С30) алкиламино-группы, которая может содержать заместитель, включают метиламино-группу, этиламино-группу, бутиламино-группу, изопропиламино-группу, циклогексиламино-группу, бензиламино-группу, 4-фенилбутиламино-группу, диметиламино-группу, диэтиламино-группу, дибутиламино-группу, диизопропиламино-группу, дициклогексиламино-группу, дибензиламино-группу, дифенилбутиламино-группу, N-этилметиламино-группу, N-метилфениламино-группу и N-метил-4-фенилбутиламино-группу, и среди них предпочтительна этиламино-группа, бензиламино-группа и 4-фенилбутиламино-группа.
[0058] Q в производном α-аминокислоты, представленном формулой (III), предпочтительно представляет собой боковую цепь незаменимой аминокислоты, и ее примеры могут включать атом водорода, метильную группу, бензильную группу и изобутильную группу. Бензильная группа, которая представляет собой боковую цепь фенилаланина, особенно предпочтительна. Кроме того, примеры (С1-С10) алкильной группы, которая может содержать заместитель, в Z могут включать заместители, упомянутые выше в качестве примеров, и среди них предпочтительна метильная группа, этильная группа, фенильная группа, бензильная группа и 4-фенил-1-бутильная группа.
Примеры (С1-С10) алкильной группы, которая может содержать заместитель, и (С6-С10) арильной группы для Т могут включать те же группы, которые упомянуты для Т в формуле (II), и предпочтительные группы также являются такими же.
Примеры (С1-С10) алкокси-группы, которая может содержать фенильную группу, для Z могут включать метокси-группу, этокси-группу, н-пропокси-группу, изопропокси-группу, трет-бутокси-группу, бензилокси-группу, фенетилокси-группу и 4-фенилбутокси-группу.
Примеры (С6-С10) арилокси-группы для Z могут включать фенокси-группу и нафтокси-группу.
Если Z представляет собой -NR12CONHR13, примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, для R12 и R13 могут включать такие же группы, как упомянуты выше для R6 и R7 в W в формуле (II), и предпочтительные группы также являются такими же.
Среди них в качестве Z особенно предпочтительна бензилокси-группа.
[0059] Примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, для R9 и R10 в -NR9CONHR10 для R5 в формуле (I) могут включать такие же группы, как упомянуты выше для R6 и R7 в W в формуле (II), и предпочтительные группы также являются такими же.
[0060] Заместители R5 формулы (I) в одной молекуле могут быть одинаковыми или различными, и можно использовать один заместитель или смесь заместителей в молекулах полимерного конъюгата гексакоординированного комплекса платины.
Особенно предпочтительные примеры заместителя для R5 в формуле (I) могут включать остатки, полученные отщеплением Н от аминогрупп бензилового эфира фенилаланина, бензилового эфира N-метилфенилаланина, бензилового эфира N-этилфенилаланина и бензилового эфира N-бензилфенилаланина; и -NR9CONHR10, упомянутый выше.
[0061] Индекс а в формуле (I) представляет собой целое число от 5 до 11500 и предпочтительно а составляет от 10 до 2000.
[0062] Каждый индекс d, е, f, g, h, i и j в формуле (I) представляет собой целое число от 0 до 200, и d+e представляет собой целое число от 1 до 200, причем d+e+f+g+h+i+j представляет собой целое число от 2 до 200. Предпочтительно, каждый d, е, f, g, h, i и j представляет собой целое число от 0 до 100, d+e представляет собой целое число от 1 до 100, f+g представляет собой целое число от 0 до 99, h+i представляет собой целое число от 0 до 30, и d+e+f+g+h+i+j представляет собой целое число от 4 до 100.
В отношении полимерного конъюгата гексакоординированного комплекса платины, представленного формулой (I), порядок связи различных составных звеньев полиаспарагиновой кислоты является произвольным.
[0063] Полимерный конъюгат гексакоординированного комплекса платины согласно настоящему изобретению, в котором гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, напрямую или через спейсер связан с карбоксильной группой боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиглутаминовой кислоты, представлен, например, формулой (VI), описанной выше.
[0064] Примеры (С1-С10) алкильной группы, которая может иметь заместитель для R11 формулы (VI), могут включать заместители, примеры которых приведены выше, и среди них предпочтительна (С1-С3) алкильная группа, которая может иметь заместитель, и особенно предпочтительна метильная группа.
Примеры (С6-С10) арильной группы для R11 в формуле (VI) могут включать заместители, упомянутые выше в качестве примеров.
[0065] Примеры связывающей группы, представленной как R19 в формуле (VI), могут включать такие же группы, как связывающие группы для R2 в формуле (I), и предпочтительные группы являются такими же.
[0066] Примеры (С1-С6) ацильной группы для R20 в формуле (VI) могут включать такие же группы, как (С1-С6) ацильная группа для R3 в формуле (I), и предпочтительные группы являются такими же.
[0067] R21 в формуле (VI) представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель формулы (VII), описанный выше.
Остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, представляет собой группу, полученную отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, описанного выше.
Примеры (С1-С10) алкильной группы, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, и (С6-С10) арилокси-группы для W в формуле (VII), а также примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, для R16 и R17 в -NR16CONHR17 могут включать такие же группы, как (С1-С10) алкильная группа, которая может содержать заместитель, (С1-С10) алкокси-группа, которая может содержать фенильную группу, и (С6-С10) арилокси-группа для W в формуле (II), и (С3-С6) циклическая алкильная группа и (С1-С5) алкильная группа, которая может быть замещена третичной аминогруппой, для R6 и R7 в -NR6CONHR7, соответственно. Предпочтительные группы также являются такими же.
[0068] Примеры (С1-С10) алкильной группы, которая может иметь заместитель, для Т в формуле (VII) могут включать заместители, упомянутые выше в качестве примеров, и предпочтительные примеры могут включать метильную группу, этильную группу, н-пропильную группу и бензильную группу.
Примеры (С6-С10) арильной группы для Т в формуле (VII) могут включать заместители, упомянутые выше в качестве примеров.
Особенно предпочтительные примеры для Т в формуле (VII) могут включать атом водорода, метильную группу, этильную группу и бензильную группу.
[0069] Примеры (С1-С10) алкильной группы, которая может содержать заместитель, и аминокислотного остатка, содержащего защищенную карбоксильную группу, для R8 в формуле (VII) могут включать такие же группы, как (С1-С10) алкильная группа, которая может содержать заместитель, и аминокислотный остаток, содержащий защищенную карбоксильную группу, для R8 в формуле (II), и предпочтительные группы также являются такими же.
[0070] Заместитель, представленный формулой (VII), для R21 в формуле (VI) предпочтительно представляет собой заместитель, представленный формулой (IX) [где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (VII), соответственно], и заместитель, представленный формулой (X) [где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и -NR16CONHR17; оба R16 и R17 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащей защищенную карбоновую кислоту], является особенно предпочтительным.
[0071] R22 в формуле (VI) представляет собой группу, выбранную из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, производного α-аминокислоты, представленного формулой (VIII): [где Q представляет собой α-аминокислотный остаток боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR24CONHR25; и R24 и R25 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой], и -NR14CONHR15. R14 и R15 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой.
[0072] В данном случае примеры (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, и ди(С1-С30) алкиламино-группы, которая может содержать заместитель, могут включать такие же группы, как (С1-С30) алкокси-группа, (С1-С30) аралкилокси-группа, (С6-С10) арилокси-группа, (С1-С30) алкиламино-группа, которая может содержать заместитель, и ди(С1-С30) алкиламино-группа, которая может содержать заместитель, для R5 в формуле (I), соответственно, и предпочтительные группы также являются такими же.
[0073] Примеры Q и Т в производном α-аминокислоты, представленном формулой (VIII), могут включать такие же группы, как Q и Т в производном α-аминокислоты, представленном формулой (III), и предпочтительные группы также являются такими же. Кроме того, примеры (С1-С10) алкильной группы, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, и (С6-С10) арилокси-группы для Z в формуле (VIII), а также (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, для R24 и R25 в -NR24CONHR25, могут включать такие же группы, как (С1-С10) алкильная группа, которая может содержать заместитель, (С1-С10) алкокси-группа, которая может содержать фенильную группу, и (С6-С10) арилокси-группа для Z в формуле (III), а также (С3-С6) циклическая алкильная группа и (С1-С5) алкильная группа, которая может быть замещена третичной аминогруппой, для R12 и R13 в -NR12CONHR13, упомянутом выше, соответственно, и предпочтительные группы также являются такими же.
Среди них в качестве Z особенно предпочтительна бензилокси-группа.
[0074] Примеры (С3-С6) циклической алкильной группы и (С1-С5) алкильной группы, которая может быть замещена третичной аминогруппой, для R14 и R15 в -NR14CONHR15 для R22 в формуле (VI) могут включать такие же группы, как упомянуты выше для R6 и R7 в -NR6CONHR7 для W в формуле (II), и предпочтительные группы также являются такими же.
Заместители R22 формулы (VI) в одной молекуле могут быть одинаковыми или различными, и можно использовать один заместитель или смесь заместителей в молекулах полимерного конъюгата гексакоординированного комплекса платины.
Особенно предпочтительные примеры заместителя для R22 в формуле (VI) включают остатки, полученные отщеплением Н от аминогрупп бензилового эфира фенилаланина, бензилового эфира N-метилфенилаланина, бензилового эфира N-этилфенилаланина и бензилового эфира N-бензилфенилаланина; и -NR14CONHR15, описанный выше.
[0075] Индекс b в формуле (VI) представляет собой целое число от 5 до 11500, и предпочтительно представляет собой целое число от 10 до 2000.
[0076] Индекс k в формуле (VI) представляет собой целое число от 1 до 200, каждый m и n представляет собой целое число от 0 до 200, и k+m+n представляет собой целое число от 2 до 200. Предпочтительно, k представляет собой целое число от 1 до 100, каждый m и n представляет собой целое число от 0 до 100, и k+m+n составляет от 3 до 100. Более предпочтительно, m равен от 0 до 99, и n равен от 0 до 30.
В отношении полимерного конъюгата гексакоординированного комплекса платины, представленного формулой (VI), порядок связи различных составных звеньев полиглутаминовой кислоты является произвольным.
[0077] В отношении гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, согласно настоящему изобретению, предпочтительно можно использовать гексакоординированный комплекс платины, представленный формулой (XI) [где оба X1 и Х2 представляют собой атом галогена или связаны друг с другом с образованием дикарбоксилата, выбранного из группы, состоящей из оксалата, малоната, сукцината и о-фталата; и Y1 представляет собой атом галогена].
[0078] Предпочтительно, что оба X1 и Х2 в формуле (XI) представляют собой атом хлора или атом брома или связаны друг с другом с образованием дикарбоксилата, и Y1 предпочтительно представляет собой атом хлора или атом брома.
[0079] Дикарбоксилат не имеет специального ограничения; однако группа, в которой две карбоксильные группы связаны напрямую, (С1-С6) алкильная группа, содержащая две карбоксильные группы, или (С6-С10) арильная группа, содержащая две карбоксильные группы в орто-положениях, является особенно предпочтительной, и ее примеры могут включать оксалат (i), малонат (ii), сукцинат (iii) и о-фталат (iv), представленные ниже.
[Химическая формула 12]
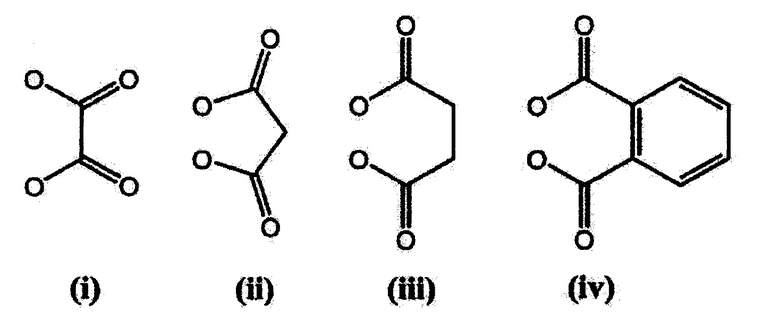
[0080] Пространственная структура циклогексан-1,2-диаминного лиганда, который предпочтительно используют для предложенного гексакоординированного комплекса платины, предпочтительно является транс-конфигурацией 1R и 2R.
[0081] В отношении предложенного гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, особенно предпочтительны соединения следующих формул (XII) и (XIII).
[0082] [Химическая формула 13]
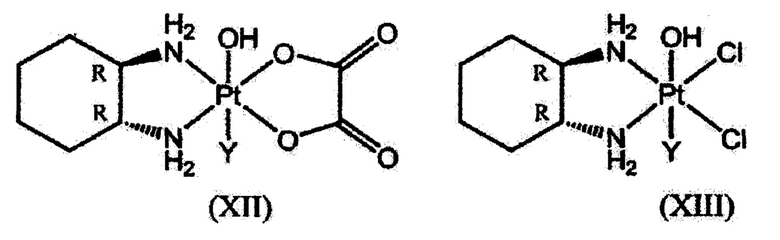
где Y1 представляет собой атом хлора или атом брома.
[0083] Полимерный конъюгат гексакоординированного комплекса платины, представленный формулой (I) или (VI), может образовывать мицеллу в воде, в которой полиэтиленгликолевый структурный фрагмент образует внешнюю оболочку, а фрагмент конъюгата платинового комплекса образует внутреннюю оболочку. В таком случае размер частицы мицеллы, измеренный с помощью анализатора размера частиц/дзета-потенциала (Malvern Instruments Ltd; Zetasizer Nano ZS), составляет от примерно 3 до 100 нм.
[0084] Гексакоординированный комплекс платины, используемый согласно настоящему изобретению, можно получать способом, описанным в таком документе, как непатентный документ 10. То есть используют способ получения гексакоординированного комплекса платины посредством обработки тетракоординированного комплекса платины окислительным агентом с пероксидом водорода или подобным агентом, или посредством окислительного галогенирования в растворителе; или способ получения заданного гексакоординированного комплекса платины в результате участия гексакоординированного комплекса платины в реакции замещения или в реакции конденсации. Пример указанного способа получения описан в следующем эталонном примере.
[0085] Предложенный полимерный конъюгат гексакоординированного комплекса платины получают посредством сложноэфирного связывания карбоксильной группы боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, с гидроксильной группой гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, который можно получать способом получения, описанным выше, с применением дегидратирующего конденсирующего агента или подобного агента в органическом растворителе, и предложенный способ получения также входит в объем настоящего изобретения. Так, например, способ получения включает взаимодействие блок-сополимера полиэтиленгликолевого структурного фрагмента и фрагмента полиаспарагиновой кислоты, который получают со ссылкой на способ, описанный в JP 3268913 В, и гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, в котором все функциональные группы, отличные от группы, которая должна участвовать в реакции, при необходимости защищены, в условиях реакции конденсации с дегидратацией с применением дициклогексилкарбодиимида (DCC), диизопропилкарбодиимида (DIPC), 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорида (WSC), 1-этоксикарбонил-2-этокси-1,2-дигидроксихинолинона (EEDQ), (бензотриазол-1-илокси)трипирролидинофосфония гексафторфосфата (PyBOP), N,N,N',N'-тетраметил-O-(7-азабензотриазол-1-ил)урония гексафторфосфата (HATU) или подобного агента, в растворителе, предпочтительно в апротонном полярном растворителе, таком как N,N-диметилформамид (ДМФА), 1,3-диметил-2-имидазолидинон (DMI) или N-метилпирролидинон (NMP), при температуре от 0°C до 180°C, и предпочтительно при температуре от 5°C до 50°C. Кроме того, во время реакции конденсации также можно использовать вспомогательный реагент, такой как N,N-диметиламинопиридин (DMAP), 1-гидроксибензотриазола гидрат (HOBt⋅H2O) или этил-(гидроксиимино)цианоацетат. После реакции конденсации при необходимости осуществляют снятие защиты, и после стадии стандартного разделения, очистки и т.п. получают полимерный конъюгат гексакоординированного комплекса платины. Предложенный полимерный конъюгат гексакоординированного комплекса платины получают таким же образом, используя блок-сополимер полиэтиленгликолевого структурного фрагмента и фрагмента полиглутаминовой кислоты, ссылаясь на способ, описанный в JP 4745664 В.
[0086] В отношении способа внедрения структуры, представленной формулой (II) или (VII), в R4 или R21 в соединении формулы (I) или (VI), например, указанное соединение можно получать посредством амидного связывания карбоксильной группы боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, с производным аминокислоты, содержащим защищенную карбоновую кислоту, или N-моноалкильной формой производного аминокислоты с помощью дегидратирующего конденсирующего агента, снятия защиты с карбоновой кислоты, с последующим внедрением заместителя, представленного как W в формуле (II) или (VII), с применением дегидратирующего конденсирующего агента.
[0087] В отношении способа внедрения необходимого заместителя в R5 или R22 в соединении формулы (I) или (VI), можно использовать способ активации карбоксильной группы блок-сополимера с помощью способа применения стандартного синтеза сложного эфира или синтеза амида, с последующим взаимодействием соответствующего спирта, соответствующего амина или производного аминокислоты, содержащего защищенную карбоксильную группу, с указанной активированной карбоксильной группой в таком количестве, которое необходимо для образования связей в щелочных условиях; способ активации соответствующего спирта, соответствующего амина, производного аминокислоты, содержащего защищенную карбоксильную группу, или подобного соединения, с последующим взаимодействием полученного активированного соединения с карбоксильной группой блок-сополимера; и подобные способы. После очистки продукта можно повторно активировать не прореагировавшие карбоксильные группы в полимере с помощью аналогичной реакции, а гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, можно конденсировать с повторно активированными карбоксильными группами. Альтернативно, можно повторно привести во взаимодействие другие спирты, амины и подобные соединения с повторно активированными карбоксильными группами, в результате чего синтезируют гибрид различных заместителей R5 или R22, а затем гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, можно конденсировать с указанным гибридом. Кроме того, порядок реакций в указанных способах может быть различным. Способ получения предложенного полимерного конъюгата гексакоординированного комплекса платины не ограничен до указанных способов. Примеры способов получения также описаны в следующих примерах.
[0088] Лекарственное средство, содержащее предложенный полимерный конъюгат гексакоординированного комплекса платины в качестве активного ингредиента, также входит в объем настоящего изобретения. Практическое применение не имеет специального ограничения, при условии, что практическое применение является медицинским применением, в котором предложенный полимерный конъюгат гексакоординированного комплекса платины демонстрирует эффективность; однако предпочтительным является практическое применение в качестве противоопухолевого агента. Указанный полимерный конъюгат в качестве противоопухолевого агента можно использовать в чистом виде или после смешивания с фармацевтически приемлемыми добавками, такими как носитель препарата, вспомогательное вещество, разрыхлитель, связующее вещество, смазывающее вещество, разжижитель, агент покрытия, суспендирующий агент, эмульгатор, стабилизатор, консервант, корригирующее вещество, ароматизатор, разбавители и вспомогательный агент растворения, и указанное лекарственное средство можно вводить перорально или парентерально (системное введение, местное введение или т.п.) в форме таких препаратов, как порошкообразный препарат, гранулированный препарат, таблетка, капсуловидная таблетка, капсула, препарат для инъекций, суппозиторий и мазь. Применение в качестве препарата для инъекций является особенно предпочтительным, и обычно используют, например, воду, физиологический солевой раствор, 5% раствор глюкозы или маннита, водорастворимый органический растворитель (например, глицерин, этанол, диметилсульфоксид, N-метилпирролидон, полиэтиленгликоль, CREMOPHOR или их жидкие смеси) или жидкую смесь воды и водорастворимого органического растворителя.
[0089] Доза вводимого полимерного конъюгата гексакоординированного комплекса платины согласно настоящему изобретению может варьироваться в зависимости от пола, возраста и физиологического состояния пациента, стадии заболевания и т.п.; однако предложенный полимерный конъюгат гексакоординированного комплекса платины обычно вводят парентерально в количестве от 0,01 до 1500 мг/м2, и предпочтительно от 0,1 до 250 мг/м2, в пересчете на активный ингредиент, в сутки для взрослого человека. Введение посредством инъекции осуществляют через вены, артерии, пораженные области (опухолевые области) или т.п.
ПРИМЕРЫ
[0090] Далее настоящее изобретение более подробно описано с помощью примеров. Однако настоящее изобретение не ограничено указанными примерами.
В примерах настоящего изобретения использованы следующие сокращения.
ох: оксалат
R,R-dach: (1R,2R)-циклогександиамин
l-OHP: оксалиплатин
[0091] Содержание лекарственного соединения в представленных примерах определяли, количественно измеряя содержание платины с применением анализатора эмиссионной спектроскопии с индуктивно-связанной плазмой, ICP-OES (Agilent Technologies, Inc.; тип 720-ES), и рассчитывали содержание лекарства на основании содержания платины.
[0092] Размер частиц и дзета-потенциал соединения в представленных примерах определяли с помощью анализатора размера частиц/дзета-потенциала (Malvern Instruments Ltd; Zetasizer Nano ZS).
[0093] Измерение чистоты низкомолекулярного соединения в представленном эталонном примере проводили с помощью высокоэффективной жидкостной хроматографии, используя L-колонку 2 ODS (внутренний диаметр 4,6 мм × 250 мм; приобретенную у компании Chemicals Evaluation and Research Institute, Япония) в качестве колонки; буферный раствор, полученный растворением 2,72 г дигидрофосфата калия, 1,89 г 1-пентансульфоната натрия и 0,5 мл триэтиламина в 2000 мл дистиллированной воды, который доводили до pH 4,3 фосфорной кислотой, в качестве подвижной фазы (А); и метанол в качестве подвижной фазы (В), при следующих аналитических условиях 1 или 2.
[0094] Аналитические условия 1 (изократический анализ):
Концентрация подвижной фазы (В): от 15% (0 мин.) до 15% (20 мин.)
Скорость потока подвижной фазы: 1 мл/мин., обнаружение: 210 нм.
[0095] Аналитические условия 2 (градиентный анализ):
Концентрация подвижной фазы (В): от 15% (0 мин.) до 90% (10 мин.)
Скорость потока подвижной фазы: 1 мл/мин., обнаружение; 210 нм.
[0096] Молекулярную массу низкомолекулярного соединения в представленном эталонном примере измеряли с помощью ЖХ/МС (Shimadzu LCMS-2020), и используя Inertsil ODS-3 (внутренний диаметр 2,1 мм × 100 мм) в качестве колонки; ацетонитрил/муравьиную кислоту (99,9/0,1) в качестве подвижной фазы (А); и воду/муравьиную кислоту (99,9/0,1) в качестве подвижной фазы (В), при следующих аналитических условиях 3 или 4.
[0097] Аналитические условия 3
Градиент
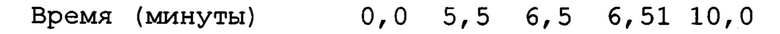

Скорость потока подвижной фазы: 0,3 мл/мин.
[0098] Аналитические условия 4
Градиент
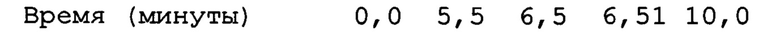
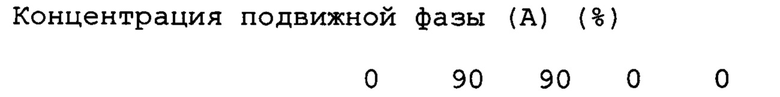
Скорость потока подвижной фазы: 0,3 мл/мин.
[0099] Эталонный пример 1. Синтез транс,цис,цис-[PtCl(OH)(R,R-dach)(ox)]: гексакоординированного комплекса платины, в котором Y в формуле (XII) представляет собой атом хлора
N-Хлорсукцинимид (66,8 мг) растворяли в 14 мл дистиллированной воды, к раствору добавляли жидкость, полученную суспендированием l-OHP (200 мг) в 6 мл дистиллированной воды, и перемешивали смесь в течение 4 часов при комнатной температуре в темноте. После завершения реакции нерастворимые вещества в реакционной жидкости отделяли фильтрованием, а фильтрат концентрировали при пониженном давлении с получением твердого вещества. Полученное таким образом твердое вещество перекристаллизовывали из этанола/воды с получением указанного в заголовке соединения (114 мг). 1H-ЯМР (D2O): δ 2,89-2,72 (2Н, м), 2,15 (2Н, д, J=12,2 Гц), 1,53-1,41 (4Н, м), 0,97-0,90 (2Н, м), МС (ИЭР): 450 (М+1), 451 (М+2), чистота (ВЭЖХ, аналитические условия 2); 99,4%.
[0100] Пример 1. Получение соединения примера 1 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43, с транс,цис,цис-[PtCl(ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ac (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты; примерно 43; 1,98 г), полученный способом, описанным в JP 3268913 В, и гексакоординированный комплекс платины (899 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (70 мл) при 35°C, а затем добавляли к нему диметиламинопиридин (61 мг). Реакционную жидкость доводили до 25°C, а затем к ней добавляли диизопропилкарбодиимид (0,38 мл). По истечении 4 часов добавляли гидрохлорид бензилового эфира фенилаланина (875 мг), диизопропилэтиламин (0,52 мл) и диизопропилкарбодиимид (0,38 мл) и перемешивали полученную смесь в течение 18,5 часа. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (70 мл), этанола (70 мл) и диизопропилового эфира (700 мл), и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Полученный таким образом осадок дополнительно промывали этанолом/диизопропиловым эфиром (1/4 (об./об.); 100 мл) и собирали неочищенный продукт (3,1 г) фильтрованием. Полученный таким образом неочищенный продукт (1,4 г) растворяли в холодной воде (28 мл), а затем пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 14 мл), и элюировали холодной водой (40 мл). Полученную таким образом элюированную фракцию сушили замораживанием с получением указанного в заголовке соединения (1,04 г). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 21,5% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 33 нм, и соединение образовывало мицеллы.
[0101] Пример 2. Получение соединения примера 2 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ox)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 0,93 г), полученный способом, описанным в JP 3268913 В, и гексакоординированный комплекс платины (633 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (40 мл) при 35°С, а затем добавляли к нему диметиламинопиридин (29 мг). Реакционную жидкость доводили до 25°С, затем к ней добавляли диизопропилкарбодиимид (0,43 мл) и перемешивали смесь в течение 5,5 часа. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (40 мл), этанола (40 мл) и диизопропилового эфира (400 мл), и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Полученный таким образом осадок дополнительно промывали этанолом/диизопропиловым эфиром (1/4 (об./об.); 40 мл) и собирали неочищенный продукт (1,5 г) фильтрованием. Полученный таким образом неочищенный продукт (1,45 г) растворяли в холодной воде (29 мл), а затем пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 14,5 мл), и элюировали холодной водой (40 мл). Полученную таким образом элюированную фракцию сушили замораживанием с получением указанного в заголовке соединения (1,25 г). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 31,1% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Однако интенсивность рассеянного излучения была слабой, поэтому предположили, что соединение не образовывало мицеллы.
[0102] Пример 3. Получение соединения примера 3 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 22, с транс,цис,цис-[PtCl (ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (VI) R11=Me (метильная группа), R19 = триметиленовая группа, R20=Ас (ацетильная группа), R21 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R22 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), k+m+n=22, и b=273)
Указанное в заголовке соединение получали таким же способом, как пример 1, используя блок-сополимер (1,18 г), содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 22, который получали способом, описанным в JP 4745664 В, гидрохлорид бензилового эфира фенилаланина (0,31 г), гексакоординированный комплекс платины, полученный в эталонном примере 1 (0,32 г), диизопропилэтиламин (0,18 мл), диметиламинопиридин (21 мг) и диизопропилкарбодиимид (0,27 мл). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 9,9% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 17 нм, и соединение образовывало мицеллы.
[0103] Пример 4. Получение соединения примера 4 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 11, с транс,цис,цис-[PtCl(ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=11, и а=46)
Указанное в заголовке соединение получали таким же способом, как пример 1, используя блок-сополимер (0,61 г), содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 11, который получали способом, описанным в JP 3268913 В, гексакоординированный комплекс платины, полученный в эталонном примере 1 (0,38 г), гидрохлорид бензилового эфира фенилаланина (0,35 г), диизопропилэтиламин (0,21 мл), диметиламинопиридин (24 мг) и диизопропилкарбодиимид (0,29 мл). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 14,8% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял менее 10 нм, и соединение образовывало мицеллы.
[0104] Пример 5. Получение соединения примера 5 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 40000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 41, с транс,цис,цис-[PtCl(ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=41, и а=909)
Указанное в заголовке соединение получали таким же способом, как пример 1, используя блок-сополимер (1,00 г), содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 40000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 41, который получали способом, описанным в JP 3268913 В, гексакоординированный комплекс платины, полученный в эталонном примере 1 (0,17 г), гидрохлорид бензилового эфира фенилаланина (0,19 г), диизопропилэтиламин (0,12 мл), диметиламинопиридин (11 мг) и диизопропилкарбодиимид (0,15 мл). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 7,0% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 80 нм, и соединение образовывало мицеллы.
[0105] Эталонный пример 2. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 3,03 г), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (25 мл) при 35°C и добавляли к нему гидрохлорид бензилового эфира фенилаланина (2,33 г), диизопропилэтиламин (1,42 мл), диметиламинопиридин (93 мг) и диметилформамид (5 мл). Жидкость охлаждали до температуры 25°С, а затем к смеси добавляли диизопропилкарбодиимид (2,34 мл). Смесь перемешивали в течение 18 часов при той же температуре, затем температуру повышали до 30°C и перемешивали смесь 5 часов. Затем к ней добавляли диизопропилкарбодиимид (0.23 мл) и перемешивали в течение 2 часов. После завершения реакции смесь медленно добавляли к смешанному растворителю из этанола (60 мл) и диизопропилового эфира (240 мл) и перемешивали полученную смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Осадок, полученный таким образом, собирали фильтрованием и сушили при пониженном давлении с получением неочищенного продукта (4,6 г). Неочищенный продукт (4,6 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (60 мл) и воды (20 мл), и пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 40 мл), и элюировали 20% водным раствором ацетонитрила (110 мл). Ацетонитрил удаляли упариванием элюированной фракции, полученной таким образом, при пониженном давлении, и сушили полученный остаток замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (4,52 г). Бензил-защищенную форму (3,14 г), полученную таким образом, растворяли в диметилформамиде (63 мл) при 35°С, к нему добавляли водный Pd/C (10%) (688 мг) и перемешивали смесь в течение 22 часов при 33°C в атмосфере водорода. После завершения реакции смесь обрабатывали поглотителем металла (SiliaMetS TAAcOH), фильтровали смесь через целит и медленно, по каплям добавляли фильтрат к смешанному растворителю из гептанов (570 мл) и этилацетата (114 мл). Смесь перемешивали при комнатной температуре, а затем оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Приемы добавления смешанного растворителя из гептанов и этилацетата к осадку, полученному таким образом, и удаления надосадочной жидкости повторяли два раза и собирали осадок фильтрованием, и сушили при пониженном давлении. В результате получали указанное в заголовке соединение (1,8 г).
[0106] Пример 6. Получение соединения примера 6 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, с транс,цис,цис-[PtCl(OH)(R,R-dach)(ox)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер (0,6 г), полученный в эталонном примере 2, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, и гексакоординированный комплекс платины (460 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (30 мл) при 35°С, а затем к раствору добавляли диметиламинопиридин (12 мг). Реакционную жидкость доводили до 30°С, а затем к ней добавляли диизопропилкарбодиимид (0,31 мл). По истечении 21 часа к ней добавляли диизопропилкарбодиимид (0,31 мл). Через 3 часа температуру раствора повышали до 35°С и перемешивали раствор в течение 2 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этанола (43 мл) и диизопропилового эфира (257 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этанол/диизопропиловый эфир (1/6 (об./об.); 150 мл) и собирали неочищенный продукт (807 мг) фильтрованием. Неочищенный продукт (785 мг), полученный таким образом, растворяли в холодной воде (80 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN 20 (НОММ; 3 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (424 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 14,1% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 68 нм, и соединение образовывало мицеллы.
[0107] Пример 7. Получение соединения примера 7 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 10, с транс,цис,цис-[PtCl(ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (VI) R11=Me (метильная группа), R19 = триметиленовая группа, R20=Ас (ацетильная группа), R21 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R22 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), k+m+n=10, и b=46)
Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 10 (степень полимеризации глутаминовой кислоты: примерно 10; 750 мг), полученный способом, описанным в JP 4745664 В, растворяли в диметилформамиде (29 мл) при 35°С, а затем к раствору добавляли гексакоординированный комплекс платины (400 мг), полученный в эталонном примере 1, и диметиламинопиридин (27,6 мг). Реакционную жидкость доводили до 25°С, а затем к ней добавляли диизопропилкарбодиимид (0,17 мл). По истечении 5 часов добавляли гидрохлорид бензилового эфира фенилаланина (390 мг), диизопропилэтиламин (0,38 мл) и диизопропилкарбодиимид (0,34 мл) и перемешивали смесь в течение 17,5 часа. Затем к ней добавляли изопропилкарбодиимид (0,17 мл) и перемешивали полученную смесь еще 5 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (31 мл) и диизопропилового эфира (589 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Затем к остатку добавляли смешанный растворитель из этилацетата (31 мл) и диизопропилового эфира (589 мл) и перемешивали смесь в течение ночи. Затем удаляли надосадочную жидкость, остаток сушили при пониженном давлении с получением неочищенного продукта (1,52 г). Неочищенный продукт, полученный таким образом, растворяли в холодной воде (72 мл), а затем проводили очистку, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG). Раствор, полученный таким образом, сушили замораживанием с получением указанного в заголовке соединения (994 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 14,5% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 9,9 нм, и соединение образовывало мицеллы.
[0108] Пример 8. Получение соединения примера 8 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиглутаминовой кислоты, имеющий степень полимеризации примерно 8, с транс,цис,цис-[PtCl(ОН)(R,R-dach)ox] и бензиловым эфиром фенилаланина; в формуле (VI) R11=Me (метильная группа), R19 = триметиленовая группа, R20=Ас (ацетильная группа), R21 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R22 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), k+m+n=8, и b=46)
Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 8 (степень полимеризации глутаминовой кислоты: примерно 8; 1001 мг), полученный способом, описанным в JP 4745664 В, растворяли в диметилформамиде (36 мл) при 35°C, а затем к раствору добавляли гексакоординированный комплекс платины (461 мг), полученный в эталонном примере 1, и диметиламинопиридин (31,5 мг). Реакционную жидкость доводили до 25°C, а затем к ней добавляли диизопропилкарбодиимид (0,20 мл). По истечении 4,5 часа добавляли гидрохлорид бензилового эфира фенилаланина (450 мг), диизопропилэтиламин (0,44 мл) и диизопропилкарбодиимид (0,40 мл) и перемешивали смесь в течение 16 часов. Затем к ней добавляли диизопропилкарбодиимид (0,20 мл) и перемешивали полученную смесь еще 4 часа. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (38 мл) и диизопропилового эфира (722 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Затем к остатку добавляли смешанный растворитель из этилацетата (38 мл) и диизопропилового эфира (722 мл) и перемешивали смесь в течение ночи. Затем удаляли надосадочную жидкость, остаток сушили при пониженном давлении, а затем получали неочищенный продукт (1,77 г). Неочищенный продукт (1,68 г), полученный таким образом, растворяли в холодной воде (72 мл), а затем проводили очистку, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG). Раствор, полученный таким образом, сушили замораживанием с получением указанного в заголовке соединения (1270 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 14,3% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 9,6 нм, и соединение образовывало мицеллы. [0109] Эталонный пример 3. Синтез транс,цис,цис-[PtCl(ОН)(R,R-dach)Cl2]: гексакоординированного комплекса платины, в котором Y в формуле (XIII) представляет собой атом хлора
N-Хлорсукцинимид (534 мг) растворяли в 50 мл дистиллированной воды и добавляли этот раствор к жидкости, полученной суспендированием Pr(R,R-dach)Cl2 (1,52 г), который получали в соответствии с описанием, представленным в J. Med. Chem., 52, 5474-5484 (2009), в 500 мл тетрагидрофурана. Смесь перемешивали в течение 3 часов при комнатной температуре в темноте. После завершения реакции нерастворимые вещества в реакционной жидкости отделяли фильтрованием, а фильтрат концентрировали при пониженном давлении с получением твердого вещества. Твердое вещество, полученное таким образом, суспендировали в этаноле и снова собирали суспензию фильтрованием. В результате получали требуемый продукт (1,55 г). 1H-ЯМР (ДМСО-d6): δ 7,53-7,29 (2Н, м), 6,89-6,78 (2Н, м), 2,75-2,60 (2Н, м), 2,10-2,00 (2Н, м), 1,47 (2Н, д, J=8,0 Гц), 1,10-0,93 (2Н, м), МС (ИЭР): 433 (М+1), чистота (ВЭЖХ, аналитические условия 2): 98,1%.
[0110] Пример 9. Получение соединения примера 9 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43, с транс,цис,цис-[PtCl(OH)(R,R-dach)Cl2] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 43; 0,577 г), полученный способом, описанным в JP 3268913 В, и гексакоординированный комплекс платины (251 мг), полученный в эталонном примере 3, растворяли в диметилформамиде (20 мл) при 35°C, а затем добавляли к полученному раствору диметиламинопиридин (17,8 мг). Реакционную жидкость доводили до 25°C, а затем к ней добавляли диизопропилкарбодиимид (0,112 мл). По истечении 4,5 часа добавляли гидрохлорид бензилового эфира фенилаланина (254,8 мг), диизопропилэтиламин (0,112 мл) и диизопропилкарбодиимид (0,152 мл) и перемешивали полученную смесь в течение 18,5 часа. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (20 мл), этанола (20 мл) и диизопропилового эфира (160 мл), и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Полученный таким образом осадок дополнительно промывали этанолом/диизопропиловым эфиром (1/4 (об./об.); 50 мл) и собирали неочищенный продукт (0,791 г) фильтрованием. Неочищенный продукт (0,7 г), полученный таким образом, растворяли в 10% водном растворе ацетонитрила (30 мл), а затем проводили очистку, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG). Раствор, полученный таким образом, сушили замораживанием с получением указанного в заголовке соединения (0,68 г). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 6,4% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 87 нм, и соединение образовывало мицеллы.
[0111] Пример 10. Получение соединения примера 10 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, с транс,цис,цис-[PtCl(OH)(R,R-dach)Cl2]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер (360 мг), полученный в эталонном примере 2, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, и гексакоординированный комплекс платины (225 мг), полученный в эталонном примере 3, растворяли в диметилформамиде (5 мл) при 35°С, а затем к раствору добавляли диметиламинопиридин (8 мг). Реакционную жидкость доводили до 30°С, а затем к ней добавляли диизопропилкарбодиимид (0,20 мл). По истечении 23 часов к ней добавляли дополнительное количество диизопропилкарбодиимида (0,10 мл). Через один час температуру раствора повышали до 35°С и перемешивали раствор в течение 2 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (6 мл), этанола (6 мл) и диизопропилового эфира (48 мл), и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К полученному таким образом осадку добавляли дополнительное количество смешанного растворителя из этилацетата (1 мл), этанола (1 мл) и диизопропилового эфира (8 мл) и собирали неочищенный продукт (408 мг) фильтрованием. Неочищенный продукт (399 мг), полученный таким образом, растворяли в 10% водном растворе ацетонитрила (16 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (241 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 8,2% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 17 нм, и соединение образовывало мицеллы.
[0112] Эталонный пример 4. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 12; 2,04 г), который получали способом, описанным в JP 3268913 В, растворяли в диметилформамиде (20 мл) при 35°С. Температуру жидкости понижали до 25°С, а затем к раствору добавляли гидрохлорид бензилового эфира фенилаланина (2,17 г; 1,05 эквивалента относительно карбоксильных групп), диизопропилэтиламин (1,33 мл), диметиламинопиридин (86 мг) и диизопропилкарбодиимид (2,19 мл). Смесь перемешивали в течение 15 часов при той же температуре, а затем температуру повышали до 30°С. К ней добавляли дополнительное количество диизопропилкарбодиимида (0,22 мл) и перемешивали смесь еще 2 часа. После завершения реакции реакционную смесь медленно добавляли к смешанному растворителю из этилацетата (20 мл) и диизопропилового эфира (380 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения в осадок требуемого продукта. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (19/1 (об./об.); 400 мл) и собирали неочищенный продукт (5,4 г) фильтрованием. Неочищенный продукт (5,4 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (18 мл) и воды (12 мл), и пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 70 мл), и элюировали 60% водным раствором ацетонитрила (225 мл). Элюированную фракцию, полученную таким образом, концентрировали при пониженном давлении для удаления ацетонитрила и сушили остаток замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (3,8 г). Бензил-защищенную форму (3,75 г), полученную таким образом, растворяли в диметилформамиде (67 мл), к нему добавляли водный Pd/C (5%) (375 мг) и перемешивали смесь в течение 20 часов при комнатной температуре в атмосфере водорода. После завершения реакции реакционную жидкость обрабатывали поглотителем металла (SiliaMetS ТААсОН), и фильтровали полученную смесь через фильтр из гидрофильного политетрафторэтилена. Затем фильтрат медленно, по каплям добавляли к диизопропиловому эфиру (1340 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К полученному таким образом осадку добавляли диизопропиловый эфир (1005 мл) и собирали осадок фильтрованием, и сушили при пониженном давлении. В результате получали указанное в заголовке соединение (2,5 г).
[0113] Пример 11. Получение соединения примера 11 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, с транс,цис,цис-[PtCl(OH)(R,R-dach)Cl2]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=12, и а=46)
Блок-сополимер, полученный способом, описанным в эталонном примере 4 (0,3 г), содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, и гексакоординированный комплекс платины (303 мг), полученный в эталонном примере 3, растворяли в диметилформамиде (15 мл) при 25°С, а затем к раствору добавляли диметиламинопиридин (17 мг) и диизопропилкарбодиимид (0,22 мл). Смесь перемешивали в течение 15 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (15 мл) и диизопропилового эфира (135 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, добавляли этилацетат/диизопропиловый эфир (1/9 (об./об.)/ 150 мл) и собирали неочищенный продукт (550 мг) фильтрованием. Неочищенный продукт (550 мг), полученный таким образом, растворяли в холодной воде (35 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 3 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (173 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 19,3% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 21 нм, и соединение образовывало мицеллы.
[0114] Эталонный пример 5. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 12; 2,05 г), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (21 мл) при 35°С и добавляли к полученному раствору гидрохлорид бензилового эфира фенилаланина (2,25 г; 1,05 эквивалента относительно карбоксильных групп), диизопропилэтиламин (1,35 мл) и диметиламинопиридин (90 мг). Температуру жидкости понижали до 25°С, а затем к ней добавляли диизопропилкарбодиимид (2,26 мл). Смесь перемешивали в течение 19 часов при той же температуре, а затем температуру повышали до 30°С. Затем к ней добавляли дополнительное количество диизопропилкарбодиимида (0,23 мл) и перемешивали смесь в течение 5,5 часа. После завершения реакции реакционную смесь медленно добавляли к смешанному растворителю из этанола (20 мл) и диизопропилового эфира (380 мл) и перемешивали смесь при комнатной температуре. Надосадочную жидкость удаляли, а остаток сушили при пониженном давлении с получением неочищенного продукта (4,6 г). Неочищенный продукт (4,6 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (18 мл) и воды (12 мл), и пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 69 мл), и элюировали 60% водным раствором ацетонитрила (375 мл). Элюированную фракцию, полученную таким образом, концентрировали при пониженном давлении для удаления ацетонитрила и сушили остаток замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (4,5 г). Бензил-защищенную форму (4,5 г), полученную таким образом, растворяли в смешанном растворителе из диметилформамида (89 мл) и уксусной кислоты (4,5 мл) при 35°С, к раствору добавляли водный Pd/C (10%) (450 мг) и перемешивали смесь при 30°С в течение 67 часов в атмосфере водорода. После завершения реакции реакционную смесь обрабатывали поглотителем металла (SiliaMetS ТААсОН) и фильтровали обработанную реакционную смесь через целит. Фильтрат медленно, по каплям добавляли к диизопропиловому эфиру (1800 мл) и перемешивали смесь при комнатной температуре. Надосадочную жидкость удаляли и два раза повторяли приемы добавления диизопропилового эфира к осадку, полученному таким образом, и удаления надосадочной жидкости. Остаток сушили при пониженном давлении с получением указанного в заголовке соединения (1,7 г).
[0115] Пример 12. Получение соединения примера 12 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]/ в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=12, и а=46)
Блок-сополимер (733 мг), полученный в эталонном примере 5, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, и гексакоординированный комплекс платины (756 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (78 мл) при 35°С, а затем к нему добавляли диметиламинопиридин (21 мг). Реакционную жидкость доводили до 30°С, затем добавляли диизопропилкарбодиимид (0,52 мл) и перемешивали смесь. По истечении 20 часов добавляли дополнительное количество диизопропилкарбодиимида (0,52 мл) и повышали температуру раствора до 35°С, и перемешивали раствор в течение 2 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (78 мл) и диизопропилового эфира (1482 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (1/19 (об./об.); 780 мл) и собирали неочищенный продукт (1,30 г) фильтрованием. Неочищенный продукт (642 мг), полученный таким образом, растворяли в 5% водном растворе ацетонитрила (36 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (389 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 18,1% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 10 нм, и соединение образовывало мицеллы.
[0116] Пример 13. Получение соединения примера 13 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 =структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=12, и а=46)
Блок-сополимер (0,9 г), полученный в эталонном примере 4, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, растворяли в диметилформамиде (39 мл) при 35°С. Реакционную жидкость доводили до 30°С, затем к ней добавляли гексакоординированный комплекс платины (532 мг), полученный в эталонном примере 1, диметиламинопиридин (24 мг) и диизопропилкарбодиимид (0,61 мл), и перемешивали смесь. По истечении 45 часов добавляли дополнительное количество диизопропилкарбодиимида (0,61 мл) и повышали температуру раствора до 35°С, и перемешивали раствор в течение 3 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (39 мл) и диизопропилового эфира (351 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (1/9 (об./об.); 390 мл) и собирали неочищенный продукт (1,27 г) фильтрованием. Неочищенный продукт (1,2 г), полученный таким образом, растворяли в 5% водном растворе ацетонитрила (36 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (863 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 14,4% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 13 нм, и соединение образовывало мицеллы.
[0117] Эталонный пример 6. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 7
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 7; 1,0 г), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (10 мл) при 35°С и добавляли к полученному раствору гидрохлорид бензилового эфира фенилаланина (770 мг), диизопропилэтиламин (0,47 мл) и диметиламинопиридин (31 мг). Температуру жидкости понижали до 25°С, а затем к ней добавляли диизопропилкарбодиимид (0,77 мл). Смесь перемешивали в течение 19 часов при той же температуре, а затем температуру повышали до 30°С. Затем к ней добавляли дополнительное количество диизопропилкарбодиимида (0,08 мл) и перемешивали смесь в течение 4 часа. После завершения реакции реакционную смесь медленно добавляли к смешанному растворителю из этилацетата (10 мл) и диизопропилового эфира (190 мл) и перемешивали смесь при комнатной температуре. Надосадочную жидкость удаляли, а к остатку добавляли этилацетат/диизопропиловый эфир (1/19 (об./об.)/ 100 мл). Смесь перемешивали при комнатной температуре, а затем удаляли надосадочную жидкость. Остаток сушили при пониженном давлении с получением неочищенного продукта (2,0 г). Неочищенный продукт (2,0 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (7,5 мл) и воды (7,5 мл), и пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 30 мл), и элюировали 50% водным раствором ацетонитрила (120 мл). Элюированную фракцию, полученную таким образом, концентрировали при пониженном давлении для удаления ацетонитрила и сушили остаток замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (1,56 г). Бензил-защищенную форму (1,54 г), полученную таким образом, растворяли в диметилформамиде (30 мл) при 35°С и добавляли к нему водный Pd/C (5%) (159 мг). Смесь перемешивали при 30°С в течение 19 часов в атмосфере водорода. Затем смесь обрабатывали активированным углеродом и фильтровали через фильтровальную бумагу. Фильтрат концентрировали при пониженном давлении для удаления растворителя. Затем остаток растворяли в N-метилпирролидоне при 30°С и добавляли к полученному раствору водный Pd/C (5%) (159 мг). Смесь перемешивали при 30°С в течение 14 часов в атмосфере водорода. После завершения реакции реакционную смесь обрабатывали активированным углеродом и фильтровали через фильтровальную бумагу. Фильтрат медленно, по каплям добавляли к диизопропиловому эфиру (500 мл) и перемешивали смесь при комнатной температуре. Надосадочную жидкость удаляли и добавляли диизопропиловый эфир к осадку, полученному таким образом. Надосадочную жидкость удаляли и сушили остаток при пониженном давлении. Остаток, полученный таким образом, растворяли в воде и сушили замораживанием с получением указанного в заголовке соединения (1,0 г).
[0118] Пример 14. Получение соединения примера 14 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 7, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=7, и а=46)
Блок-сополимер (838 мг), полученный в эталонном примере 6, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 7, и гексакоординированный комплекс платины (416 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (31 мл) при 35°С, а затем к раствору добавляли диметиламинопиридин (19 мг). Реакционную жидкость доводили до 30°С, затем добавляли к ней диизопропилкарбодиимид (0,47 мл) и перемешивали смесь. По истечении 45 часов добавляли дополнительное количество диизопропилкарбодиимида (0,47 мл) и повышали температуру раствора до 35°С, и перемешивали смесь в течение 3 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (31 мл) и диизопропилового эфира (585 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (1/19 (об./об.); 308 мл) и перемешивали смесь при комнатной температуре. Затем удаляли надосадочную жидкость, остаток сушили при пониженном давлении с получением неочищенного продукта (1,15 г). Неочищенный продукт (1,15 г), полученный таким образом, растворяли в холодной воде (36 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (774 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 9,3% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 8,8 нм, и соединение образовывало мицеллы. [0119] Эталонный пример 7. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 16; 998 мг), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (12 мл) при 35°С и добавляли к полученному раствору гидрохлорид бензилового эфира фенилаланина (1,27 г; 1,05 эквивалента относительно карбоксильных групп), диизопропилэтиламин (0,77 мл) и диметиламинопиридин (51 мг). Температуру жидкости понижали до 25°С, затем к ней добавляли диизопропилкарбодиимид (1,27 мл) и перемешивали смесь при той же температуре. По истечении 21 часа добавляли дополнительное количество диизопропилкарбодиимида (0,64 мл) и перемешивали в течение 2 часов. После завершения реакции смесь медленно добавляли к смешанному растворителю из этилацетата (23 мл) и диизопропилового эфира (207 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К полученному таким образом осадку добавляли этилацетат/диизопропиловый эфир (1/19 (об./об.); 230 мл) и собирали осадок фильтрованием, и сушили при пониженном давлении. Таким образом, получали неочищенный продукт (2,7 г). Неочищенный продукт (2,7 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (20 мл) и воды (20 мл), и обрабатывали раствор ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 25 мл) в течение 5 часов с охлаждением на льду. Ионообменную смолу отфильтровывали, а затем концентрировали фильтрат при пониженном давлении для удаления ацетонитрила. Затем остаток сушили замораживанием с получением бензил-защищенной формы указанного в заголовке соединения (1,94 г). Бензил-защищенную форму (1,88 г), полученную таким образом, растворяли в N-метилпирролидоне (34 мл) при 35°С. Реакционную жидкость доводили до 30°С, а затем к ней добавляли водный Pd/C (10%) (188 мг). Смесь перемешивали с течение 25 часов при той же температуре в атмосфере водорода. После завершения реакции смесь обрабатывали активированным углеродом и медленно добавляли фильтрат к диизопропиловому эфиру (646 мл). Смесь перемешивали при комнатной температуре, затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, добавляли смешанный растворитель из этилацетата и диизопропилового эфира, и растворяли осадок в воде, и сушили замораживанием. В результате получали указанное в заголовке соединение (1,5 г).
[0120] Пример 15. Получение соединения примера 15 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=16, и а=46)
Блок-сополимер (0,8 г), полученный в эталонном примере 7, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16, растворяли в диметилформамиде (40 мл) при 35°С. Реакционную жидкость доводили до 30°С, затем к реакционной жидкости добавляли гексакоординированный комплекс платины (532 мг), полученный в эталонном примере 1, диметиламинопиридин (24 мг) и диизопропилкарбодиимид (0,61 мл), и перемешивали смесь. По истечении 45 часов добавляли дополнительное количество диизопропилкарбодиимида (0,61 мл) и повышали температуру раствора до 35°С, и перемешивали раствор в течение 3 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (40 мл) и диизопропилового эфира (360 мл) и перемешивали смесь при комнатной температуре. Смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (1/9 (об./об.); 400 мл) и собирали неочищенный продукт (1,2 г) фильтрованием. Неочищенный продукт (1,1 г), полученный таким образом, растворяли в 5% водном растворе ацетонитрила (60 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (719 мг). Содержание лекарственного средства в указанном в заголовке соединении составляло 13,3% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 32 нм, и соединение образовывало мицеллы.
[0121] Эталонный пример 8. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 12; 1,54 г), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (97 мл) при 35°С и добавляли к полученному раствору гидрохлорид бензилового эфира фенилаланина (1,04 г; 0,66 эквивалента относительно карбоксильных групп), диизопропилэтиламин (0,70 мл), диметиламинопиридин (66 мг) и диметилформамид (11 мл). Температуру жидкости понижали до 25°С, а затем к ней добавляли диизопропилкарбодиимид (1,67 мл). Смесь перемешивали в течение 22 часов при той же температуре, а затем к ней добавляли диизопропилкарбодиимид (0,23 мл). Температуру смеси повышали до 35°С и перемешивали смесь в течение 3 часов. После завершения реакции реакционную смесь медленно добавляли к смешанному растворителю из этилацетата (87 мл) и диизопропилового эфира (1,65 л) и перемешивали смесь при комнатной температуре. Затем к ней добавляли диизопропиловый эфир (200 мл), затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Приемы добавления этилацетата/диизопропилового эфира (1/19 (об./об.); 1,08 л) к осадку, полученному таким образом, и удаления надосадочной жидкости повторяли два раза и собирали осадок фильтрованием, и сушили при пониженном давлении. Таким образом, получали неочищенный продукт (2,5 г). Неочищенный продукт (2,5 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (50 мл) и воды (50 мл), и добавляли к полученному раствору ионообменную смолу (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 78 мл). Смесь перемешивали в течение одного часа, ионообменную смолу удаляли фильтрованием при пониженном давлении, а затем фильтрат промывали 50% водным раствором ацетонитрила (30 мл). Фильтрат концентрировали при пониженном давлении для удаления ацетонитрила, а затем сушили замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (2,23 г). Бензил-защищенную форму (2,19 г), полученную таким образом, растворяли в диметилформамиде (44 мл) при 35°С и добавляли к нему водный Pd/C (5%) (219 мг). Смесь перемешивали при 30°С в течение 25 часов в атмосфере водорода. После завершения реакции реакционную смесь обрабатывали активированным углеродом и фильтровали через целит. Фильтрат медленно, по каплям добавляли к смешанному растворителю из этилацетата (44 мл) и диизопропилового эфира (836 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Приемы добавления этилацетата/диизопропилового эфира (1/19 (об./об.); 440 мл) к осадку, полученному таким образом, и удаления надосадочной жидкости повторяли еще два раза и собирали осадок фильтрованием, и сушили при пониженном давлении. В результате получали указанное в заголовке соединение (1,27 г).
[0122] Пример 16. Получение соединения примера 16 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа и остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, d+e+f+g+h+i+j=12, и а=46)
Блок-сополимер (1,27 г), полученный в эталонном примере 8, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, растворяли в диметилформаиде (2 9 мл) при 35°С, а затем к полученному раствору добавляли диметиламинопиридин (27 мг), гексакоординированный комплекс платины (986 мг), полученный в эталонном примере 1, и диметилформамид (44 мл). Реакционную жидкость доводили до 30°С, а затем к ней добавляли диизопропилкарбодиимид (0,68 мл). По истечении 22 часов добавляли дополнительное количество диизопропилкарбодиимида (0,68 мл) и повышали температуру раствора до 35°С, и перемешивали раствор в течение 3 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (73 мл) и диизопропилового эфира (1,39 л) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, добавляли этилацетат/диизопропиловый эфир (1/19 (об./об.); 731 мл) и повторяли удаление надосадочной жидкости еще два раза, и собирали неочищенный продукт (2,23 г) фильтрованием. Неочищенный продукт (2,20 г), полученный таким образом, растворяли в холодной воде (80 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN 20 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (893 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 13,2% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 10 нм, и соединение образовывало мицеллы.
[0123] Эталонный пример 9. Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16
Блок-сополимер метокси-полиэтиленгликоля и полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 16; 1,18 г), полученный способом, описанным в JP 3268913 В, растворяли в диметилформамиде (24 мл) при 35°С и добавляли к полученному раствору гидрохлорид бензилового эфира фенилаланина (942 мг; 0,66 эквивалента относительно карбоксильных групп). Температуру жидкости понижали до 25°С, затем к ней добавляли диизопропилэтиламин (0,64 мл), диметиламинопиридин (60 мг) и диизопропилкарбодиимид (1,51 мл) и перемешивали смесь при той же температуре. По истечении 21 часа к смеси добавляли дополнительное количество диизопропилкарбодиимида (0,61 мл) и повышали температуру раствора до 35°С, и перемешивали смесь в течение 4 часов. После завершения реакции смесь медленно добавляли к смешанному растворителю из этилацетата (12 мл) и диизопропилового эфира (228 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Осадок, полученный таким образом, собирали фильтрованием и сушили при пониженном давлении с получением неочищенного продукта (2,9 г). Неочищенный продукт (2,9 г), полученный таким образом, растворяли в жидкой смеси ацетонитрила (9 мл) и воды (б мл), и пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 40 мл), и элюировали 20% водным раствором ацетонитрила (120 мл). Элюированную фракцию, полученную таким образом, концентрировали при пониженном давлении для удаления ацетонитрила и затем сушили остаток замораживанием. В результате получали бензил-защищенную форму указанного в заголовке соединения (2,09 г). Бензил-защищенную форму (2,0 г), полученную таким образом, растворяли в диметилформамиде (36 мл) при 30°С и добавляли к полученному раствору водный Pd/C (5%) (300 мг). Смесь перемешивали с течение 24 часов при той же температуре в атмосфере водорода. После завершения реакции реакционную смесь обрабатывали активированным углеродом и медленно, по каплям добавляли фильтрат к смешанному растворителю из этилацетата (36 мл) и диизопропилового эфира (684 мл). Смесь перемешивали при комнатной температуре, а затем оставляли стоять до выпадения требуемого продукта в осадок. Надосадочную жидкость удаляли. К осадку, полученному таким образом, добавляли смешанный растворитель из этилацетата и диизопропилового эфира, и собирали осадок фильтрованием, и сушили при пониженном давлении. В результате получали указанное в заголовке соединение (1,5 г).
[0124] Пример 17. Получение соединения примера 17 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16, с транс,цис,цис-[PtCl(OH)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = атом водорода), R5 = изопропиламинокарбонилизопропиламино-группа и остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, d+e+f+g+h+i+j=16, и а=46)
Блок-сополимер (0,9 г), полученный в эталонном примере 9, содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой фенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 16, растворяли в диметилформамиде (34 мл) при 35°С. Реакционную жидкость доводили до 30°С, затем добавляли гексакоординированный комплекс платины (7 65 мг), полученный в эталонном примере 1, диметиламинопиридин (21 мг) и диизопропилкарбодиимид (0,53 мл), и перемешивали смесь. По истечении 45 часов к смеси добавляли дополнительное количество диизопропилкарбодиимида (0,61 мл) и повышали температуру раствора до 35°С, и перемешивали раствор в течение 3 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (34 мл) и диизопропилового эфира (306 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этилацетат/диизопропиловый эфир (1/9 (об./об.); 390 мл) и собирали неочищенный продукт (1,61 г) фильтрованием. Неочищенный продукт (1,5 г), полученный таким образом, растворяли в 5% водном растворе ацетонитрила (60 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN TURBO 15 (НОММ: 10 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (882 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 15,2% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 11 нм, и соединение образовывало мицеллы.
[0125] Пример 18. Получение соединения примера 18 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой 4-фенил-1-бутиловый эфир аспарагиновой кислоты-аланина связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (vii) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа; Т = атом водорода; и R8 = остаток, полученный отщеплением Н от аминогруппы 4-фенил-1-бутилового эфира аланина), R5 = изопропиламинокарбонилизопропиламино-группа, d+е+f+g+h+i+j=43, и а=273)
Блок-сополимер (364 мг), содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой 4-фенил-1-бутиловый эфир аланина связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, который был получен способом, описанным в WO 2010/131675, и гексакоординированный комплекс платины (135 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (10 мл) при 35°С, а затем к нему добавляли диметиламинопиридин (6 мг). Реакционную жидкость доводили до 25°С, а затем к ней добавляли диизопропилкарбодиимид (0,07 мл). По истечении 22 часов добавляли дополнительное количество диизопропилкарбодиимида (0,07 мл) и перемешивали в течение 4 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этанола (20 мл), этилацетата (20 мл) и диизопропилового эфира (160 мл), и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этанол/этилацетат/диизопропиловый эфир (1/1/8 (об./об./об.); 100 мл) и собирали неочищенный продукт (441 мг) фильтрованием. Неочищенный продукт (420 мг), полученный таким образом, растворяли в 30% водном растворе ацетонитрила (30 мл), а затем проводили диализ, используя прибор SPECTRA/POR 6 (НОММ: 3,5 кДа) (Spectrum, Inc.) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (399 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 21,9% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 75 нм, и соединение образовывало мицеллы.
[0126] Пример 19. Получение соединения примера 19 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент, имеющий структуру, в которой этиловый эфир аспарагиновой кислоты-глицина связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, с транс,цис,цис-[PtCl(ОН)(R, R-dach)(ох)] и бензиновым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (vii) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), или изопропиламинокарбонилизопропиламино-группа; Т = атом водорода; и R8 = остаток, полученный отщеплением Н от аминогруппы этилового эфира глицина), R5 = изопропиламинокарбонилизопропиламино-группа и остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=43, и а=273)
Блок-сополимер (510 мг), содержащий метокси-полиэтиленгликолевый фрагмент и фрагмент, имеющий структуру, в которой этиловый эфир аспарагиновой кислоты-глицина связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 43, который был получен способом, описанным в WO 2010/131675, растворяли в диметилформамиде (4,8 мл) при 35°С, а затем к раствору добавляли гексакоординированный комплекс платины (158 мг), полученный в эталонном примере 1, диметиламинопиридин (11 мг) и диметилформамид (4,0 мл). Реакционную жидкость доводили до 25°С, а затем к ней добавляли диизопропилкарбодиимид (0,067 мл). По истечении 4 часов добавляли гидрохлорид бензилового эфира фенилаланина (153 мг), диизопропилэтиламин (0,089 мл) и диизопропилкарбодиимид (0,067 мл) и перемешивали смесь еще 20 часов. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этанола (13 мл) и диизопропилового эфира (75 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. К осадку, полученному таким образом, дополнительно добавляли этанол/диизопропиловый эфир (1/6 (об./об.); 88 мл) и собирали неочищенный продукт (643 мг) фильтрованием. Неочищенный продукт (501 мг), полученный таким образом, растворяли в холодной воде (50 мл), а затем проводили диализ, используя прибор SPECTRA/POR 6 (НОММ: 3,5 кДа) (Spectrum, Inc.) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (440 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 18,1% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 33 нм, и соединение образовывало мицеллы.
[0127] Пример 20. Получение соединения примера 20 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 7, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=7, и а=46)
Блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты, имеющей степень полимеризации примерно 7 (степень полимеризации аспарагиновой кислоты: примерно 7; 50 мг), полученный способом, описанным в JP 3268913 В, и гексакоординированный комплекс платины (22,5 мг), полученный в эталонном примере 1, растворяли в диметилформамиде (2,15 мл) при 35°С, а затем добавляли к полученному раствору диметиламинопиридин (1,53 мг). Реакционную жидкость доводили до 25°С, а затем к ней добавляли диизопропилкарбодиимид (0,009 мл). По истечении 5 часов добавляли гидрохлорид бензилового эфира фенилаланина (22 мг), диизопропилэтиламин (0,013 мл) и диизопропилкарбодиимид (0,009 мл) и перемешивали смесь еще 21 час. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этилацетата (4,3 мл) и диизопропилового эфира (48,7 мл) и перемешивали смесь при комнатной температуре. Затем реакционную смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Осадок, полученный таким образом, дополнительно промывали этилацетатом/диизопропиловым эфиром (1/9 (об./об.); 20 мл) и удаляли надосадочную жидкость. Неочищенный продукт (79 мг), полученный таким образом, растворяли в холодной воде (12 мл), а затем проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN 6 (НОММ: 3 кДа) (Sartorius AG) для удаления низкомолекулярных соединений. Раствор, полученный после очистки, сушили замораживанием с получением указанного в заголовке соединения (48,8 мг). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 12,1% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 5 мг/мл и измеряли размер частиц. Размер частиц составлял 10,4 нм, и соединение образовывало мицеллы.
[0128] Эталонный пример 10. Синтез транс,цис,цис-[Pt(OH)(ОАс)(R,R-dach)(ох)]
0,135 мл 30% водного раствора пероксида водорода добавляли к жидкости, полученной суспендированием l-ОНР (200 мг) в 9 мл уксусной кислоты, и перемешивали смесь в течение 19 часов при комнатной температуре в темноте. После завершения реакции смесь несколько раз концентрировали при пониженном давлении, добавляя в систему воду, и получали твердое вещество. Полученное таким образом твердое вещество перекристаллизовывали из этанола/метанола с получением указанного в заголовке соединения (55 мг), 1Н-ЯМР (D2O): δ 2,78-2,73 (2Н, м), 2,17 (2Н, д, J=9,2 Гц), 1,94 (3Н, с), 1,54-1,44 (4Н, м), 1,20-1,05 (2Н, м), чистота (ВЭЖХ, аналитические условия 1): 94,0%.
[0129] Эталонный пример 11. Синтез транс,цис,цис-[Pt(OCOCH(CH2Ph)N(CH3)-Boc)(Cl)(R,R-dach)(ox)]
Гексакоординированный комплекс платины (300 мг), полученный в эталонном примере 1, N-α-Boc-N-α-метилфенилаланин (223,6 мг, Watanabe Chemical Industries, Ltd.) и HOBt⋅H2O (10,2 мг) суспендировали в диметилформамиде (3 мл) и охлаждали суспензию до 0°С. Затем к ней добавляли диизопропилкарбодиимид (0,155 мл) и перемешивали смесь в течение одного часа. Затем смесь снова доводили до комнатной температуры и оставляли смесь взаимодействовать в течение еще 6 часов. После завершения реакции к смеси добавляли этилацетат и воду и разделяли смесь. Органический слой промывали водой и водным раствором гидрокарбоната натрия, и сушили органический слой над сульфатом натрия. Сульфат натрия отделяли фильтрованием, а фильтрат концентрировали при пониженном давлении. К остатку, полученному таким образом, добавляли диэтиловый эфир, в результате чего в осадок выпадало твердое вещество. Твердое вещество собирали фильтрованием с получением указанного в заголовке соединения (178 мг). ЖХ/МС (аналитические условия 3): время удерживания 5,5 минуты, m/z 711 (М+1).
[0130] Эталонный пример 12. Синтез транс,цис,цис-[Pt(OCOCH(CH2Ph)NH(CH3))(Cl)(R,R-dach)(ox)] трифторацетата
Гексакоординированный комплекс платины (96 мг), полученный в эталонном примере 11, растворяли в дихлорметане (3 мл), раствор охлаждали до 0°С, а затем к нему добавляли трифторуксусную кислоту (1 мл). Смесь перемешивали в течение 15 минут при той же температуре и удаляли растворитель при пониженном давлении. К остатку, полученному таким образом, добавляли диэтиловый эфир, в результате чего в осадок выпадало твердое вещество, которое собирали фильтрованием. В результате получали указанное в заголовке соединение (76 мг). ЖХ/МС (аналитические условия 4): время удерживания 4,1 минуты, m/z 611 (М+1).
[0131] Пример 21. Получение соединения примера 21 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент, имеющий структуру, в которой N-метилфенилаланин связан с боковой цепью полиаспарагиновой кислоты, имеющей степень полимеризации примерно 12, с транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)]; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = структура (i) формулы (II) (W = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, или изопропиламинокарбонилизопропиламино-группа, Т = метильная группа), R5 = изопропиламинокарбонилизопропиламино-группа, d+e+f+g+h+i+j=12, и а=46)
Указанное в заголовке соединение получали таким же способом, как пример 12, используя блок-сополимер, содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 2000, и фрагмент полиаспарагиновой кислоты (степень полимеризации аспарагиновой кислоты: примерно 12; 22 мг), полученный способом, описанным в JP 3268913 В, гексакоординированный комплекс платины (23 мг), полученный в эталонном примере 12, HOBt⋅Н2О (2,4 мг), диизопропилэтиламин (0,016 мл), диметилформамид (0,5 мл) и диизопропилкарбодиимид (0,048 мл). Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 19,0% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 10,5 нм, и соединение образовывало мицеллы.
[0132] Сравнительный пример 1. Получение соединения сравнительного примера 1 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43, с транс,цис,цис-[Pt(ОН)(ОАс)(R,R-dach)(ох)] и бензиловым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+е+f+g+h+i+j=43, и а=273)
Указанное в заголовке соединение получали таким же способом, как пример 1, используя транс,цис,цис-[Pt(ОН)(ОАс)(R,R-dach)(ох)], который представлял собой гексакоординированный комплекс платины, полученный в эталонном примере 10, содержащий ацетокси-группу и гидроксильную группу в аксиальных положениях, и который использовали вместо транс,цис,цис-[PtCl(ОН)(R,R-dach)(ох)] примера 1. Содержание лекарственного средства в указанном в заголовке соединении составляло 20,2% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 15 нм, и соединение образовывало мицеллы.
[0133] Эталонный пример 13. Синтез транс,цис,цис-[Pt(ОН)2(R,R-dach)(ох)]
2,58 мл 30% водного раствора пероксида водорода добавляли к жидкости, полученной суспендированием l-ОНР (900 мг) в 12 мл дистиллированной воды, и перемешивали смесь в течение 20,5 часа при комнатной температуре в темноте. После завершения реакции реакционную смесь несколько раз концентрировали при пониженном давлении, добавляя в систему воду, и получали твердое вещество. Полученное таким образом твердое вещество перекристаллизовывали из воды с получением указанного в заголовке соединения (422 мг). 1H-ЯМР (D2O): δ 2,74-2,72 (2Н, м), 2,17 (2Н, д, J=12,8 Гц), 1,54-1,45 (4Н, м), 1,18-1,12 (2Н, м), чистота (ВЭЖХ, аналитические условия 1): >98,0%.
[0134] Сравнительный пример 2. Получение соединения сравнительного примера 2 (конъюгата блок-сополимера, содержащего метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиаспарагиновой кислоты, имеющий степень полимеризации примерно 43, с транс,цис,цис-[Pt(ОН)2(R,R-dach)(ох)] и бензиновым эфиром фенилаланина; в формуле (I) R1=Me (метильная группа), R2 = триметиленовая группа, R3=Ас (ацетильная группа), R4 = остаток, полученный отщеплением Н от гидроксильной группы гексакоординированного комплекса платины, R5 = изопропиламинокарбонилизопропиламино-группа или остаток, полученный отщеплением Н от аминогруппы бензилового эфира фенилаланина (Т = атом водорода), d+e+f+g+h+i+j=43, и а=273)
Указанное в заголовке соединение получали таким же способом, как пример 1, используя транс,цис,цис-[Pt(ОН)2(R,R-dach)(ох)], который представлял собой гексакоординированный комплекс платины, полученный в эталонном примере 13, в котором оба лиганда в аксиальных положениях представляли собой гидроксильную группу, вместо транс,цис,цис-[PtCl(ОН) (R,R-dach)(ох)] примера 1. Содержание лекарственного средства в указанном в заголовке соединении составляло 12,5% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 44 нм, и соединение образовывало мицеллы.
[0135] Сравнительный пример 3. Получение соединения сравнительного примера 3 (полимерного конъюгата, в котором DACH-платин (Pt(R,R-dach)Cl2), который представляет собой тетракоординированный комплекс платины, координационно связан с блок-сополимером, содержащим метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 37)
Блок-сополимер (0,7 г), содержащий метокси-полиэтиленгликолевый фрагмент, имеющий молекулярную массу 12000, и фрагмент полиглутаминовой кислоты, имеющей степень полимеризации примерно 37, который получали способом, описанным в JP 4745664 В, и гидрохлорид бензилового эфира фенилаланина (243 мг) растворяли в диметилформамиде (18 мл) при 35°С. Затем к раствору добавляли 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (260 мг) и диизопропилэтиламин (0,15 мл) и перемешивали смесь в течение 17 часов при той же температуре. После завершения реакции реакционную жидкость медленно добавляли к смешанному растворителю из этанола (36 мл) и диизопропилового эфира (144 мл) и перемешивали смесь при комнатной температуре. Затем смесь оставляли стоять до выпадения требуемого продукта в осадок, и удаляли надосадочную жидкость. Осадок, полученный таким образом, собирали фильтрованием и сушили при пониженном давлении с получением неочищенного продукта (0,8 г) полимера, который использовали в качестве носителя. Неочищенный продукт (0,8 г), полученный таким образом, растворяли в 50% водном растворе ацетонитрила (25 мл), а затем пропускали раствор через колонку, упакованную ионообменной смолой (DOWEX 50 (Н+) производства компании The Dow Chemical Company; 35 мл), и элюировали 50% водным раствором ацетонитрила (17 мл) и 50% водным раствором изопропилового спирта. Элюированную фракцию, полученную таким образом, концентрировали при пониженном давлении и удаляли органический растворитель. Остаток сушили замораживанием с получением полимерного носителя (0,6 г). Полимерный носитель (0,5 г), полученный таким образом, растворяли в 50% водном растворе изопропилового спирта (22 мл), затем к нему добавляли 0,56 н. водный раствор гидроксида натрия (0,9 мл) и перемешивали смесь в течение 1,5 часа при 40°С. Затем к ней добавляли водный раствор комплекса [Pt(R,R-dach)(ОН2)2](NO3)2 (10,75 мМ; 24 мл), полученного из K2PtCl4 способом, описанным в JP 1989-313488, и перемешивали смесь в течение 19,5 часа. После завершения реакции низкомолекулярные компоненты удаляли, используя диализную мембрану (НОММ = 14 кДа), затем к диализированному продукту добавляли мальтозу (2,0 г) и сушили полученную смесь замораживанием. Содержание лекарственного средства в указанном в заголовке соединении, полученном таким образом, составляло 2,9% (массовая доля). Затем указанное в заголовке соединение растворяли в воде до концентрации 1 мг/мл и измеряли размер частиц. Размер частиц составлял 44 нм, и соединение образовывало мицеллы.
[0136] Испытательный пример 1. Испытание способности соединения примера 1, соединения сравнительного примера 1 и соединения сравнительного примера 2 высвобождать комплекс платины в восстановительных условиях
Соединение примера 1, соединение сравнительного примера 1 и соединение сравнительного примера 2, соответственно, растворяли в 10 мМ фосфатном буферном растворе, содержащем аскорбиновую кислоту в концентрации 600 мкМ, при концентрации соединения 1 мг/мл, и встряхивали раствор при 37°С в темноте. Через некоторое время раствор собирали и проводили центрифужную ультрафильтрацию, используя прибор VIVASPIN 500 (НОММ: 5 кДа) (Sartorius AG). Количественно измеряли содержание платины в фильтрате, определяя способность к высвобождению платинового комплекса из полимерного конъюгата. Для сравнения испытывали также способность к высвобождению соединения примера 1 в том случае, в котором указанное соединение не растворяли в 10 мМ фосфатном буферном растворе, без добавления аскорбиновой кислоты. Затем количественно определяли содержание платины в фильтрате с помощью ICP-OES, и процентное количество высвобожденной платины относительно содержания платины в исходном растворе, взятого за 100%, представлено в таблице 1.

[0138] В отношении соединения примера 1, через 2 часа после начала испытания в восстановительных условиях, созданных добавлением аскорбиновой кислоты, наблюдали высвобождение 76,4% комплекса платины, связанного с полимером. В то же время, в отношении соединения сравнительного примера 1 и соединения сравнительного примера 2, высвобождение комплекса платины, связанного с полимером, почти не наблюдали даже через 6 часов после начала испытания, и стало понятно, что комплекс платины не будет высвобождаться даже в восстановительных условиях. Кроме того, в отношении соединения примера 1, поскольку степень высвобождения комплекса платины через 2 часа после начала испытания без добавления аскорбиновой кислоты составляла 17,8%, и степень высвобождения в условиях, созданных с добавлением аскорбиновой кислоты, как описано выше, составляла 16,4%, подтвержден тот факт, что высвобождение комплекса платины ускоряется в восстановительных условиях. На основании вышеуказанного было установлено, что выбирая гексакоординированный комплекс платины, конъюгированный с блок-сополимером, содержащим полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, можно получать полимерный конъюгат гексакоординированного комплекса платины, который высвобождает комплекс платины в восстановительных условиях.
[0139] Испытательный пример 2. Испытание способности соединения примера 1, соединения сравнительного примера 3 высвобождать комплекс платины в восстановительных условиях
Испытание высвобождения для соединения сравнительного примера 3, представляющего собой тетракоординированный комплекс платины, имеющий другой способ связывания, чем соединение примера 1, представляющее собой гексакоординированный комплекс платины, проводили таким же образом, как в испытательном примере 1. Результаты представлены в таблице 2.
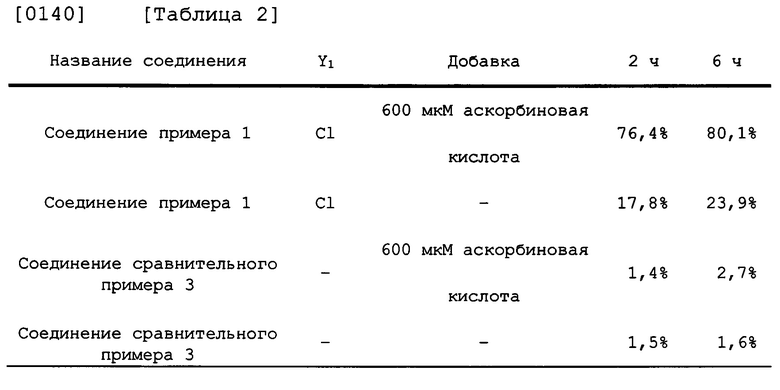
[0141] В отношении соединения сравнительного примера 3, высвобождение комплекса платины почти не наблюдали даже через 24 часа после начала испытания в восстановительных условиях, созданных добавлением аскорбиновой кислоты. Такое же испытание проводили также в условиях без добавления аскорбиновой кислоты; однако степень высвобождения была почти такой же, как степень высвобождения в условиях с добавлением аскорбиновой кислоты, и добавление аскорбиновой кислоты не оказывало какого-либо заметного влияния. Таким образом, очевидно, что если тетракоординированный комплекс платины, использованный в патентном документе 1 и т.п., конъюгирован с полимером посредством обмена лигандами, способность к высвобождению является низкой.
[0142] Испытательный пример 3. Противоопухолевый эффект у мышей с трансплантированным раком желудка 4-1ST человека
[0143] <Животные и трансплантированная опухоль>
Рак желудка 4-1ST человека подкожно инокулировали мышам BALB/cA-nu/nu (далее «голым» мышам). Рак желудка 4-1ST человека приобретали у Центрального института экспериментальных животных (Central Institute for Experimental Animals).
[0144] <Противоопухолевое испытание 1>
Рак желудка 4-1ST человека подкожно собирали из «голых» мышей и разрезали на блоки с размером каждой стороны примерно 3 мм. Блоки опухоли, полученные таким образом, подкожно трансплантировали в спинку «голых» мышей с помощью троакара. На 15 день после трансплантации, когда средний объем опухоли достигал примерно 100-200 мм3, через хвостовую вену вводили различные лекарства. Ниже описано применение и дозы (в пересчете на лекарство) различных введенных лекарств. В отношении соединения примера 1, соединение растворяли в 5% растворе глюкозы для инъекций и вводили полученный раствор однократно в дозе 25 мг/кг или 12,5 мг/кг. В отношении соединения примера 2, соединение растворяли в 5% растворе глюкозы для инъекций и вводили полученный раствор однократно в дозе 25 мг/кг или 12,5 мг/кг. В отношении соединения примера 3, соединение растворяли в 5% растворе глюкозы для инъекций и вводили полученный раствор однократно в дозе 20 мг/кг или 10 мг/кг. В отношении соединения примера 4, соединение растворяли в 5% растворе глюкозы для инъекций и вводили полученный раствор однократно в дозе 20 мг/кг или 10 мг/кг. В отношении соединения примера 5, соединение растворяли в 5% растворе глюкозы для инъекций и вводили полученный раствор однократно в дозе 20 мг/кг или 10 мг/кг. В качестве контрольного лекарства однократно вводили l-ОНР в дозе 20 мг/кг, и однократно вводили цисплатин в дозе 10 мг/кг. В отношении доз введенного l-ОНР и цисплатина и высоких доз введенных соединений различных примеров, использовали максимально переносимые дозы (MTD дозы) для всех соединений. После введения с помощью штангенциркуля измеряли размер большой оси (L) и малой оси (W) опухоли в зависимости от времени, и рассчитывали объем опухоли (L×W×W×0,5). Испытание проводили, используя по четыре животных на группу для всех групп без лечения, а также для всех групп, которым вводили различные лекарства. В течение периода от начала введения до 21 дня после введения по приведенной ниже формуле рассчитывали относительный объем опухоли (Т/С (%)) для каждой группы с лечением в сравнении с относительным объемом опухоли в группе без лечения, взятым за 100, в качестве показателя противоопухолевого эффекта. Значения Т/С (%) в группах, которым вводили различные лекарства, представлены в таблице 3.
Формула: Т/С (%) = Относительный объем опухоли в группе с лечением/относительный объем опухоли в группе без лечения × 100
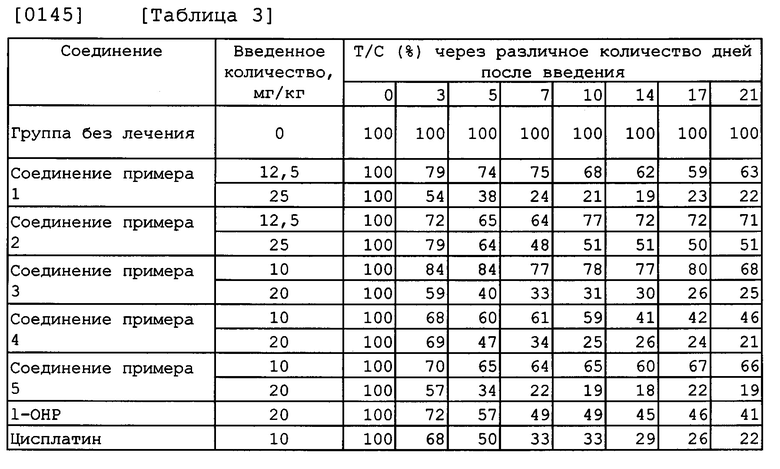
[0146] Соединения всех примеров, за исключением соединения примера 2, демонстрировали более высокий противоопухолевый эффект, по сравнению с l-ОНР. В частности, в отношении соединения примера 4, такой противоопухолевый эффект, как для l-ОНР, сохранялся даже при низкой дозе. Соединение примера 2 демонстрировало такой же противоопухолевый эффект, как l-ОНР. На основании результатов, описанных выше, очевидно, что полимерный конъюгат гексакоординированного комплекса платины согласно настоящему изобретению обладает противоопухолевым эффектом, равным или превосходящим противоопухолевый эффект l-ОНР.
[0147] <Противоопухолевое испытание 2>
Рак желудка 4-1ST человека подкожно собирали из «голых» мышей и разрезали на блоки с размером каждой стороны примерно 3 мм. Блоки опухоли, полученные таким образом, подкожно трансплантировали в спинку «голых» мышей с помощью троакара. На 17 день после трансплантации, когда средний объем опухоли достигал примерно 100-200 мм3, через хвостовую вену вводили различные лекарства. Ниже описано применение и дозы (в пересчете на лекарство) различных введенных лекарств. В отношении соединения примера 1, соединение растворяли в 5% растворе глюкозы для инъекций и вводили раствор однократно в дозе 15 мг/кг или 7,5 мг/кг. В отношении соединения примера 12, соединение растворяли в 5% растворе глюкозы для инъекций и вводили раствор однократно в дозе 30 мг/кг или 15 мг/кг. В качестве контрольного лекарства однократно вводили l-ОНР в дозе 18 мг/кг, и однократно вводили цисплатин в дозе 10 мг/кг. В отношении доз введенного l-ОНР и цисплатина и высоких доз введенных соединений различных примеров, использовали максимально переносимые дозы (MTD дозы) для всех соединений. После введения с помощью штангенциркуля измеряли размер большой оси (L) и малой оси (W) опухоли в зависимости от времени, и рассчитывали объем опухоли (L×W×W×0,5). Испытание проводили, используя по четыре животных на группу для всех групп без лечения, а также для всех групп, которым вводили различные лекарства. В течение периода от начала введения до 21 дня после введения по приведенной ниже формуле рассчитывали относительный объем опухоли (Т/С (%)) для каждой группы с лечением в сравнении с относительным объемом опухоли в группе без лечения, взятым за 100, в качестве показателя противоопухолевого эффекта. Значения Т/С (%) в группах, которым вводили различные лекарства, представлены в таблице 4.
Формула: Т/С (%) = Относительный объем опухоли в группе с лечением/относительный объем опухоли в группе без лечения × 100
После введения измеряли массу тела мышей в зависимости от времени. В течение периода от начала введения до 21 дня после введения рассчитывали изменения относительной массы тела в сравнении с массой тела в день начала введения, взятой за 1, и результаты представлены в таблице 5.
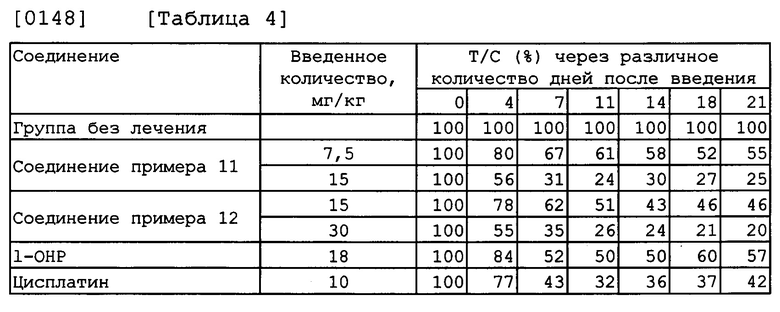
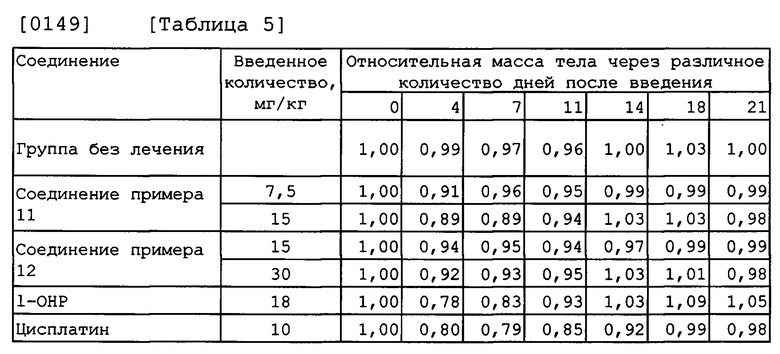
[0150] Соединение примера 11 и соединение примера 12 демонстрировали более сильный противоопухолевый эффект, чем l-ОНР и цисплатин. В то же время снижение массы для соединения примера 11 и соединения примера 12 было низким, по сравнению с l-ОНР и цисплатином на 4 день после введения.
[0151] <Противоопухолевое испытание 3>
Рак желудка 4-1ST человека подкожно собирали из «голых» мышей и разрезали на блоки с размером каждой стороны примерно 3 мм. Блоки опухоли, полученные таким образом, подкожно трансплантировали в спинку «голых» мышей с помощью троакара. На 20 день после трансплантации, когда средний объем опухоли достигал примерно 100-200 мм3, через хвостовую вену вводили различные лекарства. Ниже описано применение и дозы (в пересчете на лекарство) различных введенных лекарств. В отношении соединения примера 7, соединение растворяли в 5% растворе глюкозы для инъекций и вводили раствор однократно в дозе 15 мг/кг или 7,5 мг/кг. В отношении соединения примера 16, соединение растворяли в 5% растворе глюкозы для инъекций и вводили раствор однократно в дозе 30 мг/кг или 15 мг/кг. В качестве контрольного лекарства однократно вводили l-ОНР в дозе 18 мг/кг или 9 мг/кг, и однократно вводили цисплатин в дозе 10 мг/кг. В отношении доз введенного l-ОНР и цисплатина и высоких доз введенных соединений различных примеров, использовали максимально переносимые дозы (MTD дозы) для всех соединений. После введения с помощью штангенциркуля измеряли размер большой оси (L) и малой оси (W) опухоли в зависимости от времени, и рассчитывали объем опухоли (L×W×W×0,5). Испытание проводили, используя по четыре животных на группу для всех групп без лечения, а также для всех групп, которым вводили различные лекарства. В течение периода от начала введения до 21 дня после введения по приведенной ниже формуле рассчитывали относительный объем опухоли (Т/С (%)) для каждой группы с лечением в сравнении с относительным объемом опухоли в группе без лечения, взятым за 100, в качестве показателя противоопухолевого эффекта. Значения Т/С (%) в группах, которым вводили различные лекарства, представлены в таблице 6.
Формула: Т/С (%) = Относительный объем опухоли в группе с лечением/относительный объем опухоли в группе без лечения × 100
После введения измеряли массу тела мышей в зависимости от времени. В течение периода от начала введения до 21 дня после введения рассчитывали изменения относительной массы тела в сравнении с массой тела в день начала введения, взятой за 1, и результаты представлены в таблице 7.
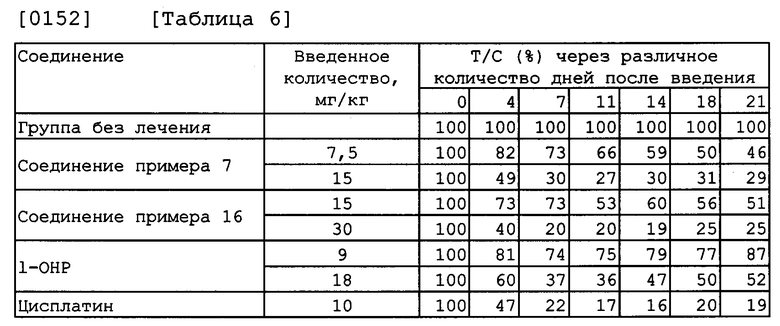
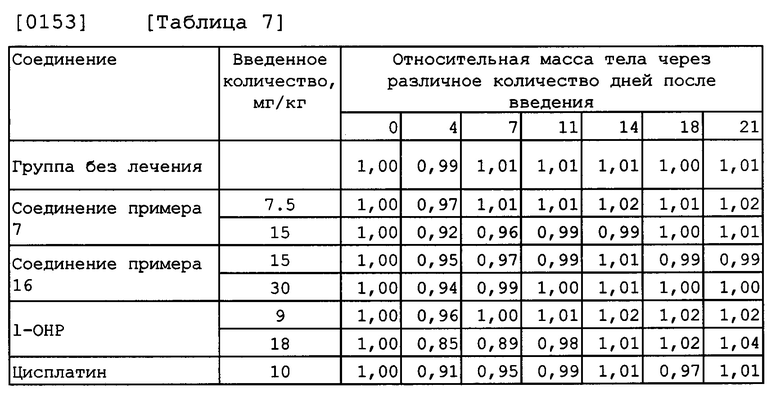
[0154] Соединение примера 7 и соединение примера 16 демонстрировали более сильный противоопухолевый эффект, по сравнению с l-ОНР, в MTD дозах. В то же время снижение массы для соединения примера 7 и соединения примера 16 было низким, по сравнению с l-ОНР и цисплатином на 4 день после введения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМЕРНЫЙ КОНЪЮГАТ КООРДИНАЦИОННОГО КОМПЛЕКСА ПЛАТИНЫ (II) С ПРОИЗВОДНЫМ СУЛЬФОКСИДА | 2016 |
|
RU2721725C2 |
| ВЫСОКОМОЛЕКУЛЯРНЫЙ КОНЪЮГАТ ПОДОФИЛЛОТОКСИНОВ | 2007 |
|
RU2447095C2 |
| БЛОК-СОПОЛИМЕРНЫЙ КОНЪЮГАТ ФИЗИОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА | 2016 |
|
RU2732612C2 |
| ПОЛИМЕРНОЕ ПРОИЗВОДНОЕ АНТИМЕТАБОЛИТА ЦИТИДИНА | 2006 |
|
RU2404980C2 |
| ВЫСОКОМОЛЕКУЛЯРНЫЕ ПРОИЗВОДНЫЕ КАМПТОТЕЦИНОВ | 2003 |
|
RU2315782C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЛОК-СОПОЛИМЕРА | 2012 |
|
RU2623426C2 |
| ИНГИБИТОР СВЯЗЫВАНИЯ СФИНГОЗИН-1-ФОСФАТА | 2007 |
|
RU2395499C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМОТИРУЮЩАЯ ДЕФЕКАЦИЮ | 2001 |
|
RU2294762C2 |
| ИНГИБИТОРЫ ФАКТОРА VIIA | 2000 |
|
RU2248359C2 |
| ПРОИЗВОДНЫЕ (ТИО)МОЧЕВИНЫ, ИНГИБИРУЮЩИЕ ФАКТОР VIIa, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2286337C2 |
Изобретение относится к полимерным конъюгатам гексакоординированного комплекса платины. Предложен полимерный конъюгат гексакоординированного комплекса платины, в котором гексакоординированный комплекс платины, содержащий галогены и гидроксильные группы в аксиальных положениях, напрямую или через спейсеры связаны с карбоксильными группами боковой цепи блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты. Технический результат – предложенный конъюгат эффективно высвобождает высокоактивный комплекс платины в восстановительных условиях, в том числе в клетках. 6 н. и 10 з.п. ф-лы, 2 ил., 7 табл., 21 пр.
1. Полимерный конъюгат гексакоординированного комплекса платины, содержащий блок-сополимер, который содержит полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты; и гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, где гексакоординированный комплекс платины прямо или через спейсер связан с карбоксильной группой боковой цепи указанного блок-сополимера.
2. Полимерный конъюгат гексакоординированного комплекса платины по п. 1, отличающийся тем, что полимерный конъюгат представлен следующей формулой (I):
[Химическая формула 1]
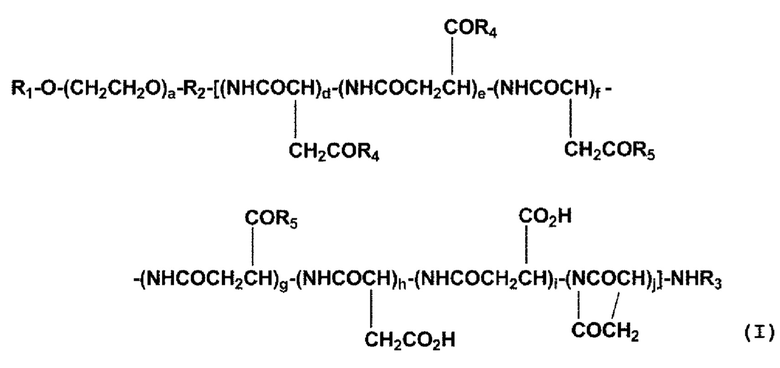
где R1 представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; R2 представляет собой связывающую группу; R3 представляет собой атом водорода или (С1-С6) ацильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, представленной следующей формулой (II):
[Химическая формула 2]

[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, гидроксильной группы, аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR6CONHR7; R6 и R7 могут быть одинаковыми или различными и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; и R8 представляет собой (С1-С10) алкильную группу, которая может содержать заместитель, бензильную группу или остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, заместителя, представленного следующей формулой (III), полученного отщеплением Н от α-аминогруппы производного α-аминокислоты:
[Химическая формула 3]
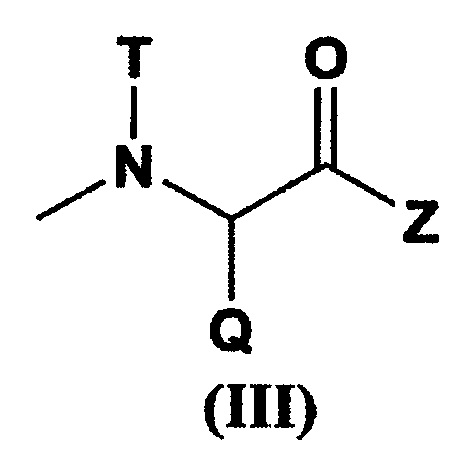
[где Q представляет собой α-аминокислотный остаток боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR12CONHR13; и R12 и R13 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой],
и -NR9CONHR10; R9 и R10 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; а представляет собой целое число от 5 до 11500; каждый d, е, f, g, h, i и j представляет собой целое число от 0 до 200; d+е представляет собой целое число от 1 до 200; d+е+f +g+h+i+j представляет собой целое число от 2 до 200; и порядок связывания различных составных звеньев полиаспарагиновой кислоты является произвольным.
3. Полимерный конъюгат гексакоординированного комплекса платины по п. 2, отличающийся тем, что R1 представляет собой (С1-С3) алкильную группу, которая может содержать заместитель; R2 представляет собой (С2-С6) алкиленовую группу; R3 представляет собой (С1-С3) ацильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, состоящей из следующей формулы (IV):
[Химическая формула 4]
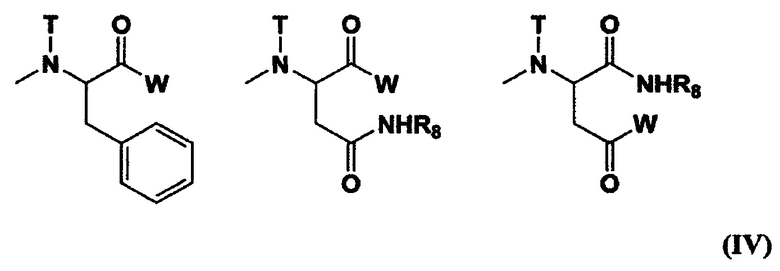
[где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (II), соответственно],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; а представляет собой целое число от 10 до 2000; каждый d, е, f, g, h, i и j представляет собой целое число от 0 до 100; d+е представляет собой целое число от 1 до 100; и d+е+f+g+h+i+j представляет собой целое число от 4 до 100.
4. Полимерный конъюгат гексакоординированного комплекса платины по п. 2 или 3, отличающийся тем, что R1 представляет собой метильную группу; R2 представляет собой триметиленовую группу; R3 представляет собой ацетильную группу; R4 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой заместитель, выбранный из группы, состоящей из остатка, полученного отщеплением Н от аминогруппы бензилового эфира фенилаланина, и -NR9CONHR10; и оба R9 и R10 представляют собой циклогексильную группу или изопропильную группу.
5. Полимерный конъюгат гексакоординированного комплекса платины по п. 2 или 3, отличающийся тем, что R1 представляет собой метильную группу; R2 представляет собой триметиленовую группу; R3 представляет собой ацетильную группу; R4 представляет собой заместитель, выбранный из группы, представленной следующей формулой (V):
[Химическая формула 5]
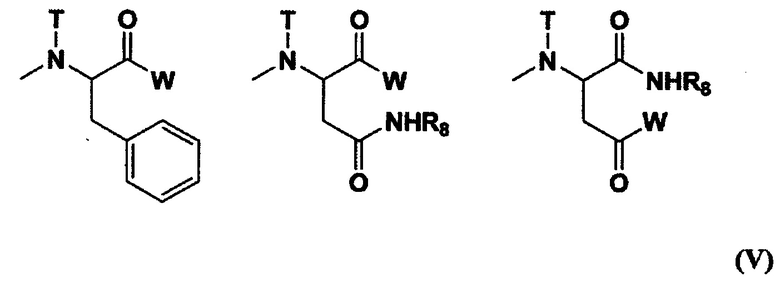
[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и -NR6CONHR7; оба R6 и R7 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R5 представляет собой -NR9CONHR10; и оба R9 и R10 представляют собой циклогексильную группу или изопропильную группу.
6. Полимерный конъюгат гексакоординированного комплекса платины по п. 1, отличающийся тем, что полимерный конъюгат представлен следующей формулой (VI):
[Химическая формула 6]
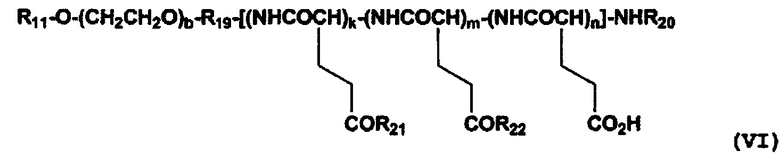
где R11 представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; R19 представляет собой связывающую группу; R20 представляет собой атом водорода или (С1-С6) ацильную группу; R21 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, представленной следующей формулой (VII):
[Химическая формула 7]
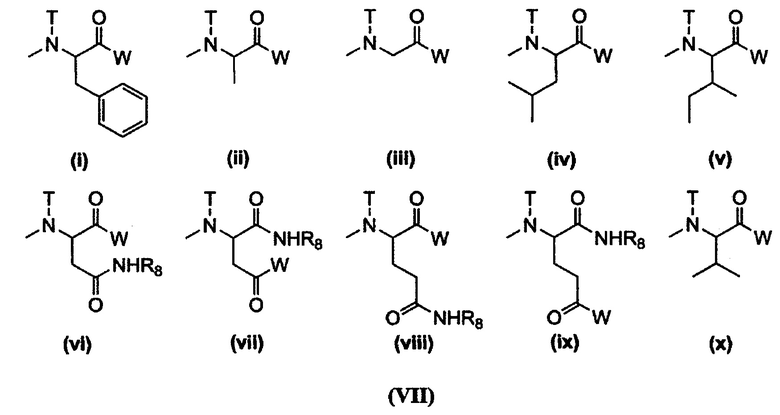
[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, гидроксильной группы, аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может иметь заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR16CONHR17; R16 и R17 могут быть одинаковыми или различными и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу, R8 представляет собой (С1-С10) алкильную группу, которая может содержать заместитель, бензильную группу или остаток α-аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой заместитель, выбранный из группы, состоящей из (С1-С30) алкокси-группы, (С1-С30) аралкилокси-группы, (С6-С10) арилокси-группы, (С1-С30) алкиламино-группы, которая может содержать заместитель, ди(С1-С30) алкиламино-группы, которая может содержать заместитель, остатка, представленного следующей формулой (VIII), полученного отщеплением Н от α-аминогруппы производного α-аминокислоты:
[Химическая формула 8]
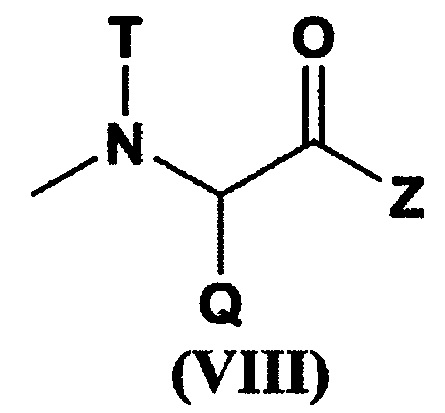
[где Q представляет собой α-аминокислотный остаток боковой цепи; Т представляет собой атом водорода, (С1-С10) алкильную группу, которая может содержать заместитель, или (С6-С10) арильную группу; Z представляет собой заместитель, выбранный из группы, состоящей из аминогруппы, содержащей бензильную группу или (С1-С10) алкильную группу, которая может содержать заместитель, (С1-С10) алкокси-группы, которая может содержать фенильную группу, (С6-С10) арилокси-группы и -NR24CONHR25; R24 и R25 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой],
и -NR14CONHR15; R14 и R15 могут быть одинаковыми или различными, и каждый из них представляет собой (С3-С6) циклическую алкильную группу или (С1-С5) алкильную группу, которая может быть замещена третичной аминогруппой; b представляет собой целое число от 5 до 11500; k представляет собой целое число от 1 до 200; каждый m и n представляет собой целое число от 0 до 200; k+m+n представляет собой целое число от 2 до 200; и порядок связывания различных составных звеньев полиглутаминовой кислоты является произвольным.
7. Полимерный конъюгат гексакоординированного комплекса платины по п. 6, отличающийся тем, что R11 представляет собой (С1-С3) алкильную группу, которая может содержать заместитель; R19 представляет собой (С2-С6) алкиленовую группу; R20 представляет собой (С1-С3) ацильную группу; R21 представляет собой остаток гексакоординированного комплекса, содержащего атом галогена и гидроксильную группу в аксиальных положениях, или заместитель, выбранный из группы, состоящей из следующей формулы (IX):
[Химическая формула 9]
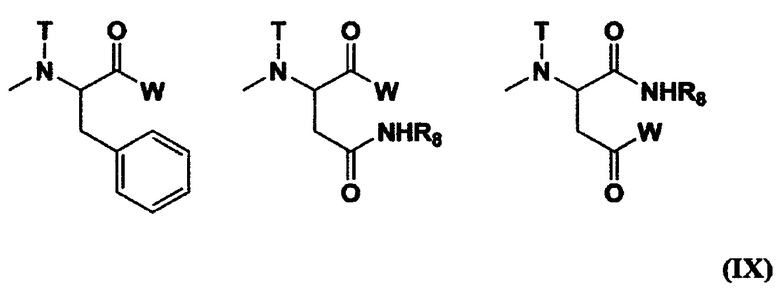
[где W, Т и R8 означают такие же группы, как W, Т и R8 в формуле (VII), соответственно],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; b представляет собой целое число от 10 до 2000; k представляет собой целое число от 1 до 100; каждый m и n представляет собой целое число от 0 до 100; и k+m+n представляет собой целое число от 3 до 100.
8. Полимерный конъюгат гексакоординированного комплекса платины по п. 6 или 7, отличающийся тем, что R11 представляет собой метильную группу; R19 представляет собой триметиленовую группу; R20 представляет собой ацетильную группу; R21 представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой заместитель, выбранный из группы, состоящей из остатка, полученного отщеплением Н от аминогруппы бензилового эфира фенилаланина, и -NR14CONHR15; и оба R14 и R15 представляют собой циклогексильную группу или изопропильную группу.
9. Полимерный конъюгат гексакоординированного комплекса платины по п. 6 или 7, отличающийся тем, что R11 представляет собой метильную группу; R19 представляет собой триметиленовую группу; R20 представляет собой ацетильную группу; R21 представляет собой заместитель, выбранный из группы, представленной следующей формулой (X):
[Химическая формула 10]
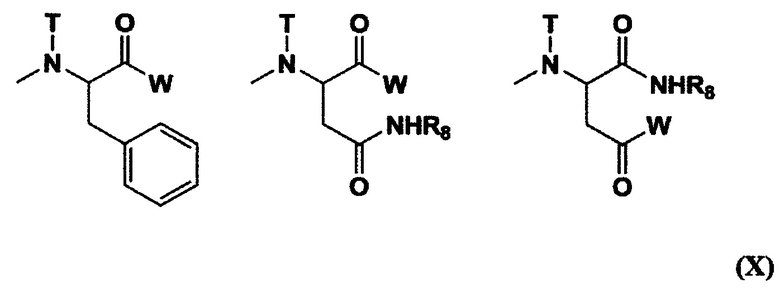
[где W представляет собой заместитель, выбранный из группы, состоящей из остатка гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, и NR16CONHR17; оба R16 и R17 представляют собой циклогексильную группу или изопропильную группу; Т представляет собой атом водорода, метильную группу, этильную группу или бензильную группу; и R8 представляет собой остаток аминокислоты, содержащий защищенную карбоновую кислоту],
при условии, что по меньшей мере один W из указанных заместителей представляет собой остаток гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях; R22 представляет собой -NR14CONHR15; и оба R14 и R15 представляют собой циклогексильную группу или изопропильную группу.
10. Полимерный конъюгат гексакоординированного комплекса платины по любому из пп. 1-9, отличающийся тем, что гексакоординированный комплекс платины, содержащий атом галогена и гидроксильную группу в аксиальных положениях, представляет собой гексакоординированный комплекс платины, представленный следующей формулой (XI):
[Химическая формула 11]

где оба X1 и Х2 представляют собой атом галогена, или они связаны друг с другом с образованием дикарбоксилата, выбранного из группы, состоящей из оксалата, малоната, сукцината и о-фталата; и Y1 представляет собой атом галогена.
11. Полимерный конъюгат гексакоординированного комплекса платины по п. 10, отличающийся тем, что Y1 в гексакоординированном комплексе платины представляет собой атом хлора или атом брома; оба X1 и Х2 представляют собой атом хлора или атом брома, или они связаны друг с другом с образованием оксалата.
12. Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. 1, в котором карбоксильную группу в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связывают сложноэфирной связью с помощью дегидратирующего конденсирующего агента.
13. Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. 1, в котором линкер, с которым посредством сложноэфирной связи связывают гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связан с карбоксильной группой в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты.
14. Способ получения полимерного конъюгата гексакоординированного комплекса платины по п. 1, в котором линкер, связанный с карбоксильной группой в боковой цепи указанного блок-сополимера, содержащего полиэтиленгликолевый структурный фрагмент и фрагмент полиаспарагиновой кислоты или фрагмент полиглутаминовой кислоты, и гидроксильную группу гексакоординированного комплекса платины, содержащего атом галогена и гидроксильную группу в аксиальных положениях, связывают сложноэфирной связью.
15. Лекарственное средство, содержащее полимерный конъюгат гексакоординированного комплекса платины по любому из пп. 1-11 в качестве активного ингредиента.
16. Противоопухолевый агент, содержащий полимерный конъюгат гексакоординированного комплекса платины по любому из пп. 1-11 в качестве активного ингредиента.
| FR 2954321 A1, 24.06.2011 | |||
| ЧУВСТВИТЕЛЬНЫЙ ЭЛЕМЕНТ ЛОТОВЫХ УРОВНЕМЕРОВ | 2004 |
|
RU2305275C2 |
| КООРДИНАЦИОННЫЙ КОМПЛЕКС ДИАМИНОЦИКЛОГЕКСАНА ПЛАТИНЫ (II) С БЛОКСОПОЛИМЕРОМ, СОДЕРЖАЩИМ СЕГМЕНТ ПОЛИ(КАРБОНОВОЙ КИСЛОТЫ), И ВКЛЮЧАЮЩИЙ ЕГО ПРОТИВОРАКОВЫЙ АГЕНТ | 2004 |
|
RU2335512C2 |
| Турбоциклон | 1986 |
|
SU1695991A1 |
Авторы
Даты
2020-02-25—Публикация
2016-09-08—Подача