Настоящее изобретение относится к соединениям формулы I,
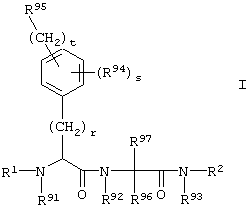
в которой R1, R2, R91, R92, R93, R94, R95, R96, R97, r, s и t имеют значения, указанные ниже. Соединения формулы I являются полезными фармакологически активными соединениями. Они обладают мощным антитромботическим действием и являются пригодными, например, для лечения и профилактики тромбоэмболических заболеваний или повторного стеноза. Они являются обратимыми ингибиторами фермента свертывания крови фактора VIIa (F VIIa) и могут в основном применяться при состояниях, когда имеет место нежелательная активность фактора VIIa, или при состояниях, для лечения и профилактики которых может оказаться полезным ингибирование фактора VIIa. Кроме того, данное изобретение относится к способам получения соединений формулы I, их применению, в особенности, в качестве активных ингредиентов лекарственных препаратов, и к включающим их лекарственным препаратам.
Способность образовывать сгустки крови является жизненно необходимой. Образование сгустка крови или тромба обычно является результатом повреждения ткани, которое инициирует каскад коагуляции, и обладает эффектом замедления или предотвращения кровотечения при излечивании раны. Другие факторы, которые непосредственно не связаны с повреждением ткани, такие как атеросклероз и воспаление, могут также инициировать каскад коагуляции. Как правило, существует связь между воспалением и каскадом коагуляции. Медиаторы воспаления регулируют каскад коагуляции, а компоненты коагуляции влияют на продукцию и активность медиаторов воспаления. Однако при некоторых болезненных состояниях образование сгустков крови в кровеносной системе достигает нежелательной степени и является источником болезненного состояния, потенциально приводящего к патологическим последствиям. Тем не менее, при таких болезненных состояниях нежелательно полностью ингибировать систему свертывания крови, так как это может привести к кровотечению, представляющему собой угрозу для жизни. При лечении таких состояний требуется хорошо сбалансированное вмешательство в систему свертывания крови, и все еще существует потребность в веществах, проявляющих подходящую для достижения такого результата фармакологическую активность.
Коагуляция крови представляет собой сложный процесс, включающий постепенно расширяющиеся серии реакций активации ферментов, в которых зимогены плазмы последовательно активируются путем ограниченного протеолиза. Механически каскад коагуляции крови разделяется на внутренний и внешний пути, которые сходятся в момент активации фактора X. Последующее образование тромбина протекает через единственный общий путь (см. схему 1). Данные факты позволяют предположить, что внутренний путь играет важную роль в поддержании и росте образования фибрина, тогда как внутренний путь играет важную роль в фазе инициации коагуляции крови (Н.Cole, Aust. J.Med. Sci. 16 (1995) 87-93; G.J.Broze, Blood Coagulation и Fibrinolysis 6, Suppl. 1 (1995) S7-S13). Обычно считают, что коагуляция крови физически инициируется при образовании комплекса фактор VIIa/тканевый фактор (ТФ). После образования данный комплекс быстро инициирует коагуляцию посредством активации факторов IX и X. Вновь образованный активированный фактор X, например, фактор Ха, затем образует один-к-одному комплекс с фактором Va и фосфолипидами с образованием протромбиназного комплекса, который отвечает за превращение растворимого фибриногена в нерастворимый фибрин посредством активации тромбина из его предшественника протромбина. Со временем активность комплекса фактор VIIa/тканевый фактор (внешний путь) подавляется под действием белка, ингибитора протеазы типа Куница (Kunitz), TFPI, который при образовании комплекса с фактором Ха может непосредственно ингибировать протеолитическую активность комплекса фактор VIIa/тканевый фактор.
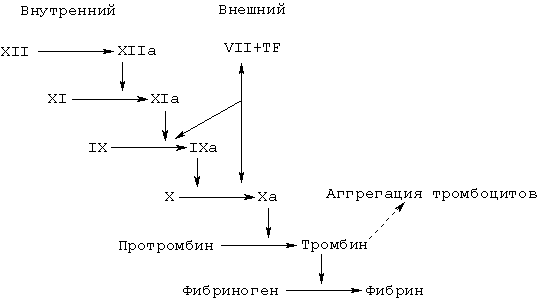
Схема 1: Каскад коагуляции крови
Для поддержания процесса коагуляции при ингибированной внешней системе дополнительный фактор Ха продуцируется посредством тромбин-опосредованной активности внутреннего пути. Таким образом, тромбин играет двойную автокаталитическую роль, опосредуя его собственную продукцию и превращение фибриногена в фибрин. Автокаталитическая природа образования тромбина является важной защитой от неконтролируемого кровотечения и гарантирует, что при наличии данного порогового уровня коагуляция крови будет происходить полностью. Таким образом, наиболее желательно разрабатывать агенты, которые ингибируют коагуляцию, не ингибируя непосредственно тромбин, но ингибируя другие стадии каскада коагуляции, такие как активность фактора VIIa.
При многих клинических применениях существует насущная необходимость в предотвращении образования сгустков крови внутри сосудов, или в лечении некоторыми антикоагулянтами. Например, приблизительно у 50% пациентов, подвергающихся полной замене бедра, развивается тромбоз глубокой вены (DVT). Доступные в настоящее время лекарственные препараты, такие как гепарин и его производные, не удовлетворяют существующих потребностей при многих конкретных клинических применениях. Утвержденные в настоящее время терапии включают применение низкомолекулярного гепарина (LMWH) в фиксированных дозах и гепарина в изменяющихся дозах. Даже при таких режимах приема лекарственного препарата у 10%-20% пациентов развивается DVT, и у 5%-10% развиваются осложнения, связанные с кровотечением.
Другая клиническая ситуация, при которой требуются улучшенные антикоагулянты, касается субъектов, подвергающихся коронарной внутрипросветной ангиопластике, а также субъектов с риском инфаркта миокарда или страдающих от грудной жабы, возникающей с нарастающими частотой, интенсивностью и продолжительностью. В настоящее время традиционно принятая терапия, которая заключается во введении гепарина и аспирина, связана с 6-8% частотой внезапной закупорки сосудов в пределах 24 часов проведения процедуры. Частота связанных с кровотечением осложнений после применения гепарина, при которых требуется терапия с переливанием крови, также составляет приблизительно 7%. Кроме того, даже несмотря на то, что количество задержанных закупорок является значительным, введение гепарина после окончания процедур не имеет большой ценности и может быть вредным.
Широко использующиеся ингибиторы свертывания крови, такие как гепарин и родственные сульфированные полисахариды, такие как LMWH и гепаринсульфат, проявляют свои антикоагуляционные эффекты путем стимуляции связывания природного регулятора процесса свертывания, антитромбина III, с тромбином и фактором Ха. Ингибиторная активность гепарина в основном направлена на тромбин, который инактивируется приблизительно в 100 раз быстрее, чем фактор Ха. Хирудин и хирулог представляют собой два дополнительных тромбин-специфичных антикоагулянта, которые в настоящее время проходят клинические испытания. Однако данные антикоагулянты, ингибирующие тромбин, также могут вызывать связанные с кровотечением осложнения. Доклинические исследования на обезьянах и собаках показали, что, если мишенью являются ферменты, включенные в ранние стадии каскада коагуляции, такие как фактор Ха или фактор VIIa, то предотвращение образования сгустков происходит без связанных с кровотечением побочных эффектов, которые наблюдаются при действии непосредственных ингибиторов тромбина (L.A.Marker et al., Thromb. Hemostas. 74 (1995) 464-472). Некоторые пептиды и аналоги пептидов, которые ингибируют свертывание крови путем специфического ингибирования фактора Ха раскрыты, например, в WO-A-95/29189.
Специфическое ингибирование каталитического комплекса фактор VIIa/тканевый фактор с помощью моноклональных антител (WO-A-92/06711) или такого белка, как инактивированный под действием хлорметилкетона фактор VIIa (WO-A-96/12800 и WO-A-97/47651) является крайне эффективным средством подавления тромбообразования, вызванного сильным повреждением артерии, или тромбозных осложнений, связанных с бактериальной септицемией. Существуют также экспериментальные данные, свидетельствующие о том, что ингибирование активности фактор VIIa/тканевый фактор подавляет повторный стеноз, возникающий после ангиопластики с использованием баллона (L.A.Marker et al., Haemostasis 26 (1996) S1:76-82). Исследования кровотечения, проводимые на обезьянах, показали, что ингибирование комплекса фактор VIIa/тканевый фактор имеет широчайший диапазон безопасности относительно терапевтической эффективности и риска кровотечения любого исследуемого подхода с использованием антикоагулянта, включая ингибирование тромбина, аггрегации тромбоцитов и фактора Ха (L.A.Harker et al., Thromb. Hemostas. 74 (1995) 464-472).
Специфический ингибитор фактора VIIa, имеющий благоприятный профиль свойств, может иметь большое практическое значение в медицинской практике. В особенности, ингибитор фактора VIIa может быть эффективным в тех случаях, когда использующиеся в настоящее время лекарственные средства, такие как гепарин и родственные сульфатированные полисахариды, являются неэффективными или малоэффективными. Некоторые ингибиторы фактора VIIa уже были описаны, например, в WO-A-89/09612. ЕР-А-987274 раскрывает соединения, содержащие трипептидную единицу, которая ингибирует фактор VIIa. Однако профиль свойств данных соединений все еще не является идеальным, и существует потребность в дополнительных низкомолекулярных ингибиторах свертывания крови, специфичных к фактору VIIa, которые являются эффективными и не вызывают нежелательных побочных эффектов. Настоящее изобретение удовлетворяет данную потребность путем предоставления новых соединений формулы I, ингибирующих активность фактора VIIa.
Таким образом, предметом настоящего изобретения являются соединения формулы I,
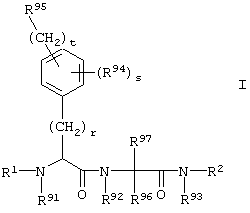
где r обозначает 0, 1, 2 или 3;
s обозначает 0, 1, 2, 3 или 4;
t обозначает 0, 1 или 2;
R1 выбран из группы, включающей водород, R11-CO- и R12-SO2-;
R11 выбран из группы, включающей водород, (C1-С8)-алкил, (C6-C14)-арил, (С6-С14)-арил-(C1-C4)-алкил-, Het-, Het-(C1-C4)-алкил-, (C1-C8)-алкилокси-, (C6-C14)-арилокси-, (С6-С14)-арил-(C1-C4)-алкилокси-, амино, (C1-С8)-алкиламино-, (C6-C14)-ариламино- и (С6-С14)-арил-(C1-C4)-алкиламино-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R12 выбран из группы, включающей (C1-C8)-алкил, (С6-С14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het-, Het-(C1-C4)-алкил-, ди((C1-C8)-алкил)амино- и ди((С6-С14)арил-(C1-C4)-алкил)амино-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R2 обозначает водород, R21(R22)СН-, R23-Het-(СН2)k-, R23(R24)N-(CH2)m-D-(CH2)n- или R25(R26)N-CO-(СН2)p-D-(CH2)q-, где D обозначает двухвалентный остаток -C(R31)(R32)-, двухвалентный (C6-C14)-ариленовый остаток или двухвалентный остаток, полученный из ароматической группы Het, содержащей от 5 до 10 атомов в цикле, из которых 1, 2, 3 или 4 являются одинаковыми или различными гетероатомами, выбранными из группы, включающей азот, кислород и серу, а числа k, m, n, р и q, которые являются независимыми друг от друга и могут быть одинаковыми или разными, равны 0, 1, 2, 3, 4 или 5, при условии, что в случае, если D обозначает -C(R31) (R32) - сумма m+n не может быть равна 0 и сумма p+q не может быть равна 0;
R21 и R22, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (C1-C12)-алкил, (C6-C14)-арил, (С6-С14)-арил-(C1-C4)-алкил-, Het- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями из группы, включающей R40, (C1-C8)-алкиламино-, ди-((C1-C8)-алкил)-амино-, (С6-С14)-арил-(C1-C4)-алкиламино-, (С6-С14)-ариламино-, аминокарбонил- и аминокарбонил-(C1-С8)-алкил-, или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют насыщенную или ненасыщенную 3-8-членную карбоциклическую структуру, которая может быть конденсированной с одной или двумя циклическими системами, представляющими собой гетероароматические циклы, содержащие от 5 до 10 атомов в цикле, из которых 1, 2 или 3 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот, кислород и серу, и/или (C6-C10) карбоциклические ароматические структуры, где получившаяся группа R21(R22)CR- является незамещенной или замещенной одним или несколькими одинаковыми или разными заместителями, выбранными из группы, включающей R40, (C1-C8)-алкиламино-, ди-((C1-C8)-алкил)-амино-, (C6-C14)-арил-(C1-C4)-алкиламино-, (С6-C14)-ариламино-, аминокарбонил- и аминокарбонил-(C1-C8)-алкил-;
R23 обозначает водород, R27-SO2- или R28-CO-;
R24 выбран из группы, включающей водород, (C1-C8)-алкил, (C6-C14)-арил и (C6-C14)-арил-(C1-C4)-алкил-;
R25 и R26, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (C1-C8)-алкил, (C6-C14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R27 выбран из группы, включающей (C1-C8)-алкил, (С6-С14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het-, Het-(C1-C4)-алкил-, амино, (C1-C8)-алкиламино-, ди-((C1-C8)-алкил) амино-, (С6-С14)-ариламино- и (C6-C14)-арил-(C1-C4)-алкиламино-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R28 выбран из группы, включающей R27, (C1-C8)-алкилокси-, (C6-C14)-арилокси- и (С6-С14)-арил-(C1-C4)-алкилокси-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R31 и R32, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, являются выбранными из группы, включающей водород, (C1-C12)-алкил, (C6-C14)-арил, (С6-С14)-арил-(C1-C4)-алкил-, Het- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R40 выбран из группы, включающей галоген, гидрокси, (C1-С8)-алкилокси-, (C6-C14)-арил-(C1-C8)-алкилокси-, (C6-C14)-арилокси-, (C1-C8)-алкил, (C6-C14)-арил, (C6-C14)-арил-(C1-C8)-алкил-, (C1-C8)-алкилсульфонил-, трифторметил, ацетиламино-, амино, амидино, гуанидино, оксо, нитро и циано, где группы R40 являются независимыми друг от друга и могут быть одинаковыми или разными;
R91, R92 и R93, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (C1-C8)-алкил, (C6-C14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het- и Het-(C1-C4)-алкил-;
R94 выбран из группы, включающей (C1-C4)-алкил, (С6-С14)-арил, амино, нитро, галоген, трифторметил, гидрокси, (C1-C4)-алкилокси-, где группы R94 являются независимыми друг от друга и могут быть одинаковыми или разными;
R95 выбран из группы, включающей амидино, гуанидино, ((C1-C4)-алкил)оксикарбониламидино-, ((C1-C4)-алкил)оксикарбонилгуанидино- и гидроксиамидино-;
R96 выбран из группы, включающей водород, R98-(C1-C8)-алкил-, R98-(C1-С8)-арил-, R98-(С6-С14)арил-(C1-C4)-алкил-, R98-Het- и R98-Het-(C1-C4)-алкил-;
R97 выбран из группы, включающей R99-(C1-C8)-алкил-, R99-(С6-С14)арил-, R99-(С6-С14)арил-(C1-C4)-алкил-, R99-Het- и R99-Het-(C1-С4)-алкил-;
R98 и R99, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей гидроксикарбонил-, (C1-C8)-алкилоксикарбонил-, (С6-C14)-арилоксикарбонил-, (C6-C14)-арил-(C1-C4)-алкилоксикарбонил-, аминокарбонил-, (C1-C8)-алкиламинокарбонил-, тетразолил, Р(O)(ОН)2, -S(O)2OH и -S(O)2NH2;
Het обозначает насыщенную, частично ненасыщенную или ароматическую моноциклическую или бициклическую гетероциклическую структуру, содержащую от 3 до 10 атомов в цикле, из которых 1, 2, 3 или 4 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот, кислород и серу;
во всех их стереоизомерных формах, а также их смеси в любых соотношениях, и их физиологически приемлемые соли.
Все остатки, которые могут встречаться несколько раз в соединениях формулы I, например остатки R40, R94 или Het, могут независимо друг от друга иметь указанные значения, и в каждом случае могут быть одинаковыми или разными.
В данном документе термин алкил, который следует понимать в самом широком смысле, обозначает углеводородные остатки, которые могут быть линейными, т.е. прямоцепочечными, или разветвленными, и которые могут быть ациклическими или циклическими остатками или включать любое сочетание ациклических и циклических субъединиц. Кроме того, термин алкил в данном документе специально включает насыщенные группы, а также ненасыщенные группы, причем последние группы содержат одну или несколько, например одну, две или три двойные связи и/или тройные связи, при условии, что двойные связи не локализованы в циклической алкильной группе с образованием ароматической системы. Все данные утверждения также применимы, если алкильная группа несет заместители, или встречается в качестве заместителя на другом остатке, например, на алкилоксильном остатке, алкилоксикарбонильном остатке или арилалкильном остатке. Примерами алкильных остатков, содержащих от 1 до 20 атомов углерода, являются метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тетрадецил, гексадецил, октадецил и эйкозил, н-изомеры всех данных остатков, изопропил, изобутил, 1-метилбутил, изопентил, неопентил, 2,2-диметилбутил, 2-метилпентил, 3-метилпентил, изогексил, 2,3,4-триметилгексил, изодецил, втор-бутил, трет-бутил или трет-пентил.
Ненасыщенными алкильными остатками являются, например, алкенильные остатки, такие как винил, 1-пропенил, 2-пропенил (=аллил), 2-бутенил, 3-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 5-гексенил или 1,3-пентадиенил, или алкинильные остатки, такие как этинил, 1-пропинил, 2-пропинил (=пропаргил) или 2-бутинил. Алкильные остатки также могут быть ненасыщенными, если они являются замещенными.
Примерами циклических алкильных остатков являются циклоалкильные остатки, содержащие 3, 4, 5, 6, 7 или 8 атомов углерода в цикле, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил, которые также могут быть замещенными и/или ненасыщенными. Ненасыщенные циклические алкильные группы и ненасыщенные циклоалкильные группы, такие как, например, циклопентенил или циклогексенил, могут быть связаны через любой атом углерода. Термин алкил в данном документе также включает циклоалкил-замещенные алкильные группы, такие как циклопропилметил-, циклобутилметил-, циклопентилметил-, циклогексилметил-, циклогептилметил-, циклооктилметил-, 1-циклопропилэтил-, 1-циклобутилэтил-, 1-циклопентилэтил-, 1-циклогексилэтил- 1-циклогептилэтил-, 1-циклооктилэтил-, 2-циклопропилэтил-, 2-циклобутилэтил-, 2-циклопентилэтил-, 2-циклогексилэтил-, 2-циклогептилэтил-, 2-циклооктилэтил-, 3-циклопропилпропил, 3-циклобутилпропил-, 3-циклопентилпропил, 3-циклогексилпропил-, 3-циклогептилпропил-, 3-циклооктилпропил- и т.д., в данных группах циклоалкильная подгруппа, а также ациклическая подгруппа также могут быть ненасыщенными и/или замещенными.
Конечно, циклическая алкильная группа должна содержать по меньшей мере три атома углерода и ненасыщенная алкильная группа должна содержать по меньшей мере два атома углерода. Таким образом, следует понимать, что такая группа, как (C1-C8)-алкил включает, в числе других, насыщенный ациклический (C1-С8)-алкил, (С3-С8)-циклоалкил, циклоалкил-алкильные группы, такие как (С3-С7)-циклоалкил-(C1-C5)-алкил-, где общее число атомов углерода может варьировать от 4 до 8, и ненасыщенный (C2-C8)-алкил, такой как (С2-С8)-алкенил или (C2-C8)-алкинил. Подобным образом, следует понимать, что такая группа, как (C1-С4)-алкил включает, в числе других, насыщенный ациклический (C1-C4)-алкил, (С3-С4)-циклоалкил, циклопропилметил-, и ненасыщенный, такой как (С2-С4)-алкенил или (C2-C4)-алкинил.
Если не определено иначе, термин алкил предпочтительно включает ациклические насыщенные углеводородные остатки, содержащие от 1 до 6 атомов углерода, которые могут быть линейными или разветвленными, ациклические ненасыщенные углеводородные остатки, содержащие от 2 до 6 атомов углерода, которые могут быть линейными или разветвленными, такие как (С2-С6)-алкенил и (С2-С6)-алкинил, а также циклические алкильные группы, содержащие от 3 до 8 атомов углерода в цикле, особенно, от 3 до 6 атомов углерода в цикле. Представляющие особый интерес насыщенные ациклические алкильные остатки образованы такими (C1-C4)-алкильными остатками, как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил.
Вышеприведенные определения, относящиеся к алкильным группам, применяются не только к моновалентным остаткам, но и соответственно к двухвалентным остаткам, таким как алкандиильные группы, алкиленовые группы или полиметиленовые группы, примерами которых являются метилен, 1,2-этилен (=этан-1,2-диил), 1,1-этилен (=1-метил-метилен), 1-изобутилметилен, 1,3-пропилен, 2,2-диметил-1,3-пропилен, 1,4-бутилен, бут-2-ен-1,4-диил, 1,2-циклопропилен, 1,2-циклогексилен, 1,3-циклогексилен или 1,4-циклогексилен.
Если не определено иначе, и независимо от какого-либо конкретного заместителя, связанного с алкильными группами, указанного в определении соединений формулы I, алкильные группы в основном могут быть незамещенными или замещенными одним или несколькими, например, одним, двумя, тремя или четырьмя одинаковыми или разными заместителями. Заместители любого вида, присутствующие в замещенных алкильных остатках, могут присутствовать в любом желательном положении, при условии, что замещение не приводит к образованию нестабильной молекулы. Примерами замещенных алкильных остатков являются алкильные остатки, в которых один или несколько, например, 1, 2, 3, 4 или 5, атомов водорода замещены атомами галогенов, в частности, атомами фтора.
Примерами замещенных циклоалкильных групп являются циклоалкильные группы, которые несут в качестве заместителя одну или несколько, например, одну, две, три или четыре, одинаковые или разные ациклические алкильные группы, например, ациклические (C1-C4)-алкильные группы, такие как метильные группы. Примерами замещенных циклоалкильных групп являются 4-метилциклогексил, 4-трет-бутилциклогексил или 2,3-диметилциклопентил.
Термин арил относится к моноциклическому или полициклическому углеводородному остатку, в котором присутствует по меньшей мере одна карбоциклическая структура, которая имеет сопряженную пи-электронную систему. В (С6-С14)-арильном остатке присутствует от 6 до 14 атомов углерода в цикле. Примерами (С6-С14)-арильных остатков являются фенил, нафтил, бифенилил, флуоренил или антраценил. Примерами (С6-С10)-арильных остатков являются фенил или нафтил. Если не определено иначе, и независимо от какого-либо конкретного заместителя, связанного с арильными группами, указанного в определении соединений формулы I, арильные остатки, включая, например, фенил, нафтил и флуоренил, как правило, могут быть незамещенными или замещенными одним или несколькими, например одним, двумя, тремя или четырьмя одинаковыми или разными заместителями. Арильные остатки могут быть связаны через любое желательное положение, и в замещенных арильных остатках заместители могут находиться в любом желательном положении.
В монозамещенных фенильных остатках заместитель может находиться в положении 2, 3 или 4, причем положения 3 и 4 являются предпочтительными. Если фенильная группа несет два заместителя, они могут находиться в положениях 2,3, 2,4, 2,5, 2,6, 3,4 или 3,5. В фенильных остатках, несущих три заместителя, заместители могут находиться в положениях 2,3,4, 2,3,5, 2,3,6, 2,4,5, 2,4,6 или 3,4,5. Нафтильные остатки могут представлять собой 1-нафтил и 2-нафтил. В замещенных нафтильных остатках заместители могут находиться в любых положениях, например, в монозамещенных 1-нафтильных остатках, в положениях 2, 3, 4, 5, 6, 7 или 8 и в монозамещенных 2-нафтильных остатках в положениях 1, 3, 4, 5, 6, 7 или 8. Бифенилильные остатки могут представлять собой 2-бифенилил, 3-бифенилил или 4-бифенилил. Флуоренильные остатки могут представлять собой 1-, 2-, 3-, 4- или 9-флуоренил. В монозамещенных флуоренильных остатках, связанных через положение 9, заместитель предпочтительно присутствует в положениях 1, 2, 3 или 4.
Если не определено иначе, заместители, которые могут присутствовать в замещенных арильных группах, представляют собой, например, (C1-С8)-алкил, особенно, (C1-C4)-алкил, такой как метил, этил или трет-бутил, гидрокси, (C1-C8)-алкилокси, особенно, (C1-C4)-алкилокси, такой как метокси, этокси или трет-бутокси, метилендиокси, этилендиокси, F, Cl, Br, I, циано, нитро, трифторметил, трифторметокси, гидроксиметил, формил, ацетил, амино, моно- или ди-(C1-C4)-алкиламино, ((C1-C4)-алкил)карбониламино, такой как ацетиламино, гидроксикарбонил, ((C1-C4)-алкилокси)карбонил, карбамоил, необязательно замещенный фенил, бензил необязательно замещенный по фенильной группе, необязательно замещенный фенокси, или бензилокси, необязательно замещенный по фенильной группе. Замещенная арильная группа, которая может находиться в конкретном положении соединений формулы I, может независимо от другой арильной группы быть замещенной заместителями, выбранными из любой желательной подгруппы заместителей, перечисленных ранее, и/или приведенных в определении данной группы. Например, замещенная арильная группа может быть замещена одним или несколькими одинаковыми или разными заместителями, выбранными из группы, включающей (C1-C4)-алкил, гидрокси, (C1-C4)-алкилокси, F, Cl, Br, I, циано, нитро, трифторметил, амино, фенил, бензил, фенокси и бензилокси. Предпочтительно, в соединениях формулы I присутствует не более двух нитрогрупп.
Вышеприведенные определения, относящиеся к арильным группам, соответственно применимы к двухвалентным остаткам, полученным из арильной группы, т.е. к ариленовым группам, таким как фениленовые, которые могут представлять собой незамещенный или замещенный 1,2-фенилен, 1,3-фенилен или 1,4-фенилен, или нафтиленовые, которые могут представлять собой незамещенный или замещенный 1,2-нафталиндиил, 1,3-нафталиндиил, 1,4-нафталиндиил, 1,5-нафталиндиил, 1,6-нафталиндиил, 1,7-нафталиндиил, 1,8-нафталиндиил, 2,3-нафталиндиил, 2,6-нафталиндиил или 2,7-нафталиндиил. Вышеприведенные определения также соответственно применимы к арильной подгруппе в группах арилалкил-. Примерами групп арилалкил-, которые также могут быть незамещенными или замещенными по арильной подгруппе, а также по алкильной подгруппе, являются бензил, 1-фенилэтил, 2-фенилэтил, 3-фенилпропил, 4-фенилбутил, 1-метил-3-фенил-пропил, 1-нафтилметил, 2-нафтилметил, 1-(1-нафтил)этил, 1-(2-нафтил)этил, 2-(1-нафтил)этил, 2-(2-нафтил)этил, или 9-флуренилметил. Все приведенные формулировки также могут применяться к ароматическим циклам, которые могут быть конденсированными (или сопряженными) с циклом, образованным группами R21 и R22 и атомом углерода, к которому присоединены данные группы.
Группа Het включает группы, содержащие 3, 4, 5, 6, 7, 8, 9 или 10 атомов в цикле в исходной моноциклической или бициклической гетероциклической системе. В моноциклической группе Het гетероциклическая структура предпочтительно представляет собой 3-членный, 4-членный, 5-членный, 6-членный или 7-членный цикл, особенно предпочтительно 5-членный или 6-членный цикл. В бициклической группе Het предпочтительно присутствуют два сопряженных цикла, один из которых представляет собой 5-членный цикл или 6-членную гетероциклическую структуру, а другой представляет собой 5-членную или 6-членную гетероциклическую или карбоциклическую структуру, т.е. бициклическая структура Het предпочтительно содержит 8, 9 или 10 атомов в цикле, особенно предпочтительно 9 или 10 атомов в цикле.
Het включает насыщенные гетероциклические структуры, которые не содержат в циклах двойных связей, а также мононенасыщенные и полиненасыщенные гетероциклические системы, которые содержат в циклах одну или несколько, например, одну, две, три, четыре или пять, двойных связей, при условии, что полученная система является стабильной. Ненасыщенные циклы могут быть неароматическими или ароматическими, т.е. двойные связи в циклических структурах группы Het могут располагаться таким образом, что в результате образуется сопряженная система пи-электронов. Ароматические циклы в группе Het могут представлять собой 5-членные или 6-членные циклы, т.е. ароматические группы в группе Het содержат от 5 до 10 атомов в цикле. Таким образом, ароматические циклы в группе Het включают 5-членные и 6-членные моноциклические гетероциклы и бициклические гетероциклы, состоящие из двух 5-членных циклов, одного 5-членного цикла и одного 6-членного цикла, или двух 6-членных циклов. В бициклических ароматических группах в группе Het один или оба цикла могут содержать гетероатомы. Ароматические группы Het также могут обозначаться традиционным термином гетероарил, для которого соответственно могут применяться приведенные выше и ниже для Het определения и формулировки. Все данные формулировки также соответственно применяются к гетероароматическим циклам, которые могут быть конденсированными (или сопряженными) с циклом, образованным группами R21 и R22 и атом углерода, к которому присоединены данные группы.
Если не определено иначе, в группах Het и любых других гетероциклических группах предпочтительно присутствуют 1, 2, 3 или 4 одинаковых или разных гетероатома в цикле, выбранных из группы, включающей атомы азота, кислорода и серы. Особенно предпочтительно, если в данных группах присутствуют 1 или 2 одинаковых или разных гетероатома, выбранных из группы, включающей азот, кислород и серу. Циклические гетероатомы могут присутствовать в любом желательном количестве и в любом положении по отношению друг к другу, при условии, что полученная гетероциклическая система известна в данной области и является стабильной и подходящей в качестве подгруппы в лекарственном веществе. Примерами исходных структур гетероциклов, из которых может быть получена группа Het, являются азиридин, оксиран, азетидин, пиррол, фуран, тиофен, диоксол, имидазол, пиразол, оксазол, изоксазол, тиазол, изотиазол, 1,2,3-триазол, 1,2,4-триазол, тетразол, пиридин, пиран, тиопиран, пиридазин, пиримидин, пиразин, 1,2-оксазин, 1,3-оксазин, 1,4-оксазин, 1,2-тиазин, 1,3-тиазин, 1,4-тиазин, 1,2,3-триазин, 1,2,4-триазин, 1,3,5-триазин, азепин, 1,2-диазепин, 1,3-диазепин, 1,4-диазепин, индол, изоиндол, бензофуран, бензотиофен, 1,3-бензодиоксол, индазол, бензимидазол, бензоксазол, бензотиазол, хинолин, изохинолин, хроман, изохроман, циннолин, хиназолин, хиноксалин, фталазин, пиридоимидазолы, пиридопиридины, пиридопиримидины, пурин, птеридин и др., а также циклические системы, которые получаются из перечисленных гетероциклов путем сопряжения (или конденсации) с карбоциклической структурой, например, бензо-сопряженные, циклопента-сопряженные, циклогекса-сопряженные или циклогепта-сопряженные производные указанных гетероциклов.
Тот факт, что многие из приведенных ранее названий гетероциклов являются химическими названиями ненасыщенных или ароматических циклических систем, не означает, что группы Het могут быть получены только из соответствующей ненасыщенной циклической системы. В данном случае названия служат только для описания циклической системы в соответствии с размером цикла и числом гетероатомов, а также их относительными положениями. Как разъясняется выше, группа Het может быть насыщенной, или частично ненасыщенной, или ароматической, и, следовательно, может быть получена не только из самих перечисленных выше гетероциклов, то также из всех их частично или полностью гидрированных аналогов, а также из их аналогов с более высокой степенью ненасыщенности, если они являются пригодными. В качестве примеров полностью или частично гидрированных аналогов перечисленных ранее гетероциклов, из которых могут быть получены группы Het, могут быть упомянуты следующие группы: пирролин, пирролидин, тетрагидрофуран, тетрагидротиофен, дигидропиридин, тетрагидропиридин, пиперидин, 1,3-диоксолан, 2-имидазолин, имидазолидин, 4,5-дигидро-1,3-оксазол, 1,3-оксазолидин, 4,5-дигидро-1,3-тиазол, 1,3-тиазолидин, пергидро-1,4-диоксан, пиперазин, пергидро-1,4-оксазин (=морфолин), пергидро-1,4-тиазин (=тиоморфолин), пергидроазепин, индолин, изоиндолин, 1,2,3,4-тетрагидрохинолин, 1,2,3,4-тетрагидроизохинолин и др.
Остаток Het может быть присоединен через любой циклический атом углерода, и, в случае азот-содержащих гетероциклов, через любой подходящий циклический атом азота. Так, например, пирролильный остаток может представлять собой 1-пирролил, 2-пирролил или 3-пирролил, пирролидинильный остаток может представлять собой 1-пирролидинил (=пирролидино), 2-пирролидинил или 3-пирролидинил, пиридильный остаток может представлять собой 2-пиридил, 3-пиридил или 4-пиридил, пиперидинильный остаток может представлять собой 1-пиперидинил (=пиперидино), 2-пиперидинил, 3-пиперидинил или 4-пиперидинил. Фурил может представлять собой 2-фурил или 3-фурил, тиенил может представлять собой 2-тиенил или 3-тиенил, имидазолил может представлять собой 1-имидазолил, 2-имидазолил, 4-имидазолил или 5-имидазолил, 1,3-оксазолил может представлять собой 1,3-оксазол-2-ил, 1,3-оксазол-4-ил или 1,3-оксазол-5-ил, 1,3-тиазолил может представлять собой 1,3-тиазол-2-ил, 1,3-тиазол-4-ил или 1,3-тиазол-5-ил, пиримидинил может представлять собой 2-пиримидинил, 4-пиримидинил (=6-пиримидинил) или 5-пиримидинил, пиперазинил может представлять собой 1-пиперазинил (=4-пиперазинил=пиперазино) или 2-пиперазинил. Индолил может представлять собой 1-индолил, 2-индолил, 3-индолил, 4-индолил, 5-индолил, 6-индолил или 7-индолил. Подобным образом, остатки бензимидазолил, бензоксазолил и бензотиазолил могут присоединяться через положение 2 и через любое из положений 4, 5, 6, и 7, бензимидазолил также через положение 1. Хинолил может представлять собой 2-хинолил, 3-хинолил, 4-хинолил, 5-хинолил, 6-хинолил, 7-хинолил или 8-хинолил, изохинолил может представлять собой 1-изохинолил, 3-изохинолил, 4-изохинолил, 5-изохинолил, 6-изохинолил, 7-изохинолил или 8-изохинолил. Кроме присоединения через любое из положений, указанных для хинолила и изохинолила, 1,2,3,4-тетрагидрохинолил и 1,2,3,4-тетрагидроизохинолил могут также присоединяться через атомы азота в положении 1 и 2, соответственно.
Если не определено иначе, и независимо от каких-либо заместителей, связанных с группами Het, или с любыми другими гетероциклическими группами, которые указаны в определении соединений формулы I, группа Het может быть незамещенной или замещенной по атомам углерода в цикле одним или несколькими, например одним, двумя, тремя, четырьмя или пятью одинаковыми или разными заместителями, такими как (C1-C8) -алкил, особенно (C1-C4)-алкил, (C1-C8)-алкилокси, особенно (C1-C4)-алкилокси, (C1-C4)-алкилтио, галоген, нитро, амино, ((C1-C4)-алкил)карбониламино, такой как ацетиламино, трифторметил, трифторметокси, гидрокси, оксо, гидрокси-(C1-C4)-алкил, такой как, например, гидроксиметил, или 1-гидроксиэтил, или 2-гидроксиэтил, метилендиокси, этилендиокси, формил, ацетил, циано, метилсульфонил, гидроксикарбонил, аминокарбонил, (C1-С4)-алкилоксикарбонил, необязательно замещенный фенил, необязательно замещенный фенокси, бензил, необязательно замещенный по фенильной группе, бензилокси, необязательно замещенный по фенильной группе, и др. Заместители могут присутствовать в любом желательном положении, при условии, что в результате получается стабильная молекула. Конечно, оксогруппа не может присутствовать в ароматическом цикле. Каждый подходящий циклический атом азота в группе Het независимо от другого может быть незамещенным, т.е. нести атом водорода, или может быть замещенным, т.е. нести заместитель, такой как (C1-C8)-алкил, например, (C1-C4)-алкил, такой как метил или этил, необязательно замещенный фенил, фенил-(C1-C4)-алкил, например, бензил, необязательно замещенный по фенильной группе, гидрокси-(С2-С4)-алкил такой как, например, 2-гидроксиэтил, ацетил или другую ацильную группу, метилсульфонил или другую сульфонильную группу, аминокарбонил, (C1-C4)-алкилоксикарбонил, и др. Содержащие азот гетероциклы могут также находиться в виде N-оксидов или в виде четвертичных солей. Циклические атомы серы могут быть окислены до сульфоксида или до сульфона. Так, например, тетрагидротиенильный остаток может присутствовать как S,S-диоксотетрагидротиенильный остаток, или тиоморфолинильный остаток, такой как 4-тиоморфолинил, может присутствовать как 1-оксо-4-тиоморфолинил или 1,1-диоксо-4-тиоморфолинил. Замещенная группа Het, которая может находиться в определенном положении соединений формулы I, может независимо от другой группы Het быть замещенной заместителями, выбранными из любой желательной подгруппы заместителей, перечисленных выше, и/или в определении данной группы.
Разъяснения, касающиеся остатка Het, соответственно, могут применяться к двухвалентным остаткам Het, включая двухвалентные гетероароматические остатки, которые могут быть связаны через любые два циклические атома углерода и в случае азот-содержащих гетероциклов, через любой атом углерода и любой подходящий атом азота в цикле, или через любые два подходящие атома азота. Например, пиридиндиильный остаток может представлять собой 2,3-пиридиндиил, 2,4-пиридиндиил, 2,5-пиридиндиил, 2,6-пиридиндиил, 3,4-пиридиндиил или 3,5-пиридиндиил, а пиперидиндиильный остаток может представлять собой, в числе прочих, 1,2-пиперидиндиил, 1,3-пиперидиндиил, 1,4-пиперидиндиил, 2,3-пиперидиндиил, 2,4-пиперидиндиил или 3,5-пиперидиндиил, а пиперазиндиильный остаток может представлять собой, в числе прочих, 1,3-пиперазиндиил, 1,4-пиперазиндиил, 2,3-пиперазиндиил, 2,5-пиперазиндиил, и др. Выше приведенные определения также соответственно применяются к подгруппе Het в группах Het-алкил-. Примерами таких групп Het-алкил-, которые также могут быть незамещенными или замещенными по подгруппе Het, а также по алкильной подгруппе, являются (2-пиридил)метил, (3-пиридил)метил, (4-пиридил)метил, 2-(2-пиридил)этил, 2-(3-пиридил)этил или 2-(4-пиридил)этил.
Галоген обозначает фтор, хлор, бром или иод, предпочтительно фтор, хлор или бром, особенно предпочтительно хлор или бром.
Оптически активные атомы углерода, присутствующие в соединениях формулы I, могут независимо друг от друга иметь конфигурацию R или S. Соединения формулы I могут присутствовать в виде чистых энантиомеров, или чистых диастереомеров, или в виде смесей энантиомеров и/или диастереомеров, например, в виде рацематов. Настоящее изобретение относится к чистым энантиомерам и смесям энантиомеров, а также к чистым диастереомерам и смесям диастереомеров. Данное изобретение включает смеси двух или более стереоизомеров формулы I, а также оно включает все соотношения стереоизомеров в смесях. В случае, если соединения формулы I могут присутствовать в виде Е-изомеров или Z-изомеров (или цис-изомеров или транс-изомеров), данное изобретение относится как к чистым Е-изомерам, так и к чистым Z-изомерам, а также к смесям E/Z в любых соотношениях. Данное изобретение также включает все таутомерные формы соединения формулы I.
Диастереомеры, включая E/Z изомеры, могут быть разделены на индивидуальные изомеры, например, с помощью хроматографии. Рацематы могут быть разделены на два энантиомера обычными методами, например, методом хроматографии на хиральных фазах, или методом кристаллизации диастереомерных солей, полученных с оптически активными кислотами или основаниями. Стереохимически однородные соединения формулы I также могут быть получены путем применения стереохимически однородных исходных веществ, или путем использования стереоселективных реакций.
Выбор введения в соединение формулы I билдинг-блока с конфигурацией R или S, или, в случае присутствия в соединении формулы I аминокислотной единицы, введения билдинг-блока, представляющего собой D-аминокислоту или L-аминокислоту, может зависеть, например, от желаемых характеристик соединения формулы I. Например, введение D-аминокислотного билдинг-блока может обеспечивать повышенную стабильность in vitro или in vivo. Введение D-аминокислотного билдинг-блока может также способствовать достижению желаемого увеличения или уменьшения фармакологической активности данного соединения. В некоторых случаях может быть желательным, чтобы соединение оставалось активным в течение только короткого промежутка времени. В таких случаях, введение в соединение L-аминокислотного билдинг-блока создает возможность для расщепления соединения in vivo под действием эндогенных пептидаз субъекта, ограничивая таким образом воздействие активного соединения на субъекта. Подобный эффект может также наблюдаться в соединениях данного изобретения в результате изменения конфигурации другого билдинг-блока с S на R, или наоборот. Принимая во внимание медицинские нужды, специалист в данной области может определить желаемые характеристики, например, подходящую стереохимию, требуемого соединения данного изобретения.
Физиологически приемлемыми солями соединений формулы I являются нетоксичные соли, которые являются физиологически допустимыми, в особенности соли, используемые в фармацевтике. Такими солями соединений формулы I, содержащих кислые группы, например, карбоксильную группу СООН, являются, например, соли щелочных металлов или соли щелочноземельных металлов, такие как соли натрия, соли калия, соли магния и соли кальция, а также соли, образованные с физиологически приемлемыми четвертичными ионами аммония, такими как тетраметиламмоний или тетраэтиламмоний, и соли кислотного добавления с аммиаком и физиологически приемлемыми органическими аминами, такими как метиламин, диметиламин, триметиламин, этиламин, триэтиламин, этаноламин или трис-(2-гидроксиэтил)амин. Основные группы, содержащиеся в соединениях формулы I, например, аминогруппы, амидиногруппы или гуанидиногруппы, образуют адитивные кислотные соли, например, с такими неорганическими кислотами, как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота или фосфорная кислота, или с органическими карбоновыми и сульфоновыми кислотами, такими как муравьиная кислота, уксусная кислота, щавелевая кислота, лимонная кислота, молочная кислота, яблочная кислота, янтарная кислота, малоновая кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, виннокаменная кислота, метансульфоновая кислота или п-толуолсульфоновая кислота. Соединения формулы I, которые одновременно содержат основную группу и кислотную группу, например, амидиногруппу и карбоксильную группу, могут также присутствовать в виде цвиттерионов (бетаинов), которые также включены в объем настоящего изобретения.
Соли соединений формулы I могут быть получены с помощью обычных методов, известных специалистам в данной области, например, путем объединения соединения формулы I с неорганическими или органическими кислотой или основанием в растворителе или дисперсанте, или из другой соли путем катионного или анионного обмена. Настоящее изобретение также включает все соли соединений формулы I, которые, вследствие низкой физиологический переносимости, не являются непосредственно подходящими для применения в фармацевтике, но могут использоваться, например, как промежуточные соединения для проведения дальнейших химических модификаций соединений формулы I, или как исходные вещества для получения физиологически приемлемых солей.
Кроме того, настоящее изобретение включает все сольваты соединений формулы I, например, гидраты, или аддукты со спиртами. Данное изобретение также включает производные и модификации соединений формулы I, например, пролекарства, защищенные формы и другие физиологически приемлемые производные, включая сложные эфиры и амиды, а также активные метаболиты соединений формулы I. Такие сложные эфиры и амиды представляют собой, например, (C1-C4)-алкильные сложные эфиры, незамещенные амиды или (C1-C4)-алкиламиды. Данное изобретение в особенности относится к пролекарственным и защищенным формам соединений формулы I, которые могут быть превращены в соединения формулы I в физиологических условиях. Подходящие пролекарственные формы соединения формулы I, т.е. химически модифицированные производные соединений формулы I, обладающие улучшенными в желательном направлении свойствами, например, в отношении растворимости, биодоступности или длительности действия, известны специалистам в данной области. Более детальную информацию, касающуюся пролекарственных форм, можно найти в обычной литературе, такой, как, например, Design of Prodrugs, H.Bundgaard (ed.), Eisevier, 1985, Fleisher et al., Advanced Drug Delivery Reviews 19 (1996) 115-130; или H.Bundgaard, Drugs of the Future 16 (1991) 443, которые все включены в данный документ в качестве ссылки. Подходящими пролекарственными формами соединений формулы I в особенности являются сложноэфирные и амидные пролекарственные формы карбоксильных кислотных групп, а также ацильные и карбаматные пролекарственные формы способных к ацилированию азотсодержащих групп, таких как аминогруппы, амидиногруппы и гуанидиногруппы. В ацильных и карбаматных пролекарственных формах один или несколько, например, один или два, атома водорода на атомах азота таких групп замещены на ацильную группу или карбаматную группу. Подходящими ацильными и карбаматными группами для ацильных и карбаматных пролекарственных форм являются, например, группы Rp1-CO- и Rp2O-СО-, в которых Rp1 обозначает водород, (C1-C18)-алкил, (С3-С8)-циклоалкил, (С3-С8)-циклоалкил-(C1-C4)-алкил-, (C6-C14)-арил, Het-, (C6-C14)-арил-(C1-C4)-алкил- или Het-(C1-C4)-алкил-, и в которых Rp2 имеет значения, определенные для Rp1, за исключением водорода.
С другой стороны, концепция превращения соединения формулы I в производное или пролекарственную форму может также рассматриваться с точки зрения защиты или маскировки таких функциональных групп, как аминогруппы, амидиногруппы, гуанидиногруппы, карбоксильные группы и др., которые присутствуют в соединении формулы I. Как уже указано, настоящее изобретение также относится ко всем таким защищенным формам, для которых некоторые детали далее приведены в примерах.
Например, соединения данного изобретения могут быть химически модифицированы или защищены по любой аминогруппе так, что аминогруппа несет в качестве заместителя, например, ацетил, циклопентилкарбонил, аллилоксикарбонил, пропилоксикарбонил, бензоил или другую такую группу, в данных группах, как описано выше, могут необязательно присутствовать дополнительные заместители. Термин аминогруппа в данном документе используется в широком смысле для обозначения любой, способной к ацетилированию, аминогруппы, включая первичную или вторичную аминогруппу. Такие аминогруппы могут находиться, например, на N-конце соединения формулы I, или в качестве заместителей на алкильных или арильных группах, или на боковой цепи аминокислотного билдинг-блока, например, в группах R96, R97 или R2. Термин N-конец относится к α-аминогруппе первой аминокислотной единицы, присутствующей в соединении формулы I, записанном в традиционной манере представления пептида, т.е. к группе R1(R91)N. Конкретно, N-конец соединения данного изобретения может быть защищен путем связывания его с аминозащитной группой.
Термин защитная группа (или блокирующая группа) используется в данном документе в широком смысле для обозначения традиционной химической группы, которая может замещать атом водорода, присутствующий в аминогруппе, и которую вводят путем взаимодействия аминогруппы с аминозащитным реагентом, включая, например, α-аминогруппу, находящуюся на N-конце соединения данного изобретения. Аминозащитная группа защищает другую реакционноспособную аминогруппу от нежелательных реакций, которые могут происходить, например, в результате действия экзопептидазы на конечное соединение формулы I, а также, например, в процессе процедуры синтеза или хранения соединения. Как уже упомянуто, модификация аминогруппы может также обеспечивать дополнительные преимущества, включая, например, увеличение растворимости или биодоступности соединения. Различные аминозащитные группы известны в данной области и включают, например, ацильные группы, такие как формильная, ацетильная, пиколоильная, трет-бутилацетильная, трет-бутилоксикарбонильная, аллилоксикарбонильная, бензилоксикарбонильная или бензоильная группы, а также аминоацильные остатки, которые сами могут быть модифицированы с помощью аминозащитной группы. Другие аминозащитные группы описаны, например, в Gross and Meienhofer (eds.), The Peptides, vol. 3, Academic Press, 1981, или в Greene and Wuts, Protective Группы в Organic Synthesis, 2nd ed., pages 309-405, John Wiley&Sons, 1991, каждый из которых включен в данный документ в качестве ссылки. Продукт любой такой модификации N-концевой аминогруппы соединения формулы I называют N-концевым производным.
Выше приведенные утверждения, относящиеся к защитным группам аминогрупп соединений формулы I, соответственно применяются к защитным группам амидиногрупп и гуанидиногрупп. Как и в аминогруппе, в данных последних группах, которые, например, могут представлять остаток R95, атом водорода может быть замещен ацильной группой, такой, как, например, формил, ((C1-C4)-алкил)карбонил, ((C1-C4)-алкил)оксикарбонил, (С6-С14)-арилкарбонил, (С6-С14)-арил-(C1-C4)-алкилоксикарбонил и др., для того, чтобы улучшить профиль свойств соединения формулы I желательным образом.
Подобным образом, соединения данного изобретения могут быть химически модифицированы по любой карбоксильной группе путем введения карбоксизащитной группы. Термин защитная группа (или блокирующая группа) также используется в данном документе в широком смысле для обозначения традиционной химической группы, которая может замещать атом водорода, или гидроксильную группу, или оксогруппу карбоксильной группы (СООН) или всю карбоксильную группу. Карбоксильные группы, которые преимущественно могут присутствовать в защищенной или модифицированной форме, могут находиться, например, в качестве заместителей на алкильных или арильных группах или на боковых цепях аминокислотных билдинг-блоков, например, в группах R96, R97 и R2. Карбоксильная группа может быть защищена или модифицирована, например, путем обычного восстановления карбоксильной группы или ее производного, такого как сложный эфир, что приводит к образованию спиртовой группы СН2OН или альдегидной группы СНО, которые замещают группу СООН. Карбоксильная группа также может быть защищена путем превращения группы СООН в сложноэфирную группу, например, путем образования сложного эфира, пригодного для перорального применения. Сложные эфиры, пригодные для перорального применения, хорошо известны в данной области и включают, например, алкилоксиметиловые сложные эфиры, такие как (C1-C4)-алкилоксиметиловые сложные эфиры, такие как метоксиметиловый, этоксиметиловый, изопропоксиметиловый сложные эфиры и т.п.; 1-(C1-C4)-алкилоксиэтиловые сложные эфиры, такие как 1-метоксиэтиловый, 1-этоксиэтиловый, 1-пропоксиэтиловый, 1-изопропоксиэтиловый сложные эфиры и т.п.; 2-оксо-1,3-диоксолен-4-илметиловые сложные эфиры, такие как 5-метил-2-оксо-1,3-диоксолен-4-илметиловый, 5-фенил-2-оксо-1,3-диоксо-лен-4-илметиловый сложные эфиры и т.п.; (C1-C4)-алкилтиометиловые сложные эфиры, такие как метилтиометиловый, этилтиометиловый, изопропилтиометиловый сложные эфиры и т.п.; ацилоксиметиловые сложные эфиры, такие как пивалоилоксиметиловый, ацетоксиметиловый сложные эфиры и т.п.; 1-этоксикарбонилметиловый сложный эфир; 1-ацилокси-1-замещенные метиловые сложные эфиры, такие как 1-ацетоксиэтиловый; 3-фталидиловый или 5,6-диметил-3-фталидиловый сложные эфиры; 1-((C1-C4)-алкилоксикарбонилокси)этиловые сложные эфиры, такие как 1-(этоксикарбонилокси)этиловый сложный эфир; и 1-((C1-C4)-алкиламинокарбонилокси)этиловые сложные эфиры, такие как 1-(метиламинокарбонилокси)этиловый сложный эфир. Карбоксильная группа может быть также модифицирована путем замены всей карбоксильной группы на такой заместитель, как 2-тиазолил, тетразолил, циклогексил или на другую группу. Карбоксизащитные группы, подобные описанным выше, хорошо известны в данной области (см., например, Greene and Wuts, loc. cit, pages 224-276, который включен в данный документ в качестве ссылки) и защищают карбоксильную группу от нежелательных реакций, как разъяснялось выше в отношении аминозащитной группы.
Структурная единица -N(R92)-С(R96)(R97)-CO-, присутствующая в соединениях формулы I, представляет остаток α-аминокислоты, который формально получают из соответствующей α-аминокислоты путем удаления атома водорода из N-концевой аминогруппы и гидроксильной группы из С-концевой карбоксильной группы, что является обычной процедурой в пептидной химии. Группы R9 и/или R97 могут таким образом относиться к соответствующим группам, связанным с центральным атомом углерода α-аминокислоты, т.е. в случае α-монозамещенной α-аминокислоты группа R96 соответствует атому водорода, присоединенному к центральному атому углерода, а группа R97 соответствует боковой цепи аминокислоты. Как отмечено ниже, структурная единица -N(R92)-C(R96)(R97)-CO- может быть включена в соединения формулы I с помощью синтетических методов путем применения в качестве билдинг-блока соответствующей аминокислоты формулы HN(R92)-C(R96)(R97)-СООН. Исходные аминокислоты, из которых может быть получена структурная единица -N(R92)-С(R96)(R97)-СО-, могут быть природными или неприродными аминокислотами, примерами которых являются Aad, Asn, Asp, Gln, Glu, hGIn или hGlu. Функциональные группы в таких аминокислотах могут находиться в защищенном виде, или могут быть дериватизированными. Подобным образом, единица -N(R91)-CH(-(CH2)-(замещенный фенил))-СО-, присутствующая в соединениях формулы I, представляет остаток α-аминокислоты.
Помимо соединений формулы I, определение которых описано вначале, вторым предметом настоящего изобретения являются также соединения формулы I, в которых все остатки, группы и количества определены, как описано в начале, за исключением того, что остатки R98 и R99, которые во втором воплощении данного изобретения являются независимыми друг от друга и могут быть одинаковыми или разными, и являются выбранными из группы, включающей водород, гидроксикарбонил-, (C1-C8)-алкилоксикарбонил-, (C6-C14)-арилоксикарбонил-, (С6-С14)-арил-(C1-C4)-алкилоксикарбонил-, аминокарбонил-, (C1-C8)-алкиламинокарбонил-, тетразолил, -P(O)(OH)2, -S(O)2OH и S(O)2NH2, во всех их стереоизомерных формах, а также их смесях в любых соотношениях, и их физиологически приемлемые соли, при условии, что в данном втором воплощении настоящего изобретения соединения ацетил-(4-амидинофенилаланил)-циклогексилглицил-(4-метилпиридинийметил)амид, ацетил-(4-амидинофенилаланил)-циклогексилглицил-(2-(3-метилпиридиний)этил)амид, ацетил-(4-амидинофенилаланил)-циклогексилглицил-(2-(4-метилпиридиний)этил)амид, ацетил-(4-амидинофенилаланил)-циклогексилглицил-(4-амидинобензил)амид, ацетил-(4-амидинофенилаланил)-циклогексилглицил-(3-амидинобензил)амид и ацетил-(4-амидинофенилаланил)-циклогексилглицил-(1-(4-метилпиридиний)этил)амид исключаются. Для данного второго воплощения настоящего изобретения соответственно могут применяться определения, приведенные выше и ниже, например, относящиеся к алкильным группам, арильным группам или гетероциклическим группам, или к солям или стереоизомерным формам соединений, а также относящиеся к предпочтительным значениям. В данном втором воплощении настоящего изобретения более предпочтительным значением R98 и R99, независимо друг от друга, является водород. В качестве примеров исходных аминокислот, из которых в данном втором воплощении настоящего изобретения может быть получена структурная единица -N(R92)-C(R96)(R97)-CO-, могут быть упомянуты Aad, Ala, Asn, Asp, Gln, Glu, hAla, hGln, hGlu, His, hIle, hLeu, hPhe, hTrp, hTyr, Ile, Leu, Nle, Nva, Phe, Phg, Thi, Trp, Tyr, Val, трет-бутилглицин (Tbg), неопентилглицин (Npg), циклогексилглицин (Chg), циклогексилаланин (Cha), 2-тиенилаланин (Thia), 2,2-дифениламиноуксусная кислота или 2-(п-хлорфенил)аминоуксусная кислота (cf. Houben-Weyl, Methoden der organischen Chemie [Methods of Organic Chemistry], Volume 15/1 и 15/2, Georg Thieme Verlag, Stuttgart, 1974), где функциональные группы данных аминокислот могут находиться в защищенной форме или могут быть дериватизированы.
Структурные элементы в соединениях формулы I имеют следующие предпочтительные значения, которые они могут иметь независимо от значений других элементов.
Число r, т.е. количество групп СН2 в полиметиленовой цепи, связывающей фенильную группу, изображенную на формуле I, и атом углерода, который несет аминогруппу R1(R91)N, предпочтительно равно 0, 1 или 2, более предпочтительно 0 или 1, особенно предпочтительно 1. Таким образом, предпочтительно группа -(СН2)r- представляет собой прямую связь, или одну из групп -СН2- или -СН2-СН2-, более предпочтительно, прямую связь или группу -СН2-, особенно предпочтительно, группу -CH2-.
Число s, т.е. количество заместителей R94, присутствующих на фенильной группе, изображенной на формуле I, предпочтительно равно 0, 1 или 2, более предпочтительно 0 или 1, особенно предпочтительно 0. В случае, если все заместители R94, присутствующие на фенильной группе, представляют собой атомы галогенов, особенно, атомы фтора, более предпочтительным значением s является 4. Положения на фенильной группе, с которыми не связаны ни заместитель R94, ни группа R95-(CH2)t-, несут атомы водорода. Если, например, s равно 0, фенильная группа несет группу R95-(CH2)t-, которая присутствует в соединениях формулы I с любой частотой, и четыре атома водорода. Группа R95-(CH2)t- может присутствовать в любом желательном положении фенильного цикла, т.е. в положении 2, 3 или 4. Предпочтительно, группа R95-(СН2)t- находится в положении 3 или 4, более предпочтительно, она находится в положении 4 (по отношению к группе (СН2)r). Заместители R94 могут находиться в любом желательном положении фенильной группы, не занятом группой R95-(CH2)t-. Таким образом, если группа R95-(СН2)t- находится в положении 4 и s равно 1, единственный заместитель R94 может находиться в положении 2 или 3, где положение 3 является предпочтительным, если группа R95-(CH2)t- находится в положении 3 (по отношению к группе (СН2)r) и s равно 1, единственный заместитель R94 может находится в положении 2, 4, 5 или 6, где положение 4 является предпочтительным. Если группа R95-(CH2)t- находится в положении 4 и s равно 2, два заместителя R94 могут находиться в положениях 2,3, 2,5, 2,6 или положениях 3,5, где положения 3,5 являются предпочтительными.
Число t, т.е. количество групп CH2 в полиметиленовой цепи, связывающей фенильную группу, изображенную на формуле I, и группу R95, предпочтительно равно 0 или 1, более предпочтительно, 0. Таким образом, предпочтительно, группа -(CH2)t- представляет собой прямую связь или группу -СН2-. Более предпочтительно, группа -(CH2)t- представляет собой прямую связь, т.е. группа R95 непосредственно связана с фенильной группой.
R1 предпочтительно представляет R11-CO- или R12-SO2-, более предпочтительно, R11-СО-.
R11 предпочтительно обозначает (C1-C8)-алкил, (С6-С14)-арил, (C6-C14)-арил-(C1-C4)-алкил, (C1-C8)-алкилокси- или (С6-С14)-арил-(C1-C4)-алкилокси-, где все указанные группы могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. Более предпочтительно, R11 обозначает (C1-C8)-алкил, (C6-C14)-арил или (C1-C8)-алкилокси-, особенно предпочтительно, (С6-С14)-арил или (C1-C8)-алкилокси-, где все указанные группы могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. (C1-C8)-алкильная группа, представляющая R11, или присутствующая в группе, представляющей R11, предпочтительно, представляет собой (C2-C8)-алкильную группу, более предпочтительно, (С2-С6)-алкильную группу, например, аллильную группу или группу циклопропилметил-. (С6-С14)-арильная группа, представляющая R11, или присутствующая в группе, представляющей R11, предпочтительно, представляет собой (С6-С10)-арильную группу, более предпочтительно, фенильную группу. Таким образом, среди особенно предпочтительных групп, представляющих R11, присутствуют, например, (C2-C6)-алкилокси- и фенил, причем указанные группы могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40.
Как указано выше по отношению к алкильным группам в общем, алкильная группа, представляющая R11, или присутствующая в группе, представляющей R11, может быть насыщенной или ненасыщенной и может быть ациклической или циклической. Предпочтительно, алкильная группа, представляющая R11, или присутствующая в группе, представляющей R11, представляет собой ненасыщенную ациклическую алкильную группу или насыщенную алкильную группу, содержащую циклическую группу, такую как циклоалкильную группу, или группу циклоалкил-алкил-. Более предпочтительно, такая алкильная группа представляет собой ненасыщенную ациклическую алкильную группу, например, алкильную группу, содержащую одну или две двойные связи и/или тройные связи, предпочтительно одну или две двойные связи или одну тройную связь, особенно предпочтительно, одну двойную связь, или группу циклоалкил-алкил-. Особенно предпочтительно, такая алкильная группа представляет собой ненасыщенную ациклическую алкильную группу. Примерами таких предпочтительных алкильных групп, представляющих R11, или присутствующих, например, в группе алкилокси-, представляющей R11, являются этенил (=винил) СН2=СН-, 1-пропенил СН3-СН=СН-, 2-пропенил (=аллил) СН2=СН-СН2-, Е- и Z-2-бутенил СН3-СН=СН-СН2-, 3-метил-2-бутенил (СН3)2С=СН-СН2, 1,3-пентадиенил СН3-СН=СН-СН=СН-, циклопропил, циклопропилметил-, 2-циклопропилэтил-, циклопентил, циклопентилметил-, циклогексил или циклогексилметил-. Таким образом, в предпочтительном воплощении настоящего изобретения R11 представляет собой ненасыщенную (С2-С8)-алкилокси-, особенно, ненасыщенную (С2-С6)-алкокси-, особенно, ненасыщенную (С3-С6)-алкилокси-, содержащую одну или две двойные связи, особенно, одну двойную связь, или представляет собой насыщенную (С3-С6)-циклоалкил-(C1-C2)-алкилокси-, особенно, насыщенную (С3-С6)-циклоалкил-метилокси-, особенно, циклопропилметилокси-, или представляет собой фенил, где алкилокси-, циклоалкилалкилокси- и фенильная группы могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. В более предпочтительном воплощении настоящего изобретения R11 представляет собой ненасыщенную (C2-C6)-алкилокси-, содержащую одну двойную связь, особенно, ненасыщенную (С3-С6)-алкилокси-, особенно аллилокси-, или циклопропилметилокси-, где группы алкилокси-, аллилокси- и циклопропилметилокси- могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. В особенно предпочтительном воплощении настоящего изобретения R11 представляет собой ненасыщенную (С2-С6)-алкилокси-, содержащую одну двойную связь, особенно, ненасыщенную (С3-С6)-алкилокси-, особенно аллилокси-, где группы алкилокси- и аллилокси- могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40.
Если группа R11 замещена одним или несколькими заместителями R40, она предпочтительно замещена одним, двумя или тремя одинаковыми или разными заместителями R40, особенно предпочтительно, одним или двумя заместителями R40. Заместители R40, присутствующие на группе R11, предпочтительно являются одинаковыми или разными группами, выбранными из группы, включающей галоген, (C1-C4)-алкил и трифторметил, где галоген предпочтительно представляет собой фтор, хлор или бром, особенно, бром или хлор. Заместители R40 могут присутствовать в любом желательном положении группы R11.
R12 предпочтительно представляет собой (C1-C8)-алкил, (С6-С14)-арил, особенно предпочтительно, (C1-C8) -алкил или (С6-С10)-арил, где все указанные группы могут быть незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. Если группа R12 замещена одним или несколькими заместители R40, она предпочтительно замещена одним, двумя или тремя одинаковыми или разными заместителями R40, особенно предпочтительно, одним или двумя заместителями R40. Заместители R40, присутствующие на группе R12, предпочтительно являются одинаковыми или разными группами, выбранными из группы, включающей галоген, (C1-C4)-алкил, ацетиламино, нитро и трифторметил, где галоген предпочтительно представляет собой фтор, хлор или бром, особенно, бром или хлор. Заместители R40 могут присутствовать в любом желательном положении группы R12.
R2 предпочтительно представляет собой R21(R22)CH-, R23-Het-(CH2)k-, R23(R24)N-(CH2)m-D-(CH2)n- или R25(R26)N-CO-(CH2)p-D-(CH2)q-, особенно предпочтительно, R21(R22)CH-, R23-Het-(CH2)k- или R23(R24)N-(CH2)m-D-(CH2)n-.
Группа Het, которая присутствует в группе R23-Het-(СН2)k-, предпочтительно, представляет собой 5- или 6-членную моноциклическую или 9- или 10-членную бициклическую насыщенную или ароматическую гетероциклическую группу, содержащую 1 или 2, особенно, 1, одинаковых или разных гетероатома, которые выбраны из группы, включающей азот, кислород и серу, и которые предпочтительно представляют собой атомы азота. Более предпочтительно, такая группа Het представляют собой 5- или 6-членную моноциклическую насыщенную или ароматическую гетероциклическую группу. Группа Het в группе R23-Het-(СН2)k- может быть связана с группой -(CH2)k- через атом углерода или подходящий атом азота. Предпочтительно, она связана через атом углерода. Группа Het в группе R23-Het-(CH2)k- может быть незамещенной, т.е. нести только группу R23, и не нести никаких дополнительных заместителей, или она может быть замещенной, т.е. нести, кроме R23, дополнительные заместители, как описано выше для гетероциклических групп в общем. Если группа Het несет, кроме R23, дополнительные заместители, она предпочтительно несет один, два или три одинаковых или разных заместителя, выбранных из группы, включающей (C1-C4)-алкил, (C1-C4)-алкилокси, галоген, амино, (C1-C4)-алкиламино-, ди-((C1-C4)-алкил)-амино, трифторметил, гидрокси и оксо.
Группа R23, присутствующая в группе R23-Het-(CH2)k-, может быть связана с любым желательным и подходящим положением в группе Het. В случае, если группа R23 в группе R23-Het-(CH2)k- представляет собой R27-SO2- или R28-CO-, группа Het предпочтительно представляет собой частично ненасыщенную или насыщенную группу, особенно, насыщенную группу, и содержит циклический атом азота, который не связан с группой (CH2)k, с указанным циклическим атомом азота связана группа R23. В случае, если R23 в группе R23-Het-(CH2)k- представляет собой R27-SO2- или R28-CO-, группа Het в группа R23-Het-(CH2)r особенно предпочтительно представляет собой насыщенный 5-членный или 6-членный цикл, который содержит один атом азота в качестве циклического гетероатома, т.е. группу пирролидин или пиперидин, и который связан с группой (CH2)k через положение 3 в случае пирролидиновой группы, или через положение 3 или 4, особенно, через положение 4, в случае пиперидиновой группы, и атом азота которого несет группу R23. В случае, если группа Het в группе R23-Het-(СН2)k- представляет собой ароматическую гетероциклическую группу, то группа R23 в группе R23-Het-(CH2)k- предпочтительно представляет собой водород.
D предпочтительно представляет собой двухвалентный остаток -C(R31)(R32)-, двухвалентный (C6-C10)-ариленовый остаток или двухвалентный остаток, полученный из ароматической моноциклической или бициклической группы Het, содержащей от 5 до 10 циклических атомов, из которых 1 или 2 являются одинаковыми или разными циклическими гетероатомами, выбранными из группы, включающей азот, кислород и серу. D более предпочтительно представляет собой двухвалентный остаток -С(R31)(R32)-, двухвалентный фениленовый остаток, особенно, 1,3-фенилен или 1,4-фенилен, или двухвалентный остаток, полученный из ароматической моноциклической группы Het, содержащей 5 или 6 циклических атомов, из которых 1 или 2 являются одинаковыми или разными циклическими гетероатомами, выбранными из группы, включающей азот, кислород и серу. D особенно предпочтительно представляет собой двухвалентный остаток -C(R31)(R32) - или двухвалентный фениленовый остаток. В ароматической группе Het, представляющей D, предпочтительно 1 или 2 атома азота присутствуют в виде циклических гетероатомов. Ариленовые группы и группы Het, представляющие D, могут быть замещенными, как описано выше для таких групп в общем.
Числа k, m, n, р и q предпочтительно равны независимо друг от друга 0, 1, 2 или 3, более предпочтительно, 0, 1 или 2, особенно предпочтительно, 0 или 1, при условии, что в случае, если D представляет собой -C(R31)(R32)-, сумма m+n не может быть равна 0, и сумма p+q не может быть равна 0. Число k особенно предпочтительно равно 0. В соединениях формулы I, в которых D представляет собой -C(R31)(R32)- и оба R31 и R32 представляют собой водород, сумма m+n предпочтительно равна 2.
(C1-C12)-алкильная группа, представляющая группы R21 или R22, предпочтительно представляет собой ациклическую (C1-C8)-алкильную группу, (С3-С8)-циклоалкильную группу, или группу (С3-С8)-циклоалкил-(C1-C4)-алкил-, где (C1-C4)-алкильная группа является ациклической. R21 и R22 предпочтительно независимо друг от друга представляют собой водород, ациклический (C1-C8)-алкил, (С3-С8)-циклоалкил, (С3-С8)-циклоалкил-(C1-C4)-алкил-, (С6-С10)-арил, (С6-С10)-арил-(C1-C4)-алкил-, Het- или Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными, как указанно выше, и где (C1-C4)-алкильная группа является ациклической, или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют цикл, как указано выше. Более предпочтительно, одна из групп R21 и R22 представляет собой водород или (C1-C4)-алкил, а другая из групп R21 и R22 представляет собой водород, ациклический (C1-C8)-алкил, (С3-С8)-циклоалкил, (С3-С8)-циклоалкил-(C1-C4)-алкил, (С6-С10)-арил, (С6-С10)-арил-(C1-C4)-алкил-, Het- или Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными, как указано выше, и где (C1-C4)-алкильная группа является ациклической, или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют цикл, как указано выше. Особенно предпочтительно, одна из групп R21 и R22 представляет собой водород или ациклический (C1-C4)-алкил, а другая из групп R21 и R22 представляет собой водород, ациклический (C1-C4)-алкил, (С3-С7)-циклоалкил, (С6-С10)-арил или Het-, где все указанные группы являются незамещенными или замещенными, как указанно выше, или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют цикл, как указано выше.
Группа Het, присутствующая в R21 или R22, предпочтительно представляет собой моноциклическую или бициклическую насыщенную или ароматическую гетероциклическую группу, содержащую от 5 до 10 циклических атомов, предпочтительно моноциклическую насыщенную или ароматическую группу, содержащую 5 или 6 циклических атомов, из которых 1 или 2, предпочтительно 1, являются гетероатомами, выбранными из группы, включающей азот, кислород и серу, и предпочтительно представляют собой азот. Группа R21 или R22, которая замещена одним или несколькими заместителями, предпочтительно является замещенной 1, 2 или 3 одинаковыми или разными заместителями. Заместители, присутствующие в R21 или R22, предпочтительно являются выбранными из группы, включающей галоген, гидрокси, (C1-C4)-алкилокси-, (C1-C4)-алкил, (C1-C4)-алкилсульфонил-, трифторметил, ацетиламино-, амино, амидино, гуанидино, оксо, нитро, циано, (C1-C4)-алкиламино-, ди-((C1-C4)-алкил)-аминоаминокарбонил- и аминокарбонил-(C1-C4)-алкил-.
Насыщенная или ненасыщенная карбоциклическая структура, которая может быть образована R21 и R22 вместе с атомом углерода, с которым они связаны, может содержать 3, 4, 5, 6, 7 или 8 циклических атомов. Предпочтительно, такой цикл представляет собой насыщенную или ненасыщенную циклопентановую или циклогексановую структуру. По одной или двум связям цикл, образованный R21 и R22 вместе с атомом углерода, с которым они связаны, может быть конденсированным (или сопряженным) с одинаковыми или разными ароматическими циклами, которые предпочтительно выбраны из группы, включающей бензол, нафталин, 5- или 6-членные моноциклические гетероароматические структуры, и 9- или 10-членные бициклические гетероароматические структуры, где гетероароматические структуры предпочтительно содержат 1 или 2 одинаковых или разных гетероатома, выбранных из группы, включающей азот, кислород и серу. Более предпочтительно, ароматические циклы, конденсированные по связи углерод-углерод цикла, образованного R21 и R22 вместе с атомом углерода, с которым они связаны, выбраны из группы, включающей бензол и 5- или 6-членные моноциклические гетероароматические циклы, содержащие 1 или 2 одинаковых или разных гетероатома, особенно, 1 гетероатом, выбранных из группы, включающей азот, кислород и серу. Особенно предпочтительным ароматическим циклом, который может быть конденсированным по связи, находящейся в цикле, образованном R21 и R22 вместе с атомом углерода, с которым они связаны, является бензольный цикл.
Полученная группа R21(R22)CH-, в которой R21 и R22 вместе с атомом углерода, с которым они связаны, образуют цикл, и которая необязательно содержит конденсированные ароматические циклы, может быть незамещенной или замещенной по любому желательному положению цикла, образованного R21 и R22 вместе с атомом углерода, с которым они связаны, и/или по любому желательному положению необязательно конденсированных ароматических циклов. Если полученная циклическая группа R21(R22)CH- является замещенной, она предпочтительно замещена одним или несколькими, например 1, 2 или 3, одинаковыми или разными заместителями, как указанно выше. Предпочтительно, заместители, присутствующие в полученной циклической группе R21(R22)CH-, выбраны из группы, включающей галоген, гидрокси, (C1-C4)-алкилокси-, (C1-C4)-алкил, (C1-C4)-алкилсульфонил-, трифторметил, ацетиламино-амино, амидино, гуанидино, оксо, нитро, циано, (C1-C4)-алкиламино-, ди-((C1-C4)-алкил)-амино-, аминокарбонил- и аминокарбонил-(C1-C4) -алкил-, особенно, из группы, включающей ацетиламино-, амино, (C1-C4)-алкиламино- и ди-((C1-C4)-алкил)-амино-.
R24 предпочтительно представляет собой водород, (C1-C8)-алкил или (C6-C14)-арил-(C1-C4)-алкил-, более предпочтительно, водород, (C1-C4)-алкил или фенил-(C1-C4)-алкил-, особенно, водород или (C1-C4)-алкил, где алкильные группы предпочтительно являются ациклическими. Особенно предпочтительно, R24 представляет собой водород.
R25 и R26 предпочтительно представляют собой независимо друг от друга водород, (C1-C8)-алкил или (С6-С14)-арил-(C1-C4)-алкил-, более предпочтительно, водород, (C1-C4)-алкил или фенил-(C1-C4)-алкил-, особенно предпочтительно, водород или (C1-C4)-алкил, где все указанные группы являются незамещенными или замещенными одним или несколькими, например одним, двумя или тремя, одинаковыми или разными заместителями R40, и где алкильные группы предпочтительно являются ациклическими. Особенно предпочтительно, одна из двух групп R25 и R26 представляет собой водород, а другая представляет собой водород или отличается от водорода. Более предпочтительно, обе группы R25 и R26 представляют собой водород.
R27 предпочтительно представляет собой (C1-С8)-алкил, (C6-C14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het- или ди-((С1-С8)-алкил)амино-, более предпочтительно, (C1-C4)-алкил, (С6-С10)-арил, Het- или ди-((C1-C4)-алкил)амино-, особенно предпочтительно, (C1-C4)-алкил или (С6-С10)-арил, особенно предпочтительно, (С6-С10)-арил, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40, и где алкильные группы предпочтительно являются ациклическими. Группа Het, представляющая R27, предпочтительно представляет собой моноциклическую или бициклическую ароматическую гетероциклическую группу, содержащую от 5 до 10 атомов в цикле, предпочтительно, моноциклическую группу, содержащую 5 или 6 атомов в цикле, из которых 1 или 2 представляют собой гетероатомы, выбранные из группы, включающей азот, кислород и серу, предпочтительно, из группы, включающей азот и серу. Группа R27, которая замещена заместителями R40, предпочтительно замещена 1, 2 или 3, особенно, 1 или 2, одинаковыми или разными заместителями R40. Заместители R40, присутствующие в группе R27, предпочтительно выбраны из группы, включающей галоген, особенно, бром, хлор и фтор, (C1-C4)-алкилокси-, (C1-С4)-алкил, трифторметил, ацетиламино-, нитро и циано.
R28 предпочтительно представляет собой (C1-C8)-алкил, (С6-С14)-арил, (C6-C14)-арил-(C1-C4)-алкил-, Het-, (C1-С8)-алкилокси- или (C6-C14)-арил-(C1-C4)-алкилокси-, более предпочтительно, (C1-C4)-алкил, (С6-С10)-арил, Het-, (C1-C4)-алкилокси- или (C6-С10)-арил-(C1-C4)-алкилокси-, особенно предпочтительно, (C1-C4)-алкил, (С6-С10)-арил, (C1-C4)-алкилокси- или (С6-С10)-арил-(C1-C4)-алкилокси-, особенно предпочтительно, (C1-C4)-алкил, (C1-C4)-алкилокси- или фенил-(C1-C4)-алкилокси-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40, и где алкильные группы предпочтительно являются ациклическими. Группа Het, представляющая R28, предпочтительно представляет собой моноциклическую или бициклическую ароматическую гетероциклическую группу, содержащую от 5 до 10 циклических атомов, предпочтительно моноциклическую группу, содержащую 5 или 6 циклических атомов, из которых 1 или 2 представляют собой гетероатомы, выбранные из группы, включающей азот, кислород и серу. Группа R28, которая замещена заместителями R40, предпочтительно замещена 1, 2 или 3, особенно, 1 или 2, одинаковыми или разными заместителями R40. Заместители R40, присутствующие в группе R28, предпочтительно являются выбранными из группы, включающей галоген, особенно, бром, хлор и фтор, (C1-C4)-алкилокси-, (C1-C4)-алкил, трифторметил, ацетиламино-, нитро и циано.
(C1-C12)-алкильная группа, представляющая группы R31 или R32, предпочтительно представляет собой ациклическую (C1-C8)-алкильную группу, (С3-С8)-циклоалкильную группу, или группу (С3-С8)-циклоалкил-(C1-C4)-алкил-, где (C1-C4)-алкильная группа является ациклической. R31 и R32 предпочтительно представляют собой независимо друг от друга водород, ациклический (C1-C8)-алкил, (С6-С14)-арил-(C1-C4)-алкил, (С3-С8)-циклоалкил-(C1-C4)-алкил- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими, например одним, двумя или тремя, одинаковыми или разными заместителями R40, и где (C1-C4)-алкильные группы являются ациклическими. Предпочтительно, одна из двух групп R31 и R32 представляет собой водород, а другая представляет собой водород, или отличается от водорода. Ациклический (C1-С8)-алкил, присутствующий в группе R31 или R32, предпочтительно представляет собой ациклическую (C1-C4)-алкильную группу, а (С6-С14)-арил, присутствующий в группе R31 или в группе R32, предпочтительно представляет собой (C6-C10)-арильную группу, более предпочтительно, фенильную группу, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40. Группа Het, присутствующая в группе R31 или R32, предпочтительно представляет собой моноциклическую или бициклическую насыщенную или ароматическую гетероциклическую группу, содержащую один или два одинаковых или разных циклических гетероатома, выбранных из группы, включающей азот, кислород и серу, особенно, содержащую в качестве циклических гетероатомов один или два атома азота. Заместители R40, присутствующие в группе R31 или R32, предпочтительно, являются выбранными из группы, включающей галоген, особенно, бром, хлор и фтор, (C1-C4)-алкилокси-, (C1-C4)-алкил и трифторметил.
R91, R92 и R93 предпочтительно представляют собой независимо друг от друга водород или (C1-C4)-алкил, более предпочтительно, независимо друг от друга представляют собой водород или метил, особенно предпочтительно, водород.
R94 предпочтительно является выбранным из группы, включающей (C1-C4)-алкил и галоген, причем группы R94 являются независимыми друг от друга и могут быть одинаковыми или разными. Более предпочтительно, заместители R94 являются одинаковыми или разными атомами галогенов. Атомы галогенов, представляющие группы R34, предпочтительно представляют собой хлор и/или фтор.
R95 предпочтительно представляет собой амидиногруппу, или ее производное, такое как ((C1-C4)-алкил)оксикарбониламидино, гидроксиамидино-, или другую защищенную форму или производное амидиногруппы, как описано выше. Более предпочтительно, R95 представляет собой амидино, ((C1-C4)-алкил)оксикарбониламидино или гидроксиамидино-. Особенно предпочтительно, R95 представляет собой амидиногруппу, т.е. группу H2N-C(=NH)-, которая также называется группа аминоиминометил-, или карбамимидоильная группа.
R96 предпочтительно представляет собой водород или R98-(C1-C8)-алкил-, более предпочтительно, водород или R98-(C1-C4)-алкил. Особенно предпочтительно, R96 представляет собой водород. R98 предпочтительно представляет собой гидроксикарбонил-, (C1-C8)-алкилоксикарбонил- или аминокарбонил-, более предпочтительно, гидроксикарбонил-(C1-C4)-алкилоксикарбонил- или аминокарбонил-.
R97 предпочтительно представляет собой R99-(C1-C8)-алкил- или R99-(C6-C14)-арил-(C1-C4)-алкил-. Более предпочтительно, R97 представляет собой R99-(C1-C8)-алкил-. Как объяснялось выше для алкильной группы в общем, (C1-C8)-алкил, присутствующий в группе R97, может быть насыщенным или ненасыщенным и может быть ациклическим или циклическим. Предпочтительно, такая алкильная группа представляет собой насыщенную ациклическую алкильную группу, или насыщенную циклическую алкильную группу (=циклоалкильная группа) или насыщенную группу типа циклоалкилалкил-, более предпочтительно, насыщенную ациклическую алкильную группу, или насыщенную циклоалкильную группу, особенно предпочтительно, насыщенную ациклическую алкильную группу. В случае, если (C1-C8)-алкил, присутствующий в группе R97, представляет собой насыщенную ациклическую алкильную группу, то группа R97 предпочтительно представляет собой группу R99-(C1-C4)-алкил-, где (C1-C4)-алкил представляет собой насыщенный ациклический алкил, более предпочтительно, один из группы R99-CH2-, R99-CH2-CH2-, R99-CH2-CH2-CH2- или R99-CH2-CH2-CH2-СН2-, особенно предпочтительно, группу R99-CH2-CH2-. В случае, если (C1-C8)-алкил, присутствующий в группе R97, представляет собой насыщенную циклическую алкильную группу, то группа R97 предпочтительно представляет собой группу R99-(С3-С7)-циклоалкил-, более предпочтительно, группа R99-(С3-С6)-циклоалкил-, где циклоалкильная группа является насыщенной, особенно предпочтительно, группу R99-циклопропил-, R99-циклопентил- или R99-циклогексил-. В такой группе, как R99-(С3-С7)-циклоалкил-, например R99-циклопропил-, R99-циклопентил- или R99-циклогексил-, группа R99 может присутствовать в любом желательном положении циклоалкильной группы, в случае циклопропильной группы, например, в положении 2, в случае циклопентильной группы, например, в положении 2 или 3, в случае циклогексильной группы, например, в положении 2, 3 или 4, где положение 4 является предпочтительным. Особенно предпочтительными группами R97 являются группы R99-CH2CH2- и 2-(R99)-циклопропил, особенно предпочтительной является группа R99-CH2-CH2-.
R99 предпочтительно представляет собой гидроксикарбонил-, (C1-C8) -алкилоксикарбонил-, (C6-C14)-арил-(C1-C4)-алкилоксикарбонил, аминокарбонил-, (C1-C8)-алкиламинокарбонил- или другое производное или защищенную форму гидроксикарбонильной группы, как, например, сложный эфир или амид, как описано выше. Более предпочтительно, R99 представляет собой гидроксикарбонил-, (C1-C8)-алкилоксикарбонил-, (C6-C14)-арил-(C1-C4)-алкилоксикарбонил, аминокарбонил-, или (C1-C8)-алкиламинокарбонил-, особенно предпочтительно, гидроксикарбонил-, (C1-С8)-алкилоксикарбонил-, аминокарбонил- или (C1-C8)-алкиламинокарбонил. Более того, предпочтительно, R99 представляет собой гидроксикарбонил- или (C1-C8)-алкилоксикарбонил-. Группа (C1-C8)-алкилокси-, присутствующая в группе R99, предпочтительно представляет собой группу (C1-C4)-алкилокси-. Дпкильная группа, присутствующая в группе R99, предпочтительно представляет собой насыщенную ациклическую группу.
Предпочтительными соединениями формулы I являются такие соединения, в которых один или несколько из остатков, имеющих предпочтительные значения, или имеющих одно или несколько конкретных значений из значений, перечисленных в их соответствующих определениях и в общих разъяснениях для соответствующих остатков, причем все сочетания таких предпочтительных значений и конкретных значений являются предметом настоящего изобретения. А также все предпочтительные соединения формулы I являются предметом настоящего изобретения во всех их стереоизомерных формах и их смесях в любом соотношении, а также в виде их физиологически приемлемых солей. Кроме того, также все предпочтительные соединения формулы I являются предметом настоящего изобретения в виде их пролекарственных форм и других производных, как разъяснялось выше, например в виде их сложных эфиров, таких как (C1-C4)-алкиловые и другие сложные эфиры, и их амидов, таких как незамещенные амиды, (C1-C4)-алкиламиды и другие амиды.
Например, предпочтительными соединениями формулы I являются соединения, в которых
R1 обозначает R11-CO-;
R91 обозначает водород;
r равно 0 или 1;
s равно 0, 1 или 2;
t равно 0;
R94 выбран из группы, включающей хлор и фтор;
R95 обозначает амидино или ((C1-C4)-алкил)оксикарбониламидино-, и группа R95 присоединена по положению 4 фенильного цикла формулы I; во всех их стереоизомерных формах и их смесях в любом соотношении, а также их физиологически приемлемые соли. Соединения данного типа содержат структурную единицу, полученную из 4-амидинофенилглицина или 4-амидинофенилаланина, которая является необязательно замещенной по амидиногруппе группой ((C1-C4)-алкил)оксикарбонил-, и необязательно замещенной по фенильной группе хлором и/или фтором, и замещенной по N-концевой аминогруппе группой R11-CO-. В особенно предпочтительной группе данных соединений s равно 0 и амидиногруппа не является замещенной, т.е. особенно предпочтительными соединениями данного типа являются соединения, полученные из 4-амидинофенилглицина или 4-амидинофенилаланина, особенно предпочтительными являются соединения, полученные из 4-амидинофенилаланина, замещенные по N-концевой аминогруппе группой R11-CO-.
Предпочтительными соединениями формулы I являются также соединения, в которых
R92 и R96 обозначают водород;
R97 обозначает R99-CH2-CH2-;
R99, R97 обозначают гидроксикарбонил- или ((C1-C8)-алкил)оксикарбонил-; во всех их стереоизомерных формах и их смесях в любых соотношениях, а также их физиологически приемлемые соли. Соединения данного типа содержат структурную единицу, которая представляет собой остаток глютаминовой кислоты или ее производное, где карбоксильная кислотная группа в боковой цепи превращена в (C1-C8)-алкиловый сложный эфир.
Особенно предпочтительными соединениями формулы I являются соединения, в которых
r равно 1;
s равно 0;
t равно 0;
R1 обозначает алкилоксикарбонил-;
R95 обозначает амидиногруппу, которая присоединена по положению 4 фенильного цикла формулы I;
R91, R92, R93 и R96 обозначают водород;
R97 обозначает R99-CH2-CH2-;
R99 обозначает гидроксикарбонил- или ((C1-C4)-алкил)оксикарбонил-;
во всех их стереоизомерных формах и их смесях в любых соотношениях, а также их физиологически приемлемые соли.
Кроме того, предпочтительными соединениями формулы I являются соединения, в которых хиральные центры присутствуют по существу в одинаковой конфигурации. Особенно предпочтительно, если хиральный атом углерода, с которым связаны группы R1(R91)N- и -(СН2)r-, имеет S-конфигурацию, т.е. структурная единица R1(R91)N-CH(-(CH2)r(замещенный фенил))-СО- предпочтительно является полученной из производного L-аминокислоты. В случае, если R96 обозначает водород, особенно предпочтительно, чтобы хиральный атом углерода, с которым связаны группы R96 и R97 имел S-конфигурацию, т.е. структурная единица -(R92)N-CH(R97)-СО- предпочтительно является полученной из производного L-аминокислоты.
Настоящее изобретение также относится к способу получения, с помощью которого могут быть получены соединения формулы I. Соединения формулы I в основном могут быть получены путем соединения двух или более фрагментов (или билдинг-блоков), которые могут быть получены ретросинтетически из формулы I. При получении соединений формулы I обычно может быть полезно или необходимо в ходе синтеза вводить функциональные группы, присутствие которых может приводить к нежелательным или побочным реакциям на стадии синтеза, в виде предшественников, которые позже превращаются в целевые функциональные группы, или временно блокировать функциональные группы, используя защитные группы. Такие методы защиты хорошо известны специалистам в данной области (см., например, Greene and Wuts, Protective Groups в Organic Synthesis, 2nd ed., John Wiley and Sons, 1991). В качестве примеров группы-предшественника могут быть упомянуты нитрогруппы, которые впоследствии могут быть превращены путем восстановления, например, путем каталитического гидрирования, в аминогруппы, или могут быть упомянуты цианогруппы, которые впоследствии могут быть превращены в амидиногруппы, или, в результате восстановления, в аминометильные группы. Защитные группы (или блокирующие группы), которые могут находиться на функциональных группах, включают аллил, трет-бутил, бензил, трет-бутилоксикарбонил (Воc), бензилоксикарбонил (Z) и 9-флуоренилметилоксикарбонил (Fmoc) как защитные группы для гидроксильной, карбоксильной, амино-, гуанидино- и амидино- групп.
В частности, при получении соединения формулы I билдинг-блоки соединяют путем проведения одного или нескольких амидных сочетаний (или конденсаций), т.е. путем образования амидных связей между карбоксильной кислотной группой (или подобной группой, такой как сульфоновая кислотная группа) одного билдинг-блока и аминогруппой (или подобной группой) другого билдинг-блока. Например, соединения формулы I могут быть получены путем соединения билдинг-блоков формул II, III и IV посредством образования по существу известным способом амидной связи между группой производного карбоновой кислоты CO-Y1, изображенного на формуле II, и атомом азота соединения, изображенного на формуле III, и путем образования дополнительной амидной связи между производным карбоновой кислоты CO-Y2, изображенным на формуле III, и атомом азота соединения, изображенного на формуле IV.
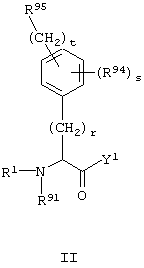
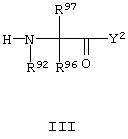
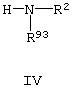
В соединениях формул II, III и IV группы R1, R2, R91, R92, R93, R94, R95, R96, R97 и r, s и t имеют указанные выше определения, но функциональные группы в данных соединениях также могут присутствовать в виде групп-предшественников, которые впоследствии превращают в группы, присутствующие в соединениях формулы I, или функциональные группы могут присутствовать в защищенном виде. Y1 и Y2, которые могут быть одинаковыми или разными, представляют собой гидроксильные или другие, способные к нуклеофильному замещению, уходящие группы, т.е. группы COY1 и COY2 в соединениях формул II и III представляют собой карбоксильные кислотные группы СООН или активированные производные карбоновых кислот, такие как, например, хлорангидриды кислот, сложные эфиры, такие как (C1-C4)-алкиловые сложные эфиры, или активированные эфиры, или смешанные ангидриды.
Исходные соединения формул II, III и IV, а также другие соединения, которые используются в синтезе соединений формулы I для введения некоторых структурных единиц, являются коммерчески доступными или могут быть легко получены из коммерчески доступных соединений с помощью описанных ниже или аналогичных способов, или способов, которые могут быть найдены в легко доступной для специлистов в данной области литературе.
Для получения соединений формулы I вначале соединения формул II и III могут быть подвергнуты конденсации и затем полученный промежуточный продукт подвергают конденсации с соединением формулы IV с получением соединения формулы I, или вначале соединения формул III и IV могут быть подвергнуты конденсации и затем полученный промежуточный продукт подвергают конденсации с соединением формулы II с получением соединения формулы I. После любой такой стадии в ходе синтеза могут быть проведены стадии блокировки и деблокировки, а также превращения групп-предшественников в целевые конечные группы, и могут быть осуществлены дальнейшие модификации. Например, такая группа, как R1, которая является отличной от водорода, может уже присутствовать в соединении формулы II, которое используется в реакции сочетания с соединением формулы III или с промежуточным соединением, полученным из соединений формул III и IV, но группа R1 также может быть введена после проведения только одной реакции сочетания, или после обоих реакций сочетания. Стратегия синтеза для получения соединения формулы I, таким образом, может широко варьировать, и она зависит от того, какой способ синтеза является предпочтительным в данном конкретном случае.
Различные общие методы образования амидной связи, которые могут использоваться в синтезе соединений формулы I, известны специалистам в данной области, например из пептидной химии. Стадия сочетания может проводиться путем использования свободной карбоновой кислоты, т.е. соединения формулы II или III, или промежуточного продукта взаимодействия, в котором группа COY1 или COY2, взаимодействующая на данной стадии, представляет собой группу СООН, активации карбоксильной кислотной группы, предпочтительно in situ, с помощью обычного конденсирующего реагента, такого как карбодиимид, например, дициклогексилкарбодиимид (DCC) или диизопропилкарбодиимид (DIC), или карбонилдиазол, например, карбонилдиимидазол, или соль урония, например, О-((циано-(этоксикарбонил)-метилен)амино)-1,1,3,3-тетраметилурония тетрафторборат (TOTU) или О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HATU), или эфир хлормуравьиной кислоты, например, этилхлорформат или изобутилхлорформат, или тозилхлорид, или ангидрид пропилфосфоновой кислоты, или другие, и затем взаимодействия активированного производного карбоновой кислоты с аминосоединением. Амидная связь также может быть образована путем взаимодействия аминосоединения с галогенангидридом карбоновой кислоты, особенно, с хлорангидридом карбоновой кислоты, который может быть получен на отдельной стадии, или in situ из карбоновой кислоты и, например, тионилхлорида, или эфира или тиоэфира карбоновой кислоты, например метилового эфира, этилового эфира, фенилового эфира, нитрофенилового эфира, пентафторфенилового эфира, метилтиолового эфира, фенилтиолового эфира или 2-пиридилтиолового эфира, т.е. соединения формулы II или III, или с промежуточным продуктом взаимодействия, в котором Y1 или Y2 представляет собой Cl, метокси, этокси, необязательно замещенные фенилокси, метилтио, фенилтио или 2-пиридилтио.
Реакции активации и реакции сочетания обычно проводят в присутствии инертного растворителя (или разбавителя), например, в присутствии апротонного растворителя, такого, как диметилформамид (DMF), тетрагидрофуран (THF), диметилсульфоксид (DMSO), гексаметилтриамид фосфорной кислоты (НМРТ), 1,2-диметоксиэтан (DME), диоксан, или другие, или в смеси таких растворителей. В зависимости от конкретного способа, температура реакции может варьировать в широком диапазоне и может составлять, например, приблизительно от -20°С до температуры кипения растворителя или разбавителя.
Также в зависимости от конкретного способа может оказаться необходимым или полезным добавление в подходящем количестве одного или нескольких вспомогательных агентов, например, основания, такого, как четвертичный амин, например, триэтиламин или диизопропилэтиламин, или алкоголята щелочного металла, например, метоксида натрия или трет-бутоксида калия, для доведения рН, или для нейтрализации образующейся кислоты, или для высвобождения свободного основания из аминосоединения, использующегося в виде соли кислотного добавления, или N-гидроксиазола, такого как 1-гидроксибензотриазол, или катализатора, такого как 4-диметиламинопиридин. Подробные описания методов получения активированных производных карбоновых кислот и образования амидных связей, а также источники литературы, приведены в различных стандартных ссылках, таких, как, например, J.March, Advanced Organic Chemistry, 4th ed., John Wiley&Sons, 1992; или Houben-Weyl, Methoden der organischen Chemie [Methods of Organic Chemistry], Georg Thieme Verlag.
Затем защитные группы, которые еще могут присутствовать в продуктах, полученных с помощью реакции сочетания, удаляют с помощью стандартных методов. Например, трет-бутильная защитная группа, особенно, трет-бутильная сложноэфирная группа, которая представляет собой защитную форму группы СООН, может быть удалена, т.е. превращена в карбоксильную группу, в случае сложного эфира, путем обработки трифторуксусной кислотой. Бензильные группы могут быть удалены путем гидрирования.
Флуоренилметоксикарбонильные группы могут быть удалены с помощью вторичных аминов, таких, как пиперидин. Как уже разъяснялось, после реакции сочетания функциональные группы также могут быть образованы из подходящих групп-предшественников, или, если желательно, с помощью обычных способов могут проводиться дополнительные реакции с продуктами сочетания, например, реакции ацилирования или реакции этерификации. Кроме того, затем с помощью известных способов может проводиться превращение в физиологически приемлемую соль или пролекарственную форму соединения формулы I.
В качестве примеров введения конкретных функциональных групп могут быть приведены процедуры введения амидиногрупп и гуанидиногрупп, которые представляют, например, группу R95. Амидины могут быть получены из циано-содержащих соединений путем добавления спирта в кислых безводных условиях, например, в метаноле, или этаноле, насыщенном хлористым водородом, и с последующим аминолизом. Следующим способом получения амидинов является добавление сульфида водорода к цианогруппе, с последующим метилированием полученного тиоамида и затем взаимодействие с аммиаком. Другим способом является добавление гидроксиламина к цианогруппе, что приводит к образованию гидроксиамидина. При желании связь N-O в гидроксиамидине можно расщепить, например, путем каталитического гидрирования, с получением амидина.
Аминогруппу, которая может быть получена из нитро-предшественника, можно превратить в гуанидино или нитрогуанидино группу, причем в последней нитрогруппа является защитной группой. Для гуанилирования или нитрогуанилирования аминогруппы могут быть использованы следующие реагенты, которые хорошо известны специалистам в данной области, и которые все описаны в литературе: O-метилизомочевина, S-метилизотиомочевина, нитро-3-метилизотиомочевина, формамидинсульфоновая кислота, 3,5-диметил-1-пиразолилформамидиния нитрат, N,N'-ди-трет-бутилоксикарбонил-S-метилизотиомочевина, или N-алкилоксикарбонил- и N,N'-диaлкилoкcикapбoнил-S-метилизотиомочевина.
В основном, реакционную смесь, содержащую целевое соединение формулы I или промежуточное соединение, обрабатывают и, при необходимости, продукт затем очищают с помощью традиционных способов, известных специалистам в данной области. Например, синтезированное соединение может быть очищено с помощью таких хорошо известных методов, как кристаллизация, хроматография или высокоэффективная жидкостная хроматография на обращенной фазе (ОФ-ВЭЖХ), или с помощью других методов разделения, основанных, например, на различиях в размере, заряде или гидрофобности данного соединения. Подобным образом для характеристики соединения данного изобретения могут использоваться хорошо известные методы, такие как анализ аминокислотной последовательности, ЯМР, ИК и масс-спектрометрия (МС).
Реакции, описанные выше и ниже, которые проводят в рамках синтеза соединений формулы I, как правило, могут быть проведены в соответствии с методами традиционной жидкофазной химии, а также в соответствии с методами твердофазной химии, обе данные области традиционно используются в пептидном синтезе. Среди различных методов, которые могут применяться, если соединения формулы I получают на твердой фазе, может быть упомянут следующий метод, использующийся для получения соединений, в которых гидроксикарбонильная группа присутствует в группе R96 или группе R97. В качестве исходного вещества используют соединение формулы Fmoc-HN-C(R96)(R97)-CO-OPG, в котором Fmoc представляет собой 9-флуоренилметоксикарбонил, PG представляет собой защитную группу карбоновой кислоты, а R96 и R97 такие, как определены выше, при условии, что в одной из групп R96 и R97 присутствует свободная гидроксикарбонильная группа СООН. Упомянутое исходное соединение присоединяют к смоле Wang (S.S.Wang, J.Am. Chem. Soc. 95 (1973) 1328) путем взаимодействия СООН группы со смолой. Затем проводят удаление защитной группы Fmoc и соединение формулы II подвергают взаимодействию с аминогруппой. После чего проводят удаление защитной группы PG и полученную карбоксильную группу подвергают взаимодействию с соединением формулы IV. В конце соединение удаляют со смолы с помощью трифторуксусной кислоты. Если используются методы твердофазного синтеза, присутствующие функциональные группы могут быть модифицированы или функциональные группы могут быть введены в образующееся соединение, пока оно присоединено к смоле, или после удаления соединения со смолы, для получения, например, N-концевого производного, такого, как аллилоксикарбонилированное соединение по N-концу, или производного по карбоксильной группе, данная группа, например, может быть амидирована. Соединение данного изобретения можно также синтезировать путем объединения стадий, проводимых в соответствии с методами жидкофазной органической химии, и с помощью стадий, проводимых в соответствии с методами твердофазной органической химии. Соединение данного изобретения можно также синтезировать с помощью автоматического синтезатора.
Соединения настоящего изобретения ингибируют фермент коагуляции крови фактор VIIa. В частности, они являются специфическими ингибиторами фактора VIIa. В данном документе термин специфический, если используется в отношении ингибирования активности фактора VIIa, означает, что соединение формулы I может ингибировать активность фактора VIIa, не ингибируя по существу активность других специфических протеаз, включенных в процесс коагуляции крови и/или фибринолиза, включая, например, фактор Ха, плазмин и тромбин (при использовании одинаковых концентраций ингибитора). Активность соединения формулы I может быть определена, например, с помощью описанного ниже анализа, или с помощью других анализов, известных специалистам в данной области. Предпочтительными соединениями настоящего изобретения являются такие соединения, которые имеют Ki≤10 мкМ, особенно предпочтительно, ≤1 мкМ, для ингибирования фактора VIIa, как определяли в анализе, описанном ниже, и которые предпочтительно по существу не ингибируют активность других протеаз, включенных в процессы коагуляции и фибринолиза, по сравнению с ингибированием фактора VIIa (при использовании одинаковых концентраций ингибитора). Соединения данного изобретения ингибируют каталитическую активность фактора VIIa либо непосредственно в протромбиназном комплексе или в виде растворимой субъединицы, либо косвенно, путем ингибирования включения фактора VIIa в протромбиназный комплекс.
Вследствие того, что соединения формулы I обладают ингибиторной активностью по отношению к фактору VIIa, они являются полезными фармакологически активными соединениями, которые могут применяться, например, для воздействия на процесс коагуляции крови (или свертывания) и фибринолиза, а также для лечения и профилактики, например, сердечно-сосудистых заболеваний, тромбоэмболических заболеваний или повторных стенозов. Соединения формулы I и их физиологически приемлемые соли и пролекарственные формы могут быть введены животным, предпочтительно млекопитающим, и, особенно, людям, в качестве лекарственных препаратов, для лечения или профилактики. Они могут быть введены по отдельности, или в смесях друг с другом, или в виде фармацевтических препаратов, которые допускают энтеральное или парентеральное введение, и которые содержат в качестве активного ингредиента эффективное количество по меньшей мере одного соединения формулы I, и/или его физиологически приемлемых солей, и/или его пролекарственных форм, а также фармацевтически приемлемый носитель.
Следовательно, настоящее изобретение также относится к соединениям формулы I и/или их физиологически приемлемым солям и/или их пролекарственным формам, предназначенным для применения в качестве фармацевтических препаратов (или лекарственных средств), к применению соединений формулы I, и/или их физиологически приемлемых солей, и/или их пролекарственных форм, для получения фармацевтических препаратов для ингибирования фактора VIIa или для воздействия на процесс коагуляции крови или фибринолиэа, или для лечения или профилактики заболеваний, упомянутых выше или ниже, например, для получения фармацевтического препарата для лечения и профилактики сердечно-сосудистых заболеваний, тромбоэмболических заболеваний или повторных стенозов. Данное изобретение также относится к применению соединений формулы I, и/или их физиологически приемлемых солей, и/или их пролекарственных форм, для ингибирования фактора VIIa, или для воздействия на процесс коагуляции крови или фибринолиза, или для лечения или профилактики заболеваний, упомянутых выше или ниже, например, для применения в лечении и профилактике сердечно-сосудистых заболеваний, тромбоэмболических заболеваний или повторных стенозов, а также к способам лечения, направленного на указанные цели, включая способы, относящиеся к упомянутым лечению и профилактике. Кроме того, настоящее изобретение относится к фармацевтическим препаратам (или фармацевтическим композициям), которые содержат эффективное количество по меньшей мере одного соединения формулы I, и/или его физиологически приемлемых солей, и/или его пролекарственных форм, а также фармацевтически приемлемый носитель, т.е. одно или несколько фармацевтически приемлемых несущих веществ (или сред для лекарства) и/или добавочных средств (или эксципиентов).
Фармацевтические препараты могут быть введены перорально, например, в виде пиллюль, таблеток, лакированных таблеток, покрытых таблеток, гранул, твердых и мягких желатиновых капсул, растворов, сиропов, эмульсий, суспензий или аэрозольных смесей. Введение, однако, может проводиться ректально, например, в виде свечей, или парентерально, например, внутривенно, внутримышечно или подкожно, в виде растворов для инъекций или растворов для вливаний, микрокапсул, имплантантов или палочек, или чрезкожно или местно, например в виде мазей, растворов или настоек, или другими путями, например, аэрозолей или назальных спреев.
Фармацевтические препараты в соответствии с данным изобретением получают известным по существу способом, хорошо знакомым специалистам в данной области, причем фармацевтически приемлемые инертные неорганические и/или органические носители используют в добавление к по меньшей мере одному соединению формулы I и/или его (их) физиологически приемлемым солям и/или его (их) пролекарственным формам. Для получения пилюль, таблеток, покрытых таблеток и твердых желатиновых капсул можно применять, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и др.
Носителями для мягких желатиновых капсул и свечей могут служить, например, жиры, воски, полутвердые и жидкие полиолы, природные или отвержденные масла и др. Подходящими носителями для получения растворов, например, растворов для инъекций, или эмульсий или сиропов являются, например, вода, соляной раствор, спирты, глицерин, полиолы, сахароза, инвертированный сахар, глюкоза, растительные масла и др. Подходящими носителями для микрокапсул, имплантантов или палочек являются, например, сополимеры гликолевой кислоты и молочной кислоты. Фармацевтические препараты обычно содержат приблизительно от 0,5 до 90% по массе соединений формулы I и/или их физиологически приемлемых солей и/или пролекарственных форм. Количество активного ингредиента формулы I и/или его физиологически приемлемых солей и/или пролекарственных форм в фармацевтических препаратах обычно составляет приблизительно от 0,5 до 1000 мг, предпочтительно, приблизительно от 1 до 500 мг.
В дополнение к активным ингредиентам формулы I, и/или их физиологически приемлемым солям, и/или пролекарственным формам, и носителям фармацевтические препараты могут содержать добавки, такие как, например, наполнители, дезинтегрирующие средства, связующие средства, связывающие средства, увлажняющие агенты, стабилизаторы, эмульгаторы, консерванты, подсластители, окрашивающие средства, вкусовые добавки, ароматизаторы, загустители, разбавители, буферные вещества, растворители, солюбилизаторы, агенты, улучшающие способность к хранению, соли, для изменения осмотического давления, покрывающие агенты или антиоксиданты. Они могут также содержать два или более соединения формулы I, и/или их физиологически приемлемых солей, и/или пролекарственных форм. В случае, если фармацевтический препарат содержит два или более соединения формулы I, выбор индивидуальных соединений осуществляют на основе конкретного полного фармакологического профиля фармацевтического препарата. Например, высокоэффективное соединение с небольшой продолжительностью действия может быть объединено с долгодействующим соединением, имеющим более низкую эффективность. Гибкость, допускаемая в отношении выбора заместителей в соединениях формулы I, дает возможность в высокой степени контролировать биологические и физико-химические свойства соединений и таким образом создает возможность для отбора таких желательных соединений. Кроме того, в добавление к по меньшей мере одному соединению формулы I, и/или его физиологически приемлемым солям, и/или пролекарственным формам, фармацевтические препараты могут также содержать одно или несколько других терапевтически или профилактически активных ингредиентов.
В качестве ингибиторов фактора VIIa соединения формулы I и их физиологически приемлемые соли и пролекарственные формы являются в основном подходящими для лечения и профилактики состояний, при которых активность фактора VIIa имеет значение, или имеет нежелательный уровень, или на которые может оказать благоприятное влияние ингибирование фактора VIIa или уменьшение его активности, или для предотвращения, облегчения или излечения которых, по мнению врача, необходимо ингибирование фактора VIIa или уменьшение его активности. Так как ингибирование фактора VIIa оказывает влияние на коагуляцию крови и фибринолиз, соединения формулы I и их физиологически приемлемые соли и пролекарственные формы обычно являются подходящими для уменьшения свертывания крови, или для лечения и профилактики состояний, при которых активность фактора VIIa имеет значение или имеет нежелательный уровень, или на которые может оказывать благоприятное влияние уменьшение свертывания крови, или для предотвращения, облегчения или излечения которых, по мнению врача, необходимо уменьшение активности системы свертывания крови. Таким образом, отдельным предметом настоящего изобретения является уменьшение или ингибирование нежелательного свертывания крови, особенно, у субъекта, путем введения эффективного количества соединения I, или его физиологически приемлемой соли или пролекарственной формы, а также содержащих его фармацевтических препаратов.
Состояния, при которых применение соединения формулы I может иметь благоприяный эффект, включают, например, сердечно-сосудистые заболевания, тромбоэмболические заболевания или осложнения, связанные, например, с инфекцией или хирургическим вмешательством. Соединения настоящего изобретения также могут использоваться для уменьшения воспалительного ответа. Примерами отдельных заболеваний, для лечения или профилактики которых могут использоваться соединения формулы I, являются коронарная болезнь сердца, инфаркт миокарда, грудная жаба, повторный стеноз сосудов, например, повторный стеноз после ангиопластики, такой как ангиопластика PICA (задней нижней мозжечковой артерии), респираторный дистресс-синдром взрослых, множественная недостаточность, удар и нарушение, связанное с рассеянным внутрисосудистым свертыванием. Примерами родственных осложнений, связанных с хирургическим вмешательством, являются тромбозы, такие как тромбоз глубокой и проксимальной вены, которые могут встречаться после хирургического вмешательства. С точки зрения фармакологической активности соединения данного изобретения могут заменять другие антикоагулянты, такие как гепарин. Применение соединения данного изобретения может привести к снижению себестоимости по сравнению с другими антикоагулянтами.
При использовании соединений формулы I доза может варьировать в широких пределах и обычно, как известно терапевту, дозу устанавливают в соответствии с индивидуальными состояниями в каждом конкретном случае. Она зависит, например, от конкретного применяемого соединения, от природы и тяжести заболевания, подлежащего лечению, от способа и режима введения, или от того, подлежит ли лечению острое или хроническое состояние, или проводится профилактика. Соответствующая дозировка может быть установлена с помощью клинических подходов, хорошо известных в данной области. Как правило, дневная доза, необходимая для достижения желаемых результатов у взрослых весом приблизительно 75 кг, составляет приблизительно от 0,01 до 100 мг/кг, предпочтительно, приблизительно от 0,1 до 50 мг/кг, особенно, приблизительно от 0,1 до 10 мг/кг (в каждом случае в мг на кг массы тела). Ежедневная доза может быть разделена, особенно, в случае введения относительно больших количеств, на несколько, например, 2, 3 или 4 отдельных введения. Обычно, в зависимости от индидуальной реакции организма, может возникнуть необходимость отклонения в большую или меньшую сторону от установленной дневной дозы.
Соединение формулы I может выгодно использоваться в качестве антикоагулянта вне субъекта. Например, эффективное количество соединения данного изобретения может быть приведено в контакт со свежеполученным образцом крови для предотвращения в нем коагуляции. Кроме того, соединение формулы I и его соли могут применяться для диагностических целей, например, в in vitro диагнозах, и в качестве вспомогательного вещества в биохимических исследованиях. Например, соединение формулы I можно использовать в анализе для определения присутствия фактора VIIa, или для выделения фактора VIIa в по существу чистом виде. Соединение данного изобретения можно пометить, например, радиоактивным изотопом, и затем наличие меченого соединения, связанного с фактором VIIa, можно определить с помощью рутинного метода, использующегося для определения конкретной метки. Таким образом, соединение формулы I или его соль можно успешно использовать в качестве зонда для определения локализации или количества активности фактора VIIa in vivo, in vitro или ex vivo.
Кроме того, соединения формулы I могут использоваться как промежуточные соединения для получения других соединений, в особенности, других фармацевтически активных соединений, которые могут быть получены из соединений формулы I, например, путем введения заместителей или модификации функциональных групп.
Следует понимать, что модификации, которые не оказывают существенного влияния на различные воплощения данного изобретения, включены в изобретение, раскрытое в данном описании. Соответственно, следующие примеры предназначаются для иллюстрации, а не для ограничения настоящего изобретения.
Примеры
Сокращения
Аллилоксикарбонил Alloc
L-4-Амидинофенилаланил pAph
L-Аспартил Asp
трет-Бутил tBu
Дихлорметан DCM
N,N'-Диизопропилкарбодиимид DIC
N,N-Диизопропил-N-этиламин DIEA
N,N-Диметилформамид DMF
Диметилсульфоксид DMSO
N-Этилморфолин NEM
9-Флуренилметилоксикарбонил Fmoc
L-Глутамил Glu
N-Гидроксибензотриазол HOBt
Пентафторфенил Pfp
Тетрагидрофуран THF
Трифторуксусная кислота TFA
О-((Циан(этоксикарбонил)метилен)амино)-1,1,3,3-
тетраметилурония тетрафторборат TOTU
О-(7-Азабензотриазол-1-ил)-1,1,3,3-
тетраметилурония гексафторфосфат HATU
Соединения формулы I называют в соответствии с правилами пептидной химии. Таким образом, например, такое название, как Alloc-pAph-Glu-(4-аминобензил)амид означает, что в соответствующем соединении единица L-4-амидинофенилаланил связана посредством пептидной связи с единицей L-глутамил, и что α-аминогруппа L-4-амидинофенилаланила несет аллилоксикарбонильную группу, и что в положении 1 глутамила вместо свободной карбоксильной группы присутствует группа N-(4-аминобензил)карбоксамид, т.е., что соответствующее соединение имеет следующую структурную формулу.
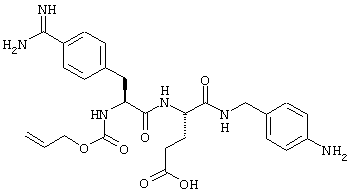
Если на конечной стадии синтеза соединения используют кислоту, такую, как трифторуксусная или уксусная кислота, например, если для удаления трет-бутильной группы используют трифторуксусную кислоту, или если соединение очищают хроматографией, используя элюент, который содержит такую кислоту, но в некоторых случаях, в зависимости от процедуры обработки, например, деталей процесса замораживания-высушивания, соединение получают частично или полностью в виде соли используемой кислоты, например, в виде соли уксусной или трифторуксусной кислоты.
Пример 1: Alloc-pAph-Glu-(4-аминобензил)амид
a) (S)-2-Аллилоксикарбониламино-3-(4-цианофенил)пропионовая кислота
Суспензию 50 г (0,221 моль) (S)-2-амино-3-(4-цианофенил)пропионовой кислоты в 150 мл воды доводят до рН 8 с помощью 1 N NaOH. При температуре от 0 до 5°С медленно добавляют 26,6 г (0,221 моль) аллилхлорформиата в 225 мл диоксана (значение рН, равное 8, поддерживают путем добавления 1 N NaOH). После завершения реакции (контроль осуществляют с помощью тонкослойной хроматографии (ТСХ)) смесь экстрагируют DCM и водный слой подкисляют до рН 2 с помощью KHSO4. Осадок растворяют в DCM, сушат (Na2SO4) и упаривают. Остаток перекристаллизовывают из смеси эфир/нефтяной бензин, получая 31 г (51%) указанного в заголовке соединения. МС 275,1 (М+1)+.
b) Гидрохлорид этилового эфира (S)-2-аллилоксикарбониламино-3-(4-карбамимидоил)пропионовой кислоты (гидрохлорид Alloc-pAph-OC2H5)
Сухую газообразную хлористоводородную кислоту пропускают через раствор 15 г (0,055 моль) (S)-2-аллилоксикарбониламино-3-(4-цианофенил)пропионовой кислоты в 200 мл этанола. Через 5 ч смесь выдерживают в течение ночи при 0°С. Растворитель упаривают и остаток обрабатывают 250 мл 3 М раствора аммиака в этаноле в течение 12 ч при комнатной температуре. Растворитель упаривают и остаток промывают DCM и кристаллизуют из эфира, получая 17,5 г (90%) указанного в заголовке соединения. МС 320,3.
c) Гидрохлорид (S)-2-аллилоксикарбониламино-3-(4-карбамимидоилфенил)пропионовой кислоты (гидрохлорид Alloc-pAph-OH)
17 г (0,048 моль) гидрохлорида этилового эфира (S)-2-аллилоксикарбониламино-3-(4-карбамимидоилфенил)пропионовой кислоты обрабатывают 400 мл полуконцентрированной хлористоводородной кислоты в течение 3 ч при комнатной температуре. Растворитель упаривают (<30°С) и остаток перемешивают с эфиром. Выход 15 г (95%). МС 292,2 (М+1)+.
d) Гидрохлорид Alloc-pAph-Glu(OtBu)-ОСН3
К раствору 1,3 г (3,97 ммоль) гидрохлорида Alloc-pAph-OH и 1,0 г (3,97 ммоль) гидрохлорида H-Glu(OtBu)-ОСН3 в 15 мл DMF добавляют 1,63 г (4,96 ммоль) TOTU и 1,14 г (9,9 ммоль) NEM. Через 5 ч при комнатной температуре раствор выливают в 150 мл соляного раствора и экстрагируют DCM. Органический слой сушат (NB2SO4) и упаривают, получая 1,7 г (81%) указанного в заголовке соединения. МС 491,2 (M+1)+.
e) Alloc-pAph-Glu(OtBu)-OH
1,7 г (3,17 ммоль) гидрохлорида Alloc-pAph-Glu(OtBu)-ОСН3 в 15 мл THF и 50 мл воды обрабатывают 0,16 г (3,8 ммоль) моногидрата гидроксида лития. Через 3 ч растворитель удаляют и остаток сушат из замороженного состояния, получая 1,25 г (82%) указанного в заголовке соединения. МС 477,5 (M+1)+.
f) Alloc-pAph-Glu(OtBu-4-аминобензил)амид
К раствору 56 мг (0,12 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 13 мкл (0,12 ммоль) п-аминобензиламина в 10 мл DMF добавляют 39 мг (0,12 ммоль) TOTU и 15 мкл (0,12 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют, получая 0,15 г указанного в заголовке соединения, которое используют на следующей стадии без дополнительной очистки. МС 581,4 (М+1)+.
g) Alloc-pAph-Glu-(4-аминобензил)амид
150 мг Alloc-pAph-Glu(OtBu)-4-аминобензиламида обрабатывают 1 мл 90% TFA. Через 12 ч добавляют смесь этилацетат/DСМ/метанол и осадок фильтруют и сушат, получая 55 мг указанного в заголовке соединения. МС 525,3 (М+1)+.
Пример 2: Alloc-pAph-Glu-(3-аминобензил)амид
К раствору 30 мг (0,064 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 8 мг (0,064 ммоль) 3-аминобензиламина в 5 мл DMF добавляют 21 мг (0,064 ммоль) TOTU и 8 мкл (0,064 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат и осадок фильтруют и сушат, получая 30 мг указанного в заголовке соединения. МС 525,4 (M+1)+.
Пример 3: Alloc-pAph-Glu-(2-(4-аминофенил)этил)амид
К раствору 30 мг (0,064 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 8,5 мкл (0,064 ммоль) 2-(4-аминофенил)этиламина в 4 мл DMF добавляют 21 мг (0,064 ммоль) TOTU и 8 мкл (0,064 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат и осадок фильтруют и сушат, получая 30 мг указанного в заголовке соединения. МС 539,4 (М+1)+.
Пример 4: Alloc-pAph-Glu-(2,4-дигидроксибензил)амид
К раствору 30 мг (0,064 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 14 мг (0,064 ммоль) 3,4-дигидроксибензиламина в 5 мл DMF добавляют 21 мг (0,064 ммоль) TOTU и 16 мкл (0,128 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат и осадок фильтруют и сушат, получая 45 мг указанного в заголовке соединения. МС 542,4 (M+1)+.
Пример 5: Alloc-pAph-Glu-(2-аминобензил)амид
К раствору 59 мг (0,124 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 15 мг (0,124 ммоль) 2-аминобензиламина в 1,5 мл DMF добавляют 41 мг (0,124 ммоль) TOTU и 28 мг (0,248 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре растворитель упаривают и остаток очищают методом ВЭЖХ, получая 1,5 мг указанного в заголовке соединения. МС 525,4 (М+1)+.
Пример 6: Alloc-pAph-Glu-((RS)-2-амино-9Н-флуорен-9-ил) амид
К раствору 60 мг (0,126 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 34 мг (0,126 ммоль) (RS)-2,9-диамино-9Н-флурена в 5 мл DMF добавляют 42 мг (0,126 ммоль) TOTU и 32 мкл (0,252 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. После 8 ч при комнатной температуре добавляют этилацетат и осадок фильтруют и сушат, получая 50 мг указанного в заголовке соединения. МС 598,7 (М+1)+.
Пример 7: Alloc-pAph-Glu-(3-этоксикарбониламинопропил)амид
a) 3-Этоксикарбониламинопропиламин
К раствору 0,5 г (2,9 ммоль) 3-трет-бутилоксикарбониламинопропиламина в 8 мл DCM и 0,37 г (2,9 ммоль) NEM добавляют раствор 0,32 г (0,29 ммоль) этилхлорформата в 2 мл DCM. Через 24 ч при комнатной температуре смесь промывают водой и сушат. Растворитель упаривают и остаток перемешивают с 5 мл TFA (90%). Через 1 ч растворитель упаривают, получая 0,6 г указанного в заголовке соединения. МС 147,0 (М+1)+.
b) Alloc-pAph-Glu-(3-этоксикарбониламинопропил)амид
К раствору 59 мг (0,124 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 16 мг (0,124 ммоль) 3-этоксикарбониламинопропиламина в 1,5 мл DMF добавляют 41 мг (0,124 ммоль) TOTU и 28 мг (0,248 ммоль) DIEA при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре растворитель упаривают и остаток очищают методом ВЭЖХ, получая 1,4 мг указанного в заголовке соединения. МС 549,2 (M+1)+.
Пример 8: Alloc-pAph-Glu-((R)-1-(3-аминофенил)этил)амид и Alloc-pAph-Glu-((S)-1-(3-аминофенил)этил)амид
a) (RS)-3-(1-Аминоэтил)фениламин гидрохлорид
Смесь 0,69 г (5,123 ммоль) 1-(3-аминофенил)-этанона, 0,43 г (6,15 ммоль) гидроксиламина, 0,50 г (6,15 ммоль) ацетата натрия и 15 мл этанола нагревают при 80°С в течение 8 ч. Растворитель удаляют и остаток распределяют между водой и этилацетатом. Органическую фазу сушат, фильтруют и растворитель упаривают, получая 0,53 г оксима (МС 151,2 (М+1)+. 0,53 г оксима растворяют в 100 мл метанола и гидрируют в аппарате Парра (Parr apparatus) при комнатной температуре. Через 2 дня смесь фильтруют через целит и растворитель упаривают. Остаток перемешивают с эфиром, насыщенным хлористым водородом. Растворитель упаривают, получая 0,46 г указанного в заголовке соединения. МС 137,1 (М+1)+.
b) Alloc-pAph-Glu-((R)-1-(3-аминофенил)этил)амид and Alloc-pAph-Glu-((S)-1-(3-аминофенил))этиламид
К раствору 59 мг (0,124 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 18 мг (0,125 ммоль) (RS)-3-(1-аминоэтил)фениламина в 5 мл DMF добавляют 41 мг (0,124 ммоль) TOTU и 28 мг (0,248 ммоль) DIEA при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре растворитель упаривают и остаток очищают методом ВЭЖХ, получая 0,7 мг диастереомера I (МС 539,2 (М+1)+) и 0,9 мг диастереомера II (МС 539,2 (М+1)+.
Пример 9: Alloc-pAph-Glu-((R)-1-(4-аминофенил)бутил)амид и Alloc-pAph-Glu-((S)-1-(4-аминофенил)бутил)амид
(RS)-4-(1-Аминобутил)фениламин синтезируют по способу, описанному в примере 8, начиная с соответствующего кетона. К раствору 60 мг (0,126 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 24 мг (0,121 ммоль) (RS)-4-(1-аминобутил)фениламин в 5 мл DMF добавляют 42 мг (0,126 ммоль) TOTU и 32 мкл (0,252 ммоль) NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре растворитель упаривают и остаток очищают методом ВЭЖХ, получая 3 мг диастереомера I (МС 567,3 (M+l)+) и 3 мг диастереомера II (МС 567,3 (М+1)+).
Пример 10: Alloc-pAph-Glu(3-(3,5-дихлорбензолсульфониламино)пропил)амид
a) N-(3-Аминопропил)-3,5-дихлорбензолсульфонамид
1,3-Диаминопропан (6 г, 81,5 ммоль) растворяют в 45 мл 1,4-диоксана и при 15-20°С в течение 3 часов при перемешивании медленно добавляют раствор 3,5-дихлорбензолсульфонилхлорида (2 г, 8,15 ммоль) в 5 мл 1,4-диоксане. Перемешивание продолжают при комнатной температуре. Через 30 часов образовавшийся осадок отфильтровывают и фильтрат концентрируют в вакууме. Остаток распределяют между этилацетатом и водой. Органический слой отделяют, сушат сульфатом магния, фильтруют и концентрируют в вакууме, получая 2,0 г неочищенного вещества. 750 мг данного вещества очищают методом ВЭЖХ, получая 675 мг указанного в заголовке соединения в виде соли TFA (МС 283,0 (М+Н)+). 200 мг данного продукта растворяют в этилацетате и обрабатывают 5 мл разбавленного раствора карбоната калия. Органический слой отделяют, сушат, фильтруют и концентрируют в вакууме, получая не содержащий TFA указанный в заголовке амин.
b) Alloc-pAph-Glu-3-((3,5-дихлорбензолсульфониламино)пропил) амид
N-(3-Аминопропил)-3,5-дихлорбензолсульфонамид (7 мг, 23,4 мкмоль), Alloc-pAph-Glu(OtBu)-ОН (10 мг, 19,5 мкмоль) и гидрат HOBt (9 мг, 58,5 мкмоль) растворяют в 2 мл смеси DMF и DCM 1:3. Затем добавляют DIC (6 мкл, 39 мкмоль). После перемешивания в течение 3 ч раствор оставляют на выходные при комнатной температуре, затем растворитель удаляют и остаток очищают методом ВЭЖХ, получая 6,5 мг продукта конденсации. Его перемешивают в 4 мл смеси TFA и DCM 1:1 в течение 2 ч. После стояния в течение ночи растворитель упаривают и остаток растворяют в DCM. После упаривания растворителя остаток очищают методом ВЭЖХ и лиофилизируют, получая 3,5 мг указанного в заголовке соединения. МС 685,4 (M+Н)+.
Пример 11: Alloc-pAph-Glu-(3-((нафталин-2-сульфониламино)метил)бензил)амид
а) (3-Аминометилбензил)амид нафталин-2-сульфоновой кислоты
α,α'-Диамино-м-ксилол (24 г, 176 ммоль) растворяют в 50 мл 1,4-диоксана, и при 15-20°С медленно добавляют в течение 3 часов при перемешивании нафталин-2-сульфонилхлорид (4 г, 17,6 ммоль), растворенный в 50 мл 1,4-диоксана. Перемешивание продолжают при комнатной температуре. После стояния в течение ночи образовавшийся осадок отфильтровывают и фильтрат концентрируют в вакууме. Остаток распределяют между DCM и водой. Органический слой отделяют и промывают водой и 1 N НСl. Маслянистый слой, образовавшийся между органическим и водным слоем, отделяют. Он отвердевает при стоянии. Полученное твердое вещество обрабатывают этилацетатом, отсасывают и промывают этилацетатом. Остаток растворяют в воде и обрабатывают раствором карбоната калия. Водный раствор экстрагируют три раза этилацетатом и объединенные органические фазы сушат над сульфатом магния, фильтруют и концентрируют, получая 3,2 г указанного в заголовке соединения. МС 327,3 (M+H)+.
b) Alloc-pAph-Glu-(3-((нафталин-2-сульфониламино) метил) бензил)амид
(3-Аминометилбензил)амид нафталин-2-сульфоновой кислоты (8 мг, 23,4 мкмоль), Alloc-pAph-Glu (OtBu)-ОН (10 мг, 19,5 мкМ) и гидрат HOBt (9 мг, 58,5 мкмоль) растворяют в 2 мл смеси DMF и DCM 1:3. Затем добавляют DIC (6 мкл, 39 мкмоль). Через 3 ч реакционную смесь концентрируют и обрабатывают, как описано в примере 10. После лиофилизации получают 7,6 мг указанного в заголовке соединения. МС 729,4 (М+Н)+.
Пример 12: Alloc-pAph-Glu-(4-карбамоилметилтиазол-2-ил)амид
a) Fmoc-Glu(OtBu)-(4-карбамоилметилтиазол-2-ил)амид
К раствору 1,24 г (2,1 ммоль) Fmoc-Glu(OtBu)-OPfp в 10 мл DMF добавляют раствор 0,33 г (2,1 ммоль) 2-(2-аминотиазол-4-ил)-ацетамида в 10 мл DMF в течение 15 мин. После 2 дней при комнатной температуре растворитель упаривают и остаток промывают эфиром, получая 0,86 г указанного в заголовке соединения. МС 565,4 (M+H)+.
b) H-Glu(OtBu)-(4-карбамоилметилтиазол-2-ил)амид
Раствор 0,86 г (1,52 ммоль) Fmoc-Glu(OtBu)-(4-карбамоилметилтиазол-2-ил)амида в 5 мл смеси DMF/пиперидин (1:1) перемешивают в течение 3 ч при комнатной температуре. Растворитель упаривают и остаток фильтруют через целит, получая 0,37 г указанного в заголовке соединения. МС 343,4 (М+Н)+.
c) Alloc-pAph-Glu-(4-карбамоилметилтиазол-2-ил)амид
К раствору 50 мг (0,17 ммоль) Alloc-pAph-OH и 39,1 мг TOTU в 10 мл DMF добавляют 58,8 мг (0,17 ммоль) H-Glu(OtBu)-(4-карбамоилметилтиазол-2-ил)амид и 21,8 мкл NEM. Через 24 ч при комнатной температуре растворитель удаляют и остаток распределяют между водным раствором NaHCO3 и этилацетатом. Органическую фазу сушат, фильтруют и упаривают. Остаток перемешивают 16 ч с 0,6 мл TFA. Добавляют 50 мл этилацетата и 10 мл лигроина и осадок отфильтровывают, получая 59 мг указанного в заголовке соединения. МС 560,4 (M+1)+.
Пример 13: Alloc-pAph-Glu-(4-амино-2-метилпиримидин-5-илметил)амид
К раствору 53 мг (0,11 ммоль) Alloc-pAph-Glu(OtBu)-ОН и 15 мг (0,11 ммоль) 4-амино-5-аминометил-2-метилпиримидина в 5 мл DMF добавляют 37 мг (0,115 ммоль) TOTU и 14 мкл NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат, изопропанол и метанол и осадок отфильтровывают, получая 46 мг указанного в заголовке соединения. МС 541,3 (М+1)+.
Пример 14: Alloc-pAph-Asp-(3-аминобензил)амид
К раствору 50 мг (0,153 ммоль) Alloc-pAph-OH и 50,3 мг (0,153 ммоль) гидрохлорида H-Asp(OtBu)-3-аминобензиламида в 5 мл DMF добавляют 50 мг (0,153 ммоль) TOTU и 60 мкл NEM при 3°С. Через 12 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат и маслянистый осадок отделяют и сушат из замороженного состояния, получая 82 мг указанного в заголовке соединения. МС 511,3 (М+1)+.
Пример 15: Alloc-pAph-2-Aad-(3-аминобензил)амид
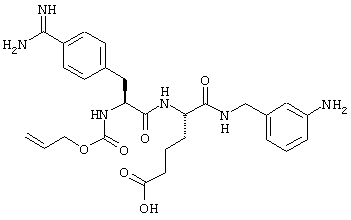
К раствору 100 мг гидрохлорида (0,305 ммоль) Alloc-pAph-OH и 139 мг (0,305 ммоль) гидрохлорида H-2-Aad(OtBu)-(3-аминобензил)амида в 5 мл DMF добавляют 128 мг (0,389 ммоль) TOTU и 150 мкл NEM при 3°С. Через 16 ч при комнатной температуре растворитель удаляют и остаток обрабатывают 1 мл 90% TFA. Через 8 ч при комнатной температуре добавляют этилацетат и осадок фильтруют, очищают методом ВЭЖХ и лиофилизируют, получая 43 мг указанного в заголовке соединения. МС 539,2 (М+1)+.
Пример 16: Аllос-рАph-Glu(ОСН3)-(3-аминобензил)амида
50 мг (0,153 ммоль) гидрохлорида Alloc-pAph-OH и 75 мг (0,153 ммоль) гидрохлорида Н-Glu(ОСН3)-(3-аминобензил) амида подвергают взаимодействию в соответствии со способом, описанным в примере 15, получая 22 мг указанного в заголовке соединения. МС 539,3 (М+1)+.
Следующие примеры соединений получают по способам, аналогичным описанным в вышеприведенных примерах.
Примеры соединений формулы Iа:
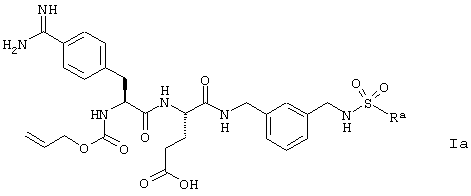
Примеры соединений формулы Ib:
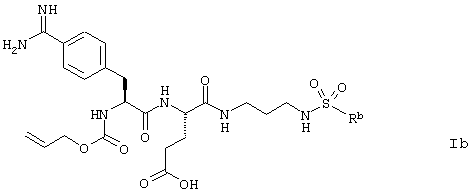
Примеры соединений формулы Iс:
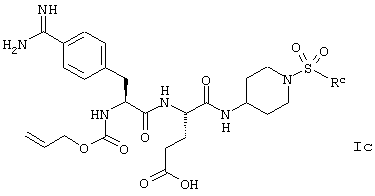
Пример 35: ((S)-2-Аллилоксикарбониламино-3-(4-карбамимидоилфенил)пропионил)-Glu-(3-(пиридин-3-илсульфониламино)фенил)амид (Alloc-pAph-Glu-(3-(пиридин-3-илсульфониламино)фенил)амид) МС 652,4 (М+1)+.
Пример 36: ((R)-2-Аллилоксикарбониламино-3-(4-карбамимидоилфенил)пропионил)-Glu-(3-(пиридин-3-илсульфониламино)фенил)амид (Alloc-D-pAph-Glu-(3-(пиридин-3-илсульфониламино)фенил)амид) МС 652,4 (М+1)+.
Примеры соединений формулы Id:
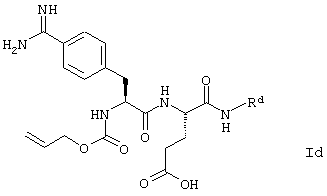
(а) выделяют в виде гидрохлорида
Примеры соединений формулы Iе:
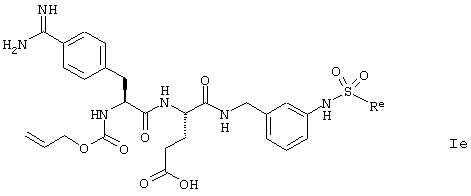
Пример 70: ((S)-2-(3-Бромбензолсульфониламино)-3-(4-карбамимидоилфенил)пропионил)-Glu-(3-аминобензил)амид. МС 659,1 (М+1)+.
Пример 71: ((S)-2-(3-Хлорбензоиламино)-3-(4-карбамимидоилфенил)пропионил)-Glu-(3-аминобензил)амид. МС 579,2 (M+1)+.
Фармакологическое тестирование
Способность соединения формулы I ингибировать фактор VIIa или другие ферменты, такие как фактор Ха, тромбин, плазмин или трипсин, можно оценить путем определения концентрации соединения формулы I, при которой происходит 50% ингибирование активности фермента, т.е. значения IC50, которое связано с константой ингибирования Ki. В хромогенных анализах используют очищенные ферменты. Концентрацию ингибитора, которая вызывает 50% уменьшение скорости гидролиза субстрата, определяют методом линейной регрессии после построения графика зависимости относительных скоростей гидролиза (по сравнению с неингибированным контролем) от log концентрации соединения формулы I. Для расчета константы ингибирования Ki значение IC50 корректируют с учетом конкуренции субстрата с помощью формулы Ki=IС50/{1+(концентрация субстрата/Кm)}, где Km представляет собой константу Михаэлиса-Ментен (Chen и Prusoff, Biochem. Pharmacol. 22 (1973), 3099-3108; I.H.Segal, Enzyme Kinetics, 1975, John Wiley&Sons, New York, 100-125 включена в данный документ в качестве ссылки).
а) Анализ на фактор VIIa
Ингибиторную активность (выраженную как константа ингибирования Ki (FVIIa)) соединений формулы I по отношению к активности комплекса фактор VIIa/тканевый фактор определяют с помощью хромогенного анализа по существу, как описано ранее (J.A.Ostrem et al., Biochemistry 37 (1998) 1053-1059 включена в данный документ в качестве ссылки). Кинетические анализы проводят при 25°С в половинных микротитровочных планшетах (Costar Corp., Cambridge, Massachusetts), используя кинетический планшет-ридер (Molecular Devices Spectramax 250). Для обычного анализа требуется 25 мкл раствора человеческого фактора VIIa и TF (конечная концентрация составляет соответственно 5 нМ и 10 нМ), который объединяют с 40 мкл раствора ингибитора в разных разведениях в смеси 10% DMSO/TBS-PEG буффер (50 mm Трис, 15 мМ NaCl, 5 mM CaCl2, 0,05% PEG 8000, рН 8,15). После 15-минутного периода преинкубации анализ инициируют путем добавления 35 мкл хромогенного субстрата S-2288 (D-Ile-Pro-Arg-п-нитроанилид, Pharmacia Hepar Inc., конечная концентрация 500 мкМ).
Были получены следующие результаты анализа (константы ингибирования Ki (FVIIa)).
Следующие тесты могут служить для исследования ингибирования других выбранных ферментов, участвующих в процессе коагуляции, и других сериновых протеаз под действием соединений формулы I и, следовательно, для определения их специфичности.
b) Анализ фактора Ха
Для данного анализа используют буфер TBS-PEG (50 мМ Трис-Сl, рН 7,8, 200 мМ NaCl, 0,05% (мас./об.) PEG-8000, 0,02% (мас./об.) NaN3). IC50 определяют путем объединения в соответствующих лунках половинного микротитровочного планшета Costar 25 мкл раствора человеческого фактора Ха (Enzyme Research Laboratories, Inc.; South Bend, Indiana) в TBS-PEG; 40 мкл 10% (об./об.) DMSO в TBS-PEG (неингибируемый контроль) или рстворов тестируемого соединения с различными концентрациями, разбавленных 10% (об./об.) DMSO в TBS-PEG; и субстрата S-2765 (N(а)-бензилоксикарбонил-D-Arg-Gly-L-Arg-п-нитроанилида; Kabi Pharmacia, Inc.; Franklin, Ohio) в TBS-PEG.
Анализ проводят путем преинкубации соединения формулы I с ферментом в течение 10 мин. Затем анализ инициируют путем добавления субстрата до получения конечного объема 100 мкл. Начальную скорость гидролиза хромогенного субстрата определяют путем измерения изменения поглощения при 405 нм с помощью кинетического планшет-ридера Biotek Instruments (Ceres UV900HDi) при 25°С на линейном участке кривой временной зависимости (обычно 1,5 мин после добавления субстрата). Концентрация фермента составляет 0,5 нМ, а концентрация субстрата составляет 140 мкМ.
c) Тромбиновый анализ
Для данного анализа используют буфер TBS-PEG. Значение IС50 определяют по методике, описанной выше для анализа фактора Ха, за исключением того, что субстратом является S-2366 (L-PyroGlu-L-Pro-L-Arg-п-нитроанилид; Kabi), а ферментом является человеческий тромбин (Enzyme Research Laboratories, Inc.; South Bend, Indiana). Концентрация фермента составляет 175 мкМ.
d) Плазминовый анализ
Для данного анализа используют буфер TBS-PEG. Значение IC50 определяют по методике, описанной выше для анализа фактора Ха, за исключением того, что субстратом является S-2251 (D-Val-L-Leu-L-Lys-п-нитроанилид; Kabi), а ферментом является человеческий плазмин (Kabi). Концентрация фермента составляет 5 нМ, а концентрация субстрата составляет 300 мкМ.
e) Трипсиновый анализ
Для данного анализа используют буфер TBS-PEG, содержащий 10 мМ CaCl2. Значение IC50 определяют по методике, описанной выше для анализа фактора Ха, за исключением того, что субстратом является BAPNA (бензоил-L-Arg-п-нитроанилид; Sigma Chemical Co.; St. Louis, Missouri), а ферментом является бычий трипсин поджелудочной железы (Type XIII, обработанный ТРСК; Sigma). Концентрация фермента составляет 50 нМ, а концентрация субстрата составляет 300 мкМ.
Крысиная артериовенная модель шунтирования тромбоза
Антитромбозную активность соединений данного изобретения можно оценить с помощью крысиного экстракорпорального артериовенного (AV) шунта. AV шунтирующий контур состоит из трубки длиной 20 см из полиэтилена (РЕ) 60, вставленной в правую сонную артерию, трубки длиной 6 см из РЕ 160, содержащей мерсеризованную хлопковую нить длиной 6,5 см (на 5 см погруженную в кровоток), и второй трубки из РЕ 60 (20 см), завершающей контур в левой яремной вене. Перед вставкой весь контур заполняют обычным физиологическим раствором.
Тестируемое соединение вводят путем непрерывного вливания в хвостовую вену с помощью шприца и катетера типа бабочка. Соединение вводят в течение 30 мин, затем шунт открывают и крови дают течь в течение 15 мин (общее время инфузии 45 мин). В конце 15-минутного периода шунт зажимают, нить осторожно удаляют и взвешивают на аналитических весах. Процент ингибирования образования тромба рассчитывают, используя массу тромба, полученного от контрольных крыс, которым вливали физиологический раствор.
| название | год | авторы | номер документа |
|---|---|---|---|
| Ингибиторы фактора VIIa | 1999 |
|
RU2223967C2 |
| ПРОИЗВОДНЫЕ (ТИО)МОЧЕВИНЫ, ИНГИБИРУЮЩИЕ ФАКТОР VIIa, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2286337C2 |
| N-ГУАНИДИНОАЛКИЛАМИДЫ, ИХ ПОЛУЧЕНИЕ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ | 2000 |
|
RU2253651C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛИДИНА, СПОСОБ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1998 |
|
RU2239641C2 |
| НОВЫЕ ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ, ИХ ПОЛУЧЕНИЕ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ | 1998 |
|
RU2240326C2 |
| ГЕТЕРОАРИЛЗАМЕЩЕННЫЕ АМИДЫ, СОДЕРЖАЩИЕ НАСЫЩЕННУЮ СВЯЗЫВАЮЩУЮ ГРУППУ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2006 |
|
RU2412181C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛИДИНА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ VLA-4 | 2002 |
|
RU2318815C2 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| СОСТАВ ДЛЯ ПОЛУЧЕНИЯ МЕТАТЕЗИСНЫХ ПОЛИМЕРИЗАТОВ | 1995 |
|
RU2171815C2 |
| ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ АДГЕЗИИ ЛЕЙКОЦИТОВ И VLA-4-АНТАГОНИСТОВ | 1997 |
|
RU2229296C2 |
Изобретение относится к соединениям формулы (I)
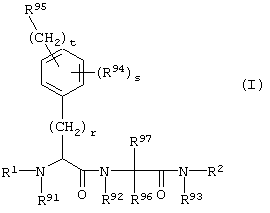
где r равно 1, 2 или 3; s равно 0; t равно 0; R1 выбран из группы, включающей R11-CO и R12-SO2-; R11 выбран из группы, включающей (С6-С14)-арил, (C1-C8)-алкилокси, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40; R12 обозначает (С6-С14)-арил, где указанная группа является незамещенной или замещенной одним или несколькими одинаковыми или разными заместителями R40; R2 обозначает R21(R22)CH-, R23-Het-(CH2)k-, R23(R24)N-(CH2)m-D-(CH2)n- или R25(R26)N-CO-(CH2)p-D-(CH2)q-, где D обозначает двухвалентный остаток -C(R31)(R32)-, двухвалентный (С6-С14)-ариленовый остаток или двухвалентный остаток, полученный из ароматической группы Het, содержащей 5 или 6 атомов в цикле, из которых 1 или 2 являются одинаковыми или различными циклическими гетероатомами, выбранными из группы, включающей азот и серу; числа k, m, n, р и q равны 0, 1, 2; R21 и R22, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (С1-С12)алкил, (С6-С14)-арил, и т.д.; R23 обозначает водород; R27-SO2- или R28-CO-; R24, R25 и R26 обозначают водород; R27 выбран из группы, включающей (С1-С8)-алкил, (С6-С14)-арил, и т.д.; R28 выбран из группы, включающей R27, (С1-С8)-алкилокси; R31 и R32 обозначают водород; R40 выбран из группы, включающей галоген, гидрокси, (С1-С8)-алкилокси, (С1-С8)-алкил, (С6-С14)-арил, и т.д.; R91, R92, R93 и R96 обозначают водород; R95 обозначает амидино; R97 обозначает R99-(C1-С8)алкил; R99 выбран из группы, включающей гидроксикарбонил- и (C1-С8)алкилоксикарбонил-; Het обозначает насыщенную, частично ненасыщенную или ароматическую моноциклическую структуру, содержащую от 3 до 6 атомов в цикле, из которых 1 или 2 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот и серу; во всех его стереоизомерных формах, а также их смеси в любых соотношениях, и его физиологически приемлемые соли. Предложен способ получения соединения формулы (I). Также предложен фармацевтический препарат, обладающий ингибирующей активностью в отношении фактора VIIa, включающий, по меньшей мере, одно соединение формулы (I) и/или его физиологически приемлемые соли и фармацевтически приемлемый носитель. Технический результат соединения формулы (I), обладающие мощным антитромботическим действием и полезные для лечения и профилактики тромбоэмболических заболеваний. 3 н. и 7 з.п. ф-лы.
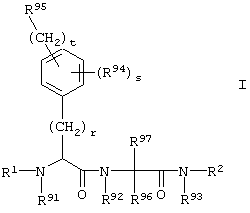
где r равно 1, 2 или 3;
s равно 0;
t равно 0;
R1 выбран из группы, включающей водород, R11-СО- и R12-SO2-;
R11 выбран из группы, включающей (С6-С14)-арил, (С1-С8)-алкилокси-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R12 выбран из группы, включающей (С6-С14)-арил, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R2 обозначает R21(R22)CH-, R23-Het-(CH2)k-, R23(R24)N-(СН2)m-D-(СН2)n-или R25(R26)N-CO-(CH2)p-D-(CH2)q-, где D обозначает двухвалентный остаток -C(R31) (R32)-, двухвалентный (С6-С14)-ариленовый остаток или двухвалентный остаток, полученный из ароматической группы Het, содержащей 5 или 6 атомов в цикле, из которых 1 или 2 являются одинаковыми или различными циклическими гетероатомами, выбранными из группы, включающей азот, и серу, а числа k, m, n, p и q, которые являются независимыми друг от друга и могут быть одинаковыми или разными, равны 0, 1, 2, при условии, что в случае, если D обозначает -C(R31) (R32)- сумма m+n не может быть равна 0 и сумма p+q не может быть равна 0;
R21 и R22, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (C1-С12)-алкил, (С6-С14)-арил, (С6-С14)-арил-(С1-С4)-алкил-, Het- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями из группы, включающей R40, ди-((С1-С8)-алкил)-амино-, аминокарбонил-,
или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют насыщенную или ненасыщенную 3-8-членную карбоциклическую структуру, которая может быть конденсированной с одной или двумя циклическими системами, представляющими собой гетероароматические циклы, содержащие 5-10 атомов в цикле, из которых один представляет собой кислород, и/или (С6-С10) карбоциклические ароматические структуры, где получившаяся группа R21(R22)CH- является незамещенной или замещенной одним или несколькими одинаковыми или разными заместителями, выбранными из группы, включающей R40,
R23 обозначает водород, R27-SO2- или R28-СО-;
R24, R25 и R26 обозначают водород;
R27 выбран из группы, включающей (С1-С8)-алкил, (С6-С14)-арил, (С6-С14)-арил-(С1-С4)-алкил-, амино-, Het-, ди-((С1-С8)-алкил) амино-,
где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R28 выбран из группы, включающей R27, (С1-С8)-алкилокси-;
R31 и R32 обозначают водород;
R40 выбран из группы, включающей галоген, гидрокси, (С1-С8)-алкилокси-, (С1-С8)-алкил, (С6-С14)-арил, (С1-С8)-алкилсульфонил-, трифторметил, ацетиламино-, амино, амидино, гуанидино, оксо, нитро и циано, где группы R40 являются независимыми друг от друга и могут быть одинаковыми или разными;
R91, R92 и R93, R96 обозначают водород;
R95 обозначает амидино;
R97 обозначает R99-(С1-С8)-алкил-;
R99 выбран из группы, включающей гидроксикарбонил-, (C1-C8)-алкилоксикарбонил-;
Het обозначает насыщенную, частично ненасыщенную или ароматическую моноциклическую или бициклическую гетероциклическую структуру, содержащую 3-6 атомов в цикле, из которых 1 или 2 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот и серу; во всех его стереоизомерных формах, а также их смеси в любых соотношениях, и его физиологически приемлемые соли.
r равно 1;
s равно 0;
t равно 0;
R1 обозначает аллилоксикарбонил;
R2 обозначает R21(R22)CH-, R23-Het-(CH2)k или R23(R24)N-(CH2)m-D-(CH2)n;
D обозначает двухвалентный остаток -C(R31) (R32)-, двухвалентный фениленовый остаток или двухвалентный остаток, полученный из ароматической моноциклической группы Het;
R95 обозначает амидино;
R91, R92, R93 и R96 обозначают водород;
R97 обозначает R99-CH2-CH2-;
R99 обозначает гидроксикарбонил- или ((С1-С4)-алкил)оксикарбонил-; во всех его стереоизомерных формах, а также их смеси в любых соотношениях, и его физиологически приемлемые соли.
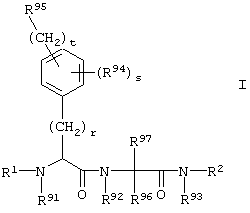
где
r равно 1, 2 или 3;
s равно 0;
t равно 0;
R1 выбран из группы, включающей водород, R11-CO- и R12-SO2-;
R11 выбран из группы, включающей (С6-С14)-арил, (С1-С8)-алкилокси-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R12 выбран из группы, включающей (С6-С14)-арил, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R2 обозначает R21(R22)CH-, R23-Het-(CH2)k-, R23(R24)N-(СН2)m-D-(СН2)n- или R25(R26)N-CO-(CH2)p-D-(CH2)q-, где D обозначает двухвалентный остаток -C(R31) (R32)-, двухвалентный (С6-С14)-ариленовый остаток или двухвалентный остаток, полученный из ароматической группы Het, содержащей 5 или 6 атомов в цикле, из которых 1 или 2 являются одинаковыми или различными циклическими гетероатомами, выбранными из группы, включающей азот, и серу, а числа k, m, n, p и q, которые являются независимыми друг от друга и могут быть одинаковыми или разными, равны 0, 1, 2, при условии, что в случае, если D обозначает -C(R31) (R32) - сумма m+n не может быть равна 0 и сумма p+q не может быть равна 0;
R21 и R22, которые являются независимыми друг от друга, и могут быть одинаковыми или разными, выбраны из группы, включающей водород, (С1-С12)-алкил, (С6-С14)-арил, (С6-С14)-арил-(С1-С4)-алкил-, Het- и Het-(C1-C4)-алкил-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями из группы, включающей R40, ди-((С1-С8)-алкил)-амино-, аминокарбонил-,
или R21 и R22 вместе с атомом углерода, с которым они связаны, образуют насыщенную или ненасыщенную 3-8-членную карбоциклическую структуру, которая может быть конденсированной с одной или двумя циклическими системами, представляющими собой гетероароматические циклы, содержащие от 5 до 10 атомов в цикле, из которых один представляет собой кислород, и/или (С6-С10) карбоциклические ароматические структуры, где получившаяся группа R21(R22)CH- является незамещенной или замещенной одним или несколькими одинаковыми или разными заместителями, выбранными из группы, включающей R40,
R23 обозначает водород, R27-SO2- или R28-СО-;
R24, R25 и R26 обозначают водород;
R27 выбран из группы, включающей (С1-С8)-алкил, (С6-С14)-арил, (С6-С14)-арил-(С1-С4)-алкил-, Het-, ди-((С1-С8)-алкил)амино-, где все указанные группы являются незамещенными или замещенными одним или несколькими одинаковыми или разными заместителями R40;
R28 выбран из группы, включающей R27, (C1-C8)-алкилокси-;
R31 и R32 обозначают водород;
R40 выбран из группы, включающей галоген, гидрокси, (С1-С8)алкилокси-, (С1-С8)-алкил, (С6-С14)-арил, (С1-С8)-алкилсульфонил-, трифторметил, ацетиламино-, амино, амидино, гуанидино, оксо, нитро и циано, где группы R40 являются независимыми друг от друга и могут быть одинаковыми или разными;
R91, R92 и R93, R96 обозначают водород;
R95 обозначает амидино;
R97 обозначает R99-(С1-С8)-алкил-;
R99 выбран из группы, включающей гидроксикарбонил-, (C1-C8)-алкилоксикарбонил-;
Het обозначает насыщенную, частично ненасыщенную или ароматическую моноциклическую или бициклическую гетероциклическую структуру, содержащую от 3 до 6 атомов в цикле, из которых 1 или 2 являются одинаковыми или разными гетероатомами, выбранными из группы, включающей азот и серу, включающий конденсацию соединения формул II
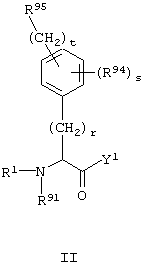
с соединением III
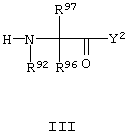
и последующую конденсацию полученного промежуточного продукта с соединением формулы IV
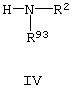
с получением соединения формулы I, причем группы R1, R2, R91, R92, R93, R95, R96, R97 и r, s и t имеют значения указанные выше, или функциональные группы присутствуют в виде групп-предшественников, или в защищенном виде, и Y' и Y2 представляют собой гидроксильные или способные к нуклеофильному замещению уходящие группы.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, ОБЛАДАЮЩИЕ АНТИКОАГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2088591C1 |
Авторы
Даты
2005-03-20—Публикация
2000-05-27—Подача