Область техники, к которой относится изобретение
Настоящее изобретение касается новых противогельминтных депсипептидных соединений с улучшенной активностью против эндопаразитов и эктопаразитов. Настоящее изобретение касается также композиций, содержащих указанные соединения, способов и применения указанных соединений для избавления, борьбы и предотвращения заражения паразитами и/или паразитных инфекций у животных. Соединения по настоящему изобретению можно вводить животным, в частности млекопитающим, рыбам и птицам, для предотвращения или лечения паразитных инфекций и/или заражений.
Предшествующий уровень техники
Животные, включая млекопитающих (включая человека), рыбы и птицы, часто подвержены паразитным заражениям и инфекциям. Эти паразиты могут представлять собой эктопаразиты, такие как блохи и клещи. Животные также страдают также от эндопаразитических инфекций, включая, например, гельминтиаз, который чаще всего вызывается группой паразитических червей, называемых нематодами или круглыми червями. Эти паразиты являются причиной больших экономических потерь в свиноводстве, овцеводстве, коневодстве и разведении крупного рогатого скота, а также поражают домашних животных и птиц в птицеводстве. Другие паразиты, обитающие в желудочно-кишечном тракте животных и людей, включают Ancylostoma, Necator, Ascaris, Strongyloides, Trichinella, Capillaria, Toxocara, Toxascaris, Trichuris, Enterobius, и паразитов, которые встречаются в крови или других тканях и органах, таких как филярийные черви и внекишечные стадии Strongyloides, Toxocara и Trichinella.
Одним типом эндопаразитов, который серьезно вредит млекопитающим, является Dirofilaria immitis, известный также как сердечный гельминт. Другие филярийные эндопаразиты включают Dirofilaria repens и Dirofilaria honkongensis, которые заражают также людей. Наиболее частыми хозяевами являются кошки и собаки, но могут подвергаться заражению также другие млекопитающие, такие как хорьки и еноты. Сердечный гельминт проходит несколько жизненных стадий перед тем как стать взрослым, заражающим легочную артерию гостя-млекопитающего. Червям требуется комар в качестве промежуточного хозяина для завершения своего жизненного цикла. Период между изначальным заражением, когда собаку кусает комар, и превращением червей во взрослых особей, живущих в сердце и легочных артериях, составляет от шести до семи месяцев у собак и известен как «препатентный период». L3 личинки мигрируют во время сосания комаром крови в кончик ротового аппарата комара (лабиум), покидают комара и остаются на коже собаки, где они затем мигрируют в хозяина через ранку от укуса. Большинство L3 личинок переходят в личинок четвертой стадии (L4) в подкожных тканях собаки в течение 1-3 дней после заражения. Затем они мигрируют в мышцы груди и брюшной полости, и через 45-60 дней после заражения переходят в пятую стадию (L5, незрелая взрослая особь). Примерно через 75-20 дней после заражения, эти незрелые сердечные гельминты затем попадают в кровоток и проходят через сердце, задерживаясь в легочной артерии. Примерно через семь месяцев после заражения, взрослые особи Dirofilaria immitis достигают зрелости и приступают к половому размножению в легочных артериях и правом желудочке. Взрослые самцы имеют длину около 15см, а самки около 25см, и их нормальная продолжительность жизни во взрослом состоянии составляет около 5 лет.
Заражение сердечными гельминтами представляет собой тяжелое и угрожающее жизни заболевание. Инфицирование сердечными гельминтами собак можно предотвратить, и профилактическое лечение является приоритетом в областях, эндемичных по заболеванию сердечными гельминтами. Лечение инфекции зрелых сердечных гельминтов препаратами, убивающими взрослых гельминтов (например, меларсомина дигидрохлорид) является дорогостоящим и может вызвать серьезные побочные эффекты, поэтому широко применяется предотвращение заражения посредством ежемесячного введения лекарств, прерывающих развитие личинок. Целью доступных методов терапии сердечных гельминтов у собак является предотвращение развития паразита во взрослых червей путем прерывания жизненного цикла Dirofilaria immitis после заражения.
Макроциклические лактоны (МЛ, например, ивермектин, милбемицин оксим, моксидектин и селамектин) представляют собой наиболее широко используемые средства химиопрофилактики и вводятся ежемесячно или каждые шесть месяцев. Эти лекарственные средства эффективны против инвазионных личинок третьей стадии (L3) Dirofilaria immitis, распространяемых комарами, а также против взрослеющих личинок четвертой стадии (L4). При ежемесячном введении, МЛ убивают L3 и L4 личинок, попавших в организм в течение предыдущих 30 дней, и таким образом предотвращают заболевание, вызываемое взрослыми червями. МЛ можно также применять ежемесячно у инфицированных собак для подавления размножения взрослых червей и удаления микрофиллярий, тем самым уменьшая передачу и постепенно избавляя от взрослых червей (Vet. Parasitol. 2005 Oct 24 133(2-3) 197-206).
В последние годы сообщается об увеличивающемся числе случаев отсутствия эффективности (LOE), при которых у собак развивается инфекция зрелых сердечных гельминтов, несмотря на ежемесячное введение профилактических доз лекарственных средств, представляющих собой макроциклические лактоны. Например, Atkins с соавторами (Veterinary Parasitology 206 (2014) 106-113) недавно сообщали об увеличивающемся числе случаев собак, у которых наблюдалась положительная реакция на антиген сердечных гельминтов при получении профилактической терапии против сердечных гельминтов, что говорит о том, что некоторые популяции Dirofilaria immitis выработали селективную устойчивость к профилактическим средствам против сердечных гельминтов (American Heartworm Society, 2010. Heartworm Preventive Resistance. Is it Possible, vol. 37. Bulletin of the American Heartworm Society, pp. 5.). Таким образом, существует насущная потребность в разработке новых противогельминтных средств с улучшенной активностью против Dirofilaria immitis и других эндопаразитов.
Существуют различные паразитицидные средства для лечения инфекций эндопаразитов у животных. Помимо макроциклических лактонов, известны циклические депсипептиды с антипаразитической активностью. Было обнаружено, что PF1022A, 24-членное циклооктадепсипептид, выделенный из гриба Mycelia sterilia группой Sasaki с соавторами (см. J. Antibiotics 45: 692-697 (1992)), демонстрирует широкий спектр противогельминтной активности против различных эндопаразитов in vivo при низкой токсичности. Эти соединения описаны, например, в Патентах США 5,514,773; 5,747,448; 5,646,244; 5,874,530; среди прочих, которые включены в настоящий текст посредством ссылки. Эмодепсид представляет собой полусинтетический аналог PF1022A, содержащий морфолиновую группу в пара-положении фениллактатных групп. Эмодепсид представляет собой сильное противогельминтное средство, применяемое в комбинации с празиквантелом в продукте Profender® для лечения паразитических червей у кошек и собак. Недавно Scherkenbeck с соавторами описали синтез аналогов PF1022A, в которых фенильные группы в фениллактатных фрагментах молекулы замещены на гетероароматические группы (Letters in Organic Chemistry, 2016, 13, 441-445). Однако, антипаразитическая активность PF1022А и эмодепсида недостаточна для лечения от некоторых паразитов, в особенности для борьбы с Dirofilaria immitis у млекопитающих для предотвращения развития заболевания сердечными гельминтами. Таким образом, имеется потребность в более эффективных антипаразитических средствах для лечения и защиты животных, например млекопитающих, рыб и птиц, от паразитов, в частности от внутренних паразитов, включая нематод и филярийных червей, таких как сердечные гельминты.
Следует отметить, что цитирование или упоминание какого-либо документа в настоящей заявке не является признанием того, что такой документ является частью предшествующего уровня техники для настоящего изобретения. Все предшествующие заявки и все документы, процитированные в них или во время их рассмотрения («процитированные в заявках документы»), и все документы, процитированные или упомянутые в процитированных в заявках документах, и все документы, процитированные или упомянутые в настоящем тексте («процитированные в настоящем тексте документы»), и все документы, процитированные или упомянутые в процитированных в настоящем тексте документах, вместе со всеми инструкциями производителей, описаниями, спецификациями продуктов и технологическими картами продуктов для всех упомянутых в настоящем тексте продуктов, или в любом документе, включенном в настоящий текст посредством ссылки, включены в настоящий текст посредством ссылки и могут использоваться в практической реализации настоящего изобретения.
Краткое описание изобретения
В настоящем изобретении описаны новые и инновационные циклические депсипептидные соединения с улучшенной противогельминтной активностью, а также, возможно, повышенной активностью в отношении эктопаразитов в некоторых вариантах осуществления. Кроме того, в настоящем изобретении описаны композиции, содержащие новые депсипептидные соединения, и способы лечения и профилактики паразитных инфекций и, возможно, заражения животных паразитами, с применением указанных соединений. В некоторых вариантах осуществления, циклические депсипептидные соединения, имеющие формулу I, можно применять для лечения паразитных инфекций у людей.
В одном варианте осуществления, в настоящем изобретении описаны циклические депсипептидные соединения, имеющие изображенную ниже формулу (I):
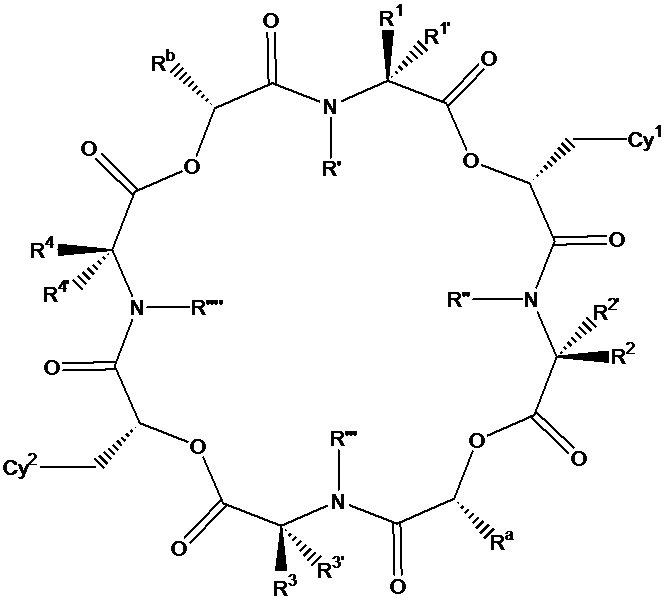 (I)
(I)
или их ветеринарно приемлемая соль, где значения переменных R1, R1’, R2, R2’, R3, R3’, R4, R4’ Cy1, Cy2, Ra, Rb, R', R'', R''' и R'''' соответствуют приведенным ниже. В настоящем изобретении описаны также ветеринарные композиции, содержащие указанные инновационные соединения или их соли, в комбинации с фармацевтически приемлемым носителем или разбавителем.
Соединения по настоящему изобретению охватывают рацемические смеси, отдельные стереоизомеры и таутомерные формы указанного соединения. Другим аспектом настоящего изобретения является солевая форма соединения по настоящему изобретению.
Указанные инновационные соединения и композиции, содержащие указанные соединения, обладают высокой эффективностью в лечении и профилактике внутренних паразитов у животных, включая млекопитающих, рыб и птиц, и, в частности, у людей, кошек, собак, лошадей, цыплят, свиней и крупного рогатого скота, с конечной целью избавить указанных хозяев от всех эндопаразитов, обычно встречающихся у млекопитающих, рыб и птиц.
В одном варианте осуществления, соединения и композиции по настоящему изобретению обладают высокой эффективностью против эндопаразитов, таких как филярии (например, сердечный гельминт), анкилостомы, власоглавы и круглые черви пищеварительного тракта животных (включая людей). В некоторых вариантах осуществления, соединения и композиции по настоящему изобретению эффективны против Dirofilaria immitis (сердечный гельминт), который менее чувствителен к лечению макроциклическими лактонами. В другом варианте осуществления, новые и инновационные депсипептиды по настоящему изобретению эффективны для лечения и предотвращения инфицирования животных круглыми червями, которые менее чувствительны к лечению коммерчески доступными или известными макроциклическими лактонами.
В некоторых вариантах осуществления, в настоящем изобретении описаны композиции, содержащие комбинацию нового депсипептида по настоящему изобретению в комбинации с по меньшей мере одним вторым действующим веществом, которое расширяет спектр защиты животных от эндопаразитов и, возможно, также эктопаразитов.
Настоящее изобретение касается также способов лечения и предотвращения паразитной инфекции или заражения у животного, включающих введение млекопитающему по меньшей мере одного из соединений, имеющих формулу (I) по настоящему изобретению. Также в настоящее изобретение входит применение указанных соединений для лечения и/или предотвращения паразитных инфекций и заражений животных, и применение указанных соединений в получении лекарственного средства для лечения и/или предотвращения паразитных инфекций у животного.
Задачей настоящего изобретения является не включать в настоящее изобретение любые ранее известные продукты, способы изготовления таких продуктов или способы применения таких продуктов, так что Заявитель сохраняет права на настоящее изобретение и заявляет отсутствие притязаний на любой ранее известный продукт, процесс или способ.
Следует отметит, что в настоящем описании, и в частности в формуле изобретения и/или абзацах, такие термины как «содержит», «содержащий» и т.п. имеют значение, указанное для них в патентном законодательстве США; например, они могут означать «включает», «включающий» и т.п.; и что такие термины как «состоящий главным образом из» и «состоит главным образом из» имеют значение, указанное для них в патентном законодательстве США, например они допускают наличие элементов, не указанных явным образом, но исключают элементы, известные в предшествующем уровне техники или которые влияют на основные или новые отличительные черты настоящего изобретения. Эти и другие варианты осуществления раскрыты или являются очевидными из приведенного далее подробного описания, и охватываются им.
Подробное описание изобретения
В настоящем изобретении описаны новые и инновационные циклические депсипептидные соединения, имеющие формулу (I), обладающие паразитицидным действием против эндопаразитов и также против эктопаразитов в некоторых вариантах осуществления, или их ветеринарно приемлемые соли, и композиции, содержащие соединения или их соли, для лечения или предотвращения паразитных инфекций и/или заражений у животного. Также описаны способы для лечения или предотвращения заражений и/или инфекций паразитами у животных, включающие введение млекопитающему эффективного количества депсипептидного соединения по настоящему изобретению или его соли.
Новые и инновационные циклические депсипептиды, имеющие описанную в настоящем тексте формулу (I), и их фармацевтически приемлемые соли особенно эффективны для борьбы с эндопаразитами. Эндопаразиты включают (но не ограничиваются только ими) нематоды (такие как круглые черви, анкилостомы и власоглавы) и филярийные черви, такие как Dirofilaria immitis (сердечный гельминт). В некоторых вариантах осуществления, было обнаружено, что новые циклические депсипептиды по настоящему изобретению имеют значительно более высокую эффективность против эндопаразитов, по сравнению с известными циклическими депсипептидами, включая PF1022A и эмодепсид. В других вариантах осуществления, было неожиданно обнаружено, что новые циклические депсипептиды по настоящему изобретению имеют улучшенный профиль безопасности (более низкую токсичность для млекопитающих) по сравнению с известными циклическими депсипептидами, включая PF1022A и эмодепсид. Кроме того, было обнаружено, что новые циклические депсипептиды по настоящему изобретению значительно более устойчивы к метаболической модификации в теле животных, так что они могут поддерживать высокую концентрацию в теле животного-хозяина и высокий уровень активности против внутренних паразитов в течение более длительного периода времени.
В одном варианте осуществления, было обнаружено, что циклические депсипептиды по настоящему изобретению высоко эффективны против филярийных червей, таких как Dirofilaria immitis (микрофилярийные и личиночные стадии), включая изоляты паразитов, которые менее чувствительны к лечению макроциклическими лактонами. В других вариантах осуществления, соединения по настоящему изобретению эффективны против эндопаразитов, для борьбы с которыми недостаточно эффективны известные циклические депсипептиды, такие как PF1022A и эмодепсид.
В другом варианте осуществления, было обнаружено, что циклические депсипептиды по настоящему изобретению обладают активностью против эктопаразитов, таких как блохи и клещи. Так, в некоторых вариантах осуществления циклические депсипептиды могут иметь эндектоцидную активность как против внутренних, так и против внешних паразитов.
Настоящее изобретение включает по меньшей мере следующие отличительные черты:
(a) В одном варианте осуществления, в настоящем изобретении описаны новые циклические депсипептидные соединения, имеющие формулу (I), или их фармацевтически или ветеринарно приемлемые соли, которые активны против эндопаразитов, и в некоторых случаях также против эктопаразитов;
(b) ветеринарные и фармацевтические композиции, содержащие паразитицидно эффективное количество циклических депсипептидных соединений, имеющих формулу (I), или их фармацевтически или ветеринарно приемлемой соли, в комбинации с фармацевтически или ветеринарно приемлемым носителем или разбавителем;
(c) ветеринарные и фармацевтические композиции, содержащие паразитицидно эффективное количество циклических депсипептидных соединений по настоящему изобретению, или их фармацевтически или ветеринарно приемлемых солей, в комбинации с еще одним другим действующим веществом и фармацевтически или ветеринарно приемлемым носителем или разбавителем;
(d) описаны способы лечения заражений/инфекций паразитами в организме животного или на его покровах, включающие введение паразитицидно эффективного количества циклического депсипептидного соединения, имеющего формулу (I), или его фармацевтически или ветеринарно приемлемых солей, нуждающемуся в этом млекопитающему;
(e) способы предотвращения заражений/инфекций паразитами у животного, которые включают введение паразитицидно эффективного количества циклического депсипептидного соединения, имеющего формулу (I), или его фармацевтически или ветеринарно приемлемых солей, с одним или больше дополнительными действующими веществами, нуждающемуся в этом млекопитающему;
(f) применение циклических депсипептидных соединений, имеющих формулу (I), или их фармацевтически или ветеринарно приемлемых солей, для лечения или предотвращения паразитных инфекций и, возможно, заражения паразитами у животного;
(g) применение циклических депсипептидных соединений, имеющих формулу (I), или их фармацевтически или ветеринарно приемлемых солей, в производстве лекарственного средства для лечения или предотвращения паразитных инфекций у животного; и
(h) способы получения соединений, имеющих формулу (I).
Определения
Применяемые в настоящем тексте термины имеют общепринятое в данной области значение, если не указано иное. Органические фрагменты, указанные в определениях переменных, присутствующих в циклически депсипептидах, имеющих формулу (I), являются - как термин «галоген» - собирательными терминами для списков отдельных членов групп - в случае «галогена» это фтор, хлор, бром и иод. Приставка Cn-Cm в каждом случае указывает возможное число атомов углерода в группе.
Термин «алкил» относится к насыщенным линейным, разветвленным, первичным, вторичным или третичным углеводородам, включая углеводороды, содержащие от 1 до 12 атомов. В некоторых вариантах осуществления, алкильные группы включают C1-C10, C1-C8, C1-C6, C1-C4 или C1-C3 алкильные группы. Примеры C1-C10 алкилов включают (но не ограничиваются только ими) метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, гексил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, гептил, октил, 2-этилгексил, нонил и децил, и их изомеры. C1-C4-алкил означает, например, метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил или 1,1-диметилэтил.
Предпочтительно, если не указано иное, когда «алкильная» группа является заместителем в другом заместителе, алкильная группа является незамещенной. Кроме того, предпочтительно, если не указано иное, «алкил» в контексте алкильного компонента в алкиламино-группе, ди(алкил)амино-группе, алкокси-группе, алкоксиалкокси-группе, алкиловом эфире, галогеналкокси-группе, алкилтио-группе, тиоалкиле, алкилтиоалкиле, галогеналкилтио-группе, гетероалкиле, гидроксиалкиле, алкоксиалкиле, алкилсульфиниле, галогеналкилсульфиниле, алкилсульфониле, галогеналкилсульфониле, триалкилсилиле и т.д. означает алкил, определение которому дано выше, где алкильный компонент не имеет дополнительных заместителей.
Карбоциклические группы представляют собой циклические группы, состоящие исключительно из углерода. Карбоциклические группы включают и ароматические кольца, такие как фенил, и неароматические кольца, такие как циклогексил, и включают группы, содержащие 3-14 атомов углерода, имеющие одно или несколько сконденсированных колец.
Циклические алкильные группы, входящие в понятие алкила, именуемые также «циклоалкил», включают группы с 3-10 атомами углерода, содержащие один или несколько конденсированных циклов. Неограничивающие примеры циклоалкильных групп включают адамантил, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и т.п. Предпочтительно, если не указано иное, когда «циклоалкильная» группа является заместителем в другом заместителе, циклоалкильная группа является незамещенной.
Описанные в настоящем документе алкильные и циклоалкильные группы могут быть незамещенными или замещены одним или более фрагментами, выбранными из группы, состоящей из алкила, галогена, галогеналкила, гидроксила, карбоксила, ацила, ацилокси-группу, амино-группу, алкил- или диалкиламино-группу, амидо, ариламино-группу, алкокси-группу, арилокси-группу, нитро, циано, азидо, тиола, имино, сульфокислоты, сульфата, сульфонила, сульфанила, сульфинила, сульфамоила, сложного эфира, фосфонила, фосфинила, фосфорила, фосфина, тио-сложного эфира, тио-простого эфира, галогенангидрида, ангидрида, оксима, гидразина, карбамата, фосфоновой кислоты, фосфата, фосфоната или любой другой возможной функциональной группы, которая не подавляет биологическую активность соединений по настоящему изобретению, в незащищенном или при необходимости защищенном виде, как известно квалифицированным специалистам в данной области техники, например, как описано в книге Greene, et al., Protective Groups in Organic Synthesis, John Wiley и Sons, Third Edition, 1999, включенной в настоящий документ посредством ссылки.
Термин «алкенил» относится к линейным и разветвленным углеродным цепям, содержащим по меньшей мере одну углерод-углеродную двойную связь. Предпочтительно, если не указано иное, когда «алкенильная» группа является заместителем в другом заместителе, алкенильная группа является незамещенной. В некоторых вариантах осуществления, алкенильные группы могут включать C2-C12 алкенильные группы. В других вариантах осуществления, «алкенил» включает C2-C10, C2-C8, C2-C6 или C2-C4 алкенильные группы. В одном варианте алкенила, число двойных связей составляет 1-3, в другом варианте алкенила число двойных связей равно одному. Другие количества двойных связей углерод-углерод и атомов углерода также входят в определение данного термина, в зависимости от расположения алкенильного фрагмента в молекуле. «C2-C10-алкенильные» группы могут содержать больше одной двойной связи в цепи. Примеры включают (но не ограничиваются только ими) этенил, 1-пропенил, 2-пропенил, 1-метил-этенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-метил-1-пропенил, 2-метил-1-пропенил, 1-метил-2-пропенил, 2-метил-2-пропенил; 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-метил-1-бутенил, 2-метил-1-бутенил, 3-метил-1-бутенил, 1-метил-2-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 1-метил-3-бутенил, 2-метил-3-бутенил, 3-метил-3-бутенил, 1,1-диметил-2-пропенил, 1,2-диметил-1-пропенил, 1,2-диметил-2-пропенил, 1-этил-1-пропенил, 1-этил-2-пропенил, 1-гексенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-метил-1-пентенил, 2-метил-1-пентенил, 3-метил-1-пентенил, 4-метил-1-пентенил, 1-метил-2-пентенил, 2-метил-2-пентенил, 3-метил-2-пентенил, 4-метил-2-пентенил, 1-метил-3-пентенил, 2-метил-3-пентенил, 3-метил-3-пентенил, 4-метил-3-пентенил, 1-метил-4-пентенил, 2-метил-4-пентенил, 3-метил-4-пентенил, 4-метил-4-пентенил, 1,1-диметил-2-бутенил, 1,1-диметил-3-бутенил, 1,2-диметил-1-бутенил, 1,2-диметил-2-бутенил, 1,2-диметил-3-бутенил, 1,3-диметил-1-бутенил, 1,3-диметил-2-бутенил, 1,3-диметил-3-бутенил, 2,2-диметил-3-бутенил, 2,3-диметил-1-бутенил, 2,3-диметил-2-бутенил, 2,3-диметил-3-бутенил, 3,3-диметил-1-бутенил, 3,3-диметил-2-бутенил, 1-этил-1-бутенил, 1-этил-2-бутенил, 1-этил-3-бутенил, 2-этил-1-бутенил, 2-этил-2-бутенил, 2-этил-3-бутенил, 1,1,2-триметил-2-пропенил, 1-этил-1-метил-2-пропенил, 1-этил-2-метил-1-пропенил и 1-этил-2-метил-2-пропенил.
Термин «циклоалкенил» означает одновалентные циклические алкенильные группы, содержащие от 4 до 10 атомов углерода, предпочтительно от 5 до 8 атомов углерода, имеющие одно или несколько конденсированных циклов, которые могут быть или не быть циклоалкенильными, при условии, что точкой присоединения к остальной части молекулы является атом циклоалкенильного кольца. Примеры циклоалкенильных групп включают, например, циклопентен-4-ил, циклооктен-5-ил и т.п. Алкенильные и циклоалкенильные группы могут быть незамещенными или могут быть замещены одним или больше заместителями, описанными выше для алкила.
Термин «алкинил» относится к линейным и разветвленным углеродным цепям, содержащим по меньшей мере одну углерод-углеродную тройную связь. Предпочтительно, если не указано иное, когда «алкинильная» группа является заместителем в другом заместителе, алкинильная группа является незамещенной. В одном варианте алкинила, число тройных связей составляет 1-3; в другом варианте алкинила число тройных связей равно одному. В некоторых вариантах осуществления, алкинильные группы включают C2-C12 алкинильные группы. В других вариантах осуществления, алкинильные группы могут включать C2-C10, C2-C8, C2-C6 или C2-C4 алкинильные группы. Другие количества тройных связей углерод-углерод и атомов углерода также входят в определение данного термина, в зависимости от расположения алкинильного фрагмента в молекуле. «C2-C10-алкинил» при использовании в настоящем тексте относится к линейным или разветвленным ненасыщенным углеводородным группам, содержащим от 2 до 10 атомов углерода и содержащим по меньшей мере одну тройную связь, таким как этинил, проп-1-ин-1-ил, проп-2-ин-1-ил, н-бут-1-ин-1-ил, н-бут-1-ин-3-ил, н-бут-1-ин-4-ил, н-бут-2-ин-1-ил, н-пент-1-ин-1-ил, н-пент-1-ин-3-ил, н-пент-1-ин-4-ил, н-пент-1-ин-5-ил, н-пент-2-ин-1-ил, н-пент-2-ин-4-ил, н-пент-2-ин-5-ил, 3-метилбут-1-ин-3-ил, 3-метилбут-1-ин-4-ил, н-гекс-1-ин-1-ил, н-гекс-1-ин-3-ил, н-гекс-1-ин-4-ил, н-гекс-1-ин-5-ил, н-гекс-1-ин-6-ил, н-гекс-2-ин-1-ил, н-гекс-2-ин-4-ил, н-гекс-2-ин-5-ил, н-гекс-2-ин-6-ил, н-гекс-3-ин-1-ил, н-гекс-3-ин-2-ил, 3-метилпент-1-ин-1-ил, 3-метилпент-1-ин-3-ил, 3-метилпент-1-ин-4-ил, 3-метилпент-1-ин-5-ил, 4-метилпент-1-ин-1-ил, 4-метилпент-2-ин-4-ил или 4-метилпент-2-ин-5-ил и т.п.
Термин «галогеналкил» относится к алкильной группе, определение которой дано в настоящем тексте, которая замещена одним или больше атомами галогена. Например, C1-C4-галогеналкил включает (но не ограничивается только ими) хлорметил, бромметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлордифторметил, 1-хлорэтил, 1-бромэтил, 1-фторэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2-хлор-2-фторэтил, 2-хлор-2,2-дифторэтил, 2,2-дихлор-2-фторэтил, 2,2,2-трихлорэтил, пентафторэтил и т.п.
Термин «фторалкил» при использовании в настоящем тексте означает алкил, в котором один или больше атомов углерода заменены на атомы фтора, например дифторметил, трифторметил, 1-фторэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 1,1,2,2-тетрафторэтил или пентафторэтил.
Термин «галогеналкенил» относится к алкенильной группе, определение которой дано в настоящем тексте, которая замещена одним или больше атомами галогена.
Термин «галогеналкинил» относится к алкинильной группе, определение которой дано в настоящем тексте, которая замещена одним или больше атомами галогена.
Термин «алкокси» относится к группе алкил-O-, где алкил имеет указанное выше значение. Аналогично, термины «алкенилокси», «алкинилокси», «галогеналкокси», «галогеналкенилокси», «галогеналкинилокси», «циклоалкокси», «циклоалкенилокси», «галогенциклоалкокси» и «галогенциклоалкенилокси» относятся к группам алкенил-O-, алкинил-O-, галогеналкил-O-, галогеналкенил-O-, галогеналкинил-O-, циклоалкил-O-, циклоалкенил-O-, галогенциклоалкил-O- и галогенциклоалкенил-O-, соответственно, где алкенил, алкинил, галогеналкил, галогеналкенил, галогеналкинил, циклоалкил, циклоалкенил, галогенциклоалкил и галогенциклоалкенил имеют указанные выше значения. Примеры C1-C6-алкокси включают (но не ограничиваются только ими) метокси, этокси, OCH2-C2H5, OCH(CH3)2, н-бутокси, OCH(CH3)-C2H5, OCH2-CH(CH3)2, OC(CH3)3, н-пентокси, 1-метилбутокси, 2-метилбутокси, 3-метилбутокси, 1,1-диметилпропокси, 1,2-диметилпропокси, 2,2-диметил-пропокси, 1-этилпропокси, н-гексокси, 1-метилпентокси, 2-метилпентокси, 3-метилпентокси, 4-метилпентокси, 1,1-диметилбутокси, 1,2-диметилбутокси, 1,3-диметилбутокси, 2,2-диметилбутокси, 2,3-диметилбутокси, 3,3-диметилбутокси, 1-этилбутокси, 2-этилбутокси, 1,1,2-триметилпропокси, 1,2,2-триметилпропокси, 1-этил-1-метилпропокси, 1-этил-2-метилпропокси и т.п.
Термин «арил» относится к одновалентной карбоциклической группе, содержащей от 6 до 14 атомов углерода, имеющей один цикл или несколько конденсированных циклов. Арильные группы включают (но не ограничиваются только ими) фенил, бифенил и нафтил. В некоторых вариантах осуществления, арил включает тетрагидронафтил, фенилциклопропил и инданил. Арильные группы могут быть незамещенными или быть замещены одним или более заместителями, выбранными из следующих: атом галогена, циано-группа, нитро-группа, гидрокси-группа, меркапто-группа, амино-группа, алкил, алкенил, алкинил, циклоалкил, циклоалкенил, галогеналкил, галогеналкенил, галогеналкинил, галогенциклоалкил, галогенциклоалкенил, алкокси-группа, алкенилокси-группа, алкинилокси-группа, галогеналкокси-группа, галогеналкенилокси-группа, галогеналкинилокси-группа, циклоалкокси-группа, циклоалкенилокси-группа, галогенциклоалкокси-группа, галогенциклоалкенилокси-группа, алкилтио-группа, галогеналкилтио-группа, галогентио-группа, циклоалкилтио-группа, галогенциклоалкилтио-группа, алкилсульфинил, алкенилсульфинил, алкинил-сульфинил, галогеналкилсульфинил, галогеналкенилсульфинил, галогеналкинилсульфинил, алкилсульфонил, алкенилсульфонил, алкинилсульфонил, галогеналкил-сульфонил, галогеналкенилсульфонил, галогеналкинилсульфонил, -SF5, алкиламино-группа, алкениламино-группа, алкиниламино-группа, ди(алкил)амино-группа, ди(алкенил)-амино-группа, ди(алкинил)амино-группа или триалкилсилил.
Термин «аралкил» относится к арильной группе, которая связана с остальной частью соединения через дирадикальный алкиленовый мостик, (-CH2-)n, где n равно 1-12 и где «арил» имеет указанное выше значение.
Термин «Гетероарил» относится к одновалентной ароматической группе, содержащей 1 - 15 атомов углерода, предпочтительно от 1 до 10 атомов углерода, содержащей один или более гетероатомов кислорода, азота и серы в цикле, предпочтительно 1 - 4 гетероатома или 1 - 3 гетероатома. Гетероатомы азота и серы опционально могут быть окислены. Такие гетероарильные группы могут иметь один цикл (например, пиридил или фурил) или несколько конденсированных циклов, при условии, что точка присоединения находится на атоме гетероарильного цикла. Предпочтительные гетероарилы включают пиридил, пиридазинил, пиримидинил, пиразинил, триазинил, пирролил, индолил, хинолинил, изохинолинил, хиназолинил, хиноксалиннил, фуранил, тиофенил, фурил, пирролил, имидазолил, оксазолил, изоксазолил, изотиазолил, пиразолил, бензофуранил, бензотиофенил, имидазопиридил, имидазопиримидил или пирролопиримидил. Гетероарильные циклы могут быть незамещенными или замещены одним или более фрагментами, определенными выше для термина «арил».
Термины «Гетероциклил», «гетероциклический» или «гетероцикло» относится к полностью насыщенным или ненасыщенным циклическим группам, например, 3-7-членным моноциклическим, 7-11-членным бициклическим или 10-15-членным трициклическим системам, которые могут содержать по меньшей мере один гетероатом в цикле, содержащем по меньшей мере один атом углерода. Каждый цикл гетероциклической группы, содержащий гетероатом, может содержать 1, 2, 3 или 4 гетероатома, выбранных из атомов азота, атомов кислорода и/или атомов серы, где гетероатомы азота и серы опционально могут быть окислены, и гетероатомы азота опционально могут быть кватернизованы. Если не указано иное, гетероциклическая группа может быть присоединена по любому гетероатому или атому углерода в цикле или в циклической системе, и может быть незамещенной или замещенной одним или больше заместителями, как описано выше для арильных групп.
Примеры моноциклических гетероциклических групп включают (но не ограничиваются только ими) азиридинил, азетидинил, оксетанил, пирролидинил, пирролил, пиразолил, оксетанил, пиразолинил, имидазолил, имидазолинил, имидазолидинил, оксазолил, оксазолидинил, изоксазолинил, изоксазолил, тиазолил, тиадиазолил, тиазолидинил, изотиазолил, изотиазолидинил, фурил, тетрагидрофурил, тиенил, оксадиазолил, пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, 4-пиперидонил, пиридинил, пиразинил, пиримидинил, пиридазинил, тетрагидропиранил, морфолинил, тиаморфолинил, тиаморфолинил сульфоксид, тиаморфолинил сульфон, 1,3-диоксолан и тетрагидро-1,1-диоксотиенил, триазолил, триазинил и т.п.
Примеры бициклических гетероциклических групп включают (но не ограничиваются только ими) индолил, бензотиазолил, бензоксазолил, бензодиоксолил, бензотиенил, хинуклидинил, хинолинил, тетра-гидроизохинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофурил, хромонил, кумаринил, бензопиранил, циннолинил, хиноксалинил, индазолил, пирролопиридил, фуропиридинил (такой как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолил, дигидрохиназолинил (такой как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинил и т.п.
Термин «алкилтио» относится к группе алкил-S-, где алкил имеет указанное выше значение. В некоторых вариантах осуществления, алкильный компонент алкилтио-группы включает C1-C10, C1-C8, C1-C6 C1-C4 или C1-C3 алкильные группы. Например, C1-C4-алкилтио-группа включает (но не ограничивается только ими) метилтио-группу, этилтио-группу, пропилтио-группу, 1-метилэтилтио-группу, бутилтио-группу, 1-метилпропилтио-группу, 2-метилпропилтио-группу или 1,1-диметилэтилтио-группу.
Аналогично, термины «галогеналкилтио», «циклоалкилтио», «галогенциклоалкилтио» относятся к группам -S-галогеналкил, -S-циклоалкил и -S-галогенциклоалкил, соответственно, где термины «галогеналкил», «циклоалкил» и «галогенциклоалкил» имеют указанные выше значения.
Термин «галогентио» относится к группам, имеющим формулу Xn-S-, где X это атом галогена, и n равен 1, 3 или 5. Термин «галогентио» включает -SF5.
Термин «алкилсульфинил» означает группу алкил-S(=O)-, где «алкил» имеет указанное выше значение. В некоторых вариантах осуществления, алкильный компонент алкилсульфинильных групп включает C1-C12, C1-C10, C1-C8, C1-C6, C1-C4 или C1-C3 алкильные группы. Примеры включают (но не ограничиваются только ими) -SO-CH3, -SO-C2H5, н-пропилсульфинил, 1-метилэтилсульфинил, н-бутилсульфинил, 1-метилпропилсульфинил, 2-метилпропилсульфинил, 1,1-диметилэтилсульфинил, н-пентилсульфинил, 1-метилбутилсульфинил, 2-метилбутилсульфинил, 3-метилбутилсульфинил, 1,1-диметилпропилсульфинил, 1,2-диметилпропилсульфинил, 2,2-диметилпропилсульфинил, 1-этилпропилсульфинил, н-гексилсульфинил, 1-метилпентилсульфинил, 2-метилпентилсульфинил, 3-метилпентилсульфинил, 4-метилпентилсульфинил, 1,1-диметилбутилсульфинил, 1,2-диметилбутилсульфинил, 1,3-диметилбутилсульфинил, 2,2-диметилбутилсульфинил, 2,3-диметилбутилсульфинил, 3,3-диметилбутилсульфинил, 1-этилбутилсульфинил, 2-этилбутилсульфинил, 1,1,2-триметилпропилсульфинил, 1,2,2-триметилпропилсульфинил, 1-этил-1-метилпропилсульфинил или 1-этил-2-метилпропилсульфинил.
Аналогично, термины «алкенилсульфинил», «алкинилсульфинил», «галогеналкилсульфинил», «галогеналкенилсульфинил» и «галогеналкинилсульфинил» относятся к группам алкенил-S(=O)-, алкинил-S(=O)- и галогеналкил-S(=O)-, галогеналкенил-S(=O)- и галогеналкинил-S(=O)-, где термины «алкенил», «алкинил», «галогеналкил», «галогеналкенил» и «галогеналкинил» имеют указанные выше значения.
Термин «алкилсульфонил» означает группу алкил-S(=O)2-, где термин «алкил» имеет указанное выше значение. В некоторых вариантах осуществления, алкильный компонент в алкилсульфонильных группах включает C1-C12, C1-C10, C1-C8, C1-C6 или C1-C4 алкильные группы. Примеры включают (но не ограничиваются только ими) -SO2-CH3, -SO2-C2H5, н-пропилсульфонил, -SO2-CH(CH3)2, н-бутилсульфонил, 1-метилпропилсульфонил, 2-метилпропилсульфонил, -SO2-C(CH3)3, н-пентилсульфонил, 1-метилбутилсульфонил, 2-метилбутилсульфонил, 3-метилбутилсульфонил, 1,1-диметилпропилсульфонил, 1,2-диметилпропилсульфонил, 2,2-диметилпропилсульфонил, 1-этилпропилсульфонил, н-гексилсульфонил, 1-метилпентилсульфонил, 2-метилпентилсульфонил, 3-метилпентилсульфонил, 4-метилпентилсульфонил, 1,1-диметилбутилсульфонил, 1,2-диметилбутилсульфонил, 1,3-диметилбутилсульфонил, 2,2-диметилбутилсульфонил, 2,3-диметилбутилсульфонил, 3,3-диметилбутилсульфонил, 1-этилбутилсульфонил, 2-этилбутилсульфонил, 1,1,2-триметилпропилсульфонил, 1,2,2-триметилпропилсульфонил, 1-этил-1-метилпропилсульфонил или 1-этил-2-метилпропилсульфонил и т.п.
Термины «алкенилсульфонил», «алкинилсульфонил», «галогеналкилсульфонил», «галогеналкенилсульфонил» и «галогеналкинилсульфонил» относятся к группам алкенил -S(=O)2-, алкинил-S(=O)2- и галогеналкил-S(=O)2-, галогеналкенил-S(=O)2- и галогеналкинил-S(=O)2-, где термины «алкенил», «алкинил», «галогеналкил», «галогеналкенил» и «галогеналкинил» имеют указанные выше значения.
Термины «алкиламино-группа», «диалкиламино-группа», «алкениламино-группа», «алкиниламино-группа», «ди(алкенил)амино-группа» и «ди(алкинил)амино-группа» относятся к группам -NH(алкил), -N(алкил)2, -NH(алкенил), -NH(алкинил), -N(алкенил)2 и -N(алкинил)2, где термины «алкил», «алкенил» и «алкинил» имеют указанные выше значения. В некоторых вариантах осуществления, алкильный компонент в алкиламино-группах или диалкиламино-группах включают C1-C12, C1-C10, C1-C8, C1-C6 или C1-C4 алкильные группы.
Соединения по настоящему изобретению:
Соединения по настоящему изобретению представляют собой 24-членные циклические депсипептидные соединения, которые обладают высокой активностью против эндопаразитов, таких как нематоды и филярийные черви (микрофилярийные и личиночные стадии), а также против эктопаразитов, таких как блохи и клещи. В одном варианте осуществления, в настоящем изобретении описаны циклические депсипептидные соединения, имеющие формулу (I), или их фармацевтически или ветеринарно приемлемые соли:

(I)
где:
Cy1 и Cy2 независимо представляют собой арил, карбоцикл, гетероарил или гетероцикл, каждый из которых может быть необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель в Cy1 и Cy2 необязательно дополнительно независимо замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2;
R5 и R6 независимо представляют собой атом водорода, алкил, галогеналкил, тиоалкил, алкилтио-группу, алкилтиоалкил, гидроксиалкил, алкоксиалкил, алкенил, галогеналкенил, алкинил, галогеналкинил или группу -CH2C(O)NHCH2CF3; или R5 и R6 вместе с атомом(-ами), с которыми они связаны, образуют C3-C6 циклическую группу;
R', R'', R''' и R''''' каждый независимо представляют собой атом водорода или C1-C3 алкил;
Ra и Rb независимо представляют собой атом водорода, C1-C3 алкил или C1-C3 галогеналкил; и
(a) R1 представляет собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или R1 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ представляет собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R3, R3’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(b) R2 представляет собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или R2 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2’ представляет собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R3, R3’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(c) R3 представляет собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или R3 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членной карбоциклической или 3-8-членной гетероциклической группой; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R3’ представляет собой атом водорода или C1-C3 алкил; или
R3 и R3’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2, R2’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(d) R4 представляет собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или R4 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R4’ представляет собой атом водорода или C1-C3 алкил; или
R4 и R4’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2, R2’, R3 и R3’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(e) R1 и/или R2 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R2’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R3, R3’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(f) R1 и/или R3 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(g) R1 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, галогеналкилсульфинила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R3 и R3’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(h) R2 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R3 и R3’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(i) R2 и/или R3 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2’ и/или R3’ независимо представляют собой атом водорода или C1-C 3 алкил; или
R2 и R2’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R4 и R4’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(j) R3 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R3’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2 и R2’ каждый независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(k) R1 и/или R2 и/или R3 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R2’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R4 и R4’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(l) R2 и/или R3 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2’ и/или R3’и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1 и R1’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(m) R1 и/или R3 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R3’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2 и R2’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(n) R1 и/или R2 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R2’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R3 и R3’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой; или
(o) R1 и/или R2 и/или R3 и/или R4 каждый независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1’ и/или R2’ и/или R3’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе и/или R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла.
Cy1 и Cy2 группы
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2, где R5 и R6 имеют указанные выше значения. Следует понимать, что заместители в фенильном кольце могут находиться в любом положении кольца, включая орто-, мета- и пара-положения к точке присоединения к макроциклу.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, гетероарил или гетероциклил, необязательно независимо замещенные одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой 6-12 членную бициклическую арильную, 6-12 членную бициклическую гетероарильную или 6-12 членную бициклическую гетероциклильную группы, каждая из которых необязательно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель дополнительно независимо замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой бициклические гетероциклические группы, каждая из которых необязательно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный и гетероарильный заместитель дополнительно независимо замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, бифенил, нафтил, тетрагидронафтил, фенилциклопропил, бифенилен (бифениленил), флуорен (флуоренил), антрацен (антраценил), аценафтен (аценафтенил), фенантрен (фенантренил) или инданил, каждый из которых необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой пиридил, пиридазинил, пиримидинил, пиразинил, триазинил, пирролил, индолил, хинолинил, изохинолинил, хиназолинил, хиноксалинил, фуранил, тиофенил, пирролил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, бензоксазолил, бензотиазолил, пиразолил, бензофуранил, дигидробензофуранил, бензотиофенил, имидазопиридил, имидазопиримидил или пирролопиримидил, каждый из которых необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила и гетероарила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой пирролидинил, пирролил, пиразолил, оксетанил, пиразолинил, имидазолил, имидазолинил, имидазолидинил, оксазолил, оксазолидинил, изоксазолинил, изоксазолил, тиазолил, тиадиазолил, тиазолидинил, изотиазолил, изотиазолидинил, фурил, тетрагидрофуранил, тиенил, оксадиазолил, пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, 4-пиперидонил, пиридинил, пиразинил, пиримидинил, пиридазинил, тетрагидропиранил, морфолинил, тиаморфолинил, тиаморфолинил сульфоксид, тиаморфолинил сульфон, 1,3-диоксолан и тетрагидро-1,1-диоксотиенил, триазолил или триазинил, каждый из которых необязательно независимо замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила, гетероарила, -O-гетероарила, -S-гетероарила, -O-гетероциклила или -S-гетероциклила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой индолил, изоиндолил, бензотиазолил, бензоксазолил, бенз[d]изоксазолил, бензотриазолил, бензодиоксолил, бензотиенил, хинуклидинил, хиназолинил, хиноксалинил, хинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофуранил, дигидробензофуранил, хромонил, кумаринил, циннолинил, индазолил, пирролопиридил, фталазинил, 1,2,3-бензотриазинил, 1,2,4-бензотриазинил, фуропиридинил (такой как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолил, дигидрохиназолинил (такой как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинил или тетрагидроизохинолинил, каждый из которых необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкила, гетероалкила, гетероциклила, арила, гетероарила, -O-гетероарила, -S-гетероарила, -O-гетероциклила или -S-гетероциклила, где каждый циклоалкильный, гетероалкильный, гетероциклильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный гетероциклилом. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой 6-членную гетероарильную группу, замещенную гетероциклилом. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой гетероциклил, замещенный гетероциклильной группой. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, каждый из которых замещен гетероциклилом.
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, замещенный морфолино-группой, тетрагидропирановой группой, тетрагидрофурановой группой, пирролидиновой или пиперидиновой группой, где указанные морфолино-группа, тетрагидропирановая группа, тетрагидрофурановая группа, пирролидиновая или пиперидиновая группа могут необязательно быть замещены одним или больше галогенами, алкилами или галогеналкилами.
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил или 5-членное или 6-членное гетероарильный цикл, каждый из которых необязательно замещен одним или больше галогенами, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, тиоамидо-группой, -SF5, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил или 5-членное или 6-членное гетероарильный цикл, каждый из которых необязательно замещен одним или больше алкилом, галогеналкилом, алкенилом, галогеналкенилом, алкинилом, галогеналкинилом.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил или 5-членное или 6-членное гетероарильное кольцо, каждое из которых необязательно замещено одним или больше метилом, этилом, пропилом, изопропилом, бутилом, изобутилом, трет-бутилом, CF3, -CH2CF3, -CHFCF3 или -CF2CF3.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил или 5-членное или 6-членное гетероарильное кольцо, каждое из которых необязательно замещено фтором, хлором, бромом или иодом.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил или 5-членное или 6-членное гетероарильное кольцо, каждое из которых необязательно замещено одной или больше гидрокси-группой, метокси-группой, трифторметокси-группой, -OCH2CF3, -OCHFCF3, -OCF2CF3, -SCH3, -SCF3, -SCH2CF3, -SCHFCF3, -SCF2CF3, -S(O)CH3, -S(O)CF3, -S(O)CH2CF3, -S(O)CHFCF3, -S(O)CF2CF3, -S(O)2CH3, -S(O)2CF3, -S(O)2CH2CF3, -S(O)2CHFCF3, -S(O)2CF2CF3 или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, тиенил, оксазолил, тиазолил, изотиазолил, 1,3-4-тиадиазолил, пиразолил, фурил, имидазолил, пирролил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, каждый из которых необязательно замещен одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, тиоамидо-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, тиенил, оксазолил, тиазолил, изотиазолил, 1,3-4-тиадиазолил, пиразолил, фурил, имидазолил, пирролил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, каждый из которых необязательно замещен одним или больше алкилом, галогеналкилом, алкенилом, галогеналкенилом, алкинилом или галогеналкинилом.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, 5-членное или 6-членное гетероарильное кольцо, каждое из которых необязательно замещено метилом, этилом, пропилом, изопропилом, бутилом, изобутилом, трет-бутилом, CF3, -CH2CF3, -CHFCF3 или -CF2CF3.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, тиенил, оксазолил, тиазолил, изотиазолил, 1,3-4-тиадиазолил, пиразолил, фурил, имидазолил, пирролил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, каждый из которых необязательно замещен фтором, хлором, бромом или иодом.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, тиенил, оксазолил, тиазолил, изотиазолил, 1,3-4-тиадиазолил, пиразолил, фурил, имидазолил, пирролил, пиридинил, пиридазинил, пиримидинил, пиразинил или тетразинил, каждый из которых необязательно замещен гидрокси-группой, метокси-группой, трифторметокси-группой, -OCH2CF3, -OCHFCF3, -OCF2CF3, -SCH3, -SCF3, -SCH2CF3, -SCHFCF3, -SCF2CF3, -S(O)CH3, -S(O)CF3, -S(O)CH2CF3, -S(O)CHFCF3, -S(O)CF2CF3, -S(O)2CH3, -S(O)2CF3, -S(O)2CH2CF3, -S(O)2CHFCF3, -S(O)2CF2CF3 или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный C1-C6 алкилом, C1-C6-галогеналкилом, C1-C3 алкокси-группой, C1-C3-галогеналкокси-группой, C3-C8 циклоалкилом, тетрагидропиранилом, морфолинилом или пиперидинилом, где каждый C1-C6 алкил, C3-C8 циклоалкил, тетрагидропиранил, морфолинил или пиперидинил необязательно замещен одним или больше галогеном, C1-C4 алкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный трет-бутилом, втор-бутилом, изобутилом, изопропилом, трифторметилом, метокси-группой, этокси-группой, пропокси-группой, трифторметокси-группой, циклопентилом, циклогексилом, тетрагидропиранилом, морфолинилом или пиперидинилом, где каждый трет-бутил, втор-бутил, изобутил, изопропил, циклопентил, циклогексил, тетрагидропиранил, морфолинил или пиперидинил необязательно замещен одним или больше галогеном, C1-C4 алкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный трет-бутилом, изопропилом, циклогексилом, трифторметокси-группой, трифторметилом, тетрагидропиранилом, морфолинилом или пиперидинилом, где каждый циклогексил, тетрагидропиранил, морфолинил или пиперидинил необязательно замещен одним или больше галогеном, C1-C4 алкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой фенил, замещенный трет-бутилом, трифторметилом, трифторметокси-группой, циклогексилом, тетрагидропиранилом, морфолинилом или пиперидинилом, где каждый циклогексил, тетрагидропиранил, морфолинил или пиперидинил необязательно замещен одним или больше атомами фтора.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой одну из изображенных ниже групп R1 - R8:
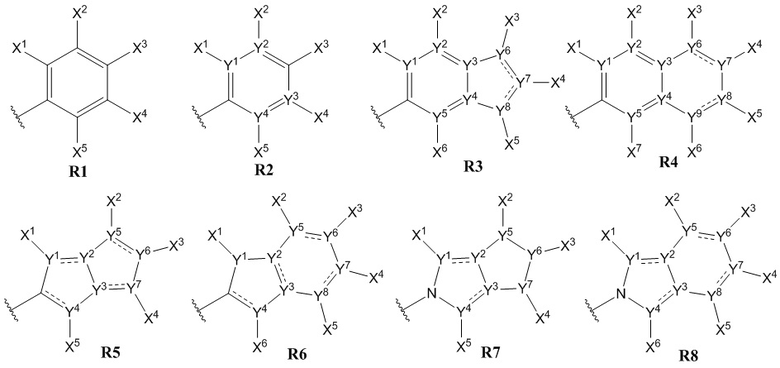
где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, галоген, гидрокси-группу, алкокси-группу, галогеналкокси-группу, алкилтио-группу, галогеналкилтио-группу, тиоамидо-группу, амино-группу, алкиламино-группу, диалкиламино-группу, алкил, галогеналкил, алкенил, галогеналкенил, алкинил, галогеналкинил, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкил, гетероалкил, арил или гетероарил, где каждый циклоалкильный, гетероалкильный, арильный или гетероарильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2, где R5 и R6 имеют указанные выше значения; и пунктирные линии вместе со сплошными линиями, т.е. ---- представляют собой простые или двойные связи.
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой R1 - R8, где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, галоген, гидрокси-группу, алкокси-группу, галогеналкокси-группу, алкилтио-группу, галогеналкилтио-группу, R5R6NC(O)-, R5R6NC(O)NR5-, тиоамидо-группу, амино-группу, алкиламино-группу или диалкиламино-группу.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R1 - R8, где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, алкил, галогеналкил, алкенил, галогеналкенил, алкинил, галогеналкинил.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R1 - R8, где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, CF3, -CH2CF3, -CHFCF3 или CF2CF3.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R1 - R8, где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, атом фтора, хлор, бром или иод.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R1 - R8, где Y1, Y2, Y3, Y4, Y5, Y6, Y7, Y8 и Y9 каждый независимо представляют собой C, CH или N; и X1, X2, X3, X4, X5, X6 и X7 независимо представляют собой атом водорода, гидрокси-группу, метокси-группу, трифторметокси-группу, -OCH2CF3, -OCHFCF3, -OCF2CF3, метилтио-группу, трифторметилтио-группу, -SCH2CF3, -SCHFCF3, -SCF2CF3 или SF5.
В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой изображенные ниже R9 - R11:
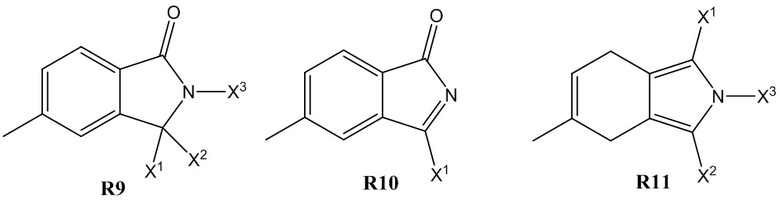
где X1, X2 и X3 независимо представляют собой атом водорода, галоген, гидрокси-группу, алкокси-группу, галогеналкокси-группу, алкилтио-группу, галогеналкилтио-группу, тиоамидо-группу, амино-группу, алкиламино-группу, диалкиламино-группу, алкил, галогеналкил, алкенил, галогеналкенил, алкинил, галогеналкинил, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN, -NO2, циклоалкил, гетероалкил, арил или гетероарил, где каждый циклоалкил, гетероалкил, арил или гетероарил необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, тиоамидо-группы, амино-группы, алкиламино-группы, диалкиламино-группы, алкила, галогеналкила, алкенила, галогеналкенила, алкинила, галогеналкинила, SF5, R5S(O)-, R5S(O)2-, R5C(O)-, R5R6NC(O)-, R5R6NC(O)NR5-, R5OC(O)-, R5C(O)O-, R5C(O)NR6-, -CN и -NO2.
В одном варианте осуществления, Cy1 и Cy2 независимо представляют собой R9 - R11, где X1, X2 и X3 независимо представляют собой атом водорода, галоген, алкил или галогеналкил. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R9 - R11, где X1, X2 и X3 независимо представляют собой атом водорода, атом фтора, хлом, бром или иод. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R9 - R11, где X1, X2 и X3 независимо представляют собой атом водорода, метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, CF3, -CH2CF3, -CHFCF3 или CF2CF3. В другом варианте осуществления, Cy1 и Cy2 независимо представляют собой R9 - R11, где X1, X2 и X3 независимо представляют собой атом водорода, гидрокси-группу, метокси-группу, трифторметокси-группу, -OCH2CF3, -OCHFCF3, -OCF2CF3, метилтио-группу, трифторметилтио-группу, -SCH2CF3, -SCHFCF3, -SCF2CF3 или SF5.
В другом варианте осуществления, Cy1 и/или Cy2 независимо представляют собой фенил, п-морфолинофенил, п-фторфенил, п-OCF3-фенил, п-CF3-фенил, 3,4,5-трифтор-фенил, п-тетрагидропиранил-фенил, 4-морфолино-2-пиридинил, 4-морфолино-3-пиридинил, п-тиосульфонилморфолино-фенил, п-NH2-фенил, п-S-тетразолил-фенил, п-NH2-фенил, дигидробензофуранил, 4-морфолиноциклогексил, п-иодфенил, п-бромфенил, п-нитрофенил и п-трет-бутилфенил.
В другом варианте осуществления, Cy1 и Cy2 представляют собой группы, перечисленные ниже в Таблице 1:
Таблица 1:
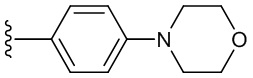

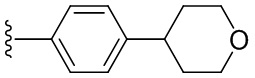

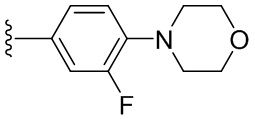

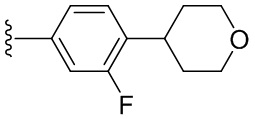

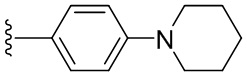

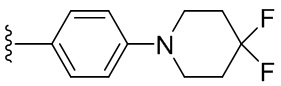

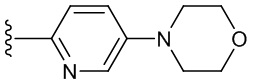

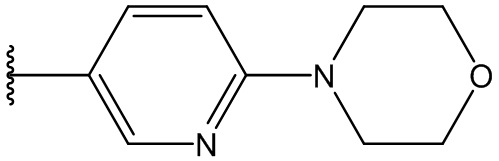

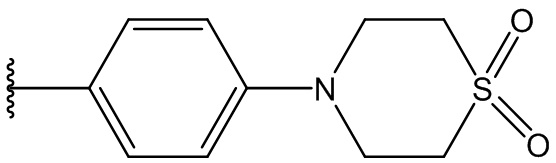

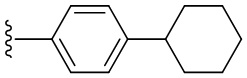

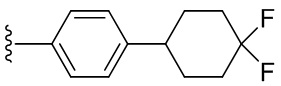


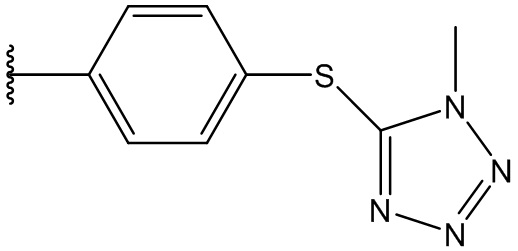
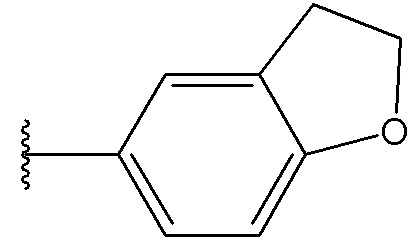



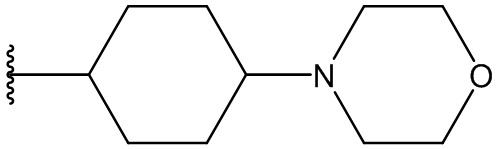


Ra и Rb
Ra и Rb могут независимо представлять собой атом водорода, C1-C3 алкил или C1-C3 галогеналкил. В одном варианте осуществления, Ra и Rb независимо представляют собой атом водорода или метил. В другом варианте осуществления, Ra и Rb независимо представляют собой атом водорода, метил, этил или пропил. В другом варианте осуществления, Ra и Rb независимо представляют собой атом водорода, метил или CF3. В другом варианте осуществления, Ra и Rb оба представляют собой метил. В другом варианте осуществления, Ra и Rb оба представляют собой атом водорода.
R', R'', R''' и R''''
В одном варианте осуществления, R', R'', R''' и R'''' независимо представляют собой атом водорода или C1-C3 алкил. В другом варианте осуществления, R', R'', R''' и R'''' независимо представляют собой атом водорода или метил. В другом варианте осуществления, каждый из R', R'', R''' и R'''' независимо представляют собой атом водорода, метил или этил.
R1, R1’, R2, R2’, R3, R3’ R4 и R4’
Следует понимать, что настоящее изобретение включает соединения, где различные группы Cy1 и Cy2, описанные в приведенных выше вариантах осуществления, комбинируются с любой комбинацией R1, R1’, R2, R2’, R3, R3’ R4 и R4’, описанных выше для формулы (I) и в описанных ниже вариантах осуществления.
В одном варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, алкилсульфинила, галогеналкилсульфинила, галогентио-группы, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные два из R1 - R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой. В другом варианте осуществления, R1 и R3 независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 представляют собой C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В одном варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, алкилсульфинила, галогеналкилсульфинила, галогентио-группы, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные два из R1 - R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C8 алкил, необязательно независимо замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 представляет собой C1-C8 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) или 3-8-членное карбоциклическое или 3-8-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо(кольца) или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные два из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо(кольца) или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо(кольца) или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо(кольца) или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 представляет собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим или 3-6-членным гетероциклическим кольцом; где указанное 3- или 4-членное карбоциклическое или 3- или 4-членное гетероциклическое кольцо(кольца) или 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо(кольца) могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ образуют 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, R2 и R4 вместе с соответствующим R2’ и R4’ независимо образуют 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом; и
R1, R1’, R3 и R3’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, R1 и R3 вместе с соответствующим R1’ и R3’ независимо образуют 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом; и
R2, R2’, R4 и R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ образуют 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, все четыре из R1 - R4 вместе с соответствующим R1’ - R4’ образуют 2-6-членную углеродную цепочку с формированием цикла, который необязательно замещен одним или больше галогеном, C1-C3 алкилом или C1-C3 галогеналкилом.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо может дополнительно быть замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой циклопропил, циклобутил, циклопентил, циклогексил или фенил или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо(кольца) или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные два из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой циклопропил, циклобутил, циклопентил, циклогексил или фенил или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо(кольца) или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой циклопропил, циклобутил, циклопентил, циклогексил или фенил или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо(кольца) или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой циклопропил, циклобутил, или фенил; и R1 и R3 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой циклопропил, циклобутил или фенил; и R2 и R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой циклопропил, циклобутил, циклопентил, циклогексил или фенил или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное, циклобутильное, циклопентильное, циклогексильное или фенильное кольцо(кольца) или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 представляет собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой циклопропил, циклобутил, циклопентил, циклогексил или фенил или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-5-членным карбоциклическим или 3-5-членным гетероциклическим кольцом, где указанное циклопропильное кольцо(кольца) или 3-5-членное карбоциклическое или 3-5-членное гетероциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2-4-членную углеродную цепочку, формируя циклопропильное, циклобутильное или циклопентильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ образуют 2-4-членную углеродную цепочку, формируя циклопропильное, циклобутильное или циклопентильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ образуют 2-4-членную углеродную цепочку, формируя циклопропильное, циклобутильное или циклопентильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные R1 - R4 и соответствующие R1’ - R4’ независимо представляют собой атом водорода или C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные два из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; в то время как остальные из R1 - R4 представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или больше атомами галогена, который дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-H2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода или C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, все четыре из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, каждое из которых необязательно замещено одним или больше атомом фтора, метилом или трифторметилом.
В другом варианте осуществления, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или больше атомами галогена, который дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R2 и R4 представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, R1 и R3 представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой C1-C4 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанными карбоциклическими или гетероциклическими группами), где указанная карбоциклическая или гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанной 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные два из R1 - R4 независимо представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанной 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанной 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен указанной 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанные 3-6-членные карбоциклические или 3-6-членные гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные два из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанные 3-6-членные карбоциклические или 3-6-членные гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанные 3-6-членные карбоциклические или 3-6-членные гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой, где указанные 3-6-членные карбоциклические или 3-6-членные гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно заменен указанной карбоциклической или гетероциклической группой), где указанная карбоциклическая или гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно заменен указанной карбоциклической или гетероциклической группой), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно заменен указанной карбоциклической или гетероциклической группой), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно заменен указанной карбоциклической или гетероциклической группой), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно заменен указанной карбоциклической или гетероциклической группой), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, один из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, который независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, фенил, гетероарил, алкокси-группа, галогеналкокси-группа, алкилтио, галогеналкилтио, галогентио, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, все четыре из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из нафтила, инданила, бифенила, индолила, изоиндолила, бензотиазолила, бензоксазолила, бенз[d]изоксазолила, бензотриазолила, бензодиоксолила, бензотиенила, хинуклидинила, хиназолинила, хиноксалинила, хинолинила, изохинолинила, бензимидазолила, бензопиранила, индолизинила, бензофуранила, дигидробензофуранила, хромонила, кумаринила, циннолинила, индазолила, пирролопиридила, фталазинила, 1,2,3-бензотриазинила, 1,2,4-бензотриазинила, фуропиридинила (такого как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолила, дигидрохиназолинила (такого как 3,4-дигидро-4-оксо-хиназолинил), тетрагидрохинолинила и тетрагидроизохинолинила (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и соответствующие R1’ - R4’ независимо представляют собой атом водорода, 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой и диалкиламино-группой.
В другом варианте осуществления, один из R1 - R4 представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или больше атомами галогена, который дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, один из R1 - R4 независимо представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или больше атомами галогена, который дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может быть дополнительно замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, два из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут дополнительно быть независимо замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, в то время как остальные из R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, один из R1 - R4 независимо представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами фтора(-CHF- или -CF2-), который замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами фтора, который дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанная карбоциклическая или гетероциклическая группа может быть дополнительно замещена одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, два из R1 - R4 независимо представляет собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами фтора(-CHF- или -CF2), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами фтора, каждый из которых дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно независимо замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой, в то время как остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, R2 и R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами фтора(-CHF- или -CF2), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами фтора, каждый из которых дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно независимо замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой; и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, R1 и R3 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами фтора(-CHF- или -CF2), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами фтора, каждый из которых дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно независимо замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой; и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, три из R1 - R4 независимо представляют собой метилен (-CH2-) или метилен, замещенный одним или двумя атомами фтора(-CHF- или -CF2), которые независимо замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана (другими словами, метил или метил, замещенный одним или двумя атомами фтора, каждый из которых дополнительно замещен одной из указанных карбоциклических или гетероциклических групп), где указанные карбоциклические или гетероциклические группы могут быть дополнительно независимо замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой, в то время как остальные из R1 - R4 представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления настоящего изобретения, один из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, два из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, которое необязательно замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления настоящего изобретения, три из R1 - R4 вместе с соответствующим R1’ - R4’ независимо образуют 2- или 3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, каждое из которых необязательно независимо замещено одним или больше атомом фтора, метилом или трифторметилом; и
остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В одном варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R1 и R3 независимо выбраны из C1-C8 алкила, необязательно независимо замещенного одним или больше из следующих заместителей: галоген, гидрокси-группа, алкокси-группа, галогеналкокси-группа, алкилтио-группа, галогеналкилтио-группа, галогентио-группа, алкилсульфинил, галогеналкилсульфинил, алкилсульфонил, галогеналкилсульфонил, алкоксиалкокси-группа, оксо-группа, циано-группа, амино-группа, алкиламино-группа или диалкиламино-группа.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба, предпочтительно оба, из R1 и R3 независимо выбраны из C2-C6 алкила, необязательно независимо замещенного одним или больше галогенами, предпочтительно фтором, хлором или иодом, более предпочтительно фтором или хлором, и наиболее предпочтительно фтором.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R1 и R3 оба независимо выбраны из C3-C5 алкила, независимо замещенного одним или больше галогенами, предпочтительно фтором, хлором или иодом, более предпочтительно фтором или хлором, и наиболее предпочтительно фтором.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R1 и R3 оба независимо выбраны из C3-C5 алкила, независимо замещенного одним или больше атомами фтора, и предпочтительно где R1 и R3 оба независимо выбраны из -CH2-CF(CH3)2.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий описанную выше формулу (I), где R1 и R3 одинаковые.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба R1’ и R3’ представляют собой H или алкил, предпочтительно H.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R1’ и R3’ одинаковые, и предпочтительно оба представляют собой H.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R2 и R4 представляют собой 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо, или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-6-членное карбоциклическое или гетероциклическое кольцо или 3-8-членное карбоциклическое или гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, алкилсульфинила, галогеналкилсульфинила, галогентио-группы, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R2 и R4 представляют собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-8-членное карбоциклическое или гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, циклоалкила, гетероциклила, арила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, алкилсульфинила, галогеналкилсульфинила, галогентио-группы, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R2 и R4 представляют собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом; где указанное 3-8-членное карбоциклическое или гетероциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, алкилсульфинила, галогеналкилсульфинила, галогентио-группы, алкилсульфонила, галогеналкилсульфонила, оксо-группы, циано-группы.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R2 и R4 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным карбоциклическим кольцом; где указанное 3-8-членное карбоциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, алкокси-группы и галогеналкокси-группы.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба из R2 и R4 представляет собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным карбоциклическим кольцом; где указанное 3-6-членное карбоциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, алкокси-группы и галогеналкокси-группы.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый независимо представляют собой C1-C3 алкил или C1-C3 галогеналкил, каждый из которых замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана, где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой.
В другом варианте осуществления, описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый независимо представляют собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана, где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше галогеном, C1-C4 алкилом, C1-C4 галогеналкилом, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, фенилом или оксо-группой.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый независимо представляют собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен карбоциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила и фенила.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый независимо представляют собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен карбоциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила или циклопентила.
В другом варианте осуществления, описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый независимо представляют собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен циклопропилом.
В другом варианте осуществления, описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 каждый представляют собой метил, замещенный 3-5 членным карбоциклическим кольцом, предпочтительно циклопропилом, и предпочтительно где R2 и R4 каждый представляют собой -CH2-циклопропил.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R2 и R4 одинаковые.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где один или оба R1’ и R3’ представляют собой H или алкил, предпочтительно H.
В другом варианте осуществления, описан антигельминтный циклический депсипептид, имеющий формулу (I), где R1’ и R3’ одинаковые, и предпочтительно оба представляют собой H.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где R', R'', R''' и R'''' каждый независимо представляют собой C1-C3 алкил, предпочтительно метил.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где Cy1 и Cy2 каждый независимо выбраны из группы, состоящей из следующих: фенил, замещенный гетероциклилом, предпочтительно где гетероциклил выбран из группы, состоящей из следующих: пирролидинил, фурил, тетрагидрофурил, тиенил, пиперидинил, пиперазинил и морфолинил, и более предпочтительно где гетероциклил представляет собой морфолинил.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где Cy1 и Cy2 одинаковые и каждый представляют собой фенил, замещенный морфолинилом, предпочтительно N-морфолинилом, и более предпочтительно пара-N-морфолинилфенил:
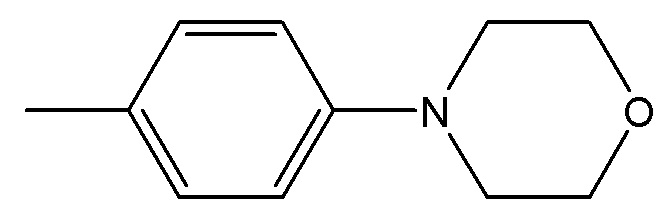 .
.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где Cy1 и Cy2 одинаковые и каждый представляют собой фенил, замещенный тетрагидропиранилом, предпочтительно пара-тетрагидропиранилом, и более предпочтительно пара-тетрагидропиранилфенил:
 .
.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где Ra и Rb независимо представляют собой C1-C3 алкил или C1-C3 галогеналкил, предпочтительно C1-C3 алкил, и более предпочтительно метил.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где:
R1 и R3 оба независимо выбраны из C3-C5 алкила, независимо замещенного одним или больше атомами фтора, и предпочтительно где R1 и R3 оба независимо выбраны из -CH2-CF(CH3)2;
R2 и R4 каждый представляют собой метил, замещенный 3-5 членным карбоциклическим кольцом, предпочтительно циклопропилом, и предпочтительно где R2 и R4 каждый представляют собой -CH2-циклопропил;
R1’, R2’, R3’ и R4’ представляют собой H;
R', R'', R''' и R'''' каждый независимо представляют собой C1-C3 алкил;
Cy1 и Cy2 каждый независимо выбраны из группы, состоящей из следующих: фенил, замещенный гетероциклилом, предпочтительно где гетероциклил выбран из группы, состоящей из следующих: пирролидинил, фурил, тетрагидрофурил, тетрагидропиранил, тиенил, пиперидинил, пиперазинил и морфолинил; и
Ra и Rb независимо представляют собой C1-C3 алкил.
В другом варианте осуществления, в настоящем изобретении описан антигельминтный циклический депсипептид, имеющий формулу (I), где:
R1 и R3 оба независимо выбраны из C3-C5 алкила, независимо замещенного одним или больше атомами фтора, и предпочтительно где R1 и R3 оба независимо выбраны из -CH2-CF(CH3)2;
R2 и R4 каждый представляют собой метил, замещенный 3-5 членным карбоциклическим кольцом, предпочтительно циклопропилом, и предпочтительно где R2 и R4 каждый представляют собой -CH2-циклопропил;
R1’, R2’, R3’ и R4’ представляют собой H;
R', R'', R''' и R'''' каждый независимо представляют собой C1-C3 алкил;
Cy1 и Cy2 каждый независимо выбраны из группы, состоящей из следующих: фенил, замещенный гетероциклилом, предпочтительно где гетероциклил выбран из группы, состоящей из следующих: пирролидинил, фурил, тетрагидрофурил, тиенил, пиперидинил, пиперазинил и морфолинил; и
Ra и Rb независимо представляют собой C1-C3 алкил.
В другом варианте осуществления настоящего изобретения, один, два или три из R1 - R4 представляют собой циклопропил, циклобутил, фенил или оксетан, или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые независимо замещены 3-6-членной карбоциклической или 3-6-членной гетероциклической группой (другими словами, метил или метил, замещенный одним или двумя атомами галогена, каждый из которых независимо дополнительно замещен 3-6-членной карбоциклической или 3-6-членной гетероциклической группой), где указанная 3-6-членная карбоциклическая или 3-6-членная гетероциклическая группа может дополнительно быть независимо замещена одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, и остальные из R1 - R4 представляют собой группу G-1:
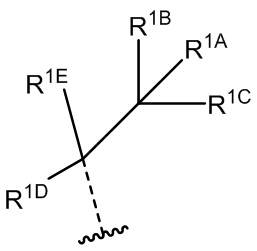
G-1;
где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, галоген, алкил или галогеналкил.
В одном варианте осуществления, один, два или три из R1 - R4 независимо представляют собой циклопропил или фенил, или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксирана, оксетана, тиирана, тиетана, азиридина, азетидина, пирролидина, пиррола, тиофена, оксазола, изоксазола, изоксазолина, тиазола, изотиазола, 1,3,4-тиадиазола, пиразола, имидазола, триазола, тетразола, фурана, тетрагидрофурана и дигидрофурана, где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, и остальные из R1 - R4 независимо представляют собой G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, галоген, C1-C3-алкил или C1-C3-галогеналкил.
В другом варианте осуществления, один, два или три из R1 - R4 независимо представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила, оксетана, пиррола, тетрагидрофурана и дигидрофурана, где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, и остальные из R1 - R4 независимо представляют собой G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, атом фтора, C1-C3-алкил или C1-C3-галогеналкил.
В другом варианте осуществления, один, два или три из R1 - R4 представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены карбоциклической или гетероциклической группой, выбранной из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила, фенила и оксетана, где указанные карбоциклические или гетероциклические группы могут быть дополнительно замещены одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкила, галогеналкила, C3-C6 циклоалкила, гетероциклила, фенила, гетероарила, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы, и остальные из R1 - R4 независимо представляют собой G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, атом фтора, C1-C3-алкил или C1-C3-галогеналкил.
В другом варианте осуществления, один, два или три из R1 - R4 представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены циклопропилом, необязательно замещенным галогеном, и остальные из R1 - R4 независимо представляют собой G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, атом фтора, метил или трифторметил.
В одном варианте осуществления, один, два или три из R1 - R4 представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены циклопропилом, необязательно замещенным галогеном, и остальные из R1 - R4 независимо представляют собой G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, атом фтора, C1-C3 алкил или C1-C3 галогеналкил.
В другом варианте осуществления, один, два или три из R1 - R4 представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены циклопропилом, необязательно замещенным галогеном, и остальные из R1 - R4 независимо представляют собой G-1, где R1D и R1E независимо представляют собой H или галоген. В другом варианте осуществления, R1D и R1E независимо представляют собой C1-C3 алкил или C1-C3 галогеналкил. В другом варианте осуществления, R1A представляет собой H или галоген. В другом варианте осуществления, R1A представляет собой C1-C3 алкил или C1-C3 галогеналкил. В другом варианте осуществления, R1A представляет собой галоген, и R1B и R1C независимо представляют собой C1-C3 алкил или C1-C3 галогеналкил. В другом варианте осуществления, R1D и R1E представляют собой H, R1A представляет собой галоген, и R1B и R1C независимо представляют собой C1-C3 алкил или C1-C3 галогеналкил.
В другом варианте осуществления, один, два или три из R1 - R4 представляют собой циклопропил или метилен (-CH2-) или метилен, замещенный одним или двумя атомами галогена (-CHX- или -CX2-, где X это галоген), которые замещены циклопропилом, необязательно замещенным галогеном, и остальные из R1 - R4 независимо представляют собой G-1, где R1D и R1E независимо представляют собой H или F. В другом варианте осуществления, R1D и R1E независимо представляют собой метил или трифторметил. В другом варианте осуществления, R1A представляет собой H или F. В другом варианте осуществления, R1A представляет собой метил или трифторметил. В другом варианте осуществления, R1A представляет собой F, и R1B и R1C представляют собой метил или трифторметил. В другом варианте осуществления, R1D и R1E представляют собой H, R1A представляет собой F, R1B и R1C представляют собой метил или трифторметил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C28, изображенные ниже:
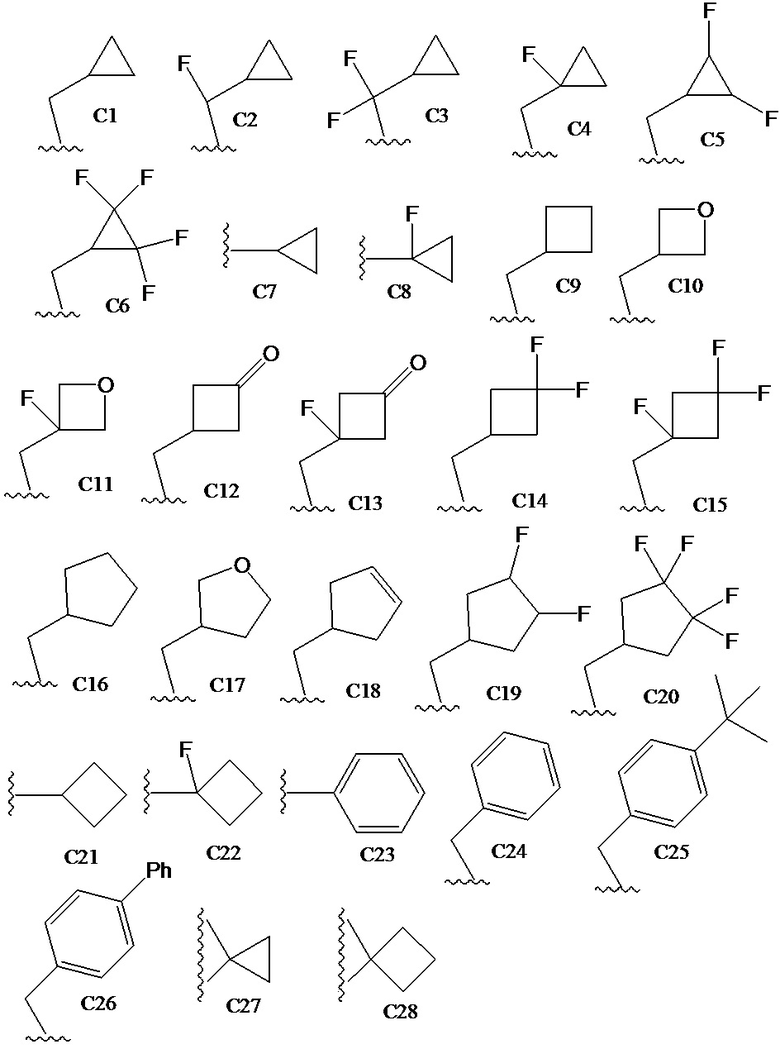
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C8. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C9 - C15. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C16 - C20. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C21 - C26. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 вместе с соответствующим R1’ - R4’ представляют собой C27 или C28. В другом варианте осуществления, один, два, три или все четыре из R1 - R4, независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой C1-C6 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой C1-C3 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 вместе с соответствующим R1’ - R4’ представляют собой C27 или C28, и остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода или C1-C3 алкил, необязательно замещенный одним или больше галогеном, гидрокси-группой, алкокси-группой, галогеналкокси-группой, алкилтио-группой, галогеналкилтио-группой, галогентио-группой, алкилсульфинилом, галогеналкилсульфинилом, алкилсульфонилом, галогеналкилсульфонилом, алкоксиалкокси-группой, оксо-группой, циано-группой, амино-группой, алкиламино-группой или диалкиламино-группой. В другом варианте осуществления, один, два, три или все четыре из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой C27 или C28, и остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода, 2-метилпропил или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой C27 или C28, и остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода или 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше заместителями, выбранными из группы, состоящей из галогена, гидрокси-группы, алкокси-группы, галогеналкокси-группы, алкилтио-группы, галогеналкилтио-группы, галогентио-группы, алкилсульфинила, галогеналкилсульфинила, алкилсульфонила, галогеналкилсульфонила, алкоксиалкокси-группы, оксо-группы, циано-группы, амино-группы, алкиламино-группы и диалкиламино-группы.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой C27 или C28, и остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода или 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой C27 или C28, и остальные из R1 - R4 и соответствующий R1’ - R4’ независимо представляют собой атом водорода или 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 - C26, и остальные из R1 - R4 независимо представляют собой группу G-1, где R1A, R1B, R1C, R1D и R1E независимо представляют собой атом водорода, галоген, алкил или галогеналкил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C1 или C2, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C3, C4 или C5, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C6, C7 или C8, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C9, C10 или C11, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C12, C13, C14 или C15, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, один, два, три или все четыре из R1 - R4 независимо представляют собой C16 - C20, и остальные из R1 - R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил. В другом варианте осуществления, R1 и R3 независимо представляют собой C1 - C26, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C1 или C2, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C3, C4, C5 или C6, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C7 или C8, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C9, C10 или C11, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C12, C13, C14 или C15, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C16, C17, C18, C19 или C20, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 и R3 независимо представляют собой C21, C22, C23, C24, C25 или C26, и R2 и R4 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R1 вместе с R1’ и/или R3 вместе с R3’ образуют 2-3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, и R2, R2’, R4 и R4’ независимо представляют собой атом водорода, 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C1 - C26, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C1 или C2, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C3, C4, C5 или C6, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C7 или C8, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C9, C10 или C11, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C12, C13, C14 или C15, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C16, C17, C18, C19 или C20, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 и R4 независимо представляют собой C21, C22, C23, C24, C25 или C26, и R1 и R3 независимо представляют собой 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В другом варианте осуществления, R2 вместе с R2’ и/или R4 вместе с R4’ образуют 2-3-членную углеродную цепочку, формируя циклопропильное или циклобутильное кольцо, и R1, R1’, R3 и R3’ независимо представляют собой атом водорода, 2-метилпропил, замещенный одним или двумя атомами фтора, или 2,2-диметилпропил.
В одном варианте осуществления, в настоящем изобретении описаны соединения, имеющие формулу (I), где R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или C1-C3 алкил; и Cy1, Cy2, Ra, Rb, R1, R2, R3 и R4 имеют значения, указанные ниже в Таблицах 2 - 38. В соединениях, представленных в Таблицах 2 - 38, переменные R1’, R2’, R3’ и R4’ представляют собой атом водорода, за исключением случаев, когда они образуют углеродную цепочку с соответствующими R1 - R4 с образованием кольца (например, когда формируют C27 или C28).
Соединения в Таблицах 2 - 38 где все из Ra, Rb, R', R'', R''' и R'''' представляют собой метил обозначены номером X-YA, где X это номер таблицы, и Y это последовательный номер в таблице. Соединения в Таблицах 2 - 38, где Ra, Rb каждый представляют собой атом водорода, и R', R'', R''' и R'''' представляют собой метил, обозначены номером X-YB. Соединения в Таблицах 2 - 38, где Ra, Rb каждый представляют собой метил, и R', R'', R''' и R'''' представляют собой атом водорода, обозначены номером X-YC; и Соединения в Таблицах 2 - 38, где Ra, Rb каждый представляют собой атом водорода, и R', R'', R''' и R'''' представляют собой метил, обозначены номером X-YD.
Таблица 2: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой незамещенный фенил, R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил, и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 3: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-фторфенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 4: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-трифторметилфенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 5: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-трифторметоксифенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 6: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 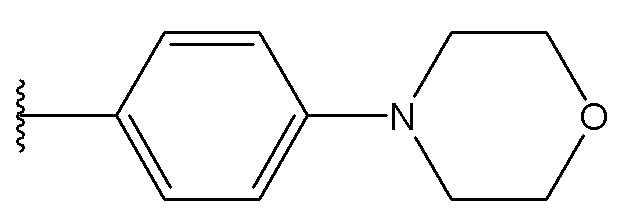 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 7: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
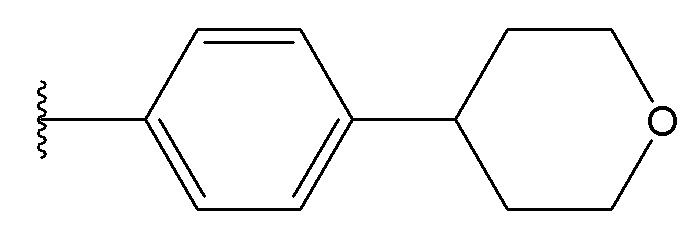 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 8: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
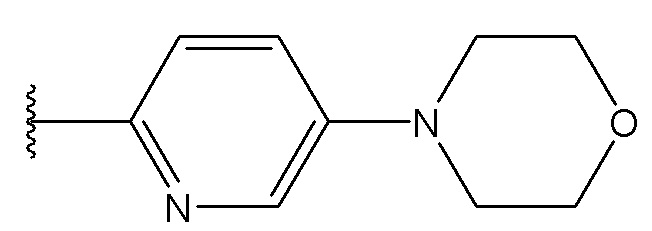 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 9: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
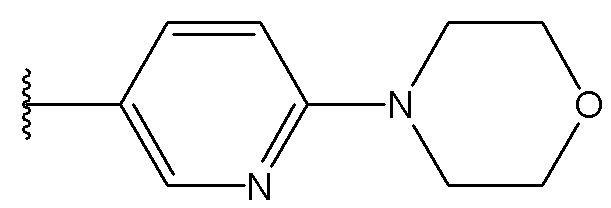 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 10: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
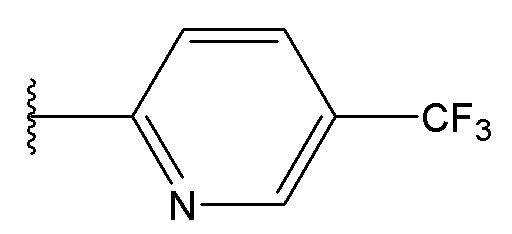 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 11: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
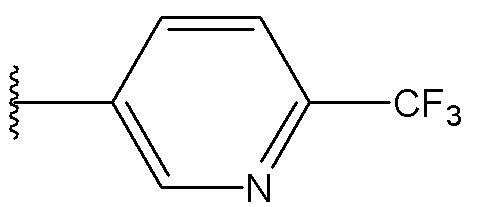 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 12: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
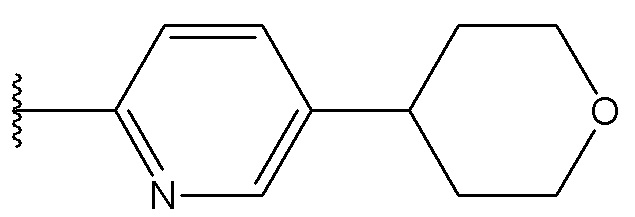 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 13: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
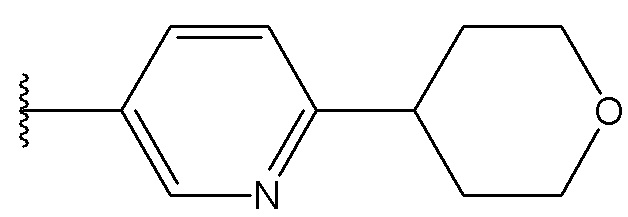 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 14: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
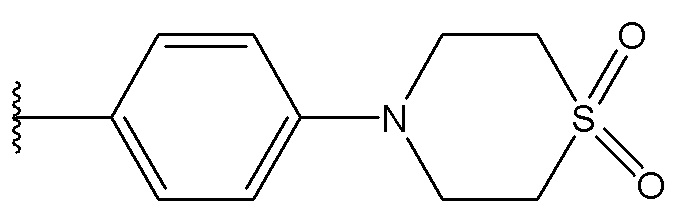 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 15: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
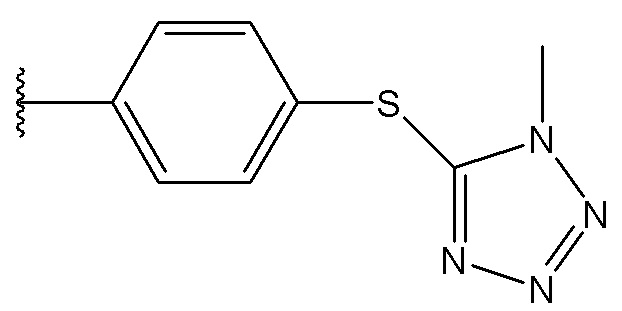 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 16: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
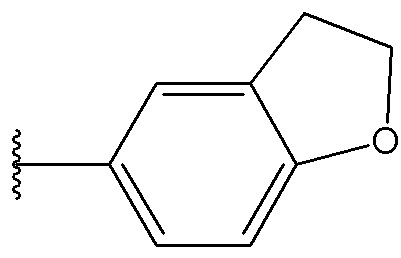 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 17: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
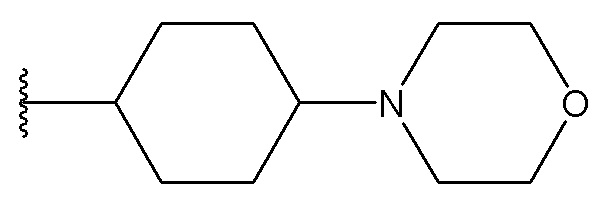 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 18: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
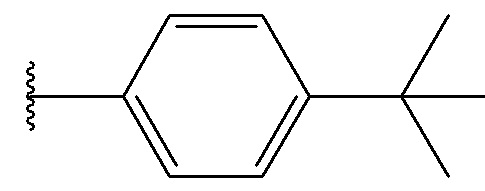 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 19: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
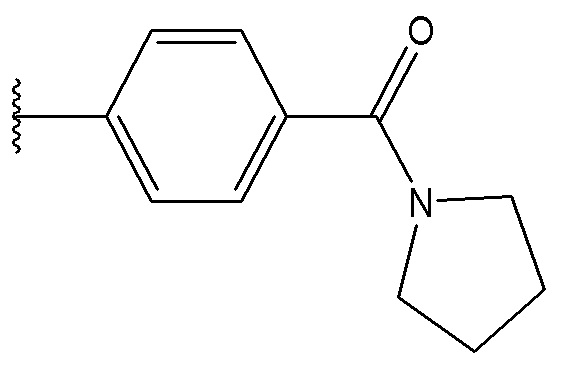 ; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 20: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 3,4,5-трифторфенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 21: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-аминофенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 22: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-иодфенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 23: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-бромфенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 24: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-цианофенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 25: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
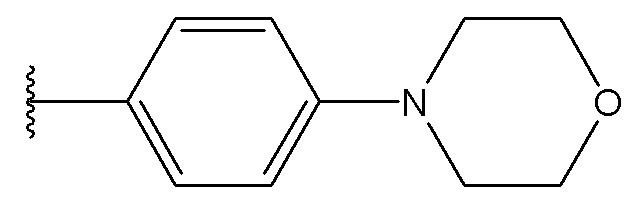 и незамещенный фенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
и незамещенный фенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 26: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
 и п-иодфенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
и п-иодфенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 27: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой
 и незамещенный фенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
и незамещенный фенил, соответственно; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 28: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой п-нитрофенил; R', R'', R''' и R'''' каждый независимо представляют собой атом водорода или метил; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 29: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 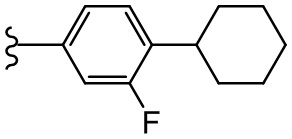 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 30: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 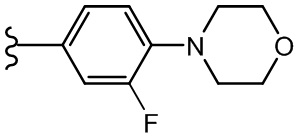 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 31: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 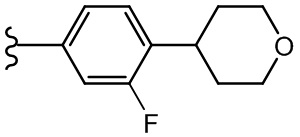 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 32: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 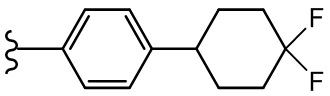 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 33: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 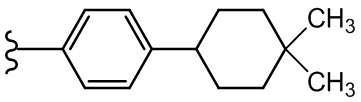 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 34: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 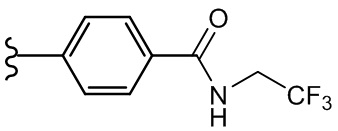 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 35: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 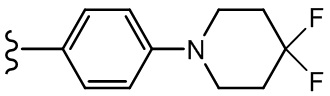 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 36: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 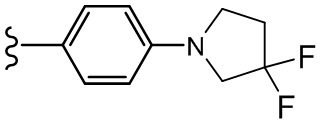 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 37: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 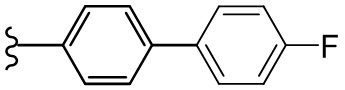 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Таблица 38: Соединения, имеющие формулу (I), в которых Cy1 и Cy2 представляют собой 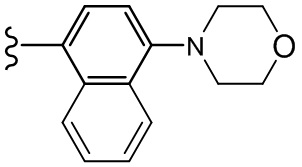 ; и Ra, Rb и R1 - R4 имеют указанные значения.
; и Ra, Rb и R1 - R4 имеют указанные значения.
Частные варианты соединений по настоящему изобретению дополнительно описаны в Таблицах 39-1037, где значения переменных Cy1, Cy2, Ra, Rb и R1 - R4 имеют значения, указанные в Таблицах 2-38, за исключением того, что группа C1 в Таблицах 2-38 заменена на группы C2 - C28.
Неожиданно было обнаружено, что замещение описанными в настоящем тексте определенными группами алкильных групп R1, R2, R3 и R4, которые представляют собой 2-метилпропильные группы в материнском циклическом депсипептиде PF1022A, а также в эмодепсиде, улучшает метаболическую устойчивость соединений, а также повышает активность данных соединений против эндопаразитов и, в некоторых случаях, эктопаразитов. В некоторых случаях, соединения по настоящему изобретению могут демонстрировать более низкую токсичность для млекопитающих. Кроме того, неожиданно было обнаружено, что замещение в соединениях, имеющих формулу (I), описанными в настоящем тексте определенными группами Cy1 и/или Cy2 также значительно улучшает метаболическую устойчивость соединений по настоящему изобретению, по сравнению с PF1022A и эмодепсидом. Таким образом, было обнаружено, что соединения по настоящему изобретению, в которых группы Cy1 и/или Cy2 и по меньшей мере один из R1, R2, R3 и R4 замещены описанными в настоящем тексте определенными заместителями, обладают значительно улучшенной метаболической устойчивостью и равной или значительно более высокой эффективностью против эндопаразитов, включая (но не ограничиваясь только ими) Dirofilaria immitis микрофилярии и/или L3 и L4 личинки и/или личинки Haemonchus contortus. Соединения по настоящему изобретению активны также против анкилостом, власоглавов и круглых червей пищеварительного тракта животных. В частных вариантах осуществления, соединения, имеющие формулу (I), с определенными заместителями также демонстрируют улучшенную активность против эктопаразитов.
В некоторых вариантах осуществления, некоторые соединения по настоящему изобретению, в которой по меньшей мере один из R1 - R4 представляет собой необязательно замещенное 3-6-членное карбоциклическое или 3-6-членное гетероциклическое кольцо или C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен необязательно замещенным 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом, могут демонстрировать улучшенные профили токсичности по сравнению с соединениями, содержащими ациклические алкильные группы в этих положениях. В других вариантах осуществления настоящего изобретения, где один или больше из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2-6-членную углеродную цепочку с формированием цикла такие циклические депсипептиды могут демонстрировать улучшенные профили токсичности по сравнению с соединениями, содержащими ациклические алкильные группы в этих положениях.
Также неожиданно было обнаружено, что пространственный порядок замещения R1 - R4 также оказывает значительное влияние на активность соединений. Например, было обнаружено, что когда модифицируются встречающиеся в природе 2-метилпропильные группы в положениях, идентифицированных как R1 и R3 в соединении, имеющем формулу (I), то активность таких соединений значительно увеличивается по сравнению с соединениями, где заместителями в положениях R2 и R4 являются 2-метилпропильные группы.
Влияние определенных заместителей в природной 2-метилпропильной группе в N-метил лейциновых остатках PF1022A, соответствующих одному или больше из R1, R2, R3 и R4 в формуле (I), также является неожиданным. Так, было обнаружено, что замещение одного или больше 2-метилпропилов в R1, R2, R3 и R4 на фтор значительно повышает активность соединений, имеющих формулу (I), на подвижность личинок Haemonchus contortus и микрофилярий Dirofilaria immitis in vitro по сравнению с незамещенными соединениями (например, PF1022A или аналоги, где Cy1 и/или Cy2 представляют собой замещенный фенил, но R1 - R4 представляют собой 2-метилпропил) или соединениями, в которых природные 2-метилпропильные группы замещены метильной группой. Кроме того, было обнаружено, что замещение 2-метилпропильных групп в группах R1 и R3 атомом фтора приводит к значительному повышению активности против микрофилярий H. contortus и D. immitis по сравнению с соединениями, замещенными атомом фтора в R2 и R4, или с другими комбинациями. Кроме того, в некоторых вариантах осуществления включение в переменные R1 - R4 по меньшей мере одного необязательно замещенного 3-6-членного карбоциклического или 3-6-членного гетероциклического кольца, или C1-C3 алкила или C1-C3 галогеналкила, где C1-C3 алкил или C1-C3 галогеналкил замещен необязательно замещенным 3-8-членным карбоциклическим или 3-8-членным гетероциклическим кольцом, или где один или больше из R1 - R4 вместе с соответствующим R1’ - R4’ образует 2-6-членную углеродную цепочку с формированием цикла, может улучшить профиль безопасности и/или метаболическую устойчивость соединений, тем самым расширяя терапевтическое окно. Несомненно, что тип замещения в группах R1, R2, R3 и R4, а также то, в каком из R1, R2, R3 и R4 происходит замещение, оказывает значительное влияние на активность, устойчивость и безопасность рассматриваемых соединений.
Scherkenbeck с соавторами (Bioorg. Med. Chem. Lett. 8 (1998), 1035-1040) описал, что замена N-метил лейциновых заместителей на серию родственных N-метилированных аминокислот, таких как изолейцин, валин, норвалин, аланин и фенилаланин, приводила к почти полной потере противогельминтной эффективности при пероральном введении овцам. роме того, в данной публикации сообщалось, что модификация половины N-метил лейциновых остатков метильными или н-пропильными боковыми цепочками также неожиданно приводила к значительно пониженной активности. Был сделан вывод, что (L)-N-метил лейциновые остатки в циклическом депсипептиде PF1022A являлись критически важной частью фармакофора и необходимыми для in vivo активности.
Таким образом, является неожиданным тот факт, что модификация групп R1 - R4 в соединении, имеющем формулу (I), которые соответствуют N-метил лейциновым остаткам в PF1022A или эмодепсиде, приводит к повышению метаболической устойчивости и/или пониженной токсичности и/или повышенной активности по сравнению с соединениями, содержащими немодифицированные N-метил лейциновые остатки. Также очень неожиданным является тот факт, что соединения, имеющие формулу (I), в которых алкильные группы, представленные R1 и R3, замещены определенными группами, описанными в настоящем изобретении, демонстрируют значительно более высокую эффективность против эндопаразитов, по сравнению с соединениями, которые замещены теми же группами в положениях R2 и R4, или в других комбинациях. Кроме того, включение определенных заместителей, описанных в настоящем изобретении, в группы R1 - R4 и Cy1 и Cy2 приводит к повышению метаболической устойчивости и пониженной токсичности, в сравнении с незамещенными соединениями. Из этого следует, что определенная комбинация заместителей в Cy1 и Cy2 и R1 - R4 в соединениях, имеющих формулу (I), приводит к значительному повышению активности против эндопаразитов и улучшенной метаболической устойчивости.
Кроме того, было обнаружено, что замещение встречающихся в природе 2-метилпропильных групп некоторыми заместителями, включая фтор и метил, улучшает in vitro проницаемость и биодоступность данных соединений (см. Метод С в Примерах). Например, было обнаружено, что соединения, имеющие формулу (I), где Cy1 и Cy2 оба представляют собой незамещенные фенильные или п-фторфенильные группы, и R2 и R4, соответственно, представляют собой фтор, имеют значительно улучшенную проницаемость, по сравнению с соединениями, где R2 и R4 представляют собой незамещенный 2-метилпропил. Кроме того, было обнаружено, что соединения, в которых Cy1 и Cy2 представляют собой п-морфолино-фенил, и R2 и R4 представляют собой метил, имеют значительно улучшенную проницаемость, по сравнению с эмодепсидом (R2 и R4 = H).
Ожидается, что характеристики, описанные выше для соединений, имеющих формулу (I), приводят в итоге к соединениям с более высокой антипаразитической эффективностью против эндопаразитов и эктопаразитов в организме животных или на их покровах.
Стереоизомеры и полиморфные формы
Специалистам в данной области понятно, что соединения по настоящему изобретению могут существовать и быть выделенными в виде оптически активных и рацемических форм Соединения, имеющие один или более хиральных центров, включая таковой на атоме серы, могут присутствовать в виде единственных энантиомеров или диастереомеров или в виде смесей энантиомеров и/или диастереомеров. Например, хорошо известно, что сульфоксидные соединения могут быть оптически активными и могут существовать в виде отдельных энантиомеров или рацемических смесей. Кроме того, соединения по настоящему изобретению могут включать один или больше хиральных центров, которые приводят к существованию теоретического числа оптически активных изомеров. Там, где соединения по настоящему изобретению включают n хиральных центров, соединения могут иметь до 2n оптических изомеров. Настоящее изобретение охватывает частные энантиомеры или диастереомеры каждого соединения, а также смеси различных энантиомеров и/или диастереомеров соединений по настоящему изобретению, которые обладают полезными свойствами, описанными в настоящем документе. Оптически активные формы могут быть получены, например, путем разделения рацемических форм методами селективной кристаллизации, синтеза из оптически активных предшественников, хирального синтеза, хроматографического разделения с использованием хиральной неподвижной фазы или с помощью ферментативного разделения.
Соединения по настоящему изобретению также могут присутствовать в различных твердых формах, таких как различные кристаллические формы, или в форме аморфного твердого вещества. Настоящее изобретение охватывает различные кристаллические формы, а также аморфные формы соединений по настоящему изобретению.
Кроме того, соединения по настоящему изобретению могут существовать в виде гидратов или сольватов, в которых определенные стехиометрические количества воды или растворителя ассоциированы с молекулой в кристаллической форме. Гидраты и сольваты соединений, имеющих формулу (I), также являются объектом изобретения.
Соли
Помимо нейтральных соединений формулы (I), соли данных соединений также обладают активностью против паразитов. Термин "ветеринарно приемлемая соль" и "фармацевтически приемлемая соль" используются в настоящем документе для описания любых солей соединений, которые приемлемы для введения в ветеринарии, и которые при введении обеспечивают доставку активного соединения.
В случаях, когда соединения являются в достаточной степени основными или кислыми для образования устойчивых нетоксичных солей с кислотами или основаниями, соединения могут находиться в форме ветеринарно приемлемой соли, фармацевтически приемлемой соли или соли, приемлемой для сельского хозяйства. Приемлемые для ветеринарии соли включают соли, полученные из приемлемых для ветеринарии или для сельского хозяйства неорганических или органических оснований и кислот. Подходящие соли включают включают соли щелочных металлов, таких как литий, натрий или калий, щелочноземельных металлов, таких как кальций, магний и барий. Также могут применяться соли переходных металлов, включая (но не ограничиваясь только ими) магний, медь, цинк и железо. Кроме того, соли, содержащие катионы аммония (NH4+), а также замещенные катионы аммония, в которых один или более атомов водорода замещены на алкильные или арильные группы, также входят в объем настоящего изобретения.
Особенно хорошо подходят соли, полученные из неорганических кислот, включая (но не ограничиваясь только ими) гидрогалогенидные кислоты (HCl, HBr, HF, HI), серную кислоту, азотную кислоту, фосфорную кислоту, и т.п. Подходящие неорганические соли также включают (но не ограничиваются только ими) бикарбонатные и карбонатные соли. В некоторых вариантах осуществления, примеры приемлемых для ветеринарии и для сельского хозяйства солей представляют собой соли с органическими кислотами, образуемые с органическими кислотами, включая (но не ограничиваясь только ими) малеат, дималеат, фумарат, тозилат, метансульфонат, ацетат, цитрат, малонат, тартрат, сукцинат, бензоат, аскорбат, 〈-кетоглютарат и 〈-глицерофосфат. Разумеется, можно применять другие приемлемые органические кислоты.
Соли описанных соединений со щелочными металлами (например, натрий, калий или литий) или с щелочноземельными металлами (например, кальций) также можно получать введением в реакцию достаточно кислого остатка соединений с гидроксидом щелочного или щелочно-земельного металла.
Приемлемые для ветеринарии соли можно получать по обычным методикам, хорошо известным в данной области техники, например, введением в реакцию достаточно основного соединения, такого как амин, с подходящей достаточно кислой функциональной группой, содержащейся в соединении, или введением подходящей кислоты в реакцию с достаточно основной функциональной группой соединения по настоящему изобретению.
Способы получения соединений, имеющих формулу (I):
Соединения, имеющие формулу (I) можно получить способами, являющимися адаптацией способов, описанных в Патентах США 5,514,773; 5,747,448; 5,874,530; 5,856,436; 6,033,879; 5,763,221; 6,329,338, 5,116,815; 6,468,966; 6,369,028; 5,777,075; и 5,646,244, которые все полностью включены в настоящий текст посредством ссылки. Кроме того, в химической литературе описаны различные способы синтеза циклических депсипептидов (см. Luttenberg et al., Tetrahedron 68 (2012), 2068-2073; Byung H. Lee, Tetrahedron Letters, 1997, 38 (5), 757-760; Scherkenbeck et al., Letters in Organic Chemistry, 2016, 13, 441-445; Eur. J. Org. Chem., 2012, 1546-1553; Biosci. Biotech. Biochem., 1994, 58(6), 1193-1194; и Scherkenbeck et al., Tetrahedron, 1995, 51(31), 8459-8470). Квалифицированному специалисту в данной области будет понятно, что определенные функциональные группы в соединениях и интермедиатах могут быть незащищенными или защищенными подходящими защитными группами, как описано в книге Greene et al., Protective Groups in Organic Synthesis, John Wiley и Sons, Inc., 4th edition 2006. Кроме того, квалифицированному специалисту в данной области будет понятно, что соединения и интермедиаты можно выделять в стандартных условиях водной обработки реакционных смесей и, опционально, очищать. Например, соединения или интермедиаты можно очистить хроматографическими методами или перекристаллизовать, получая целевой продукт приемлемой чистоты.
В одном варианте осуществления, соединения, имеющие формулу (I), где R1, R1’, R2, R2’, R3, R3’, R4, R4’, Ra, Rb, Cy1 и Cy2 имеют указанные выше значения, R', R'', R''' и R'''' представляют собой метил, получают общим способом, изображенным ниже на Схеме 1:
Схема 1
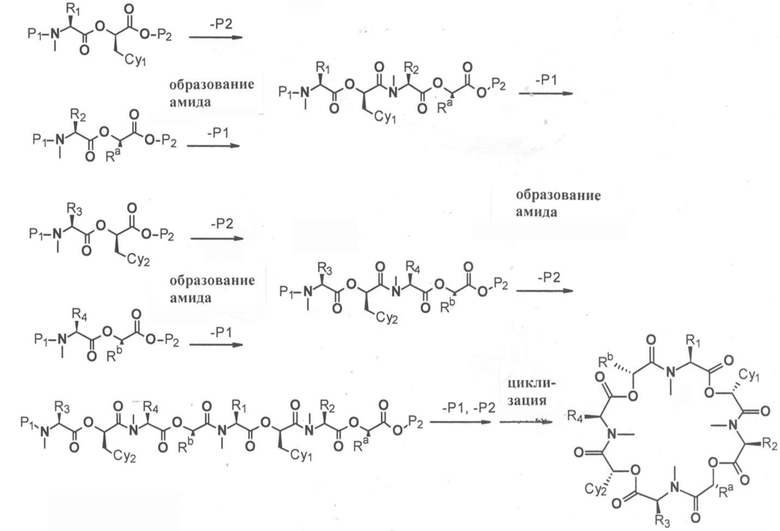
На Схеме 1, P1 и P2 представляют собой, соответственно, защитные группы для аминной и карбоксильной групп, общеизвестные в данной области (см., например, Greene et al. Protective Groups in Organic Synthesis, John Wiley и Sons, Inc., 4th edition 2006), и R1, R2, R3, R4, Ra, Rb, Cy1 и Cy2 имеют указанные выше значения.
Кроме того, сочетание аминов с карбоновыми кислотами с образованием амидов хорошо известно в данной области, и можно применять стандартные реагенты в данном сочетании фрагмента с незащищенным амином и второго фрагмента, содержащего свободную карбоксильную группу (см., например, Peptide Synthesis by Miklos Bodanszky и Miguel Ondetti, Interscience Publishers, 1966; Амино Acid и Peptide Synthesis, 2nd Ed. By John Jones, Oxford University Press, 2002). Соединения можно получить синтезом в растворе или с применением твердофазного синтеза на полимерной подложке. Например, формирование амидных связей можно осуществлять с применением активирующих реагентов, таких как карбодиимидные реагенты (например, дициклогексилдиимид, диизопропилдиимид и (N-(3-диметиламинопропил)-N’-этилкарбодиимид HCl), в комбинации с такими добавками, как N-гидроксибензотриазол (HOBt) и т.п. Кроме того, формирование амидных связей в данном синтезе можно осуществлять с применением фосфониевых реагентов, таких как BOP (Бензотриазол-1-илокси-трис(диметиламино)-фосфония гексафторфосфат), PyBOP (Бензотриазол-1-илокси-трипирролидинo-фосфония гексафторфосфат), PyBrOP (Бром-трипирролидинo-фосфония гекса-фторфосфат) и т.п. Другими подходящими реагентами для образования амидных связей в соединениях по настоящему изобретению являются так называемые аминий/уроний-имониевые реагенты, такие как TBTU/HBTU (2-(1H-Бензотриазол-1-ил)-N,N,N’,N’- тетраметиламиния тетрафторборат/гексафторфосфат), HATU (2-(7-аза-1H-бензотриазол-1-ил)-N,N,N’,N’-тетраметиламиния гексафторфосфат) и т.п. Эти реагенты и способы применения этих реагентов для получения амидных связей хорошо известны в данной области.
Ветеринарные композиции:
Соединения, имеющие формулу (I), и композиции, содержащие указанные соединения, можно применять для предотвращения и лечения паразитных заражений/инфекций у животных. Композиции по настоящему изобретению содержат эффективное количество по меньшей мере одного циклического депсипептидного соединения, имеющего формулу (I), или его ветеринарно приемлемой соли, в комбинации с ветеринарно приемлемым носителем или разбавителем и, необязательно, другими неактивными вспомогательными соединениями. Композиции могут иметь вид различных твердых или жидких готовых форм, которые подходят для различных способов применения или введения животным. Например, ветеринарные композиции, содержащие инновационные соединения, могут иметь вид препаратов, подходящих для перорального введения, введения в виде инъекций, включая подкожное и парентеральное введение, и наружное применение (например, точечное нанесение или препарат для обливания), кожное или подкожное введение. Готовые формы предназначены для введения животному, включая (но не ограничиваясь только ими) млекопитающих, птиц и рыб. Примеры млекопитающих включают (но не ограничиваются только ими) человека, крупный рогатый скот, овец, коз, лам, альпаков, свиней, лошадей, ослов, собак, кошек и других сельскохозяйственных или домашних млекопитающих. Примеры птиц включают индеек, цыплят, страусов и других сельскохозяйственных или домашних птиц. В особенности полезно применение соединений, имеющих формулу (I), для защиты животных-компаньонов, таких как собаки и кошки, от эндопаразитов.
Композиции по настоящему изобретению могут иметь подходящую для перорального применения форму (см., например, Патент США № 4,564,631, включенный в настоящий документ посредством ссылки), пищевых добавок, пастилок, ромбовидных пастилок, жевательных таблеток, таблеток, твердых или мягких капсул, болюсов, эмульсий, водных или масляных суспензий, водных или масляных растворов, препаратов для вливания в ротовую полость, диспергируемых порошков или гранул, готовых смесей, сиропов или эликсиров, кишечнорастворимых препаратов или паст. Предназначенные для перорального применения композиции можно получать согласно любому известному в данной области техники способу получения фармацевтических композиций, и данные композиции могут содержать один или более подсластителей, горечей, ароматизаторов, красителей и консервантов, для получения превосходных в фармацевтическом смысле и внешне привлекательных препаратов.
Таблетки могут содержать активный ингредиент в смеси с нетоксичным фармацевтически приемлемым наполнителем, подходящим для производства таблеток. Такими наполнителями могут быть, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция и фосфат натрия; гранулирующие и дезинтегрирующие агенты, например, кукурузный крахмал или альгиновая кислота; связующие средства, например, крахмал, желатин или смола акации, и смазывающие вещества, например, стеарат магния, стеариновая кислота или тальк, таблетки могут быть без покрытия или с нанесенным известными методами покрытием для задержки распада и всасывания в желудочно-кишечном тракте, что обеспечивает продолжительное действие в течение большего промежутка времени. Например, могут применяться такие материалы для увеличения продолжительности действия, как глицерил моностеарат или глицерил дистеарат. На таблетки также можно наносить покрытие по методике, описанной в патентах США № 4,256,108; 4,166,452; и 4,265,874 (включенных в настоящий текст посредством ссылки), для получения осмотических терапевтических таблеток с контролируемым высвобождением.
Препараты для перорального применения включают твердые желатиновые капсулы, в которых активный ингредиент смешан с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином. Капсулы также могут представлять собой мягкие желатиновые капсулы, в которых активный ингредиент смешан с водой или со смешивающимся с водой растворителем, таким как пропиленгликоль, полиэтиленгликоли (PEG) и этанол, или с масляной средой, например, с арахисовым маслом, жидким парафином или оливковым маслом.
В одном варианте осуществления, соединения, имеющие формулу (I), можно вводить в виде мягких таблетированных композиций или мягких жевательных композиций, таких как описанные в US 2013/0203692 A1, US 2010/0087492, US 2006/0222684, US 2004/0151759, US 7955632, все включены в настоящий текст посредством ссылки. Ветеринарные композиции могут иметь вид мягких жевательных препаратов (“мягкая жвачка”), которые привлекательны и приемлемы для млекопитающих. Помимо действующего вещества (веществ), мягкие жвачки по настоящему изобретению могут включать один или больше из следующих компонентов: растворитель или смесь растворителей, один или больше наполнителей, один или больше связующих, одно или больше поверхностно-активных веществ, один или больше увлажнителей, одно или больше смазывающих веществ, один или больше разрыхлителей, один или больше красителей, один или больше противомикробных агентов, один или больше антиоксидантов, один или больше модификаторов рН, и один или больше ароматизаторов.
Растворители, которые могут быть использованы в композициях по настоящему изобретению, включают, без ограничения перечисленным, различные категории жидкого полиэтиленгликоля (PEG), включая PEG 200, PEG 300, PEG 400 и PEG 540; пропилен карбонат; спирты, включая этанол, изопропанол и бензиловый спирт; пропиленгликоль; триглицериды, включая, без ограничения перечисленным, каприловый/каприновый триглицерид, каприловый/каприновый/линолевый триглицерид (например, MIGLYOL® 810 и 812, каприловый/каприновый/янтарный триглицерид, пропиленгликоль дикаприлат/дикапрат, и т.п.; воду, раствор сорбита, глицерин каприлат/капрат и полигликозилированные глицериды (GELUCIRE®) или их комбинации.
Различные наполнители, известные в данной области, могут быть использованы в мягких жевательных композициях изобретения. Наполнители включают, без ограничения перечисленным, кукурузный крахмал, предварительно клейстеризованный кукурузный крахмал, тонкоизмельченный соевый белок, мука из зёрен кукурузы с початками, кукурузная глютеновая мука и т.п. В некоторых воплощениях в композициях может быть использована комбинация двух или большего количества наполнителей.
Связующие, которые могут быть использованы в композициях изобретения, включают, без ограничения перечисленным, поливинилпирролидон (например, повидон), перекрестно-связанный поливинилпиррролидон (кросповидон), полиэтиленгликоли различных категорий, включая PEG 3350, PEG 4000, PEG 6000, PEG 8000 и даже PEG 20,000, кополимеры винилпирролидона и винилацетата (например, коповидона), такие как продукты, продаваемые BASF под торговой маркой Kollidon® VA 64 и т.п., крахмал, такой как картофельный крахмал, крахмал из тапиоки, и кукурузный крахмал; меласса, кукурузный сироп, мед, кленовый сироп и сахара различных типов; или комбинация двух или нескольких связующих.
Увлажнители, которые могут быть использованы в композициях, включают, без ограничения перечисленным, глицерол (также упоминается в данном документе как глицерин), пропиленгликоль, цетиловый спирт или глицерин моностеарат, и т.п. Полиэтиленгликоли различных категорий также могут быть использованы в качестве увлажнителей.
В композициях могут присутствовать поверхностно-активные вещества для улучшения растворимости и всасывания после переваривания. Поверхностно-активные вещества в типичном случае присутствуют в концентрации примерно от 1 до 10% (вес/вес), более типично от примерно 1 до примерно 5% (вес/вес). Примеры поверхностно-активных веществ, которые могут быть использованы в композициях, включают, но не ограничиваются ими, глицерил моноолеат, полиоксиэтиленовые сложные эфиры сорбита и жирных кислот, сложные эфиры сорбита, в том числе моноолеат сорбита (Span® 20), поливиниловый спирт, полисорбаты в том числе полисорбат 20 и полисорбат 80, d-α-токоферил полиэтиленгликоль 1000 сукцинат (TPGS), лаурилсульфат натрия, сополимеры окиси этилена и окиси пропилена (например, полоксомеры, такие как LUTROL® F87 и т.п.), полиэтиленгликоль производные касторового масла, включая полиоксил 35 касторовое масло (Cremophor® EL), полиоксил 40 гидрогенизированное касторовое масло (Cremophor® RH 40), полиоксил 60 касторовое масло (Cremophor® RH60); пропиленгликольмонолаурат (LAUROGLYCOL®); сложные эфиры глицерина включая каприлат/капрат глицерина (CAPMUL® MCM), полигликолизированные глицериды (GELUCIRE®), PEG 300 каприловые/каприновые триглицериды (Softigen® 767), PEG 400 каприловые/каприновые триглицериды (Labrasol®), PEG 300 олеиновые глицериды (Labrafil® M-1944CS), PEG 300 линолевые глицериды (Labrafil® M-2125CS); полиэтиленгликоль стеараты и полиэтиленгликоль гидроксистеараты, в том числе полиоксил 8 стеарат (PEG 400 моностеарат), полиоксилстеарат 40 (PEG 1750, моностеарат) и т.п.
Инновационные составы могут содержать другие инертные ингредиенты, такие как антиоксиданты, консерванты или стабилизаторы pH. Эти соединения также хорошо известны в области приготовления составов. Антиоксиданты могут быть добавлены к композициям изобретения для ингибирования деградации активных агентов. Подходящие антиоксиданты включают, без ограничения перечисленным, альфа токоферол, аскорбиновую кислоту, аскорбил пальмитат, фумаровую кислоту, яблочную кислоту, аскорбат натрия, метабисульфат натрия, н-пропил галлат, BHA (бутилированный гидроксианизол), BHT (бутилированный гидрокситолуол), монотиоглицерин и т.п.
Композиции по настоящему изобретению могут также включать один или несколько смазывающих веществ/вспомогательных веществ. В некоторых случаях смазывающее вещество может также выполнять роль растворителя, и, соответственно, некоторые компоненты оригинальных композиций могут выполнять двойные функции. Смазывающие вещества/вспомогательные вещества включают, без ограничения перечисленным, полиэтиленгликоли различных диапазонов молекулярных масс, включая PEG 3350 (Dow Chemical) и PEG 4000, кукурузное масло, минеральное масло, гидрогенизированные растительные масла (STEROTEX или LUBRITAB), арахисовое масло и/или касторовое масло.
Многие вкусоароматические агенты могут быть использованы в композициях изобретения для улучшения вкусовых качеств пероральных ветеринарных композициях. Предпочтительными вкусоароматическими агентами являются те, которые не получают из животных источников. В различных воплощениях могут быть использованы вкусовые ароматические компоненты, полученные из фруктов, мяса (включая, без ограничения перечисленным, свинину, говядину, курятину, рыбу, домашнюю птицу и т.п.), овощей, сыра, бекона, сыра-бекона и/или искусственных вкусовых ароматизирующих веществ. Вкусовой ароматический компонент, как правило, выбирают на основании рассмотрения организма, который будет проглатывать мягкую жвачку. Например, лошадь может предпочитать яблочный вкусовой ароматизирующий компонент, а собака может предпочитать мясной вкусовой ароматизирующий компонент. Хотя вкусовые компоненты, полученные из неживотных источников являются предпочтительными, в некоторых воплощениях могут быть использованы натуральные вкусоароматические добавки, содержащие экстракты говядины или печени и т.п., такие как добавка со вкусом тушеного мяса, искусственная порошкообразная добавка со вкусом говядины, добавка со вкусом жареной говядины, и добавка со вкусом говяжьей солонины в числе прочих.
В другом варианте осуществления настоящего изобретения, активную композицию можно вводить в виде жидких композиций, и можно применять либо наружно, либо перорально. Жидкие препараты - это жидкость-содержащие композиции по настоящему изобретению, их вводят в рот или горло животным, или выливают на кожу или покровы животного.
Композиции по настоящему изобретению могут также иметь форму эмульсий масло-в-воде или вода-в-масле. Масляная фаза может представлять собой растительное масло, например, оливковое масло или арахисовое масло, или минеральное масло, например, жидкий парафин, или их смесь. Подходящие эмульгаторы включают природные фосфатиды, например, соевое масло, лецитин, и сложные эфиры или частичные сложные эфиры, полученные из жирных кислот и ангидридов гекситолов, например, сорбитан моноолеат, и продукты конденсации указанных частичных сложных эфиров с этиленоксидом, например, полиоксиэтилен сорбитан моноолеат. Эмульсии могут также содержать подсластители, горечи, ароматизаторы и/или консерванты.
В одном варианте осуществления, композиция по настоящему изобретению может быть в форме микроэмульсии. Микроэмульсии хорошо подходят в качестве жидкого носителя. Микроэмульсии представляют собой четырехкомпонентные системы, содержащие водную фазу, масляную фазу, поверхностно-активное вещество и ко-сурфактант. Они представляют собой прозрачные и изотропные жидкости.
Микроэмульсии состоят из стабильных дисперсий микрокапель водной фазы в масляной фазе, или наоборот - микрокапель масляной фазы в водной фазе. Размер таких микрокапель может быть менее 200 нм (от 1000 до 100000 нм для эмульсий). Пленка на границе раздела фаз может состоять из чередования молекул поверхностно-активного вещества и ко-сурфактанта, которые благодаря уменьшению коэффициента поверхностного натяжения делают возможным спонтанное образование микроэмульсии.
В одном варианте осуществления масляной фазы, масляная фаза может быть образована из минеральных или растительных масел, из ненасыщенных полигликозилированных глицеридов или из триглицеридов, или, альтернативно, из смесей перечисленных соединений. В одном варианте масляной фазы, масляная фаза образована триглицеридами; в другом варианте осуществления масляной фазы, триглицериды представляют собой триглицериды со средней длиной цепочки, например, C8-C10 каприловый/каприновый триглицерид. В другом варианте осуществления, процентное содержание (об/об) масляной фазы выбрано из группы, состоящей из следующих интервалов: от около 2 до около 15%; от около 7 до около 10%; и от около 8 до около 9% (об/об) микроэмульсии.
Водная фаза включает, например, воду или гликолевые производные, такие как пропиленгликоль, простые эфиры гликолей, полиэтиленгликоль или глицерин. В одном варианте гликолевого производного, гликоль может представлять собой пропиленгликоль, моноэтиловый эфир диэтиленгликоля, моноэтиловый эфир дипропиленгликоля и их смеси. В целом, водная фаза составляет от около 1 до около 4% (об/об) микроэмульсии.
Поверхностно-активные вещества для микроэмульсии включают моноэтиловый эфир диэтиленгликоля, монометиловый эфир дипропиленгликоля, полигликолезированные C8-C10 глицериды или полиглицерил-6-диолеат. Помимо перечисленных поверхностно-активных веществ, вспомогательные поверхностно-активные вещества включают короткоцепочечные спирты, такие как этанол и пропанол.
Некоторые вещества являются общими для обсужденных выше трех компонентов, т.е. водной фазы, поверхностно-активного вещества и вспомогательного поверхностно-активного вещества. Однако, квалифицированный специалист в данной области может использовать различные вещества для каждого компонента в составе одного препарата. В одном варианте соотношения ПАВ/со-ПАВ, соотношение со-ПАВ к ПАВ составляет от около 1/7 до около 1/2. В другом варианте количества со-ПАВ, указанное соотношение составляет от около 25 до около 75% (об/об) поверхностно-активного вещества и от около 10 до около 55% (об/об) со-ПАВ в микроэмульсии.
Масляные суспензии можно приготовить суспендированием активного ингредиента в растительном масле, например, в арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, например, пчелиный воск, твердый парафин или цетиловый спирт. Можно добавлять подсластители, такие как сахароза, сахарин или аспартам, горечи и ароматизаторы, чтобы приготовить приятный на вкус препарат для перорального введения. Описанные композиции можно законсервировать добавлением антиоксиданта, такого как аскорбиновая кислота, или других известных консервантов.
Водные суспензии могут содержать действующее вещество в смеси с наполнителями, подходящими для приготовления водных суспензий. Такие наполнители включают суспендирующие средства, например, натрия карбоксиметилцеллюлоза, метилцеллюлоза, гидрокси-пропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и смола акации; диспергирующими или увлажняющими средствами могут быть природные фосфатиды, например, лецитин, или продукты конденсации алкиленоксида с жирными кислотами, например, полиоксиэтилен стеарат, или продукты конденсации этиленоксида с длинноцепочечными алифатическими спиртами, например, гептадекаэтиленоксицетанол, или продукты конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и гекситола, такие как полиоксиэтилен сорбитол моноолеат, или продукты конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и ангидридов гекситола, например, полиэтилен сорбитан моноолеат. Водные суспензии могут содержать один или более консервантов, например, этил- или н-пропил, п-гидроксибензоат, один или более красителей, один или более ароматизаторов, и один или более подсластителей и/или горечей, таких как описано выше.
Диспергируемые порошки и гранулы, подходящие для приготовления водной суспензии путем добавления воды, содержат активный ингредиент в смеси с диспергирующим или увлажняющим средством, суспендирующим средством и одним или более консервантами. Примерами подходящих диспергирующих или увлажняющих средств, а также суспендирующих средств, являются уже перечисленные выше. Могут также присутствовать дополнительные наполнители, например, подсластители, горечи, ароматизаторы и красители.
В состав сиропов и эликсиров могут входить подсластители, например, глицерин, пропиленгликоль, сорбит или сахароза. Такие препараты могут также содержать средство, уменьшающее раздражение, консервант, подсластитель(-ли) и/или краситель(-ли).
В другом варианте осуществления настоящего изобретения, композиция может иметь вид пасты. Примеры вариантов пастообразной готовой формы включают (но не ограничены только ими) описанные в Патенты США № 6,787,342 и 7,001,889, которые оба включены в настоящий текст посредством ссылки. Помимо соединений по настоящему изобретению, паста может также содержать высокодисперсный диоксид кремния; модификатор вязкости; носитель; опционально, адсорбент; и, опционально, краситель, стабилизирующее средство, поверхностно-активное вещество или консервант.
В одном варианте препарата, препарат может представлять собой пасту, содержащую соединения по настоящему изобретению, высокодисперсный диоксид кремния, модификатор вязкости, адсорбент, краситель; и гидрофильный носитель, который представляет собой триацетин, моноглицерид, диглицерид или триглицерид.
Паста может также включать модификатор вязкости. Подходящие модификаторы вязкости включают (но не ограничиваются только ими) полиэтиленгликоли (PEG), включающие (но не ограничивающиеся только ими) PEG 200, PEG 300, PEG 400, PEG 600, моноэтаноламин, триэтаноламин, глицерин, пропиленгликоль, полиоксиэтилен (20) сорбитан моно-олеат (полисорбат 80 или Tween 80), и полиоксамеры (например, Pluronic L 81); адсорбент, такой как карбонат магния, карбонат кальция, крахмал, и целлюлозу и ее производные; и краситель, включающий (но не ограничивающийся только ими) диоксид титана, оксид железа, FD&C Blue #1 Aluminum Lake.
В некоторых вариантах осуществления, композиции могут иметь форму стерильных инъецируемых водных или масляных суспензий. Такую суспензию можно получать согласно известным в данной области методикам с применением подходящих диспергирующих или смачивающих агентов и суспендирующих агентов, которые были упомянуты выше. Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально-приемлемом разбавителе или растворителе, например, раствор в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, подходящих для применения, находятся вода, раствор Рингера и изотонический раствор хлорида натрия. Можно также применять сорастворители, такие как этанол, пропиленгликоль, глицерин формаль или полиэтиленгликоли. Можно применять консерванты, такие как фенол или бензиловый спирт.
Кроме того, можно применять стерильные жирные масла в качестве растворителя или суспендирующей среды. Для этой цели можно применять любую марку жирного масла, включая синтетические моно- и диглицериды. Кроме того, в приготовлении инъецируемых композиций находят применение жирные кислоты, такие как олеиновая кислота.
Препараты для наружного, кожного и подкожного применения могут включать, в качестве неограничивающих примеров, эмульсии, кремы, мази, гели, пасты, порошки, шампуни, препараты для обливания, готовые к применению препараты, растворы и суспензии для точечного нанесения, растворы для погружения и спреи. Наружное нанесение инновационного соединения или композиции, содержащей по меньшей мере одно инновационное соединение среди других действующих веществ, в форме препарата для точечного нанесения, опрыскивания или обливания, позволяет добиться абсорбции инновационных композиций через кожу и достижения системной концентрации, распределения через сальные железы или по поверхности кожи, обеспечивая достижения желательной концентрации по всей площади покровов. Когда соединение распределяется через сальные железы, они могут играть роль резервуара, благодаря чему можно достичь продолжительного (до нескольких месяцев) эффекта. Препараты для точечного нанесения обычно наносят на локализованный участок, составляющий область, отличную от всего животного в целом. В одном варианте осуществления, локализованный участок может представлять собой область между лопатками. В другом варианте осуществления, это может быть полоса, например, полоса от головы до хвоста животного.
Препараты для обливания описаны в Патенте США 6,010,710, который также включен в настоящий текст посредством ссылки. Препараты для обливания преимущественно могут быть масляными и обычно содержат разбавитель или носитель, а также растворитель (например, органический растворитель) для действующего вещества, если он нерастворим в разбавителе.
Органические растворители, которые можно применять по настоящему изобретению, включают (но не ограничиваются только ими) ацетилбутил цитрат, сложные эфиры жирных кислот, такие как диметиловый эфир, диизобутил адипат, ацетон, ацетонитрил, бензиловый спирт, этиловый спирт, бутилдигликоль, диметилацетамид, диметилформамид, диметилсульфоксид, дипропиленгликоля н-бутиловый эфир, этанол, изопропанол, метанол, этиленгликоля моноэтиловый эфир, этиленгликоля монометиловый эфир, монометилацетамид, дипропиленгликоля монометиловый эфир, жидкие полиоксиэтиленгликоли, пропиленгликоль, 2-пирролидон (например, N-метилпирролидон), пропиленкарбонат, диэтиленгликоля моноэтиловый эфир, этиленгликоль, триацетин, C1-C10 эфиры карбоновых кислот, такие как бутил- или октилацетат, и диэтилфталат, или смесь по меньшей мере двух из перечисленных растворителей.
Растворитель применяют пропорционально концентрации действующего вещества и его растворимости в данном растворителе. Следует применять наименьший возможный объем. Носитель составляет оставшееся до 100% количество.
Носители или разбавители для данных препаратов могут включать диметилсульфоксид (ДМСО), гликолевые производные, такие как, например, пропиленгликоль, простые эфиры гликолей, полиэтиленгликоли или глицерин. В качестве носителя или разбавителя можно также указать растительные масла, такие как (но не ограничиваясь только ими) соевое масло, арахисовое масло, касторовое масло, кукурузное масло, хлопковое масло, оливковое масло, масло виноградных косточек, подсолнечное масло, минеральные масла, такие как (но не ограничиваясь только ими) петролатум, парафин, силикон и т.д.; алифатические или циклические углеводороды или, альтернативно, например, среднецепочечные (такие как C8 - C12) триглицериды.
В другом варианте осуществления настоящего изобретения, можно добавлять умягчитель и/или растекатель и/или пленкообразующее средство. В одном варианте осуществления, умягчитель и/или растекатель и/или пленкообразующий агент может представлять собой:
(a) поливинилпирролидон, поливиниловые спирты, сополимеры винилацетата и винилпирролидона, полиэтиленгликоли, бензиловый спирт, маннит, глицерин, сорбит, полиоксиэтиленированные сложные эфиры сорбитана, лецитин, натрия карбоксиметилцеллюлоза, силиконовые масла, полидиорганосилоксановые масла (такие как полидиметилсилоксановые (PDMS) масла), например, содержащие силанольные функциональные группы, или масло 45V2,
(b) анионогенные ПАВ, такие как стеараты щелочных металлов, стеараты натрия, калия или аммония; стеарат кальция, стеарат триэтаноламина; абиетат натрия; алкилсульфаты (например, лаурилсульфат натрия и цетилсульфат натрия); додецилбензолсульфонат натрия, диоктилсульфосукцинат натрия; жирные кислоты (например, производные кокосового масла),
(c) катионогенные ПАВ, такие как водорастворимые четвертичные соли аммония формулы N+R'R''R'''R''''Y-, в которой радикалы R представляют собой при желании гидроксилированные углеводородные радикалы, а Y- представляет собой анион сильной кислоты, такой как галогенидные, сульфатные и сульфонатные анионы; среди подходящих катионогенных ПАВ также находится цетилтриметиламмония бромид,
(d) соли аминов формулы N+ R'R''R''', в которой радикалы R представляют собой при желании гидроксилированные углеводородные радикалы; среди подходящих катионогенных ПАВ также находится октадециламина гидрохлорид,
(e) неионогенные ПАВ, такие как сложные эфиры сорбитана, которые при желании являются полиоксиэтиленированными (например, полисорбат 80), полиоксиэтиленированные алкиловые эфиры; полиоксипропиленированные жирные спирты, такие как полиоксипропилен-стироловый эфир; полиэтиленгликоль стеарат, полиоксиэтиленированные производные касторового масла, сложные эфиры полиглицерина, полиоксиэтиленированные жирные спирты, полиоксиэтиленированные жирные кислоты, сополимеры этиленоксида и пропиленоксида,
(f) амфотерные ПАВ, такие как замещенные лауриловые соединения бетаина, и
(g) смесь по меньшей мере двух из перечисленных средств.
В одном варианте осуществления, количество умягчителя составляет примерно от 0.1 до 50% или от 0.25 до 5%, по объему. В другом варианте осуществления, количество умягчителя составляет от примерно 0.1% до примерно 30%, от примерно 1% до примерно 30%, от примерно 1% до примерно 20%, или от примерно 5% до примерно 20%, по объему.
В другом варианте осуществления настоящего изобретения, композиции могут быть готовым к применению раствором, как описано, например, в U.S. Patent No. 6,395,765, который включен в настоящий текст посредством ссылки. Помимо соединений по настоящему изобретению, готовый к применению раствор может содержать ингибитор кристаллизации, органический растворитель или органический сорастворитель. В некоторых вариантах осуществления, вместе с органическим растворителем в состав может входить вода.
В различных вариантах осуществления настоящего изобретения, композиции могут включать ингибитор кристаллизации в количестве от примерно 1 до примерно 50% (вес/об) или от примерно 5 до примерно 40% (вес/об) из расчета на общий вес препарата. В других вариантах осуществления, количество ингибитора кристаллизации в инновационных препаратах может составлять от примерно 1% до примерно 30%, от примерно 5% до примерно 20%, от примерно 1% до примерно 15%, или от примерно 1% до примерно 10% (вес/вес). Тип ингибитора кристаллизации, применяемого в инновационных препаратах, не ограничивается, при условии, что он подавляет кристаллизацию действующих или инертных веществ из препарата. Например, в некоторых вариантах осуществления настоящего изобретения, растворитель или сорастворитель в препарате также может выполнять роль ингибитора кристаллизации, если он в достаточной степени подавляет формирование кристаллов после введения препарата.
Ингибиторы кристаллизации, которые могут применяться в настоящем изобретении, включают (но не ограничены только ими):
(a) поливинилпирролидон, поливиниловые спирты, сополимеры винилацетата и винилпирролидона, полиэтиленгликоли, бензиловый спирт, диметилформамид, диметилацетамид, диметилсульфоксид, 2-пирролидон, N-метилпирролидон, маннит, глицерин, сорбит или полиоксиэтиленированные сложные эфиры сорбитана; лецитин или натрия карбоксиметилцеллюлоза; или акриловые производные, такие как акрилаты или метакрилаты или их полимеры или сополимеры, полиэтиленгликоли (PEG) или полимеры, содержащие полиэтиленгликоли, такие как гликофуролы и т.п., и другие;
(b) анионогенные ПАВ, такие как стеараты щелочных металлов (например, стеараты натрия, калия или аммония); стеарат кальция или стеарат триэтаноламина; абиетат натрия; алкилсульфаты, которые включают (но не ограничиваются только ими) лаурилсульфат натрия и цетилсульфат натрия; додецилбензолсульфонат натрия или диоктилсульфосукцинат натрия; или жирные кислоты (например, кокосовое масло),
(c) катионогенные ПАВ, такие как водорастворимые четвертичные соли аммония формулы N+R'R''R'''R''''Y-, в которой радикалы R представляют собой одинаковые или разные при желании гидроксилированные углеводородные радикалы, а Y- представляет собой анион сильной кислоты, такой как галогенидные сульфатные и сульфонатные анионы; цетилтриметиламмония бромид является одним из подходящих для применения катионогенных ПАВ,
(d) соли аминов формулы N+R'R''R''', в которой радикалы R представляют собой одинаковые или разные при желании гидроксилированные углеводородные радикалы; октадециламина гидрохлорид является одним из подходящих для применения катионогенных ПАВ;
(e) неионогенные ПАВ, такие как при желании полиоксиэтиленированные сложные эфиры сорбитана, например, полисорбат 80, или полиоксиэтиленированные алкиловые эфиры; полиэтиленгликоль стеарат, полиоксиэтиленированные производные касторового масла, сложные эфиры полиглицерина, полиоксиэтиленированные жирные спирты, полиоксиэтиленированные жирные кислоты или сополимеры этиленоксида и пропиленоксида;
(f) амфотерные ПАВ, такие как замещенные лауриловые соединения бетаина, или
(g) смесь по меньшей мере двух из перечисленных выше в пунктах (a)-(f) соединений, или
(h) органический растворитель или смесь растворителей, которые подавляют образование кристаллов или аморфного твердого вещества после введения препарата.
В одном варианте ингибитора кристаллизации, может применяться пара ингибиторов. Такие пары включают, например, комбинацию пленкообразующего средства полимерного типа и поверхностно-активного вещества. Указанные средства могут быть выбраны из соединений, перечисленных выше в качестве ингибиторов кристаллизации.
В некоторых вариантах осуществления, органический растворитель(-ли) могут иметь диэлектрическую константу от примерно 10 до примерно 35 или от примерно 20 до примерно 30. В других вариантах осуществления, органический растворитель может иметь диэлектрическую константу от примерно 10 до примерно 40 или от примерно 20 до примерно 30. Содержание органического растворителя или смеси растворителей в композиции не ограничивается, и он присутствует в количестве, достаточном для растворения целевых компонентов в желаемой концентрации. Как обсуждено выше, органический растворитель может также играть роль ингибитора кристаллизации в препарате.
В некоторых вариантах осуществления, один или больше органических растворителей могут иметь температуру кипения ниже примерно 100°C, или ниже примерно 80°C. В других вариантах осуществления, органический растворитель(-ли) могут иметь температуру кипения ниже примерно 300°C, ниже примерно 250°C, ниже примерно 230°C, ниже примерно 210°C или ниже примерно 200°C.
В некоторых вариантах осуществления, когда присутствует смесь растворителей, т.е. растворитель и сорастворитель, растворители могут присутствовать в композиции в вес/вес соотношении от примерно 1/50 до примерно 1/1. В типичном случае растворители присутствуют в соотношении от примерно 1/30 до примерно 1/1, от примерно 1/20 до примерно 1/1, или от примерно 1/15 до примерно 1/1 по весу. Предпочтительно, два растворителя присутствуют в вес/вес соотношении от примерно 1/15 до примерно 1/2. В некоторых вариантах осуществления, по меньшей мере один из присутствующих растворителей может улучшать растворимость действующего вещества или выступать в роли ускорителя высыхания. В частных вариантах осуществления, по меньшей мере один из растворителей смешивается с водой.
Препарат может также содержать антиоксидант, предназначенный для ингибирования окисления на воздухе, и этот антиоксидант может присутствовать в количестве от примерно 0.005 до примерно 1% (вес/об), от примерно 0.01 до примерно 0.1%, или от примерно 0.01 до примерно 0.05%.
В одном варианте пленкообразующего средства, данные средства являются средствами полимерного типа, которые включают (но не ограничиваются только ими) различные марки поливинилпирролидона, поливиниловые спирты и сополимеры винилацетата и винилпирролидона.
В одном варианте поверхностно-активных веществ, данные вещества включают (но не ограничиваются только ими) вещества, изготовленные из неионогенных ПАВ; в другом варианте поверхностно-активных веществ, данные вещества представляют собой полиоксиэтиленированный сложный эфир сорбитана. В другом варианте поверхностно-активных веществ, данные вещества включают различные марки полисорбата, например, Полисорбат 80.
В другом варианте осуществления настоящего изобретения, пленкообразующее средство и поверхностно-активное вещество могут присутствовать в близких или одинаковых количествах, в указанных выше рамках границ общего количества ингибитора кристаллизации.
Ингибитор кристаллизации подавляет образование кристаллов на покровах и улучшает сохранение косметического вида на коже или мехе; при этом без создания ощущения липкости или липкого вида, несмотря на высокую концентрацию действующего вещества. В настоящем изобретении можно также применять в качестве ингибиторов кристаллизации вещества, отличные от указанных в настоящем тексте. В одном варианте осуществления, эффективность ингибитора кристаллизации можно продемонстрировать в ходе теста, согласно которому 0.3 мл раствора, содержащего 10% (вес/об) действующего вещества в указанном выше подходящем растворителе, и 10% (вес/об) соединения, играющего роль ингибитора кристаллизации, помещают на стеклянную пластинку при 20°C на 24 часа, после чего на поверхности стекла менее 10 кристаллов, предпочтительно 0 кристаллов, видны невооруженным глазом.
В одном варианте антиоксидантов, данными агентами являются известные в данной области и включают (но не ограничиваются только ими) бутилированный гидроксианизол, бутилированный гидрокситолуол, аскорбиновая кислота, метабисульфит натрия, пропил галлат, тиосульфат натрия или смесь по меньшей мере двух соединений, обладающих антиоксидантными свойствами.
Вспомогательные вещества для составления готовых форм хорошо известны практикующим специалистам в данной области и могут быть приобретены у коммерческих поставщиков или получены по известным методикам. Описанные концентрированные композиции в целом готовят простым смешиванием описанных выше компонентов; преимущественно, отправной точкой служит смешивание действующего вещества с основным растворителем, с последующим добавлением других ингредиентов или вспомогательных веществ.
Объем применяемого препарата зависит от типа животного размера животного, а также от силы препарата и активности действующих веществ. В одном варианте осуществления, для млекопитающего можно применять количество от примерно 0.1 до примерно 20 мл препарата. В другом варианте осуществления, объем может составлять от примерно 0.1 до примерно 10 мл, от примерно 0.1 до примерно 5 мл, от примерно 0.5 мл до примерно 10 мл, или от примерно 0.3 до примерно 3 мл.
В другом варианте осуществления настоящего изобретения, нанесение препарата для точечного нанесения по настоящему изобретению может также оказывать продолжительное действие широкого спектра, когда раствор наносится на животное или птицу. Препараты для точечного нанесения обеспечивают местное нанесение концентрированного раствора, суспензии, микроэмульсии или эмульсии для периодического нанесения на определенный участок животного, обычно между двумя плечами (раствор для точечного нанесения).
В случае препаратов для точечного нанесения, носитель может представлять собой жидкий носитель, как описано в Патенте США 6,426,333 (включен в настоящий текст посредством ссылки), который в одном варианте препарата для точечного нанесения может содержать растворитель или смесь растворителей, включая (но не ограничиваясь только ими) ацетон, алифатический спирт, такой как метанол, этанол, пропанол, бутанол, изопропанол, пентанол, гексанол, гептанол, октанол, нонанол, циклопентанол, циклогексанол, этиленгликоль, пропиленгликоль и т.п.; ароматический спирт, такой как фенол, крезол, нафтол, бензиловый спирт и т.п.; ацетонитрил, бутил дигликоль, органический амид, такой как диметилацетамид, диметилформамид, монометилацетамид, 2-пирролидон, N-метилпирролидон, винилпирролидон и т.п.; пропилен или этилен карбонат, диметилсульфоксид (ДМСО), полимер гликоля или его простой эфир, такой как полиэтиленгликоль (PEG) различных марок, полипропиленгликоли различных марок, дипропиленгликоля н-бутиловый эфир, этиленгликоля моноэтиловый эфир, этиленгликоля монометиловый эфир, дипропиленгликоля монометиловый эфир, диэтиленгликоля моноэтиловый эфир, этиленгликоль, диэтилфталат, сложные эфиры жирных кислот, такие как диэтил- или диизобутиладипат, или смесь по меньшей мере двух из перечисленных растворителей.
Жидкий носитель необязательно можно содержать ингибитор кристаллизации, включая (но не ограничиваясь только ими) описанные выше в пунктах (a)-(h), или соединение, которое может одновременно играть роль растворителя и ингибитора кристаллизации (как описано выше), или смесь указанных ингибиторов кристаллизации.
Препараты для точечного нанесения можно приготовить растворением активных ингредиентов в фармацевтически или ветеринарно приемлемом носителе. Альтернативно, препарат для точечного нанесения можно приготовить инкапсулированием активного ингредиента, чтобы остаток терапевтического средства оставался на покровах животного. Состав таких препаратов может варьироваться в отношении содержания терапевтического средства в комбинации, в зависимости от вида животного, подвергающегося лечению, степени и типа инфекции, и веса животного.
Дозированные формы в типичном случае содержат от примерно 0.1 мг до примерно 5 г действующего вещества. В других вариантах осуществления, дозированная форма может содержать от примерно 0.5 мг до примерно 5 г действующего вещества. В одном варианте дозированной формы, дозировка может составлять от примерно 1 мг до примерно 500 мг действующего вещества, в типичном случае примерно 25 мг, примерно 50 мг, примерно 100 мг, примерно 200 мг, примерно 300 мг, примерно 400 мг, примерно 500 мг, примерно 600 мг, примерно 800 мг или примерно 1000 мг.
В одном варианте осуществления настоящего изобретения, действующее вещество может присутствовать в препарате в концентрации от примерно 0.05 до примерно 10% вес/объем. В другом варианте осуществления настоящего изобретения, действующее вещество может присутствовать в препарате в концентрации от примерно 0.1 до примерно 2% вес/объем. В другом варианте осуществления настоящего изобретения, действующее вещество может присутствовать в препарате в концентрации от примерно 0.25 до примерно 1.5% вес/объем. В другом варианте осуществления настоящего изобретения, действующее вещество может присутствовать в препарате в концентрации примерно 1% вес/объем.
II. Способы лечения:
Как описано выше, соединения, имеющие формулу (I), эффективны против эндопаразитов и могут применяться для лечения или предотвращения паразитных инфекций в организме животных или на их покровах. Во избежание сомнений следует указать, что понятие «животные» включает млекопитающих (включая людей), птиц или рыб. В одном варианте осуществления, в настоящем изобретении описан способ лечения или предотвращения эндопаразитной инфекции в организме животных или на их покровах, включающий введение животному эндопаразитицидно эффективного количества соединения, имеющего формулу (I), или их ветеринарно или фармацевтически приемлемых солей, или композиции по настоящему изобретению.
Соединения, имеющие формулу (I), также эффективны против эктопаразитов и могут применяться для лечения или предотвращения заражения животных эктопаразитами. В другом варианте осуществления, в настоящем изобретении описан способ лечения или предотвращения заражения животных эктопаразитами, включающий введение животному эктопаразитицидно эффективного количества соединения, имеющего формулу (I), или их фармацевтически приемлемых солей, или композиции по настоящему изобретению.
В другом варианте осуществления, в настоящем изобретении описан способ лечения или предотвращения эндопаразитной инфекции в организме животных или на их покровах или предотвращения заражения животных эктопаразитами, включающий введение млекопитающему композиции, содержащей эффективное количество соединения, имеющего формулу (I), в комбинации с эффективным количеством по меньшей мере одного второго действующего вещества, или его фармацевтически приемлемой соли.
В другом варианте осуществления настоящего изобретения, описан способ для лечения или предотвращения заражения паразитами в очаге, который включает введение или нанесение на очаг паразитицидно эффективного количества соединения, имеющего формулу (I), или его фармацевтически приемлемой соли. В применении к охране здоровья животных, под "очагом" понимается место обитания, размножения, площадь, материал или окружение, в котором паразит растет или может расти, исключая организм животного или его покровы.
В другом варианте осуществления, в настоящем изобретении описаны способы и применения соединений, имеющих формулу (I), для борьбы с вредителями растений или круп, или для защиты дерево-содержащих конструкций.
Млекопитающие, которые могут подвергаться обработке, включают (но не ограничиваются только ими) людей, кошек, собак, крупный рогатый скот, кур, бизонов, оленей, коз, лошадей, лам, верблюдов, свиней, овец и яков. В одном варианте осуществления настоящего изобретения, обрабатываемыми животными являются люди, кошки или собаки.
В одном варианте осуществления настоящего изобретения, соединения, имеющие формулу (I), обладают повышенной эффективностью против эндопаразитов, и в частности против эндопаразитов, резистентных к действующим веществам из класса макроциклических лактонов. В одном варианте осуществления, соединения и композиции по настоящему изобретению эффективны для борьбы с Haemonchus contortus, Ostertagia circumcincta и Trichostrongylus colubriformis у млекопитающих или птиц.
В другом варианте осуществления, в настоящем изобретении описан способ лечения паразитной инфекции или заражения паразитами у животного, включающий введение эффективного количества противогельминтного соединения по настоящему изобретению в комбинации с эффективным количеством активаторов ГАМК-рецепторов беспозвоночных, включая авермектин или милбемицин, млекопитающему, нуждающемуся в этом. Авермектины, которые можно применять в комбинации с соединениями по настоящему изобретению, включают (но не ограничиваются только ими) абамектин, димадектин, дорамектин, эмамектин, эприномектин, ивермектин, латидектин, лепимектин и селамектин. Милбемицины, которые можно применять в комбинации с соединениями по настоящему изобретению, включают (но не ограничиваются только ими) милбемиктин, милбемицин D, моксидектин и немадктин. Также включены 5-оксо и 5-оксимные производные указанных авермектинов и милбемицинов.
В одном варианте осуществления, соединения и композиции по настоящему изобретению можно применять для лечения или предотвращения эндопаразитной инфекции следующих паразитов: Anaplocephala (Anoplocephala), Ancylostoma, Necator, Ascaris, Brugia, Bunostomum, Capillaria, Chabertia, Cooperia, Cyathostomum, Cylicocyclus, Cylicodontophorus, Cylicostephanus, Craterostomum, Dictyocaulus, Dipetalonema, Dipylidium, Dirofilaria, Dracunculus, Echinococcus, Enterobius, Fasciola, Filaroides, Habronema, Haemonchus, Metastrongylus, Moniezia, Necator, Nematodirus, Nippostrongylus, Oesophagostomum, Onchocerca, Ostertagia, Oxyuris, Parascaris, Schistosoma, Strongylus, Taenia, Toxocara, Strongyloides, Toxascaris, Trichinella, Trichuris, Trichostrongylus, Triodontophorus, Uncinaria, Wuchereria, и их комбинаций.
В особенно предпочтительном варианте осуществления настоящего изобретения, соединения и композиции по настоящему изобретению применяют для лечения или предотвращения инфекции Dirofilaria immitis. Было обнаружено, что соединения, имеющие формулу (I), высоко эффективны против микрофилярий и L4 личинок D. Immitis, а также эффективны для защиты животных от инфекции Dirofilaria immitis in vivo. Так, соединения, имеющие формулу (I) можно применять для защиты животных от развития заболевания сердечными гельминтами посредством истребления незрелых стадий D. immitis до того, как они разовьются в зрелых червей. В одном варианте осуществления, соединения, имеющие формулу (I), и композиции, содержащие данные соединения, можно применять для предотвращения развития заболевания сердечными гельминтами посредством истребления незрелых стадий D. immitis, устойчивых к макроциклическим лактонам. В другом варианте осуществления, соединения и композиции по настоящему изобретению применяют для лечения или предотвращения инфекции Dirofilaria repens или Dirofilaria hongkongensis.
В другом варианте осуществления настоящего изобретения, паразит представляет собой Haemonchus contortus, Ostertagia circumcincta, Trichostrongylus axei, Trichostrongylus colubriformis, Cooperia curticei, Nematodirus battus и их комбинации.
В другом варианте лечения против эндопаразитов и эктопаразитов, при комбинировании с эктопаразитицидными веществами, эктопаразит представляет собой одно или больше насекомое или паукообразное, включая представителей родов Ctenocephalides, Rhipicephalus, Dermacentor, Ixodes, Boophilus, Amblyomma, Haemaphysalis, Hyalomma, Sarcoptes, Psoroptes, Otodectes, Chorioptes, Hypoderma, Damalinia, Linognathus, Haematopinus, Solenoptes, Trichodectes и Felicola.
В другом воплощении лечения эктопаразитов, эктопаразит происходит из родов Ctenocephalides, Rhipicephalus, Dermacentor, Ixodes и/или Boophilus. Обрабатываемые эктопаразиты включают, без ограничения перечисленным, блох, паразитиформных клещей, акариформных клещей, москитов, мух, вшей, мясных мух и их комбинаций. Конкретные примеры включают, без ограничения перечисленным, блох котов и собак (Ctenocephalides felis, Ctenocephalides sp. и т.п.), паразитиформных клещей (Rhipicephalus sp., Ixodes sp., Dermacentor sp., Amblyomma sp., и т.п.), и акариформных клещей (Demodex sp., Sarcoptes sp., Otodectes sp. и т.п.), вшей (Trichodectes spp., Cheyletiella spp., Linognathus spp., и т.п.), комаров (Aedes spp., Culex spp., Anopheles spp., и т.п.) и мух (Haematobia spp., Musca spp., Stomoxys spp., Dermatobia spp., Cochliomyia spp., и т.п.). В другом воплощении лечения эктопаразитов, эктопаразит представляет собой блоху и/или клеща.
Дополнительные примеры эктопаразитов включают, без ограничения перечисленным, род клещей Boophilus, особенно видов microplus (клещ кольчатый), decoloratus и annulatus; миазы, такие как Dermatobia hominis (известна как Berne in Brazil) и Cochliomyia hominivorax (падальница зелёная); миазы овец, такие как Lucilia sericata, Lucilia cuprina (известна как падальная муха в Австралии, Новой Зеландии и Южной Африке), собственно мухи, а именно те, чьи взрослые формы являются паразитами, такие как Haematobia irritans (жигалка коровья малая); вши, такие как Linognathus vituli и т.п.; и акариформные клещи, такие как Sarcoptes scabiei и Psoroptes ovis. Вышеуказанный перечень не является исчерпывающим, и другие эктопаразиты хорошо известны в данной области как опасные для животных и людей. Они включают, например, мигрирующие личинки двукрылых.
В другом варианте осуществления настоящего изобретения, соединения и композиции по настоящему изобретению пригодны для борьбы с вредителями, выбранными из группы, состоящей из Blatella germanica, Heliothis virescens, Leptinotarsa decemlineata, Tetramorium caespitum и их комбинации.
Фитопаразитические нематоды включают, например, виды родов Anguina, Aphelenchoides, Belonolaimus, Bursaphelenchus, Ditylenchus dipsaci, Globodera, Helicotylenchus, Heterodera, Longidorus, Meloidogyne, Pratylenchus, Radopholus similis, Rotylenchus, Trichodorus, Tylenchorhynchus, Tylenchulus, Tylenchulus semipenetrans и Xiphinema.
Кроме того, с добавлением или без добавления других пестицидных средств в композицию, настоящее изобретение может также применяться для избавления от других вредителей, которые включают (но не ограничиваются только ими) следующих вредителей:
(1) из отряда Isopoda, например, Oniscus asellus, Armadillidium vulgare и Porcellio scaber;
(2) из отряда Diplopoda, например, Blaniulus guttulatus;
(3) из отряда Chilopoda, например, Geophilus sarcophagus и Scutigera spp.;
(4) из отряда Symphyla, например, Scutigerella immaculata;
(5) из отряда Thysanura, например, Lepisma saccharina;
(6) из отряда Collembola, например, Onychiurus armatus;
(7) из отряда Blattaria, например, Blatta orientalis, Periplaneta americana, Leucophaea maderae и Blattella germanica;
(8) из отряда Hymenoptera, например, виды родов Diprion, Hoplocampa, Lasius, Monomorium pharaonis и Vespa;
(9) из отряда Siphonaptera, например, Xenopsylla cheopis и виды родов Ceratophyllus;
(10) из отряда Anoplura (Phthiraptera), например, виды родов Damalinia, Haematopinus, Linognathus, Pediculus, Trichodectes;
(11) из класса Arachnida, например, Acarus siro, Aceria sheldoni, виды родов Aculops, Aculus, Amblyomma, Argas, Boophilus, Brevipalpus, Bryobia praetiosa, Chorioptes, Dermanyssus gallinae, Eotetranychus, Epitrimerus pyri, Eutetranychus, Eriophyes, Hemitarsonemus, Hyalomma, Ixodes, Latrodectus mactans, Metatetranychus, Oligonychus, Ornithodoros, Panonychus, Phyllocoptruta oleivora, Polyphagotarsonemus latus, Psoroptes, Rhipicephalus, Rhizoglyphus, Sarcoptes, Scorpio maurus, Stenotarsonemus, Tarsonemus, Tetranychus, Vasates lycopersici;
(12) из класса Bivalva, например, виды рода Dreissena;
(13) из отряда Coleoptera, например, Acanthoscelides obtectus, виды родов Adoretus, Agelastica alni, Agriotes, Amphimallon solstitialis, Anobium punctatum, Anoplophora, Anthonomus, Anthrenus, Apogonia, Atomaria, Attagenus, Bruchidius obtectus, Bruchus, Ceuthorhynchus, Cleonus mendicus, Conoderus, Cosmopolites, Costelytra zealandica, Curculio, Cryptorhynchus lapathi, Dermestes, Diabrotica, Epilachna, Faustinus cubae, Gibbium psylloides, Heteronychus arator, Hylamorpha elegans, Hylotrupes bajulus, Hypera postica, Hypothenemus, Lachnosterna consanguinea, Leptinotarsa decemlineata, Lissorhoptrus oryzophilus, Lixus, Lyctus, Meligethes aeneus, Melolontha melolontha, Migdolus, Monochamus, Naupactus xanthographus, Niptus hololeucus, Oryctes rhinoceros, Oryzaephilus surinamensis, Otiorrhynchus sulcatus, Oxycetonia jucunda, Phaedon cochleariae, Phyllophaga spp., Popillia japonica, Premnotrypes, Psylliodes chrysocephala, Ptinus, Rhizobius ventralis, Rhizopertha dominica, Sitophilus, Sphenophorus, Sternechus, Symphyletes, Tenebrio molitor, Tribolium, Trogoderma, Tychius, Xylotrechus, Zabrus;
(14) из отряда Diptera, например, виды родов Aedes, Anopheles, Bibio hortulanus, Calliphora erythrocephala, Ceratitis capitata, Chrysomyia, Cochliomyia, Cordylobia anthropophaga, Culex, Cuterebra, Dacus oleae, Dermatobia hominis, Drosophila, Fannia, Gastrophilus, Hylemyia, Hyppobosca, Hypoderma, Liriomyza, Lucilia, Musca, Nezara, Oestrus, Oscinella frit, Pegomyia hyoscyami, Phorbia, Stomoxys, Tabanus, Tannia, Tipula paludosa, Wohlfahrtia;
(15) из класса Gastropoda, например, виды родов Arion, Biomphalaria, Bulinus, Deroceras, Galba, Lymnaea, Oncomelania, Succinea;
(16) из класса гельминтов, например, Ancylostoma duodenale, Ancylostoma ceylanicum, Acylostoma braziliensis, виды родов Ancylostoma, Ascaris lubricoides, Ascaris, Brugia malayi, Brugia timori, Bunostomum, Chabertia, Clonorchis, Cooperia, Dicrocoelium Dictyocaulus filaria, Diphyllobothrium latum, Dracunculus medinensis, Echinococcus granulosus, Echinococcus multilocularis, Enterobius vermicularis, Faciola, Haemonchus, Heterakis, Hymenolepis nana, Hyostrongulus, Loa Loa, Nematodirus, Oesophagostomum, Opisthorchis, Onchocerca volvulus, Ostertagia, Paragonimus, Schistosomen, Strongyloides fuelleborni, Strongyloides stercoralis, Stronyloides, Taenia saginata, Taenia solium, Trichinella spiralis, Trichinella nativa, Trichinella britovi, Trichinella nelsoni, Trichinella pseudopsiralis, Trichostrongulus, Trichuris trichuria, Wuchereria bancrofti;
(17) из отряда Heteroptera, например, Anasa tristis, виды родов Antestiopsis, Blissus, Calocoris, Campylomma livida, Cavelerius, Cimex, Creontiades dilutus, Dasynus piperis, Dichelops furcatus, Diconocoris hewetti, Dysdercus, Euschistus, Eurygaster, Heliopeltis, Horcias nobilellus, Leptocorisa, Leptoglossus phyllopus, Lygus, Macropes excavatus, Miridae, Nezara, Oebalus, Pentomidae, Piesma quadrata, Piezodorus, Psallus seriatus, Pseudacysta persea, Rhodnius, Sahlbergella singularis, Scotinophora, Stephanitis nashi, Tibraca, Triatoma;
(18) из отряда Homoptera, например, виды родов Acyrthosipon, Aeneolamia, Agonoscena, Aleurodes, Aleurolobus barodensis, Aleurothrixus, Amrasca, Anuraphis cardui, Aonidiella, Aphanostigma piri, Aphis, Arboridia apicalis, Aspidiella, Aspidiotus, Atanus, Aulacorthum solani, Bemisia, Brachycaudus helichrysii, Brachycolus, Brevicoryne brassicae, Calligypona marginata, Carneocephala fulgida, Ceratovacuna lanigera, Cercopidae, Ceroplastes, Chaetosiphon fragaefolii, Chionaspis tegalensis, Chlorita onukii, Chromaphis juglandicola, Chrysomphalus ficus, Cicadulina mbila, Coccomytilus halli, Coccus, Cryptomyzus ribis, Dalbulus, Dialeurodes, Diaphorina, Diaspis, Doralis, Drosicha, Dysaphis, Dysmicoccus, Empoasca, Eriosoma, Erythroneura, Euscelis bilobatus, Geococcus coffeae, Homalodisca coagulata, Hyalopterus arundinis, Icerya, Idiocerus, Idioscopus, Laodelphax striatellus, Lecanium, Lepidosaphes, Lipaphis erysimi, Macrosiphum, Mahanarva fimbriolata, Melanaphis sacchari, Metcalfiella, Metopolophium dirhodum, Monellia costalis, Monelliopsis pecanis, Myzus, Nasonovia ribisnigri, Nephotettix, Nilaparvata lugens, Oncometopia, Orthezia praelonga, Parabemisia myricae, Paratrioza, Parlatoria, Pemphigus, Peregrinus maidis, Phenacoccus, Phloeomyzus passerinii, Phorodon humuli, Phylloxera, Pinnaspis aspidistrae, Planococcus, Protopulvinaria pyriformis, Pseudaulacaspis pentagona, Pseudococcus, Psylla, Pteromalus, Pyrilla, Quadraspidiotus, Quesada gigas, Rastrococcus, Rhopalosiphum, Saissetia, Scaphoides titanus, Schizaphis graminum, Selenaspidus articulatus, Sogata, Sogatella furcifera, Sogatodes, Stictocephala festina, Tenalaphara malayensis, Tinocallis caryaefoliae, Tomaspis, Toxoptera, Trialeurodes vaporariorum, Trioza, Typhlocyba, Unaspis, Viteus vitifolii;
(19) из отряда Isoptera, например, виды родов Reticulitermes, Odontotermes;
(20) из отряда Lepidoptera, например, Acronicta major, Aedia leucomelas, виды родов Agrotis, Alabama argillacea, Anticarsia, Barathra brassicae, Bucculatrix thurberiella, Bupalus piniarius, Cacoecia podana, Capua reticulana, Carpocapsa pomonella, Cheimatobia brumata, Chilo, Choristoneura fumiferana, Clysia ambiguella, Cnaphalocerus, Earias insulana, Ephestia kuehniella, Euproctis chrysorrhoea, Euxoa, Feltia, Galleria mellonella, Helicoverpa, Heliothis, Hofmannophila pseudospretella, Homona magnanima, Hyponomeuta padella, Laphygma, Lithocolletis blancardella, Lithophane antennata, Loxagrotis albicosta, Lymantria, Malacosoma neustria, Mamestra brassicae, Mocis repanda, Mythimna separata, Oria, Oulema oryzae, Panolis flammea, Pectinophora gossypiella, Phyllocnistis citrella, Pieris, Plutella xylostella, Prodenia spp., Pseudaletia, Pseudoplusia includens, Pyrausta nubilalis, Spodoptera, Thermesia gemmatalis, Tinea pellionella, Tineola bisselliella, Tortrix viridana, Trichoplusia;
(21) из отряда Orthoptera, например, Acheta domesticus, Blatta orientalis, Blattella germanica, Gryllotalpa spp., Leucophaea maderae, виды родов Locusta, Melanoplus, Periplaneta americana, Schistocerca gregaria;
(22) из отряда Thysanoptera, например, Baliothrips biformis, Enneothrips flavens, виды родов Frankliniella, Heliothrips, Hercinothrips femoralis, Kakothrips, Rhipiphorothrips cruentatus, Scirtothrips, Taeniothrips cardamoni, Thrips;
(23) из класса Protozoa, например, виды рода Eimeria.
В каждом аспекте настоящего изобретения, соединения и композиции по настоящему изобретению можно применять против одного вредителя или их комбинации.
III. Смеси с другими действующими веществами
В другом варианте осуществления, композиции, содержащие циклические депсипептиды, имеющие формулу (I), могут также включать другие ветеринарные терапевтические средства. Ветеринарные фармацевтические агенты, которые можно включать в композиции по настоящему изобретению, хорошо известны в данной области техники (смотри, например, Plumb’ Veterinary Drug Handbook, 5th Edition, ed. Donald C. Plumb, Blackwell Publishing, (2005) или The Merck Veterinary Manual, 9th Edition, (January 2005)) и включают (но не ограничиваются только ими) акарбоза, ацепромазина малеат, ацетаминофен, ацетазоламид, ацетазоламид натрий, уксусная кислота, ацетогидроксамовая кислота, ацетилцистеин, ацитрецин, ацикловир, албендазол, албутерол сульфат, алфентанил, аллопуринол, алпразолам, альтреногест, амантадин, амикацин сульфат, аминокапроновая кислота, аминопентамида гидросульфат, аминофиллин/теофиллин, амиодарон, амитриптилин, амлодипина безилат, хлорид аммония, молибдат аммония, амоксициллин, клавуланат калия, амфотрецин В деоксихолат, амфотрецин В на липидной основе, ампициллин, ампролиум, антациды (для перорального применения), антивенин, апоморфион, апрамицина сульфат, аскорбиновая кислота, аспрагиназа, аспирин, атенолол, атипамезол, атракурия безилат, атропина сульфат, ауранофин, ауротиоглюкоза, азаперон, азатиоприн, азитромицин, баклофен, барбитураты, беназеприл, бетаметазон, бетанехол хлорид, бисакодил, субсалицилат висмута, блеомицин сульфат, болденона ундециленат, бромиды, бромокриптина мезилат, будесонид, бупренорфин, бусирон, бусульфан, буторфанола тартрат, каберголин, кальцитонин лососевых рыб, кальцитрол, соли кальция, каптоприл, карбенициллин инданил натрий, карбимазол, карбоплатин, карнитин, карпрофен, карведилол, цефадроксил, цефазолин натрий, цефиксим, клорсулон. цефоперазон натрий, цефотаксим натрий, цефотетан динатрий, цефокситин натрий, цефподоксим проксетил, цефтазидим, цефтиофур натрий, цефтиофур, цефтриаксон натрий, цефалексин, цефалоспорины, цефапирин, активированный уголь, хлорамбуцил, хлорамфеникол, хлордиазэпоксид, хлордиазэпоксид +/- клидиниум бромид, хлортиазид, хлорфенирамина малеат, хлорпромазин, хлорпропамид, хлортетрациклин, хорионический гонадотропин (ХГЧ), хром, циметидин, ципрофлоксацин, цисаприд, цисплатин, цитратные соли, кларитромицин, клемастина фумарат, кленбутерол, клиндамицин, клофазимин, кломипрамин, клаоназепам, клонидин, клопростенол натрий, клоразепат дикалий, клорсулон, клоксациллин, кодеина фосфат, колхицин, кортикотропин (АКТГ), косинтропин, циклофосфамид, циклоспорин, циклогептадин, цитарабин, дакарбазин, дактиномицин/актиномицин D, далтепарин натрий, даназол, дантролен натрий, дапсон, декохинат, дефероксамина мезилат, деракоксиб, деслорелина ацетат, десмопрессина ацетат, дезоксикортиокстерона пивалат, детомидин, дексаметазон, декспантенол, дексраазоксан, декстран, диазепам, диазоксид (перорально), дихлорфенамид, диклофенак натрий, диклоксациллин, диэтилкарбамазина цитрат, диэтилстилбестрол (DES), дифлоксацин, дигоксин, дигидротахистерол (DHT), дилтиазем, дименгидринат, димеркапрол/BAL, диметилсульфоксид, динопрост трометамин, дифенилгидрамин, дисопирамида фосфат, добутамин, докузат/DSS, доласетрона мезилат, домперидон, допамин, дорамектин, доксапрам, доксепин, доксорубицин, доксициклин, едетат кальция динатрия, кальция ЭДТА, эдрофония хлорид, эналаприл/эналаприлат, эноксапарин натрий, энрофлоксацин, эфедрина сульфат, эпинефрин, эпоетин/эритропоетин, эприномектин, эпсипрантел, эритромицин, эсмолол, эстрадиол ципионат, этакриновая кислота/этакринат натрия, этанол (спирт), этидронат натрия, этодолак, этомидат, средства для эвтаназии с пентобарбиталом, фамотидин, жирные кислоты (незаменимые/омега), фелбамат, фентанил, сульфат железа, филграстим, финастерид, фипронил, флорфеникол, флуконазол, флуцитозин, флудрокортизона ацетат, флумазенил, флуметазон, флуниксин меглумин, фторурацил (5-FU), флуоксетин, флутиказона пропионат, флувоксамина малеат, фомепизол (4-MP), фуразолидон, фуросемид, габапентин, гемцитабин, гентамицина сульфат, глимепирид, глипизид, глюкагон, глюкокортикоидные средства, глюкозамин/хондроитин сульфат, глутамин, глибурид, глицерин (перорально), гликопирролат, гонадорелин, гриссеофульвин, гвайфенезин, галотан, гемоглобин глутамер-200 (оксиглобин®), гепарин, гидроксиэтилкрахмал, гиалуронат натрия, гидразалин, гидрохлортиазид, гидрокодона битартрат, гидрокортизон, гидроморфон, гидроксимочевина, гидроксизин, ифосфамид, имидаклоприд, имидокарб дипропионат, импенем-циластатин натрий, имипрамин, инамринон лактат, инсулин, интерферон альфа-2а (человеческий рекомбинантный), иодид (натрия/калия), ипекак (сироп), иподат натрия, декстран железа, изофлуран, изопротеренол, изотретиноин, изокссуприн, итраконазол, каолин/пектин, кетамин, кетоконазол, кетопрофен, кеторолак трометамин, лактулоза, левпролид, левамизол, левитирацетам, левотироксин натрий, лидокаин, линкомицин, лиотиронин натрий, лизиноприл, ломустин (CCNU), луфенурон, лизин, магний, маннит, марбофлоксацин, мехлорэтамин, меклизин, меклофенамовая кислота, медетомидин, среднецепочечные триглицериды, медроксипрогестерона ацетат, мегестрола ацетат, меларсомин, мелатонин, мелоксикан, мелфалан, меперидин, меркаптопурин, меропенем, метформин, метадон, метазоламид, метенамина манделат/гиппурат, метимазол, метионин, метокарбамол, метогекситал натрий, метотрексат, метоксифлуран, метиленовый синий, метилфенидат, метилпреднизолон, метоклопрамид, метопролол, метронидаксол, мексилетин, миболерлон, мидазолам, милбемицин оксим, минеральное масло, миноциклин, мисопростол, митотан, митоксантрон, морфина сульфат, моксидектин, налоксон, мандролон деканоат, напроксен, наркотические (опиатные) агонистические анальгетики, неомицина сульфат, неостигмин, ниацинамид, нитазоксанид, нитенпирам, нитрофурантоин, нитроглицерин, нитропруссид натрия, низатидин, новобиоцин натрий, нистатин, октреотида ацетат, олсалазин натрий, омепрозол, ондансетрон, опиатные противодиарейные средства, орбифлоксацин, оксациллин натрий, оксазепам, оксибутинин хлорид, оксиморфон, окситетрациклин, окситоцин, памидронат динатрия, панкреплипаза, панкурония бромид, паромомицина сульфат, парозетин, пеницилламин, общеизвестные пенициллины, пенициллин G, пенициллин V калий, пентазоцин, пентобарбитал натрий, пентосан полисульфат натрия, пентоксифиллин, перголида мезилат, фенобарбитал, феноксибензамин, фенилбутазон, фенилэфрин, фенилпропаноламин, фенитоин натрий, феромоны, парентеральный фосфат, фитонадион/витамин К-1, пимобендан, пиперазин, пирлимицин, пироксикам, полисульфатированный гликозамингликан, поназурил, хлорид калия, пралидоксим хлорид, празосин, преднизолон/преднизон, примидон, прокаинамид, прокарбазин, прохлорперазин, пропантелина бромид, инъекция пропионовой бактерии акне, пропофол, пропранолол, протамина сульфат, псевдоэфедрин, объемное слабительное из подорожника, пиридостигмина бромид, пириламина малеат, пириметамин, хинакрин, хинидин, ранитидин, рифампин, s-аденозил-метионин (SAMe), физраствор/гиперосмотическое слабительное, селамектин, селегилин/l-депренил, сертралин, севеламер, севофлуран, силимарин/расторопша, бикарбонат натрия, полистиролсульфонат натрия, стибоглюконат натрия, сульфат натрия, тиосульфат натрия, соматотропин, соталол, спектиномицин, спиронолактон, станозолол, стрептокиназа, стрептозоцин, сукцимер, сукцинилхолин хлорид, сукралфат, суфентанила цитрат, сульфахлорпиридазин натрий, сульфадиазин/триметроприм, сульфаметоксазол/триметоприм, сульфадиментоксин, сульфадиментоксин/орметроприм, сульфасалазин, таурин, тепоксалин, тербинафлин, тербуталина сульфат, тестостерон, тетрациклин, тиабедазол, тиацетарсамид натрий, тиамин, тиогуанин, тиопентал натрий, тиотепа, тиротропин, тиамулин, тикарцилин динатрий, тилетамин/золазепам, тилмоксин, тиопронин, тобрамицина сульфат, токаинид, толазолон, телфенамовая кислота, топирамат, трамадол, тримцинолона ацетонид, триентин, трилостан, тримепраксина тартрат с преднизолоном, трипеленнамин, тилосин, урдосиол, вальпроевая кислота, ванадий, ванкомицин, вазопрессин, векурония бромид, верапамил, винбластина сульфат, винкристина фульфат, витамин Е/селен, варфарин натрий, ксилазин, йохимбин, зафирлукаст, зидовудин (АЗТ), ацетат цинка/сульфат цинка, зонисамид и их смеси.
В одном варианте осуществления настоящего изобретения, арилпиразольные соединения, такие как фенилпиразолы, можно включать в ветеринарные композиции по настоящему изобретению. Арилпиразолы известны в данной области техники и подходят для комбинирования с циклическими депсипептидами, имеющими формулу (I), в композициях по настоящему изобретению. Примеры таких арилпиразольных соединений включают (но не ограничиваются только ими) описанные в Патентах США 6,001,384; 6,010,710; 6,083,519; 6,096,329; 6,174,540; 6,685,954, 6,998,131 и 7,759,381 (все они включены в настоящий текст посредством ссылок). Особенно предпочтительным арилпиразольным действующим веществом является фипронил.
В другом варианте осуществления настоящего изобретения, один или больше макроциклических лактонов, которые работают как акарицид, противогельминтное средство и/или инсектицид, можно включать в композиции по настоящему изобретению в комбинации с соединениями, имеющими формулу (I). Во избежание сомнений, термин “макроциклический лактон” при использовании в настоящем тексте включает как природные, так и синтетические или полусинтетические авермектин и милбемицин.
Макроциклические лактоны, которые можно применять в композициях по настоящему изобретению, включают (но не ограничиваются только ими) природные авермектины (например, включая компоненты, обозначенные как A1a, A1b, A2a, A2b, B1a, B1b, B2a и B2b) и милбемицины, полусинтетические авермектины и милбемицины, моносахаридные авермектины и агликоновые авермектины. Примеры макроциклических лактоновых соединений, которые можно применять в композициях по настоящему изобретению, включают (но не ограничиваются только ими) абамектин, димадектин, дорамектин, эмамектин, эприномектин, ивермектин, латидектин, лепимектин, селамектин, мл-1,694,554, и милбемицины, включая (но не ограничиваясь только ими) милбемектин, милбемицин D, милбемицин A3, милбемицин A4, милбемицин оксим, моксидектин и немадектин. Также включены 5-оксо и 5-оксимные производные указанных авермектинов и милбемицинов.
Макроциклические лактоны известны в данной области техники и могут быть легко получены из коммерческих источников или известными методами синтеза. Широко доступна техническая и коммерческая литература по данному вопросу. Для авермектинов, ивермектина и абамектина можно указать, например, работу “Ivermectin and Abamectin”, 1989, by M.H. Fischer and H. Mrozik, William C. Campbell, опубликованную издательством Springer Verlag., или Albers-Schönberg et al. (1981), “Avermectins Structure Determination”, J. Am. Chem. Soc., 103, 4216-4221. В случае дорамектина можно порекомендовать работу “Veterinary Parasitology”, vol. 49, No. 1, July 1993, 5-15. В случае милбемицинов можно указать, среди прочих, работы Davies H.G. et al., 1986, “Avermectins and Milbemycins”, Nat. Prod. Rep., 3, 87-121, Mrozik H. et al., 1983, Synhesis of Milbemycins from Avermectins, Tetrahedron Lett., 24, 5333-5336, Патент США 4,134,973 и EP 0 677 054, которые оба включены в настоящий текст посредством ссылки.
Структуры авермектинов и милбемицинов являются близко родственными, например, они все содержат сложный 16-членный макроциклический лактоновый цикл. Природные авермектины описаны в Патенте США 4,310,519, а 22,23-дигидро авермектиновые соединения описаны в Патенте США 4,199,569. Следует также упомянуть, среди прочих, Патенты США 4,468,390, 5,824,653, EP 0 007 812 A1, Патент Великобритании 1 390 336, EP 0 002 916, и Патент Новой Зеландии 237 086. Природные милбемицины описаны в Патенте США 3,950,360, а также в многочисленных публикациях, процитированных в “The Merck Index” 12th ed., S. Budavari, Ed., Merck & Co., Inc. Whitehouse Station, New Jersey (1996). Латидектин описан в “International Nonproprietary Names for Pharmaceutical Substances (INN)”, WHO Drug Information, vol. 17, no. 4, pp. 263- 286, (2003). Полусинтетические производные этих классов соединений хорошо известны в данной области и описаны, например, в Патентах США 5,077,308, 4,859,657, 4,963,582, 4,855,317, 4,871,719, 4,874,749, 4,427,663, 4,310,519, 4,199,569, 5,055,596, 4,973,711, 4,978,677, 4,920,148, и в EP 0 667 054, все включены в настоящий текст посредством ссылки.
В одном варианте осуществления, ветеринарные композиции по настоящему изобретению содержат эффективное количество по меньшей мере одного из следующих веществ: абамектин, димадектин, дорамектин, эмамектин, эприномектин, ивермектин, латидектин, лепимектин, селамектин, милбемектин, милбемицин D, милбемицин A3, милбемицин A4, милбемицин оксим, моксидектин и немадектин, или их комбинации. В другом варианте осуществления, в настоящем изобретении описана ветеринарная композиция, содержащая эффективное количество по меньшей мере одного из следующих веществ: абамектин, эмамектин, эприномектин, ивермектин, дорамектин и селамектин, или их комбинации. В другом варианте осуществления, который является особенно предпочтительным, ветеринарные композиции по настоящему изобретению содержат эффективное количество по меньшей мере одного из следующих веществ: ивермектин, эприномектин, милбемицин оксим или моксидектин, или их комбинации.
В другом варианте осуществления настоящего изобретения, описана композиция, содержащая соединение, имеющее формулу (I), в комбинации с классом акарицидов или инсектицидов, известных как регуляторы роста насекомых (IGR). Соединения, принадлежащие к данной группе, хорошо известны практикующим специалистам и представляют собой широкий спектр различных химических классов. Эти соединения работают посредством нарушения развития или роста насекомых-вредителей. Регуляторы роста насекомых описаны, например, в Патентах США 3,748,356, 3,818,047, 4,225,598, 4,798,837, 4,751,225, EP 0 179 022 или U.K. 2 140 010, а также в Патентах США 6,096,329 и 6,685,954 (все включены в настоящий текст посредством ссылки).
В одном варианте осуществления, композиции по настоящему изобретению могут включать IGR соединение, которое является мимиком ювенильного гормона или модулирует концентрацию ювенильных гормонов у насекомого. Примеры мимиков ювенильного гормона включают азадирахтин, диофенолан, феноксикарб, гидропрен, кинопрен, метопрен, пирипроксифен, тетрагидроазадирахтин и 4-хлор-2(2-хлор-2-метил-пропил)-5-(6-иод-3-пиридилметокси)пиридазин-3(2H)-он. В другом варианте осуществления, композиции по настоящему изобретению содержат соединение, имеющее формулу (I), в комбинации с метопреном или пирипроксифеном, и фармацевтически приемлемый носитель.
В другом варианте осуществления, композиции по настоящему изобретению включают IGR соединение, которое представляет собой ингибитор синтеза хитина. Ингибиторы синтеза хитина включают хлорфлуазурон, циромазин, дифлубензурон, флуазурон, флуциклоксурон, флуфеноксурон, гексафлуморон, луфенурон, тебуфенозид, тефлубензурон, трифлумурон, 1-(2,6-дифторбензоил)-3-(2-фтор-4-(трифторметил)-фенилмочевину, 1-(2,6-дифтор-бензоил)-3-(2-фтор-4-(1,1,2,2-тетрафторэтокси)-фенилмочевину и 1-(2,6-дифторбензоил)-3-(2-фтор-4-трифторметил)фенилмочевину.
В некоторых вариантах осуществления, композиции по настоящему изобретению могут включать один или больше противонематодных средств, включая (но не ограничиваясь только ими) действующие вещества из классов бензимидазолов, имидазотиазолов, тетрагидропиримидинов и органических фосфатов. В некоторых вариантах осуществления, в композиции могут входить бензимидазолы, включая (но не ограничиваясь только ими) тиабендазол, камбендазол, парбендазол, оксибендазол, мебендазол, флубендазол, фенбендазол, оксфендазол, албендазол, циклобендазол, фебантел, тиофанат и его o,o-диметильные аналоги.
В других вариантах осуществления, композиции могут включать имидазотиазольные соединения, включая (но не ограничиваясь только ими) тетрамизол, левамизол и бутамизол.
В других вариантах осуществления, композиции по настоящему изобретению могут включать тетрагидропиримидиновые активные соединения, включая (но не ограничиваясь только ими) пирантел, оксантел и морантел.
Подходящие органофосфатные активные соединения включают (но не ограничиваются только ими) кумафос, трихлорфон, галоксон, нафталофос и дихлорфос, гептенофос, мевинфос, монокротофос, тетраэтилпирофосфат и тетрахлорвинфос.
В других вариантах осуществления, композиции могут включать противонематодные соединения фенотиазин, пиперазин в виде нейтральных соединений и в виде различных солей, диэтилкарбамазин, фенолы, такие как дисофенол, соединения мышьяка, такие как арсенид, этаноламины, такие как бефений, тений клозилат и метиридин; цианиновые красители, включая пирвиний хлорид, пирвиний памоат и дитиазанин иодид, изотиоцианаты, включая битосканат, сурамин натрий, фталофин, и различные природные вещества, включая (но не ограничиваясь только ими), гигромицин B, α-сантонин и каиновую кислоту.
В других вариантах осуществления, композиции по настоящему изобретению могут включать противотрематодозные средства. Подходящие противотрематодозные средства включают (но не ограничиваются только ими) мирацилы, такие как мирацил D и мирасан, празиквантел, клоназепам и его 3-метильное производное, олтипраз, лукантон, гикантон, оксамнихин, амосканат, ниридазол, нитроксинил, различные бисфенольные соединения, известные в данной области техники, включая гексахлорофен, битионол, битионол сульфоксид и менихлофолан; различные салициланилидные соединения, включая трибромсалан, оксиклозанид, клиоксанид, рафоксанид, бротианид, бромоксанид и клосантел; триклабендазол, диамфенетид, клорсулон, гетолин и эметин.
В композиции по настоящему изобретению также могут с пользой применяться противоцестодозные средства, включая (но не ограничиваясь только ими) ареколин в виде различных солей, бунамидин, никлозамид, нитросканат, паромомицин, паромомицин II и празиквантел. В особенно предпочтительном варианте осуществления, композиции по настоящему изобретению могут содержать празиквантел.
В других вариантах осуществления, композиции по настоящему изобретению могут включать другие активные средства, эффективные против членистоногих паразитов. Подходящие активные средства включают (но не ограничиваются только ими) бромциклен, хлордан, ДДТ, эндосульфан, линдан, метоксихлор, токсафен, бромофос, бромофос-этил, карбофенотион, хлорфенвинфос, хлорпирифос, кротоксифос, цитиоат, диазинон, дихлорентион, диэмтоат, диоксатион, этион, фамфур, фенитротион, фентион, фосфпират, иодофенфос, малатион, налед, фосалон, фосмет, фоксим, пропетамфос, роннел, стирофос, бензилбензоат, дисульфид углерода, кротамитон, дифлубензурон, дифениламин, дисульфирам, изоборнилтиоцианатоацетат, моносульфирам, пиренонилбутоксид, ротенон, трифенилолова ацетат, трифенилолова гидроксид, ДЭТА, диметилфталат и соединения 1,5a,6,9,9a,9b-гексагидро-4a(4H)-дибензофуранкарбоксальдегид (MGK-11), 2-(2-этилгексил)-3a,4,7,7a-тетрагидро-4,7-метано-1H-изоиндол-1,3(2H)дион (MGK-264), дипропил-2,5-пиридиндикарбоксилат (MGK-326) и 2-(октилтио)этанол (MGK-874).
В другом варианте осуществления настоящего изобретения, в композицию по настоящему изобретению можно также добавлять инсектициды и акарициды, поражающие взрослых особей. Они включают пиретрины (которые включают цинерин I, цинерин II, жасмолин I, жасмолин II, пиретрин I, пиретрин II и их смеси) и синтетические пиретроиды. Пиретроиды представляют собой синтетические аналоги пиретринов с повышенной активностью и устойчивостью. Пиретроиды, которые можно применять в композициях по настоящему изобретению, включают (но не ограничиваются только ими) перметрин, альфа-циперметрин, цифлутрин, бета-цифлутрин, цигалотрин, циперметрин, цифенотрин, дельтаметрин, фенвалерат, флуцитринат, флуметрин, тау-флувалинат, аллетрин, биоаллетрин, фенотрин, ресметрин, тетраметрин, трансфлутрин и этофенпрокс.
Карбаматные инсектициды, которые можно применять в композициях по настоящему изобретению, включают (но не ограничиваются только ими) беномил, карбанолат, карбарил, карбофуран, метиокарб, метолкарб, промацил, пропоксур, алдикарб, бутокарбоксим, оксамил, тиокарбоксим и тиофанокс.
В другом варианте осуществления, антипаразитарным средством, которое можно включать в ветеринарную композицию, содержащую соединение, имеющее формулу (I), может быть биологически активный пептид или белок, включая (но не ограничиваясь только ими) депсипептиды, отличные от соединений, имеющих формулу (I). Они включают PF1022A или его аналоги, и эмодепсид. Эти соединения работают в нейромышечном соединении посредством стимулирования пресинаптических рецепторов, принадлежащих к семейству секретиновых рецепторов, что приводит к параличу и смерти паразитов. В одном варианте депсипептида, депсепептид представляет собой эмодепсид (смотри Willson et al., Parasitology, Jan. 2003, 126(Pt 1):79-86).
В другом варианте осуществления, композиции по настоящему изобретению могут содержать действующее вещество из неоникотиноидного класса паразитицидов. Неоникотиноиды связываются и ингибируют специфические для насекомых никотиновые ацетилхолиновые рецепторы. В одном варианте осуществления, неоникотиноидным инсектицидом, который можно комбинировать с соединением, имеющим формулу (I), в композиции по настоящему изобретению является имидаклоприд. Средства из данного класса описаны, например, в Патенте США 4,742,060 или в EP 0 892 060 (оба включены в настоящий текст посредством ссылки). В другом варианте осуществления, композиции по настоящему изобретению могут содержать нитенпирам, другое действующее вещество из неоникотиноидного класса пестицидов. Применение нитенпирама для борьбы с блохами описано в Патенте США 5,750,548, который включен в настоящий текст в полном объеме посредством ссылки.
В некоторых других вариантах осуществления настоящего изобретения, циклические депсипептиды, имеющие формулу (I), можно комбинировать с композициями по настоящему изобретению, содержащими семикарбазон, такой как метафлумизон.
В другом варианте осуществления, композиции по настоящему изобретению могут содержать одно или больше других изоксазолиновых соединений, известных в данной области, включая (но не ограничиваясь только ими) афоксоланер, сароланер, лотиланер и флураланер. Этот класс действующих веществ описан в US7,964,204, US 8410153, WO 2014/036056, US 2010/0254960 A1, US2011/0159107, US2012/0309620, US2012/0030841, US2010/0069247, WO 2007/125984, WO 2012/086462, US 8318757, US 8466115, US 8618126, US 8822466, US8383659, US8853186, US 2011/0144349, US 8,053,452; US 8952175, US 2010/0254959, US 2011/152081, WO 2007/075459 и US 2009/0133319, WO 2009/025983 и US 8513431, WO 2009/003075 и US 2010/0173948, WO 2008/150393, WO 2008/154528 и US 8623875, WO 2010/003877 и US 8597688, WO 2010/003923 и US 8563474, WO 2009/045999 и US 8367584, WO 2009/126668 и US 8546618, WO 2009/051956, WO 2012/089623, WO 2012/089622, US 8,119,671; US 7,947,715; WO 2102/120135, WO 2012/107533, WO 2011/157748, US 2011/0245274, US 2011/0245239, US 2012/0232026, US 2012/0077765, US 2012/0035122, US 2011/0251247, WO 2011/154433, WO 2011/154434, US 2012/0238517, US 2011/0166193, WO 2011/104088, WO 2011/104087, WO 2011/104089, US 2012/015946, US 2009/0143410, WO 2007/123855 A2, US 2011/0118212, US7951828 & US7662972, US 2010/0137372 A1, US 2010/0179194 A2, US 2011/0086886 A2, US 2011/0059988 A1, US 2010/0179195 A1, US 7897630, и U.S. 7951828, которые все включены в настоящий текст в полном объеме посредством ссылки.
В другом варианте осуществления настоящего изобретения, в композиции по настоящему изобретению можно добавлять нодулиспоровую кислоту и ее производные. Данные соединения применяются для лечения или профилактики инфекций у человека и животных и описаны, например, в Патенте США № 5,399,582, 5,962,499, 6,221,894 и 6,399,786, которые все включены в текст настоящего изобретения посредством ссылки во всем своем объеме. Композиции могут включать одно или больше известных в данной области производных нодулиспоровой кислоты, включая все стереоизомеры, такие как описанные в процитированных выше литературных источниках.
В другом варианте осуществления, в композиции по настоящему изобретению можно добавлять противогельминтные соединения из класса аминоацетонитрилов (AAD), такие как монепантел (ZOLVIX) и т.п. Данные соединения описаны, например, в Патенте США 7,084,280, выданном Ducray с соавторами (включен в настоящий текст посредством ссылки); Sager et al., Veterinary Parasitology, 2009, 159, 49-54; Kaminsky et al., Nature vol. 452, 13 March 2008, 176-181.
Композиции по настоящему изобретению могут также включать арилоазол-2-ил цианоэтиламиновые соединения, такие как описанные в Патенте США 8,088,801, выданном Soll с соавторами, который включен в настоящий текст посредством ссылки, и тиоамидные производные данных соединений, как описано в Патенте США 7,964,621, выданном Le Hir de Fallois, который также включен в настоящий текст посредством ссылки.
Композиции по настоящему изобретению могут также включать парагерквамиды и производные этих соединений, включая дерквантел (см. Ostlind et al., Research in Veterinary Science, 1990, 48, 260-61; и Ostlind et al., Medical and Veterinary Entomology, 1997, 11, 407-408). Семейство парагерквамидных соединений является известным классом соединений, которые содержат спиродиоксепиноиндольное ядро, обладающее активностью в отношении определенных паразитов (см. Tet. Lett. 1981, 22, 135; J. Antibiotics 1990, 43, 1380, и J. Antibiotics 1991, 44, 492). Кроме того, структурно родственное семейство маркфортинов, таких как маркфортины A-C, также известно и может комбинироваться с препаратами по настоящему изобретению (см. J. Chem. Soc. - Chem. Comm. 1980, 601 и Tet. Lett. 1981, 22, 1977). Дополнительную информацию по производным парагерквамидов можно найти, например, в WO 91/09961, WO 92/22555, WO 97/03988, WO 01/076370, WO 09/004432 и US 2010/0197624, Патенте США 5,703,078 и Патенте США 5,750,695, которые все включены в настоящий текст в полном объеме посредством ссылки.
В другом варианте осуществления настоящего изобретения, композиции могут включать спинозиновое действующее вещество, вырабатываемое почвенным актиномицетом Saccharopolyspora spinosa (см., например, Salgado V.L. and Sparks T.C., “The Spinosyns: Chemistry, Biochemistry, Mode of Action, and Resistance,” в Comprehensive Molecular Insect Science, vol. 6, pp. 137-173, 2005) или полусинтетическое спинозиновое действующее вещество. Спинозины обычно называют факторами или компонентами A, B, C, D, E, F, G, H, J, K, L, M, N, О, P, Q, R, S, T, U, V, W или Y, и любой из этих компонентов или их комбинация могут применяться в композициях по настоящему изобретению. Спинозиновое соединение может представлять собой 5,6,5-трициклическую кольцевую систему, сконденсированную с 12-членным макроциклическим лактоном, нейтральным сахаром (рамноза) и аминосахаром (форосамин). Эти и другие природные спинозиновые соединения, включая 21-бутенил спинозин, вырабатываемый Saccharopolyspora pagona, которые можно применять в композициях по настоящему изобретению, можно получить ферментацией согласно известным в данной области методикам. Другие спинозиновые соединения, которые можно применять в композициях по настоящему изобретению, описаны в Патентах США 5,496,931; 5,670,364; 5,591,606; 5,571,901; 5,202,242; 5,767,253; 5,840,861; 5,670,486; 5,631,155 и 6,001,981, которые все включены в настоящий текст в полном объеме посредством ссылки. Спинозиновые соединения могут включать (но не ограничиваются только ими) спинозин A, спинозин D, спиносад, спинеторам или их комбинации. Спиносад представляет собой комбинацию спинозина A и спинозина D, и спинеторам представляет собой комбинацию 3’-этокси-5,6-дигидро спинозина J и 3’-этокси спинозина L.
В целом, дополнительные действующие вещества (отличные от соединения, имеющего описанную выше формулу (I)) включают в дозированные лекарственные формы по настоящему изобретению в количестве от примерно 0.1 мкг до примерно 1000 мг. В типичном случае, действующее вещество можно включать в количестве от примерно 10 мкг до примерно 500 мг, от примерно 10 мкг до примерно 400 мг, от примерно 1 мг до примерно 300 мг, от примерно 10 мг до примерно 200 мг, или от примерно 10 мг до примерно 100 мг. В более типичном случае дополнительное действующее вещество присутствует в композициях по настоящему изобретению в количестве от примерно 5 мг до примерно 50 мг.
Концентрация дополнительного действующего вещества в композициях по настоящему изобретению в типичном случае составляет от примерно 0.01% до примерно 30% (вес/вес), в зависимости от активности действующего вещества. В некоторых вариантах осуществления для очень активных действующих веществ, включая (но не ограничиваясь только ими) макроциклические лактоны, концентрация действующего вещества в типичном случае составляет от примерно 0.01% до примерно 10% (вес/вес), от примерно 0.01 до примерно 1% (вес/вес), от примерно 0.01% до примерно 0.5% (вес/вес), от примерно 0.1% до примерно 0.5% (вес/вес), или от примерно 0.01% до примерно 0.1% (вес/вес). В других вариантах осуществления, концентрация действующего вещества в типичном случае составляет от примерно 0.1% до примерно 2% (вес/вес), или от примерно 0.1% до примерно 1% (вес/вес).
В других вариантах осуществления, дополнительное действующее вещество в типичном случае присутствует в более высоких концентрациях, для достижения целевой эффективности. В некоторых вариантах осуществления, действующее вещество присутствует в концентрации от примерно 1% до примерно 30% (вес/вес), от примерно 1% до примерно 20% (вес/вес), или от примерно 1% до примерно 15% (вес/вес). В других вариантах осуществления, действующее вещество присутствует в композиции в концентрации от примерно 5% до примерно 20% (вес/вес), или от примерно 5% до примерно 15% (вес/вес).
В различных вариантах осуществления настоящего изобретения, дополнительное действующее вещество может входить в состав композиция в таком количестве, чтобы обеспечить введение дозы от примерно 0.001 мг/кг до примерно 50 мг/кг, или от примерно 0.5 мг/кг до примерно 50 мг/кг веса тела животного. В других вариантах осуществления, действующее вещество в типичном случае присутствует в количестве, достаточном для создания дозы от примерно 0.05 мг/кг до примерно 30 мг/кг, от примерно 0.1 мг/кг до примерно 20 мг/кг. В других вариантах осуществления, действующее вещество присутствует в количестве, достаточном для создания дозы от примерно 0.1 мг/кг до примерно 10 мг/кг, от примерно 0.1 мг/кг до примерно 1 мг/кг, или от примерно 0.5 мг/кг до примерно 50 мг/кг веса тела животного.
В некоторых вариантах осуществления настоящего изобретения, когда дополнительное действующее вещество представляет собой очень активное соединение, такое как макроциклический лактон или другие активные соединения, действующее вещество присутствует в концентрации, достаточной для создания дозы от примерно 0.001 мг/кг до примерно 5 мг/кг, от примерно 0.001 мг/кг до примерно 0.1 мг/кг, или от примерно 0.001 мг/кг до примерно 0.01 мг/кг. В других вариантах осуществления, действующее вещество присутствует в концентрации, достаточной для создания дозы от примерно 0.01 мг/кг до примерно 2 мг/кг или от примерно 0.1 мг/кг до примерно 1 мг/кг веса тела животного. В других вариантах осуществления, дополнительное действующее вещество присутствует в количестве, достаточном для создания дозы от примерно 1 мкг/кг до примерно 200 мкг/кг, или от примерно 0.1 мг/кг до примерно 1 мг/кг веса животного.
В дополнение к указанным выше другим действующим веществам, можно применять комбинации двух или больше действующих веществ с соединениями по настоящему изобретению в композиции для лечения от целевого спектра вредителей и паразитов. Решение о том, какое конкретное соединение можно применять в инновационных препаратах для лечения конкретного заражения насекомыми, находится в рамках компетенции специалиста, реализующего настоящее изобретение на практике.
Настоящее изобретение далее описано подробнее с привлечением частных неограничивающих примеров.
Примеры
В приведенных ниже Примерах используются следующие сокращения:
DAST: трифторид диэтиламиносеры;
DCC: N,N’-дициклогексилкарбодиимид;
DMAP: 4-диметиламинопиридин;
DIEA: диизопропилэтиламин;
HOBt: гидроксибензотриазол;
rt: комнатная температура;
LiHMDS: бис(триметилсилил)амид лития;
TBAF: тетрабутиламмония фторид;
TBDMSCl: трет-бутилдиметилсилил хлорид;
4A-MS: молекулярные сита с размером пор 4 ангстрема;
DEAD: диэтилазодикарбоксилат;
BOP-Cl: бис(2-оксо-3-оксазолидинил)фосфин хлорид;
MS: масс-спектрометрия;
ESI: ионизация методом электроспрея;
X-phos: 2-дициклогексилфосфино-2′,4′,6′-триизопропилбифенил;
XantPhos: 4,5-бис(дифенилфосфино)-9,9-диметилксантен;
AD-mix альфа: коммерчески доступная смесь гексацианоферрата(II) калия, карбоната калия, тетрагидроксодиоксоосмата(VI) калия и хирального лиганда (DHQ)2-PHAL на основе фталазина и дигидрохинона;
ТФУК: трифторуксусная кислота;
ДХМ: дихлорметан.
Примеры получения
Приведенные ниже примеры получения являются неограничивающими примерами способов, применявшихся для получения соединений по настоящему изобретению. 4-Фтор-N-метиллейцин, защищенный трет-бутилоксикарбонильной группой (BOC), изображенный ниже, используется в получении соединений по настоящему изобретению, содержащих -CH2C(CH3)2F группу в положениях, соответствующих - R1, R2, R3 или R4.
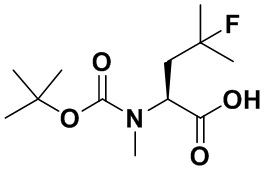
Это соединение получают по стандартным методикам из коммерчески доступного 4-фторлейцина (Chemical Abstracts Registry Number 857026-04-1). Следует понимать, что другие группы R1 - R4 могут также быть получены из различных аналогов лейцина аналогичным образом. Например, 3-фторлейцин (Chemical Abstracts Registry No. 171077-98-8, например, см. Kaneko et al., Chem. Pharm Bull., 1995, 43(5), 760-765) и 5-фторлейцин (Chemical Abstracts Registry No. 159415-71-1, см. Moody et al., Tett. Lett., 1994, 35(30), 5485-8) также известны и могут использоваться для получения соединений, в которых R1 - R4 представляют собой различным образом замещенные остатки фторлейцина. Кроме того, следует понимать, что могут также применяться альтернативные аминокислоты с различными боковыми цепочками для получения альтернативных соединений по настоящему изобретению.
N-BOC-L-3-циклопропилаланин, изображенный ниже, также используется в получении некоторых соединений по настоящему изобретению, где R1, R2, R3 или R4 представляют собой C1. Это соединение известно (CAS 89483-06-7) и коммерчески доступно в виде дициклогексиламиновой соли.
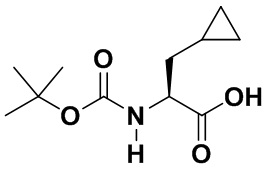
Бензил (R)-2-гидрокси-3-(4-морфолинофенил)пропаноат, изображенный ниже, также применяется в получении некоторых соединений по настоящему изобретению. Это соединение известно, и его получение описано, например, в работе Scherkenbeck et al., Eur. J. Org. Chem. 2012, 1546-1553.
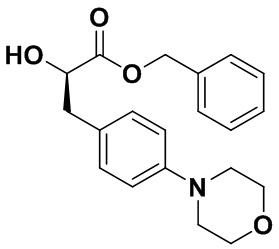
Сходным образом, изображенное ниже соединение применяется в получении соединений по настоящему изобретению. Это соединение известно и описано, например, в работе Dutton et al., J. Antibiotics 1994, 47(11), 1322-1327, помимо других источников.
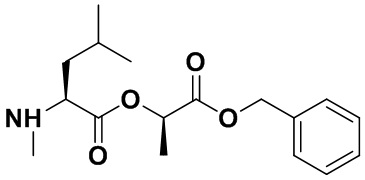
Как показано выше на Схеме 1, получение соединений по настоящему изобретению осуществляют циклизацией прекурсора 1-7 после снятия защиты с терминальной амино-группы и карбоксильной группы. Квалифицированным специалистам в данной области будет понятно, что при использовании общего способа, изображенного на Схеме 1, можно получить широкий ряд разнообразных соединений по настоящему изобретению, выбирая подходящие мономерные исходные вещества с желаемыми группами R1, R2, R3, R4, Cy1 и Cy2, и получая димеры с общими формулами 1-1, 1-2, 1-3 и 1-4 путем снятия защитных групп с подходящих карбоксильных групп и амино-групп и формирования амида.
На изображенных ниже Примерах получения 1-16 приведены способы получения различных мономерных соединений M1 - M16, замещенных широким рядом групп R1, R2, R3, R4, Cy1 и Cy2, что позволяет получать диверсифицированный набор димерных соединений, применяющихся для получения соединений по настоящему изобретению.
Пример синтеза 1: Получение мономера M1.
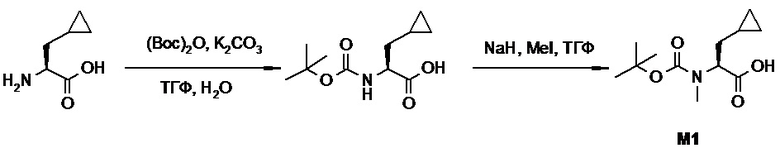
Подробное описание эксперимента
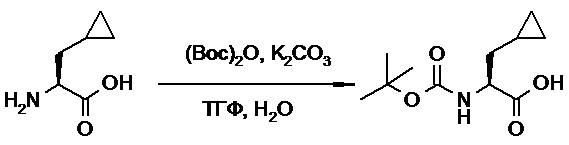
(2S)-2-[[(трет-бутокси)карбонил]амино]-3-циклопропилпропановая кислота: В 3-горлую круглодонную колбу объемом 1000 мл помещали (2S)-2-амино-3-циклопропилпропановую кислоту (10 г, 77.43 ммоль, 1.00 экв.), тетрагидрофуран (120 мл), воду (120 мл), карбонат калия (36.7 г, 265.54 ммоль, 3.40 экв.). После этого добавляли ди-трет-бутил дикарбонат (21.9 г, 100.35 ммоль, 0.80 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение в течение ночи при комнатной температуре. Полученный раствор экстрагировали 2x60 мл эфира, и органические слои объединяли. Значение pH раствора доводили до 3 с помощью лимонной кислоты (2 ммоль/л). Результирующий раствор экстрагировали 3x100 мл дихлорметана, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 17.2 г (97%) (2S)-2-[[(трет-бутокси)карбонил]амино]-3-циклопропилпропановой кислоты в виде бесцветного масла. MS (ESI, m/z): 228 (M-H).
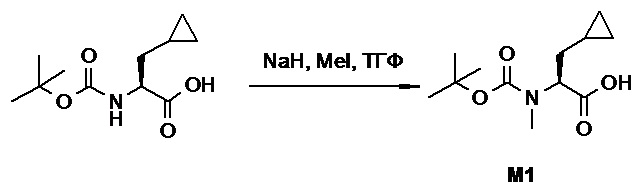
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановая кислота (M1): В 3-горлую круглодонную колбу объемом 1000 мл помещали (2S)-2-[[(трет-бутокси) карбонил]амино]-3-циклопропилпропановую кислоту (8 г, 34.89 ммоль, 1.00 экв.), тетрагидрофуран (450 мл). После этого добавляли гидрид натрия (2.8 г, 83.33 ммоль, 3.00 экв.) по каплям при перемешивании при 0°C. В полученную смесь добавляли CH3I (40 г, 281.81 ммоль, 8.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1.5 ч при комнатной температуре. Результирующий раствор оставляли для прохождения реакции, при перемешивании, на ночь при комнатной температуре. Затем реакцию гасили добавлением 100 мл смеси вода/лед. Результирующий раствор экстрагировали 2x100 мл МТБЭ, и водные слои объединяли. Значение pH раствора доводили до 4 с помощью лимонной кислоты (2 моль/л). Результирующий раствор экстрагировали 3x200 мл этилацетата, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 6 г (71%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановой кислоты в виде желтого масла. MS (ESI, m/z): 242 (M-H);
1H ЯМР (ДМСО, 300 МГц) δ: 12.59 (ушир.с, 1 H), 4.55-4.29 (м, 1 H), 3.31 (с, 3 H), 1.90-1.51 (м, 2 H), 1.47-1.41 (м, 9 H), 0.70-0.50 (м, 1 H), 0.50-0.30 (м, 2 H), 0.20-0.00 (м, 2 H).
Пример синтеза 2: Получение мономера M2.

Подробное описание эксперимента
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-2-циклопропилуксусная кислота (M2): В 3-горлую круглодонную колбу объемом 250 мл помещали (2S)-2-[[(трет-бутокси)карбонил] амино]-2-циклопропилуксусную кислоту (5 г, 23.23 ммоль, 1.00 экв.), тетрагидрофуран (120 мл). После этого добавляли гидрид натрия (1 г, 41.67 ммоль, 3.00 экв.) порциями при 0°C. В полученную смесь добавляли CH3I (16 г, 112.72 ммоль, 8.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Затем реакцию гасили добавлением 20 мл смеси вода/лед. Результирующий раствор экстрагировали 2x30 мл МТБЭ, и водные слои объединяли. Значение pH водной фазы доводили до 4 с помощью лимонной кислоты. Результирующий раствор экстрагировали 3x80 мл этилацетата, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 3.4 г (64%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-2-циклопропилуксусной кислоты в виде желтого масла. MS (ESI, m/z): 228 (M-H).
Пример синтеза 3: Получение мономера M3.
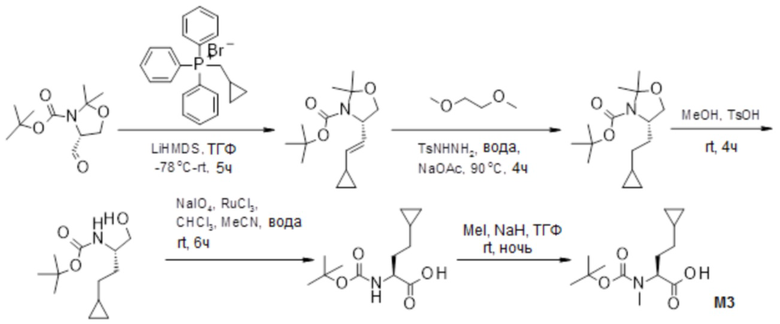
Подробное описание эксперимента
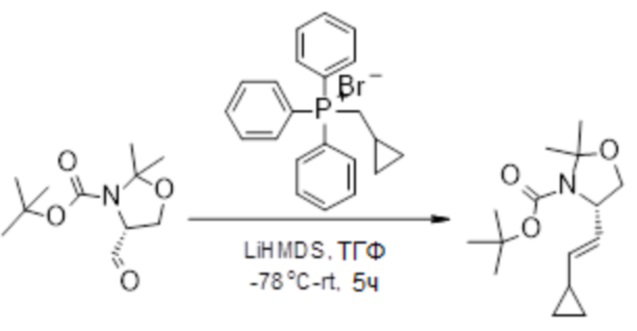
Трет-бутил (4S)-4-[(E)-2-циклопропилэтенил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат: В 3-горлую круглодонную колбу объемом 500 мл помещали тетрагидрофуран (105 мл) в атмосфере азота, (циклопропилметил)трифенилфосфоний (9.1 г, 28.67 ммоль, 1.50 экв.). После этого добавляли LiHMDS (1M) (23 мл, 23 ммоль, 1.50 экв.) по каплям при перемешивании при -78°C. Полученный оранжевый раствор нагревали до комнатной температуры на 1 час, затем охлаждали до -78°C. В описанный выше раствор добавляли раствор трет-бутил (4R)-4-формил-2,2-диметил-1,3-оксазолидин-3-карбоксилата (3.5 г, 15.27 ммоль, 1.00 экв.) в ТГФ (20 мл). Результирующий раствор перемешивали в течение 5 ч при комнатной температуре. Полученный раствор гасили добавлением 105 мл метанола. Результирующий раствор упаривали в вакууме. Остаток растворяли в 200 мл этилацетата и 200 мл воды. Органическую фазу отделяли. Водный раствор экстрагировали 2x200 мл этилацетата, органические слои объединяли и сушили над сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:10). В результате получали 2.3 г (56%) трет-бутил (4S)-4-[(E)-2-циклопропилэтенил]-2,2-диметил-1,3-оксазолидин-3-карбоксилата в виде светло-желтого масла. MS (ESI, m/z): 268 (M+H).
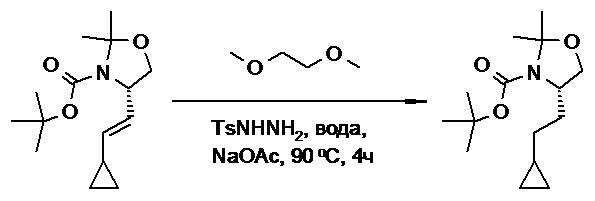
Трет-бутил (4S)-4-(2-циклопропилэтил)-2,2-диметил-1,3-оксазолидин-3-карбоксилат: В 3-горлую круглодонную колбу объемом 1000 мл помещали трет-бутил (4S)-4-[(E)-2-циклопропилэтенил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат (4.5 г, 16.83 ммоль, 1.00 экв.) и Tos-NH-NH2 (31.5 г, 168.3 ммоль, 10.00 экв.) в диметиловом эфире этиленгликоля (150 мл). Смесь нагревали до 90°C и добавляли по каплям раствор NaOAc (39.4 г, 504.9 ммоль, 30.00 экв.) в воде (400 мл). Результирующий раствор перемешивали в течение 4 ч при 90°C. После добавления, реакционную смесь охлаждали до комнатной температуры и экстрагировали 3x200 мл этилацетата, органические слои объединяли. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:7). В результате получали 1.9 г (42%) трет-бутил (4S)-4-(2-циклопропилэтил)-2,2-диметил-1,3-оксазолидин-3-карбоксилата в виде желтого масла. MS (ESI, m/z): 270 (M+H).
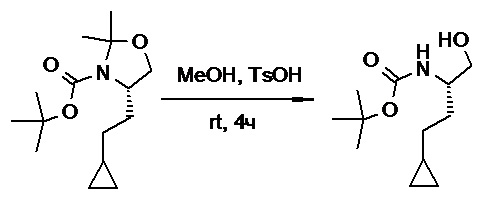
Трет-бутил N-[(2S)-4-циклопропил-1-гидроксибутан-2-ил]карбамат: В круглодонную колбу объемом 100 мл помещали трет-бутил (4S)-4-(2-циклопропилэтил)-2,2-диметил-1,3-оксазолидин-3-карбоксилат (1.7 г, 6.31 ммоль, 1.00 экв.), метанол (34 мл), TsOH (119 мг, 0.69 ммоль, 0.11 экв.). Результирующий раствор перемешивали в течение 4 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт (2.0 г) очищали методом флэш-препаративной ВЭЖХ в следующих условиях (CombiFlash-1): Колонка, С18 силикагель; подвижная фаза, CH3CN:H2O=30/70 с повышением до CH3CN:H2O=100:0 в течение 40 мин; Детектор, УФ 220 нм. В результате получали 1.4 г (97%) трет-бутил N-[(2S)-4-циклопропил-1-гидроксибутан-2-ил]карбамата в виде желтого масла. MS (ESI, m/z): 230 (M+H).
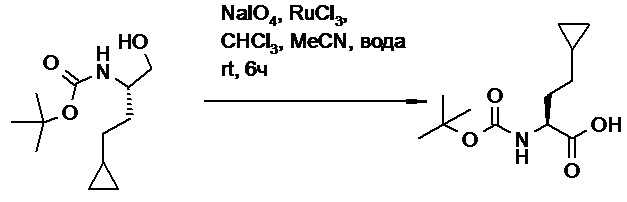
(2S)-2-[[(трет-бутокси)карбонил]амино]-4-циклопропилбутановая кислота: В 3-горлую круглодонную колбу объемом 500 мл помещали трет-бутил N-[(2S)-4-циклопропил-1-гидроксибутан-2-ил]карбамат (1.2 г, 5.23 ммоль, 1.00 экв.), хлороформ (24 мл), воду (36 мл), CH3CN (24 мл), RuCl3 (324 мг, 1.57 ммоль, 0.30 экв.), NaIO4 (5.6 г, 5.00 экв.). Результирующий раствор перемешивали в течение 6 ч при комнатной температуре. Затем реакцию гасили добавлением 500 мл NaS2O3 (насыщенный раствор). Результирующий раствор экстрагировали 300 мл МТБЭ и водные слои объединяли. Значение pH водной фазы доводили до 4 с помощью лимонной кислоты. Результирующий раствор экстрагировали 3x300 мл этилацетата, органические слои объединяли и сушили над сульфатом натрия и упаривали в вакууме. В результате получали 2.4 г (сырой) (2S)-2-[[(трет-бутокси)карбонил] амино]-4-циклопропилбутановой кислоты в виде черного масла. MS (ESI, m/z): 244 (M+H).
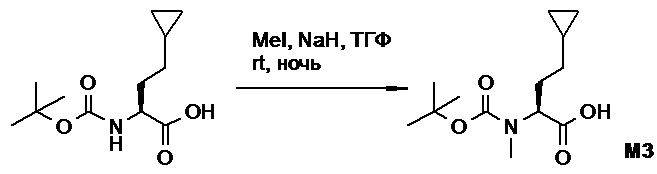
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-циклопропилбутановая кислота (M3): В 3-горлую круглодонную колбу объемом 250 мл помещали тетрагидрофуран (100 мл), (2S)-2-[[(трет-бутокси)карбонил]амино]-4-циклопропилбутановую кислоту (2.4 г, 9.86 ммоль, 1.00 экв.). После этого добавляли гидрид натрия (2.37 г, 98.75 ммоль, 10.00 экв.) порциями при 0°C. Результирующий раствор перемешивали 1 ч при 0°C. В полученную смесь добавляли CH3I (14 г, 98.63 ммоль, 10.00 экв.) по каплям при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Затем реакцию гасили добавлением 200 мл смеси вода/лед. Полученный раствор экстрагировали 200 мл МТБЭ и водные слои объединяли. Значение pH водной фазы доводили до 4 с помощью лимонной кислоты. Результирующий раствор экстрагировали 3x200 мл этилацетата, органические слои объединяли и сушили над сульфатом натрия и упаривали в вакууме. В результате получали 1.5 г (59%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-циклопропилбутановой кислоты в виде желтого масла. MS (ESI, m/z): 258 (M+H).
Пример синтеза 4: Получение мономера M4.

Подробное описание эксперимента
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклобутилпропановая кислота (M4): В круглодонную колбу объемом 50 мл помещали тетрагидрофуран (200 мл), (2S)-2-[[(трет-бутокси)карбонил]амино]-3-циклобутилпропановую кислоту (2 г, 8.22 ммоль, 1.00 экв.), CH3I (24 г, 169.09 ммоль, 20.57 экв.), гидрид натрия (6.6 г, 275.00 ммоль, 33.45 экв.). Результирующий раствор перемешивали в течение ночи при 38°C. Затем реакцию гасили добавлением смеси вода/лед. Значение pH раствора доводили до 4 хлороводородом (2 моль/л). Результирующий раствор экстрагировали 3x20 мл этилацетата, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 1.8 г (85%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклобутилпропановой кислоты в виде бесцветного масла. MS (ESI, m/z): 258 (M+H).
Пример синтеза 5: Получение мономера M5.
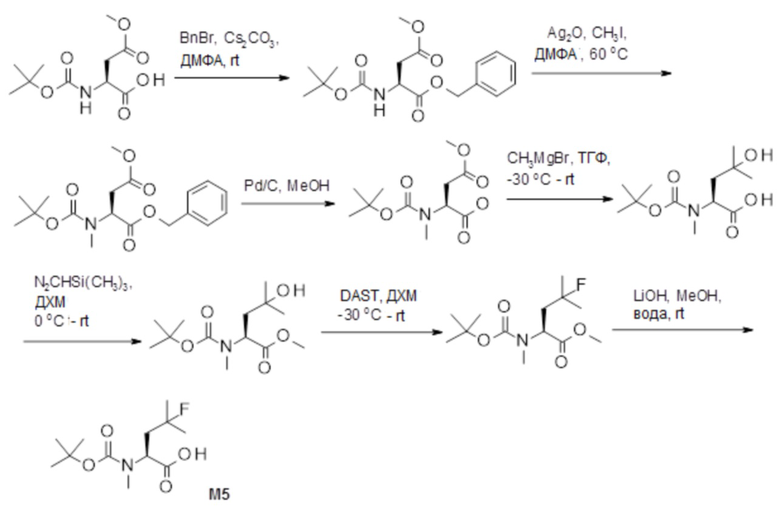
Подробное описание эксперимента
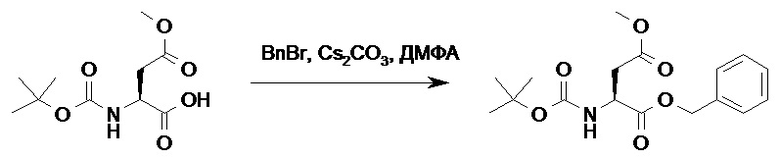
1-Бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил]амино]бутандиоат: В 20-литровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор (2S)-2-[[(трет-бутокси)карбонил]амино]-4-метокси-4-оксобутановой кислоты (150 г, 606.69 ммоль, 1.00 экв.) в N,N-диметилформамиде (5 л), Cs2CO3 (396 г, 1.22 моль, 2.00 экв.), BnBr (124 г, 725.02 ммоль, 1.20 экв.). Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Полученный раствор разбавляли 10 л этилацетата. Полученную смесь промывали 3x5 л H2O. Полученную смесь промывали 3x5 л насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 170 г (83%) 1-бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил]амино]бутандиоата в виде белого твердого вещества. MS (ESI, m/z): 338 (M+H).
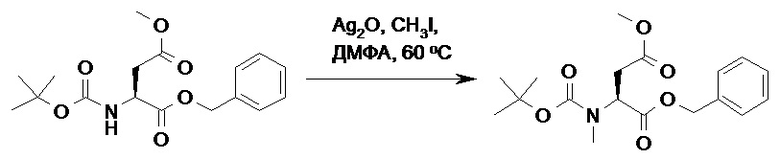
1-Бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]бутандиоат: В 10-литровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор 1-бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил]амино]бутандиоата (170 г, 503.90 ммоль, 1.00 экв.) в N,N-диметилформамиде (5 мл), Ag2O (348 г, 3.00 экв.), CH3I (1433 г, 10.10 моль, 20.00 экв.). Полученный раствор перемешивали в течение 1 часа при 60°C на масляной бане. Полученный раствор разбавляли 10 л этилацетата. Полученную смесь промывали 3x8 л H2O. Смесь промывали 3x8 л насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 159 г (90%) 1-бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]бутандиоата в виде желтого масла. MS (ESI, m/z): 352 (M+H).
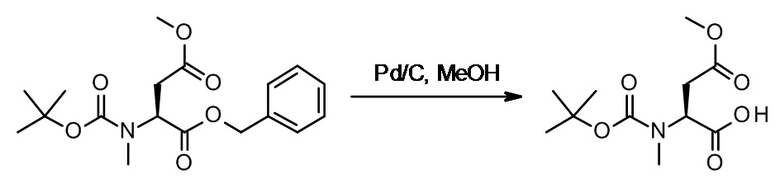
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метокси-4-оксобутановая кислота: В 10-литровую 3-горлую круглодонную колбу помещали раствор 1-бензил 4-метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]бутандиоата (159 г) в метаноле (3 л), палладий на угле (15.9 г, 0.10 экв.), H2 (газ) (достаточное количество). Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 115 г (97%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метокси-4-оксобутановой кислоты в виде желтого масла. MS (ESI, m/z): 262 (M+H).
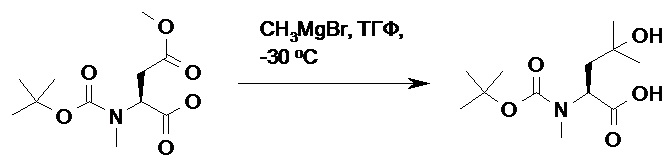
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-гидрокси-4-метилпентановая кислота: В 3-литровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метокси-4-оксобутановой кислоты (114 г) в тетрагидрофуране (4 л), CH3MgBr (874 мл, 6.00 экв.). Полученный раствор перемешивали в течение 3 часов при -30°C в охлаждающей бане. Затем реакцию гасили добавлением 1000 мл раствора NH4Cl/H2O. Значение pH раствора доводили до 3~4 добавлением раствора хлороводород/H2O. Полученный раствор разбавляли 6 л H2O. Полученный раствор экстрагировали 3x4 л этилацетата, органические слои объединяли. Полученную смесь промывали 2x5 л насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 90 г (сырой продукт) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-гидрокси-4-метилпентановой кислоты в виде желтого масла. MS (ESI, m/z): 262 (M+H).
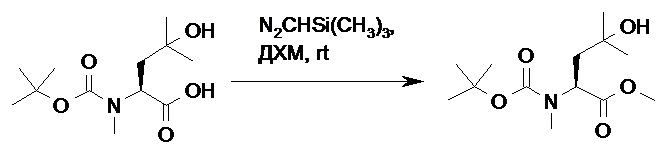
Метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-гидрокси-4-метилпентаноат: В 3-литровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-гидрокси-4-метилпентановой кислоты (90 г) в дихлорметане (4 л), (диазометил)триметилсилан (340 мл, 2.00 экв, 2M). Полученный раствор перемешивали в течение 2 часов при комнатной температуре в бане лед/соль. Полученную смесь промывали 2x3 л H2O. Смесь промывали 2x3 л насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 92 г (сырой продукт) метил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-гидрокси-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 276 (M+H).
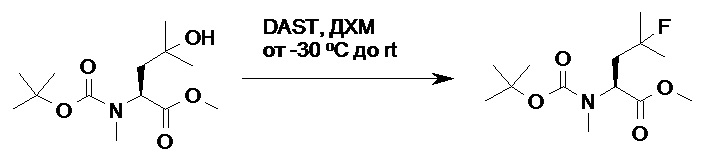
Метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат: В 3-литровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-гидрокси-4-метилпентаноата (90 г) в дихлорметане (3.0 л), DAST (106 г, 2.00 экв.). Полученный раствор перемешивали в течение 2 часов при -30°C в охлаждающей бане. Затем реакцию гасили добавлением 1 литра раствора NaHCO3 при 0°C. Полученную смесь промывали 2x1 л H2O. Смесь промывали 2x1 л насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:100~1:20). В результате получали 15 г (16%) метил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 278 (M+H).
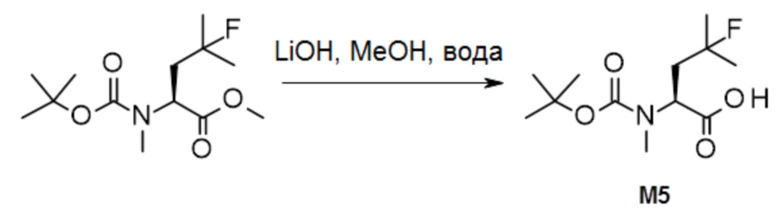
(S)-2-(трет-бутоксикарбонил(метил)амино)-4-фтор-4-метилпентановая кислота (M1): В 500-миллилитровую 3-горлую круглодонную колбу помещали раствор (S)-метил 2-(трет-бутоксикарбонил(метил)амино)-4-фтор-4-метилпентаноата (15 г) в MeOH (80 мл), LiOH (11.4 г, 5.00 экв.) в H2O (150 мл). Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Раствор экстрагировали 3x100 мл этилацетата. Значение pH водных слоев доводили до 3~4 добавлением раствора хлороводород/H2O. Полученный раствор экстрагировали 3x100 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 2x5 л насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 12.6 г (89%) (S)-2-(трет-бутоксикарбонил(метил)амино)-4-фтор-4-метилпентановой кислоты в виде желтого масла. MS (ESI, m/z): 264 (M+H).
Пример синтеза 6: Получение мономера M6.
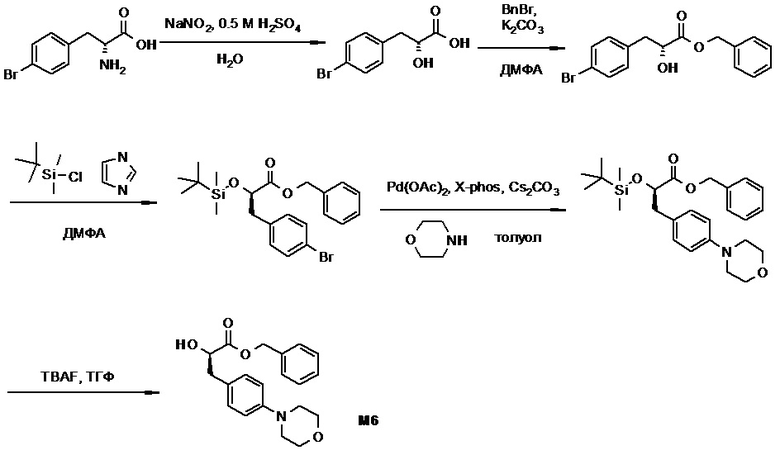
Подробное описание эксперимента
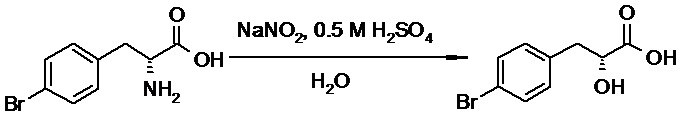
(2R)-3-(4-бромфенил)-2-гидроксипропановая кислота: В 2000-миллилитровую 4-горлую круглодонную колбу помещали (2R)-2-амино-3-(4-бромфенил)пропановую кислоту (150 г, 614.54 ммоль, 1.00 экв.), серную кислоту (0.5M/л) (2500 мл). Затем добавляли раствор NaNO2 (256 г, 3.71 моль, 6.00 экв.) в воде (900 мл) по каплям при перемешивании. Полученный раствор перемешивали в течение 48 часов при комнатной температуре. Твердый осадок отделяли фильтрованием. Полученное твердое вещество сушили в термошкафу при пониженном давлении. В результате получали 240 г (80%) (2R)3-(4-бромфенил)-2-гидроксипропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 243 (M-H); 1H ЯМР (ДМСО, 300 МГц) δ: 12.59 (ушир.с, 1 H), 7.51-7.44 (м, 2 H), 7.27-7.14 (м, 2 H), 5.34 (ушир.с, 1 H), 4.16-4.12 (м, 1 H), 2.97-2.91 (м, 1 H), 2.80-2.70 (м, 1 H).
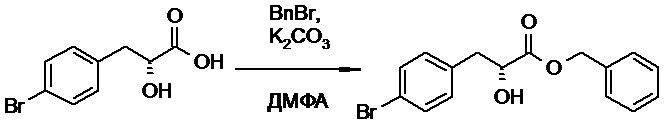
Бензил (2R)-3-(4-бромфенил)-2-гидроксипропаноат: В 2000-миллилитровую 4-горлую круглодонную колбу помещали (2R)-3-(4-бромфенил)-2-гидроксипропановую кислоту (60 г, 244.83 ммоль, 1.00 экв.), карбонат калия (67.6 г, 489.11 ммоль, 2.00 экв.), N,N-диметилформамид (1000 мл). Затем добавляли BnBr (50.3 г, 294.10 ммоль, 1.20 экв.) по каплям при перемешивании. Полученный раствор перемешивали в течение ночи при комнатной температуре. Полученный раствор разбавляли 2000 мл H2O. Полученный раствор экстрагировали 3x500 мл этилацетата, и органические слои объединяли. Органические слои промывали 3x500 мл воды и 1x500 мл насыщенного раствора хлорида натрия. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:5). В результате получали 62 г (76%) бензил (2R)-3-(4-бромфенил)-2-гидроксипропаноата в виде белого твердого вещества. 1H ЯМР (ДМСО, 300 МГц) δ: 7.49 (д, J=3.9 Гц, 2 H), 741-7.34 (м, 5 H), 7.15 (д, J=4.4 Гц, 2 H), 5.28-5.15 (м, 2 H), 4.55-4.51 (м, 1 H), 3.23-3.16 (м, 1 H), 3.07-3.01 (м, 1 H).
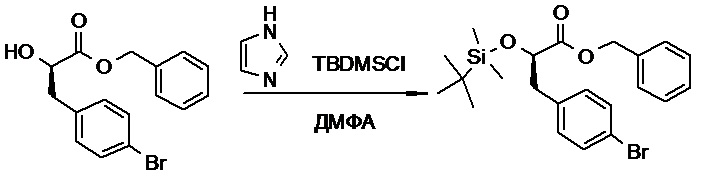
Бензил (2R)-3-(4-бромфенил)-2-[(трет-бутилдиметилсилил)окси]пропаноат: В 2-литровую 4-горлую круглодонную колбу помещали бензил (2R)-3-(4-бромфенил)-2-гидроксипропаноат (60 г, 179.00 ммоль, 1.00 экв.), N,N-диметилформамид (1000 мл), 1H-имидазол (24.5 г, 359.89 ммоль, 2.00 экв.). Затем добавляли TBDMSCl (32.4 г, 1.20 экв.) по каплям при перемешивании. Полученный раствор перемешивали в течение 16 часов при комнатной температуре. Полученный раствор разбавляли 2 л H2O. Раствор экстрагировали 3x500 мл этилацетата, органические слои объединяли. Органические слои промывали 3x500 мл насыщенного раствора хлорида натрия. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:50). В результате получали 78 г (97%) бензил (2R)-3-(4-бромфенил)-2-[(трет-бутилдиметилсилил)окси] пропаноата в виде желтого масла. MS (ESI, m/z): 449 (M+H); 1H ЯМР (ДМСО, 300 МГц) δ: 7.44 (д, J=4.2 Гц, 2 H), 7.40-7.31 (м, 5 H), 7.16 (д, J=4.0 Гц, 2 H), 5.13 (с, 2 H), 4.50-4.46 (м, 1 H), 3.03-2.98 (м, 1 H), 2.86-2.79 (м, 1 H), 0.73 (с, 9 H), -0.15 (с, 3 H), -0.25 (с, 3 H).
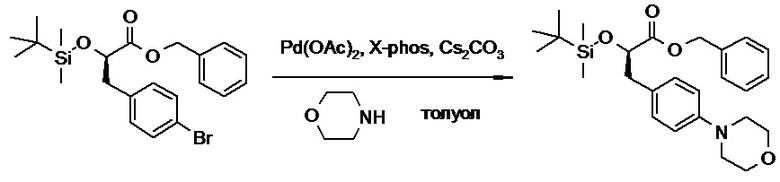
Бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(морфолин-4-ил)фенил]пропаноат: В 2-литровую 4-горлую круглодонную колбу в инертной атмосфере азота помещали бензил (2R)-3-(4-бромфенил)-2-[(трет-бутилдиметилсилил)окси]пропаноат (78 г, 173.54 ммоль, 1.00 экв.), X-phos (8.27 г, 0.10 экв.), Pd(OAc)2 (1.95 г, 8.69 ммоль, 0.05 экв.), толуол (1500 мл), морфолин (45.3 г, 519.97 ммоль, 3.00 экв.), Cs2CO3 (170 г, 3.00 экв.). Полученный раствор перемешивали в течение 16 часов при 90°C. Твердый осадок отфильтровывали. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/ петролейный эфир (1:5). В результате получали 64 г (81%) бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(морфолин-4-ил)фенил]пропаноата в виде желтого масла. MS (ESI, m/z): 456 (M+H); 1H ЯМР (CDCl3, 300 МГц) δ: 7.34-7.31 (м, 5 H), 7.12 (д, J=4.2 Гц, 2 H), 6.90-6.80 (м, 2 H), 5.20-5.10 (м, 2 H), 4.36-4.32 (м, 1 H), 3.90-3.80 (м, 4 H), 3.13-3.05 (м, 4 H), 3.04-2.95 (м, 1 H), 2.89-2.82 (м, 1 H), 0.79 (с, 9 H), -0.15 (с, 3 H), -0.20 (с, 3 H).
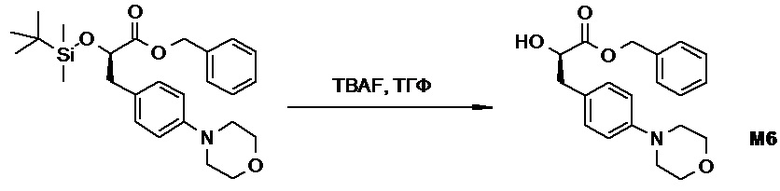
Бензил (2R)-2-гидрокси-3-[4-(морфолин-4-ил)фенил]пропаноат (M6): В 2000-миллилитровую 4-горлую круглодонную колбу помещали бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(морфолин-4-ил)фенил]пропаноат (60 г, 131.68 ммоль, 1.00 экв.), тетрагидрофуран (1200 мл). Затем добавляли TBAF (51.7 г, 197.74 ммоль, 1.20 экв.) порциями при 0°C. Полученный раствор перемешивали в течение 20 минут при комнатной температуре. Полученный раствор разбавляли 2000 мл H2O. Полученный раствор экстрагировали 3x500 мл этилацетата, и органические слои объединяли. Органические слои промывали 3x500 мл воды и 1x500 мл насыщенного раствора хлорида натрия. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:3). В результате получали 42 г (93%) бензил (2R)-2-гидрокси-3-[4-(морфолин-4-ил)фенил]пропаноата в виде желтого твердого вещества. MS (ESI, m/z): 342 (M+H); 1H ЯМР (ДМСО, 300 МГц) δ: 7.40-7.27 (м, 5H), 7.06 (д, J=8.4 Гц, 2H), 6.82 (д, J=8.7 Гц, 2H), 5.57 (д, J=6.3 Гц, 1H), 5.08 (с, 2H), 4.27-4.21 (м, 1H), 3.75-3.71 (м, 4H), 3.06-3.03 (м, 4H), 2.91-2.74 (м, 2H).
Пример синтеза 7: Получение мономера M7.
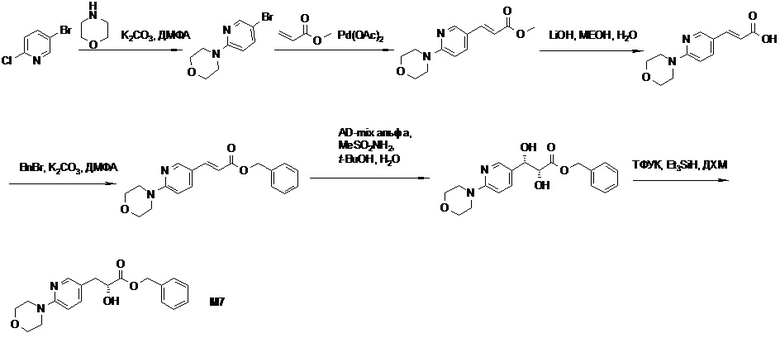
Подробное описание эксперимента
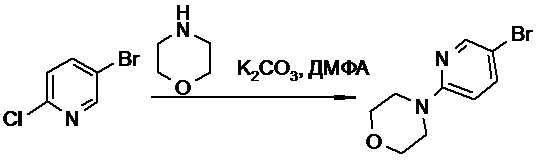
4-(5-бромпиридин-2-ил)морфолин: В 1-литровую круглодонную колбу помещали раствор 5-бром-2-хлорпиридина (50 г, 259.82 ммоль, 1.00 экв.) в N,N-диметилформамиде (300 мл), морфолин (91 г, 1.04 моль, 4.00 экв.), карбонат калия (108 г, 781.42 ммоль, 3.00 экв.). Полученный раствор перемешивали в течение ночи при 120°C. Полученный раствор экстрагировали 5x150 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x100 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. Полученную смесь промывали смесью петролейный эфир:этилацетат = 1:5. В результате получали 80 г (63%) 4-(5-бромпиридин-2-ил)морфолина в виде белого твердого вещества. MS (ESI, m/z): 243 (M+H); 1H ЯМР (CDCl3, 300 МГц) δ: 8.22 (с, 1 H), 7.57 (д, J=4.5Гц, 1 H), 6.54 (д, J=2.4Гц, 1 H), 3.82 (т, J=5.1 Гц, 4 H), 3.48 (т, J = 5.1 Гц, 4 H).
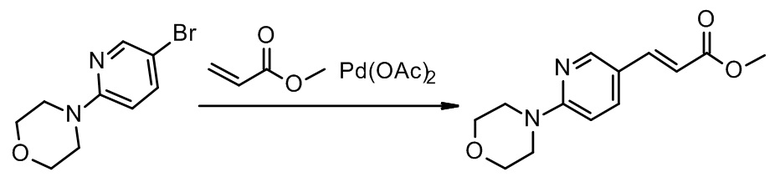
Метил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноат: В 250-миллилитровую круглодонную колбу в инертной атмосфере азота помещали раствор 4-(5-бромпиридин-2-ил)морфолина (5 г, 20.57 ммоль, 1.00 экв.) в N,N-диметилформамиде (120 мл), метил проп-2-еноат (3.54 г, 41.12 ммоль, 2.00 экв.), Pd(OAc)2 (92 мг, 0.41 ммоль, 0.02 экв.), бикарбонат натрия (3.46 г, 41.19 ммоль, 2.00 экв.), Bu4NCl (11.4 г, 41.02 ммоль, 2.00 экв.). Полученный раствор перемешивали в течение 3 дней при 100°C. Полученный раствор экстрагировали 5x150 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x100 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. Твердый осадок отфильтровывали. В результате получали 11.5 г (56%) метил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноата в виде светло-коричневого твердого вещества. MS (ESI, m/z): 249 (M+H); 1H ЯМР (CDCl3, 300 МГц) δ: 8.30 (с, 1 H), 7.72-7.58 (м, 2 H), 6.64 (д, J=4.5Гц, 1 H), 6.27 (д, J=8.0 Гц, 1 H), 3.84-3.80 (м, 7 H), 3.62 (т, J=4.8 Гц, 4 H).
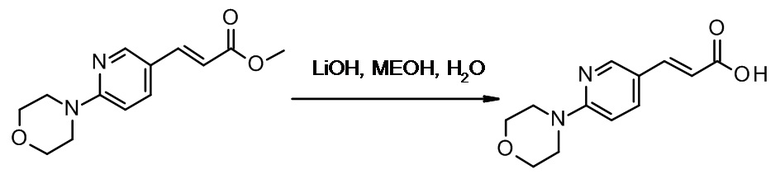
(2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еновая кислота: В 500-миллилитровую круглодонную колбу помещали раствор метил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноата (11 г, 44.31 ммоль, 1.00 экв.) в смеси метанол/H2O (60:60 мл), LiOH (10.6 г, 442.59 ммоль, 10.00 экв.). Полученный раствор перемешивали в течение 1 часа при 80°C. Полученный раствор разбавляли 150 мл воды. Значение pH раствора доводили до 6~7 добавлением насыщенного раствора NaHCO3. Полученный раствор экстрагировали 5x150 мл этилацетата, и органические слои объединяли. Органическую фазу промывали 3x150 мл насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 10.4 г (сырой продукт) (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еновой кислоты в виде светло-коричневого твердого вещества. MS (ESI, m/z): 245 (M+H).
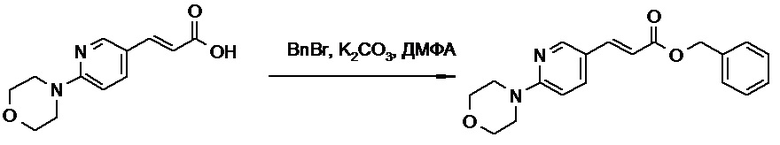
бензил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноат: В 250-миллилитровую круглодонную колбу помещали раствор (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еновой кислоты (4 г, 17.08 ммоль, 1.00 экв.) в N,N-диметилформамиде (70 мл), карбонат калия (7.1 г, 51.37 ммоль, 3.00 экв.), (бромметил)бензол (4.4 г, 25.73 ммоль, 1.50 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре. Раствор экстрагировали 5x150 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x150 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. Полученную смесь промывали 1x70 мл петролейного эфира. Твердый осадок отделяли фильтрованием. В результате получали 10 г (72%) бензил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноата в виде желтого твердого вещества. MS (ESI, m/z): 325 (M+H); 1H ЯМР (CDCl3, 300 МГц) δ: 8.30 (с, 1 H), 7.70-7.62 (м, 2 H), 7.45-7.32 (м, 5 H), 6.63 (д, J=4.5Гц, 1 H), 6.32 (д, J=8.0 Гц, 1 H), 5.25 (с, 2 H), 3.82 (т, J=4.5 Гц, 4 H), 3.63-3.60 (м, 4 H).
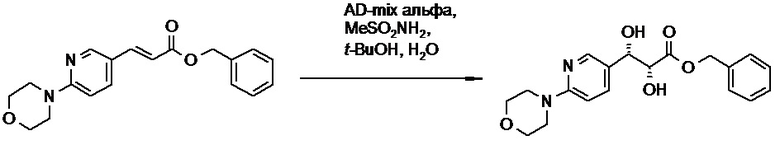
(2R,3S)-2,3-дигидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноат: В 100-миллилитровую 3-горлую круглодонную колбу помещали смесь трет-бутанол:H2O (20:20 мл), AD-mix (8.6 г). Затем добавляли бензил (2E)-3-[6-(морфолин-4-ил)пиридин-3-ил]проп-2-еноата (2 г, 6.17 ммоль, 1.00 экв.) и MeSO2NH2 (586 г, 6.17 моль, 1.00 экв.) при перемешивании при 0°C. Полученный раствор перемешивали в течение 3 дней при комнатной температуре. Затем реакцию гасили добавлением Na2SO3. Полученный раствор экстрагировали 3x150 мл этилацетата, и органические слои объединяли, сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:1). В результате получали 5.4 г (49%) бензил (2R, 3S)-2,3-дигидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноата в виде светло-желтого твердого вещества. MS (ESI, m/z): 359 (M+H).
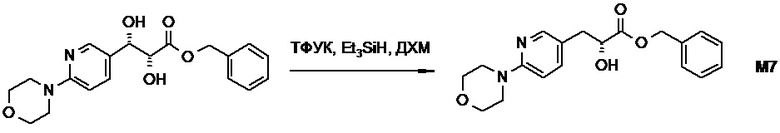
бензил (2R)-2-гидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноат (M7): В 100-миллилитровую круглодонную колбу помещали раствор бензил (2R, 3S)-2,3-дигидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноата (1.5 г, 4.19 ммоль, 1.00 экв.) в дихлорметане (15 мл), трифторуксусную кислоту (5 мл), Et3SiH (10 мл). Полученный раствор перемешивали в течение 3 дней при 50°C. Полученную смесь упаривали в вакууме. Затем реакцию гасили добавлением смеси вода/лед. Значение pH раствора доводили до 9 добавлением водного раствора бикарбоната натрия. Полученный раствор экстрагировали 3x40 мл дихлорметана, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:2). В результате получали 2.3 г (27%) бензил (2R)-2-гидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноата в виде желтого масла. MS (ESI, m/z): 343 (M+H); 1H ЯМР (CDCl3, 300 МГц) δ: 8.02 (с, 1 H), 7.43-7.32 (м, 6 H), 6.54 (д, J=4.4 Гц, 1 H), 5.21 (с, 2 H), 4.52-4.46 (м, 1 H), 3.84 (т, J=7.8Гц, 4 H), 3.48 (т, J=4.8Гц, 4 H) 3.05-3.01 (м, 1H), 2.91-2.85 (м, 1H).
Пример синтеза 8: Получение мономера M8.
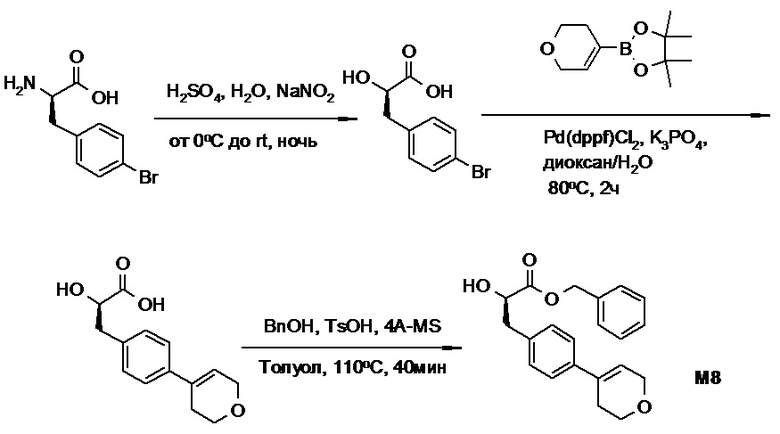
Подробное описание эксперимента
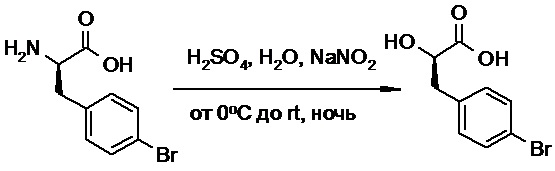
(2R)-3-(4-бромфенил)-2-гидроксипропановая кислота: В 5-литровую 4-горлую круглодонную колбу помещали смесь серная кислота/H2O (0.5моль/л) (3.2 л), (2R)2-амино-3-(4-бромфенил)пропановую кислоту (100 г, 409.69 ммоль, 1.00 экв.). Затем добавляли раствор NaNO2 (350 г, 5.07 моль, 12.38 экв.) в H2O (500 мл) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отделяли фильтрованием. Полученное твердое вещество сушили в термошкафу при пониженном давлении. В результате получали 146 г (73%) (2R)3-(4-бромфенил)-2-гидроксипропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 243 (M-H).
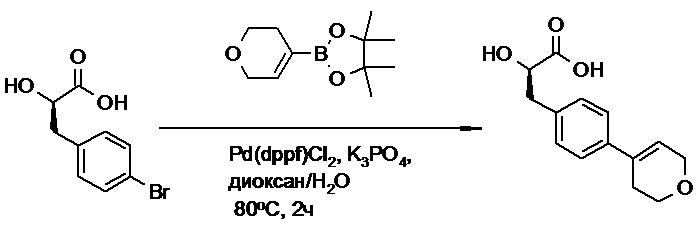
(2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропановая кислота: В 1-литровую круглодонную колбу в инертной атмосфере азота помещали диоксан (500 мл), H2O (50 мл), (2R)-3-(4-бромфенил)-2-гидроксипропановую кислоту (30 г, 122.41 ммоль, 1.00 экв.), 2-(3,6-дигидро-2H-пиран-4-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (40 г, 190.41 ммоль, 1.60 экв.), K3PO4 (65 г, 306.21 ммоль, 2.50 экв.), Pd(dppf)Cl2 (4.5 г, 6.15 ммоль, 0.05 экв.). Полученный раствор перемешивали в течение 2 часов при 75°C на масляной бане. Реакционную смесь охлаждали. Полученную смесь упаривали в вакууме. Остаток растворяли в 100 мл эфира. Твердый осадок отфильтровывали. Твердую фазу растворяли в 10 мл H2O и 500 мл ТГФ. Значение pH раствора доводили до 4-5 добавлением раствора хлороводорода (12 моль/л). Твердый осадок отфильтровывали. Фильтрат сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 28 г (92%) (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропановой кислоты в виде светло-коричневого твердого вещества. MS (ESI, m/z): 249(M+H).
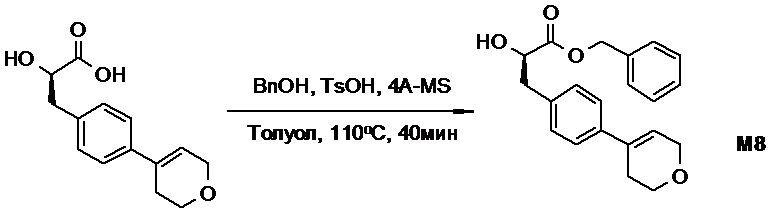
Бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноат (M8): В 500-миллилитровую круглодонную колбу помещали толуол (300 мл), (2R)3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропановую кислоту (9 г, 36.25 ммоль, 1.00 экв.), фенилметанол (10.3 г, 95.25 ммоль, 2.50 экв.), TsOH (2 г, 11.61 ммоль, 0.30 экв.), 4А молекулярные сита (5.4 г). Полученный раствор перемешивали в течение 40 минут при 110°C на масляной бане. Реакционную смесь охлаждали. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10-1:3). В результате получали 24 г (98%) бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноата в виде белого твердого вещества. MS (ESI, m/z): 339 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.62-7.30 (м, 7H), 7.13 (д, J=8.4 Гц, 2H), 6.12-6.10 (м, 1H), 5.24 (с, 2H), 4.52-4.48 (м, 1H), 4.35-4.32 (м, 2H), 3.96-3.92 (м, 2H), 3.16-2.95 (м, 2H), 2.67-2.49 (м, 2H).
Пример синтеза 9: Получение мономера M9.
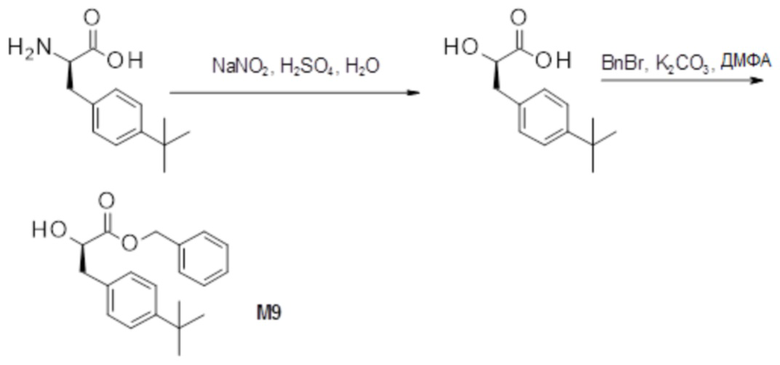
Подробное описание эксперимента
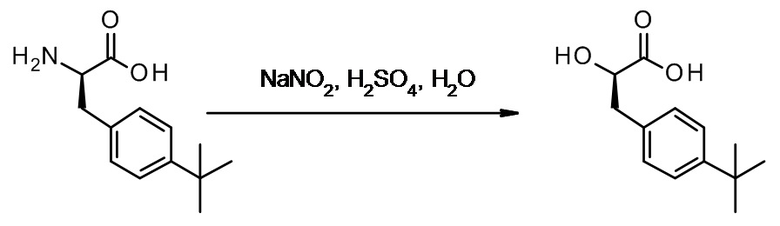
(2R)-3-(4-трет-бутилфенил)-2-гидроксипропановая кислота: В 2000-миллилитровую 3-горлую круглодонную колбу помещали раствор (2R)-2-амино-3-(4-трет-бутилфенил) пропановой кислоты (30 г, 135.57 ммоль, 1.00 экв.) в серной кислоте (0.5M) (480 мл), раствор NaNO2 (94 г, 1.36 моль, 10.00 экв.) в воде (180 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре в бане лед/соль. Твердый осадок отделяли фильтрованием. В результате получали 20.0 г (66%) (2R)-3-(4-трет-бутилфенил)-2-гидроксипропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 221 (M-H).
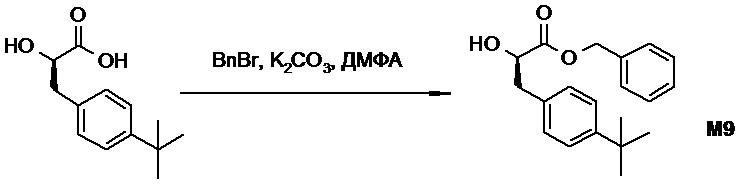
(2R)-3-(4-трет-бутилфенил)-2-гидроксипропаноат (M9): В 2000-миллилитровую 3-горлую круглодонную колбу помещали раствор (2R)3-(4-трет-бутилфенил)-2-гидроксипропановой кислоты (40 г, 179.95 ммоль, 1.00 экв.) в N,N-диметилформамиде (1000 мл), карбонат калия (50 г, 361.77 ммоль, 2.00 экв.), BnBr (61 г, 356.66 ммоль, 2.00 экв.). Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Полученный раствор разбавляли 2000 мл этилацетата. Смесь промывали 3x2000 мл воды. Полученную смесь промывали 2x2000 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:50~1:10). В результате получали 42 г (75%) бензил (2R)-3-(4-трет-бутилфенил)-2-гидроксипропаноата в виде желтого масла. 1H ЯМР (300 МГц, CDCl3): δ 7.40-7.27 (м, 7H), 7.10 (д, J=8.1 Гц, 2H), 5.20 (с, 2H), 4.49 (т, J=5.4 Гц, 1H), 3.14-2.93 (м, 2H), 1.31 (с, 9H).
Пример синтеза 10: Получение мономера M10.
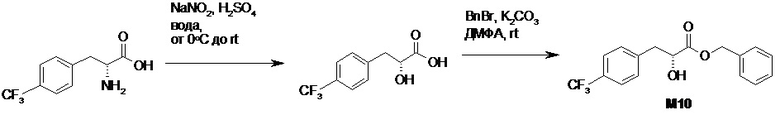
Подробное описание эксперимента
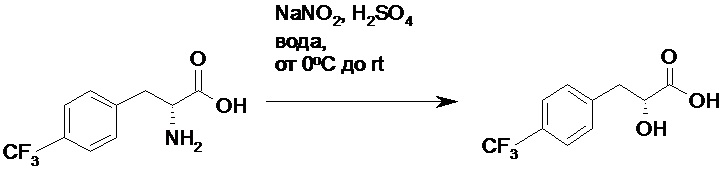
2-Гидрокси-3-[4-(трифторметил)фенил]пропановая кислота: В 500-миллилитровую 3-горлую круглодонную колбу помещали 2-амино-3-[4-(трифторметил)фенил]пропановую кислоту (20 г, 85.77 ммоль, 1.00 экв.), серную кислоту (0.5 M) (340 мл). Затем добавляли раствор NaNO2 (35.5 г, 514.49 ммоль, 6.00 экв.) в воде (80 мл) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение 1 часа при 0°C. Полученный раствор оставляли реагировать при перемешивании на ночь при комнатной температуре. Твердый осадок отделяли фильтрованием. В результате получали 17.5 г (87%) 2-гидрокси-3-[4-(трифторметил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 233 (M-H); 1H ЯМР (ДМСО, 300 МГц) δ: 7.63 (д, J=3.9 Гц, 2 H), 7.46 (д, J=4.0 Гц, 2 H), 4.21-4.17 (м, 1 H), 3.09-3.03 (м, 1 H), 2.91-2.84 (м, 1 H).
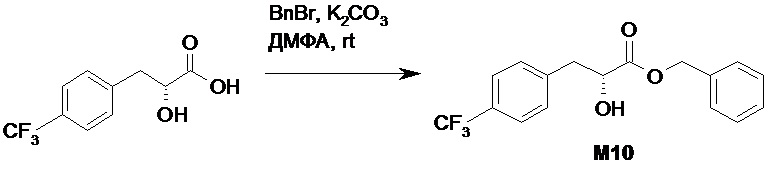
Бензил (2R)-2-гидрокси-3-[4-(трифторметил)фенил]пропаноат (M10): В 500-миллилитровую 3-горлую круглодонную колбу помещали (2R)-2-гидрокси-3-[4-(трифторметил)фенил]пропановую кислоту (17.5 г, 74.73 ммоль, 1.00 экв.), (бромметил)бензол (15.3 г, 89.46 ммоль, 1.20 экв.), карбонат калия (31 г, 224.30 ммоль, 3.00 экв.), N,N-диметилформамид (100 мл). Полученный раствор перемешивали в течение 30 минут при 0°C и оставляли нагреваться до комнатной температуры при перемешивании в течение ночи. Затем реакцию гасили добавлением 250 мл воды. Полученный раствор экстрагировали 3x150 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x250 мл насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток от упаривания очищали на колонке с силикагелем со смесью этилацетат/петролейный эфир (1:6), получая 10.6 г (44%) бензил (2R)-2-гидрокси-3-[4-(трифторметил)фенил]пропаноата в виде белого твердого вещества. 1H ЯМР (ДМСО, 300 МГц) δ: 7.60 (д, J=4.0 Гц, 2 H), 7.42 (д, J=4.0 Гц, 2 H), 7.39-7.27 (м, 5 H), 5.72 (д, J=3 Гц, 1 H), 5.10 (с, 2 H), 4.40-4.33 (м, 1 H), 3.10-3.04 (м, 1 H), 2.99-2.91 (м, 1 H).
Пример синтеза 11: Получение мономера M11.
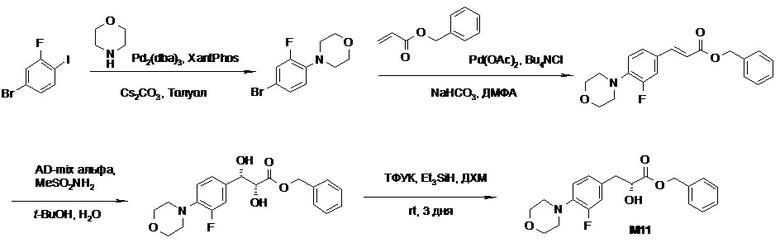
Подробное описание эксперимента
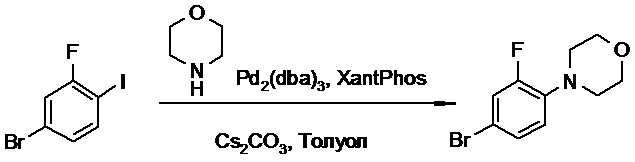
4-(4-Бром-2-фторфенил)морфолин: В 1-литровую круглодонную колбу в инертной атмосфере азота помещали раствор 4-бром-2-фтор-1-иодбензола (15 г, 49.85 ммоль, 1.00 экв.) в толуоле (300 мл). Добавляли Pd2(dba)3 (1.3 г, 1.42 ммоль, 0.03 экв.), Cs2CO3 (41 г, 125.45 ммоль, 2.50 экв.), XantPhos (2.9 г, 5.01 ммоль, 0.10 экв.), морфолин (4.3 г, 49.36 ммоль, 1.00 экв.). Полученный раствор перемешивали в течение ночи при 100°C. Затем реакцию гасили добавлением 150 мл воды. Полученный раствор экстрагировали 3x100 мл этилацетата, органические слои объединяли и сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:15). В результате получали 10.5 г (81%) 4-(4-бром-2-фторфенил)морфолина в виде желтого твердого вещества. MS (ESI, m/z): 260 (M+H).
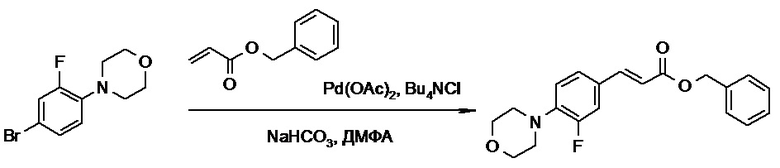
Бензил (2E)-3-[3-фтор-4-(морфолин-4-ил)фенил]проп-2-еноат: В 100-миллилитровую круглодонную колбу в инертной атмосфере азота помещали 4-(4-бром-2-фторфенил)морфолин (1.25 г, 4.81 ммоль, 1.00 экв.), Pd(OAc)2 (50 мг, 0.22 ммоль, 0.05 экв.), раствор бикарбоната натрия (810 мг, 9.64 ммоль, 2.00 экв.) в N,N-диметилформамиде (30 мл), Bu4NCl (2.7 г, 9.72 ммоль, 2.00 экв.), бензил проп-2-еноат (1.6 г, 9.87 ммоль, 2.00 экв.). Полученный раствор перемешивали в течение 36 часов при 100°C. Затем реакцию гасили добавлением воды. Полученный раствор экстрагировали 4x100 мл этилацетата, и органические слои объединяли. Органическую фазу промывали 3x60 мл насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:5). В результате получали 10.5 г (80%) бензил (2E)-3-[3-фтор-4-(морфолин-4-ил)фенил]проп-2-еноата в виде желтого твердого вещества. MS (ESI, m/z): 342 (M+H).
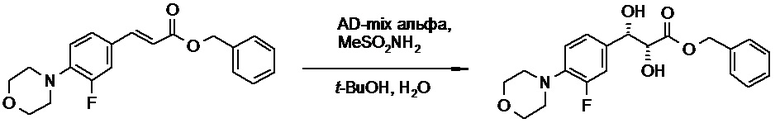
Бензил (2R, 3S)-3-[3-фтор-4-(морфолин-4-ил)фенил]-2,3-дигидроксипропаноат: В 250-миллилитровую 3-горлую круглодонную колбу помещали раствор AD-mix (12.3 г) в смеси трет-бутанол/H2O (60:60 мл). Затем добавляли бензил (2E)-3-[3-фтор-4-(морфолин-4-ил)фенил]проп-2-еноат (3 г, 8.79 ммоль, 1.00 экв.) порциями при 0°C. Затем добавляли MeSO2NH2 (1.23 г, 1.00 экв.) порциями при 0°C. Полученный раствор перемешивали в течение 3 дней при комнатной температуре. Затем реакцию гасили добавлением Na2SO3. Полученный раствор экстрагировали 3x100 мл этилацетата, и органические слои объединяли. Органическую фазу промывали 3x60 мл насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:1). В результате получали 9.5 г (72%) бензил (2R, 3S)-3-[3-фтор-4-(морфолин-4-ил)фенил]-2,3-дигидроксипропаноата в виде желтого масла. MS (ESI, m/z): 376 (M+H).
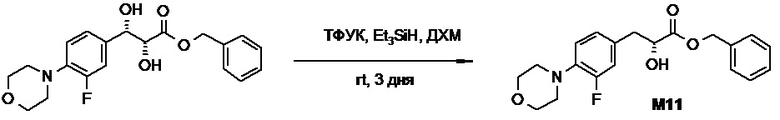
Бензил (2R)-3-[3-фтор-4-(морфолин-4-ил)фенил]-2-гидроксипропаноат (M11): В 40-миллилитровую виалу помещали раствор бензил (2R,3S)-3-[3-фтор-4-(морфолин-4-ил)фенил]-2,3-дигидроксипропаноата (900 мг, 2.40 ммоль, 1.00 экв.) в дихлорметане (2 мл), Et3SiH (4 мл), трифторуксусную кислоту (2 мл). Полученный раствор перемешивали в течение 3 дней при комнатной температуре. Затем реакцию гасили добавлением смеси вода/лед. Полученный раствор экстрагировали 3x80 мл этилацетата, и органические слои объединяли. Органическую фазу промывали 3x60 мл насыщенного раствора хлорида натрия. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:3). В результате получали 4.1 г (48%) бензил (2R)-3-[3-фтор-4-(морфолин-4-ил)фенил]-2-гидроксипропаноата в виде красноватого масла. MS (ESI, m/z): 360 (M+H).
Пример синтеза 12: Получение мономера M12.
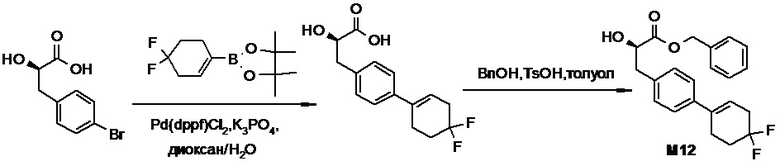
Подробное описание эксперимента
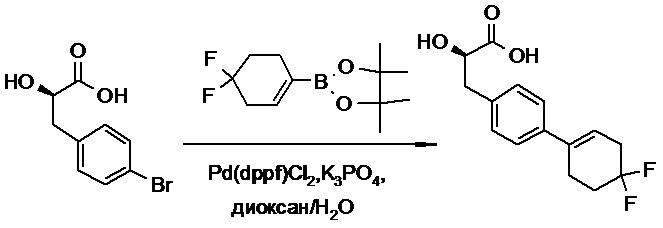
(2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропановая кислота: В 250-миллилитровую круглодонную колбу в инертной атмосфере азота помещали смесь диоксан/H2O (88 мл), (2R)-3-(4-бромфенил)-2-гидроксипропановую кислоту (4 г, 16.32 ммоль, 1.00 экв.), 2-(4,4-дифторциклогекс-1-ен-1-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (4.0 г, 16.39 ммоль, 1.00 экв.), Pd(dppf)Cl2 (640 мг, 0.87 ммоль, 0.05 экв.), K3PO4 (11 г, 51.82 ммоль, 3.00 экв.). Полученный раствор перемешивали в течение 4 часов при 80°C на масляной бане. Реакционную смесь охлаждали. Полученную смесь упаривали в вакууме. Остаток растворяли в 50 мл эфира. Твердый осадок отделяли фильтрованием. Твердую фазу растворяли в 50 мл ТГФ. Значение pH раствора доводили до 5 добавлением раствора хлороводорода (12 моль/л). Полученный раствор разбавляли 200 мл этилацетата. Твердый осадок отделяли фильтрованием. Фильтрат сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 4.5 г (98%) (2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропановой кислоты в виде светло-желтого масла. MS (ESI, m/z): 281 (M-H).
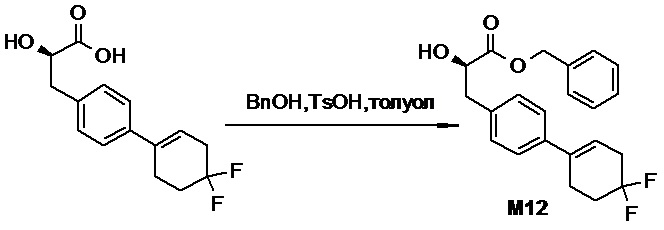
Бензил-(2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропаноат (M12): В 500-миллилитровую круглодонную колбу помещали толуол (200 мл), (2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропановую кислоту (4.5 г, 15.94 ммоль, 1.00 экв.), BnOH (2.24 г, 1.30 экв.), TsOH (540 мг, 3.14 ммоль, 0.20 экв.), 4А молекулярные сита (2 г). Полученный раствор перемешивали в течение 4 часов при 110°C на масляной бане. Реакционную смесь охлаждали. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:20-1:10). В результате получали 5 г (84%) бензил (2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропаноата в виде светло-желтого твердого вещества. 1H ЯМР (300 МГц, CDCl3): δ 7.62-7.30 (м, 7H), 7.11 (д, J=8.4 Гц, 2H), 5.89 (ушир, 1H), 5.21 (с, 2H), 4.52-4.48 (м, 1H), 3.16-2.95 (м, 2H), 2.71-2.67 (м, 4H), 2.25-2.12 (м, 2H).
Пример синтеза 13: Получение мономера M13.
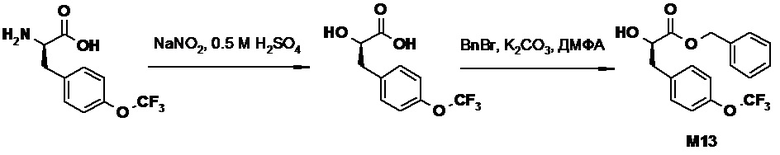
Подробное описание эксперимента
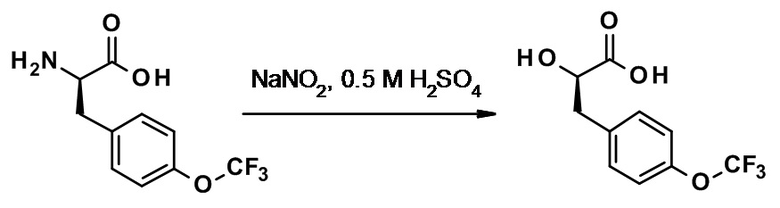
(2R)-2-гидрокси-3-[4-(трифторметокси)фенил]пропановая кислота: В 1000-миллилитровую 3-горлую круглодонную колбу помещали (2R)2-амино-3-[4-(трифторметокси)фенил]пропановой кислоты гидрохлорид (10 г, 35.01 ммоль, 1.00 экв.). Затем добавляли раствор NaNO2 (29 г, 420.29 ммоль, 12.00 экв.) в воде (150 мл) по каплям при перемешивании при 0°C. Затем добавляли серную кислоту (0.5M/л) (300 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре. Полученный раствор экстрагировали 3x200 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x200 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 11 г (сырой продукт) (2R)-2-гидрокси-3-[4-(трифторметокси)фенил]пропановой кислоты в виде желтого масла. MS (ESI, m/z): 249 (M-H).
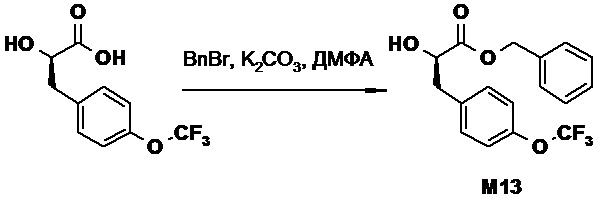
Бензил (2R)-2-гидрокси-3-[4-(трифторметокси)фенил]пропаноат (M13): В 1000-миллилитровую 3-горлую круглодонную колбу помещали (2R)2-гидрокси-3-[4-(трифторметокси)фенил]пропановую кислоту (11 г, 43.97 ммоль, 1.00 экв.), N,N-диметилформамид (300 мл), карбонат калия (12 г, 86.82 ммоль, 2.00 экв.). Затем добавляли (бромметил)бензол (9 г, 52.62 ммоль, 1.20 экв.) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Затем реакцию гасили добавлением 100 мл воды. Полученный раствор экстрагировали 3x150 мл этилацетата, и органические слои объединяли. Полученную смесь промывали 3x200 мл насыщенного раствора хлорида натрия. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 7.6 г (51%) бензил (2R)-2-гидрокси-3-[4-(трифторметокси)фенил]пропаноата в виде желтого масла. 1H ЯМР (ДМСО, 300 МГц) δ: 7.45-7.30 (м, 7 H), 7.25-7.17 (м, 2 H), 5.70 (д, J=2.7 Гц, 1 H), 5.10 (с, 2 H), 4.34-4.32 (м, 1 H), 3.04-2.98 (м, 1 H), 2.92-2.85 (м, 1 H).
Пример синтеза 14: Получение мономера M14.
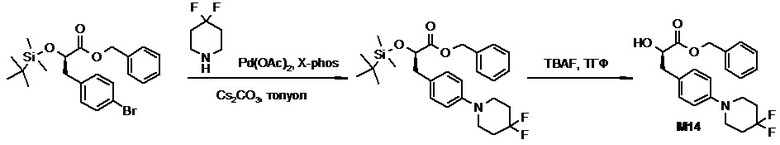 Подробное описание эксперимента
Подробное описание эксперимента
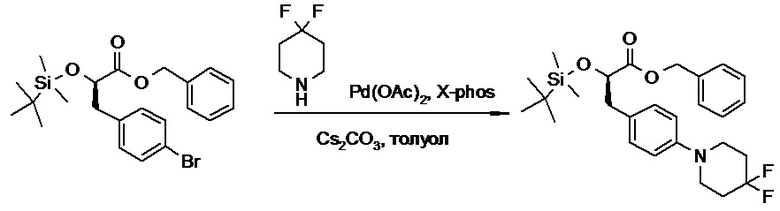
Бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(4,4-дифторпиперидин-1-ил)фенил] пропаноат: В 250-миллилитровую круглодонную колбу в инертной атмосфере азота помещали бензил (2R)-3-(4-бромфенил)-2-[(трет-бутилдиметилсилил)окси] пропаноат (14.53 г, 32.33 ммоль, 1.00 экв.), 4,4-дифторпиперидин (6.2 г, 51.19 ммоль, 1.20 экв.), Cs2CO3 (19 г, 3.00 экв.), X-PhOS (309 мг, 0.02 экв.), толуол (50 мл), Pd(OAc)2 (145 мг, 0.65 ммоль, 0.02 экв.). Полученный раствор перемешивали в течение 16 часов при 90°C. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:6). В результате получали 12.28 г (78%) бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(4,4-дифторпиперидин-1-ил)фенил] пропаноата в виде бесцветного масла.
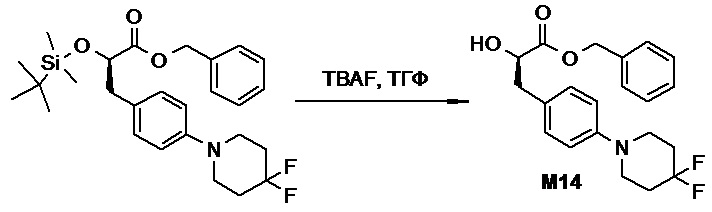
Бензил (2R)-3-[4-(4,4-дифторпиперидин-1-ил)фенил]-2-гидроксипропаноат (M14): В 100-миллилитровую 3-горлую круглодонную колбу помещали бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(4,4-дифторпиперидин-1-ил)фенил]пропаноат (12.28 г, 25.08 ммоль, 1.00 экв.), тетрагидрофуран (30 мл), TBAF (8.4 г, 32.13 ммоль, 1.20 экв.). Полученный раствор перемешивали в течение 20 минут при комнатной температуре. Полученную смесь упаривали в вакууме. Полученный раствор разбавляли 100 мл этилацетата. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10). В результате получали 6.8 г (72%) бензил (2R)-3-[4-(4,4-дифторпиперидин-1-ил)фенил]-2-гидроксипропаноата в виде белого твердого вещества. MS (ESI, m/z): 376 (M+H).
Пример синтеза 15: Получение мономера M15.
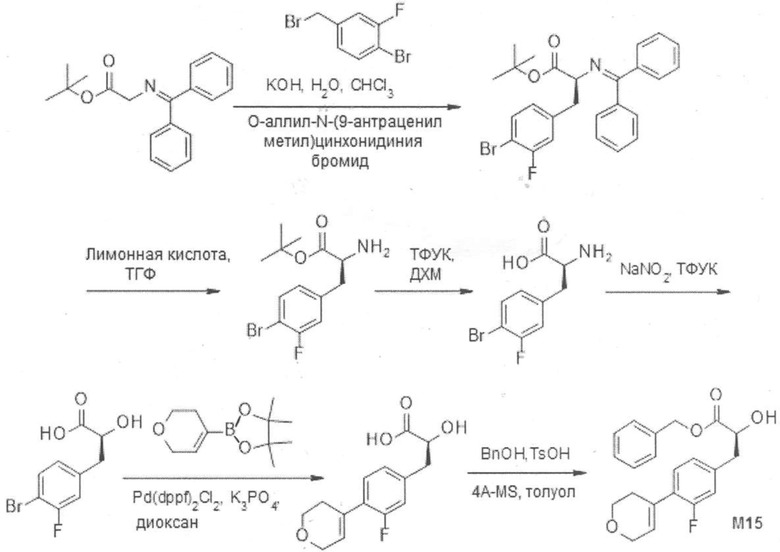
Подробное описание эксперимента
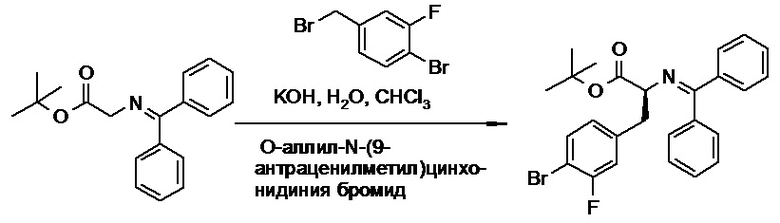
трет-бутил (2S)-3-(4-бром-3-фторфенил)-2-[(дифенилметилиден)амино]пропаноат: В 1000-миллилитровую 3-горлую круглодонную колбу помещали трет-бутил 2-[(дифенилметилиден)амино]ацетат (30 г, 101.57 ммоль, 1.00 экв.), толуол (315 мл), раствор 1-бром-4-(бромметил)-2-фторбензола (54 г, 201.55 ммоль, 1.98 экв.) в хлороформе (135 мл), O-аллил-N-(9-антраценилметил)цинхонидиния бромид (1.1 г, 2.09 ммоль, 0.02 экв.), гидроксид калия (56 г, 998.04 ммоль, 9.83 экв.). Полученный раствор перемешивали в течение 3 дней при -20°C. Полученный раствор разбавляли 1000 мл этилацетата. Смесь промывали 3x1000 мл H2O. Органический слой сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на С18 обращенно-фазную колонку с H2O/ACN (1/9). В результате получали 28 г (57%) трет-бутил (2S)-3-(4-бром-3-фторфенил)-2-[(дифенилметилиден)амино]пропаноата в виде светло-желтого масла. MS (ESI, m/z): 482 (M+H).
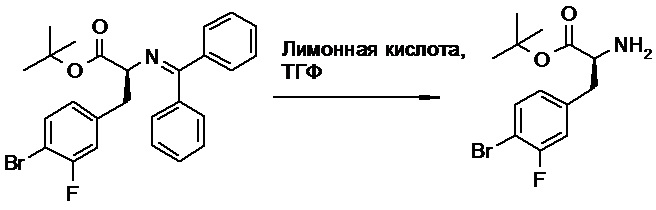
трет-бутил (2S)-2-амино-3-(4-бром-3-фторфенил)пропаноат: В 2-литровую 3-горлую круглодонную колбу помещали трет-бутил (2S)-3-(4-бром-3-фторфенил)-2-[(дифенилметилиден)амино]пропаноат (28 г, 58.04 ммоль, 1.00 экв.), тетрагидрофуран (580 мл), лимонную кислоту (580 мл). Полученный раствор перемешивали в течение 4 часов при комнатной температуре. Смесь упаривали в вакууме. Полученный раствор разбавляли 1000 мл воды. Раствор экстрагировали 3x200 мл эфира и водные слои объединяли. Значение рН водного слоя доводили до 8 добавлением бикарбоната натрия и экстрагировали 3x300 мл этилацетата. Органические слои объединяли, сушили над сульфатом натрия и упаривали в вакууме. В результате получали 14.8 г (80%) трет-бутил (2S)-2-амино-3-(4-бром-3-фторфенил)пропаноата в виде светло-желтого масла. MS (ESI, m/z): 318 (M+H).
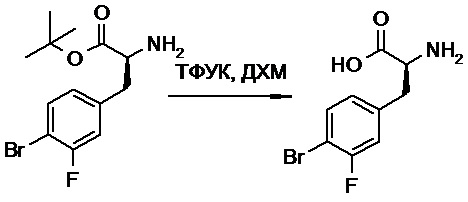
(2S)-2-амино-3-(4-бром-3-фторфенил)пропановая кислота: В 500-миллилитровую круглодонную колбу помещали трет-бутил (2S)-2-амино-3-(4-бром-3-фторфенил)пропаноат (5.9 г, 18.54 ммоль, 1.00 экв.), дихлорметан (200 мл), трифторуксусную кислоту (21 г, 185.77 ммоль, 10.02 экв.). Полученный раствор перемешивали в течение 3 дней при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на С18 обращенно-фазную колонку с H2O/ACN (1/3). В результате получали 5.4 г (сырой продукт) (2S)-2-амино-3-(4-бром-3-фторфенил)пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 262 (M+H).
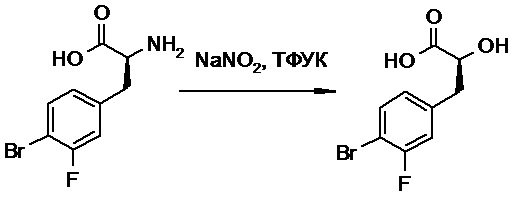
(2S)-3-(4-бром-3-фторфенил)-2-гидроксипропановая кислота: В 500-миллилитровую 3-горлую круглодонную колбу помещали (2S)-2-амино-3-(4-бром-3-фторфенил)пропановую кислоту (5.4 г, 20.60 ммоль, 1.00 экв.), трифторуксусную кислоту (28.3 г, 250.35 ммоль, 12.15 экв.), воду (180 мл) и медленно добавляли раствор NaNO2 (17.1 г, 247.83 ммоль, 12.03 экв.) в воде (180 мл). Полученный раствор перемешивали в течение 16 часов при комнатной температуре. Твердый осадок отделяли фильтрованием. В результате получали 3.1 г (57%) (2S)-3-(4-бром-3-фторфенил)-2-гидроксипропановой кислоты в виде светло-желтого твердого вещества.
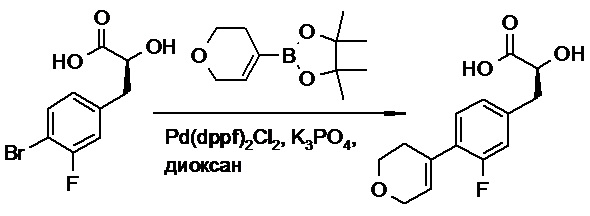
(2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропановая кислота: В 500-миллилитровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали (2S)-3-(4-бром-3-фторфенил)-2-гидроксипропановую кислоту (3 г, 11.40 ммоль, 1.00 экв.), 2-(3,6-дигидро-2H-пиран-4-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (4.8 г, 22.85 ммоль, 2.00 экв.), K3PO4 (7.28 г, 34.30 ммоль, 3.01 экв.), диоксан (180 мл), воду (18 мл), Pd(dppf)Cl2 (1.67 г, 2.28 ммоль, 0.20 экв.). Полученный раствор перемешивали в течение 5 часов при 80°C. Полученную смесь упаривали в вакууме. Полученную смесь разбавляли 900 мл эфира. Твердый осадок отделяли фильтрованием. Твердую фазу растворяли в 200 мл тетрагидрофурана. Значение pH раствора доводили до 3-4 добавлением раствора хлороводорода. Выпавший осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1/10). В результате получали 2.63 г (87%) (2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропановой кислоты в виде коричневого твердого вещества. MS (ESI, m/z): 265 (M-H).
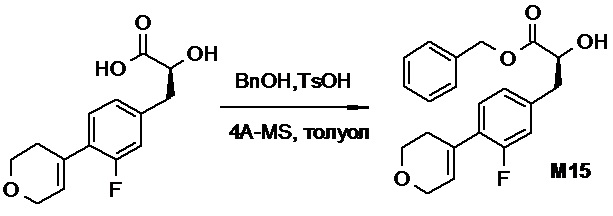
Бензил(2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропаноат (M33): В 100-миллилитровую круглодонную колбу помещали (2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропановую кислоту (1 г, 3.76 ммоль, 1.00 экв.), BnOH (1.1 г), TsOH (160 мг, 0.93 ммоль, 0.25 экв.), 4А молекулярные сита (1 г), толуол (20 мл). Полученный раствор перемешивали в течение 4 часов при 110°C. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1/4). В результате получали 350 мг (26%) бензил (2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропаноата в виде коричневого масла. 1H ЯМР (300 МГц, CD3OD): δ 7.37-7.29 (м, 5H), 7.20-7.15 (м, 1H), 6.97-6.92 (м, 2H), 6.02 (ушир, 1H), 5.19 (с, 2H), 4.44-4.40 (м, 1H), 4.30-4.27 (м, 2H), 3.92-3.885 (м, 2H), 3.33-2.90 (м, 2H), 2.47-2.46 (м, 2H).
Пример синтеза 16: Получение мономера M16.

Подробное описание эксперимента
1-[[(трет-бутокси)карбонил](метил)амино]циклопропан-1-карбоновая кислота (M16): В круглодонную колбу объемом 100 мл помещали 1-[[(трет-бутокси)карбонил] амино]циклопропан-1-карбоновую кислоту (2 г, 9.94 ммоль, 1.00 экв.), тетрагидрофуран (30 мл). После этого добавляли MeI (5 мл, 8.00 экв.) при 0°C в течение 10 минут. В полученную смесь добавляли гидрид натрия (1.32 г, 55.00 ммоль, 5.50 экв.) порциями при 0°C в течение 10 минут. Результирующий раствор перемешивали в течение 24 ч при комнатной температуре. Реакционную смесь медленно выливали в 150 мл воды при 0°C. Результирующий раствор промывали 30 мл эфира. Водный раствор отделяли и значение pH доводили до 3 с помощью лимонной кислоты (1 моль/л). Результирующий раствор экстрагировали 3x40 мл этилацетата, органические слои объединяли и упаривали в вакууме. В результате получали 2.5 г (сырой) 1-[[(трет-бутокси)карбонил](метил)амино]циклопропан-1-карбоновой кислоты в виде желтого твердого вещества. MS (ESI, m/z): 216 (M+H).
В приведенных ниже Примерах синтеза 17-32 описаны способы получения различных димерных соединений D1 - D16, замещенных широким рядом групп R1, R2, R3, R4, Cy1 и Cy2, что делает возможным получение диверсифицированного набора димерных соединений, использующихся для получения соединений по настоящему изобретению.
Пример синтеза 17: Получение димера D1.
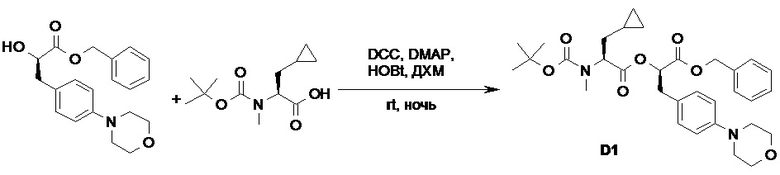
(2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D1): В 3-горлую круглодонную колбу объемом 250 мл помещали бензил (2R)-2-гидрокси-3-[4-(морфолин-4-ил)фенил]пропаноат (2.8 г, 8.20 ммоль, 1.00 экв.), (2S)-2-[[(трет-бутокси)карбонил]амино]-3-циклопропилпропановую кислоту (2 г, 8.72 ммоль, 1.00 экв.), дихлорметан (80 мл). После этого добавляли DCC (1.9 г, 9.21 ммоль, 1.10 экв.), 4-диметиламинопиридин (1.1 г, 9.00 ммоль, 1.10 экв.) и HOBt (1.2 г, 8.88 ммоль, 1.10 экв.) порциями при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:5). В результате получали 4.2 г (90%) (2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде желтого твердого вещества. MS (ESI, m/z): 567 (M+H).
Пример синтеза 18: Получение димера D2.
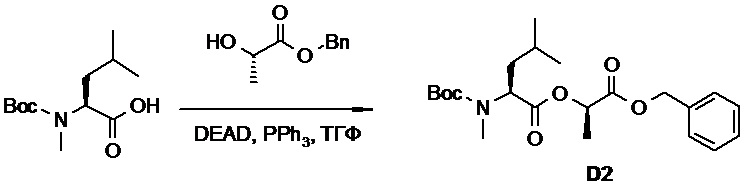
(2R)-1-(бензилокси)-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-метилпентаноат (D2): В 2-литровую круглодонную колбу в инертной атмосфере азота помещали тетрагидрофуран (1.5 л), (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метилпентановую кислоту (50 г, 203.82 ммоль, 1.00 экв.), бензил (2S)-2-гидроксипропаноат (36.7 г, 203.66 ммоль, 1.00 экв.), трифенилфосфин (85 г, 324.07 ммоль, 1.50 экв.). Затем добавляли DEAD (56.5 г, 324.43 ммоль, 1.20 экв.) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:50-1:10). В результате получали 82 г (99%) (2R)1-(бензилокси)-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-метилпентаноата в виде розового масла. MS (ESI, m/z): 408 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.41-7.31 (м, 5H), 5.31-5.10 (м, 3H), 5.01-4.73 (м, 1H), 2.77-2.74 (м, 3H), 1.72-1.65 (м, 2H), 1.60-1.58 (м, 1H), 1.52-1.50 (м, 3H), 1.47 (с, 9H), 0.96-0.94 (м, 6H).
Пример синтеза 19: Получение димера D3.
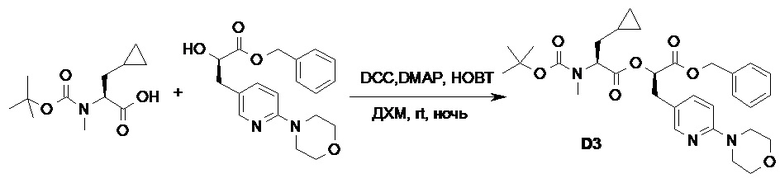
(2R)-1-(бензилокси)-3-[6-(морфолин-4-ил)пиридин-3-ил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D3): В круглодонную колбу объемом 100 мл помещали раствор (2S)-2-[[(трет-бутокси)карбонил] (метил)амино]-3-циклопропилпропановой кислоты (700 мг, 2.88 ммоль, 1.00 экв.) в дихлорметане (20 мл), бензил (2R)-2-гидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноат (1 г, 2.92 ммоль, 1.00 экв.). После этого добавляли DCC (660 мг, 3.20 ммоль, 1.10 экв.), порциями при 0°C. В полученную смесь добавляли 4-диметиламинопиридин (400 мг, 3.27 ммоль, 1.10 экв.), порциями при 0°C. В полученную смесь добавляли HOBT (440 мг, 3.26 ммоль, 1.10 экв.), порциями при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:3). В результате получали 1 г (61%) (2R)-1-(бензилокси)-3-[6-(морфолин-4-ил)пиридин-3-ил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде белого твердого вещества. MS (ESI, m/z): 568 [M+H]+.
Пример синтеза 20: Получение димера D4.
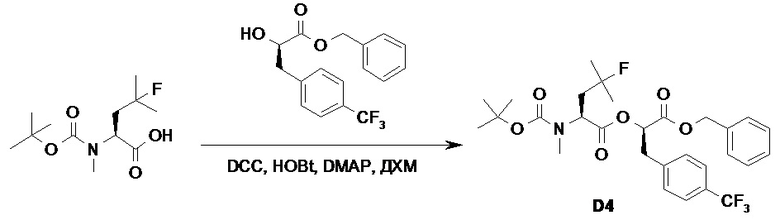
(2R)-1-(бензилокси)-1-оксо-3-[4-(трифторметил)фенил]пропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D4): В 1000-миллилитровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали раствор (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановой кислоты (15 г, 56.97 ммоль, 1.00 экв.) в дихлорметане (400 мл), бензил (2R)2-гидрокси-3-[4-(трифторметил)фенил]пропаноат (12 г, 37.00 ммоль, 1.00 экв.). Затем добавляли HOBT (7.5 г, 55.51 ммоль, 1.20 экв.), DCC (11 г, 53.31 ммоль, 1.20 экв.) и 4-диметиламинопиридин (6.8 г, 55.66 ммоль, 1.20 экв.) порциями при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10). В результате получали 21 г (65%) (2R)-1-(бензилокси)-1-оксо-3-[4-(трифторметил)фенил]пропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-фтор-4-метилпентаноата в виде красного масла. MS (ESI, m/z): 570 (M+H).
Пример синтеза 21: Получение димера D5.
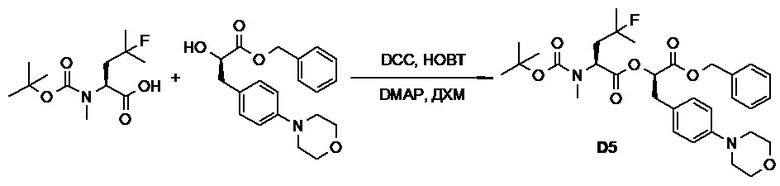
(2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D5): В 100-миллилитровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали дихлорметан (10 мл, 1.10 экв.), бензил (2R)-2-гидрокси-3-[4-(морфолин-4-ил)фенил]пропаноат (130 мг, 0.38 ммоль, 1.00 экв.), (2S)-2-[(трет-бутокси)карбонил](метил)амино-4-фтор-4-метилпентановую кислоту (100 мг, 0.38 ммоль, 1.00 экв.). Затем добавляли HOBT (57 мг, 0.42 ммоль, 1.10 экв.), DCC (86 мг, 0.42 ммоль, 1.10 экв.) и 4-диметиламинопиридин (51 мг, 0.42 ммоль, 1.10 экв.) порциями при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10). В результате получали 180 мг (80.5%) (2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде светло-желтого твердого вещества. MS (ESI, m/z): 587 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.38-7.36 (м, 4H), 7.29-7.25 (м, 1H), 7.20-6.99 (м, 4H), 5.27-5.18 (м, 1H), 5.18-5.09 (м, 2H), 5.08-4.83 (м, 1H), 4.01 (ушир, 4H), 3.23 (ушир, 4H), 3.15-3.05 (м, 2H), 2.68 (с, 3H), 2.28-1.91 (м, 2H), 1.51-1.28 (м, 15H).
Пример синтеза 22: Получение димера D6.
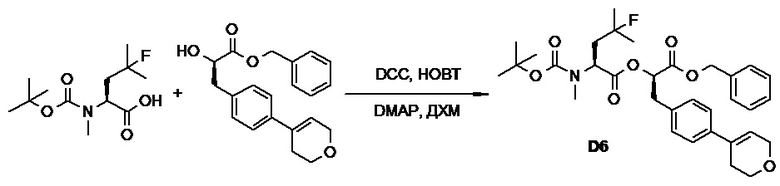
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D6): В 500-миллилитровую круглодонную колбу помещали дихлорметан (400 мл), (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановую кислоту (20 г, 75.96 ммоль, 1.00 экв.), бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноат (25.8 г, 76.24 ммоль, 1.00 экв.). Затем добавляли HOBT (12 г, 88.81 ммоль, 1.15 экв.), DCC (18 г, 87.24 ммоль, 1.15 экв.) и 4-диметиламинопиридин (10.7 г, 87.58 ммоль, 1.15 экв.) порциями при перемешивании при 0°C. Полученный раствор перемешивали в течение 4 часов при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10-1:5). В результате получали 80 г (90%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде бесцветного масла. MS (ESI, m/z): 584 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.37-7.16 (м, 7H), 7.14 (д, J=8.4 Гц, 2H), 6.12 (с, 1H), 5.28-5.25 (м, 1H), 5.15-5.13 (м, 2H), 5.12-4.81 (м, 1H), 4.35-4.33 (м, 2H), 3.95 (т, J=8.7 Гц, 2H), 3.18-3.14 (м, 2H), 2.68 (д, J=12.9 Гц, 3H), 2.53-2.49 (м, 2H), 2.22-2.10 (м, 1H), 2.06-1.85 (м, 1H), 1.48 (д, J=16.8 Гц, 9H), 1.39 (с, 3H), 1.32 (с, 3H).
Пример синтеза 23: Получение димера D7.
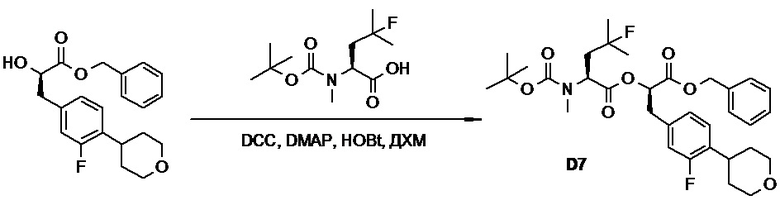
(2R)-1-(бензилокси)-3-[3-фтор-4-(оксан-4-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D7): В 100-миллилитровую круглодонную колбу помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановую кислоту (700 мг, 2.66 ммоль, 1.00 экв.), ДХМ (30 мл), бензил (2S)-3-[3-фтор-4-(оксан-4-ил)фенил]-2-гидроксипропаноат (513 мг, 1.43 ммоль, 1.00 экв.). Затем добавляли HOBT (262 мг, 1.94 ммоль, 1.10 экв.), DCC (442 мг, 2.14 ммоль, 1.10 экв.) и 4-диметиламинопиридин (290 мг, 2.37 ммоль, 1.10 экв.) порциями при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:5). В результате получали 850 мг (53%) (2R)-1-(бензилокси)-3-[3-фтор-4-(оксан-4-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде бесцветного масла. MS (ESI, m/z): 604 (M+H).
Пример синтеза 24: Получение димера D8.
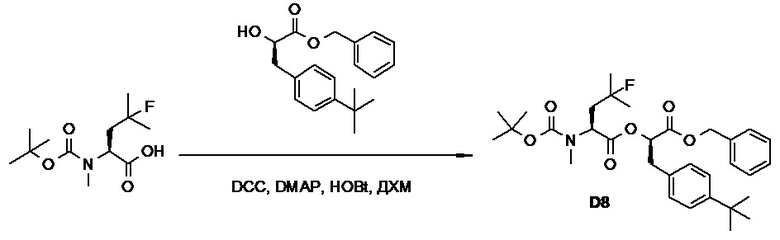
(2R)-1-(бензилокси)-3-(4-трет-бутилфенил)-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноат (D8): В 1000-миллилитровую 3-горлую круглодонную колбу помещали раствор (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентановой кислоты (25 г, 94.95 ммоль, 1.00 экв.) в дихлорметане (1000 мл), бензил (2R)-3-(4-трет-бутилфенил)-2-гидроксипропаноат (30 г, 96.03 ммоль, 1.00 экв.), DCC (40 г, 193.86 ммоль, 2.00 экв.), HOBT (26 г, 192.42 ммоль, 2.00 экв.), 4-диметиламинопиридин (23.5 г, 192.35 ммоль, 2.00 экв.). Полученный раствор перемешивали в течение 2 часов при комнатной температуре в бане лед/соль. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:50~1:10). В результате получали 50 г (94%) (2R)-1-(бензилокси)-3-(4-трет-бутилфенил)-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде бесцветного масла. MS (ESI, m/z): 558 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.35-7.27 (м, 7H), 7.12-7.09 (м, 2H), 5.27-4.62 (м, 4H), 3.15-3.09 (м, 2H), 2.69-2.61 (м, 3H), 2.20-1.82 (м, 2H), 1.61-1.31 (м, 24H).
Пример синтеза 25: Получение димера D9
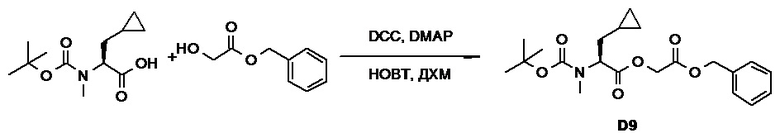
2-(Бензилокси)-2-оксоэтил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D9): В круглодонную колбу объемом 100 мл помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановую кислоту (1.5 г, 6.17 ммоль, 1.00 экв.), бензил 2-гидроксиацетат (1.02 г, 6.14 ммоль, 1.00 экв.) в дихлорметане (30 мл). После этого добавляли DCC (1.52 г, 7.37 ммоль, 1.20 экв.), 4-диметиламинопиридин (900 мг, 7.37 ммоль, 1.20 экв.) и HOBt (1.0 г, 7.40 ммоль, 1.20 экв.) соответственно порциями при перемешивании при 0°C. Результирующий раствор перемешивали в течение 12 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (3:1). В результате получали 2 г (83%) 2-(бензилокси)-2-оксоэтил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде желтого масла. MS (ESI, m/z): 392 (M+H); 1H ЯМР (300 МГц,CDCl3, м.д.): δ 7.42-7.32 (м, 5H), 5.19 (с, 2H), 4.96-4.91 (м, 0.5H), 4.71-4.65 (м, 2H), 4.65-4.63 (м, 0.5H), 2.87 (д, J = 14.1 Гц, 3H), 1.90-1.62 (м, 2H), 1.47 (д, J = 6.0 Гц, 9H), 0.78-0.67 (м, 1H), 0.49-0.42 (м, 2H), 0.13-0.09 (м, 2H).
Пример синтеза 26: Получение мономера D10.
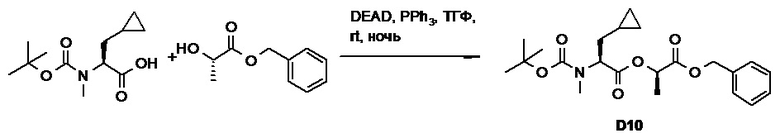
(S)-((R)-1-(бензилокси)-1-оксопропан-2-ил) 2-(трет-бутоксикарбонил(метил)амино)-3-циклопропилпропаноат (D10): В 3-горлую круглодонную колбу объемом 500 мл помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановую кислоту (4 г, 16.44 ммоль, 1.00 экв.), бензил (2S)-2-гидроксипропаноат (3 г, 16.65 ммоль, 1.00 экв.), PPh3 (5.2 г, 19.83 ммоль, 1.20 экв.), тетрагидрофуран (150 мл). После этого добавляли раствор DEAD (3.5 г, 20.10 ммоль, 1.20 экв.) в тетрагидрофуране (30 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:20). В результате получали 7 г (сырой) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде бесцветного масла. MS (ESI, m/z): 406 (M+H).
Пример синтеза 27: Получение мономера D11.
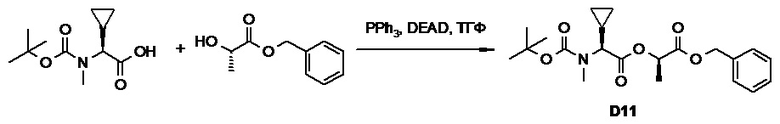
Бензил (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-2-циклопропилацетил] окси]пропаноат (D11): В 3-горлую круглодонную колбу объемом 250 мл в инертной атмосфере азота помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-2-циклопропилуксусную кислоту (3.4 г, 14.83 ммоль, 1.00 экв.), бензил (2S)-2-гидроксипропаноат (2.7 г, 14.98 ммоль, 1.00 экв.), тетрагидрофуран (100 мл), PPh3 (3.1 г, 11.82 ммоль, 1.20 экв.). После этого добавляли DEAD (4.7 г, 26.99 ммоль, 1.20 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:15). В результате получали 4.2 г (72%) бензил (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-2-циклопропилацетил]окси]пропаноата в виде желтого масла. MS (ESI, m/z): 392 (M+H); 1H ЯМР (300 МГц, CDCl3, м.д.): δ 7.41-7.34 (м, 5H), 5.24-5.15 (м, 3H), 4.08-3.66 (м, 1H), 2.97 (ушир, 3H), 1.53 (д, J = 6.9 Гц, 3H), 1.46 (с, 9H), 1.25-1.14 (м, 1H), 0.78-0.72 (м, 1H), 0.60-0.55 (м, 2H), 0.39-0.34 (м, 1H).
Пример синтеза 28: Получение мономера D12.
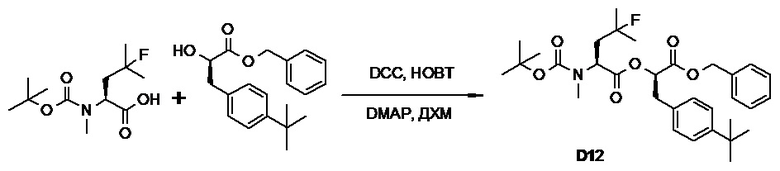
(2R)-1-(бензилокси)-3-[4-(циклогекс-1-ен-1-ил)-3-фторфенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D12): В 100-миллилитровую 3-горлую круглодонную колбу в инертной атмосфере азота помещали тетрагидрофуран (25 мл), бензил (2S)-3-[4-(циклогекс-1-ен-1-ил)-3-фторфенил]-2-гидроксипропаноат (710 мг, 2.00 ммоль, 1.00 экв.), (2S)-2-[(трет-бутокси)карбонил] (метил)амино-4-фтор-4-метилпентановую кислоту (527 мг, 2.00 ммоль, 1.00 экв.), PPh3 (790 мг, 3.01 ммоль, 1.50 экв.). Затем добавляли DEAD (517 мг, 2.97 ммоль, 1.50 экв.) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток очищали методом тонкослойной хроматографии, используя в качестве элюента смесь этилацетат/петролейный эфир (1/5). В результате получали 710 мг (59%) (2R)-1-(бензилокси)-3-[4-(циклогекс-1-ен-1-ил)-3-фторфенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде бесцветного масла. MS (ESI, m/z): 600 (M+H).
Пример синтеза 29: Получение мономера D13.
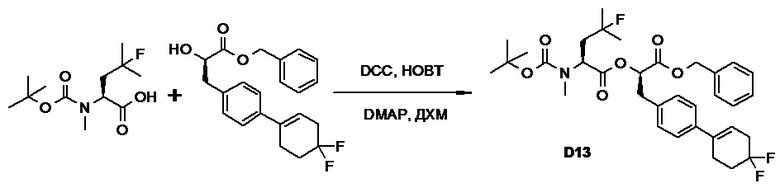
(2R)-1-(бензилокси)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D13): В 100-миллилитровую круглодонную колбу помещали дихлорметан (50 мл), бензил (2R)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-2-гидроксипропаноат (2 г, 5.37 ммоль, 1.00 экв.), (2S)-2-[(трет-бутокси)карбонил](метил)амино-4-фтор-4-метилпентановую кислоту (1.42 г, 5.39 ммоль, 1.10 экв.). Затем порциями добавляли HOBT (870 мг, 6.44 ммоль, 1.20 экв.). Затем порциями добавляли DCC (1.33 г, 6.45 ммоль, 1.20 экв.). В смесь порциями добавляли 4-диметиламинопиридин (780 мг, 6.38 ммоль, 1.20 экв.). Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:20-1:15). В результате получали 3.2 г (96%) (2R)-1-(бензилокси)-3-[4-(4,4-дифторциклогекс-1-ен-1-ил)фенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде бесцветного масла. MS (ESI, m/z): 618 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.36-7.34 (м, 5H), 7.26-7.25 (м, 2H), 7.14-7.11 (м, 2H), 5.89 (ушир, 1H), 5.29-5.23 (м, 1H), 5.18-5.06 (м, 2H), 4.89-4.78 (м, 1H), 3.17-3.10 (м, 2H), 2.77-2.65 (м, 7H), 2.23-1.97 (м, 2H), 1.59-1.15 (м, 17H).
Пример синтеза 30: Получение мономера D14.
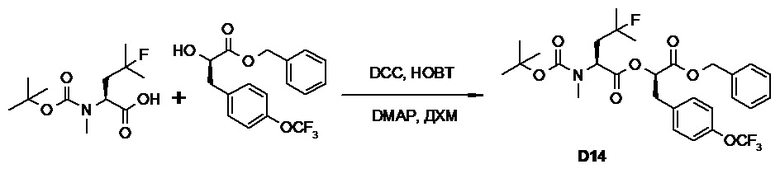
(2R)-1-(бензилокси)-1-оксо-3-[4-(трифторметокси)фенил]пропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D14): В 250-миллилитровую 3-горлую круглодонную колбу помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановую кислоту (3.1 г, 11.77 ммоль, 1.00 экв.), бензил (2R)-2-гидрокси-3-[4-(трифторметокси)фенил]пропаноат (4 г, 11.75 ммоль, 1.00 экв.), дихлорметан (120 мл). Затем добавляли DCC (2.7 г, 13.09 ммоль, 1.10 экв.), 4-диметиламинопиридин (1.6 г, 13.10 ммоль, 1.10 экв.) и HOBt (1.7 г, 12.58 ммоль, 1.10 экв.) порциями при перемешивании при 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1:10). В результате получали 3.5 г (51%) (2R)-1-(бензилокси)-1-оксо-3-[4-(трифторметокси)фенил]пропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 586 (M+H); 1H ЯМР (300 МГц, CDCl3): δ 7.39-7.37 (м, 4H), 7.28-7.26 (м, 1H), 7.19-7.08 (м, 4H), 5.30-5.27 (м, 1H), 5.22-5.10 (м, 2H), 5.05-4.82 (м, 1H), 3.19-3.16 (м, 2H), 2.66 (д, J=22.5 Гц, 3H), 2.28-2.16 (м, 1H), 2.07-1.92 (м, 1H), 1.51-1.33 (м, 15H).
Пример синтеза 31: Получение мономера D15.
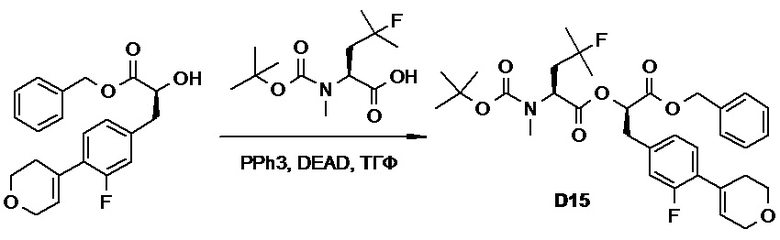
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-1-оксопропан-2-ил-(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D15): В 250-миллилитровую круглодонную колбу в инертной атмосфере азота помещали бензил (2S)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-2-гидроксипропаноат (700 мг, 1.96 ммоль, 1.00 экв.), (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановую кислоту (776 мг, 2.95 ммоль, 1.50 экв.), PPh3 (1.03 г, 3.93 ммоль, 2.00 экв.), тетрагидрофуран (50 мл). Затем добавляли DEAD (684 мг, 3.93 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Полученный раствор перемешивали в течение 2 часов при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем, используя в качестве элюента смесь этилацетат/петролейный эфир (1/4). В результате получали 950 мг (80%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)-3-фторфенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде светло-желтого масла. MS (ESI, m/z): 602 (M+H); 1H ЯМР (300 МГц, CD3OD): δ 7.36-7.28 (м, 5H), 7.14-7.12 (м, 1H), 6.97-6.93 (м, 2H), 6.03 (ушир, 1H), 5.33-5.31 (м, 1H), 5.17-5.12 (м, 2H), 4.93-4.90 (м, 0.5H), 4.73-4.56 (м, 0.5H), 4.34-4.23 (м, 2H), 3.88-3.83 (м, 2H), 3.15-3.12 (м, 2H), 2.75-2.71 (м, 3H), 2.50 (ушир, 2H), 2.31-1.97 (м, 2H), 1.47-1.23 (м, 15H).
Пример синтеза 32: Получение мономера D16.
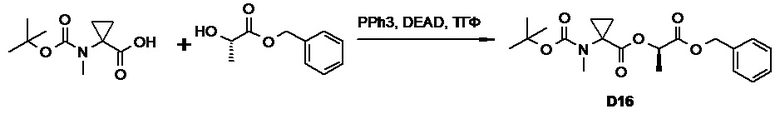
Бензил (2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)- карбонилокси] пропаноат (D16): В 3-горлую круглодонную колбу объемом 100 мл в инертной атмосфере азота помещали 1-[[(трет-бутокси)карбонил](метил)амино]циклопропан-1-карбоновую кислоту (2 г, 9.29 ммоль, 1.00 экв.), PPh3 (7.3 г, 27.83 ммоль, 3.00 экв.), тетрагидрофуран (35 мл), бензил (2S)-2-гидроксипропаноат (2.02 г, 11.21 ммоль, 1.20 экв.). После этого добавляли DEAD (4.86 г, 27.91 ммоль, 3.00 экв.) по каплям при перемешивании при 0°C в течение 10 минут. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Затем реакцию гасили добавлением 100 мл воды. Результирующий раствор экстрагировали 3x40 мл этилацетата, органические слои объединяли и промывали 1x30 мл насыщенного раствора хлорида натрия. Органические слои отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:3). В результате получали 2.8 г (80%) бензил (2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-пропаноата в виде оранжевого масла. MS (ESI, m/z): 378 (M+H).
Приведенные ниже Примеры синтеза 33 - 40 представляют собой неограничивающие иллюстрации способов получения соединений по настоящему изобретению. Квалифицированному специалисту будет понятно, что данные способы можно адаптировать для получения других соединений по настоящему изобретению.
Пример синтеза 33: Получение соединения 6-7A в Таблице 6, где Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил
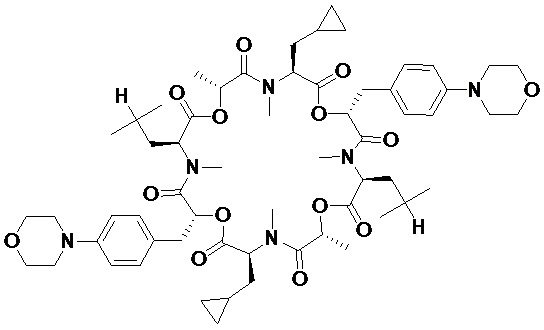
6-7A
Соединение 6-7A получали согласно Схемам 2 и 3, изображенным ниже.
Схема 2
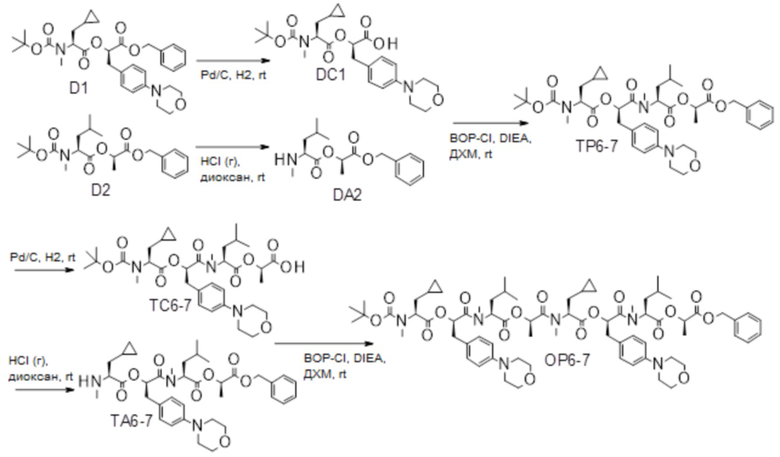
Схема 3
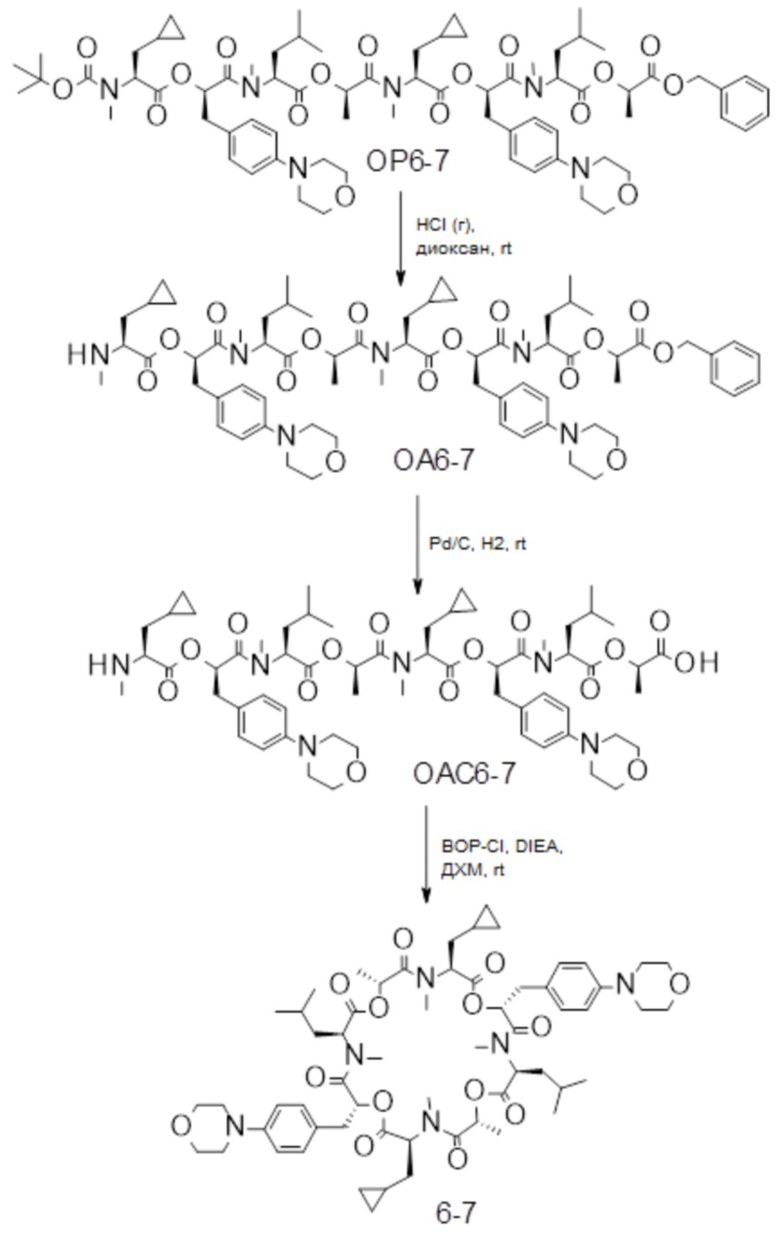
Подробное описание эксперимента
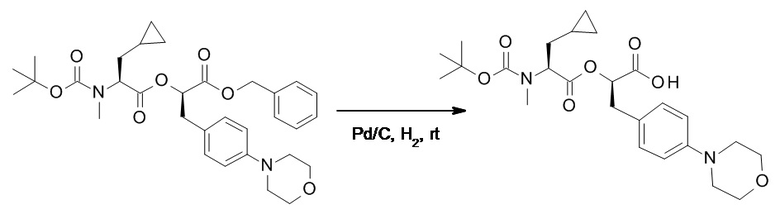
(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил] окси]-3-[4-(морфолин-4-ил)фенил]пропановая кислота (DC1): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (2.5 г, 4.41 ммоль, 1.00 экв.), метанол (100 мл), палладий на угле (500 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 2 г (95%) (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-3-[4-(морфолин-4-ил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 477 (M+H).
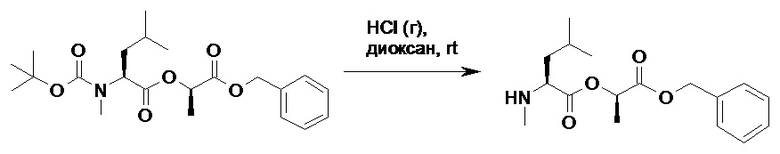
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-4-метил-2-(метиламино)пентаноат (DA2): В 3-горлую круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метилпентаноат (3.50 г, 8.35 ммоль, 1.00 экв.), дихлорметан (20 мл), HCl(газ)/диоксан (50 мл). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (насыщенный раствор). Результирующий раствор экстрагировали 3x100 мл дихлорметана, органические слои объединяли и промывали 3x100 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 2.42 г (94%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-4-метил-2-(метиламино)пентаноата в виде бесцветного масла. MS (ESI, m/z): 308 (M+H).
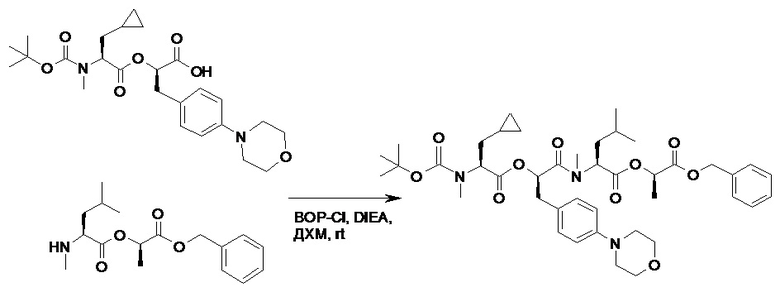
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил] (метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил] пропанамидо]-4-метилпентаноат (TP6-7): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-4-метил-2-(метиламино) пентаноат (1.35 г, 4.39 ммоль, 1.00 экв.), (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-3-[4-(морфолин-4-ил)фенил]пропановую кислоту (2 г, 4.20 ммоль, 1.00 экв.), дихлорметан (100 мл). После этого добавляли BOP-Cl (2.14 г, 8.41 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (1.08 г, 8.36 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/ петролейный эфир (1:3). В результате получали 2 г (59%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 766 (M+H).
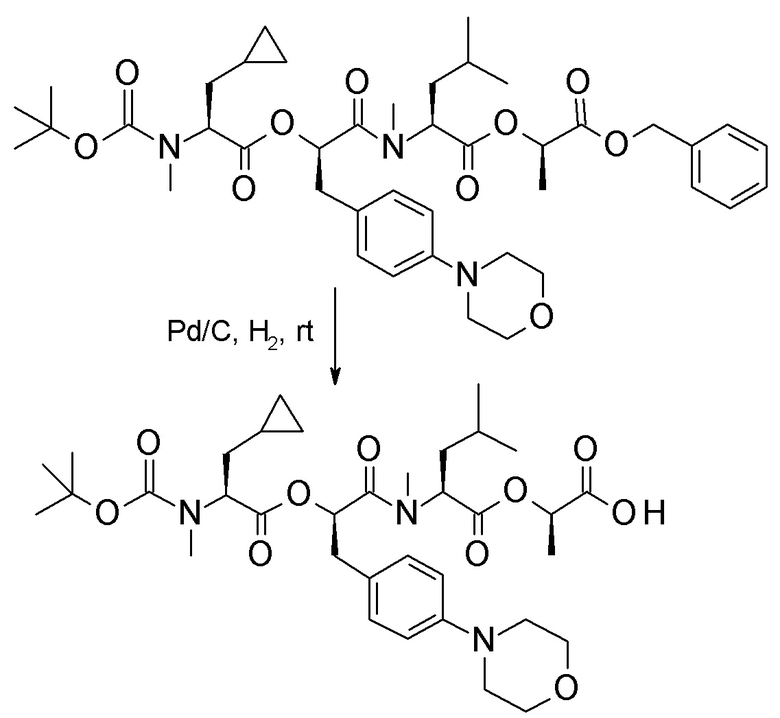
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил]окси]пропановая кислота (TC6-7): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси) карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил) фенил]пропанамидо]-4-метилпентаноат (1 г, 1.31 ммоль, 1.00 экв.), метанол (100 мл), палладий на угле (300 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 800 мг (91%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 676 (M+H).
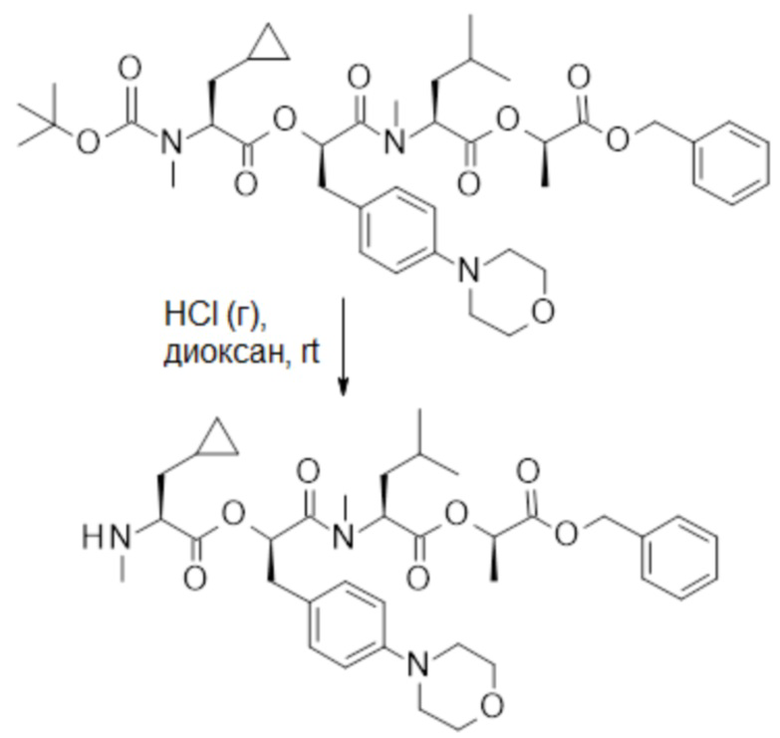
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноат (TA6-7): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил) амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноат (1 г, 1.31 ммоль, 1.00 экв.), HCl(газ)/диоксан (50 мл). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный насыщенный раствор). Результирующий раствор экстрагировали 3x100 мл дихлорметана, органические слои объединяли и промывали 3x100 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 820 мг (94%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил] пропанамидо]-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 666 (M+H).
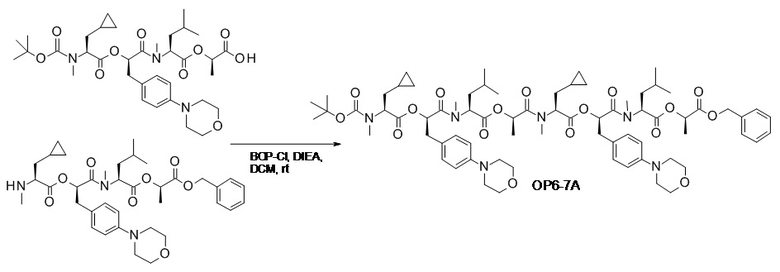
[(1R)-2-[[(1S)-2-[(1R)-2-[[(1S)-1-[(1R)-2-бензилокси-1-метил-2-оксо-этокси]карбонил-3-метил-бутил]-метил-амино]-1-[(4-морфолинофенил)метил]-2-оксо-этокси]-1-(циклопропилметил)-2-оксо-этил]-метил-амино]-1-метил-2-оксо-этил] (2S)-2-[[(2R)-2-[(2S)-2-[трет-бутоксикарбонил(метил)амино]-3-циклопропил-пропаноил]окси-3-(4-морфолинофенил)пропаноил]-метил-амино]-4-метил-пентаноат (OP6-7): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил]окси]пропановую кислоту (800 мг, 1.18 ммоль, 1.00 экв.), (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноат (788 мг, 1.18 ммоль, 1.00 экв.), дихлорметан (120 мл). После этого добавляли BOP-Cl (602 мг, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (304 мг, 2.35 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:1). В результате получали 850 мг (54%) OP6-7 в виде желтого твердого вещества. MS (ESI, m/z): 1324 (M+H).
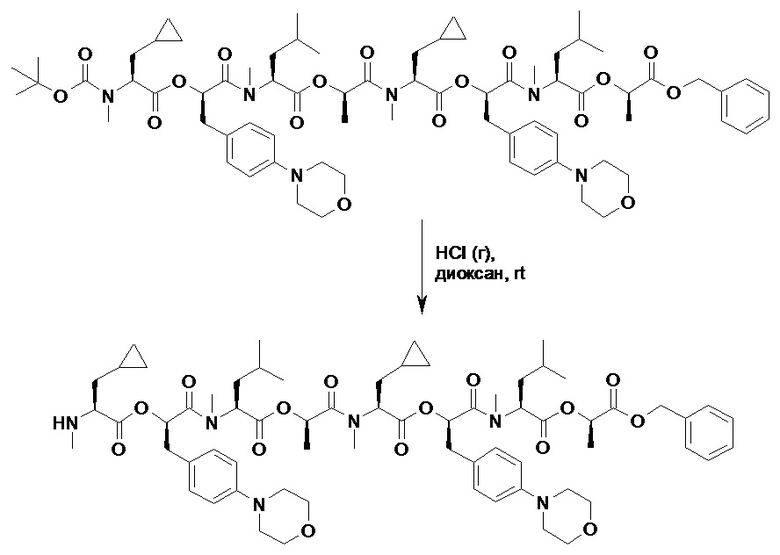
(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-4-метил-1-оксопентан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]этил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил] пропанамидо]-4-метилпентаноат (OA6-7): В круглодонную колбу объемом 100 мл помещали OP6-7 (850 мг, 0.64 ммоль, 1.00 экв.), HCl(газ)/диоксан (20 мл). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x60 мл дихлорметана, органические слои объединяли и промывали 3x100 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 800 мг (сырой) (1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-4-метил-1-оксопентан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]этил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино) пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноата (OA6-7) в виде желтого твердого вещества. MS (ESI, m/z): 1224 (M+H).
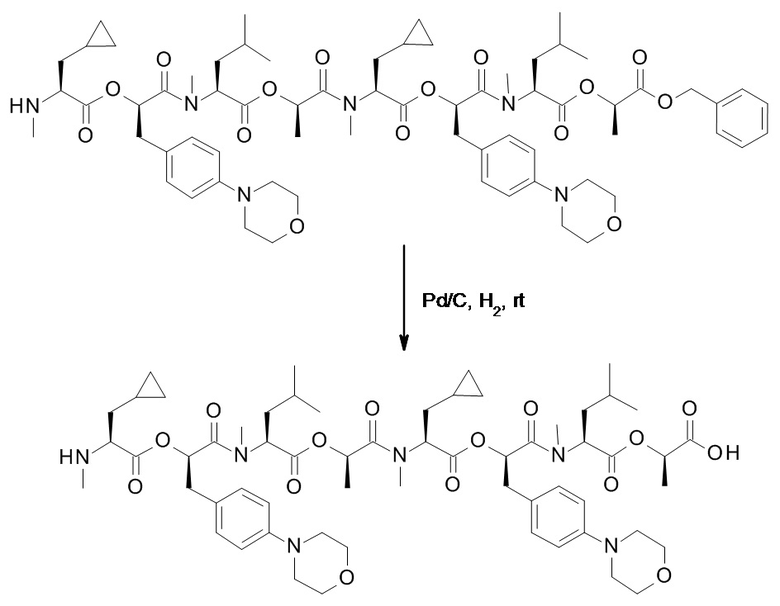
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил] пропанамидо]-4-метилпентаноил]окси]-N-метилпропанамидо]пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил]окси]пропановая кислота (OAC6-7): В круглодонную колбу объемом 100 мл помещали OA6-7 (800 мг, 0.65 ммоль, 1.00 экв.), метанол (50 мл), палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 720 мг (97%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил]окси]-N-метилпропанамидо] пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-4-метилпентаноил] окси]пропановой кислоты (OAC6-7) в виде белого твердого вещества. MS (ESI, m/z): 1134 (M+H).
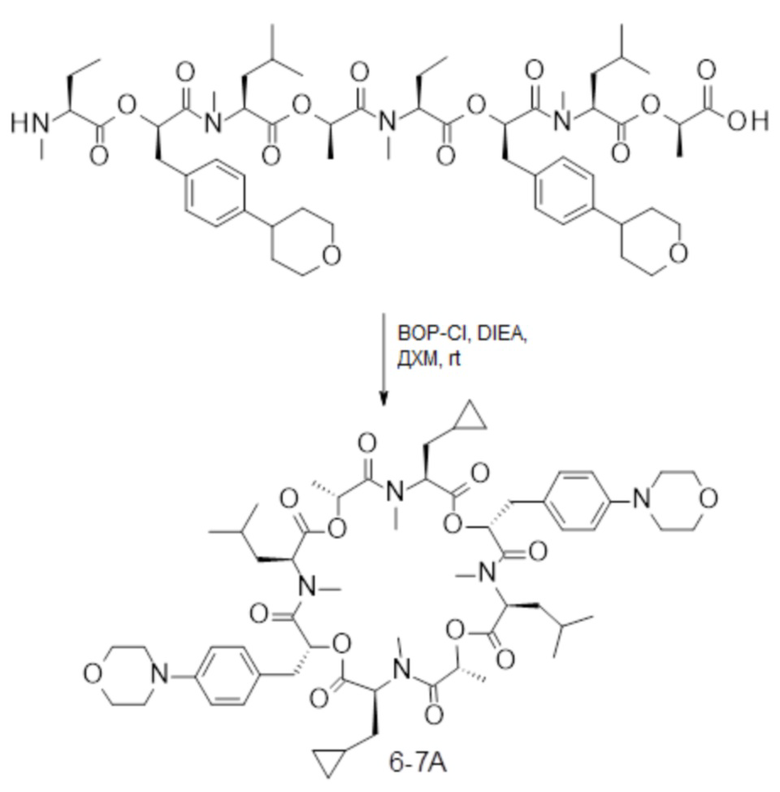
(3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-4,6,10,16,18,22-гексаметил-9,21-бис(2-метилпропил)-12,24-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (6-7A): В 3-горлую круглодонную колбу объемом 250 мл помещали OAC6-7 (720 мг, 0.64 ммоль, 1.00 экв.), дихлорметан (200 мл). После этого добавляли BOP-Cl (324 мг, 1.27 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (164 мг, 1.27 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, вода и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 220 нм. В результате получали 53.6 мг (8%) (3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-4,6,10,16,18,22-гексаметил-9,21-бис(2-метилпропил)-12,24-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона (6-7A) в виде белого твердого вещества. 1H-ЯМР (CD3OD, 300 МГц) δ: 7.22-7.15 (м, 4H), 6.94-6.85 (м, 4H), 5.73-5.62 (м, 2H), 5.55-5.15 (м, 5H), 4.82-4.72 (м, 1H), 3.85-3.75 (м, 8H), 3.15-2.98 (м, 18H), 2.98-2.86 (м, 6H), 2.22-1.35 (м, 12H), 1.01-0.98 (м, 3H), 0.94-0.69 (м, 14H), 0.69-0.05 (м, 9H); MS (ESI, m/z): 1116.0 (M+H); ; [α]= -91.66o, T=27.2 °C, C=0.90 г/100 мл в MeOH.
Пример синтеза 34: Получение соединения 9-7A в Таблице 9, где Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил
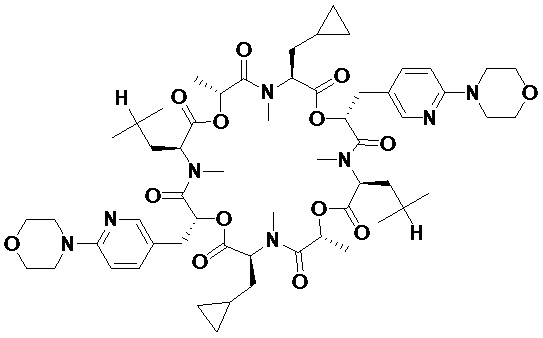
9-7A
Соединение 9-7A получали аналогично синтезу соединения 6-7A согласно Схемам 4 и 5, изображенным ниже.
Схема 4
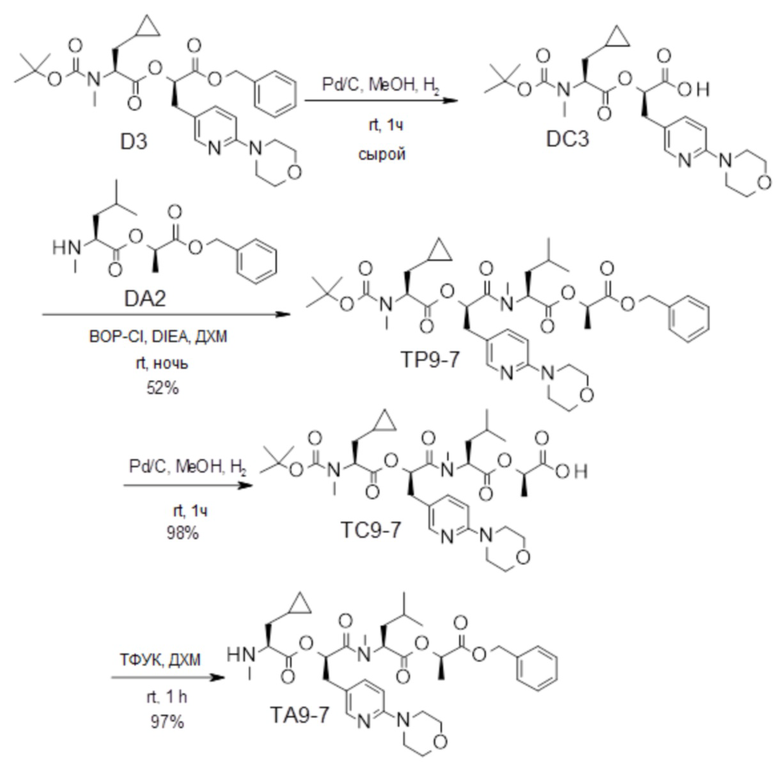
Схема 5
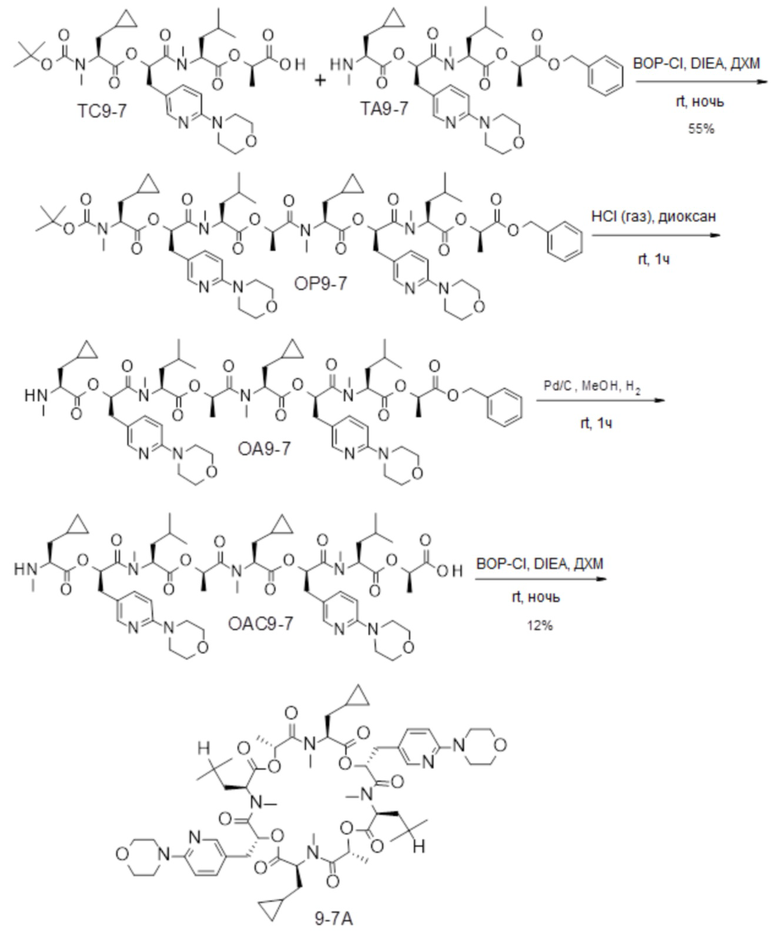
Подробное описание эксперимента
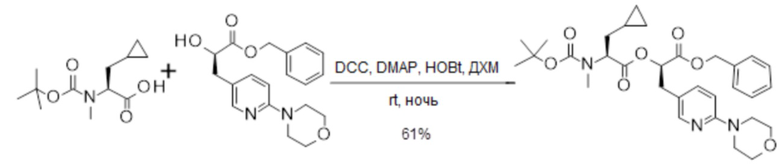
(2R)-1-(бензилокси)-3-[6-(морфолин-4-ил)пиридин-3-ил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D3): В круглодонную колбу объемом 100 мл помещали раствор (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановой кислоты (700 мг, 2.88 ммоль, 1.00 экв.), дихлорметан (20 мл), бензил (2R)-2-гидрокси-3-[6-(морфолин-4-ил)пиридин-3-ил]пропаноат (1 г, 2.92 ммоль, 1.00 экв.). После этого добавляли DCC (660 мг, 3.20 ммоль, 1.10 экв.), 4-диметиламинопиридин (400 мг, 3.27 ммоль, 1.10 экв.) и HOBT (440 мг, 3.26 ммоль, 1.10 экв.) порциями при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:3). В результате получали 1 г (61%) (2R)-1-(бензилокси)-3-[6-(морфолин-4-ил) пиридин-3-ил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D3) в виде белого твердого вещества. MS (ESI, m/z): 568 [M+H]+.
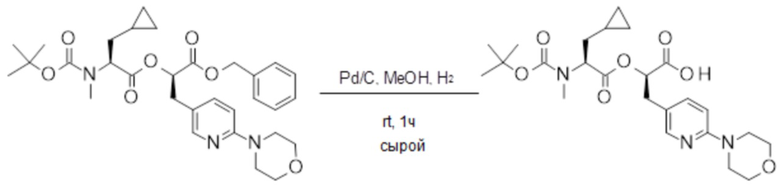
(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил] окси]-3-[6-(морфолин-4-ил)пиридин-3-ил]пропановая кислота (DC3) В круглодонную колбу объемом 250 мл помещали раствор (2R)-1-(бензилокси)-3-[6-(морфолин-4-ил)пиридин-3-ил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D3, 1.1 г, 1.94 ммоль, 1.00 экв.), метанол (15 мл) и палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1 г (сырой) (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-3-[6-(морфолин-4-ил)пиридин-3-ил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 478 [M+H]+.
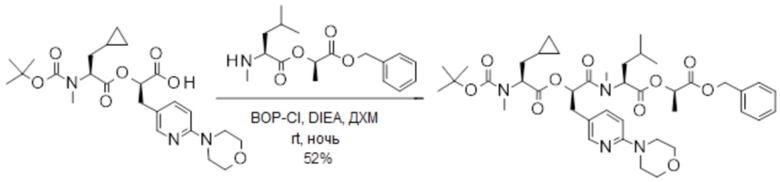
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил] (метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил]пропанамидо]-4-метилпентаноат (TP9-7): В 3-горлую круглодонную колбу объемом 100 мл помещали раствор (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-4-метил-2-(метиламино)пентаноата (1 г, 3.25 ммоль, 1.00 экв.), дихлорметан (30 мл) и (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-3-[6-(морфолин-4-ил)пиридин-3-ил]пропановую кислоту (650 мг, 1.36 ммоль, 1.00 экв.). После этого добавляли BOP-Cl (1.1 г, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (540 мг, 4.18 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:2). В результате получали 1.3 г (52%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси) карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил) пиридин-3-ил]пропанамидо]-4-метилпентаноата в виде белого твердого вещества. MS (ESI, m/z): 767 [M+H]+.
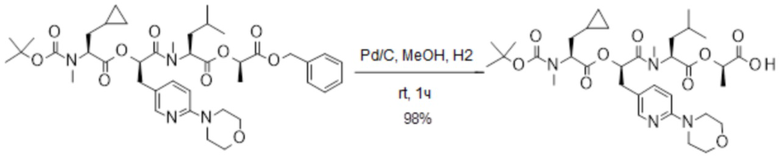
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил] пропанамидо]-4-метилпентаноил]окси]пропановая кислота (TC9-7): В круглодонную колбу объемом 100 мл помещали раствор (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил]пропанамидо]-4-метилпентаноата (650 мг, 0.85 ммоль, 1.00 экв.), метанол (15 мл) и палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 560 мг (98%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил] (метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил] пропанамидо]-4-метилпентаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 677 [M+H]+.
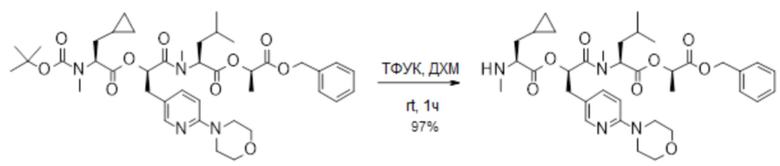
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил] пропанамидо]-4-метилпентаноат (TA9-7): В круглодонную колбу объемом 100 мл помещали раствор (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил]пропанамидо]-4-метилпентаноата (650 мг, 0.85 ммоль, 1.00 экв.), дихлорметан (10 мл). В полученную смесь добавляли трифторуксусную кислоту (1 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 9 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x20 мл дихлорметана и органические слои объединяли. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 550 мг (97%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино) пропаноил]окси]-N-метил-3-[6-(морфолин-4-ил)пиридин-3-ил]пропанамидо]-4-метилпентаноата в виде светло-желтого полутвердого вещества. MS (ESI, m/z): 667 [M+H]+.
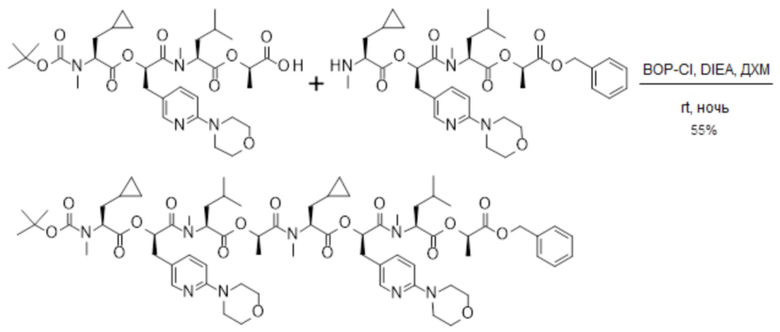
OP9-7: В 3-горлую круглодонную колбу объемом 250 мл помещали раствор TC9-7 (560 мг, 0.83 ммоль, 1.00 экв.), дихлорметан (50 мл) и TA9-7 (550 мг, 0.82 ммоль, 1.00 экв.). После этого добавляли BOP-Cl (421 мг, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (210 мг, 1.62 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:1). В результате получали 600 мг (55%) 9-7-6 в виде бесцветного масла. MS (ESI, m/z): 1326 [M+H]+.
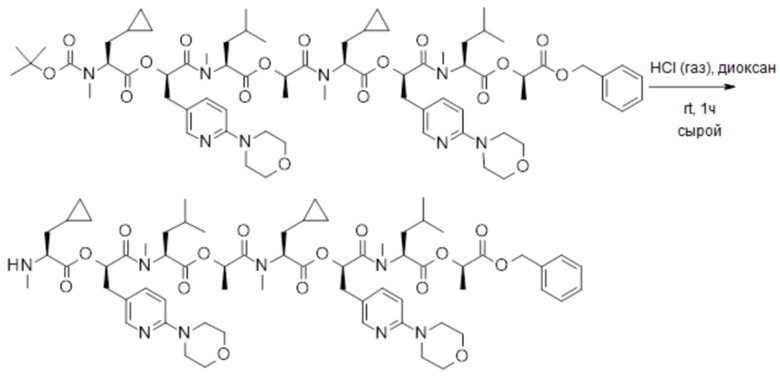
OA9-7: В 3-горлую круглодонную колбу объемом 100 мл помещали раствор OP9-7 (600 мг, 0.45 ммоль, 1.00 экв.), диоксан (20 мл). В полученную смесь вводили газообразный хлороводород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 9 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x20 мл дихлорметана и органические слои объединяли. Органическую фазу сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 510 мг (сырой) OA9-7 в виде желтого полутвердого вещества. MS (ESI, m/z): 1226 [M+H]+.
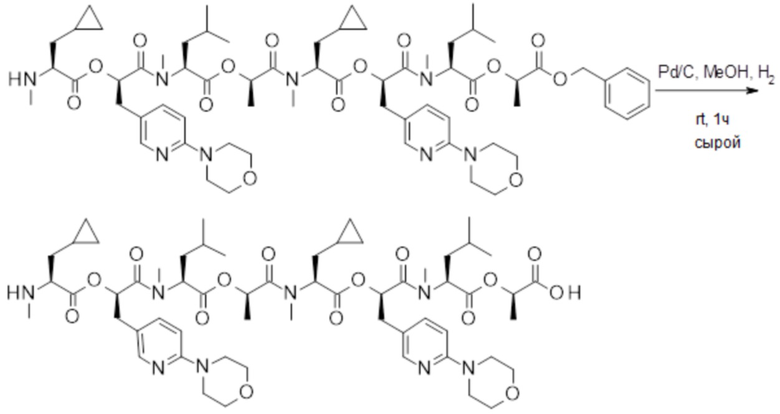
OAC9-7: В круглодонную колбу объемом 100 мл помещали раствор OA9-7 (510 мг, 0.42 ммоль, 1.00 экв.), метанол (10 мл) и палладий на угле (50 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 480 мг (сырой) OAC9-7 в виде белого твердого вещества. MS (ESI, m/z): 1136 [M+H]+.
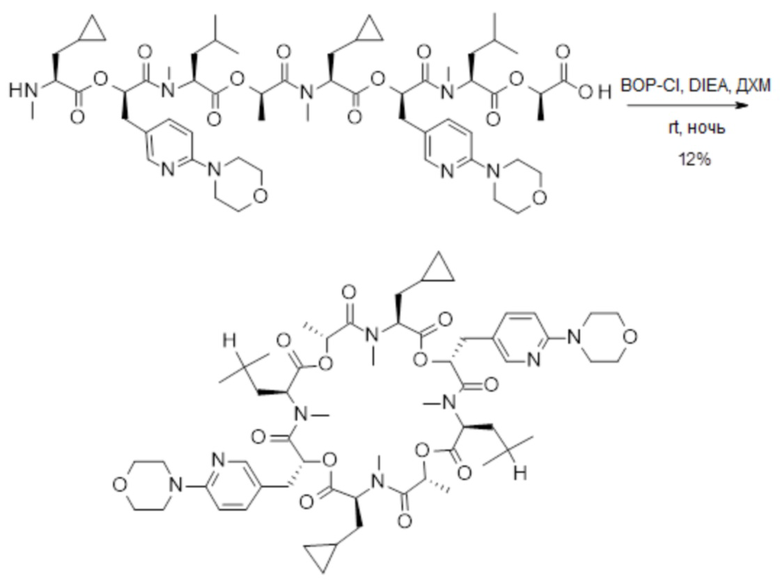
9-7A
(3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-4,6,10,16,18,22-гексаметил-9,21-бис(2-метилпропил)-12,24-бис([[6-(морфолин-4-ил)пиридин-3-ил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (9-7A): В 3-горлую круглодонную колбу объемом 250 мл помещали раствор OAC9-7 (480 мг, 0.042 ммоль, 1.00 экв.) и ДХМ (100 мл). После этого добавляли BOP-Cl (216 мг, 0.85 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (110 мг, 0.85 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, 0.05% Трифторуксусная кислота в воде и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 254 нм. В результате получали 57.2 мг (12%) (3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-4,6,10,16,18,22-гексаметил-9,21-бис(2-метилпропил)-12,24-бис([[6-(морфолин-4-ил)пиридин-3-ил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона (9-7) в виде белого твердого вещества. 1H ЯМР (CD3OD, 300 МГц) δ: 8.1-7.9 (м, 2H), 7.60-7.50 (м, 2H), 6.85-6.65 (м, 2H), 5.90-5.10 (м, 7H), 4.80-4.70 (м, 1H), 3.85-3.65 (м, 8H), 3.55-3.40 (м, 8H), 3.20-2.80 (м, 16H), 2.25-1.30 (м, 12H), 1.10 -0.70 (м, 17H), 0.70-0.35 (м, 5H), 0.30-0.01 (м, 4H); MS (ESI, m/z): 1118 [M+H]+ ; [α]= -77.34o, T=27.2°C, C=1.00 г/100 мл, MeOH.
Пример синтеза 35: Синтез соединения 6-34A в Таблице 6, где Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил
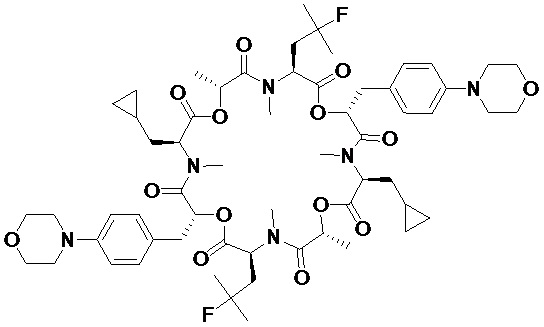
6-34A
Соединение 6-30A получали аналогично синтезу соединения 6-7A согласно Схемам 6 и 7, изображенным ниже.
Схема 6
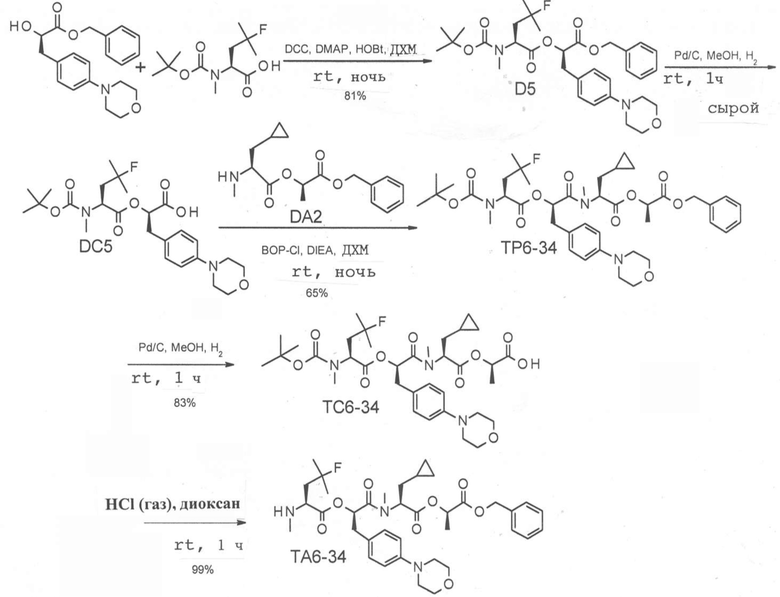
Схема 7
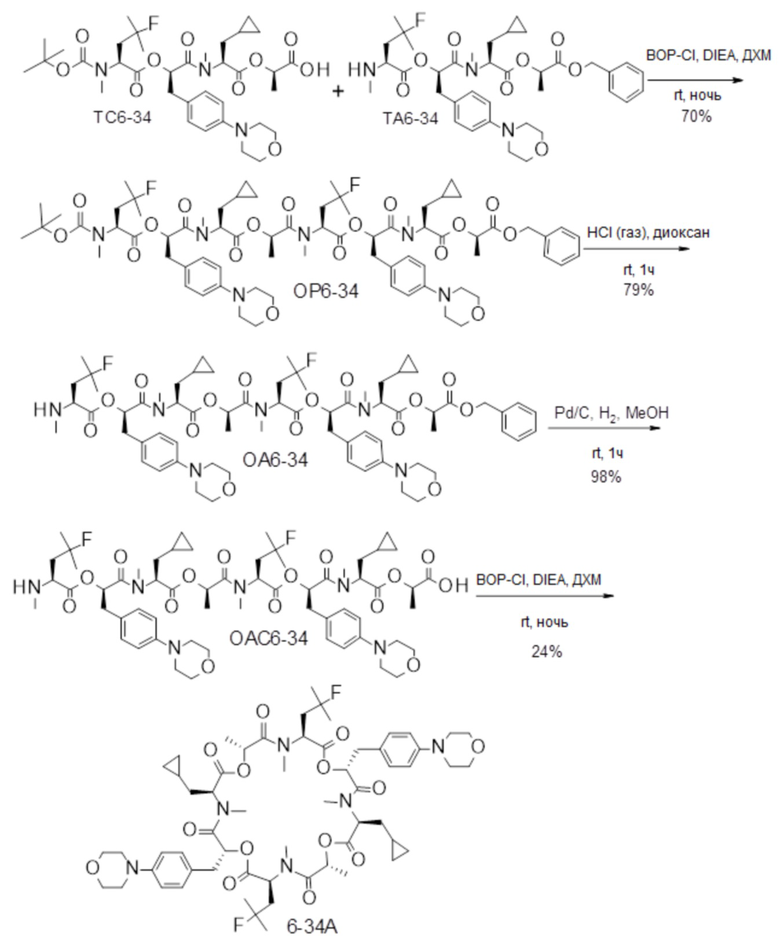
Подробное описание эксперимента
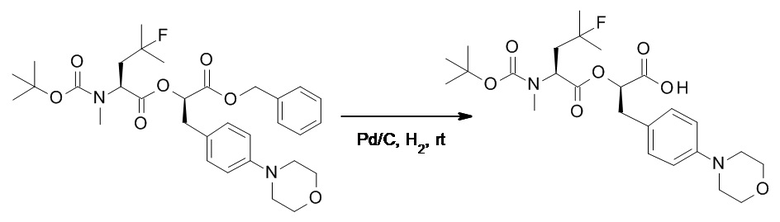
(R)-2-((S)-2-(трет-бутоксикарбонил(метил)амино)-4-фтор-4-метилпентаноилокси)-3-(4-морфолинофенил)пропановая кислота (DC5): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-3-[4-(морфолин-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D5, 3.5 г, 5.97 ммоль, 1.00 экв.), метанол (100 мл), палладий на угле (1 г). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 3 г (сырой) (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил] окси]-3-[4-(морфолин-4-ил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 497 (M+H).
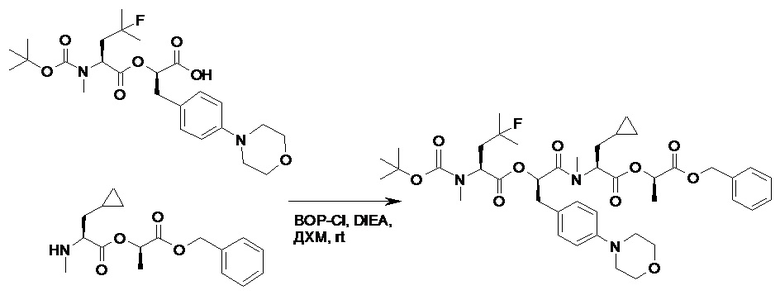
(S)-((R)-1-(((S)-1-((R)-1-(бензилокси)-1-оксопропан-2-илокси)-3-циклопропил-1-оксопропан-2-ил)(метил)амино)-3-(4-морфолинофенил)-1-оксопропан-2-ил) 2-(трет-бутоксикарбонил(метил)амино)-4-фтор-4-метилпентаноат (TP6-34): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-3-циклопропил-2-(метиламино)пропаноат (DA2, 1.8 г, 5.89 ммоль, 1.00 экв.), (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-3-[4-(морфолин-4-ил)фенил]пропановую кислоту (DC5, 3 г, 6.04 ммоль, 1.00 экв.), дихлорметан (120 мл). После этого добавляли BOP-Cl (3.1 г, 12.18 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (1.6 г, 12.38 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:6). В результате получали 3 г (65%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI,m/z): 784 (M+H).
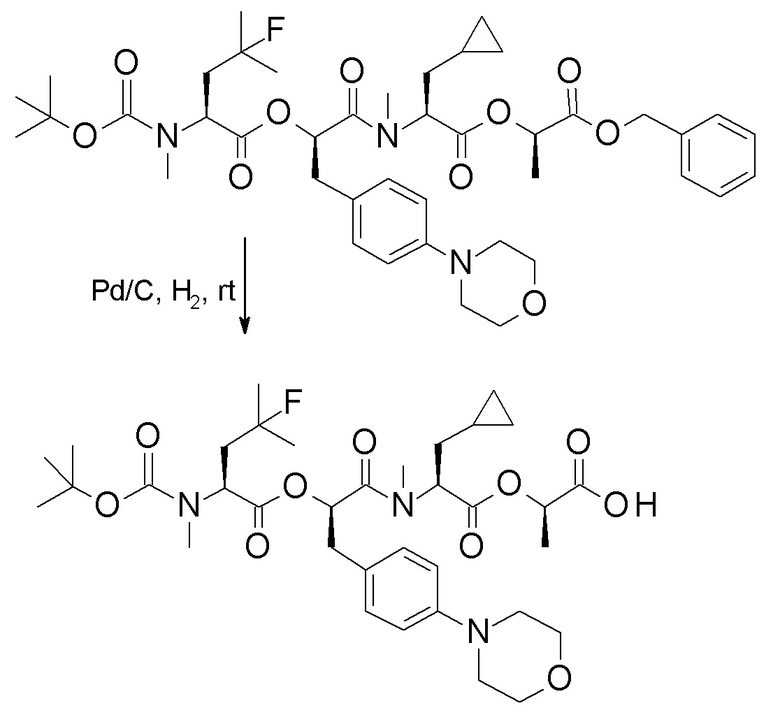
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановая кислота (TC6-34): В круглодонную колбу объемом 250 мл помещали (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (TP6-34, 1.5 г, 1.91 ммоль, 1.00 экв.), метанол (100 мл), палладий на угле (500 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1.1 г (83%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI,m/z): 694 (M+H).
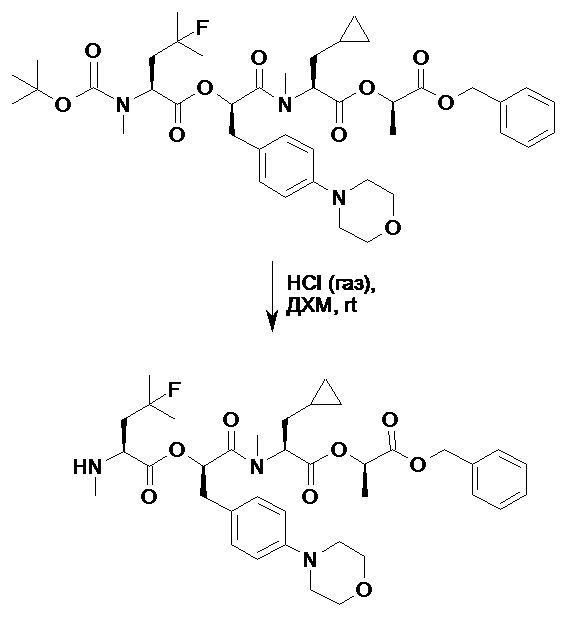
(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (TA6-34): В 3-горлую круглодонную колбу объемом 250 мл помещали (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (TP6-34, 1.5 г, 1.91 ммоль, 1.00 экв.), дихлорметан (100 мл). В полученный раствор пропускали HCl (газ). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x80 мл дихлорметана, органические слои объединяли и промывали 3x100 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 1.3 г (99%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино) пентаноата в виде желтого масла. MS (ESI,m/z): 684 (M+H).
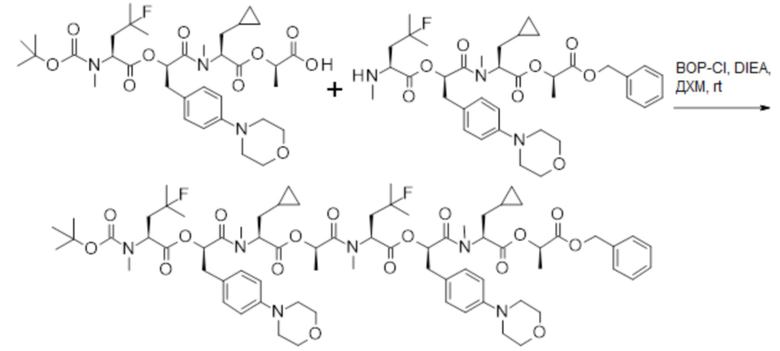
[(1R)-2-[[(1S)-2-[(1R)-2-бензилокси-1-метил-2-оксо-этокси]-1-(циклопропилметил)-2-оксо-этил]-метил-амино]-1-[(4-морфолинофенил)метил]-2-оксо-этил] (2S)-2-[[(2R)-2-[(2S)-2-[[(2R)-2-[(2S)-2-[трет-бутоксикарбонил(метил)амино]-4-фтор-4-метил-пентаноил] окси-3-(4-морфолинофенил)пропаноил]-метил-амино]-3-циклопропил-пропаноил] оксипропаноил]-метил-амино]-4-фтор-4-метил-пентаноат (OP6-34): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановую кислоту (TC6-34, 1.1 г, 1.59 ммоль, 1.00 экв.), (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (TA6-34, 1.1 г, 1.61 ммоль, 1.00 экв.), дихлорметан (120 мл). После этого добавляли BOP-Cl (808 мг, 3.17 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (409 мг, 3.16 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:1). В результате получали 1.5 г (70%) OP6-34 в виде желтого твердого вещества. MS (ESI, m/z): 1360 (Ms+H).
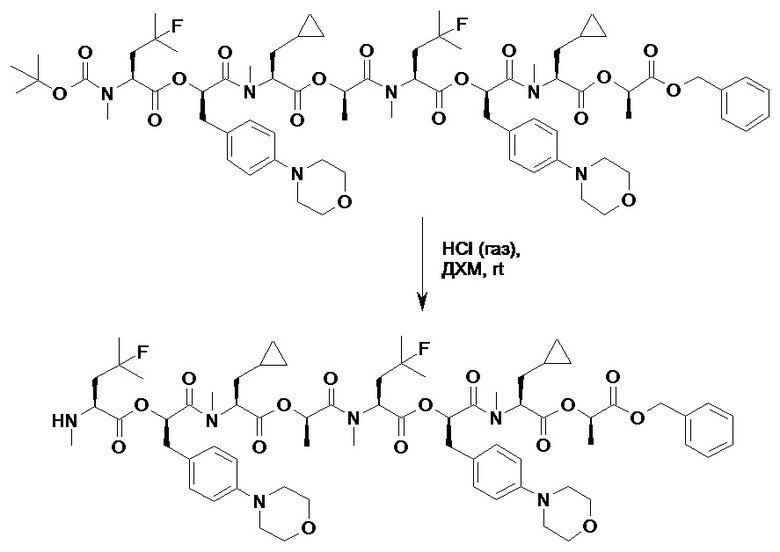
(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил] окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил) фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (OA6-34): В 3-горлую круглодонную колбу объемом 250 мл помещали OP6-34 (1.5 г, 1.10 ммоль, 1.00 экв.), дихлорметан (100 мл). В полученный раствор пропускали HCl (газ). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x100 мл дихлорметана, органические слои объединяли и промывали 3x100 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 1.1 г (79%) (1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил] (метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноата в виде желтого твердого вещества. MS (ESI,m/z): 1260 (M+H).
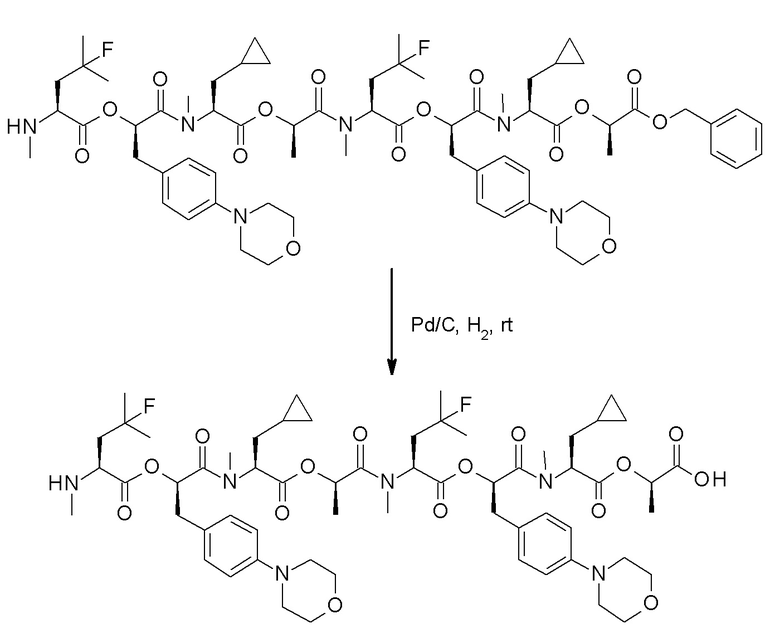
(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил]окси]-N-метил-3-[4-(морфолин-4-ил) фенил]пропанамидо]пропаноил]окси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил] окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]пропаноил]окси]пропановая кислота (OAC6-34): В круглодонную колбу объемом 250 мл помещали 1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (OA6-34, 1.1 г, 0.87 ммоль, 1.00 экв.), метанол (100 мл), палладий на угле (300 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1 г (98%) (2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил] окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]пропаноил]окси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил] пропанамидо]пропаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI,m/z): 1170 (M+H).
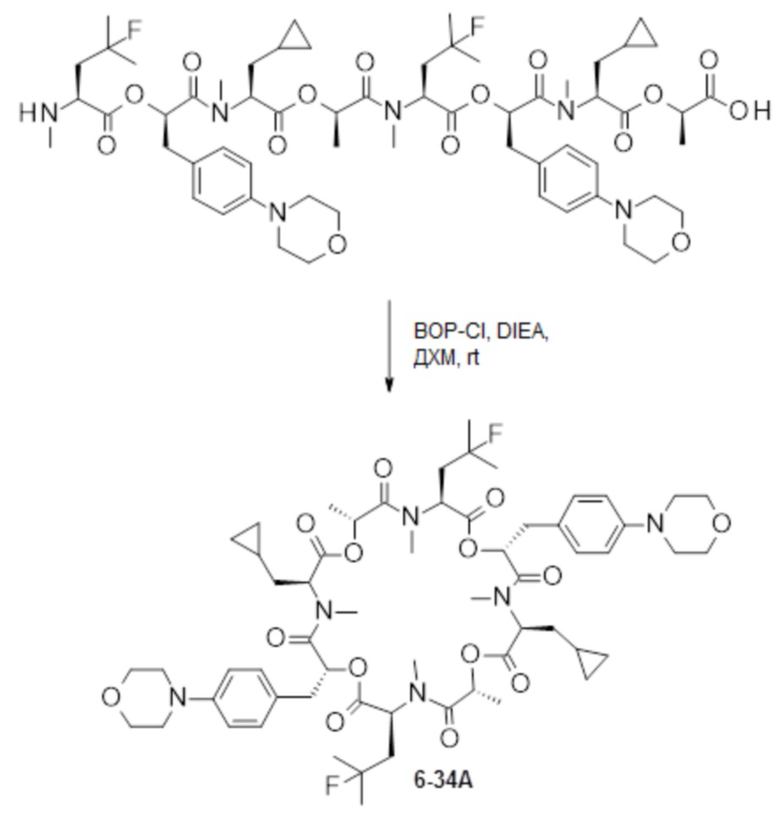
(3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,10,12,16,22,24-гексаметил-6,18-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (6-34A): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо] пропаноил]окси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]пропаноил]окси]пропановую кислоту (OAC6-34, 300 мг, 0.26 ммоль, 1.00 экв.), дихлорметан (150 мл). После этого добавляли BOP-Cl (131 мг, 0.51 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (66 мг, 0.51 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, вода и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 220 нм. В результате получали 72.3 мг (24%) (3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,10,12,16,22,24-гексаметил-6,18-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона в виде белого твердого вещества. MS (ESI,m/z): 1152 (M+H); 1H ЯМР: (300 МГц,CD3OD, м.д.): δ 7.19-7.12 (м, 4H), 6.98-6.81 (м, 4H), 5.88-5.55 (м, 2H), 5.55-5.16 (м, 5H), 5.01-4.88 (м, 1H), 3.92-3.78 (м, 8H), 3.19-2.82 (м, 24H), 2.35-2.00 (м, 4H), 1.92-1.55 (м, 3H), 1.55-1.20 (м, 18H), 1.02-0.91 (м, 1H), 0.55-0.11 (м, 10H); MS (ESI, m/z): 1152 [M+H]+; [a]= -71.7o, T=27.2°C, C = 0.75 г/100мл в MeOH.
Пример синтеза 36: Синтез соединения 6-1A в Таблице 6, где R', R'', R''' и R'''' каждый представляют собой метил
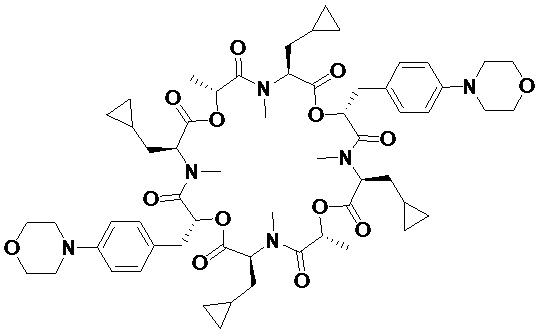
6-1A
Соединение 6-1A получали аналогично синтезу соединения 6-7A согласно Схемам 8 и 9, изображенным ниже.
Схема 8
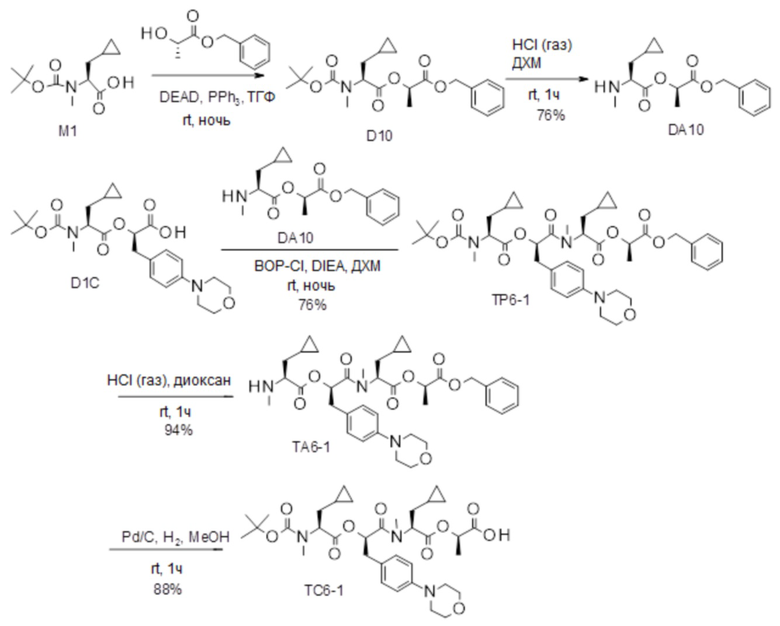
Схема 9
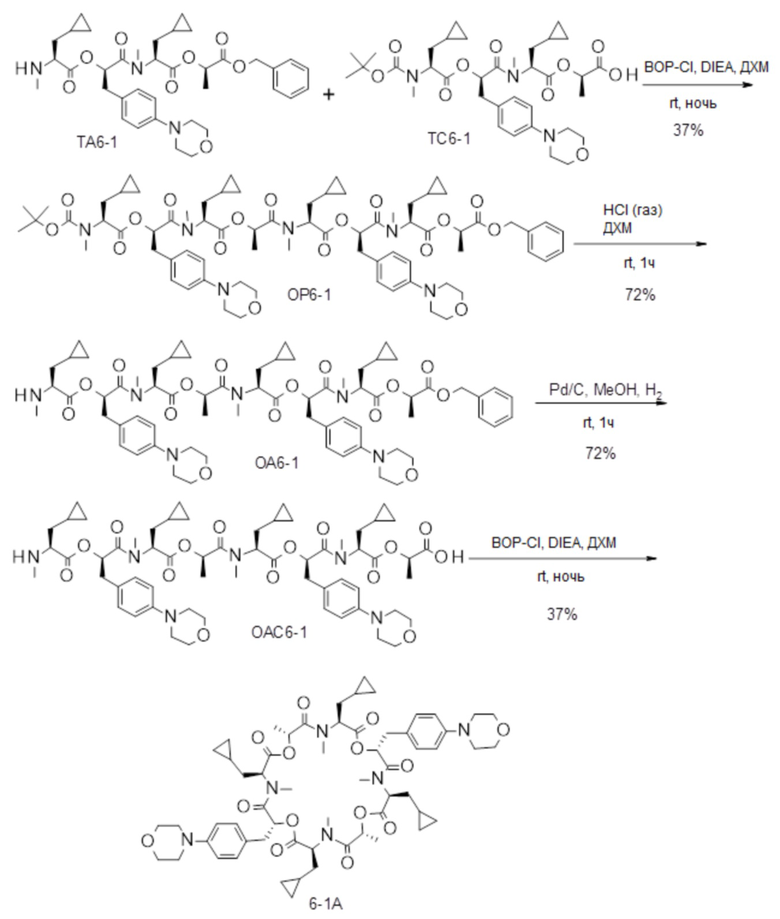
Подробное описание эксперимента
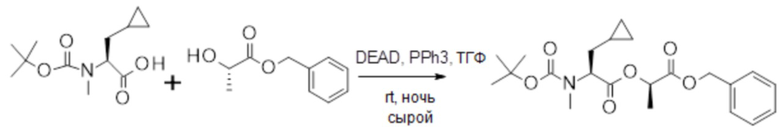
(S)-((R)-1-(бензилокси)-1-оксопропан-2-ил) 2-(трет-бутоксикарбонил(метил)амино)-3-циклопропилпропаноат (D10): В 3-горлую круглодонную колбу объемом 500 мл помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановую кислоту (4 г, 16.44 ммоль, 1.00 экв.), бензил (2S)-2-гидроксипропаноат (3 г, 16.65 ммоль, 1.00 экв.), PPh3 (5.2 г, 19.83 ммоль, 1.20 экв.), тетрагидрофуран (150 мл). После этого добавляли раствор DEAD (3.5 г, 20.10 ммоль, 1.20 экв.) в тетрагидрофуране (30 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:20). В результате получали 7 г (сырой) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде бесцветного масла. MS (ESI, m/z): 406 [M+H]+.
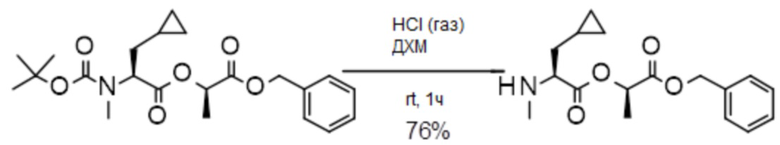
(S)-((R)-1-(бензилокси)-1-оксопропан-2-ил) 3-циклопропил-2-(метиламино)пропаноат (DA10): В круглодонную колбу объемом 500 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D10, 7 г, 17.26 ммоль, 1.00 экв.), дихлорметан (200 мл). В полученный раствор пропускали HCl (газ). Полученный раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x200 мл дихлорметана и органические слои объединяли. Органические слои промывали 3x200 мл насыщенного раствора хлорида натрия. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 4 г (76%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-3-циклопропил-2-(метиламино)пропаноата в виде желтого масла. MS (ESI, m/z): 306 [M+H]+.
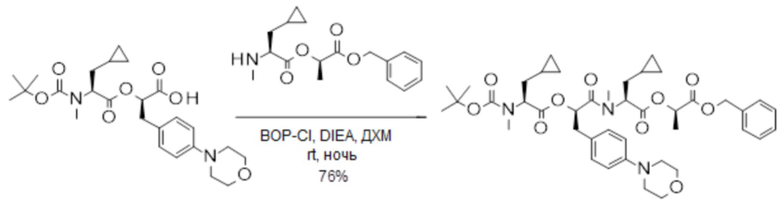
(S)-((R)-1-(((S)-1-((R)-1-(бензилокси)-1-оксопропан-2-илокси)-3-циклопропил-1-оксопропан-2-ил)(метил)амино)-3-(4-морфолинофенил)-1-оксопропан-2-ил) 2-(трет-бутоксикарбонил(метил)амино)-3-циклопропилпропаноат (TP6-1): В 3-горлую круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-3-циклопропил-2-(метиламино)пропаноат (DA10, 900 мг, 2.95 ммоль, 1.00 экв.), (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-3-[4-(морфолин-4-ил)фенил]пропановую кислоту (DC1, 1.3 г, 2.73 ммоль, 1.00 экв.), дихлорметан (80 мл). После этого добавляли BOP-Cl (1.5 г, 5.89 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (770 мг, 5.96 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:4). В результате получали 1.7 г (76%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-3-циклопропилпропаноата в виде желтого масла. MS (ESI, m/z): 764 [M+H]+.
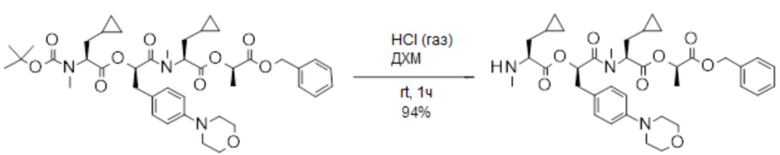
(S)-((R)-1-(бензилокси)-1-оксопропан-2-ил) 3-циклопропил-2-((R)-2-((S)-3-циклопропил-2-(метиламино)пропаноилокси)-N-метил-3-(4-морфолинофенил)пропанамидо) пропаноат (TA6-1): В круглодонную колбу объемом 100 мл помещали (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (TP6-1) (800 мг, 1.05 ммоль, 1.00 экв.), дихлорметан (60 мл). В полученный раствор пропускали HCl (газ). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x50 мл дихлорметана и органические слои объединяли. Органические слои промывали 3x60 мл насыщенного раствора хлорида натрия. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 650 мг (94%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-3-циклопропил-2-(метиламино)пропаноата в виде желтого масла. MS (ESI, m/z): 664 [M+H]+.
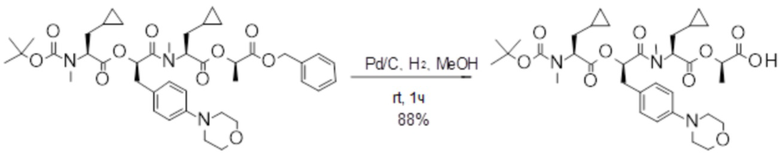
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановая кислота (TC6-1): В круглодонную колбу объемом 250 мл помещали (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (TP6-1, 800 мг, 1.05 ммоль, 1.00 экв.), палладий на угле (100 мг), метанол (80 мл). В полученный раствор пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Полученную смесь упаривали в вакууме. В результате получали 620 мг (88%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 674 [M+H]+.
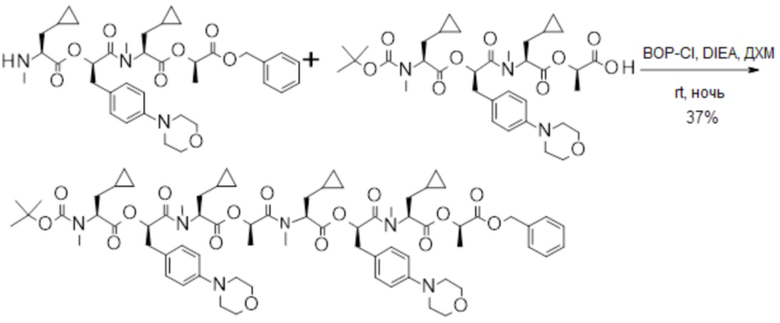
Соединение OP6-1: В 3-горлую круглодонную колбу объемом 250 мл помещали раствор TC6-1 (620 мг, 0.92 ммоль, 1.00 экв.), дихлорметан (100 мл), TA6-1 (611 мг, 0.92 ммоль, 1.00 экв.). После этого добавляли BOP-Cl (469 мг, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (237 мг, 1.83 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1/1). В результате получали 450 мг (37%) OP6-1 в виде желтого масла. MS (ESI, m/z): 1320 [M+H]+.
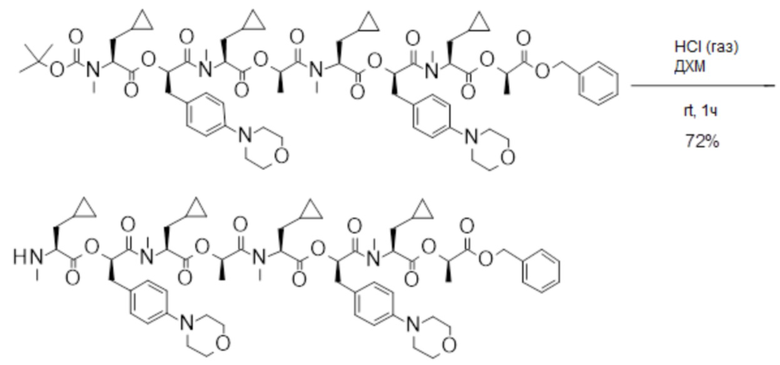
(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил] окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил) фенил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-3-циклопропил-2-(метиламино)пропаноат (OA6-1): В круглодонную колбу объемом 100 мл помещали OP6-1 (450 мг, 0.34 ммоль, 1.00 экв.), дихлорметан (50 мл). В полученный раствор пропускали HCl (газ). Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 3x50 мл дихлорметана и органические слои объединяли. Органический слой промывали 3x70 мл насыщенного раствора хлорида натрия. Органический слой сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 300 мг (72%) (1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-3-циклопропил-2-(метиламино)пропаноата в виде желтого масла. MS (ESI, m/z): 1220 [M+H]+.
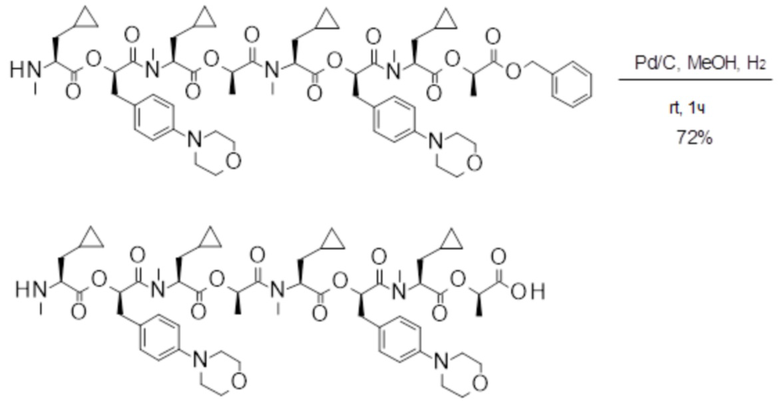
(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]пропаноил]окси]-N-метилпропанамидо] пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо]пропаноил]окси] пропановая кислота (OAC6-1): В круглодонную колбу объемом 100 мл помещали (1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(морфолин-4-ил)фенил]этил (2S)-3-циклопропил-2-(метиламино) пропаноат (OAC6-1) (300 мг, 0.25 ммоль, 1.00 экв.), метанол (50 мл), палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 200 мг (72%) (2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-3-циклопропил-2-(метиламино)пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил)фенил]пропанамидо] пропаноил]окси]-N-метилпропанамидо]пропаноил]окси]-N-метил-3-[4-(морфолин-4-ил) фенил]пропанамидо]пропаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 1130 [M+H]+.
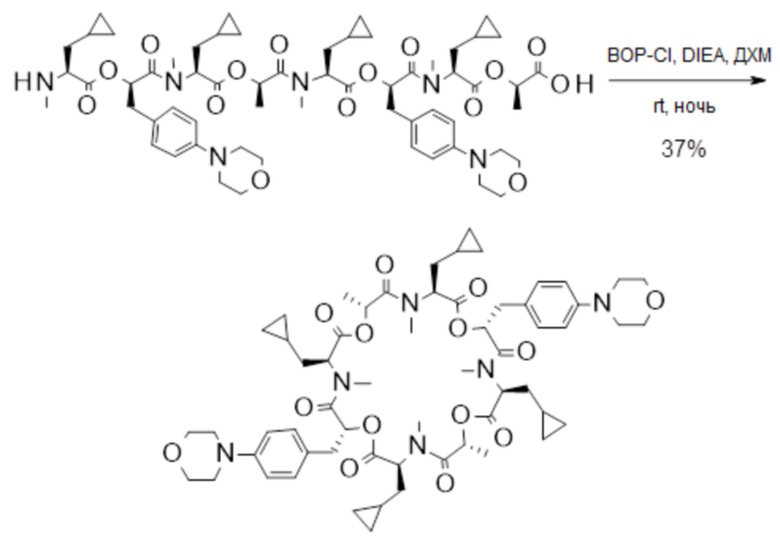
6-1A
(3S,6R,9S,12R,15S,18R,21S,24R)-3,9,15,21-тетракис(циклопропилметил)-4,10,12,16,22,24-гексаметил-6,18-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (6-1A): В 3-горлую круглодонную колбу объемом 250 мл помещали OAC6-1 (200 мг, 0.18 ммоль, 1.00 экв.), дихлорметан (120 мл). После этого добавляли BOP-Cl (90 мг, 0.35 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (46 мг, 0.36 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, вода и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 254 нм. В результате получали 24.7 мг (13%) (3S,6R,9S,12R,15S,18R,21S,24R)-3,9,15,21-тетракис(циклопропилметил)-4,10,12,16,22,24-гексаметил-6,18-бис([[4-(морфолин-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона в виде белого твердого вещества. 1H ЯМР (CD3OD, 300 МГц) δ: 7.31-7.08 (м, 4H), 6.98-6.81 (м, 4H), 5.08-5.02 (м, 7H), 4.82-4.68 (м, 1H), 3.92-3.76 (м, 8H), 3.25-2.82 (м, 24H), 2.51-1.18 (м, 13H), 1.08-0.95 (м, 2H), 0.78-0.03 (м, 19H); (ESI, m/z): 1111 [M+H]+. [α] = -110.72o, T=27.2°C, C = 0.23 г/100мл в MeOH.
Пример синтеза 37: Синтез соединения 7-34A в Таблице 7, где Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил
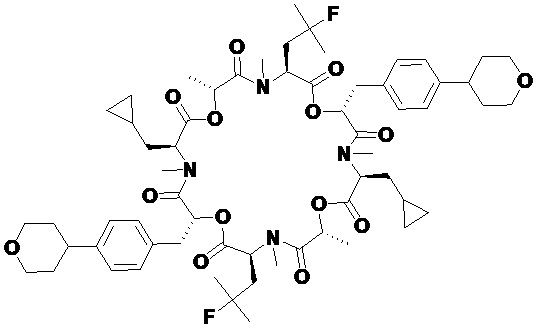
7-34A
Соединение 7-34A получали аналогично синтезу соединения 6-7A согласно Схемам 10 - 12, изображенным ниже.
Схема 10
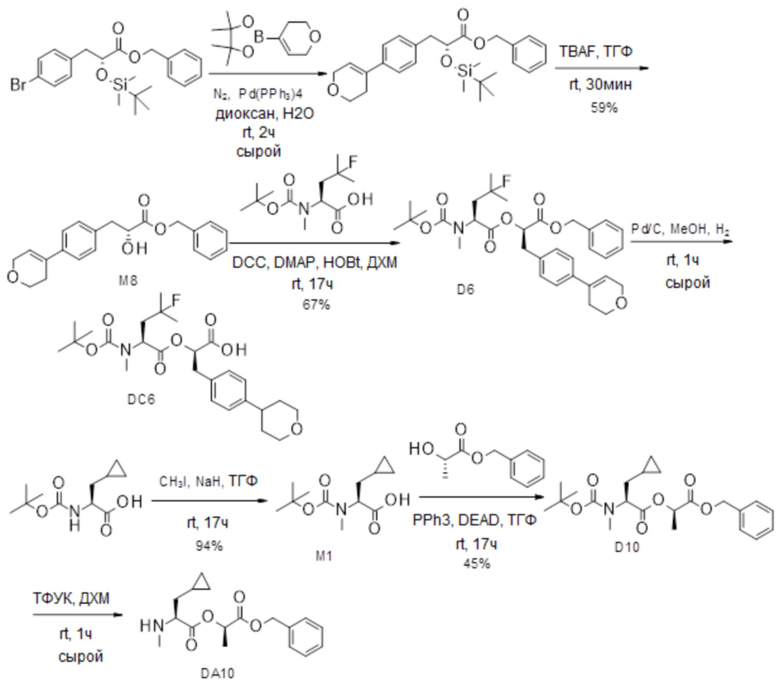
Схема 11
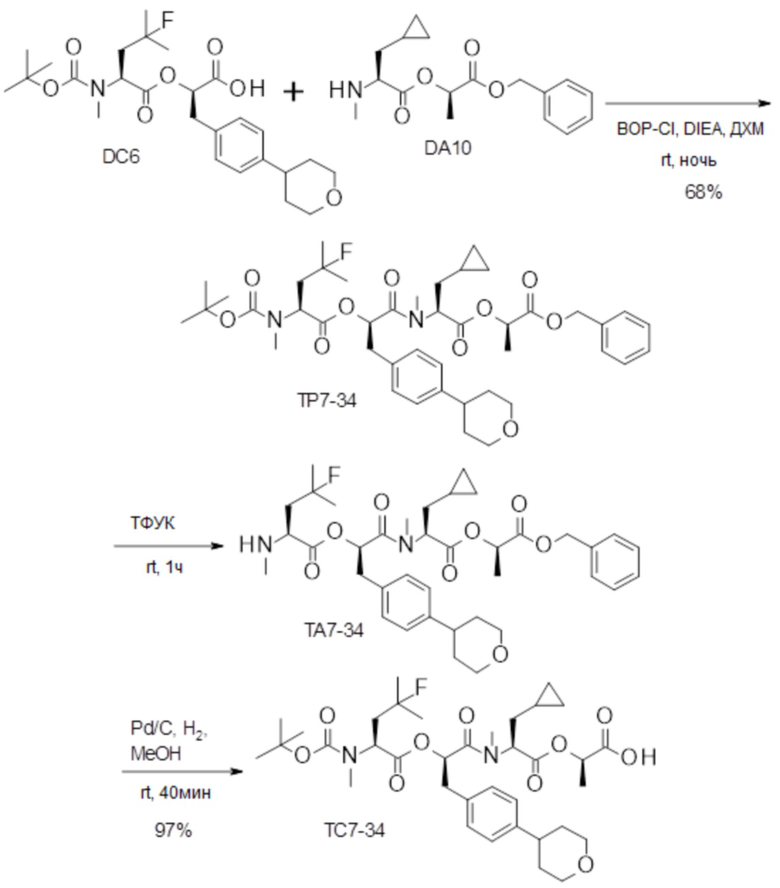
Схема 12
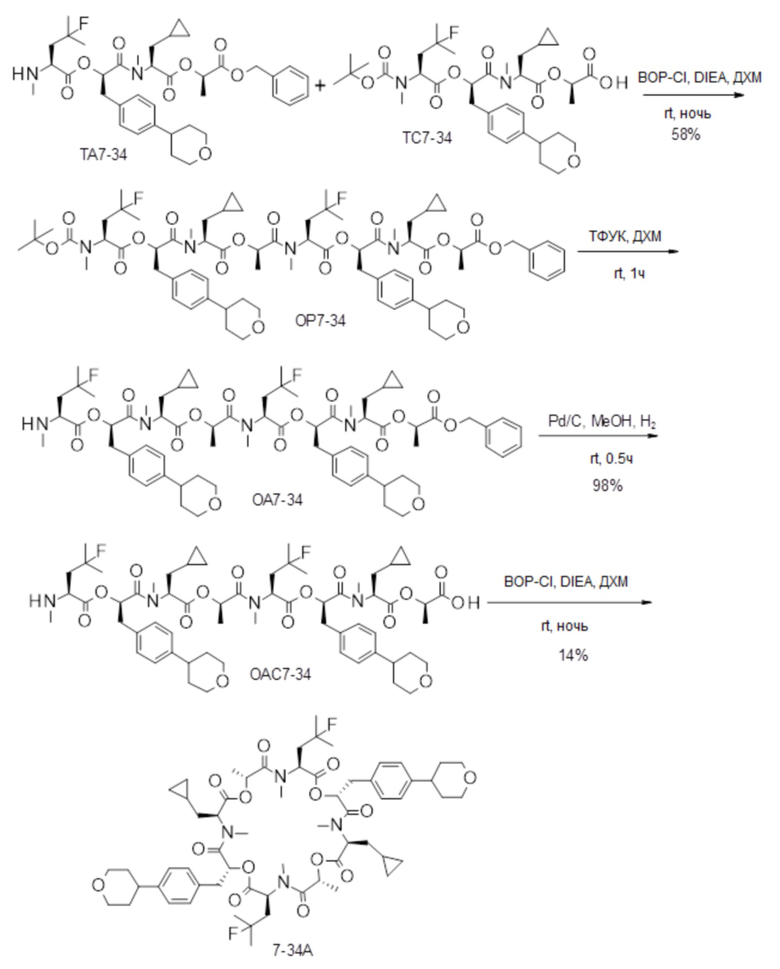
Подробное описание эксперимента
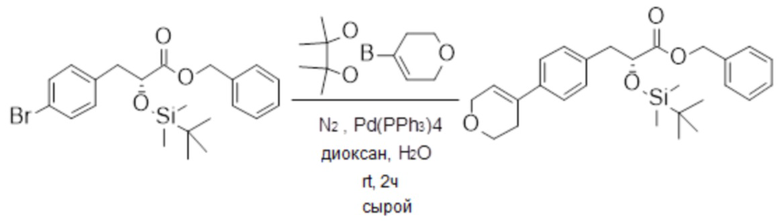
Бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил] пропаноат: В круглодонную колбу объемом 250 мл в инертной атмосфере азота помещали бензил (2R)-3-(4-бромфенил)-2-[(трет-бутилдиметилсилил)окси]пропаноат (7 г, 15.57 ммоль, 1.00 экв.), 2-(3,6-дигидро-2H-пиран-4-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (3.3 г, 15.71 ммоль, 1.00 экв.), карбонат натрия (5 г, 47.17 ммоль, 3.00 экв.), диоксан (50 мл), воду (10 мл), Pd(PPh3)4 (900 мг, 0.78 ммоль, 0.05 экв.). Результирующий раствор перемешивали в течение 2 ч при 75°C. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:10). В результате получали 8 г (сырой) бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]пропаноата в виде бесцветного масла. MS (ESI, m/z): 453 [M+H]+.
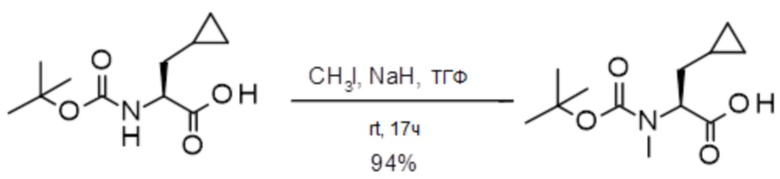
(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановая кислота: В 3-горлую круглодонную колбу объемом 1000 мл помещали (2S)-2-[[(трет-бутокси) карбонил]амино]-3-циклопропилпропановую кислоту (9 г, 39.25 ммоль, 1.00 экв.), тетрагидрофуран (500 мл), После этого добавляли гидрид натрия (4.7 г, 117.50 ммоль, 3.00 экв., 60%) порциями при 0°C. В полученную смесь добавляли CH3I (45 г, 317.04 ммоль, 8.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 17 ч при комнатной температуре. Затем реакцию гасили добавлением воды (500 мл). Результирующий раствор экстрагировали 3x500 мл метил-трет-бутилового эфира и водные слои объединяли. Значение pH раствора доводили до 4 с помощью лимонной кислоты. Результирующий раствор экстрагировали 3x500 мл этилацетата, органические слои объединяли. Органический слой промывали 1x500 мл насыщенного раствора хлорида натрия. Органический слой сушили над сульфатом натрия и упаривали в вакууме. В результате получали 8.99 г (94%) (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановой кислоты в виде желтого масла. MS (ESI, m/z) : 242 [M-H]-.
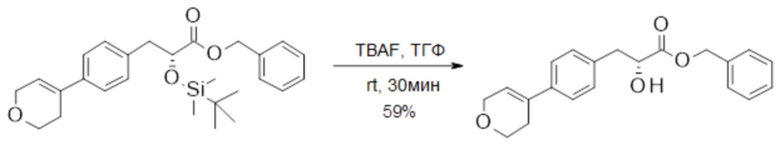
Бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноат: В 3-горлую круглодонную колбу объемом 250 мл помещали бензил (2R)-2-[(трет-бутилдиметилсилил)окси]-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]пропаноат (8 г, 17.67 ммоль, 1.00 экв.), тетрагидрофуран (60 мл), затем добавляли TBAF (6 г, 22.95 ммоль, 1.20 экв.) порциями при 0°C. Результирующий раствор перемешивали в течение 30 минут при комнатной температуре. Затем реакцию гасили добавлением воды (200 мл). Результирующий раствор экстрагировали 3x50 мл этилацетата, органические слои объединяли. Органический слой промывали 3x50 мл воды и 1x50 мл насыщенного раствора хлорида натрия. Органический слой сушили над сульфатом натрия и упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:7). В результате получали 3.5 г (59%) бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноата в виде белого твердого вещества.
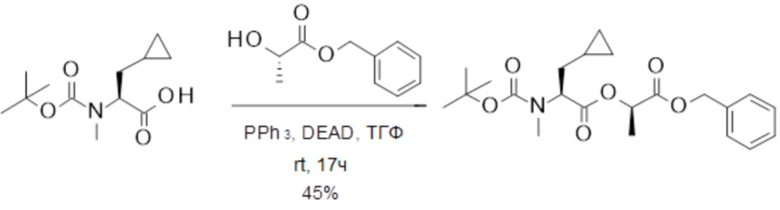
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропил-пропаноат: В 3-горлую круглодонную колбу объемом 100 мл в инертной атмосфере азота помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановую кислоту (4 г, 16.44 ммоль, 1.00 экв.), бензил (2S)-2-гидроксипропаноат (3 г, 16.65 ммоль, 1.00 экв.), тетрагидрофуран (30 мл), PPh3 (5.2 г, 19.83 ммоль, 1.20 экв.). В полученную смесь добавляли DEAD (3.5 г, 20.10 ммоль, 1.20 экв.) в тетрагидрофуране (10 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 17 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:20). В результате получали 3 г (45%) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде белого масла. MS (ESI, m/z): 406 [M+H]+.
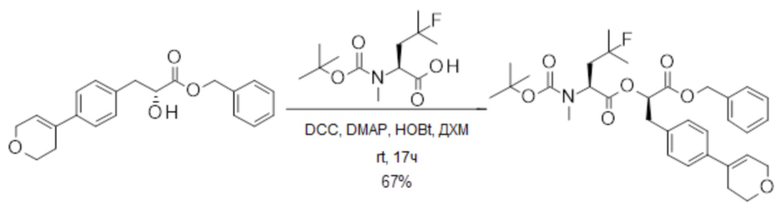
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D6): В 3-горлую круглодонную колбу объемом 50 мл помещали бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил) фенил]-2-гидроксипропаноат (1.3 г, 3.84 ммоль, 1.00 экв.), (2S)-2-[[(трет-бутокси)карбонил] (метил)амино]-4-фтор-4-метилпентановую кислоту (1 г, 3.80 ммоль, 1.00 экв.), дихлорметан (15 мл), После этого добавляли DCC (872 мг, 4.23 ммоль, 1.10 экв.), 4-диметиламинопиридин (516 мг, 4.22 ммоль, 1.10 экв.) и HOBT (571 мг, 4.23 ммоль, 1.10 экв.) порциями при 0°C. Результирующий раствор перемешивали в течение 17 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:8). В результате получали 1.5 г (67%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде белого твердого вещества. MS (ESI, m/z): 584 [M+H]+.
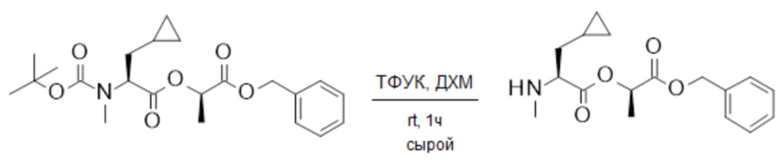
(2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-3-циклопропил-2-(метиламино)пропаноат (DA10): В 3-горлую круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D10, 1.5 г, 3.70 ммоль, 1.00 экв.), дихлорметан (30 мл), После этого добавляли трифторуксусную кислоту (7 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 100 мл дихлорметана, органические слои объединяли и сушили над сульфатом натрия и упаривали в вакууме. В результате получали 1.4 г (сырой) (2R)-1-(бензилокси)-1-оксопропан-2-ил (2S)-3-циклопропил-2-(метиламино)пропаноата в виде белого твердого вещества. MS (ESI, m/z): 306 [M+H]+.
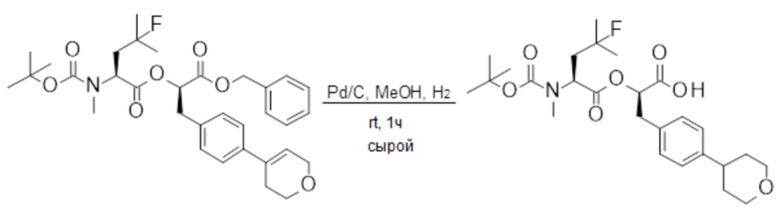
(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-3-[4-(ox-an-4-ил)фенил]пропановая кислота (DC6): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D6, 1.5 г, 2.57 ммоль, 1.00 экв.), MeOH (80 мл) и палладий на угле (800 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1.3 г (сырой) (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 496 [M+H]+.
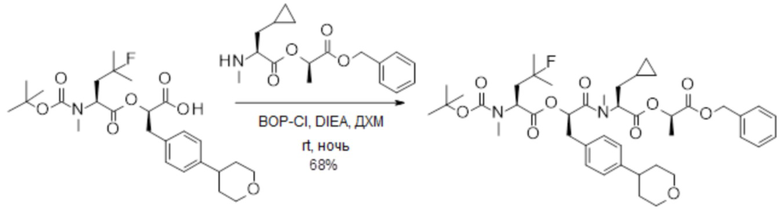
(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноат (TP7-34): В 3-горлую круглодонную колбу объемом 100 мл помещали DC6 (1.3 г, 2.62 ммоль, 1.00 экв.), DA10 (801 мг, 2.62 ммоль, 1.00 экв.), дихлорметан (20 мл), затем добавляли BOP-Cl (1.3 г, 5.11 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (678 мг, 5.25 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:8). В результате получали 1.4 г (68%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил] этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде белого твердого вещества. MS (ESI, m/z): 783 [M+H]+.
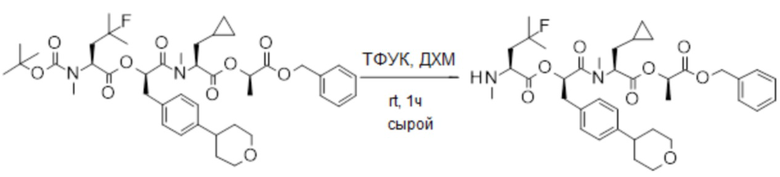
(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (TA7-34): В 3-горлую круглодонную колбу объемом 50 мл помещали TP7-34 (700 мг, 0.89 ммоль, 1.00 экв.), дихлорметан (15 мл). После этого добавляли трифторуксусную кислоту (3 мл), по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 50 мл дихлорметана и органические слои объединяли. Органические слои сушили над безводным сульфатом натрия и упаривали в вакууме. В результате получали 650 мг (сырой) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноата (TA7-34) в виде белого твердого вещества. MS (ESI, m/z): 683 [M+H]+.
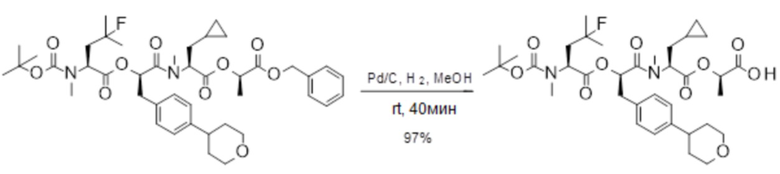
(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановая кислота (TC7-34): В круглодонную колбу объемом 100 мл помещали TP7-34 (700 мг, 0.89 ммоль, 1.00 экв.), метанол (30 мл), палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 40 мин при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 600 мг (97%) (2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 693 [M+H]+.
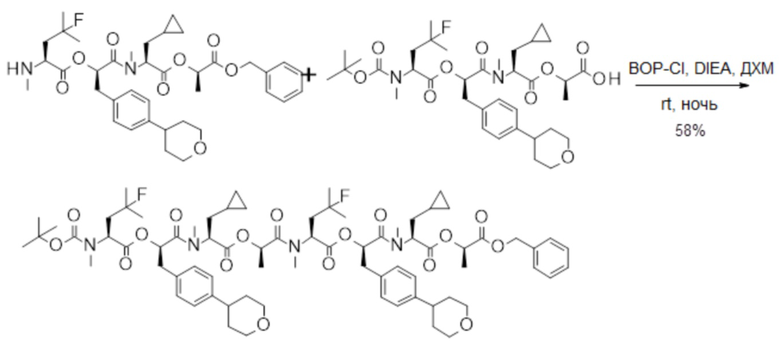
Соединение OP7-34: В 3-горлую круглодонную колбу объемом 50 мл помещали TA7-34 (650 мг, 0.95 ммоль, 1.00 экв.), TC7-34 (600 мг, 0.87 ммоль, 1.00 экв.), дихлорметан (15 мл). После этого добавляли BOP-Cl (486 мг, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (246 мг, 1.90 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем и элюировали смесью этилацетат/петролейный эфир (1:3). В результате получали 750 мг (58%) OP7-34 в виде белого твердого вещества. MS (ESI, m/z): 1358 [M+H]+.
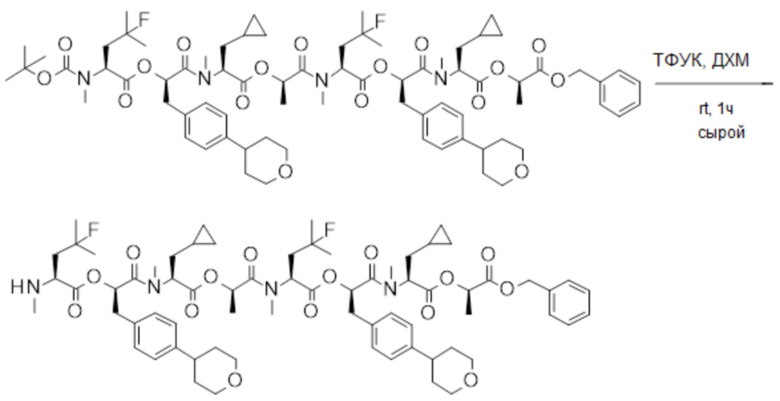
(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил] окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил] этокси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (OA7-34): В 3-горлую круглодонную колбу объемом 50 мл помещали OP7-34 (750 мг, 0.55 ммоль, 1.00 экв.), дихлорметан (8 мл), Затем добавляли трифторуксусную кислоту (2 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 8 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 30 мл дихлорметана, органические слои объединяли и сушили в термошкафу при пониженном давлении и упаривали в вакууме. В результате получали 700 мг (1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-1-оксопропан-2-ил]окси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этокси]-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино) пентаноата (OA7-34) в виде белого твердого вещества. MS (ESI, m/z): 1258 [M+H]+.
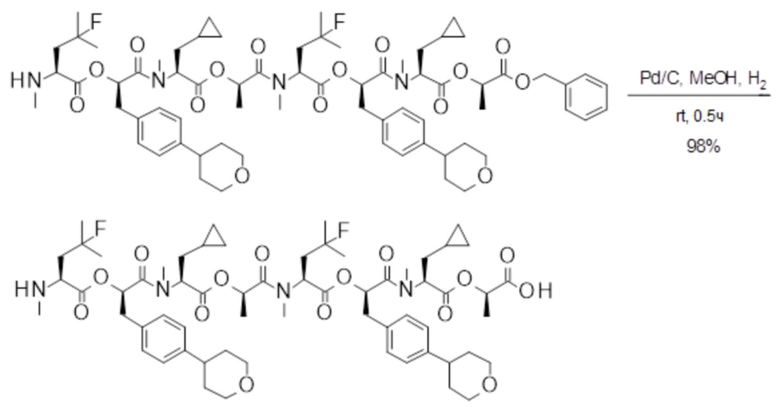
(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо-]пропаноил]окси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]пропаноил]окси] пропановая кислота (OAC7-34): В круглодонную колбу объемом 50 мл помещали OA7-34 (700 мг, 0.56 ммоль, 1.00 экв.), метанол (30 мл), палладий на угле (100 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 0.5 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 640 мг (98%) (2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-[(2R)-2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]пропаноил]окси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]пропаноил]окси] пропановой кислоты (OAC7-30) в виде белого твердого вещества. MS (ESI, m/z): 1168 [M+H]+.
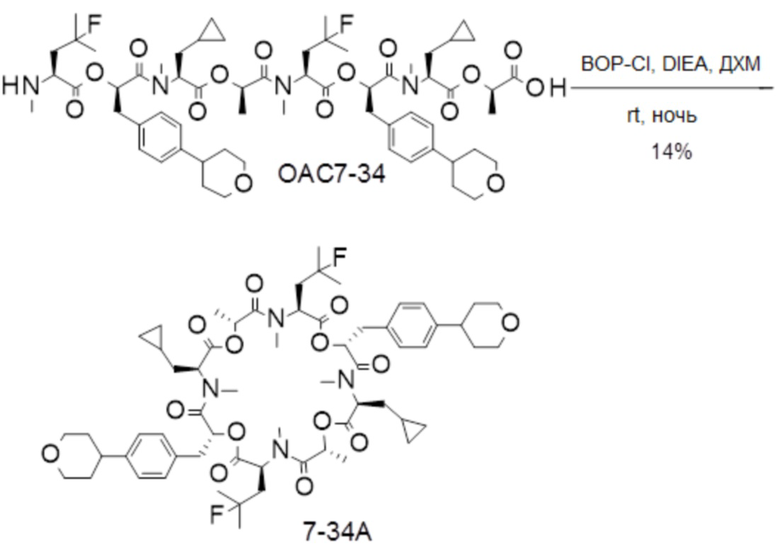
(3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,-10,12,16,22,24-гексаметил-6,18-бис([[4-(оксан-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (7-34A): В 3-горлую круглодонную колбу объемом 500 мл помещали OAC7-34 (640 мг, 0.55 ммоль, 1.00 экв.), дихлорметан (200 мл). После этого добавляли BOP-Cl (280 мг, 1.10 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (141 мг, 1.09 ммоль, 1.99 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, вода и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 254 нм. В результате получали 85.8 мг (14%) (3S,6R,9S,12R,15S,18R,21S,24R)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,10,12,16,22,24-гексаметил-6,18-бис([[4-(оксан-4-ил)фенил]метил])-1,7,-13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона (7-34A) в виде белого твердого вещества. 1H ЯМР (CD3OD, 300 МГц) δ: 7.5-7.0 (м, 8H), 5.96-4.9 (м, 8H), 4.19-3.94 (м, 4H), 3.7-3.47 (м, 4H), 3.28-2.69 (м, 18H), 2.39-1.2(м, 33H), 1.00-0.97 (м, 1H), 0.69-0.01 (м, 10H); MS (ESI, m/z): 1150 [M+H]+; [α]= -57.2o, T=27.2°C, C =1.0 г/100мл в MeOH.
Пример синтеза 38: Синтез соединения 7-30B в Таблице 7 где Ra и Rb представляют собой атом водорода, и R', R'', R''' и R'''' каждый представляют собой метил
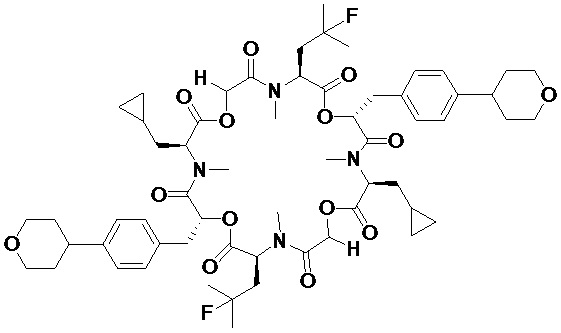
Соединение 7-34B получали аналогично синтезу соединения 6-7A согласно Схемам 13 и 14, изображенным ниже.
Схема 13
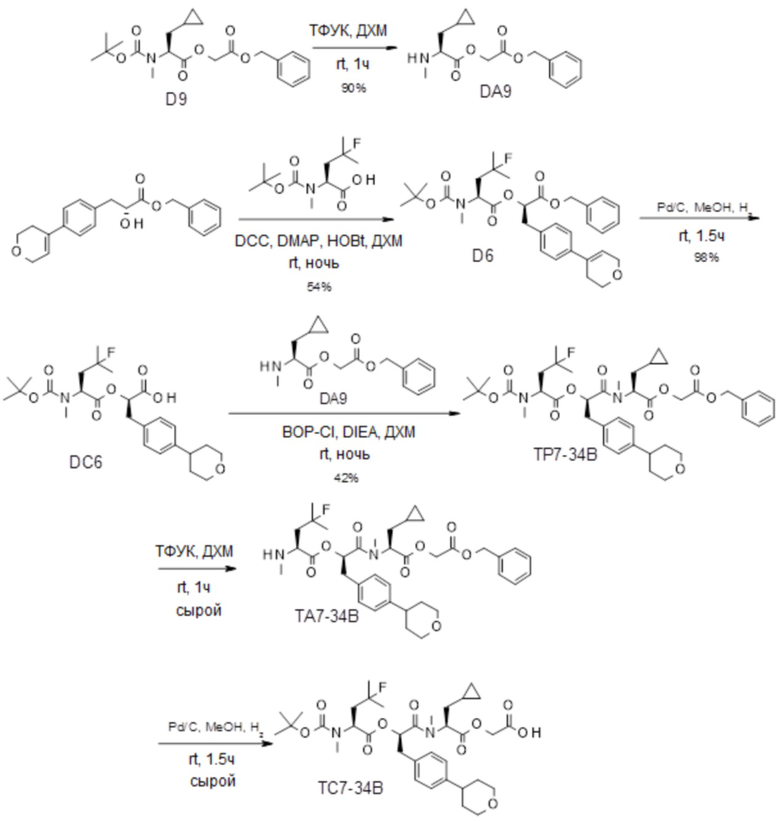
Схема 14
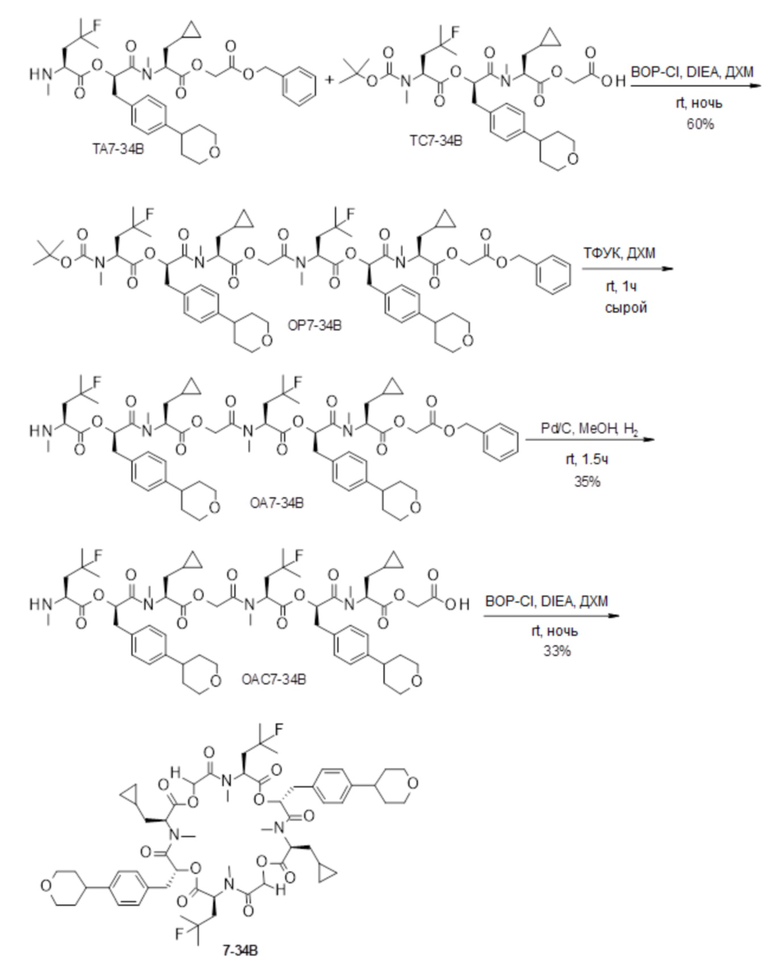
Подробное описание эксперимента
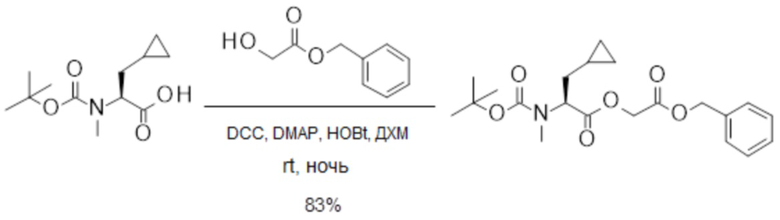
2-(бензилокси)-2-оксоэтил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D9): В круглодонную колбу объемом 100 мл помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропановую кислоту (1.5 г, 6.17 ммоль, 1.00 экв.), бензил 2-гидроксиацетат (1.02 г, 6.14 ммоль, 1.00 экв.) и дихлорметан (30 мл). После этого добавляли DCC (1.52 г, 7.37 ммоль, 1.20 экв.), 4-диметиламинопиридин (900 мг, 7.37 ммоль, 1.20 экв.) и HOBt (1.0 г, 7.40 ммоль, 1.20 экв.) порциями при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:3). В результате получали 2 г (83%) 2-(бензилокси)-2-оксоэтил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноата в виде желтого масла. MS (ESI, m/z): 392 [M+H]+.

2-(бензилокси)-2-оксоэтил (2S)-3-циклопропил-2-(метиламино)пропаноат (DA9): В круглодонную колбу объемом 50 мл помещали 2-(бензилокси)-2-оксоэтил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-3-циклопропилпропаноат (D9, 1.8 г, 4.60 ммоль, 1.00 экв.) и дихлорметан (16 мл). В полученную смесь добавляли трифторуксусную кислоту (3 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 9 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 2x20 мл дихлорметана, и органические слои объединяли. Органические слои сушили над сульфатом натрия и упаривали в вакууме. В результате получали 1.2 г (90%) 2-(бензилокси)-2-оксоэтил (2S)-3-циклопропил-2-(метиламино) пропаноата в виде светло-желтого масла. MS (ESI, m/z): 292 [M+H]+.
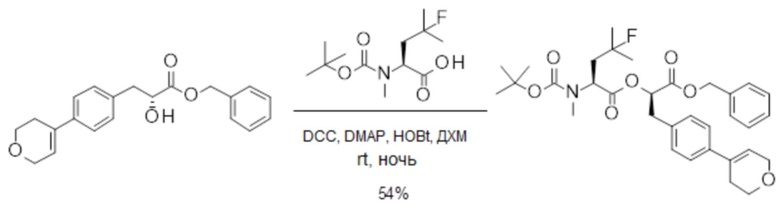
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D6): В круглодонную колбу объемом 50 мл помещали (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентановую кислоту (1 г, 3.80 ммоль, 1.00 экв.), бензил (2R)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-2-гидроксипропаноат (770 мг, 2.28 ммоль, 1.00 экв.) и дихлорметан (20 мл), После этого добавляли DCC (730 мг, 3.54 ммоль, 1.20 экв.), 4-диметиламинопиридин (430 мг, 3.52 ммоль, 1.20 экв.) и HOBt (480 мг, 3.55 ммоль, 1.20 экв.). Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:3). В результате получали 1.2 г (54%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 584 [M+H]+.
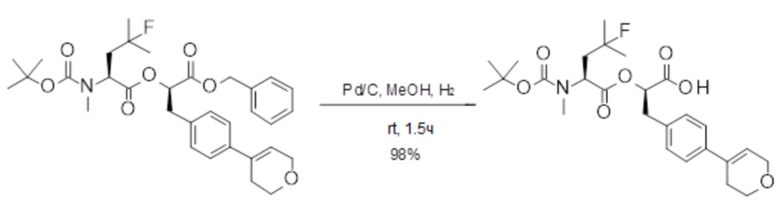
(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановая кислота (DC6): В круглодонную колбу объемом 50 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (1.2 г, 2.06 ммоль, 1.00 экв.), метанол (20 мл) и палладий на угле (200 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1.5 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1.0 г (98%) (2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 496 [M+H]+.
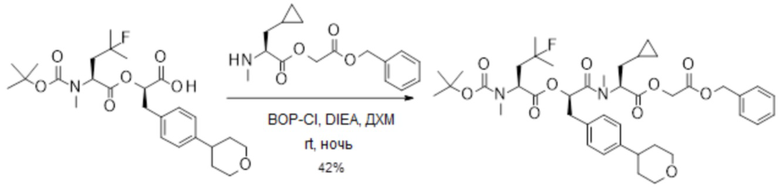
(1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-фтор-4-метилпентаноат (TP7-34B): В круглодонную колбу объемом 50 мл помещали 2-(бензилокси)-2-оксоэтил (2S)-3-циклопропил-2-(метиламино)пропаноат (1.0 г, 3.43 ммоль, 1.00 экв.), (2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (580 мг, 0.99 ммоль, 1.00 экв.), дихлорметан (20 мл), Затем добавляли BOP-Cl (1.03 г, 4.05 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (520 мг, 4.02 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/гексан (1:3). В результате получали 1.1 г (42%) (1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 769 [M+H]+.
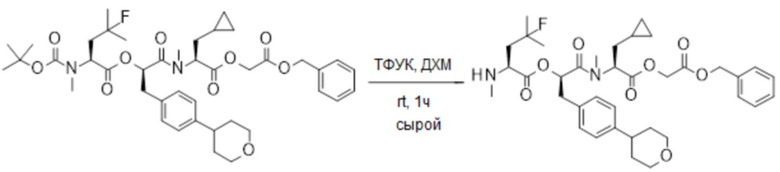
(1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (TA7-34B): В круглодонную колбу объемом 50 мл помещали (1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил] этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (TP7-34B, 560 мг, 0.73 ммоль, 1.00 экв.) и дихлорметан (20 мл). В полученную смесь добавляли трифторуксусную кислоту (3 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1 часа при комнатной температуре. Значение pH раствора доводили до 9 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 2x20 мл дихлорметана и органические слои объединяли. Органические слои сушили над сульфатом натрия и упаривали в вакууме. В результате получали 0.50 г (сырой) (1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил) карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноата в виде коричневого масла. MS (ESI, m/z): 669 [M+H]+.
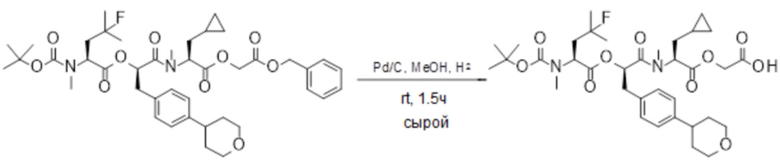
2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]уксусная кислота (TC7-34B): В круглодонную колбу объемом 50 мл помещали (1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноат (TP7-34B, 560 мг, 0.73 ммоль, 1.00 экв.), метанол (20 мл) и палладий на угле (50 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 1.5 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 0.50 г (сырой) 2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]уксусной кислоты в виде бесцветного масла. MS (ESI, m/z): 679 [M+H]+.
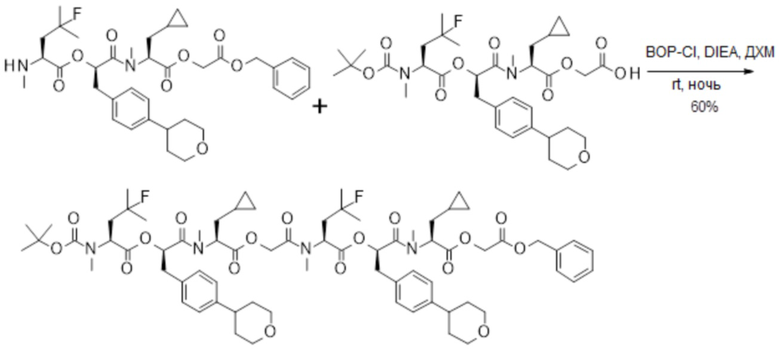
Соединение OP7-34B: В круглодонную колбу объемом 50 мл помещали (1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (TA7-34B, 500 мг, 0.75 ммоль, 1.00 экв.), 2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]уксусную кислоту (TC7-34B, 500 мг, 0.74 ммоль, 1.00 экв.), дихлорметан (20 мл), Затем добавляли BOP-Cl (420 мг, 1.65 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (210 мг, 1.62 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:10). В результате получали 0.6 г (60%) OP7-34B в виде коричневого масла. MS (ESI, m/z): 1330 [M+H]+.
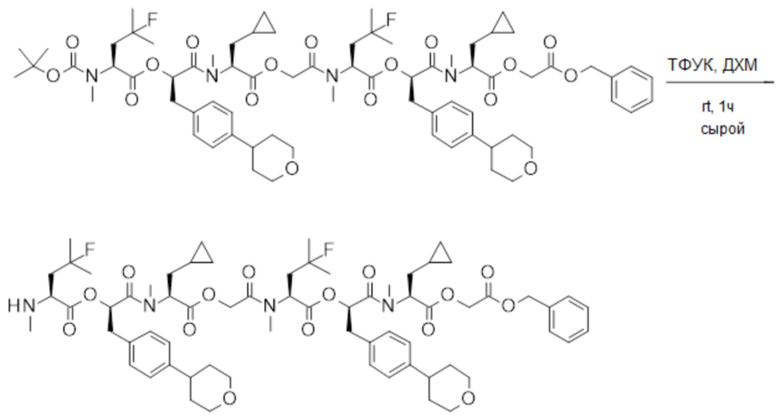
(1R)-1-[[(2S)-1-([[(2S)-1-[(1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]метокси)-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино) пентаноат (OA7-34B): В круглодонную колбу объемом 50 мл помещали OP7-34B (600 мг, 0.45 ммоль, 1.00 экв.) и дихлорметан(20 мл). В полученную смесь добавляли трифторуксусную кислоту (3 мл) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение 1.5 ч при комнатной температуре. Значение pH раствора доводили до 9 с помощью бикарбоната натрия (водный раствор). Результирующий раствор экстрагировали 2x10 мл дихлорметана и органические слои объединяли. Органические слои сушили над сульфатом натрия и упаривали в вакууме. Получали 560 мг (сырой) (1R)-1-[[(2S)-1-([[(2S)-1-[(1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил] (метил)карбамоил]метокси)-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноата в виде желтого масла. MS (ESI, m/z): 1230 [M+H]+.
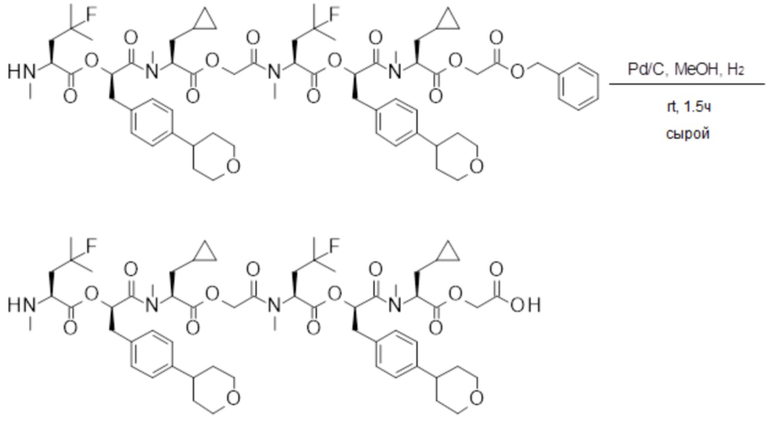
2-[[(2S)-2-[(2R)-2-[[(2S)-2-(2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси)карбонил](метил) амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]-N-метилацетамидо)-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]уксусная кислота (OAC7-34B): В круглодонную колбу объемом 50 мл помещали (1R)-1-[[(2S)-1-([[(2S)-1-[(1R)-1-[[(2S)-1-[2-(бензилокси)-2-оксоэтокси]-3-циклопропил-1-оксопропан-2-ил] (метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этокси]-4-фтор-4-метил-1-оксопентан-2-ил] (метил)карбамоил]метокси)-3-циклопропил-1-оксопропан-2-ил](метил)карбамоил]-2-[4-(оксан-4-ил)фенил]этил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (OA7-34B, 560 мг, 0.46 ммоль, 1.00 экв.), метанол (30 мл) и палладий на угле (100 мг). В полученный раствор пропускали водород. Результирующий раствор перемешивали в течение 1.5 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 200 мг (35%) 2-[[(2S)-2-[(2R)-2-[[(2S)-2-(2-[[(2S)-2-[(2R)-2-[[(2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил] пропанамидо]-3-циклопропилпропаноил]окси]-N-метилацетамидо)-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]-3-циклопропилпропаноил]окси]уксусной кислоты в виде светло-желтого масла. MS (ESI, m/z): 1140 [M+H]+.
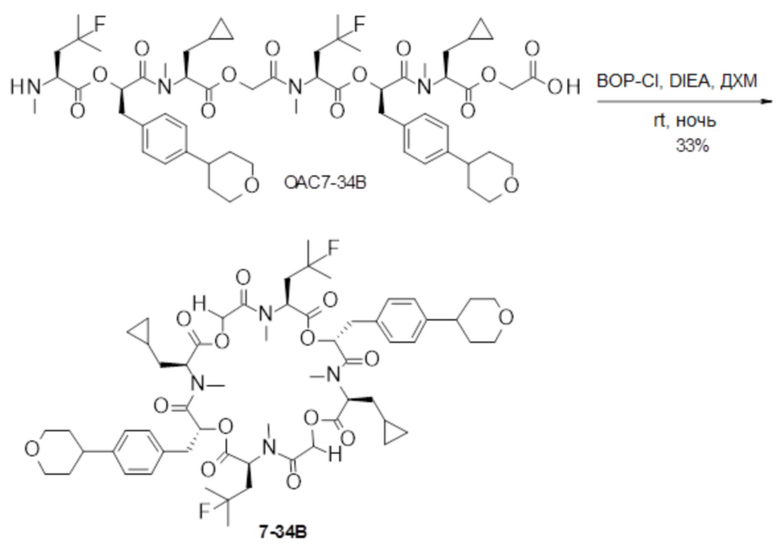
(3S,6R,9S,15S,18R,21S)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,10,16,22-тетраметил-6,18-бис([[4-(оксан-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октон (7-34B): В круглодонную колбу объемом 250 мл помещали 2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-2-(2-[[(2S)-3-циклопропил-2-[(2R)-2-[[(2S)-4-фтор-4-метил-2-(метиламино)пентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]пропаноил]окси]-N-метилацетамидо)-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]пропаноил]окси] уксусную кислоту (OAC7-34B, 200 мг, 0.18 ммоль, 1.00 экв.) и дихлорметан (70 мл). После этого добавляли BOP-Cl (89 мг, 0.35 ммоль, 2.00 экв.) порциями при 0°C. В полученную смесь добавляли DIEA (45 мг, 0.35 ммоль, 2.00 экв.) по каплям при перемешивании при 0°C. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (waters-2767): Колонка, SunFire Prep C18, 5 мкм, 19*150 мм; подвижная фаза, вода и CH3CN (70% CH3CN до 80% за 8 минут); Детектор, УФ 254 нм. В результате получали 64 мг (33%) (3S,6R,9S,15S,18R,21S)-3,15-бис(циклопропилметил)-9,21-бис(2-фтор-2-метилпропил)-4,10,16,22-тетраметил-6,18-бис([[4-(оксан-4-ил)фенил]метил])-1,7,13,19-тетраокса-4,10,16,22-тетраазациклотетракозан-2,5,8,11,14,17,20,23-октона в виде белого твердого вещества. 1H ЯМР (CD3OD, 300 МГц) δ: 7.26-7.16 (м, 8H), 5.65-5.35 (м, 5H), 4.90-4.72 (м, 5H), 4.06-4.02 (м, 4H), 3.61-3.52 (м, 4H), 3.15-2.78 (м, 18H), 2.35-2.12 (м, 4H), 1.90-1.32 (м, 24H), 0.65-0.08 (м, 10H); MS (ESI, m/z): 1150 [M+H]+; [α]= -90.83o, T=27.2°C, C =0.48 г/100мл в MeOH.
Пример синтеза 39: Синтез соединения F4, где Cy1 и Cy2 каждый представляют собой 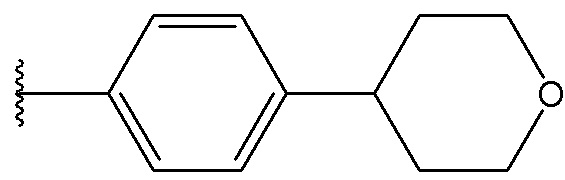 ; R1 и R3 каждый представляют собой -CH2CF(CH3)2; R2 представляет собой -CH2CH(CH3)2; R4 представляет собой C27; и Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил.
; R1 и R3 каждый представляют собой -CH2CF(CH3)2; R2 представляет собой -CH2CH(CH3)2; R4 представляет собой C27; и Ra, Rb, R', R'', R''' и R'''' каждый представляют собой метил.
Соединение 7-30B получали согласно способу, приведенному на Схемах 15 и 16, изображенных ниже.
Схема 15
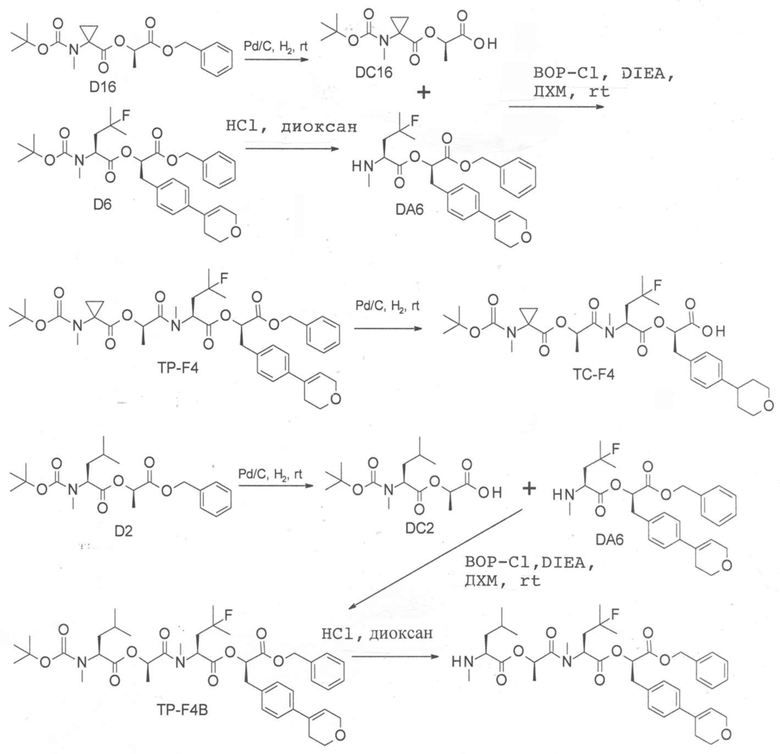
Схема 16
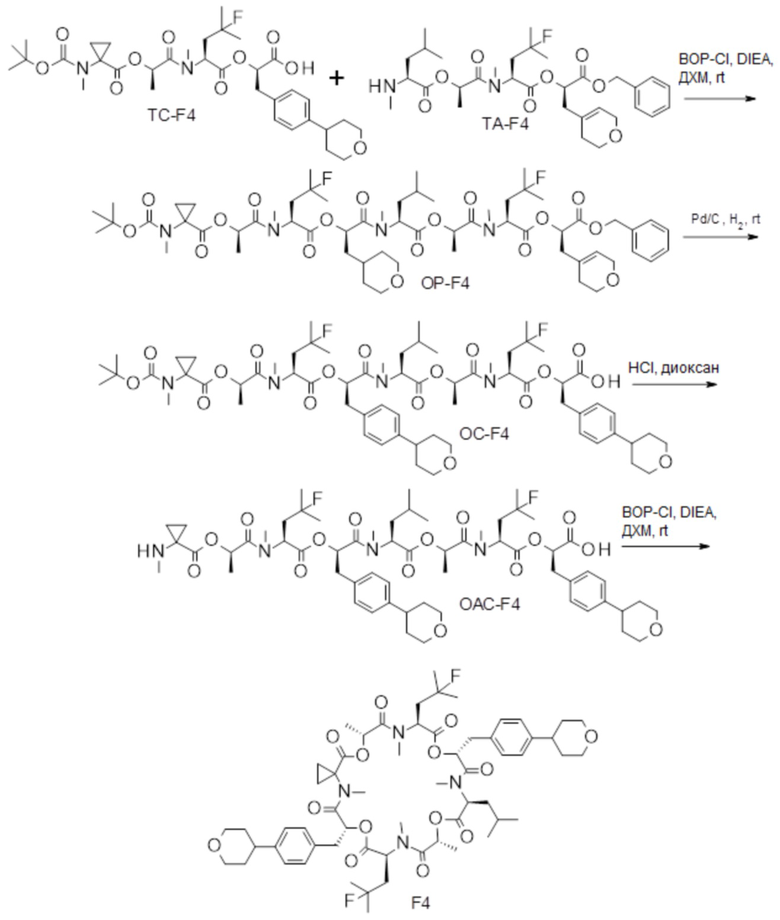
Подробное описание эксперимента
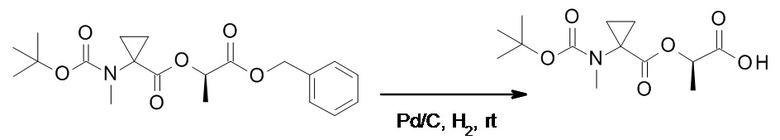
(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси] пропановая кислота (DC16): В круглодонную колбу объемом 100 мл помещали бензил (2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]пропаноат (D16, 1 г, 2.65 ммоль, 1.00 экв.), этилацетат (20 мл), палладий на угле (400 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 750 мг (99%) (2R)-2-[(1-[[(трет-бутокси)карбонил](метил) амино]циклопропил)карбонилокси]пропановую кислоту в виде розового масла. MS (ESI, m/z): 288 (M+H).
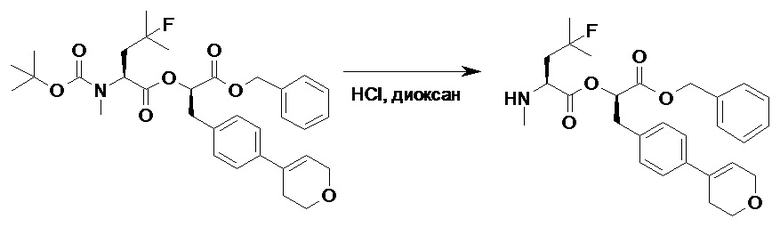
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (DA6): В круглодонную колбу объемом 250 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-фтор-4-метилпентаноат (D6, 2 г, 3.43 ммоль, 1.00 экв.), ДХМ (10 мл), хлороводород (диоксан, 20 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 40 мл насыщенного раствора хлорида натрия. Органический слой отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 1.6 г (97%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-(метиламино) пентаноата в виде желтого масла. MS (ESI, m/z): 484 (M+H).
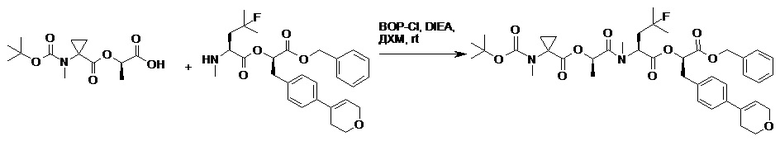
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноат (TP-F4): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (DA6, 1.5 г, 3.10 ммоль, 1.00 экв.), (2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси] пропановую кислоту (DC16, 890 мг, 3.10 ммоль, 1.00 экв.), дихлорметан (30 мл). После этого добавляли BOP-Cl (1.58 г, 6.21 ммоль, 2.00 экв.) при 0°C в течение 10 минут. В полученную смесь добавляли DIEA (800 мг, 6.19 ммоль, 2.00 экв.) при 0°C в течение 10 минут. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:2). В результате получали 1.4 г (60%) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 753 (M+H).
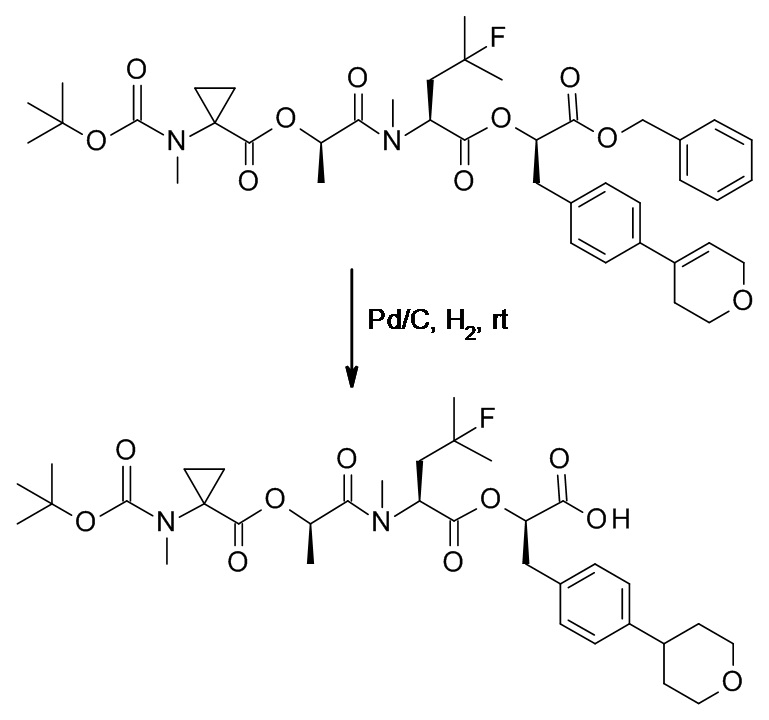
(2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил) карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил) фенил]пропановая кислота (TC-F4): В круглодонную колбу объемом 100 мл в инертной атмосфере азота помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил) карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноат (TP-F4, 900 мг, 1.20 ммоль, 1.00 экв.), этилацетат (20 мл), палладий на угле (200 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 660 мг (83%) (2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино] циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановой кислоты в виде белого твердого вещества. MS (ESI, m/z): 665 (M+H).
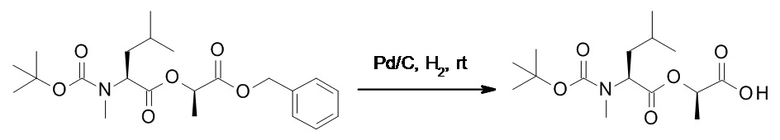
(R)-2-((S)-2-(трет-бутоксикарбонил(метил)амино)-4-метилпентаноилокси)пропановая кислота (DC2): В круглодонную колбу объемом 100 мл помещали (S)-((R)-1-(бензилокси)-1-оксопропан-2-ил) 2-(трет-бутоксикарбонил(метил)амино)-4-метилпентаноат (D2, 1 г, 2.40 ммоль, 1.00 экв.), ЭА (30 мл), палладий на угле (400 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 720 мг (сырой) (R)-2-((S)-2-(трет-бутоксикарбонил(метил)амино)-4-метилпентаноилокси) пропановой кислоты в виде желтого масла. MS (ESI, m/z): 484 (M+H).
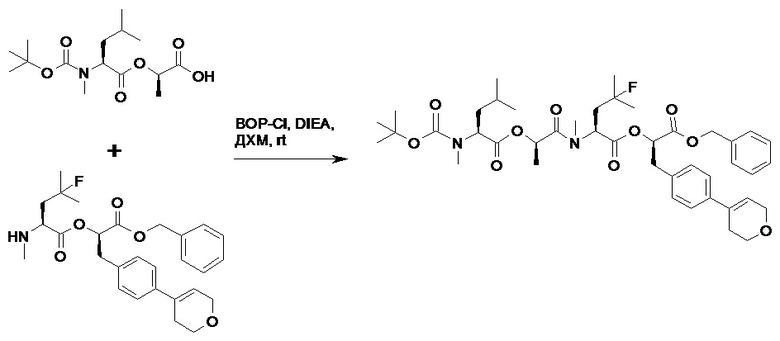
(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил]окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-2-[[(трет-бутокси) карбонил](метил)амино]-4-метилпентаноат (TP-F4B): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-(метиламино)пентаноат (DA6, 500 мг, 1.03 ммоль, 1.00 экв.), (R)-2-((S)-2-(трет-бутоксикарбонил(метил)амино)-4-метилпентаноилокси)пропановую кислоту (DC2, 330 мг, 1.03 ммоль, 1.00 экв.) в ДХМ (30 мл). После этого добавляли BOP-Cl (528 мг, 2.06 ммоль, 2.00 экв.) при 0°C в течение 5 минут. В полученную смесь добавляли DIEA (267 мг, 2.06 ммоль, 2.00 экв.) при 0°C в течение 5 минут. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Остаток наносили на колонку с силикагелем со смесью этилацетат/петролейный эфир (1:5). В результате получали 615 мг (76%) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил) фенил]-1-оксопропан-2-ил]окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метилпентаноата в виде желтого масла. MS (ESI, m/z): 783 (M+H).
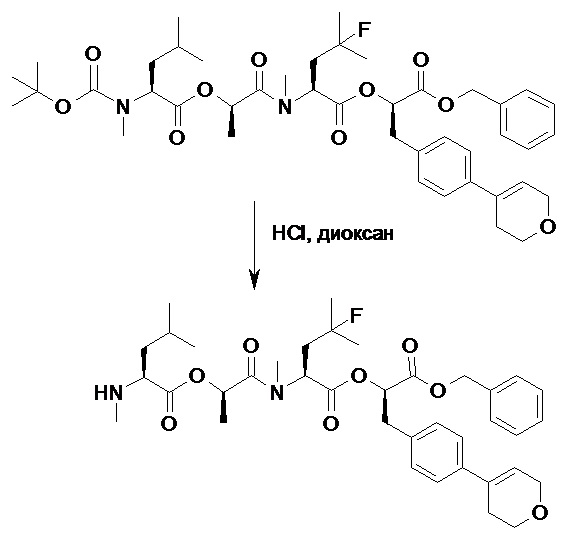
(1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил]окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-4-метил-2-(метиламино) пентаноат (TA-F4): В круглодонную колбу объемом 100 мл помещали (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил]окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-2-[[(трет-бутокси)карбонил](метил)амино]-4-метилпентаноат (TP-F4B, 400 мг, 0.51 ммоль, 1.00 экв.), хлороводород (диоксан, 10 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 30 мл насыщенного раствора хлорида натрия. Органическую фазу отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 400 мг (сырой) (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил] окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-4-метил-2-(метиламино)пентаноата в виде желтого масла. MS (ESI, m/z): 683 (M+H).
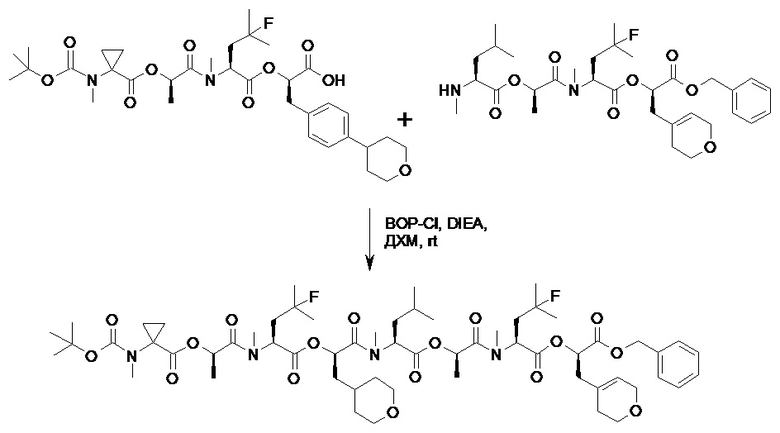
[(1R)-2-[[(1S)-1-[(1R)-2-[[(1S)-1-[(1R)-2-[[(1S)-1-[(1R)-2-бензилокси-1-(3,6-дигидро-2H-пиран-4-илметил)-2-оксо-этокси]карбонил-3-фтор-3-метил-бутил]-метил-амино]-1-метил-2-оксо-этокси]карбонил-3-метил-бутил]-метил-амино]-2-оксо-1-(тетрагидропиран-4-илметил)этокси]карбонил-3-фтор-3-метил-бутил]-метил-амино]-1-метил-2-оксо-этил] 1-[трет-бутоксикарбонил(метил)амино]циклопропанкарбоксилат (OP-F4): В круглодонную колбу объемом 100 мл помещали (2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановую кислоту (TC-F4, 340 мг, 0.51 ммоль, 1.00 экв.), (1R)-1-[[(2S)-1-[[(2R)-1-(бензилокси)-3-[4-(оксан-4-ил)фенил]-1-оксопропан-2-ил]окси]-4-фтор-4-метил-1-оксопентан-2-ил](метил)карбамоил]этил (2S)-4-метил-2-(метиламино)пентаноат (TA-F4, 350 мг, 0.51 ммоль, 1.00 экв.), дихлорметан (15 мл). После этого добавляли BOP-Cl (261 мг, 1.03 ммоль, 2.00 экв.) при 0°C в течение 5 минут. В полученную смесь добавляли DIEA (132 мг, 1.02 ммоль, 2.00 экв.) при 0°C в течение 5 минут. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Сырой продукт очищали методом флэш-препаративной ВЭЖХ в следующих условиях (IntelFlash-1): Колонка, С18 силикагель; подвижная фаза, H2O и CH3CN (от 50% CH3CN до 80% за 15 минут, и от 80% CH3CN до 100% за 15 минут); Детектор, УФ 220 нм. В результате получали 400 мг (59%) OP-F4 в виде желтого масла. MS (ESI, m/z): 1330 (M+H).
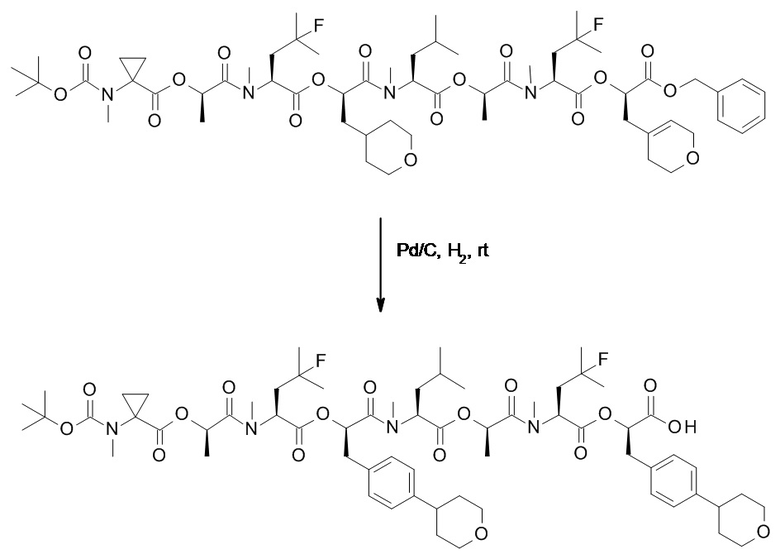
(2R)-2-[(2S)-2-[[(2R)-2-[(2S)-2-[[(2R)-2-[(2S)-2-[[(2R)-2-[1-[трет-бутоксикарбонил(метил) амино]циклопропанкарбонил]оксипропаноил]-метил-амино]-4-фтор-4-метил-пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропаноил]-метил-амино]-4-метил-пентаноил]оксипропаноил]-метил-амино]-4-фтор-4-метил-пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропановая кислота (OC-F4): В круглодонную колбу объемом 100 мл помещали OP-F4 (400 мг, 0.30 ммоль, 1.00 экв.), этилацетат (15 мл), палладий на угле (160 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 350 мг (94%) OC-F4 в виде желтого масла. MS (ESI, m/z): 1242 (M+H).
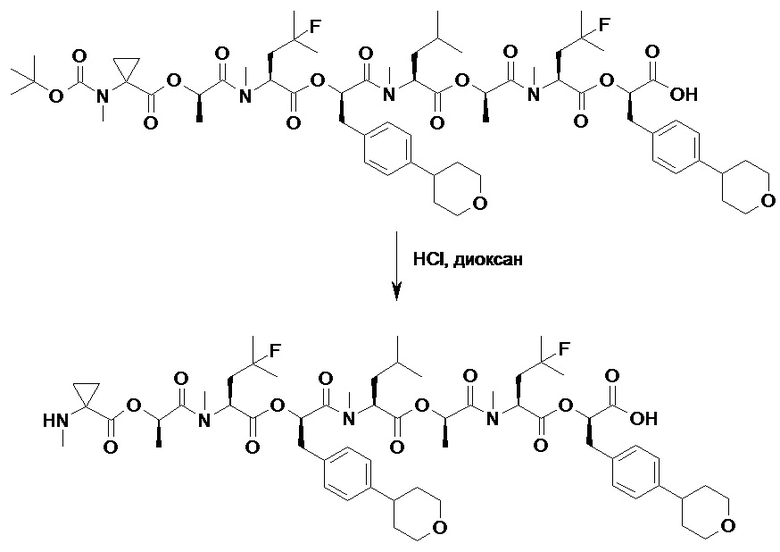
(2R)-2-[(2S)-4-фтор-2-[[(2R)-2-[(2S)-2-[[(2R)-2-[(2S)-4-фтор-4-метил-2-[метил-[(2R)-2-[1-(метиламино)циклопропанкарбонил]оксипропаноил]амино]пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропаноил]-метил-амино]-4-метил-пентаноил] оксипропаноил]-метил-амино]-4-метил-пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропановая кислота (OAC-F4): В круглодонную колбу объемом 100 мл помещали OC-F4 (350 мг, 0.28 ммоль, 1.00 экв.), ДХМ (5 мл), хлороводород (диоксан, 10 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 40 мл насыщенного раствора хлорида натрия. Органический слой отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 350 мг (сырой) OAC-F4 в виде желтого масла. MS (ESI, m/z): 1142 (M+H).
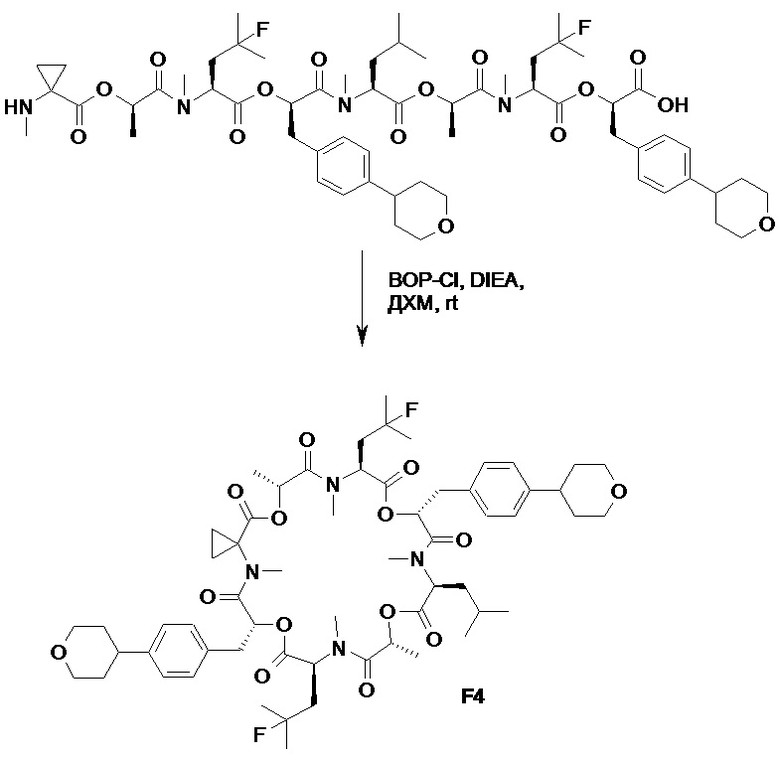
(6R,9S,12R,15S,18R,21S,24R)-9,21-бис(2-фтор-2-метилпропил)-4,10,12,16,22,24-гексаметил-15-(2-метилпропил)-6,18-бис([[4-(оксан-4-ил)фенил]метил])-7,13,19,25-тетраокса-4,10,16,22-тетраазаспиро[2.23]гексакозан-5,8,11,14,17,20,23,26-октон (F4): В круглодонную колбу объемом 250 мл помещали OAC-F4 (300 мг, 0.26 ммоль, 1.00 экв.), дихлорметан (300 мл). После этого добавляли BOP-Cl (134 мг, 0.53 ммоль, 2.00 экв.) при 0°C в течение 5 минут. В полученную смесь добавляли DIEA (102 мг, 0.79 ммоль, 3.00 экв.) при 0°C в течение 5 минут. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Полученную смесь упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (Waters I): Колонка, X Bridge Prep RP18, 5 мкм, 19x150 мм; подвижная фаза, вода и CH3CN (от 70% CH3CN до 90% ацетонитрила за 7 минут); Детектор, УФ 220 нм. В результате получали 116.5 мг (39%) (6R,9S,12R,15S,18R,21S,24R)-9,21-бис(2-фтор-2-метилпропил)-4,10,12,16,22,24-гексаметил-15-(2-метилпропил)-6,18-бис([[4-(оксан-4-ил)фенил]метил])-7,13,19,25-тетраокса-4,10,16,22-тетраазаспиро[2.23]гексакозан-5,8,11,14,17,20,23,26-октона (F4) в виде белого твердого вещества. MS (ESI, m/z): 1098.0 (M+H); 1H ЯМР (CD3OD, 300 МГц, м.д.): δ 7.31-7.23 (м, 8H), 5.96-5.83 (м, 1H), 5.81-5.72 (м, 1H), 5.71-5.60 (м, 1H), 5.59-5.31 (м, 2H), 5.31-5.09 (м, 2H), 4.18-3.95 (м, 4H), 3.71-3.43 (м, 4H), 3.21-3.09 (м, 6H), 3.06-2.94 (м, 6H), 2.85-2.77 (м, 6H), 2.26-2.18 (м, 4H), 2.05 -1.61 (м, 11H), 1.49-1.26 (м, 18H), 1.18-0.97 (м, 4H), 0.96-0.75 (м, 6H); [α]=-89.93o, T= 24.7°C, C = 0.29 г/100мл, MeOH.
Пример синтеза 40: Синтез соединения 969-34A в Таблице 699 где каждый из Ra, Rb, R', R'', R''' и R'''' представляют собой метил
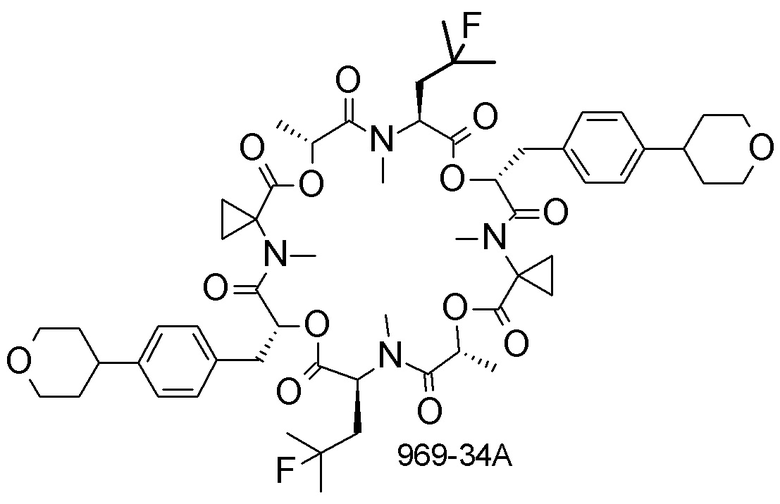
Соединение 969-34A получали аналогично синтезу соединения 6-7A согласно Схеме 17, изображенной ниже.
Схема 17
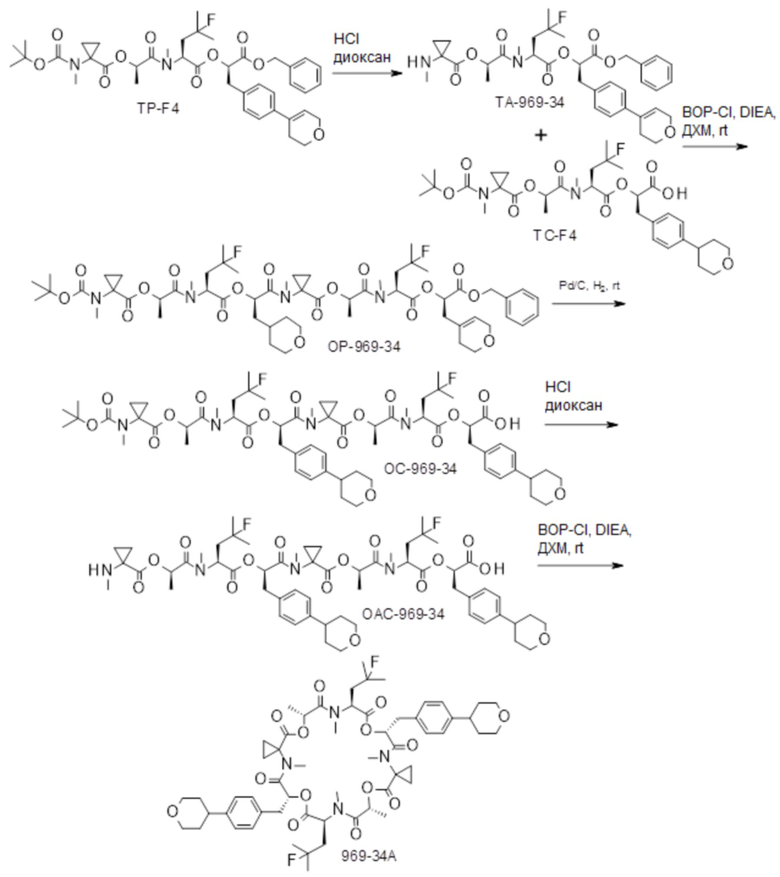
Подробное описание эксперимента
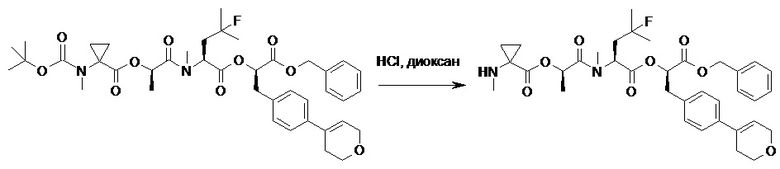 (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-[(2R)-N-метил-2-[[1-(метиламино)циклопропил]карбонилокси] пропанамидо]пентаноат (TA-969-34): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноат (TP-F4) (300 мг, 0.40 ммоль, 1.00 экв.), ДХМ (8 мл), хлороводород (диоксан, 15 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 30 мл насыщенного раствора хлорида натрия. Органический слой отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 350 мг (сырой) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-[(2R)-N-метил-2-[[1-(метиламино) циклопропил]карбонилокси]пропанамидо]пентаноата в виде желтого масла. MS (ESI, m/z): 653 (M+H).
(2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-[(2R)-N-метил-2-[[1-(метиламино)циклопропил]карбонилокси] пропанамидо]пентаноат (TA-969-34): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноат (TP-F4) (300 мг, 0.40 ммоль, 1.00 экв.), ДХМ (8 мл), хлороводород (диоксан, 15 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 30 мл насыщенного раствора хлорида натрия. Органический слой отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 350 мг (сырой) (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-[(2R)-N-метил-2-[[1-(метиламино) циклопропил]карбонилокси]пропанамидо]пентаноата в виде желтого масла. MS (ESI, m/z): 653 (M+H).
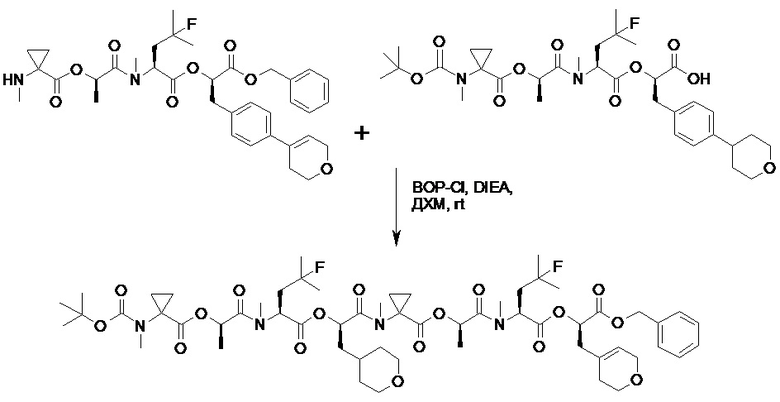
[(1R)-2-[[(1S)-1-[(1R)-2-бензилокси-1-(3,6-дигидро-2H-пиран-4-илметил)-2-оксо-этокси] карбонил-3-фтор-3-метил-бутил]-метил-амино]-1-метил-2-оксо-этил] 1-[[(2R)-2-[(2S)-2-[[(2R)-2-[1-[трет-бутоксикарбонил(метил)амино]циклопропанкарбонил] оксипропаноил]-метил-амино]-4-фтор-4-метил-пентаноил]окси-3-тетрагидропиран-4-ил-пропаноил]-метил-амино]циклопропанкарбоксилат (OP-969-34): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил) фенил]-1-оксопропан-2-ил (2S)-4-фтор-4-метил-2-[(2R)-N-метил-2-[[1-(метиламино) циклопропил]карбонилокси]пропанамидо]пентаноат (TA-969-34) (350 мг, 0.54 ммоль, 1.00 экв.), (2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил) карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил) фенил]пропановую кислоту (TC-F4) (330 мг, 0.50 ммоль, 1.00 экв.), дихлорметан (20 мл). После этого добавляли BOP-Cl (274 мг, 1.08 ммоль, 2.00 экв.) при 0°C в течение 5 минут. В полученную смесь добавляли DIEA (138 мг, 1.07 ммоль, 2.00 экв.) при 0°C в течение 5 минут. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом флэш-препаративной ВЭЖХ в следующих условиях (IntelFlash-1): Колонка, С18 силикагель; подвижная фаза, H2O и CH3CN (от 50% CH3CN до 100% за 20 минут); Детектор, УФ 220 нм. В результате получали 220 мг (34%) OP-969-34 в виде желтого масла. MS (ESI,m/z): 1230 (M+H).
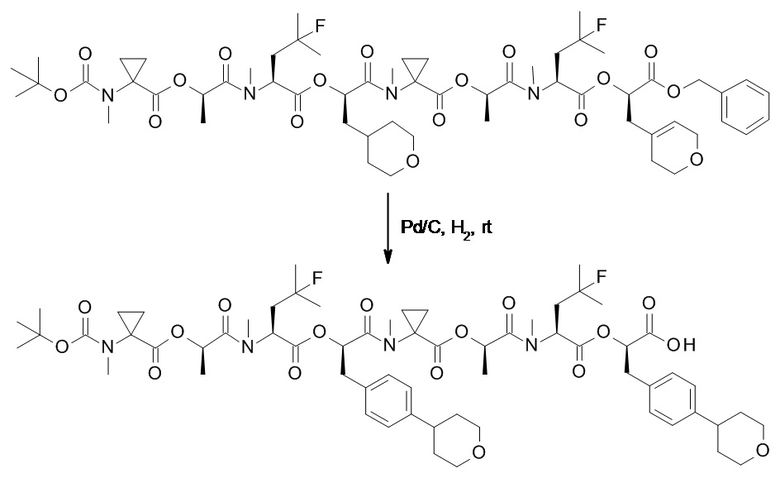
(2R)-2-[[(2S)-2-[(2R)-2-([1-[(2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил) амино]циклопропил)карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил] окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]циклопропил]карбонилокси)-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил] пропановая кислота (OC-969-34): В круглодонную колбу объемом 100 мл помещали (2R)-1-(бензилокси)-3-[4-(3,6-дигидро-2H-пиран-4-ил)фенил]-1-оксопропан-2-ил (2S)-2-[(2R)-2-([1-[(2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил) карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]циклопропил]карбонилокси)-N-метилпропанамидо]-4-фтор-4-метилпентаноат (OP-969-34) (200 мг, 0.15 ммоль, 1.00 экв.), этилацетат (10 мл), палладий на угле (80 мг). Через полученную смесь пропускали водород. Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 200 мг (сырой) (2R)-2-[[(2S)-2-[(2R)-2-([1-[(2R)-2-[[(2S)-2-[(2R)-2-[(1-[[(трет-бутокси)карбонил](метил)амино]циклопропил) карбонилокси]-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-N-метил-3-[4-(оксан-4-ил)фенил]пропанамидо]циклопропил]карбонилокси)-N-метилпропанамидо]-4-фтор-4-метилпентаноил]окси]-3-[4-(оксан-4-ил)фенил]пропановой кислоты в виде желтого масла. MS (ESI, m/z): 1212 (M+H).
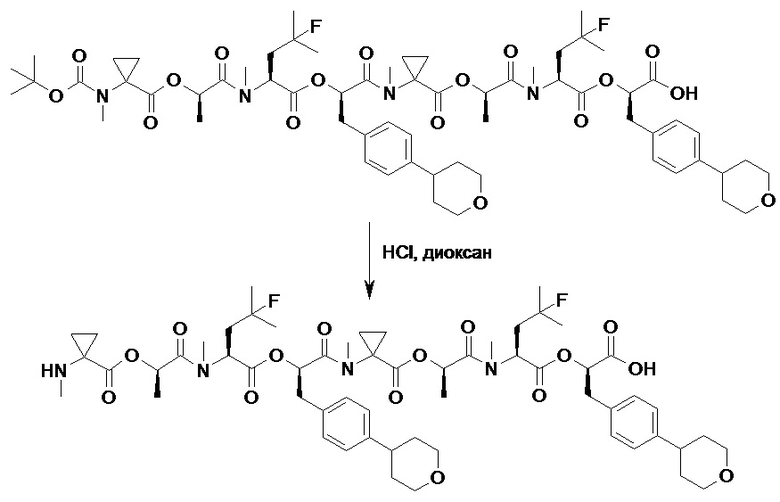
(2R)-2-[(2S)-4-фтор-2-[[(2R)-2-[1-[[(2R)-2-[(2S)-4-фтор-4-метил-2-[метил-[(2R)-2-[1-(метиламино)циклопропанкарбонил]оксипропаноил]амино]пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропаноил]-метил-амино]циклопропанкарбонил] оксипропаноил]-метил-амино]-4-метил-пентаноил]окси-3-(4-тетрагидропиран-4-илфенил)пропановая кислота (OAC-969-34): В круглодонную колбу объемом 100 мл помещали OC-969-34 (200 мг, 0.17 ммоль, 1.00 экв.), ДХМ (5 мл), хлороводород (диоксан, 8 мл). Результирующий раствор перемешивали в течение 2 ч при комнатной температуре. Полученную смесь упаривали в вакууме. Значение pH раствора доводили до 9 водным раствором бикарбоната натрия. Результирующий раствор экстрагировали 2x30 мл дихлорметана, органические слои объединяли и промывали 40 мл насыщенного раствора хлорида натрия. Органический слой отделяли и сушили над сульфатом натрия. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. В результате получали 200 мг (сырой) OAC-969-34 в виде желтого масла. MS (ESI, m/z): 1112 (M+H).
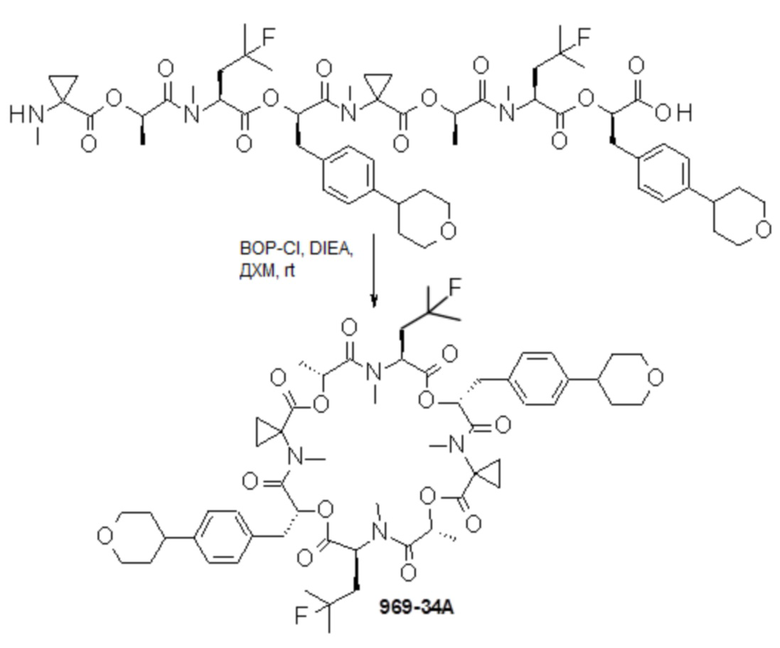
(6R,9S,12R,20R,23S,26R)-9,23-бис(2-фтор-2-метилпропил)-4,10,12,18,24,26-гексаметил-6,20-бис([[4-(оксан-4-ил)фенил]метил])-7,13,21,27-тетраокса-4,10,18,24-тетраазадиспиро[2.11.2^[15].11^[3]]октакозан-5,8,11,14,19,22,25,28-октон (969-34A): В круглодонную колбу объемом 250 мл помещали OAC969-34 (180 мг, 0.16 ммоль, 1.00 экв.), дихлорметан (50 мл). После этого добавляли BOP-Cl (83 мг, 0.33 ммоль, 2.00 экв.) при 0°C в течение 2 минут. В полученную смесь добавляли DIEA (63 мг, 0.49 ммоль, 3.00 экв.) при 0°C в течение 2 минут. Результирующий раствор перемешивали в течение ночи при комнатной температуре. Твердый осадок отфильтровывали. Фильтрат упаривали в вакууме. Сырой продукт очищали методом препаративной ВЭЖХ в следующих условиях (Waters I): Колонка, X Bridge Prep RP18, 5 мкм, 19x150 мм; подвижная фаза, фаза A: вода и CH3CN (от 60% CH3CN до 80% в течение 7 минут); Детектор, УФ 220 нм. В результате получали 51.5 мг (29%) (6R,9S,12R,20R,23S,26R)-9,23-бис(2-фтор-2-метилпропил)-4,10,12,18,24,26-гексаметил-6,20-бис([[4-(оксан-4-ил)фенил]метил])-7,13,21,27-тетраокса-4,10,18,24-тетраазадиспиро [2.11.2^[15].11^[3]]октакозан-5,8,11,14,19,22,25,28-октона (969-34A) в виде белого твердого вещества. MS (ESI, m/z): 1094 (M+H); 1H ЯМР (CD3OD, 300 МГц, м.д.): δ 7.22-7.20 (м, 8H), 5.93-4.93 (м, 6H), 4.07-4.03 (м, 4H), 3.61-3.53 (м, 4H), 3.11-2.79 (м, 18H), 2.41-2.08 (м, 4H), 2.05-1.81 (м, 1H), 1.81-1.76 (м, 9H), 1.76-1.24 (м, 20H), 1.08-1.06 (м, 3H), 0.85-0.72 (м, 1H); [a]= -62.98o, T=27.4 °C, C = 0.10 г/100мл в MeOH.
Помимо депсипептидных соединений по настоящему изобретению, описанных в Примерах 33-40, были получены дополнительные пронумерованные соединения, представленные ниже в Таблице 1038 (которые описаны выше, где R', R'', R''' и R'''' каждый представляют собой метил), в соответствии с синтетическими методиками, описанными в примерах, за исключением того, что для получения целевых депсипептидных соединений были выбраны другие димерные соединения, имеющие целевую функциональность. Выбранные димеры, в свою очередь, получены из соответствующих мономерных соединений. Квалифицированному специалисту в данной области будет понятно, что с применением описанной методологии можно получить дополнительные депсипептидные соединения по настоящему изобретению с применением других мономерных и димерных компонентов.
Таблица 1038: Дополнительные полученные соединения, имеющие формулу (I)
*Cy1 и Cy2 представляют собой п-THPфенил (см. Таблицу 7); R1, R3 = -CH2CF(CH3)2, и R2, R4 представляют собой -CH2CH2циклопропил
Примеры биологической активности
Метод A: Метод скрининга на предмет активности соединений против Haemonchus contortus.
Двадцать личинок L1 Haemonchus contortus помещали в лунки микропланшета, содержащие питательную среду и испытуемое соединение в ДМСО. Анализ проводили через 4 дня, определяя степень развития личинок. Личинки, подвергавшиеся воздействию только ДМСО, служили в качестве контроля. Соединения 228-34A и 969-34A показали средние значения EC50 между 1.0 и 10 мкM, соединение 7-58A показало среднее значение EC50 между 0.1 мкM и 1.0 мкM, и соединения 4-34A, 5-34A, 7-34A, 18-34A, 30-34A, 32-34A, 35-34A, 229-34A и 303-34A показали средние значения EC50 меньше 0.1 мкM при оценке через 4 дня. Для сравнения, эмодепсид показал среднее значение EC50 между 1 мкM и 10 мкM в данном тесте.
Соединение 6-1A показало среднее значение MIC90 между 1.0 и 10 мкM, соединения 6-7A и 6-34A показали средние значения MIC90 между 0.1 мкM и 1.0 мкM, и соединения 7-34A и 7-58A показали средние значения MIC90 меньше 0.1 мкM при оценке через 4 дня. Для сравнения, эмодепсид показал среднее значение EC50 между 0.1 мкM и 1 мкM в данном тесте. Измерения EC50 и MIC90 проводили с применением разных приборов.
Метод B: Метод скрининга на предмет активности соединений против микрофилярий Dirofilaria immitis.
Микрофилярии Dirofilaria immitis помещали в лунки микропланшета, содержащие буферный раствор и испытуемые соединения в ДМСО. Оценку проводили через 72 часа, определяя выживаемость микрофилярий. Микрофилярии, подвергавшиеся воздействию только ДМСО, служили в качестве контроля. Соединения 6-58A, 9-7A, 31-34A и 969-34A показали средние значения EC50 между 1 мкM и 10 мкM, соединения 6-1A, 6-7A и 6-34A показали средние значения EC50 между 0.1 мкM и 1.0 мкM, и соединения 4-34A, 5-34A, 7-34A, 7-58A, 18-34A, 30-34A, 32-34A, 228-34A, 229-34A и 303-34A показали средние значения EC50 меньше 0.1 мкM. Для сравнения, эмодепсид показал среднее значение EC50 между 0.1 мкM и 1 мкM в данном тесте.
Метод C: Метод скрининга на предмет активности соединений против Dirofilaria immitis in vivo.
Собак породы бигль тестировали на микрофилярии и антиген сердечного гельминта, а также проводили полное физическое обследование перед включением в данное исследование. Каждую собаку заражали 50 инвазионными личинками D. immitis третьей стадии в День -30, используя изолят, сензитивный к макроциклическим лактонам в стандартных дозировках. Определение антигена, проведенное на образцах крови, собранных в День 90, подтвердило, что животные не подвергались заражению D. immitis до индуцированного инфицирования.
В данном исследование формировали пять блоков по четыре или пять собак в каждом, по результатам снижения веса со Дня -3 до Дня 0. Внутри данных блоков, собак случайным образом распределяли в одну из пяти групп и вводили им пять раз с интервалом в один месяц перорально раствор соединения по настоящему изобретению в соответствии с приведенной ниже Таблицей 1039. Контрольным особям собак ничего не вводили. Группам 2 и 3 вводили соединения, не входящие в объем настоящего изобретения.
Всех животных гуманно умерщвляли в День 159, проводили вскрытие для подсчета паразитов и определяли число живых D. Immitis для каждой отдельной собаки. Выраженная в процентах эффективность для каждой группы приведена в Таблице 1039.
Таблица 1039. Эффективность против D. immitis у собак породы бигль.
В данном исследовании, соединение 18-34A по настоящему изобретению (в дозировке 0.1 и 0.5 мг/кг) при пероральном введении (в растворе) в виде пяти ежемесячных доз обеспечило 100% эффективность против индуцированной инфекции изолятов Dirofilaria immitis, чувствительных к макроциклическим лактонам.
* * *
Несмотря на подробное описание предпочтительных вариантов осуществления настоящего изобретения, следует понимать, что описанное выше изобретение не ограничивается частными деталями, приведенными выше в описании, поскольку возможны его многочисленные вариации без выхода за рамки сути и объема настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОГЕЛЬМИНТНЫЕ ДЕПСИПЕПТИДНЫЕ СОЕДИНЕНИЯ | 2016 |
|
RU2707298C2 |
| N-СОДЕРЖАЩИЕ ГЕТЕРОАРИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK3 КИНАЗЫ | 2010 |
|
RU2553681C2 |
| ПРОИЗВОДНЫЕ ХРОМЕНА | 2011 |
|
RU2574164C2 |
| 4-АМИНОХИНАЗОЛИНОВЫЕ АНТАГОНИСТЫ СЕЛЕКТИВНЫХ НАТРИЕВЫХ И КАЛЬЦИЕВЫХ ИОННЫХ КАНАЛОВ | 2004 |
|
RU2378260C2 |
| ВВОДИМЫЕ ПЕРОРАЛЬНО КОМБИНАЦИИ БЕТА-ЛАКТАМНЫХ АНТИБИОТИКОВ И ПРОИЗВОДНЫХ АВИБАКТАМА ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2020 |
|
RU2825281C1 |
| КОМБИНАЦИЯ MCL-1 ИНГИБИТОРА И ТАКСАНОВОГО СОЕДИНЕНИЯ, ИХ ПРИМЕНЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2018 |
|
RU2763544C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ СИНТЕЗА | 1993 |
|
RU2119917C1 |
| ПОЛУЧЕНИЕ ЗАМЕЩЕННОГО АКРИЛАТНОГО СОЕДИНЕНИЯ | 2021 |
|
RU2830161C1 |
| ПРОПИТОЧНАЯ СМОЛЯНАЯ СИСТЕМА ДЛЯ ИЗОЛЯЦИОННЫХ МАТЕРИАЛОВ В РАСПРЕДЕЛИТЕЛЬНЫХ УСТРОЙСТВАХ | 2010 |
|
RU2499006C2 |
| ЗАМЕЩЕННЫЕ ЦИКЛИЧЕСКИЕ АМИДЫ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2016 |
|
RU2772956C2 |
Изобретение относится к циклическим депсипептидным соединениям формулы (I), где значения R1-R4, R1’-R4’, Cy1 и Cy2 определены в формуле изобретения, и композициям, содержащим указанные соединения. Описанные соединения и композиции могут применяться для борьбы с паразитами у животных, включая млекопитающих и птиц. 4 н. и 46 з.п. ф-лы, 1039 табл., 40 пр.
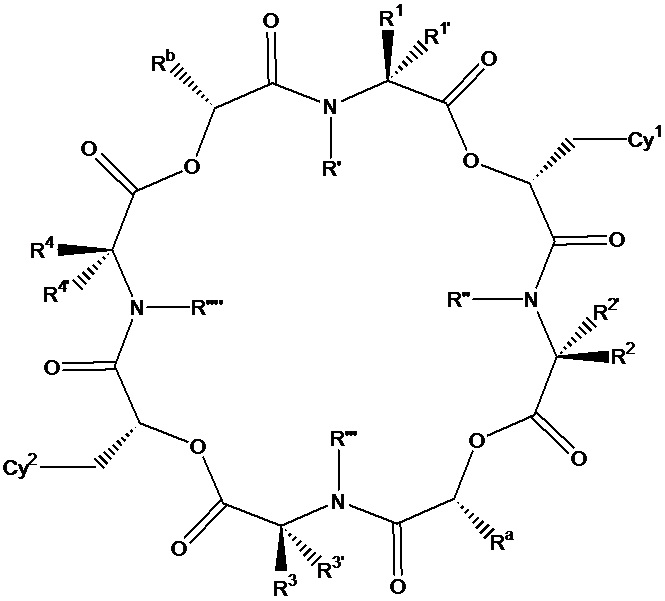
1. Циклическое депсипептидное соединение, имеющее формулу (I), или его фармацевтически или ветеринарно приемлемая соль:
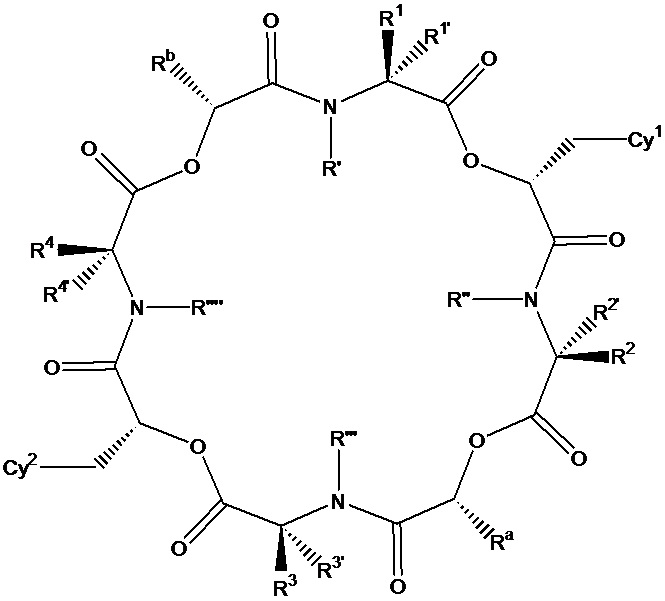
(I)
где:
Cy1 и Cy2 независимо представляют собой фенил, нафтил, 6-членный гетероарил, содержащий 1-3 атома азота, каждый из которых необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, C1-C3 алкокси-группы, C1-C3 галогеналкокси-группы, амино-группы, C1-C3 алкиламино-группы, C1-C3 диалкиламино-группы, C1-C6 алкила, C1-C6 галогеналкила, R5R6NC(O)-, -CN, -NO2, C3-C8 циклоалкила, 3-7-членного моноциклического гетероциклила, содержащего 1-3 атома кислорода или азота, и фенила, где указанный циклоалкильный, гетероциклильный или фенильный заместитель в Cy1 и Cy2 дополнительно независимо замещен одним или больше из галогена, C1-C6 алкила или C1-C6 галогеналкила;
R5 и R6 независимо представляют собой атом водорода или C1-C6 алкил или R5 и R6 вместе с атомом(-ами), к которому(-ым) они присоединены, формируют C3-C6 циклическую группу;
R', R'', R''' и R'''' каждый независимо представляет собой атом водорода или C1-C3 алкил;
Ra и Rb независимо представляют собой атом водорода, C1-C3 алкил или C1-C3 галогеналкил; и
(a) R1 представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ представляет собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R3, R3’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(b) R2 представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’ представляет собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R3, R3’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(c) R3 представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членной неароматической карбоциклической группой; где указанное 3-6-членное карбоциклическое, 3-6-членное гетероциклическое кольцо, 3-8-членное неароматическое карбоциклическое кольцо может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; или
R3 и R3’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2, R2’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(d) R4 представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R4’ представляет собой атом водорода или C1-C3 алкил; или
R4 и R4’ вместе образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2, R2’, R3 и R3’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(e) R1 и/или R2 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R2’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R3, R3’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(f) R1 и/или R3 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(g) R1 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R3 и R3’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(h) R2 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше заместителями, выбранными из группы, состоящей из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R3 и R3’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(i) R2 и/или R3 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(j) R3 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R3’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2 и R2’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(k) R1, и/или R2, и/или R3 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’, и/или R2’, и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе, и/или R2 и R2’ вместе, и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R4 и R4’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(l) R2, и/или R3, и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’, и/или R3’. и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе, и/или R3 и R3’ вместе, и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1 и R1’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(m) R1, и/или R3, и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’, и/или R3’, и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе, и/или R3 и R3’ вместе, и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2 и R2’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(n) R1, и/или R2, и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’, и/или R2’, и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе, и/или R2 и R2’ вместе, и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R3 и R3’ независимо представляют собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(o) R1, и/или R2, и/или R3, и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’, и/или R2’, и/или R3’, и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе, и/или R2 и R2’ вместе, и/или R3 и R3’ вместе, и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла.
2. Соединение по п. 1, где
(e) R1 и/или R2 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть независимо замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R2’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R2 и R2’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R3, R3’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(f) R1 и/или R3 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(g) R1 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R1’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R1 и R1’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R2, R2’, R3 и R3’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(h) R2 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R3 и R3’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(i) R2 и/или R3 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R2’ и/или R3’ независимо представляют собой атом водорода или C1-C3 алкил; или
R2 и R2’ вместе и/или R3 и R3’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R4 и R4’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном; или
(j) R3 и/или R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, замещенный 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше из C1-C6 алкила, C1-C6 галогеналкила или галогена; и R3’ и/или R4’ независимо представляют собой атом водорода или C1-C3 алкил; или
R3 и R3’ вместе и/или R4 и R4’ вместе независимо образуют 2-6-членную углеродную цепочку с формированием цикла; и
R1, R1’, R2 и R2’ каждый независимо представляет собой атом водорода или C1-C8 алкил, необязательно замещенный одним или больше галогеном.
3. Соединение по п. 1, где один, два, три или четыре из R1-R4 представляют собой метилен или метилен, замещенный одним или двумя атомами галогена, которые дополнительно замещены неароматическим карбоциклическим кольцом(кольцами), выбранным из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила и циклогексила, где указанное неароматическое карбоциклическое кольцо(кольца) может дополнительно быть замещено одним или больше галогеном; и остальные из R1-R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогеном.
4. Соединение по п. 1, где один или оба из R1 и R3 независимо выбраны из C1-C8 алкила, необязательно независимо замещенного одним или больше галогеном.
5. Соединение по п. 4, где один или оба из R1 и R3 представляют собой независимо C2-C6 алкил, необязательно независимо замещенный одним или больше галогенами.
6. Соединение по п. 4 или 5, где R1 и R3 оба представляют собой независимо C3-C5 алкил, независимо замещенный одним или больше фтором.
7. Соединение по любому из пп. 4-6, где R1 и R3 представляют собой -CH2-CF(CH3)2.
8. Соединение по любому из пп. 4-6, где R1 и R3 одинаковые.
9. Соединение по любому из пп. 4-8, где R1’ и R3’ представляют собой H.
10. Соединение по любому из пп. 4-9, где один или оба из R2 и R4 представляют собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо может быть дополнительно замещено одним или больше из галогена, C1-C6 алкила или C1-C6 галогеналкила.
11. Соединение по любому из пп. 4-10, где один или оба из R2 и R4 представляют собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-8-членным неароматическим карбоциклическим кольцом; где указанное 3-8-членное неароматическое карбоциклическое кольцо может быть дополнительно замещено одним или больше галогенами.
12. Соединение по любому из пп. 4-10, где один или оба из R2 и R4 представляют собой C1-C3 алкил или C1-C3 галогеналкил, где C1-C3 алкил или C1-C3 галогеналкил замещен 3-6-членным неароматическим карбоциклическим кольцом; где указанное 3-6-членное неароматическое карбоциклическое кольцо может быть дополнительно замещено одним или больше заместителями, выбранными из группы, состоящей из галогена, C1-C6 алкила и C1-C6 галогеналкила.
13. Соединение по любому из пп. 4-10, где R2 и R4 каждый независимо представляет собой C1-C3 алкил или C1-C3 галогеналкил, каждый из которых замещен неароматическим карбоциклическим кольцом, выбранным из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила и циклогексила, где указанные карбоциклические кольца могут быть дополнительно замещены одним или больше галогеном, C1-C4 алкилом или C1-C4 галогеналкилом.
14. Соединение по любому из пп. 4-10, где R2 и R4 каждый независимо представляет собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен неароматическим карбоциклическим кольцом, выбранным из группы, состоящей из циклопропила, циклобутила, циклопентила, циклопентенила и циклогексила, где указанные неароматические карбоциклические кольца могут быть дополнительно замещены одним или больше галогеном, C1-C4 алкилом или C1-C4 галогеналкилом.
15. Соединение по любому из пп. 4-14, где R2 и R4 каждый независимо представляет собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен неароматическим карбоциклическим кольцом, выбранным из группы, состоящей из циклопропила, циклобутила, циклопентила и циклопентенила.
16. Соединение по любому из пп. 4-15, где R2 и R4 каждый независимо представляет собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен неароматическим карбоциклическим кольцом, выбранным из группы, состоящей из циклопропила, циклобутила или циклопентила.
17. Соединение по любому из пп. 4-16, где R2 и R4 каждый независимо представляет собой метил, моно-фтор-замещенный метил или ди-фтор-замещенный метил, каждый из которых замещен циклопропилом.
18. Соединение по любому из пп. 4-17, где R2 и R4 каждый представляет собой -CH2-циклопропил.
19. Соединение по любому из пп. 4-17, где R2 и R4 одинаковые.
20. Соединение по любому из пп. 4-19, где один или оба из R1’ и R3’ представляют собой H или C1-C3 алкил.
21. Соединение по любому из пп. 4-20, где R1’ и R3’ представляют собой H.
22. Соединение по любому из пп. 4-21, где R', R'', R''' и R'''' представляют собой метил.
23. Соединение по любому из пп. 4-22, где Cy1 и Cy2 каждый независимо представляет собой фенил или пиридил, каждый из которых необязательно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, C1-C4 алкила, C1-C4 галогеналкила, C1-C3 галогеналкокси-группы, C3-C8 циклоалкила, 3-7-членного гетероциклила, содержащего 1-3 атома кислорода или азота, и фенила.
24. Соединение по любому из пп. 4-23, где Cy1 и Cy2 каждый независимо представляет собой фенильную группу, замещенную одним или больше заместителями, выбранными из группы, состоящей из галогена, C1-C4 алкила, C1-C4 галогеналкила, C1-C3 галогеналкокси-группы, C3-C8 циклоалкила, 3-7-членного гетероциклила, содержащего 1-3 атома кислорода или азота, и фенила.
25. Соединение по любому из пп. 4-24, где Cy1 и Cy2 каждый независимо представляет собой фенил, замещенный 3-7-членным гетероциклилом, содержащим 1-3 атома кислорода или азота; и где указанный гетероциклил выбран из группы, состоящей из пирролидинила, пирролила, пиразолила, оксетанила, пиразолинила, имидазолила, имидазолинила, имидазолидинила, оксазолила, оксазолидинила, изоксазолинила, изоксазолила, фурила, тетрагидрофурила, оксадиазолила, пиперидинила, пиперазинила, азепинила, 4-пиперидонила, пиридинила, пиразинила, пиримидинила, пиридазинила, тетрагидропиранила, морфолинила, 1,3-диоксолана, триазолила и триазинила.
26. Соединение по любому из пп. 4-25, где Cy1 и Cy2 каждый независимо представляет собой фенил, замещенный 3-7-членным гетероциклилом, содержащим 1-3 атома кислорода или азота; где указанный гетероциклил выбран из группы, состоящей из пирролидинила, фурила, тетрагидрофурила, пиперидинила, пиперазинила и морфолинила.
27. Соединение по любому из пп. 4-26, где Cy1 и Cy2 одинаковые и каждый представляет собой пара-N-морфолинилфенил:
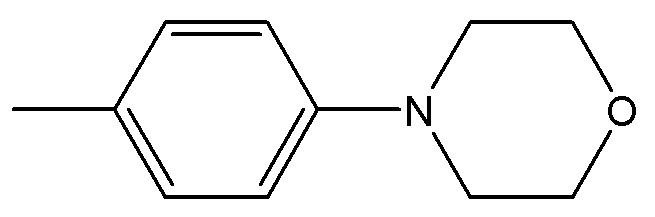 .
.
28. Соединение по любому из пп. 4-25, где Cy1 и Cy2 одинаковые и каждый представляет собой пара-тетрагидропиранилфенил:
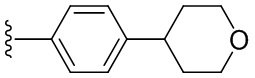 .
.
29. Соединение по любому из пп. 4-28, где Ra и Rb независимо представляют собой C1-C3 алкил.
30. Соединение по любому из пп. 4-28, где Ra и Rb представляют собой метил.
31. Соединение по п. 1, где:
R1 и R3 оба независимо выбраны из C3-C5 алкила, замещенного одним или больше атомами фтора;
R2 и R4 каждый представляет собой метил, замещенный 3-5-членным неароматическим карбоциклическим кольцом;
R1’, R2’, R3’ и R4’ представляют собой H;
R', R'', R''' и R'''' каждый независимо представляет собой C1-C3 алкил;
Cy1 и Cy2 каждый независимо представляет собой фенил, замещенный галогеном, C1-C6 алкилом, C1-C6 галогеналкилом, C1-C3 галогеналкокси-группой, 3-7-членным гетероциклилом, содержащим 1-3 атома кислорода или азота, где гетероциклил выбран из группы, состоящей из пирролидинила, фурила, тетрагидрофурила, тетрагидропиранила, пиперидинила, пиперазинила и морфолинила; и
Ra и Rb независимо представляют собой C1-C3 алкил.
32. Соединение по п. 1, где:
R1 и R3 оба независимо представляют собой -CH2-CF(CH3)2;
R2 и R4 каждый представляет собой -CH2-циклопропил;
R1’, R2’, R3’ и R4’ представляют собой H;
R', R'', R''' и R'''' каждый независимо представляет собой C1-C3 алкил;
Cy1 и Cy2 каждый независимо представляет собой фенил, замещенный галогеном, трет-бутилом, -CF3, -ОCF3 и 3-7-членным гетероциклилом, содержащим 1-3 атома кислорода или азота, предпочтительно где гетероциклил выбран из группы, состоящей из пиперидинила, тетрагидропиранила и морфолинила; и
Ra и Rb независимо представляют собой C1-C3 алкил.
33. Соединение по п. 1, где один, два, три или четыре из R1, R2, R3 и R4 независимо представляют собой C1-С6, С9, С14-С16 или С18-С20:
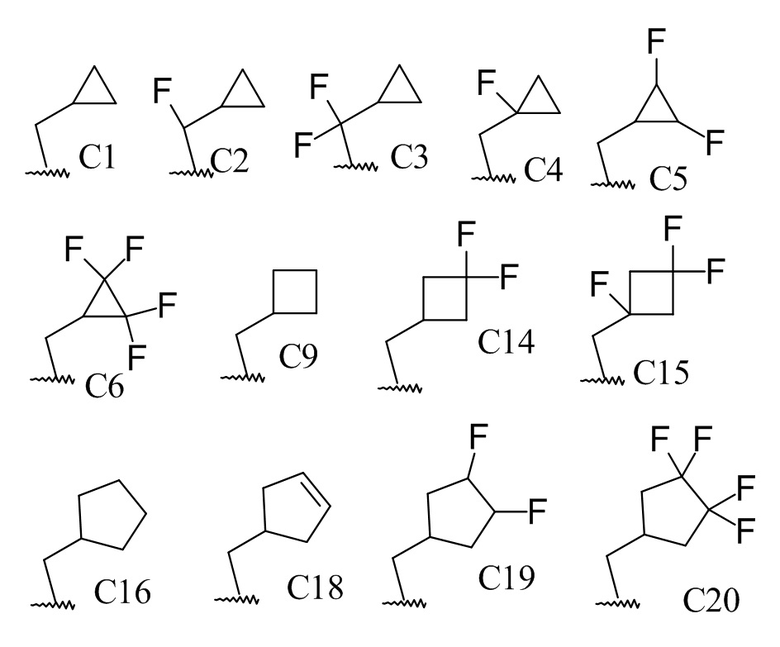
и остальные из R1, R2, R3 и R4 независимо представляют собой C1-C3 алкил, необязательно замещенный одним или больше галогеном, C1-C3 алкокси-группой, C1-C3 галогеналкокси-группой, циано-группой, амино-группой, C1-C6 алкиламино-группой или C1-C6 диалкиламино-группой.
34. Соединение по п. 33, где один, два, три или все четыре из R1-R4 каждый независимо представляет собой один из C1-С6, С9, С14-С16 или С18-С20 и остальные из R1-R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогенами.
35. Соединение по п. 33, где R1 и R3 каждый независимо представляет собой один из C1-С6, С9, С14-С16 или С18-С20 и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогенами.
36. Соединение по п. 33, где R2 и R4 каждый независимо представляет собой один из C1-С6, С9, С14-С16 или С18-С20 и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше галогенами.
37. Соединение по п. 33, где R2 и R4 каждый независимо представляет собой C1, C9 или С16 и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
38. Соединение по п. 33, где R1 и R3 каждый независимо представляет собой C1, C9 или С16 и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или больше атомами фтора.
39. Соединение по п. 38, где R1 и R3 представляют собой C1 и R2 и R4 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
40. Соединение по п. 37, где R2 и R4 представляют собой C1 и R1 и R3 независимо представляют собой 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
41. Соединение по п. 1, где один, два, три или четыре из R1 вместе с R1’, и/или R2 вместе с R2’, и/или R3 вместе с R3’, и/или R4 вместе с R4’ независимо представляют собой C27 или C28:
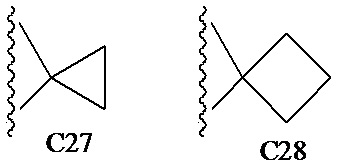 ; и
; и
остальные из R1, R1’, R2, R2’, R3, R3’, R4 и R4’ независимо представляют собой атом водорода, 2,2-диметилпропил или 2-метилпропил, замещенный одним или двумя атомами фтора.
42. Соединение по любому из пп. 33-41, где Cy1 и Cy2 независимо представляют собой необязательно замещенный нафтил.
43. Соединение по любому из пп. 33-41, где Cy1 и Cy2 независимо представляют собой фенил или пиридинил, каждый из которых необязательно независимо замещен одним или больше галогеном, C1-C3 галогеналкокси-группой, C1-C6 алкилом, C1-C6 галогеналкилом, C3-C8 циклоалкилом, 3-7-членным гетероциклилом, содержащими 1-3 атома кислорода или азота, или фенилом, где каждый циклоалкильный, гетероциклильный или фенильный заместитель необязательно дополнительно замещен одним или больше заместителями, выбранными из группы, состоящей из галогена, C1-C6 алкила или C1-C6 галогеналкила.
44. Соединение по п. 43, где Cy1 и Cy2 независимо представляют собой фенил, необязательно независимо замещенный галогеном, C1-C4 алкилом, C1-C4 галогеналкилом или гетероциклилом.
45. Соединение по п. 43, где Cy1 и Cy2 независимо представляют собой фенил или пиридинил, необязательно независимо замещенный гетероциклилом, фтором, трифторметилом или трифторметокси-группой.
46. Соединение по п. 43, где Cy1 и Cy2 независимо представляют собой фенил или пиридинил, необязательно независимо замещенный морфолинилом или тетрагидропиранилом.
47. Соединение по п. 43, где Cy1 и Cy2 независимо представляют собой фенил, независимо необязательно замещенный трет-бутилом.
48. Антигельминтная ветеринарная композиция, содержащая эффективное количество циклического депсипептидного соединения по п. 1 или его фармацевтически или ветеринарно приемлемую соль, в комбинации с фармацевтически приемлемым носителем.
49. Способ лечения или профилактики паразитной инфекции или заражения у животного, включающий введение животному паразитицидно эффективного количества циклического депсипептидного соединения по п. 1.
50. Применение циклического депсипептидного соединения по п. 1 для изготовления лекарственного средства для лечения или профилактики паразитной инфекции у животного.
| Способ измерений пульсаций давления | 1971 |
|
SU626375A1 |
| ЭНДОПАРАЗИТИЦИДНОЕ СРЕДСТВО | 2000 |
|
RU2250779C2 |
| Способ изготовления копира | 1976 |
|
SU662326A1 |
| SCHERKENBECK J ET AL | |||
| ПРЕДОХРАНИТЕЛЬ ОТ ВЗРЫВА ХРАНИЛИЩ ЛЕГКО ВОСПЛАМЕНЯЮЩИХСЯ ЖИДКОСТЕЙ | 1923 |
|
SU1022A1 |
| Modification and exchange of the N-methyl leucine residues", BIOORGANIC & MEDICINAL CHEMISTRY LETTERS, 1998, vol | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
2020-03-02—Публикация
2016-12-14—Подача