Настоящее изобретение относится к способу конъюгации полипептида, такого как белок, с полезной нагрузкой в условиях, которые не повреждают полипептид, с получением стабильной молекулы. Настоящее раскрытие также относится к молекулам, полученным или получаемым с помощью указанных способов, и композициям, содержащим их. Настоящее раскрытие дополнительно относится к применению молекул, полученных этим способом, в терапии, например в иммунотерапии и/или в терапии рака.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Методики конъюгации очень важны в контексте фармацевтических препаратов, например, ряд имеющихся на рынке лекарственных препаратов/биологических препаратов конъюгированы с молекулой полиэтиленгликоля (PEG). PEG имеет одну из нескольких функций, среди которых, как полагают, снижение иммуногенности некоторых молекул и/или увеличение периода полураспада молекул. Примеры имеющихся на рынке медикаментов включают: пегинезатид, пеглотиказу, цертолизумаб пэгол (Cimzia), метоксиполиэтиленгликоль-эпоэтин бета (Mircera), пегаптаниб (Macugen), пегфилграстим (Neulasta), пегвисомант (Somavert), пегинтерферон альфа-2a (Pegasys), липосомальный доксорубицин HCl (Doxil/Caelyx), пегинтерферон альфа-2b (PegIntron), пэгаспаргазу (Oncaspar) и пегадемазу бычью (Adagen).
Конъюгаты антитело-лекарственный препарат (ADC) также представляют собой важную категорию терапевтических молекул. Они являются сильнодействующими и похожи на "управляемую ракету", где компонент-антитело конъюгирован с полезной нагрузкой, например цитотоксином, который направляется к намеченной цели с помощью компонента-антитела. Примеры ADC включают брентуксимаб ведотин и трастузумаб эмтанзин. Линкер, образованный с использованием химии конъюгации, имеет жизненно важное значение для ADC.
Во многих методиках конъюгации используется малеимидный элемент в реакции 1,4-присоединения по Михаэлю, дающий сукцинимидный компонент в конъюгированной молекуле. Однако, как обсуждается в WO2013/173337, эта реакция является обратимой, и по-видимому, находится в состоянии динамического равновесия. То есть очистка не решает проблемы получения отдельной чистой структурной единицы.
Есть несколько публикаций, которые свидетельствуют, что это происходит в плазме, и часть конъюгированной молекулы может замещаться сывороточным альбумином Alley et al., Bioconjugate Chem. 2008, 19, 759-765. Это представляет собой проблему, особенно в контексте ADC.
Одним из ответов является гидролиз полученного сукцинимида. Тем не менее, это требует сравнительно жестких условий, например, 50 мM боратный буфер при pH 9,2 и 45°C в течение приблизительно 12 часов. Это может привести к агрегации/деградации антитела, а также деградации полезной нагрузки или поражающего элемента.
Решение этой проблемы раскрывается в WO2013/173337 (Seattle Genetics Inc.), в котором используется производное малеимида с заместителем амином в бета-положении относительно азота в малеимидном кольце. Полученный сукцинимид можно гидролизовать в более мягких условиях. Тем не менее, по-видимому имеет место значительный гидролиз малеимида до стадии конъюгации с тиолом. Кроме того, стадию конъюгации проводят при щелочном рН приблизительно 8. Последние условия могут способствовать агрегации белковых материалов, таких как антитела и фрагменты антител, тем самым вызывая потерю этого ценного материала на стадии конъюгации. Кроме того, соотношение полезной нагрузки и антитела в целом должно быть увеличено, чтобы гарантировать конъюгацию всех антител.
Механизмы деконьюгации, катализируемой амином, обсуждаются в статье Md. Rowshon Alam et al. (Bioconjugate Chem 2011, 22, 1673-1681), в которой показано, что стратегия Seattle Genetics не является универсально применимой (см. схему 2 в ней).
Альтернативное решение предоставлено в WO2013/121175, где раскрывается применение бромсодержащих производных малеимида в так называемой реакции SN2. Однако в условиях низкого pH реакционноспособные виды, а именно малеиновый ангидрид, преобразуются, см., например, стр. 54:
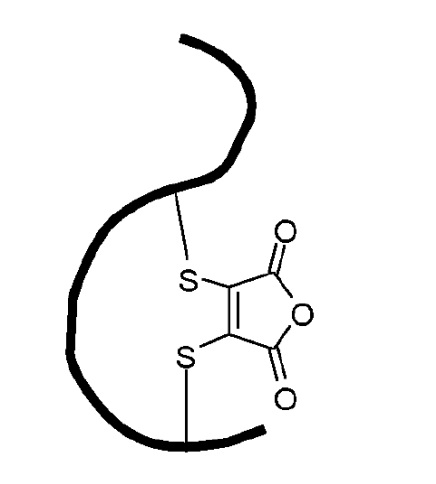
"Затем pH изменяли путем ультрафильтрации ……..до pH 4,5. Конъюгат антитела инкубировали при 37°C и анализировали аликвоты через 2, 6, 24, 48 и 72 часа с помощью LCMS. Доксорубицин высвобождался после разъединения линкера и образовывался трастузумаб-Fab-малеиновый ангидрид".
Авторы настоящего изобретения полагают, что эта нестабильность в конъюгатах, то есть способность образовывать малеиновое кольцо, является недостатком, поскольку в организме существует ряд сред с низким рН, и это ограничивает полезность молекул WO2013/1211175, так как полезная нагрузка может отсоединиться.
Настоящее раскрытие относится к способам, в которых используют мягкие условия, что дает молекулы, которые стабильны после получения и, следовательно, пригодны для введения in vivo, и в частности, которые пригодны для применения в терапии.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО РАСКРЫТИЯ
Таким образом, изобретение относится к способу получения полипептида, конъюгированного с полезной нагрузкой, включающему стадию:
a) проведения реакции присоединения по Михаэлю с малеимидной структурной единицей в молекуле формулы (I),
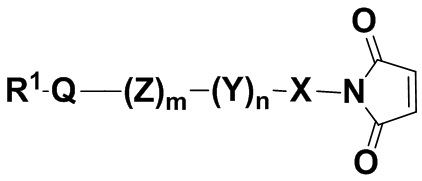 (I),
(I),
и полипептидной молекулой, содержащей по меньшей мере одну тиоловую группу,
где для формулы (I)
n равняется 0 или 1;
m равняется 0 или 1;
p равняется 0 или 1;
q равняется 0 или целому числу в диапазоне от 1 до 12, например, от 1 до 6, такому как 2 или 3;
Q представляет собой связь или остаток из компонента для конъюгации;
X представляет собой C0-18алкилен-C6-36арил(-CR2=CH-)p, C0-18алкилен-C6-36арил-CH2-CR2=CH-, C0-18алкилен-5-36-членный-гетероарил(-CR=CH-)p, C0-18алкилен-5-36-членный-гетероарил-CH2CR2=CH-, C0-18алкилен-CR2=CH-, C0-18алкилен-C≡C-,
где арил или гетероарил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4, -(OCH2CH2)q-OR3;
Y представляет собой оксо;
Z представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-30алкиленовую цепь, где один или несколько атомов углерода (например, 1, 2, 3, 4, 5, 6, 7 или 8) необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько (например, 1, 2, 3 или 4) оксо-заместителей;
R1 представляет собой H, поверхность твердой фазы или молекулу полезной нагрузки;
R2 представляет собой заместитель, например, выбранный из H, галогена, гидроксила, -C1-6алкила,
-C1-6алкокси, -COOR3, -COR3, -CN, -CF3, NO2, -SO2, -SO3, -NR4R5,
-PO4, C6-10арил-C0-6алкилена-, 6-10-членного-гетероарил-C0-6алкилена-;
R3 представляет собой H или C1-6алкил;
R4 представляет собой H или C1-6алкил;
R5 представляет собой H или C1-6алкил и
их фармацевтически приемлемые соли,
b) при этом R1 представляет собой молекулу полезной нагрузки или поверхность твердой фазы, способ включает дополнительную стадию гидролиза полученной тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (I) и полипептида, или
c) при этом R1 представляет собой H, причем способ включает дополнительную стадию осуществления конъюгации с полезной нагрузкой или поверхностью твердой фазы с последующим гидролизом тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (I) и полипептидной молекулы.
Предпочтительно, конъюгаты по настоящему раскрытию можно получать при кислых значениях рН, таких как рН приблизительно 5, и гидролиз тиосукцинимида можно выполнять в мягких условиях. В некоторых вариантах осуществления тиосукцинимид в конъюгатах можно быстро гидролизовать в мягких условиях. Кроме того, сразу после получения молекулы по настоящему раскрытию являются стабильными при использовании, например, стабильны в сыворотке.
Не желая быть связанными теорией, предположительно, что резонансные возможности ненасыщенной системы, такой как арил, фенил, винил, алкинил или их комбинации, являются важными, поскольку они облегчают мягкий гидролиз. В схематической диаграмме на Фигуре 1 показано, как ненасыщенная система, присоединенная к атому азота в сукцинимидном кольце, может облегчать нуклеофильную атаку воды на любую из карбонильных групп в кольце.
В одном из вариантов осуществления арил несет 1, 2, 3 или 4 заместителя - атома фтора.
Настоящее раскрытие также распространяется на соединение/продукт, полученный или который может быть получен с помощью указанного способа, например, продукт, полученный после конъюгации, или продукт, полученный после гидролиза сукцинимида.
В одном из аспектов изобретение относится к соединению, раскрытому здесь, например, формулы (I), (II), (IIa), (IIaa), (IIaa'), (IIaaa), (IIb), (IIbb), (IIbb'), (IIIbbb), (IIc), (IIcc), (IId), (IIdd), (IIddd), (III), (IIIa), (IIIaa), (IIIaa'), (IIIaaa), (IIIb), (IIIbb), (IIIc), (IIIcc) и (IIIcc'), или его производному, конъюгированному с полипептидом и/или полезной нагрузкой.
В одном из вариантов осуществления изобретение относится к молекуле/соединению, показанным в примерах.
В одном из вариантов осуществления изобретение также относится к применению соединения, раскрытого здесь, в химии конъюгации.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фигура 1 Схематическое представление гидролиза соединений по данному раскрытию
Фигура 1A Спектральные характеристики не вступившего в реакцию mAb
Фигура 1B Спектральные характеристики конъюгата алкилмалеимид-PEG-биотин
Фигура 2А Спектральная характеристика алкилмалеимид-PEG-биотина (компаратора)
Фигура 2В Спектральная характеристика фенилмалеимид-PEG-биотина
Фигура 2С Спектральная характеристика фторфенилмалеимид-PEG-биотина
Фигура 3 Эффективность конъюгации x-малеимид-PEG-биотинов с mAb T289C при 22°C
Фигура 4 Эффективность конъюгации x-малеимид-PEG-биотинов с mAb T289C при 22°C
Фигура 5 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 5,5, при 22°C
Фигура 6 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 7,4, при 22°C
Фигура 7 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 8,6, при 22°C
Фигура 8 Кинетика реакции x-малеимид-PEG-биотинов с mAb T289C после предварительной инкубации: непрямое измерение гидролиза малеимида
Фигура 9 Кинетика гидролиза малеимида, pH 5,5, 22°C
Фигура 10 Кинетика гидролиза малеимида, pH 7,4, 22°C
Фигура 11 Кинетика гидролиза малеимида, pH 8,6, 22°C
Фигура 12 Гидролиз тиосукцинимида, pH 7,4, 22°C, для конъюгатов PEG-биотин-mAb T289C
Фигура 13 Гидролиз тиосукцинимида, pH 7,4, 37°C, для PEG-биотин-mAb T289C
Фигура 14 Гидролиз тиосукцинимида, pH 8,6, 22°C, для PEG-биотин-mAb T289C
Фигура 15 Гидролиз x-тиосукцинимида для конъюгатов PEG-биотин-mAb T289C после инкубации длительностью 1 час, n=3
Фигура 16 Гидролиз x-тиосукцинимид-PEG-биотина для конъюгатов PEG-биотин-mAb T289C в присутствии молибдата натрия
Фигура 17 Чувствительность конъюгатов mAb T289C к замене тиолов в буфере, содержащем тиолы
Фигура 18 Стабильность конъюгатов PEG-биотин-mAb T289C в буфере, содержащем BME
Фигура 19 Гидролиз тиосукцинимида при pH 7,2, 37°C для конъюгатов PEG-биотин-mAb T289C, наблюдаемый в анализе испытания с BME
Фигура 20 Взаимосвязь между деконъюгацией и гидролизом тиосукцинимида, наблюдаемыми в анализе испытания с BME
Фигура 21 Чувствительность конъюгатов mAb T289C к замене тиолов в буфере после мягкого гидролиза
Фигура 22 Анализ ADC mc-PAB-MMAE-mAb T289C
Фигура 23 Стабильность конъюгатов MMAE-mAb T289C в буфере, содержащем тиол (BME)
Фигура 24 Гидролиз MMAE-тиосукцинимидов в конъюгатах с mAb T289C
Фигура 25 Стабильность конъюгатов MMAE-mAb T289C в буфере, содержащем тиол (BME)
Фигура 26 Сравнение гидролиза тиосукцинимида в PEG-биотине и MMAE, наблюдаемого в испытании с BME
Фигура 27 Сравнение деконъюгации в присутствии β-меркаптоэтанола: PEG-биотин по сравнению с MMAE-полезной нагрузкой
Фигура 28 Стабильность ADC MMAE-T289C в сыворотке мыши
Фигура 29 Стабильность ADC MMAE-T289C в сыворотке мыши
Фигура 30 Активность ADC в отношении раковых клеток MDA-MB-361 после инкубации в сыворотке мыши
Фигура 31 Альтернативный формат для стабилизации связанных с тиолом ADC
Фигура 32 Масс-спектрометрический анализ конъюгата N-фенилмалеимид-PEG-BCN-mAb
Фигура 33 Масс-спектрометрический анализ конъюгата N-фторфенилмалеимид-PEG-BCN-mAb
Фигура 34 Масс-спектрометрический анализ конъюгата N-алкилмалеимид-PEG-BCN-mAb
Фигура 35 Эффективность конъюгации x-малеимид-PEG-BCN с mAb T289C
Фигура 36 Кинетика гидролиза тиосукцинимида для конъюгатов x-малеимид-PEG-BCN
Фигура 37 Анализ конъюгатов mAb-BCN-Ac4GlcNAz
Фигура 38 Реакционноспособность конъюгата mAb-BCN после хранения
Фигура 39 Анализ конъюгатов mAb-PBD
Фигура 40 Активность In Vitro ADC mAb-BCN-PBD по отношению к клетками рака молочной железы MDA-MB-361
ПОДРОБНОЕ ОПИСАНИЕ РАСКРЫТИЯ
В одном из вариантов осуществления n равняется 0. В одном из вариантов осуществления n равняется 1. В одном из вариантов осуществления m равняется 0. В одном из вариантов осуществления m равняется 1. В одном из вариантов осуществления p равняется 0. В одном из вариантов осуществления p равняется 1.
В одном из вариантов осуществления X представляет собой C0-18алкилен-C6-10арил(-CR2=CH-)p, C0-18алкилен-C6-10арил-CH2-CR2=CH-, C0-18алкилен-5-10-членный-гетероарил(-CR=CH-)p, C0-18алкилен-5-10-членный-гетероарил-CH2CR2=CH-, C0-18алкилен-CR2=CH-, C0-18 алкилен-C≡C-,
где арил или гетероарил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления X представляет собой C0-15алкилен-C6-10арил(-CR2=CH-)p, C0-15алкилен-C6-10арил-CH2-CR2=CH-, C0-18алкилен-5-10-членный-гетероарил(-CR=CH-)p, C0-15алкилен-5-10-членный-гетероарил-CH2CR2=CH-, C0-15алкилен-CR2=CH-, C0-15алкилен-C≡C-,
где арил или гетероарил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4, -(CH2-O-CH2)q-O-R3.
В одном из вариантов осуществления X представляет собой C0-15алкилен-C6-10арил(-CR2=CH-)p, где арил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления X представляет собой C0-15алкилен-C6-10арил(-CH2CR2CH2-)p, например, C0-6алкилен-C6-10арил, такой как C6-10арил, в частности, фенил.
Z представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-25алкиленовую цепь, где один или несколько атомов углерода (например, 1, 2, 3, 4, 5, 6, 7 или 8) необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько (например, 1, 2, 3 или 4) оксо-заместителей.
Как правило, арил, такой как фенил, будет связан ковалентной связью непосредственно с атомом азота малеимидного кольца за исключением того, где р равняется 1.
В одном из вариантов осуществления арил, такой как фенил, несет "R1-Q-(Z)m"-содержащий заместитель в орто-, мета- или пара-положении, например, мета- или пара-, в таком как пара-положение.
В одном из вариантов осуществления арил, такой как фенил, может быть заменен одним, двумя, тремя или четырьмя заместителями, которые независимо выбраны из электронодонорных, электроноакцепторных и нейтральных заместителей. В одном из вариантов осуществления арил, такой как фенил, заменен одной, двумя, тремя или четырьмя электроноакцепторными группами. В одном из вариантов осуществления арил, такой как фенил, заменен одной, двумя, тремя или четырьмя электронодонорными группами. В одном из вариантов осуществления арил, такой как фенил, заменен одной, двумя, тремя или четырьмя группами с нейтральными электронными свойствами. Подобные модели замен также могут быть применены к гетероарилам в случае необходимости.
В одном из вариантов осуществления арил, такой как фенил, заменен одним, двумя, тремя или четырьмя заместителями, например, независимо выбранными из галогена, С1-3алкила, трифторметила, такого как хлор- или фтор-, в частности, одного, двух, трех или четырех атомов фтора. Молекулы, содержащие один или несколько атомов фтора, могут быть пригодны в методиках визуализации, таких как позитронно-эмиссионная томография.
В одном из вариантов осуществления арил, такой как фенил, несет один заместитель в орто-, мета- или пара-положении, например в мета- или пара-положении кольца, соединенного с малеимидом.
В одном из вариантов осуществления арил, такой как фенил, несет два заместителя, например в мета-, пара-положении; мета-, орто-положении; орто-, пара-положении; мета-, мета-положении или орто-, орто-положении кольца, соединенного с малеимидом.
В одном из вариантов осуществления арил, такой как фенил, несет три заместителя, например, в орто-, мета- и пара-положении; орто-, мета-, мета-положении; орто-, орто-, пара-положении или мета-, мета-, пара-положении кольца, соединенного с малеимидом.
В одном из вариантов осуществления арил, такой как фенил, не имеет заместителей.
Настоящее раскрытие также распространяется на модели заместителей, описанные выше в отношении арила и фенила, применительно к гетероарилу.
В одном из вариантов осуществления гетероарил не является пиридином.
Конъюгация с поверхностью твердой фазы является важным аспектом настоящего раскрытия, поскольку позволяет присоединять полипептиды к гранулам или планшетам, например, из синтетического материала, такого как пластик или смола, для облегчения очистки или скрининга, такого как высокопроизводительный скрининг.
В одном из вариантов осуществления R1 представляет собой молекулу полезной нагрузки, примеры которой даны ниже в разделе определений. В одном из вариантов осуществления R1 представляет собой H. В одном из вариантов осуществления R1 представляет собой поверхность твердой фазы.
В одном из вариантов осуществления в способе согласно настоящему раскрытию, где n равняется 1, используют соединение формулы (II),
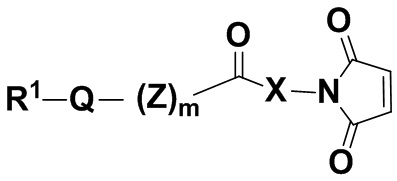 (II),
(II),
и его фармацевтически приемлемые соли, где R1, Q, Z, X и m определены выше для соединений формулы (I).
В одном из вариантов осуществления в способе согласно настоящему раскрытию, где n равняется 0, используют соединение формулы (III),
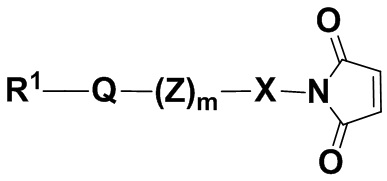 (III),
(III),
и его фармацевтически приемлемые соли, где R1, Q, Z, X и m определены выше для соединений формулы (I).
В одном из вариантов осуществления молекула малеимида находится в соединении формулы (IIa),
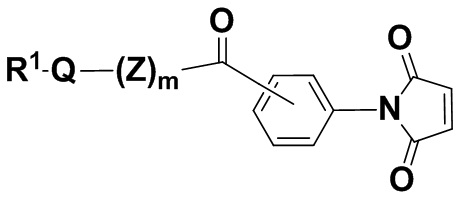 (IIa),
(IIa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIaa),
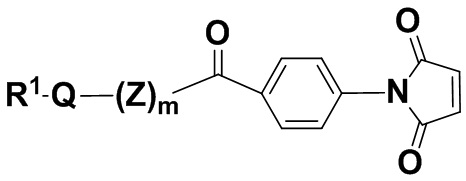 (IIaa),
(IIaa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы галогена, гидроксила, C1-6алкила, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в мета-положении, как показано в соединении формулы (IIaa'),
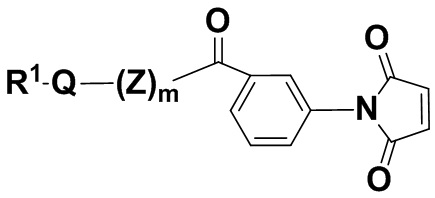 (IIaa'),
(IIaa'),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы галогена, гидроксила, C1-6алкила, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления молекула малеимида находится в соединении формулы (IIaaa),
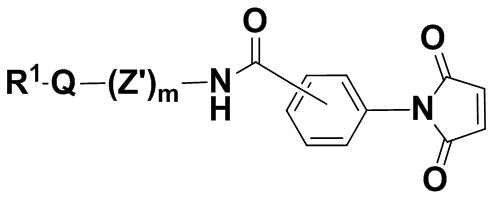 (IIaaa),
(IIaaa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), фенил несет 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 -(OCH2CH2)q-OR3, и Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в пара-положении. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в мета-положении.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIb),
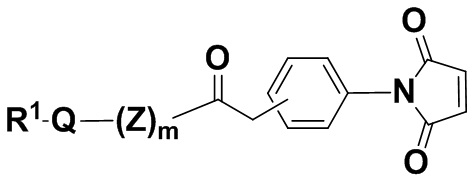 (IIb),
(IIb),
и ее фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIbb),
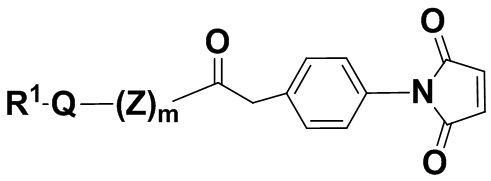 (IIbb),
(IIbb),
и его фармацевтически приемлемых солях, где Q, Z, X, R1 и m определены выше для соединений формулы (I).
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в мета-положении, как показано в соединении формулы (IIbb'),
 (IIbb'),
(IIbb'),
и его фармацевтически приемлемых солях, где Q, Z, X, R1 и m определены выше для соединений формулы (I).
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIbbb),
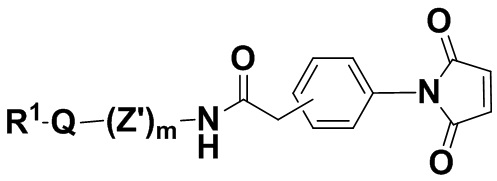 (IIbbb),
(IIbbb),
и ее фармацевтически приемлемых солях, где R1, Q и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3,
Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в пара-положении фенильного кольца. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в мета-положении фенильного кольца.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIc),
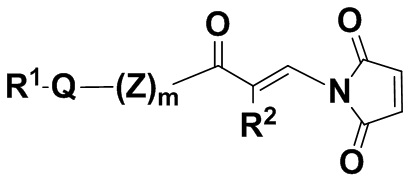 (IIc),
(IIc),
или ее изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами, при этом Q, Z, R1, R2 и m определены выше для соединений формулы (I), и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIcc),
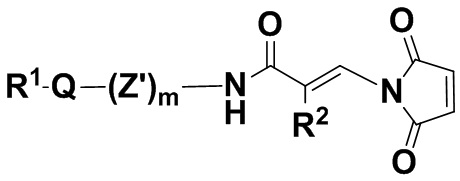 (IIcc),
(IIcc),
или ее изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами,
где Q, Z, R1, R2 и m определены выше в п. 1, и Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IId),
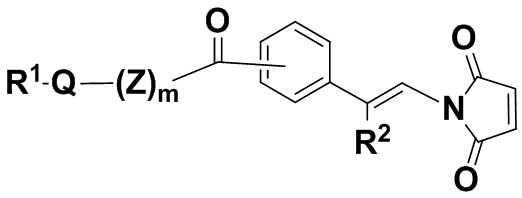 (IId),
(IId),
или ее изомере, где R2 и R1Q(Z')mNHC(O)Ph- поменяны местами,
или где Q, Z, R1, R2 и m определены выше в п. 1, и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и
-(OCH2CH2)q-OR3, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIdd),
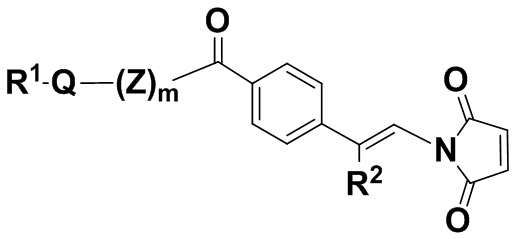 (IIdd),
(IIdd),
или его изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами,
где Q, Z, R1, R2 и m определены выше в п. 1, и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3, и его фармацевтически приемлемых солях.
В одном из вариантов осуществления группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIdd'),
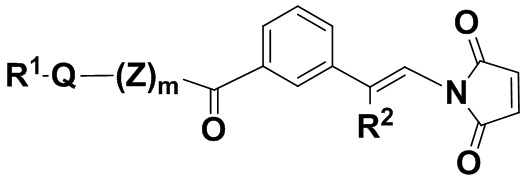 (IIdd'),
(IIdd'),
или его изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами,
где Q, Z, R1, R2 и m определены выше в п. 1, и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3, и его фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIddd),
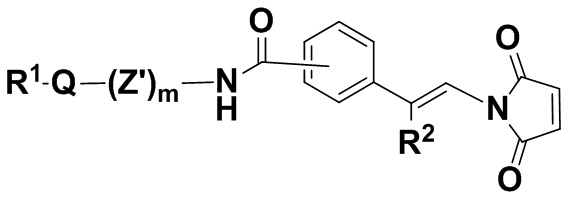 (IIddd),
(IIddd),
или ее изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами,
фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3,
Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей, и ее фармацевтически приемлемых солях. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в пара-положении фенильного кольца. В одном из вариантов осуществления группа R1Q(Z')mNC(O)- находится в мета-положении фенильного кольца.
В одном из вариантов осуществления соединение формулы IIc, IIcc, IId, IIdd или его производное предоставлено в виде Е-изомера.
В одном из вариантов осуществления соединение формулы IIc, IIcc, IId, IIdd или его производное предоставлено в виде Z-изомера.
В одном из вариантов осуществления молекула малеимида находится в соединении формулы (IIIa),
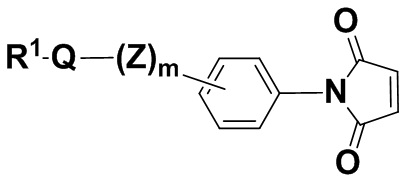 (IIIa),
(IIIa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления группа R1Q(Z)m- находится в пара-положении, как показано в соединении формулы (IIIaa),
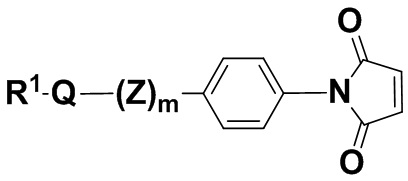 (IIIaa),
(IIIaa),
или его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3,
-COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления группа R1Q(Z)m- находится в мета-положении, как показано в соединении формулы (IIIaa'),
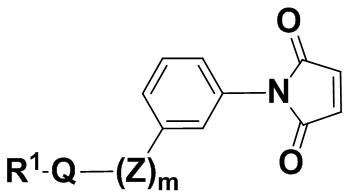 (IIIaa'),
(IIIaa'),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
В одном из вариантов осуществления молекула малеимида находится в соединении формулы (IIIaaa),
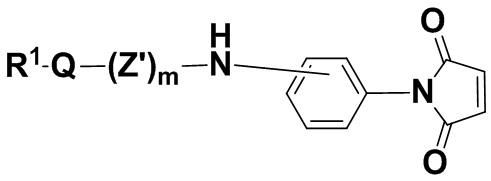 (IIIaaa),
(IIIaaa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3 и
Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей. В одном из вариантов осуществления R1Q(Z')mNH- находится в пара-положении фенильного кольца. В одном из вариантов осуществления R1Q(Z')mNH- находится в мета-положении фенильного кольца.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIIb),
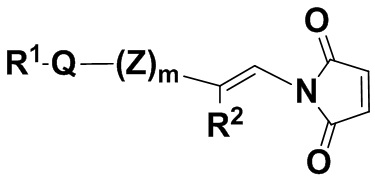 (IIIb),
(IIIb),
или его изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами, при этом Q, Z, R1, R2 и m имеют значения, указанные для соединений формулы (I), и его фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIIbb),
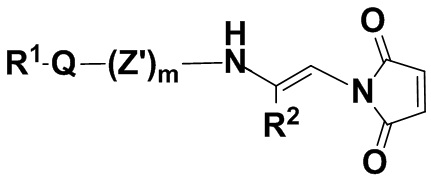 (IIIbb),
(IIIbb),
или ее изомере, где R2 и R1Q(Z')mNHC(O)- поменяны местами,
где Q, Z, R1, R2 и m имеют значения, указанные для соединений формулы (I), и Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIIc),
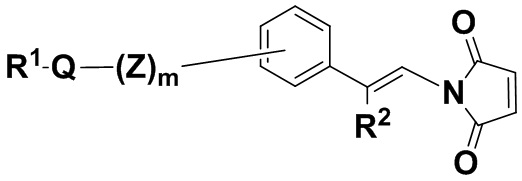 (IIIc),
(IIIc),
или ее изомере, где R2 и R1Q(Z')mNHC(O)Ph- поменяны местами,
или где Q, Z, R1, R2 и m имеют значения, указанные для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIIcc),
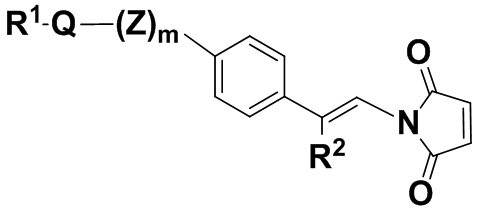 (IIIcc),
(IIIcc),
или ее изомере, где R2 и R1Q(Z')mNHC(O)Ph- поменяны местами,
или где Q, Z, R1, R2 и m имеют значения, указанные для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления малеимидная структурная единица находится в молекуле формулы (IIIcc'),
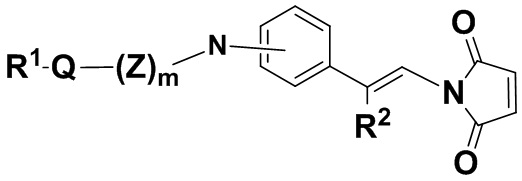 (IIIccc),
(IIIccc),
или ее изомере, где R2 и R1Q(Z')mNHC(O)Ph- поменяны местами,
или где n, Q, Z, R1, R2 и m имеют значения, указанные для соединений формулы (I), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3, и ее фармацевтически приемлемых солях.
В одном из вариантов осуществления соединение формулы IIc, IIcc, IId, IIdd, IIdd', IIddd, IIIb, IIIbb, IIIc, IIIcc, IIIccc, IIId или его производное предоставлено в виде Е-изомера.
В одном из вариантов осуществления соединение формулы IIc, IIcc, IId, IIdd, IIdd', IIddd, IIIb, IIIbb, IIIc, IIIcc, IIIccc, IIId или его производное предоставлено в виде Z-изомера.
В одном из вариантов осуществления R2 представляет собой фтор.
В одном из вариантов осуществления фрагмент -QZ (т.e. когда m равняется 1) или -QZ'NH (когда m равняется 1), в случае необходимости в данной структуре, представляет собой:
-QOC(O)(CH2CH2O)1-8(CH2)0-1NH, например -QOC(O)(CH2CH2O)1-6(CH2)0-1NH, такой как -QOC(O)(CH2CH2O)2,3,4,5(CH2)0-1NH, более конкретно,
-QOC(O)(CH2CH2O)4NH.
В одном из вариантов осуществления Q представляет собой связь. В одном из вариантов осуществления Q представляет собой компонент для конъюгации. Компонент для конъюгации представляет собой структурную единицу, которую можно использовать для конъюгации одной молекулы или фрагмента с другой молекулой или фрагментом.
В одном из вариантов осуществления Q содержит или представляет собой функциональную группу, например, выбранную из группы, включающей тетразин, функционализированный тетразин, сложный эфир NHS (сложный эфир N-гидроксисукцимида), сложный эфир тетрафторфенила и их комбинации.
В одном из вариантов осуществления Q представляет собой полимеризируемую функциональную группу, например, выбранную из группы, включающей алкин, тетразин, дериватизированный тетразин, липид, наночастицу, дендример, хелатор металла и их комбинации.
В одном из вариантов осуществления компоненты для конъюгации Q представляет собой компонент клик-химии. Примеры компонентов клик-химии включают остатки коллекции Click-matesTM, такие как:
алкины Click-matesTM, которые включают 5-пропаргилокси-dU CEP, 5-октадиинил-dU CEP, алкинил-модификатор-C6-dT CEP, 5-(пропаргилокси)-2'-дезоксиуридин, 5-(1,7-октадиин-1-ил)-2'-дезоксиуридин, 5-октадиинил-TMS-dU CEP, 5-октадиинил-TMS-dC CEP, 5-октадиинил-dC CEP, 5-октадиинил-TIPS-dU CEP и
алкины Click-easy® (для клик-модификаций без меди), которые включают BCN CEP I, BCN CEP II, BCN-N-гидроксисукцинимидный сложный эфир I, BCN-N-гидроксисукцинимидный сложный эфир II, MFCO-N-гидроксисукцинимидный сложный эфир и MFCO CEP.
Остатки, как используется в данном документе, относятся к структуре, которая остается после того, как имеет место соответствующая реакция с присоединением молекулы к одному или нескольким молекулярным фрагментам (компонентам).
В одном из вариантов осуществления компонент для конъюгации представляет собой BCN.
В одном из вариантов осуществления компонент для конъюгации Q представляет собой биотин. В одном из вариантов осуществления Q представляет собой фрагмент:
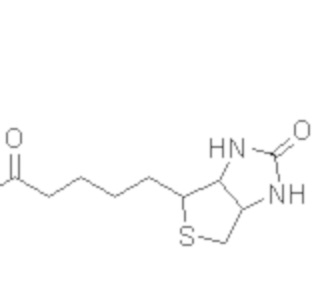
В одном из вариантов осуществления Z независимо выбран из -C1-12алкилена,
-OC(O)(CH2CH2O)1-8(CH2)0-1NH, например -OC(O)(CH2CH2O)1-6(CH2)0-1NH, такого как -OC(O)(CH2CH2O)2,3,4,5(CH2)0-1NH, более конкретно -OC(O)(CH2CH2O)4NH.
В одном из вариантов осуществления Z' независимо выбран из -C1-12алкилена,
-OC(O)(CH2CH2O)1-8(CH2)0-1, например -OC(O)(CH2CH2O)1-6(CH2)0-1, такого как
-OC(O)(CH2CH2O)2,3,4,5(CH2)0-1, более конкретно -OC(O)(CH2CH2O)4.
В одном из вариантов осуществления Y-X в молекулах формулы (I) представляет собой C(O)CH2фенил(малеимид или сукцинимид), и m равняется 0, и Q представляет собой связь, и полезная нагрузка связана через амидную связь с оксогруппой в фрагменте Y-X.
В одном из вариантов осуществления полезная нагрузка связана посредством лабильной связи, например гидразоновой (высвобождение при низком рН), дисульфидной, иминной или аналогичной.
Предпочтение, приведенное в данном документе для соединений формулы (I), в равной степени применимы для соединений с другими формулами, описанными в данном документе, в случае необходимости.
Можно использовать фармацевтически приемлемые соли, например соли минеральных кислот, такие как гидрохлориды, гидробромиды, фосфаты и сульфаты, или соли органических кислот, такие как ацетаты, пропионаты, малонаты и бензоаты.
В одном из вариантов осуществления малеимидную структурную единицу конъюгируют с помощью нативного цистеина в полипептиде. В одном из вариантов осуществления малеимид конъюгируют с помощью цистеина, сконструированного в полипептиде (также называемого в данном документе сконструированным цистеином). В одном из вариантов осуществления цистеин представляет собой подвергнутый воздействию растворителя цистеин.
В одном из вариантов осуществления одну или несколько стадий конъюгации, например, конъюгацию малеимида с полипептидом, проводят при pH в диапазоне от 5 до 9, например, pH 5,5-8,6, таком как 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1, 8,2, 8,3, 8,4, 8,5 или 8,6, или комбинации одного или нескольких из указанных значений pH.
В одном из вариантов осуществления одну или несколько стадий конъюгации, например, конъюгацию малеимида с полипептидом, проводят при температуре в диапазоне от приблизительно 4°C до приблизительно 37°C, например, от 8°C до 37°C, от 8°C до 30°C, от 8°C до 25°C или от 21°C до 31°C, такой как 5°C, 6°C, 7°C, 8°C, 9°C, 10°C, 11°C, 12°C, 13°C, 14°C, 15°C, 16°C, 17°C, 18°C, 19°C, 20°C, 21°C, 22°C, 23°C, 24°C, 25°C, 26°C, 27°C, 28°C, 29°C, 30°C, 31°C, 32°C, 33°C, 34°C, 35°C, 36°C или 37°C, или комбинации одной или нескольких из указанных температур.
В одном из вариантов осуществления одну или несколько стадий конъюгации проводят в подходящем буфере, например буфере, выбранном из группы, включающей фосфатный буфер, цитратный буфер, боратный буфер, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота), MES (2-(N-морфолино)этансульфоновая кислота)), PIPES (пиперазин-N,N′-бис(2-этансульфоновая кислота)), MOPS (3-(N-морфолино)пропансульфоновая кислота)), таком как фосфатный.
В одном из вариантов осуществления буфер не содержит первичного амина, например TRIS и тому подобного.
В одном из вариантов осуществления эффективность одной или нескольких реакций конъюгации, например, конъюгации малеимида с полипептидом, составляет 50% или более, например 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%.
Таким образом, в одном из вариантов осуществления присутствует низкий процент неконъюгированного полипептида (такого как антитело) после реакции, например 5% или менее, такой как 4%, 3%, 2%, 1% или менее.
В одном из вариантов осуществления отношение соединения формулы (I) и другими формулами, описанными в данном документе, к полипептиду на стадии конъюгации составляет от 1 к 1, соответственно, до 5 к 1, такое как 2 к 1, 3 к 1 или 4 к 1.
В одном из вариантов осуществления тиол-конъюгат дополнительно вступает в реакцию с полезной нагрузкой, наночастицей или поверхностью твердой фазы с помощью Cu(I)-катализируемого азид-алкинового циклоприсоединения (CuAAC) с использованием солей меди, восстанавливающих средств, таких как аскорбат натрия, и/или Cu(I)-стабилизирующих лигандов, таких как 2-[4-{(бис[(1-трет-бутил-1H-1,2,3-триазол-4-ил)метил]амино)-
метил}-1H-1,2,3-триазол-1-ил]этилгидросульфат ( BTTES); трис[(1-
бензил-1H-1,2,3-триазол-4-ил)метил]амин (TBTA); трис[(1-гидроксипропил-
1H-1,2,3-триазол-4-ил)метил]амин (THTPA) и тому подобных, с образованием триазольной связи.
В одном из вариантов осуществления тиол-конъюгат дополнительно вступает в реакцию с полезной нагрузкой, наночастицей или поверхностью твердой фазы с помощью азид-алкинового циклоприсоединения, облегченного напряжением (SPAAC), с использованием циклических алкинов, таких как биарилазациклооктинон (BARAC); дибензоциклооктин (DBCO), бицикло[6.1.0]нонин (BCN) и тому подобных, с образованием триазольной связи.
В одном из вариантов осуществления тиол-конъюгат дополнительно вступает в реакцию с полезной нагрузкой, наночастицей или поверхностью твердой фазы с помощью реакции тетразина и транс-циклооктена с образованием дигидропиразиновой связи.
В одном из вариантов осуществления в данном способе используют стадию гидролиза, например, гидролиз полученного сукцинимида проводят при pH в диапазоне от 7 до 12, например pH от 7,4 до 9, таком как 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1, 8,2, 8,3, 8,4, 8,5, 8,6, 8,7, 8,8, 8,9 или 9,0 или комбинации одного или нескольких из них.
В одном из вариантов осуществления на стадии гидролиза используют буфер, например буфер, выбранный из группы, включающей фосфатный буфер, цитратный буфер, боратный буфер, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота), MES (2-(N-морфолино)этансульфоновая кислота)), PIPES (пиперазин-N,N′-бис(2-этансульфоновая кислота)), MOPS (3-(N-морфолино)пропансульфоновая кислота)), такой как фосфатный.
В одном из вариантов осуществления одну или несколько стадий гидролиза, например, гидролиз сукцинимида, проводят при температуре в диапазоне от приблизительно 4°C до приблизительно 37°C, например, от 8°C до 37°C, от 8°C до 30°C, от 8°C до 25°C или от 21°C до 31°C, такой как 5°C, 6°C, 7°C, 8°C, 9°C, 10°C, 11°C, 12°C, 13°C, 14°C, 15°C, 16°C, 17°C, 18°C, 19°C, 20°C, 21°C, 22°C, 23°C, 24°C, 25°C, 26°C, 27°C, 28°C, 29°C, 30°C, 31°C, 32°C, 33°C, 34°C, 35°C, 36°C или 37°C, или комбинации одной или нескольких из указанных температур.
В одном из вариантов осуществления одну или несколько реакций в настоящем способе, например, реакцию конъюгации, проводят в присутствии катализатора. Примеры катализаторов включают катализаторы на основе переходных металлов, таких как медь, олово, неорганические оксиды, такие как молибдат.
В одном из вариантов осуществления в одной или нескольких реакциях в настоящем способе, например, в реакции конъюгации, не используют катализатор.
Следует также отметить, что в широком диапазоне условий гидролиз происходит с высокой эффективностью после конъюгации, поэтому легко можно выбрать условия таким образом, что конъюгация и гидролиз осуществляются последовательно в той же самой реакции. Фактически, это желательно, поскольку минимизирует количество стадий. Альтернативные/дополнительные условия для последующих стадий (например, фильтрации, хранения, замены буфера, очистки на колонке) можно выбрать для обеспечения гидролиза конъюгата. В одном из вариантов осуществления при гидролизе не используют комбинацию низкого рН и низкой температуры.
Настоящее раскрытие также распространяется на гидролизованные молекулы, например, полученные или получаемые по настоящему способу. В одном из вариантов осуществления эти молекулы имеют формулу (IV),
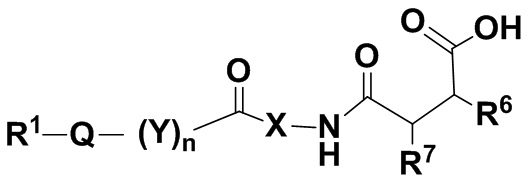 (IV),
(IV),
и ее фармацевтически приемлемые соли, где
Q, R1, Z и m определены выше для соединений формулы (I), и
R6 представляет собой H или полипептидный остаток, R7 представляет собой H или полипептидный остаток, где по меньшей мере один из R6 или R7 представляет собой полипептидный остаток, а другой представляет собой H.
Гидролиз может иметь место в одном из двух положений, как показано в схеме 1:
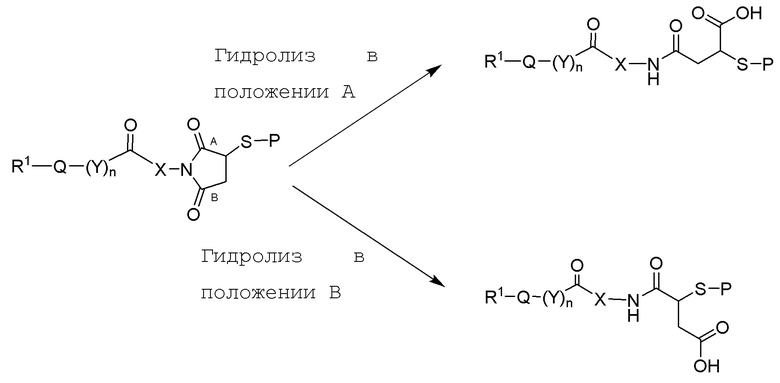
где Р представляет собой полипептид.
Настоящее раскрытие распространяется на соединения/молекулы, полученные или получаемые по способу данного документа.
В одном из вариантов осуществления полученные молекулы являются стабильными или, например, физически, химически и термически стабильными. Доказательством физической нестабильности является, например, агрегация, которую можно измерить с помощью обычных методов, таких как эксклюзионная хроматография. Доказательством химической нестабильности является, например, деградация или распад молекулы, такой как отсоединение полезной нагрузки. Доказательством термической нестабильности является, например, денатурация.
В одном из вариантов осуществления в гидролизованных молекулах по настоящему раскрытию имеется 20% потерь полезной нагрузки или менее после инкубации с бета-меркаптоэтанолом, например 10% потерь или менее, такое как 5% потерь или менее. В одном из вариантов осуществления потеря происходит в течение периода от 1 до 36 часов, такого как от 2 до 24 часов.
В одном из вариантов осуществления в гидролизованных молекулах по настоящему раскрытию имеется 20% потерь полезной нагрузки или менее после инкубации с сывороткой (например, мышиной сывороткой или бычьей сывороткой), например 10% потерь или менее, такое как 5% потерь или менее. В одном из вариантов осуществления потеря происходит в течение периода от 1 до 36 часов, такого как 24 часа.
В одном из вариантов осуществления снижение активности, например, как измерено с помощью IC50, при инкубации с сывороткой составляет 20% или менее, например 10% или менее, такое как 5% или менее, более конкретно 4%, 3%, 2% или 1%.
ОПРЕДЕЛЕНИЯ
Присоединение по Михаэлю (также называемое в данном документе как 1,4-присоединение по Михаэлю) представляет собой нуклеофильное присоединение карбаниона или другого аниона к альфа, бета-ненасыщенному карбонильному соединению.
Выражение алкил, используемое в данном документе, относится к алкилу с прямой или разветвленной цепью, такому как, без ограничения, метил, этил, пропил, изопропил, бутил и трет-бутил. В одном из вариантов осуществления алкил относится к алкилу с прямой цепью. Алкил представляет собой концевую группу, то есть на конце цепи. C1-6алкил включает в себя C1, C2, C3, C4, C5 и C6.
Выражение алкокси-, используемое в данном документе, относится к алкокси- с прямой или разветвленной цепью, например, метокси-, этокси-, пропокси-, бутокси-. Выражение алкокси-, используемое в данном документе, также распространяется на варианты осуществления, в которых атом кислорода находится в пределах алкильной цепи, например -CH2CH2OCH3 или -CH2OCH3. В одном из вариантов осуществления алкокси- связана через кислород с остальной частью молекулы. В одном из вариантов осуществления настоящее раскрытие относится к алкокси- с прямой цепью.
Выражение арил, используемое в данном документе, относится к C6-C36 карбоциклической системе, например, C6-C10 карбоциклической системе, содержащей по меньшей мере одно ароматическое кольцо, например, нафталин, фенил, инден, индан, 1, 2, 3,4-тетрагидронафтален, азулен, например, нафталин или фенил, такое как фенил.
Гетероарил представляет собой 5-36-членное ароматическое карбоциклическое кольцо или бициклическую кольцевую систему, содержащую один или несколько (например 1, 2, 3 или 4) гетероатомов, независимо выбранных из O, N и S. Примеры гетероарилов включают: пиррол, оксазол, тиазол, изотиазол, имидазол, пиразол, изоксазол, пиридин, пиридазин, пиримидин, пиразин, бензотиофен, бензофуран или 1,2,3- и 1,2,4-триазол. В бициклической кольцевой системе определение гетероарил будет выполнено, если по меньшей мере одно кольцо содержит гетероатом и по меньшей мере одно кольцо является ароматическим. Гетероарил может быть связан с остальной частью молекулы через карбоциклическое кольцо или кольцо, содержащее гетероатом.
Выражение оксо-, используемое в данном документе, относится к C=O и будет, как правило, представлено в виде C(O).
Относительно насыщенной или ненасыщенной, разветвленной или неразветвленной C1-25алкиленовой цепи, где по меньшей мере один атом углерода (например 1, 2 или 3 атома углерода, соответственно 1 или 2, в частности 1) заменен гетероатомом, выбранным из O, N, и указанная цепь необязательно заменена одной или несколькими оксогруппами, специалисту в данной области техники будет ясно, что гетероатом может заменять первичный, вторичный или третичный атом углерода, то есть CH3, -CH2- или -CH-, или разветвленную углеродную группу, как подходит технически. Данное определение также применимо там, где этот язык используется в контексте цепей другой длины, чем от 1 до 25 атомов углерода.
Алкилен представляет собой связывающую группу, т.е. соединенную на каждом конце с другими частями/компонентами молекулы. C1-25алкилен включает C1, C2, C3, C4, C5, C6, C7, C8 или C9, C10, C11, C12, C13, C14, C15, C16, C17, C18, C19, C20, C21, C22, C23, C24 и C25.
C0 там, где "особенность" отсутствует.
Выражение галоген- или галоген, используемое в данном документе, относится к йод-, бром-, хлор- или фтор-, такому как фтор-.
Выражение конъюгированный, используемое в данном документе, относится к соединению/молекуле, образованной путем объединения двух соединений или молекул или фрагментов вместе.
Выражение гидролиз, используемое в данном документе, относится к реакциям с расщеплением колец или молекул путем добавления молекулы воды.
Выражение электроноакцепторная группа, используемое в данном документе, относится к заместителю, который привлекает электроны (или притягивает электроны) из структурной единицы, к которой он присоединяется.
Выражение электронодонорная группа, используемое в данном документе, относится к заместителю, который дает, "жертвует" электроны структурной единице, к которой он присоединяется.
Выражение нейтральная группа в контексте настоящего раскрытия не имеет отношения к заряду как таковому, но относится к электронодонорным или акцепторным свойствам. Такие группы не имеют никакого влияния на электронные свойства структурной единицы, к которой они присоединяются.
Полипептиды для применения в настоящем раскрытии
Выражения "полипептид", "пептид" и "белок" используются в данном документе взаимозаменяемо для обозначения полимеров из аминокислот любой длины. Полимер может быть линейным или разветвленным, может содержать модифицированные аминокислоты и может быть разделен соединениями, отличными от аминокислот. Выражения также охватывают полимер из аминокислот, который был модифицирован в естественных условиях или посредством вмешательства; например, посредством образования дисульфидной связи, гликозилирования, липидизации, ацетилирования, фосфорилирования или любой другой манипуляции или модификации, такой как конъюгация с метящим компонентом. В данное определение также включены, например, полипептиды, содержащие один или несколько аналогов аминокислоты (в том числе, например, не встречающиеся в природе аминокислоты и т. п.), а также другие модификации, известные из уровня техники. Понятно, что полипептиды настоящего раскрытия основаны на антителах.
Выражение полипептид, используемое в данном документе, относится к последовательности из 5 или более аминокислот с наличием или без вторичной или третичной структуры, которая содержит по меньшей мере одну тиоловую группу. Таким образом, в настоящем раскрытии выражение "полипептиды" включает пептиды, полипептиды и белки. Они используются взаимозаменяемо, если не указано иное.
В одном из вариантов осуществления полипептид представляет собой белок. Белки обычно содержат вторичную и/или третичную структуру и могут быть мономерными или мультимерными по форме.
В одном из вариантов осуществления белок представляет собой антитело в виде одиночных цепей или связанных цепей, или их связывающих фрагментов.
Выражения "антитело" или "иммуноглобулин", используемые в данном документе взаимозаменяемо, включают целые антитела и любой их антигенсвязывающий фрагмент или любые их одиночные цепи.
Типичное антитело содержит по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, связанные между собой дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (в настоящем документе сокращенно VH, VH-область или VH-домен) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех или четырех константных доменов, CH1, CH2, CH3, и CH4. Fc-область включает в себя полипептиды, содержащие константную область антитела за исключением первого домена константной области иммуноглобулина, и их фрагменты. Таким образом, для IgG "Fc-область" относится к CH2 и CH3 и, необязательно, ко всей или к части гибкой шарнирной области с N-конца этих доменов. Выражение "Fc-область" может относиться к данной области в отдельности или к данной области в контексте антитела, фрагмента антитела или Fc-гибридного белка.
Каждая легкая цепь состоит из вариабельной области легкой цепи (в данном документе сокращенно VL, VL-область или VL-домен) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена CL.
Области VH и VL можно дополнительно подразделять на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), чередующиеся с более консервативными областями, называемыми каркасными областями (FW). Каждая VH и VL состоит из трех CDR и четырех FW, расположенных от амино-конца к карбокси-концу в следующем порядке: FW1, CDR1, FW2, CDR2, FW3, CDR3, FW4. Каркасные области можно обозначить согласно их соответствующим VH и VL-областям. Следовательно, например, VH-FW1 будет относиться к первой каркасной области VH. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплемента.
Выражение "антитело" означает молекулу иммуноглобулина или его антигенсвязывающий фрагмент, который распознает и специфически связывается с мишенью, такой как белок, полипептид, пептид, углевод, полинуклеотид, липид или комбинации вышеуказанных, посредством по меньшей мере одного антиген-распознающего участка (также называемого связывающий участок) вариабельной области молекулы иммуноглобулина. Используемое в данном документе выражение "антитело" охватывает интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител (такие как Fab, Fab', F(ab')2 и Fv-фрагменты), фрагменты одноцепочечных антител (scFv и стабилизированный дисульфидом scFv (dsFv)), полиспецифические антитела, такие как биспецифические антитела, полученные по меньшей мере из двух различных антител, или полиспецифические антитела, образованные из фрагментов антител (см., например, публикации PCT WO96/27011, WO2007/024715, WO2009018386, WO2009/080251, WO2013006544, WO2013/070565 и WO2013/096291), химерные антитела, гуманизированные антитела, человеческие антитела, гибридные белки, содержащие антиген-связывающий фрагмент антитела, а также любую другую модифицированную молекулу иммуноглобулина, содержащую антигенсвязывающий фрагмент, до тех пор, пока антитела проявляют желаемую биологическую активность.
Антитело может быть любым из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, или подклассов (изотипов) (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), или аллотипов (например, Gm, например G1m(f, z, a или x), G2m(n), G3m(g, b или c), Am, Em и Km(1, 2 или 3)). Разные классы иммуноглобулинов характеризуются разными и хорошо известными структурами субъединиц и пространственными конфигурациями. Антитела могут быть получены от любого млекопитающего, включая без ограничения людей, обезьян, свиней, лошадей, кроликов, собак, котов, мышей и т.д., или других животных, таких как птицы (например, куры).
Выражение "антигенсвязывающий фрагмент" относится к фрагменту, включающему в себя вариабельные области интактного антитела, распознающие антиген. Из уровня техники известно, что антигенсвязывающая функция антитела может быть представлена фрагментами полноразмерного антитела. Примеры фрагментов антитела включают без ограничения Fab, Fab', F(ab')2, Fv-фрагменты, scFvs, линейные антитела, одноцепочечные антитела и полиспецифические антитела, образованные из фрагментов антитела.
Таким образом, в одном из вариантов осуществления антитело, используемое в настоящем изобретении, может содержать полную молекулу антитела, имеющую полноразмерные тяжелые и легкие цепи, или ее фрагмент, и может представлять собой без ограничения Fab, модифицированный Fab, Fab', модифицированный Fab', F(ab')2, Fv, однодоменные антитела (например, VH или VL или VHH), scFv, би-, три- или тетравалентные антитела, Bis-scFv, диатела, триатела, тетратела, комбинации вышеупомянутого и эпитоп-связывающие фрагменты любого из вышеуказанного.
Другими специфически рассматриваемыми антителами являются "олигоклональные" антитела, которые представляют собой заранее определенную смесь различных моноклональных антител. См., например, публикацию PCT WO 95/20401; патенты США №№ 5789208 и 6335163. Предпочтительно олигоклональные антитела состоят из заранее определенной смеси антител против одного или нескольких эпитопов, которые генерируются в отдельной клетке. Более предпочтительно, олигоклональные антитела включают множество тяжелых цепей, способных к спариванию с общей легкой цепью с получением антител с несколькими специфичностями (например, публикация PCT WO 04/009618). Олигоклональные антитела являются особенно полезными, когда желательно нацелиться на несколько эпитопов на одной молекуле-мишени. Специалисты в данной области техники будут знать или смогут определить, какой тип антитела или смеси антител применим для предполагаемой цели и желаемой потребности.
Другие фрагменты, конкретно рассматриваемые для применения в настоящем раскрытии, представляют собой небольшие сконструированные белковые домены, такие как каркас (см., например, публикации патентов США №№ 2003/0082630 и 2003/0157561). Каркасы основаны на известных природных семействах доменов, не принадлежащих к антителам, в частности белковых внеклеточных доменов, которые, как правило, имеют небольшой размер (от ~100 AA до ~300 AA) и содержат высоко структурированное ядро, связанное с вариабельными доменами с высокой конформационной устойчивостью, допускающей вставки, делеции или другие замены. Такие вариабельные домены могут создавать предполагаемую связывающую поверхность для любого целевого белка. В целом, конструирование общего белкового каркаса состоит из двух основных стадий: (i) выбор подходящего корового белка с требуемыми особенностями и (ii) получение комплексных комбинаторных библиотек путем мутагенеза части или всех доменов, допускающих высокую структурную вариабельность, отображение этих библиотек в соответствующем формате (т.e. фаговом, рибосомальном, бактериальном или дрожжевом) и скрининг библиотеки на мутированный каркас, имеющий желаемые характеристики связывания (например, целевую специфичность и/или аффинность). Структура исходных каркасов может быть весьма разнообразной и включать высоко структурированные белковые домены, включая без ограничения домены FnIII (например, AdNectin, см., например, Protein Eng. Des. Sel. 18, 435-444 (2005), US2008/00139791 и WO2005/056764, TN3, см., например, WO2009/058379 и WO2011/130324); Z-домены белка A (Affibody (аффитело), см., например Protein Eng. Des. Sel. 17, 455-462 (2004) и EP1641818A1); домен A из рецептора к LDL (Avimer (авимеры), см., например, Nature Biotechnology 23(12), 1556-1561 (2005), и Expert Opinion on Investigational Drugs 16(6), 909-917 (June 2007)); домены анкириновых повторов (DARPin (дарпины), J. Mol. Biol. 332,489-503 (2003), PNAS (2003), и Biol. 369, (2007), и WO02/20565); домены лектина C-типа (тетранектины, см., например, WO02/48189). При необходимости два или более таких сконструированных каркасных домена можно соединить вместе с образованием поливалентного связывающего белка. Отдельные домены могут нацеливать один тип белка или несколько, в зависимости от показаний к применению/заболеванию.
Практически любая молекула (или ее часть, например, субъединицы, домены, мотивы или эпитоп) может быть нацелена с помощью и/или встроена в фрагмент, включая без ограничения интегральные мембранные белки, в том числе ионные каналы, ионные насосы, сопряженные с G-белком рецепторы, структурные белки; адгезивные белки, такие как интегрины; транспортеры; белки, участвующие в передаче сигнала, и закрепленные липидами белки, включая G-белки, ферменты, такие как киназы, включая закрепленные в мембранах киназы, связанные с мембранами ферменты, протеазы, липазы, фосфатазы, синтетазы жирных кислот, пищеварительные ферменты, такие как пепсин, трипсин и химотрипсин, лизоцим, полимеразы; рецепторы, такие как рецепторы гормонов, рецепторы к лимфокинам, рецепторы к монокинам, рецепторы факторов роста, рецепторы к цитокинам; цитокины и много другое.
В некоторых аспектах полипептид, используемый в настоящем раскрытии, нацеливает и/или включает в себя весь или часть (например, субъединицы, домены, мотивы или эпитоп) фактора роста, цитокина, родственного цитокину белка, фактора роста, лиганда рецептора или рецептора, выбранного из числа, например, BMP1, BMP2, BMP3B (GDF10), BMP4, BMP6, BMP8, CSF1(M-CSF), CSF2 (GM-CSF), CSF3 (G-CSF), EPO, FGF1 (αFGF), FGF2 (βFGF), FGF3 (int-2), FGF4 (HST), FGF5, FGF6 (HST-2), FGF7 (KGF), FGF9, FGF10, FGF11, FGF12, FGF12B, FGF14, FGF16, FGF17, FGF19, FGF20, FGF21, FGF23, FGFR, FGFR1, FGFR2, FGFR3, FGFR4, FGFRL1, FGFR6, IGF1, IGF2, IGF1R, IGF2R, IFNA1, IFNA2, IFNA4, IFNA5, IFNA6, IFNA7, IFNAR1, IFNAR2, IFNB1, IFNG, IFNW1, FIL1, FIL1 (EPSILON), FIL1 (ZETA), IL1A, IL1B, IL2, IL3, IL4, IL5, IL6, IL7, IL8, IL9, IL10, IL11, IL12A, IL12B, IL13, IL14, IL15, IL16, IL17, IL17B, IL18, IL19, IL20, IL22, IL23, IL24, IL25, IL26, IL27, IL28A, IL28B, IL29, IL30, IL2RA, IL1R1, IL1R2, IL1RL1, IL1RL2, IL2RA, IL2RB, IL2RG, IL3RA, IL4R, IL5RA, IL6R, IL7R, IL8RA, IL8RB, IL9R, IL10RA, IL10RB, IL11RA, IL12RB1, IL12RB2, IL13RA1, IL13RA2, IL15RA, IL17R, IL17RA, IL17RB, IL17RC, IL17RD, IL18R1, IL20RA, IL20RB, IL21R, IL22R, IL22RA1, IL23R, IL27RA, IL28RA, PDGFA, PDGFB, PDGFRA, PDGFRB, TGFA, TGFB1, TGFB2, TGFB3, TGFBR1, TGFBR2, TGFBR3, ACVRL1, GFRA1, LTA (TNF-бета), LTB, TNF (TNF-альфа), TNFSF4 (лиганд OX40), TNFSF5 (лиганд CD40), TNFSF6 (FasL), TNFSF7 (лиганд CD27), TNFSF8 (лиганд CD30), TNFSF9 (лиганд 4-1BB), TNFSF10 (TRAIL), TNFSF11 (TRANCE), TNFSF12 (APO3L), TNFSF13 (April), TNFSF13B, TNFSF14 (HVEM-L), TNFSF15 (VEGI), TNFSF18, TNFRSF1A, TNFRSF1B, TNFRSF10A (Trail-рецептор), TNFRSF10B (Trail-рецептор 2), TNFRSF1°C (Trail-рецептор 3), TNFRSF10D (Trail-рецептор 4), FIGF (VEGFD), VEGF, VEGFB, VEGFC, KDR, FLT1, FLT4, NRP1, IL1HY1, IL1RAP, IL1RAPL1, IL1RAPL2, IL1RN, IL6ST, IL18BP, IL18RAP, IL22RA2, AIF1, HGF, LEP (лептин), PTN, ALK и THPO.
В некоторых аспектах полипептид, используемый в настоящем раскрытии, нацеливает и/или включает в себя весь или часть (например, субъединицы, домены, мотивы или эпитоп) хемокина, рецептора хемокина или родственного хемокину белка, выбранного из числа, например, CCL1(I-309), CCL2 (MCP-1/MCAF), CCL3 (MIP-1a), CCL4 (MIP-1b), CCL5 (RANTES), CCL7 (MCP-3), CCL8 (mcp-2), CCL11 (эотаксин), CCL13 (MCP-4), CCL15 (MIP-1d), CCL16 (HCC-4), CCL17 (TARC), CCL18 (PARC), CCL19 (MIP-3b), CCL20 (MIP-3a), CCL21 (SLC/exodus-2), CCL22 (MDC/STC-1), CCL23 (MPIF-1), CCL24 (MPIF-2/эотаксин-2), CCL25 (TECK), CCL26 (эотаксин-3), CCL27 (CTACK/ILC), CCL28, CXCL1(GRO1), CXCL2 (GRO2), CXCL3 (GRO3), CXCL5 (ENA-78), CXCL6 (GCP-2), CXCL9 (MIG), CXCL10 (IP 10), CXCL11 (I-TAC), CXCL12 (SDF1), CXCL13, CXCL14, CXCL16, PF4 (CXCL4), PPBP (CXCL7), CX3CL1 (SCYD1), SCYE1, XCL1 (лимфотактин), XCL2 (SCM-1b), BLR1 (MDR15), CCBP2 (D6/JAB61), CCR1 (CKR1/HM145), CCR2 (mcp-1RB/RA), CCR3 (CKR3/CMKBR3), CCR4, CCR5 (CMKBR5/ChemR13), CCR6 (CMKBR6/CKR-L3/STRL22/DRY6), CCR7 (CKR7/EBI1), CCR8 (CMKBR8/TER1/ CKR-L1), CCR9 (GPR-9-6), CCRL1 (VSHK1), CCRL2 (L-CCR), XCR1 (GPR5/CCXCR1), CMKLR1, CMKOR1 (RDC1), CX3CR1 (V28), CXCR4, GPR2 (CCR10), GPR31, GPR81 (FKSG80), CXCR3 (GPR9/CKR-L2), CXCR6 (TYMSTR/STRL33/Bonzo), HM74, IL8RA (IL8Ra), IL8RB (IL8Rb), LTB4R (GPR16), TCP10, CKLFSF2, CKLFSF3, CKLFSF4, CKLFSF5, CKLFSF6, CKLFSF7, CKLFSF8, BDNF, C5R1, CSF3, GRCC10 (C10), EPO, FY (DARC), GDF5, HIF1A, IL8, PRL, RGS3, RGS13, SDF2, SLIT2, TLR2, TLR4, TREM1, TREM2, и VHL.
В некоторых аспектах полипептид, используемый в настоящем раскрытии, нацеливает и/или включает в себя весь или часть (например, субъединицы, домены, мотивы или эпитоп) белка, выбранного из числа, например, ренина; гормона роста, включая человеческий гормон роста и бычий гормон роста; соматотропин-рилизинг-фактора; паратиреоидного гормона; тиреотропного гормона; липопротеинов; альфа-1-антитрипсина; A-цепи инсулина; B-цепи инсулина; проинсулина; фолликулостимулирующего гормона; кальцитонина; лютеинизирующего гормона; глюкагона; факторов свертывания крови, таких как фактор VII, фактор VIIIC, фактор IX, тканевой фактор (TF) и фактор фон Виллебранда; факторов, препятствующих свертыванию крови, таких как C-белок; предсердного натрийуретического фактора; легочного сурфактанта; активатора плазминогена, такого как урокиназа или мочи или тканевого типа активатор плазминогена человека (t-PA); бомбезина; тромбина; гемопоэтического фактора роста; фактора некроза опухоли альфа и бета; энкефалиназы; RANTES (regulated on activation normally T-cell expressed and secreted, хемокин, экспрессируемый и секретируемый T-клетками при активации); воспалительного белка макрофагов человека (MIP-1-альфа); сывороточного альбумина, такого как человеческий сывороточный альбумин; мюллеровой ингибирующей субстанции; A-цепи релаксина; B-цепи релаксина; прорелаксина; мышиного гонадотропин-ассоциированного белка; микробного белка, такого как бета-лактамаза; ДНКазы; IgE; цитотоксического T-лимфоцит-ассоциированного антигена (CTLA), такого как CTLA-4; ингибина; активина; белка A или D; ревматоидных факторов; нейротрофического фактора, такого как костный нейротрофический фактор (BDNF), нейротрофин-3,-4,-5 или -6 (NT-3, NT-4, NT-5 или NT-6), или фактора роста нервов; эпидермального фактора роста (EGF); белков, связывающих инсулиноподобный фактор роста; CD-белков, таких как CD2, CD3, CD4, CD 8, CD11a, CD14, CD18, CD19, CD20, CD22, CD23, CD25, CD33, CD34, CD40, CD40L, CD52, CD63, CD64, CD80 и CD147; эритропоэтина; остеоиндуктивных факторов; иммунотоксинов; супероксиддисмутазы; рецепторов T-клеток; поверхностных мембранных белков; фактора ускорения распада; вирусного антигена, такого как, например, часть оболочки вируса AIDS, например, gp120; транспортных белков; "хоминг"-рецепторов; адрессинов; регуляторных белков; молекул клеточной адгезии, таких как LFA-1, Mac 1, p150.95, VLA-4, ICAM-1, ICAM-3 и VCAM, интегрин a4/p7 и интегрин Xv/p3, в том числе весь или его субъединицы, альфа-субъединицы интегрина, такие как CD49a, CD49b, CD49c, CD49d, CD49e, CD49f, альфа7, альфа8, альфа9, альфаD, CD11a, CD11b, CD51, CD11c, CD41, альфаIIb, альфаIELb; бета-субъединицы интегрина, такие как CD29, CD 18, CD61, CD104, бета5, бета6, бета7 и бета8; комбинации субъединиц интегрина, включая без ограничения αVβ3, αVβ5 и α4β7; компонента пути апоптоза; IgE; антигенов группы крови; рецептора flk2/flt3; рецептора ожирения (OB); рецептора mpl; CTLA-4; C-белка; Eph-рецептора, такого как EphA2, EphA4, EphB2 и т.д.; человеческого лейкоцитарного антигена (HLA), такого как HLA-DR; белков комплемента, таких как рецептор комплемента CR1, C1Rq и другие факторы комплемента, такие как C3 и C5; гликопротеинового рецептора, такого как GpIbα, GPIIb/IIIa и CD200.
Рассматриваются также фрагменты, которые специфически связывают и/или содержат антигены рака, включая без ограничения ALK-рецептор (рецептор плеотрофина), плеотрофин, KS 1/4 панкарциномный антиген; антиген карциномы яичника (CA125); кислую фосфатазу предстательной железы; простатспецифический антиген (PSA); меланома-ассоциированный антиген p97; антиген меланомы gp75; высокомолекулярный антиген меланомы (HMW-MAA); простатспецифический мембранный антиген; карциноэмбриональный антиген (CEA); полиморфный эпителиальный муциновый антиген; антиген жировых глобул грудного молока; антигены, ассоциированные с колоректальными опухолями, такие как: CEA, TAG-72, CO17-1A, GICA 19-9, CTA-1 и LEA; антиген-38.13 лимфомы Беркитта; CD19; антиген-CD20 В-клеточной лимфомы человека; CD33; меланома-специфические антигены, такие как ганглиозид GD2, ганглиозид GD3, ганглиозид GM2 и ганглиозид GM3; опухолеспецифичный поверхностный антиген трансплантационного типа (TSTA); антигены вирусно-индуцированных опухолей, включая Т-антиген, опухолевые ДНК-вирусы и антигены оболочки опухолевых РНК-вирусов; онкофетальный антиген альфа-фетопротеин, такой как CEA кишечника, онкофетальный трофобластный гликопротеин 5T4 и онкофетальный антиген опухоли мочевого пузыря; антиген дифференцировки, такой как антиген карциномы легких человека L6 и L20; антигены фибросаркомы; T-клеточный антиген-Gp37 лейкоза человека; неогликопротеин; сфинголипиды; антигены рака молочной железы, такие как EGFR (рецептор эпидермального фактора роста); NY-BR-16, NY-BR-16, антиген HER2 (p185HER2) и HER3; полиморфный эпителиальный муцин (PEM); антиген-APO-1 злокачественных лимфоцитов человека; антиген дифференцировки, такой как антиген I, обнаруженный в фетальных эритроцитах; антиген I первичной эндодермы, обнаруженный в эритроцитах взрослых; предимплантационные эмбрионы; I(Ma), обнаруженный при аденокарциномах желудка; M18, M39, обнаруженный в эпителии молочной железы; SSEA-1, обнаруженный в миелоидных клетках; VEP8; VEP9; Myl; VIM-D5; D156-22, обнаруженный при колоректальном раке; TRA-1-85 (группа крови H); SCP-1, обнаруженный при раке яичка и яичника; C14, обнаруженный при аденокарциноме толстой кишки; F3, обнаруженный при аденокарциноме легкого; AH6, обнаруженный при раке желудка; гаптен Y; Ley, обнаруженный в клетках эмбриональной карциномы; TL5 (группа крови A); EGF-рецептор, обнаруженный в клетках A431; серию E1 (группа крови B), обнаруженную при раке поджелудочной железы; FC10.2, обнаруженный в клетках эмбриональной карциномы; антиген аденокарциномы желудка; CO-514 (группа крови Lea), обнаруженный при аденокарциноме; NS-10, обнаруженный при аденокарциномах; CO-43 (группа крови Leb); G49, обнаруженный в EGF-рецепторе клеток A431; MH2 (группа крови ALeb/Ley), обнаруженный при аденокарциноме толстой кишки; 19.9, обнаруженный при раке толстой кишки; муцины рака желудка; T5A7, обнаруженный в миелоидных клетках; R24, обнаруженный при меланоме; 4.2, GD3, D1.1, OFA-1, GM2, OFA-2, GD2 и M1:22:25:8, обнаруженный в клетках эмбриональной карциномы, и SSEA-3 и SSEA-4, обнаруженный в эмбрионах на 4-8-клеточной стадии; кожный антиген Т-клеточной лимфомы; антиген MART-1; антиген сиалил-Tn (STn); антиген рака толстой кишки NY-CO-45; вариант A антигена рака легкого NY-LU-12; антиген аденокарциномы ART1; ассоциированный с паранеопластическим синдромом антиген рака яичка-головного мозга (онконейрональный антиген MA2; паранеопластический нейрональный антиген); нейроонкологический вентральный антиген 2 (NOVA2); ген антигена 520 гепатоцеллюлярной карциномы; опухоль-ассоциированный антиген CO-029; опухоль-ассоциированные антигены MAGE-C1 (раково-тестикулярный антиген CT7), MAGE-B1 (антиген MAGE-XP), MAGE-B2 (DAM6), MAGE-2, MAGE-4a, MAGE-4b и MAGE-X2; раково-тестикулярный антиген (NY-EOS-1) и фрагменты любого из выше перечисленных полипептидов.
В одном из вариантов осуществления используемый полипептид является рекомбинантным. "Рекомбинантный" полипептид или белок относится к полипептиду или белку, полученному посредством технологии рекомбинантных ДНК. Полученные рекомбинантным путем полипептиды и белки, экспрессирующиеся в сконструированных клетках-хозяевах, считаются выделенными для цели настоящего раскрытия, также как и нативные или рекомбинантные полипептиды, разделенные, фракционированные или частично или в значительной степени очищенные с помощью любой подходящей методики. Раскрытые в данном документе полипептиды можно получить рекомбинантным путем с использованием известных в данной области техники способов. Альтернативно, раскрытые в данном документе белки и пептиды можно синтезировать химическим путем.
Молекулы полезной нагрузки
Выражение полезная нагрузка, используемое в данном документе, относится к молекуле или компоненту, который предназначен для "доставки" до места целевой области путем конъюгации с полипептидом. Как правило, полезная нагрузка обычно будет эффекторной молекулой, например, выбранной из группы, состоящей из токсина, например, цитотоксина, такого как химиотерапевтическое средство, лекарственное средство, пролекарство, фермент, иммуномодулятор, антиангиогенное средство, проапоптическое средство, цитокин, гормон, антитело или его фрагмент, синтетические или природные полимеры, нуклеиновые кислоты и их фрагменты, например, ДНК, РНК и их фрагменты (например, антисмысловая молекула или ген), радионуклиды, в частности, радиоактивный йодид, радиоизотопы, хелатированные металлы, наночастицы и репортерные группы, такие как флуоресцентные соединения или соединения, которые могут быть обнаружены с помощью ЯМР или ESR-спектроскопии.
В одном из вариантов осуществления полезную нагрузку выбирают из группы, включающей токсин, лекарственное средство, радионуклид, иммуномодулятор, цитокин, лимфокин, хемокин, фактор роста, фактор некроза опухоли, гормон, антагонист гормона, фермент, олигонуклеотид, ДНК, РНК, фермент, олигонуклеотид, ДНК, РНК, siRNA, RNAi, микроРНК, пептидо-нуклеиновую кислоту, фотоактивное терапевтическое средство, антиангиогенное средство, проапоптотическое средство, не встречающуюся в природе аминокислоту, пептид, липид, полимер, углевод, каркасную молекулу, флуоресцентную метку, пептид для визуализации, биотин, средство, продлевающее период полувыведения из сыворотки, метку захвата, хелатирующее средство, твердую подложку или их комбинацию.
В одном из вариантов осуществления полезная нагрузка представляет собой молекулу лекарственного средства (также называемую в данном документе лекарственным средством). Примеры молекул лекарственного средства для применения в настоящем раскрытии включают азотистый иприт, производное этиленамина, алкилсульфонаты, нитрозомочевину, гемцитабин, триазен, аналог фолиевой кислоты, антрациклин, таксан, ингибитор СОХ-2, аналог пиримидина, аналог пурина, антибиотик, ингибитор фермента, эпиподофиллотоксин, платиновый координационный комплекс, алкалоид барвинка, замещенную мочевину, производное метилгидразина, средство для адренокортикальной супрессии, антагонист гормона, эндостатин, таксол, камптотецин, доксорубицин, аналог доксорубицина, антиметаболит, алкилирующее средство, антимитотическое средство, антиангиогенное средство, ингибитор тирозинкиназы, ингибитор mTOR, ингибитор белка теплового шока (HSP90), ингибитор протеосомы, ингибитор HDAC, проапоптотическое средство, метотрексат, СРТ-11 или их комбинации, и в которых присутствует конъюгация.
В конкретных аспектах лекарственное средство представляет собой амифостин, цисплатин, дакарбазин, дактиномицин, мехлорэтамин, стрептозоцин, циклофосфамид, кармустин, ломустин, инкапсулированный в липосомы доксорубицин, гемцитабин, даунорубицин, инкапсулированный в липосомы даунорубицин, прокарбазин, митомицин, цитарабин, этопозид, метотрексат, 5-фторурацил, винбластин, винкристин, блеомицин, паклитаксел, доцетаксел, альдеслейкин, аспарагиназу, бусульфан, карбоплатин, кладрибин, 10-гидрокси-7-этилкамптотецин (SN38), гефитиниб, дакарбазин, флоксуридин, флударабин, гидроксимочевину, ифосфамид, идарубицин, месну, интерферон альфа, интерферон бета, иринотекан, митоксантрон, топотекан, лейпролид, мегестрол, мелфалан, меркаптопурин, пликамицин, митотан, пэгаспаргазу, пентостатин, пипоброман, пликамицин, стрептозоцин, тамоксифен, тенипозид, тестолактон, тиогуанин, тиотепу, урациловый иприт, винорелбин, хлорамбуцил, ингибиторы ароматазы и их комбинации.
В одном из вариантов осуществления лекарственное средство выбрано из группы, включающей алкилфосфохолины, ингибиторы топоизомеразы I, таксоиды и сурамин.
В одном из вариантов осуществления токсин включает в себя цитотоксины или цитотоксические средства, в том числе любые средства, которые наносят ущерб (например убивают) клеткам. Примеры включают аплидин, анастрозол, азацитидин, бортезомиб, бриостатин-1, бусульфан, комбрестатины, кармустин, доластатины, эпотилоны, стауроспорин, майтанзиноиды, спонгистатины, ризоксин, галихондрины, роридины, гемиастерлины, таксол, цитохалазин В, грамицидин D, этидия бромид, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин и их аналоги или гомологи.
В одном из вариантов осуществления лекарственное средство (также цитотоксин в данном случае) содержит антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацил декарбазин), алкилирующие средства (например, мехлорэтамин, тиоэпахлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромоманнитол, стрептозотоцин, митомицин C и цис-дихлородиамин платины (II) (DDP) цисплатин), карбоплатин, антрациклины (например, даунорубицин (ранее дауномицин) и доксорубицин или доксорубицина глюкуронид), антибиотики (например, дактиномицин (ранее актиномицин), блеомицин, митрамицин, антрамицин (АМС), калихеамицин или дуокармицины) и антимитотические средства (например, винкристин и винбластин).
В некоторых аспектах лекарственное средство представляет собой ауристатин (патенты США №№ 5635483; 5780588), например, MMAE (монометилауристатин E) или MMAF (монометилауристатин F). В других аспектах лекарственное средство представляет собой доластатин или пептидный аналог или производное доластатина. Было показано, что доластатины и ауристатины нарушают динамику микротрубочек, гидролиз GTP и деление ядер и клеток (Woyke et al., Antimicrob. Agents and Chemother. 45:3580-3584 (2001)), а также обладают противораковой активностью (патент США № 5663149). Лекарственный фрагмент доластатина или ауристатина может быть присоединен к соединению-конъюгату через N (амино)-конец или С (карбокси)-конец пептидного лекарственного фрагмента. См., например, международную публикацию № WO2002/088172, которая включена в данный документ посредством ссылки во всей своей полноте.
В других аспектах лекарственное средство представляет собой майтанзиноид. В некоторых аспектах майтанзиноид представляет собой N-2'-деацетил-N-2'-(3-меркапто-1-оксопролил)-майтанзин (DM1), N-2'-деацетил-N2'-(4-меркапто-1-оксопентил)-майтанзин (DM3) или N-2'-деацетил-N-2'(4-метил-4-меркапто-1-оксопентил)-майтанзин (DM4). Майтанзиноиды являются митотическими ингибиторами, действие которых заключается в ингибировании полимеризации тубулина. Майтанзин впервые был выделен из восточноафриканского кустарника Maytenus serrata (патент США № 3896111). Позднее было обнаружено, что определенные микроорганизмы также продуцируют майтанзиноиды, такие как майтанзинол и C-3 сложные эфиры майтанзинола (патент США № 4151042). Синтетический майтанзинол и его производные и аналоги раскрыты, например, в патентах США №№ 4137230; 4248870; 4256746; 4260608; 4265814; 4294757; 4307016; 4308268; 4308269; 4309428; 4313946; 4315929; 4317821; 4322348; 4331598; 4361650; 4364866; 4424219; 4450254; 4362663 и 4371533, которые включены в данный документ посредством ссылки во всей своей полноте.
Фрагменты лекарственного средства в виде майтанзиноида являются перспективными фрагментами лекарственного средства для конъюгатов антитело-лекарственное средство в связи с тем, что они: (i) относительно доступны для получения с помощью ферментации или химической модификации, дериватизации продуктов ферментации, (ii) поддаются дериватизации с помощью функциональных групп, подходящих для конъюгации посредством не содержащих дисульфидные связи линкеров с антителами, (iii) стабильны в плазме и (iv) эффективны в отношении широкого разнообразия линий опухолевых клеток. Конъюгаты, содержащие майтанзиноиды, способы получения таковых и их терапевтическое применение раскрыты, например, в патентах США №№ 5208020, 5416064 и Европейском патенте EP0425235B1; Liu et al., Proc. Natl. Acad. Sci. USA 93:8618-8623 (1996) (описаны иммуноконъюгаты, содержащие майтанзиноид, обозначенный DM1) и Chari et al., Cancer Research 52:127-131 (1992), которые включены в данный документ посредством ссылки во всей своей полноте.
Майтанзиноиды хорошо известны из уровня техники, и их можно синтезировать с помощью известных методик или выделить из природных источников. Подходящие майтанзиноиды раскрыты, например, в патенте США № 5 208 020. Иллюстративные фрагменты лекарственного средства в виде майтанзиноида включают таковые с модифицированным ароматическим кольцом, например, C-19-дехлор (патент США США № 4256746) (полученный посредством восстановления ансамитоцина P2 с помощью алюмогидрида лития); C-20-гидрокси (или C-20-деметил)+/-C-19-дехлор (патенты США №№ 4361650 и 4307016) (полученные посредством деметилирования с использованием Streptomyces или Actinomyces или дехлорирования с использованием LAH) и C-20-деметокси, C-20-ацилокси (-OCOR), +/-дехлор (патент США № 4294757) (полученный посредством ацилирования с использованием хлорангидридов), а также таковые с модификациями в других положениях. Иллюстративные фрагменты лекарственного средства в виде майтанзиноида также включают таковые с такими модификациями, как C-9-SH, полученная с помощью реакции майтанзинола с H2S или P2S5 (патент США № 4424219); C-14-алкоксиметил(деметокси/CH2OR) (патент США № 4331598); C-14-гидроксиметил или ацилоксиметил (CH2OH или CH2OAc), полученный из Nocardia (патент США № 4450254); C-15-гидрокси/ацилокси, полученный посредством превращения майтанзинола с помощью Streptomyces (патент США № 4364866); C-15-метокси, выделенный из Trewia nudiflora (патент США №№ 4313946 и 4315929); C-18-N-деметил, полученный посредством деметилирования майтанзинола с помощью Streptomyces (патент США №№ 4 362 663 и 4 322 348) и 4,5-деокси, полученного восстановлением майтанзинола с помощью трихлорида титана/LAH (патент США № 4371533). Известно много положений соединений майтанзина, пригодных в качестве положения для связывания, в зависимости от типа связи. Например, для образования сложноэфирной связи подходящими являются все из положения C-3 с гидроксильной группой, положения C-14, модифицированного гидроксиметилом, положения C-15, модифицированного гидроксильного группой, и положения C-20 с гидроксильной группой.
В некоторых аспектах лекарственное средство представляет собой калихеамицин. Антибиотики калихеамицинового семейства способны образовывать двунитевые разрывы ДНК в субпикомолярных концентрациях. Касательно получения конъюгатов на основе калихеамицинового семейства, см., например, патенты США №№ 5712374, 5714586, 5739116, 5767285, 5770701, 5770710, 5773001, 5877296, все из которых включены в данный документ посредством ссылки во всей своей полноте. Структурные аналоги калихеамицина, которые можно применять, включают без ограничения γ1I, α2I, α3I, N-ацетил-γ1I, PSAG и θ11 (Hinman et al., Cancer Research 53:3336-3342 (1993), Lode et al., Cancer Research 58:2925-2928 (1998) и вышеупомянутые патенты США, закрепленные за American Cyanamid).
В некоторых аспектах лекарственное средство представляет собой тубулизин. Тубулизины являются представителями класса природных веществ, выделенных из видов миксобактерий (Sasse et al., J. Antibiot. 53:879-885 (2000)). Как средства, взаимодействующие с цитоскелетом, тубулизины являются митотическими ядами, которые ингибируют полимеризацию тубулина и приводят к блокированию клеточного цикла и апоптозу (Steinmetz et al., Chem. Int. Ed. 43:4888-4892 (2004); Khalil et al., ChemBioChem. 7:678-683 (2006); Kaur et al., Biochem. J. 396: 235-242 (2006)). Тубулизины являются весьма эффективными цитотоксическими молекулами, превышая в отношении ингибирования роста клеток любые подходящие с клинической точки зрения традиционные химиотерапевтические средства, например, эпотилоны, паклитаксел и винбластин. Кроме того, они эффективны в отношении линий клеток с устойчивостью ко многим лекарственным средствам (Domling et al., Mol. Diversity 9:141-147 (2005)). Такие соединения продемонстрировали высокую цитотоксичность при исследовании в отношении панели раковых линий клеток со значениями IC50 в узком пикомолярном диапазоне; таким образом, они представляют интерес в качестве противораковых терапевтических средств. См., например международную публикацию № WO/2012019123, которая включена в данный документ посредством ссылки во всей своей полноте. Конъюгаты с тубулизином раскрыты, например, в патенте США № 7 776 814.
В некоторых аспектах лекарственное средство представляет собой пирролобензодиазепин (PBD). PBD представляют собой относительно малые молекулы, при этом некоторые из них обладают способностью распознавать и ковалентно связываться со специфичными последовательностями в малой бороздке ДНК и, следовательно, характеризуются антибиотической/противоопухолевой активностью. Ряд PBD и их производных известны из уровня техники, например, димеры PBD (например, SJG-136 или SG2000), C2-ненасыщенные димеры PBD, пирролобензодиазепиновые димеры с арильными заменами в C2 (например, SG2285), пролекарство на основе димеров PBD, активируемое гидролизом (например, SG2285), и полипиррол-PBD (например, SG2274). PBD дополнительно описаны в международных публикациях №№ WO2000/012507, WO2007/039752, WO2005/110423, WO2005/085251 и WO2005/040170, и в патенте США № 7612062, каждый из которых включен в данный документ посредством ссылки во всей своей полноте.
В некоторых аспектах токсин включает, например, абрин, бруцин, цикутоксин, дифтерийный токсин, ботулотоксин, шига-токсин, эндотоксин, тетанотоксин, коклюшный токсин, сибиреязвенный токсин, холерный токсин, фалкаринол, альфа-токсин, гелданамицин, гелонин, лотавстралин, рицин, стрихнин, тетродотоксин, сапонин, рибонуклеазу (РНКазу), ДНКазу I, стафилококковый энтеротоксин-A, противовирусный белок лаконоса, экзотоксин синегнойной палочки, эндотоксин синегнойной палочки или их комбинацию. В других аспектах токсин включает, например, цепь А модессина, альфа-сарцин, белки Aleurites fordii (тунгового дерева), диантиновые белки, белки Phytolaca americana (лаконоса американского) (PAPI, PAPII и PAP-S), ингибитор Momordica charantia, курцин, кротин, ингибитор Saponaria officinalis (мыльнянки лекарственной), митогеллин, рестриктоцин, феномицин, неомицин, трихотецины или их комбинацию. См., например, международную публикацию № WO1993/021232.
В некоторых аспектах хелатирующее средство представляет собой DTPA, EC, DMSA, EDTA, Cy-EDTA, EDTMP, DTPA, CyDTPA, Cy2DTPA, BOPTA, DTPA-MA, DTPA-BA, DTPMP, DOTA, TRITA, TETA, DOTMA, DOTA-MA, HP-DO3A, pNB-DOTA, DOTP, DOTMP, DOTEP, DOTPP, DOTBzP, DOTPME, HEDP, DTTP, триамидотиол N3S, DADS, MAMA, DADT, диаминотетратиол N2S4, дитиол-бисфосфин N2P2, 6-гидразиноникотиновую кислоту, пропиленаминооксим, тетраамин, циклам или их комбинацию.
В одном из вариантов осуществления лекарственное средство представляет собой ауристатин, тубулизин или пирролобензодиазепин (PBD).
В одном из вариантов осуществления ауристатин представляет собой MMAE (монометилауристатин E) или MMAF (монометилауристатин F).
В одном из вариантов осуществления лекарственное средство представляет собой майтанзиноид, например, N 2'-деацетил-N 2'-(3-меркапто-1-оксопропил)-майтанзин (DM1), N 2'-деацетил-N2'-(4-меркапто-1-оксопентил)-майтанзин (DM3) или N 2'-деацетил-N 2'(4-метил-4-меркапто-1-оксопентил)-майтанзин (DM4).
Примеры радионуклидов включают 3H, 11C, 13N, 15O, 18F, 32P, 33P, 35S, 47Sc, 51Cr, 54Mn, 57Co, 58Co, 59Fe, 62Cu, 65Zn, 67Cu, 67Ga, 68Ge, 75Br, 75Se, 76Br, 77Br, 77As, 80mBr, 85Sr, 89Sr, 90Y, 95Ru, 97Ru, 99Mo и 99mTc, 103Pd, 103m Rh, 103 Ru, 105Rh, 105Ru, 107Hg, 109Pd, 109Pt, 111Ag, 111In, 112In, 113mIn, 113Sn, 115In, 117Sn, 119Sb, 121mTe, 121I, 122mTe, 125mTe, 125I, 126I, 131I, 133I, 133Xe, 140La, 142Pr, 143Pr, 149Pm, 152Dy, 153Sm, 153Gd, 159Gd, 161Ho, 161Tb, 165Tm, 166Dy, 166Ho, 167Tm, 168Tm, 169Er, 169Yb, 175Yb, 177Lu, 186Re, 188Re, 188W, 189mOs, 189Re, 192Ir, 194Ir, 197Pt, 198Au, 199Au, 201T1, 203Hg, 211At, 211Bi, 211Pb, 212Pb, 212Bi, 213Bi, 215Po, 217At, 219Rn, 221Fr, 223Ra, 224Ac, 225Ac, 225Fm, 252Cf и их комбинацию.
В одном из вариантов осуществления радионуклид выбран из группы, включающей или состоящей из хрома (51Cr), кобальта (57Co), фтора (18F), гадолиния (153Gd, 159Gd), германия (68Ge), гольмия (166Ho), индия (115In, 113In, 112In, 111In), йода (131I, 125I, 123I, 121I), лантана (140La), лютеция (177Lu), марганца (54Mn), молибдена (99Mo), палладия (103Pd), фосфора (32P), празеодима (142Pr), прометия (149Pm), рения (186Re, 188Re), родия (105Rh), рутения (97Ru), самария (153Sm), скандия (47Sc), селена (75Se), стронция (85Sr), серы (35S), технеция (99Tc), таллия (201Tl), олова (113Sn, 117Sn), трития (3H), ксенона (133Xe), иттербия (169Yb, 175Yb), иттрия (90Y), цинка (65Zn) или их комбинации.
В одном из вариантов осуществления радионуклид присоединен к соединению-конъюгату по настоящему раскрытию с помощью хелатирующего средства.
В одном из вариантов осуществления R1 представляет собой средство, продлевающее период полувыведения из сыворотки, например, содержащее альбумин, альбумин-связывающий полипептид, PAS, β-субъединицу C-концевого пептида (CTP) человеческого хорионического гонадотропина, полиэтиленгликоль (PEG), гидроксиэтилкрахмал (HES), XTEN, альбумин-связывающие малые молекулы и их комбинацию.
Там, где эффекторная молекула представляет собой полимер, он может, в целом, являться синтетическим или природным полимером, например, полимером с необязательно замененной прямой или разветвленной цепью полиалкилена, полиалкенилена или полиоксиалкилена, или разветвленным или неразветвленным полисахаридом, например гомо- или гетерополисахаридом.
Конкретные необязательные заместители, которые могут присутствовать в указанных выше синтетических полимерах, включают одну или несколько гидрокси-, метил- или метокси-групп.
Конкретные природные полимеры включают лактозу, гиалуроновую кислоту, гепарансульфат, хондроитинсульфат, альгинат, целлюлозу, амилозу, декстран, гликоген или их производные.
В некоторых вариантах осуществления полимер представляет собой полиэтиленгликоль (PEG), разветвленный PEG, полисиаловую кислоту (PSA), гидроксиалкилкрахмал (HAS), гидроксилэтилкрахмал (HES), углевод, полисахариды, пуллуланы, хитозан, гиалуроновую кислоту, хондроитинсульфат, дерматансульфат, крахмал, декстран, карбоксиметилдекстран, полиалкиленоксид (PAO), полиалкиленгликоль (PAG), полипропиленгликоль (PPG) полиоксазолин, полиакрилоилморфолин, поливиниловый спирт (PVA), поликарбоксилат, поливинилпирролидон, полифосфазин, полиоксазолин, сополимер полиэтилена и ангидрида малеиновой кислоты, сополимер полистирола и ангидрида малеиновой кислоты, поли(1-гидроксиметилэтилен гидроксиметилформаль) (PHF), 2-метакрилоилокси-2'-этилтриметиламмония фосфат (MPC). В некоторых вариантах осуществления полимер представляет собой полиэтиленгликоль. В одном из вариантов осуществления настоящего изобретения полиэтиленгликоль имеет молекулярную массу в диапазоне от 300 Да до 10000000 Да, от 500 Да до 100000 Да, от 1000 Да до 50000 Да, 1500 Да до 30000 Да, от 2000 Да до 20000 Да, от 3000 Да до 5000 Да и от 4000 Да до 5000 Да. В других вариантах осуществления полиэтиленгликоль имеет молекулярную массу приблизительно 1000 Да, приблизительно 1500 Да, приблизительно 2000 Да, приблизительно 3000 Да, приблизительно 4000 Да, приблизительно 5000 Да, приблизительно 10000 Да или приблизительно 20000 Да.
В одном из вариантов осуществления R1 или полипептид (в частности, R1) содержит метку для визуализации. Метки для визуализации включают без ограничения хромофор, флуорофор, флуоресцентный белок, фосфоресцентный краситель, тандемный краситель, частицу, гаптен, фермент, радиоактивный изотоп или их комбинацию.
В одном из вариантов осуществления метка для визуализации представляет собой пептид для визуализации. В некоторых аспектах пептид для визуализации обеспечивает визуализацию или определение расположения соединения-конъюгата in vitro, in vivo, ex vivo или при любой их комбинации. В некоторых аспектах пептид для визуализации представляет собой, например, биотин-акцепторный пептид, акцепторный пептид с липоевой кислотой, флуоресцентный белок, цистеин-содержащий пептид для лигирования мышьяксодержащего красителя или для конъюгации метастабильного технеция, пептид для конъюгации клатратов с европием для анализов с определением расстояния на основе резонансного переноса энергии флуоресценции (FRET) или любую их комбинацию. В некоторых аспектах флуоресцентный белок представляет собой, например, зеленый флуоресцентный белок (GFP), красный флуоресцентный белок (RFP), желтый флуоресцентный белок (YFP), усиленный зеленый флуоресцентный белок (EGFP), усиленный желтый флуоресцентный белок (EYFP) или любую их комбинацию. В некоторых аспектах флуоресцентный белок представляет собой фикобилипротеин или его производное.
Флуоресцентные белки, в особенности фикобилипротеин, пригодны для получения метящих реактивов на основе тандемных красителей. Эти тандемные красители содержат флуоресцентный белок и флуорофор с целью получения большего стоксового сдвига, где спектр испускания дальше смещен от длины волны спектра поглощения флуоресцентного белка. Это может быть эффективным для выявления небольшого количества мишени в образце, где испускаемый флуоресцентный свет максимально оптимизирован, другими словами, испускаемый свет повторно поглощается флуоресцентным белком в незначительном количестве или совсем не поглощается. С этой целью флуоресцентный белок и флуорофор функционируют в качестве пары для переноса энергии, при этом флуоресцентный белок испускает при длине волны, при которой флуорофор поглощает, а затем флуорофор испускает при длине волны, смещенной относительно флуоресцентных белков дальше, чем можно было бы получить с помощью только флуоресцентного белка. Функциональная комбинация может представлять собой фикобилипротеины и сульфородаминовые флуорофоры или сульфированные цианиновые флуорофоры, известные из уровня техники. Флуорофор в некоторых случаях функционирует в качестве донора энергии, при этом акцептором энергии является флуоресцентный белок.
В других аспектах мышьяксодержащий краситель представляет собой 4ʹ,5ʹ-бис(1,3,2-дитиоарсолан-2-ил)флуоресцеин (FlAsH). В некоторых аспектах биотин-акцепторный пептид способствует конъюгированию реактивов на основе авидина и стрептавидина. В некоторых аспектах акцепторный пептид с липоевой кислотой способствует конъюгированию зондов с реакционноспособной тиоловой группой со связанной липоевой кислотой или непосредственному лигированию флуоресцентных аналогов липоевой кислоты.
В одном из вариантов осуществления R1 или полипептид (в частности, R1) содержит флуоресцентную метку. В некоторых аспектах флуоресцентная метка включает, например, краситель флуоресцеинового типа, краситель родаминового типа, краситель данзилового типа, краситель лиссаминового типа, краситель цианинового типа, краситель фикоэритринового типа, краситель типа техасский красный или любую их комбинацию. Флуорофоры, подходящие для конъюгации с раскрытыми в данном документе сконструированными с цистеином антителами или их антигенсвязывающими фрагментами, включают без ограничения пирен (в том числе любое из соответствующих производных соединений), антрацен, нафталин, акридин, стильбен, индол или бензиндол, оксазол или бензоксазол, тиазол или бензотиазол, 4-амино-7-нитробенз-2-окса-1,3-диазол (NBD), цианин (в том числе любые соответствующие соединения), карбоцианин (в том числе любые соответствующие соединения), карбостирил, порфирин, салицилат, антранилат, азулен, перилен, пиридин, хинолин, бораполиазаиндацен (в том числе любые соответствующие соединения), ксантен (в том числе любые соответствующие соединения), оксазин (в том числе любые соответствующие соединения) или бензоксазин, карбазин (в том числе любые соответствующие соединения), феналенон, кумарин (в том числе любые раскрытые соответствующие соединения), бензофуран (в том числе любые соответствующие соединения) и бензфеналенон (в том числе любые соответствующие соединения) и их производные. В контексте данного документа оксазины включают резоруфины (в том числе любые соответствующие соединения), аминооксазиноны, диаминооксазины и их бензозамещенные аналоги или любую их комбинацию.
В определенных аспектах флуорофоры включают, например, ксантен (родол, родамин, флуоресцеин и их производные), кумарин, цианин, пирен, оксазин, бораполиазаиндацен или любую их комбинацию. В некоторых вариантах осуществления такие флуорофоры представляют собой, например, сульфированные ксантены, фторированные ксантены, сульфированные кумарины, фторированные кумарины, сульфированные цианины или любую их комбинацию. Также включены красители, реализуемые под торговыми марками, и, как правило, известные как ALEXA FLUOR®, DYLIGHT®, CY DYES®, BODIPY®, OREGON GREEN®, PACIFIC BLUE®, IRDYES®, FAM®, FITC® и ROX®.
Выбор флуорофора, присоединяемого через линкер "Z", как раскрыто в данном документе, будет определять свойства поглощения и испускания флуоресценции конечного соединения. Физические свойства флуорофорной метки, которую можно применять, включают без ограничения спектральные характеристики (поглощение, испускание и стоксов сдвиг), интенсивность, длительность, поляризацию флуоресценции и скорость обесцвечивания или их комбинацию. Все эти физические свойства можно применять для того, чтобы отличить один флуорофор от другого, и, таким образом, способствовать мультиплексному анализу. В определенных аспектах флуорофор имеет максимум поглощения при длинах волн более 480 нм. В некоторых аспектах флуорофор поглощает при 488-514 нм или вблизи этих значений (что особенно подходит для возбуждения излучением аргонового ионного лазерного источника возбуждения) или вблизи 546 нм (что особенно подходит для возбуждения ртутной дуговой лампой). В некоторых аспектах флуорофор может испускать в NIR (ближней инфракрасной области) для применения в тканях или во всем организме. Другие необходимые свойства флуоресцентной метки могут включать клеточную проницаемость и низкую токсичность, например, если мечение антитела необходимо проводить в клетке или организме (например, живом животном).
В одном из вариантов осуществления R1 или полипептид (в частности, R1) содержит метку захвата. В некоторых аспектах метка захвата представляет собой биотин или His6-метку. Биотин является подходящим, поскольку он может функционировать в ферментной системе для дополнительного усиления выявляемого сигнала, и он также может функционировать в качестве метки для применения в аффинной хроматографии в целях выделения. В целях выявления можно применять конъюгат фермента, который характеризуется аффинностью к биотину, такой как авидин-HRP.
Затем можно добавить субстрат пероксидазы для получения выявляемого сигнала. Помимо биотина можно применять и другие гаптены, в том числе гормоны, встречающиеся в природе и синтетические лекарственные средства, загрязнители, аллергены, эффекторные молекулы, факторы роста, хемокины, цитокины, лимфокины, аминокислоты, пептиды, промежуточные химические соединения, нуклеотиды и т. п.
В одном из вариантов осуществления R1 содержит фермент. Ферменты являются эффективными метками, поскольку можно получить усиление выявляемого сигнала, приводящее к повышению чувствительности анализов. Зачастую сам фермент не вызывает выявляемого ответа, а действует путем разрушения субстрата при контакте с подходящим субстратом, так что превращаемый субстрат испускает флуоресцентный, колориметрический или люминесцентный сигнал. Ферменты усиливают выявляемый сигнал, поскольку один фермент в метящем реактиве может приводить к превращению нескольких субстратов в выявляемый сигнал. Субстрат для фермента выбирают так, чтобы получить измеримый продукт, например колориметрический, флуоресцентный или хемилюминесцентный. Такие субстраты широко применяются в данной области техники и известны из уровня техники.
В некоторых вариантах осуществления в комбинации колориметрического или флуорогенного субстрата и фермента применяются оксидоредуктазы, такие как пероксидаза хрена, и субстрат, такой как 3,3'-диаминобензидин (DAB) и 3-амино-9-этилкарбазол (AEC), которые дают отличительный цвет (коричневый и красный, соответственно). Другие колориметрические субстраты оксидоредуктаз, которые дают выявляемые продукты, включают, без ограничения: 2,2-азино-бис(3-этилбензотиазолин-6-сульфоновую кислоту (ABTS), o-фенилендиамин (OPD), 3,3',5,5'-тетраметилбензидин (TMB), o-дианизидин, 5-аминосалициловую кислоту, 4-хлор-1-нафтол. Флуорогенные субстраты включают без ограничения гомованилиновую кислоту или 4-гидрокси-3-метоксифенилуксусную кислоту, восстановленные феноксазины и восстановленные бензотиазины, в том числе реактив Amplex® Red и его варианты, и восстановленные дигидроксантены, в том числе дигидрофлуоресцеины, и дигидрородамины, в том числе дигидрородамин 123.
Настоящее раскрытие распространяется на использование субстратов пероксидазы, которыми являются тирамиды, представляющие уникальный класс субстратов пероксидазы, поскольку по своей природе они могут быть выявлены до действия фермента, но под действием пероксидазы "фиксируются на месте" в процессе, описанном как тирамидное усиление сигнала (TSA). Эти субстраты широко используются для мечения мишеней в образцах, которыми являются клетки, ткани или монослои, для их последующего выявления с помощью микроскопии, проточной цитометрии, оптического сканирования и флуорометрии.
Настоящее раскрытие распространяется на комбинацию колориметрического (и в некоторых случаях флуорогенного) субстрата и фермента, где применяется фермент фосфатаза, такой как кислая фосфатаза, щелочная фосфатаза или рекомбинантный вариант такой фосфатазы, в комбинации с колориметрическим субстратом, таким как 5-бром-6-хлор-3-индолилфосфат (BCIP), 6-хлор-3-индолилфосфат, 5-бром-6-хлор-3-индолилфосфат, п-нитрофенилфосфат или o-нитрофенилфосфат, или с флуорогенным субстратом, таким как 4-метилумбеллиферилфосфат, 6,8-дифтор-7-гидрокси-4-метилкумаринилфосфат (DiFMUP, патент США № 5830912), флуоресцеиндифосфат, 3-O-метилфлуоресцеинфосфат, резоруфинфосфат, 9H-(1,3-дихлор-9,9-диметилакридин-2-он-7-ил) фосфат (DDAO фосфат) или ELF 97, ELF 39 или родственные фосфаты.
Настоящее раскрытие также распространяется на R1, который включает гликозидазу, в частности, бета-галактозидаза, бета-глюкуронидаза и бета глюкозидаза представляют собой дополнительные подходящие ферменты. Подходящие колориметрические субстраты включают без ограничения 5-бром-4-хлор-3-индолил-бета-D-галактопиранозид (X-gal) и подобные индолилгалактозиды, глюкозиды и глюкурониды, o-нитрофенил-бета-D-галактопиранозид (ONPG) и п-нитрофенил-бета-D-галактопиранозид. В некоторых вариантах осуществления флуорогенные субстраты включают резоруфин-бета-D-галактопиранозид, флуоресцеиндигалактозид (FDG), флуоресцеиндиглюкуронид и их структурные варианты, 4-метилумбеллиферил-бета-D-галактопиранозид, карбоксиумбеллиферил-бета-D-галактопиранозид и фторированные кумарин-бета-D-галактопиранозиды. Дополнительные ферменты включают, без ограничения, гидролазы, такие как холинэстеразы и пептидазы, оксидазы, такие как глюкозооксидаза и цитохромоксидазы, и редуктазы, для которых известны подходящие субстраты.
Ферменты и их соответствующие субстраты, которые дают хемилюминесценцию, пригодны для включения в молекулы настоящего изобретения. Они включают, без ограничения, природные и рекомбинантные формы люцифераз и экворинов. Дополнительно продуктивными являются дающие хемилюминесценцию субстраты фосфатаз, гликозидаз и оксидаз, как, например, содержащие стабильные диоксетаны, люминол, изолюминол и сложные эфиры акридиния.
где такой гетерологичный фрагмент представляет собой нуклеиновую кислоту. Нуклеиновая кислота может быть выбрана из группы, состоящей из ДНК, РНК, короткой интерферирующей РНК (siRNA), микроРНК, шпильки или миметиков нуклеиновых кислот, таких как пептидо-нуклеиновые кислоты. В определенных аспектах конъюгированная нуклеиновая кислота состоит из по меньшей мере 10 пар оснований, по меньшей мере 20 пар оснований, по меньшей мере 30 пар оснований, по меньшей мере 40 пар оснований, по меньшей мере 50 пар оснований, по меньшей мере 60 пар оснований, по меньшей мере 100 пар оснований, по меньшей мере 200 пар оснований, по меньшей мере 500 пар оснований, по меньшей мере 1000 пар оснований, по меньшей мере 5000 или более пар оснований. Конъюгированная нуклеиновая кислота может быть однонитевой. В различных аспектах конъюгированная нуклеиновая кислота может быть двунитевой. В некоторых аспектах конъюгированная нуклеиновая кислота кодирует открытую рамку считывания. В некоторых аспектах открытая рамка считывания, кодируемая конъюгированной нуклеиновой кислотой, соответствует индуцирующему апоптоз белку, вирусному белку, ферменту или подавляющему рост опухоли белку. Методики доставки таких нуклеиновых кислот известны из уровня техники.
Другие определения
Прежде чем описывать предусмотренные варианты осуществления более подробно, следует понимать, что настоящее раскрытие не ограничивается конкретными композициями или стадиями способа, и в связи с этим они могут изменяться. Используемые в настоящем описании и прилагаемой формуле изобретения формы единственного числа включают определяемые объекты и во множественном числе, если из контекста явно не следует иное. Выражения "один или несколько" и "по меньшей мере один" можно использовать в данном документе взаимозаменяемо.
Кроме того, выражение "и/или", если оно используется в данном документе, следует рассматривать как конкретное раскрытие каждого из двух указанных признаков или компонентов с другим или без другого. Таким образом, подразумевается, что выражение "и/или", используемое в данном документе в такой фразе, как "А и/или В", включает "А и В", "А или В", "А" (отдельно) и "В" (отдельно). Аналогично, выражение "и/или", используемое в такой фразе, как "А, В и/или С", должно охватывать каждый из следующих аспектов: A, B и C; A, B или C; A или C; A или B; B или C; A или C; A или B; B или C; A (отдельно); B (отдельно) и C (отдельно).
Если не определено иное, все используемые в настоящем документе технические и научные термины имеют то же значение, которое обычно понимает специалист обычной квалификации в данной области техники, к которой относится данное раскрытие. Например, Concise Dictionary of Biomedicine and Molecular Biology, Juo, Pei-Show, 2nd ed., 2002, CRC Press; The Dictionary of Cell and Molecular Biology, 3rd ed., 1999, Academic Press; а также Oxford Dictionary Of Biochemistry And Molecular Biology, Revised, 2000, Oxford University Press предоставляют специалисту общий словарь многих терминов, используемых в настоящем раскрытии.
Единицы измерения, префиксы и символы обозначены в их форме, принятой согласно Международной системе единиц (SI). Числовые диапазоны включают числа, определяющие диапазон. Если не указано иное, то аминокислотные последовательности записаны слева направо в направлении от амино- к карбокси-концу. Приведенные в данном документе заголовки не ограничивают различные аспекты, которые могут обеспечиваться ссылкой на описание в целом. Соответственно термины, приведенные непосредственно ниже, более полно определены посредством ссылки на описание во всей его полноте.
В данном документе аминокислоты обозначены либо с помощью их общеизвестных трехбуквенных символов, либо с помощью однобуквенных символов, рекомендованных Комиссией по биохимической номенклатуре IUPAC-IUB. Аналогично, нуклеотиды обозначены с помощью их общепринятых однобуквенных кодов.
Выражение "субъект" относится к любому животному (например, млекопитающему), в том числе без ограничения к людям, отличным от человека приматам, грызунам и т. п., которое будет реципиентом конкретного лечения. Как правило, выражения "субъект" и "пациент" можно использовать взаимозаменяемо в отношении субъекта-человека.
Выражение "фармацевтическая композиция" относится к препарату, который пребывает в такой форме, которая обеспечивает биологическую активность активного компонента (например, раскрытого в данном документе соединения-конъюгата), и который не содержит дополнительных компонентов, которые неприемлемо токсичны для субъекта, которому будут вводить композицию. Такая композиция может содержать один или несколько фармацевтически приемлемых наполнителей. Такая композиция может быть стерильной.
"Эффективное количество" раскрытого в данном документе соединения-конъюгата представляет собой количество, достаточное для осуществления конкретно установленной цели. "Эффективное количество" в отношении поставленной цели можно определить опытным путем и стандартным способом.
Выражение "терапевтически эффективное количество" относится к количеству раскрытого в данном документе соединения-конъюгата или другого лекарственного средства, эффективного для "лечения" заболевания или нарушения у субъекта или млекопитающего.
Слово "метка" при использовании в данном документе относится к выявляемому соединению или композиции, которая конъюгирована прямо или косвенно со сконструированным антителом или его фрагментом, раскрытым в данном документе (например, сконструированное с цистеином антитело или его фрагмент), с тем, чтобы генерировать "меченое" соединение-конъюгат. Метка может быть выявляемой сама по себе (например, радиоизотопные метки или флуоресцентные метки) или, в случае ферментной метки, может катализировать химическое превращение субстратного соединения или композиции, которое является выявляемым.
Такие выражения как "осуществление лечения", или "лечение", или"лечить" относится как к (1) терапевтическим мерам, с помощью которых излечивают, замедляют, ослабляют симптомы диагностированного патологического состояния или расстройства и/или останавливают его прогрессирование, так и к (2) профилактическим или предупреждающим мерам, с помощью которых предупреждают и/или замедляют развитие патологического состояния или нарушения, на которое осуществляют нацеливание. Таким образом, к нуждающимся в лечении относят тех, у кого уже есть нарушение; тех, кто предрасположен к развитию нарушения и тех, у кого нужно предупредить развитие нарушения. В некоторых аспектах субъекта успешно "лечат" от заболевания или состояния, например, рака, в соответствии со способами по настоящему раскрытию, если пациент характеризуется, например, общей, частичной или временной ремиссией заболевания или состояния, например, определенного типа рака.
Термины "полинуклеотид" и "нуклеинова кислота" используются в данном документе взаимозаменяемо и относятся к полимерам нуклеотидов любой длины, в том числе к ДНК и РНК. Нуклеотиды могут представлять собой дезоксирибонуклеотиды, рибонуклеотиды, модифицированные нуклеотиды или основания, и/или их аналоги, или любой субстрат, который можно встроить в полимер с помощью ДНК- или РНК-полимеразы. Полинуклеотид может содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды и их аналоги.
Используемое в данном документе выражение "вектор" относится к конструкции, которая способна доставлять, а в некоторых аспектах экспрессировать, один или несколько представляющих интерес генов или последовательностей в клетку-хозяин. Примеры векторов включают без ограничения вирусные векторы, векторы экспрессии "голой" ДНК или РНК, плазмиды, космиды или фаговые векторы, векторы экспрессии ДНК или РНК, ассоциированные с катионными конденсирующими средствами, векторы экспрессии ДНК или РНК, инкапсулированные в липосомы, и некоторые эукариотические клетки, такие как клетки-продуценты.
Используемое в данном документе выражение "содержащий" в контексте настоящего описания следует интерпретировать как "включающий в себя".
Выражение "используемый в настоящем раскрытии", используемое в данном документе, относится к используемому в способе, раскрытом в данном документе, используемому в молекулах, в том числе промежуточных соединениях, раскрытых в данном документе, или в обоих, соответственно контексту используемого термина.
Следует понимать, что какие бы аспекты ни описывались в настоящем документе формулировкой "содержащий", другие аналогичные аспекты, описываемые выражениями "состоящий из" и/или "состоящий по сути из", также предусмотрены.
Любой положительный вариант осуществления или их комбинация, описанная в данном документе, может быть основанием для негативного исключения, т.е. отказа от прав.
Композиции
Настоящее раскрытие распространяется на композиции, содержащие молекулу, описанную в данном документе (такую как гидролизованные молекулы по настоящему раскрытию), в частности, фармацевтическую композицию (или диагностическую композицию), содержащую молекулу по настоящему раскрытию и фармацевтический наполнитель, разбавитель или носитель.
Композиция, как правило, будет поставляться в виде части стерильной фармацевтической композиции, которая будет, как правило, включать фармацевтически приемлемый носитель. Фармацевтическая композиция по настоящему изобретению может дополнительно включать фармацевтически приемлемый адъювант в контексте состава вакцины.
Настоящее раскрытие также распространяется на способы получения указанных композиций, например получение фармацевтической или диагностической композиции, включающее добавление и смешивание молекулы по настоящему раскрытию, такой как гидролизованная молекула по раскрытию настоящего изобретения, вместе с одним или более фармацевтически приемлемым наполнителем, разбавителем или носителем.
Антитело по настоящему раскрытию может быть единственным активным компонентом в фармацевтической или диагностической композиции или может сопровождаться другими активными компонентами.
Фармацевтические композиции, соответственно, содержат терапевтически эффективное количество молекулы по настоящему раскрытию. Выражение "терапевтически эффективное количество", используемое в данном документе, относится к количеству терапевтического средства, необходимому для лечения, ослабления или профилактики целевого заболевания или состояния, или для достижения выявляемого терапевтического или профилактического эффекта. Терапевтически эффективное количество можно оценить первоначально либо в анализах на клеточных культурах, или на животных моделях, как правило, у грызунов, кроликов, собак, свиней или приматов. Животную модель можно также использовать для определения подходящего диапазона концентраций и способа введения. Затем такую информацию можно использовать для определения подходящих доз и способов для введения человеку.
Точное терапевтически эффективное количество для субъекта-человека будет зависеть от тяжести течения заболевания, общего состояния здоровья субъекта, возраста, веса и пола субъекта, диеты, времени и частоты введения, комбинации (комбинаций) лекарственных средств, чувствительности реакции и толерантности/ответа на терапию. Это количество может быть определено с помощью обычных экспериментов и находится на усмотрении клинициста. Как правило, терапевтически эффективное количество будет составлять от 0,01 мг/кг до 50 мг/кг, например, от 0,1 мг/кг до 20 мг/кг. Фармацевтические композиции могут быть в целях удобства представлены в виде единичных дозированных форм, содержащих заранее определенное количество активного средства по настоящему изобретению на дозу. Фактическая доза, в которой вводят молекулу по настоящему раскрытию, зависит от природы состояния, подлежащего лечению, например, степени имеющегося заболевания/воспаления, и от того, используется ли молекула профилактически или для лечения существующего состояния.
Композиции можно вводить пациенту по отдельности или можно вводить в комбинации (например, одновременно, последовательно или раздельно) с другими средствами, лекарственными средствами или гормонами.
Фармацевтически приемлемый носитель не должен сам по себе индуцировать выработку антител, вредных для индивидуума, получающего композицию, и не должен быть токсичными. Подходящими носителями могут быть крупные, медленно метаболизируемые макромолекулы, такие как белки, полипептиды, липосомы, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот и неактивные вирусные частицы.
Фармацевтически приемлемые носители в терапевтических композициях могут дополнительно содержать жидкости, такие как вода, физиологический раствор, глицерин и этанол. Кроме того, вспомогательные вещества, такие как увлажняющие или эмульгирующие средства, или рН-буферные вещества, могут присутствовать в таких композициях. Такие носители позволяют составлять фармацевтические композиции в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, взвесей и суспензий для приема внутрь пациентом.
Подходящие формы для введения включают формы, пригодные для парентерального введения, например, путем инъекции или инфузии, например, путем болюсной инъекции или непрерывной инфузии. Там, где продукт предназначен для инъекции или инфузии, он может иметь форму суспензии, раствора или эмульсии в масляном или водном носителе и может содержать вспомогательные средства, такие как суспендирующие, консервирующие, стабилизирующие и/или диспергирующие средства. В качестве альтернативы, молекула по настоящему раскрытию может быть в сухом виде для восстановления перед применением с соответствующей стерильной жидкостью.
Соответственно, в составах по настоящему раскрытию значение рН конечного состава не аналогично значению изоэлектрической точки антитела, например, если значение рН состава равняется 7, то pI 8-9 или выше может быть целесообразным. Не желая быть связанными теорией, полагают, что это может, в перспективе, обеспечить конечному составу улучшенную стабильность, например, антитело остается в растворе.
Фармацевтические композиции данного изобретения могут быть введены любым числом способов, включая, но без ограничений, пероральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интратекальный, внутрижелудочковый, трансдермальный, чрескожный (например, см. WO98/20734), подкожный, внутрибрюшинный, интраназальный, энтеральный, местный, сублингвальный, интравагинальный или ректальный. Безыгольные шприцы также могут быть использованы для введения фармацевтических композиций по настоящему изобретению. Как правило, терапевтические композиции могут быть приготовлены либо как инъецируемые, либо в виде жидких растворов, или суспензий. Твердые формы, подходящие для растворения или суспендирования в жидких носителях перед инъекцией, также могут быть получены.
Прямая доставка композиций обычно будет выполняться путем инъекции, подкожно, внутрибрюшинно, внутривенно или внутримышечно, или доставляться в интерстициальное пространство ткани. Композиции также можно ввести в место поражения. Дозирование лечения может проходить в режиме однократного приема или в режиме многократных приемов.
Следует принять во внимание, что композиция содержит полипептид, и, как таковой, он может подвергаться разложению в желудочно-кишечном тракте. Таким образом, если композиция будет вводиться путем использования желудочно-кишечного тракта, эта композиция должна будет содержать средства, которые защищают полипептид от разложения, но которые высвобождают антитело после его всасывания из желудочно-кишечного тракта.
Подробное обсуждение фармацевтически приемлемых носителей доступно в Remington's Pharmaceutical Sciences (Mack Publishing Company, Нью-Джерси 1991).
В одном из вариантов осуществления состав предоставляется в виде состава для местного применения, в том числе ингаляции.
Подходящие ингаляционные препараты включают ингаляционные порошки, дозированные аэрозоли, содержащие газы-пропелленты, или ингаляционные растворы, свободные от газов-пропеллентов. Ингаляционные порошки по настоящему раскрытию, содержащие активное вещество, могут состоять исключительно из вышеуказанных активных веществ или смеси вышеуказанных активных веществ с физиологически приемлемым наполнителем.
Эти ингаляционные порошки могут включать моносахариды (например, глюкозу или арабинозу), дисахариды (например, лактозу, сахарозу, мальтозу), олиго- и полисахариды (например, декстраны), полиспирты (например, сорбит, маннит, ксилит), соли (например, хлорид натрия, карбонат кальция) или их смеси друг с другом. Удобны к применению моно- или дисахариды, а именно, применение лактозы или глюкозы, в частности, но не исключительно, в виде их гидратов.
Частицам для осаждения в легких требуется размер частиц менее 10 мкм, такой как 1-9 мкм, например от 0,1 мкм до 5 мкм, в частности, от 1 мкм до 5 мкм. Размер частиц активного компонента (такого как антитело) имеет первостепенное значение.
Газы-пропелленты, которые могут быть использованы для получения ингаляционных аэрозолей, известны из уровня техники. Подходящие газы-пропелленты выбирают из числа углеводородов, таких как н-пропан, н-бутан или изобутан, и галогенсодержащих углеводородов, таких как хлорированные и/или фторированные производные метана, этана, пропана, бутана, циклопропана или циклобутана. Вышеприведенные газы-пропелленты могут быть использованы сами по себе или в виде их смесей.
Особенно подходящими газами-пропеллентами являются галогенированные производные алканов, выбранные из числа TG 11, TG 12, TG 134а и TG227. Из вышеприведенных галогенированных углеводородов TG134a (1,1,1,2-тетрафторэтан) и TG227 (1,1,1,2,3,3,3-гептафторпропан) и их смеси являются особенно подходящими.
Содержащие газ-пропеллент ингаляционные аэрозоли могут также содержать другие компоненты, такие как сорастворители, стабилизаторы, поверхностно-активные вещества (сурфактанты), антиокислители, смазочные материалы и средства для регулирования рН. Все эти компоненты известны из уровня техники.
Содержащие газ-пропеллент ингаляционные аэрозоли по настоящему изобретению могут содержать до 5% по массе активного вещества. Аэрозоли по настоящему изобретению содержат, например, от 0,002% до 5% по массе, от 0,01% до 3% по массе, от 0,015% до 2% по массе, от 0,1% до 2% по массе, от 0,5% до 2% по массе или от 0,5% до 1% по массе активного компонента.
Альтернативными вариантами местного введения в легкие может также быть введение препарата в виде жидкого раствора или суспензии, например, с использованием устройства, такого как небулайзер, например, небулайзер, соединенный с компрессором (например небулайзер Pari LC-Jet Plus(R), соединенный с компрессором Pari Master(R) производства Pari Respiratory Equipment, Inc., Ричмонд, Вирджиния).
Молекулы настоящего изобретения могут быть доставлены диспергированными в растворителе, например, в виде раствора или суспензии. Их можно суспендировать в соответствующем физиологическом растворе, например, растворе хлорида натрия или другом фармакологически приемлемом растворителе или буферном растворе.
Терапевтические составы в виде суспензий и растворов могут также содержать один или несколько наполнителей. Наполнители хорошо известны в данной области техники и включают буферы (например, цитратный буфер, фосфатный буфер, ацетатный буфер и бикарбонатный буфер), аминокислоты, мочевину, спирты, аскорбиновую кислоту, фосфолипиды, белки (например, сывороточный альбумин), EDTA, хлорид натрия, липосомы, маннит, сорбит и глицерин. Растворы или суспензии могут быть инкапсулированы в липосомы или биоразлагаемые микросферы. Состав, как правило, будет предоставлен в по существу стерильной форме с использованием стерильных процессов производства.
Это может включать в себя получение и стерилизацию путем фильтрации буферного растворителя/раствора, используемого для состава, асептическое суспендирование молекулы в стерильном буферном растворе растворителя и разлив состава в стерильные сосуды при помощи способов, известных специалистам в данной области техники.
Лечение
Настоящее раскрытие также распространяется на способы лечения пациента, нуждающегося в этом, путем введения терапевтически эффективного количества молекулы по настоящему раскрытию или композиции, такой как фармацевтическая композиция, содержащая вышеупомянутое.
В одном из вариантов осуществления предусмотрена молекула по настоящему раскрытию или композиция, содержащая вышеупомянутое, для применения в лечении, в частности, для применения в лечении заболевания или состояния, описанного в данном документе, такого как рак.
В одном из вариантов осуществления предусмотрено применение молекулы по настоящему раскрытию или композиции, содержащей вышеупомянутое, в производстве лекарственного препарата для лечения состояния или заболевания, описанного в данном документе, такого как рак.
Следовательно, молекулы по настоящему изобретению пригодны для лечения и/или профилактики патологического состояния.
Таким образом, предусмотрена молекула по настоящему изобретению для применения в лечении путем введения ее терапевтически эффективного количества, например, в виде фармацевтического состава. В одном из вариантов осуществления молекулу по настоящему раскрытию вводят местно в легкие, например, с помощью ингаляции.
Антитела, предусмотренные в настоящем изобретении, являются пригодными для лечения заболеваний или нарушений, в том числе воспалительных заболеваний и нарушений, иммунных заболеваний и нарушений, фиброзирующих нарушений и рака.
Термин "воспалительное заболевание" или "нарушение" и "иммунное заболевание или нарушение" включает в себя ревматоидный артрит, псориатический артрит, болезнь Стилла, болезнь Макла-Уэльса, псориаз, болезнь Крона, неспецифический язвенный колит, SLE (системную красную волчанку), астму, аллергический ринит, атопический дерматит, рассеянный склероз, васкулит, сахарный диабет I типа, вторичную болезнь и реакцию трансплантат против хозяина.
Термин "фиброзирующее нарушение" включает идиопатический легочный фиброз (IPF), системный склероз (или склеродермию), фиброз почек, диабетическую нефропатию, IgA-нефропатию, артериальную гипертензию, терминальную стадию хронической почечной недостаточности, перитонеальный фиброз (постоянный амбулаторный перитонеальный диализ), цирроз печени, возрастную макулярную дегенерацию (ARMD), ретинопатию, кардиальный реактивный фиброз, рубцевание, келоиды, ожоги, кожные язвы, ангиопластику, коронарное шунтирование, артропластику и хирургическое лечение катаракты.
Термин "рак" включает в себя злокачественный новый рост, который возникает из эпителия, обнаруженный в коже или, что чаще, в выстилке органов тела, например молочной железы, яичника, предстательной железы, толстой кишки, легкого, почки, поджелудочной железы, желудка, мочевого пузыря или кишечника. Рак имеет тенденцию проникать в окружающие ткани и распространяться (метастазировать) в отдаленные органы, например в кости, печень, легкие или головной мозг.
Субъекты, подлежащие лечению, могут являться животными. Однако в одном или нескольких вариантах осуществления композиции адаптированы для введения субъекту-человеку.
ПРИМЕРЫ
В Примерах ниже используется моноклональное антитело, названное в данном документе T289C.
AC4GlcNAz Тетраацилированный N-азидоацетилглюкозамин
ADC конъюгат антитело-лекарственное средство
BCN бицикло[6.1.0]нонин
BME β-меркаптоэтанол
DTT дитиотреитол
MMAE трис(2-карбоксиэтил)фосфин
PAB пара-аминобензиловый спирт
Пример 1 Синтез малеимидопропионил-PEG7-биотина
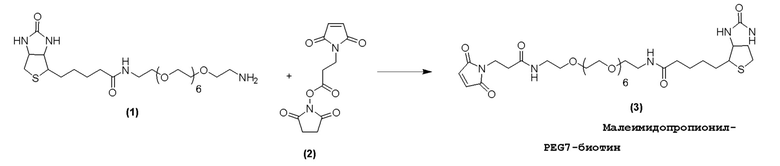
К перемешиваемому раствору биотин-PEG7 амина (1) (100 мг, 0,168 ммоль) в безводном дихлорметане (7 мл) при комнатной температуре в атмосфере N2 добавляли малеимидопропионовый сложный эфир NHS (2) (49,2 мг, 0,186 ммоль, 1,1 экв.). После перемешивания в течение 1 ч. анализ TLC показал завершение реакции, после чего добавляли 1 N HCl (2 мл). Органический раствор отделяли, промывали насыщенным раствором соли и сушили над Na2SO4. Неочищенный продукт, полученный после выпаривания в вакууме, очищали с применением колоночной флеш-хроматографии на силикагеле, элюируя ступенчатым градиентом MeOH в дихлорметане (об./об.=1:30, 1:20 и 1:10), с получением целевого соединения, малеимидопропионил-PEG7-биотина (3) (65 мг, 0,087 ммоль, выход 52%), в виде твердого воска. 1H ЯМР (CDCl3) d 7,01 (br s, 1H), 6,96 (br s, 1H), 6,70 (s, 2H), 5,86 (s, 1H), 5,06 (s, 1H), 4,51 (m, 1H), 4,33 (m, 1H), 3,84 (t, J= 7,2 Гц, 2H), 3,62-3,66 (m, 24H), 3,53 (m, 4H), 3,40 (m, 4H), 3,15 (m, 1H), 2,88-2,96 (m, 1H), 2,73 (d, J= 12,6 Гц, 1H), 2,52 (t, J= 7,2 Гц, 2H), 2,24 (t, J= 7,0 Гц, 2H), 1,66 (m, 4H), 1,45 (m, 2H).
Пример 2 Синтез малеимидофенилацетил-PEG7-биотина
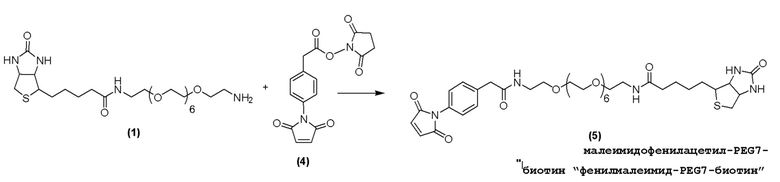
Смесь биотин-PEG7-NH2 (1) (0,25 г, 0,42 ммоль) и малеимидофенилуксусного сложного эфира NHS (4) (0,2 г, 0,609 ммоль) в ацетонитриле (10 мл) перемешивали в течение ночи при температуре окружающей среды в атмосфере N2. Растворитель удаляли в вакууме и полученный остаток очищали с помощью колоночной флэш-хроматографии на силикагеле, элюируя ступенчатыми градиентами дихлорметана к МеОН в дихлорметане при соотношении об./об. 1:30, 1:20, 1:10:1 и 1:5 с получением целевого продукта малеимидофенилацетил-PEG7-биотина (5) в виде масла (70 мг, 0,087 ммоль, выход 21%) вместе с 190 мг смеси желаемого продукта и гидролизованной формы в соотношении 3:1, как это показано с помощью 1H ЯМР, а также 15 мг смеси 1:2. 1H ЯМР (CDCl3) d 7,41, 7,30 (AB-тип, JAB=8,3 Гц, 4H) [7,64, 7,24 (AB-тип, JAB=9,2 Гц, 4H) второстепенный компонент], 6,85 (s, 2H) [6,23 (d, J=7,5 Гц, 1H), 6,47 (d, J=7,5 Гц, 1H), второстепенный компонент], 6,63 (br s, 1H), 6,55 (br s, 1H), 5,83 (s, 1H), 5,18 (s, 1H), 4,49 (m, 1H), 4,31 (m, 1H), 3,63-3,40 (m, 34H), 3,15 (m, 1H), 2,90 (d-AB-тип, JAB=12,9, J=4,7 Гц, 1H), 2,72 (AB Type, JAB=12,9Гц, 1H), 2,22 (t, J= 7,1 Гц, 2H), 1,68 (m, 4H), 1,46 (m, 2H). MS (ESI) масса/заряд 830 (M+Na), 825 (M+NH4, основной пик), 808 (M+1).
Пример 3 Синтез 2-фтор-5- малеимидофенил-PEG7-биотина
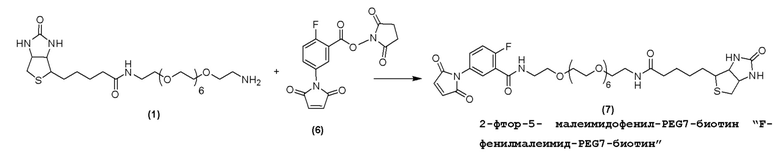
Смесь биотин-PEG7-NH2 (1) (0,1 г, 0,168 ммоль, 1 экв.) и 2-фтор-5-малеимидофенольного сложного эфира NHS (6) (0,084 г, 0,252 ммоль, 1,5 экв.) в дихлорметане (1 мл) перемешивали в течение ночи при температуре окружающей среды в атмосфере N2. Растворитель удаляли в вакууме и полученный остаток очищали с помощью эксклюзионной хроматографии (SEC) на колонке LH20, элюируя смесью МеОН/дихлорметан (об./об. 1:1), с получением целевого продукта 2-фтор-5-малеимидофенил-PEG7-биотина (7) в виде масла (28 мг, 0,034 ммоль, выход 20,5%), который содержал приблизительно 10% гидролизованной формы, как это показано с помощью HPLC. Также получили дополнительно 90 мг смеси желаемого продукта и гидролизованной формы в соотношении 3:2. 1H ЯМР (CDCl3) d 8,05 (dd, J=6,7, 2,9 Гц, 1H), 7,47 (dd, J=4,5, 2,7 Гц, 1H), 7,23 (m, 1H) [8,20 (m, 1H), 7,46 (m, 1H), 7,19 (m, 1H), второстепенный компонент], 6,88 (s, 2H) [6,45, 6,24 (AB-тип, JAB=12,9 Гц, 2H), второстепенный компонент], 6,63 (br s, 1H), 6,05 (s, 1H), 4,49 (m, 1H), 4,31 (m, 1H), 3,66-3,54 (m, 32H), 3,43 (m, 2H), 3,14 (m, 1H), 2,90 (d-AB-тип, JAB=12,7, J=5,0 Гц, 1H), 2,73 (AB-тип, JAB=12,7 Гц, 1H), 2,22 (m, 2H), 1,73 (m, 4H), 1,44 (m, 2H). MS (ESI) масса/заряд 835 (M+Na), 829 (M+NH4), 813 (M+1, основной пик).
Пример 4 Общая процедура конъюгации x-малеимид-PEG-биотинов с mAb
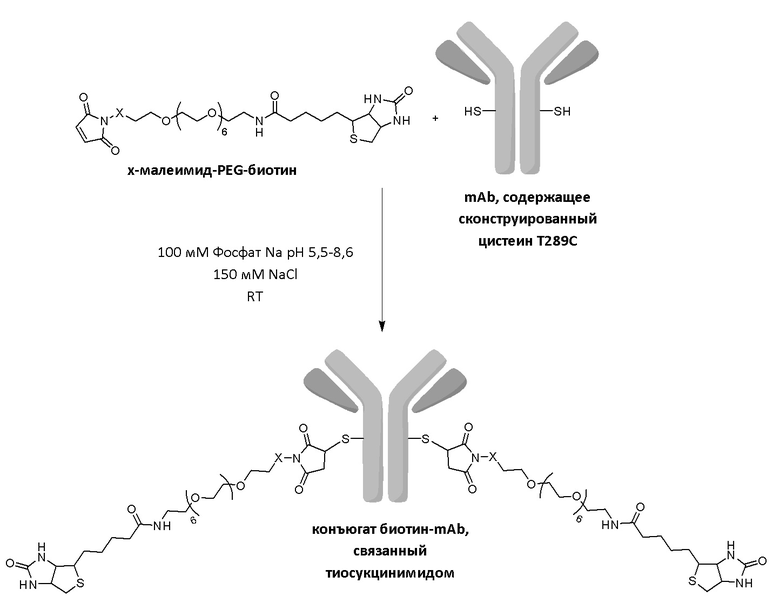
где x представляет собой X, как определено выше для соединений формулы (I), и необязательно дополнительно содержит Y, как определено для соединений формулы (I).
x-Малеимид-PEG-биотины конъюгировали с mAb (содержащим мутацию T289C в Fc) в несколько стадий. Сначала mAb мягко восстанавливали с получением свободных сульфгидрильных групп путем объединения 5 мл раствора 1,6 мг/мл mAb в 10 мM PBS, pH 7,2 (8 мг mAb, 53,3 нM, 1 экв.), с 43 мкл раствора 50 мM TCEP в воде (2,15 мкмоль, 40 экв.) с последующим осторожным перемешиванием при 37°С в течение 1 ч. Восстановленное mAb переносили в кассету для диализа Slide-A-Lyzer® (10K MWCO) и подвергали диализу против PBS, 1 мM EDTA, pH 7,2-7,8, 4°C в течение 24 ч. с некоторыми изменениями буфера. Восстановленное mAb окисляли с повторным образованием внутренних дисульфидных связей путем добавления дегидроаскорбиновой кислоты (21 мкл 50 мM исходного раствора в DMSO, 1,1 мкмоль, 20 экв.) с последующим осторожным перемешиванием в течение 4 ч. при комнатной температуре. Раствор окисленного mAb доводили до нужного рН добавлением 1 М фосфата натрия (однозамещенный для рН 5,5, двузамещенный для рН 8,6, или исходный раствор, доведенный до рН 7,4) до конечной концентрации фосфата 100 мМ и концентрации mAb 1,3 мг/мл. Затем 1,15 мл раствора mAb (1,5 мг, 10 нмоль, 1 экв.) разделяли на аликвоты во флакон с последующим добавлением исходного раствора x-малеимид-PEG-биотина (2 мкл 10 мM исходного раствора в DMAc, 20 нмоль, 2 экв.). Реакционную смесь кратковременно встряхивали и дополнительно инкубировали в течение требуемого количества времени с последующим добавлением N-ацетилцистеина (10 мкл 100 мM раствора в воде, 1 мкмоль, 100 экв.) и дополнительно инкубировали в течение 15 минут, чтобы погасить не вступивший в реакцию малеимид. Все реакции конъюгации выполняли при комнатной температуре (22oC) в атмосфере окружающей среды. Отметим, что 2 экв. x-малеимид-PEG-биотина относительно mAb=1 экв. x-малеимид-PEG-биотина относительно свободного цистеина, содержащегося в mAb. Эту общую процедуру модифицировали по мере необходимости для достижения желаемой стехиометрии реакции (т.e. начальные растворы с различным малеимид:mAb).
Образцы ADC анализировали с использованием масс-спектрометра Agilent 6520B Q-TOF, оснащенного колонкой RP-HPLC (Agilent Poroshell 300SB-C3; 5 мкм, 2,1 мм x 75 мм; Part# 660750-909). Параметры высокоэффективной жидкостной хроматографии (HPLC) были следующими: скорость потока 0,4 мл/мин; подвижная фаза A представляла собой 0,1% (об./об.) муравьиную кислоту в H2O HPLC-класса, и подвижная фаза B представляла собой 0,1% (об./об.) муравьиную кислоту в ацетонитриле. Колонку уравновешивали в смеси 90%A/10%B, которую также использовали для обессоливания образцов ADC, с последующим элюированием в смесь 40%A/60%B. Данные масс-спектров собирали для 100-3000 масса/заряд, положительной полярности, температуры газа 350°C, давления распылителя 48 фунт/дюйм2 и капиллярного напряжения 5000 В. Данные анализировали с использованием поставляемого изготовителем программного обеспечения для качественного анализа MassHunter (Agilent v.B.04.00) и интенсивности пиков спектров после деконволюции использовали для получения относительной доли реагентов и продуктов и кинетики реакции.
Пример 5 Расчет эффективности конъюгации и процента гидролиза
Расчет эффективности конъюгации
Эффективность конъюгации и соотношение лекарственное средство:антитело (DAR) рассчитывали, исходя из интенсивностей пиков масс-спектров после деконволюции, используя следующие уравнения:
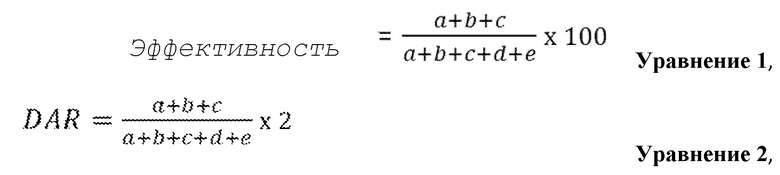
a=интенсивность пика G0+1;
b=интенсивность пика G0+1+Na/H2O;
c=интенсивность пика G0+1+Na/H2O+Na;
d=интенсивность пика G0;
e=интенсивность пика G0+Na/H2O;
DAR= соотношение лекарственное средство:антитело;. Для данного исследования любую молекулу, конъюгированную с mAb, рассматривают в качестве "лекарственного средства"
Способ расчета процента гидролиза для конъюгированных с mAb T289C тиосукцинимидов
Значения процента гидролиза рассчитывали, исходя из интенсивностей пиков масс-спектров после деконволюции, используя следующее уравнение:
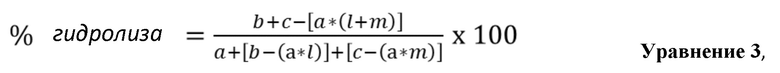
Уравнение 3,
a= интенсивность пика конъюгата тяжелой цепи= (HC+1 );
b= интенсивность пика конъюгата тяжелой цепи +H2O/Na= (HC+1+H2O/Na);
примечание: Конъюгат тяжелой цепи+23 а.е.м. и +18 а.е.м., оба были включены в это значение; при промежуточных значениях гидролиза эти пики не могут быть разделены и одиночный пик появился между значениями, ожидаемыми для (HC+1+H2O) и (HC+1+Na);
c= интенсивность пика конъюгата тяжелой цепи+H2O+ Na=(HC+1+H2O+Na);
l= b/a при T=0;
m= c/a при T=0.
Пример 6 Расчеты периода полувыведения
Полупериоды рассчитывали из полученных констант скоростей, используя уравнение 4 для реакций псевдо-первого порядка (гидролиз и деконьюгация) и уравнение 5 для реакций второго порядка (конъюгация):
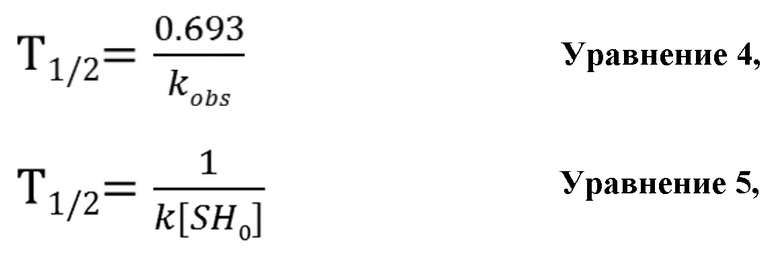
[SH]0=Начальная концентрация тиола
Пример 7 Анализ конъюгации x-малеимид-PEG-биотина при 1 экв. малеимида:тиола
Конъюгаты x-малеимид-PEG-биотин-mAb подготавливали для анализа LC/MS путем разбавления до 0,2 мг/мл с PBS pH 7,2 с последующим комбинированием 50 мкл раствора mAb с 5 мкл TCEP (0,5 M в воде). Эту смесь инкубировали в течение 5 мин. при комнатной температуре для восстановления дисульфидных связей перед впрыском (15 мкл) в LC/MS. Типичные данные показаны на Фигуре 1A и 1B.
Пример 8 Анализ конъюгации x-малеимид-PEG-биотина при 0,5 экв. малеимида:тиола
Конъюгаты x-малеимид-PEG-биотин-mAb подготавливали, как описано выше в Примере 7, за исключением того, что использовали 1 экв. малеимида:mAb. Отметим, что 1 эквивалент x-малеимид-PEG-биотина равен 0,5 эквивалента x-малеимид-PEG-биотина:тиола.
1) Алкилмалеимид-PEG-биотин (компаратор), см. Фигуру 2A
2) Фенилмалеимид-PEG-биотин, см. Фигуру 2B
3) Фторфенилмалеимид-PEG-биотин, см. Фигуру 2C
Эти данные показывают, что способ расчета является надежным, то есть 50% исходная реакционная смесь дала нам ~ 50% конъюгации.
Пример 9 Эффективность конъюгации x-малеимид-PEG-биотинов с mAb T289C при 22oC
Конъюгаты x-малеимид-PEG-биотин-mAb подготавливали, как описано выше, с использованием 2 экв. малеимида:mAb. Отметим, что 2 экв. x-малеимид-PEG-биотина:mAb равняется 1 экв. x-малеимид-PEG-биотина:тиола. Продукты реакции анализировали с помощью масс-спектрометрии восстановленных и гликозилированных продуктов и эффективность конъюгации рассчитывали с использованием уравнения 1. Результаты показаны на Фигуре 3 и Фигуре 4.
Пример 10 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 5,5, 22oC
Данные конъюгации анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости второго порядка определяли по наклонам кривых, полученных при нанесении на график 1/[SH] в зависимости от времени, и линейному регрессионному анализу. Результаты показаны на Фигуре 5.
Пример 11 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 7,4, 22oC
Данные конъюгации анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости второго порядка определяли по наклонам кривых, полученных при нанесении на график 1/[SH] в зависимости от времени, и линейному регрессионному анализу. Результаты показаны на Фигуре 6.
Пример 12 Кинетика конъюгации x-малеимид-PEG-биотинов с mAb T289C, pH 8,6, 22oC
Данные конъюгации анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости второго порядка определяли по наклонам кривых, полученных при нанесении на график 1/[SH] в зависимости от времени, и линейному регрессионному анализу. Результаты показаны на Фигуре 7.
Краткое описание кинетики x-малеимид-PEG-биотина для конъюгации с mAb T289C
(k2, M-1с-1)
(k2, M-1с-1)
(k2, M-1с-1)
Сравнения из литературы:
1) Реакция N-этилмалеимида с цистеином при pH 7,0, k2=1,62×103 M-1с-1
Li, J.; Xu, Q.; Cortes, D.; et al. Reaction of cysteines substituted in the amphipathic N-terminal tail of a bacterial potassium channel with hydrophilic and hydrophobic maleimides. PNAS 2002, 99(18), 11605-11610.
2) Реакция N-этилмалеимида с β-меркаптоэтанолом при pH 7,0, k2=0,71×103 M-1с-1
Mosser, G. N-Substituted maleimide inactivation of the response of taste cell stimulation. J. Neurobiol. 1976, 7(5), 457-468.
Пример 13 Кинетика реакции x-малеимид-PEG-биотинов с mAb T289C после предварительной инкубации: непрямое измерение гидролиза малеимида
х-Малеимид-PEG-биотины предварительно инкубировали в буферных растворах с различным рН для оценки их стабильности и эффективности конъюгации с тиолами с течением времени. Данный анализ косвенно контролирует гидролиз малеимида, поскольку гидролизованные малеинимиды не активны по отношению к тиолам. Антитело, имеющее мутацию T289C FC, восстанавливали и окисляли, как описано выше, и доводили до 1,5 мг/мл в PBS, содержащем 50 мM фосфата натрия, pH 7,4. Растворы малеимида подготавливали в буфере (100 мM фосфата натрия, pH 5,5, 7,4, 8,6) путем объединения 20 мкл раствора x-малеимид-PEG-биотина (10 мM раствор в DMAc) с 180 мкл буфера при желаемом pH (конечная концентрация x-малеимид-PEG-биотина=1 мM) и инкубировали при 22°C в течение определенных промежутков времени перед проведением реакции с mAb. Для реакций конъюгации 267 мкл mAb (1,5 мг/мл, 2,7 нмоль, 1 экв.) объединяли с 5,3 мкл инкубированного в буфере раствора x-малеимид-PEG-биотина (5,4 нмоль, 2 экв.). Добавление раствора малеимида не влияло на рН раствора mAb. Реакция конъюгации протекала при 22°C в течение 1,5 ч. при pH 7,4. После реакции образцы восстанавливали с DTT при комнатной температуре в течение 5 мин. и анализировали с помощью масс-спектрофотометрии. Процент конъюгации рассчитывали с использованием уравнения 1. Результаты показаны на Фигуре 8.
Эти данные показывают, что реакционная способность малеимида теряется с течением времени из-за гидролиза. Скорость гидролиза малеимида увеличивается в случае N-арилмалеимидов. В целом, гидролиз малеимида происходит медленнее, чем тиол-малеимидная конъюгация, что объясняет, почему наблюдалась эффективная конъюгация для N-арилмалеимидов при рН 8,6. Полупериоды можно сравнить с использованием нижеследующих данных.
Пример 14 Кинетика гидролиза малеимида, pH 5,5, 22°C
Данные гидролиза малеимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 9.
Пример 15 Кинетика гидролиза малеимида, pH 7,4, 22°C
Данные гидролиза малеимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 10.
Пример 16 Кинетика гидролиза малеимида, pH 8,6, 22°C
Данные гидролиза малеимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 11.
Краткое описание кинетики гидролиза x-малеимида
гидролиза (ч.)
гидролиза (ч.)
a) После 60-минутной инкубации существенного гидролиза не выявлено
Сравнения из литературы:
1) Гидролиз N-фенилмалеимида при pH 7,6, 25°C kobs=7×10-5 с-1
Oleksandr, K.; Leriche, G.; et al. Selective Irreversible chemical tagging of cysteine with 3-arylpropiolonitriles. Bioconjug. Chem. 2014, 25, 202-206.
2) Гидролиз малеимида (незамещенного) при pH 8,38, 30oC, kobs=1,51×10-4 с-1
Khan, M.N. Kinetics and mechanism of the alkaline hydrolysis of maleimide. J. Pharm. Sci. 1984, 73(12), 1767-1171.
Эти данные показывают, что гидролиз малеимида происходит намного медленнее, чем тиол-малеимидная конъюгация, таким образом, N-арилмалеимиды являются пригодными реагентами для конъюгации. Даже в самом крайнем случае F-фенилмалеимидов при рН 8,6 полупериод гидролиза малеимида составляет 6 минут, в то время как конъюгация тиолов завершается за 15 секунд.
Пример 17 Кинетика гидролиза тиосукцинимида для конъюгатов x-малеимид-PEG-биотин-mAb T289C
Конъюгаты x-малеимид-PEG-биотин-mAb инкубировали в буферных растворах и контролировали с помощью LC/MS во времени для наблюдения гидролиза тиосукцинимида. Сначала mAb, содержащее мутацию T289C Fc (0,75 мг, 5 нмоль, 1 экв.), подвергали взаимодействию с x-малеимид-PEG-биотином (50 нмоль, 5 мл 10 мM исходного раствора в DMAC, 10 экв.) в 577 мл PBS, pH 7,2. Реакции конъюгации давали протекать в течение 5 минут, а затем гасили N-ацетилцистеином (500 нмоль, 4 мл 100 мМ в воде, 100 экв.) и дополнительно инкубировали в течение 5 минут. Реакционную смесь затем объединяли с PBS, содержащим 0,5 мМ EDTA и 1 М фосфата натрия при желаемом рН, чтобы достичь конечных концентраций 0,65 мг/мл mAb, 100 мМ фосфата, 0,5 М EDTA и 150 мМ NaCl. После подготовки образца аликвоту удаляли и разбавляли 1:3 75 мМ фосфатным буфером с pH 5,5 для получения исходного момента времени образца. Затем образцы дополнительно инкубировали в требуемых условиях с аликвотами, удаляемыми в определенные моменты времени. Все образцы немедленно разбавляли 1:3 75 мМ фосфатным буфером с рН 5,5 для прекращения реакции гидролиза. Затем образцы стерильно фильтровали, восстанавливали с помощью TCEP и анализировали с использованием LC/MS. Гидролиз тиосукцинимида подтверждали добавлением 18 а.е.м. к пику конъюгата mAb в масс-спектре. Полуколичественный анализ гидролиза проводили с использованием интенсивностей пиков в масс-спектрах после деконволюции и уравнения 3, который включает вычитание фона с использованием измерения Т=0. Затем данные превращали в потерю тиосукцинимида (М) с течением времени и наносили на график в виде ln [тиосукцинимида] против секунд. Наклон линии наилучшего соответствия дал константу скорости псевдо-первого порядка для гидролиза тиосукцинимида. Дополнительные эксперименты проводили для определения гидролиза тиосукцинимида в течение 1 часа, n=3.
Пример 18 Гидролиз тиосукцинимида, pH 7,4, 22oC, для конъюгатов PEG-биотин-mAb T289C
Данные гидролиза тиосукцинимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 12.
Пример 19 Гидролиз тиосукцинимида, pH 7,4, 37oC, для конъюгатов PEG-биотин-mAb T289C
Данные гидролиза тиосукцинимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 13.
Пример 20 Гидролиз тиосукцинимида, pH 8,6, 22oC, для конъюгатов PEG-биотин-mAb T289C
Данные гидролиза тиосукцинимида также анализировали в единицах молярной концентрации для определения констант скорости реакции. Константы скорости псевдо-первого порядка определяли исходя из наклонов кривых, полученных при нанесении на график ln[малеимида] в зависимости от времени, и линейного регрессионного анализа. Результаты показаны на Фигуре 14.
Краткое описание кинетики гидролиза тиосукцинимида для конъюгатов mAb T289C-PEG-биотин
Таблица 6. Константы скорости реакции для гидролиза тиосукцинимида конъюгатов PEG-биотин в положении mAb T289C
(kobs, с-1)
Эти данные показывают, что гидролиз N-арилтиосукцинимидов происходит во временном масштабе, который легко может быть применен к производству без существенных изменений стандартных процедур конъюгации. Например, при выполнении конъюгации полезной нагрузки при рН 7,4, 22°C в течение 24 ч. можно было бы проводить как конъюгацию, так и гидролиз тиосукцинимида на одной стадии.
Пример 21 Гидролиз x-тиосукцинимида для конъюгатов PEG-биотин-mAb-T289C после инкубации длительностью 1 час, n=3
Результаты показаны на Фигуре 15 в виде среднего ± стандартное отклонение, n=3. Эти данные подтверждают тенденцию, наблюдаемую в экспериментах по кинетике с отдельными образцами, с расширенным набором образцов. Легкость гидролиза тиосукцинимида зависит от химической структуры, присоединенной к азоту кольцевой головки, следующим образом: N-алкил<<N-фенил<N-фторфенил. Относительная погрешность для этих экспериментов обычно составляла менее 5%.
Пример 22 Гидролиз x-тиосукцинимида для конъюгатов PEG-биотин-mAb-T289C в присутствии молибдата натрия
Конъюгаты x-малеимид-PEG-биотин-mAb инкубировали в буферных растворах, содержащих молибдат натрия, для исследования того, способно ли это соединение увеличивать гидролиз тиосукцинимида. Образцы контролировали с помощью LC/MS в течение времени для наблюдения гидролиза тиосукцинимида, как описано выше. Сначала mAb, содержащее мутацию T289C Fc (0,5 мг, 3,3 нмоль, 1 экв.), подвергали взаимодействию с x-малеимид-PEG-биотином (50 нмоль, 5 мл 10 мM исходного раствора в DMAC, 15 экв.) в 0,365 мл PBS, pH 7,2. Реакции конъюгации давали протекать в течение 5 минут, а затем гасили N-ацетилцистеином (500 нмоль, 4 мл 100 мМ в воде, 151 экв.) и дополнительно инкубировали в течение 5 минут. Затем реакционную смесь объединяли с 1 М PBS, содержащим 1 М молибдат натрия, при желаемом рН, чтобы достичь конечной концентрации 100 мМ фосфата и 100 мМ молибдата. После добавления молибдата смесь инкубировали при 22°C в течение 1 ч. Через 1 ч. образцы разбавляли 1:5 75 мМ фосфатным буфером с рН 6,5 для прекращения гидролиза. Затем образцы стерильно фильтровали, восстанавливали с помощью TCEP и анализировали с использованием LC/MS. Гидролиз тиосукцинимида подтверждали добавлением 18 а.е.м. к пику конъюгата mAb в масс-спектре. Полуколичественный анализ гидролиза проводили с использованием интенсивностей пиков в масс-спектрах после деконволюции и уравнения 3. Результаты показаны на Фигуре 16.
Заметное усиление гидролиза наблюдалось для 2 образцов:
A) F-фенилмалеимид-PEG-биотин с pH 5,5
B) F-фенилмалеимид-PEG-биотин с pH 7,4
(+ молибдат натрия/ - молибдат натрия)
a) образцы, демонстрирующие менее чем 10% гидролиз, не анализировали
Эти данные показывают, что только N-фторфенилтиосукцинимиды чувствительны к катализируемому молибдатом гидролизу, другие нет. Кроме того, эффекты катализатора уменьшаются при высоком рН, как и ожидалось.
Пример 23 Чувствительность конъюгатов mAb T289C к замене тиолов в буфере, содержащем тиолы
Конъюгаты биотин-mAb инкубировали в водном буфере, содержащем β-меркаптоэтанол (BME), чтобы испытать тиосукцинимидную связь на деконьюгацию. х-Малеимид-PEG-биотины конъюгировали с mAb, содержащим мутацию T289C, как описано выше, с незначительной модификацией. Реакции конъюгации проводили при 1 эквиваленте x-PEG-малеимида:тиола в течение 15 мин при 22°C с последующим немедленным разбавлением до 0,2 мг/мл (1,33 мкМ mAb) с помощью 1X PBS, pH 7,2, содержащего 0,5 мM EDTA. Стадию гашения N-ацетилцистеином пропускали. Для BME-содержащих образцов BME добавляли до конечной концентрации 1% об./об. (143 мМ). Образцы дополнительно инкубировали при 37°C в атмосфере окружающей среды без перемешивания. Аликвоты удаляли в различные моменты времени, стерильно фильтровали, восстанавливали с помощью DTT и затем анализировали с использованием LC/MS. Процент конъюгированного mAb и гидролиза тиосукцинимида определяли по высотам пиков масс-спектров, используя уравнение 1 и уравнение 2, соответственно. Данные по деконъюгированному mAb гидролизу тиосукцинимида наносили на график в виде ln[концентрации] в зависимости от времени (с) с получением констант скорости псевдо-первого порядка исходя из наклона лини наилучшего соответствия. Результаты показаны на Фигуре 17.
Пример 24 Стабильность конъюгатов PEG-биотин-mAb T289C в буфере, содержащем BME
Результаты показаны на Фигуре 18. Эти данные показывают, что 1) вариабельная стабильность наблюдалась между различными типами тиосукцинимидов в присутствии свободного тиола. Виды с более быстрым гидролизом показали меньшую деконъюгацию, 2) N-алкилтиосукцинимид деконъюгировал в простом буфере, не содержащем свободного тиола.
Кроме того, эти данные показывают, что быстрая дестабилизация может быть достигнута сразу после конъюгации без какой-либо специальной обработки в случае N-фторфенилтиосукцинимида.
Пример 25 Гидролиз тиосукцинимида при pH 7,2, 37°C для конъюгатов PEG-биотин-mAb T289C, наблюдаемый в анализе испытания с BME
Результаты показаны на Фигуре 19.
Эти данные показывают, что N-фенил и N-фторфенилтиосукцинимиды полностью гидролизуются в течение первых 24 часов, что согласуется с другими данными гидролиза. N-алкилтиосукцинимиды гидролизуются значительно медленнее.
Пример 26 Взаимосвязь между деконъюгацией и гидролизом тиосукцинимида, наблюдаемыми в анализе испытания с BME
Результаты показаны на Фигуре 20.
Эти данные наносят на график в виде деконъюгации на левой оси и гидролиза на правой оси. Гидролиз и деконьюгация явно связаны между собой. Более высокая скорость гидролиза ограничивает максимальную степень деконьюгации.
Пример 27 Стабильность конъюгатов mAb-биотина в присутствии свободного тиола после мягкого гидролиза
Конъюгаты биотина-mAb инкубировали в водном буфере, содержащем β-меркаптоэтанол (BME), чтобы испытать тиосукцинимидную связь на деконьюгацию. В этом эксперименте конъюгаты тиосукцинимида подвергали кратковременной инкубации в мягко основных условиях для облегчения гидролиза тиосукцинимида перед испытанием на стабильность. x-Малеимид-PEG-биотины конъюгировали с mAb, содержащим мутацию T289C, как описано выше, с незначительной модификацией Реакции конъюгации проводили при 1 эквиваленте x-PEG-малеимида:тиола в течение 15 мин. при 22°C с последующим гашением N-ацетилцистеином (100 экв. относительно mAb) и дополнительной реакцией в течение 5 минут. Реакционные смеси доводили до рН 8,6 добавлением 10% об./об. фосфата натрия (1 М, двузамещенный) и затем инкубировали при 37°С в течение 1 ч. Затем реакции диализовали против PBS (pH 7,2), содержащего 0,5 мМ EDTA, в течение 24 ч. при 4oC. После диализа концентрации mAb подтверждали путем измерения A280 (NanoDrop) и образцы разбавляли до 0,2 мг/мл (1,33 мкM mAb) 1X PBS, pH 7,2, содержащим 0,5 мM EDTA. Для BME-содержащих образцов BME добавляли до конечной концентрации 1% об./об. (143 мМ). Образцы дополнительно инкубировали при 37°C в атмосфере окружающей среды без перемешивания. Аликвоты удаляли в различные моменты времени, стерильно фильтровали, восстанавливали с помощью DTT и затем анализировали с использованием LC/MS. Процент конъюгированного mAb и гидролиза тиосукцинимида определяли по высотам пиков масс-спектров, используя уравнение 1 и уравнение 2, соответственно. Данные по деконъюгированному mAb гидролизу тиосукцинимида наносили на график в виде ln[концентрации] в зависимости от времени (с) с получением констант скорости псевдо-первого порядка исходя из наклона лини наилучшего соответствия.
Пример 28 Чувствительность конъюгатов mAb T289C к замене тиолов в буфере после мягкого гидролиза
Эти данные показывают, что 1) мягкий гидролиз полностью стабилизировал N-арилтиосукцинимиды, но не N-алкилтиосукцинимид. Кроме того, константа скорости псевдо-первого порядка для опосредованной тиолами деконъюгации N-алкилтиосукцинимидов из этого эксперимента точно соответствует значению из эксперимента без предварительного гидролиза (данные воспроизводимы).
Пример 29 Синтез N-алкилмалеимидо-Val-Cit-PAB-MMAE
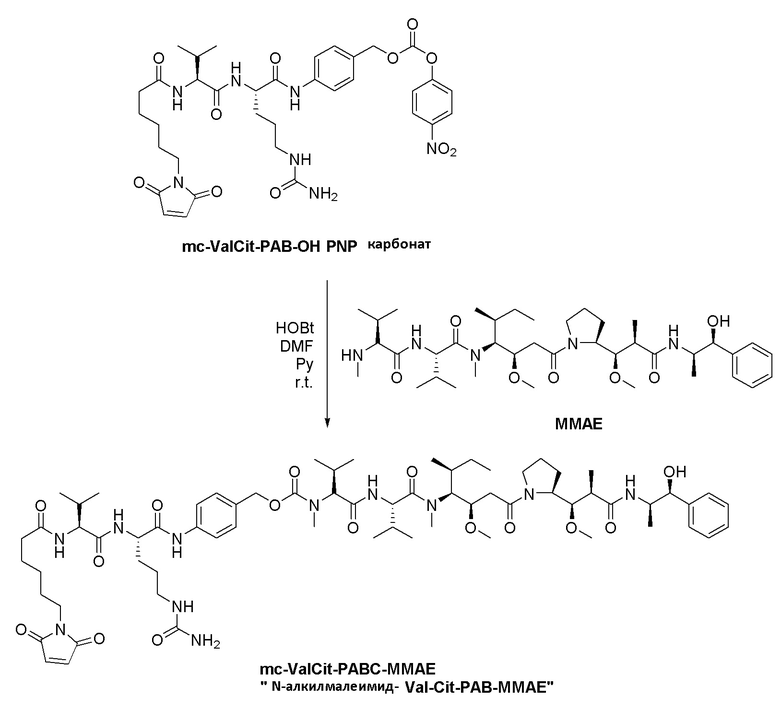
Малеимидокапроил-валин-цитруллин-p-амидобензилкарбонил-моно-метил-ауристатин-E (mc-ValCit-PABC-MMAE) получали в соответствии с литературным способом с модификациями.1 Таким образом, смесь mc-Val-Cit-p-аминобензиловый спирт p-нитрофенилкарбоната (8), свежеприготовленного в соответствии с литературным способом2 (265 мг, 0,36 ммоль, 1,5 экв.), MMAE (9) (169 мг, 0,24 ммоль, 1 экв.) и N-гидроксибензотриазола (HOBt) (6,48 мг, 0,048 ммоль, 0,2 экв.) перемешивали в DMF (5 мл) при комнатной температуре в течение 2 мин. с последующим добавлением пиридина (38 мг, 0,48 ммоль, 2 экв.). После перемешивания в течение 24 ч. летучие органические вещества удаляли в вакууме. Полученный остаток растирали с этилацетатом и метанолом (1 л), получая mc-Val-Cit-PAB-MMAE (10) в виде белого порошка (220 мг, 0,17 ммоль, выход 71%), который был обычно > 95% чистоты согласно анализу RP-HPLC. Если необходимо, дальнейшую очистку можно проводить с помощью препаративной HPLC с обращенной фазой на C18 или эксклюзионной колоночной хроматографии. Электроспрей (ES)-MS масса/заряд 1339 (M+Na, основной пик), 1317 (M+1).
Список литературы: 1) Doronina SO, Toki BE, Torgov MY, Mendelsohn BA, Cerveny CG, Chace DF, DeBlanc RL, Gearing RP, Bovee TD, Siegall CB, Francisco JA, Wahl AF, Meyer DL, Senter PD. Development of potent monoclonal antibody auristatin conjugates for cancer therapy. Nat Biotechnol. 2003;21:778-784.
2) Dubowchik GM, Firestone RA, Padilla L, Willner D, Hofstead SJ, Mosure K, Knipe JO, Lasch, SJ, Trail PA. Cathepsin B-labile dipeptide linkers for lysosomal release of doxorubicin from internalizing immunoconjugates: model studies of enzymatic drug release и antigen-specific in vitro anticancer activity. Bioconjug Chem. 2002;13:855-869.
Пример 30 Синтез N-фенилацетилмалеимидо-Val-Cit-PAB-MMAE
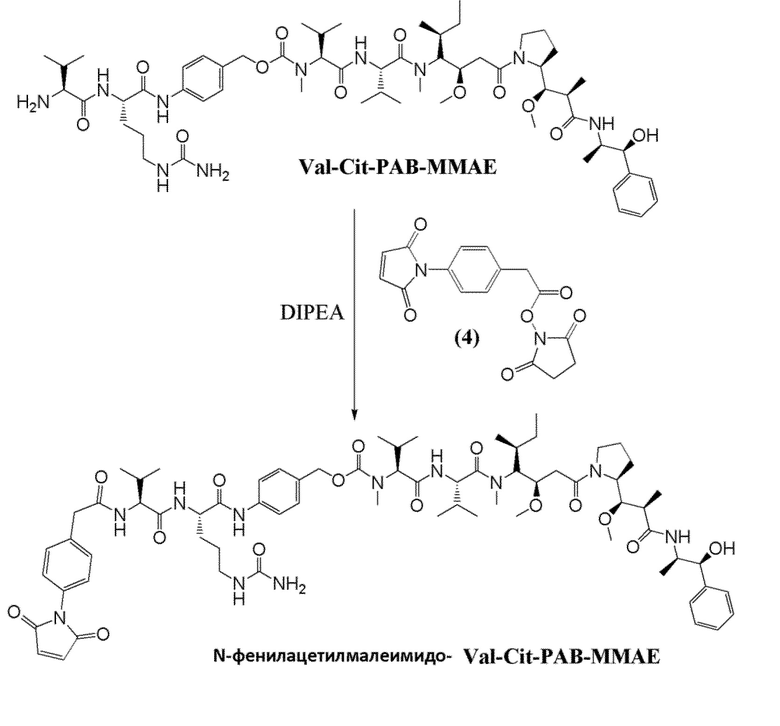
К перемешиваемому раствору Val-Cit-PAB-MMAE (100 мг, 0,089 ммоль) и малеимидофенилуксусного сложного эфира NHS (4) (43,8 мг, 0,133 ммоль) в DMF (1 мл) при температуре окружающей среды под атмосферой N2добавляли DIPEA (57,5 мг, 0,445 ммоль). После перемешивания в течение ночи MS-анализ показал образование продукта с присутствием небольшого количества исходного материала. Смесь инициировали, разделяли методом эксклюзионной хроматографии (SEC) на колонке LH-20, элюируя смесью МеОН/дихлорметан (об./об. 1: 1). Фракции контролировали с помощью MS и те, которые содержали желаемый продукт, объединяли. После выпаривания досуха в вакууме получали 25 мг (0,0187 ммоль, выход 21%) маслянистого материала. MS демонстрировала кластер ионов с масса/заряд 1391 (M+Cl+Na), 1369 (M+Cl, основной пик), 1360 (M+Na) и 1337 (M+1), в то время как HPLC показывала два пика в соотношении приблизительно 2:1. Дополнительная очистка с помощью полупрепаративной HPLC давала после выпаривания 2 основные фракции 5 мг и 6 мг, соответственно. Однако эти два образца показали по существу такие же результаты HPLC и MS.
Пример 31 Получение конъюгатов N-фенилмалеимид Val-Cit-PAB-MMAE-mAb T289C
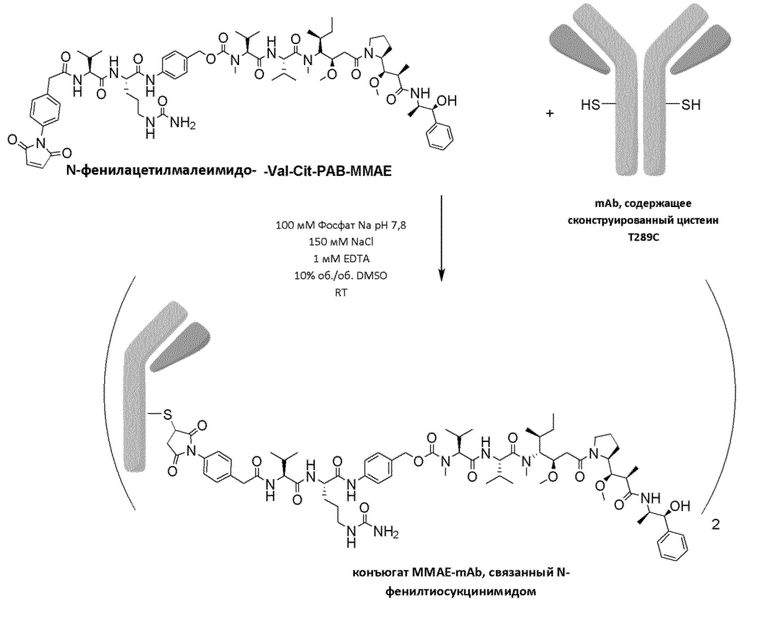
N-фенилацетилмалеимидо-Val-Cit-PAB-MMAE конъюгировали с mAb (содержащим мутацию T289C в Fc) в несколько стадий. Сначала mAb мягко восстанавливали с получением свободных сульфгидрильных групп путем объединения 5 мл раствора 1,6 мг/мл mAb в 10 мM PBS, pH 7,2 (8 мг mAb, 53,3 нM, 1 экв.), с 43 мкл раствора 50 мM TCEP в воде (2,15 мкмоль, 40 экв.) с последующим осторожным перемешиванием при 37°С в течение 1 ч. Восстановленное mAb переносили в кассету для диализа Slide-A-Lyzer® (10K MWCO) и подвергали диализу против PBS, 1 мM EDTA, pH 7,2-7,8, 4°C в течение 24 ч. с некоторыми изменениями буфера. Восстановленное mAb окисляли с повторным образованием внутренних дисульфидных связей путем добавления дегидроаскорбиновой кислоты (21 мкл 50 мM исходного раствора в DMSO, 1,1 мкмоль, 20 экв.) с последующим осторожным перемешиванием в течение 4 ч. при комнатной температуре. Раствор окисленного mAb (2,5 мл, 27 нмоль, 1 экв.) объединяли с 10% об./об. DMSO с последующим добавлением N-фенилацетилмалеимидо-Val-Cit-PAB-MMAE (27 мкл 10 мM исходного раствора в DMSO, 270 нмоль, 10 экв.). Реакцию проводили при комнатной температуре при перемешивании в течение 1 ч., а затем добавляли N-ацетилцистеин (21 мкл 100 мМ исходного раствора в воде, 2,2 мкмоль, 80 экв.) для прекращения реакции. Затем реакционную смесь разбавляли в 3 раза дистиллированной водой и подвергали CHT-хроматографии для удаления свободного неконъюгированного лекарственного средства (колонка Bio-Scale Mini Cartridge CHT Type II 40 мкм среды). ADC элюировали градиентом от буфера A (10 мM фосфата, pH 7,0) к буферу B (10 мM фосфата, pH 7,0, содержащий 2M NaCl) в течение 25 минут. После CHT-хроматографии образец подвергали замене буфера на 1X PBS, дополненный 0,5 мМ EDTA, pH 7,2, путем диализа в кассете slide-a-lyzer при 4oC. Для образцов, подвергнутых мягкому гидролизу, добавляли 10% об./об. раствора фосфата натрия (1М, двузамещенный) и раствор инкубировали при 37°С в течение 1 ч. Затем гидролизованные образцы подвергали замене буфера с помощью диализа на 1X PBS (pH 7,2), дополненный 0,5 мМ EDTA. ADC характеризовали с помощью LC/MS восстановленных и гликозилированных продуктов, как описано выше. Эффективность конъюгации и DAR рассчитывали, используя уравнение 1 и уравнение 2, соответственно.
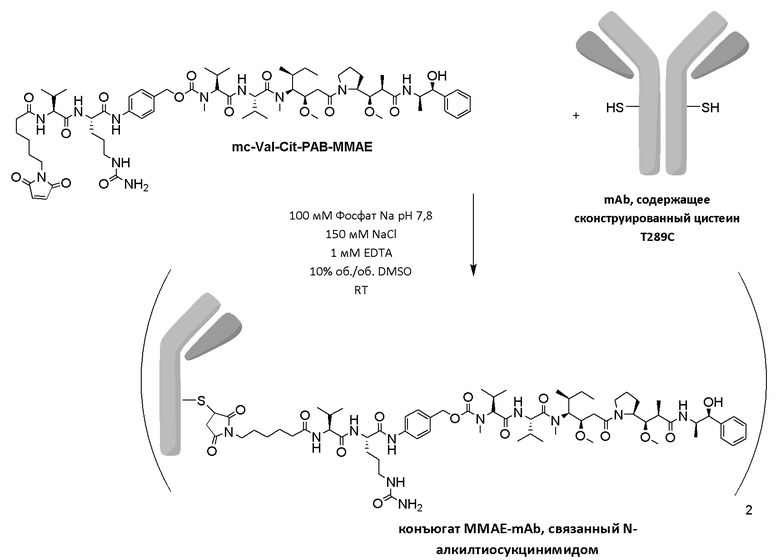
N-алкилмалеимидо-Val-Cit-PAB-MMAE конъюгировали с mAb (содержащим мутацию T289C в Fc) таким же образом, как и N-фенилмалеимидо-Val-Cit-PAB-MMAE (см. выше).
Пример 32 Анализ ADC mc-PAB-MMAE-mAb T289C
Типичные данные масс-спектрометрии восстановленных и гликозилированных продуктов для конъюгатов x-малеимид-Val-Cit-PAB-MMAE-mAb T289C показаны на Фигуре 22.
Краткое описание данных конъюгации MMAE mAb T289C
Конъюгация 2
(%)
(%)
(%)
(%)
Конъюгация 3
(%)
(%)
(%)
(%)
Пример 32 Стабильность конъюгатов MMAE-mAb T289C в буфере, содержащем тиолы
Конъюгаты MMAE-mAb инкубировали в водном буфере, содержащем β-меркаптоэтанол (BME), чтобы испытать тиосукцинимидную связь относительно реакций обмена тиолов. MMAE конъюгировали с mAb, содержащим мутацию T289C, как описано выше. После конъюгации конъюгаты немедленно очищали с помощью CHT-хроматографии для удаления неконъюгированного лекарственного средства. Затем образцы подвергали кратковременному диализу (кассета Slide-a-lizer, 10 кДа MWCO, 4oC, 2 ч.) для замены буфера на 1X PBS, pH 7,2, содержащий 0,5 мM EDTA. После диализа образцы разбавляли до 0,2 мг/мл (1,33 мкM mAb) 1X PBS, pH 7,2, содержащим 0,5 мM EDTA. Для BME-содержащих образцов BME добавляли до конечной концентрации 1% об./об. (143 мМ). Образцы дополнительно инкубировали при 37°C в атмосфере окружающей среды без перемешивания. Аликвоты удаляли в различные моменты времени, стерильно фильтровали, восстанавливали с помощью DTT и затем анализировали с использованием LC/MS. Процент конъюгированного mAb и гидролиза тиосукцинимида определяли по высотам пиков масс-спектров, используя уравнение 1 и уравнение 2, соответственно. Данные по деконъюгированному mAb гидролизу тиосукцинимида наносили на график в виде ln[концентрации] в зависимости от времени (с) с получением констант скорости псевдо-первого порядка исходя из наклона лини наилучшего соответствия.
Пример 33 Стабильность конъюгатов MMAE-mAb T289C в буфере, содержащем тиол (BME)
Результаты показаны на Фигуре 23.
(kobs, с-1)
Эти данные показывают, что MMAE деконьюгирует в тиолсодержащем буфере и что конъюгаты, полученные с N-алкилмалеимидом, являются менее стабильными, чем MMAE, конъюгированный с N-фенилмалеимидом.
Пример 34 Гидролиз MMAE-тиосукцинимидов в конъюгатах mAb-T289C
Результаты показаны на Фигуре 24.
(kobs, с-1)
Эти данные показывают, что MMAE, конъюгированный с N-алкилмалеимидом, является менее стабильным, чем MMAE, конъюгированный с N-фенилмалеимидом в присутствии свободных тиолов. Графики Ln, используемые для расчета констант скорости, не показаны.
Пример 35 Стабильность конъюгатов MMAE-mAb T289C в буфере, содержащем тиол (BME)
Результаты показаны на Фигуре 25.
Эти данные показывают, что: 1) MMAE, конъюгированный с N-алкилмалеимидом, является менее стабильным, чем MMAE, конъюгированный с N-фенилмалеимидом, в присутствии свободных тиолов; 2) конъюгаты N-алкилмалеимид-MMAE менее чувствительны к мягкому гидролизу, чем аналоги PEG-биотин, 3) мягкий гидролиз не улучшает стабильность конъюгатов N-алкилмалеимид-ММАЕ, 4) конъюгаты N-фенилмалеимид-ММАЕ очень чувствительны к мягкому гидролизу, но данная стадия не является необходимой для достижения высокой стабильности, 5) N-фенилмалеимид спонтанно гидролизуется значительно больше, чем N-алкилмалеимид, когда подвергается идентичным способам очистки.
Пример 36 Сравнение гидролиза тиосукцинимида в PEG-биотине и MMAE, наблюдаемого в испытании с BME
Результаты показаны на Фигуре 26.
Эти данные показывают, что на медленно гидролизующие тиосукцинимиды значительно влияет химия, предшествующая малеимиду. Химия гидрофильного PEG-биотина повышает скорость гидролиза в ~3-5 раз по сравнению гидрофобным конъюгатом MMAE-полезная нагрузка.
Пример 37 Сравнение деконъюгации в присутствии β-меркаптоэтанола: PEG-биотин по сравнению с MMAE-полезной нагрузкой
Результаты показаны на Фигуре 27.
Таблица 23. Кинетические параметры для гидролиза тиосукцинимида и деконъюгации, определенные в анализе с BME
(kobs, с-1)
Пример 38 Стабильность ADC MMAE-T289C в мышиной сыворотке
ADC MMAE инкубировали в мышиной сыворотке, чтобы испытать тиосукцинимидную связь относительно деконъюгации. MMAE конъюгировали с mAb, содержащим мутацию T289C, с получением желаемого ADC, как описано выше. После конъюгации лекарственного средства ADC немедленно очищали с помощью CHT-хроматографии для удаления неконъюгированного лекарственного средства. Затем образцы подвергали кратковременному диализу (кассета slide-a-lyzer, 10 кДа MWCO, 4oC, 2 ч.) для замены буфера на 1X PBS, pH 7,2, содержащий 0,5 мM EDTA. После диализа концентрации mAb определяли по измерению A280 (NanoDrop), а затем добавляли к нормальной мышиной сыворотке (Jackson Immunoresearch) для достижения конечной концентрации 0,2 мг/мл (1,33 мкМ mAb). Общий объем ADC, добавленного в сыворотку, был менее 10%. Смесь ADC-сыворотки стерильно фильтровали и инкубировали при 37°C в герметичном контейнере без перемешивания. Аликвоты удаляли в различные моменты времени и замораживали. Конъюгированное и неконъюгированное человеческое антитело извлекали из мышиной сыворотки иммунопреципитацией с использованием FC-специфической против человеческого IgG агарозной смолы (Sigma-Aldrich). Сначала смолу дважды промывали PBS, один раз буфером для элюирования IgG и затем еще дважды с PBS. Затем образцы мышиной ADC-сыворотки объединяли со смолой против человеческого IgG (100 мкл смеси ADC-сыворотки, 50 мкл суспензии смолы) и осторожно перемешивали в течение 15 минут при комнатной температуре. Смолу извлекали центрифугированием и затем дважды промывали PBS. Осадок смолы ресуспендировали в 100 мкл буфера для элюирования IgG (Thermoscientific) и дополнительно инкубировали в течение 5 минут при комнатной температуре. Смолу удаляли центрифугированием и затем к надосадочной жидкости добавляли 20 мкл 1 М Трис, рН 8,0. Раствор восстановленных человеческих антител подвергали стерильной фильтрации, восстанавливали с помощью DTT и затем анализировали с использованием LC/MS. Процент конъюгированного mAb и гидролиза тиосукцинимида определяли по высотам пиков масс-спектров, используя уравнение 1 и уравнение 2, соответственно. Данные по деконъюгированному mAb гидролизу тиосукцинимида наносили на график в виде ln[концентрации] в зависимости от времени (с) с получением констант скорости псевдо-первого порядка исходя из наклона лини наилучшего соответствия.
Результаты показаны на Фигуре 28.
скорости деконъюгации псевдо-первого порядка
(kobs, с-1)
(kobs, с-1)
Эти данные свидетельствуют о том, что 1) ADC, полученные с N-фенилмалеимидом, являются более стабильными, чем ADC, полученные с N-алкилмалеимидами; 2) гидролиз N-фенилтиосукцинимида происходит быстрее, чем гидролиз N-алкилтиосукцинимида; 3) тиоловая деконъюгация происходит несколько медленнее, чем гидролиз тиосукцинимида для N-алкилтиосукцинимида, поэтому полной деконъюгации не наблюдается, скорости сходны для растворимых и нерастворимых полезных нагрузок. В случае растворимых полезных нагрузок максимальная наблюдаемая деконьюгация ниже, предположительно, из-за более высокой скорости гидролиза тиосукцинимида.
На Фигуре 29А показана деконъюгация и гидролиз алкилтиосукцинимида, рН 7,2, 37°С, плюс BME. Эти данные демонстрируют, что деконъюгация связана с гидролизом тиосукцинимида. Достигнуты плато деконъюгации после максимального гидролиза тиосукцинимида, что согласуется с экспериментами по испытанию с BME.
На Фигуре 29B показана деконъюгация ADC в мышиной сыворотке через 7 дней при 37°C как среднее +/- стандартное отклонение (n=3). Этот эксперимент представляет собой тот же самый описанный выше анализ стабильности в сыворотке, который проводят в трех повторах в один момент времени. Данные показывают, что ADC N-алкилмалеимид-Val-Cit-PAB-MMAE менее устойчив, чем ADC N-фенилмалеимид-Val-Cit-PAB-MMAE. Относительная погрешность для этого эксперимента обычно составляла менее 10%.
Пример 39 Активность ADC по отношению к раковым клеткам MDA-MB-361 после инкубации в мышиной сыворотке
В этих исследованиях использовали клетки рака молочной железы MDA-MB-361 с высокой экспрессией 5T4. Клетки высевали в 80 мкл RPMI1640 с 10% FBS в 96-луночные плоскодонные планшеты при 2000 MDA-MB-361 клеток/лунку. Клетки оставляли на ночь для прилипания. Концентрацию 5Х каждого ADC получали разбавлением тестируемых образцов в культуральной среде. Двадцать микролитров каждого тестируемого образца добавляли к клеткам в двух повторах, так что диапазон конечной дозовой кривой составлял от 50 нг/мл до 0,76 пг/мл в серии при ступенчатом серийном разведении 1:4. Обработанные клетки культивировали при 37°C/5% CO2 в течение 6 дней и жизнеспособность клеток оценивали с помощью люминесцентного анализа жизнеспособности CellTiter-Glo от Promega. 100 мкл восстановленного реагента CTG добавляли в каждую лунку, слегка встряхивали в течение 10 минут при комнатной температуре и абсорбцию каждого образца при 560 нм считывали с использованием люминометра Perkin Elmer EnVision. Процент жизнеспособности клеток рассчитывали по следующей формуле: (средняя люминесценция обработанных образцов/средняя люминесценция необработанных контрольных образцов) × 100. Значения EC50 определяли с использованием анализа методом логистической нелинейной регрессии с помощью программного обеспечения GraphPad Prism.
Результаты показаны на Фигуре 30 в виде среднего ± относительная погрешность, n=2. Эти данные показывают, что активность ADC сохраняется для стабильных (N-фенил) ADC и теряется для нестабильных (N-алкилмалеимид) ADC.
Пример 40 Гетеробифункциональные линкеры для стабилизации тиосукцинимида и конъюгации полезной нагрузки
1) N-фторфенилмалеимидо-PEG4-BCN
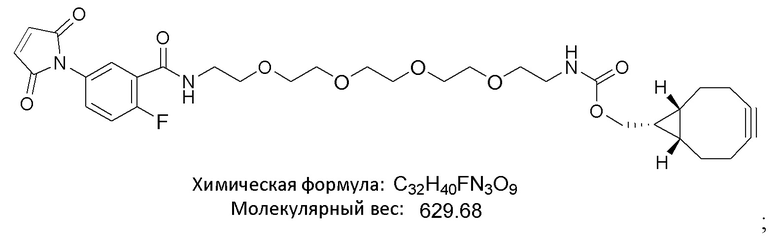
2) N-фенилмалеимидо-PEG4-BCN
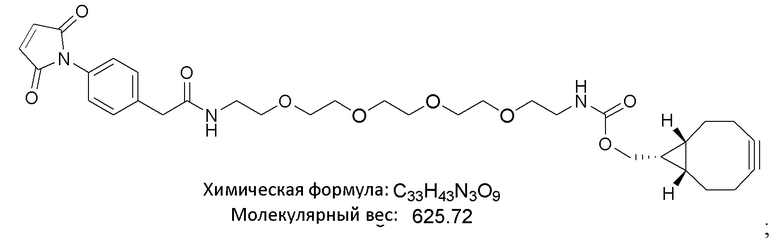
3) N-алкилмалеимидо-PEG4-BCN продукт каталога SynChem #SC50094 95% чистота
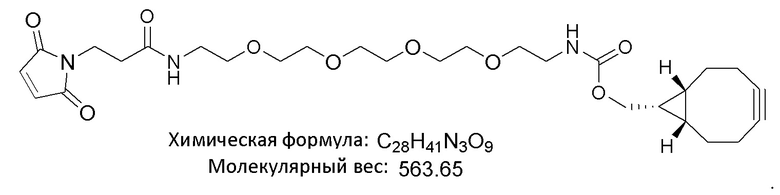
Приготовили серию гетеробифункциональных линкеров, содержащих как малеимиды на основе алкила- или N-арила, так и функциональные группы PEG-BCN. Группа BCN является реакционноспособной по отношению к азидам в реакции, известной как "клик-конъюгация без меди".
Пример 41 Синтез N-фторфенилмалеимидо-PEG-BCN
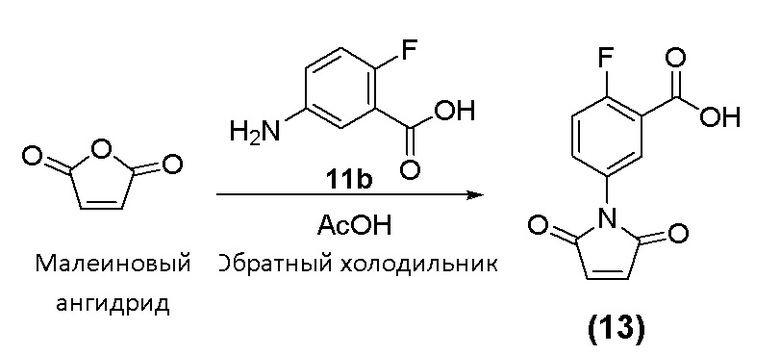
Реакция малеинового ангидрида (10a, 0,313 г, 3,19 ммоль) и 5-амино-2-фторбензойной кислоты (11b, 0,5 г, 3,22 ммоль) в ледяном AcOH при кипячении с обратным холодильником дает неочищенный 9c (0,72 г) в виде желтого твердого вещества после обработки. Неочищенный продукт дополнительно очищали колоночной хроматографией на силикагеле с получением 0,21 г (0,89 ммоль, выход 28%) 9c в виде светло-желтого твердого вещества.
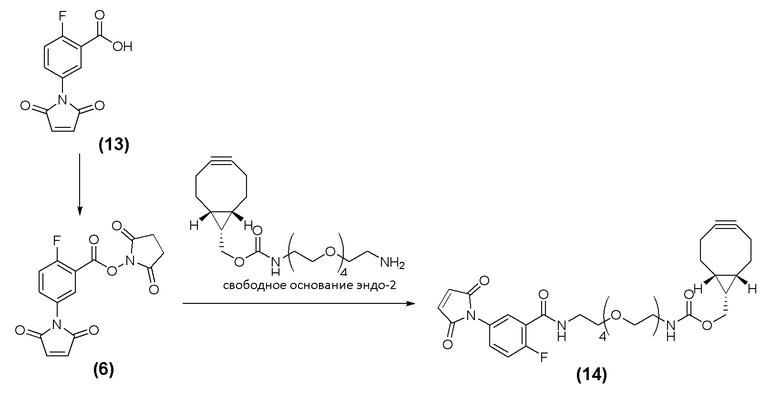
NHS-активированный малеимид (6) получали in situ из (13) и использовали без очистки. Таким образом, (13) (0,137 г, 0,582 ммоль) подвергали взаимодействию с N-гидроксисукцинимидом (0,074 г, 0,64 ммоль) в присутствии DCC (0,144 г, 0,698 ммоль) в DME (5 мл) при комнатной температуре в течение 1 ч. После удаления осажденного твердого вещества (DCU) фильтрованием фильтрат, содержащий активированный сложный эфир (6), добавляли по каплям к раствору эндо-2 (0,2 г, 0,485 ммоль) в DME (2 мл) при комнатной температуре при перемешивании в атмосфере N2. Через 1 ч. анализы TLC и MS указали на завершение реакции. Избыток DME концентрировали в вакууме и полученный неочищенный остаток очищали колоночной хроматографией на силикагеле в атмосфере N2, элюируя этилацетатом, затем 4% MeOH в DCM, получая (14) (0,24 г, 0,38 ммоль, выход 78,6%) в виде светло-желтого масла. Данные 1H ЯМР и MS подтвердили химическую структуру; HPLC показала 94% чистоту. MS (ESI) масса/заряд 629,3 (M+1), 647,8 (M+H2O), 652,8 (M+Na, основной пик).
Пример 42 Синтез N-фенилмалеимидо-PEG-BCN
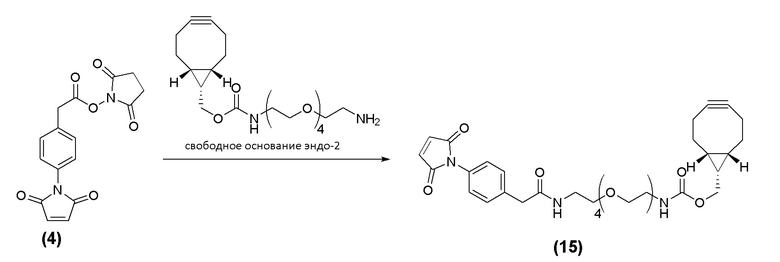
Реакцию между (4) (0,191 г, 0,582 ммоль) и эндо-2 (0,2 г, 0,485 ммоль) в DME (5 мл) завершали за 1 ч. при комнатной температуре в атмосфере N2, как указано одновременно с помощью TLC и MS. Избыток DME удаляли в вакууме и полученный неочищенный остаток очищали колоночной хроматографией на силикагеле под давлением N2, элюируя этилацетатом, затем 4% MeOH в DCM. Фракции, содержащие продукт, объединяли и концентрировали в вакууме. Остаток растворяли в DCM и переносили во флакон под N2. Избыток растворителя удаляли барботированием с N2, получая (15) (0,26 г, выход 85%) в виде светло-желтого масла. Данные 1H ЯМР и MS подтвердили химическую структуру с примесью остаточных растворителей. MS (ESI) масса/заряд 626,5 (M+1), 643,5 (M+H2O), 648,8 (M+Na, основной пик).
Пример 43 Общая процедура конъюгации x-малеимид-PEG-BCN с mAb
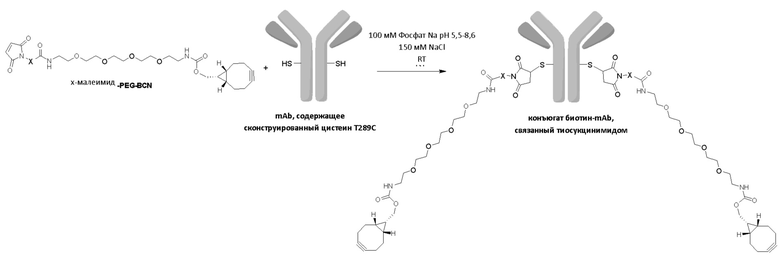
x-Малеимид-PEG-BCN конъюгировали с mAb (содержащим мутацию T289C в Fc) в несколько стадий. Сначала mAb мягко восстанавливали с получением свободных сульфгидрильных групп путем объединения 5 мл раствора 1,6 мг/мл mAb в 10 мM PBS, pH 7,2 (8 мг mAb, 53,3 нM, 1 экв.), с 43 мкл раствора 50 мM TCEP в воде (2,15 мкмоль, 40 экв.) с последующим осторожным перемешиванием при 37°С в течение 1 ч. Восстановленное mAb переносили в кассету для диализа Slide-A-Lyzer® (10K MWCO) и подвергали диализу против PBS, 1 мM EDTA, pH 7,2-7,8, 4°C в течение 24 ч. с некоторыми изменениями буфера. Восстановленное mAb окисляли с повторным образованием внутренних дисульфидных связей путем добавления дегидроаскорбиновой кислоты (21 мкл 50 мM исходного раствора в DMSO, 1,1 мкмоль, 20 экв.) с последующим осторожным перемешиванием в течение 4 ч. при комнатной температуре. Раствор окисленного mAb доводили до 1,3 мг/мл mAb добавлением PBS. Затем 1,15 мл раствора mAb (1,5 мг, 10 нмоль, 1 экв.) разделяли на аликвоты во флакон с последующим добавлением исходного раствора x-малеимид-PEG-BCN (10 мM исходный раствор в DMAc, 20 нмоль, 2 экв.). Реакционную смесь кратковременно встряхивали и инкубировали в течение 1 ч. при 22°C с последующим добавлением N-ацетилцистеина (10 мкл 100 мM раствора в воде, 1 мкмоль, 100 экв.) и дополнительно инкубировали в течение 15 минут, чтобы погасить не вступивший в реакцию малеимид. Все реакции конъюгации выполняли при комнатной температуре (22oC) в атмосфере окружающей среды. Отметим, что 2 экв. x-малеимид-PEG-BCN относительно mAb=1 экв. x-малеимид-PEG-BCN относительно свободного цистеина, содержащегося в mAb. Эту общую процедуру модифицировали по мере необходимости для достижения желаемой стехиометрии реакции (т.e. начальные растворы с различным малеимид:mAb). Конъюгаты анализировали с помощью масс-спектрометрии восстановленных и гликозилированных продуктов и эффективность конъюгации определяли с использованием уравнения 1.
Пример 44 Масс-спектрометрический анализ конъюгата N-фенилмалеимид-PEG-BCN-mAb
Типичные данные масс-спектрометрии для конъюгата N-фенил-PEG-BCN-mAb, полученного с 4 эквивалентами сшивающего средства, показаны на Фигуре 31 и в Таблице 25:
N-фенилмалеимид-PEG-BCN конъюгирован эффективно и специфично с mAb, содержащим мутацию T289C. Дополнительной конъюгации не наблюдалось на тяжелой цепи или легкой цепи до 10 молярных эквивалентов сшивающего средства.
Пример 45 Масс-спектрометрический анализ конъюгата N-фторфенилмалеимид-PEG-BCN-mAb
Типичные данные масс-спектрометрии для конъюгата N-фторфенил-PEG-BCN-mAb, полученного с 4 эквивалентами сшивающего средства, на Фигуре 32 и в Таблице 26:
N-фторфенилмалеимид-PEG-BCN конъюгирован эффективно и специфично с mAb, содержащим мутацию T289C. Дополнительной конъюгации не наблюдалось на тяжелой цепи или легкой цепи до 10 молярных эквивалентов сшивающего средства.
Пример 46 Масс-спектрометрический анализ конъюгата N-алкилмалеимид-PEG-BCN-mAb
Краткое описание данных масс-спектрометрии для конъюгата N-алкил-PEG-BCN-mAb, полученного с 4 эквивалентами сшивающего средства, на Фигуре 33 и ниже:
N-алкилмалеимид-PEG-BCN конъюгирован эффективно и специфично с mAb, содержащим мутацию T289C. Дополнительной конъюгации не наблюдалось на тяжелой цепи или легкой цепи до 10 молярных эквивалентов сшивающего средства.
Пример 47 Эффективность конъюгации x-малеимид-PEG-BCN с mAb T289C
Результаты показаны на Фигуре 35. Все сшивающие средства эффективно конъюгировали с mAb, содержащим мутацию T289C. Полная конъюгация наблюдается выше 2 эквивалентов малеимида.
Пример 48 Кинетика гидролиза тиосукцинимида для конъюгатов PEG-BCN
Конъюгаты x-малеимид-PEG-BCN-mAb инкубировали в буферных растворах и контролировали с помощью LC/MS во времени для наблюдения гидролиза тиосукцинимида. Конъюгированные mAb T289C разбавляли до 0,22 мг/мл 1X PBS, содержащим 0,5 мM EDTA, pH 7,2, и затем добавляли дитиотреитол (0,5 M исходный раствор в воде) до достижения конечной концентрации 42 мM. Образцы помещали в автоматический пробоотборник LC/MS при 22°C и периодически вводили. Гидролиз тиосукцинимида подтверждали добавлением 18 а.е.м. к пику конъюгата mAb в масс-спектре. Полуколичественный анализ гидролиза проводили с использованием интенсивностей пиков в масс-спектрах после деконволюции и уравнения 3, который включает вычитание фона с использованием измерения Т=0. Затем данные превращали в потерю тиосукцинимида (М) с течением времени и наносили на график в виде ln [тиосукцинимида] против секунд. Наклон линии наилучшего соответствия дал константу скорости псевдо-первого порядка для гидролиза тиосукцинимида. Эти результаты показаны на Фигуре 36 и в Таблице 28.
Конъюгаты х-малеимид-PEG-BCN гидролизуются с аналогичной тенденцией, которая наблюдается для конъюгатов PEG-биотин; т.e. F-фенилтиосукцинимид>фенилтиосукцинимид>>алкилтиосукцинимид.
Пример 49 Последовательное добавление полезных нагрузок к mAb T289C
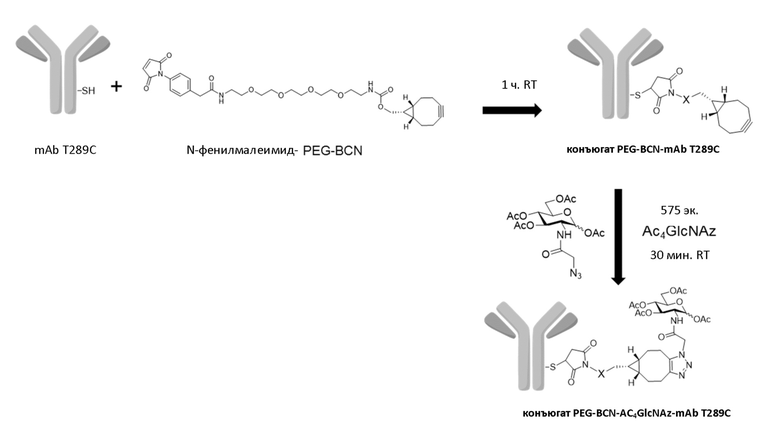
Конъюгат N-фенилмалеимид-PEG-BCN-mAb (100 мкл раствора 1,3 мг/мл в PBS с 0,5 мM EDTA, 0,87 нмоль) объединяли с AC4GlcNAz (1 мкл 500 мM исходного раствора в DMSO, 500 нмоль). Реакционный раствор инкубировали при комнатной температуре без перемешивания в течение 1 ч. при 22°С. Для исследований долговременной реакционной способности конъюгат mAb-BCN хранили при 4°C в PBS с 0,5 мМ EDTA, pH 7,2, и аликвоты удаляли и подвергали взаимодействию с AC4GlcNAz, как описано выше. Конъюгаты анализировали с помощью масс-спектрометрии восстановленных и гликозилированных продуктов и эффективность конъюгации определяли с использованием уравнения 1.
Анализ конъюгатов mAb-BCN-Ac4GlcNAz показан на Фигуре 37. Группы BCN полностью реагировали с AC4GlcNAz.
Пример 50 Реакционноспособность конъюгата mAb-BCN после хранения
Результаты показаны на Фигуре 38 и в Таблице 29.
Таблица 29. Краткое описание реакционноспособности BCN после конъюгации сшивающего средства с mAb и хранения при 4oC
Количественная реакция BCN наблюдалась для всех образцов. Непрореагировавший mAb-BCN можно обнаружить с помощью масс-спектрометрии. Группы BCN не показали снижения реакционноспособности в течение > 21 дня после конъюгации и хранения при 4oC.
Пример 51 Конъюгация азидо-PBD с BCN-модифицированным mAb
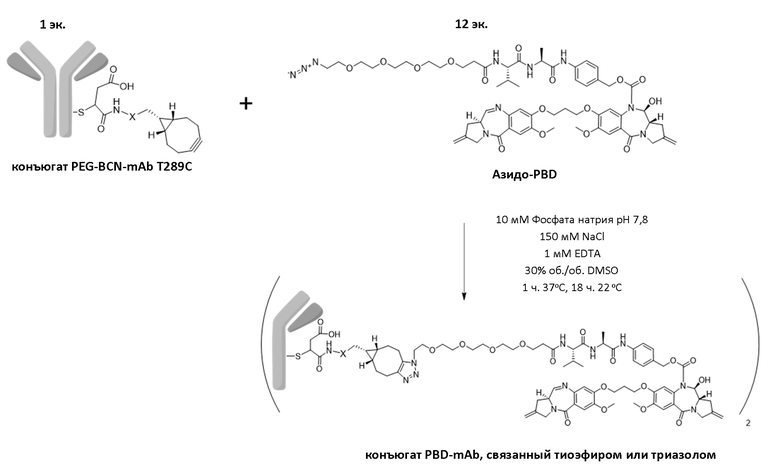
Конъюгаты N-фенилмалеимид-PEG-BCN-mAb T289C готовили, как описано выше (с 1,5 мг/мл mAb), и хранили при 4°C до реакции с азидо-PBD. Для конъюгации PBD раствор mAb сначала объединяли с DMSO для достижения конечной концентрации 30% об./об. DMSO и 1,05 мг/мл mAb-BCN. Затем раствор mAb-BCN/DMSO (1,89 мл, 13 нмоль mAb, 1 экв.) переносили в сосуд и добавляли азидо-PBD (16 мкл 10 мM исходного раствора в DMSO, 160 нмоль, 12 экв.). Реакционную смесь инкубировали при 37°C в течение одного часа и затем при 22°C в течение 18 часов. Реакционную смесь сначала очищали диализом (кассета 10 К MWCO slide-a-lyzer, 1X PBS с 0,5 мМ EDTA, pH 7,2, 4oC, 18 часов) и затем CHT-хроматографией, как описано выше. Продукты реакции анализировали с использованием масс-спектрометрии восстановленных и гликозилированных продуктов. Эффективность конъюгации и DAR рассчитывали, используя уравнение 1 и уравнение 2, соответственно.
Пример 52 Анализ конъюгатов mAb-PBD
Типичные масс-спектрометрические данные для 5T4-нацеленого конъюгата mAb T289C- N-фенилмалеимид-PEG-BCN показаны на Фигуре 38.
(%)
a) Рассчитано относительно групп BCN
b) Рассчитано относительно mAb. Непрореагировавшие mAb и mAb+BCN рассматривались как неконъюгированные
Пример 53 Активность In vitro ADC mAb-BCN-PBD относительно клеток молочной железы MDA-MB-361.
В этих исследованиях использовали клетки рака молочной железы MDA-MB-361 с высокой экспрессией 5T4. Клетки высевали в 80 мкл RPMI1640 с 10% FBS в 96-луночные плоскодонные планшеты при 2000 MDA-MB-361 клеток/лунку. Клетки оставляли на ночь для прилипания. Концентрацию 5Х каждого ADC получали разбавлением тестируемых образцов в культуральной среде. Двадцать микролитров каждого тестируемого образца добавляли к клеткам в трех повторах, так что диапазон конечной дозовой кривой составлял от 50 нг/мл до 0,76 пг/мл в серии при ступенчатом серийном разведении 1:4. Обработанные клетки культивировали при 37°C/5% CO2 в течение 6 дней и жизнеспособность клеток оценивали с помощью люминесцентного анализа жизнеспособности CellTiter-Glo от Promega. 100 мкл восстановленного реагента CTG добавляли в каждую лунку, слегка встряхивали в течение 10 минут при комнатной температуре и абсорбцию каждого образца при 560 нм считывали с использованием люминометра Perkin Elmer EnVision. Процент жизнеспособности клеток рассчитывали по следующей формуле: (средняя люминесценция обработанных образцов/средняя люминесценция необработанных контрольных образцов) × 100. Значения EC50 определяли с использованием анализа методом логистической нелинейной регрессии с помощью программного обеспечения GraphPad Prism.
Результаты показаны на Фигуре 40 и в Таблице 25.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАТЕРИАЛЫ И СПОСОБЫ, СВЯЗАННЫЕ С ЛИНКЕРАМИ ДЛЯ ПРИМЕНЕНИЯ В КОНЪЮГАТАХ ЛЕКАРСТВЕННОГО СРЕДСТВА И БЕЛКА | 2015 |
|
RU2737553C2 |
| СПОСОБЫ КОНЪЮГАЦИИ АГЕНТА С ТИОЛЬНЫМ КОМПОНЕНТОМ В БЕЛКЕ, КОТОРЫЙ СОДЕРЖИТ ПО МЕНЬШЕЙ МЕРЕ ОДНУ ТРИСУЛЬФИДНУЮ СВЯЗЬ | 2015 |
|
RU2744978C2 |
| СПОСОБ ДВОЙНОЙ КОНЪЮГАЦИИ ДЛЯ ПОЛУЧЕНИЯ КОНЪЮГАТОВ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2018 |
|
RU2771310C2 |
| КОНЪЮГИРОВАННЫЕ ИММУНОГЛОБУЛИНЫ С C-КОНЦЕВЫМ ЛИЗИНОМ | 2016 |
|
RU2747581C2 |
| КОНЪЮГАТЫ МЕЧЕННЫХ РАДИОАКТИВНЫМ ЦИРКОНИЕМ СКОНСТРУИРОВАННЫХ АНТИТЕЛ С ЦИСТЕИНОВЫМИ ЗАМЕНАМИ | 2010 |
|
RU2562862C2 |
| СПОСОБЫ КОНЪЮГАЦИИ | 2010 |
|
RU2765240C2 |
| КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, НАГРУЖЕННЫЙ БИНАРНЫМИ ТОКСИНАМИ, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2795148C2 |
| КОНЪЮГАТ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА, КОМПОЗИЦИИ НА ЕГО ОСНОВЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2728235C2 |
| САЙТ-СПЕЦИФИЧЕСКАЯ КОНЪЮГАЦИЯ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО ПОСРЕДСТВОМ ГЛИКОИНЖЕНЕРИИ | 2014 |
|
RU2711935C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2436796C9 |
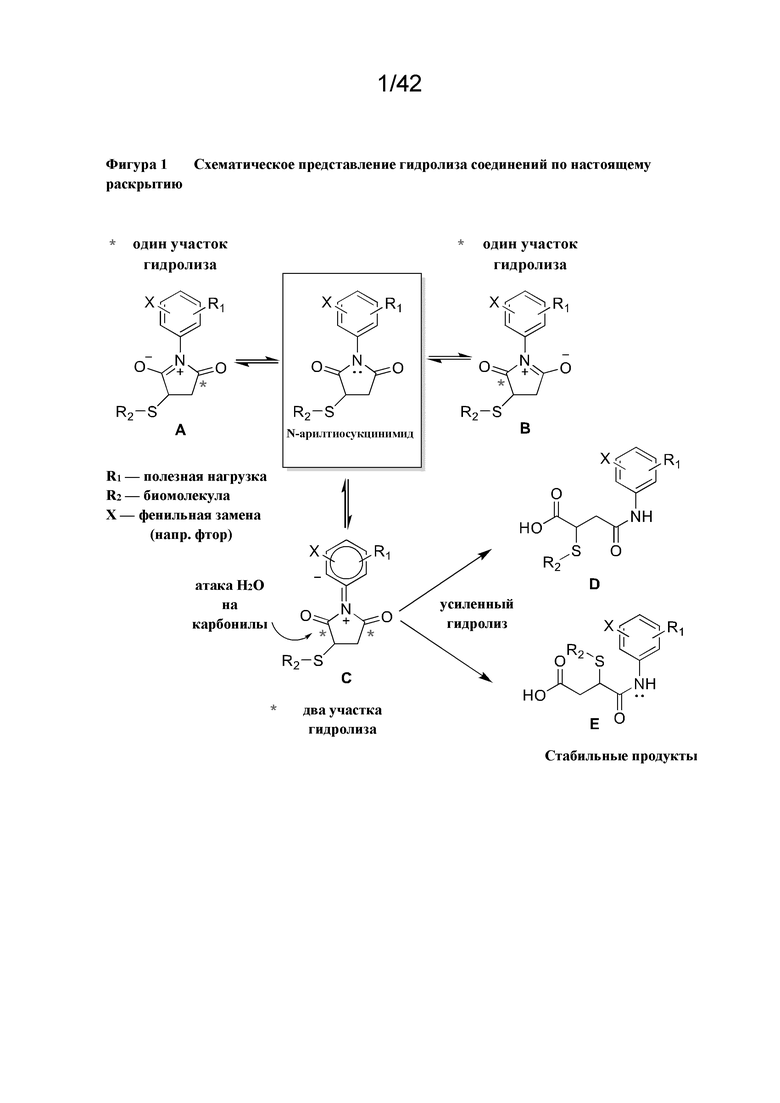
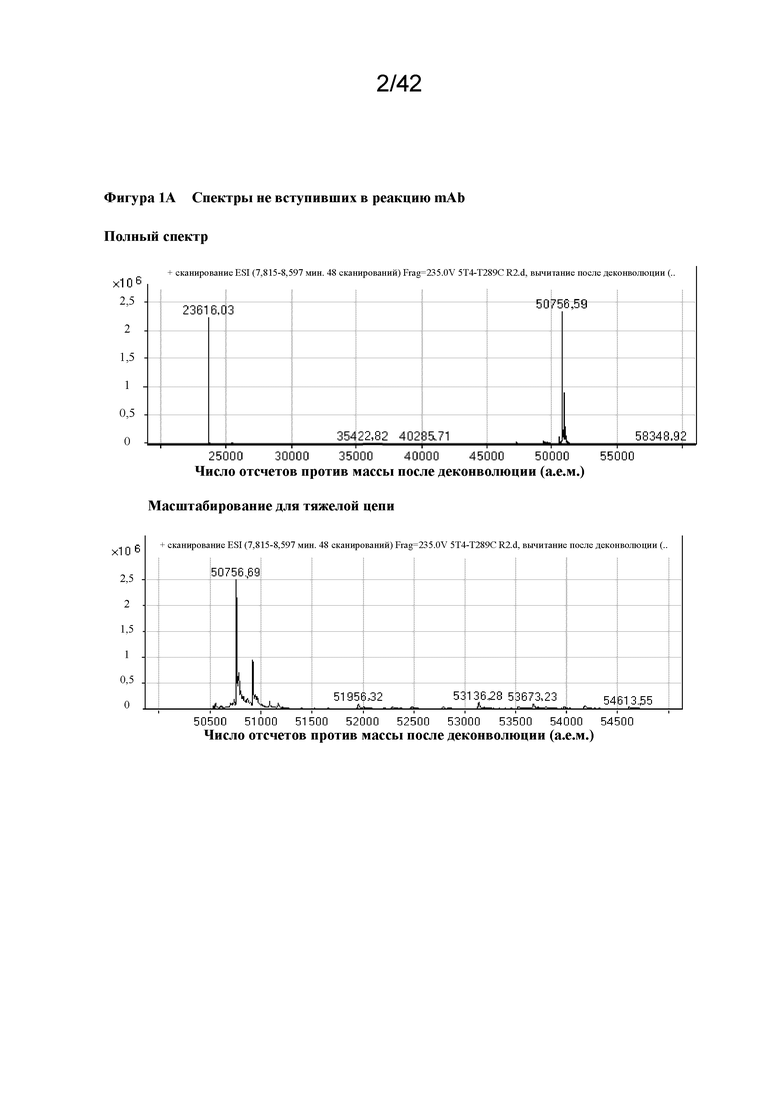
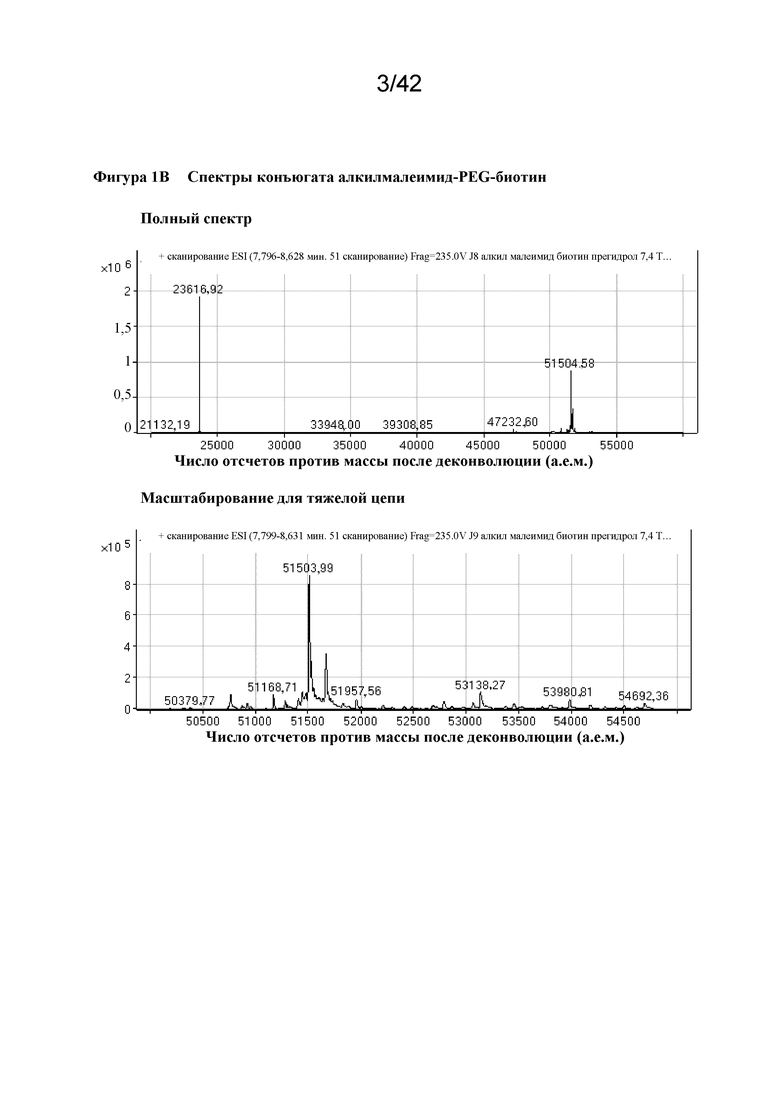
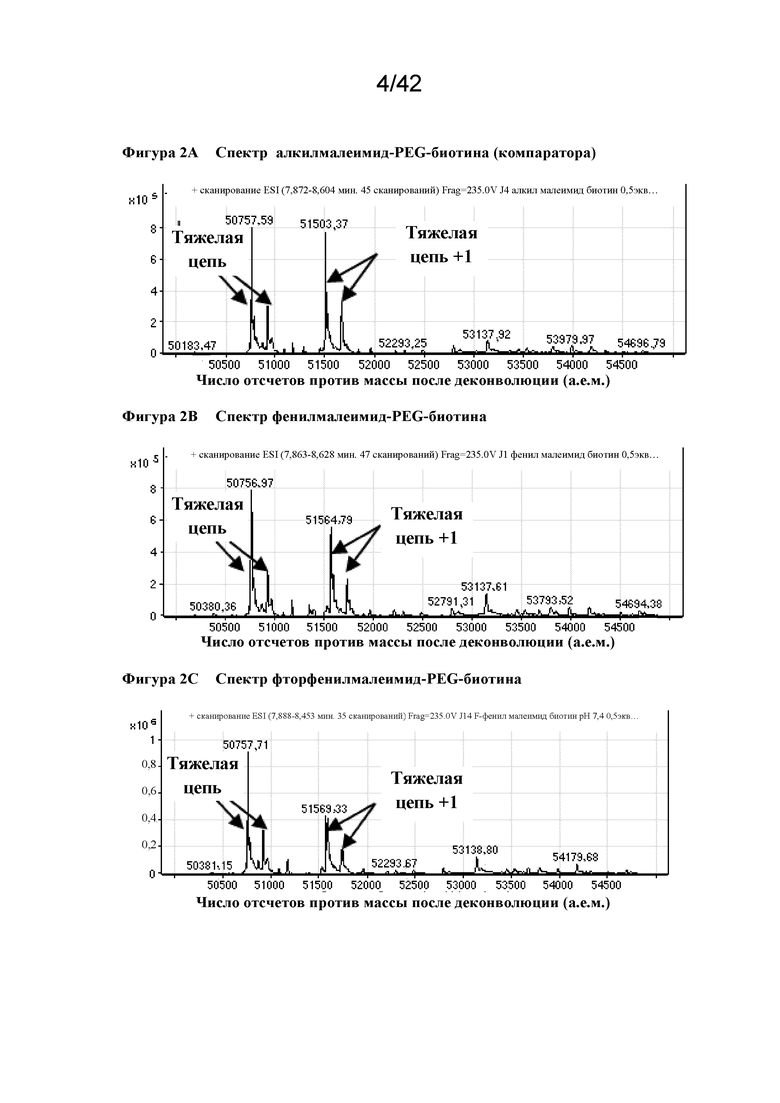
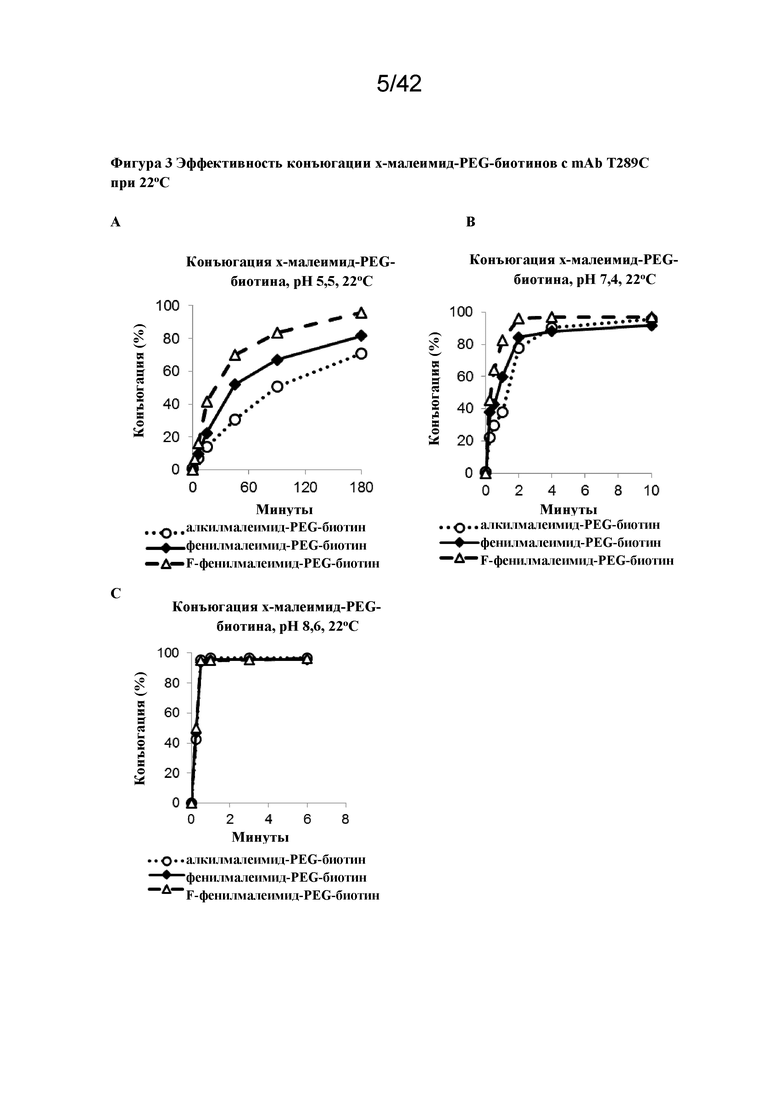
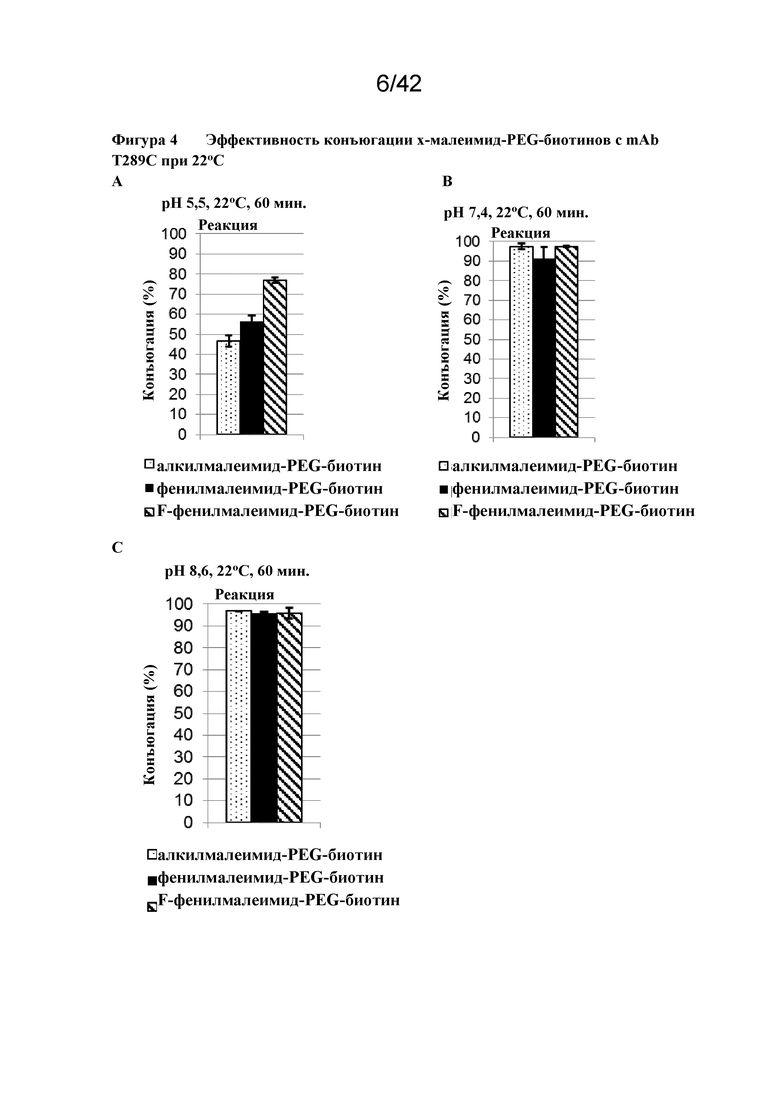
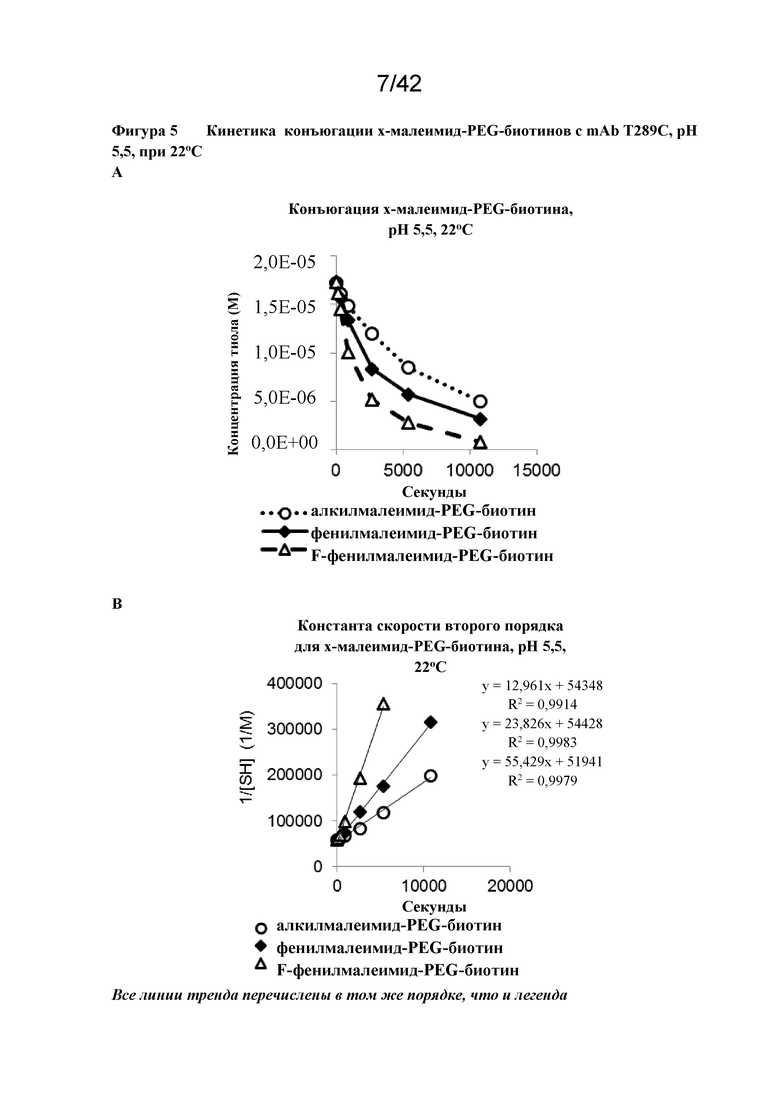
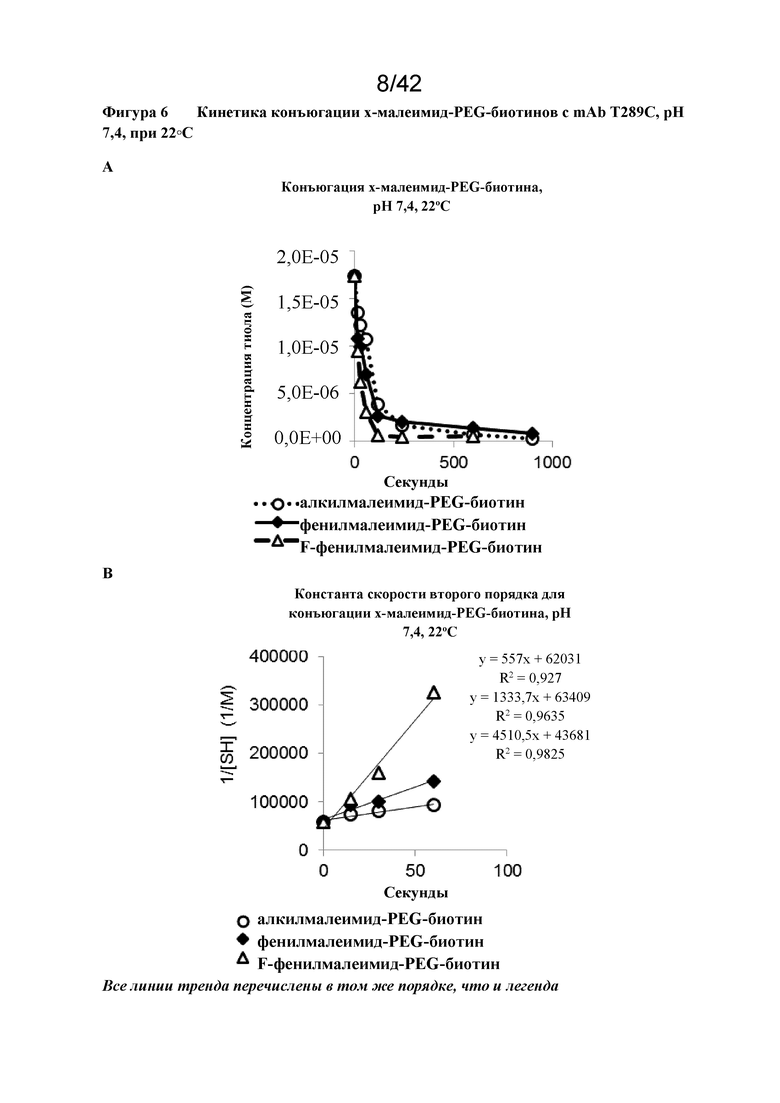
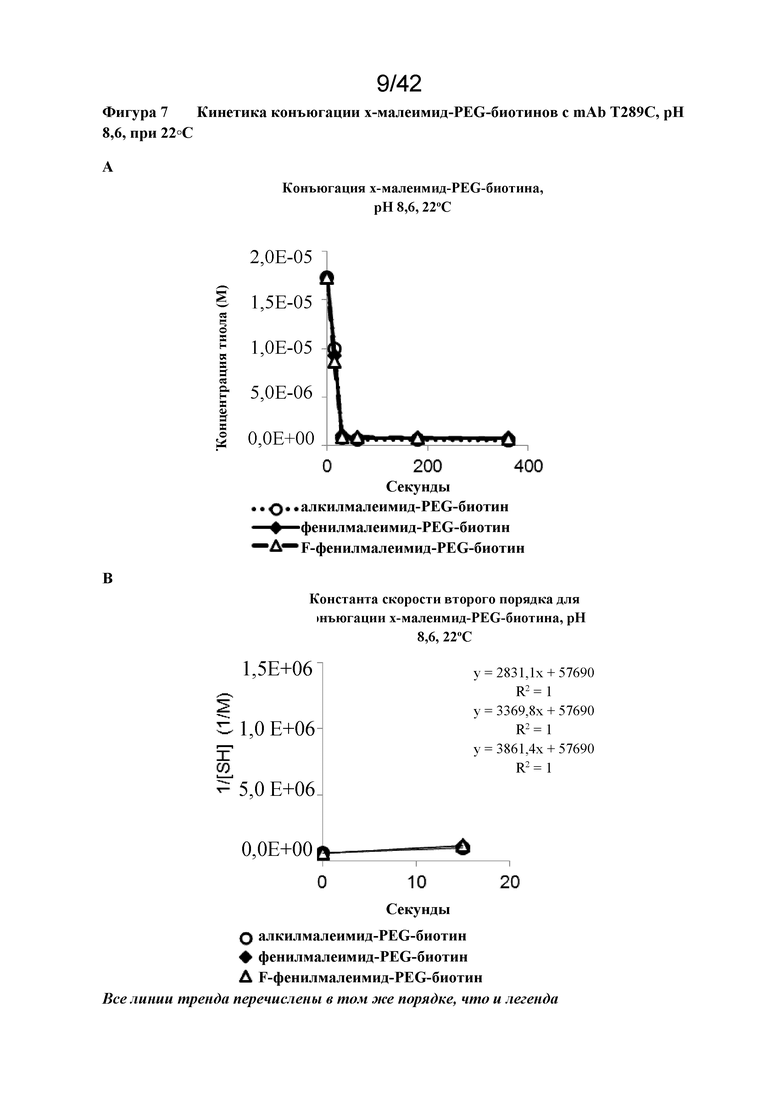
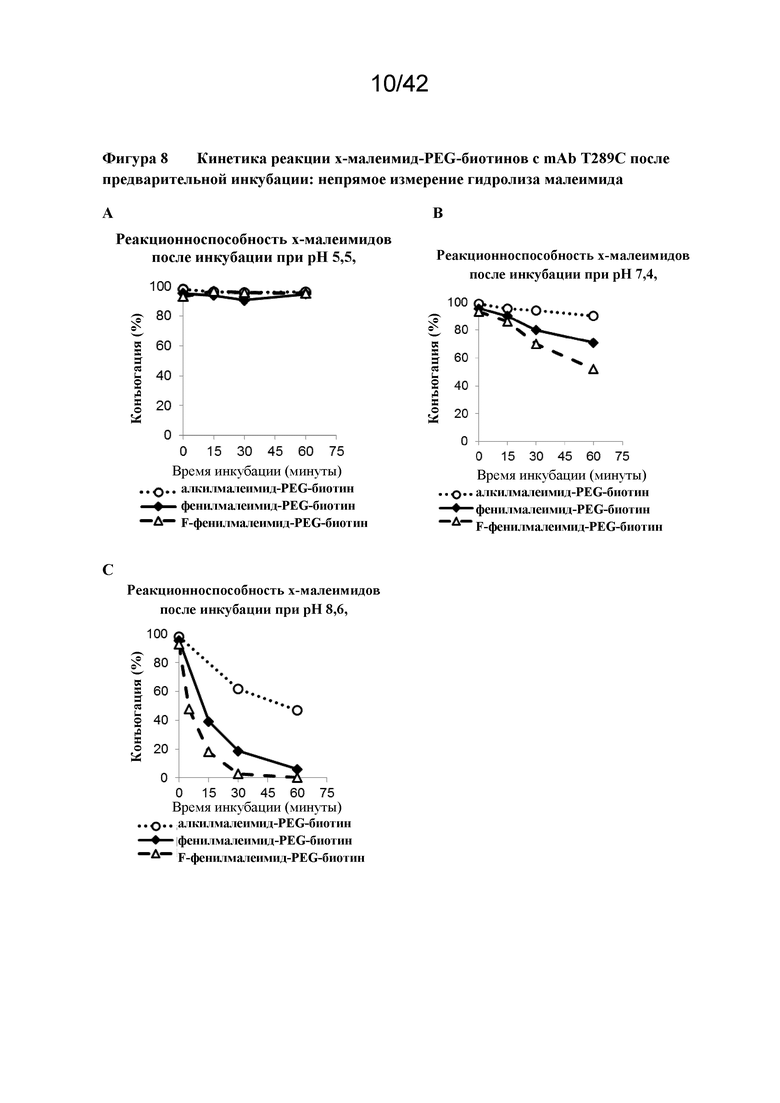
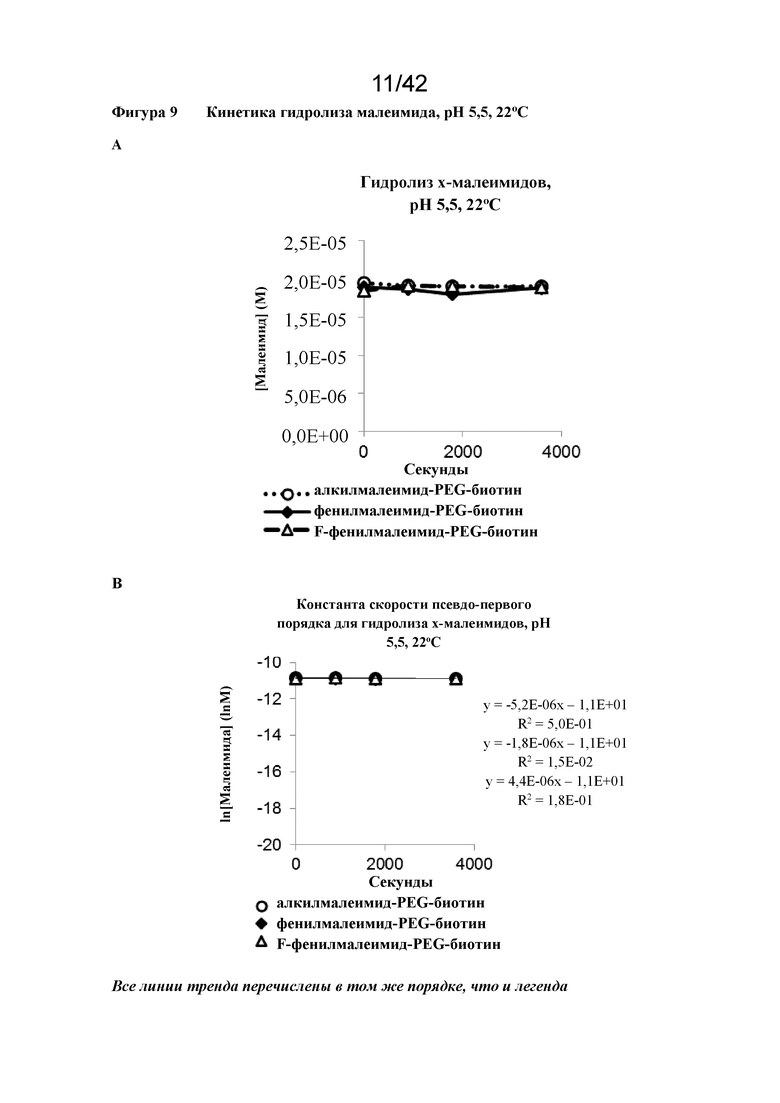
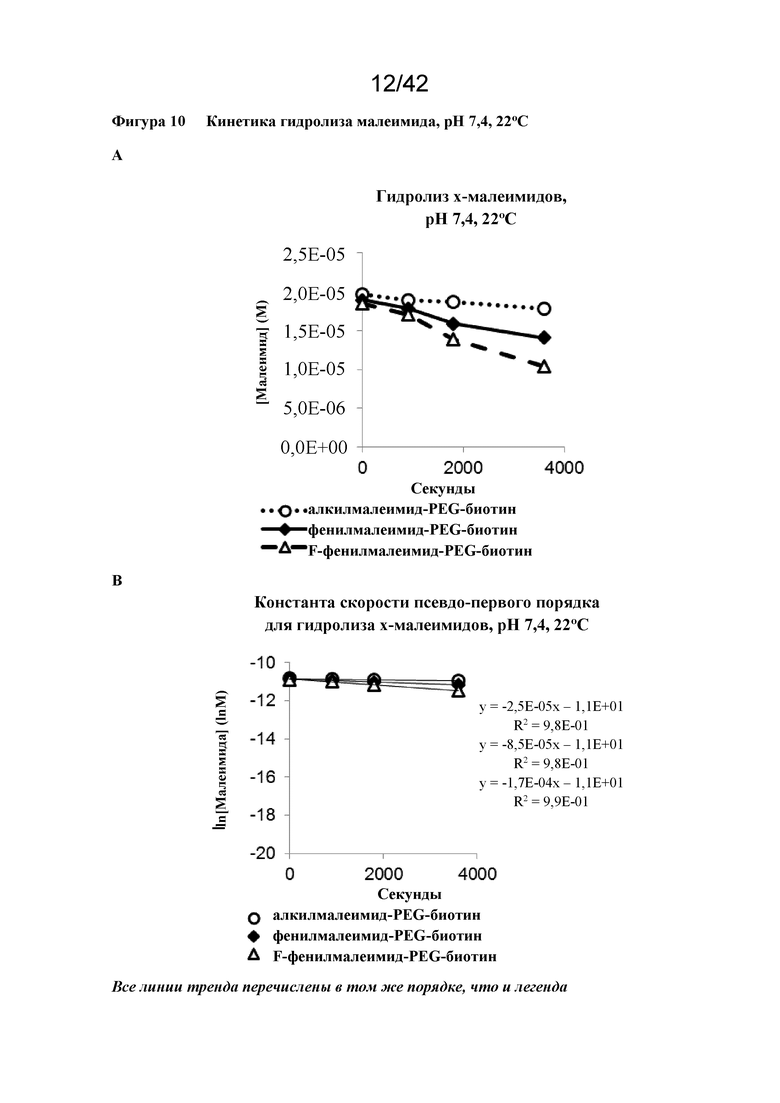
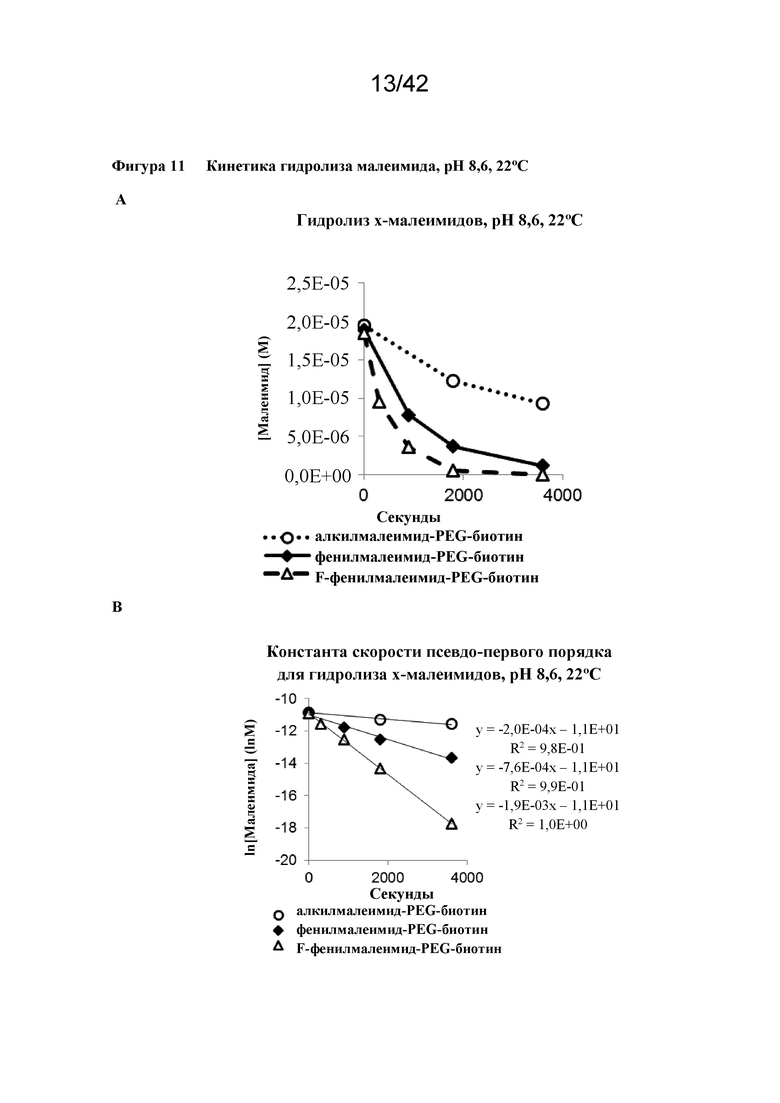
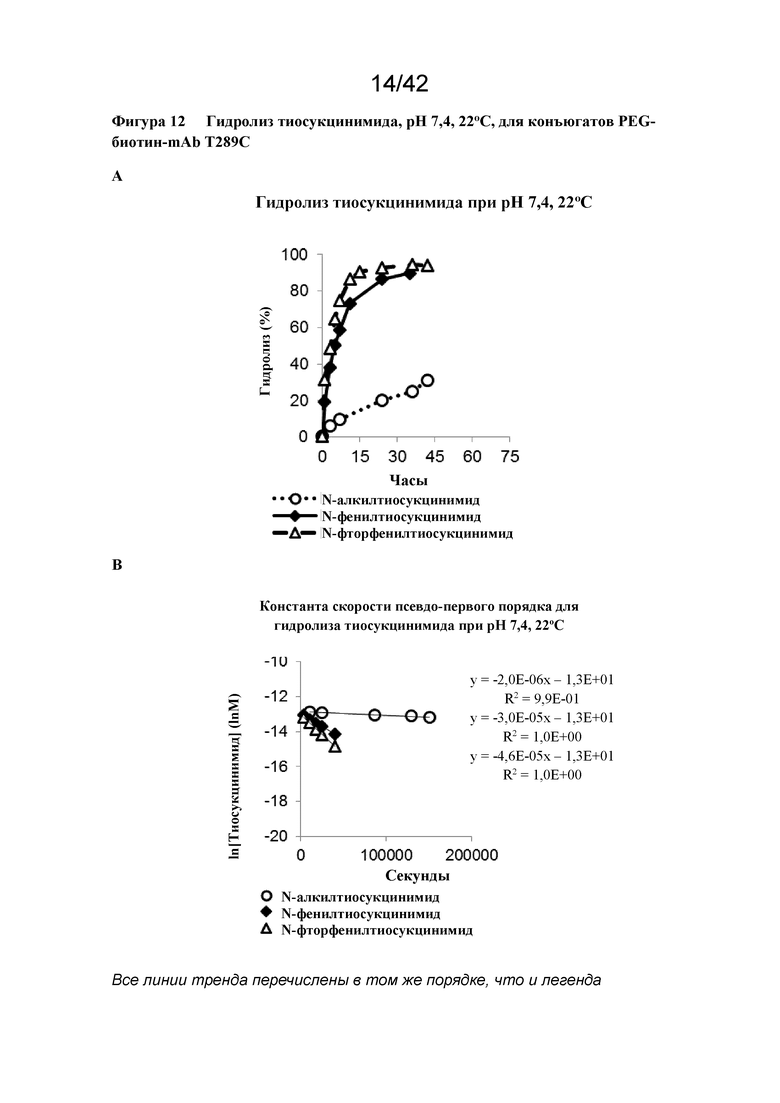
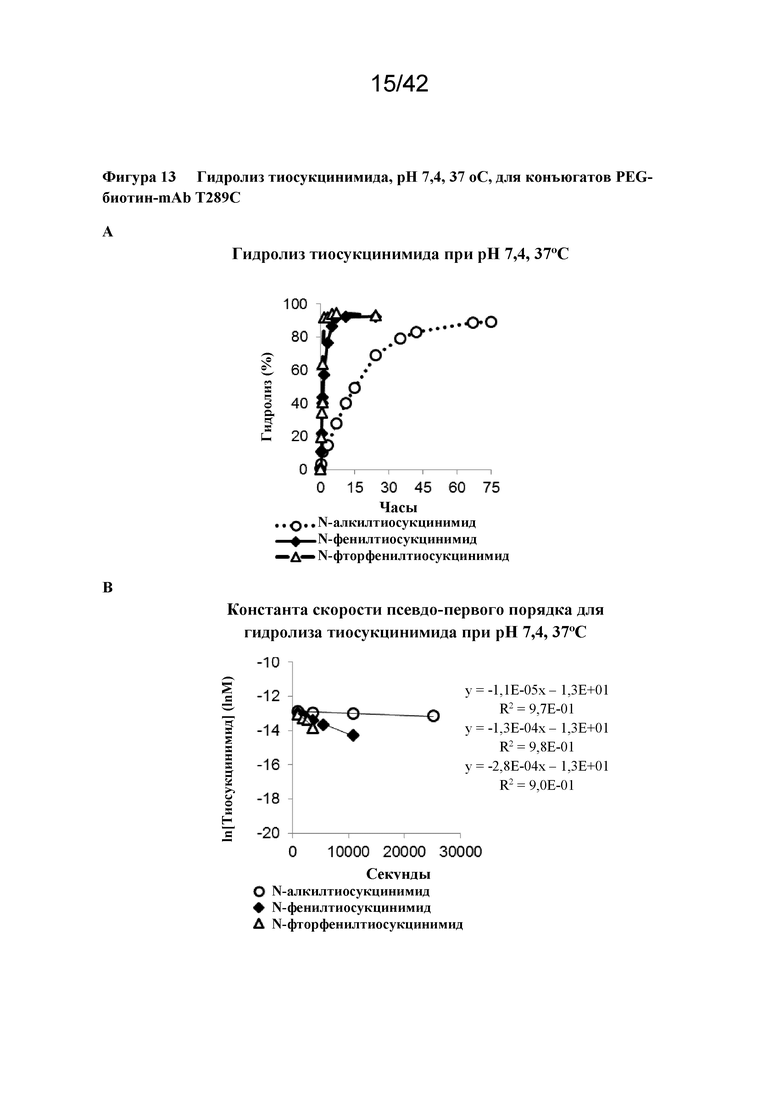
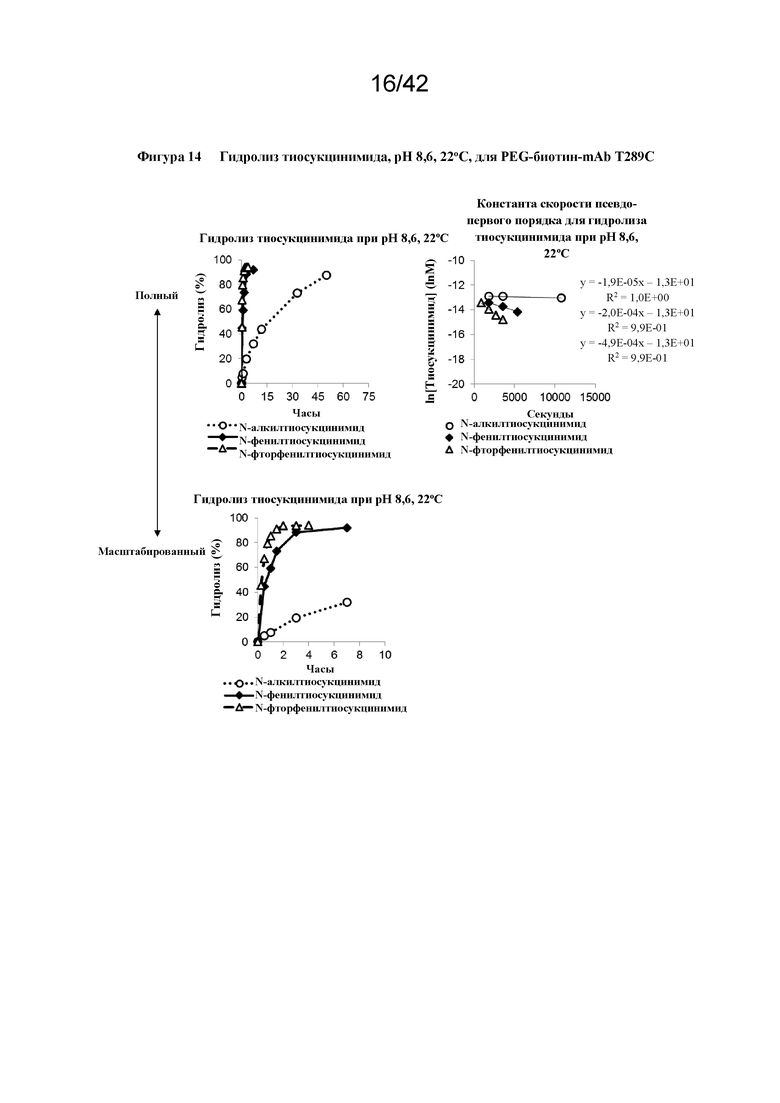
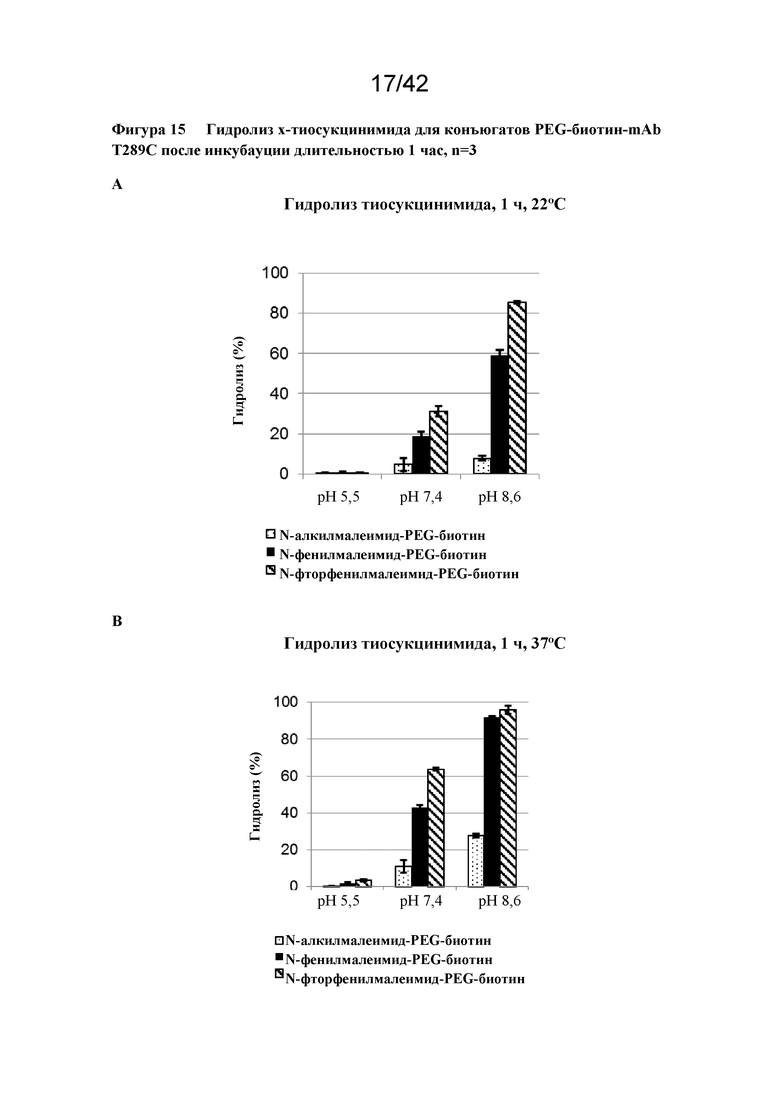
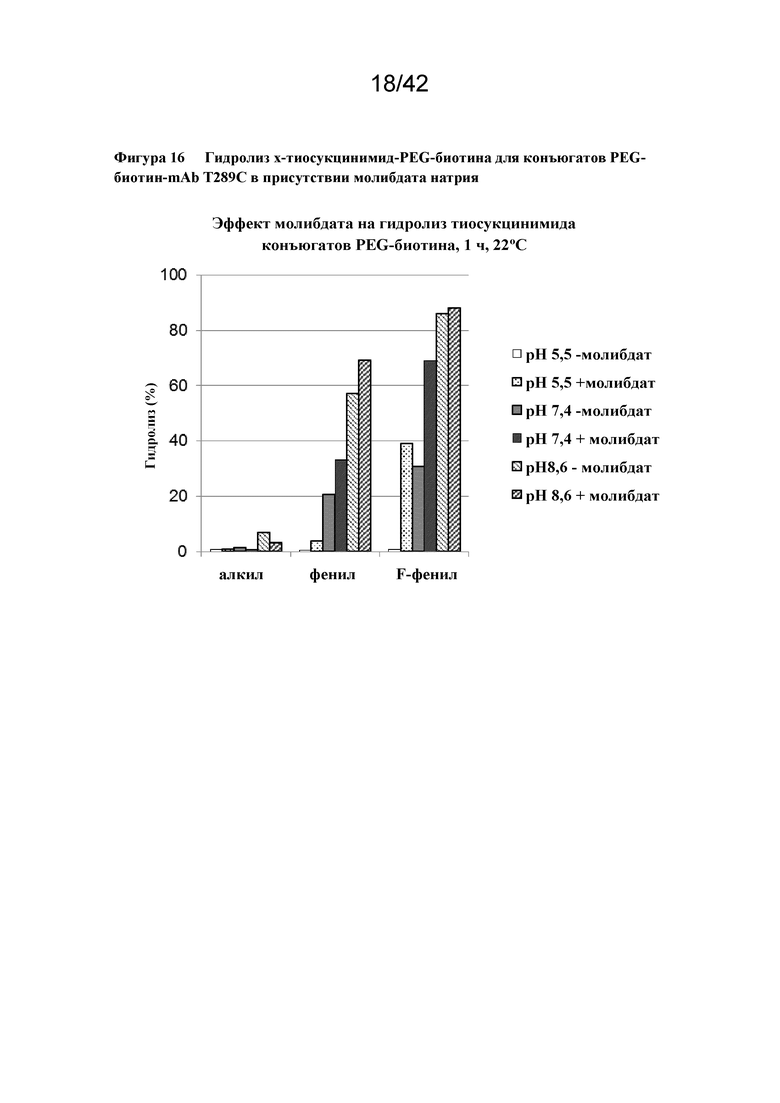

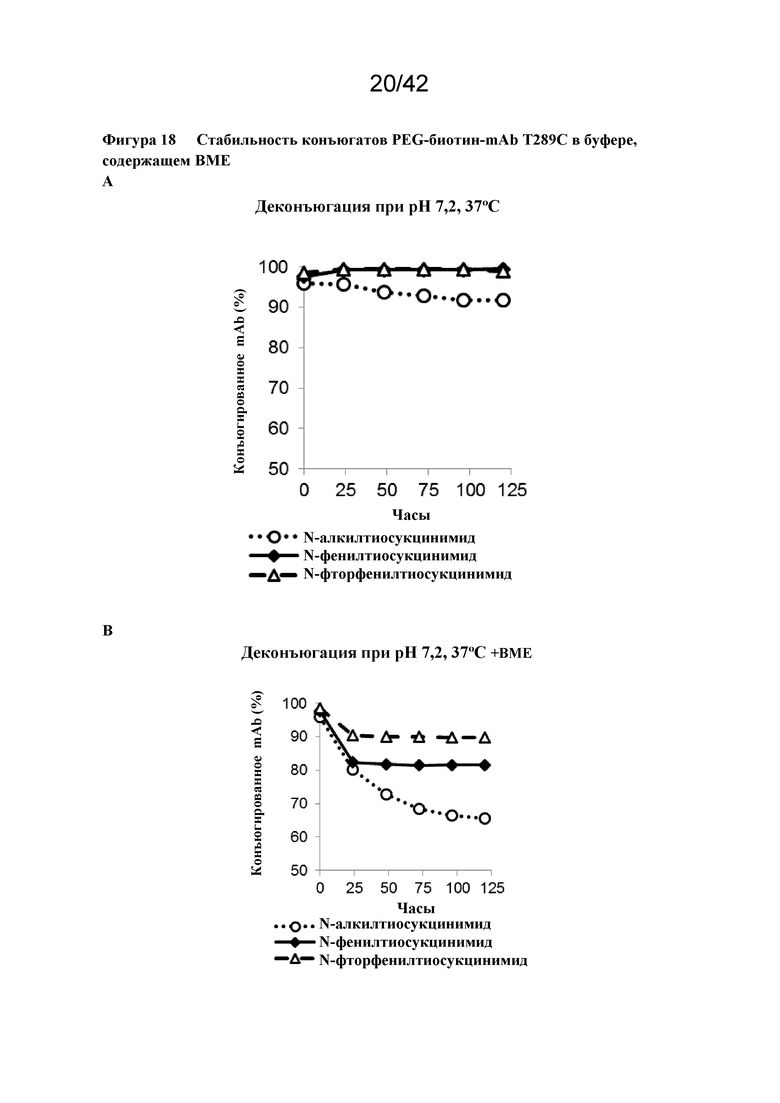
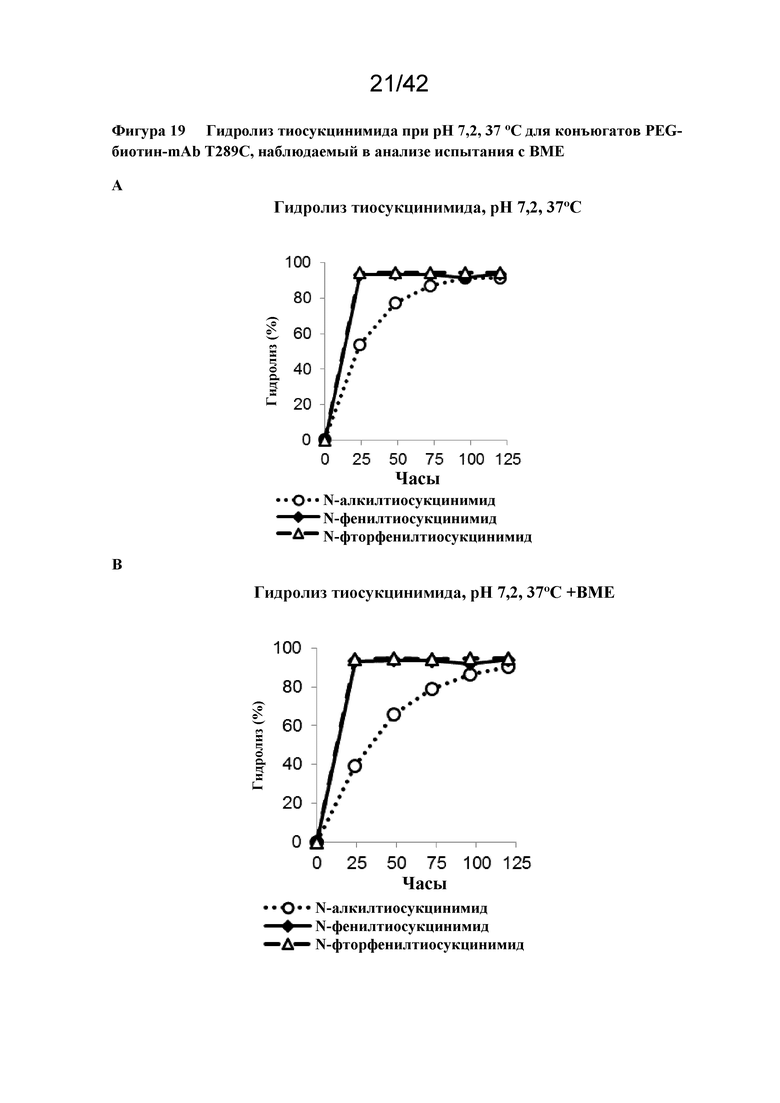
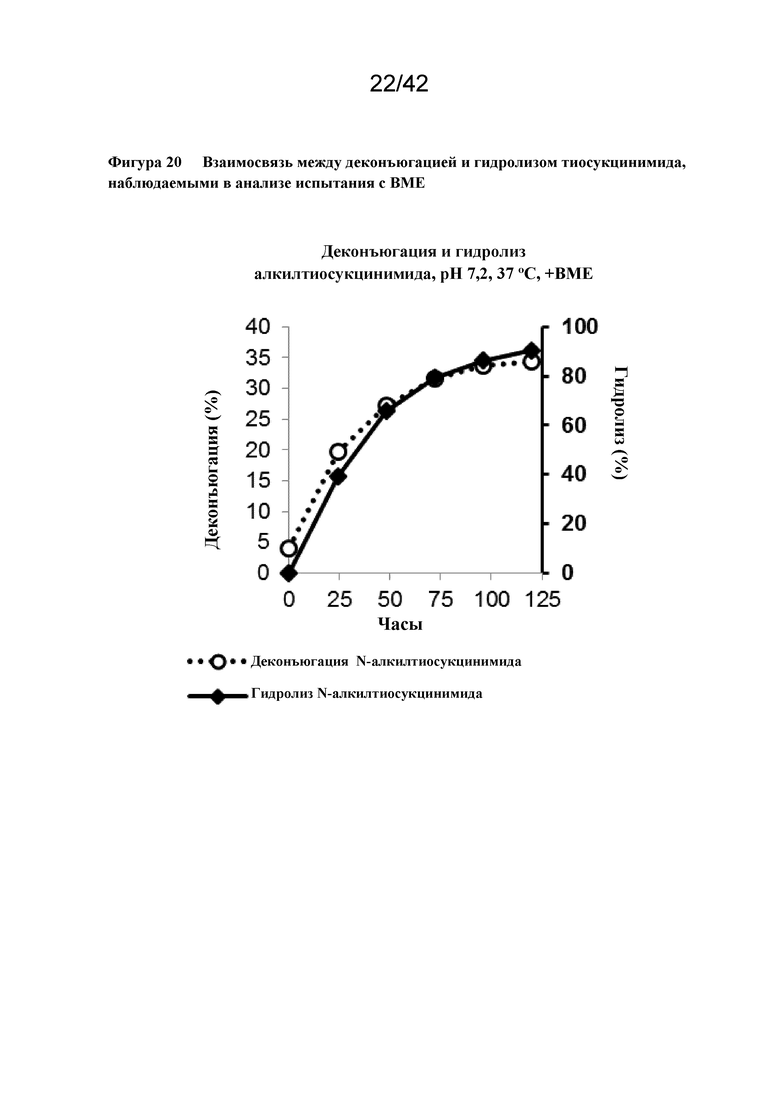
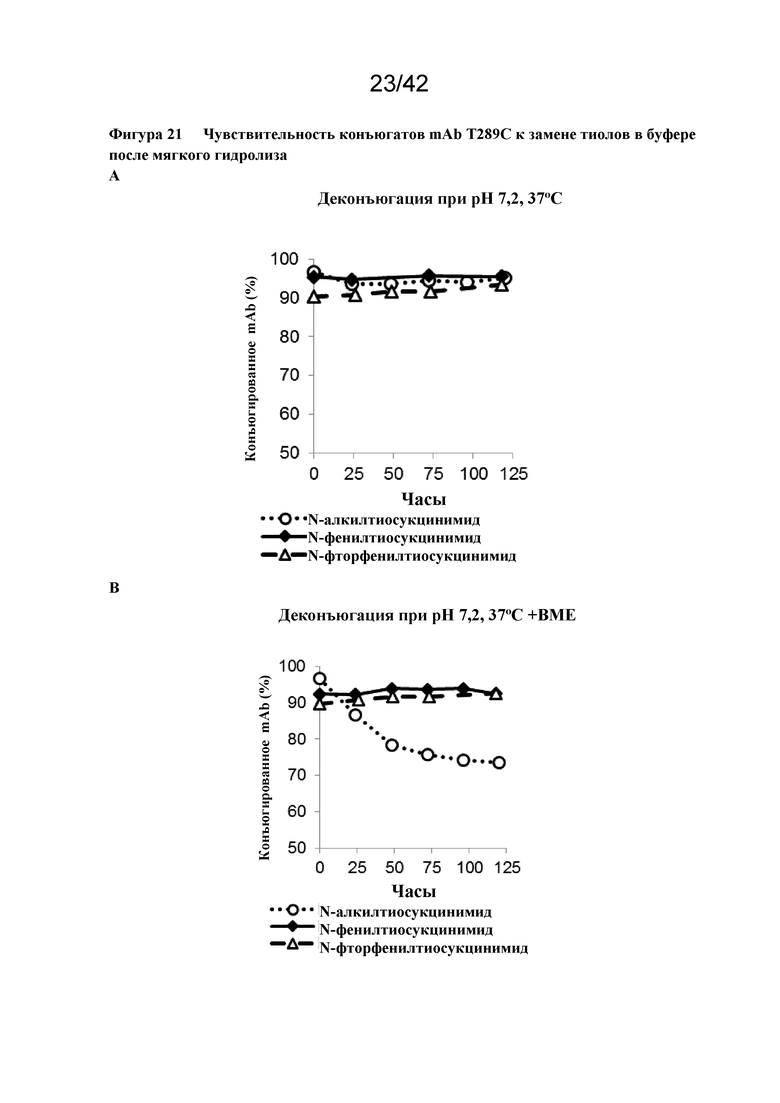

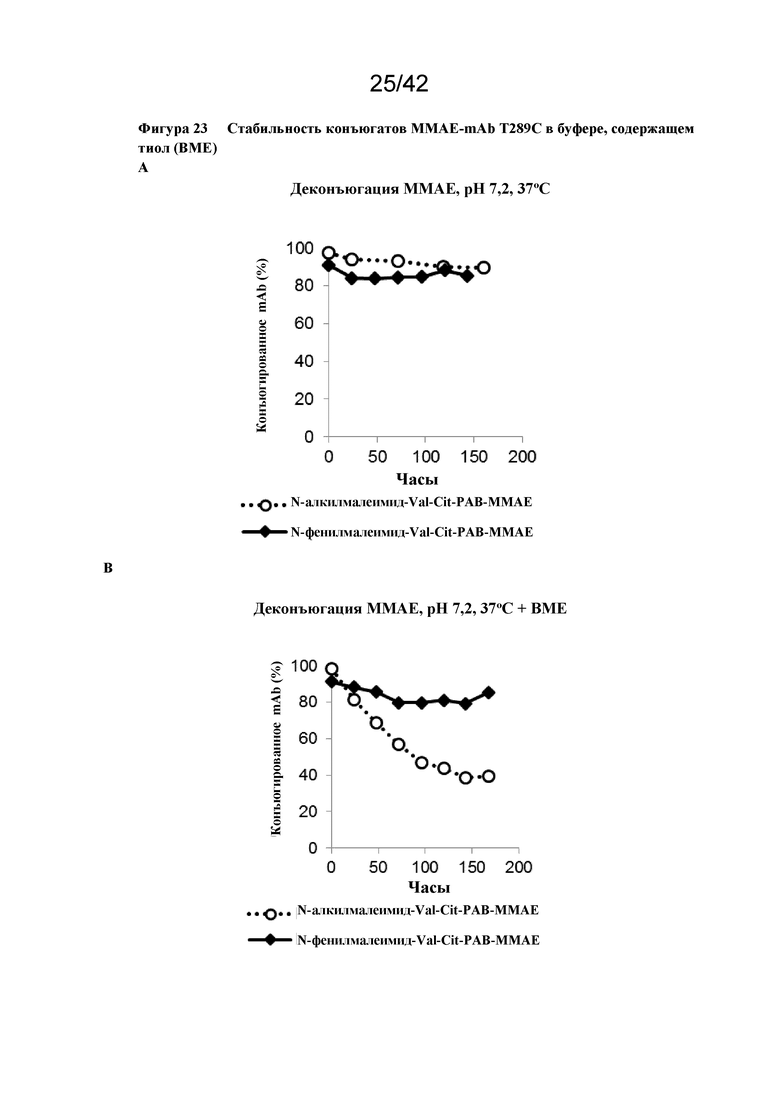
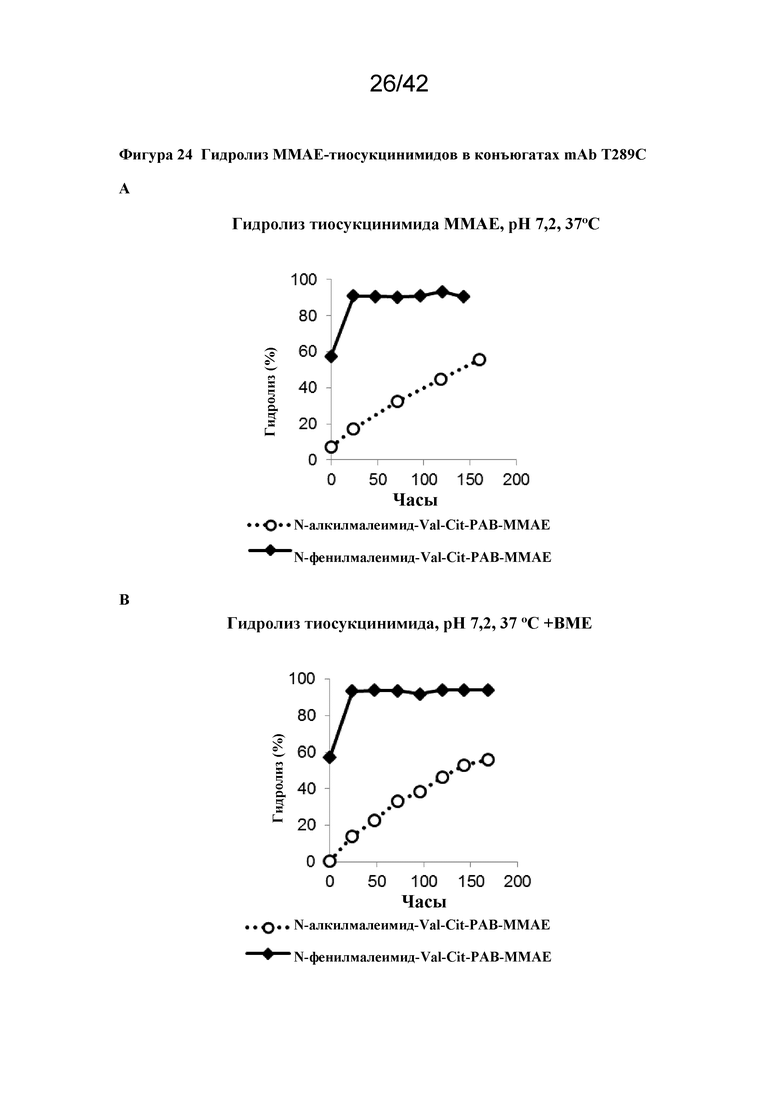
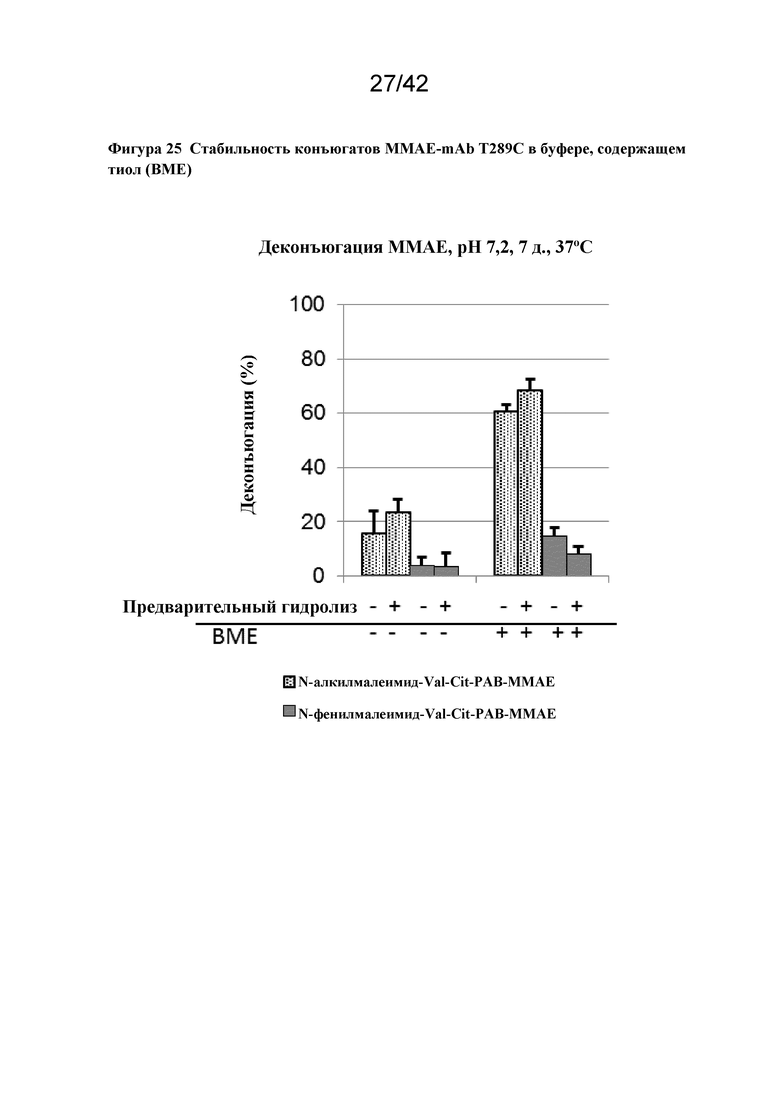
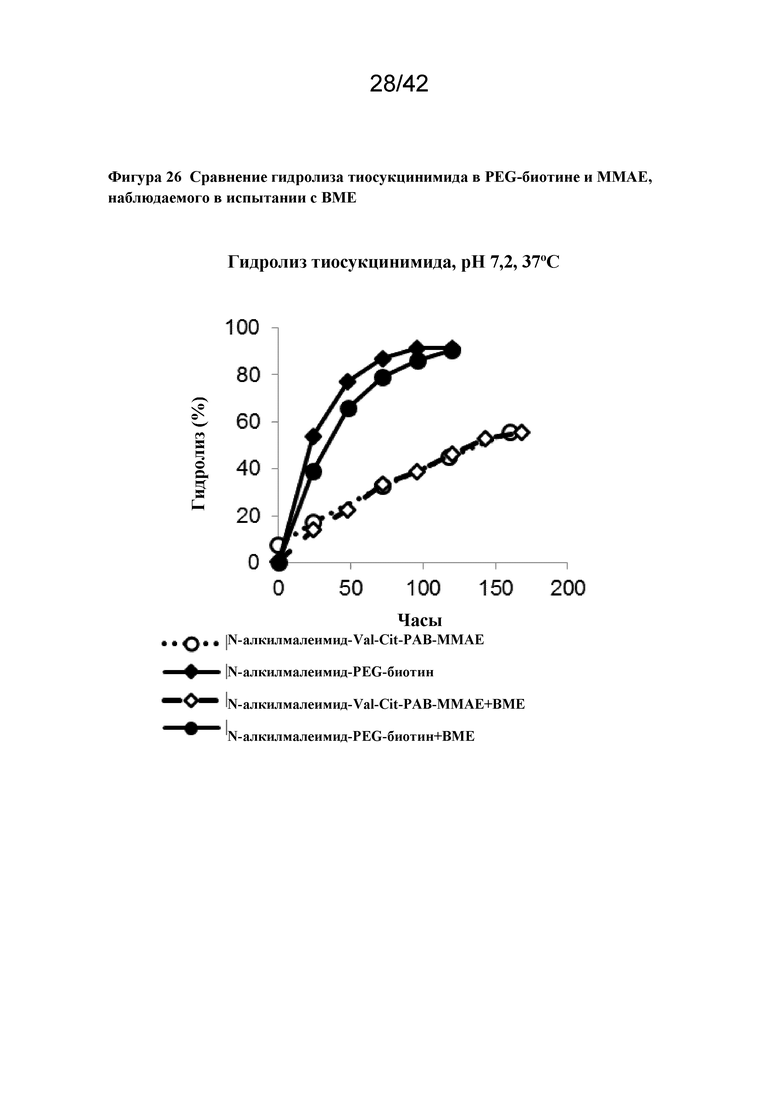
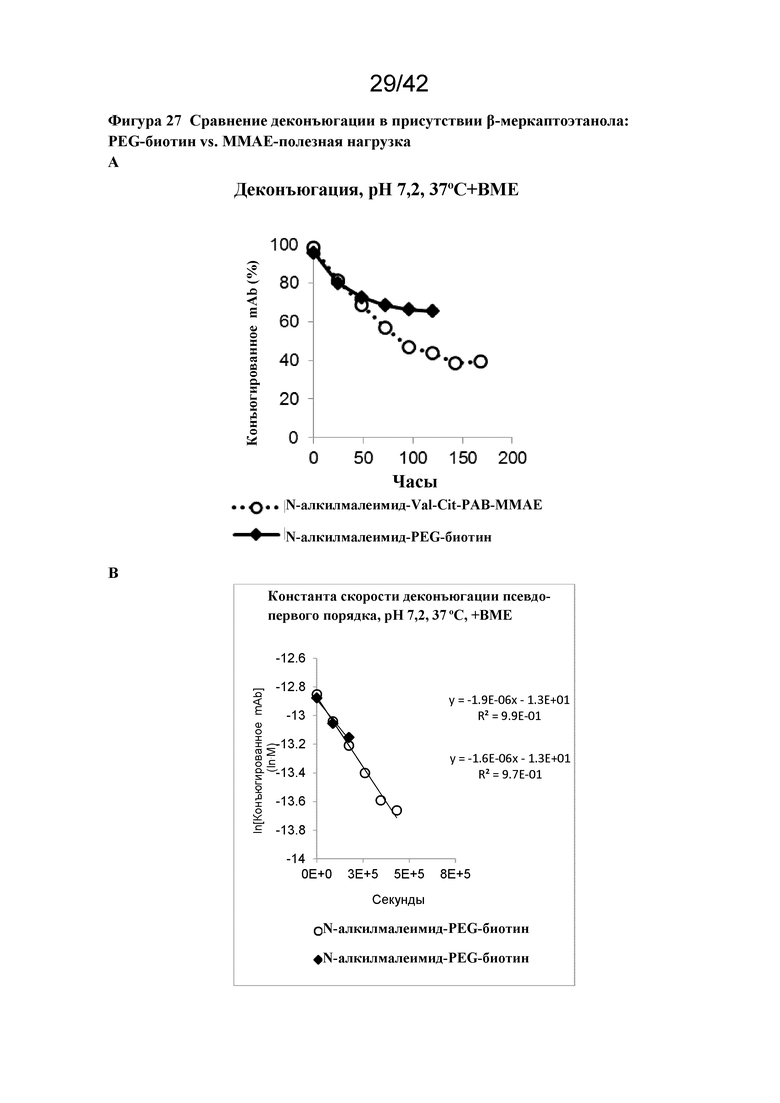
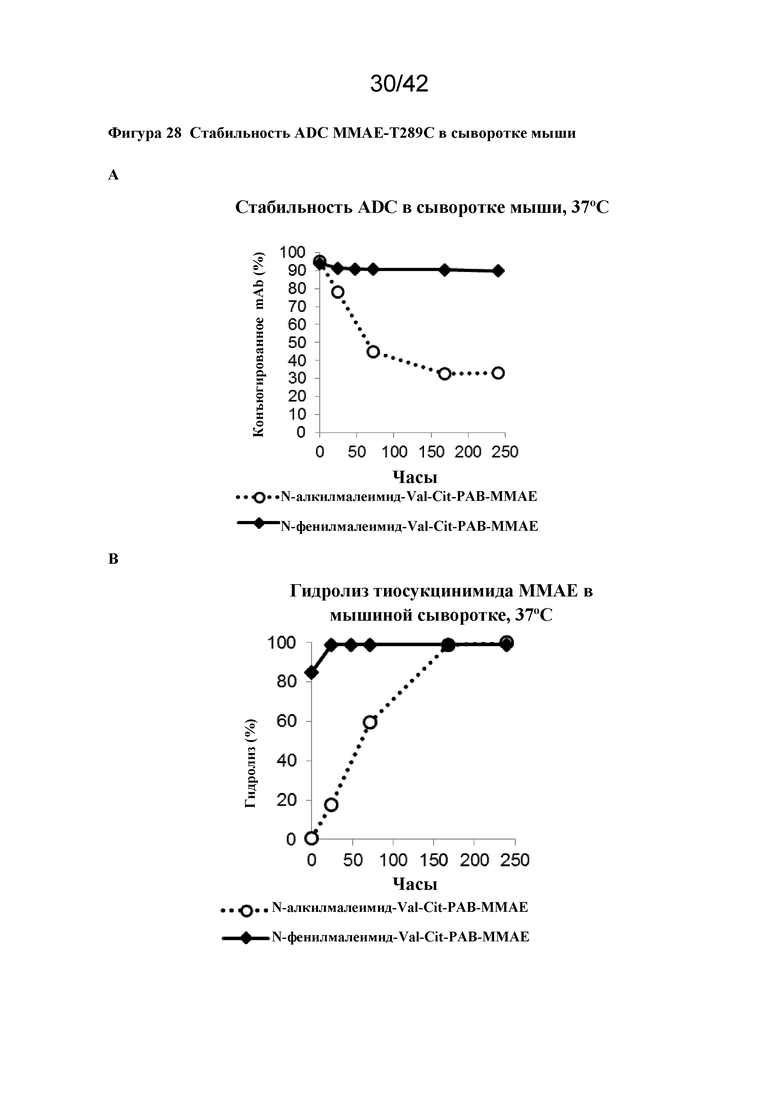
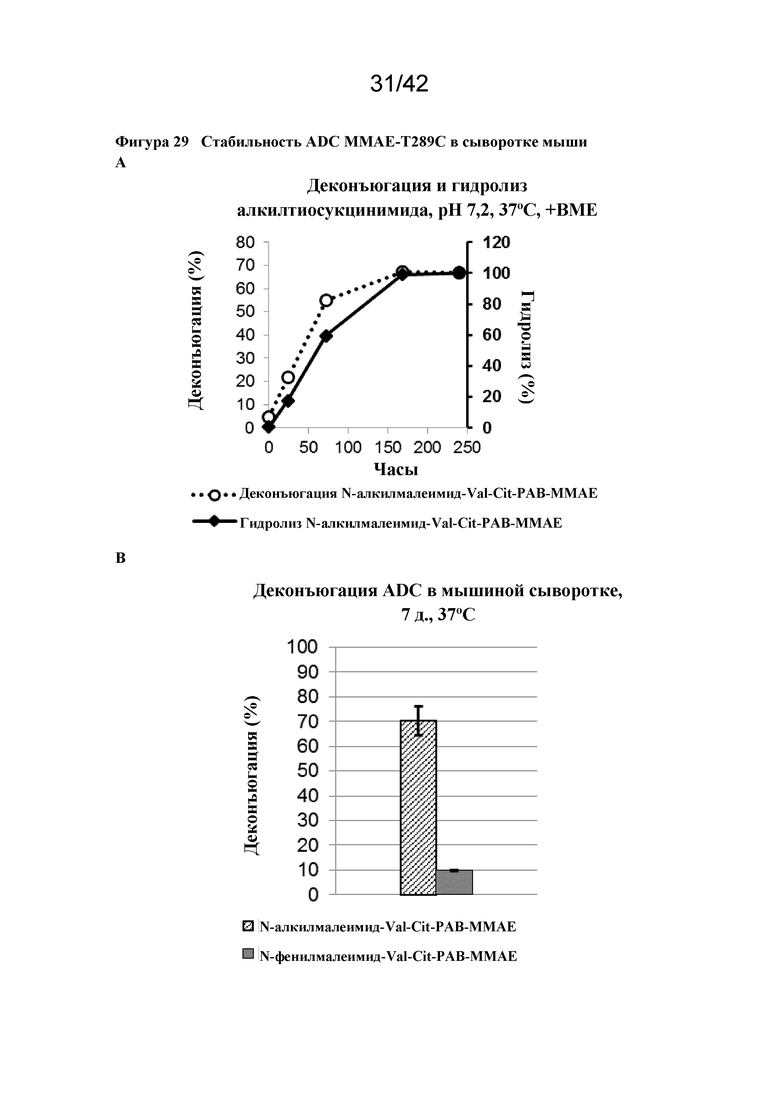
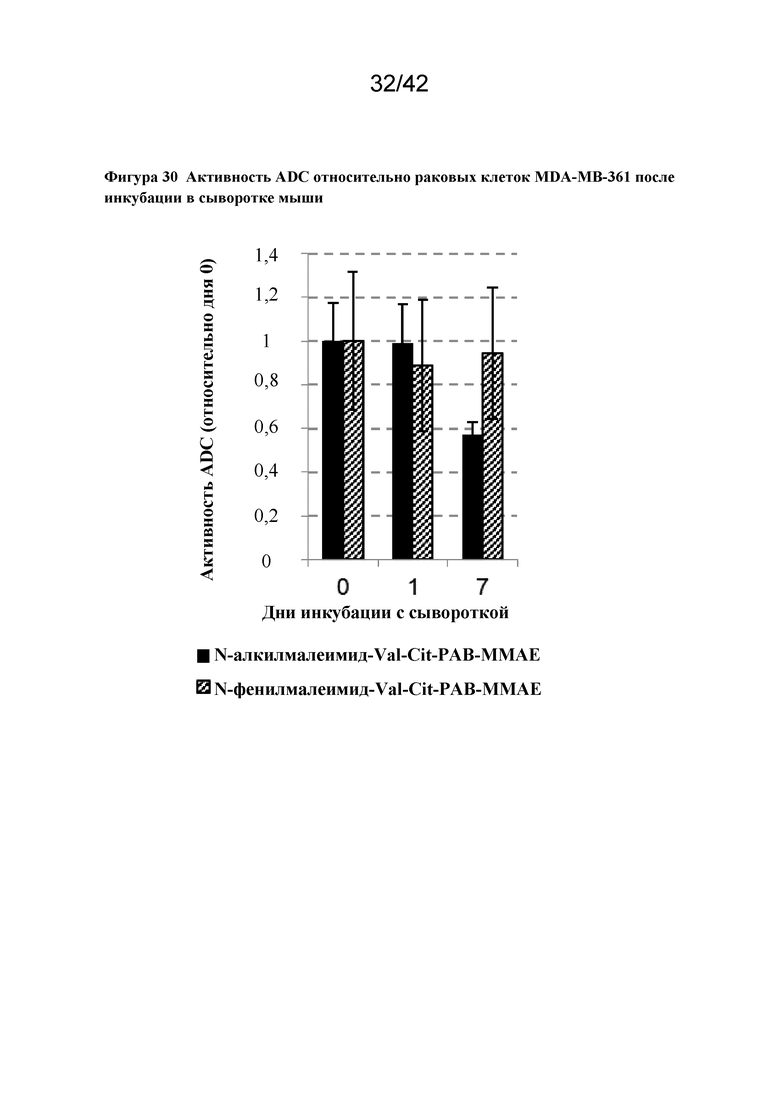



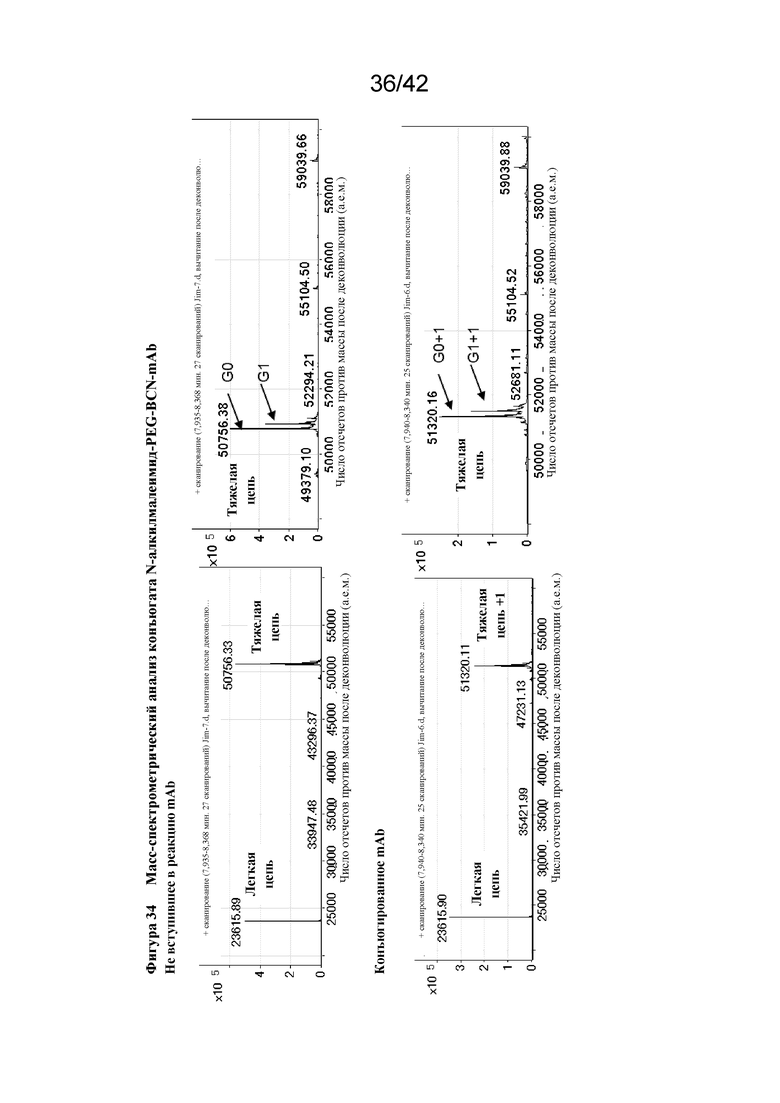
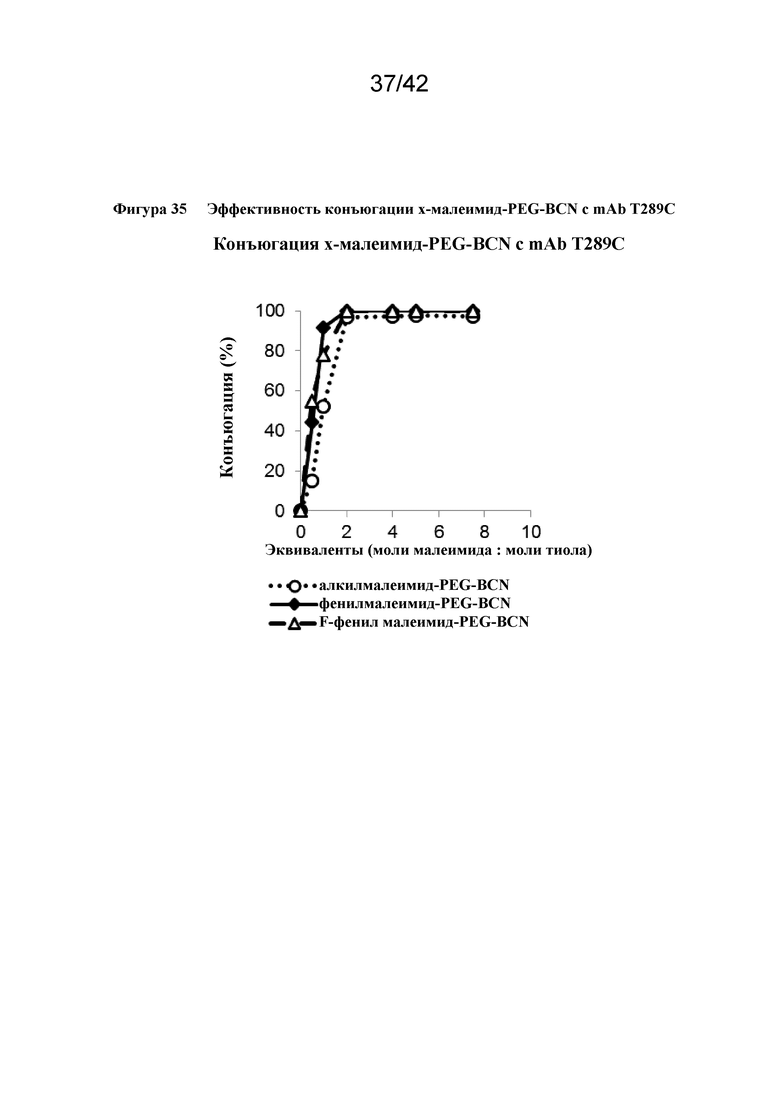
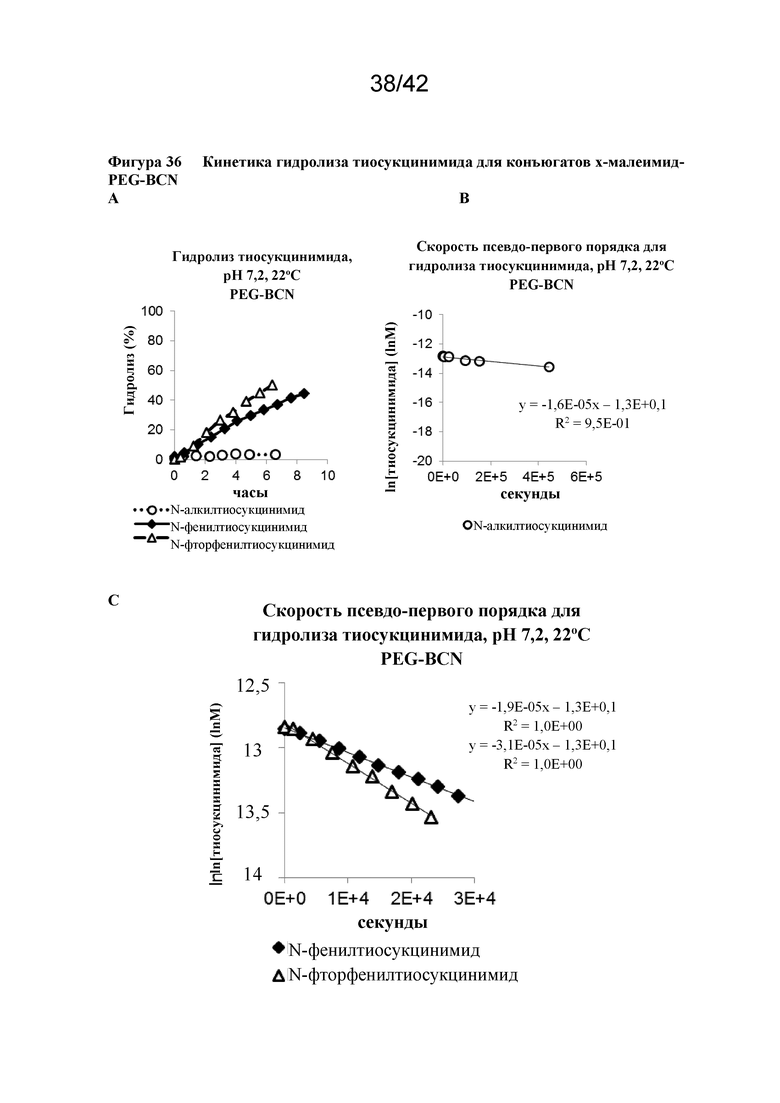
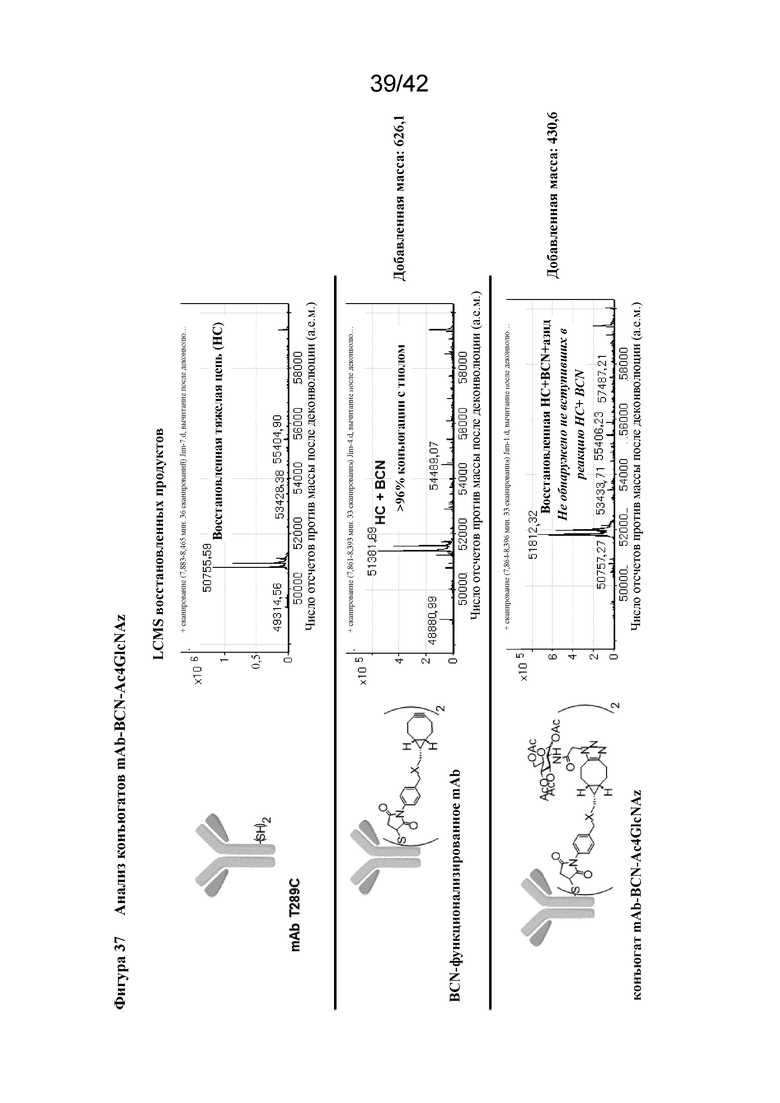

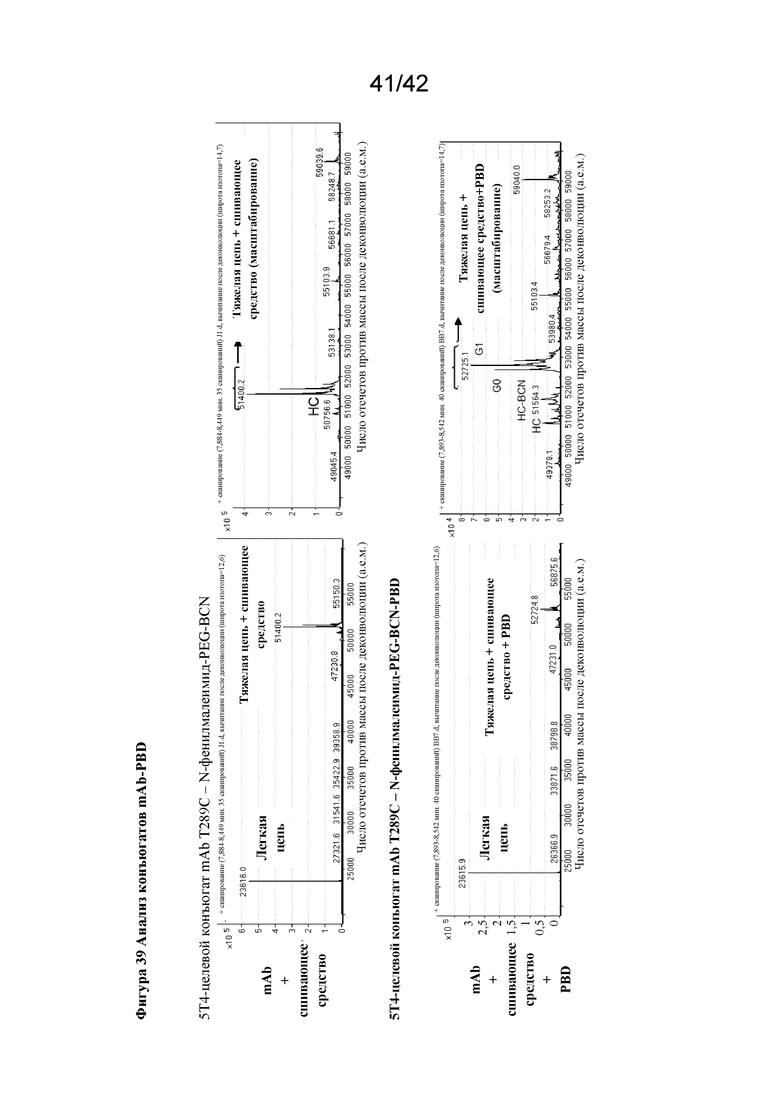
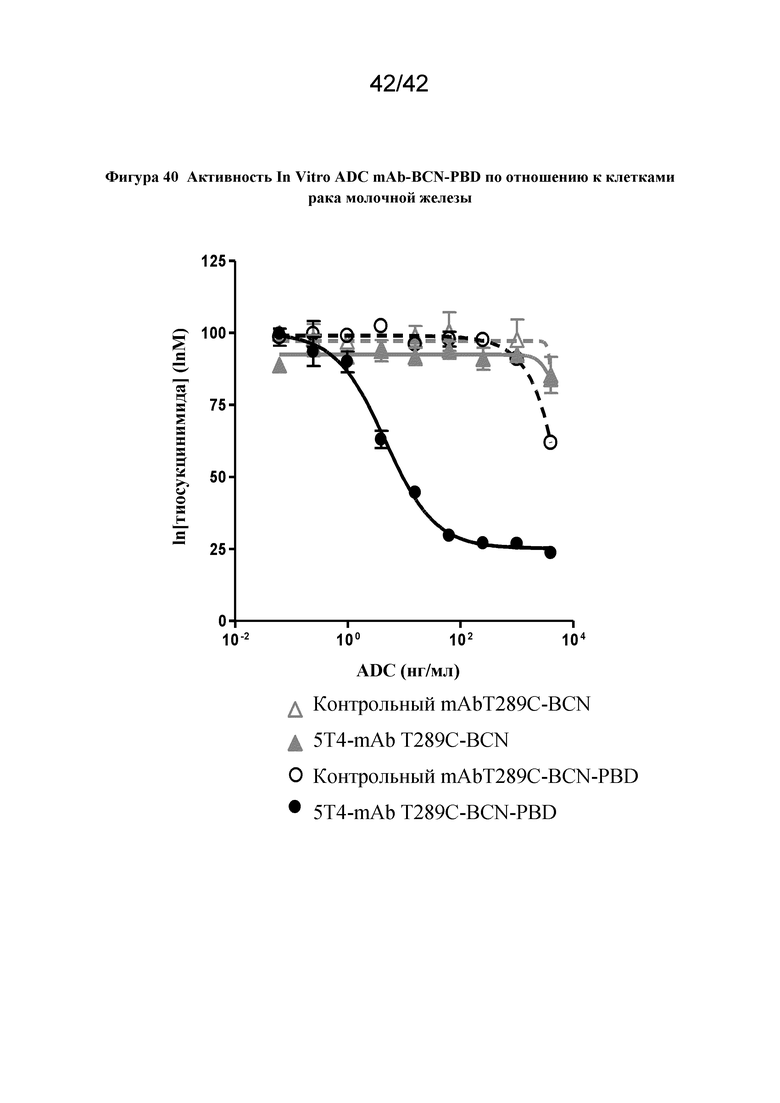
Настоящее изобретение относится к способу получения антитела или его связывающего фрагмента, конъюгированного с полезной нагрузкой, включающему конъюгацию соединения формулы (I), с антителом или его связывающим фрагментом, содержащим по меньшей мере одну тиоловую группу. В способе используют мягкие условия, что дает молекулы, которые стабильны после получения и, следовательно, пригодны для введения in vivo. 2 н. и 19 з.п. ф-лы, 40 ил., 31 табл., 53 пр.
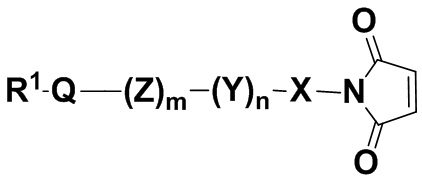
1. Способ получения антитела или его связывающего фрагмента, конъюгированного с полезной нагрузкой, включающий стадии:
a) проведения реакции присоединения по Михаэлю с малеимидной структурной единицей в молекуле формулы (IIa)
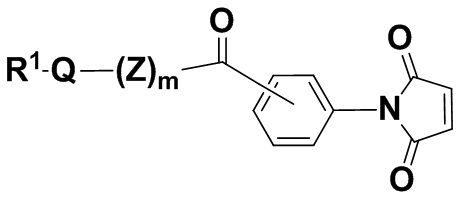 (IIa)
(IIa)
и антителом или его связывающим фрагментом, содержащим по меньшей мере одну тиоловую группу, где
фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3;
m равняется 0 или 1;
q равняется 0 или целому числу в диапазоне от 1 до 12, например от 1 до 6, такому как 2 или 3;
Q представляет собой связь или остаток из компонента для конъюгации;
Z представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-30алкиленовую цепь, где один или несколько атомов углерода (например, 1, 2, 3, 4, 5, 6, 7 или 8) необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько (например, 1, 2, 3 или 4) оксо-заместителей;
R1 представляет собой H, поверхность твердой фазы или молекулу полезной нагрузки, выбранную из списка, состоящего из токсина, молекулы лекарственного средства (такого как цитотоксическое средство), полимера, антитела или его связывающего фрагмента;
R3 представляет собой H или C1-6алкил;
R4 представляет собой H или C1-6алкил;
R5 представляет собой H или C1-6алкил; и
b) если R1 представляет собой молекулу полезной нагрузки или поверхность твердой фазы, способ дополнительно включает стадию гидролиза полученной тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (IIa) и антитела или его связывающего фрагмента, или
c) если R1 представляет собой H, способ дополнительно включает стадию проведения конъюгации с полезной нагрузкой или компонентом для конъюгации, или поверхностью твердой фазы с последующим гидролизом тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (IIa) и антитела или его связывающего фрагмента.
2. Способ по п.1, где группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIaa)
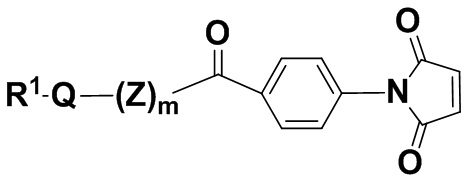 (IIaa),
(IIaa),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (IIa), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
3. Способ по п.1, где группа R1Q(Z)mC(O)- находится в мета-положении, как показано в соединении формулы (IIaa')
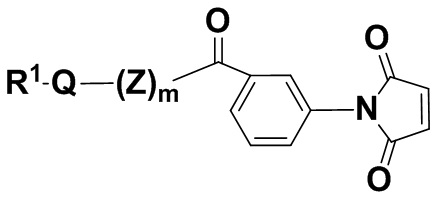 (IIaa'),
(IIaa'),
и его фармацевтически приемлемых солях, где R1, Q, Z и m определены выше для соединений формулы (IIa), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3.
4. Способ по п.1, где молекула малеимида находится в соединении формулы (IIааa)
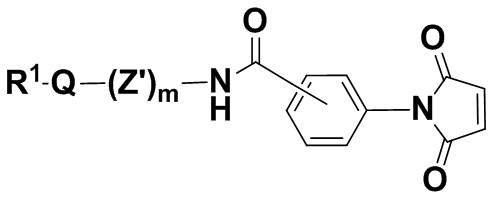 (IIaaa),
(IIaaa),
и его фармацевтически приемлемых солях, где R1, Q и m определены выше для соединений формулы (IIa),
фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3, и
Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей.
5. Способ по п.4, где группа R1Q(Z')mNC(O)- находится в мета- или пара-положении.
6. Способ получения антитела или его связывающего фрагмента, конъюгированного с полезной нагрузкой, включающий стадии:
a) проведения реакции присоединения по Михаэлю с малеимидной структурной единицей в молекуле формулы (IIb)
 (IIb)
(IIb)
и антителом или его связывающим фрагментом, содержащим по меньшей мере одну тиоловую группу, где
фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3;
m равняется 0 или 1;
q равняется 0 или целому числу в диапазоне от 1 до 12, например от 1 до 6, такому как 2 или 3;
Q представляет собой связь или остаток из компонента для конъюгации;
Z представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-30алкиленовую цепь, где один или несколько атомов углерода (например, 1, 2, 3, 4, 5, 6, 7 или 8) необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько (например, 1, 2, 3 или 4) оксо-заместителей;
R1 представляет собой H, поверхность твердой фазы или молекулу полезной нагрузки, выбранную из списка, состоящего из токсина, молекулы лекарственного средства (такого как цитотоксическое средство), полимера, антитела или его связывающего фрагмента;
R3 представляет собой H или C1-6алкил;
R4 представляет собой H или C1-6алкил;
R5 представляет собой H или C1-6алкил; и
b) если R1 представляет собой молекулу полезной нагрузки или поверхность твердой фазы, способ дополнительно включает стадию гидролиза полученной тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (IIb) и антитела или его связывающего фрагмента, или
c) если R1 представляет собой H, способ дополнительно включает стадию проведения конъюгации с полезной нагрузкой или компонентом для конъюгации, или поверхностью твердой фазы с последующим гидролизом тиосукцинимидной структурной единицы, образованной посредством реакции соединения формулы (IIb) и антитела или его связывающего фрагмента.
7. Способ по п.6, где группа R1Q(Z)mC(O)- находится в пара-положении, как показано в соединении формулы (IIbb)
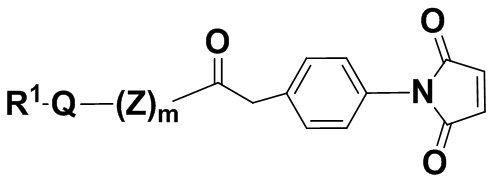 (IIbb),
(IIbb),
и его фармацевтически приемлемых солях, где n, Q, Z, X, R1 и m определены выше в п.6.
8. Способ по п.6, где группа R1Q(Z)mC(O)- находится в мета-положении, как показано в соединении формулы (IIbb')
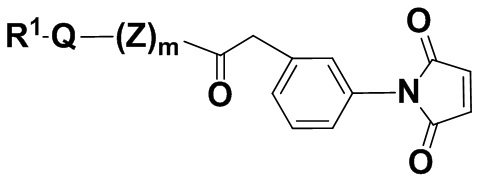 (IIbb'),
(IIbb'),
и его фармацевтически приемлемых солях, где Q, Z, X, R1 и m определены выше в п.6.
9. Способ по п.6, где малеимидная структурная единица находится в молекуле формулы (IIbbb)
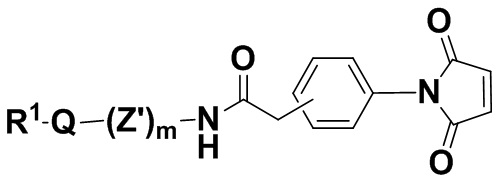 (IIbbb),
(IIbbb),
где R1, Q и m определены выше для соединений формулы (IIb), и фенил содержит 0, 1, 2, 3 или 4 заместителя, независимо выбранных из группы, включающей галоген, гидроксил, C1-6алкил, C1-6алкокси, -COOR3, -COR3, -CN, -CF3, -NO2, -SO2, -SO3, -NR4R5, -PO4 и -(OCH2CH2)q-OR3
Z' представляет собой насыщенную или ненасыщенную, разветвленную или неразветвленную C1-24алкиленовую цепь, где один или несколько атомов углерода необязательно независимо заменены -O-, N, и цепь необязательно несет один или несколько оксо-заместителей.
10. Способ по п.9, где группа R1Q(Z')mNC(O)- находится в мета- или пара-положении фенильного кольца.
11. Способ по любому из пп. 1-10, где Z или Z' представляет собой -C1-12алкилен- или -(CH2CH2O)1-8-.
12. Способ по любому из пп. 1-11, где молекула лекарственного средства выбрана из таковой, включающей ауристатин, например выбрана из группы, включающей тубулизин или пирролобензодиазепин (PBD), MMAE (монометилауристатин Е) и MMAF (монометилауристатин F).
13. Способ по любому из пп. 1-11, где молекула лекарственного средства выбрана из таковой, включающей майтанзиноид, например N2'-деацетил-N2'-(3-меркапто-1-оксопропил)-майтанзин (DM1), N2'-деацетил-N2'-(4-меркапто-1-оксопентил)-майтанзин (DM3) и N2'-деацетил-N2'-(4-метил-4-меркапто-1-оксопентил)-майтанзин (DM4).
14. Способ по любому из пп. 1-11, где R1 представляет собой токсин.
15. Способ по любому из пп. 1-11, где полимер представляет собой природный полимер, например крахмал или альбумин, или синтетический полимер, такой как PEG.
16. Способ по любому из пп. 1-15, где присоединение по Михаэлю проводят при рН в диапазоне от 5 до 9, например от 5,5 до 8,6.
17. Способ по любому из пп. 1-16, где присоединение по Михаэлю проводят при температуре в диапазоне от приблизительно 4°C до приблизительно 37°C, например от 8°C до 37°C, от 8°C до 30°C, от 8°C до 25°C или от 21°C до 31°C.
18. Способ по любому из пп. 1-17, где реакцию присоединения по Михаэлю проводят с буфером, выбранным из группы, включающей фосфатный буфер, цитратный буфер, боратный буфер, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновую кислоту), MES (2-(N-морфолино)этансульфоновую кислоту)), PIPES (пиперазин-N,N′-бис(2-этансульфоновую кислоту)), MOPS (3-(N-морфолино)пропансульфоновую кислоту)), например фосфатным.
19. Способ по любому из пп. 1-18, где стадию гидролиза проводят при рН в диапазоне от 7 до 12, например рН от 7,4 до 9.
20. Способ по любому из пп. 1-19, где стадию гидролиза проводят в буфере, выбранном из группы, включающей фосфатный буфер, цитратный буфер, боратный буфер, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновую кислоту), MES (2-(N-морфолино)этансульфоновую кислоту)), PIPES (пиперазин-N,N′-бис(2-этансульфоновую кислоту)), MOPS (3-(N-морфолино)пропансульфоновую кислоту)), например фосфатном.
21. Способ по любому из пп. 1-20, где стадию гидролиза проводят при температуре в диапазоне от приблизительно 4°C до приблизительно 37°C, например от 8°C до 37°C, от 8°C до 30°C, от 8°C до 25°C или от 21°C до 31°C.
| EA 201401254 A1, 20.09.2015 | |||
| KRATZ F | |||
| et al | |||
| "A NOVEL MACROMOLECULAR PRODRUG CONCEPT EXPLOITING ENDOGENOUS SERUM ALBUMIN AS A DRUG CARRIER FOR CANCER CHEMOTHERAPY" | |||
| JOURNAL OF MEDICINAL CHEMISTRY, 2000, vol | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| Передвижное опорное приспособление (якорь) для удерживания, при работе, корчевальных машин, экскаваторов, драг и т.п. | 1923 |
|
SU1253A1 |
| Z | |||
| T | |||
| SHEN et al | |||
| "Bi-specific MHC Heterodimers for Characterization of Cross-reactive T Cells" | |||
| JOURNAL OF BIOLOGICAL | |||
Авторы
Даты
2020-03-04—Публикация
2015-10-01—Подача