Изобретение относится к медицине, а именно к онкологии, абдоминальной хирургии и касается хирургического лечения больных с опухолевым поражением (первичные опухоли или вторичная опухолевая инвазия извне) двенадцатиперстной кишки (ДПК).
Гастропанкреатодуоденальная резекция (ГПДР) является стандартным объемом хирургического вмешательства при опухолевом поражении двенадцатиперстной кишки [Journal Annals of Surgery 2006; 244 (6): 931-939]. Способ состоит в том, что одномоментно, единым блоком удаляются вся двенадцатиперстная кишка с начальным отделом тощей кишки, головка поджелудочной железы, выходной отдел желудка с прилежащим малым сальником и правой половиной большого сальника, желчный пузырь, общий желчный проток, прилежащая к головке поджелудочной железы клетчатка, фасциально-клетчаточные футляры общей и собственной печеночной артерий, стволов верхнебрыжеечных сосудов и воротной вены.
Операция выполняется из срединного лапаротомного доступа. После рассечения желудочно-ободочной связки выполняется мобилизация ДПК по Кохеру с выделением верхнебрыжеечной и воротной вен. Далее выполняется мобилизация желчного пузыря с лимфодиссекцией по ходу гепатодуоденальной связки и пересечением общего желчного протока выше слияния с пузырным протоком. Желудок мобилизуется по обеим кривизнам с перевязкой правых желудочных и желудочно-сальниковых сосудов. Отдельно выделяется и перевязывается гастродуоденальная артерия. Между перешейком поджелудочной железы и воротной веной формируется туннель. На этом уровне пересекается поджелудочная железа. Следующим этапом линейными степлерными аппаратами производится пересечение желудка и тощей кишки. В проксимальном направлении пересекается брыжейка резецированной тощей кишки. Далее весь комплекс мобилизуется от верхнебрыжеечных сосудов и удаляется. В процессе мобилизации удаляются лимфоузлы следующих регионарных групп: супра- и инфрапилорические (№4 и 5), гепатодуоденальной связки (№12 а, b, с, р и h), по верхнему и нижнему краю головки поджелудочной железы (№11 и 18), передние и задние панкреатодуоденальные (№13) и проксимальные мезентериальные (№14). Существуют различные вариации реконструктивного этапа, который состоит восстановлении непрерывности ЖКТ с обязательным включением поджелудочной железы и общего печеночного протока.
Недостатки ГПДР являются: высокая послеоперационная морбидность (послеоперационные осложнения развиваются у 30-70% больных), высокая послеоперационная летальность (до 5% в специализированных клиниках и до 7-12% в непрофильных клиниках), а также высокий уровень функциональных нарушений в отдаленные сроки послеоперационного периода. Основной проблемой операции является несостоятельность панкреатикоеюноанастомоза, частота которой достигает 30% и панкреонекроз культи ПЖ, встречающийся в 0,5-9% случаев. Несостоятельность билиодигестивного анастомоза развивается у 9% больных. Более чем у 2/3 пациентов развиваются экзокринная и эндокринная недостаточность поджелудочной железы, которые проявляются синдромом мальабсорбции и инсулинозависимым сахарным диабетом, что осложняет реабилитацию больных, и в большинстве случаев приводят к их инвалидизации.
По данным литературы при неэпителиальных опухолях (за исключением лимфом) оправданы экономные, органосохранные операции. В результате выполнения экономных резекций значительно улучшаются непосредственные результаты и качество жизни больных. При этом показатели общей выживаемости не отличаются от результатов расширенных хирургических вмешательств. Обязательными требованиями к хирургическому вмешательству являются отрицательные края резекции и сохранение целостности капсулы опухоли [Zhou В, Zhang М, Wu J. Pancreaticoduodenectomy versus local resection in the treatment of gastrointestinal stromal tumours of the duodenum. World Journal of Surgical Oncology. 2013; 11(1): 196. https://doi.org/10.1186/1477-7819-11-196]. Аналогичные данные описаны и у больных с аденокарциномой двенадцатиперстной кишки (АДПК). По данным многих авторов, сравнивших результаты хирургического лечения больных с АДПК, различия в отдаленных результатах после экономных резекций и ГПДР не были обнаружены [Hu JX, Miao XY, Zhong DW, Dai WD, Liu W, Hu W. Surgical treatment of primary duodenal adenocarcinoma. Hepatogastroenterology. 2006; 53: 858-862].
Другим способом хирургического лечения больных неэпителиальными опухолями двенадцатиперстной кишки является выполнение клиновидных резекций ДПК. Способ состоит в том, что опухоль иссекается в пределах здоровых тканей стенки кишки. Технически вектор резекции и последующего прошивания дефекта стенки кишки должен быть выполнен в поперечном направлении относительно вектора ДПК. Основными критериями радикальности операции являются отрицательные края резекции. Поэтому интраоперационно выполняется срочное гистологическое исследование, и при наличии опухолевых клеток по линии резекции необходимо расширить объем хирургического вмешательства. [Chung JC, Kim НС, Hur SM. Limited resections for duodenal gastrointestinal stromal tumours and their oncologic outcomes. Surg. Today. 2016; 46(1): 110-116. https://doi.org/10.1007/s00595-015-1163-х].
Недостатком данного способа является риск развития стеноза просвета кишки при большой площади опухолевого поражения. Клиновидная резекция допустима только при небольших опухолях или в случаях, когда опухоли исходит из стенки кишки на «тонкой ножке».
При локализации опухоли в нисходящей части ДПК в литературе описаны способы панкреатосохранной дуоденэктомии (ПСД). Существуют два вида ПСД: типичная и папиллосохранная ПСД (Yusuke Nakayama, Masaru Konishi, Naoto Gotohda et al. Comparison of postoperative early and late complications between pancreas-sparing duodenectomy and pancreatoduodenectomy. Surgery Today June 2017, Volume 47, Issue 6, pp. 705-711). Способ состоит в полной мобилизации и удалении ДПК с последующим формированием анастомоза между петлей тощей кишки и ампулой холедохо-панкреатического протока по типу «конец в бок». По показателям послеоперационной морбидности и функциональным характеристикам значительным преимуществом по сравнению с панкреатодуоденалной резекцией обладает только папиллосохранные ПСД. Послеоперационные осложнения и функциональные нарушения после выполнения типичных ПСД примерно одинаковы по сравнению с ПДР, по некоторым авторам даже выше (Michael W.  , M.D.a,b, Rolf Dahmen, et al. Is there an advantage in performing a pancreas-preserving total duodenectomy in duodenal adenomatosis? The American Journal of Surgery. 2008, 195, 741-748).
, M.D.a,b, Rolf Dahmen, et al. Is there an advantage in performing a pancreas-preserving total duodenectomy in duodenal adenomatosis? The American Journal of Surgery. 2008, 195, 741-748).
Наиболее близким к заявляемому является способ выполнения дистальных сегментарных (ограниченных) резекций ДПК (Ankush Golhar,*Vivek Mangla, et al. Limited distal duodenal resection: Surgical approach and outcomes. A case series. Ann Med Surg (Lond). 2018 Jun; 30: 36-41. doi:10.1016/j.amsu.2018.04.005). Данный способ применяется при локализации опухоли в нижнегоризонтальном и вертикальном отделах ДПК и состоит в ограниченной циркулярной резекции дистальной части двенадцатиперстной кишки с формированием дуоденоеюноанастомоза по типу «конец в конец», «конец в бок» или «бок в бок».
Недостатком данного способа является ограничение его применения при локализации опухоли в нисходящей части ДПК.
Задачей заявляемого изобретения является созданием нового способа хирургического лечения больных с опухолевым поражением нисходящей части двенадцатиперстной кишки, свободного от недостатков прототипа.
Поставленная задача решается тем, что выполняют мобилизацию и циркулярную резекцию дистальной части нисходящего отдела, нижнего угла, нижне-горизонтального и вертикального отделов ДПК с последующим перемещением начального отдела тощей кишки вправо от верхнебрыжеечных сосудов и формированием дуоденоеюноанастомоза по типу «бок в бок». Ограничивающим критерием выполнения данного объема оперативного вмешательства является расстояние от макроскопического края опухоли до Фатерова сосочка. Минимальное расстояние, при котором нам удалось выполнить радикальную дистальную резекцию двенадцатиперстной кишки (ДР ДПК) у больной с ГИСО, составила 3 см. При расположении опухолевой инфильтрации по наружному контуру ДПК возможно пересечение кишки в косом направлении, тем самым, расширяя показания к выполнению дистальной резекции ДПК при расстоянии менее чем 3 см от Фатерова соска. Для достижения оптимальных условий (уменьшение и девитализация опухоли) для выполнения ДР ДПК необходимо расширить показания к неоадъювантой терапии.
Техническим результатом заявляемого способа является возможность более широкого его применения, высокая надежность и функциональность анастомоза.
Заявляемый способ иллюстрируется примерами 1-2 и фигурами 1 (A-D) и 2 (A-D).
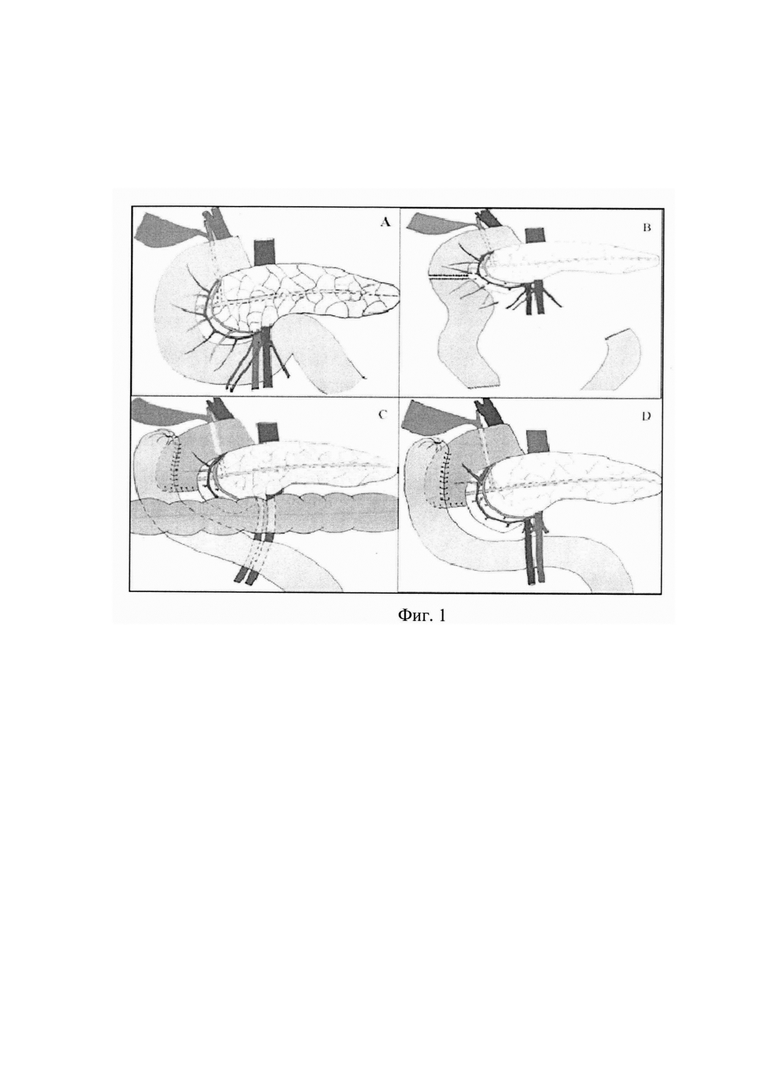
На фиг. 1 (A-D) представлена схема технического выполнения дистальной резекции (ДР) ДПК.
На фиг. 2 (A-D) представлены интраоперационные фотографии отдельных этапов выполнения ДР ДПК.
Способ осуществляется следующим образом.
Для выполнения дистальной резекции двенадцатиперстной кишки применяется срединный лапаротомный доступ. Выполняют мобилизацию ДПК по Кохеру с применением приема Cattel-Braash. Рассекают листок брюшины по ходу правого латерального канала от уровня гепатодуоденальной связки до купола слепой кишки. Далее разрез брюшины продолжают влево и краниально до уровня связки Трейтца с мобилизацией правой половины ободочной кишки и всей тонкой кишки с брыжейкой, которые смещаются влево и кверху. В результате этого маневра двенадцатиперстная кишка обнажается на всем ее протяжении. Далее выполняют мобилизацию нижне-горизонтального, вертикального отделов ДПК и дуоденоеюнального перехода с пересечением брыжейки с питающими сосудами. Мобилизованная часть тощей кишки переводят (выводят) справа от брыжейки тонкой кишки (фиг. 1В и 2А). Наиболее сложным этапом является мобилизация нижнего угла и нисходящей части ДПК. В процессе их мобилизации отдельно перевязывают передние и задние короткие дуоденальные сосуды с сохранением соответствующих панкреатодуоденальных сосудистых дуг. При необходимости выполняют забрюшинную лимфодиссекцию. Сшивающим линейным степлерным аппаратом пересекают двенадцатиперстную кишку и начальный отдел тощей кишки (фиг. 1В и 2В). Механический шов на культе тощей кишки погружают в кисетный шов. Шов на культе нисходящей части ДПК, с учетом ограниченного расстояния до Фатерова соска, укрывают отдельными узловыми серозно-мышечными швами (фиг. 1С). С нашей точки зрения, и по данным литературы наиболее надежным способом восстановления непрерывности кишечного тракта является выполнение дуоденоеюноанастомоза по типу «бок-в-бок» (фиг. 1С, D; 2С, D).
Технически анастомозы можно сформировать как изо-, так и антиперистальтические.
Дистальную часть тощей кишки оптимальнее всего подводить для формирования анастомоза позадиободочно (через окно в брыжейке поперечно-ободочной кишки) и кпереди от верхнебрыжеечных сосудов (фиг. 1С и 2D). При технических сложностях возможно проведение анастомозируемой петли тощей кишки позади верхнебрыжеечных сосудов (в ложе удаленной нижнегоризонтальной и вертикальной части ДПК) (фиг. 1D).
Предлагаемый способ отличается от прототипа возможностью выполнения более обширной резекции двенадцатиперстной кишки, включающей удаление не только нижнегоризонтальной части, но и нисходящей части двенадцатиперстной кишки, а также анатомически обоснованной методикой мобилизации двенадцатиперстной кишки от ткани головки поджелудочной железы, позволяющей уменьшить вероятность повреждения паренхимы поджелудочной железы и частоту панкреатогенных осложнений (панкреатита, панкреонекроза панкреатического свища).
Данный способ резекции двенадцатиперстной кишки отличается от известных высокой надежностью и функциональностью анастомоза и возможностью более широкого его применения.
Пример №1 Пациентка Б. 69 лет.
Диагноз: ГИСО двенадцатиперстной кишки pT4N0M0, МИ - высокий, IIIB ст. Состояние после неоадьювантной терапии иматинибом 400 мг в сутки в 2017-2018 гг. Частичная регрессия.
Гистологический диагноз: стромальная опухоль двенадцатиперстной кишки, веретеноклеточного типа строения, с высоким митотическим индексом (15 митозов в 50 ПЗ х 400).
Пациентке с августа 2017 г. по октябрь 2018 г. проведена неоадъювантная терапия иматинибом 400 мг в сутки с положительным эффектом в виде уменьшения опухоли с 15.5 см до 7,5 см. В ноябре 2018 г. в ФГБУ «НМИЦ онкологии имени Н.Н. Блохина» Минздрава РФ выполнена операция по заявленному способу. После операции начата адъювантная терапия по принятым стандартам лечения в течение 3 лет. В настоящее время пациентка жива без признаков прогрессирования заболевания.
Пример №2
Пациент А. 60 лет.
Диагноз: Рак поперечно-ободочной кишки pT4bN0M0 - IIC ст.
Гистологический диагноз: аденокарцинома поперечноободочной кишки, прорастающая все слои стенки ободочной кишки и врастающая в нисходящую часть двенадцатиперстной кишки.
Пациенту в июле 2017 г. в ФГБУ «НМИЦ онкологии имени Н.Н. Блохина» Минздрава РФ выполнена операция по заявленному способу. После операции проведены 6 курсов адьювантной ПХТ по схеме XELOX. В настоящее время пациент наблюдается без признаков прогрессирования заболевания.
Хирургическое лечение по заявленному способу было проведено 11 пациентам с опухолевым поражением 12-перстной кишки. Средний возраст больных составил 56 лет (от 28 до 74 лет). Во всех 11 случаях была выполнена R0 резекции (без элементов опухолевого роста по линии резекции ДПК). Из них у 9 больных ДР ДПК выполнялась по поводу первичных опухолей двенадцатиперстной кишки: в 1-м случае лейомиосаркома ДПК, в остальных 8 случаях ГИСО ДПК. Из 8 больных с ГИСО двенадцатиперстной кишки 4 пациентам проводилась неоадьювантная терапия иматинибом в дозировке 400 мг в сутки с частичной регрессией опухоли. В остальных 2 случаях дистальная резекция двенадцатиперстной кишки выполнялась по поводу опухолевой инвазии извне: в 1 случае рака поперечно-ободочной кишки и во втором - забрюшинной неорганной опухоли.
Во всех случаях нами были сформированы анастомозы по типу «бок-в-бок» между передне-наружной стенкой оставшейся нисходящей части двенадцатиперстной кишки и начальным отделом тощей кишки. В 10 (90,9%) случаях нами сформированы изоперистальтические анастомозы, в одном (9,1%) случае - антиперистальтический.
Послеоперационная морбидность была оценена с учетом классификации Clavien Dindo. В раннем послеоперационном периоде осложнения 1-2 степени развились у 4 (36,4%) больных. Осложнения 2 степени имелись у 2-х пациентов, из них у одного (9,1%) - в виде панкреатического свища, который закрылся на фоне консервативного лечения. У одного пациента диагностирована полисегментарная пневмония. Несостоятельности культи двенадцатиперстной кишки и дуодено-еюно анастомоза во всех случаях не наблюдались. Летальных исходов в послеоперационном периоде также не было. В отдаленные сроки функциональные нарушения желудочно-кишечного тракта нами не отмечались. Локальных рецидивов за весь период наблюдения также не выявлено. Послеоперационное пребывание в стационаре составило в среднем 13 суток (от 10 до 16 суток).
Таким образом, заявляемый способ ассоциируются с низкой послеоперационной морбидностью, хорошей функциональностью и качеством жизни больных, а также меньшим количеством суток пребывания в стационаре по сравнению с расширенными операциями. С учетом отсутствия различий в отдаленных результатах, экономные резекции ДПК, в частности ДР ДПК, являются методом выбора у больных с неэпителиальными (за исключением лимфом), нейроэндокринными опухолями и вторичной опухолевой инвазией двенадцатиперстной кишки извне.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ С ОПУХОЛЕВЫМ ПОРАЖЕНИЕМ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ БЕЗ ВОВЛЕЧЕНИЯ ФАТЕРОВА СОСОЧКА И ПЕРИПАПИЛЛЯРНОЙ ОБЛАСТИ | 2022 |
|
RU2779945C1 |
| Способ реконструкции желудочно-кишечного тракта при хронической артериомезентериальной компрессии двенадцатиперстной кишки | 2015 |
|
RU2607512C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОСЛОЖНЕННОГО ХРОНИЧЕСКОГО ПАНКРЕАТИТА | 2000 |
|
RU2181027C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЯЗВЕННОЙ БОЛЕЗНИ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ, СОЧЕТАЮЩЕЙСЯ С ХРОНИЧЕСКИМИ НАРУШЕНИЯМИ ДУОДЕНАЛЬНОЙ ПРОХОДИМОСТИ | 1996 |
|
RU2124863C1 |
| СПОСОБ ЛЕЧЕНИЯ МОТОРНО-ЭВАКУАТОРНЫХ НАРУШЕНИЙ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 1997 |
|
RU2153854C2 |
| СПОСОБ ДИСТАЛЬНОЙ РЕЗЕКЦИИ ЖЕЛУДКА | 2006 |
|
RU2290879C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ СИНДРОМА ЗОЛЛИНГЕРА-ЭЛЛИСОНА И ЯЗВ КАРДИАЛЬНОГО ОТДЕЛА ЖЕЛУДКА | 1996 |
|
RU2142740C1 |
| СПОСОБЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ДУОДЕНАЛЬНОЙ НЕПРОХОДИМОСТИ (ВАРИАНТЫ) | 2004 |
|
RU2264179C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ПОСТБУЛЬБАРНОЙ ЯЗВЫ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 1997 |
|
RU2159581C2 |
| СПОСОБ ФОРМИРОВАНИЯ ТЕРМИНОЛАТЕРАЛЬНОГО ПАНКРЕАТОЕЮНОАНАСТОМОЗА ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 2006 |
|
RU2293530C1 |

Изобретение относится к медицине, а именно к онкологии и абдоминальной хирургии и может быть использован для хирургического лечения больных с опухолевым поражением двенадцатиперстной кишки (ДПК). Мобилизация двенадцатиперстной кишки от ткани поджелудочной железы осуществляется с раздельной перевязкой передних и задних коротких дуоденальных сосудов и сохранением передней и задней панкреатодуоденальных сосудистых дуг. Проводят циркулярную резекцию не только нижне-горизонтального, но и дистальной части нисходящего отдела двенадцатиперстной кишки, отступя не менее 3 см от фатерова сосочка с формированием изо- или антиперистальтического дуоденоеюноанастомоза по типу «бок в бок». Способ обеспечивает высокую надежность и функциональность анастомоза за счет анатомически обоснованной мобилизации ДПК от ткани поджелудочной железы. 2 ил., 2 пр.
Способ хирургического лечения больных с опухолевым поражением двенадцатиперстной кишки, заключающийся в дистальной резекции двенадцатиперстной кишки с формированием дуоденоеюноанастомоза и отличающийся тем, что мобилизация двенадцатиперстной кишки от ткани поджелудочной железы осуществляется с раздельной перевязкой передних и задних коротких дуоденальных сосудов и сохранением передней и задней панкреатодуоденальных сосудистых дуг, циркулярной резекцией не только нижне-горизонтального, но и дистальной части нисходящего отдела двенадцатиперстной кишки, отступя не менее 3 см от фатерова сосочка с формированием изо- или антиперистальтического дуоденоеюноанастомоза по типу «бок в бок».
| Ankush Golhar,Vivek Mangla, et al | |||
| Limited distal duodenal resection: Surgical approach and outcomes | |||
| A case series | |||
| Ann Med Surg (Lond) | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| СПОСОБ ДУОДЕНОЕЮНОСТОМИИ | 1995 |
|
RU2111709C1 |
| СПОСОБ НАЛОЖЕНИЯ ДУОДЕНОЕЮНОАНАСТОМОЗА ПРИ КОЛЬЦЕВИДНОЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЕ | 1999 |
|
RU2150243C1 |
| Шариковый подшипник | 1924 |
|
SU832A1 |
| Ankush Golhar, et al | |||
| Limited distal duodenal resection: Surgical approach and | |||
Авторы
Даты
2020-03-11—Публикация
2019-06-19—Подача