ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к области экспериментальной медицины и медицинской микробиологии и предназначено для моделирования брюшного тифа на мелких лабораторных животных с искусственной иммуносупрессией. Для создания состояния иммуносупрессии животным в течение 3 суток ежедневно однократно внутрибрюшинно вводят дексаметазон в дозе эквивалентной среднетерапевтической для человека, что составляет 2 мг/кг для белых мышей и 0,8 мг/кг для морских свинок. Через 2 суток после последней инъекции животным производят парентеральную аппликацию культуры возбудителя брюшного тифа. В зависимости от моделируемых проявлений инфекционного процесса микробы вводят белым мышам внутривенно (системная инфекция) или внутрибрюшинно (эндотоксемия), морским свинкам интратестикулярно (локальный воспалительный очаг инфекции). Данное изобретение позволяет обеспечить диссеминацию, приживление и размножение в организме лабораторных животных возбудителя с развитием некоторых проявлений инфекционного процесса, использование которых необходимо для решения ряда практических задач, связанных с оценкой патогенных свойств микробов, анимализацией лабораторных культур, оценкой эффективности средств этиотропного лечения.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В медицинской микробиологии существует необходимость воспроизведения инфекционных заболеваний человека на лабораторных животных с целью изучения особенностей их течения, оценки эффективности и безопасности средств профилактики и лечения, для изучения патогенных свойств и анимализации микробных культур. В данной связи огромную проблему представляет собой группа микроорганизмов - антропонозов, типичным представителем которой является возбудитель брюшного тифа Salmonella enterica enterica серотип Typhi (S.Typhi). За многолетнюю историю исследований установлено, что в эксперименте заражение возбудителем брюшного тифа различных видов животных, вплоть до высших обезьян, не приводит к развитию типичного заболевания, сопоставимого с наблюдаемым у человека.
Известно, что ранее для изучения патогенетических особенностей брюшного тифа проводились исследования на мышах, инфицированных Salmonella enterica enterica серотип Typhimurium, вызывающей у них системную инфекцию, похожую на брюшнотифозную. Однако развивающееся при этом заболевание существенно отличается по механизму развития и проявлениям инфекции у человека, отсутствует возможность получения данных в отношении конкретных культур самого возбудителя брюшного тифа [Bhan, М.К. Typhoid and paratyphoid fever/ M.K. Bhan, R. Bahl, S. Bhatnagar // Lancet. - 2005. - №366. - P. 749-762].
Известны попытки воспроизведения брюшного тифа при различных способах аппликации возбудителя (внутрибрюшинно, субъконъюктивально, в полость трубчатых костей) белым мышам, морским свинкам и кроликам [Моргунов, И.Н. Экспериментальное воспроизведение брюшного тифа у морских свинок и кроликов / И.Н. Моргунов, С.Л. Ягуд, Ю.А. Барштейн // Журн. микробиол. - 1962. - №1. - С. 40-45.; Джикидзе, Э.К. Моделирование кишечных инфекций человека в эксперименте на различных животных / Э.К. Джикидзе [и др.] // Вестник академии мед. наук СССР. - 1965. -№11.-С.38-49.; Ведибеда, Д.К. Роль костного мозга в формировании носительства тифозных бактерий в эксперименте / Д.К. Ведибеда, Т.Л. Сакун, А.А. Заднепрянский // Журн. микробиол. - 1972. - №4. - С. 71-77]. Недостатками данных способов является то, что при этом развивается нетипичная форма заболевания, получаемые данные противоречивы и в большинстве своем трудно воспроизводимы на практике.
Известны попытки воспроизведения брюшного тифа при энтеральном заражении приматов [Шабалин, Б.А. Воспроизведение брюшного тифа в опытах на лабораторных животных / Б.А. Шабалин, В.Ю. Охапкина, С.Л. Кузнецов // Материалы юбилейной научной конференции, посвященной 70-летию образования научно-исследовательского института микробиологии МО РФ «Диагностика, лечение и профилактика опасных инфекционных заболеваний. Биотехнология. Ветеринария», 30 ноября - 1 декабря 1998 г, г. Киров. - Киров, 1998. - С. 271-272]. Недостатком данного способа является то, что у инфицированных даже высокими дозами 5. Typhi животных при отсутствии типичных внешних клинических проявлений обнаруживались лишь сдвиги лабораторных показателей: появление специфических антител в сыворотке крови, лейкопения, в половине случаев возбудитель удавалось выделить в копрокультуре. При этом приматы являются дорогостоящей и малодоступной моделью.
Имеются указания на возможность воспроизведения брюшного тифа на модели гуманизированных алимфоидных мутантных мышей линии RAG 2 [Firoz Mian, М. Humanized mice are susceptible to Salmonella typhi infection / M. Firoz Mian, E.A. Pek, M.J. Chenoweth, A.A. Ashkar // Cell. Mol. Immunol. -2011. - Jan; 8(1). - P. 83-87.; Song, J. A mouse model for the human pathogen Salmonella typhi I J. Song [et al.] // Cell Host Microbe. - 2010. - Oct 21; 8(4). - P. 369-376]. При этом данная модель является весьма редкой, дорогой и малодоступной.
В литературе приводятся сведения о том, что в ряде случаев для моделирования проявлений инфекционного процесса, вызываемого микроорганизмами-антропонозами и возбудителями нелетальных инфекций возможно применение методического подхода, связанного с созданием искусственной иммуносупрессии. На фоне сниженного иммунного ответа нивелируются индивидуальные различия отдельных используемых в опыте особей и полученные данные более воспроизводимы, облегчается приживление, диссеминация и размножение микробов в организме, инфекционный процесс протекает более интенсивно. Подобные методики были разработаны в отношении возбудителей таких антропонозных и зоонозных инфекций как сифилис [Зудин, Б.И. Кожные и венерические болезни / Б.И. Зудин. - М: «Медицина», 1990. - 255 с], клебсиеллез [Пат. №2279721 Российская Федерация. Способ моделирования кишечной инфекции у мелких лабораторных животных / О.В.Васильева [и др.]; заявитель и патентообладатель ГОУ ВПО Омская государственная медицинская академия. - №2004100928/14: заявл. 09.01.2004; опубл. 10.07.2006], микобактериоз [Брудная, Е.Ю. Новый метод определения вирулентности атипичных и слабовирулентных туберкулезных микобактерий / Е.Ю. Брудная, Н.Ф. Амфитеатрова, Н.М. Калугина // Журн. микробиол. -1987. - №11.- С. 9-12], сальмонеллез [Пат. №2058599 Российская Федерация. Способ моделирования грамотрицательного сальмонеллезного сепсиса / М.С. Абидов [и др.]; заявитель и патентообладатель Абидов М.С.. - №93 93009421: заявл. 18.02.1993; опубл. 20.04.1996], бруцеллез [Пат. №2209251 Российская Федерация. Способ оценки вирулентных свойств S-форм бруцелл / Л.Н. Гордиенко [и др.]; заявитель и патентообладатель Всероссийский научно-исследовательский институт бруцеллеза и туберкулеза животных. -№2001113031/13: заявл. 10.05.2001; опубл. 27.07.2003].
В приведенной группе изобретений описан наиболее близкий к заявляемому существующий способ моделирования антропонозной кишечной инфекции у мелких лабораторных животных, при котором предварительно у крыс создают иммунодефицитное состояние путем введения 2,5% суспензии гидрокортизона ацетата в дозе 0,125 мг/100 г массы тела трехкратно с интервалом в 2 суток, а затем их заражают культурой клебсиелл через зонд в полость желудка. У прототипа имеются следующие недостатки, имеющие значение при моделировании брюшного тифа. Среди мелких лабораторных животных не крысы, а морские свинки и белые мыши отличаются наибольшей чувствительностью к факторам патогенности (в частности, токсину) возбудителя брюшного тифа.
Алиментарный способ аппликации возбудителя не обеспечивает воспроизводимое развитие системной формы заболевания и не позволяет получать локальные варианты инфекционного процесса, то есть не пригоден для решения различных практических задач. При парентеральных способах аппликации (в частности, внутривенном) для моделирования системных форм заболевания обеспечивается наиболее быстрое поступление возбудителя в кровоток, полный контакт с макрофагальными клетками иммунной системы, незавершенный фагоцитоз бактерий в которых является одним из ведущих механизмов развития заболевания. При анимализации большей способностью обеспечивать приживление и размножение культур прихотливых патогенных бактерий обладает интратестикулярный метод аппликации, который имеет целый ряд преимуществ. Отсутствие необходимости преодолевать иммунные барьеры, обильное кровоснабжение паренхимы органа, относительная изолированность ввиду наличия гематотестикулярного барьера создает щадящие условия и облегчает приживление и последующее размножение бактерий. Таким образом, тестикулы выполняют роль «живого резервуара», создавая в процессе взаимодействия макроорганизма и микробной популяции определенные условия для восстановления патогенных свойств возбудителя.
Используемый для создания иммунодефицита гидрокортизон не является наиболее эффективным препаратом из группы глюкокортикоидов, а при введении в требуемых больших дозах приводит к нарушению общего состояния и возможной гибели лабораторных моделей, искажающих получаемые результаты. Из числа глюкокортикоидов дексаметазон обладает меньшей токсичностью, выраженным, воспроизводимым и универсальным для разных биологических моделей иммуносупрессивным эффектом, интенсивность которого превышает таковую гидрокортизона ацетата в 7 раз, его максимальное действие наступает через 12 ч за счет более медленного метаболизма в организме и сохраняется на протяжении 3 суток [«Регистр лекарственных средств России» 2000-2014].
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачей предлагаемого способа является моделирование брюшного тифа на мелких лабораторных животных с искусственной иммуносупрессией.
Технический результат заключается в том, что, в зависимости от моделируемых проявлений инфекционного процесса, обеспечивается возможность решения ряда практических задач, связанных с оценкой патогенных свойств микробов, анимализацией культур при поддержании в лабораторных условиях, оценкой эффективности средств этиотропного лечения.
Для выполнения заявленного технического результата предлагаются: метод создания у мелких лабораторных моделей (белых мышей и морских свинок) состояния искусственной иммуносупрессии, позволяющего нивелировать индивидуальные различия животных и обеспечивающее последующее приживление, диссеминацию и размножение в организме возбудителя при его аппликации;
метод парентеральной аппликации животным культуры возбудителя брюшного тифа в зависимости от решаемой практической задачи.
Состояние искусственной иммуносупрессии у животных создают путем введения дексаметазона ежедневно однократно в течение 3 суток внутрибрюшинно в дозе эквивалентной среднетерапевтической для человека, что составляет 2 мг/кг для белых мышей и 0,8 мг/кг для морских свинок. Через 2 суток после последней инъекции глюкокортикоида животным производят парентеральную аппликацию культуры возбудителя брюшного тифа.
Аппликацию возбудителя осуществляют в зависимости от моделируемых проявлений инфекционного процесса:
белым мышам внутрибрюшинно для моделирования эндотоксемии с целью количественного определения токсического летального эффекта (ЛД50) по методу подгрупп и сравнительной характеристики патогенных свойств штаммов;
белым мышам внутривенно в сублетальной дозе 10 млн живых микробов для моделирования системной инфекции, в частности, для оценки антимикробной эффективности антибактериальных препаратов in vivo;
морским свинкам интратестикулярно в сублетальной дозе 100 млн живых микробов для моделирования локального воспалительного очага инфекции с целью проведения анимализации культур возбудителя брюшного тифа для восстановления свойств при поддержании в лабораторных условиях.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Заявляемое изобретение подтверждается следующими примерами практического применения. Пример 1.
Характеристика иммунологических показателей у белых мышей на фоне введения дексаметазона
Белым мышам опытной группы массой 18-22 г вводили дексаметазон ежедневно однократно внутрибрюшинно в дозе 40 мкг в течение 3 суток. Для проведения исследования у каждого животного на 2, 5, 10, 20 сутки эксперимента забирали кровь в объеме 50 мкл из ретробульбарного венозного сплетения в пробирку типа «Эппендорф», куда заранее добавляли 5 мкл 0,1 М Трилон Б («SIGMA-ALDRICH», США). В качестве контроля были использованы образцы крови, взятые у тех же животных перед введением им препаратов.
Количественную оценку различных популяций (субпопуляций) лимфоцитов в крови у подопытных животных на фоне введения препаратов проводили методом проточной цитофлуориметрии, используя моноклональные антитела, окрашенные флуорохромами («Bioscience», США): CD3-РЕ-Су7, CD45-РЕ-Су5,5, CD8-PE, CD4-APC, CD19-FITC. Для подсчета абсолютного количества лимфоцитов использовали референсные частицы Flow-Count Fluorospheres («Beckman Coulter», США). Пробоподготовку образцов крови проводили согласно инструкциям, прилагаемым к моноклональным антителам и референсным частицам. Для лизиса образцов крови использовали лизирующий раствор OptiLyse® С («Beckman Coulter», Франция). Исследование окрашенных образцов осуществляли на проточном цитофлуориметре Navios («Beckman Coulter», США).
Параллельно с цитометрическим анализом оценивали динамику гематологических показателей подопытных животных, используя ветеринарный геманализатор («Exigo», Sweden).
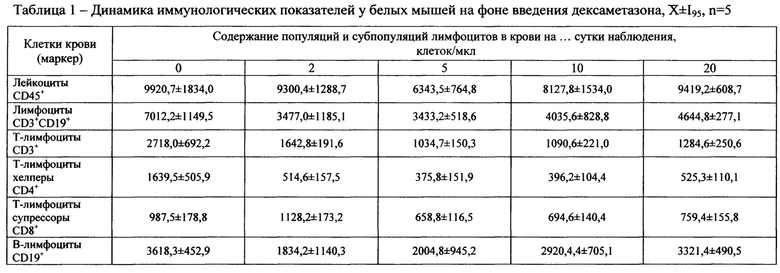
При введении дексаметазона в дозе 40 мкг на животное ежедневно однократно внутрибрюшинно в течение трех суток отмечается быстрое и интенсивное снижение содержания лимфоцитов, преимущественно за счет популяции Т-лимфоцитов. При этом максимально подавлялась субпопуляция Т-лимфоцитов хелперов, количество которых в динамике от 3,1 до 4,4 раза ниже по сравнению с фоновыми показателями. Данный эффект продолжителен и сохраняется в течение 20 суток после окончания курса введения препарата.
Начиная со 2 суток отмечается достоверное снижение абсолютного содержания В-лимфоцитов в крови животных, которое в динамике составляет от 1,1 до 2,0 раз относительно фона. При этом содержание В-лимфоцитов восстанавливается к 10 дню после последнего введения дексаметазона.
Таким образом, предложенная схема введения дексаметазона обеспечивает эффективное максимально выраженное на 5 сутки (на 2 сутки после последней инъекции) ингибирование клеточного звена иммунитета, компонентам которого принадлежит ведущая роль в формировании защиты организма от возбудителя брюшного тифа.
Пример 2.
Изучение патогенных свойств возбудителя брюшного тифа при внутрибрюшинной аппликации белым мышам с искусственной иммуносупрессией
Одним из ведущих факторов патогенности, имеющих приоритетное значение в патогенезе брюшнотифозной инфекции, является эндотоксин микробов, для количественной оценки которого используется величина летального эффекта (ЛД50) культур возбудителя брюшного тифа.
Изучение токсического летального эффекта культур S.Typhi проводили на модели белых мышей с искусственной иммуносупрессией. Для подавления иммунной системы белым мышам массой 18-22 г вводили дексаметазон ежедневно однократно внутрибрюшинно в дозе 40 мкг в течение 3 суток.
Определение величин показателя ЛД50 осуществляли по методу подгрупп. Заражение производили через 2 суток после последнего введения гормона. Наблюдение за инфицированными животными осуществляли в течение 10 суток. В качестве контроля служила группа интактных белых мышей.
В таблице 2 представлены величины показателя ЛД50 для культур нескольких штаммов возбудителя брюшного тифа.
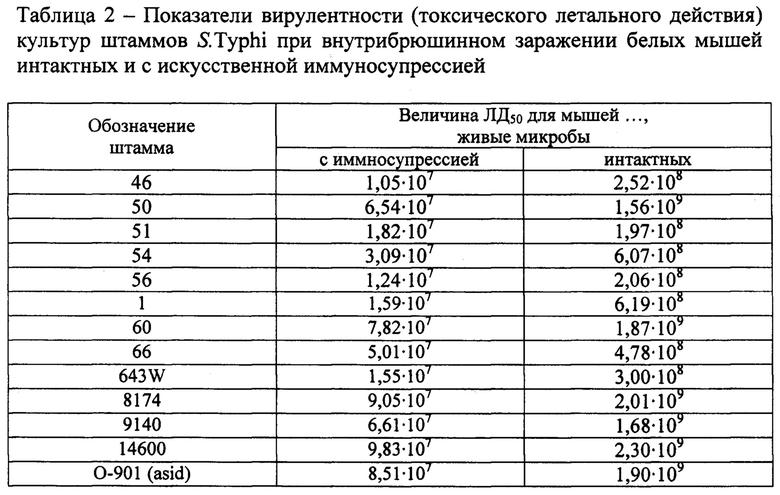
Величина показателя ЛД50 штаммов брюшнотифозных бактерий для интактных белых мышей характеризуется значительно более высокими значениями, при этом отмечается существенная вариабельность индивидуальной реактивности белых мышей к токсическому действию, искажающая параметры зависимости «доза-эффект».
В условиях искусственной иммуносупрессии токсический эффект введенных микробных культур увеличился практически на порядок, дексаметазон нивелировал индивидуальные различия в клинической картине инфекционного процесса у животных и обеспечивал закономерное проявление зависимости «доза-эффект». Получаемые данные позволяют осуществлять сравнительную оценку патогенных свойств штаммов возбудителя брюшного тифа, в том числе и стабильность этого признака в процессе поддержания.
Пример 3.
Анимализация культур штаммов возбудителя брюшного тифа при интратестикулярной аппликации морским свинкам-самцам с искусственной иммуносупрессией
Наиболее эффективным из известных к настоящему времени способов восстановления основных биологических свойств патогенных микроорганизмов при поддержании в лабораторных условиях является пассаж через организм восприимчивой лабораторной модели (анимализация).
Изучена приживляемость, уровень и динамика накопления микробов типичного штамма S.Typhi 1 при интратестикулярной аппликации морским свинкам с искусственной иммуносупрессией. Предварительно самцам массой от 450 до 550 г вводили трехкратно ежедневно дексаметазон в дозе 400 мкг внутрибрюшинно. Инфицирование осуществляли на вторые сутки после последнего введения препарата в сублетальной дозе 100 млн микробов по оптической концентрации в объеме 0,2 мл с обеих сторон. В течение срока наблюдения животных эвтаназировали, проводили экстирпацию тестикул, готовили из них гомогенат в расчетном количестве физраствора и определяли содержание в нем брюшнотифозных бактерий методом серийных десятикратных разведений (таблица 3).
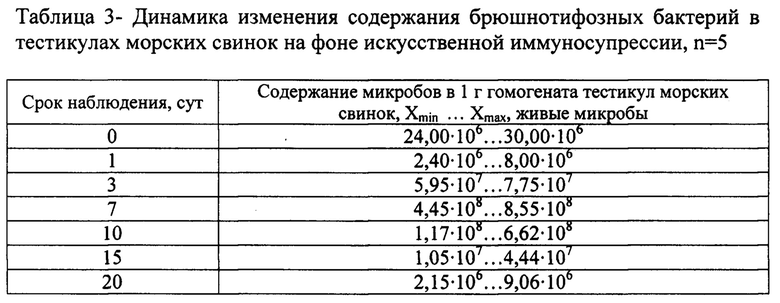
Полученные данные свидетельствуют, что искусственная иммуносупрессия обеспечивает не только приживление, но и размножение микробов в период на 3-7 сутки, затем идет постепенное снижение содержания брюшнотифозных бактерий, но без их полной элиминации. Следовательно, для получения анимализированной культуры, микробов целесообразно выделять в период максимального их накопления (3-7 сутки).
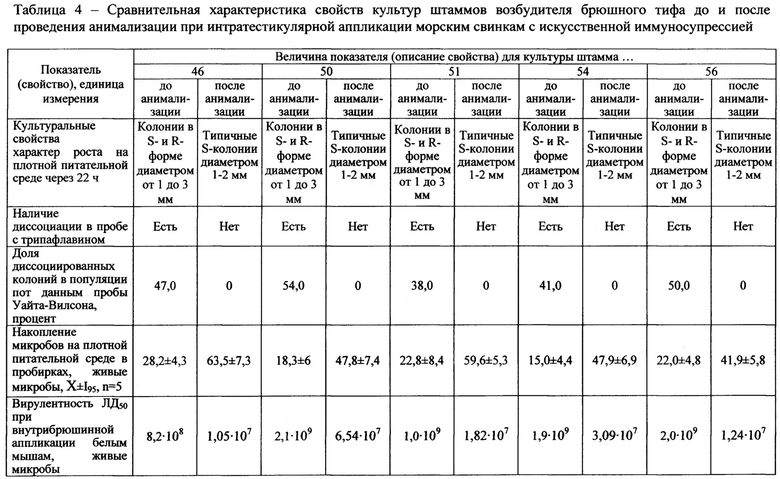
Подобным образом путем тестикулярного пассажа через организм морских свинок были анимализированы культуры нескольких клинических изолятов S.Typhi 46, 50, 51, 54, 56, которые после поддержания в лабораторных условиях обнаруживали признаки нарушения основных биологических свойств (диссоциация, ухудшение ростовых свойств, снижение патогенности). Выделение культуры осуществляли на 5 сутки из гомогената тестикул на плотную питательную среду в чашках Петри по методу Дригальского.
Выделенные после анимализации культуры морфологически представляли собой стойкую S-форму, сохраняли исходную антигенную структуру и при этом характеризовались более быстрым и интенсивным ростом на искусственных питательных средах. Так, накопление микробов анимализированных культур на агаризованной среде в пробирках увеличилось от 1,9 до 3,2 раза по сравнению с исходными величинами (таблица 4).
Пример 4.
Воспроизведение системной брюшнотифозной инфекции при внутривенной аппликации возбудителя белым мышам с искусственной иммуносупрессией
Опыты проводили на белых мышах. Предварительно определили величину оптимальной дозы возбудителя брюшного тифа для внутривенного инфицирования белых мышей. Она должна быть максимально возможной, чтобы обеспечить эффективное приживление и размножение микробов в органах, но при этом не вызывать гибели подопытных животных. Величина показателя ЛД50 культуры штамма S. Typhi 46 при внутривенной аппликации белым мышам в условиях искусственной иммуносупресии составила 121 млн живых бактерий, а требуемая сублетальная инфицирующая доза находится в пределах от 1 до 10 млн живых микробов. При использовании указанной дозы в отсутствие гибели животных в течение более 20 суток удается стабильно выделять возбудитель брюшного тифа из гомогената печени и селезенки мышей на плотной питательной среде в чашках Петри.
Изучали динамику накопления бактерий типичного штамма S. Typhi 46 во внутренних органах внутривенно инфицированных белых мышей. Для создания искусственной иммуносупрессии животным предварительно в течение трех суток внутрибрюшинно вводили дексаметазон в дозе 40 мкг. Через 2 суток после последней инъекции мышей инфицировали суспензией агаровой культуры сальмонелл в ретробульбарное венозное сплетение в дозе порядка 10 млн микробов по оптической концентрации.
Накопление микробов оценивали путем высева серийных разведений гомогената внутренних органов на плотную питательную среду в чашках Петри с последующим подсчетом числа выросших колоний. Изучение данного показателя проводили через 30 мин, 1, 2, 3, 4, 7, 15, 20 и 30 сут с момента заражения. Для приготовления гомогената использовали пробы органов общей массой 0,4 г, состоящие из целой селезенки (0,2 г) и кусочка ткани печени (0,2 г). Полученные результаты представлены в таблице 5.
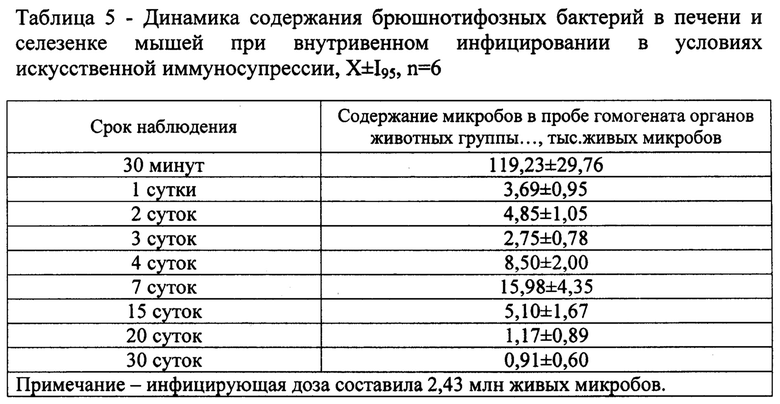
Полученные данные показывают, что у мышей с иммуносупрессией отмечается быстрая диссеминация, приживление и последующая персистенция возбудителя брюшного тифа (системная инфекция). В отсутствие воздействия внешних факторов, численный уровень микробной популяции во внутренних органах инфицированных мышей сохраняется достаточно стабильно на протяжении 15 сут наблюдения и лишь к 30 сут отмечается его естественное снижение. Следовательно, в течение указанных 15 сут с момента инфицирования возможно проводить оценку влияния внешних факторов на параметры популяции сальмонелл во внутренних органах.
Пример 5.
Оценка антимикробной активности антибактериальных препаратов на модели системной брюшнотифозной инфекции при внутривенной аппликации возбудителя белым мышам с искусственной иммуносупрессией
Моделирование системной брюшнотифозной инфекции и контроль динамики процесса по накоплению микробов во внутренних органах осуществляли аналогично примеру 4.
Белых мышей с искусственной иммуносупрессией инфицировали внутривенно в дозе 10 млн микробов по оптической концентрации культурой типичного штамма 5. Typhi 46. Одновременно с инфицированием белым мышам начинали вводить антибактериальные препараты в дозах эквивалентных среднетерапевтическим для человека. Препараты вводили в течение 5 суток в соответствии с инструкциями по применению.
Антимикробную активность препаратов оценивали по влиянию на динамику накопления микробов во внутренних органах, которое определяли путем высева серийных разведений их гомогената на плотную питательную среду с последующим количественным учетом числа выросших колоний. Пробы гомогената печени и селезенки готовили, как описано в примере 4. Для удобства интерпретации результатов рассчитывали показатель отношения содержания микробов в пробах гомогената контрольной и опытных групп («индекс антимикробной активности») на 7 суток наблюдения (через 2 суток после последнего введения антибиотика). Наличие промежутка времени от момента окончания курсов антибиотиков до начала исследования дает возможность отследить вероятность рецидива инфекции в случае, если препараты не обеспечивают необходимого клинического эффекта. Полученные результаты представлены в таблице 6.
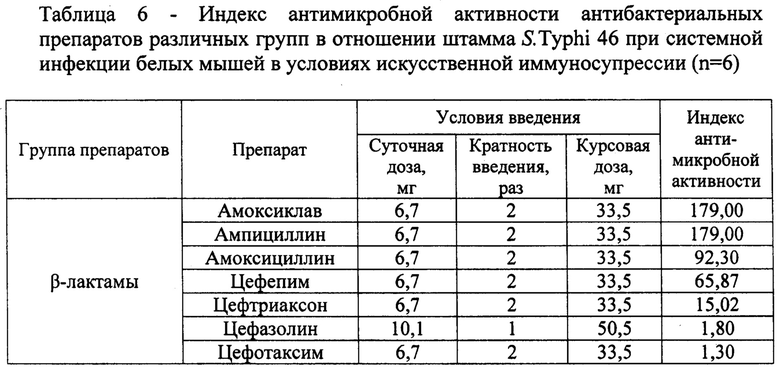
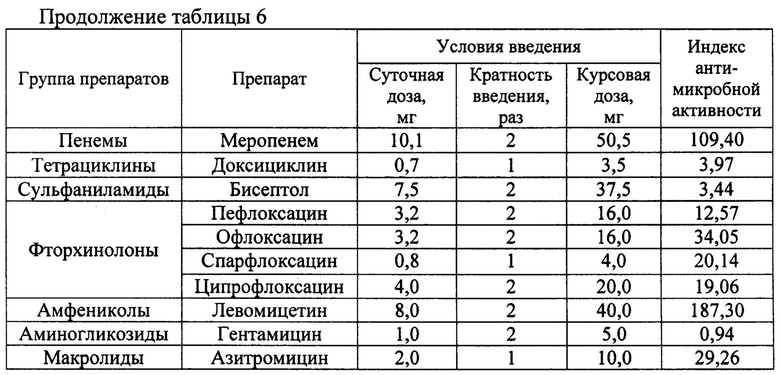
Полученные данные свидетельствуют, что при оценке антимикробной активности антибактериальных препаратов в отношении возбудителя брюшного тифа на модели системной инфекции у белых мышей с искусственной иммуносупрессией их влияние на количественное содержание бактерий во внутренних органах лабораторных животных значительно отличается (величина индекса антимикробной активности варьирует в пределах от 0,94 до 187,30), что сопоставимо с их эффективностью при практическом использовании для лечения брюшного тифа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАСЧЕТА ДОЗЫ ДЕКСАМЕТАЗОНА ДЛЯ РАЗРАБОТКИ БИОЛОГИЧЕСКОЙ МОДЕЛИ ИММУНОСУПРЕССИИ НА МЫШАХ | 2020 |
|
RU2748123C1 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ ВАКЦИОННОГО ШТАММА ЧУМНОГО МИКРОБА | 2019 |
|
RU2727258C1 |
| Вакцина и способ повышения иммуногенности и специфической активности средств профилактики инфекций | 2020 |
|
RU2741834C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЛЕГОЧНОГО САПА | 1998 |
|
RU2141135C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ КИШЕЧНОГО ИЕРСИНЕОЗА У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2014 |
|
RU2566188C1 |
| ВАКЦИННЫЙ ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ БРЮШНОГО ТИФА | 1997 |
|
RU2111012C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИВАЛЕНТНОЙ ВАКЦИНЫ ПРОТИВ КИШЕЧНЫХ ИНФЕКЦИЙ | 1992 |
|
RU2080875C1 |
| Способ эрадикации бактерий Helicobacter pylori при экспериментальном хеликобактериозе у конвенциональных белых мышей и средство для его осуществления | 2020 |
|
RU2746590C1 |
| ИММУНОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 1989 |
|
RU2032403C1 |
| СПОСОБ ПРЕДОТВРАЩЕНИЯ РАЗВИТИЯ КИШЕЧНОЙ ИНФЕКЦИИ БАКТЕРИАЛЬНОЙ ПРИРОДЫ | 2012 |
|
RU2526806C2 |
Изобретение относится к области экспериментальной медицины и медицинской микробиологии. Морским свинкам в течение 3 суток ежедневно однократно внутрибрюшинно вводят дексаметазон в дозе 0,8 мг/кг. Через 2 суток после последней инъекции животным вводят интратестикулярно культуру возбудителя в сублетальной дозе 100 млн живых микробов. Способ позволяет получить развитие некоторых проявлений инфекционного процесса, использование которых необходимо для решения ряда практических задач, связанных с оценкой патогенных свойств микробов, анимализацией лабораторных культур, оценкой эффективности средств лечения и профилактики. 6 табл., 5 пр.
Способ моделирования брюшного тифа на мелких лабораторных животных с искусственной иммуносупрессией, заключающийся в том, что морским свинкам в течение 3 суток ежедневно однократно внутрибрюшинно вводят дексаметазон в дозе 0,8 мг/кг, через 2 суток после последней инъекции животным вводят интратестикулярно культуру возбудителя в сублетальной дозе 100 млн живых микробов для получения локального воспалительного очага инфекции.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Renee M | |||
| Tsolis et al | |||
| How To Become a Top Model: Impact of Animal Experimentation on Human Salmonella Disease Research, Infect Immun, 2011, May, 79, 5, 1806-1814 | |||
| Song J | |||
| et al | |||
| A mouse model for the human pathogen Salmonella typhi, Cell Host Microbe, 2010, Oct, 21, 8,4, 369 | |||
| Carter PB et al | |||
| Growth of typhoid and | |||
Авторы
Даты
2020-03-16—Публикация
2019-03-26—Подача