Изобретение относится к медицине, в частности, к препарату для профилактики и лечения брюшного тифа на основе Ви-антигена, выделенного из возбудителя заболевания.
Брюшной тиф - инфекционное заболевание, вызываемое Salmonella typhi. Возбудитель, попав в пищеварительный тракт, поступает в лимфоидную ткань и мезентериальные узлы, где происходит его интенсивное размножение. Размножившись в местах первичной локализации, к концу инкубационного периода бактерии проникают в кровь и вызывают период длительной бактериемии. Трудности диагностики данного заболевания, а также появление штаммов с множественной устойчивостью к антибиотикам затрудняют проведение эффективной терапии, увеличивают количество осложнений, повышают уровень смертности. В настоящее время брюшной тиф все еще остается серьезным заболеванием.
Наиболее эффективным методом борьбы с инфекционными заболеваниями является вакцинация. Ранее для вакцинации в основном использовали препараты аттенуированных штаммов возбудителя Salmonella typhi (патент Франции 2538703, 1984).
Исследования последних лет показали, что вирулентность бактерии обусловлена капсулярным Ви-антигеном, полисахаридом по своей химической природе.
Наиболее близким аналогом предлагаемому препарату является Тифим Ви на основе Ви-антигена, который представляет собой дорогостоящий зарубежный препарат (Morand P., Stahl J.P., 1992).
Задачей изобретения является создание отечественной высокоочищенной вакцины на основе капсулярного Ви-антигена, выделенного и очищенного особым способом.
Для приготовления вакцины используют Ви-антиген, полученный следующим образом. Микроорганизмы S.typhi культивируют на питательной среде, бактериальные клетки отделяют центрифугированием, супернатант стерилизуют микрофильтрацией с использованием мембран с размером пор 0,22 мк, фильтрат концентрируют с помощью системы "Пелликон" или "Амикон" до объема 0,1-0,2% от исходного и подвергают ультрацентрифугированию при 105,000 g. Полученный супернатант обрабатывают дезоксирибо- и рибонуклеазами, затем проназой. Реакционную смесь наносят на колонку, заполненную сефадексом на Трис-НСl/NaCl буфере, рН 8,0, содержащем ЭДТА и NaNO3, после гель-хроматографии получают Ви-антиген. Очищенный антиген является апирогенным полисахаридом и содержит менее 1% белка и менее 1,5% нуклеиновых кислот.
На основе очищенного антигена готовят вакционный препарат, смешивая следующие компоненты в определенных количествах, мас.%: Ви-антиген 0,004-0,006; гидроортофосфат натрия 0,01-0,02; дигидроортофосфат натрия 1,75-1,85; хлорид натрия 0,84-0,90; фенол 0,10-0,15; вода дистиллированная до 100.
Полученный препарат можно хранить при 2-8oС в течение 18 мес.
Действие вакцины, условно обозначенной ВИАНВАК исследовано на экспериментальных животных, где показаны иммуногенные свойства препарата.
Пример 1. В основе защитного эффекта Ви-антигенных тифоидных вакцин лежит индукция выраженного гуморального иммунного ответа у иммунизированных индивидуумов. В периферической крови определяются специфические анти-Ви антитела, нейтрализующие возбудитель и предотвращающие возникновение инфекции.
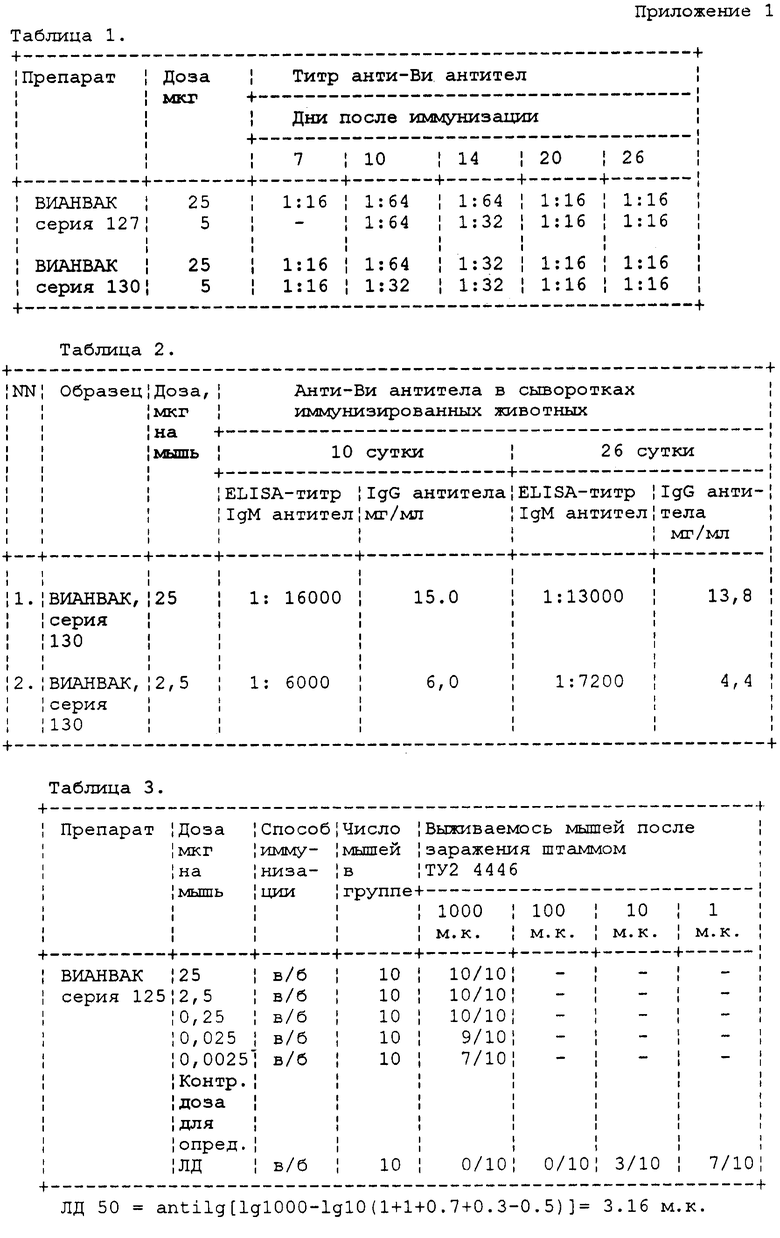
Мышей линии (СВАхС57В1/6)FI иммунизируют сериями вакцины ВИАНВАК в дозах 25 и 5 мкг. Первая доза является вакцинальной человеческой дозой, вторая иммуногенной дозой для мышей. Через 7, 10, 14, 20, 26 дней у животных забирают сыворотку периферической крови и определяют специфические анти-Ви антитела различными методами иммуноанализа. В табл. 1 представлены данные о специфических антителах, определяемых в реакции пассивной гемагглютинации с Виантигенным диагностикумом.
Как видно из табл. 1, препарат развивает существенный иммунный ответ после однократного введения, титр анти-Ви антител достигает на пике ответ на 10-е сутки и сохраняется достаточно долго на высоком уровне.
Основные классы специфических анти-Ви антител определяют с помощью иммуноферментного анализа, используя изотип-специфические анти-IgG и анти-IgM антитела, конъюгированные с пероксидазой. Содержание IgG антител оценивают, используя в качестве стандарта препаративно выделенные из сыворотки мыши анти-Ви антитела в определенной концентрации. Содержание IgM в сыворотке оценивают по конечному титру (табл. 2).
После иммунизации животных препаратом вакцины ВИАНВАК в периферической крови определяется существенное количество основных классов антител IgG, IgM К Ви-антигену. Таким образом, два важнейших в плане нейтрализации возбудителя класса антител представлены в сыворотках иммунизированных животных.
Оценку препарата проводят в соответствии с протоколом заражения, рекомендованным ВОЗ для испытания протективной активности живой аттенуированной вакцины Ту-21А, тифопаратифоидной вакцины. Настоящая модель использовалась и для изучения защитных свойств ближайшего аналога настоящего препарата Ви-антигенной вакцины Ви-Тифум производства компании "Пастер&Мерье" (Франция). Оценка протективной активности проводится на лабораторных животных мышах весом 18-20 г, иммунизированных вакционным препаратом. Заражение животных высоковирулентным контрольно-производственным штаммом S. typhi Ty2 N4446 проводят с сенсибилизатором муцином, полученным из желудка поросенка (Sigma, CША), который добавляют в стерильный физраствор для инъекций до конечной концентрации 5%. Для иммунизации и заражения используется интраперитонеальный путь введения. Интервал между иммунизацией и заражением составляет 10-14 дней.
Доза заражения 1000 микробных клеток (м.к.) на мышь. Она также стандартна и применяется для тестирования вакцин Ви-Тифум и тифоидно-паратифоидной. Вирулентность суспензии клеток в муцине, используемой для заражения иммунизированных вакциной мышей, должна быть высокой и обязательно параллельно контролируется по параметру ЛД 50. Для этого интактных мышей той же партии заражают рабочей суспензией клеток в стандартной концентрации 1000 м.к. на мышь и дозами 100, 10, 1 м.к. на мышь, полученными в результате серийных 10-кратных разведений рабочей суспензии стерильным физиологическим раствором с 5% содержанием муцина.
Учет гибели животных в опыте и контроле проводят в течение 3-х суток. Расчет ЛД 50 проводят по методу Рида и Менча. Заражающий штамм считают удовлетворяющим требованиям контрольной модели, если его ЛД 50 меньше 20 м.к. Если ЛД 50 шт мм более 20 м.к., то результаты основного эксперимента по оценке протективной активности считают недостоверными.
Пример 2. Мышей линии (СВАхС57В1/6)F1 иммунизировали препаратом вакцины ВИАНВАК серия 125 в дозах 25; 2,5; 0,25; 0,025; 0,0025 мкг внутрибрюшинно. На 12 день мышей заражали штаммом Ту2 N4446 в дозе 1000 м.к. Данные о выживаемости животных представлены в табл. 3.
Как видно из табл. 3, препарат обеспечивает прочную 100%-ную защиту животных как при введении в дозе 25 мкг - 1 человеческая доза, так и при введении в дозе 2,5 и 0,25 мкг. ЛД 50 вирулентного штамма при заражении в рамках требований ВОЗ.
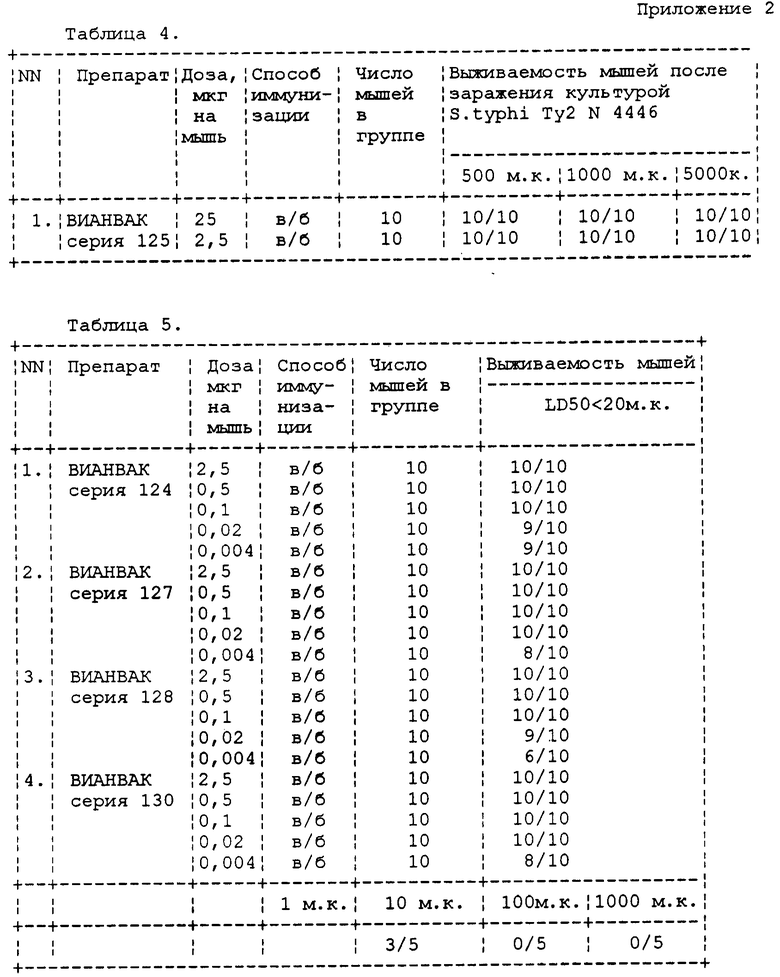
Мышей линии (СВАхС57В1/6)А1 иммунизировали препаратом вакцины ВИАНВАК серия 125 в человеческой дозе 25 мкг и 1/10 человеческой дозы - 2,5 мкг внутрибрюшинно. На 12 день мышей заражали штаммом Ту2 N4446 в дозах 500, 1000, 5000 м.к. Выживаемость животных представлена в табл. 4.
Как видно из табл. 4, препарат обеспечивает защиту животных при введении в дозе 25 мкг - 1 человеческая доза, так и при введении в 1/10 человеческой дозы 2,5 мкг. При этом максимальная доза заражения 5000 м.к. в 5 раз превышает стандартную.
Пример 3. Сравнение протективных активностей серий препарата на мышах (СВАхС57В1/6)F1 представлено в табл. 5. Введены дозы 2,5; 0,5; 0,1; 0,02; 0,004 мкг на мышь. Мышей заражали стандартной дозой 1000 м.к. на мышь.
Как представлено в табл. 5, все испытанные серии ВИАНВАК надежно защищают мышей в широком диапазоне доз иммунизации: 2,5; 0,5; 0,1 мкг. ЛД 50 для всех серий препаратов находится ниже уровня 0,004 мкг. Таким образом, протективный эффект серий препарата является стандартным и воспроизводимым.
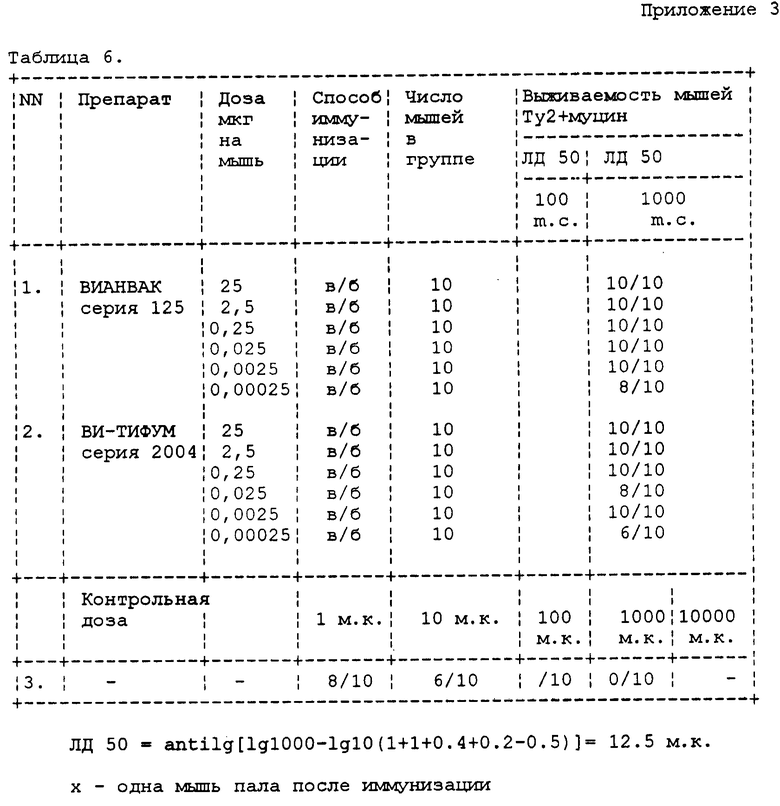
Пример 4. Проведено сравнение протективных свойств препарата ВИАНВАК с его ближайшим аналогом - вакциной Ви-Тифум. Препараты в эквивалентной по Ви-антигену дозах вводили мышам в широком диапазоне доз: 25, 2,5, 0,25, 0,025, 0,0025, 0,00025 мкг и заражали их на 12 и 13 сут. Данные о выживаемости животных представлены в табл. 6.
Как представлено в табл. 6, протективная активность препарата ВИАНВАК сопоставима с протективной активностью вакцины Ви-Тифум (Франция).
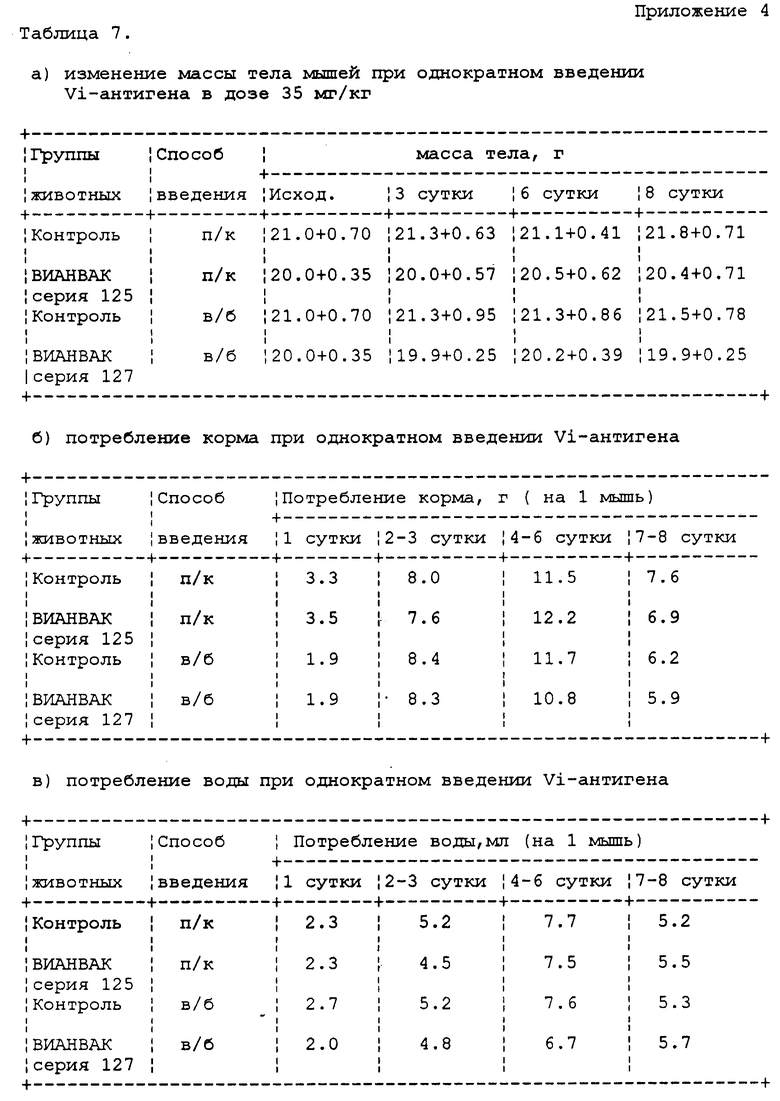
Пример 5. Изучение острой токсичности субстанции ВИАНВАК - проведено на 28 мышах самках гибридах (СВАхС57В1/6)F1 массой 19-21 г и морских свинках самках массой 240-260 г при однократном внутрибрюшинном и подкожном способах введения препарата, растворенного в физиологическом растворе. ВИАНВАК вводили в дозе 35 мг/кг, что в 10 раз превышает рекомендуемую для человека дозу вакцины: 25 мкг на 70 кг или 0,35 мкг/кг. Визуальные наблюдения за животными проводились в течение 8 дней, следили за поведением, внешним видом животных, потреблением корма и воды, изменением массы тела. На 8 сутки животных забивали и брали внутренние органы на морфологическое исследование.
Результаты наблюдений показали, что после введения препарата опытные животные по внешнему виду не отличались от контрольных, были активны, признаков интоксикации не отмечалось. В табл. 7 (а, б, в) представлены данные по изменению массы тела мышей, потребления корма и воды при подкожном введении ВИАНВАК.
Из приведенных данных следует, что как при внутрибрюшинном, и так и при подкожном способах введения ВИАНВАК отсутствует потеря массы мышей. Потребление корма и воды опытными животными также не отличалось от потребления контрольными.
Наблюдение за морскими свинками, которым ВИАНВАК вводили внутрибрюшинно, показало, что опытные морские свинки прибавляют в весе как и контрольные животные (табл. 8).
Таким образом, можно сделать заключение, что введение ВИАНВАКА в дозе, превышающей рекомендуемую для человека в 10 раз, не вызывает токсических эффектов как при подкожном, так и внутрибрюшинном способах введения. Дальнейший расход препарата на проведение исследования по установлению LD 50 ВИАНВАК представлялось нецелесообразным из-за отсутствия сколько-нибудь выраженного токсического эффекта при столь значительной передозировке вакцины в 100000 раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ ФРАКЦИИ (БАФ), СОДЕРЖАЩЕЙ S-ЛИПОПОЛИСАХАРИДЫ (S-ЛПС) ИЗ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ, БАФ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЕМЫХ ГРАМОТРИЦАТЕЛЬНЫМИ БАКТЕРИЯМИ, ПРОИЗВОДЯЩИМИ ЭНДОТОКСИЧНЫЕ S-ЛПС, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБЫ ИНДУКЦИИ ПРОТЕКТИВНОГО ИММУНИТЕТА И УЛУЧШЕНИЯ СОСТОЯНИЯ ПАЦИЕНТА ПРИ СОСТОЯНИЯХ, ТРЕБУЮЩИХ ПОВЫШЕНИЯ ИММУННОГО СТАТУСА | 2002 |
|
RU2260053C2 |
| СПОСОБ ПОЛУЧЕНИЯ VI-АНТИГЕНА | 1993 |
|
RU2088244C1 |
| НИЗКОТОКСИЧНЫЙ, НИЗКОПИРОГЕННЫЙ ЛИПООЛИГОСАХАРИД ИЗ NEISSERIA MENINGITIDIS | 1998 |
|
RU2161037C2 |
| ШТАММ БАКТЕРИЙ HAEMOPHILUS INFLUENZAE В №326, СТАБИЛЬНЫЙ ПРОДУЦЕНТ КАПСУЛЬНОГО ПОЛИСАХАРИДА | 2011 |
|
RU2465316C1 |
| ШТАММ БАКТЕРИЙ SHIGELLA SONNEI, ФАЗА 1, СТАБИЛЬНЫЙ ПРОДУЦЕНТ S-ЛИПОПОЛИСАХАРИДА | 2001 |
|
RU2241031C2 |
| ШТАММ БАКТЕРИЙ Shigella flexneri № 1605-8 СЕРОТИП 2a, ДЕПОНИРОВАННЫЙ В ФГУН ГИСК ИМ. Л.А.ТАРАСЕВИЧА ПОД НОМЕРОМ 285, СТАБИЛЬНЫЙ ПРОДУЦЕНТ S-ЛИПОПОЛИСАХАРИДА | 2009 |
|
RU2415921C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСНОГО ШИГЕЛЛЕЗНОГО ПРЕПАРАТА | 2015 |
|
RU2614123C1 |
| Вакцина и способ повышения иммуногенности и специфической активности средств профилактики инфекций | 2020 |
|
RU2741834C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К КАПСУЛЬНОМУ ПОЛИСАХАРИДУ Haemophilus influenzae ТИПА b | 2006 |
|
RU2331075C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕКТИВНОЙ БЕЛОКСОДЕРЖАЩЕЙ ФРАКЦИИ БАКТЕРИЙ | 2013 |
|
RU2533815C1 |

Вакцинный препарат содержит Ви-антиген из Salinonella typhi, обработанный рибонуклеазами и проназой и очищенный гель-фильтрацией, а также гидрофосфат и ортофосфат натрия и фенол для консервации. Препарат по своим иммуногенным свойствам не уступает наиболее близкому зарубежному аналогу и может быть успешно использован в качестве специфического протективного средства при брюшном тифе. 8 табл.
Вакцинный препарат для профилактики брюшного тифа на основе физиологического раствора капсулярного Ви-антигена, выделенного из Salmonella typhi, содержащий вспомогательные вещества, отличающийся тем, что препарат содержит антиген, дополнительно обработанный дезокси- и рибонуклеазой, затем проназой и очищенный гель - фильтрацией, а в качестве вспомогательных веществ содержит гидроортофосфат и дигидроортофосфат натрия и фенол при следующем соотношении компонентов, мас.%:
Ви-антиген - 0,004 - 0,006
Гидроортофосфат натрия - 0,01 - 0,02
Дигидроортофосфат натрия - 1,75 - 1,85
Хлорид натрия - 0,84 - 0,90
Фенол - 0,10 - 0,15
Вода дистиллированная - До 100с
| Robbins J.D | |||
| et al | |||
| Resxamination of the protective role of the capsular polysaccharides (Vi-antigen of S.typhi) J.Infect | |||
| Dis., 1984, 150 (3), 436 - 449 | |||
| DE 297331 (Coopers Animal Health Lim.GB.), 09.01.92, A 61 K 39/39 | |||
| EP 047726 (The Wellcome Faundation Lim.), 15.11.90, A 61 K 39/00. |
Авторы
Даты
1998-05-20—Публикация
1997-04-15—Подача