[0001] Настоящая заявка испрашивает приоритет на основании находящейся на одновременном рассмотрении предварительной заявки на патент США №62/178956, поданной 23 апреля 2015 года, и предварительной заявки на патент США №62/159145, поданной 8 мая 2015 года; обе эти заявки включены в настоящий документ посредством ссылки.
Область техники
[0002] Областью настоящего изобретения являются неоэпитопы рака, и, в частности, идентификация и применение неоэпитопов в получении специфичных к неоэпитопам антител, а также применению неоэпитопов и специфичных к неоэпитопам антител в профилактике и терапии.
Уровень техники
[0003] Описание уровня техники включает информацию, которая может быть полезна для понимания настоящего изобретения. Это не является признанием того, что какая-либо представленная в настоящем документе информация является предшествующим уровнем техники или имеет отношение к заявленному изобретению, или что какая-либо упомянутая напрямую или косвенным образом публикация является предшествующим уровнем техники.
[0004] В данной области техники хорошо известно, что большинство, если не все неопластические заболевания сопровождаются относительно большим количеством мутаций, включая точечные мутации, вставки, делеции и транслокации. Таким образом, по меньшей мере теоретически разумно предположить, что неопластические клетки также могут характеризоваться присутствием одного или более мутированных белков. Позднее в результате многочисленных исследований стала доступна довольно небольшая коллекция опухолевых антигенов человека, определяемых Т-клетками (см., например, Cancer Immunity (15 июля 2013 г.), Vol. 13, р. 15) для ограниченного числа типов опухолей. К сожалению, эти антигены не обеспечили получение эффективного терапевтического агента для конкретного типа опухоли. Все процитированные в настоящем документе публикации включены посредством ссылки в той же степени, как если бы для каждой отдельной публикации или заявки на патент было конкретно и отдельно указано, что она включена посредством ссылки. Кроме того, если определение или использование термина во включенном цитируемом источнике не согласуется или противоречит определению данного термина, приведенного в настоящем документе, применяется определение этого термина, приведенное в настоящем документе, а определение этого термина, данное в цитируемом источнике, не применяется.
[0005] В числе других возможных причин неудач с получением иммунотерапевтического агента для конкретной опухоли, наблюдаемое случайное распределение мутаций в большинстве опухолей у различных пациентов с одинаковым типом опухоли серьезно усложнило задачу идентификации одного или более антигенов, которые можно было бы применять в качестве иммунологически эффективного агента. Более того, поскольку иммунный ответ на конкретный антиген также зависит от способности индивидуума к связыванию и презентации антигена HLA-комплексом (комплексом лейкоцитарных антигенов человека), статистическая вероятность идентификации подходящего антигена для лечения опухоли у нескольких пациентов является очень низкой. Таким образом, идентификация пациент-специфичных опухолевых антигенов по меньшей мере теоретически должна с большой долей вероятности привести к эффективному получению терапевтического агента.
[0006] К сожалению, поскольку многие опухоли выработали различные механизмы «ускользания» от иммунологического надзора, потенциально подходящий пациент и опухолеспецифичные антигены обычно не вызывают терапевтически эффективный иммунный ответ или даже выработку антител, которые могли бы связываться с пациент-специфичным и опухолеспецифичным антигеном. Более того, даже если бы у пациента вырабатывались В-клетки, которые образуют антитела со специфичностью к пациент-специфичномй и опухолеспецифичному антигену, выделение таких В-клеток является довольно сложным и трудоемким процессом. Аналогичным образом, выделение терапевтически полезных количеств антител от таких пациентов так же трудоемко и времязатратно, и вероятно превысит ожидаемое время жизни пациента. Кроме того, даже если было бы возможным получать достаточное количество антител против одного пуциент-специфичного и опухолеспецифичного антигена, гетерогенность многих опухолей может, тем не менее, сделать лечение неэффективным, поскольку возможно не все клетки в массе опухоли экспрессируют тот же антиген. Кроме того, даже если было бы возможным продуцировать в или выделить различные терапевтические антитела из млекопитающего для применения у отдельно взятого пациента, такой подход был бы совершенно неподходящим в качестве платформы для массового производства для большого числа пациентов, нуждающихся в иммунотерапии. Действительно, традиционное получение моноклональных антител против единственного антигена зачастую занимает много месяцев.
[0007] Таким образом, даже несмотря на то, что способы получения антител хорошо и широко известны в данной области техники, до сих пор существует потребность в системах и способах, которые позволяют быстро идентифицировать пациент-опухолевые антигены и в сжатые сроки получать антитела, нацеленные на такие антигены, для диагностического или терапевтического применения.
Краткое описание изобретения
[0008] Заявленное изобретение относится к идентификации и применению различных неоэпитопов рака у этого пациента, в частности, в тех случаях, когда такие неоэпитопы не вызывают защитного иммунного ответа у указанного пациента.
[0009] В одном аспекте заявленного изобретения предложен способ получения фармацевтического агента для иммунотерапии раковых заболеваний. Особенно предпочтительные способы включают этап применения «омных» данных опухоли, для которых есть парные (matched: син. - соответствующие, сопоставляемые) нормальные данные, для получения с применением методов компьютерного моделирования (in silico) множества n-меров, которые содержат по меньшей мере один пациент- и рак-специфичный неоэпитоп рака, и дополнительный этап отбора (filtering) in silico n-меров с получением подмножества последовательностей неоэпитопов. На еще одном этапе по меньшей мере один синтетический n-мерный пептид получают с применением информации о последовательности из подмножества последовательностей неоэпитопов, и затем указанный синтетический n-мерный пептид используют для выделения рекомбинантного антитела. Получают информацию о последовательности определяющего комплементарность участка рекомбинантного антитела, и получают синтетическое антитело с применением указанной информации о последовательности определяющего комплементарность участка рекомбинантного антитела. Затем на еще одном этапе синтетическое антитело можно присоединить к терапевтическому или диагностическому агенту с получением фармацевтического агента.
[0010] В целом предусмотрено, что омные данные, для которых есть парные нормальные данные, представляют собой данные полногеномного секвенирования, данные экзомного секвенирования и/или данные транскриптома, и что омные «данные», для которых есть парные нормальные данные, сопоставляют с нормальными данными до лечения пациента. Кроме того предполагается, что каждый из множества n-мерных пептидов имеет длину от 7 до 11 аминокислот, и/или что множество n-мерных пептидов составляет по меньшей мере 1000 n-мерных пептидов. В наиболее типичном варианте различные n-мерные пептиды из множества n-мерных пептидов содержат разные неоэпитопы. Без ограничения заявленного изобретения предполагается также, что этап отбора включает отбор по типу мутации, отбор по силе экспрессии, отбор по субклеточной локализации и/или отбор по аффинности связывания с некоторым типом HLA у пациента.
[0011] Кроме того предусмотрено, что этап применения синтетического n-мерного пептида с выделением рекомбинантного антитела включает фаговый пэннинг, которая может дополнительно включать этап созревания аффинности. Также предусмотрено, что информация о последовательности определяющего комплементарность участка рекомбинантного антитела включает информацию о последовательности CDR1-H, CDR2-Н и CDR3-H и необязательно CDR1-L, CDR2-L и CDR3-L, и/или что синтетическое антитело получают с применением методики «пересадки» (grafting) CDR или SDR на скаффолд человеческого антитела.
[0012] Предусмотренные синтетические антитела обычно получают путем рекомбинантной экспрессии в виде IgG, F(ab')2, Fab', Fab или scFv, а предусмотренные терапевтические или диагностические агенты включают неклеточные агенты (например, химиотерапевтическое лекарственное средство, радиоизотоп, изотоп, детектируемый методом позитронно-эмиссионной томографии (PET), изотоп, детектируемый методом однофотонной эмиссионной компьютерной томографии (SPECT), аффинный агент и т.д.) и иммунокомпетентные клетки (например, Т-клетка, клетка-природный киллер (NK-клетка) и т.д.). Например, в том случае, когда клетка представляет собой Т-клетку, указанная Т-клетка может экспрессировать химерный рецептор, содержащий scFv в качестве эктодомена, причем синтетическое антитело представляет собой scFv. В альтернативном или дополнительном варианте, в том случае, когда клетка представляет собой NK-клетку, указанная NK-клетка может экспрессировать высокоаффинный Fcγ-рецептор (CD16), и синтетическое антитело в таком случае может представлять собой IgG, который связывается с указанной NK-клеткой через указанный высокоаффинный Fcγ-рецептор. В первую очередь, соответственно, следует принимать во внимание, что пациент- и рак-специфические антитела и композиции, содержащие такие антитела, можно получить за исключительно короткое время (например, за менее, чем 8 недель или менее, чем 6 недель или даже менее, чем 4 недели), даже в тех случаях, когда у пациента не вырабатывается эффективный и защитный иммунный ответ на неоэпитоп.
[0013] Таким образом, авторы настоящего изобретения также предлагают способ получения синтетического антитела против неоэпитопа рака у этого пациента, при этом указанный неоэпитоп рака не способен вызывать защитный иммунный ответ. Предусмотренные способы обычно включают этап применения неоэпитопа рака (обычно полностью синтетического) для выбора связывающего рекомбинантного антитела из библиотеки рекомбинантных антител, причем указанный неоэпитоп рака является пациент- и рак-специфичным. Затем на другом этапе гипервариабельные петли анализируют в связывающем рекомбинантном антителе, получая таким образом информацию о специфичности связывающего рекомбинантного антитела, и ген, кодирующий по меньшей мере часть антитела человека, модифицируют с применением указанной информации о специфичности. В заключение затем указанный ген рекомбинантно экспрессируют с получением синтетического антитела. Следует отметить, что таким образом получают пациент- и рак-специфичное антитело без применения иммунной системы млекопитающих.
[0014] В отдельно предусмотренных способах неоэпитоп рака представляет собой HLA-парный неоэпитоп и/или библиотека рекомбинантных антител представляет собой библиотеку на основе фагового дисплея. При желании указанный способ может дополнительно включать этап созревания аффинности связывающего рекомбинантного антитела с получением оптимизированного связывающего рекомбинантного антитела. Независимо от дополнительных этапов, гипервариабельные петли предпочтительно анализируют путем секвенирования ДНК, которая кодирует указанные гипервариабельные петли, а этап модификации предпочтительно включает «пересадку» (grafting) CDR или SDR (например, когда часть антитела человека представляет собой scFv). Рекомбинантная экспрессия модифицированного гена затем приведет к получению синтетического антитела в форме IgG, F(ab')2, Fab', Fab или scFv. В наиболее типичном варианте неоэпитоп рака экспрессируется в раковых клетках пациента, и/или указанный неоэпитоп является уникальным для пациента и конкретного рака у этого пациента.
[0015] С другой стороны, авторы настоящего изобретения также предусматривают композицию, которая содержит синтетическое антитело, обладающее аффинностью связывания пациент- и рак-специфичным HLA-парный неоэпитопом рака, при этом указанный неоэпитоп является уникальным для пациента и конкретного рака у этого пациента.
[0016] В особенно предпочтительных аспектах HLA-парный неоэпитоп рака, соответствует презентации главным комплексом гистосовместимости класса I (ГКГС-I), а синтетическое антитело выбрано из группы, состоящей из IgG, F(ab')2, Fab', Fab и scFv. При желании терапевтический агент можно присоединить к синтетическому антителу, и терапевтический агент представляет собой неклеточный агент (например, химиотерапевтическое лекарственное средство, радиоизотоп, изотоп, детектируемый методом PET, изотоп, детектируемый методом SPECT или аффинный агент). В альтернативном варианте терапевтический агент может также представлять собой клетку, и в особенности иммунокомпетентную клетку (например, Т-клетку или NK-клетку). Например, в том случае, когда указанная клетка представляет собой Т-клетку, она может экспрессировать химерный рецептор, содержащий scFv в качестве эктодомена, при этом синтетическое антитело представляет собой указанный scFv. С другой стороны, в том случае, когда указанная клетка представляет собой NK-клетку, она может экспрессировать высокоаффинный Fcγ-рецептор (CD 16), при этом синтетическое антитело представляет собой IgG, который связывается с указанной NK-клетку посредством указанного высокоаффинного Fcγ-рецептора. Среди других композиций предполагаемый неоэпитоп рака может содержать последовательность, выбранную из группы, состоящей из SEQ ID №: 1 - SEQ ID №: 1408729.
[0017] В еще одном аспекте заявленного изобретения авторы также предусматривают композицию, которая содержит твердую фазу, с которой связывается HLA-парный пациент- и рак-специфичный неоэпитоп рака, при этом указанный неоэпитоп рака является уникальным для пациента и конкретного рака у этого пациента. Например, подходящие твердые фазы будут включать стенку емкости с реагентом, магнитную гранулу или индивидуально маркированный элемент, а в особенно предпочтительном варианте длина неоэпитопов рака будет составлять от 7 до 9 аминокислот. Среди других неоэпитопов предусмотренные неоэпитопы включают неоэпитопы, которые имеют последовательность, соответствующую любой из SEQ ID №: 1 - SEQ ID №: 1408729. Предусмотрено, что в соответствующих случаях синтетическое антитело (например, IgG, F(ab')2, Fab', Fab и scFv) связывается с неоэпитопом рака, который, в свою очередь, может быть присоединен к вирусной частице.
[0018] Различные объекты, признаки, аспекты и преимущества заявленного изобретения станут более очевидными, исходя из последующего подробного описания предпочтительных вариантов реализации совместно с прилагаемыми чертежами, на которых одинаковые цифры представляют аналогичные компоненты.
Краткое описание чертежей
[0019] На Фигуре 1 в качестве примера показана схематическая блок-схема одного аспекта заявленного изобретения.
[0020] На Фигуре 2 в качестве примера показан график, изображающий результаты отбора для вычисленных неоэпитопов.
Подробное описание
[0021] Авторы настоящего изобретения обнаружили, что различные диагностические и терапевтические композиции и агенты можно получать с применением теоретически простого, но эффективного подхода, который сочетает в себе методы компьютерного моделирования (in silico) и методы in vitro.
[0022] Понятно, что применение систем и способов, разработанных авторами настоящего изобретения будет понятно, позволяет получить полностью синтетические антитела против одного или более пациент-специфичных неоэпитопов и, в частности, против антигенов, которые либо не вызывают защитный иммунный ответ, и/или против антигенов, которые демонстрируют подавленный иммунный ответ. Следует отметить, что, в еще более предпочтительном варианте, такие синтетические антитела можно получить при помощи компьютерного анализа (анализа in silico) омных данных пациента с получением относительно большого количества потенциально подходящих неоэпитопов, которые затем можно дополнительно подвергнуть отбору для повышения терапевтической эффективности. С другой стороны, предполагаемые синтетические моноклональные антитела получают без фактического времязатратного выделения опухолеспецифичных пептидов из опухоли и без проведения какой-либо процедуры иммунизации млекопитающего (или другого животного с иммунной системой). Кроме того следует отметить, что предусмотренные в настоящем документе способы позволят быстро получать синтетические антитела, обычно в пределах от нескольких дней до нескольких недель (например, от 5 до 21 дня).
[0023] Вкратце, и как в качестве примера показано на блок-схеме Фигуры 1, один предусмотренный способ 100 будет включать аналитическую часть in silico 110 и синтетическую часть in vitro 120. В наиболее типичном варианте проведение анализа in silico начинается с омного анализа 112 для идентификации мутаций в опухоли относительно нормальной ткани того же пациента, и этапа 114 вычисления одного или более неоэпитопов для определения пациент- и опухоль-специфичных неоэпитопов. Полученные таким образом неоэпитопы дополнительно подвергают этапу отбора 116, например, для удаления неоэпитопов, экспрессируемых слабо или не экспрессируемых вовсе. Идентифицированные экспрессируемые неоэпитопы можно затем подвергать дополнительным алгоритмам отбора 118, например, для того, чтобы ограничить неоэпитопы экспонируемыми вне клетки или связываемыми ГКГС-1 неоэпитопами. На Фигуре 2 в качестве примера показан результат ряда этапов отбора. В этом примере полногеномное секвенирование образца трижды отрицательного рака молочной в сравнении с парными нормальными данными (т.е. в сравнении с тканью, не пораженной заболеванием, полученной от того же пациента) выявило относительно большое количество (~ 18000) неоэпитопов в образце опухоли. Следует отметить, что на первом этапе отбора, основываясь на силы экспрессии, было исключено более 50% всех идентифицированных неоэпитопов. На этом же этапе исключили последовательности неоэпитопов с уровнем экспрессии менее 20% от уровня экспрессии по сравнению с парным нормальным образцом. Оставшиеся последовательности подвергали анализу in silico для определения тех последовательностей, которые должны свяхываться (например, с аффинностью менее, чем 500 нМ) с одним конкретным типом HLA того же образца. Следует еще раз отметить, что была исключена значительная часть неоэпитопов, и что в конечном итоге подходящими для применения оказалось только менее 1,3% от всего числа неоэпитопов.
[0024] Обращаясь снова к Фигуре 1, после идентификации подходящих последовательностей неоэпитопов с применением методов компьютерного моделирования, соответствующие синтетические пептиды затем получают in vitro (например, с применением твердофазного синтеза) и применяют в анализе с использованием фагового дисплея, обычно применяя библиотеку с большим количеством различных конструкций scFv (например, по меньшей мере 109 различных членов), как показано на этапе 122. Следует понимать, что активно связывающиеся фаги будут связываться через перный scFv, представляемый фагом, который кодируется соответствующей нуклеиновой кислотой, присутствующей в указанном связываемом фаге. Анализ последовательности такой фаговой ДНК позволяет обнаружить последовательности для определяющих комплементарность (обычно по меньшей мере CDR1-H, CDR2-H и CDR3-H и CDR1-L, CDR2-L и CDR3-L) участков в scFv, как показано на этапе 124. Затем эту информацию можно применять в качестве руководства для модификации нуклеиновой кислоты, кодирующей человеческое или гуманизированное scFv или другое антитело. После экспрессии в подходящей системе экспрессии затем синтетическое антитело (синтело (synbody)) вводят в состав желаемого терапевтического объекта, например, путем связывания антитела с NK-клеткой или с применением технологии «пересадки» (grafting) соответствующего scFv на химерный рецептор Т-клеток.
[0025] В частности, что касается получения омных данных пациента для идентификации одного или более неоэпитопов, в целом предполагается, что омные данные получают из одного или более образцов биопсии пациента в соответствии со стандартным протоколом обработки ткани и протоколами секвенирования. Без ограничения настоящего изобретения, обычно предпочтительно, чтобы данные представляли собой данные опухоли, для которых есть парные данные от того же пациента (например, опухоль в сравнении с нормальной тканью того же пациента), и чтобы данные имели формат SAM, ВАМ, GAR или VCF. Однако данные, имеющие парные референсные данные (например, более ранние данные нормальной или опухолевой ткани того же пациента, или homo statisticus) или без них, также считаются подходящими для применения. Таким образом, омные данные могут представлять собой «свежие» омные данные или могут представлять собой данные, которые были получены в предшествующей процедуре (или даже от другого пациента). Например, на первом этапе неоэпитопы из опухоли пациента могут быть идентифицированы с применением полногеномного и/или полноэкзомного анализа биопсии опухоли (или биопсии лимфы, или биопсии метастатической области) и парной нормальной ткани (т.е., с тканью, которая не поражена заболеванием, полученной от того же пациента, как, например, периферическая кровь) путем одновременного сравнения по местоположению (located-guided) полученной таким образом омной информации.
[0026] В числе других вариантов предусмотрено, что геномный анализ можно выполнять с применением ряда аналитических способов, однако особенно предпочтительные аналитические способы включают WGS (полногеномное секвенирование) и экзомное секвенирование как опухоли, так и парного нормального образца с применением методик секвенирования следующего поколения, таких как методы массивного параллельного секвенирования, полупроводниковое секвенирование (ion torrent), пиросеквенирование и т.д. Также следует понимать, что компьютерный анализ данных последовательностей можно осуществлять многочисленными способами. Однако в наиболее предпочтительных способах анализ проводят in silico путем одновременного выравнивания по местоположению данных по образцам опухоли и нормальным (здоровым) образцам, как, например, описано в патенте США 2012/0059670 А1 и патенте США 2012/0066001 А1 с использованием файлов ВАМ и серверов ВАМ. В Безусловно, настоящий документ также предусматривает применение и других файловых форматов для анализа последовательностей (например, SAM, GAR, FASTA и т.д.).
[0027] Следует отметить, что любое выражение, относящееся к «компьютеру» следует понимать как включающее любую подходящую комбинацию вычислительных устройств, включая серверы, интерфейсы, системы, базы данных, агенты, узлы сети, механизмы, контроллеры или другие типы вычислительных устройств, работающих совместно или по отдельности. Следует понимать, что вычислительные устройства содержат процессор, сконфигурированный для выполнения программных инструкций, хранящихся на материальном, энергонезависимом машиночитаемом носителе данных (например, жестком диске, диске, ОЗУ, флэш-накопителе, ПЗУ и т.д.). В предпочтительном варианте программные инструкции конфигурируют вычислительное устройство для выполнения функций, выполнения операций или других функциональных возможностей, описанных ниже в отношении описанного устройства. Кроме того, раскрытые технологии можно реализовать в виде компьютерного программного продукта, который включает энергонезависимый машиночитаемый носитель, хранящий инструкции для программного обеспечения, которые запускают процессор для выполнения описанных этапов, связанных с реализацией компьютерных алгоритмов, процессов, способов или других инструкций. В особенно предпочтительных вариантах реализации различные серверы, системы, базы данных или интерфейсы обмениваются данными с использованием стандартизированных протоколов или алгоритмов, возможно, на основе HTTP, HTTPS, AES, открытых/личных ключей обмена, API-интерфейсов веб-сервисов, известных протоколов финансовых транзакций или других способов электронного обмена информацией. Обмен данными между устройствами может осуществляться через сеть с пакетной коммутацией, Интернет, LAN, WAN, VPN или другую сеть с пакетной коммутацией, сеть с коммутацией каналов, сеть сотовой коммутации или другой тип сети.
[0028] Безусловно следует понимать, что можно выполнить последующий анализ для таких идентифицированных различий в последовательностях, чтобы идентифицировать те, которые приводят к появлению новой последовательности пептида, в основе которой лежит пациент- или рак-специфичная мутация. Таким образом, неоэпитопы можно идентифицировать, рассматривая тип мутации (например, делецию, вставку, трансверсию, транзицию, транслокацию) и характер воздействия мутации (например, нонсенс-мутация, миссенс-мутация, сдвиг рамки и т.д.), и, таким образом, они могут выполнять роль фильтра содержимого, исключающего молчащие и другие несущественные (например, неэкспрессируемые) мутации.
[0029] Кроме того следует понимать, что предусмотренные настоящим документом последовательности неоэпитопов можно определить как фрагменты последовательности (stretch) относительно короткой длины (например, 5-30-мерные, наиболее типично 7-11-мерные или 12-25-мерные), при этом такие фрагменты содержат изменение (изменения) в последовательностях аминокислот. В наиболее типичном варианте такое изменение(измененияя) располагается(-ются) по центру или вблизи центра (например, на расстоянии менее, чем 4 или менее, чем 5, или менее, чем 6 аминокислот от центрального положения). Соответственно, с другой точки зрения, предусмотренные в настоящем документе последовательности неоэпитопов будут, в частности, включать последовательности, в которых отдельная аминокислота была заменена относительно парной нормальной последовательности, и в которых измененная аминокислота расположена по центру или вблизи центра последовательности неоэпитопа (например, в 9-мере измененная аминокислота находится в положении 2, 3, 4 или 5, более типично в положении 3, 4 или 5, и в наиболее типичном случае в положении 4 или 5). Таким образом, следует понимать, что одно изменение аминокислоты может быть представлено в многочисленных последовательностях неоэпитопов, которые содержат эту измененную аминокислоту, в зависимости от местоположения измененной аминокислоты. Полезно, что такая вариабельность последовательности допускает множественный выбор неоэпитопов и, следовательно, увеличивает количество потенциально подходящих мишеней, которых затем можно подвергнуть отбору на основе одного или более необходимых признаков (например, самой высокой аффинности к некоторому типу HLA пациента, самой высокой структурной стабильности и т.д.). В наиболее типичном варианте неоэпитопы будут вычисляться таким образом, чтобы их длина составляла от 2 до 50 аминокислот, более типично от 5 до 30 аминокислот и в наиболее типичном варианте от 9 до 15 аминокислот, причем измененная аминокислота предпочтительно расположена по центру или расположена иным образом, обеспечивающим улучшение ее связывания с ГКГС. Например, в том случае, когда эпитоп будет презантироваться главным комплексом гистосовместимости-I, обычная длина такого эпитопа будет составлять примерно 8-11 аминокислот, тогда как обычная длина эпитопа для презентации) через ГКГС-II будет составлять примерно 13-17 аминокислот. Хорошо понятно, что поскольку положение измененной аминокислоты в неоэпитопе может быть отличным от центрального, фактическая последовательность пептида и, соответственно, фактическая топология неоэпитопа, может значительным образом варьировать. Кроме того, в том случае, если неоэпитоп презентируется иммунокомпетентной (или другой) клетке в качестве синтетического пептида, следует понимать, что указанный синтетический пептид может быть значительно длиннее области пептида, которая в конечном итоге связывается системой ГКГС-I или ГКГС-II, чтоб обеспечивает протеолитический процессинг в клетке. Таким образом, например, предусмотренные синтетические пептиды могут содержать от 8 до 15 аминокислот, расположенных перед и после измененной аминокислоты.
[0030] Что касается отбора идентифицированных неоэпитопов, то в целом предполагается, что неоэпитопы особенно предпочтительны для применения в настоящем изобретении в том случае, если «омный» (или другой) анализ показывает, что происходит фактическая экспрессия неоэпитопа. Идентификация экспрессии и уровня экспрессии неоэпитопа может быть выполнена с применением любых известных в данной области способов, и предпочтительные способы включают количественный анализ на определение содержания РНК (гяРНК или мРНК) и/или количественный протеомический анализ. В наиболее типичном варианте пороговым уровнем для включения в исследование неоэпитопов будет являться по меньшей мере 20% уровень экспрессии и более типично по меньшей мере 50% уровень экспрессии относительно уровня экспрессии соответствующей парной нормальной последовательности, что обеспечивает по меньшей мере потенциальную «видимость» (нео)эпитопа для иммунной системы. Следовательно, в целом предпочтительно, чтобы «омный» анализ также включал анализ экспрессии генов (транскриптомный анализ), чтобы обеспечить идентификацию уровня экспрессии гена с мутацией. Существует множество способов проведения транскриптомного анализа, известных в данной области техники, и все известные способы считаются подходящими для применения в настоящем изобретении. Например, предпочтительные материалы включают мРНК и первичные транскрипты (гяРНК), а информацию о последовательности РНК можно получить из обратной транскрибируемой полиА+-РНК, которую, в свою очередь, получают из образца опухоли и перного нормального (здорового) образца от того же пациента. Аналогичным образом следует отметить, что хотя полиА+-РНК в целом предпочтительна в качестве представления транскриптома, другие формы РНК (гяРНК, неполиаденилированная РНК, миРНК, микроRNA и т.д.) также считаются подходящими для применения в настоящем изобретении. Предпочтительные способы включают количественный анализ на определение РНК (гяРНК или мРНК) и/или количественный протеомный анализ. В наиболее типичном варианте количественное определение и секвенирование РНК осуществляют с применением способов на основе количественной ПЦР (кPCR) и/или ПЦР с обратной транскриптазой (отПЦР), хотя другие способы (например, способы на основе твердофазной гибридизации) также считаются подходящими. С другой стороны, транскриптомный анализ может быть подходящим (отдельно или в сочетании с геномным анализом) для идентификации и количественной оценки генов, содержащих пациент- или рак-специфичную мутацию.
[0031] Аналогичным образом, протеомный анализ можно осуществить различными способами для определения экспрессии неоэпитопа, и в настоящем документе предполагаются все известные способы протеомного анализа. Однако особенно предпочтительные протеомные методы включают методы на основе применения антител и масс-спектроскопические методы. Более того, следует отметить, что протеомный анализ может не только обеспечивать качественную или количественную информацию о белке как таковом, но также может включать данные об активности белка в том случае, когда белок обладает каталитической или другой функциональной активностью. Один из примеров методик проведения протеомнных исследваний включает патент США №7473532 от Darfler и др. под названием «Liquid Tissue Preparation from Histopathologically Processed Biological Samples, Tissues, and Cells», поданный 10 марта 2004 года.
[0032] Кроме того, также можно провести детальный анализ и отбор неоэпитопов с применением предварительно определенных структурных переметров и/или параметров субклеточной локализации. Например, предполагается, что последовательности неоэпитопов выбирают для дальнейшего применения, если они идентифицированы как последовательности, местоположение которых связано с мембраной (например, они располагаются снаружи клеточной мембраны клетки), и/или если расчет структуры in silico подтверждает, что неоэпитоп, вероятнее всего, будет экспонирован в растворители или представляет собой структурно стабильный эпитоп и т.д.
[0033] Следовательно, следует принять во внимание, что пациент- и рак-специфичные неоэпитопы можно идентифицировать на основании омной информации исключительно в среде in silico, которая, в конечном итоге, позволяет сделать прогноз в отношении потенциальных эпитопов, уникальных для пациента и типа опухоли. Идентифицированные и выбранные таким образом неоэпитопы затем можно дополнительно подвергнуть отбору in silico на основании идентифицированного у пациента типа HLA. Считается, что такое соответствие HLA обеспечивает сильное связывание неоэпитопов с комплексом ГКГС-I ядерных клеток и с комплексом ГКГС-II специфичных антигенпрезентирующих клеток. В частности, предполагается, что нацеливание на эти две антигенпрезентирующие системы даст терапевтически эффективный и продолжительный иммунный ответ, включающего как клеточную, так и гуморальную составляющие иммунной системы. Безусловно, следует также понимать, что проверку идентифицированных таким образом HLA-парных неоэпитопов можно осуществить биохимическими методами in vitro.
[0034] Определение типа HLA как для ГКГС-I, так и для ГКГС-II можно осуществить с применением различных методов жидкостной химии, которые хорошо известны в данной области техники, и все эти методы считаются подходящими для применения в настоящем изобретении. Однако особенно предпочтительные также позволяют предсказать тип HLA по омным данным in silico с применением референсной последовательности, содержащей большинство или все известные и/или общераспространенные типы HLA, как это более подробно показано ниже. Вкратце, у пациента определяют тип HLA (с применением методов жидкостной химии обработки или определения in silico), и рассчитывают или получают на основе базы данных структуру для типа HLA, которое затем применяют в качестве модели «докинга» (docking model) in silico для определения аффинности связывания неоэпитопа с определенной структурой HLA. Подходящие системы для определения аффинности связывания включают платформу NetMHC (см., например, Nucleic Acids Res. 2008 от 1 июля; 36 (веб-издание): W509-W512.), HLAMatchmaker (http://www.epitopes.net/downloads.html) и ресурс для проведения анализа IEDB (http://tools.immuneepitope.org/mhcii/). Затем выбирают неоэпитопы с высокой аффинностью (например, с аффинностью менее 100 нМ, менее 75 нМ, менее 50 нМ для ГКГС-I, менее 500 нМ, менее 300 нМ, менее 100 нМ для ГКГС-II) в отношении ранее определенного типа HLA. При расчете самого высокого показателя аффинности, можно произвести модификации неоэпитопов путем добавления N- и/или С-концевых модификаций к эпитопу для дальнейшего увеличения связывания синтетического неоэпитопа с типом HLA пациента. Таким образом, неоэпитопы могут быть нативными, т.е. просто идентифицированными, или дополнительно модифицированными для лучшего соответствия конкретному типу HLA.
[0035] В еще одном аспекте отбора неоэпитопы можно сравнивать с базой данных, которая содержит известные последовательности человека и таким образом позволяет избежать применения последовательности, идентичной последовательности человека. Более того, отбор может также включать удаление последовательностей неоэпитопов, которые возникают в результате однонуклеотидного полиморфизма (SNP) у пациента. Например, база данных однонуклеотидных полиморфизмом (dbSNP) представляет собой бесплатный общедоступный архив генетических вариантов внутри видов и между различными видами, который разработан и поддерживается Национальным центром биотехнологической информации (NCBI) в сотрудничестве с Национальным научно-исследовательским институтом генома человека (NHGRI). Хотя название базы данных подразумевает собрание только одного класса полиморфизмов (а именно, однонуклеотидных полиморфизмов (SNP)), по факту она содержит относительно широкий диапазон молекулярных вариантоы: (1) SNP, (2) делеционные и инсерционные полиморфизмы коротких последовательностей (инделы/DIP-полиморфизмы инсерции/делеции) (3) микросателлитные маркеры или короткие тандемные повторы (STR), (4) мультинуклеотидные полиморфизмы (MNP), (5) гетерозиготные последовательности и (6) именованные варианты. Очевидно, в базе dbSNP возможно размещение и нейтральных полиморфизмов, полиморфизмов, соответствующих известным фенотипам, и областей без вариаций. Применяя такую базу данных, можно провести дополнительный отбор пациент- и рак-специфичных неоэпитопов, чтобы удалить такие известные последовательности, что позволяет получить набор терапевтических последовательностей со множеством последовательностей неоэпитопов.
[0036] Соответственно следует понимать, что идентифицированные таким образом неоэпитопы рака являются уникальными для пациента и конкретного рака у этого пациента (например, с частотой менее 0,1% от числа всех неоэпитопов и, более типично, с частотой менее 0,01% в популяция пациентов с раком, у которых диагностирован один и тот же вид рака), однако идентифицированные таким образом неоэпитопы рака будут с высокой вероятностью присутствовать в опухоли и, следовательно, обеспечивать высокую вероятность того, что на них будет специфически нацеливаться синтетическое антитело даже в том случае, если микроокружение рака подавляет иммунную систему.
[0037] На практике можно оценить/ранжировать неоэпитопы на основании частоты аллелей, умноженной на число транскриптов на миллион, для получения оценки возможности. Затем эту оценку можно также дополнить, применяя информацию по HLA и расчетной или фактической аффинности связывания с типом HLA пациента. Например, в качестве примера формат ранжирования может представлять собой:

[0038] В данном примере файл представляет собой файл формата FASTA, и записи начинаются с символа «>», который сообщает только информацию об образце. Следующая строка - это неоэпитоп. В информационной строке примера содержится номер, применяемый для индексирования образца (например, 254), ID-номер гена Refseq (например, NM_001000.3), общее имя HUGO (например, RPL39), тип варианта (например, Missense - миссенс), изменение в белке (например, p.M29K), изменение пары оснований (например, А->Т), нормальный эпитоп (например, Normal: WIRMKTGNK), частота аллеля (например, AF: 0.1779104477612), число транскриптов на миллион для данного гена (например, ТРМ: 1023.96), TPM_MEDIAN, которое является средним уровнем экспрессии всех генов (например, TPM_MEDIAN: 7.35), оценка LL, которая представляет собой AF х ТРМ (например, LL: 183.395820896), прогнозируемое значение величины связывания по платформе netMHC (например, netMHC: 242.96) и HLA-специфичный аллель, который связывает неоэпитоп (например, Allele: HLA-A0301). Следующая строка - это неоэпитоп (например, WIRKKTGNK).
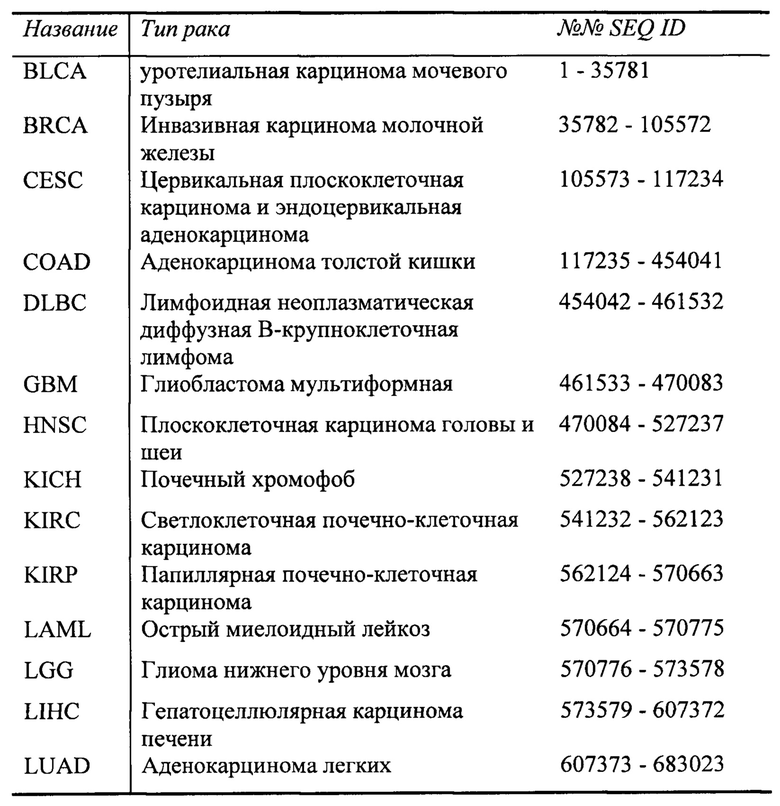
[0039] Возможность применения такого подхода была продемонстрирована авторами настоящего изобретения с применением омных данных из общедоступной базы данных TCGA, охватывающей многочисленные виды рака, которая для каждого из видов рака содержит данные от множества пациентов. В таблице 1 ниже перечислены название и тип рака, за которым следуют неоэпитопы, обнаруженные для каждого типа рака.

[0040] Таким образом, следует принимать во внимание, что можно собрать полную рационально сконструированную коллекцию неоэпитопов конкретного пациента с конкретным типом рака, которую затем можно дополнительно исследовать in vitro для поиска или получения высокоаффинных антител. Действительно, предполагаемые коллекции могут содержать один, два, три, четыре, пять, от шести до десяти, 10-50, 50-150, 1000 и даже больше пациент- и рак-специфичных неоэпитопов. С другой точки зрения, рационально сконструированная коллекция неоэпитопов может охватывать от 1 до 10% или от 10 до 25%, или от 25 до 60%, или от 60 до 100% от числа всех неоэпитопов, которые экспрессируются и связываются с типом HLA пациента. Таким образом, предполагаемые коллекции будут содержать по меньшей мере 15%, по меньшей мере 25%, по меньшей мере 50%, по меньшей мере 70% или по меньшей мере 90% иммуномов рака (неоэпитопов, которые экспрессируются и связываются с типом HLA пациента). Следовательно, следует также понимать, что даже для пациентов, у которых опухоль подавляет иммунную систему, или для пациентов с поврежденной в результате химиотерапии иммунной системой, теперь доступны многочисленные мишени для иммунотерапии.
[0041] Чтобы получить синтетическое антитело против идентифицированного неоэпитопа(-ов), предусмотрено, что идентифицированный in silico неоэпитоп получают in vitro с получением синтетического пептида. Существует множество способов, известных в данной области техники, для получения синтетических пептидов и все известные способы считаются подходящими для применения в настоящем изобретении. Например, пептиды с последовательностями неоэпитопов рака можно получить на твердой фазе (например, с применением синтеза Меррифильда), путем жидкофазного синтеза или из более мелких пептидных фрагментов. В менее предпочтительных аспектах пептиды также можно получить путем экспрессии рекомбинантной нуклеиновой кислоты в подходящем хозяине (особенно в тех случаях, когда множественные неоэпитопы находятся на одной пептидной цепи, необязательно со спейсерами между неоэпитопами или сайтами расщепления).
[0042] Таким образом, структура синтетических пептидов, соответствующих или содержащих последовательности неоэпитопов, может представлять собой X-L1-(An-L2)mQ, где X представляет собой необязательную связывающую группу или фрагмент, который подходит для ковалентного или нековалентного присоединения указанного синтетического пептида к твердой фазе, L1 представляет собой необязательный линкер, который ковалентно связывает синтетический пептид с твердой фазой или указанной связующей группой. An представляет собой синтетический пептид, имеющий последовательность неоэпитопа, где А представляет собой природную (протеиногенную) аминокислоту, а n представляет собой целое число от 7 до 30 и в наиболее типичном варианте от 7 до 11 или от 15 до 25. L2 представляет собой необязательный линкер, который может присутствовать, особенно в том случае, когда в конструкции имеется множество синтетических пептидных последовательностей (одинаковых или разных), a m представляет собой целое число, обычно от 1 до 30 и в наиболее типичном варианте от 2 до 15. Наконец, Q представляет собой концевую группу, которую можно применять для присоединения конца синтетического пептида к указанной твердой фазе (например, чтобы обеспечить стерическое ограничение пептида) или репортерной группе (например, флуоресцентному маркеру) или другому функциональному фрагменту (например, аффинному маркеру). Следовательно, следует отметить, что в том случае, когда синтетический пептид применяют для непосредственного связывания с MHC-I, его общая длина будет составлять от 8 до 10 аминокислот. Аналогичным образом, в том случае, если синтетический пептид применяют для непосредственного связывания с ГКГС-II, его общая длина будет составлять от 14 до 20 аминокислот. С другой стороны, в том случае, когда происходит процессинг синтетического пептида в клетке (как правило, за счет процессинга с участием протеасом) до презентации ГКГС, общая длина обычно будет составлять от 10 до 40 аминокислот с учетом того, что синтетический пептид содержит измененную аминокислоту в центральном положении или вблизи центрального положения.
[0043] Например, X может представлять собой нековалентный аффинный фрагмент (например, биотин), который связывает соответствующий связывающий агент (например, авидин) на твердой фазе, или химическую группу (со спейсером или без), которая вступает в реакцию с N- или С-концевой амино- или карбоксильной группой указанного пептида, или селективную реакционноспособную группу (например, иодацетильную или малеимидную группу), которая вступает в реакцию с сульфгидрильной группой указанного пептида или линкером L1. L1 можно применять для увеличения расстояния между синтетическим пептидом и твердой фазой и, следовательно, он обычно будет содержать гибкий линейный фрагмент (например, содержащий гликолевые группы, алкоксигруппы, глицин и т.д.), имеющий длину, эквивалентную примерно 2-20 углерод-углеродным связям (например, от 0,3 нм до 3 нм). Безусловно, следует также понимать, что при получении синтетического пептида может применяться твердая фаза, на которой синтезировали указанный пептид, и поэтому не требуется отдельная связывающая группа или линкер.
[0044] Следует понимать, что в зависимости от конкретного синтетического пептида и способа связывания природа твердой фазы может значительно варьировать, и все известные твердые фазы для присоединения пептидов считаются подходящими для применения в настоящем изобретении. Например, подходящие твердые фазы включают гранулы агарозы, полимерные гранулы (окрашенные или иным образом индивидуально маркированные), поверхности стенки лунки планшета для микротитрования, бумагу, нитроцеллюлозу, стекло и т.д. Специалист в данной области техники легко сделает подходящий выбор твердой фазы и химических реагентов для присоединения. Также следует отметить, что в других предпочтительных аспектах твердая фаза в целом подходит для протоколов, связанных со способами на основе фагового дисплея, например, будет позволять представленным на фаге (или на другом носителе-каркасе(скаффолде)) пептидам обратимо связываться с твердой фазой через синтетический пептид. В дополнительно предусмотренных применениях также предполагается, что твердая фаза может представлять собой белок-носитель, применяемый при вакцинации (например, альбумин, гемоцианин моллюска (KLH), столбнячный токсоид, дифтерийный токсин и т.д.), в частности в том случае, когда синтетический белок применяют в качестве вакцины для млекопитающего или в качестве иммуногенного соединения для млекопитающего, не являющегося человеком, для выработки антител. Аналогичным образом, синтетический белок можно также применять в качестве вакцины или иммуногенного соединения без какого-либо носителя.
[0045] В еще более предпочтительных способах следует понимать, что в том случае, когда синтетический пептид (содержащий или соответствующий неоэпитопу рака) иммобилизуют на твердой фазе, аффинные агенты и, в частности, антитела против неоэпитопа можно выделить и/или очистить. В наиболее предпочтительном варианте такое выделение будет включать применение заранее созданной библиотеки с большим количеством различных антител. В контексте настоящего и в случае отсутствия другого определения термин «антитело» или «антитела» включает все изотипы и подтипы антител (например, IgG, IgM, IgE и т.д.), а также все их фрагменты, включая одновалентный IgG, F(ab')2, Fab', Fab, scFv, scFv-Fc, VhH и т.д. Кроме того, предусмотренные антитела могут представлять собой гуманизированные антитела человеческого или нечеловеческого происхождения (например, грызунов), или могут быть химерными. В типичном способе библиотека с большим количеством различных антител может представлять собой библиотеку на фаговом дисплее, содержащую по меньшей мере в 109 различных членов или по меньшей мере в 1010 различных членов или даже более, обычно на основе фагов М13 и презентации посредством pIII, pVIII, pVI или pIX, или на основе фагов Т7 и гена 10 белка капсида. Будет легко понять, что применение библиотек с большим количеством различных элементов обеспечит за сравнительно короткое время обнаружение нескольких кандидатов для связывающих антител, из которых можно дополнительно выбрать самых лучших по связыванию. Действительно, в том случае, если аффинность связывания с иммобилизованным синтетическим пептидом меньше требуемой, следует принимать во внимание, что аффинность можно улучшить за счет этапа созревания аффинности, применяя протоколы, хорошо известные в данной области техники. Например, связывающие антитела с низкой аффинностью (KD>10-7 M) или члены из более мелких библиотек можно подвергнуть этапу созревания аффинности для улучшения аффинности и/или кинетики связывания с применением способов, хорошо известных в данной области техники (см., например, Briefings In Functional Genomics And Proteomics. Вып. 1., №2, стр. 189-203, июль 2002.). Кроме того, следует отметить, что в то время как в целом библиотеки антител являются предпочтительными, другие каркасы также считаются подходящими и включают бета-бочонки (beta-barrel), рибосомный дисплей, дисплей клеточной поверхности и т.д. (см., например, Protein Sci., 2006, Январь, 15 (1): 14-27). Таким образом, следует понимать, что в предпочтительных аспектах синтетический пептид используют в качестве «приманки» в библиотеке антител, чтобы таким образом идентифицировать антитела с высокой (KD<10-7 М и более типично KD<10-8 М) аффинностью связывания.
[0046] Поскольку антитела присоединяют непосредственно к клетке, которая содержит нуклеиновую кислоту, кодирующую эти антитела, следует также принять во внимание, что затем такую нуклеиновую кислоту можно исследовать для идентификации элементов последовательности, кодирующих гипервариабельные петли, CDR1, CDR2 и CDR3, для легкой и тяжелой цепи соответственно, и/или SDR (определяющие специфичность остатки). В наиболее типичном варианте определение выполняют с применением стандартных способов секвенирования. Далее, предполагается, что после определения гипервариабельные петли или CDR1-H, CDR2-H и/или CDR3-H, и/или CDR1-L, CDR2-L и/или CDR3-L, и/или SDR «пересаживают» (graft) на каркас человеческого или гуманизированного антитела или антитело. Как это легко понять, такую «пересадку» можно осуществить при помощи генной инженерии нуклеиновой кислоты, которая кодирует каркас человеческого или гуманизированного антитела или антитело. Например, в каждом CDR существуют положения с большей вариабельностью, которые непосредственно участвуют во взаимодействии с антигеном, т.е. определяющие специфичность остатки (SDR), в то время как существуют и более консервативные остатки, которые поддерживают конформации петель CDR. SDR можно идентифицировать по трехмерной структуре комплекса антиген-антитело и/или в результате мутационного анализа CDR. Гуманизированное антитело с «пересаженными» SDR (SDR-grafted humanized antibody) конструируют путем «пересадки» SDR и остатков, поддерживающих конформацию CDR, на человеческую матрицу для сборки молекул. Следовательно, следует принимать во внимание, что человеческие или гуманизированные антитела со специфичностью к неоэпитопам рака можно получить полностью синтетическим образом, при этом антитело экспрессируется в клетке, которая ранее не вступала в контакт с антигеном. Кроме того, предусмотренные способы позволяют получать пациент- и рак-специфичные антитела для лечения пациента, организм которого не способен вырабатывать или эффективно использовать антитела против неоэпитопов.
[0047] Без ограничения заявленного изобретения, полученные таким образом синтетические антитела можно применять непосредственно в виде IgG (или другого изотипа), в виде фрагмента (например, биспецифичного Fab или другого биспецифичного фрагмента) и/или в виде химерного белка (например, scFv в качестве эктодомена в химерном Т-клеточном рецепторе) по отдельности или в виде конъюгата с терапевтическим или диагностическим агентом, и/или в виде белка слияния с трансмембранным доменом для обеспечения заякоривания антитела на мембране клетки. Соответственно, авторы настоящего изобретения предусмотрели способ получения фармацевтического агента для иммунотерапии рака, в котором идентифицированные синтетические антитела присоединены к терапевтическому или диагностическому агенту (который может содержать клеточный или неклеточный компонент), с получением фармацевтического агента.
[0048] Например, предусмотренные неклеточные агенты включают различные химиотерапевтические лекарственные средства, обеспечивающие доставку указанного химиотерапевтического лекарственного средства непосредственно в раковую клетку. Например, подходящие химиотерапевтические лекарственные средства включают ингибиторы киназы (например, эрлотиниб, иматиниб, бортезомиб и т.д.), ингибиторы топоизомераз (например, топотекан, этопозид, тенипозид и т.д.), аналоги нуклеотидов (например, фторурацил, гемцитабин, азацитидин и т.д.), агенты на основе платины (например, цисплатин, карбоплатин и т.д.), алкилирующие агенты (например, циклофосфамид, хлорамбуцил, темозоломид и т.д.), таксаны (например, доцетаксел, паклитаксел и т.д.), ингибиторы микротубулина (например, винкристин, винбластин и т.д.). С другой стороны, можно применять направленную и специфическую лучевую терапию путем связывания радиологического агента с антителом для селективного разрушения раковой клетки. Подходящие радиологические агенты включают всех агенты, подходящие для брахитерапии, и в особенности 125I, 103Pd или 192Ir. В альтернативном варианте можно применять 10B в том случае, когда требуется применение нейтронно-захватной терапии с тепловыми нейтронами низкой энергии. Аналогичным образом, агенты для визуализации можно присоединять к антителу или его фрагменту, и особенно предпочтительные агенты для визуализации включают метки для проведения PET- (например, 11C, 13N, 15O и 18F) и SPECT-томографии (например, 123I, 99mTc, 133Хе, 201Tl и 18F). В контексте настоящего описания и если отсутствует другое определение предполагается, что термин «присоединенный к» включает как непосредственное присоединение (при котором два элемента, которые присоединены друг к другу, контактируют друг с другом), так и присоединение, которое не является непосредственным (при котором по меньшей мере один дополнительный элемент расположен между этими двумя элементами). Следовательно, термины «присоединенный к» и «соединенный с» используются в качестве синонимов. В других предусмотренных аспектах антитело можно модифицировать с применением антигена, о котором известно, что он является иммуногенным антигеном. Такая модификация является особенно преимущественной в том случае, когда пациент был ранее иммунизирован этем же антигеном. В таком случае предусмотрено, что содержащие неоэпитопы раковые клетки «окрашиваются» модифицированным антителом, представляющим собой иммуногенный антиген, которое обладает особенным преимуществом в том случае, когда иммунный ответ на исходный неоэпитоп не был иммуногенным или подавлялся.
[0049] Следует отметить, что когда неоэпитопы используют для нацеливания иммунных клеток на опухоль, антитело также можно присоединить к части Т-клеточного рецептора или цитотоксической Т-клетки или NK-клетки. Например, когда антитело присоединено к химерному Т-клеточному рецептору цитотоксической Т-клетки, антигенсвязывающая часть указанного химерного Т-клеточного рецептора может содержать scFv в качестве эктодомена, и указанный scFv обладает аффинностью связывания в отношении одного из неоэпитопов (например, соответствующих SEQ ID №: 1 - SEQ ID №: 1408729). С другой стороны, в том случае, когда антитело присоединено к NK-клетке, предпочтительные NK-клетки являются производными NK-92, которые модифицированы так, чтобы обладать пониженной или подавленной экспрессией по меньшей мере одного иммуноглобулиноподобного рецептора клетки-киллера (KIR), что будет приводить к константной активации таких клеток (из-за отсутствия или уменьшенного ингибирования). Такие NK-клетки можно получить из компании NantKwest (см. Nantkwest.com) в виде aNK-клеток (активированных клеток-природных киллеров), и их можно дополнительно модифицировать для экспрессии связанного с мембраной синтетического антитела, обладающего аффинностью связывания с неоэпитопом (например, соответствующего SEQ ID №: 1 - SEQ ID №: 1408729).
[0050] В альтернативном варианте NK-клетка может также являться производной NK-92, которая модифицирована для экспрессии высокоаффинного Fcγ-рецептора (CD16), и отдельно предусмотрено, что антитела, предусмотренные в настоящем документе, могут связываться с такими модифицированными NK-клетками. Такие клетки можно получить из компании NantKwest в виде ваNK-клеток (высокоаффинных клеток-природныхкиллеров). Аналогичным образом, NK-клетку также можно генетически модифицировать для экспрессии химерного Т-клеточного рецептора. В особенно предпочтительных аспектах химерный Т-клеточный рецептор будет содержать участок scFv или другого эктодомена, обладающего специфичностью связывания с неоэпитопом (например, соответствующим SEQ ID №: 1 - SEQ ID №: 1408729). Безусловно, следует также отметить, что в том случае, когда терапевтический агент содержит клеточный компонент, указанная клетка может представлять собой аутологичную клетку, полученную от пациента, или гетерологичную клетку.
[0051] Следовательно, следует отметить, что можно вызвать эффективный иммунный ответ в отношении неоэпитопа рака, с применением процесса, который не требует иммунизации пациента или другого организма, что значительно сокращает время ответа и доступность терапевтических антител. Действительно, применение предусмотренных композиций и способов позволяет стимулировать или даже вызвать иммунный ответ в отношении неоэпитопа у пациента в том случае, когда иммунная система такого пациента недостаточно эффективна для формирования защитного ответа (например, вследствие химиотерапии или подавления иммунитета опухолью или регуляторными Т-клетками (Treg), или супрессорными клетками миелоидного происхождения).
[0052] Следовательно, следует принимать во внимание, что в зависимости от конкретной композиции фармацевтический агент можно вводить пациенту in vivo или в клетку или ткань in vitro. Например, когда синтетическое антитело применяют для целей диагностики, указанное антитело можно добавить к образцу ткани ex vivo (например, на предметное стекло микроскопа к фиксированному формалином, залитому парафином образцу с использованием флуоресцентного меченого антитела) или in vivo (например, когда указанное антитело метят РЕТ-меткой). С другой стороны, в том случае, когда антитело связывается с иммунокомпетентной клеткой, указанное антитело можно вводить пациенту in vivo.
[0053] В некоторых вариантах реализации числа, выражающие количества ингредиентов, свойства, как, например, концентрация, условия реакции и т.п., применяемые для описания и заявления определенных вариантов реализации настоящего изобретения, следует понимать как модифицированные в некоторых случаях термином «примерно». Соответственно, в некоторых вариантах реализации числовые параметры, изложенные в письменном описании и прилагаемой формуле изобретения, являются приближениями, которые могут варьировать в зависимости от требуемых свойств, получаемых в конкретном варианте реализации. В некоторых вариантах реализации численные параметры следует рассматривать с учетом числа приводимых значащих разрядов и с применением обычных методов округления. Несмотря на то, что диапазоны численных значений и параметры, определяющие широкий объем некоторых вариантов реализации настоящего изобретения, являются приближениями, численные значения, указанные в конкретных примерах, приведены с максимальной возможной точностью. Если контекст не указывает на иное, все указанные в настоящем документе диапазоны следует интерпретировать как включающие их конечные точки, а не открытые диапазоны следует интерпретировать как включающие значения, применимые на практике с коммерческой точки зрения. Аналогичным образом, все перечисленные значения следует рассматривать как включающие промежуточные значения, если иное не следует из контекста.
[0054] Для специалистов в данной области техники будет очевидно, что может быть сделано гораздо больше модификаций кроме тех, которые уже описаны, без отклонения от концепции настоящего изобретения. Следовательно, заявленное изобретение не ограничивается, за исключением объема прилагаемой формулы изобретения. Более того, при интерпретации как описания, так и формулы изобретения все термины следует интерпретировать максимально широко в соответствии с контекстом. В частности, термины «содержит» и «содержащий» следует интерпретировать как указывающие элементы, компоненты или этапы неисключающим образом, т.е. в том смысле, что указанные элементы, компоненты или этапы могут присутствовать, применяться или комбинироваться с другими элементами, компонентами или этапами, на которые не указаны в явном виде. В тех случаях, когда у описании или формуле упоминается по меньшей мере один элемент, выбранный из группы, состоящей из А, В, С … и N, текст следует интерпретировать в том смысле, что обязательно присутствие только одного элемент из группы, а не А совместно с N или В совместно с N и т.д.
| название | год | авторы | номер документа |
|---|---|---|---|
| КЛЕТКИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ АКТИВИРУЮЩИЕ РЕЦЕПТОРЫ И ХИМЕРНЫЕ СТИМУЛИРУЮЩИЕ РЕЦЕПТОРЫ, И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2780020C2 |
| АНТИ-CD 16 СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2006 |
|
RU2491294C2 |
| Способ отбора неоэпитопов | 2019 |
|
RU2826184C2 |
| ПОЛУЧЕНИЕ АНТИГЕНСПЕЦИФИЧЕСКИХ T-КЛЕТОК | 2017 |
|
RU2745319C2 |
| ДЕТЕРМИНАНТЫ ОТВЕТА РАКОВОЙ ОПУХОЛИ НА ИММУНОТЕРАПИЮ | 2014 |
|
RU2707530C2 |
| БИОЛОГИЧЕСКИЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2432363C9 |
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ ПРИМЕНИМОСТИ СПЕЦИФИЧНЫХ ДЛЯ ЗАБОЛЕВАНИЯ АМИНОКИСЛОТНЫХ МОДИФИКАЦИЙ ДЛЯ ИММУНОТЕРАПИИ | 2018 |
|
RU2799341C2 |
| ВЫСОКОАФФИННЫЕ АНТИТЕЛА К GD2 | 2014 |
|
RU2680267C2 |
| КОНСТРУИРОВАНИЕ ОБЛИГАТНОГО ВЕКТОРА НА ОСНОВЕ ОНКОЛИТИЧЕСКИХ ВИРУСОВ ПРОСТОГО ГЕРПЕСА (oHSV) И КОНСТРУКЦИИ ДЛЯ ТЕРАПИИ РАКА | 2016 |
|
RU2831084C2 |
| АНТИТЕЛА К РОДСТВЕННОЙ РАКОВО-ЭМБРИОНАЛЬНОМУ АНТИГЕНУ МОЛЕКУЛЕ КЛЕТОЧНОЙ АДГЕЗИИ (СЕАСАМ) | 2012 |
|
RU2650869C2 |


Изобретение относится к области биотехнологии. Предложен способ получения фармацевтического агента для иммунотерапии рака. Способ включает применение омных данных опухоли, для которых есть парные нормальные данные, для получения in silico множества содержащих пациент- и рак-специфичный неоэпитоп рака n-меров, отбор in silico n-меров с получением подмножества последовательностей неоэпитопов, получение синтетического n-мерного пептида с применением информации о последовательности подмножества последовательностей неоэпитопов, применение синтетического n-мерного пептида для выделения рекомбинантного антитела, получение информации о последовательности определяющего комплементарность участка рекомбинантного антитела, получение синтетического антитела с применением информации о последовательности определяющего комплементарность участка рекомбинантного антитела и присоединение синтетического антитела к терапевтическому или диагностическому агенту с получением фармацевтического агента. Изобретение обеспечивает быстрое идентифицирование пациент-опухолевых антигенов и в сжатые сроки получение антител, нацеленных на такие антигены, для диагностического или терапевтического применения. 18 з.п. ф-лы, 2 ил., 1 табл.
1. Способ получения фармацевтического агента для иммунотерапии рака, включающий:
применение омных данных опухоли, для которых есть парные нормальные данные, для получения in silico множества n-меров, которые содержат по меньшей мере один пациент- и рак-специфичный неоэпитоп рака, причем указанные омные данные по каждой опухоли и парному нормальному образцу пациента включают данные, выбранные из группы, состоящей из данных полногеномного секвенирования, данных экзомного секвенирования, транскриптомных данных и их комбинаций;
отбор in silico n-меров с получением подмножества последовательностей неоэпитопов, причем отбор представляет собой отбор по типу мутации, отбор по силе экспрессии, отбор по субклеточной локализации и/или отбор по аффинности связывания в отношении типа HLA пациента;
получение по меньшей мере одного синтетического n-мерного пептида с применением информации о последовательности указанного подмножества последовательностей неоэпитопов;
применение указанного синтетического n-мерного пептида для выделения рекомбинантного антитела;
получение информации о последовательности определяющего комплементарность участка указанного рекомбинантного антитела;
получение синтетического антитела с применением информации о последовательности определяющего комплементарность участка указанного рекомбинантного антитела и
присоединение указанного синтетического антитела к терапевтическому или диагностическому агенту с получением фармацевтического агента.
2. Способ по п. 1, где омные «данные», для которых есть парные нормальные данные, сопоставляют с нормальными данными до лечения пациента.
3. Способ по п. 1, где длина каждого из множества n-мерных пептидов составляет от 7 до 11 аминокислот.
4. Способ по п. 1, где указанное множество n-мерных пептидов содержит по меньшей мере 1000 n-мерных пептидов.
5. Способ по п. 1, где различные n-мерные пептиды из указанного множества n-мерных пептидов имеют различные неоэпитопы.
6. Способ по п. 1, где стадия отбора включает по меньшей мере два из: отбора по типу мутации, отбора по силе экспрессии, отбора по субклеточной локализации и отбора по аффинности связывания в отношении типа HLA пациента.
7. Способ по п. 1, где стадия отбора включает по меньшей мере три из: отбора по типу мутации, отбора по силе экспрессии, отбора по субклеточной локализации и отбора по аффинности связывания в отношении типа HLA пациента.
8. Способ по п. 1, где стадия применения указанного синтетического n-мерного пептида для выделения рекомбинантного антитела включает фаговый пэннинг.
9. Способ по п. 8, где стадия фагового пэннинга дополнительно включает этап созревания аффинности.
10. Способ по п. 1, где указанная информация о последовательности определяющего комплементарность участка рекомбинантного антитела включает CDR1-H, CDR2-H и CDR3-H.
11. Способ по п. 1, где указанное синтетическое антитело получают с применением пересадки CDR или SDR на каркас человеческого антитела.
12. Способ по п. 1, где указанное синтетическое антитело получают посредством рекомбинантной экспрессии в форме IgG, F(ab')2, Fab', Fab или scFv.
13. Способ по п. 1, где указанный терапевтический или диагностический агент представляет собой неклеточный агент.
14. Способ по п. 13, где указанный неклеточный агент представляет собой химиотерапевтическое лекарственное средство, радиоизотоп, изотоп, детектируемый методом PET, изотоп, детектируемый методом SPECT, или аффинный агент.
15. Способ по п. 1, где указанный терапевтический агент представляет собой клетку.
16. Способ по п. 15, где указанная клетка представляет собой Т-клетку или NK-клетку.
17. Способ по п. 16, где указанная клетка представляет собой Т-клетку, экспрессирующую химерный рецептор, содержащий scFv в качестве эктодомена, и при этом указанное синтетическое антитело представляет собой указанный scFv.
18. Способ по п. 16, где указанная клетка представляет собой NK-клетку, экспрессирующую высокоаффинный Fcγ-рецептор (CD16), и при этом указанное синтетическое антитело представляет собой IgG и связано с указанной NK-клеткой через указанный высокоаффинный Fcγ-рецептор.
19. Способ по п. 1, где указанный фармацевтический агент получают в терапевтически эффективных количествах в течение менее чем 6 недель после применения омных данных, для которых есть парные нормальные данные.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| REUSCHENBACH M | |||
| A multiplex method for the detection of serum antibodies against in silico‑predicted tumor antigens // Cancer Immunol Immunother, 2014, 63, p | |||
| Фрикционная передача | 1923 |
|
SU1251A1 |
| ХАРКЕВИЧ Г.Ю., ДЕМИДОВ Л.В | |||
| Современный взгляд на лекарственное лечение | |||
Авторы
Даты
2020-04-16—Публикация
2016-04-25—Подача