Изобретение относится к области медицины и может быть использовано при экспериментальных исследованиях в области колопроктологии детского возраста для моделирования периоперационной ишемии неоректум путем нарушения регионарного кровообращения кишки.
При значительной вариабельности аноректальных пороков развития и технической сложности их хирургической коррекции количество новорожденных, госпитализируемых в отдельную клинику, чаще всего невелико. В таких условиях приобретение опыта затруднительно. Открытое информационное пространство (Интернет, специальная литература), а также обучение детских хирургов в разных клиниках страны и мира определяют современную тенденцию широкого внедрения большого спектра вариантов хирургического лечения и тактических схем послеоперационного ведения пациентов с аноректальными мальформациями. При такой вариабельности оказываемого лечения трудно определить основные факторы, влияющие на отдаленные результаты оперативных вмешательств. В литературе достаточно часто освящаются проблемы стенозирования и нарушения функции неоректум (недержание кала, запоры) в отдаленном послеоперационном периоде. Моделирование периоперационной ишемии неоректум, имеющей место быть после радикальной коррекции аноректальных мальформаций у детей, при которой производилась чрезмерная мобилизация прямой кишки, позволит изучить и определить роль множества факторов, влияющих на исход коррекции порока, в лечебной тактике пациентов с аноректальными пороками развития.
Из уровня техники известны экспериментальные исследования, посвященные изучению анатомического строения прямой кишки и сфинктерного аппарата у животных [Баширов С.Р., Гайдаш А.А., Тихонов В.И. «Строение анального канала и анальных сфинктеров собак в норме и после проктэктомии с низведением ободочной кишки». Бюллетень Сибирской Медицины 14, вып. 6 (2015 г. ): 25-32; Гольдберг О.А., Ким А.Д. «Строение стенки анального канала и дистального отдела прямой кишки белой крысы линии Wistar». Acta Biomedica Scientifica 1, вып. 4 (110) (2016 г.)]. Баширов С.Р. с соавторами, помимо изучения нормального анатомического строения анального канала и анального сфинктера собак, также выполняли резекцию прямой кишки, но при этом пытались воссоздать должную анатомию анального канала путем формирования гладкомышечного сфинктера, резервуара и гладкомышечного лоскута-леватора в промежностном отделе низведенной кишки. Однако предложенная в данном эксперименте модель формирования внутреннего сфинктера и неоануса не позволяет производить экспериментальные исследования в условиях, близких к таковым у детей после радикальной коррекции аноректальных мальформаций, так как в практике такой метод не используется.
Известны также исследования, посвященные значению сохранения внутреннего анального сфинктера в функции прямой кишки [Yoo, S. Y., K. S. Bae, S. J. Kang, S. Y. Kim, и Е. Н. Hwang. «How Important Is the Role of the Internal Anal Sphincter in Fecal Continence? An Experimental Study in Dogs». Journal of Pediatric Surgery 30, вып. 5 (1995 г. ): 687-91]. Yoo S. Y с соавторами также выполняли резекцию участков прямой кишки разной протяженности в эксперименте, но после операции оценивали только клинические показатели (держание кала, аноректальное давление, местный статус) для оценки роли внутреннего анального сфинктера в функции прямой кишки. В проведенных экспериментах у собак резецировали участки прямой кишки длиной 2 и 4 см, при этом оценку кровоснабжения неоректум не производили. Резекция участка прямой кишки такой длины у собак может быть недостаточно для достижения значимой ишемии неоректум.
Известно исследование влияния терапевтических препаратов, ингибирующих процесс фиброзирования тканей, на заживление послеоперационной раны после аноректопластики [Lampus H.F., Kusmayadi D.D., Nawas В.А. «The influence of topical mitomycin-C on total fibroblasts, epithelialization, and collagenization in anoplasty wound healing in Wistar rats». Journal of Pediatric Surgery. 2015 Aug; 50(8): 1347-51]. В данном экспериментальном исследовании Lampus H.F. с соавторами не производили резекцию участка прямой кишки, а только выполняли циркулярный разрез вокруг ануса с последующей анопластикой. Такая модель не соответствует состоянию кишки после радикальной коррекции аноректальных пороков, так как не производилась ректопластика.
При изучении патентной литературы не было найдено способов моделирования периоперационной ишемии неоректум.
Технической проблемой, решаемой изобретением, является воспроизведение периоперационной ишемии неоректум, возникающей после радикальной коррекции аноректальных мальформаций с чрезмерной мобилизацией прямой кишки, при которой нарушается регионарное кровообращение неоректум.
Техническим результатом, на достижение которого направлено заявленное изобретение, является обеспечение возможности воспроизведения периоперационной ишемии неоректум, возникающей после радикальной коррекции аноректальных мальформаций с чрезмерной мобилизацией прямой кишки. Изобретение позволяет получить точную и адекватную модель, соответствующую данной патологии, обеспечивающую возможность дальнейшего изучения факторов, влияющих на исход лечения порока, разработку способов его коррекции и тактики послеоперационного ведения пациентов с аноректальными мальформациями.
Технический результат достигается за счет реализации способа создания модели послеоперационной ишемии неоректум у лабораторных животных массой от 350 г, включающего круговой разрез кожи и подкожно-жировой клетчатки вокруг ануса, мобилизацию участка прямой кишки непосредственно по стенке кишки до наружного анального сфинктера протяженностью не менее 35 мм с одновременной коагуляцией всех сосудов на ее поверхности, циркулярную коагуляцию серозной оболочки выделенного участка прямой кишки в двух местах - в самом проксимально доступном месте выделенного участка кишки, и на его середине, с нарушением регионарного и сохранением внутристеночного кровоснабжения дистальной части прямой кишки, создание неоануса посредством наложения узловых швов между кожей ануса и кишкой по всей окружности кишки с получением модели ишемии неоректум на третьи сутки после операции.
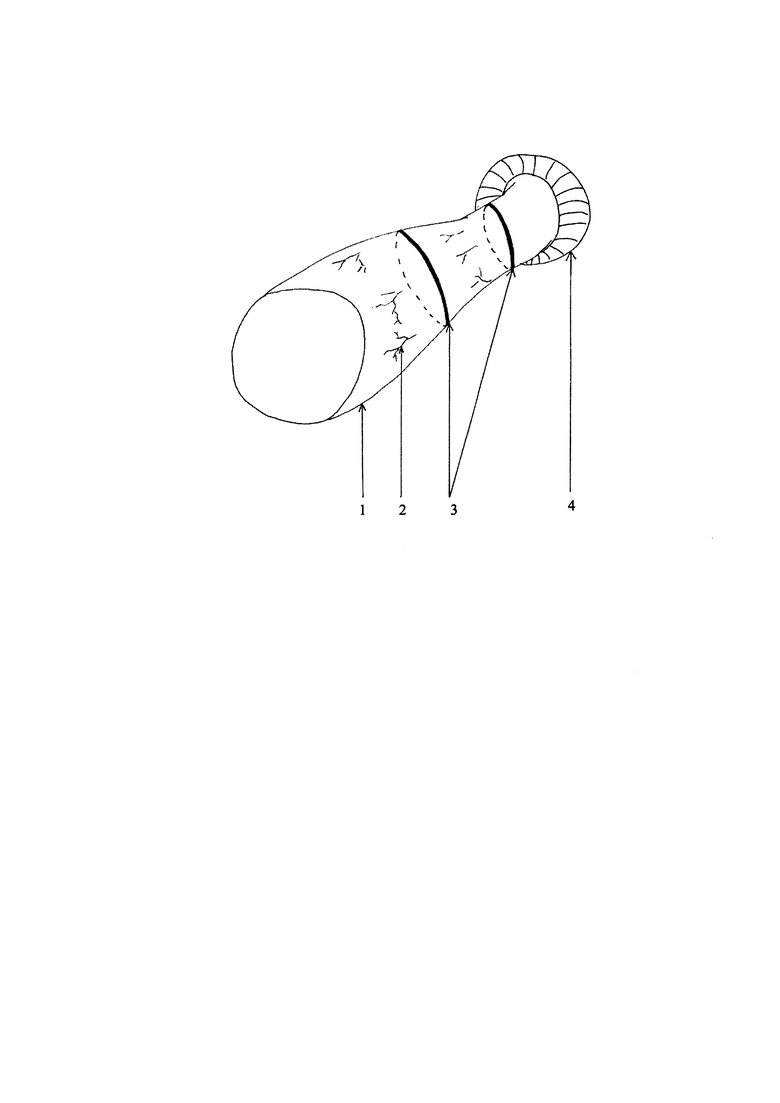
Изобретение поясняется чертежом, на котором позициями обозначены: 1 - прямая кишка, 2 - сосуды на поверхности прямой кишки (подлежащие коагуляции), 3 - два «кольца» коагуляции серозной оболочки, 4 - наружный сфинктер прямой кишки.
Способ осуществляют следующим образом.
Берут опытное животное массой от 350 г (например, крысу), дают внутримышечный наркоз, дополненный местной анестезией перианальной области (Новокаин 0,5% 0,2 мл/кг). После чего скальпелем выполняют круговой разрез вокруг анального отверстия на расстоянии 1-2 мм, рассекая кожу и подкожно-жировую клетчатку. Прямую кишку 1 выделяют непосредственно по стенке органа до наружного сфинктера 4, длиной не менее 35 мм (см. чертеж), используя монополярный коагулятор в режиме «резания» (допускается использование биполярного коагулятора). При этом коагулируют все сосуды 2 на поверхности прямой кишки посредством монополярного коагулятора. Затем на режиме усиленной коагуляции на выделенном участке кишки циркулярно линейно повреждают серозную оболочку в двух местах - в самом проксимально доступном месте выделенного участка кишки, и примерно на его середине, с образованием двух «колец» 3 коагуляции серозной оболочки. Второе «кольцо» выполняют для достоверного нарушения регионарного кровоснабжения ректум, тем самым сохраняя только внутристеночное кровоснабжение дистальной части прямой кишки (см. чертеж). Затем кишку возвращают на свое место. Окончанием оперативного вмешательства является создания неоануса, путем наложения 8-12 узловых швов между кожей и кишкой по всей окружности операционной
раны: кожу прокалывают снаружи внутрь в 2 мм от края, следом так же прокалывают кишку через все слои на расстоянии 2-4 мм от края (расстояние между швами 4-6 мм). Используемый шовный материал - полифиламентный синтетический рассасывающийся 4-0. Ишемия неоректум присутствует на третьи сутки после операции.
Предлагаемый способ позволяет изучать морфологические и функциональные изменения неоректум и неоануса в зависимости от проводимого лечения или без него в условиях близких к таковым у детей после радикальной коррекции аноректальных мальформаций с чрезмерной мобилизацией прямой кишки.
Созданная периоперационная ишемия неоректум подтверждается морфологическими исследованиями и иммуноферментным анализом (ИФА) кишечного гомогената. Материал для лабораторных исследований забирался на 3-й сутки после оперативного вмешательства у 10 животных. Эксперимент был выполнен на базе центрального вивария Сеченовского университета.
Проведенное гистологическое исследование выявило нарушение венозного дренажа, выраженная воспалительная реакция диффузного характера за счет миграции клеток «острой фазы» - нейтрофилов и эозинофилов преимущественно в подслизистую основу стенки кишки; полнокровие вен и венул, повышение их проницаемости с развитием мелких кровоизлияний, образование тромбов (по структуре смешанных и красных) в сосудах венозного типа подслизистой основы. В мышечном слое воспаление носит фокальный и менее интенсивный характер. Морфологические изменения соответствуют ишемии ткани кишки.
Ишемия неоректум также подтверждалась концентрацией биомаркеров гипоксии HIF-1a (5,127 нг/мл), VEGF-C (594,4 пг/мл) в кишечном гомогенате.
Пример реализации способа.
Нелинейной крысе массой 545 г внутримышечно ввели золазепама гидрохлорид, тилетамина гидрохлорид в равных пропорциях из расчета 15 мг/кг, выполнили местную анестезию перианальной области (Новокаин 0,5% 0,2 мл/кг). Произвели круговой разрез кожи вокруг ануса на расстоянии 2 мм от анального отверстия, используя скальпель, после чего выделили кишку непосредственно по ее стенке коагулируя монополярным коагулятором все сосуды на поверхности ректум, до наружного анального сфинктера. Длина выделенного участка составила 38 мм. После чего монополярным коагулятором повреждали серозный слой выделенного участка в двух местах циркулярно линейно (в самом проксимально доступном месте выделенного участка кишки, и на его середине). Далее приступили к наложению швов между кожей и кишкой для создания неоануса. Кишку прошивали через все слои. Первые швы создавались на «12 часах», «6 часах», «9 часах» и «3 часах» окружности, затем швы накладывались между соседними уже наложенными швами до полного закрытия операционной раны по всей окружности (расстояние между швами 4-6 мм). Использовался полифиламентный синтетический рассасывающийся шовный материал 4-0.
У крысы в течение трех дней после оперативного вмешательства наблюдался стул, но его количество было снижено. При этом дефекация была нарушена, стул задерживался на выходе из ануса, перианальная область загрязнялась фекалиями.
На 3-й сутки после операции забиралась ткань неоректум для лаборатных исследований. Морфологическое исследование и ИФА установили ишемию кишки.
Таким образом, предлагаемый способ позволяет создать периоперационную ишемию неоректум, путем нарушения регионарного кровообращения ткани кишки. Создаются условия близкие к клиническому течению послеоперационного периода пациентов после радикальной хирургической коррекции аноректального порока развития, при которой выполнялась чрезмерная мобилизация прямой кишки. Модель может использоваться при экспериментальных исследованиях для изучения влияния различных факторов в послеоперационном ведении таких пациентов, а также роли различных оперативных факторов на исход хирургического лечения. Летальность при создании модели составила 0%, воспроизводимость модели 100%. Способ обеспечивает получение во всех случаях ишемии неоректум однотипную по тяжести патологического процесса и по клинической картине. При апробации модели установлено, что нет необходимости каждый раз выполнять биомикроскопию, достоверно получение ишемии ткани кишки можно прогнозировать на основании коагуляции всех поверхностных сосудов прямой кишки, а также выполненной циркулярной коагуляции серозной оболочки в двух местах, тем самым сохраняя только внутристеночное кровоснабжение.
Предлагаемый способ создания ишемии неоректум также позволяет исследовать роль чрезмерной мобилизации кишки при хирургических коррекциях аноректальных мальформаций, влияние данного фактора на клиническое течение послеоперационного периода, а также на исход выполненного лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОЗДАНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ ПОСЛЕОПЕРАЦИОННОЙ ИШЕМИИ НЕОРЕКТУМ ПУТЕМ НАТЯЖЕНИЯ ПРЯМОЙ КИШКИ | 2019 |
|
RU2719661C1 |
| Способ парциальной пластики наружного анального сфинктера у детей | 2023 |
|
RU2820000C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ НИЗКИХ ФОРМ АНОРЕКТАЛЬНЫХ ПОРОКОВ У НОВОРОЖДЕННЫХ | 2013 |
|
RU2523639C1 |
| СПОСОБ БРЮШНО-АНАЛЬНОЙ РЕЗЕКЦИИ ПРЯМОЙ КИШКИ | 1999 |
|
RU2171635C2 |
| Способ хирургического лечения ректального пролапса у детей, оперированных по поводу аноректальной мальформации | 2023 |
|
RU2829051C1 |
| СПОСОБ НЕПРЕРЫВНОГО СЕРОЗНО-МЫШЕЧНО-ПОДСЛИЗИСТОГО ОДНОРЯДНОГО КИШЕЧНОГО ШВА С ВИЗУАЛЬНЫМ КОНТРОЛЕМ ПО ВСЕЙ ОКРУЖНОСТИ КИШКИ | 2019 |
|
RU2718281C1 |
| Способ хирургического лечения параректальных свищей | 2023 |
|
RU2818747C1 |
| СПОСОБ ТРАНСАНАЛЬНОЙ РЕЗЕКЦИИ ПРЯМОЙ КИШКИ ПРИ БОЛЕЗНИ ГИРШПРУНГА У ДЕТЕЙ | 2009 |
|
RU2410046C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ НАРУЖНЫХ ПОЛОВЫХ ОРГАНОВ У ЖЕНЩИН ПРИ ВОВЛЕЧЕНИИ АНУСА В ОПУХОЛЕВЫЙ ПРОЦЕСС И КЛОАГЕННОМ РАКЕ | 2000 |
|
RU2157121C1 |
| СПОСОБ ВАГИНОПРОКТОАНОСФИНКТЕРОПЛАСТИКИ ПРИ ЛЕЧЕНИИ КЛОАКАЛЬНЫХ АТРЕЗИЙ ЗАДНЕГО ПРОХОДА | 2001 |
|
RU2209043C1 |
Изобретение относится к области медицины, а именно к колопроктологии. У лабораторных животных массой от 350 г проводят круговой разрез кожи и подкожно-жировой клетчатки вокруг ануса. Выделяют участок прямой кишки непосредственно по стенке кишки до наружного анального сфинктера протяженностью не менее 35 мм с одновременной коагуляцией всех сосудов на ее поверхности. Проводят циркулярную коагуляцию серозной оболочки выделенного участка прямой кишки в двух местах - в самом проксимально доступном месте выделенного участка кишки и на его середине, с нарушением регионарного и сохранением внутристеночного кровоснабжения дистальной части прямой кишки. Создание неоануса посредством наложения узловых швов между кожей ануса и кишкой по всей окружности кишки. Получают модель ишемии неоректум на третьи сутки после операции. Способ позволяет воспроизвести послеоперационную ишемию неоректум, возникающую после радикальной коррекции аноректальных мальформаций с чрезмерной мобилизацией прямой кишки. 1 ил., 1 пр.
Способ создания послеоперационной модели ишемии неоректум у лабораторных животных массой от 350 г, включающий круговой разрез кожи и подкожно-жировой клетчатки вокруг ануса, выделение участка прямой кишки непосредственно по стенке кишки до наружного анального сфинктера протяженностью не менее 35 мм с одновременной коагуляцией сосудов на ее поверхности, циркулярную коагуляцию серозной оболочки выделенного участка прямой кишки в двух местах - в самом проксимально доступном месте выделенного участка кишки и на его середине, с нарушением регионарного и сохранением внутристеночного кровоснабжения дистальной части прямой кишки, создание неоануса посредством наложения узловых швов между кожей ануса и кишкой по всей окружности кишки с получением модели ишемии неоректум на третьи сутки после операции.
| СПОСОБ МОДЕЛИРОВАНИЯ ОСТРОЙ КИШЕЧНОЙ НЕПРОХОДИМОСТИ | 2009 |
|
RU2422913C1 |
| Баширов С.Р | |||
| и др | |||
| Строение анального канала и анальных сфинктеров собак в норме и после проктэктомии с низведением ободочной кишки, Бюллетень сибирской медицины, 2015, т.14, 6, с.25-32 | |||
| Яновой В.В | |||
| Низкая резекция прямой кишки, хронология проблем, Хирургия, 2012, 1, 49-52 | |||
| Araki, J.et al | |||
| Anorectal autotransplantation | |||
Авторы
Даты
2020-04-21—Публикация
2019-09-27—Подача