Настоящее изобретение относится к медицине, а именно к психиатрии, и позволяет прогнозировать степень риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией.
Сердечно-сосудистые заболевания являются одной из первостепенных причин преждевременной смертности у больных шизофренией, обусловливая тем самым значительное сокращение продолжительности жизни данной категории больных по сравнению с общей популяцией [1]. Больные шизофренией имеют более высокие показатели распространенности метаболического синдрома, ускоряющего развитие кардиоваскулярных заболеваний [2, 3]. В соответствии с критериями Международной Федерацией Диабета, метаболический синдром определяется как абдоминальное (висцеральное) ожирение в сочетании с двумя и более признаками из четырех: повышение сывороточных уровней триглицеридов (специфическое лечение по поводу данного нарушения), повышенное содержание глюкозы в плазме крови натощак (ранее диагностированный сахарный диабет 2-го типа), снижение сывороточных концентраций холестерина липопротеинов высокой плотности (специфическое лечение по поводу данного нарушения), а также повышенное артериальное давление (лечение ранее диагностированной артериальной гипертензии).
Согласно данным многочисленных исследований, причинами повышения частоты возникновения метаболического синдрома или его компонентов среди больных шизофренией по сравнению с общей популяцией являются терапия антипсихотическими препаратами, в особенности атипичными антипсихотиками [4], внутренние механизмы шизофренического процесса [5, 6], специфический образ жизни пациентов с шизофренией, а также генетические факторы [7]. Примерами таких генетических факторов могут быть однонуклеотидные мутации в генах NOS3 и GLP-1R, кодирующих эндотелиальную синтазу оксида азота и рецептор глюкагоноподобного пептида-1. Нарушения функционирования эндотелиальной синтазы оксида азота при метаболическом синдроме и, как следствие, снижение вазопротекторных эффектов продуцируемого под ее действием оксида азота способствуют формированию эндотелиальной дисфункции и инсулинорезистентности [8]. Недостаточность секреции и снижение чувствительности тканей к гормону глюкагоноподобному пептиду-1, синтезируемого в желудочно-кишечном тракте и усиливающего глюкозозависимую секрецию инсулина, также вносят значимый вклад в развитие инсулинорезистентности при метаболическом синдроме и компенсируются применением агонистов рецепторов данного гормона [9, 10].
Известен способ прогнозирования риска метаболического синдрома, выявляющий степень выраженности метаболических нарушений на основе определения блока антропометрических показателей, показателей липидного обмена, показателей липопероксидации, показателей функционального состояния печени и показателей центральной гемодинамики с вычислением прогностического индекса [11]. По рассчитываемому значению данного индекса прогнозируют отсутствие риска развития метаболического синдрома, низкий риск, средний риск или высокий риск развития метаболического синдрома. Одним из недостатков данного способа является его недостаточная специфичность, так как нарушения в содержании определяемых биохимических показателей зависят от множества факторов, включающих пол, возраст, наличие различных заболеваний, сопровождаемых хроническим системным воспалением или поражением печени и т.д. Кроме того, используемые функциональные и биохимические методы требуют использования сложной, дорогостоящей аппаратуры (многофункционального компьютерного реографа, иммуноферментного анализатора) и большого количества наборов реагентов, что может ограничивать применение данного способа.
Известен способ прогнозирования метаболического синдрома у больных хронической обструктивной болезнью легких, заключающийся в интегральной оценке маркеров перекисного окисления липидов, эндотелиальной дисфункции, инсулинорезистентности, гликемического профиля, липидного спектра и антропометрических данных для вычисления значения дискриминантной функции [12]. Недостатком данного способа является необходимость выполнения большого количества антропометрических измерений и трудоемких этапов по оценке концентраций вышеперечисленных маркеров в сыворотке (плазме) крови, ограничивает применение этого способа в клинической практике.
Наиболее близким по технической сущности к предлагаемому изобретению является способ прогнозирования риска развития метаболического синдрома у пациентов с абдоминальным ожирением [13], взятый за прототип. В основе данного метода лежит генотипирование однонуклеотидного полиморфного варианта T45G гена адипонектина. Недостатками данного способа являются его относительно низкая эффективность, поскольку для прогнозирования риска метаболического синдрома используется только один ген, а также длительное выполнение методики ввиду проведения анализа полиморфизма длин рестрикционных фрагментов ДНК в агарозном геле.
Оценка генетической предрасположенности к развитию метаболического синдрома на фоне терапии антипсихотическими препаратами позволит выделить группы высокого риска даже при отсутствии у пациентов выраженных метаболических нарушений или изменений антропометрических показателей. Прогнозирование степени риска развития данного симптомокомплекса на фоне антипсихотической терапии у больных шизофренией на основе молекулярно-генетических маркеров может являться одним из критериев выбора антипсихотических препаратов для проведения терапии, позволит своевременно проводить лечебные мероприятия по профилактике клинических проявлений метаболического синдрома у пациентов в группе высокого риска.
Задачей настоящего изобретения является разработка способа прогнозирования степени риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией на основе генетических маркеров.
Поставленную задачу решают путем прогнозирования степени риска развития метаболического синдрома у пациентов с шизофренией в результате определения генотипов полиморфных вариантов rs2070744 гена NOS3 и rs6923761 гена GLP-1R методом полимеразной цепной реакции в режиме реального времени.
Способ состоит из 4 этапов и осуществляется следующим образом:
На первом этапе из цельной крови пациентов выделяют геномную ДНК при помощи коммерческих наборов «ДНК-Экстран-1» («Синтол», Россия), согласно инструкции производителя, или другими известными методами.
На втором этапе проводят полимеразную цепную реакцию в режиме реального времени для определения генотипов полиморфного варианта rs2070744 гена NOS3 при помощи коммерческих наборов для определения данного полиморфизма («Синтол», Россия). В лунки планшета или эппендорфы объемом 0,2 мл вносят по 10 мкл 2,5-кратной реакционной смеси, содержащей специфические праймеры (5'-GGCACAGAACTACAAACCCC-3'; 5'-GTCAGCAGAGAGACTAGGGC-3') и зонды (FAM-CAGGGTCAGCCAGCCAGG-RTQ1; R6G-GATCCTCCTCAGCTTCA-BHQ2), 10 мкл разбавителя, 5 мкл ДНК и 0,5 мкл Taq-полимеразы. Анализ осуществляют в дублях и используют положительные контрольные образцы, соответствующие генотипам ТТ, ТС и СС полиморфизма rs2070744 гена NOS3, а также отрицательный контрольный образец. Планшет или эппендорфы с образцами загружают в термоблок амплификатора LightCycler 480 Instrument II («Roche», Швейцария) и запускают программу амплификации ДНК со считыванием флуоресцентного сигнала по двум каналам для флуорофоров FAM и R6G. Протокол амплификации для полиморфизма Т-786С гена NOS3 включает нагрев реакционной смеси при 95°С продолжительностью 3 мин и 40 циклов в следующем режиме: 95°С - 15 сек, 65°С - 40 сек. В процессе амплификации ДНК Taq-полимераза расщепляет олигонуклеотидные зонды, что приводит к увеличению расстояния между «гасителями» (RTQ1 или BHQ-1) и флуорофорами (FAM или R6G) и соответствующей регистрации флуоресцентного сигнала. Если регистрируется флуоресцентный сигнал только по каналу FAM, то пациент является носителем генотипа ТТ полиморфизма Т-786С гена NOS3. Если детекция флуоресцентного сигнала происходит по обоим каналам FAM и R6G, то это означает, что пациент является носителем гетерозиготного генотипа ТС данного полиморфизма. Если флуоресцентный сигнал считывается только по каналу R6G, то пациент имеет генотип СС полиморфизма Т-786С гена NOS3.
На третьем этапе по аналогии с предыдущим проводят полимеразную цепную реакцию в режиме реального времени для определения генотипов полиморфизма rs6923761 гена GLP-1R при помощи коммерческих наборов для определения данного полиморфизма с соответствующими олигонуклеотидными зондами (FAM-CCTCGGCTTCAGGTAAGGT-RTQ1; R6G-GATCCTCCTCAGCTTCA-BHQ2) и специфическими праймерами (5'-CGCACTCTCCTTCTCT-3'; 5'-GTTGGGCTGCTTCATTCCTC-3') («Синтол», Россия). Анализ проводят в дублях с использованием отрицательного контрольного образца и положительных контрольных образцов, соответствующих генотипам GG, GA и АА полиморфизма rs6923761 гена GLP-1R. После загрузки планшета или эппендорфы с образцами в термоблок амплификатора LightCycler 480 Instrument II ("Roche", Швейцария) запускают программу амплификации ДНК со считыванием флуоресцентного сигнала в реальном времени по двум каналам для флуорофоров FAM и R6G. Данная программа для полиморфизма rs6923761 гена GLP-1R включает предварительную денатурацию ДНК-матрицы (95°С в течение 3 мин) и 40 циклов амплификации (95°С в течение 15 сек, 63°С в течение 40 сек). На основании результатов полимеразной цепной реакции в режиме реального времени идентифицируется один из трех возможных генотипов однонуклеотидного полиморфизма rs6923761 гена GLP-1R у пациента: генотип GG (при регистрации флуоресценции по каналу FAM), гетерозиготный генотип GA (при регистрации флуоресценции по каналам FAM и HEX) или генотип АА (при детекции флуоресцентного сигнала по каналу HEX).
На четвертом этапе проводят оценку степени риска развития метаболического синдрома на фоне антипсихотической терапии у обследуемых лиц. При выявлении генотипов ТС или СС полиморфизма rs2070744 гена NOS3 и генотипа GG полиморфизма rs6923761 гена GLP-1R прогнозируют высокий риск развития метаболического синдрома, а при выявлении генотипа ТТ полиморфизма rs2070744 гена NOS3 и генотипов GG или GA полиморфизма rs6923761 гена GLP-1R прогнозируют низкий риск развития метаболического синдрома. Риск развития метаболического синдрома отсутствует, если установлено носительство генотипов ТС или СС полиморфизма rs2070744 гена NOS3, а также генотипов GA или АА полиморфизма rs6923761 гена GLP-1R.
В популяционное исследование по типу «случай-контроль» было включено 255 больных с диагнозом «шизофрения» (F20 по МКБ-10), относившихся к европеоидной расе и проходивших стационарное лечение в отделении эндогенных расстройств клиники НИИ психического здоровья Томского национального исследовательского медицинского центра Российской академии наук. В исследуемую группу вошли 65 больных шизофренией с метаболическим синдромом (46 женщин и 19 мужчин, средний возраст - 47±13 лет). В данной группе терапию атипичными антипсихотиками получали 46 пациентов (71%), терапию типичными антипсихотиками - 8 пациентов (12%), комбинированную терапию типичными и атипичными антипсихотиками - 11 пациентов (17%). В контрольную группу были включены 190 больных шизофренией (68 женщин и 122 мужчины, средний возраст - 44±9 лет) с нормальными значениями индекса массы тела (ИМТ). В данной выборке терапию атипичными антипсихотиками получали 140 пациентов (74%), терапию типичными антипсихотиками - 12 пациентов (6%), комбинированную терапию типичными и атипичными антипсихотическими препаратами - 38 больных шизофренией (20%). Спектр назначаемых атипичных антипсихотиков включал рисперидон, амисульприд, палиперидон, клозапин, оланзапин и сертиндол. Наиболее используемым типичным антипсихотиком был галоперидол.
Метаболический синдром у пациентов с шизофренией устанавливался на основании критериев Международной Федерации Диабета. Исследование было одобрено локальным независимым этическим комитетом НИИ психического здоровья Томского НИМЦ. При проведении исследования были соблюдены принципы информированного согласия Хельсинской Декларации Всемирной Медицинской Ассоциации.
В обеих группах пациентов с шизофренией были измерены следующие антропометрические характеристики: масса тела, рост, объем талии (ОТ) и объем бедер (ОБ). ОТ определяли с помощью сантиметровой ленты по линии, находящейся на середине расстояния между гребнем подвздошной кости и нижним краем реберной дуги. ОБ измеряли на уровне вертелов бедренных костей. Для расчета ИМТ использовали формулу: ИМТ = масса тела (кг)/рост (м)2. Исследование биохимических показателей нарушений углеводного и липидного обменов в сыворотке или плазме крови проводились на автоматическом биохимическом анализаторе СА-180 («Furuno Electric Co., Ltd.», Япония) с использованием наборов реагентов «Triglycerides FS», «Glucose GOD FS» и «HDL-C Immuno FS» («DiaSys Diagnostic Systems GmbH», Германия). Материалом для исследования служила венозная кровь. Геномная ДНК из крови пациентов с шизофренией была выделена с использованием наборов «ДНК-Экстран-1» («Синтол», Россия). Исследование генотипов изучаемых полиморфных вариантов проводили на амплификаторе LightCycler 480 Instrument II ("Roche", Швейцария) с применением наборов для определения полиморфизмов rs2070744 гена NOS3 и rs6923761 гена GLP-1R («Синтол», Россия).
Статистическую обработку полученных данных проводили в программе Statistica 10.0. Критерий Колмогорова-Смирнова применяли для проверки нормальности распределения. Для сравнения средних значений двух нормально распределенных выборок использовали t-критерий Стьюдента. С помощью критерия согласия Пирсона (хи-квадрат) проводили сравнение частот аллелей и генотипов в выборках. Различия считались статистически значимыми при уровне значимости р<0,05. Значения отношения шансов (OR) и 95% доверительного интервала (95% CI) были определены с применением статистического онлайн-калькулятора VassarStats. Значения OR>1 указывали на ассоциацию генотипов (аллелей) с повышенным риском развития метаболического синдрома у больных шизофренией. Значения OR<1 служили индикатором ассоциации генотипов (аллелей) со сниженным риском развития метаболического синдрома у больных шизофренией.
Сравнение групп пациентов с шизофренией по антропометрическим характеристикам и показателям нарушений углеводного и липидного обменов выявило следующие результаты. Среднее значение ИМТ в группе больных шизофренией с метаболическим синдромом (34,06±4,13 кг/м2) было выше, чем в контрольной группе (21,56±2,09 кг/м2) (р<0,001). Среднее значение ОТ в группе больных шизофренией с метаболическим синдромом (103,31±13,19 см) было также более высоким, чем в контрольной группе (77,90±6,71 см) (р<0,001). Различий в значениях ОБ между исследуемой (104±20,58 см) и контрольной (95,17±9,95 см) группами не было найдено. Уровни глюкозы в плазме натощак (5,55±0,70 ммоль/л), сывороточные уровни триглицеридов (1,50±0,50 ммоль/л) и холестерина липопротеинов высокой плотности (1,01±0,27 ммоль/л) в группе больных шизофренией с метаболическим синдромом не отличались от таковых в группе пациентов с нормальными значениями ИМТ (5,14±0,65 ммоль/л, 1,15±0,53 ммоль/л, 1,2±0,43 ммоль/л).
Распределения частот аллелей и генотипов полиморфизма rs2070744 гена NOS3 в исследуемой и контрольной группах соответствовали равновесию Харди-Вайнберга. Частоты аллеля Т (55,4% против 67,4%, р=0,01) и генотипа ТТ (26,2% против 45,3%, р=0,007) в исследуемой группе были статистически значимо ниже, чем в контрольной группе. Аллель Т (OR=0,60; 95% CI 0,40-0,90) и генотип ТТ (OR=0,45; 95% CI 0,23-0,80) полиморфизма rs2070744 гена NOS3 были ассоциированы с низким риском формирования метаболического синдрома у данной категории больных.
В группе больных шизофренией с метаболическим синдромом частоты аллелей G и А полиморфного варианта rs6923761 гена GLP-1R составили 81,5% и 18,5%, в контрольной группе - 72,7% и 27,3%. Распределение частот генотипов полиморфизма rs6923761 гена GLP-1R в группе больных шизофренией с метаболическим синдромом соответствовало равновесию Харди-Вайнберга (р=0,52) и было следующим: GG - 67,7%, GA - 27,7%, АА - 4,6%. В контрольной группе распределение частоты генотипов данного полиморфного варианта также соответствовало равновесию Харди-Вайнберга (р=0,23) и составило: GG - 54,7%, GT - 36%, ТТ - 9,3%. Носители генотипа GG полиморфизма rs6923761 гена GLP-1R в исследуемой группе встречались чаще, чем в контрольной (р=0,011). Установлено, что генотип GG данного полиморфизма у больных шизофренией ассоциирован с высоким риском развития метаболического синдрома (OR=1,74, 95% CI 0,95-3,17).
Таким образом, приведенные результаты исследования подтверждают то, что определение генотипов полиморфных вариантов rs2070744 гена NOS3 и rs6923761 гена GLP-1R позволяет прогнозировать риск развития метаболического синдрома при шизофрении. Описанный способ прост в осуществлении, в его основе лежит анализ данных полимеразной цепной реакции в режиме реального времени с последующим расчетом отношения шансов развития метаболического синдрома, что позволяет преждевременно формировать группы высокого риска, корректировать антипсихотическую терапию и проводить профилактические мероприятия с учетом индивидуальных генетических особенностей пациентов с шизофренией.
Пример 1. Пациентка Ю., 26 лет. Находилась на лечении в ТОКПБ с диагнозом параноидной шизофрении, непрерывного типа течения. Родилась в состоянии асфиксии, с интранатальным поражением ЦНС. Росла агрессивным ребенком (мучила животных, обижала сверстников). Страдала энурезом до 5 лет. С 7 лет наблюдалась у психиатра с диагнозом «органического поражения ЦНС, эпилептиформного синдрома». В юношестве госпитализировалась в ТОКПБ с диагнозом эпилепсии и изменениями личности по эпилептоидному типу со снижением интеллекта. Вышла замуж за мужчину, страдающего шизофренией, от брака двое детей, вскоре была лишена родительских прав. Не работала, проживала с родителями. 2 года назад появились вербальные псевдогаллюцинации императивного содержания, был выставлен диагноз параноидной шизофрении, установлена II группа инвалидности. В дальнейшем часто госпитализировалась в ТОКПБ, до 6 раз за год. При поступлении жаловалась на преследование со стороны бывших работодателей, бессонницу и тревогу. Психический статус при поступлении характеризовался фрагментарными идеями отношения с инсомническим компонентом на фоне специфических эмоционально-волевых и ассоциативных расстройств. Артериальное давление при поступлении 145/88 мм.рт.ст. В лечении получала галоперидол 30 мг/сут., с последующим переводом на пролонгированную форму галоперидола 100 мг, хлорпромазин до 300 мг. Была проконсультирована терапевтом. Выставлен диагноз гипертонической болезни II ст, риск 3, назначен бисопролол 5 мг/сут. В отношении данной больной проводилась диагностика сопутствующего метаболического синдрома на основании критериев Международной ассоциации диабета: основной критерий - обхват талии более 80 см присутствовал (у пациентки он составил 134 см), однако среди дополнительных критериев выполнялся только один: повышенный уровень артериального давления более 130/85 мм.рт.ст. (у пациентки 145/88 мм.рт.ст.). В результате проведения полимеразной цепной реакции в режиме реального времени было установлено, что данная пациентка является носителем генотипа ТС полиморфизма rs2070744 гена NOS3 и генотипа GG полиморфизма rs6923761 гена GLP-1R, что говорит о высоком риске развития метаболического синдрома. В динамике через 4 недели лечения при повторном биохимическом обследовании уровень триглицеридов составил 1,8 ммоль/л. Таким образом, у данной пациентки был верифицирован метаболический синдром на фоне антипсихотической терапии. Следовательно, предложенный способ прогнозирования степени риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией в отношении данной пациентки подтвердился.
Пример 2. Пациентка К., 64 года. Находилась на лечении в ТОКПБ с диагнозом параноидной шизофрении, непрерывного типа течения. Родилась первым ребенком в полной семье. Росла замкнутой, стеснительной, предпочитала общению со сверстниками уединенные игры. В раннем детском возрасте перенесла ветряную оспу, часто болела ангиной. В школу пошла с 7 лет. Училась удовлетворительно. Окончила 10 классов средней школы, получить среднее специальное образование не смогла, пропускала занятия, была отчислена за неуспеваемость из училища. Диагноз параноидной шизофрении был установлен в 19-летнем возрасте. Ежегодно госпитализировалась в ТОКПБ с симптоматикой по типу «клише» в виде актуализации галлюцинаторно-бредовой симптоматики. Не работала, проживала с родителями. Установлена II группа инвалидности. Наблюдалась в ПНД, в лечении преимущественно получала пролонгированные формы конвенциональных антипсихотиков из-за низкой приверженности к лечению. С 45 лет страдает гипертонической болезнью, постоянно принимает бисопролол. В настоящее поступление высказывала идеи отношения в адрес родителей, слышала голоса внутри головы императивного содержания, бессонницу и тревогу. Психический статус при поступлении характеризовался галлюцинаторно-бредовым синдромом на фоне специфических эмоционально-волевых и ассоциативных расстройств. Артериальное давление при поступлении 130/85 мм.рт.ст. (на фоне гипотензивной терапии бисопрололом 5 мг). В биохимическом анализе крови: содержание глюкозы 5,1 ммоль/л, триглицеридов - 1,7 ммоль/л, холестерина ЛПВП - 1,5 ммоль/л. Принимала галоперидол 30 мг/сут., с последующим переводом на пролонгированную форму галоперидола 100 мг внутримышечно 1 раз месяц. Была проконсультирована терапевтом. В результате проведения полимеразной цепной реакции в режиме реального времени было установлено, что данная пациентка является носителем генотипа ТТ полиморфизма rs2070744 гена NOS3 и генотипа АА полиморфизма rs6923761 гена GLP-1R, что говорит о низком риске развития метаболического синдрома. В отношении данной больной проводилась диагностика сопутствующего метаболического синдрома на основании критериев Международной ассоциации диабета: основной критерий - обхват талии более 80 см присутствовал (у пациентки он составил 134 см), однако среди дополнительных критериев выполнялся только один: повышенный уровень триглицеридов равен или более 1,7 ммоль/л (у пациентки 1,7 ммоль/л). Таким образом, диагноз метаболического синдрома у данной пациентки подтвержден не был. Следовательно, предложенный способ прогнозирования степени риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией в отношении данной пациентки подтвердился.
Таким образом, предлагаемый способ прост в осуществлении и на основе определения генетических полиморфизмов позволяет прогнозировать степень риска метаболического синдрома у больных шизофренией на фоне антипсихотической терапии и целенаправленно проводить индивидуальную терапевтическую тактику для больных с высоким риском метаболического синдрома.
Список использованной литературы:
1. Robinson D.G. Early mortality among people with schizophrenia // Am J Psychiatry. - 2016. - Vol. 173. - P. 554-555.
2. Enez Darcin A., Yalcin Cavus S., Dilbaz N., Kaya H., Dogan E. Metabolic syndrome in 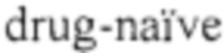 and drug-free patients with schizophrenia and in their siblings // Schizophr Res. - 2015. - Vol. 166, №1-3. - P. 201-206.
and drug-free patients with schizophrenia and in their siblings // Schizophr Res. - 2015. - Vol. 166, №1-3. - P. 201-206.
3. Vancampfort D., Stubbs В., Mitchell A.J., De Hert M., Wampers M., Ward P.B., Rosenbaum S., Correll C.U. Risk of metabolic syndrome and its components in people with schizophrenia and related psychotic disorders, bipolar disorder and major depressive disorder: a systematic review and meta-analysis // World Psychiatry. - 2015. - Vol. 14, №3. P. 339-347.
4. Pramyothin P., Khaodhiar L. Metabolic syndrome with the atypical antipsychotics // Curr Opin Endocrinol Diabetes Obes. - 2010. - Vol. 17, №5. - P. 460-466.
5. Ryan M.C., Collins P., Thakore J.H. Impaired fasting glucose tolerance in first-episode, drug-naive patients with schizophrenia // Am J Psychiatry. - 2003. - Vol. 160, №2. - P. 284-289.
6. Thakore J.H., Mann J.N., Vlahos I., Martin A., Reznek R. Increased visceral fat distribution in drug-naive and drug-free patients with schizophrenia // Int J Obes Relat Metab Disord. - 2002. - Vol. 26, №1. - P. 137-141.
7. 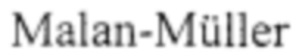 S., Kilian S., van den Heuvel L.L., Bardien S., Asmal L., Warnich L., Emsley R.A., Hemmings S.M., Seedat S. A systematic review of genetic variants associated with metabolic syndrome in patients with schizophrenia // Schizophr Res. - 2016. - Vol. 170, №1. - P. 1-17.
S., Kilian S., van den Heuvel L.L., Bardien S., Asmal L., Warnich L., Emsley R.A., Hemmings S.M., Seedat S. A systematic review of genetic variants associated with metabolic syndrome in patients with schizophrenia // Schizophr Res. - 2016. - Vol. 170, №1. - P. 1-17.
8. Huang P.L. eNOS, metabolic syndrome and cardiovascular disease // Trends Endocrinol Metab. - 2009. - Vol. 20, №6. - P. 295-302.
9. Baggio L.L., Drucker D.J. Biology of incretins: GLP-1 and GIP // Gastroenterology. - 2007. - Vol. 132, №6. - P. 2131-2157.
10. Levin P.A., Nguyen H., Wittbrodt E.T., Kim S.C. Glucagon-like peptide-1 receptor agonists: a systematic review of comparative effectiveness research // Diabetes Metab Syndr Obes. - 2017. - Vol. 10. - P. 123-139.
11. Гвозденко Т.А., Юбицкая H.C., Антонюк M.B., Веремчук Л.В. Патент РФ №2530770 Способ прогнозирования риска метаболического синдрома. Опубл. 10.10.2014. Бюл. №28.
12. Танченко О.А., Нарышкина С.В. Патент РФ №2633931 Способ прогнозирования метаболического синдрома у больных хронической обструктивной болезнью легких. Опубл. 19.10.2017. Бюл. №29.
13. Беляева О.Д., Березина А.В., Чубенко Е.А., Беркович О.А., Баранова Е.И. Патент РФ №2471193 Способ прогнозирования риска развития метаболитического синдрома у пациента с абдоминальным ожирением. Опубл. 27.12.2012. Бюл. №36.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАННЕЙ ГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ РИСКА РАЗВИТИЯ САХАРНОГО ДИАБЕТА 2 ТИПА | 2017 |
|
RU2655635C1 |
| Способ прогнозирования функционального исхода у больных шизофренией | 2021 |
|
RU2757728C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТЕПЕНИ РИСКА РАЗВИТИЯ ЭКСТРАПИРАМИДНЫХ ПОБОЧНЫХ ЭФФЕКТОВ НА ФОНЕ ТЕРАПИИ ГАЛОПЕРИДОЛОМ У ПАЦИЕНТОВ С РАССТРОЙСТВАМИ ШИЗОФРЕНИЧЕСКОГО СПЕКТРА | 2021 |
|
RU2771180C1 |
| Способ прогнозирования развития метаболического синдрома у больных шизофренией, получающих антипсихотическую терапию | 2018 |
|
RU2703424C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ ПАЦИЕНТОВ С АНТИПСИХОТИК-ИНДУЦИРОВАННЫМИ ЭКСТРАПИРАМИДНЫМИ РАССТРОЙСТВАМИ | 2022 |
|
RU2810798C1 |
| Способ прогнозирования развития висцерального ожирения у больных шизофренией, получающих терапию кветиапином | 2017 |
|
RU2659638C1 |
| Способ прогнозирования риска развития сахарного диабета 2 типа у жителей Центральной России на основе генотипирования полиморфизма rs755892 гена DNAJB1 | 2023 |
|
RU2803637C1 |
| Способ поддержки принятия врачебных решений выбора антипсихотической терапии у больных шизофренией с целью профилактики акатизии | 2021 |
|
RU2756614C1 |
| СПОСОБ ГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ ПОДВЕРЖЕННОСТИ К СЕРДЕЧНО-СОСУДИСТЫМ ЗАБОЛЕВАНИЯМ | 2007 |
|
RU2376372C2 |
| Способ прогнозирования риска развития гиперпролактинемии у женщин с шизофренией, принимающих антипсихотическую терапию | 2023 |
|
RU2810398C1 |





Изобретение относится к области биотехнологии. Изобретение представляет собой способ прогнозирования степени риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией. С помощью полимеразной цепной реакции в режиме реального времени проводят анализ полиморфизмов rs2070744 гена NOS3 и rs6923761 гена GLP-1R. Согласно изобретению среди пациентов с шизофренией носителям генотипов ТС или СС полиморфизма rs2070744 гена NOS3 и генотипа GG полиморфизма rs6923761 гена GLP-1R прогнозируют высокий риск развития метаболического синдрома, а носителям генотипа ТТ полиморфизма rs2070744 гена NOS3 и генотипов GA или GG полиморфизма rs6923761 гена GLP-1R прогнозируют низкий риск развития метаболического синдрома. Изобретение позволяет прогнозировать степень риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией на основе генетических маркеров. 2 пр.
Способ прогнозирования степени риска развития метаболического синдрома на фоне антипсихотической терапии у больных шизофренией, включающий выделение геномной ДНК из крови с последующим проведением полимеразной цепной реакции в режиме реального времени, отличающийся тем, что оценку степени риска развития метаболического синдрома проводят на основе выявления генотипов полиморфизмов rs2070744 гена NOS3 и rs6923761 гена GLP-1R, и при выявлении генотипов ТС или СС полиморфизма rs2070744 гена NOS3 и генотипа GG полиморфизма rs6923761 гена GLP-1R прогнозируют высокий риск развития метаболического синдрома, а при выявлении генотипа ТТ полиморфизма rs2070744 гена NOS3 и генотипа GA или GG полиморфизма rs6923761 гена GLP-1R прогнозируют низкий риск метаболического синдрома.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ МЕТАБОЛИТИЧЕСКОГО СИНДРОМА У ПАЦИЕНТА С АБДОМИНАЛЬНЫМ ОЖИРЕНИЕМ | 2010 |
|
RU2471193C2 |
| Способ прогнозирования метаболического синдрома у больных хронической обструктивной болезнью легких | 2016 |
|
RU2633931C1 |
| HUANG P., eNOS, metsbolic syndrome and cardiovascular disease, Trends Endocrinol Metab, fugust, 2009, 20 (6), p | |||
| УСТРОЙСТВО ПАРОПЕРЕГРЕВАТЕЛЯ | 1920 |
|
SU295A1 |
Авторы
Даты
2020-06-02—Публикация
2019-03-21—Подача