Область техники
Изобретение относится к способам идентификации химических соединений, в частности, наркотических, отравляющих веществ или лекарственных препаратов. Особенностью изобретения является принцип идентификации химического соединения при помощи увеличенного набора структурных дескрипторов, что позволяет проводить идентификацию на разных моделях хромато-масс-спектрометров, и использовать для идентификации существующие базы данных химических соединений.
Уровень техники
В настоящее время общепринятый подход для идентификации малых молекул (лекарств, метаболитов, наркотиков) основывается на применение газовой или жидкостной хроматографии в сочетании с масс-спектрометрией высокого разрешения (GC-MS/MS или LC-MS/MS) (Dettmer, K., Aronov, P. A. And Hammock, B. D. (2007), Mass spectrometry-based metabolomics. MassSpectrom. Rev., 26: 51-78). Вещество идентифицируется, если измеренные параметры такие как время выхода из хроматографической колонки, точная масса и спектр фрагментации совпадают с ранее измеренными значениями, хранящимися в базе данных (US20160231341A1). Например, решение по анализу токсинов, поставляемое компанией Брукер, требует от пользователя иметь систему идентичную той, для которой производителем создана база данных: аналитический хроматограф Elute и времяпролетный масс-спектрометр определенной марки. Соединение идентифицируется, если для него совпали время выхода, масса и три фрагментных иона из базы. Фрагментируются все ионы без изоляции. Недостатками данного подхода являются необходимость использования оборудования, идентичного тому, которое использовалось для наполнения базы данных, что приводит к несопоставляемости результатов, полученных на разных инструментах. Кроме того, небольшие, плохо контролируемые отклонения от стандартного подхода приводят к большому числу ложно-положительных или ложно-отрицательных идентификаций, что недопустимо в задачах нарко-контроля, судебно-медицинской экспертизы или допинг-контроля. Идентификация соединения также ограничена его присутствием в предоставляемой компанией-производителем базе данных, что существенно ограничивает возможность идентификации неизвестного вещества.
В настоящее время методика идентификации химических веществ в Российской Федерации регламентируется ГОСТ Р 8.795-2012. Согласно данному стандарту, А.9.5 Идентификацию проводят на основании следующих критериев идентификации: - время удерживания (определяемое на газохроматографических колонках различной полярности), с, мин;- индексы удерживания, ед.; усл. ед.; - сравнение масс-спектра при электронной ионизации с масс-спектром стандартного образца, полученным в аналогичных условиях, %;- наличие трех подтверждающих ионов при электронной ионизации в режиме селективного мониторинга ионов; - наличие молекулярных ионов при химической ионизации; - наличие, как минимум, двух m/z фрагментов в режиме мониторинга множественных реакций (ММР), так называемом режиме детектирования заданных масс, при использовании тандемной масс-спектрометрии.
Таким образом, получаемые данные зависят от конкретной модели хромато-масс-спектрометра, и возможность идентификации неизвестного соединения ограничена его присутствием в предоставляемой компанией-производителем базе данных. Существует потребность в способе идентификации вещества на основе расширенного набора структурных дескрипторов, что позволит снизить зависимость эффективности идентификации от конкретной модели хромато-масс-спектрометра, а также использовать для идентификации существующие публичные базы данных химических соединений.
Сущность изобретения
Задачей настоящего изобретения является повышение эффективности идентификации неизвестных химических соединений (наркотических, лекарственных препаратов, метаболитов, липидов, пептидов и др.) с использованием хроматографа, соединенного с масс-спектрометром. Авторами предложен подход к идентификации соединения, основанный на сравнении нескольких структурных дескрипторов, характерных для этого соединения и слабо зависящих от конкретной модели используемого хромато-масс-спектрометра, с аналогичными дескрипторами из одной из доступных баз данных. Указанные дескрипторы получают, проводя реакции дейтеро/водородного и 16О/18О изотопных обменов в регламентируемых условиях, позволяющих произвести обогащение изотопами у строго определенных групп анализируемого соединения. Далее производят идентификацию посредством сопоставления масс исходного соединения, соединения, модифицированного двумя разными изотопными обменами, а также масс фрагментов этих соединений при заданном режиме фрагментации в масс-спектрометре, с соответствующими значениями масс из базы данных химических соединений.
Указанная задача решается путем создания способа идентификации химического соединения с использованием жидкостного хроматографа, совмещенного с ним масс-спектрометра с источником электроспрей ионизации и соединяющего их переходного тройника, включающего следующие стадии: а) вводят растворенное в полярном растворителе химическое соединение в хроматограф, после чего после выхода с колонки хроматографа соединение поступает в совмещенный с хроматографом источник электроспрей ионизации, представляющий собой полую иглу; б) подают электрическое напряжение на иглу, распыляя раствор химического соединения в спрей заряженных капель для ионизации, при этом заряженные капли, образованные химическим соединением, попадают в один из выходов нагреваемого переходного тройника, образующего Т-образное соединение с вакуумной частью масс-спектрометра и с камерой, содержащей дейтерирующий агент, при этом соединение с камерой, содержащей дейтерирующий агент, обеспечивают при помощи клапана, регулирующего пропускание дейтерирующего агента; в) удерживая клапан, регулирующий пропускание дейтерирующего агента в пространство переходного тройника, в закрытом состоянии, определяют молекулярную массу химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре; г) повторяют стадии а) и б) по меньшей мере один раз при закрытом клапане, регулирующем пропускание дейтерирующего агента, используя определяемое химическое соединение, модифицированное путем изотопного обмена атомов кислорода, при этом модификацию химического соединения проводят до введения в хроматограф при помощи инкубации высушенного химического соединения в тяжелой воде H218О; д) определяют молекулярную массу химического соединения, модифицированного изотопом 18О атома кислорода, а также массу его фрагментов при заданном режиме фрагментации в масс- спектрометре; е) повторяют стадии а) и б) по меньшей мере один раз при открытом клапане, регулирующем пропускание дейтерирующего агента, и при этом нагревают пространство переходного тройника, создавая в нем атмосферу, насыщенную дейтерирующим агентом, при этом получают заряженные капли, образованные дейтерированным химическим соединением в пространстве переходного тройника; ж) определяют молекулярную массу дейтерированного химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре; е) идентифицируют химическое соединение, используя полученные значения массы химического соединения, массы его фрагментов при заданном режиме фрагментации, а также полученные значения массы и массы фрагментов при заданном режиме фрагментации для дейтерированного химического соединения, а также для химического соединения, модифицированного изотопом 18О атома кислорода, при помощи сравнения этих значений со соответствующими значениями из базы данных химических соединений.
В предпочтительных вариантах изобретения данный способ характеризуется тем, что в качестве дейтерирующего агента используют тяжелую воду 2H2О. В других вариантах изобретения данный способ характеризуется тем, что модификацию химического соединения путем изотопного обмена атомов кислорода проводят при помощи инкубации высушенного химического соединения в тяжелой воде H218О при температуре от 80 до 100°С. В других вариантах изобретения данный способ характеризуется тем, что полярным растворителем является вода, метанол, ацетонитрил или их смесь. Оптимальный тип растворителя для конкретных классов соединений может быть подобран методами, известными специалистам.
Указанная задача также решается путем создания системы, состоящей из жидкостного хроматографа, совмещенного с ним масс-спектрометра с источником электроспрей ионизации и соединяющего их нагреваемого переходного тройника для осуществления вышеуказанного способа, характеризующейся тем, что нагреваемый переходной тройник образует Т-образное соединение, один из выходов которого соединен с областью поступления полученного в результате электроспрей ионизации спрея заряженных капель анализируемого вещества, другой выход соединен с вакуумной частью масс-спектрометра, а третий - с камерой, содержащей дейтерирующий агент, при этом соединение с камерой, содержащей дейтерирующий агент, происходит при помощи клапана, регулирующего пропускание дейтерирующего агента, и при этом при открытии клапана в переходном тройнике образуется атмосфера, насыщенная дейтерирующим агентом.
Техническим результатом настоящего изобретения является повышение эффективности и достоверности идентификации неизвестных химических соединений при использовании разных моделей хромато-масс-спектрометров за счет использования для идентификации нескольких структурных дескрипторов, присущих соединению и не зависящих от модели используемого хромато-масс-спектрометра. Также, еще одним техническим результатом является повышение универсальности процедуры идентификации за счет возможности использования различных существующих баз данных химических соединений.
Краткое описание чертежей
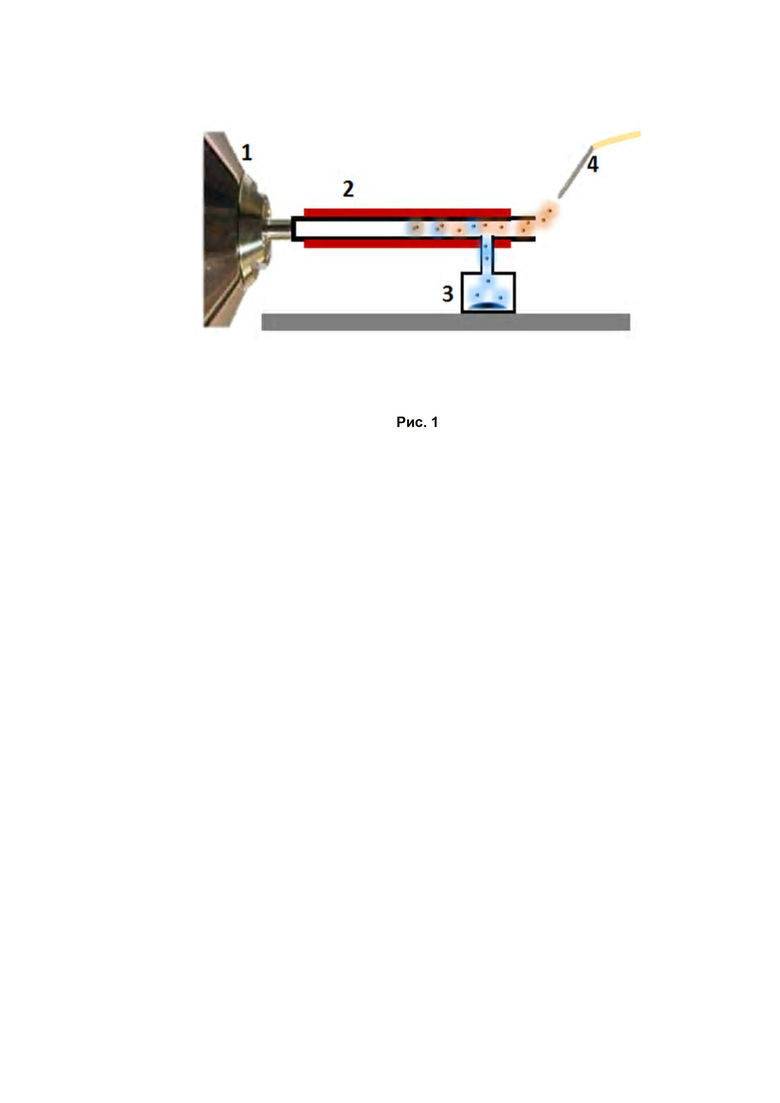
Фиг. 1. Схема модифицированного источника ионизации. 1 - масс-спектрометр, 2 - нагреваемый капилляр, с установленным тройником, 3 - контейнер с дейтерирующим агентом, 4 - источник ионизации.
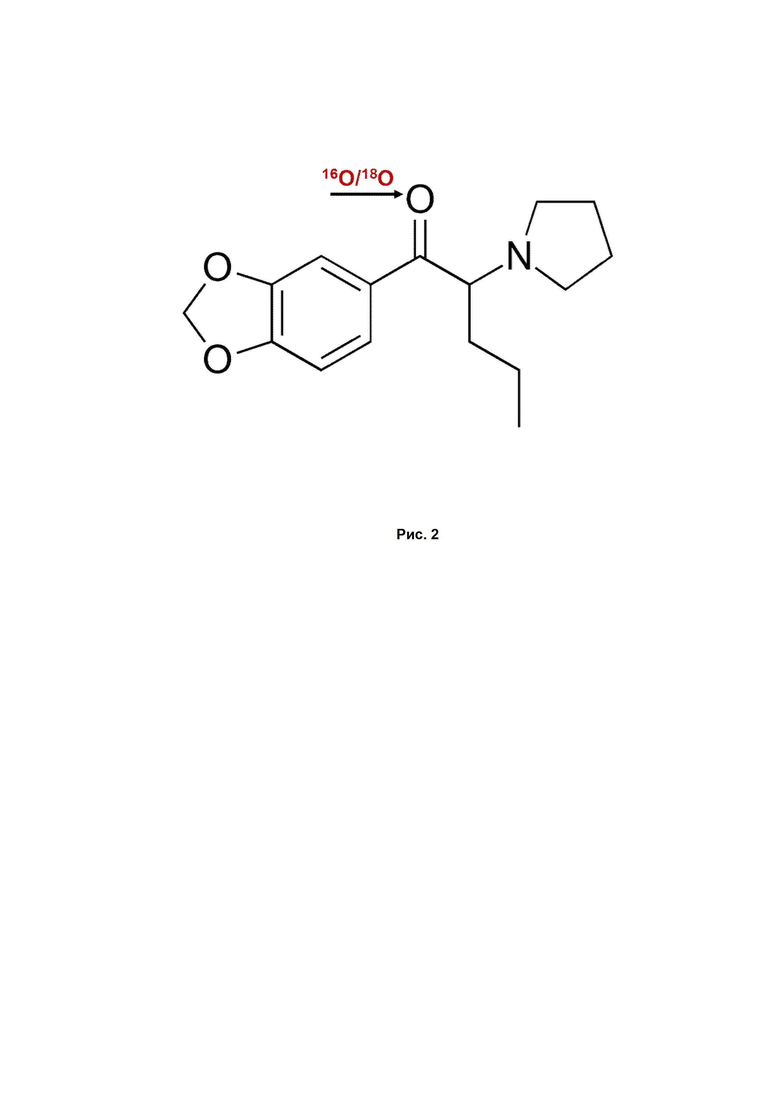
Фиг. 2. Структура наркотического вещества МДПВ. Из структуры можно предсказать один подвижный атом кислорода и отсутствие подвижных атомов водорода.
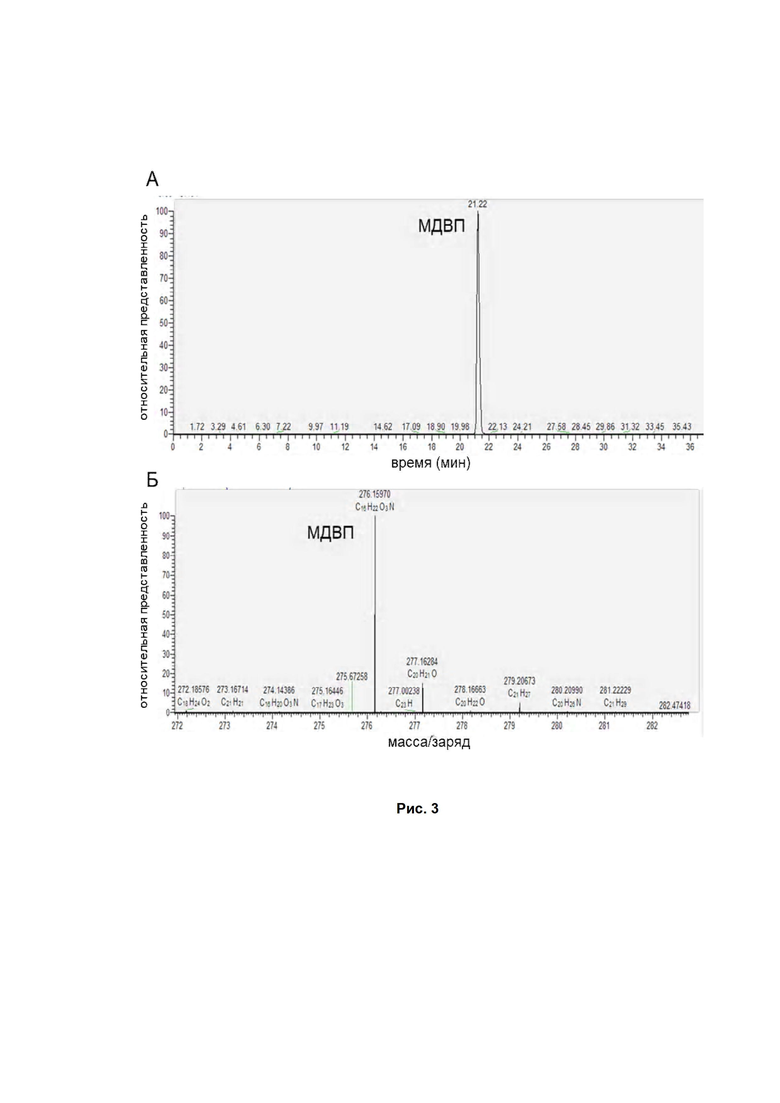
Фиг. 3. Определение характеристик МДПВ. (А) Хроматограмма для пика МДВП при разделении на колонке хроматографа. (Б) Масс спектр раствора МДВП (25 нг/мл).
Фиг. 4. Использование метода изотопного обмена для сокращения пространства поиска. А – Масс-спектр после реакции дейтеро-водородного обмена, Б - масс-спектр после реакции обмена 16О/18О, В - MS2 спектр вещества, хранящийся в базе MzCloud, Г - MS2 спектр после реакции обмена 16О/18О, Д - MS2 спектр после реакции дейтеро-водородного обмена.
Фиг. 5. Алгоритм сокращения пространства поиска при использовании информации о количестве изотопных обменов.
Подробное раскрытие изобретения
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из». Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Предлагаемая система по настоящему изобретению включает в себя хромато-масс-спектрометр, оснащенный модифицированным источником электроспрей ионизации, позволяющим проводить анализ масс соединения и его фрагментов как в стандартных условиях, так и в условиях эффективно происходящего дейтеро/водородного обмена. В уровне техники описано использование дейтеро/водородного обмена во время ионизации (RU2548387C1, JP2004028993A, Kostyukevich et.al., (2013) Anal Chem, 85(11):5330–5334; Kostyukevich et al., (2014) In-ESI source Hydrogen/Deuterium exchange of carbohydrates ions. AnalChem, 86(5):2595–2600), однако данные методы предлагают проведение обмена в условиях лимитированного времени или дейтерирующего агента, что негативно отражается на эффективности реакции.
В настоящем изобретении используют модификацию хромато-масс-спектрометра, адаптированную для проведения эффективного дейтеро/водородного обмена в процессе ионизации образца. Модификация состоит в использовании нагреваемого переходного тройника, соединяющего выход хроматографа и вход в масс-спектрометра, характеризующегося тем, что нагреваемый переходной тройник образует Т-образное соединение, один из выходов которого соединен с областью поступления полученного в результате электроспрей ионизации спрея заряженных капель анализируемого вещества, другой выход соединен с вакуумной частью масс-спектрометра, а третий - с камерой, содержащей дейтерирующий агент, при этом соединение с камерой, содержащей дейтерирующий агент, происходит при помощи клапана, регулирующего пропускание дейтерирующего агента, и при этом при открытии клапана в переходном тройнике образуется атмосфера, насыщенная дейтерирующим агентом. Данное устройство позволяет эффективно осуществлять реакцию дейтеро/водородного обмена в газовой фазе, а также управлять эффективностью данной реакции путем изменения температуры нагреваемого тройника и температуры камеры с дейтерирующим агентом. Кроме того, установленный клапан между камерой с дейтерирующим агентом и тройником позволяет запускать или прекращать реакцию обмена.
Кроме того, в данном изобретении используется методика обмена подвижных атомов кислорода в анализируемом соединении на изотоп кислорода 18О. Данный подход основывается на ранее описанном авторами способе (Kostyukevich Y, et.al., Anal Bioanal Chem. 2014 Oct;406(26):6655-64 и Kostyukevich Y, et.al., Anal Bioanal Chem (2019) 411: 3331), заключающимся в том, что предварительно высушенное соединение растворяется в тяжелой воде Н218О и запаивается в стеклянной ампуле и нагревается в термостате в течении 24 часов при температуре 95°С. При таких условиях подвижные атомы кислорода из групп =О, -СООН заменяются на изотоп, при этом молекулы исходных соединений не разрушаются.
Авторами были определены режимы реализации обмена подвижных атомов кислорода. Например, при работе с водорастворимыми соединениями, такими как многие лекарственные препараты, растительные и почвенные экстракты для обмена атомов кислорода из групп =О, -СООН реакция проводится в течении 24 часов при температуре от 80 до 100°С. Для обмена кислорода из спиртовых групп (-ОН) реакция проводится в течении 20 дней при температуре от 80 до 100°С.
При работе с водонерастворимыми соединениями, такими как нафтеновые кислоты, может применяться метод обмена в сверхкритической или околокритической воде. Для этого к соединению добавляется тяжелая вода и данная система (в общем случае несмешивающаяся) помещается в герметично закрытый автоклав и нагревается в течении часа при температуре 300-450°С. При таких температурах и давлениях вода переходит в сверхкритическое состояние и растворяет многие (в том числе неполярные) соединения. При этих условиях также происходит обмен в =О и –СООН группах.
Эффективность реакции обмена возрастает при увеличении времени и температуры реакции, однако, также увеличивается скорость реакции гидролиза, которая разрушает исходное соединение. Таким образом, конкретные параметры реакции подбираются индивидуально для соединений различных классов.
Для проведения реакции дейтеро/водородного обмена в газовой фазе могут использоваться следующие соединения: D2O, дейтерированные по гидроксильной группе спирты (MeOD, EtOD), дейтерированный аммиак. Объем дейтерирующего агента в контейнере влияет только на продолжительность устойчивой работы изобретения и не влияет на глубину реакции обмена.
Схема модифицированного источника ионизации показана на Фиг. 1. Геометрические размеры нагреваемого капилляра могут варьироваться в широких пределах: длина от 5 см до 50 см, и внутренний диаметр от 0.3 мм до 3 мм. Нагреваемый капилляр изготавливается из нержавеющей стали или других устойчивых к окислению сплавов.
Увеличение длины и внутреннего диаметра капилляра увеличивает глубину реакции обмена, однако уменьшает чувствительность из-за гибели ионов на стенках. Для эффективного прохождения реакции необходимо использовать повышенную температуру от 200 до 400°С. Более высокие значения температуры приводят к термической фрагментации ионов. В качестве клапана в настоящем изобретении используется шаровой кран с регулирующим элементом сферической формы.
В настоящем изобретении для идентификации соединения используется время выхода из хроматографической колонки, точная масса, массы фрагментов, полученных с использованием фрагментации под действием столкновений, количество подвижных атомов водорода, количество подвижных атомов кислорода, определяемых путем сравнения спектров исходного и меченного соединений, а также распределение изотопов в спектре фрагментации. Использование изотопного обмена является существенной особенностью данного изобретения.
Измеренные параметры используются для идентификации соединения с использованием доступных баз данных MzCloud, Metlin, PubChem. Изобретение включает в себя специализированное программное обеспечение, обеспечивающее фильтрацию соединений по количеству обменных атомов.
Настоящий способ включает следующие стадии:
1) Проведение классического хромато-масс-спектрометрического эксперимента с фрагментацией. Измерение для соединений времени выхода из хроматографической колонки, точной массы и спектра фрагментных ионов.
2) Проведение реакции дейтеро/водородного обмена в источнике ионизации, измерение точной массы соединения после внедрения изотопной метки, измерение спектра фрагментации после внедрения изотопной метки.
3) Проведение реакции обмена кислорода, измерение точной массы соединения после внедрения изотопной метки, измерение спектра фрагментации после внедрения изотопной метки.
4) Использование точной массы и спектра фрагментации исходного соединения для предварительной идентификации в публичных базах данных MzCloud, Metlin, HMDB. Определение списка соединений, потенциально соответствующих исходному.
5) В случае множества кандидатов использовать информацию о количестве подвижных атомов водорода и кислорода и отфильтровать из определенного списка те соединения, которые удовлетворяют измеренным в эксперименте параметрам.
6) В случае, если фильтрация по изотопным меткам по-прежнему оставляет множество кандидатов, использовать информацию о распределении изотопных меток по фрагментным ионам. Отфильтровать те соединения, для которых положение изотопных меток в фрагментных ионах удовлетворяет измеренным в эксперименте параметрам.
7) В случае если, ни одно из соединений из данных баз данных не подходит под измеренные экспериментальные параметры, провести поиск в базе данных PubChem и отфильтровать те соединения, для которых точная масса и количество подвижных атомов кислорода и водорода удовлетворяет измеренным в эксперименте параметрам.
Пример фильтрации по подвижным атомам для наркотика МДПВ:
Выгрузим из базы данных PubChem все соединения с брутто-формулой C10H21O3N. Таких соединений 20022.
Отфильтруем все соединения, у которых нет подвижных протонов, т.е. групп –OH, -NH, -COOH и т.д. Таких уже 6179.
Отфильтруем все соединения, у которых есть только 1 группа =O (один кислородный обмен). Таких 2016.
Таким образом, пространство поиска даже при использовании самой наполненной базы данных PubChem (около 100 миллионов соединений) сократилось в 10 раз.
Нижеследующие примеры осуществления способа приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1.
Пример использования данных по количеству изотопных обменов (количеству определенных функциональных групп) приведен в Таблице 1.
Был проведен анализ количества химических соединений, имеющих одинаковый элементный состав и одинаковое количество функциональных групп. Элементный состав может быть определен, измеряя точную массу, используя масс-спектрометр высокого разрешения. Количество различных функциональных групп может быть определено, используя заявляемый в изобретении метод.
Можно видеть, что применение заявляемого метода позволяет более чем в 10 раз сократить химическое пространство для поиска и идентификации соединений.
Таблица 1. Уменьшение числа потенциальных соединений, имеющих одинаковый элементный состав, при добавлении в анализ структурных дескрипторов. Столбцы: название соединения; химическая формула; количество соединений, присутствующих в базе данных PubChem/HMDB и имеющих ту же молекулярную формулу (PC1/H1); количество соединений, присутствующих в базе данных PubChem/HMDB и имеющих ту же молекулярную формулу и то же количество подвижных атомов водорода (PC2/H2); количество соединений, присутствующих в базе данных PubChem/HMDB и имеющих ту же молекулярную формулу, то же количество подвижных атомов водорода и то же количество подвижных атомов кислорода (PC3/H3); наличие или отсутствие соединения в базе HMBD; наличие спектра MS2 в базе HMDB.
Пример 2.
Использование заявляемого метода для анализа реального наркотического вещества МДВП приведено на Фиг. 2-4.
Для осуществления заявляемого метода был использован хромато-масс- спектрометр в составе хроматографа Dionex 3000 Ultimate, использовалась хроматографическая колонка Acclaim PepMap 100 C18, 50см*75млм*3мкм. Подвижная фаза A: вода, 0.05% раствор трифторуксусной кислоты (ТФУ), подвижная фаза B: 20% вода, 80% ацетонитрил, 0.04% ТФУ; растворитель для загрузки на колонку: 98% вода, 2% ацетонитрил, 0.05% ТФУ. Хроматограф был совмещен с ионным источником нано-электроспрей. Напряжение на игле электроспрея составляло 2.5 кВ. Регистрировались положительно заряженные ионы. Для детектирования ионов использовался масс-спектрометр Orbitrap Q Exactive (Бремен, Германия). Разрешающая способность прибора была установлена на значение 140 000. Фрагментация ионов осуществлялась с использованием метода диссоциации, индуцированной столкновением HCD (Higher-energy collisional dissociation). Энергия фрагментации была установлена на значении 30 ед.
Отметим, что описанная конфигурация не ограничивает сферу применения заявляемого изобретения. Изобретение может использоваться в сочетании с другими моделями хроматографов, а также с методом прямого ввода. Кроме ионизации методом электроспрей, ионы могут быть получены методами химической ионизации, методом фотоионизации, а также ионизацией, вызванной взаимодействием с бета-частицами (электронами). В качестве масс-спектрометра может использоваться любой масс- спектрометр, оснащенный источником ионизации при атмосферном давлении и специальным капилляром для транспорта ионов из области атмосферного давления в область низкого вакуума. В качестве метода фрагментации могут быть использованы методы фрагментации, индуцированной столкновениями (при высоких и низких энергиях), методы фрагментации, индуцированной поглощением фотона (или нескольких фотонов), а также фрагментация, вызванная захватом электрона.
Структура наркотического вещества приведена на Фиг. 2; из структуры можно предвидеть отсутствие в нейтральной молекуле подвижных атомов водорода и наличие одного подвижного атома кислорода. Далее были определены характеристики МДПВ – время задержки на колонке (retention time) (Фиг. 3А) и масса вещества с помощью жидкостной хромато-масс-спектрометрии (масс спектр раствора МДВП (25 нг/мл) изображен на Фиг. 3Б). После проведения реакции изотопного обмена в протонированном ионе наблюдался один обмен водорода на дейтерий (Фиг. 4А) и один обмен 16О на 18О (Фиг. 4Б). Для идентификации соединения необходимо провести процедуру сравнения измеренного спектра фрагментации (MS2 спектра) со спектром фрагментации данного соединения, хранящимся в верифицированных базах данных (MzCloud, Metlin и др.). Спектр фрагментации соединения МДВП, хранящийся в базе MzCloud приведен на Фиг. 4В. Экспериментально измеренные спектры фрагментации для соединения МДВП после прохождения реакции обмена представлены на Фиг. 4Г и Фиг. 4Д. Видно, что данные спектры совпадают с спектром, хранящимся в базе MzCloud; кроме того, можно видеть, что некоторые фрагментные ионы несут в себе изотопную метку, что также может использоваться для повышения достоверности идентификации.
На Фиг. 5 представлен алгоритм сокращения пространства поиска, используя информацию о количестве обменов. Можно видеть, что применение заявляемого в изобретении подхода позволяет существенно сократить пространство поиска.
Данное сокращение будет особенно полезно при работе с идентификацией соединений в низких концентрациях в составе сложных биологических матриц, таких как физиологические жидкости, экстракты растений и т.д. Именно в этом случает возникают такие эффекты, как присутствие внутри хроматографического пика нескольких различных соединений, присутствие в смеси химически близких соединений, дающих близкие спектры фрагментации, а также другие эффекты, затрудняющие однозначную идентификацию. В заявляемом изобретении разработан набор дескрипторов, определяемых с использованием масс-спектрометра и реакции изотопного обмена, применение которых позволит значительно повысить достоверность идентификации.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные случаи приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть, понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИДЕНТИФИКАЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДОМ ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ | 2015 |
|
RU2599900C2 |
| СПОСОБ ПРОВЕДЕНИЯ ДЕЙТЕРО-ВОДОРОДНОГО ОБМЕНА В ИОННОМ ИСТОЧНИКЕ МАСС-СПЕКТРОМЕТРА | 2013 |
|
RU2548387C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ФОСФОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДОМ ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ С ЦИЛИНДРИЧЕСКОЙ ИОННОЙ ЛОВУШКОЙ | 2020 |
|
RU2741955C1 |
| Способ контроля содержания противотуберкулёзных препаратов основного ряда и их токсичных метаболитов в плазме крови | 2018 |
|
RU2702998C1 |
| Способ количественного мультиплексного анализа альфа-2-макроглобулина, фетуина А и сывороточного амилоида А1 как факторов воспаления в сыворотке крови с использованием MALDI-TOF масс-спектрометрии | 2022 |
|
RU2789503C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ СПИРТА ЭТИЛОВОГО И ЭТАНОЛСОДЕРЖАЩИХ ЖИДКОСТЕЙ | 2007 |
|
RU2348032C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ НА ОСНОВЕ МЕТОДА ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ И МАСС-СПЕКТРОМЕТРИИ | 2011 |
|
RU2469314C2 |
| ПРОТЕОТИПИЧЕСКИЙ ПЕПТИД Q9Y4W6-02 И СПОСОБ МАСС-СПЕКТРОМЕТРИЧЕСКОГО АНАЛИЗА СОДЕРЖАНИЯ AFG3-ПОДОБНОГО БЕЛКА ЧЕЛОВЕКА НА ЕГО ОСНОВЕ | 2012 |
|
RU2673551C2 |
| СПОСОБ МАСС-СПЕКТРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ КОМПОНЕНТНОГО СОСТАВА ГАЗОВОЙ СМЕСИ | 2020 |
|
RU2754084C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ВЫСОКОТОКСИЧНЫХ СОЕДИНЕНИЙ РЯДА O-АЛКИЛАЛКИЛФТОРФОСФОНАТОВ И ПРОГНОЗИРОВАНИЯ МАСС-СПЕКТРОВ ХИМИКАТОВ ЭТОГО РЯДА | 2008 |
|
RU2391657C2 |


Группа изобретений относится к идентификации химических соединений с применением хромато-масс-спектрометра. Раскрыт способ идентификации химического соединения, включающий следующие стадии: вводят растворенное в полярном растворителе химическое соединение в хроматограф, после чего после выхода с колонки хроматографа соединение поступает в совмещенный с хроматографом источник электроспрей ионизации; подают электрическое напряжение на иглу, распыляя раствор химического соединения в спрей заряженных капель для ионизации, при этом заряженные капли, образованные химическим соединением, попадают в один из выходов нагреваемого переходного тройника, образующего Т-образное соединение с вакуумной частью масс-спектрометра и с камерой, содержащей дейтерирующий агент; определяют молекулярную массу химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре; повторяют указанные стадии, используя определяемое химическое соединение, модифицированное путем изотопного обмена атомов кислорода; определяют молекулярную массу химического соединения, модифицированного изотопом 18О атома кислорода, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре; повторяют указанные стадии и при этом нагревают пространство переходного тройника до температуры 200-400°С, создавая в нем атмосферу, насыщенную дейтерирующим агентом, определяют молекулярную массу дейтерированного химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре; идентифицируют химическое соединение, используя полученные значения масс при помощи сравнения этих значений со соответствующими значениями из базы данных химических соединений. Также раскрыта система для осуществления указанного способа. Группа изобретений позволяет повысить достоверность, эффективность и универсальность идентификации неизвестных химических соединений. 2 н. и 3 з.п. ф-лы, 5 ил., 1 табл., 2 пр.
1. Способ идентификации химического соединения с использованием жидкостного хроматографа, совмещенного с ним масс-спектрометра с источником электроспрей ионизации и нагреваемого переходного тройника, включающий следующие стадии:
а) вводят растворенное в полярном растворителе химическое соединение в хроматограф, после чего после выхода с колонки хроматографа соединение поступает в совмещенный с хроматографом источник электроспрей ионизации, представляющий собой полую иглу;
б) подают электрическое напряжение на иглу, распыляя раствор химического соединения в спрей заряженных капель для ионизации, при этом заряженные капли, образованные химическим соединением, попадают в один из выходов нагреваемого переходного тройника, образующего Т-образное соединение с вакуумной частью масс-спектрометра и с камерой, содержащей дейтерирующий агент, при этом длина ответвления переходного тройника, присоединяющего вакуумную часть масс-спектрометра, составляет от 5 до 50 см, и соединение с камерой, содержащей дейтерирующий агент, обеспечивают при помощи клапана, регулирующего пропускание дейтерирующего агента;
в) удерживая клапан, регулирующий пропускание дейтерирующего агента в пространство переходного тройника, в закрытом состоянии, определяют молекулярную массу химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре;
г) повторяют стадии а) и б) по меньшей мере один раз при закрытом клапане, регулирующем пропускание дейтерирующего агента, используя определяемое химическое соединение, модифицированное путем изотопного обмена атомов кислорода, при этом модификацию химического соединения проводят до введения в хроматограф при помощи инкубации высушенного химического соединения в тяжелой воде H218О;
д) определяют молекулярную массу химического соединения, модифицированного изотопом 18О атома кислорода, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре;
е) повторяют стадии а) и б) по меньшей мере один раз при открытом клапане, регулирующем пропускание дейтерирующего агента, и при этом нагревают пространство переходного тройника до температуры 200-400°С, создавая в нем атмосферу, насыщенную дейтерирующим агентом, при этом получают заряженные капли, образованные дейтерированным химическим соединением в пространстве переходного тройника;
ж) определяют молекулярную массу дейтерированного химического соединения, а также массу его фрагментов при заданном режиме фрагментации в масс-спектрометре;
е) идентифицируют химическое соединение, используя полученные значения массы химического соединения, массы его фрагментов при заданном режиме фрагментации, а также полученные значения массы и массы фрагментов при заданном режиме фрагментации для дейтерированного химического соединения, а также для химического соединения, модифицированного изотопом 18О атома кислорода, при помощи сравнения этих значений с соответствующими значениями из базы данных химических соединений.
2. Способ по п. 1, характеризующийся тем, что в качестве дейтерирующего агента используют тяжелую воду 2H2О.
3. Способ по п. 1, характеризующийся тем, что модификацию химического соединения путем изотопного обмена атомов кислорода проводят при помощи инкубации высушенного химического соединения в тяжелой воде H218О при температуре от 80 до 100°С.
4. Способ по п. 1, характеризующийся тем, что полярным растворителем является вода, метанол, ацетонитрил или их смесь.
5. Система, состоящая из жидкостного хроматографа, совмещенного с ним масс-спектрометра с источником электроспрей ионизации и соединяющего их нагреваемого переходного тройника для осуществления способа по п. 1, характеризующаяся тем, что нагреваемый переходной тройник образует Т-образное соединение, один из выходов которого соединен с областью поступления полученного в результате электроспрей ионизации спрея заряженных капель анализируемого вещества, другой выход соединен с вакуумной частью масс-спектрометра, причем длина данного ответвления составляет от 5 до 50 см, а третий - с камерой, содержащей дейтерирующий агент, при этом соединение с камерой, содержащей дейтерирующий агент, происходит при помощи клапана, регулирующего пропускание дейтерирующего агента, и при этом при открытии клапана в переходном тройнике образуется атмосфера, насыщенная дейтерирующим агентом, нагретая до температуры 200-400°С.
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| KOSTYUKEVICH Y | |||
| et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Bional | |||
| Chem., 2014, V.406, pp.6655-6664 | |||
| HEMLING M.E | |||
| et al | |||
| Gas Phase | |||
Авторы
Даты
2020-06-02—Публикация
2019-06-11—Подача