Изобретение относится к исследованию или анализу материалов путем определения их химических или физических свойств, конкретно путем разделения на составные части (компоненты) с использованием адсорбции и их масс-спектрометрического исследования.
Изобретение может быть использовано для идентификации органических соединений с применением метода высокоэффективной жидкостной хроматографии и масс-спектрометрического детектирования.
Современная масс-спектрометрия представляет собой эффективный метод исследования состава, строения, термодинамических и кинетических свойств веществ, находящихся в любом агрегатном состоянии. Высокая чувствительность, большой объем получаемой информации, почти универсальная применимость обусловили чрезвычайно бурный рост широты и разнообразия приложений масс-спектрометрических методов.
Хромато-масс-спектрометрические методы широко используются для качественного и количественного анализа смесей различных органических соединений. В основе хромато-масс-спектрометрии лежат колоночная газовая (ГХ-МС) или жидкостная хроматография (ВЭЖХ-МС) и масс-спектрометрия. С помощью хроматографических методов осуществляется разделение смеси на отдельные компоненты, а с помощью масс-спектрального метода - количественный анализ, идентификация и установление строения веществ.
Несмотря на общность методов, лежащих в основе хромато-масс-спектрометрии, и решаемых при анализе задач существуют принципиальные различия в ГХ-МС и ВЭЖХ-МС.
В методе ГХ-МС поток, вытекающий из капиллярной колонки газожидкостного хроматографа (элюата), состоит из газа-носителя (обычно гелия) и паров разделяемых веществ. Элюат можно непосредственно вводить в ионный источник масс-спектрометра, поскольку скорость потока газа в капиллярных колонках невелика (1…2 см3/мин) и вакуумный насос успевает откачать поступающий газ, не допуская создания повышенного давления в источнике. Если учесть высокую разрешающую способность капиллярной колоночной хроматографии, то станет понятно, почему именно она в сочетании с масс-спектрометрией вот уже в течение полувека является одним из наиболее эффективных методов исследования малых количеств смесей органических соединений.
Элюат, выходящий из колонки высокоэффективного жидкостного хроматографа, представляет собой раствор разделяемых веществ в элюенте. Такой раствор невозможно ввести в ионный источник без резкого повышения давления. Проблема сочетания жидкостного хроматографа с масс-спектрометром долгое время препятствовала широкому применению ВЭЖХ-МС. Решением этой проблемы, в частности, было использование другого метода ионизации по сравнению с тем методом ионизации, который традиционно используют в методе ГХ-МС.
Речь идет о наиболее распространенном в ГХ-МС методе ионизации электронным ударом (ЭУ), заключающемся в воздействии на анализируемое вещество пучка электронов (обычно при давлении 1·10-6 мм рт.ст.). Источником электронов является нагретая катодная нить, ускоряются электроны электрическим полем при разности потенциалов от 0 до 100 В.
Альтернативным методом является метод "мягкой" ионизации (химическая ионизация при атмосферном давлении и электростатическое распыление при атмосферном давлении). При "мягкой" ионизации масс-спектры содержат меньшее количество осколочных ионов, чем при ионизации электронным ударом. В результате "мягкая" ионизация позволяет обнаруживать молекулярные ионы (или протонированные молекулярные ионы), отсутствующие в масс-спектрах с ионизацией электронным ударом (Д.Броун, А.Флойд, М.Сейнзбери. Спектроскопия органических веществ. Перевод с английского А.А.Кирюшкина [Текст] / М.: Мир, 1992 - 300 с.).
В масс-спектрометрии жесткой ионизации (электронным ударом) за более чем полувековую историю метода накоплен обширный справочный материал по масс-спектрам органических соединений, позволяющий по набору пиков и соотношению их интенсивностей осуществлять надежную идентификацию практически любого неизвестного соединения.
Этому в немалой степени способствовало развивавшееся в течение последних 20…25 лет все более активное применение вычислительной техники для целей регистрации и обработки масс-спектрометрических данных. Благодаря универсальности и воспроизводимости именно спектры электронной ионизации стали основой компьютерных библиотек масс-спектров. Наиболее эффективной в настоящее время является масс-спектральная библиотека NIST/EPA/NIH Mass Spectral Library, очередная версия которой NIST08 выпущена в 2008 г. В нее включено 220460 спектров для 192108 соединений. Кроме того, она содержит 224038 литературных и оценочных величин газохроматографических индексов удерживания для 21847 соединений библиотеки электронной ионизации, а также 5308 спектров МС/МС для 5308 прекурсор-ионов (Лебедев А.Т., Лебедев К.С., Мясоедов Б.Ф., Рыбальченко И.В., Сигейкин Г.И., Суворкин В.Н. Масс-спектрометрическая идентификация высокотоксичных алкилфторфосфонатов. Масс-спектрометрия. Т. 3, №4 (2006). Интернет-ресурс: www.sisweb.com/nist.).
Известны различные вариации способа идентификации на основе ГХ-МС, например способ, предусматривающий проведение хроматографического и масс-спектрометрического анализа и генерацию хотя бы одного профиля элюции в трехмерном измерении, координатами которого являются время удерживания соединения (хроматографический параметр), отношение m/z (масс-спектрометрический параметр) и интенсивность сигнала. Способ предусматривает также автоматическое присвоение профилей элюции (Способ и система для проведения хроматографического и масс-спектрометрического анализа. G01N 30/86. Патент № WO 2005015199 А1, приоритет от 06.07.2004 г. Изобретения стран мира (Реферативный журнал) 2006, №6).
Способ идентификации органических соединений на основе ГХ-МС электронной ионизации является ближайшим из аналогов предлагаемого изобретения.
Несмотря на несомненные достоинства способа идентификации органических соединений методом газовой хроматографии в сочетании с масс-спектрометрическим детектированием с ионизацией электронным ударом решение ряда аналитических задач требует применения метода высокоэффективной жидкостной хроматографии.
Возможность анализа высокомолекулярных органических соединений, отсутствие температурного воздействия на анализируемую пробу, масс-спектрометрическое детектирование с "мягкой" ионизацией, например электростатическим распылением при атмосферном давлении, создают условия преимущественного использования этого способа как для количественного, так и для качественного анализа. При этом в методе ВЭЖХ-МС для идентификации используют лишь два параметра: время удерживания и массу псевдомолекулярного иона.
Обнаружение молекулярных ионов (или протонированных псевдомолекулярных ионов) при "мягкой" ионизации, отсутствующих в масс-спектрах с ионизацией электронным ударом, с одной стороны, облегчает идентификацию соединения особенно в том случае, когда известна предполагаемая химическая формула вещества. С другой стороны, при отсутствии каких-либо данных о неизвестном соединении этих двух параметров оказывается недостаточно для надежной и достоверной идентификации.
Задача настоящего изобретения заключается в совершенствовании способа идентификации органических соединений на основе метода высокоэффективной жидкостной хроматографии и масс-спектрометрии.
Решение поставленной задачи предполагает технический результат, заключающийся в повышении достоверности и объективности идентификации, расширении функциональных возможностей масс-спектрометрического метода. На базе полученных результатов в перспективе представляется возможной реализация программного продукта для идентификации органических соединений.
Поставленная задача решается тем, что в способе идентификации органических соединений на основе метода высокоэффективной жидкостной хроматографии и масс-спектрометрии согласно предлагаемому решению после хроматографического разделения веществ и ионизации способом электростатического распыления при атмосферном давлении производят детектирование разделенных компонентов в режиме регистрации положительных и отрицательных ионов и выбирают режим детектирования по максимальной информативности; измеряют спектр масс первой полярности и определяют вероятную молярную массу посредством распознавания аддуктов с учетом возможного изотопного состава атомов, входящих в молекулу; измеряют масс-спектры дочерних ионов; на основании масс-спектра первой полярности и дочерних спектров рассчитывают идентификационные коэффициенты; сравнивают хроматографические параметры и результаты масс-спектрометрических измерений с данными библиотеки спектров масс известных веществ.
Объектами настоящего исследования являются пестициды, принадлежащие к различным классам органических веществ. В таблице 1 приведены объекты исследований и их характеристики.
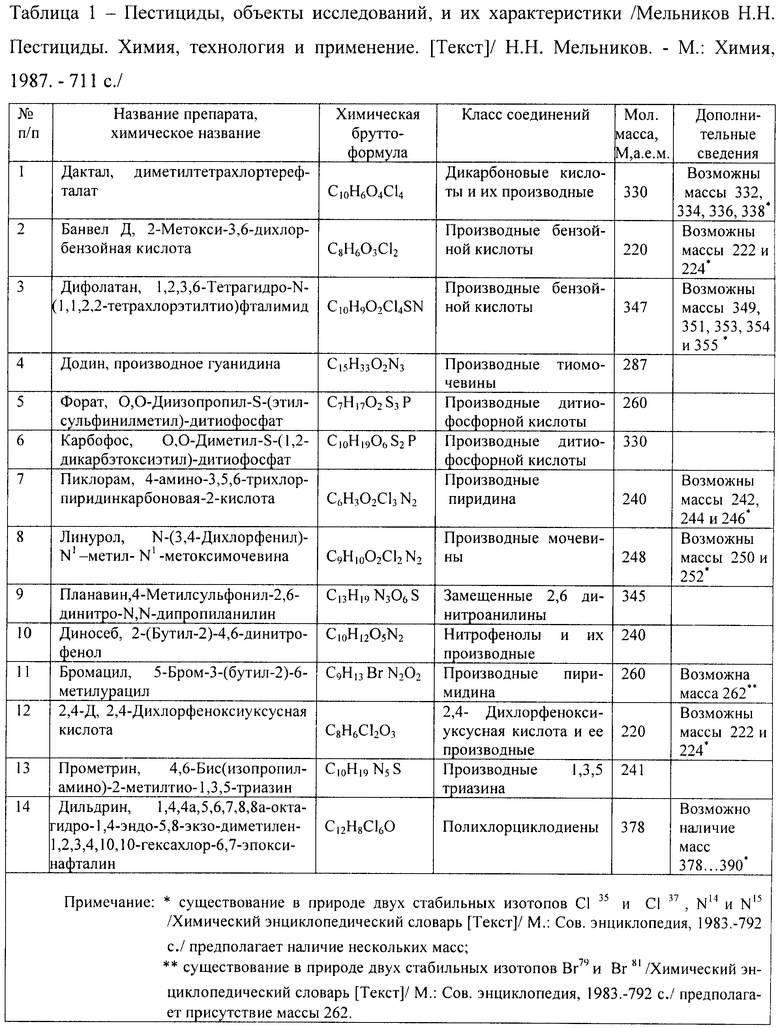
Учитывая тот факт, что большинство исследуемых соединений является полярными веществами с несколькими возможными ионизируемыми химическими центрами, можно предположить возможность их детектирования в условиях "мягкой" ионизации за счет электростатического распыления и при этом ожидать более простую по количеству образующихся ионов-осколков картину по сравнению с условиями жесткой ионизации электронным ударом.
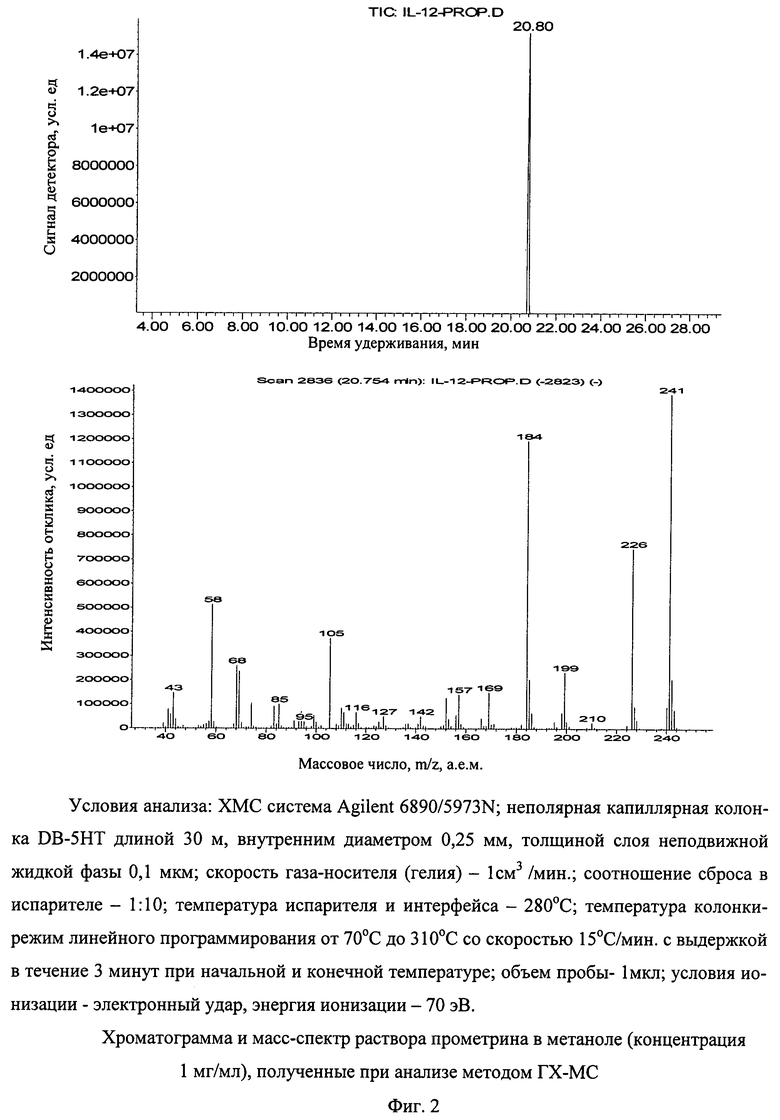
На первом этапе работы по идентификации органических соединений методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием был проведен сравнительный анализ раствора одного из исследуемых соединений в метаноле (раствор прометрина в концентрации 1 мг/мл) методами ВЭЖХ-МС и ГХ-МС. На фигурах 1, 2 приведены хроматограммы и масс-спектры прометрина, полученные методами ВЭЖХ-МС и ГХ-МС.
Анализ приведенных спектральных данных позволяет сделать следующие выводы:
спектрограмма прометрина, полученная методом ВЭЖХ-МС, содержит всего три характеристических пика, в то время как спектрограмма, полученная методом ГХ-МС, содержит целый спектр пиков разной интенсивности;
идентификация исследуемого соединения при использовании метода ВЭЖХ-МС облегчается тем, что из трех ионов наиболее интенсивным ионом первой полярности является псевдомолекулярный ион [М+Н]+ с массой, на единицу большей молекулярной массы соединения;
с другой стороны, в масс-спектрометрии жесткой ионизации (электронным ударом) использование известного программного аппарата позволяет по набору пиков и соотношению их интенсивностей надежно идентифицировать неизвестное соединение (в данном случае применение библиотеки масс-спектров NIST08 с высокой степенью вероятности подтвердило структуру прометрина).
На следующем этапе работы все объекты исследований, представленные в таблице 1, были подвергнуты анализу методом ВЭЖХ с масс-селективным детектированием в режиме регистрации положительных или отрицательных ионов. Было обнаружено, что соединения, детектируемые в режиме регистрации положительных ионов, не детектируются в режиме регистрации отрицательных ионов. Некоторые соединения не детектируются ни в том, ни в другом режиме; вероятно, для их детектирования необходимо использовать режим химической ионизации.
Для повышения надежности идентификации органических соединений при использовании "мягкой" ионизации (метод ВЭЖХ-МС) были проведены исследования по изучению соотношений образующихся псевдомолекулярных ионов.
Анализ исследованных органических соединений методом ВЭЖХ с масс-селективным детектированием по положительным ионам позволил выделить в масс-спектре кроме основного псевдомолекулярного иона с массой [М+Н]+ при том же времени удерживания дочерние псевдомолекулярные ионы с массой [М+2]+ и [М+3]+, соответствующие молекулярным массам соединения [М+1] и [М+2]. Их появление обусловлено изотопным составом атомов углерода и водорода, в первую очередь, входящих в молекулу соединения.
При работе с отрицательными ионами основным детектируемым ионом является ион [М-Н]-. Возможно образование дочернего отрицательного иона [М+е]-. Причем в соответствии с таблицей 1 возможно существование псевдомолекулярных ионов с несколькими массами, обусловленное наличием в природе нескольких изотопов атомов, входящих в состав молекулы органического соединения.
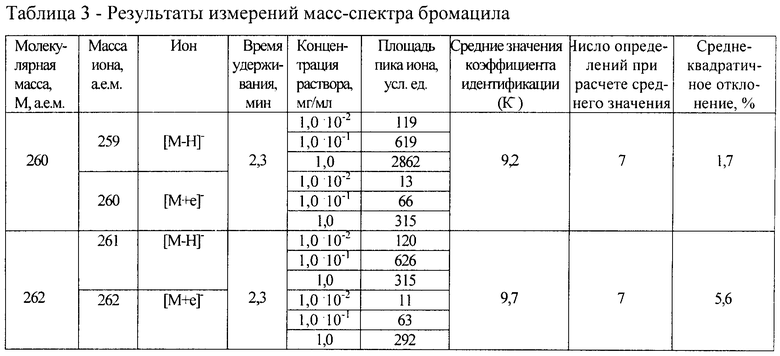
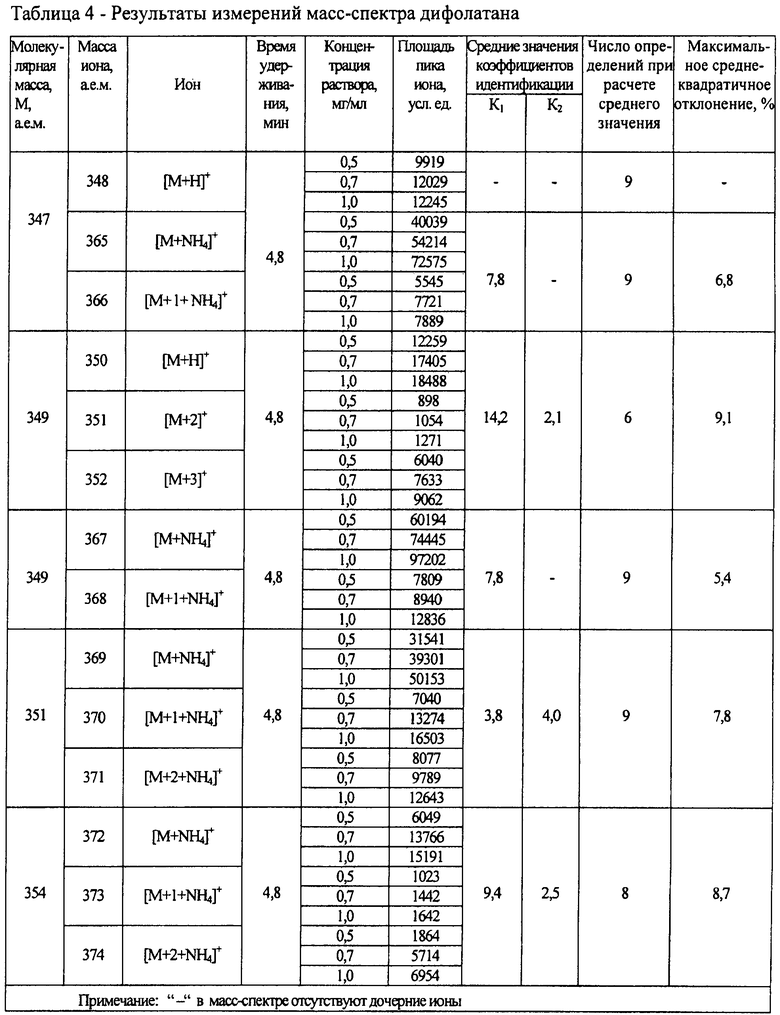
В таблицах 2-4 приведены результаты измерений масс-спектров метанольных растворов с концентрацией в диапазоне от 1,0·10-2 до 1,0 мг/мл прометрина и дифолатана (детектирование в режиме регистрации положительных ионов) и бромацила, детектируемого по отрицательным ионам.
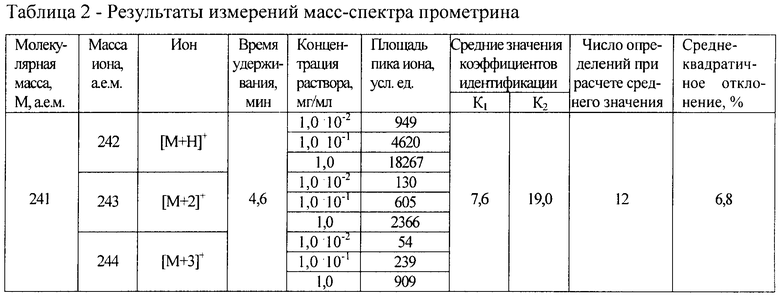
Анализ данных таблиц 2 и 4 при детектировании в режиме регистрации положительных ионов и сопоставление величин площадей ионов первой полярности и дочерних ионов, принадлежащих одному соединению, позволили сделать вывод о том, что соотношение этих величин является индивидуальной характеристикой рассматриваемого соединения.
Так, для прометрина (таблица 2), время удерживания которого в условиях анализа методом ВЭЖХ с масс-селективным детектированием в режиме регистрации положительных ионов составляет 4,6 минуты, характерны следующие коэффициенты: K1=7,6; K2=19,0.
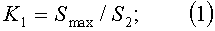
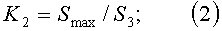
где К1 и К2 - относительные коэффициенты,
Smax - максимальная площадь иона, усл. ед. (в режиме детектирования положительных ионов это площадь иона первой полярности, псевдомолекулярного иона [M+H]+),
S2 и S3 - площади дочерних ионов с массой [М+2]+ и [М+3]+ соответственно, усл. ед.
Найденные коэффициенты (коэффициенты идентификации) прометрина сохраняют свое значение в интервале концентраций раствора от 1,0·10-2 до 1,0 мг/мл при относительном среднеквадратичном отклонении, не превышающем 6,8% (количество определений 12).
В случае дифолатана (таблица 4) картина осложняется наличием нескольких возможных ионов первой полярности за счет различного изотопного состава атомов молекулы, содержащей четыре атома хлора, атомы серы и азота. В масс-спектре дифолатана присутствуют псевдомолекулярные ионы первой полярности и их дочерние ионы, образованные присоединением аддукта (NH4)+, наличие которого возможно при использовании ацетата аммония в качестве компонента подвижной фазы. При этом характерно отсутствие дочерних ионов для иона первой полярности с массой 347.
При работе с отрицательными ионами соотношение площадей ионов определяет коэффициент идентификации (K-) для соответствующей молекулярной массы:
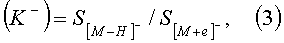
где (K-) - коэффициент идентификации для соответствующей молекулярной массы при детектировании в режиме регистрации отрицательных ионов;
S[M-H] - и S[М+е] - - соответственно площадь пика иона с массой [М-Н]- и [М+е]-.
Для бромацила (таблица 3) значения коэффициента идентификации для двух возможных масс с учетом изотопного состава молекулы составляют 9,2 и 9,7 и сохраняют свое значение в широком концентрационном интервале.
Анализируя результаты, приведенные в таблицах 2-4, можно сделать вывод о том, что не только сами значения коэффициентов, но и наличие или отсутствие второго коэффициента являются индивидуальными характеристиками соединения, зависящими от его химического состава и строения.
Аналогичным образом были исследованы и другие представители пестицидов, выбранных в качестве объектов настоящей работы. Из них, кроме прометрина и дифолатана, в режиме регистрации положительных ионов детектируются форат, карбофос и его примесь, линурол, планавин, дактал. При этом для этих соединений не наблюдалось образования отрицательных ионов.
По отрицательным ионам было возможно детектирование, кроме бромацила, бан-вела, 2,4-Д, диносерба, пиклорама. Некоторые соединения (из класса полициклических галогенпроизводных - дильдрин; из производных тиомочевины - додин) не детектируются ни в том, ни в другом режиме.
В таблице 5 приведены результаты расчетов коэффициентов идентификации K1 и К2 для исследованных пестицидов при детектировании в режиме регистрации положительных ионов.
** - ионы [М+NH4]+, соответствующие молекулярным массам 347 и 349, образование которых возможно при использовании ацетата аммония в качестве одного из компонентов подвижной фазы;
*** - ион [М+NH4]+, соответствующий молекулярной массе 351, образование которого возможно при использовании ацетата аммония в качестве одного из компонентов подвижной фазы;
**** - ион [М+NH4]+, соответствующий молекулярной массе 354 при учете изотопного состава, образование которого возможно при использовании ацетата аммония в качестве одного из компонентов подвижной фазы.
Анализ данных таблицы 5 показывает, что для фората, карбофоса и его примеси, прометрина и планавина характерно наличие одного псевдомолекулярного иона [М+Н]+ и его дочерних ионов. Все эти соединения не содержат атомов галогенов (таблица 1).
В случае линурола, как и в случае дифолатана, наблюдается спектр ионов. Оба эти соединения содержат в своем составе атомы хлора, для которого возможно существование в природе двух изотопов, отличающихся по массе на 2 а.е.м., что согласуется с основными представлениями по ионизации галогенсодержащих соединений (Д.Броун, А.Флойд, М.Сейнзбери. Спектроскопия органических веществ. Перевод с английского А.А.Кирюшкина [Текст] / М.: Мир, 1992. - 300 с.). Все это подтверждает тот факт, что картина "мягкой" ионизации электрораспылением при атмосферном давлении уникальна для каждого соединения и отражает его индивидуальность.
В таблице 6 приведены результаты расчетов коэффициентов идентификации (K-) для исследованных пестицидов при детектировании в режиме регистрации отрицательных ионов.
Анализ результатов детектирования исследованных пестицидов в режиме регистрации отрицательных ионов позволяет сделать следующие выводы:
коэффициент идентификации (K-) является индивидуальной характеристикой соединения и сохраняет свое значение в концентрационном интервале от 1,0·10-2 до 1,0 мг/мл;
для тех соединений, для которых возможно существование нескольких молекулярных масс, наблюдается близость значений коэффициента (K-), определенных для каждой из масс;
как и в случае детектирования в режиме регистрации положительных ионов, совокупность параметров: массовое число, время удерживания, а также значения коэффициента идентификации (K-) - позволит повысить надежность идентификации исследуемых соединений.
Пример осуществления способа
1. При анализе методом ВЭЖХ с масс-селективным детектированием (условия анализа приведены на фигуре 1) смеси пестицидов неизвестного состава обнаружен хроматографический пик с временем удерживания, равным 1,1…1,3 мин. Измеренный масс-спектр первой полярности позволяет определить молекулярную массу соединения. Эта величина составляет 240 а.е.м.
Близкими по значению молекулярной массы являются соединения: диносеб, пиклорам и прометрин. Идентификация только по хроматографическому параметру и массе основного псевдомолекулярного иона позволяет сделать предположение, что этот пик не может принадлежать прометрину, поскольку его время удерживания составляет 4,6 мин (таблица 2). Дополнительным подтверждением правильности сделанного предположения является тот факт, что его детектирование осуществляется в режиме регистрации положительных ионов, в то время как неизвестное соединение детектировалось по отрицательным ионам, как диносеб и пиклорам.
После сравнения хроматографических параметров, ионов первой полярности и режима детектирования следующей стадией идентификации является измерение дочерних масс-спектров и определение идентификационных коэффициентов. В случае детектирования по отрицательным ионам речь идет о коэффициенте (K-). Согласно таблице 6 диносеб имеет лишь один коэффициент, равный 8,3 для молекулярной массы 240. Пиклорам характеризуется двумя значениями коэффициента: для массы 240 он составляет 16,0, а для массы 242 - 14,5 (таблица 6). Существенные различия в значении коэффициента и в количестве коэффициентов позволяют с высокой достоверностью отличить пиклорам от диносеба.
2. Более сложным случаем распознавания двух соединений является случай 2,4-Д и банвела: оба они имеют одинаковую молекулярную массу, равную 220; одинаковое время удерживания в условиях хроматографирования методом ВЭЖХ с масс-селективным детектированием, равное 1,1…1,4 мин; оба соединения детектируются по отрицательным ионам. Поэтому использование идентификационного коэффициента (K-) - единственная возможность надежного различения этих двух соединений: для банвела характерно наличие лишь одного значения коэффициента для массы 220, равного 13,2; для 2,4-Д характерно наличие двух близких значений коэффициента для масс (220 и 222), равных 11,2 и 11,0 (таблица 6).
3. При анализе методом ВЭЖХ с масс-селективным детектированием в режиме регистрации положительных ионов обнаружено неизвестное соединение с массой иона первой полярности, равной 348, и временем удерживания, равным 4,3 мин. По массе иона первой полярности и времени удерживания наиболее близким соединением является дифолатан с временем удерживания, равным 4,8 мин (таблицы 4, 5).
Как известно (Вигдергауз М.С. Расчеты в газовой хроматографии [Текст] / М.С.Вигдергауз. - М.: Химия, 1978. - 248 с.), при хроматографическом анализе уменьшение концентрации соединения в растворе может привести к увеличению времени удерживания. В этом случае вполне возможно увеличение времени удерживания с 4,3 мин до (4,7…4,8) мин, что может привести к ошибке в идентификации. Использование идентификационных коэффициентов позволяет повысить достоверность идентификации.
Так, в приведенном примере неизвестное соединение характеризовалось наличием лишь одного первого коэффициента, равного 3,6. Для дифолатана, наоборот, характерно отсутствие первого коэффициента для массы, равной 347, но при этом имеются коэффициенты K1 и K2 для массы 349, равные 14,2 и 2,1 соответственно, и коэффициенты, рассчитанные для масс 347 и 349 и дочерних ионов, образованных за счет присоединения аддукта (таблица 4).
Все это подтверждает тот факт, что картина "мягкой" ионизации электрораспылением при атмосферном давлении уникальна для каждого соединения и отражает его индивидуальность. Не только сами значения коэффициентов, но и наличие или отсутствие второго коэффициента являются индивидуальными характеристиками органического соединения, зависящими от его химического состава и строения. Использование дополнительной информации наряду с массой исследуемого иона и параметром удерживания позволит повысить надежность и достоверность идентификации органических соединений и расширить функциональные возможности масс-спектрометрического метода.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИДЕНТИФИКАЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДОМ ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ | 2015 |
|
RU2599900C2 |
| СПОСОБ ВЫЯВЛЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ПАЦИЕНТОВ, ПРИНИМАВШИХ НАРКОТИЧЕСКИЕ ИЛИ ПСИХОАКТИВНЫЕ ВЕЩЕСТВА | 2009 |
|
RU2419788C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ ФОСФОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕТОДОМ ХРОМАТО-МАСС-СПЕКТРОМЕТРИИ С ЦИЛИНДРИЧЕСКОЙ ИОННОЙ ЛОВУШКОЙ | 2020 |
|
RU2741955C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ НАРКОТИЧЕСКИХ И ПСИХОАКТИВНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2009 |
|
RU2390771C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КСЕНОБИОТИКОВ В МОЧЕ ЧЕЛОВЕКА ПРИ ДОПИНГОВОМ КОНТРОЛЕ | 2008 |
|
RU2390773C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРИЕМА КОРТИКОТРОПИНОВ ПРИ ДОПИНГОВОМ КОНТРОЛЕ СПОРТСМЕНОВ | 2008 |
|
RU2384846C1 |
| СПОСОБ ВЫЯВЛЕНИЯ И ОПРЕДЕЛЕНИЯ ПРОИСХОЖДЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В СПИРТНЫХ НАПИТКАХ | 2009 |
|
RU2392616C1 |
| СПОСОБ ОБНАРУЖЕНИЯ КОМПЛЕКСА КСЕНОБИОТИКОВ В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ ПРИ ДОПИНГОВОМ КОНТРОЛЕ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2011 |
|
RU2473079C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРИЕМА ЭРИТРОПОЭТИНА ПРИ ДОПИНГОВОМ КОНТРОЛЕ СПОРТСМЕНОВ | 2008 |
|
RU2390779C2 |
| Способ определения дабигатрана в сыворотке крови человека | 2018 |
|
RU2683032C1 |
Изобретение относится к исследованию или анализу материалов путем определения их химических или физических свойств, конкретно путем разделения на составные части (компоненты) с использованием адсорбции и их масс-спектрометрического исследования. Способ идентификации органических соединений на основе метода высокоэффективной жидкостной хроматографии и масс-спектрометрии заключается в том, что после хроматографического разделения веществ и ионизации электростатическим распылением при атмосферном давлении производят детектирование разделенных компонентов в режиме регистрации положительных и отрицательных ионов и выбирают режим детектирования по максимальной информативности. Затем измеряют спектр масс первой полярности и определяют вероятную молекулярную массу посредством распознавания аддуктов с учетом возможного изотопного состава атомов, входящих в молекулу. Далее измеряют масс-спектры дочерних ионов. При этом на основании масс-спектра первой полярности и дочерних масс-спектров рассчитывают идентификационные коэффициенты. Затем сравнивают хроматографические параметры и результаты масс-спектрометрических измерений с данными библиотеки спектров масс известных веществ.
Техническим результатом изобретения является повышение достоверности и надежности идентификации, расширение функциональных возможностей масс-спектрометрического метода. 6 табл., 2 ил.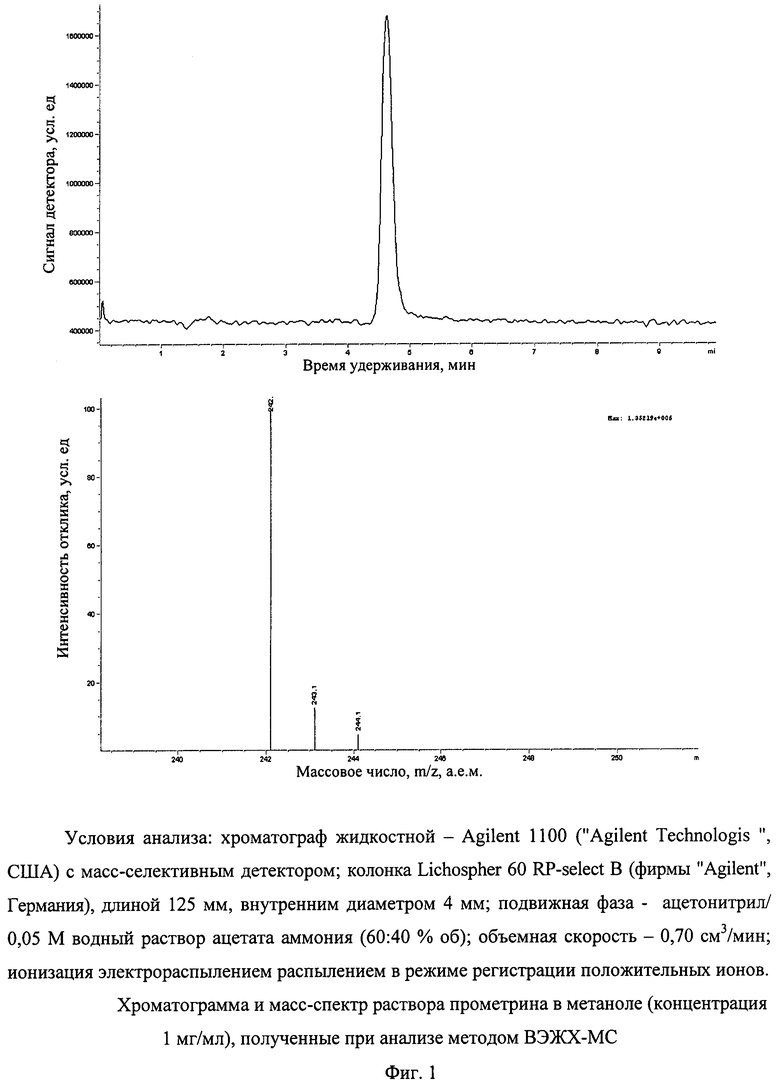
Способ идентификации органических соединений на основе метода высокоэффективной жидкостной хроматографии и масс-спектрометрии, отличающийся тем, что после хроматографического разделения веществ и ионизации электростатическим распылением при атмосферном давлении производят детектирование разделенных компонентов в режиме регистрации положительных и отрицательных ионов и выбирают режим детектирования по максимальной информативности; измеряют спектр масс первой полярности и определяют вероятную молекулярную массу посредством распознавания аддуктов с учетом возможного изотопного состава атомов, входящих в молекулу; измеряют масс-спектры дочерних ионов; на основании масс-спектра первой полярности и дочерних масс-спектров рассчитывают идентификационные коэффициенты; сравнивают хроматографические параметры и результаты масс-спектрометрических измерений с данными библиотеки спектров масс известных веществ.
| СПОСОБ ПРОИЗВОДСТВА АРОМАТИЗИРОВАННОГО ВАФЕЛЬНОГО ХЛЕБА | 2009 |
|
RU2409102C1 |
| RU 2007104231 A, 10.08.2008 | |||
| US 20050215764 A1, 29.09.2005 | |||
| Лебедев А.Т., Лебедев К.С., Мясоедов Б.Ф., Рыбальченко И.В., Сигейкин Г.И., Суворкин В.Н | |||
| Масс-спектрометрическая идентификация высокотоксичных алкилфторфосфонатов | |||
| - Масс-спектрометрия, т | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2012-12-10—Публикация
2011-02-10—Подача