Изобретение относится к области медицины и может использоваться в анестезиологии и реаниматологии для плановой катетеризации подключичной вены.
Центральная венозная катетеризация является одной из основополагающих манипуляций в анестезиологии и реаниматологии [1] и представляет собой установку катетера в центральную вену -верхнюю или нижнюю полые - через подключичную вену (ПВ), внутреннюю яремную, бедренную, плечеголовную или периферическую вену конечностей. Инфекционные и тромботические осложнения встречаются при катетеризации ПВ с наименьшей частотой, по сравнению с другими доступами [2-4]. Механические осложнения, в большей степени присущие катетеризации ПВ, такие как пневмоторакс, пункция артерии, гематома, предотвращаются с помощью ультразвуковой навигации [5, 6].
Тем не менее, имеются сведения о том, что низкая частота успеха катетеризации ПВ при использовании ультразвукового контроля с первой попытки выделяется как одна из основных проблем при катетеризации ПВ [7]. Таким образом, в настоящее время повышение показателей эффективности катетеризации ПВ под контролем УЗ является актуальной задачей.
Известны способы катетеризации вены под контролем УЗ в продольном сечении сосуда, поперечном и косом:
Способ катетеризация вены под контролем УЗ в продольном сечении сосуда, описан Fragou at al. (2011) [5]. Сосудистый пучок в подключичной области визуализируется в поперечном сечении. По совокупности факторов (сжимаемость, спадение на вдохе, форма и размер сосуда, пульсация, взаимное расположение с артерией) определяется ПВ. Ультразвуковое изображение вены выводится в продольное сечение. Пункция ПВ осуществляется по ходу сосуда под углом 30°. Игла или след от смещения тканей иглой визуализируется по всей длине.
Главным недостатком методики является высокий риск утраты изображения вены при малейшем смещении датчика и/или движении больного и отсутствие визуализации окружающих вену структур.
Пункция вены под контролем УЗ в поперечном сечении сосуда описана Vezzani at al. (2017) [6]. Сосуды выводятся в поперечном сечении. По совокупности вышеописанных параметров определяется вена. Пункция кожи осуществляется на расстоянии, равном глубине залегания ПВ, от поперечно располагающегося над веной датчика. Пункция ПВ иглы осуществляется под углом 45° к поверхности кожи. Визуализируются окружающие структуры.
В вышеуказанном источнике сравнивалась пункция под контролем УЗ в поперечном сечении с пункцией под контролем УЗ в продольном сечении, описанной выше. Для поперечного сечения продемонстрирована большая частота успешных пункций, в том числе с первой попытки, меньшее число пункций кожи и вены, изменений направления иглы, меньшее время до введения проводника. В обеих группах отсутствовали механические осложнения.
Недостатком методики является отсутствие визуализации продвигающейся к вене иглы, а также большая частота пункций задней стенки вены (ПЗС) [8].
Пункция вены под контролем УЗ в косом сечении сосуда предложена Brescia et al. [9]. Предполагает выведение вены в косое сечение с пункцией иглой под углом 30° к поверхности кожи, как в продольном сечении, при этом визуализируется и игла, и окружающие структуры. Продемонстрирован практически 100% успех процедуры по предлагаемой технике, однако в исследовании не изучалась частота ПЗС и изменений направления иглы.
По наиболее близкой технической сущности в качестве прототипа нами выбран способ катетеризации ПВ подключичным доступом под контролем УЗ в продольном сечении сосуда. Способ заключается в следующем: сосудистый пучок в подключичной области визуализируют в поперечном сечении, осматривают окружающие структуры. По совокупности факторов (сжимаемость, спадение на вдохе, форма и размер сосуда, пульсация, взаимное расположение с артерией) идентифицируют ПВ. Изображение вены выводят в продольное сечение. Датчик располагают в подключичной области параллельно ключице. Пункцию ПВ осуществляют по ходу сосуда под углом 30°. Частота успешного введения проводника после единственной пункции кожи и вены без изменений направления иглы составляет 48% [6].
Недостатками способа, выбранного в качестве прототипа, являются:
• высокий риск утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного;
• низкая вероятность успешного введения проводника после единственной пункции кожи и ПВ без изменения направления иглы, составляющая 48% [6].
Техническим результатом, достигаемым с помощью изобретения, является:
• снижение риска утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного;
• повышение частоты успешного введения проводника после выполнения единственного вкола в кожу и ПВ без изменения направления иглы.
Технический результат изобретения достигается тем, что катетеризацию ПВ выполняют под контролем УЗ в продольном сечении. Датчик устанавливают в дельтовидно-грудной борозде. Выполняют катетеризацию ПВ с наибольшим передне-задним диаметром, но не менее 0,7 см. При величине передне-заднего диаметра ПВ менее 0,7 см изменяют укладку больного до получения значения передне-заднего диаметра ПВ не менее 0,7 см. Срез иглы и кончик J-образного проводника направляют в каудальном направлении.
Способ осуществляется следующим образом:
Используют линейный датчик с частотой эмиссии УЗ волн 7,5 МГц. Ультразвуковой аппарат располагают со стороны, противоположной процедуре, таким образом, чтобы его экран находился перед глазами оператора. Катетеризацию проводят с соблюдением правил асептики и антисептики.
Осуществляют сканирование подключичной области с двух сторон. Визуализацию сосудистого пучка осуществляют с помощью различных движений датчика: скольжения, наклонов, качания и вращения. Осматривают окружающие ткани и исключают из исследования пациентов с аномалиями и тромбозом ПВ. По совокупности факторов, а именно: форма и размер сосуда, пульсация, сжимаемость, спадение на вдохе и взаимное расположение, идентифицируют ПВ. Выбирают вену с наибольшим передне-задним диаметром, но не менее 0,7 см. При отсутствии различий отдают предпочтение правой ПВ, ввиду возможного разрыва правой стенки при катетеризации левой ПВ, вследствие отсутствия углов между левой ПВ, левой плечеголовной и верхней полой венами [10]. При величине передне-заднего диаметра менее 0,7 см изменяют укладку больного: с выбранной стороны манипуляции подкладывают валик под плечо и на 15-20° отводят в сторону во фронтальной плоскости верхнюю конечность [11] до получения значения передне-заднего диаметра подключичной вены не менее 0,7 см.
После описанного выше сканирования сосудистого пучка в поперечной плоскости датчик разворачивают для пункции вены в продольном сечении. Датчик должен располагаться строго над веной перпендикулярно поверхности тела в дельтовидно-грудной борозде. С помощью иглы малого диаметра, то есть первой иглой, осуществляют вкол на коже у латерального края датчика и ведут эту иглу по направлению к вене строго по средней линии датчика, контролируя смещение тканей или продвижение самой иглы и предпосылая раствор местного анестетика. Затем по той же траектории осуществляют продвижение второй, то есть «рабочей» иглы до ПВ. При потере следа от смещения тканей первой или второй иглой осуществляют скольжение датчика вправо и влево от первоначальной позиции и одновременно оказывают давление на иглу, причем с такой силой, которая не позволяет игле продвинуться дальше, и находят утерянный след. Попадание «рабочей» иглы в вену подтверждается аспирацией крови. Срез иглы и J-образный кончик вводимого в иглу проводника направляют каудально [12]. Далее по проводнику заводят катетер. Правильное положение катетера, т.е. в устье верхней полой вены, подтверждают с помощью ультразвукового сканирования вен шеи, подключичных областей, трансторакальной эхокардиографии [13]. Пневмоторакс исключают с помощью ультразвукового исследования легких [14].
Существенные отличительные признаки изобретения и причинно-следственная связь между ними и достигаемым техническим результатом:
• УЗ датчик устанавливают в дельтовидно-грудной борозде, катетеризацию подключичной вены выполняют при величине передне-заднего диаметра не менее 0,7 см в плоскости ультразвукового сканирования, а при величине передне-заднего диаметра менее 0,7 см изменяют укладку больного до получения значения передне-заднего диаметра не менее 0,7 см.
Установка УЗ датчика в дельтовидно-грудной борозде обоснована на основании следующих фактов:
- в 7 случаях из 32 на экране ультразвукового аппарата визуализировалось изображение-«призрак» сосудистого пучка (Фиг. 1), обусловленное преломлением некоторых волн при прохождении через край дельтовидной или большой грудной мышцы. Поэтому датчик, в отличие от способа прототипа, необходимо устанавливать в дельтовидно-грудной борозде, где нет краев вышеуказанных мышц и преломление ультразвуковых волн минимально;
- вена у некоторых пациентов сжималась лишь от интенсивного давления на датчик; складывалось впечатление, что сосуд сжимался передаточной силой;
- было замечено, что при проведении катетеризации ПВ под контролем УЗ в продольном сечении сосуда визуализируется лишь след от смещения тканей иглой, но практически никогда - сама игла;
- сложно предположить другие причины, объясняющие низкую частоту успеха с первой попытки после единственной пункции кожи и вены - 48% - при катетеризации ПВ в продольном сечении в исследовании Vezzani et al. (2017) [6];
В процессе исследования установлено, что величина передне-заднего диаметра ПВ не менее 0,7 см в плоскости ультразвукового сканирования позволяет найти след от смещения тканей иглой, в случае его утраты, скольжением датчика в стороны, не теряя при этом вену и не меняя направление иглы. При величине передне-заднего диаметра менее 0,7 см маловероятно обнаружить утерянный след, и поэтому изменяют укладку больного до получения значения передне-заднего диаметра не менее 0,7 см.
Увеличение вены в размере уменьшает время на выведение удовлетворительного изображения сосуда на экране УЗ аппарата. Увеличенная вена пунктируется легко, предотвращается ПЗС.
• Срез иглы и кончик J-образного проводника направляют в каудальном направлении. Существуют способы направления среза иглы и кончика J-образного проводника под контролем УЗ [15] и с их каудальным направлением [12]. В последнем случае частота правильного расположения проводника, т.е. в устье верхней полой вены, составляет 84%, что сопоставимо с аналогичным показателем под контролем УЗ, поэтому для удобства оператора достаточно каудального направления среза иглы и J-образного кончика проводника.
Совокупность существенных отличительных признаков снижает риск утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного, а также повышает частоту успешного введения проводника после выполнения единственного вкола в кожу и ПВ без изменения направления иглы.
Пример конкретного выполнения способа:
Пример 1.
Пациентка К., 70 лет, пункция периферических вен у которой была невозможна вследствие их невыраженности. Передне-задний диаметр обеих ПВ 0,9 см. Под контролем УЗ в продольном сечении сосуда по заявляемому способу с первого раза, после единственной пункции кожи и вены, без изменения направления иглы в правую ПВ был введен проводник. Технических сложностей, механических осложнений (пневмоторакс, пункция артерии, гематома) не было. Катетер, заведенный по проводнику, находился в верхней полой вене. Утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного не наблюдалось.
Пример 2.
Пациент М., 70 лет, нуждался в постановке центрального венозного катетера вследствие необходимости катехоламиновой поддержки кровообращения, вызванной острым инфарктом миокарда. Передне-задний диаметр левой ПВ 0,9 см, правой - 1,2 мм. Под контролем УЗ в продольном сечении сосуда по вышеописанной методике с первого раза, после единственной пункции кожи и вены, без изменения направления иглы в правую ПВ был введен проводник. Технических сложностей, механических осложнений (пневмоторакс, пункция артерии, гематома) не было. Катетер, заведенный по проводнику, находился в верхней полой вене.
Утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного не наблюдалось.
Пример 3.
Пациентке К., 81 год, требовалась катетеризация ПВ с целью проведения массивной инфузионной терапии. Вследствие гиповолемии наибольший среди правой и левой ПВ передне-задний диаметр при ультразвуковом сканировании составлял 0,5 см. Было утрачено изображение вены в продольном сечении при смещении датчика. Под правое плечо был подложен валик, и правая верхняя конечность была отведена в сторону на 20°. После этого передне-задний диаметр правой ПВ составлял 1,1 см, что позволило найти утраченное изображение вены. Под контролем УЗ в продольном сечении сосуда по заявляемому способу с первого раза, после единственной пункции кожи и вены, без изменения направления иглы в ПВ введен проводник. Механических осложнений (пневмоторакс, пункция артерии, гематома) не было. Катетер, заведенный по проводнику, находился в верхней полой вене.
Заявляемый способ апробирован у 17 больных. Способ прототип был нами использован у 15 больных. Успех пункции с первой попытки после единственной пункции кожи и вены без изменения направления иглы имел место значительно чаще, в 94% наблюдений, по заявляемому способу в сравнении со способом прототипом (48% по данным авторов способа прототипа [8], 20% по собственным данным). Различия статистически достоверны (р=0,0001).
Полной утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного в заявляемом способе не наблюдалось, после изменения укладки увеличенный размер вены позволял обнаружить след от смещения тканей иглой при его утрате. В способе прототипе этот показатель не исследовался, вероятность утраты изображения вены обсуждалась как недостаток методики.
Таким образом, заявляемый способ катетеризации ПВ снижает риск утраты изображения вены в продольном сечении при малейшем смещении датчика и/или движении больного, а также повышает частоту успешного введения проводника после выполнения единственного вкола в кожу и ПВ без изменения направления иглы.
Список литературы
1. Лебединский К.М. Под ред., Кровообращение и анестезия, "Человек", СПб, Человек, 2012, 1076 С.
2. J.-J. Parienti, N. Mongardon, 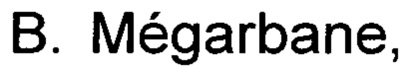 J.-P. Mira, P. Kalfon, A. Gros,
J.-P. Mira, P. Kalfon, A. Gros,  M. Thuong, V. Pottier, M. Ramakers, B. Savary, A. Seguin, X. Valette, N. Terzi, B. Sauneuf, V. Cattoir, L.A. Mermel, D. du Cheyron, 3SITES Study Group, Intravascular Complications of Central Venous Catheterization by Insertion Site, N. Engl. J. Med. 373 (2015) 1220-1229. doi: 10.1056/NEJMoa1500964.
M. Thuong, V. Pottier, M. Ramakers, B. Savary, A. Seguin, X. Valette, N. Terzi, B. Sauneuf, V. Cattoir, L.A. Mermel, D. du Cheyron, 3SITES Study Group, Intravascular Complications of Central Venous Catheterization by Insertion Site, N. Engl. J. Med. 373 (2015) 1220-1229. doi: 10.1056/NEJMoa1500964.
3. D.C. McGee, M.K. Gould, Preventing complications of central venous catheterization, N. Engl. J. Med. 348 (2003) 1123-1133. doi: 10.1056/NEJMra011883.
4. P.E. Marik, M. Flemmer, W. Harrison, The risk of catheter-related bloodstream infection with femoral venous catheters as compared to subclavian and internal jugular venous catheters: a systematic review of the literature and meta-analysis, Crit. Care Med. 40 (2012) 2479-2485. doi: 10.1097/CCM.0b013e318255d9bc.
5. M. Fragou, A. Gravvanis, V. Dimitriou, A. Papalois, G. Kouraklis, A. Karabinis, T. Saranteas, J. Poularas, J. Papanikolaou, P. Davlouros, N. Labropoulos, D. Karakitsos, Real-time ultrasound-guided subclavian vein cannulation versus the landmark method in critical care patients: A prospective randomized study*:, Critical Care Medicine. 39 (2011) 1607-1612. doi: 10.1097/CCM.0b013e318218a1ae.
6. A. Vezzani, T. Manca, C. Brusasco, G. Santori, L. Cantadori, A. Ramelli, G. Gonzi, F. Nicolini, T. Gherli, F. Corradi, A randomized clinical trial of ultrasound-guided infra-clavicular cannulation of the subclavian vein in cardiac surgical patients: short-axis versus long-axis approach, Intensive Care Medicine. 43 (2017) 1594-1601. doi: 10.1007/s00134-017-4756-6.
7. J.-F. Timsit, M. Rupp, E. Bouza, V. Chopra,  K. Laupland, T. Lisboa, L. Mermel, O. Mimoz, J.-J. Parienti, G. Poulakou, B. Souweine, W. Zingg, A state of the art review on optimal practices to prevent, recognize, and manage complications associated with intravascular devices in the critically ill, Intensive Care Med. (2018). doi: 10.1007/s00134-018-5212-y.
K. Laupland, T. Lisboa, L. Mermel, O. Mimoz, J.-J. Parienti, G. Poulakou, B. Souweine, W. Zingg, A state of the art review on optimal practices to prevent, recognize, and manage complications associated with intravascular devices in the critically ill, Intensive Care Med. (2018). doi: 10.1007/s00134-018-5212-y.
8. J.A. Vogel Haukoos, J.S. Haukoos, C.L. Erickson, M.M. Liao, J. Theoret, G.E. Sanz, J. Kendall, Is Long-Axis View Superior to Short-Axis View in Ultrasound-Guided Central Venous Catheterization?*:, Critical Care Medicine. 43 (2015) 832-839. doi: 10.1097/CCM.0000000000000823.
9. F. Brescia, D.G. Biasucci, F. Fabiani, M. Favarato, F. Costa, F. Longo, M. Martuscelli, M. Vitiello, M. Pittiruti, A novel ultrasound-guided approach to the axillary vein: Oblique-axis view combined with in-plane puncture, J Vase Access. (2019) 1129729819826034. doi: 10.1177/1129729819826034.
10. P. Marino, Marino's The ICU Book, 4th Edition, Wolters Kluwer Health/Lippincott Williams & Wilkins, n.d.
11. M. Pittiruti, D.G. Biasucci, A. La Greca, A. Pizza, G. Scoppettuolo, How to make the axillary vein larger? Effect of 90° abduction of the arm to facilitate ultrasound-guided axillary vein puncture, J Crit Care. 33 (2016) 38-41. doi:10.1016/j.jcrc.2015.12.018.
12. Быков M.B., Ультразвуковые исследования в обеспечении инфузионной терапии в отделениях реанимации и интенсивной терапии., ООО «Издательство «Триада», Тверь, 2011.
13. J.M. Smit, R. Raadsen, M.J. Blans, M. Petjak, P.M. Van de Ven, P.R. Tuinman, Bedside ultrasound to detect central venous catheter misplacement and associated iatrogenic complications: a systematic review and meta-analysis, Critical Care. 22 (2018). doi: 10.1186/s13054-018-1989-x.
14. E.A. Ablordeppey, A.M. Drewry, A.B. Beyer, D.L. Theodoro, S.A. Fowler, B.M. Fuller, C.R. Carpenter, Diagnostic Accuracy of Central Venous Catheter Confirmation by Bedside Ultrasound Versus Chest Radiography in Critically III Patients: A Systematic Review and Meta-Analysis, Critical Care Medicine. 45 (2017) 715-724. doi: 10.1097/CCM.0000000000002188.
15. A.-Y. Oh, Y.-T. Jeon, E.-J. Choi, J.-H. Ryu, J.-W. Hwang, H.-P. Park, S.-H. Do, The influence of the direction of J-tip on the placement of a subclavian catheter: real time ultrasound-guided cannulation versus landmark method, a randomized controlled trial, BMC Anesthesiology. 14 (2014). doi:10.1186/1471-2253-14-11.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КАТЕТЕРИЗАЦИИ ВНУТРЕННЕЙ ЯРЕМНОЙ ВЕНЫ ЛАТЕРАЛЬНЫМ ДОСТУПОМ | 2017 |
|
RU2655449C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ ВНУТРЕННЕЙ ЯРЕМНОЙ ВЕНЫ ЦЕНТРАЛЬНЫМ ДОСТУПОМ ПОД УЛЬТРАЗВУКОВОЙ НАВИГАЦИЕЙ | 2011 |
|
RU2471516C1 |
| Способ пункции нижней полой вены | 2023 |
|
RU2817477C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ ЦЕНТРАЛЬНЫХ ВЕН У ДЕТЕЙ | 2013 |
|
RU2527163C1 |
| СПОСОБ ДОСТУПА К КРУПНЫМ ВЕНАМ ВЕРХНИХ КОНЕЧНОСТЕЙ (V.BASILICA и V.CEPHALILCA) ДЛЯ ПРОВЕДЕНИЯ ДИАГНОСТИЧЕСКИХ И ЛЕЧЕБНЫХ ИНТЕРВЕНЦИОННЫХ ВМЕШАТЕЛЬСТВ | 2016 |
|
RU2613562C1 |
| СПОСОБ ДЕКОМПРЕССИИ ГРУДНОГО ЛИМФАТИЧЕСКОГО ПРОТОКА | 2023 |
|
RU2807939C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ ВНУТРЕННЕЙ ЯРЕМНОЙ ВЕНЫ ПРИ НАХОЖДЕНИИ ПАЦИЕНТА В ПРОН-ПОЗИЦИИ | 2020 |
|
RU2753579C1 |
| Способ установки венозной порт-системы | 2022 |
|
RU2790238C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ ВНУТРЕННЕЙ ЯРЕМНОЙ ВЕНЫ | 2014 |
|
RU2573337C1 |
| Способ формирования артериовенозной фистулы для профилактики нарушения проходимости магистральных артерий нижних конечностей | 2021 |
|
RU2780929C1 |
Изобретение относится к области медицины, а именно к ультразвуковой диагностике, и может быть использовано для катетеризации подключичной вены (ПВ) подключичным доступом под контролем ультразвука в продольном сечении. Ультразвуковой датчик устанавливают в дельтовидно-грудной борозде и выполняют катетеризацию ПВ с наибольшим передне-задним диаметром, но не менее 0,7 см. При величине передне-заднего диаметра ПВ менее 0,7 см изменяют укладку больного до получения значения передне-заднего диаметра ПВ не менее 0,7 см. Способ обеспечивает успешную катетеризацию ПВ за счет ультразвукового контроля. 1 ил., 3 пр.
1. Способ катетеризации подключичной вены подключичным доступом под контролем ультразвука в продольном сечении, отличающийся тем, что ультразвуковой датчик устанавливают в дельтовидно-грудной борозде и выполняют катетеризацию подключичной вены с наибольшим передне-задним диаметром, но не менее 0,7 см, а при величине передне-заднего диаметра подключичной вены менее 0,7 см изменяют укладку больного до получения значения передне-заднего диаметра подключичной вены не менее 0,7 см.
2. Способ катетеризации подключичной вены по п. 1, отличающийся тем, что срез иглы и кончик J-образного проводника направляют в каудальном направлении.
| СПОСОБ УЗИ- НАВИГАЦИИ ПРИ ПРОВЕДЕНИИ ВЕРТИКАЛЬНОЙ ПОДКЛЮЧИЧНОЙ БЛОКАДЫ ПЛЕЧЕВОГО СПЛЕТЕНИЯ У ДЕТЕЙ | 2016 |
|
RU2648224C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ ВНУТРЕННЕЙ ЯРЕМНОЙ ВЕНЫ | 2014 |
|
RU2573337C1 |
| Способ катетеризации подключичной вены | 1983 |
|
SU1132925A1 |
| WO 2006122001 A2, 16.11.2006 | |||
| БЫКОВ М | |||
| В | |||
| и др | |||
| Ультразвуковой контроль при катетеризации центральных вен у детей | |||
| SonoAce International | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| FORTUNE J | |||
| B | |||
| et al | |||
| Effect of Patient Position on Size and Location of the Subclavian Vein for | |||
Авторы
Даты
2020-06-04—Публикация
2019-11-05—Подача