Изобретение относится к молекулярной биологии и медицине, а именно к медицинской генетике, диагностике, иммунологии и аллергологии. Изобретение представляет собой способ прогнозирования риска возникновения болезней, связанных с уровнем иммуноглобулина Е (IgE) в сыворотке крови человека, таких как атопический дерматит, хроническая крапивница, астма, аллергический ринит, аллергический риноконъюнктивит, аллергический конъюнктивит. С выделенной из биологического материала человека ДНК проводят полимеразно-цепную реакцию в реальном времени в присутствии олигонуклеотидных зондов и праймеров и анализируют полиморфизмы rs2251746 и rs2427837 гена FCER1A методом аллельной дискриминации.
Изобретение обеспечивает получение новых критериев оценки риска развития заболеваний, связанных с уровнем сывороточного IgE на основе данных о сочетаниях генетических вариантов локусов rs2251746 и rs2427837.
IgE был открыт в связи с его участием в развитии аллергических реакций, связанных с I-типом гиперчувствительности, при котором первичное поступление аллергена вызывает продукцию плазмоцитами специфичного IgE, вызывающего каскад реакций, приводящих к клиническим проявлениям аллергии. [1, 2]
Позже было показано, что доминирующая роль IgE с точки зрения эволюции заключается в защите хозяина от паразитарных инфекций, в особенности гельминтозов, представлявших большую опасность для выживания человека в природных условиях. [1, 3]
С развитием цивилизации частота заражения паразитами существенно снизилась, а высокий уровень сывороточного IgE, закрепившийся в популяции, при частом контакте с различными агентами стал приводить к возникновению аллергических реакций. [4, 5]
Дальнейшие исследования обнаружили связь между концентрацией IgE в крови и некоторыми заболеваниями человека. Высокие уровни IgE в крови повышают риск развития таких заболеваний, как атопический дерматит, хроническая крапивница, астма, аллергический ринит, аллергический риноконъюнктивит, аллергический конъюнктивит.[6, 7, 8, 9, 10, 11] В свою очередь, низкие уровни IgE связывают с меньшей устойчивостью к паразитарным заболеваниям и токсинам животного происхождения. [1, 12, 13, 14]
Таким образом, можно говорить о том, что высокие уровни сывороточного IgE связаны с развитием аллергических реакций и являются маркерами некоторых заболеваний, в то время как низкие уровни сывороточного IgE связаны с пониженной устойчивостью к паразитарным заболеваниям и токсинам животного происхождения.
rs2251746 и rs2427837 - это однонуклеотидные полиморфизмы (SNP) в гене, кодирующем альфа-цепь высокоаффинного рецептора IgE (FCER1A) на хромосоме 1q23. Различные исследования показали высокий уровень корреляции между присутствием в геноме человека rs2251746 или rs2427837 и уровнем IgE в сыворотке крови, а также вероятностью развития аллергических реакций. [3, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26]
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития заболеваний, связанных с уровнем сывороточного IgE на основе генетических полиморфизмов rs2251746 и rs2427837.
В патенте RU2275863 C1 (дата публикации 10.04.2015) предложен «Способ прогнозирования риска возникновения бронхиальной астмы», заключающийся в проведении аллергических проб и определении таких показателей как: наличие родственников, страдающих астмой; подверженность пациента респираторным инфекциям более двух раз в году и подверженность вазомоторному риниту, наличие атонического дерматита, экземы, крапивницы и других аллергических синдромов, заболеваний желудочно-кишечного тракта или печени, а также наличие профессиональной вредности и рассчитывают риск возникновения бронхиальной астмы по формуле. [27] Недостатком данного метода является его трудоемкость, необходимость сбора анамнеза, субъективность оценки, непосредственное присутствие пациента для постановки аллергических проб, невозможность оценить риски развития других заболеваний, связанных с уровнем сывороточного IgE и недостаточная информативность, так как метод не включает генетические маркеры и не позволяет оценить передачу данного признака потомкам.
В патенте RU 2424528 C2 (дата публикации 10.04.2015) предложен «Способ прогнозирования формирования бронхиальной астмы у детей раннего возраста, перенесших острый обструктивный бронхит», заключающийся в проведении исследования периферического кровообращения у детей раннего возраста, перенесших 1-2 эпизода острого обструктивного бронхита, методом компьютерной капилляроскопии капилляров ногтевого ложа и определении отклонения различных показателей микроциркуляторного русла от доверительного среднего показателя. [28] Недостатком данного метода является его трудоемкость, применимость только для небольшой группы населения, невозможность оценить риски развития других заболеваний, связанных с уровнем сывороточного IgE и недостаточная информативность, так как метод не включает генетические маркеры и не позволяет оценить передачу данного признака потомкам.
В патенте RU 2330291 C1 (дата публикации 27.07.2008) предложен «Способ прогнозирования развития атопического дерматита у новорожденных», заключающийся в определении в пуповинной крови новорожденных абсолютного количества мононуклеаров, синтезирующих интерферон-гамма (INFγ) и не имеющих маркера активации CD69 (фенотип клеток - INFγ+CD69-). [29] Недостатком данного метода является необходимость сохранения пуповинной крови новорожденного ребенка, применимость только для небольшой группы населения, невозможность оценить риски развития других заболеваний, связанных с уровнем сывороточного IgE и недостаточная информативность, так как метод не включает генетические маркеры и не позволяет оценить передачу данного признака потомкам.
В патенте RU 2568738 C1 (дата публикации 20.11.2015) предложен «Способ прогнозирования формирования атопического дерматита у детей», заключающийся в определении таких прогностических предикторов, как наличие затянувшейся неонатальной желтухи, пневмонии на 1 -м году жизни ребенка, острой респираторной вирусной инфекции на 1-м году жизни ребенка, паратрофии, синдрома избыточного бактериального роста кишечника на 1-м году жизни ребенка, лямблиоза кишечника на 1-м году жизни, острого простого бронхита на 2-м году жизни, хронического тонзилофарингита на 2-м году жизни ребенка, острого простого бронхита в возрасте после 2-х лет жизни ребенка, бронхообструктивного синдрома в возрасте после 2-х лет жизни ребенка, хронического тонзилофарингита в возрасте после 2-х лет жизни ребенка, хронического аденоидита в возрасте после 2-х лет жизни ребенка, внутричерепной гипертензии, хронического гастродуоденита, аллергического ринита у отца ребенка, бронхиальной астмы у родственников матери пациента и расчете зависимой переменной по математической формуле. [30] Недостатком данного метода является его трудоемкость, необходимость сбора анамнеза, субъективность оценки, невозможность оценить риски развития других заболеваний, связанных с уровнем сывороточного IgE и недостаточная информативность, так как метод не включает генетические маркеры и не позволяет оценить передачу данного признака потомкам.
В патенте RU 2187817 C2 предложен «Способ прогнозирования риска развития аллергических реакций у детей раннего возраста», заключающийся в том, что выделяют лейкоциты из пуповинной крови новорожденного, тестируют их количество при жизнеспособности 95-98%, образец инкубируют раздельно с аллергеном домашней пыли и фактором активации тромбоцитов, в надосадочной жидкости с помощью жидкостной хроматографии высокого разрешения выявляют лейкотриены, и при их обнаружении в пробе с аллергеном и/или при уровне лейкотриена Е4 более 3 нг/107 лейкоцитов и лейкотриена E4 более 4 нг/10 7 лейкоцитов в пробе с фактором активации тромбоцитов прогнозируют развитие аллергической патологии на первом году жизни. [31] Недостатками данного метода являются необходимость сохранения пуповинной крови новорожденного ребенка, применимость только для небольшой группы населения, невозможность оценить риски развития других заболеваний, связанных с уровнем сывороточного IgE и недостаточная информативность, так как метод не включает генетические маркеры и не позволяет оценить передачу данного признака потомкам.
Методом, позволяющим проанализировать состояние полиморфизмов rs2251746 и rs2427837 является секвенирование по Сэнгеру - метод, применяемый для детекции любых изменений нуклеотидной последовательности, разработанный Ф. Сэнгером в 1977 году и широко использующийся для изучения нуклеотидной последовательности ДНК человека. [15] Недостатками данного метода являются его трудоемкость, необходимость в приобретении дорогостоящего оборудования и реактивов, значительно более долгое получение результатов и повышенные риски контаминации лаборатории продуктами полимеразно-цепной реакции (ПНР) и реакций секвенирования.
За прототип нами был выбран патент US 5538848 A (US 5538848 A, Kenneth J. Livak, Susan J., A. Flood, Jeffrey Marmaro, Method for detecting nucleic acid amplification using self-quenching fluorescence probe, 23.07.1996), представляющий собой метод анализа ДНК путем проведения полимеразно-цепной реакции в реальном времени в присутствии меченых флуорофорами, аллель-специфичных (TaqMan) зондов и праймеров. [32] Недостатком прототипа является то, что для использования описанного в прототипе метода на практике, с целью исследования различных полиморфизмов, требуется разработка TaqMan зондов и праймеров для каждого отдельного исследуемого полиморфизма.
Новизна и изобретательский уровень нашего исследования заключаются в том, что на данный момент не известна возможность индивидуального прогноза риска развития заболеваний, связанных с уровнем сывороточного IgE по данным о сочетании полиморфизмов rs2251746 и rs2427837.
Техническим результатом изобретения является разработка TaqMan зондов и праймеров для анализа полиморфизмов rs2251746 и rs2427837 методом аллельной дискриминации, что позволит расширить число способов прогнозирования развития IgE-зависимых заболеваний.
Для достижения указанного технического результата был разработан способ прогнозирования риска развития IgE-зависимых заболеваний, который осуществляется следующим образом:
1. Выделение ДНК из биологического материала пациента
Выделение ДНК из биологического материала пациента осуществляется при помощи коммерческого набора GeneJet Whole Blood Genomic DNA Purification Mini Kit фирмы ThermoFisher Scientific или любым альтернативным методом выделения ДНК, например, методом фенол-хлороформной экстракции по Мэтью.
2. Анализ полиморфизмов rs2251746 и rs2427837
Анализ полиморфизмов rs2251746 и rs2427837 проводят методом ПЦР в реальном времени на амплификаторе Bio-Rad CFX96 Real-Time System с последующим анализом методом аллельной дискриминации.
Для исследования полиморфизма rs2251746 авторами были разработаны следующие TaqMan зонды и праймеры:
Зонды:
Probe 1: FAM - ATATGATACAGAAAACATTTCCTTCTGCT - BHQ-1
Probe 2: ROX - ATATGACACAGAAAACATTTCCTTCTGCT - BHQ-2
Праймеры: Pr Fw: CACAGCTGATGGGTTAA
Pr rev: CTGGAGAGATCTAAGGC
Реакционная смесь объемом 18 мкл включает в себя:
1. ДНК=2.5 мкл,
2. Pr Fw=2 мкл,
3. Pr rev=2 мкл,
4. Probe 1=0.5 мкл,
5. Probe 2=0.5 мкл,
6. DreamTaq PCR Master Mix фирмы ThermoFisher Scientific=9 мкл,
7. MgCl2=1,5 мкл.
После денатурации (3 минуты при t=95°C) выполняют 40 циклов амплификации по схеме: 10 секунд при t=95°C, 30 секунд при t=64°C, регистрация флуоресценции Для исследования полиморфизма rs2427837 были разработаны следующие TaqMan зонды и праймеры:
Зонды:
Probe 1: FAM - AGTTCATCATGGGGAGAAAGTCAATTAAAAA - BHQ1
Probe 2: ROX - AGTCCATCATGGGGAGAAAGTCAATTAAAAA - BHQ2
Праймеры:
Pr Fw: CTACTGTAGGTCTCTCTGTGTTACTACC
Pr rev: CAGGACCAAGGAAAGGATGAG
Реакционная смесь объемом 18 мкл включает в себя:
1. ДНК = 2.5 мкл,
2. PrFw = 2 мкл,
3. Prrev = 2 мкл,
4. Probe 1 = 0.5 мкл,
5. Probe 2 = 0.5 мкл,
6. DreamTaq PCR Master Mix фирмы ThermoFisher Scientific = 9 мкл,
7. MgCl2 = 1,5 мкл.
После денатурации (3 минуты при t=95°C) выполняют 40 циклов амплификации по схеме: 10 секунд при t=95°C, 45 секунд при t=64°C, регистрация флуоресценции
При проведении ПЦР в амплификаторе Bio-Rad CFX96 Real-Time System с флюоресцентной детекцией генотипирование осуществляют методом TaqMan зондов по величине RFU (относительных единиц флуоресценции). Для rs2251746 зонд с флуоресцентным красителем FAM соответствует аллелю Т, зонд с красителем ROX - аллелю С. Для rs2427837 зонд с флуоресцентным красителем FAM соответствует аллелю А, зонд с красителем ROX - аллелю G.
Изобретение охарактеризовано на фигурах 1 и 2.
Фиг. 1. Аллельная дискриминация методом детекции TaqMan зондов по данным величин RFU каждого зонда на амплификаторе CFX96 с детектирующей системой в режиме реального времени полиморфизма rs2251746:  - отрицательный контроль,
- отрицательный контроль,  - гомозиготы СС,
- гомозиготы СС,  -гетерозиготы СТ,
-гетерозиготы СТ,  - гомозиготы ТТ.
- гомозиготы ТТ.
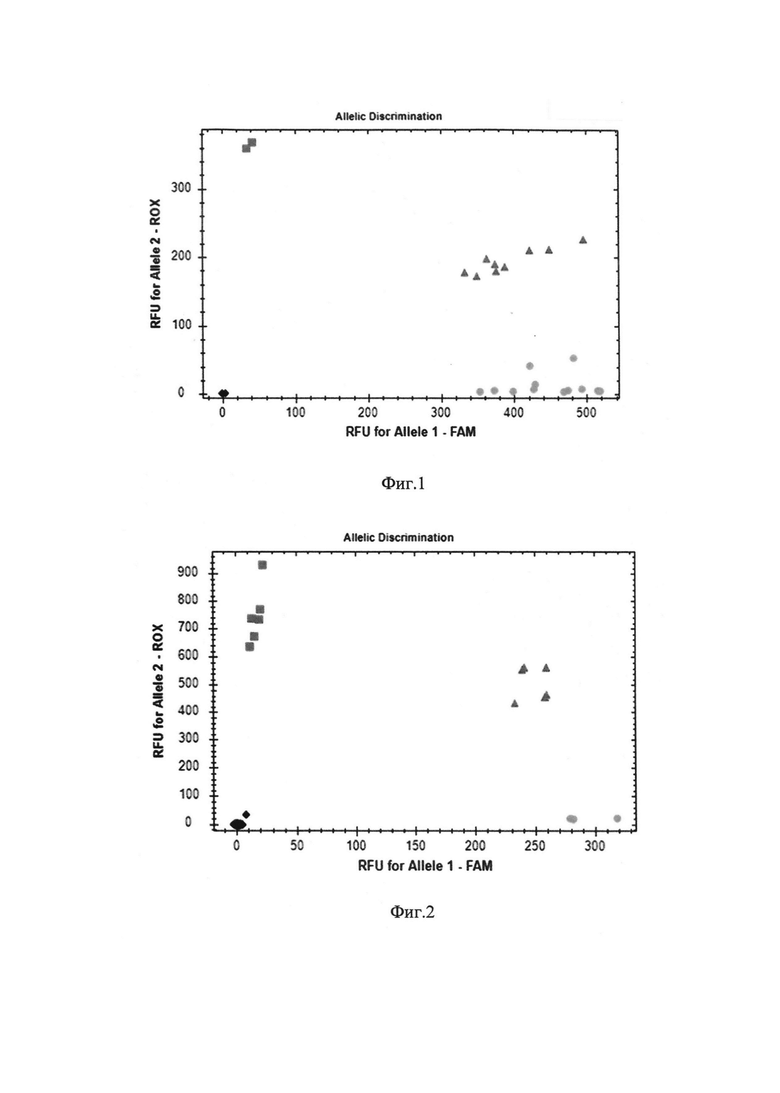
Фиг. 2. Аллельная дискриминация методом детекции TaqMan зондов по данным величин RFU каждого зонда на амплификаторе CFX96 с детектирующей системой в режиме реального времени полиморфизма rs2427837:  - отрицательный контроль,
- отрицательный контроль,  - гомозиготы GG,
- гомозиготы GG,  -гетерозиготы AG,
-гетерозиготы AG,  - гомозиготы АА.
- гомозиготы АА.
3. Прогнозирование риска развития заболеваний, связанных с уровнем сывороточного IgE
rs2251746
В случае выявления аллеля ТТ в гене прогнозируется высокое содержание IgE в сыворотке крови человека.
В случае выявления аллеля СТ прогнозируется сниженное содержание IgE в сыворотке крови человека.
В случае выявления аллеля СС прогнозируется низкое содержание IgE в сыворотке крови человека.
rs2427837
В случае выявления аллеля GG в гене прогнозируется высокое содержание IgE в сыворотке крови человека.
В случае выявления аллеля AG прогнозируется сниженное содержание IgE в сыворотке крови человека.
В случае выявления аллеля АА прогнозируется низкое содержание IgE в сыворотке крови человека.
Интерпретация результатов:
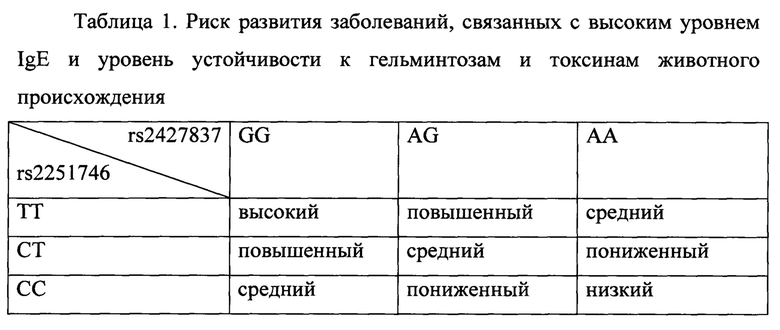
При сочетании аллелей ТТ (rs2251746) и GG (rs2427837) прогнозируется высокий риск развития заболеваний, связанных с высоким уровнем сывороточного IgE и высокая устойчивость к гельминтозам и токсинам животного происхождения.
При сочетании аллелей ТТ (rs2251746) и AG (rs2427837) или СТ (rs2251746) и GG (rs2427837) прогнозируется повышенный риск развития заболеваний, связанных с высоким уровнем IgE и повышенная устойчивость к гельминтозам и токсинам животного происхождения.
При сочетании аллелей СТ (rs2251746) и AG (rs2427837) или СС (rs2251746) и GG (rs2427837) или ТТ (rs2251746) и АА (rs2427837) прогнозируется средний риск развития заболеваний, связанных с высоким уровнем IgE и средняя устойчивость к гельминтозам и токсинам животного происхождения.
При сочетании аллелей СС (rs2251746) и AG (rs2427837) или СТ (rs2251746) и АА (rs2427837) прогнозируется сниженный риск развития заболеваний, связанных с высоким уровнем IgE и сниженная устойчивость к гельминтозам и токсинам животного происхождения.
При сочетании аллелей СС (rs2251746) и АА (rs2427837) прогнозируется низкий риск развития заболеваний, связанных с высоким уровнем IgE и низкая устойчивость к гельминтозам и токсинам животного происхождения.
К заболеваниям, связанным с высоким уровнем IgE в сыворотке крови относят: атопический дерматит, хроническую крапивницу, астму, аллергический ринит, аллергический риноконъюнктивит, аллергический конъюнктивит.
Для интерпретации результатов можно воспользоваться таблицей 1.
В качестве примеров применения разработанного способа приведено исследование ДНК добровольцев, не являющихся родственниками, для которых был проведен анализ полиморфизма генов rs2251746 и rs2427837.
Пример 1.
У пациента O22 была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено, что генотип пациента по локусу rs2251746 - СС, генотип по локусу rs2427837 - AG. Сочетание аллелей СС (rs2251746) и AG (rs2427837) позволяет отнести пациента в группу с пониженным риском развития заболеваний, связанных с высоким уровнем сывороточного IgE. Полученные результаты были подтверждены секвенированием.
Пример 2.
У пациента 015 была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено, что генотип пациента по локусу rs2251746 - СТ, генотип по локусу rs2427837 - GG. Сочетание аллелей СТ (rs2251746) и GG (rs2427837) позволяет отнести пациента в группу с повышенным риском развития заболеваний, связанных с высоким уровнем сывороточного IgE. Полученные результаты были подтверждены секвенированием.
Пример 3.
У пациента N9 была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено, что генотип пациента по локусу rs2251746 - ТТ, генотип по локусу rs2427837 - GG. Сочетание аллелей ТТ (rs2251746) и GG (rs2427837) позволяет отнести пациента в группу с высоким риском развития заболеваний, связанных с высоким уровнем сывороточного IgE. Полученные результаты были подтверждены секвенированием.
Разработанный нами метод обладает следующими преимуществами:
1. Позволяет охватить широкий спектр IgE зависимых заболеваний,
2. Является точным, простым, быстрым и недорогим в исполнении,
3. Не требует медицинских знаний, сбора анамнеза или присутствия пациента,
4. Может быть проведен с использованием различных видов биологического материала, содержащих ДНК пациента (венозная кровь, буккальный эпителий, волосяные фолликулы и др.),
5. Может использоваться для любой группы населения,
6. Позволяет оценить вероятность передачи данного признака потомкам,
7. Результат исследования не зависит от образа жизни и состояния здоровья пациента.
Применение данного способа позволит формировать на доклиническом этапе группы риска по развитию заболеваний, связанных с уровнем сывороточного IgE и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития этих заболеваний.
Список литературы:
1. Amarasekera М. "Immunoglobulin Е in health and disease". Asia Рас Allergy. 2011;1(1):12-15
2. Galli SJ, Tsai M. "IgE and mast cells in allergic disease". Nat Med. 2012;18(5):693-704.
3. Weidinger S. et al. "Genome-wide scan on total serum IgE levels identifies FCER1A as novel susceptibility locus". PLoS Genet. 2008 Aug;4(8):el000166.
4. https://www.ncbi.nlm.nih.gov/variation/tools/1000genomes/
5. Satwani H, Rehman A, Ashraf S, Hassan A. "Is serum total IgE levels a good predictor of allergies in children?" J Pak Med Assoc. 2009 Oct;59(10):698-702
6.  Eva Serrano-Candelas, Gustavo-J Molina-Molina,
Eva Serrano-Candelas, Gustavo-J Molina-Molina,  . "IgE-Related Chronic Diseases and Anti-IgE-Based Treatments." Journal of Immunology Research, vol. 2016, Article ID 8163803, 12 pages, 2016
. "IgE-Related Chronic Diseases and Anti-IgE-Based Treatments." Journal of Immunology Research, vol. 2016, Article ID 8163803, 12 pages, 2016
7. Kessel A, Helou W, Bamberger E, Sabo E, Nusem D, Panassof J, Toubi E. Elevated serum total IgE-a potential marker for severe chronic urticaria. Int Arch Allergy Immunol. 2010;153:288-293
8.  Serrano-Candelas E, Molina-Molina GJ,
Serrano-Candelas E, Molina-Molina GJ, 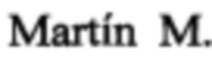 IgE-Related Chronic Diseases and Anti-IgE-Based Treatments. J Immunol Res. 2016; 2016:8163803. doi:10.1155/2016/8163803
IgE-Related Chronic Diseases and Anti-IgE-Based Treatments. J Immunol Res. 2016; 2016:8163803. doi:10.1155/2016/8163803
9. Sudha S Deo et al. "Relationship of Total IgE, Specific IgE, Skin Test Reactivity and Eosinophils in Indian Patients with Allergy". JIACM 2010; 11(4): 265-71
10. Akikatsu K., Tetsuo K. "The Clinical Significance of Serum IgE in Allergic Rhinitis". Auris Nasus Larynx, Volume 1, Issue 1, 1974, Pages 43-51, ISSN 0385-8146
11. Miguel A. Sanjuan, Divya Sagar, Roland Kolbeck. "Role of IgE in autoimmunity". Journal of Allergy and Clinical Immunology vol. 137, 6. 2016:1651-1661
12. Mukai, Kaori et al. "IgE and mast cells in host defense against parasites and venoms." Seminars in immunopathology vol. 38,5 (2016): 581-603
13. Marichal, Thomas et al. "A beneficial role for immunoglobulin E in host defense against honeybee venom." Immunity vol. 39,5 (2013): 963-75
14. Tsai, Mindy et al. "Testing the 'toxin hypothesis of allergy': mast cells, IgE, and innate and acquired immune responses to venoms." Current opinion in immunology vol. 36 (2015): 80-7. doi:10.1016/j.coi.2015.07.001
15. Sanger F. "Determination of nucleotide sequences in DNA". Biosci Rep. - 2004. - V. 24(4-5). - P.237-253
16. Zhou J. et al. "Association of polymorphisms in the promoter region of FCER1A gene with atopic dermatitis, chronic uticaria, asthma, and serum immunoglobulin E levels in a Han Chinese population." PLoS Genet. 2008 Aug;4(8):el000166
17. Chen CM et al. "Common variants in FCER1A influence total serum IgE levels from cord blood up to six years of life." Allergy. 2009 Sep;64(9): 1327-32.
18. Hindorff LA et al. "Potential etiologic and functional implications of genome-wide association loci for human diseases and traits." Proc Natl Acad Sci USA. 2009 Jun 9;106(23):9362-7
19. Niwa Y et al. "FcepsilonRIalpha gene (FCER1A) promoter polymorphisms and total serum IgE levels in Japanese atopic dermatitis patients." Int J Immunogenet. 2010 Apr;37(2): 139-41
20. Nica AC et al. "Candidate causal regulatory effects by integration of expression QTLs with complex trait genetic associations." PLoS Genet. 2010 Apr 1;6(4):e1 000895
21. Potaczek DP et al. "Different FCER1A polymorphisms influence IgE levels in asthmatics and non-asthmatics." Pediatr Allergy Immunol. 2013 Aug; 24(5):441-9.
22. Hsieh CW et al. "A disease marker for aspirin-induced chronic urticaria." Int J Mol Sci. 2014 Jul 15;15(7):12591-603
23. Liao EC et al. "An Exploratory Pilot Study of Genetic Marker for IgE-Mediated Allergic Diseases with Expressions of FcsRla and Ce." Int J Mol Sci. 2015 Apr27; 16(5):9504-19
24. Amo G et al. "FCERI and Histamine Metabolism Gene Variability in Selective Responders to NSAIDS." Front Pharmacol. 2016 Sep 29;7:353. eCollection 2016
25. Dar SA et al. "FcεR1α gene polymorphism shows association with high IgE and anti- FcεR1α in Chronic Rhinosinusitis with Nasal Polyposis." J Cell Biochem. 2018 May;119(5):4142-4149
26. Sharma V et al. "A role of FCER1 A and FCER2 polymorphisms in IgE regulation." Allergy. 2014 Feb; 69(2):231-6
27. RU 2275863 C1, 10.05.2006. Углева Елена Михайловна (RU), Способ прогнозирования риска возникновения бронхиальной астмы, МПК А61В 10/00, Бюл. №13, 10.05.2006
28. RU 2548140 C, Бережанский Павел Вячеславович (RU), Мельникова Ирина Михайловна (RU), Мизерницкий Юрий Леонидович (RU), Способ прогнозирования формирования бронхиальной астмы у детей раннего возраста, перенесших острый обструктивный бронхит, МПК А61В 5/00, Бюл. №10, 10.04.2015
29. RU 330291 C1, 26.02.2004, Терещенко Сергей Юрьевич (RU) Васильева Людмила Викторовна (RU) Исаков Игорь Викторович (RU) Новицкий Иван Александрович (RU) Ольховский Игорь Алексеевич (RU) Шакина Наталья Александровна (RU) Прохоренко Виктор Иванович (RU), Способ прогнозирования развития атопического дерматита у новорожденных, МПК G01N 33/53, Бюл. №21, 27.07.2008
30. RU2568738C, 16.09.2014, Левашева Светлана Владимировна (RU), Эткина Эсфирь Исааковна (RU), Фазылова Алла Аркадьевна (RU), Сакаева Гульнара Дабировна (RU), Бабенкова Любовь Иосифовна (RU), Орлова Наталья Анатольевна (RU), Способ прогнозирования формирования атопического дерматита у детей, МПК А61В 5/00; А61В 10/00, Бюл. №32, 20.11.2015
31. RU2187817C2, 15.05.2000, Погомий Н.Н., Святкина О.Б., Пампура А.Н., Чебуркин А.А., Морозова О.В., Окунева Т.С., Способ прогнозирования развития аллергических реакций у детей раннего возраста, МПК G01N 33/53, 20.08.2002
32. US 5538848 A, Kenneth J. Livak, Susan J., A. Flood, Jeffrey Marmaro, Method for detecting nucleic acid amplification using self-quenching fluorescence probe, 23.07.1996
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения наличия генетической предрасположенности к долголетию человека | 2020 |
|
RU2741838C1 |
| Способ прогнозирования риска развития первичной открытоугольной глаукомы у мужчин по генетическим данным | 2021 |
|
RU2775430C1 |
| Способ прогнозирования риска развития преэклампсии у женщин с учетом генетических маркеров | 2022 |
|
RU2795660C1 |
| Способ прогнозирования риска развития преэклампсии тяжелого течения | 2024 |
|
RU2834809C1 |
| Способ прогнозирования риска развития остеоартроза коленного сустава у мужчин | 2023 |
|
RU2816024C1 |
| Способ прогнозирования риска развития гипертонической болезни с учетом генетических и средовых факторов | 2018 |
|
RU2678441C1 |
| Способ прогнозирования риска развития хронической истинной экземы у женщин с учетом генетических факторов | 2021 |
|
RU2753274C1 |
| Способ прогнозирования риска развития эссенциальной гипертензии | 2017 |
|
RU2661604C1 |
| Способ прогнозирования аллергического ринита у детей с пищевой аллергией к коровьему молоку | 2022 |
|
RU2796318C1 |
| Способ прогнозирования риска развития преэклампсии на основе генетического тестирования | 2024 |
|
RU2834808C1 |
Изобретение относится к области молекулярной биологии и медицины. Предложен способ прогнозирования риска развития заболеваний, связанных с уровнем иммуноглобулина Е (IgE) в сыворотке крови человека. Исследуют полиморфизмы rs2251746 и rs2427837 методом аллельной дискриминации при помощи TaqMan зондов и праймеров. В случае выявления сочетания аллеля ТТ (rs2251746) с аллелем GG (rs2427837) прогнозируют высокий риск развития заболеваний, связанных с высоким уровнем сывороточного IgE. При сочетании аллелей ТТ (rs2251746) и AG (rs2427837) или СТ (rs2251746) и GG (rs2427837) - повышенный риск. При сочетании аллелей AG (rs2427837) и СТ (rs2251746), или GG (rs2427837) и СС (rs2251746), или АА (rs2427837) и ТТ (rs2251746) - средний риск. При сочетании аллелей AG (rs2427837) и СС (rs2251746) или АА (rs2427837) и СТ (rs2251746) - сниженный риск. При сочетании аллелей АА (rs2427837) и СС (rs2251746) - низкий риск. Изобретение обеспечивает расширение числа способов прогнозирования развития IgE-зависимых заболеваний. 2 ил., 1 табл., 3 пр.
Способ прогнозирования риска развития заболеваний, связанных с уровнем иммуноглобулина Е (IgE) в сыворотке крови человека, включающий анализ ДНК из биологического материала человека путем проведения полимеразно-цепной реакции в реальном времени в присутствии меченых флуорофорами аллель-специфичных (TaqMan) зондов и праймеров, отличающийся тем, что исследуют полиморфизмы rs2251746 и rs2427837 методом аллельной дискриминации при помощи следующих TaqMan зондов и праймеров:
rs2251746:
Probe 1: FAM - ATATGATACAGAAAACATTTCCTTCTGCT - BHQ-1
Probe 2: ROX - ATATGACACAGAAAACATTTCCTTCTGCT - BHQ-2
Pr Fw: CACAGCTGATGGGTTAA
Pr rev: CTGGAGAGATCTAAGGC
rs2427837:
Probe 1: FAM - AGTTCATCATGGGGAGAAAGTCAATTAAAAA - BHQ1
Probe 2: ROX - AGTCCATCATGGGGAGAAAGTCAATTAAAAA - BHQ2
Pr Fw: CTACTGTAGGTCTCTCTGTGTTACTACC
Pr rev: CAGGACCAAGGAAAGGATGAG,
а затем осуществляют прогнозирование риска развития заболеваний, связанных с уровнем IgE в сыворотке крови, при этом прогнозируют высокий риск развития заболеваний, связанных с высоким уровнем сывороточного IgE в случае выявления сочетания аллеля ТТ (rs2251746) с аллелем GG (rs2427837), повышенный риск при сочетании аллелей ТТ (rs2251746) и AG (rs2427837) или СТ (rs2251746) и GG (rs2427837), средний риск при сочетании аллелей AG (rs2427837) и СТ (rs2251746), или GG (rs2427837) и СС (rs2251746), или АА (rs2427837) и ТТ (rs2251746), сниженный риск при сочетании аллелей AG (rs2427837) и СС (rs2251746) или АА (rs2427837) и СТ (rs2251746) и низкий риск при сочетании аллелей АА (rs2427837) и СС (rs2251746).
| ZHOU J | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Hum Immunol | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ АТОПИЧЕСКОГО ДЕРМАТИТА У НОВОРОЖДЕННЫХ | 2007 |
|
RU2330291C1 |
| US 5538848 A, 23.07.1996 | |||
| WEIDINGER S | |||
| et al | |||
| Genome-wide scan on total serum IgE levels | |||
Авторы
Даты
2020-06-11—Публикация
2019-07-04—Подача