ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет по дате подачи предварительной заявки на патент США № 62/090138, поданной 10 декабря 2014, содержание которой во всей ее полноте включено здесь в качестве ссылки, и согласно которой заявляется приоритет.
Область техники, к которой относится изобретение
Раскрываемый здесь предмет изобретения относится к соединениям, которые модулируют активность вкусового рецептора умами, и к вкусоароматическим композициям, которые включают, по меньшей мере, одно такое соединение, а также к способам идентификации таких соединений. Вкусоароматические композиции можно использовать для усиления или изменения вкусовой привлекательности, вкуса и/или аромата пищевых продуктов для домашних животных. Вкусоароматические композиции могут включать комбинации соединений и могут быть добавлены в пищевые продукты для домашних животных в различных форматах системы доставки. Соединения, которые модулируют активность вкусового рецептора умами, могут включать одно или более трансмембранных соединений, нуклеотидных производных, нуклеотидов, первой аминокислоты, второй аминокислоты или их комбинации.
Уровень техники
Профили вкуса для съедобных композиций включают основные вкусы, такие как сладкий, соленый, горький, кислый, умами и кокуми. Профили вкуса также были описаны как вкусы, появляющиеся за счет образования свободных жирных кислот. Химические соединения, которые вызывают эти вкусы, часто упоминаются как тастанты. Предполагается, что тастанты воспринимаются рецепторами вкуса в ротовой полости и горле, откуда передаются сигналы в мозг, где регистрируются тастанты и возникающие профили вкуса. Вкусовые рецепторы включают класс вкусовых рецепторов T1R, таких как T1R1, T1R2 и T1R3, которые взаимодействуют в виде гетеродимеров для функционирования в качестве вкусовых рецепторов. Например, T1R2/T1R3 реагирует на сладкие раздражители, а гетеродимер T1R1/T1R3 распознает вкус умами. Кошки и члены семейства Felidae не могут экспрессировать функциональный мономер T1R2, указывая на то, что основным классом вкусовых рецепторов T1R у кошек является рецептор умами, T1R1/T1R3. Кроме того, кошки проявляют предпочтение для кормовых композиций со вкусом умами.
Существует несколько значительных различий между рецепторами T1R1/T1R3 человека и T1R1/T1R3 кошки. Например, человеческий T1R1/T1R3 реагирует на аминокислоту глутамат в качестве агониста и на нуклеотиды, в частности, IMP и GMP, в качестве положительных аллостерических модуляторов. Человеческий T1R1/T1R3 также реагирует на соединения, которые связываются трансмембранным доменом рецептора. Например, в опытах со свопингом доменов было показано, что N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамид, который представляет положительный аллостерический модулятор рецептора, связывается с трансмембранным доменом T1R1 человека (Zhang et.al, Proc. Natl. Acad. Sci. USA, 105 (52): 20930-4, 2008). Известно также, что аллостерические модуляторы, которые связываются с трансмембранным доменом, модулируют активность многочисленных членов GPCR класса III, включая рецепторы mGluR и рецептор CaSR. Однако T1R1/T1R3 человека и кошки реагируют синергетически на комбинации нуклеотидов и аминокислот.
Производители пищевых продуктов для домашних животных имеют давнее желание обеспечить пищевые продукты для домашних животных, имеющие высокую питательную ценность. Кроме того, относясь с особым вниманием к кошачьим и собачьим кормам, производители пищевых продуктов для домашних животных стремятся достичь высокой степени их вкусовой привлекательности, чтобы домашние животные могли получать полноценную питательную пользу от своего корма. Домашние животные, особенно кошки, являются, как известно, непостоянными в своих пищевых предпочтениях и часто отказываются потреблять пищевой продукт для домашних животных, который они потребляли в течение некоторого времени, или отказываются поедать больше, чем минимальное количество корма для домашних животных. В результате владельцы домашних животных часто меняют типы и марки пищевых продуктов для животных, чтобы поддерживать своих питомцев в здоровом и удовлетворительном состоянии.
Несмотря на недавние достижения в технологиях создания вкуса и аромата, остается потребность в соединениях, которые могут улучшать или изменять вкусовую привлекательность пищевых продуктов для домашних животных путем усиления или модификации профилей вкуса, текстуры и/или аромата пищевого продукта для домашних животных. Усиление или модификация может заключаться в повышении интенсивности требуемого атрибута, замещении требуемого атрибута, который отсутствует или каким-то образом утерян в пищевом продукте для домашних животных, или уменьшении интенсивности нежелательного атрибута. В частности, желательно усилить интенсивность тастанта в пищевом продукте для домашних животных. Следовательно, в данной области техники существует потребность в композициях для повышения вкусовой привлекательности и/или вкуса умами пищевых продуктов для домашних животных.
Сущность изобретения
Раскрываемый здесь предмет изобретения относится к вкусоароматическим композициям и способам получения и модификации таких композиций в различных пищевых продуктах для домашних животных. В частности, настоящее раскрытие относится к композициям, содержащим одно или более трансмембранных соединений и/или нуклеотидных производных, которые усиливают, увеличивают и/или модулируют активность рецептора умами, T1R1/T1R3.
В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция содержит нуклеотидное производное формулы Nt-1:
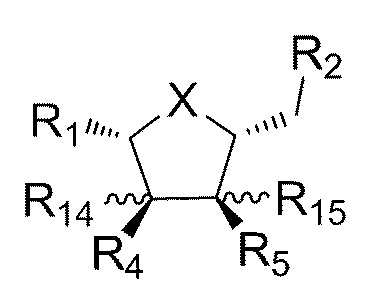
где X, R1, R2, R4, R5, R14 и R15 имеют значения, раскрытые здесь ниже. Настоящее раскрытие обеспечивает соли и стереоизомеры соединений формулы Nt-1.
В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция содержит одно или более нуклеотидных производных формул от Nt-2 до Nt-55, как здесь описано.
В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция дополнительно содержит одно или более трансмембранных соединений формул от Tm-1 до Tm-104, как здесь описано.
В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит одну или более первых аминокислот и/или одну или более вторых аминокислот. В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит, по меньшей мере, одну, две, три, четыре, пять или более первых аминокислот и/или, по меньшей мере, одну, две, три, четыре, пять или более вторых аминокислот. В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит, по меньшей мере, одну первую аминокислоту и/или, по меньшей мере, одну вторую аминокислоту. В некоторых вариантах осуществления вкусоароматическая композиция содержит, по меньшей мере, две первые аминокислоты и/или, по меньшей мере, одну вторую аминокислоту. В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит, по меньшей мере, одну первую аминокислоту и/или, по меньшей мере, две вторые аминокислоты. В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит, по меньшей мере, две первые аминокислоты и/или, по меньшей мере, две вторые аминокислоты.
Неограничивающие примеры первой аминокислоты включают триптофан, фенилаланин, гистидин, глицин, цистеин, аланин, тирозин, серин, метионин, аспарагин, лейцин и их комбинации.
Неограничивающие примеры второй аминокислоты включают аспарагин, треонин, изолейцин, пролин, глутаминовую кислоту, аспарагиновую кислоту, гидроксипролин, аргинин, цистин, глутамин, лизин, валин, орнитин, глутамат мононатрия, таурин и их комбинации.
В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит аланин.
В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит глицин.
В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит гистидин.
В некоторых вариантах осуществления вкусоароматическая композиция может дополнительно содержать, по меньшей мере, один нуклеотид или нуклеотидное производное. Неограничивающие примеры нуклеотидов включают гуанозинмонофосфат (GMP), гуанозиндифосфат (GDP), гуанозинтрифосфат (GTP), аденозинмонофосфат (AMP), аденозиндифосфат (ADP), аденозинтрифосфат (ATP), цитидинмонофосфат (CMP), цитидиндифосфат (CDP), цитидинтрифосфат (CTP), инозинмонофосфат (IMP), инозиндифосфат (IDP), инозинтрифосфат (ITP), уридинмонофосфат (UMP), уридиндифосфат (UDP), уридинтрифосфат (UTP), тимидинмонофосфат TMP), тимидиндифосфат (TDP), тимидинтрифосфат (TTP), ксантозинмонофосфат (XMP), ксантозиндифосфат (XDP), ксантозинтрифосфат (XTP) и их комбинации.
В одном варианте осуществления вкусоароматическая композиция может дополнительно содержать нуклеотид, выбранный из группы, состоящей из гуанозинмонофосфата (GMP), инозинмонофосфата (IMP) и их комбинации.
В других вариантах вкусоароматическая композиция дополнительно содержит аланин и гуанозинмонофосфат (GMP).
В еще одних вариантах вкусоароматическая композиция дополнительно содержит глицин и гуанозинмонофосфат (GMP).
В еще одних вариантах вкусоароматическая композиция дополнительно содержит гистидин и гуанозинмонофосфат (GMP).
В еще одних вариантах вкусоароматическая композиция дополнительно содержит аланин и инозинмонофосфат (IMP).
В еще одних вариантах вкусоароматическая композиция дополнительно содержит глицин и инозинмонофосфат (IMP).
В еще одних вариантах вкусоароматическая композиция дополнительно содержит гистидин и инозинмонофосфат (IMP).
В еще одних вариантах осуществления вкусоароматическая композиция дополнительно содержит пролин и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
В еще одних вариантах осуществления вкусоароматическая композиция дополнительно содержит треонин и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
В некоторых вариантах осуществления вкусоароматическая композиция дополнительно содержит глутаминовую кислоту и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
В некоторых вариантах осуществления настоящее изобретение относится к пищевому продукту, содержащему вкусоароматическую композицию, как здесь описано, где вкусоароматическая композиция присутствует в концентрации примерно от 0,0001 мас.% до примерно 10 мас.% к общей массе пищевого продукта. В других вариантах осуществления вкусоароматическая композиция присутствует в концентрации примерно от 0,001 ppm до примерно 1000 ppm к общей массе пищевого продукта. В еще одних вариантах осуществления вкусоароматическая композиция присутствует в концентрации примерно от 1 пМ до примерно 1 М, или примерно от 1 мкМ до примерно 1 М к общей массе пищевого продукта.
В некоторых вариантах осуществления вкусоароматическая композиция присутствует в количестве, эффективном для повышения вкусовой привлекательности пищевого продукта, как определяется панелью дегустаторов.
В еще одних вариантах осуществления настоящее раскрытие обеспечивает способ усиления интенсивности вкуса умами в пищевом продукте, включающий смешивание пищевого продукта с вкусоароматическими композициями, описанными здесь, где вкусоароматическая композиция присутствует в концентрации примерно от 0,0001 мас.% до примерно 10 мас.% к общей массе смеси. В еще одних вариантах осуществления вкусоароматическая композиция присутствует в концентрации примерно от 0,001 ppm до примерно 1000 ppm к общей массе смеси. В еще одних вариантах осуществления вкусоароматическая композиция присутствует в концентрации примерно от 1 пМ до примерно 1 М, или примерно от 1 мкМ до примерно 1 М 0,001 ppm до примерно 1000 ppm к общей массе смеси.
В еще одних вариантах осуществления настоящее раскрытие обеспечивает способ усиления интенсивности вкуса умами в пищевом продукте, включающий смешивание пищевого продукта с вкусоароматическими композициями, описанными здесь, где вкусоароматическая композиция присутствует в количестве, эффективном для повышения вкусовой привлекательности пищевого продукта, как определяется панелью дегустаторов. В некоторых вариантах осуществления усиление интенсивности вкуса умами включает усиление послевкусия умами.
Настоящее раскрытие также обеспечивает способы получения пищевого продукта, содержащего вкусоароматическую композицию, описанную здесь, где способ включает термическую обработку предшественника пищевого продукта, где вкусоароматическую композицию получают во время термической обработки. Примеры термической обработки включают, например, стерилизацию, перегонку в реторте, экструзию, литье под давлением или их комбинации.
В некоторых вариантах осуществления пищевые продукты, описанные здесь, включают пищевые продукты для домашних животных, например, пищевые продукты для домашних кошек, такие как влажные и/или сухие пищевые продукты для домашних кошек. В других примерах пищевые продукты для домашних животных включают пищевые продукты для домашних собак, такие как влажные и/или сухие пищевые продукты для домашних собак.
В еще одних вариантах осуществления пищевые продукты, описанные здесь, включают пищевые продукты для человека.
Вышеизложенное в общих чертах довольно широко описывает признаки и технические преимущества настоящего изобретения, чтобы последующее подробное описание изобретения могло быть лучше понято. Дополнительные отличительные признаки и преимущества изобретения будут описаны ниже, которые образуют предмет формулы изобретения. Специалистам в данной области техники должно быть понятно, что описываемые концепция и конкретный вариант осуществления могут быть легко использованы в качестве основы для модификации и конструирования других структур для осуществления тех же задач данного изобретения. Специалистам в данной области техники должно быть понятно, что такие эквивалентные конструкции не выходят за рамки сущности и объема изобретения, изложенных в прилагаемой формуле изобретения. Новые признаки, которые, как полагают, являются характерными для изобретения, как в отношении его организации, так и способа функционирования, вместе с другими объектами и преимуществами будут лучше поняты из следующего описания.
Краткое описание фигур
На фиг. 1 представлены кривые зависимости доза-эффект для гуанозинмонофосфата (GMP), использованного в качестве испытуемого соединения в активации рецептора умами T1R1/T1R3 кошек in vitro. На данной фигуре (а также на фигурах 2-12, 14 и 38-45 представлены четыре кривые: испытуемое соединение в буфере, испытуемое соединение в буфере с 20 мМ аланина, испытуемое соединение в буфере с 0,2 мМ IMP и испытуемое соединение в 20 мМ аланина и 0,2 мМ IMP. На горизонтальных осях отложены концентрации испытуемого соединения, выраженные в мМ. На вертикальных осях находятся рецепторные ответы, измеренные в виде ΔF/F во флуоресцентном анализе или в виде Lum в люминесцентном анализе.
На фиг. 2 представлены кривые зависимости доза-эффект для 2'-деоксиаденозин-3',5'-O-бисфосфата.
На фиг. 3 представлены кривые зависимости доза-эффект для инозин-5'-дифосфата натриевой соли (IDP).
На фиг. 4 показаны кривые зависимости доза-эффект для 2'-/ 3'-O-(2-аминоэтилкарбамоил)аденозин-5'-монофосфата.
На фиг.5 показаны кривые зависимости доза-эффект для 2'-/ 3'-O-(2-аминоэтилкарбамоил)гуанозин-5'-O-монофосфата.
На фиг. 6 представлены кривые зависимости доза-эффект для инозинтрифосфата тринатриевой соли (ITP).
На фиг. 7 представлены кривые зависимости доза-эффект для N6-бензоиладенозин-5'-О-монофосфата.
На фиг. 8 представлены кривые зависимости доза-эффект для аденозин-5'-O-тиомонофосфата дилитиевой соли.
На фиг. 9 представлены кривые зависимости доза-эффект для аденозин-3',5'-дифосфата натриевой соли и аланина (1:1000).
На фиг. 10 представлены кривые зависимости доза-эффект для аденозин-3',5'-дифосфата натриевой соли и аланина (1:100).
На фиг. 11 представлены кривые зависимости доза-эффект для аденозин-3',5'-дифосфата натриевой соли и аланина (1:10).
На фиг. 12 представлены кривые зависимости доза-эффект для аденозин-3',5'-дифосфата натриевой соли.
На фиг. 13 представлены кривые зависимости доза-эффект для инозинмонофосфата (IMP) в активации T1R1/T1R3 кошки. IMP использовали в качестве контроля для экспериментов, представленных на фиг. 1-13 и 38-45.
На фиг. 14 представлена общая структурная модель домена VFT T1R1/T1R3 кошки, связанного с IMP и L-аланином. L-аланин и IMP показаны связанными в активном сайте между верхней и нижней глобулами домена VFT.
На фиг. 15 представлена модель домена VFT T1R1 кошки, связанного с L-аланином. L-аланин связывается с шарнирной областью домена VFT. Гипотетические взаимодействия водородной связью, солевым мостиком и катион-пи взаимодействия показаны между L-аланином и следующими аминокислотами T1R1: Thr149, Ser172, Tyr220, Thr148, Glu170 и Asp302. Взаимодействия показаны пунктирными линиями. Glu170 и Asp302 координируют цвиттерионный азот связанных аминокислот, одновременно с отсутствием электростатического связывания L-глутамата и L-аспарагиновой кислоты, нативных лигандов рецептора умами человека.
На фиг. 16 показана in silico модель домена VFT T1R1 кошки, связанная с GMP. Гипотетические взаимодействия водородной связью и солевым мостиком показаны пунктирными линиями между фосфатом GMP и His47, His71, Arg277 и Asn69; сахаром GMP и Asp302 и Ser306; и основанием GMP и Ser384, His308 и Ala380.
На фиг. 17 представлена in silico модель домена VFT T1R1 кошки, которая показывает, что Asp302 в T1R1 может одновременно координировать цвиттерионный азот скелета связанной аминокислоты (L-аланин слева) и молекулу сахара связанного нуклеотида (GMP справа).
На фиг. 18 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным аденозин-3',5'-дифосфатом.
На фиг. 19 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным XMP.
На фиг. 20 показана in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным N-ацетил-5'-GMP.
На фиг. 21 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным 2'-3' AEC-5'-AMP.
На фиг. 22 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным 5'd-GMPS.
На фиг. 23 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным 5'-O-2-тиодифосфатом.
На фиг. 24 представлена in silico модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным 6-тиогуанозин-5'-O-монофосфатом.
На фиг. 25 представлена in silico-модель домена VFT T1R1 кошки, которая показывает гипотетические взаимодействия между T1R1 и связанным CMP.
На фиг. 26 представлена in silico модель домена VFT T1R1 кошки, связанного с аденозин-3',5'-дифосфатом. Гипотетические взаимодействия водородной связью и солевым мостиком показаны пунктирными линиями между фосфатами аденозин-3',5'-дифосфата и His71, His47, Asn69, Arg281, Arg277, His308 и Ile309; сахаром аденозин-3',5'-дифосфата и Asp302 и Ser306; и основанием аденозин-3',5'-дифосфата и Ser384.
На фиг. 27 представлена in silico модель трансмембранного домена T1R1 кошки. Трансмембранное соединение метиловый эфир N-бензил-L-фенилаланина показан состыкованным в трансмембранной области T1R1.
На фиг. 28 представлена in silico модель метилового эфира N-бензил-L-фенилаланина, состыкованного в трансмембранной области T1R1.
На фиг. 29 представлена in silico модель 2-амино-N-фенетилбензамида, состыкованного в трансмембранной области T1R1.
На рис. 30 представлена in silico модель N-(2-(1H-индол-3-ил)этил) никотинамида, состыкованного в трансмембранной области T1R1.
На фиг. 31 представлена in silico модель 1-бензил-3-(2-(5-хлортиофен-2-ил)-2-оксоэтил)имидазолидин-2,4,5-триона, состыкованного в трансмембранной области T1R1.
На фиг. 32 представлена in silico модель этил(2,2-дифенилацетил)карбамата, состыкованного в трансмембранной области T1R1.
На фиг. 33 представлена in silico модель 2-((3,5-дихлорфенил)карбамоил)циклогексанкарбоновой кислоты, состыкованная в трансмембранной области T1R1.
На фиг. 34 представлена in silico модель N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида, состыкованного в трансмембранной области T1R1.
На фиг. 35 представлена in silico модель 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-триона, состыкованного в трансмембранной области T1R1.
На фиг. 36 представлена in silico модель производного 1Н-имидазо[4,5-с]пиридин-2(3H)-она, состыкованного в трансмембранной области T1R1.
На фиг. 37 представлены кривые зависимости доза-эффект для 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-триона.
На фиг. 38 представлены кривые зависимости доза-эффект для 1-(2-бромфенил)-3-((1R,2S)-2-гидрокси-2,3-дигидро-1Н-инден-1-ил) мочевины.
На фиг. 39 представлены кривые зависимости доза-эффект для N-(бензо[d][1,3]диоксол-5-ил)-2-пропилпентанамида.
На фиг. 40 представлены кривые зависимости доза-эффект для N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида.
На фиг. 41 представлены кривые зависимости доза-эффект для N-(2-амино-2-оксо-1-фенилэтил)-3-хлор-4,5-диметоксибензамида.
На фиг. 42 представлены кривые зависимости доза-эффект для (E)-3-(4-метоксифенил)-N-(пентан-3-ил)акриламида.
На фиг. 43 представлены кривые зависимости доза-эффект для 2-((5-(4-(метилтио)фенил)-2H-тетразол-2-ил)метил)пиридина.
На фиг. 44 представлены кривые зависимости доза-эффект для N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида в присутствии GMP и фенилаланина.
На фиг. 45 представлен график значений ΔF/F0 для N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида в присутствии GMP и фенилаланина.
На фиг. 46 представлены кривые зависимости доза-эффект для положительного и отрицательного контролей в активации T1R1/T1R3 кошки для экспериментов, представленных на фиг. 1-14 и 38-45. Кривые зависимости доза-эффект для аминокислот определяли в присутствии 0,2 мМ IMP. Кривые зависимости доза-эффект для нуклеотидов определяли в присутствии 20 мМ аланина.
На фиг. 47 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 48 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 49 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 50 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 51 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 52 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 53 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 54 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 55 представлено in silico моделирование трансмембранного соединения по одному примерному варианту осуществления раскрытого предмета изобретения, состыкованного в трансмембранной области T1R1.
На фиг. 56A-B показано: (A) активация T1R1/T1R3 под действием 1,3-дибензилпиримидин-2,4,6(1H,3H,5H)-триона в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (В) активация T1R1/T1R3 под действием одного 1,3-дибензилпиримидин-2,4,6(1H,3H,5H)-триона в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фигуре 57А-В показано: (A) активация T1R1/T1R3 под действием 4-бензил-3-бутил-1-(2-оксо-2-(пирролидин-1-ил)этил)-1Н-1,2,4-триазол-5(4Н)-она в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного 4-бензил-3-бутил-1-(2-оксо-2-(пирролидин-1-ил)этил)-1Н-1,2,4-триазол-5(4Н)-она в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 58А-В показано: (A) активация T1R1/T1R3 под действием 2-((3,5-дихлорфенил)карбамоил)циклогексанкарбоновой кислоты в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одной 2-((3,5-дихлорфенил)карбамоил)циклогексанкарбоновой кислоты в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или оюоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 59А-В показано: (A) активация T1R1/T1R3 под действием 4-ацетамидо-N-(1-(2-гидроксиэтил)-3-фенил-1Н-пиразол-5-ил)бензамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP, и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного 4-ацетамидо-N-(1-(2-гидроксиэтил)-3-фенил-1Н-пиразол-5-л)бензамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 60A-B показано: (A) активация T1R1/T1R3 под действием этилового эфира (дифенилацетил)карбаминовой кислоты в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного этилового эфира (дифенилацетил)карбаминовой кислоты в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 61А-В показано: (A) активация T1R1/T1R3 под действием N,N'-(бутан-1,4-диил)диникотинамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (В) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N,N'-(бутан-1,4-диил)диникотинамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих20 мМ L-аланина и 0,2 ММ IMP.
На фиг. 62A-B показано: (A) активация T1R1/T1R3 под действием N-фенэтилникотинамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N-фенэтилникотинамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 63A-B показано: (A) активация T1R1/T1R3 под действием 2-амино-N-фенэтилбензамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного 2-амино-N-фенэтилбензамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 64A-B показано: (A) активация T1R1/T1R3 под действием N-фенэтилбензо[d][1,3]диоксол-5-карбоксамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N-фенэтилбензо[d][1,3]диоксол-5-карбоксамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина И 0,2 мМ IMP.
На фиг. 65A-B показано: (A) активация T1R1/T1R3 под действием N-фенэтилбензамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N-фенэтилбензамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 66A-B показано: (A) активация T1R1/T1R3 под действием N-бензоил-DL-лейцинамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N-бензоил-DL-лейцинамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 67А-В показано: (A) активация T1R1/T1R3 под действием N-(2-(1Н-индол-3-ил)этил)никотинамида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (В) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного N-(1Н-индол-3-ил)этил)никотинамида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 68A-B показано: (A) активация T1R1/T1R3 под действием метилового эфира N-бензил-L-фенилаланина гидрохлорида в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного метилового эфира N-бензил-L-фенилаланина гидрохлорида в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На фиг. 69A-B показано: (A) активация T1R1/T1R3 под действием 6-тиогуанозин-5'-O-дифосфата (6-T-GDP) в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного 6-тиогуанозин-5'-O-дифосфата (6-T-GDP) в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 мМ L-аланина и 0,2 мМ IMP.
На рис. 70А-В показано: (A) активация T1R1/T1R3 под действием 6-хлорпуринрибозид-5'-О-трифосфата (6-Cl-PuTP) в присутствии 20 мМ L-аланина или 0,2 мМ IMP и (B) кривые зависимости доза-эффект для активации T1R1/T1R3 под действием одного 6-хлорпуринрибозид-5'-О-трифосфата (6-Cl-PuTP) в буфере или в присутствии 20 мМ L-аланина, 0,2 мМ IMP или обоих 20 ММ L-аланина и 0,2 мМ IMP.
На фиг. 71 показаны кривые зависимости доза-эффект для положительных и отрицательных контролей в активации T1R1/T1R3 кошки для экспериментов, представленных на фиг. 57-75. Кривые зависимости доза-эффект для нуклеотидов определяли в присутствии 20 мМ аланина.
На фиг. 72A-D показана активация T1R1/T1R3: (A) под действием трансмембранного соединения 1-бензил-3-(2-(3,4-дигидро-2H-бензо[b][1,4]диоксепин-7-ил)-2-оксоэтил)имидазолидин-2,4,5-триона (оценка агонистического профиля) и (B) и (C) в присутствии GMP и аланина (оценка профиля PAM). На (D) представлено графическое изображение данных, приведенных на (A) и (B). Трансмембранное соединение проявляло активность PAM.
На фиг. 73A-F показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения 1-бензил-3-(2-(5-хлортиофен-2-ил)-2-оксоэтил)имидазолидин-2,4,5-триона (оценка агонистического профиля), и (B) и (C) в присутствии GMP и аланина (оценка профиля PAM). На (D) представлено графическое изображение данных, приведенных на (A) и (B). На (E) и (F) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки). Трансмембранное соединение проявляло активность PAM.
На фиг. 74A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка профиля PAM). На (С) представлено графическое изображение данных, приведенных на (A) и (B). На (D) и (E) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность PAM.
На фиг. 75A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения метилового эфира N-бензил-L-фенилаланина гидрохлорида (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка профиля PAM). На (С) представлено графическое изображение данных, прведенных на (A) и (B). На (D) и (E) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность агониста и PAM.
На фиг. 76A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения метилового эфира N-бензил-D-фенилаланина гидрохлорида (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка PAM профиля). На (С) представлено графическое изображение данных, приведенных на (а) и (В). На (D) и (E) представлены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность агониста и PAM.
На фиг. 77A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения метилового эфира бензил-L-лейцина гидрохлорида (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка PAM профиля). На (С) представлено графическое изображение данных, приведенных на (A) и (B). На (C) и (E) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность агониста и PAM.
На фиг. 78A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения метил-2-бензиламино-2-фенилацетата (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка PAM профиля). На (С) представлено графическое изображение данных, прведенных на (A) и (B). На (D) и (E) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность агониста и PAM.
На фиг. 79A-E показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения бензилового эфира L-фенилаланина гидрохлорида (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка PAM профиля). На (С) представлено графическое изображение данных, прведенных на (A) и (B). На (D) и (E) приведены кривые зависимости доза-эффект для трансмембранного соединения, при этом концентрация GMP поддерживалась постоянной и концентрацию Ala изменяли, и когда концентрация Ala поддерживалась постоянной, то изменяли концентрацию GMP, в клетках, экспрессирующих T1R1/T1R3 (индуцированные клетки, (D)), и контрольных клетках, которые не экспрессировали T1R1 (неиндуцированные клетки, (E)). Трансмембранное соединение проявляло активность агониста и PAM.
На фиг. 80A-B показана активация T1R1/T1R3: (A) под действием одного трансмембранного соединения 1,3-дибензилпиримидин-2,4,6(1H,3H,5H)-триона (оценка агонистического профиля) и (B) в присутствии GMP и аланина (оценка PAM профиля). Трансмембранное соединение проявляло активность агониста.
На фиг. 81 представлена последовательность нуклеиновой кислоты рецептора T1R1 кошки (SEQ ID NO: 1).
На фиг. 82 представлена аминокислотная последовательность рецептора T1R1 кошки (SEQ ID NO: 2).
На фиг. 83 представлена последовательность нуклеиновой кислоты рецептора T1R3 кошки (SEQ ID NO: 3).
На фиг. 84 представлена аминокислотная последовательность рецептора T1R3 кошки (SEQ ID NO: 4).
Подробное описание изобретения
К настоящему времени остается необходимость в модификаторе вкуса, который может обеспечить требуемый уровень вкуса умами для увеличения и/или повышения вкусовой привлекательности различных пищевых продуктов для домашних кошек. Настоящая заявка относится к вкусоароматическим композициям, которые содержат, по меньшей мере, одно нуклеотидное производное и/или трансмембранное соединение. Вкусоароматические композиции могут быть использованы для повышения вкусовой привлекательности и/или улучшения или изменения вкуса различных пищевых продуктов для домашних животных, таких как питательно полноценный корм для домашних животных. В некоторых вариантах осуществления вкусоароматические композиции могут быть использованы для усиления вкуса умами пищевого продукта для домашних животных. Вкусоароматические композиции могут дополнительно содержать комбинации соединений, включающие нуклеотиды и/или аминокислоты, и могут быть добавлены к пищевым продуктам для домашних животных в различных форматах системы доставки.
1. Определения
Термины, использованные в данном описании, как правило, имеют свои обычные значения в данной области техники в контексте настоящего изобретения и в конкретном контексте, где используется каждый термин. Некоторые термины обсуждаются ниже или в другом месте по тексту описания для предоставления дополнительных указаний практику при описании композиций и способов по изобретению, и как осуществить их приготовление и применение.
Как здесь используется, применение артикля «a» или «an», при использовании в сочетании с термином «содержащий» в формуле изобретения и/или описании может означать «один», но также согласуется со значением «один или более», «по меньшей мере, один» и «один или более чем один». Кроме того, термины «имеющий», «включающий», «содержащий» и «состоящий» являются взаимозаменяемыми, и специалист в данной области техники понимает, что эти термины являются открытыми.
Термин «примерно» или «приблизительно» означает допустимый диапазон погрешностей для конкретного значения, определенного специалистом в данной области техники, что будет частично зависеть от того, как измеряется или определяется значение, то есть ограничений измерительной системы. Например, «примерно» может означать в пределах 3 или более 3 стандартных отклонений в соответствии с практикой в данной области техники. Альтернативно, «примерно» может означать диапазон до 20%, предпочтительно до 10%, более предпочтительно до 5% и более предпочтительно еще до 1% от заданного значения. Альтернативно, особенно в отношении биологических систем или процессов, данный термин может означать порядок величины, предпочтительно в пределах 5 раз и более предпочтительно в пределах 2 раз от значения.
Как здесь используется, «вкус» относится к ощущению, вызванному активацией или ингибированием рецепторных клеток в ротовой полости субъекта. В некоторых вариантах осуществления вкус может быть выбран из группы, состоящей из сладкого, кислого, соленого, горького, кокуми и умами. В некоторых вариантах осуществления «вкус» может включать вкус, придаваемый образованием свободных жирных кислот. См., например, Cartoni et al., J. of Neuroscience, 30 (25): 8376-8382 (2010), содержание данной публикации включено сюда посредством ссылки. В некоторых вариантах осуществления вкус у субъекта вызывается «тастантом». В некоторых вариантах осуществления тастант вкуса является синтетическим тастантом. В некоторых вариантах осуществления тастант получают из природного источника.
Как здесь используется, «профиль вкуса» относится к комбинации вкусов, например, таких как один или более из сладкого, кислого, соленого, горького, умами, кокуми и вкуса, появляющегося за счет образования свободных жирных кислот. В некоторых вариантах осуществления профиль вкуса получают с использованием одного или более тастантов, которые присутствуют в композиции в одинаковых или разных концентрациях. В некоторых вариантах осуществления профиль вкуса относится к интенсивности вкуса или комбинации вкусов, например, сладкого, кислого, соленого, горького, умами, кокуми и вкуса, появляющегося за счет образования свободных жирных кислот, которые детектируются субъектом или любым тестом, известным в данной области техники. В некоторых вариантах осуществления модификация, изменение или варьирование комбинации вкусов в профиле вкуса может изменить сенсорный опыт субъекта.
В некоторых вариантах осуществления термин «послевкусие» относится к интенсивности вкуса пищевого продукта, который воспринимается после удаления пищевого продукта изо рта или ротовой полости.
Как здесь используется, термин «вкусоароматическое вещество» относится к одному или более сенсорным стимулам, например, таким как один или более вкусовых (пищевых), ароматных (обонятельных), осязательных (тактильных) и температурных (термических) стимулов. В некоторых неограничивающих вариантах осуществления сенсорный опыт субъекта, подвергшийся воздействию вкусоароматического вещества, может быть классифицирован как специфический опыт для конкретного вкусоароматического вещества. Например, вкусоароматическое вещество может быть идентифицировано субъектом как имеющее, не ограничиваясь этим, цветочный, цитрусовый, ягодный, ореховый, карамельный, шоколадный, перечный, копченый, сырный, мясной вкус и т.д.. Как здесь используется, вкусоароматическая композиция может быть выбрана из жидкости, раствора, сухого порошка, спрея, пасты, суспензии и любой их комбинации. Вкусоароматическое вещество может быть природной композицией, искусственной композицией, идентичной природной или любой их комбинацией.
Как здесь используется взаимозаменяемо, «аромат» и «запах» относятся к обонятельной реакции на стимул. Например, и не в качестве ограничения, аромат может быть создан ароматическими веществами, которые воспринимаются обонятельными рецепторами обонятельной системы.
Как здесь используется, термин «профиль вкуса» относится к комбинации сенсорных стимулов, например вкусов, таких как сладкий, кислый, горький, соленый, умами, кокуми, и вкус, придаваемый свободными жирными кислотами, и/или обонятельных, осязательных и/или термических стимулов. В некоторых вариантах осуществления профиль вкуса включает одно или более вкусоароматических веществ, которые способствуют возникновения сенсорного опыта у субъекта. В некоторых вариантах осуществления модификация, изменение или варьирование комбинации стимулов в профиле вкуса может изменить сенсорный опыт у субъекта.
Как здесь используется, термин «смешивание», например, «смешивание вкусоароматической композиции или ее комбинаций по настоящему изобретению с пищевым продуктом» относится к способу, где вкусоароматическая композиция или отдельные компоненты вкусоароматической композиции смешиваются с или добавляются к готовому продукту или смешиваются с некоторыми или всеми компонентами продукта во время получения продукта или некоторой комбинации этих стадий. При использовании в контексте смешивания термин «продукт» относится к продукту или любому из его компонентов. Эта стадия смешивания может включать способ, выбранный из стадии добавления вкусоароматической композиции к продукту, распыления вкусоароматической композиции на продукт, нанесения вкусоароматической композиции на продукт, суспендирования продукта во вкусоароматической композиции, окрашивания вкусоароматической композицией продукта, намазывания вкусоароматической композиции на продукт, инкапсулирования продукта вкусоароматической композицией, смешивания вкусоароматической композиции с продуктом и любой их комбинации. Вкусоароматическая композиция может представлять раствор, жидкий, сухой порошок, спрей, пасту, суспензию и любую их комбинацию.
В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения вкусоароматической композиции могут быть получены во время термической обработки пищевого продукта для домашних животных, например, стерилизации, перегонки в реторте, литья под давлением и/или экструзии, из соединений-предшественников, присутствующих в пищевом продукте для домашних животных. В некоторых вариантах осуществления нуклеотидное производное и/или трансмембранное соединение вкусоароматической композиции могут быть получены во время обработки пищевого продукта для домашних животных, и дополнительные компоненты вкусоароматической композиции, например, нуклеотид и/или аминокислоту, можно добавить к пищевому продукту для домашних животных путем смешивания.
Как здесь используется, термин «ppm» означает части на миллион и является относительным весовым параметром. Часть на миллион представляет собой микрограмм на грамм, например, если компонент присутствует в количестве 10 ppm, то это означает 10 микрограмм конкретного компонента присутствует в 1 грамме общей смеси.
Как здесь используется, термин «вкусовая привлекательность» может относиться к общей готовности человека или животного, не относящегося к человеку, например, животного-компаньона, потреблять определенный пищевой продукт. Повышение «вкусовой привлекательности» пищевого продукта может привести к увеличению потребления и принятия пищи человеком или животным, отличным от человека, для гарантии того, что человек или животное, не относящееся к человеку, потребляет «здоровое количество» пищи. Как здесь используется, термин «здоровое количество» относится к количеству, которое позволяет человеку или животному, не относящемуся к человеку, поддерживать или достигать приема пищи, способствующего его общему здоровью в отношении микронутриентов, макронуриентов и калорий, например, как указано в «Mars Petcare Essential Nutrient Standards». В некоторых вариантах осуществления «вкусовая привлекательность» может означать относительное предпочтение человеком или животным, не относящимся к человеку, одного пищевого продукта над другим. Например, когда человек или животное, не относящееся к человеку, демонстрирует предпочтение одного из двух или более пищевых продуктов, то предпочтительный пищевой продукт является более «привлекательным» и имеет «улучшенную вкусовую привлекательность». В некоторых вариантах осуществления относительная вкусовая привлекательность одного пищевого продукта по сравнению с одним или более другими пищевыми продуктами может быть определена, например, расположенных рядом вариантов сравнения со свободным выбором, например, путем относительного потребления пищевых продуктов или других соответствующих показателей предпочтения, указывающих на вкусовые качества. Вкусовая привлекательность может определяться стандартным протоколом тестирования, где животное имеет одинаковый доступ к обоим пищевым продуктам, таким как тест под названием «тест с двумя кормушками» или «сравнительный тест». Такое предпочтение может возникать в результате любого ощущения у животного, но может быть связанно, среди прочего, со вкусом, послевкусием, запахом, ощущением во рту и/или текстурой.
Термин «пищевой продукт» или «пищевой продукт для домашних животных» означает продукт или композицию, предназначенные для потребления животным-компаньоном, например, кошками, собаками, морскими свинками, кроликами, птицами и лошадьми. Например, но не в качестве ограничения, животное-компаньон может быть «домашним» котом, например, Felis domesticus. В некоторых вариантах осуществления животное-компаньон может быть «домашней» собакой, например, Canis lupus familiaris. «Пищевой продукт» или «пищевой продукт для домашних животных» включает любой продукт, корм, закуску, пищевую добавку, жидкость, напитки, лакомство, игрушку (жевательные и/или съедобные игрушки), заменитель пищи или заместитель пищи.
Термин «пищевой продукт для человека» или «продукт питания человека» означает продукт или композицию, предназначенную для потребления человеком. «Пищевой продукт для человека» или «продукт питания человека» включает любой продукт, корм, закуску, пищевую добавку, жидкость, напитки, лакомство, игрушку (жевательные и/или съедобные игрушки), заменитель пищи или заместитель пищи.
В некоторых вариантах осуществления «пищевой продукт» включает пищевые продукты для человека и/или домашних животных.
Как здесь используется, термин «питательно полноценный» относится к пищевому продукту, например, пищевому продукту для домашних животных, который содержит все известные необходимые питательные вещества для предполагаемого реципиента пищевого продукта в соответствующих количествах и пропорциях, основанных, например, на рекомендациях признанных или компетентных органов в области кормления животных-компаньонов. Следовательно, такие продукты могут служить в качестве единственного источника питания для поддержания жизни без добавления дополнительных источников питания.
Как здесь используется, термин «вкусоароматическая композиция» относится, по меньшей мере, к одному соединению или его биологически приемлемой соли, которое модулирует, включая усиление, увеличение, потенцирование, уменьшение, подавление или индуцирование вкусов, запахов, ароматов и/или текстур природного или синтетического тастанта, вкусоароматического агента, профиля вкуса, профиля аромата и/или профиля текстуры у животного или человека. В некоторых вариантах осуществления вкусоароматическая композиция включает комбинацию соединений или их биологически приемлемых солей. В некоторых вариантах осуществления вкусоароматическая композиция включает один или более эксципиентов.
Как здесь используется, термин «агонист» относится, по меньшей мере, к одному соединению или его биологически приемлемой соли, которое модулирует, включая усиление, увеличение, потенцирование, уменьшение, подавление или индуцирование активности рецептора, с которым оно связывается или взаимодействует иным образом. В некоторых вариантах осуществления этот термин используется для описания соединений, которые действуют самостоятельно для активации рецептора, или для описания соединений, представляющих «положительный аллостерический модулятор» (также известных как «РАМ»), которые положительно усиливают действие других агонистов.
Как здесь используется, термин «синергия», «синергетический» или «синергетический эффект» относится к эффекту, создаваемому двумя или более отдельными компонентами, где общий эффект, производимый этими компонентами при их использовании в комбинации, больше, чем сумма отдельных эффектов каждого компонента, действующего самостоятельно. Как здесь используется, термин «синергически эффективный» относится к любому объединенному количеству нуклеотидного производного и/или трансмембранного соединения, и дополнительного соединения (например, аминокислоты, нуклеотида или соединения, которое связывается с трансмембранными доменами T1R1 или T1R3 (см., например, Zhang et al., Proc. Natl. Acad. Sci. USA, 2008, Dec. 30, 105(52): 20930-4, Epub 2008 Dec 22)), которое проявляет синергическую активацию рецептора T1R1/T1R3 или повышает вкусовую привлекательность корма для домашних животных.
Термин «алкил» относится к линейной или разветвленной С1-С20 (предпочтительно С1-С6) углеводородной группе, состоящей исключительно из атомов углерода и водорода, не содержащей ненасыщенности и присоединенной к остальной части молекулы простой связью, например, метил, этил, н-пропил, 1-метилэтил (изопропил), н-бутил, н-пентил, 1,1-диметилэтил (трет-бутил).
Термин «алкенил» относится к C2-C20 (предпочтительно C2-C12) алифатической углеводородной группе, содержащей, по меньшей мере, одну углерод-углеродную двойную связь, и которая может иметь прямую или разветвленную цепь, например, этенил, 1-пропенил, 2-пропенил (аллил), изопропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил.
Термин «алкинил» относится к алифатической углеводородной группе С2-С20 (предпочтительно С2-С12), содержащей, по меньшей мере, одну тройную углерод-углеродную связь, и которая может иметь прямую или разветвленную цепь, например, этинил, 1-пропинил, 2-пропинил.
Термин «циклоалкил» означает ненасыщенную, неароматическую моно- или полициклическую углеводородную кольцевую систему (содержащую, например, C3-C6), такую как циклопропил, циклобутил, циклопентил, циклогексил. Примеры полициклических циклоалкильных групп (содержащих, например, C6-C15) включают пергидронафтил, адамантил и норборнил с мостиковой циклической группой или спиробициклические группы, например, спиро(4,4)нон-2-ил.
Термин «циклоалкил» относится к циклоалкилу, как определено выше, непосредственно присоединенному к алкильной группе, как определено выше, что приводит к созданию стабильной структуры, такой как циклопропилметил, циклобутилэтил или циклопентилэтил.
Термин «простой эфир» относится к алкильной группе или циклоалкильной группе, как определено выше, содержащей, по меньшей мере, один атом кислорода, включенный в алкильную цепь, например, метилэтиловый эфир, диэтиловый эфир, тетрагидрофуран. Такие группы также могут быть описаны как алкоксиалкильные или алкоксициклоалкильные группы.
Термин «аминоалкил» относится к алкильной группе или циклоалкильной группе, как определено выше, содержащей, по меньшей мере, один атом азота, например, н-бутиламин и тетрагидрооксазин.
Термин «арил» относится к ароматическим радикалам, содержащим примерно от 6 до примерно 14 атомов углерода, таким как фенил, нафтил, тетрагидронаптил, инданил, бифенил.
Термин «арилалкил» относится к арильной группе, как определено выше, непосредственно связанной с алкильной группой, как определено выше, например, -CH2C6H5 и -C2H4C6H5.
Термин «гетероциклический» относится к стабильному 3-15-членному циклическому радикалу, который состоит из атомов углерода и одного или более, например, от одного до пяти гетероатомов, выбранных из группы, состоящей из атома азота, кислорода и серы. Для целей этой заявки гетероциклический кольцевой радикал может представлять моноциклическую или бициклическую кольцевую систему, которая может включать конденсированные или мостиковые кольцевые системы, и атомы азота, углерода, кислорода или серы в гетероциклическом кольцевом радикале могут быть необязательно окислены до различного состояния окисления. Кроме того, атом азота может быть необязательно кватернизирован; и кольцевой радикал может быть частично или полностью насыщенным или кольцевой радикал может быть полностью ненасыщенным (то есть гетероароматическим или гетероарильным ароматическим). Гетероциклический кольцевой радикал может быть присоединен к основной структуре по любому гетероатому или атому углерода, что приводит к образованию стабильной структуры.
Термин «гетероарил» относится к гетероциклическому кольцу, в котором кольцо является ароматическим.
Термин «гетероарилалкил» относится к гетероарильному циклическому радикалу, как определено выше, непосредственно связанному с алкильной группой. Гетероарилалкильный радикал может быть присоединен к основной структуре по любому атому углерода в алкильной группе, что приводит к образованию стабильной структуры.
Термин «гетероциклил» относится к гетероциклическому кольцевому радикалу, как определено выше. Гетероциклический кольцевой радикал может быть присоединен к основной структуре по любому гетероатому или атому углерода, что приводит к образованию стабильной структуры.
В некоторых вариантах осуществления термин «рецептор умами» относится к рецептору, сопряженному с G-белком (GPCR), например, GPCR T1R1/T1R3. Рецептор умами может представлять, например, рецептор умами кошки, собаки, человека или млекопитающего, не относящегося к человеку.
В некоторых вариантах осуществления T1R1 кошки представляет белок, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, или последовательность, по меньшей мере, на 99, 98, 97, 96, 95, 90, 85 или 80%, гомологичную ей (как здесь используется термин «гомология», ее можно определить с использованием стандартного программного обеспечения, такого как BLAST или FASTA), и кодированный, например, нуклеиновой кислотой, содержащей последовательность, показанную в SEQ ID NO: 1, или последовательность, по меньшей мере, на 99, 98, 97, 96, 95, 90, 85 или 80% гомологичную ей (как здесь используется термин «гомология», ее можно определить с использованием стандартного программного обеспечения, такого как BLAST или FASTA).
В некоторых вариантах осуществления T1R3 кошки представляет собой белок, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 4, или последовательность, по меньшей мере, на 99, 98, 97, 96, 95, 90, 85 или 80%, гомологичную ей (как здесь используется термин «гомология», ее можно определить с использованием стандартного программного обеспечения, такого как BLAST или FASTA), и кодированный, например, нуклеиновой кислотой, содержащей последовательность, показанную в SEQ ID NO: 3, или последовательность, по меньшей мере, на 99, 98, 97, 96, 95, 90, 85 или 80% гомологичную ей (как здесь используется термин «гомология», ее можно определить с использованием стандартного программного обеспечения, такого как BLAST или FASTA).
2. Нуклеотидные производные
Настоящее раскрытие относится к вкусоароматическим композициям, которые содержат, по меньшей мере, одно нуклеотидное производное. В некоторых вариантах осуществления нуклеотидное производное представляет соединение, усиливающее вкус умами. Нуклеотидные производные, раскрытые здесь, идентифицировали с помощью in silico моделирования нуклеотидных производных в связывающем кармане рецептора T1R1/T1R3 кошки («рецептора умами»). Вкусоароматические композиции могут использоваться для повышения или модификации вкусовой привлекательности, вкуса или аромата пищевого продукта для домашних животных. Вкусоароматические композиции могут включать комбинации соединений, например, комбинации одного или более нуклеотидных производных и/или одной или более аминокислот, и/или одного или более нуклеотидов и/или одного или более трансмембранных соединений, как здесь описано, и могут быть добавлены в композиции пищевых продуктов для домашних животных в различных форматах системы доставки.
В некоторых вариантах осуществления нуклеотидное производное может представлять соединение, приведенное в таблицах 2 и 5-13 ниже.
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-1, имеющее следующую структуру:
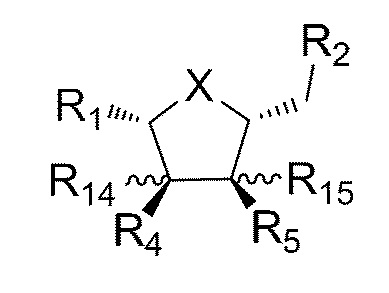
где R1 выбран из группы, состоящей из замещенного или незамещенного пурина или замещенного или незамещенного пиримидина;
где R2 выбран из монофосфата, дифосфата, трифосфата,
OP(W)(OH)2, -OP(W)(OH)OP(W)(OH)2, -OP(W)(OH)OP(W)(OH)OP(W)(OH)2, -OS(O)2арил(H), -OS(O)2арил(CH3), -P(W)(OH)2, -OP(W)(OH)OS(O)2(OH), -OP(W)(OH)Z, -P(W)(OH)OP(W)(OH)2, -O(CH2)1-4OP(W)(OH)2, -OS(W)(OH)2, -OP(W)(OH) CH2OP(W)(OH)2, -OP(W)(OH)OP(W)O(CH2)1-4R18, -(CH2)0-4COOH, -(CH2)0-4S(O)(OH)2, -(CH2)0-4C(O)NHOH и -(CH2)0-4B(OH)2;
где Х выбран из O, S, N (R3) и CH2;
где W выбран из O и S;
где R3 выбран из H и CH3;
где R4, R5, R14, R15, R18 независимо выбраны из H, OH, SH, CH2, CH3, OR6, SR6, CH2CH3, разветвленного или неразветвленного низшего (C1-C6) алкила, XC(O)низшего алкила, -XC(O)CH2Ph, -P(W)(OH)2, -XC(O)PhR11, -OP(O)(OH)O, OCH3, N(R11,R17), -O(C)nR11, R17O-, N(H или независимо низший алкил)2-3 и COOR11, -OC(W)NH(CH2)1-6NH2, -OC(W)NH(CH2)1-6R44,
где R44 представляет H, OH, SH, CH2, CH3, OR6, SR6, CH2CH3, разветвленный или неразветвленный низший алкил (C1-C6), XC(O)низший алкил, -XC(O)CH2Ph, -P(W)(OH)2, - XC(O)PhR11, -OP(O)(OH)O, OCH3, N(R11, R17), -O(C)nR11, R17O-, N(H или независимо низший алкил)2-3 или COOR11, -OC(W)NH(CH2)1-6NH2;
где Z выбран из пиперидина, морфолина, пиперазина, N-метилпиперазина, N(R16)(R17); и
где R6, R11, R16 и R17 независимо выбраны из H, OH, SH, CH2, CH3, OCH3, COOR, N(R12)(R13), CH2CH3, разветвленного и неразветвленного низшего алкила (C1-C6), XC(O)низшего алкила, -XC(O)CH2Ph, -P(W)(OH)2, -XC(O)PhR12, -OP(O)(OH)O, OCH3, N(R12,R13), -O(C)nR12, R13O-, N(H или независимо низший алкил)2-3 и COOR12; и
где R12 и R13 независимо выбраны из H, OH, SH, CH2, CH3, OCH3 и CH2CH3.
В некоторых вариантах осуществления R1 в формуле Nt-1 выбран из:
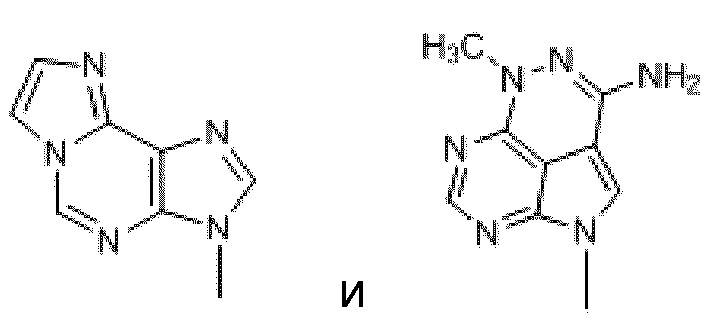 .
.
В некоторых вариантах осуществления R1 в формуле Nt-1 выбран из соединений, приведенных в таблице 1.
Группа R1 в нуклеотидных производных формулы Nt-1
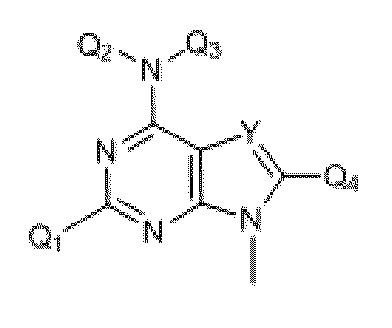
где Q6 выбран из Me и Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразвевленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 and -CH2CH2CH2CH2-; и
где Y выбран из C или N.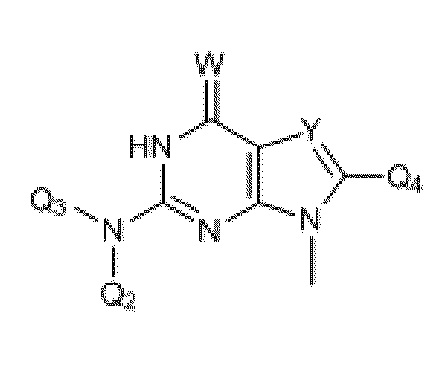
где Q6 выбран из Me и Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где Y или W независимо выбраны из O, S, C или N.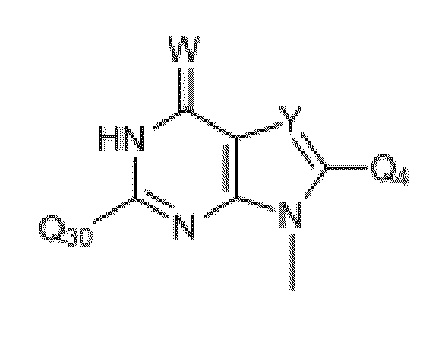
где Q6 выбран из Me и Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где Y или W независимо выбраны из O, S, C или N.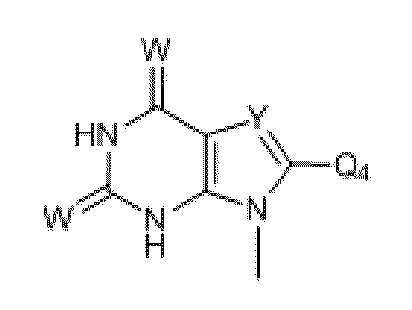
где Q6 выбран из Me and Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где Y или W независимо выбраны из O, S, C или N.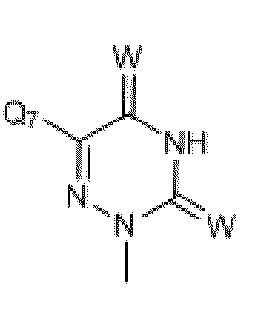
где Q6 выбран из Me and Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где W выбран из O, S, C или N.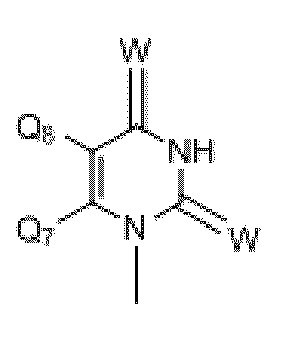
где Q6 выбран из Me and Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где W выбран из O, S, C или N.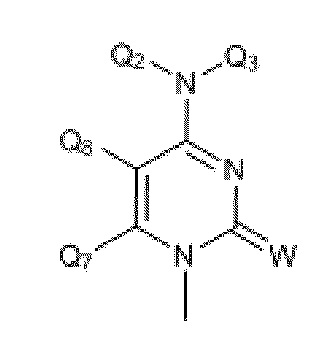
где Q6 выбран из Me and Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где W выбран из O, S, C или N.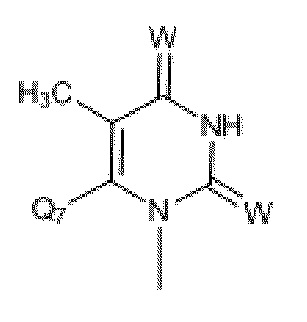
где Q6 выбран из Me и Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где W выбран из O, S, C или N.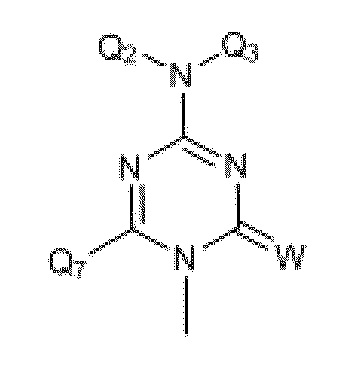
где Q6 выбран из Me and Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-; и
где W выбран из O, S, C или N.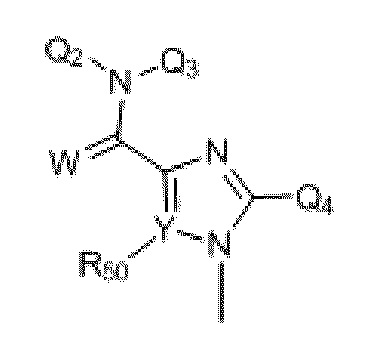
где Q6 выбран из Me и Ph;
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-;
где W выбран из O и S;
где Y выбран из C и N, и когда Y представляет атом азота, то R50 отсутствует, и когда Y представляет атом углерода, то R50 выбран из H, CH3, -SCH3, -N(R19)(R20), F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), арила, -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, COOH, c-C4H7, c-C5H9, c-C6H10 и -CH2CH2CH2CH2-;
где Q6 выбран из Me и Ph; и
где R19 и R20 независимо выбраны из H, CH3, -SCH3, F, Cl, Br, I, -OCH3, O, S, разветвленного или неразветвленного низшего алкила (C1-C10), -(CH2)1-4арила, SCH3, S(O)1-2Q6, COOCH3, COOEt, -(CH2)0-4Ph, c-C4H7, c-C4H7, c-C5H9, c-C6H10, -CH2CH2CH2CH2 и арила.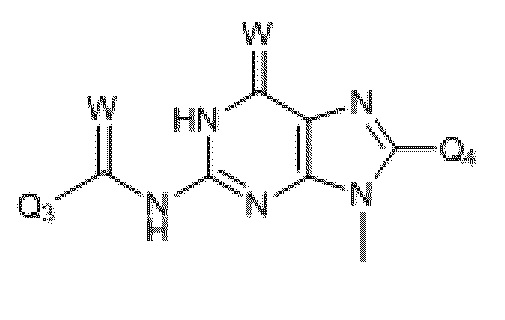
где Q3 выбран из замещенного или незамещенного, разветвленного или неразветвленного низшего алкила (C1-C15), замещенного или незамещенного арила, замещенного или незамещенного фурана, замещенного или незамещенного тиофена, замещенного или незамещенного фенила, замещенного или незамещенного пиридина и замещенного или незамещенного нафталена; и
где Q4 выбран из O, S, CH3, SCH3, H, Br, F, Cl и I.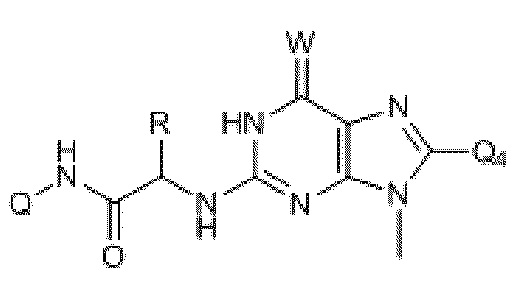
где R получен из боковых цепей 21 встречающихся в природе аминокислот;
где Q выбран из замещенного или незамещенного, разветвленного или неразветвленного низшего алкила (C1-C15), замещенного или незамещенного арила, замещенного или незамещенного фурана, замещенного или незамещенного тиофена, замещенного или незамещенного фенила, замещенного или незамещенного пиридина и замещенного или незамещенного нафталена; и
где Q4 выбран из O, S, CH3, SCH3, H, Br, F, Cl и I.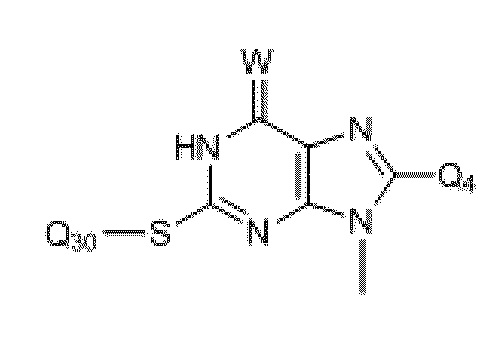
где Q30 выбран из замещенного или незамещенного, разветвленного или неразветвленного низшего алкила (C1-C15), замещенного или незамещенного арила, замещенного или незамещенного фурана, замещенного или незамещенного тиофена, замещенного или незамещенного фенила, замещенного или незамещенного пиридина и замещенного или незамещенного нафталена; и
где Q4 выбран из O, S, CH3, SCH3, H, Br, F, Cl и I.
Заместители в замещенных группах, описанных здесь, таких как «замещенный алкил», «замещенный арил», «замещенный фуран», «замещенный тиофен», «замещенный алкил», «замещенный фенил», «замещенный пиримидин» или «замещенный нафтален» могут быть одинаковыми или различными с одним или более, выбранных из групп, описанных в настоящей заявке, и атома водорода, атома галогена, метила, амидо, ацетила, нитро (-NO2), гидроксила (-ОН), оксо (=O), тио (=S), OCH3, метилендиокси, CN, NO2, COOH, SO3H, S(O)1-2CH3, S(O)1-2арила, SCH3, OH, N(R)1-2, COOCH3, OC(O)CH3, SH, сульфонила, сульфонамидо, сульфата, циано, азидо, трифторметила (-CF3), метокси (-OCH3), трет-бутилкарбамат (-Boc) или необязательно замещенных групп, выбранных из алкила, циклоалкила, алкенила, алкинила, алкокси, арила, арилокси, арилалкил, простого эфира, карбокси, гидроксила, гетероарила, гетероарилалкила, сульфонила и гетероциклила. «Замещенная» функциональная группа может иметь один или более заместителей.
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-2, имеющее следующую структуру:
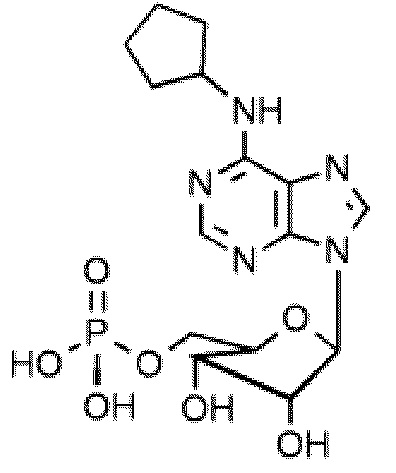
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-3, имеющее следующую структуру:
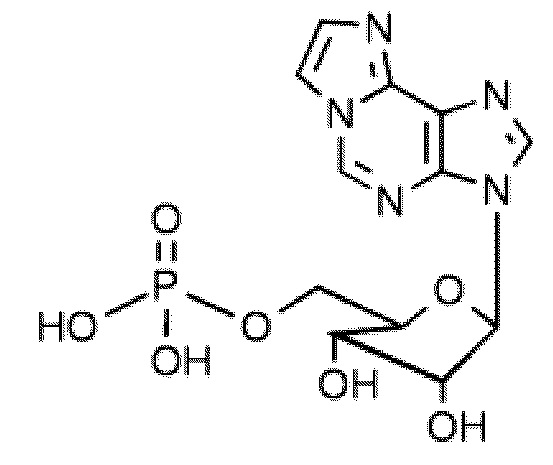
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-4, имеющее следующую структуру:
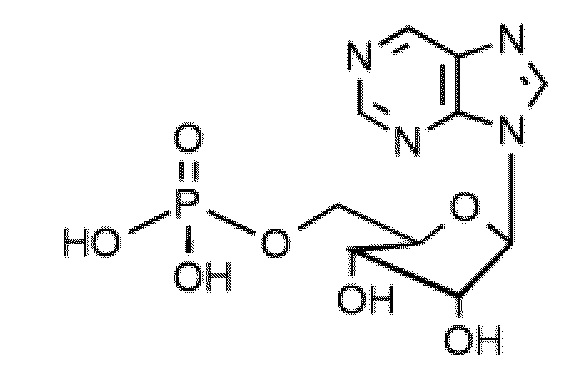
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-5, имеющее следующую структуру:
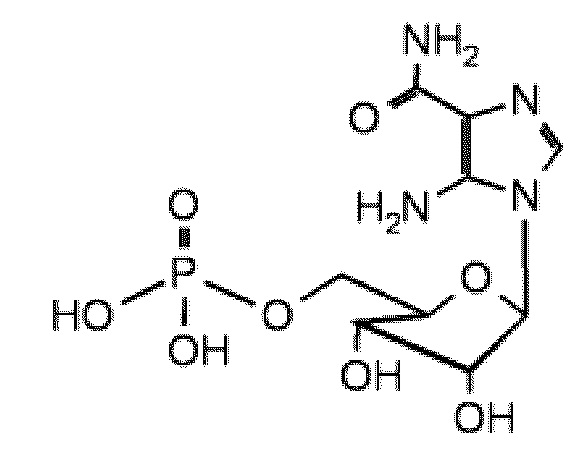
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-6, имеющее следующую структуру:
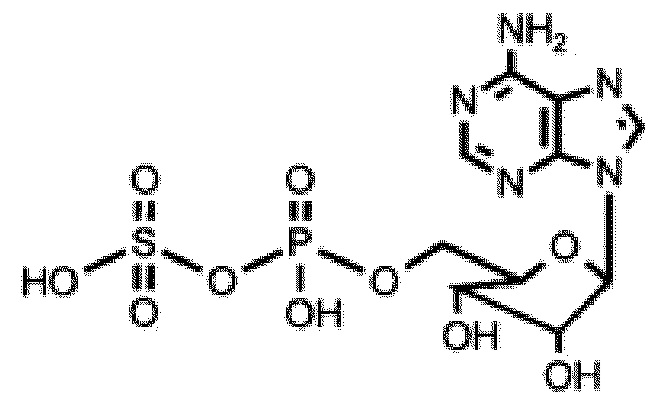
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-7, имеющее следующую структуру:
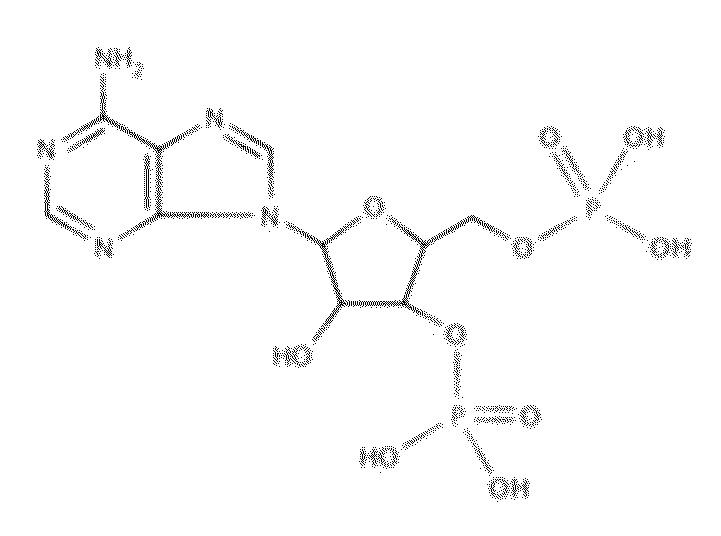
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-8, имеющее следующую структуру:
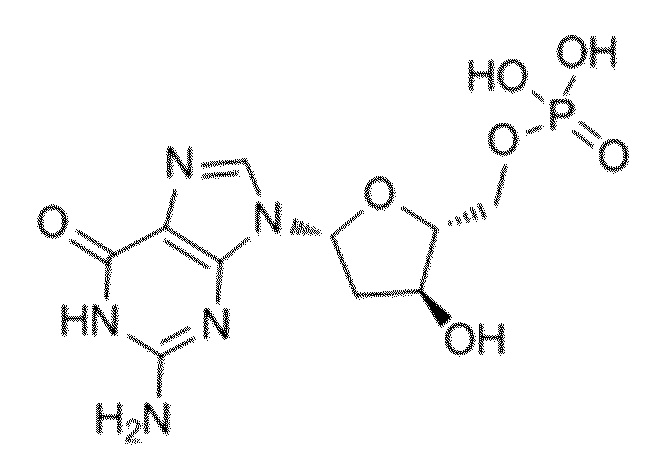
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-9, имеющее следующую структуру:
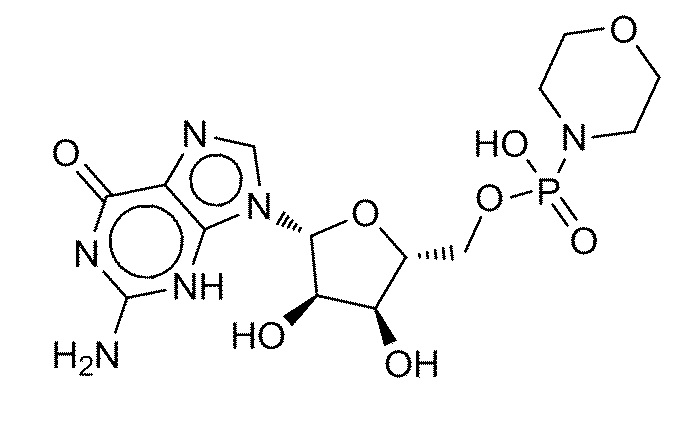
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-10, имеющее следующую структуру:
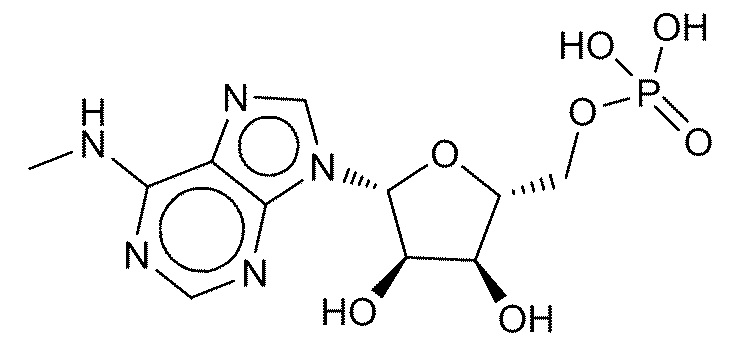
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-11, имеющее следующую структуру:
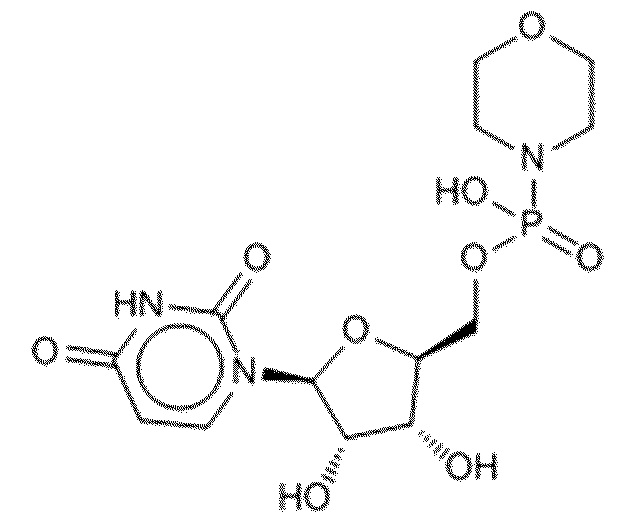
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-12, имеющее следующую структуру:
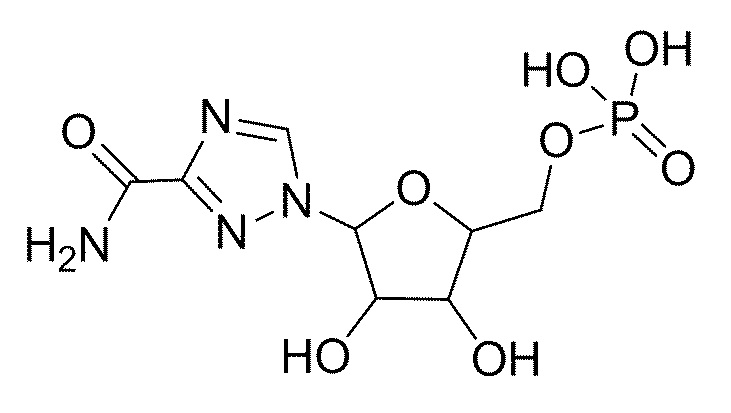
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-13, имеющее следующую структуру:
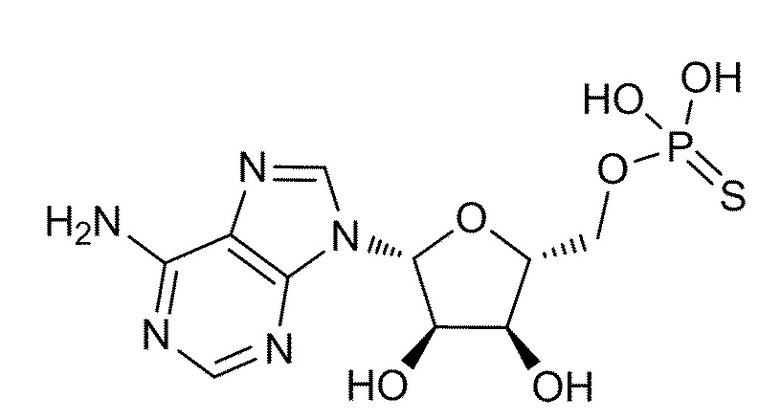
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-14, имеющее следующую структуру:
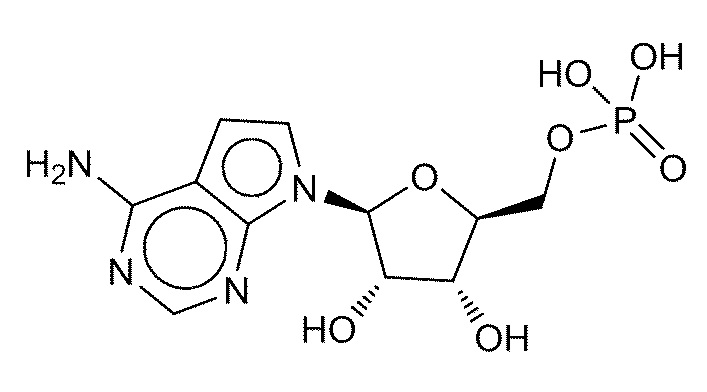
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-15, имеющее следующую структуру:
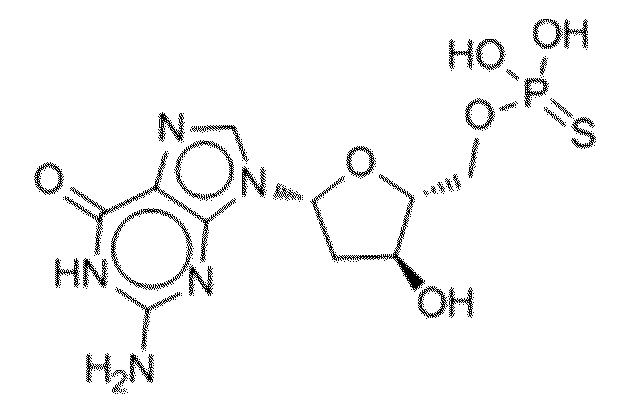
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-16, имеющее следующую структуру:
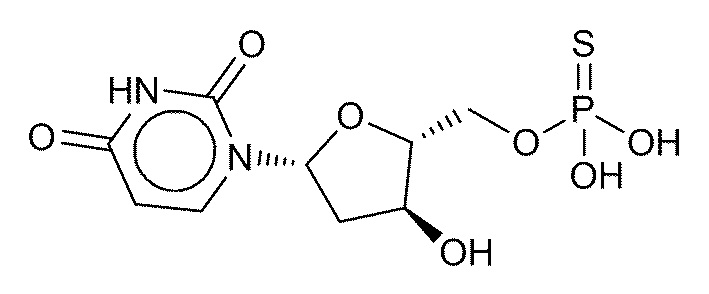
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-17, имеющее следующую структуру:
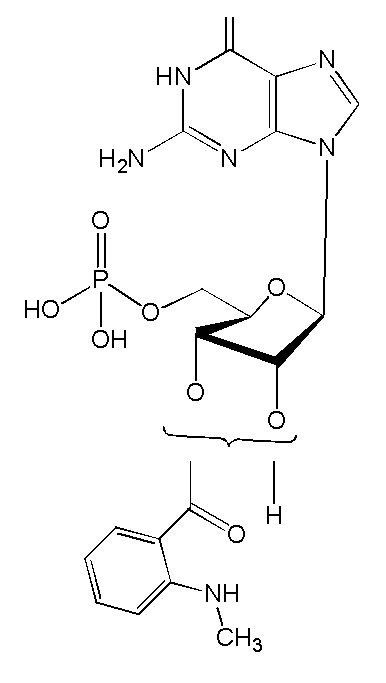
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-18, имеющее следующую структуру:
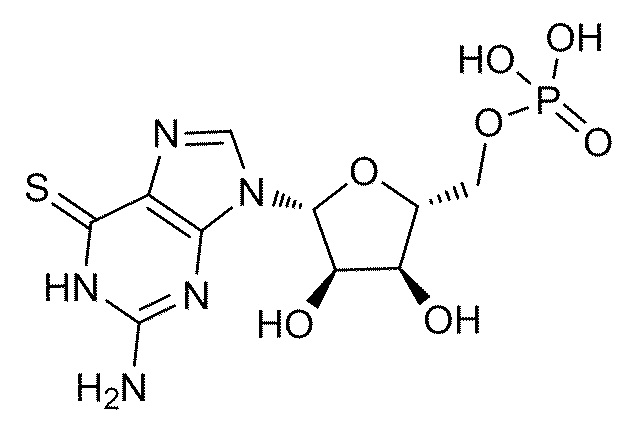
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-19, имеющее следующую структуру:
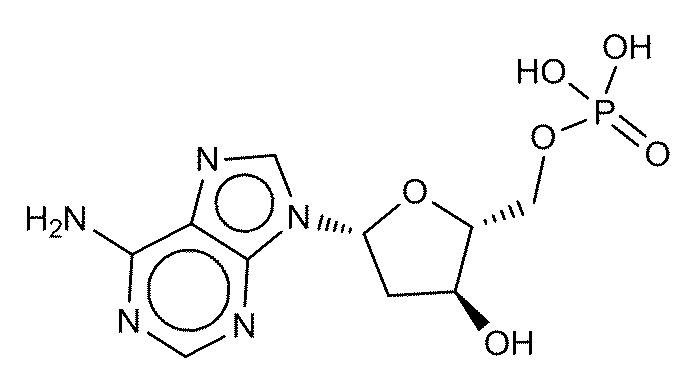
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-20, имеющее следующую структуру:
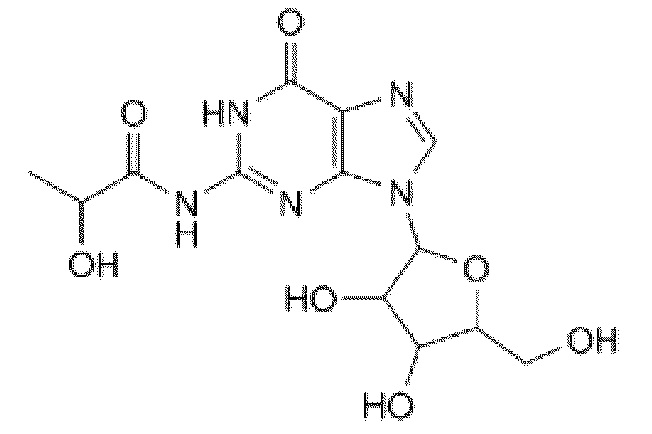
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-21, имеющее следующую структуру:
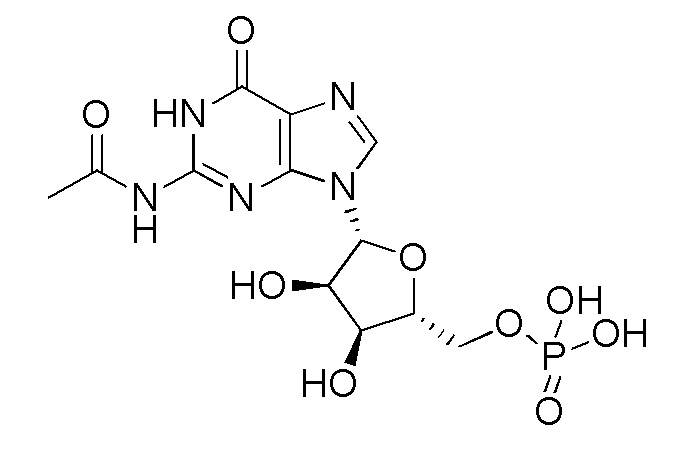
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-22, имеющее следующую структуру:
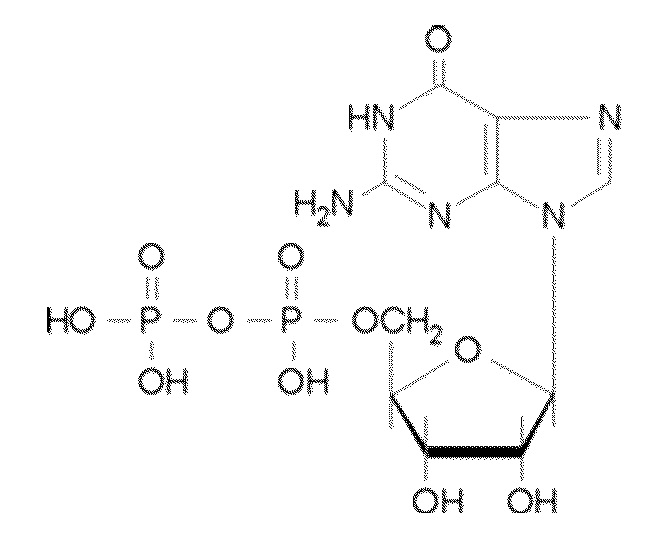
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-23, имеющее следующую структуру:
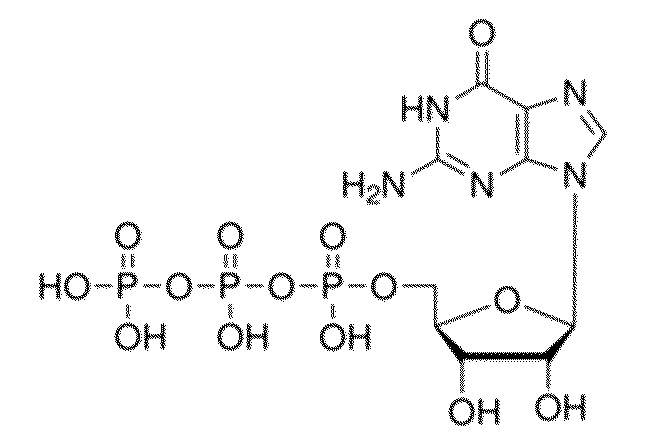
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-24, имеющее следующую структуру:
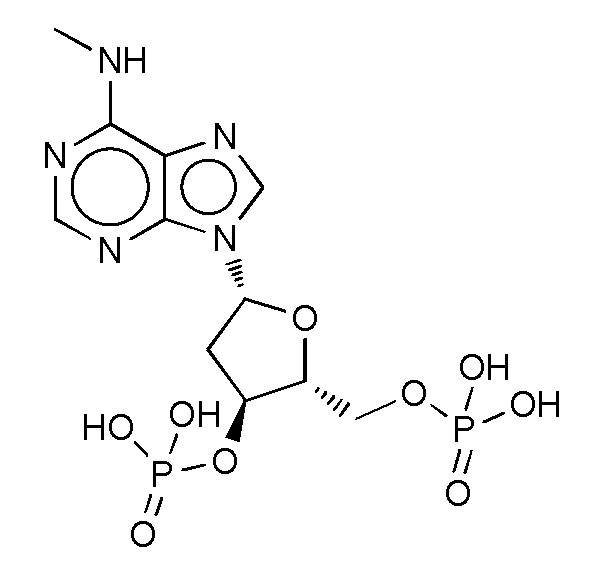
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-25, имеющее следующую структуру:
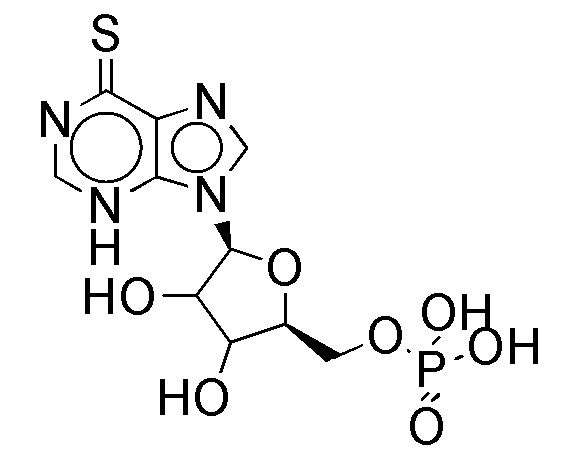
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-26, имеющее следующую структуру:
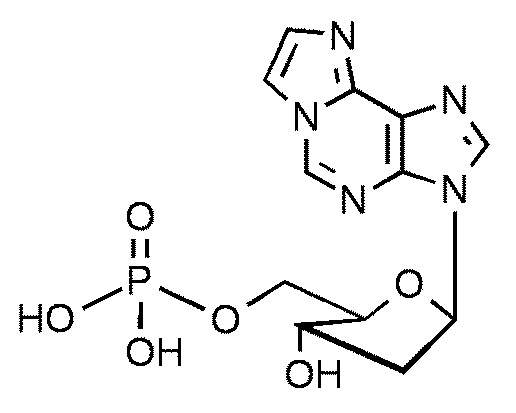
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-27, имеющее следующую структуру:
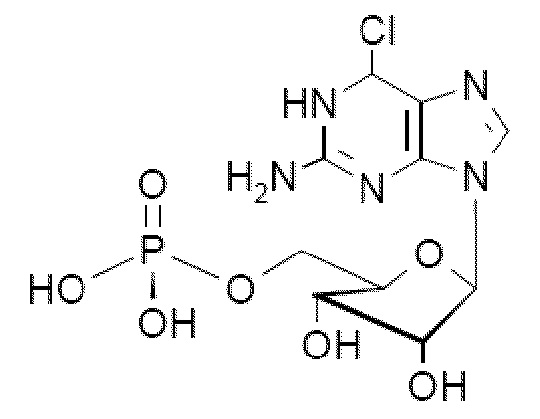
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-28, имеющее следующую структуру:
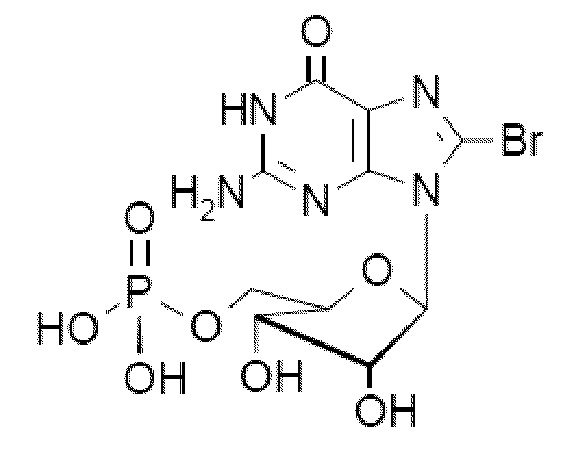
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-29, имеющее следующую структуру:
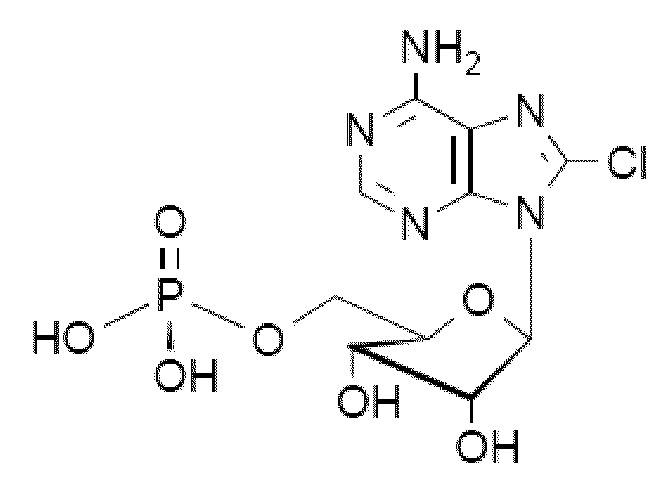
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-30, имеющее следующую структуру:
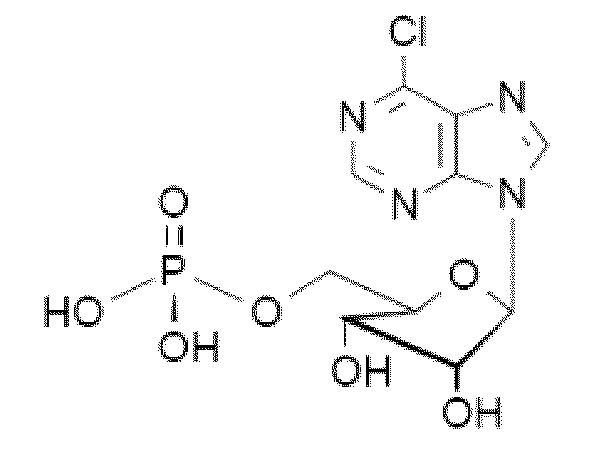
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-31, имеющее следующую структуру:
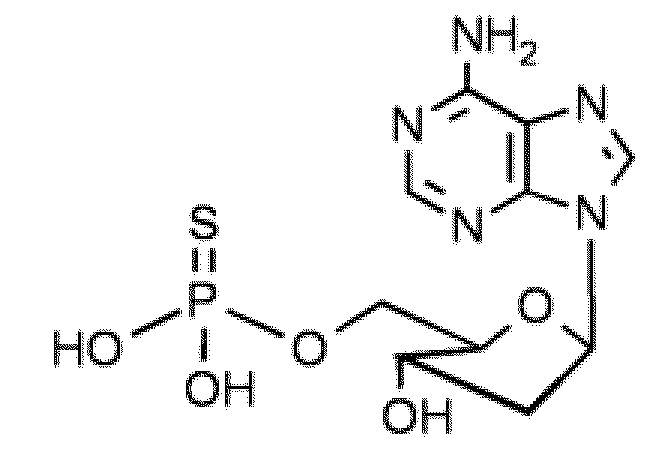
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-32, имеющее следующую структуру:
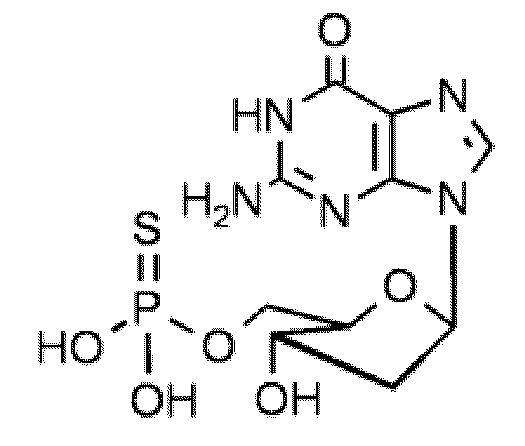
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-33, имеющее следующую структуру:
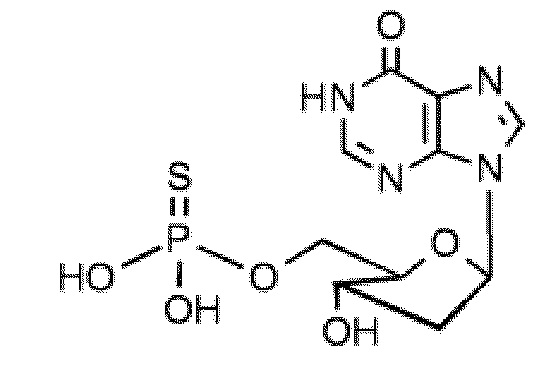
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-34, имеющее следующую структуру:
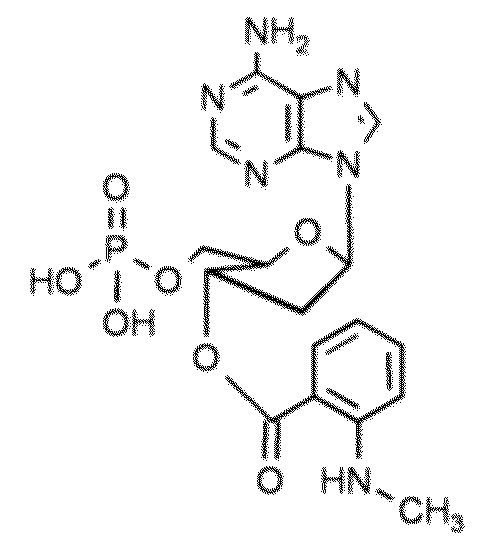
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-35, имеющее следующую структуру:
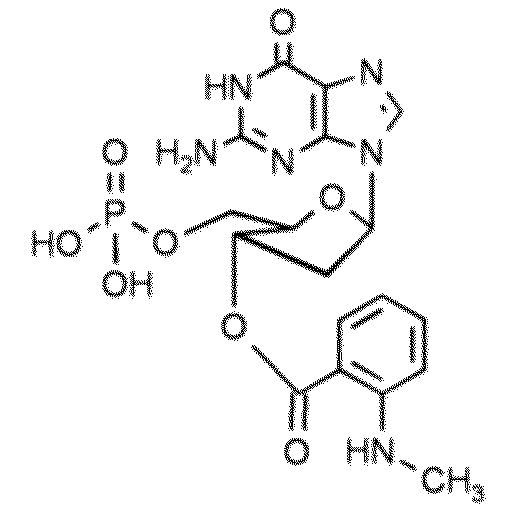
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-36, имеющее следующую структуру:
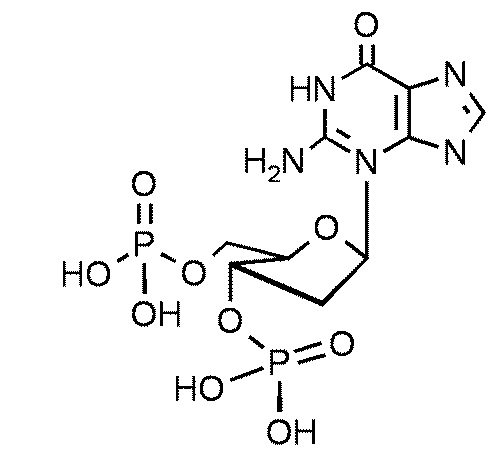
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-37, имеющее следующую структуру:
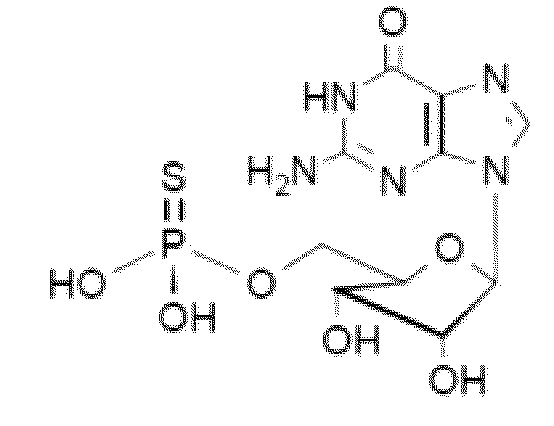
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-38, имеющее следующую структуру:
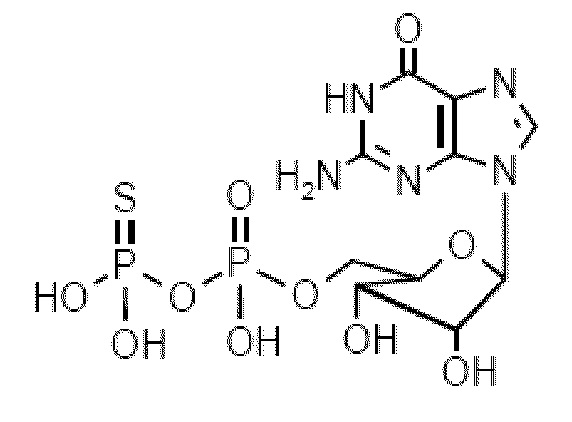
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-39, имеющее следующую структуру:
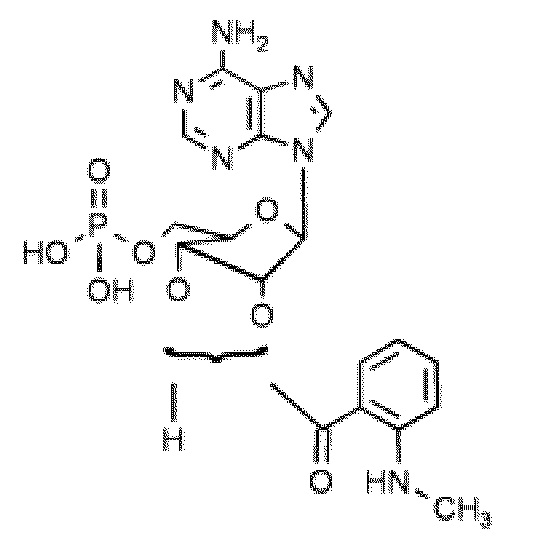
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-40, имеющее следующую структуру:
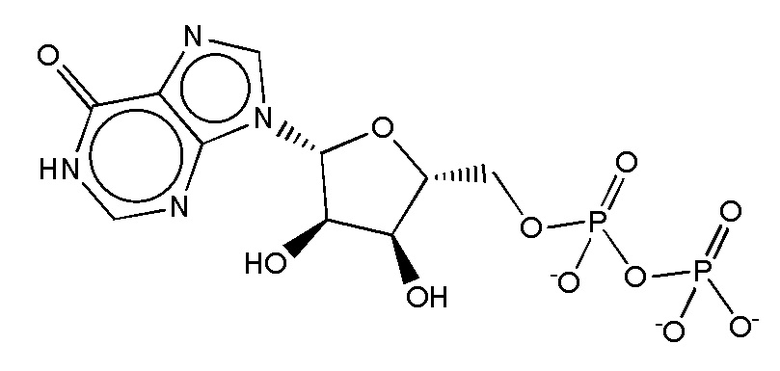
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-41, имеющее следующую структуру:
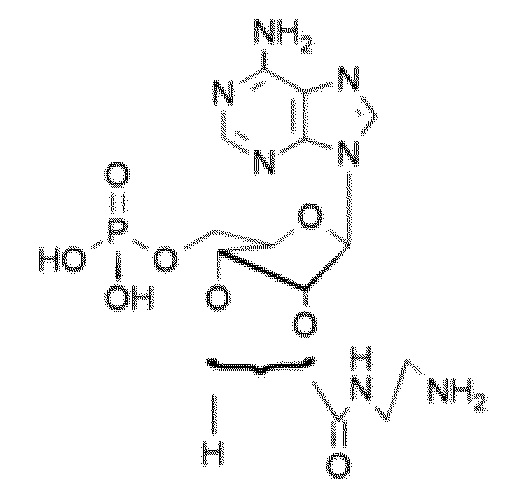
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-42, имеющее следующую структуру:
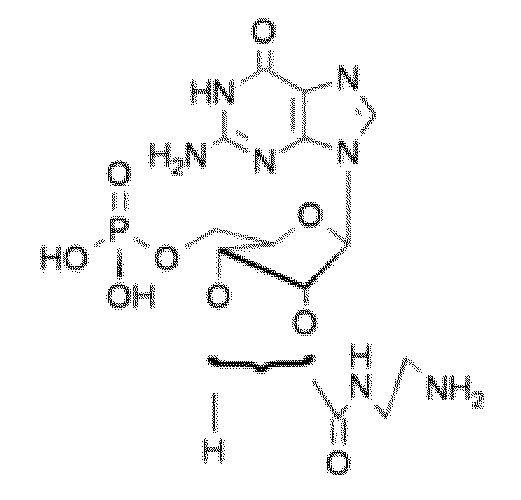
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-43, имеющее следующую структуру:
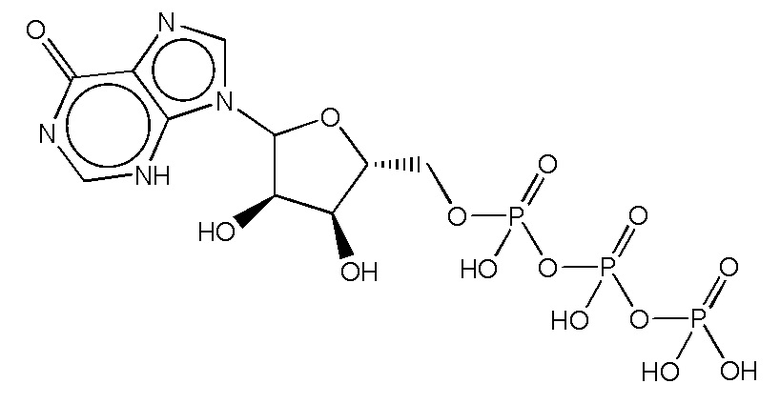
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-44, имеющее следующую структуру:
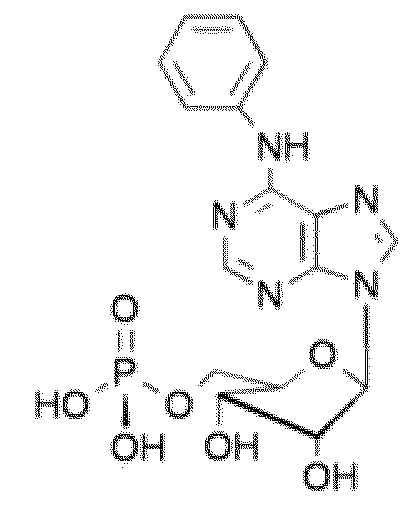
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-45, имеющее следующую структуру:
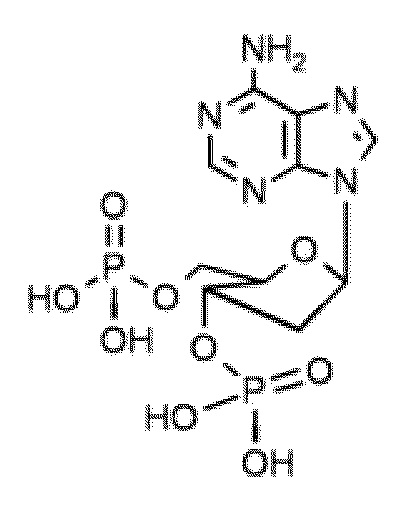
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-46, имеющее следующую структуру:
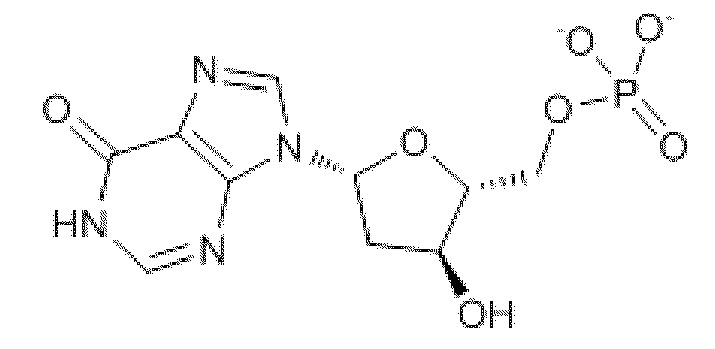
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-47, имеющее следующую структуру:
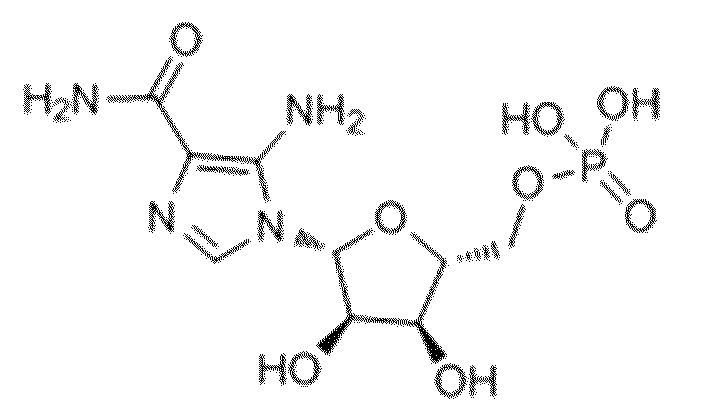
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-48, имеющее следующую структуру:
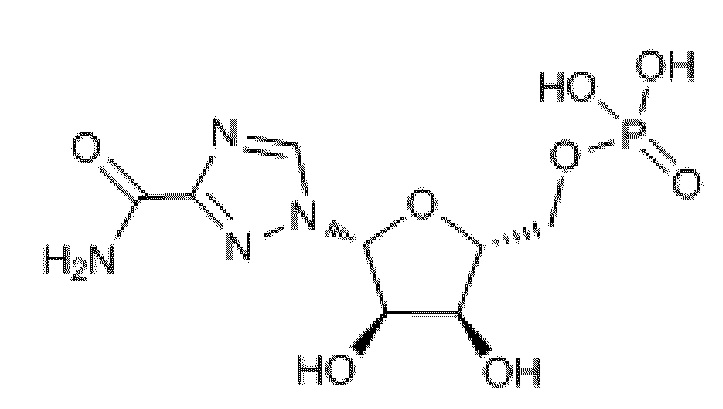
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-49, имеющее следующую структуру:
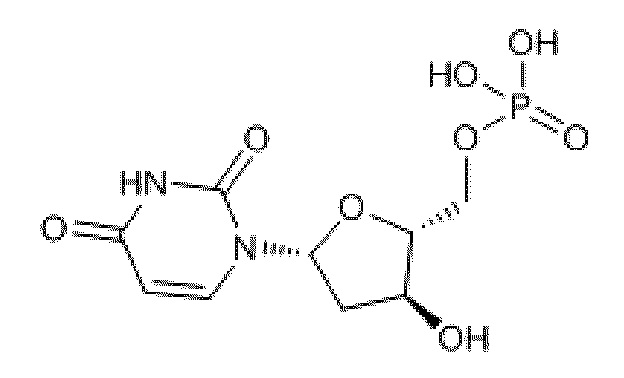
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-50, имеющее следующую структуру:
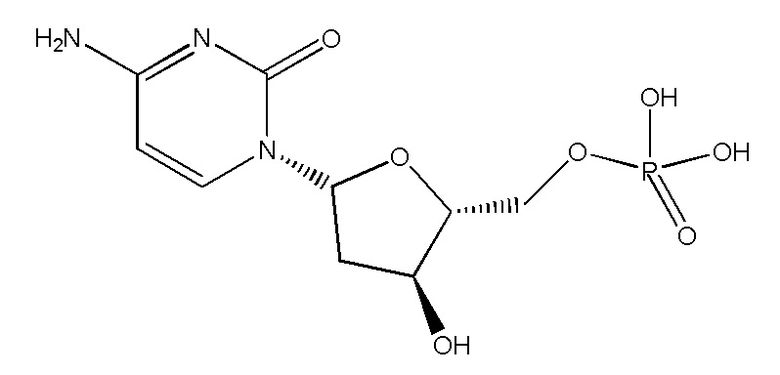
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-51, имеющее следующую структуру:
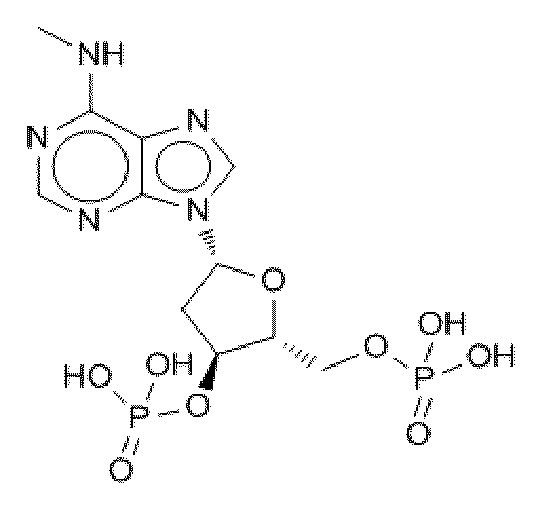
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-52, имеющее следующую структуру:
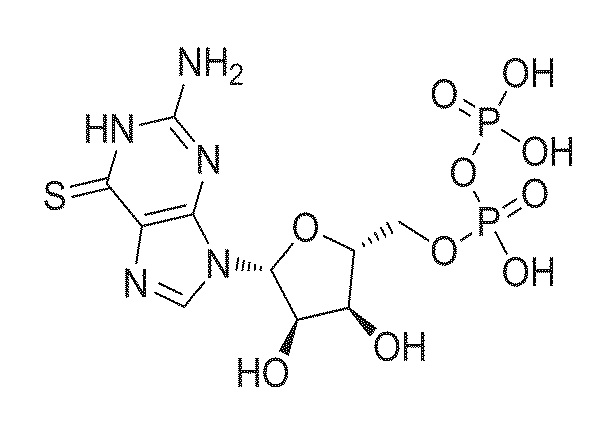
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-53, имеющее следующую структуру:
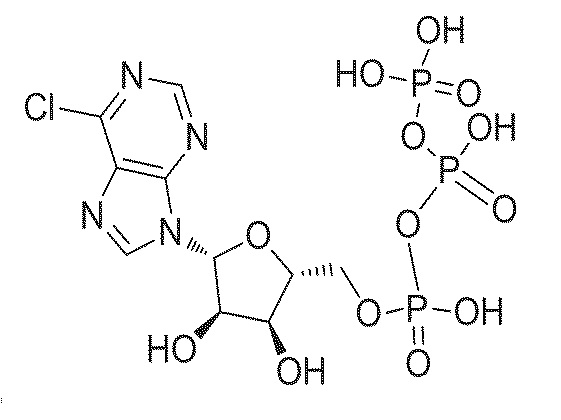
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-54, имеющее следующую структуру:
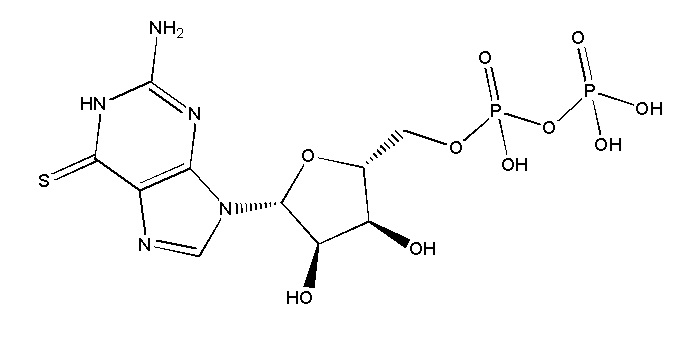
В некоторых вариантах осуществления нуклеотидное производное включает соединение формулы Nt-55, имеющее следующую структуру:
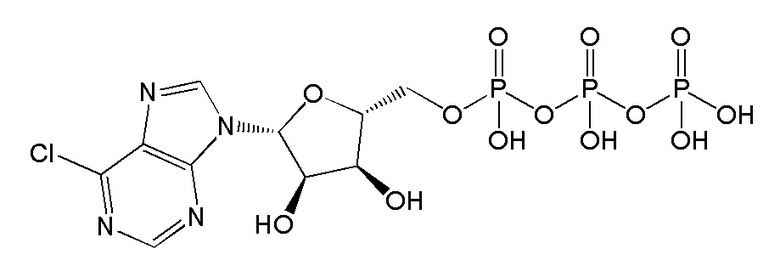
В некоторых вариантах осуществления нуклеотидное производное может представлять собой соль, стереоизомер или приемлемую форму соединений формул от Nt-1 до Nt-55 и/или соединений, приведенных в таблицах 2 и 6-14.
Нуклеотидные производные
В некоторых вариантах осуществления нуклеотидные производные по настоящему изобретению включают соль нуклеотидного производного, например, не ограничиваясь этим, ацетатную соль или формиатную соль. В некоторых вариантах осуществления соль нуклеотидного производного включает анион (-) (например, не ограничиваясь этим, Cl-, O2-, CO32-, HCO3-, OH-, NO3-, PO43-, SO42-, CH3COO-, HCOO- и C2O42-), связанный ионной связью с катионом (+) (например, не ограничиваясь этим, Al3+, Ca2+, Na+, K+, Cu2+, H+, Fe3+, Mg2+, NH4+ и H3O+). В еще одних вариантах осуществления соль нуклеотидного производного содержит катион (+), связанный ионной связью с анионом (-).
В некоторых вариантах осуществления нуклеотидные производные по настоящему изобретению идентифицируют с использованием in silico моделирования рецептора T1R1/T1R3 кошки («рецептора умами»), где нуклеотидные производные по настоящему изобретению имеют структуру, которая помещается в сайте связывания рецептора T1R1/T1R3 кошки.
В некоторых вариантах осуществления нуклеотидные производные по настоящему изобретению идентифицируют с помощью анализа in vitro, где производные нуклеотидов активируют рецептор T1R1/T1R3 кошки, экспрессируемый клетками in vitro. В некоторых вариантах осуществления нуклеотидные производные активируют рецептор одни или в комбинации с другими связывающимися с T1R1/T1R3 агентами, такими как нуклеотиды, аминокислоты и трансмембранные соединения, описанные здесь, и/или в комбинации с аминокислотами, описанными здесь, которые связываются с одним или более другими рецепторами. В некоторых вариантах осуществления анализ in vitro включает анализы in vitro, описанные в разделе «Примеры» настоящей заявки.
2.1. Сайт связывания T1R1 с нуклеотидами
Настоящая заявка также обеспечивает композиции, которые модулируют рецептор умами, например, рецептор T1R1/T1R3, где композиции взаимодействуют с одной или более аминокислотами в домене Venus Flytrap рецептора умами. В некоторых вариантах осуществления домен Venus Flytrap (VFT) находится в T1R1. В некоторых вариантах осуществления аминокислоты, с которыми взаимодействует композиция, включают одну или более аминокислот из Thr449, Ser172, Glu170, Glu301, His71, His47, Arg277, His308, Asn69, Asn302, Ser306, Ser384, Asp302, Ser306 и Ala380.
В одном неограничивающем варианте осуществления композиция содержит нуклеотид и/или нуклеотидное производное, где нуклеотид и/или нуклеотидное производное взаимодействует с одной, двумя, тремя, четырьмя, пятью, семью, восемью или более аминокислотами из His71, Arg277, His308, Ser306, Ser384, Ala380, His47, Asn69 и Asp302 T1R1.
В еще одном неограничивающем варианте осуществления композиция содержит нуклеотид и/или нуклеотидное производное, где нуклеотид и/или нуклеотидное производное взаимодействует с одной, двумя, тремя, четырьмя или более аминокислотами из Met383, Ser385, Ile309, Ser107 и Asp49 T1R1.
При связывании нуклеотида и/или нуклеотидного производного аминокислотные остатки VFT могут координировать фосфаты, дифосфаты, трифосфаты, бисфосфаты, фосфатные миметики (например, кислотные функциональные группы, такие как COOH, SO3H, NHOH и т. д.) нуклеотида и/или нуклеотидного производного, и включают одну или более аминокислот из His71, His47, Arg277, His308, Ile309, Asn69, Ser107 и Asp49 T1R1.
В некоторых вариантах осуществления, по меньшей мере, один фосфат нуклеотида и/или нуклеотидного производного взаимодействует с одной, двумя, тремя, четырьмя или более аминокислотами из His71, His47, Arg277, His308 и Asn69 T1R1. В неограничивающем примере связывание нуклеотида и/или нуклеотидного производного с VFT включает взаимодействия между отрицательно заряженными группами аминокислот в области связывания фосфатов VFT и фосфата нуклеотида и/или нуклеотидного производного.
Аминокислотные остатки VFT могут координировать атомы сахара нуклеотида и/или нуклеотидного производного (или, например, модифицированный сахар или замещение сахара) и могут включать Asp302 и/или Ser306 T1R1.
В некоторых вариантах осуществления, по меньшей мере, одна молекула сахара нуклеотида и/или нуклеотидного производного взаимодействует с аминокислотами Asp302 и/или Ser306 T1R1.
Аминокислотные остатки VFT могут координировать азотистое основание нуклеотида и/или нуклеотидного производного и могут включать одну или более аминокислот из Ser384, Ser385, Ala380, Met383, Glu170 и Asp302 T1R1.
В некоторых вариантах осуществления азотистое основание нуклеотида и/или нуклеотидного производного взаимодействует с одной, двумя или более аминокислотами из Ser384, His308 и Ala380 T1R1.
В еще одних неограничивающих вариантах осуществления молекула сахара нуклеотида и/или нуклеотидного производного взаимодействует с Asp302 VFT, где Asp302 ориентирована на одновременную координацию цвиттерионного азота скелета связанной аминокислоты и сахара нуклеотида и/или нуклеотидного производного.
В некоторых вариантах осуществления композиция взаимодействует с доменом Venum Flyprap (VFT) умами посредством любой комбинации взаимодействий, описанных здесь, например, одним, двумя, тремя или более взаимодействиями. Взаимодействия между нуклеотидом и/или нуклеотидным производным и VFT могут также включать дополнительные гидрофобные взаимодействия, которые дополняют энергию взаимодействия нуклеотида и/или нуклеотидного производного с VFT.
В некоторых вариантах осуществления взаимодействие между композицией и одной или более аминокислотами включает одно или более из водородных связей, ковалентной связи, нековалентной связи, солевого мостика, физического взаимодействия и их комбинаций. Взаимодействия также могут представлять любую характеристику взаимодействия лиганд-рецепторного взаимодействия, известного в данной области техники. Такие взаимодействия можно определить, например, сайт-направленным мутагенезом, рентгеновской кристаллографией, рентгеновскими или другими спектроскопическими методами, ядерным магнитным резонансом (ЯМР), оценкой возникновения поперечной сшивки, масс-спектроскопией или электрофорезом, анализом вытеснения на основе известных агонистов, определением структуры и их комбинацией. В некоторых вариантах осуществления взаимодействия определяют in silico, например, с помощью теоретических способов, таких как докинг соединения в домен VFT с использованием молекулярного докинга, молекулярного моделирования, молекулярной симуляции или других способов, известных специалистам в данной области техники.
В настоящей заявке также обеспечиваются способы идентификации соединения, которое модулирует активность рецептора умами, например, T1R1, где соединение идентифицируется на основе его способности взаимодействовать с одной или более из указанных здесь аминокислот, которые присутствуют в домене VFT T1R1.
В некоторых вариантах осуществления способ включает контактирование испытуемого агента с рецептором умами T1R1 кошки, детектирование взаимодействия между испытуемым агентом и одной или более аминокислотами в сайте взаимодействия VFT рецептора умами T1R1 кошки и выбор в качестве соединения испытуемого агента, который взаимодействует с одной или более аминокислотами.
3. Трансмембранные соединения
Настоящее раскрытие относится к вкусоароматическим композициям, которые включают, по меньшей мере, одно трансмембранное соединение. В некоторых вариантах осуществления трансмембранное соединение представляет собой соединение, усиливающее вкус умами. Трансмембранные соединения, описанные здесь, идентифицировали с помощью in silico моделирования гипотетических агонистов в трансмембранной области T1R1 кошачьего рецептора T1R1/T1R3 («рецептора умами»). Следовательно, в некоторых вариантах осуществления трансмембранное соединение представляет собой композицию, которая взаимодействует (например, связывается) с областью T1R1, содержащей трансмембранный домен T1R1. В некоторых вариантах осуществления такие взаимодействия с трансмембранным доменом T1R1 действуют агонистически на рецептор T1R1/T1R3 или умами. В других вариантах осуществления трансмембранное соединение функционирует синергически с другими агонистами или модуляторами T1R1 для модуляции активности рецептора T1R1/T1R3 или умами.
Вкусоароматические композиции могут использоваться для улучшения или модификации вкусовой привлекательности, вкуса или аромата пищевого продукта для домашних животных. Вкусоароматические композиции могут включать комбинации соединений, например, комбинации трансмембранных соединений и/или нуклеотидов, и/или нуклеотидных производных, и/или аминокислот, и могут быть добавлены в композиции пищевых продуктов для домашних животных в различных форматах системы доставки.
3.1. Производные аминов формулы I
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-1, имеющее следующую структуру:
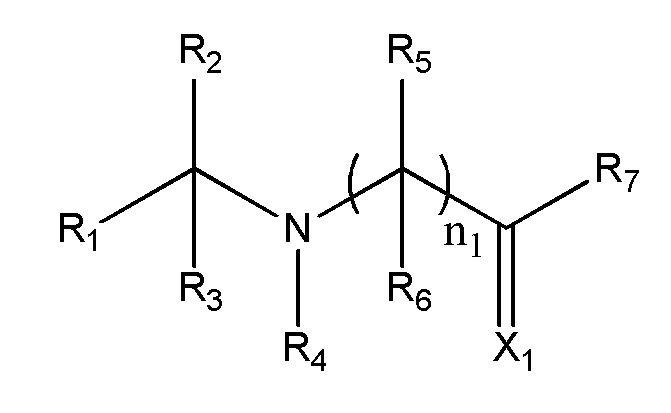
где X1 выбран из группы, состоящей из О и S;
где n1 равно 1-3;
где n2 равно 0-4 (где, когда n равно 0, то присутствует химическая связь);
где n4 равно 0-3;
где R1, R2 и R3 независимо выбраны из группы, состоящей из H, =O, =S, разветвленного или неразветвленного, замещенного или незамещенного низшего алкила (C1-C8), и R5;
где R4 выбран из группы, состоящей из H, разветвленного или неразветвленного низшего алкила (C1-C8) и (CH2)n2арила;
где R5 выбран из группы, состоящей из H, CH3, CH(CH3)2, CH2CH(CH3)2, CH(CH3)CH2CH3, CH2CH2SCH3, CH2SH, CH2SeH, CH2OH, CH(OH)CH3, CH2C(O)NH2, CH2CH2C(O)NH2, CH2CH2CH2NHC(NH)NH2, CH2(1H-имидазолила), CH2(CH2)2CH2NH2, CH2COOH, CH2CH2COOH, CH2C6H5, CH2(4-гидроксифенила), CH2[3-ил-(1H-индола)], CH2(циклопентила), CH2(циклогексила), CH2(инданила), независимо разветвленного или неразветвленного низшего алкила (С1-С10), (CH2)0-4PH, c-C3H5, c-C4H7, c-C5H9, c-C6H10, фенила, биарила, (CH2)n2арила, пиридина, тиофина, CH2Ph, CH2пиридина и CH2тиофена,
арильные и алкильные (как разветвленные, так и неразветвленные) группы могут быть необязательно замещены метилом, OH, SH, OCH3, SCH3, COOH, COOR13, S(O)n4R1, C(O)R11, C(O)NR11R12, CN, NR11R12, NR11C(O)R12, арилом, метилендиокси, алкилом (C1-C5), CH2SSCH2CH(COOH)(NH2), атомом галогена (F, Cl, Br, I), NO2, NHC(=NH)NH2, CHO, CF3, P(=X1)(OR1)2, OP(=X1)(OR1)2;
где R5 и R6, взятые вместе, могут образовать циклические кольца, такие как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил (т.е. спироциклические группы);
где R6 выбран из группы, состоящей из H, и разветвленного или неразветвленного низшего алкила (C1-C4);
где R7 выбран из группы, состоящей из H, AA, OH, O, разветвленного или неразветвленного низшего алкила (C1-C6), O(CH2)n1арила, NR11R12, N(R14)OH, C(R8)(R9), арила и гетероарила;
где R8 и R9 независимо выбраны из группы, состоящей из H, разветвленного или неразветвленного низшего алкила (C1-C6), арила, алкиларила и алкилгетероарила;
где R11 и R12 независимо выбраны из группы, состоящей H, CH3, разветвленного или неразветвленного низшего алкила (C1-C6), фенила, арила и (CH2)n1арила;
где R13 выбран из группы, состоящей из H, CH3, CH2CH3, CH2арила и трет-бутила;
где R14 выбран из группы, состоящей из H и CH3; и
где АА выбран из группы, состоящей из встречающейся в природе альфа-аминокислоты или (R)- или (S)-конфигурации (т.е. протеогенных аминокислот).
В одном неограничивающем варианте осуществления предусмотрены все асимметричные конфигурации для раскрытых в настоящем изобретении композиций.
В некоторых вариантах осуществления арил имеет свое обычное химическое значение и может включать следующие группы, не ограничиваясь этим, Ph, пиридин, тиофен, фуран, нафтил, индол, бензотиофен, бензофуран, хинолон, изохинолин, пиррол, N-(метил)пиррол, имидазол, тиазол, пиримидин, изоксазол, оксазол, изоиндол, индолизин, пурин, пиразин и пиперазин.
В некоторых вариантах осуществления присоединения арильной группы могут находиться в различных углеродных центрах, что должно быть понятно специалисту в данной области техники.
В еще одних неограничивающих вариантах осуществления, когда соединение содержит два арильных кольца (например, фенилы), то одно или оба кольца могут быть замещены биарильной кольцевой системой. Такие биарильные кольцевые системы включают, например, фенилфенил, фенилпиридил, фенилтиофен, тиофентиофен и фенилфуран.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-2, имеющее следующую структуру:
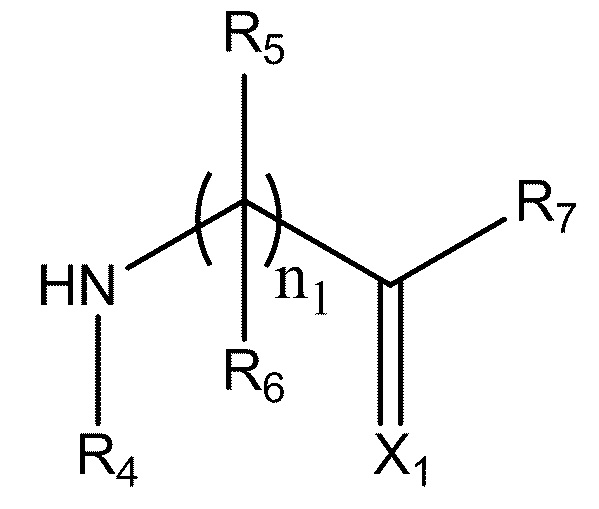
где R4, R5, R6, R7, X1 и n1 имеют значения, определенные для формулы Tm-1.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-20, имеющее следующую структуру:
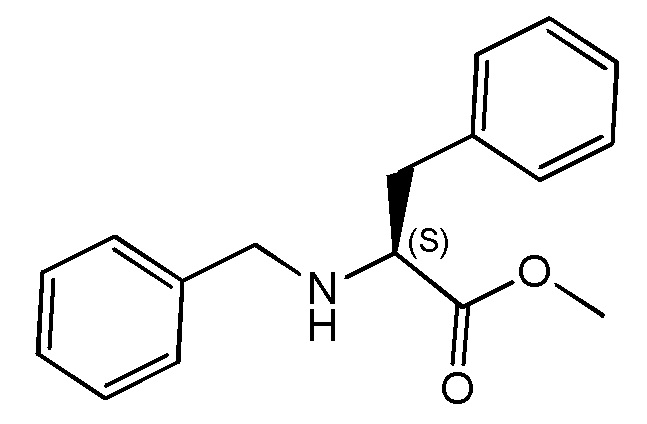
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-21, имеющее следующую структуру:
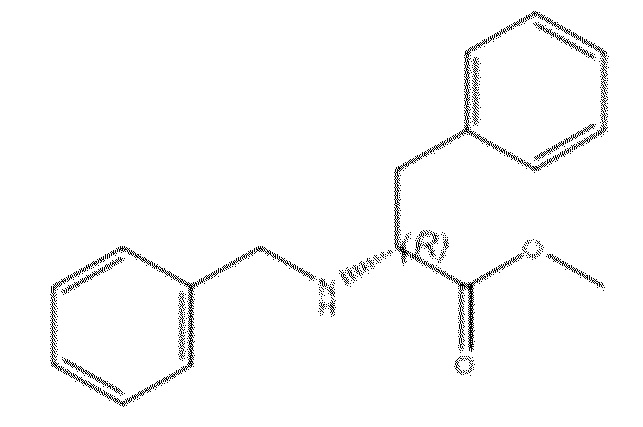
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-22, имеющее следующую структуру:
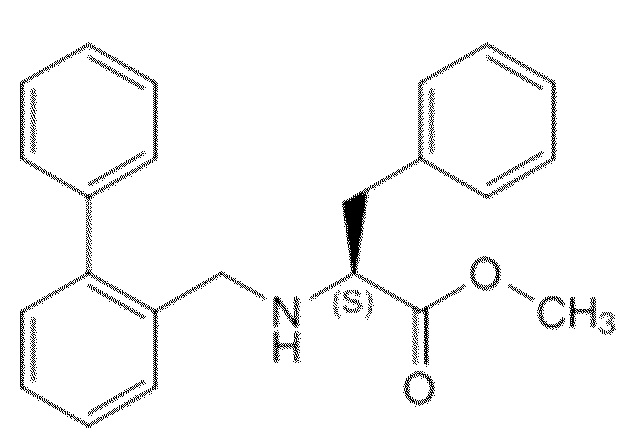
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-23, имеющее следующую структуру:
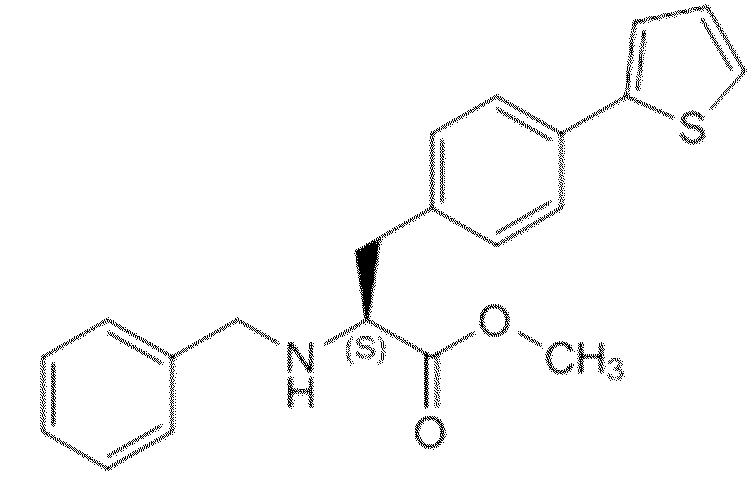
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-24, имеющее следующую структуру:
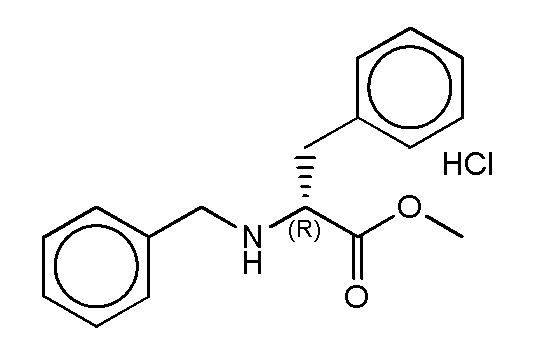
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-25, имеющее следующую структуру:
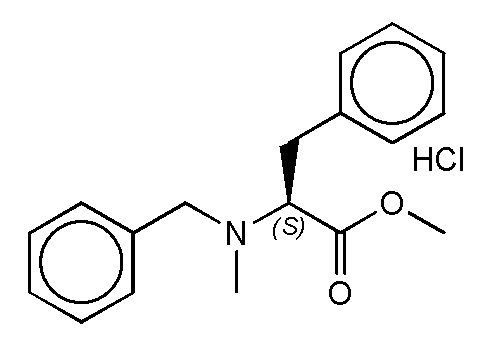
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-26, имеющее следующую структуру:
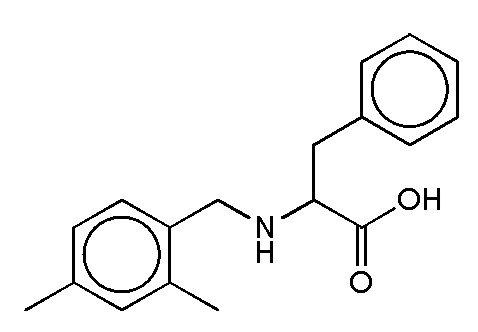
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-27, имеющее следующую структуру:
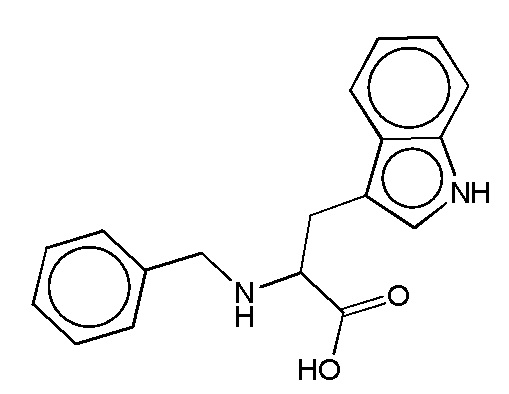
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-28, имеющее следующую структуру:
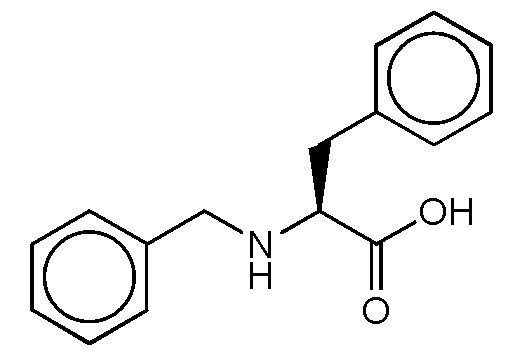
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-29, имеющее следующую структуру:
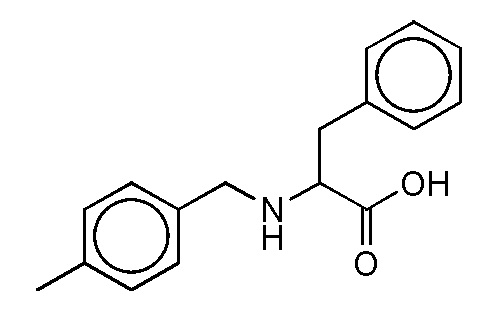
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-30, имеющее следующую структуру:
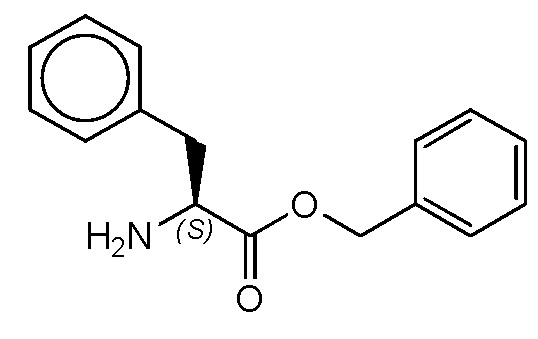
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-31, имеющее следующую структуру:
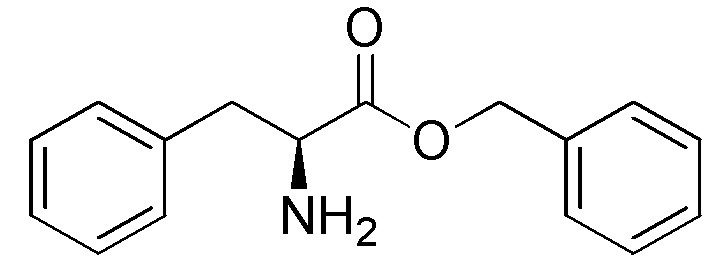
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-32, имеющее следующую структуру:
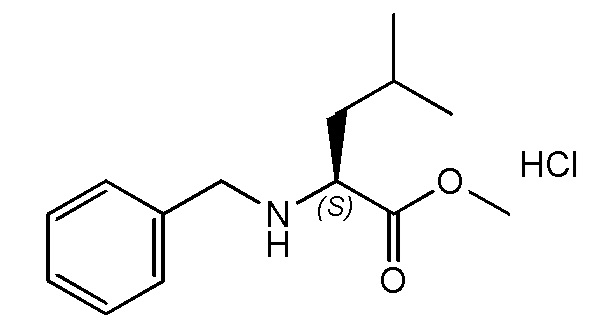
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-33, имеющее следующую структуру:
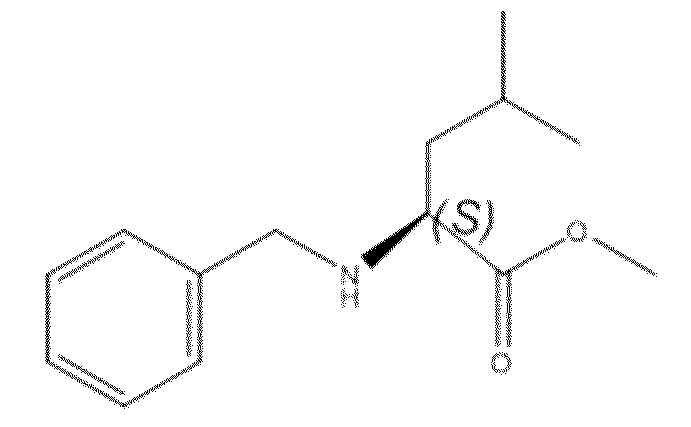
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-34, имеющее следующую структуру:
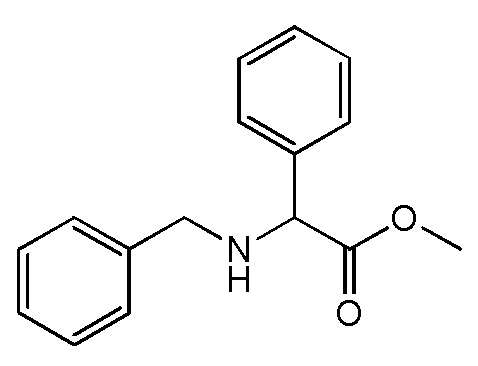
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-35, имеющее следующую структуру:
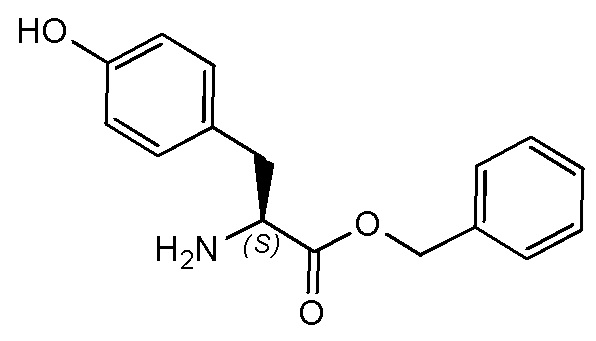
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-36, имеющее следующую структуру:
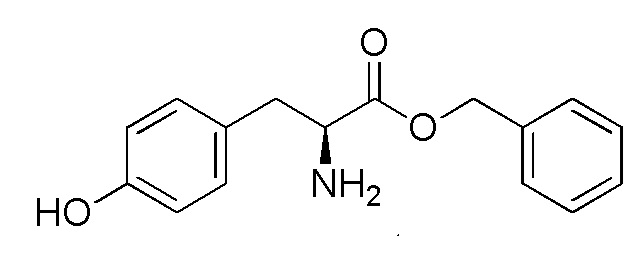
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-37, имеющее следующую структуру:
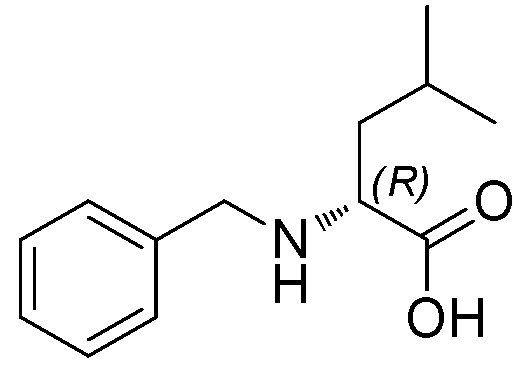
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-38, имеющее следующую структуру:
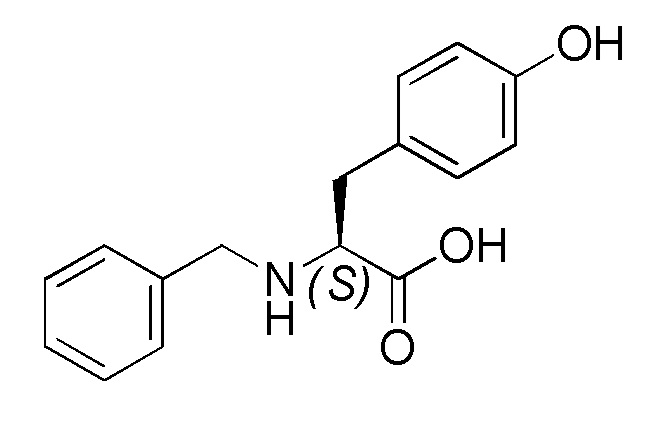
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-39, имеющее следующую структуру:
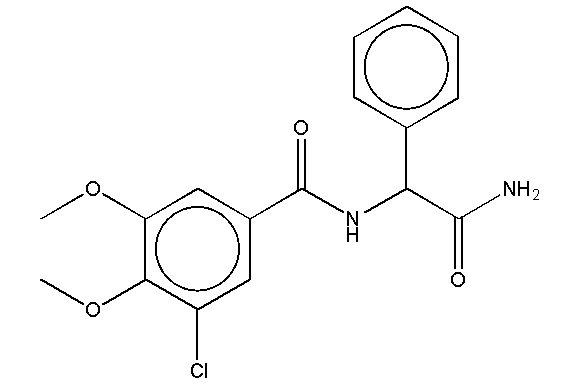
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-40, имеющее следующую структуру:
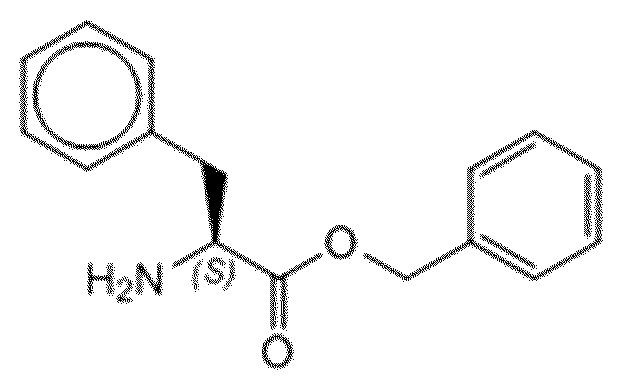
3.2. Производные аминов формулы II
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-3, имеющее следующую структуру:
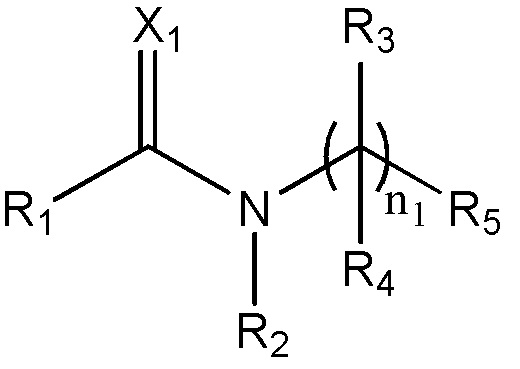
где X1 выбран из группы, состоящей из О и S;
где n1 и n2 равны 0-4 (где, когда n1 и/или n2 равно 0, то присутствует химическая связь);
где R1 выбран из группы, состоящей из разветвленного или неразветвленного низшего алкила (С1-С10), (CH2)n2Ph, c-C3H5, c-C4H7, c-C5H9, c-C6H10, фенила, (CH2)n2арила, Ph, пиридина, тиофина, CH2Ph, CH2пиридина, CH2тиофена, O-арила, Ph, пиридина, тиофена, фурана, нафтила, индола, бензотиофена, бензофурана, хинолона, изохинолина, пиррола, N-(метил)пиррола, имидазола, тиазола, пиримидина, изоксазола, оксазола, изоиндола, индолизина, пурина, пиразина, пиперазина, O-алкил(C1-C6), биарила и OR1 (например, карбаматов),
арильные и алкильные (как разветвленные, так и неразветвленные) группы могут быть необязательно замещены метилом, OH, SH, OCH3, SCH3, COOH, COOR13, S(O)n4R1, C(O)R11, C(O)NR11R12, CN, NR11R12, NR11C(O)R12, арилом, метилендиокси, алкилом (C1-C5), CH2SSCH2CH(COOH)(NH2), атомом галогена (F, Cl, Br, I), NO2, NHC(=NH)NH2, CHO, CF3, P(=X1)(OR1)2, OP(=X1)(OR1)2;
где R2 выбран из группы, состоящей из H, CH3, (CH2) и арила;
где R3, R4 и R5 независимо выбраны из группы, состоящей из Н, разветвленного или неразветвленного низшего алкила (C1-C8), (CH2)n2арила и R1;
где R11 и R12 независимо выбраны из группы, состоящей из H, CH3, разветвленного или неразветвленного низшего алкила (C1-C6), фенила, арила и (CH2)n1арила;
где R13 выбран из группы, состоящей из H, CH3, CH2CH3, CH2арила и трет-бутила;
В некоторых вариантах осуществления арил имеет свое обычное химическое значение и может включать, не ограничиваясь этим, Ph, пиридин, тиофен, фуран, нафтил, индол, бензотиофен, бензофуран, хинолон, изохинолин, пиррол, N-(метил)пиррол, имидазол, тиазол, пиримидин, изоксазол, оксазол, изоиндол, индолизин, пурин, пиразин и пиперазин.
В некоторых вариантах осуществления присоединения арильной группы могут находиться в различных углеродных центрах, что должно быть понятно специалисту в данной области техники.
В некоторых вариантах осуществления асимметричные центры могут быть (R)- или (S)-конфигурации, как это должно быть понятно специалисту в данной области техники.
В одном неограничивающем варианте осуществления все асимметричные конфигурации предусмотрены для раскрытых в настоящем изобретении композиций.
В еще одних неограничивающих вариантах осуществления, когда соединение содержит два арильных кольца (например, фенилы), то одно или оба кольца могут быть замещены биарильной кольцевой системой. Такие биарильные кольцевые системы включают, например, фенилфенил, фенилпиридил, фенилтиофен, тиофентиофен и пенилфуран.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-4, имеющее следующую структуру:
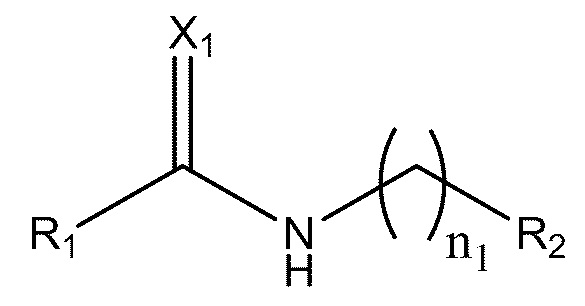
где R1 и R2 независимо выбраны из группы, состоящей из арила, циклоалкила (например, циклопропила, циклобутила, циклопентила, циклогексила, циклогептила) и гетероарила (например, не ограничиваясь этим, Ph, пиридина, тиофена, фурана, нафтила, индола, бензотиофена, бензофурана, хинолона, изохинолина, пиррола, N-(метил)пиррола, имидазола, тиазола, пиримидина, изоксазола, оксазола, изоиндола, индолизина, пурина, пиразина и пиперазина);
арильные и алкильные (как разветвленные, так и неразветвленные) группы могут быть необязательно замещены метилом, OH, SH, OCH3, SCH3, COOH, COOR13, S(O)n4R1, C(O)R11, C(O)NR11R12, CN, NR11R12, NR11C(O)R12, арилом, метилендиокси, алкилом (C1-C5), CH2SSCH2CH(COOH)(NH2), атомом галогена (F, Cl, Br, I), NO2, NHC(=NH)NH2, CHO, CF3, P(=X1)(OR1)2 или OP(=X1)(OR1)2;
где циклоалкильные группы могут необязательно содержать гетероатомы в кольцах (например, O, N и/или S), например, пиперидин, пиперазин, тетрагидротиофен, пиран, пирролидин или тетрагидрофуран;
где n1=0-4;
где R11, R12, R13 и X1 имеют значения, определенные здесь; и
где n4=0-4.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-41, имеющее следующую структуру:
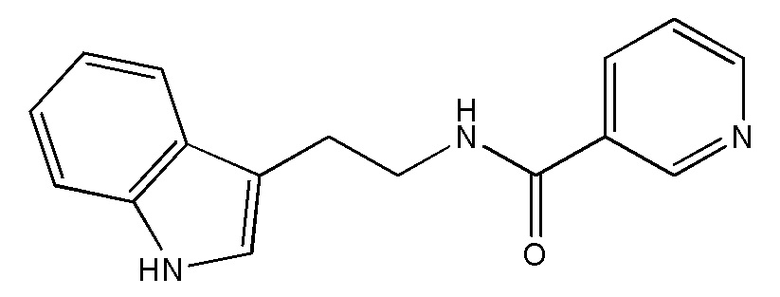
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-42, имеющее следующую структуру:
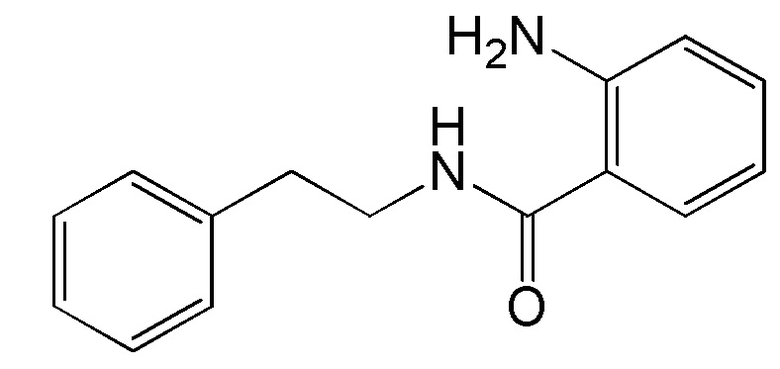
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-43, имеющее следующую структуру:
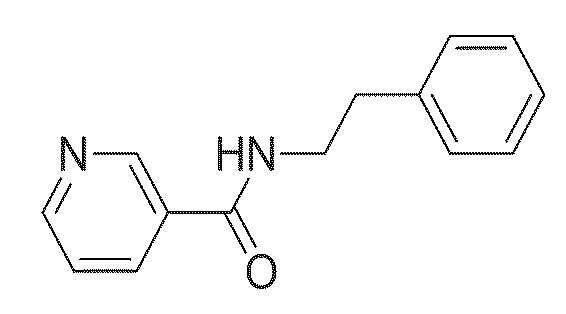
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-44, имеющее следующую структуру:
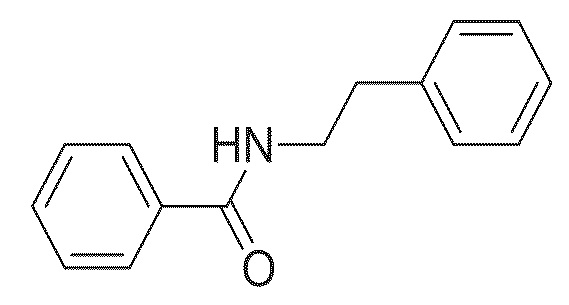
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-45, имеющее следующую структуру:
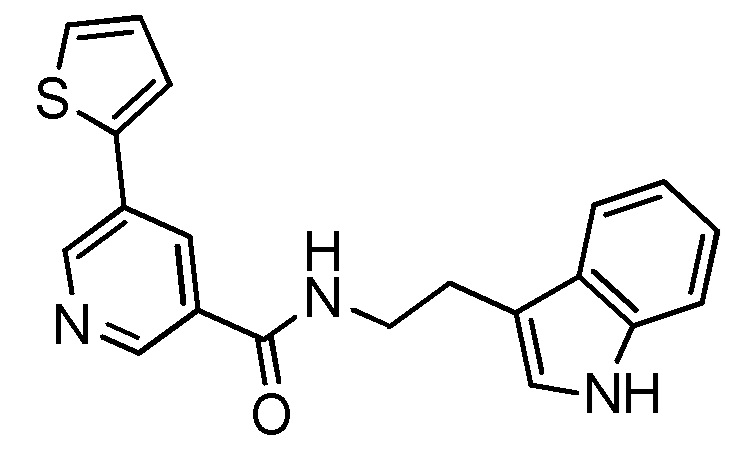
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-46, имеющее следующую структуру:
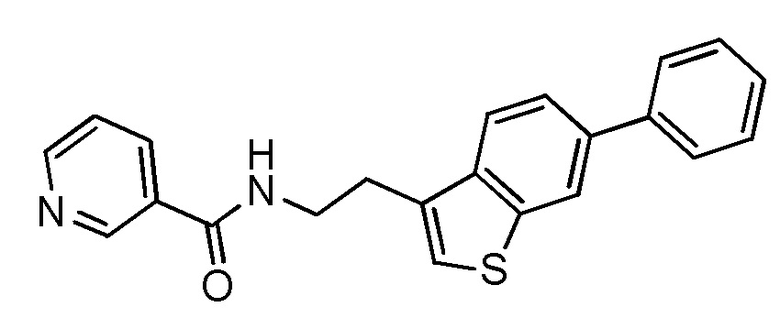
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-47, имеющее следующую структуру:
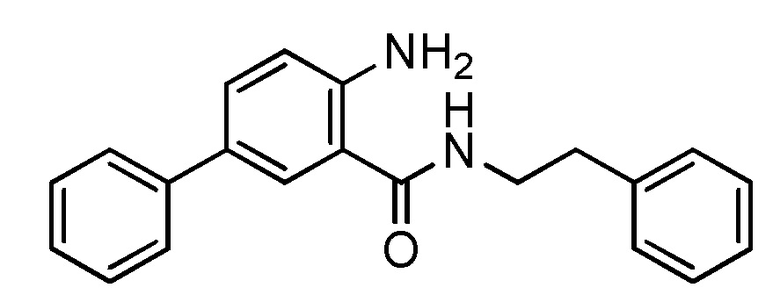
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-48, имеющее следующую структуру:
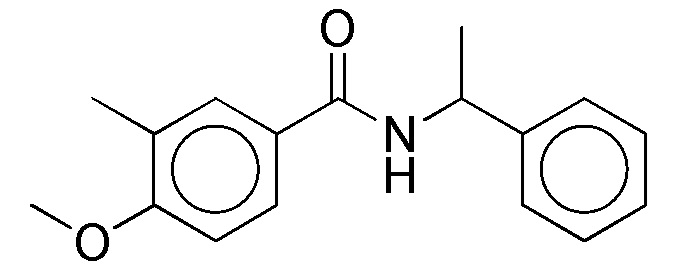
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-49, имеющее следующую структуру:
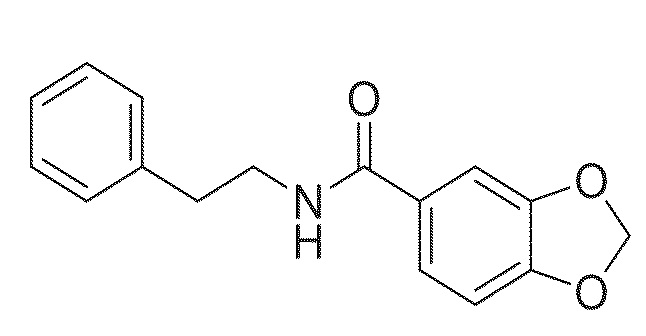
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-50, имеющее следующую структуру:
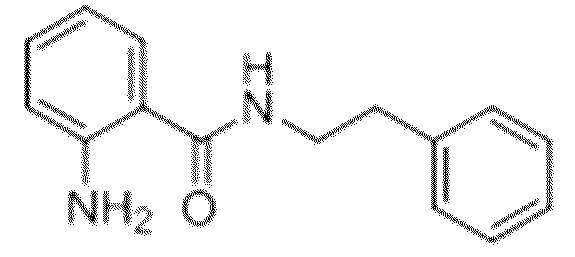
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-51, имеющее следующую структуру:
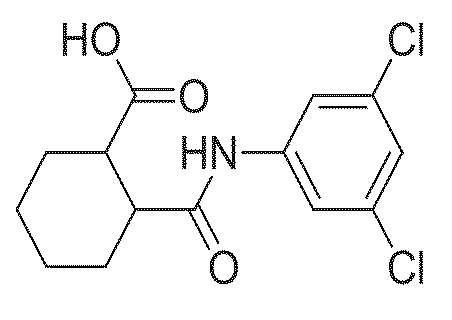
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-52, имеющее следующую структуру:
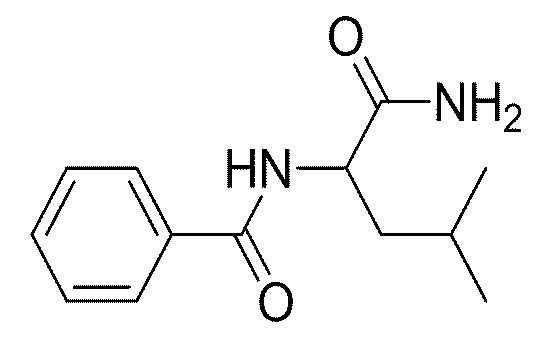
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-53, имеющее следующую структуру:
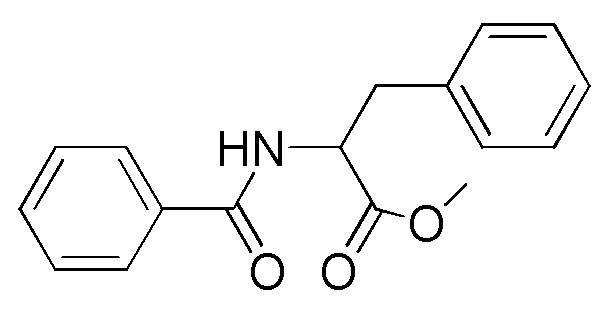
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-54, имеющее следующую структуру:
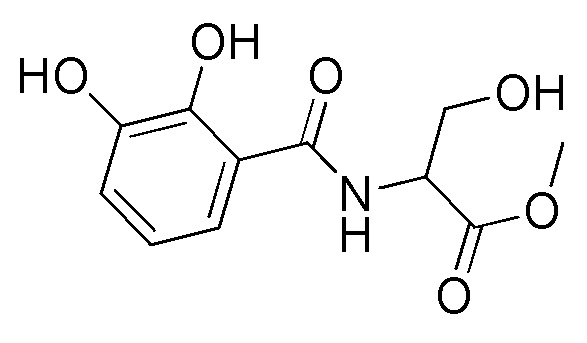
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-55, имеющее следующую структуру:
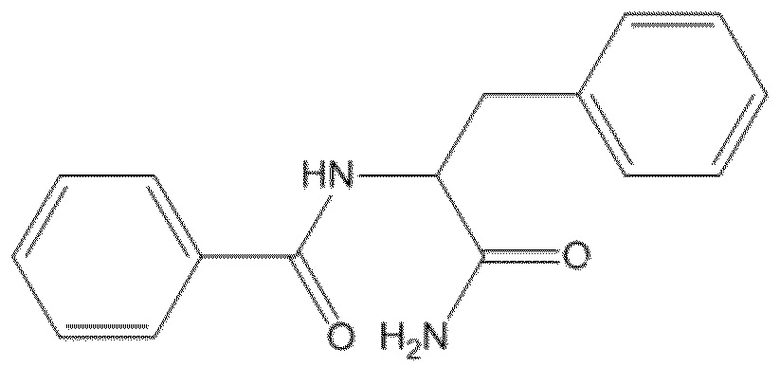
3.3. Производные парабановой кислоты
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-6, имеющее следующую структуру:
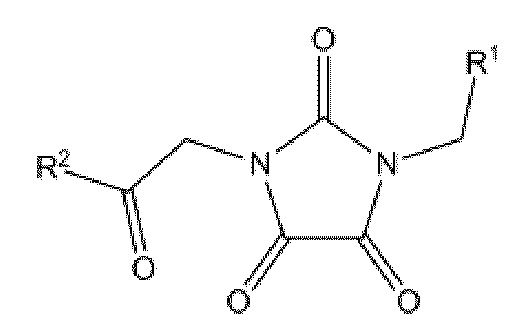
где R1 или R2 независимо выбраны из группы, состоящей из замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного алкинила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, гидроксила, атома водорода, замещенного или незамещенного простого эфира, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила, замещенного или незамещенного инденила или замещенного или незамещенного инданила.
В некоторых вариантах осуществления R1 или R2 могут содержать следующую структуру:
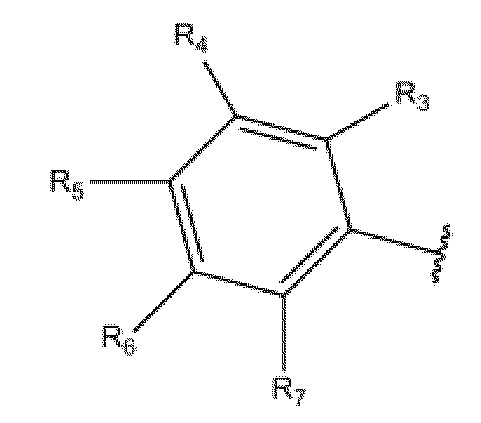
где R3, R4, R5, R6 и R7 независимо выбраны из группы, состоящей из атома водорода, атома галогена, циано, азидо, гидроксила, замещенного или незамещенного сульфонила, замещенного или незамещенного сульфонамидо, замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного амидо, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, замещенного или незамещенного простого эфира, замещенного или незамещенного карбокси, замещенного или незамещенного ацила, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила или замещенного или незамещенного гетероаренила, или замещенного или незамещенного индена, или замещенного или незамещенного инданила. В некоторых вариантах осуществления два или более из R3, R4, R5, R6 и R7, взятые вместе, образуют кольцо, которое может быть гетероциклическим (т.е. содержать один или более гетероатомов) или которое может быть полностью карбоциклическим и которое независимо может быть насыщенным или ненасыщенным.
Заместители в замещенных группах, описанных здесь, таких как «замещенный простой эфир», «замещенный карбокси», «замещенный ацил», «замещенный сульфонил», «замещенный алкил», «замещенный алкенил», «замещенный циклоалкил», «замещенный циклоалкалкил», «замещенный арилалкил», «замещенный арил», «замещенный гетероциклил», «замещенный гетероарилалкил», «замещенный гетероарил», «замещенный нафтил», «замещенный фенил», «замещенный тиенил», «замещенный бензотиенил», «замещенный пиридил» «замещенный индолил», «замещенный изохинолил», «замещенный хинолил», «замещенный бензотиазолил», «замещенный гетероарил», «замещенный инденил» или «замещенный инданил», могут быть одинаковыми или различными, с одной или более из групп, описанных здесь, и атома водорода, атома галогена, амидо, ацетила, нитро (-NO2), гидроксила (-ОН), оксо (=O), тио (=S), сульфонила, сульфонамидо, сульфата, тио, циано, азидо, трифторметила (-CF3), метокси (-CH3), трет-бутилкарбамата (-Boc), или необязательно замещенных групп, выбранных из алкила, циклоалкила, алкенила, алкинила, алкокси, арила, арилокси, арилалкила, простого эфира, карбокси, гидроксила, гетероарила, сульфонила и гетероциклила. «Замещенная» функциональная группа может иметь один или более заместителей.
В одном неограничивающем варианте осуществления R1 и R2 представляют незамещенные фенильные группы.
В одном неограничивающем варианте осуществления R1 представляет незамещенную фенильную группу, и R2 представляет замещенную фенильную группу.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-7, имеющее следующую структуру:
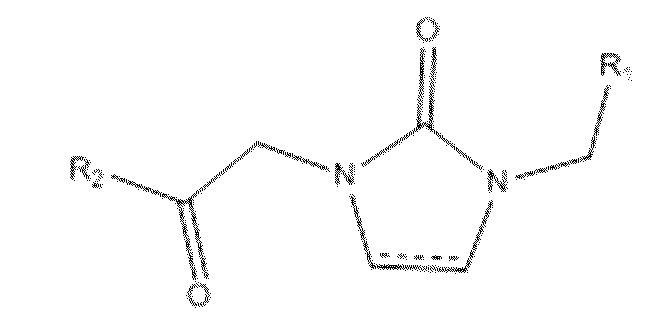
где R1 и R2 имеют значения, определенные для формулы Tm-6.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-5, имеющее следующую структуру:
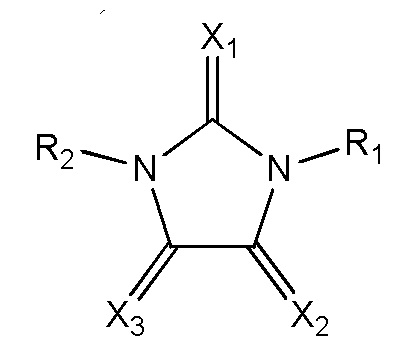
где X1 выбран из группы, состоящей из O, N(R3), S;
где Х2 и Х3 независимо выбраны из группы, состоящей из О и S;
где R3 выбран из группы, состоящей из H и разветвленного или неразветвленного низшего алкила (C1-C4); и
где R1 и R2 имеют значения, определенные выше для формулы Tm-6, и могут также представлять (CH2)nC(=X1)R1, (CH2)nC(=X1)R2, где X1 представляет О или S, и n равно 0-4.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-9, имеющее следующую структуру:
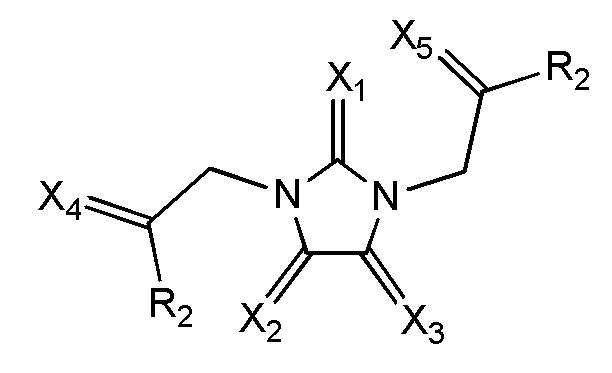
где X1-5 независимо выбраны из группы, состоящей из О и S;
и где R1 и R2 имеют значения, определенные выше для формулы Tm-6.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-10, имеющее следующую структуру:
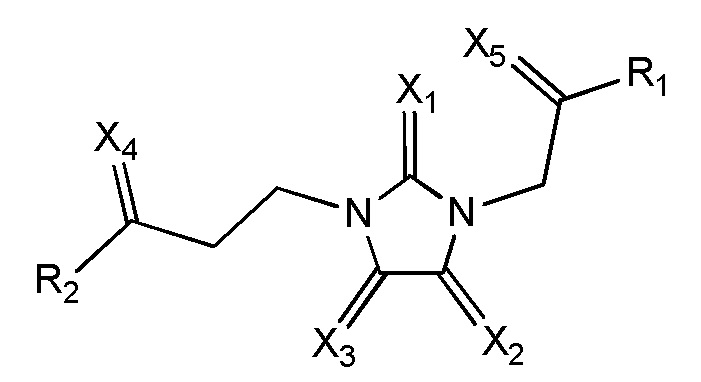
где X1-5 независимо выбраны из группы, состоящей из О и S;
и где R1 и R2 имеют значения, определенные выше для формулы Tm-6.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-11, имеющее следующую структуру:
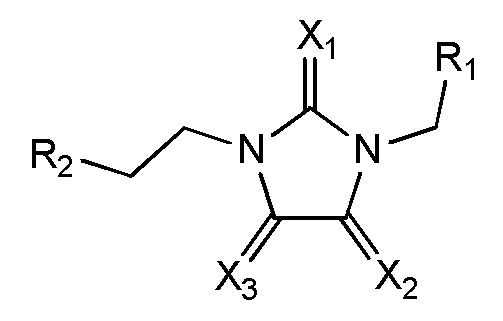
где X1-3 независимо выбраны из группы, состоящей из О и S;
и где R1 и R2 имеют значения, определенные выше для формулы Tm-6.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-56, имеющее следующую структуру:
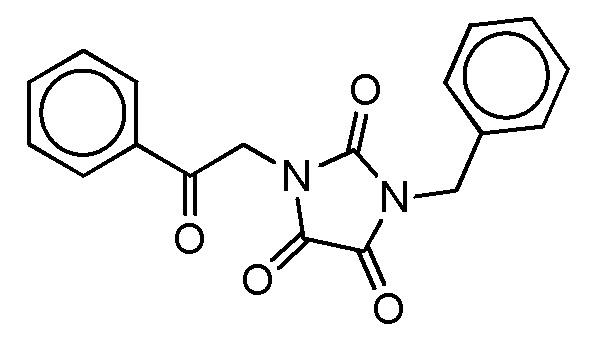
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-57, имеющее следующую структуру:
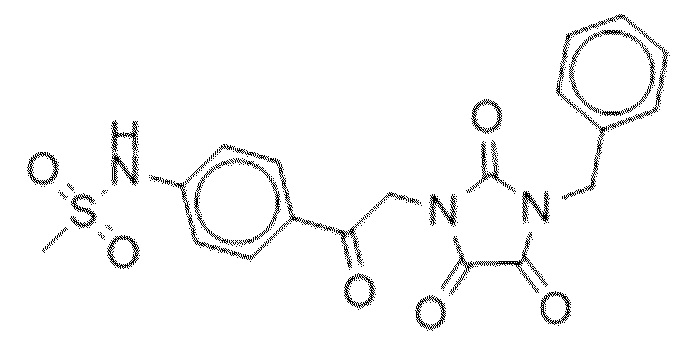
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-58, имеющее следующую структуру:
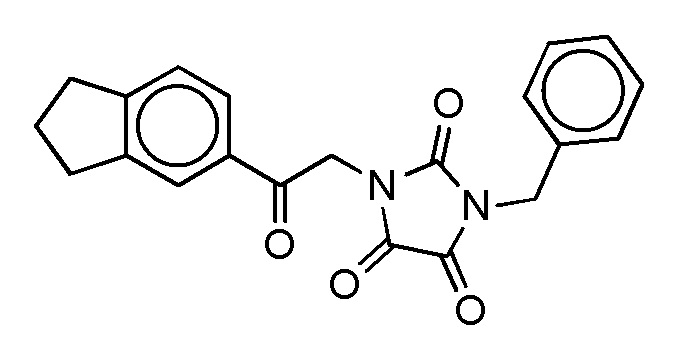
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-59, имеющее следующую структуру:
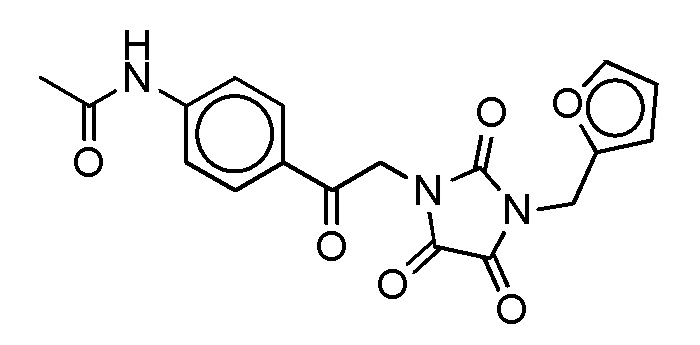
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-60, имеющее следующую структуру:
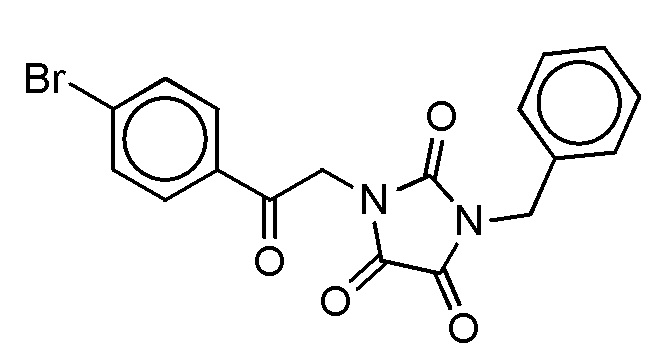
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-61, имеющее следующую структуру:
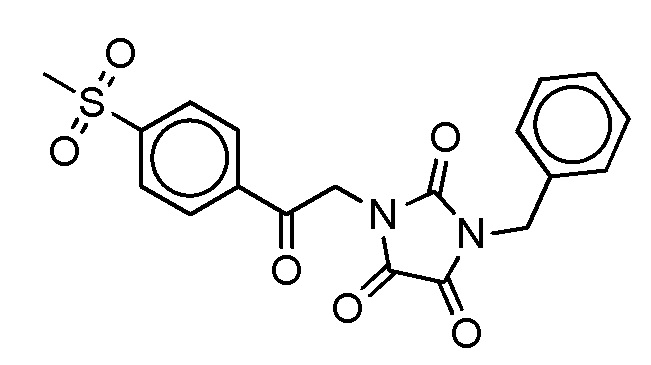
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-62, имеющее следующую структуру:
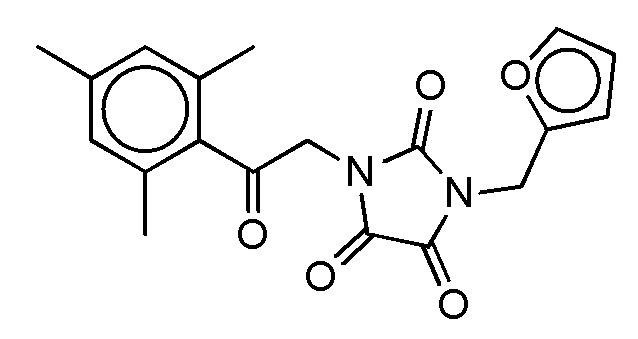
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-63, имеющее следующую структуру:
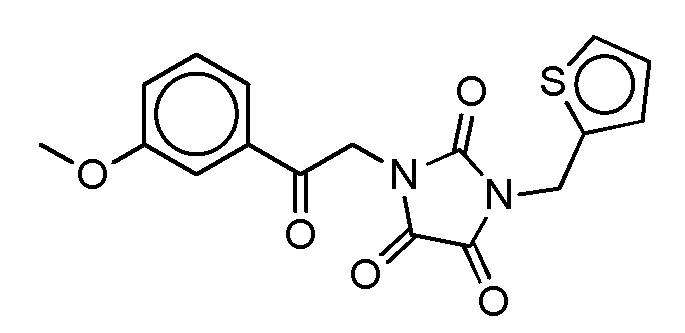
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-64, имеющее следующую структуру:
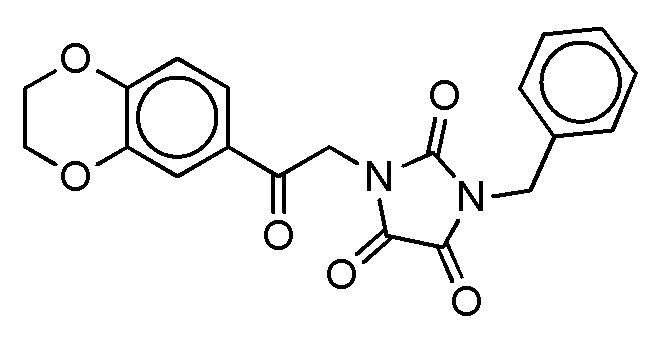
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-65, имеющее следующую структуру:
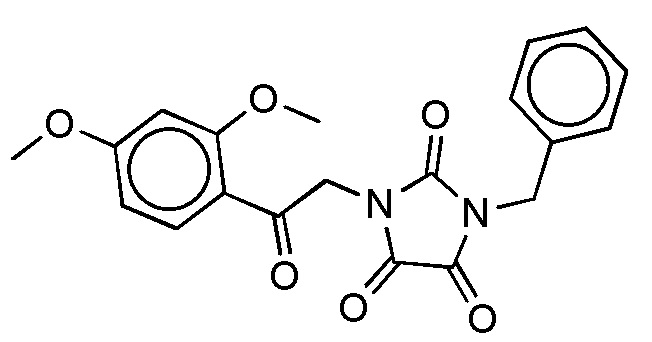
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-66, имеющее следующую структуру:
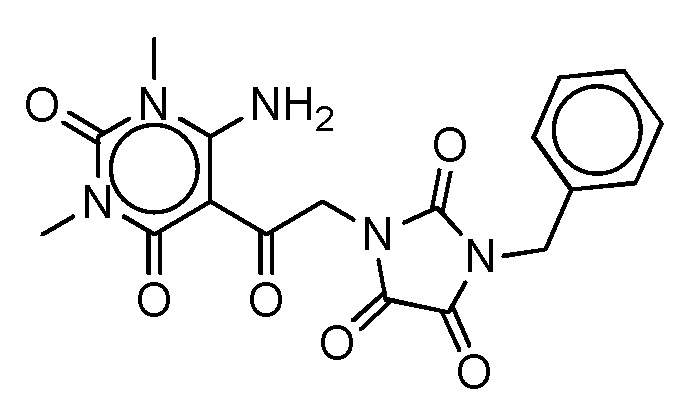
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-67, имеющее следующую структуру:

В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-68, имеющее следующую структуру:
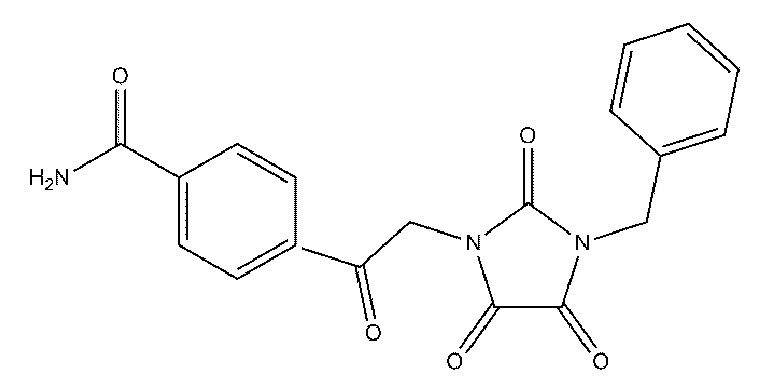
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-69, имеющее следующую структуру:
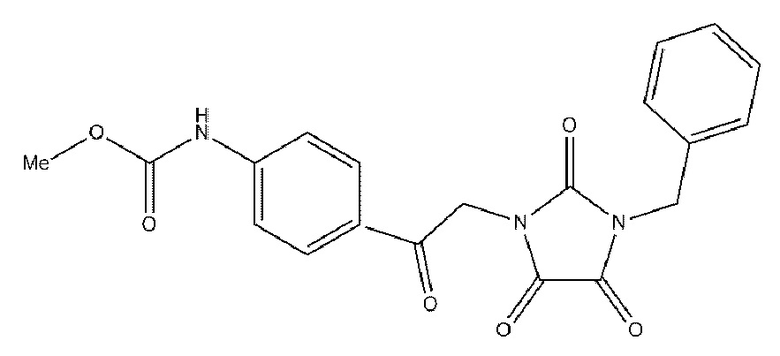
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-70, имеющее следующую структуру:
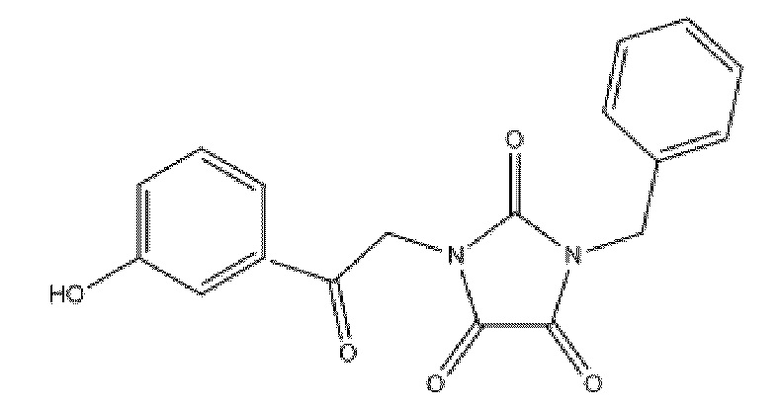
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-71, имеющее следующую структуру:
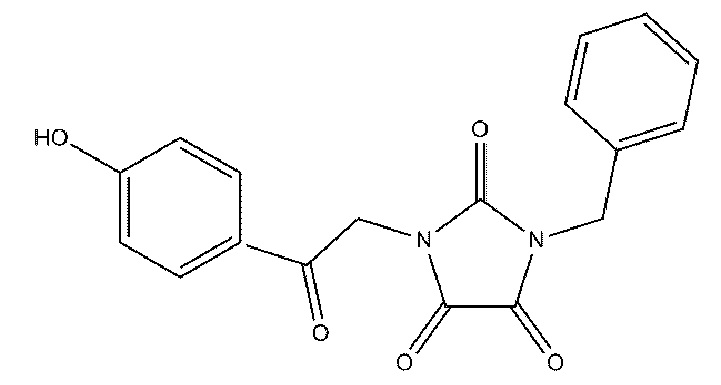
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-72, имеющее следующую структуру:
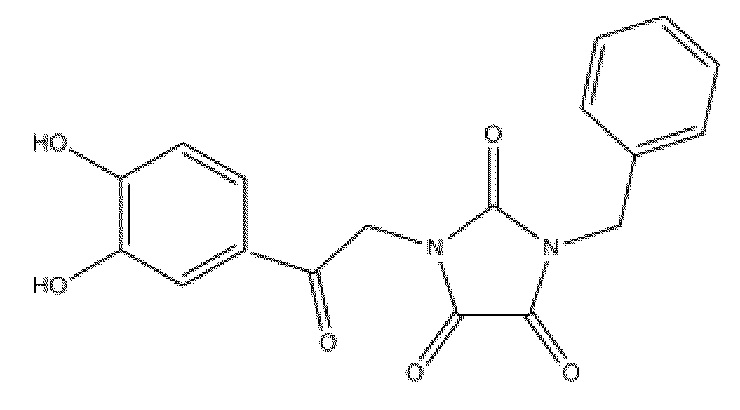
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-73, имеющее следующую структуру:
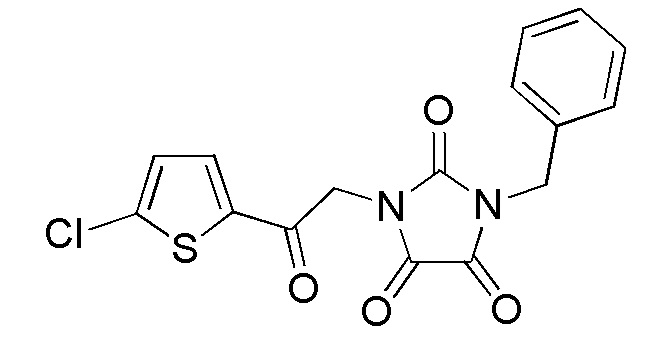
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-74, имеющее следующую структуру:
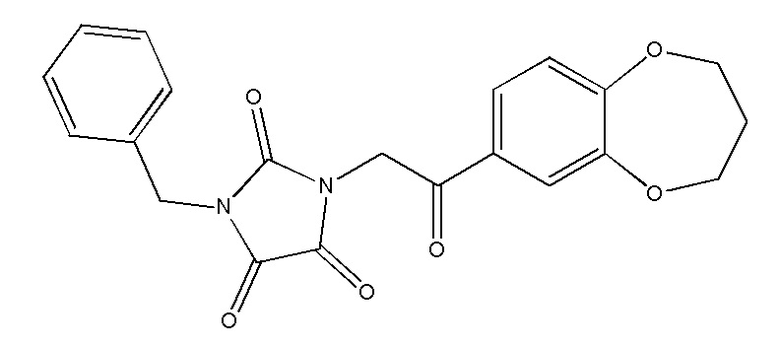
3.4. Производные имидазопиридинона
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-19, имеющее следующую структуру:
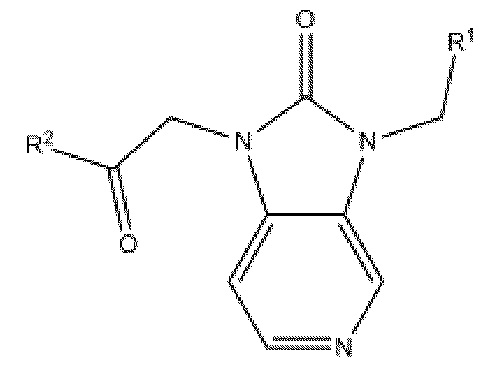
где R1 или R2 независимо выбраны из группы, состоящей из замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного алкинила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, гидроксила, атома водорода, замещенного или незамещенного простого эфира, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила, замещенного или незамещенного инденила или замещенного или незамещенного инданила.
В некоторых вариантах осуществления R1 или R2 могут содержать следующую структуру:
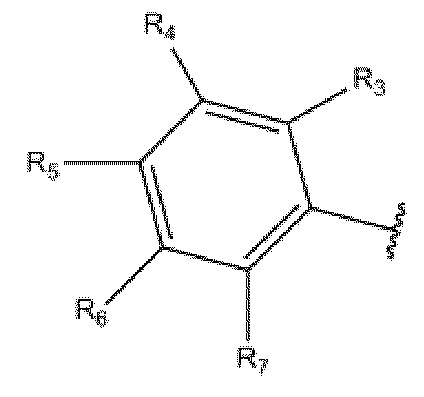
где R3, R4, R5, R6 и R7 независимо выбраны из группы, состоящей из атома водорода, атома галогена, циано, азидо, гидроксила, замещенного или незамещенного сульфонила, замещенного или незамещенного сульфонамидо, замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного амидо, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, замещенного или незамещенного простого эфира, замещенного или незамещенного карбокси, замещенного или незамещенного ацила, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила или замещенного или незамещенного гетероаренила, или замещенного или незамещенного индена или замещенного или незамещенного инданила. В некоторых вариантах осуществления два или более из R3, R4, R5, R6 и R7, взятые вместе, образуют кольцо, которое может быть гетероциклическим (т.е. содержать один или более гетероатомов) или которое может быть полностью карбоциклическим и которое независимо может быть насыщенным или ненасыщенным.
Заместители в замещенных группах, описанных здесь, таких как «замещенный простой эфир», «замещенный карбокси», «замещенный ацил», «замещенный сульфонил», «замещенный алкил», «замещенный алкенил», «замещенный циклоалкил», «замещенный циклоалкалкил» «замещенный арилалкил», «замещенный арил», «замещенный гетероциклил», «замещенный гетероарилалкил», «замещенный гетероарил», «замещенный нафтил», «замещенный фенил», «замещенный тиенил», «замещенный бензотиенил», «замещенный пиридил», «замещенный индолил», «замещенный изохинолил», «замещенный хинолил», «замещенный бензотиазолил», «замещенный гетероарил», «замещенный инденил» или «замещенный инданил», могут быть одинаковыми или различными, с одной или более группами, выбранными из групп, описанных здесь, и атома водорода, атома галогена, амидо, ацетила, нитро (-NO2), гидроксила (-ОН), оксо (=O), тио (=S), сульфонила, сульфонамидо, сульфата, тио, циано, азидо, трифторметила (-CF3), метокси (-CH3), трет-бутилкарбамата (-Boc), или необязательно замещенных групп, выбранных из алкила, циклоалкила, алкенила, алкинила, алкокси, арила, арилокси, арилалкила, простого эфира, карбокси, гидроксила, гетероарила, сульфонила и гетероциклила. «Замещенная» функциональная группа может иметь один или более заместителей.
В одном неограничивающем варианте осуществления R1 и R2 представляют незамещенные фенильные группы.
В одном неограничивающем варианте осуществления R1 представляет незамещенную фенильную группу, и R2 представляет замещенную фенильную группу.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-12, имеющее следующую структуру:
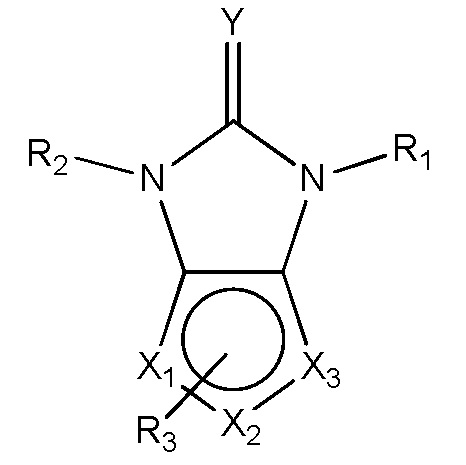
где Y выбран из группы, состоящей из O, S и N(R4);
где X1-3 независимо выбраны из группы, состоящей из С, О, N и S;
где R3 представляет замещенный или незамещенный ароматический заместитель, где заместитель представляет, например, H, OR4, S(O)nR4, N(R4)(R5), CN, COOH, COOR, C(O)N(R4)(R5), SO2N(R4)(R5), атом галогена (например, Cl, Br, Fl, I), разветвленный или неразветвленный, замещенный или незамещенный низший алкил (C1-C8), арил, биарил, P(O)(OH)2, NHOH, B(OH)2, C(=NH)NH2, NHC(=NH)NH2, NO2, CF3, -OCH2O- (т.е. метилендиокси), разветвленный или неразветвленный, замещенный или незамещенный низший алкин (C2-C6), разветвленный или неразветвленный, замещенный или незамещенный низший алкен (C2-C6), (CH2)nарил;
где R4 и R5 независимо представляют H, разветвленный или неразветвленный, замещенный или незамещенный низший алкил (C1-C8), разветвленный или неразветвленный, замещенный или незамещенный низший алкин (C2-C6), разветвленный или неразветвленный, замещенный или незамещенный низший алкен (C2-C6), арил, (CH2)nарил;
где n равно 0-4; и
где R1 и R2 имеют значения, определенные для формулы Tm-19.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-13, имеющее следующую структуру:
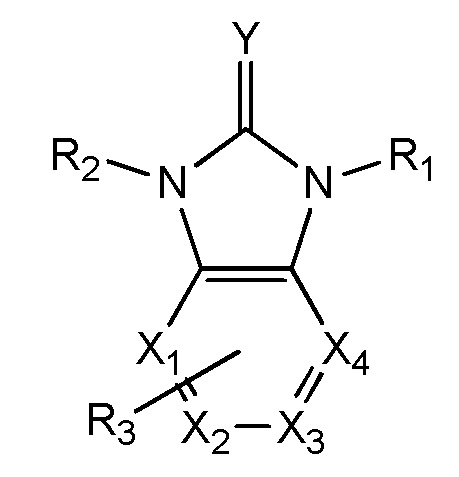
где Y выбран из группы, состоящей из O, S и N(R4);
где X1-4 независимо выбраны из группы, состоящей из С, О, N и S;
где R3 представляет замещенный или незамещенный ароматический заместитель, где заместитель представляет, например, H, OR4, S(O)nR4, N(R4)(R5), CN, COOH, COOR, C(O)N(R4)(R5), SO2N(R4)(R5), атом галогена (например, Cl, Br, Fl, I), разветвленный или неразветвленный, замещенный или незамещенный низший алкил (C1-C8), арил, биарил, P(O)(OH)2, NHOH, B(OH)2, C(=NH)NH2, NHC(=NH)NH2, NO2, CF3, -OCH2O- (т.е. метилендиокси), разветвленный или неразветвленный, замещенный или незамещенный низший алкин (C2-C6), разветвленный или неразветвленный, замещенный или незамещенный низший алкен (C2-C6), (CH2)nарил;
где R4 и R5 независимо представляют H, разветвленный или неразветвленный, замещенный или незамещенный низший алкил (C1-C8), разветвленный или неразветвленный, замещенный или незамещенный низший алкин (C2-C6), разветвленный или неразветвленный, замещенный или незамещенный низший алкен (C2-C6), арил, (CH2)nарил;
где n равно 0-4; и
где R1 и R2 имеют значения, определенные для формулы Tm-19.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-14, имеющее следующую структуру:
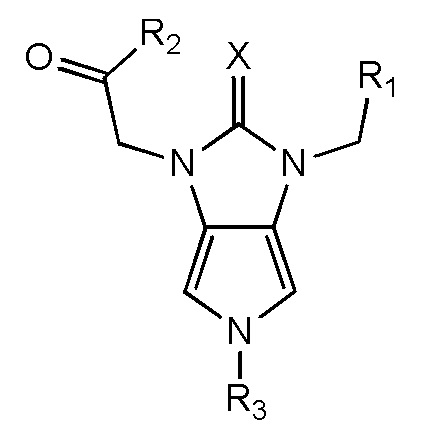
где Х выбран из группы, состоящей из С, О, N и S; и
где R1-3 имеют значения, определенные для формул Tm-19, Tm-12 и Tm-13.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-15, имеющее следующую структуру:
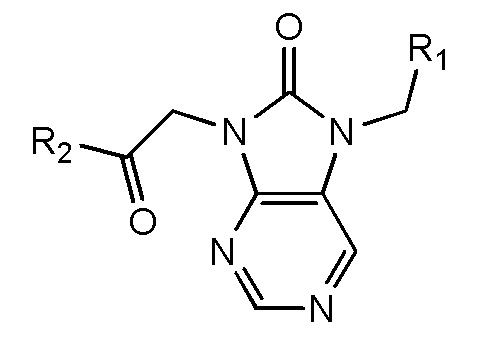
где R1-2 имеют значения, определенные для формул Tm-19, Tm-12 и Tm-13.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-16, имеющее следующую структуру:
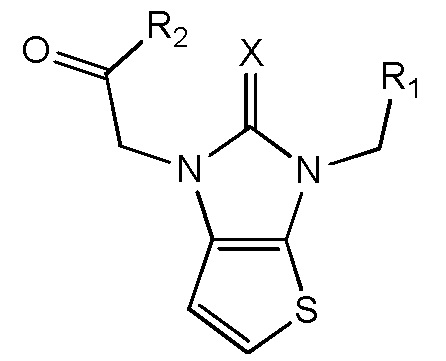
где Х выбран из группы, состоящей из С, О, N и S; и
где R1-2 имеют значения, определенные для формул Tm-19, Tm-12 и Tm-13.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-17, имеющее следующую структуру:
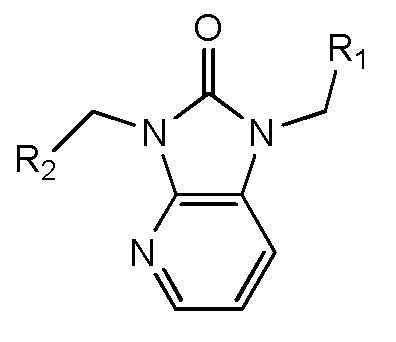
где R1-2 имеют значения, определенные для формул Tm-19, Tm-12 и Tm-13.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-18, имеющее следующую структуру:
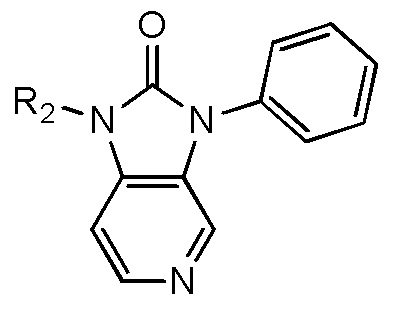
где R1 имеет значения, определенные для формул Tm-19, Tm-12 и Tm-13.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-75, имеющее следующую структуру:
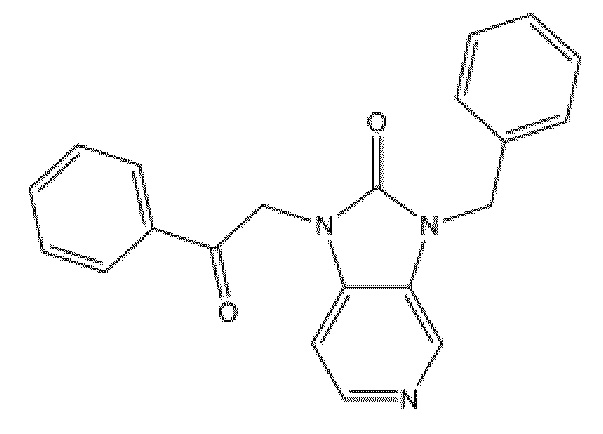
3.5. Производные пиримидин-2,4,6-триона
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-8, имеющее следующую структуру:
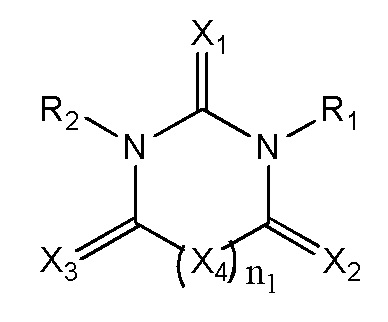
где X1 выбран из группы, состоящей из O, N(R12) и S;
где Х2 и Х3 независимо выбраны из группы, состоящей из О и S;
где X4 выбран из группы, состоящей из NH, N(R7) и C(R8,R9);
где n1 равно 0-1, и когда n1 равно 0, то химическая связь находится между двумя атомами углерода, несущими X2 и X3;
где R7, R8 и R9 независимо выбраны из группы, состоящей из Н, замещенного или незамещенного, разветвленного или неразветвленного низшего алкила (С1-С20), арила, гетероарила, циклоалкила (С3-С7) и замещенного или незамещенного, разветвленного или неразветвленного низшего алкила, C(CH2)n2арила,
замещение в алкильных и арильных группах включает функциональные группы, известные специалистам в данной области, такие как OH, NH2, атом галогена, SH, нитро, арил, алкен, COOH, COOR, C(O)N(R4)(R5), SO2N(R4)(R5), NO2, P(O)(OH)2, NHOH, B(OH)2, C(=NH)NH2, NHC(=NH)NH2, NO2 и CF3;
где R4 и R5 независимо представляют H, разветвленный или неразветвленный, замещенный или незамещенный низший алкил (C1-C8), разветвленный или неразветвленный, замещенный или незамещенный низший алкин (C2-C6), разветвленный или неразветвленный, замещенный или незамещенный низший алкен (C2-C6), арил, (CH2)nарил;
где n2 равно 0-10;
где R12 выбран из группы, состоящей из H, разветвленного или неразветвленного низшего алкила (C1-C4); и
где R1 или R2 независимо выбраны из группы, состоящей из замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного алкинила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, гидроксила, атома водорода, замещенного или незамещенного простого эфира, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила, замещенного или незамещенного инденила или замещенного или незамещенного инданила.
В некоторых вариантах осуществления R1 и/или R2 могут содержать следующую структуру:
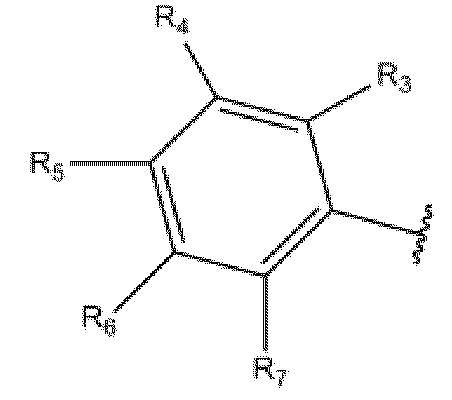
где R3, R4, R5, R6 и R7 независимо выбраны из группы, состоящей из атома водорода, атома галогена, циано, азидо, гидроксила, замещенного или незамещенного сульфонила, замещенного или незамещенного сульфонамидо, замещенного или незамещенного алкила, замещенного или незамещенного алкенила, замещенного или незамещенного циклоалкила, замещенного или незамещенного арила, замещенного или незамещенного циклоалкалкила, замещенного или незамещенного арилалкила, замещенного или незамещенного гетероарилалкила, замещенного или незамещенного гетероарила, замещенного или незамещенного амидо, замещенного или незамещенного гетероциклила, замещенного или незамещенного алкокси, замещенного или незамещенного арилокси, замещенного или незамещенного простого эфира, замещенного или незамещенного карбокси, замещенного или незамещенного ацила, замещенного или незамещенного бензотиазолила, замещенного или незамещенного пиридила, замещенного или незамещенного нафтила, замещенного или незамещенного тиенила, замещенного или незамещенного бензотиенила, замещенного или незамещенного индолила, замещенного или незамещенного изохинолила, замещенного или незамещенного хинолила или замещенного или незамещенного гетероаренила, или замещенного или незамещенного индена, или замещенного или незамещенного инданила. В некоторых вариантах осуществления два или более из R3, R4, R5, R6 и R7, взятые вместе, образуют кольцо, которое может быть гетероциклическим (т.е. содержать один или более гетероатомов) или которое может быть полностью карбоциклическим и которое независимо может быть насыщенным или ненасыщенным.
В одном неограничивающем варианте осуществления R1 и R2 представляют незамещенные фенильные группы.
В одном неограничивающем варианте осуществления R1 представляет незамещенную фенильную группу, и R2 представляет замещенную фенильную группу.
В одном неограничивающем варианте осуществления R1 и R2, имеют значения, определенные выше для формул Tm-6, Tm-19, Tm-12 и Tm-13, и также могут представлять (CH2)nC(=X1)R1, (CH2)nC(=X1)R2, где X1 представляет О или S, и n равно 0-4.
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-76, имеющее следующую структуру:
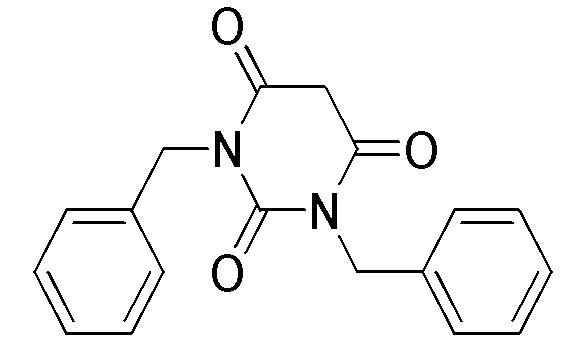
3.6. Дополнительные трансмембранные соединения
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-77, имеющее следующую структуру:
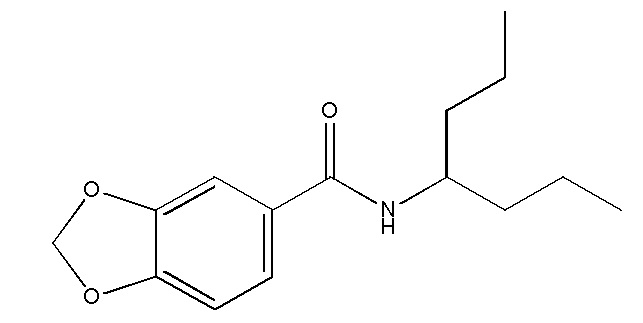
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-78, имеющее следующую структуру:
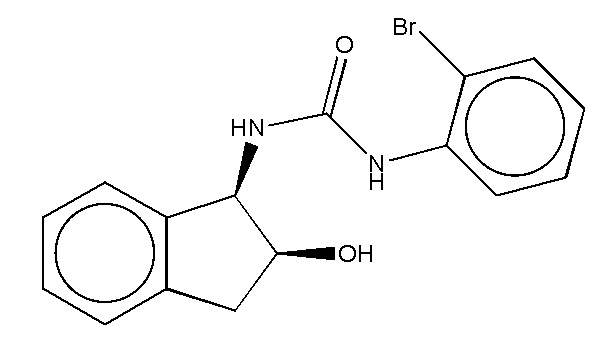
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-79, имеющее следующую структуру:
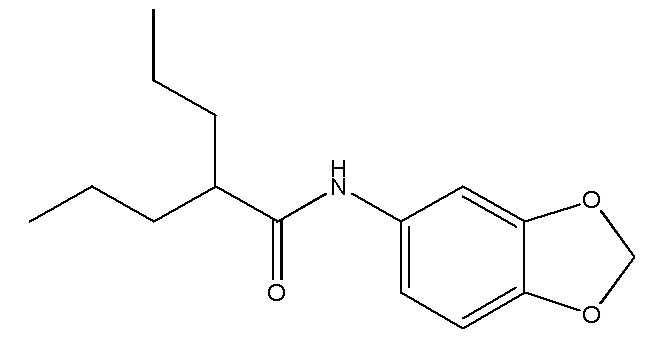
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-80, имеющее следующую структуру:
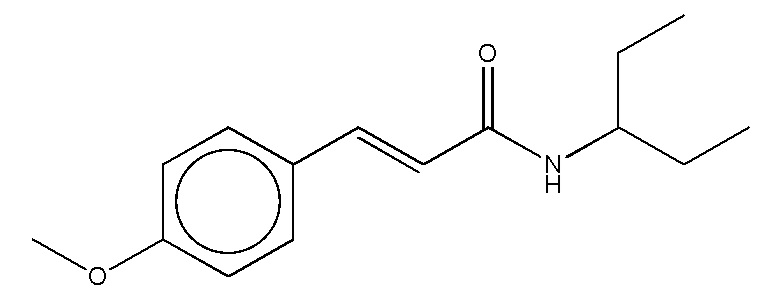
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-81, имеющее следующую структуру:
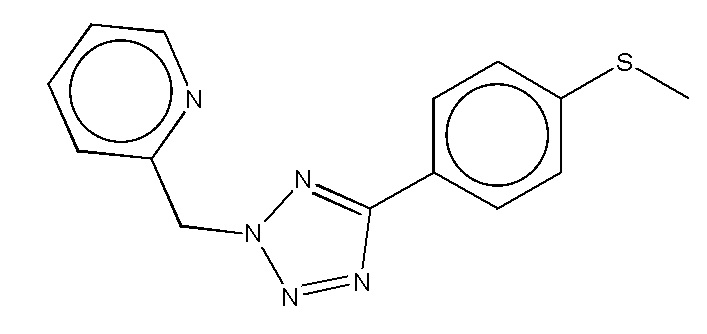
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-82, имеющее следующую структуру:
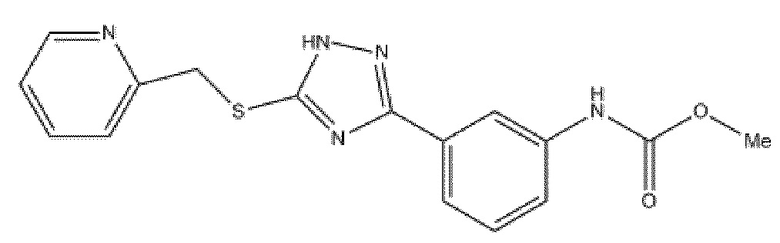
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-83, имеющее следующую структуру:
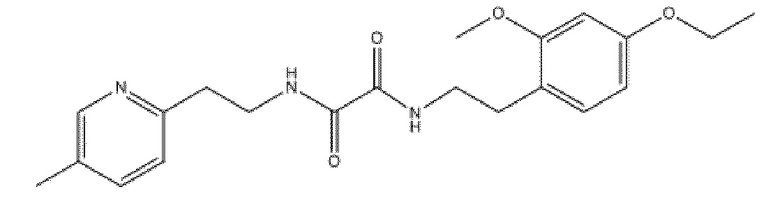
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-84, имеющее следующую структуру:
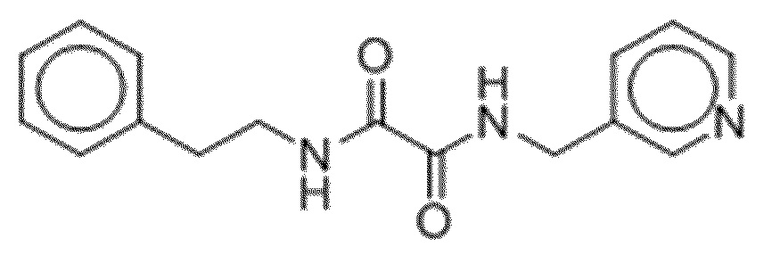
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-85, имеющее следующую структуру:
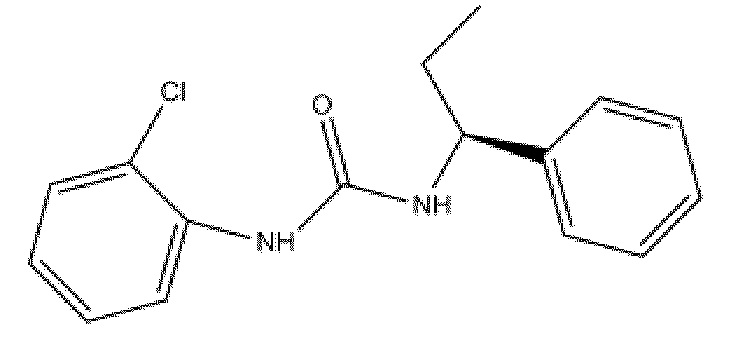
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-86, имеющее следующую структуру:
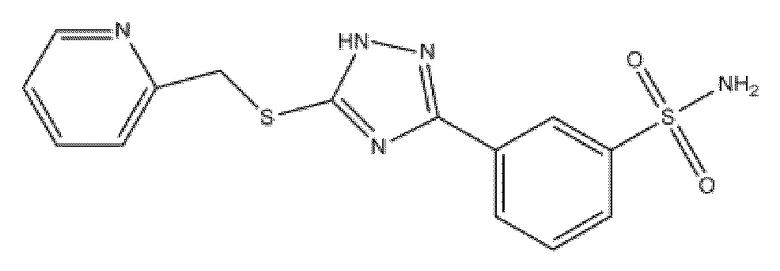
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-87, имеющее следующую структуру:
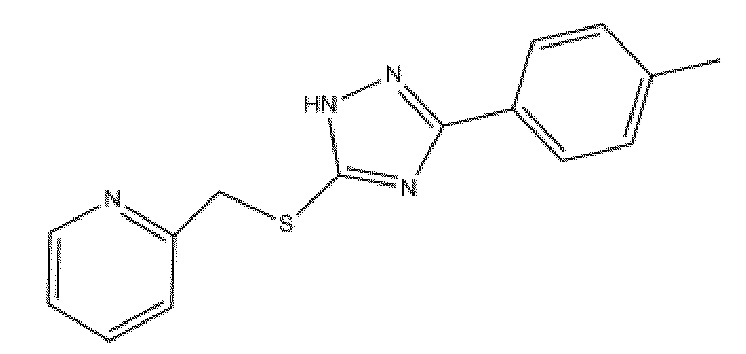
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-88, имеющее следующую структуру:
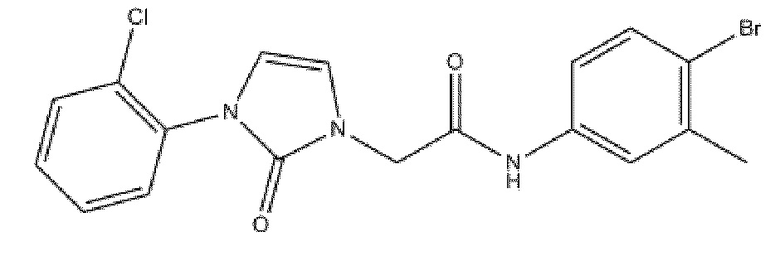
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-89, имеющее следующую структуру:
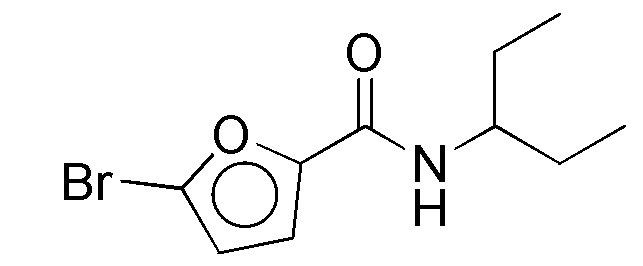
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-90, имеющее следующую структуру:
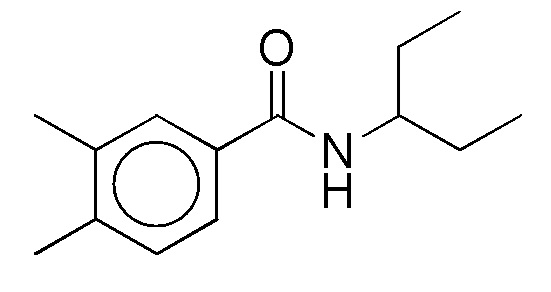
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-91, имеющее следующую структуру:
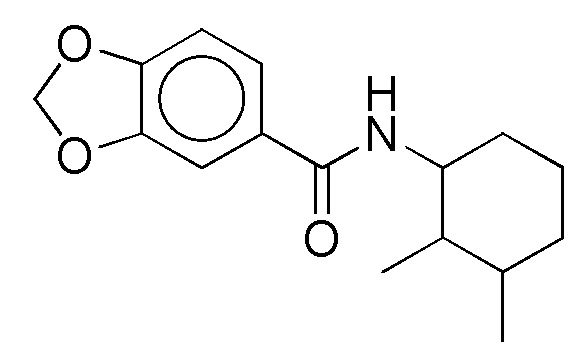
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-92, имеющее следующую структуру:
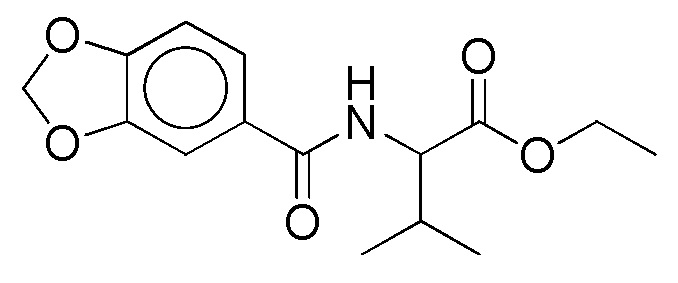
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-93, имеющее следующую структуру:
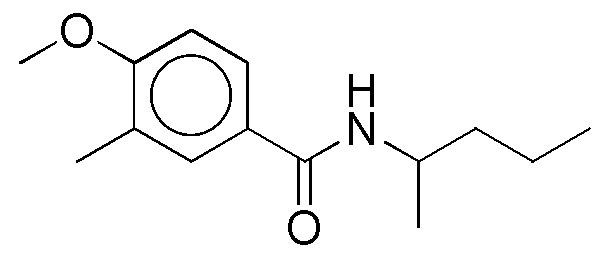
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-94, имеющее следующую структуру:
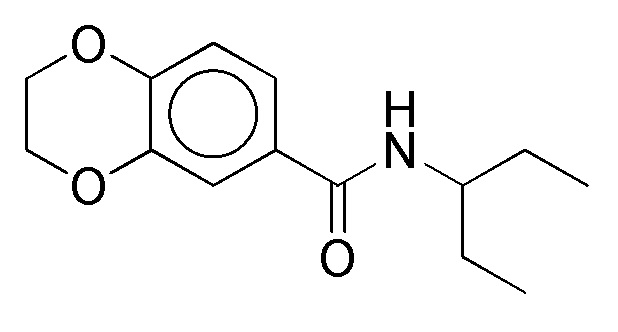
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-95, имеющее следующую структуру:
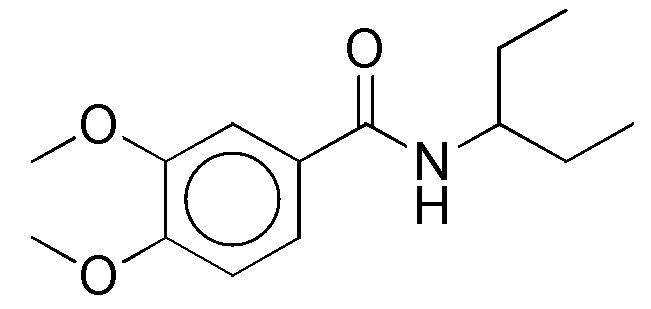
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-96, имеющее следующую структуру:
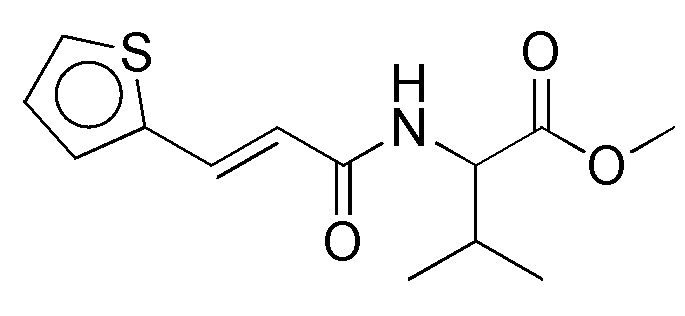
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-97, имеющее следующую структуру:
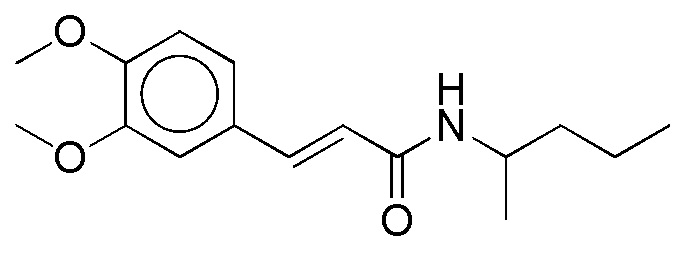
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-98, имеющее следующую структуру:
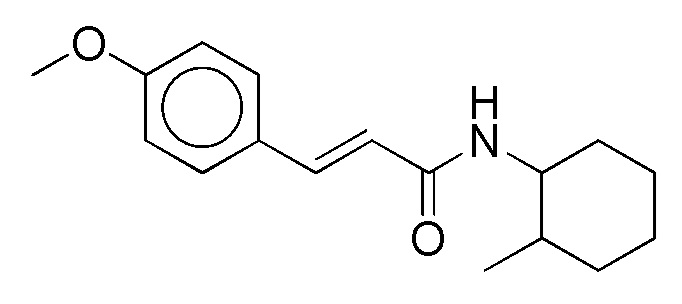
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-99, имеющее следующую структуру:
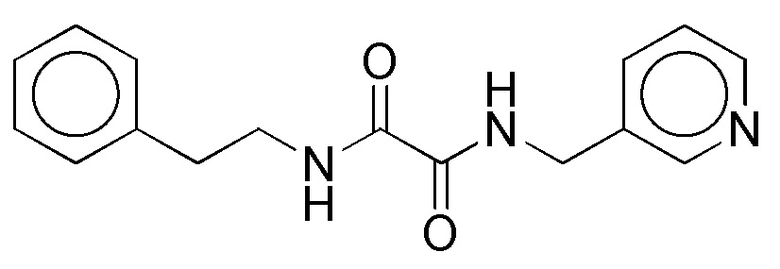
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-100, имеющее следующую структуру:
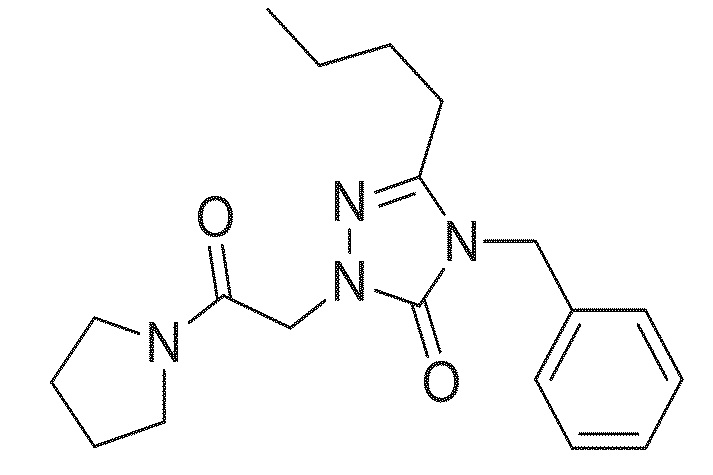
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-101, имеющее следующую структуру:
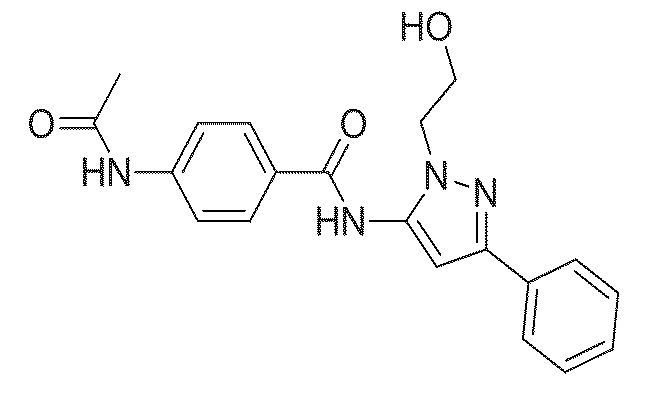
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-102, имеющее следующую структуру:
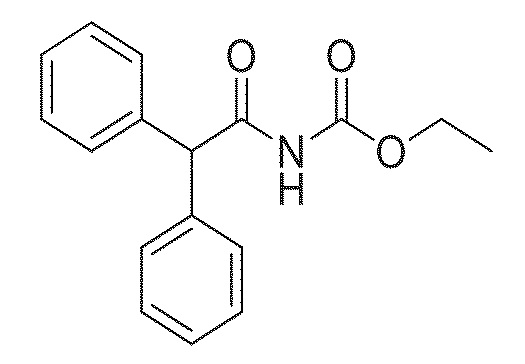
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-103, имеющее следующую структуру:
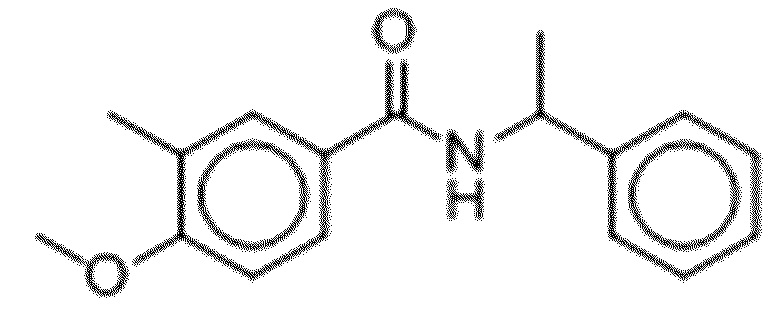
В некоторых вариантах осуществления трансмембранное соединение включает соединение формулы Tm-104, имеющее следующую структуру:
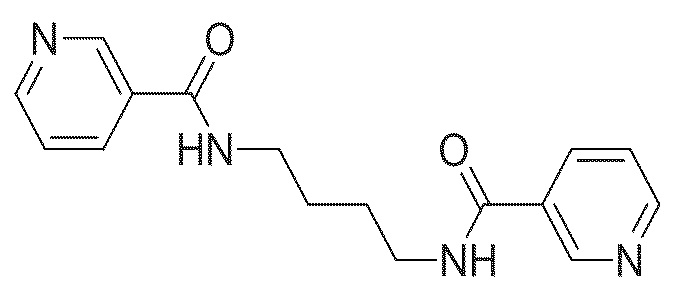
В некоторых вариантах осуществления настоящего раскрытия трансмембранное соединение включает соединение, приведенное в таблице 3 ниже.
Трансмембранные соединения
3.7. Соли трансмембранных соединений
В некоторых вариантах осуществления трансмембранные соединения по настоящему изобретению включают соль трансмембранного соединения, например, не ограничиваясь этим, ацетатную соль, TFA соль или формиатную соль. В некоторых вариантах осуществления соль трансмембранного соединения содержит анион (-) (например, не ограничиваясь этим, Cl-, F-, Br-, O2-, CO32-, HCO3-, OH-, NO3-, PO43-, SO42-, CH3COO-, HCOO-, C2O42- и CN-), связанный ионной связью с катионом (+)(например, не ограничиваясь этим, Al3+, Ca2+, Na+, K+, Cu2+, H+, Fe3+, Mg2+, Ag+, NH4+, H3O+, Hg22+). В еще одних вариантах осуществления соль трансмембранного соединения включает катион (+), связанный ионной связью с анионом (-).
В некоторых вариантах осуществления трансмембранное соединение может представлять собой соль, стереоизомер или съедобную форму трансмембранного соединения, описанного здесь, например, соединений формул от Tm-1 до Tm-104.
3.8. Сайт связывания T1R1 с трансмембранным соединением
В настоящей заявке обеспечены композиции, которые модулируют активность рецептора умами, например, рецептора T1R1/T1R3, где композиции взаимодействуют с одной или более аминокислотами в трансмембранном домене рецептора умами, например, семь трансмембранных доменов (7TM) в T1R1. В некоторых вариантах осуществления аминокислоты, с которыми взаимодействуют композиции, включают 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более аминокислот из Ala795, Ala796, Asn792, Trp773, Phe776, Ala731, Phe728, Leu730, Phe732, Asn735, Ala689, Ser686, Gln690, Ile693, Cys694, Leu695, Arg634, Gln635, Phe642, Ala639, Ala643 и Leu638.
В конкретном неограничивающем варианте осуществления аминокислоты, с которыми взаимодействуют композиции, включают аминокислоты Asn735 и/или Ser686.
В еще одних неограничивающих вариантах осуществления аминокислоты, с которыми взаимодействуют композиции, включают 1, 2, 3, 4, 5, 6, 7 или более аминокислот из Trp773, Phe776, Phe732, Phe728, Leu730, Leu695, Leu638 и Phe642.
В еще одних неограничивающих вариантах осуществления аминокислоты, с которыми взаимодействуют композиции, включают 1, 2, 3, 4 или более аминокислот из Trp773, Phe776, Phe732, Phe728 и Phe642. В неограничивающем примере аминокислоты, которые взаимодействуют с композицией, подвергаются кольцевым стэкинг-взаимодействиям со связанной композицией.
В некоторых вариантах осуществления композиция взаимодействует с доменом 7ТМ умами посредством любой комбинации взаимодействий, описанных здесь, например, одним, двумя, тремя или более взаимодействиями. Взаимодействия между нуклеотидом и/или нуклеотидным производным и 7ТМ могут также включать дополнительные гидрофобные взаимодействия, которые дополняют энергию взаимодействия нуклеотида и/или нуклеотидного производного с 7ТМ.
В некоторых вариантах осуществления взаимодействие между композицией и одной или более аминокислотами домена 7ТМ T1R1 включает одно или более из водородных связей, ковалентной связи, нековалентной связи, солевого мостика, физического взаимодействия и их комбинаций. Взаимодействия также могут представлять любую характеристику взаимодействия лиганд-рецепторного взаимодействия, известного в данной области техники. Такие взаимодействия можно определить, например, сайт-направленным мутагенезом, рентгеновской кристаллографией, рентгеновскими или другими спектроскопическими методами, ядерным магнитным резонансом (ЯМР), оценкой возникновения поперечной сшивки, масс-спектроскопией или электрофорезом, анализом вытеснения на основе известных агонистов, определением структуры и их комбинацией. В некоторых вариантах осуществления взаимодействия определяют in silico, например, с помощью теоретических способов, таких как докинг соединения в домен 7ТМ T1R1 с использованием молекулярного докинга, молекулярного моделирования, молекулярной симуляции или других способов, известных специалистам в данной области техники.
В настоящей заявке также обеспечиваются способы идентификации соединения, которое модулирует активность рецептора умами, например, T1R1, где соединение идентифицируется на основе его способности взаимодействовать с одной или более из указанных здесь аминокислот, которые присутствуют в домене 7ТМ T1R1.
В некоторых вариантах осуществления способ включает контактирование испытуемого агента с рецептором умами T1R1 кошки, детектирование взаимодействия между испытуемым агентом и одной или более аминокислотами в сайте взаимодействия 7ТМ рецептора умами T1R1 кошки и выбор в качестве соединения испытуемого агента, который взаимодействует с одной или более аминокислотами.
4. Вкусоароматические композиции
В некоторых вариантах осуществления вкусоароматические композиции по настоящему изобретению могут быть использованы для усиления вкуса умами и/или повышения вкусовой привлекательности пищевых продуктов для домашних животных, таких как пищевые продукты для кошек. Вкусоароматические композиции могут включать комбинации соединений и могут быть добавлены к пищевому продукту для домашних животных в различных системах доставки.
В некоторых вариантах осуществления настоящее раскрытие относится к способам модуляции вкуса умами пищевого продукта для домашних животных, включающим: а) обеспечение, по меньшей мере, одного пищевого продукта для домашних животных или его предшественника и b) объединение пищевого продукта для домашних животных или его предшественника, по меньшей мере, с количеством, модулирующим вкус умами, по меньшей мере, одной вкусоароматической композиции, например, содержащей одно или более нуклеотидных производных и/или одно или более трансмембранных соединений или их съедобной приемлемой соли, для получения улучшенного пищевого продукта для домашних животных.
В некоторых вариантах осуществления вкусоароматические композиции по настоящему изобретению могут усиливать вкус умами и/или вкусовую привлекательность пищевого продукта для домашних животных, например, такого как пищевой продукт для домашних животных, включая влажные пищевые продукты для домашних животных, сухие пищевые продукты для домашних животных, сырые пищевые продукты для домашних животных, напитки для домашних животных и/или закуски для домашних животных.
В некоторых вариантах осуществления одна или более вкусоароматических композиций по настоящему изобретению могут быть добавлены к пищевому продукту для домашних животных в количестве, эффективном для модификации, улучшения или иного изменения вкуса или профиля вкуса пищевого продукта для домашних животных. Модификация может включать, например, повышение или усиление вкуса умами пищевого продукта для домашних животных, как определяется животными, например, кошками и/или собаками, или в случае тестирования композиции определяется группой животных-дегустаторов вкуса, например, кошками и/или собаками, с помощью процедур, известных в данной области.
В некоторых вариантах осуществления настоящего раскрытия может быть получен пищевой продукт для домашних животных, который содержит достаточное количество, по меньшей мере, одной вкусоароматической композиции, описанной здесь, например, содержащей нуклеотидное производное, например соединение формулы Nt-1, с получением пищевого продукта для домашних животных, имеющего желаемый вкус, например, умами.
В некоторых вариантах осуществления настоящего раскрытия может быть получен пищевой продукт для домашних животных, который содержит достаточное количество, по меньшей мере, одной вкусоароматической композиции, описанной здесь, например, содержащей трансмембранное соединение, например соединение формулы от Tm-1 до Tm-19, с получением пищевого продукта для домашних животных, имеющего желаемый вкус, например, умами.
В некоторых вариантах осуществления настоящего раскрытия может быть получен пищевой продукт для домашних животных, который содержит достаточное количество вкусоароматической композиции, содержащей, по меньшей мере, одно, два, три, четыре, пять, шесть или более нуклеотидных производных.
В некоторых вариантах осуществления настоящего изобретения может быть получен пищевой продукт для домашних животных, который содержит достаточное количество вкусоароматической композиции, содержащей, по меньшей мере, одно, два, три, четыре, пять, шесть или более трансмембранных соединений.
В некоторых вариантах осуществления модулирующее количество одной или более вкусоароматических композиций по настоящему изобретению может быть добавлено к пищевому продукту для домашних животных для того, чтобы пищевой продукт для домашних животных обладал повышенной вкусовой привлекательностью по сравнению с пищевым продуктом для домашних животных, приготовленным без вкусоароматической композиции, как определяется животными, например, кошками и/или собаками, или в случае тестирования композиции группой животных-дегустаторов вкуса, например, кошками и/или собаками, с помощью процедур, известных в данной области.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция добавляется к пищевому продукту для домашних животных в количестве, эффективном для повышения, усиления и/или модификации вкусовой привлекательности пищевого продукта для домашних животных.
Концентрация вкусоароматической композиции, смешанной с пищевым продуктом для домашних животных, для модуляции и/или улучшения вкусовой привлекательности и/или вкуса умами пищевого продукта для домашних животных, может варьироваться в зависимости от переменных факторов, например, таких как, конкретный тип пищевого продукта для домашних животных, какие соединения, придающие вкус умами, уже присутствуют в пищевом продукте для домашних животных и их концентрации, и также усиливающий эффект конкретной вкусоароматической композиции для таких соединений умами.
Широкий диапазон концентраций вкусоароматических композиций может быть использован для обеспечения такой модификации вкусовой привлекательности и/или вкуса умами. В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция смешивается с пищевым продуктом для домашних животных, где вкусоароматическая композиция присутствует в количестве примерно от 0,001 ppm до примерно 1000 ppm. Например, и не в качестве ограничения, вкусоароматическая композиция может присутствовать в количестве примерно от 0,001 ppm до примерно 750 ppm, примерно от 0,001 ppm до примерно 500 ppm, примерно от 0,001 ppm до примерно 250 ppm, примерно от 0,001 ppm до примерно 150 ppm, примерно от 0,001 ppm до примерно 100 ppm, примерно от 0,001 ppm до примерно 75 ppm, примерно от 0,001 ppm до примерно 50 ppm, примерно от 0,001 ppm до примерно 25 ppm, примерно от 0,001 ppm до примерно 15 ppm, примерно от 0,001 ppm до примерно 10 ppm, примерно от 0,001 до примерно 5 ppm, примерно от 0,001 ppm до примерно 4 ppm, примерно от 0,001 ppm до примерно 3 ppm, примерно от 0,001 ppm до примерно 2 ppm, примерно от 0,001 ppm до примерно 1 ppm, примерно от 0,01 ppm до примерно 1000 ppm, примерно от 0,1 ppm до примерно 1000 ppm, примерно от 1 ppm до 1000 ppm, примерно от 2 ppm до примерно 1000 ppm, примерно от 3 ppm до примерно 1000 ppm, примерно от 4 ppm до примерно 1000 ppm, примерно от 5 ppm до примерно 1000 ppm, примерно от 10 ppm до примерно 1000 ppm, примерно от 15 ppm до примерно 1000 ppm, примерно от 25 ppm до примерно 1000 ppm, примерно от 50 ppm до примерно 1000 ppm, примерно от 75 до примерно 1000 ppm, примерно от 100 ppm до примерно 1000 ppm, примерно от 150 ppm до примерно 1000 ppm, примерно от 250 ppm до примерно 1000 ppm, примерно от 250 ppm до примерно 1000 ppm, примерно от 500 ppm до примерно 1000 ppm или примерно от 750 ppm до примерно 1000 ppm, и значения между ними.
В некоторых вариантах осуществления вкусоароматическая композиция присутствует в пищевом продукте для домашних животных в количестве выше примерно 0,001 ppm, выше примерно 0,01 ppm, выше примерно 0,1 ppm, выше примерно 1 ppm, выше примерно 2 ppm, выше примерно 3 ppm, выше примерно 4 ppm, выше примерно 5 ppm, выше примерно 10 ppm, выше примерно 25 ppm, выше примерно 50 ppm, выше примерно 75 ppm, выше примерно 100 ppm, выше примерно 250 ppm, выше примерно 500 ppm, выше примерно 750 ppm или выше примерно 1000 ppm, и значения между ними.
В некоторых вариантах осуществления нуклеотидное производное по настоящему раскрытию присутствует в пищевом продукте в количестве, достаточном для модуляции, активации и/или усиления рецептора умами, например, рецептора T1R1/T1R3. Например, не ограничиваясь этим, нуклеотидное производное может присутствовать в пищевом продукте в количестве примерно от 1 пМ до примерно 1 М, примерно от 1 нМ до примерно 1 М, примерно от 1 мкМ до примерно 1 М, примерно от 1 мМ до примерно 1 М, примерно от 10 мМ до примерно 1 М, примерно от 100 мМ до примерно 1 М, примерно от 250 мМ до примерно 1 М, примерно от 500 мМ до примерно 1 М, примерно от 750 мМ до примерно 1 М, примерно от 0,001 мкМ до примерно 1 М, примерно от 0,001 мкМ до примерно 750 мМ, примерно от 0,001 мкМ до примерно 500 мМ, примерно от 0,001 мкМ до примерно 250 мМ, примерно от 0,001 мкМ до примерно 100 мМ, примерно от 0,001 мкМ до примерно 50 мМ, примерно от 0,001 мкМ до примерно 25 мМ, примерно от 0,001 мкМ до примерно 10 мМ, примерно от 0,001 мкМ до примерно 1 мМ, примерно от 0,001 мкМ до примерно 100 мкМ или примерно от 0,001 мкМ до примерно 10 мкМ, и значения между ними.
В некоторых вариантах осуществления трансмембранное соединение по настоящему раскрытию присутствует в количестве соединения, достаточном для модуляции, активации и/или усиления рецептора умами, например, рецептора T1R1/T1R3 кошки. Например, не ограничиваясь этим, трансмембранное соединение может присутствовать в пищевом продукте в количестве примерно от 1 пМ до примерно 10 М, примерно от 1 пМ до примерно 1 М, примерно от 1 мкМ до примерно 1 М, примерно от 1 мМ до примерно 1 М, примерно от 10 мМ до примерно 1 М, примерно от 100 мМ до примерно 1 М, примерно от 250 мМ до примерно 1 М, примерно от 500 мМ до примерно 1 М, примерно от 750 мМ до примерно 1 М, примерно от 1 мкМ до примерно 1 М, примерно от 1 мкМ до примерно 750 мМ, примерно от 1 мкМ до примерно 500 мМ, примерно от 1 мкМ до примерно 250 мМ, примерно от 1 мкМ до примерно 100 мМ, примерно от 1 мкМ до примерно 50 мМ, примерно от 1 мкМ до примерно 25 мМ, примерно от 1 мкМ до примерно 10 мМ, примерно от 1 мкМ до примерно 1 мМ, примерно от 1 мкМ до примерно 100 мкМ или примерно от 1 мкМ до примерно 10 мкМ, и значения между ними.
В некоторых вариантах осуществления настоящей заявки вкусоароматическая композиция смешивается с пищевым продуктом, где вкусоароматическая композиция присутствует в количестве примерно от 0,0001 до около 10 мас.% (мас./мас.) к общей массе пищевого продукта. Например, но не в качестве ограничения, вкусоароматическая композиция может присутствовать в количестве примерно от 0,00001 мас.% до примерно 10 мас.%, примерно от 0,0001 мас.% до примерно 1 мас.%, примерно от 0,0001 мас.% до примерно 0,1 мас.%, примерно от 0,0001 мас.% до примерно 0,01 мас.%, примерно от 0,0001 мас.% до примерно 0,001 мас.%, примерно от 0,001 мас.% до примерно 10 мас.%, примерно от 0,001 мас.% до примерно 1 мас.%, примерно от 0,01 мас.% до примерно 1 мас.% или примерно от 0,1 мас.% до примерно 1 мас.%, и значения между ними.
В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения по настоящему изобретению смешиваются вместе в различных соотношениях или смешиваются вместе с другими соединениями, например, нуклеотидами и/или аминокислотами, и/или фуранонами, с образованием различных вкусоароматических композиций. Неограничивающие примеры нуклеотидов, аминокислот и фуранонов раскрыты в патентных заявках PCT/EP2013/072788, PCT/EP2013/072789, PCT/EP2013/072790 и PCT/EP2013/072794, которые включены здесь во всей их полноте в качестве ссылки. В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения, которые смешиваются с другими соединениями, представляют одно или более соединений формулы от Nt-1 до Nt-55 и/или одно или более соединений формулы от Tm-1 до Tm-104.
В некоторых вариантах осуществления нуклеотидные производные, которые смешиваются с другими соединениями, включают нуклеотидные производные формул от Nt-1 до Nt-55 и приведенные в таблицах 2 и 6-14.
В некоторых вариантах осуществления трансмембранные соединения, которые смешиваются с другими соединениями, включают трансмембранные соединения формул от Tm-1 до Tm-104.
4.1. Нуклеотиды
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, одно нуклеотидное производное и/или, по меньшей мере, одно трансмембранное соединение и, по меньшей мере, один нуклеотид, как здесь описано.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, два, три, четыре, пять или более нуклеотидов, как здесь описано. Неограничивающие примеры нуклеотидов включают гуанозинмонофосфат (GMP), гуанозиндифосфат (GDP), гуанозинтрифосфат (GTP), аденозинмонофосфат (AMP), аденозиндифосфат (ADP), аденозинтрифосфат (АТФ), цитидинмонофосфат (CMP), цитидиндифосфат (CDP), цитидинтрифосфат (CTP), инозинмонофосфат (IMP), инозиндифосфат (IDP, инозинтрифосфат (ITP), уридинмонофосфат (UMP), уридиндифосфат (UDP), уридинтрифосфат (UTP), тимидинмонофосфат (TMP), тимидиндифосфат (TDP), тимидинтрифосфат (TTP) и ксантозинмонофосфат (XMP), ксантозиндифосфат (XDP) и ксантозинтрифосфат (XTP), или любое нуклеотидное производное, описанное формулой Nt-1.
В некоторых вариантах осуществления вкусоароматическая композиция может включать нуклеотид, присутствующий в пищевом продукте, который может присутствовать в количестве примерно от 1 пМ до примерно 1 М, примерно от 1 нМ до примерно 1 М, примерно от 1 мкМ до примерно 1 М, примерно от 1 мМ до примерно 1 М, примерно от 10 мМ до примерно 1 М, примерно от 100 мМ до примерно 1 М, примерно от 250 мМ до примерно 1 М, примерно от 500 мМ до примерно 1 М, примерно от 750 мМ до примерно 1 М, примерно от 1 мкМ до примерно 1 М, примерно от 1 мкМ до примерно 750 мМ, примерно от 1 мкМ до примерно 500 мМ, примерно от 1 мкМ до примерно 250 мМ, примерно от 1 мкМ до примерно 100 мМ, примерно от 1 мкМ до примерно 50 мМ, примерно от 1 мкМ до примерно 25 мМ, примерно от 1 мкМ до примерно 10 мМ, примерно от 1 мкМ до примерно 1 мМ, примерно от 1 мкМ до примерно 100 мкМ или примерно от 1 мкМ до примерно 10 мкМ, и значения между ними.
В некоторых вариантах осуществления нуклеотид может присутствовать в количестве выше примерно 1 мМ или выше примерно 2,5 мМ к общей массе пищевого продукта для домашних животных. В некоторых неограничивающих вариантах осуществления нуклеотид и/или нуклеотидное производное может присутствовать в количестве ниже примерно 100 мМ, ниже примерно 50 мМ, ниже примерно 20 мМ или ниже примерно 10 мМ к общей массе пищевого продукта для домашних животных. В некоторых неограничивающих вариантах осуществления нуклеотид присутствует в количестве примерно 5 мМ к общей массе пищевого продукта для домашних животных.
В некоторых вариантах осуществления вкусоароматическая композиция содержит, по меньшей мере, одно трансмембранное соединение и, по меньшей мере, один нуклеотид и/или нуклеотидное производное, которое может представлять IMP, GMP или их смесь. В некоторых вариантах осуществления, по меньшей мере, один нуклеотид может представлять комбинацию GMP и IMP, содержащую примерно от 1% до примерно 99% GMP и примерно от 1% до примерно 99% IMP, или примерно от 20% до примерно 80% GMP и примерно от 20% до примерно 80% IMP, или примерно 50% GMP и примерно 50% IMP, или примерно 10% GMP и примерно 90% IMP, или примерно 20% GMP и примерно 80% IMP, или примерно 30% GMP и примерно 70% IMP, или примерно 40% GMP и примерно 60% IMP, или примерно 60% GMP и примерно 40% IMP, или примерно 70% GMP и примерно 30% IMP, или примерно 80% GMP и примерно 20% IMP или примерно 10% GMP и примерно 90% IMP.
В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция дополнительно содержит, по меньшей мере, одну аминокислоту, как здесь описано.
4.2. Аминокислоты
В некоторых вариантах осуществления настоящего изобретения вкусоароматическая композиция содержит, по меньшей мере, одно нуклеотидное производное и/или, по меньшей мере, одно трансмембранное соединение и, по меньшей мере, одну аминокислоту, как здесь описано. В некоторых вариантах осуществления вкусоароматическая композиция содержит, по меньшей мере, две, три, четыре, пять или более аминокислот, как здесь описано.
В некоторых вариантах осуществления вкусоароматическая композиция содержит, по меньшей мере, одну, две, три, четыре, пять или более первых аминокислот и/или, по меньшей мере, одну, две, три, четыре, пять или более вторых аминокислот.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, одну первую аминокислоту и, по меньшей мере, одну вторую аминокислоту.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, две первые аминокислоты и, по меньшей мере, одну вторую аминокислоту.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, одну первую аминокислоту и, по меньшей мере, две вторые аминокислоты.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция содержит, по меньшей мере, две первые аминокислоты и, по меньшей мере, две вторые аминокислоты.
В некоторых вариантах осуществления настоящего раскрытия вкусоароматическая композиция дополнительно содержит, по меньшей мере, один нуклеотид, как здесь описано.
Неограничивающие примеры первой аминокислоты включают триптофан, фенилаланин, гистидин, глицин, цистеин, аланин, тирозин, серин, метионин, аспарагин, лейцин и их комбинации.
Неограничивающие примеры второй аминокислоты включают аспарагин, треонин, изолейцин, пролин, глутаминовую кислоту, аспарагиновую кислоту, гидроксипролин, аргинин, цистин, глутамин, лизин, валин, орнитин, таурин, глутамат мононатрия (MSG) и их комбинации.
В некоторых вариантах осуществления, по меньшей мере, одна первая аминокислота и/или вторая аминокислота, одна или в комбинации, могут присутствовать в количестве примерно от 1 мМ до примерно 1 М или примерно от 250 мМ до примерно 1 М, или примерно от 5 мМ до примерно 500 мМ или примерно от 10 мМ до примерно 100 мМ или примерно от 15 мМ до примерно 50 мМ или примерно от 20 мМ до примерно 40 мМ к общей массе пищевого продукта для домашних животных. В некоторых вариантах осуществления аминокислота(ы) может присутствовать в количестве ниже примерно 1 М, ниже примерно 200 мМ, ниже примерно 100 мМ, ниже примерно 50 мМ, ниже примерно 20 мМ или ниже примерно 10 мМ к общей массе пищевого продукта для домашних животных. В некоторых вариантах осуществления первая аминокислота и/или вторая аминокислота, одна или в комбинации, может присутствовать в количестве примерно 25 мМ к общей массе пищевого продукта для домашних животных.
4.2.1. Сайт связывания T1R1 с аминокислотами
Аминокислоты композиций, описанных здесь, которые модулируют рецептор умами, например, рецептор T1R1/T1R3, могут взаимодействовать с одной или более аминокислотами в домене Venus Flytrap рецептора умами. В некоторых вариантах осуществления домен Venus Flytrap (VFT) присутствует в T1R1. В некоторых вариантах осуществления аминокислоты VFT, с которыми взаимодействует композиция, включают одну или более аминокислот из Thr149, Tyr220, Thr148, Thr449, Ser172, Glu170, Glu301, His71, His47, Arg277, His308, Asn69, Asn302, Ser306, Ser384, Asp302, Ser306 и Ala380.
В одном неограничивающем варианте осуществления композиция содержит аминокислоту, где аминокислота взаимодействует с одной, двумя, тремя, четырьмя, пятью, шестью или более аминокислотами из Ser172, Thr149, Thr148, Glu301, Tyr220, Glu170 и Asp302 T1R1.
В еще одних неограничивающих вариантах осуществления композиция взаимодействует с одной, двумя, тремя, четырьмя, пятью или более аминокислотами из Thr149, Ser172, Tyr220, Thr148, Glu170 и/или Asp302, где взаимодействия могут включать, например, водородные связи, солевые мостики и/или катион-пи взаимодействия.
В неограничивающем примере композиция взаимодействует с Glu170 и/или Asp302 в домене VFT, где композиция не содержит L-глутамат или L-аспарагиновую кислоту. В одном варианте осуществления Glu170 и Asp302 помогают координировать цвиттерионный азот аминокислотного лиганда композиции, который подходит активному сайту T1R1, одновременно создавая электростатическую среду, которая является «негостеприимной» для связывания L-глутамата и L-аспарагиновой кислоты.
В некоторых вариантах осуществления композиция взаимодействует с доменом VFT посредством любой комбинации взаимодействий, описанных здесь, например, одним, двумя, тремя или более взаимодействиями. Взаимодействия между аминокислотой и VFT могут также включать дополнительные гидрофобные взаимодействия, которые дополняют энергию взаимодействия аминокислоты с VFT.
В некоторых вариантах осуществления взаимодействие между композицией и одной или более аминокислотами включает одно или более из водородных связей, ковалентной связи, нековалентной связи, солевого мостика, физического взаимодействия и их комбинаций. Взаимодействия также могут представлять любую характеристику взаимодействия лиганд-рецепторного взаимодействия, известного в данной области техники. Такие взаимодействия можно определить, например, сайт-направленным мутагенезом, рентгеновской кристаллографией, рентгеновскими или другими спектроскопическими методами, ядерным магнитным резонансом (ЯМР), оценкой возникновения поперечной сшивки, масс-спектроскопией или электрофорезом, анализом вытеснения на основе известных агонистов, определением структуры и их комбинацией. В некоторых вариантах осуществления взаимодействия определяют in silico, например, с помощью теоретических способов, таких как докинг соединения в домен VFT с использованием молекулярного докинга, молекулярного моделирования, молекулярной симуляции или других способов, известных специалистам в данной области техники.
В настоящей заявке также обеспечиваются способы идентификации соединения, которое модулирует активность рецептора умами, например, T1R1, где соединение идентифицируется на основе его способности взаимодействовать с одной или более из указанных здесь аминокислот, которые присутствуют в домене VFT T1R1.
В некоторых вариантах осуществления способ включает контактирование испытуемого агента с рецептором умами T1R1 кошки, детектирование взаимодействия между испытуемым агентом и одной или более аминокислотами в сайте взаимодействия VFT рецептора умами T1R1 кошки и выбор в качестве соединения испытуемого агента, который взаимодействует с одной или более аминокислотами.
5. Системы доставки
В некоторых вариантах осуществления вкусоароматические композиции по настоящему изобретению могут быть включены в систему доставки для применения в пищевых продуктах для домашних животных. Системы доставки могут быть жидкими или твердыми, водными или неводными. Системы доставки, как правило, адаптированы в соответствии с потребностями вкусоароматической композиции и/или пищевого продукта для домашних животных, в который будет включена вкусоароматическая композиция.
Вкусоароматические композиции можно использовать в жидкой форме, высушенной форме и/или твердой форме. При использовании в высушенной форме могут использоваться подходящие методы сушки, такие как распылительная сушка. Альтернативно, вкусоароматическая композиция может быть инкапсулирована или абсорбирована на водорастворимых материалах, включая, не ограничиваясь этим, такие материалы, как целлюлоза, крахмал, сахар, мальтодекстрин, гуммиарабик и тому подобное. Фактические методы получения таких высушенных форм хорошо известны в данной области и могут быть применены к раскрытому здесь предмету изобретения.
Вкусоароматические композиции по раскрытому здесь предмету изобретения можно использовать во многих различных физических формах, хорошо известных в данной области, для обеспечения первоначального всплеска вкуса, аромата и/или текстуры; и/или пролонгированного ощущения вкуса, аромата и/или текстуры. Не ограничиваясь ими, такие физические формы включают свободные формы, такие как высушенные распылением, порошкообразные и гранулированные формы, и инкапсулированные формы и их смеси.
В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения вкусоароматической композиции могут быть получены во время обработки пищевого продукта для домашних животных. Например, и не в качестве ограничения, нуклеотидные производные и/или трансмембранные соединения могут быть получены из соединений-предшественников во время термической обработки, например, перегонки в реторте, экструзии и/или стерилизации пищевого продукта для домашних животных.
В некоторых вариантах осуществления, как было отмечено выше, для модификации вкусоароматических систем можно использовать методы инкапсуляции. В некоторых вариантах осуществления вкусоароматические соединения, вкусоароматические компоненты или вся вкусоароматическая композиция могут быть полностью или частично инкапсулированы. Инкапсулирующие материалы и/или методы инкапусулирования могут быть выбраны для определения типа модификации вкусоароматической системы.
В некоторых вариантах осуществления инкапсулирующие материалы и/или методы инкапусулирования выбраны для повышения стабильности вкусоароматических соединений, вкусоароматических компонентов или вкусоароматических композиций; в то время, как в других вариантах осуществления инкапсулирующие материалы и/или методы инкапусулирования выбраны для модификации профиля высвобождения вкусоароматических композиций.
Подходящие инкапсулирующие материалы могут включать, не ограничиваясь этим, гидроколлоиды, такие как альгинаты, пектины, агары, гуаровые камеди, целлюлозы и тому подобное, белки, поливинилацетат, полиэтилен, сшитый поливинилпирролидон, полиметилметакрилат, полимолочная кислота, полигидроксиалканоаты, этилцеллюлоза, поливинилацетатфталат, сложные эфиры полиэтиленгликоля, метакриловая кислота-со-метилметакрилат, сополимер этилена и винилацетата (EVA) и тому подобное, и их комбинации. Подходящие методы инкапсулирования могут включать, не ограничиваясь этим, покрытие распылением, распылительную сушку, замораживание распылением, адсорбцию, комплексообразование с включением (например, получение комплекса вкусоароматическое соединение/циклодекстрин), коацервацию, покрытие в псевдоожиженном слое, или можно использовать другой процесс для инкапсулирования ингредиента инкапсулирующим материалом.
Инкапсулированные системы доставки вкусоароматических агентов или подсластителей могут содержать гидрофобную матрицу из жира или воска, окружающую ядро с подсластителем или вкусоароматическим агентом. Жиры могут быть выбраны из любого ряда обычных материалов, таких как жирные кислоты, глицериды или полиглицериновые эфиры, сложные эфиры сорбита и их смеси. Примеры жирных кислот включают, не ограничиваясь этим, гидрогенизированные и частично гидрогенизированные растительные масла, такие как пальмовое масло, пальмоядровое масло, арахисовое масло, рапсовое масло, масло рисовых отрубей, соевое масло, хлопковое масло, подсолнечное масло, сафлоровое масло и их комбинации. Примеры глицеридов включают, не ограничиваясь этим, моноглицериды, диглицериды и триглицериды.
Воска могут быть выбраны из группы, состоящей из природных и синтетических восков и их смесей. Неограничивающие примеры включают парафиновый воск, вазелин, карбовакс, микрокристаллический воск, пчелиный воск, карнаубский воск, воск канделилы, ланолин, душистый воск, воск сахарного тростника, спермацетовый воск, воск из рисовых отрубей и их смеси.
Жиры и воска можно использовать по отдельности или в комбинации в количествах примерно от 10 мас.% до примерно 70 мас.% и, альтернативно в количествах примерно от 30 мас.% до примерно 60 мас.% к общей массе инкапсулированной системы. При использовании в комбинации жир и воск могут находиться в соотношении примерно от 70:10 до 85:15 соответственно.
Типичные инкапсулированные системы доставки вкусоароматических композиций, вкусоароматического агента или подсластителя раскрыты в патентах США № 4597970 и 4722845, раскрытия которых включены здесь в виде ссылки во всей их полноте.
Жидкие системы доставки могут включать, не ограничиваясь этим, системы с дисперсией вкусоароматических композиций по настоящему изобретению, например, в виде сиропов и/или эмульсий углеводов. Жидкие системы доставки также могут включать экстракты, в которых нуклеотидное производное, трансмембранное соединение и/или вкусоароматические композиции солюбилизированы в растворителе. Твердые системы доставки можно получить распылительной сушкой, покрытием распылением, замораживанием распылением, сушкой в псевдоожиженном слое, абсорбцией, адсорбцией, коацервацией, комплексообразованием или любой другой стандартной методикой. В некоторых вариантах осуществления система доставки может быть выбрана таким образом, чтобы быть совместимой или функционировать в съедобной композиции. В некоторых вариантах осуществления система доставки должна включать масляный материал, такой как жир или масло. В некоторых вариантах осуществления система доставки будет включать кондитерский жир, такой как какао-масло, заменитель какао-масла, заместитель какао-масла или эквивалент какао-масла.
Для применения в высушенном виде могут использоваться подходящие способы для сушки, такие как распылительная сушка. Альтернативно, вкусоароматическая композиция может быть адсорбирована или абсорбирована на субстратах, таких как водорастворимые материалы, такие как целлюлоза, крахмал, сахар, мальтодекстрин, гуммиарабик и тому подобное, и таким образом могут быть инкапсулированы. Фактические методики получения таких высушенных форм хорошо известны в данной области.
6. Пищевые продукты для домашних животных
Вкусоароматические композиции по настоящему раскрытому предмету изобретения можно использовать в широком ряде пищевых продуктов для домашних животных. Неограничивающие примеры подходящих пищевых продуктов для домашних животных включают влажные пищевые продукты, сухие пищевые продукты, сырые пищевые продукты, пищевые добавки для домашних животных (например, витамины), напитки для домашних животных, закуски и лакомства, и категории пищевых продуктов для животных, описанные здесь.
Комбинация вкусоароматической композиции(й) по раскрытому здесь предмету изобретения, вместе с пищевым продуктом для домашних животных и необязательными ингредиентами, когда это требуется, обеспечивает вкусоароматический агент, который обладает неожиданным вкусом и придает, например, сенсорный опыт умами и/или чабера. Вкусоароматические композиции, описанные здесь, можно добавить до, во время или после обработки композиции или упаковки пищевого продукта для домашних животных, и компоненты вкусоароматической композиции могут добавляться последовательно или одновременно. В некоторых вариантах осуществления один или более компонентов вкусоароматических композиций, описанных здесь, могут быть получены во время производства пищевого продукта для домашних животных из соединений-предшественников, например, во время термической обработки пищевых продуктов. Например, и не в качестве ограничения, нуклеотидное производное и/или трансмембранное соединение вкусоароматической композиции могут быть получены во время производства пищевого продукта для домашних животных, и дополнительные компоненты вкусоароматической композиции могут быть добавлены до, во время или после обработки композиции или упаковки пищевого продукта для домашних животных.
В некоторых вариантах осуществления пищевой продукт для домашних животных является питательно полноценным сухим пищевым продуктом. Сухой или с низким содержанием влаги питательно полноценный пищевой продукт для домашних животных может содержать ниже примерно 15% влаги и содержать примерно от 10% до примерно 60% жира, примерно от 10% до примерно 70% белка и примерно от 30% до примерно 80% углеводов, например, диетическое волокно и золу.
В некоторых вариантах осуществления пищевой продукт для домашних животных является питательно полноценным влажным пищевым продуктом. Влажный или с высоким содержание влаги, питательно полноценный пищевой продукт может содержать выше 50% влаги. В некоторых вариантах осуществления влажный пищевой продукт для домашних животных содержит примерно 40% жира, примерно 50% белка и примерно 10% углеводов, например, пищевого волокна и золы.
В некоторых вариантах осуществления пищевой продукт для домашних животных представляет питательно полноценный сырой пищевой продукт. Сырой, например, полусырой или полусухой, или мягкий сухой или мягкий сырой или с промежуточной или средней влажностью, питательно полноценный пищевой продукт для домашних животных, содержит примерно от 15% до примерно 50% влаги.
В некоторых вариантах осуществления пищевой продукт для домашних животных представляет закуску для домашних животных. Неограничивающие примеры закусок для домашних животных включают закусочные палочки, жевательные конфеты для домашних животных, хрустящие угощения, хлопья, закуски, печенье и сладкие продукты.
В некоторых вариантах осуществления источник белка можно получить из растительного источника, такого как протеин люпина, протеин пшеницы, соевый белок и их комбинации. Альтернативно или дополнительно источник белка может быть получен из множества животных источников. Неограничивающие примеры животного белка включают говядину, свинину, птицу, баранину или рыбу, включая, например, мышечное мясо, мясные субпродукты, мясную муку или рыбную муку.
7. Методы определения вкусовых атрибутов
В некоторых вариантах осуществления настоящего изобретения атрибуты вкуса, аромата и/или вкусовой привлекательности пищевого продукта для домашних животных могут быть модифицированы смешиванием вкусоароматической композиции с пищевым продуктом, или получены в условиях получения пищевого продукта, как здесь описано. В некоторых вариантах осуществления атрибут(ы) может быть усилен или снижен путем повышения или снижения концентрации вкусоароматической композиции, смешанной или полученной с пищевым продуктом. В некоторых вариантах осуществления атрибуты вкуса модифицированного пищевого продукта могут быть оценены, как здесь описано, и концентрация вкусоароматической композиции, смешанной или полученной с пищевым продуктом, может быть повышена или снижена в зависимости от результатов оценки.
В некоторых вариантах осуществления настоящего изобретения атрибуты вкуса и/или вкусовой привлекательности можно оценить с использованием анализа in vitro, где измеряется способность соединения активировать рецептор умами кошки, экспрессированный клетками in vitro, в разных концентрациях. В некоторых вариантах осуществления повышение активации рецептора коррелирует с увеличением атрибутов вкуса и/или вкусовой привлекательности соединения. В некоторых вариантах осуществления композицию оценивают одну или в комбинации с другими соединениями. В некоторых вариантах осуществления анализ in vitro включает тесты in vitro, описанные в разделе «Примеры» настоящей заявки. В некоторых вариантах осуществления анализ in vitro включает рекомбинантные клетки, экспрессирующие рецептор умами, кодированный нуклеиновой кислотой, введенной в клетки (например, экзогенной нуклеиновой кислотой). В других неограничивающих вариантах осуществления анализ in vitro включает клетки, экспрессирующие рецептор умами, который является нативным для клеток. Примеры таких клеток, экспрессирующих нативный рецептор умами, включают, например, не ограничиваясь этим, вкусовые клетки кошки и/или собаки. В некоторых вариантах осуществления вкусовые клетки кошки и/или собаки, экспрессирующие рецептор умами, выделяют из организма кошки и/или собаки и культивируют in vitro.
В некоторых вариантах осуществления настоящего изобретения атрибуты вкуса и/или вкусовой привлекательности могут быть оценены с помощью панели дегустаторов. Например, но не в качестве ограничения, панель может включать кошек-дегустаторов. В некоторых вариантах осуществления панель может включать собак-дегустаторов. В некоторых вариантах осуществления вкусовую привлекательность пищевого продукта для домашних животных можно определить по потреблению пищевого продукта для домашних животных, содержащего только вкусоароматическую композицию (например, тест с одной кормушкой, монадическое ранжирование). В некоторых вариантах осуществления вкусовую привлекательность пищевого продукта для домашних животных можно определить по предпочтительному потреблению пищевого продукта для домашних животных, содержащего вкусоароматическую композицию, описанную здесь, в сравнении с пищевым продуктом для домашних животных, который не содержит вкусоароматической композиции или содержит другую вкусоароматическую композицию (например, тест с двумя кормушками для оценки предпочтения, различия и/или выбора).
В некоторых вариантах осуществления вкусовую привлекательность и/или вкус умами вкусоароматической композиция можно определить по предпочтительному потреблению водного раствора, содержащего вкусоароматическую композицию, описанную здесь, в сравнении с водным раствором, который не содержит вкусоароматическую композицию или содержит другую вкусоароматической композиции (например, тест с двумя бутылями). Например, панель растворов можно использовать для сравнения вкусовой привлекательности ряда концентраций соединений в монадическом воздействии. В некоторых вариантах осуществления раствор может содержать усилитель вкусовой привлекательности, например, L-гистидин, в качестве пищеварительного/положительного тастанта для увеличения потребления исходного раствора, что позволяет идентифицировать потенциальное отрицательное влияние испытуемого соединения.
Степень потребления каждого пищевого продукта для домашних животных или водного раствора можно определить путем измерения количества одного потребляемого рациона, деленного на общее потребление. Затем можно рассчитать коэффициент потребления (CR) для сравнения потребления одного рациона в пересчете на другой рацион для определения предпочтительного потребления одного пищевого продукта или водного раствора над другим. Альтернативно или дополнительно разницу в потреблении (г) можно использовать для оценки средней разницы в потреблении между двумя растворами в тесте с двумя бутылями или между двумя пищевыми продуктами для домашних животных в тесте с двумя кормушками на выбранном уровне значимости, например, на уровне значимости 5%, чтобы определить среднюю разницу в потреблении с 95% доверительным интервалом. Однако может быть использован любой уровень значимости, например, уровень значимости 1, 2, 3, 4, 5, 10, 15, 20, 25 или 50%. В некоторых вариантах осуществления процентные оценки предпочтений, например, процентное предпочтение одного раствора или пищевого продукта животным, представляет собой процент от общего количества жидкости или пищевого продукта, поглощенного во время теста, который также может быть рассчитан для этого раствора или пищевого продукта.
8. Способы получения
В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения по настоящему изобретению могут быть получены с использованием обычных способов химического синтеза. В некоторых вариантах осуществления способ химического синтеза обеспечивает нуклеотидное производное и/или трансмембранное соединение, имеющее чистоту, по меньшей мере, 99,999% или, по меньшей мере, 99% или, по меньшей мере, 95% или, по меньшей мере, 90% или, по меньшей мере, 85% или, по меньшей мере, 80%. В некоторых вариантах осуществления нуклеотидные производные и/или трансмембранные соединения можно получить с использованием обычных способов гидролиза, таких, в которых используются кислоты, ферменты или комбинация кислот и ферментов.
Нуклеотидные производные и/или трансмембранные соединения по настоящему раскрытию также можно получить в условиях приготовления корма, например, во время производства пищевого продукта для домашних животных. Например, не ограничиваясь этим, нуклеотидные производные и/или трансмембранные соединения по настоящему изобретению могут быть получены во время термической обработки пищевого продукта, например, стерилизации, перегонки на реторте и/или экструзии из соединений-предшественников, присутствующих в пищевом продукте для домашних животных. В некоторых вариантах осуществления жидкий и/или порошкообразный палатант также может быть добавлен для улучшения вкуса пищевого продукта для домашних животных, например, сухого пищевого продукта для домашних животных, и для повышения вкусовой привлекательности пищевого продукта для домашних животных. Палатант может представлять мясной перевар (например, печени) и/или перевар растительного продукта и может необязательно содержать другие палатанты, известные в данной области. В некоторых вариантах осуществления нуклеотидное производное и/или трансмембранное соединение можно смешивать с или получать в жидком и/или порошкообразном палатанте перед его добавлением в пищевой продукт для домашних животных. Альтернативно или дополнительно, нуклеотидное производное и/или трансмембранное соединение можно смешивать или получать в жидком и/или растительном палатанте после его добавления в пищевой продукт для домашних животных.
В некоторых вариантах осуществления вкусоароматические композиции по настоящему раскрытию содержат одно или более трансмембранных соединений формул от Tm-1 до Tm-104. В некоторых вариантах осуществления такие соединения можно, без ограничений, синтезировать любыми способами, известными в данной области. В некоторых вариантах осуществления трансмембранные соединения на основе производных парабановой кислоты можно синтезировать согласно следующей схеме синтеза:
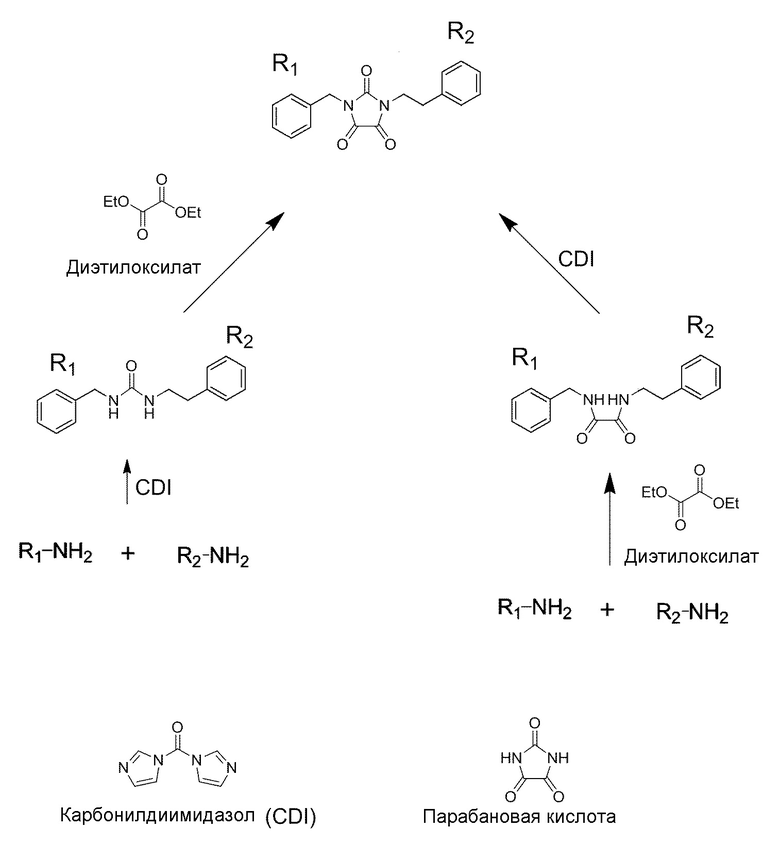
9. Неограничивающие примеры вкусоароматических композиций по настоящему изобретению
Как здесь описано, имеется, по меньшей мере, три различных сайта связывания, присутствующих в рецепторе T1R1/T1R3 кошки (т.е. рецепторе умами), что позволяет связывать небольшие молекулы и/или соединения. Один из сайтов связывания, присутствующих в рецепторе T1R1/T1R3 кошки, может связывать нуклеотиды и/или нуклеотидные производные, описанные здесь. Второй сайт связывания, присутствующий в рецепторе T1R1/T1R3 кошки, может связывать аминокислоты первой группы, как здесь описано, и третий сайт связывания, присутствующий в рецепторе T1R1/T1R3 кошки (то есть в домене 7TM T1R1), может связывать трансмембранные соединения, описанные здесь. Не желая связываться с какой-либо конкретной теорией, связывание аминокислот первой группы, как здесь раскрыто, может изменить конформацию рецептора T1R1/T1R3 кошки для обеспечения большего контакта со связанным нуклеотидом и/или нуклеотидным производным и привести к синергической активации рецептора умами. Аминокислоты второй группы, раскрытые здесь, могут взаимодействовать с одним или более другими рецепторами и не конкурировать с первыми аминокислотами за связывание с рецептором умами. Добавление аминокислот второй группы во вкусоароматическую композицию может улучшить восприятие вкусоаромата композиции. Связывание трансмембранного соединения с рецептором, как здесь описано, дополнительно активирует рецептор, тем самым улучшая или изменяя вкусовую привлекательность пищевого продукта, содержащего такие соединения.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, один нуклеотид и/или нуклеотидное производное, которые связываются с первым сайтом связывания в рецепторе умами и/или, по меньшей мере, с одной аминокислотой первой группы, которая связывается со вторым сайтом связывания в рецепторе умами и/или, по меньшей мере, одно трансмембранное соединение, которое связывается с третьим сайтом связывания в рецепторе умами (например, внутри домена 7TM рецептора умами) и/или, по меньшей мере, с одной аминокислотой второй группы, которая связывается с другим рецептором.
Раскрываемый здесь предмет изобретения обеспечивает вкусоароматические композиции, которые содержат, по меньшей мере, одно, два, три, четыре, пять или более нуклеотидных производных и/или, по меньшей мере, один, два, три, четыре, пять или более нуклеотидов и/или, по меньшей мере, одно, три, четыре, пять или более трансмембранных соединений и/или, по меньшей мере, одну, две, три, четыре, пять или более аминокислот первой группы, и/или, по меньшей мере, одну, две, три, четыре, пять или более аминокислот второй группы.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, одну, две, три, четыре, пять или более аминокислот первой группы и/или, по меньшей мере, одну, два, три, четыре, пять или более аминокислот второй группы, выбранных из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, одну аминокислоту первой группы, выбранную из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, одну аминокислоту второй группы, выбранную из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, одну аминокислоту первой группы и, по меньшей мере, одну аминокислоту второй группы, выбранные из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, две аминокислоты первой группы и, по меньшей мере, одну аминокислоту второй группы, выбранные из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, одну аминокислоту первой группы и, по меньшей мере, две аминокислоты второй группы, выбранные из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, две аминокислоты первой группы и, по меньшей мере, две аминокислоты второй группы, выбранные из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, один нуклеотид и, по меньшей мере, одну аминокислоту первой группы, выбранную из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, один нуклеотид и, по меньшей мере, одну аминокислоту второй группы, выбранную из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное и, по меньшей мере, один нуклеотид и, по меньшей мере, одну, две, три, четыре, пять или более аминокислот первой группы и/или, по меньшей мере, одну, две, три, четыре, пять или более аминокислот второй группы, выбранных из таблицы 4.
В некоторых вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, по меньшей мере, один нуклеотид и, по меньшей мере, одну аминокислоту первой группы и, по меньшей мере, одну аминокислоту второй группы, выбранные из таблицы 4.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, гистидин и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, аланин и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, глицин и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, фенилаланин и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, триптофан и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, тирозин и пролин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, гистидин и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, аланин и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, глицин и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, фенилаланин и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, триптофан и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, тирозин и треонин.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, гистидин и глутаминовую кислоту.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, аланин и глутаминовую кислоту.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, глицин и глутаминовую кислоту.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, фенилаланин и глутаминовую кислоту.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, триптофан и глутаминовую кислоту.
В некоторых неограничивающих вариантах осуществления настоящее раскрытие обеспечивает вкусоароматическую композицию, содержащую, по меньшей мере, одно нуклеотидное производное, тирозин и глутаминовую кислоту.
В некоторых вариантах осуществления любая из вкусоароматических композиций, раскрытых выше, может дополнительно содержать, по меньшей мере, один нуклеотид и/или, по меньшей мере, одно трансмембранное соединение, как здесь описано.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей аденозин-3',5'-дифосфат и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 6-тиогуанозин-5'-О-монофосфат и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 2'-,3'-O-(N'-метилантраниноил)гуанозин-5'-O-монофосфат и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 2-амино-6-хлорпуринрибозид-5'-О-монофосфат и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 6-хлорпуринрибозид-5'-O-монофосфат и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей инозинтрифосфат (ITP) и аланин.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей инозинтрифосфат (ITP), аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 1-(2-бромфенил)-3-((1R,2S)-2-гидрокси-2,3-дигидро-1Н-инден-1-ил)мочевину, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей N-(бензо[d][1,3]диоксол-5-ил)-2-пропилпентанамид, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамид, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей N-(2-амино-2-оксо-1-фенилэтил)-3-хлор-4,5-диметоксибензамид, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей (E)-3-(4-метоксифенил)-N-(пентан-3-ил)акриламид, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-трион, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей 1Н-имидазо [4,5-с]пиридин-2(3Н)-он, аланин и IMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамид, фенилаланин и GMP.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей комбинацию N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида с первой аминокислотой (аминокислота группы А), второй аминокислотой (аминокислота группы B) и одним или более нуклеотидов, как описано ниже.
Вкусоароматические композиции, содержащие трансмембранное соединение, первую аминокислоту (группа А), вторую аминокислоту (группа В) и нуклеотид.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к пищевому продукту для домашних животных, содержащему вкусоароматическую композицию, описанную здесь, где вкусоароматическая композиция присутствует в количестве примерно от 0,001 ppm до примерно 1000 ppm.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к пищевому продукту для домашних животных, содержащему вкусоароматическую композицию, описанную здесь, где вкусоароматическая композиция присутствует в концентрации примерно от 0,0001 мас.% до примерно 10 мас.% к общей массе пищевого продукта для домашних животных.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к пищевому продукту для домашних животных, содержащему вкусоароматическую композицию, описанную здесь, где вкусоароматическая композиция присутствует в количестве выше примерно 1 ppm.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к пищевому продукту для домашних животных, содержащему вкусоароматическую композицию, описанную здесь, где вкусоароматическая композиция присутствует в количестве выше примерно 10 ppm.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к вкусоароматической композиции, содержащей в количестве выше примерно 100 ppm.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к пищевому продукту для домашних животных, содержащему нуклеотидное производное, описанное здесь, где нуклеотидное производное присутствует в количестве примерно от 1 пМ до примерно 1 М.
10. Неограничивающие примеры способов по настоящему изобретению
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к способу повышения вкусовой привлекательности пищевого продукта для домашних животных, включающему смешивание пищевого продукта для домашних животных с вкусоароматической композицией, содержащей нуклеотидное производное и/или трансмембранное соединение, как здесь описано, где нуклеотидное производное и/или трансмембранное соединение присутствует в концентрации примерно от 1 пМ до примерно 10 М или примерно от 1 пМ до примерно 1 М к общей массе смеси.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к способу повышения вкусовой привлекательности пищевого продукта для домашних животных, включающему получение пищевого продукта для домашних животных с вкусоароматической композицией, содержащей нуклеотидное производное и/или трансмембранное соединение, как здесь описано, где нуклеотидное производное и/или трансмембранное соединение присутствует в концентрации примерно от 1 пМ до примерно 10 М или примерно от 1 пМ до примерно 1 М к общей массе продукта.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к способу усиления вкуса умами пищевого продукта для домашних животных, включающему смешивание пищевого продукта для домашних животных с вкусоароматической композицией, содержащей нуклеотидное производное и/или трансмембранное соединение, как здесь описано, где нуклеотидное производное и/или трансмембранное соединение присутствует в концентрации от 0,001 ppm до 1000 ppm к общей массе смеси.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к способу повышения вкусовой привлекательности пищевого продукта для домашних животных, включающему смешивание пищевого продукта для домашних животных с вкусоароматической композицией, содержащей нуклеотидное производное и/или трансмембранное соединение, как здесь описано, где вкусоароматическая композиция присутствует в концентрации примерно от 0,001 ppm до 1000 ppm к общей массе смеси.
В некоторых неограничивающих вариантах осуществления настоящее изобретение относится к способу усиления вкуса умами пищевого продукта для домашних животных, включающему смешивание пищевого продукта для домашних животных с вкусоароматической композицией, содержащей нуклеотидное производное и/или трансмембранное соединение, как здесь описано, где вкусоароматическая композиция присутствует в концентрации примерно от 0,0001 мас.% до примерно 10 мас.% к общей массе смеси.
11. Примеры
Раскрываемый здесь предмет изобретения будет лучше понят со ссылкой на следующие примеры, которые представлены в качестве примера изобретения, но не в качестве ограничения.
Пример 1 - активация рецептора T1R1/T1R3 под действием нуклеотидных производных.
В настоящем примере описывается активация рецептора T1R1/T1R3 кошки под действием нуклеотидных производных in vitro.
Нуклеотидные производные, которые могут функционировать в качестве активаторов T1R1/T1R3, были идентифицированы с помощью in silico моделирования рецептора умами кошки, T1R1/T1R3, и выбраны для дальнейшего тестирования in vitro. Функциональную характеристику in vitro выбранных нуклеотидных производных использовали для оценки эффективности нуклеотидного производного в активации рецептора T1R1/T1R3 одного и в комбинации с аминокислотами и/или нуклеотидами.
Методы: клетки HEK293, которые стабильно экспрессируют T1R3 и индуцибельно экспрессируют T1R1, подвергали воздействию одних нуклеотидных производных для активации рецептора умами. Активацию рецептора T1R1/T1R3 детектировали по изменению уровней внутриклеточного кальция с использованием флуоресцентного красителя, чувствительного к кальцию. Клетки, которые экспрессируют T1R3, но не T1R1, использовали в качестве контроля. Для сбора данных использовали систему FLIPR® Tetra или ридер FlexStation® 3.
Для каждого нуклеотидного производного были получены кривые зависимости доза-эффект и определены следующие показатели: EC50 одного нуклеотидного производного; EC50 нуклеотидного производного с 20 мМ аланина; EC50 нуклеотидного производного с 0,2 мМ IMP; и EC50 нуклеотидного производного с 20 мМ аланина и 0,2 мМ IMP.
Термин половинная максимальная эффективная концентрация (EC50) относится к концентрации соединения, которая вызывает половинный ответ между базовой линией и максимумом после определенного времени воздействия. В каждом эксперименте к клеткам, экспрессирующим T1R1/T1R3, добавляли серийные разведения нуклеотидного производного до 0,1 мМ, 1 мМ или 10 мМ.
Результаты: обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3, одним 2'-дезоксиаденозин-3',5'-O-бисфосфатом (например, в буфере) или в комбинации с 20 мМ аланина, приводила к активации рецептора T1R1/T1R3, о чем свидетельствует изменение уровня внутриклеточного кальция (ΔF/F0). В присутствии аланина или в буфере 2'-дезоксиаденозин-3',5'-O-бисфосфат приводил к наблюдаемому значению EC50, равному 0,02 мМ (таблица 6 и фиг. 2). Эти результаты показали, что 2'-дезоксиаденозин-3',5'-O-бисфосфат является положительным активатором рецептора T1R1/T1R3.
Было обнаружено, что нуклеотидное производное, один аденозин-5'-О-тиомонофосфат дилитиевая соль действует в качестве активатора T1R1/T1R3 (фиг. 8 и таблица 6). В присутствии 20 мМ аланина, который один имеет значение EC50, равное 13,6 мМ, EC50 аденозин-5'-O-тиомонофосфата дилитиевой соли уменьшилось с более чем 1 мМ до 0,06 мМ, а значений ΔF/F0 достоверно повысилось (фиг. 8 и таблица 6). Эти результаты дают основание предположить, что аланин и нуклеотидные производные, например аденозин-5'-О-тиомонофосфат, действуют синергически в активации T1R1/T1R3.
Не желая свызываться с конкретной теорией, данные результаты показывают, что нуклеотидные производные одни или в комбинации с аминокислотой, например аланином, могут функционировать в качестве положительных модуляторов рецептора T1R1/T1R3.
Активация рецептора T1R1/T1R3 под действием нуклеотидных производных
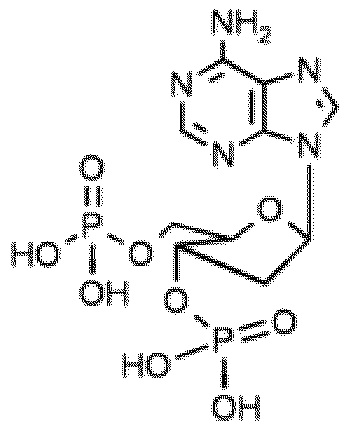
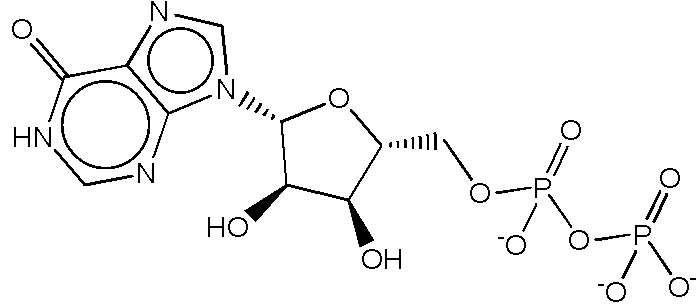
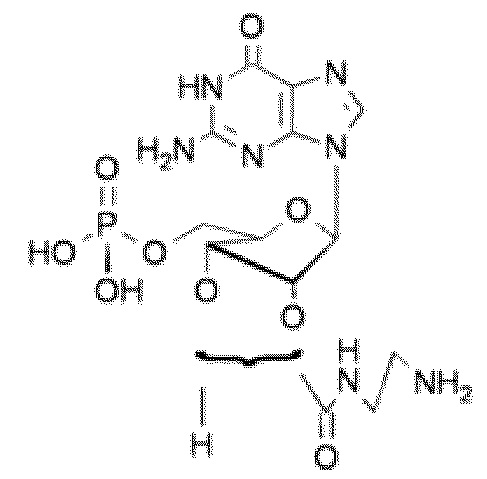
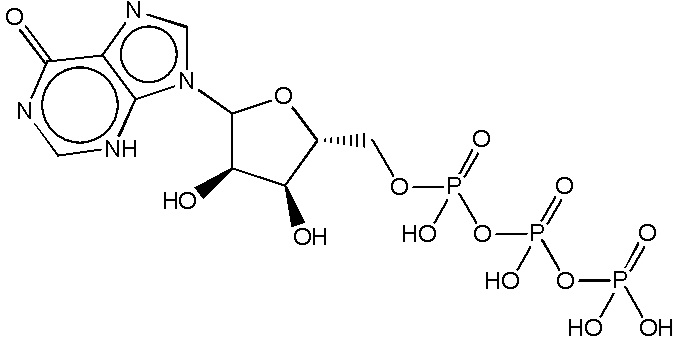
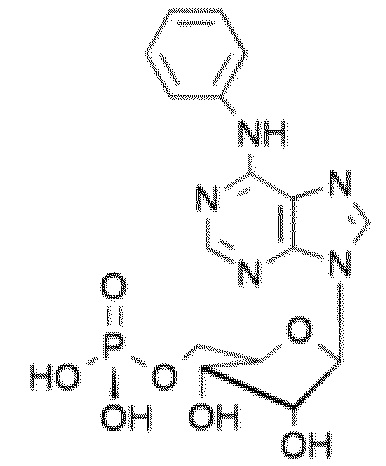
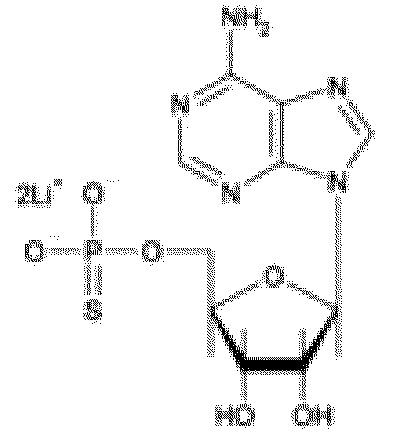
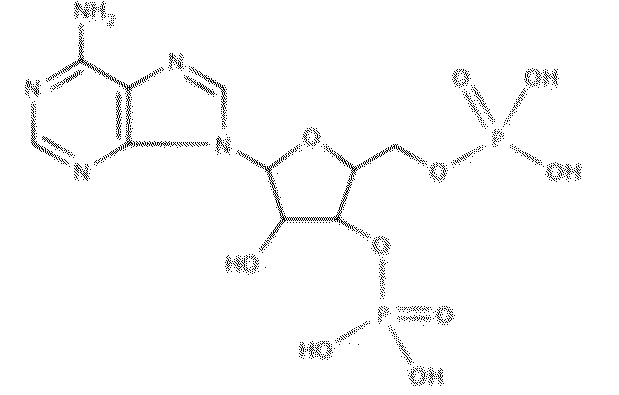
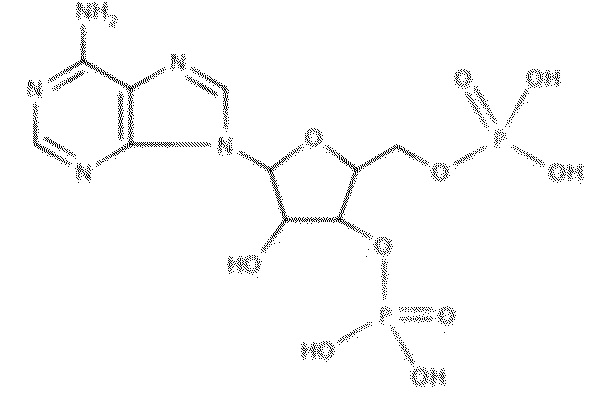
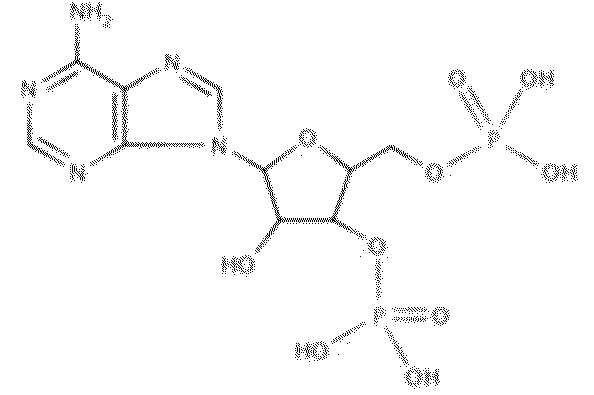
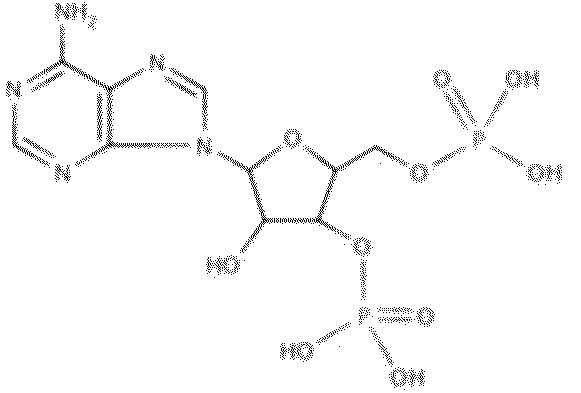
Пример 2 - Активация рецептора T1R1/T1R3 под действием нуклеотидных производных в комбинации с аминокислотой.
В настоящем примере описывается активация рецептора T1R1/T1R3 кошки под действием нуклеотидных производных в комбинации с аминокислотой in vitro.
Нуклеотидные производные оценивали для определения эффективности нуклеотидных производных в активации рецептора T1R1/T1R3 в комбинации с одним или более нуклеотидами и/или одной или более аминокислотами.
Методы: клетки HEK293, которые стабильно экспрессируют T1R3 и индуцибельно экспрессируют T1R1, подвергали воздействию нуклеотидных производных одних или в комбинации с одной или более аминокислотами и/или одним или более нуклеотидами для активации рецептора умами. Активацию рецептора T1R1/T1R3 детектировали по изменению уровней внутриклеточного кальция с использованием флуоресцентного красителя, чувствительного к кальцию, и/или люминесцентной репортерной системы. Клетки, которые экспрессируют T1R3, но не T1R1, использовали в качестве контроля. Для сбора данных использовали систему FLIPR® Tetra или ридер FlexStation® 3.
Для каждого нуклеотидного производного были получены кривые зависимости доза-эффект и определены следующие показатели в присутствии 20 мМ аланина: EC50 нуклеотидного производного, максимальный ответ рецептора в присутствии нуклеотидного производного, максимальный ответ рецептора в присутствии нуклеотидного производного по сравнению с ответом рецептора в присутствии IMP и пороговое количество нуклеотидного производного, которое приводит к активации рецептора T1R1/T1R3. Значения EC50 для используемого положительного и отрицательного контроля приведены в таблице 16.
Результаты: эффект всех нуклеотидных производных, тестированных в отношение активации T1R1/T1R3, показан в таблице 15. Обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3, нуклеотидным производным, аденозином-3',5'-дифосфатом (ADP) натриевой солью в комбинации с 20 мМ аланина, приводила к активации рецептора T1R1/T1R3, о чем свидетельствует максимальное изменение уровней внутриклеточного кальция (ΔF/F0) и установленное значение EC50, равное 0,001 мМ. В противоположность, нуклеотид, аденозинмонофосфат (AMP), в присутствии 20 мМ аланина имел установленное значение EC50, равное 0,011 мМ (таблица 7). Эти результаты показывают, что нуклеотидное производное на основе аденозина проявило более высокую активность в активации рецептора T1R1/T1R3 по сравнению с обычным нуклеотидом, из которого он был получен. Аналогичные результаты наблюдали для 2'-/3'-O-(N'-метилантранилоил) аденозин-5'-O-монофосфата натриевой соли (таблица 7). Кроме того, нуклеотидные производные на основе аденозина также имели более низкое пороговое количество для активации рецепторов по сравнению с AMP (таблица 7).
Как было установлено нуклеотидные производные на основе гуанозина, 6-тиогуанозин-5'-О-монофосфат, 2'-дезоксигуанозин-5'-О-монофосфоротиоат (натриевая соль); 2'-,3'-O-(N'-метилантранилоил)гуанозин-5'-О-монофосфат; гуанозин-5'-монофосфоротиоат (натриевая соль); 2'-дезокси-3'-O-(N'-метилантранилоил)гуанозин-5'-O-монофосфат; гуанозин-5'-O-(2-тиодифосфат), 2'-дезоксигуанозин-3',5'-O-бисфосфат и 2'-деоксигуанозин-5'-О-монофосфоротиоат функционировали в качестве активаторов T1R1/T1R3 в присутствии аланина (таблица 8). Как показано в таблице 8, данные нуклеотидные производные на основе гуанозина обладали повышенной активностью по сравнению с обычным нуклеотидом, гуанозинмонофосфатом (GMP). Например, 6-тиогуанозин-5'-О-монофосфат показал значение EC50, равное 0,0009 мМ, в присутствии аланина и пороговое количество 0,0002 мМ; в то время как GMP демонстрировал значение EC50 0,02 мМ и пороговое значение 0,008 мМ (таблица 8 и фиг. 1).
Также было установлено, что нуклеотидные производные на основе пурина, 2-амино-6-хлорпуринрибозид-5'-O-монофосфат (2-NH2-6-Cl-5'-PuMP) и 6-хлорпуринрибозид-5'-O-монофосфат, функционируют в качестве активаторов рецептора T1R1/T1R3 (таблица 9). Например, 2-амино-6-хлорпуринрибозид-5'-O-монофосфат в присутствии аланина показал значение EC50 0,0005 мМ с пороговым значением 0,00013 мМ и 6-хлорпуринрибозид-5'-O-монофосфат в присутствии аланина показал значение EC50 0,002 мМ с пороговым значением 0,0005 мМ (таблица 9). В противоположность, пуринрибозид-5'-О-монофосфат (5'-PuMP) показал значение EC50 0,02 мМ с пороговым значением 0,005 мМ в присутствии аланина, что указывает на то, что нуклеотиды на основе пурина активировали рецептор умами кошки в более низкой концентрации по сравнению с обычным нуклеотидом 5'-PuMP (таблица 9).
Было обнаружено, что нуклеотидные производные на основе инозина активируют рецептор в присутствии аланина (таблица 11). 6-Тиоинозинфосфат показал значение EC50 0,02 мМ в присутствии аланина, и инозинтрифосфат (ITP) имел значение EC50 0,08 мМ в присутствии аланина (таблица 11 и фиг. 6). Обычный нуклеотид, инозинмонофосфат (IMP), имел значение EC50, равное 0,07 мМ, указывая на то, что 6-тиоинозинфосфат проявлял повышенную активность по сравнению с IMP. Аналогичные результаты наблюдали для нуклеотидных производных на основе уридина, где нуклеотидные производные проявляли повышенную активность по сравнению с уридинмонофосфатом (UMP). Например, нуклеотидное производное на основе уридина, уридин-5'-монофосфоморфолидат 4-морфолин-N,N'-дициклогексилкарбоксамидин, показал значение EC50 выше 3 мМ по сравнению с EC50 для UMP выше 30 мМ (таблица 12).
Не желая связываться с конкретной теорией, полученные результаты свидетельствуют о том, что нуклеотидные производные функционируют в качестве положительных модуляторов рецептора T1R1/T1R3 и обладают повышенной активностью по сравнению с обычными нуклеотидами.
Активация T1R1/T1R3 под действием аденозина и нуклеоидных производных на основе аденозина
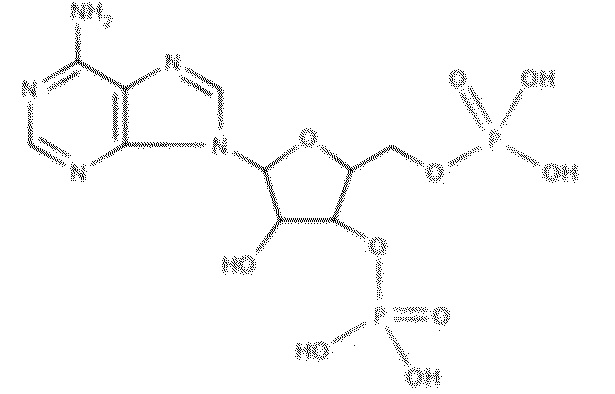
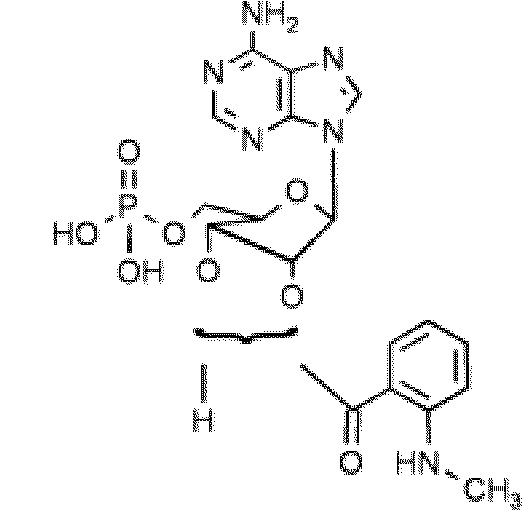
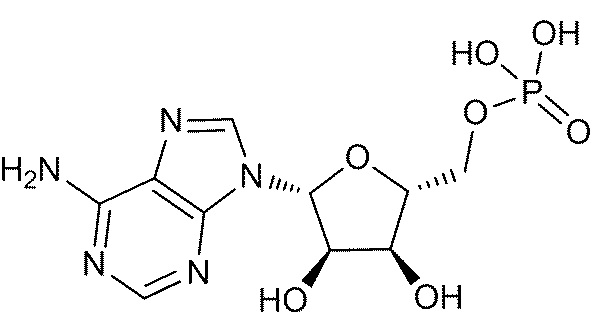
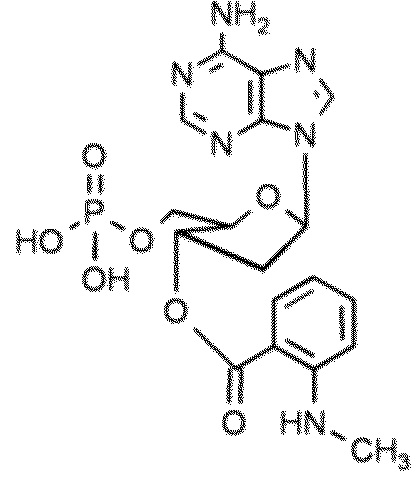
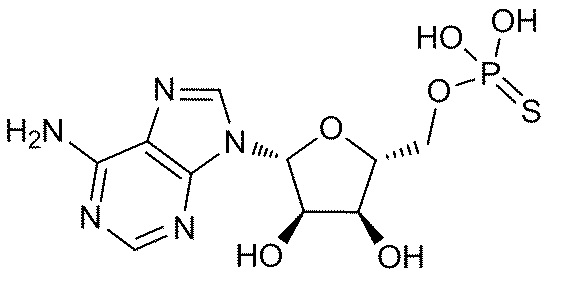
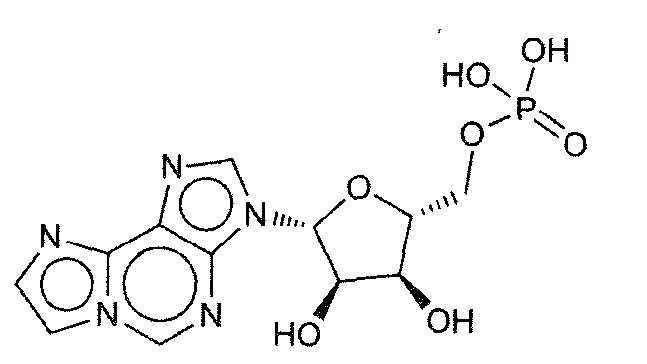
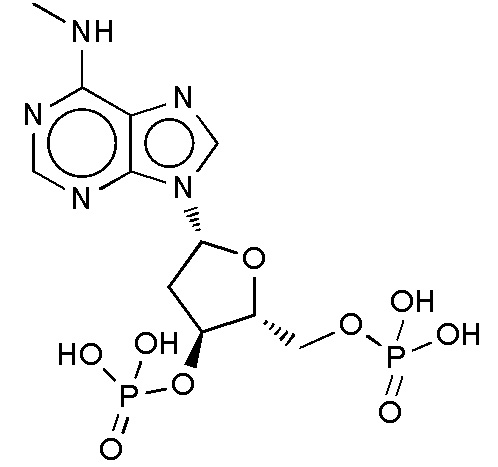
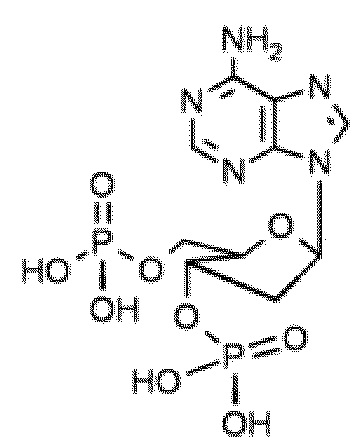
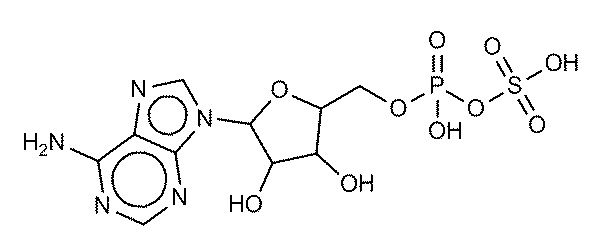
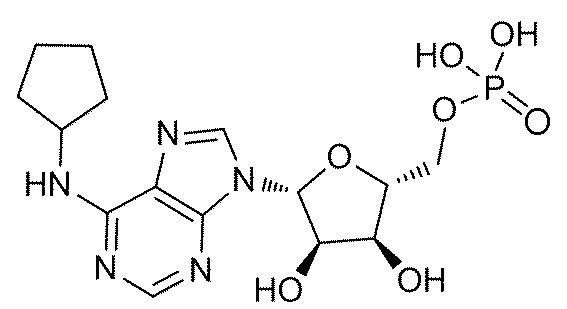
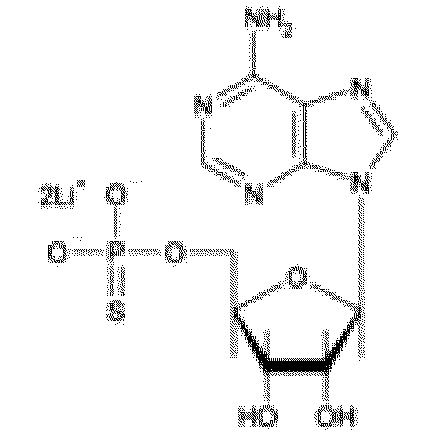
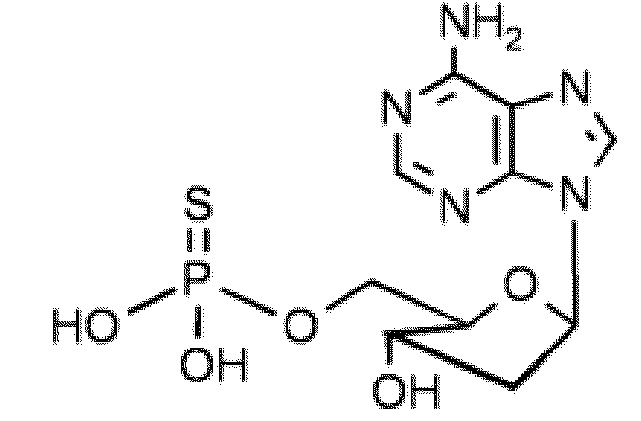
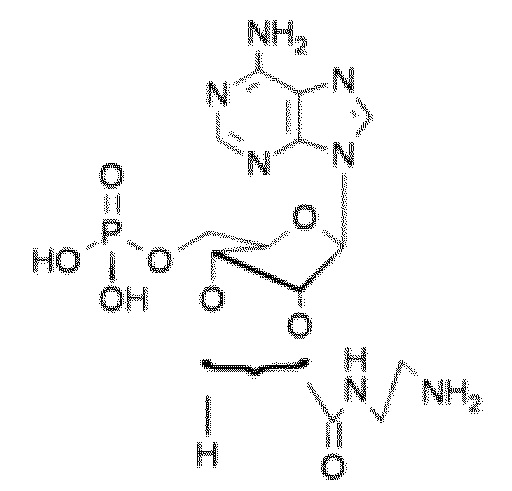
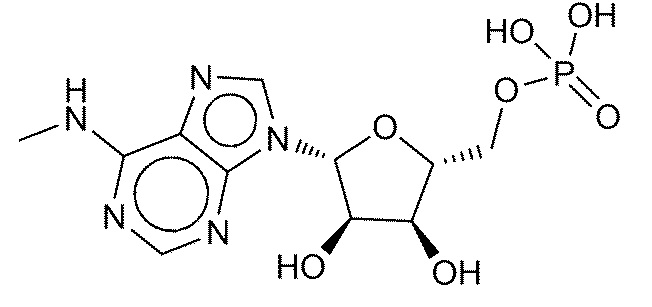
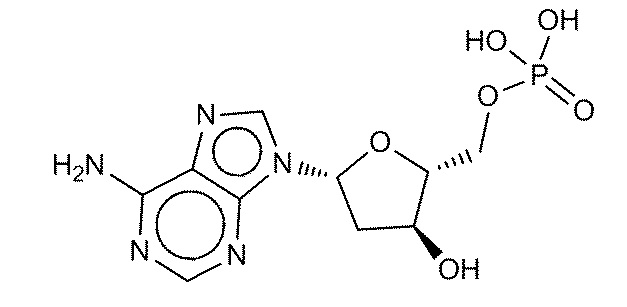
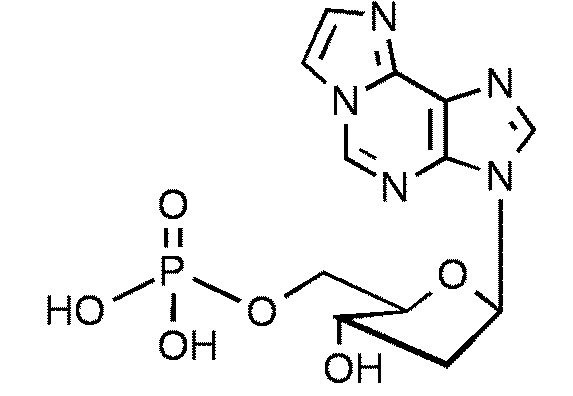
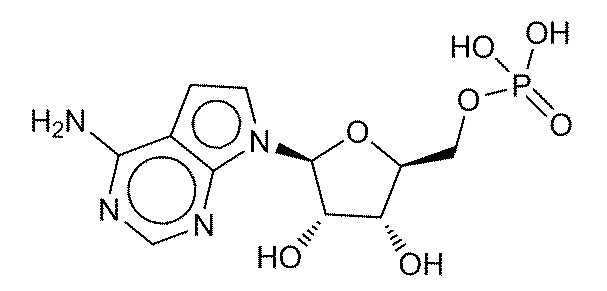
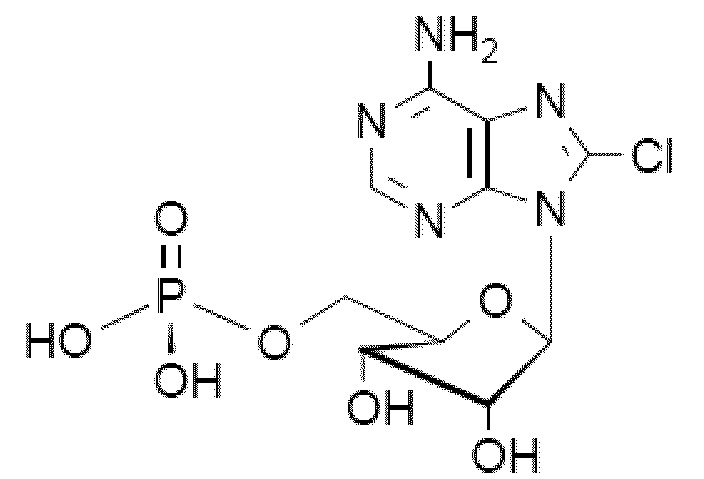
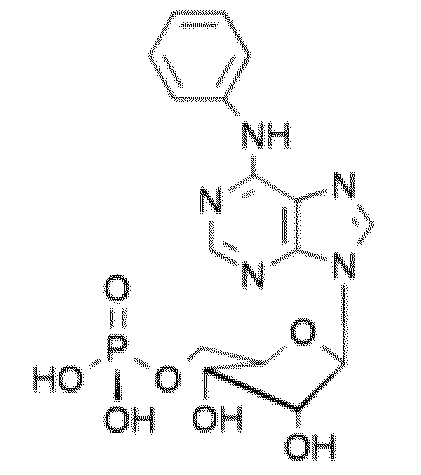
Активация T1R1/T1R3 под действием гуанозина и нуклеоидных производных на основе гуанозина
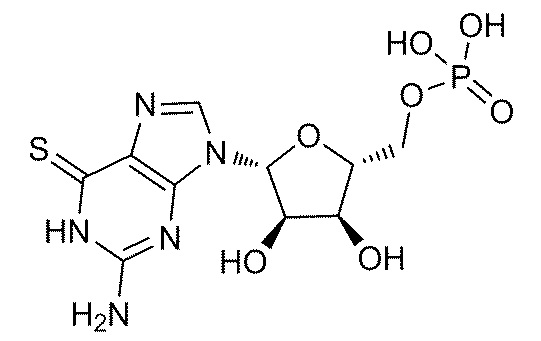
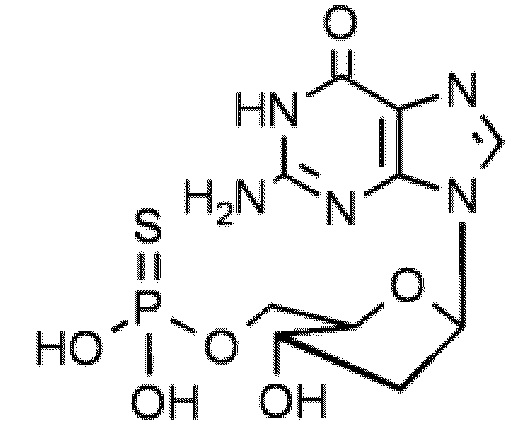
гуанозин-5'-O-монофосфат (MANT-5'-GMP)
Флуоресцентный аналог 5'-GMP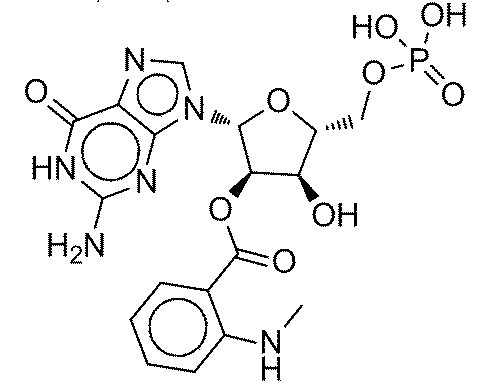
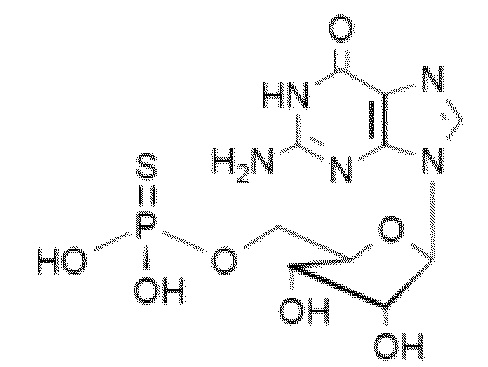
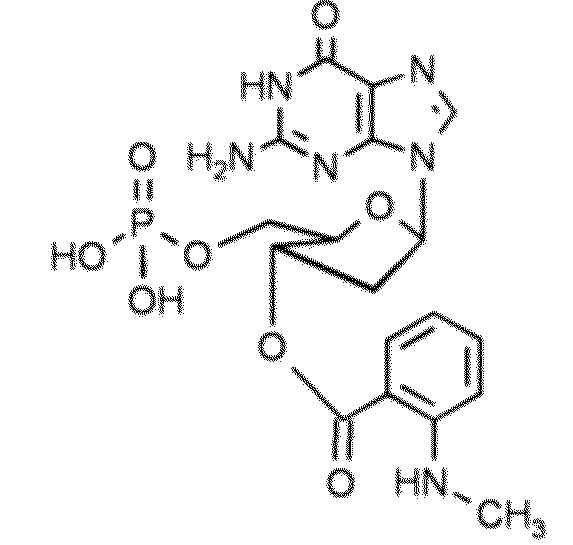
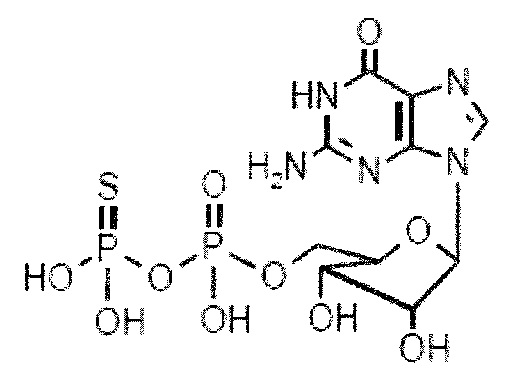
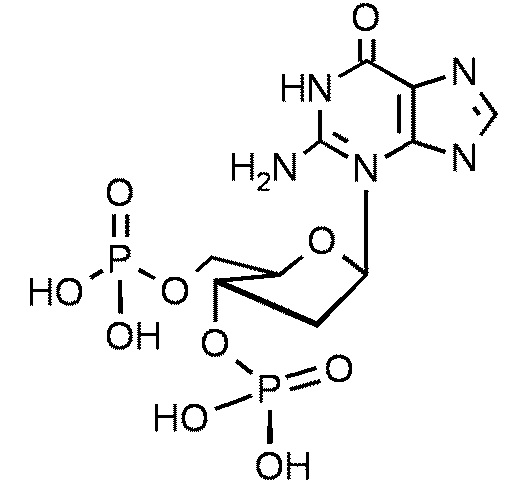
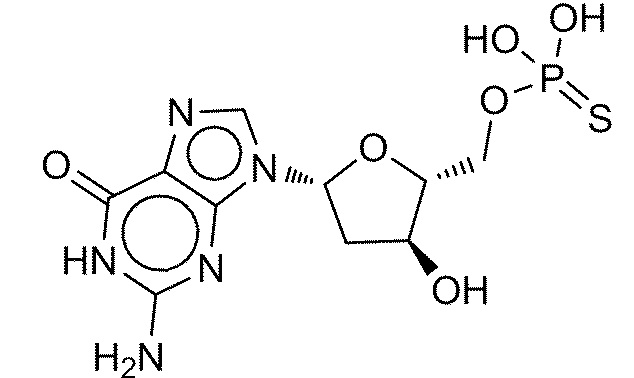
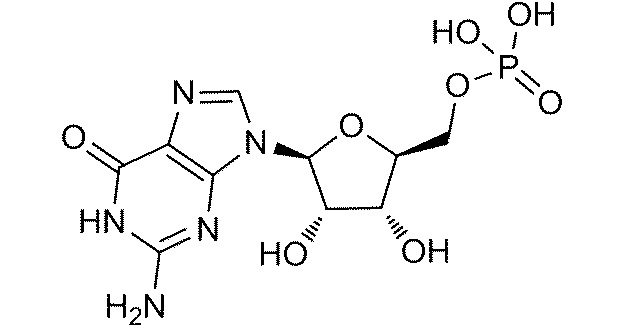
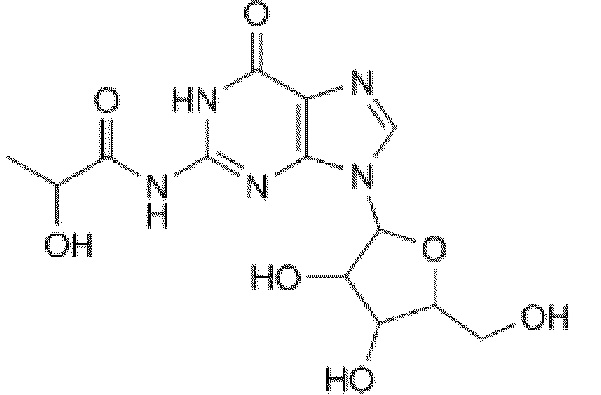
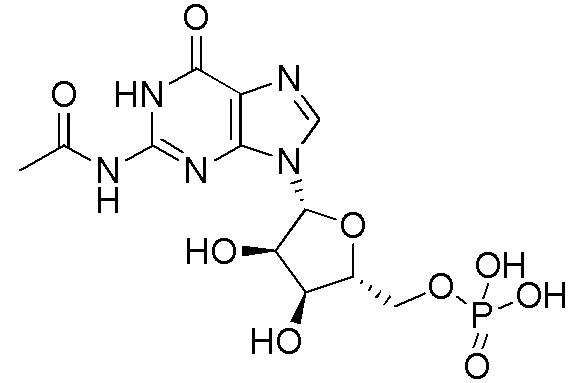
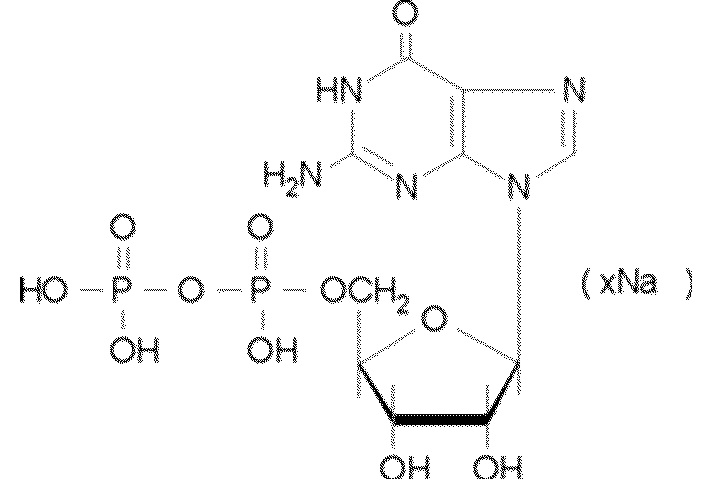
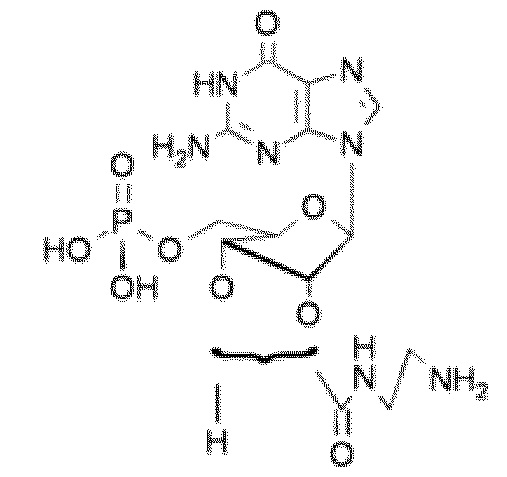
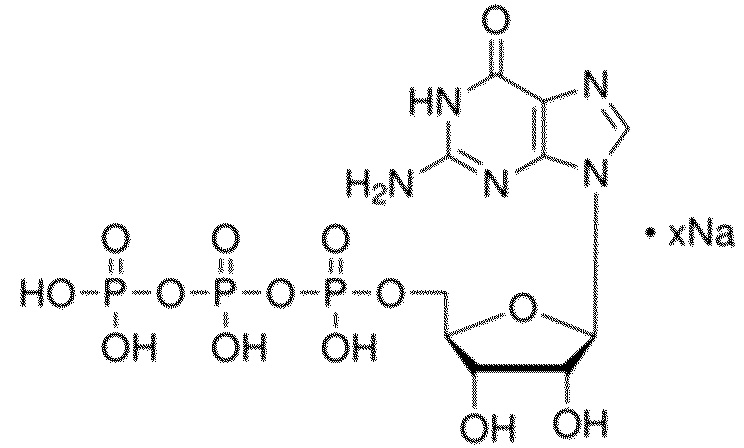
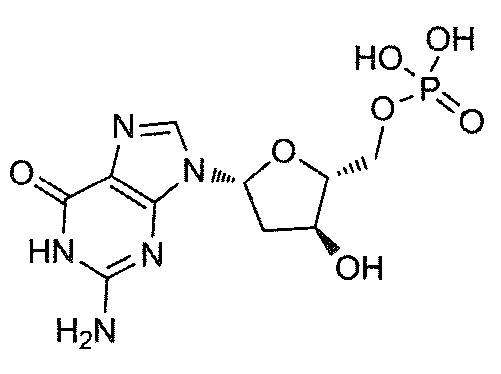
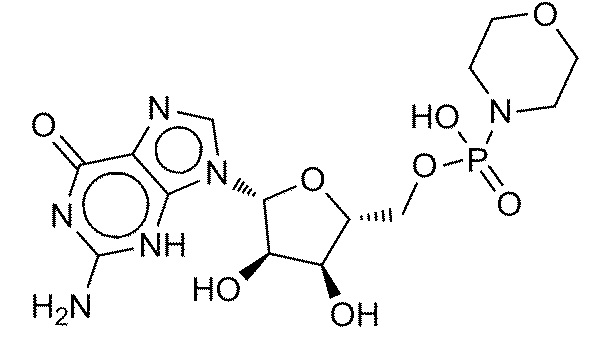
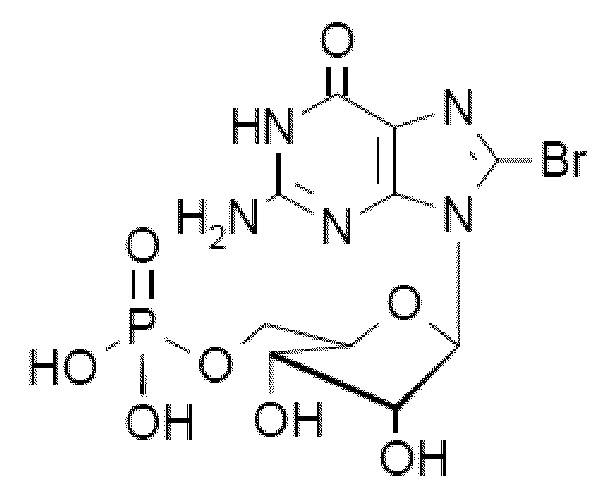
Активация T1R1/T1R3 под действием нуклеоидных производных на основе пурина
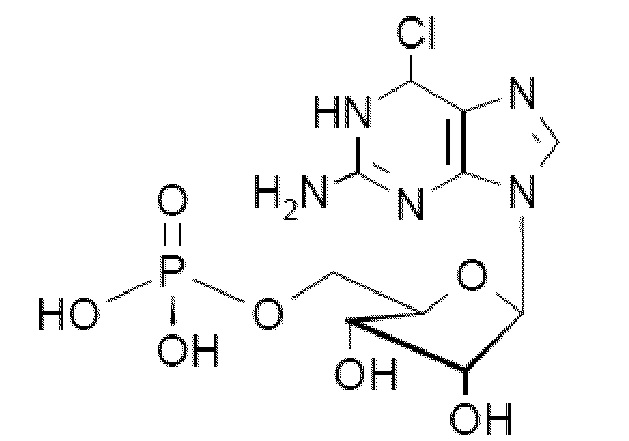
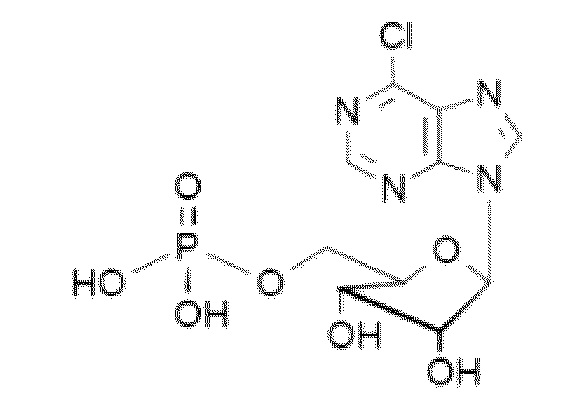
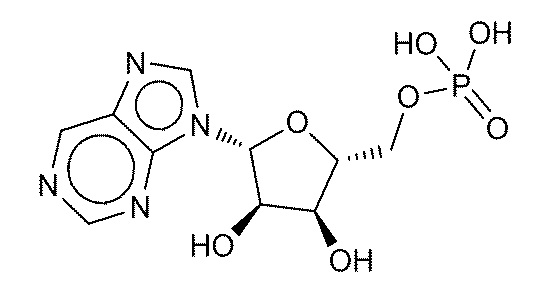
Активация T1R1/T1R3 под действием ксантозина
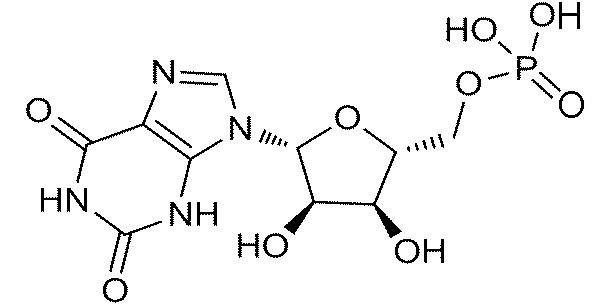
Активация T1R1/T1R3 под действием инозина и нуклеоидных производных на основе инозина
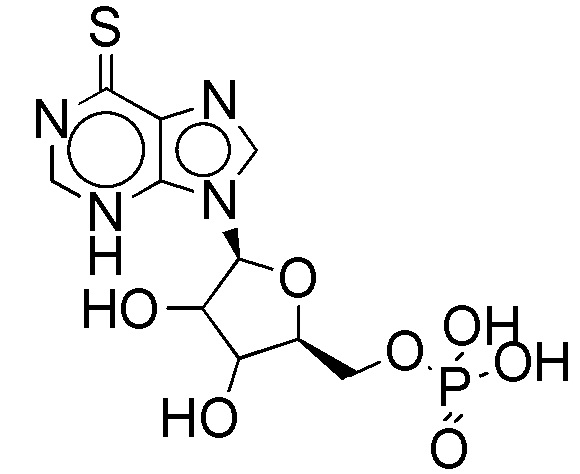
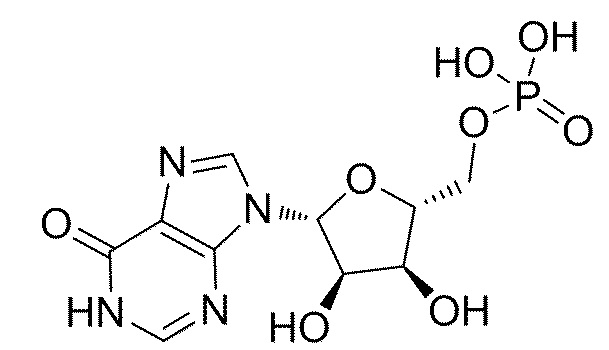
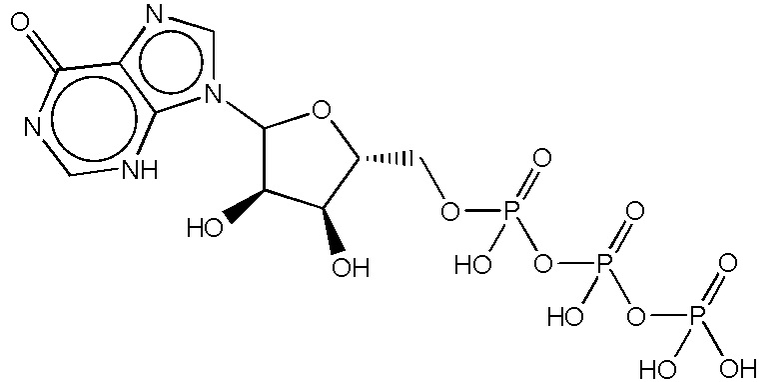
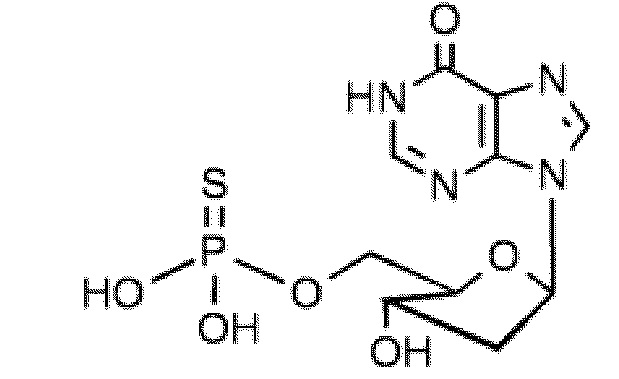
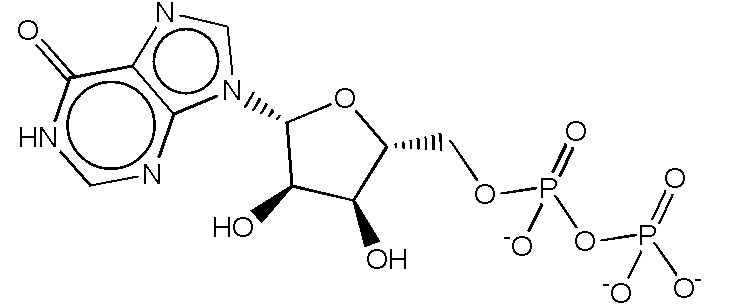
Активация T1R1/T1R3 под действием уридина и нуклеоидных производных на основе уридина
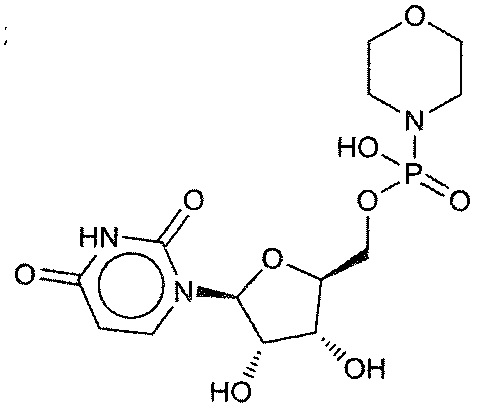
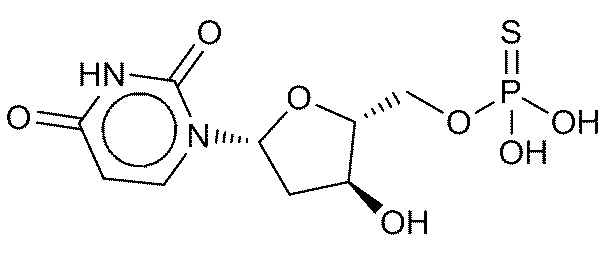
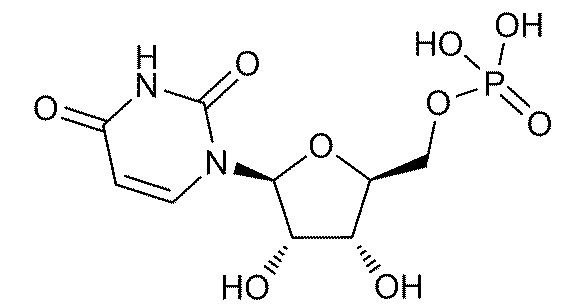
Активация T1R1/T1R3 под действием цитидина
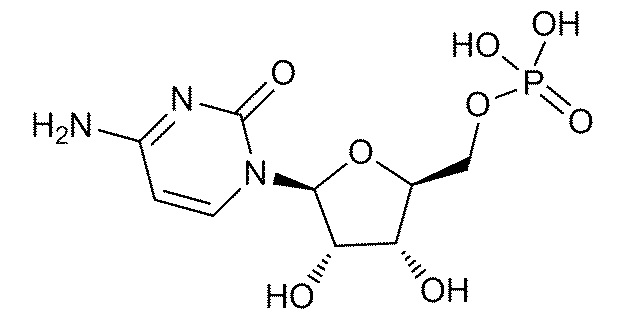
Активация T1R1/T1R3 под действием различных нуклеоидных производных
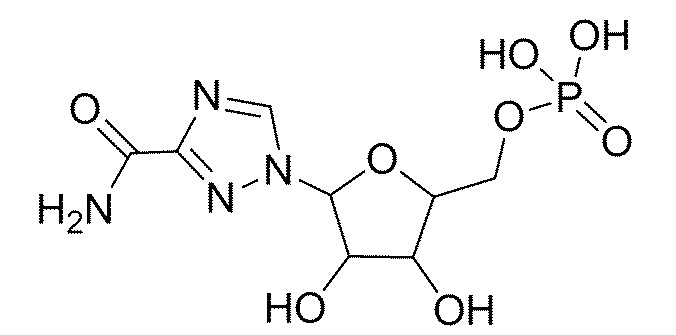
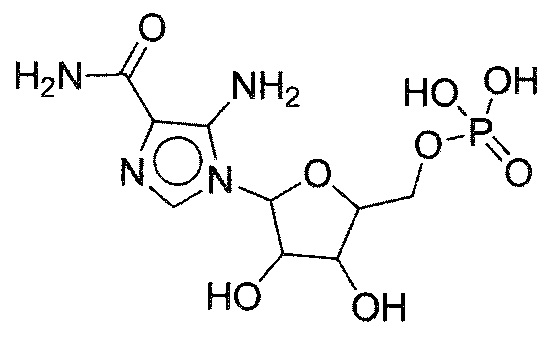
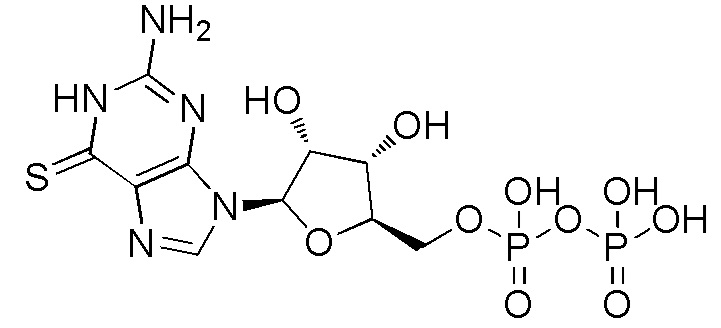
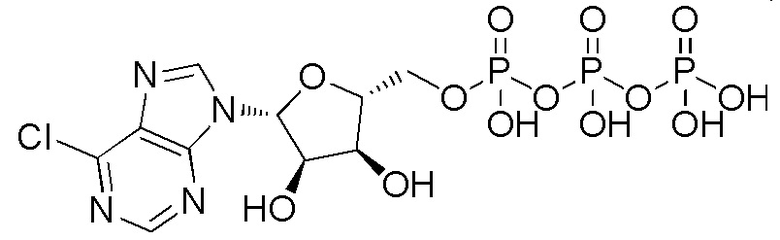
Модуляция T1R1/T1R3 под действием нуклеотидных производных
Н/Т=не тестировали
Н/А=Н/А
CNBD=невозможно определить
6-Аза-D-уридин-5'-монофосфат
Ациклогуанозинмонофосфат
Аденозин-5'-O-монофосфоротиоат (5'-AMPS)
Флуоресцентный аналог 5'-GMP
Трициклический нуклеозидмонофосфат (TCN-P)
6-cPe-ADP
5'-dAMPS
MANT-dGDP
5'-GMPS
MANT-AMP
6-PhEt-ADP
2-MeS-AMP
/5'-dTuMP)
Положительные и отрицательные контроли. EC50 для аминокислот определяли в присутствии 0,2 мМ IMP
Пример 3 - идентификация доменов T1R1, взаимодействующих с нуклеотидами и аминокислотами
В настоящем примере описывается in silico идентификация аминокислот в T1R1, которые взаимодействуют с нуклеотидами и аминокислотами, которые связываются с T1R1.
Методы: T1R1 кошки представляет рецептор, сопряженный с белком G, группы C (GPCR), который комплексуется с T1R3 с образованием гетеродимера рецептора вкуса умами. Модель домена Venus Flytrap (домена VFT) T1R1 кошки была построена с использованием кристаллической структуры метаботропного глутаматного рецептора 1EWT, другая группа C GPCR (Kunishima et al., Nature, 407: 971-977 (2000)), которая доступна из Банка данных белков (Berman et al., Nucleic Acids Research, 28: 235-242 (2000)). Кристаллические структуры VFT группы С GCR, включая метаботропные глутаматные рецепторы mGluR1, mGluR3, mGluR5 и mGluR7, демонстрируют удивительно похожие способы связывания лиганда с углублением активного сайта VFT. Эти способы связывания лиганда использовали для ручного выравнивания последовательности VFT T1R1 кошки с профилем последовательности метаботропных глутаматных рецепторов. Затем данное выравнивание использовали для моделирования по гомологии с использованием программного пакета Modeller (Eswar и др., Curr Protoc Bioinformatics, John Wiley & Sons, Inc., Supplement 15, 5.6.1-5.6.30 (2006)).
Моделирование аминокислот в активный сайт T1R1: аланин (L-аланин) первоначально располагали в активном сайте модели VFT T1R1 кошки, следуя размещению цвиттерионного скелета глутамата в кристаллических структурах mGluR. Полученный комплекс был уточнен с использованием молекулярной динамики и минимизации энергии. Энергию связывания оценивали вычислением разности между рассчитанной энергией комплекса и рассчитанной энергией выделенного лиганда и белка apo с использованием континуальной модели для воды. Другие аминокислоты встраивали в связанный аланиновый каркас с использованием Discovery Studio (Dassault Systemes, BIOVIA Corp., San Diego, CA, USA) и уточняли с использованием молекулярной динамики и минимизации энергии (Brooks et al., J. Comput. Chem., 30 (10): 545-614 (2009)). Для аминокислот были выбраны конечные модели, для которых рассчитанные энергии связывания были сопоставимы с таковыми для аланина, и которые также сохраняли консервативные взаимодействия с шарнирной областью, наблюдаемые в кристаллических структурах mGluR.
Моделирование нуклеотидов в активный сайт T1R1: IMP и GMP первоначально располагали в активном сайте VFT T1R1 кошки, следуя ранее опубликованному моделированию IMP в человеческий T1R1, как описано Zhang et al. (Zhang et al., Proc. Natl. Acad. Sci. USA, 105 (52): 20930-4 (2008)). Торсионные связи нуклеотида варьировали, и полученные модели уточняли с использованием молекулярной динамики и минимизации энергии. Были выбраны конечные модели, для которых энергии связывания были сопоставимы с таковыми для GMP, и которые также проявляли взаимодействия нуклеотидов с консервативными остатками, которые были установлены как важные для связывания IMP с человеческим T1R1 с помощью сайт-направленного мутагенеза (Zhang et al., Proc. Natl. Acad. Sci. USA, 105 (52): 20930-4 (2008)). Другие нуклеотиды и нуклеотидные аналоги первоначально перекрывались с моделями IMP и GMP и затем подвергались той же процедуре уточнения, оценки и выбора, описанной для IMP и GMP.
Результаты. Домен VTR T1R1 кошки состоит из двух долей, как показано на фиг. 14. Верхняя доля и нижняя доля связаны тремя нитями белка, называемого шарниром. На фиг. 14 верхняя доля находится в верхней части фигуры; нижняя доля находится в нижней части фигуры. Шарнир находится слева. Домен flytrap переходит от открытой к замкнутой конформации при связывании агониста. Активные аминокислоты и нуклеотиды связываются с доменом VFT между двумя долями (см. фиг. 14). Аминокислоты связываются с областью вблизи шарнира (см. фиг. 14: аланин показан в пространстве заполнения CPK на фигуре слева). Нуклеотиды связываются с областью, находящейся дистальнее к шарниру, но все еще расположенной между долями flytrap (см. фиг. 14: IMP показан в пространстве заполнения CPK на фигуре справа).
Связывание аминокислот: аминокислотные лиганды связываются с шарнирной областью VFT, как показано на фиг. 14, и хорошо скоординированы взаимодействиями вблизи шарнира. На фиг. 15 показан примерный способ связывания для L-аланина, иллюстрирующий возможные взаимодействия на основе водородных связей, солевых мостиков и катион-пи взаимодействия с Thr149, Ser172, Tyr220, Thr148, Glu170 и Asp302. Эти взаимодействия показаны пунктирными линиями.
С помощью сайт-направленного мутагенеза было установлено, что остатки Thr149, Ser172 и Tyr220 являются важными для связывания L-глутамата в рецепторе умами человека (Zhang et al., Proc. Natl. Acad. Sci. USA, 105 (52): 20930-4 (2008)). Было показано, что мышиная аминокислота Asn149, которая соответствует Thr148 кошки, имеет важное значение для связывания аминокислот у мыши (Toda et al., J. Biol. Chem., 288: 36863-36877 (2013)). Glu170 и Asp302 присутствуют в T1R1 кошки и мыши, но не у человека. У людей аминокислотами в этих положениях является аланин. Человеческий T1R1/T1R3 является высокоселективным для L-глутамата и L-аспарагиновой кислоты. В противоположность, T1R1/T1R3 кошки и мыши отвечают на широкий диапазон аминокислот. В модели, описанной в настоящем примере, Glu170 и Asp302 помогают координировать цвиттерионный азот аминокислотных лигандов, которые подходят активному сайту T1R1, одновременно создавая электростатическую среду, которая является «негостеприимной» для связывания L-глутамата и L-аспарагиновой кислоты. Используя сайт-направленный мутагенез, Toda et al. показали, что Glu170 и Asp302 ответственны за наблюдаемое различие в предпочтениях аминокислотных лигандов между кошкой и человеком (Toda et al., J. Biol. Chem., 288: 36863-36877 (2013)).
Связывание нуклеотидов: нуклеотиды связываются с положением, которое находится дистальнее к шарниру, чем аминокислоты, как показано на фиг. 14. На фиг. 16 показан примерный способ связывания GMP. Возможные взаимодействия на основе водородных связей и солевого мостика фосфата GMP и His47, His71, Arg277 и Asn69T1R1; сахара GMP и Asn302 и Ser306T1R1; и основания GMP и Ser384, His308 и Ala380 T1R1. Эти взаимодействия показаны пунктирными линиями.
Показано, что His308 координирует основание GMP, но также может координировать фосфат GMP. Также имеются дополнительные гидрофобные взаимодействия, которые дополняют энергию взаимодействия лиганда с VFT, и гибкость различных сайтов связывания может варьироваться (данные не показаны). Различные нуклеотиды могут проявлять различные взаимодействия с T1R1, но могут перекрываться с взаимодействиями, описанными здесь для GMP. На основании взаимосвязи структура-активность (SAR) и модели T1R1 можно предположить, что наличие отрицательно заряженной группы в области связывания фосфата T1R1 имеет важное значение для связывания нуклеотида с T1R1. На основании SAR и моделирования можно предположить, что присутствие азотистого основания, расширенного основания, замещенного основания или другого биоизостерического замещения азотистого основания, которое может образовывать взаимодействия в области связывания азотистого основания T1R1, также имеет важное значение для связывания (примеры оснований см. у Limbach et al., Nucleic Acids Research, 22 (12): 2183-2196 (1994)).
Аналогично на основании SAR и моделирования можно предположить, что взаимодействие между нуклеотидным сахаром (или молекулой замещения сахара) важно для успешного связывания нуклеотида с T1R1. Сахар может ориентировать соответствующую отрицательно заряженную группу для обеспечения взаимодействий между T1R1 и фосфатной областью и областью азотистого основания нуклеотида.
Несмотря на то, что различные нуклеотиды могут проявлять различные взаимодействия с T1R1, такие взаимодействия, вероятно, будут в значительной степени соответствовать описанному ряду возможных взаимодействий.
Мостиковые взаимодействия между связанными аминокислотой и нуклеотидом: Asp302 представляет собой остаток, присутствующий в VFT T1R1 у нескольких видов, включая кошку и мышь. Однако у людей аминокислота в этом положении представляет собой аланин. Asp302 имеет гибкую боковую цепь, которая может ориентироваться для координации цвиттерионного азота или боковой цепи связанного аминокислотного лиганда (фиг. 15), или может альтернативно ориентироваться для координации сахара связанного нуклеотида (фиг. 16). Кроме того, Asp302 также может быть ориентирована на одновременную координацию цвиттерионного азота скелета связанной аминокислоты и сахара нуклеотида (фиг. 17). Такое мостиковое взаимодействие может усилить синергетический эффект между связанной аминокислотой и связанным нуклеотидом. Поскольку аминокислотой в этом положении у людей является аланин, то такое мостиковое взаимодействие у человека невозможно. Альтернативная конформация азотистого основания может установить дополнительные мостиковые взаимодействия между Glu170 и выбранными азотистыми основаниями нуклеотидов (данные не показаны).
Пример 4 - in silico идентификация трансмембранных соединений
В настоящем примере описывается вычислительное моделирование рецептора T1R1/T1R3 для идентификации гипотетических трансмембранных соединений.
Вычислительные подходы были использованы для анализа трехмерной структуры T1R1 для идентификации трансмембранных областей, которые могут быть использованы для селективной активации рецептора T1R1/T1R3. Несмотря на то, что кристаллическая структура T1R1 кошки не была установлена, структурная модель трансмембранной области T1R1 была создана на основе кристаллической структуры человеческого метаботропного глутаматного рецептора 1 GPCR (mGluR1) (Wu et al., 2014 Science, Vol. 344, P. 58-64) и метаботропного глутаматного рецептора 5 GPCR (mGluR5) (Dore et al., Nature, 2014, Jul 31, 511 (7511): 557-62. Epub 2014, July 6). Затем использовали in silico моделирование для определения низкомолекулярных химических соединений, которые могли бы потенциально взаимодействовать с трансмембранным доменом мономера T1R1 рецептора T1R1/T1R3.
На фиг. 28 показано взаимодействие метилового эфира N-бензил-L-фенилаланина с T1R1. Можно видеть, что аспарагин (Asn) 735 трансмембранного домена T1R1 взаимодействует с эфирным лигандом. Кластер арильных остатков расположен в активном сайте, который может координироваться с лигандом путем образования кольцевых стэкинг-взаимодействий с фенильной группой лиганда на фигуре справа. На фиг. 35 показано моделирование 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-триона в трансмембранной области T1R1. Phe642 спирали 6 и Phe776 спирали 2 взаимодействуют с фенильным кольцом 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-триона и Asn792 спирали 6 взаимодействует с карбонильной группой посредством водородной связи (фиг. 35). Моделирование 1H-имидазо[4,5-c]пиридин-2(3H)-она в трансмембранной области T1R1 показывает образование водородной связи между Asn735 трансмембранной области T1R1 и 1H-имидазо[4,5-c]пиридин-2(3H)-оном (фиг. 36).
Пример 5 - активация рецептора T1R1/T1R3 под действием трансмембранных соединений
В настоящем примере описывается активация рецептора T1R1/T1R3 под действием трансмембранных соединений in vitro.
На основе in silico моделирования, описанного в примере 4, были идентифицированы и отобраны для дальнейшего тестирования in vitro гипотетические трансмембранные соединения для T1R1/T1R3. Функциональную характеристику in vitro выбранных соединений использовали для оценки эффективности гипотетических трансмембранных соединений в активации рецептора T1R1/T1R3 одних или в комбинации с одним или более нуклеотидами и/или одной иди более аминокислотами.
Методы: клетки HEK293, которые стабильно экспрессируют T1R3 и индуцибельно экспрессируют T1R1, подвергали воздействию трансмембранных соединений одних или в комбинации с одной или более аминокислотами и/или одним или более нуклеотидами для активации рецептора умами. Активацию рецептора T1R1/T1R3 детектировали по изменению уровней внутриклеточного кальция с использованием флуоресцентного красителя, чувствительного к кальцию. Клетки, которые экспрессируют T1R3, но не T1R1, использовали в качестве контроля. Для сбора данных использовали систему FLIPR® Tetra или ридер FlexStation® 3.
Для каждого трансмембранного соединения были получены кривые зависимости доза-эффект и определены следующие показатели: EC50 одного трансмембранного соединения; EC50 трансмембранного соединения с 20 мМ аланина; EC50 трансмембранного соединения с 0,2 мМ IMP; EC50 трансмембранного соединения с 20 мМ аланина и 0,2 мМ IMP. Термин половинная максимальная эффективная концентрация (EC50) относится к концентрации соединения, которая вызывает половинный ответ между базовой линией и максимумом после определенного времени воздействия. В каждом эксперименте к клеткам, экспрессирующим T1R1/T1R3, добавляли серийные разведения трансмембранного соединения до 10 мМ.
Результаты: обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3, одним 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-трионом (например, в буфере) или в комбинации с 20 мМ аланина приводила к активации рецептора T1R1/T1R3, о чем свидетельствует изменение уровней внутриклеточного кальция (ΔF/F0) и приводит к установленному значению EC50 выше 1 мМ. В противоположность, обработка клеток 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-трионом в присутствии 0,2 мМ IMP или в присутствии 20 мМ аланина и 0,2 мМ IMP, приводила к снижению значения EC50 до 0,32±0,05 мМ и 0,33±0,04 соответственно (фиг. 37 и таблица 17). Эти результаты показывают, что IMP представляет собой положительный аллостерический модулятор трансмембранного соединения 1-бензил-3-(2-оксо-2-фенилэтил)имидазолидин-2,4,5-триона, то есть соединения являются синергетическими по отношению к T1R1/T1R3.
Было установлено, что одно соединение N-(бензо[d][1,3]диоксол-5-ил)-2-пропилпентанамид функционирует в качестве агониста T1R1/T1R3 (фиг. 39 и таблица 17). В присутствии IMP или IMP и аланина значение EC50 N-(бензо[d][1,3]диоксол-5-ил)-2-пропилпентанамида снижалось, и значение ΔF/F0 достоверно увеличивалось (фиг. 39 и таблица 17). Эти результаты показывают, что аланин и IMP действуют синергически с N-(бензо[d][1,3]диоксол-5-ил)-2-пропилпентанамидом в активации T1R1/T1R3. Аналогичные результаты наблюдали для трансмембранного соединения N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида (фиг. 40 и таблица 17). IMP функционировал как положительный аллостерический модулятор N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида.
Одно предполагаемое трансмембранное соединение, N-(2-амино-2-оксо-1-фенилэтил)-3-хлор-4,5-диметоксибензамид, не активировало T1R1/T1R3; однако в присутствии IMP или IMP и аланина, N-(2-амино-2-оксо-1-фенилэтил)-3-хлор-4,5-диметоксибензамид приводил к активации T1R1/T1R3, о чем свидетельствовало повышение ΔF/F0 в более низких концентрациях и снижение значения EC50 (фиг. 41 и таблица 17). Аналогичные результаты наблюдали с 2-((5-(4-(метилтио)фенил)-2Н-тетразол-2-ил)метил)пиридином (фиг. 43 и таблица 17).
Соединение, (E)-3-(4-метоксифенил)-N-(пентан-3-ил)акриламид, функционирует как трансмембранное соединение для T1R1/T1R3 с EC50, равной 0,45±0,01. В присутствии IMP или IMP и аланина активность (E)-3-(4-метоксифенил)-N-(пентан-3-ил)акриламида была значительно усилена, что привело к значениям EC50 0,15±0,02 и 0,08±0,01 соответственно, указывая на то, что IMP и аланин функционируют в качестве аллостерических модуляторов (E)-3-(4-метоксифенил)-N-(пентан-3-ил)акриламида (фиг. 42 и таблица 17).
Затем анализировали трансмембранное соединение, N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамид. На фиг. 44 представлены кривые зависимости доза-эффект для N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида в присутствии GMP и фенилаланина; GMP, фенилаланина и аланина; GMP, фенилаланина и IMP; или GMP, фенилаланина, аланина и IMP. Присутствие аланина и IMP достоверно снижало значение EC50 N-(гептан-4-ил)бензо[d] [1,3]диоксол-5-карбоксамида по сравнению с значением EC50 N- (гептан-4-ил)бензо[D][1,3]диоксол-5-карбоксамида в присутствии фенилаланина и GMP или только в присутствии IMP (таблица 19). Как указывалось выше, IMP функционирует в качестве аллостерического модулятора агонистической активности N- (гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида; однако полученные результаты показывают, что комбинация IMP и аланина приводила к более низкому значению EC50 и более резкому изменению значения ΔF/F0 по сравнению с одним IMP, указывая на то, что эта комбинация проявляла синергетический эффект с N-(гептан-4-ил)бензо[D][1,3]диоксол-5-карбоксамидом в активации T1R1/T1R3 (фиг. 44 и таблица 19). Кроме того, значение ΔF/F0 было примерно в 10 раз выше в присутствии тройной смеси, состоящей из N-(гептан-4-ил)бензо[d][1,3]диоксол-5-карбоксамида, фенилаланина и GMP, по сравнению с комбинацией фенилаланина и GMP в отсутствие агониста (фиг. 45).
На фиг. 46 приведены кривые зависимости доза-эффект для использованных положительных и отрицательных контролей, и результаты для активных соединений обобщены в таблице 17. В таблице 18 представлены результаты для всех тестированных соединений. Для положительного и отрицательного контроля были определены кривые зависимости доза-эффект для аминокислот в присутствии 0,2 мМ IMP. Кривые зависимости доза-эффект для нуклеотидов определяли в присутствии 20 мМ аланина.
Не желая связываться с конкретной теорией, данные результаты показывают, что одни нуклеотиды, например IMP, или комбинации нуклеотидов и аминокислот, например IMP и аланин, функционируют в качестве положительных модуляторов описанных трансмембранных соединений, что приводит к снижению количества агониста, необходимого для достаточной активации рецептора T1R1/T1R3.
Трансмемебранные соединения, которые модулируют активность T1R1/T1R3
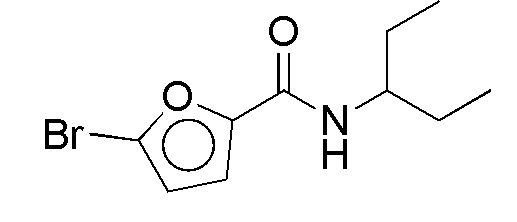
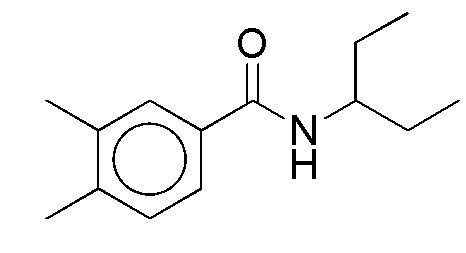
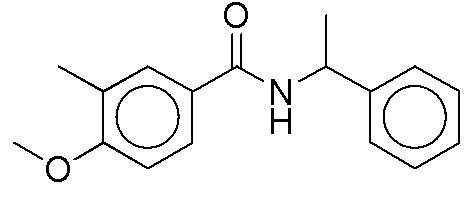
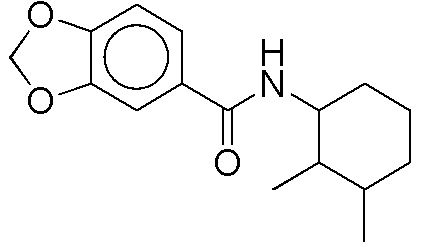
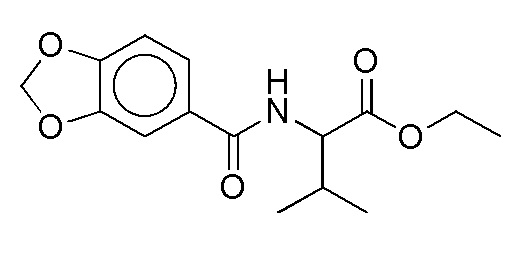
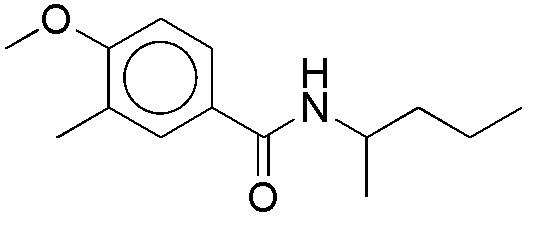
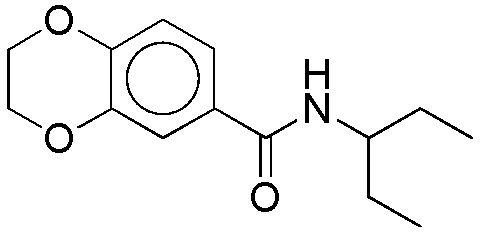
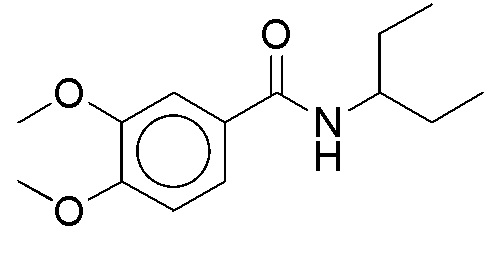
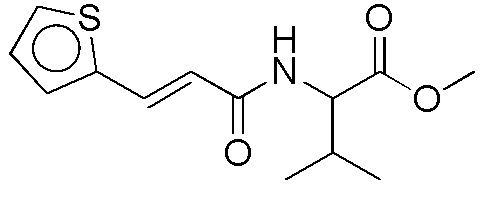
(2E)-3-(3,4-диметоксифенил)-N-(пентан-2-ил)проп-2-енамид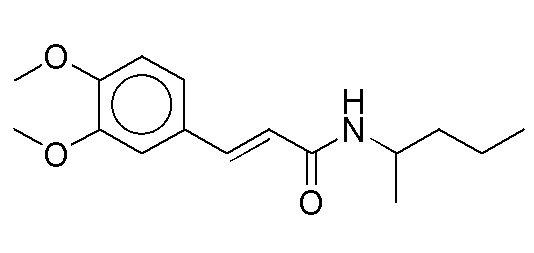
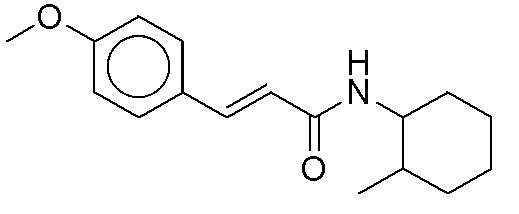
N-(2-фенилэтил)-N'-(пиридин-3-илметил)этандиамид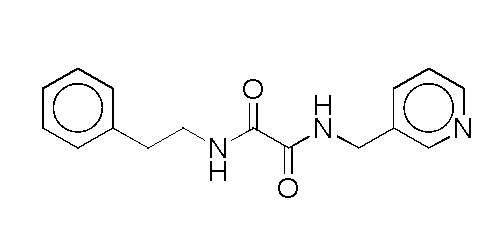
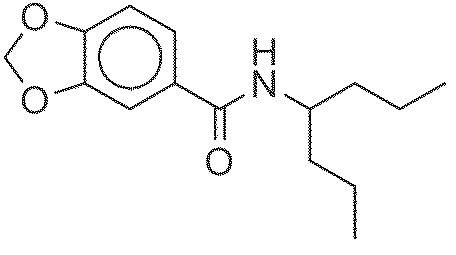
1H-инден-1-ил)мочевина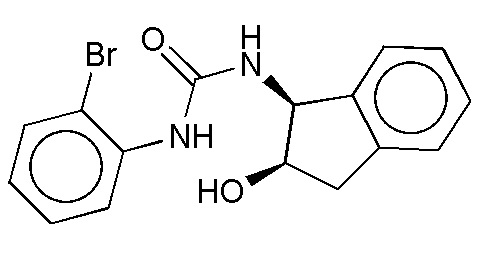
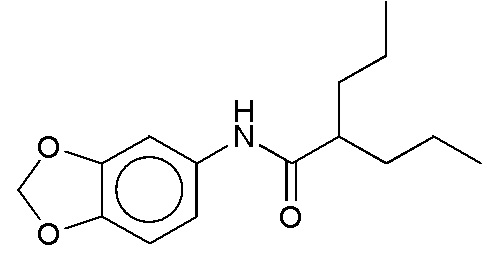
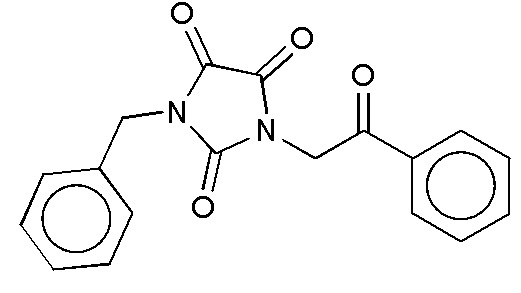
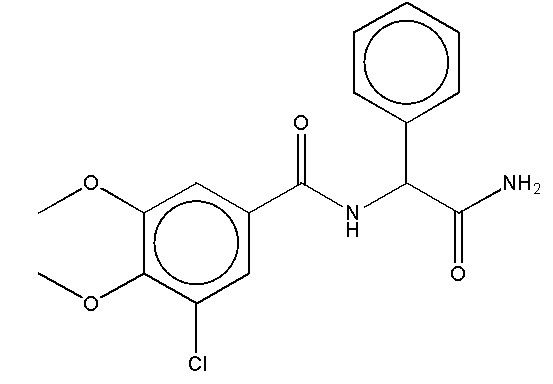
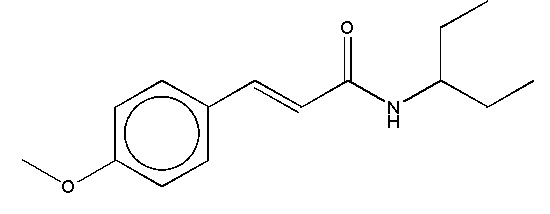
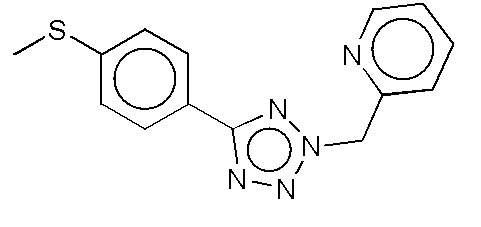
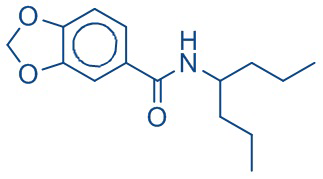
CNBD: невозможно определить
Активация T1R1/T1R3 под действием трансмембранных соединений
Н/Т=не тестировали
Н/А=неактивный
CNBD=невозможно определить
N-(1-этилпропил)-3,4-диметилбензамид
этил N-(1,3-бензодиоксол-5-илкарбонил)валинат
(2E)-3-(3,4-диметoксифенил)-N-(пентан-2-ил)проп-2-енамид
N-(2-фенилэтил)-N'-(пиридин-3-илметил)этaндиамид
1-(4-хлорфенил)-3-(1-(п-толил)пропил)мочевина
Активация T1R1/T1R3 под действием комбинаций нуклеотидов, аминокислот и трансмембранных соединений
Положительные и отрицательные контроли с 0,2 мМ IMP
Пример 6 - активация рецептора T1R1/T1R3 под действием трансмембранных соединений
В настоящем примере описывается активация рецептора T1R1/T1R3 под действием трансмембранных соединений in vitro.
Основываясь на in silico моделировании, описанном в примере 4, были идентифицированы и отобраны для дальнейшего тестирования in vitro гипотетические трансмембранные соединения для T1R1/T1R3. Функциональную характеристику in vitro выбранных соединений использовали для оценки эффективности гипотетических трансмембранных соединений в активации рецептора T1R1/T1R3 одних или в комбинации с одним или более нуклеотидами и/или одной или более аминокислотами.
Методы. Функциональную характеристику выбранных соединений in vitro проводили, как описано в примере 5.
Результаты. Как показано в таблице 21, обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3, только одним метиловым эфиром N-бензил-L-фенилаланина HCl (например, в буфере) приводила к активации рецептора T1R1/T1R3 с EC50 0,03±0,002 мМ. Объединение соединения с 20 мМ L-аланина повысило EC50 до 0,05±0,001 мМ. Объединение соединения с 0,2 мМ IMP снижало значение EC50 до 0,02±0,001 мМ, и объединение соединения с 20 мМ L-аланина и 0,2 мМ IMP понижало EC50 до 0,02±0,021 мМ.
EC50 метилового эфира N-бензил-L-фенилаланина HCl в активации T1R1/T1R3
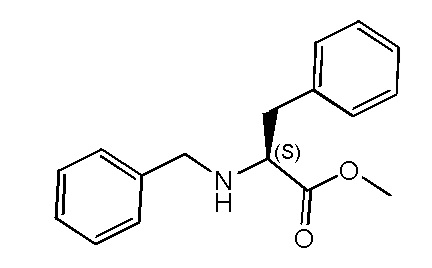
Как показано в таблице 22, обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3, только одним N-(2-(1H-индол-3-ил)этил)никотинамидом (например, в буфере) приводила к активации рецептора T1R1/T1R3 с EC50 0,15±0,03 мМ. Объединение соединения с 20 мМ L-аланина повышало EC50 до более чем 0,1 мМ. Объединение соединения с 0,2 мМ IMP снижало значение EC50 до 0,05±0,01 мМ, и объединение соединения с 20 мМ L-аланина и 0,2 мМ IMP снижало EC50 до 0,04±0,01 мМ.
EC50 N-(2-(1Н-индол-3-ил)никотинамида в активации T1R1/T1R3
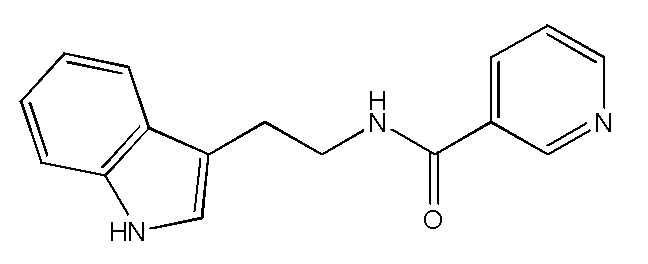
Как показано в таблице 23, обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3 только одним 2-амино-N-фенэтилбензамидом (например, в буфере) приводила к активации рецептора T1R1/T1R3 с EC50 0,42±0,01 мМ. Объединение соединения с 20 мМ L-аланина повышало значение EC50 до 0,48±0,01 мМ. Объединение соединения с 0,2 мМ IMP понижало EC50 до 0,14±0,03 мМ, и объединение соединения с 20 мМ L-аланина и 0,2 мМ IMP понижало EC50 до 0,09±0,01 мМ.
EC50 2-амино-N-фенэтилбензамида в активации T1R1/T1R3
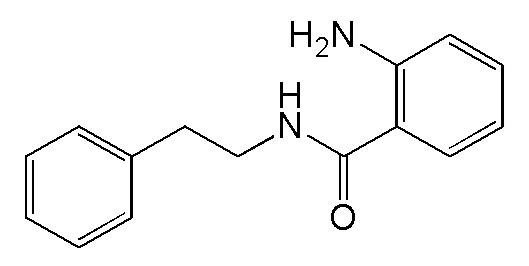
Не желая связываться с какой-либо конкретной теорией, данные результаты показывают, что одни нуклеотиды, например IMP, или комбинации нуклеотидов и аминокислот, например IMP и аланин, функционируют в качестве положительных модуляторов описанных трансмембранных соединений, что приводит к снижению количества агониста, необходимого для достаточной активации рецептора T1R1/T1R3.
Пример 7 - активация рецептора T1R1/T1R3 под действием трансмембранных соединений и нуклеотидных производных
В настоящем примере описывается активация рецептора T1R1/T1R3 под действием трансмембранных соединений и нуклеотидных производных in vitro.
Основываясь на in silico моделировании, описанным в примере 4, были идентифицированы и отобраны для дальнейшего тестирования in vitro гипотетические трансмембранные соединения для T1R1/T1R3. Функциональную характеристику in vitro выбранных соединений использовали для оценки эффективности гипотетических трансмембранных соединений в активации рецептора T1R1/T1R3 одних или в комбинации с одним или более нуклеотидами и/или одной или более аминокислотами. Также выбранные нуклеотидные производные тестировали одни или в комбинации с одним или более нуклеотидами и/или одной или более аминокислотами.
Методы. Функциональную характеристику выбранных соединений in vitro проводили, как описано в примерах 1, 2 и 5.
Результаты. Эффект всех трансмембранных соединений и нуклеотидных производных, которые были тестированы в активации T1R1/T1R3, показан в таблице 26. Обработка клеток HEK293, экспрессирующих рецепторы T1R1/T1R3 одними несколькими трансмембранными соединениями в буфере, привела к активации T1R1/T1R3, о чем свидетельствует изменение уровней внутриклеточного кальция (ΔF/F0), как показано в таблице 24A-O. Когда данные соединения комбинировали с 0,2 мМ IMP или смесью 0,2 мМ IMP и 20 мМ аланина, то трансмембранные соединения были более эффективными в активации T1R1/T1R3, о чем свидетельствует снижение значения EC50 трансмембранных соединений (таблица 24A-O и фиг. 58-75). В таблице 24A-O приведены значения EC50 для каждого активного трансмембранного соединения одного (в буфере) и в присутствии L-аланина, IMP и L-аланина+IMP. В таблице 25 и на фиг. 71 показаны значения EC50 и кривые зависимости доза-эффект для контрольных соединений (20 мМ аминокислоты в присутствии 0,2 мМ IMP). Не желая связываться с какой-либо конкретной теорией, данные результаты показывают, что одни нуклеотиды, например IMP, или комбинации нуклеотидов и аминокислот, например IMP и аланина, функционируют в качестве положительных модуляторов описанных трансмембранных соединений, что приводит к снижению количества агониста, необходимого для достаточной активации рецептора T1R1/T1R3.
Таблицы 24А-О. EC50 трансмембранных соединений в активации T1R1/T1R3.
Таблица 25
Модуляция T1R1/T1R3 под действием трансмембранных соединений
Н/Т=не тестировали
Н/А=Н/А
CNBD=невозможно определить
Пример 8 - активация рецептора T1R1/T1R3 под действием трансмембранных соединений
В настоящем примере описывается активация рецептора T1R1/T1R3 под действием трансмембранных соединений in vitro, где трансмембранные соединения функционируют в качестве агонистов рецептора и/или положительных аллостерических модуляторов (PAM). При функционировании в качестве PAM трансмембранные соединения повышают эффект нуклеотидов и аминокислот в отношение активности рецептора.
Основываясь на in silico моделировании, описанном в примере 4, были идентифицированы и отобраны для дальнейшего тестирования in vitro гипотетические трансмембранные соединения для T1R1/T1R3 в качестве агониста и/или рецептора. Функциональную характеристику in vitro выбранных соединений использовали для оценки эффективности гипотетических трансмембранных соединений в качестве агонистов и/или PAM в активации рецептора T1R1/T1R3.
Метод скрининга агонистов: клетки HEK293, которые стабильно экспрессируют T1R3 и индуцибельно экспрессируют T1R1, подвергали воздействию трансмембранного соединения. Активацию рецептора T1R1/T1R3 детектировали по изменению уровней внутриклеточного кальция с использованием флуоресцентного красителя, чувствительного к кальцию, и/или люминесцентной репортерной системы. Клетки, которые не экспрессируют рецептор T1R1/T1R3, использовали в качестве контроля. Для сбора данных использовали систему FLIPR® Tetra или ридер FlexStation® 3.
Каждое трансмембранное соединение тестировали в концентрациях 0,01 мМ, 0,1 мМ и 1 мМ. Строили кривые зависимости доза-эффект для каждого трансмембранного соединения, которое активировало T1R1/T1R3. Для построения кривых зависимости доза-эффект трансмембранное соединение тестировали в концентрациях от 0,0001 мМ до 1,0 мМ в присутствии GMP и Ala. Были построены кривые зависимости доза-эффект, где концентрацию Ala поддерживали постоянной на 20 мМ, и концентрацию GMP увеличивали с 0,001 до 1 мМ (в частности, 0,001; 0,003; 0,01; 0,03; 0,1; 0,3; 0,6 и 1 мМ). Аналогично, концентрацию GMP поддерживали постоянной на 1 мМ и концентрацию Ala изменяли в пределах от 0,1 до 100 мМ (в частности, 0,1; 0,3; 1; 3; 10; 30; 60 и 100 мМ).
Метод скрининга PAM: клетки HEK293, которые стабильно экспрессируют T1R3 и индуцибельно экспрессируют T1R1, подвергали воздействию трансмембранного соединения одного или в комбинации с Ala и GMP для активации рецептора умами. Активацию рецептора T1R1/T1R3 детектировали по изменению уровней внутриклеточного кальция с использованием флуоресцентного красителя, чувствительного к кальцию, и/или люминесцентной репортерной системы. Клетки, которые не экспрессируют рецептор T1R1/T1R3, использовали в качестве контроля. Для сбора данных использовали систему FLIPR® Tetra или ридер FlexStation® 3.
Строили кривые зависимости доза-эффект для каждого трансмембранного соединения в концентрациях 0 (только буфер), 0,01; 0,1 и 1 мМ, где каждую из трех концентраций трансмембранного соединения тестировали в комбинации с 0,03 мМ GMP+100 мМ Ala (T1); 0,6 мМ GMP+10 мМ Ala (T2); 0,1 мМ GMP+60 мМ Ala (T3) и 0,3 мМ GMP+60 мМ Ala (T4). Смесь T4 также тестировали в серии двукратных разведений (концентрация T4 (X)). В этих экспериментах первая испытанная концентрация составляла 2Х (2 раза) концентрации Т4. Последующие испытанные концентрации представляли 2-кратные разведения (1X, 0,5X и т.д.). Эту серию разведений тестировали с добавлением испытуемого соединения или без него в постоянной концентрации, равной 0,3 мМ.
Активацию рецептора умами также определяли в присутствии 1 мМ GMP+100 мМ Ala для получения «максимального» уровня активации рецептора умами. Соединение классифицировали как PAM, если ответ на любую комбинацию соединение+Ala+GMP был выше, чем суммарный ответ на одно соединение и ответ на GMP+аланин один.
Результаты. Как показано в таблице 27, было тестировано 24 различных трансмембранных соединения, и девять были идентифицированы как агонист T1R1/T1R3, PAM или обладающие обеими активностями.
Трансмембранные соединения, которые функционируют в качестве агониста, PAM для T1R1/T1R3 или обоих
Как показано в таблице 28, девять из испытанных соединений были активными в качестве агонистов и/или PAM T1R1/T1R3. На фиг. 72-80 показаны кривые зависимости доза-эффект для определения профиля агониста и PAM для каждого соединения, идентифицированного как агонист и/или PAM T1R1/T1R3.
Не желая связываться с какой-либо конкретной теорией, полученные результаты показывают, что одни трансмембранные соединения могут активировать T1R1/T1R3 в качестве агонистов и могут также функционировать как положительные аллостерические модуляторы активации GMP и Ala T1R1/T1R3, тем самым уменьшая количество необходимого агониста, необходимое для достаточного активирования рецептора T1R1/T1R3.
Пример 9 - идентификация остатков T1R1, взаимодействующих с трансмембранным соединением.
В настоящем примере описывается in silico идентификация аминокислот в T1R1, которые взаимодействуют с трансмембранными соединениями, которые связываются с T1R1.
Методы: T1R1 кошки представляет собой сопряженный с G-белком рецептор группы C (GPCR), как и T1R2, T1R3, CaSR, GabaB и mGlu. GPCR группы С содержит (1) большой внешний домен, называемый областью Venus Flyprap (VFT), (2) 7 трансмембранных доменов (7TM) и (3) домен, богатый цистеином, который соединяет VFT и 7TM. Модель по гомологии кошачьего домена 7TM T1R1 была сконструирована на основе кристаллических структур 4OR2 и 4OO9 из Банка данных белков (Berman et al., Nucleic Acids Research, 28: 235-242 (2000)). 4OR2 и 4OO9 представляют кристаллические структуры частей двух метаботропных глутаматных рецепторов, которые представляют GPCR группы C. 4OR2 представляет кристаллическую структуру трансмембранного домена mGluR1 со связанным отрицательным аллостерическим модулятором (NAM) (Wu et al., Science, 2014 4 Apr, 344 (6179): 58-64. Epub 2014 6 марта). 4OO9 является кристаллической структурой трансмембранного домена mGluR5 со связанным NAM (Dore et al., Nature, 2014, 31 Jul, 511 (7511): 557-62. Epub 2014 6 Jul). Модели были построены с использованием программ I-TASSER Suite (Yang et al., Nature Methods, 12: 7-8 (2015)) и программного пакета Modeller (Eswar и др., Burrinformatics Curr Protoc, John Wiley & Sons, Inc., Supplement 15, 5.6.1-5.6.30 (2006)), который является частью набора программ DiscoveryStudio (DS) от Dassault Systemes, BIOVIA Corp., Сан-Диего, Калифорния, США. Имеется примерно 25% идентичность последовательностей между доменами mGluR1 и 7TM T1R1 кошки. Метиловый эфир N-бензил-L-фенилаланина был подвергнут докингу к аллостерическому сайту 7TM T1R1 кошки в модели T1R1, с использованием программы докинга BioDock от BioPredict, Inc. (Oradell, NJ, USA). Для докинга аминокислот и нуклеотидов к домену VFT был использован аналогичный протокол, описанный для моделирования докинга нуклеотидов с доменом VFT.
Результаты. На модели докинга метиловый эфир N-бензил-L-фенилаланина взаимодействует со следующими аминокислотами аллостерического сайта связывания 7TM T1R1 кошки: Ala795, Ala796 и Asn792, которые находятся в спирали 7 7TM; Trp773 и Phe776, которые находятся в спирали 6 7TM; Ala731, Phe728, Leu730, Phe732 и Asn735, которые находятся в спирали 5 7TM; Ala689, Ser686, Gln690, Ile693, Cys694 и Leu695, которые находятся в спирали 4 7TM; и Arg634, Gln635, Phe642, Ala639, Ala643 и Leu638, которые находятся в спирали 3 7TM (фиг. 28. Эфирная группа метилового эфира N-бензил-L-фенилаланина образует водородную связь с Asn735. Модели других трансмембранных соединений показывают, что лиганд может образовывать водородные связи с Asn735, Ser686 или обоими.
Большинство гидрофобных взаимодействий между метиловым эфиром N-бензил-L-фенилаланина и 7TM-доменом T1R1 имеют место между лигандом и Trp773, Phe776, Phe732, Phe728, Leu730, Leu695, Leu638 и Phe642. Эти аминокислоты также обеспечивают большую часть гидрофобных взаимодействий между другими трансмембранными лигандами T1R1 и трансмембранным доменом T1R1.
Примечательным признаком активного сайта T1R1 является количество остатков, которые могут подвергаться стэкинг-взаимодействию со связанным лигандом. Модель метилового эфира N-бензил-L-фенилаланина, связанного с T1R1 7TM, показывает стэкинг-взаимодействия бензильной группы с трансмембранным доменом. Этот признак характерен для моделей других активных трансмембранных соединений, связанных с T1R1 7TM. Они могут способствовать как связыванию, так и стабилизации активной конформации T1R1/T1R3. Аминокислоты 7TM T1R1, которые могут образовывать такие взаимодействия, включают Trp773, Phe776, Phe732, Phe728 и Phe642.
Несмотря на то, что раскрытый в настоящее время предмет изобретения и его преимущества были подробно описаны, следует понимать, что здесь могут быть сделаны различные изменения, замены и модификации, не отступая от сущности и объема изобретения, что определено прилагаемой формулой изобретения. Кроме того, объем настоящей заявки не ограничивается конкретными вариантами осуществления способа, устройства, производства и композиции вещества, средств, способов и стадий, описанных в заявке. Как должно быть понятно специалистам в данной области техники, из раскрытия раскрытого здесь предмета изобретения, что могут быть использованы способы, устройства, производства и композиции вещества, средства, способы и стадии, существующие или разрабатываемые в настоящее время, которые выполняют по существу одинаковую функцию или достигают практически того же результата, что и соответствующие варианты осуществления, описанные здесь, в соответствии с раскрытым предметом изобретения. Следовательно, прилагаемая формула изобретения должна включать в свой объем такие способы, устройства, производство, композиции вещества, средства, способы и стадии.
Патенты, патентные заявки, публикации, описания продуктов и протоколы приводятся во всей этой заявке, раскрытие которых включено в настоящее описание посредством ссылки во всей их полноте для всех целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ МОДУЛЯЦИИ ВКУСОВЫХ РЕЦЕПТОРОВ | 2015 |
|
RU2740310C2 |
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ АКТИВНОСТЬ КАЛЬЦИЙЧУВСТВИТЕЛЬНЫХ РЕЦЕПТОРОВ, ДЛЯ МОДУЛЯЦИИ ВКУСА КОКУМИ И КОРМОВЫЕ ПРОДУКТЫ ДЛЯ ДОМАШНИХ ЖИВОТНЫХ, СОДЕРЖАЩИЕ ИХ | 2017 |
|
RU2759563C2 |
| СОЕДИНЕНИЯ, ВКЛЮЧАЮЩИЕ СВЯЗАННЫЕ ГЕТЕРОАРИЛЬНЫЕ ФРАГМЕНТЫ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ НОВЫХ МОДИФИКАТОРОВ ВКУСО-АРОМАТА УМАМИ, ТАСТАНТОВ (СТИМУЛЯТОРОВ СЕНСОРНЫХ КЛЕТОК ВКУСОВЫХ СОСОЧКОВ ЯЗЫКА) И УСИЛИТЕЛЕЙ ВКУСА В ПИЩЕВЫХ КОМПОЗИЦИЯХ | 2006 |
|
RU2410383C2 |
| ВКУСОАРОМАТИЧЕСКИЕ ДОБАВКИ | 2013 |
|
RU2639888C2 |
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ АКТИВНОСТЬ РЕЦЕПТОРОВ GPR92, И КОРМОВЫЕ ПРОДУКТЫ ДЛЯ ДОМАШНИХ ЖИВОТНЫХ, СОДЕРЖАЩИЕ ИХ | 2019 |
|
RU2807217C2 |
| НОВЫЕ АРОМАТИЗИРУЮЩИЕ ВЕЩЕСТВА, МОДИФИКАТОРЫ ВКУСА, СОЕДИНЕНИЯ, ПРИДАЮЩИЕ ВКУС, УСИЛИТЕЛИ ВКУСА, СОЕДИНЕНИЯ, ПРИДАЮЩИЕ ВКУС "УМАМИ" ИЛИ СЛАДКИЙ ВКУС, И/ИЛИ УСИЛИТЕЛИ И ИХ ПРИМЕНЕНИЕ | 2004 |
|
RU2419602C2 |
| СТОЙКАЯ В ХРАНЕНИИ КУЛИНАРНАЯ ДОБАВКА И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 2006 |
|
RU2414148C2 |
| Вариант фосфорибозилпирофосфатамидотрансферазы и способ получения пуринового нуклеотида с его использованием | 2019 |
|
RU2736372C1 |
| СПОСОБЫ ИДЕНТИФИКАЦИИ МОДУЛЯТОРОВ GPR92 | 2017 |
|
RU2742608C2 |
| СТАБИЛЬНОЕ ВСПОМОГАТЕЛЬНОЕ КУЛИНАРНОЕ СРЕДСТВО И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2005 |
|
RU2381719C2 |
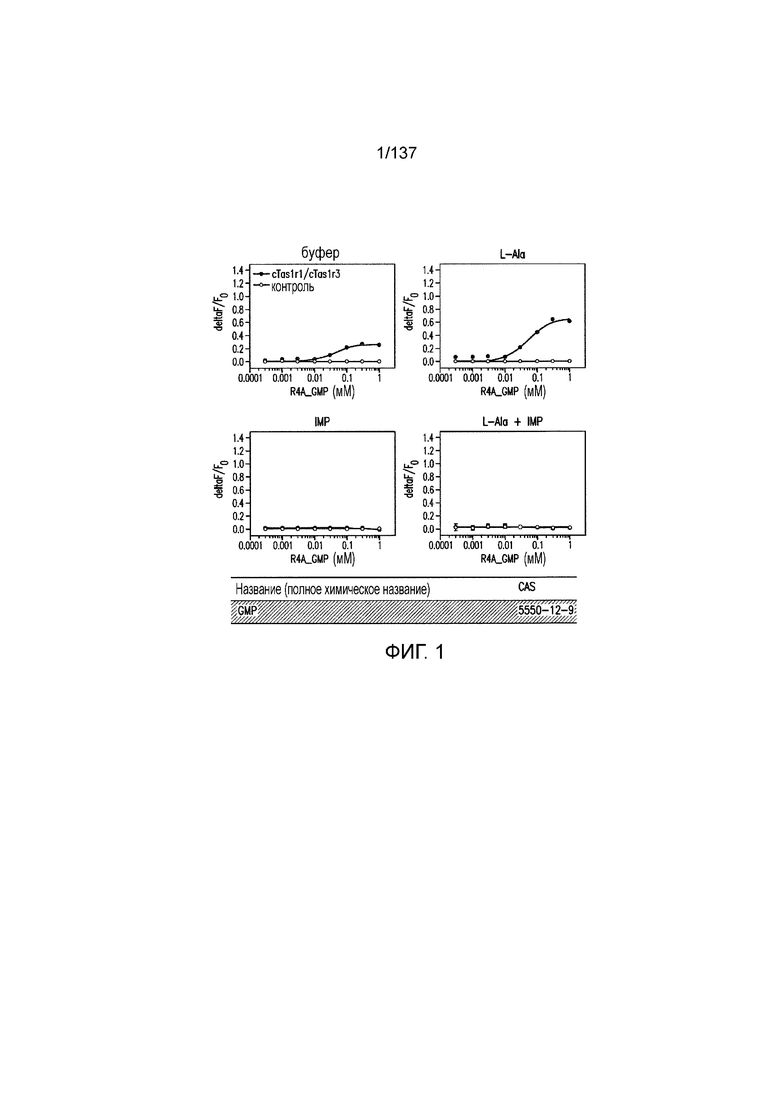
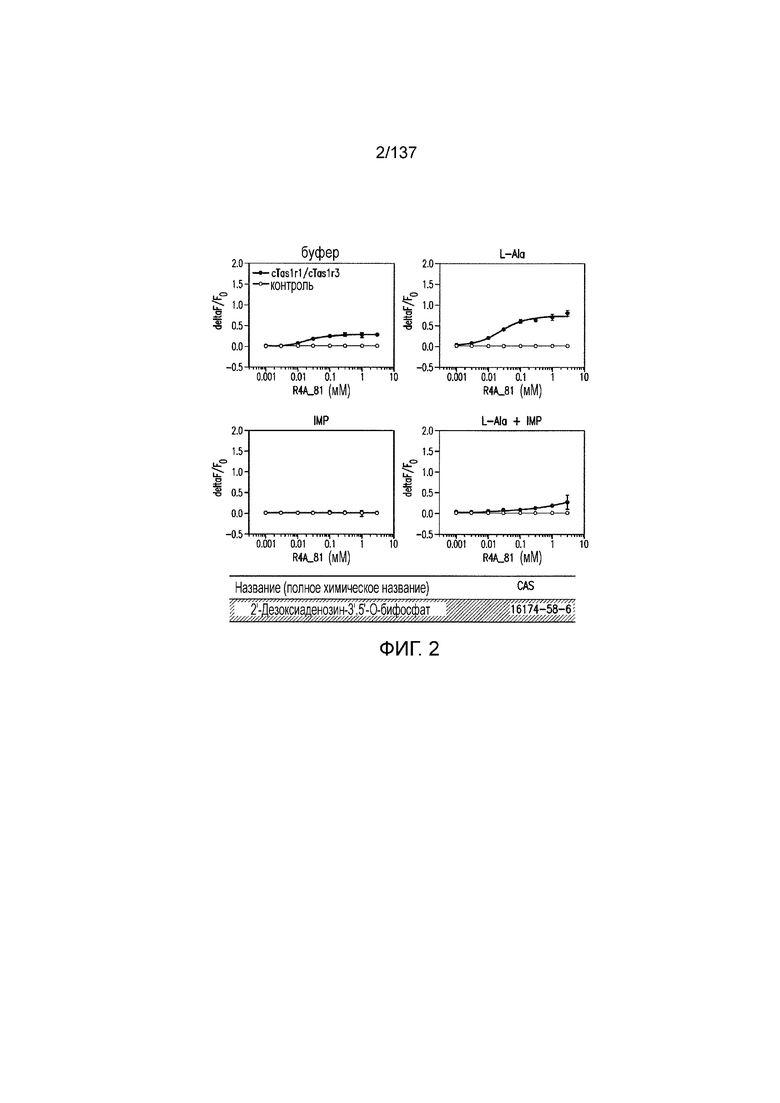
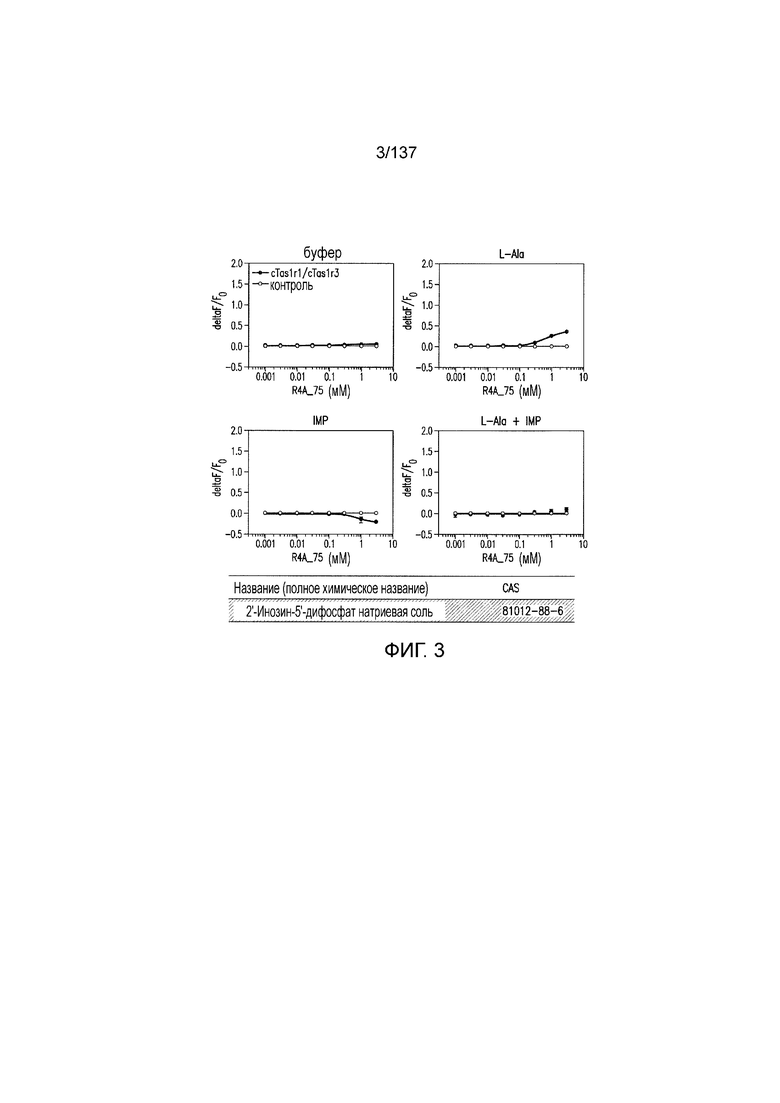
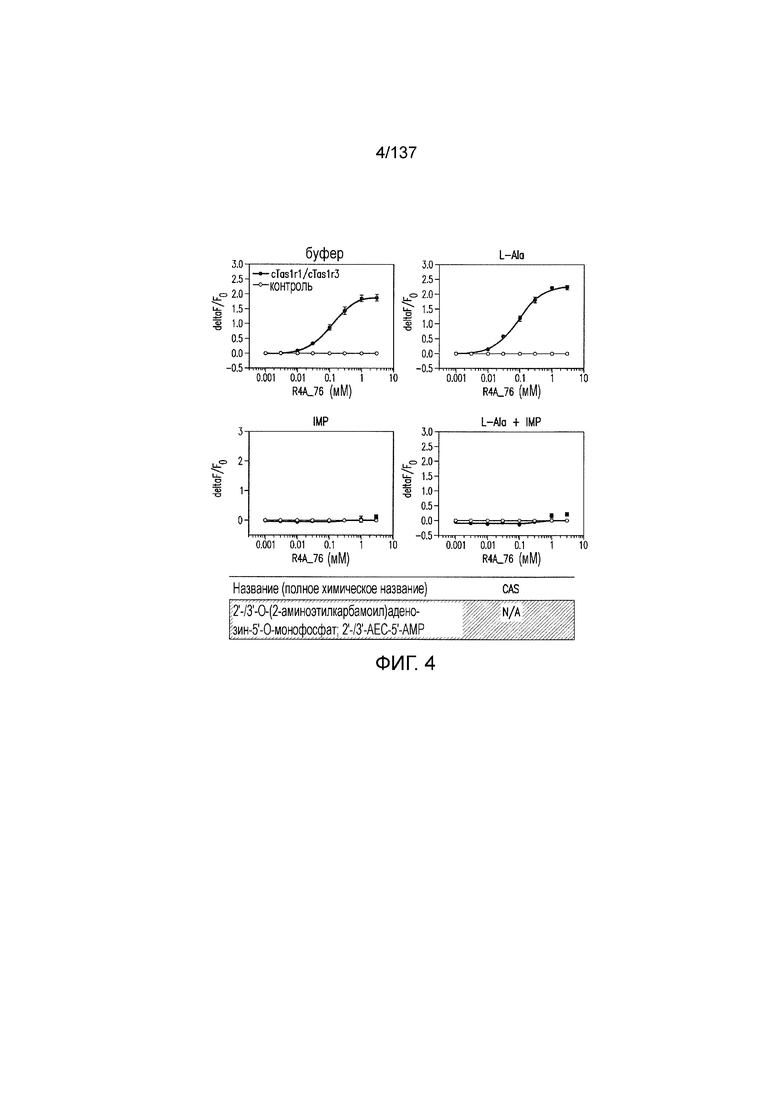
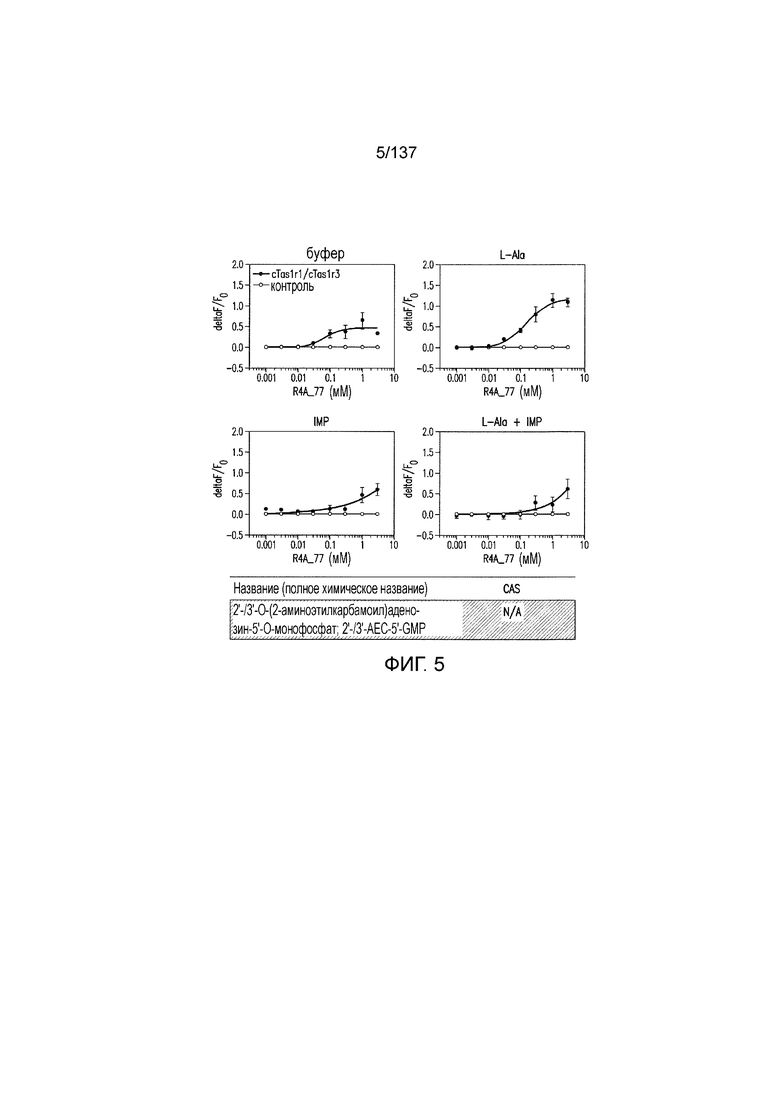
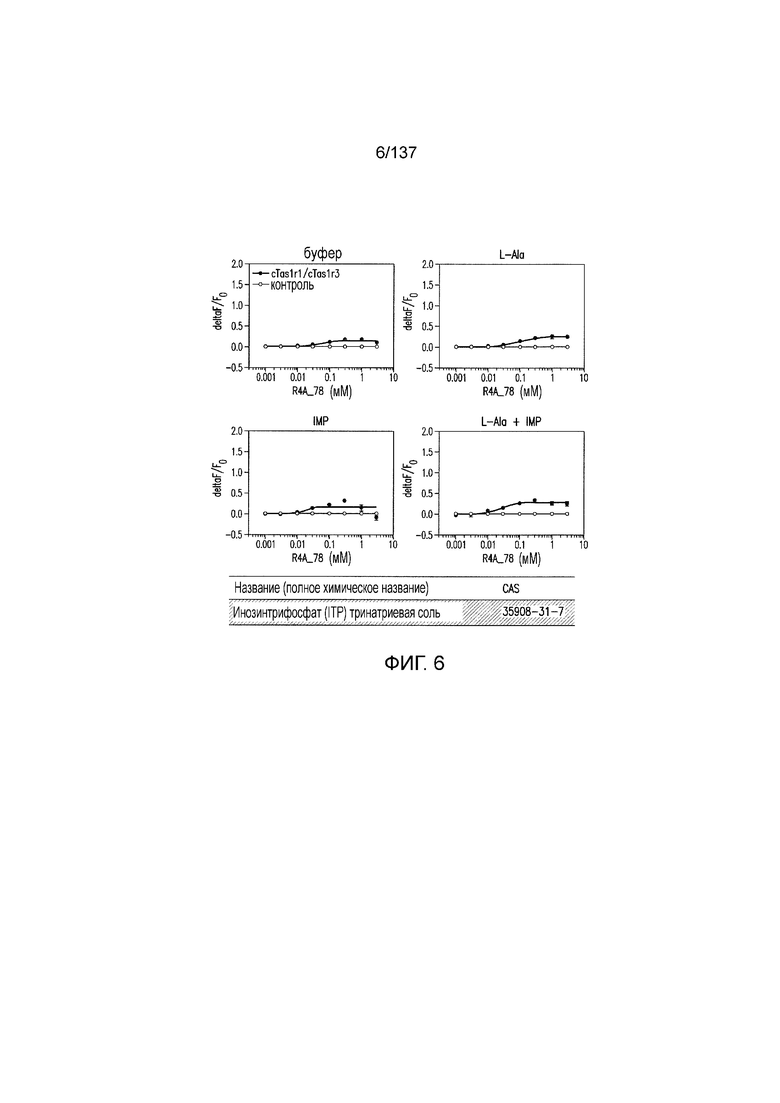
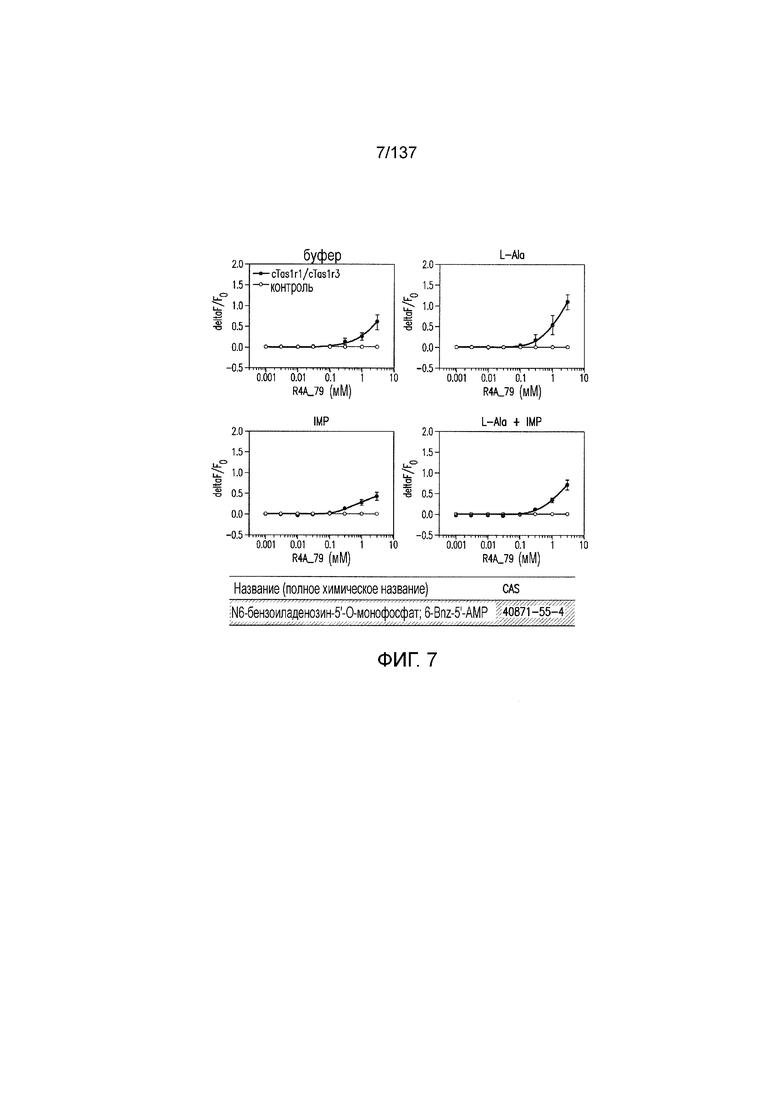
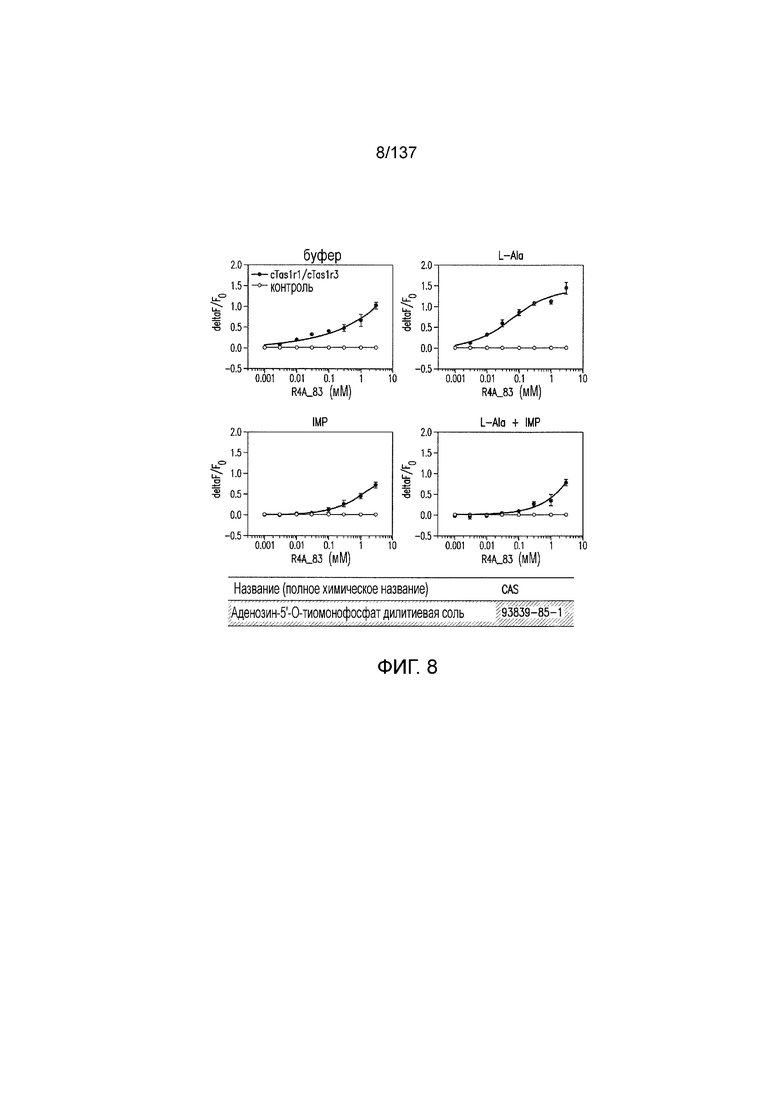
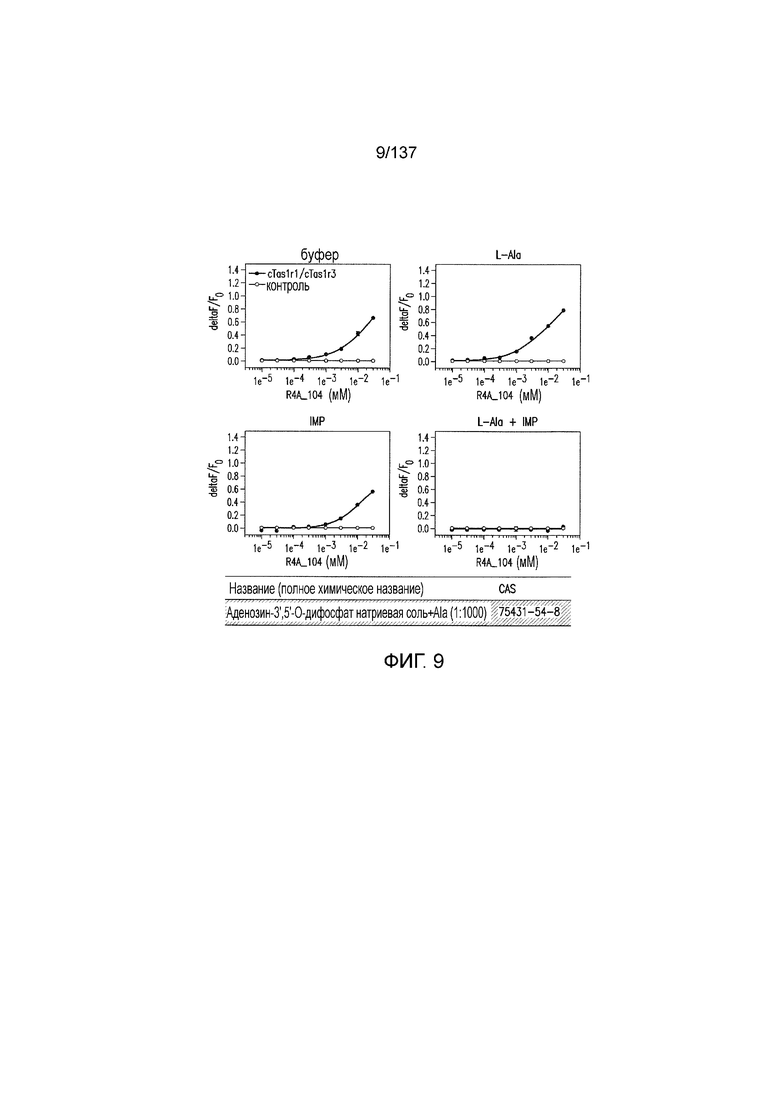
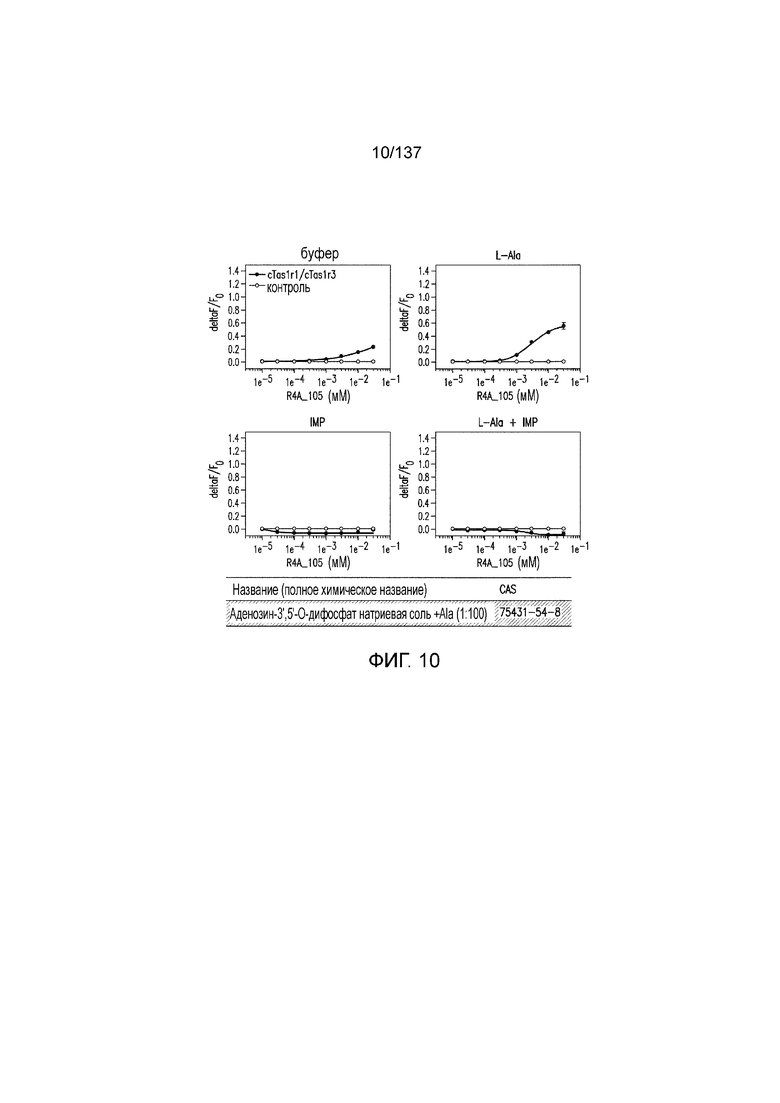
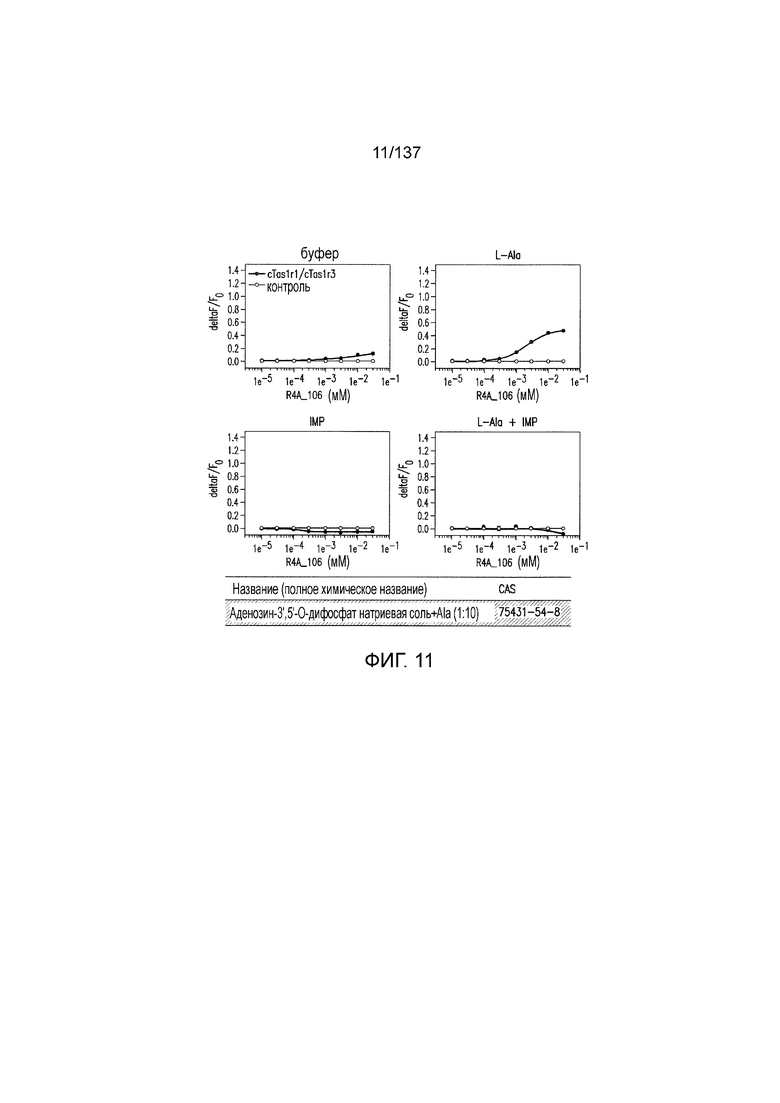
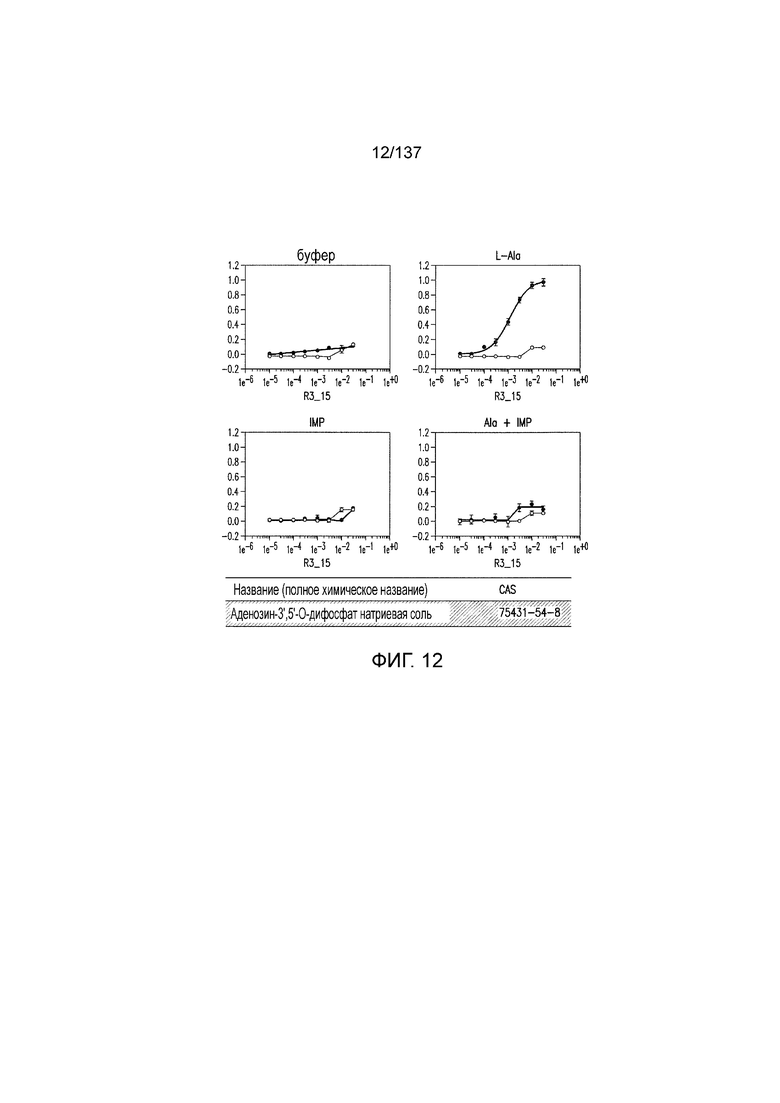
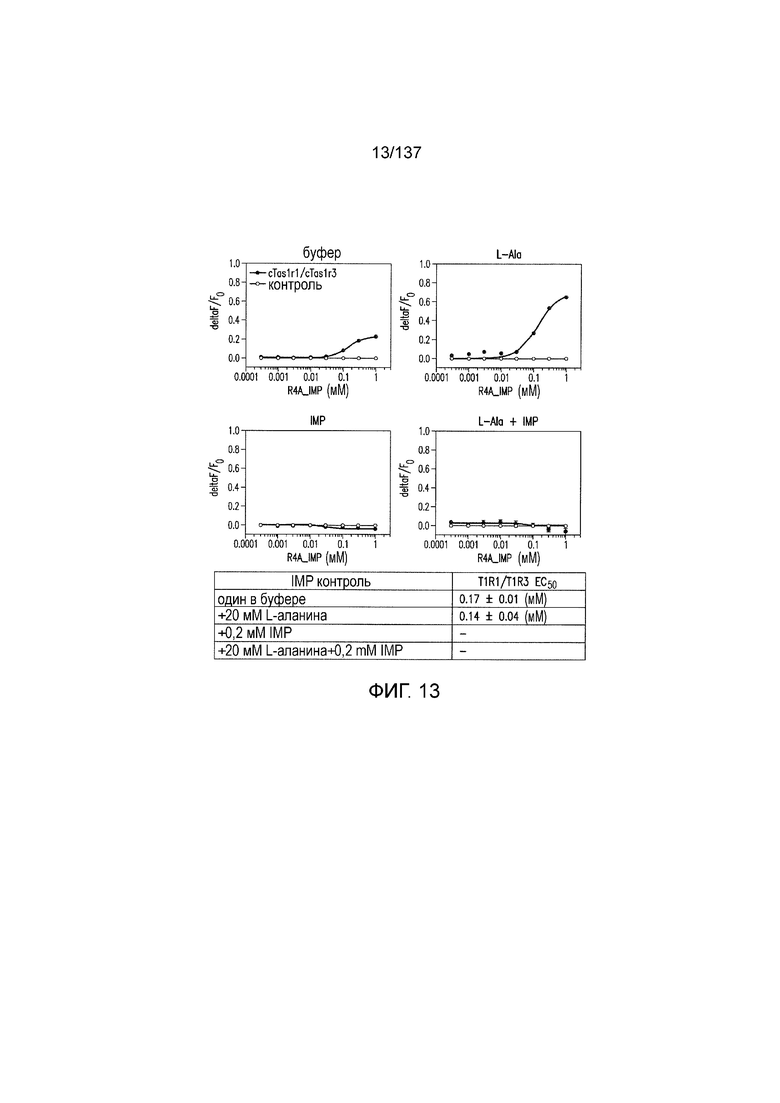
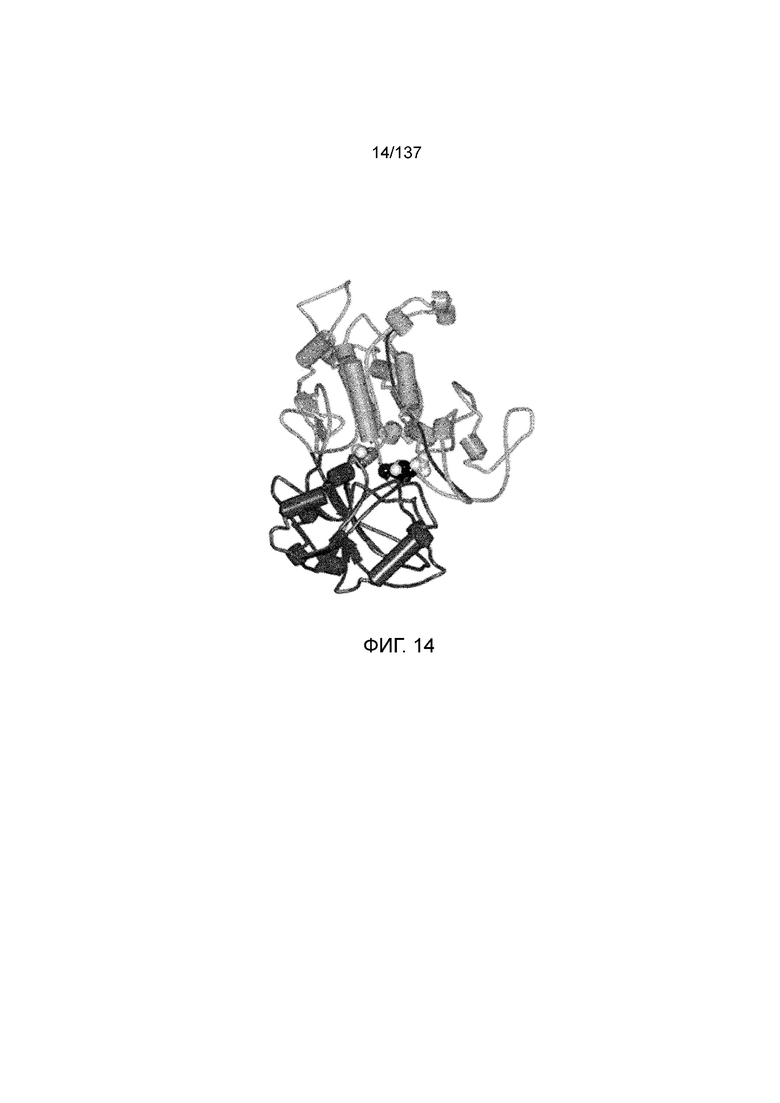
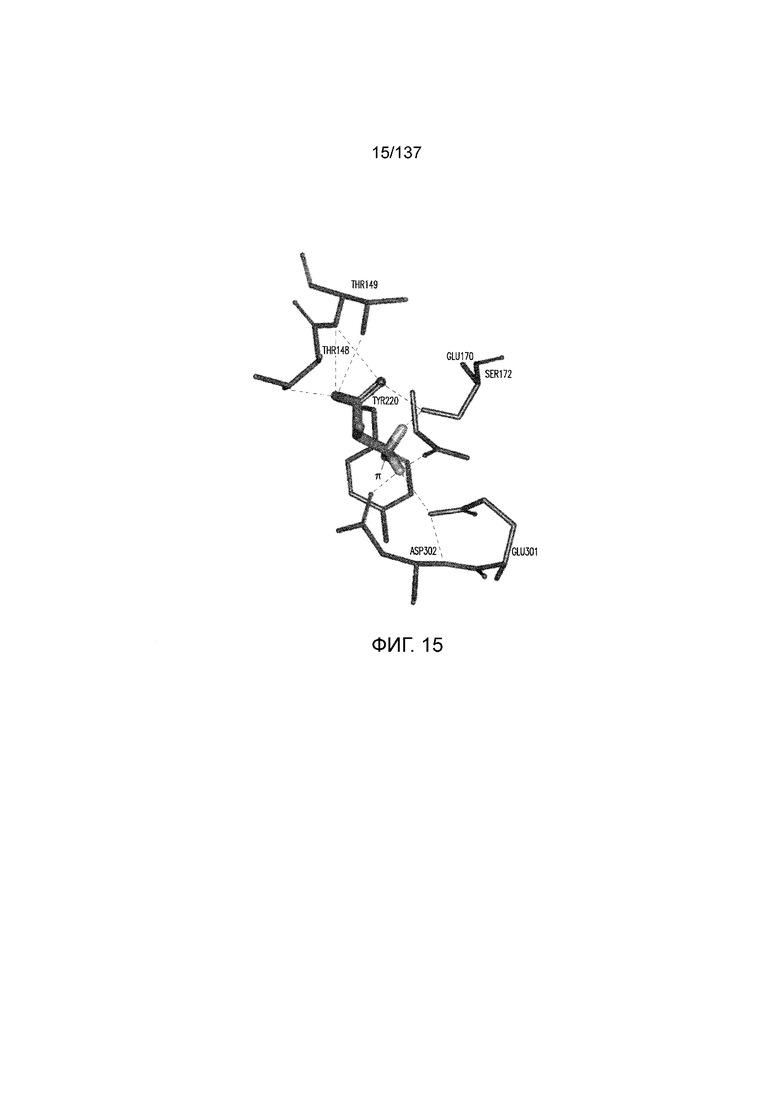
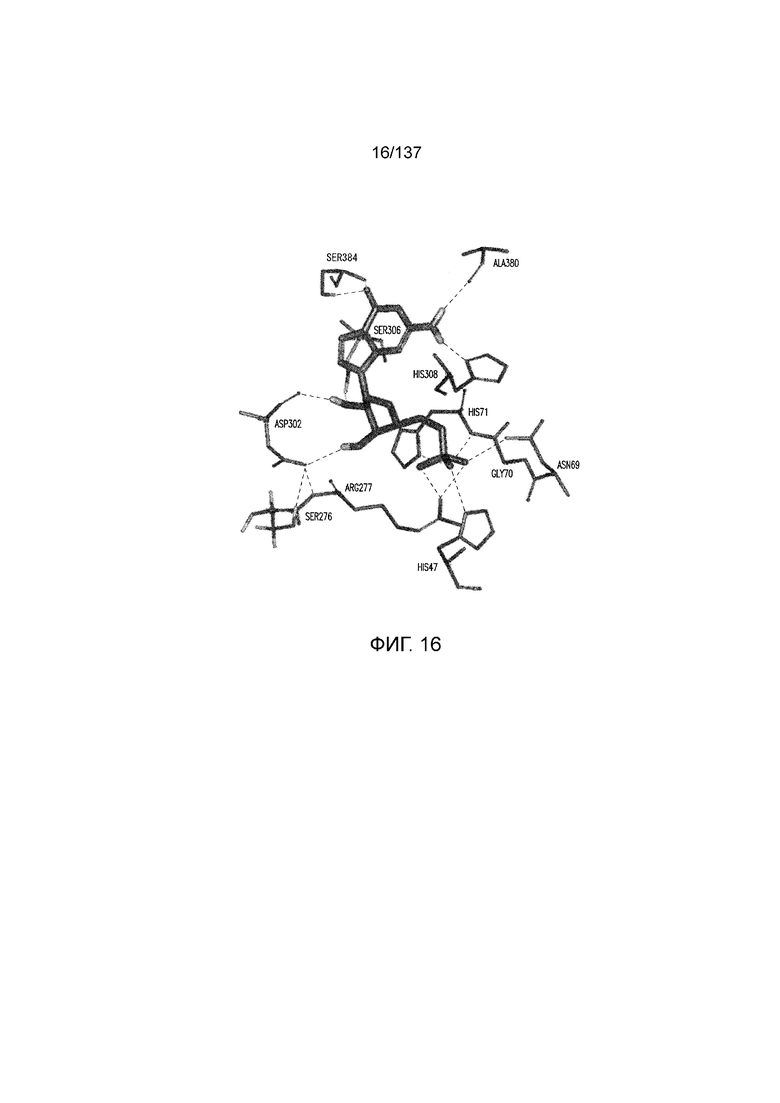
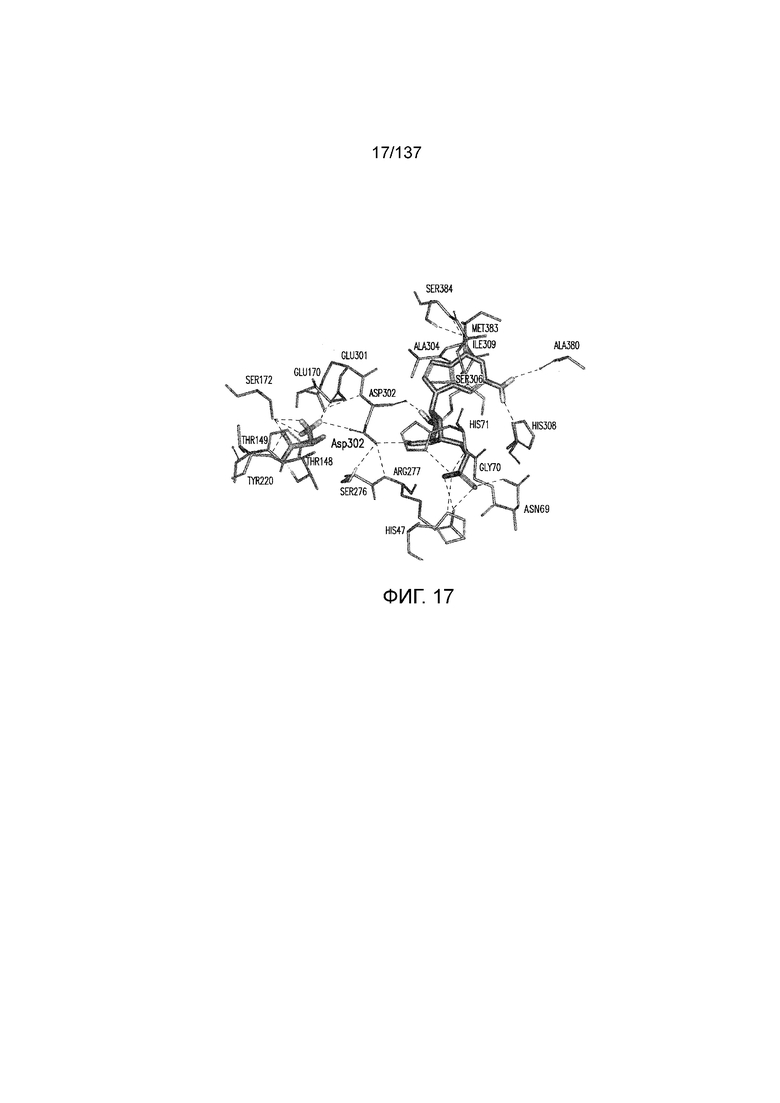
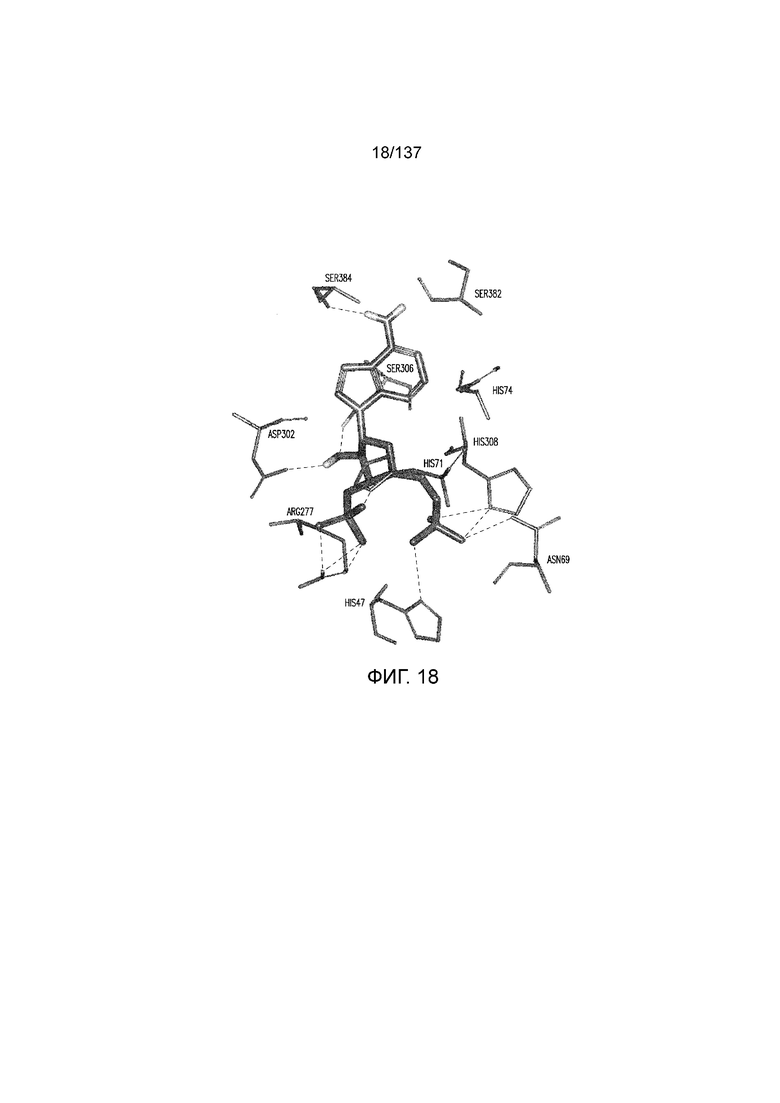
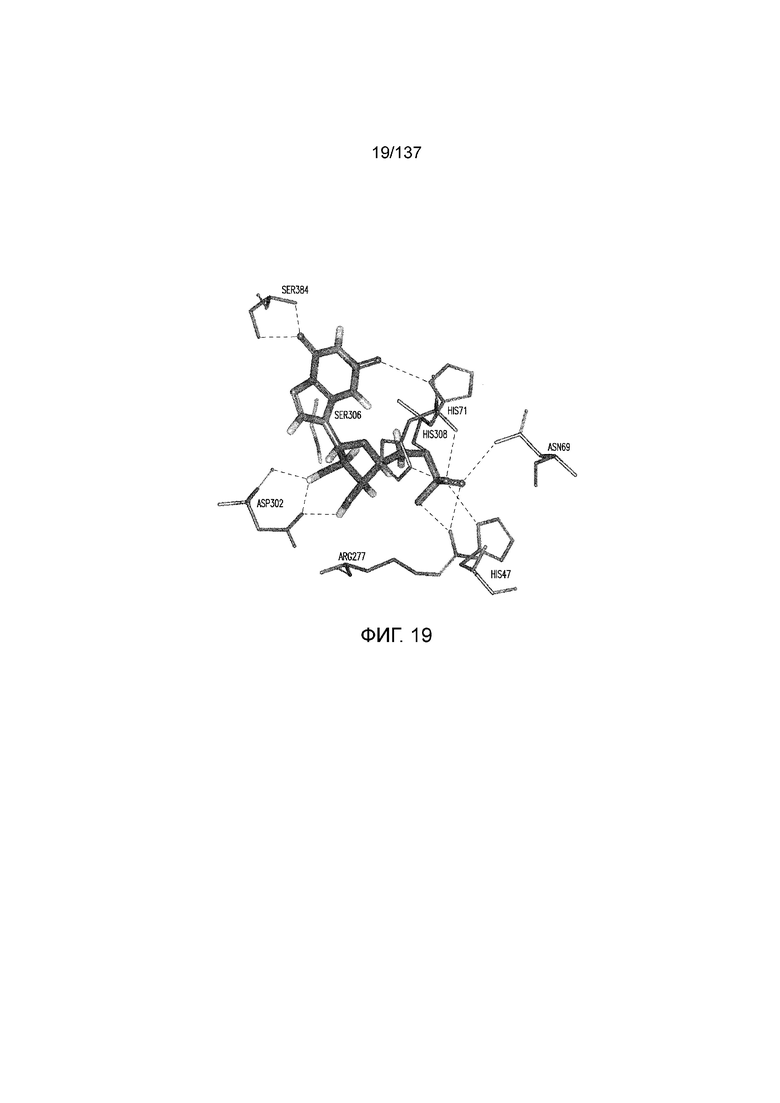
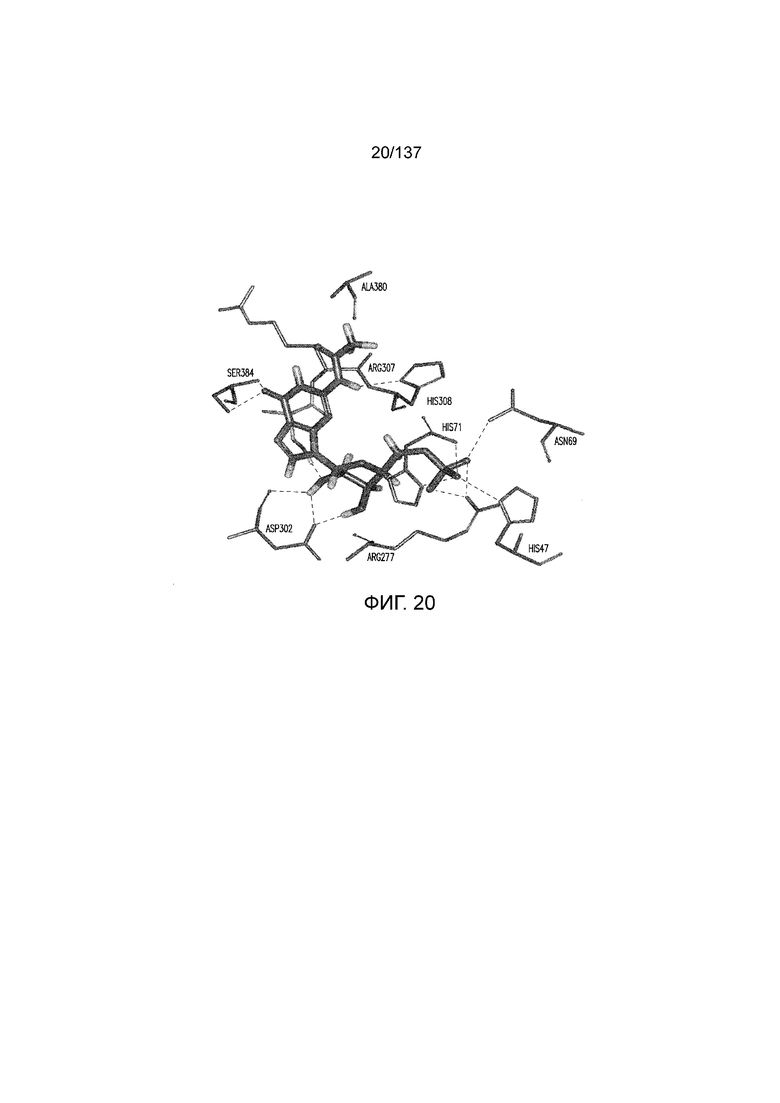
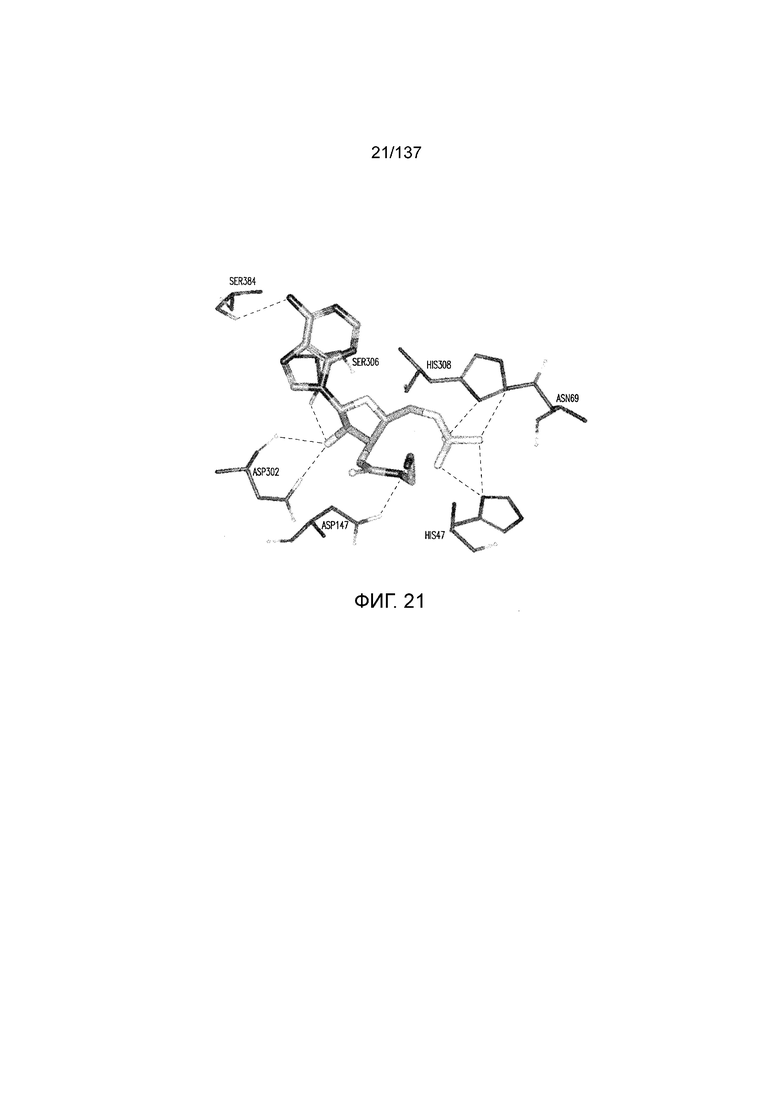
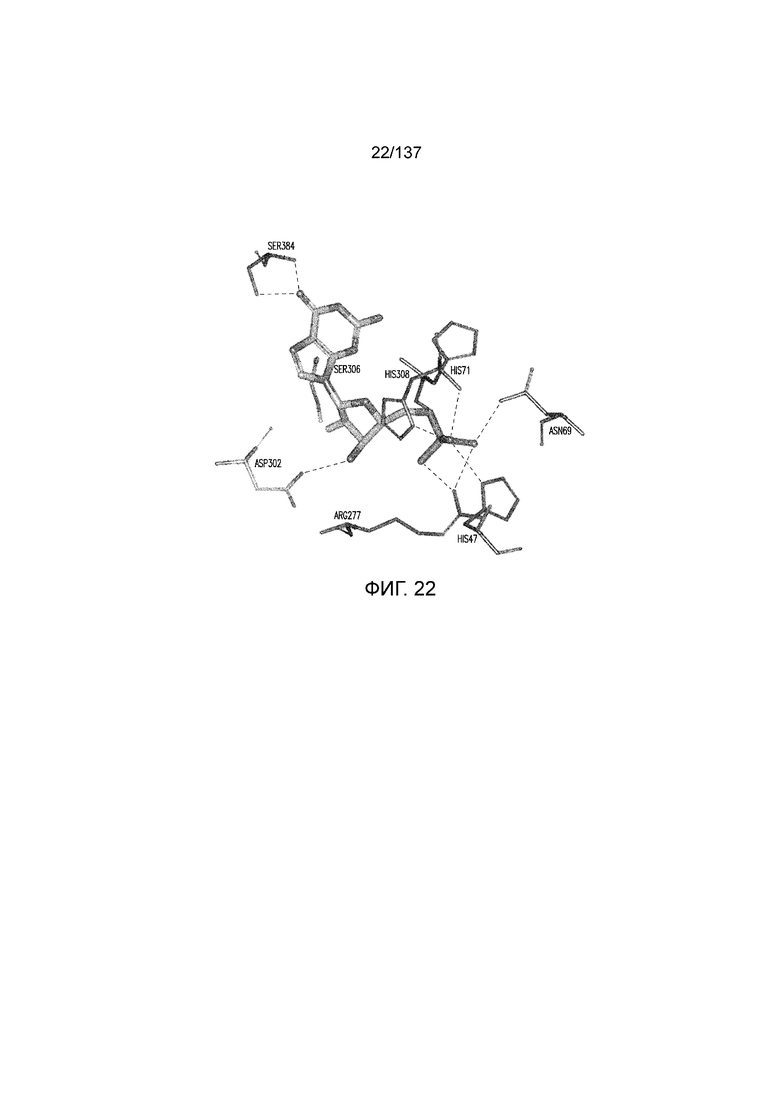
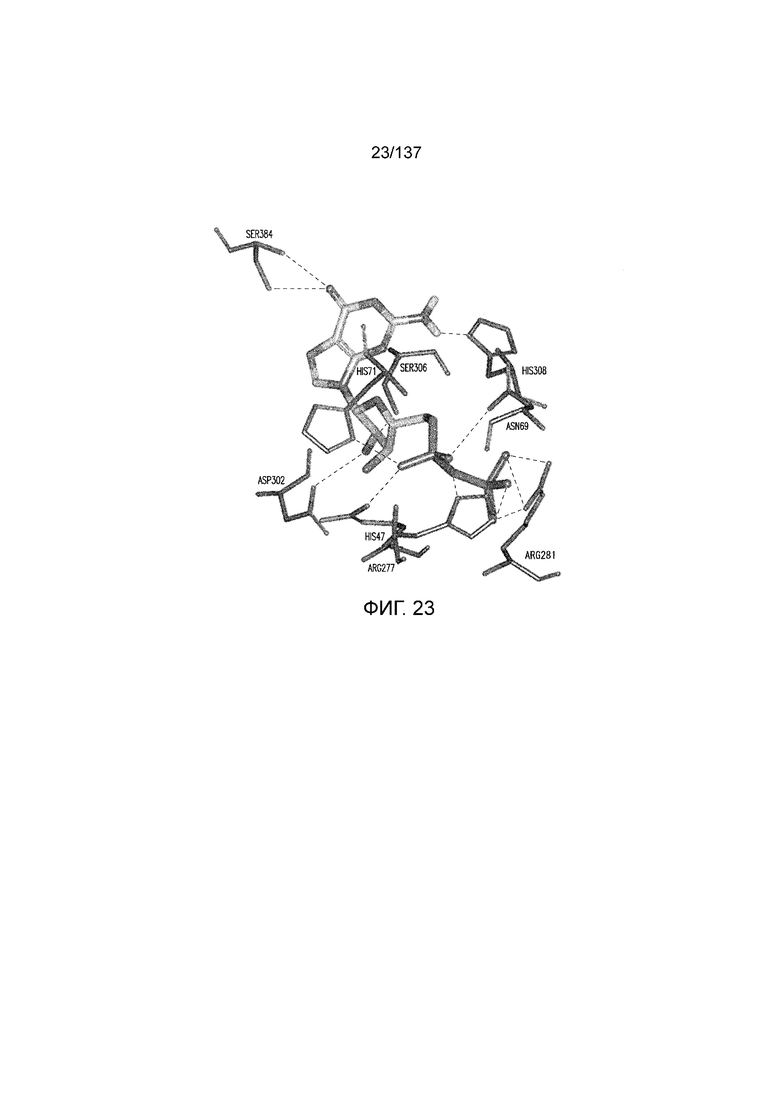
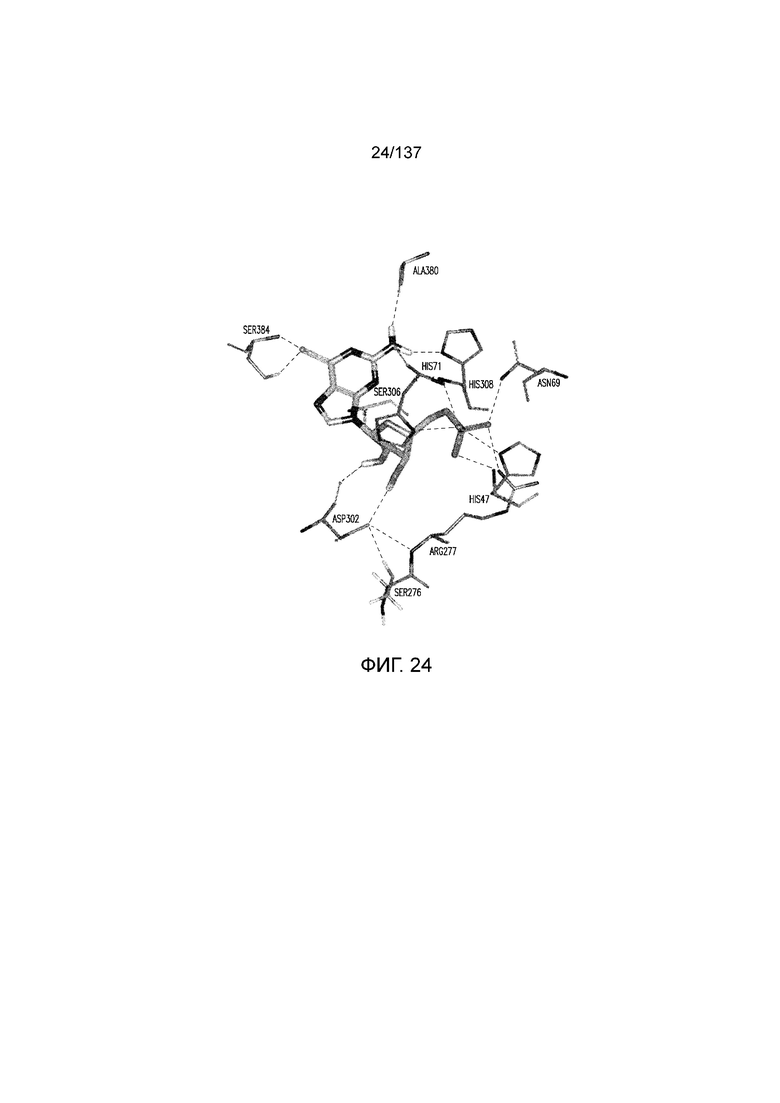
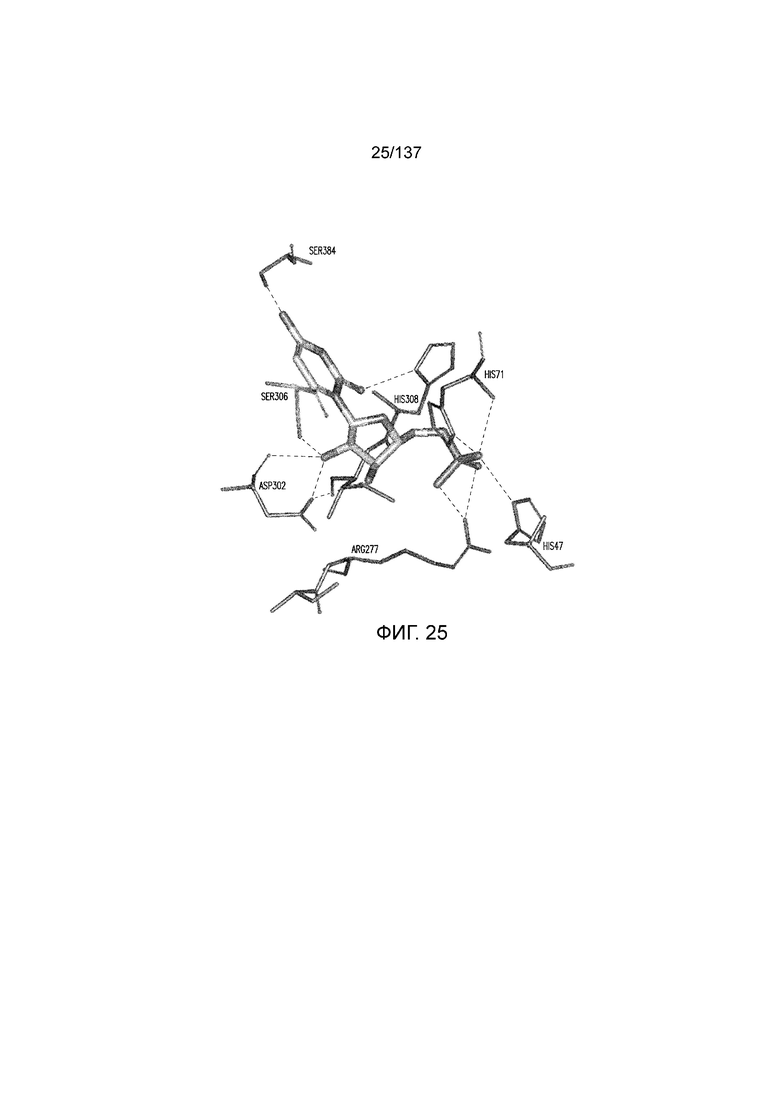
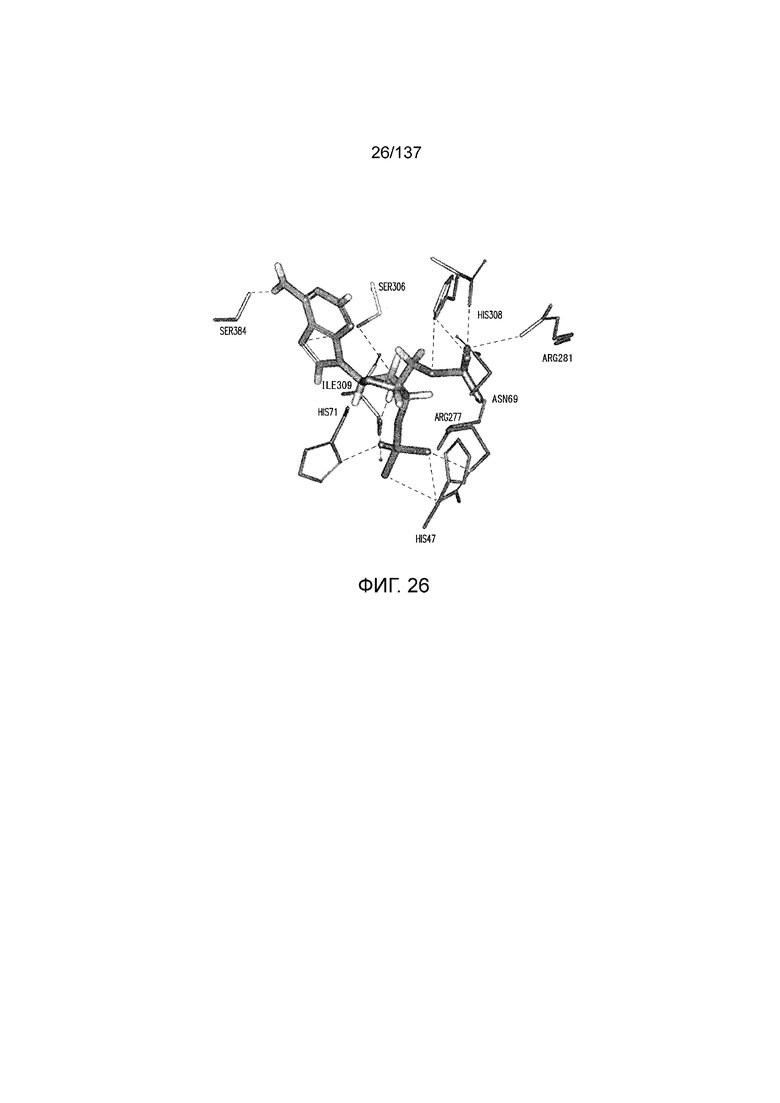
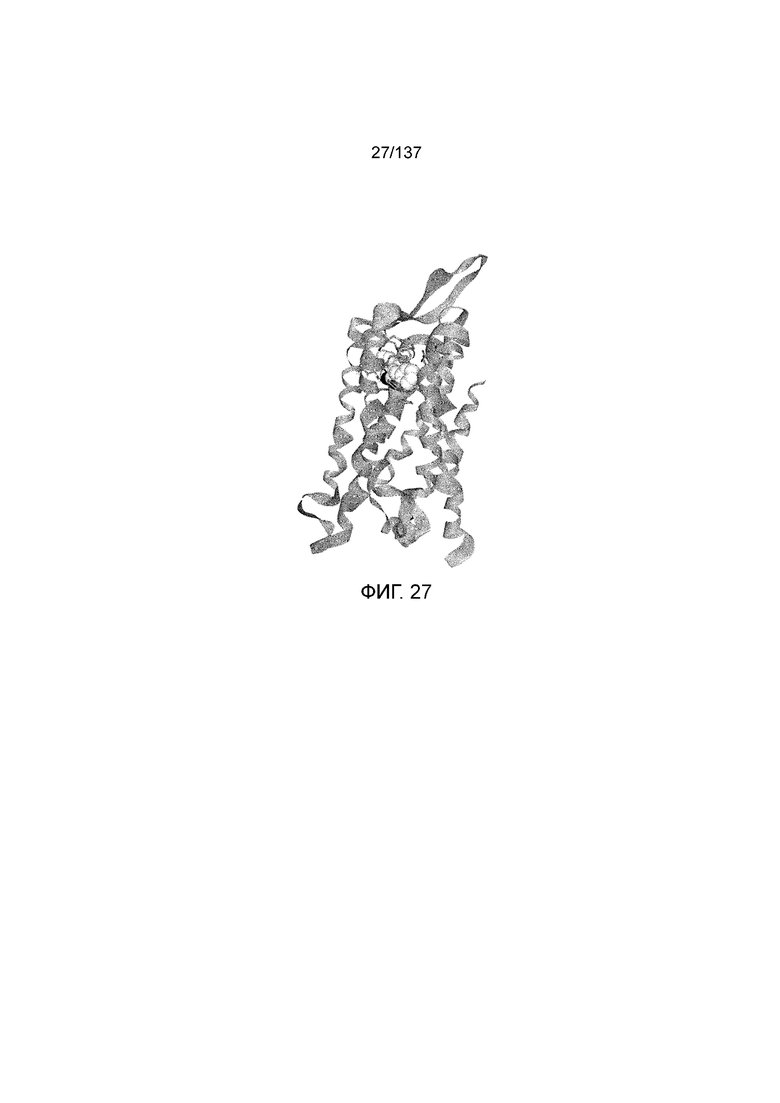
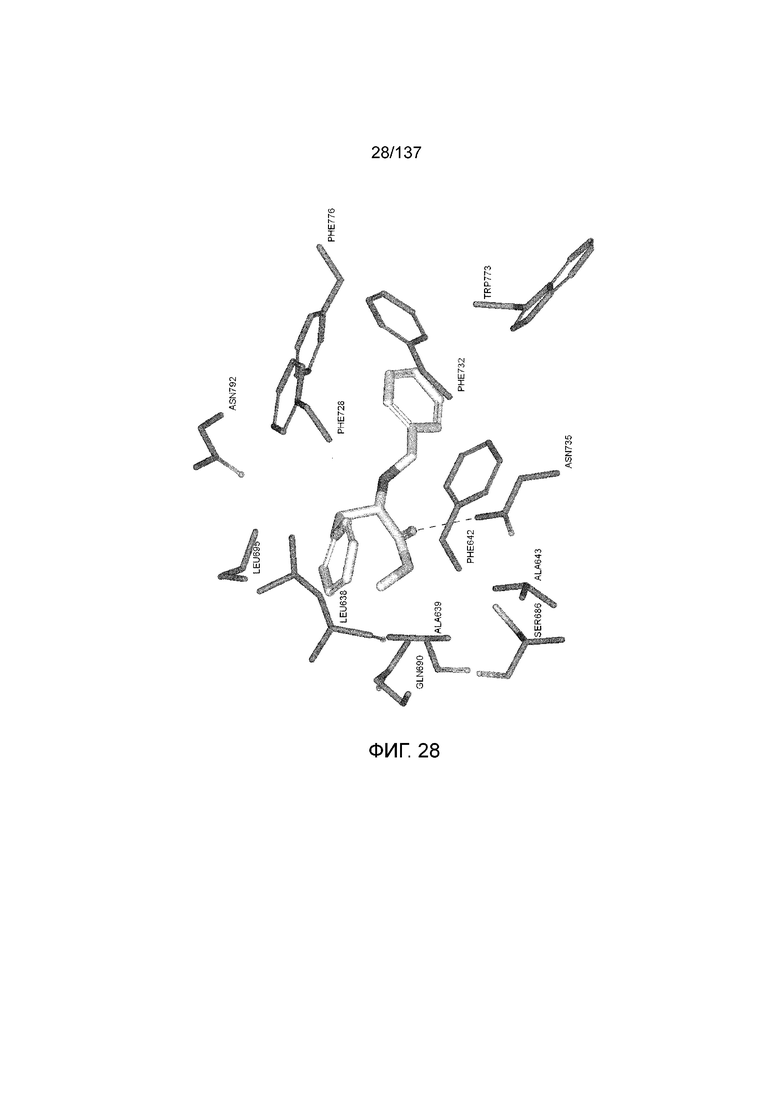
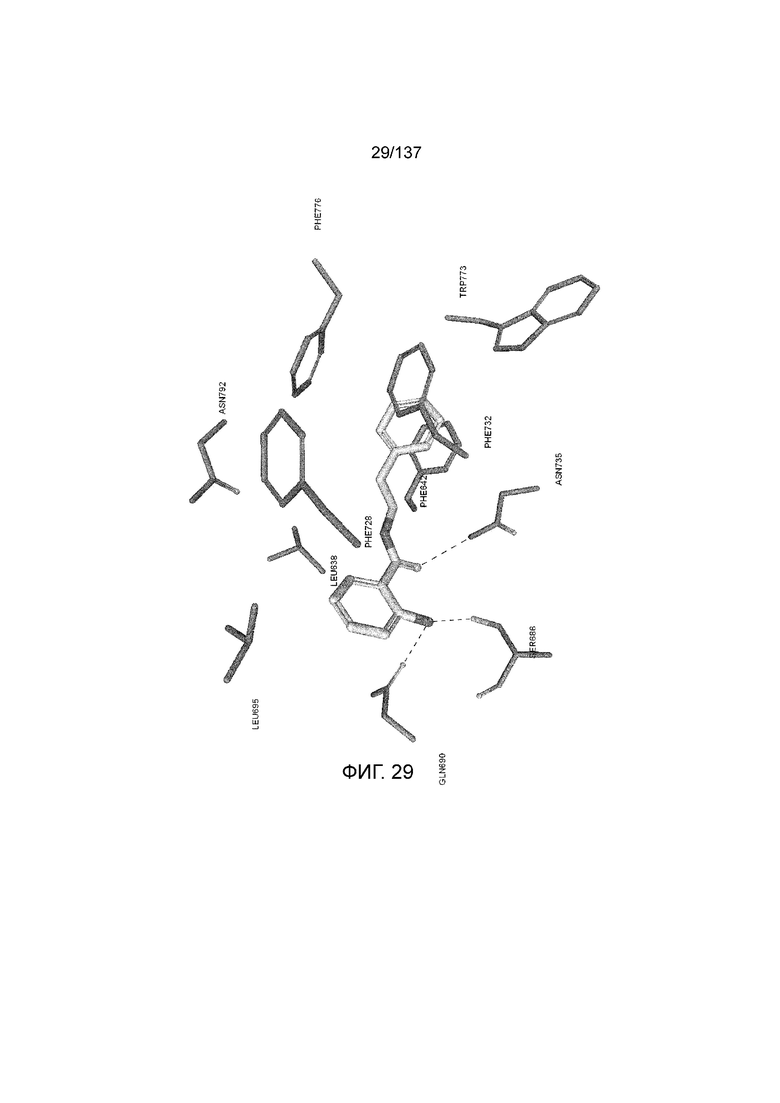
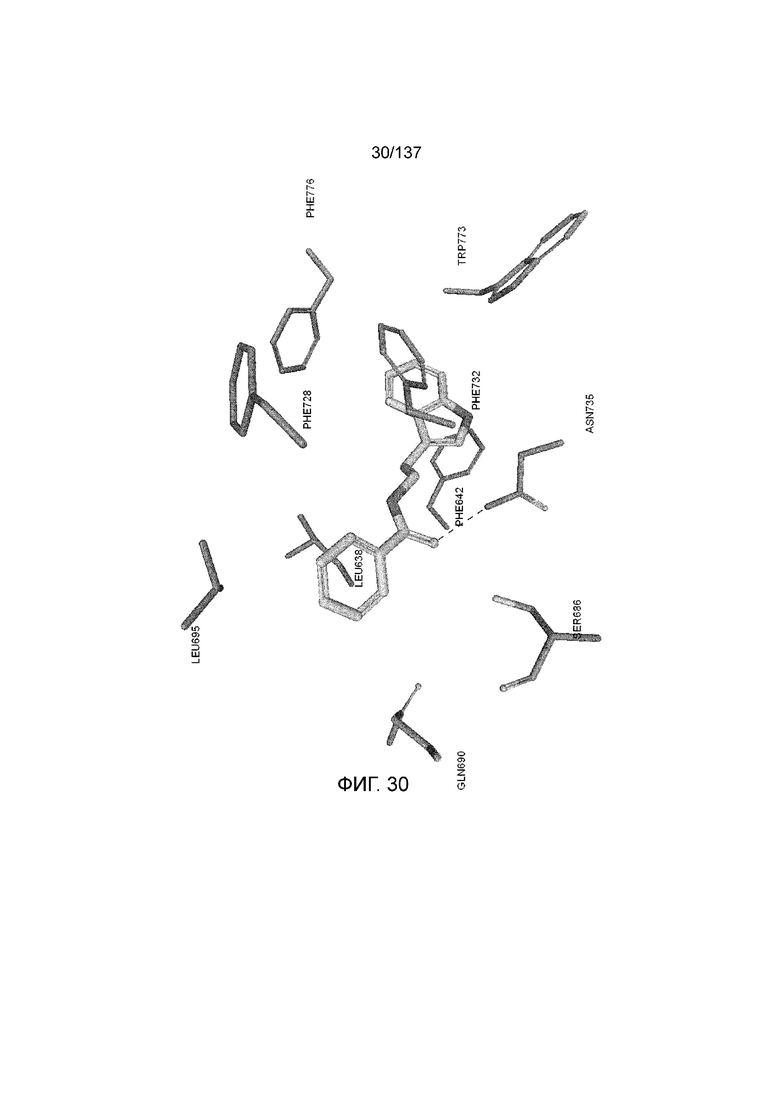
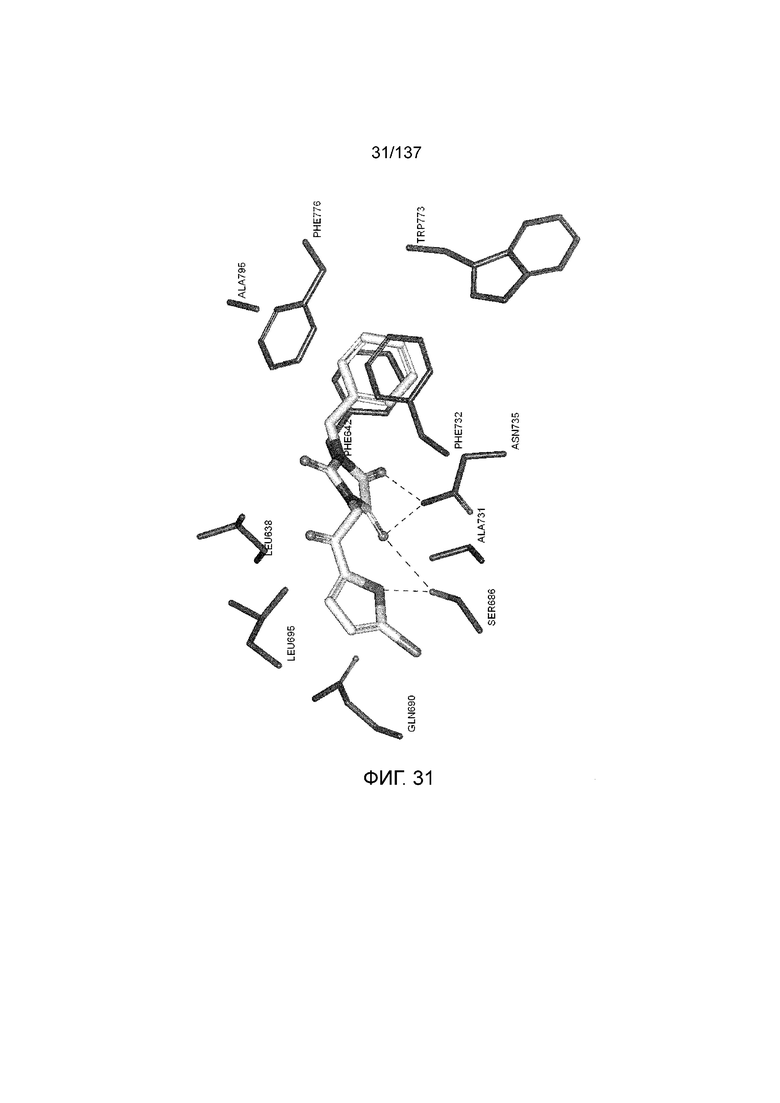
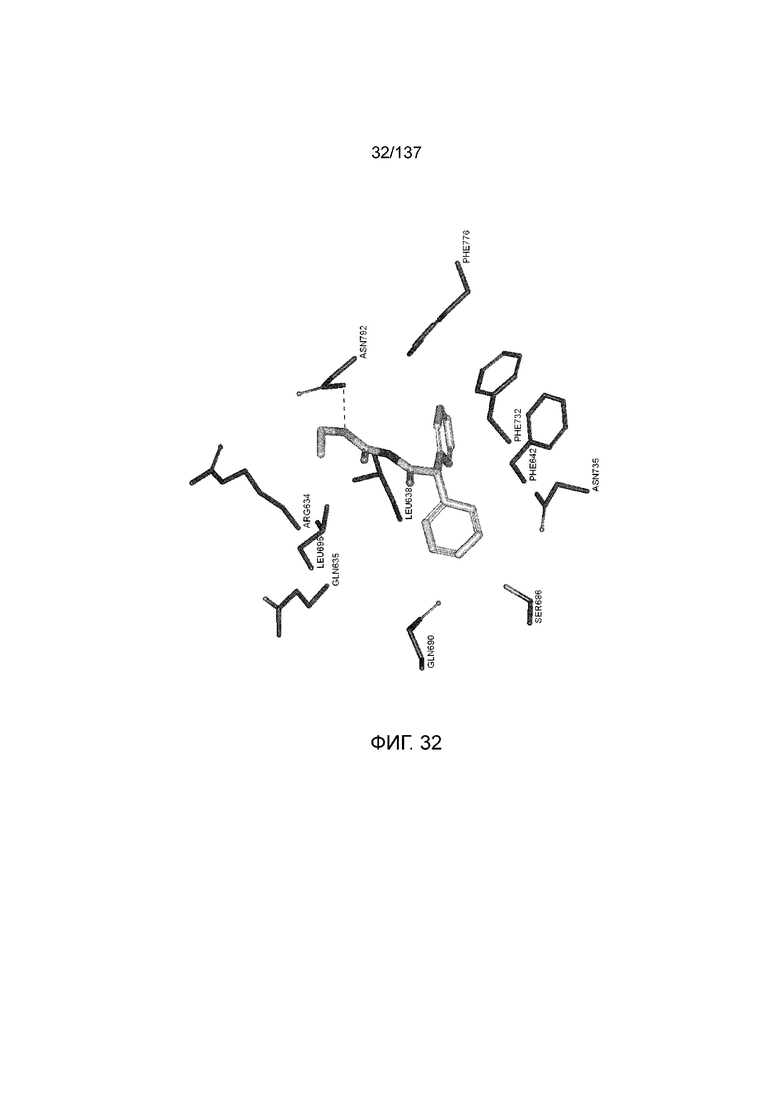
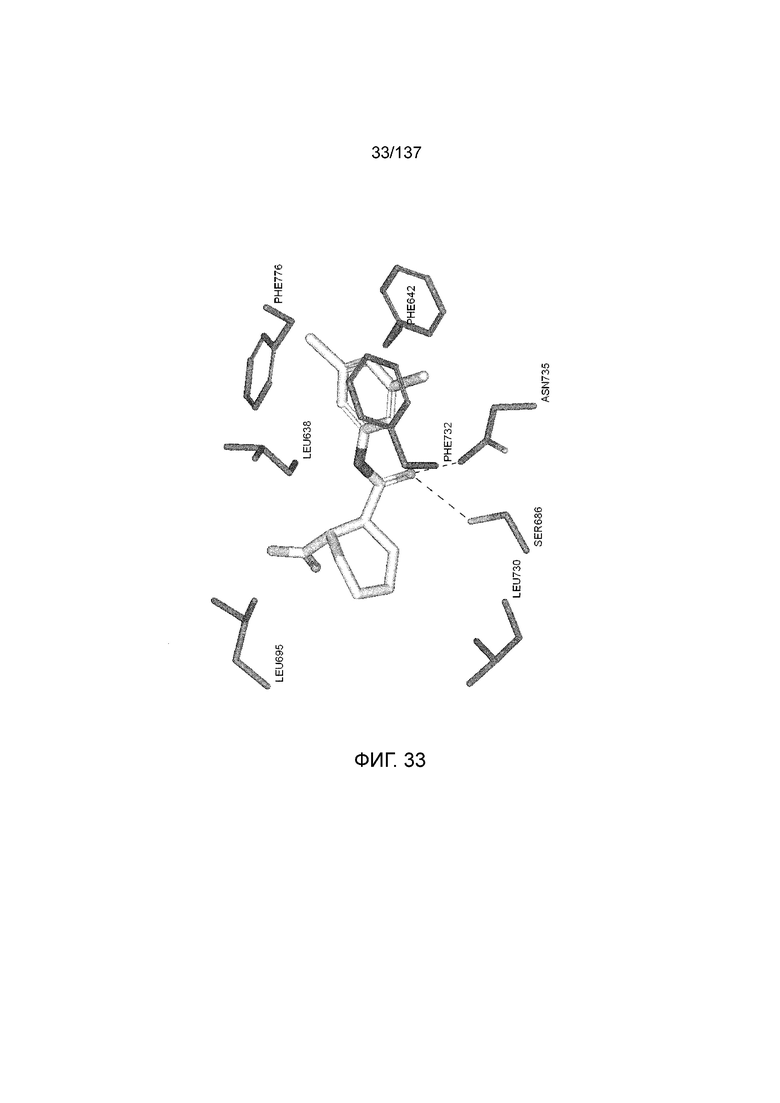
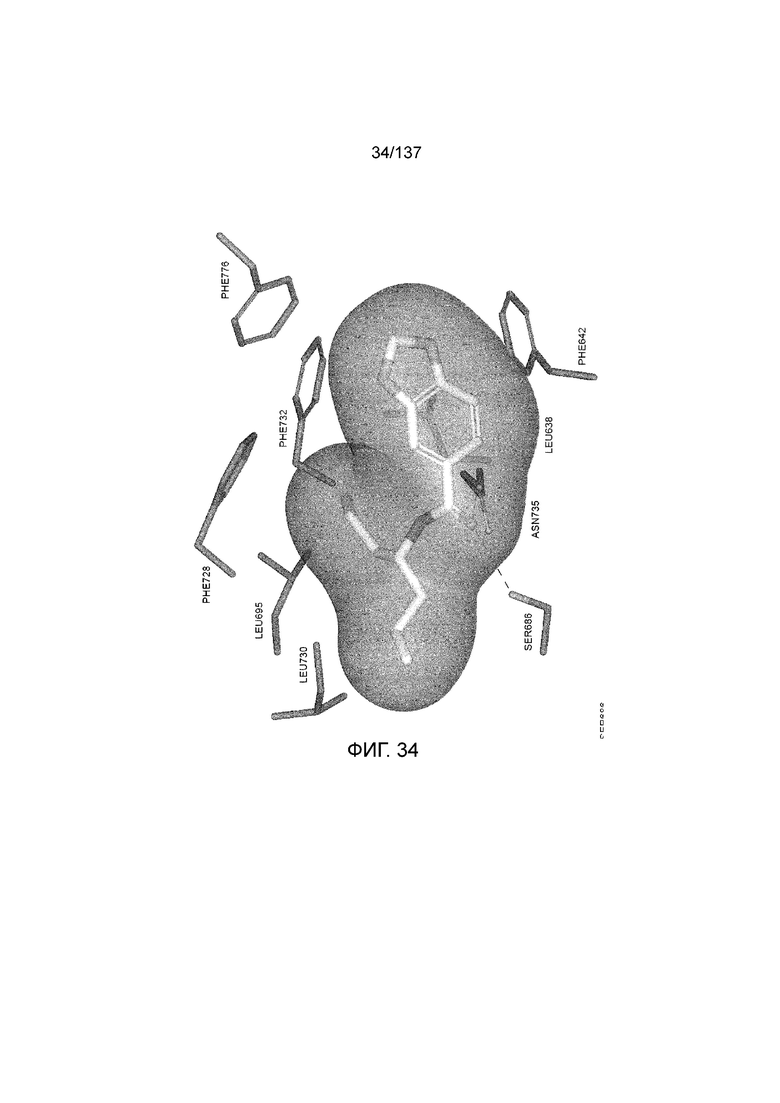

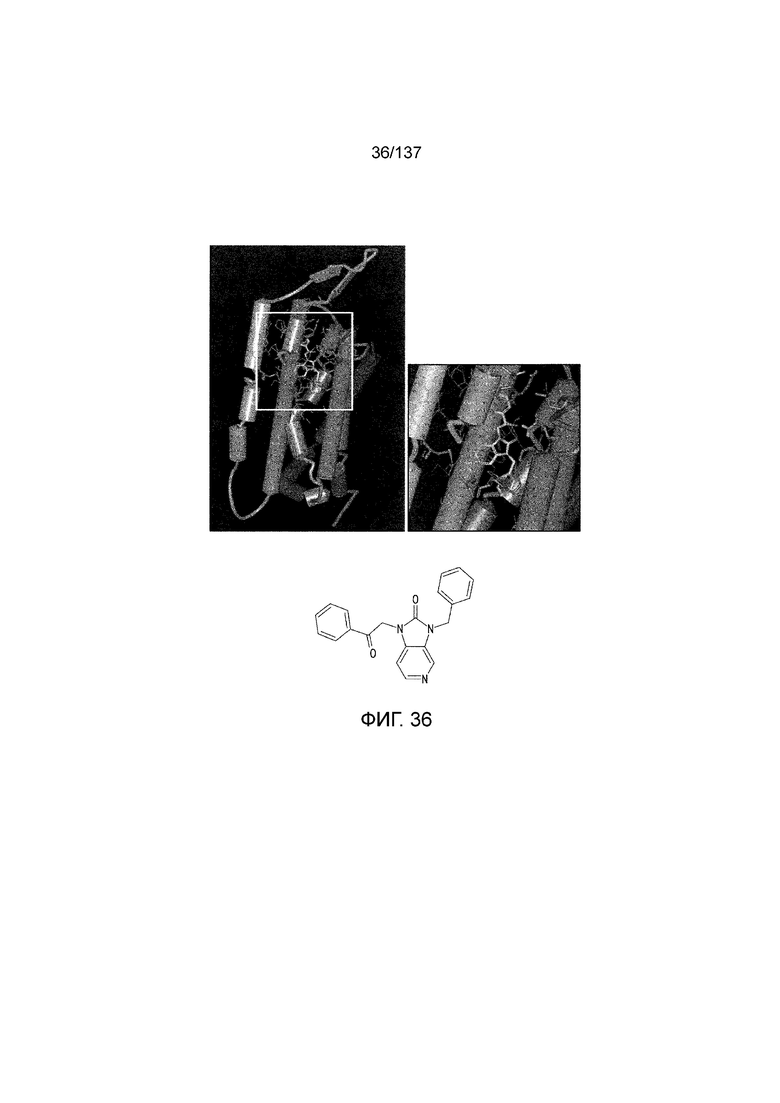
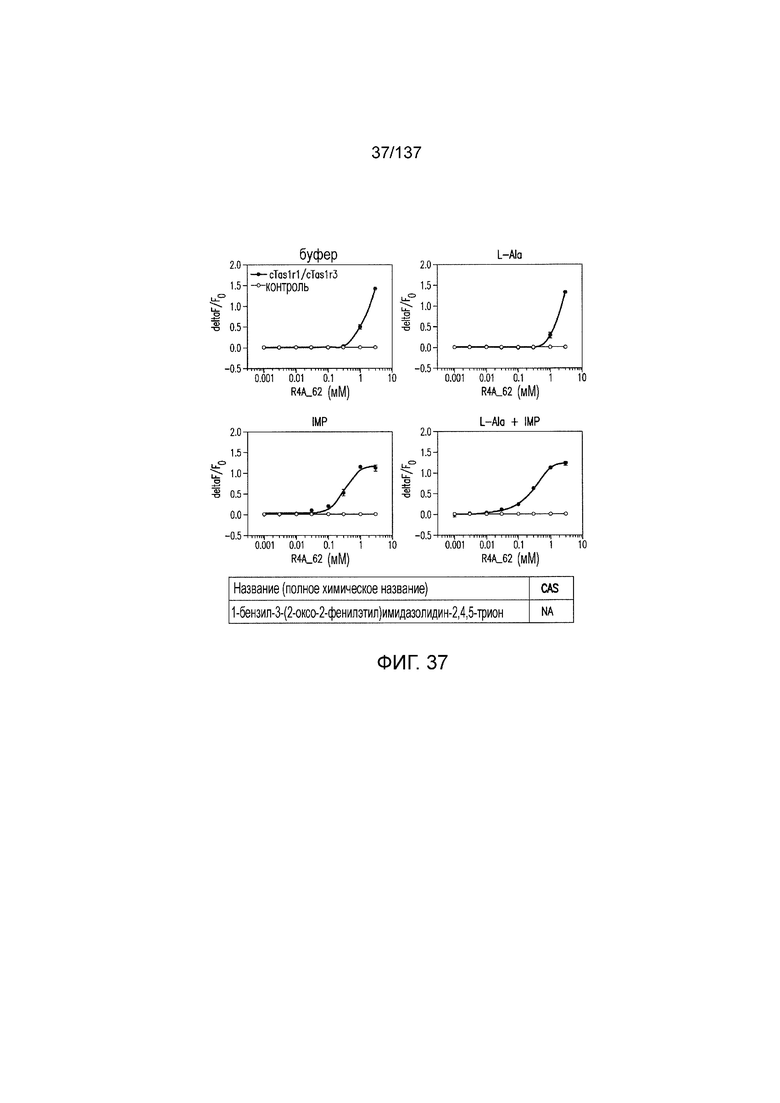
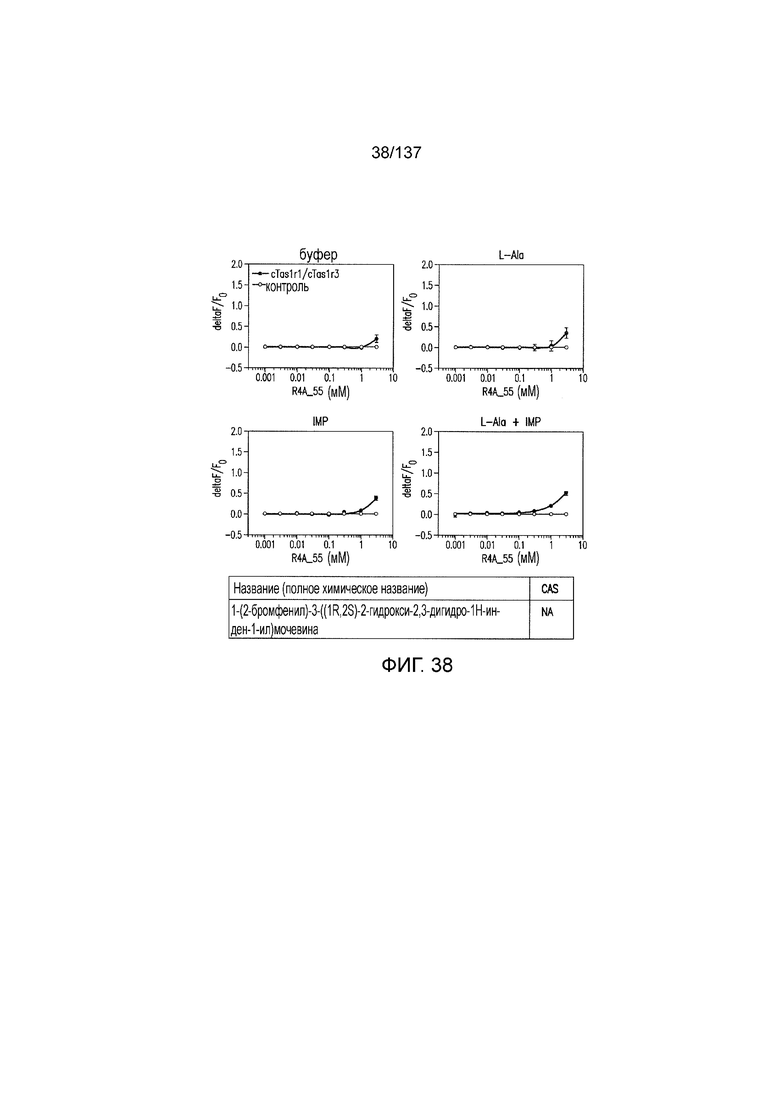
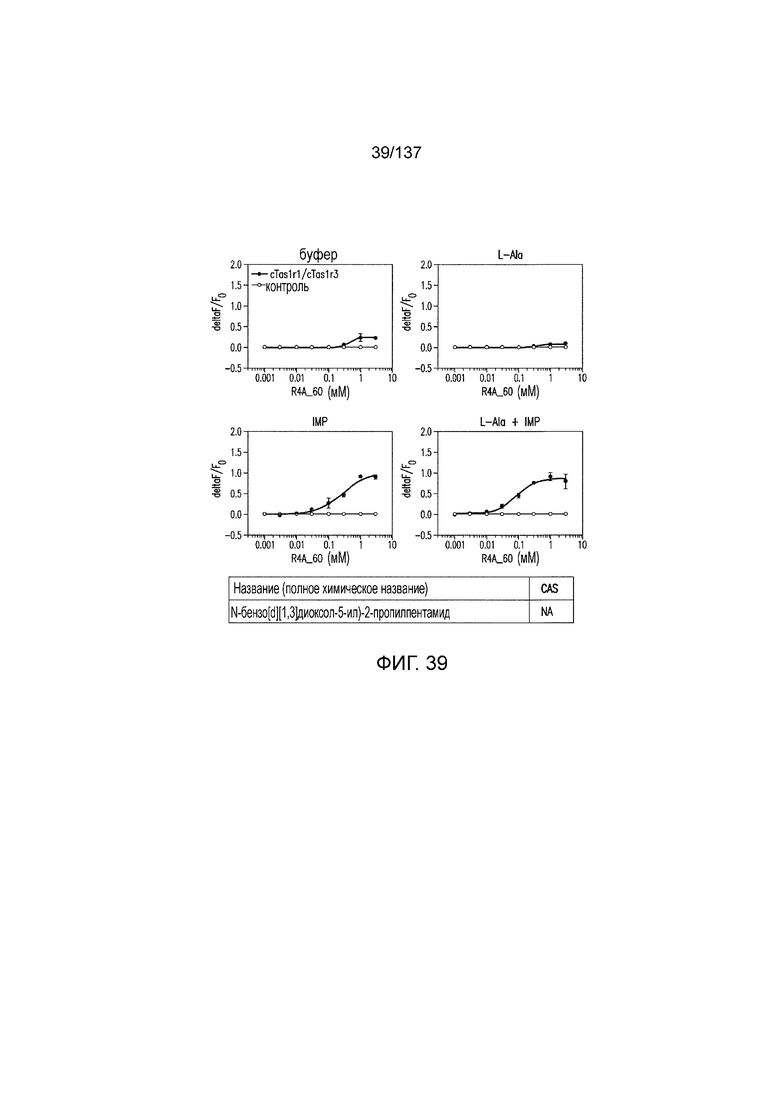
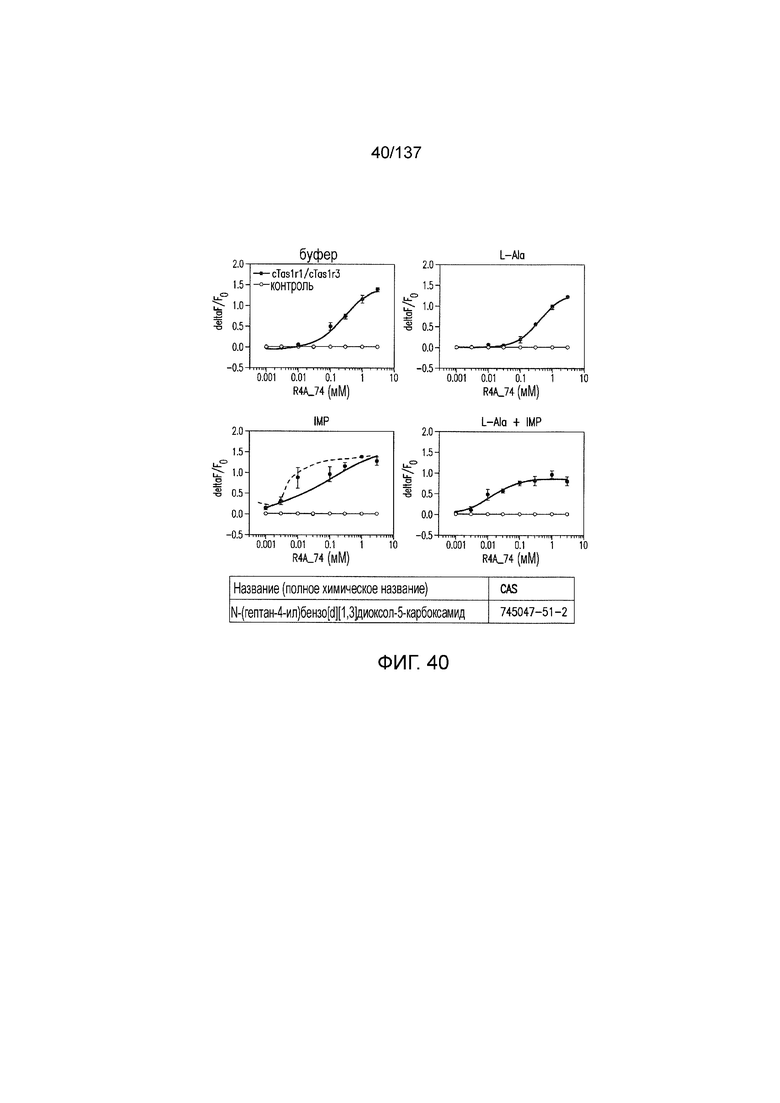
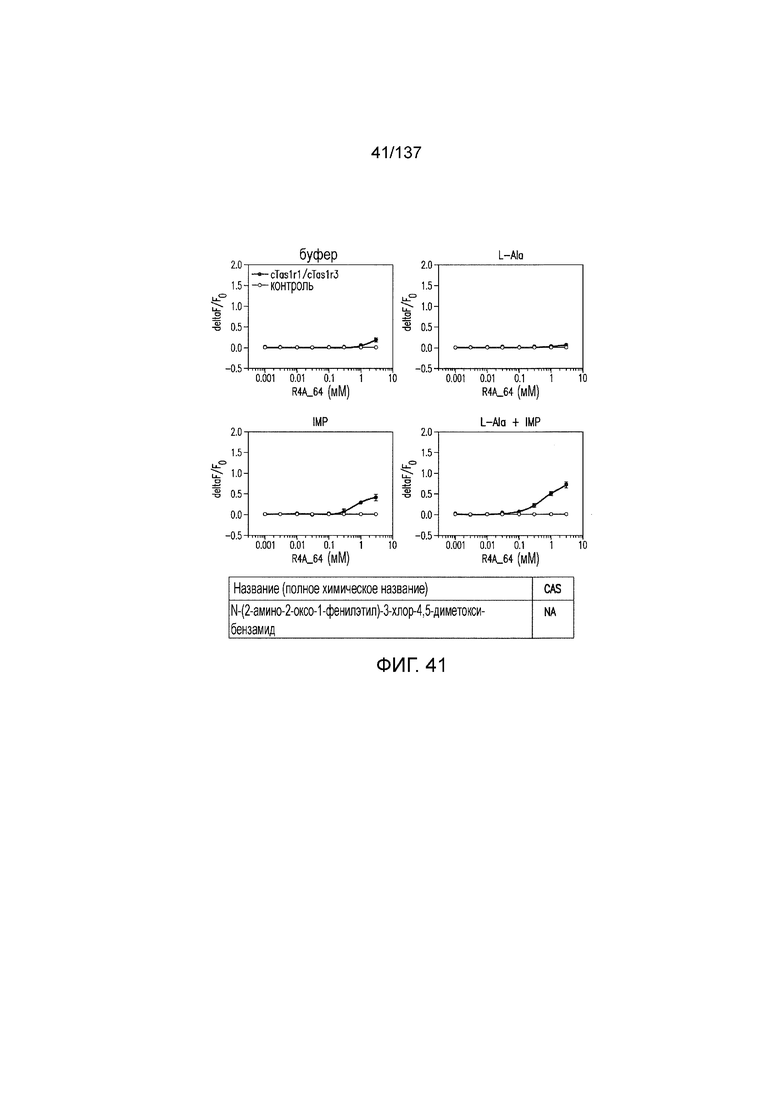
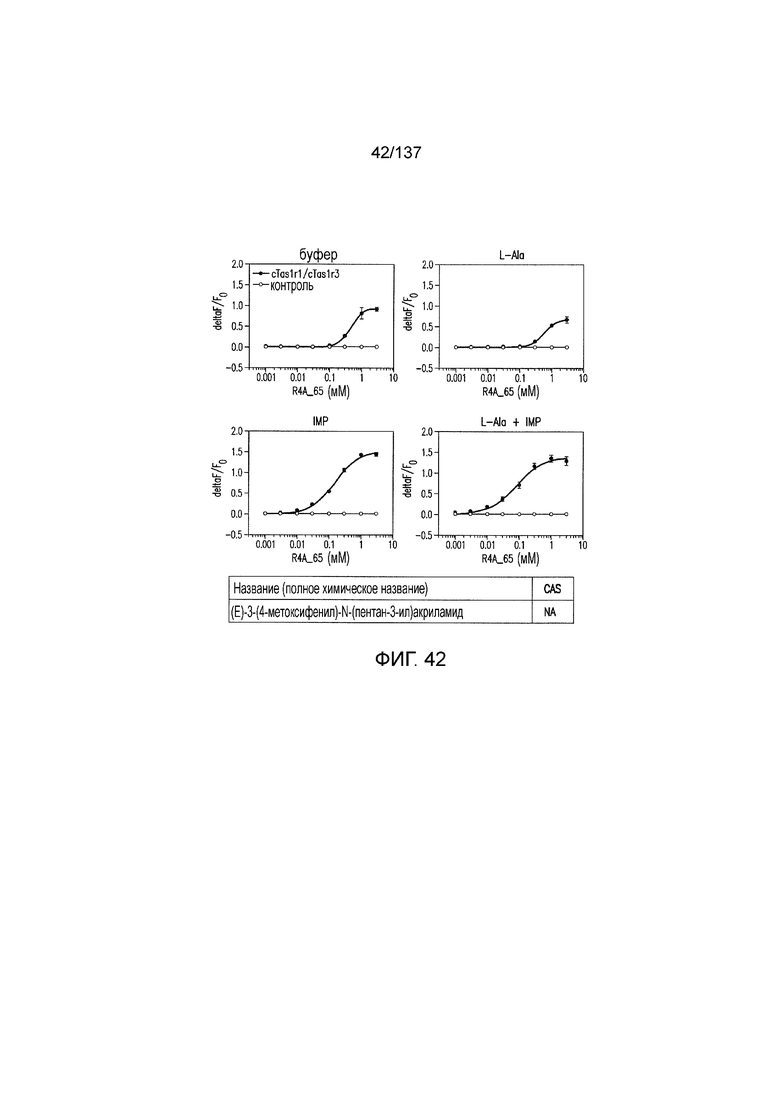
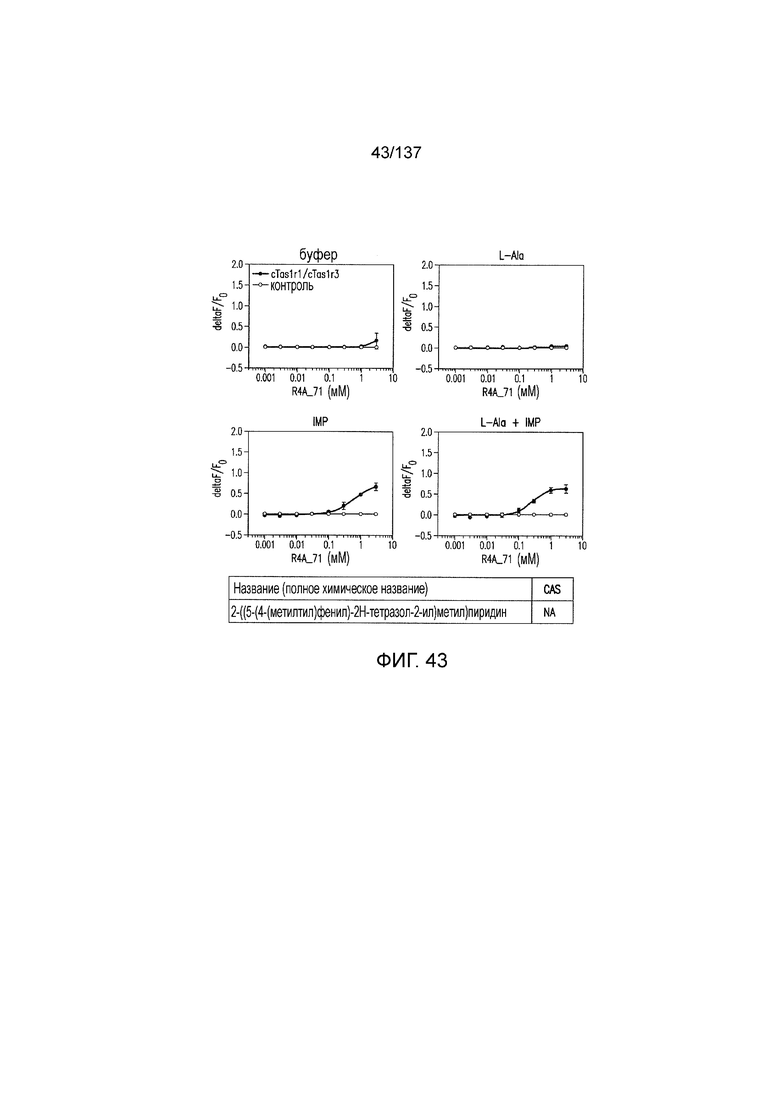
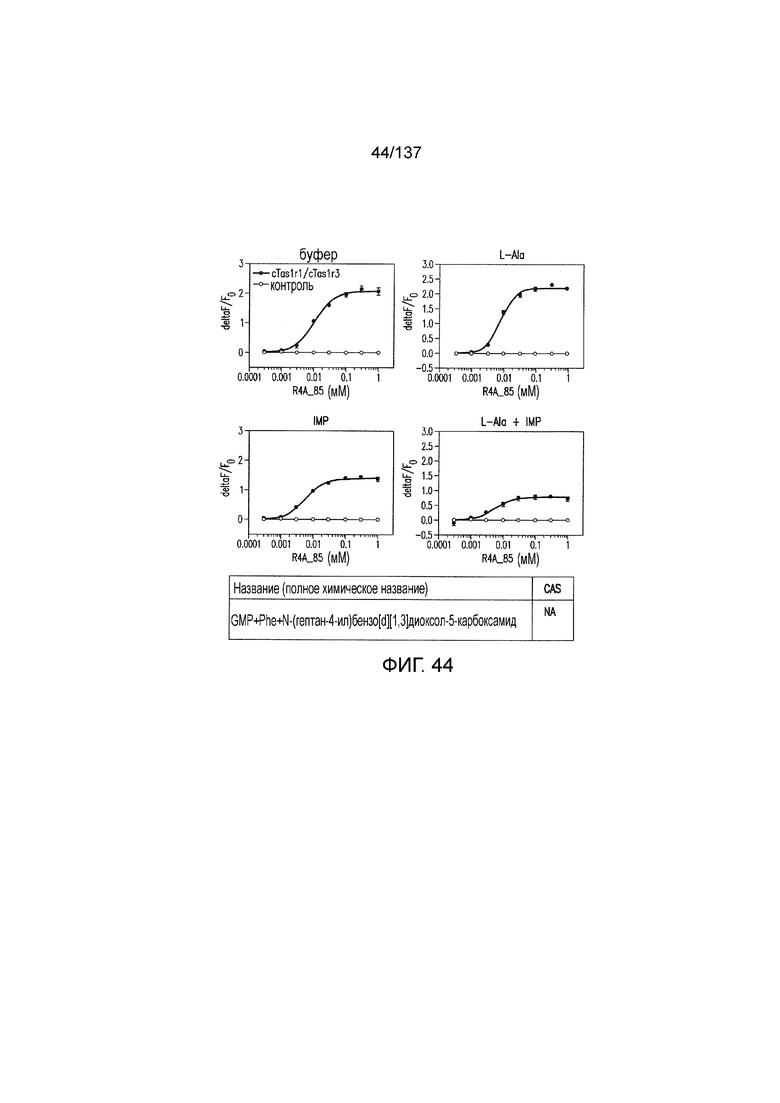
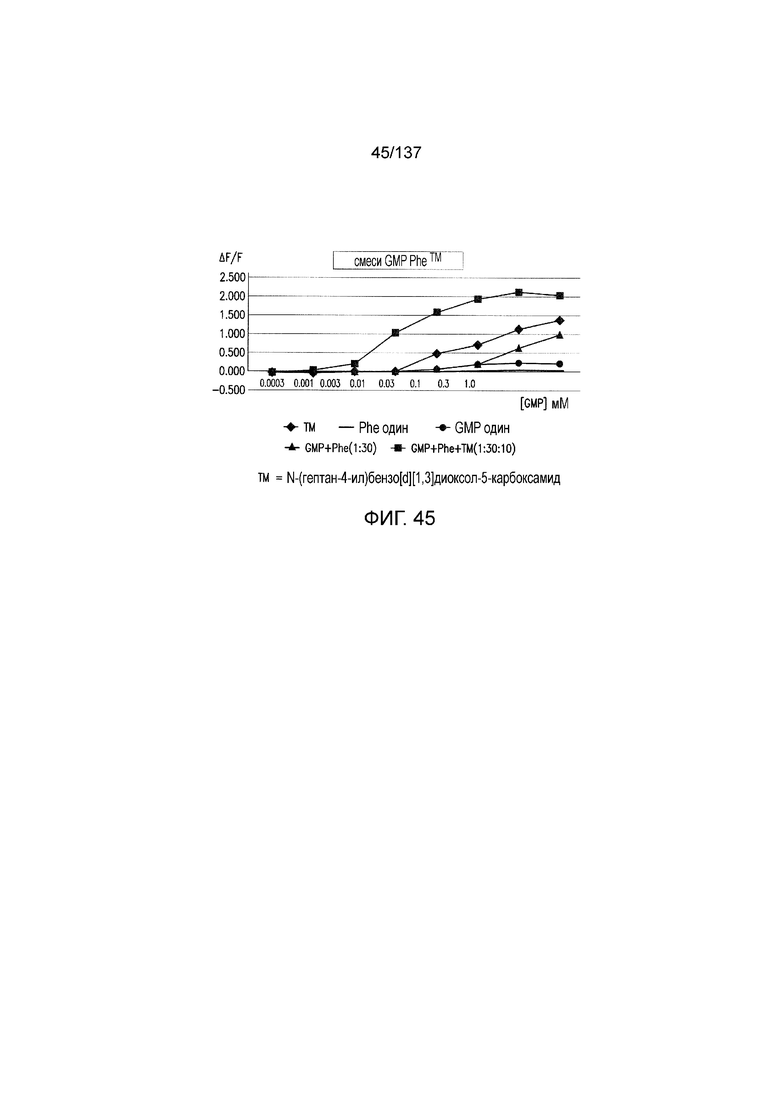
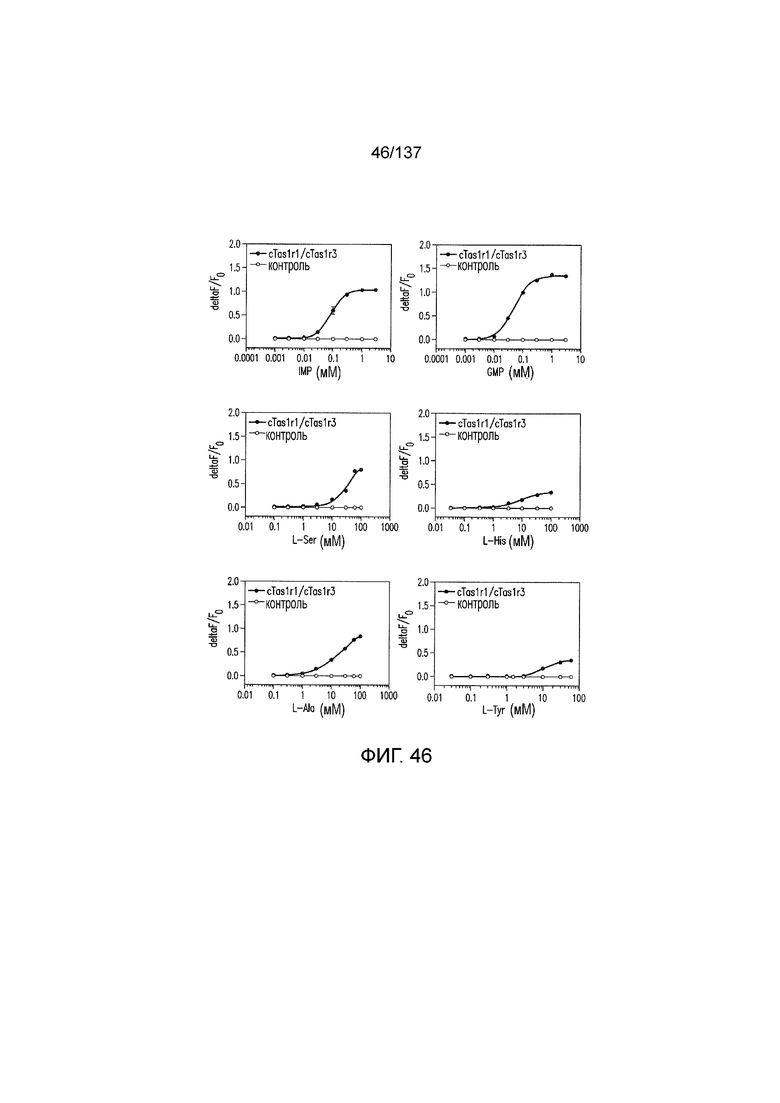
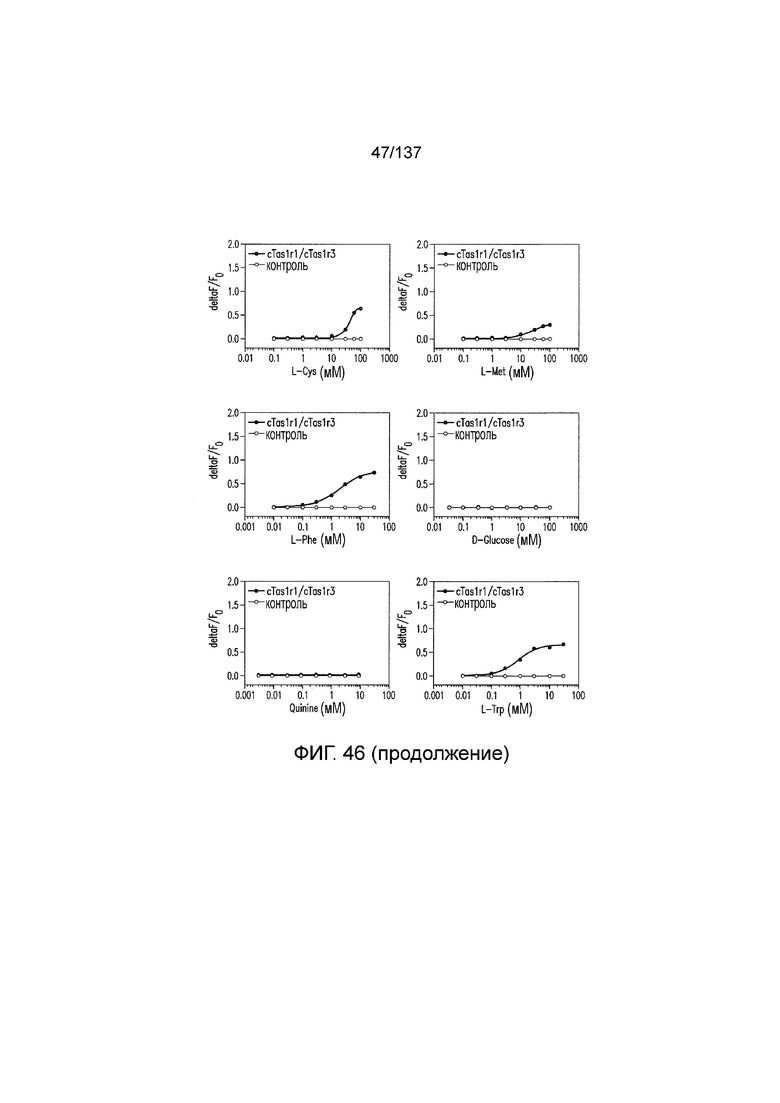




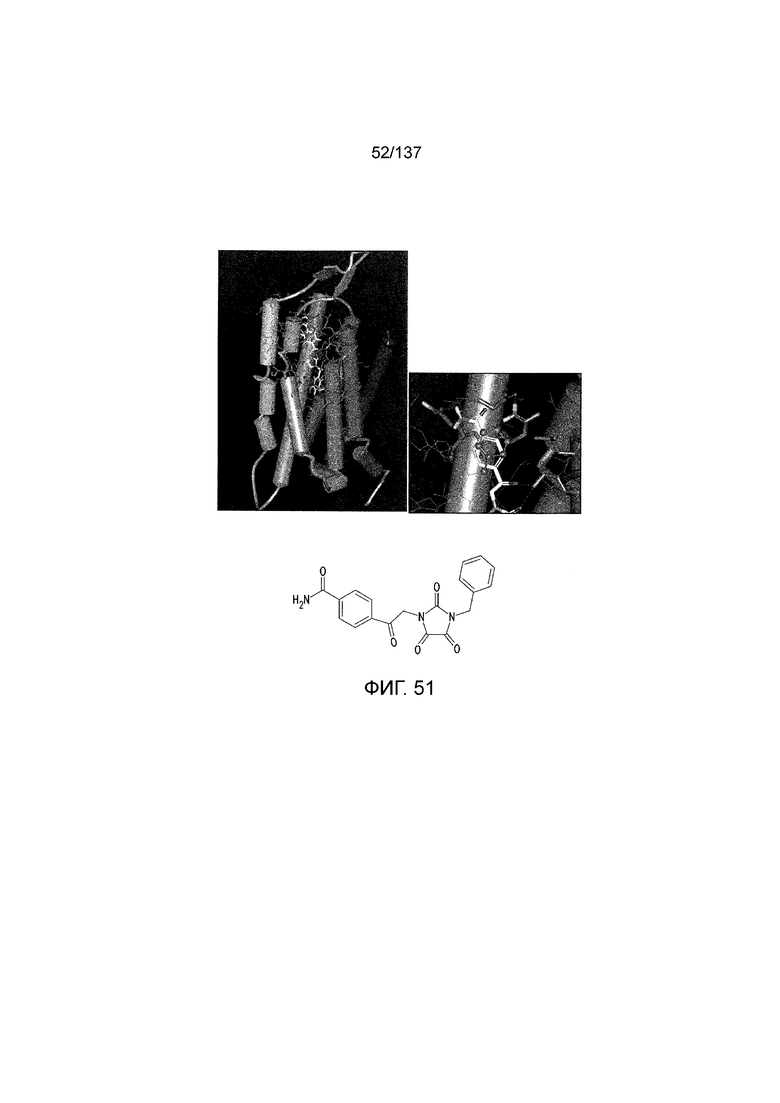
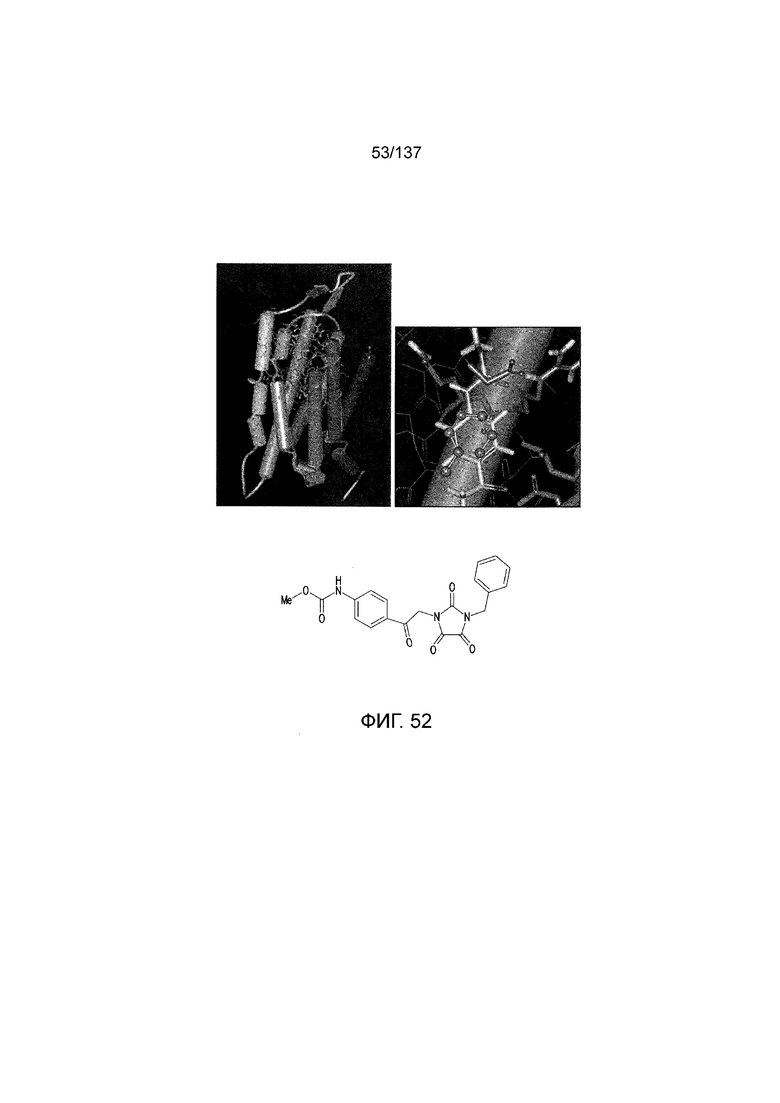
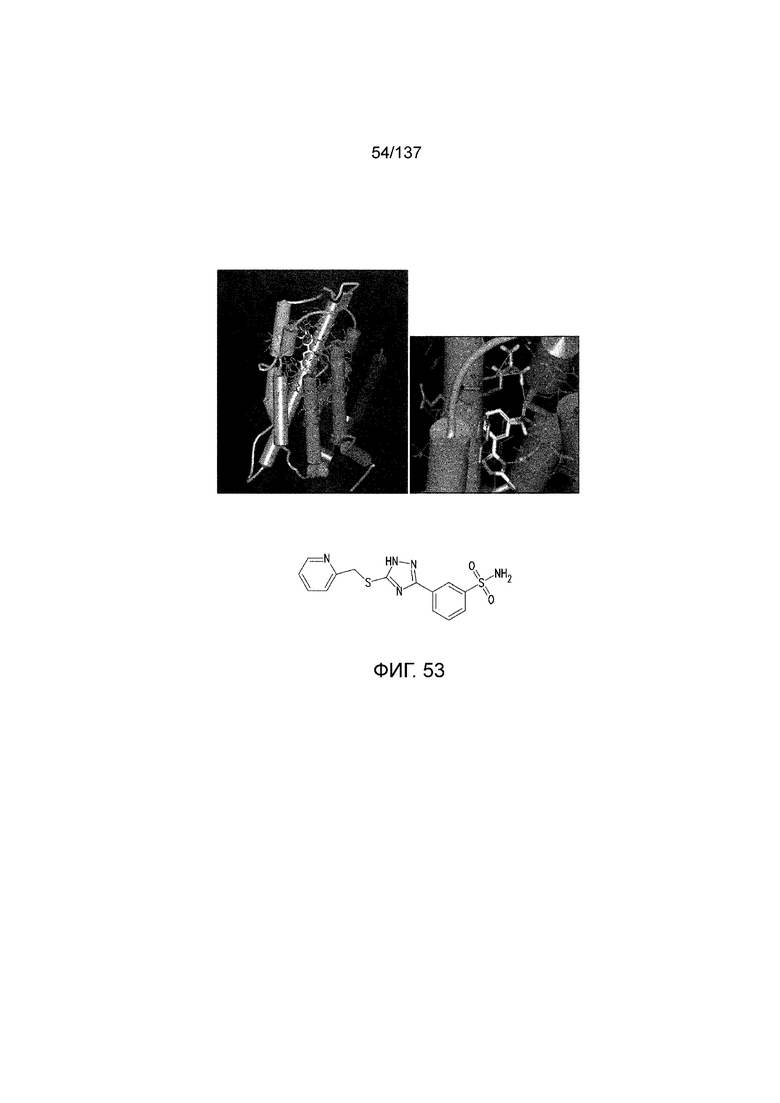



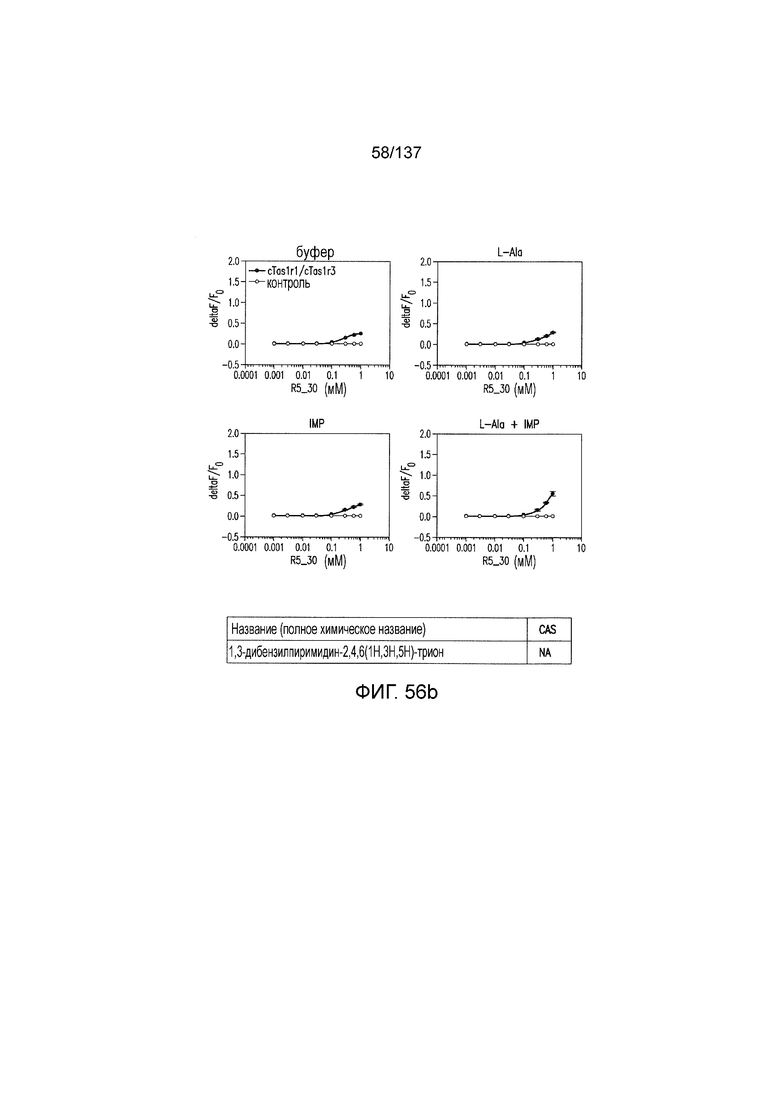
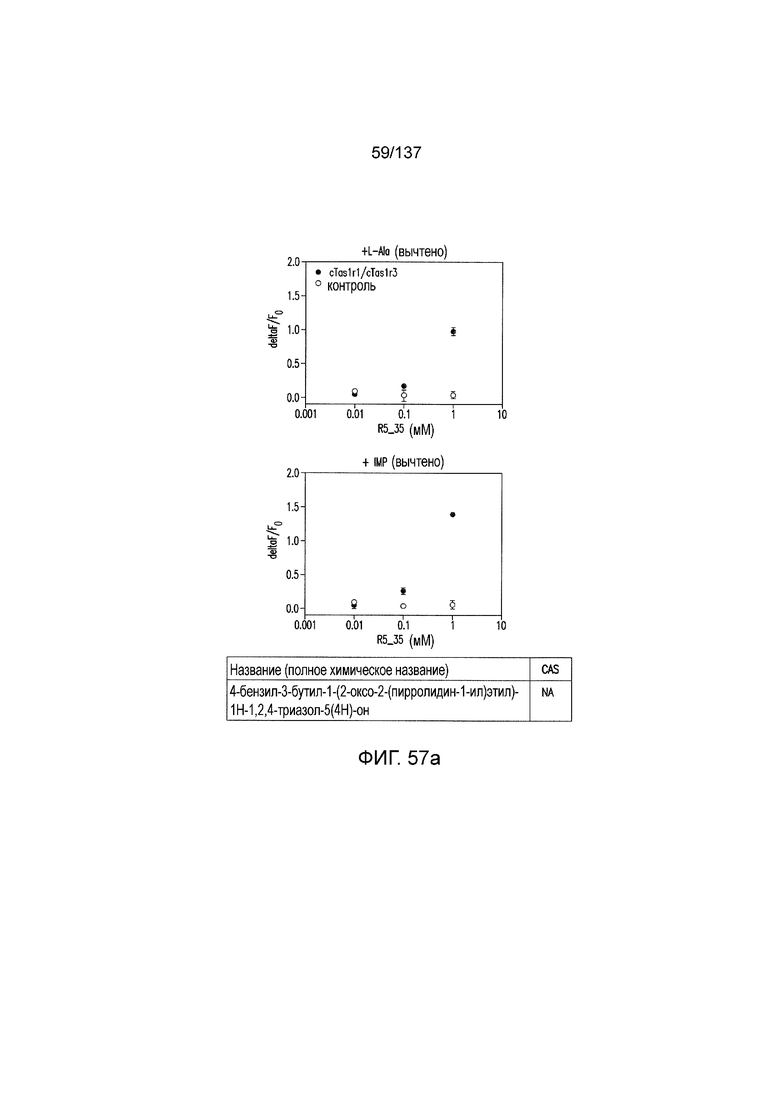
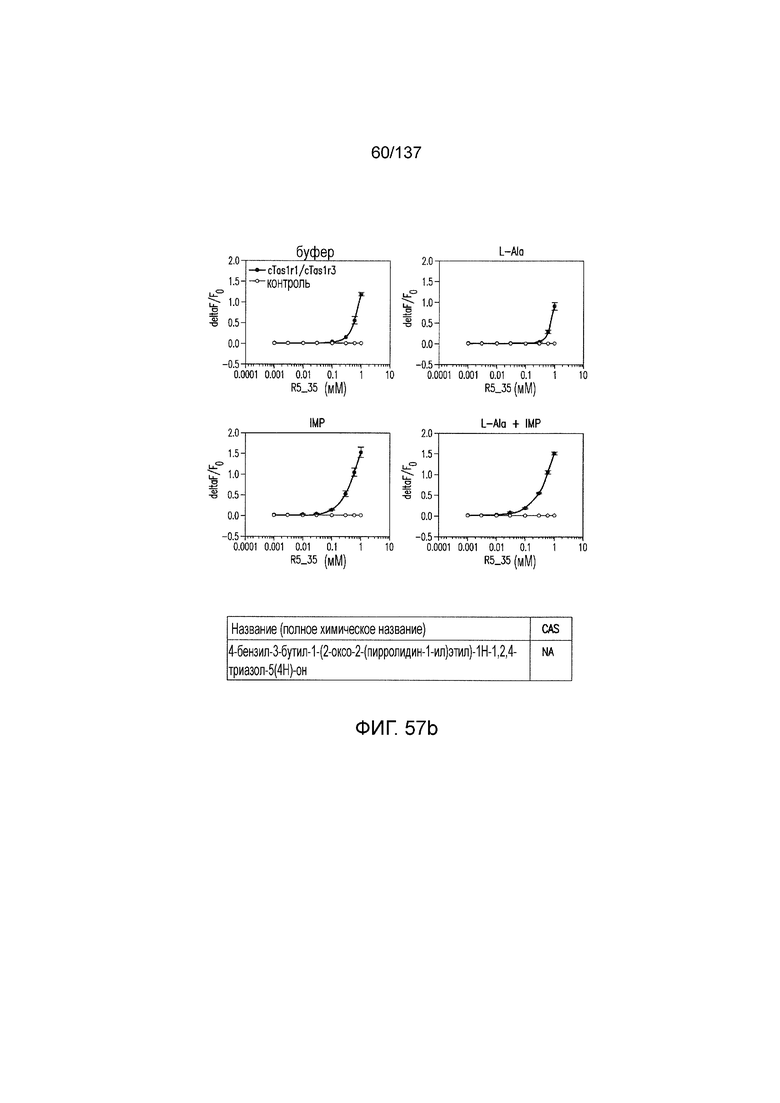

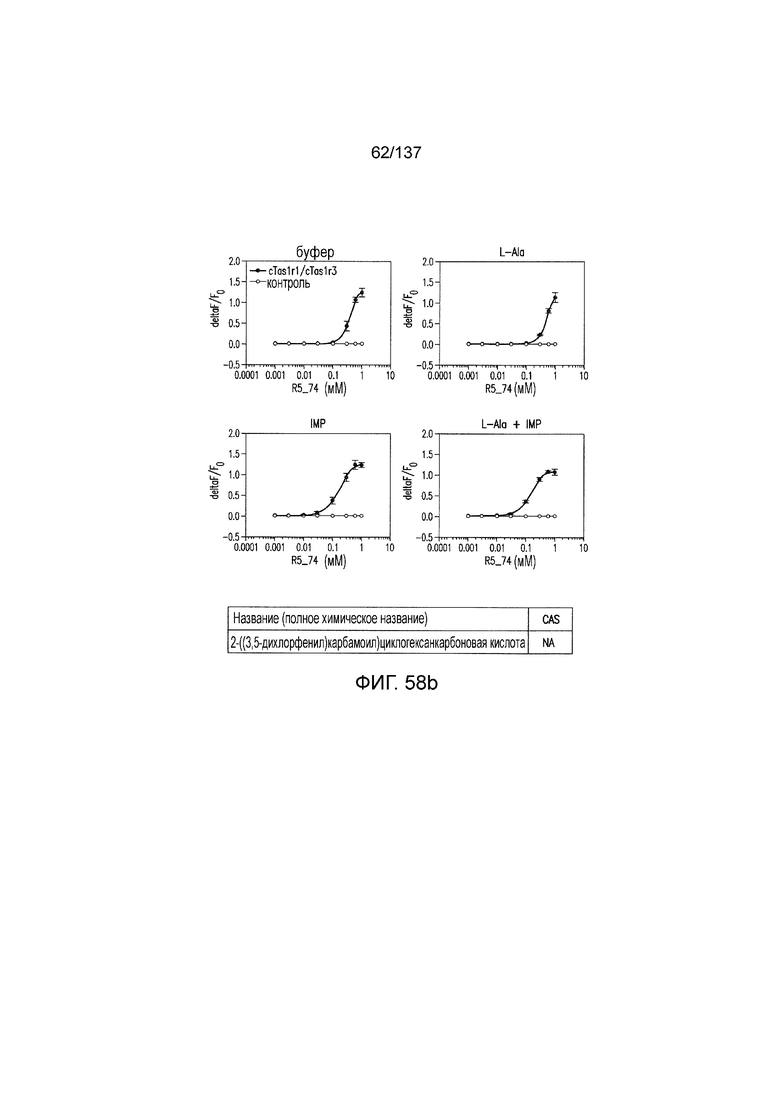

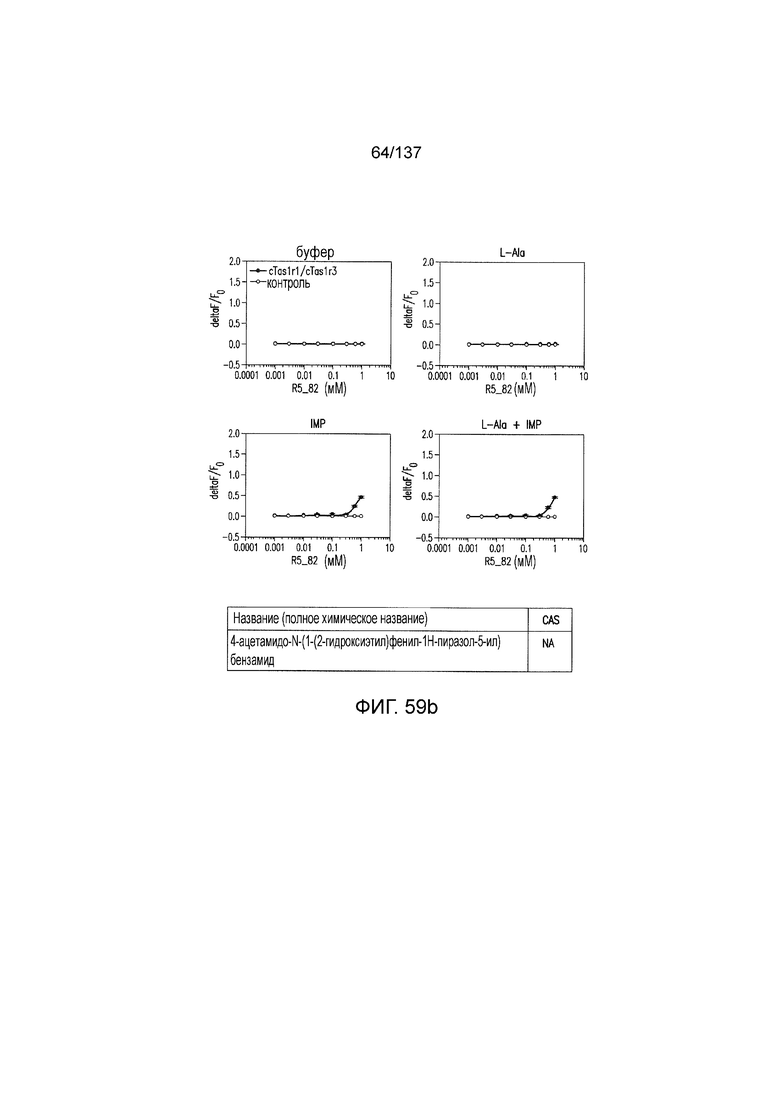
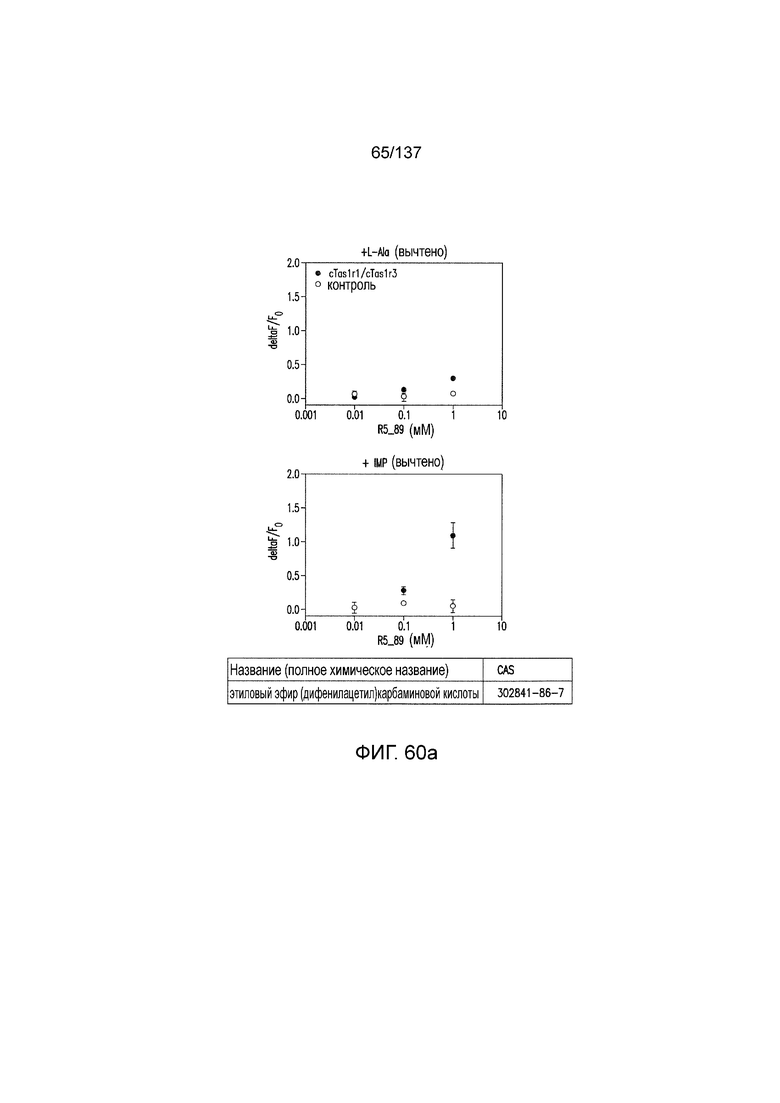
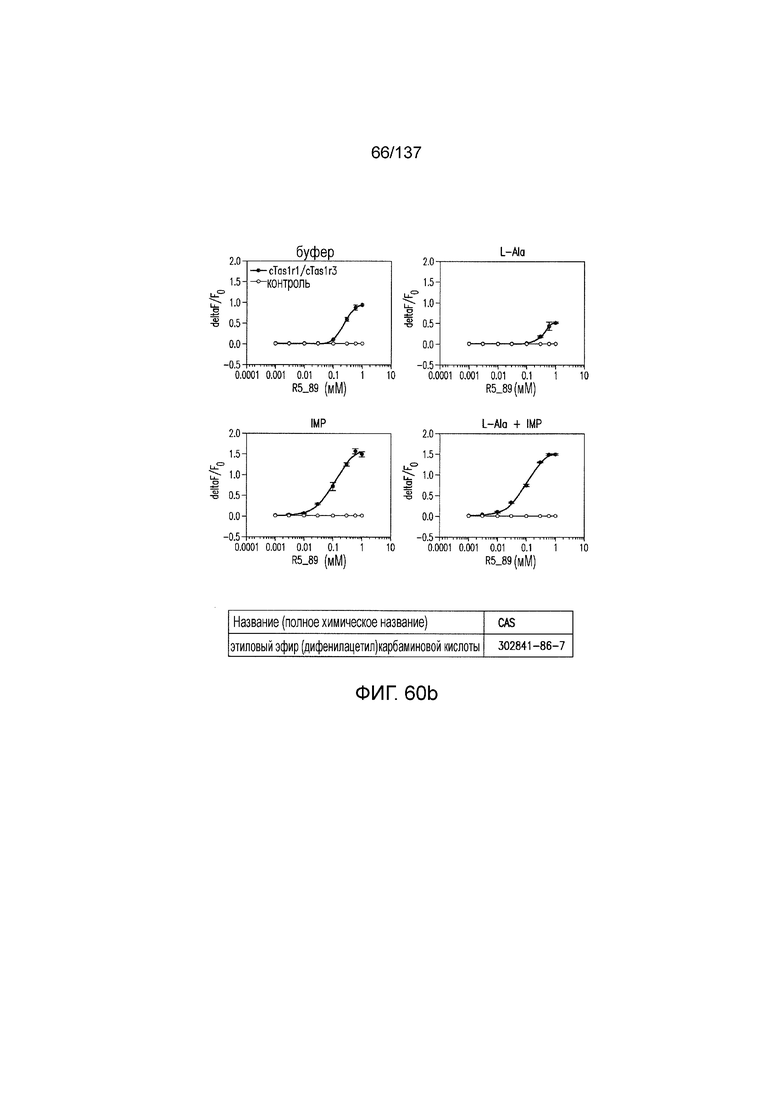

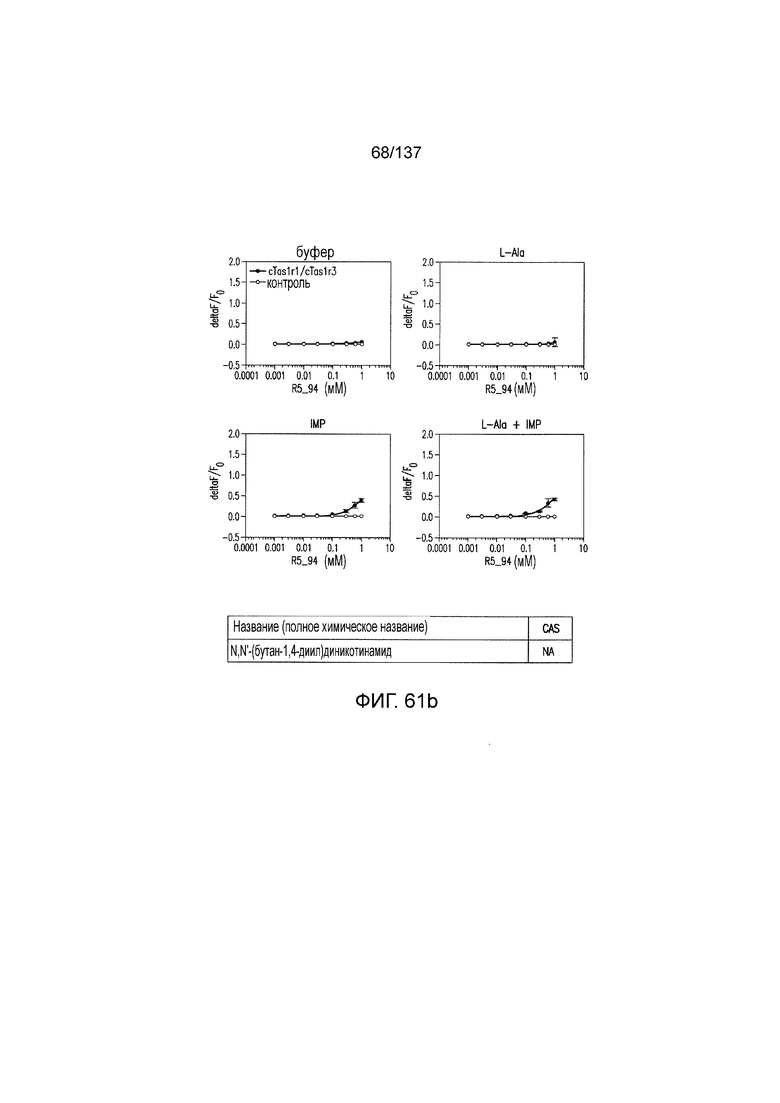

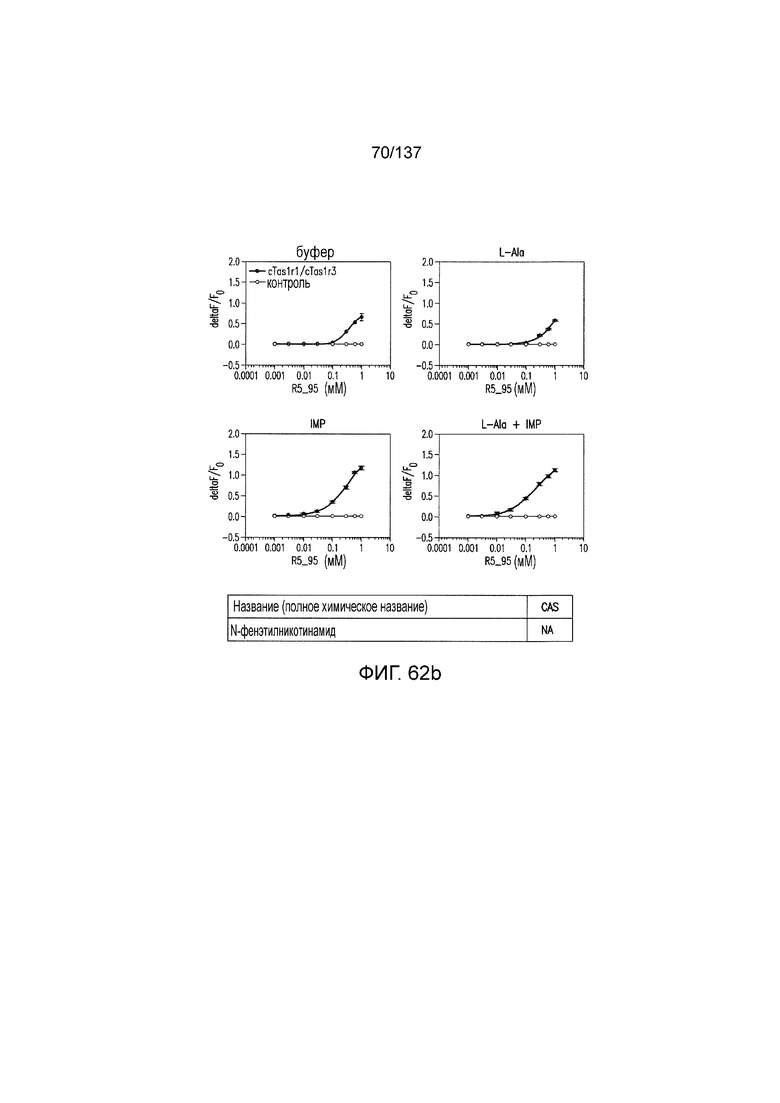

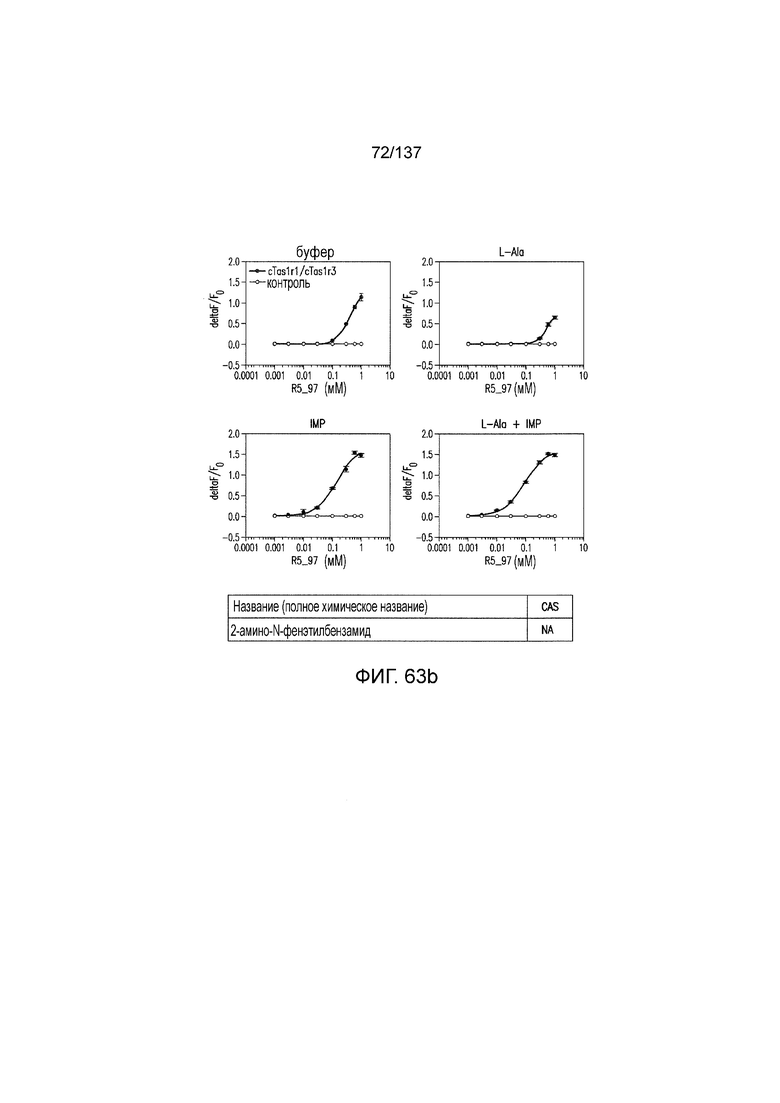
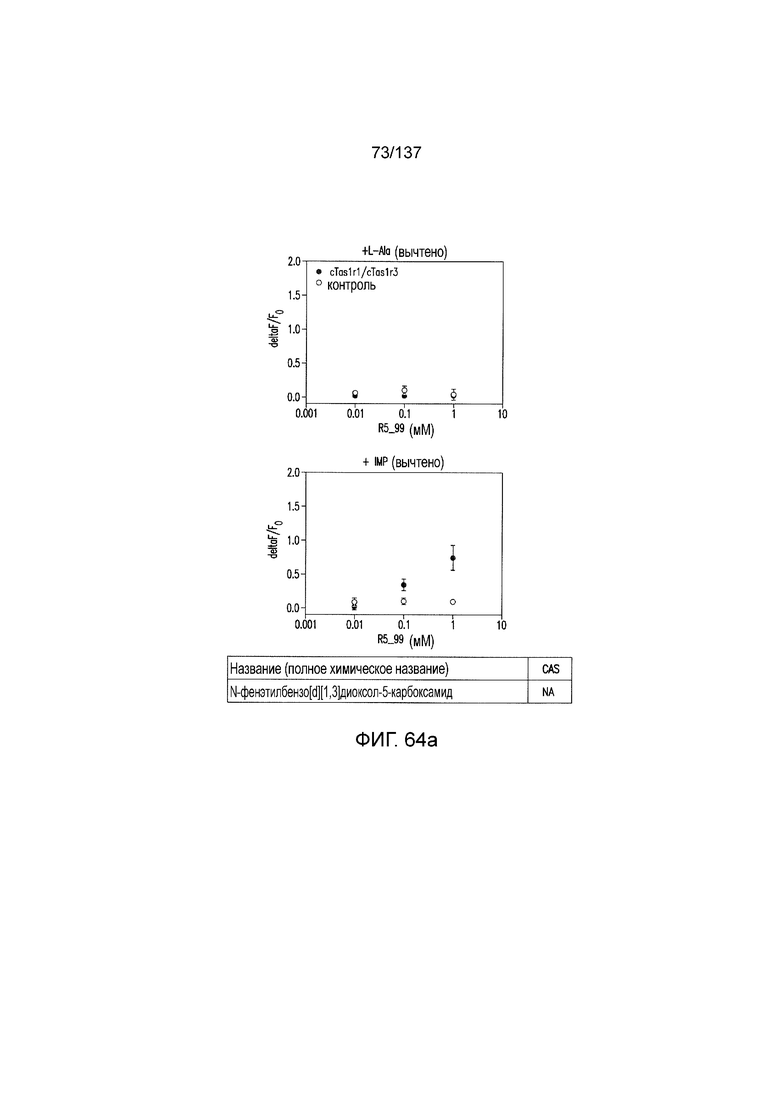
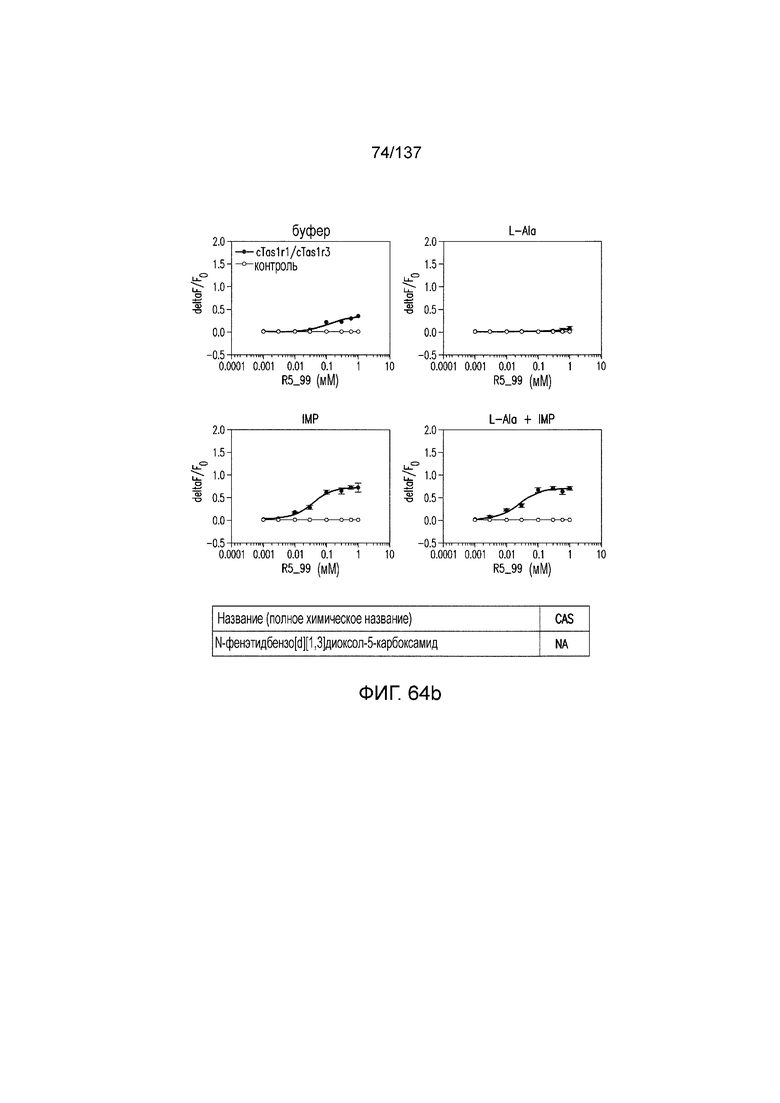
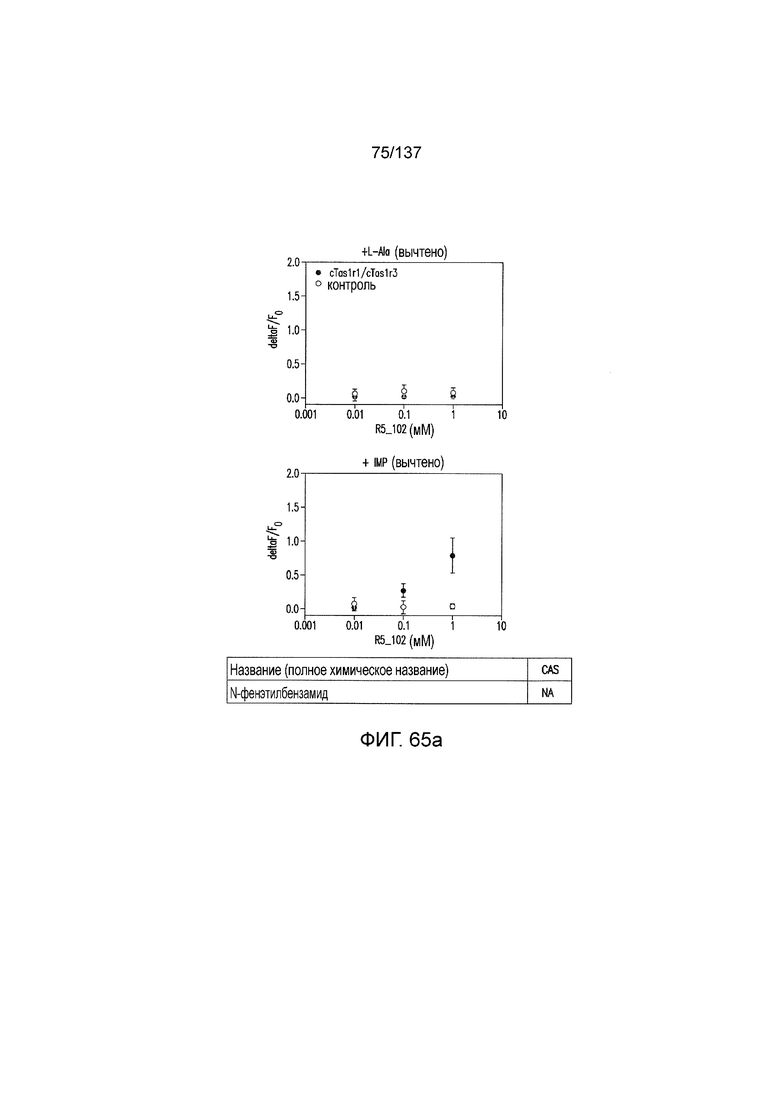
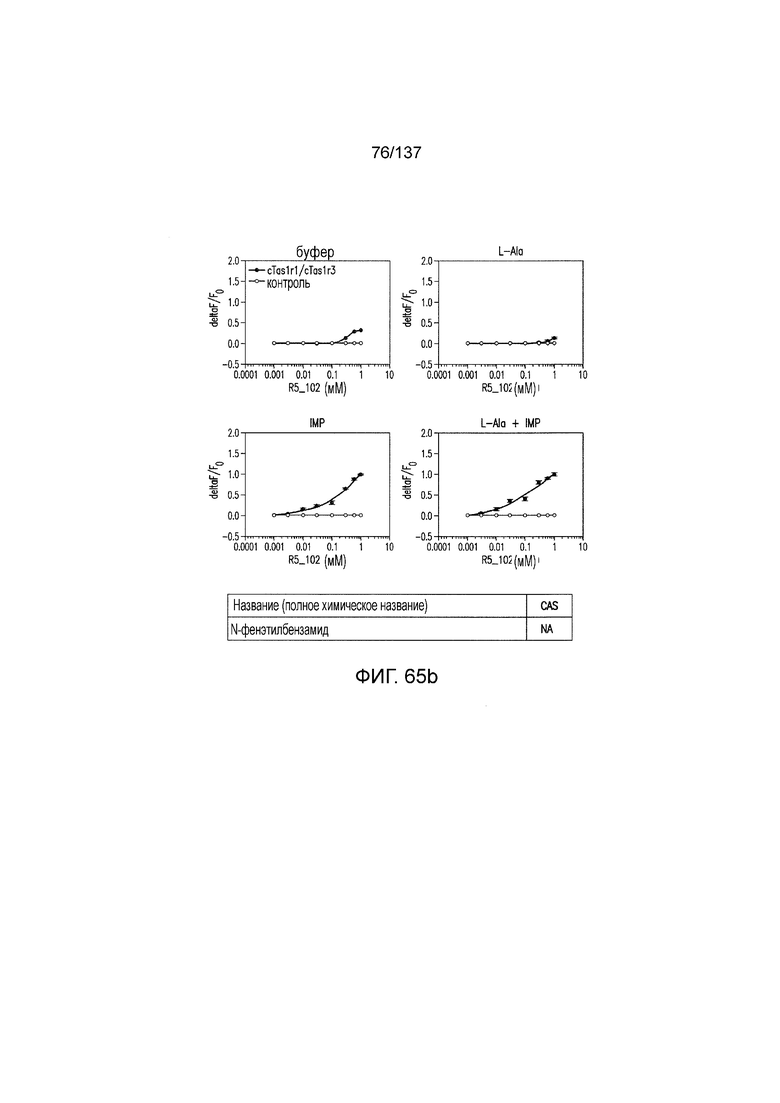
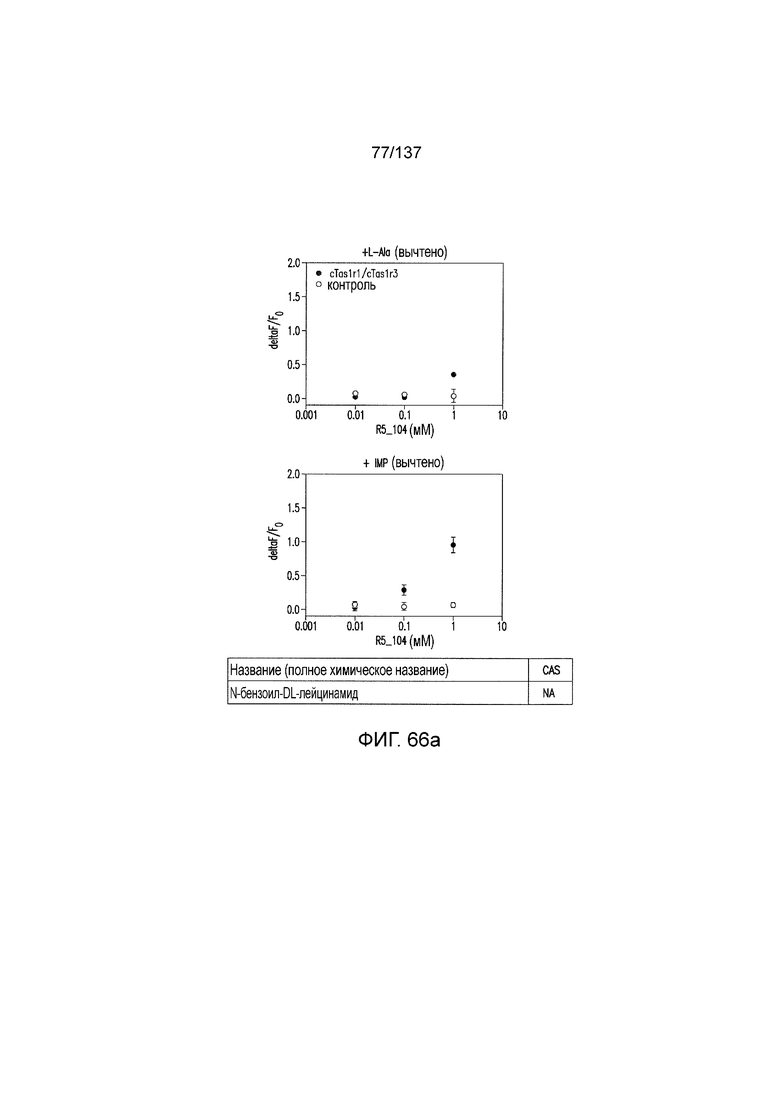
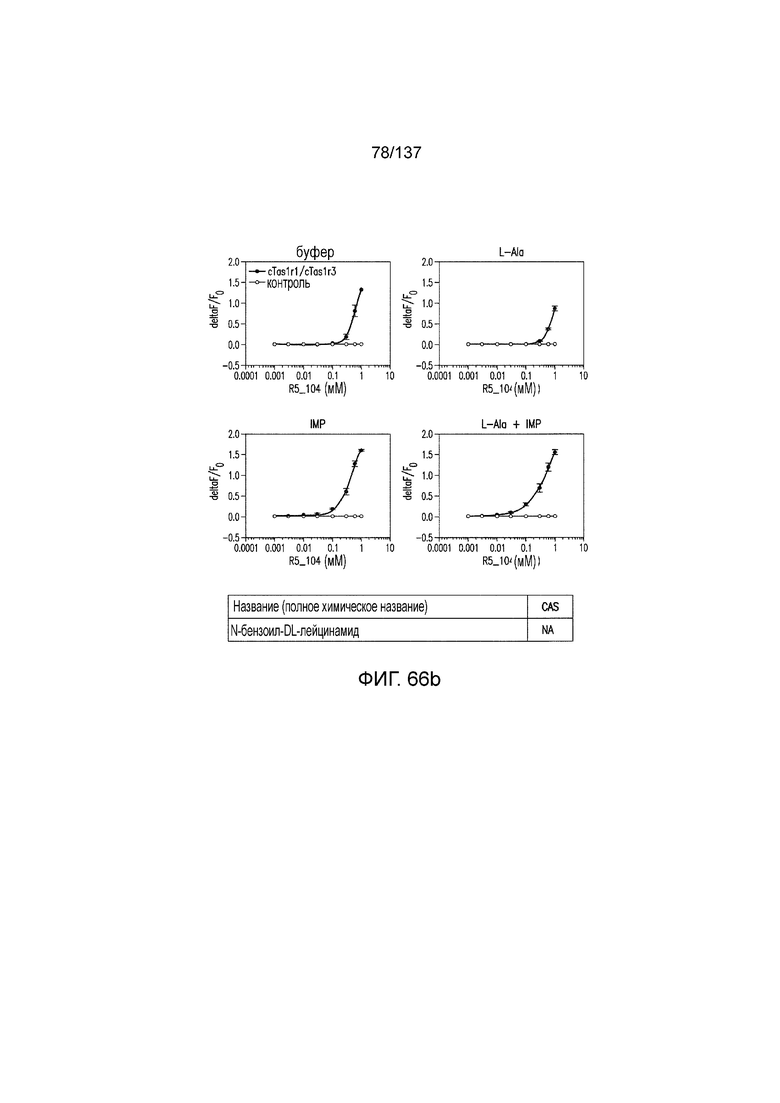

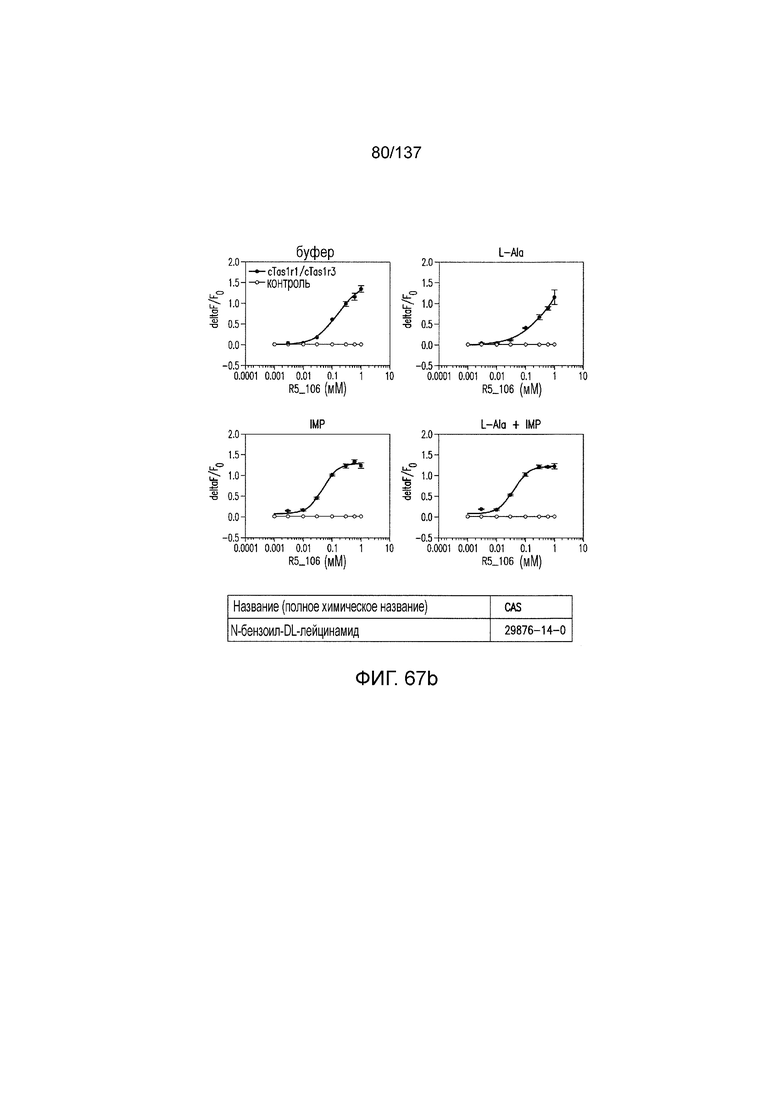
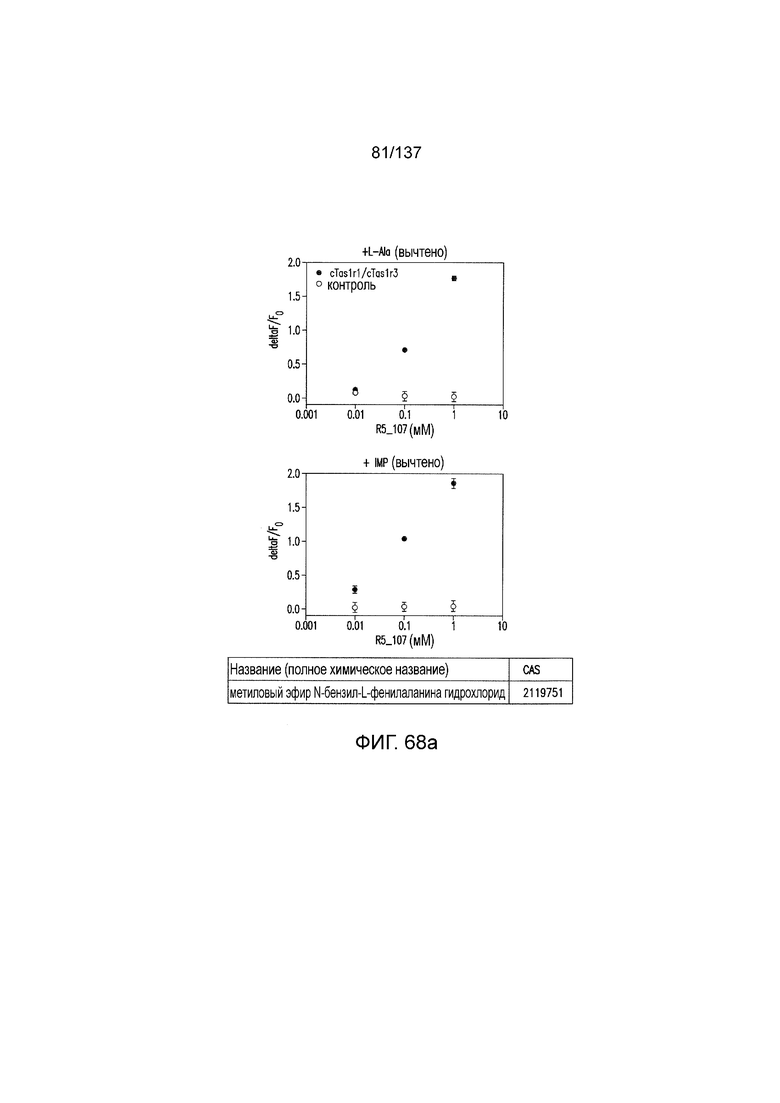
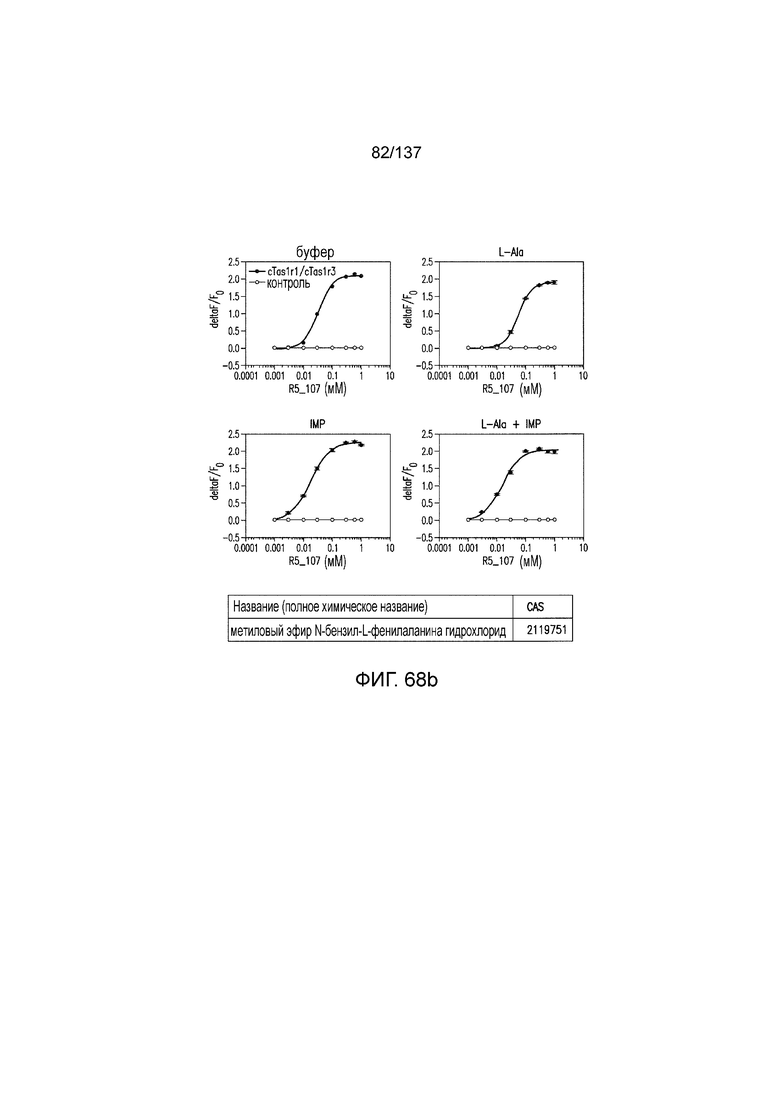

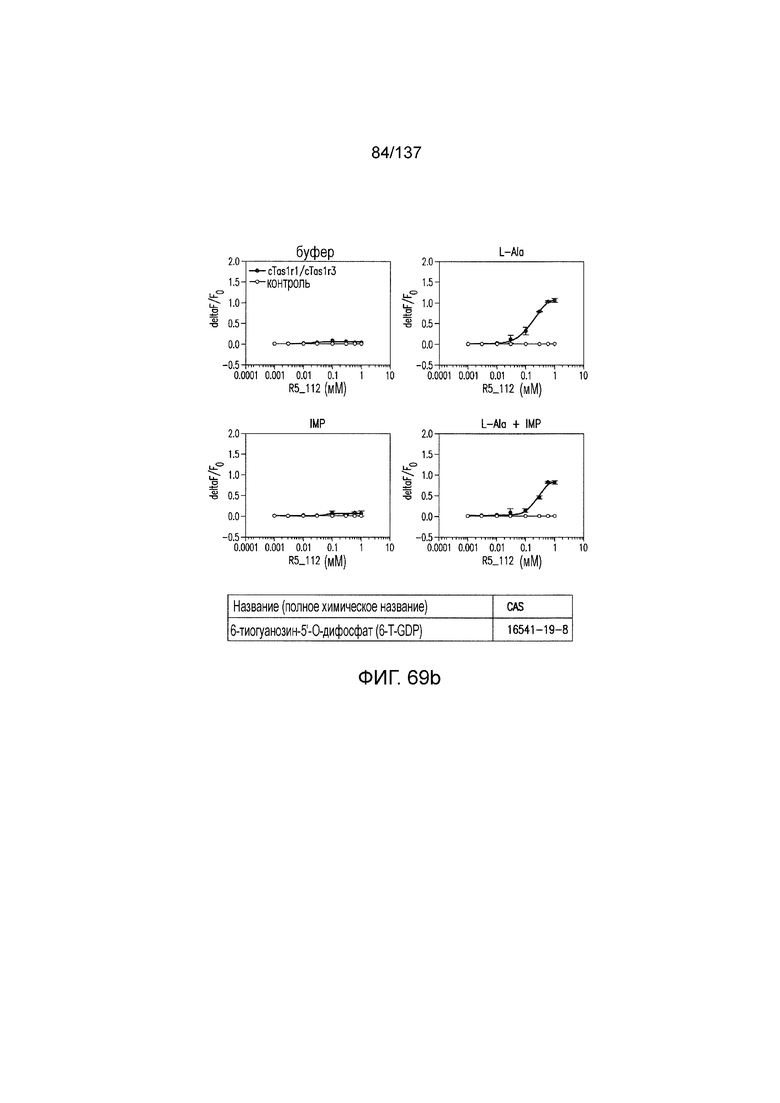

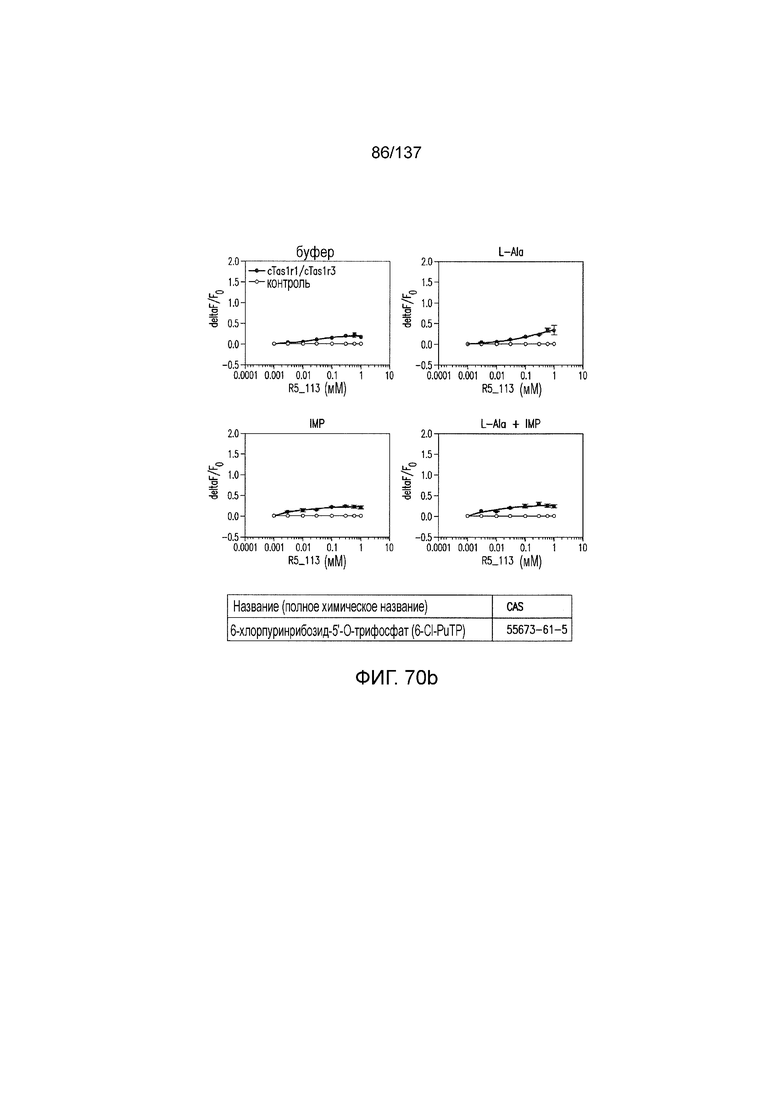
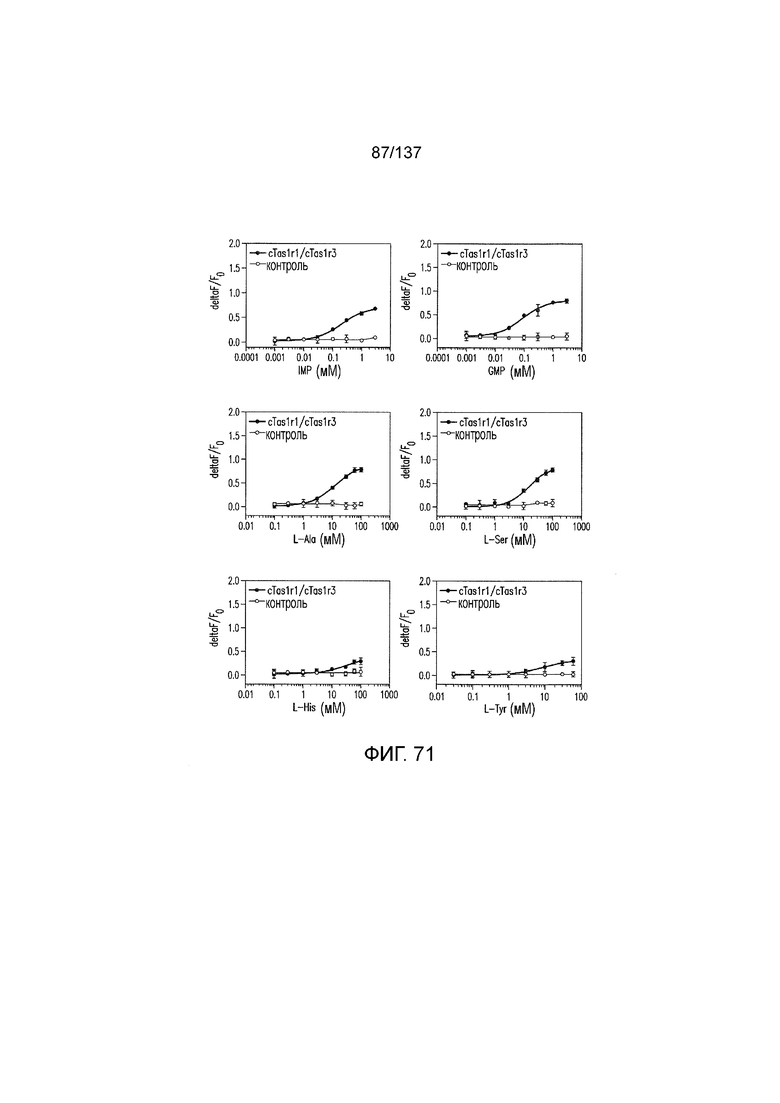
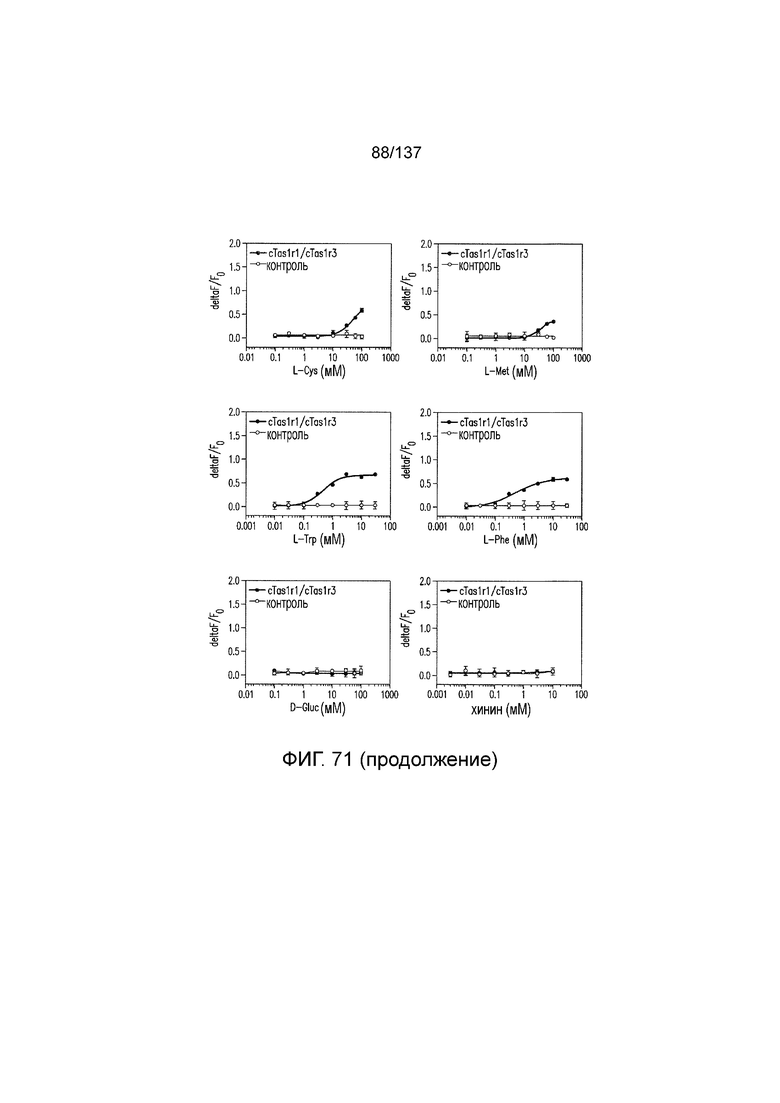
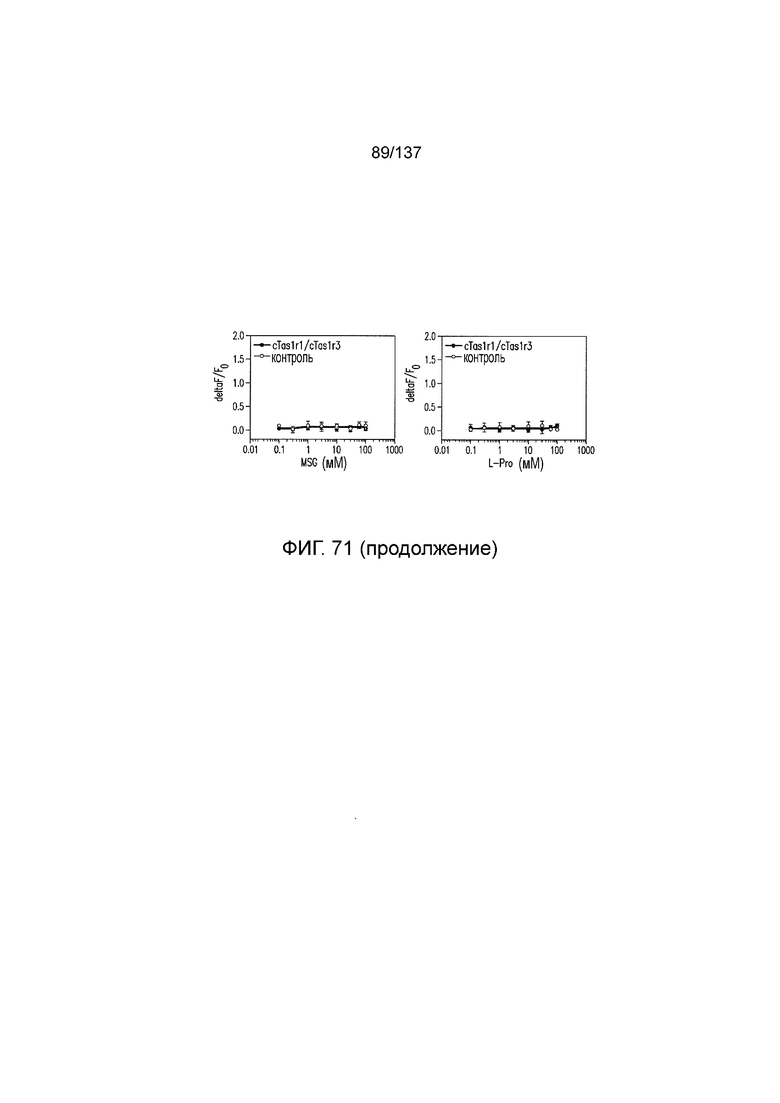
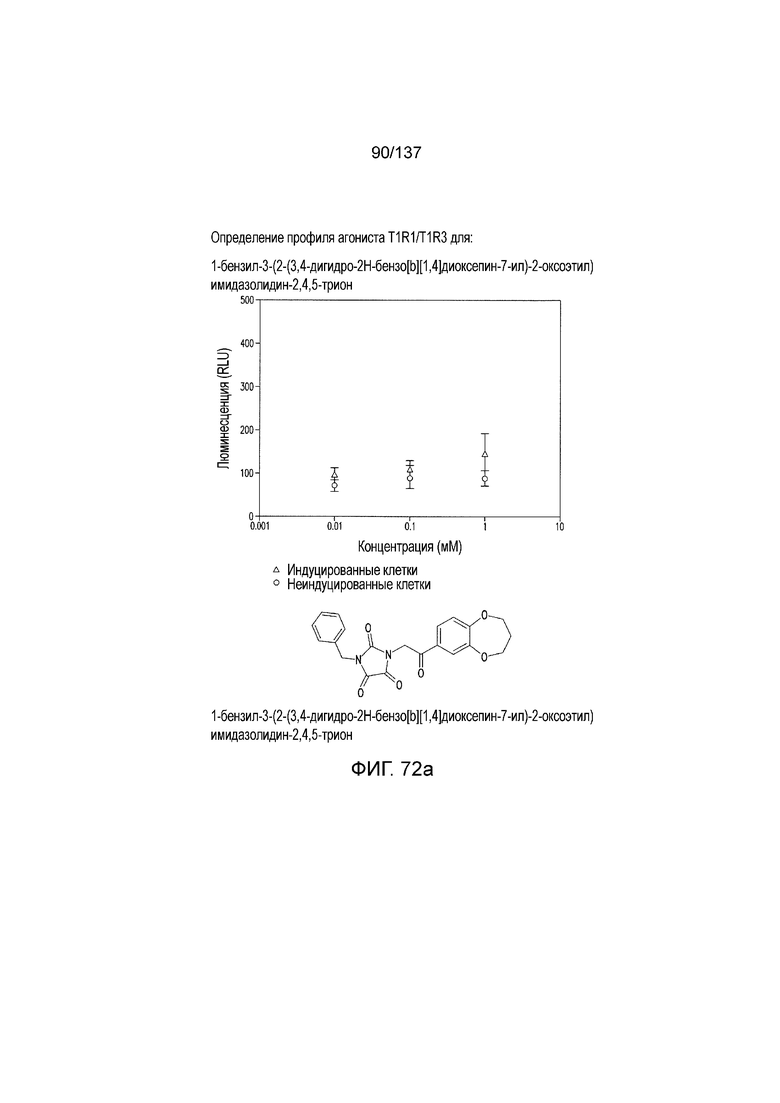
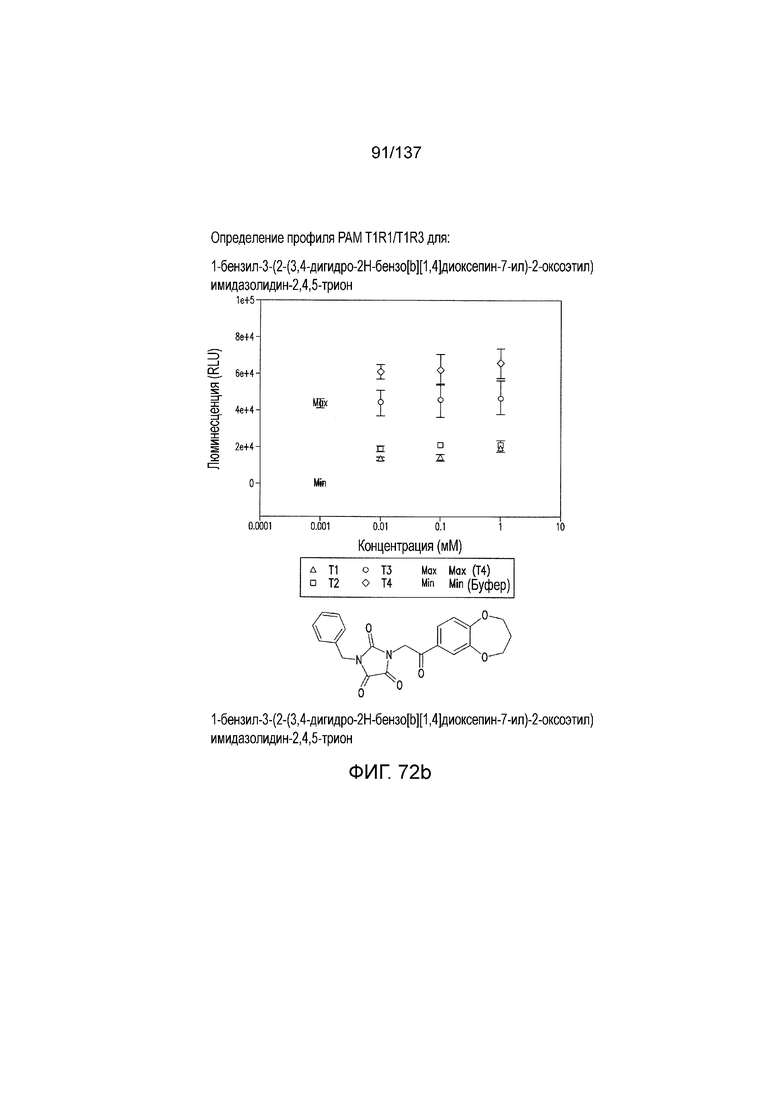
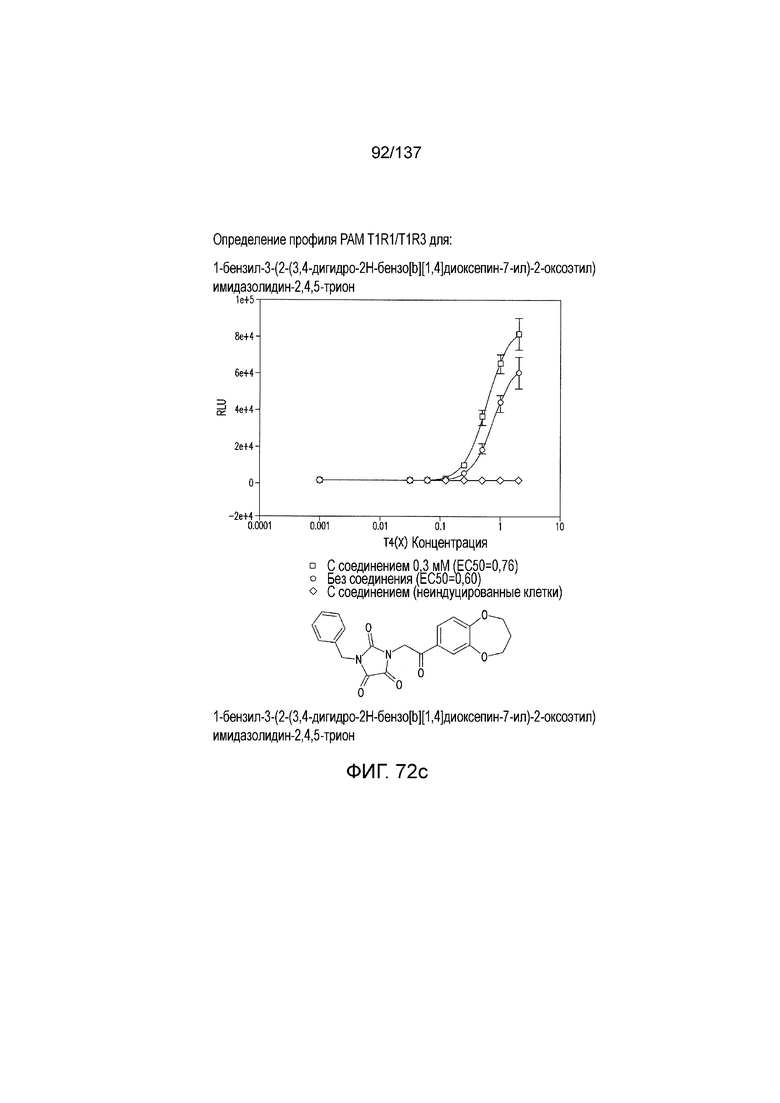
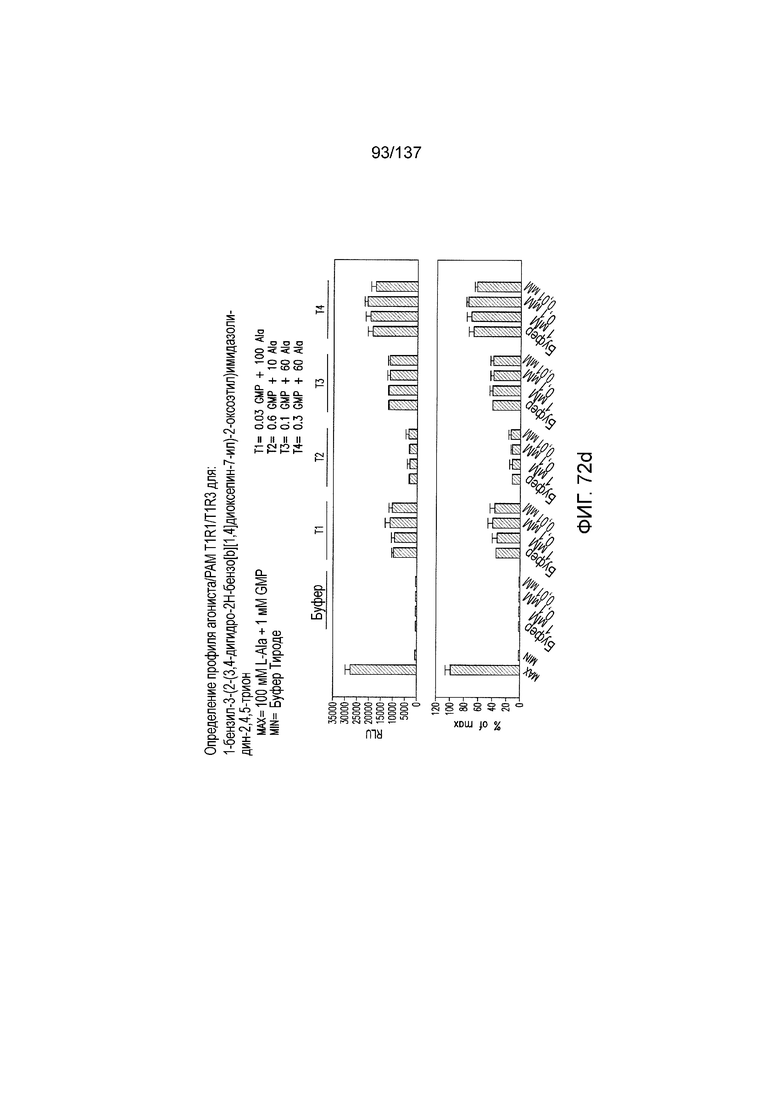
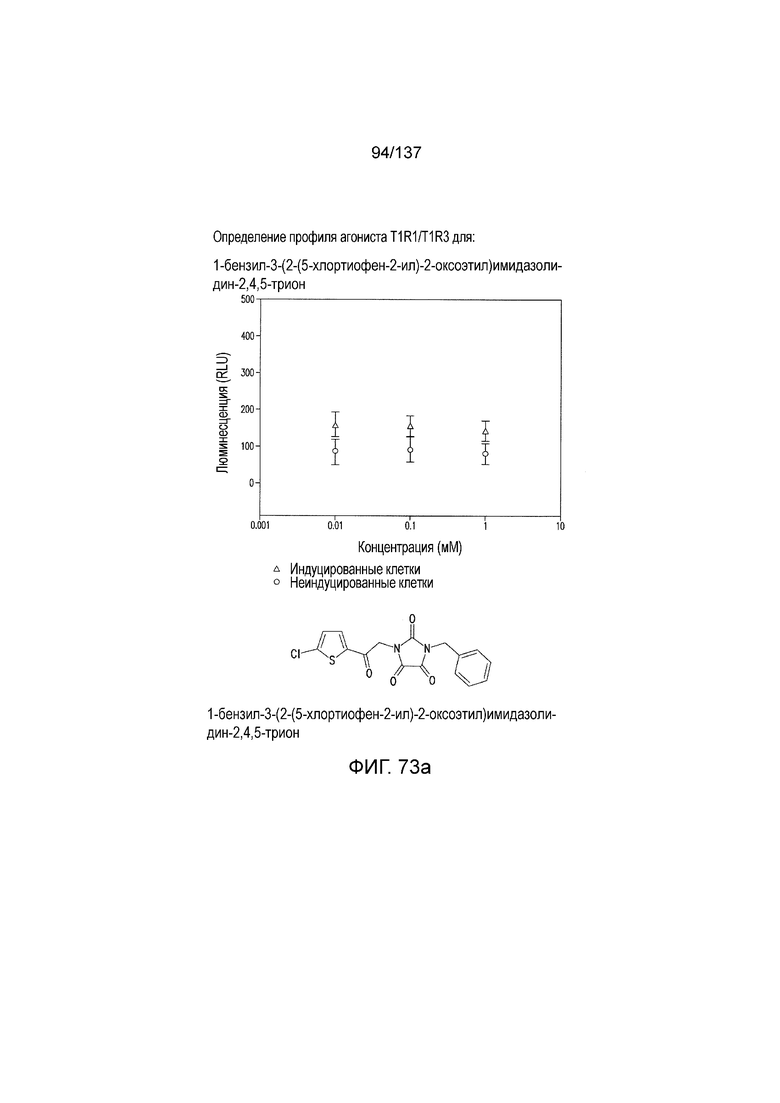
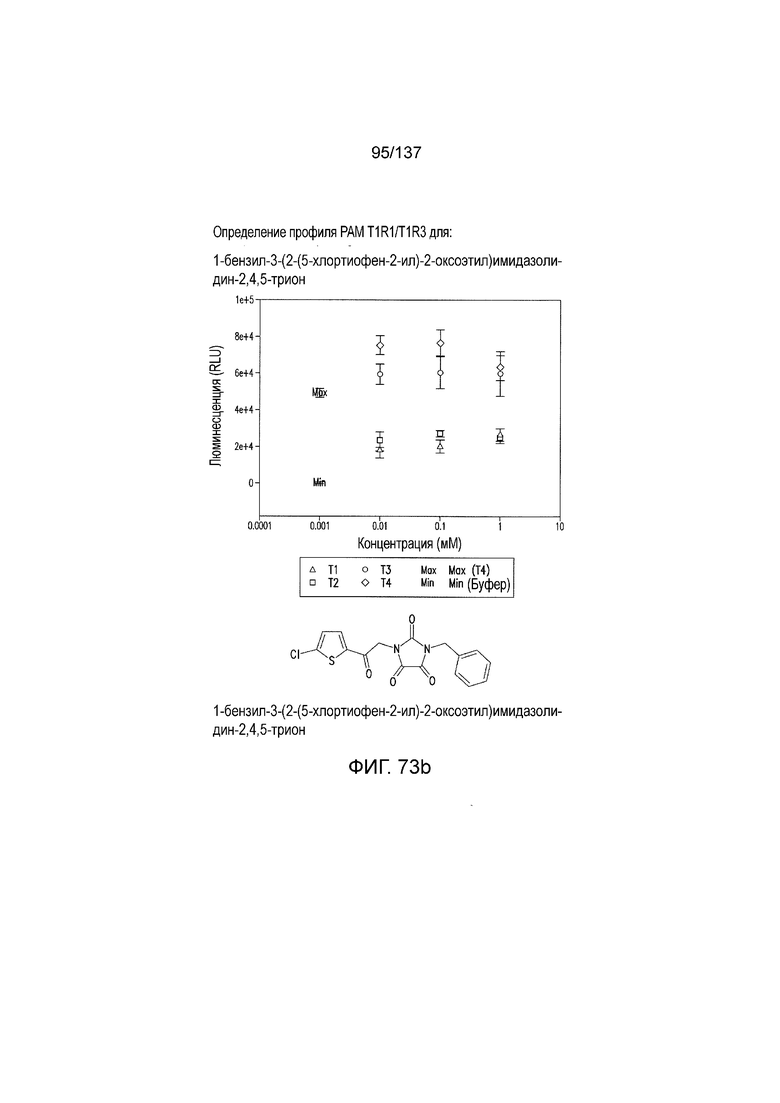
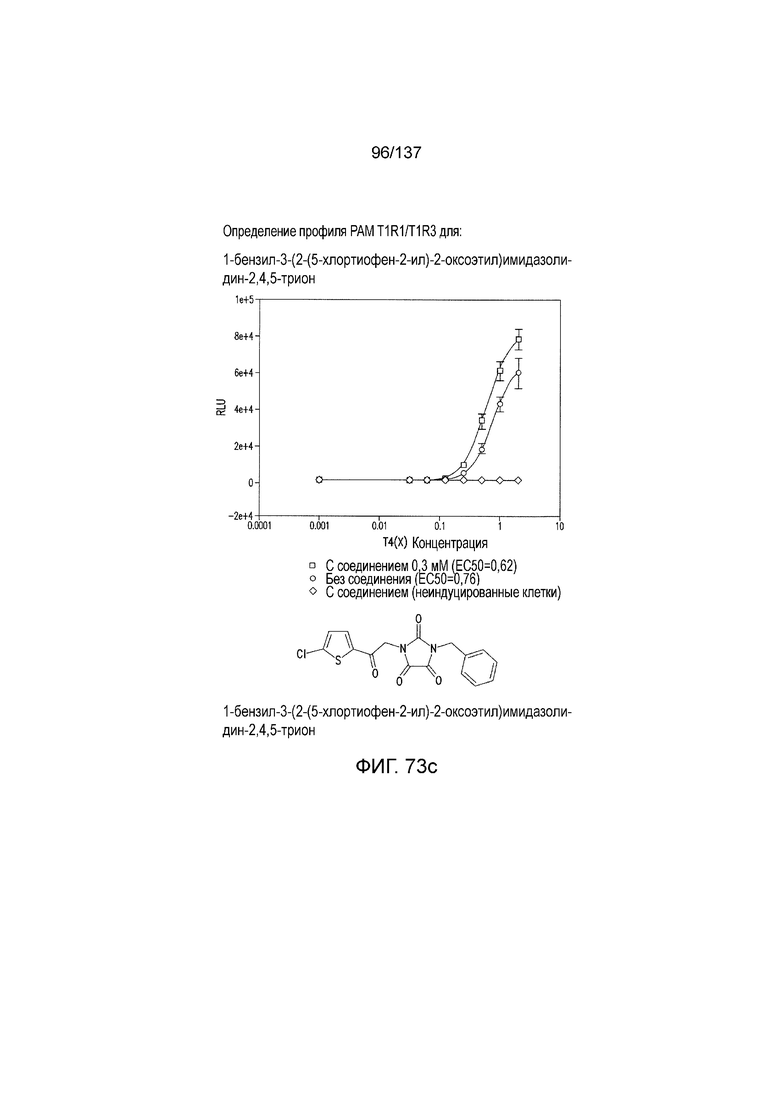
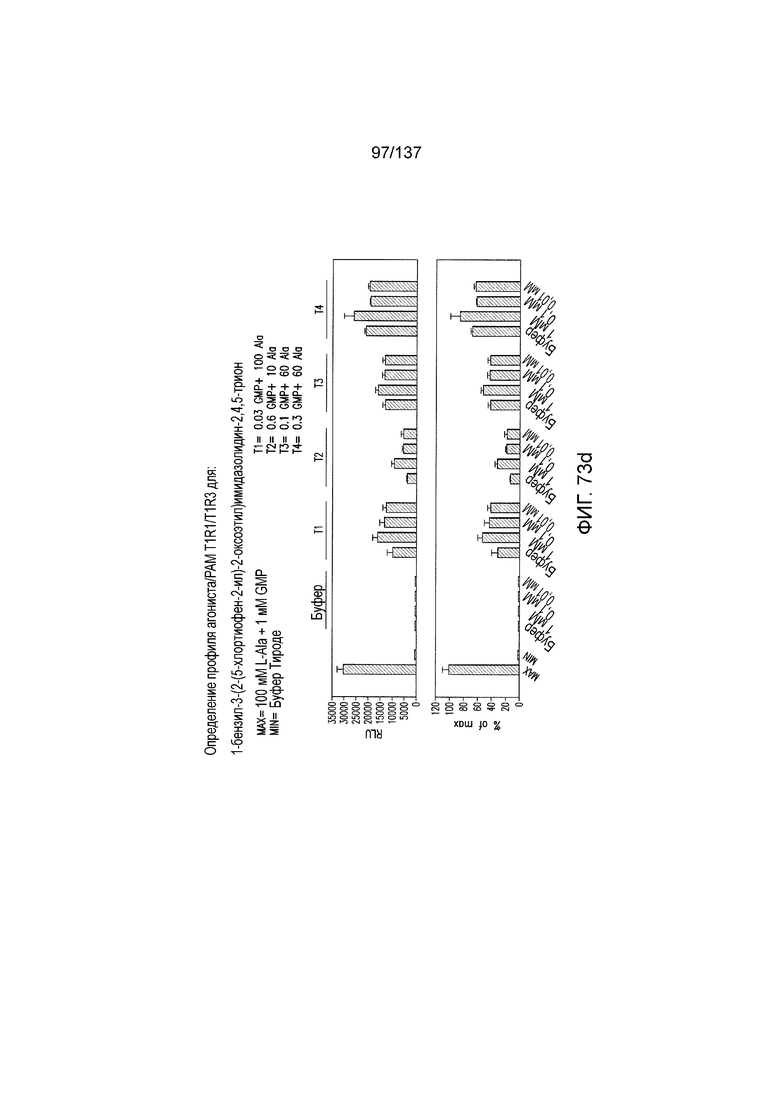
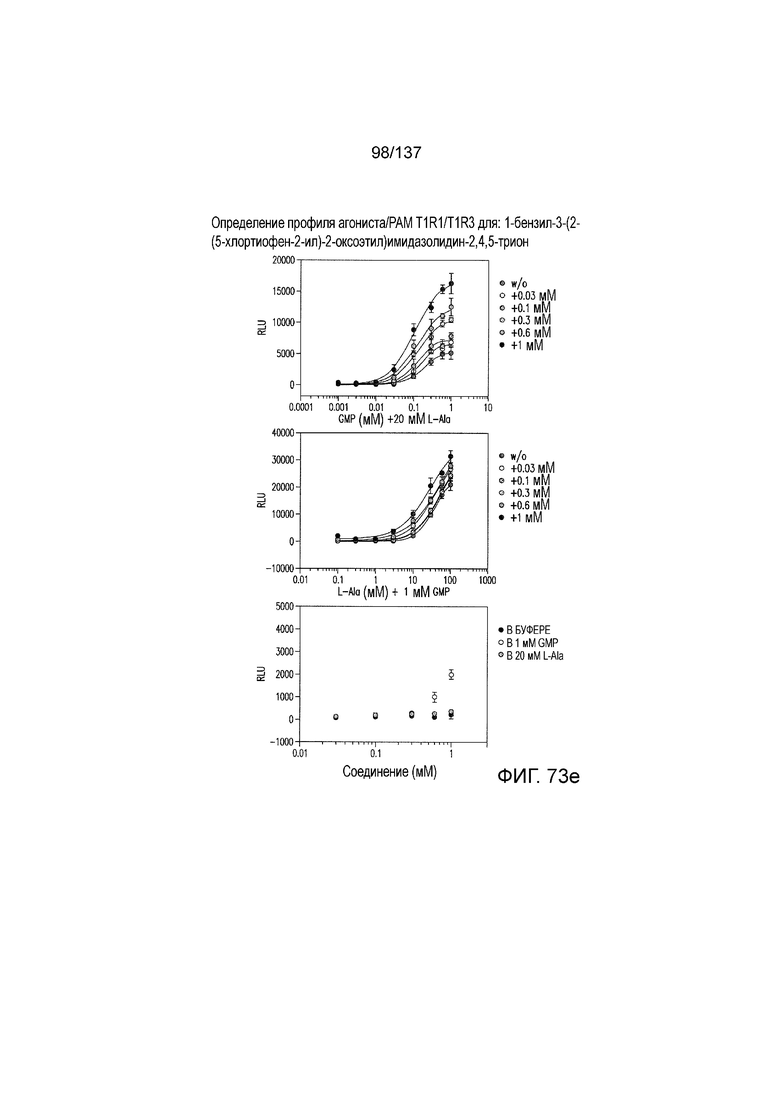
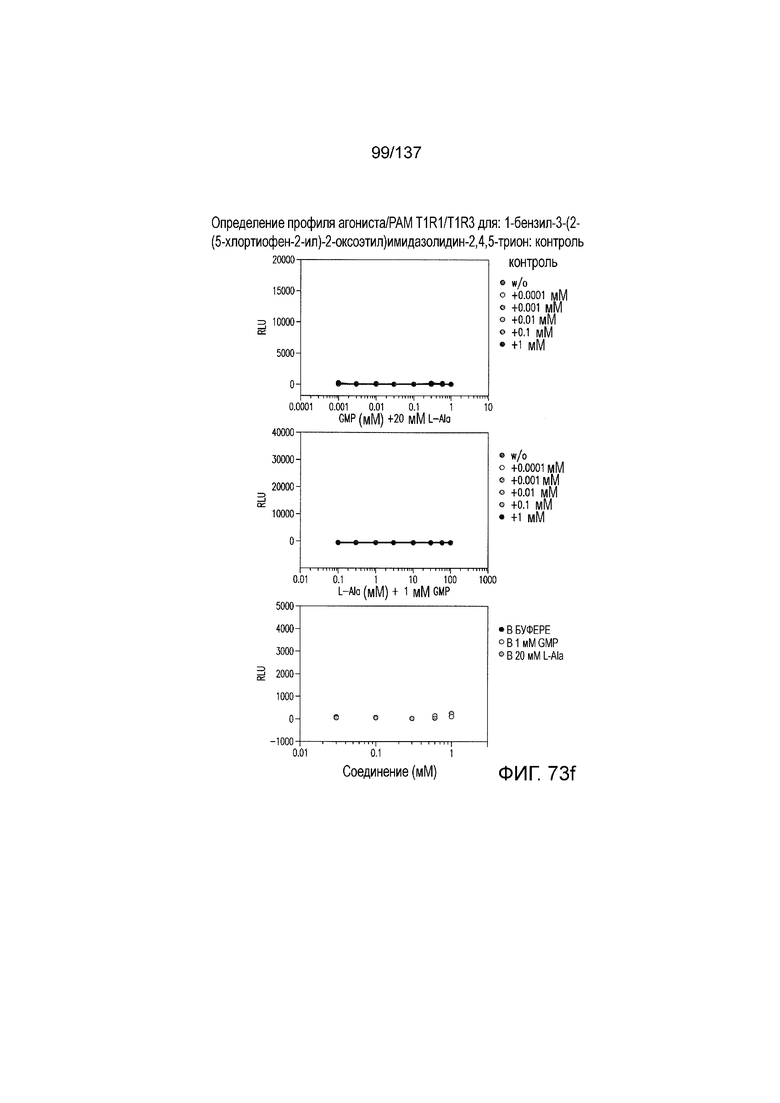
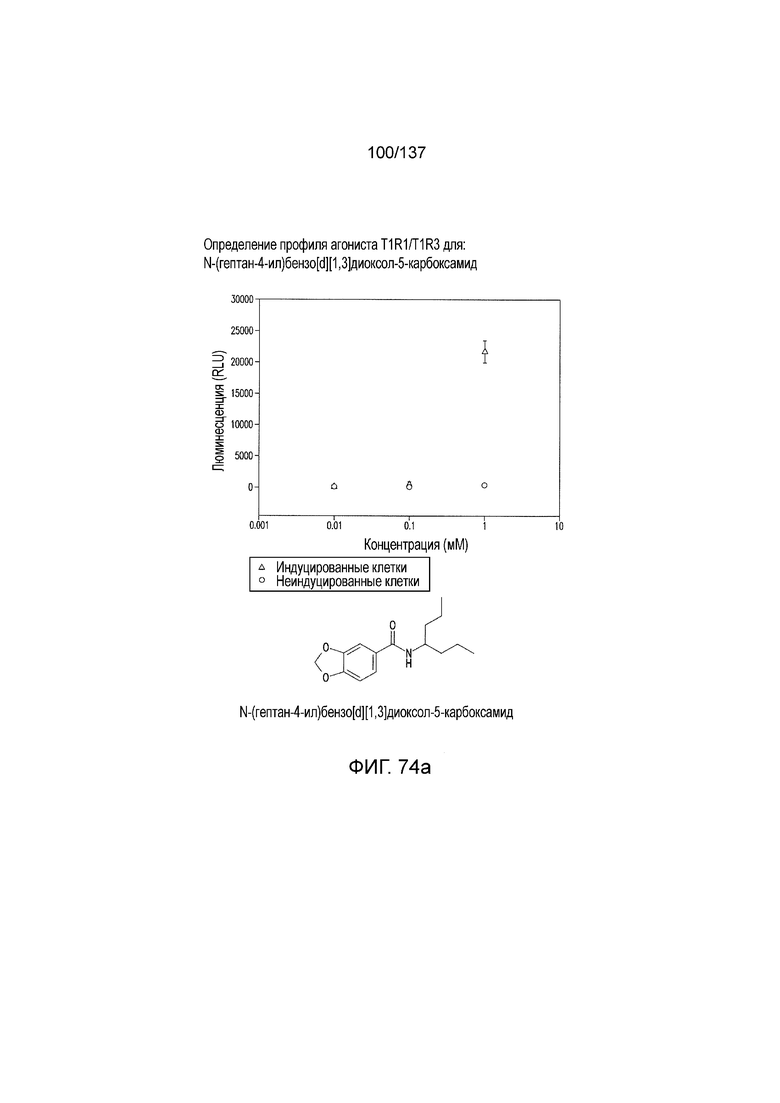
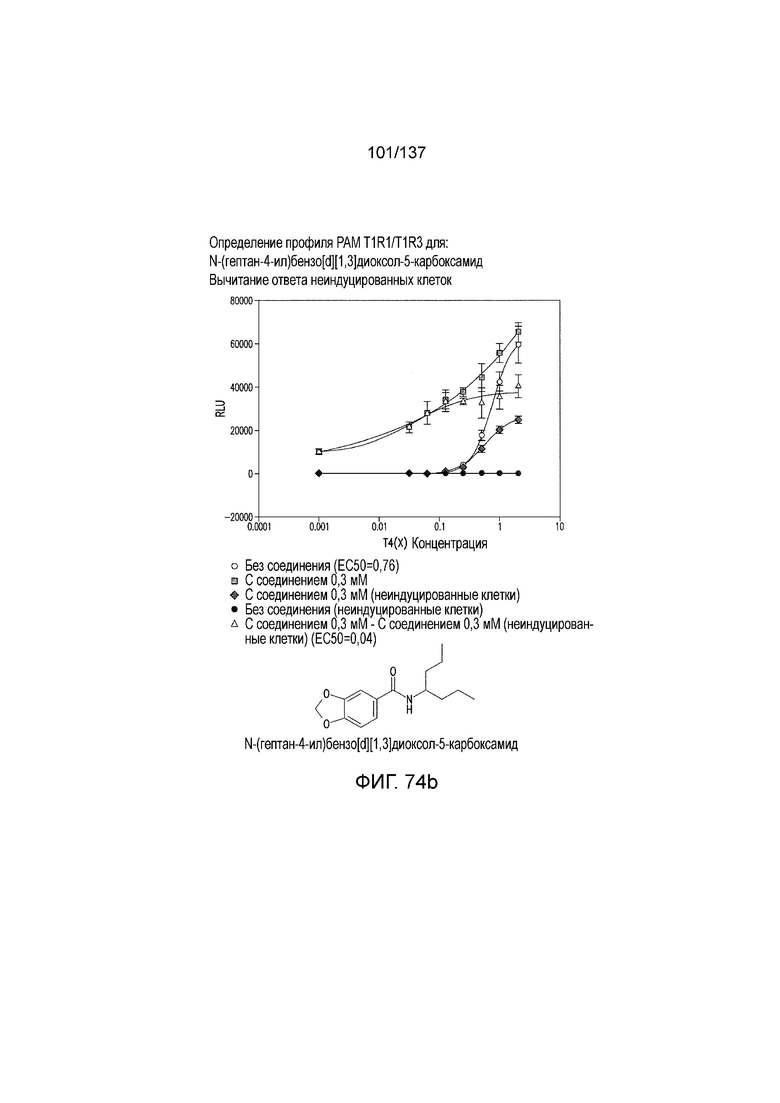
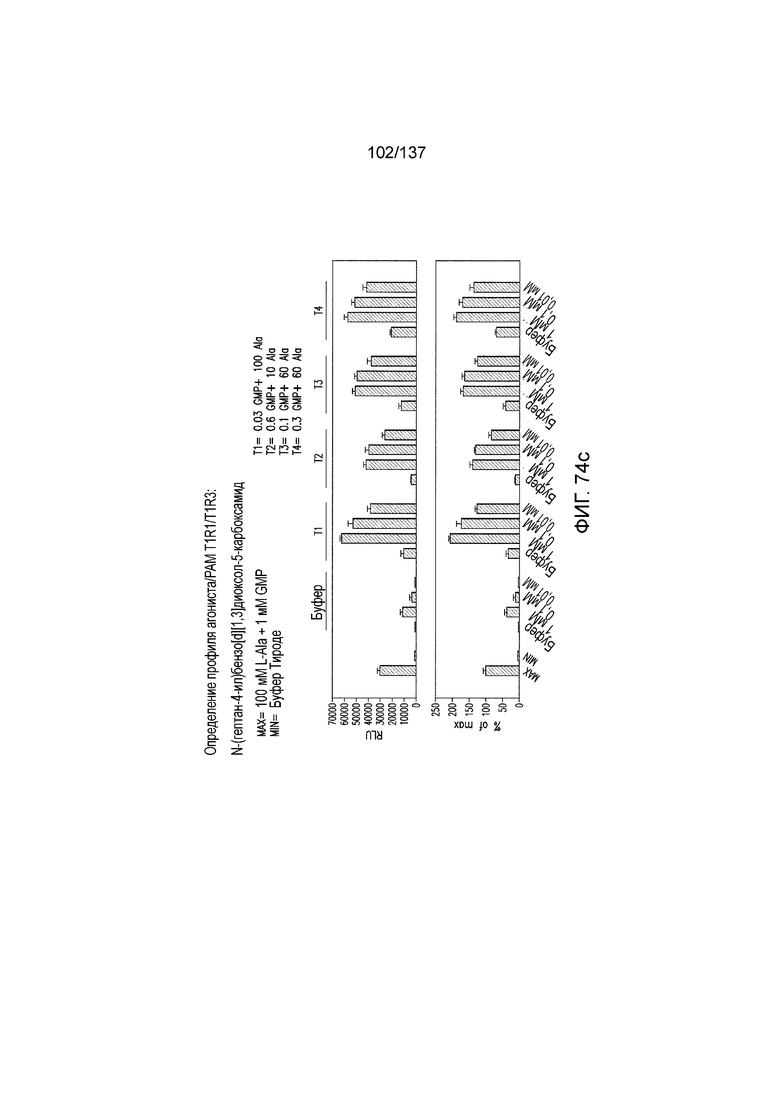


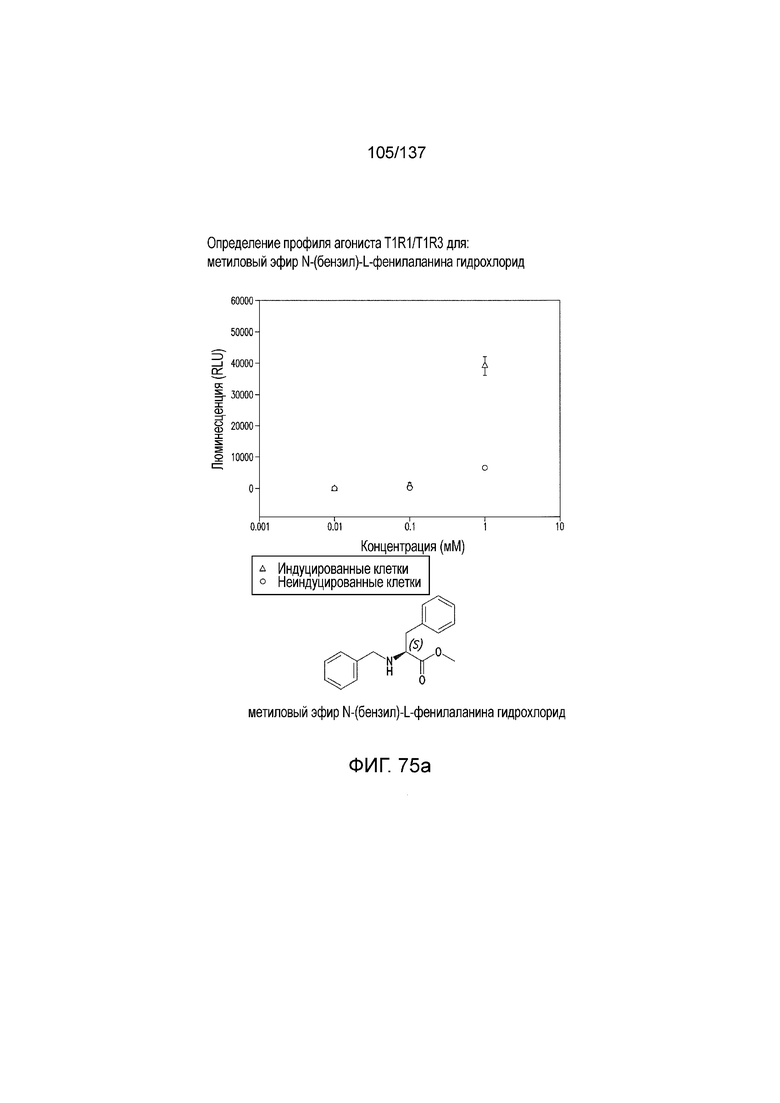
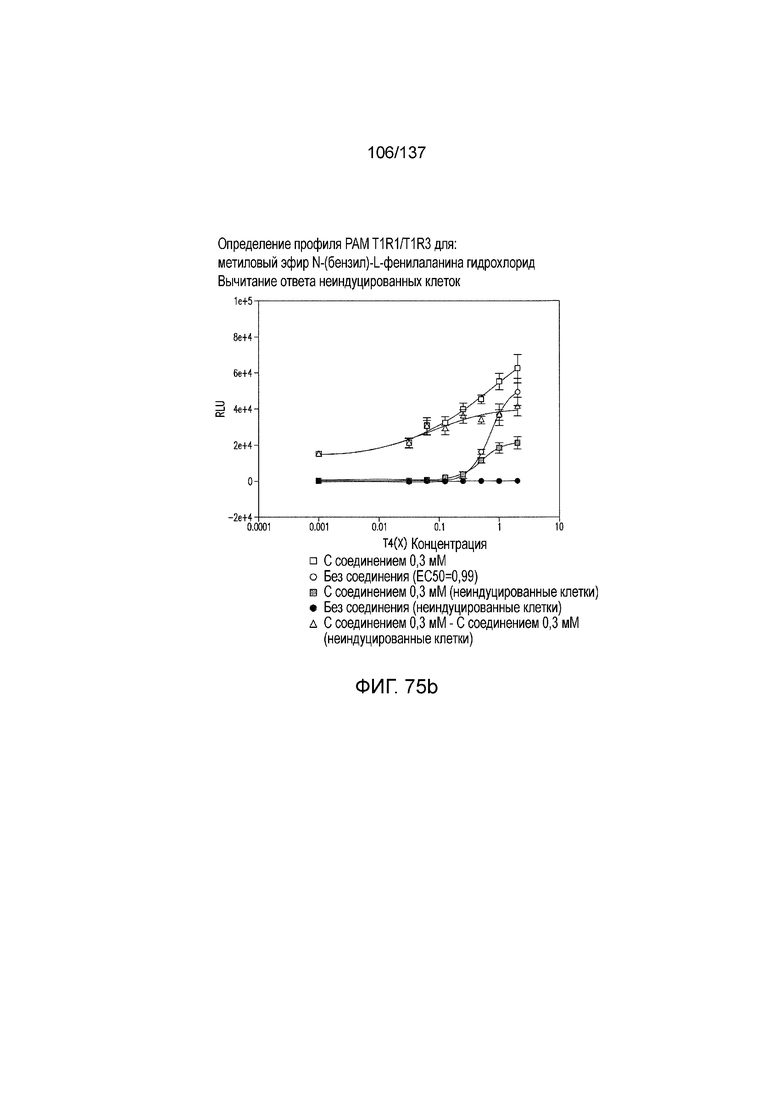
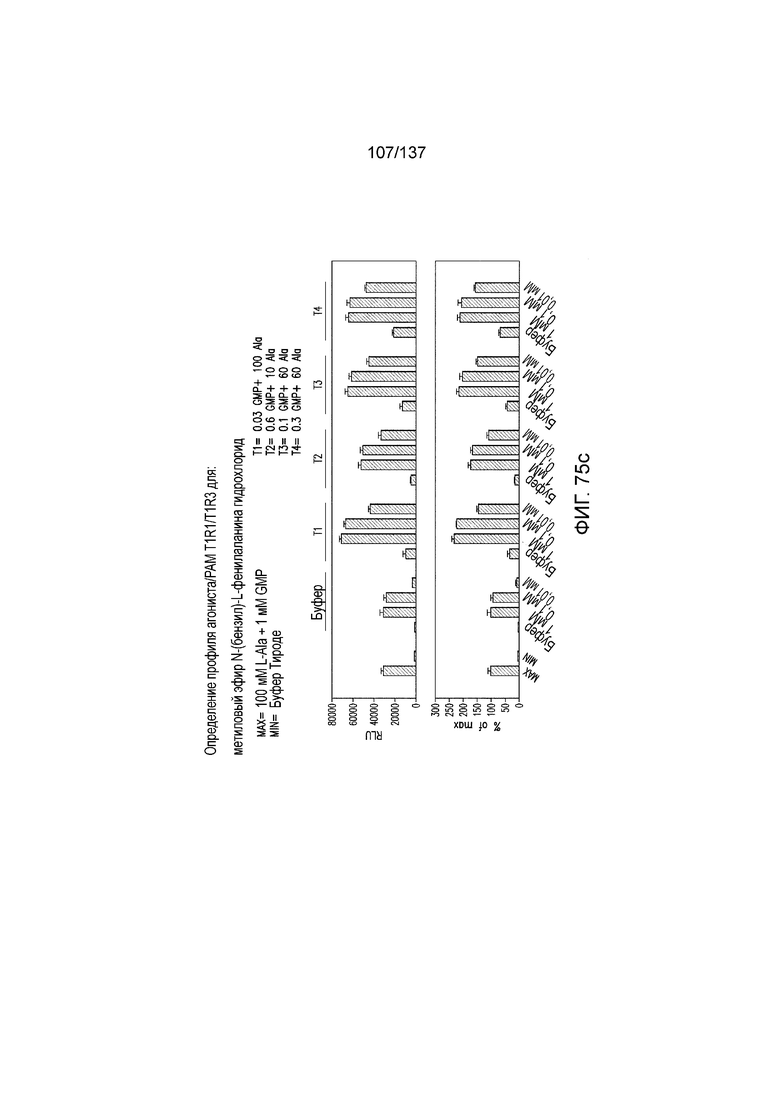
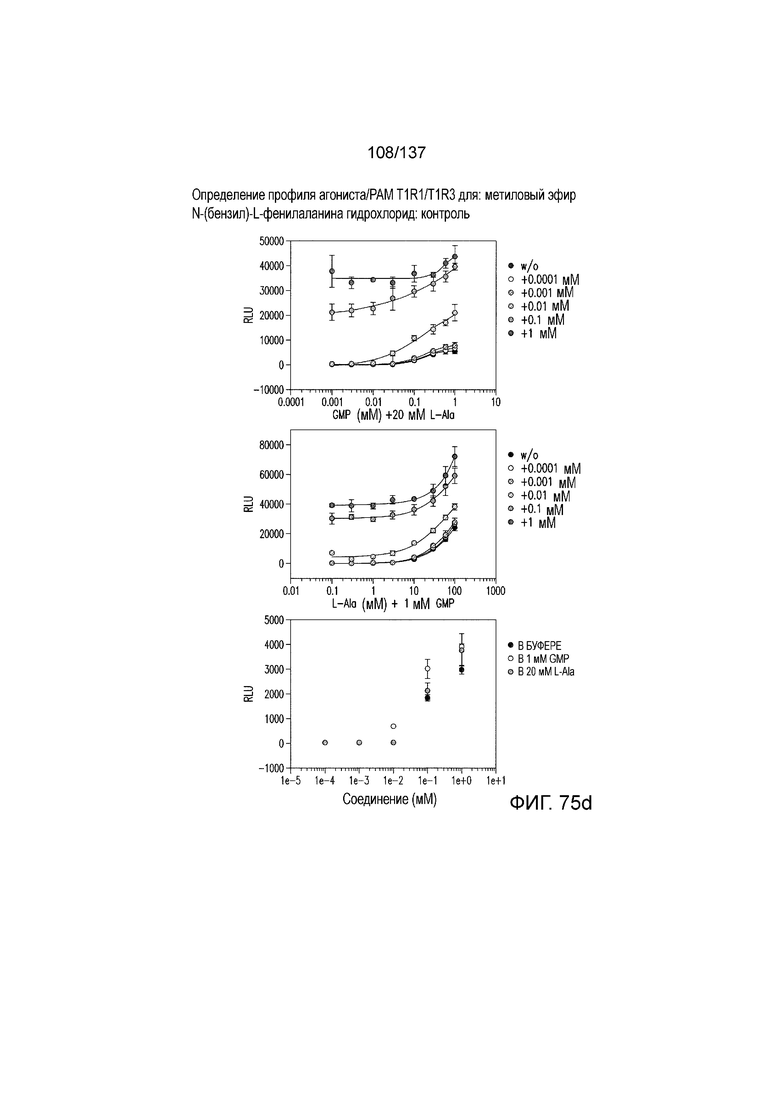

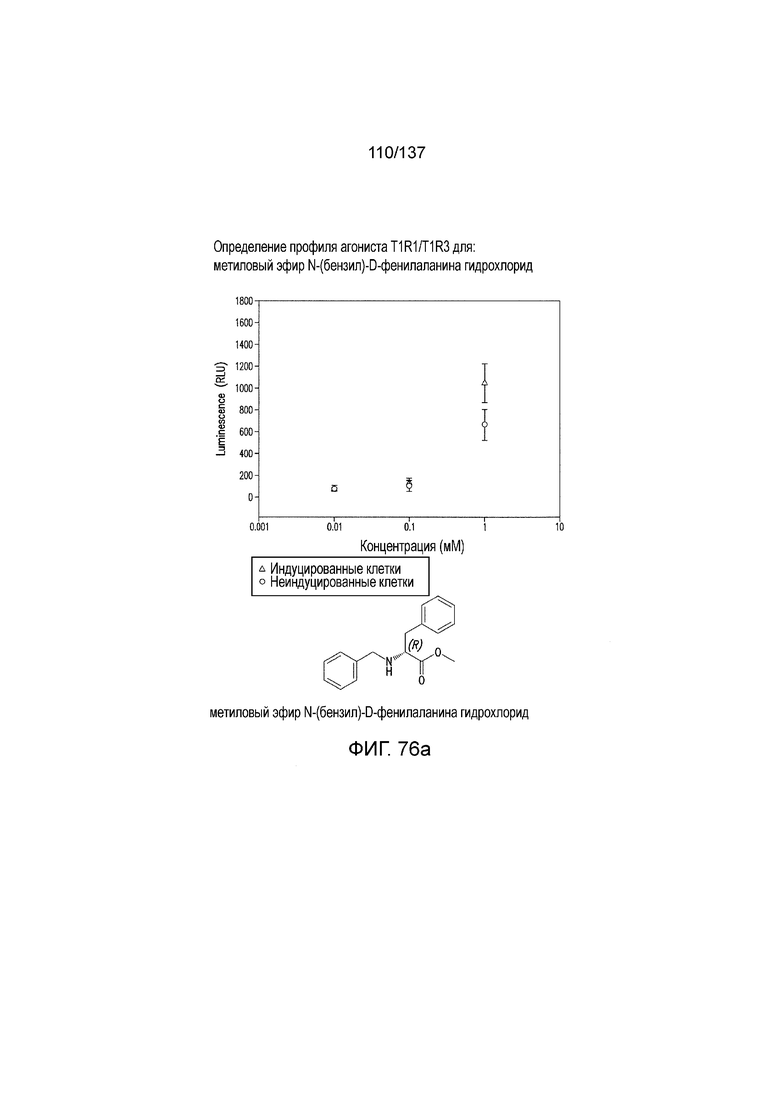
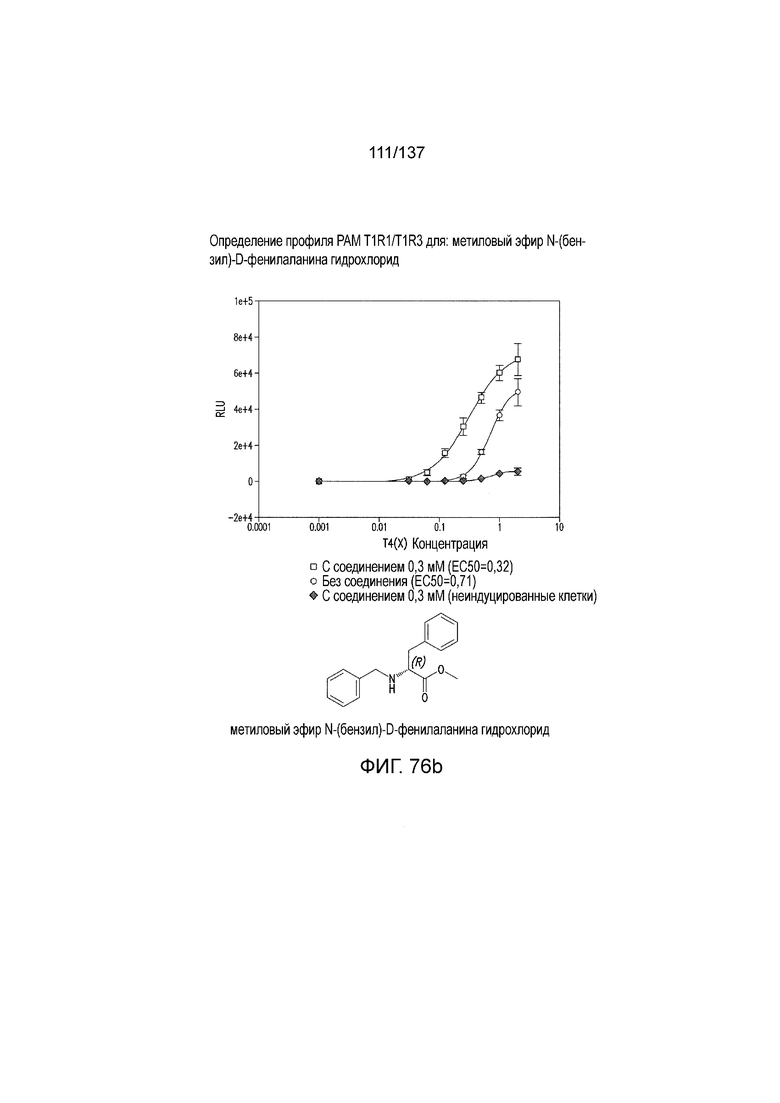
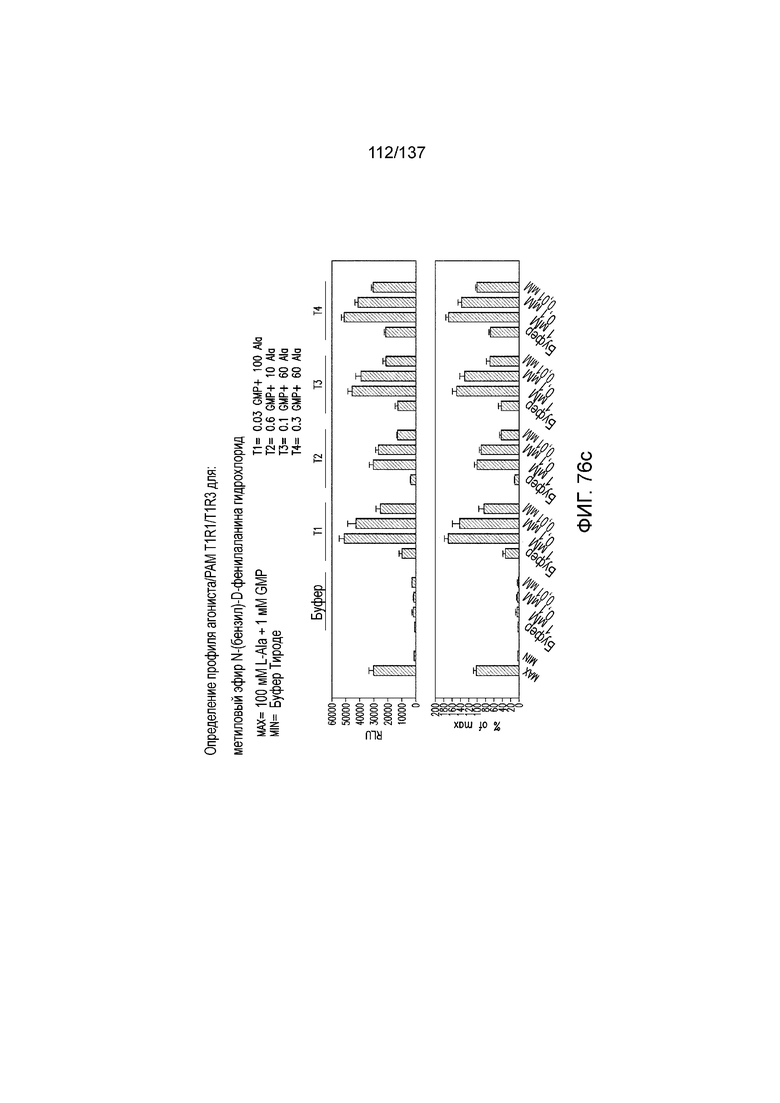
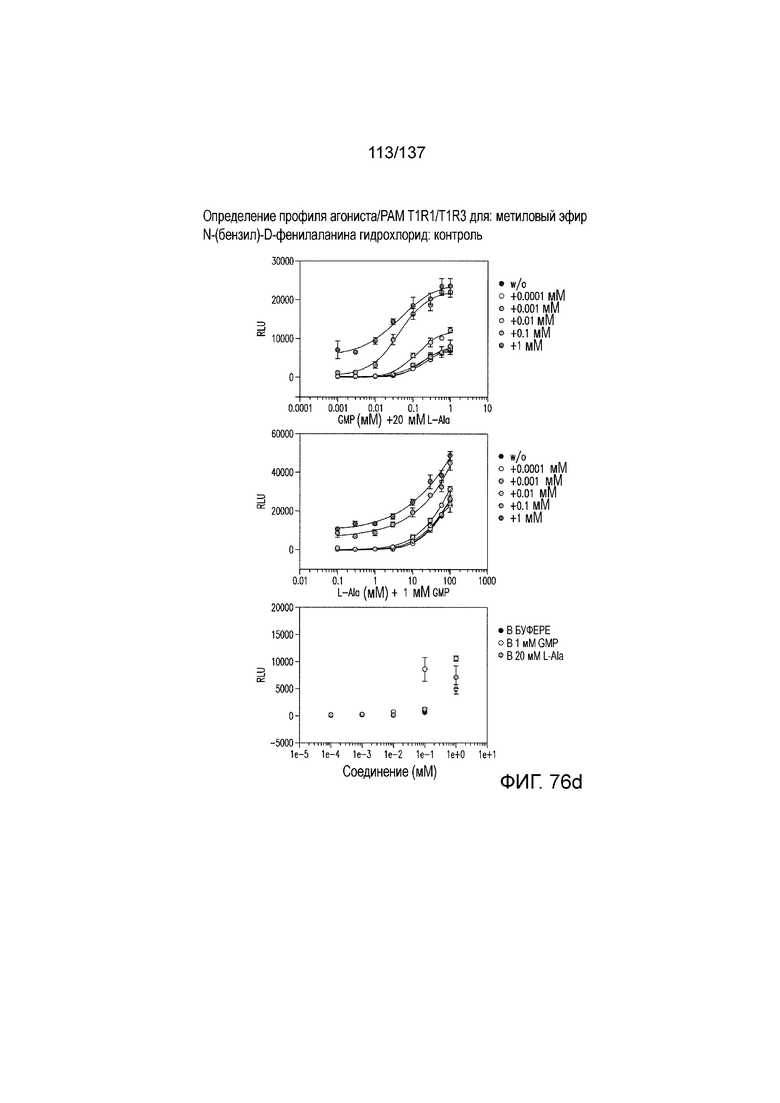

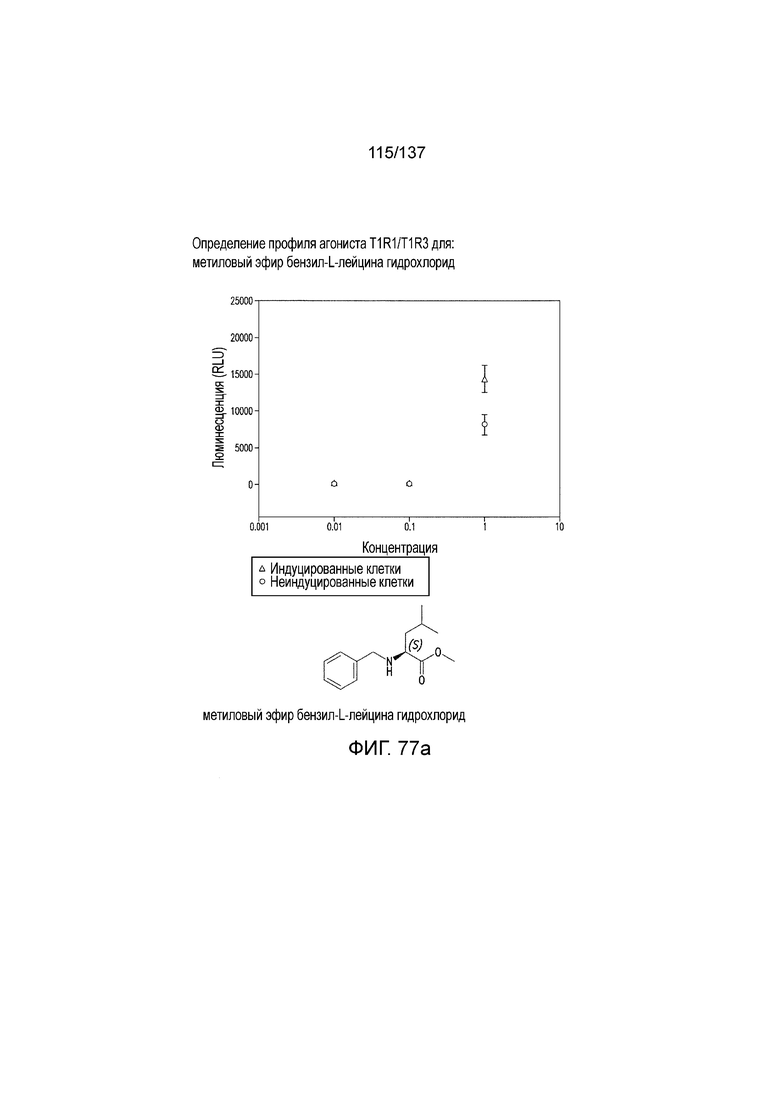
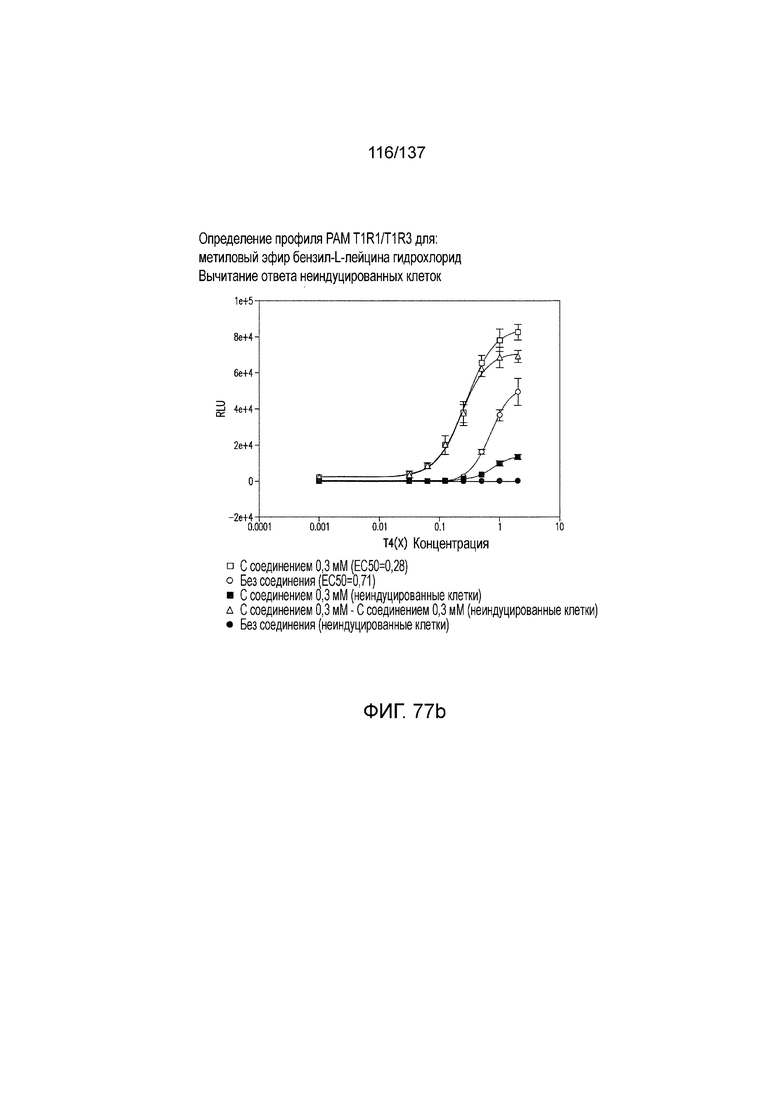
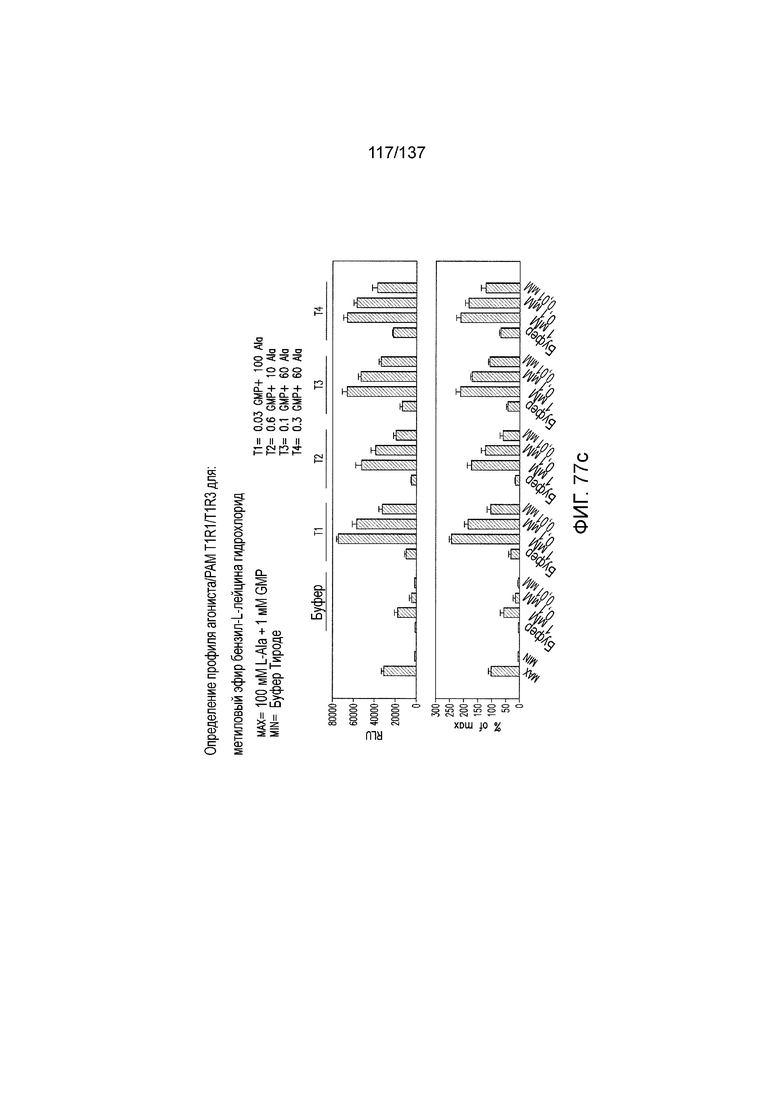
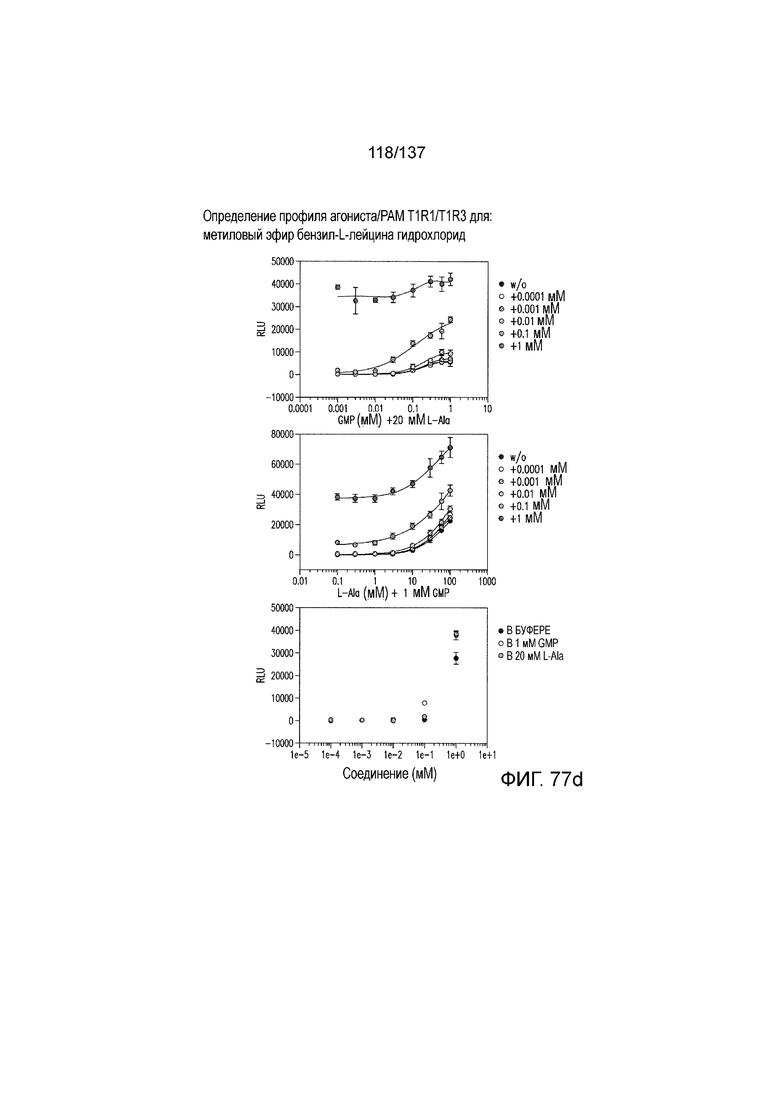
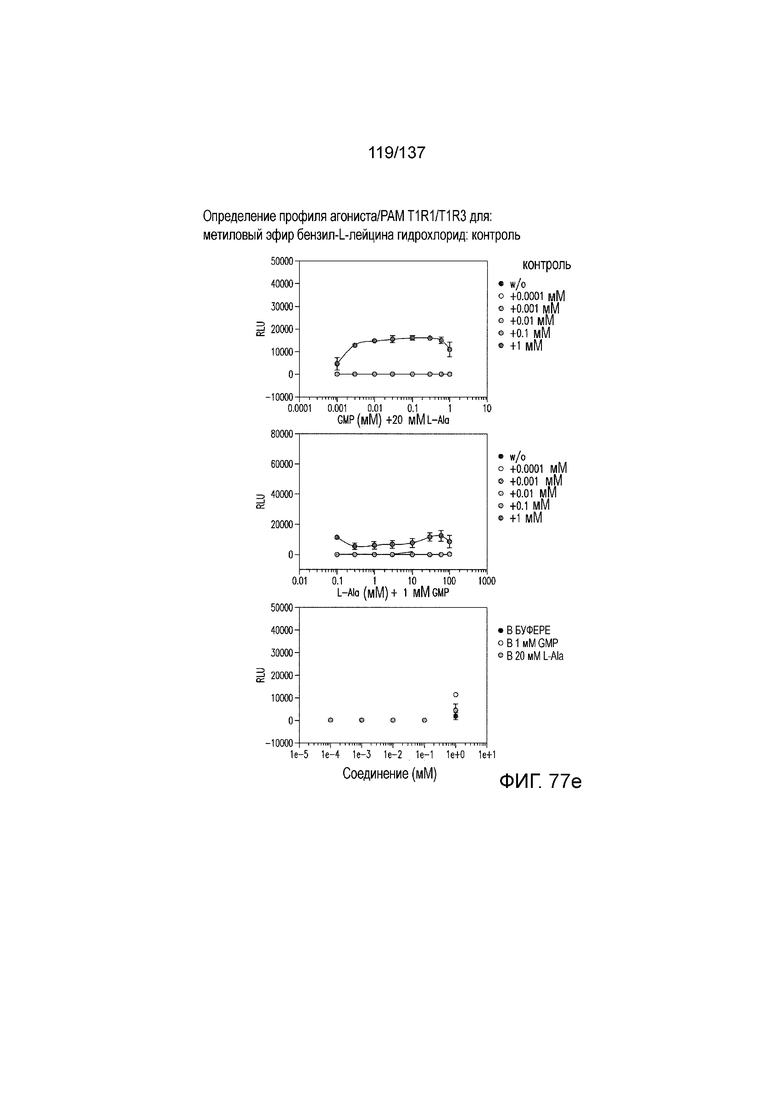
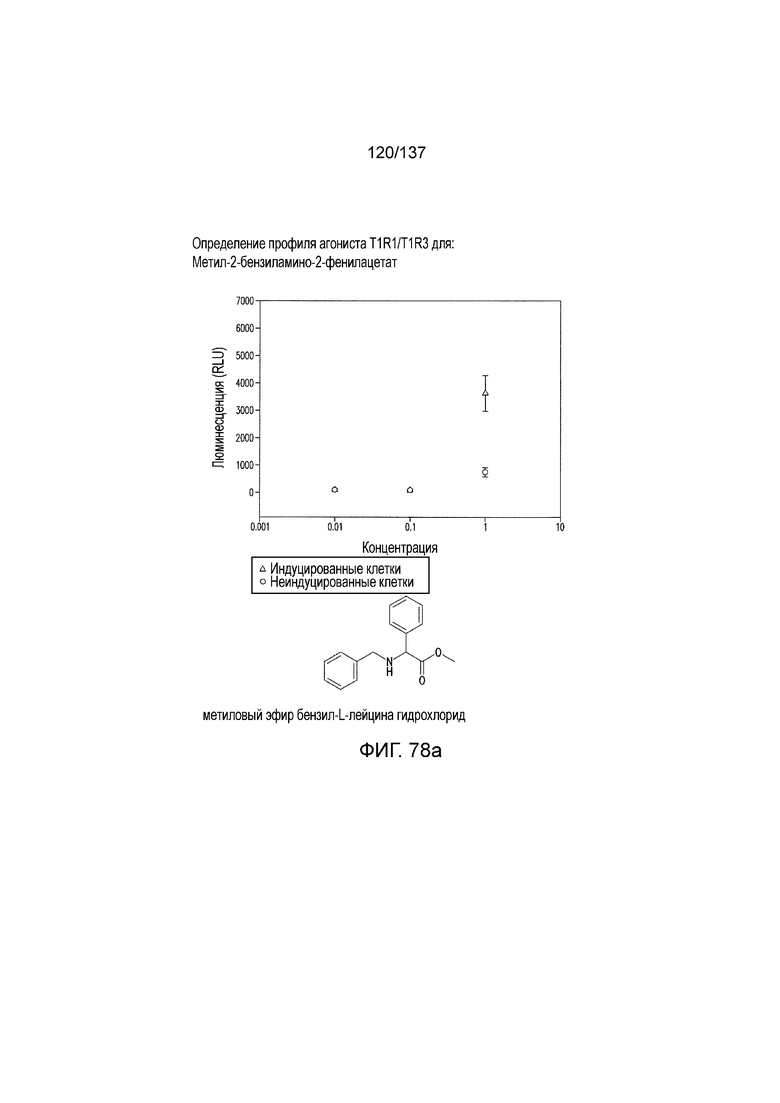
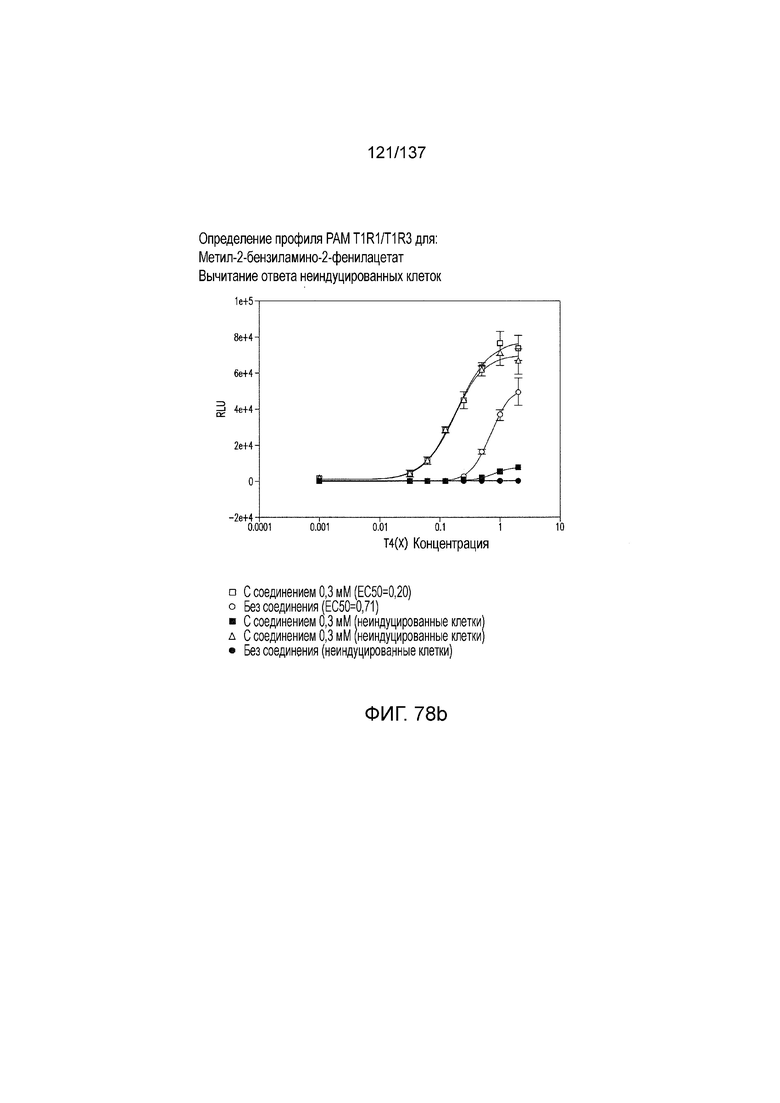
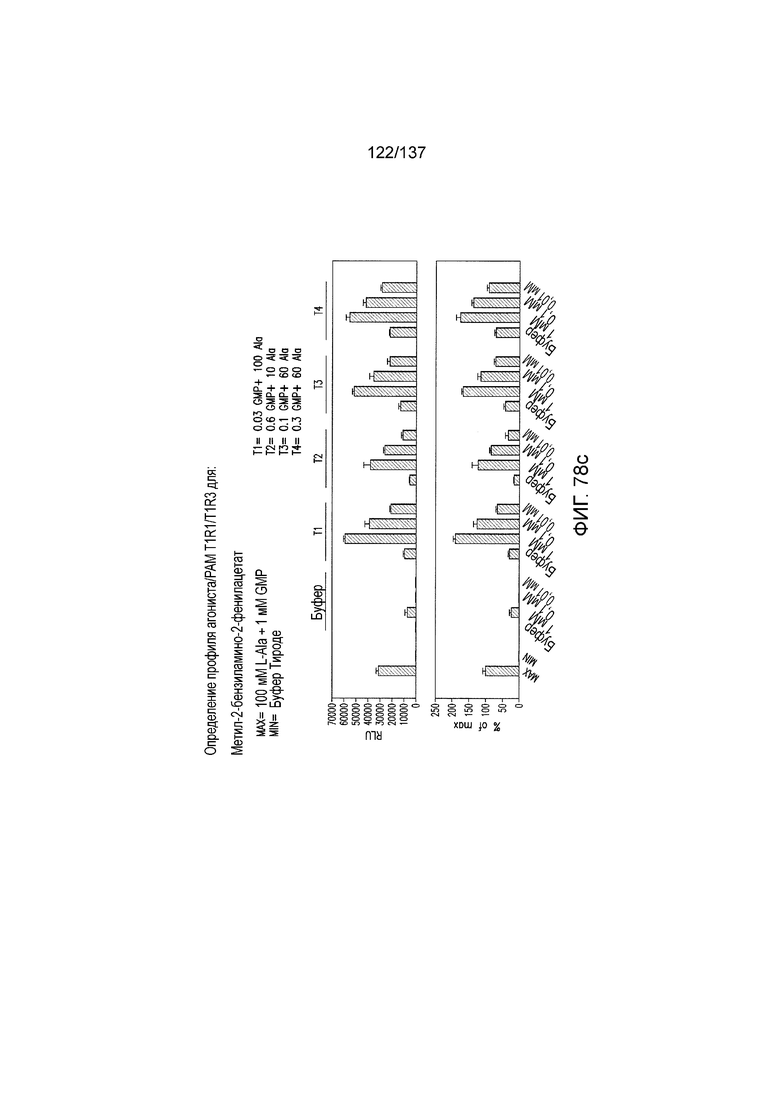
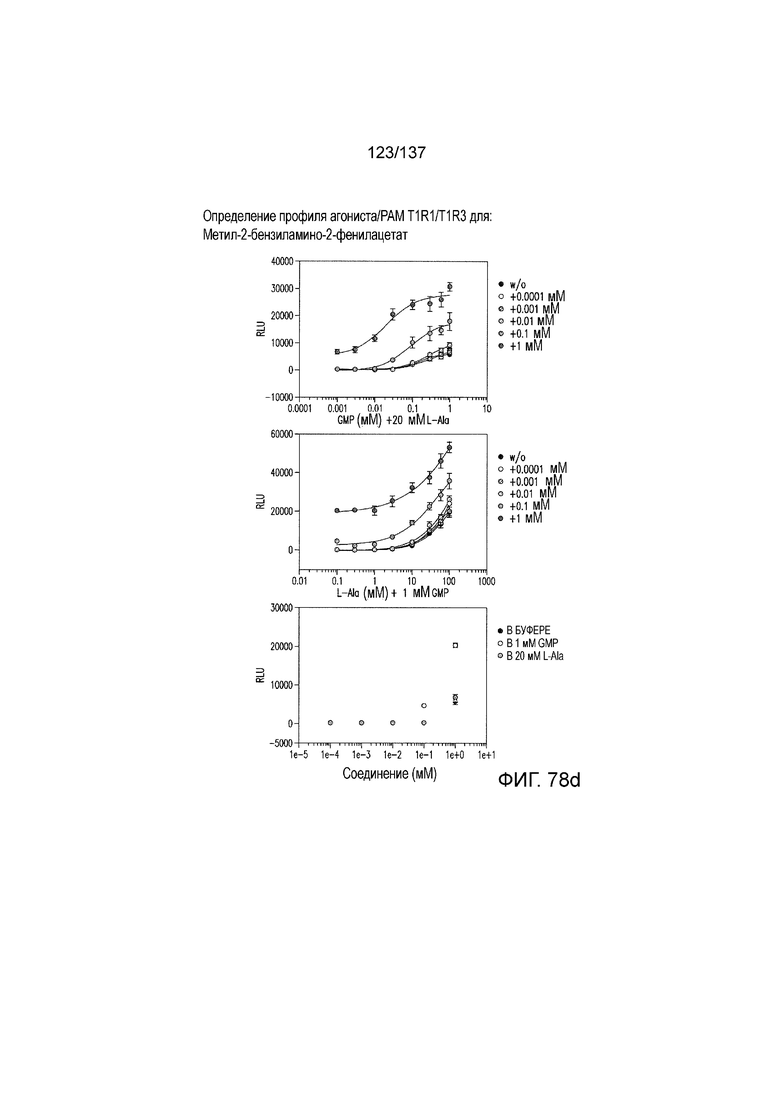

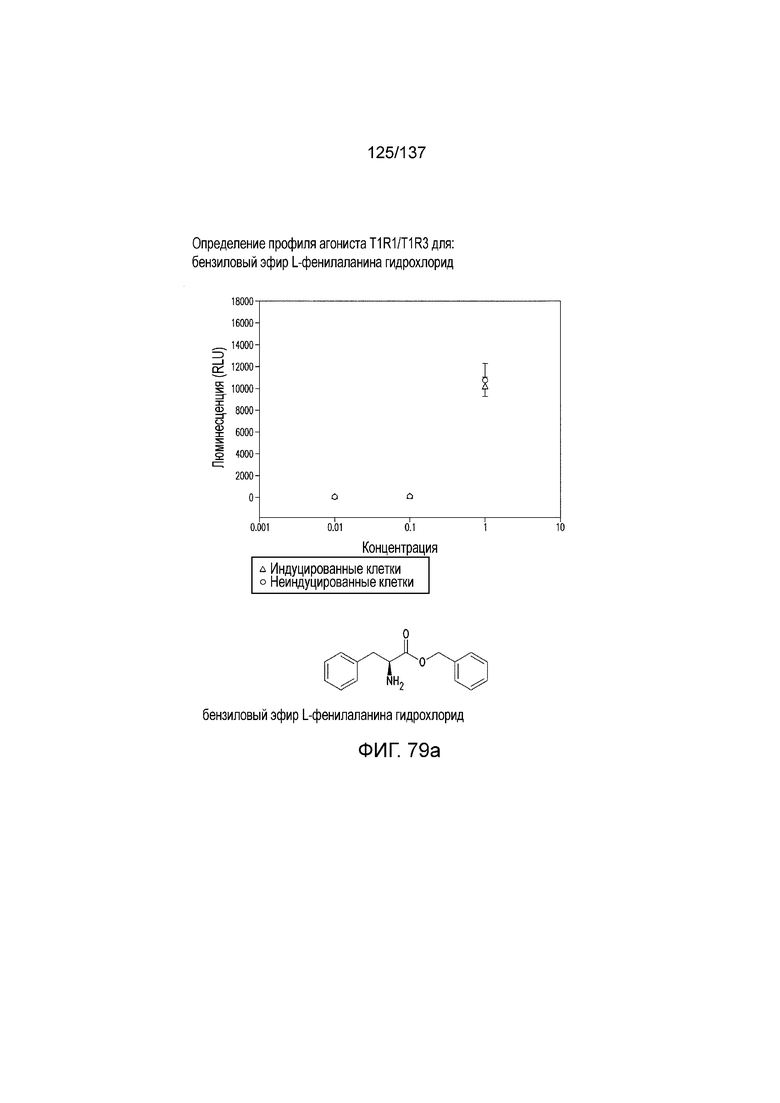
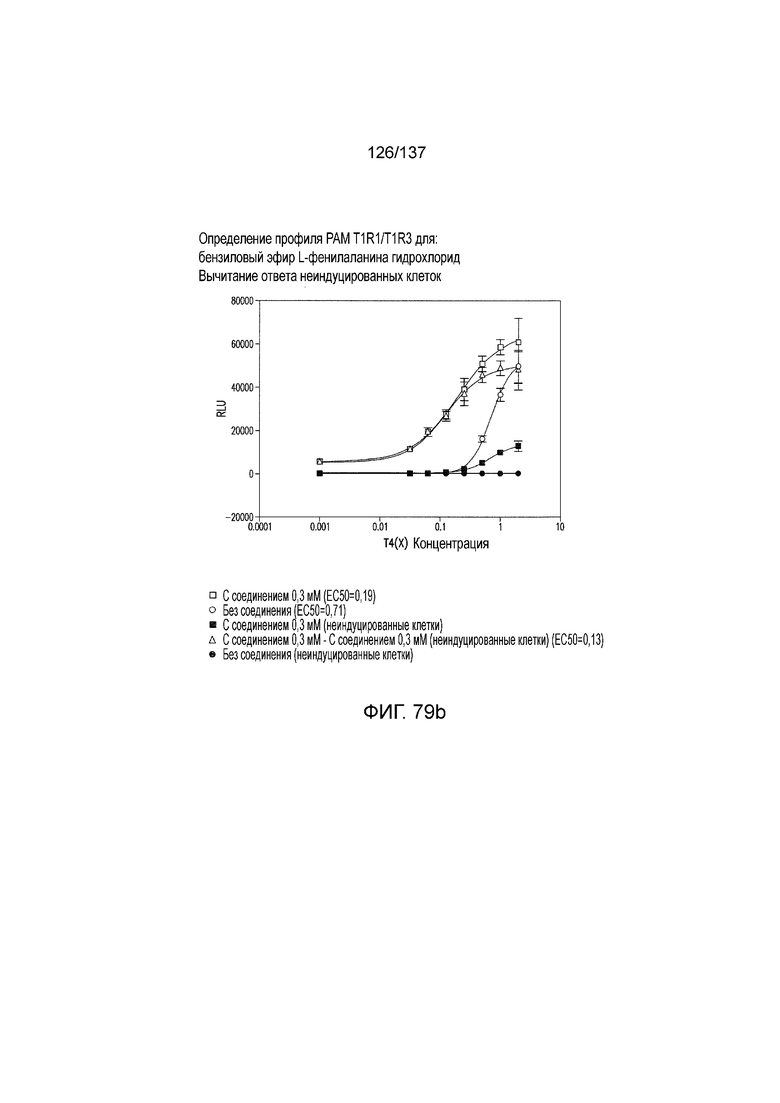
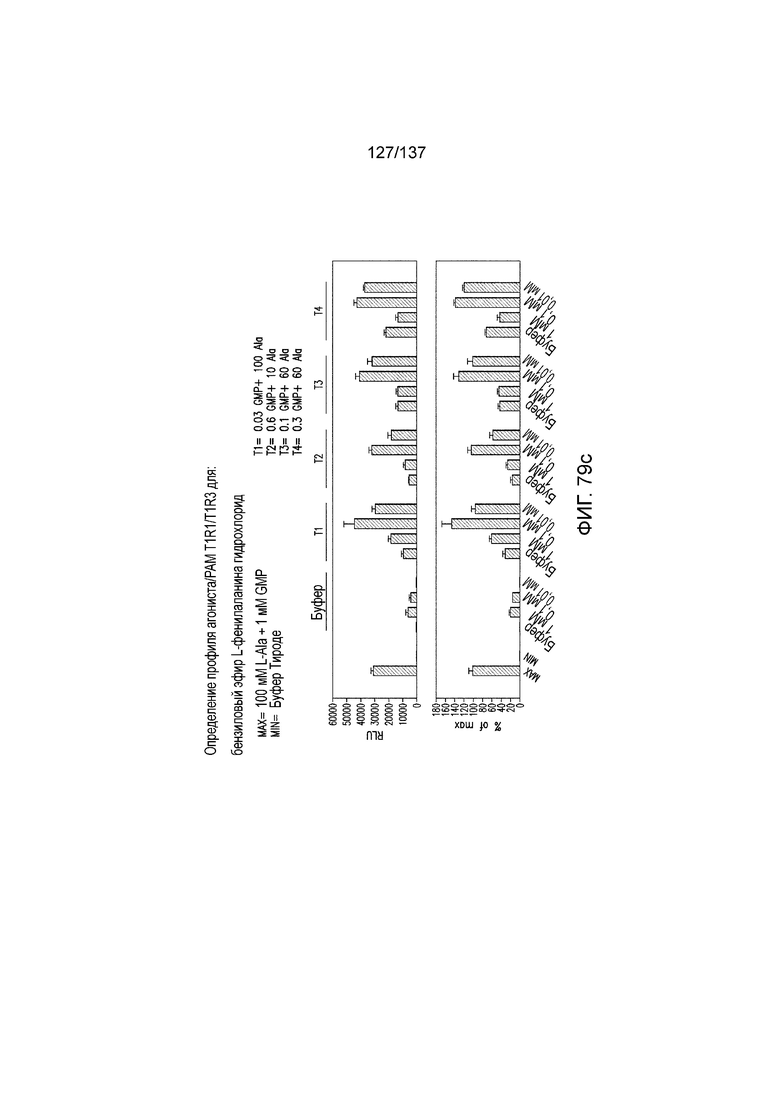
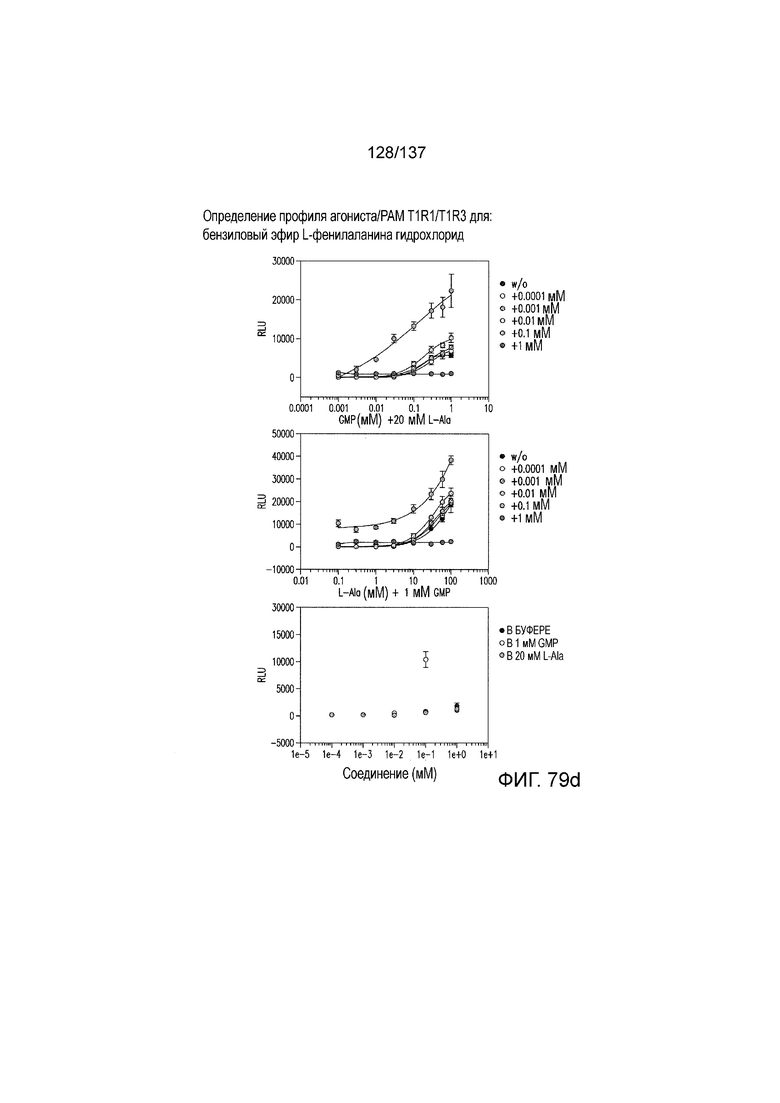
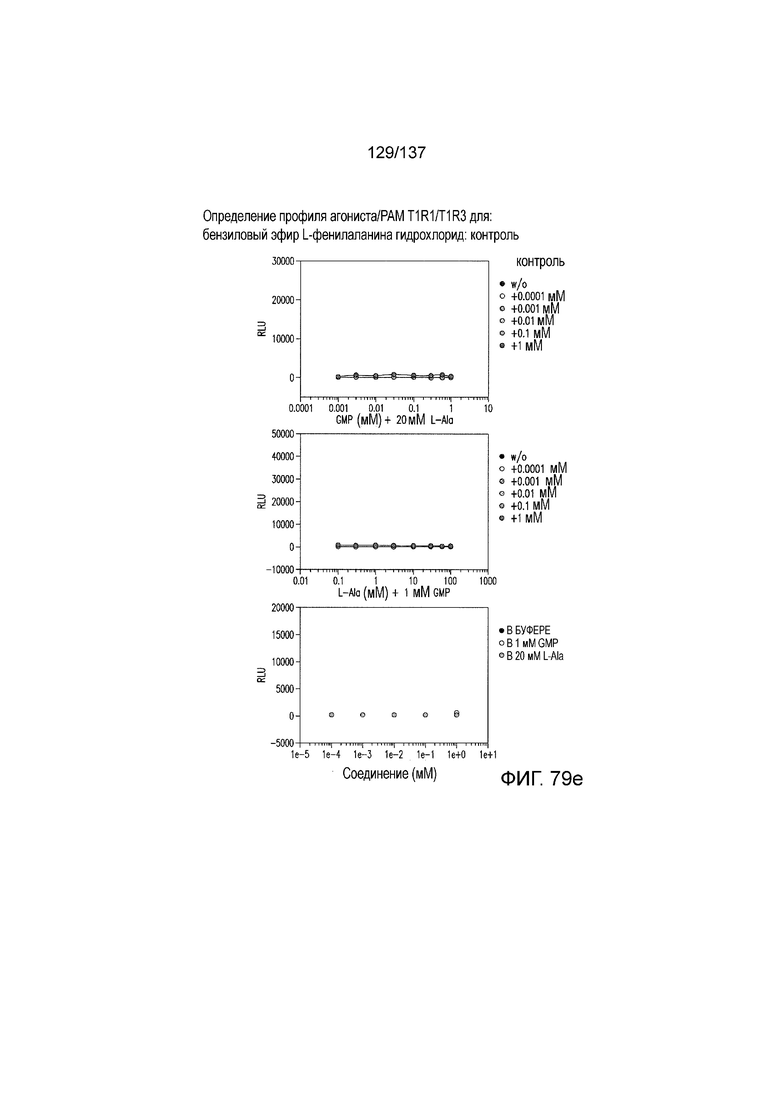
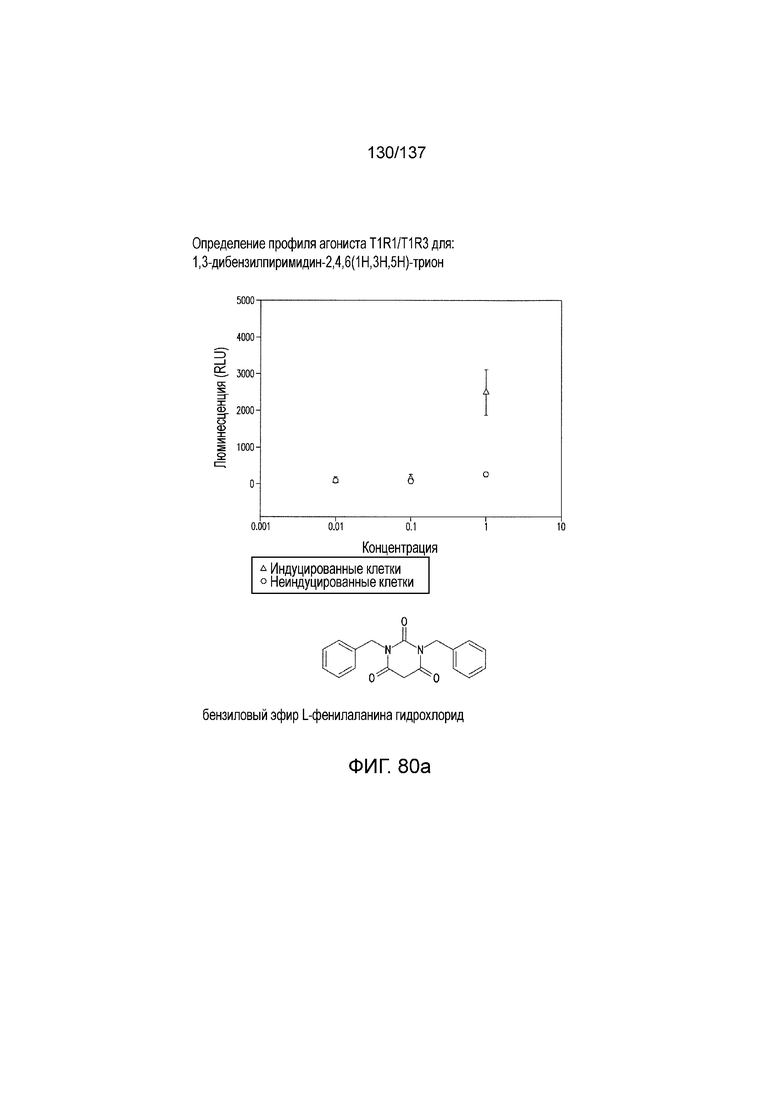
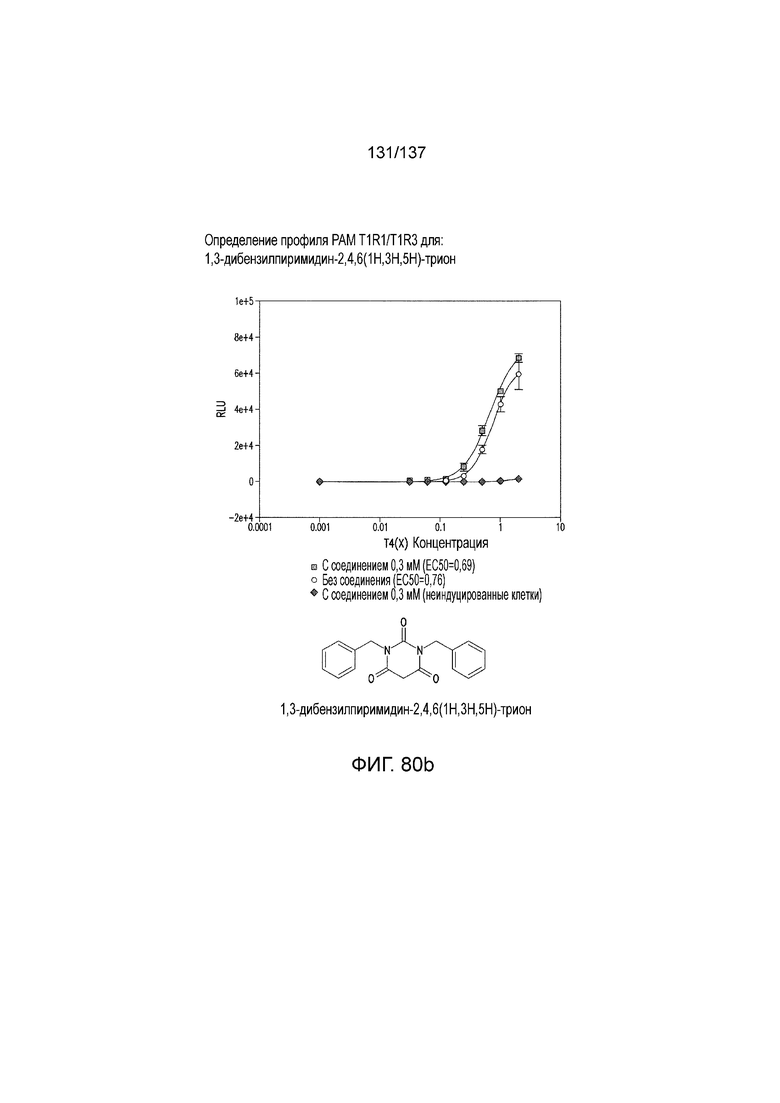






Изобретение относится к области биотехнологии, конкретно к композиции для усиления вкуса умами, и может быть использовано в пищевой промышленности. Изобретение позволяет получить вкусоароматическую композицию, содержащую по меньшей мере одно модифицированное нуклеотидное производное, которое усиливает активность группы рецепторов вкуса умами. Изобретение может быть применимо в качестве пищевой добавки для усиления вкуса и/или вкусовой привлекательности кормовых продуктов для домашних животных. 8 н. и 33 з.п. ф-лы, 27 табл., 9 пр., 84 ил.
1. Композиция для усиления вкуса умами в кормовых продуктах для домашних животных, включающая соединение формулы Nt-1, содержащее структуру
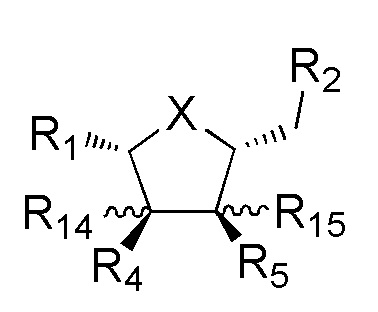 ,
,
где R1 выбран из группы, состоящей из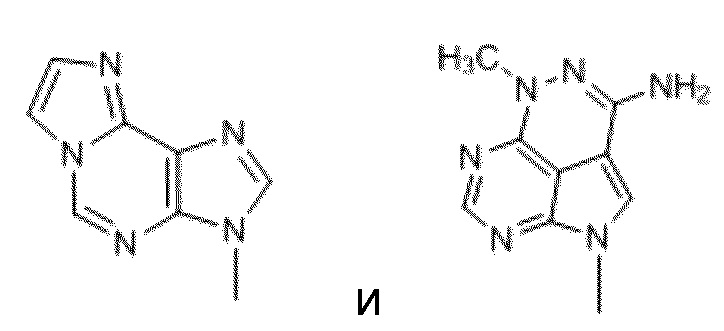 ;
;
где R2 выбран из монофосфата, дифосфата, трифосфата, OP(W)(OH)2, -OP(W)(OH)OP(W)(OH)2,
-OP(W)(OH)OP(W)(OH)OP(W)(OH)2,
-OS(O)2арил(H), -OS(O)2арил(CH3),
-P(W)(OH)2, -OP(W)(OH)OS(O)2(OH), -OP(W)(OH)Z,
-P(W)(OH)OP(W)(OH)2, -O(CH2)1-4OP(W)(OH)2, -OS(W)(OH)2, -OP(W)(OH) CH2OP(W)(OH)2, -OP(W)(OH)OP(W)O(CH2)1-4R18, -(CH2)0-4COOH, -(CH2)0-4S(O)(OH)2, -(CH2)0-4C(O)NHOH и -(CH2)0-4B(OH)2;
где Х выбран из O, S, N (R3) и CH2;
где W выбран из O и S;
где R3 выбран из H и CH3;
где R4, R5, R14, R15, R18 независимо выбраны из H, OH, SH, CH2, CH3, OR6, SR6, CH2CH3, разветвленного или неразветвленного низшего алкила (C1-C6), XC(O)низшего алкила, -XC(O)CH2Ph, -P(W)(OH)2,
-XC(O)PhR11, -OP(O)(OH)O, OCH3, N(R11,R17), -O(C)nR11, R17O-, N(H или независимо низший алкил)2-3 и COOR11, -OC(W)NH(CH2)1-6NH2,
-OC(W)NH(CH2)1-6R4,
где Z выбран из пиперидина, морфолина, пиперазина, N-метилпиперазина, N(R16)(R17); и
где R6, R11, R16 и R17 независимо выбраны из H, OH, SH, CH2, CH3, OCH3, COOR, N(R12)(R13), CH2CH3, разветвленного и неразветвленного низшего алкила (C1-C6), XC(O)низшего алкила, -XC(O)CH2Ph, -P(W)(OH)2, -XC(O)PhR12, -OP(O)(OH)O, OCH3, N(R12,R13), -O(C)nR12, R13O-, N(H или независимо низший алкил)2-3 и COOR12; и
где R12 и R13 независимо выбраны из H, OH, SH, CH2, CH3, OCH3 и CH2CH3.
2. Вкусоароматическая композиция по п.1, где соединение выбрано из группы, состоящей из:
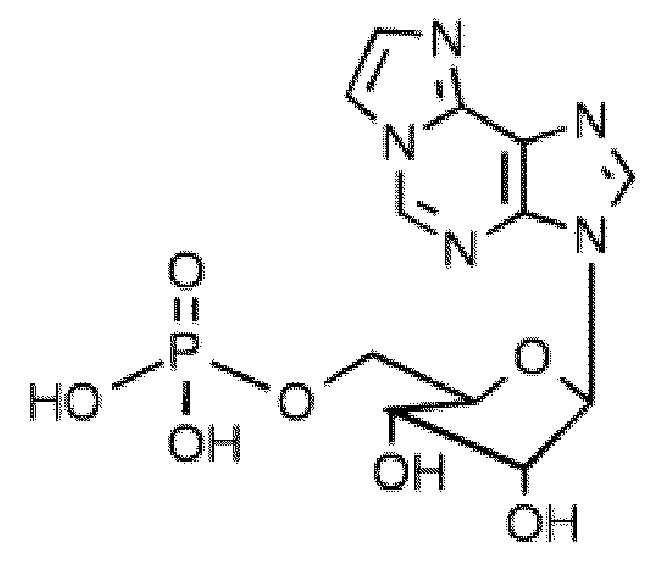 ,
,
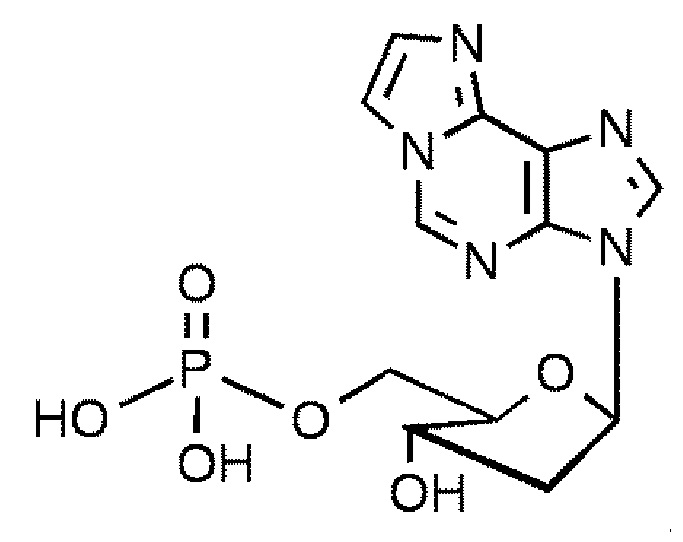
и их комбинации.
3. Композиция по п.1 или 2, дополнительно содержащая соединение, выбранное из группы, состоящей из:
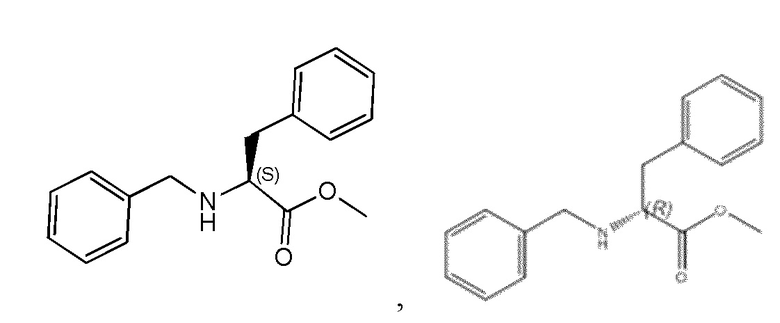
и их комбинации.
4. Композиция по п.1 или 2, дополнительно содержащая соединение, выбранное из группы, состоящей из:
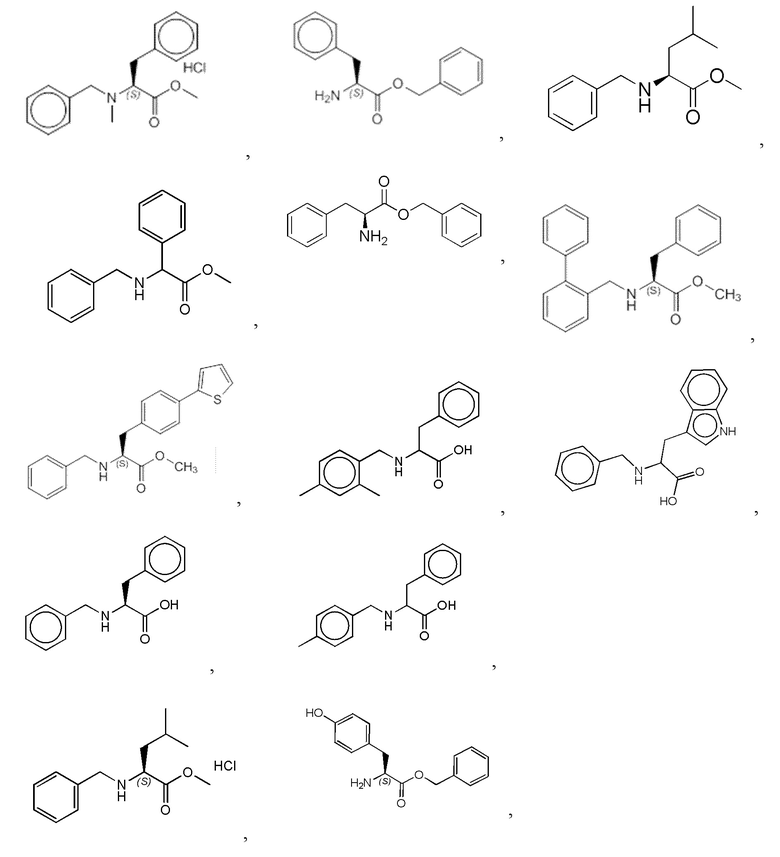
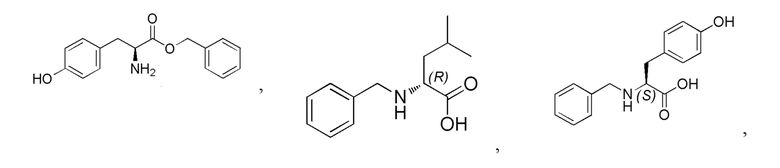
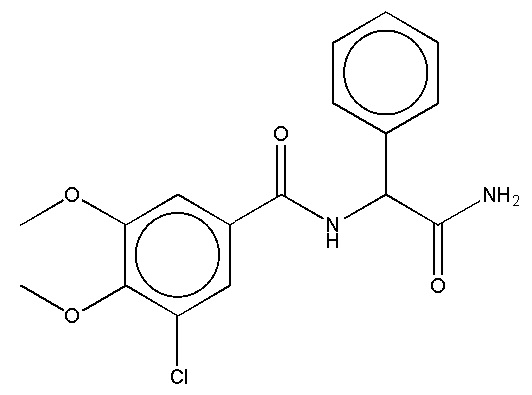
и их комбинаций.
5. Композиция по п.1 или 2, дополнительно содержащая соединение, имеющее структуру
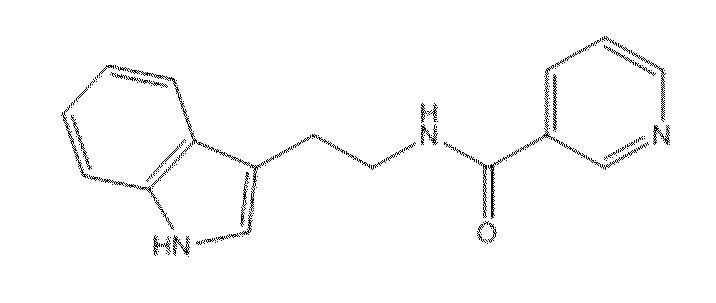 .
.
6. Композиция по п.1 или 2, дополнительно содержащая соединение, имеющее структуру
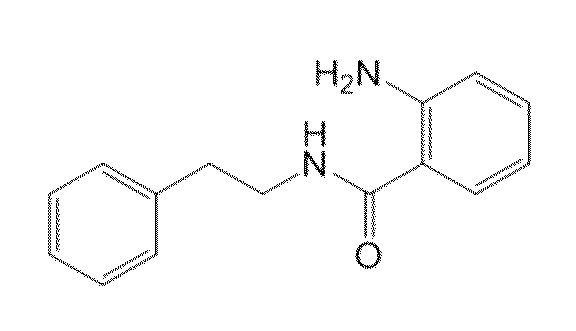 .
.
7. Композиция по п.1 или 2, дополнительно содержащая соединение, выбранное из группы, состоящей из:
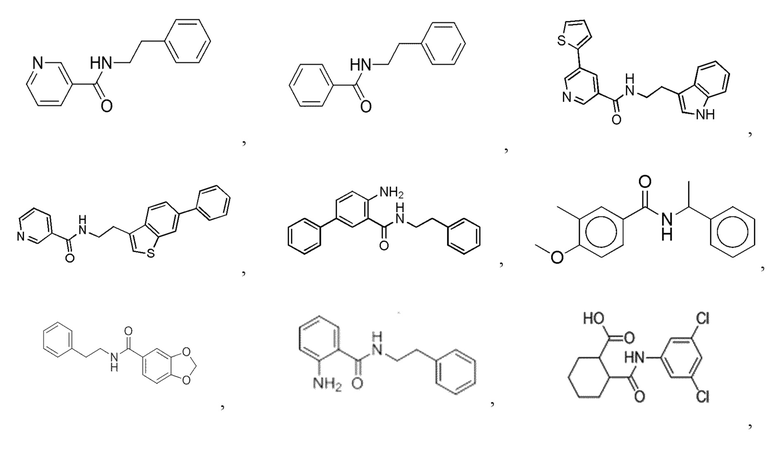
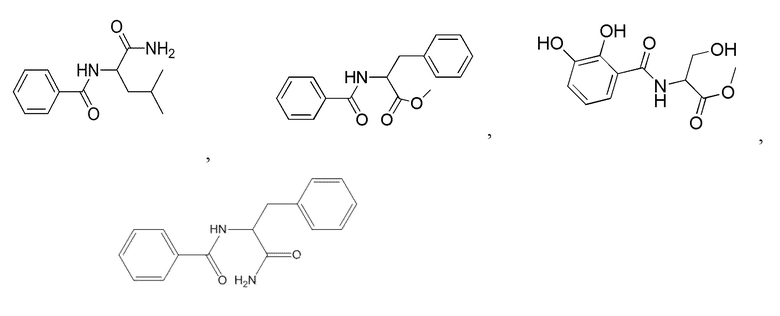
и их комбинаций.
8. Композиция по п.1 или 2, дополнительно содержащая соединение, имеющее структуру
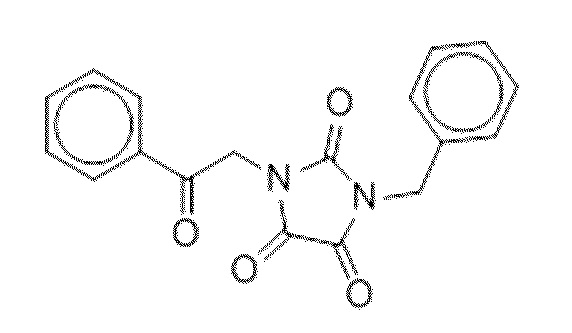 .
.
9. Композиция по п.1 или 2, дополнительно содержащая соединение, выбранное из группы, состоящей из:
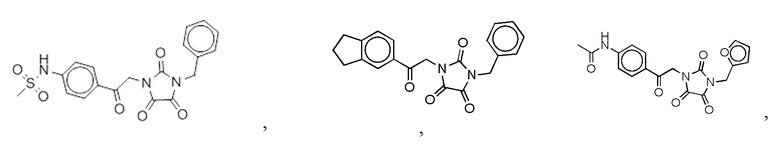
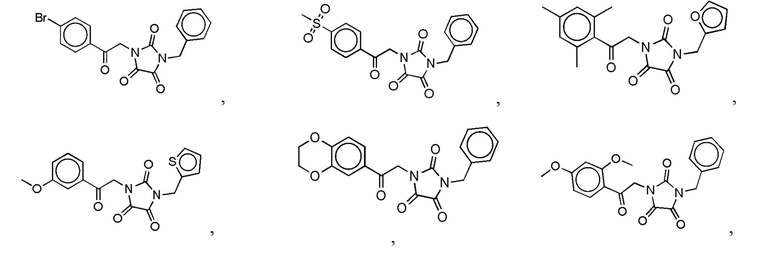
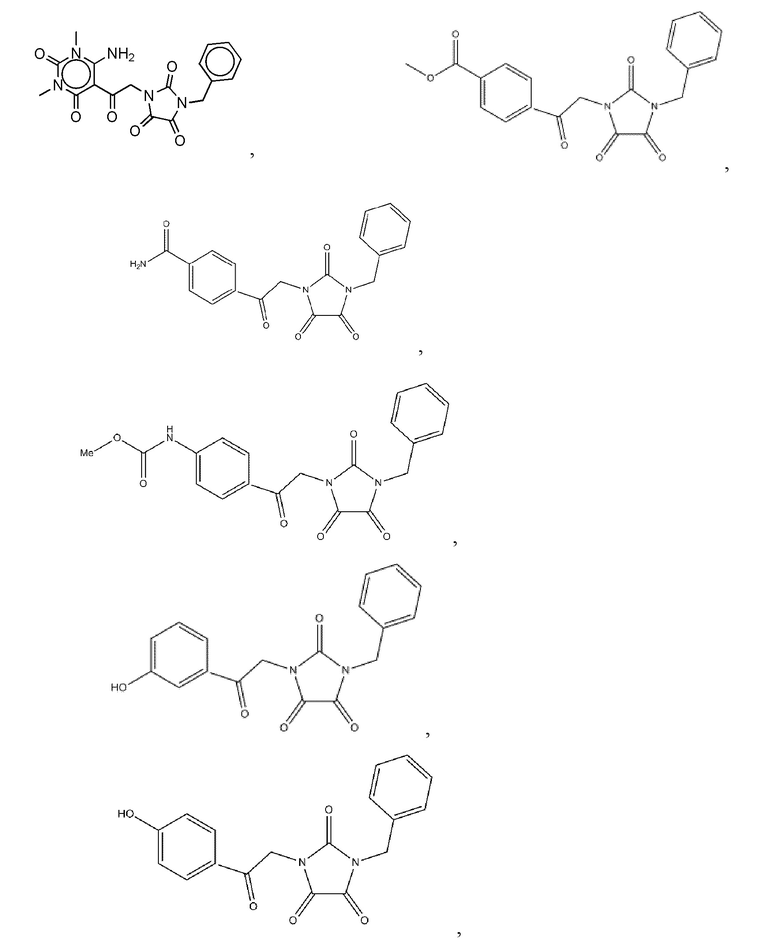
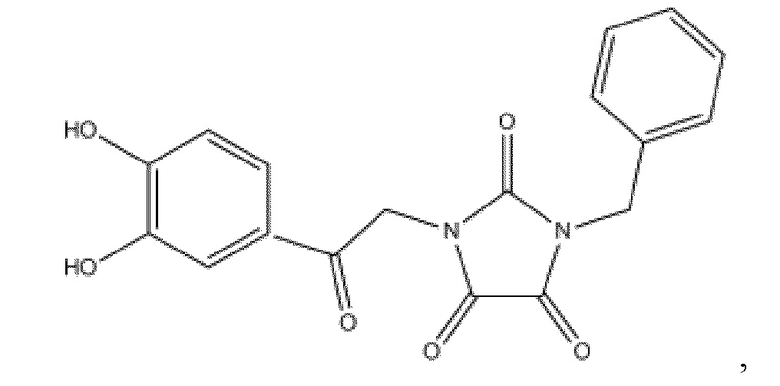
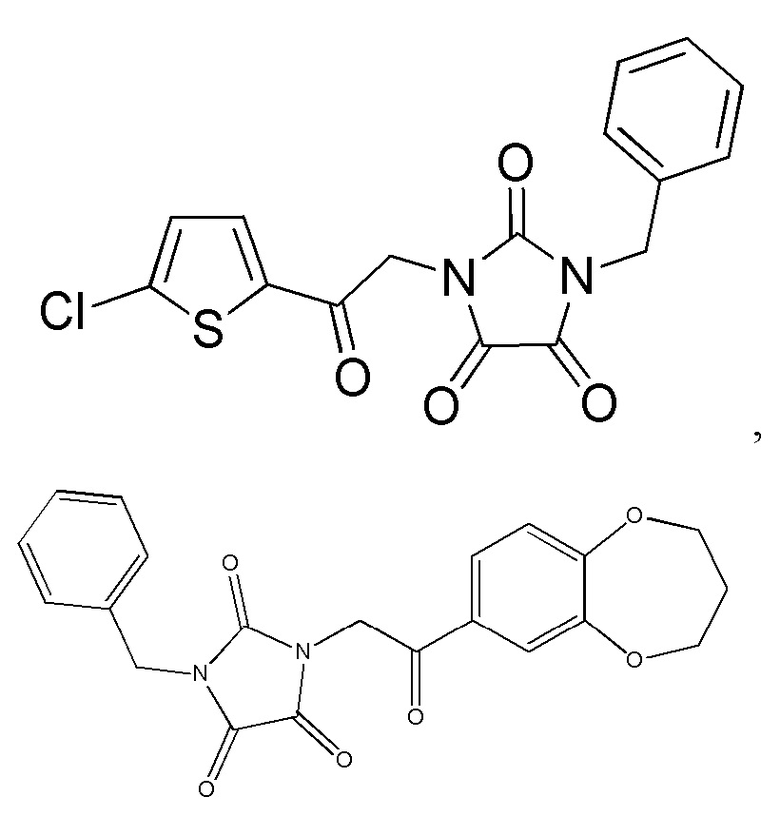
и их комбинаций.
10. Композиция по п.1 или 2, дополнительно содержащая соединение, имеющее структуру
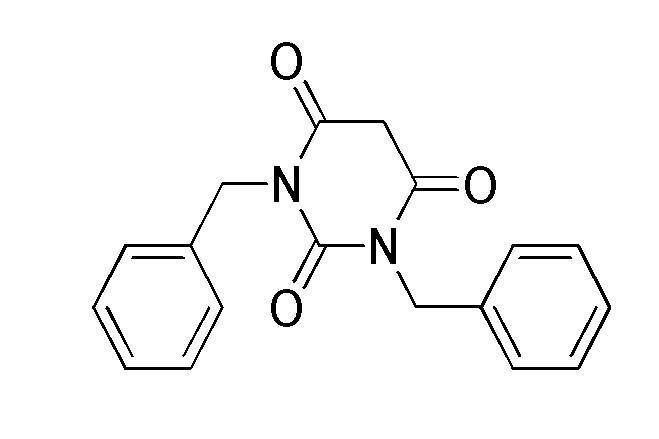 .
.
11. Композиция по п.1 или 2, дополнительно содержащая соединение, имеющее структуру
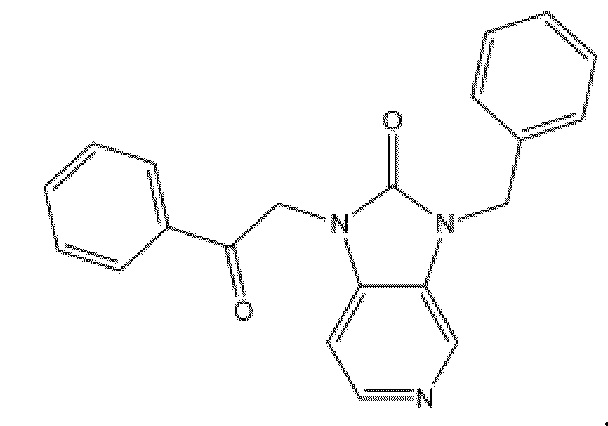
12. Композиция по п.1 или 2, дополнительно содержащая соединение, выбранное из группы, состоящей из:
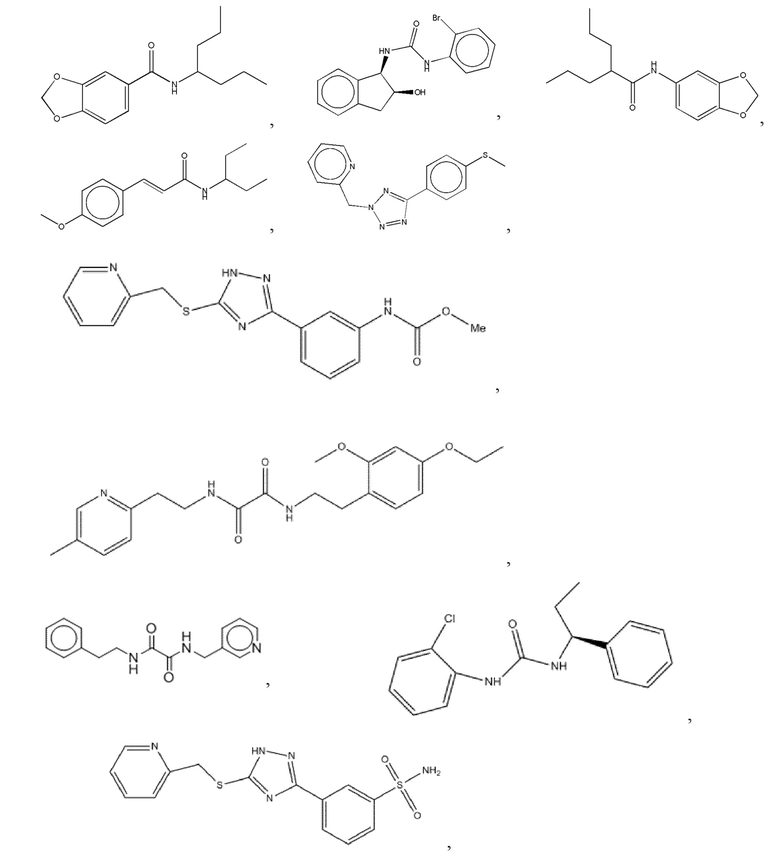
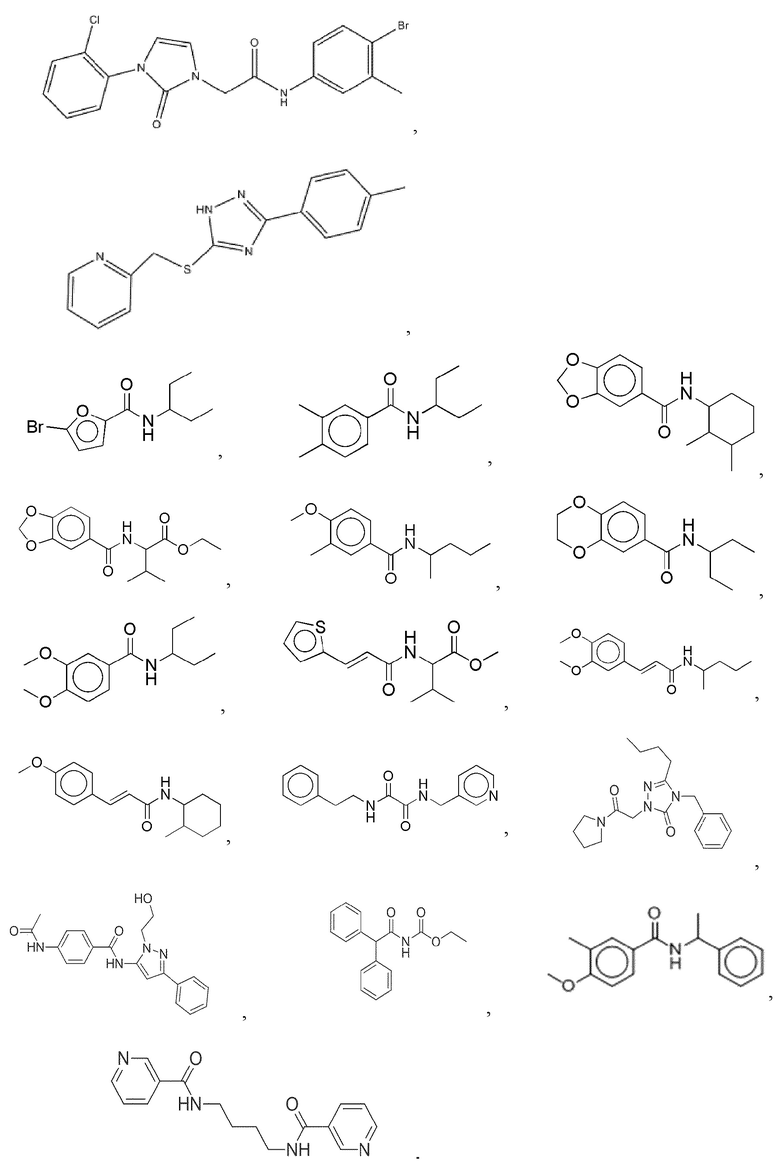
13. Композиция по любому из пп.1-12, дополнительно содержащая аминокислоту, выбранную из группы, состоящей из триптофана, фенилаланина, гистидина, глицина, цистеина, аланина, тирозина, серина, метионина, аспарагина, лейцина и их комбинаций.
14. Композиция по п.13, где аминокислота представляет собой аланин.
15. Композиция по любому из пп.1-14, дополнительно содержащая аминокислоту, выбранную из группы, состоящей из аспарагина, треонина, изолейцина, пролина, глутаминовой кислоты, аспарагиновой кислоты, гидроксипролина, аргинина, цистина, глутамина, лизина, валина, орнитина, глутамата мононатрия, таурина и их комбинаций.
16. Композиция по любому из пп.1-12, дополнительно содержащая первую аминокислоту по п.12 и вторую аминокислоту по п.14.
17. Композиция по любому из пп.1-16, дополнительно содержащая нуклеотид, выбранный из группы, состоящей из гуанозинмонофосфата (GMP), гуанозиндифосфата (GDP), гуанозинтрифосфата (GTP), аденозинмонофосфата (AMP), аденозиндифосфата (ADP), аденозинтрифосфата (ATP), цитидинмонофосфата (CMP), цитидиндифосфата (CDP), цитидинтрифосфата (CTP), инозинмонофосфата (IMP), инозиндифосфата (IDP), инозинтрифосфата (ITP), уридинмонофосфата (UMP), уридиндифосфата (UDP), уридинтрифосфата (UTP), тимидинмонофосфата (TMP), тимидиндифосфата (TDP), тимидинтрифосфата (TTP), ксантозинмонофосфата (XMP), ксантозиндифосфата (XDP), ксантозинтрифосфата (XTP) и их комбинаций.
18. Композиция по п.17, где нуклеотид выбран из группы, состоящей из гуанозинмонофосфата (GMP), инозинмонофосфата (IMP) и их комбинации.
19. Композиция по любому из пп.1-12, дополнительно содержащая аланин и гуанозинмонофосфат (GMP).
20. Композиция по любому из пп.1-12, дополнительно содержащая глицин и гуанозинмонофосфат (GMP).
21. Композиция по любому из пп.1-12, дополнительно содержащая гистидин и гуанозинмонофосфат (GMP).
22. Композиция по любому из пп.1-12, дополнительно содержащая аланин и инозинмонофосфат (IMP).
23. Композиция по любому из пп.1-12, дополнительно содержащая глицин и инозинмонофосфат (IMP).
24. Композиция по любому из пп.1-12, дополнительно содержащая гистидин и инозинмонофосфат (IMP).
25. Композиция по любому из пп.1-12, дополнительно содержащая пролин и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
26. Композиция по любому из пп.1-12, дополнительно содержащая треонин и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
27. Композиция по любому из пп.1-12, дополнительно содержащая глутаминовую кислоту и аминокислоту, выбранную из группы, состоящей из гистидина, аланина, глицина, фенилаланина, триптофана и тирозина.
28. Кормовой продукт для домашних животных, содержащий композицию по любому из пп.1-27, где композиция присутствует в концентрации примерно от 0,0001 до примерно 10 мас.% к общей массе кормового продукта.
29. Кормовой продукт для домашних животных, содержащий композицию по любому из пп.1-27, где композиция присутствует в концентрации примерно от 0,001 до примерно 1000 ppm к общей массе кормового продукта.
30. Кормовой продукт для домашних животных, содержащий композицию по любому из пп.1-27, где композиция присутствует в концентрации примерно от 1 мкМ до примерно 1 М к общей массе кормового продукта.
31. Кормовой продукт для домашних животных, содержащий композицию по любому из пп.1-27, где композиция присутствует в количестве, эффективном для повышения вкусовой привлекательности кормового продукта, как определяется панелью дегустаторов вкуса.
32. Кормовой продукт по любому из пп.28-31, где кормовой продукт для домашних животных представляет кормовой продукт для домашних кошек.
33. Кормовой продукт по п.32, где кормовой продукт для домашних кошек представляет влажный кормовой продукт для домашних кошек.
34. Кормовой продукт по п.32, где кормовой продукт для домашних кошек представляет сухой кормовой продукт для домашних кошек.
35. Кормовой продукт по любому из пп.28-31, где кормовой продукт для домашних животных представляет кормовой продукт для домашних собак.
36. Кормовой продукт по п.35, где кормовой продукт для домашних животных представляет влажный кормовой продукт для домашних собак.
37. Кормовой продукт по п.35, где кормовой продукт для домашних животных представляет сухой кормовой продукт для домашних собак.
38. Способ усиления интенсивности вкуса умами в кормовом продукте для домашних животных, включающий смешивание кормового продукта с композицией по любому из пп.1-27, где композиция присутствует в концентрации примерно от 0,0001 до примерно 10 мас.% к общей массе смеси.
39. Способ усиления интенсивности вкуса умами в кормовом продукте для домашних животных, включающий смешивание кормового продукта с композицией по любому из пп.1-27, где композиция присутствует в концентрации примерно от 0,001 до примерно 1000 ppm к общей массе смеси.
40. Способ усиления интенсивности вкуса умами в кормовом продукте для домашних животных, включающий смешивание кормового продукта с композицией по любому из пп.1-27, где композиция присутствует в концентрации примерно от 1 мкМ до примерно 1 М к общей массе смеси.
41. Способ по любому из пп.38-40, где усиление интенсивности вкуса умами включает усиление послевкусия умами.
| US 4826824 A1, 02.05.1989 | |||
| WO 2014068044 A1, 08.05.2014 | |||
| WO 2014068045 A1, 08.05.2014 | |||
| КОЛЕСО ТУРБОПРИВОДА | 1988 |
|
RU2042043C1 |
| TODA Y | |||
| et al., Two distinct determinants of ligand specificity in T1R1/T1R3 (the umami taste receptor), J.BIO.CHEM., 2013, v | |||
| ДВОЙНОЙ ГАЕЧНЫЙ КЛЮЧ | 1920 |
|
SU288A1 |
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Прибор для сигнализации о появлении вредных газов с применением электрической цепи со звонком | 1931 |
|
SU36863A1 |
| WO 2014068043 A1, 08.05.2014 | |||
| YOSHII K | |||
| et al., Synergistic effects of | |||
Авторы
Даты
2020-07-22—Публикация
2015-12-10—Подача