Настоящее изобретение относится к способу изготовления приспособления для лечения костей, например, для ортогнатического остеосинтеза и/или для матриц.
Способы, родственные этому способу, известны, например, из патентов США US 8 855 389 B1 и US 2014/0094924 A1. В патенте US 8 855 389 B1 раскрыт автоматизированный способ использования метода конечных элементов для систем костных имплантатов. В настоящем контексте также предоставляется доступ к библиотеке, содержащей данные предварительно сконструированных имплантатов. Однако вышеупомянутые данные применяют/адаптируют к интактной кости. В патенте US 2014/0094924 A1, с другой стороны, используется зеркальное отображение интактной/неповрежденной контралатеральный кости. Дальнейшая информация о существующем уровне техники предоставляется в патенте US 2011/0 151 400 A1.
При существующих способах изготовления приспособления для лечения кости, а именно: или имплантатов, или матриц для резекции кости/распила кости, их качество не является удовлетворительным. Поэтому необходимо улучшить качество таких приспособлений. Кроме того, приспособление для лечения кости необходимо адаптировать к конкретным пациентам, кому оно предписано, и чтобы его можно было сделать быстрее, чтобы оно было менее дорогим и более удобным. Кроме того, необходимо обеспечить более высокую надежность планирования. Планирование также должно быть упрощено. Наконец, необходимо повысить удобство такого способа для пользователя.
В способе изготовления приспособления для лечения кости эта цель достигается с использованием различных этапов. На первом этапе, например, необходимо обнаружить/получить/использовать (исходные) 3D-данные кости или части кости конкретного пациента, подлежащего лечению, при этом участок, подлежащий лечению, должен находиться внутри кости или части кости. Вышеупомянутый участок, как правило, представляет собой дефект или дефект костного материала. Вышеупомянутые (исходные) 3D-данные кости или части кости конкретного пациента, подлежащего лечению, формируются на основе других данных, например, данных, полученных на этапе сбора, таких как, например, данные, полученные с помощью компьютерной томографии (CT), магнитно-резонансной томографии (MRT), магниторезонансной визуализации (MRI), цифрового изображения и коммуникации в медицине, стандарта (DICOM) или с помощью аналогичных способов и устройств. На третьем реконструктивном этапе два набора данных связаны друг с другом, таким образом, 3D-данные дополняются или их сбор завершается для реконструкции участка, подлежащего лечению. Соответственно, обрезка исходных 3D-данных или полученных дополнительных данных на основе 3D-данных выбранного контрольного пациента включена или может быть включена, что позволяет получать восстановленные и обрезанные 3D-данные для перекрытия или восполнения дефекта костного материала у пациента, подлежащего лечению. Это помогает достичь существенного улучшения, по сравнению с предыдущими способами. Данные «контрольного пациента» могут в большей степени относиться к набору данных, который был составлен, исходя из данных различных конкретных пациентов. Соответственно, например, может использоваться форматирование средних значений, форматирование медиан и/или другие/подобные алгоритмы. Следовательно, под термином «контрольный пациент», необязательно, но может подразумеваться «конкретный человек». Представляется перспективным составить «искусственного» «контрольного пациента», исходя из существующих наборов данных. Наконец, используется статистическая модель. Под пациентом понимают живого или мертвого человека или животного и/или их части. Этап зеркального отображения используется для получения объединенных 3D-данных участка, подлежащего лечению, посредством наложения 3D-данных конкретного пациента, подлежащего лечению, на соответствующий участок, при этом наложенные 3D-данные берут свое происхождение на зеркально-симметричной другой стороне пациента, а точнее, на участке, соответствующем кости или части кости. Несмотря на то, что уже используемые статистические данные, то есть, данные, которые были предоставлены, по меньшей мере, одним контрольным пациентом, показывают улучшение, такое улучшение в значительной мере продолжается за счет использования этапа зеркального отображения и за счет использования зеркальных данных интактной стороны определенного конкретного пациента, подлежащего лечению. Таким образом, предлагается также этап включения 3D-данных, при этом вышеупомянутые 3D-данные соответствуют кости или части кости с участком, подлежащим лечению (однако на интактной стороне), и, следовательно, берут свое происхождение на стороне, зеркально-симметричной стороне, подлежащей лечению.
Преимущество вариантов осуществления настоящего изобретения отражено в подпунктах формулы изобретения, подробное объяснение которых приведено ниже.
Преимущество состоит в том, что результат, по меньшей мере, трех этапов используется для планирования производственной операции.
Дополнительное преимущество состоит в том, что три этапа предоставления исходных 3D-данных пациента, подлежащего лечению, включения 3D-данных контрольного пациента и дополнений выполняются последовательно или по меньшей мере частично параллельно. Таким образом, можно отследить процессы планирования в течение 5-10 минут, и даже можно отследить весь процесс изготовления в течение < 12 часов, если изготовление проводится на месте локализации, или в течение < 48 часов, если предприятие по изготовлению медицинского оборудования находится в другом месте.
Когда после третьего этапа приспособление для лечения кости производят на четвертом этапе в форме имплантата или матрицы остеотомии, то компонент, который должен быть прикреплен к кости, можно получить относительно быстро.
Также преимущество состояло в том, что на этапе подготовки исходные 3D-данные пациента и/или 3D-данные по меньшей мере одного контрольного пациента вводятся, например, в базу данных на интернет-основе и/или собираются из нее.
Также преимущественный вариант осуществления настоящего изобретения отличается тем, что перед этапом зеркального отображения и/или после первого этапа выполняется автоматизированная 2D- или 3D-визуализация. Таким образом, удобство такого способа для пользователя повышается.
Для того, чтобы было возможно провести идентификацию костей конкретного человека и, соответственно, костных фрагментов легко и эффективно, предпочтительно, чтобы перед или после этапа зеркального отображения, в предпочтительном варианте осуществления настоящего изобретения – после этапа визуализации, на кости были выбраны / выбраны в дальнейшем точки, отмечаемые маркером, например, в виде «ориентиров» или маркеровок. Для того, чтобы укрепить не только существующие кости, но и заменить фактически отсутствующий материал, предпочтительно, чтобы дефект костного материала пациента, подлежащего лечению, закрывался или перекрывался, или заполнялся по типу отверстия. Таким образом, область применения способа может быть значительно расширена. Конечно, также возможно использовать приспособление для лечения кости, с тем, чтобы после закрепления на кости/части кости оно служило направляющим и/или указывающим приспособлением для осуществления перфорирования, распила и прокалывания кости.
Пациенту может быть предоставлена помощь быстрее, чем это было прежде, если перед четвертым этапом, то есть, перед изготовлением, на этапе получения 3D-данных и/или данных изготовления для управления производственными машинами, создаются, например, данные СК или ЧПУ и, в преимущественном варианте осуществления настоящего изобретения вышеупомянутые данные СК или ЧПУ непосредственно или опосредованно подаются в производственное устройство, такое как устройство управления системой фрезерования, обтачивания, спекания или сварки. Формирование, формирование, в частности, механообрабатывающим и/или аддитивным способом производства может быть использовано быстро и эффективно. Особенно эффективным является использование технологий быстрого прототипирования, таких как технологии 3D-печати, особенно те, которые используют формат данных *.3mf. В дополнение к информации о геометрии должна быть включена и информация об аддитивном и/или механообрабатывающем способе производстве.
Дополнительное преимущество состоит в том, что в предпочтительном варианте осуществления настоящего изобретения непосредственно после третьего этапа и/или перед четвертым этапом выполняется этап моделирования для получения поверхностей, осей, локализаций и/или коэффициентов отклонения.
Рекомендуется выполнять этап планирования производственной операции перед четвертым этапом или вместо четвертого этапа.
Преимущественный вариант осуществления настоящего изобретения также отличается тем, что 3D-данные пациента, подлежащего лечению, и/или 3D-данные контрольного пациента(ов) хранятся в базе данных больницы или на облачном сервере в интернете (или на аналогичном устройстве), или в базе данных предприятия по изготовлению медицинского оборудования. Затем могут использоваться как данные, хранящиеся в больнице, за пределами больницы, так и все доступные данные. Именно с помощью решения на интернет-основе происходит улучшение способа и облегчается его использование.
Когда 3D-данные контрольного пациента(ов) содержат критерии отбора, такие как информацию, касающуюся курения/не курения, пола, возраста, размера, профессии, национальной принадлежности и/или физиологии телосложения, то выбор соответствующих (индивидуальных) данных для реконструкции кости облегчается. Что касается информации о физиологии телосложения, то подходит классификация по Кречмеру, хотя его классификация вызывает споры.
Настоящее изобретение также относится к устройству для осуществления способа планирования и/или изготовления, при этом в нем содержится/создается и подготавливается приспособление для осуществления способа по настоящему изобретению.
Разработка состоит в том, что компьютер включает/содержит информацию, которая подготовлена и установлена для автоматического осуществления этапов способа. Таким образом, взаимодействие с операционным персоналом сводится к минимуму.
Применение в соответствии с настоящим изобретением заключается в использовании неровностей в кости и, таким образом, для получения лучшего диагноза.
Другими словами, описан способ или процесс, в котором при использовании моделей статистической формы создается поверхность и/или объем, и/или в котором реконструкция имплантата и матрицы для остеотомии хранятся в базе данных. Таким образом, этапы лечения кости и/или приспособления для лечения кости можно автоматически адаптировать и рассчитать для каждого конкретного человека. Приспособление для лечения кости также может быть произведено с адаптацией к конкретному человеку и особенно быстро.
Статистические модели анатомических областей подходят для планирования оказания медицинской помощи. Это – виртуальные модели, которые позволяют восполнять или заменять недостающие или дефектные области с использованием имеющейся информации об особенностях человека.
Оказалось, что статистические модели для реконструкции устройства укрепления кости человека обеспечивают/показывают более высокую точность, по сравнению с простым/сингулярным зеркальным отображением интактной стороны на дефектную сторону. Важное преимущество состоит в том, что при автоматизированной реконструкции патологически или травматологически модифицированной кости требуется просто ориентация посредством точек или поверхностей на локальных костях для применения модели статистической формы и для получения реконструкции, независимо от более сложных способов сегментации. Кроме того, тип и качество имеющейся информации о 3D-изображении человека теперь не зависит от результата реконструкции посредством статистической модели. Это также означает, что имеющиеся артефакты, например, из-за металлических болтов, которые вызывают размытые зоны при диагностике способом визуализации, можно отделить и, следовательно, удалить.
Когда статистическая модель сочетается с конструкциями имплантатов, это означает, что конструкции имплантатов можно адаптировать к соответствующему человеку с помощью автоматизированной процедуры. Таким образом, выбрав типичные локализации переломов, можно создать, например, индивидуальные имплантаты посредством автоматизированной процедуры. Также можно собрать информацию о реконструкциях конкретного человека, чтобы таким образом получить оптимизацию имплантатов для стандартизированных заготовок имплантатов.
Тот же принцип может быть применен и к так называемым «направляющим распила». «Направляющие распила» необходимы для выполнения расчетов остеотомий на кости. Например, при реконструкции нижней челюсти, для которой необходимо провести костную трансплантацию из малоберцовой кости, заранее рассчитывается, каким образом должна быть распилена приподнятая кость, чтобы можно было восстановить анатомическую форму нижней челюсти. Если вышеупомянутые дефекты хранятся в базе данных, то можно рассчитать «направляющие распила» с помощью автоматизированной процедуры. Кроме того, таким способом в дальнейшем можно пропустить дополнительное рентгеновское облучение донорской области, если статистическая модель адаптирована к предоставлению вышеуказанной информации в качестве среднего значения автоматическим способом, который предлагается в настоящем документе.
Технологическая цепочка для изготовления имплантатов выглядит следующим образом:
1. сбор данных (компьютерная томография, магнитно-резонансная томография, УЗИ, статистическая модель (пол, возраст, размер, профессия ...))
2. выбор области и/или имплантата по точкам или поверхностям
3. применение статистической модели к выбранной области
4. подгонка имплантата к конкретной области
5. экспорт файла с готовой конструкцией имплантата.
Технологическую цепочку для «направляющей распила» можно охарактеризовать следующим образом:
1. сбор данных
2. выбор области, подлежащей реконструированию
3. применение статистической модели к выбранной области
4. выбор донорской области и расчет требуемых остеотомий
5. представление требуемой коррекции репозиции и автоматическое построение направляющей распила
6. экспорт файла с готовой конструкцией
Все это создает различные преимущества, по сравнению с другими способами. Например, не обязательно использовать зеркальное отображение стороны. Таким образом, можно принять во внимание индивидуальную асимметрию. Не требуется новая конструкция имплантата. Можно хранить любое количество «заготовок имплантатов». Их можно получать в зависимости от показаний и рекомендаций оперирующего хирурга. «Направляющие распила» также могут быть рассчитаны по способу планирования производственной операции. Таким образом, технологическая цепочка значительно сокращается. Необходимый осмотр врачом пропускается, поскольку он выполняется на том же сеансе создания имплантата лицом, ведущим планирование. Приложение на интернет-основе позволяет быстро и эффективно проводить планирование без какого-либо дополнительного программного обеспечения. Программное обеспечение может непрерывно улучшать имплантаты и поверхности в режиме самообучения. Становится возможным размещать «стандартные параметры» и «стандартные оси» для того, чтобы выявлять патологические изменения и предлагать соответствующую коррекцию. Дополнительная рентгенограмма и связанное с ней облучение донорской области можно пропустить.
Следовательно, отличительной особенностью является автоматическая реконструкция поверхности кости с помощью 3D-данных, в частности, с использованием имеющихся данных определенного конкретного пациента, которые дополняются данными из статистической модели. Сочетание имеющихся (сохранившихся) данных конкретного пациента с дополнительными 3D-данными из статистической модели приводит, таким образом, к осуществлению точечной поверхностной реконструкции кости, подлежащей лечению.
Модель статистической формы служит для автоматизированного планирования. Модель формы интегрирована в соответствующее программное обеспечение планирования (например, в качестве набора данных стандартной библиотеки шаблонов (STL)) и может использоваться для «виртуальной реконструкции» в хирургической навигации. Преимущество этого способа заключается в том, что зеркальное отображение не является обязательным, но оно может быть осуществлено для реконструкции. Таким образом, можно осуществлять навигацию по двусторонним (находящимся на двух сторонах) дефектам. Одновременный захват виртуальных имплантатов позволяет точно контролировать хирургическое позиционирование путем навигации.
Кроме того, специальное приложение учитывает тот факт, что стандартизированный имплантат уже «сконструирован» для области. То есть, «заготовка имплантата» уже была создана с помощью стандартных средних значений. Вышеупомянутая заготовка имплантата хранится в базе данных. Благодаря точкам конструкции она привязана к статистической модели и автоматически помещается в соответствующий участок человека. На втором этапе адаптируется поверхность зоны имплантата, обращенной к кости. Файл конструкции изменяется, когда модель статистической формы адаптируют к конкретной кости.
Также отличительной особенностью является то, что стандартный имплантат удерживается на соответствующем участке кости (максимально соответствует участку). Посредством способа обрезки материалом заполняют пространство между поверхностью имплантата, обращенной к кости, и костью.
В дальнейшем изобретение будет подробно проиллюстрировано на нескольких фигурах, при этом:
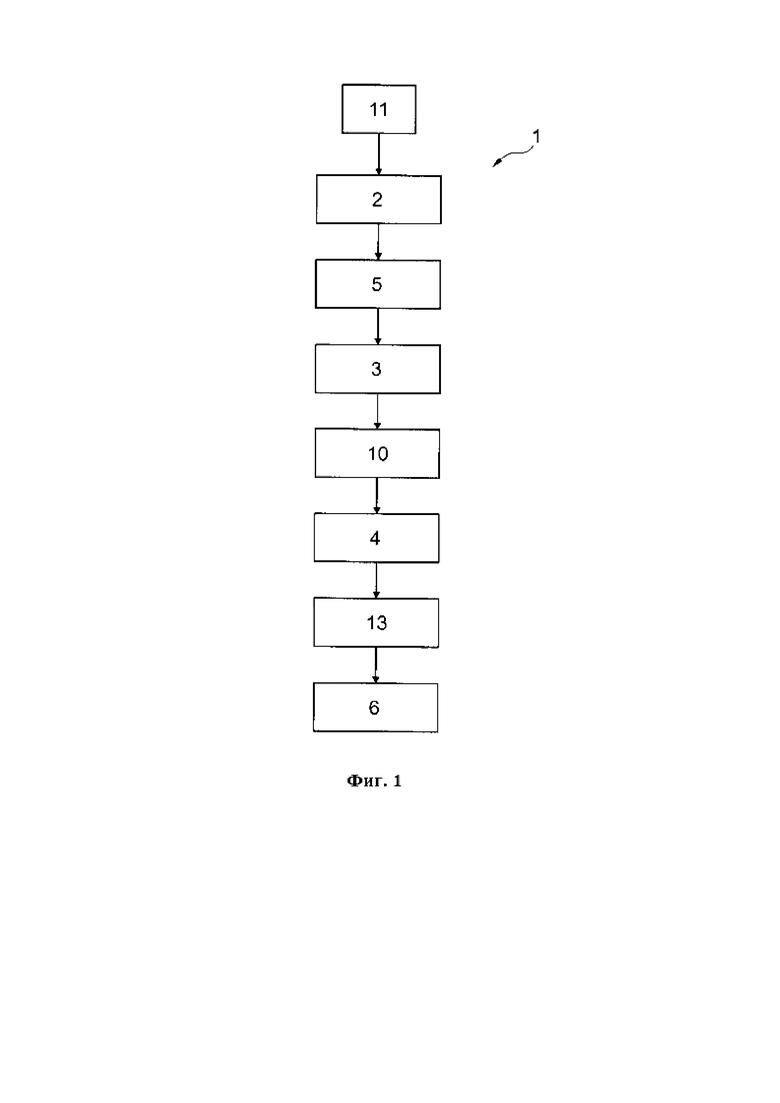
На Фигуре 1 показана блок-схема осуществления способа, в соответствии с настоящим изобретением.
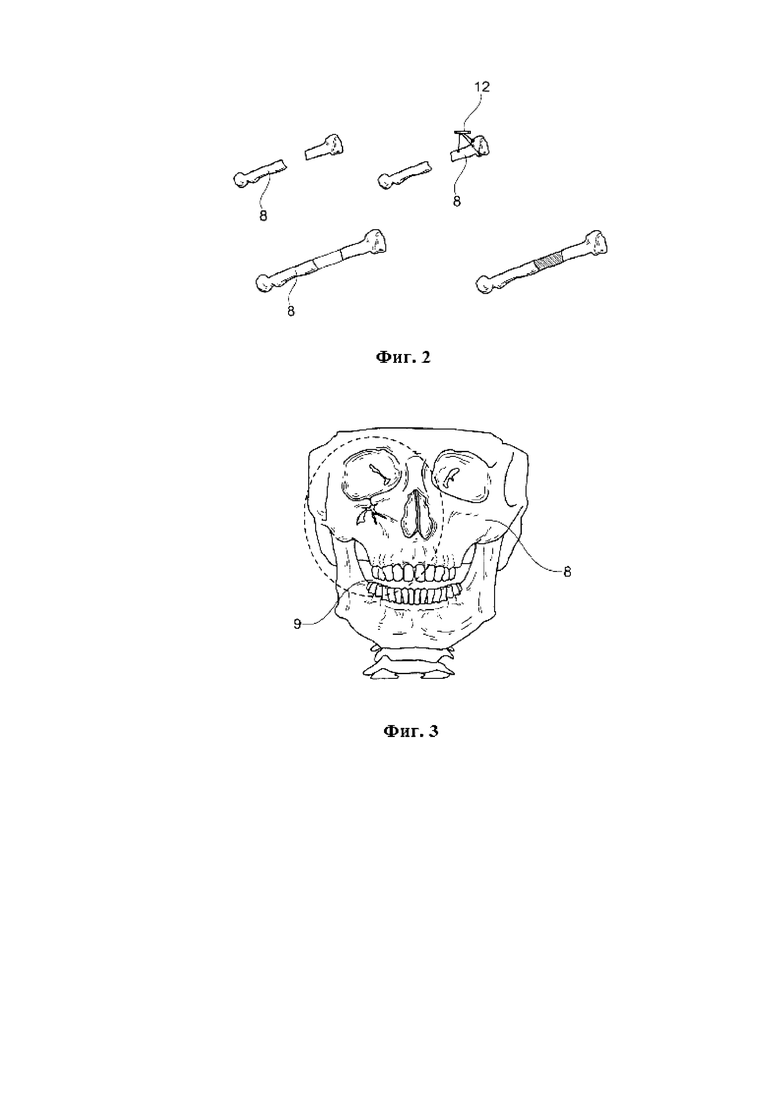
На Фигуре 2 показан процесс ремоделирования на кости.
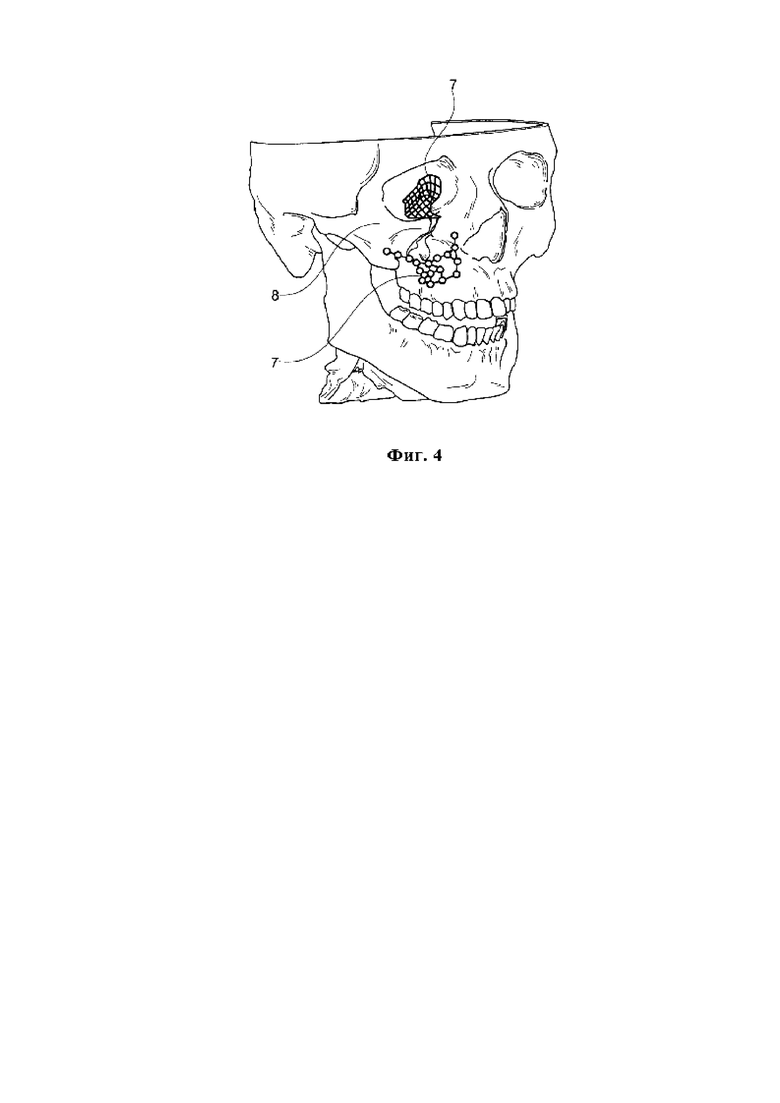
На Фигуре 3 показано положение зоны, подлежащей лечению, на образце черепа.
На Фигуре 4 показана установка крепежных приспособлений для кости по типу имплантата глазного яблока и имплантата челюсти.
Фигуры представляют собой просто схематическое изображение и служат только для понимания настоящего изобретения. Подобные элементы имеют одинаковые позиционные обозначения.
Настоящее изобретение подходит для использования в хирургии черепа и лица, но, в конечном итоге, оно может быть использовано и/или для любой костной структуры человека или млекопитающего.
В способе 1, в соответствии с настоящим изобретением, существует первый этап 2 создания доступных исходных 3D-данных кости или части кости конкретного пациента, подлежащего лечению. Затем следует второй этап 3, в котором происходит включение 3D-данных контрольного пациента, который был выбран в соответствии с предопределенными критериями, а именно 3D-данные собираются в сопоставимой области, которая подлежит лечению. На следующем третьем этапе 4 выполняется дополнение, возможно содержащее обрезку 3D-данных, объединенных на этапе 2 и этапе 3, при этом объединение данных происходит на частичном этапе.
Между первым этапом 2 и вторым этапом 3 также может выполняться этап зеркального отображения 5. На вышеупомянутом этапе зеркального отображения 3D-данные, которые противопоставлены продольной оси или плоскости симметрии, включая продольную ось тела, собираются из интактного участка больного (конкретного) пациента, подлежащего лечению, и накладываются на 3D-данные больной стороны, подлежащей лечению. Рекомендуется использовать этот этап.
На четвертом этапе 6, также называемой этапом изготовления, приспособление для лечения кости 7 изготавливается, например, по типу имплантата или матрицы остеотомии. Таким образом, возможно также «виртуальное хирургическое планирование». Такое приспособление для лечения кости 7, которое прикреплено к кости 8 определенного конкретного пациента, подлежащего лечению, показано на Фигуре 4.
На Фигуре 3 показана зона 9, подлежащая лечению, на черепе, включая кость 8. И если глазное яблоко вышеупомянутого черепа имеет дефект в зоне области 9, подлежащей лечению, на правой стороне, если смотреть со стороны пациента, то глазное яблоко не имеет дефектов на левой стороне, если смотреть со стороны пациента.
Соответствующие данные интактной стороны передаются на дефектный участок на этапе зеркального отображения 10, изображенного на Фигуре 1. Их адаптируют к нему/для него. Предшествующие предыдущие этапы включают этап подготовки 11, в которых 3D-данные пациента и/или 3D-данные по меньшей мере одного контрольного пациента вводятся в локальную базу данных или базу данных на интернет-основе и, соответственно, собираются из нее.
На Фигуре 2 показано, каким образом, начиная с дефекта кости, создаются ориентиры, затем выполняется «корректировка», в которой используется модель наложенной формы, которая еще не адаптирована к последующей вставке модели статистической формы в расчетный распил для того, чтобы получить адаптированную модель с замененным дефектом кости. Маркеры 12, которые формирую «ориентиры», отмечены позиционным обозначением 12.
Следовательно, дело в том, что до настоящего времени, исключительно для примера, дефекты черепа реконструировали, в большинстве случаев, путем зеркального отображения интактной стороны на дефектную сторону. Однако такой способ подходит только в ограниченной степени, или результатов недостаточно. В настоящем способе оценивается множество моделей черепа для формирования статистической модели. Благодаря статистической модели дефектный участок на дефектном черепе теперь может быть реконструирован.
В способе 1 по настоящему изобретению используется этап производства 13.
Позиционные обозначения:
1 способ
2 первый этап (данные для предоставления)
3 второй этап (включающий статистическую модель)
4 третий этап (дополняющий плюс обрезки, где требуется)
5 этап зеркального отображения
6 четвертый этап/этап производства
7 приспособление для лечения кости
8 кость
9 область, подлежащая лечению
10 этап зеркального отображения
11 этап подготовки
12 маркер
13 этап производства
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хирургического лечения пациентов с посттравматическими дефектами и деформациями средней зоны лицевого черепа | 2024 |
|
RU2834340C1 |
| СПОСОБ ПРЕВЕНТИВНОГО ИЗГОТОВЛЕНИЯ ИНДИВИДУАЛИЗИРОВАННОГО ИМПЛАНТАТА ДЛЯ ОДНОМОМЕНТНОГО ВОСПОЛНЕНИЯ ПЛАНИРУЕМОГО ДЕФЕКТА ПРИ ХИРУРГИЧЕСКОМ УДАЛЕНИИ ОПУХОЛИ НИЖНЕЙ ЧЕЛЮСТИ | 2000 |
|
RU2164391C1 |
| Имплантат для протезирования костей черепа и способ изготовления имплантата для протезирования костей черепа | 2016 |
|
RU2638894C2 |
| СПОСОБ ТРЕХМЕРНОГО МОДЕЛИРОВАНИЯ ПЕРСОНИФИЦИРОВАННЫХ ЧЕЛЮСТНО-ЛИЦЕВЫХ ИМПЛАНТАТОВ ДЛЯ МОДЕЛИРОВАНИЯ ФОРМЫ ПОДБОРОДКА | 2021 |
|
RU2797494C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНДИВИДУАЛИЗИРОВАННОГО ПРЕЦИЗИОННОГО ИМПЛАНТАТА ДЛЯ ВОСПОЛНЕНИЯ СЛОЖНОГО СУБТОТАЛЬНОГО ПОЛИОССАЛЬНОГО ДЕФЕКТА ГЛАЗНИЦЫ | 2000 |
|
RU2164392C1 |
| Способ замещения дефекта костей черепа с применением аддитивных технологий | 2023 |
|
RU2825748C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТОВ ПРОКСИМАЛЬНОГО ОТДЕЛА БОЛЬШЕБЕРЦОВОЙ КОСТИ ПРИ ВЫПОЛНЕНИИ ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2019 |
|
RU2730985C1 |
| Способ укладки и стабилизации гранулированных костнопластических материалов в реципиентном ложе при устранении сложных дефектов костей челюстей | 2021 |
|
RU2766977C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТОВ ДИСТАЛЬНОГО ОТДЕЛА БЕДРЕННОЙ КОСТИ ПРИ ВЫПОЛНЕНИИ ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2019 |
|
RU2724490C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТЕЙ ЧЕРЕПА ПРИ ГРУБЫХ КОСМЕТИЧЕСКИХ ДЕФЕКТАХ В ВИСОЧНОЙ ОБЛАСТИ И ИМПЛАНТАТ ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТЕЙ ЧЕРЕПА ПРИ ГРУБЫХ КОСМЕТИЧЕСКИХ ДЕФЕКТАХ В ВИСОЧНОЙ ОБЛАСТИ | 2020 |
|
RU2740567C1 |
Изобретение относится к медицине. Способ изготовления имплантата для лечения кости содержит первый этап, в котором имеются исходные 3D-данные кости или части кости конкретного пациента, подлежащего лечению, при этом участок, подлежащий лечению, находится внутри кости или части кости, второй этап включения 3D-данных контрольного пациента, который был выбран в соответствии с предопределенными критериями, при этом включенные 3D-данные контрольного пациента соответствуют кости или части кости с участком, подлежащим лечению, и включают 3D-данные различных конкретных пациентов путем форматирования среднего значения и/или с использованием статистической модели, и третий и восстановительный этап для дополнения или завершения 3D-данных, объединенных с данными, полученными на первом этапе и втором этапе, для восстановления участка, подлежащего лечению. Далее заготовка имплантата, сконструированная с помощью стандартных средних значений, хранится в базе данных и привязана к статистической модели с помощью точек конструкции и автоматически помещается в соответствующий ранее реконструированный участок, подлежащий лечению, и где впоследствии адаптируется поверхность зоны имплантата, обращенная к кости. Технический результат заявленного изобретения заключается в повышении адаптации приспособления для лечения кости к конкретным пациентам. 9 з.п. ф-лы, 4 ил.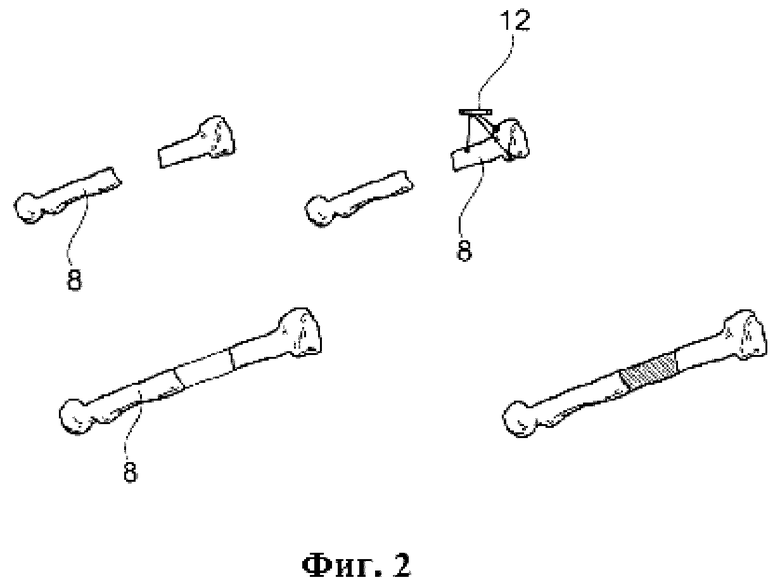
1. Способ (1) изготовления имплантата для лечения кости (7), содержащий первый этап (2), в котором имеются исходные 3D-данные кости (8) или части кости конкретного пациента, подлежащего лечению, при этом участок, подлежащий лечению, находится внутри кости (8) или части кости, второй этап (3) включения 3D-данных контрольного пациента, который был выбран в соответствии с предопределенными критериями, при этом включенные 3D-данные контрольного пациента соответствуют кости (8) или части кости с участком, подлежащим лечению, и включают 3D-данные различных конкретных пациентов путем форматирования среднего значения и/или с использованием статистической модели, и третий и восстановительный этап (4) для дополнения или завершения 3D-данных, объединенных с данными, полученными на первом этапе (2) и втором этапе (3), для восстановления участка, подлежащего лечению, отличающийся тем, что далее заготовка имплантата, сконструированная с помощью стандартных средних значений, хранится в базе данных и привязана к статистической модели с помощью точек конструкции и автоматически помещается в соответствующий ранее реконструированный участок, подлежащий лечению, и где впоследствии адаптируется поверхность зоны имплантата, обращенная к кости.
2. Способ (1) по п. 1, отличающийся тем, что используют этап зеркального отображения (5), в котором 3D-данные конкретного пациента, подлежащего лечению, изначально берут на другой зеркально-симметричной стороне пациента, накладывают на участок, соответствующий кости (8) или части кости, для получения объединенных 3D-данных.
3. Способ (1) по п. 1 или 2, отличающийся тем, что три или четыре этапа (2, 3, 4 и/или 5) выполняют последовательно или параллельно.
4. Способ (1) по любому из пп. 1-3, отличающийся тем, что после третьего этапа (4) на следующем этапе (6) приспособление для лечения кости (7) изготавливают в форме имплантата или матрицы остеотомии.
5. Способ (1) по п. 4, отличающийся тем, что на этапе подготовки (11) исходные 3D-данные пациента и/или 3D-данные по меньшей мере одного контрольного пациента вводят в базу данных и/или собирают из нее.
6. Способ (1) по любому из пп. 2-5, отличающийся тем, что перед этапом зеркального отображения (5) и/или после первого этапа (2) выполняют автоматизированную 2D- или 3D-визуализацию.
7. Способ (1) по любому из пп. 2-6, отличающийся тем, что перед или после этапа зеркального отображения (5) выбирают определенные точки на кости, отмеченные маркером (12).
8. Способ (1) по любому из пп. 1-7, отличающийся тем, что дефект костного материала пациента, подлежащего лечению, по типу отверстия, закрывают, или перекрывают, или заполняют.
9. Способ (1) по любому из пп. 4-8, отличающийся тем, что перед следующим этапом (6) на этапе изготовления генерируют 3D-данные и/или данные об изготовлении для управления производственными машинами.
10. Способ (1) по любому из предшествующих пунктов, отличающийся тем, что результат по меньшей мере трех этапов (2, 3, 4) используют для планирования производственной операции.
| DE 19922279 А1, 16.11.2000 | |||
| МАШИНА ДЛЯ НАНЕСЕНИЯ ТОРКРЕТ-БЕТОНА | 0 |
|
SU185040A1 |
| US 5741215 A, 21.04.1998 | |||
| ЧУГУН | 2006 |
|
RU2318058C1 |
| US 4976737 A, 11.12.1990. | |||
Авторы
Даты
2020-07-22—Публикация
2016-10-27—Подача