Изобретение относится к медицине, а именно к онкологии, и может быть использовано для стимуляции презентации опухолевых антигенов дендритными клетками.
Из литературных источников известно о низкой иммуногенности опухолевых антигенов, т.к. они являются аутологичными, а микроокружение опухоли способствует не только формированию дормантного состояния опухолевых клеток, но и их росту и распространению (см. В.М. Перельмутер, Л.А. Таширева, В.Н. Манских, Е.В. Денисов, О.Е. Савельева, Е.В. Кайгородова, М.В. Завьялова Иммуновоспалительные реакции в микроокружении гетерогенны, пластичны, определяют противоопухолевый эффект или агрессивное поведение опухоли // Журнал общей биологии, 2017, том 78, №5, с. 15-36; см. Dunn, Gavin Р.; см. Old, Lloyd J.; Schreiber, Robert D. (2004). «The Three Es of Cancer Immunoediting"». Annual Review of Immunology. 22 (1): 329-360. doi: 10.1146/annurev.immunol.22.012703.104803. PMID 15032581; см. Kim, Ryungsa; Emi, Manabu; Tanabe, Kazuaki (2007). «Cancer immunoediting from immune surveillance to immune escape"». Immunology. 121 (1): 1-14. doi: 10.1111/j.1365-2567.2007.02587.x. PMC 2265921. PMID 17386080).
Инициальным этапом иммунного ответа на опухоль является распознавание антигена, который обеспечивается антиген-презентирующими клетками (АПК), важнейшими среди них являются дендритные клетки (ДК). От их функционального состояния зависят и последующие этапы ответа, связанные с вовлечением в него Т-клеток: Т-хелперов (CD4+) и Т-цитотоксических (CD8+) лимфоцитов. Повышение иммуногенности опухолевых антигенов является актуальной задачей современной иммуноонкологии и клеточных технологий, на решение которой направлены разработка и применение различных адъювантов.
Применение в противоопухолевых вакцинах, приготовленных на основе неоантигенов опухолевых клеток, иммуностимулирующих адъювантов, которые позволяют преодолеть толерантность опухолевого микроокружения и вызывают мощный противоопухолевый иммунный ответ, может повысить эффективность вакцинотерапии (см. Барышникова М.А., Кособокова Е.Н., Косоруков B.C. Неоантигены в иммунотерапии опухолей // Российский биотерапевтический журнал. 2018. - N 2. - С. 6-14).
Сама идея использования адъювантов - неспецифических усилителей иммунного ответа - пришла, как и вакцинация, из области специфической профилактики инфекционных заболеваний. Адъюванты подразделяются на две основные группы, эффекты которых частично пересекаются: средства доставки (минеральные соли, например, гидроксид алюминия, эмульсии, липосомы) и иммуностимуляторы. Представляется важным, какие преимущественно звенья иммунной системы стимулируют тот или иной адъювант. Так, соединения алюминия стимулируют ответ по Th2 типу, поэтому используются для усиления антибактериального иммунитета. Эмульсия сквалена обладает мощным адъювантным эффектом, сбалансированным по действию на обе субпопуляции Т-хелперов (Th1 и Th2) (см. Seubert A., et al., J Immunol, 2008. 180(8): p. 5402-12). Классический адъювант Фрейнда, известный в полном и неполном вариантах, вызывает выраженное усиление ответа по Th1 (полный) и Th2 типу при слабом действии на ответ по Th1 типу (неполный). Эффект полного адъюванта Фрейнда, содержащего БЦЖ, на Th1 типа, по-видимому, реализуется с помощью белка микобактерий Antigen85A (Ag85A), относящегося к семейству Ag85, который участвует в синтезе миколиновой кислоты в клеточной стенке (см. Belisle J.Т., Vissa V.D., Sievert Т. et al. Role of the major antigen of Mycobacterium tuberculosis in cell wall biogenesis. Science 1997; 276(5317): 1420-2. PMID: 9162010], индуцирует пролиферацию Т-хелперов и продукцию цитокинов Th1 у людей, вакцинированных БЦЖ, и мышей, инфицированных микобактериями (см. Huygen K., Content J., Denis О. et al. Immunogenicity and protective efficacy of a tuberculosis DNA vaccine. Nat Med 1996; 2(8): 893-8. PMID: 8705859].
В обзоре A.C. Ильницкой и соавт. (2018) приводятся данные о том, что модификация дендритных клеток (ДК) для повышения их способности индуцировать иммунный ответ может быть достигнута за счет использования различных белков-носителей, адъювантов, цитокинов или генетически модифицированных вирусов (см. А.С. Ильницкая, А.Б. Данилова, И.А. Балдуева Иммунотерапия на основе дендритных клеток в лечении рака мочевого пузыря // Успехи молекулярной онкологии, 2018 т. 5, №2. С. 16-23; см. Engleman E.G. Dendritic cell-based cancer immunotherapy. Semin Oncol 2003; 30 (3 Suppl 8): 23-9. PMID: 12881809; Aarntzen E.H., de Vries I.J.,  J.H. et al. Humoral anti-KLH responses in cancer patients treated with dendritic cell-based immunotherapy are dictated by different vaccination parameters. Cancer Immunol Immunother 2012; 61 (11): 2003-11. DOI: 10.1007/s00262-012-1263-z.).
J.H. et al. Humoral anti-KLH responses in cancer patients treated with dendritic cell-based immunotherapy are dictated by different vaccination parameters. Cancer Immunol Immunother 2012; 61 (11): 2003-11. DOI: 10.1007/s00262-012-1263-z.).
В группу адъювантов-иммуностимуляторов включены также вещества, нацеленные на рецепторы распознавания патогена (PRRs) врожденной иммунной системы - патоген-связанные молекулярные паттерны (PAMPs) и компоненты, выделяющихся из травмированных или умирающих клеток - молекулярные паттерны, связанные с повреждениями (DAMPS). Взаимодействие PAMPs и DAMPS с PRRs вызывает воспалительную реакцию, которая в свою очередь, усиливает адаптивный иммунный ответ (см. Medzhitov R. and С. Janeway Jr., N Engl J Med, 2000. 343(5): p. 338-44). В качестве адъюванта для усиления противоопухолевого иммунного ответа был успешно использован олигонуклеотид - лиганд для TLR9 (см. А.С. Ильницкая, А.Б. Данилова, И.А. Балдуева Иммунотерапия на основе дендритных клеток в лечении рака мочевого пузыря // Успехи молекулярной онкологии, 2018 т. 5, №2. С. 16-23).
К эволюционно древним механизмам защиты принадлежат также белки теплового шока (например, HSP70), которые могут, наряду с другими эндогенными «сигналами опасности», выделяться из опухолевых клеток при их облучении (см. Xie X.F., Ding Q., Hou J.G., Chen G. Inhibitory effects of a dendritic cell vaccine loaded with radiation-induced apoptotic tumor cells on tumor cell antigens in mouse bladder cancer. Genet Mol Res 2015; 14(3): 7548-55. DOI: 10.4238/2015.July.3.30 PMID: 26214433), и регулировать экспрессию клетками антигенов МНС I, ICAM-1, VCAM-1 и других молекул адгезии, что способствует хемотаксису иммунных клеток к опухолевой ткани.
Использование погибающих опухолевых клеток в качестве пула антигенов для иммунизации антиген-презентирующих клеток, в частности, ДК является широко разрабатываемым подходом для клеточной иммунотерапии опухолей. В виде индукторов такой гибели могут выступать различные воздействия.
Известно использование апоптотически погибающих опухолевых клеток как источника антигена для стимуляции ДК с целью получения антиген-специфических Т-лимфоцитов, продуцирующих интерферон-гамма (см. S. Carluccio, S. Delbue, L. Signorini et al. Generation of tumor-specific cytotoxic T-lymphocytes from the peripheral blood of colorectal cancer patients for adoptive T-cell transfer // J Cell Physiol. - 2015. - Vol. 230, No. 7. - P. 1457-65). Полученные данные были включены авторами в протокол клеточной иммунотерапии колоректального рака с использованием Т-лимфоцитарной фракции, обогащенной CD8+ клетками, и ДК; индукция гибели опухолевых клеток достигалась с помощью ультрафиолетового облучения.
Известен способ применения химиопрепаратов в режиме метрономной терапии, вызывающей гибель опухолевых клеток, совместно с бактериальными вакцинами или вирусами в качестве адъювантов, обеспечивающих, с одной стороны, формирование специфического иммунного ответа против опухоли, а с другой - дополнительную стимуляцию неспецифического иммунитета для усиления цитолитической активности проводимой терапии (см. Патент RU 2500392 С2, опубл. 10.12.2013, Бюл. №34).
Ряд работ посвящен действию фотосенсибилизаторов в качестве адъювантов. Известен способ иммунотерапии плоскоклеточного рака у экспериментальных животных с помощью фотомодифицированых опухолевых клеток в состоянии апоптоза, тормозящий развитие опухоли у большинства вакцинированных животных (см. KorbelikM., Stott В., Sun J. Photodynamic therapy-generated vaccines: relevance of tumor cell death expression. - Br. J. Cancer, 2007, Vol. 97, pp. 1381-1387).
Кроме того, известно применение коллекционной клеточной линии меланомы кожи человека 369 ADmel, экспрессирующей раково-тестикулярные антигены, для приготовления биомедицинских клеточных продуктов и тестирования противоопухолевых препаратов, согласно которому ДК стимулируются лизатом клеток данной линии меланомы, полученном при действии фотосенсибилизатора фотодитазина с последующим облучением опухолевых клеток лазером с λ=662 нм (см. Балдуева И.А., Данилова А.Б., Нехаева Т.Л., Беляев А.М. Применение клеточной линии меланомы кожи человека 369 ADMEL, Патент RU №2642265, опубл. 24.01.2018 Бюл. №3). Лизат получали методом многократной шоковой заморозки и одномоментной разморозки клеток. Теми же авторами предложен способ противоопухолевой иммунотерапии, предполагающий последовательное применение сеанса фотодинамической терапии и аутологичных костномозговых предшественников дендритных клеток (см. Патент RU 2376033 С1, опубл. 20.12.2009, Бюл. №35).
Все указанные авторы ссылаются на иммуностимулирующее действие ФДТ, однако, стимуляция разных звеньев иммунной системы может привести к неоднозначным результатам, например, к активации иммуносупрессивных Т-регуляторных клеток.
Применение непатогенных вирусов с адъювантной целью также описано в литературе. Вирусы используются как средства доставки целевого (опухолевого) антигена, однако, с учетом того, что они и сами являются экзогенными антигенами, ответ на которые развивается через Т-клеточное звено, они могут быть применены и как иммуностимуляторы Т-лимфоцитов, т.к. вызывают продукцию цитокинов, включая TNF-a, стимулирующего как факторы неспецифической защиты, так и специфического иммунитета, частности, Т-хелперную активность (см. Russell SJ, Peng K.W. Viruses as anticancer drugs // Trends Pharmacol Sci. - 2007. - Vol. 28, No. 7. - P. 326-33). Поскольку у некоторых вирусов установлено онколитическое действие (см. С.В. Нетёсов, Г.В. Кочнева, В.Б. Локтев и др. Онколитические вирусы: достижения и проблемы // Медицинский алфавит. - 2011. - N 3. - С. 26-33; см. О.В. Матвеева, Г.В. Кочнева, С.В. Нетесов и др. Механизмы онколитического действия парамиксовируса Сендай // ActaNaturae - 2015. - N 7 (2). - С. 6-17; см. S.  I.
I.  G. Proboka et al. ЕСНО-7 virus Rigvir immunotherapy (oncolytic virotherapy) prolongs survival in melanoma patients after surgical excision of the tumour in a retrospective study // Melanoma research. - 2015. - Vol. 25, No. 5. - P. 421; см. Schirrmacher V. Immunobiology of Newcastle disease virus and its use for prophylactic vaccination in poultry and as adjuvant for therapeutic vaccination in cancer patients // International journal of molecular sciences - 2017. - Vol. 18, No. 5. - P. 1103), возможно их участие в усилении иммунного ответа через индукцию PAMPs и DAMPS, образующихся при разрушении опухолевых клеток, что может быть одним из механизмов адъювантного эффекта. Известны способы применения ВБН в качестве адъюванта при проведении вакцинотерапии у онкологических больных. Однако в качестве самой вакцины использовались аутологичные опухолевые клетки (Schlag Р, Manasterski М, Gerneth Т, Hohenberger Р, Dueck М, Herfarth С, Liebrich W, Schirrmacher V. Active specific immunotherapy with Newcastle-disease-virus-modified autologous tumor cells following resection of liver metastases in colorectal cancer. First evaluation of clinical response of a phase II-trial. Cancer Immunol Immunother. 1992; 35(5): 325-30; Liang W, Wang H, Sun TM, Yao WQ, Chen LL, Jin Y, Li CL, Meng FJ. Application of autologous tumor cell vaccine and NDV vaccine in treatment of tumors of digestive tract. World J Gastroenterol. 2003 Mar; 9(3): 495-8; Mosolits S, Nilsson B, Mellstedt H. Towards therapeutic vaccines for colorectal carcinoma: a review of clinical trials. Expert Rev Vaccines. 2005 Jun; 4(3): 329-50). Недостатком данного способа вакцинирования является необходимость в наращивании аутологичного опухолевого материала, что является сложным, длительным и трудоемким процессом, поскольку выживание клеток и их пролиферация возможны только лишь при воссоздании всех внешних условий, которые были in vivo.
G. Proboka et al. ЕСНО-7 virus Rigvir immunotherapy (oncolytic virotherapy) prolongs survival in melanoma patients after surgical excision of the tumour in a retrospective study // Melanoma research. - 2015. - Vol. 25, No. 5. - P. 421; см. Schirrmacher V. Immunobiology of Newcastle disease virus and its use for prophylactic vaccination in poultry and as adjuvant for therapeutic vaccination in cancer patients // International journal of molecular sciences - 2017. - Vol. 18, No. 5. - P. 1103), возможно их участие в усилении иммунного ответа через индукцию PAMPs и DAMPS, образующихся при разрушении опухолевых клеток, что может быть одним из механизмов адъювантного эффекта. Известны способы применения ВБН в качестве адъюванта при проведении вакцинотерапии у онкологических больных. Однако в качестве самой вакцины использовались аутологичные опухолевые клетки (Schlag Р, Manasterski М, Gerneth Т, Hohenberger Р, Dueck М, Herfarth С, Liebrich W, Schirrmacher V. Active specific immunotherapy with Newcastle-disease-virus-modified autologous tumor cells following resection of liver metastases in colorectal cancer. First evaluation of clinical response of a phase II-trial. Cancer Immunol Immunother. 1992; 35(5): 325-30; Liang W, Wang H, Sun TM, Yao WQ, Chen LL, Jin Y, Li CL, Meng FJ. Application of autologous tumor cell vaccine and NDV vaccine in treatment of tumors of digestive tract. World J Gastroenterol. 2003 Mar; 9(3): 495-8; Mosolits S, Nilsson B, Mellstedt H. Towards therapeutic vaccines for colorectal carcinoma: a review of clinical trials. Expert Rev Vaccines. 2005 Jun; 4(3): 329-50). Недостатком данного способа вакцинирования является необходимость в наращивании аутологичного опухолевого материала, что является сложным, длительным и трудоемким процессом, поскольку выживание клеток и их пролиферация возможны только лишь при воссоздании всех внешних условий, которые были in vivo.
Известен способ лечения онкологических заболеваний, заключающийся в применении вируса болезни Ньюкасла (ВБН) в составе композиции, содержащей сам вирус и извлеченные из него антигены, и обладающей противоопухолевым эффектом, осуществляющимся за счет лизиса опухолевых клеток (см. патент США №7223389, МПК А61К 48/00, опубл. 29.05.2007 г. «Композиция и способ лечения опухолей»). Однако данный способ предусматривает только использование цитолитического потенциала ВБН, но не формирование специфического иммунитета у опухоленосителя, что необходимо для профилактики рецидивирования заболевания. Кроме того, для культивирования ВБН необходимы куриные эмбрионы, что технически сложнее, чем использование культур клеток.
Следует отметить, что опухоли, против которых получали указанные вакцины, были преимущественно меланомами и карциномами толстой кишки. Известен патент на «Способ лечения первичных больных местно-распространенным раком шейки матки», где применялась ДКВ, лизат опухолевых клеток для приготовления которой получали с помощью шести последовательных циклов моментального замораживания суспензии клеток культуры HeLa в жидком азоте и оттаивания до комнатной температуры без применения адъювантов (см. Кит О.И. Водолажский Д.И. Моисеенко Т.И. Франциянц Е.М. Меньшенина А.П. Патент №2616531, опубл. 17.04.2017, Бюл. №11).
Учитывая приведенные выше данные о важности применения адъювантов с целью повышения иммуногенности опухолевых антигенов при получении дендритноклеточных вакцин, нами было предпринято использование для этого вирусов, способных лизировать опухолевые культуры, в частности, культуру рака шейки матки HeLa.
Техническим результатом предлагаемого нами изобретения является повышение антиген-презентирующей активности дендритных клеток путем использования для их нагрузки антигена в виде лизата культуры HeLa, полученного с помощью культивирования в течение 5 суток с реовирусом Р-92.
Технический результат достигают тем, что для получения лизата клеток HeLa используют апатогенный реовирус Р-92, с которым их сокультивируют в среде 199 с L-глютамином в течение 5 суток (37°С в атмосфере 5% CO2), достигая полного цитопатического действия, нагружают полученным лизатом незрелые дендритные клетки и сокультивируют с лимфоцитами 5 дней, в течение которых проводят иммунофенотипирование с оценкой экспрессии активационных маркеров на CD4+ и CD8+ Т-лимфоцитах, после чего оценивают их активность против клеток-мишеней путем 2-х суточного сокультивирования и констатируют 100% гибель последних.
Предлагаем рисунки для пояснения способа.
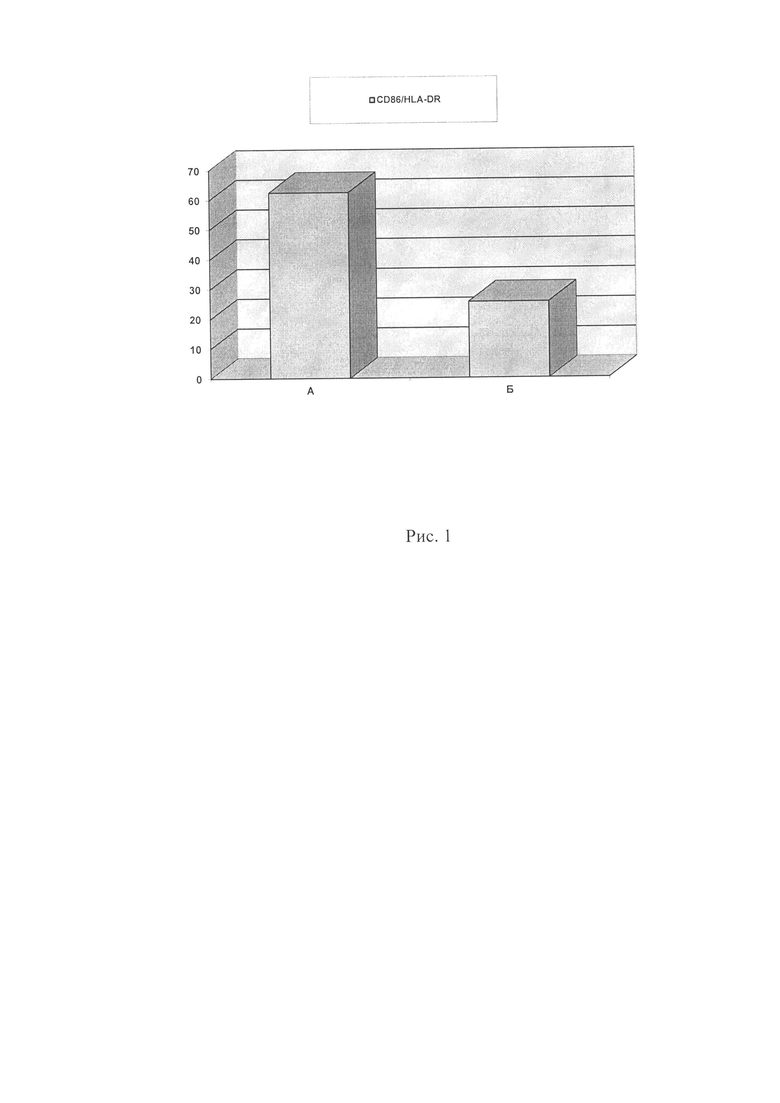
На рис. 1 изображено количество ДК, коэкспрессирующих CD86 и HLA-DR, после нагрузки опытным и контрольным антигенами. Ось Y - % от нелимфоидных клеток.
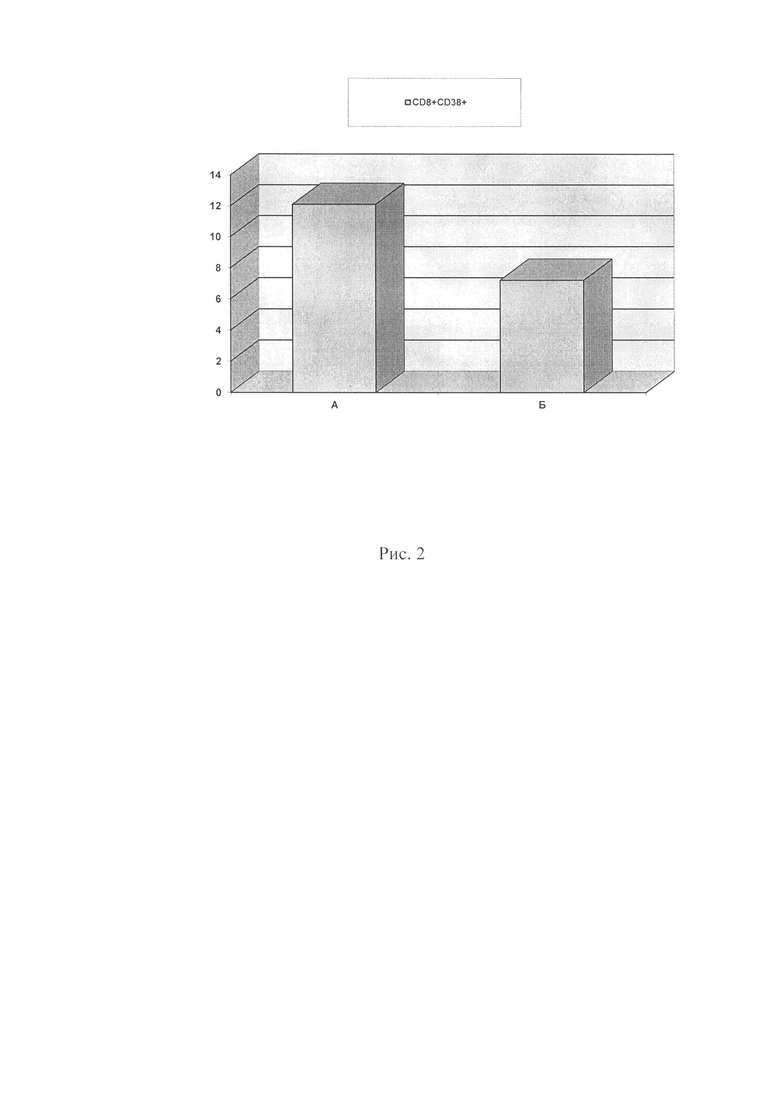
На рис. 2 изображено количество активированных CD8+ Т-клеток через 1 сутки после инкубации с ДК, нагруженных опытным и контрольным антигенами. Ось Y - % от CD3+ CD8+.
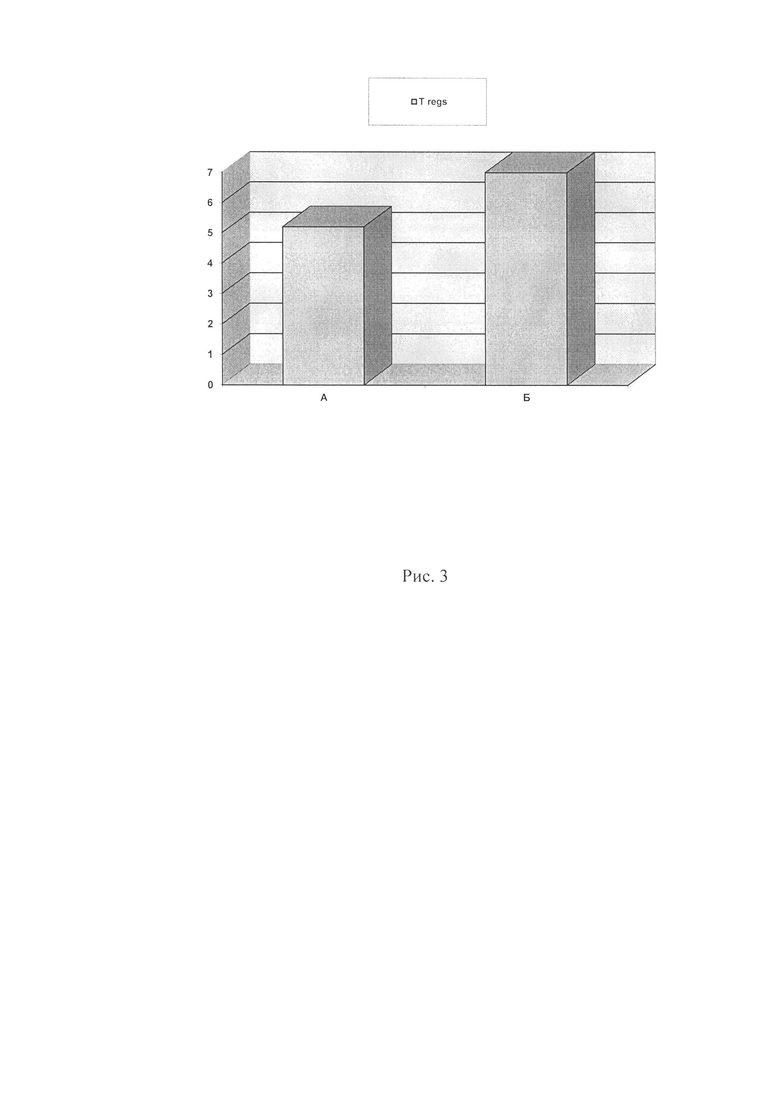
На рис. 3 изображено количество Т regs (CD4+CD25+CD127low) клеток через 1 сутки после инкубации с ДК, нагруженных опытным и контрольным антигенами. Ось Y - % Т regs от CD4+ клеток.
На рис. 4 изображено количество активированных CD4+ и CD8+ Т-клеток через 2 суток после инкубации с ДК, нагруженных опытным и контрольным антигенами. Ось Y - % от CD4+ и CD8+ клеток.
Рис. 5 изображено количество активированных CD4+ и CD8+ Т-клеток через 5 суток после инкубации с ДК, нагруженных опытным и контрольным антигенами. Ось Y - % от CD4+ и CD8+ клеток.
Рис. 6 изображено количество активированных CD4+ и CD8+ Т-клеток через 7 суток после инкубации с ДК, нагруженных опытным и контрольным антигенами. Ось Y - % от CD4+ и CD8+ клеток.
Штамм реовируса человека Р-92, используемый в качестве производственного для создания диагностического препарата «Реотест» депонирован в коллекции НИИ Вирусологии им. Д.И. Ивановского 17.02.2003, ему присвоен номер ГКВ №2363. Штамм выделен из фекального экстракта больного инфекционным гепатитом в 1992 г. старшим научным сотрудником Ростовского НИИ микробиологии и паразитологии к.м.н. С.А. Колпаковым. Выделение проводили на перевиваемой культуре СПЭВ, штамм прошел 12 пассажей, адаптирован к росту на данной культуре. Ранее охарактеризован электронно-микроскопическими, серологическими методами и ПЦР, как относящийся предположительно к 3 серотипу (см. Колпаков С.А., Колпакова Е.П. Неклассифицированные вирусы человека семейства Reoviridae // Сб. конф. Актуальные вопросы диагностики и профилактики инфекционных и паразитарных заболеваний на юге России. Материалы межрегиональной научно-практической конференции с международным участием. - 2016. - С. 243-247). Инфекционная активность штамма - 107 ТЦД50/мл. По морфологии и диаметру вирионов (70 нм) соответствует реовирусам. Геном имеет 10 сегментов РНК с их распределением по классам 3-3-4 и молекулярными массами от 2,7 до 0,8 мегедальтон. Используется в качестве производственного штамма для создания диагностического препарата «Реотест», является непатогенным.
Для получения лизата с помощью реовируса Р-92 использовали линию опухолевых клеток: HeLa (рак шейки матки), полученную из Российской коллекции культур клеток ФГБУН Института цитологии РАН. Для наращивания реовируса Р-92 использовали культуру СПЭВ (клетки почки эмбриона свиньи), культивируемые в среде 199.
Культуру HeLa наращивали во флаконах Т25 до 100% конфлюентности монослоя в полной питательной среде RPMI-1640 с L-глутамином, 10% фетальной бычьей сыворотки и 0,5% пенициллина-стрептомицина в условиях 5% CO2 при температуре 37°С. Затем декантировали питательную среду, промывали клетки раствором Хенкса. Далее в каждый флакон добавляли по 100 мкл Р-92, выращенного на культуре клеток СПЭВ, и 200 мл питательной среды RPMI-1640, равномерно распределяли раствор по поверхности флакона с клетками, инкубировали в течение 3 минут при постоянном покачивании, после чего вносили по 10 мл той же питательной среды и культивировали в условиях 5% CO2 при температуре 37°С.
Визуализацию проводили с помощью инвертированного микроскопа Zeiss Axio Vert при увеличении ×100. Реовирусное происхождение лизиса культуры подтверждали в серологических реакциях РНГА и РТНГА. Титр реовируса в культуральной жидкости определяли с помощью тест-системы «Реотест», представляющей собой эритроцитарный иммуноглобулиновый диагностикум для РИГА и РТНГА, разработанный в Ростовском НИИ микробиологии и паразитологии Роспотребнадзора; чувствительность метода составляет 1-2 нг по вирусному белку. Тест-система позволяет обнаруживать реовирусы непосредственно в биологическом материале, которым в данном случае являлась культуральная жидкость.
С целью усиления антиген-презентирующей активности ДК этап нагрузки незрелых ДК антигеном проводили с помощью лизата культуры HeLa, полученного при сокультивировании с реовирусом Р-92 в течение 5 суток при 37° с 5% СO2.
Для выполнения заявляемого способа проводились следующие этапы получения и контроля лизата:
1. Инкубацию монослоя культуры клеток HeLa (рак шейки матки) с реовирусом Р-92 в среде 199 с L-глютамином проводили в течение 5 суток (37°С в атмосфере 5% CO2), на протяжении которых отмечалось частичное, а впоследствии и полное разрушение монослоя, уменьшение адгезии клеток с потерей ими типичного вида и полным откреплением их от поверхности флакона. При развитии цитопатического действия (ЦПД) титры РНГА реовируса в культуральной жидкости с тест-системой «Реотест» составляли 1:32-1:64. На данном этапе контрольной пробой служила культура реовируса Р-92, растущего на среде СПЭВ. Результаты РНГА в опытной и контрольной пробах были аналогичны, следовательно, полученное ЦПД связано с репликацией Р-92.
2. Мононуклеарные клетки (МНК) выделяли из периферической крови, взятой из локтевой вены в объеме 100 мл в пробирки для выделения МНК BD Vacutainer® CPT™ (Cell Preparation Tube), реактив гепарин натрия/Ficoll™. 2-х часовую адгезию моноцитов выполняли в питательной среде RPMI-1640 на 2 флаконах Т75, после чего питательную среду с неприкрепленными клетками (лимфоцитами) переносили в стерильные центрифужные пробирки и аликвотировали по 10 млн клеток в 1 мл криосреды в криопробирках и замораживали при температурном режиме - 80°С для дальнейших исследований.
3. Дифференцировку прикрепившихся клеток (моноцитов) в незрелые ДК проводили в течение 7 дней в питательной среде для дифференцировки ДК (CellGenix), добавляя на 1-й, 3-й и 5-й день инкубации IL-4 (20 нг/мл) и GM-CSF (72 нг/мг). На 7-й день инкубации клетки снимали с флакона раствором Версена, определяли фенотип на проточном цитофлуориметре (FACSCantoII, BD). Маркер незрелых ДК CD1а был обнаружен на 25% клеток.
После снятия ДК их в равной пропорции переносили на 2 флакона Т25 в кондиционированной среде (т.е. в среде, в которой ранее культивировались ДК), добавляли IL-4 (20 нг/мл), GM-CSF (72 нг/мг) и TNF-a (20 нг/мл), а также проводили индивидуальную антигенную нагрузку для каждого флакона: А) опытным антигеном, представляющим собой лизат HeLa, полученный в результате сокультивирования реовируса Р-92 с культурой в течение 5 сут., как описано в п 1; Б) контрольным антигеном - лизатом культуры HeLa, который готовили путем многократной шоковой заморозки и одномоментной разморозки клеток. Через 48 часов нагруженные ДК снимали с культуральных флаконов раствором Версена и фенотипировали с использованием панели антител CD80/CD83/CD86/HLA-DR/CD1a/CD45, позволяющей охарактеризовать созревание ДК.
Результаты иммунофенотипирования показали, что в опытных пробах ДК отмечено увеличение в 2,4 раза процента ДК, коэкспрессирующих маркеры CD86 и HLA-DR, по сравнению с нагрузкой контрольным опухолевым лизатом (рис. 1).
4. Для оценки способности полученных ДК активировать лимфоциты проводили их сокультивирование в течение 5 суток с аутологичными лимфоцитами в соотношении 3:1 в лунках 6-луночных планшетов в питательной среде RPMI-1640 с добавлением 10% телячьей эмбриональной сыворотки. Для контроля активации Т-лимфоцитов субпопуляций CD4+ и CD8+ в течение данного срока несколько раз проводили иммунофенотипирование.
Результаты иммунофенотипирования, выполненного через 1 сутки совместного культивирования, показали, что на CD8+ лимфоцитах определялась в 1,7 раза более высокая экспрессия маркера ранней активации CD38 в опытном образце с ДК, нагруженными лизатом HeLa, полученном при действии реовируса (рис. 2).
Кроме того, в тот же срок исследования среди этих же лимфоцитов после их сокультивирования с ДК, нагруженными опытным лизатом, отмечен в 1,4 раза более низкий процент Т-регуляторных клеток с фенотипом CD4+CD25+CD127low, чем после сокультивирования с ДК, нагруженными контрольным лизатом HeLa (рис. 3.)
В последующие сроки культивирования (2-е и 5-е сутки) происходила постепенная смена лимфоцитарного маркера ранней активации (CD38) на маркер поздней активации (HLA-DR). Различия экспрессии активационных маркеров на Т-лимфоцитах между опытной и контрольной пробами сохранялись, причем они были выявлены не только на CD8+, но и на CD4+ клетках (рис. 4, 5).
На рис. 4 представлено сравнение доли активированных Т-лимфоцитов с маркерами ранней и поздней активации на 2-е сутки сокультивирования ДК опытных и контрольных проб с аутологичными лимфоцитами.
Как видно из рис. 4, доля активированных лимфоцитов была выше после их сокультивирования с ДК, нагруженными лизатом, полученным с помощью реовируса Р-92: в 3,4 раз для CD4+HLA-DR+ клеток, в 2,7 раз для CD8+HLA-DR+ клеток и в 2,9 раз для CD8+CD38+ клеток.
На 5-е сут. сокультивирования различия сохраняются и даже возрастают для лимфоцитов обеих основных субпопуляций, экспрессирующих маркеры поздней активации (рис. 5). Как видно из рис. 5, на 5-е сутки доля активированных лимфоцитов была выше после их сокультивирования с ДК, нагруженными лизатом, полученным с помощью реовируса Р-92: в 18,5 раз для CD4+HLA-DR+ клеток, в 5,0 раз для CD8+HLA-DR+ клеток и в 2,3 раз для CD8+CD38+ клеток.
5. Оценивали цитотоксическое действие сокультивируемых лимфоцитов и ДК против клеток-мишеней, для чего на 5-е сут. к опытным и контрольным пробам добавляли культуру HeLa по 1,5×105 клеток (в соотношении с ДК 1:1) и продолжали инкубацию. Через 2 суток совместного культивирования зрелых ДК, аутологичных лимфоцитов и HeLa, все клетки извлекали из образцов, и проводили их фенотипирование. Отмечено, что в контрольных образцах, где ДК нагружали лизатом HeLa, сохранялись опухолевые клетки в количестве, равном первоначально внесенному, хотя в тех же образцах была отмечена наибольшая популяция зрелых ДК (CD83) (81,9% против 33,6% в опытных пробах), что говорит об их низкой антиген-презентирующей активности. Напротив, в опытных пробах, опухолевые клетки-мишени полностью отсутствовали.
Как видно из рис. 6, доля активированных Т-лимфоцитов и в этих пробах, культивированных 7 суток, была выше при использовании ДК, нагруженных лизатом, полученным с помощью реовируса Р-92: в 2,3 раз для CD4+CD38+ клеток, в 2,9 раз для CD4+HLA-DR+ клеток, в 1,5 раза для CD8+CD38+ клеток и в 3,2 раз для CD8+HLA-DR+ клеток.
Полученные результаты свидетельствуют о преимуществе предлагаемого способа стимуляции презентирующей активности ДК под действием реовируса штамма Р-92, позволяющего получить после сокультивирования с ними активированные Т-лимфоциты хелперного и цитотоксического звеньев, проявляющие противоопухолевый эффект в модельной системе in vitro.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ иммунотерапии рака молочной железы с помощью антиген-активированных дендритных клеток | 2016 |
|
RU2645464C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕН-СПЕЦИФИЧЕСКИХ ЦИТОТОКСИЧЕСКИХ КЛЕТОК, ОБЛАДАЮЩИХ АКТИВНОСТЬЮ ПРОТИВ КЛЕТОК РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2596920C2 |
| Способ получения in vitro популяций активированных антигенспецифических противоопухолевых цитотоксических Т-лимфоцитов, специфичных к эпитопам опухоль-ассоциированного антигена | 2016 |
|
RU2619186C1 |
| Полиэпитопная противоопухолевая вакцинная конструкция, содержащая эпитопы опухоль-ассоциированных антигенов, фармацевтическая композиция и ее применение для стимуляции специфического противоопухолевого иммунного ответа | 2016 |
|
RU2684235C2 |
| КЛЕТОЧНЫЙ ПРОДУКТ ДЛЯ НАГРУЗКИ И АКТИВАЦИИ ДЕНДРИТНЫХ КЛЕТОК ЧЕЛОВЕКА | 2019 |
|
RU2714208C1 |
| СПОСОБ ИММУНОТЕРАПИИ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА С | 2016 |
|
RU2637631C2 |
| СПОСОБ ИММУНОТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА | 2018 |
|
RU2686756C1 |
| Способ получения аутологичных дендритных клеток с высоким уровнем экспрессии HLA-DR и костимуляторных молекул при онкологических заболеваниях | 2020 |
|
RU2767631C1 |
| СПОСОБ ГЕНЕРАЦИИ АНТИГЕН-СПЕЦИФИЧЕСКИХ ЦИТОТОКСИЧЕСКИХ КЛЕТОК С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ ПРИ РАКЕ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2521506C1 |
| СПОСОБ ИММУНОТЕРАПИИ ОПУХОЛЕВЫМ ЛИЗАТОМ С АДЪЮВАНТОМ БЕТАЛЕЙКИН БОЛЬНЫХ СОЛИДНЫМИ ОПУХОЛЯМИ | 2004 |
|
RU2267326C2 |



Изобретение относится к биотехнологии и может быть использовано для клеточной иммунотерапии опухолей. Сущностью изобретения является получение и использование в качестве антигена для нагрузки незрелых дендритных клеток лизата опухолевой культуры HeLa, образующегося после ее сокультивирования с реовирусом Р-92. Нагрузка таким лизатом способствует стимуляции созревания дендритных клеток и повышению их антиген-презентирующей активности, оцениваемой по иммунофенотипу и по способности их активировать Т-лимфоциты. Разработанный способ обеспечивает усиление презентации опухолевых антигенов дендритными клетками, что представляется важным для клеточной иммунотерапии опухолей. 1 пр., 6 ил.
Способ стимуляции презентирующей активности дендритных клеток, включающий культивирование незрелых дендритных клеток в присутствии лизата культуры HeLa, цитокинов и ростовых добавок в течение 7 дней, отличающийся тем, что для получения лизата клеток HeLa используют апатогенный реовирус Р-92.
| Xiaojun Xia et al, Porous Silicon Microparticle Potentiates Anti-Tumor Immunity by Enhancing Cross-Presentation and Inducing Type I Interferon Response, Cell Reports, Volume 11, Issue 6, 2015, Pages 957-966 | |||
| Курилин В | |||
| В., Хантакова Ю | |||
| Н., Облеухова И | |||
| А., Шевченко Ю | |||
| А., Куликова Е | |||
| В., Якушенко В | |||
| К., Соколов А | |||
| В., Сенников С | |||
| В., Стимуляция |
Авторы
Даты
2020-07-30—Публикация
2019-08-20—Подача