Область Техники
Изобретение относится к способу генерирования аэрозоля для терапевтических целей. Более конкретно, изобретение относится к способу распыления композиции, содержащей иммуноглобулин (Ig), конкретно, поликлональные иммуноглобулины, такие как иммуноглобулин G (IgG), иммуноглобулин A (IgA) или иммуноглобулин M (IgM) или их комбинации.
Уровень техники
Иммуноглобулины (Ig) представляют собой компоненты плазмы крови человека, которые играют важную роль в иммунологических реакциях. Эти специфические иммунные белки синтезируются В-лимфоцитами и присутствуют в плазме крови, лимфе и в других секретах организма у всех позвоночных. Иммуноглобулины составляют приблизительно 20% белков плазмы у людей. Три класса иммуноглобулинов, IgG, IgA и IgM, более важны, чем другие. Человеческий IgG представляет собой наиболее распространенный иммуноглобулин в плазме, тогда как IgA представляет основной класс антител в экзокринных секретах, таких как слюна, слезы и слизь дыхательных путей и желудочно-кишечного тракта. IgA образует одну из первых линий защиты против бактериальных и вирусных патогенов. IgM, без сомнения, представляет собой физически самое крупное антитело в системе кровообращения человека, появляется рано в процессе инфекции и обычно появляется повторно в меньшей степени после следующего экспонирования.
На протяжении прошлого века препараты иммуноглобулинов успешно применяли в качестве заместительной терапии для лечения инфекционных заболеваний у пациентов с первичными расстройствами иммунодефицита и для профилактики и лечения различных воспалительных и аутоиммунных патологических состояний, а также некоторых неврологических расстройств. Эти препараты иммуноглобулинов были разработаны для системного введения, и они, по большей части, состояли из IgG. В настоящее время эти препараты выделяют из суммарной плазмы тысячей здоровых доноров (1000-60000 доноров), и они содержат как специфичные, так и природные антитела, отражая кумулятивный опыт встреч с антигенами в донорской популяции. Этот большой спектр специфичных и природных антител может распознавать широкий интервал антигенов (например, патогены, чужеродные антигены и свои/аутоантигены).
Как правило, иммуноглобулины вводят внутривенно или подкожно. Некоторые коммерческие составы доступны для этих путей введения. Кроме того, предлагалось местное введение иммуноглобулинов, более конкретно, введение в дыхательные пути (включая верхние дыхательные пути: нос и носовой проход, околоносовые пазухи, горло, ротоглотку, глотку, гортань, дыхательное горло и трахею; а также нижние дыхательные пути: дыхательные пути, в которых происходит газообмен, легкие, бифуркация, бронхи и бронхиолы, дыхательные бронхиолы, альвеолярные каналы, альвеолярные мешочки и альвеолы).
Например, в US 4994269 описан способ местного введения антител P. aeruginosa. Антитела могут вводиться в форме аэрозоля, например, посредством нанесения в нос, в виде аэрозоля для легких или посредством внутритрахейного введения.
В WO 92/01473 описан способ, который включает введение в нижние дыхательные пути восприимчивого реципиента небольшой частицы (< 2 мкм) аэрозоля смеси конкретных моноклональных антител, направленных против различных защитных антигенных сайтов, присутствующих на большинстве защитных антигенов вирусной поверхности.
В Rimensberger and Roth («Physical Properties of Aerosolized Immunoglobulin for Inhalation Therapy», Journal of Aerosol Medicine, Vol. 8(3), pp 255-262, 1995) распыление раствора иммуноглобулинов (IVIG) оценивали с использованием четырех пневматических небулайзеров.
В US 2002/0136695 описано аэрозольное введение иммуноглобулина A с помощью дозирующего ингалятора или небулайзера для предотвращения или лечения заболевания, включающего иммунодефициты и инфекции.
В WO 03/059424 описан контроллер, который может контролировать аэрозольный генератор на основе идентификации содержимого распыляемого вещества, имеющего маркер идентификации/метку. Система может использоваться для распыления нескольких лекарственных групп. Антитела упоминаются в качестве одной из таких лекарственных групп.
В WO 2004/004798 описаны способы и композиции для системной доставки терапевтических средств путем введения аэрозоля, содержащего антитела или конъюгаты терапевтического агента с FcRn-связывающим партнером, в эпителий центральных дыхательных путей легкого. Способы и продукты имеют преимущество, связанное с тем, что нет потребности во введения глубоко в легкое с целью осуществления системной доставки. Предполагается использование аэрозольных генераторов с различным принципом работы.
В WO 2006/122257 описаны способы и композиции, применяющие антитело, которое ингибирует активацию системы комплемента, и которые могут использоваться для предотвращения или лечения заболевания или патологического состояния легких. Для введения моноклональных антител предлагаются небулайзеры различных типов.
В WO 2011/098552 описаны способы получения аэрозоля единственного вариабельного домена иммуноглобулинов, где количество образованных агрегатов значительно уменьшено.
Хотя в этих документах предложено несколько методов применения различных типов антител, существует потребность в способе распыления поликлональных Ig, например, IgG, IgA, IgM, или их комбинаций, особенно быстрым и эффективным образом.
Таким образом, целью настоящего изобретения является предложение способа генерирования аэрозоля композиции, содержащей поликлональные Ig, например, IgG, IgA, IgM или их комбинаций, для доставки поликлональных Ig в дыхательные пути пациента эффективным образом, например, доставляемая доза (DD) аэрозольного генератора может составлять, по меньшей мере, 40%, или, предпочтительно, по меньшей мере, 50%, вдыхаемая фракция (размер частиц менее 5мкм MMD) должна составлять, по меньшей мере, 70% или, предпочтительно, по меньшей мере, 80%, и, кроме того, пенообразующие свойства и остаточный объем жидкости, заполненной в жидкостной резервуар, после получения аэрозоля может уменьшаться, например, ниже 1 мл или, предпочтительно, ниже 0,5 мл, или, более предпочтительно, ниже 0,3 мл.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В изобретении предлагается способ получения аэрозоля, включающий стадии (a) получения жидкой водной композиции, содержащей поликлональные Ig, например, IgG, IgA, IgM или их комбинации, где концентрация Ig составляет 20-200 мг/мл; (b) обеспечения мембранного небулайзера, имеющего резервуар, в который заполняется композиция, и (c) распыления композиции с применением небулайзера для получения аэрозоля (генерирование аэрозоля).
В предпочтительных воплощениях, Ig является поликлональным. Предпочтительно, Ig представляет собой поликлональный IgG, поликлональный мономерный IgA, поликлональный димерный IgA, поликлональный IgM или их комбинации. В некоторых воплощениях, композиция может дополнительно содержать секреторный компонент, предпочтительно, рекомбинантно полученный человеческий секреторный компонент.
В некоторых воплощениях, концентрация Ig, например, IgG, IgA, IgM или их комбинации в жидкой водной композиции составляют 20-100 мг/мл. Кроме того, композиция может содержать стабилизатор. Стабилизатор может представлять собой пролин. Другие вспомогательные вещества, такие как ПАВ, также могут содержаться в композиции.
В конкретных воплощениях, резервуар небулайзера изолирован от атмосферы, так что давление внутри резервуара уменьшается перед или во время стадии (c). В предпочтительном воплощении, небулайзер представляет собой вибрационный мембранный небулайзер. В некоторых воплощениях, небулайзер конкретно адаптирован для генерирования аэрозоля с направленным воздействием либо на нижние дыхательные пути и/или на верхние дыхательные пути.
В одном аспекте, с помощью способа по изобретению получают аэрозоль, содержащий по меньшей мере, 40%, предпочтительно, по меньшей мере 50%, более предпочтительно, по меньшей мере, 60% дозы Ig, например, IgG, IgA, IgM или их комбинации, заполненные в резервуар. В другом аспекте, с помощью способа получают аэрозоль, где активность Ig, например, IgG, IgA, IgM или их комбинаций, составляет, по меньшей мере, 60%, предпочтительно, по меньшей мере, 70%, более предпочтительно, по меньшей мере, 80%, еще более предпочтительно, по меньшей мере, 90% активности в композиции, заполненной в резервуар.
Дополнительные воплощения изобретения будут очевидны на основе следующего подробного описания, примеров и формулы изобретения.
Краткое описание чертежей
На Фигуре 1 представлено схематическое изображение известного мембранного небулайзера, который может использоваться в настоящем изобретении.
На Фигуре 2 представлено изображение компьютерной томографии (КТ) известной мембраны, которая может использоваться в настоящем изобретении.
На Фигуре 3 представлены результаты структурного анализа нераспыленной и распыленной композиции IgG (PrivigenTM), проведенного с помощью SDS-PAGE в восстанавливающих (A) и не восстанавливающих (B) условиях.
На Фигуре 4 представлены результаты структурного анализа нераспыленных и распыленных композиций IgG (в PBS или в глицерине), IgA и IgAM, проведенного с помощью SDS-PAGE в восстанавливающих (A) и не восстанавливающих (B) условиях. На (C) представлен SDS-PAGE-анализ дополнительных IgA (p, q), IgAM (r, s), SIgAM (t, u) и IgG (v, w, x, y) в восстанавливающих (левая панель) и не восстанавливающих (правая панель) условиях.
На Фигуре 5 представлено связывание различных составов с S. pneumonia до (-) и после (N) распыления.
На Фигуре 6 представлен эффект распыления в отношении активности различных составов до и после распыления при различных аспектах инфекции Shigella flexneri монослоев эпителиальных клеток: (A) эффект секреции эпителиальными клетками воспалительных цитокинов в ответ на Shigella flexneri индивидуально (C+), или в комплексе с нераспыляемыми (-) или распыляемыми (N) составами различных иммуноглобулиновых композиций; (B) эффект инфекции Shigella flexneri индивидуально (C+), или в комплексе с нераспыляемыми (-) или распыляемыми (N) составами различных иммуноглобулиновых композиций в отношении трансэпителиальной мембранной устойчивости клеточного монослоя; (C) инфицированная область (левая панель) и количество очагов инфекции (правая панель) после инфекции Shigella flexneri индивидуально (C+), или в комплексе с нераспыляемым (-) или распыляемым (N) составом различных иммуноглобулиновых композиций.
На Фигуре 7 представлено легочное депонирование распыляемых иммуноглобулиновых составов и динамика их присутствия в БАЛ в животной модели.
На Фигуре 8 представлены Вестерн-блоты образцов БАЛ, взятых в моменты времени 0, 1ч, 6ч, 12ч и 24ч, которые гибридизовали с антителом к цепи гамма (a), к цепи альфа (b), и к цепи мю (c).
Подробное описание изобретения
Способ по изобретению представляет собой способ генерирования аэрозоля путем распыления жидкой водной композиции. Жидкие водные композиции представляют собой жидкие системы, где жидкий носитель или растворитель в основном или полностью состоит из воды. В конкретных случаях, жидкий носитель может содержать небольшие фракции одной или нескольких жидкостей, которые, по меньшей мере, частично смешиваются с водой.
Композиции содержат поликлональный иммуноглобулин, который обычно получают из плазмы людей-доноров. Предпочтительно, плазму от множества доноров объединяют, например, от более чем 100 доноров, предпочтительно, от более чем 500 доноров, еще более предпочтительно от более чем 1000 доноров. Как правило, пулы плазмы подвергают фракционированию в этаноле с последующими стадиями очистки, такими как стадии преципитации и/или колоночной хроматографии, а также стадиями для инактивации и удаления вирусных и других патогенов, таким как нанофильтрация или обработка растворителем/детергентом.
Композиция содержит поликлональный иммуноглобулин, который также обозначают Ig. Такие поликлональные Ig, например IgG, IgA, IgM или их комбинации могут быть получены из плазмы крови людей-доноров. Нормальный человеческий IgG может быть получен с чистотой, составляющей, по меньшей мере, 95% IgG. Таким образом, в одном воплощении, IgG, содержащийся в композиции, используемой в способе по изобретению, как правило, имеет чистоту, составляющую по меньшей мере, 95% IgG, предпочтительно, по меньшей мере, 96% IgG, более предпочтительно, по меньшей мере, 98% IgG, еще более предпочтительно, по меньшей мере, 99% IgG. Предпочтительно, он содержит минорные количества IgA. Например, в одном воплощении, композиция содержит максимально 25 мкг IgA на 1 мл.
В другом аспекте воплощения, композиция содержит IgA с чистотой, по меньшей мере, 90%, предпочтительно, по меньшей мере, 92%, более предпочтительно, по меньшей мере, 94%, еще более предпочтительно, по меньшей мере, 96%, наиболее предпочтительно, по меньшей мере, 98%. Предпочтительно, IgA очищают из человеческой плазмы; однако также могут использоваться другие источники IgA, такие как молоко, слюна или другие IgA-содержащие физиологические жидкости. В другом конкретном воплощении, IgA представляет собой мономерный IgA. Еще в одном конкретном воплощении, IgA обогащен димерным IgA; предпочтительно, по меньшей мере, 20% IgA представлено в димерной форме, более предпочтительно, по меньшей мере, 30%, еще более предпочтительно, по меньшей мере, 40%, наиболее предпочтительно, по меньшей мере, 50%. Необязательно, композиция IgA может дополнительно содержать секреторный компонент, предпочтительно, рекомбинантно полученный секреторный компонент. Например, могут использоваться композиции, раскрытые в WO2013/132052, который включен в данный документ ссылкой в полном объеме.
Еще в одном конкретном воплощении, композиция содержит IgM. В одном воплощении, композиция содержит IgM и IgA. В предпочтительном воплощении, композиция содержит IgM и димерный IgA, который также содержит J-цепь. Необязательно, композиция также может содержать секреторный компонент, предпочтительно, рекомбинантно полученный секреторный компонент. Еще в одном воплощении, композиция содержит IgM, IgA и IgG. В конкретном воплощении, такая композиция может содержать 76% IgG, 12% IgA и 12% IgM.
В способе по изобретению используются относительно высокие концентрации Ig, например, IgG, IgA, IgM или их комбинаций. Более конкретно, концентрация Ig, особенно IgG, IgA, IgM или их комбинаций составляет от 20 до 200 мг/мл. Предпочтительно, концентрация составляет от 20 до 190 мг/мл, 20-180 мг/мл, 20-170 мг/мл, 20-160 мг/мл, 20-150 мг/мл, 30-200 мг/мл, 30-190 мг/мл, 30-180 мг/мл, 30-170 мг/мл, 30-160 мг/мл, 30-150 мг/мл, 40-200 мг/мл, 40-190 мг/мл, 40-180 мг/мл, 40-170 мг/мл, 40-160 мг/мл, 40-150 мг/мл. Более предпочтительно, концентрация составляет от 20 до 140 мг/мл, 20-130 мг/мл, 20-120 мг/мл, 30-140 мг/мл, 30-130 мг/мл, 30-120 мг/мл, 40-140 мг/мл, 40-130 мг/мл, 40-120 мг/мл, 50-140 мг/мл, 50-130 мг/мл или 50-120 мг/мл, еще более предпочтительно, концентрация составляет примерно 50 мг/мл, 60 мг/мл, 70 мг/мл, 80 мг/мл, 90 мг/мл, 100 мг/мл, 110 мг/мл, или 120 мг/мл. Относительно высокие концентрации важны для возможности достижения низких объемов заполнения и короткого времени распыления, гарантируя таким образом, терапевтическую эффективность способа.
Мембранный небулайзер используется для генерирования аэрозоля согласно способу по изобретению. Небулайзер определяют в данном документе как устройство, способное к аэрозолизации жидкого вещества в диспергированную жидкую фазу. Аэрозоль определяют в данном документе как систему, содержащую непрерывную газовую фазу, и диспергированную в ней дискретную или диспергированную фазу жидких частиц.
Генератор аэрозоля может содержать жидкостной резервуар, сконструированный для поддержания исходного объема жидкости, например, содержащей Ig, IgG, IgA, IgM или их комбинацию, мембрану, имеющую отверстия, причем жидкостной резервуар сообщается с мембраной для подачи жидкости, например, путем силы гравитации к одной стороне мембраны, причем мембрана колеблется для транспортировки жидкости сквозь отверстия, посредством чего жидкость испускается в форме аэрозоля с другой стороны мембраны.
Генератор аэрозоля может содержать мембрану, которая генерирует капли жидкости из жидкости, присутствующей на одной стороне, и высвобождает их в виде аэрозоля на другой стороне, когда часть стенки жидкостного резервуара вибрирует, и устройство генерирования вибрации, например, пьезоэлектрический элемент, которое связано с частью стенки жидкостного резервуара так, чтобы часть стенки жидкостного резервуара вибрировала (пассивный мембранный небулайзер типа I).
Генератор аэрозоля может содержать мембрану, которая генерирует капли жидкости из жидкости, присутствующей на одной стороне, и высвобождает их в виде аэрозоля на другой стороне, когда часть стенки устройства подачи жидкости (например, трубка) вибрирует, и устройство генерирования вибрации, например, пьезоэлектрический элемент, которое связано с устройством подачи жидкости так, чтобы устройство подачи жидкости вибрировало (пассивный мембранный небулайзер типа II).
Генератор аэрозоля может содержать мембрану, которая генерирует капли жидкости из жидкости, присутствующей на одной стороне, и высвобождает их в виде аэрозоля на другой стороне, когда мембрана вибрирует, и устройство генерирования вибрации, например, пьезоэлектрический элемент, которое связано с мембраной так, чтобы мембрана вибрировала (активный мембранный небулайзер).
Диспергированная фаза по существу состоит из капель жидкости. Капли диспергированной фазы содержат поликлональный Ig, например, IgG, IgA, IgM или их комбинации в жидкой окружающей среде. Жидкая окружающая среда в основном представляет собой водную фазу, содержащую или не содержащую дополнительные вспомогательные вещества, как описано дополнительно ниже. Специалисту в данной области будет понятно, что признаки и предпочтения в отношении жидкой композиции, раскрытой в данном документе, также могут применяться к диспергированной фазе аэрозоля, генериированной из него, и наоборот.
Непрерывная газовая фаза аэрозоля может быть выбрана из любого газа или смеси газов, которые являются фармацевтически приемлемыми. Например, газ может быть просто воздухом, который наиболее широко распространен в ингаляционной терапии при использовании небулайзеров в качестве аэрозольных генераторов. Альтернативно, могут использоваться другие газы и газовые смеси, такие как воздух, обогащенный кислородом, диоксид углерода или смеси азота и кислорода.
Две величины могут быть определены экспериментально и могут быть полезны для описания размера частиц или размера капель генерированного аэрозоля: медианный диаметр массы (MMD), медианный аэродинамический диаметр массы (MMAD). Различие между двумя значениями таково, что MMAD нормализован к плотности воды (эквивалентно аэродинамичности).
MMAD может измеряться с помощью импактора, например каскадного импактора Андерсона (ACI) или импактора следующего поколения (NGI). Альтернативно, могут использоваться методы лазерной дифракции, например, Malvern MasterSizer XTM, для измерения MMD.
Диспергированная фаза аэрозоля, генерированного способом по изобретению, демонстрирует размер частиц, например, MMD предпочтительно менее чем 10 мкм, предпочтительно примерно от 1 примерно до 6 мкм, более предпочтительно, примерно от 1,5 примерно до 5 мкм и еще более предпочтительно примерно от 2 примерно до 4,5 мкм. Альтернативно, размер частиц может иметь MMAD предпочтительно менее чем 10 мкм, предпочтительно примерно от 1 примерно до 6 мкм, более предпочтительно, примерно от 1,5 примерно до 5 мкм и еще более предпочтительно, примерно от 2 примерно до 4,5 мкм. Другой параметр, описывающий диспергированную фазу аэрозоля, представляет собой распределение размеров аэрозолизированных частиц жидкости или капель. Геометрическое стандартное отклонение (GSD) представляет собой часто используемую величину для широты распределения размера частиц или капель, генерированных аэрозольных частиц или капель.
Выбор точного MMD внутри описанного выше интервала должен принимать во внимание целевую область или ткань для депонирования аэрозоля. Например, оптимальный диаметр капель будет отличаться в зависимости от того, какая назначена ингаляция - пероральная, назальная или трахейная, и от пути доставки - в верхние и/или нижние дыхательные пути (например, в ротоглотку, горло, трахею, бронхи, альвеолы, легкие, нос и/или околоносовые пазухи).
Кроме того, зависимая от возраста анатомическая геометрия (например, геометрия носа, рта или дыхательных путей), а также респираторные заболевания и состояния пациентов и их профиль дыхания принадлежат к важным факторам, определяющим оптимальный размер частиц (например, MMD и GSD) для доставки лекарственного средства в нижние или верхние дыхательные пути.
Как правило, небольшие дыхательные пути, которые определяются внутренним диаметром менее чем 2 мм, составляют почти 99% от объема легких и, следовательно, играют важную роль в функции легких. Альвеолы представляют собой участки, расположенные глубоко в легких, где происходит обмен кислорода и диоксида углерода с кровью. Воспаление в альвеолах, вызванное некоторыми вирусами или бактериями, приводит к секреции жидкости на месте воспаления и непосредственно влияет на поглощение кислорода в легких. Для терапевтической направленности аэрозолей на глубокие легочные пути требуются аэрозоли, имеющие MMD ниже 5 мкм, предпочтительно менее 4 мкм, более предпочтительно менее 3,5 мкм и еще более предпочтительно менее 3 мкм.
Для доставки аэрозоля в дыхательные пути, аэрозоль имеет MMD менее 10 мкм, предпочтительно менее 5 мкм, более предпочтительно менее 3,3 мкм, и еще более предпочтительно менее 2 мкм. Предпочтительно, ММД (размеры капель) составляют примерно от 1 примерно до 5 мкм, и распределение по размерам имеет GSD менее чем 2,2, предпочтительно менее 2, более предпочтительно, менее чем 1,8 или даже более предпочтительно менее чем 1,6. Такие параметры размеров частиц и распределения частиц по размерам особенно полезны для достижения высокой местной концентрации лекарственного средства в дыхательных путях (например, в легких) человека, в том числе в бронхах и бронхиолах, по отношению к количеству лекарственного средства, которое аэрозолизируется. В этом контексте следует учитывать, что депонирование глубоко в легких требует меньших MMD, чем депонирование в центральных дыхательных путях взрослых и детей, а для младенцев и новорожденных более предпочтительны меньшие размеры капель (MMD) в диапазоне примерно от 1 примерно до 3,3 мкм, и диапазон менее 2 мкм является еще более предпочтительным. Таким образом, в аэрозольной терапии является обычной оценка фракции капель меньше чем 5 мкм (представляющих фракцию, которая вдыхается взрослым) и меньше, чем 3,3 мкм (представляющих фракцию, которая вдыхается ребенком или депонируется более глубоко в легких взрослого). Кроме того, фракция капель меньше 2 мкм часто оценивается так, как будто она представляет собой фракцию аэрозоля, которая может оптимально достичь терминальных бронхиол и альвеол взрослых и детей и может проникать в легкие младенцев и новорожденных.
В способе по настоящему изобретению, фракция капель, имеющих размер частиц менее чем 5 мкм, предпочтительно составляет более, чем 65%, более предпочтительно более чем 70% и еще более предпочтительно больше, чем 80%. Фракция капель, имеющих размер частиц менее, чем 3,3 мкм, предпочтительно составляет более, чем 25%, более предпочтительно более чем 30%, еще более предпочтительно более чем 35% и еще более предпочтительно более чем 40%. Фракция капель, имеющих размер частиц, менее чем 2 мкм, предпочтительно составляет более чем 4%, более предпочтительно более чем 6% и еще более предпочтительно более чем 8%.
Аэрозоль также может быть охарактеризован с помощью его доставляемой дозы (DD), как определено в опытах моделирования дыхания. Доставляемая доза может быть использована для расчета вдыхаемой дозы (RD), например, на основе вдыхаемой фракции (RF), измеренной с помощью лазерной дифракции (например, Malvern Mastersizer XTM) или с помощью импактора (например, каскадного импактора Андерсона - ACI или импактора следующего поколения - NGI). При применении способа по изобретению в эксперименте моделирования дыхания (например, с помощью дыхательного тренажера типа BRS3000 от Copley или Compass IITM от PARI) к профилю дыхания взрослого (синусоидальный поток, 500 мл дыхательного объема, 15 вдохов/мин) и при заполнении композиции до 2 мл (например, 200 мг Ig, 200 мг IgG, 200мг IgA, 200мг IgM, или их комбинации) в мембранный небулайзер, то доставляемая доза (DD), предпочтительно выше чем 40% (80 мг Ig, например, IgG, IgA, IgM, или их комбинации), более предпочтительно выше чем 45% (90 мг Ig, например, IgG, IgA, IgM, или их комбинации), и еще более предпочтительно выше чем 50% (100 мг Ig, например, IgG, IgA, IgM, или их комбинации).
Для лечения верхних дыхательных путей, в частности, носа, слизистой носа и/или придаточных пазух носа, остиомеатального комплекса и околоносовых полостей, особенно подходит ММД менее примерно 5 мкм, или менее примерно 4,5 мкм, или менее примерно 4 мкм, или менее примерно 3,3 или менее примерно 3 мкм.
Пригодность генерируемого аэрозоля для нанесения на верхние дыхательные пути может оцениваться на моделях назальной ингаляции, таких как человеческая назальная модель в виде слепка, описанная в WO 2009/027095. Для доставки аэрозоля в нос существует, например, устройство SinusTM (струйный небулайзер) от PARI, а также мембранный небулайзер (прототипы технологии Vibrent™).
Небулайзер, используемый в способе по изобретению, представляет собой мембранный небулайзер. Предпочтительно, мембранный небулайзер представляет собой вибрационный мембранный небулайзер. Небулайзеры последнего типа содержат резервуар, в который заполнена жидкость для распыления. При работе небулайзера жидкость подается нa мембрану, сделанную так, что она способна колебаться, т.е. вибрировать (например, с помощью пьезоэлектрического элемента). Жидкость, присутствующая на одной стороне вибрирующей мембраны, транспортируется таким образом через отверстия в вибрирующей мембране (также обозначаемые как «поры» или «дыры») и принимает форму аэрозоля на другой стороне вибрирующей мембраны. (Например, eFlow rapid и eRapid от PARI, HL100 от Health and Life, а также AeronebGo и AeronebSolo от Aerogen). Такие небулайзеры могут обозначаться как «активные мембранные небулайзеры».
В других полезных мембранных небулайзерах, композицию можно распылять с помощью вибрации жидкости, а не мембраны. Такой колебательный жидкостной мембранный небулайзер содержит резервуар, в который заполняют жидкость, которую предстоит распылить. При работе небулайзера жидкость подается на мембрану через систему подачи жидкости, причем система сконструирована так, что она способна колебаться (т.е. вибрировать, например, с помощью пьезоэлектрического элемента). Эта система подачи жидкости может представлять собой вибрирующую заднюю стенку резервуара (например, AerovectRxTM Technology, Pfeifer Technology) или вибрирующий скользящий элемент транспортировки жидкости (например, устройство I-NebTM от Respironics или устройство U22TM от Omron). Эти небулайзеры могут обозначаться как «пассивные мембранные небулайзеры».
Различные типы мембран доступны для распыления жидкостей с использованием мембранного небулайзера. Эти мембраны характеризуются различными размерами пор, которые генерируют аэрозоли с различными размерами капель (MMD и GSD). В зависимости от характеристик композиции и желаемых характеристик аэрозоля, могут быть использованы мембраны различного типа (то есть различные модифицированные мембранные небулайзеры или аэрозольные генераторы). В способе по настоящему изобретению, предпочтительно использовать типы мембран, которые генерируют аэрозоль с MMD в диапазоне от 2 мкм до 5, предпочтительно в диапазоне от 3 мкм до 4,9 и более предпочтительно в диапазоне от 3,4 мкм до 4,5 мкм. В другом воплощении изобретения, предпочтительно использовать типы мембран, встроенных в устройства аэрозольных генераторов, которые генерируют аэрозоль, например, изотонический солевой раствор (NaCl 0,9%) с MMD в диапазоне от 2,8мкм до 5,5 мкм, предпочтительно в диапазоне от 3,3 мкм до 5 мкм и более предпочтительно в диапазоне от 3,3 мкм до 4,4 мкм. В другом воплощении изобретения, предпочтительно использовать типы мембран, встроенных в устройства аэрозольных генераторов, которые генерируют аэрозоль, например, изотонический солевой раствор, с MMD в диапазоне от 2,8 мкм до 5,5 мкм, предпочтительно в диапазоне от 2,9 мкм до 5 мкм и более предпочтительно в диапазоне от 3,8 мкм до 5 мкм.
Авторы настоящего изобретения обнаружили, что способ по изобретению действует особенно хорошо, когда резервуар изолирован от атмосферы, так что давление в резервуаре снижается до или во время стадии распыления жидкой водной композиции, содержащей поликлональные Ig, например, IgG, IgA, IgM или их комбинации (т.е. стадия (с)). Другими словами, способ особенно эффективен, если жидкая водная композиция подается на мембрану под давлением, которое немного ниже атмосферного давления области, в которую испускаются капли аэрозоля. Исходное давление в резервуаре, перед стадией распыления жидкости, предпочтительно составляет, по меньшей мере, 50 мбар, более предпочтительно, по меньшей мере, 75 мбар, и наиболее предпочтительно, по меньшей мере, 100 мбар.
Кроме того, генератор аэрозоля имеет устройство, создающее отрицательное давление, взаимодействующее с жидкостным резервуаром таким образом, чтобы увеличить объем (V1) жидкостного резервуара в герметичном состоянии жидкостного резервуара до объема (V2) до того, как мембрана начнет колебаться (то есть до начала введения или использования). Такое устройство, создающее отрицательное давление, может быть сделано, как описано в патенте США 6983747 В2, который включен с помощью ссылки в полном объеме. В качестве альтернативы, устройство, создающее отрицательное давление, также может быть сконфигурировано, как описано в публикации WO 2007/020073 А1, которая включена с помощью ссылки в полном объеме.
Для того, чтобы реализовать уменьшение давления в резервуаре, особенно предпочтительно изолировать резервуар от атмосферы уплотнительным элементом (16), расположенный на отверстии в резервуаре (10), чтобы обеспечить герметичное уплотнение для отверстия, и скользящий элемент (21), соединенный с уплотнительным элементом (16) таким образом, что движение скользящего элемента (21) осуществляет перемещение, по меньшей мере, одной секции (18) уплотнительного элемента (16), в результате чего в резервуаре (10) генерируется отрицательное давление, как показано на рисунке 1. Такой способ уменьшения давления внутри резервуара описан в публикации WO 02/064265, которая включена с помощью ссылки в полном объеме. В качестве альтернативы, устройство, создающее отрицательное давление, также может быть сконфигурирован так, как описано в публикации ЕР 1353759 В1, которая включена с помощью ссылки в полном объеме. В других полезных мембранных небулайзерах отрицательное давление генерируется в герметичном жидкостном резервуаре с помощью запирающего элемента или механической системы, например, с помощью сильфонов, увеличивающих объем, перемещение, всасывание, прокачивание или тому подобное.
В качестве альтернативы, устройство, создающее отрицательное давление в резервуаре, может быть также сконфигурировано с возможностью генерирования почти постоянного диапазона отрицательного давления в резервуаре в течение всего процесса генерирования аэрозоля из жидкой среды или жидкости. Диапазон отрицательного давления в резервуаре, во время стадии распыления жидкости, предпочтительно, составляет от 50 до 400 мбар, более предпочтительно от 100 до 400 мбар, еще более предпочтительно от 100 до 350 мбар, и наиболее предпочтительно, от 100 до 200 мбар. Такое устройство с диапазоном отрицательного давления может быть сделано, как описано в публикации WO 2012/069531 А2, которая включена с помощью ссылки в полном объеме.
Однако отрицательное давление также может генерироваться индивидуально во время распыления, или отрицательное давление, генерируемое с помощью запирающего элемента, как описано выше, может поддерживаться на достаточно постоянном уровне при проведении распыления (т.е. на стадии (c)).
Если способ предназначен для направленного воздействия на нижние дыхательные пути, такие как бронхи или глубоко в легких, особенно предпочтительно выбирать пьезоэлектрический перфорированный небулайзер мембранного типа для генерирования аэрозоля. Примеры подходящих небулайзеров включают пассивный мембранный небулайзер, такой как I-Neb™, U22™, U1™, Micro Air™, ультразвуковой небулайзер, например Multisonic™, и/или активный мембранный небулайзер, такой как HL100™, Respimate™, небулайзеры Технология eFlow™, Aeroneb™, Aeroneb Pro™, AeronebGo™ и устройства семейства AeroDose™, а также прототип Пфайфер, Chrysalis (Philip Morris) или устройства AerovectRxTM. Особенно предпочтительным небулайзером для направленного воздействия лекарственного средства на нижние дыхательные пути является вибрационный небулайзер с перфорированной мембраной или так называемый активный мембранный небулайзер, такой как, например, небулайзер eFlow™ (электронный вибрационный мембранный небулайзер доступен от PARI, Германия). В качестве альтернативы может быть использован пассивный мембранный небулайзер, например, U22™ или U1™ от компании Omron или небулайзер на основе метода Telemaq.fr или метода Ing. Erich Pfeiffer GmbH.
Предпочтительный мембранный небулайзер для направленного воздействия на верхние дыхательные пути, представляет собой небулайзер, который генерирует аэрозоль посредством принципа перфорированной вибрирующей мембраны, такой как модифицированный исследовательский мембранный небулайзер с использованием технологии eFlow™, но который также способен испускать пульсирующий поток воздуха таким образом, чтобы аэрозольное облако пульсировало (т.е. испытывает флуктуации давления) в целевом месте или во время транспортировки аэрозольного облака в целевое место (например, синоназальные или околоносовые пазухи). Этот тип небулайзера содержит сопло для направления потока, переносящего облако аэрозоля в нос. Аэрозоли, доставляемые таким модифицированным электронным небулайзером, могут достигать синоназальных или околоносовых полостей намного лучше, чем когда аэрозоль доставляется в непрерывном режиме (не пульсирующем). Волны пульсирующего давления достигают более интенсивной вентиляции пазух таким образом, что одновременно с этим применяемый аэрозоль лучше распределяется и депонируется в этих полостях.
Более конкретно, предпочтительный небулайзер для направленного воздействия на верхние дыхательные пути пациента, представляет собой небулайзер, приспособленный для генерирования аэрозоля с эффективной скоростью потока менее примерно 5 л/мин и для одновременно действующих средств для осуществления пульсации давления аэрозоля с частотой в диапазоне примерно от 10 примерно до 90 Гц, где эффективная скорость потока представляет собой скорость потока аэрозоля при его поступлении в дыхательную систему пациента. Примеры таких электронных устройств распыления раскрыты в WO 2009/027095.
В предпочтительном воплощении изобретения, небулайзер для направленного воздействия на верхние дыхательные пути представляет собой небулайзер, который использует транспортный поток, который может быть прерван, когда аэрозольное облако достигает целевого участка, и затем запускает пульсацию аэрозольного облака, например, в периодическом режиме. Подробности описаны в WO 2010/097119 A1 и WO 2011/134940 A1.
Небулайзер, либо адаптированнный для легочной, либо для синоназальной доставки, предпочтительно, должен быть выбран или адаптированы так, чтобы быть способным к аэрозолизации однократной дозы с предпочтительной скоростью выходящего потока. Однократная доза определяется в данном документе как объем жидкой водной композиции, содержащей эффективное количество активного соединения, т.е. Ig, IgG, IgA, IgM или их комбинации, предназначенные для введения во время однократного введения. Предпочтительно, небулайзер может доставлять такую однократную дозу со скоростью, составляющей, по меньшей мере, 0,1 мл/мин, или, если предположить, что относительная плотность композиции обычно составляет около 1, то со скоростью по меньшей мере 100 мг/мин. Более предпочтительно, небулайзер способен генерировать скорость выходящего потока, составляющую, по меньшей мере, 0,4 мл/мин или 400 мг/мин, соответственно. В других воплощениях скорости выходящего потока жидкости из небулайзера или генератора аэрозоля составляют, по меньшей мере, 0,5 мл/мин, предпочтительно, по меньшей мере, 0,55 мл/мин, более предпочтительно, по меньшей мере, 0,60 мл/мин, еще более предпочтительно, по меньшей мере, 0,65 мл/мин, и наиболее предпочтительно, по меньшей мере, 0,7 мл/мин, причем такие устройства, называют аэрозольными генераторами с высоким выходом и высокой скоростью выходящего потока. Предпочтительно, диапазоны скоростей выходящих потоков жидкости составляют примерно от 0,35 примерно до 1 мл/мин или примерно от 350 примерно до 1000 мг/мин; предпочтительно диапазоны скоростей выходящего потока жидкости на выходе составляют примерно от 0,5 примерно до 0,9 мл/мин или примерно от 500 примерно до 800 мг/мин. Скорости выходящего потока жидкости означает количество жидкой композиции, распыляемой через небулайзер за единицу времени. Жидкость может содержать активное соединение, лекарственное средство, Ig, IgG, IgA, IgM, или их комбинации и/или заменитель, такой как хлорид натрия 0,9%.
Было установлено, что для способа по изобретению, то есть для генерирования аэрозоля из поликлональных Ig, например, IgG, IgA, IgM или их комбинации для интенсификации выходящего потока может использоваться композиция в концентрации от 20 до 200 мг/мл, специфические типы мембраны в небулайзере. Например, было обнаружено, что особенно предпочтительно по отношению к интенсивности выходящего потока использовать мембрану (122), имеющую первую сторону (124) для контакта с жидкостью, и противоположную вторую сторону (125), мембрану, имеющую множество сквозных отверстий (126), пронизывающих мембрану в направлении удлинения (E) от первой стороны ко второй стороне, в результате чего жидкость проходит через сквозные отверстия от первой стороны ко второй стороне, когда мембрана вибрирует для генерирования аэрозоля на второй стороне, причем каждое сквозное отверстие (126), имеет вдоль его направления удлинения (E) наименьший диаметр (ДС), больший диаметр (DL), который больше, чем наименьший диаметр и определяется диаметром, который ближе всего к утроенному, предпочтительно к удвоенному наименьшему диаметру, причем каждое сквозное отверстие имеет сопло (132), ограниченное непрерывным участком сквозного отверстия в направлении удлинения, содержащим наименьший диаметр сквозного отверстия и ограниченным более крупным диаметром сквозного отверстия, отличающимся тем, что отношение общей длины каждого сквозного отверстия (126) в направлении удлинения к соответствующей длине указанных частей сопла (132) в направлении улинения составляет, по меньшей мере, 4. Такая мембрана описана в публикации WO 2012/168181 A1 и показана на Фигуре 2, на которой представлено изображение компьютерной томографии (КТ) с прилагаемым описанием.
Интенсивность выходящего потока небулайзера должна быть выбрана для достижения короткого времени распылении жидкой композиции. Обычно время распыления будет зависеть от объема композиции, которую следует аэрозолизировать, и от интенсивности выходящего потока. Предпочтительно, небулайзер должен быть выбран или адаптирован так, чтобы быть способным к аэрозолизации объема жидкой композиции, содержащей эффективную дозу поликлонального Ig, например, IgG, IgA, IgM, или их комбинации, в течение не более чем 20 минут. Более предпочтительно, время распыления для однократной дозы не должно составлять более чем 15 минут. В следующем воплощении небулайзер выбирают или адаптируют так, чтобы время распыления на однократную дозу могло составлять не более чем 10 минут, и более предпочтительно не более чем 6 минут, а еще более предпочтительно, не более чем 3 минуты. В настоящее время наиболее предпочтительным является время распыления, составляющее от 0,5 до 5 минут.
Объем композиции, которую распыляют на стадии (с) способа по изобретению, предпочтительно является низким, чтобы была возможность короткого времени распыления. Объем, также обозначаемый как объем дозы или единицы объема дозы, или объем единицы дозы, следует понимать, как объем, который предназначен для использования в течение одного однократного введения или одного сеанса терапии с использованием небулайзера. В частности, объем может составлять от 0,3 мл до 6 мл, предпочтительно от 0,5 мл до 4 мл, или более предпочтительно от 1 мл до 3 мл, или еще более предпочтительно примерно 2 мл. В случае если желателен или полезен остаточный объем, то этот остаточный объем должен составлять менее, чем 1 мл, более предпочтительно менее чем 0,5 мл и наиболее предпочтительно менее чем 0,3 мл. Эффективно распыляемый объем следовательно предпочтительно составляет от 0,2 до 3 мл или от 0,5 до 2,5 мл, или более предпочтительно, от 0,75 до 2,5 мл или от 1 до 2,5 мл.
Предпочтительно, небулайзер адаптирован для генерирования аэрозоля, где основная фракция загруженной дозы жидкой композиции доставляется в виде аэрозоля, то есть имеет высокий выход. Более конкретно, небулайзер выполнен с возможностью генерирования аэрозоля, который содержит по меньшей мере 50% дозы Ig, например, IgG, IgA, IgM или их комбинации, в композиции, или, другими словами, испускает по меньшей мере, 50% жидкой композиции, заполненной в резервуар. Особенно по сравнению с моноклональными антителами, из которых дозы не должны быть столь же высоким из-за своей специфичности, важно выбрать небулайзер, который может генерировать такой высокий выход поликлональных Ig, например, IgG, IgA, IgM или их комбинации. Было установлено, что мембранный небулайзер, используемый в способе по изобретению, способен генерировать аэрозоль поликлональных Ig, например, IgG, IgA, IgM или их комбинации, композиции с особенно высоким выходом.
Кроме того, небулайзер может содержать камеру с клапаном вдоха и выдоха, также обозначаемую как аэрозольная камера или смесительная камера. Резервуар мембранного небулайзера заполняют жидкостью, и мембрана генерирует аэрозоль в смесительной камере. Предпочтительно клапан выдоха расположен рядом с соплом, и клапан вдоха расположен вблизи входного отверстия окружающего воздуха. Это уменьшает потерю аэрозоля во время фазы выдоха пациента, так как аэрозоль, который образуется во время этой фазы, в основном сохраняется в смесительной камере, пока пациент не вдыхает. Мембранный небулайзер с такой смесительной камерой описан в WO 2001/34232 и WO 2010/066714.Могут использоваться смесительные камеры разного размера. В способе по настоящему изобретению, предпочтительно использовать большую смесительную камеру, имеющую объем, по меньшей мере, 45 мл, более предпочтительно по меньшей мере 50 мл, еще более предпочтительно, по меньшей мере, 60 мл. В качестве альтернативы можно использовать большую смесительную камеру, имеющую объем, составляющий от 60 до 150 мл. Мембранный небулайзер с такой большой смесительной камерой описан в публикации ЕР 1927373, которая включена с помощью ссылки в полном объеме.
Предпочтительно, жидкая водная композиция, используемая в способе по изобретению, содержит один или более стабилизаторов. Часто встречающейся проблемой при разработке составов жидких композиций иммуноглобулинов является то, что иммуноглобулины имеют тенденцию к агрегации и образуют преципитаты, если они не стабилизированы в достаточной степени с помощью соответствующих добавок. Некоторые аминокислоты, такие как пролин, глицин и гистидин, или сахариды, или сахарные спирты, или белки, такие как альбумин, или их комбинации, как известно, стабилизируют иммуноглобулины в жидких композициях и могут использоваться в жидкой водной композиции.
Для легочного введения Ig с помощью распыления, например IgG, IgA, IgM, или их комбинации, предпочтительно использовать высокие концентрации Ig, например IgG, IgA, IgM или их комбинации. Как правило, высокие дозы поликлональных Ig необходимы, но важно свести к минимуму распыляемый объем настолько, насколько это возможно для того, чтобы сохранить время распыления как можно более коротким. Последнее имеет отношение к соблюдению пациентом схемы лечения. Таким образом, композиции Ig с высокой концентрацией Ig являются предпочтительными в способе по изобретению. Однако было установлено, что увеличение концентрации Ig приводит к нелинейному увеличению вязкости.
В общем известно, что динамическая вязкость жидкой композиции оказывает влияние на распределение размера капель аэрозоля, образованного при распылении этой композиции, и на эффективность распыления. Для распылении жидких композиций с использованием мембранного небулайзера, как правило, предпочтительно, чтобы жидкая композиция, используемая в способе по изобретению, демонстрировала динамическую вязкость, составляющую примерно от 0,8 примерно до 4 мПа⋅с при температуре 20°С +/- 0,1°С).Более предпочтительно, динамическая вязкость составляет примерно от 1 примерно до 3,5 мПа⋅с при температуре 20°C +/- 0,1°С при измерении с помощью вискозиметра с падающим шариком («Kugelfallviskosimeter») согласно Höppler в соответствии с Европейской Фармакопеей версии 6.0, 2.2.49 и требованиям DIN 53015. Таким образом, определяют время прокатки шара или сферы в трубе или капилляра определенных размеров, и имеющего определенный наклон. На основе времени прокатки может быть определена вязкость жидкости в трубке или капилляре. Измерения, как правило, производятся при температуре 20°С +/- 0,1°C.
Одно из воплощений изобретения представляет собой способ генерирования аэрозоля раствора иммуноглобулина, где раствор иммуноглобулина имеет вязкость от 1 до 17 мПа·с, от 1 до 16 мПа·с, от 1 до 15 мПа·с, от 1 до 14 мПа·с, 1 до 13 мПа·с, от 1 до 12 мПа·с, от 1 до 11 мПа·с, от 1 до 10 мПа·с, от 2 до 17 мПа·с, от 2 до 16 мПа·с, от 2 до 15 мПа·с, от 2 до 14 мПа·с, от 2 до 13 мПа·с, от 2 до 12 мПа·с, от 2 до 11 мПа·с, от 2 до 10 мПа·с, от 3 до 17 мПа·с, от 3 до 16 мПа·с, от 3 до 15 мПа·с, от 3 до 14 мПа·с, от 3 до 13 мПа·с, от 3 до 12 мПа·с, от 3 до 11 мПа·с, от 3 до 10 мПа·с; предпочтительно раствор иммуноглобулина имеет вязкость от 1 до 9 мПа·с, от 1 до 8 мПа·с, от 1 до 7 мПа·с, от 1 до 6 мПа·с, 2 до 9 мПа·с, от 2 до 8 мПа·с, от 2 до 7 мПа·с, от 2 до 6 мПа·с, от 3 до 9 мПа·с, от 3 до 8 мПа·с, от 3 до 7 мПа·с, или от 3 до 6 мПа·с; более предпочтительно раствор иммуноглобулина имеет вязкость от 1 до 5 мПа·с, от 1 до 4 мПа·с, от 2 до 5 мПа·с, от 2 до 4 мПа·с, от 3 до 5 мПа·с, или от 3 до 4 мПа·с.
Для того, чтобы избежать проблем распыления, вызванных высокой вязкостью, было установлено, что пролин, предпочтительно используют в качестве стабилизатора, так как при этом может быть достигнута относительно низкая вязкость препаратов Ig, например, IgG, IgA, IgM или их комбинации, даже если концентрация Ig является высокой, как описано в WO2011/095543. Таким образом, было установлено, что особенно предпочтительным является добавление пролина к композициям поликлональных Ig, когда эти композиции предназначены для использования в способах генерирования аэрозоля с использованием небулайзера. Пролин обеспечивает с одной стороны, целевую стабильность Ig в жидкой композиции, а с другой стороны, это снижает вязкость композиции, таким образом, позволяя распыление небольшого объема жидкости с высокой концентрацией Ig, что приводит к быстрому и эффективному лечению с помощью небулайзера.
При использовании пролина в качестве стабилизирующего агента, особенно предпочтительно использовать L-пролин. L-пролин, как правило, присутствует в организме человека, и имеет очень благоприятный профиль токсичности. Безопасность L-пролина была изучена в исследованиях при многократном введении доз токсичности, в исследованиях воспроизведения токсичности, мутагенности и безопасности фармакологии, и при этом не было отмечено никаких побочных эффектов.
Как правило, количество пролина, и более предпочтительно L-пролина, которое добавляют в композицию, таково, что концентрация пролина в композиции иммуноглобулина составляет примерно от 10 примерно до 1000 ммоль/л, более предпочтительно примерно от 100 примерно до 500 ммоль/л, и наиболее предпочтительно, составляет примерно 250 ммоль/л.
В одном воплощении изобретения, вязкость жидкой водной композиции, содержащей поликлональные IgG и стабилизирующее количество пролина составляет от 1 мПа⋅с до 17 мПа⋅с (при температуре 20°C +/- 0,1°C).Вязкость композиции, содержащей 100 мг/мл поликлональных IgG и 250 мМ пролина, составляет примерно 3 мПа⋅с при температуре 20°С +/- 0,1°C.
Композиция IgG, используемая согласно изобретению и содержащая пролин, имеет рН от 4,2 до 5,4, предпочтительно от 4,6 до 5, наиболее предпочтительно примерно 4,8, что дополнительно обеспечивает высокую стабильность препарата.
Использование пролина позволяет приготовить композицию таким образом, что стабильность состава увеличивается, и вязкость композиции уменьшается с использованием одного единственного агента. Это приводит к получению композиции, которая особенно полезна в способах генерирования аэрозоля с использованием мембранного небулайзера.
Жидкая композиция, используемая в способе по изобретению, может также содержать другие фармацевтически приемлемые вспомогательные вещества, которые служат для оптимизации характеристик композиции и/или характеристик аэрозоля. Примеры таких вспомогательных веществ представляют собой вспомогательные вещества для доведения или буферизация рН, вспомогательные вещества для регуляции осмоляльности, антиоксиданты, поверхностно-активные вещества, вспомогательные вещества для замедленного высвобождения или пролонгированного местного удерживания, агенты, маскирующие вкус, подсластители и ароматизаторы. Эти вспомогательные вещества используются для получения оптимального рН, осмоляльности, вязкости, поверхностного натяжения и вкуса, которые поддерживают стабильность состава, аэрозолизацию, переносимость и/или эффективность состава при ингаляции.
Растворы иммуноглобулина, используемые в изобретении, имеют поверхностное натяжение от 60 до 75 мН/м, предпочтительно примерно от 64 до 71 мН/м.
Например, в композицию могут быть добавлены поверхностно-активные вещества. Они могут помогать контролировать скорость агрегации иммуноглобулинов в композиции (то есть во время хранения и в резервуаре), и во время распыления (то есть во время и после прохождения через мембрану небулайзера), тем самым оказывая влияние на активность Ig, например, IgG, IgA, IgM, или их комбинации, в аэрозоле. Примеры полезных поверхностно-активных веществ представляют собой полисорбаты, такие как полисорбат 80.
В общем, было установлено, что применение способа согласно изобретению приводит к получению аэрозоля, в котором активность Ig, например, IgG, IgA, IgM, или их комбинации, составляет, по меньшей мере 80% активности иммуноглобулина в композиции, заполненной в резервуар небулайзера. Таким образом, способ по изобретению не приводит ни к значительной агрегации Ig, ни к значительной денатурации Ig. Активность Ig может быть определена с помощью стандартных иммунологических методов (например, тИФА, проточная цитометрия и клеточные анализы).
Аэрозоль, полученный с помощью способа согласно изобретению, может быть использован для лечения и профилактики ряда патологических состояний, где проявляются поликлональные Ig, например, IgG, IgA, IgM, или их комбинации.
Конкретно, аэрозоль, генерированный с помощью способа согласно изобретению, может использоваться для пациентов, нуждающихся в заместительной терапии, т.е. для пациентов, имеющих заболевание легких, синусит, пациентов с риском рецидивирующих инфекций, так как они не имеют достаточного количества антител, или, другими словами, которые имеют синдром иммунодефицита. Более конкретно, аэрозоль может использоваться при лечении пациентов с первичным иммунодефицитом (PID), вторичным иммунодефицитом (SID), например, гипогаммаглобулинемией и рецидивирующими бактериальными инфекциями, вызванными хроническим лимфолейкозом или множественной миеломой, гипогаммаглобулинемии после аллогенной трансплантации стволовых клеток крови (HSCT), гипогаммаглобулинемии, вызванной химиотерапией для лечения злокачественных опухолей, гипогаммаглобулинемии, вызванной обработкой биологическими препаратами, например, ритуксимабом, для лечения злокачественных опухолей или аутоиммунных заболеваний, восприимчивости к инфекции дыхательных путей в результате иммуноподавляющих препаратов для лечения аутоиммунного заболевания или трансплантации твердых органов, и для пациентов с приобретенным синдромом иммунодефицита (AIDS, HIV). Кроме того, аэрозоль может использоваться при лечении патологических состояний с хроническими инфекциями дыхательных путей, таких как кистозный фиброз и первичная цилиарная дискинезия, хроническая обструктивная болезнь легких (COPD), хронический бактериальный синусит, патологических состояний с хроническим воспалением дыхательных путей, таких как бронхиолит облитерирующий, облитерирующий бронхиолит с организующейся пневмонией, не кистозно-фиброзный бронхоэктаз, хронический бактериальный бронхит, интерстициальная болезнь легких, бронхиальная астма, или обычная интерстициальная пневмония, или при аллергических состояниях, таких как экзогенный аллергический альвеолит, аллергическая астма или хронический синусит.
Кроме того, аэрозоль, генерированный с помощью способа по изобретению, может быть использован для иммуномодуляции у пациентов, которые имеют аномальную иммунную систему, которую следует скорректировать. Таким образом, аэрозоль может быть использован для пациентов с идиопатической (или первичной) тромбоцитопенической пурпурой (ITP), которые относятся к группе высокого риска кровотечения или которые нуждаются в коррекции количества тромбоцитов перед операцией, у пациентов с синдромом Гийена-Барре, болезнью Кавасаки или с хронической воспалительной демиелинизирующей полинейропатией (CIDP).
Коммерчески доступные составы иммуноглобулинов, перечисленные в следующей таблице, могут быть использованы в способе согласно изобретению в качестве жидкой водной композиции, содержащей поликлональный иммуноглобулин G:
*PS80=Полисорбат 80
**NR= не сообщается
Примеры
Следующие не ограничивающие примеры служат для иллюстрации изобретения.
Пример 1: Распыление IgG
Оценивали распыление композиции, содержащей 100 мг/мл нормального человеческого иммуноглобулина и 0,25 моль/л пролина в воде для инъекций. Фракцию иммуноглобулинов, которая содержала, по меньшей мере, 98% IgG, и композицию, которая содержала по большей мере 25 мкг IgA на мл; получали из плазмы доноров крови человека. Композиция имела рН 4,82, плотность 1,0336 г/мл, вязкость 3,33 мПа⋅с при 20°С, поверхностное натяжение 71,1 мН/м при температуре 20°С и осмоляльность 312 мОсм/кг.
Распыление проводили с помощью электронного вибрационного мембранного небулайзера (модифицированный мембранный небулайзер с использованием технологии eFlow™, PARI Pharma GmbH, Германия), имеющего большую смесительную камеру (с приблизительно 90 мл объема), начальное отрицательное давление в резервуаре для жидкости в диапазоне от 100 до 400 мбар, а также различные типы мембран, имеющих разные размеры отверстий и геометрию отверстий. Различные типы мембран предназначены для создания различного размера капель или частиц (характеризующихся медианным диаметром массы (MMD) и геометрическим стандартным отклонением (GSD)) и/или различных скоростей выходящего потока (например, скорости доставки лекарственного средства (DDR) или общей скорости выходящего потока (TOR или так называемый выход)). Нормальная скорость выходящего потока мембраны, помещенной в устройстве генератора аэрозоля, определяется ниже 0,55 мл/мин, и высокая выходная скорость определяется значениями по меньшей мере, мере, 0,55 мл/мин. В качестве альтернативы скорость выходящего потока может быть охарактеризована (или определена) в мг/мин; следовательно, нормальная скорость выходящего потока составляет например, ниже 550 мг/мин и высокая скорость выходящего потока составляет например, по меньшей мере, 550 мг/мин. (В качестве альтернативы предел для высокой скорости выходящего потока может быть определен с помощью по меньшей мере, 0,5 мл/мин, предпочтительно, по меньшей мере, 0,55 мл/мин, более предпочтительно, по меньшей мере, 0,6 мл/мин, или, наиболее предпочтительно, по меньшей мере, 0,65 мл/мин, и скорость выходящего потока в мг/мин соответственно). Предел зависит от характеристик жидкости, например, плотности, вязкости, поверхностного натяжения и так далее, и он может определяться для целей контроля качества устройств генератора аэрозоля, например, для суррогатного раствора типа хлорида натрия 0,9% вместо раствора Ig, например, IgG, IgA и/или IgM. Тогда нормальная скорость выходящего потока суррогатного раствора (например, хлорид натрия 0,9%), генерированная из мембраны, встроенной в устройстве генератора аэрозоля, определяется на уровне, составляющем, по меньшей мере, 0,55 мл/мин, более предпочтительно, по меньшей мере, 0,6 мл/мин и более предпочтительно, по меньшей мере, 0,65 мл/мин. В качестве альтернативы высокая скорость выходящего потока составляет по меньшей мере 550 мг/мин, предпочтительно, по меньшей мере, 600 мг/мин, и более предпочтительно, по меньшей мере, 650 мг/мин. Типы электронной мембраны, которые были использованы для распыления композиции IgG, идентифицированы и охарактеризованы в таблице 1.
Таблица 1: Типы мембран, используемые для распыления композиции IgG (с использованием технологии eFlow™)
Прибор лазерной дифракции (Malvern Mastersizer X™) использовали для определения размеров капель (выраженного в виде медианного диаметра массы (MMD)) и распределения по размерам капель (выраженного в виде геометрического стандартного отклонения (GSD)) генерируемых аэрозолей. Объем 2 мл композиции IgG заполняли в резервуар небулайзера и анализировали аэрозоль, полученный при работе небулайзера, путем направления аэрозольного облака через лазерный луч прибора MasterSizer XTM с использованием потока аспирации 20 л/мин. Температура и относительная влажность воздуха во время измерений составили 23°C±2°C) и 50%±5%), соответственно. В том же эксперименте, оценивали суммарную скорость выходящего потока (TOR). Измерение проводили дважды для каждого типа мембраны (n=2). Результаты (средние значения и стандартные отклонения (SD)), показаны в Таблице 2.
Таблица 2: Результаты экспериментов по дифракции лазерного излучения и суммарной скорости выходящего потока
Пример 2: Воспроизводимость распыления IgG
Эксперименты лазерной дифракции, описанные в Примере 1, повторяли с тремя модифицированными мембранными небулайзерами с использованием технологии eFlow™ и имеющих большую смесительную камеру (около 90 мл), начальное отрицательное давление в резервуаре для жидкости в диапазоне от 100 до 400 мбар, с использованием мембран типа 2 и типа 4 (как указано выше). Дополнительно к определению MMD, GSD и TOR, измеряли процент капель размером менее чем 5 мкм, менее чем 3,3 мкм и менее чем 2 мкм (т.е. процент различных вдыхаемых фракций (RF)). Фракция капель менее чем 5 мкм дает хорошее представление о процентах капель, ингалируемых в нижних отделах дыхательных путей взрослого, в то время как доля капель менее, чем 3,3 мкм дает оценку процента капель, ингалируемых в нижние дыхательные пути ребенка. Фракция капель размером менее 2 мкм показывает процент капель, способных достичь терминальных бронхиол и альвеол. Депонирование в легких аэрозолей с различным размером частиц можно рассчитать с помощью математических моделей, таких как, например, модель ICRP (Модель депонирования в дыхательных путях, предложенная группой дозиметрии и радиационной защиты для решения задачи ICRP (1991) 38 (1-3): 159- 165, A.C. James et al.), для разных возрастных групп, типа взрослых, детей, младенцев или новорожденных.
Эксперименты проводились дважды для каждого тестируемого небулайзера (n=2). Результаты измерений приведены в Таблице 3.
Таблица 3: Результаты экспериментов по дифракции лазерного излучения и суммарной скорости выходящего потока с различными небулайзерами
Пример 3: Распыление различных составов иммуноглобулинов
Различные выделенные из плазмы изотипы иммуноглобулинов и полимеры (IgA и IgM), а также составы IgG распыляли, и полученные аэрозоли охарактеризовывали способом, аналогичным способу, описанному в Примере 1, с использованием того же небулайзера и мембран.
Более конкретно, характеристики аэрозолей, полученных с помощью распыления из следующих составов, сравнивали с помощью лазерной дифракции.
Распределение частиц по размерам определяли с помощью измерения лазерной дифракции (Malvern Mastersizer X™) каждого из составов при распылении с использованием исследовательской системы небулайзера eFlowTM с большой смесительной камерой и резервуаром, индуцирующим отрицательное давление при закрытии каждого, с 2-мя различными типами мембран (как указано в Примере 1). Объем заполнения составил 2 мл в каждом случае. Измеряемые параметры представляли собой MMD, GSD, суммарную скорость выходящего потока (TOR) и вдыхаемую фракцию. ТОР определяли путем взвешивания заполненного небулайзера до распыления и после полного распыления и рассчитывали путем деления разности массы на время распыления.
Все измерения проводили по три раза. Результаты (средние значения трех измерений и стандартные отклонения (SD)), показаны в Таблице 4.
Таблица 4: Результаты экспериментов по дифракции лазерного излучения и суммарной скорости выходящего потока для различных композиций иммуноглобулина
%
НО: Не определено
Эти результаты демонстрируют, что все исследуемые составы могут быть распылены с хорошей производительностью.
Пример 4: Эксперименты моделирования дыхания
Распыление композиций, описанных в Примере 1 и Примере 3, также оценивали в экспериментах моделирования дыхания с тремя модифицированными мембранными небулайзерами с использованием технологии eFlow™ и имеющими большую смесительную камеру с использованием мембран типа 2 и 4 (как указано выше). Каждый из небулайзеров тестировали дважды (n= 2).
Эксперименты моделирования дыхания проводили с использованием профиля дыхания взрослых согласно Ph.Eur. 2.9.44 (т.е. синусоидальный поток с дыхательным объемом 500 мл, 15 вдохов в минуту и ингаляция:выдох (I:E) соотношение 50:50). В каждом тесте небулайзер был подключен к синусоидальному насосу (симулятор дыхания PARI Compass IITM). Инспираторный фильтр (полипропилен; 3М) был установлен между небулайзером, включая насадку и насос, и зафиксирован резиновыми коннекторами. Небулайзер заполняли 2 мл композиции, описанной в Примере 1, и распыление начинали и продолжали до тех пор, пока получения аэрозоля уже не было видно. Капли аэрозоля, содержащие лекарственное средство, собирали на фильтре для ингаляции.
Для определения доставленной дозы, то есть количества иммуноглобулина, собранного на фильтре во время распыления, фильтр для ингаляции удаляли из корпуса фильтра с помощью пинцета и помещали в 50 мл пластиковую пробирку с завинчивающейся крышкой. После этого корпус фильтра промывали 40 мл буфера, содержащего 0,9% солевой раствор и 0,5% SDS (додецилсульфат натрия, 98,5%) в очищенной воде, и промывочную жидкость затем добавляли в пробирку с фильтром. Фильтр экстрагировали в течение 1 ч при встряхивании на ротаторе.
Кроме того, небулайзер несколько раз промывали с помощью 40 мл описанного выше буфера, и промывочный раствор собирали в химический стакан для определения количества оставшегося в резервуаре лекарственного средства (остаток).
Растворы, полученные в результате экстракции фильтра и промывки небулайзера, анализировали с помощью УФ-спектрофотометрии. Образец каждого из растворов разбавляли буфером для достижения концентрации приблизительно 0,5 мг/мл иммуноглобулина. Приблизительно 0,8 мл разбавленного раствора образца помещали в одноразовую микрокювету и измеряли против буфера при 280 нм. Содержание Ig в растворе рассчитывали в соответствии с законом Ламберта-Бера (A=ε·СхL), с использованием коэффициента поглощения массы ε (0,1%)=1,38 мл/(мг⋅см). Более конкретно, формула для расчета содержания Ig:
с (мг/мл)=коэффициент разведения* A280/ε * л
Вдыхаемые дозы рассчитывали на основе доставленной дозы и средних вдыхаемых фракций, определенных с помощью лазерной дифракции в Примере 2.
В ходе экспериментов моделирования дыхания, время распыления также фиксировали.
Результаты экспериментов моделирования дыхания суммированы в Таблицах 5а и 5b. Для каждого тестируемого параметра, среднее из результатов 6 опытов для каждого типа мембраны (то есть 2 теста 3-х различных небулайзеров) представлено вместе со стандартным отклонением (SD).
Таблица 5а: Результаты, полученные для IgG (10%) в экспериментах по моделированию дыхания
(благодаря выдыханию)
Таблица 5b: Результаты, полученные для различных составов в экспериментах моделирования дыхания
Пример 5: Биохимические свойства иммуноглобулинов после распыления (характеристика молекулярного размера)
Распыляемые композиции, полученные в Примере 1 и Примере 3, были охарактеризованы для структурной целостности и мультимеризации иммуноглобулинов. С этой целью проводили (i) SDS-PAGE, (ii) эксклюзионную хроматографию (SEC) и (iii) анализ динамического рассеяния света (DLS) на образцах распыляемой композиции.
Распыляемые образцы собирали непосредственно после процесса распыления следующим образом: Пробирку Falcon соединяли непосредственно с выходным отверстием смесительной камеры небулайзера с помощью эластомерных коннекторов. Небулайзеры, коннекторы и пробирки Falcon автоклавировали перед экспериментами и распыление проводили в условиях ламинарного потока воздуха. Резервуар небулайзера заполняли с помощью 4 мл образца состава. Пробирку для забора образцов закрывали с помощью завинчивающейся крышки и замораживали при -18°C до тестирования целостности.
Суммарно 36 образцов подвергали SDS-PAGE и анализу SEC:
8 для IgG, приготовленных с пролином (Фигура 3): 2, не распыленные контрольные образцы (а), 3 распыленные образцы, полученные с помощью мембраны типа 2 (б) и 3 распыленные образцы, полученные с помощью мембраны типа 4 (с). Образцы анализировали в дубликатах (не распыленные образцы) и трехкратными повторами (распыленные образцы), соответственно.
14 для IgG в PBS (d, f, g) и глицин (e, h, i) (Фигура 4): 2, не распыленные контроли (D, E), 6 распыленные образцы, полученные с мембраной типа 2 (f, h), и 6 распыленные образцы, полученные с помощью мембраны типа 4 (g, i)). Образцы анализировали трехкратными повторами (распыленные образцы).
14 для IgA (j, l, m) и IgAM (k, n, o) (Фигура 4): 2, не распыленные контроли (j, k), 6 распыленные образцы, полученные с мембраной типа 2 (l, n) и 6 распыленные образцы, полученные мембраной типа 4 (m, o)). Образцы анализировали трехкратными повторами (распыленные образцы).
10 для IgA (p,q), IgAM (r, s), SIgAM (t, u) и IgG (v, w, x, y) (рисунок 4): 5, не распыленные контроли (р, r, t, v, х) и 5 распыленные образцы (q, s, u, w, y), полученные мембраной типа 4.
Все растворы иммуноглобулинов получали из плазмы доноров крови человека. Растворы IgG имели концентрацию белка 100 мг/мл и содержали, по меньшей мере, 98% IgG. Все три состава IgG (250 мМ пролина, 250 мМ глицин, PBS) имели рН 4,8. Раствор IgA и IgAM (полимерный IgA+IgM) имел концентрацию белка 50 мг/мл и был приготовлен в PBS с рН 7,4. Относительное содержание IgM раствора IgA составило 2%, раствора IgAM 35%. Растворы IgA и IgAM также были приготовлены в пролине (125 мм).Человеческий рекомбинантный секреторный компонент связывали с IgA и IgM в PBS, а затем готовили в пролине (125 мМ).Содержание IgM в растворах IgA, приготовленных в пролине, были следующим: IgA (<2%), IgAM (33%), SIgAM (32%).
SDS-PAGE проводили с использованием системы Mini-Cell Life Technologies в соответствии с протоколами производителя. Вкратце, образцы денатурировали в буфере для образцов в восстанавливающих или невосстанавливающих условиях, соответственно, и электрофоретически разделяли на предварительно залитых градиентных гелях NuPAGE NovexTM Бис-трис 4-12% 1 мм 15 лунок, используя NuPAGETM MES буфер для электрофореза (Life Technologies ).После электрофореза белки в гелях фиксировали и окрашивали Кумасси G-250 (SimplyBlue SafestainTM; Life Technologies) в соответствии с протоколом производителя. Картину окрашивания белка записывали в цифровом виде с использованием системы 4000 ImageQuantTM LAS (GE Healthcare LIFESCIENCES).
Белковые полосы, полученные с помощью анализа SDS-PAGE, представлены на Фигуре 3 (где метки a, b и c относятся к вышеупомянутым группам образцов) и на ФИгуре4 (где метки d, e, f, g, h, i, j, k, l, m, n, o, p, q, r, s, t, u, v, w, x и y относятся к вышеупомянутым группам образцов). Фигуры 3A, 4A, 4C (левая панель) демонстрируют результаты, полученные в восстанавливающих условиях, и на Фигурах 3B, 4B, 4C (правая панель) представлены результаты, полученные в невосстанавливающих условиях.
Для анализа SEC, образцы вводили в количестве 200 мкг/2 мкл (IgG) или 100 мкг/2 мкл (IgA, IGAM) в Agilent Technologies системы ВЭЖХ 1260 InfinityTM для эксклюзионной хроматографии при скорости потока 0,7 мл/мин на колонку с гелем TSK G3000SWXL 7,8 мм ID х 30 см (Tosoh Bioscience). Из полученных хроматограмм оценивали относительное содержание (i) иммуноглобулиновых полимеров и агрегатов, (ii) мономеров и димеров, а также (iii) фрагментов, соответственно. Результаты представлены в Таблицах 6 и 7.
Для DLS-анализа образцы измеряли с помощью Malvern Zetasizer NanoTM в режиме обратного рассеяния при идентичных, фиксированных настройках прибора для измерения положения, затухание детектора, продолжительность прогона, количество прогонов и количество измерений, и результаты измерений усредняли на образец с использованием запатентованного программного обеспечения Zetasizer. Результаты представлены в Таблице 8.
Таблица 6: SEC анализ распыляемых IgG
Таблица 7: SEC-анализ распыляемых IgA и IgAM
Таблица 8: DLS анализ распыляемых IgA/M
Сравнение нераспыляемых и соответствующих распыляемых образцов иммуноглобулинов показало, что белковые полосы, полученных с помощью анализа SDS-PAGE, были идентичными для всех анализируемых образцов одного и того же препарата иммуноглобулина (Фигура 3 и Фигура 4), как в восстанавливающих, так и в невосстанавливающих условиях, что предполагает сохранение структурной целостности иммуноглобулина в распыляемых образцах.
Это открытие существенно подкрепляется с помощью анализа молекулярного размера с использованием эксклюзионной высокоэффективной жидкостной хроматографии (Э-ВЭЖХ). Относительное содержание разных категорий размеров белка (полимеры и агрегаты, мономеры и димеры и фрагменты) было сопоставимо для всех анализируемых образцов (Таблица 6, Таблица 7). Следует отметить, что содержание агрегатов ≤1%, как это наблюдалось с составами IgG с пролином или глицином, является очень низким для аэрозолизированного, высококонцентрированного IgG, и даже удовлетворяет требованиям для внутривенного введения IgG. Кроме того, иммуноглобулиновые препараты с повышенным содержанием высокомолекулярных белковых компонентов, типа 10% (масс./масс.) IgG, приготовленные в подкисленном PBS (~3% содержания агрегатов), 5% (масс./масс.) IgA в PBS (~ 17% Ig полимеров и агрегатов), 5% (масс./масс.) IgA в пролине (~ 21% Ig полимеров и агрегатов), 5% (масс./масс.) IGAM в PBS (~ 55% Ig полимеров и агрегатов ), 5% (масс./масс.) IGAM в пролине (~ 54% Ig полимеров и агрегатов) и 5% (масс./масс.) SIGAM в пролине (~ 56% Ig полимеров и агрегатов) также заметно не изменялись в процессе распыления.
Поскольку SEC-анализ не способен делать различия между полимерами и агрегатами Ig, богатые полимерами образцы IGAM до и после распыления дополнительно анализировали с помощью динамического рассеяния света (DLS), способа, обладающего повышенной чувствительностью для более крупных частиц. Изменение распределения размера частиц белка Ig в связи с образованием белковых агрегатов будет выявлено с помощью анализа DLS. Однако, результаты DLS для Z-Средних значений, полидисперсности и скорости счета частиц показывают, что распыление не вызывает никаких изменений в распределении частиц по размерам (Таблица 8).
Суммируя, вышеуказанные биохимические анализы демонстрируют практически полное отсутствие различия между нераспыляемыми и распыляемыми образцами.
Пример 6: Активность иммуноглобулинов после распыления
Иммуноглобулины проявляют различные функции, которые напрямую зависят от их Fab- (фрагмент связывания антигена) и Fc-фрагмента (фрагмент, способный кристаллизоваться) фрагментов. В то время как Fab-часть вовлечена в распознавание антигена, Fc-часть может связываться со специализированными рецепторами и активировать нижние молекулярные пути. Важно отметить, что они также могут активировать комплемент.
6a. Fc-активность иммуноглобулинов после распыления
Композиции, описанные в Примере 1 и Примере 3, распыляли с помощью модифицированного мембранного небулайзера с использованием технологии eFlow™ и имеющего большую смесительную камеру с использованием мембран типа 2 и 4 (как указано выше), и собирали генерированные аэрозоли. Собранные растворы использовали для определения активности иммуноглобулина после распыления, которую сравнивали с активностью иммуноглобулина в композиции перед распылением для того, чтобы оценить влияние процесса распыления на активность иммуноглобулинов.
Активность была впервые определена путем тестирования способности распознавания антигена и функции Fc распыляемого иммуноглобулина. Во всех препаратах Ig человека, присутствуют ксенореактивные антитела. Добавление ксеноантигенов (эритроциты кролика) к такой композиции приводит к образованию иммунного комплекса. Полученный иммунный комплекс добавляют к полиморфноядерными нейтрофилам человека (PMN), которые затем активируют путем распознавания и связывания Fc-фрагмента IgG на их рецепторах FcγRII и FcγRIIIγ или Fc-фрагмента IgA на CD89 (IgA - рецептор).Затем генерируются свободные радикалы кислорода (респираторный взрыв), которые детектируют с помощью хемилюминесценции.Степень активации клеток зависит от целостности Fc-участка иммуноглобулинов и от количества, связанного с эритроцитами. Для получения данных, которые исключительно зависит от качества Fc-участка иммуноглобулинов, количество антител, связанных с эритроцитах кролика измеряют с помощью FACS, и вычисляют хемилюминесценцию и данные по связыванию. Иммуноглобулины с Fc-активностью ≥50% проявляют нормальную функцию Fc. Результаты представлены в Таблицах 9a и 9b. В Таблице 9b, Fc-активность представлена в процентах от активности перед распылением, которую рассчитывают следующим образом:
Fc-активность (образец)=Ig-связанный при половине максимальной хемилюминесценции до распыления/Ig-связанный при половине максимальной хемилюминесценции после распыления * 100%
Все иммуноглобулины до распыления имеют активность Fc ≥50%.
Таблица 9а: Данные средних значений, полученные в опытах респираторного взрыва (состав 6)
Таблица 9b: Данные средних значений, полученные для различных составов в экспериментах респираторного взрыва
Нормальный IgG проявлял 97% Fc-активности на нейтрофилах. Распыленный IgG демонстрировал Fc-активность, очень близкую к активности контрольного IgG (Fc-активность> 90%) в зависимости от того, мембрану какого типа использовали для распыления. Таким образом, распыляемый IgG был способен распознавать ксеноантигены и связывать и активировать PMN, также как не распыляемый IgG.
Сравнение Fc-активностей различных составов с пролином (IgG, IgA, IgAM и SIgAM) до и после распыления демонстрируют отсутствие потери функции в процессе распыления (Таблицы 9a и 9b).
Во втором анализе, функцию Fc оценивали путем измерения активации комплемента. Распыляемый IgG и контрольный IgG адсорбировались на полистирольные микросферы, образуя модель иммунного комплекса. Эти микросферы с покрытием затем инкубировали с человеческой сывороткой в качестве источника комплемента. Полученную в результате активацию комплемента количественно оценивали путем измерения депонирования активированных фрагментов С3 в микросферах с помощью FACS. Вычисляя этих данные вместе с данными о фактическом количестве IgG, связанном с микросферами, оценивали целостность Fc-части IgG.
Было установлено, что распыление IgG не влияет на способность IgG активировать комплемент.
6b. Распознавание антигена иммуноглобулинами после распыления
Дальнейшая характеристика биологических свойств иммуноглобулинов после распыления включает анализ с помощью тИФА распознавания антигенов, таких как EBV, CMV, FSME, HB, HAV, HSV, VZV, эпидемического паротита, краснухи и кори, а также реакцию связывания комплемента и тесты связывания с рецептором. Конкретно, оценивали распознавание респираторно-синцитиального вируса (RSV) и антигена пневмококкового полисахарида (PCP) для всех составов (5-9). тИФА осуществляли согласно протоколам производителя. Результаты представлены в Таблицах 10a и 10b. Антитела к антигенам RSV и PCP детектировали в каждом составе поликлональных иммуноглобулинов. Важно то, что распознавание антигенов RSV и РСР с помощью различных составов не зависит от распыления.
Таблица 10a: Распознавание антигена RSV иммуноглобулинами до и после распыления
состав
Таблица 10b: Распознавание PCP-антигена с помощью иммуноглобулинов до и после распыления
Распознавание антигенов тестировали непосредственно на бактериях. 5×107 КОЕ/мл клеток штамма A66.1 Streptococcus pneumoniae наносили на планшеты PolySorb (Nunc) в карбонатном буфере при 4°С в течение ночи. После промывания с помощью PBS-Tween (0,05%), планшеты блокировали с помощью 2,5% FCS (в PBS) в течение 1,5 ч при комнатной температуре. После промывания с помощью PBS-Tween (0,05%), добавляли составы, при 333мкг/мл (разведенные в блокирующем буфере), и инкубировали в течение 2 ч при комнатной температуре. После промывания с помощью PBS-Tween (0,05%), вторичное антитело (козье антитело к человеческому IgG/A/M-HRP (Novex); 1 мг/мл, 1:2000 в блокирующем буфере) инкубировали в течение 2 ч при комнатной температуре. После промывания с помощью PBS-Tween (0,05%), субстрат TMB добавляли в лунки и катализ останавливали добавлением HCL. Затем планшеты считывали на ридере. Результаты представлены на Фигуре 5.
Антитела к S. pneumoniae детектировали в каждом составе (5-9). IgAM и SIgAM продемонстрировали лучший титр антител к S. pneumoniae, как это изображено с помощью более высокой OD. Важно отметить, что сравнение распыляемых составов с не распыляемыми контролями не продемонстрировало никакого различия в распознавании бактерий с помощью распыляемых составов. Таким образом, распыление не влияет на распознавание бактериальных антигенов с помощью поликлональных иммуноглобулинов.
6с. Активность распыляемых иммуноглобулины в in vitro модели инфекции
Полимерные иммуноглобулины играют важную роль на поверхности слизистых оболочек. Иммуноглобулины участвуют в предотвращении попадания бактерий в организм, процесс, известный как иммунное отторжение. Он включает в себя распознавание антигенов на поверхности бактерий иммуноглобулинами, а также способность полимерных иммуноглобулинов лучше агрегировать бактерии.
Для оценки того, может ли распыление обладать вредными функциями полимерных иммуноглобулинов, составы (5-9) тестировали в in vitro модели инфекции поляризованных эпителиальных клеток слизистых оболочек. Shigella flexneri использовали в качестве инфекционного агента, известного для инфицирования эпителиальных клеток слизистой кишечника, приводящего к диарее у человека. Для этой цели использовали монослой клеток кишечника. Клеточный монослой оставляют необработанным (C-) или экспонируют в течение 14 ч с Shigella flexneri индивидуально (C+) или в комплексе с контрольным составом (-) или распыляемыми составами (N) (Фигура 6). Инфекция Shigella flexneri индуцировала секрецию воспалительных цитокинов эпителиальными клетками, таких как TNF-альфа, CXCL8 и CCL3 (Фигура 6А). Кроме того, инфекция приводила к потере целостности мембраны и плотных соединений, которые можно было оценить путем измерения ассоциированной потери трансэпителиального электрического сопротивления (Фигура.6В). Наконец, инфекцию отслеживали путем подсчета количества очагов инфекции и измерения инфицированной области (Фигура.6С). Подробные протоколы для измерения этих конечных точек опубликованы в патентной заявке WO2013132052, и в Longet S. et al, J Biol Chem. 2014 Aug 1;289(31):21617-26.
В такой in vitro модели инфекции, мономерные иммуноглобулины не являются защитными (Longet S. et al, J Biol Chem. 2014 Aug 1;289(31):21617-26). Только IgAM и SIgAM в пролине уменьшали инфекцию, секрецию воспалительных цитокинов и целостность защитной мембраны (Фигура 6А, В, С; составы 8 и 9). Важно отметить, что иммунные комплексы Shigella flexneri с распыляемыми IgAM и SIgAM могли снижать инфекционность Shigella flexneri и секрецию цитокинов настолько сильно, насколько и иммунные комплексы, образованные Shigella flexneri и не распыляемые IgAM и SIgAM.
Распыление мономерных иммуноглобулинов (Фигура 6, составы 5-7) не оказывали влияние на их активности in vitro. На самом деле, не наблюдали усиления или потери функции в данной модели инфекции.
Таким образом, в целом было установлено, что распыление поликлональных иммуноглобулинов не изменяет распознавания антигенов иммуноглобулинами и Fc-функцию.
Пример 7: Депонирование в легких распыляемых иммуноглобулинов в животной модели
Композиции, описанные в Примере 1 и в Примере 3, распыляли и вводили крысам с использованием мембранного небулайзера, соединенного с проточной камерой, где аэрозоль распределяется животным.
В разные моменты времени после нанесения аэрозоля (0, 1 ч, 6ч, 12ч и 24ч), крыс умерщвляли. Левые доли легких использовали для бронхоальвеолярных лаважей (БАЛ). С этой целью, трахею канюлировали и легкие промывали два раза стерильным PBS (2×5 мл). Выходы из каждого индивидуального БАЛ объединяли и собирали в стерильную пластиковую пробирку. Образцы БАЛ центрифугировали (при 1500 х g в течение 10 мин при температуре приблизительно 4°С), и надосадочную жидкость БАЛ собирали по аликвотам в две стерильные пробирки (примерно 5 мл в каждую ). Правые доли выделяли, фиксировали и готовили для гистологии с использованием стандартных методов. Распределение Ig в легких затем оценивали с использованием методов иммуногистохимии со специфическими вторичными антителами на парафиновых срезах. Изучают определенные части легких (например, респираторные бронхиолы, альвеолярные протоки, альвеолярные мешочки и альвеолы).
Наличие иммуноглобулинов в БАЛ измеряли с помощью тИФА. Для детектирования IgA, на планшеты (Nunc) наносили покрытие в виде козьих антител к человеческим IgA (Bethyl Laboratories, 1/500 в буфере для покрытия (1,59г Na2CO3, NaHCO3, 2,93г 1мл H2O, pH 9,6)) в течение 1 ч при комнатной температуре. После промывания с использованием PBS-Tween добавляли в лунку блокирующий раствор (PBS, 1% BSA) и инкубировали в течение 1 ч при комнатной температуре. Блокирующий буфер промывали с использованием PBS-Tween, и образцы распределяли в планшеты и инкубировали в течение 2 ч при 37°С. После промывания с использованием PBS-Tween, добавляли в лунки козьи антитела к человеческим IgA-HRP (Bethyl Laboratories, 1/8000 в буфере для разведения (буфер lowcross (Candor), 1% казеин)) в течение 1 ч при комнатной температуре. После промывания с использованием PBS-Tween добавляли в лунки субстрат TMB в течение 15 минут при комнатной температуре и катализ останавливали добавлением стоп-раствора.
Для детектирования IgG на планшеты (Nunc) наносили покрытие в виде козьих антител к человеческому IgG (Acris; конечная концентрация 1,5 мкг/мл в буфере для покрытия (1,59г Na2CO3, 2,93г NaHCO3, H2O 1 мл, рН 9,6)) в течение 2 ч при комнатной температуре. После промывания с использованием PBS-Tween добавляли в лунку блокирующий раствор (PBS, 1,6% BSA) и инкубировали в течение 1 ч при комнатной температуре. Блокирующий буфер промывали с использованием PBS-Tween, и образцы распределяли в планшеты и инкубировали в течение 2 ч при комнатной температуре. После промывания с использованием PBS-Tween добавляли в лунки козьи антитела к человеческому IgG-HRP (Acris, конечная концентрация 0,3 мкг/мл в буфере для разведения («low cross» буфер (Candor), 1% казеин)) в течение 1 ч при комнатной температуре.После промывания с использованием PBS-Tween, добавляли в лунки ТМВ субстрат в течение 15 минут при комнатной температуре и катализ останавливали добавлением стоп-раствора. Результаты представлены на Фиг 7.
Наибольшее количество иммуноглобулинов было обнаружено в БАЛ во время применения составов 5, 7 и 8 с помощью аэрозоля (время 0 ч). Со временем количество распыляемых иммуноглобулины снижалось, причем более низкое количество детектировали в конце подвижности (24ч). Важно отметить, что распыленные иммуноглобулины еще детектировались в БАЛ через 24 часа после распыления.
Наличие распыленных иммуноглобулинов в плазме крыс также анализировали. Ни один из составов IgA (IgA и IgAM) не детектировали в плазме через 24 ч после распыления. Однако распыленные IgG можно было детектировать в плазме 3 крыс через 24 ч после того, как они получили аэрозоль (Таблица 11).
Таблица 11: Распыленные IgG детектировали в плазме через 24 часа после доставки иммуноглобулинов
Нами было продемонстрировано, что распыление не влияет на структуру иммуноглобулинов. Однако, слои слизистой оболочки в легких, как известно, содержат протеазы, которые могут повлиять на целостность применяемых иммуноглобулинов. Для того чтобы дополнить результаты тИФА, полученные для БАЛ, нами была проанализирована целостность распыляемых иммуноглобулинов с помощью SDS-PAGE. SDS-PAGE проводили в соответствии со стандартными протоколами или, как это описано в патентной заявке WO2013132052. Для иммуноблоттинга использовали поликлональные кроличьи антитела: а) кроличьи антитела к человеческой гамма-цепи (Dako, конъюгированные с пероксидазой хрена (HRP); разведение 1/10000), b) кроличьи антитела к человеческой альфа-цепи (Dako, конъюгированные с пероксидазой хрена (HRP): разведение 1/5000); c) кроличьи антитела к человеческой мю-цепи (Dako, конъюгированные с пероксидазой хрена (HRP); разведение 1/3000). Все инкубации проводили в PBS, содержащем 5% сухого молока и 0,5% Tween при температуре окружающей среды в течение 3 часов. После конечной промывки PBS-Tween иммунологическое детектирование на мембранах было обнаружено с помощью хемилюминесценции и записано в цифровом виде в системе ImageQuant LAS 4000 (GE Healthcare Lifesciences). Вестерн-блоты из восстановленных гелей представлены на Фигуре 8.
В подтверждение данных тИФА, гамма-цепи IgG детектировали в каждом образце БАЛ крыс, получивших распыленный IgG (Фигура 8; 5, а). Полосы детектировали до 24 ч после распыления. В образцах БАЛ крыс, получавших распыленной IgA, детектировали альфа-цепь (7, b) в ранние моменты времени после доставки, но сигнал ослабевал через 6ч. Альфа-цепь действительно было очень трудно детектировать через 24 часа после распыления (Фигура 8, 7, b). У крыс, получавших распыленный IgAM, детектирование альфа-цепи в каждом образце БАЛ было положительным с более низким сигналом через 24 ч. В тех же образцах БАЛ, мю-цепь (с) детектировали в каждом образце до 24 часов, хотя и сигнал ослабевал в этот последний момент времени.
Образцы БАЛ также прогоняли на гелях в невосстанавливающих условиях. Не детектировали фрагментов гамма-, альфа- и мю-цепей. Иммуноглобулины, которые детектировали, были интактными.
В целом, нами было продемонстрировано, что распыленные иммуноглобулины могли эффективно достигать легких животного, и что эти иммуноглобулины оставались интактными в этой среде в течение 24 часов, даже если их количество имело тенденцию к сокращению в течение времени.
Пример 8: распыляемые иммуноглобулины для лечения и профилактики хронического синусита
Хронический синусит (CS) является одним из наиболее частых хронических инфекционных патологических состояний (распространенность 13% у пациентов с иммунодефицитом и в здоровой популяции), обуславливая значительное ухудшение качества жизни (Khalid AN, Quraishi SA, Kennedy DW. Long-term quality of life measures after functional endoscopic sinus surgery. Am J Rhinol 2004 May; 18 (3): 131-6) и значительное потребление медицинской помощи (Anand VK. Epidemiology and economic impact of rhinosinusitis. Ann Otol Rhinol Laryngol Suppl 2004 May; 193: 3-5).
Современные методы лечения включают антибиотики, долгосрочные стероиды и (повторяющиеся) операции. Однако эти меры обладают ограниченной эффективностью с высокой частотой отсутствия эффекта в группах высокого риска (например, дефицит первичного антитела, кистозный фиброз), и, кроме того, после повторных применений потенциально может развиться устойчивость к антибиотикам.
Для предотвращения или лечения CS, композицию, описанную в Примере 1, предпочтительно IgA или смесь полимерного IgA и IgM, необязательно с добавлением рекомбинантного секреторного компонента, распыляли и вводили целевым пациентам с использованием мембранного небулайзера, имеющего большую смесительную камеру и способного испускать пульсирующий поток воздуха в целевые синоназальные или околоносовые пазухи. Целевые пациенты представляют собой пациентов, о которых известно, что они принадлежат к группе высокого риска (например, дефицит первичного антитела, кистозный фиброз) или что у них были эпизоды рецидива CS.
У пациентов, страдающих CS, применение начинали после хирургического удаления полипов носа и/или лечения антибиотиками или стероидами. Пациенты распыляли 2 мл жидкой композиции, содержащей IgG (10%) или IgA (50 мг/мл) или смеси полимерного IgA и IgM (50мг/мл), предпочтительно полимерные IgA и IgM (50мг/мл), ассоциированные с рекомбинантным секреторным компонентом, по меньшей мере, один раз в день в течение 8-недельного периода. Это соответствует одному курсу лечения.
В качестве превентивной терапии, пациенты распыляли 2 мл жидкой композиции, содержащей IgG (10%) или IgA (50 мг/мл) или смеси полимерного IgA и IgM (50мг/мл), предпочтительно полимерные IgA и IgM (50мг/мл), ассоциированные с рекомбинантным секреторным компонентом, 2 курса лечения в год.
Распыленные иммуноглобулины уменьшают хронический характер эпизодов синусита в случае профилактического лечения.
При применении у пациентов с CS, распыленные иммуноглобулины уменьшали такие симптомы, как заложенность носа и отделяемое носоглотки, давление на лицо или боль, отек вокруг глаз, щек и носа.
Пример 9: распыленные иммуноглобулины в лечении хронических инфекций нижних дыхательных путей при первичном иммунодефиците (PID)
IgG-заместительная терапия у пациентов с PID эффективно снижает частоту пневмонии и тяжелых инфекций. Однако эти пациенты все еще испытывают 3-4 инфекции в год и на одного пациента. Такой высокий уровень инфекции в сочетании с воспалением указывает на то, что IgG-терапия оказывает низкое воздействие на хронические побочные эффекты инфекции, такие как бронхоэктаз, хроническая диарея, аутоиммунитет и лимфопролиферативные расстройства.
Пневмония, бронхоэктаз и сепсис при длительной заместительной терапии IgG были ассоциированы с низким уровнем IgM, в то время как имела место значительно увеличенная степень желудочно-кишечных инфекций с низким уровнем IgA (Oksenhendler Е, Gerard L, Fieschi C et al. Infections in 252 patients with common variable immunodeficiency. Clin Infect Dis 2008 May 15;46(10):1547-54; Gregersen S, Aalokken TM, Mynarek G, et al. Development of pulmonary abnormalities in patients with common variable immunodeficiency: associations with clinical and immunologic factors. Ann Allergy Asthma Immunol 2010 Jun;104(6):503-10; Quinti I, Soresina A, Guerra A, et al. Effectiveness of immunoglobulin replacement therapy on clinical outcome in patients with primary antibody deficiencies: Results from a multicenter prospective cohort study. J Clin Immunol 2011 Mar 2.), что опять же свидетельствует о том, что IgA и/или IgM могут представлять собой критические недостающие факторы.
Пациенты с бронхоэктазом восприимчивы к инфекции Pseudomonas aeruginosa. Х-связанная агаммаглобулинемия (XLA) представляет собой расстройство, затрагивающие субпопуляции пациентов с PID. Оно характеризуется дефектом в генерации зрелых В-лимфоцитов, а также специфических антител и низкой концентрацией иммуноглобулинов в сыворотке. Эти пациенты отображают хронические инфекции, которые могут привести к развитию бронхоэктаза.
Конкретная исследуемая популяция с хроническими инфекциями нижних дыхательных путей представляет собой пациентов с XLA, испытавших первый эпизод инфекции легких с P. aeruginosa. Цель лечения будет профилактика рецидива инфекции и долгосрочная профилактики бронхоэктазов. Для этого конкретного симптома предлагается либо IgA, либо смешанный продукт IgM/IgA. Пациенты распыляют 2 мл жидкой композиции, содержащей IgG (10%) или IgA (50 мг/мл) или смесь полимерного IgA и IgM (50мг/мл), предпочтительно полимерные IgA и IgM (50мг/мл), ассоциированные с рекомбинантным секреторным компонентом, по меньшей мере, один раз в день, в течение 8-недельного периода (= один курс лечения). Пациенты должны получать 2 курса лечения в год.
Параметры эффективности четко определены, включая частоту рецидивов инфекции, скорость развития бронхоэктаза, микробную нагрузку/параметры воспаления в индуцированной мокроте.
Пример 10: Распыление вязких составов иммуноглобулинов
Как представлено в предыдущих примерах, распыление иммуноглобулинов с использованием исследовательской модифицированной технологии eFlow не вредит ни структуре иммуноглобулинов, ни их функции. Для того чтобы обеспечить более короткое время распыления при ориентации на определенное количество иммуноглобулинов, которые будут доставлены в дыхательные пути (верхние и/или нижние), предпочтительными являются более высокие концентрации иммуноглобулинов. Высокая молекулярная масса иммуноглобулинов (150кДа - 1040кДа), а также высокая концентрация молекул, как известно, или по отдельности или в сочетании, влияет на вязкость композиции. Вязкость напрямую влияет на производительность распыления.
Для того, чтобы лучше понять, как вязкость влияет на производительность распыления, несколько составов тестировали на трех различных устройствах. Использовали исследовательский небулайзер eFlow (модифицированный мембранный типа 4) Omron Micro Air U22 и Aerogen Aeroneb®Go.
Составы представлены в таблице 12.
Таблица 12: Характеристика тестриуемых составов
Эксперименты лазерной дифракции проводили, как описано в Примере 1, 2 и 3. Для этого исследования использовали 3 исследовательских модифицированных небулайзера eFlow (активный вибрационный мембранный и с отрицательным давлением) 3 Omron Micro Air U22 (пассивный вибрационный мембранный), и 1 Aerogen Aeroneb®Go (активный вибрационный мембранный), образцы тестировали в двух экземплярах (Aeroneb®Go) или в трех (исследовательский модифицированный eFlow, Micro Air U22).Небулайзеры Omron и Aerogen использовали в соответствии с инструкцией соответствующих производителей. Все составы тестировали в случайном порядке. Результаты представлены в Таблицах 13 и 14.
Таблица 13: Результаты распылений IgG-составов
н.п.: не применяется; MMD: медианный диаметр массы; TOR: суммарная скорость выходящего потока; RF: вдыхаемая фракция; GSD: геометрическое стандартное отклонение; IM-eFlow: исследовательский модифицированный eFlow
Таблица 14: Результаты распылений составов с IgAM
н.п.: не применяется; MMD: медианный диаметр массы; TOR: суммарная скорость выходящего потока; RF: вдыхаемая фракция; GSD: геометрическое стандартное отклонение; IM-eFlow: исследовательский модифицированный eFlow
Как представлено в Таблицах 13 и 14, увеличение концентрации одного и того же белка (например, мономерного поликлонального иммуноглобулина) было связано с повышением вязкости (1,75 до 14,52 мПа*с для IgG в интервале от 5% до 20%, соответственно). Для больших и более сложных белков, таких как полимерные иммуноглобулины (IgA и IgM), вязкость увеличилась быстрее, чем у мономерных иммуноглобулинов. 5% и 9% IgG демонстрировали вязкость 1,75 и 2,65 мПа*с, соответственно, в то время как композиция полимерного IgA и IgM при концентрации 5% и 9% демонстрировали вязкость 3,88 и 15,87 мПа*с. Повышенная вязкость была связана с уменьшением суммарной скорости выходящего потока (TOR). Размер капель снижался минимально, в то время как вязкость увеличилась.
Распыление повышенных концентраций поликлональных IgG было выполнимо с использованием исследовательского модифицированного небулайзера eFlow (IM-eFlow) до концентрации 13%. Для 15% IgG, 1 небулайзер из 3-х может распылять IgG. 20% IgG также мог распыляться с помощью 1 небулайзера из 3-х, но с очень низкой TOR (6 мг/мин). Небулайзер Omron Micro Air U22 не мог распылять состав с концентрацией выше, чем 7% IgG, и с очень низкой TOR (160 мг/мин) и с более крупным размером капель (> 6 мкм; IM-eFlow <4 мкм), Aerogen Aeroneb®Go мог распылять составы 7% и 9%, но с очень низкой TOR (117 и 20 мг/мин, соответственно). Для IgG с концентрацией 7% и 9%, небулайзеры eFlow проявили высокую производительности (например, TOR> 550 мг/мин).
Распыление составов IgA и IgM составов (например, IgAM 5% и 8%) осуществимо с использованием небулайзеров eFlow и с хорошей производительностью. IgAM с концентрацией 9% могут быть распылены только один раз с нормальной производительностью. Небулайзер Omron Micro Air U22 был не способен распылять эти составы, содержащие полимерные поликлональные иммуноглобулины. Устройства Omron и Aerogen были не способны генерировать аэрозоль из составов иммуноглобулинов с вязкостью выше чем 3 мПа*с.
В общем, данный способ генерирования аэрозоля путем распыления композиции поликлональных иммуноглобулинов демонстрирует превосходную производительность при распылении высококонцентрированных мономерных и полимерных иммуноглобулинов с помощью способа по изобретению.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ОСТРЫХ ОСЛОЖНЕНИЙ С ИСПОЛЬЗОВАНИЕМ ПОЛИКЛОНАЛЬНОГО ИММУНОГЛОБУЛИНА | 2019 |
|
RU2806443C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЦИКЛОСПОРИН | 2006 |
|
RU2421209C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СЕКРЕТОРНОПОДОБНЫЕ ИММУНОГЛОБУЛИНЫ | 2013 |
|
RU2644240C2 |
| ВОДНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АРБЕКАЦИН | 2012 |
|
RU2604767C2 |
| ДОСТАВКА В ЛЕГКИЕ АЛЬФА-1-ИНГИБИТОРА ПРОТЕИНАЗ | 2007 |
|
RU2433841C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРОДУКТ С УВЕЛИЧЕННОЙ СТАБИЛЬНОСТЬЮ, СОДЕРЖАЩИЙ ИММУНОГЛОБУЛИНЫ | 2015 |
|
RU2748841C2 |
| ВОДНЫЙ АЭРОЗОЛЬНЫЙ ПРЕПАРАТ | 2004 |
|
RU2363449C2 |
| ВВЕДЕНИЕ ИЛОПРОСТА В ВИДЕ АЭРОЗОЛЬНЫХ БОЛЮСОВ | 2012 |
|
RU2605849C2 |
| ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2009 |
|
RU2396278C1 |
| ИГАЛЯЦИОННОЕ УСТРОЙСТВО ДЛЯ ИСПОЛЬЗОВАНИЯ В АЭРОЗОЛЬНОЙ ТЕРАПИИ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2700650C2 |

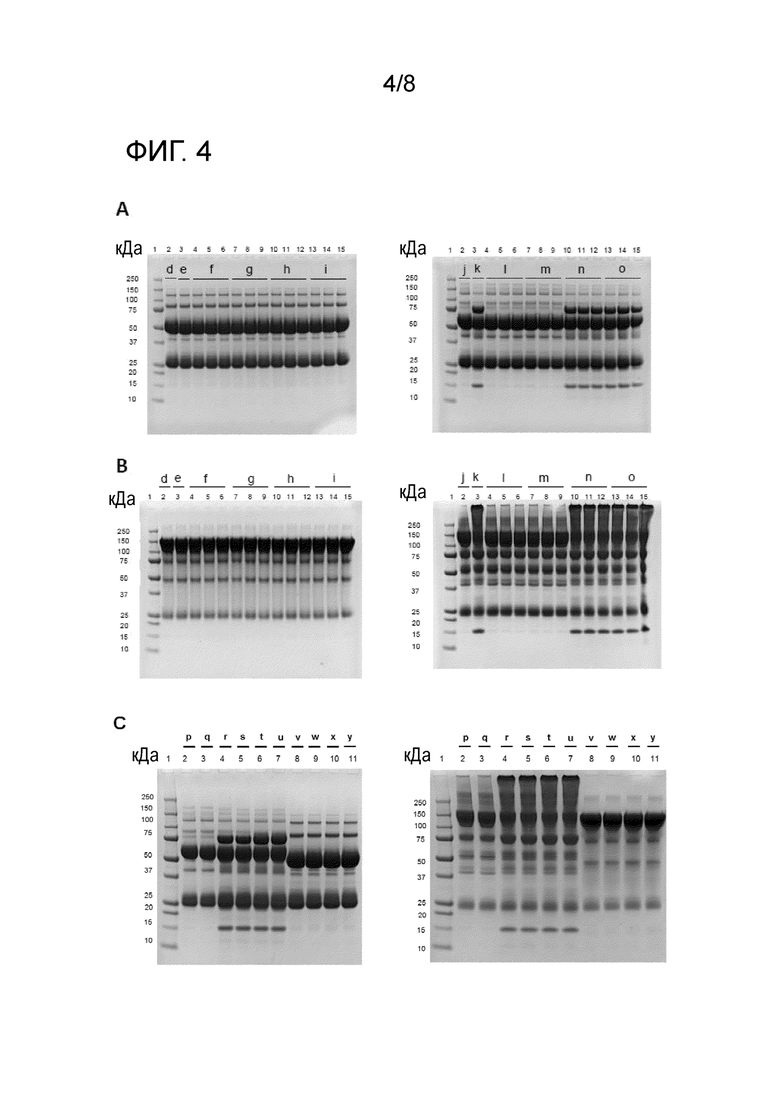
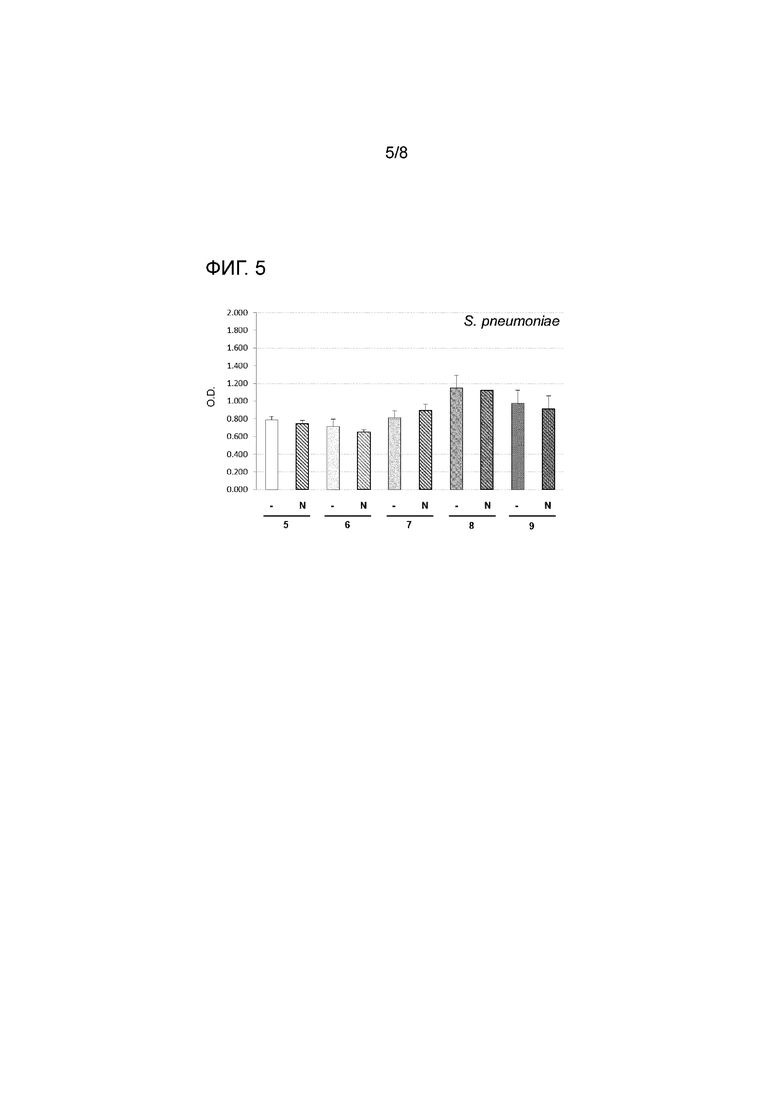
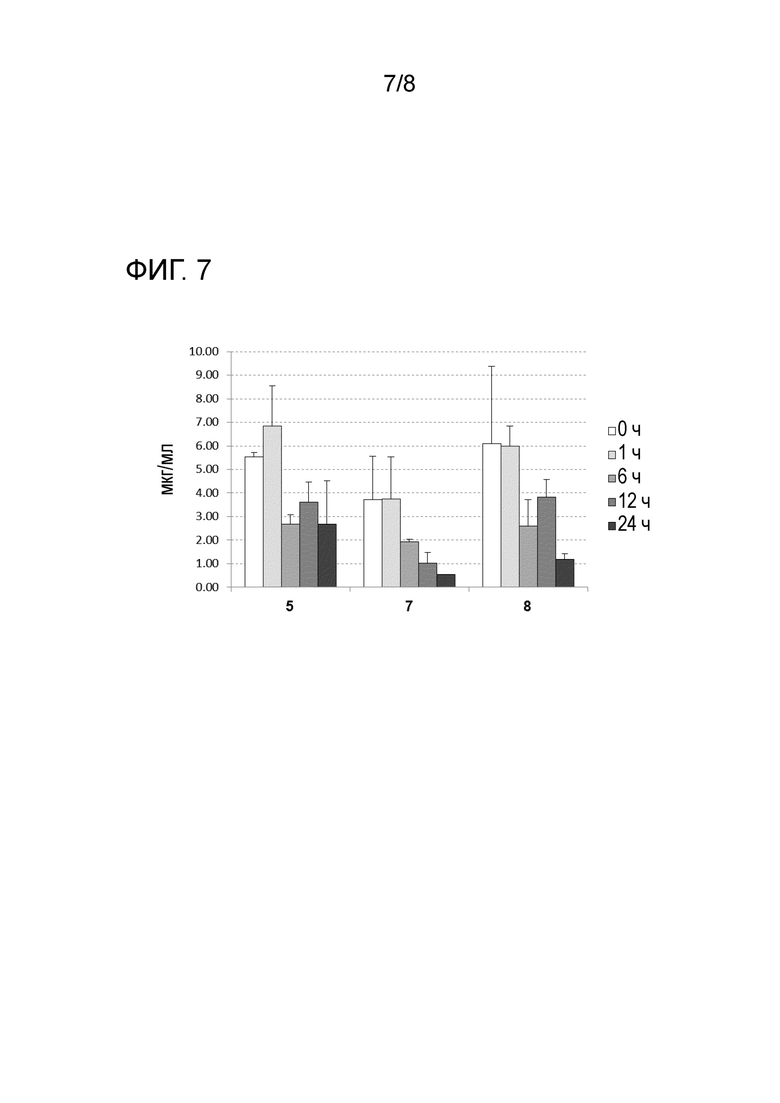
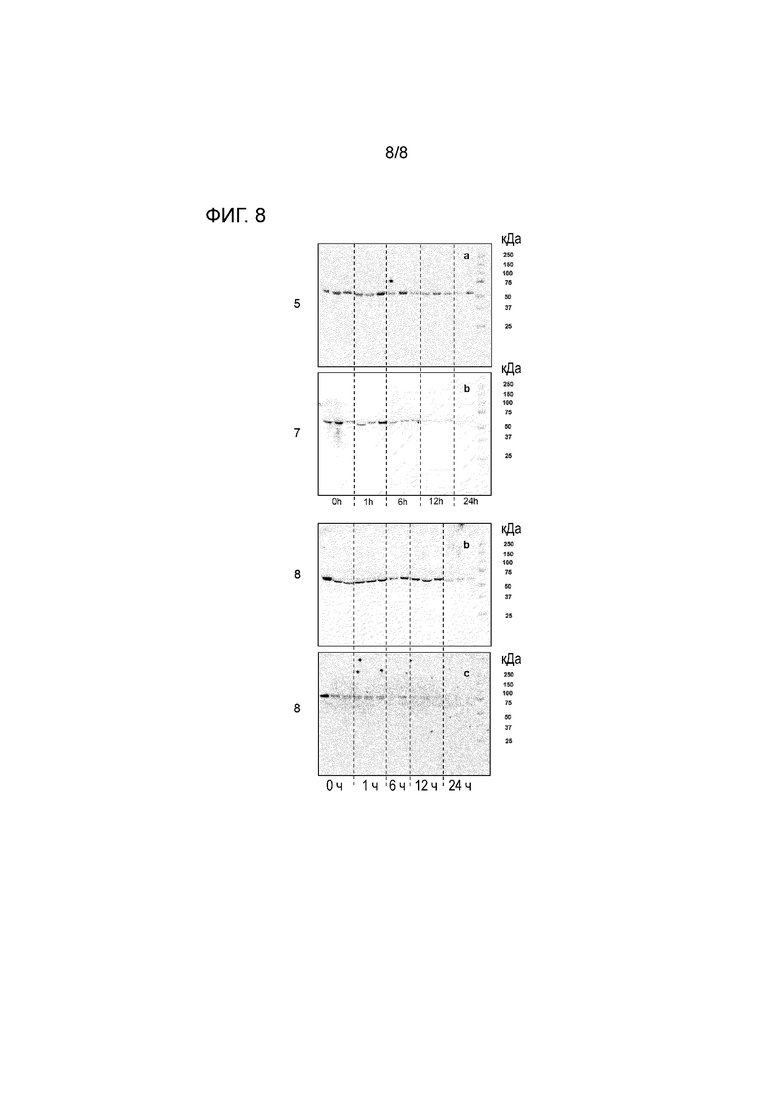
Изобретение относится к генерированию аэрозоля для терапевтических целей. Применение способа распыления композиции, содержащей поликлональный иммуноглобулин (Ig), где концентрация Ig составляет 40-200 мг/мл и где вязкость композиции, измеренная с помощью вискозиметра с падающим шариком при температуре 20±0,1С°, составляет 1-17 мПа·с. При этом способ включает стадии: (a) получения жидкой водной композиции, содержащей иммуноглобулин (Ig); (b) обеспечения мембранного небулайзера, имеющего резервуар, который заполняется композицией; и (c) распыления композиции с применением небулайзера с получением аэрозоля. Изобретение обеспечивает успешное распылении концентрированных иммуноглобулиновых композиций. 14 з.п. ф-лы, 8 ил., 19 табл., 9 пр.
1. Применение способа распыления композиции, содержащей иммуноглобулин (Ig), где способ включает стадии:
(a) получения жидкой водной композиции, содержащей иммуноглобулин (Ig);
(b) обеспечения мембранного небулайзера, имеющего резервуар, который заполняется композицией; и
(c) распыления композиции с применением небулайзера с получением аэрозоля,
для распыления композиции, содержащей поликлональный иммуноглобулин (Ig), где концентрация Ig составляет 40-200 мг/мл и где вязкость композиции, измеренная с помощью вискозиметра с падающим шариком при температуре 20±0,1°C, составляет 1-17 мПа·с.
2. Применение по п. 1, где концентрация Ig в композиции составляет 50-120 мг/мл.
3. Применение по п. 1 или 2, где композиция дополнительно содержит стабилизатор.
4. Применение по п. 3, где стабилизатор представляет собой пролин.
5. Применение по п. 1 или 2, где композиция дополнительно содержит ПАВ.
6. Применение по п. 1 или 2, где резервуар изолирован от атмосферы, так что давление внутри резервуара уменьшается перед или во время стадии (c).
7. Применение по п. 6, где резервуар изолирован от атмосферы с помощью уплотнительного элемента (16), расположенного на отверстии в резервуаре (10) с получением газонепроницаемого уплотнения для отверстия и скользящего элемента (21), связанного с уплотнительным элементом (16) так, что движение скользящего элемента (21) воздействует на движение, по меньшей мере, одной секции (18) уплотнительного элемента (16), посредством чего в резервуаре (10) генерируется отрицательное давление.
8. Применение по п. 1 или 2, где мембранный небулайзер представляет собой вибрационный мембранный небулайзер.
9. Применение по п. 1 или 2, где мембранный небулайзер содержит способную к вибрации мембрану (122), имеющую первую сторону (124) для контакта с жидкостью и противоположную вторую сторону (125), причем мембрана имеет множество сквозных отверстий (126), пронизывающих мембрану в направлении удлинения (E) от первой стороны ко второй стороне, причем жидкость проходит сквозь отверстия от первой стороны ко второй стороне, когда мембрана вибрирует для генерирования аэрозоля на второй стороне, каждое сквозное отверстие (126) имеет наряду с его направлением удлинения (E) наименьший диаметр (DS), больший диаметр (DL), который более чем в три раза больше, чем наименьший диаметр, каждое сквозное отверстие содержит область сопла (132), ограниченную непрерывной областью сквозного отверстия в направлении удлинения, включающей наименьший диаметр сквозного отверстия, и ограниченную большим диаметром сквозного отверстия, отличающуюся тем, что соотношение суммарной длины каждого сквозного отверстия (126) в направлении удлинения к соответствующей длине областей сопла (132) в направлении удлинения составляет, по меньшей мере 4.
10. Применение по п. 1 или 2, где небулайзер адаптирован для генерирования аэрозоля с направленным воздействием на нижние дыхательные пути пациента.
11. Применение по п. 1 или 2, где небулайзер адаптирован для генерирования аэрозоля с направленным воздействием на верхние дыхательные пути пациента.
12. Применение по п. 1 или 2, где небулайзер представляет собой небулайзер с активной мембраной, которая соединена с устройством генерирования вибрации.
13. Применение по любому из пп. 1-12, где иммуноглобулин (Ig) представляет собой поликлональный иммуноглобулин G (IgG), поликлональный иммуноглобулин A (IgA) и/или поликлональный иммуноглобулин M (IgM).
14. Применение по любому из пп. 1-13, где доза Ig в доставляемом аэрозоле составляет, по меньшей мере, 50% дозы Ig в композиции, которой заполняют резервуар небулайзера.
15. Применение по любому из пп. 1-14, где активность Ig в аэрозоле составляет, по меньшей мере, 80% Ig в композиции, заполненной в резервуар небулайзера.
| US 2013019860 A1, 24.01.2013 | |||
| US 2012308557 А1, 06.12.2012 | |||
| Шихта для изготовления керамического материала | 1986 |
|
SU1353759A1 |
| WO 2012168181 А1, 06.12.2012 | |||
| US 2010260853 A1, 14.10.2010. | |||
Авторы
Даты
2020-08-07—Публикация
2015-04-02—Подача