Изобретение относится к ветеринарии и медицине, в частности, к использованию препаратов, предназначенных для профилактики и лечения радиационных поражений, достигается путем ингибирования образование продуктов пираксидации липидов (ПОЛ), индуцированных ионизирующей радиацией.
Известен способ лечения радиационного поражения организма с использованием экстрактов из растительных (настойка календулы, цветочная пыльца, полиэкстракт из ягод рябины) продуктов, обладающих противолучевым действием (см. статью Л.М. Овсянникова и др. - Основные принципы коррекции поражений окислительного гомеостаза у лиц, подвергавшихся воздействию факторов аварий на ЧАЭС // Проблемы противолучевой защиты: Матер, конф. М.: РАН, 1998. - С. 116-117).
Известен способ лечения (реабилитации) облученных лиц с использованием базового комплекса биологически активных пищевых добавок, содержащего настои осиновой коры, гриба чаги, морс калины или рябины и витаминый травяной чай (заявка на изобретение RU №2004109896, кл. A23L 1/30, дата публ. 10.10.05).
Недостатком указанных способов является то, что во - первых, они предполагают пероральнное применение водных или спиртовых экстрактов апифитопродуктов, во-вторых, радиозащитный эффект указанных средств проявляется только при длительном (в течение года или течение не менее 21 дня) непрерывном применении препаратов в виде пищевых добавок к основному рациону. В случае необходимости экстренного радиопрофилактического или радиотерапевтического применение указанные способы не обеспечивают экстренной защиты.
Известен способ профилактики и лечении радиационных поражений организма путем однократного подкожного введения противолучевой сыворотки в дозах 100-125 мг/кг массы тела молодым и 200-250 мг/кг взрослым в течение первых 10 суток после облучения с лечебной целью (Патент RU №2169372, МПК А61К 35/28, 27.06.2001 г.). Недостатком указанного способа является сложная технология получения препарата (двукратное облучение крупных животных с использованием мощной радиационно-опасной гамма-установки и самое главное - использование высоких лечебных доз дорогостоящего препарата - противолучевой лошадиной сыворотки, расход которой для крупных животных составляет 200-400 мл препарата на голову).
Известен способ лечения и профилактики радиационных поражений с пролонгированным применением БАВ из древесной зелени, ели и сосны, которые при скармливании из расчета 0,2 мл/кг массы тела обеспечивали выживаемость 60% летально облученных животных (Курило А.И. Ветеринарно-гигиенические основы применения биологически активных веществ растительного происхождения для профилактики лучевых поражений: Автореф. дисс… доктора ветеринарных наук - С. Петербург, 1977-46 с).
Наиболее близким по технической сущности является использование тритерпеноида растительного происхождения - милиацина, для ингибирования токсических радикалов, внутрибрюшинное введение которого в дозе 2 мг/кг оказывало стресспротекторное действие, путем ингибирования стрессиндуцированных токсических радикалов - продуктов липопероксидации липидов (ПОЛ) (см. статью Т.В. Панфиловой, А.А. Штиль, Б.А. Фролова - Тритерпеноид мелиацина снижает индуцируемое стрессом ПОЛ // Бюлл. эксперемент. биология и медицина. - 2006. - Т. (4). - №6. - С. 633-635).
Недостатком этого способа является низкая эффективность лечения от радиационных поражений, сложность получения препарата и длительность его применения (30 дней).
Препараты растительного происхождения - терпеноиды из сосны обладают важнейшим механизмом - протекторным действием при стрессорных поражениях путем блокирования образования токсических радикалов на фоне воздействия на организм стрессоров (ионизирующее излучение, патогенные агенты, химические токсиканты и т.д.). Одним из важнейших терпенов, применяемых в медицине и ветеринарии, является терпентинное масло - скипидар, обладающий широким спектром биологического действия (противовоспалительное, болеутоляющее, антибактериальное, активация грануляции, центральной нервной системы, иммуно- и гемопоэза) (И.Е. Мозгов - Фармакология: Руководство для ветеринарных врачей. - М.: Сельхозгиз. - 1954. - с. 207-209).
Технический результат, на достижение которого направлено изобретение, заключается в повышении эффективности защиты организма от радиационного поражения, в упрощении и удешевлении способа лечения и в сокращении срока лечения.
Для достижения названного технического результата в предлагаемом способе, включающем введение в организм биологического препарата растительного происхождения, в качестве биологического препарата используют композицию, полученную путем смешивания очищенного скипидара с высокоочищенным рафинированным подсолнечным маслом в соотношении 70:30 соответственно, которую вводят животным однократно внутримышечно в дозе 1,0-2,0 мл мелким животным и 5,0-8,0 мл крупным животным в течение 1-12 дней до облучения и в течение первых 1-4 суток после облучения.
Использование композиции, полученной путем смешивания 70 частей очищенного скипидара (ГОСТ 1571-82) и 30 частей высокоочищенного рафинированного подсолнечного масла «Solpro» (ТУ 9141 -006-70316851-2012) производства АО «Актарский МЭЗ» (Россия) и введение ее внутримышечно однократно в дозах 1,0-2,0 мл мелким и 5,0-8,0 мл взрослым животным в течение 1-12 суток до облучения и в течение первых 1-4 суток после облучения, позволяет повысить эффективность лечения, создать радиозащитную, радиотерапевтическую дозу препарата, упростить технологию получения биологического препарата и использовать вместо перорального и длительного (в течение 30 дней) введения БАВ из древесной зелени или сосны на однократное внутримышечное парентеральное введение.
Выбор оптимального пути введения препарата и снижение демаркационного эффекта скипидара в сочетании с высокоочищенным растительным маслом обеспечивает экстренное и эффективное действие композиции за счет прямого действия на биомембраны пораженных радиацией клеток и, стабилизируя их функцию и повышая их устойчивость к продуктам пероксидации липидов и токсических продуктов распада, мишенью атаки которых являются высокочувствительные к радиации клетки - лимфоциты, подвергающиеся радиационному апоптозу. Таким образом, используемый препарат, экстренно достигая пораженные ионизирующей радиацией клетки мишени - лимфоциты, защищает их от атакующего агента - липидных радиотоксинов (продуктов липопероксидации - ПОЛ) путем стабилизации мембран и блокируя метаболические (биохимические и патохимические) эффекты токсических агентов.
Способ лечения радиационных поражений иллюстрируется следующими примерами.
Пример 1. Изучение возможности парентерального способа применения очищенного скипидара.
В качестве биологической модели для проведения этих исследований использовали белых мышей, а в качестве испытуемого препарата - очищенный чистый скипидар. Препарат вводили белым мышам подкожно, внутримышечно и внутрибрюшинно в дозах 0,1; 0,2; 0,3; 0,4 и 0,5 мл соответственно. За животными вели клиническое наблюдение, регистрируя количество павших и сроки падежа животных после введения препарата.
Установлено, что наиболее приемлемым способом применения скипидара является его подкожное введение. При внутрибрюшинном введении препарат оказывает токсический эффект, а при внутримышечном вызывает некроз тканей на месте введения и гибель животных при всех испытуемых дозах (0,1-0,5 мл) применения.
Однако, несмотря на отсутствия токсического эффекта при подкожном введении очищенного (нативного) скипидара, применение его в неразведенном виде нежелательно, поскольку при этом способе на месте введения образуется разлитой отек в виде небольшого валика без явных границ.
Сказанное предполагает поиск разбавителя (растворителя) для ускорения рассасывания препарата и адресной доставки его к пораженным ионизирующей радиацией клеткам - мишеням.
Пример 2. Подбор оптимального растворителя (депонирующего агента) скипидара.
Учитывая, что скипидар не растворяется в воде, но легко растворяется в спирте, хлороформе, смешивается в любых соотношениях с эфиром, хлороформом, бензином и растительными маслами, свой выбор мы остановили на растительных маслах, поскольку другие выше перечисленные компоненты высокотоксичны для организма.
В качестве потенциальных растворителей (разбавителей) использовали подсолнечные масла: нерафинированное, рафинированное и высокоолеиновое рафинированное подсолнечное масло. С использованием различных масел готовили эмульсии скипидара в различных соотношениях компонентов (очищенный скипидар: масло): 70:30; 50:50; 30:70; 20:80.
Приготовленных вышеописанным способом 70, 50, 30 и 20%-ные эмульсии скипидара и подсолнечного масла вводили подкожно, внутрибрюшинно и внутримышечно белым мышам по 3 животных на каждый вариант опыта (12 вариантов с различным соотношением компонентов (4) и 3 видов использованных масел).
Установлено, что из всех испытанных эмульсий на основе подсолнечных масел различной степени очистки, наиболее приемлемыми оказались эмульсии (композиции), полученные путем смешивания высокоочищенного рафинированного подсолнечного масла «Solpro», которые, в отличие от эмульсий на основе нерафинированных и рафинированных масел, при внутримышечном введении не вызывали образования отека, быстрее рассасывались на месте инъекции без образования отека и валика с расширенными границами. Внутрибрюшинное введение оказывало токсическое действие на животных, которое сопровождалось гибелью 70% белых мышей. При подкожном введении образовался отек в виде небольшого валика с четкими границами, что свидетельствует о плохом рассасывании и длительном депонировании препарата на месте введения.
Следовательно, оптимальным растворителем (разбавителем) для очищенного скипидара является высокоочищенное высокоолеиновое подсолнечное масло «Solpro» (ТУ 9141-006-70316851-2012) производства АО «Аткарский МЭЗ» (Россия), а метод парентерального введения - внутримышечный.
Пример 3. Изучение радиозащитной эффективности эмульсии (композиции) на основе очищенного скипидара и подсолнечного масла.
Для оценки радиозащитной эффективности очищенного скипидара и подсолнечного масла готовили различные соотношения компонентов: 70:30 (70%-ная эмульсия), 50:50 (50%-ная), 30:70 (30%-ная) и 20:80 (20%-ная эмульсия). Опыты проводили на 45 белых мышах, разделенных на 9 групп по 5 животных в каждой. Приготовленные композиции с указанными соотношениями компонентов вводили внутримышечно белым мышам однократно в дозе 0,1 мл на мышь за 24 часа до (1-я, 2-я, 3-й и 4-я группы) и через 24 часа после (5-я, 6-я, 7-я, 8-я группы) облучения в летальной дозе (8,0 Гр, ЛД100/30) 9-я группа служила контролем облучения.
За животными вели наблюдения в течение 30 дней, до и после облучения вводили испытуемые препараты, учитывая количество павших и выживших животных в каждой группе.
Результаты изучения радиозащитной эффективности испытуемых композиций представлены в таблице 1.
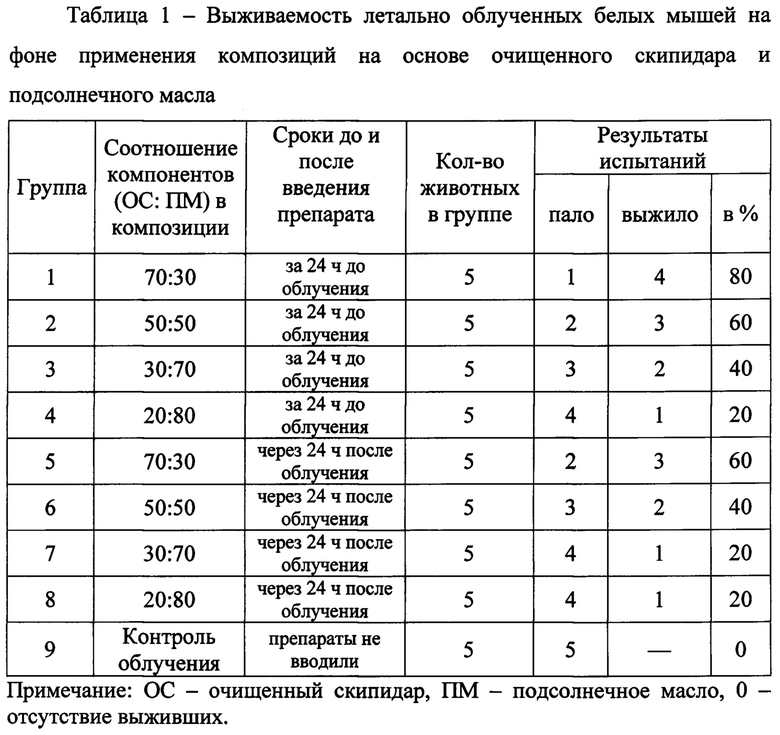
Из данных таблицы видно, что испытуемые композиции обладают радиозащитной активностью как при профилактическом (введение препарата за 24 ч до облучения), так и лечебном применяли (введение препарата через 24 ч после облучения), обеспечивая 80%- и 60%-ную выживаемость летально облученных животных соответственно. При этом оптимальным соотношением компонентов в обоих вариантах применения препарата является 7 частей очищенного скипидара и 3 части подсолнечного масла (ОС:ПМ=70:30). Любые изменения этого соотношения компонентов приводит к снижению радиозащитной эффективности компонентов (группы 2, 3 ,4 и 6, 7 ,8 соответственно).
Пример 4. Определение оптимальной лечебно-профилактической дозы радиозащитного препарата при парентеральном (внутримышечном) введении.
Для определения оптимальной лечебно-профилактической дозы радиозащитного препарата композиции на основе очищенного скипидара и подсолнечного масла, готовили различные разведения препарата, содержащие в 0,1 мл 0,1; 0,01; 0,05; 0,025 и 0,0012 мл исходного (70%-ного +30%-ного) раствора - эмульсии, которые однократно внутримышечно вводили 5 белым мышам (живая масса - 20 г) на каждое разведение (дозу) за 24 ч до и через 24 ч после летального облучения (7,7 Гр).
Установлено, что максимальный радиозащитный эффект (60-80%-ная защита при лечебном и профилактическом применении соответственно) проявлялся при введении доз 0,1; 0,01 и 0,005 мл. Введение препарата в дозе 0,0025 мл приводит к снижению радиозащитного эффекта (20%-ная выживаемость). Следовательно, оптимальными лечебно-профилактическими дозами препарата являются 0,01-0,005 мл на мышь, что в пересчете на 1 кг массы тела составляет 0,5-0,25 мл.
При практическом применении композиционного препарата эффективная лечебно-профилактическая доза для животных живой массой 100-500 кг составляет 5,0-8,0 мл, 50-100 кг - 1,0-2,0 мл.
Пример 5. Изучение стресспротекторного антиоксидантного действия композиции на основе очищенного скипидара и подсолнечного масла.
Для оценки антиоксидантной активности испытуемого препарата, опыты проводили на 30 белых крысах, разделенных на три группы по 10 животных в каждой. Животных 1-й и 2-й групп подвергали радиационному стрессу путем облучения их на гамма-установке «Пума» в дозе 9,0 Гр. Через 24 ч после летального облучения животным 2-й группы однократно внутримышечно вводили 70%-ую эмульсию очищенного скипидара и подсолнечного масла в дозе 0,5 мл. Животных 3-й группы не облучали и не лечили - они служили биологическим контролем. У всех животных через 3,7 и 14 суток после облучения и лечения брали пробы крови и в плазме определяли концентрацию стрессиндуцированных продуктов пероксидации липидов (ПОЛ). Содержание гидроперекисей липидов (ПОЛ) определяли в сыворотке крови по М.С. Гончаренко и A.M. Латиновой (Методика определения малонового диальдегида в сыворотке крови животных. - //Лабораторное дело. - 1985. - №1. - С. 60-61). Содержание ПОЛ выражали в эквивалентном количестве малонового диальдегида (МДА), используя коэффициент молярной экотинции, равной 1,56 к 105 (моль/л) см-1.
Спектр поглощения окрашенного продукта с тиобарбитуровой кислотой (ТБК) записывали на двулучевом спектрофотометре «СФ-6».
Результаты проведенных исследований представлены в таблице 2.

Как видно из таблицы, радиогенный стресс у белых крыс сопровождается резким усилением интенсивности пероксидации липидов - уже через 3 суток концентрации МДА в крови облученных крыс возрастала в 1,21 раза (Р<0,05) и постепенно увеличиваясь к 14 суткам достигала максимального значения (10,13±0,57 мкмоль/л против 4,65±0,09 в контроле).
Применение композиции полученной путем смешивание 70%-ного очищенного скипидара и 30%-ного высокоочищенного рафинированного подсолнечного масла через 24 ч после летального облучения приводило к длительному снижению интенсивности пероксидации липидов (ПОЛ) по сравнению с только облученными животными, что и обусловило повышение выживаемости летально облученных животных на фоне применения испытуемого препарата.
Таким образом, использование очищенного скипидара в смеси с высокоочищенным рафинированным подсолнечным маслом оказывает на организм радиозащитный эффект, основанный на ингибировании образования токсических продуктов пероксидации липидов (ПОЛ - радиотоксинов), мишенью атаки которых являются иммунокомпетентные клетки - лимфоциты, опустошающий апоптоз которых при летальном облучении ведет к радиационной гибели животного. Ингибирование образования ПОЛ под воздействием смеси терпенов (скипидара и подсолнечного масла) на фоне летального облучения усиливает сопротивляемость организма к разрушительному действию ионизирующих излучений.
Пример 6. Определение оптимальных сроков применение композиции до (с профилактической целью) и после (с лечебной целью) летального облучения животных.
Для этой цели проводили опыты на 80 белых мышах, разделенных на 16 групп. Проверяли противолучевую эффективность композиции на основе очищенного скипидара и подсолнечного масла до и после летального обучения животных. Сорока белым мышам первых 8-ми групп вводили внутримышечно по 0,1 мл 70%-ной эмульсии препарата с профилактической целью за 1,2,4, 6, 8, 10,12 и 14 суток (по 5 белых мышей на каждый срок) до летального облучения. Сорока белым мышам второй подгруппы (8 групп по 5 животных в каждой) спустя 1, 2, 4, 6, 8, 10, 12 и 14 суток после летального облучения вводили препарат в аналогических дозах и способом, что и первой подгруппе животных.
Белых мышей всех групп облучали в летальной дозе 8,0 Гр (ЛД100/30) на гамма-установке «Пума» и в течение 30 дней после облучения вели наблюдение за ними, учитывая количество павших и выживших в каждой группе животных.
Результаты опытов показали, что достаточно высокий профилактический (70-80%-ная выживаемость) и лечебный (60%-ная выживаемость) эффект достигается в течение первых 1-12 суток до и в течение первых 1-4 суток после летального облучения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТРОГО ЛУЧЕВОГО ПОРАЖЕНИЯ | 2021 |
|
RU2770991C2 |
| Способ лечения радиационных поражений организма и способ получения биологического препарата для лечения радиационных поражений организма | 2020 |
|
RU2760551C1 |
| Способ получения препарата для лечения радиационных поражений организма животных | 2024 |
|
RU2837739C1 |
| Способ лечения комбинированных радиационно-термических поражений и средство для его реализации | 2018 |
|
RU2686843C1 |
| Способ лечения радиационных поражений организма | 2018 |
|
RU2675598C1 |
| СПОСОБ ЛЕЧЕНИЯ РАДИАЦИОННО-КАДМИЕВОГО ПОРАЖЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ РАДИАЦИОННО-КАДМИЕВОГО ПОРАЖЕНИЯ | 2011 |
|
RU2484830C1 |
| Способ получения препарата для лечения животных при радиационно-кадмиевом поражении | 2024 |
|
RU2837735C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ РАДИАЦИОННЫХ ПОРАЖЕНИЙ ОРГАНИЗМА | 2006 |
|
RU2338546C2 |
| СПОСОБ ПОВЫШЕНИЯ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА МЛЕКОПИТАЮЩИХ ПРИ РАДИАЦИОННОМ ПОРАЖЕНИИ | 2012 |
|
RU2508100C1 |
| СПОСОБ ЛЕЧЕНИЯ КОМБИНИРОВАННОГО РАДИАЦИОННО-ТЕРМИЧЕСКОГО ПОРАЖЕНИЯ | 2013 |
|
RU2549451C2 |
Изобретение относится к ветеринарии и медицине, в частности к использованию препаратов, предназначенных для профилактики и лечения радиационных поражений, достигаемых путем ингибирования продуктов пераксидации липидов (ПОЛ) индуцированных ионизирующей радиацией. Способ лечения радиационных поражений организма заключается во введении в организм биологического препарата растительного происхождения - композиции, полученной путем смешивания очищенного скипидара и высокоочищенного рафинированного подсолнечного масла, однократно внутримышечно в дозах 0,25-0,5 мл/кг живого веса в течение первых 12 суток до и в течение первых 1-4 суток после летального облучения. 2 табл., 6 пр.
Способ лечения радиационных поражений организма, предусматривающий введение в организм биологического препарата растительного происхождения, отличающийся тем, что в качестве биологического препарата используют композицию, полученную путем смешивания 70 частей очищенного скипидара и 30 частей высокоочищенного рафинированного подсолнечного масла, которую вводят животным однократно внутримышечно в течение первых 1-12 суток до облучения и в течение первых 1-4 суток после облучения в дозе 0,25-0,5 мл/кг живой массы.
| Способ лечения комбинированных радиационно-термических поражений и средство для его реализации | 2018 |
|
RU2686843C1 |
| RU 94002337 A1, 27.08.1996 | |||
| Н | |||
| В | |||
| Марухненко и др., Новые перспективные радиопротекторы растительного происхождения, Сопроводительная фитотерапия в онкологии: материалы 2-й междунар | |||
| науч.-практ | |||
| конф., Москва, 23 мая 2015 г., под ред | |||
| В | |||
| Ф | |||
| Корсуна, М., 2015, стр | |||
| Светоэлектрический измеритель длин и площадей | 1919 |
|
SU106A1 |
Авторы
Даты
2020-10-13—Публикация
2019-07-23—Подача