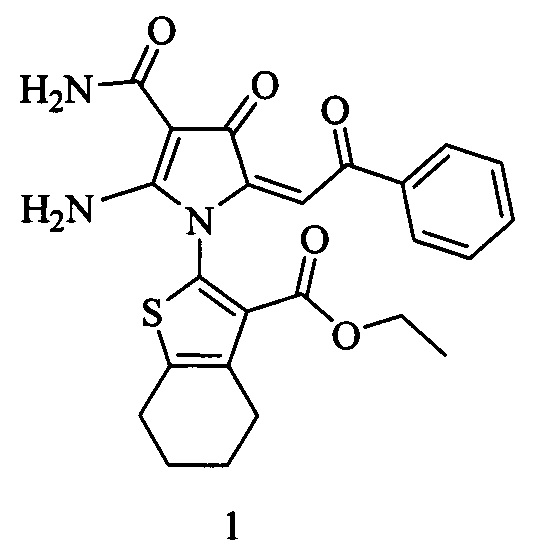
Изобретения относится к области органической химии, к новым биологически активным веществам класса замещенных амидов (Е)-2-амино-4-оксо-1-гетарил-4,5-дигидро-1Н-пиррол-3-карбоновых кислот, а именно к амиду (Е)-2-амино-4-оксо-5-(2-оксо-2-фенилэтилиден)-1-(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1H-пиррол-3-карбоновой кислоты 1 формулы:
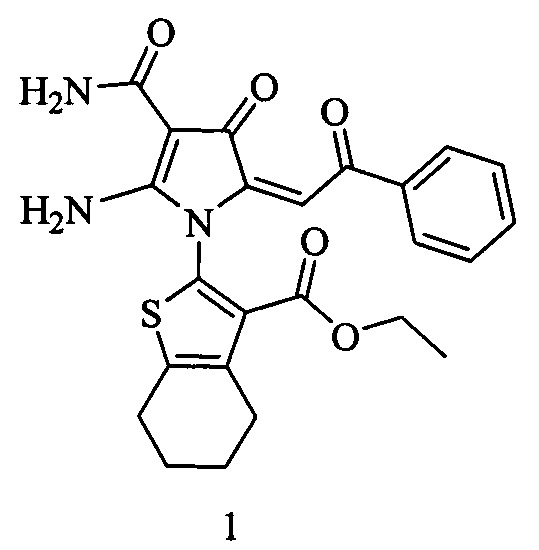
Соединение 1 обладает противомикробной активностью, что позволяет предположить его использование в медицине в качестве лекарственного средства с противомикробными свойствами.
Аналогом по структуре заявляемому соединению является амид 2-амино-1-(пиридин-3-ил)-4-(4-хлорфенил)-1Н-пиррол-3-карбоновой кислоты 2, обладающий противомикробной активностью [Open Journal of Medicinal Chemistry, 2015, 5, 49-96, doi: 10.4236/ojmc.2015.54005] формулы:
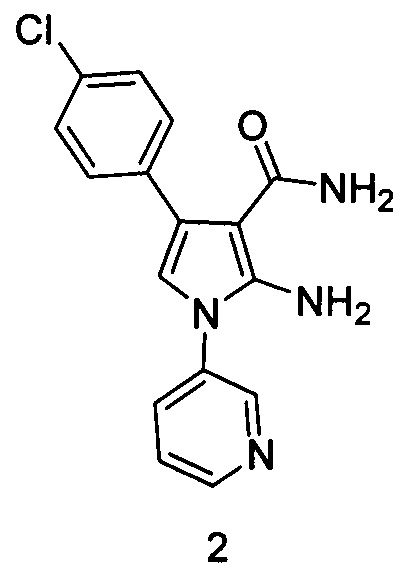
Эталоном сравнения биологической активности был выбран фенилсалицилат формулы:
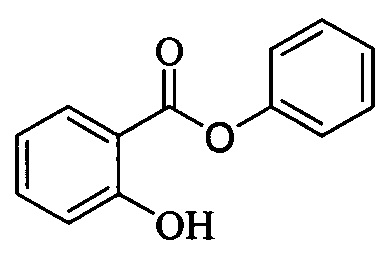
который широко применяется в лечебной практике, и являются аналогом по действию [Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - с. 950].
Задачей изобретения является поиск в ряду замещенных амидов (Е)-2-амино-4-оксо-1-гетарил-4,5-дигидро-1H-пиррол-3-карбоновых кислот веществ с выраженным противомикробным действием и низкой токсичностью.
Поставленная задача достигается получением амида (E)-2-амино-4-оксо-5-(2-оксо-2-фенилэтилиден)-1-(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1H-пиррол-3-карбоновой кислоты, который обладает противомикробной активностью.
Заявляемое соединение 1 синтезируют взаимодействием амида циануксусной кислоты с этиловым эфиром (Е)-2-[(2-оксо-5-фенилфуран-3(2H)-илиден)амино]-4,5,6,7-тетрагидробензо[6]тиофен-3-карбоновой кислоты в среде безводного толуола при 50°С с последующим выделением целевого продукта известными методами по схеме:
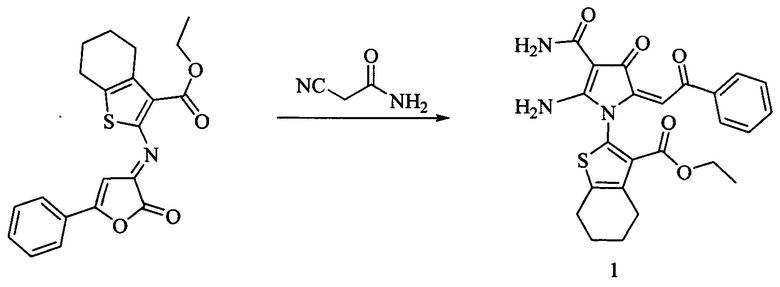
Пример 1. Получение соединения 1. К раствору 3.81 г (0.01 моль) этилового эфира (Е)-2-[(2-оксо-5-фенил фуран-3(2H)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты в 50 мл безводного диоксана прибавляли 0.84 г амида цианоуксусной кислоты, с последующим добавлением 1.01 г триэтиламина. Полученный раствор перемешивали при 50°С в течении 10 ч. Раствор охлаждали до комнатной температуры, выпавший осадок отфильтровывали и перекристаллизовывали из ацетонитрила. Выход 87%. Тразл.=234-235°С. Найдено, %: С 61.90, Н 4.98, N 9.00, S 6.89. C24H23N3O5S. Вычислено, %: С 61.92, Н 4.98, N 9.03, S 6.89. ИК спектр, v, см'1: 1664 (CONH2), 1711 (COOEt), 3208, 3359 (NH2). Спектр ЯМР 'Н, (400 МГц, DMSOd6), δ, м.д.: 1.13 (т, J 7.1 Гц, 3Н, Me), 1.81 (м, 4Н, 2СН2), 2.82 (м, 4Н, 2СН2), 4.20 (м, 2Н, CH2O), 5.79 (с, 1Н, С=СН), 6.89 (с, 1Н, NH2), 7.11 (с, 1Н, NH2), 7.50 (м, 2Н, HAr), 7.60 (м, 1Н, HAr), 7.82 (м, J 7.1 Гц, 2Н, HAr), 8.60 (с, 1Н, NH2), 8.64 (с, 1Н, NH2). Спектр ЯМР 13С (100 МГц, DMSOd6), δ, м.д.: 13.56, 21.81, 22.16, 24.65, 25.69, 60.41, 66.20, 89.16, 109.60, 128.31, 128.37, 129.70, 133.11, 133.91, 135.39, 136.96, 137.35, 142.50, 160.91, 165.86, 166.16, 175.9, 192.83. Полученное соединение 1 представляет собой желтое кристаллическое вещество, растворимое в хлороформе, толуоле, ацетоне, не растворимое в воде и гексане.
Пример 2. Для характеристики антибактериальной активности использовали стандартные параметры: минимальная подавляющая концентрация (МПК), которую определяли модифицированным методом двукратных серийных разведений (МУК 4.2.1890-04 Определение чувствительности микроорганизмов к антибактериальным препаратам) и минимальная бактерицидная концентрация (МБК) (Медицинские лабораторные технологии: Руководство по клинической лабораторной диагностике, п/р Каприщенко, 2013, Т. 2, стр. 407). Тесты проводили с использованием культур модельных микроорганизмов Escherichia coli МС4100 и Staphylococcus epidermidis АТСС29887 на питательной среде Луриа-Бертани в 96-луночных полистироловых планшетах. Конечная концентрация микроорганизмов в лунках составляла 5*105 КОЕ/мл. Культивирование проводили при 37°С без перемешивания. Определение МПК и высевы для определения МБК производили через 24 ч. На первом этапе исследуемые соединения растворяли в диметилсульфоксиде (ДМСО), дальнейшие разведения производили в метаноле. В качестве начальных в тестах использовали концентрации, которые при внесении в питательную среду Луриа-Бертани не образовывали осадка (от 0,2 до 4 мг/мл).
Пример 3. Острую токсичность (ЛД50, мг/мл) соединения 1 определяли по методу Г.Н. Першина [Першин Г.Н. Методы экспериментальной химиотерапии // М., С. 100, 109-117 (1971)]. Соединение 1 вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемых соединений 1-3 ЛД50 составляет > 1500 мг/кг.
Согласно классификации токсичности препаратов, соединение 1 относится к V классу практически нетоксичных препаратов [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977. - с. 196]. Результаты испытаний представлены в таблице:
Противомикробная активность и острая токсичность соединения 1.
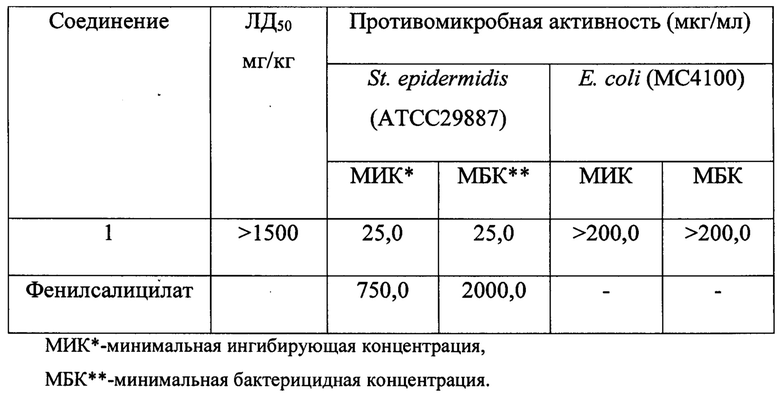
Как видно из таблицы, заявляемое соединение 1 превышает по противомикробной активности препарат сравнения (Фенилсалицилат) в 30 раз по отношению к St. epidermidis. Таким образом, амид (E)-2-амино-4-оксо-5-(2-оксо-2-фенилэтилиден)-1-(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1H-пиррол-3-карбоновой кислоты 1 проявляет более высокую активность по сравнению с эталоном сравнения в отношении грамположительных микроорганизмов, что делает возможным его использование для создания новых лекарственных средств, целенаправленного действия.
Изобретение относится к амиду (E)-2-амино-4-оксо-5-(2-оксо-2-фенилэтилиден)-1-(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1H-пиррол-3-карбоновой кислоты формулы 1:
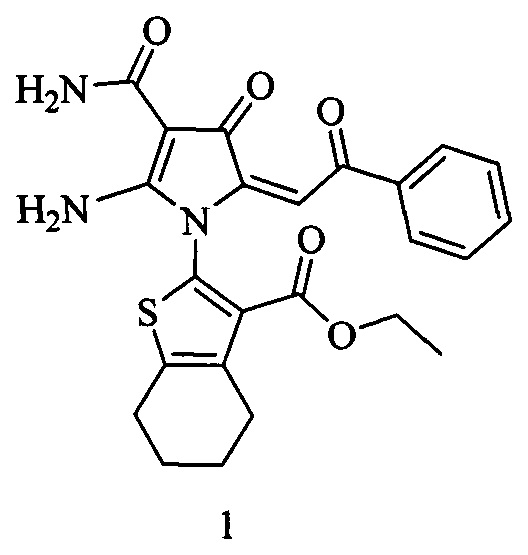
Технический результат: получено соединение с высоким выходом, обладающее выраженной противомикробной активностью в отношении грамположительных микроорганизмов, а также низкой токсичностью. 1 табл., 3 пр.
Амид (E)-2-амино-4-оксо-5-(2-оксо-2-фенилэтилиден)-1-(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1Н-пиррол-3-карбоновой кислоты:
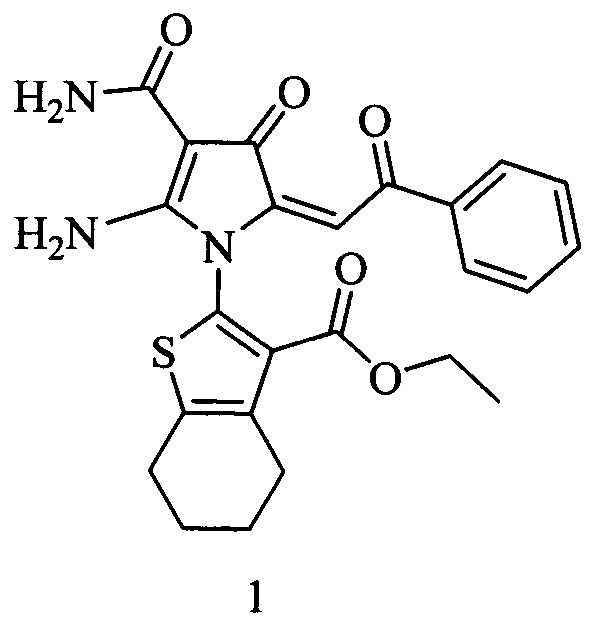
обладающий противомикробной активностью.
| M | |||
| T | |||
| Sarg, M | |||
| M | |||
| Koraa, A | |||
| H | |||
| Bayoumi, S | |||
| M | |||
| Abd El Gilil | |||
| "Synthesis of Pyrroles and Condensed Pyrroles as Anti-Inflammatory Agents with Multiple Activities and Their Molecular Docking Study", Open Journal of Medicinal Chemistry, 2015, 5, 49-96, doi: 10.4236/ojmc.2015.54005 | |||
| WO 2010122012 A1, 28.10.2010 | |||
| WO 2006012642 A2, 02.02.2006 | |||
| RU |
Авторы
Даты
2020-12-11—Публикация
2020-05-26—Подача