Изобретение относится к экспериментальной медицине и онкологии, а именно, к способу фото динамической терапии (ФДТ) перевивной опухоли меланома В-16 мышей.
При проведении ФДТ животным вводится фотосенсибилизатор (ФС), избирательно накапливающийся в злокачественных новообразованиях. Затем опухоль подвергается дистанционному облучению лазерным светом определенной длины волны, в соответствии со спектром возбуждения ФС. В результате облучения происходит фотохимическая реакция, где ФС фактически играет роль катализатора, и происходит образование активных форм кислорода и различных радикалов, которые являются цитотоксическими агентами и вызывают разрушение клеток опухоли. Второй механизм ФДТ - деструкция эндотелия кровеносных сосудов в зоне лазерного облучения, в результате которой имеет место тромбоз сосудов и нарушение питания в опухоли.
Избирательность разрушения опухоли связана с избирательностью накопления ФС в опухоли по отношению к здоровой ткани и с воздействием света определенной длины волны. Не пораженные опухолью ткани в меньшей степени поглощают ФС, но в результате лазерного облучения имеет место нежелательная частичная деструкция здоровых тканей.
Из уровня техники [патент RU 2119363 С1, опубл. 27.09.1998] известен способ ФДТ злокачественных опухолей, включающий системное введение ФС с последующим дистанционным лазерным облучением опухоли в световой дозе 124 Дж/см2 и 98 Дж/см2 на курс лечения.
Однако в известном способе при минимальных побочных реакциях в зоне облучения достичь полной регрессии возможно лишь при воздействии на небольшие поверхностные опухоли.
Известен также способ ФДТ злокачественных опухолей [RU 2146159 С1, опубл. 10.03.2000], включающий системное введение ФС и лазерное дистанционное облучение зоны опухолевого роста световой дозой 300-500 Дж/см2.
Однако данный способ применим, в основном, к поверхностным опухолям, так как лазерное облучение с используемыми параметрами приводит к развитию геморрагического некроза в здоровых тканях во время и после ФДТ.
Известен способ ФДТ злокачественных опухолей [патент RU 2169015 С2, опубл. 20.06.2001], в котором ФДТ осуществляют путем введения ФС "Фотосенс" в дозе 0,3-0,8 мг/кг веса тела больного с последующим воздействием на зону опухолевого роста дистанционным лазерным излучением мощностью 100-500 мВт/см2.
Однако в этих условиях интенсивное лазерное воздействие, осуществляемое за короткий промежуток времени после введения ФС, приводит к полному терапевтическому эффекту при воздействии на поверхностные опухоли и сопровождается глубоким некрозом опухоли и части окружающих нормальных тканей.
Известен также способ ФДТ злокачественных новообразований [патент RU 2704202 С1, опубл. 24.10.2019], включающий введение в организм пациента фотосенсибилизатора Фоторан Е6 и лазерное облучение зоны опухолевого роста световой дозой 150-300 Дж/см2.
Однако этот способ направлен на терапию соединительнотканной солидной опухоли - саркома М-1 и не рассчитан на применение для ФДТ других видов опухолей, в частности такой агрессивной опухоли, как меланома В-16.
Проблема лечения меланомы методом ФДТ - недостаточная селективность накопления препаратов - фотосенсибилизаторов в клетках меланомы по сравнению с накоплением в окружающих здоровых тканях для полной эрадикации опухоли без глубоких повреждений окружающих тканей.
Из уровня техники [патент RU 2670087 С1, опубл. 18.10.2018] известен ФС на основе хлорина е6 с присоединенным ПСМА-лигандом для лечения рака предстательной железы и способ его получения.
Однако из уровня техники не известна возможность использования данного ФС для терапии перевивной опухоли меланома В-16 мышей.
В предлагаемом изобретении предложен способ фотодинамической терапии перевивной опухоли меланома В-16 мышей с использованием фотосенсибилизатора на основе хлорина е6 с присоединенным ПСМА-лигандом.
Техническая задача предлагаемого изобретения состояла в определении оптимального лекарственно-светового интервала (ЛСВИ) - времени от момента введения ФС до облучения лазером, подбор дозы введенного ФС и подбор плотности мощности лазерного излучения для достижения полной эрадикации опухоли меланома В-16 с минимальным повреждением окружающих здоровых тканей.
Технический результат заключается в повышении эффективности фото динамической терапии и в обеспечении полной эрадикации опухоли меланома В-16 экспериментальных животных с минимальным повреждением окружающих здоровых тканей за счет селективного накопления ФС в опухоли, обусловленного захватом ПСМА-лиганда фотосенсибилизатора рецепторами ПСМА клеток меланомы, а также за счет оптимально подобранных параметров и режима лазерного воздействия.
Технический результат достигается способом фотодинамической терапии перевивной опухоли меланома В-16 мышей, согласно которому внутривенно вводят хлориновый фотосенсибилизатор с ПСМА-лигандом в организм животного в дозе 2,5-5,0 мг/кг и далее облучают опухоль лазерным светом с параметрами: длина волны 650-670 нм, плотность мощности Ps=0,4-0,5 Вт/см2, плотность энергии Е=100-200 Дж/см2, причем время между введением фотосенсибилизатора и сеансом облучения составляет от 45 мин до 1 ч. Хлориновый фотосенсибилизатор с ПСМА-лигандом имеет структурную формулу (I):
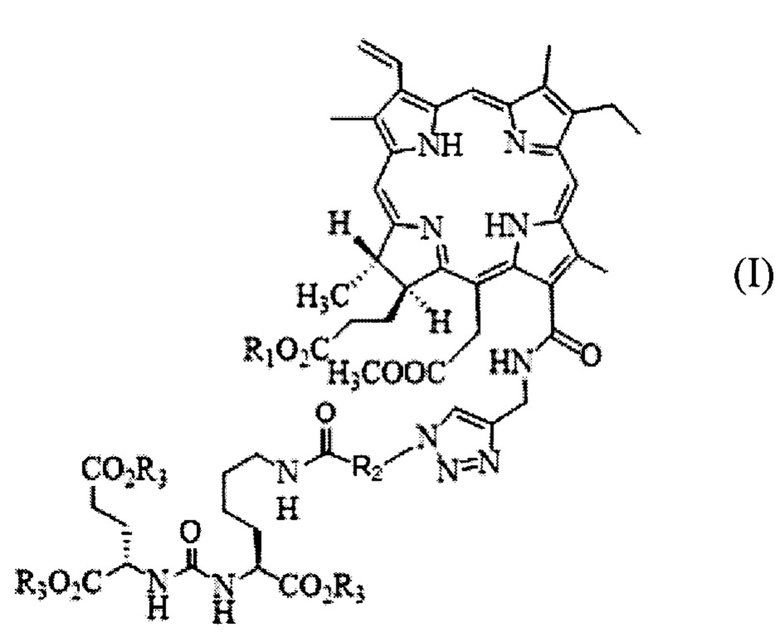
где R1 выбирается из водорода (Н), натрия (Na), калия (К) или C1-С2-алкила; R2 представляет собой соединение общей формулы CxH2x, где х=4÷17; R3 выбирается из водорода (Н), натрия (Na) или калия (К).
В предлагаемом способе в экспериментальных исследованиях получено 100% полное излечение животных с меланомой В-16 при проведении ФДТ с применением хлоринового фотосенсибилизатора с ПСМА-лигандом.
Изобретение поясняется подробным описанием, сериями опытов и иллюстрациями, на которых изображено:
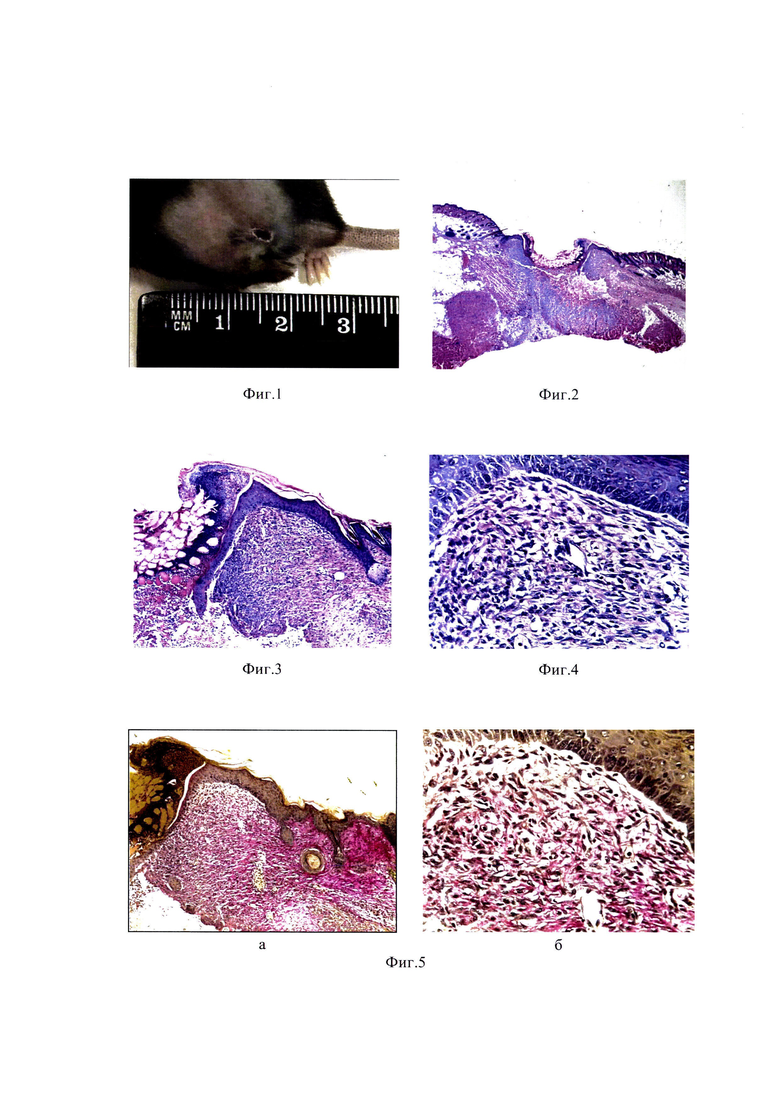
Фиг. 1 - Формирование струпа на коже бедра через 21 сутки после ФДТ (макрофото).
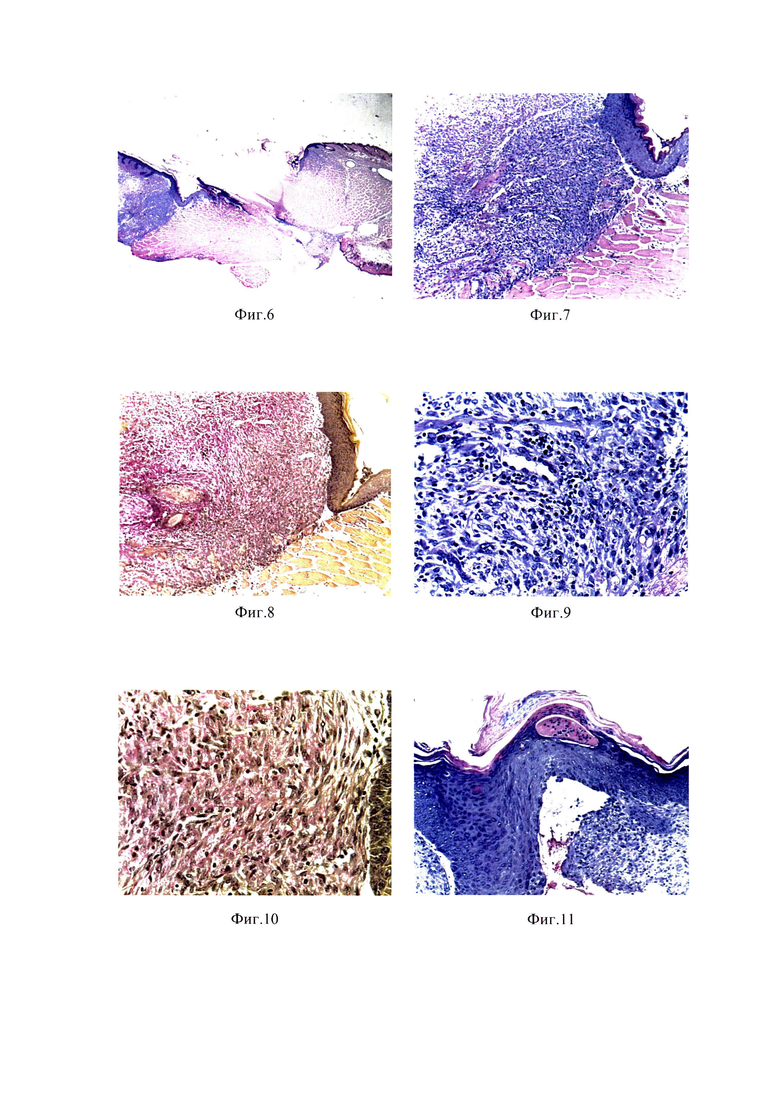
Фиг. 2 - Зона элиминации меланомы В-16 на 21 сутки после ФДТ; окрашивание гематоксилином и эозином (Об. ×2,5).
Фиг. 3-Эпителизация и замещение зоны фотодинамической деструкции соединительной тканью на 21 сутки после ФДТ, окрашивание гематоксилином и эозином (Об. ×10).
Фиг. 4 - Фрагмент фиг. 3 (Об. ×40).
Фиг. 5 - Формирование плотной соединительной ткани под базальным слоем эпидермиса в зоне фото динамического воздействия на 21 сутки после ФДТ, окрашивание по Ван Гизону: а) Об. ×10; б) Об. ×40.
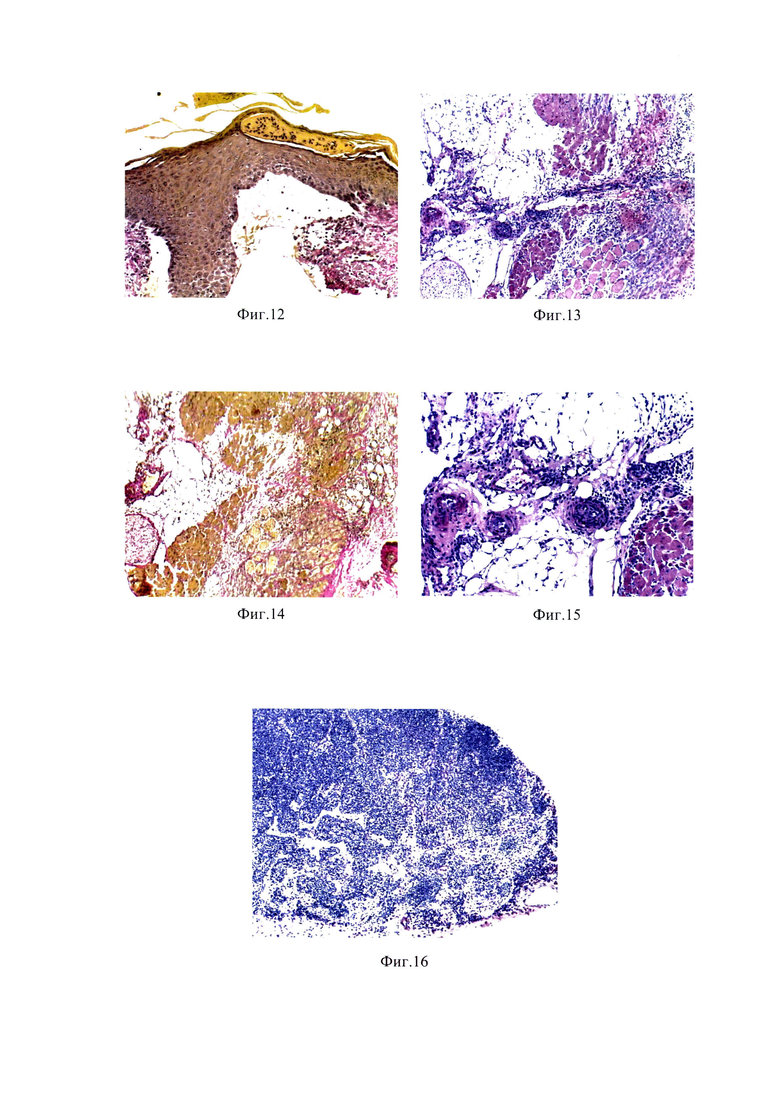
Фиг. 6 - Деструктивные изменения мягких тканей бедра под поверхностным струпом на 21 сутки после ФДТ, окрашивание гематоксилином и эозином (Об. ×2,5).
Фиг. 7 - Фрагмент фиг. 6, окрашивание гематоксилином и эозином (Об. ×10).
Фиг. 8 - Замещение зоны фотодинамического повреждения фиброзной тканью, окрашивание по Ван Гизону (Об. ×10).
Фиг. 9 - Пролиферация фибробластов в зоне роста соединительной ткани (Об. ×40).
Фиг. 10 - Коллагеновые волокна в зоне роста соединительной ткани (Об. ×40).
Фиг. 11 - Локальная гиперплазия эпидермиса в кожном рубце через 21 сутки после ФДТ, окрашивание гематоксилином и эозином (Об. ×20).
Фиг. 12 - Плотная соединительная ткань под гиперплазированным эпидермисом, окрашивание по Ван Гизону (Об. ×20).
Фиг. 13 - Репаративные процессы в мышечной ткани через 21 сутки после ФДТ, окрашивание гематоксилином и эозином (Об. ×10).
Фиг. 14 - Разрастание соединительной ткани в глубокой зоне повреждения бедра через 21 сутки после ФДТ, окрашивание по Ван Гизону (Об. ×10).
Фиг. 15 - Окклюзия артериол в соединительной ткани бедра через 21 сутки после ФДТ, окрашивание гематоксилином и эозином (Об. ×20).
Фиг. 16 - Регионарный подвздошный лимфатический узел мыши опытной группы, окрашивание гематоксилином и эозином (Об. ×10).
Способ осуществляют следующим образом.
Работа выполнена с соблюдением международных рекомендаций по проведению исследований с использованием лабораторных животных, изложенных в «Европейской конвенции по защите позвоночных животных, используемых в экспериментальных и других научных целях» (Страсбург, 1987), на 20 мышах С57 BL/6j массой 18-20 г с имплантированной подкожно с внешней стороны бедра меланомой В-16. Меланому перевивали мышам в виде суспензии в объеме 0,10-0,15 мл. Штамм опухоли получен в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Животные получены из питомника лабораторных животных ФГБУН НЦБМТ ФМБА России (филиал «Андреевка»). Они были здоровы, имели ветеринарный сертификат качества и состояния здоровья и прошли 20-суточный карантин в виварии МРНЦ им. А.Ф. Цыба.
При достижении наибольшего диаметра опухолевых узлов 0,4-0,6 см животных методом рандомизации распределяли на опытные и контрольные группы. Опухоли мышей контрольных групп не подвергались воздействиям.
Экспериментальным мышам со злокачественной эктодермальной опухолью меланома В16 вводят фотосенсибилизатор Фоторан Е6 (препарат сравнения) в дозе 5 мг/кг, внутривенно или внутрибрюшинно, через оптимальный ЛСВИ (при внутривенном введении - от 45 мин до 1 ч, при внутрибрюшинном введении - от 1,5 до 2 ч), и далее опухоли у животных облучают лазерным светом с длиной волны 662 нм, Ps=0,25 Вт/см2, Е=152 Дж/см2.
В соответствии с предлагаемым способом вводили внутривенно в дозе 2,5 мг/кг хлориновый фотосенсибилизатор с ПСМА-лигандом структурной формулы (I), в которой: R1 - СН3, R2 - С10Н20, R3 - Na. Лазерное облучение проводили в период максимального индекса контрастности опухоль/здоровая ткань после введения ФС. Для воздействия лазерным излучением на опухоли мышей использовали полупроводниковый аппарат «Аткус-2» (ЗАО «Полупроводниковые приборы», Санкт-Петербург). Длина волны излучения 662 нм, параметры лазерного излучения: Е=100 Дж/см2, Р=0,44 Вт/см2, диаметр светового пятна - 1,0 см. Для фиксации животных использовали известное устройство [патент RU190718 U1, опубл. 09.07.2019].
Для оценки противоопухолевой эффективности на 21 сутки после ФДТ животные были выведены для патоморфологического анализа.
Выделенную ткань опухоли в виде пластинок, ориентированных вдоль длинной оси, и регионарные подвздошные лимфатические узлы фиксировали 24 ч в жидкости Буэна. После стандартной гистологической проводки ориентированные фрагменты тканей заключали в парафиновую среду Гистомикс на станции заливки HistoStar (Thermo Scientific).
Для морфологических исследований депарафинированные срезы толщиной 5 мкм, полученные на микротоме Leica RM2235, окрашивали гематоксилином и эозином (БиоВитрум) и по Ван Гизону для выявления соединительной ткани.
Гистологические срезы изучали под микроскопом Leica DM 1000 с микрофотосъемкой на цифровую камеру Leica ICC50 HD при 4-х уровнях увеличений: объективы ×2,5, ×10, ×20 и ×40.
На 21 сутки после ФДТ в зоне имплантации меланомы макроскопически и при пальпировании опухоли не определялись; на коже бедра в зоне облучения были видны небольшие плотные струпы (Фиг. 1) или рубцы.
При гистологическом изучении зон фотодинамического воздействия у всех мышей опытной группы выявлена полная деструкция опухолей. В зоне воздействия лазерным излучением наблюдалось кратерообразное повреждение кожного покрова, ограниченное краевой эпителизацией и узким валом полиморфноядерных лейкоцитов (Фиг. 2 и Фиг. 3).
Кроме того, в зонах повреждения выявлялись небольшие полости, заполненные межтканевой жидкостью, эритроцитами и распадающимися мышечными волокнами. Зоны фотодинамической деструкции тканевых структур замещались соединительной тканью (Фиг. 4 и Фиг. 5 а, б).
В области образования поверхностного струпа были видны более выраженные деструктивные изменения мягких тканей бедра до поперечнополосатых мышц (Фиг. 6).
На границе с погибшими мышечными волокнами также отмечалось замещение зон повреждения фиброзной тканью (Фиг. 7, Фиг. 8, Фиг. 9 и Фиг. 10).
В зоне формирования рубцовых изменений наблюдалась локальная гиперплазия эпидермиса с его утолщением и неравномерным разрастанием (Фиг. 11).
Под эпидермисом были видны небольшие полости, заполненные клеточным детритом, и ограниченные формирующейся плотной волокнистой соединительной тканью (Фиг. 12).
В более глубоких зонах повреждения тканей бедра отмечались репаративные процессы со стороны поврежденных мышечных волокон (Фиг. 13) и разрастание соединительной ткани (Фиг. 14).
Обращали на себя внимание изменения со стороны сосудов. Так, в артериолах, расположенных в рыхлой соединительной и жировой ткани была видна окклюзия просветов за счет разрастания эндотелия и гладкомышечных клеток (Фиг. 15).
При микроскопическом исследовании тканей бедра мышей опытной группы в зоне имплантации меланомы В16 на 21 сутки после фотодинамической терапии опухолевые клетки не выявлены. В регионарных лимфатических узлах мышей этой группы, увеличенных за счет разрастания лимфоидной ткани, метастазы меланомы не обнаружены (Фиг. 16).
Анализ полученных макро- и микроскопических результатов свидетельствует, что на 21 сутки после фото динамической терапии меланомы В-16 с применением хлоринового фотосенсибилизатора с ПСМА-лигандом у мышей опытной группы в зонах воздействия лазерным излучением выживших опухолевых клеток не обнаружено.
Таким образом, после ФДТ, проведенной в оптимальные сроки после введения ФС и при оптимальных параметрах лазерного излучения, был достигнут результат 100% эрадикации меланомы В-16. Высокий терапевтический эффект при данных параметрах лазерного воздействия был обусловлен снижением повреждения нормальных тканей за счет высокого индекса контрастности опухоль/здоровая ткань, достигаемого за счет селективного накопления ФС в опухоли, обусловленного захватом ПСМА-лиганда фотосенсибилизатора рецепторами ПСМА клеток меланомы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ОПУХОЛИ КАРЦИНОМА ЭРЛИХА МЫШЕЙ С ФОТОСЕНСИБИЛИЗАТОРОМ ХЛОРИНОВОГО РЯДА | 2022 |
|
RU2788766C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ЭКТОДЕРМАЛЬНОЙ ОПУХОЛИ МЕЛАНОМЫ B16 МЫШЕЙ | 2020 |
|
RU2724867C2 |
| СПОСОБ НИЗКОИНТЕНСИВНОГО ЛАЗЕРНОГО ИЗЛУЧЕНИЯ ПРИ ПРОВЕДЕНИИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ФОТОСЕНСИБИЛИЗАТОРОМ ФОТОРАН Е6 ПЕРЕВИВНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ ОПУХОЛИ САРКОМА М-1 КРЫС, ПОЛОЖИТЕЛЬНОЙ ПО МУТАНТНОМУ ГЕНУ р53 | 2020 |
|
RU2736261C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ПОВЕРХНОСТНОЙ СОЛИДНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС | 2019 |
|
RU2704202C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕВИВНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС ПРИ КОМБИНИРОВАННОМ ВОЗДЕЙСТВИИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И ЛУЧЕВОЙ ТЕРАПИИ | 2021 |
|
RU2763663C2 |
| Способ проведения фотодинамической терапии солидной карциномы Эрлиха мышей | 2021 |
|
RU2774589C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ПОВЕРХНОСТНОЙ СОЛИДНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС | 2021 |
|
RU2776449C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕВИВНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС ПРИ КОМБИНИРОВАННОМ ВОЗДЕЙСТВИИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И ЛУЧЕВОЙ ТЕРАПИИ | 2021 |
|
RU2767272C2 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ В КОМБИНИРОВАННОМ ЛЕЧЕНИИ МЕСТНО-РАСПРОСТРАНЕННЫХ САРКОМ МЯГКИХ ТКАНЕЙ | 2020 |
|
RU2737704C2 |
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА сТ1N0M0 ПРИ ГЛУБИНЕ ИНВАЗИИ ОПУХОЛИ ДО 5 ММ | 2023 |
|
RU2824427C2 |
Изобретение относится к экспериментальной медицине и онкологии, а именно к способу фотодинамической терапии перевивной опухоли меланомы В-16 мышей. Согласно предложенному способу внутривенно вводят хлориновый фотосенсибилизатор с ПСМА-лигандом в организм животного в дозе 2,5-5,0 мг/кг и далее облучают опухоль лазерным светом с параметрами: длина волны 650-670 нм, плотность мощности Ps=0,4-0,5 Вт/см2, плотность энергии Е=100-200 Дж/см2, причем время между введением указанного фотосенсибилизатора и сеансом облучения составляет от 45 мин до 1 ч. Хлориновый фотосенсибилизатор с ПСМА-лигандом имеет структурную формулу (I):
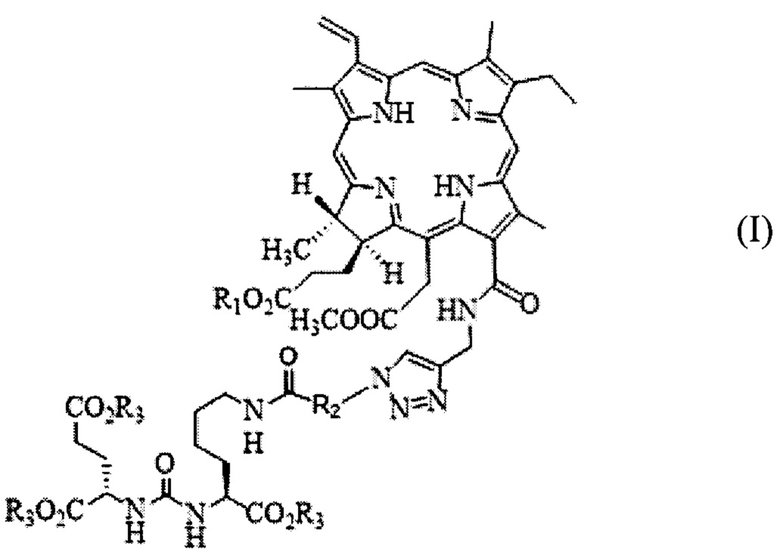
где R1 выбирается из водорода (Н), натрия (Na), калия (К) или С1-С2-алкила, R2 представляет собой группу общей формулы СхН2х, где х=4÷17, R3 выбирается из водорода (Н), натрия (Na) или калия (К). Способ обеспечивает повышение эффективности фотодинамической терапии и приводит к полной эрадикации опухоли меланомы В-16 экспериментальных животных с минимальным повреждением окружающих здоровых тканей за счет селективного накопления фотосенсибилизатора в опухоли, обусловленного захватом ПСМА-лиганда фотосенсибилизатора рецепторами ПСМА клеток меланомы, а также за счет оптимально подобранных параметров и режима лазерного воздействия. 17 ил.
Способ фотодинамической терапии перевивной опухоли меланома В-16 мышей, характеризующийся тем, что внутривенно вводят хлориновый фотосенсибилизатор с ПСМА-лигандом в организм животного в дозе 2,5-5,0 мг/кг и далее облучают опухоль лазерным светом с параметрами: длина волны 650-670 нм, плотность мощности Ps=0,4-0,5 Вт/см2, плотность энергии Е=100-200 Дж/см2, причем время между введением указанного фотосенсибилизатора и сеансом облучения составляет от 45 мин до 1 ч, где хлориновый фотосенсибилизатор с ПСМА-лигандом имеет структурную формулу (I):
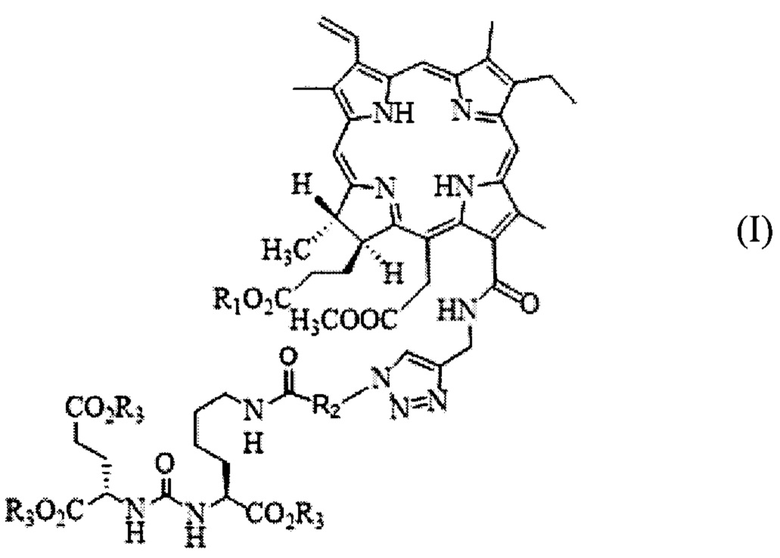
где R1 выбирается из водорода (Н), натрия (Na), калия (К) или С1-С2-алкила; R2 представляет собой группу общей формулы СхН2х, где х=4÷17; R3 выбирается из водорода (Н), натрия (Na) или калия (К).
| Фотосенсибилизатор для лечения рака предстательной железы и способ его получения | 2018 |
|
RU2670087C1 |
| ОСИПЧУК Ю.В | |||
| и др., Фотодинамическая терапия меланомы В16 у мышей с новым фотосенсибилизатором, борированным хлорином, Фотодинамическая терапия и Фотодиагностика, 2015, номер 2, с | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ изготовления электрических нагревательных приборов | 1928 |
|
SU19704A1 |
| ФОТОСЕНСИБИЛИЗАТОР НА ОСНОВЕ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ИСПОЛЬЗОВАНИЕМ ЭТОГО ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2411943C2 |
| ПРОИЗВОДНЫЕ 13(1)-N-{2-[N-(КЛОЗО-МОНОКАРБАДОДЕКАБОРАН-1-ИЛ)-МЕТИЛ]АМИНОЭТИЛ}АМИД-15(2),17(3)-ДИМЕТИЛОВОГО ЭФИРА ХЛОРИНА e, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2406726C1 |
| HUANG Y.-Y | |||
| et al, Melanoma resistance to photodynamic | |||
Авторы
Даты
2020-12-21—Публикация
2020-03-24—Подача