ОБЛАСТЬ
[0001] Эта заявка претендует на приоритет в соответствии с 35 §1 19 (e) Свода законов US согласно Предварительной патентной Заявке № 62/345,086, поданной 3 июня 2016 и имеющей название «СПОСОБ ЛЕЧЕНИЯ ФИБРОЗА ПЕЧЕНИ», которая включена здесь полностью посредством этой ссылка.
[0002] Настоящее раскрытие описывает способы лечения фиброза печени CCR2 антагонистами. Фиброз печени может быть связан с неалкогольным стеатогепатитом (NASH), неалкогольным жировым заболеванием печени (NAFLD), развивающимся циррозом, нецирротическим фиброзом печени, сахарным диабетом 2 типа (T2DM) или метаболическим синдромом (MS).
ПРЕДПОСЫЛКИ
[0003] Фиброз печени является результатом чрезмерного накопления белков внеклеточного матрикса, включая коллаген, которое встречается в большинстве типов хронических заболеваний печени. Неалкогольная жировая болезнь печени (NAFLD) - это медицинское состояние, которое характеризуется накоплением жира (называемым жировой инфильтрацией) в печени. До 85% пациентов с NAFLD имеют диабет или нарушенную толерантность к глюкозе. Неалкогольный стеатогепатит (NASH) - это самая тяжелая форма NAFLD, которая сопровождается жировой инфильтрацией вместе с воспалением печени (стеатогепатитом). NASH поражает 2-5% американцев.
[0004] Как NASH, так и NAFLD более распространены возможно из-за увеличенного уровня ожирения. Ожирение также способствует диабету и повышенному холестерину крови, что может дополнительно осложнить здоровье пациента с NASH. В настоящее время имеется потребность в улучшенных способах лечения фиброза печени, который может быть связан с неалкогольным стеатогепатитом (NASH), неалкогольной жировой болезнью печени (NAFLD), развивающимся циррозом, нецирротическим фиброзом печени, сахарным диабетом 2 типа (T2DM) или метаболическим синдромом (MS).
[0005] CCR2 антагонисты были описаны в патентах US № 8,519, 135, US 7,622,583, 7,884, 1 10, и US 8,093,247 и патентной публикации US 2006/0173019.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ
[0006] Настоящее раскрытие направлено на способы лечения фиброза печени в пациенте, включающие назначение нуждающемуся в этом пациенту эффективного количества соединения Формулы I:
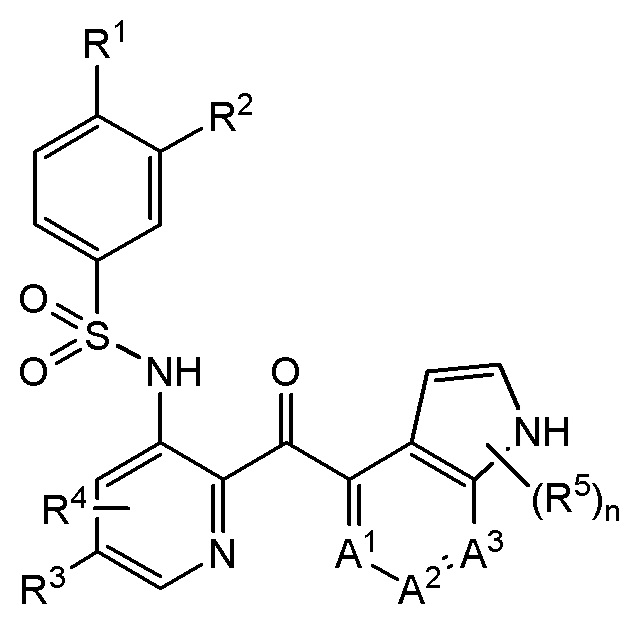
Формула I
или фармацевтически приемлемой его соли, где
R1 - это галоген или C1-6 алкил;
R2 - водород, галоген, C1-6 алкил, C1-6 алкокси, C1-6 галоалкил, C1-6 галоалкокси или -CN;
R3 - водород, галоген или C1-6 алкил;
R4 - водород, галоген или C1-6 алкил;
каждый R5 независимо - C1-6 алкил, - О, или -NH2;
n - 0, 1, 2, или 3; и
каждый из A1, A2 и A3 - это -CH- или -N-, где по меньшей мере один из A1, A2 или A3 - это - N-.
ФИГУРЫ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
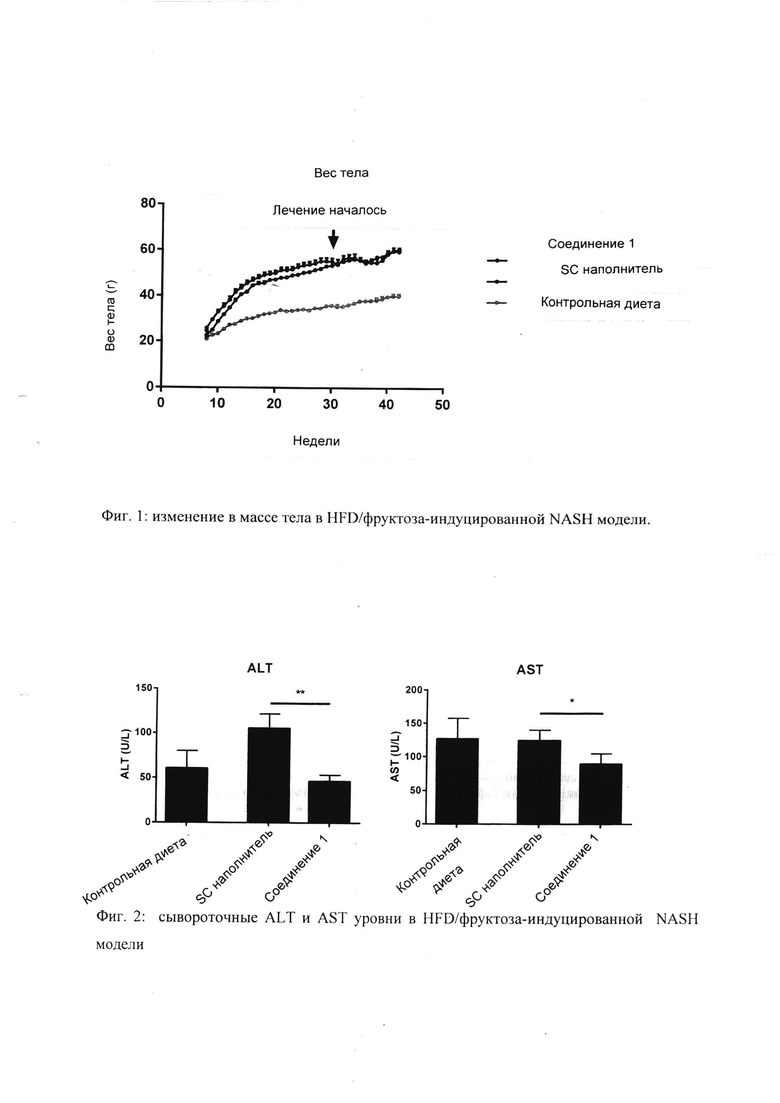
[0007] Фиг. 1 иллюстрирует изменение в массе тела в HFD/фруктоза-индуцированной NASH модели.
[0008] Фиг. 2 показывает сывороточные ALT и AST уровни в HFD/фруктоза-индуцированной NASH модели.
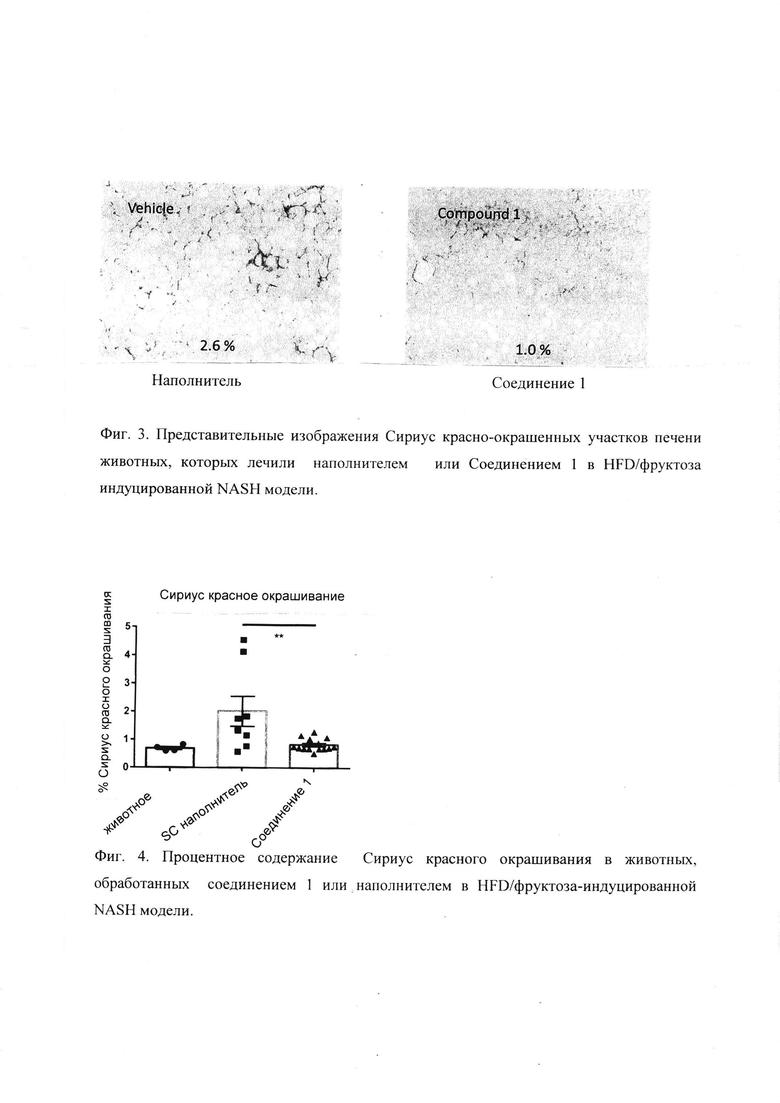
[0009] Фиг. 3 показывает представительные изображения Сириус красно-окрашенных участков печени животных, обработанных наполнителем или Соединением 1 в FHD/фруктоза-индуцированной NASH модели.
[0010] Фиг. 4 показывает процентное содержание Сириус красного окрашивания в животных, обработанных соединением 1 или наполнителем в HFD/фруктоза-индуцированной NASH модели.
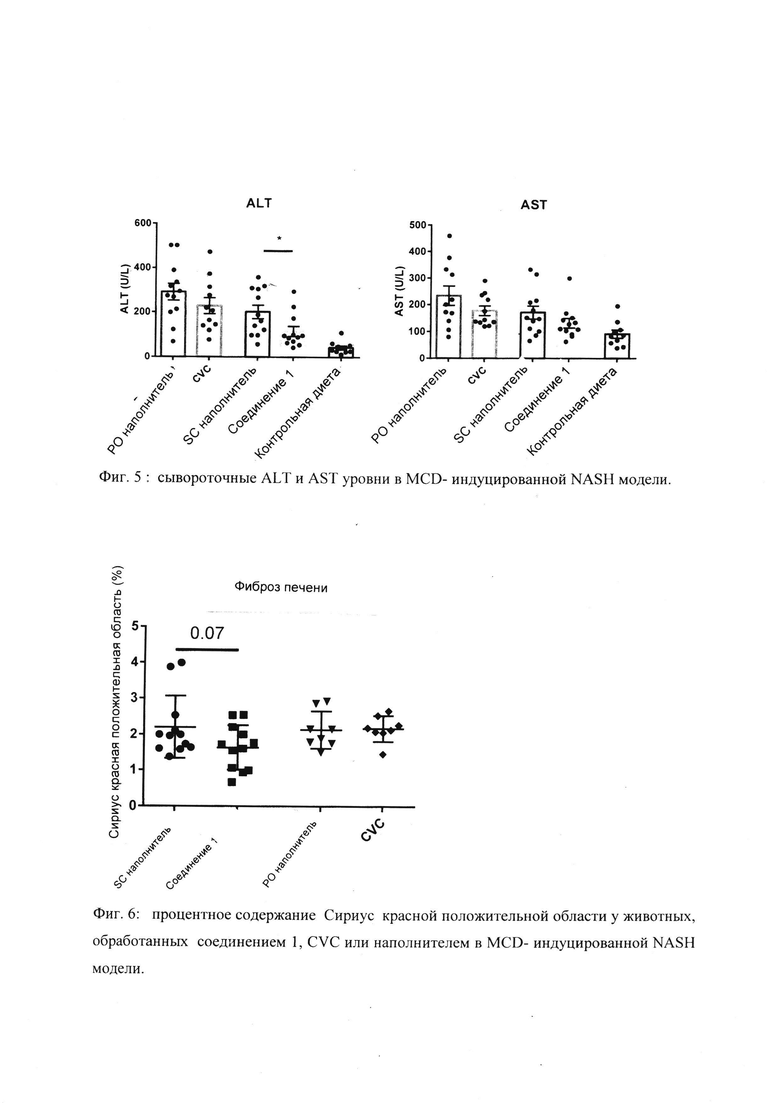
[0011] Фиг. 5 показывает сывороточные ALT и AST уровни в MCD- индуцированной NASH модели.
[0012] Фиг. 6 показывает процентное содержание Сириус красной положительной области у животных, обработанных соединением 1, CVC или наполнителем в MCD- индуцированной NASH модели.
ПОДРОБНОЕ ОПИСАНИЕ
Сокращения и определения
[0013] При описании соединений, композиций, способов и процессов этого раскрытия следующие термины имеют следующие значения, если не указано иначе.
[0014] «Алкил» как таковой или в качестве части другого заместителя относится к углеводородной группе, которая может быть линейной, цикличной или разветвленной или их комбинацией, имеющей указанное количество атомов углерода (т.е. C1-8 означает один - восемь атомов углерода). Примеры алкильных групп включают метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, изобутил, втор-бутил, циклогексил, циклопентил, (циклогексил)метил, циклопропилметил, бицикло[2.2.1]гептан, бицикло[2.2.2]октан и т.д. Алкильные группы являются незамещенными, если не указано иначе. Примеры замещенного алкила включают галоалкил, тиоалкил, аминоалкил и т.п.
[0015] «Алкокси» относится к - O-алкилу. Примеры алкокси группы включают метокси, этокси, н-пропокси и т.д.
[0016] «Алкенил» относится к группе ненасыщенного углеводорода, которая может быть линейной, цикличной или разветвленной или их комбинацией. Группы алкенила с 2-8 атомами углерода предпочтительны, несмотря на то, что алкенил может иметь больше чем 8 атомов углерода. Группа алкенила может содержать 1, 2 или 3 углерод- углерод двойные связи. Примеры групп алкенила включают этенил, н-пропенил, изопропенил, н-бут-2-енил, н-гекс-3-енил, циклогексенил, циклопентенил и т.п. Группы алкенила являются незамещенными, если не указано иначе.
[0017] «Алкинил» относится к группе ненасыщенного углеводорода, которая может быть линейной, цикличной или разветвленной или их комбинацией. Группы алкинила с 2-8 атомами углерода предпочтительны. Группа алкинила может содержать 1, 2 или 3 углерод-углерод тройные связи. Примеры групп алкинила включают этинил, н-пропинил, н-бут-2-инил, н-гекс-3-инил и т.п. Группы алкинила являются незамещенными, если не указано иначе.
[0018] «Арил» относится к группе полиненасыщенного ароматического углеводорода, имеющей единственное кольцо (моноциклический) или множественные кольца (бициклический), которые могут быть сплавлены вместе или связаны ковалентно. Арильные группы с 6-10 атомами углерода предпочтительны, при этом это количество атомов углерода может указываться как C6-10, например. Примеры арильных групп включают фенил и нафтален-1-ил, нафтален-2-ил, бифенил и т.п. Арильные группы являются незамещенными, если не указано иначе.
[0019] «Гало» или «галоген», как таковой или в качестве части заместителя относится к атому хлора, брома, йода или фтора.
[0020] «Галоалкил» в качестве замещенной алкильной группы относится к моногалоалкильной или полигалоалкильной группе, как правило замещенной 1 - 3 атомами галогена.
Примеры включают 1-хлороэтил, 3-бромопропил, трифторометил и т.п.
[0021] «Гетероциклил» относится к насыщенному или ненасыщенному неароматическому кольцу, содержащему, по меньшей мере, один гетероатом (как правило, 1-5 гетероатомов), выбранный из азота, кислорода или серы. Гетероциклическое кольцо может быть моноциклическим или бициклическим.
Предпочтительно, эти группы содержат 0-5 атомов азота, 0-2 атома серы и 0-2 атома кислорода. Более предпочтительно эти группы содержат 0-3 атома азота, 0-1 атом серы и 0-1 атом кислорода. Примеры гетероциклических групп включают пирролидин, пиперидин, имидазолидин, пиразолидин, бутиролактам, валеролактам, имидазолидинон, гидантоин, диоксолан, фталимид, пиперидин, 1,4-диоксан, морфолин, тиоморфолин, тиоморфолин-S-оксид, тиоморфолин-S, S-диоксид, пиперазин, пиран, пиридон, 3-пирролин, тиопиран, пирон, тетрагидрофуран, тетрагидротиофен, хинуклидин и подобное. Предпочтительными гетероциклическими группами являются моноциклические, хотя они могут быть сплавлены или связаны ковалентно с арильной или гетероарильной кольцевой системой.
[0022] В одном предпочтительном варианте гетероциклические группы могут быть представлены формулой (AA) ниже:
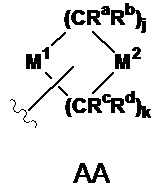
где формула (AA) присоединена посредством свободной валентности или на M1 или на M2; M1 представляет собой 0, NRe или S (0)I; M2 представляет собой CRfRg, 0, S (O), или NRe; I – это 0, 1 или 2; j равняется 1, 2 или 3, и k равняется 1, 2 или 3, при условии, что j + k равняется 3, 4, или 5; а Rа, Rb, Rc, Rd, Rе, Rf и Rg независимо выбраны из группы, состоящей из водорода, галогена, незамещенного или замещенного C1-8 алкила, незамещенного или замещенного C1-8 алкенила, незамещенного или замещенного C2-8 алкинила, -CORh, -C02Rh, -CONRhRI , -NRhCOR', -S02Rh, - SO2NRhRI,
-NS02RhRI-NRhRI, -NRhRI-, -ORh, -Q1CORh, -Q1CO2Rh, -Q1CONRhRI, Q1NRhCORI,
-Q1NSO2RhRI, -Q1NRhRI, -Q1ORh, где Q1 – это член, выбранный из группы, состоящей из C1-4 алкилена, C2-4 алкенила и C2-4 алкинила, и Rh и R' независимо выбраны из группы, состоящей из водорода и C1 -8 алкила, и где алифатические части каждого из Rа, Rb, Rc, Rd, Rе, Rf , Rg, Rh и Ri заместителей необязательно являются замещенными от одного до трех членов, выбранных из группы, состоящей из: галогена, - ОH, -ORn, -OC(O)NHRn, -OC(O)NRnRo, -SH, -SRn, -S(O)Rn, -S(O)2Rn, -SO2NH2, -S(O)2NHRn, -S(O)2NRnR°, NHS(O)2Rn, -NRnS(O)2R°, -C(O)NH2, -C(O)NHRn, -C(O)NRnRo, -C(O)Rn, -NHC(O)R°, -NRnC(O)R°, -NHC(O)NH2, -NRnC(O)NH2, -NRnC(O)NHR°, -NHC(O)NHRn, -NRnC(O)NR°Rp, -NHC(O)NRnRo, -CO2H, -CO2Rn, -NHCO2Rn, -NRnCO2R° , -CN, -NO2, -NH2,-NHRn, -NRnR°, -NRnS(O)NH2 и -NRnS(O)2NHR°, где Rn, R° и Rp являются независимо незамещенным C1-8 алкилом. Кроме того, любые два из Rа, Rb, Rc, Rd, Rе, Rf и Rg могут быть объединены, чтобы сформировать соединенную или спироциклическую кольцевую систему.
[0023] В одном предпочтительном варианте количество Rа + Rb + Rc + Rd групп, которые отличаются от водорода, равняется 0, 1 или 2. В более предпочтительном варианте Rа, Rb, Rc, Rd, Rе, Rf и Rg независимо выбраны из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила, , -CORh, -CO2Rh, -CONRhRh, -NRhCORh, -SO2Rh, –SO2NRhRi, -NSO2RhRi, -NRhR', и -ORh, где Rh и R' независимо выбраны из группы, состоящей из водорода и незамещенного C1-8 алкила, и где алифатические части каждого Rа, Rb, Rc, Rd, Rе, Rf и Rg заместителя необязательно замещены от одного до трех членами, выбранными из группы, состоящей из галогена, -ОH, -ORn, -OC(O)NHRn, -OC(O)°NRnR, -SH, -SRn, -S(O)R°, -S(O)2Rn, -SO2NH2, -S(O)2NHRn, -S(O)2NRnR°, -NHS(O)2Rn, -NRnS(O)2R°, -C(O)NH2, -C(O)NHRn , -C(O)°NRnR, -C(O)Rn, - NHC(O)Rn, -NRnC(O)R°, -NHC(O)NH2, -NRnC(O)NH2 , -NRnC(O)NHR°, - NHC(О)NHRn, -NRnC(О)NR°Rp , -NHC(О)°NRnR, -CО2H, -CО2Rn, -NHCО2Rn, -NRnCО2R°, -CN, -NO2, -NH2, -NHRn, -NRnR°, -NRnS(О)NH2 и -NRnS(О)2NHR°, где Rn, R ° и Rp независимо являются незамещенным C1-8 алкилом.
[0024] В более предпочтительном варианте Rа, Rb, Rc, Rd, Rе, Rf и Rg - независимо являются водородом или C1-4 алкилом. В другом предпочтительном варианте по меньшей мере три из Rа, Rb, Rc, Rd, Rе, Rf и Rg - это водород.
[0025] «Гетероарил» относится к ароматической группе, содержащей по меньшей мере один гетероатом, где группа гетероарила может быть моноциклической или бициклической. Примеры включают пиридил, пиридазинил, пиразинил, пиримидинил, тиазинил, хинолинил, хиноксалинил, хиназолинил, циннолинил, фталазинил, бензотриазинил, пуринил, бензимидазолил, бензопиразолил, бензотриазолил, бензисоксазолил, изобензофурил, изоиндолил, индолизинил, бензотриaзинил, тиенопиридинил, тиенопиримидинил, пиразолопиримидинил, имидазопиридины, бензотиазолил, бензофуранил, бензотиенил, индолил, азаиндолил, азаиндазолил, хинолил, изохинолил, изотиазолил, пиразолил, индазолил, птеридинил, имидазолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, пирролил, тиазолил, фурил или тиенил. Предпочтительные группы гетероарила – это те, которые имеют по меньшей мере один арилзамещенный кольцевой атом азота, такие как хинолинил, хиноксалинил, пуринил, бензимидазолил, бензопиразолил, бензотриазолил, бензотиазолил, индолил, хинолил, изохинолил и т.п. Предпочтительные системы гетероарила с 6 кольцами включают пиридил, пирадазинил, пиразинил, пиримидинил, триазинил и т.п. Предпочтительные системы гетероарила с 5 кольцами включают изотиазолил, пиразолил, имидазолил, тиенил, фурил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, пирролил, тиазолил и т.п.
[0026] Гетероциклил и гетероарил могут быть присоединены на любом доступном кольцевом углероде или гетероатоме. Каждый гетероциклил и гетероарил могут иметь одно или более колец. Когда присутствуют многократные кольца, они могут быть сплавлены вместе или связаны ковалентно. Каждый гетероциклил и гетероарил должны содержать по меньшей мере один гетероатом (как правило, 1 - 5 гетероатомов), выбранных из азота, кислорода или серы. Предпочтительно, эти группы содержат 0-5 атомов азота, 0-2 атома серы и 0-2 атома кислорода. Более предпочтительно эти группы содержат 0-3 атома азота, 0-1 атом серы и 0-1 атом кислорода. Группы гетероциклила и гетероарила являются незамещенными, если не указано иначе. Для замещенных групп замещение может быть на углероде или гетероатоме. Например, когда заместитель это oксo (=0 или-O''), полученная группа может иметь карбонил (-C(O)-) или N-оксид (-N+-0-).
[0027] Подходящие заместители для замещенного алкила, замещенного алкенила и замещенного алкинила включают галоген, -CN, -CO2R', -C(O)R', -C(O)NR'R'', oксo (=O или –O-), -OR', -OC(O)R', -OC(O)NR'R'' -NO2, -NR'C(O)R'', -NR'''C(O)NR'R'', -NR'R'', -NR'CO2R'', -NR'S(O)R'', -NR'S(O)2R''', -NR'''S(O)NR'R'', -NR'''S(O)2NR''R'', -SR', -S(O)R', -S(O)2R', -S(O)2NR'R'', -NR'-C(NHR'''=NR''', -SiR'R''R''', -N3, замещенный или незамещенный C6-10 арил, замещенный или незамещенный 5- 10-членный гетероарил, и замещенный или незамещенный 3- 10-членный гетероциклил. Количество возможных заместителей колеблется от ноля до (2 m' +1), где m' является общим количеством атомов углерода в таком радикале.
[0028] Подходящие заместители для замещенного арила, замещенного гетероарила и замещенного гетероциклила включают галоген, -CN, -CO2R', -C(O)R’, -C(O)NR'R'', oксo (=O или -O''), - OR', -OC(O)R', -OC(O)NR'R'', -NO2, -NR'C(O)R'', -NR'''C(O)NR'R'', -NR'R'', -NR'CO2R'', -NР(O)R''', -NР(O)2R'', -NR'''S(O)NR'R'', -NR'''S(O)2NR'R'', -SR', -S(O)R', -S(O)2R', -S(O)2N R'R'', -NR'-C(NHR'')=NR''', -SiR'R''R''', -N3, замещенный или незамещенный C1-8 алкил, замещенный или незамещенный C2-8 алкенил, замещенный или незамещенный C2-8 алкинил, замещенный или незамещенный C6-10 арил, замещенный или незамещенный 5-10-членный гетероарил, и замещенный или незамещенный 3-10-членный гетероциклил. Количество возможных заместителей колеблется от ноля до общего количества открытых валентностей на ароматической кольцевой системе.
[0029] Как выше использовалось, R', R'' и R''' каждый независимо относится к ряду групп, включающих водород, замещенынй или незамещенный C1-8 алкил, замещенный или незамещенный C2-8 алкенил, замещенный или незамеещнный C2-8 алкинил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арилалкил, замещенный или незамещенный арилоксиалкил. Когда R' и R'' присоединены к одному и тому же атому азота, они могут быть объединены с атомом азота, чтобы формировать 3-, 4-, 5-, 6- или 7-членное кольцо (например, -NR'R'' включает 1-пирролидинил и 4-морфолинил). Кроме того, R' и R'', R'' и R''' , или R' и R''' вместе с атомом (атомами), на который они присоединены, формируют замещенное или незамещенное 5-, 6-, или 7-членное кольцо.
[0030] Два из заместителей на соседних атомах арила или кольца гетероарила могут необязательно быть заменены заместителем Формулы -T-C(O)-(CH2)q-U-, где T и U независимо - это -NR'''', -O-, -CH2- или единственная связь, и q – это целое число от 0 до 2. Также два из заместителей на соседних атомах арила или кольца гетероарила необязательно могут быть заменены заместителем Формулы -A '-(CH2)i-B'-, где А' и B' являются независимо -CH2-, -О-, NR'''', -S-, -S(O)-, -S(О)2-, -S(О)2NR''''- или единственной связью, и r - это целое число от 1 до 3. Одна из единственных связей нового кольца, таким образом сформированного, необязательно может быть замещена двойной связью. Также два из заместителей на соседних атомах арила или кольца гетероарила необязательно могут быть заменены заместителем формулы -(CH2)S-X-(CH2)t, где s и t - независимо целые числа от 0 до 3, и X - это - O-, - NR'''', -S-, -S(O)-, -S (О)2- или -S(O)2NR'-. R'''' выбран из водорода или незамещенного C1-8 алкила.
[0031] «Гетероатом» означает атом, который включает кислород (O), азот (N), серу (S) и кремний (Si).
[0032] «Выше природной изотопной распространенности» относится к распространению изотопов химического элемента, как измерено в естественных условиях .
[0033] «Фармацевтически приемлемый» носитель, разбавитель или эксципиент – это носитель, разбавитель или эксципиент, совместимый с другими ингредиентами состава и не вредный его реципиенту.
[0034] «Фармацевтически приемлемая соль» относится к соли, которая приемлема для назначения пациенту, такому как млекопитающее (например, соли, имеющие приемлемую безопасность для млекопитающего в данном режиме дозировки). Такие соли могут быть получены из фармацевтически приемлемого неорганического вещества или органических оснований и из фармацевтически приемлемых неорганических кислот или органических кислот, в зависимости от конкретных заместителей, обнаруженных на соединениях, здесь описанных. Когда соединения настоящего раскрытия содержат относительно кислые функциональные группы, основные аддитивные соли могут быть получены путем связывания нейтральной формы таких соединений с достаточным количеством требуемого основания, или неразбавленного или в подходящем инертном растворителе. Соли, полученные из фармацевтически приемлемых неорганических оснований, включают алюминий, аммоний, кальций, медь, железо (3), железо (2), литий, магний, марганец, калий, натрий, цинк и т.п. Соли, полученные из фармацевтически приемлемых органических оснований, включают соли первичных, вторичных, третичных и четвертичных аминов, включая замещенные амины, циклические амины, естественные амины и т.п., такие как аргинин, бетаин, кофеин, холин, Ν, Ν'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламоноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, тетрагидрооксазин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и т.п. Когда соединения настоящего раскрытия содержат относительно основные функциональные группы, кислотно-аддитивные соли могут быть получены путем связывания нейтральной формы таких соединений с достаточным количеством требуемой кислоты, или неразбавленной или в подходящем инертном растворителе. Соли, полученные из фармацевтически приемлемых кислот, включают уксусную, аскорбиновую, бензолсульфоновую, бензойную, камфосульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глюкороновую, глутаминовую, гиппуровую, бромистоводородную, соляную, изэтиновую, молочную, лактобионовую, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, нафталенсульфоновую, никотиновую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную, п-толуолсульфоновую и т.п.
[0035] Также включены соли аминокислот, такие как аргинаты и т.п. и соли органических кислот, такие как глюкуроновая или галактуроновая кислоты и т.п. (см., например, Berge, S.M. et al., «Pharmaceutical Salts», J. Pharmaceutical Science, 1977, 66: 1-19). Некоторые определенные соединения настоящего раскрытия содержат и основные, и кислые функциональные группы, которые позволяют преобразовывать соединения как в основные, так и в кислотно-аддитивные соли.
[0036] Нейтральные формы соединений могут быть восстановлены путем взаимодействия соли с основанием или кислотой и выделением исходного соединения обычным образом. Исходная форма соединения отличается от различных солевых форм определенными физическими свойствами, такими как растворимость в полярных растворителях, но по другим свойствам соли эквивалентны исходной форме соединения в целях настоящего раскрытия.
[0037] В дополнение к солевым формам настоящее раскрытие обеспечивает соединения, которые находятся в форме пролекарства. Пролекарства соединений, описанных здесь, это соединения, которые быстро претерпевают химические изменения в физиологических условиях для обеспечения соединения настоящего раскрытия. Кроме того, пролекарства могут быть преобразованы в соединения настоящего раскрытия химическими или биохимическими методами в ex vivo среде. Например, пролекарства могут быть медленно преобразованы в соединения настоящего раскрытия, когда помещаются в резервуар трансдермального пластыря с подходящим ферментным или химическим реактивом.
[0038] «Терапевтически эффективное количество» относится к количеству, достаточному, чтобы произвести терапевтический эффект при назначении нуждающемуся в лечении пациенту.
[0039] Как здесь используется, «лечение» или «терапия» относится к лечению или терапии заболевания или медицинского состояния у пациента, такого как млекопитающее (особенно человек или домашнее животное), которое включает улучшение заболевания или медицинского состояния, т.е. устранение или вызов регрессии заболевания или медицинского состояния у пациента; подавление заболевания или медицинского состояния, например, замедление или прекращение развития заболевания или медицинского состояния в пациенте; или облегчение симптомов заболевания или медицинского состояния в пациенте; или предотвращение развития заболевания.
[0040] Определенные соединения настоящего раскрытия могут существовать в несольватных формах, а также сольватных формах, включая гидратированные формы. В целом как сольватные, так и несольватные формы охвачены рамками настоящего раскрытия.
[0041] Для специалиста в области будет очевидно, что определенные соединения настоящего раскрытия могут существовать в таутомерных формах, при этом все такие таутомерные формы соединений находятся в рамках этого раскрытия. Определенные соединения настоящего раскрытия обладают асимметричными атомами углерода (оптические центры), или двойными связями; рацематы, диастереомеры, геометрические изомеры и индивидуальные изомеры (например, отдельные энантиомеры) - все охватываются рамками настоящего раскрытия.
[0042] Соединения могут быть получены таким образом, что любое количество атомов водорода заменено изотопом дейтерием (2H). Соединения настоящего раскрытия могут также содержать неестественные соотношения изотопов атомов в одном или большем количестве атомов, которые составляют такие соединения. Неестественные соотношения изотопа могут быть определены в диапазоне от количеств, найденных в природе, до количества 100% рассматриваемого атома. Например, соединения могут включать радиоактивные изотопы, такие как например, тритий (3H), йод 125 (125 I) или углерод 14 (14C), или нерадиоактивные изотопы, такие как дейтерий (2H) или углерод 13 (13C). Такие изотопные вариации могут обеспечить дополнительные применения для тех, которые описаны в этой заявке. Все изотопные вариации соединений настоящего раскрытия, или радиоактивные или нет, охватываются рамками настоящего раскрытия. Например, изотопные вариации соединений раскрытия могут найти дополнительные применения, без ограничения включающие как диагностические, так и/или отображающие реактивы, или в качестве цитотоксических/радиотоксических терапевтических компонентов. Кроме того, изотопные вариации соединений раскрытия могут иметь измененные фармакокинетические и фармакодинамические характеристики, которые могут способствовать улучшенной безопасности, толерантности или эффективности во время лечения.
Способ лечения фиброза печени
[0043] Настоящее раскрытие обеспечивает способы лечения фиброза печени у пациента, включающие назначение пациенту, нуждающемуся в этом, эффективного количества соединения Формулы la:

или фармацевтически приемлемой его соли, где
[0044] Ar1 выбирают из группы, состоящей из замещенного или незамещенного C 6-10 арила и замещенныого или незамещенного 5- 10-членного гетероарила;
[0045] R1 выбирают из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила;
[0046] Y1 выбирают из группы, включающей -CR2a-, -N-, и - N+(О)-;
[0047] Y2 выбирают из группы, состоящей из -CR2b-,-N-, и - N+(О)-;
[0048] Y3 выбирают из группы, включающей -CR2c-, -N-, и - N+(О)-;
[0049] R2a, R2b и R2c - каждый независимо выбирают из группы, состоящей из водорода, галогена, -CN, -C(О)R3a, -CО2R3a,- C(О)NR3aR4a, -OR3a, -OC(О)R3a, -OC(О)NR3aR4a, -SR3a, -S(О)R3a, - S(О)2R3a, -S(О)2NR3aR4a, -NО2, -NR3aR4a, -NR3aC(О)R4a, -NR3aC(О)R4a, - NR3aS(O)2R4a, - NR3aC(O)NR4aR5a, замещенного или незамещенного C1- 8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила;
[0050] R3a, R4a и R5a - каждый независимо выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила, и замещенного или незамещенного 3- 10-членного гетероциклила;
[0051] R3a и R4a, R4a и R5a или R3a и R5a могут, вместе с атомами, на которые они присоединены, формировать замещенное или незамещенное 5-, 6-, или 7-членное кольцо;
[0052] L выбирают из группы, включающей связь, -0-, -S-, - S(O) -, S(О)2-, -CR6R7-, -NR8-, -C(O) - и -NR8C (О)-;
[0053] R6 и R7 - каждый независимо выбирают из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила, -CN, -OR9, -NR10R11, -S(O)R9 и -S(O)2R9;
[0054] R6 и R7 могут вместе с атомом углерода, на который они присоединены, формировать замещенный или незамещенный C3-8 циклоалкил, замещенное или незамещенное 3- 10-членное гетероциклическое кольцо;
[0055] R9 выбирают из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила и замещенного или незамещенного 3-10-членного гетероциклила;
[0056] R10 и R11 - каждый независимо выбраны из группы, включающей замещенный или незамещенный C1-8 алкил, замещенный или незамещенный 3-10-членный гетероциклил, замещенный или незамещенный C 6-10 арил, замещенный или незамещенный 5- 10-членный гетероарил, замещенный или незамещенный C2-8 алкенил, замещенынй или незамещенный C2-8 алкинил;
[0057] R10 и R11 из -NR10R11 могут вместе с азотом формировать замещенный или незамещенный C3-8 циклоалкил, замещенный или незамещенный 3- 10-членный гетероциклил;
[0058] R8 выбирают из группы, состоящей из водорода, C(О)R12, S(О)2R12, CО2R12, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного 3-10-членного гетероциклила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила;
[0059] R12 выбирают из группы, состоящей из замещенного или незамещённого C1-8 алкила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила;
[0060] Z1 выбирают из группы, состоящей из замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила, замещенного или незамещенного 3- 10-членного гетероциклила, и - NR13R14;
[0061] R13 и R14 - каждый независимо выбирают из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила, замещенного или незамещенного (C1-4 алкил) - (C6-10 арил), и замещенного или незамещенного (C1-4 алкил) - (5- 10-членный гетероарил);
[0062] R13 и R14 могут вместе с азотом формировать замещенный или незамещенный 4-, 5-, 6-, или 7-членный гетероциклил;
[0063] Y4 выбирают из группы, включающей -N- и -N + (О)- -.
[0064] В некоторых вариантах воплощения соединения Формулы CC исключены из Формулы (la):
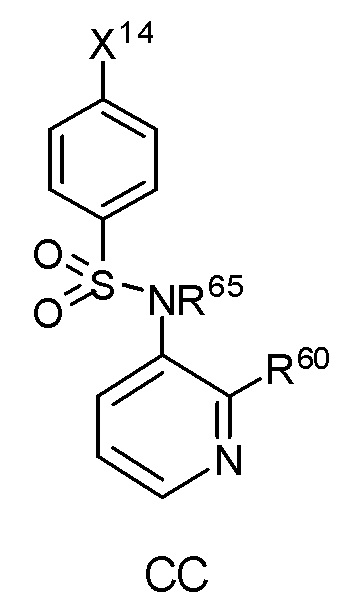
[0065] где X14 выбирают из группы, включающей -CI, -NО2, - OCH3, -CH3, -NHC(О)CH3 и -CH2CH2-(фенил);
[0066] R65 выбирают из группы, состоящей из водорода, замещенного или незамещенного C1-4 алкила, замещенного или незамещенного - SО2 (фенил); и
[0067] R60 выбирают из группы, состоящей из -NR61CH2CH2OR62, - NR61CH2CH2NR63R64, -NR61CH2CH2SR62,
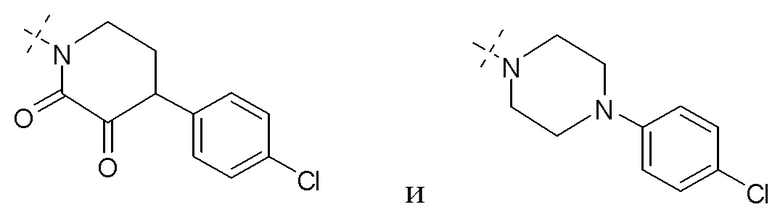
[0068] где R61 выбирают из группы, состоящей из водорода и замещенного или незамещенного фенила;
[0069] R62 выбирают из группы, состоящей из замещенного или незамещенного фенила, замещенного или незамещенного C1-4 алкила, и
[0070] R63 и R64 - каждый независимо выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного фенила, замещенного или незамещенного -SО2(фенил), -C(О)CH3, - C(О)C(О), О, и -C(О)2C(CH3)3.
[0071] В некоторых вариантах воплощения Z1 – это замещенный или незамещенный 5-10-членный гетероарил.
[0072] В некоторых вариантах воплощения L - это -C(O)-.
[0073] В некоторых вариантах воплощения Y1 это -CR2a-; Y2- это CR2b-; Y3 это -CR2c-; и R2a, R2b и R2c - каждый независимо выбран из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила.
[0074] В некоторых вариантах воплощения R1а выбран из группы, состоящей из водорода или замещенного или незамещенного C1-8 алкила.
[0075] В некоторых вариантах воплощения Ar1 - это замещенный или незамещенный C6-10 арил.
[0076] В некоторых вариантах воплощения Y4 - это -N-.
[0077] В некоторых вариантах воплощения Z1 - это замещенный или незамещенный 5-10-членный гетероарил; L – это -C(O)-; Y1 – это -CR2a-; Y2- это -CR2b-; Y3- это -CR2c-; R2a, R2b и R2c - каждый независимо выбран из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила; R1а выбран из группы, состоящей из водорода или замещенного или незамещенного C1-8 алкила; Ar1 - это замещенный или незамещенный C6-10 арил; и Y4- это -N-.
[0078] Настоящее раскрытие представляет способы лечения фиброза печени у пациента, включающие назначение пациенту, нуждающемуся в этом, эффективного количества соединения Формулы I:

Формула I
или фармацевтически приемлемой его соли, где
[0079] R1 – галоген или C1-6 алкил;
[0080] R2 – водород, галоген, C1-6 алкил, C1-6 алкокси, C1-6 галоалкил, C1-6 галоалкокси, или -CN;
[0081] R3 - водород, галоген или C1-6 алкил;
[0082] R4 – водород, галоген или C1-6 алкил;
[0083] каждый R5 независимо – C1-6 алкил, - О, или -NH2;
[0084] n - это 0, 1, 2, или 3; и
[0085] каждый из A1, A2 и A3- это -CH- или -N-, где по меньшей мере один из A1, A2 или A3 это -N-.
[0086] В некоторых вариантах воплощения R1 – галоген или метил; R2 – галоген или C1-6 галоалкил; R3 – галоген или C1-6 алкил; R4 – водород; n - это 0; A2 – это -CH-; и A3- это -N-.
[0087] В некоторых вариантах воплощения соединение выбирают из группы, включающей:
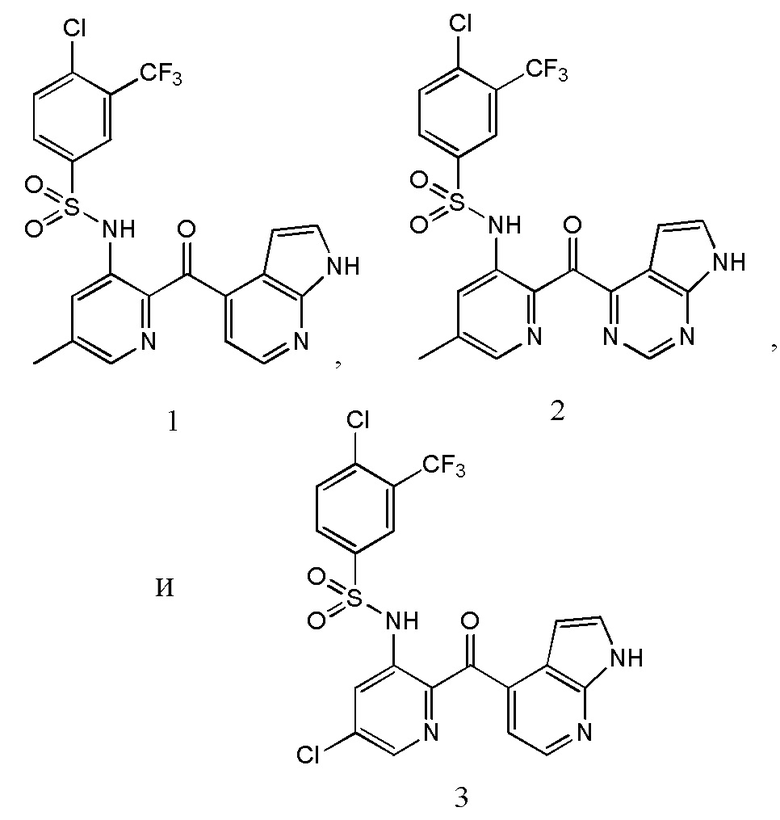
или фармацевтически приемлемую их соль.
[0088] В некоторых вариантах воплощения соединение это -
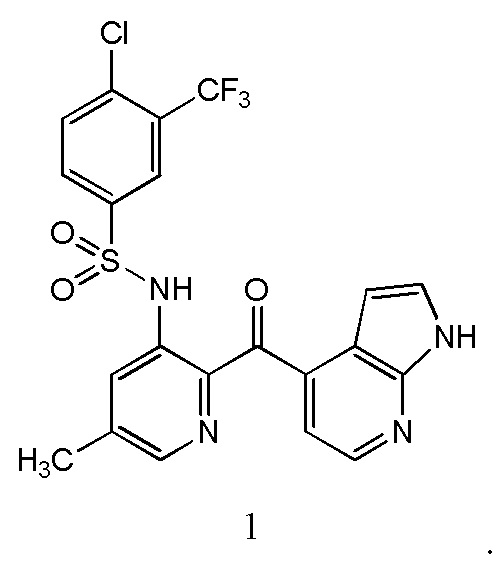
или фармацевтически приемлемая его соль.
[0089] В некоторых вариантах воплощения фиброз печени связан с неалкогольным стеатогепатитом (NASH).
[0090] В некоторых вариантах воплощения NASH связан с сахарным диабетом 2 типа (T2DM).
[0091] В некоторых вариантах воплощения NASH связан с метаболическим синдромом (MS).
[0092] В некоторых вариантах воплощения фиброз печени связан с неалкогольной жировой болезнью печени (NAFLD).
[0093] В некоторых вариантах воплощения NAFLD связан с сахарным диабетом 2 типа (T2DM).
[0094] В некоторых вариантах воплощения NAFLD связан с метаболическим синдромом (MS).
[0095] В некоторых вариантах воплощения фиброз печени связан с развивающимся циррозом. В некоторых вариантах воплощения цирроз связан с алкогольным повреждением.
[0096] В некоторых вариантах воплощения фиброз печени включает нецирротический фиброз печени.
[0097] В некоторых вариантах воплощения фиброз печени связан с инфекцией гепатита, включая, без ограничения, гепатит B, гепатит С и гепатит D.
[0098] В некоторых вариантах воплощения фиброз печени связан с одним или более развивающимся циррозом, первичным желчным холангитом, первичным склерозирующим холангитом, желчной атрезией, холестатическим заболеванием печени, хроническим заболеванием печени, алкогольной болезнью печени, холистеринемией и гиперлипидемией.
[0099] В некоторых вариантах воплощения фиброз печени связан с первичным желчным циррозом (PBC), желчной атрезией или первичным склерозирующим холангитом.
[00100] В некоторых вариантах воплощения фиброз печени связан с первичным желчным холангитом, первичным склерозирующим холангитом или желчной атрезией.
[00101] В некоторых вариантах воплощения пациент, подвергающийся лечению, заражен вирусом. В некоторых вариантах воплощения вирус – это вирус гепатита, без ограничения, включая HCV (вирус гепатита С), HBV и HDV. В некоторых вариантах воплощения у субъекта имеется диабет. В некоторых вариантах воплощения у субъекта имеется диабет 2 типа. В некоторых вариантах воплощения у субъекта имеется диабет 1 типа. В некоторых вариантах воплощения у субъекта имеется метаболический синдром (MS). В некоторых вариантах воплощения субъект имеет одно или более этих заболеваний или нарушений. В некоторых вариантах воплощения субъект подвергается риску получить одно или более этих заболеваний. В некоторых вариантах воплощения у субъекта имеется устойчивость к инсулину. В некоторых вариантах воплощения субъект имеет повышенную концентрацию глюкозы в крови, высокое кровяное давление, повышенные уровни холестерина, увеличенные уровни триглицерида или ожирение. В некоторых вариантах воплощения у субъекта имеется синдром поликистозного яичника.
[00102] В некоторых вариантах воплощения пациент, подвергающийся лечению, имеет риск развития фиброза печени или цирроза.
[00103] В некоторых вариантах воплощения фиброз включает нецирротический печеночный фиброз.
[00104] В некоторых вариантах воплощения фиброз печени прогрессирует.
[00105] В некоторых вариантах воплощения соединение или фармацевтически приемлемая его соль назначается перорально.
[00106] В некоторых вариантах воплощения соединение или фармацевтически приемлемая его соль назначается один раз в день или дважды в день.
[00107] В некоторых вариантах воплощения соединение или фармацевтически приемлемая его соль назначается один раз в день.
[00108] В некоторых вариантах воплощения способ дополнительно включает назначение пациенту одного или более дополнительного терапевтического соединения.
[00109] В некоторых вариантах воплощения одно или более дополнительное терапевтическое соединение выбирают из одного или более ингибитора транспортера-2 глюкозы натрия, агониста подобного глюкагону пептида 1, ингибитора галектина-3, стимулятора трансаминазы, агониста IL-10, сенсибилизатора инсулина, агониста PPAR гамма, агониста бета рецептора тироидного гормона, ингибитора каспазы, ингибитора дипептидил пептидазы IV, агониста PPAR альфа; агониста PPAR дельта, агониста PPAR, агониста фарнезоидного X рецептора, ингибитора гомолога лизилоксидазы 2, ингибитора протеинкиназы MEKK-5, модулятора метил CpG 2 связывающего белка, ингибитора трансглутаминазы, стимулятора миелин основного белка, стимулятора канала хлорида, антагониста хемокина CCR3, антагониста хемокина CCR5, антагониста ангиотензин В-1 рецептора, ингибитора транскрипционного фактора SREBP 1, модулятора бета рецептора PDGF, лиганда FGF-21, антагониста IL-17, ингибитора rho связаной протеинкиназы 2, ингибитора котранспортера желчнокислого натрия, ингибитора стеароил CoA десатуразы-1, агониста рецептора FGF1, стимулятора клото бета, ингибитора лиганда фактора роста соединительной ткани, липопротеинового ингибитора липазы; ингибитора транскрипционного фактора SREBP, лиганда FGF-19, антагониста CD3, ингибитора кавеолина 1, агониста амилинового рецептора; агониста кальцитонина, стимулятора NAD-зависимой деацетилазы сиртуина, ингибитора PDE 5, ингибитора NADPH 1 оксидазы, ингибитора NADPH 4 оксидазы, ингибитора NADPH оксидазы, агониста фактора роста гепатоцита, антагониста интегрин альфа -V/бета-6, антагониста TGF бета, стимулятора NAD-зависимого деацетилазы сиртуина, агониста рецептора никотиновой кислоты 1, стимулятора гидроксилазы фенилаланина, ингибитора мембранной медной аминоксидазы, ингибитора рибосомного белка киназы S6 1, ингибитора высоко мобильной группы белка B1, антагониста TLR 4, ингибитора катепсина B, лиганда фактора роста гепатоцита, лиганда гамма интерферона, ингибитора АСЕ, ингибитора HMG CoA редуктазы или фармацевтически приемлемой их соли.
[00110] В некоторых вариантах воплощения один или более дополнительного терапевтического соединения выбирают из одного или более агониста фарнезоидного X рецептора (FXR), двойного агониста TGR5/FXR, агониста PPAR альфа, агониста PPAR гамма, агониста PPAR дельта или фармацевтически приемлемой их соли.
[00111] В некоторых вариантах воплощения одно или более дополнительное терапевтическое соединение выбирают из одного или более дапаглифлозинпропандиола, дапаглифлозина, лираглютида, GR-MD-02, семаглютида, сенекривирока, F-351, пег-илодецикина, ипраглифлозина, урсодезоксихолевой кислоты, целесвелама, пиоглитазона, VK-2809, эмрикасана, линаглиптина, элафибранора, DS-102, Px 102, Px 103, GS-4997, симтузумаба, DUR-928, меркаптамина, олезокцима, кобипростона, бертидимумаба, MDV-4463, ирбесартана, GS-9674, BOT-191, MGL-3196, BMS-986171, PEG-FGF21, LJN-452, CF-102, KD-025, воликсибата, калия этанолата гидрата воликсибата, арамхола, типелукаста, NGM-313, FG-3019, CAT-2003, NGM-282, TRX-318, IONIS-DGAT2Rx, IMM-124-E, RG-125, норурсодеоксихолиевой кислоты, KBP 042, лейцина, метформина, силденафила, A-4250, GKT-831, BB-3, сароглатазара, BG-0001 1, алипоген типарвовека, MB-12066, безводного бетаина, ARI-3037MO, ГепаСтема, PXS-4728A, CIGB-500, олтипраза, омега 3 карбоновых кислот, дапаглифлозина, ремоглифлозин этабоната, ремоглифлозина, LC-280126, JKB-121, DWP-10292, VBY-376, VBY-825, изосапент этилового эфира, капсулы Фучжэн Хиайю, интерферона, ацетилсалициловой кислоты, гидрохлоротиазида, эналаприла, аторвастатина, NC-101, TCM-606F, обетихолиновой кислоты, INT 767, GNF-5120, криптохинона-D, фексарамина, каприлового триглицерида, эвоглиптина, GM-CT-01, витамина Е высокой дозировки (> 400 iU/d) или фармацевтически приемлемой их соли.
[00112] В некоторых вариантах воплощения одно или более дополнительное терапевтическое соединение может назначаться одновременно с соединением Формулы (I), (la), соединением 1, 2 или 3 или фармацевтически приемлемой их солью, или назначаться отдельно, включая назначение в разное время и с различными частотами. Одно или более дополнительное терапевтическое соединение может назначаться любым известным путем, таким как: перорально, внутривенно, внутримышечно, через нос, подкожно, внутривлагалищным образом, внутриректально, и т.п.; и соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль также могут быть применены любым обычным путем. В некоторых вариантах воплощения одно или более дополнительное терапевтическое соединение и соединение Формулы (I), (la), соединение 1, 2 или 3 или фармацевтически приемлемая их соль назначаются перорально.
[00113] Когда два или более лекарств используются в комбинации, дозировка каждого медикамента обычно идентична дозировке медикамента при независимом использовании, но когда медикамент вмаимодействует с метаболизмом других лекарств, дозировка каждого медикамента соответствующим образом регулируется. Каждый медикамент может назначаться одновременно или отдельно во временном интервале, например, меньше чем 12 часов, 24 часов, 36 часов. Форма дозировки как здесь описано, такая как капсула, может назначаться в адекватных интервалах. Например, один раз в день, дважды в день, три раза в день и т.п. В частности, форма дозировки назначается, например, несколько раз в день. И более конкретно форма дозировки назначается один раз в день.
[00114] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3 или фармацевтически приемлемая их соль улучшают чувствительность к инсулину.
[00115] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль улучшают переносимость глюкозы.
[00116] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают накопление триглицерида в печени.
[00117] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают концентрацию аланин аминотрансферазы (АЛТ).
[00118] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают концентрацию аспартатаминотрансферазы (AST).
[00119] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают содержание коллагена печени.
[00120] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают содержание макрофагов в печени.
[00121] В некоторых вариантах воплощения соединение Формулы смеси (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают содержание макрофагов жировой ткани.
[00122] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают сальниковое содержание жировой ткани.
[00123] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают уровни холестерина печени.
[00124] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль понижают уровни билирубина.
[00125] В некоторых вариантах воплощения соединение Формулы (I), (la), соединение 1, 2 или 3, или фармацевтически приемлемая их соль уменьшают фиброз печени.
Соединения, которые Модулируют CCR2 Активность
[00126] Настоящее раскрытие представляет соединения, которые модулируют CCR2 активность. Рецепторы хемокина являются интегральными мембранными белками, которые взаимодействуют с внеклеточным лигандом, таким как хемокин, и содействуют клеточной реакции на лиганд, например, хемотаксису, увеличивающему внутриклеточную концентрацию ионов кальция и т.д.
Поэтому модуляция функции рецептора хемокина, например, интерференция со взаимодействием лиганда рецептора хемокина, будет модулировать опосредованный ответ рецептора хемокина и лечить или предотвращать обусловленное рецептором хемокина состояние или заболевание. Модуляция функции рецептора хемокина включает как стимуляцию, так и торможение функции. Тип достигнутой модуляции будет зависеть от характеристик соединения, т.е. антагонист или полный, частичный или обратный агонист.
[00127] Без связи с какой-либо конкретной теорией считается, что соединения, представленные здесь, вмешиваются во взаимодействие между рецептором хемокина и одним или более сродственными лигандами. В частности, считается, что соединения вмешиваются во взаимодействие между CCR2 и CCR2 лигандом, таким как MCP-1. Соединения, рассмотренные этим раскрытием, включают, но без ограничения, типичные соединения, представленные здесь, и их соли.
[00128] Соединения этого раскрытия, как полагают, вмешиваются в несоответствующий трекинг Т-клеток, специфично модулируя или ингибируя функцию рецептора хемокина. Соединения, рассмотренные в этом описании, включают, но без ограничения, типичные представленные здесь соединения и фармацевтически приемлемые их соли и соединения, представленные в US 8,519,135, US 2006/0173019, US 7,622,583, US 7,884,110 и US 8,093,247, которые включены здесь посредством ссылки.
[00129] В некоторых вариантах воплощения соединения этого раскрытия не ингибируют CCR5.
[00130] В некоторых вариантах воплощения соединения этого раскрытия представляют собой селективные CCR2 ингибиторы по сравнению с CCR5.
[00131] В некоторых вариантах воплощения соединения этого раскрытия имеют более чем 10-кратную селективность для CCR2 ингибирования перед CCR5 ингибированием.
[00132] В некоторых вариантах воплощения соединения этого раскрытия имеют более чем 100-кратную селективность для CCR2 ингибирования перед CCR5 ингибированием.
[00133] В некоторых вариантах воплощения соединения этого раскрытия - избирательно действующие CCR2 ингибиторы.
Композиции
[00134] Фармацевтически приемлемые композиции могут быть назначены людям и другим животным перорально, ректально, парентерально, внутриполостным образом, внутривлагалищно, интраперитонеально, местно (в виде порошков, мазей или капель), букально, в качестве орального или назального спрея, и т.п.
[00135] Жидкие формы дозировки для перорального приема включают, но без ограничения, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активному соединению (соединениям) жидкая форма дозировки может содержать инертные разбавители, обычно используемые в области, такие как, например, вода или другие растворители, солюбилизирующие компоненты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, масло семян хлопчатника, арахисовое, кукурузное, ростков пшеницы, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирной кислоты сорбитана и их смеси. Помимо инертных разбавителей оральные композиции могут также включать адъюванты, такие как увлажняющие компоненты, эмульгирующие вещества и суспендирующие компоненты, подслащивающие, вкусовые и ароматизирующие агенты.
[00136] Впрыскиваемые препараты, например, стерильные впрыскиваемые водные или маслянистые суспензии могут быть составлены в соответствии со знаниями из уровня техники с использованием подходящих диспергирующих веществ или увлажняющих агентов и суспендирующих агентов. Стерильный впрыскиваемый препарат может также быть стерильным впрыскиваемым раствором, суспензией или эмульсией в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в качестве раствора - в 1,3-бутандиоле. Среди приемлемых транспортных веществ и растворителей, которые могут использоваться, - вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные, жирные масла традиционно используются в качестве растворителя или суспендирующей среды. С этой целью любое мягкое жирное масло может использоваться, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, могут быть включены во впрыскиваемый продукт. Впрыскиваемые составы могут стерилизоваться, например, фильтрацией через удерживающий бактерии фильтр, или введением стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной впрыскиваемой среде перед применением.
[00137] Чтобы продлить действие соединения этого раскрытия часто желательно замедлить абсорбцию соединения из подкожной или внутримышечной инъекции. Это может быть достигнуто при помощи жидкой суспензии кристаллического или аморфного вещества с низкой водорастворимостью. Уровень абсорбции соединения в этом случае будет зависеть от его уровня растворения, что, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. Альтернативно отсроченная абсорбция парентерально назначенной формы соединения достигается путем растворения или суспендирования соединения в масляном наполнителе. Впрыскиваемые депо-препараты изготавливают путем формирования микроинкапсулированных матриксов соединения в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от отношения соединения к полимеру и природе конкретного используемого полимера, можно управлять скоростью высвобождения состава. Примеры других биоразлагаемых полимеров включают поли(орто-эфиры) и поли(ангидриды). Впрыскиваемые депо-препараты также получают путем включения соединения в липосомы или микроэмульсии, которые совместимы с тканями тела.
[00138] Композиции для ректального или вагинального назначения – это предпочтительно свечи, которые могут быть получены путем смешивания соединения этого раскрытия с подходящими нераздражающими эксципиентами или носителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела и поэтому тают в прямой кишке или влагалище и высвобождают активное соединение.
[00139] Твердые формы дозировки для перорального приема включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых формах дозировки активное соединение смешано, по меньшей мере, с одним инертным, фармацевтически приемлемым эксципиентом или носителем, таким как цитрат натрия или дикальцийфосфат и/или (a) наполнителями или разбавителями, такими как крахмал, лактоза, сахароза, глюкоза, маннитол и кремневая кислота, (b) связующими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и акация, (c) влагоудерживающими веществами, такими как глицерин, (d) дизинтегрирующими агентами, такими как агар, карбонат кальция, картофельный крахмал или крахмал тапиоки, альгиновая кислота, определенные силикаты и натрия карбонат, (e) замедляющими растворение агентами, такими как парафин, (f) ускорителями абсорбции, такими как соединения четвертичного аммония, (g) увлажняющими компонентами, такими как, например, цетиловый спирт и глицеринмоностеарат, (h) абсорбентами, такими как каолин и бентонитовая глина, и (i) смазывающими веществами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль, форма дозировки может также включать буферные вещества.
[00140] Твердые композиции подобного типа могут также использоваться в качестве наполнителей в мягких и твердо- заполненных желатиновых капсулах, использующих такие эксципиенты, как лактоза или молочный сахар, а также полиэтиленгликоли высокого молекулярного веса и т.п. Твердые формы дозировок таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеральные покрытия и другие покрытия, широко известные в области фармацевтики. Они могут необязательно содержать замутняющие компоненты и могут также быть композициями, которые высвобождают активный ингредиент (ингредиенты) только, или избирательно, в определенной части кишечного тракта, необязательно, отсроченным образом. Примеры наполнителей, которые могут быть использованы, включают полимерные вещества и воски. Твердые композиции подобного типа могут также использоваться в качестве наполнителей в мягких и твердо- заполненных желатиновых капсулах, использующих такие эксципиенты как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п.
[00141] Соединения настоящего раскрытия или фармацевтически приемлемая их соль могут быть получены с использованием нанотехнологии. Наночастицы привлекательны для медицинских целей благодаря своим характерным особенностям, таким как отношение их поверхности к массе, которое больше, чем у других частиц, их квантовым свойствам и их способности адсорбировать и нести другие соединения. Наночастицы могут иметь размеры ниже 0,1 мкм или 100 нм. Также фармацевтическая композиция может включать относительно большие (размер> 100 нм) наночастицы, по мере необходимости, для загрузки достаточного количества лекарственного средства в частицы. Кроме того, для доставки лекарственных средств не только сконструированные частицы могут быть использованы в качестве носителя, но также и само лекарственное средство может быть составлено в наноразмерной форме, и затем действовать как свой собственный носитель. Композиция сконструированных наночастиц может изменяться. Исходные вещества могут иметь биологическое происхождение как фосфолипиды, липиды, молочная кислота, декстран, хитозан, или иметь больше химических характеристик как различные полимеры, углерод, оксид кремния и металлы. Особенно в области сконструированных наночастиц полимерного происхождения имеется обширная область возможностей для химической композиции. Например, см. Martins et al., Nanoparticle Drug Delivery Systems: Recent Patents and Applications in Nanomedicine, Recent Patents on Nanomedicine, 2013, 3(2), pp. 1 – 14.
[00142] Соединения настоящего раскрытия или фармацевтически приемлемая их соль могут также быть в микроинкапсулированной форме с одним или более эксципиентами, как отмечалось выше. Твердые формы дозировки таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с покрытиями и оболочками, такими как энтеральные покрытия, покрытия с контролируемым высвобождением и другие покрытия, известные в области фармацевтики. В таких твердых формах дозировки активное соединение может быть смешано, по меньшей мере, с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие формы дозировки могут также включать, в качестве нормальной практики, дополнительные вещества кроме инертных разбавителей, например, таблетирующие лубриканты и другие таблетирующие агенты, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль формы дозировки могут также включать буферные вещества. Они могут необязательно содержать замутняющие агенты и могут также быть композицией, так что высвобождают активный ингредиент (ингредиенты) только или избирательно в определенной части кишечного тракта, необязательно, отсроченным образом. Примеры неактивных носителей, которые могут быть использованы, включают полимерные вещества и воски.
[00143] Формы дозировки для местного или трансдермального назначения соединения этого раскрытия включают мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, летучие препараты или пластыри. Активный компонент смешивается в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами, или буферами, как может потребоваться. Офтальмологический состав, ушные капли и глазные капли также рассматриваются в объеме этого раскрытия.
Кроме того, это раскрытие рассматривает применение трансдермальных пластырей, которые имеют дополнительное преимущество обеспечения контролируемой доставки соединения к телу. Такие формы дозировки получают путем растворения или диспергирования соединения в надлежащей среде. Ускорители абсорбции также могут использоваться для увеличения выделения соединения через кожу. Скорость может управляться или за счет обеспечения контролирующей скорость мембраны, или за счет растворения соединения в полимерной матрице или геле.
[00144] Соединения и композиции настоящего раскрытия могут быть применены оральным, парентеральным (например, внутримышечной, интраперитонеальной, внутривенной, ICV, внутриполостной инъекцией или инфузией, подкожной инъекцией или имплантатом), ингаляцией, назальным, влагалищным, ректальным, подъязычным или местным путями введения и могут быть составлены отдельно или вместе, в подходящих составах дозировки, содержащих обычные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители, адекватные для каждого пути назначения. Настоящее раскрытие также рассматривает назначение соединений и композиций настоящего раскрытия в форме депо-препарата.
[00145] В лечении или профилактике состояний, которые требуют модуляции рецептора хемокина, адекватный уровень дозировки соединения Формулы (I), (la), соединения 1, 2 или 3 или фармацевтически приемлемой их соли, в общем случае будет приблизительно составлять от 0,001 до 100 мг на кг массы тела пациента в день, который может быть применен в единственной или многократных дозах. Предпочтительно, уровень дозировки будет от приблизительно 0,01 до приблизительно 25 мг/кг в день; более предпочтительно от приблизительно 0,05 до приблизительно 10 мг/кг в день. Подходящий уровень дозировки может быть приблизительно от 0,01 до 25 мг/кг в день, приблизительно от 0,05 до 10 мг/кг в день или приблизительно от 0,1 до 5 мг/кг в день. В этом диапазоне дозировка может составлять 0,005 - 0,05; 0,05 - 0,5; 0,5 - 5,0; или 5,0 - 50 мг/кг в день. Для перорального приема композиции предпочтительно обеспечены в форме таблеток, содержащих от 1,0 до 1 000 миллиграммов активного ингредиента, в частности, 1.0, 5.0, 10.0, 15.0, 20.0, 25.0, 50.0, 75.0, 80.0, 90.0, 100.0, 110.0, 120.0, 130.0, 140.0, 150.0, 160.0, 170.0, 180.0, 190.0, 200.0, 250.0, 300.0, 400.0, 500.0, 600.0, 750.0, 800.0, 900.0, и 1 000,0 миллиграммов активного ингредиента для симптоматического регулирования дозировки пациенту, которого лечат. Соединения могут назначаться в режиме 1 - 4 раза в день, предпочтительно несколько раз в день.
[00146] Понятно, однако, что определенный уровень дозы и частота дозировки для какого-либо конкретного пациента могут быть изменены и будут зависеть от ряда факторов, включая активность определенного используемого соединения, метаболическую стабильность и продолжительность действия этого соединения, возраста, массы тела, наследственных характеристик, общего состояния здоровья, пола, диеты, способа и время назначения, скорости экскреции, сочетания лекарств, серьезности конкретного состояния и хозяина, переносящего терапию.
[00147] Соединения и композиции настоящего раскрытия могут быть объединены с другими соединениями и композициями, имеющими соответствующее применение, чтобы предотвратить и лечить фиброз печени, NASH, NAFLD, развивающийся цирроз и/или нецирротический печеночный фиброз. Выбор адекватных компонентов для использования в комбинированной терапии может быть осуществлен специалистом в области. Комбинация терапевтических компонентов может действовать синергично для осуществления лечения или профилактики различных нарушений. Используя этот подход, можно достигнуть терапевтическую эффективность с более низкими дозировками каждого компонента, таким образом уменьшая потенциал для неблагоприятных побочных эффектов.
[00148] Весовое отношение соединения настоящего раскрытия к другому активному ингредиенту может быть изменено и будет зависеть от эффективной дозы каждого ингредиента. Обычно будет использоваться эффективная доза каждого. Таким образом, например, когда соединение настоящего раскрытия объединено со вторым терапевтическим соединением, весовое отношение соединения настоящего раскрытия ко второму терапевтическому соединению будет в общем случае лежать в диапазоне от приблизительно 1000:1 до приблизительно 1:1000, предпочтительно от приблизительно 200: 1 до приблизительно 1:200.
[00149] В еще одном аспекте настоящее раскрытие обеспечивает способы лечения или предотвращения фиброза печени, NASH, NAFLD, развивающегося цирроза и/или нецирротического печеночного фиброза путем назначения субъекту, имеющему такое состояние или заболевание, терапевтически эффективного количества любого соединения настоящего раскрытия. Соединения для использования в настоящих способах включают соединения в соответствии с Формулой (I), (la), соединения 1, 2 или 3 или фармацевтически приемлемую их соль, которые представлены как варианты, т.е. которые являются соединениями, представленными в US 8,519,135, US 2006/0173019, US 7,622,583, US 7,884,110 и US 8,093,247, которые включены здесь посредством ссылки. Соединения могут быть полезными для лечения субъекта, который нуждается в таком лечении. «Субъект» определен здесь, как включающий животных, таких как млекопитающие, включая, но без ограничения, приматов (например, людей), коров, овец, козлов, лошадей, собак, кошек, кроликов, крыс, мышей и т.п. В предпочтительных вариантах воплощения субъект – это человек.
[00150] Как здесь используется, фраза «терапевтически эффективное количество» означает количество соединения, которое вызовет биологический или медицинский ответ клетки, ткани, системы или животного, такого как человек, который исследуется исследователем, ветеринаром, врачом или другим лицом, осуществляющим лечение.
[00151] В одном варианте воплощения настоящее раскрытие обеспечивает способы лечения или предотвращение фиброза печени, NASH, NAFLD, развивающегося цирроза и/или нецирротического печеночного фиброза, включающие назначение субъекту эффективного количества соединения или композиции этого раскрытия, где назначение является оральным, парентеральным, ректальным, трансдермальным, подъязычным, назальным или местным.
CCR2 Модуляторы
[00152] Следующие примеры предлагаются, чтобы проиллюстрировать, но без ограничения, настоящее раскрытие.
[00153] Определенные молекулы, раскрытые в этом патенте, могут существовать в различных энантиомерических и диастериомерических формах, и все такие варианты этих соединений находятся в рамках настоящего раскрытия.
[00154] Определенные фармакологические наблюдаемые ракции могут изменяться в соответствии и в зависимости от конкретного активного выбранного соединения или того, присутствуют ли фармацевтические носители, а также от типа состава и способа используемого введения, и такие ожидаемые разбросы значений или отличия в результатах рассмотрены в соответствии с практикой настоящего раскрытия.
[00155] Несмотря на то, что определенные варианты воплощения настоящего раскрытия здесь проиллюстрированы и описаны подробно, раскрытие ими не ограничено. Вышеупомянутые подробные описания предоставлены как типичные для настоящего раскрытия и не должны быть истолкованы как составляющие любое ограничение раскрытия. Модификации будут очевидны для специалистов области, и все модификации, которые не отступают от замысла раскрытия, предназначены для включения в него с объемом приложенных пунктов формулы.
ПРИМЕРЫ
[00156] Соединение 1:
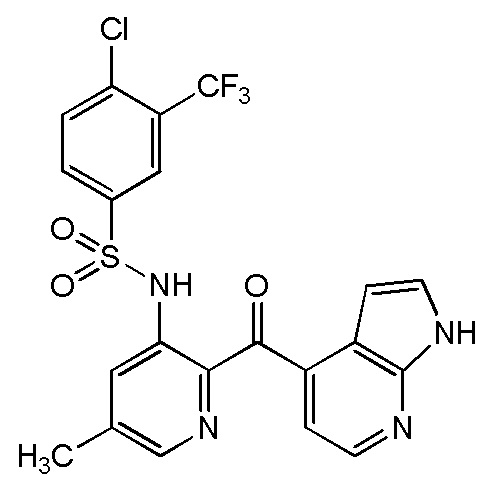
[00157] CVC – это сенекривирок.
Пример 1: Диета с высоким содержанием жира (HFD) вызвала модель NASH
[00158] Мужской дикий тип (VVT) мыши C57BI/6 получили из Лаборатории Джексона и кормили любой диетой с высоким содержанием жира (D12492, 60 кал % жира, Research Diets, New Brunswick, NJ) с 30%-й фруктозой в питьевой воде или минимизированной диетой контроля (D12450B, 10 кал % жира Research Diets) в возрасте 6-8 недель и поддерживали на соответствующей диете в течение продолжительности исследования (16-32 недели). Соединение 1 было составлено в форме раствора в 1% гидроксипропилметилцеллюлозе (Sigma-Aldrich, St. Louis, USA). Мышам вводили подкожно один раз в день 30 мг/кг Соединения 1 или наполнитель в течение 8 недель. Как показывает Фиг. 1, лечение соединением 1 не изменяло массу тела по сравнению с наполнителем. Как показано на Фиг. 2, Соединение 1 снизило серологические уровни ALT и AST. Сириус Красное окрашивание было использовано, чтобы оценить серьезность фиброза печени. Фиг. 3 показывает представительные изображения Сириус красного окрашивания участков печени животных, которых лечили Соединением 1 или наполнителем. Фиг. 4 показывает, что лечение соединением 1 снизило процент Сириус окрашивания и, следовательно, фиброз печени, по сравнению с наполнителем.
Пример 2: дефицит метионин-холина (MCD) вызвал модель NASH
[00159] Мужской дикий тип (VVT) мышей C57BI/6 получили из Лаборатории Джексона и кормили любой MCD диетой (MP Biomedicals, № 960439) или минимизированной диетой контроля в 8-недельном возрасте в течение 8 недель. Соединение 1 составлено в форме раствора в 1% гидроксипропилметилцеллюлозе (Sigma-Aldrich, St. Louis, USA). Мышам вводили подкожно один раз в день Соединение 1 30 мг/кг или наполнитель в течение 8 недель. Соединение 1 назначено подкожно, чтобы обеспечить высокие системные уровни. Соединение CVC (сенекривирок) составлено в форме раствора в 1% гидроксипропилметилцеллюлозе и протестировано при 30мг/мг перорально. Для обоих - соединения 1 и CVC, уровень препарата был по IC50. Фиг. 5 показывает, что соединение 1 значительно снижает серологические уровни ALT, тогда как CVC - нет. Фиг. 6 показывает, что соединение 1 уменьшает Сириус красное положительное окрашивание и, поэтому, фиброз печени, тогда как CVC нет.
Пример 3: Гистопатологический анализ
[00160] Фиксированные формалином, заключенные в парафин участки печени окрашены отдельно гематоксилином & эозином (Г-Э) и для Сириус красного Picrosirius(#365548, Sigma) и оценены на серьезность фиброза печени. Все патологические оценки были выполнены паталогом на рандомизированном и слепом основании. Поверхностная плотность коллагена определена количественно с использованием Изображения J (NIH). Два Сириус красных окрашенных препарата на животное взяты на различной глубине с 18 изображениями, взятыми рандомизированно на слайд в общей сложности для 36 изображений на животное для определения количества коллагена.
Пример 4: анализ сыворотки и ткани
[00161] Ферменты печени анализировали с помощью Antech GLP (Morrisville, NC). Инсулин измерили c помощью Ultrsasensitive. Набор ELISA инсулина мыши (Crystal Chem Inc: # 90080); глюкоза Крови и уровни инсулина определены после ночного голодания (14-16 ч). Чувствительность инсулина определена гомеостатическим исследованием модели устойчивости к инсулину (HOMA-IR). Липиды измерили в сыворотке и печени с помощью набора для триглицеридного колориметрического анализа (Cayman Chemical Company: # 10010303), набора для Определения количества Свободной Жирной кислоты, (Abcam , ab65341) и набора для Определения количества Холестерина (Abcam, ab65359).
Пример 5: анализ CCR5 миграции
[00162] Обычную пробу миграции использовали для определения эффективности антагонистов потенциальных рецепторов в блокировании миграции, опосредованной через MIP 1b. Эта проба выполнена обычным образом с использованием ChemoTX(R) (Neuroprobe) микрокамерной системы с поликарбонатной мембраной с 5-mum размерами пор. Клетки, выражающие CCR5 (IL-2 Лимфоциты или L1.2CCR5 клетки), получены центрифугированием клеточной суспензии при 1000 об/мин на GS-6R центрифуге Бекмана. Клетки осадка повторно суспендированы в хемотаксисном буфере (HBSS с 0,1% BSA) при 5x106 клетки/мЛ. Тестовые соединения при требуемых концентрациях приготовлены из 10 мМ запасенных растворов последовательными разбавлениями в хемотаксисном буфере. Равный объем клеток и соединений смешивали и инкубировали при комнатной температуре в течение 15 минут.
Впоследствии, 20 мкл смеси переданы на пористую мембрану миграционной микрокамеры, с 29 мкл лиганда MIP 1b (0,1 нм белка MIP 1b), помещенного в нижнюю камеру. После инкубации при температуре 37оС (90 минут), проба закончена, капли клеток удалены с верха фильтра. Для определения количества клеток, мигрировавших через мембрану, 5 мкл _ 7X CyQUANT(R) (ТECAN, Durham, NC) раствора добавлено в каждую лунку в нижней камере, и сигнал флуоресценции измерен на Spectrafluor Plus ридере флуоресцентных пластин (TECAN, Durham, NC). Степень ингибирования определена путем сравнения сигналов миграции между подвергшимися лечению соединением клетками и необработанными клетками. Вычисление IC50 далее выполнено нелинейным регрессионным анализом площадей, используя Graphpad Prism (Graphpad Software, San Diego , CA).
[00163] Как представлено в Таблице 1, соединения 1, 2 и 3 не ингибируют CCR5, тогда как CVC – является мощным ингибитором CCR5.
Таблица 1. CCR5 IC50
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения фокально-сегментарного гломерулосклероза | 2017 |
|
RU2765737C2 |
| Ингибиторы цитохрома 11В2 человека | 2022 |
|
RU2800378C1 |
| ИЗОКСАЗОЛИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ АМИДГИДРОЛАЗЫ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2539595C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКИХ И ПЕЧЕНОЧНЫХ РАССТРОЙСТВ | 2022 |
|
RU2833318C1 |
| ЦИАНОТИЕНОТРИАЗОЛОДИАЗЕПИНЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2750164C2 |
| ИНГИБИТОРЫ α-АМИНО-β-КАРБОКСИМУКОНАТ-ε-СЕМИАЛЬДЕГИД-ДЕКАРБОКСИЛАЗЫ | 2015 |
|
RU2746405C2 |
| 19-НОР C3, 3-ДИЗАМЕЩЕННЫЕ C21-N-ПИРАЗОЛИЛЬНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2675855C2 |
| НОВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА И ФИБРОЗА | 2017 |
|
RU2762280C2 |
| ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ СОЕДИНЕНИЯ ГЕКСАГИДРОДИБЕНЗО[A, G]ХИНОЛИЗИНА | 2014 |
|
RU2704257C2 |
| НЕЙРОАКТИВНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2764702C2 |
Изобретение относится к способу лечения фиброза печени у пациента, который включает назначение пациенту, который в этом нуждается, эффективного количества соединения Формулы I или фармацевтически приемлемой его соли, где R1 - галоген, R2 - C1-6 галоалкил, R3 - C1-6 алкил, R4 - водород, и каждый из A1, A2 - это -CH-, и A3 - это -N-. Технический результат - разработан новый способ лечения фиброза печени, в котором фиброз печени связан с неалкогольным стеатогепатитом (NASH). 5 з.п. ф-лы, 6 ил., 1 табл., 5 пр.
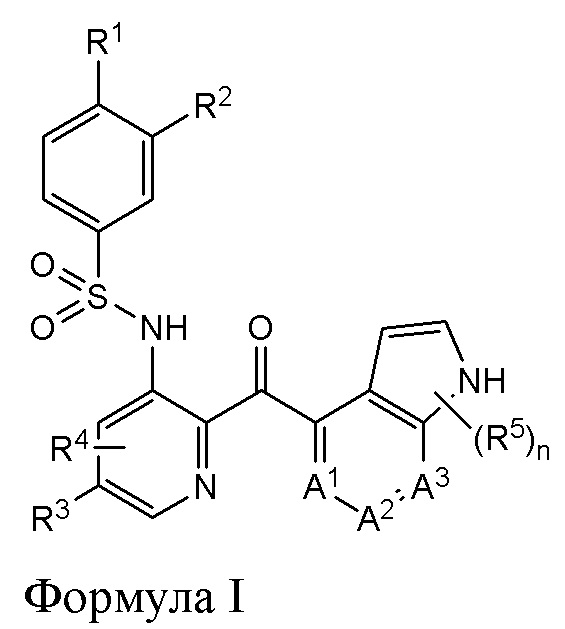
1. Способ лечения фиброза печени у пациента, включающий назначение пациенту, который в этом нуждается, эффективного количества соединения Формулы I
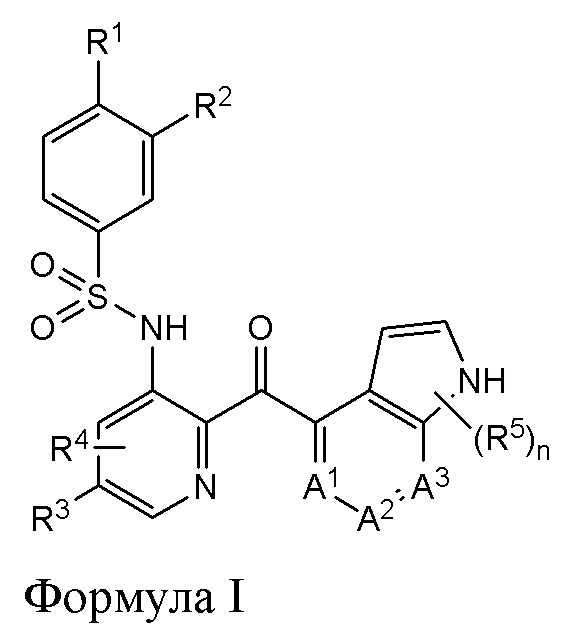
или фармацевтически приемлемой его соли, где
R1 - галоген;
R2 - C1-6 галоалкил;
R3 - C1-6 алкил;
R4 - водород; и
каждый из A1, A2 - это -CH-, и A3 - это -N-.
2. Способ по п. 1, в котором соединение это
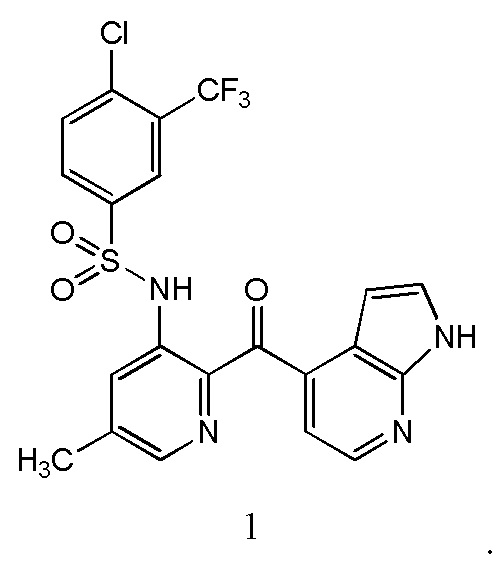
3. Способ по п. 1, в котором фиброз печени связан с неалкогольным стеатогепатитом (NASH).
4. Способ по п. 1, в котором соединение понижает концентрацию аланин аминотрансферазы (АLT).
5. Способ по п. 1, в котором соединение понижает концентрацию аспартат аминотрансферазы (AST).
6. Способ по п. 1, в котором соединение уменьшает фиброз печени.
| WO 2016040860 A1, 17.03.2016 | |||
| WO 2009009740 A1, 15.01.2009 | |||
| WO 2008008431 A2, 17.01.2008 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| EA 23207 B1, 31.05.2016. | |||
Авторы
Даты
2021-01-21—Публикация
2017-06-02—Подача