РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет на основании предварительной заявки на патент США № 62/043853, поданной 29 августа 2014, полностью включенной в настоящее описание в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ РАСКРЫТИЕ
Настоящее раскрытие относится к соединениям, способным модулировать активность α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD). Раскрытые соединения можно использовать в способах предупреждения и/или лечения заболеваний и расстройств, связанных с дефектами в биосинтезе NAD+, например, метаболических нарушений, нейродегенеративных заболеваний, хронических воспалительных заболеваний, болезней почек и заболеваний, связанных со старением.
ПРЕДПОСЫЛКИ СОЗДАНИЯ РАСКРЫТИЯ
ACMSD является критичным ферментом для метаболизма триптофана и регулирует биосинтез NAD+ из триптофана. ACMSD является цинказависимой амидогидролазой, которая участвует в гомеостазе пиколиновой кислоты (РА), хинолиновой кислоты (QA) и NAD. ACMSD стоит в точке ветвления пути биосинтеза NAD+ из триптофана и определяет конечную судьбу аминокислоты, т.е. трансформацию в РА, полное окисление через цикл лимонной кислоты или конверсию в NAD+ через синтез QA.
ACMSD выделена из тканей печени, почек и головного мозга человека. Существует две изоформы ACMSD1 и ACMSD2, образующиеся при различном сплайсинге транскрипции гена ACMSD, но только ACMSD1 наделена ферментативной активностью. ACMSD1 направляет ACMS (семиальдегид α-амино-ω-карбоксимуконовой кислоты) в каскад ацетил-СоА, и когда ACMSD1 ингибирована, ACMS не превращается ферментативно в хинолиновую кислоту (QA), приводя к образованию NAD+ и повышению внутриклеточного уровня NAD+.
Показано, что повышенные уровни NAD+ защищают от нейронной дегенерации, улучшают мышечную функцию и окислительный метаболизм у мышей и увеличивают продолжительность жизни у червей. В то же время пониженные уровни NAD+ ассоциируются с рядом патофизиологических состояний, включая диабет типа 2 (T2D), гиперлипидемию (повышенный холестерин и TAG), митохондриальные заболевания, нейтропению, раковые заболевания и почечные расстройства.
Таким образом, ингибирование ACMSD представляет новый подход к повышению уровней NAD+ и модификации патофизиологии заболеваний, связанных с дефектами в биосинтезе NAD+.
СУЩНОСТЬ РАСКРЫТИЯ
Задачей настоящего изобретения является новый ряд соединений, способных модулировать активность α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), которые применимы для предупреждения и/или лечения заболеваний и расстройств, связанных с дефектами биосинтеза NAD+, например, метаболических расстройств, нейродегенеративных заболеваний, хронических воспалительных заболеваний, болезней почек и заболеваний, связанных со старением.
Соединения формулы (I), определенные в настоящем описании, можно использовать при лечении заболевания или расстройства, в котором играет роль ACMSD. Раскрытие показывает способы лечения заболевания или расстройства, связанного с дисфункцией ACMSD или с анормальностями в биосинтезе NAD+, путем введения субъектам, страдающим от или восприимчивым к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений, которые повышают внутриклеточный NAD+ путем ингибирования ACMSD1, в количестве, достаточном для активации сиртуинов (SIRT), и отрицательно регулируют мишени SIRT, такие как PGC-1α, FoxO1 и/или супероксиддисмутаза (SOD). Способы по настоящему раскрытию можно использовать для лечения ACMSD-зависимых заболеваний путем ингибирования ACMSD. Ингибирование ACMSD может предоставить новый подход к предупреждению и лечению метаболических расстройств, хронических воспалительных заболеваний, болезней почек, заболеваний, связанных со старением, и других ACMSD-зависимых заболеваний или заболеваний, характеризующихся несовершенным синтезом NAD+.
Соответственно, первый аспект настоящего раскрытия относится к соединению, представленному формулой (I)
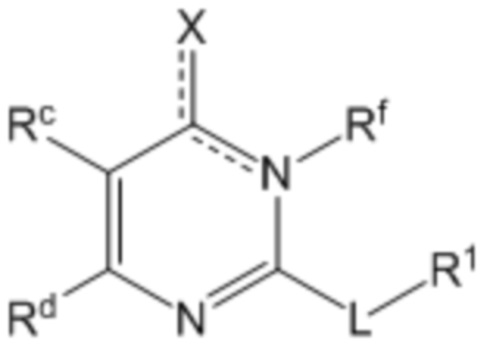
или его фармацевтически приемлемой соли или таутомеру,
где в указанной формуле
X представляет собой O, OH или Cl;
L представляет собой -(CH2)mCH2CH2-, -(CH2)mY(CH2)p-, -(CH2)mC(O)(CH2)p-, -(CH2)mC(O)O(CH2)p-, -(CH2)mC(O)NR2(CH2)p- или -(CH2)mNR2C(O)(CH2)p;
Y представляет собой O, N или S(O)q;
R1 представляет собой (C6-C10)арил или гетероарил, где арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re;
R2 представляет собой H или (C1-C6)алкил;
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx при каждом появлении представляет собой независимо водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
Rf представляет собой H или отсутствует;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил;
каждый m и p равен независимо 0, 1 или 2, где m+p <3;
q равен 0, 1 или 2;
r равен 0 или 1; и
пунктирная линия представляет собой необязательную двойную связь;
при условии, что Rc не является водородом или -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой метил, и что Rc не является -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
Второй аспект настоящего раскрытия относится к фармацевтическим композициям, включающим соединение формулы (I) или его фармацевтически приемлемую соль и по меньшей мере одни фармацевтически приемлемый носитель, разбавитель или эксципиент.
Третий аспект раскрытия относится к способу лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Четвертый аспект раскрытия относится к способу предупреждения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Пятый аспект раскрытия относится к способу снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Шестой аспект раскрытия относится к способу лечения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Седьмой аспект раскрытия относится к способу предупреждения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Восьмой аспект раскрытия относится к способу снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I).
Девятый аспект раскрытия относится к способу лечения расстройства, связанного с митохондриальной дисфункцией, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), что повышает внутриклеточный никотинамидадениндинуклеотид (NAD+).
Десятый аспект раскрытия относится к способу промотирования окислительного метаболизма, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), что повышает внутриклеточный никотинамидадениндинуклеотид (NAD+).
Одиннадцатый аспект раскрытия относится к способу изготовления лекарственного средства для лечения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I) или его фармацевтически приемлемую соль.
Двенадцатый аспект раскрытия относится к фармацевтической композиции для применения в способе лечения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I) или его фармацевтически приемлемую соль.
Тринадцатый аспект раскрытия относится к способу лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений следующих формул:
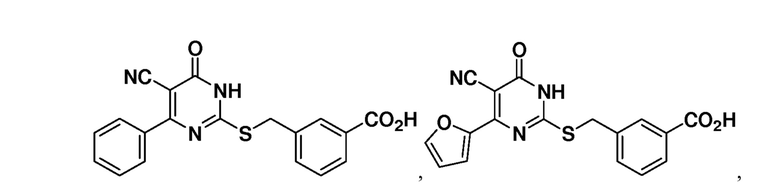
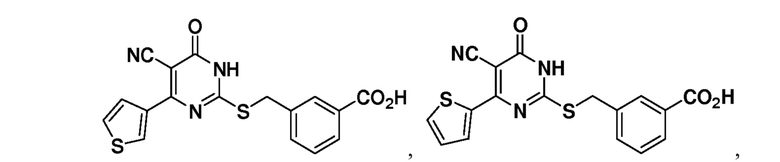
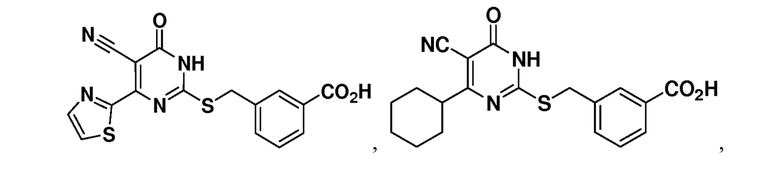
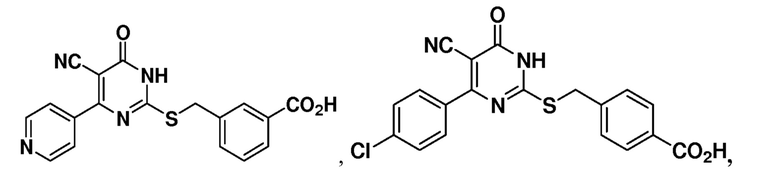
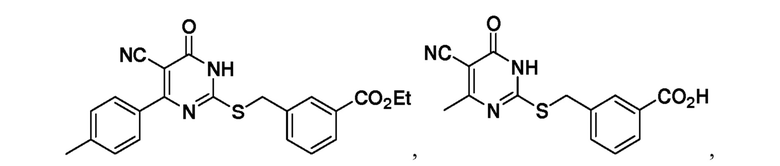
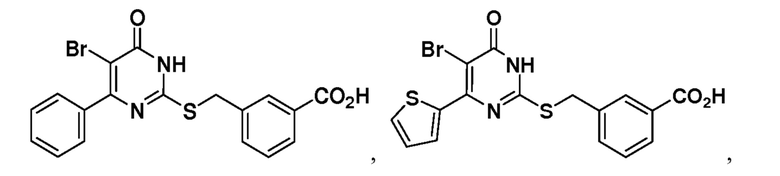
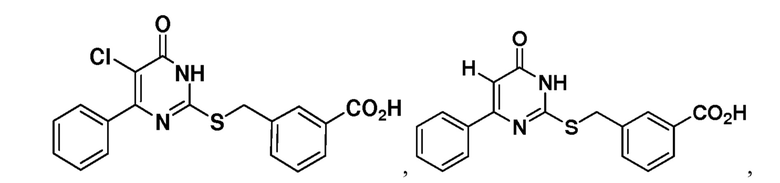
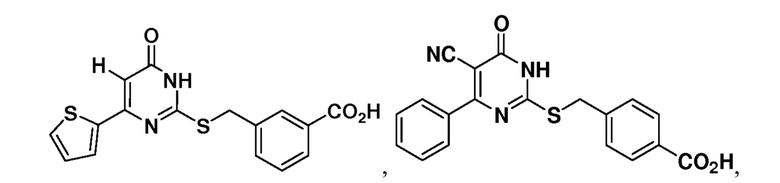
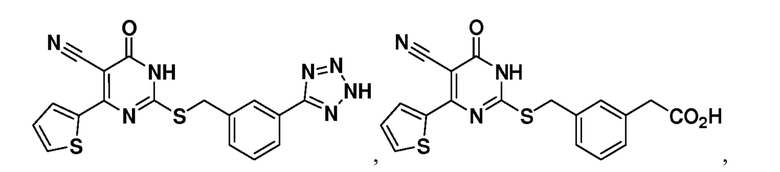
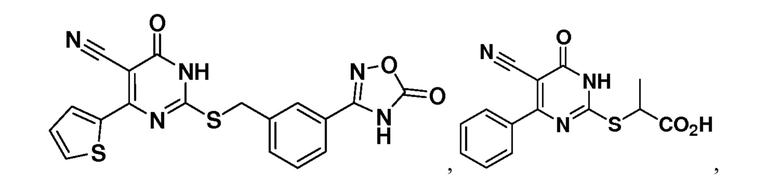
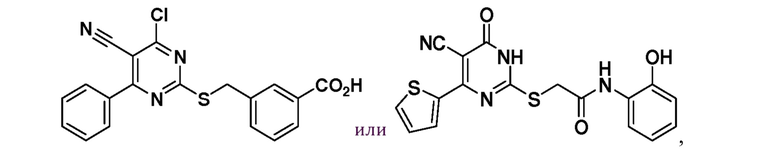
или их фармацевтически приемлемых солей.
Четырнадцатый аспект раскрытия относится к применению соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Пятнадцатый аспект раскрытия относится к применению соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Шестнадцатый аспект раскрытия относится к применению соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
Семнадцатый аспект раскрытия относится к применению соединения формулы (I) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для промотирования окислительного метаболизма.
Восемнадцатый аспект раскрытия относится к применению соединения формулы (I), его фармацевтически приемлемой соли для при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Девятнадцатый аспект раскрытия относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Двадцатый аспект раскрытия относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с митохондриальной дисфункцией.
Двадцать первый аспект раскрытия относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения при лечении, предупреждении или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Двадцать второй аспект раскрытия относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения при лечении, предупреждении или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
Двадцать третий аспект раскрытия относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения при промотировании окислительного метаболизма.
Двадцать четвертый аспект раскрытия относится к соединению, имеющему одну из следующих формул:











или его фармацевтически приемлемой соли,
при изготовлении лекарственного средства для лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Двадцать пятый аспект раскрытия относится к соединению, имеющему одну из следующих формул:











или его фармацевтически приемлемой соли,
для применения в качестве лекарственного средства для лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Двадцать шестой аспект раскрытия относится к соединению, имеющему одну из следующих формул:










или его фармацевтически приемлемой соли,
для применения при лечении заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В некоторых аспектах модулирующие ACMSD соединения можно вводить одни или в комбинации с другими соединениями, включая другие модулирующие ACMSD соединения или другие терапевтические средства.
Если не определено иначе, все технические и научные термины, используемые в настоящем описании, имеют те же значения, какие им обычно придают специалисты в данной области техники, к которым относится раскрытие. В описании формы единственного числа также включают формы множественного числа, если контекст не указывает четко иное. Хотя на практике и при проверке раскрытия можно использовать способы и материалы, схожие с или эквивалентные описанным в настоящем описании, подходящие способы и материалы описаны ниже. Все публикации, заявки на патент, патенты и другие ссылки, упомянутые в настоящем описании, включены в него в качестве ссылок. Ссылки, цитированные в настоящем описании, не допускают претензий известного уровня техники к заявляемому раскрытию. В случае конфликта настоящее описание, включая определения, будет контролем. Кроме того, материалы, способы и примеры являются только иллюстративными и не предназначены для ограничения.
Другие особенности и преимущества раскрытия будут очевидны из следующих далее подробного описания и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 представляет собой диаграмму измеренных уровней NAD+ в первичных гепатоцитах человека, обработанных соединением 4, обнаруженных ЖХ-МС/МС.
Фиг. 2 представляет собой диаграмму измеренных уровней NAD+ в первичных мышиных гепатоцитах, обработанных различными концентрациями соединения 17 в течение 24 часов и обнаруженных ЖХ-МС/МС. Данные показывают возрастание уровней NAD+ в первичных гепатоцитах мыши, обработанных соединением 17.
Фиг. 3 представляет собой диаграмму измеренного содержания NAD+ в первичных гепатоцитах человека, обработанных различными концентрациями соединения 1 и моно(2-этилгексил)фталатом (МЕНР) в качестве контроля.
Фиг. 4А представляет собой диаграмму экспрессии генов Acmsd, Sod-1 и Sod-2 при определении RT-qPCR в клетках AML-12, обработанных соединением 1 в течение 24 часов. Фиг. 4B представляет собой диаграмму экспрессии генов Sod-1 и Sod-2 при определении RT-qPCR в клетках Hepa-1.6, обработанных соединением 1 в течение 24 часов. Фиг. 4C представляет собой диаграмму экспрессии генов Acmsd, Sod-1, Sod-2 и Pgc1a при определении RT-qPCR в первичных мышиных гепатоцитах, обработанных соединением 17 в течение 24 часов. Столбиковые диаграммы представляют среднее ± SEM, ***p ≤ 0,005.
Фиг. 5А представляет собой диаграмму, показывающую модуляцию активности SOD2 в клетках AML-12, обработанных в течение 24 часов соединением 1. Фиг. 5В представляет диаграмму, показывающую модуляцию активности SOD2 в клетках AML-12, обработанных в течение 24 часов соединением 17. Фиг. 5С представляет диаграмму, показывающую модуляцию активности SOD2 в первичных мышиных гепатоцитах, обработанных в течение 24 часов соединением 17.
Фиг. 6А отображает гель, показывающий действие соединения 1 на уровни фосфорилирования EoxO1. Фиг. 6В отображает гель, показывающий действие соединения 17 на уровни фосфорилирования EoxO1.
Фиг. 7А представляет собой диаграмму изменений экспрессии acsmd-1 и sod-3 по уровням мРНК, измеренным у червей N2 дикого типа в день 2 взрослого состояния с помощью сайленсинга РНКи acmsd-1 у Caenorhabditis elegans (C. elegans). Фиг. 7B представляет собой диаграмму индукции экспрессии sod-3 по уровням белков у червей N2 в день 3 взрослого состояния, полученных количественно с использованием репортерного штамма SOD-3 gfp, после сайленсинга РНКи acmsd-1 у C. elegans. Фиг. 7C представляет собой график, показывающий выживаемость червей после отрицательной регуляции acmsd-1 путем подкормки специфической РНКи, у C. elegans. Фиг. 7C показывает, что отрицательная регуляция acmsd-1 улучшает выживаемость червей в зависмости от SIR-2.1 и DAF-16. Фиг. 7D представляет собой график, показывающий, что отрицательная регуляция acmsd-1 улучшает стрессоустойчивость червей, когда они подвергаются вызванному паракватом окислительному стрессу. Фиг. 7Е представляет собой график, показывающий мобильность червей со временем, питаемых РНКи acmsd-1, в состоянии вызванного паракватом окислительного стресса. Как показывают фиг. 7С-7Е, сниженная экспрессия acmsd-1 улучшает выживаемость и выносливость червей при вызванном паракватом окислительном стрессе. Фиг. 7F представляет собой график, который показывает выживаемость червей в условиях вызванного паракватом окислительного стресса, когда подвергаются РНКи acmsd-1 на различных стадиях развития. Фиг. 7F иллюстрирует, что улучшение выживаемости червей в условиях с паракватом не зависит от стадии развития, на которой черви подвергаются воздействию РНКи acmsd-1. Фиг. 7G представляет собой график, показывающий выживаемость червей в условиях вызванного паракватом окислительного стресса при отрицательной регуляции acmsd-1 в комбинации с отрицательной регуляцией daf-16 путем подкормки специфической РНКи у C. elegans. Фиг. 7G показывает, что улучшенная выживаемость червей, подвергнутых отрицательной регуляции acmsd-1, является зависимой от daf-16 в условиях вызванного паракватом окислительного стресса.
Фиг. 8А представляет собой диаграмму вызванных циспалатином изменений в активности каспазы 3/7 в клетках MDCK при обработке различными концентрациями соединения 18 в комбинации с цисплатином. Фиг. 8В представляет собой диаграмму вызванных циспалатином изменений в активности каспазы 3/7 в клетках MDCK при обработке различными концентрациями соединения 18 за один час до добавления цисплатина.
ПОДРОБНОЕ ОПИСАНИЕ РАСКРЫТИЯ
Соединения формулы (I)
Настоящее раскрытие относится к соединениям формулы (I)

или их фармацевтически приемлемым солям или таутомерам,
где в указанной формуле
X представляет собой O, OH или Cl;
L представляет собой -(CH2)mCH2CH2-, -(CH2)mY(CH2)p-, -(CH2)mC(O)(CH2)p-, -(CH2)mC(O)O(CH2)p-, -(CH2)mC(O)NR2(CH2)p- или -(CH2)mNR2C(O)(CH2)p;
Y представляет собой O, N или S(O)q;
R1 представляет собой (C6-C10)арил или гетероарил, где арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re;
R2 представляет собой H или (C1-C6)алкил;
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx при каждом появлении представляет собой независимо водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
Rf представляет собой H или отсутствует;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил;
каждый m и p равен независимо 0, 1 или 2, где m+p <3;
q равен 0, 1 или 2;
r равен 0 или 1; и
пунктирная линия представляет собой необязательную двойную связь;
при условии, что Rc не является водородом или -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой метил, и что Rc не является -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (I) Х представляет собой О, ОН или Cl. В других воплощениях Х представляет собой О. В других воплощениях Х представляет собой ОН. В других воплощениях Х представляет собой Cl.
В некоторых воплощениях формулы (I) L представляет собой -(CH2)mCH2CH2-, -(CH2)mY(CH2)p-, -(CH2)mC(O)(CH2)p-, -(CH2)mC(O)O(CH2)p-, -(CH2)mC(O)NR2(CH2)p- или -(CH2)mNR2C(O) (CH2)p. В других воплощениях L представляет собой -CH2CH2-, -CH2CH2CH2-,-SCH2-, -SCH2CH2-, -CH2S-, -CH2SCH2-, -CH2CH2S-, -S(O)CH2-, -S(O)CH2CH2-, -CH2S(O)-, -CH2S(O)CH2-, -CH2CH2S(O)-, -S(O)2CH2-, -S(O)2CH2CH2-, -CH2S(O)2-, -CH2S(O)2CH2-, -CH2CH2S(O)2-, -OCH2-, -OCH2CH2-, -CH2O-, -CH2OCH2-, -CH2CH2O-, -NR2CH2-, - CH2NR2-, -CH2NR2CH2-, - CH2CH2NR2-, -NR2CH2CH2-, -C(O)CH2-, -C(O)CH2CH2-, -C(O)O-, -C(O)OCH2-, -CH2C(O)O-, -C(O)NR2-, -C(O)NR2CH2-, -NR2C(O), -NR2C(O)CH2 или -CH2NR2C(O). В других воплощениях L представляет собой -CH2CH2-, -CH2CH2CH2-, -SCH2-, -SCH2CH2-, -S(O)CH2-, -S(O)CH2CH2-, -S(O)2CH2-, -S(O)2CH2CH2-, -OCH2-, -OCH2CH2-, -NR2CH2-, -NR2CH2CH2-, -C(O)CH2-, -C(O)CH2CH2-, -C(O)O-, -C(O)OCH2-,-CH2C(O)O-, -C(O)NR2-, -C(O)NR2CH2-, - NR2C(O) или - NR2C(O)CH2. В других воплощениях L представляет собой -CH2CH2-, -CH2C(O)-, -C(O)CH2-, -NR2CH2-, -CH2NR2-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -S(O)CH2-, -CH2S(O)-, -CH2S(O)2- или -S(O)2CH2-.
В некоторых воплощениях формулы (I) R1 представляет собой (C6-C10)арил или гетероарил, где арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re. В других воплощениях R1 представляет собой (C6-C10)арил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re. В других воплощениях R1 представляет собой гетероарил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re. В других воплощениях R1 представляет собой фенил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re.
В некоторых воплощениях формулы (I) Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Ra представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Ra представляет собой водород, СО2Н, СН2СО2Н, тетразол или 1,2,4-оксадиазол-5(4Н)-он.
В некоторых воплощениях формулы (I) Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Rb представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, CO2Н, CH2CO2Н, тетразол или 1,2,4-оксадиазол-5(4Н)-он. В других воплощениях Rb представляет собой водород.
В некоторых воплощениях формулы (I) Rс представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rс представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rс представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rс представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rс представляет собой Н, -CN или галоген. В других воплощениях Rс представляет собой -CN или галоген.
В некоторых воплощениях формулы (I) Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл. В других воплощениях Rd представляет собой метил, необязательно замещенный циклогексил, необязательно замещенный пиридинил, необязательно замещенный тиазолил, необязательно замещенный фенил или необязательно замещенный тиенил. В других воплощениях Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, выбранными независимо из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, -ОН, CN и амино. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, выбранными независимо из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила и (C1-C6)галогеналкокси. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими атомами галогена. В еще других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил, 4-хлорфенил, 4-метилфенил или тиенил.
В некоторых воплощениях формулы (I) каждый Rе представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN. В других воплощениях Rе представляет собой (C1-C4)алкил, (C2-C4)алкенил, (C2-C4)алкинил, галоген, -ORy, (C1-C4)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (I) Rf представляет собой Н или отсутствует. В других воплощениях Rf представляет собой Н. В других воплощениях Rf отсутствует, когда N, к которому он присоединен, участвует в двойной связи.
В некоторых воплощениях формулы (I) Rх представляет собой водород или (C1-C6)алкил. В других воплощениях Rх представляет собой водород или (C1-C3)алкил. В других воплощениях Rх представляет собой водород, метил, этил, н-пропил или изопропил.
В некоторых воплощениях формулы (I) Ry представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Ry представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (I) каждый Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Rz представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (I) m равен 0, 1 или 2. В других воплощениях m равен 0. В других воплощениях m равен 1. В еще других воплощениях m равен 2.
В некоторых воплощениях формулы (I) р равен 0, 1 или 2. В других воплощениях р равен 0. В других воплощениях р равен 1. В еще других воплощениях р равен 2.
В некоторых воплощениях формулы (I) m+р <3.
В некоторых воплощениях формулы (I) q равен 0, 1 или 2. В других воплощениях q равен 0. В других воплощениях q равен 1. В других воплощениях q равен 2.
В некоторых воплощениях формулы (I) r равен 0 или 1. В других воплощениях r равен 0. В других воплощениях r равен 1.
В некоторых воплощениях формулы (I) пунктирная линия представляет собой простую связь. В других воплощениях пунктирная линия представляет собой двойную связь.
В некоторых воплощениях формулы (I) один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (I) Rb представляет собой водород, Rc представляет собой -CN, Rd представляет собой тиенил, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол 5(4H)-он.
В некоторых воплощениях формулы (I) Rc представляет собой галоген, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (I) Rc представляет собой галоген, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой тетразол, и Rb представляет собой H.
В некоторых воплощениях формулы (I) Rc представляет собой галоген, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CH2CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (I) Rc представляет собой галоген, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (I) Rc представляет собой -CN, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой тетразол, и Rb представляет собой H. В еще других воплощениях Rc представляет собой -CN, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (I) Rc не является водородом или -CN, и X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил. В других воплощениях Rc не является (C1-C6)алкилом, и X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой метил. В других воплощениях Rc не является -CN, и X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (I) Rc не является водородом или -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил.
В некоторых воплощениях формулы (I) Rc не является (C1-C6)алкилом, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой метил.
В некоторых воплощениях формулы (I) Rc не является -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В одном воплощении соединение формулы (I) представляет собой соединение формулы (Ia)
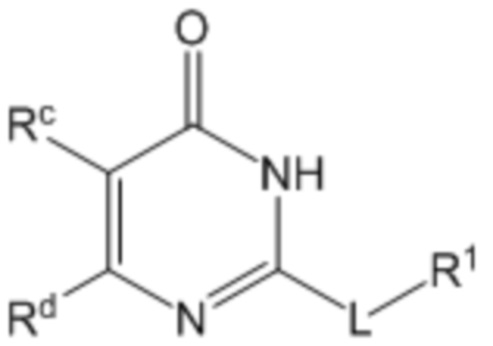 (Ia)
(Ia)
или его фармацевтически приемлемую соль или таутомер,
где в указанной формуле
L представляет собой -(CH2)mCH2CH2-, -(CH2)mY(CH2)p-, -(CH2)mC(O)(CH2)p-, -(CH2)mC(O)O(CH2)p-, -(CH2)mC(O)NR2(CH2)p- или -(CH2)mNR2C(O)(CH2)p;
Y представляет собой O, N или S(O)q;
R1 представляет собой (C6-C10)арил или гетероарил, где арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re;
R2 представляет собой H или C1-C6 алкил;
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил;
каждый m и p независимо равен 0, 1 или 2, причем m+p <3;
q равен 0, 1 или 2; и
r равен 0 или 1;
при условии, что Rc не является водородом или -CN, когда L представляет собой -SCH2- и Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда L представляет собой -SCH2-, и Rd представляет собой метил, и что Rc не является -CN, когда L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ia)
L представляет собой -CH2CH2-, -CH2C(O)-, -C(O)CH2-, -NR2CH2-, -CH2NR2-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -S(O)CH2-, -CH2S(O)-, -CH2S(O)2- или -S(O)2CH2-;
Y представляет собой O, N или S(O)q;
R1 представляет собой (C6-C10)арил или гетероарил, причем арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re;
R2 представляет собой H или (C1-C6)алкил;
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил;
каждый m и p независимо равен 0, 1 или 2, причем m+p <3;
q равен 0, 1 или 2; и
r равен 0 или 1;
при условии, что Rc не является -CN, когда L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда L представляет собой -SCH2-, и Rd представляет собой метил, и что Rc не является -CN, когда L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ia) L представляет собой -(CH2)mCH2CH2-, -(CH2)mY(CH2)p-, -(CH2)mC(O)(CH2)p-, -(CH2)mC(O)O(CH2)p-, -(CH2)mC(O)NR2(CH2)p- или -(CH2)mNR2C(O)(CH2)p. В других воплощениях L представляет собой -CH2CH2-, -CH2CH2CH2-,-SCH2-, -SCH2CH2-, -CH2S-, -CH2SCH2-, -CH2CH2S-, -S(O)CH2-, -S(O)CH2CH2-, -CH2S(O)-, -CH2S(O)CH2-, -CH2CH2S(O)-, -S(O)2CH2-, -S(O)2CH2CH2-, -CH2S(O)2-, -CH2S(O)2CH2-, -CH2CH2S(O)2-, -OCH2-, -OCH2CH2-, -CH2O-, -CH2OCH2-, -CH2CH2O-,-NR2CH2-, - CH2NR2-, -CH2NR2CH2-, - CH2CH2NR2-, -NR2CH2CH2-, -C(O)CH2-, -C(O)CH2CH2-, -C(O)O-, -C(O)OCH2-, -CH2C(O)O-, -C(O)NR2-, -C(O)NR2CH2-, -NR2C(O), -NR2C(O)CH2 или -CH2NR2C(O). В других воплощениях L представляет собой -CH2CH2-, -CH2CH2CH2-, -SCH2-, -SCH2CH2-, -S(O)CH2-, -S(O)CH2CH2-, -S(O)2CH2-, -S(O)2CH2CH2-, -OCH2-, -OCH2CH2-, -NR2CH2-, -NR2CH2CH2-, -C(O)CH2-, -C(O)CH2CH2-, -C(O)O-, -C(O)OCH2-,-CH2C(O)O-, -C(O)NR2-, -C(O)NR2CH2-, - NR2C(O) или - NR2C(O)CH2. В других воплощениях, L представляет собой -CH2CH2-, -CH2C(O)-, -C(O)CH2-, -NR2CH2-, -CH2NR2-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -S(O)CH2-, -CH2S(O)-, -CH2S(O)2- или -S(O)2CH2-.
В некоторых воплощениях формулы (Ia) R1 представляет собой (C6-C10)арил или гетероарил, где арил и гетероарил замещены Ra и Rb и, необязательно, замещены одним или несколькими Re. В других воплощениях R1 представляет собой (C6-C10)арил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re. В других воплощениях, R1 представляет собой гетероарил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re. В других воплощениях R1 представляет собой фенил, замещенный Ra и Rb и, необязательно, замещенный одним или несколькими Re.
В некоторых воплощениях формулы (Ia) Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Ra представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Ra представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ia) Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Rb представляет соой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Rb представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он. В других воплощениях Rb представляет собой водород.
В некоторых воплощениях формулы (Ia) Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C3)алкил. В других воплощениях Rc представляет собой H, -CN или галоген. В других воплощениях Rc представляет собой -CN или галоген.
В некоторых воплощениях формулы (Ia) Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл. В других воплощениях Rd представляет собой метил, необязательно замещенный циклогексил, необязательно замещенный пиридинил, необязательно замещенный тиазолил, необязательно замещенный фенил или необязательно замещенный тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, -OH, CN и амино. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила и (C1-C6)галогеналкокси. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими атомами галогена. В других воплощениях Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил. В еще других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил, 4-хлорфенил, 4-метилфенил или тиенил.
В некоторых воплощениях формулы (Ia) каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN. В других воплощениях Re представляет собой (C1-C4)алкил, (C2-C4)алкенил, (C2-C4)алкинил, галоген, -ORy, (C1-C4)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (Ia) Rx представляет собой водород или (C1-C6)алкил. В других воплощениях Rx представляет собой водород или (C1-C3)алкил. В других воплощениях Rx представляет собой водород, метил, этил, н-пропил или изопропил.
В некоторых воплощениях формулы (Ia) Ry представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Ry представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (Ia) каждый Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Rz представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (Ia) m равен 0, 1 или 2. В других воплощениях m равен 0. В других воплощениях m равен 1. В еще других воплощениях m равен 2.
В некоторых воплощениях формулы (Ia) p равен 0, 1 или 2. В других воплощениях p равен 0. В других воплощениях p равен 1. В еще других воплощениях p равен 2.
В некоторых воплощениях формулы (Ia) q равен 0, 1 или 2. В других воплощениях q равен 0. В других воплощениях q равен 1. В других воплощениях q равен 2.
В некоторых воплощениях формулы (Ia) r равен 0 или 1. В других воплощениях r равен 0. В других воплощениях r равен 1.
В некоторых воплощениях формулы (Ia) один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ia) Rb представляет собой водород, Rc представляет собой -CN, Rd представляет собой тиенил, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ia) Rc представляет собой галоген, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (Ia) Rc представляет собой галоген, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой тетразол, и Rb представляет собой H.
В некоторых воплощениях формулы (Ia) Rc представляет собой галоген, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CH2CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (Ia) Rc представляет собой галоген, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (Ia) Rc представляет собой -CN, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой тетразол, и Rb представляет собой H. В еще других воплощениях Rc представляет собой -CN, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (Ia) Rc не является водородом или -CN, и L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил. В других воплощениях Rc не является (C1-C6)алкилом, и L представляет собой -SCH2-, и Rd представляет собой метил. В других воплощениях Rc не является -CN, и L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ia) Rc не является водородом или -CN, когда L представляет собой -SCH2-, и Rd представляет собой необязательно замещенный фенил.
В некоторых воплощениях формулы (Ia) Rc не является (C1-C6)алкилом, когда L представляет собой -SCH2-, и Rd представляет собой метил.
В некоторых воплощениях формулы (Ia) Rc не является -CN, когда L представляет собой -SCH2-, и Rd представляет собой 2-фурил.
В другом воплощении соединение формулы (I) представляет собой соединение формулы (Ib)
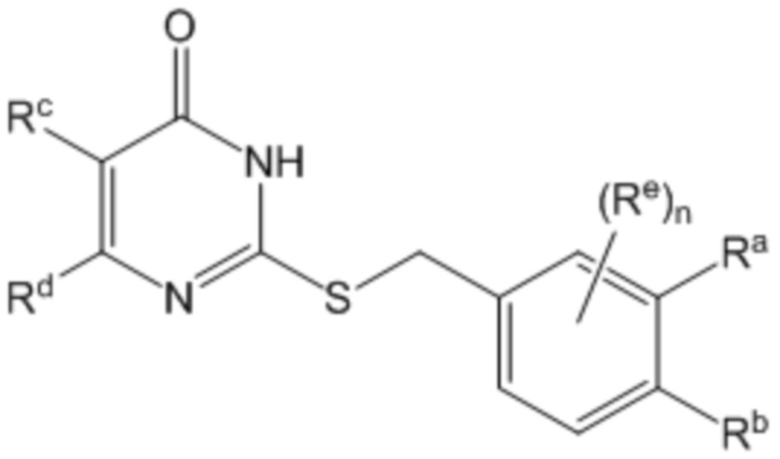 (Ib),
(Ib),
или его фармацевтически приемлемую соль,
где в указанной формуле
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил; и
n равен 0, 1, 2 или 3;
при условии, что Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ib)
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
при условии, что Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ib)
один из Ra и Rb представляет собой водород, и другой представляет собой -CO2Rx, CH2CO2Rx, тетразол или оксадиазолон; -
Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл; и
Rx представляет собой водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил; и
n равен 0, 1, 2 или 3;
при условии, что Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ib) Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Ra представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Ra представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ib) Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Rb представляет соой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Rb представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он. В других воплощениях Rb представляет собой водород.
В некоторых воплощениях формулы (Ib) Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C3)алкил. В других воплощениях Rc представляет собой H, -CN или галоген. В других воплощениях Rc представляет собой -CN или галоген.
В некоторых воплощениях формулы (Ib) Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл. В других воплощениях Rd представляет собой метил, необязательно замещенный циклогексил, необязательно замещенный пиридинил, необязательно замещенный тиазолил, необязательно замещенный фенил или необязательно замещенный тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, -OH, CN и амино. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила и (C1-C6)галогеналкокси. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими атомами галогена. В других воплощениях Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил. В еще других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил, 4-хлорфенил, 4-метилфенил или тиенил.
В некоторых воплощениях формулы (Ib) каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN. В других воплощениях Re представляет собой (C1-C4)алкил, (C2-C4)алкенил, (C2-C4)алкинил, галоген, -ORy, (C1-C4)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (Ib) Rx представляет собой водород или (C1-C6)алкил. В других воплощениях Rx представляет собой водород или (C1-C3)алкил. В других воплощениях Rx представляет собой водород, метил, этил, н-пропил или изопропил.
В некоторых воплощениях формулы (Ib) Ry представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Ry представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (Ib) каждый Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Rz представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (Ib) n равен 0, 1, 2 или 3. В других воплощениях n равен 0 или 1. В еще других воплощениях n равен 0.
В некоторых воплощениях формулы (Ib) один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ib) Rb представляет собой водород, Rc представляет собой -CN, Rd представляет собой тиенил, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (Ib) Rc представляет собой галоген, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (Ib) Rc представляет собой галоген, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой тетразол, и Rb представляет собой H.
В некоторых воплощениях формулы (Ib) Rc представляет собой галоген, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CH2CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (Ib) Rc представляет собой галоген, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (Ib) Rc представляет собой -CN, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой тетразол, и Rb представляет собой H. В еще других воплощениях Rc представляет собой -CN, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (Ib) Rc не является водородом или -CN, и Rd представляет собой необязательно замещенный фенил. В других воплощениях Rc не является (C1-C6)алкилом, и Rd представляет собой метил. В других воплощениях Rc не является -CN, и Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (Ib) Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил.
В некоторых воплощениях формулы (Ib) Rc не является (C1-C6)алкилом, когда Rd представляет собой метил.
В некоторых воплощениях формулы (Ib) Rc не является -CN, когда Rd представляет собой 2-фурил.
В другом воплощении соединение формулы (I) представляет собой соединение формулы (II)
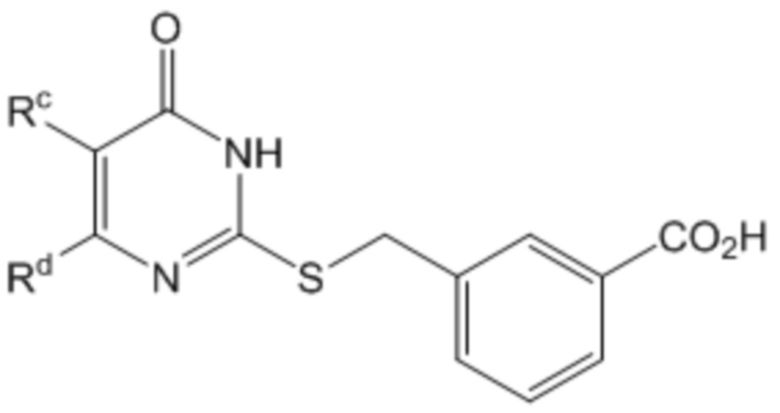 (II)
(II)
или его фармацевтически приемлемую соль,
где в указанной формуле
Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл; и
Rx представляет собой водород или (C1-C6)алкил;
при условии, что Rc не является -CN, когда Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (II) Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил; Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл; и Rx представляет собой водород или (C1-C6)алкил, при условии, что Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (II) Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C3)алкил. В других воплощениях Rc представляет собой -CN или галоген.
В некоторых воплощениях формулы (II) Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, -OH, CN и амино. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила и (C1-C6)галогеналкокси. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими атомами галогена. В других воплощениях Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил.
В некоторых воплощениях формулы (II) Rb представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он. В других воплощениях Rb представляет собой водород.
В некоторых воплощениях формулы (II) Ra представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Ra представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (II) каждый Rе представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (II) каждый Ry представляет собой независимо водород, (C1-C4)алкил или (C1-C4)галогеналкил.
В некоторых воплощениях формулы (II) каждый Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил.
В некоторых воплощениях формулы (II) n равен 0, 1, 2 или 3. В других воплощениях n равен 0 или 1. В других воплощениях n равен 0.
В некоторых воплощениях формулы (II) один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (II) Rb представляет собой водород, Rс представляет собой -CN, Rd представляет собой тиенил, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (II) Rс представляет собой галоген, Ra представляет собой -CO2H, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Br, Ra представляет собой -CO2H, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Cl, Ra представляет собой -CO2H, и Rb представляет собой Н.
В некоторых воплощениях формулы (II) Rс представляет собой галоген, Ra представляет собой тетразол, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Br, Ra представляет собой тетразол, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Cl, Ra представляет собой тетразол, и Rb представляет собой Н.
В некоторых воплощениях формулы (II) Rс представляет собой галоген, Ra представляет собой -CH2CO2H, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Br, Ra представляет собой -CH2CO2H, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Cl, Ra представляет собой -CH2CO2H, и Rb представляет собой Н.
В некоторых воплощениях формулы (II) Rс представляет собой галоген, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Br, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой Н. В других воплощениях Rс представляет собой -Cl, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой Н.
В некоторых воплощениях формулы (II) Rс представляет собой -CN, Ra представляет собой -CO2H, и Rb представляет собой Н. В других воплощениях Rс представляет собой -CN, Ra представляет собой -CH2CO2H, и Rb представляет собой Н. В других воплощениях В других воплощениях Rс представляет собой -CN, Ra представляет собой тктразол, и Rb представляет собой Н. В еще других воплощениях Rс представляет собой -CN, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой Н.
В другом воплощении соединение формулы (I) представляет собой соединение формулы (III)
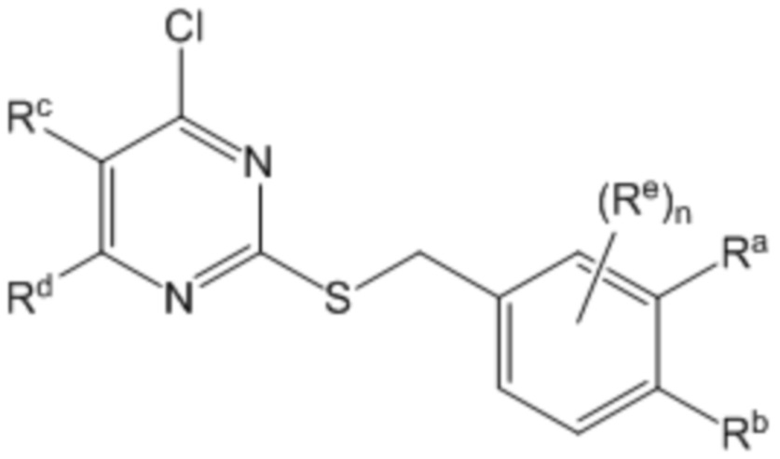 (III),
(III),
или его фармацевтически приемлемую соль,
где в указанной формуле
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил; и
n равен 0, 1, 2 или 3.
В некоторых воплощениях формулы (III)
один из Ra и Rb представляет собой водород, и другой представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил;
Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл;
каждый Rx представляет собой независимо при каждом появлении водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (III)
один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон;
Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил;
Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл; и
Rx представляет собой водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил; и
n равен 0, 1, 2 или 3;
при условии, что Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил, и что Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (III) Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Ra представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Ra представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Ra представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (III) Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, -(CH2)rтетразол, -(CH2)rоксадиазолон, -(CH2)rтетразолон, -(CH2)rтиадиазолол, -(CH2)rизоксазол-3-ол, -(CH2)rP(O)(OH)ORx, -(CH2)rS(O)2OH, -(CH2)rC(O)NHCN или -(CH2)rC(O)NHS(O)2алкил. В других воплощениях Rb представляет собой -(CH2)rCO2Rx, -OCH2CO2Rx, тетразол, -(CH2)тетразол, оксадиазолон, -(CH2)оксадиазолон, тетразолон, -(CH2)тетразолон, тиадиазолол, -(CH2)тиадиазолол, изоксазол-3-ол, -(CH2)изоксазол-3-ол, -P(O)(OH)ORx, -(CH2)P(O)(OH)ORx, -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN, -(CH2)C(O)NHCN, -C(O)NHS(O)2алкил или -(CH2)C(O)NHS(O)2алкил. В других воплощениях Rb представляет собой водород, CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, CO2H, CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он. В других воплощениях Rb представляет собой водород.
В некоторых воплощениях формулы (III) Rc представляет собой H, (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой (C1-C6)алкил, (C1-C6)галогеналкил, галоген, -CN, -ORx, CO2Rx или NO2. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C6)алкил. В других воплощениях Rc представляет собой галоген, -CN, -ORx или (C1-C3)алкил. В других воплощениях Rc представляет собой H, -CN или галоген. В других воплощениях Rc представляет собой -CN или галоген.
В некоторых воплощениях формулы (III) Rd представляет собой метил, необязательно замещенный 5-10-членный арил, необязательно замещенный 5- или 6-членный гетероарил или необязательно замещенный 5- или 6-членный карбоцикл. В других воплощениях Rd представляет собой метил, необязательно замещенный циклогексил, необязательно замещенный пиридинил, необязательно замещенный тиазолил, необязательно замещенный фенил или необязательно замещенный тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)галогеналкокси, -OH, CN и амино. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил фенил или тиенил, причем каждый необязательно замещен одним или несколькими заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкокси, (C1-C6)галогеналкила и (C1-C6)галогеналкокси. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил, причем каждый необязательно замещен одним или несколькими атомами галогена. В других воплощениях Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил. В еще других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил или тиенил. В других воплощениях Rd представляет собой циклогексил, пиридинил, тиазолил, фенил, 4-хлорфенил, 4-метилфенил или тиенил.
В некоторых воплощениях формулы (III) каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN. В других воплощениях Re представляет собой (C1-C4)алкил, (C2-C4)алкенил, (C2-C4)алкинил, галоген, -ORy, (C1-C4)галогеналкил, -NHRz, -OH или -CN.
В некоторых воплощениях формулы (III) Rx представляет собой водород или (C1-C6)алкил. В других воплощениях Rx представляет собой водород или (C1-C3)алкил. В других воплощениях Rx представляет собой водород, метил, этил, н-пропил или изопропил.
В некоторых воплощениях формулы (III) Ry представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Ry представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (III) каждый Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил. В других воплощениях Rz представляет собой водород, (C1-C3)алкил или (C1-C3)галогеналкил.
В некоторых воплощениях формулы (III) n равен 0, 1, 2 или 3. В других воплощениях n равен 0 или 1. В других воплощениях n равен 0.
В некоторых воплощениях формулы (III) один из Ra и Rb представляет собой водород, и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон. В других воплощениях Rb представляет собой водород, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (III) Rb представляет собой водород, Rc представляет собой -CN, Rd представляет собой тиенил, и Ra представляет собой CH2CO2H, тетразол или 1,2,4-оксадиазол-5(4H)-он.
В некоторых воплощениях формулы (III) Rc представляет собой галоген, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (III) Rc представляет собой галоген, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой тетразол, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой тетразол, и Rb представляет собой H.
В некоторых воплощениях формулы (III) Rc представляет собой галоген, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой -CH2CO2H, и Rb представляет собой H.
В некоторых воплощениях формулы (III) Rc представляет собой галоген, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Br, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H. В других воплощениях Rc представляет собой -Cl, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (III) Rc представляет собой -CN, Ra представляет собой -CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой -CH2CO2H, и Rb представляет собой H. В других воплощениях Rc представляет собой -CN, Ra представляет собой тетразол, и Rb представляет собой H. В еще других воплощениях Rc представляет собой -CN, Ra представляет собой 1,2,4-оксадиазол-5(4H)-он, и Rb представляет собой H.
В некоторых воплощениях формулы (III) Rc не является водородом или -CN, когда Rd представляет собой необязательно замещенный фенил, Rc не является (C1-C6)алкилом, когда Rd представляет собой метил, и Rc не является -CN, когда Rd представляет собой 2-фурил.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) один из Rа или Rb представляет собой карбоновую кислоту или биоизостеру карбоновой кислоты.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой -CO2Н, -(CH2)CO2Н или -ОCH2CO2Н. В других воплощениях Rа представляет собой -CO2СН3, -CO2CH2CН3, -CO2CH2CH2CН3, -CO2CH(CH3)2, -(CH2)CO2CH3, -(CH2)CO2CH2CH3, -(CH2)CO2CH2CH2CH3 или -(CH2)CO2CH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой -P(O)(OH)OH, -(CH2)P(O)(OH)OH, -P(O)(OH)OCH3, -P(O)(OH)OCH2CH3, -P(O)(OH)OCH2CH2CH3, -P(O)(OH)OCH(CH3)2, -(CH2) P(O)(OH)OCH3, -(CH2)P(O)(OH)OCH2CH3, -(CH2)P(O)(OH)OCH2CH2CH3 или -(CH2)P(O)(OH)OCH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN или -(CH2)C(O)NHCN.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой -C(O)NHS(O)2CH3, -C(O)NHS(O)2CH2CH3, -C(O)NHS(O)2CH2CH2CH3, -C(O)NHS(O)2CH(CH3)2, -(CH2)C(O)NHS(O)2CH3, -(CH2)C(O)NHS(O)2CH2CH3, -(CH2)C(O)NHS(O)2CH2CH2CH3 или -(CH2)C(O)NHS(O)2CH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой
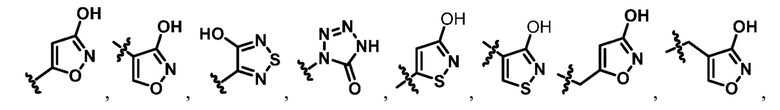
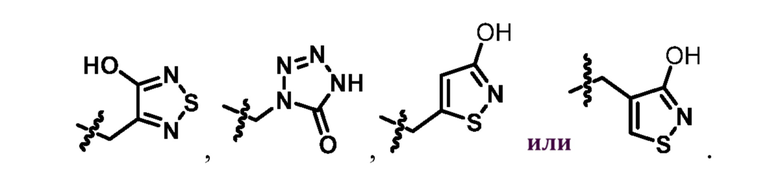 В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rа представляет собой
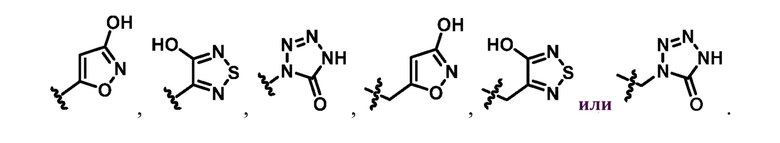 В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой -CO2Н, -(CH2)CO2Н или -ОCH2CO2Н. В других воплощениях Rb представляет собой -CO2СН3, -CO2CH2CН3, -CO2CH2CH2CН3, -CO2CH(CH3)2, -(CH2)CO2CH3, -(CH2)CO2CH2CH3, -(CH2)CO2CH2CH2CH3 или -(CH2)CO2CH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой -CO2Н, -(CH2)CO2Н или -ОCH2CO2Н. В других воплощениях Rb представляет собой -CO2СН3, -CO2CH2CН3, -CO2CH2CH2CН3, -CO2CH(CH3)2, -(CH2)CO2CH3, -(CH2)CO2CH2CH3, -(CH2)CO2CH2CH2CH3 или -(CH2)CO2CH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой -P(O)(OH)OH, -(CH2)P(O)(OH)OH, -P(O)(OH)OCH3, -P(O)(OH)OCH2CH3, -P(O)(OH)OCH2CH2CH3, -P(O)(OH)OCH(CH3)2, -(CH2) P(O)(OH)OCH3, -(CH2)P(O)(OH)OCH2CH3, -(CH2)P(O)(OH)OCH2CH2CH3 или -(CH2)P(O)(OH)OCH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой -S(O)2OH, -(CH2)S(O)2OH, -C(O)NHCN или -(CH2)C(O)NHCN.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой -C(O)NHS(O)2CH3, -C(O)NHS(O)2CH2CH3, -C(O)NHS(O)2CH2CH2CH3, -C(O)NHS(O)2CH(CH3)2, -(CH2)C(O)NHS(O)2CH3, -(CH2)C(O)NHS(O)2CH2CH3, -(CH2)C(O)NHS(O)2CH2CH2CH3 или -(CH2)C(O)NHS(O)2CH(CH3)2.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой
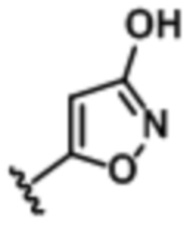 ,
,  ,
, 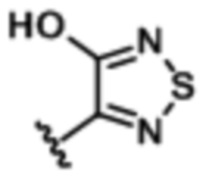 ,
,  ,
, 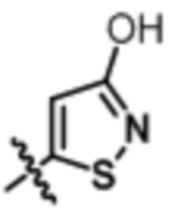 ,
, 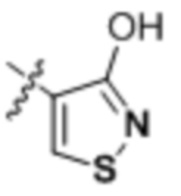 ,
, 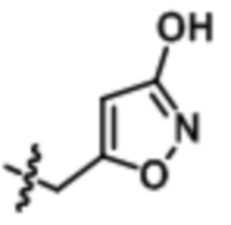 ,
,
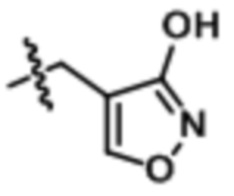 ,
, 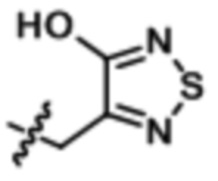 ,
, 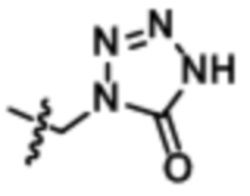 ,
, 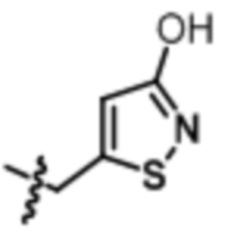 или
или 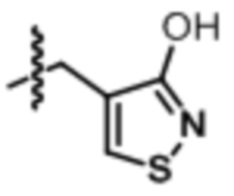 .
.
В некоторых воплощениях формулы (I), (Ib), (II) и (III) Rb представляет собой
 ,
,  ,
,  ,
,  ,
,  или
или  .
.
В некоторых воплощениях соединение формулы (I) представляет собой соединение, имеющее одну из следующих структур:


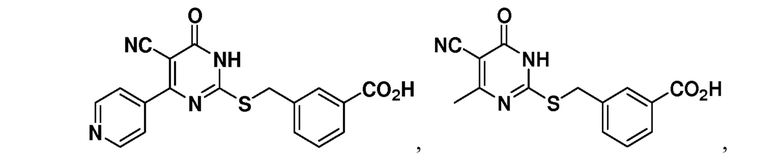

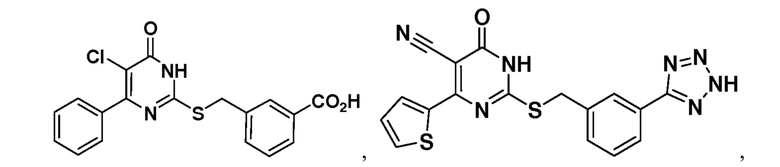

или 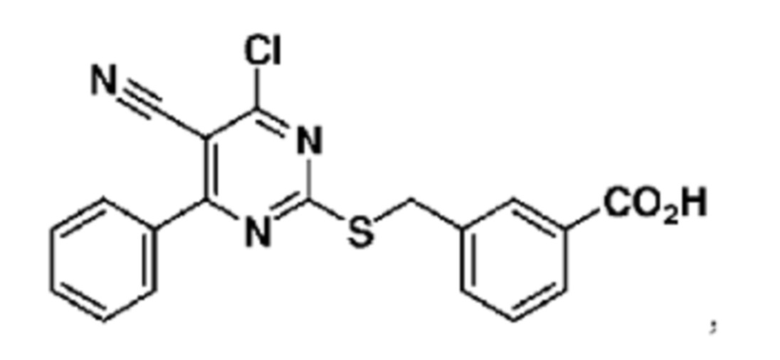 ,
,
или его фармацевтически приемлемую соль.
Приведенное выше определение соединений формулы (I) упоминается в настоящем описании как выражения «соединение формулы (I)», определенное в настоящем описании, или просто «соединения формулы (I)», и т.д. Приведенное выше определение соединений формулы (Iа) упоминается в настоящем описании как выражения «соединение формулы (Iа)», определенное в настоящем описании, или просто «соединения формулы (I)», и т.д. Приведенное выше определение соединений формулы (Ib) упоминается в настоящем описании как выражения «соединение формулы (Ib)», определенное в настоящем описании, или просто «соединения формулы (I)», и т.д. Приведенное выше определение соединений формулы (II) упоминается в настоящем описании как выражения «соединение формулы (II)», определенное в настоящем описании, или просто «соединения формулы (II)», и т.д. Приведенное выше определение соединений формулы (III) упоминается в настоящем описании как выражения «соединение формулы (III)», определенное в настоящем описании, или просто «соединения формулы (III)», и т.д. Следует иметь в виду, что предполагается, что такие упоминания охватывают не только приведенные выше формулы, но также каждое и все воплощения и т.д., обсуждаемые далее. Также следует иметь в виду, что если не указано противоположное, такие упоминания также охватывают изомеры, смеси изомеров, фармацевтически приемлемые соли, сольваты и пролекарства соединений формулы (I), формулы (Ia), формулы (Ib), формулы (II) и формулы (III).
Определения
Термин «алкил», используемый в настоящем описании, относится к насыщенной линейной или разветвленной углеводородной цепи. Углеводородная цепь предпочтительно содержит от одного до восьми атомов углерода (С1-8-алкил), предпочтительнее от одного до шести атомов углерода (С1-6-алкил), в частности, от одного до четырех атомов углерода (С1-4-алкил), включая метил, этил, пропил, изопропил, бутил, изобутил, вторичный бутил, третичный бутил, пентил, изопентил, неопентил, третичный пентил, гексил, изогексил, гептил и октил. В предпочтительном воплощении «алкил» представляет собой С1-4-алкильную группу, которая может включать, в частности, метил, этил, пропил, изопропил, бутил, изобутил, вторичный бутил и третичный бутил. Соответственно, термин «алкилен» обозначает соответствующий бирадикал (-алкил-).
Термин «циклоалкил» или «карбоцикл», используемый в настоящем описании, относится к циклической алкильной группе, предпочтительно содержащей от трех до десяти атомов углерода (С3-10-циклоалкил или С3-10-карбоцикл), например, от трех до восьми атомов углерода (С3-8-циклоалкил или С3-8-карбоцикл), предпочтительно, от трех до шести атомов углерода (С3-6-циклоалкил или С3-6-карбоцикл), включая циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Кроме того, термин «циклоалкил» используемый в настоящем описании, также может включать полициклические группы, такие как, например, бицикло[2.2.2]октил, бицикло[2.2.2]гептанил, декалинил и адамантил. Соответственно, термин «циклоалкилен» обозначает соответствующий бирадикал (-циклоалкил-). Алкильные и циклоалкильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей алкильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил, карбамоил, оксо и -CN.
Термин «алкенил», используемый в настоящем описании, относится к линейной или разветвленной углеводородной цепи или циклическим углеводородам, содержащим одну или больше двойных связей, включая диены, триены и полиены. Типично алкенильная группа включает от двух до восьми атомов углерода (С2-8-алкенил), например, от двух до шести атомов углерода (С2-6-алкенил), в частности, от двух до четырех атомов углерода (С2-4-алкенил), включающих по меньшей мере одну двойную связь. Примеры алкенильных группа включают этенил; 1- или 2-пропенил; 1-, 2- или 3-бутенил или 1,3-бутдиенил; 1-, 2-, 3-, 4- или 5-гексенил или 1,3-гексдиенил или 1,3,5-гекстриенил; 1-, 2-, 3-, 4-, 5-, 6- или 7-октенил или 1,3-октадиенил, или 1,3,5-октатриенил, или 1,3,5,7-октатетраенил, или циклогексенил. Соответственно, термин «алкенилен» обозначает соответствующий бирадикал (-алкенил-). Алкенильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей алкенильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил, карбамоил, оксо и -CN.
Термин «алкинил», используемый в настоящем описании, относится к линейной или разветвленной углеводородной цепи, содержащей одну или больше тройных связей, включая диины, триины и полиины. Типично алкинильная группа включает от двух до восьми атомов углерода (С2-8-алкинил), например, от двух до шести атомов углерода (С2-6-алкинил), в частности, от двух до четырех атомов углерода (С2-4-алкинил), включающих по меньшей мере одну тройную связь. Примеры предпочтительных алкинильных групп включают этинил; 1- или 2-пропинил; 1-, 2- или 3-бутинил или 1,3-бутдиинил; 1-, 2-, 3-, 4- или 5-гексинил или 1,3-гексдиинил или 1,3,5-гекстриинил; 1-, 2-, 3-, 4-, 5-, 6- или 7-октинил или 1,3-октдиинил, или 1,3,5-окттриинил, или 1,3,5,7-окттетраинил. Соответственно, термин «алкинилен» обозначает соответствующий бирадикал (-алкинил-). Алкинильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей алкинильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил, карбамоил, оксо и -CN.
Термины «гало» и «галоген», используемые в настоящем описании, относятся к фтору, хлору, брому или иоду. Таким образом, тригалогенметильная группа представляет собой, например, трифторметильную группу или трихлорметильную групп. Предпочтительно термины «гало» и «галоген» обозначают фтор или хлор.
Термин «галогеналкил», используемый в настоящем описании, относится к алкильной группе, определенной в настоящем описании, которая замещена один или несколько раз одним или несколькими атомами галогена. Примеры галогеналкильных групп включают, но не ограничиваются перечисленным, трифторметил, дифторметил, пентафторэтил, трихлорметил и т.д.
Термин «алкокси», используемый в настоящем описании, относится к группе «алкил-О-», где алкил имеет значения, указанные выше.
Термин «гидроксиалкил», используемый в настоящем описании, относится к алкильной группе (определенной в настоящем описании выше), которая замещена один или несколько раз гидрокси. Примеры гидроксиалкильных групп включают HO-CH2-, HO-CH2-CH2- и CH3-CH(OH)-.
Термин «окси», используемый в настоящем описании, относится к группе «-О-».
Термин «оксо», используемый в настоящем описании, относится к группе «=О».
Термин «амин», используемый в настоящем описании, относится к первичным (R-NH2, R≠H), вторичным ((R)2-NH, (R)2≠H) и третичным ((R)3-N, R≠H) аминам. Замещенный амин обозначает амин, в котором по меньшей мере один из атомов водорода заменен заместителем.
Термин «карбамоил», используемый в настоящем описании, относится группе «H2N(C=О)-».
Термин «арил», используемый в настоящем описании, если не указано иное, включает карбоциклические ароматические системы, образованные от ароматического углеводорода путем удаления атома водорода. Арил также включает би-, три- и полициклические системы. Примеры предпочтительных арильных групп включают фенил, нафтил, инденил, инданил, флуоренил, бифенил, антраценил, фенантренил, пенталенил, азуленил и бифениленил. Предпочтительный «арил» представляет собой фенил, нафтил или инденил, в частности, фенил, если не указано иное. Любой используемый арил может быть замещенным. Соответственно, термин «арилен» обозначает соответствующий бирадикал (-арил-). Арильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей арильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил и -CN.
Термин «гетероарил», используемый в настоящем описании, относится к ароматическим группам, содержащим один или несколько гетероатомов, выбранных из O, S и N, предпочтительно один-четыре гетероатома, и предпочтительнее от одного до трех гетероатомов. Гетероарил также включает би-, три- и полициклические группы, где по меньшей мере один цикл группы является ароматическим, и по меньшей мере один из циклов содержит гетероатом, выбранный из O, S и N. Гетероарил также включает циклические системы, замещенные одной или несколькими оксогруппами. Примеры предпочтительных гетероарильных групп включают N-гидрокситетразолил, N-гидрокситриазолил, N-гидроксиимидазолил, фуранил, триазолил, пиранил, тиадиазинил, бензотиофенил, дигидробензо[b]тиофенил, ксантенил, изоинданил, акридинил, бензизоксазолил, хинолинил, изохинолинил, птеридинил, азепинил, диазепинил, имидазолил, тиазолил, карбазолил, пиридинил, пиридазинил, пиримидинил, пиразолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, оксазолил, изотиазолил, пирролил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, триазинил, изоиндолил, пуринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотриазолил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил, дигидрохинолил, тетрагидрохинолил, дигидроизохинолил, тетрагидроизохинолил, бензофурил, фуропиридинил, пиролопиримидинил, азаиндолил, пиразолинил, 1,2,4-оксадиазол-5(4Н)-он и пиразолидинил. Неограничительными примерами частично гидрированных производных являются 1,2,3,4-тетрагидронафтил, 1,4-дигидронафтил и 1-окталин. Соответственно, термин «гетероарилен» обозначает соответствующий бирадикал (-гетероарил-). Гетероарильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей гетероарильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил и -CN.
Термин «гетероциклил», используемый в настоящем описании, относится к циклическим неароматическим группам, содержащим один или несколько гетероатомов, выбранных из O, S и N, предпочтительно один-четыре гетероатома, и предпочтительнее от одного до трех гетероатомов. Гетероциклил также включает би-, три- и полициклические неароматические группы, и по меньшей мере один из циклов содержит гетероатом, выбранный из O, S и N. Гетероциклил также включает циклические системы, замещенные одной или несколькими оксогруппами. Примерами гетероциклических групп являются оксетан, пирролидинил, пирролил, 3Н-пирролил, оксоланил, фуранил, тиоланил, тиофенил, пиразолил, пиразолидинил, имидазолил, имидазолидинил, 3Н-пиразолил, 1,2-оксазолил, 1,3-оксазолил, 1,2-тиазолил, 1,3-тиазолил, 1,2,5-оксадиазолил, пиперидинил, пиридинил, оксанил, 2-Н-пиранил, 4-Н-пиранил, тианил, 2Н-тиопиранил, пиридазинил, 1,2-диазинанил, пиримидинил, 1,3-диазинанил, пиразинил, пиперазинил, 1,4-диксинил, 1,4-диксанил, 1,4-оксазинил, морфолинил, тиоморфолинил, 1,4-оксатианил, бензофуранил, изобензофуранил, индазолил, бензимидазолил, хинолинил, изохинолинил, изохроманил, 4Н-хроменил, 1Н-изохроменил, циннолинил, хиназолинил, хиноксалинил, фталазинил, пуринил, нафтиридинил, птеридинил, индолизинил, 1Н-пирролизинил, 4Н-хинолизинил и аза-8-бицикло[3.2.1]октан. Соответственно, термин «гетероциклилен» обозначает соответствующий бирадикал (-гетероциклил-). Гетероциклильные группы могут быть необязательно замещены 1-4 заместителями. Примеры заместителей гетероциклильных групп включают, но не ограничиваются перечисленным, алкил, алкенил, алкинил, галоген, галогеналкил, алкокси, гетероарил, арил, карбоциклил, гидроксил и -CN.
Термин «N-гетероцикл», используемый в настоящем описании, относится к гетероциклилу или гетероарилу, определенным выше, имеющим по меньшей мере один атом азота и связывающимся через атом азота. Примерами таких N-гетероциклилов являются пирролидинил, пирролил, 3Н-пирролил, пиразолил, пиразолидинил, имидазолил, имидазолидинил, 3Н-пиразолил, 1,2-оксазолил, 1,2-тиазолил, 1,3-тиазолил, пиперидинил, пиридинил, пиридазинил, пиразинил, пиперазинил, морфолинил, пиримидинил, тетразолил и т.д.
Изомеры
В настоящем описании структурная формула соединения в некоторых случаях для удобства представляет определенный изомер, но настоящее раскрытие включает все изомеры, такие как геометрические изомеры, оптические изомеры на основе асимметричного углерода, стереоизомеры, таутомеры и т.п. Соответственно, следует иметь в виду, что определение соединений формул (I), (Ia), (Ib), (II) и (III) включает каждый и все отдельные изомеры, соответствующие формулам (I), (Ia), (Ib), (II) и (III), включая цис-транс-изомеры, стереоизомеры и таутомеры, а также их рацемические смеси и их фармацевтически приемлемые соли. Следовательно, также предполагается, что определение соединений формул (I), (Ia), (Ib), (II) и (III) охватывает все R- и S-изомеры химической структуры в любом соотношении, например, при обогащении (т.е. энантиомерном избытке или диастереомерном избытке) одного из возможных изомеров и соответствующих меньших долях других изомеров. Кроме того, в случае соединений, представленных формулами (I), (Ia), (Ib), (II) и (III), может иметь место кристаллический полиморфизм. Отмечается, что любая кристаллическая форма, смесь кристаллических форм или их ангидриды или гидраты включены в объем настоящего раскрытия. Кроме того, в объем настоящего раскрытия включен так называемый метаболит, который образуется путем разрушения соединения по настоящему изобретению in vivo.
«Изомеризм» обозначает соединения, которые имеют идентичные молекулярные формулы, но различаются последовательностью их атомов или расположением их атомов в пространстве. Изомеры, которые различаются расположением их атомов в пространстве, называются «стереоизомерами». Стереоизомеры, которые не являются зеркальными изображениями друг друга, называются «диастереомерами», и стереоизомеры, которые являются несовмещаемыми зеркальными изображениями друг друга, называются «энантиомерами» или иногда оптическими изомерами. Смесь, содержащая равные количества отдельных энантиомерных форм противоположной хиральности, называется «рацемической смесью».
Атом углерода, связанный с четырьмя неидентичными заместителями, называется «хиральным центром».
«Хиральный изомер» обозначает соединение по меньшей мере с одним хиральным центром. Соединения с более чем одним хиральным центром могут существовать или как отдельные диастереомеры или как смесь диастереомеров, называемая «диастереомерной смесью». Когда присутствует один хиральный центр, стереоизомер можно характеризовать абсолютной конфигурацией (R или S) такого хирального центра. Абсолютная конфигурация относится к расположению в пространстве заместителей, присоединенных к хиральному центру. При рассмотрении заместители, присоединенные к хиральному центру, классифицируют согласно правилу последовательностей Кана, Ингольда и Прелога (Cahn et al., Angew. Chem. Inter. Edit., 1966, 5, 385; errata 511; Cahn et al., Angew. Chem., 1966, 78, 413; Cahn and Ingold, J. Chem. Soc., 1951 (London), 612; Cahn et al., Experientia, 1956, 12, 81; Cahn, J. Chem. Educ., 1964, 41, 116).
Диастереомеры, т.е. несовмещаемые стереохимические изомеры, можно разделить обычными способами, такими как хроматография, перегонка, кристаллизация или сублимация. Оптические изомеры можно получить путем расщепления рацемических смесей согласно обычным способам, например, путем образования диастереомерных солей путем обработки оптически активной кислотой или основанием. Примеры соответствующих кислот включают, без ограничения, винную, диацетилвинную, дибензоилвинную, дитолуоилвинную и камфорсульфоновую кислоту. Смесь диастереомеров можно разделить кристаллизаций с последующим освобождением оптически активных оснований из таких солей. Альтернативный способ разделения оптических изомеров включает использование колонки для хиральной хроматографии, оптимально выбранной для максимального разделения энантиомеров. Еще один доступный способ включает синтез ковалентных диастереоизомерных молекул путем взаимодействия соединений формулы (I), (Ia), (Ib), (II) или (III) с оптически чистой кислотой в активированной форме или оптически чистым изоцианатом. Синтезированные диастереоизомеры можно разделить обычными способами, такими как хроматография перегонка, кристаллизация или сублимация, и затем гидролизовать и получить энантиомерно чистое соединение. Оптически активные соединения формул (I), (Ia), (Ib), (II) и (III) можно получить подобным образом, используя оптически активные исходные материалы и/или используя хиральный катализатор. Такие изомеры могут быть в форме свободной кислоты, свободного основания, сложного эфира или соли. Примеры методов хирального разделения приводятся в Chiral Separation Techniques, A Practical Approach, 2nd ed. by G. Subramanian, Wiley-VCH, 2001.
«Геометрический изомер» обозначает диастереомеры, которые обязаны своим существованием затрудненному вращению вокруг двойных связей. Такие конфигурации различаются в их названиях префиксами цис и транс или Z и E, которые показывают, что группы находятся с одной и той же или противоположных сторон двойной связи в молекуле согласно правилам Кана-Ингольда-Прелога.
Кроме того, структуры и другие соединения, обсуждаемые в настоящем раскрытии, включают все их атропические изомеры. «Атропические изомеры» представляют собой тип стереоизомеров, в которых атомы двух изомеров по-разному располагаются в пространстве. Атропические изомеры обязаны своим существованием ограниченному вращению, вызванному затруднением вращения крупных групп вокруг центральной связи. Такие атропические изомеры типично существуют в виде смеси, однако в результате последних достижений в хроматографических методах в отдельных случаях возможно разделение смесей двух атропических изомеров.
«Таутомер» является одним из двух или большего числа структурных изомеров, которые существуют в равновесии и легко превращаются из одной изомерной формы в другую. Такое превращение приводит к кажущейся миграции атома водорода, сопровождаемой смещением соседних конъюгированных двойных связей. Таутомеры существуют в растворе в виде смеси таутомерного набора. В твердой форме, как правило, преобладает один из таутомеров. В растворах, где таутомеризация возможна, будет достигаться химическое равновесие таутомеров. Точное соотношение таутомеров зависит от нескольких факторов, включая температуру, растворитель и рН. Концепция таутомеров, которые взаимопревращаются путем таутомеризации, называется таутомеризмом.
Из различных типов таутомеризма, которые возможны, обычно наблюдают два. При кето-енольном таутомеризме происходит одновременный сдвиг электронов и атома водорода. Цикло-цепной таутомеризм возникает в результате взаимодействия альдегидной группы (-СНО) в молекуле с цепью сахара с одной или несколькими гидроксильными группами (-ОН) в той же молекуле с образованием ее циклической (в форме кольца) формы, которую показывает глюкоза.
Обычными таутомерными парами являются кетон-енол, амид-нитрил, лактам-лактим, таутомеризм амид-имидокислота в гетероциклах (например, в нуклеиновых основаниях, таких как гуанин, тимин и цитозин), амин-енамин и енамин-енамин. Следует представлять, что соединения по настоящему раскрытию можно изобразить в виде различных таутомеров. Также следует иметь в виду, что когда соединения имеют таутомерные формы, предполагается, что все таутомерные формы включены в объем настоящего раскрытия, и названия соединений не исключают никакую таутомерную форму.
Термины «кристаллические полиморфы», «полиморфы» или «кристаллические формы» обозначают кристаллические структуры, в которых соединение (или его соль или сольват) может кристаллизоваться в различных кристаллических упаковках, которые все имеют один и тот же элементный состав. Различные кристаллические формы обычно имеют различные рентгеновские дифракционные картины, инфракрасные спектры, температуры плавления, плотность, твердость, форму кристаллов, оптические и электрические свойства, устойчивость и растворимость. Растворитель для перекристаллизации, скорость кристаллизации, температура хранения и другие факторы могут вызвать преобладание одной кристаллической формы. Кристаллические полиморфы соединений можно получить кристаллизацией в различных условиях.
Кроме того, соединения по настоящему раскрытию, например, соли соединений, могут существовать в гидратированной или негидратированной (безводной) форме или в виде сольватов с молекулами других растворителей. Неограничительные примеры гидратов включают моногидраты, дигидраты и т.д. Неограничительные примеры сольватов включают сольваты этанола, сольваты ацетона и т.д.
«Сольват» обозначает формы присоединения растворителей, которые содержат стехиометрические или нестехиометрические количества растворителя. Некоторые соединения имеют склонность захватывать молекулы растворителя в фиксированном молярном отношении в кристаллическом твердом состоянии, образуя таким образом сольват. Если растворителем является вода, образованный сольват представляет собой гидрат; и если растворителем является спирт, образованный сольват представляет собой алкоголят. Гидраты образуются путем объединения одной или нескольких молекул воды с одной молекулой вещества, в котором вода сохраняет свое молекулярное состояние как Н2О.
Предполагается, что настоящее раскрытие включает все изотопы атомов, встречающихся в соединениях по настоящему изобретению. Изотопы включают атомы, имеющие один и тот же атомный номер, но различные массовые числа. Как общий пример и без ограничения, изотопы водорода включают тритий и дейтерий, и изотопы углерода включают С-13 и С-14.
В описании и формуле изобретения слова «включать» и «содержать» и вариации слов, например, «включающий» и «включает», означают «включая, но не ограничиваясь» и не исключают другие группы, добавки, компоненты, целые числа или стадии. В описании и формуле изобретения единственное число включает множественное, если контекст не требует иного. В частности, при использовании неопределенного артикля описание следует понимать как рассматривающее множественную форму, а также единственную форму, если контекст не требует иного.
Все ссылки, включая любой патент или заявку на патент, цитированные в настоящем описании, включены в настоящее описание в качестве ссылок. Не делается допущение, что какая-то ссылка составляет уровень техники. Также не делается допущение, что что-то из уровня техники составляет часть общего знания в технике.
Способ лечения
В другом аспекте настоящее раскрытие относится к способу лечения заболевания или расстройства, в котором играет роль α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилаза (ACMSD), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В другом аспекте настоящее раскрытие относится к способу предупреждения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В еще одном аспекте настоящее раскрытие относится к способу снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу уменьшения интенсивности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В другом аспекте настоящее раскрытие относится к способу лечения заболевания или расстройства, в котором играет роль модуляция никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу предупреждения заболевания или расстройства, в котором играет роль модуляция никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В другом аспекте настоящее раскрытие относится к способу снижения опасности заболевания или расстройства, в котором играет роль модуляция никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу уменьшения интенсивности заболевания или расстройства, в котором играет роль модуляция никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В другом аспекте настоящее раскрытие относится к способу лечения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Настоящее раскрытие также относится к способу предупреждения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
В другом аспекте настоящее раскрытие относится к способу уменьшения интенсивности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающему введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей.
Другой аспект настоящего раскрытия относится к способу лечения расстройства, связанного с митохондриальной дисфункцией, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей. В одном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой наследственное митохондриальное заболевание, обыкновенное метаболическое расстройство, нейродегенеративное заболевание, расстройство, связанное со старением, почечное расстройство или хроническое воспалительное заболевание. В предпочтительном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой обыкновенное метаболическое расстройство, такое как ожирение или диабет типа II.
В другом аспекте настоящее раскрытие относится к способу предупреждения расстройства, связанного с митохондриальной дисфункцией, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей. В одном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой наследственное митохондриальное заболевание, обыкновенное метаболическое расстройство, нейродегенеративное заболевание, расстройство, связанное со старением, почечное расстройство или хроническое воспалительное заболевание. В предпочтительном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой обыкновенное метаболическое расстройство, такое как ожирение или диабет типа II.
Другой аспект настоящего раскрытия относится к способу снижения опасности расстройства, связанного с митохондриальной дисфункцией, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей. В одном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой наследственное митохондриальное заболевание, обыкновенное метаболическое расстройство, нейродегенеративное заболевание, расстройство, связанное со старением, почечное расстройство или хроническое воспалительное заболевание. В предпочтительном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой обыкновенное метаболическое расстройство, такое как ожирение или диабет типа II.
Другой аспект настоящего раскрытия относится к способу уменьшения интенсивности расстройства, связанного с митохондриальной дисфункцией, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей. В одном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой наследственное митохондриальное заболевание, обыкновенное метаболическое расстройство, нейродегенеративное заболевание, расстройство, связанное со старением, почечное расстройство или хроническое воспалительное заболевание. В предпочтительном воплощении расстройство, связанное с митохондриальной дисфункцией, представляет собой обыкновенное метаболическое расстройство, такое как ожирение или диабет типа II.
В другом аспекте настоящее раскрытие относится к способу промотирования окислительного метаболизма, включающему введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества одного или нескольких соединений формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей, что повышает внутриклеточный никотинамидадениндинуклеотид (NAD+).
В еще одном аспекте настоящее расстройство относится к способу изготовления лекарственного средства для лечения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Другой аспект настоящего раскрытия относится к способу изготовления лекарственного средства для предупреждения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В другом аспекте настоящее раскрытие относится к способу изготовления лекарственного средства для снижения опасности заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В еще одном аспекте настоящее раскрытие относится к способу изготовления лекарственного средства для уменьшения интенсивности заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В другом аспекте настоящее раскрытие относится к фармацевтической композиции для применения в способе лечения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В другом аспекте настоящее раскрытие относится к фармацевтической композиции для применения в способе предупреждения заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В другом аспекте настоящее раскрытие относится к фармацевтической композиции для применения в способе снижения опасности заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Другой аспект настоящего раскрытия относится к фармацевтической композиции для применения в способе уменьшения интенсивности заболевания или состояния, опосредуемого ACMSD, причем лекарственное средство включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В еще одном аспекте настоящее раскрытие относится к соединению для применения в способе лечения заболевания или состояния, опосредуемого ACMSD, причем соединение включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Другой аспект настоящего раскрытия относится к соединению для применения в способе предупреждения заболевания или состояния, опосредуемого ACMSD, причем соединение включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
В другом аспекте настоящее раскрытие относится к соединению для применения в способе снижения опасности заболевания или состояния, опосредуемого ACMSD, причем соединение включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Другой аспект настоящего раскрытия относится к соединению для применения в способе уменьшения интенсивности заболевания или состояния, опосредуемого ACMSD, причем соединение включает соединение формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для предупреждения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для уменьшения интенсивности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для предупреждения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для уменьшения интенсивности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для предупреждения расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для снижения опасности расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для уменьшения интенсивности расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к применению соединения формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли при изготовлении лекарственного средства для промотирования окислительного метаболизма.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при изготовлении лекарственного средства для лечения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при изготовлении лекарственного средства для предупреждения заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при изготовлении лекарственного средства для снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при изготовлении лекарственного средства для уменьшения интенсивности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для предупреждения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для уменьшения интенсивности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для лечения расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для предупреждения расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для снижения опасности расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для уменьшения интенсивности расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения в качестве лекарственного средства для промотирования окислительного метаболизма.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при лечении, предупреждении или снижении опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при лечении заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при предупреждении заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при снижении опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при уменьшении интенсивности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при лечении, предупреждении или снижении опасности расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при лечении расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при предупреждении расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при снижения опасности расстройства, связанного с митохондриальной дисфункцией.
В другом аспекте настоящее раскрытие относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при уменьшении интенсивности расстройства, связанного с митохондриальной дисфункцией.
Другой аспект настоящего раскрытия относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли для применения при промотировании окислительного метаболизма.
В другом аспекте настоящее раскрытие относится к способу лечения, предупреждения, уменьшения интенсивности или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения, имеющего следующие формулы:










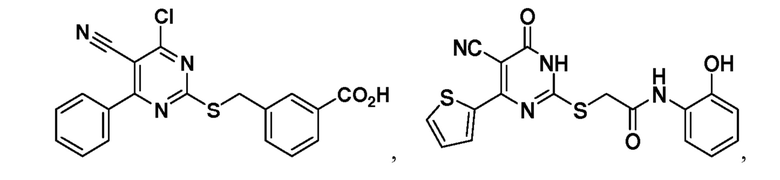
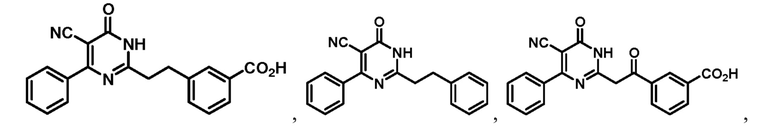
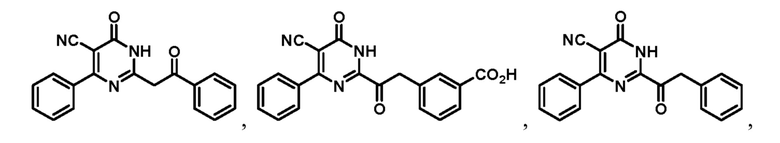
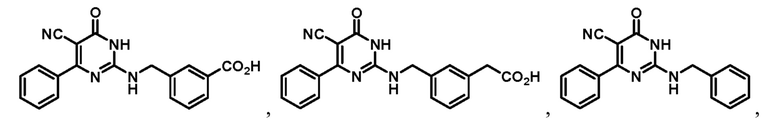
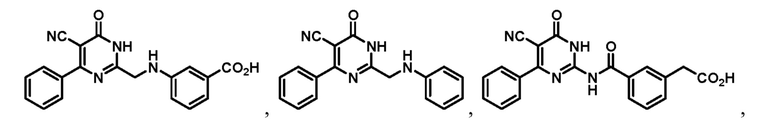
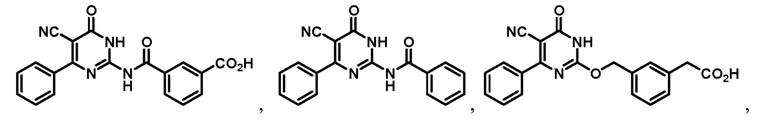
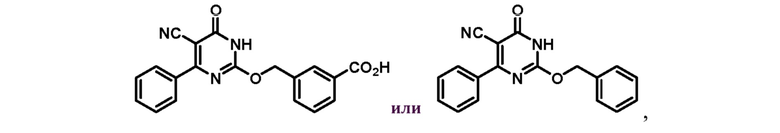
или его фармацевтически приемлемой соли.
В другом аспекте настоящее раскрытие относится к способу лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения, имеющего следующие формулы:











или его фармацевтически приемлемой соли.
Следовательно, раскрытие также относится к соединению формулы (I), формулы (Iа), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли, описанных в настоящем описании, для применения в качестве лекарственного средства.
Другой аспект настоящего раскрытия относится к применению соединения, имеющего одну из следующих формул:

















или его фармацевтически приемлемой соли при изготовлении лекарственного средства для лечения, предупреждения, уменьшения интенсивности или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к применению соединения, имеющего одну из следующих формул:











или его фармацевтически приемлемой соли
при изготовлении лекарственного средства для лечения, предупреждения, уменьшения интенсивности или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению, имеющему одну из следующих формул:

















или его фармацевтически приемлемой соли
для применения в качестве лекарственного средства для лечения, предупреждения, уменьшения интенсивности или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению, имеющему одну из следующих формул:











или его фармацевтически приемлемой соли
для применения в качестве лекарственного средства для лечения, предупреждения, уменьшения интенсивности или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
Другой аспект настоящего раскрытия относится к соединению, имеющему одну из следующих формул:

















или его фармацевтически приемлемой соли
для применения при лечении, предупреждении, уменьшении интенсивности или снижении опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
В другом аспекте настоящее раскрытие относится к соединению, имеющему одну из следующих формул:











или его фармацевтически приемлемой соли
для применения при лечении, предупреждении, уменьшении интенсивности или снижении опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
При использовании в настоящем описании «лечение» или «лечить» описывает оказание помощи и наблюдения за пациентом с целью изменения направления, ингибирования или борьбы с заболеванием, состоянием или расстройством, и включает введение соединения по настоящему раскрытию (т.е. соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III)) или его фармацевтически приемлемой соли, пролекарства, метаболита, полиморфа или сольвата для реверсии заболевания, состояния или расстройства.
Соединение по настоящему раскрытию (т.е. соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III)) или его фармацевтически приемлемую соль, пролекарство, метаболит, полиморф или сольват также можно использовать для предупреждения заболевания, состояния или расстройства. При использовании в настоящем описании «предупреждение» или «предупреждать» описывает ослабление или устранение начала симптомов или осложнений заболевания, состояния или расстройства.
Соединение по настоящему раскрытию (т.е. соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III)) или его фармацевтически приемлемую соль, пролекарство, метаболит, полиморф или сольват также можно использовать для уменьшения интенсивности одного или нескольких симптомов заболевания, состояния или расстройства. При использовании в настоящем описании «уменьшение интенсивности» предназначено для описания процесса, с помощью которого снижается тяжесть признака или симптома расстройства. Что важно, признак или симптом может быть ослаблен без устранения. Предпочтительно лечение является куративным или уменьшающим интенсивность.
Способы получения соединений формул (I), (Ia), (Ib), (II) и (III)
Соединения по настоящему раскрытию (например, соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) и формулы (III)) можно получить многими путями, хорошо известными специалистам в области органического синтеза. Как пример, соединения по настоящему раскрытию можно синтезировать с использованием способов, описанных ниже, вместе со способами синтеза, известными в области синтетической органической химии, или их вариантов, признанных специалистами в данной области техники. Предпочтительные способы включают, но не ограничиваются перечисленным, способы, описанные ниже. Конечные продукты реакций, описанных в настоящем описании, можно выделить обычными методами, например, экстракцией, кристаллизацией, перегонкой, хроматографией и т.д.
Соединения по настоящему раскрытию можно синтезировать, следуя стадиям, отображенным на общих схемах А-Е, которые включают различную последовательность «сборки» промежуточных соединений Ia-Ih и Ij-Io. Исходные материалы или являются коммерчески доступными или получают известными процедурами, описанными в литературе или которые поясняются. Применимые стадии, которые можно использовать на стадиях получения соединений, будут известны специалистам в данной области техники. Ниже приводится способ как пример, не являющийся ограничивающим, или как можно получить соединения.
Общая схема А
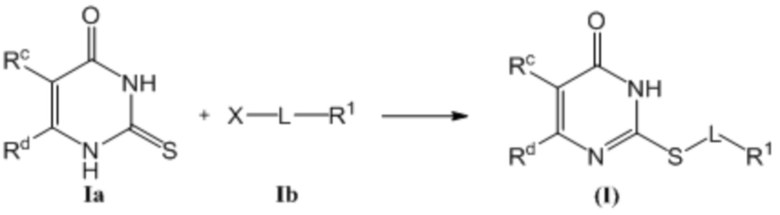 ,
,
где R1, Rc и Rd имеют значения, указанные для формулы (I).
Общий путь получения соединений формулы (I) с использованием промежуточных соединений Ia и Ib, отображен на общей схеме А. Сочетание Ia с Ib с использованием основания, т.е. карбоната калия (К2СО3), в растворителе, т.е. ацетонитриле (CH3CN), необязательно при повышенной температуре дает нужный продукт формулы (I). Основания, которые можно использовать, включают, но не ограничиваются перечисленным, карбонат натрия (Na2CO3), карбонат калия (К2СО3), N,N-диизопропилэтиламин (DIPEA) и триэтиламин. Растворители, используемые в реакции сочетания, могут представлять собой полярные или неполярные растворители. Например, растворитель может представлять собой ацетонитрил (CH3CN), ацетон или диметилсульфоксид (ДМСО).
Общая схема В
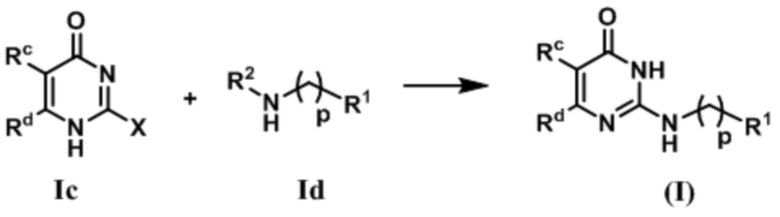 ,
,
где Х представляет собой легко удаляемую группу, т.е. Cl, Br, -SCH3 или S(O)2CH3, и R1, R2, Rc, Rd и р имеют значения, указанные для формулы (I).
С другой стороны, соединения формулы (I) можно получить с использованием промежуточных соединений Iс и Id, как отображено на общей схеме В. Аминирование промежуточного соединения Iс с помощью Id с использованием основания, т.е. гидроксида натрия (NaOH), гидроксида калия (КОН) и т.д. в растворителе, т.е. метаноле (МеОН), этаноле (EtOH), воде (Н2О) и т.д., дает соединения формулы (I).
Общая схема С
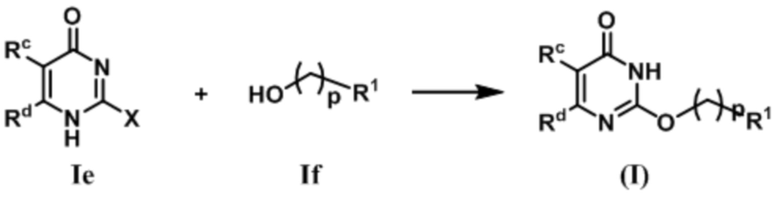 ,
,
где Х представляет собой легко удаляемую группу, т.е. Cl, Br, -SCH3 или S(O)2CH3, и R1, R2, Rc, Rd и р имеют значения, указанные для формулы (I).
Соединения формулы (I) также можно получить с использованием промежуточных соединений Iе и If, как отображено на общей схеме C. Аминирование промежуточного соединения Ie с If с использованием основания, т.е. гидроксида натрия (NaOH), гидроксида калия (КОН) и т.д. в растворителе, т.е. метаноле (МеОН), этаноле (EtOH), воде (Н2О) и т.д., дает соединения формулы (I).
Общая схема D
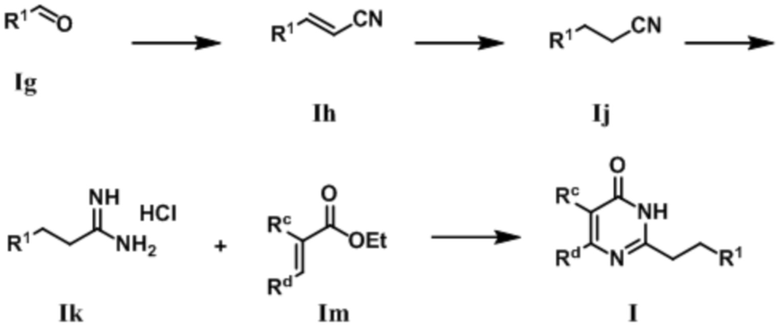
где R1, Rc и Rd имеют значения, указанные для формулы (I).
С другой стороны, соединения формулы (I) также можно получить с использованием промежуточных соединений Ig, Ih, Ij, Ik и Im, как отображено на общей схеме D. Олефинирование промежуточного соединения Ig с использованием основания, т.е. карбоната калия (К2СО3), и диэтил(цианометил)фосфоната в растворителе, т.е. тетрагидрофуране (ТГФ), воде (Н2О), необязательно при повышенной температуре дает промежуточное соединение Ih. Гидрирование Ih с использованием металлического катализатора, т.е. палладия на угле (Pd/C), диоксида платины (PtO2) и т.д., и газа водорода (Н2) в растворителе, т.е. этаноле (EtOH) и/или тетрагидрофуране (ТГФ), дает промежуточное соединение Ij. Промежуточное соединение Ik получают путем обработки промежуточного соединения Ij кислотой, т.е. хлороводородной кислотой (HCl) в растворителе, т.е. этаноле (EtOH), дихлорметане (CH2Cl2) и т.д., и затем последующей обработки основанием, т.е. аммиаком (NH3). Циклизация промежуточного соединения Ik и Im с использованием основания, т.е. гидроксида натрия (NaOH), гидроксида калия (КОН) и т.д., в растворителе, т.е. диметилацетамиде (DMA), необязательно при повышенной температуре дает соединения формулы (I).
Общая схема Е
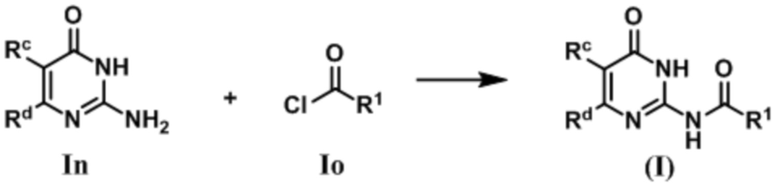 ,
,
где R1, Rc и Rd имеют значения, указанные для формулы (I).
С другой стороны, соединения формулы (I) можно получить с использованием промежуточных соединений In и Io, как отображено на общей схеме E. Ацилирование промежуточного соединения In с помощью Io с использованием основания, т.е. гидроксида натрия (NaOH), гидроксида калия (КОН) и т.д., в растворителе, т.е. метаноле (МеОН), этаноле (EtOH), воде (Н2О) и т.д., дает соединения формулы (I).
Смесь энантиомеров, диастереомеров, цис/транс-изомеров, образующаяся в процессе, описанном выше, можно разделить на ее отдельные компоненты методом с хиральной солью, хроматографией с использованием нормальной фазы, обращенной фазы или хиральной колонки, в зависимости от характера разделения.
Следует иметь в виду, что в описании и формулах, показанных выше, различные группы R1, R2, X, L, Y, Ra, Rb, Rc, Rd, Re, Rf, Rx, Ry, Rz, m, n, p, q, r и другие переменные определены в настоящем описании выше, за исключением случаев, где указано иное. Кроме того, для целей синтеза, соединения на общих схемах 1 и 2 с выбранными радикалами более характерны для пояснения общей методологии синтеза соединений формулы (I), определенной выше.
Биологические анализы и исследования на животных
Способ скрининга ингибирования ACMSD1
Активность соединений как ингибиторов ACMSD1 определяют спектрофотометрическим анализом in vitro. Предварительную смесь для анализа инкубируют, и затем добавляют соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль и раствор ACMSD1. Влияние концентрации ACMS на ферментативную активность исследуют, изменяя концентрацию 3-гидроксиантраниловой кислоты (3ОН-НА) в предварительной смеси для анализа. Кинетические параметры вычисляют из данных по начальной скорости с использованием графика Лайнуивера-Бэрка.
Методы клеточного анализа
Линии мышиных гепатоцитов выращивают и высевают на чашки. Клетки поддерживают в культуре при 37°С, и как только клетки прикрепляются, добавляют различные концентрации соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли или ДМСО. Первичные гепатоциты харвестируют примерно 24 часами позже.
Определение модуляции ACMSD-1 в клетках НЕК293Т
Клетки НЕК293Т высевают и трансфицируют для временной экспрессии ACMSD. Затем клетки стимулируют различными концентрациями соединения 1 и затем лизируют для измерения активности ACMSD спектрофотометрическим анализом in vitro. Количество всего белка в клеточных лизатах детектируют анализом Бредфорда и используют для вычисления специфической активности фермента, нормализованного во всех образцах.
Определение содержания NAD+ в первичных гепатоцитах человека
Первичные гепатоциты после посева обрабатывают различными концентрациями соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли или МЕНР (контроль). Соединение заменяют каждые 24 часа, и затем клетки непосредственно харвестируют и лизируют для детекции содержания NAD+ с помощью ЖХ-МС/МС (жидкостная хроматография-масс-спектрометрия/масс-спектроскопия).
Модуляция активности SOD2 в клетках AML12 и мышиных первичных гепатоцитах
Первичные гепатоциты или клетки AML-12 лизируют, и определяют общую концентрацию белка с использованием анализа Бредфорда. Активность SOD2 определяют в указанное время после обработки соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью с использованием набора для анализа SOD Assay Kit. Определяют поглощение, и результаты выражают в Е/мл/мг белка согласно стандартной кривой и измеренной концентрации белка.
Определение содержания NAD+ в мышиных первичных гепатоцитах
NAD+ экстрагируют с использованием метода кислотной экстракции, и образцы собирают и гомогенизируют. После осаждения нерастворимых белковых частей образцы разделяют высокоэффективной жидкостной хроматографией (ВЭЖХ) и анализируют масс-спектрометрией. Белки в осадке определяют количественно анализом Бредфорда и используют для нормализации.
Получение РНК и анализ RT-qPCR ACMSD и SIRT1-регулированных генов в клетках
Клетки (AML-12, Hepa-1.6, НЕК-293, первичные гапатоциты человека и мыши) обрабатывают различными концентрациями соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли, и определяют экспрессию генов ACMSD, Pgc1a, Sod1 и Sod2 (MnSOD) с использованием RT-qPCR. Всю РНК экстрагируют из клеток, и экстрагированную РНК обрабатывают ДНКазой и используют для обратной транскрипции (RT).
Модуляция активности каспазы 3/7 в клетках MDCK
Клетки MDCK культивируют в базальной среде до конечной концентрации 10%. Клетки высевают в 96 лунок, и после 24-часового культивирования среду заменяют свежей средой с добавлением 1% FBS. Затем используют цисплатин для индукции повреждения клеток. Различные концентрации соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли (в ДМСО) добавляют в комбинации с цисплатином или перед добавлением цисплатина. Активность каспазы 3/7 (Promega) определяют согласно стандартной процедуре с использованием считывания люминесцентного сигнала на планшет-ридере. Каждый эксперимент/условие выполняют в трехкратном повторении. Активность каспазы анализируют как действие в процентах, нормализованное к одному цисплатину и клеткам, обработанным средой.
Цитотоксичность и скрининг hERG
Клетки НеРG2 и AML-12 высевают, и определяют зависимость реакции от дозы соединения при различных концентрациях. Клетки стимулируют, и супернатант используют для высвобождения LDH как меры некроза, в то время как клетки лизируют для детекции уровней АТФ для определения жизнеспособности клеток.
Набор Predictor hERG assay устойчиво трансфицируют калиевым каналом hERG и высокоаффинным красным флуоресцентным лигандом каналов hERG и используют для определения аффиности связывания каналов hERG соединений формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемых солей. Соединения, которые связываются с белком канала hERG (конкуренты), идентифицируют по их способности заменять индикатор, что приводит к более низкой поляризации флуоресценции.
Эксперименты с C.elegans - сайленсинг ACMSD1, анализы продолжительности жизни, оценка мобильности и количественное определение GFP
Сайленсинг ACMSD1. Бактериальные эксперименты с питанием РНКи для определения влияния отрицательной регуляции или сайленсинга acmsd-1 на экспрессию генов и выживаемость осуществляют на нематоде Caenorhabditis elegans (C. elegans). Клонами, используемыми для экспериментов с питанием, являются acmsd-1, SIR-2.1 и DAF-16. Всю РНК экстрагируют из клеток, и экстрагированную РНК обрабатывают ДНКазой и используют для обратной транскрипции (RT).
Червей выращивают на агаровых пластинах NGM, дополнительно содержащих карбенициллин и IPTG, и высевают с бактериальными культурами. После обработки РНКи червей переносят на чашки, содержащие паракват, и высевают с бактерями с РНКи. Контрольных животных выращивают на бактериях с РНКи, содержащих пустой вектор (контроль), и затем переносят на чашки, содержащие паракват, и высевают с бактериями с РНКи. Выполняют количественное определение экспрессии гена sod-3 при уровнях мРНК и уровнях белка с использованием RT-qPCR и анализы на выживаемость. Движение червей регистрируют в дни 1, 3 и 5 взрослого состояния.
Исследование противодиабетического действия на мышах С57BL/6J и КК-Ау
Мышам дают правильный рацион или рацион с высоким содержанием жира (HFD). Соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль дают ежедневно, и берут кровь и ткани для выделения РНК, измерения липидов и гистологии. Измеряют потребление кислорода, и выполняют гистологический анализ и трансмиссионную электронную микроскопию. Также выполняют тест на пероральную переносимость глюкозы и интраперитонеальный тест толерантности к инсулину для количественного определения глюкозы и измерения концентраций инсулина в плазме.
Исследование противодиабетического действия и действия против ожирения на мышах db/db с мутацией LepR
Животным дают рацион с высоким содержанием жира (HFD). Для субхронического вмешательства животных обрабатывают один раз в день соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью в течение 14 дней. Берут образцы крови, и определяют концентрации глюкозы в каждом образце крови. В случае резкого вмешательства сначала берут образцы крови, и затем вводят соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемые соли. Затем ограничивают доступ к рациону, и берут второй образец крови. Мышей подвергают тесту на пероральную переносимость глюкозы, и определяют концентрации глюкозы в крови.
Для анализа эугликемических гиперинсулинемических клэмпов животные получают первичную непрерывную инфузию [3-3H]глюкозы, и затем берут образец крови, определяют концентрации в плазме инсулина, глюкозы и [3-3H]глюкозы, и вычисляют базальные скорости появления эндогенной глюкозы. Затем мыши получают среду или соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль через желудочный зонд. Затем животные получают инфузию [3-3H]глюкозы, содержащей инсулин, вызывая умеренное общее повышение концентраций инсулина в плазме. Измеряют концентрации глюкозы в крови, и устанавливают целевую гликемию, подбирая скорость инфузии глюкозы. Затем вводят внутривенно 2-дезокси-D-[1-14C]глюкозу, и берут образцы крови. Затем мышей умерщвляют. Икроножную мышцу и эпидидимальную жировую ткань собирают, и определяют [3H]- и [14C] радиоактивность плазмы в депротеинезированной плазме.
Оценивают массу тела, и иссекают и взвешивают бурую жировую ткань (ВАТ) и гонадную белую жировую ткань (WAT). Измеряют объем кислорода (VO2) и продуцирование диоксида углерода (VCO2), и приводят средний объем VO2 в час, нормализованный к массе тела (мл/час/кг). Активность считают по прерываниям инфракрасного пучка, и одновременно измеряют поглощение пищи.
Исследования неалкогольной жировой болезни печени (NAFLD) и неалкокгольнного стеатогепатита (NASH) на самцах мышей С57BL/6J
Мышам дают рацион «Western» HF-HSD (рацион с высоким содержанием жира и сахарозы) или обычный рацион (NCD) в качестве контроля. Затем животных обрабатывают соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью в течение 4, 12 или 20 недель и затем умерщвляют. Еженедельно контролируют массу тела и поглощение рациона, и анализируют общую массу жира. Также выполняют интраперитонеальный тест на толерантность к глюкозе (IPGTT), и после введения глюкозы измеряют уровни глюкозы в крови из хвостовой вены. Инсулинорезистентность вычисляют с использованием модели гомеостаза инсулинорезистентности. Затем мышей умерщвляют, забирая кровь через кардиальную пункцию. Получают плазму, и вместе с плазмой собирают ткани для дальнейших биохимических и молекулярных анализов или для гистологического анализа.
Исследования неалкогольной жировой болезни печени (NAFLD) и неалкокгольнного стеатогепатита (NASH) на мышах с дефицитом метионина и холина
Мышам массой 25 г дают или рацион с недостатком метионина и холина (MCD для индукции NASH) или обычный рацион (как контроль). Эксперименты на животных и оценку NAFLD и NASH проводят так, как описано выше для мышей С57BL/6J, получавших рацион с высоким содержанием жира и сахарозы.
Исследования атеросклероза на мышах с нокаутом LDL-R, получавших рацион с высоким содержанием холестерина
Мышей с нокаутом LDL-R (КО) умерщвляют через примерно 12 недель после начала атерогенного питания, после чего сердце и аорту перфузируют PBS и затем фиксируют. Атеросклероз и биохимические параметры оценивают с помощью соответствующих коммерчески доступных наборов. Для исследования на липополисахариды (ЛПС) in vivo мышам интраперитонеально инъецируют ЛПС, и берут кровь из хвостовой вены. Уровни TNFα определяют количественно анализом ELISA на мышиный TNFα. Определяют числа клеток крови.
Исследования наследственного митохондриального заболевания на мышах Sco2KO/KI
Соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) растворяют в воде и добавляют к стандартному порошковому рациону в соответствующей концентрации. Подачу питания изменяют каждые три дня и назначают ad libitum в течение одного месяца. Ткани собирают для гистологического анализа. Для образцов четырехглавой мышцы измеряют спектрофотометрическую активность cI, cII, cIII и cIV, а также CS. NAD+ экстрагируют из тканей с использованием кислотных и щелочных методов экстракции, соответственно, и анализируют масс-спетрометрией.
Исследования наследственного митохондриального заболевания на делеторных мышах
Самцам делеторных мышей и мышей WT назначают или обычный рацион (CD) или соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III), смешанные с СD. Мышей регулярно контролируют на массу, потребление корма и физическую выносливость, и измеряют способность переносить физическую нагрузку. Регистрируют потребление кислорода и продуцирование диоксида углерода, а также спонтанное движение и активность при питании. Собирают и препарируют срезы тканей из четырехглавой мышцы, печени и ВАТ. Замороженные срезы четырехглавой мышцы анализируют на гистохимический СОХ in situ и активность сукцинатдегидрогеназы (SDH). Содержание крист как в ВАТ, так и в мышце определяют из электронных микрофотографий, и образцы скелетной мышцы анализируют на активность цитратсинтазы.
Исследования заболевания почек
Мышам C57BL/6J WT дают стандартный коммерческий рацион и делят на четыре группы: контроль; цисплатин; соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемая соль и цисплатин; и только соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемая соль. Мышей умерщвляют, и собирают образцы тканей и сыворотку. Измеряют сывороточный креатинин и уровни BUN, и определяют количественно провоспалительные цитокины TNF-α, IL-1b и IL-6 из сыворотки или гомогенатов из почечной ткани. Почки мышей собирают и окрашивают для анализа. Проверяют тубулярное повреждение и оценивают на основании процента кортикального тубулярного некроза. Нейтрофильную инфильтрацию оценивают количественно на окрашенной ткани путем подсчета числа нейтрофилов в поле зрения под большим увеличением.
С другой стороны, мышей C57BL/6J WT нумеруют и выдерживают некоторое время для акклиматизации и затем рандомизируют на группы различной обработки на основании их массы тела. Различные группы держат на специфическом рационе в течение некоторого периода времени. Проводят измерения массы тела, и оценивают потребление корма. Собирают кровь ретроорбитальной пункцией при умеренной анестезии и используют для анализа базальных уровней азота мочевины крови (BUN).
Мышам дают наркоз и помещают на хирургическую платформу. Обе почки надрезают, и почечные ножки пережимают, используя сосудистые зажимы. Затем зажим удаляют, и место операции сшивают. Ложно оперируемую группу подвергают схожим хирургическим операциям за исключением того, что зажим не применяют. Животных контролируют до восстановления от наркоза и возвращают в их клетки. Животных наблюдают каждый день на общие клинические признаки и симптомы и смертность.
За день до окончания эксперимента животных по отдельности помещают в метаболические клетки, и собирают урину для оценки на мочевину, креатинин, натрий и калий. Также собирают кровь ретроорбитальной пункцией при умеренной анестезии, и плазму используют для анализа на уровни азота мочевины крови (BUN) и сывороточный креатинин. Затем животных усыпляют, и собирают органы. Одну почку фиксируют, а другую быстро замораживают и используют для оценки перокисления липидов, GSH, MPO и уровней SOD.
Исследования острого повреждения почек, вызванного ишемией/реперфузией
Мышей CD-1 (ICR) обрабатывают соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью с помощью перорального зонда один раз в день. Мышей CD-1 делят на четыре группы: (1) молодые мыши с имитацией повреждения; (2) молодые мыши с повреждением от ишемии/реперфузии (I/R); (3) взрослые мыши с имитацией повреждения и (4) взрослые мыши с повреждением I/R. Дополнительных 27 взрослых мышей произвольно делят на две группы: мышей, получающих соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль, и мышей, получающих среду, как контроль. Измеряют уровень сывороточного креатинина, и регистрируют измерения BUN. Затем оценивают почечную ткань и регистрируют тубулярное повреждение.
Определение влияния на уровни фосфорилирования FoxО1
Клетки AML-12 обрабатывают различными концентрациями соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли. Затем клетки лизируют и анализируют SDS-PAGE/вестерн-блоттингом. Затем осуществляют блокирование и инкубацию с антителами, и затем детектируют каждый присутствующий белок с помощью специфических для него антител.
Ингибирующее действие
Настоящее раскрытие также относится к соединению формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли, определенных в настоящем описании, в способе ингибирования активности ACMSD. Способ включает контактирование клетки с соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью. В родственном воплощении способ дополнительно обеспечивает присутствие соединения в количестве, эффективном для получения концентрации, достаточной для селективного ингибирования ACMSD в клетке.
Таким образом, предпочтительно в анализе на ингибирование ACMSD (т.е. анализе ACMSD, описанном в настоящем описании, например, примере 29, или анализах ACMSD, известных из литературы) предпочтительными соединениями формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемыми солями являются соединения, способные уменьшать или, предпочтительно, ингибировать ACMSD и повышать уровни NAD+ и/или активировать SIRT и отрицательно регулирующие мишени SIRT, такие как PGC-1α, FoxO1 и/или SOD. Предпочтительно указанное ингибирование определяют как IC50 указанного соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) в связи с указанным анализом на ингибирование ACMSD. Предпочтительные соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемые соли имеют IC50 на уровне или ниже 1 мкМ, предпочтительнее, менее 300 нМ, например, менее 100 нМ, например, менее 50 нМ в отношении ингибирования ACMSD.
Фармацевтически приемлемые соли
Соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) может быть представлено в любой форме, подходящей для предполагаемого введения, в частности, включая фармацевтически приемлемые соли, сольваты и пролекарства соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III).
Фармацевтически приемлемыми солями называют соли соединений формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III), которые считаются приемлемыми для применения в медицине и/или ветеринарии. Типичные фармацевтически приемлемые соли включают соли, полученные взаимодействием соединений формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) и минеральной или органической кислоты или органического или неорганического основания. Такие соли известны как соли присоединения кислот и соли присоединения оснований, соответственно. Следует иметь в виду, что определенный противоион, образующий часть любой соли, не является критичным по природе до тех пор, пока соль как целое является фармацевтически приемлемой, и до тех пор, пока противоион не придает нежелательные качества соли как целому. Такие соли можно получить способами, известными специалистам. Фармацевтически приемлемыми солями являются соли, например, описанные и обсуждаемые в Remington's Pharmaceutical Sciences, 17. Ed. Alfonso R. Gennaro (Ed.), Mack Publishing Company, Easton, PA, U.S.A., 1985, и более поздних изданиях, и в Encyclopedia of Pharmaceutical Technology.
Примеры фармацевтически приемлемых солей присоединения включают соли присоединения кислот, образованные с неорганическими кислотами, например, хлороводородной, бромоводородной, серной, азотной, иодоводородной, метафосфорной или фосфорной кислотой; и органическими кислотами, например, янтарной, малеиновой, уксусной, фумаровой, лимонной, винной, бензойной, трифторуксусной, яблочной, молочной, муравьиной, пропионовой, гликолевой, глюконовой, камфорсульфоновой, изотионовой, слизевой, гентизиновой, изоникотиновой, сахарной, глюкуроновой, фуроиновой, глутамовой, аскорбиновой, антраниловой, салициловой, фенилуксусной, миндальной, эмбоновой (памовой), этансульфоновой, пантотеновой, стеариновой, сульфаниловой, альгиновой и галактуроновой кислотой; и арилсульфоновой, например, бензолсульфоновой, п-толуолсульфоновой, метансульфоновой или нафталинсульфоновой кислотой; и соли присоединения оснований, образованные с щелочными металлами и щелочноземельными металлами и органическими основаниями, такими как N,N-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин (N-метилглюкамин), лизин и прокаин; и образованные внутренние соли. Следует иметь в виду, что все ссылки на фармацевтически приемлемые соли включают формы с присоединением растворителя (сольваты) или кристаллические формы (полиморфы), определенные в настоящем описании, той же соли.
Соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемая соль могут предлагаться в растворимых или нерастворимых формах вместе с фармацевтически приемлемым растворителем, таким как вода, этанол и т.п. Растворимые формы также могут включать гидратированные формы, такие как моногидрат, дигидрат, гемигидрат, тригидрат, тетрагидрат и т.п.
Соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемая соль могут предлагаться в виде пролекарства. Термин «пролекарство», используемый в настоящем описании, предназначен для обозначения соединения, которое - после воздействия некоторых физиологических условий - будет освобождать соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль, которые затем будут способны проявлять нужное биологическое действие. Типичным примером является лабильный карбамат амина.
Так как известно, что пролекарства усиливают многие желательные качества фармацевтических препаратов (например, растворимость, биодоступность, изготовление и т.д.), соединения по настоящему раскрытию могут доставляться в форме пролекарств. Таким образом, предполагается, что настоящее раскрытие распространяется на пролекарства заявляемых в настоящем изобретении соединений, способы их доставки и композиции, содержащие их. Предполагается, что «пролекарства» включают любые ковалентно связанные носители, которые высвобождают активное лекарственное средство по настоящему раскрытию in vivo, когда такое пролекарство вводят пациенту. Пролекарства в настоящем раскрытии получают путем модификации функциональных групп, присутствующих в соединении, таким образом, что модификации расщепляются или при обычной манипуляции или in vivo до исходного соединения. Пролекарства включают соединения по настоящему раскрытию, в которых группа гидрокси, амино, сульфгидрил, карбокси или карбонильная группа связана с любой группой, которая может отщепляться in vivo с образованием свободной гидроксильной группы, свободной аминогруппы, свободной сульфгидрильной группы, свободной карбоксигруппы или свободной карбонильной группы, соответственно.
Примеры пролекарств включают, но не ограничиваются перечисленным, сложные эфиры (например, ацетат, диалкиламиноацетаты, формиаты, фосфаты, сульфаты и бензоаты) и карбаматы (например, N,N-диметиламинокарбонил) функциональных гидроксигрупп, эфиры (например, С1-6-алкилэфиры, например, метиловые эфиры, этиловые эфиры, 2-пропиловые эфиры, фениловые эфиры, 2-аминоэтиловые эфиры, эфиры морфолиноэтанола и т.д.) карбоксильных функциональных групп, N-ацилпроизводные (например, N-ацетил) N-оснований Манниха, оснований Шиффа и енаминоны аминофункциональных групп, оксимы, ацетали, кетали и сложные енолэфиры кетоновых и альдегидных функциональных групп в соединениях по раскрытию и т.п. См. Bundegaard H., Design of Prodrugs, p1-92, Elesevier, New York-Oxford (1985).
Соединения или их фармацевтически приемлемые соли, эфиры или пролекарства вводят перорально, назально, трансдермально, легочно, ингаляцией, трансбуккально, сублингвально, интраперитонеально, подкожно, внутримышечно, внутривенно, ректально, интраплеврально, интратекально и парентерально. В одном воплощении соединение вводят перорально. Специалистам в данной области техники будут понятны преимущества некоторых путей введения.
Схему приема лекарственных средств с использованием соединений выбирают согласно ряду факторов, включая тип, вид, возраст, массу, пол и состояние здоровья пациента; тяжесть состояния, от которого лечат; путь введения; функцию почек и печени пациента и конкретное используемое соединение или его соль. Лечащий врач или ветеринар легко определит и назначит эффективное количество лекарственного средства, требуемое для предупреждения, противодействия или остановки развития состояния.
Методы получения препаратов и введения раскрытых соединений можно найти в Remington: the Science and Practice of Pharmacy, 19th edition, Mack Publishing Co., Easton, PA (1995). В одном воплощении соединения, описанные в настоящем описании, и их фармацевтически приемлемые соли используют в фармацевтических препаратах в комбинации с фармацевтически приемлемым носителем или разбавителем. Подходящие фармацевтически приемлемые носители включают инертные твердые наполнители или разбавители и стерильные водные или органические растворы. Соединения будут присутствовать в таких фармацевтических композициях в количествах, достаточных для обеспечения желательной дозировки в интервале, описанном в настоящем описании.
В одном аспекте настоящее раскрытие относится к фармацевтической композиции, включающей в качестве активного ингредиента по меньшей мере одно соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль, определенные в настоящем описании, и необязательно один или несколько фармацевтически приемлемых эксципиентов, разбавителей и/или носителей. Соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемые соли можно вводить одни или в комбинации с фармацевтически приемлемыми носителями, разбавителями или эксципиентами или в однократных или в нескольких дозах. Подходящие фармацевтически приемлемые носители, разбавители и эксципиенты включают инертные твердые разбавители или наполнители, стерильные водные растворы и различные органические растворители.
«Фармацевтическая композиция» представляет собой композицию, содержащую соединения по настоящему раскрытию в форме, подходящей для введения субъекту. Фармацевтические композиции можно получить с фармацевтически приемлемыми носителями или рабавителями, а также любыми другими известными адъювантами и эксципиентами согласно обычным методам, таким, как раскрытые в Remington: The Science and Practice of Pharmacy, 21st Edition, 2000, Lippincott Williams & Wilkins.
Используемое в настоящем описании выражение «фармацевтически приемлемый» относится к таким соединениям, материалам, композициям, носителям и/или лекарственным формам, которые, в рамках здравого медицинского суждения, подходят для применения в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соизмеримо с разумным соотношением польза/риск.
«Фармацевтически приемлемый эксципиент» обозначает эксципиент, который применим при получении фармацевтической композиции, которая обычно безопасна, нетоксична ни биологически ни как-либо иначе, и включает эксципиент, который приемлем для применения в ветеринарии, а также применения в фармацевтических препаратах для людей. «Фармацевтически приемлемый эксципиент», используемый в настоящем описании, включает как один, так и более одного такого эксципиента.
Фармацевтические композиции, образованные комбинацией соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли, определенных в настоящем описании, с фармацевтически приемлемыми носителями, разбавителями или эксципиентами, можно легко вводить в различных лекарственных формах, таких как таблетки, порошки, лепешки, сиропы, суппозитории, растворы для инъекции и т.п. В порошках носитель представляет собой тонко измельченное твердое вещество, такое как тальк или крахмал, которое находится в смеси с тонко измельченным активным компонентом. В таблетках активный компонент смешан в подходящих пропорциях с носителем, имеющим необходимые связывающие свойства, и спрессован в нужной форме и размере.
Фармацевтические композиции можно конкретно получить для введения подходящим путем, таким как пероральный и парентеральный (включая подкожный, внутримышечный, интратекальный, внутривенный и интрадермальный) путь. Следует признать, что предпочтительный путь будет зависеть от общего состояния и возраста субъекта, которого лечат, природы состояния, от которого лечат, и выбранного активного ингредиента.
Фармацевтические композиции для перорального введения включают твердые лекарственные формы, такие как капсулы, таблетки, пилюли, лепешки, порошки и гранулы. В соответствующем случае их можно получить с покрытием, таким как энтеросолюбильное покрытие, или их можно получить, например, для обеспечения регулируемого высвобождения активного ингредиента, например, длительного или пролонгированного высвобождения, согласно способам, хорошо известным в технике.
Для перорального введения в форме таблетки или капсулы соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль, определенные в настоящем описании, можно соответственно комбинировать с пероральным нетоксичным фармацевтически приемлемым носителем, таким как этанол, глицерин, вода или подобное. Кроме того, в смесь в соответствующем случае можно добавить подходящие связующие вещества, лубриканты, дезинтеграторы, корригенты и красители. Подходящие связующие вещества включают, например, лактозу, глюкозу, крахмал, желатин, аравийскую камедь, трагакантовую камедь, альгинат натрия, карбоксиметилцеллюлозу, полиэтиленгликоль, воски или подобное. Лубриканты включают, например, олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия или подобное. Дезинтеграторы включают, например, крахмал, метилцеллюлозу, агар, бентонит, ксантановую смолу, натрий крахмалгликолят, кросповидон, кроскармеллозу натрия или подобное. Другие эксципиенты для капсул включают макрогели или липиды.
Для получения твердых композиций, таких как таблетки, активное соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль смешивают с одним или несколькими эксципиентами, такими как описанные выше, и другими фармацевтическими разбавителями, такими как вода, и получают твердую предварительную композицию, содержащую гомогенную смесь соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли. Предполагается, что термин «гомогенная» означает, что соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемая соль равномерно диспергированы в композиции, так что композицию можно легко разделить на равно эффективные стандартные лекарственные формы, такие как таблетки или капсулы.
Жидкие композиции для перорального или парентерального введения соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли включают, например, водные растворы, сиропы, эликсиры, водные или масляные суспензии и эмульсию со съедобными маслами, такими как хлопковое масло, сезамаовое масло, кокосовое масло или арахисовое масло. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические или природные смолы, такие как трагакант, альгинат, аравийская камедь, декстран, карбоксиметилцеллюлоза натрия, желатин, метилцеллюлоза или поливинилпирролидон.
Фармацевтические композиции для парентерального введения включают стерильные водные и неводные растворы, дисперсии, суспензии или эмульсии для инъекции, а также стерильные порошки, которые восстанавливают до стерильных растворов или дисперсий для инъекции перед применением.
Для внутривенного введения подходящие носители включают физиологический раствор, бактериостатическую воду, кремофор EL™ (BASF, Parsippany, N.J.) или забуференный фосфатом физиологический раствор (PBS). Во всех случаях композиция должна быть стерильной и должна быть жидкой до такой степени, которая допускает легкое введение шприцом. Она должна быть устойчивой в условиях изготовления и хранения и должна быть сохранена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль, и т.п.) и их подходящие смеси. Соответствующую текучесть можно поддерживать, например, путем использования покрытия, такого как лецитин, путем сохранения требуемого размера частиц в случае дисперсии, и используя поверхностно-активные вещества. Предотвращения действия микроорганизмов можно достичь с помощью различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола, аскорбиновой кислоты, тимеросаля и т.п. Во многих случаях предпочтительным будет включение в композицию изотоничных средств, например, сахаров, многоатомных спиртов, таких как маннит, сорбит, и хлорида натрия. Пролонгированная абсорбция инъецируемых композиций может быть вызвана путем включения в композицию средства, которое замедляет абсорбцию, например, моностеарата алюминия и желатина.
Получение всех таких растворов в стерильном состоянии легко осуществляется с помощью стандартных фармацевтических методов, хорошо известных специалистам в данной области техники.
Например, стерильные растворы для инъекции можно получить путем включения активного соединения в требуемом количестве в соответствующий растворитель с одним или комбинацией ингредиентов, перечисленных выше, что необходимо, с последующей стерилизацией фильтрованием. Как правило, дисперсии получают, включая активное соединение в стерильную среду, которая содержит основную дисперсную среду и требуемые другие ингредиенты из перечисленных выше. В случае стерильных порошков для получения стерильных растворов для инъекции способами получения являются вакуумная сушка и сушка вымораживанием, которые дают порошок активного ингредиента с добавлением любого дополнительного нужного ингредиента из их предварительно стерилизованного фильтрованием раствора. Депо-композиции для инъекции также рассматриваются как входящие в объем настоящего раскрытия.
Для парентерального введения можно использовать растворы, содержащие соединение формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемую соль в сезамовом или арахисовом масле, водном пропиленгликоле или в стерильном водном растворе. Такие водные растворы при необходимости должны быть соответственно забуферены, и жидкому разбавителю должна быть придана изотоничность достаточным количеством физиологического раствора или глюкозы. Такие специфические водные растворы особенно подходят для внутривенного, внутримышечного, подкожного и интраперитонеального введения. Масляные растворы подходят для целей внутрисуставной, внутримышечной и подкожной инъекции.
Кроме вышеуказанных ингредиентов композиции соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли могут включать один или несколько дополнительных ингредиентов, таких как разбавители, буферы, корригенты, краситель, поверхностно-активные вещества, загустители, консерванты, например, метилгидроксибензоат (включая антиоксиданты), эмульгаторы и т.п.
Термин «терапевтически эффективное количество», используемый в настоящем описании, относится к количеству фармацевтического средства для лечения, ослабления симптомов или предупреждения идентифицированного заболевания, расстройства или состояния, или для проявления детектируемого терапевтического или ингибирующего действия. Действие можно обнаружить любым методом анализа, известным в технике. Точное эффективное количество для субъекта будет зависеть от массы тела, размера и здоровья субъекта; характера и степени состояния и терапевтического средства или комбинации терапевтических средств, выбранных для введения. Терапевтически эффективные количества в данной ситуации можно определить обычным экспериментом, которым владеет специалист, и который осмыслен лечащим врачом. В предпочтительном аспекте заболевание или расстройство, от которого лечат, представляет собой заболевание или расстройство, связанное с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD).
Для любого соединения терапевтически эффективное количество сначала можно оценить или в анализах в клеточной культуре, например, в клетках, или на животных моделях, обычно, крысах, мышах, кроликах, собаках или свиньях. Животную модель также можно использовать для определения соответствующего интервала концентраций и пути введения. Затем такую информацию можно использовать для определения применимых доз и путей введения для людей. Терапевтическую/Профилактическую эффективность и токсичность можно определить стандартными фармацевтическими процедурами в клеточных культурах или на подопытных животных, например, ED50 (доза, терапевтически эффективная для 50% популяции). Соотношение доз между токсическим и терапевтическим действиями представляет собой терапевтический индекс, и его можно выразить как отношение LD50/ED50. Фармацевтические композиции, которые показывают большие терапевтические индексы, являются предпочтительными. Дозировка может изменяться в интервале, зависящем от используемой лекарственной формы, чувствительности пациента и пути введения.
Дозировку и введение регулируют для обеспечения достаточных уровней активного(ых) средства(средств) или для поддержания желательного действия. Факторы, которые можно принять в расчет, включают тяжесть болезненного состояния, состояние здоровья субъекта, возраст, массу тела и пол субъекта, время и частоту введения, комбинацию(и) лекарственных средств, чувствительность и переносимость/реакцию на терапию. Длительно действующие фармацевтические композиции можно вводить каждые 3-4 дня, каждую неделю или один раз каждые две недели, в зависимости от периода полувыведения и скорости клиренса определенного препарата.
Подходящая дозировка соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли будет зависеть от возраста и состояния пациента, тяжести заболевания, от которого лечат, и других факторов, хорошо известных практическому врачу. Соединение можно вводить, например, перорально, парентерально или топически согласно различным программам приема лекарственных средств, например, ежедневно или с интервалами, такими как недельные интервалы. Как правило, однократная доза будет находиться в интервале от 0,01 до 500 мг/кг массы тела, предпочтительно от примерно 0,05 до 100 мг/кг массы тела, предпочтительнее от 0,1 до 50 мг/кг массы тела, и наиболее предпочтительно от 0,1 до 25 мг/кг массы тела. Соединение можно вводить как болюс (т.е. всю дневную дозу вводят за один раз) или в раздельных дозах два или больше раз в день. Изменения на основе вышеуказанных дозировочных интервалов могут быть сделаны врачом с учетом известных соображений, таких как масса, возраст и состояние пациента, которого лечат, тяжести недуга и конкретного пути введения.
При использовании в настоящем описании «субъект» или «субъект, нуждающийся в этом» представляет собой субъекта, имеющего заболевание или расстройство, связанное с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD). «Субъект» включает млекопитающего. Млекопитающее может представлять собой, например, любое млекопитающее, например, человека, примата, птицу, мышь, крысу, домашнюю птицу, собаку, кошку, корову, лошадь, козу, верблюда, овцу или свинью. Предпочтительно млекопитающим является человек.
Соединения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемые соли также можно получить в фармацевтической композиции, включающей одно или больше дополнительных активных веществ одних или в комбинации с фармацевтически приемлемыми носителями, разбавителями или эксципиентами или в одной дозе или в нескольких дозах. Подходящими фармацевтически приемлемыми носителями, разбавителями и эксципиентами являются описанные в настоящем описании выше, и одно или больше дополнительных активных веществ могут представлять собой любые активные вещества или, предпочтительно, активное вещество, описанное в настоящем описании ниже в разделе «Комбинированное лечение».
Клинические состояния и другие применения соединений
Соединения согласно формуле (I), формуле (Ia), формуле (Ib), формуле (II) или формуле (III) или их фармацевтически приемлемые соли, композиции, лекарственные средства и соединения для применения, определенные в настоящем описании, применимы для лечения заболевания или расстройства, в котором играет роль модуляция α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD). Соединения можно использовать или в медицине или в ветеринарии, и пациент может представлять собой любое млекопитающее, но в особенности человека. Лечение может включать введение любому млекопитающему, но в особенности человеку, страдающему от заболевания или расстройства, в котором играет роль модуляция α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD), терапевтически эффективного количества соединения согласно формуле (I), формуле (Ia), формуле (Ib), формуле (II) или формуле (III) или его фармацевтически приемлемой соли, определенных в настоящем описании.
Настоящее раскрытие также относится к соединению формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой соли, определенным в настоящем описании, для применения при заболевании или расстройстве, связанном с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD), таком как ожирение, диабет типа II и его осложнения (например, диабетическая ретинопатия и нефропатия), неалкогольная жировая болезнь печени (NaFLD), неалкогольный стеатогепатит (NASH) или хроническая болезнь почек.
Термином «заболевание или расстройство, связанное с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-карбоксилазы (ACMSD)» обозначается заболевание, характеризующееся сниженной экспрессией никотинамидадениндинуклеотида (NAD+) и/или активностью по меньшей мере в некоторых случаях заболевания, или заболевание, симптомы которого облегчают путем оценки уровней NAD+.
Способы, лекарственные средства и соединения для применения по настоящему раскрытию применимы для лечения, уменьшения интенсивности или отсрочки начала расстройства, связанного с аберрантной митохондриальной функцией. Расстройства, связанные с аберрантной митохондриальной функцией, включают, например, метаболические расстройства, нейродегенеративные расстройства, расстройства, связанные с возрастом, и хронические воспалительные расстройства. Митохондриальные расстройства также включают заболевания с наследственной и/или приобретенной митохондриальной дисфункцией (т.е. болезнь Шарко-Мари-Тута, тип 2А2, митохондриальную энцефалопатию с лактоцидозом и инсультом (MELAS), синдром Лейха, синдром Барта и оптическую нейропатию Лебера), нарушения окисления жирных кислот, наследственные формы глухоты и слепоты и метаболические анормальности, вызванные воздействием токсических химических веществ и/или лекарственных средств (например, глухота, вызванная цисплатином).
Метаболические расстройства включают, например, диабет типа II, ожирение, гипергликемию, непереносимость глюкозы, инсулинорезистентность (т.е. гиперинсулиненмию, метаболический синдром, синдром Х), гиперхолестеринемию, гипертензию, гиперлипопротеинемию, гиперлипидемию (например, дислипидемию), гипертриглицеридемию, сердечно-сосудистую болезнь, атеросклероз, заболевание периферических сосудов, болезнь почек, кетоацидоз, тромботические нарушения, нефропатию, диабетическую невропатию, диабетическую ретинопатию, половую дисфункцию, дерматопатию, диспепсию, гипогликемию, рак и отек.
Нейродегенеративные расстройства включают такие заболевания, как дегенерация фоторецепторов (т.е. пигментный ретинит), деменцию, болезнь Альцгеймера, болезнь Паркинсона и болезнь Гентингтона.
Хронические воспалительные заболевания включают такие заболевания, как глютеновая болезнь, васкулит, волчанка, хроническая обструктивная легочная болезнь (COPD), синдром раздраженной толстой кишки, атеросклероз, артрит и псориаз.
Заболевания, связанные с возрастом, включают такие болезни, как рак, деменция, сердечно-сосудистая болезнь (т.е. артериосклероз), гипертензия, сахарный диабет (типа I или типа II), артрит, катаракта, болезнь Альцгеймера, дегенерация желтого пятна и остеопороз.
Субъект может страдать от восприимчивости к развитию метаболического расстройства. Субъектов, страдающих от опасности развития метаболического расстройства, идентифицируют методами, известными в технике. Например, диабет можно диагностировать, измеряя уровни глюкозы в крови натощак или инсулина, или с помощью теста переносимости глюкозы. Нормальные уровни глюкозы у взрослых находятся между примерно 60-126 мг/дл. Нормальные уровни инсулина составляют примерно 7 мЕ/мл±3 мЕ. Гипертензию можно диагностировать по кровяному давлению, согласно показаниям примерно или выше 140/90. Сердечно-сосудистую болезнь можно диагностировать, измеряя уровни холестерина. Например, LDL холестерин выше примерно 137 или общий холестерин выше примерно 200 являются показателями сердечно-сосудистого заболевания. Гипергликемию можно диагностировать по уровням глюкозы в крови выше примерно 10 ммоль/л (180 мг/дл). Непереносимость глюкозы можно диагностировать по уровням глюкозы 140-199 мг на дл (7,8-11,0 ммоль) после проведения перорального двухчасового теста с 75 г глюкозы. Инсулинорезистентность можно диагностировать по уровню инсулина в сыворотке натощак, превышающему приблизительно 60 пмоль/л. Гипогликемию можно диагностировать по уровню глюкозы в крови ниже примерно 2,8-3,0 ммоль/л (50-54 мг/дл). Ожирение можно диагностировать, например по индексу массы тела. Индекс массы тела (BMI) измеряют в кг/м2 (или ф/д2 × 704,5). С другой стороны, можно измерить окружность талии (оценивает распределение жира), отношение талии к бедрам (оценивает распределение жира), толщину кожной складки (если измерена в нескольких местах, оценивает распределение жира) или биоимпеданс (основанный на принципе, что тощая масса проводит ток лучше, чем жировая масса (т.е. жировая масса не пропускает ток), оценивает % жира). Параметры для индивидуумов нормальных, с избыточным весом или с ожирением следующие: BMI <18,5 пониженная масса; BMI от примерно 18,5 до примерно 24,9 нормальная масса; BMI=примерно 25 - примерно 29,9 это избыточная масса. Индивидуумы с избыточной массой характеризуются как имеющие объем талии >94 см для мужчин или >80 см для женщин и отношения талии к бедрам >0,95 у мужчин и >0,80 у женщин. Индивидуумы с ожирением характеризуются как имеющие BMI 30-34,9, с более чем 20% выше «нормальной» массы для роста, имеющие процент жира >30% для женщин и 25% для мужчин, и имеющие окружность талии >102 см (40 дюймов) для мужчин или 88 см (35 дюймов) для женщин. Индивидуумы с тяжелым или морбидным ожирением характеризуются как имеющие BMI >35.
Способы, описанные в настоящем описании, могут привести к уменьшению тяжести или уменьшению интенсивности одного или нескольких симптомов метаболического расстройства. Например, симптомы диабета включают повышенные уровни глюкозы в крови натощак, кровяное давлении примерно или выше 140/90 мм/Hg; анормальные уровни жира в крови, такого как липопротеины высокой плотности (HDL), менее или равные 35 мг/дл, или триглицеридов большие или равные 250 мг/дл (мг/дл=миллиграмм глюкозы на децилитр крови). Эффективность лечения определяют в ассоциации с любым известным способом диагностики метаболического расстройства. Уменьшение интенсивности одного или нескольких симптомов метаболического расстройства показывает, что соединение приносит клиническую пользу.
Способы по настоящему раскрытию применимы для лечения, уменьшения интенсивности симптомов или отсрочки начала почечного расстройства. Почечные расстройства включают острое повреждение почек (AKI) и хроническую болезнь почек (CKD).
Субъект может страдать от или быть восприимчивым к развитию острого повреждения почек (AKI). Острое повреждение почек можно охарактеризовать одним или несколькими клиническими критериями или состояниями (т.е. резким снижением способности почек выводить азотсодержащие продукты жизнедеятельности из крови, что приводит к азотемии). Субъектов, страдающих от или в опасности развития острого повреждения почек (AKI), идентифицируют способами, известными в технике. Например, острое повреждение почек может характеризоваться повышением сывороточного креатинина по меньшей мере на 50% от базового уровня, абсолютным повышением сывороточного креатинина по меньшей мере на 0,3 мг/мл от базового уровня, снижением диуреза до 0,5 мл на килограмм массы тела или меньше в час, сохраняющимся по меньшей мере в течение 6 часов, или их любой комбинацией. Острое повреждение почек может вызываться ишемией, лекарственными средствами или токсическими средствами (т.е. радиоконтрастными средами, нестероидными противовоспалительными лекарственными средствами (NSAID), спиртом или химическим веществом), вирусами и закупоркой.
Субъект может страдать от или быть восприимчивым к развитию хронической болезни почек (CKD). Хроническую болезнь почек (CKD) определяют как (1) наличие поражения почек, определенное структурными или функциональными анормальностями почек в течение 3 месяцев или долее с или без пониженной скорости гломерулярной фильтрации (GFR), или (2) наличие GFR меньше 60 мл/мин/1,73 м2 в течение 3 месяцев или долее с или без поражения почек. Субъектов, страдающих от или в опасности развития хронической болезни почек (CKD), идентифицируют способами, известными в технике. Структурные или функциональные анормальности проявляются симптомами, такими как патологические анормальности или маркеры поражения почек, включая анормальности, идентифицированные в визуальных исследованиях, или состав крови или мочи.
Например, CKD диагностируют проверкой на специфический маркер. Например, маркеры поражения почек включают концентрацию креатинина в плазме выше примерно 1,6 мг/дл и концентрацию азота мочи в крови (BUN) выше примерно 20 мг/дл. Типично оба эти маркера у индивидуума с CKD повышаются. Дополнительные маркеры поражения почек могут включать гематурию (т.е. любое детектируемое количество крови в моче), протеинурию (т.е. концентрацию белка в моче выше примерно 100 мг/дл), альбуминурию (т.е. концентрацию альбумина в моче выше примерно 100 мг/дл), концентрацию интактного паратиреоидного гормона в крови выше примерно 150 пг/мл или уровни фосфатов в крови выше примерно 4,5 мг/дл. Одним из специфических маркеров болезни почек является скорость CFR выше нормальной (т.е. CFR выше примерно 90 мл/мин/1,73 м2), однако CFR ниже нормальной также указывает на CKD.
Способы по настоящему раскрытию применимы для лечения, уменьшения интенсивности симптомов или отсрочки начала неалкогольной жировой болезни печени (NAFLD) и/или неалкогольного стеатогепатита (NASH). Субъект может страдать от или или быть восприимчивым к развитию неалкогольной жировой болезни печени (NAFLD) и/или неалкогольного стеатогепатита (NASH). Субъектов, страдающих от или в опасности развития неалкогольной жировой болезни печени (NAFLD) и/или неалкогольного стеатогепатита (NASH), идентифицируют способами, известными в технике. Например, NAFLD и/или NASH можно диагностировать по биопсии печени.
Неалкогольная жировая болезнь печени (NAFLD), как определяется в настоящем описании, является болезнью с отложением жира в печени, которое происходит у пациентов, чья история потребления алкоголя не является достаточно длительной, чтобы вызвать повреждение печени. Неалкогольную жировую болезнь печени (NAFLD) можно дополнительно распределить на простую жировую печень, стеатогепатит и цирроз. Неалкогольный стеатогепатит (NASH) относится к патологии, связанной с воспалением, некрозом, баллонированием и фиброзом клеток печени. Начало простой жировой печени вызывается отложением жира в клетках печени, и накопление этого жира определяют по балансу между факторами возрастания (приток и синтез жиров в клетках печени) и факторами снижения (катаболизм жиров и их высвобождение из клеток печени). Как только происходит поражение клеток печени, в дополнение к осаждению жира, неалкогольная простая жировая печень будет прогрессировать до неалкогольного стеатогепатита. Неалкогольный стеатогепатит развивается и может в итоге развиться до цирроза и гепатоцеллюлярной карциномы.
Комбинированное лечение
Соединение, композиции, лекарственные средства и соединения для применения формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или их фармацевтически приемлемые соли также можно использовать с выгодой в комбинации с одним или несколькими другими терапевтическими средствами. Такие терапевтические средства включают, но не ограничиваются перечисленным, другие ингибиторы ACMSD; противодиабетические средства, такие как агонисты PPARy, двойные агонисты PPARα/γ, агонисты PPARδ, бигуаниды, ингибиторы протеинтирозинфосфатазы-1В (РТР-1В), ингибиторы дипептидилпептидазы IV (DPP-IV), сульфонилмочевины, меглитиниды, ингибиторы альфа-глюкозидгидролазы, ингибиторы альфа-амилазы, секретагоги инсулина, антагонисты А2, инсулин или инсульиномиметики, ингибиторы гликогенфосфорилазы, агонисты GLP-1, не-тиазолидиндионы, гликокиназу и ингибитор 11 β HSD-1; средства против ожирения, такие как активаторы разобщающего белка (UCP-1, UCP-2 UCP-3), β3-адренергический рецептор (β3), β-агонисты тиреоидного гормона, ингибиторы синтазы жирных кислот (PAS), ингибиторы фосфодиэстеразы (PDE), ингибиторы липазы, ингибиторы повторного поглощения серотонина, ингибиторы повторного поглощения моноамина, агонисты Mc4r, агонисты 5НТ2с, агонисты секретагога гормона роста (GHS), производные CNTF, цилиарные нейротрофные факторы (CNTh), агонисты холецистокинина-А (ССК-А), опиоидные антагонисты, орексиновые антагонисты, ацилэстрогены, лептин, антагонисты NPY 5, антагонисты нейропептида Y5 (NPY5), агонисты нейропептида Y2 (NPY2), антагонисты рецептора меланинконцентрирующего гормона (MCHLR) и антагонисты рецептора меланинконцентрирующего гормона 2 (MCH2R), антагонисты MCH1R, антагонисты нейропептида Y1, антагонисты глерина, антагонисты/обратные агонисты каннабиноидного рецептора 1 (СВ-1), ингибиторы переноса серотонина (5НТ), агонисты ССК-А и антагонисты/обратные агонисты гистамина 3; средства, снижающие холестерин, такие как ингибиторы 3-гидрокси-3-метилглутарилкофермент-А-(HMG-CoA)-редуктазы, ингибиторы HMG-CoA-синтазы, ингибиторы скваленэпоксидазы, фиброевые кислоты, связывающие желчные кислоты смолы, пробукол и ниацин (никотиновая кислота); соединения, которые повышают уровни NAD+, такие как предшественники NAD+ (т.е. никотинамидрибоза (NA), никотинамидмононуклеотид (NMN), никотиновая кислота (NA) и никотинамид); и соединения, которые ингибируют расход NAD+, такие как ингибиторы PARP и ингибиторы CD38.
Агонисты PPARy, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, глитазоны (например, балаглитазон, циглитазон, дарглитазон, энглитазон, изаглитазон (МСС-555), пиоглитазон, розиглитазон, троглитазон, CLX-0921, 5-BTZD и т.п.); GW-0207, LG-100641, LY-300512, LY-519818, R483 (Roche), T131 (Tularik) и соединения, раскрытые в W097/27857, 97/28115, 97/28137 и 97/27847; и их фармацевтически приемлемые соли или эфиры. Двойные агонисты PPARα/γ, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, CLX-0940, GW-1536, GW1929, GW-2433, KRP-297, L-796449, LR-90, MK-0767, SB 219994 и мураглитазар и их фармацевтически приемлемые соли или эфиры. KRP-297 представляет собой 5-[(2,4-диоксо-5-тиазолидинил)метил]-2-метокси-N-[[4-(трифторметил)фенил]метил]бензамид и его фармацевтически приемлемые соли или эфиры. Агонисты PPARδ, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, GW 501516, GW 590735 и соединения, раскрытые в JP 10237049 и WO 02/14291; и их фармацевтически приемлемые соли или эфиры.
Бигуаниды, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, буформин, метформин и фенформин и их фармацевтически приемлемые соли или эфиры. Метформин (Glucophage®) показан для пациентов с инсулиннезависимым сахарным диабетом, особенно пациентам с рефракторным ожирением. Physician's Desk Reference®, page 1080-1086, (56th ed. 2002).
Ингибиторы протеинтирозинфосфатазы-1В (РТР-1), применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, A-401,674, KR 61639, OC-060062, OC-83839, OC-297962, MC52445, MC52453 и соединения, раскрытые в WO 02/26707, WO 02/26743, JP 2002114768, и их фармацевтически приемлемые соли или эфиры.
Ингибиторы дипептидилпептидазы IV (DPP-IV), включают такие средства, как изолейцинтиазолидид; NVP-DPP728; P32/98; и LAP 237, P 3298, TSL 225, валинпирролидид, TMC-2A/2B/2C, ингибиторы CD-26, FE 999011, P9310/K364, VIP 0177, DPP4, SDZ 274A444 и соединения, раскрытые в WO 03/00449; WO 03/004496; EP 1258476; WO 02/083128; WO 021062764; WO 03/000250; WO 03/002530; WO 03/002531; WO 03/002553; WO 03/002593; WO 03/000180 и WO 03/000181.
Сульфонилмочевины, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, ацетогексамид, хлорпропамид, диабинез, глибенкламид, глипизид, глибурид, глимепирид, гликлазид, глипентид, гликвидон, глизоламид, толазамид и толбутамид, их фармацевтически приемлемые соли или эфиры. Меглиниды, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, репаглинид и натеглинид и их фармацевтически приемлемые соли или эфиры.
Ингибиторы альфа-глюкозидгидролазы (или ингибиторы глюкозидов), применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, акарбозу, адипозин, камиглибозу, эмиглитат, миглитол, воглибозу, прадимицин-Q, сальбостатин, CKD-711, MDL-25,637, MDL-73,945 и MOR 14 и их фармацевтически приемлемые соли или эфиры, и соединения, раскрытые в пат. США №№ 4062950, 4174439, 4254256, 4701559, 4639436, 5192772, 4,634,765, 5157116, 5504078, 5091418, 5217877 и 5091524. Ингибиторы альфа-амилазы, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, тендамистат, трестатин и A1-3688 и их фармацевтически приемлемые соли и эфиры, и соединения, раскрытые в пат. США №№ 4451455, 4623714 и 4273765.
Секретагоги инсулина, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, линоглирид и А1-3688 и их фармацевтически приемлемые соли и эфиры.
Ингибиторы окисления жирных кислот, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, кломоксир и этомоксир и их фармацевтически приемлемые соли и эфиры. Антагонисты А2, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, мидаглизол, изаглидол, дериглидол, идазоксан, эароксан, флупароксан и их фармацевтически приемлемые соли и эфиры. Инсулин или инсулиномиметики, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, биоту, LP-100, новарапид, инсулин детемир, инсулин лиспро, инсулин гларгин, суспензию цинк-инсулина (ленте и ультраленте), инсулин Lys-Pro, GLP-1 (73-7) (инсулинтропин) и GLP-1 (73-6)-NH2) и их фармацевтически приемлемые соли или эфиры.
Ингибиторы гликогенфосфорилазы, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, CP-368, 296, CP-316,819, BAYR3401 и соединения, раскрытые в WO 01/94300, и WO 02/20530, и их фармацевтически приемлемые соли или эфиры. Агонисты GLP-1, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, экзендин-3 и экзендин-4 и соединения, раскрытые в US 2003087821 и NZ 504256, и их фармацевтически приемлемые соли или эфиры.
Не-тиазолидиндионы, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, JT-501 и фарглитазар (GW-2570/GI-262579) и их фармацевтически приемлемые соли или эфиры. Активаторы гликокиназы, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, конденсированные гетероароматические соединения, такие как соединения, раскрытые в US 2002103199, и изоиндолин-1-онзамещенные производные пропионамида, такие как раскрытые в WO 02/48106.
Ингибиторы переноса серотонина (5НТ), применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, пароксетин, флуоксетин, фенфлурамин, флувоксамин, сертралин и имипрамин. Ингибиторы переноса норэпинефрина (NE), применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, GW 320659, деспирамин, талсупрам и номифензин. Антагонисты/Обратные агонисты каннабиноидного рецептора 1 (CB-1), применимые в настоящем раскрытии, включают раскрытые в пат. США №№ 5532237, 4973587, 5013837, 5081122, 5112820, 5292736, 5624941 и пат. США № 6028084, и заявках согласно PCT №№ WO 96/33159, WO 98/33765, W098/43636, W098/43635, WO 01/09120, WO 98/31227, WO 98/41519, WO 98/37061, WO 00/10967, WO 00/10968, WO 97/29079, WO 99/02499, WO 01/58869, WO 02/076949, WO 01/64632, WO 01/64633, WO 01/64634 и WO 03/007887, и в заявке EPO № EP-658546. Конкретные антагонисты/обратные агонисты CB-1, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, римонбант (Sanofi Synthelabo), SR-147778 (Sanofi Synthelabo), BAY 65-2520 (Bayer) и SLY 319 (Solvay). Агонисты CCK-A, применимые в настоящем раскрытии, включают GI 181771 и SR 146131. Антагонисты грелина, применимые в настоящем раскрытии, включают антагонисты, раскрытые в заявках PCT №№ WO 01/87335 и WO 02/08250. Антагонисты/Обратные агонисты гистамина 3 (H3), применимые в настоящем раскрытии, включают раскрытые в заявке согласно PCT № WO 02/15905, и O-[3-(1H-имидазол-4-ил)пропанол]карбаматы (Kiec-Kononowicz K. et al., Pharmazie, 55:349-55 (2000)), антагонисты рецептора пиперидинсодержащего гистамина H3 (Lazewska D. et al., Pharmazie, 56:927-32 (2001), производные бензофенона и родственные соединения (Sasse A. et al., Arch. Pharm.(Weinheim), 334:45-52 (2001)), замещенные N-фенилкарбаматы (Reidemeister S. et al., Pharmazie, 55:83-6 (2000)) и производные проксифана (Sasse A. et al., J. Med. Chem., 43:3335-43 (2000)). Конкретные антагонисты/обратные агонисты Н3, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, тиоперамид, 3-(1H-имидазол-4-ил)пропил-N-4-пентенил)карбамат, клобенпропит, иодфенпропит, имопроксифан, GT2394 (Gliatech) и A331440.
Антагонисты рецептора меланинконцентрирующего гормона (MCHLR) и агонисты/антагонисты рецептора меланинконцентрирующего гормона 2 (MCH2R), применимые в настоящем раскрытии, включают соединения, раскрытые в заявках на патент согласно PCT №№ WO 01/82925, WO 01/87834, WO 02/06245, WO 02/04433 и WO 02/51809 и заявке на патент Японии № JP 13226269. Конкретные антагонисты MCH1R, применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, T-226296 (Takeda), SB 568849 и SNAP 7941. Антагонисты нейропептида Y1 (NPY1), применимые в настоящем раскрытии, включают соединения, раскрытые в пат. США № 6001836 и заявках согласно PCT №№ WO 96/14307, WO 01/23387, WO 99/51600, WO 01/85690, WO 01/85098, WO 01/85173 и WO 01/89528. Конкретные примеры антагонистов NPY1, применимых в настоящем раскрытии, включают, но не ограничиваются перечисленным, BIBP3226, J-115814, BIBO 3304, LY-357897, CP-671906 и GI-264879A. Агонисты нейропептида Y2 (NPY2), применимые в настоящем раскрытии, включают пептид YY (PYY) и PYY3_36, аналоги пептида YY, агонисты PYY и соединения, раскрытые в WO 03/026591, WO 03/057235 и WO 03/027637. Антагонисты нейропептида Y5 (NPY5), применимые в настоящем раскрытии, включают, но не ограничиваются перечисленным, соединения, раскрытые в пат. США №№ 6140354, 6191160, 6258837, 6313298, 6337332, 6329395 и 6340683, пат. США №№ 6326375, 6329395, 6337332, 6335345, Европейских патентах №№ EP-01010691 и EP 01044970, и в международных патентных публикациях согласно PCT №№ WO 97/19682, WO 97/20820, WO 97/20821, WO 97/20822, WO 97/20823, WO 98/27063, WO 00/107409, WO00/185714, WO 00/185730, WO 00/64880, WO 00/68197, WO 00/69849, wo 01/09120, WO 01/85714, WO 01/85730, WO 01/07409, WO 01/02379, WO 01/02379, WO 01/23388, WO 01/23389, WO 01/44201, WO 01/62737, WO 01/62738, WO 01/09120, WO 02/20488, WO 02/22592, WO 02/48152, WO 02/49648 и WO 01/14376. Конкретные антагонисты NPY5, применимые в комбинациях по настоящему раскрытию, включают, но не ограничиваются перечисленным, GW-569180A, GW-594884A, GW-587081X, GW-548118X, FR 235,208, FR226928, FR 240662, FR252384, 1229U91, GI-264879A, CGP71683A, LY-377897, LY366377, PD-160170, SR-120562A, SR-120819A, JCF-104 и H409/22. Другие конкретные антагонисты NPY5, применимые в комбинациях по настоящему раскрытию, включают, но не ограничиваются перечисленным, соединения, раскрытые в Norman et al., J. Med. Chem., 43:42884312 (2000). Лептин включает, но не ограничивается перечисленным, рекомбинантный лептин человека (PEG-OB, Hoffman La Roche) и рекомбинантный метиониллептин человека (Amgen). Производные лептина (например, усеченные формы лептина), применимые в настоящем раскрытии, включают раскрытые в пат. США №№ 5552524, 5552523, 5552522, 5521283 и международных публикациях согласно PCT №№ WO 96/23513, WO 96/23514, WO 96/23515, WO 96/23516, WO 96/23517, WO 96/23518, WO 96/23519 и WO 96/23520.
Опиоидные антагонисты, применимые в настоящем раскрытии, включают соединения, раскрытые в заявке РСТ № WO 00/21509. Конкретные опиоидные антагонисты, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, налмефен (ревекс®), 3-метоксиналтрексон, налоксон и налтрексон. Антагонисты орексина, применимые в настоящем раскрытии, включают соединения, раскрытые в заявках на патент согласно РСТ №№ WO 01/96302, WO 01/68609, WO 02/51232, WO 02/51838 и WO 03/023561. Конкретные антагонисты орексина, применимые в настоящем раскрытии, включают, но не ограничивается, SB-334867-A. Ацилэстрогены, применимые в настоящем раскрытии, включают олеоилэстрон (del Mar-Grasa M. et al., Obesity Research, 9:202-9 (2001)). Агонисты холецистокинина-А (CCK-A), применимые в настоящем раскрытии, включают соединения, раскрытые в пат. США № 5739106. Конкретные агонисты CCK-A включают, но не ограничивается перечисленным, AR-R 15849, GI181771, JMv-180, A-71378, A-71623 и SR146131. Конкретные цилиарные нейротрофные факторы (CNTh), применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, GI-181771 (Glaxo-SmithKline), SR146131 (Sanofi Synthelabo), бутабиндид, PD170,292, PD 149164 (Pfizer). Приизводные CNTF, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, аксокин (Regeneron) и соединения, раскрытые в заявках согласно PCT №№ WO 94/09134, WO 98/22128 и WO 99/43813. Агонисты секретагога гормона роста (GHS), применимые в настоящем раскрытии, включают соединения, раскрытые в пат. США № 6358951 и в заявках на патент США №№ 2002/049196 и 2002/022637, и в заявках согласно PCT №№ WO 01/56592 и WO 02/32888. Конкретные агонисты GHS включают, но не ограничивается перечисленным, NN703, гексарелин, MK-0677, SM-130686, CP424 391, L-692429 и L-163255.
Агонисты 5НТ2, применимые в настоящем раскрытии, включают соединения, раскрытые в пат США № 3914250 и в заявках согласно PCT №№ WO 02/36596, WO 02/48124, WO 02/10169, WO 01/66548, WO 02/44152, WO 02/51844, WO 02/40456 и WO 02/40457. Конкретные агонисты 5HT2c, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, BVT933, DPCA37215, 1K264, PNU 22394, WAY161503, R-1065 и YM 348.
Агонисты Mc4r, применимые в настоящем раскрытии, включают соединения, раскрытые в заявках согласно PCT №№ WO 99/64002, WO 00/74679, WO 01/991752, WO 01/74844, WO 01/70708, WO 01/70337, WO 01/91752, WO 02/059095, WO 02/059107, WO 02/059108, WO 02/059117, WO 02/12166, WO 02111715, WO 02/12178, WO 02/15909, WO 02/068387, WO 02/068388, WO 02/067869, WO 03/007949 и WO 03/009847. Конкретные агонисты Mc4r, применимые в настоящем раскрытии, включают CIR86036 (Chiron), ME-10142 и ME-10145 (Melacure).
Ингибиторы повторного поглощения моноамина, применимые в настоящем раскрытии, включают соединения, раскрытые в заявках согласно PCT №№ WO 01/27068 и WO 01/62341. Конкретные ингибиторы повторного поглощения моноамина, применимые в настоящем раскрытии, включают, но не ограничиваются, сибутрамин (Meridia O/редуктил®), раскрытый в пат. США №№ 4746680, 4806570 и 5436272 и публикации патента США № 2002/0006964.
Ингибиторы повторного поглощения серотонина и высвободители, применимые в настоящем раскрытии, включают дексфенфлурамин, флуоксетин и другие ингибиторы повторного поглощения серотонина, включая, но не ограничиваясь перечисленным, соединения, раскрытые в пат США № 6365633 и заявках на патент согласно PCT №№ WO 01/27060 и WO 01/162341.
Ингибитор 11 β HSD-1, применимый в настоящем раскрытии, включает, но не ограничивается перечисленным, BVT 3498, BVT 2733 и соединения, раскрытые в WO 01/90091, WO 01/90090, WO 01/90092. Активаторы разобщающего белка (UCP-1, UCP-2 и UCP-3), применимые в настоящем раскрытии, включают соединения, раскрытые в заявке на патент согласно PCT № WO 99/00123. Конкретные активаторы разобщающего белка (UCP-1, UCP-2 и UCP-3), применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, фитановую кислоту, 4-[(E)-2-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафталенил)-1-пропенил]бензойную кислоту (TTNPB) и ретиноевую кислоту.
Агонисты адренергического рецептора β3 (β3), применимые в настоящем раскрытии, включают соединения, раскрытые в пат. США № 5705515 и пат. США № 5451677 и заявках на патент согласно PCT №№ 01/74782 и WO 02/32897. Конкретные агонисты β, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, AD9677/TAK677 (Dainippon/Takeda), CL-316,243, SB 418790, BRL-37344, L-796568, BMS-196085, BRL-35135A, CGP12177A, BTA-243, GW 427353, трекадрин, Zeneca D7114 и SR 59119A.
Агонисты тиреоидного гормона β, применимые в настоящем раскрытии, включают соединения, раскрытые в заявке согласно PCT №№ WO 02/15845 и заявке на патент Японии № JP 2000256190. Конкретные агонисты тиреоидного гормона β, применимые в настоящем раскрытии, включают, но не ограничивается, КВ-2611 (KaroBioBMS). Конкретные ингибиторы синтазы жирных кислот (PAS), применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, церуленин и C75. Конкретные ингибиторы фосфодиэстеразы (PDE), применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, теофиллин, пентоксифиллин, запринаст, силденафил, арнринон, милринон, цилостамид, ролипрам и циломиласт.
Ингибиторы липазы, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, ингибиторы, раскрытые в заявке согласно РСТ № WO 01/77094 и пат. США №№ 4598089, 4452813, 5512565, 5391571, 5602151, 4405644, 4189438 и 4242453. Конкретные ингибиторы липазы, применимые в настоящем раскрытии, включают, но не ограничивается перечисленным, тетрагидролипстатин (орлистат/ксеникал®), тритон WR1339, RHC80267, липстатин, теасапонин и диэтилумбеллиферилфосфат, FL-386, WAY-121898, Bay-N-3176, валилактон, эстерацин, эбелактон A, эбелактон B и RHC 80267.
Примеры ингибиторов HMG-CoA-редуктазы включают, но не ограничивается перечисленным, ловастатин, симвастатин, правастатин и флувастатин. Примерами ингибиторов HMG-CoA-синтазы являются производные бета-лактона, раскрытые в патентах США 4806564, 4816477, 4847271 и 4751237; производные бета-лактама, раскрытые в U.S. 4983597 и U.S.S.N. 07/540992, поданной 20 июня 1990; и замещенные аналоги оксациклопропана, раскрытые в публикации Европейского патента EP 0411703. Примеры ингибиторов скваленэпоксидазы раскрыты в публикации Европейского патента EP 0318860 и в публикации патента Японии J02 169-571A. Примеры молекул-индукторов гена LDL-рецептора раскрыты в патенте США 5182298, зарегистрированном 18 марта 1991. Другие снижающие холестерин средства, которые можно вводить, включают ниацин, пробукол, фиброевые кислоты (т.е. клофибрат и гемфиброзил) и индукторы гена LDL-рецептора.
Примеры ингибиторов PARP включают, но не ограничиваются перечисленным, иоднитокумарин, 5-иод-6-нитрокумарин, 3,4-дигидро-5-метилизохинолинон, 4-амино-l,8-нафталимид, 3-метоксибензамид, 8-гидрокси-2-метил-3-гидрохиназолин-4-он, 2-{3-[4-(4-фторфенил)-3,6-дигидро-l(2h)-пиридинил]пропил}-8-метил-4(3h)хиназолинон, 5-фтор-l-[4-(4-фенил-3,6-дигидропиридин-l-бутил)]хиназолин-2,4(lh,3h)дион, 3-(4-хлорфенил)хиноксалин-5-карбоксамид, 2-(3'-метоксифенил)бензимидазол-4-карбоксамид, бензамид, 3-аминобензамид, 3-аминофталгидразид и 1,5-дигидроксиизохинолин.
Вышеуказанные соединения, которые можно использовать в комбинации с соединением формулы (I), формулы (Ia), формулы (Ib), формулы (II) или формулы (III) или его фармацевтически приемлемой солью, можно получить и вводить так, как описано в технике, и так, как в документах, цитированных выше.
Вышеуказанные соединения являются только пояснениями ингибиторов ACMSD, противодиабетических средств, средств против ожирения, средств, снижающих холестерин, соединений, которые поддерживают уровни NAD+, соединений, которые подавляют расход NAD+, которые можно использовать в композициях по настоящему раскрытию. Так как этот список соединений не предназначен быть исчерпывающим, в способах по настоящему раскрытию можно использовать любые средства против ожирения и любые противодиабетические средства, которые не ограничиваются каким-либо определенным структурным классом соединений.
При использовании в настоящем описании «комбинированная терапия» включает введение соединения по настоящему раскрытию или его фармацевтически приемлемой соли, пролекарства, метаболита, полиморфа или сольвата и по меньшей мере второго средства как части специфической схемы лечения, предполагаемой для получения благоприятного действия от совместного введения таких терапевтических средств. Благоприятное действие комбинации включает, но не ограничивается перечисленным, совместное, например, синергичное действие и/или фармакокинетическое или фармакодинамическое совместное действие или их любую комбинацию, являющиеся результатом комбинации терапевтических средств. Введение таких терапевтических средств в комбинации типично осуществляют в течение определенного периода времени (обычно минут, часов, дней или недель, в зависимости от выбранной комбинации). «Комбинированная терапия» может быть предназначена, но как правило, не предназначена, для включения введения двух или больше таких терапевтических средств как части раздельных схем лечения, которые в связи с этим и произвольно приводят к комбинациям по настоящему раскрытию.
«Комбинированная терапия» предназначена для включения введения таких терапевтических средств последовательно, где каждое терапевтическое средство вводят в различное время и в любом порядке или чередуя и в любом порядке, а также введения таких терапевтических средств или по меньшей мере двух терапевтических средств по существу одновременно. Введение по существу одновременно можно выполнить, например, вводя субъекту одну капсулу, имеющую фиксированную долю каждого терапевтического средства, или несколько отдельных капсул для каждого терапевтического средства. Последовательное или по существу одновременное введение каждого терапевтического средства можно выполнить любым соответствующим путем, включая, но без ограничения, пероральные пути, внутривенные пути, внутримышечные пути и прямое поглощение через ткани слизистой оболочки. Терапевтические средства можно вводить одинаковым путем или различными путями. Например, первое терапевтическое средство выбранной комбинации можно ввести внутримышечной инъекцией, в то время как другие терапевтические средства можно ввести перорально. С другой стороны, например, все терапевтические средства можно вводить перорально, или все терапевтические средства можно вводить внутривенной инъекцией. Последовательность, в которой вводят терапевтические средства, являтся не слишком критической.
Все проценты и соотношения, используемые в настоящем описании, если не указано иное, являются массовыми. Другие особенности и преимущества настоящего раскрытия станут очевидны из различных примеров. Предлагаемые примеры иллюстрируют различные компоненты и методологию, применимые при практическом осуществлении настоящего раскрытия. Вообще говоря, раскрытие расширяется до любой новой особенности или любой новой комбинации особенностей, раскрытых в настоящем описании (включая прилагаемые формулу изобретения и чертежи). Примеры не ограничивают заявленное раскрытие. Таким образом, признаки, целые числа, характеристики, соединения или химические группы, описанные в сочетании с определенным аспектом, воплощением или примером раскрытия, должны пониматься как применимые к любому другому аспекту, воплощению или примеру, описанным в настоящем описании, если не являются вследствие этого несовместимыми. На основании настоящего раскрытия специалисты могут идентифицировать и использовать другие компоненты и методологию, применимые для практического осуществления настоящего раскрытия. Кроме того, если не указано иное, любая особенность, раскрытая в настоящем описании, может быть заменена альтернативной особенностью, служащей такой же или схожей цели.
Теперь раскрытие будет описываться с помощью примеров только с обращением к примерам, приведенным ниже.
ПОЯСНЕНИЕ ПРИМЕРАМИ
1. ПОЛУЧЕНИЕ СОЕДИНЕНИЙ
Общие способы и материалы
Все химикаты закупают у Sigma-Aldrich, Alfa Aesar. Спектры 1H ЯМР регистрируют при 200 и 400 МГц, и спектры 13C ЯМР регистрируют при 100,6 и 50,3 МГц, используя дейтерированные растворители, указанные ниже. TCХ осуществляют на силикагелевых пластинах на алюминиевой поверхности (силикагель 60 F254). Все реакции выполняют в атомсфере азота с использованием перегнанных растворителей. Найдено, что все испытываемые соединения имеют чистоту >95%, определенную ВЭЖХ анализом. Воду чистотой для ВЭЖХ получают из тандемного аппарата Milli-Ro/Milli-Q. Аналитические измерения ВЭЖХ осуществляют на Shimadzu LC-20AProminence, снабженном передающим модулем шины CBM-20A, двумя плунжерными сдвоенными насосами LC-20AD, фотодиодным матричным детектором SPD-M20A и инжектором 7725i с 20-мкл петлей из нержавеющей стали.
Схема 1. Получение промежуточного соединения 1.4
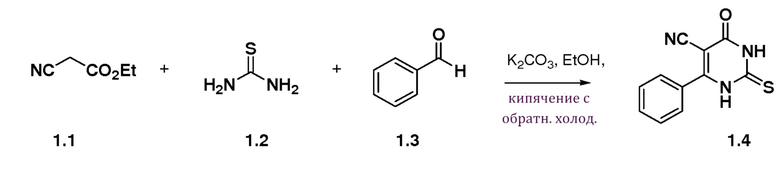
Пример 1. Получение промежуточного соединения 1.4
К раствору соединения 1.1 (0,52 мл, 4,9 ммоль), 1.2 (372 мг, 4,9 ммоль) и 1.3 (0,5 мл, 0,83 мл, 4,9 ммоль) в этаноле (25 мл) при перемешивании добавляют К2СО3 (812 мг, 5,88 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. После охлаждения собирают бледно-желтое твердое вещество, растворяют в кипящей воде и снова фильтруют. Водную фазу подкисляют до рН 5 АсОН (15 капель), выпавшее в осадок вещество отфильтровывают и сушат в вакууме. Получают названное в заголовке соединение 1.4 в виде бледно-желтого твердого вещества (500 мг, 2,18 ммоль). Выход 44%.
Схема 2. Получение промежуточного соединения 2.2
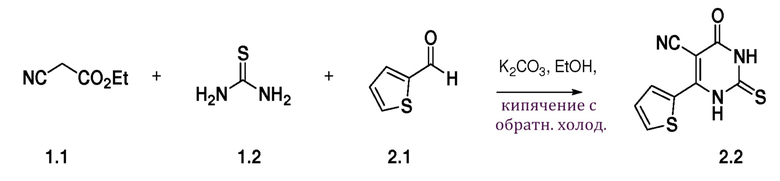
Пример 2. Получение промежуточного соединения 2.2
К раствору соединения 1.1 (0,96 г, 8,8 ммоль), 1.2 (672 мг, 8,8 ммоль) и 2.1 (1 г, 0,83 мл) в этаноле (55 мл) при перемешивании добавляют К2СО3 (1,57 г, 11,44 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. После охлаждения собирают желтоватое твердое вещество, растворяют в горячей воде и снова фильтруют. Водную фазу подкисляют до рН 1, выпавшее в осадок вещество отфильтровывают и сушат в вакууме. Получают названное в заголовке соединение 2.2 в виде желтоватого твердого вещества (1 г, 4,25 ммоль). Выход 49%. 1H ЯМР (200 МГц, ДМСО) δ 7,22 (м, 1H), 7,68 (м, 1H), 7,85 (д, J=4,8 Гц, 1H), 8,05 (с, 1H).
Схема 3. Получение промежуточного соединения 3.2
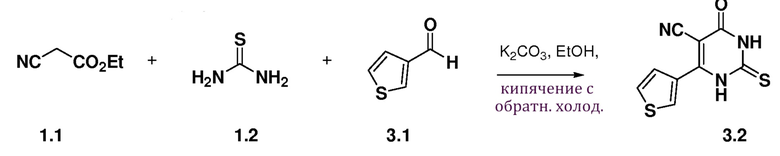
Пример 3. Получение промежуточного соединения 3.2
К раствору соединения 1.1 (0,96 г, 8,8 ммоль), 1.2 (672 мг, 8,8 ммоль) и 3.1 (1 г, 1,29 мл) в этаноле (55 мл) при перемешивании добавляют К2СО3 (1,57 г, 11,44 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. После охлаждения собирают желтоватое твердое вещество, растворяют в горячей воде и снова фильтруют. Водную фазу подкисляют до рН 1, выпавшее в осадок вещество отфильтровывают и сушат в вакууме. Получают названное в заголовке соединение 3.2 в виде желтоватого твердого вещества (1 г, 4,25 ммоль). Выход 49%.
Схема 4. Получение промежуточного соединения 4.2
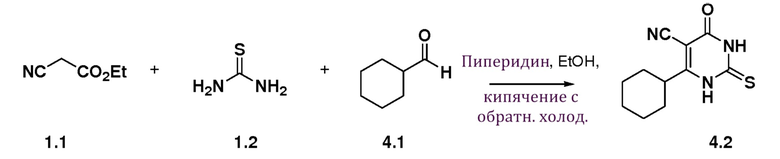
Пример 4. Получение промежуточного соединения 4.2
К раствору соединения 1.1 (1,42 г, 13,37 ммоль), 1.2 (1,01 г, 13,3 ммоль) и 4.1 (1,62 мл, 13,3 ммоль) в этаноле (50 мл) при перемешивании добавляют пиперидин (2,64 мл, 26,7 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. После охлаждения собирают твердое вещество, растворяют в горячей воде и снова фильтруют. Водную фазу подкисляют до рН 1 и экстрагируют EtOAc (3×25 мл). Органическую фазу промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией (CHCl3/МеОН, градиент от 0 до 2% для продукта), и получают названное в заголовке соединение 4.2 в виде белого твердого вещества (930 мг, 3,25 ммоль). Выход 30%.
Схема 5. Получение промежуточного соединения 5.2
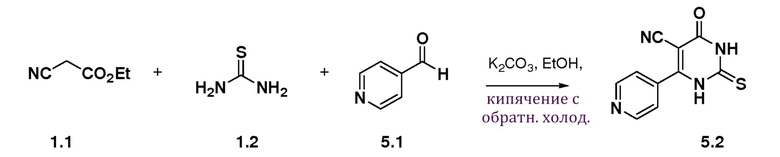
Пример 5. Получение промежуточного соединения 5.2
К раствору соединения 1.1 (0,49 мл, 4,67 ммоль), 1.2 (355 мг, 4,67 ммоль) и 5.1 (0,44 мл, 4,67 ммоль) в этаноле (25 мл) при перемешивании добавляют К2СО3 (773 мг, 5,6 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. После охлаждения собирают белое твердое вещество и используют на следующей стадии без дополнительной очистки. Получают названное в заголовке соединение 5.2 в виде белого твердого вещества (300 мг, 1,3 ммоль). Выход 29%. 1H ЯМР (400 МГц, ДМСО) δ 7,64 (д, J=4,7 Гц, 2H), 8,78 (д, J=4,7 Гц, 2H), 12,98 (с, 1H).
Схема 6. Получение промежуточного соединения 6.2
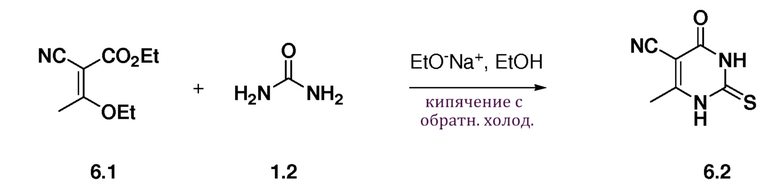
Пример 6. Получение промежуточного соединения 6.2
К раствору NaOEt (1,02 мл, 2,73 ммоль) в абс. EtOH (20 мл) при перемешивании добавляют соединение 6.1 (500 мг, 2,73 ммоль) и 1.2 (207 мг, 2,73 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение 4 час. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде и подкисляют АсОН. Выпавшее в осадок вещество собирают растворенным в воде и промывают смесью CHCl3 и МеОН. Водную фазу экстрагируют EtOAc (3×20 мл). Собранную органическую фазу промывают рассолом и сушат над Na2SO4. Получают названное в заголовке соединение 6.2 в виде белого твердого вещества (250 мг, 1,49 ммоль). Выход 55%.
Схема 7. Получение промежуточного соединения 7.3
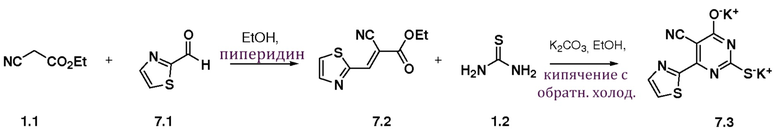
Пример 7а. Получение промежуточного соединения 7.2
К раствору соединения 1.1 (0,14 мл, 1,3 ммоль) и соединения 7.1 (150 мг, 1,3 мл) в EtOH (5 мл) при перемешивании добавляют пиперидин (1 капля). Перемешивание продолжают при комнатной температуре в течение ночи. Растворитель удаляют в вакууме. Сырой продукт реакции очищают флэш-хроматографией, и получают названное в заголовке соединение 7.2 (160 мг, 0,77 ммоль) в виде желтоватого твердого вещества. Выход 58%.
Пример 7b. Получение промежуточного соединения 7.3
К суспензии соединения 7.2 (150 мг, 0,72 ммоль) и соединения 1.2 (55 мг, 0,72 ммоль) в EtOH (5 мл) при перемешивании добавляют К2СО3 (99 мг, 0,72 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. Выпавшее в осадок белое твердое вещество собирают и используют как таковое на следующей стадии без дополнительной очистки. Получают названное в заголовке соединение 7.3 (150 мг, 0,48 ммоль) в виде желтоватого твердого вещества как дикалиевую соль. Выход 67%.
Схема 8. Получение промежуточного соединения 8.5
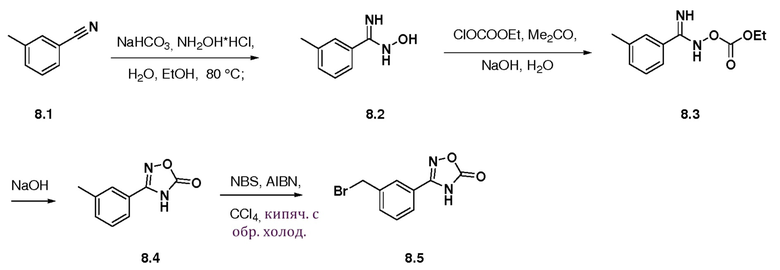
Пример 8а. Получение промежуточного соединения 8.2
К раствору NH2OH*HCl и NaHCO3 в воде (7 мл) при перемешивании постепенно добавляют раствор м-толунитрила (8.1) (2 мл, 17,0 ммоль) в EtOH (13,3 мл). Перемешивание продолжают при 80°С в течение 4 час. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде и экстрагируют EtOAc (3×25 мл). Органическую фазу собирают, промывают рассолом, сушат над Na2SO4, и получают названное в заголовке соединение 8.2 (1,5 г, 9 ммоль) в виде белого твердого вещества. Выход 59%.
Пример 8b. Получение промежуточного соединения 8.3
К раствору соединения 8.2 (1 г, 6 ммоль) в сухом ацетоне (5 мл) добавляют по каплям при 0°С EtOCOCl (0,63 мл, 6,6 ммоль). Продолжают перемешивание при этой температуре в течение 1 часа. Затем к смеси добавляют 5% раствор NaOH. Продолжают перемешивание еще в течение 1 часа. Растворитель удаляют в вакууме. Сырую реакционную смесь выливают в воду и экстрагируют EtOAc (3×50 мл). Собранную органическую фазу промывают рассолом и сушат над Na2SO4. Получают названное в заголовке соединение 8.3 (600 мг, 2,7 ммоль) в виде белого твердого вещества. Выход 45%.
Пример 8с. Получение промежуточного соединения 8.4
К раствору соединения 8.3 (300 мг, 1,35 ммоль) в абс. EtOH (5 мл) добавляют по частям натрий (50 мг). Продолжают перемешивание при комнатной температуре еще в течение 4 час. Реакцию гасят, добавляя МеОН. Растворитель удаляют при пониженном давлении, и сырой остаток очищают флэш-хроматографией. Получают названное в заголовке соединение 8.4 (150 мг, 0,85 ммоль) в виде белого твердого вещества. Выход 63%.
Пример 8d. Получение промежуточного соединения 8.5
К суспензии соединения 8.4 (326 мг, 1,85 ммоль) в CCl4 (10 мл) добавляют AIBN (60,7 мг, 0,37 ммоль) и NBS (493 мг, 2,77 ммоль). Продолжают перемешивание при кипячении с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении. Продукт реакции растворяют в воде, экстрагируют EtOAc (3×20 мл), экстракт промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью петролейный эфир (петр.эфир)/EtOAc (30% для продукта), и получают названное в заголовке соединение 8.5 (280 мг, 1,09 ммоль) в виде белого твердого вещества. Выход 59%.
Схема 9. Получение промежуточного соединения 9.2
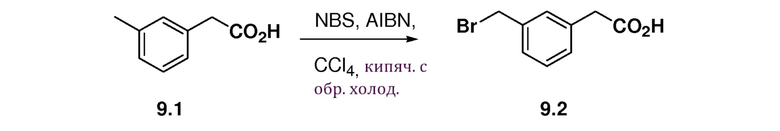
Пример 9. Получение промежуточного соединения 9.2
К суспензии соединения 9.1 (750 мг, 5 ммоль) в CCl4 (15 мл) добавляют AIBN (41 мг, 0,25 ммоль) и NBS (933,7 мг, 5,24 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении. Продукт реакции растворяют в воде, экстрагируют EtOAc (3×20 мл), экстракт промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью CH2Cl2/МеОН (3% для продукта), и получают названное в заголовке соединение 9.2 (800 мг, 3,49 ммоль) в виде белого твердого вещества. Выход 70%.
Схема 10. Получение промежуточного соединения 10
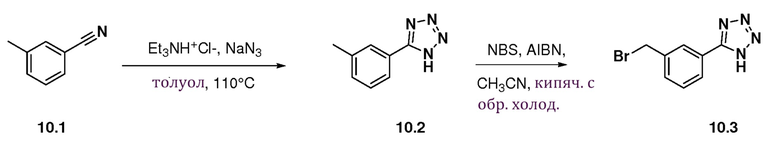
Пример 10а. Получение промежуточного соединения 10.2
Смесь соединения 10.1 (1,02 мл, 8,54 ммоль), NaN3 (832 мг, 12,8 ммоль) и Et3N.HCl (1,76 г, 12,6 ммоль) кипятят с обратным холодильником 4 часа. Растворитель удаляют при пониженном давлении. Сырой продукт выливают в воду, подкисляют до рН 1 3 N HCl и экстрагируют EtOAc (3×20 мл). Органическую фазу промывают рассолом, сушат над Na2SO4 и концентрируют при пониженном давлении. Получают названное в заголовке соединение 10.2 (1,22 г, 7,6 ммоль) в виде белого твердого вещества. Выход 89%.
Пример 10b. Получение промежуточного соединения 10.3
К суспензии соединения 10.2 (300 мг, 1,87 ммоль) в CН3CN (15 мл) добавляют AIBN (31 мг, 0,18 ммоль) и NBS (333 мг, 1,87 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении. Продукт реакции растворяют в воде, экстрагируют EtOAc (3×20 мл), экстракт промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью CH2Cl2/МеОН (7% для продукта), и получают названное в заголовке соединение 10.3 (150 мг, 0,62 ммоль) в виде светло-желтого твердого вещества. Выход 34%.
Схема 11. Получение промежуточного соединения 11.3
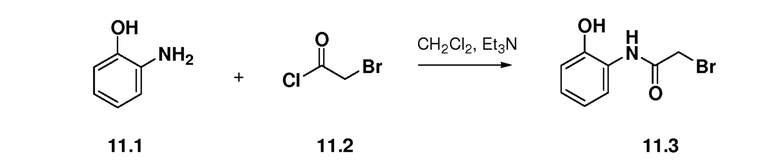
Пример 11. Получение промежуточного соединения 11.3
К раствору соединения 11.1 (2,5 г, 23 ммоль) в CH2Cl2 (25 мл) добавляют пиридин (1,63 мл, 20,3 ммоль) и соединение 11.2 (1,68 мл, 20,3 ммоль). Перемешивание продолжают при комнатной температуре в течение ночи. Растворитель удаляют при пониженном давлении. Продукт реакции растворяют в воде, экстрагируют CH2Cl2 (3×30 мл), экстракт промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью петр.эфир/EtOAc (25% для продукта), и получают названное в заголовке соединение 11.3 (735 мг, 3,19 ммоль) в виде коричневатого твердого вещества. Выход 14%.
Схема 12. Получение промежуточного соединения 12.2
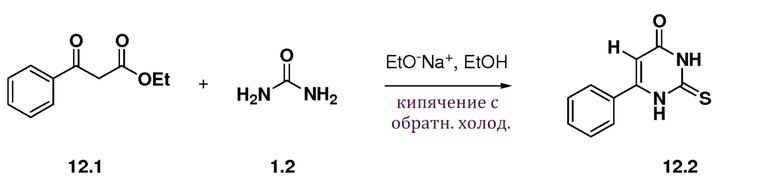
Пример 12. Получение промежуточного соединения 12.2
К раствору соединения 12.1 (2 г, 10,41 ммоль) в EtOH (15 мл) добавляют EtONa (7 мл, 18,7 ммоль) и соединение 1.2 (1,18 г, 15,61 ммоль). Продолжают перемешивание при кипячении с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении. Продукт реакции растворяют в воде, подкисляют до рН 3, экстрагируют EtOAc (3×20 мл), экстракт промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью CH2Cl2/МеОН (2,5% для продукта), и получают названное в заголовке соединение 12.2 (500 мг, 2,44 ммоль) в виде белого твердого вещества. Выход 24%.
Схема 13. Получение промежуточного соединения 13.2
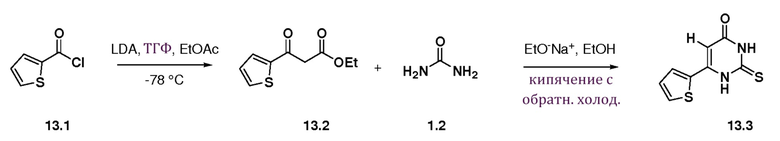
Пример 13а. Получение промежуточного соединения 13.2
К раствору DIPA (7,6 мл, 54 ммоль) в ТГФ (53 мл) при перемешивании при 0°С добавляют н-BuLi (21,6 мл). Перемешивание продолжают при такой температуре в течение 10 минут. Затем смесь охлаждают до -78°С, и добавляют по каплям EtOAc (2,4 мл, 27 ммоль). Перемешивание продолжают при такой температуре в течение 30 минут. После этого добавляют по каплям раствор соединения 13.1 (3 мл, 27 ммоль) в ТГФ (20 мл). Реакционной смеси позволяют нагреваться до комнатной температуре и перемешивают в течение ночи. Сырой продукт реакции выливают в воду и экстрагируют EtOAc (3×30 мл). Собранную органическую фазу промывают рассолом, сушат над Na2SO4 и концентрируют в вакууме. Получают названное в заголовке соединение 13.2 в виде коричневатого масла (4,8 г, 24,3 ммоль). Выход 90%.
Пример 13b. Получение промежуточного соединения 13.3
К раствору промежуточного соединения 13.2 (2 г, 10 ммоль) в EtOH (15 мл) добавляют EtONa (21% раствор, мас./мас., в EtOH) (7,5 мл, 20 ммоль) и соединение 1.2 (1,15 г, 15,1 ммоль). Перемешивание продолжают при кипячении с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении. Реакционную смесь растворяют в воде. При рН 10 извлекают непрореагировавший исходный материал. Затем смесь подкисляют до рН 5, экстрагируют EtOAc (3×20 мл), экстракты промывают рассолом и сушат над Na2SO4. Сырой продукт реакции очищают флэш-хроматографией, элюируя смесью CH2Cl2/МеОН (7% для продукта), и получают названное в заголовке соединение 13.3 (435 мг, 2,06 ммоль) в виде желтоватого твердого вещества. Выход 21%.
Схема 14. Получение соединения 1
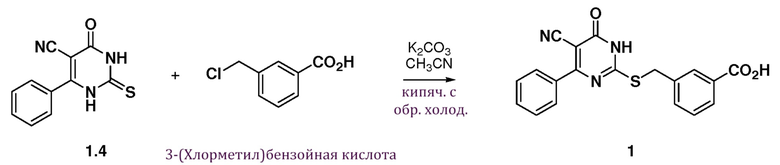
Пример 14. Получение соединения 1
К суспензии промежуточного соединения 1.4 (1,6 г, 6,98 ммоль) и К2СО3 (2,88 г, 20,9 ммоль) в CH3CN (80 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (1,19 г, 6,98 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, подкисляют до рН 5 и промывают EtOAC для удаления примесей. Затем рН доводят до 3/4, и смесь экстрагируют EtOAc (3×50 мл). Растирание в ацетоне дает соединение 1 (936 мг, 2,78 ммоль) в виде желтоватого твердого вещества. Выход 40%. 1H ЯМР (400 МГц, ДМСО) δ 4,58 (с, 2H), 7,44 (т, J=7,5 Гц, 1H), 7,54-7,61 (м, 3H), 7,67 (д, J=7,1 Гц, 1H), 7,83 (д, J=7,5 Гц, 1H), 7,91 (д, J=7,27 Гц, 2H), 8,04 (с, 1H), 13 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 33,5, 93,2, 115,6, 128,2, 128,4, 128,4, 128,5, 128,5, 128,6, 129,7, 130,8, 131,5, 133,3, 135,1, 137,4, 165,4, 166,8, 167,3. ВЭЖХ: 96,3%.
Схема 15. Получение соединения 4
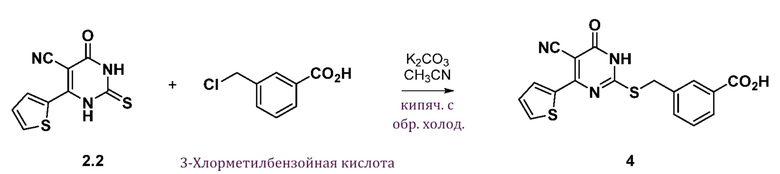
Пример 15. Получение соединения 4
К суспензии промежуточного соединения 2.2 (250 мг, 1,06 ммоль) и К2СО3 (440 мг, 3,18 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (180 мг, 1,06 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 1 и экстрагируют EtOAc (3×50 мл). Растирание в горячем ацетоне дает соединение 4 (45 мг, 0,12 ммоль) в виде желтоватого твердого вещества. Выход 12%. 1H ЯМР (400 МГц, ДМСО) δ 4,62 (с, 2H), 7,33 (т, J=4,3 Гц, 1H), 7,44 (т, J=7,6 Гц, 1H), 7,72 (д, J=7,5 Гц, 1H), 7,82 (д, J=7,5 Гц, 1H), 8,05 (м, 2H), 8,26 (д, J=3,8 Гц, 1H), 12,99 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 33,9, 88,7, 116,5, 128,8, 129,3, 129,9, 130,2, 131,5, 132,1, 133,7, 135,4, 137,9, 139,7, 159,0, 161,2, 165,3, 167,4. ВЭЖХ: 97,2%.
Схема 16. Получение соединения 3
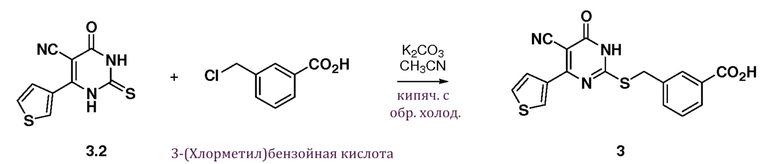
Пример 16. Получение соединения 3
К суспензии промежуточного соединения 3.2 (250 мг, 1,06 ммоль) и К2СО3 (440 мг, 3,18 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (180 мг, 1,06 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 1 и экстрагируют EtOAc (3×50 мл). Растирание в смеси Et2O/ацетон дает соединение 3 (260 мг, 0,7 ммоль) в виде желтоватого твердого вещества. Выход 70%. 1H ЯМР (400 МГц, ДМСО) δ 4,63 (с, 2H), 7,44 (т, J=7,6 Гц, 1H), 7,69 (д, J=7,7 Гц, 1H), 7,74 (дд, J=5 Гц, J=2,9 Гц, 1H), 7,84 (м, 2H), 8,05 (с, 1H), 8,58 (м, 1H), 13,0 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 35,3, 90,1, 118,0, 130,2, 130,7, 131,3, 131,6, 132,9, 133,5, 135,1, 136,8, 139,3, 141,1, 160,4, 162,7, 166,7, 168,8. ВЭЖХ: 95,0%.
Схема 17. Получение соединения 6
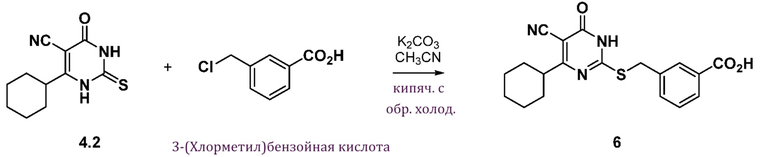
Пример 17. Получение соединения 6
К суспензии промежуточного соединения 4.2 (280 мг, 1,18 ммоль) и К2СО3 (495 мг, 3,56 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (202 мг, 1,18 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 1 и экстрагируют EtOAc (3×50 мл). Растирание в Et2O дает соединение 6 (90 мг, 0,24 ммоль) в виде белого твердого вещества. Выход 21%. 1H ЯМР (400 МГц, ДМСО) δ 1,24 (м, 3H), 1,60 (м, 7H), 2,74 (м, 1H), 4,52 (с, 2H), 7,45 (т, J=7,18 Гц, 1H), 7,67 (д, J=6,83 Гц, 1H), 7,82 (д, J=7,17 Гц, 1H), 8,04 (с, 1H), 13,0 (с, 1H). 13C ЯМР (100 МГц, ДМСО) δ 25,4, 25,7, 25,7, 30,3, 30,3, 33,8, 44,9, 94,1, 115,3, 128,6, 129,2, 130,1, 131,3, 133,6, 138,5, 161,1, 166,2, 167,4, 177,9. ВЭЖХ: 98,1%.
Схема 18. Получение соединения 7
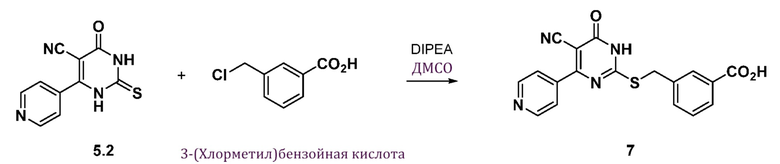
Пример 18. Получение соединения 7
К суспензии промежуточного соединения 5.2 (220 мг, 0,95 ммоль) и DIPEA (0,18 мл, 1,05 ммоль) в ДМСО (5 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (178 мг, 1,05 ммоль). Перемешивание продолжают в течение ночи при комнатной температуре. Светло-желтое твердое вещество собирают, промывают смесью толченого льда и воды и сушат в вакууме. Растирание в горячем EtOАс дает соединение 7 (180 мг, 0,49 ммоль) в виде светло-желтого твердого вещества. Выход 53%. 1H ЯМР (400 МГц, ДМСО) δ 4,55 (с, 2H), 7,44 (м, 1H), 7,66 (д, J=6 Гц, 1H), 7,81 (м, 3H), 8,02 (с, 1H), 8,80 (с, 2H), 13,1 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 34,1, 94,8, 115,8, 122,8, 122,8, 128,7, 129,2, 130,4, 131,3, 133,9, 138,1, 143,1, 150,5, 150,5, 161,8, 165,7, 167,4, 167,4. ВЭЖХ: 95,1%.
Схема 19. Получение соединения 11
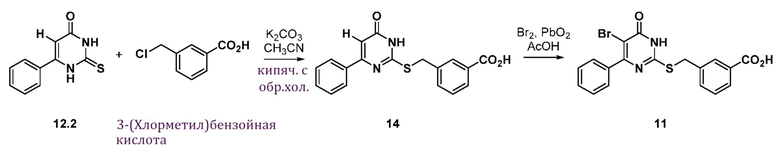
Пример 19а. Получение соединения 14
К суспензии промежуточного соединения 12.2 (100 мг, 0,4 ммоль) и К2СО3 (178 мг, 1,29 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (74 мг, 0,43 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Растирание в смеси Et2O/ацетон дает соединение 14 (30 мг, 0,088 ммоль) в виде белого твердого вещества. Выход 21%. 1H ЯМР (400 МГц, ДМСО) δ 4,59 (с, 2H), 6,69 (с, 1H), 7,41 (м, 1H), 7,46 (м, 3H), 7,71 (д, J=7,5 Гц, 1H), 7,81 (д, J=7,74 Гц, 1H), 8,06 (м, 3H), 12,85 (с, 2H). 13C ЯМР (100 МГц, ДМСО) δ 33,8, 127,3, 127,3, 128,5, 129,1, 129,2, 130,1, 131,0, 131,3, 131,5, 133,6, 136,3, 138,8, 167,5.
Пример 19b. Получение соединения 11
К раствору соединения 14 (100 мг, 0,29 ммоль) в уксусной кислоте (5 мл) при перемешивании добавляют диоксид свинца (77,2 мг, 0,32 ммоль) и бром (0,02 мл, 0,32 ммоль). Перемешивание продолжают в течение 6 час при комнатной температуре. Смесь выливают в раствор Na2S2O5 и экстрагируют EtOAc (3×20 мл). Собранные органические фазы промывают водой и рассолом, и затем их сушат над Na2SO4. Растирание в смеси Et2O/ацетон дает соединение 11 (40 мг, 0,09 ммоль) в виде белого твердого вещества. Выход 33%. 1H ЯМР (400 МГц, ДМСО) δ 4,44 (с, 2H), 7,42 (т, J=7,6 Гц, 1H), 7,48 (м, 3H), 7,61-7,65 (м, 3H), 7,82 (д, J=7,5 Гц, 1H), 8,0 (с, 1H), 13,1 (м, 2H). 13C ЯМР (100 МГц, ДМСО) δ 33,9, 128,4, 128,6, 129,14, 129,3, 129,3, 129,3, 130,1, 130,2, 131,3, 133,9, 138,1, 138,4, 167,5. ВЭЖХ: 94,2%.
Схема 20. Получение соединения 12

Пример 20а. Получение соединения 15
К суспензии промежуточного соединения 13.3 (235 мг, 1,11 ммоль) и К2СО3 (460 мг, 3,33 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (190 мг, 1,11 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Растирание в смеси Et2O/ацетон дает соединение 15 (150 мг, 0,44 ммоль) в виде белого твердого вещества. Выход 39%. 1H ЯМР (400 МГц, ДМСО) δ 4,55 (с, 2H), 6,64 (с, 1H), 7,19 (дд, J=4,9 Гц, J=3,8 Гц, 1H), 7,43 (т, J=7,7 Гц, 1H), 7,74 (д, J=7,6 Гц, 1H), 7,77 (д, J=4,9 Гц, 1H), 7,81 (д, J=7,8 Гц, 1H), 7,90 (д, J=3,6 Гц, 1H), 8,08 (с, 1H), 12,80 (с, 2H). 13C ЯМР (100 МГц, ДМСО) δ 33,5, 101,6, 128,1, 128,6, 129,1, 129,1, 130,1, 131,1, 131,4, 133,7, 138,9, 141,7, 167,4.
Пример 20b. Получение соединения 12
К раствору соединения 15 (134 мг, 0,39 ммоль) в уксусной кислоте (5 мл) при перемешивании добавляют диоксид свинца (102 мг, 0,42 ммоль) и бром (0,022 мл, 0,42 ммоль). Перемешивание продолжают в течение 6 час при комнатной температуре. Смесь выливают в раствор Na2S2O5 и экстрагируют EtOAc (3×20 мл). Собранные органические фазы промывают водой и рассолом, и затем их сушат над Na2SO4. Сырой продукт реакции подвергают очистке флэш-хроматографией с элюированием смесью CH2Cl2/МеОН (10% для продукта). Получают соединение 12 (45 мг, 0,11 ммоль) в виде белого твердого вещества. Выход 27%. 1H ЯМР (400 МГц, ДМСО) δ 4,56 (с, 2H), 7,27 (т, J=3,5 Гц, 1H), 7,44 (т, J=7,6 Гц, 1H), 7,72 (д, J=7,5 Гц, 1H), 7,82 (д, J=7,7 Гц, 1H), 7,92 (д, J=4,5 Гц), 8,07 (с, 1H), 8,33 (д, J=2,9 Гц, 1H), 13,1 (м, 2H). 13C ЯМР (100 МГц, ДМСО) δ 33,8, 128,6, 128,7, 128,7, 129,2, 130,1, 131,4, 132,3, 132,8, 133,6, 138,3, 141,1, 152,1, 158,5, 159,6, 167,4. ВЭЖХ: 95,2%.
Схема 21. Получение соединения 13
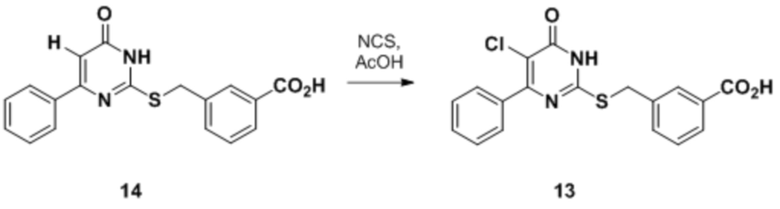
Пример 21. Получение соединения 13
К раствору соединения 14 (100 мг, 0,29 ммоль) в уксусной кислоте (5 мл) при перемешивании добавляют диоксид свинца (55,8 мг, 0,35 ммоль) и N-хлорсукцинимид (47 мг, 0,35 ммоль). Перемешивание продолжают в течение 6 час при комнатной температуре. Смесь выливают в воду и экстрагируют EtOAc (3×20 мл). Собранные органические фазы промывают водой и рассолом, и затем их сушат над Na2SO4. Растирание в смеси Et2O/ацетон дает соединение 13 (40 мг, 0,1 ммоль) в виде белого твердого вещества. Выход 37%. 1H ЯМР (400 МГц, ДМСО) δ 4,47 (с, 2H), 7,43 (т, J=7,7 Гц, 1H), 7,49 (м, 3H), 7,64 (д, J=7,2 Гц, 1H), 7,71 (м, 2H), 7,83 (д, J=7.5 Гц, 1H), 8,02 (с, 1H), 13,1 (с, 1H), 13,25 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 33,9, 128,4, 128,4, 128,6, 129,1, 129,4, 130,2, 131,3, 131,3, 133,8, 136,5, 138,3, 167,5. ВЭЖХ: 95,3%.
Схема 22. Получение соединения 22
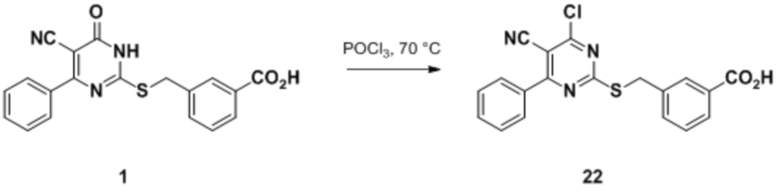
Пример 22. Получение соединения 22
Суспензию соединения 1 (160 мг, 0,44 ммоль) и POCl3 (3 мл) при перемешивании греют при 70°С в течение 6 час. Белая суспензия превращается в красную. Избыток POCl3 осторожно разрушают толченым льдом и затем водой. Смесь экстрагируют EtOAc (3×20 мл). Собранные органические фазы промывают рассолом, сушат над Na2SO4 и упаривают. Очистка флэш-хроматографией (градиент CH2Cl2/МеОН) дает названное в заголовке соединение 22 (60 мг, 0,16 ммоль) в виде белого твердого вещества. Выход 36%. 1H ЯМР (400 МГц, ДМСО) δ 4,58 (с, 2H), 7,44 (т, J=7,7 Гц, 1H), 7,58-7,62 (м, 2H), 7,66 (д, J=7,17 Гц, 1H), 7,70 (д, J=7,7 Гц, 1H), 7,82 (д, J=7,7 Гц, 1H), 7,94 (д, J=7,1 Гц, 2H), 8,08 (с, 1H), 12,98 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 34,9, 102,5, 115,2, 128,7, 129,2, 129,2, 129,6, 129,6, 130,4, 131,4, 132,7, 133,9, 134,7, 138,0, 162,9, 167,5, 169,0, 174,3. ВЭЖХ: 98,8%.
Схема 23. Получение соединения 10
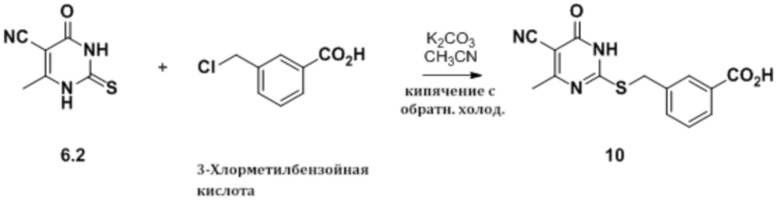
Пример 23. Получение соединения 10
К суспензии промежуточного соединения 6.2 (145 мг, 0,86 ммоль) и К2СО3 (599 мг, 4,33 ммоль) в CH3CN (15 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (148 мг, 0,86 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Сырой продукт реакции очищают флэш-хроматографией с элюированием смесью (CH2Cl2/МеОН+АсОН 3%), и получают названное в заголовке соединение 10 (60 мг, 0,2 ммоль) в виде белого твердого вещества. Выход 23%. 1H ЯМР (400 МГц, ДМСО) δ 2,44 (с, 3H), 4,49 (с, 2H), 7,45 (т, J=7,6 Гц, 1H), 7,68 (д, J=7,4 Гц, 1H), 7,82 (д, J=7,6 Гц, 1H), 8,05 (м, 1H), 13,1 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 23,3, 33,9, 95,3, 115,6, 128,7, 129,1, 130,6, 131,2, 134,1, 138,0, 161,1, 165,7, 167,4, 170,9. ВЭЖХ 96,5%.
Схема 24. Получение соединения 5
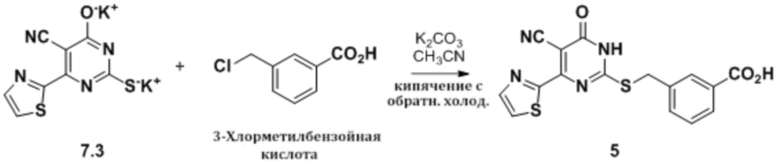
Пример 24. Получение соединения 5
К суспензии промежуточного соединения 7.3 (414 мг, 1,27 ммоль) и К2СО3 (526 мг, 3,81 ммоль) в CH3CN (20 мл) при перемешивании добавляют 3-(хлорметил)бензойную кислоту (217 мг, 1,27 ммоль). Перемешивание продолжают в течение ночи при кипячении с обратным холодильником. Летучие вещества удаляют в вакууме. Сырой продукт реакции растворяют в воде, промывают EtOAC, подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Названное в заголовке соединение 5 (260 мг, 0,5 ммоль) получают в виде чистого светло-желтого твердого вещества после растирания в смеси Et2O/ацетон. Выход 55%. 1H ЯМР (400 МГц, ДМСО) δ 4,62 (с, 2H), 7,45 (м, 1H), 7,74 (д, J=5,9 Гц, 1H), 7,82 (д, J=6,1 Гц, 1H), 8,08 (с, 1H), 8,21 (д, J=7,2 Гц, 2H), 12,9 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 34,0, 90,5, 114,9, 127,7, 128,8, 129,3, 130,1, 131,4, 133,7, 138,1, 146,2, 156,7, 161,9, 163,8, 166,5, 167,4. ВЭЖХ 96,5%.
Схема 25. Получение соединения 19
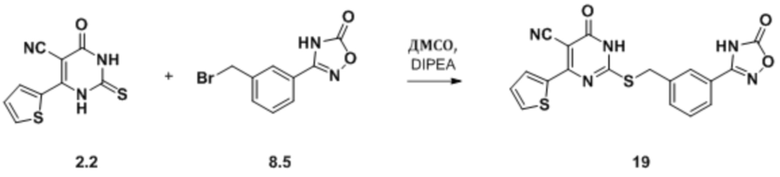
Пример 25. Получение соединения 19
К суспензии промежуточного соединения 2.2 (100 мг, 0,42 ммоль) и DIPEA (0,07 мл, 0,47 ммоль) в ДМСО (5 мл) при перемешивании добавляют промежуточное соединение 8.5 (120 мг, 0,47 ммоль). Перемешивание продолжают в течение ночи при комнатной температуре. Сырой продукт выливают в воду, промывают EtOАс, затем подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Названное в заголовке соединение 19 (65 мг, 0,15 ммоль) получают в виде чистого оранжевого твердого вещества после очистки флэш-хроматографией с элюированием смесью CH2Cl2/МеОН (10% для продукта). Выход 38%. 1H ЯМР (400 МГц, ДМСО) δ 4,37 (с, 2H), 7,20 (т, J=4 Гц, 1H), 7,45 (т, J=7,6 Гц, 1H), 7,63 (т, J=7,2 Гц, 2H), 7,75 (д, J=4,3 Гц, 1H), 7,88 (с, 1H), 8,07 (д, J=3 Гц, 1H); 13C ЯМР (100 МГц, ДМСО) δ 33,7, 85,7, 120,4, 124,9, 125,4, 126,7, 128,7, 128,8, 129,5, 131,1, 132,3, 140,6, 142,2, 159,1, 159,9, 163,3, 170,4, 171,3. ВЭЖХ 94,1%.
Схема 26. Получение соединения 18
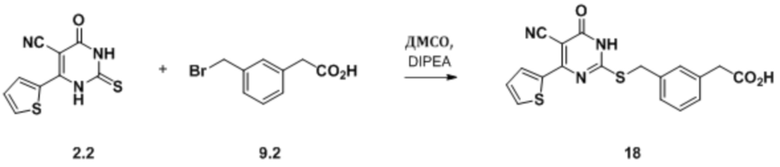
Пример 26. Получение соединения 18
К суспензии промежуточного соединения 2.2 (500 мг, 0,… ммоль) и DIPEA (0,4 мл, 2,12 ммоль) в ДМСО (5 мл) при перемешивании добавляют промежуточное соединение 9.2 (487 мг, 2,12 ммоль). Перемешивание продолжают в течение ночи при комнатной температуре. Сырой продукт выливают в воду, промывают EtOАс, затем подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Названное в заголовке соединение 18 (200 мг, 0,52 ммоль) получают в виде чистого желтоватого твердого вещества после очистки флэш-хроматографией с элюированием смесью CH2Cl2/МеОН (10% для продукта) и растирания в смеси Et2O/ацетон. Выход 25%. 1H ЯМР (400 МГц, ДМСО) δ 3,49 (с, 2H), 4,53 (с, 2H), 7,16 (д, J=6,8 Гц, 1H), 7,26 (т, J=7,2 Гц, 1H), 7,36 (м, 3H), 8,05 (д, J=4,4 Гц, 1H), 8,27 (с, 1H), 12,13 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 34,3, 40,9, 88,5, 116,8, 127,6, 128,9, 129,1, 129,8, 130,4, 131,9, 135,2, 135,8, 137,0, 139,9, 159,1, 161,6, 165,7, 172,9. ВЭЖХ 95,8%.
Схема 27. Получение соединения 17
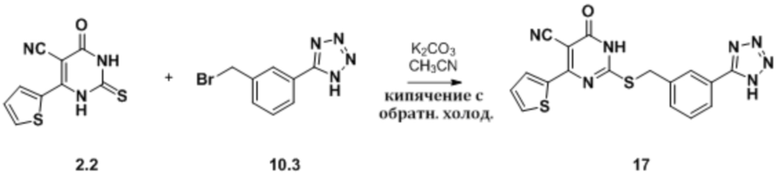
Пример 27. Получение соединения 17
К суспензии промежуточного соединения 2.2 (160 мг, 0,66 ммоль) и DIPEA (0,09 мл, 0,55 ммоль) в ДМСО (3 мл) при перемешивании добавляют промежуточное соединение 10.3 (171 мг, 0,55 ммоль). Перемешивание продолжают в течение ночи при комнатной температуре. Сырой продукт выливают в воду, промывают EtOАс, затем подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Названное в заголовке соединение 17 (90 мг, 0,22 ммоль) получают в виде чистого оранжевого твердого вещества после очистки флэш-хроматографией с элюированием смесью CH2Cl2/МеОН (5% для продукта) и предварительного растирания в смеси Et2O/ацетон. Выход 25%. 1H ЯМР (400 МГц, ДМСО) δ 4,59 (с, 2H), 7,29 (т, J=4,6 Гц, 1H), 7,54 (т, J=7,6 Гц, 1H), 7,68 (т, J=7,8 Гц, 1H), 7,91 (д, J=7,7 Гц, 1H), 7,96 (д, J=4,9 Гц, 1H), 8,16 (с, 1H), 8,22 (д, J=3,8 Гц, 1H); 13C ЯМР (100 МГц, ДМСО) δ 33,9, 88,9, 117,6, 125,0, 126,2, 127,9, 129,6, 129,9, 131,2, 131,9, 134,4, 139,3, 140,4, 155,8, 159,1, 163,8, 167,0. ВЭЖХ 96,2%.
Схема 28. Получение соединения 23
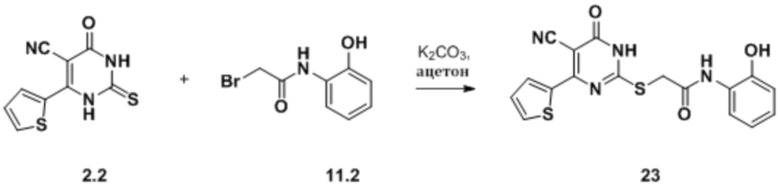
Пример 28. Получение соединения 23
К суспензии промежуточного соединения 2.2 (150 мг, 0,63 ммоль) и К2СО3 (96,6 мг, 0,70 ммоль) в ацетоне (10 мл) при перемешивании добавляют промежуточное соединение 11.2 (173 мг, 0,72 ммоль). Перемешивание продолжают в течение ночи при комнатной температуре. Летучие вещества удаляют в вакууме. Сырой продукт растворяют в воде, подкисляют до рН 3 и экстрагируют EtOAc (3×50 мл). Названное в заголовке соединение 23 (150 мг, 0,39 ммоль) получают в виде чистого оранжевого твердого вещества после очистки флэш-хроматографией с элюированием смесью CH2Cl2/МеОН (5% для продукта) и предварительного растирания в горячем EtOAc. Выход 62%. 1H ЯМР (400 МГц, ДМСО) δ 3,92 (с, 2H), 6,72 (т, J=7,7 Гц, 1H), 6,79 (д, J=7,6 Гц, 1H), 6,88 (т, J=7,3 Гц, 1H), 7,20 (т, J=4,26 Гц, 1H), 7,77 (д, J=4,7 Гц, 1H); 7,92 (д, J=7,8 Гц, 1H), 8,0 (д, J=3,5 Гц, 1H); 9,59 (с, 1H), 9,80 (с, 1H); 13C ЯМР (100 МГц, ДМСО) δ 35,12, 86,2, 115,5, 119,2, 120,1, 121,0, 124,4, 127,0, 128,7, 129,2, 131,4, 141,8, 147,3, 159,2, 167,9, 169,1, 170,5. ВЭЖХ 97,7%.
II. БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
Пример 29. Определение ингибирования ACMSD1
Активность соединений 1-19 и 21-23 как ингибиторов ACMSD1 определяют путем измерения конверсии 3ОН-антраниловой кислоты в продукт (т.е. ACMS) в спектрофотометрическом анализе in vitro.
Предварительную смесь для анализа, содержащую 3-гидроксиантраниловую кислоту (3ОН-НА), 3,4-диоксигеназу (HAО) и диализованный неочищенный экстракт клеток E. coli BL21 (DE3), экспрессирующих рекомбинантный фермент, инкубируют при 25°С, контролируя повышение поглощения при 360 нм из-за образования ACMS из 3ОН-НА. По завершении реакции в пределах ~2 мин добавляют аликвоту раствора ACMSD1 (полученной и очищенной из Pichia Pastoris, сверхэкспрессирущей рекомбинантный фермент), и за этим следует снижение поглощения при 300 нм с 15-секундными интервалами. Влияние концентрации ACMS на активность фермента исследуют, изменяя концентрацию 3ОН-НА от 2 до 20 мкМ. Кинетические параметры вычисляют из данных по начальной скорости, используя график Лайнувира-Берка.
Скорость снижения поглощения, вызванная ACMSD1, вычисляют, вычитая поглощение контрольной реакционной смеси без ACMSD из поглощения смеси, описанной выше. Одну единицу активности ACMSD указывают как количество фермента, которое приводит к 1 ммоль ACMS в минуту при 25°С. Отсутствие или восстановление активности ACMSD1 (например, за счет использования ингибиторов ACMSD) приводит к слабой спонтанной деградации до ACMS (т.е. циклизации до формы хинолиновой кислоты).
Ферментативную активность определяют при концентрации НАА 10 мкМ в присутствии соединений, указанных ниже в таблице 1. Соединения испытывают при концентрации примерно 5 мкМ и 10 мкМ, и вычисляют IC50 для соединений, показывающих ингибирующую активность выше 50%. Результаты приводятся в таблице 1.
Таблица 1
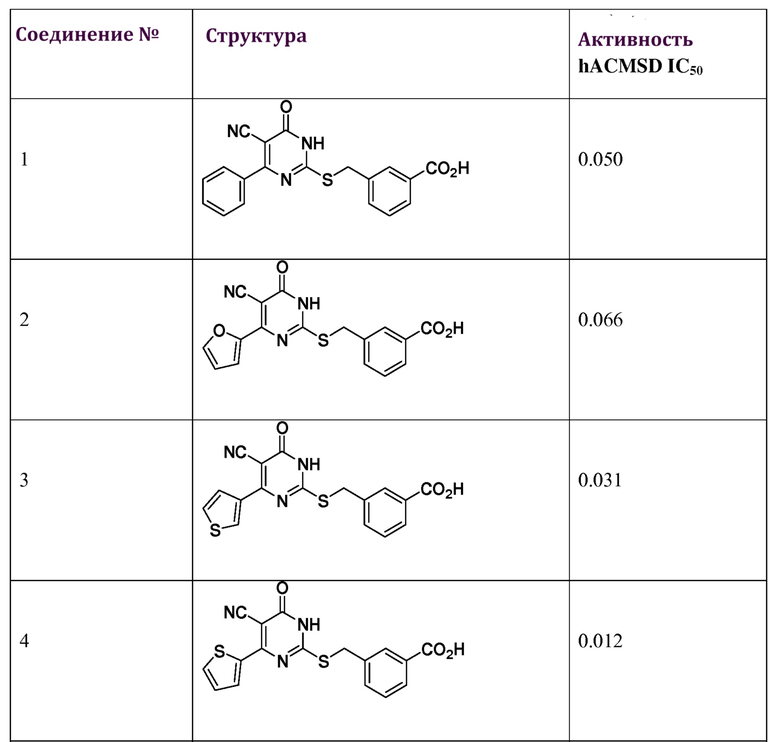
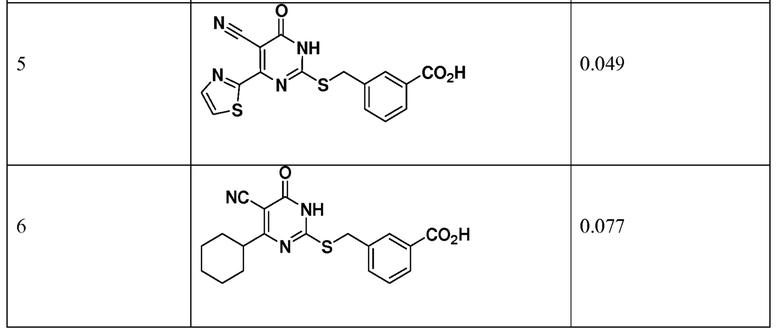
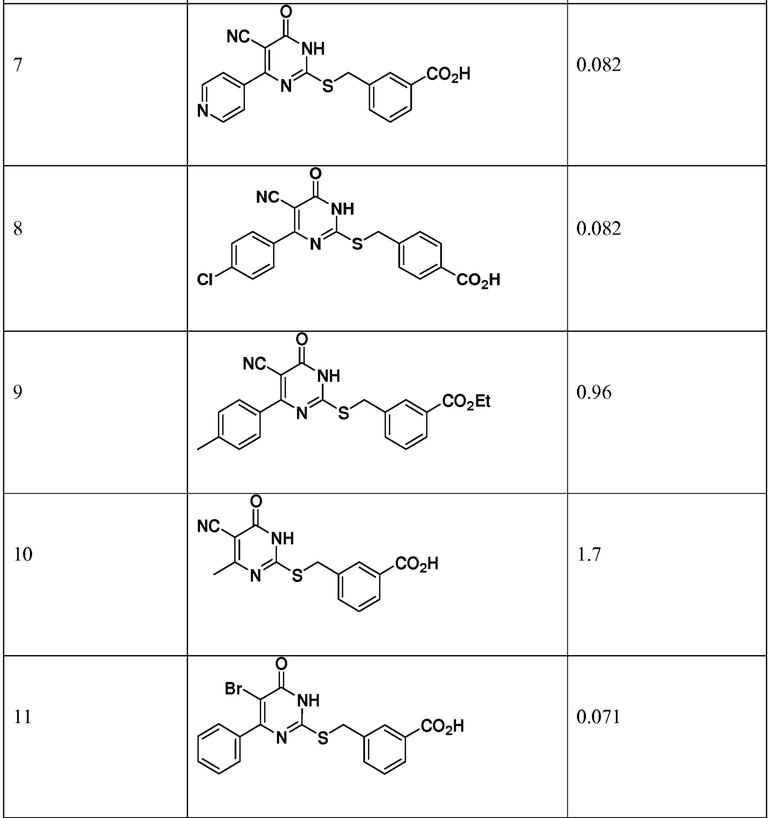
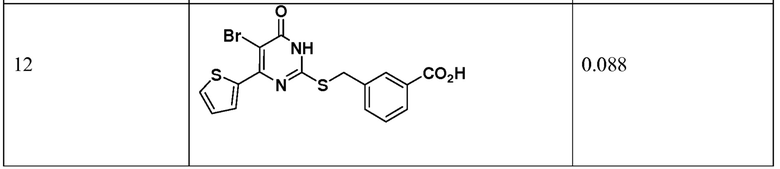

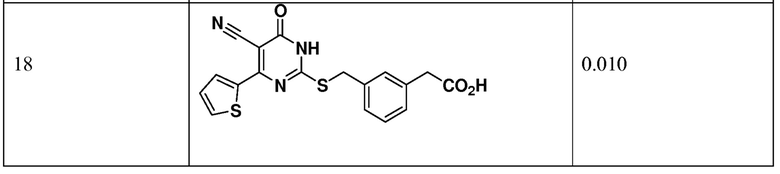
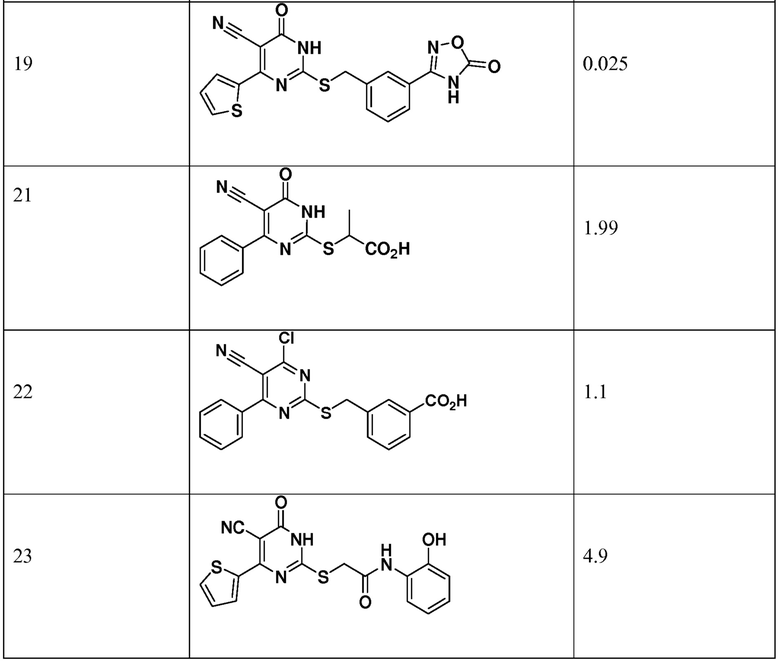
Пример 30. Определение модуляции ACMSD-1 в клетках НЕК293Т
Клетки НЕК293Т (АТСС) высевают в шестилуночные планшеты и трансфицируют с использованием Fugene HD для временной экспрессии ACMSD. Через 24 часа после трансфекции клетки стимулируют в течение 48 час - 72 час различными концентрациями соединения 1 и затем лизируют для измерения активности ACMSD путем измерения конверсии 3ОН-антраниловой кислоты в продукт (т.е. α-амино-бета-карбоксимуконат-ε-семиальдегид, ACMS) в спектрофотометрическом анализе in vitro. Количество общего белка, содержащегося в клеточных лизатах, детектируют анализом Бредфорда. Эту величину используют для вычисления специфической активности фермента, нормализованной ко всем образцам (мЕ/мл или ΔE/Δt/мг всего белка).
Известно, что фермент ACMSD-1 экспрессируется в печени, почках и головном мозгу; поэтому для определения уровней экспрессии ACMSD испытывают доступные клеточные линии для таких типов клеток. Авторы определили, что ACMSD-1 не экспрессируется в траснформированных клеточных линиях из печени и почек, таких как НерG2, НЕК293Т, Hep3B и т.д. Трансфекцию ACMSD выполняют для экспрессии фермента в различных клеточных теневых фенотипах, таких как COS-7, HEK293T и HepG2. HEK293T-клеточный теневой фенотип опробован как наилучшая система с самым высоким продуцированием белка, дающая возможность надежного измерения активности фермента ACMSD1. Это имеет место вероятно из-за более хорошей эффективности трансфекции, наблюдаемой в НЕК293Т.
Имея определенное оптимальное время стимуляции и протокол трансфекции, клетки стимулируют различными концентрациями соединения 1 (примерно 50 нМ - примерно 5 мкМ). Соединение 1 в таком анализе на основе сверхэкспрессии клетками ингибирует активность ACMSD-1 в зависимости от дозы.
Пример 31. Определение содержания NAD+ в первичных гепатоцитах человека, обработанных соединением 4
Концентрацию или содержание NAD+ определяют в первичных гепатоцитах человека, обработанных соединением 4. Среду (NT) используют как контроль.
В по меньшей мере трех экспериментах обрабатывают первичные гепатоциты различными концентрациями соединения 4 (0,5 мкМ и 5 мкМ) через 48 час после посева. Соединение 4 заменяют каждые 24 часа, и затем клетки непосредственно харвестируют и лизируют смесью ACN/H2O (отношение 5:1). Используют ЖХМС/МС для детекции и измерения концентрации/содержания NAD+. Результаты скрининга показывают, что соединение 4 ингибирует фермент ACMSD-1 в таких низких концентрациях как 0,5 мкМ и 5 мкМ (фиг. 1).
Пример 32. Определение содержания NAD+ в первичных гепатоцитах человека, обработанных соединением 1
Концентрацию или содержание NAD+ определяют в первичных гепатоцитах человека, обработанных соединением 1 и известным ингибитором МЕНР. МЕНР используют как контроль.
В по меньшей мере трех экспериментах обрабатывают первичные гепатоциты различными концентрациями соединения 1 (0,5 мкМ, 5 мкМ и 50 мкМ) через 48 час после посева. Соединение 1 заменяют каждые 24 часа, и затем клетки непосредственно харвестируют и лизируют смесью ACN/H2O (отношение 5:1). Используют ЖХМС/МС для детекции и измерения концентрации/содержания NAD+. Результаты скрининга показывают, что 500 мкМ МЕНР ингибируют 70% очищенного фермента ACMSD-1, и что 0,5 мкМ соединения 1 имеют такую же ингибирующую активность, как 250 мкМ МЕНР (фиг. 3).
Пример 33. Модуляция активности SOD2 в клетках AML-12 и мышиных первичных гепатоцитах
Измеряют модуляцию активности SOD2 в клетках AML-12 и мышиных первичных гепатоцитах, обработанных соединением 1 или 17.
Клеточную линию гепатоцитов мыши AML-12 (альфа 12 печени мыши) получают из АТСС и выращивают при 37°С в увлажненной атмосфере из 5% СО2 и 95% воздуха в смеси модифицированная по способу Дульбекко среда Игла/питательная смесь F-12 (DMEM/F-12) с добавлением 0,005 мг/мл инсулина, 0,005 мг/мл трансферрина, 5 нг/мл селена, 40 нг/мл дексаметазона и 1% гентамицина. Ингибитор ACMSD сначала разводят из порошка в ДМСО до исходной концентрации 1 мМ. Исходный раствор дополнительно разбавляют водой до концентрации 100 мкМ, которую используют для обработок клеток.
Первичные гепатоциты получают от 8-12-недельных мышей C57BL/6J методом перфузии коллагеназой. Печени мышей перфузируют сбалансированным солевым раствором Хэнкса (HBSS, KCl, 5,4 мM; KH2PO4, 0,45 мM; NaCl, 138 мM; NaHCO3, 4,2 мM; Na2HPO4, 0,34 мM; глюкоза, 5,5 мM; HEPES, 1 M; EGTA, 50 мM; CaCl2, 50 мM; pH 7,4). Затем печени промывают со скоростью 5 мл/мин через воротную вену. После промывки печени перфузируют раствором коллагеназы (0,025%). Жизнеспособность клеток оценивают методом с трипановым синим. Изолированные первичные гепатоциты высевают со средой DMEM (Gibco), включающей 10% FCS, 10 единиц на мл пенициллина и HEPES для забуферивания. Клетки поддерживают в культуре при 37°С в увлажненной атмосфере 5% СО2/95% воздуха. После 6-8-часового присоединения эту среду заменяют средами, содержащими различные концентрации ингибитора ACMSD (т.е. соединения 1 или соединения 17) или соответствующую концентрацию ДМСО (как контроль). Первичные гепатоциты собирают примерно через 24 часа, если не указано иное.
Затем первичные гепатоциты или клетки AML-12 лизируют в буфере 20 мМ HEPES (Gibco), pH 7,2, содержащем 1 мМ EGTA (Sigma), 210 мМ маннита (Sigma) и 70 мM сахарозы (AMRESCO). Общую концентрацию белка определяют с использованием анализа по Бредфорду (BioRad). Активность SOD-2 определяют в указанное время после обработки ингибитором ACMSD с помощью набора для анализа SOD Assay Kit (Cayman Chemical) согласно инструкциям изготовителя. Для того, чтобы специфически обнаружить активность SOD2, в анализ добавляют 2 мM цианида калия, который ингибирует как Cu/Zn-SOD, так и внеклеточный SOD, что приводит к детекции только активности Mn-SOD (SOD-2). Поглощение определяют с помощью многофункционального планшет-ридера Victor X4 (Perkin-Elmer) при 450 нм. Результаты выражают в Е/мл/мг белка согласно стандартной кривой и измеренной концентрации белка.
Путь сопротивления окислительному стрессу, которое, как представляется, появляется после ингибирования ACMSD, изучают, измеряя активность SOD2. Результаты показывают, что активность SOD2 индуцируется в зависимости от дозы как в AML-12, так и в первичных гепатоцитах как соединением 17, так и соединением 1. В первичных гепатоцитах, которые экспрессируют ACMSD на существенно более высоких уровнях, чем AML-12, действие наблюдают при дозе примерно 5 нМ, и максимум достигается при дозе примерно 50 нМ. Как соединение 17, так и соединение 1 способны индуцировать активность SOD2 в зависимости от дозы (фиг. 5А и фиг. 5В).
Пример 34. Определение содержания NAD+ в первичных гепатоцитах человека
Определяют уровни NAD+ в первичных гепатоцитах человека, обработанных соединением 17.
NAD+ экстрагируют с использованием метода экстракции кислотой. Образцы собирают и гомогенизируют в 70% охлажденной льдом перхлорной кислоте (HClO3). После осаждения нерастворимых частей белков путем добавления карбоната калия (К2СО3) образцы разделяют высокоэффективной жидкостной хроматографией (ВЭЖХ) и анализируют методом масс-спектрометрии. Белки в осадке определяют количественно анализом по Бредфорду и используют для нормализации.
Воздействие на первичные гепатоциты 5 нМ, 10 нМ и 50 нМ ингибитора ACMSD соединения 17 в течение 24 часов вызывает существенное и зависимое от дозы возрастание уровней внутриклеточного NAD+. Существенное воздействие на уровни NAD+ наблюдают при таких низких концентрациях, как 5 нМ (фиг. 2).
Пример 35. Анализ методом RT-qPCR SIRT1-регулируемых генов в клетках AML-12, клетках Нepа-1.6 и первичных гепатоцитах мыши, обработанных соединением 1 или 17
Экспрессию ACMSD и генов, известных как регулируемые SIRT1 (фермент, который является строго NAD+-зависимым), таких как Pgc1a, Sod1, Sod2 (MnSOD), анализируют в клетках AML-12, клетках Hepa-1.6 и первичных гепатоцитах мыши, обработанных соединением 1 или 17.
Клетки (AML-12, Hepa-1.6, НЕК-293, первичные гепатоциты человека и мыши) обрабатывают различными концентрациями соединения 1 и соединения 17. Всю РНК экстрагируют из клеток с использованием TRIzol (Invitrogen) согласно инструкциям изготовителя. РНК обрабатывают ДНказой, и 2 мкг ДНК используют для обратной транскрипции (RT). Разведенную 50Х кДНК используют для реакций RT-количественной ПЦР (RT-qPCR). Реакции RT-qPCR выполняют с использованием системы Light-Cycler (Roche Applied Science) и qPCR Supermix (QIAGEN) с указанными праймерами. Используют по меньшей мере три технических повтора для каждой точки биологических данных.
Возрастание в зависимости от дозы уровней экспрессии генов мРНК, известных как регулируемые SIRT1 (фермент, который является строго NAD+-зависимым), таких как Pgc1a и Sod2 (MnSOD), но не Sod1 (Cu-Zn SOD), наблюдают в первичных гепатоцитах мыши, обработанных в течение 24 час соединением 17 (интервал 5 нМ - 500 нМ). Наблюдаемое возрастание экспрессии генов является зависимым от дозы, которое соответствует зависимому от дозы возрастанию ферментативной активности SOD2, наблюдаемому в примере 32 (фиг. 5). Уровни мРНК Sod2 также возрастают в зависимость от дозы в клетках AML-12 и линиях гепатоцитов Нера-1.6 после 24-час обработки соединением 1. Такие изменения в экспрессии мРНК совместимы с активацией SIRT1, являющейся результатом индукции в уровнях NAD+ путем ингибирования активности ACMSD соединением 17 (фиг. 4 и фиг. 5).
Пример 36. Модуляция активности каспазы 3/7 в клетках MDCK
Выполняют исследование in vitro в клетках MDCK для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на острое повреждение почек.
Клетки MDCK (MDCK (NBL-2) ATCC® CCL-34™) культивируют в базовой составленной ATCC среде минимальной эссенциальной среде Игла, каталожный № 30-2003, с сывороткой плода коровы (FBS) до конечной концентрации 10%. Высевают 10000 клеток в 96 лунок, и через 24 часа после посева среду заменяют на свежую среду с добавлением 1% FBS. Затем используют цисплатин (50 мкМ, в течение 16 час) для индукции повреждения клеток. Добавляют различные концентрации соединения 18 (в 1% ДМСО) (фиг. 1) в комбинации с цисплатином или за 1 час до добавления цисплатина (фиг. 2).
Активность каспазы 3/7 (Promega) определяют согласно стандартным процедурам с использованием люминисцентного сигнала, считываемого на планшет-ридере Victor V (PerkinElmer). Каждый эксперимент/условие выполняют при трехкратном повторе.
Каспазную активность анализируют как влияние в процентах, нормализованное к клеткам, обработанным одним цисплатином (100%) и средой как 0% каспазной активности. Данные анализируют с помощью программы GraphPad. Используют однофакторный дисперсионный анализ (критерий множественного сравнения Дуннетта) для статистического анализа.
Как видно на фиг. 8А, клетки MDCK обрабатывают различными концентрациями соединения 18 (0,01 мкМ - 100 мкМ) в комбинации с цисплатином (цисп). Величину ЕС50 вычисляют как равную 70 кмМ. Клетки, обработанные соединением 18, значительно снижают каспазную активность при концентрации 100 мкМ по сравнению с одним цисплатином (p<0,001).
Клетки MDCK также обрабатывают различными (1 мкМ - 125 мкМ) концентрациями соединения 18 за один час до добавления цисплатина (cisp). Как видно на фиг. 8В, клетки, обработанные соединением 18, снижают каспазную активность в значительной степени при концентрации примерно 30 мкМ - примерно 125 мкМ по сравнению с одним цисплатином (p<0,001). Величину ЕС50 вычисляют как равную 30 кмМ.
Результаты показывают, что соединение 18 снижает, существенным образом, активность каспазы 3/7, вызываемую цисплатином (фиг. 8А); защитное действие особенно заметно, если перед повреждением повреждающим средством (цисплатином) добавляют соединение 18, как видно на фиг. 8В.
Пример 37. Цитотоксичность и скрининг hERG
Цитотоксичность. Высевают 20000 клеток HePG2 и AML-12 в 96-луночный планшет (Viewplate PerkinElmer). Зависимость эффекта от дозы для соединений в таблице 2 определяют с использованием цифрового распределителя HP D300 в интервале от 10 нМ до 300 мкМ при постоянном 1% ДМСО в среде. Клетки стимулируют в течение 4 час при 37°C; супернатант используют для выполнения высвобождения LDH (Cytotox-one, Promega) как меры некроза, в то время как клетки лизируют для детекции уровня АТФ для определения жизнеспособности клеток (Celltiter-glo, Promega) согласно инструкциям изготовителя.
Набор для анализа предшественников hERG (Invitrogen), содержащий мембранные препараты из клеток яичника китайского хомячка, устойчиво трансфицированных калиевым каналом hERG и высокоаффинным красным флуоресцентным лигандом канала hERG (индикатор), используют для определения аффинности связывания канала hERG испытываемых соединений в таблице 2. Соединения, которые связываются с белком канала hERG (конкуренты), идентифицируют по их способности заменять индикатор, что приводит к более низкой поляризации флуоресценции. Конечную концентрацию ДМСО в каждой лунке поддерживают при 1%. Анализы выполняют согласно протоколу изготовителя (Invitrogen).
Результаты приводятся в таблице 2.
Таблица 2
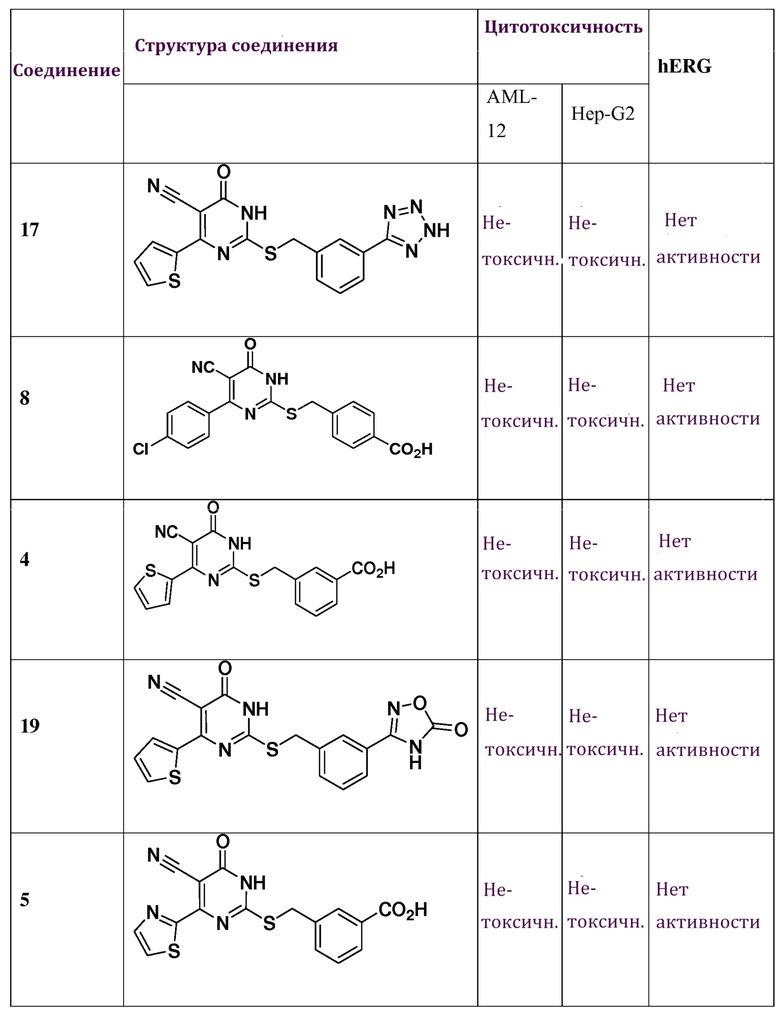
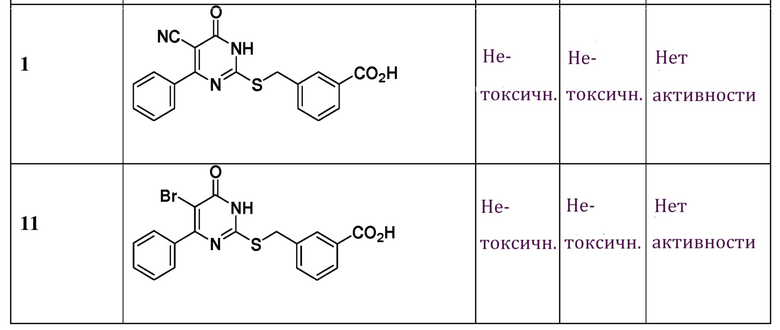
Пример 38. Эксперименты с C.elegans - сайленсинг ACMSD1, анализы продолжительности жизни, оценка подвижности и количественное определение флуоресценции GFP
Штаммы C. elegans (Caenorhabditis elegans) предоставляются Caenorhabditis Genetics Center (University of Minnesota). Червей поддерживают на агаровых пластинах со средой для роста нематод (NGM), засеянных бактерией E. coli OP50, при 20°C, если не указано иное. Штаммы, используемые для экспериментов, следующие: Bristol N2, NL2099 (rrf-3(pk1426)II), KN259 (huIs33[sod-3::GFP+pRF4(rol-6(su1006))]).
Эксперименты с кормлением бактериальной РНКи выполняют следующим образом: червей выращивают на агаровых пластинах NGM, содержащих карбенициллин и IPTG в конечных концентрациях 25 мкг/мл и 1 мМ, соответственно, и засеянных бактериальными культурами, полученными из библиотеки Ahringer. Используемые клоны acmsd-1 (Y71D11A.3), sir-2.1 (R11A8.4) и daf-16 (R13H8.1). Клоны закупают у GeneService, и их идентичность подтверждают секвенированием. Для двойных экспериментов с РНКи бактериальные культуры перед посевом на пластины NGM смешивают. Контрольная РНКи в такого рода экспериментах разведена на 50% контрольными бактериями с пустым вектором РНКи.
Нематоду Caenorhabditis elegans используют в качестве модельной системы для подтверждения активации защиты от окислительного стресса, которую наблюдают в клетках на уровне интактного организма. Влияние РНКи acmsd-1 оценивают на C. elegans с помощью RT-qPCR. Всю РНК экстрагируют из клеток с использованием TRIzol (Invitrogen) согласно инструкциям изготовителя. РНК обрабатывают ДНказой, и 2 мкг РНК используют для обратной транскрипции (RT). Разведенную 50X кДНК используют для реакций RT-количественной ПЦР (RT-qPCR). Реакции RT-qPCR выполняют с использованием системы Light-Cycler (Roche Applied Science) и qPCR Supermix (QIAGEN) с указанными праймерами. Используют по меньшей мере три технических повтора для каждой точки биологических данных.
Анализы продолжительности жизни C. elegans выполняют при 20°C следующим образом. На животных воздействуют NAC (N-ацетилцистеин) в конечной концентрации 5 мМ из 0,5 M водного исходного раствора на стадии от молодых до взрослых. К пластинам NGM, содержащим карбенициллин (100 lg mL)1), добавляют пируват натрия в конечной концентрации 2,5 мМ, и засевают УФ-убитыми OP50. После 5 дней обработки РНКи червей переносят на пластины, содержащие паракват и засеянные бактериями с РНКи acmsd-1. Контрольных животных выращивают в течение первых 5 дней взросления на бактериях с РНКи, содержащих пустой вектор, и затем переносят на пластины, содержащие паракват и засеянные бактериями с РНКи acmsd-1. Анализы на выживаемость выполняют с использованием метода Каплана-Мейера, и значимость различий между кривыми выживаемости вычисляют с использованием логарифмического рангового критерия. Используют статистическую программу XLSTAT 2007 (XLSTAT, Brooklyn, NY, USA), и все значения P <0,05 считаются значимыми. Используют 100 червей на условие и оценивают каждые 2 дня. Причинами вычеркивания являются фенотип «exploded vulva» или черви, которые сползают с пластины. Где указано, сверху на агаровые пластины добавляют паракват в указанной концентрации. Как только раствор параквата полностью высохнет, червей L4 переносят на такие агаровые пластины и проверяют в течение 5-6 дней каждый день. В день 6 все тесты с паракватом прекращают, поскольку небольшой процент популяции червей может начать погибать естественно, а не из-за действия параквата.
Движение червей регистрируют в течение 45 секунд в дни 1, 3 и 5 взросления с использованием камеры Nikon DS-L2/DS-Fi1 и управляющего устройства, присоединенных как к компьютеру, так и к стандартному светлопольному микроскопу. Для каждого условия используют пять пластин с 10 червями на пластину. Движение червей во время старения вычисляют, беря интеграл значения скорости, которую оценивают, следуя центроидам червей с помощью модифицированной версии свободного доступа для Parallel Worm Tracker для MATLАВ.
Интенсивность флуоресценции в шатаммах червей, экспрессирующих GFP-репортерные белки, оценивают количественно с использованием планшет-ридера Victor X4 (Perkin Elmer). Животных получают следующим путем: восемьдесят червей на условие (в соответствующем возрасте) пикируют (20 червей на лунку 96-луночного планшета с темными лунками) и помещают в среду М9. Каждый эксперимент повторяют по меньшей мере дважды.
Уровень экспрессии мРНК acmsd-1 существенно снижается, подтверждая эффективность РНКи-опосредуемого нокдауна (фиг. 7А). Ортолог червя MnSOD SOD3 индуцируют на уровне его мРНК с сопутствующей даунрегуляцией гена acmsd-1 РНКи. Существенное возрастание уровня белка SOD3 также наблюдают в день 3 взросления (фиг. 7В). Даунрегуляция ACMSD улучшает продолжительность жизни червей, и такое улучшение является SIR-2,1- и DAF-16-зависимым (фиг. 7С).
Кроме того, черви, на которые воздействовали РНКи acmsd-1, живут дольше и показывают улучшенное поведение в анализах на подвижность, когда обработаны паркватом, хорошо известным индуктором ROS, который широко используется для имитации окислительного стресса у C. elegans (фиг. 7D и 7Е).
Более хорошая выживаемость в условиях с паракватом не зависит от стадии развития, на которой на червей воздействуют РНКи acmsd-1 (фиг. 7F).
Возрастание продолжительности жизни в условиях окислительного стресса более не наблюдают, когда ортолог червей FoxO1 DAF-16 даунрегулируют, что означает, что устойчивость к окислительному стрессу является DAF-16-зависимой (фиг. 7G).
Пример 39. Исследование противодиабетического действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на мышах C57BL/6J и KK-Ay
Тест на переносимость глюкозы выполняют на самцах мышей C57BL/6J и KK-Ay для того, чтобы определить действие соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на уровни глюкозы и инсулина.
Самцов мышей C57BL/6J и KK-Ay в возрасте 6-7 недель получают, например, от Charles River Laboratories, Франция, и CLEA, Япония, соответственно. Мышей кормят, начиная с возраста 8 недель, обычным кормом (CD-Harlan 2018) и кормом с высоким содержанием жира (HFD-Harlan 06414). Соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль смешивают с HFD в количестве 180 мг.кг-1 корма. На основании ежедневного потребления корма это приводит к ежедневной дозе примерно 15 мг.кг-1 массы тела. Мышей не кормят в течение 4 час перед взятием крови и тканей для выделения РНК, измерения липидов и гистологии. Потребление кислорода измеряют прибором Oxymax (Columbus Instruments). Выполняют гистологический анализ и микроскопию в проходящем пучке электронов.
Пероральный тест на переносимость глюкозы выполняют на животных, которых не кормили в течение ночи. Глюкозу вводят с помощью зонда в дозе 2 г/кг. Интраперитонеальный тест на переносимость инсулина выполняют на животных, голодавших в течение 4 час. Инсулин инъецируют в дозе 0,75 Е/кг массы тела. Глюкозу определяют количественно глюкометром 4 из набора Maxi (Bayer Diagnostic) или RTU глюкозы (bioMerieux Inc.), и концентрации инсулина измеряют ELISA (Cristal Chem Inc.). Статистические различия определяют с помощью или ANOVA или t-критерия Стъюдента.
Пример 40. Исследование противодиабетического действия и действия против ожирения соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на мышах db/db с мутацией LepR
Исследование противодиабетического действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей проводят на мышах с генетическим ожирением LepRdb/J (db/db).
Животных размножают и содержат в среде с регулируемой температурой и влажностью в соответствии с протоколами FELASA. С возраста три недели животных кормят кормом с высоким содержанием жира (Harlan 06414). Большинство фармакологических исследований начинают с восьминедельными db/db и дикого типа (wt) как эталона.
Подострое вмешательство
Мышей db/db обрабатывают соединением формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемой солью в течение 14 дней между 5-6 часами пополудни до наступления темной фазы (6 РМ). Образцы крови берут после 4-час голодания мышей перед первой дозой и через 18±2 час после последней дозы. Определяют концентрацию глюкозы в каждом образце крови.
Острое вмешательство глюкозы
Исходные образцы крови собирают произвольно у мышей db/db между 6-8 часами до полудня после наступления светлой фазы (6 АМ), затем вводят соединения формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемые соли, ограничивают доступ к корму, и через 4 часа после обработки берут второй образец крови. Затем мышей подвергают пероральному тесту на переносимость глюкозы (OGTTI: 1 г глюкозы/кг массы тела), и определяют концентрации глюкозы через 0,5, 1, 2, 3 и 4 часов после нагрузки.
Эугликемический гиперинсулинемический клэмп-тест
Мышам db/db ставят временный катетер в яремную вену под анестезией кетамином/ксилазином. В течение 6-7 дней ограничивают поздний доступ к пище (после 6 АМ). Мышей в сознании помещают в большие рестрейнеры для крыс и греют, нагревая лапы. Затем концы катетеров соединяют со шприцами в насосах CMA402 (Axel Semrau, Sprockhoevel, Германия). После 110-минутной непрерывной с подкачиванием инфузии [3-3H]глюкозы (1,85 кБк/мин) берут образец крови для определения инсулина в плазме, концентраций глюкозы и [3-3H]глюкозы и вычисляют базальные скорости образования эндогенной глюкозы. Затем мыши получают через зонд среду или соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль.
Затем начинаются клэмпы глюкозы-1 с инфузией [3-3H]глюкозы (3,7 кБк/мин), содержащей инсулин (36 пмоль/кг⋅мин-1; HumulinR, Lilly, USA), вызывающие умеренное общее возрастание концентраций инсулина в плазме. Концентрации глюкозы в крови измеряют каждые 10 минут, и целевую гликемию устанавливают, подбирая скорость инфузии 20% глюкозы (GIR). В минуту 120 дают внутривенно 2-дезокси-D-[1-14C]глюкозу (370 кБк). Образцы крови берут в минуту 30, 60, 90, 100, 110, 120, 122, 125, 130 и 140. Затем мышей умерщвляют (т.е. дают внутривенно сверхдозу кетамина/ксилазина). Икроножную мышцу и эпидидемальную жировую ткань собирают и сразу же быстро замораживают в жидком азоте и хранят при -80°С. Из ткани экстрагируют 2-[14C]дезоксиглюкоза-6-фосфат, и вычисляют степени поглощения глюкозы (Rg).
Определяют радиоактивность [3H] и [14C] в депротеинизированной плазме после выпаривания [3H2O]. Потоки глюкозы в базальных условиях и между минутой 60-90 и 90-120 глюкозного клэмпа оценивают следующим образом: скорость исчезновения глюкозы во всем теле (Rd)=[3-3H]GIR (dpm/мин)/специфическая активность [3-3H]глюкозы в плазме (dpm/мин*моль); базальная конечная Ra=[3-3H]GIR (dpm/мин)/специфическая активность [3-3H]глюкозы в плазме (dpm/мин*моль) (dpm - распад в минуту); конечная Ra глюкозного клэмпа=GIR˗Rd. Сцинтилляционный коктейль Ultima, радиоизотопы и Tri-Carb2910TR получают от Perkin Elmer (Германия).
Анализы крови, плазмы и мочи
Образцы крови берут из латеральной хвостовой вены. Глюкозу в крови измеряют глюкометром (Contour, Bayer Vital, Германия), глюкозу в моче и плазме колориметрическим анализом Glucose LabAssay (Wako, Germany) и HbA1c с помощью A1cNow+ (Bayer Vital) или анализатора Clover (Inopia, Южная Корея).
Анализы начала заболевания и продолжительности жизни
Начало заболевания определяют по последнему дню пика массы тела индивидуума перед тем, как происходит постепенная потеря массы. Стадии заболевания определяют следующим образом: раннюю стадию заболевания определяют как время между пиком массы тела до потери массы на 10% от пика массы. Позднюю стадию заболевания определяют как время между потерей массы на 10% от пика массы и до конечной стадии заболевания. Конечную стадию заболевания определяют как день, когда животное не может само выпрямляться долее 30 с в течение трех последовательных испытаний, когда его кладут на бок. Животных эфтанизируют на конечной стадии заболевания.
Измерения состава тела
Массу тела оценивают еженедельно в течение по меньшей мере 13 недель. Бурую жировую ткань (ВАТ) и гонадную белую жировую ткань (WAT) иссекают и взвешивают при указанном возрасте. Общую тощую массу, % WAT и BMD (минеральная плотность кости) определяют DEXA (PIXImus DEXA; GE).
Косвенная калориметрия, поглощение корма и активность
Животных изначально взвешивают и оставляют для акклиматизации в клетке для опытов. Объем кислорода (VO2) и объем выработки диоксида углерода (VCO2) измеряют каждые 20 мин с использованием контрольной системы Oxymax Comprehensive Laboratory Animal Monitoring System (CLAMS) (Columbus Instruments) и записывают как средний VO2 в час, нормализованный к массе тела (мл/час/кг). С использованием прибора CLAMS одновременно измеряют активность по разрывам инфракрасного луча и поглощение корма. Конкретнее, поглощение корма измеряют путем вычитания массы измельченных в порошок гранул корма в конце эксперимента из начальной массы в начале эксперимента. Для того, чтобы дополнить этот эксперимент и контролировать в случае новой окружающей среды, которая может влиять на пищевое поведение, авторы также выполняют более «ручной» эксперимент, в котором в чистую клетку, в которой содержат животных, в одно и то же время каждый день помещают установленную массу кормовых гранул. На следующий день регистрируют массу оставшихся гранул и вычитают из начальной массы. Эксперимент выполняют в течение 14 дней подряд. Массу тела каждой мыши также регистрируют ежедневно. Результаты для каждого генотипа схожи с полученными с CLAMS.
Статистический анализ
Считая 1-β статистически более сильным, чем 0,9, авторы оценивают соответствующих членов группы из пилотных исследований a priori. Выполняют одно- или двухпараметрический дисперсионный анализ (заключительные тесты) или t-критерии.
Пример 41. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на неалкогольную жировую болезнь печени (NAFLD) и неалкогольный стеатогепатит (NASH) у мышей
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на неалкогольную жировую болезнь печени (NAFLD) и неалкогольный стеатогепатит (NASH) выполняют на мышах C57BL/6J, питающихся кромом с высоким содержанием жира и высоким содержанием сахарозы.
Мышей C57BL/6J (The Jackson Laboratory, Bar Harbor, Maine, USA) содержат при цикле 14 часов света-10 час темноты при 21-23°C и доступе к воде ad libitum во время всего эксперимента. С возраста 6 недель мышей кормят «Western» HF-HSD с 44,6% ккал, получаемыми из жира (в котором 61% насыщенных жирных кислот) и 40,6% ккал, получаемыми из углеводов (корм с, главным образом, сахарозой - 340 г/кг) (TD.08811, 45% ккал от жирного корма, Harlan Laboratories Inc., Madison, Wisconsin, USA) или обычным кормом (NCD) в качестве контроля (V1534-000 ssniff R/M-H, ssniff Spezialdiäten GmbH, Soest, Германия). Затем животных обрабатывают соединением формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемой солью или контролем в течение 4, 12 или 20 недель (n=8 на группу для каждого момента времени), после чего их умерщвляют.
Массу тела и потребление корма контролируют еженедельно в один и тот же день. После воздействия седативным средством пентабарбиталом натрия (интраперитонеальная инъекция, 50 мг/кг массы тела) анализируют общую массу жира двухэнергетической рентгеновской абсорбиометрией (DEXA) (PIXImus densitometer, Lunar Corp., Madison, Wisconsin, USA). Интраперитонеальный тест на толерантность к глюкозе (IPGTT) выполняют на голодавших 6 час мышах. Уровни глюкозы в хвостовой вене измеряют глюкометром Bayer Contour непосредственно перед (момент времени 0 мин) и через 15, 30, 60, 90 и 150 мин после введения глюкозы (1 г глюкозы/кг массы тела). Инсулинорезистентность вычисляют с использованием индекса инсулинорезистентности из модели гомеостаза (HOMA-IR): (инсулин натощак (нг/мл) × глюкоза натощак (мг/дл))/405.
Умерщвление
После 6-часового голодания мышам дают анестезию пентобарбиталом натрия (интраперитонеальная инъекция, 50 мг/кг массы тела) и умерщвляют, отбирая кровь через кардиальную пункцию. Плазму получают центрифугированием крови (6000 об/мин в течение 5 мин при 4°С) и собирают в гепаринизированные шприцы. Ткани или быстро замораживают в жидком азоте или хранят при -80°С вместе с плазмой до дальнейших биохимических и молекулярных анализов или сохраняют для гистологического анализа.
Гистологические анализы
Образцы печени обычным образом фиксируют в забуференном формалине (4%) и заливают парафином. Серию срезов толщиной 4 мм окрашивают H&E и пикросириусом красным для оценки фиброза. Замороженные срезы печени окрашивают жировым красным О для оценки накопления липидов. Все биопсии печени анализирует патоморфолог специалист по печени вслепую без знания состояния питания или хирургического вмешательства. Стеатоз, активность и фиброз оценивают полуколичественно согласно сетевым критериям клинических исследований NASH. Количество стеатоза (процент гепатоцитов, содержащих капли жира) оценивают как 0 (<5%), 1 (5-33%), 2 (>33-66%) и 3 (>66%). Баллонирование гепатоцитов классифицируют как 0 (отсутствие), 1 (незначительное) или 2 (многих клеток/заметное баллонирование). Очаги воспаления долей оценивают как 0 (отсутствие очагов), 1 (<2 очагов в поле 200×), 2 (2-4 очага в поле 200×) и 3 (>4 очагов в поле 200×). Фиброз оценивают как стадия F0 (отсутствие фиброза), стадия F1a (слабый, зона 3, перисинусоидальный фиброз), стадия F1b (умеренный, зона 3, перисинусоидальный фиброз), стадия F1c (портальный/перипортальный фиброз), стадия F2 (перисинусоидальный и портальный/перипортальный фиброз), стадия F3 (мостовидный фиброз) и стадия F4 (цирроз). Диагноз NASH основан на признанных гистологических критериях. Тяжесть заболевания оценивают с использованием NAS (оценка активности NAFLD) как невзвешенной суммы оценок стеатоза, баллонирования гепатоцитов и воспаления долей. Процент фиброза определяют количественно морфометрией из оцифрованных срезов, окрашенных сириусом красным, с использованием системы Aperio после регулировки порога детекции фиброза при визуальном контроле. Результаты выражают в виде площади пропорции коллагена.
Пример 42. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на неалкогольную жировую болезнь печени (NAFLD) и неалкогольный стеатогепатит (NASH) у мышей с дефицитом метионина и холина
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на неалкогольную жировую болезнь печени (NAFLD) и неалкогольный стеатогепатит (NASH) выполняют на самцах мышей дикого типа, которым дают рацион с дефицитом метионина и холина.
Мышей дикого типа содержат при 12-часовом цикле свет/темнота с использованием свободного доступа к корму и воде. Анализируют по меньшей мере 5 животных на каждый момент времени. Все эксперименты повторяют по меньшей мере три раза. Для ежедневной обработки 8-12 недельных самцов мышей, весящих 25 г, кормят или кормом с дефицитом метионина и холина (MCD, для того, чтобы вызвать NASH) или обычным кормом (как контроль). Эксперименты с животными и оценку NAFLD и NASH проводят так, как описано выше в примере 40 в случае мышей, которые получали корм с высоким содержание жира и высоким содержанием сахарозы.
Пример 43. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на атеросклероз у мышей с нокаутом LDL-R, получавших рацион с высоким содержанием холестерина
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на атеросклероз проводят на мышах с нокаутом LDL-R, получавших рацион с высоким содержанием холестерина.
Мышей с нокаутом LDL-R (КО) обратно скрещивают в течение десяти поколений с линией C57LB/6J, получая конгенных животных C57LB/6J. Контрольные животные, которых используют, являются однопометными животными во всех экспериментах. Животных обрабатывают соединением формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемой солью или контролем. Мышей умерщвляют через 12 недель после начала атерогенного питания (TD94059; Harlan), после чего сердце и аорту перфузируют PBS и затем фиксируют (Shandon Formal Fixx, Thermo Scientific). Атеросклероз оценивают по окрашиванию жировым красным О корня аорты и определяют количественно с помощью программы MetaMorph. Биохимические параметры измеряют с помощью соответствующих наборов в COBAS C111 (Roche). Для исследования липосахаридов (LPS) in vivo мышам интраперитонеально инъецируют 100 мг LPS и берут кровь из хвостовой вены. Уровни TNFα определяют количественно анализом Mouse TNFα ELISA Ready-SET-Go! (eBioscience). Число клеток крови определяют с помощью Advia2120 (Siemens Healthcare Diagnostics).
Используют t-критерий Стьюдента для вычисления статистической значимости. В случае множественного испытания (т.е. сравнения более чем двух групп) такому испытанию предшествует проверка ANOVA. Статистически значимым считается P<0,05. Результаты представляют как среднее±SEM.
Пример 44. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на наследственное митохондриальное заболевание у мышей SCO2KO/KI
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на наследственное митохондриальное заболевание выполняют на мышах SCO2KO/KI.
Анти-COI, анти-COX5a, анти-Ndufa9, анти-SDH-HA и анти-Core 2 получают у Invitrogen; анти-GAPDH у Millipore; анти-FoxO1 и антиацетилированный-FoxO1 у Cell Signaling и Santa Cruz, соответственно. Антимышиные вторичные антитела получают у Amersham. Химикаты получают в Sigma. Олигонуклеотиды получают у PRIMM, Италия.
Соединения формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемые соли растворяют в воде и добавляют к стандартному порошковому корму (Mucedola, Италия) в концентрации, соответствующей 50 мг/кг/день. Гранулы, содержащие соединения формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемые соли или среды восстанавливают вручную и замораживают при -20°C до потребности в них. Подачу корма изменяют каждые три дня, и каждый раз оттаивают только необходимое количество и назначают ad libitum в течение одного месяца. Мышей Sco2KO/KI содержат при температуре и влажности, регулируемых оборудованием для ухода за животными при 12-час цикле свет/темнота и свободном доступе к воде и корму. Животных умерщвляют путем смещения шейных позвонков.
Морофлогический анализ
Для гистохимического анализа ткани замораживают в жидком азоте, предварительно охлаждая в изопентане. Серии срезов толщиной 8 мм окрашивают COX и SDH.
Биохимический анализ комплексов MRС
Образцы четырехглавой мышцы хранят в жидком азоте и гомогенизируют в 10 мМ фосфатном буфере (рН 7,4), и спектрофотометрическую активность cI, cII, cIII и cIV, а также CS измеряют как описано. Отмечается, что все панели активности сII умножают на 10 для чистоты визуализации.
Определение NAD+
NAD+ экстрагируют с использованием методов кислотной и щелочной экстракции, соответственно. NAD+ в тканях анализируют масс-спектрометрией, как описано ранее.
Пример 45. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на наследственное митохондриальное заболевание у делеторных мышей
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на наследственное митохондриальное заболевание проводят на делеторных мышах.
Модель делеторная мышь генерирована на основе конгенных C57BL/6 и охарактеризована ранее (Tyynismaa et al, 2005); мыши WT являются однопометными от той же конгенной линии мышей C57BL/6J. Самцам делеторных и WT мышей назначают или обычный рацион (CD) или в CD подмешивают соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль в соответствующих концентрациях. Гранулы корма получают вручную, подмешивая соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль в порошкообразный корм, как описано для мышей Sco2KO/KI в примере 43, и хранят при -20°С. Мышей содержат в стандартных устройствах для животных при 12-час цикле темнота/свет. Они имеют доступ ad libitum к корму и воде. Группа, предшествующая манифестации, состоит из 12 делеторных и 12 WT мышей, и группа после манифестации состоит из 24 делеторных и 24 WT мышей, получающих или соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль или рацион CD. Во время интервенции у мышей регулярно проверяют массу, потребление корма и физическую выносливость. Их способность к тренировке измеряют дважды с помощью теста с нагрузкой на беговой дорожке (Exer-6M Treadmill, Columbus Instrument) в начале и конце такого рациона. Протокол проверки с тренировкой включает начальную скорость бега 7 м/с, которую повышают каждые 2 мин на 2 м/с и продолжают до тех пор, пока животное неспособно бегать или повторно падает с дорожки в участке раздражения.
Потребление кислорода и образование диоксида углерода, а также спонтанную двигательную и пищевую активности регистрируют системой Oxymax Lab Animal Monitoring System (CLAMS; Columbus Instruments, OH, USA). Мышей содержат в отдельных клетках в камере CLAMS в течение 3 дней; первый день и ночь являются периодом настройки без записи с последующими 24 час регистрации при термонейтральности (+30°С). Результаты по потреблению О2 и образованию СО2 используют для вычисления скорости дыхательного обмена и анализа отдельно для светлого (неактивного) и темного (активного) периодов суток.
Морфологический анализ
Получают срезы тканей четырехглавой мышцы, печени и ВАТ. Образцы заделывают средой OCT Compound Embedding Medium (Tissue-Tek) и быстро замораживают в 2-метилбутане в жидком азоте. Замороженные срезы (12 мм) четырехглавой мышцы анализируют in situ гистохимическим СОХ и одновременно на активности сукцинатдегидрогеназы. Вычисляют активности из срезов четырехглавой мышцы, СОХ-положительных и СОХ-отрицательных плюс SDH-положительных и нормальных волокон. Подсчитывают приблизительно 2000 волокон из каждого мышиного образца. Интенсивность СОХ гистохимической активности из четырехглавой мышцы как для окислительных, так и неокислительных волокон измеряют с помощью программы Image J. Замороженные срезы (8 мкм) из печени и ВАТ окрашивают жировым красным О. Для заключения в пластик образцы четырехглавой мышцы, печени и ВАТ фиксируют в 2,5% глутаровом альдегиде, обрабатывают 1% тетроксидом осмия, дегидратируют в этаноле и заделывают в эпоксидной смоле. Полутонкие (1 мкм) срезы окрашивают метиловым синим (0,5% мас./об.) и борной кислотой (1%, мас./об.). Представляющие интерес области для ультраструктурного анализа выбирают, проверяя срезы в оптическом микроскопе. Для просвечивающей электронной микроскопии нарезают ультратонкие (60-90 нм) срезы на сеточках и окрашивают уранилацетатом и цитратом свинца и рассматривают с помощью трансмиссионного электронного микроскопа. Число крист как в ВАТ, так и в мышце определяют из электронных микрофотографий с использованием 1-мкм «интрамитохондриального измеряющего стержня», помещенного перпендикулярно кристам. Образцы скелетных мышц также анализируют на активность цитратсинтазы.
Пример 46. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на заболевание почек
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на заболевание почек выполняют на мышах C57BL/6J WT (Wei Q. et al., «Mouse model of ischemic acute kidney injury: technical notes and tricks», American Journal of Physiology-Renal Physiology, 303(11), F1487-F1494).
Мышей C57BL/6J закупают у Charles-River. Всех мышей кормят стандартным коммерческим кормом, и в то же время содержат при температуре окружающей среды 20-22°С и относительной влажности 50±5% при цикле свет/темнота 12 час/12 час в свободном от патогенной микрофлоры оборудовании. Подопытные мыши являются 8-недельными, и их делят на четыре группы: контроль (n=5); цисплатин (20 мг/кг; Sigma Chemical, St Louis, MO; n=5); соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемая соль и цисплатин (n=5); и только соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемая соль (40 мг/кг; n=5). Дозу и время обработки цисплатином на нейротоксичность выбирают согласно опубликованному методу. Соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль вводят перорально один раз в день в течение 4 дней. Цисплатин инъецируют один раз через 12 час после первого введения соединения формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемой соли. Мышей умерщвляют через 72 часа после единственной инъекции цисплатина.
Анализы на маркеры функции почек и провоспалительные цитокины
Для анализа функции почек выделяют сыворотку и хранят при -80°С до применения. Сывороточный креатинин и уровни BUN измеряют с использованием набора для анализа согласно инструкциям изготовителя (BioVision, Milpitas, CA). Кроме того, определяют количественно провоспалительные цитокины TNF-α, IL-1b, и IL-6 из сыворотки или гомогенатов почечной ткани с помощью ELISA (Quantikine Kit; R&D Systems, Minneapolis, MN) согласно инструкциям изготовителя. Для определения цитокинов почечную ткань гомогенизаруют в забуференном фосфатом физиологическом растворе, содержащем 0,05% твина-20. Используют аликвоты, содержащие 300 мг общего белка. Используют метаболическую клетку для сбора мочи для анализа уровня цитокинов в моче. Число образцов для каждой группы равно пяти.
Альтернативное исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на заболевание почек
С другой стороны, мышей C57BL/6J WT считают и выдерживают для акклиматизации в течение 5-7 дней перед началом эксперимента (Wei Q. et al., «Mouse model of ischemic acute kidney injury: technical notes and tricks», American Journal of Physiology-Renal Physiology, 303(11), F1487-F1494). Мышей произвольно распределяют по группам для различной обработки на основании их массы тела. Различные группы содержат на рационе Harlan 2916. Затем мышей содержат на соответствующих рационах в течение 10 дней перед билатеральным ишемическим повреждением почек. Измерение массы тела проводят один раз при рандомизации и один раз в день 7. Потребление корма оценивают один раз в день 7. Кровь берут ретроорбиталльной пункцией при умеренной анестезии изофураном и используют для анализа базальных уровней азота мочевины в крови (BUN) в день 9.
Мышам дают наркоз кетамином (80 мг/кг, i.p.) и/или ксилазином (10 мг/кг, i.p.) и помещают на хирургическую платформу в положении лежа на спине. Обнажают обе почки через боковые разрезы, и почечные ножки пережимают зажимами для сосудов в течение 25 минут. Затем зажимы удаляют, и место операции сшивают. После закрытия раны вводят интраперитонеально 1 мл физиологического раствора для предотвращения дегидратации. Ложнооперированную группу подвергают подобным хирургическим процедурам за исключением того, что не применяют пережимающие зажимы. Животных контролируют до восстановления от наркоза и возвращают в их кдетку. Животных наблюдают каждый день на общие клинические признаки и симптомы и смертность.
За день до окончания животных по отдельности помещают в метаболические клетки на 12 час, и собирают мочу для оценки на мочевину, креатинин, натрий и калий.
В дни 12, 14 и 16 берут кровь ретроорбитальной пункцией под умеренной анестезией изофураном, и плазму используют для анализа на уровни азота мочевины в крови (BUN) и сывороточный креатинин. Затем животных подвергают эвтаназии путем ингаляции СО2, и собирают органы. Одну почку фиксируют в 10% нейтральном забуференном формалине, а другую быстро замораживают в жидком азоте, хранят при -80°С и используют для оценки перокисления липидов, GSH, МРО и уровней SOD.
Гистологический анализ и подсчет нейтрофилов
Мышиные почки фиксируют в 4% формальдегиде и заливают в парафине. Срезы толщиной 5 мм депарафинизируют в ксилоле и регидратируют через градуированные концентрации этанола. Выполняют окрашивание H&E и PAS с использованием стандартных протоколов. Изображения собирают и анализируют с использованием оптического микроскопа IX71, Olympus, Tokyo, Japan) с помощью программы анализатора DP (DP70-BSW, Tokyo, Japan). Тубулярные повреждения в срезах почек, окрашенных PAS, проверяют в оптическом микроскопе и оценивают на основании процента кортикального тубулярного некроза: 0=нормально, 1=1-10, 2=11-25, 3=26-45, 4=46-75 и 5=76-100%. Слайды оценивают слепым методом, и результаты представляют собой среднее ± s.d. 10 характерных полей/группа. Критерий тяжести тубулярного некроза, отображающего утрату проксимальной щеточной каемки и образование цилиндров, используют для классификации образцов. Число образцов для каждой группы равно 10. Инфильтрацию нейтрофилов оценивает количественно на окрашенной PAS ткани специалист по патологии почек, подсчитывая число нейтрофилов в поле при большом увеличением (×400). Подсчет проводят по меньшей мере в 10 полях во внешней стороне наружного мозгового вещества для каждого слайда.
Все величины представляют как среднее ± s.d. Используют однопараметрический дисперсионный анализ для вычисления статистической значимости результатов всех анализов, и Р-значения <0,05 рассматривают как статистически значимые.
Пример 47. Исследование действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) на острое повреждение почек, вызванное ишемией/реперфузией
Исследование для определения действия соединений формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или их фармацевтически приемлемых солей на острое повреждение почек, вызванное ишемией/реперфузией (вызванное I/R), выполняют на мышах CD-1 (ICR).
Мышей CD-1 (ICR) закупают у Charles River Laboratory (Wilmington, MA). Мышей содержат в среде с регулируемыми температурой и влажностью при цикле свет-темнота 12-12 час и предоставляют свободный доступ к стандартному корму для грызунов (TekLad, Madison, WI) и водопроводной воде.
Мышам делают разрез по середине спины, и обе почечные ножки зажимают на 45 мин микрососудистыми зажимами (00396-01; Fine Science Tools, Foster City, CA). После удаления зажимов почки проверяют на восстановление тока крови. Животным дают восстановиться, и их умерщвляют через 48 час после реперфузии. Мышей обрабатывают 100 мг/кг соединения формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемой соли с помощью ротового зонда один раз в день. Мышей CD-1 делят на четыре группы: (1) молодые мыши с мнимым повреждением (n=4) (возраст 6-7 недель); (2) молодые мыши с повреждением I/R (n=8); (3) взрослые мыши с мнимым повреждением (n=4) (возраст 20-24 недели); и (4) взрослые мыши с повреждением I/R (n=11). Других 27 взрослых мышей (возраст 20-24 недели) произвольно делят на две группы: 13 мышей получают соединение формулы (I), формулы (Ia), формулы (Ib) формулы (II) или формулы (III) или его фармацевтически приемлемую соль, и другие 14 мышей получают среду как контроль.
Уровень сывороточного креатинина измеряют с использованием аналитического набора QuantiChrom Creatinine Assay Kit (DICT-500, BioAssay Systems, Hayward, CA). Измерения BUN регистрируют с использованием реагента Infinity Urea (Nitrogen) Liquid Stable Reagent (TR12421; ThermoTrace, Victoria, AU).
Оценка почечной ткани
Почки фиксируют в 4% параформальдегиде, заделывают в парафине и окрашивают гематоксилином и эозином (толщина 4 мм). Тубулярное повреждение оценивают по шкале 0-4 на основании процента трубочек с некрозом, дилатации или разбухания клеток: 0 - менее 5%; 1-5-25%; 2-25-50%; 3-50-75%; и 4 - свыше 75%. Все поля с большим увеличением (×400) в корковом слое и наружном мозговом слое оценивает патоморфолог слепым способом.
Все величины выражают как среднее±s.e. Статистический анализ выполняют с использованием GraphPad Prism 4.00 (San Diego, CA) с проверкой непарным t-критерием Стьюдента для двух наборов данных и дисперсионного анализа и после этого критерия Бонферрони для нескольких групп. P<0,05 считают значимым.
Пример 48. Определение действия соединений 1 и 17 на уровни фосфорилирования FoxO1
Клетки AML-12 обрабатывают различными концентрациями соединения 1 или соединения 17 в течение 24 часов. Затем клетки лизируют в буфере для лизиса (50 мM трис, 150 мM KCl, ЭДТК 1мM, NP40 1%), содержащем ингибиторы протеазы и фосфатазы, и анализируют SDS-PAGE/вестерн-блоттингом. Блокаду и инкубацию антител осуществляют в 5% молоке. Каждый присутствующий белок детектируют с помощью его специфического антитела. Антитела к тубулину получают от Sigma Inc., антитела к FoxO1 и фосфо-FoxO1 (Ser256) получают от Cell Signaling. Реакции детекции с антителами проявляют с помощью усиленной хемилюминисценции (Advansta, CA, USA) с использованием рентгеновских пленок.
Флсфорилирование FoxO1 в Ser256 приводит к их нуклеарному экспорту и к ингибированию активности их фактора транскрипции. Наблюдают уменьшение фосфорилирования FoxO1 в Ser256 с возрастанием дозы соединения 1 и 17 (фиг. 6), что указывает на возрастание FoxO1 с ядерной транслокацией и, следовательно, возрастание транскрипционной активности FoxO1.
Если не определено иначе, все технические и научные термины, используемые в настоящем описании, имеют те же значения, какие им обычно придают специалисты в данной области техники, к которым относится раскрытие. В описании формы единственного числа также включают формы множественного числа, если контекст не указывает четко иное. Хотя на практике и при проверке раскрытия можно использовать способы и материалы, схожие с или эквивалентные описанным в настоящем описании, подходящие способы и материалы описаны ниже. Все публикации, заявки на патент, патенты и другие ссылки, упомянутые в настоящем описании, включены в него в качестве ссылок. Ссылки, цитированные в настоящем описании, не допускают претензий известного уровня техники к заявляемому раскрытию. В случае конфликта настоящее описание, включая определения, будет контролем. Кроме того, материалы, способы и примеры являются только иллюстративными и не предназначены для ограничения.
Пример 49. Синтез примеров соединений
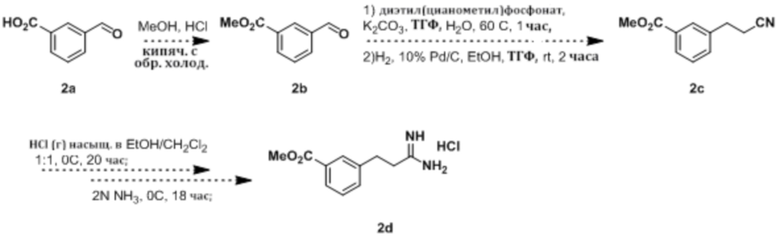
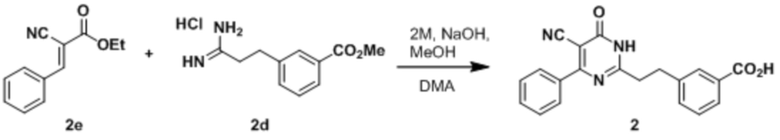
См. Hirose M, et al., «Design and synthesis of novel DFG-out RAF/vascular endothelial growth factor receptor 2 (VEGFR2) inhibitors: 3. Evaluation of 5-amino-linked thiazolo[5,4-d]pyrimidine and thiazolo[5,4-b]pyridine derivatives». Bioorg. Med. Chem., 2012, 15; 20(18): 5600-15.
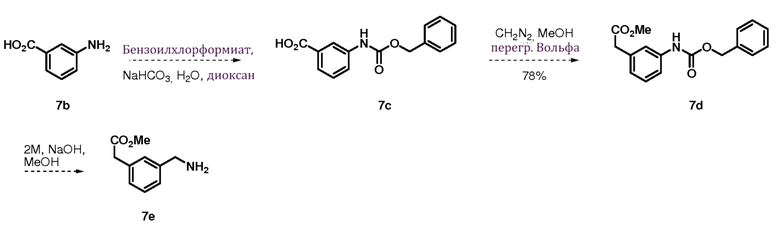
См. Clift MD, Silverman RB., «Synthesis and evaluation of novel aromatic substrates and competitive inhibitors of GABA aminotransferase», Bioorg. Med. Chem. Lett., 2008, 15; 18(10): 3122-5.
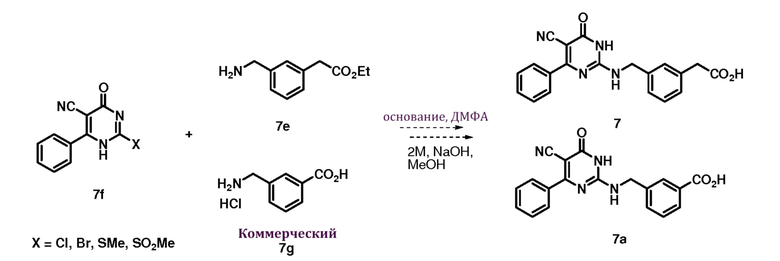
A. M. El-Reedy, A. O. Ayyad and A. S. Ali, «Azolopyrimidines and pyrimidoquinazolines from 4-chloropyrimidines», J. Het. Chem., 1989, 26, 313-16.
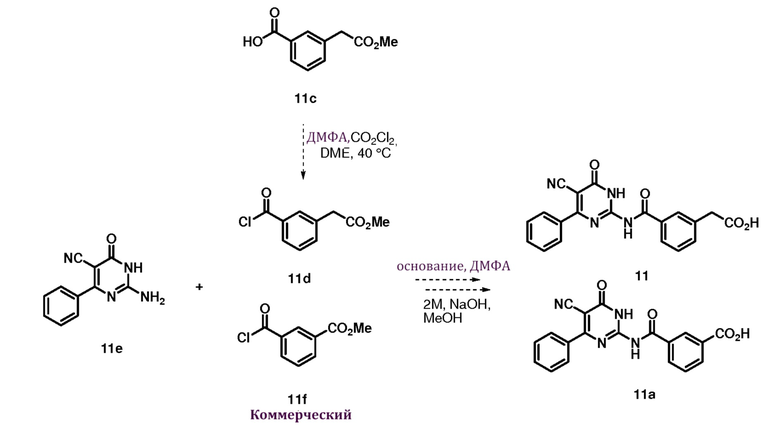
См. Iwahashi M. et al., «Design and synthesis of new prostaglandin D2 receptor antagonists», Bioorg. Med. Chem., 2011, 19(18): 5361-71.
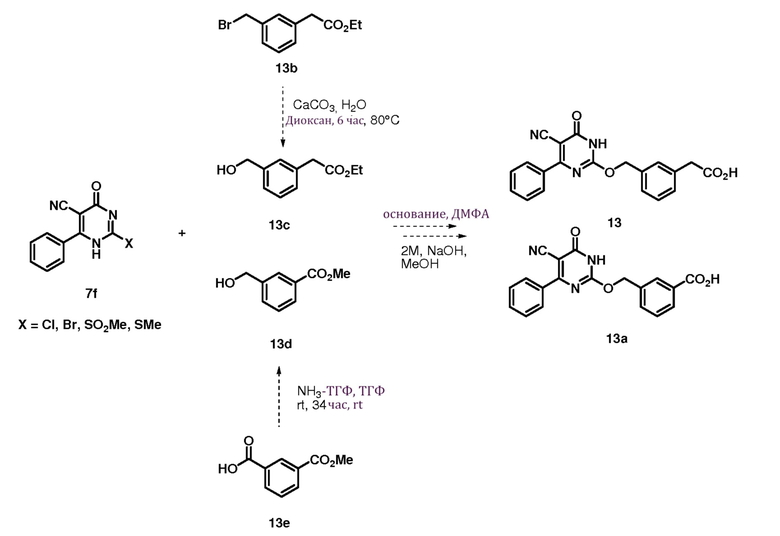
См. U.S. 2008/004302(A1); и U.S. 8716470 (B2).
ЭКВИВАЛЕНТЫ
Специалисты в данной области техники узнают или могут выяснить с использованием не более чем обычных экспериментов многие эквиваленты конкретных воплощений и способов, описанных в настоящем описании. Предполагается, что такие эквиваленты охватываются объемом настоящего раскрытия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРАЗИН-2-КАРБОКСАМИДА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR5 | 2006 |
|
RU2407739C2 |
| ИЗОКСАЗОЛИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ АМИДГИДРОЛАЗЫ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2539595C2 |
| ИНГИБИТОРЫ HDAC | 2014 |
|
RU2665554C2 |
| АНТИВИРУСНЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2505540C2 |
| МОНОМЕРНЫЕ ПРОИЗВОДНЫЕ ГЛИКОПЕПТИДНОГО АНТИБИОТИКА | 2005 |
|
RU2424248C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| АЗОЛЬНЫЕ И ТИАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2436779C2 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ, ТАКИХ КАК COPD | 2011 |
|
RU2604719C2 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ, ТАКИХ КАК COPD | 2011 |
|
RU2581839C2 |
| НОВЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2550346C2 |
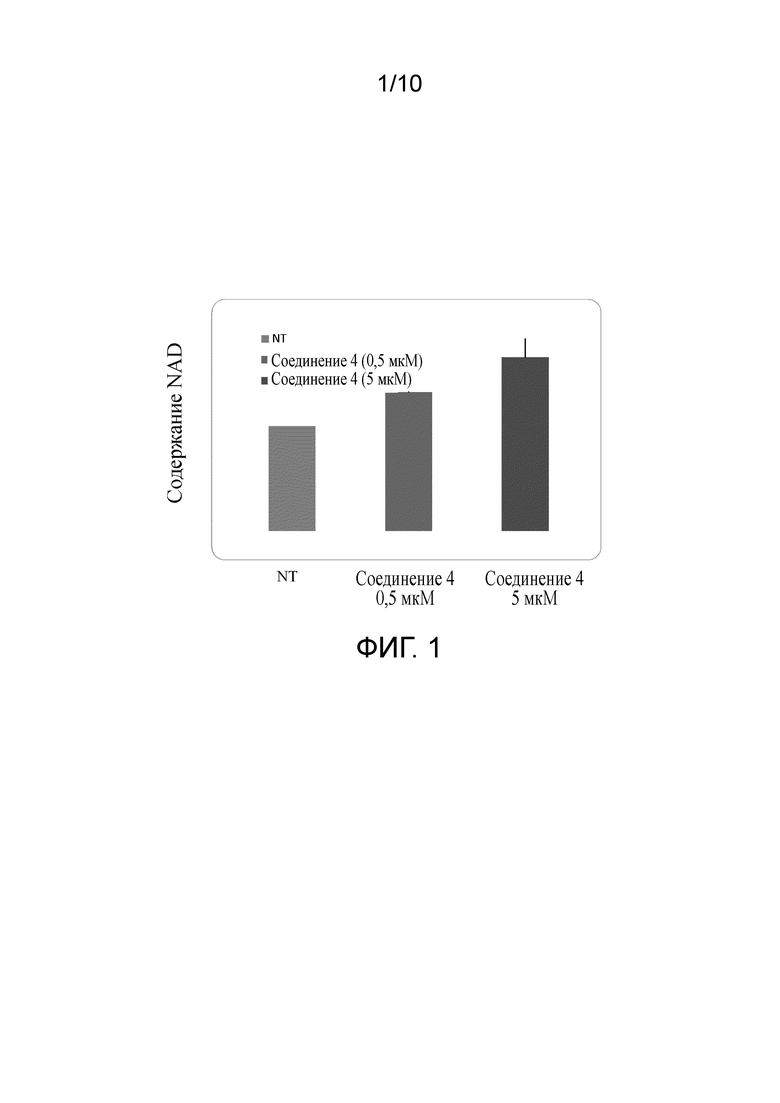
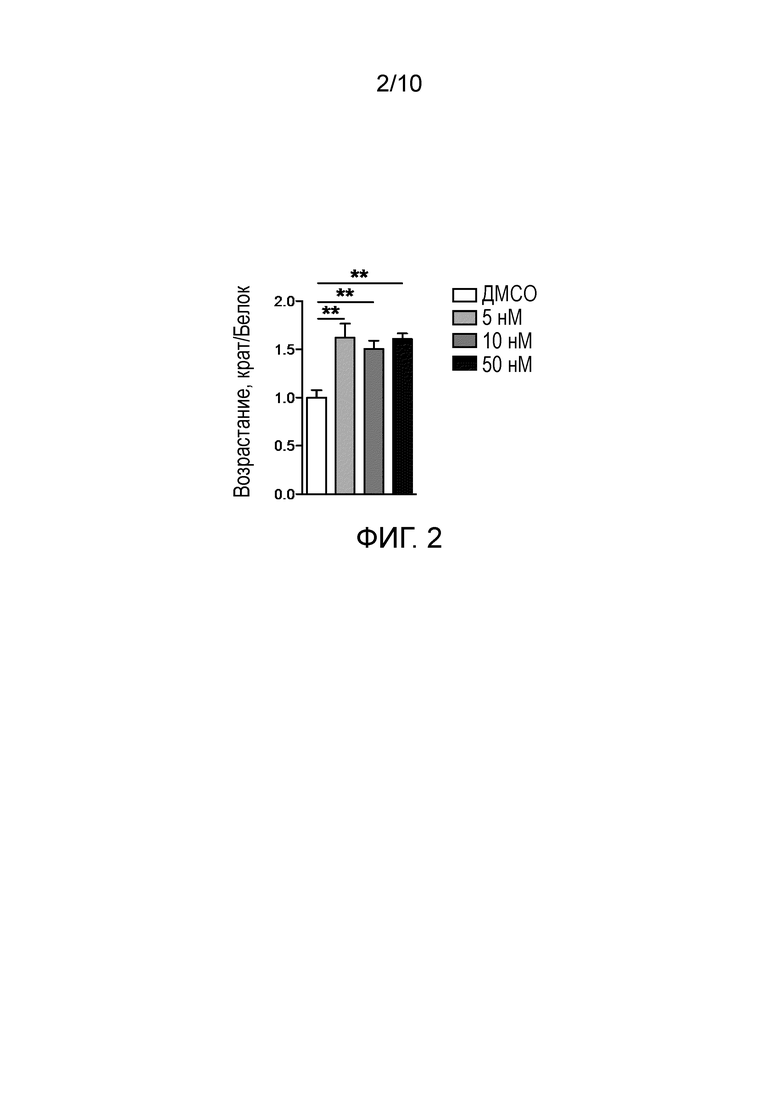
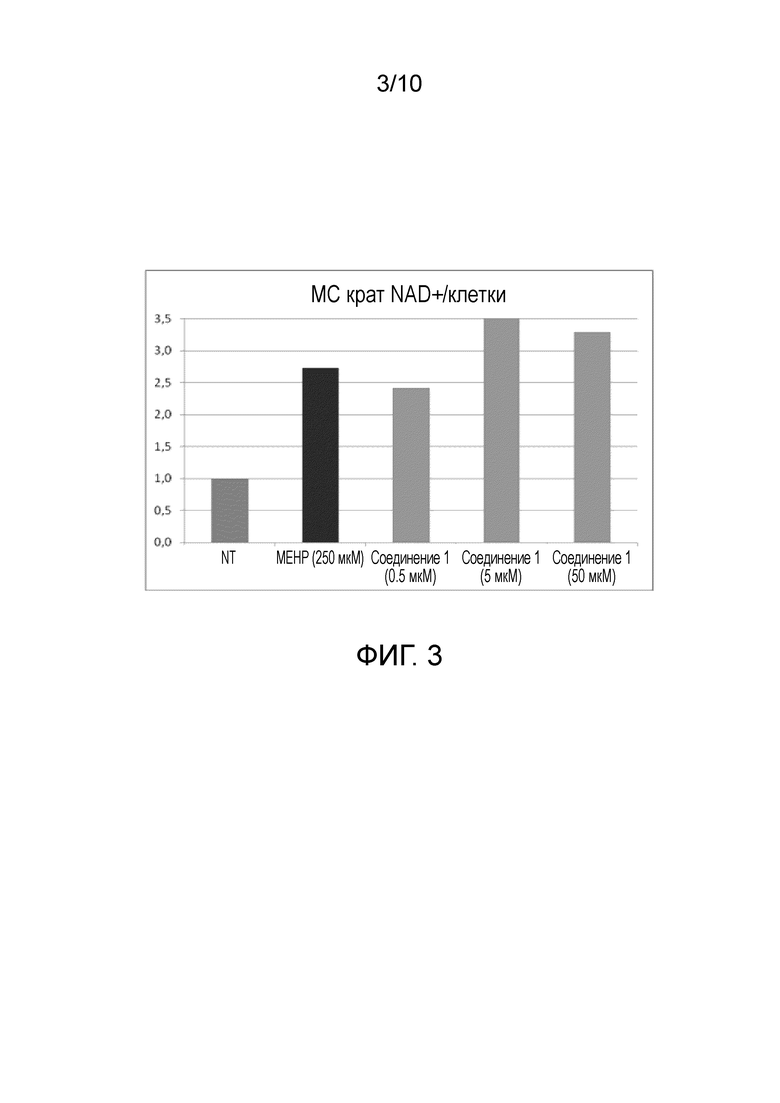
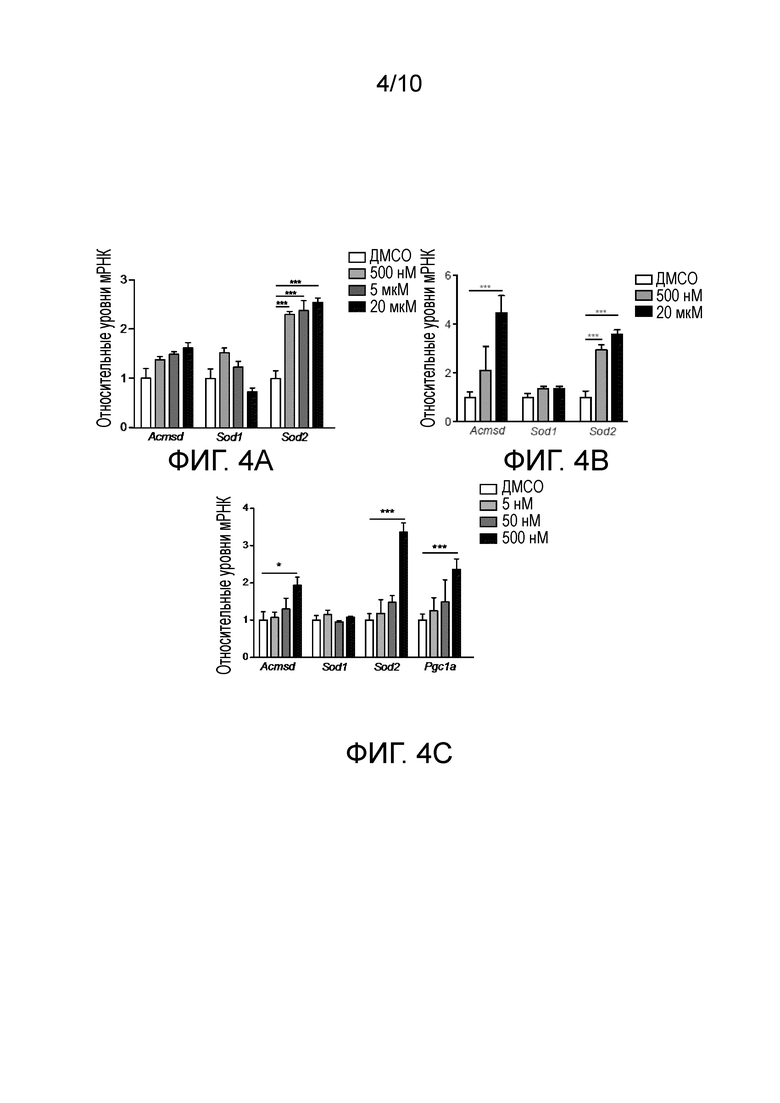
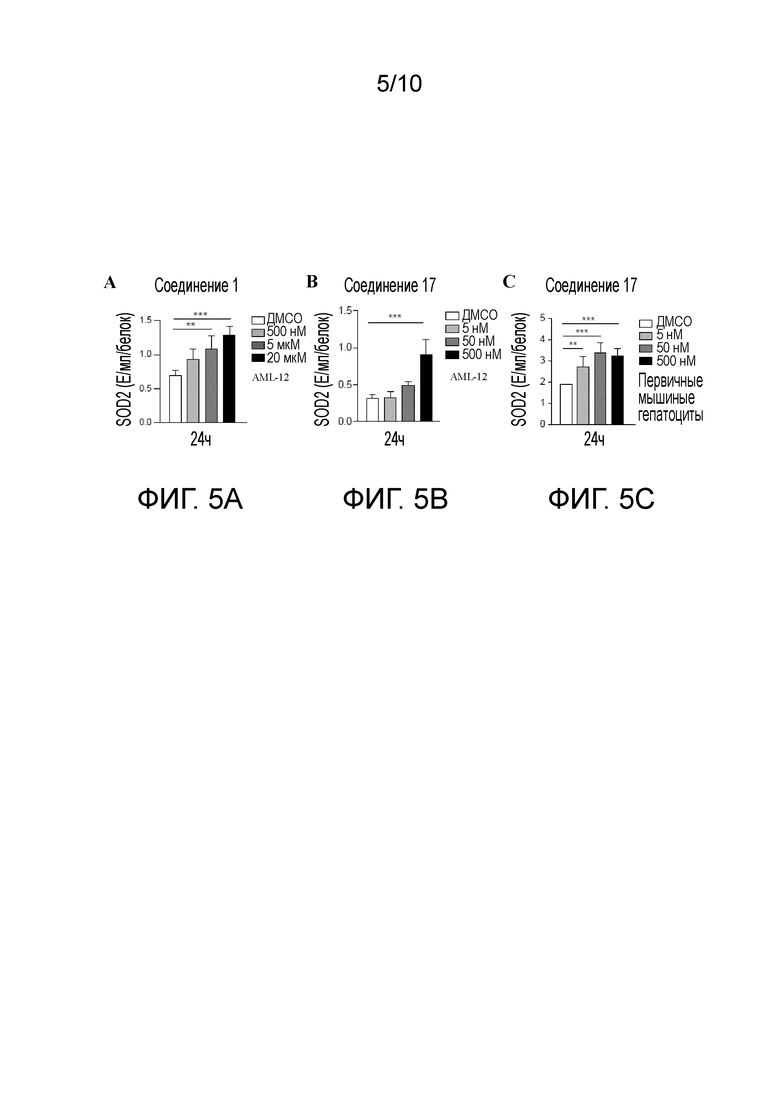
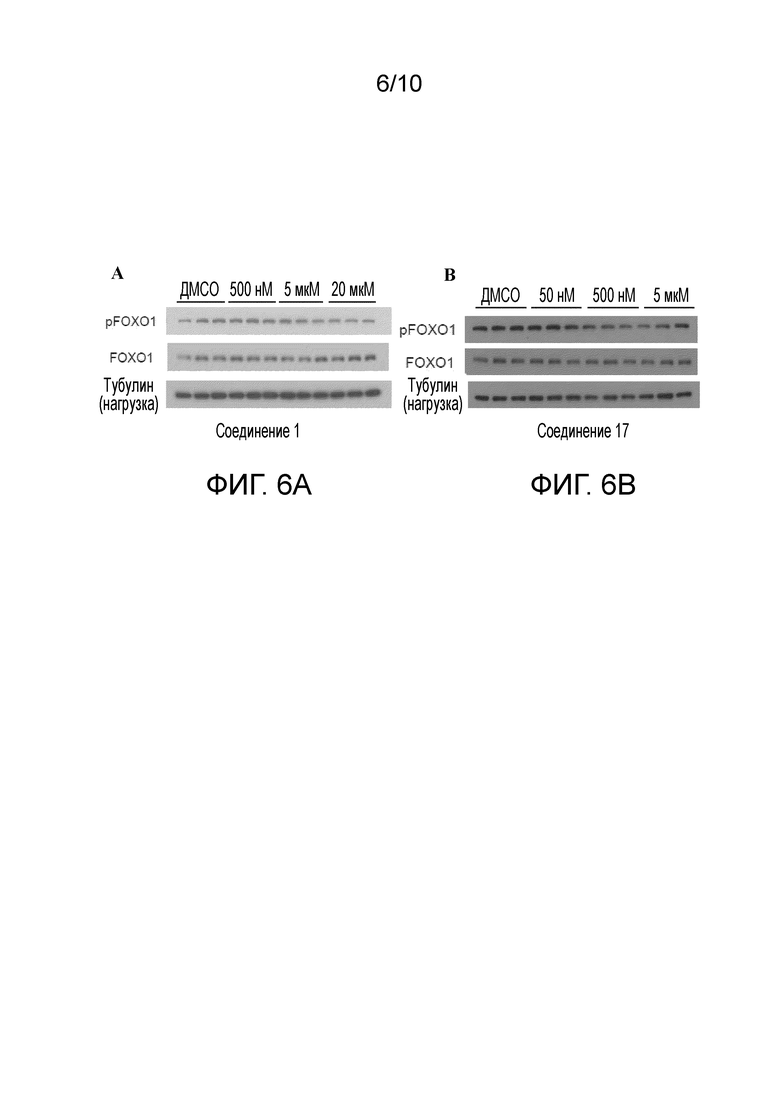
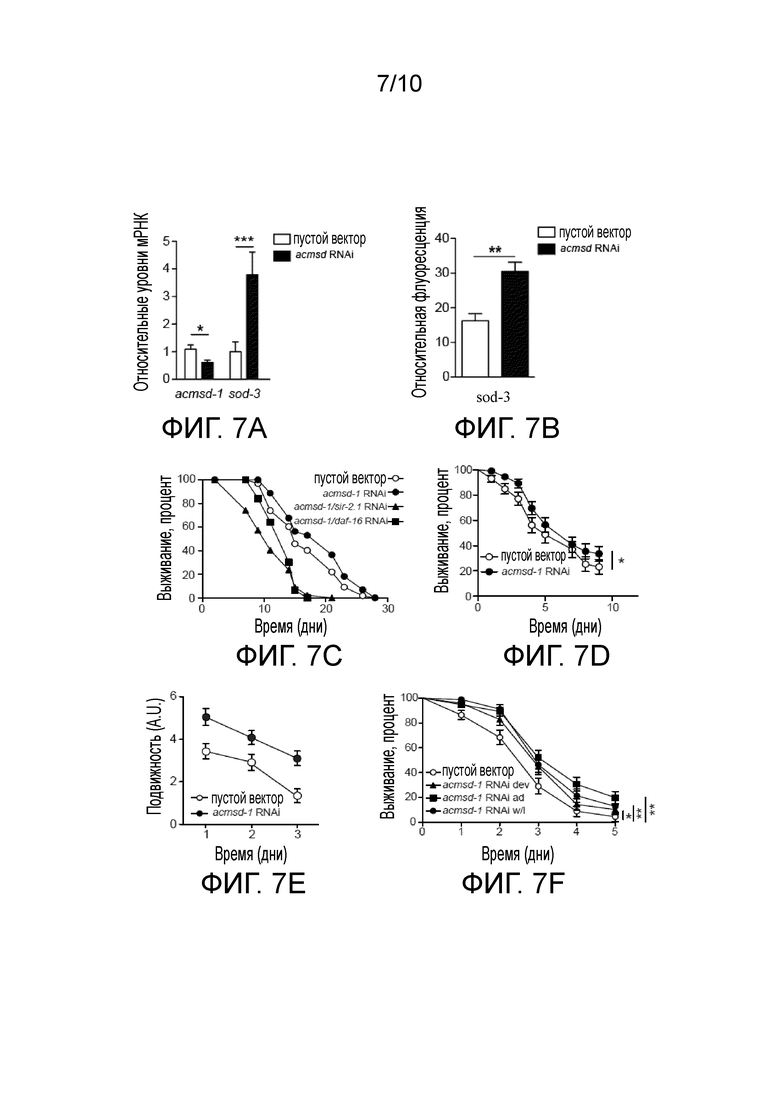
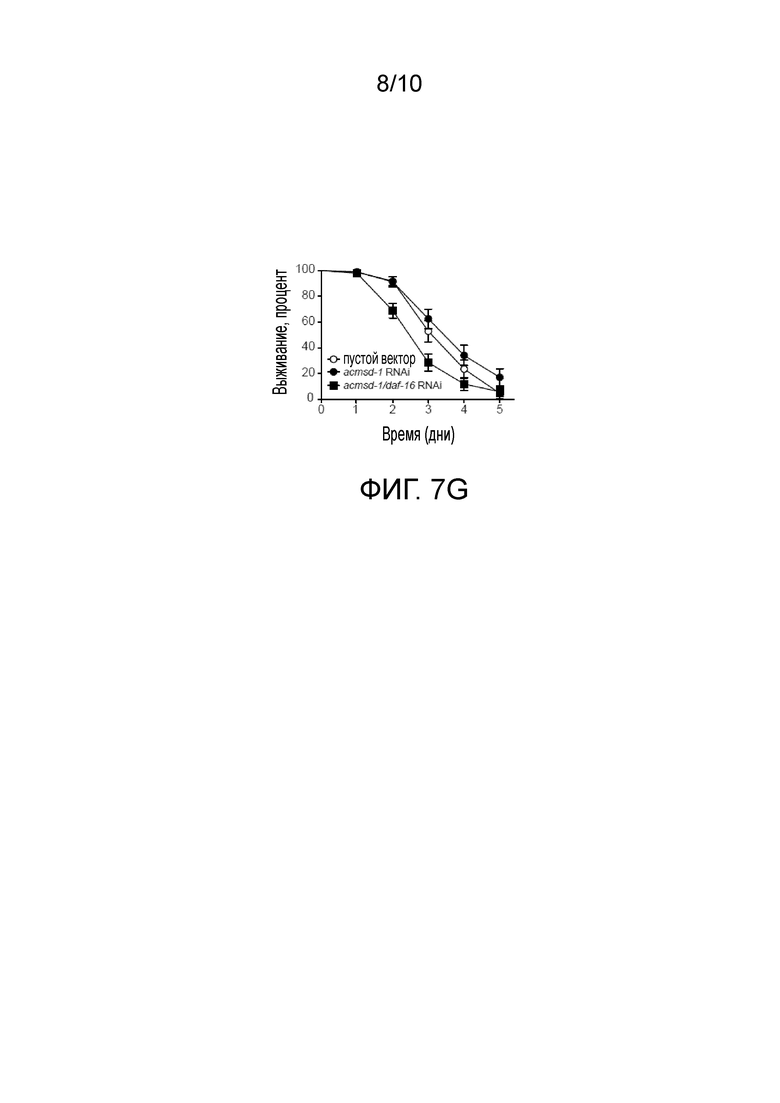
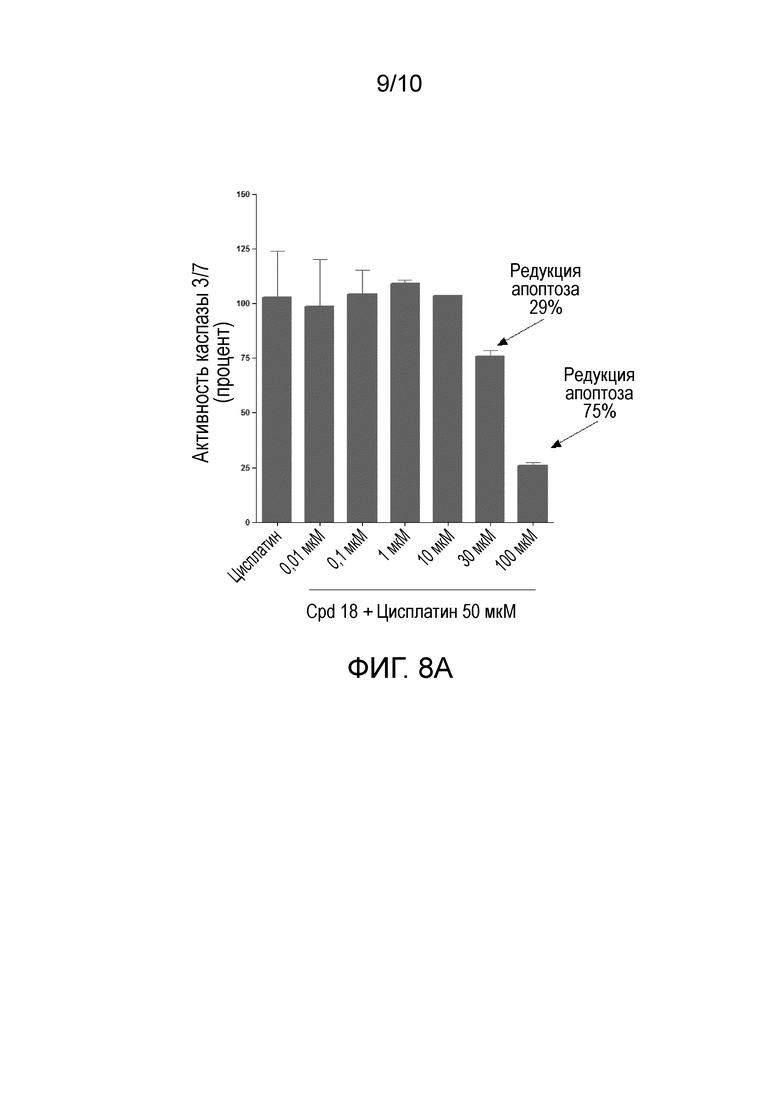
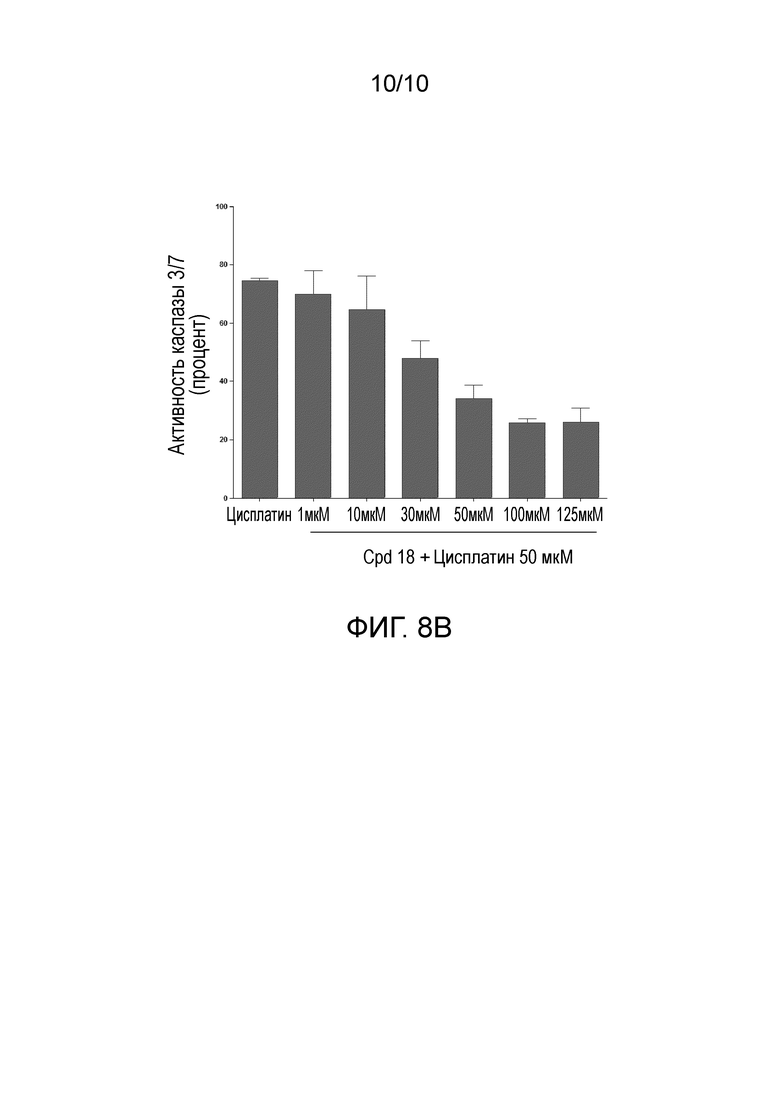
Изобретение относится к соединению, представленному формулой (I), или его фармацевтически приемлемой соли, или таутомеру, которые могут найти применение в качестве ингибиторов α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD). В формуле (I) X представляет собой O, OH или Cl; L представляет собой -(CH2)mY(CH2)p-; Y представляет собой NH или S(O)q; R1 представляет собой C6арил, где арил замещен Ra и Rb и необязательно замещен одним или несколькими Re; один из Ra и Rb представляет собой водород и другой представляет собой -(CH2)rCO2Rx, -(CH2)rтетразол или -(CH2)rоксадиазолон; Rc представляет собой галоген или -CN; Rd представляет собой метил, фенил, 5- или 6-членный гетероарил, содержащий один или два гетероатома, выбранных из азота и серы, или 5- или 6-членный карбоцикл; каждый Rx при каждом появлении представляет собой независимо водород или (C1-C6)алкил; каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN; Rf представляет собой H или отсутствует; каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил; каждый m и p равен независимо 0, 1 или 2, где m+p <3; q равен 0, 1 или 2; r равен 0 или 1; и пунктирная линия представляет собой необязательную двойную связь; при условии, что Rс не является -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой фенил. Изобретение также относится к фармацевтической композиции, обладающей свойствами ингибитора α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD) и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), включающей терапевтически эффективное количество указанного соединения и по меньшей мере один фармацевтически приемлемый носитель, разбавитель или эксципиент, и к способу лечения заболевания или расстройства путем ингибирования α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), который включает введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества указанного соединения. 15 н. и 19 з.п. ф-лы, 8 ил., 2 табл., 49 пр.
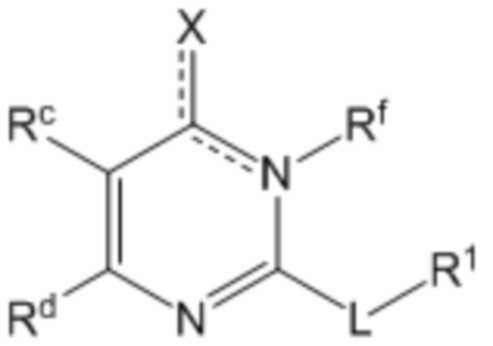 (I)
(I)
1. Соединение, представленное формулой (I)
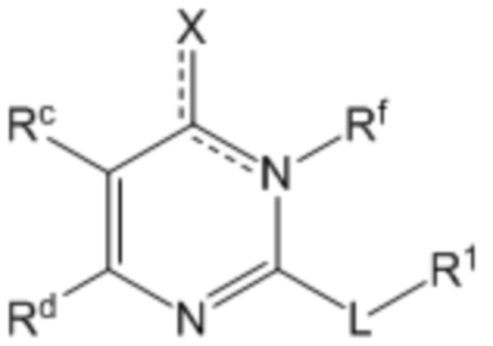 ,
,
или его фармацевтически приемлемая соль, или таутомер,
где в указанной формуле
X представляет собой O, OH или Cl;
L представляет собой -(CH2)mY(CH2)p-;
Y представляет собой NH или S(O)q;
R1 представляет собой C6арил, где арил замещен Ra и Rb и необязательно замещен одним или несколькими Re;
один из Ra и Rb представляет собой водород и другой представляет собой -(CH2)rCO2Rx, -(CH2)rтетразол или -(CH2)rоксадиазолон;
Rc представляет собой галоген или -CN;
Rd представляет собой метил, фенил, 5- или 6-членный гетероарил, содержащий один или два гетероатома, выбранных из азота и серы, или 5- или 6-членный карбоцикл;
каждый Rx при каждом появлении представляет собой независимо водород или (C1-C6)алкил;
каждый Re представляет собой независимо (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, галоген, -ORy, (C1-C6)галогеналкил, -NHRz, -OH или -CN;
Rf представляет собой H или отсутствует;
каждый Ry и Rz представляет собой независимо водород, (C1-C6)алкил или (C1-C6)галогеналкил;
каждый m и p равен независимо 0, 1 или 2, где m+p < 3;
q равен 0, 1 или 2;
r равен 0 или 1; и
пунктирная линия представляет собой необязательную двойную связь;
при условии, что Rс не является -CN, когда X представляет собой O, L представляет собой -SCH2-, и Rd представляет собой фенил.
2. Соединение по п.1, причем соединение представлено формулой (Ia)
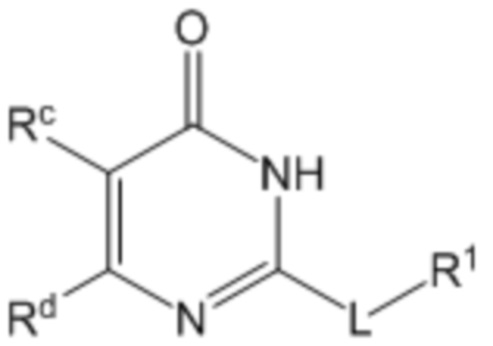 (Ia),
(Ia),
или его фармацевтически приемлемая соль, или таутомер.
3. Соединение по п. 1 или 2, причем соединение представлено формулой (Ib)
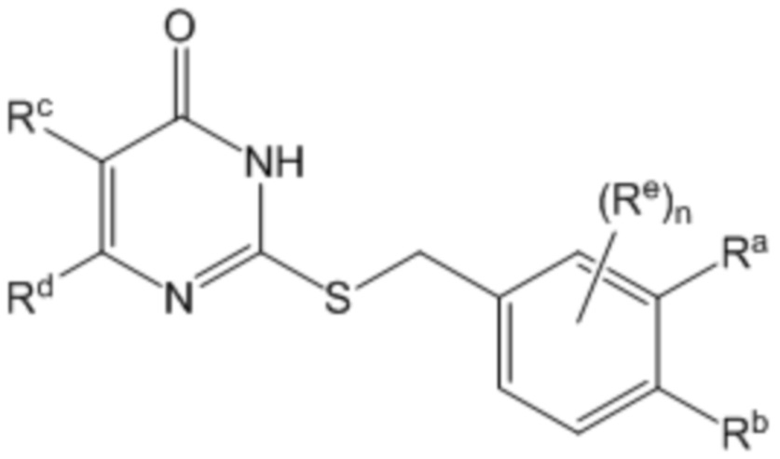 (Ib),
(Ib),
или его фармацевтически приемлемая соль, где n равен 0, 1, 2 или 3.
4. Соединение по любому из пп. 1-3,
в котором
один из Ra и Rb представляет собой водород и другой представляет собой CO2Rx, CH2CO2Rx, тетразол или оксадиазолон.
5. Соединение по любому из пп. 1-3, причем соединение представлено формулой (II)
 (II),
(II),
или его фармацевтически приемлемая соль.
6. Соединение по любому из пп. 1-5, в котором Rd представляет собой метил, циклогексил, пиридинил, тиазолил, фенил или тиенил.
7. Соединение по любому из пп. 1-4, в котором Rа представляет собой водород, СН2СО2Н, тетразол или (1,2,4-оксадиазол-5(4Н)-он).
8. Соединение по любому из пп. 1-4, в котором Rb представляет собой водород, СН2СО2Н, тетразол или (1,2,4-оксадиазол-5(4Н)-он).
9. Соединение по п. 3, в котором n равен 0.
10. Соединение по п.1, причем соединение представлено формулой (III)
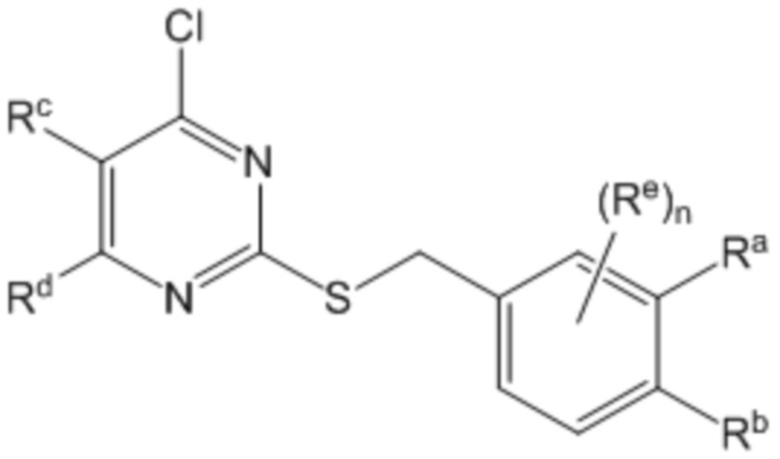 (III),
(III),
или его фармацевтически приемлемая соль.
11. Соединение по п.1, имеющее одну из следующих формул:
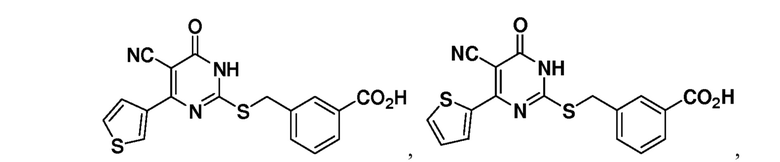
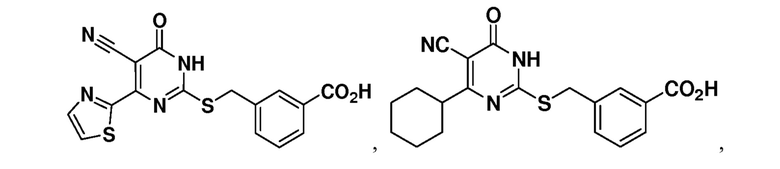
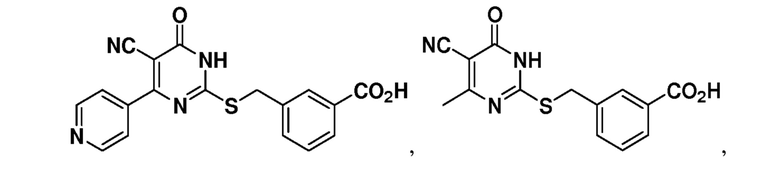
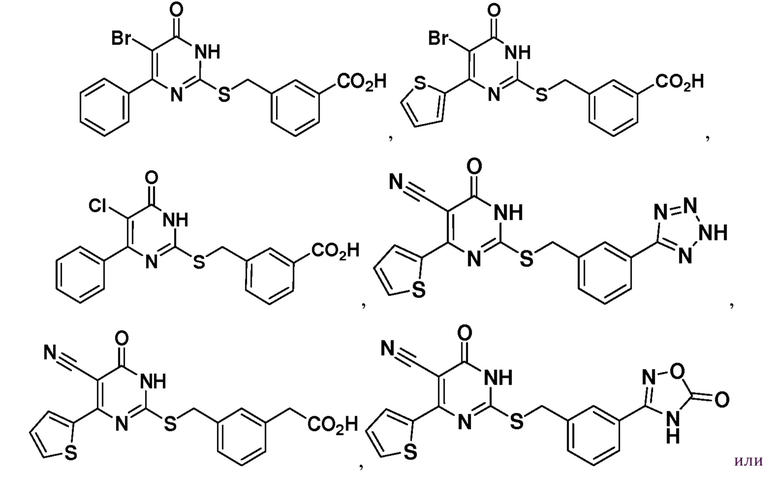

или его фармацевтически приемлемая соль.
12. Фармацевтическая композиция, обладающая свойствами ингибитора α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD) и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), включающая терапевтически эффективное количество соединения по любому из пп. 1-11 или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель, разбавитель или эксципиент.
13. Способ лечения заболевания или расстройства путем ингибирования α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
14. Способ предупреждения заболевания или расстройства путем ингибирования α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
15. Способ снижения опасности заболевания или расстройства путем ингибирования α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного с дисфункцией ACMSD, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
16. Способ лечения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
17. Способ предупреждения заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
18. Способ снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+), включающий введение субъекту, страдающему от или восприимчивому к развитию заболевания или расстройства, связанного со сниженными уровнями NAD+, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
19. Способ лечения расстройства, связанного с митохондриальной дисфункцией, включающий введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
20. Способ по п.19, причем указанное расстройство, связанное с митохондриальной дисфункцией, представляет собой наследственную митохондриальную болезнь, обыкновенное метаболическое расстройство, нейродегенеративное заболевание, расстройство, связанное со старением, почечное расстройство или хроническое воспалительное заболевание.
21. Способ по п.20, причем обыкновенное метаболическое расстройство представляет собой ожирение или диабет типа II.
22. Способ промотирования окислительного метаболизма, включающий введение субъекту, страдающему от или восприимчивому к развитию метаболического расстройства, терапевтически эффективного количества соединения по любому из пп. 1-11, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
23. Фармацевтическая композиция для применения в способе лечения заболевания или состояния, опосредуемого ACMSD, причем композиция включает терапевтически эффективное количество соединения по любому из пп. 1-11 или его фармацевтически приемлемую соль, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+).
24. Применение соединения по любому из пп. 1-11 или его фармацевтически приемлемой соли, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
25. Применение соединения по любому из пп. 1-11 или его фармацевтически приемлемой соли, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
26. Применение соединения по любому из пп. 1-11 или его фармацевтически приемлемой соли, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), при изготовлении лекарственного средства для лечения, предупреждения или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
27. Применение соединения по любому из пп. 1-11 или его фармацевтически приемлемой соли, обладающего свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), при изготовлении лекарственного средства для промотирования окислительного метаболизма.
28. Cоединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с дисфункцией α-амино-β-карбоксимуконат-ε-семиальдегид-декарбоксилазы (ACMSD).
29. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
30. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для применения в качестве лекарственного средства для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного с митохондриальной дисфункцией.
31. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для применения в качестве лекарственного средства для промотирования окислительного метаболизма.
32. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для лечения, предупреждения или снижения опасности заболевания или расстройства, связанного со сниженными уровнями никотинамидадениндинуклеотида (NAD+).
33. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для лечения, предупреждения или снижения опасности расстройства, связанного с митохондриальной дисфункцией.
34. Соединение по любому из пп. 1-11 или его фармацевтически приемлемая соль, обладающее свойствами ингибитора ACMSD и способностью повышать уровень никотинамидадениндинуклеотида (NAD+), предназначенное для промотирования окислительного метаболизма.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| DATABASE REGISTRY [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; RN 1082473-69-5, 09.12.2008, retrieved from STN | |||
| DATABASE REGISTRY [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; RN 1082520-77-1, 09.12.2008, retrieved from STN | |||
| DATABASE REGISTRY [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, | |||
Авторы
Даты
2021-04-13—Публикация
2015-08-28—Подача