[0001] По настоящей заявке испрашивается приоритет согласно предварительной заявке США № 62/425,832, поданной 23 ноября 2016. Раскрытие этой приоритетной заявки включено здесь полностью посредством ссылок.
ОБЛАСТЬ
[0002] Настоящее описание раскрывает способы лечения фокально-сегментарного гломерулосклероза (FSGS) соединением Формулы I. FSGS включает группу нарушений, характеризующих почечные повреждения, которые, как видно на световой микроскопии, включают только некоторые (фокальные) клубочки и только часть (сегментарную) из включенных клубочков. FSGS может возникнуть в контексте генетических факторов риска (генетический FSGS), гетерозиготности или гомозиготности для вариантов риска apoL1 (apoL1 FSGS), воздействия вирусов (вирусный FSGS), требований повышенной фильтрации на нефронах (адаптивный FSGS, как это может иметь место при установлении утраты нефронов, при гипертонии, ожирении, других состояниях), воздействия токсинов или лекарств (токсический FSGS), в контексте других почечных или системных заболеваний (вторичный FSGS, как может иметь место при установлении диабета, волчаночного нефрита и других болезней), в контексте распознанных или нет факторов циркуляции или может быть идиопатическим (первичный FSGS).
[0003] FSGS может быть первичным (нет известной причины) или вторичным. Вторичный FSGS может быть связан с инфекциями или вирусами, такими как HIV, заболеваниями, такими как серповидно-клеточная анемия или волчанка, токсинами или препаратами, такими как анаболические стероиды, героин или памидронат, потерей нефронов и гиперфильтрацией, такой как при хроническом пиелонефрите и рефлюксе, тяжелой формой ожирения или сахарным диабетом.
ПРЕДПОСЫЛКИ
[0004] FSGS используется для описания как заболевания, характеризуемого первичным повреждением подоцитов, так и повреждением, происходящим вторично при любом типе хронического заболевания почек (CKD). Он определяется наличием склероза в частях (сегментарный) или некоторых клубочках (фокальный) с помощью световой микроскопии. FSGS может быть обнаружен без идентифицируемой причины («первичный» или «идиопатический» FSGS представляет 80% случаев) или в ответ на предшествующее повреждение клубочков, такое как гипертония или ожирение («вторичный» FSGS представляет 20% случаев).
[0005] Наиболее распространенное проявление FSGS - это протеинурия, изменяющаяся от поднефротического до нефротического уровней (тяжелая протеинурия, гипоальбуминемия и гиперлипидемия). Тяжелая протеинурия приводит к прогрессивной потере функции почек (гломерулосклероз) и почечной недостаточности. Она составляет ~15% терминальной стадии почечной недостаточности (ESRD). Обширная протеинурия (> 10-15 г/день) приводит к быстрому ухудшению почечной функции и прогрессии до ESRD в течение 2-3 лет. Выживаемость FSGS пациентов с обширной протеинурией составляет только 45%.
[0006] Фокально-сегментарный гломерулосклероз указывается Бюро редких заболеваний (ORD) Национальных Институтов Здоровья (NIH) как «редкое заболевание» и в настоящее время нет утвержденного медикамента для FSGS. Приблизительно 5 400 пациентам в США каждый год диагностируют FSGS, но число случаев увеличивается в большей степени, чем каких-либо других причин Нефротического Синдрома. Приблизительно 1 000 FSGS пациентам каждый год осуществляют пересадки почек. В течение времени от часов до недель после пересадки почек, однако, FSGS возвращается приблизительно в 30-40% пациентов. Используемый в настоящее время стандарт медицинского ухода включает использование стероидов, ингибиторов кальциневрина, ACE или ARBs ингибиторов, иммунодепрессантов, мочегонных средств, плазмафереза, изменения диеты и статинов. Только 20% пациентов, однако, достигают полной ремиссии после 5 лет лечения, и 40% пациентов не показывают ремиссии (Focal and Segmental Glomerulosclerosis: Definition and Relevance of a Partial Remission. Troyanov et al., J Am Soc Nephrol 16: 1061-1068, 2005). Таким образом, остается потребность в разработке новых эффективных лекарств для лечения этого заболевания.
КРАТКИЙ ОБЗОР
[0007] Настоящее раскрытие относится к способам лечения фокально-сегментарного гломерулосклероза (FSGS) у нуждающегося в этом пациента, включающим назначение пациенту эффективного количества соединения Формулы I
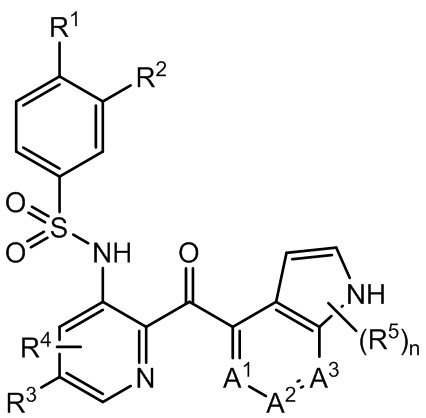
Формула I
или фармацевтически приемлемой его соли,
где R1 является галогеном или C1-6 алкилом;
R2 является водородом, галогеном, C1-6 алкилом, C1-6 алкокси, C1-6 галоалкилом, C1-6 галоалкокси или -CN;
R3 является водородом, галогеном или C1-6 алкилом;
R4 является водородом, галогеном или C1-6 алкилом;
каждый R5 независимо является C1-6 алкилом, -OH или -NH2;
n - это 0, 1, 2, или 3; и
каждый из A1, A2 и A3 является -CH- или -N-, где, по крайней мере, один из A1, A2 или A3 - это -N-.
ФИГУРЫ
[0008] Фиг. 1 показывает значения UACR в исходный момент, неделю 1 и неделю 2 при лечении соединением 3 и без него в 5/6 остаточной почечной модели.
[0009] Фиг. 2 показывает содержание макрофагов в процентах от общей площади при и без лечения соединением 3 в 5/6 остаточной почечной модели.
[0010] Фиг. 3 показывает репрезентативные изображения почечных интерстициальных макрофагов в 5/6 остаточной почечной модели при и без лечения соединением 3.
[0011] Фиг. 4 показывает количества подоцитов на поперечное сечение клубочка при и без лечения соединением 3 в 5/6 остаточной почечной модели.
[0012] Фиг. 5 показывает репрезентативные изображения подоцитов в 5/6 остаточной почечной модели при и без лечения соединением 3.
[0013] Фиг. 6 показывает процентное содержание клубочков с мезангиолизисом у здоровых мышей контроля и 5/6 нефрэктомированной мыши при и без лечения соединением 3 в 5/6 остаточной почечной модели.
[0014] Фиг. 7 показывает репрезентативное изображение клубочков с мезангиолизисом.
[0015] Фиг. 8 показывает UACR уровни в неделю 1, 2 и 3 после лечения соединением 1, кандесартаном и комбинацией соединения 1 и кандесартана в сравнении с наполнителями в модели адриамицин-нефропатии.
[0016] Фиг. 9 показывает уровни UAER в неделю 1, 2 и 3 после лечения соединением 1, кандесартаном и комбинации соединения 1 и кандесартаном по сравнению с наполнителями в модели адриамицин-нефропатии.
[0017] Фиг. 10 показывает UAER значения в исходный момент, неделю 1, 2 и 3 при лечении соединением 3, лечении кандесартаном и комбинации соединения 3 и лечения кандесартаном в 5/6 остаточной почечной модели.
[0018] Фиг. 11 показывает UACR значения в исходный момент, неделю 1 и неделю 2 при лечении соединением 3, лечении кандесартаном и при комбинации лечения соединением 3 и лечения кандесартаном в 5/6 остаточной почечной модели.
ПОДРОБНОЕ ОПИСАНИЕ
Сокращения и определения
[0019] При описании соединений, композиций, способов и процессов этого раскрытия следующие термины имеют следующие значения, если не обозначено иначе.
[0020] «Алкил» как таковой отдельно или как часть другого заместителя относится к группе углеводородов, которая может быть линейной, цикличной, или разветвленной или их комбинацией, имеющей указанное количество атомов углерода (т.е. C1-8 означает один - восемь атомов углерода). Примеры алкильных групп включают метил, этил, n -пропил, изопропил, n -бутил, t- бутил, изобутил, втор- бутил, циклогексил, циклопентил, (циклогексил)метил, циклопропилметил, бицикло [2.2.1] гептан, бицикло [2.2.2] октан и т.д. Алкильные группы являются незамещенными, если не обозначено иначе. Примеры замещенного алкила включают галоалкил, тиоалкил, аминоалкил и т.п.
[0021] «Алкокси» относится к -O-алкилу. Примеры алкокси группы включают метокси, этокси, n-пропокси и т.д.
[0022] «Алкенил» относится к группе ненасыщенных углеводородов, которая может быть линейной, цикличной или разветвленной или их комбинацией. Алкенил группы с 2-8 атомами углерода предпочтительны, несмотря на то, что алкенил может иметь больше чем 8 атомов углерода. Алкенильная группа может содержать 1, 2 или 3 углерод-углерод двойные связи. Примеры алкенильных групп включают винил, n-пропенил, изопропенил, n-бут-2-енил, n-гекс- 3-енил, циклогексенил, циклопентенил и т.п. Алкенильные группы являются незамещенными, если не обозначено иначе.
[0023] «Алкинил» относится к группе ненасыщенного углеводорода, которая может быть линейной, цикличной или разветвленной или комбинация этого. Алкинил группы с 2-8 атомами углерода предпочтительны. Алкинильная группа может содержать 1, 2 или 3 углерод - углерод тройные связи. Примеры алкинильных групп включают этинил, n-пропинил, n-бут-2-инил, n-гекс-3-инил и т.п. Алкинильные группы являются незамещенными, если не обозначено иначе.
[0024] «Арил» относится к полиненасыщенной группе ароматических углеводородов, имеющей единственное кольцо (моноциклическая) или множественные кольца (бициклическая), которые могут быть сплавлены или связаны ковалентно. Арильные группы с 6-10 атомами углерода предпочтительны, при этом это количество атомов углерода может быть указано как C6-10, например. Примеры арильных групп включают фенил и нафтален-1-ил, нафтален-2-ил, бифенил и т.п. Арильные группы являются незамещенными, если не обозначено иначе.
[0025] «Гало» или «галоген», отдельно или как часть заместителя относится к атому хлора, брома, йода или фтора.
[0026] «Галоалкил», как замещенная алкильная группа, относится к моногалоалкильной или полигалоалкильной группе, наиболее часто замещенной 1-3 атомами галогена. Примеры включают 1-хлорэтил, 3-бромпропил, трифторметил и т.п.
[0027] «Гетероциклил» относится к насыщенному или ненасыщенному неароматическому кольцу, содержащему, по крайней мере, один гетероатом (как правило, 1-5 гетероатомов), выбранных из азота, кислорода или серы. Гетероциклическое кольцо может быть моноциклическим или бициклическим. Предпочтительно эти группы содержат 0-5 атомов азота, 0-2 атома серы и 0-2 атома кислорода. Более предпочтительно эти группы содержат 0-3 атома азота, 0-1 атом серы и 0-1 атом кислорода. Примеры гетероциклических групп включают пирролидин, пиперидин, имидазолидин, пиразолидин, бутиролактам, валеролактам, имидазолидинон, гидантоин, диоксолан, фталемид, пиперидин, 1,4 диоксан, морфолин, тиоморфолин, тиоморфолин-S-оксид, тиоморфолин-S, S-диоксид, пиперазин, пиран, пиридон, 3-пирролин, тиопиран, пирон, тетрагидрофуран, тетрагидротиофен, хинуклидин и т.п. Предпочтительные гетероциклические группы являются моноциклическими, хотя они могут быть сплавлены или связаны ковалентно с арилом или гетероарильной кольцевой системой.
[0028] «Гетероарил» относится к ароматической группе, содержащей, по крайней мере, один гетероатом, где гетероарильная группа может быть моноциклической или бициклической. Примеры включают пиридил, пиридазинил, пиразинил, пиримидинил, триазинил, хинолинил, хиноксалинил, хиназолинил, циннолинил, фталазинил, бензотриазинил, пиринил, бензимидазолил, бензопаразолил, бензотриазолил, бензисоксазолил, изобензофурил, изоиндолил, индолизинил, бензотриазинил, тиенопиридинил, тиенопиримидинил, пиразолопиримидинил, имидазопиридины, бензотиазолил, бензофуранил, бензотиенил, индолил, азаиндолил, азаиндазолил, хинолил, изохинолил, изотиазолил, пиразолил, индазолил, птеридинил, имидазолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиaзолил, тиадиaзолил, пирролил, тиазолил, фурил или тиенил. Предпочтительные гетероарильные группы - те, которые имеют, по крайней мере, один атом азота арильного кольца, такие как хинолинил, хиноксалинил, пуринил, бензимидазолил, бензопиразолил, бензотриазолил, бензотиазолил, индолил, хинолил, изохинолил и т.п. Предпочтительные гетероарильные системы с 6 кольцами включают пиридил, пиридазинил, пиразинил, пиримидинил, триазинил и т.п. Предпочтительные гетероарильные системы с 5-ю кольцами включают изотиазолил, пиразолил, имидазолил, тиенил, фурил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиaзолил, тиадиaзолил, пирролил, тиазолил и т.п.
[0029] Гетероциклил и гетероарил могут быть присоединены на любом доступном кольцевом углероде или гетероатоме. Каждый гетероциклил и гетероарил могут иметь одно или более колец. Когда множественные кольца присутствуют, они могут быть сплавлены вместе или связаны ковалентно. Каждый гетероциклил и гетероарил должны содержать, по крайней мере, один гетероатом (как правило, 1-5 гетероатомов), выбранных из азота, кислорода или серы. Предпочтительно, эти группы содержат 0-5 атомов азота, 0-2 атома серы и 0-2 атома кислорода. Более предпочтительно эти группы содержат 0-3 атома азота, 0-1 атом серы и 0-1 атом кислорода. Гетероциклильные и гетероарильные группы являются незамещенными, если не обозначено иначе. Для замещенных групп замена может быть на углероде или гетероатоме. Например, когда замена это оксо (=O или -O-), получающиеся группа может иметь или карбонил (-C (O)-), или N-оксид (-N+-O-).
[0030] Подходящие заместители для замещенного алкила, замещенного алкенила, замещенного алкинила включают галоген, CN, -CO2R', -C(O)R', -C(O)NR'R''', oксo (=O или -O-), -OR', OC(O)R', OC(O)NR'R''-NO2, -NR'C(O)R'', -NR'''C(O)NR'R'', -NR'R'',
-R'CO2R'', -NR(O)R'', -NR(O)2R''', -NR'''S(O)NR'R'', -NR'''S(O)2NR'R'', -SR', -S(O)R',
-S(O)2R', S(O)2NR'R'', -NR'-C(NHR'')=NR''', -SiR'R''R''', -N3, замещенный или незамещенный C6-10 арил, замещенный или незамещенный 5- 10-членный гетероарил, и замещенный или незамещенный 3- 10-членный гетероциклил. Количество возможных заместителей колеблется от ноля до (2m' +1), где m' является общим количеством атомов углерода в таком радикале.
[0031] Подходящие заместители для замещенного арила, замещенного гетероарила и замещенного гетероциклила включают галоген, -CN, -CO2R', -C(O)R', -C(O)NR'R'', oксo (=O или -O-), -OR', C (O)R', OC(O)NR'R'', -NO2, -NR'C(O)R'', -NR'''C(O)NR'R'', -R'R'', -NR'CO2R'', -NR'(O)R'', -NR'S(O)2R'', -NR'''S(O)NR'R'', -NR'''S(O)2NR'R'', -SR', -S(O)R', -S(O)2R', -S(O)2NR'R'', -NR'-C(NHR'')=NR''', -SiR'R''R''', -N3, замещенный или незамещенный C1-8 алкил, замещенный или незамещенный C2-8 алкенил, замещенный или незамещенный C2-8 алкинил, замещенный или незамещенный C6-10 арил, замещенный или незамещенный 5-10-членный гетероарил, и замещенный или незамещенный 3-10-членный гетероциклил. Количество возможных заместителей колеблется от ноля до общего количества открытых валентностей на системе ароматического кольца.
[0032] Как использовано выше, R', R'' и R''' каждый независимо относится ко множеству групп, включая водород, замещенный или незамещенный C1-8 алкил, замещенный или незамещенный C2-8 алкенил, замещенный или незамещенный C2-8 алкинил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арилалкил, замещенный или незамещенный арилоксиалкил. Когда R' и R'' присоединены к одному и тому же атому азота, они могут быть объединены с атомом азота для формирования 3-, 4-, 5-, 6-, или 7-членного кольца (например, -NR'R'' включает 1-пирролидинил и 4-морфолинил). Кроме того, R' и R'', R'' и R''' или R' и R''' могут вместе с атомом (атомами), на который они присоединены, формировать замещенное или незамещенное 5-, 6- или 7-членное кольцо.
[0033] Два из заместителей на соседних атомах арильного или гетероарильного кольца могут произвольно быть заменены заместителем формулы -T-C(O)-(CH2)q-U-, где T и U независимо являются -NR''''-, -O-, -CH2- или одинарной связью, и q является целым числом от 0 до 2. Также два из заместителей на соседних атомах арильного или гетероарильного кольца могут произвольно быть замещены заместителем формулы -A'-(CH2)r-B'-, где А' и B' независимо являются -CH2- , -O-, -NR''''-, -S-, -S(O)-, -S(O)2-, -S(O)2NR''''- или одинарной связью, и r - это целое число от 1 до 3. Одна из одинарных связей нового кольца, таким образом сформированного, может произвольно быть заменена двойной связью. Также два из заместителей на соседних атомах арильного или гетероарильного кольца могут произвольно быть замещены заместителем формулы -(CH2)s-X-(CH2)t-, где s и t являются независимо целыми числами от 0 до 3, и X - это
-O-, -NR''''-, -S-, -S(O)-, -S(O)2- или -S(O)2NR'- . R'''' выбран из водорода или незамещенного C1-8 алкила.
[0034] «Гетероатом» обозначает включающий кислород (O), азот (N), серу (S) и кремний (Si).
[0035] Формулировка « выше естественной распространенности изотопов» относится к распространенности изотопов химического элемента, как измерено в естественных условиях.
[0036] «Фармацевтически приемлемый» носитель, разжижитель или наполнитель является носителем, разжижителем или наполнителем, совместимым с другими компонентами состава и не вредные тому, кто его принимает.
[0037] «Фармацевтически приемлемая соль» относится к соли, которая приемлема для назначения пациенту, такому как млекопитающее (например, соли, имеющие приемлемую безопасность для млекопитающих для данного режима дозировки). Такие соли могут быть получены из фармацевтически приемлемых неорганических или органических оснований и из фармацевтически приемлемых неорганических или органических кислот, в зависимости от определенных заместителей, обнаруженных на соединениях, здесь описанных. Когда соединения настоящего раскрытия содержат относительно кислые функциональности, основные дополнительные соли могут быть получены путем контакта нейтральной формы таких соединений с достаточным количеством требуемого основания, или чистого или в подходящем инертном растворителе. Соли, полученные из фармацевтически приемлемых неорганических оснований, включают алюмиевую, аммониевую, кальциевую, медную, железную, железистую, литиевую, магниевую, марганцовистую, марганцоватистую, калиевую, натриевую, цинковую и т.п. Соли, полученные из фармацевтически приемлемых органических оснований, включают соли первичных, вторичных, третичных и четвертичных аминов, включая замещенные амины, циклические амины, естественные амины и т.п., такие как аргинин, бетаин, кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, тетрагидрооксазин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометанамин и т.п. Когда соединения настоящего раскрытия содержат относительно основные функциональности, кислотные дополнительные соли могут быть получены путем контакта нейтральной формы таких соединений с достаточным количеством требуемой кислоты, или чистой, или в подходящем инертном растворителе. Соли, полученные из фармацевтически приемлемых кислот, включают уксусную, аскорбиновую, бензолсульфоновую, бензойную, камфосульфоновую, лимонную, этансульфониковую, фумаровую, глюконовую, глюкороновую, глутаминовую, гиппуровую, бромистоводородную, хлористоводородную, изэтиновую, молочную, лактобионовую, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, нафталенсульфоновую, никотиновую, азотную, памовую, пантотеническую, фосфорическую, янтарную, серную, винную, п-толуенсульфоновую и т.п.
[0038] Также входят соли аминокислот, такие как аргинат и т.п. и соли органических кислот, таких как глюкуроновые или галактуноровые кислоты и т.п. (см., например, Berge, S.M. et al, “Pharmaceutical Salts”, J. Pharmaceutical Science, 1977, 66:1-19). Некоторые определенные соединения настоящего раскрытия содержат и основные и кислые функциональности, позволяющие соединениям преобразовываться в основные и в кислотные дополнительные соли.
[0039] Нейтральные формы соединений могут быть восстановлены путем контакта соли с основанием или кислотой и изоляцией исходного соединения стандартным образом. Исходная форма соединения отличается от различных солевых форм определенными физическими свойствами, такими как растворимость в полярных растворителях, но в иных случаях соли эквивалентны исходной форме соединения в целях настоящего раскрытия.
[0040] Кроме того, для солевых форм настоящее раскрытие представляет соединения, которые находятся в форме пролекарства. Пролекарства соединений, описанных здесь, являются такими соединениями, которые легко претерпевают химические изменения при физиологических условиях для обеспечения соединений настоящего раскрытия. Кроме того, пролекарства могут быть преобразованы в соединения настоящего раскрытия химическими или биохимическими способами in vivo окружающей средой. Например, пролекарства могут медленно превращаться в соединения настоящего раскрытия, когда помещены в резервуар трансдермального пластыря, подходящим энзимом или химическим реактивом.
[0041] «Терапевтически эффективное количество» относится к количеству, достаточному для эффективного лечения, когда назначается нуждающемуся в лечении пациенту.
[0042] «Терапия» или «лечение», как используется здесь, относится к терапии или лечению заболевания или медицинского состояния в пациенте, таком как млекопитающее (особенно человек или домашнее животное), которые включают улучшение заболевания или медицинского состояния, т.е. устранение или обеспечение регрессии заболевания или медицинского состояния в пациенте; подавление заболевания или медицинского состояния, например, замедление или купирование развития заболевания или медицинского состояния у пациента; или облегчение симптомов заболевания или медицинского состояния у пациента; или предупреждение развития заболевания.
[0043] «UACR» относится к Отношению Альбумина к Креатинину в Моче.
[0044] «UAER» относится к Уровню Выделения Альбумина с Мочой.
[0045] Определенные соединения настоящего раскрытия могут существовать в несольватированных, а также в сольватированных формах, включая гидратированные формы. В целом, сольватированные и несольватированные формы охватываются рамками настоящего раскрытия.
[0046] Для специалиста области будет очевидно, что определенные соединения настоящего раскрытия могут существовать в таутомерных формах, все такие таутомерные формы соединений находятся в рамках этого раскрытия. Определенные соединения настоящего раскрытия обладают асимметричными атомами углерода (оптические центры) или двойными связями; рацематы, диастереомеры, геометрические изомеры и отдельные изомеры (например, отдельные энантиомеры) все охватываются рамками настоящего раскрытия.
[0047] Соединения могут быть получены так, что любое количество атомов водорода заменяется изотопом дейтерием (2H). Соединения настоящего раскрытия могут также содержать неестественные пропорции атомных изотопов в одном или более атомов, составляющих такие соединения. Неестественные пропорции изотопа могут быть определены как находящиеся в пределах от количества, обнаруженного в естественной природе, до количества, состоящего из 100% рассматриваемого атома. Например, соединения могут включать радиоактивные изотопы, такие как, например, тритий (3H), йод 125 (125I) или углерод 14 (14C) или нерадиоактивные изотопы, такие как дейтерий (2H) или углерод 13 (13C). Такие изотопические вариации могут обеспечить дополнительные преимущества для описанных в другом месте в этой заявке. Все изотопические вариации соединений настоящего раскрытия, или радиоактивные или нет, охвачены рамками настоящего раскрытия. Например, изотопические варианты соединений раскрытия могут найти дополнительную полезность, включая, но без ограничения, как реагенты для диагностики и/или отображения, или как цитотоксические/радиотоксические терапевтические агенты. Кроме того, изотопические варианты соединений раскрытия могут изменять фармакокинетические и фармакодинамические характеристики, которые могут способствовать повышению безопасности, переносимости или эффективности во время лечения.
Способ лечения FSGS
[0048] Настоящее раскрытие представляет способы лечения FSGS у пациента, включающие назначение нуждающемуся в этом пациенту эффективного количества соединения Формулы (Ia)
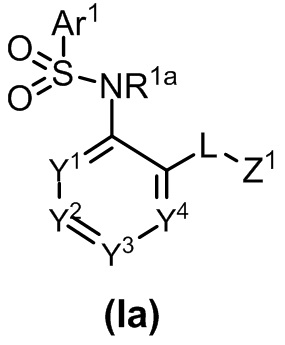
[0049] или фармацевтически приемлемой его соли, где
[0050] Ar1 выбирают из группы, состоящей из замещенного или незамещенного C6-10 арила и замещенного или незамещенного 5-10-членного гетероарила;
[0051] R1a выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного алкенила, замещенного или незамещенного C2-6 алкинила и замещенного или незамещенного 3- 10-членного гетероциклила;
[0052] Y1 выбран из группы, состоящей из -CR2a- , - N- и -N+(O)-;
[0053] Y2 выбран из группы, состоящей из -CR2b- , -N- и -N+(O)-;
[0054] Y3 выбран из группы, состоящей из -CR2c-, -N- и -N+(O)-;
[0055] R2a, R2b и R2c каждый независимо выбран из группы, состоящей из водорода, галогена, -CN, -C(O)R3a, -CO2R3a, -C(O)NR3aR4a, -OR3a, -OC(O)R3a, -OC(O)NR3aR,
-SR3a, -S(O)R3a , -S(O)2R3a , -S(O)2NR3aR4a , -NO2, -NR3aR4a, NR3aC(O)R4a,
-NR3aC(O)OR4a, -NR3aS(O)2R4a, -NR3aC(O)NR4aR5a, замещенного или незамещенного
C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила;
[0056] R3a, R4a и R5a каждый независимо выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5- 10-членного гетероарила и замещенного или незамещенного 3- 10-членного гетероциклила;
[0057] R3a и R4a , R4a и R5a или R3a и R5a могут вместе с атомами, на которые они присоединены, формировать замещенное или незамещенное 5-, 6- или 7-членное кольцо;
[0058] L выбран из группы, состоящей из связи, -O-, -S-, -S (O) - , - S (O) 2- , -CR6R7-,
-NR8-, -C (O) - и -NR8C (O)-;
[0059] R6 и R7 каждый независимо выбран из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила, -CN, -OR9, -NR10R11, -S(O)R9 и
-S(O)R9;
[0060] R6 и R7 могут, вместе с атомом углерода, на который они присоединены, формировать замещенный или незамещенный C3-8 циклоалкил или замещенное или незамещенное 3- 10-членное гетероциклическое кольцо;
[0061] R9 выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C 2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5-10-членного гетероарила и замещенного или незамещенного 3- 10-членного гетероциклила;
[0062] R10 и R11 каждый независимо выбран из группы, состоящей из замещенного или незамещенного C1-8 алкила, замещенного или незамещенного 3-10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5-10-членного гетероарила, замещенного или незамещенного C2-8 алкенила, и замещенного или незамещенного C2-8 алкинила;
[0063] R10 и R11 из -NR10R11 могут вместе с азотом формировать замещенный или незамещенный C3-8 циклоалкил, замещенный или незамещенный 3- 10-членный гетероциклил;
[0064] R8 выбран из группы, включающей водород, C(O)R12, S(O)2R12, CO2R12, замещенный или незамещенный C1-8 алкил, замещенный или незамещенный 3- 10-членный гетероциклил, замещенный или незамещенный C2-6 алкенил, замещенный или незамещенный C2-6 алкинил;
[0065] R12 выбран из группы, состоящей из замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-6 алкенила, замещенного или незамещенного C2-6 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила и замещенного или незамещенного 5- 10-членного гетероарила;
[0066] Z1 выбран из группы, состоящей из замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5-10-членного гетероарила, замещенного или незамещенного 3- 10-членного гетероциклила, и
-NR13R14;
[0067] R13 и R14 каждый независимо выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного C2-8 алкенила, замещенного или незамещенного C2-8 алкинила, замещенного или незамещенного 3- 10-членного гетероциклила, замещенного или незамещенного C6-10 арила, замещенного или незамещенного 5-10-членного гетероарила, замещенного или незамещенного (C1-4 алкил) - (C6-10 арил) и замещенного или незамещенного (C1-4 алкил) - (5- 10-членный гетероарил);
[0068] R13 и R14 могут, вместе с азотом, формировать замещенный или незамещенный 4-, 5-, 6-, или 7-членный гетероциклил;
[0069] Y4 выбран из группы, состоящей из -N- и -N+(O)-;
[0070] В некоторых воплощениях соединения формулы CC исключены из формулы (Ia)
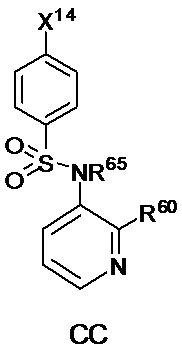
[0071] где X14 выбран из группы, состоящей из - Сl, -NO2, -OCH3, -CH3, -NHC(O)CH3 и -CH2CH2-(фенил);
[0072] R65 выбран из группы, состоящей из водорода, замещенного или незамещенного C1-4 алкила, и замещенного или незамещенного - SO2 (фенила); и
[0073] R60 выбран из группы, состоящей из - NR61CH2CH2OR62, -NR61CH2CH2NR63R64, -NR61CH2CH2SR62,
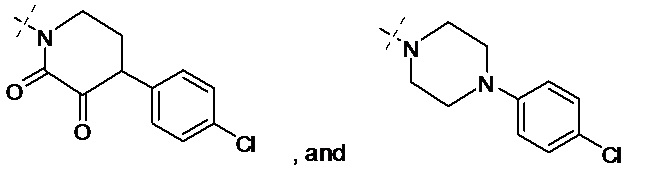
[0074] где R61 выбран из группы, состоящей из водорода, и замещенного или незамещенного фенила;
[0075] R62 выбран из группы, состоящей из замещенного или незамещенного фенила и замещенного или незамещенного C1-4 алкила; и
[0076] R63 и R64 каждый независимо выбран из группы, состоящей из водорода, замещенного или незамещенного C1-8 алкила, замещенного или незамещенного фенила, замещенного или незамещенного -SO2 (фенила), -C(O)CH3, -C(O)C(O)OH и
-C(O)2C (CH3) 3.
[0077] В некоторых воплощениях Z1 - это замещенный или незамещенный 5- 10-членный гетероарил.
[0078] В некоторых воплощениях L - это -C(O)-.
[0079] В некоторых воплощениях Y1 это -CR2а-; Y2 это -CR2b-; Y3 это -CR2c- ; и R2a, R2b и R2c каждый независимо выбран из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила.
[0080] В некоторых воплощениях R1a выбран из группы, состоящей из водорода или замещенного или незамещенного C1-8 алкила.
[0081] В некоторых воплощениях Ar1 это замещенный или незамещенный C6-10 арил. В некоторых воплощениях Ar1 - это C6-10 арил, замещенный 1-3 заместителями, выбранными из галогена, C1-6 алкила и C1-6 галоалкила. В некоторых воплощениях Ar1 это фенил, замещенный 1-3 заместителями, выбранными из галогена, C1-3 алкила и C1-3 галоалкила.
[0082] В некоторых воплощениях Y4 это -N-.
[0083] В некоторых воплощениях Z1 - это замещенный или незамещенный 5- 10-членный гетероарил; L это -C (O)-; Y1 это -CR2a-; Y2 это -CR2b-; Y3 это -CR2c-; R2a, R2b и R2c каждый независимо выбран из группы, состоящей из водорода, галогена, замещенного или незамещенного C1-8 алкила; R1a выбран из группы, состоящей из водорода или замещенного или незамещенного C1-8 алкила; Ar1 это замещенный или незамещенный C6-10 арил; и Y4 это -N-.
[0084] В некоторых воплощениях Z1 это незамещенный 9- 10-членный гетероарил; L - это -C (O)-; Y1 это -CR2a-; Y2 это CR2b- ; Y3 это -CR2c -; R2a, R2b и R2c каждый независимо выбраны из группы, состоящей из водорода, галогена и C1-8 алкила;
R1a выбран из группы, состоящей из водорода или C1-8 алкила; Ar1 является фенилом, замещенным 1 - 3 заместителями, выбранными из галогена, C1-6 алкила и C1-6 галоалкила; и Y4 - это -N-.
[0085] Настоящее раскрытие также представляет способы лечения фокально- сегментарного гломерулосклероза (FSGS) у нуждающегося в этом пациента, включающие назначение пациенту эффективного количества соединения Формулы I

(I)
[0086] или фармацевтически приемлемой его соли, где
[0087] R1 является галогеном или C1-6 алкилом;
[0088] R2 является водородом, галогеном, C1-6 алкилом, C1-6 алкокси, C1-6 галоалкилом, C1-6 галоалкокси или -CN;
[0089] R3 является водородом, галогеном или С1-6 алкилом;
[0090] R4 является водородом, галогеном или C1-6 алкилом;
[0091] каждый R5 является независимо алкилом C1-6 , - OH или -NH2;
[0092] n - это 0, 1, 2, или 3; и
[0093] каждый из A1, A2 и A3 является -CH- или -N-, где, по крайней мере, один из A1, A2 или A3 является -N-.
[0094] В некоторых воплощениях R1 является галогеном или метилом;
R2 является галогеном или C1-3 галоалкилом;
R3 является галогеном или C1-3 алкилом;
R4 является водородом;
n - это 0;
A2 является -CH-; и
A3 является -N-.
[0095] В некоторых воплощениях соединение - это:
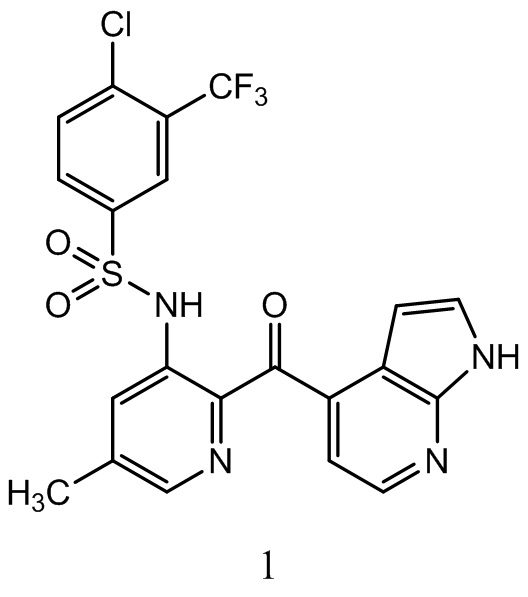
или фармацевтически приемлемая его соль.
[0096] В некоторых воплощениях соединение - это
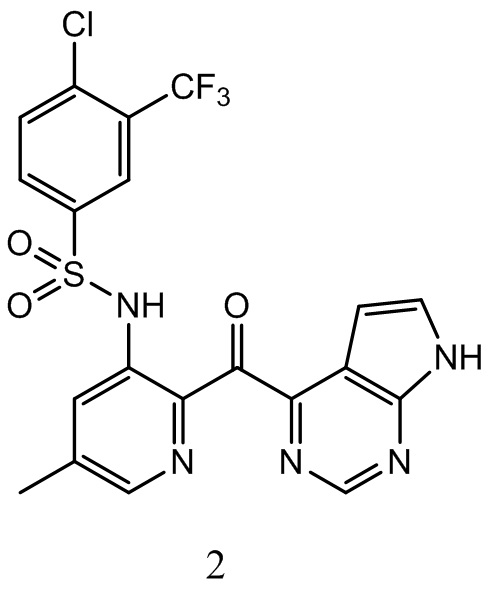
или фармацевтически приемлемая его соль.
[0097] В некоторых воплощениях соединение - это
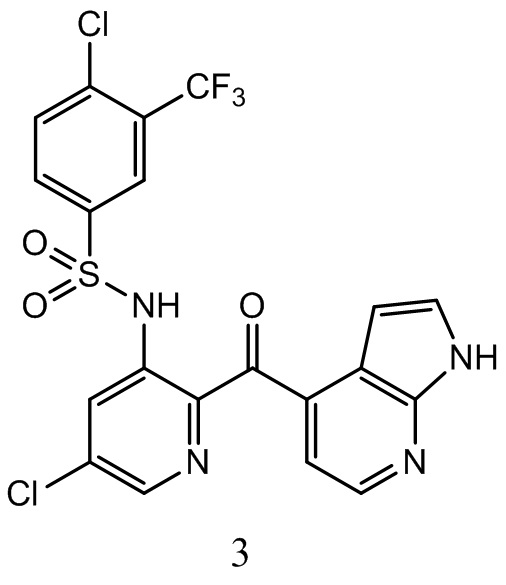
или фармацевтически приемлемая его соль.
[0098] В некоторых воплощениях способ лечения FSGS включает предотвращение, сокращение или устранение симптома или осложнения FSGS.
[0099] В некоторых воплощениях способ лечения FSGS включает предотвращение, устранение или задержку начала терминальной стадии почечного заболевания у пациента.
[0100] В некоторых воплощениях FSGS является первичным FSGS.
[0101] В некоторых воплощениях FSGS является вторичным FSGS. В некоторых воплощениях вторичный FSGS связан с инфекцией или вирусом, заболеванием, воздействием токсина или препарата, или утратой нефронов и гиперфильтрацией. В некоторых воплощениях FSGS связан с HIV, серповидно-клеточной анемией, волчанкой, воздействием анаболического стероида, героина или памидроната, хроническим пиелонефритом и рефлюксом, тяжелой формой ожирения или сахарным диабетом.
[0102] В некоторых воплощениях способ включает одно или более из: уменьшения протеинурии, замедления увеличения протеинурии, снижения UACR, замедления увеличения отношения креатинина к альбумину в моче (UACR), уменьшения UAER, замедления увеличения UAER, сокращения альбуминурии, замедления увеличения альбуминурии, повышения плотности подоцитов в клубочках, предотвращения или замедления утолщения клубочковой базисной мембраны (GBM), уменьшения клубочковой области, сокращения количества почечных интерстициальных макрофагов, уменьшения или замедления фиброза почечных тканей, остановки или уменьшения воспаления почек, остановки или уменьшения макрофаг-индуцированного повреждения почек, увеличения или нормализации предполагаемой скорости клубочковой фильтрации (eGFR), уменьшения снижения eGFR, сокращения гломерулосклероза, остановки или уменьшения расширения клубочкового внеклеточного матрикса, остановки или уменьшения смещения гиалиновых масс, остановки или сокращения клубочковых эпителиальных гиперплазийных повреждений (EPHLs) и остановки или уменьшения инфильтрации лимфоцитов.
[0103] В некоторых воплощениях соединение или фармацевтически приемлемая его соль вводятся перорально.
[0104] В некоторых воплощениях соединение или фармацевтически приемлемая его соль вводятся дважды в день.
[0105] В некоторых воплощениях соединение или фармацевтически приемлемая его соль вводятся один раз в день.
[0106] В некоторых воплощениях соединение или фармацевтически приемлемая его соль не назначаются ни с каким другим терапевтическим соединением. В некоторых воплощениях соединение или фармацевтически приемлемая его соль не назначаются ни с каким другим терапевтическим соединением одновременно или последовательно. В некоторых воплощениях назначается только одно соединение или фармацевтически приемлемая его соль. В некоторых воплощениях соединение или фармацевтически приемлемая его соль вводится с блокатором рецепторов ангиотензина II (ARB). В некоторых воплощениях соединение или фармацевтически приемлемая его соль не вводится с блокатором рецепторов ангиотензина II (ARB), одновременно или последовательно.
[0107] В некоторых воплощениях способ дополнительно включает назначение пациенту одного или более дополнительных терапевтических соединений. В некоторых воплощениях одно или более дополнительных терапевтических соединений выбирают из одного или более антигипертензивного средства, статина, вазодилататора, стероида, цитотоксического препарата, мочегонного средства, нестероидного противовоспалительного препарата (NSAID), снижающего холестерин или триглицериды агента и иммунодепрессанта.
[0108] В некоторых воплощениях одно или более дополнительных терапевтических соединений выбирают из группы, состоящей из ингибитора ангиотензинпревращающего фермента (ACE) и блокатора рецепторов ангиотензина II (ARB). В некоторых воплощениях одно или более дополнительных терапевтических соединений выбирают из группы, состоящей из рамиприла, периндоприла, лизиноприла, аргинина периндоприла, каптоприла, спираприла, хинаприла, эналаприла, имидаприла, фозиноприла, зофеноприла, беназеприла, трандолаприла, верапамила, беназеприла, амлодипина, трандолаприла, P-003, цилазаприла, делаприла, моексиприла, хинаприла, фозиноприла, темокаприла, лозартана, кандесартана, ирбесартана, телмисартана, олмесартана, валсартана, азилсартана, телмисартана, фимасартана, EMA 401, азилсартан медоксомила калия, спарсентана, кандесартана целиксетила, олмесартана медоксомила, TRV-027, лозартана калия, YH-22189, азилсартана тримэтилэтаноламина, аллисаатана изопроксила и эпросартана. В некоторых воплощениях одно или большее количество дополнительных терапевтических соединений - это кандесартан. В некоторых воплощениях одно или большее количество дополнительных терапевтических соединений - это ирбесартан.
[0109] В некоторых воплощениях соединение или фармацевтически приемлемая его соль назначаются с ингибитором ангиотензинпревращающего фермента (ACE), одновременно или последовательно.
[0110] В некоторых воплощениях соединение или фармацевтически приемлемая его соль назначается с блокатором рецепторов ангиотензина II (ARB), одновременно или последовательно.
[0111] В некоторых воплощениях одно или большее количество дополнительных терапевтических соединений выбирают из группы, состоящей из антагониста Эндотелина ETA, антиген CD20 ингибитора И-лимфоциов, ингибитора натрий глюкозного транспортера-2, CD28 ингибитора T-клеточного поверхностного гликопротеина; протеин-4 стимулятора цитотоксических Т-лимфоцитов, ингибитора 38 МАР киназы, стимулятора N ацетилманносамин киназы, лиганда адренокортикотропного гормона, антагониста интегринa альфа-V/бета-3, ингибитора лиганда фактора роста соединительной ткани и TGF бета антагонист.
[0112] В некоторых воплощениях одно или большее количество дополнительных терапевтических соединений выбирают из группы, состоящей из ритуксимаба, дапаглифлозина, спарсентана, абатасепта, DMX-200, пропагерманиума, ирбесартана, лозмапимода, X-M74, Актар-Геля, VAR-200, циленгитида, памревлумаба, DEX-M74, фрезолимумаба и SHP-627.
[0113] В некоторых воплощениях одно или большее количество дополнительных терапевтических соединений выбирают из группы, состоящей из агониста фарнезоидного X-рецептора, агониста рецептора связывающего 1 G-белок желчной кислоты, антагониста Эндотелина ETA, антагониста Эндотелина ET-1, антагониста Эндотелина ET-2, антагониста Эндотелина ET-3, антагониста Эндотелина ET-B1, антагониста Эндотелина ET-B2, антагониста Эндотелина ETC, ингибитора лиганда стимулятора B-лимфоцитов, ингибитора лиганда гормона паращитовидной железы, ингибитора ДНК-полимеразы, антиген CD20 ингибитора B-лимфоцитов, протеин-4 стимулятора цитотоксических Т-лимфоцитов, CD28 ингибитора T-клеточного поверхностного гликопротеина, ингибитора MEKK-5 протеин киназы, ингибитора лиганда фактора роста соединительной ткани, ингибитора сериновой протеазы -2 с маннан-связывающим лектином, ингибитора Syk тирозин киназы, ингибитора натрий глюкозного транспортера-2, агониста рецептора эритропоэтина, ингибитора ионизин монофосфат дегидрогеназы; ингибитора PurH пуринового биосинтезного протеина, ингибитора C5 гена, ингибитора нуклеозид обратной транскриптазы, ингибитора циклин-зависимой киназы-4; ингибитора циклин - зависимой киназы; модулятора ретинобластома-связанного протеина, сенситайзера инсулина, модулятора калликреина 1, ингибитора калиевых каналов, ингибитора Raf B протеин киназы, лиганда адренокортикотропного гормона, комплиментарного ингибитора C1s субкомпонента, антагониста минералокортикоидного рецептора, ингибитора Jak1 тирозин киназы, ингибитора Jak тирозин киназы, ингибитора Jak2 тирозин киназы, антагониста P2Y12 пуриноцептора, ингибитора комплиментарного C5 фактора, антагониста рецептора гормона роста, ингибитора альдозы-редуктазы, ингибитора сериновой протеазы, ингибитора атрипсина, агониста рецептора соматостатина, ингибитора NADPH оксидазы 1, ингибитора NADPH оксидазы 4, агониста ANP, агониста рецептора B натриуретического пептида, ингибитора I-каппа B киназы, стимулятора NFE2L2 гена, ингибитора нуклеарного фактора каппа B, ингибитора STAT3 гена, антагониста вазопрессина V2, ингибитора кальциневрина, антагониста альдостерона, антагониста минералокортикоидного рецептора, ингибитора фактора некроза опухоли, антагонист тромбоксана A2, антагонист эпидермального фактора роста, ингибитора рецептора Erbb2 тирозин киназы, ингибитора рецептора Erbb3 тирозин киназы, ингибитора рецептора Erbb4 тирозин киназы, ингибитор ренина, ингибитора галектина-3, антагониста минералокортикоидного рецептора, антагониста FGF, антагониста PDGF рецептора, TGF бета антагониста, ингибитора p38 МАР киназы, стимулятора миозина, агониста бета 2 адренорецептора, глюкокортикоидного агониста, антагониста мускаринового рецептора, ингибитора смещения амилоидного протеина, аполипопротеинового генного стимулятора, ингибитора бромодомен- содержащего протеина 4, агониста гепатоцитарного фактора роста, антагониста рецептора продвинутого продукта гликозилации, ингибитора GHR гена; ингибитора IGF1 гена, модулятора CACNA2D3 кальциевого канала, лиганда натриуретического пептида C-типа, лиганда дендроасписного натриуретичесекого протеина, агониста термостабильного рецептора энтеротоксина, агониста рецептора А натриуретического пептида, агониста рецептора B натриуретического пептида, агониста рецептора С натриуретического пептида, лигандного модулятора костно-морфогенетического протеина-7, ингибитора циклооксигеназы 1, агониста вазопрессина V1, стимулятора N-ацетилманносамин киназы, стимулятора ангиотензин-превращающего фермента 2, агониста PPAR гамма, антагониста простаноидного рецептора, антагониста тромбоксана A2, ингибитора протеин тирозин фосфатазы бета, стимулятора рецептора Tek тирозин киназы, лиганда костного морфогенетического протеина- 7, ингибитора каспазы, агониста простациклина, ингибитора альдозы-редуктазы, ингибитора циклин-зависимой киназы-2, ингибитора циклин-зависимой киназы-7, ингибитора циклин-зависимой киназы-9, ингибитора MCL1 гена, ингибитора склеростина, антагониста комплиментарного C5a рецептора, антагониста рецептора Fc IIB гамма иммуноглобулина, агониста простациклина, ингибитора p38 МАР киназы, модулятора гемоглобина, стимулятора щелочной фосфотазы, модулятора NFE2L2 гена, модулятора NFKB гена, ингибитора Rho связанной протеин киназы, антагониста CX3CR1 хемокина, модулятора PDGF рецептора бета, агониста гепарина, стимулятора эластазы, лиганда гормона роста; агониста рецептора гормона роста, ингибитора ксантин оксидазы, модулятора внеклеточного матричного протеина; модулятора протеогликана, антагониста минералокортикоидного рецептора, ингибитора лиганда моноцит хемотаксического протеина 1, ингибитора гистон деацетилазы, агониста гепатоцитарного фактора роста, агониста альбумина, ингибитора мембранной медной амин оксидазы, антагониста интегрина альфа-V/бета-3, агониста рецептора соматостатина, ингибитора циклин-зависимой киназы, ингибитора семьи носителя раствора 12A1, лигандного модулятора гепатоцитарного фактора роста, антагониста рецептора интерферон гамма, стимулятора фенилаланин гидроксилазы, модулятора почечного транспортера мочевины, антагониста фактора Xa, низкомолекулярного гепарина, агониста допамин D1 рецептора, двойного ингибитора ангиотензинпревращающего фермента (ACE) и нейтральной эндопептидазы (EP), тиазид-подобного диуретика, калий-сохраняющего диуретика, ингибитора углерод ангидразы, ингибитора нейтральной эндопептидазы, ингибитора альдостеронсинтазы; ингибитора ренина; блокатора кальциевых каналов, активатора калиевых каналов, бета-адренергического блокирующего препарата, альфа адренергического блокирующего препарата, нитрата, соединения передачи оксида азота, липид-понижающего агента, ингибитора поглощения холестерина, агониста рецептора ниацина, частичного агониста ниацинового рецептора, метаболизм преобразующего агента, ингибитора альфа-глюкозидазы, ингибитора дипептидил пептидазы, алкалоида спорыньи и ингибитора фосфодиэстеразы- 5 (PDE5).
[0114] В некоторых воплощениях один или большее количества дополнительных терапевтических соединений выбраны из группы, состоящей из антагониста Эндотелина ET-A, антагониста Эндотелина ET-1, антагониста Эндотелина ET-2, антагониста Эндотелина ET-3, антагониста Эндотелина ET-B1, антагониста Эндотелина ET-B2, антагониста Эндотелина ET-C, ингибитора лигандного стимулятора B-лимфоцитов, CD20 ингибитора антигена B-лимфоцитов, протеин-4 стимулятора цитотоксических Тлимфоцитов, CD28 ингибитора T -клеточного поверхностного гликопротеина, ингибитора протеин MEKK-5 киназы, ингибитора лигандного фактора роста соединительной ткани, ингибитора сериновой протеазы- 2 маннан- связывающего лектина, ингибитора Syk тирозин киназы, ингибитора натрий -глюкозного транспортера-2, агониста рецептора эритропоэтина, ингибитора ионизин монофосфат дегидрогеназы; ингибитора C5 гена, сенситайзера инсулина, ингибитора калиевых каналов, антагониста минералокортикоидного рецептора, ингибитора тирозин Jak1 киназы, ингибитора Jak тирозин киназы, ингибитора киназы Jak2 тирозин киназы, антагониста P2Y12 пуриноцептора, ингибитора комплиментарного C5 фактора, ингибитора кальциневрина, антагониста альдостерона, антагониста минералокортикоидного рецептора, ингибитора ренина, антагониста минералокортикоидного рецептора, антагониста FGF рецептора, антагониста PDGF рецептора, антагониста TGF бета, ингибитора p38 МАР киназы, стимулятора миозина, агониста бета 2 адренорецептора, глюкокортикоидного агониста, антагониста мускаринового рецептора, стимулятора гена аполипопротеина, ингибитора циклооксигеназы 1, агониста вазопрессина V1, стимулятора ангиотензинпревращающего фермента 2, агониста PPAR гамма, антагониста простаноидного рецептора, антагониста CX3CR1 хемокина, модулятора PDGF рецептора бета, агониста гепарина, модулятора внеклеточного матричного протеина, антагониста минералокортикоидного рецептора, двойного ингибитора ангиотензинпревращающего фермента (ACE) и нейтральной эндопептидазы (EP), и ингибитора дипептидил пептидазы.
[0115] В некоторых воплощениях одно или более дополнительных терапевтических соединений выбраны из группы, состоящей из INT 767, белимумаба, цинакальцета, ритуксимаба, лозартана, абатасепта, кандесартана, селонсертиба, мио-инозит гексафосфата, PBI-4050, OMS-721, фостаматиниба, ирбесартана, цанаглифлозина, метоксиполиэтиленгликоль-эпоэтина бета, микофенолатмофетила, ALN-CC5, обинутузумаба, ренамезина, палбоциклиба, бозентана, DM 199, будесонида, амифампридина, амифампридин фосфата, дабрафениба, дапаглифлозина, дапаглифлозин пропандиола, кортикотропина, TNT-009, дефибротида, финернона, барицитиниба, тикагрелора, амбризентан, экудизумаба, пегвисоманта, эпалрестата, камостат мезилата, октреотида, октреотида ацетата, GKT-831, уларитида, бардоксолона, бардоксолон метила, толваптана, олмесартан медоксомила, такролимуса, MT 3995, ирбесартана + пропагерманиума, атацисепта, ифетробана, ифетробана натрия, афатиниба, атрасентана, TAK-272, AST 120, фимасартана, GR-MD-02, CS-3150, пирфенидона, омекамтива мекарбила, омекамтива, беклометазона, беклометазон дипропоината, apaбеталона, спарсентана, ХронСила, азелирагона, памревлумаба, атезидозена, габапентин а энакарбила, габапентина, имидаприла, цендиритида, BMP-7, GLY-230, рекомбинантного эритропоэтин стимулирующего протеина, 2MD, терлипрессина, дихлоргидрата пиридоксамина, пиридоксамина, DEX-M74, GSK-2586881, SER-150-DN, клазосетана, блисибимода, AKB-9778, эптотермина альфа, беназеприла, эмрикасана, эпопростенола, DW-1029M, бендаcас лизина, селициклиба, BPS-804, авакопана, ALLO-ASC-DFU, SM 101, плозализумаба, берапроста натрия, берапроста, лозмапимода, PEG-bHb-CO, рекомбинантной человеческой щелочной фосфотазы, CXA-10, SAR- 407899, BI -655088, BOT -191, сулодексида, вонапанитаза, соматропина, топироксостата, SB -030, SHP-627, KBP-5074, EA-230, эмаптикапа пегола, фенилбутирата натрия, BB-3, Хемалба, тирилазада, ASP 8232, VPI-2690B, октреотида ацетата, EPO-018B, торасемида, рейна, PHN 033, эпросартана, KP-100IT, NCTX, ERC-124, сапроптерина, парнапарина натрия, парнапарина, фенолдопама и витамина D.
[0116] В некоторых воплощениях пациент также подвергается экстракорпоральной очистке крови, аллогенной трансплантации и/или терапии стволовыми клетками.
[0117] В некоторых воплощениях одно или более дополнительных терапевтических соединений назначается одновременно или последовательно.
[0118] В некоторых воплощениях одно или более дополнительных терапевтических соединений назначается как единая фармацевтическая композиция вместе с соединением формулы I или (Ia), соединением 1, соединением 2 или соединением 3 или как отдельная фармацевтическая композиция.
Соединения, Модулирующие CCR2 активность
[0119] Настоящее раскрытие представляет соединения, модулирующие CCR2 активность. Рецепторы хемокина являются интегральными мембранными протеинами, взаимодействующими с внеклеточным лигандом, таким как хемокин, и являются посредниками клеточного ответа на лиганд, например, хемотаксис, увеличивающий внутриклеточную концентрацию ионов кальция, и т.д. Поэтому модуляция функции рецептора хемокина, например, интерференция со взаимодействием лиганда рецептора хемокина, будет модулировать опосредованный ответ рецептора хемокина и лечить или предотвращать опосредованное рецептором хемокина состояние или заболевание. Модуляция функции рецептора хемокина включает и стимулирование, и ингибирование функции. Тип достигнутой модуляции будет зависеть от характеристик соединения, т.е. антагонист или полный, частичный или инверсный агонист.
[0120] Без намерения связи с какой-то конкретной теорией, представляется, что представленные здесь соединения вмешиваются во взаимодействие между рецептором хемокина и одним или более родственными лигандами. В частности считается, что соединения вмешиваются во взаимодействие между CCR2 и CCR2 лигандом, таким как MCP- 1. Соединения, рассмотренные этим раскрытием, включают, но без ограничения, типичные соединения, представленные здесь и их соли.
[0121] Соединения раскрытия, как полагают, вмешиваются в несоответствующее T-клеточное перемещение путем специфической модуляции или запрещения функции рецептора хемокина. Соединения, полезные для лечения FSGS, рассмотренные раскрытием, включают, но без ограничения, типичные представленные здесь соединения и фармацевтически приемлемые их соли и соединения, представленные в US 8,519,135, US 2006/0173019, US 2014/0031348, US 7,622,583, US 7,884,110 и US 8,093,247, которые включены здесь посредством ссылок.
[0122] В некоторых воплощениях соединения раскрытия являются селективными ингибиторами CCR2.
Композиции
[0123] Это раскрытие рассматривает назначение фармацевтически приемлемых композиций, включающих соединение Формулы I, Формулы (I а), соединение 1, соединение 2 или соединение 3 для лечения фокально-сегментарного гломерулосклероза (FSGS) в нуждающемся в этом пациенте. Фармацевтически приемлемые композиции могут включать одно или несколько дополнительных терапевтических соединений. Одно или более дополнительных терапевтических соединений могут быть выбраны из соединений, имеющих эффективность в лечении FSGS или почечных заболеваний.
[0124] Фармацевтически приемлемые композиции могут назначаться людям и другим животным перорально, ректально, парентерально, интрацестернально, внутривагинально, внутрибрюшинно, местно (как порошки, мази или капли), букально, как пероральный или назальный спрей, и т.п.
[0125] Жидкие формы дозировки для перорального приема включают, но без ограничения, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активному соединению (соединениям) жидкая форма дозировки может содержать инертные разжижители, обычно используемые в области, такие как, например, вода или другие растворители, растворяющие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, семени хлопчатника, арахисовое, кукурузное, масло зародышей пшеницы, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирной кислоты сорбитана и их смеси. Помимо инертных разжижителей оральные композиции могут также включать адъюванты, такие как смачивающие агенты, эмульсифицирующие и суспендирующие агенты, подсластители, ароматизаторы и парфюмерные агенты.
[0126] Вводимые составы, например, стерильные вводимые водные или масляные суспензии, могут быть составлены известным в области образом, используя подходящие рассеивающие или смачивающие агенты и суспендирующие агенты. Стерильный вводимый состав может также быть стерильным вводимым раствором, суспензией или эмульсией в нетоксичном парентерально приемлемом разжижителе или растворителе, например, как раствор в 1,3-бутандиоле. Среди приемлемых наполнителей и растворителей, которые могут использоваться, вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные, нелетучие масла традиционно используются в качестве растворяющей или суспендирующей среды. С этой целью любое мягкое нелетучее масло может использоваться, включая синтетические моно - или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, могут быть включены во вводимый продукт. Вводимые составы могут стерилизоваться, например, фильтрацией через бактериально-удерживающий фильтр или путем введения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной вводимой среде до использования.
[0127] Для продления действия соединения раскрытия часто желательно замедлить поглощение соединения из подкожной или внутримышечной инъекции. Это может быть достигнуто при помощи жидкой суспензии кристаллического или аморфного вещества с низкой водорастворимостью. Скорость поглощения соединения в этом случае зависит от скорости его растворения, что, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. Также задержанная абсорбция парентерально введенной формы соединения достигается путем растворения или суспендирования соединения в масляном наполнителе. Вводимые депо- формы получают путем формирования микроинкапсулированных матриц соединения в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от отношения соединения к полимеру и природы определенного используемого полимера можно контролировать скорость высвобождения соединения. Примеры других биоразлагаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Вводимые депо-составы также получают путем вовлечения соединения в липосомы или микроэмульсии, которые совместимы с тканями тела.
[0128] Композиции для ректального или вагинального введения являются предпочтительно свечами, которые могут быть получены путем смешивания соединения этого раскрытия с подходящими нераздражающими наполнителями или носителями, такими как масло какао, полиэтиленгликоль или свечной воск, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела и поэтому тают в прямой кишке или вагинальной полости и высвобождают активное соединение.
[0129] Твердые формы дозировки для перорального приема включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых формах дозировки активное соединение смешано, по крайней мере, с одним инертным фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или дикальций фосфат и/или (a) наполнителями или экстендерами, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремневая кислота, (b) связующими, такими как, например, карбоксимэтилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и акация, (c) увлажнителями, такими как глицерин, (d) дезинтегрирующими агентами, такими как агар - агар, карбонат кальция, картофельный крахмал или крахмал тапиоки, альгиновая кислота, некоторые силикаты и карбонат натрия, (e) задерживающими растворение агентами, такими как парафин, (f) акселераторами абсорбции, такими как четвертичные соединения аммония, (g) смачивающими агентами, такими как, например, цетиловый спирт и моностеарат глицерина, (h) абсорбентами, такими как каолин и бентонитовая глина и (i) лубрикантами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль форма дозировки может также включать буферные агенты.
[0130] Твердые композиции подобного типа могут также использоваться в мягких и твердых заполненных желатиновых капсулах с использованием таких наполнителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п. Твердые формы дозировки таблеток, драже, капсул, пилюль и гранул могут быть получены с использованием веществ для нанесения покрытий и оболочек, таких как энтерические покрытия и другие покрытия, известные в области фармацевтики. Они могут произвольно содержать замутняющие агенты и могут также состоять из композиции, так что высвобождают активный ингредиент (ингредиенты) только или, предпочтительно, в определенной части кишечного тракта, произвольно, с задержанием. Примеры вложенных композиций, которые могут использоваться, включают полимерные вещества и воски. Твердые композиции подобного типа могут также использоваться как наполнители в мягких и твердых заполненных желатиновых капсулах с помощью таких наполнителей как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т.п.
131] Соединения настоящего раскрытия или фармацевтически приемлемые их соли могут быть получены с помощью нанотехнологии. Наночастицы привлекательны в медицинских целях благодаря их характерным особенностям, таким как отношение площади поверхности к массе, которое больше, чем у других частиц, их квантовые свойства и их способность адсорбировать и нести другие соединения. Наночастицы могут иметь размеры менее 0,1 мкм или 100 нм. Также фармацевтическая композиция может включать относительно большие (размер> 100 нм) наночастицы, как требуется для загрузки достаточного количества препарата на частицы. Кроме того, для доставки лекарственных средств не только спроектированные частицы могут использоваться в качестве носителя, но также и сам препарат может быть сформулирован в наноразмерном диапазоне, и затем функционировать как свой собственный носитель. Композиция спроектированных наночастиц может изменяться. Исходные вещества могут иметь биологическое происхождения как фосфолипиды, липиды, молочная кислота, декстран, хитозан, или иметь больше химических характеристик, как различные полимеры, углерод, кварц и металлы. Особенно в области спроектированных наночастиц полимерного происхождения существует обширное поле возможностей для химической композиции. См., например, Martins et al., Nanoparticle Drug Delivery Systems: Recent Patents and Applications in Nanomedicine, Recent Patents on Nanomedicine, 2013, 3(2), pp. 1-14.
[0132] Соединения настоящего раскрытия или фармацевтически приемлемая их соль могут также присутствовать в микроинкапсулированной форме с одним или более наполнителями, как отмечено выше. Твердые формы дозировки таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с помощью покрытий и оболочек, таких как энтеральные покрытия, контролирующие высвобождение покрытия и другие покрытия, известные в области фармацевтических разработок. В таких твердых формах дозировки активное соединение может быть смешано, по крайней мере, с одним инертным разжижителем, таким как сахароза, лактоза или крахмал. Такие формы дозировки могут также включать, как нормальная практика, дополнительные вещества, кроме инертных разжижителей, например, таблетирующие лубриканты и другие способствующие таблетированию добавки, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль формы дозировки могут также включать буферные вещества. Они могут произвольно содержать замутняющие вещества и могут также состоять из композиции, так что высвобождают активный ингредиент (ингредиенты) только, или предпочтительно, в определенной части кишечного тракта, произвольно с задержкой. Примеры введенных композиций, которые могут использоваться, включают полимерные вещества и воски.
[0133] Формы дозировки для местного или трансдермального введения соединения этого раскрытия включают мази, пасты, сливки, лосьоны, гели, порошки, растворы, спреи, ингалянты или пластыри. Активный компонент примешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферами, как может потребоваться. Офтальмологический состав, ушные капли и глазные капли также рассматриваются как охватываемые рамками этого раскрытия. Кроме того, раскрытие рассматривает использование трансдермальных пластырей, имеющих дополнительное преимущество обеспечения контролируемой доставки соединения к телу. Такие формы дозировки получены путем растворения или распределения соединения в надлежащей среде. Усилители абсорбции могут также использоваться для увеличения поступления соединения через кожу. Скорость может контролироваться или обеспечением контролирующей скорость мембраны, или путем рассеивания соединения в полимерном матриксе или геле.
[0134] Соединения и композиции настоящего раскрытия могут вводиться перорально, парентерально (например, внутримышечно, внутрибрюшинно, внутривенно, ICV, внутриполостной инъекцией или вливанием, подкожной инъекцией или имплантатом), ингаляцией, назально, вагинально, ректально, подъязычным или местным путями введения и могут быть сформулированы, одно или вместе, в подходящих дозировках, содержащих стандартные нетоксичные фармацевтически приемлемые носители, адъюванты и носители, подходящие для каждого пути введения. Настоящее раскрытие также рассматривает введение соединений и композиций настоящего раскрытия в депо-составе.
[0135] Надлежащий уровень дозировки соединения Формулы (I), Формулы (Iа), соединения 1, 2, или 3 или фармацевтически приемлемой их соли обычно будет приблизительно от 0,001 до 100 мг на кг веса тела пациента в сутки, которая может быть введена в единственной или многократных дозах. Предпочтительно, уровень дозировки будет приблизительно от 0,01 до приблизительно 25 мг/кг в сутки; более предпочтительно от приблизительно 0,05 до приблизительно 10 мг/кг в сутки. Подходящий уровень дозировки может быть от приблизительно 0,01 до 25 мг/кг в сутки, от приблизительно 0,05 до 10 мг/кг в сутки или от приблизительно 0,1 до 5 мг/кг в сутки. В этом диапазоне дозировка может составлять от 0,005 до 0,05, от 0,05 до 0,5, от 0,5 до 5,0 или от 5,0 до 50 мг/кг в сутки. Для перорального приема композиции предпочтительно обеспечиваются в форме таблеток, содержащих от 1,0 до 1 000 миллиграмм активного ингредиента, в частности, 1.0, 5.0, 10.0, 15.0, 20.0, 25.0, 50.0, 75.0, 80.0, 90.0, 100.0, 110.0, 120.0, 130.0, 140.0, 150.0, 160.0, 170.0, 180.0, 190.0, 200.0, 250.0, 300.0, 400.0, 500.0, 600.0, 750.0, 800.0, 900.0 и 1 000,0 миллиграмм активного ингредиента для симптоматического регулирования дозировки пациенту, которого лечат. Для перорального приема в некоторых воплощениях композиции обеспечиваются в форме таблеток, содержащих 150 мг активного ингредиента. Для перорального приема в некоторых воплощениях композиции обеспечиваются в форме таблеток, содержащих 10 мг активного ингредиента. Для перорального приема в некоторых воплощениях композиции обеспечиваются в форме таблеток, содержащих 5 мг активного ингредиента. Соединения могут вводиться в режиме 1-4 раз в день, предпочтительно один или дважды в день.
[0136] Понятно, однако, что определенный уровень дозы и частота дозирования для какого-то конкретного пациента могут быть различны и будут зависеть от множества факторов, включая активность определенного используемого соединения, метаболическую стабильность и продолжительность действия этого соединения, возраст, вес тела, наследственные особенности, общее состояние здоровья, пол, диету, способ и время введения, уровень выделения, комбинацию лекарств, серьезность определенного состояния и человека, подвергающегося терапии.
[0137] Соединения и композиции настоящего раскрытия могут быть объединены с другими соединениями и композициями, имеющими пользу в предотвращении и лечении FSGS. Выбор соответствующих агентов для использования в комбинированной терапии может быть сделан обычным специалистом в области. Комбинация терапевтических агентов может действовать синергитически для осуществления лечения или профилактики различных расстройств. Используя этот подход, можно достигнуть терапевтической эффективности с более низкими дозировками каждого агента, таким образом уменьшая вероятность неблагоприятных побочных эффектов.
[0138] Весовое соотношение соединения настоящего раскрытия к другому активному ингредиенту может быть различно и будет зависеть от эффективной дозы каждого компонента. Обычно эффективная доза каждого будет использоваться. Таким образом, например, когда соединение настоящего раскрытия будет объединено со вторым терапевтическим соединением, весовое отношение соединения настоящего раскрытия ко второму терапевтическому соединению обычно составляет от приблизительно 1000:1 до приблизительно 1:1000, предпочтительно от приблизительно 200:1 до приблизительно 1:200.
[0139] В еще одном аспекте настоящее раскрытие обеспечивает способы лечения или предотвращения FSGS путем введения субъекту, имеющему такое состояние или заболевание, терапевтически эффективного количества любого соединения настоящего раскрытия. Соединения для использования в представленных способах включают соединения согласно Формуле (I), Формуле (Iа), соединение 1, 2 или 3 или фармацевтически приемлемую их соль, представленные как варианты и имеющие определенное строение, и соединения, представленные в US 8,519,135, US 2006/0173019, US 2014/0031348, US 7,622,583, US 7,884,110 и US 8,093,247, которые здесь включены посредством ссылок. Соединения могут быть полезными для лечения субъекта, который нуждается в лечении.
«Субъект» определен здесь как включающий животных, таких как млекопитающие, включая, но без ограничения, приматов (например, людей), коров, овец, коз, лошадей, собак, кошек, кроликов, крыс, мышей и т.п. В предпочтительных воплощениях субъектом является человек.
[0140] Как здесь используется, фраза «терапевтически эффективное количество» означает количество соответствующего соединения, которое вызовет биологический или медицинский ответ клетки, ткани, системы или животного, такого как человек, ожидаемый исследователем, ветеринаром, врачом или другим дающим лечение лицом.
[0141] В одном воплощении настоящее раскрытие обеспечивает способы лечения или предотвращения FSGS, включающие введение субъекту эффективного количества соединения или композиции этого раскрытия, где введение является пероральным, парентеральным, ректальным, трансдермальным, подъязыковым, назальным или местным.
Модуляторы CCR2
[0142] Следующие примеры предлагаются для иллюстрирования, но без ограничения, настоящего раскрытия.
[0143] Определенные молекулы, раскрытые в этом патенте, могут существовать в различных энантиомерических и диастереомерических формах, и все такие варианты этих соединений находятся в рамках этого раскрытия.
[0144] Определенные фармакологические наблюдаемые ответы могут изменяться согласно и в зависимости от определенного активного соединения, которое выбрано, и того существуют ли представленные фармацевтические носители, а также от типа состава и способа применяемого введения, и такие ожидаемые вариации или различия в результатах рассматриваются в соответствии с практикой настоящего раскрытия.
[0145] Несмотря на то, что определенные воплощения настоящего раскрытия здесь проиллюстрированы и описаны подробно, раскрытие ими не ограничивается. Вышеупомянутые подробные описания представлены как репрезентативные для настоящего раскрытия и не должны быть истолкованы как составляющие ограничение раскрытия. Модификации будут очевидны для специалистов в области, и все модификации, не отступающие от сущности раскрытия, охвачены объемом приложенных пунктов формулы.
Дополнительные комбинации
[0146] Соединения раскрытия могут поставляться одни или в сочетании с одним или более другими лекарственными средствами для лечения FSGS.
[0147] Примеры терапевтических веществ, которые могут быть объединены с соединением или композицией настоящего раскрытия, вводимые отдельно или в той же самой фармацевтической композиции, включают, но без ограничения: модуляторы CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CCR11, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, CXCR7, CX3CR1, ChemR23, C5aR, C5a, и C5 или любую их комбинацию. В некоторых воплощениях модулятор является антагонистом.
[0148] Примеры терапевтических агентов, которые могут быть объединены с соединением или композицией настоящего раскрытия, вводимые отдельно или в той же самой фармацевтической композиции, включают, но без ограничения: CCX354, CCX9588, CCX140, CCX872, CCX598, CCX6239, CCX9664, CCX2553, CCX 2991, CCX282, CCX025, CCX507, CCX430, CCX765, CCX224, CCX662, CCX650, CCX832, CCX168, и CCX168-M1 или любую их комбинацию.
[0149] Примеры других терапевтических агентов, которые могут быть объединены с соединением или композицией настоящего раскрытия, вводимые отдельно или в тех же фармацевтических композициях, включают, но без ограничения: терапевтическое антитело, би-специфичное антитело и «подобный антителу» терапевтический протеин (такой как DARTs®, Duobodies®, Bites®, XmAbs®, TandAbs ®, Fab производные), конъюгат антитело-препарат (ADC), вирус, онколитический вирус, генные модификаторы или редакторы, такие как CRISPR (включая CRISPR Cas9), нуклеазы «цинковые пальцы» или синтетические нуклеазы (TALENs), CAR (химерный рецептор антигена) T-клеточный иммунотерапевтический агент, цитокины, вакцины и адъюванты вакцин.
Комплекты и упаковки
[0150] Термины «комплект» и «фармацевтический комплект» относятся к коммерческому комплекту или упаковке, в одном или более подходящих контейнерах, одной или более фармацевтических композиций с инструкциями для использования. В одном воплощении обеспечиваются комплекты, включающие соединение Формулы (I) или (Ia), или соединение 1, 2 или 3, или фармацевтически приемлемую соль и инструкции для введения. В одном воплощении представлены комплекты, включающие соединение Формулы (I) или (Ia), или соединение 1, 2 или 3, или фармацевтически приемлемую его соль, в сочетании с одним или несколькими (например, один, два, три, один или два, или один - три) дополнительными терапевтическими агентами и инструкциями для их введения.
[0151] В одном воплощении соединения этого раскрытия составляются в единицы для введения, упакованные в единственную упаковку. Единственная упаковка охватывает, но без ограничения, бутылку, бутылочку для ребенка, ампулу и пробирку. В одном воплощении соединения этого раскрытия и произвольно дополнительные терапевтические агенты составляются в единицы для введения, и каждая единица для введения индивидуально упакована в единственную упаковку. Такие индивидуально упакованные единицы могут содержать фармацевтическую композицию в любой форме, включая, но без ограничения, жидкую форму, твердую форму, порошковую форму, гранулированную форму, шипучий порошок или таблетку, твердые или мягкие капсулы, эмульсии, суспензии, сироп, свечи, таблетки, лепешки, пастилки, раствор, букальный пластырь, тонкую пленку, оральный гель, жевательную таблетку, жевательную резинку и одноразовые шприцы. Такие индивидуально упакованные единицы могут быть объединены в упаковке, изготовленной из одного или более - бумаги, картона, строительного картона, металлической фольги и полимерной пленки, например, блистерная упаковка. Одна или более единиц для введения может вводиться один раз или несколько раз в день. Одна или более единиц для введения может вводиться три раза в день. Одна или более единиц для введения может вводиться два раза в день. Одна или более единиц для введения может вводиться в первый день, и одна или более единиц для введения может вводиться в последующие дни.
Другие заболевания
[0152] Соединения Формулы (I), (Iа), соединение 1, соединение 2 или соединение 3 или фармацевтически приемлемая их соль и/или их пролекарство или их композиции, использованные одни или в комбинациях, могут быть полезными для лечения других заболеваний. Эти заболевания включают, но без ограничения, хроническое заболевание почек, диабетическую нефропатию, терминальную стадию почечного заболевания, клубочковые заболевания, синдром Гудпасчура, гломерулонефрит, гломерулосклероз, igA нефропатию, мембранопролиферативный гломерулонефрит, мембранозный гломерулонефрит, грануломатоз Вегенера, васкулит, Anca-васкулит, почечную недостаточность, почечный фиброз, болезнь Барттера, нефрокальциноз, гидронефроз, пионефроз, почечно-печеночный синдром, гемолитический уремический синдром, нефрит, несахарный диабет, нефрогенный несахарный диабет, почечную недостаточность, нейрогенный несахарный диабет, синдром Вольфрама, нефротический синдром, заболевание минимальных изменений, перинефрит, болезнь вмятин, синдром Джителмена, нефросклероз, заболевание почечных трубочек, гепаторенальный синдром, азотемия, уремия, синдром Альпорта, гломерулонефрит, волчаночный нефрит, пиелит, пиелонефрит, пиелоцистит, повреждение клубочков, поликистозную болезнь почек, приобретенную поликистозную болезнь почек, аутосомальную доминирующую поликистозную болезнь почек, аутосомно-рецессивную поликистозную болезнь почек, синдром Абдергалден-Кауфман-Лигнак (нефропатический цистиноз), синдром отдела брюшной полости, ацетаминофен-индуцированную нефротоксичность, острую почечную недостаточность, острое повреждение почки, острую нефронию Лобара, острую фосфатную нефропатию, острый трубчатый некроз, недостаток аденинфосфорибозилтрансферазы, аденовирусный нефрит, синдром Альпорта, амилоидоз, ангиомиолипому, анальгетическую нефропатию, антифосфолипидный синдром, анти-TNF\U 03B1\связанный с терапией гломерулонефрит, APOL1 мутации, синдром очевидного избытка минералокортикоидов, аристолохную кислотную нефропатию, китайскую травяную нефропатию, балканскую эндемичную нефропатию, битурию, почечное заболевание β-талассемии, нефропатию выброса желчи, BK полиомную вирусную рефропатию в нативной почке, диссинергию сфинктера мочевого пузыря, тампонадный мочевой пузырь, нефропатию нарушения границ, вирус Бурбона и острое повреждение почки, острую почечную дисфункцию, баетта, C1q нефропатию, каннабиноидную гипермезию, острую почечную недостаточность, кардиренальный синдром, карфилзомиб-индуцированное почечное повреждение, CFHR5 нефропатию, заболевание Charcot-Marie-Tooth с гломерулопатией, холестериновую эмболию, синдром Хург-Штрауса, хилурию, колистиновую нефротоксичность, коллагенофибротическую гломерулопатию, коллапсирующую гломерулопатию, коллапесирующую гломерулопатию, связанную с CMV, врожденный нефротический синдром, коноренальный синдром (синдром Mainzer-Saldino или болезнь Saldino-Mainzer), контрастную нефропатию, отравление сульфатом меди, корковый некроз, кризотиниб-связанное острое повреждение почки, криоглобуинемию, кристаллоглобулин-вызванную нефропатию, кистозную болезнь почек, приобретенную цистинурию, болезнь плотного осадка, синдромом неравновесного состояния диализа, диабетическую болезнь почек, рассеянный мезангиальный склероз, дублированный мочеточник, EAST синдром, Erdheim-Chester заболевание, Болезнь Фэбри, семейную гиперкальциуриновую гиперкальцемию, синдром Fanconi, синдром Фрейзера, Фибронектиновую Гломерулопатию, волокнистый Гломерулонефрит и иммуннотактоидную гломерулопатию, синдром Fraley, фокальный Склероз, фокальный гломерулосклероз, синдром Гэллоуэя Моуэта, гигантскоклеточный артериит (Временный) с почечным включением, клубочковый трубчатый рефлюкс, гликозурию, хантавирусную инфекционную подоцитопацию, нефропатию теплового удара, истинную гематурию, нетипичный гемолитический уремический синдром (aHUS), гемофагоцитарный синдром, геморрагический цистит, эпидемическую нефропaтию, гемосидеринурию, гемосидероз, гломерулопатию, печеночную гломерулопатию, печеночную вено-окклюзивную болезнь, синусоидальный обструкционный синдром, связанное с гепатитом С почечное заболевание, гепаторенальный cиндром, cвязанную с HIV нефропатию (HIVAN), HNF1B-связанную аутосомальную доминирующую тубулоинтерстициальную болезнь почек, подковообразную почку (почечный синтез), язву Хуннера, гиперальдостеронизм, гиперкальцемию, гиперкалиемию, гипермагниемию, гипернатриемию, гипероксалурию, гиперфосфатемию, гипокальцемию, гипокомплементемический уртикариальный васкулитический синдром, гипокалиемию, вызванную гипокалиемией почечную дисфункцию, гипокалемический периодический паралич, гипомагниемию, гипонатриемию, гипофосфатемию, нефропатию IgA, нефропатию IgG4, иммуно-чекпойнт связанный с терапией промежуточный нефрит, промежуточный цистит, синдром болезненного мочевого пузыря, промежуточный нефрит, синдром Ивемарка, связанную с кетамином дисфункцую мочевого пузыря, почечные камни, нефролитиаз, токсичность чайного гриба, ведущую нефропатию и свинец-связанную нефротоксичность, почечное заболевание лептоспироза, болезнь смещения легкой цепи, моноклональную болезнь смещения иммуноглобулина, синдром Лиддла, синдром Лайтвуд-Олбрайта, липопротеиновую гломерулопатию, литиевую нефротоксичность, LMX1B мутациями вызванный наследственный FSGS, высоко болезненную гематурию, волчанку, системный волчаночный эритроматоз, волчаночную болезнь почек, волчаночный нефрит, волчаночный нефрит с антинейтрофильной цитоплазматической серопозитивной реакцией антител, подоцитопатическую волчанку, связанный с болезнью Лайма гломерулонефрит, нефропатию Лизозима, малярийную нефропатию, связанное со злокачественностью почечное заболевание, злокачественную гипертонию, малакоплакию, стеноз слухового прохода, медуллярную кистозную болезнь почек, уролодулин-связанную нефропатию, ювенильную гиперуремическую нефропатию типа 1, медуллярную губчатую почку, мегамочеточник, меламиновую токсичность и почку, мембранопролиферативный гломерулонефрит, мембранную нефропатию, мембрано-подобную Гломерулопатию с замаскированными Каппа IgG отложениями, мезоамериканскую нефропатию, метаболический ацидоз, метаболический алкалоз, связанную с метотрексатом почечную недостаточность, микроскопический поливаскулит, молочно-щелочной синдром, заболевание минимальных изменений, MDMA (Molly; Ecstacy; 3,4 -метилендиоксиметамфетам) и почечную недостаточность, нефропатию MUC1, мультикистозную диспластическую почку, множественную миелому, миелопролиферативные неоплазмы и гломерулопатию, наследственный онихоартроз, нефрокальциноз, нефрогенный системный фиброз, нефроптоз (флотирующая почка, почечный птоз), нефротический синдром, нейрогенный мочевой пузырь, узловой гломерулосклероз, негонококковый уретрит, синдром Щелкунчика, олигомеганефронию, орофациодигитальный синдром, оротовую ацидурию, ортостатическую гипотонию, ортостатическую протеинурию, осмотический диурез, осмотический нефроз, яичниковый синдром гиперстимуляции, оксалатную нефропатию, блуждающую почку, папиллярный некроз, папиллоренальный синдром (почечно-коломобный синдром, изолированная почечная гипоплазия), брюшинно-почечный синдром, задний уретральный клапан, постинфекционный гломерулонефрит, постстрептококковый гломерулонефрит, полиартериит Nodosa, поликистозную болезнь почек, задние уретральные клапаны, преэклампсию, синдром пропофол инфузии, пролиферативный гломерулонефрит с моноклональными отложениями IgG (болезнь Насра), прополис-связанную почечную недостаточность, протеинурию, псевдогиперальдостеронизм, псевдогипобакарбонатемию, псевдогипопаратироидизм, легочно-почечный синдром, пиелонефрит, пионефроз, радиационную нефропатию, синдром повторного кормления, нефропатию рефлюкса, быстро прогрессирующий гломерулонефрит, почечный абсцесс, перинефритный абсцесс, почечную агенезию, почечную дугообразную вену, связанное с микротромбами острое повреждение почки, аневризму почечной артерии, стеноз почечной артерии, клеточный рак почечного эпителия, почечную киста, почечную гипоурецемию, вызванную острой почечной недостаточностью, почечный инфаркт, почечную остеодистрофию, почечноканальцевый ацидоз, мутации ренина и аутосомальную тубулоинтерстициальную доминирующую болезнь почек, ренин-секретирующие опухоли (Юкстагломерулярная клеточная опухоль), восстановленный осмостат, ретрокавальный мочеточник, ретроперитонеальный фиброз, острый некроз скелетных мышц, острый некроз скелетных мышц, связанный с бариатрической хирургией, связанное с ревматоидным артритом почечное заболевание, почечное заболевание саркоидоза, солевая недостаточность, шистосомоз и клубочковную болезнь, шимке иммуно-костяное нарушение роста, склеродерму ренального кризиса, серпентиновый поликистозный почечный синдром, синдром Экснера, нефропатую серповидных клеток, синдром Сьегрена, использование синтетического каннабиноида и острое повреждение почки, болезнь почек после гематопоэтической клеточной трансплантации, болезнь почек, связанную с трансплантацией стволовых клеток, заболевание тонких базисных мембран, доброкачественную семейную гематурию, тригонит, туберкулез, туберозный склероз, трубчатый дисгенезис, иммунный комплексный тубулоинтерстицииальный нефрит из-за аутоантител к проксимальной тубуло-щеточной кайме, синдром лизиса опухоли, уремию, уремическую оптическую невропатию, ureteritis Cystica, уретроцеле, ральный карункул, стриктуру уретры, недержание мочи, инфекцию мочевых путей, обструкцию мочевых путей, уромодулин-связанную болезнь почек, вазомоторную Нефропатию, везикоинтестинальный свищ, везикоуретральный рефлюкс, заболевание Фон Хиппель-Линдау, макроглобулинемический гломерулонефрит Волденстрома, связанную с варфарином нефропатию, грануломатоз Вегенера, грануломатоз с поливаскулитом, западно- нильский вирус, синдромом Wunderlich, синдром Зеллвегера, цереброгепаторенальный синдром, меланому, глиобластому, опухоль пищевода, носоглоточную карциному, увеальную меланому, лимфому, лимфоцитарную лимфому, первичную лимфому CNS, T-клеточную лимфому, первичную медиастенальную обширную B-клеточную-лимфому, первичную средостеночную обширную B-клеточную-лимфому, рак простаты, кастрация-стойкий рак простаты, хроническую миелоцитарную лейкемию, фибросаркому саркомы Капоши, липосаркому, хондросаркому, остеогенную саркому, ангиосаркому, лимфангиосаркому, синовиому, менингиому, леиомиосаркому, рабдомиосаркому, саркому мягких тканей, саркому, сепсис, желчную опухоль, базально-клеточный рак, неоплазму тимуса, рак щитовидной железы, рак паращитовидной железы, утробный рак, рак надпочечника, инфекцию печени, клеточную карциному Меркель, опухоль нервов, фолликулярную центральную лимфому, рак толстой кишки, болезнь Ходжкина, неходжкинскую лимфому, лейкемию, хронические или острые лейкемии, включая острую миелоидную лейкемию, хроническую миелоидную лейкемию, острую лимфообластную лейкемию, хронический лимфолейкоз, множественную миелому, опухоль яичника, миелодиспластический синдром, кожную или внутриглазную злокачественную меланому, клеточную карциному почечного эпителия, мелкоклеточный рак легких, рак легких, мезотелиому, рак молочной железы, чешуйчатый немелкоклеточный рак легких (SCLC), нечешуйчатый NSCLC, рак ободочной и прямой кишки, рак яичника, рак желудка, гепатоцеллюлярную карциному, карциному поджелудочной железы, рак поджелудочной железы, аденокарциному протока поджелудочной железы, карциному сквамозных клеток головы и шеи, рак головы или шеи, желудочно-кишечного тракта, рак желудка, рак костей, рак кожи, рак прямой кишки, рак анальной области, тестикулярный рак, карциному фаллопиевых труб, карциному оболочки матки, карциному шейки, карциному влагалища, карциному вульвы, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак уретры, рак полового члена, рак мочевого пузыря, рак почки, рак мочеточника, карциному почечной лоханки, неоплазму центральной нервной системы (CNS), опухолевый ангиогенез, опухоли позвоночника, глиомы стволовых клеток мозга, гипофизарную аденому, рак эпидермоида, абестоз, карциному, аденокарциному, папиллярную карциному, цистаденокарциному, бронхогенную карциному, клеточную карциному почечного эпителия, переходно-клеточный рак, хориокарциному, семиному, эмбриональную карциному, опухоль Вильмса, плеоморфную аденому, папиллому клеток печени, почечноканальцевую аденому, кистозную аденому, папиллому, аденому, лейомиому, рабдомиому, гемангиому, лимфангиому, остеому, хондрому, липому и фиброму. Для любой из этих болезней соединения раскрытия могут быть объединены с другими терапевтическими агентами, включая представленные в этом раскрытии соединения.
ПРИМЕРЫ
[0153] Остаточная почечная модель и адриамицин-индуцированная модель являются обычно используемыми моделями мышевидных грызунов для FSGS (de Mik SM. Et al. Pathophysiology and treatment of focal segmental glomerulosclerosis: the role of animal models. BMC Nephrol. 2013 Apr 1; 14:74). 5/6 остаточная модель почки является репрезентативной для вторичного FSGS, тогда как модель адриамициновой нефропатии является репрезентативной для основного FSGS.
Пример 1: 5/6 Остаточная Модель Почки
[0154] 5/6 остаточная почка 129X1/SvJ мыши была получена из Лабораторий Джексона. Мыши содержались на стандартном корме и имели свободный доступ к воде. Хирургия мышей проведена в два этапа. Под анестезией изофлюраном проведена диссекция двух третей массы левой почки. Спустя 7-10 дней выполнена правая односторонняя нефрэктомия. Спустя шесть недель после 5/6 нефрэктомии, мыши рандомизированы для исследования. Соединение 3 и его носитель вводились подкожно один раз ежедневно в дозе 100 мг/кг, составленной в 1%-м HPMC. 6 животных использовались для каждой группы.
[0155] Образцы мочи собраны в первую и вторую недели индивидуально путем помещения мыши в метаболические клетки в течение 18 часов. Мочевой альбумин измерен с помощью ELISA (Bethyl Labs, Montgomery TX), и мочевой уровень выделения альбумина (UAER) вычислен в микрограммах за 24 часа. Мочевой креатинин измерен масс-спектрометрией. Отношение альбумина к креатинину (ACR) вычислено в микрограммах альбумина на миллиграмм креатинина. В конце экспериментов (после 2 недель лечения) почки были отобраны, фиксированы в формалине, интегрированы в парафин и разрезаны на секции толщиной 3 мкм. Секции окрашены для подоцитов иммуногистохимией антителом Wilms опухолевого белка 1 (Abcam, Cambridge, MA). Площадь поперечного сечения клубочков и площадь поперечного сечения и число подоцитов определены в 20-30 клубочках на мышь. Объем клубочков и плотность подоцитов вычислены по данным иммуногистохимии с помощью метода Вейбеля. Мезангиальное расширение измерено с помощью серебряной метенаминовой краски на парафиновых секциях толщиной 2 мкм стандартными методами.
[0156] Фиг. 1 показывает, что соединение 3 уменьшило глубокую протеинурию в 5/6 Остаточной Модели Почки в первую и вторую недели.
[0157] Фиг. 2 показывает, что соединение 3 сократило количество почечных интерстициальных макрофагов в 5/6 Остаточной Модели Почки.
[0158] Фиг. 3 показывает некоторые репрезентативные изображения почечных интерстициальных макрофагов в 5/6 Остаточной Модели Почки с и без лечения соединением 3.
[0159] Фиг. 4 показывает, что соединение 3 увеличило число подоцитов в 5/6 Остаточной Модели Почки.
[0160] Фиг. 5 показывает репрезентативные изображения подоцитов в 5/6 Остаточной Модели Почки с и без лечения соединением 3.
[0161] Фиг. 6 показывает, что соединение 3 имеет благоприятный эффект на процентное содержание клубочков с мезангиолизом в 5/6 Остаточной Модели Почки.
[0162] Фиг. 7 показывает репрезентативное изображение клубочков с мезангиолизом.
Пример 2: модель адриамициновой нефропатии
[0163] Эксперимент выполнялся у мышей Balb/c женского пола (Лаборатории Джексона). Мыши содержались на стандартном корме и имели свободный доступ к воде. 7,5 мг/кг адриамицина (Selleck Chemicals) или солевой раствор (контроль) введены в вену хвоста у изофлюран-обезболенных животных в день 0. Соединение 1 и его носитель (1%-й HPMC) дозировали подкожно один раз ежедневно при дозировке 90 мг/кг, составленной в 1%-м HPMC. Кандесартан и его носитель (H2O) дозировали перорально один раз ежедневно. Двенадцать животных использовались для каждой группы.
[0164] Образцы мочи собраны в неделю один и два индивидуально путем размещения мышей в метаболических клетках в течение 18 ч. Мочевой альбумин измерен ELISA (Bethyl Labs, Montgomery, TX), и мочевой уровень выделения альбумина (UAER) вычислен в микрограммах за 24 часа. Мочевой креатинин измерен масс-спектрометрией. Отношение альбумина к креатинину (ACR) вычислено в микрограммах альбумина на миллиграмм креатинина.
[0165] Фиг. 8 показывает, что соединение 1 как единственный агент и в сочетании с кандесартаном (CST) приводит к сокращению уровней UACR.
[0166] Фиг. 9 показывает, что соединение 1 в сочетании с кандесартаном (CST) приводит к сокращению уровней UAER.
Пример 3: 5/6 Остаточная Модель Почки при комбинационном лечении
[0167] 129X1/SvJ мыши с 5 /6 остаточной почкой получены из Лабораторий Джексона. Мыши содержались на стандартном корме и имели свободный доступ к воде. Хирургия мышей проведена в два этапа. Под анестезией изофлюраном диссектировали две трети массы левой почки. Спустя семь-десять дней выполнили правую одностороннюю нефрэктомию. Спустя три-шесть недель после 5/6 нефрэктомии, мыши рандомизированы для исследования (n=12 на группу). Соединение 3 и его носитель дозировали подкожно один раз ежедневно в дозе 100 мг/кг, составленной в 1%-м HPMC. Кандесартан (AK Scientific) и его носитель (H2O) дозировали один раз ежедневно перорально в дозе 5мг/кг. Два животных на группу подвергнуты эвтаназии в недели 1, 2, и 3 для выполнения гистологии и IHC.
[0168] Образцы мочи собраны в неделю один, два и три индивидуально размещением мыши в метаболических клетках в течение 18 часов. Мочевой альбумин измерен ELISA (Bethyl Labs, Montgomery, TX), и скорость выделения альбумина мочи (UAER) вычислена в микрограммах за 24 часа. Мочевой креатинин измерен масс-спектрометрией. Отношение альбумина к креатинину (ACR) вычислено в микрограммах альбумина на миллиграмм креатинина.
[0169] Фиг. 10 показывает сокращение значений UAER в недели 1, 2 и 3 при лечении одним только соединением 3, при лечении одним только кандесартаном, а также при лечении комбинацией соединения 3 и кандесартана в 5/6 Остаточной Почечной Модели.
[0170] Фиг. 11 показывает сокращение значений UACR в неделю 1 и неделю 2 при лечении одним только соединением 3, при лечении одним только кандесартаном, а также при лечении комбинацией соединения 3 и кандесартана в 5/6 Остаточной Почечной Модели.
[0171] Соединение 1 - это:
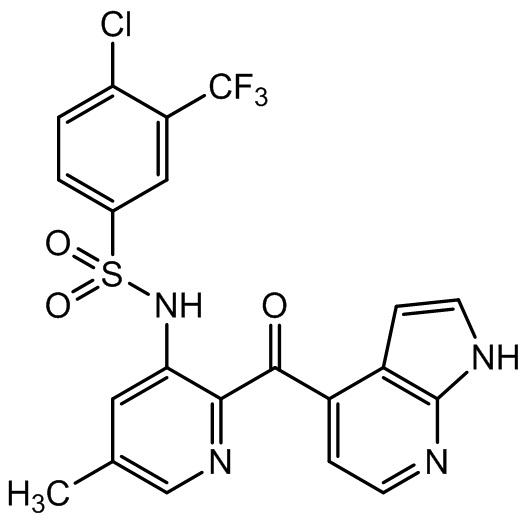
[0172] Соединение 2 - это:

[0173] Соединение 3 - это:

[0174] Специфические фармакологические наблюдаемые ответы могут изменяться согласно и в зависимости от определенного активного выбранного соединения или того, имеются ли представленные фармацевтические носители, а также от типа состава и режима примененного введения, и такие ожидаемые вариации или различия в результатах рассматриваются в соответствии с практикой настоящего раскрытия.
[0175] Несмотря на то что определенные воплощения настоящего раскрытия здесь проиллюстрированы и описаны подробно, раскрытие ими не ограничивается. Вышеупомянутые подробные описания представлены как типичные для настоящего раскрытия и не должны быть истолкованы как составляющие ограничение раскрытия. Модификации будут очевидны для специалистов области, и все модификации, не отступающие от сущности раскрытия, предназначены, чтобы охватываться объемом приложенных пунктов формулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения фиброза печени | 2017 |
|
RU2740902C2 |
| РАСТВОРИМЫЕ С5аR АНТАГОНИСТЫ | 2017 |
|
RU2748260C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2769696C2 |
| МОРФОЛИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ ИЛИ КАРБАМАТА В КАЧЕСТВЕ ИНГИБИТОРОВ MTOR | 2012 |
|
RU2616619C2 |
| ПРОИЗВОДНЫЕ 2-ПИРАЗИНОНА ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ, ПРИ КОТОРЫХ ПОЛЕЗНО ИНГИБИРОВАНИЕ АКТИВНОСТИ НЕЙТРОФИЛЬНОЙ ЭЛАСТАЗЫ | 2007 |
|
RU2448098C2 |
| НЕКОТОРЫЕ ХИМИЧЕСКИЕ СТРУКТУРЫ, КОМПОЗИЦИИ И СПОСОБЫ | 2009 |
|
RU2513636C2 |
| СПОСОБ ЛЕЧЕНИЯ С3-ГЛОМЕРУЛОПАТИИ | 2017 |
|
RU2742888C2 |
| НЕКОТОРЫЕ ХИМИЧЕСКИЕ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ | 2010 |
|
RU2582676C2 |
| НЕКОТОРЫЕ ХИМИЧЕСКИЕ СТРУКТУРЫ, КОМПОЗИЦИИ И СПОСОБЫ | 2009 |
|
RU2537549C2 |
| ПРОИЗВОДНЫЕ ИЗОТИОМОЧЕВИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2005 |
|
RU2376297C2 |
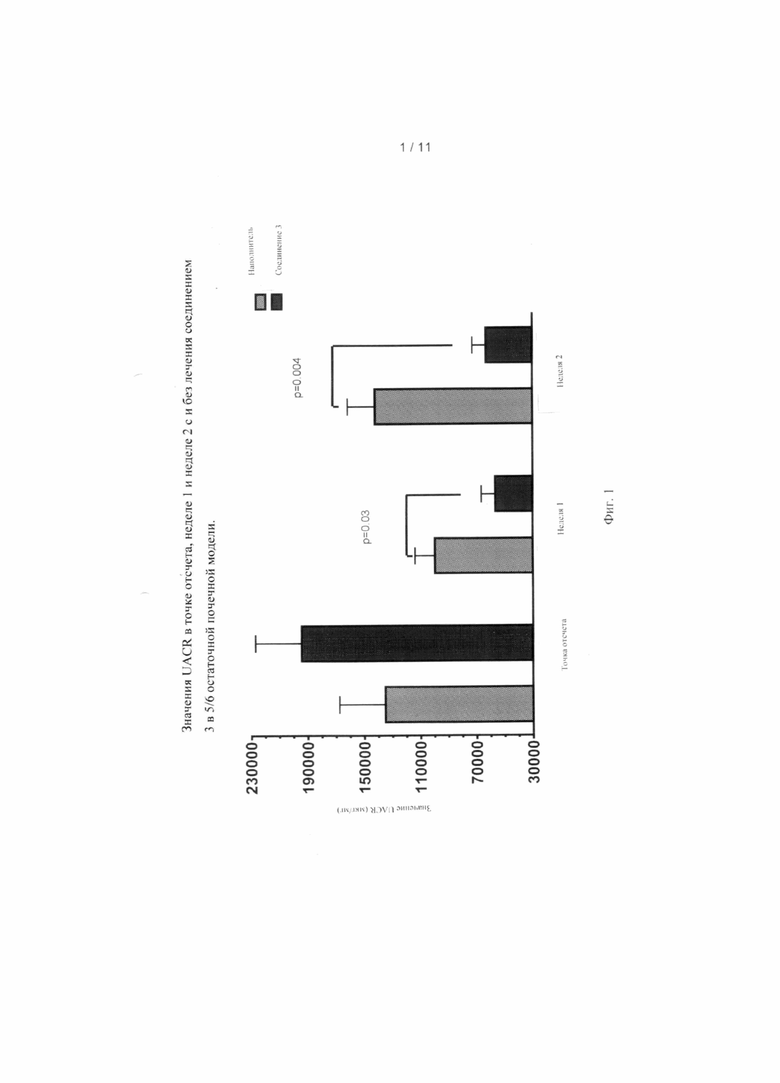
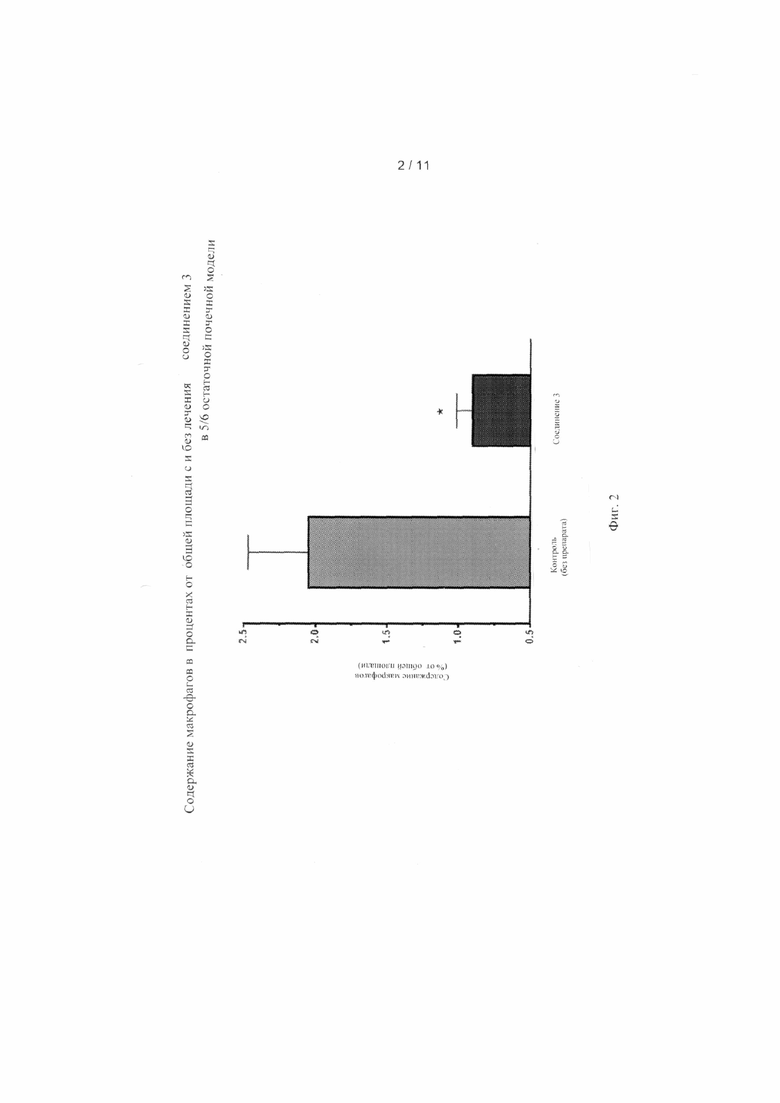


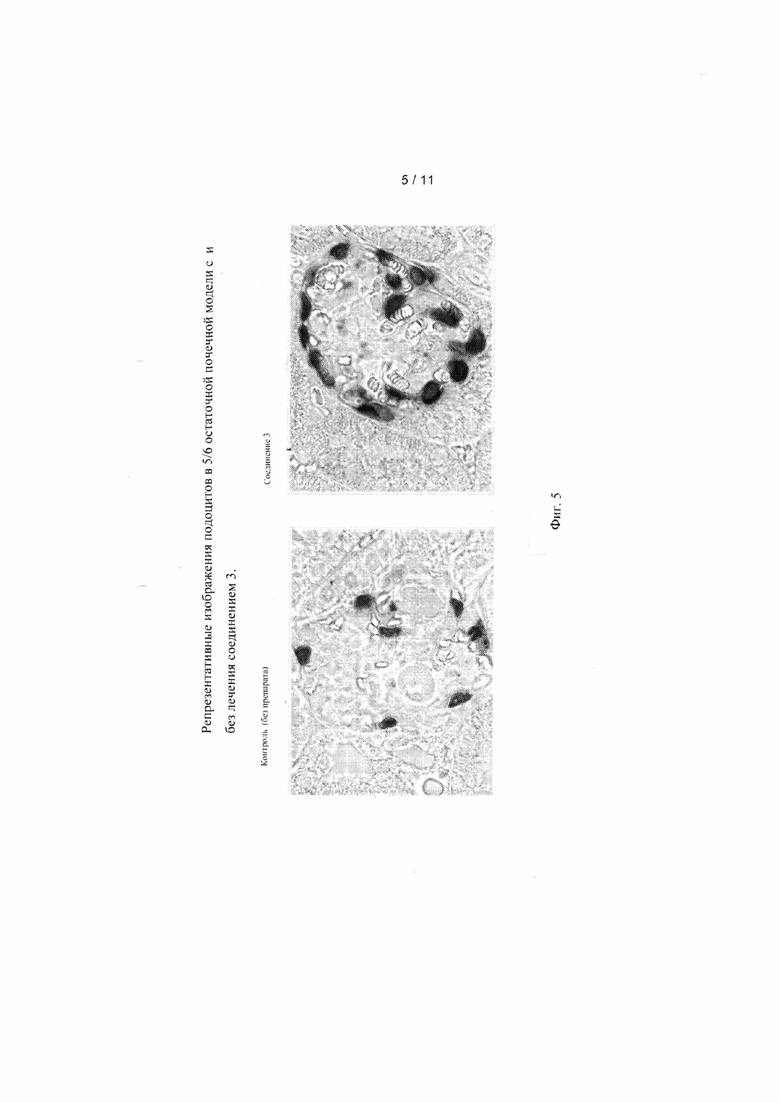
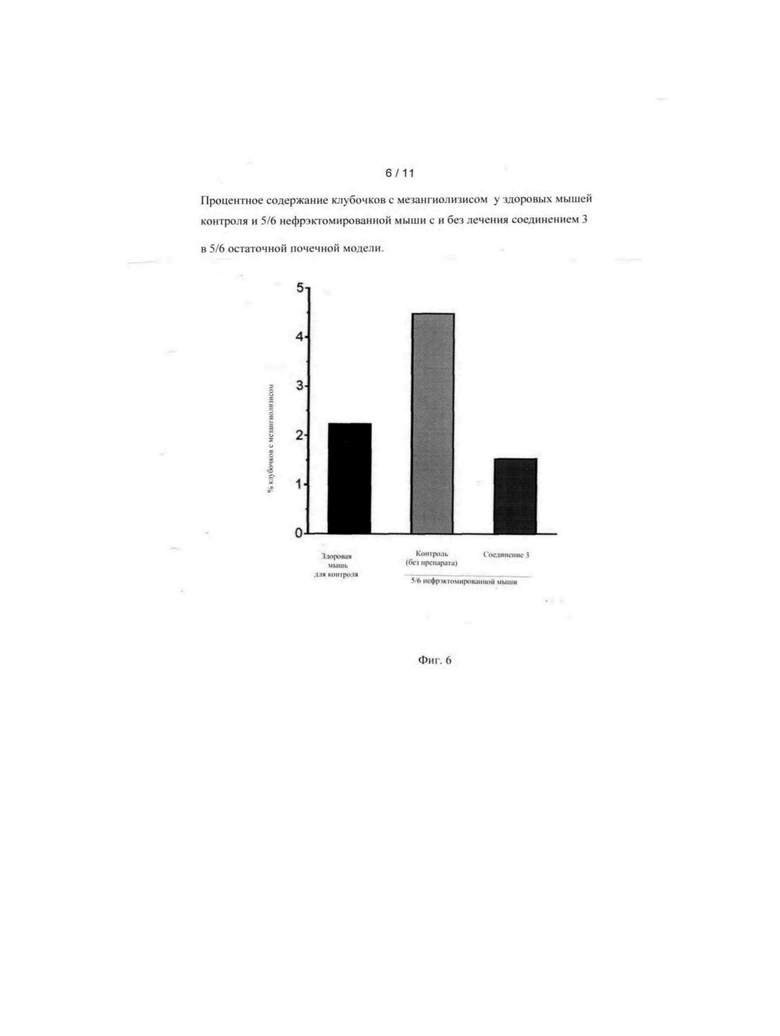
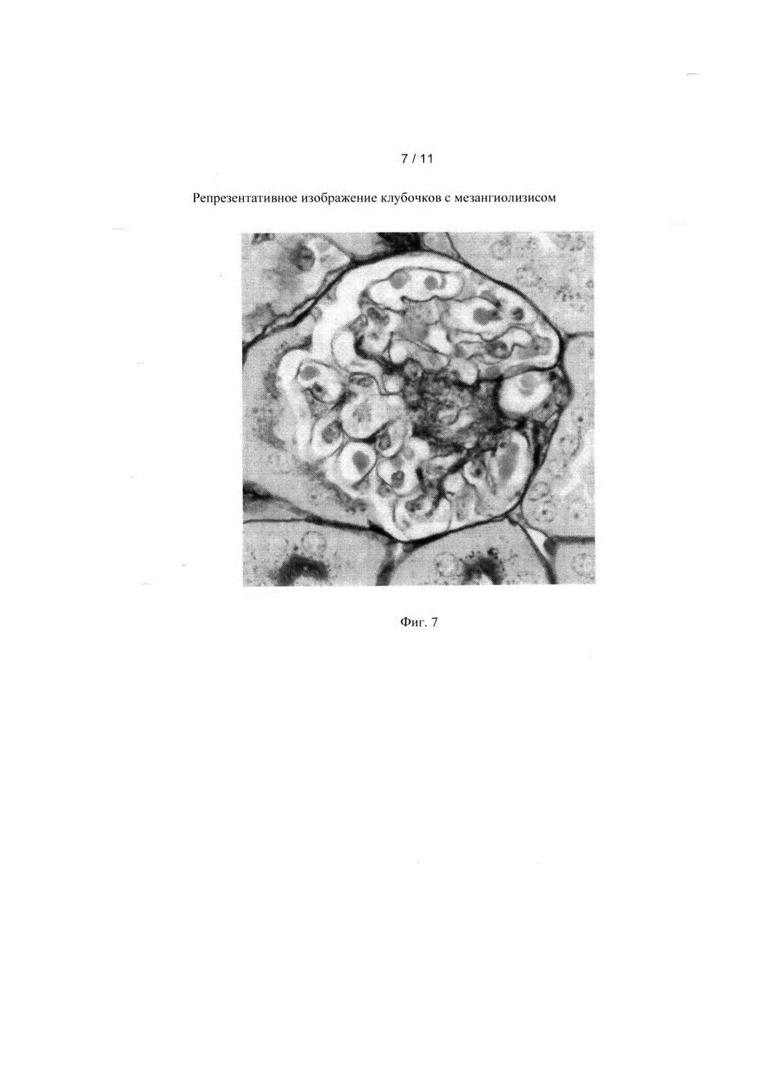

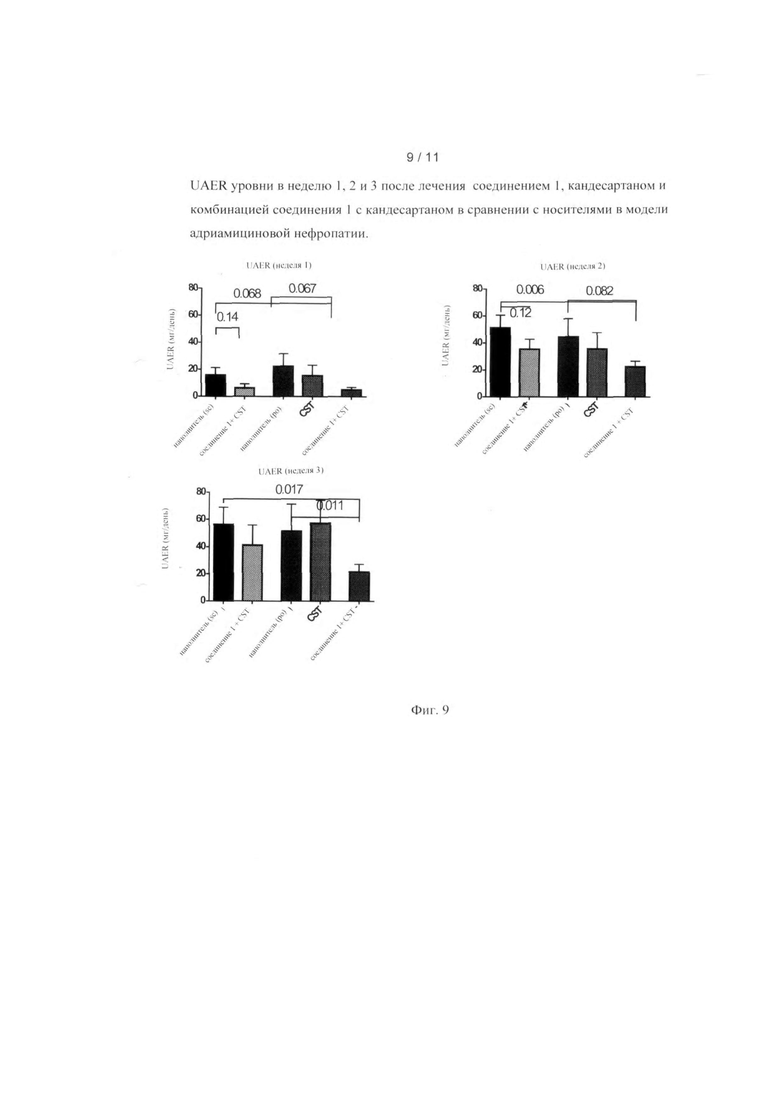
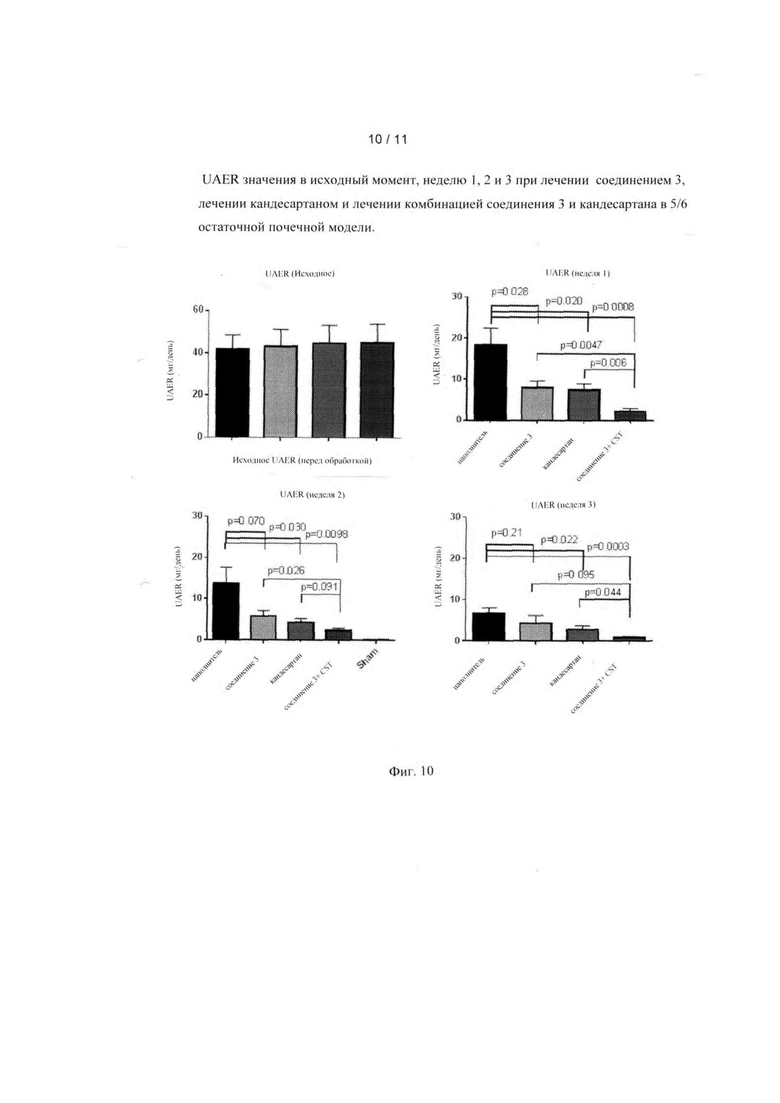

Изобретение относится к способу лечения первичного фокально-сегментарного гломерулосклероза (FSGS) у нуждающегося в этом пациента, включающему назначение пациенту эффективного количества соединения Формулы I или его фармацевтически приемлемой соли. В общей Формуле I R1 является галогеном; R2 является C1-6 галоалкилом; R3 является галогеном или C1-6 алкилом; R4 является водородом; каждый R5 независимо является C1-6 алкилом, -OH или -NH2; n - это 0; и
каждый из A1 и A2 есть -CH- ; и A3 является -N-.
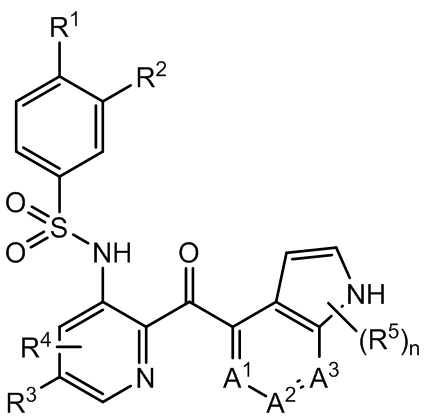 Формула I
Формула I
14 з.п. ф-лы, 11 ил., 3 пр.
1. Способ лечения первичного фокально-сегментарного гломерулосклероза (FSGS) у нуждающегося в этом пациента, включающий назначение пациенту эффективного количества соединения Формулы I
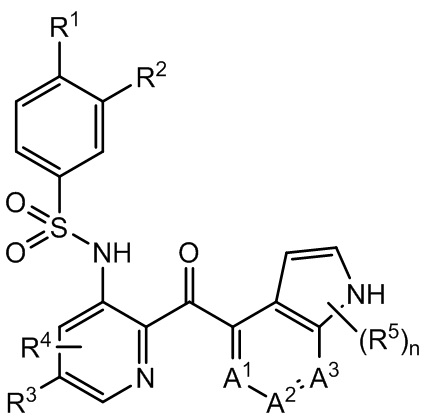 Формула I
Формула I
или фармацевтически приемлемой его соли,
где R1 является галогеном;
R2 является C1-6 галоалкилом;
R3 является галогеном или C1-6 алкилом;
R4 является водородом;
каждый R5 независимо является C1-6 алкилом, -OH или -NH2;
n - это 0; и
каждый из A1 и A2 есть -CH-;
и A3 является -N-.
2. Способ по п. 1, в котором соединение - это:
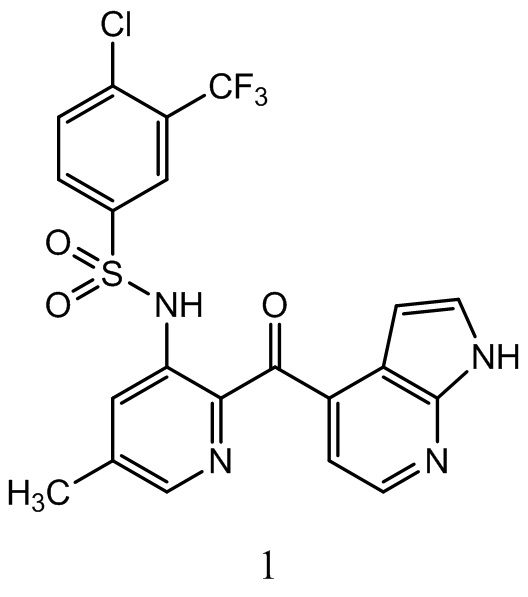
или фармацевтически приемлемая его соль.
3. Способ по п. 1, в котором соединение - это
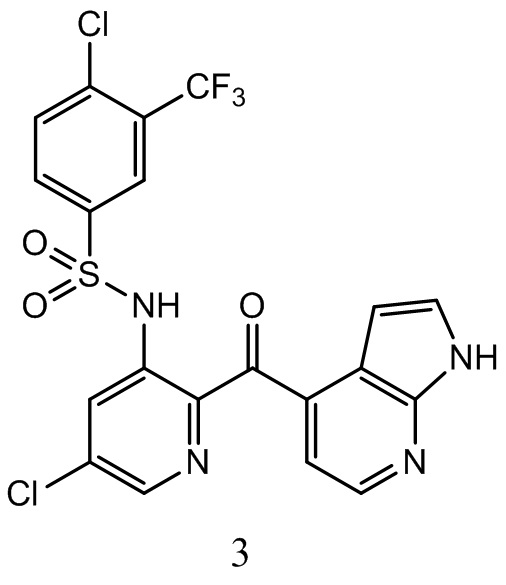
или фармацевтически приемлемая его соль.
4. Способ по любому из пп. 1-3, в котором способ лечения первичного FSGS включает предотвращение, сокращение или устранение симптома или осложнения первичного FSGS.
5. Способ по любому из пп. 1-4, в котором способ лечения FSGS включает предотвращение, устранение или задержку начала терминальной стадии почечного заболевания у пациента.
6. Способ по любому из пп. 1-5, в котором способ включает одно или более из: уменьшения протеинурии, замедления увеличения протеинурии, сокращения UACR, замедления увеличения отношения креатинина к альбумину мочи (UACR), уменьшение UAER, замедления увеличения UAER, сокращения альбуминурии, замедления увеличения альбуминурии, повышения плотности подоцитов клубочков, предотвращения или замедления утолщения базисной мембраны клубочков (GBM), уменьшения области клубочков, сокращения количества почечных интерстициальных макрофагов, уменьшения или замедления фиброза почечных тканей, остановки или уменьшения воспаления почек, остановки или уменьшения вызванного макрофагами повреждения почек, увеличения или нормализации предполагаемой скорости фильтрации клубочков (eGFR), уменьшения снижения eGFR, сокращения гломерулосклероза, остановки или уменьшения расширения внеклеточного матрикса клубочков, остановки или уменьшения смещения гиалиновых масс, остановки или сокращения эпителиальных гиперплазийных повреждений клубочков (EPHLs) и остановки или уменьшения инфильтрации лимфоцитов.
7. Способ по любому из пп. 1-6, в котором соединение или фармацевтически приемлемая его соль вводится перорально.
8. Способ по любому из пп. 1-7, в котором соединение или фармацевтически приемлемая его соль назначается дважды в день.
9. Способ по любому из пп. 1-8, в котором соединение или фармацевтически приемлемая его соль назначается один раз в день.
10. Способ по п. 1, дополнительно включающий введение пациенту одного или нескольких дополнительных терапевтических соединений, при этом одно или более дополнительных терапевтических соединений выбирают из группы, состоящей из рамиприла, периндоприла, лизиноприла, аргинина периндоприла, каптоприла, спираприла, хинаприла, эналаприла, имидаприла, фозиноприла, зофеноприла, беназеприла, трандолаприла, верапамила, беназеприла, амлодипина, трандолаприла, P-003, цилазаприла, делаприла, моексиприла, фозиноприла, темокаприла, лозартана, кандесартана, ирбесартана, телмисартана, олмесартана, валсартана, азилсартана, телмисартана, фимасартана, EMA 401, калия азилсартана медоксомила, спарсентана, кандесартан целиксетила, олмесартана медоксомила, TRV-027, калия лозартана, YH-22189, азилсартана триметилэтаноламина, аллисартана изопропоксила и эпросартана.
11. Способ по п. 1, дополнительно включающий введение пациенту одного или нескольких дополнительных терапевтических соединений, при этом одно или более дополнительных терапевтических соединений выбирают из группы, состоящей из ритуксимаба, дапаглифлозина, спарсентана, абатасепта, DMX-200, пропагерманиума, ирбесартана, лозмапимода, X-M74, Актар Геля, VAR 200, циленгитида, памревлумаба, DEX-M74, фрезолимумаба и SHP-627.
12. Способ по п. 1, дополнительно включающий введение пациенту одного или нескольких дополнительных терапевтических соединений, при этом одно или более дополнительных терапевтических соединений выбирают из группы, состоящей из INT 767, белимумаба, цинакальцета, ритуксимаба, лозартана, абатасепта, кандесартана, селонсертиба, мио-инозит гексафосфата, PBI-4050, OMS-721, фостаматиниба, ирбесартана, цанаглифлозина, метоксильной бета полиэтиленгликоля-эпоэтина, мофетила микофенолата, ALN-CC5, обинутузумаба, ренамезина, палбоциклиба, бозентана, DM 199, будесонида, амифампридина, амифампридина фосфат, дабрафениба, дапаглифлозина, дапаглифлозина пропандиола, кортикотропин, TNT-009, дефибротида, финернона, барицитиниба, тикагрелора, амбризентана, экудизумаба, пегвисоманта, эпалрестата, камостата мезилата, октреотида, октреотида ацетата, GKT-831, уларитида, бардоксолона, бардоксолона метила, толваптана, олмесартана медоксомила, такролимуса, MT 3995, ирбесартана + пропагерманиума, атацисепта, ифетробана, ифетробана натрия, афатиниба, атрасентана, TAK-272, AST 120, фимасартана, GR-MD-02, CS-3150, пирфенидона, омекамтива мекарбила, омекамтива, беклометазон, беклометазон дипропоината, apaбеталона, спарсентана, ХронСила, азелирагона, памревлумаба, атезидозена, габапентина энакарбила, габапентина, имидаприла, цендиритида, BMP-7, GLY-230, рекомбинантного эритропоэтин стимулирующего белка, 2 MD, терлипрессина, дихлоргидрата пиридоксамина, пиридоксамина, DEX-M74, GSK-2586881, SER-150-DN, клазосетана, блисибимода, AKB-9778, эптотермина альфа, беназеприла, эмрикасана, эпопростенола, DW-1029M, бендазак лизина, селициклиба, BPS-804, авакопана, ALLO-ASC-DFU, SM 101, плозализумаба, берапроста натрия, берапроста, лозмапимода, PEG-bHb-CO, рекомбинантнной человеческой щелочной фосфотазы, CXA-10, SAR 407899, BI 655088, BOT 191, сулодексида, вонапанитаза, соматропина, топироксостата, SB 030, SHP-627, KBP 5074, EA 230, эмаптикап пегола, фенилбутирата натрия, BB-3, Хемалба, тирилазада, ASP -8232, VPI-2690B, октреотида ацетата, EPO-018B, торасемида, рейна, PHN- 033, эпросартана, KP-100IT, NCTX, ERC-124, сапроптерина, парнапарина натрия, парнапарина, фенолдопама и витамина D.
13. Способ по любому из пп. 1-12, в котором пациент также подвергается экстракорпоральной очистке крови, аллогенной трансплантации и/или терапии стволовыми клетками.
14. Способ по любому из пп. 10-12, в котором одно или более дополнительных терапевтических соединений назначают одновременно или последовательно.
15. Способ по любому из пп. 10-12, в котором одно или более дополнительных терапевтических соединений назначают как единую фармацевтическую композицию вместе с соединением формулы I или как отдельную фармацевтическую композицию.
| WO 2012041817 A1, 05.04.2012 | |||
| WO 2015062743 A1, 07.05.2015 | |||
| US 20110118248 A1, 19.05.2011 | |||
| WO 2009009740 A1, 15.01.2009 | |||
| RU 2012141607 A, 10.04.2014. |
Авторы
Даты
2022-02-02—Публикация
2017-11-22—Подача