Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции для применения в лечении больного ФКУ. Далее, изобретение относится к питательной композиции, содержащей белок, липид и углеводы, где указанная композиция обеспечивает по меньшей мере все незаменимые аминокислоты, иные, чем фенилаланин.
Уровень техники
Генетическая мутация, характерная для фенилкетонурии (ФКУ), нарушает надлежащее функционирование фермента фенилаланингидроксилазы (ФАГ), которая в норме превращает фенилаланин (Фен) в тирозин (Тир). Мутация приводит к накоплению фенилаланина в крови и головном мозге до токсических уровней. Кроме того, поскольку тирозин является предшественником нейромедиаторов дофамина и норадреналина, снижение синтеза тирозина нарушает биосинтез этих катехоламинов. Параллельно фенилаланин конкурирует с тирозином и триптофаном (Трп, предшественник серотонина) на переносчиках аминокислот через гематоэнцефалический барьер (ГЭБ), и в результате высокая концентрация фенилаланина в крови также приводит к снижению поступления в головной мозг тирозина и триптофана, дополнительно влияя на их доступность для нейромедиаторов и биосинтез белка в нейронах.
Доступность дофамина и серотонина является критической, поскольку эти нейромедиаторы вовлечены в различные функции, в частности, в функции префронтального кортекса (ПФК), который является главным участком высших когнитивных функций. В ПКФ пациентов, соблюдающих диету и имеющих концентрации фенилаланина в плазме, сниженные до рекомендуемых уровней, метаболизм и дофамина, и серотонина, как предполагают, является дефицитным, поскольку анализ цереброспинальной жидкости показывает снижение уровней метаболитов этих нейромедиаторов. Параллельно, исследования у детей с ФКУ с ранним и непрерывным лечением показали дефицит исполнительного функционирования, включая оперативную обработку, скорость обработки, решение проблем, невербальное интеллектуальное развитие, рабочую память и гибкость внимания.
Ключевой чертой патофизиологии ФКУ являются повышенные уровни фенилаланина в крови. Современное лечение ФКУ в Нидерландах характеризуется контролем этих уровней между 120 мкмоль/л и 360 мкмоль/л для детей (0-12 лет) и от 120 мкмоль/л до 600 мкмоль/л после 12 лет. При отсутствии лечения уровни фенилаланина могут повышаться от 1000 до 2000 мкмоль/л. Поскольку пациентам часто трудно поддерживать диету, уровни могут находиться где-либо между ранее упомянутыми уровнями.
Современное диетическое лечение ФКУ фокусируется на снижении потребления фенилаланина в рационе. Такой рацион должен приниматься в течение всей жизни, но особенно важен в детстве и подростковом возрасте. Многие исследования показали, что полное удаление фенилаланина из рациона едва ли возможно. Пациенты всегда будут желать употреблять что-либо еще, помимо современных медицинских продуктов питания на основе аминокислот в качестве источника белка. С учетом того, что уровни фенилаланина в крови почти всегда превышают рекомендуемые, необходим продукт, который способен снизить уровни фенилаланина в крови больных ФКУ, что позволит решить реальную проблему диетического контроля у больных ФКУ.
Объектом настоящего изобретения является обеспечение композиции для применения в лечении больного ФКУ, где композиция включает комбинацию двух или более активных ингредиентов, где комбинация ингредиентов является эффективной для снижения или нормализации уровня фенилаланина в крови пациента, или эффективной в сохранении уровня фенилаланина в крови в пределах непатологического диапазона, также когда рацион больного ФКУ содержит значительное количество фенилаланина.
Другим объектом настоящего изобретения является обеспечение усовершенствованного диетического продукта, который можно применять для снижения уровня фенилаланина в крови.
Раскрытие изобретения
Авторы изобретения неожиданно установили, что композиция, содержащая ω-3 жирную кислоту, выбранную из группы, состоящей из ДГК, ДПК и ЭПК, и пиримидиновое производное, выбранное из группы, состоящей из источников уридина и источников цитидина, в частности, ДГК и УМФ, способна снижать концентрацию фенилаланина в крови. Это наблюдение было полностью неожиданным результатом исследования научно обоснованной мышиной модели ФКУ. Этих ФКУ мышей (C57/Bl6enu2), получавших рацион на основе ДГК и УМФ с добавлением разных уровней аминокислоты фенилаланина или контрольный рацион без ДГК и УМФ, сравнивали с мышами дикого типа (WT), получавшими контрольный рацион. Диетическое лечение начинали на 31 после рождения, и продолжали три месяца. Было неожиданно установлено, что ФКУ мыши, получавшие рацион с ДГК и УМФ, имели более низкие уровни фенилаланина в крови, чем ФКУ мыши, получавшие контрольный рацион (см. фигуру 1).
Соответственно, настоящее изобретение относится к композиции, содержащей: (i) одну или несколько ω-3 жирных кислот. выбранных из группы, состоящей из ДГК, ДПК и ЭПК; и (ii) одно или несколько пиримидиновых производных, выбранных из группы, состоящей из источников уридина и источников цитидина, для применения с целью снижения или нормализации уровня фенилаланина в крови больного ФКУ, или для применения в диетическом контроле уровня фенилаланина в крови больного ФКУ.
Одна или несколько ω-3 жирных кислот, выбранных из группы, состоящей из ДГК, ДПК и ЭПК, и/или одно или несколько пиримидиновых производных, выбранных из группы, состоящей из источников уридина и источников цитидина, как правило, присутствуют в композиции для применения в качестве активных ингредиентов в соответствии с изобретением. Композиция может содержать один или несколько дополнительных ингредиентов, которые могут оказывать благоприятный эффект по отношению к назначенному применению изобретения, в частности, витамин В, донор метила (такой, как холин), фосфолипид или антиоксидант (такой, как витамин С, селен, витамин Е).
Композиция может быть фармацевтической композицией, содержащей указанный активный ингредиент(ы) для применения в соответствии с изобретением, и один или несколько фармацевтически пригодных вспомогательных веществ. Предпочтительно, активный ингредиент(ы) для применения в соответствии с изобретением применяют в качестве части композиции, или в комбинации с питательной композицией.
Соответственно, изобретение также относится к питательной композиции, содержащей белок, липид и углевод, где белок обеспечивает по меньшей мере все незаменимые аминокислоты, иные, чем фенилаланин, и при необходимости фенилаланин, который, в случае наличия, присутствует в концентрации фенилаланина 0-10 мг на грамм белка; липид, включающий одну или несколько ω-3 жирных кислот, выбранных из ДГК, ДПК и ЭПК в общей концентрации по меньшей мере 0,05 масс.%, на основе общего содержания липидов; и одно или несколько производных пиримидина, выбранных из источников уридина и источников цитидина. Одно или несколько производных пиримидина, выбранных из источников уридина и источников цитидина, как правило, присутствуют в общей концентрации по меньшей мере 1 мкмоль/100 ккал питательной композиции. Такая питательная композиция особенно пригодна для применения в соответствии с настоящим изобретением.
Осуществление изобретения
Изобретение относится к композициям, содержащим одну или несколько ω-3 жирных кислот, уридин или цитидин или их эквиваленты, и к их применению с целью снижения или нормализации уровней фенилаланина в крови больных ФКУ.
Термин «или», как применяется в настоящей заявке, означает также «и», если не указано иное, или из контекста не следует противоположное. Таким образом, «вариант А или В» означает любой из вариантов А, В, и А и В.
Термины единственного числа, как применяется в настоящей заявке, означают «по меньшей мере один», если не указано противоположное.
Когда речь идет о существительном (например, соединении, добавке и т.д.) в единственном числе, подразумевается включение множественного числа, если не указано иное.
Когда упоминается кислота, например, жирная кислота, аминокислота, или фолиевая кислота, этот термин означает включение конъюгированных оснований указанной кислоты (например, фолата), солей кислот и производных кислоты, которые организм способен превратить в кислоту (например, жирнокислотных сложных эфиров, таких как триглицериды), если не указано иное.
С целью ясности и краткости описания, характеристики описаны в настоящей заявке как часть одного и того же или отдельных вариантов осуществления; однако, необходимо понять, что объем изобретения может включать варианты осуществления, имеющие комбинации из всех или некоторых из описанных характеристик.
Белок
Термин «белок» определяет любое соединение, состоящее из одной или нескольких аминокислот; термин, в частности, включает свободные аминокислоты, их соли, пептиды, гидролизованные белки и интактный белок.
Больные ФКУ должны уменьшить потребление фенилаланина (Фен) для сохранения уровней фенилаланина в крови и головном мозге в пределах нормального диапазона, по сравнению с людьми, не страдающими ФКУ. Таким образом, в предпочтительном варианте осуществления композиция (для применения) в соответствии с изобретением по существу не содержит фенилаланина, или имеет относительно низкий уровень фенилаланина. Таким образом, композиция предпочтительно содержит 0-10 мг фенилаланина на грамм белка, в частности, 0-1 мг фенилаланина на грамм белка, предпочтительно 0-0,1 мг фенилаланина на грамм белка.
Низкий уровень, как правило, означает, что содержание фенилаланина является более низким, чем в сопоставимой (питательной) композиции, такой как (питательный) продукт того же типа, не предназначенный для применения у больных ФКУ.
В предпочтительном варианте осуществления композиция (для применения) в соответствии с изобретением включает казеино-глико-макропептид (кГМП). Предпочтительно, комплементарные незаменимые аминокислоты, иные, чем фенилаланин, добавляют в качестве источника белка, в дополнение к источнику кГМП белка, для компенсации аминокислот, которые присутствуют в низких количествах в ГМП белке. Преимуществом применения кГМП в качестве источника белка для питательных продуктов является то, что кГМП имеет лучший вкус, низкую осмолярность и сбалансированный аминокислотный профиль, чем свободные аминокислоты. Далее, кГМП не содержит фенилаланина или имеет низкое содержание фенилаланина (например, аминокислотная последовательность коровьего кГМП не содержит фенилаланиновых единиц, однако коммерческий кГМП, полученный из молока, может содержать следы фенилаланина из других белковых компонентов молока). Это делает данный белок идеально пригодным для применения в рационе больных ФКУ. Источник белка предпочтительно содержит примерно от 30 масс.% до 70 масс.% казеино-глико-макропептида и примерно от 70 масс.% до 30 масс.% комплементарных свободных аминокислот.
Предпочтительно, композиция (для применения) в соответствии с изобретением обеспечивает избыток тирозина для компенсации неспособности больных ФКУ к превращению фенилаланина в тирозин. Предпочтительно, содержание тирозина в композиции (для применения) в соответствии с изобретением составляет 7-15 масс.% от общего содержания аминокислот, еще более предпочтительно 8-13 масс.%, и еще более предпочтительно 9-12 масс.% от общего содержания аминокислот.
Предпочтительно, источник белка обеспечивает примерно от 7% до 80%, более предпочтительно 7-20%, наиболее предпочтительно 7-13% от сухой массы композиции (для применения) в соответствии с изобретением. В предпочтительном варианте осуществления, пригодном для применения в детской смеси, источник белка обеспечивает примерно от 7% до 13% энергии композиции (для применения) в соответствии с изобретением. Проценты энергии можно определить на основе общеизвестного вклада ингредиентов композиции в калорийную ценность; для белка и перевариваемого углевода калорийная ценность, как правило, составляет 4 ккал/грамм, для липидов - 9 ккал/грамм.
Предпочтительно, питательная композиция (для применения) в соответствии с изобретением содержит все незаменимые аминокислоты, иные, чем фенилаланин, т.е. валин, треонин, триптофан, метионин, лейцин, изолейцин, лизин и гистидин. В другом варианте осуществления питательная композиция содержит все незаменимые аминокислоты, включая фенилаланин.
Подходящий аминокислотный профиль для специфического типа питательной композиции известен в данной области техники, и может применяться на основе известных питательных композиций для больных ФКУ, например, PKU Anamix Junior, PKU Lophlex Advance или PKU Anamix infant (все поставляются Nutricia Advanced Medical Nutrition).
Далее, питательная композиция (для применения) в соответствии с изобретением, может, например, быть основана на любой из композиций, пригодных для больных ФКУ, описанных в WO 2011/078677, содержание которого в отношении этих композиций включено посредством ссылки, в частности, в таблицах 2 и 3, с тем условием, что композиция (для применения) в соответствии с настоящим изобретением может содержать фенилаланин, и содержит пиримидиновое производное (производные) и указанную ω-3 жирную кислоту(ы).
Далее, питательная композиция может быть, например, основана на любой из композиций, пригодных для больных ФКУ, описанных в WO 2013/133711, содержание которого в отношении этих композиций включено посредством ссылки, в частности, в таблицах 1, 2А и 2В, с тем условием, что композиция (для применения) в соответствии с настоящим изобретением может содержать фенилаланин, и содержит пиримидиновое производное (производные) и указанную ω-3 жирную кислоту(ы).
Далее, питательная композиция может быть, например, основана на любой из композиций, пригодных для больных ФКУ, описанных в WO 2015/002537, содержание которого в отношении этих композиций включено посредством ссылки, в частности, композиции из Примеров 1-10, с тем условием, что композиция (для применения) в соответствии с настоящим изобретением может не содержать фенилаланин, или может содержать фенилаланин в более низком количестве (предпочтительно, меньше 10 мг/г белка), и содержит пиримидиновое производное (производные) и указанную ω-3 жирную кислоту(ы).
Далее, Nestlé [Engl] 2010; 68:58–69, таблица 2, содержание которой включено посредством ссылки, обеспечивает указания по суточному потреблению белка, энергии и фенилаланина для индивидуумов с ФКУ.
В частности, питательная композиция (для применения) в соответствии с настоящим изобретение включает одну или несколько аминокислот, предпочтительно, по меньшей мере незаменимые аминокислоты, иные, чем фенилаланин, более предпочтительно, все аминокислоты в относительном количестве, указанном в таблице 1.
Таблица 1
Липиды
Термин «липиды» включает любое съедобное жирное вещество, в целом считающееся жиром или маслом в продуктах питания, включая триглицериды, жирные кислоты и фосфолипиды.
Общее количество липидов предпочтительно составляет от 10 до 30 масс.% на основе сухого вещества, и/или от 2 до 6 г липида на 100 мл жидкой композиции.
Длинноцепочечная полиненасыщенная жирная кислота (ДЦП)
ДЦП в композиции (для применения) в соответствии с изобретением включает по меньшей мере одну ДЦП, выбранную из докозагексаеновой кислоты (22:6 ω-3; ДГК), докозапентаеновой кислоты (22:5 ω 3; ДПК) и эйкозапентаеновой кислоты (20:5 ω-3; ЭПК).
Предпочтительно, настоящая композиция содержит по меньшей мере ДГК.
Предпочтительно, композиция содержит ДГК и по меньшей мере один предшественник ДГК, выбранный из ЭПК и ДПК, более предпочтительно ДГК и ЭПК. Более предпочтительно, настоящая композиция включает ДГК, ДПК и ЭПК.
ДЦП предпочтительно обеспечивается как одно или несколько соединений, выбранных из группы из триглицеридов, диглицеридов, моноглицеридов, свободных жирных кислот, солей жирных кислот, сложных эфиров жирных кислот (иных, чем глицериды), фосфолипидов, лизофосфолипидов, эфиров глицерина, липопротеинов, церамидов, гликолипидов. Предпочтительно, настоящая композиция включает ДГК в форме триглицерида.
Композицию предпочтительно применяют для обеспечения (в целом) 400-5000 мг ω-3 жирной кислоты (кислот), выбранной из ДГК, ЭПК и ДПК в сутки, более предпочтительно 500-3000 мг в сутки, наиболее предпочтительно 1000-2500 мг в сутки. Настоящее применение предпочтительно включает применение ДГК, предпочтительно в количестве 300-4000 мг в сутки, более предпочтительно 500-2500 мг в сутки.
Количество в сутки, как описано в настоящей заявке, означает количество в ежедневной дозе, обеспеченное композицией из изобретения. Такая ежедневная доза может быть отдельной дозой, но может также быть разделена на две или три, или еще больше суточных порций.
Настоящая композиция предпочтительно включает 0,1-40 масс.% ДГК на основе общего количества жирных кислот, предпочтительно 0,3-36 масс.% ДГК на основе общего количества жирных кислот, более предпочтительно 1,0-30 масс.% ДГК на основе общего количества жирных кислот. Настоящая композиция предпочтительно содержит 0,05-20 масс.% ЭПК на основе общего количества жирных кислот, предпочтительно 0,2-10 масс.% ЭПК на основе жирных кислот, более предпочтительно 0,5-10 масс.% ЭПК на основе общего количества жирных кислот. Отношение массы ДГК к сумме ЭПК и ДПК (ω-3) предпочтительно составляет больше 1,0, более предпочтительно 1,2-10, более предпочтительно 2-8. Вышеупомянутые отношения и потребляемые количества учитывают и оптимизируют некоторые аспекты, включая вкус (слишком высокие уровни ДЦП снижают вкусовую привлекательность, приводя к снижению соблюдения режима приема), баланс ДГК и её предшественников для обеспечения оптимальной эффективности по отношению к максимальной дозировке и возможности получения композиций продукта, таких как жидкая форма, батончик или капсула.
Массовое отношение ω-6 жирных кислот, имеющих по меньшей мере 20 атомов углерода, к ω-3 жирным кислотам, имеющим по меньшей мере 20 атомов углерода в настоящей композиции предпочтительно составляет ниже 0,5, предпочтительно ниже 0,2. Предпочтительное массовое отношение ω-6 жирных кислот, имеющих по меньшей мере 18 атомов углерода, к ω-3 жирным кислотам, имеющим по меньшей мере 18 атомов углерода, составляет 0,05-1, более предпочтительно 0,1-0,6, наиболее предпочтительно 0,15-0,4.
Настоящая композиция предпочтительно содержит по меньшей мере одно масло, выбранное из жира морских организмов и яичных липидов. Жир морских организмов предпочтительно выбран из рыбьего жира и масла водорослей. Предпочтительно, настоящая композиция содержит рыбий жир, включающий ДГК, ЭПК, и предпочтительно также ДПК.
Насыщенные и мононенасыщенные жирные кислоты
Настоящая композиция предпочтительно содержит насыщенные и/или мононенасыщенные жирные кислоты. Количество насыщенных жирных кислот предпочтительно составляет 6-60 масс.%. на основе общего количества жирных кислот, предпочтительно 12-40 масс.%, более предпочтительно 20-40 масс.% на основе общего количества жирных кислот. В частности, количество С14:0 (миристиновой кислоты) + С16:0 (пальмитиновой кислоты) предпочтительно составляет 5-50 масс.%, предпочтительно 8-36, более предпочтительно 15-30 масс.% на основе общего количества жирных кислот. Общее количество мононенасыщенных жирных кислот, таких как олеиновая кислота и пальмитолеиновая кислота, предпочтительно составляет от 5 до 40 масс.%, более предпочтительно от 15 до 30 масс.%. Включение насыщенных и/или мононенасыщенных жирных кислот обеспечивает источник энергии, способствующий активности у продромальных субъектов.
Фосфолипиды
Фосфолипиды являются источником холина и могут предотвращать снижение уровней холина в плазме после физической нагрузки. Холин является необходимым для образования ацетилхолина, нейромедиатора, вовлеченного в обучение и память и в активацию мышц. Эти преимущества уже достигаются при относительно низких уровнях фосфолипидов. Таким образом, в дополнение к холину, композиция в соответствии с изобретением может включать один или несколько фосфолипидов.
Предпочтительно, настоящая композиция включает один или несколько фосфолипидов, предпочтительно 0,1-50 масс.% фосфолипидов на основе общей массы липидов, более предпочтительно 0,5-20 масс.%, более предпочтительно от 1 до 5 масс.% на основе общей массы липидов.
В случае применения суточная дозировка общих фосфолипидов обычно находится в диапазоне от 50 до 5000 мг, в частности, в диапазоне от 100 до 2000 мг, более предпочтительно в диапазоне от 150 до 1200 мг.
Как применяется в настоящей заявке, термин «фосфолипиды» включает лизофосфолипиды, деацилированные фосфолипиды и глицерофосфолипиды. В частности, фосфолипид выбран из группы из фосфатидилхолина (ФХ), фосфатидилэтаноламина (ФЭ), фосфатидилсерина (ФС), фосфатидиновой кислоты (фосфатидата), фосфоинозитидов (таких, как фосфатидилинозитол (ФИ), фосфатидилинозитол фосфат, фосфатидилинозитол дифосфат, фосфатидилинозитол трифосфат) и сфингомиелина. В специфическом варианте осуществления композиция включает по меньшей мере два различных фосфолипида, выбранных из группы, состоящей из фосфатидилсерина, фосфатидилинозитола, фосфатидилхолина и фосфатидилэтаноламина. Лецитин, например, соевый лецитин, является коммерческим источником фосфолипидов. Молочный жир можно также применять в качестве источника фосфолипидов, например, в форме фосфолипидных концентратов.
Пиримидиновое производное
Композиция (для применения) в соответствии с изобретением включает пиримидиновое производное, выбранное из группы из источников уридина и источников цитидина. Эти источники могут быть обеспечены любым соединением, предоставляющим уридиновый эквивалент, соответственно, цитидиновый эквивалент, при применении в организме человека. Термин «нуклеозидный эквивалент» (для нуклеозидов в целом), соответственно, уридиновый эквивалент или цитидиновый эквивалент (для этих специфических нуклеозидов) обычно применяется в данной области техники для соединений, включающий нуклеиновое основание, такое как нуклеиновое основание как таковое, нуклеозиды, мононуклеотиды (моно-, ди- или трифосфаты нуклеозидов), олигонуклеотиды, полинуклеотиды и их физиологически пригодные производные, которые могут быть превращены в нуклеозид как таковой, или нуклеотид как таковой in vivo.
Примеры таких производных включают различные сложные эфиры. Ацильная группа может быть любым физиологически пригодным остатком органической кислоты, в частности, остатком С2-С4 органической кислоты. Предпочтительные ацилированные формы источников пиримидина являются источниками, в которых (дезокси)рибоза ацилирована уксусной кислотой, n-капроевой кислотой, каприловой кислотой, или n-каприновой кислотой, поскольку это повышает биодоступность источника уридина или цитидина. Способы проведения реакции этих жирных кислот со средней цепью с нуклеозидами, например, в 5' положении нуклеозидов, известны в данной области техники как таковые, и включают обычные способы ацилирования. В другом варианте осуществления источник уридина ацилирован с ПНЖК, например, омега-3 ПНЖК. WO 2002/088159 относится к сложным эфирам уридина, которые можно применять в соответствии с настоящим изобретением. Содержание этой публикации, касающееся сложных эфиров (дезокси)уридина, включено посредством ссылки. Кроме того, (другие) синтетические соединения могут подходящим образом быть включены в качестве источника нуклеозидов, например, ацилированных производных нуклеозидов, например, триацетил-уридина.
Такие эквиваленты способны к повышению эндогенных уровней активных форм нуклеозидов в организме, в тканях, таких как кровь, печень и головной мозг. Пригодные ингредиенты включают экстракты из растительного, животного, бактериального, водорослевого или дрожжевого материала, а также синтетические соединения.
Настоящая композиция предпочтительно включает уридин и/или его эквивалент, предпочтительно по меньшей мере один уридин или его эквивалент, выбранный из группы, состоящей из уридина (т.е. рибозил-урацила), дезоксиуридина (дезоксирибозил-урацила), уридин-фосфатов (УМФ, дУМФ, УДФ, дУДФ, УТФ, дУТФ), нуклеотидного урацила, где при необходимости один или несколько гидроксильных компонентов (дезокси)рибозы из указанного нуклеотида ацилированы.
Подходящие источники цитидина, в частности, включают цитидин, дезоксицитидин и дериватизированные (дезокси)цитидины. Дериватизированные (дезокси)цитидины предпочтительно выбраны из группы из ЦМФ, ЦДФ, ЦТФ, дЦМФ, дЦДФ и дЦТФ, где при необходимости один или несколько гидроксильных компонентов (дезокси)рибозы из указанного нуклеотида ацилированы.
Предпочтительно, настоящая композиция включает уридина фосфат, выбранный из уридина монофосфата (УМФ), уридина дифосфата (УДФ) и уридина трифосфата (УТФ). Наиболее предпочтительно, настоящая композиция включает УМФ, поскольку УМФ наиболее эффективно усваивается организмом. Таким образом, включение УМФ в настоящем продукте обеспечивает наиболее эффективное применение наименьшей дозировки и/или низкого объема у субъекта. Предпочтительно, по меньшей мере 50 масс.% уридина в настоящей композиции обеспечивается посредством УМФ, более предпочтительно по меньшей мере 75 масс.%, наиболее предпочтительно по меньшей мере 95 масс.%. Настоящая композиция предпочтительно используется в способе, включающем применение производного пиримидина (совокупного количества источников уридина и источников цитидина) в количестве 0,08-3 г в сутки, предпочтительно 0,1-2 г в сутки, более предпочтительно 0,2-1 в сутки.
Использование композиции предпочтительно включает применение композиции, обеспечивающей источник уридина в концентрации 0,4 мг - 3000 мг, рассчитанной по УМФ, на 100 ккал, предпочтительно 0,6 мг-2000 мг, рассчитанной по УМФ, на 100 ккал продукта, более предпочтительно 1 мг - 1000 мг, рассчитанной по УМФ, на 100 ккал продукта.
Предпочтительно 1-37,5 мг уридинового эквивалента при расчете по УМФ на килограмм массы тела применяют в сутки. Необходимые дозировки эквивалентов на массовой основе могут быть рассчитаны по дозе УМФ путем приема эквимолярных количеств с применением молекулярной массы эквивалента и УМФ, последняя составляет 324 Дальтон.
Если источник(и) цитидина присутствует, то его содержание обычно составляет от 0,4 до 3000 мг, при расчете по цитидина монофосфату, на 100 ккал композиции.
Производные пиримидина, выбранные из источников уридина и источников цитидина, предпочтительно присутствуют в композиции в соответствии с изобретением в количестве, обеспечивающем в целом по меньшей мере 1,2 мкмоль/100 ккал композиции, более предпочтительно 1,2 мкмоль/100 ккал-9,26 ммоль/100 ккал композиции, более предпочтительно 1,8 мкмоль/100 ккал - 6,173 ммоль/100 ккал, более предпочтительно 3 мкмоль/100 ккал - 3,1 ммоль/100 ккал единиц указанного пиримидинового производного(ых) (уридина/цитидина).
Хотя цитидин является предшественником уридина, более выгодно и эффективно включать один или несколько уридиновых эквивалентов в настоящей композиции. Соответственно, предпочтительно 60-100 масс.%, в частности, 90-100% содержания пиримидинового производного образовано одним или несколькими источниками уридина.
Доноры метила
Из-за обедненного белками рациона больных ФКУ имеется возможность снижения потребления доноров метила, которые часто присутствуют, например, в мясных, рыбных и молочных продуктах, которые не могут употребляться в достаточных количествах больными ФКУ. Таким образом, настоящая композиция предпочтительно содержит значительные количества доноров метила.
Доноры метила являются соединениями пищевого качества, которые способны обеспечивать метильную, метиленовую или формильную группу при применении у человеческого индивидуума in vivo. Донор метила, включенный в настоящую композицию, предпочтительно выбран из серина, метионина, холина, бетаина, диметилглицина и саркозина, и их производных. Донор метила может быть включен в композицию в виде чистых соединений как таковых, их солей и соединений, где донор метила ковалентно связан с аминокислотами, и которые имеют молекулярную массу меньше 600 Дальтон.
Холин означает различные четвертичные аммонийные соли, содержащие катион N,N,N-триметилэтаноламмония. В частности, холин выбран из группы из катиона холина, холиновых солей или сложных эфиров, таких как холина хлорид, холина битартрат, холина стеарат, или тому подобные, или соединения, которые диссоциируют до холина, такие как холина альфосцерат, сфингомиелин, цитидин-дифосфо-холин или цитиколин или ЦДФ-холин, ацилглицерофосфохолины, например, лецитин, лизолецитин, глицерофосфатидилхолины, и любые их смеси. Предпочтительно, настоящая композиция содержит холиновую соль, в частности, холина хлорид, и/или фосфатидилхолин.
Настоящий способ предпочтительно включает применение более 50 мг холина в сутки, более предпочтительно 80-2000 мг холина в сутки, более предпочтительно 120-1000 мг холина в сутки, наиболее предпочтительно 150-600 мг холина в сутки. Настоящая композиция (для применения) в соответствии с изобретением предпочтительно включает 10-2000 мг холина на 100 ккал, предпочтительно по меньшей мере 10 мг/100 ккал, более предпочтительно по меньшей мере 20, 30, 40, 50, 60, 70, 80, 90, 100 мг/100 ккал. Предпочтительный верхний предел для вышеупомянутого нижнего предела составляет 2000 мг/100 ккал, более предпочтительно 1750, 1500, 1250 или 1000 мг/100 ккал.
Общая суточная доза доноров метила может быть рассчитана с учетом эквимолярных количеств, определенных по холину и скорректированных на молекулярную массу этого донора метила. Общая суточная доза предпочтительно составляет по меньшей мере 0,48 ммоль донора метила в сутки, более предпочтительно по меньшей мере 0,77 ммоль в сутки, более предпочтительно по меньшей мере 1,15 ммоль в сутки, наиболее предпочтительно по меньшей мере 1,22 ммоль в сутки. Общая суточная доза предпочтительно составляет 20 ммоль или меньше, более предпочтительно 10 ммоль или меньше, наиболее предпочтительно 10 ммоль или меньше. В случае, если композиция является жидким продуктом, настоящая композиция предпочтительно содержит 0,48-30 ммоль донора метила на 100 мл, предпочтительно 1,9-10 ммоль метила на 100 мл.
Как показано в примерах 1 и 2, больные ФКУ, вероятно, получают пользу от включения избранных доноров метила.
Витамин В
В одном варианте осуществления композиция (для применения) в соответствии с изобретением включает по меньшей мере один витамин В, выбранный из группы из витамина В6, витамина В9 и витамина В12. Витамин В6 включает пиридоксин, пиридоксаль, пиридоксамин и пиридоксиновые соли, например, гидрохлоридную или фосфатную соль. Витамин В9 также известен как фолиевая кислота или фолат. Витамин В12 также известен как кобаламины.
В частности, хорошие результаты были достигнуты с комбинацией, включающей витамин В6, витамин В12 и витамин В9.
Необходимо отметить, что один или несколько других витаминов из семейства витаминов В могут присутствовать в композиции (для применения) в соответствии с изобретением. Такие другие витамины В включают, в частности, витамин В1 (тиамин), витамин В2 (рибофлавин), витамин В3 (ниацин или ниацинамид), витамин В5 (пантотеновую кислоту), и витамин В7 (биотин).
Витамин В необходимо применять в эффективной дозе, зависящей от типа используемого витамина В. В качестве общего правила, подходящую минимальную или максимальную дозу можно выбрать на основе известных диетических рекомендаций, например, как рекомендовано Институтом медицины (IOM) Национальной Академии наук США, или Научным комитетом по питанию (научным комитетом в ЕС), с информацией, раскрытой в настоящем документе и при необходимости с ограниченным количеством рутинных экспериментов. Минимальная доза может быть основана на ожидаемой средней потребности (ОСП), хотя более низкая доза может уже быть эффективной. Максимальная доза обычно не превышает переносимых верхних уровней потребления (ВУ), как рекомендовано IOM.
Если имеется витамин В6, он обычно присутствует в количестве для обеспечения суточной дозы в диапазоне от 0,5 до 10 мг, в частности, в диапазоне от 0,75 до 5 мг, более конкретно в диапазоне от 0,9 до 2,5 мг. В случае присутствия в композиции в соответствии с изобретением, концентрация витамина В6 обычно составляет 0,05-10 мг витамина В6 на 100 ккал, предпочтительно от 0,1 до 1 мг на 100 ккал. Если витамин В12 присутствует в композиции (для применения) в соответствии с изобретением, его содержание обычно составляет 0,05-5 мкг витамина В12/100 ккал, предпочтительно 0,1-2,5 мкг/100 ккал, и еще более предпочтительно от 0,2 до 2,0 мкг/100 ккал. В случае наличия витамина В9, он обычно присутствует в количестве для обеспечения суточной дозы в диапазоне от 50 до 5000 мкг, в частности, в диапазоне от 150 до 1000 мкг, более конкретно в диапазоне от 200 до 1000 мкг.
(v) Антиоксидант
Композиция в соответствии с настоящим изобретением может включать антиоксидант, выбранный из группы из витамина С, витамина Е и селена. Витамин С может присутствовать в виде свободной кислоты (аскорбиновой кислоты) или в виде соли, например, натрия аскорбата или калия аскорбата. Подходящие источники витамина Е включают (альфа-)токоферол и токотриенол. Подходящие источники селена включают селенат и селенит.
Антиоксидант должен применяться в эффективной дозе. В качестве общего правила, подходящая минимальная или максимальная доза может быть выбрана на основе известных диетических рекомендаций, например, как рекомендовано Институтом медицины (IOM) Национальной Академии наук США, или Научным комитетом по питанию (научным комитетом в ЕС), с информацией, раскрытой в настоящем документе и при необходимости с ограниченным количеством рутинных экспериментов. Минимальная доза может быть основана на ожидаемой средней потребности (ОСП), хотя более низкая доза может уже быть эффективной. Максимальная доза обычно не превышает переносимых верхних уровней потребления (ВУ), как рекомендовано IOM. В случае присутствия в комбинации, витамин С обычно присутствует в количестве для обеспечения суточной дозы в диапазоне от 20 до 1200 мг, в частности, в диапазоне от 30 до 400 мг, более предпочтительно в диапазоне от 35 до 120 мг. В случае наличия в питательной или фармацевтической композиции в соответствии с изобретением, витамин Е обычно присутствует в количестве для обеспечения суточной дозы в диапазоне от 8 до 200 мг, в частности, в диапазоне от 20 до 140 мг, более предпочтительно в диапазоне от 35 до 100 мг.
В случае наличия в питательной или фармацевтической композиции в соответствии с изобретением, селен обычно присутствует в количестве для обеспечения суточной дозы в диапазоне от 40 до 400 мкг, в частности, в диапазоне от 5 до 200 мкг, более конкретно в диапазоне от 55 до 80 мкг.
При необходимости, может присутствовать один или несколько антиоксидантов, иных чем (v) антиоксидант, выбранный из группы из витамина С, витамина Е и селена.
Другие компоненты
Далее, композиция (для применения) в соответствии с изобретением может включать один или несколько других микронутриентов, например, один или несколько микронутриентов, выбранных из группы из (других) витаминов, минералов и микроэлементов, таурина и инозитола. В частности, в предпочтительном варианте осуществления композиция включает витамин А и/или витамин D. Кроме того, композиция может включать пищевое волокно.
Питательная композиция
Композиции в соответствии с заявленным изобретением предпочтительно являются питательными композициями, включающими углевод, липид и белок. Предпочтительно, композиция также содержит витамины, холин, антиоксидант и/или минералы (в частности, как указано выше). Предпочтительно, витамин А и D, которые часто обеспечиваются нормальными источниками белка, такими как молоко или мясо, содержатся в питательной композиции в соответствии с заявленным изобретением. Липид включает полиненасыщенные жирные кислоты, выбранные из группы, состоящей из ЭПК, ДГК и ДПК. Питательная композиция в соответствии с заявленным изобретением дополнительно содержит производное пиримидина, выбранное из источников уридина и источников цитидина, предпочтительно уридин и/или его эквивалент, предпочтительно по меньшей мере один уридин или его эквивалент, выбранный из группы, состоящей из уридина (т.е. рибозил-урацила), дезоксиуридина (дезоксирибозил-урацила), уридина фосфатов (УМФ, дУМФ, УДФ, УТФ), нуклеинового основания урацила и ацилированных производных уридина, наиболее предпочтительно, уридина монофосфата.
В специфическом варианте осуществления питательная композиция обеспечивает полное питание, т.е. питание, обеспечивающее витамины, минералы и пищевую энергию в форме углеводов, белков и жиров в подходящих количествах для обеспечения здорового поступления с пищей. Предпочтительно, полное питание также содержит пищевое волокно и/или пробиотик. Подходящие композиции для полного питания известны в данной области техники, и настоящая питательная композиция может быть основана на Указаниях по продуктам питания для специальных медицинских целей (FSMP, EC, http://eur-lex.europa.eu/legal-content/EN/ALL/?uri=CELEX:31999L0021), с тем условием, что питательная композиция (для применения) в соответствии с изобретением включает одно или несколько указанных производных пиримидина, и одну или несколько из указанных ω-3 жирных кислот.
Лечение больного ФКУ
Композиция (для применения) в соответствии с изобретением, в частности, питательная композиция, является особенно пригодной для лечения больного ФКУ. Её можно применять для снижения уровня фенилаланина в крови пациента, если уровень превышает необходимую концентрацию, или близок к максимальной необходимой концентрации. Таким образом, композицию можно также применять для нормализации концентрации фенилаланина до нормального (не патологического) уровня. Однако изобретение также очень полезно для применения в пищевом контроле (диетическом контроле) уровней фенилаланина в крови больного ФКУ. Целью диетического контроля больных ФКУ является поддержка концентраций фенилаланина в плазме, которые способствуют здоровому росту, развитию и ментальной функции, при обеспечении диетически полного рациона. Erin L. MacLeod и Denise M. NeyAnn описали, как можно осуществить диетический контроль больных ФКУ, в Nestlé [Engl] 2010;68:58–69. Субъектом, подвергаемым лечению, может быть в принципе любой больной ФКУ, хотя изобретение является особо предпочтительным для больного ФКУ, который имеет повышенный уровень фенилаланина, в частности, этот уровень является токсическим; или для лечения больного ФКУ, который не полностью соблюдает не содержащую фенилаланина диету или диету с ограниченным содержанием фенилаланина, и таким образом, имеет повышенный риск воздействия слишком высоких количеств фенилаланина.
Наименьший уровень фенилаланина в крови, который признан токсическим, зависит до определенной степени от пациента, в частности, возраста пациента. Далее, некоторые различия существуют между разными странами по рекомендациям, касающимся уровня фенилаланина в крови. Как правило, уровень примерно 1500 мкмоль/л в крови считается токсическим, но токсичность может уже проявляться при значительно более низких уровнях, среди прочего, в зависимости от таких факторов, как возраст пациента.
В следующей таблице показаны рекомендуемые уровни фенилаланина в крови для различных групп пациентов в некоторых странах.
Нормализация уровня фенилаланина в крови в соответствии с изобретением относится, в частности, к снижению концентрации фенилаланина от значения, превышающего наивысший рекомендуемый уровень, до концентрации в пределах рекомендованного диапазона. Диетический контроль нацелен на поддержку концентрации фенилаланина в крови в пределах рекомендованного диапазона.
Как правило, композиция предназначена для применения с целью снижения уровня фенилаланина в крови, нормализации уровня фенилаланина в крови, или поддержки уровня фенилаланина в крови с концентрацией ниже 1200 мкМ, в частности, ниже 900 мкмоль/л, более конкретно ниже 600 мкмоль/л.
Как правило, лечение композицией (для применения) в соответствии с изобретением ребенка в возрасте 0-10 лет нацелено на снижение, нормализацию или поддержку концентрации фенилаланина в крови пациента в диапазоне 40-360 мкмоль/л, предпочтительно 120-360 мкмоль/л.
Как правило, лечение композиций (для применения) в соответствии с изобретением ребенка в возрасте 10-12 лет нацелено на снижение, нормализацию или поддержку концентрации фенилаланина в крови пациента на уровне ниже 900 мкмоль/л, в частности, ниже 600 мкмоль/л, предпочтительно ниже 480 мкмоль/л, более предпочтительно 120-360 мкмоль/л.
Как правило, лечение композицией (для применения) в соответствии с изобретением человека в возрасте 12-20 лет нацелено на снижение, нормализацию или поддержку концентрации фенилаланина в крови пациента на уровне ниже 900 мкмоль/л, в частности, ниже 600 мкмоль/л, предпочтительно ниже 480 мкмоль/л, более предпочтительно в диапазоне 120-600 мкмоль/л.
Как правило, лечение композицией (для применения) в соответствии с изобретением человека в возрасте более 20 лет нацелено на снижение, нормализацию или поддержку концентрации фенилаланина в крови пациента на уровне ниже 1200 мкмоль/л, в частности, ниже 900 мкмоль/л, в частности, ниже 700 мкмоль/л, более конкретно, ниже 600 мкмоль/л или меньше. Нижний предел диапазона может составлять 0, в частности, 120 мкмоль/л.
В случае беременности лечение, как правило, нацелено на снижение, нормализацию или поддержку концентрации фенилаланина в крови пациентки на уровне в диапазоне 120-360 мкмоль/л.
Хотя при лечении композицией (для применения) в соответствии с изобретением также рекомендуется ограничить суточное потребление фенилаланина до более низкого суточного потребления, чем то, которое обычно рекомендуется для субъектов, не страдающих ФКУ, настоящее изобретение снижает риск побочных эффектов употребления продукта питания, содержащего значительное количество фенилаланина.
Композицию обычно применяют перорально, хотя возможен другой способ применения, например, кормление через зонд или с помощью суппозитория.
Далее, изобретение иллюстрировано посредством ряда примеров.
Пример 1. Эффект снижения фенилаланина для питательного продукта на мышиной модели ФКУ (C57Bl/6 Pahenu2).
Материалы и методы
Мышиная модель
В этом эксперименте использовали мышиную модель C57Bl/6 Pahenu2. Гомозиготных (ФКУ) мышей, самцов и самок, и однопометных животных дикого типа (WТ) получали от собственной линии. Самцов и самок мышей содержали в отдельных комнатах в одних и тех же условиях 12:12 цикла света/темноты, температуры и влажности. 60 мышей с ФКУ и 10 мышей дикого типа подразделяли на семь опытных групп, получавших разные рационы. Базовой формулой для всех рационов была AIN93G (Research Diet Services, Вейк бей Дюрстеде).
Рационы
Мыши дикого типа получали обычный корм с содержанием фенилаланина 8,8 г/кг. Шесть групп мышей с ФКУ, получавших добавку Fortasyn Connect® (N.V. Nutricia) ингредиентов и три разных количества фенилаланина, были рандомизированы. Fortasyn Connect® (FC) является комбинацией нутриентов, включающей антиоксиданты (селен, витамин Е), уридин-5'-монофосфат, холин, витамины В12 и В6, фолиевую кислоту, фосфолипид, докозагексаеновую кислоту (ДГК) и эйкозапентаеновую кислоту.
Были использованы следующие группы. Первые две группы получали тот же обычный корм AIN93G, как описано ранее для мышей дикого типа (содержание фенилаланина 8,8 г/кг). Одна из этих групп получала рацион без FC (контроль), другие получали корм с FC, эти группы были обозначены, соответственно: «Phe8.8» и «Phe8.8+FC». Контрольная группа получала более низкие количества Se, витамина Е, холина, витамина В12, В6 и фолиевой кислоты, по сравнению с группой FC. Кроме того, группа FC получала ЭПК/ДГК, УМФ и фосфолипид (лецитин), в то время как контрольные группы не получали добавок из этих ингредиентов. Две группы получали рацион с низким содержанием фенилаланина. Этот рацион содержал 4,0 г/кг фенилаланина без FC или с FC, соответственно, где группы обозначались как «Phe4.0» и «Phe4.0+FC». Наконец, были созданы две группы со средним содержанием фенилаланина, где уровни фенилаланина были установлены между уровнями групп с высоким количеством фенилаланина и низким количеством фенилаланина. Количество для рациона со средним содержанием фенилаланина составило 6,4 г/кг без FC («Phe6.4») и с FC («Phe6.4+FC»). Все рационы удовлетворяли минимальным диетическим требованиям для лабораторных животных. Животные имели свободный доступ к корму и воде в течение 12 недель. В начале эксперимента (день после рождения (ДПР) 28) животных отлучали от матери, и брали образцы крови посредством пункции хвостовой вены. На 31 ДПР животных помещали в круглую камеру «открытого поля», а затем давали различные рационы в течение 12 недель. Всех животных взвешивали каждый день между 16:00-18:00 в течение первой недели эксперимента (ДПР 31-38), а затем раз в неделю. Потребление корма измеряли ежедневно. В пределах этих 12 недель собирали крови в ДПР 59 и 87. В ДПР 115 мышей умерщвляли посредством сердечной пункции для сбора крови, с последующей перфузией. Все процедуры, касающиеся животных в данном исследовании, были разрешены этическим комитетом Университета Гронингена, Нидерланды.
Сбор крови
Образцы крови собирали с помощью трех разных методик. На ДПР 28 небольшой кусочек ткани хвоста собирали для генотипирования. Немедленно после этой процедуры собирали образцы крови из раны на конце хвоста. На ДПР 59 и 87 образцы крови собирали из хвостовой вены. При обеих методиках микропробирки для анализа гематокрита с гепарином натрия (VITREX, ISO 12772, REF 161313) использовали для сбора крови перед переносом крови на фильтровальную бумагу. На ДПР 115 у животных проводили анестезию путем интраперитонеальной (и/п) инъекции фенобарбитала. После исчезновения рефлекса задних лап проводили пункцию сердца. Собранную кровь хранили в микропробирках с гепарином лития (Sarstedt, REF 41.1393.005) перед центрифугированием образцов крови при 4°С в течение 10 мин при 12800 об./мин. Плазму крови собирали и хранили при -80°С перед анализом.
Аминокислотный анализ
В сухих пятнах крови определяли фенилаланин и тирозин с применением тандемной высокоэффективной жидкостной хроматографии - масс-спектрометрии. Кровь собирали на фильтровальной бумаге и сушили в течение по меньшей мере 24 часов. Отбирали образец из сухого пятна крови диаметром 4 мм, и оставляли для элюции в метаноле, содержащем дейтерированный фенилаланин и тирозин качестве внутренних стандартов. Жидкостную хроматографию проводили с применением Nexera LC30 (Shimadzu, Киото, Япония). Масс-спектрометрию проводили с применением API-3000 (AB-Sciex, Фремингем, США).
Для измерения аминокислоты (за исключением триптофана) в цельной плазме, образцы обрабатывали на вортексере и центрифугировали при 20800 об./мин в течение 4 минут. После центрифугирования отбирали пипеткой 85 мкл надосадочной жидкости в капсулы. Норлейцин и сульфосалициловую кислоту добавляли в качестве внутреннего стандарта (1:1 о/о). Концентрации аминокислот измеряли путем высокоэффективной жидкостной хроматографии (ВЭЖХ) с последующей дериватизацией нингидрином после колонки на анализаторе Biochrom 30 (Pharmacia Biotech, Кембридж, Соединенное Королевство).
Статистический анализ
Определяли количество фенилаланина в крови с помощью теста нормальности Шапиро-Уилка. Только мыши из групп дикого типа и Phe4.0 не имели нормально распределенных значений. Несмотря на это наблюдение, проводили односторонний тест ANOVA, и использовали тест Бонферрони в качестве ретроспективного анализа. Также тестировали нормальность значений потребления фенилаланина с тестом Шапиро-Уилка. Мыши дикого типа показали ненормальное распределение (p=0,0482). В то время как все другие группы показали нормально распределенные данные, мы проводили односторонний тест ANOVA с ретроспективным анализом Бонферрони. Корреляцию между абсолютным потреблением фенилаланина и уровнями фенилаланина в крови оценивали с помощью корреляции Пирсона. С преобразованием Фишера r-z были получены достоверные различия между корреляцией.
Ключевой характеристикой патофизиологии ФКУ являются повышенные уровни фенилаланина в крови. Современное лечение ФКУ в Нидерландах характеризуется контролем этих уровней от 120 мкмоль/л до 360 мкмоль/л для детей (0-12 лет) и от 120 мкмоль/л до 600 мкмоль/л после 12 лет. При отсутствии лечения уровни фенилаланина могут повышаться до 1000 и 2000 мкмоль/л. Поскольку пациентам часто трудно соблюдать диету, уровни могут находиться где-либо между ранее упомянутыми уровнями. В настоящем эксперименте различное содержание фенилаланина позволило имитировать у животных, до некоторой степени, эти разные группы пациентов.
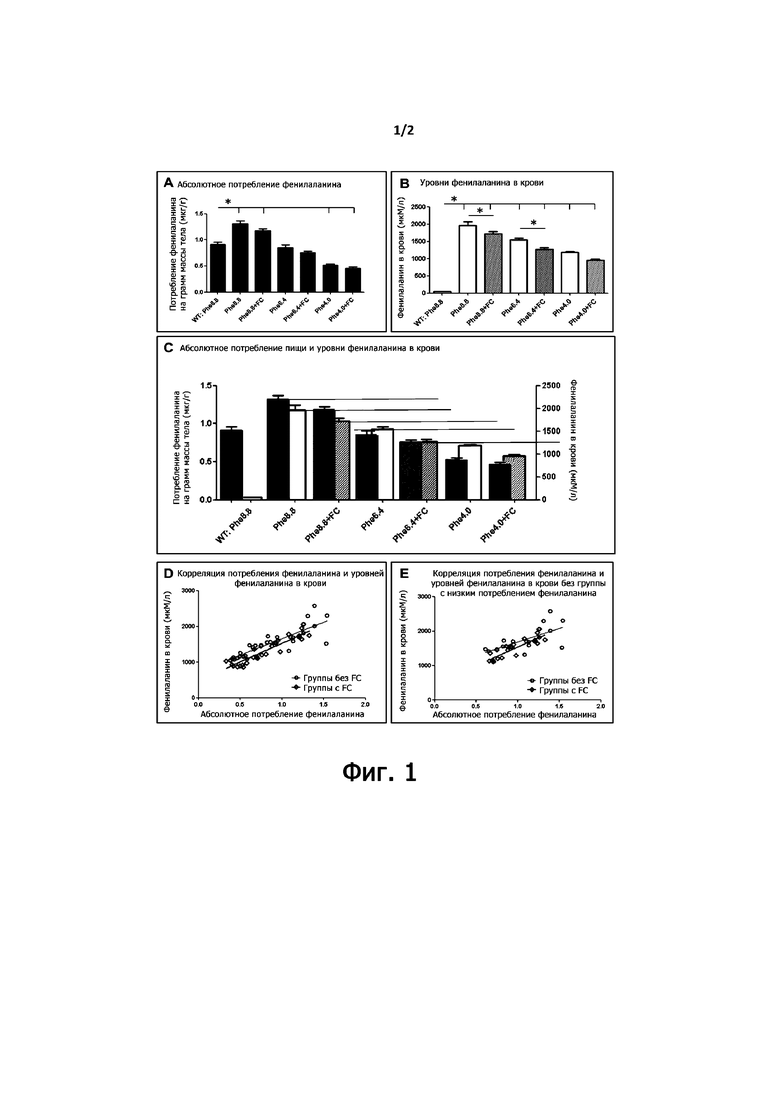
Результаты на фигурах 1А-1Е показали, что уровни фенилаланина в крови снижались с уменьшением потребления фенилаланина, но неожиданно в опытных группах, в двух группах с наивысшим потреблением фенилаланина (Phe 8 и Phe 6) были достоверно ниже, чем в группе плацебо. Это показывает, что дополнительные ингредиенты в группе FC были способны снижать уровни фенилаланина в крови.
Уровни фенилаланина в крови изображены на фигуре 1В, и односторонний ANOVA тест выявил достоверные различия между Phe8.8 и Phe8.8+FC и Phe6.4 и Phe6.4+FC у мышей с ФКУ, как указано звездочками.
Пример 2. Эффект снижения фенилаланина для продукта питания на мышиной модели ФКУ (BTBR ФКУ мыши).
В этой второй серии экспериментов проводили ту же самую процедуру, как в Примере 2, со следующими модификациями: используемые мыши имели ту же самую мутацию (Pahenu2), но на генетическом фоне BTBR вместо C57Bl/6. Кроме того, использовали 6 групп: дикого типа (WT) с обычным кормом, WT + FC, ФКУ с обычным кормом (Phe 6.2), ФКУ с обычным кормом + FC, ФКУ с низким количеством фенилаланина (2.2), и ФКУ с низким количеством фенилаланина + FC.
В возрасте 4 месяцев собирали кровь из хвостовой вены в микропробирки для гематокрита с добавлением гепарина натрия (VITREX, ISO 12772, REF 161313), затем переносили кровь на фильтровальную бумагу, и анализировали уровни фенилаланина, как описано выше.
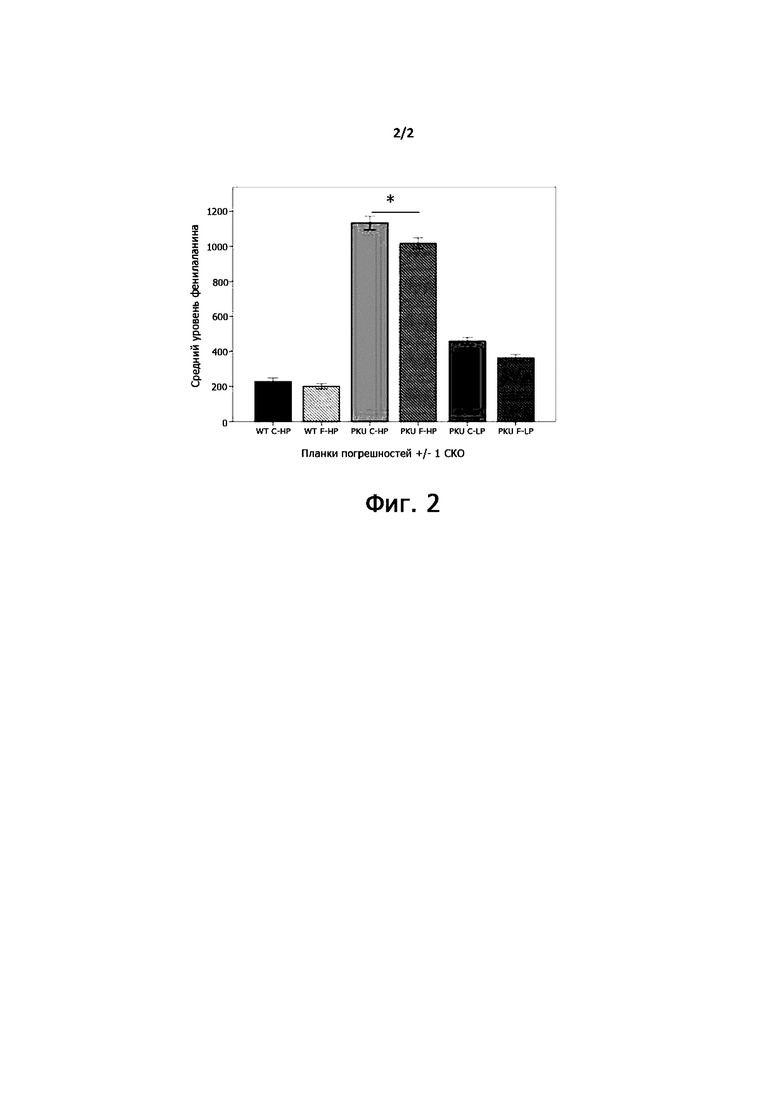
Уровни фенилаланина в крови изображены на фигуре 2, и односторонний ANOVA выявил достоверную разницу между ФКУ мышами с высоким потреблением фенилаланина, и с высоким потреблением фенилаланина + FC, как указано звездочкой.
Пример 3. Примерная композиция (для применения) в соответствии с изобретением.
Таблица 2
ДГК (22:6n-3; мг)
0,88
Кальций (мг)
Фосфор (мг)
Витамин E (мг α-токоферола)
Витамин C (мг)
Витамин D (мкг)
Витамин K (мкг)
Фолиевая кислота (мкг)
Ниацин/ Витамин B3 (мг)
Витамин B6 (мг)
Витамин B12 (мкг)
Холин (мг)
276
33,6
44,4
6
20
160
7,1
0,58
1,8
153
Уридин-5’-монофосфат (мг)
| название | год | авторы | номер документа |
|---|---|---|---|
| НУТРИТИВНАЯ КОМПОЗИЦИЯ ДЛЯ УЛУЧШЕНИЯ ФУНКЦИИ МОЗГА ПРИ ФЕНИЛКЕТОНУРИИ | 2014 |
|
RU2690660C2 |
| СПОСОБ УЛУЧШЕНИЯ ФУНКЦИОНАЛЬНОЙ СИНАПТИЧЕСКОЙ СВЯЗИ | 2013 |
|
RU2667968C2 |
| СПОСОБ ДЛЯ ОЦЕНКИ И ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ НАРУШЕННЫХ УРОВНЕЙ ПОЛЯРНЫХ ЛИПИДОВ В ПЛАЗМЕ | 2015 |
|
RU2705208C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ, СПОСОБСТВУЮЩАЯ ЗДОРОВОМУ РАЗВИТИЮ И РОСТУ | 2009 |
|
RU2501553C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ МЛАДЕНЦЕВ, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ОЖИРЕНИЯ | 2006 |
|
RU2417712C2 |
| УЛУЧШЕНИЕ ПАМЯТИ У ПАЦИЕНТОВ С ОЦЕНКОЙ 24-26 БАЛЛОВ ПО КРАТКОЙ ШКАЛЕ ОЦЕНКИ ПСИХИЧЕСКОГО СТАТУСА | 2008 |
|
RU2529815C2 |
| УЛУЧШЕНИЕ ПАМЯТИ У ПАЦИЕНТОВ С ОЦЕНКОЙ 24-26 БАЛЛОВ ПО КРАТКОЙ ШКАЛЕ ОЦЕНКИ ПСИХИЧЕСКОГО СТАТУСА | 2014 |
|
RU2677345C2 |
| КОМБИНАЦИИ И КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЖИРНЫЕ КИСЛОТЫ И АМИНОКИСЛОТЫ, ИХ ПРИМЕНЕНИЕ ДЛЯ ПРЕДУПРЕЖДЕНИЯ, ЗАМЕДЛЕНИЯ ПРОГРЕССИРОВАНИЯ ИЛИ ЛЕЧЕНИЯ ДИАБЕТА И СВЯЗАННЫХ С ДИАБЕТОМ ЗАБОЛЕВАНИЙ И СОСТОЯНИЙ, СПОСОБ СНИЖЕНИЯ ВЕСА ТЕЛА МЛЕКОПИТАЮЩЕГО, НАБОР | 2004 |
|
RU2356247C2 |
| ЖИДКИЙ ПРОДУКТ, СОДЕРЖАЩИЙ НУКЛЕОТИДЫ/НУКЛЕОЗИДЫ | 2008 |
|
RU2446807C2 |
| ДЕТСКОЕ ПИТАНИЕ | 2005 |
|
RU2404785C2 |
Изобретение относится к лечению фенилкетонурии. Раскрыто применение композиции, включающей белок, липид и углеводы, где белок обеспечивает, по меньшей мере, все незаменимые аминокислоты, кроме фенилаланина, где липид включает одну или несколько ω-3 жирных кислот, выбранных из группы, состоящей из DHA, DPA и EPA, в общей концентрации по меньшей мере 0,05 мас.% от общего содержания липидов, и одно или несколько производных пиримидина, выбранных из группы, состоящей из источников уридина и источников цитидина, обеспечивающих от 0,4 до 3000 мг источника уридина, рассчитанного как монофосфат уридина на 100 ккал композиции, и/или от 0,4 до 3000 мг источника цитидина, рассчитанного как монофосфат цитидина на 100 ккал композиции, для снижения, нормализации или поддержания уровня фенилаланина в крови пациента с фенилкетонурией ниже 1200 мкмоль/л. Изобретение обеспечивает контроль уровней фенилаланина в крови больного фенилкетонурией. 21 з.п. ф-лы, 2 ил., 2 табл., 3 пр.
1. Применение композиции, включающей белок, липид и углеводы, где белок обеспечивает, по меньшей мере, все незаменимые аминокислоты, кроме фенилаланина, где липид включает одну или несколько ω-3 жирных кислот, выбранных из группы, состоящей из DHA, DPA и EPA, в общей концентрации по меньшей мере 0,05 мас.% от общего содержания липидов, и одно или несколько производных пиримидина, выбранных из группы, состоящей из источников уридина и источников цитидина, обеспечивающих от 0,4 до 3000 мг источника уридина, рассчитанного как монофосфат уридина на 100 ккал композиции, и/или от 0,4 до 3000 мг источника цитидина, рассчитанного как монофосфат цитидина на 100 ккал композиции, для снижения, нормализации или поддержания уровня фенилаланина в крови пациента с фенилкетонурией ниже 1200 мкмоль/л.
2. Применение по п.1, где композиция дополнительно включает холин и/или фосфолипид.
3. Применение по п.2, где композицию вводят в количестве, обеспечивающем суточную дозу 0,1-5 г холина.
4. Применение по любому из предыдущих пунктов, где композиция включает 0-1 мг фенилаланина на 1 г белка, более предпочтительно 0-0,1 мг фенилаланина на 1 г белка.
5. Применение по любому из предыдущих пунктов, где композиция является питательной композицией.
6. Применение по п.5, где композиция включает от 1 до 15 мас.% липидов, 5-60 мас.% усвояемых углеводов и 1-40 мас.% белка исходя из сухой массы композиции и дополнительно включает по меньшей мере один витамин B, выбранный из группы витамина B6, витамина B9 и витамина B12, и антиоксидант, выбранный из группы витамина C, витамина E и селена.
7. Применение по любому из предшествующих пунктов, где композиция включает от 0,1 до 40 мас.% DHA от общего содержания липидов в композиции и от 0,4 до 3000 мг источника уридина в пересчете на монофосфат уридина на 100 ккал композиции.
8. Применение по любому из предшествующих пунктов, где композиция дополнительно включает по меньшей мере один витамин B, выбранный из группы витамина B6, витамина B12 и витамина B9.
9. Применение по любому из предшествующих пунктов, где композиция дополнительно включает антиоксидант, выбранный из группы, состоящей из витамина С, витамина Е и селена.
10. Применение по любому из предшествующих пунктов, где композиция предназначена для снижения уровня фенилаланина в крови пациента с фенилкетонурией, нормализации уровня фенилаланина в крови пациента с фенилкетонурией до или поддержания уровня фенилаланина в крови пациента с фенилкетонурией ниже 600 мкмоль/л.
11. Применение по п.10, где пациентом с фенилкетонурией является ребенок в возрасте от 0 до 10 лет, и уровень фенилаланина в крови снижается, нормализуется или поддерживается в диапазоне 40-360 мкмоль/л.
12. Применение по п.10, где пациентом с фенилкетонурией является человек в возрасте от 10 до 20 лет, и уровень фенилаланина в крови снижается, нормализуется или поддерживается в диапазоне 120-600 мкмоль/л.
13. Применение по п.12, где указанный уровень находится в диапазоне 120-360 мкмоль/л.
14. Применение по п.10, где пациентом с фенилкетонурией является человек в возрасте 20 лет или более.
15. Применение по п.14, где уровень фенилаланина в крови снижается, нормализуется или поддерживается в диапазоне 120-600 мкмоль/л.
16. Применение по п.10, где пациентом с фенилкетонурией является беременная женщина, и уровень фенилаланина в крови снижается, нормализуется или поддерживается в диапазоне 120-360 мкмоль/л.
17. Применение по любому из предшествующих пунктов, где композицию вводят перорально.
18. Применение по п.1, где композиция включает фенилаланин в концентрации 0-10 мг/грамм белка.
19. Применение по п.5, где композиция включает 1-15 мас.% липидов, 5-60 мас.% легкоусвояемых углеводов и 1-14 мас.% белка в расчете на сухую массу композиции.
20. Применение по п.5, где питательная композиция включает:
i) DHA и EPA,
ii) уридин и/или монофосфат уридина,
iii) по меньшей мере один витамин B, выбранный из группы витамина B6, витамина B9 и витамина B12,
iv) фосфатидилхолин и/или один или несколько других фосфолипидов,
v) антиоксидант, выбранный из группы витамина C, витамина E и селена.
21. Применение по п.5, где композиция включает по меньшей мере два различных фосфолипида, выбранных из группы, состоящей из фосфатидилсерина, фосфатидилинозита, фосфатидилхолина и фосфатидилэтаноламина.
22. Применение по п.5, где питательная композиция дополнительно включает витамин А и/или витамин D.
| WO 2014171828 A1, 23.10.2014 | |||
| CN 104012659 A, 03.09.2014 | |||
| СТУДЕНИКИН В.М | |||
| и др | |||
| Фенилкетонурия у детей и ее лечение // Лечащий врач, номер 9, 2011 г., с | |||
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
Авторы
Даты
2021-01-21—Публикация
2016-10-24—Подача