Изобретение относится к области профилактической и реабилитационной медицины, гигиены труда, в частности к способам прогнозирования преморбидных состояний у стажированных работников химических производств (например, металлургических), предшествующих развитию производственно обусловленной кардиореспираторной патологии через заболевания сердечно-сосудистой и дыхательной системы. Задачей изобретения является расширение диапазона медицинского контроля за функциональным состоянием стажированных работников химических производств, в целях повышения эффективности мероприятий, направленных на сохранение здоровья работников предпенсионного возраста химических производств, угрожаемых по развитию болезней органов дыхания и системы кровообращения, обусловленных воздействием вредных производственных факторов.
Согласно данным многоцентровых исследований основной причиной снижения производительности труда у работников предпенсионного возраста является низкий адаптационный потенциал систем жизнеобеспечения и развитие хронических заболеваний, прежде всего системы кровообращения и органов дыхания.
Результаты клинических наблюдений свидетельствуют о том, что почти у половины работников (47,1%) химической промышленности (химическая промышленность - комплекс предприятий, использующих всевозможные виды технологических процессов, основанные на химическом превращении сырья (углеводородного, минерального и т.д.) в посредствующие материалы и элементы потребления) в возрасте 50 лет и старше адаптационные резервы организма и показатели выносливости снижены более чем на 30-40% соответственно; частота сердечных сокращений (ЧСС) в течение рабочей смены достигает 100-120 уд. в мин., а систолическое артериальное давление (САД) - 160 мм.рт.ст. По результатам периодических медицинских осмотров (ПМО) и экспертизы профпригодности у 1/3 стажированных работников регистрируются 3 и более хронических заболеваний, среди которых приоритетные места занимают болезни органов дыхания (БОД) и болезни системы кровообращения (БСК). Причем БОД и БСК являются медицинскими противопоказаниями к выполнению отдельных видов работ на предприятиях химического профиля, кроме того, представляют собой наиболее частую причину временной нетрудоспособности работников предпенсионного возраста и повышают риск смерти на рабочем месте.
Исходя из вышеизложенного, выработка критериев отбора стажированных работников в группу высокого риска развития производственно обусловленной кардиореспираторной патологии является актуальной.
Под термином «кардиореспираторная патология» понимается сочетание патологии нижних дыхательных путей и системы кровообращения, имеющих единые патогенетические звенья (коморбидность хронической обструктивной болезни легких (ХОБЛ) и гипертонической болезни (ГБ) [ТН Василькова, Ю.А. Рыбина - 2013]).
Следует отметить, что в настоящее время разработаны шкалы оценки риска развития сердечно-сосудистых заболеваний (ССЗ) и их осложнений (SCORE, FRS), позволяющие определить возможность развития сердечно-сосудистых событий в течение 10 лет, опросники, направленные на выявление респираторных симптомов, для ранней диагностики ХОБЛ (CAT, опросник для больных респираторными заболеваниями госпиталя св. Георгия и др.). Однако имеются данные о том, что в 74,5% случаев инфаркт миокарда развивается у лиц с низким (менее 10% по шкале FRS) риском, а ХОБЛ вносит существенный вклад в увеличение количества случаев инвалидности и преждевременной смертности, при этом, как правило, развивается после 40 лет и медленно прогрессирует незаметно для работника, что затрудняет раннюю диагностику. Следовательно, идентификация неблагоприятного воздействия производственных факторов на риск развития у работников профессионально обусловленной сочетанной патологии систем кровообращения и дыхания является актуальной для определения прогнозирования риска развития производственно обусловленной кардиореспираторной патологии и трудового прогноза. Поэтому остается актуальным поиск новых маркеров формирования кардиореспираторной патологии и новых диагностических подходов.
Из уровня техники (патент РФ №2487663) известен способ оценки степени метаболической и кардиореспираторной адаптации кардиохирургических больных. Для этого во время операции и интенсивной терапии осуществляют последовательное вдыхание газовой смеси с 51% (FiO2=0,51) и 21% (FiO2=0,21) содержанием кислорода. Затем определяют потребление кислорода и выделение углекислого газа на каждом этапе и рассчитывают мощность анаэробного порога по FiO2 в газовой смеси, соответствующей моменту достижения анаэробного порога. При мощности анаэробного порога более >0,14 считают степень метаболической и кардиореспираторной адаптации пациента низкой. При значении показателя <0,1 считают степень метаболической и кардиореспираторной адаптации пациента высокой. При значении показателя 0,1-0,14 считают степень метаболической и кардиореспираторной адаптации пациента средней. Способ позволяет обеспечить снижение вероятности развития гипоксических осложнений у критических больных за счет определения степени метаболической и кардиореспираторной адаптации во время операции и интенсивной терапии, в том числе и в режиме мониторирования.
Однако указанный способ не может быть применим для стажированных работников химических производств.
Из уровня техники известен ряд технических решений, имеющих отношение к установлению отклонений в здоровье работников химических производств, например:
- Способ отбора стажированных работников, находящихся в контакте с парами металлической ртути, в группу риска развития хронической ртутной интоксикации (патент РФ №2460458) (способ состоит в том, что проводят нейропсихологическое тестирование с определением показателей аналитико-синтетического мышления, показателей системы счета: тройной счет, простые счетные операции; показателей понятийного мышления путем подбора противоположностей в пассивном и активном плане; зрительной и долговременной памяти; динамического и пространственного праксиса; показателей зрительного гнозиса: узнавание перечеркнутых изображений, узнавание наложенных изображений, пальцевый гнозис. Затем рассчитывают дискриминантную функцию F, сравнивают полученный результат с константой и при F больше константы стажированных работников относят к группе риска, при F меньше или равной константе - к группе без признаков влияния ртути на организм).
- Способ прогнозирования риска развития профессиональной бронхиальной астмы (патент РФ №2583948) (способ состоит в том, что определяют наличие родственников с аллергической реакцией, наличие в анамнезе ринита, крапивницы либо другой аллергической реакции, бытовой, пищевой и лекарственной аллергической реакции, профессиональной вредности, при этом дополнительно определяют концентрацию общего IgE в сыворотке крови, в качестве профессиональной вредности определяют «симптомы элиминации», «экспозиционный тест», «эффект реэкспозиции» каждый признак оценивают в баллах. Далее баллы суммируют и при их сумме менее 15 прогнозируют низкую степень риска профессиональной бронхиальной астмы, 16-30 баллов - среднюю степень риска, 31 балл и более - высокую степень риска).
- Способ прогнозирования индекса массы миокарда левого желудочка у работников химических производств в зависимости от систолического артериального давления и концентрации липопротеинов низкой плотности (патент РФ №2704788) (у обследуемых работников определяют такие предикторы ремоделирования миокарда, как возраст, систолическое артериальное давление, окружность талии и концентрация липопротеинов низкой плотности в сыворотке венозной крови. Полученные анамнестические данные и результаты обследования подставляют в разработанную математическую модель: ИММЛЖ = 1,134 × САД + 0,207 × Возр - 0,272 × ОТ + 2,256 × ЛПНП - 23,631; где: ИММЛЖ - индекс массы миокарда левого желудочка, г/м2; САД - систолическое артериальное давление, мм рт.ст.; Возр - возраст работника, лет; ОТ - окружность талии, см; ЛПНП - концентрация липопротеинов низкой плотности в сыворотке крови, ммоль/л. Согласно отечественным и зарубежным рекомендациям по лечению артериальной гипертензии за верхнюю границу нормы индекса массы миокарда левого желудочка принято 110 г/м2 для женщин и 134 г/м2 у мужского населения. При диагностированной артериальной гипертонии этот параметр снижен у мужчин до 125 г/м2. Если ИММЛЖ превышает указанные максимально допустимые значения, то диагностируется гипертрофия миокарда левого желудочка).
- Способ прогнозирования высокого риска развития производственно обусловленных и профессиональных заболеваний у работников химического комплекса, занятых во вредных условиях труда (патент РФ №2545911) (способ включает определение в сыворотке крови общего антиоксидантного статуса, при этом дополнительно в сыворотке крови определяют количественное содержание продуктов перекисного окисления липидов и при одновременном увеличении количественного содержания перекисей в липидах более 4,31 мкмоль/л и снижении общего антиоксидантного статуса менее 1,3 ммоль/л прогнозируют высокий риск развития производственно обусловленных и профессиональных заболеваний).
Однако все указанные способы не несут информационную ценность в плане установления критериев отнесения стажированных работников в группу высокого риска развития производственно обусловленной кардиореспираторной патологии.
При этом из уровня техники не были выявлены известные способы отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии, поэтому сделать выбор ближайшего аналога к заявляемому изобретению не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в обеспечении возможности выработки критериев отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии.
Поставленный технический результат достигается предлагаемым способом отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии, характеризующимся тем, что проводят медицинское обследование работников химических производств со стажем более 10 лет путем определения диагностических лабораторных и функциональных показателей, при этом в качестве лабораторных показателей определяют уровни гемоглобина (Hb), эритроцитов, гидроперекиси липидов (ГПЛ), малонового диальдегида (МДА), антиоксидантной активности плазмы (АОА), эритропоэтина, оксида азота, фактора роста эндотелия сосудов (VEGF), гомоцистеина и высокочувствительного С-реактивного белка (hs-СРБ); а в качестве функциональных показателей определяют признаки увеличения левого и правого желудочков сердца методом электрокардиографии путем установления положения электрической оси сердца, положения сегмента ST относительно изолинии в V6 и зубца Т в V1; типа желудочкового комплекса; через размер вольтажа зубца R', высоту зубца R в отведении V6 зубца Р на электрокардиограмме (ЭКГ); объем фиксированного выдоха за 1 сек. (ОФВ1), форсированную жизненную емкость легких (ФЖЕЛ); отношение ОФВ1/ФЖЕЛ и среднюю объемную скорость форсированного выдоха (СОС25-75) методом спирографии; проведение функциональной пробы с использованием бронходилататора с оценкой прироста показателя «оценка форсированного выдоха за секунду», и устанавливают ежегодное снижение ОФВ1 в сравнении с результатами предыдущего года и темп снижения реакции эндотелия за год, сравнивают результаты полученных показателей с физиологической нормой, и тех работников, у которых выявлены следующие отклонения в показателях от физиологической нормы, а именно: превышение от верхней границы нормы более чем на 10% уровня Hb, эритроцитов, ГПЛ, МДА, VEGF, гомоцистеина и hs-СРБ, превышение от верхней границы нормы более чем на 20% уровня АОА, понижение от нижней границы нормы более чем на 10% уровня эритропоэтина и оксида азота, при одновременном установлении методом электрокардиографии отклонения электрической оси сердца вправо до 100 градусов; косонисходящей депрессии сегмента ST в V6; отрицательном зубце Т в стандартных отведениях; отрицательном зубце Т в V1; желудочковом комплексе типа rSR'; вольтаже зубца R' более 7 мм, высоком зубце R в отведении V6, увеличение вольтажа Р больше 2 мм на электрокардиограмме ЭКГ; при установлении методом спирографии ОФВ1 меньше 80% от нормы; соотношении ОФВ1/ФЖЕЛ равном 65%-70%; показателя СОС25-75 - 70%-75%; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка ОФВ за секунду» на 8-12% от должного; ежегодное снижение ОФВ1 35-50 мл в год, темп снижения функциональной активности эндотелия за год больше чем на 0,3%, относят к группе работников с высоким риском развития производственно обусловленной кардиореспираторной патологии.
Указанный технический результат достигается за счет следующего.
По совокупности производственных факторов условия труда у работников основных профессий предприятий химического профиля оцениваются как вредные (степень 3.3-3.4) и рассматриваются в качестве основной причины развития профессиональных и производственно обусловленных БОД и БСК. Априорный профессиональный риск у работников основных профессий химических предприятий оценивается как высокий (непереносимый), что требует принятия неотложных мер по его снижению и предупреждению развития профессиональной и производственно обусловленной патологии органов дыхания и связанных с ней производственно обусловленных сердечно-сосудистых заболеваний.
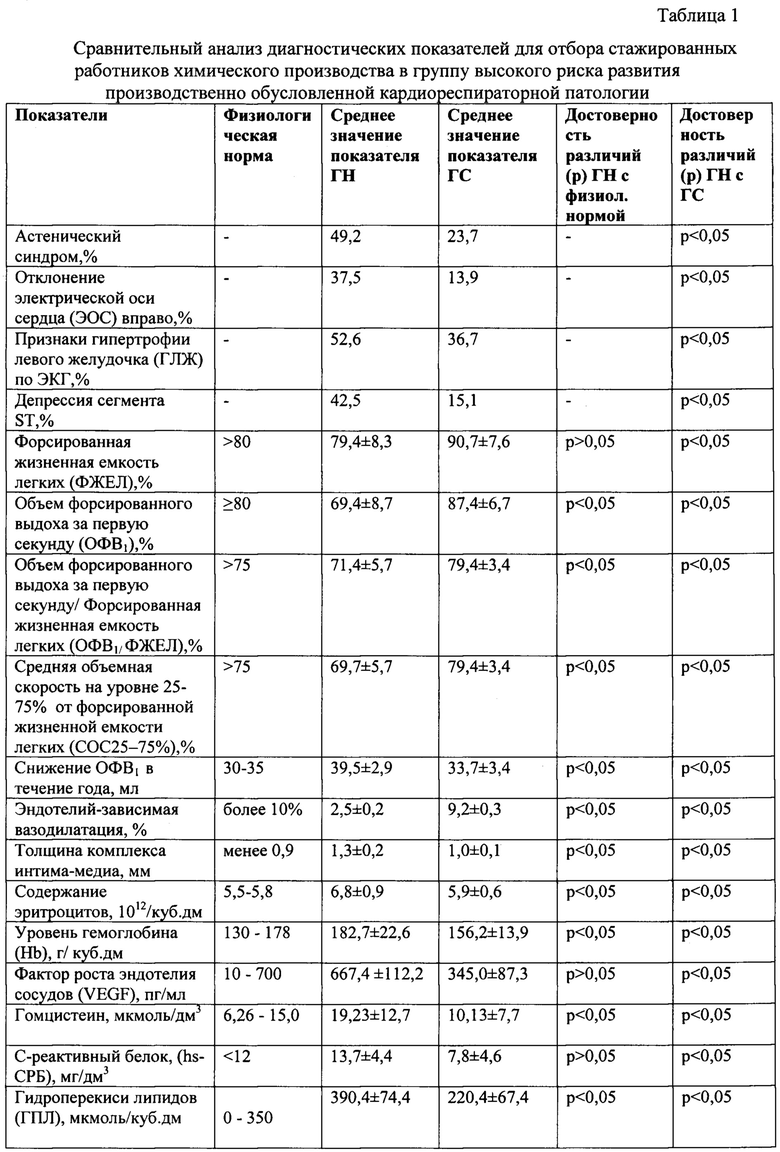
У работников основных профессий химического производства в возрасте 45 лет и старше в условиях постоянной занятости по специальности не менее 10 лет, сочетанное воздействие факторов трудового процесса повышает ежегодно на 15-20% вероятность развития неканцерогенных нарушений здоровья относительно лиц, не связанных с воздействием данных производственных факторов.
На Рис. 1 показан результат моделирования интегрального риска здоровью работников без воздействия производственных факторов и под воздействием производственных факторов.
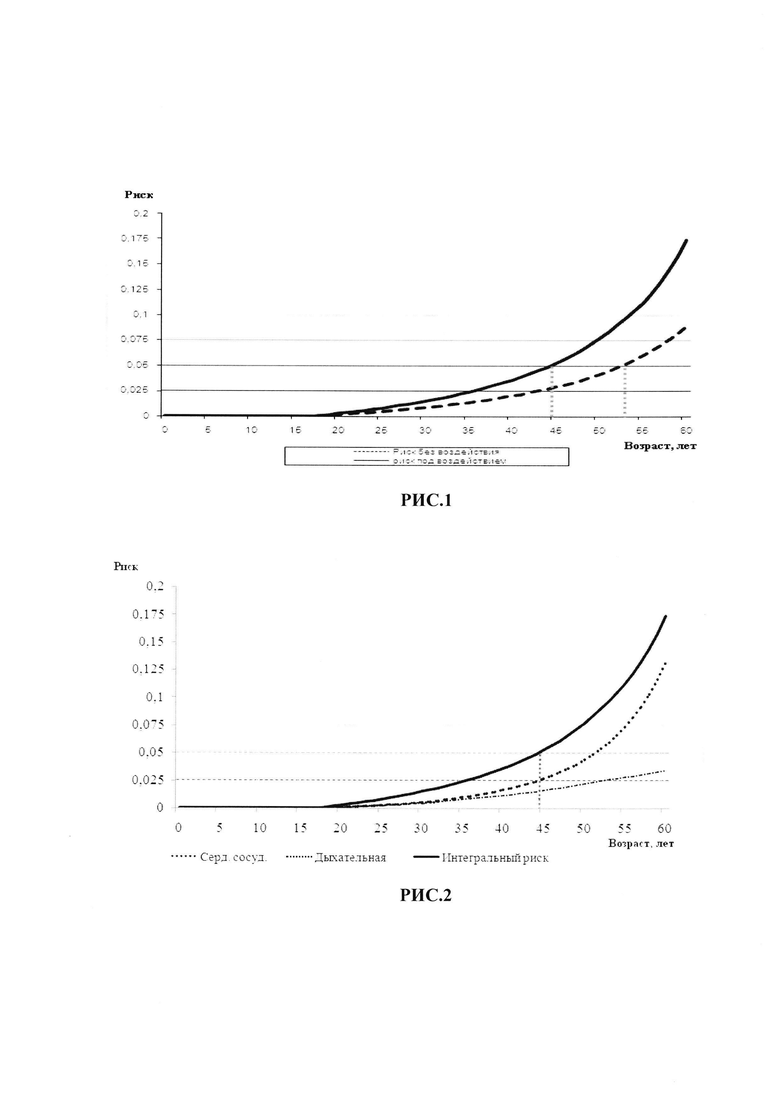
На Рис. 2 приведен результат моделирования изменения интегрального риска здоровью работников при воздействии производственных факторов при различных патологиях.
Следует отметить, что с возрастом снижается физическая активность человека за счет уменьшения физиологического резерва систем жизнеобеспечения. И в этом случае физиологическое старение будет выступать как фактор риска ХОБЛ и БСК. С возрастом функциональная активность органов и систем человека начинает постепенно снижаться. Это связано и с тем, что количество функциональных единиц органов и митотическая активность обновляющихся органов уменьшаются: количество альвеол в легких, сосудистых клубочков в различных органах, интенсивность деления клеток, других обновляющихся тканей также уменьшаются в процессе старения организма.
Обычно возрастные изменения дыхательной системы сопровождаются снижением мышечного тонуса, что способствует атрофии мышц, принимающих непосредственное участие в осуществлении дыхательного акта, пролиферация фиброзной ткани и жировым отложениям между мышечными волокнами, что обуславливает общий характер изменения структуры и функции грудной клетки.
Возрастные изменения системы кровообращения значительно ограничивают адаптационные возможности организма, создают предпосылки для развития атеросклероза, гипертонической болезни, ишемической болезни сердца и мозга. Повышается систолическое артериальное давление и пульсовое давление, происходит расширение венозного русла, снижение тонуса, эластичности венозной стенки - определяющих факторов понижения венозного давления крови. Снижение мышечного тонуса и снижение присасывающего действия грудной клетки уменьшают возврат крови к сердцу. Ослабление симпатических экстракардиальных влияний способствует урежению ЧСС. С возрастом меняется также и процесс реполяризации, происходит уширение комплекса QRS; несмотря на развитие возрастной эмфиземы легких, электрическая ось сердца отклонена влево, что свидетельствует о преимущественных изменениях миокарда левого желудочка.
Вот почему особое внимание следует уделять здоровью стажированных работников, у которых вышеприведенные факторы обостряются из-за дополнительного влияния вредных производственных факторов таких как шум, влияние токсикантов, вибрация и т.п.
Артериальная гипертензия (АГ) и хроническая обструктивная болезнь легких (ХОБЛ) имеют общие производственные и непроизводственные факторы риска, обусловливающие развитие и прогрессировании каждого из заболеваний: образ жизни (курение, низкая физическая активность, острый и хронический стресс), общебиологические процессы (физиологическое старение), наличие соматической патологии (избыточный вес, метаболический синдром), производственные факторы и условия труда.
Хроническое воздействия химических аэрозолей и пыли на эндотелий бронхов формирует дисбаланс активности про- и антиоксидантных систем, что сопровождается неконтролируемой липопероксидацией и накоплением продуктов перекисного окисления липидов, оказывающих цитотоксическое и провоспалительное действие с развитием хронического бронхита и ХОБЛ. Гипоксия, развившаяся вследствие хронического бронхита/ХОБЛ, нарушает функционирование эндотелий-зависимых вазодилатирующих механизмов, что способствует повышению артериального давления (АД). Патогенез развития пульмогенной АГ обусловлен морфологической перестройкой легочной ткани и бронхиального дерева, последующими нарушениями легочного газообмена и гемодинамики малого круга кровообращения, формированием гипоксии, гиперкапнии и нарушений метаболизма вазоактивных веществ (катехоламинов, серотонина, гистамина, кининов, ангиотензина II). Снижение содержания кислорода в крови и тканях стимулирует хеморецепторы артериальных и венозных сосудов, усиливает афферентные возбуждающие влияния на вегетативные нейроны, и усиливает эфферентную симпатическую вазоконстрикторную активность на периферии. По мере усугубления бронхиальной обструкции и прогрессирования АГ повышается центральная β-адренергическая и дофаминергическая активность. Повышение активности симпатоадреналовой системы (САС) способствует нарушению функционального состояния гипоталамо-гипофизарной системы и усилению модулирующего влияния адренокортикотропного гормона на минералокортикоидную функцию надпочечников, что приводит к увеличению секреции альдостерона. Активация ренин-ангиотензин-альдостероновой системы (РААС) происходит как при непосредственном развитии гемической гипоксии в ткани почек, так и опосредованно - через активацию САС. Хроническое сочетанное воздействие таких производственных факторов, характерных для химических производств, как наличие аэрогенных химических токсикантов, производственного шума, вибрации, тяжесть и напряженность трудового процесса, повышают на 25-30% частоту развития у работников гиперхолестеринемии и артериальной гипертензии, что обусловлено активацией симпатического отдела вегетативной нервной системы и гипоталамо-гипофизарно-надпочечниковых механизмов высвобождения кортикотропин-рилизинг-фактора, адренокортикотропного гормона и глюкокортикоидов.
Было установлено, что предикторами профессиональной и производственно обусловленной кардиореспираторной патологии у работников химических производств являются: сочетанное развитие хронических заболеваний верхних дыхательных путей и астено-невротического/астено-вегетативного синдромов с ежегодным снижением показателя объема форсированного выдоха за первую секунду (ОФВ1) (до 35 мл ежегодно) и реакции эндотелия в пробе эндотелий-зависимой вазодилатации (на 0,3% и более ежегодно); наличие рентгенологических признаков умеренного перибронхиального фиброза с прогредиентным течением; незначительное расширение правых границ сердца на фоне повышения антиоксидантной активности плазмы (АОА), эритропоэтина, оксида азота, фактора роста эндотелия сосудов (VEGF), гомоцистеина и С-реактивного белка высокочувствительного (hs-СРБ) более чем на 10% от верхней границы нормы.
Благодаря тому, что диагностику работников производят путем определения совокупности именно объективных (а не субъективных) показателей, обеспечивается наиболее надежная и точная оценка отнесения работника именно к группе высокого риска развития производственно обусловленной кардиореспираторной патологии.
Благодаря тому, что при реализации предлагаемого способа осуществляют последующее сопоставление указанных лабораторных и физиологических показателей с нормативными значениями, обеспечивается наиболее точная оценка установления вероятности нарушения здоровья стажированных работников в плане кардиореспираторной патологии, которая будет носить производственно обусловленный характер.
Исходя из вышеизложенного, можно сделать вывод, что поставленный технический результат обеспечивается за счет совокупности операций предлагаемого способа, их последовательности и режимов его реализации.
При реализации предлагаемого способа осуществляют следующие операции в нижеуказанной последовательности:
1. На первичном этапе проводят отбор для последующего медицинского обследования работников химических производств, со стажем работы 10 лет и более и с возрастом 45 лет и старше.
2. Проводят клинический осмотр рабочих на предмет выявления следующих параметров: изменения формы грудной клетки (не изменена, или эмфизематозная), снижения экскурсии нижнего края, повышения резистентности грудной клетки, перкуторный звук (притупление перкуторного звука, перкуторный звук с коробочным оттенком); характеристика дыхания (ослабление везикулярного дыхания), наличие хрипов (хрипы вне обострения не выслушиваются); границы сердца (незначительное увеличение границ вправо и влево), верхушечный толчок (высокий), акцентуация тонов (акцентуация тонов сохранена или акцент II тона на a. Puim), шумы сердечные (не выслушиваются), частота сердечных сокращений (ЧСС) - бради- или тахикардия, артериальное давление (АД) - выше 130/80 мм. рт.ст.
3. Проводят последующее определение функциональных показателей: положение электрической оси сердца, сегмента ST, зубец R, зубец Т, зубец Р, желудочковый комплекс на ЭКГ; ОФВ1, ФЖЕЛ, соотношении ОФВ1/ФЖЕЛ, остаточный объем легких, объемная скорость форсированного выдоха (СОС25-75) по результатам спирографии; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка форсированного выдоха за секунду»; ежегодное снижение ОФВ1 в сравнении с результатами предыдущего года и темпа снижения функциональной активности эндотелия в пробе эндотелий зависимая вазодилатация плечевой артерии в динамике (учитывая, что работники химических производств раз в год проходят обязательный медицинский осмотр, то реакцию эндотелия измеряют у работника ежегодно).
4. Проводят определение следующих лабораторных показателей в пробе крови: уровня гемоглобина (Hb), эритроцитов, гидроперекиси липидов (ГПЛ), малонового диальдегида (МДА), антиоксидантной активности плазмы (АОА), эритропоэтина, оксида азота, фактора роста эндотелия сосудов (VEGF), гомоцистеина и высокочувствительного С-реактивного белка (hs-СРБ).
5. Осуществляют последующее сопоставление всех указанных лабораторных и функциональных показателей с физиологической нормой (Функциональная диагностика: национальное руководство / под ред. Н.Ф. Берестень, В.А. Сандрикова, С.И. Федоровой. - М.: ГЭОТАР-Медиа, 2019. - 784 с: ил. - (Серия "Национальные руководства"). - ISBN 978-5-9704-4242-5. Клиническая лабораторная диагностика: руководство. В 2 томах / Под ред. В.В. Долгова. 2012. - 928 с. (Серия "Национальные руководства") - ISBN 978-5-9704-2129-1).
6. Обследованных работников относят к группе высокого риска развития производственно обусловленной кардиореспираторной патологии, если у них имеются следующие отклонения от физиологической нормы:
- превышение от верхней границы нормы более чем на 10% уровней Hb, эритроцитов, ГПЛ, МДА, VEGF, гомоцистеина и hs-СРБ,
- превышение от верхней границы нормы более чем на 20% уровня АОА,
- понижение от нижней границы нормы более чем на 10% уровня эритропоэтина и оксида азота,
- при одновременном установлении методом электрокардиографии отклонения электрической оси сердца вправо до 100 градусов; косонисходящей депрессии сегмента ST в V6; отрицательного зубца Т в стандартных отведениях; отрицательного зубца Т в V1; желудочкового комплекса типа rSR'; вольтажа зубца R' более 7 мм, высокого зубца R в отведении V6, зубца Р более 2 мм на электрокардиограмме (ЭКГ);
при установлении методом спирографии ОФВ1 меньше 80% от нормы; соотношении ОФВ1/ФЖЕЛ равном 65%-70%; показателя СОС25-75 - 70%-75%; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка ОФВ за секунду» на 8-12% от должного; ежегодное снижение ОФВ1 35-50 мл в год, темп снижения функциональной активности эндотелия за год больше чем на 0,3%.
При реализации предлагаемого способа лабораторная диагностика выполнялась по стандартным методикам с помощью автоматического гематологического AcT5diff AL (Beckman Coulter Inc., США, Франция), биохимического Keylab» (BPC+Biosed, Италия) анализаторов.
Ультразвуковая оценка состояния эндотелия сосудов проводилась по модифицированной методике Celermajer D.S. с соавт. (1992) на портативном ультразвуковом сканере Viamo SSA-640A (Toshiba medical, Япония) с использованием линейного датчика 7 МГц. Диаметр плечевой артерии и максимальную скорость кровотока измеряли в продольном сечении на 2-5 см выше локтевого сгиба в состоянии покоя за 30 с до компрессии, вызванной с помощью манжеты сфигмоманометра, наложенной выше места визуализации плечевой артерии и накачанной до давления, на 50 мм рт. Ст. превышающего систолическое. Продолжительность компрессии составляла 5 мин. Диаметр плечевой артерии и максимальную скорость кровотока определяли на 60-й секунде после удаления воздуха из манжеты. Изменения диаметра сосуда оценивали в процентном отношении к исходной величине. За нормальную реакцию плечевой артерии принималось ее расширение на 10 и более процентов от исходного уровня. Меньший прирост или вазоконстрикция трактовались как нарушение функции эндотелия.
Запись ЭКГ проводилась на аппарате Shiller AT-102plus по стандартной методике (Schiller AG, Швейцария, зав. номер 025.13126).
Анализ функции внешнего дыхания (ФВД) выполнен на спирометре Schiller SP-1 с применением датчика SP-20 (Schiller AG, Швейцария, зав. номер 542.10636) с использованием для расчета должных величин стандарты по ITS.
Для доказательства правомерности применяемых в предлагаемом способе оценочных вероятностных показателей (отклонения функциональных и лабораторных показателей) были использованы методы непараметрической статистики, модели логистической регрессии. Оценка параметров моделей выполнена с использованием программных продуктов, сопряженных с приложениями MS-Office. Оценку достоверности и адекватности полученных моделей осуществляли по критерию Фишера, коэффициенту детерминации [С. Гланц, 1998].
Для оценки связи условий труда с состоянием здоровья работающих использовались эпидемиологические методы исследования, включающие расчет отношения шансов (OR), относительного риска (RR) и этиологической доли ответов, обусловленной воздействием фактора профессионального риска (EF), которые позволяют изучить причинно-следственные связи между воздействием неблагоприятных факторов производственного процесса и частотой возникновения отдельных видов ответов со стороны здоровья работающих. Для оценки достоверности полученных данных использовался 95%-й доверительный интервал (CI). Наличие связи считается достоверно установленным в случае, если нижняя граница доверительного интервала больше единицы (Р 2.2.1766-03 «Руководство по оценке профессионального риска здоровья работников, организационно-методические основы. Принципы и критерии оценки»).
Пример конкретного осуществления.
Для доказательства возможности реализации способа определения диагностической значимости указанных в предлагаемом способе лабораторных и функциональных критериев, были обследованы работники химического производства, а именно, работники металлургического предприятия:
- группа наблюдения: 225 работников металлургического предприятия, средний возраст 49,7±4,7 лет, средний стаж - 25,4±5,3 лет (плавильщик цветных металлов, разливщик металла, электролизник, хлораторщик);
- группа сравнения: 97 представителей административного аппарата предприятия; средний возраст 47,4±5,5 лет (р>0,05), средний стаж 22,8±6,3 лет (р>0,05).
Все обследованные мужчины.
Условия труда указанных работников оценивали по результатам специальной оценки условий труда (СОУТ) и в соответствии с «Руководством по гигиенической оценке факторов рабочей среды и трудового процесса. Критерии и классификация условий труда. Р 2.2.2006-05».
Общая оценка условий труда у работников группы наблюдения, соответствует классу 3.2-3.3. Основные производственные вредности: пыль респирабельной фракции и химические вещества, состав которых определялся характером материалов и особенностями технологического процесса. В воздухе рабочей зоны (ВРЗ) доля взвешенных частиц (пыли) размерами до 2,5 мкм включительно составляла до 10%, а частиц размерами менее 10 мкм включительно от 28 до 47%. Шум превышал предельно допустимый уровень (ПДУ) от 1 до 7 дБА, общая вибрация превышала ПДУ от 1,5 до 1,7 раза, параметры микроклимата определяли нагревающий микроклимат в теплый период года и охлаждающий в холодный. Тепловая нагрузка среды превышала нормативный уровень от 3,4 до 10°С.
Категория априорного профессионального риска у работников группы наблюдения соответствует высокому (непереносимому).
У работников группы сравнения условия труда соответствуют классу условий труда 2 (допустимый).
Обследование включало клинический осмотр, определение функциональных показателей систем кровообращения и дыхания методом электрокардиографии (ЭКГ) и спирографии (СПГ); оценку функциональной активности эндотелия сосудов в пробе постокклюзионной эндотелий зависимой вазодилатации плечевой артерии; и лабораторных показателей крови (содержание гемоглобина и эритроцитов в крови, гидроперекиси липидов, малонового диальдегида, антиоксидантной активности плазмы, эритропоэтина, оксида азота, фактора роста эндотелия сосудов, гомоцистеина и С-реактивного белка).
Среднегрупповые значения клинических, лабораторных и функциональных показателей, характеризующих механизм развития кардиореспиратоной патологии, у работников группы наблюдения существенно превышают аналогичные показатели группы сравнения (таблица 1).
Этими испытаниями был доказан выбор достоверно значимых вероятностных показателей, посредством которых возможно оценивать вероятность нарушения здоровья, связанного с развитием производственно обусловленной кардиореспиратоной патологии у стажированных работников химических производств, подвергающихся сочетанному воздействию комплекса вредных производственных факторов: пыли респирабельной фракции и химических веществ; шума, вибрации и микроклимата, т.е. работающих во вредных условиях труда. Ниже приведено обоснование того, почему у стажированных работников химических производств может возникнуть производственно обусловленная кардиореспираторная патология.
Для доказательства негативного влияния сочетанного воздействия производственных факторов (пыль респирабельной фракции и химические веществ; шум, вибрация и микроклимат) на работников группы наблюдения в качестве критериев оценки отклонений лабораторных показателей использованы уровни лабораторных и функциональных показателей обследованного контингента группы сравнения.
Производственная пыль оказывает аддитивный эффект на развитие респираторных симптомов и вызывает воспалительные реакции на уровне эндотелия респираторного тракта, в результате чего происходят активация воспалительного ответа и образование цитокинов. Производства, связанные с ингаляционными токсинами, пылью, химическими испарениями повышает риск и могут стать причиной обструктивной болезни легких. Пыль мелких фракций способствует проникновению химических веществ в нижние отделы респираторного тракта, вызывая воспалительную реакции. Сочетанное ингаляционное воздействие мелкодисперсной пыли и химических веществ взаимно усиливают повреждающее действие на слизистую оболочку дыхательных путей. Производственная пыль, образующаяся при различных технологических процессах, вызывает механическое повреждение слизистой оболочки дыхательных путей, инициируя инфильтративно-пролиферативный воспалительный процесс, в результате чего повышается чувствительность тканей к воздействию химических веществ. Дополнительное воздействие химических веществ, обладающих выраженным раздражающим действием (хлор и его соединения и др.), усиливает альтеративно-эксудативную фазу воспаления. Мелкие частицы (такие как РМ2,5) способны проникать в нижние отделы легких и альвеолы, и запускать ряд механизмов, лежащих в основе долгосрочных эффектов: воздействие на вегетативную нервную систему (снижение вариабельности ритма сердца), процессы проведения и реполяризации, а также системные воспалительные реакции, которые включают в себя эндотелиальную дисфункцию, оксидативный стресс. Хроническое воздействия химических аэрозолей и пыли на эндотелий бронхов формирует дисбаланс активности про- и антиоксидантных систем, что сопровождается неконтролируемой липопероксидацией и накоплением продуктов перекисного окисления липидов, оказывающих цитотоксическое и провоспалительное действие с развитием хронического бронхита и хронической обструктивной болезни легких (ХОБЛ). Гипоксия, развившаяся вследствие хронического бронхита/ХОБЛ, нарушает функционирование эндотелий-зависимых вазодилатирующих механизмов, что способствует повышению артериального давления (АД). В настоящее время определены три основных механизма воздействия взвешенных в воздухе частиц на сердечно-сосудистую систему: классический путь - высвобождение в системную циркуляцию провоспалительных медиаторов, продуцированных в легких (IL-6, TNF-α, субстанция Р, нейрокинин А); альтернативный путь - непосредственное проникновение частиц из легких в системный кровоток; и центральный путь, согласно которому взвешенные частицы, стимулируя альвеолярные рецепторы, влияют на вегетативную нервную систему. Развитие легочной гипертензии запускает каскад структурно-функциональных изменений миокарда и сосудов большого круга кровообращения, что лежит в основе развития системной АГ. Механизм прогипертензивного действия пылевых частиц связан с развитием рефлекторного дисбаланса вегетативной нервной системы в сочетании с эндотелиальной дисфункцией на фоне оксидативного стресса.
Производственный шум способствует повышению систолического и/или диастолического артериального давления, дислипидемии, активацияперекисного окисления липидов и образования активных форм кислорода, системные воспалительные реакции, нарушение функциональной активности эндотелия. Прогипертензивное действие шума находится в прямой зависимости от интенсивности, частоты и продолжительности его воздействия и характеризуется развитием нейроциркуляторного синдрома, протекающего с гипертензивными реакциями и тенденцией к переходу в АГ. Шум активирует стрессовые реакции с повышением тонуса симпатической нервной системы, ростом уровня кортикостероидов, катехоламинов и ангиотензина II в крови на фоне снижения активности эндотелиальной NO-синтетазы, что в совокупности определяет развитие эндотелиальной дисфункции.
Производственная вибрация является доказанным прогипертензивным фактором и характеризуется развитием нейроциркуляторного синдрома, протекающего с гипертензивными реакциями. Вибрация вызывает нарушение вегетативно-сосудистой регуляции на сегментарном и надсегментарном, включая лимбико-ретикулярный комплекс, гипоталамус. Происходит активация симпатического отдела вегетативной нервно системы (ВНС), что приводит к вагоспазму, на фоне депрессии парасимпатического отдела ВНС. В результате повреждения мелких сосудов эндотелия происходит высвобождение эндотелиина и тромбоксана А2, которые вызывают вазоконстрикцию без регулирующего влияния вегетативной нервной системы (ВНС).
Следует учитывать также, что функциональные возможности с возрастом снижаются. Это связано и с тем, что количество функциональных единиц органов и митотическая активность обновляющихся органов уменьшаются: количество альвеол в легких, сосудистых клубочков в различных органах, интенсивность деления клеток других обновляющихся тканей также уменьшаются в процессе старения организма.
Неблагоприятный микроклимат производственных помещений обусловливает снижение адаптационных возможностей организма; происходит интенсивное биологическое старение рабочих. Происходит снижение симпатического вазоконстриктивного тонуса. Значительное напряжение гемодинамики проявляется в виде стойких нейроциркуляторных дистоний по гипертоническому типу, миокардиопатий, повышению ЧСС и соответственно увеличением минутного объема кровообращения. Хроническое тепловое воздействие сопровождается повышением функциональной активности коры надпочечников. Хроническое тепловое воздействие вызывает гиперкоагуляцию крови, в крови увеличивается количество продуктов тепловой денатурации белков крови и тканей, а также недоокисленных продуктов нарушенного тканевого обмена.
Пониженные температуры воздуха в результате активации симпатического отдела вегетативной нервной системы (ВНС) увеличивается минутный объем дыхания, усиливается легочная вентиляция; увеличивается число тромбоцитов и эритроцитов в крови, содержание холестерина, вязкость крови; повышается гликогенолиз; усиливается секреция адреналина. Охлаждение слизистой дыхательных путей способствует снижению резистентности респираторного тракта, индуцируя воспалительные реакции. Напряжение центра терморегуляции проявляется активацией симпатического отдела ВНС, ангиоспазмами. Снижение температуры вызывает увеличение концентрации тропных гормонов гипоталамуса, гормонов щитовидной железы (тироксин и др.) и надпочечников (адреналин и др.), которые усиливают окислительные процессы, активируют ферменты, катализирующие гликогенолиз в скелетных мышцах и печени, а также липолиз в жировой ткани.
Возрастные изменения дыхательной системы сопровождаются снижением мышечного тонуса, что способствует атрофии мышц, принимающих непосредственное участие в осуществлении дыхательного акта, пролиферация фиброзной ткани и жировым отложениям между мышечными волокнами), что обуславливает общий характер изменения структуры и функции грудной клетки. При форсированном вдохе и выдохе разница периметров грудной клетки, подвижность нижних краев легких и экскурсия диафрагмы уменьшаются. С возрастом изменяются и сами легкие: уменьшаются в размере, массе и становятся малоподвижными. Уменьшение упругости эластических волокон и их атрофия приводят к необратимому растяжению и утрате структуры альвеол, исчезновению межальвеолярных перегородок, расширению альвеолярных ходов. Развиваются эмфизематозные возрастные изменения, сопровождающиеся уменьшением газообменной поверхности легких. Снижается жизненная емкость легких, уменьшается ряд ее компонентов: дыхательный объем, резервный объем вдоха и выдоха. Вместе с тем возрастает объем остаточного воздуха и особенно его доля в общей емкости легких. Снижение эффективности дыхания с возрастом обусловлено увеличением вентиляции легких и возникающим в результате молекулярных, структурных и функциональных изменений снижением окислительного метаболизма и гипоксией. Возрастные изменения системы кровообращения значительно ограничивают адаптационные возможности организма, создают предпосылки для развития атеросклероза, гипертонической болезни, ишемической болезни сердца и мозга. Повышается систолическое артериальное давление и пульсовое давление, происходит расширение венозного русла, снижение тонуса, эластичности венозной стенки - определяющих факторов понижения венозного давления крови. Снижение мышечного тонуса и снижение присасывающего действия грудной клетки уменьшают возврат крови к сердцу. Ослабление симпатических экстракардиальных влияний способствует урежению ЧСС. С возрастом меняется также и процесс реполяризации, происходит уширение комплекса QRS; несмотря на развитие возрастной эмфиземы легких, электрическая ось сердца отклонена влево, что свидетельствует о преимущественных изменениях миокарда левого желудочка; удлиняется электрическая систола сердца; замедляется распространение возбуждения в предсердиях (расширение, уплощение, деформация зубца Р); несколько замедляются атриовентрикулярная проводимость и распространение возбуждения по миокарду желудочков; отмечается снижение сердечного выброса; снижается функциональный резерв сердечного выброса. В процессе биологического окисления образуются и полувосстановленные формы кислорода, обладающие большой реакционной способностью. Все активные формы кислорода: O2, ОН⋅ и H2O2 при взаимодействии со структурами клетки повреждают их вследствие переокисления липидов, инактивации белков или повреждения нуклеиновых кислот.
Сравнительный анализ изменений показателей нарушения регуляции сосудистого тонуса показал повреждающее действие комплекса производственных факторов на эпителий дыхательных путей и эндотелий сосудов, что подтверждается выявленными нарушениями в результате ЭКГ, СПГ и ультразвукового исследования (УЗИ) плечевой артерии: Р-pulmonale и признаки гипертрофии левого желудочка (ГЛЖ); ежегодное снижение ОФВ1 на 35-50 мл в год, ОФВ1/ФЖЕЛ<70%, увеличение остаточного объем легких, снижение СОС25-75 <20%; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка форсированного выдоха за секунду» на более 12%; темп снижения реакции эндотелия 0,3% за год.
Данные изменения свидетельствуют о высоком риске развития кардиореспираторной патологии.
Исследованные лабораторные параметры показали статистически значимые изменения между группами, которые отражают ряд субклинических особенностей функционирования системы кровообращения и дыхания у работников химических производств.
Таким образом, вышеприведенные данные показывают, что указанные в заявляемом способе клинические, лабораторные и функциональные показатели в группе наблюдения, уровень которых достоверно отличается от уровня в группе сравнения и направленность их отклонения от физиологической нормы, биологически правдоподобна, поэтому они могут служить в качестве критериев при оценке риска развития кардиореспираторной патологии у работников химических производств.
Ниже приведены примеры конкретного осуществления реализации предлагаемого способа для работников шахт с различной степенью риска вероятности нарушения здоровья, связанного с развитием производственно обусловленной артериальной гипертензии.
Пример 1. Работник А (возраст 46 лет, стаж работы на металлургическом производстве 11 лет 8 мес.) предъявляет жалобы при опросе на повышенную утомляемость, снижение переносимости физических нагрузок, одышку при физической нагрузке, эпизодическое повышение АД после физической нагрузки до 140/90 мм рт.ст., редкий кашель с небольшим количеством слизистой мокроты.
По результатам осмотра: состояние удовлетворительное, избыток массы тела (ИМТ 29,1 кг/м2), кожные покровы физиологической окраски, нормальной влажности. Стойкий красный дермографизм. Грудная клетка правильной формы, незначительное увеличение нижних границ; экскурсия нижнего края умеренно снижена, резистентность грудной клетки умеренно повышена. При перкуссии определяется притупление перкуторного звука; аускультативно - дыхание везикулярное, равномерно ослаблено, хрипы не выслушиваются; частота дыхания 15 в мин. Границы сердца смещены вправо на 0,5 см; верхушечный толчок высокий. При аускультации - акцентуация тонов сохранена, шумы не выслушиваются. АД 145/85 мм рт.ст., пульс 58 уд. в мин. По результатам функционального обследования:
• при ЭКГ - Сердечный ритм: синусовый с ЧСС 56. Отклонение электрической оси вправо (α+95°). Зубец Р во II и III отведениях остроконечный, 2,2 мм; RV6 37 мм; SV3 + RaVL = 2,9 мв; расширение QRS (95 мс) (признаки P-pulmonale и гипертрофии левого желудочка (ЛЖ))
• при СПГ - Форсированная жизненная емкость легких (ФЖЕЛ) 79%, объем форсированного выдоха на 1 сек (ОФВ1) 56%, ОФВ1/ ФЖЕЛ 70%, средняя объемная скорость на уровне 25-75% (СОС 25-75) 71% (Нарушение вентиляционной способности по обструктивному типу легкое снижение). Снижение ОФв1 в течение года 37 мл.
• Проба постокклюзионной реактивной гиперемии на плечевой артерии - исходные данные: диаметр артерии, D0: 0,44 см, пиковая систолическая скорость кровотока, Vmax0: 81 см/с, Параметры после реокклюзии: диаметр артерии: D1: 0,47 см, пиковая систолическая скорость кровотока, Vmax1: 92 см/с. Изменение диаметра плечевой артерии 0,03 см, относительный прирост диаметра артерии: 6,82%, напряжение сдвига на эндотелии исходное: Т0: 36,82, напряжение сдвига на эндотелии после пробы: Т1: 39,15 чувствительность плечевой артерии к напряжению сдвига, К: 1,08. Толщина комплекса интима-медиа (КИМ)=0,7 мм. Признаки дисфункции эндотелия
Оценка функционального состояния эндотелия плечевой артерии в динамике - темп снижения реакции эндотелия за год 0,4%.
По лабораторным данным наблюдается:
• Содержание эритроцитов 6,4*1012/куб.дм (превышение верхней границы нормы (ВГН) на 10,1%).
• Уровень Hb 194 г/ куб.дм (превышение ВГН на 11,2%).
• Уровень МДА 2,9 мкмоль/куб.см /л. (превышение ВГН на 11,2%)
• Уровень VEGF 799,40 пг/мл (превышение ВГН на 14,2%)
• Уровень hs-СРБ 13,2 (превышение ВГН на 10,8%)
• Уровень ГПЛ 412,4 мкмоль/куб.дм (превышение ВГН на 14,7%)
• Уровень гомоцистеина 17,23 мкмоль/куб.дм (превышение ВГН на 14,8%)
• Уровень АОА 47,2% (превышение ВГН на 22%)
• Уровень оксида азота 61,3 мкмоль/куб.дм (снижение нижней границы нормы (НГН) на 12,8%)
• Уровень эритропоэтина 7,2 мМЕ/куб.мм (снижение НГН на 11,2%).
Для данного стажированного работника вероятность развития производственно обусловленной кардиореспираторной патологии расценена как высокая и он может быть отнесен к группе высокого риска.
Пример 2. У работника Б (возраст 48 лет, стаж работы на металлургическом производстве 15 лет 2 мес.) при опросе жалобы на повышенную утомляемость, снижение переносимости физических нагрузок, одышку во время и после работы, эпизодическое повышение АД до 150/90 мм рт.ст., чаще после физической нагрузки, кашель во время физической нагрузки со слизистой мокротой.
По результатам осмотра: состояние удовлетворительное, ожирение I степени (ИМТ 32,3 кг/м2), кожные покровы бледноватые, влажные, умеренно выраженный цианоз губ. Смешанный дермографизм. Грудная клетка эмфизематозная; экскурсия нижнего края снижена, резистентность грудной клетки повышена. При перкуссии определяется перкуторный звук с коробочным оттенком; аускультативно - дыхание везикулярное, равномерно ослаблено, проводится во все отделы, хрипы не выслушиваются; частота дыхания 14 в мин. Границы сердца смещены вправо на 1 см; верхушечный толчок высокий. При аускультации - акцент II тона во II межреберье слева (на a. pulm), шумы не выслушиваются. АД 145/90 мм рт.ст., пульс 60 уд. в мин.
По результатам функционального обследования:
• при ЭКГ - Сердечный ритм: синусовый с ЧСС 56. Отклонение электрической оси вправо (α+90°). Зубец Р во II отведении остроконечный, 2,1 мм; RV6 35 мм; SV3 + RaVL = 2,7 мв; расширение QRS (98 мс) (признаки P-pulmonale и гипертрофии ЛЖ)
• при СПГ-Форсированная жизненная емкость легких (ФЖЕЛ) 61%, объем форсированного выдоха на 1 сек (ОФВ1) 70%, ОФВ1/ ФЖЕЛ 65%, средняя объемная скорость на уровне 25-75% (СОС 25-75) 75% (Нарушение вентиляционной способности по рестриктивному типу умеренное снижение). Снижение ОФВ1 в течение года 48 мл.
• Проба постокклюзионной реактивной гиперемии на плечевой артерии - исходные параметры: диаметр артерии, D0: 0,32 см, пиковая систолическая скорость кровотока, Vmax0: 26,92 см/с. Параметры после реокклюзии: диаметр артерии, D1: 0,35 см, пиковая систолическая скорость кровотока, Vmax1: 100,38 см/с. Изменение диаметра плечевой артерии: 0,03 см, относительный прирост диаметра артерии: 9,38%, напряжение сдвига на эндотелии исходное: Т0: 16,825, напряжение сдвига на эндотелии после пробы: T1: 57,36 чувствительность плечевой артерии к напряжению сдвига, К: 0,0389. Толщина КИМ: 1,1 мм. Признаки дисфункции эндотелия. Оценка функционального состояния эндотелия плечевой артерии в динамике - темп снижения реакции эндотелия 0,36%.
По лабораторным данным наблюдается:
• Содержание эритроцитов 6,6*1012 /куб.дм (превышение ВГН на 14,2%).
• Уровень Hb 196 г/куб.дм (превышение ВГН на 12,8%).
• Уровень МДА 2,7 мкмоль/куб.см /л. (превышение ВГН на 10,5%)
• Уровень VEGF 803,60 пг/мл (превышение ВГН на 14,8%)
• Уровень hs-СРБ 13,4 (превышение ВГН на 11,2%)
• Уровень ГПЛ 416,2 мкмоль/куб.дм (превышение ВГН на 15,6%)
• Уровень гомоцистеина 17,17 мкмоль/куб.дм (превышение ВГН на 14,5%)
• Уровень АОА 45,8% (превышение ВГН на 20,5%)
• Уровень оксида азота 61,3 мкмоль/куб.дм (снижение НГН на 12,8%)
• Уровень эритропоэтина 7,04 мМЕ/куб.мм (снижение НГН на 12%)
Для данного стажированного работника вероятность развития производственно обусловленной кардиореспираторной патологии также расценена как высокая и он может быть отнесен к группе высокого риска.
Данные, полученные в ходе реализации предлагаемого способа, необходимы для решения экспертных вопросов о возможности минимизации риска развития кардиореспираторной патологии у стажированных работников химических производств для сохранения работы в профессии.
Выбор числовых параметров вероятностных показателей для группы стажированных работников высокого риска развития, был обусловлен тем, что отклонения функциональных и лабораторных показателей носят стойкий патологический характер даже при отсутствии жалоб и клинической картины, характеризуются астеновегетативным синдромом и являются начальными признаками кардиореспираторной патологии.
При оценке предлагаемым способом риска развития производственно обусловленной кардиореспираторной патологии у работников химических производств принималось во внимание следующее:
структурные изменения сердца при кардиореспираторной патологии имеют общие звенья патогенеза: развитие эндотелиальной дисфункции и воспаление:
- Эндотелий зависимая вазодилатация характеризует процессы эндотелиальной дисфункции, которая является одним из основных патогенетических механизмов развития как АГ, так и ХОБЛ;
- ремоделирование сердца представляет собой компенсаторную реакцию, однако истощение функциональных резервов приводит к дезадаптивным последствиям: бессимптомное увеличение левого желудочка и перегрузка правых отделов сердца. Данные изменения могут быть связаны с производственными факторами, которые непосредственно не касаются строения сердца и его функционирования, например, тепловое излучение, физические и эмоциональные перегрузки, но способны вызывать серьезные гемодинамические нарушения, повышая риск внезапной смерти;
- нарушения функции внешнего дыхания, характеризующиеся снижением легочных объемов (рестриктивные нарушения), у работников химических производств являются ранними признаками поражения органов дыхания, часто даже при сохраненных показателях СПГ. Гипервентиляция может изначально носить компенсаторный характер (чрезмерная компенсация), связанный с возбуждением дыхательного центра (воздействие высоких температур, химических веществ);
- основные функции VEGF (сигнальный белок, вырабатываемый клетками для стимулирования васкулогенеза) - создание новых кровеносных сосудов; может быть вызвано в клетках, которые не получают достаточного количества кислорода;
- недостаточное количества кислорода также стимулирует эритропоэз;
- оксид азота (II) критически важен для регуляции нормального сосудистого тонуса, как медиатор вазодилатации (расширения сосудов). Выработка оксида азота (II) усиливается при воздействии различных факторов, таких, как гипоксия, повреждение тканей (в частности, повреждение эндотелия сосудов) и др. Через ряд промежуточных стадий это приводит к изменению активности сократительных белков гладкомышечной клетки. Конечным результатом этого является расслабление гладкомышечной клетки, вазодилатация и усиление кровотока. Оксид азота (II) также воздействует на миокард. Малые концентрации оксида азота повышают сократительную функцию миокарда, частоту сердечных сокращений и сердечный выброс, ударный и минутный объем сердца, что компенсирует вызываемую им в результате вазодилатации гипотензию, а в комплексе с вызываемой оксидом азота вазодилатацией и бронходилатацией позволяет ликвидировать гипоксию, улучшить доставку кислорода к тканям. Более высокие концентрации оксида азота, напротив, ограничивают работу сердца, понижая его сократительную функцию, частоту и силу сердечных сокращений и уменьшая потребление миокардом кислорода одновременно с увеличением коронарного кровотока. Эти свойства служат основанием для применения органических нитратов при ишемической болезни сердца и при сердечной недостаточности. В физиологических условиях оксид азота (II) является одним из важных регуляторов сократительной функции миокарда и потребления миокардом кислорода;
- в процессе жизнедеятельности в организме человека образуются свободные радикалы. Это очень активные обрывки молекул, которые вступают в химические реакции с клеточными оболочками и ДНК; образование большого количества свободных радикалов является начальной стадией кардиореспираторной патологии - свободные радикалы могут повреждать эндотелий артерий, ускорять физиологическое старение. В организме существует система антиоксидантной защиты. Срыв антиоксидантной защиты характеризуется развитием свободнорадикальных повреждений разных компонентов клетки и тканей;
- С-реактивный белок (СРБ) - это основной белок плазмы крови, отражающий воспалительные процессы в организме. Рост этого протеина также замечен при низком фоновым воспалении в организме, что может предвещать повышение риска сердечно-сосудистых заболеваний; С-реактивный белок вырабатывается в ответ на воспаление и повреждение тканей тела, например, в артериях и/или легких и можно предсказать риски кардиореспираторной патологии у работников без клинической симптоматики;
- гомоцистеин является важнейшей серосодержащей аминокислотой, которая входит в состав клеток организма. Этот компонент участвует в общем метаболизме, обеспечивает нормальный кровоток и работу сердечно-сосудистой системы. По уровню гомоцистеина определяют риски развития заболеваний болезней системы кровообращен.;
Таким образом, предлагаемый способ имеет следующие преимущества перед известными способами:
- позволяет определить для работников химических производств в условиях комплекса производственных факторов (сочетанного воздействия производственного шума и вибрации выше ПДУ и концентрации пыли и химических веществ выше ПДК, параметры микроклимата) профессиональную обусловленность донозологических показателей, характеризующих механизм развития кардиореспираторной патологии;
- выделить работников высокого риска здоровью, обусловленного вероятностью развития кардиореспираторной патологии, для проведения медико-профилактических мероприятий для минимизации риска и сохранения профессиональной трудоспособности.

Изобретение относится к медицине, а именно к профилактической и реабилитационной медицине, гигиене труда, и может быть использовано для отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии. Проводят медицинское обследование работников химических производств со стажем более 10 лет путем определения диагностических лабораторных и функциональных показателей. В качестве лабораторных показателей определяют уровни гемоглобина (Hb), эритроцитов, гидроперекиси липидов (ГПЛ), малонового диальдегида (МДА), антиоксидантной активности плазмы (АОА), эритропоэтина, оксида азота, фактора роста эндотелия сосудов (VEGF), гомоцистеина и высокочувствительного С-реактивного белка (hs-СРБ). В качестве функциональных показателей определяют признаки увеличения левого и правого желудочков сердца методом электрокардиографии путем установления положения электрической оси сердца, положения сегмента ST относительно изолинии в V6 и зубца Т в V1; типа желудочкового комплекса; через размер вольтажа зубца R', высоту зубца R в отведении V6, зубца Р на электрокардиограмме (ЭКГ). Определяют объем фиксированного выдоха за 1 сек. (ОФВ11), форсированную жизненную емкость легких (ФЖЕЛ); отношение ОФВ1/ФЖЕЛ и среднюю объемную скорость форсированного выдоха (СОС25-75) методом спирографии. Осуществляют проведение функциональной пробы с использованием бронходилататора с оценкой прироста показателя «оценка форсированного выдоха за секунду», и устанавливают ежегодное снижение ОФВ1 в сравнении с результатами предыдущего года и темп снижения реакции эндотелия за год. Сравнивают результаты полученных показателей с физиологической нормой. Тех работников, у которых выявлены следующие отклонения в показателях от физиологической нормы, а именно: превышение от верхней границы нормы более чем на 10% уровня Hb, эритроцитов, ГПЛ, МДА, VEGF, гомоцистеина и hs-СРБ, превышение от верхней границы нормы более чем на 20% уровня АОА, понижение от нижней границы нормы более чем на 10% уровня эритропоэтина и оксида азота, при одновременном установлении методом электрокардиографии отклонения электрической оси сердца вправо до 100 градусов; косонисходящей депрессии сегмента ST в V6; отрицательном зубце Т в стандартных отведениях; отрицательном зубце Т в V1; желудочковом комплексе типа rSR'; вольтаже зубца R' более 7 мм, высоком зубце R в отведении V6, увеличение вольтажа Р больше 2 мм на электрокардиограмме ЭКГ; при установлении методом спирографии ОФВ1 меньше 80% от нормы; соотношении ОФВ1/ФЖЕЛ равном 65%-70%; показателя СОС25-75 - 70%-75%; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка ОФВ за секунду» на 8-12% от должного; ежегодное снижение ОФВ1 35-50 мл в год, темп снижения функциональной активности эндотелия за год больше чем на 0,3%, относят к группе работников с высоким риском развития производственно обусловленной кардиореспираторной патологии. Способ обеспечивает возможность выработки критериев отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии за счет определения совокупности лабораторных и физиологических показателей и сопоставления показателей с нормативными значениями. 1 табл., 2 пр., 2 ил.
Способ отбора стажированных работников химического производства в группу высокого риска развития производственно обусловленной кардиореспираторной патологии, характеризующийся тем, что проводят медицинское обследование работников химических производств со стажем более 10 лет путем определения диагностических лабораторных и функциональных показателей, при этом в качестве лабораторных показателей определяют уровни гемоглобина (Hb), эритроцитов, гидроперекиси липидов (ГПЛ), малонового диальдегида (МДА), антиоксидантной активности плазмы (АОА), эритропоэтина, оксида азота, фактора роста эндотелия сосудов (VEGF), гомоцистеина и высокочувствительного С-реактивного белка (hs-СРБ); а в качестве функциональных показателей определяют признаки увеличения левого и правого желудочков сердца методом электрокардиографии путем установления положения электрической оси сердца, положения сегмента ST относительно изолинии в V6 и зубца Т в V1; типа желудочкового комплекса; через размер вольтажа зубца R', высоту зубца R в отведении V6, зубца Р на электрокардиограмме (ЭКГ); объем фиксированного выдоха за 1 сек. (ОФВ11), форсированную жизненную емкость легких (ФЖЕЛ); отношение ОФВ1/ФЖЕЛ и среднюю объемную скорость форсированного выдоха (СОС25-75) методом спирографии; проведение функциональной пробы с использованием бронходилататора с оценкой прироста показателя «оценка форсированного выдоха за секунду», и устанавливают ежегодное снижение ОФВ1 в сравнении с результатами предыдущего года и темп снижения реакции эндотелия за год, сравнивают результаты полученных показателей с физиологической нормой, и тех работников, у которых выявлены следующие отклонения в показателях от физиологической нормы, а именно: превышение от верхней границы нормы более чем на 10% уровня Hb, эритроцитов, ГПЛ, МДА, VEGF, гомоцистеина и hs-СРБ, превышение от верхней границы нормы более чем на 20% уровня АОА, понижение от нижней границы нормы более чем на 10% уровня эритропоэтина и оксида азота, при одновременном установлении методом электрокардиографии отклонения электрической оси сердца вправо до 100 градусов; косонисходящей депрессии сегмента ST в V6; отрицательном зубце Т в стандартных отведениях; отрицательном зубце Т в V1; желудочковом комплексе типа rSR'; вольтаже зубца R' более 7 мм, высоком зубце R в отведении V6, увеличение вольтажа Р больше 2 мм на электрокардиограмме ЭКГ; при установлении методом спирографии ОФВ1 меньше 80% от нормы; соотношении ОФВ1/ФЖЕЛ равном 65%-70%; показателя СОС25-75 - 70%-75%; при проведении функциональной пробы с использованием бронходилататора прирост показателя «оценка ОФВ за секунду» на 8-12% от должного; ежегодное снижение ОФВ1 35-50 мл в год, темп снижения функциональной активности эндотелия за год больше чем на 0,3%, относят к группе работников с высоким риском развития производственно обусловленной кардиореспираторной патологии.
| СПОСОБ ОТБОРА СТАЖИРОВАННЫХ РАБОТНИКОВ, НАХОДЯЩИХСЯ В КОНТАКТЕ С ПАРАМИ МЕТАЛЛИЧЕСКОЙ РТУТИ, В ГРУППУ РИСКА РАЗВИТИЯ ХРОНИЧЕСКОЙ РТУТНОЙ ИНТОКСИКАЦИИ | 2011 |
|
RU2460458C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЫСОКОГО РИСКА РАЗВИТИЯ ПРОИЗВОДСТВЕННО ОБУСЛОВЛЕННЫХ И ПРОФЕССИОНАЛЬНЫХ ЗАБОЛЕВАНИЙ У РАБОТНИКОВ ХИМИЧЕСКОГО КОМПЛЕКСА, ЗАНЯТЫХ ВО ВРЕДНЫХ УСЛОВИЯХ ТРУДА | 2013 |
|
RU2545911C1 |
| Способ диагностики профессиональной хронической обструктивной болезни легких, сформировавшейся в условиях действия токсических промаэрозолей | 2016 |
|
RU2613164C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРОИЗВОДСТВЕННО ОБУСЛОВЛЕННЫХ ЗАБОЛЕВАНИЙ У РАБОТНИКОВ, ЗАНЯТЫХ ВО ВРЕДНЫХ УСЛОВИЯХ ТРУДА | 2017 |
|
RU2655815C1 |
| СПОСОБ ОЦЕНКИ РИСКА ВОЗНИКНОВЕНИЯ ПРОФЕССИОНАЛЬНОГО ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С ВОЗДЕЙСТВИЕМ ПЫЛЕВОГО ФАКТОРА | 2014 |
|
RU2564405C1 |
| ВАЛЕЕВА Э.Т | |||
| Научное обоснование системы охраны здоровья работников химической промышленности на основе оценки профессионального риска | |||
| Автореф | |||
| Диссер | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| ШАЯХМЕТОВ С.Ф | |||
| и др | |||
| Оценка | |||
Авторы
Даты
2021-02-04—Публикация
2020-06-02—Подача