Изобретение относится к области медицины, а именно неврологии и медицинской реабилитации и может использоваться для лечения и медицинской реабилитации пациентов с задним шейным симпатическим синдромом, характеризуемым нарушением кровотока в позвоночных артериях.
В настоящее время для лечения больных с задним шейным симпатическим синдромом (ЗШСС), характеризуемым нарушением кровотока в позвоночных артериях (ПА), используются две основные стратегии: лекарственная терапия и методы консервативного лечения.
По современным литературным данным, нейропротекция представляет собой комплекс медикаментозной терапии, обращенный на компенсацию развивающегося энергетического дефицита нейронов, протекцию их от влияния повреждающих факторов, активацию процессов нейрорегенерации, коррекцию тока крови в головной мозг [1]. При ЗШСС нейропротекция представляется одним из наиболее продуктивных методов профилактики хронической ишемии головного мозга, выражающийся в виде недостаточности в вертебрально-базилярном бассейне (ВББ).
Перечень медикаментозных препаратов при лечении ЗШСС: Препараты, действующие на венозный отток: полусинтетический диосмин (детралекс, флебодиа), троксерутин, гинко-билоба. Нестероидные противовоспалительные препараты: нимесулид, лорноксикам, целекоксиб, целебрекс.
Препараты, нормализующие кровоток в ПА: пентоксифиллин, винкамин, винпоцетин, циннаризин, нимодипин, ницерголин, сермион, инстенон.
Холинергические препараты: цитиколин, цераксон, рекогнан, глиатилин.
Комплексные нейропротекторные препараты: цитофлавин, актовегин, церебролизин, пирацетам, мексидол.
Препараты для нейрометаболической терапии: цитофлавин, милдронат, тиотриазолин, триметазидин.
Препараты для симптоматической терапии - миорелаксанты: толперизон, спазмолитики: дротаверин, гистаминоподобные: бетагистин, антимигренозные: суматриптан [2].
Несмотря на большое разнообразие групп препаратов, использующихся для коррекции сосудистых нарушений, эффективность ни одного из применяющихся препаратов не является достаточной, поэтому препараты чаще всего применяются в комплексе. Кроме того, необходим длительный курсовой прием данных препаратов для развития видимого эффекта, а наличие побочных эффектов в ряде случаев ограничивает их применение. Последнее наиболее актуально для группы препаратов с холинергическим действием [3].
Консервативное лечение включает в себя: медикаментозное лечение, мануальную терапию, массаж, иглорефлексотерапию, физиотерапию, санаторно-курортное лечение [4, 5].
Данные методы имеют ряд противопоказаний, например массаж противопоказан в остром периоде заболевания, мануальная терапия, иглорефлексотерапия, физиотерапевтическое воздействие имеют ряд ограничений, что сокращает контингент пациентов.
В лечении больных с ЗШСС наряду с традиционной консервативной терапией применяются пункционные методы воздействия:
блокады ПА, звездчатого узла, нижней косой мышцы головы, дерецепции межпозвоночного диска и дугоотросчатых суставов [1]. Один из главных минусов данного подхода - сложность выполнения, связанная с тем, что пункционные методы воздействия могут выполняться только анестезиологом и нейрохирургом, а также должны выполняться при наличии реанимационного отделения, так как при выполнении пункционных методов возможны побочные эффекты, связанные с воздействием местных анестетиков.
Комплексное консервативное лечение включает в себя ортопедические воздействия на источник патологии (вытяжение шейного отдела позвоночника (ШОП), иммобилизация ШОП, мануальная терапия и др.); новокаиновые блокады спастически сокращенных и болезненных мышц ШОП; физиотерапевтические и бальнеологические методы [5].
В обзорной статье В.И. Шевцова с соавторами указано, что комплексное консервативное лечение больных с вертеброгенным синдромом позвоночной артерии включает в себя ортопедические воздействия на источник патологии на фоне проводимого медикаментозного лечения (сосудорасширяющие, десенсибилизирующие, антигистаминные, анальгезирующие средства, витамины, биостимуляторы и т.д.) [4].
В качестве прототипа по наиболее близкой технической сущности нами выбран способ лечения больных с ЗШСС, заключающийся в том, что на фоне медикаментозной терапии используют ортопедическую шейную шину Шанца, которую носят в течение дня, режим ношения и курс определяется индивидуально врачом ортопедом-травматологом [6].
В данном источнике отсутствует конкретное перечисление лекарственных препаратов или групп препаратов, составляющих медикаментозное воздействие, можно лишь предположить, что авторы использовали стандартную схему, рекомендуемую при лечении больных с задним шейным симпатическим синдромом:
Правила медикаментозного лечения синдрома ПА:
1. Препараты, действующие на венозный отток: полусинтетический диосмин (детралекс, флебодиа), троксерутин, гинко-билоба.
2. Нестероидные противовоспалительные препараты: нимесулид, лорноксикам, целекоксиб, целебрекс.
3. Препараты, нормализующие кровоток в ПА: пентоксифиллин, винкамин, винпоцетин, циннаризин, нимодипин, ницерголин, сермион, инстенон.
4. Холинергические препараты: цитиколин, цераксон, рекогнан, глиатилин.
5. Комплексные нейропротекторные препараты: цитофлавин, актовегин, церебролизин, пирацетам, мексидол.
6. Метаболическая терапия: цитофлавин, милдронат, тиотриазолин, триметазидин
7. Симптоматическая терапия - миорелаксанты: толперизон, спазмолитики: дротаверин, гистаминоподобные: бетагистин, антимигренозные: суматриптан [2].
К недостаткам способа, выбранного нами в качестве прототипа, по собственным данным, относятся:
• недостаточная эффективность лечения, так как уменьшение жалоб (головокружение, головная боль, боль в шейном отделе) происходит только на период ношения, а при снятии ортопедической шейной шины Шанца жалобы больного возвращаются, а режим ношения - ограничен;
• риск растяжения капсул межпозвоночных суставов и возможность расшатывания и без того расшатанных позвоночных сегментов, что усиливает болевую импульсацию [6];
• трудность подбора нужного размера ортопедической шейной шины Шанца, так как существуют только 4 размера по высоте изделия;
• риск нарушения венозного оттока головы, что сопровождается учащением и/или увеличением головной боли, что нередко является причиной отказа больных от использования ортопедической шейной шины Шанца;
• наличие у пациентов данной группы верхнего перекрестного синдрома (протракция головы), что требует коррекции осанки грудного отдела и плечевого пояса, но при ношении ортопедической шейной шины Шанца невозможно воздействовать на вышеописанные звенья;
• снижение тонуса всех мышц шейного отдела, что оказывает негативное влияние на гиперподвижность шейного отдела, что, в свою очередь, является риском травматизации связочного аппарата суставов шейного отдела;
• эстетическая сторона, что ограничивает применения в условиях работы.
Задачей изобретения является:
• повышение эффективности лечения, проявляющейся в увеличении линейных скоростей кровотока по ПА в экстракраниальном и интракраниальном сегментах, уменьшении клинических проявлений в виде головокружения, головной боли, боли в шейном отделе, верхнего перекрестного синдрома;
• расширение контингента больных за счет больных, отказавшихся от использования ортопедической шейной шины Шанца в связи с нарушением венозного оттока головы, что сопровождалось учащением и/или увеличением головной боли, а также тех больных, которым не всегда возможно подобрать нужный размер ортопедической шейной шины Шанца, так как существуют только 4 размера, а также за счет тех пациентов, которые отказались от использования шины Шанца по эстетическим соображениям, включая ограничение ее применения в условиях работы.
Техническим результатом изобретения является:
• возможность постоянного воздействия на мышечно-связочный аппарат и уменьшения протракции головы в течение дня, что не только повысит эффективность способа лечения, но и не ограничит его использование в рабочее время;
• возможность коррекции верхнего перекрестного синдрома (протракции головы), включающей коррекцию положения головы, плечевого пояса, а также коррекцию осанки грудного отдела, характеризуемой по плечевому индексу по О.А. Аксеновой;
• возможность стабилизации тонуса всех мышц шейного отдела, что снизит его гиперподвижность, что, в свою очередь, снизит риск травматизации связочного аппарата суставов шейного отдела;
• снижение риска растяжения капсул межпозвоночных суставов.
Технический результат изобретения достигается тем, что способ лечения больных с задним шейным симпатическим синдромом заключается в проведении медикаментозной терапии и коррекции биомеханических нарушений шейного и грудного отделов позвоночника. В качестве коррекции биомеханических нарушений шейного и грудного отделов позвоночника используют кинезиотейпирование. Нанесение тейпа проводят паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня Th12. Затем проводят поперечное нанесение тейпа по плечевой дуге в проекции горизонтальной дорзальной порции трапециевидных мышц, начиная от выступающей части перехода шейного и грудного отделов позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% на 5 дней, что составляет один курс лечения. Курсы выполняют 1-3 раза, с двухдневным перерывом между ними.
Способ осуществляется следующим образом: Пациентам с верифицированным синдромом позвоночной артерии (задний шейный симпатический синдром), на фоне базовой медикаментозной терапии, включающей венотоники, НПВП, препараты, нормализующие кровоток в позвоночных артериях, нейрометаболические препараты, миорелаксанты, спазмолитики, гистаминоподобные, антимигренозные препараты, осуществляют коррекцию биомеханических нарушений шейного и грудного отделов позвоночника путем проведения кинезиотейпирования. Пациент должен находиться в положении сидя, проводят обработку паравертебрально зон кожных покровов шейного и грудного отделов для обезжиривания и дезинфекции, а также удаляют волосяной покров в этих зонах (при наличии), что улучшает адгезивные свойства кинезиотейпов. Длину тейпа измеряют от затылочной области шейного отдела до Тн12 и по дуге сзади между акромиальными точками. Пациент находится в максимально ровном положении. Нанесение тейпа проводят паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня Th12. Затем проводят поперечное нанесение тейпа по плечевой дуге в проекции горизонтальной дорзальной порции трапециевидных мышц, начиная от выступающей части перехода шейного и грудного отделов позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50%. При этом тейп делят на две части, прикрепляют за область середины в указанном анатомическом ориентире и далее в направлении акромиальных точек до верхних частей плеч, сначала одну половину тейпа, затем другую. 2-х сантиметровые концы тейпов прикрепляют нерастянутыми. Один курс лечения составляет 5 дней Курсы выполняют 1-3 раза, с двухдневным перерывом между ними.
В основе изобретения лежит ограничение патологической подвижности шейных позвонков, стабилизация мышечного тонуса, уменьшение травматизации связочного аппарата унковертебральных и дугоотростчатых суставов, уменьшению боли в мышцах, что приводит к уменьшению влияния основных этиопатофизиологических процессов ЗШСС.
ЗШСС возникает вследствие компрессии или спазма позвоночных артерий.
Можно выделить ряд изменений, приводящих к механической компрессии позвоночных артерий и/или к раздражению симпатического сплетения артерий, которое густо иннервирует переднюю продольную связку, область фиброзного кольца, связочный аппарат дугоотросчатых суставов, что приводит к рефлекторному вазоспазму [7, 8].
Таким образом компрессия позвоночной артерии может возникать на первом отрезке до вхождения ее в канал поперечных отростков. Здесь происходит компрессия ствола позвоночной артерии лестничными мышцами. Гипертонусы средней и длинной мышцы шеи, а также их дефанс могут формировать туннельный механизм компрессии артерии [9].
Вышеописанные изменения мышечного тонуса мышц шейного отдела формируются при верхнем перекрестном синдроме, при котором также наблюдается гипертонус грудино-ключично-сосцевидных мышц [9], что формирует стойкую протракцию головы, что стимулирует гипертонус лестничных, средней и длиной мышц шеи. Эти патологические изменения являются результатом активности мышечных групп при одновременном реципрокном торможении их антагонистов [10]. Использование кинезиотейпирования с целью разгибания шейного отдела позвоночного столба, согласно мышечной теории, дает активацию мышц антагонистов за счет механического влияния на тонический рефлекс [11, 12, 13, 14], что приводит к уменьшению гипертонуса грудино-ключично-сосцевидных, лестничных, средней и длинной мышц шеи, функция которых заключается в сгибании шейного отдела позвоночного столба, что уменьшает риск компрессии позвоночных артерий на этом уровне.
На втором отрезке в канале поперечных отростков возникает механическое воздействие костных структур позвонков. Самый частый вариант рефлекторного спазма позвоночных артерий связан с раздражением симпатического сплетения вокруг позвоночной артерии, передней продольной связки, области фиброзного кольца, связочного аппарата дугоотросчатых суставов и заключается в развитии и влиянии унковертебрального артроза, экзостозов в области артроза, которые оказывают механическое раздражение артерии и волокон симпатического сплетения вышеописанных структур. Такой механизм возможен при перегрузках отдельных суставных пар, а также вследствие длительно существующего подвывиха [9], что формируется при верхнем перекрестном синдроме, который часто сопровождаются функциональными блокадами шейных позвоночно-двигательных сегментов (ПДС) или цервико-торакального перехода. В таких случаях формируется порочное кольцо, включающее блокированные ПДС, триггерные пункты перегруженных мышц, измененный двигательный стереотип. Ключевую роль в дискоординированной деятельности играет ослабление нижних фиксаторов плечевого пояса (т.е. лопатки), восходящей части трапециевидных мышц, передних зубчатых мышц, увеличение тонуса большой и малой грудных мышц, нисходящей части трапециевидных мышц, поднимающей лопатки [10].
Использование кинезиотейпирования с целью уменьшения влияния верхнего перекрестного синдрома за счет разгибания в шейном и грудном отделе и уменьшения антериоризации и супериоризации плеч, а также уменьшения количества триггерных пунктов, характеризующихся болью, согласно мышечной теории, достигается за счет активации мышц антагонистов и механического влияния на тонический рефлекс, помимо этого формируется изменение тонуса мышц, за счет воздействия на проприо- и интерорецепторы и моделирование паттерна движения, за счет векторного наложения тейпа [11, 12, 13, 14], что улучшает двигательный стереотип и ощущение схемы тела в пространстве, что ведет к увеличению постоянного контроля осанки пациентом, уравниванию тонуса мышц антагонистов, уменьшению мышечных перегрузок, и травматизации мышечно-связочного аппарата шейного и грудного отделов позвоночника.
Уменьшение болевого синдрома в триггерных пунктах реализуется за счет двух механизмов: активации афферентного потока от толстых миелиновых А-β (А-бета) волокон и активации микроциркуляции в соединительной ткани.
В соответствии с теорией «воротного контроля» (афферентного входа) болевой импульс подавляется в желатинозной субстанции, расположенной во второй пластине заднего рога (второй зоне Рекседа), импульсом приходящим по А-β толстым миелиновым волокнам, т.е импульсом от тактильных и барорецепторов.
Кинезиотейп, наложенный на поверхность кожи, раздражает, прежде всего, тактильные рецепторы и барорецепторы, от которых афферентный сигнал поступает в задние рога спинного мозга по толстым миелиновым А-β волокнам, уменьшая болевой синдром.
Второй механизм уменьшения болевого синдрома реализуется при активации микроциркуляции в тканях. Повреждение тканей сопровождается поступлением в межклеточное вещество медиаторов воспаления: субстанции Р, гистамина, простогландинов и т.д. Эти вещества вызывают сенситизацию ноцицепторов С-волокон, что понижает порог их возбудимости и возрастает болевой афферентный поток. Наложенный на кожу кинезиотейп, увеличивая пространство в соединительной ткани, активирует микроциркуляцию и способствует выведению медиаторов воспаления. [11, 12, 13, 14]
На третьем отрезке в месте выхода из канала поперечных отростков позвоночная артерия ком премируется при аномалиях верхних шейных позвонков - над верхним краем дуги атланта, где бороздка для артерии может оказаться слишком глубокой или даже превращенной в костный канал. Кроме того, позвоночная артерия может компремироваться при тоническом напряжении задней нижней косой мышцы при синдроме нижней косой мышцы. В таких случаях оказывается механическое давление на заднюю стенку артерии в области бороздки позвоночной артерии атланта, где она сзади не прикрыта суставными отростками. Патологическое напряжение этой мускулатуры возможно при гипермобильности верхне-шейных ПДС вследствие остеохондроза [9] и при верхнем перекрестном синдроме, в результате которого затылочная кость и С1-С2 находятся в гиперэкстензии.
Использование кинезиотейпирования с целью уменьшения влияния верхнего перекрестного синдрома, протракции головы за счет механизмов, описанных выше, уменьшают гиперэкстензию затылочной кости и С1-С2, что, в свою очередь, уменьшает механическое давление на позвоночные артерии.
Данная информация подтверждается в работах при хлыстовой травме шеи. Кинезиотейпы достоверно влияют на боль и объем движений в позвоночнике при хлыстовой травме шеи, при котором формируется патологическая подвижность позвонков и травматизация связочного аппарата межпозвонковых суставов [15, 16].
Кинезиотейпирование обладает высоким уровнем эффективности в снижении боли [17].
Под действием кинезиотейпирования происходит изменение характеристик мышечного сокращения, что стабилизирует мышечный тонус [18].
• Кинезиотейпирование осуществляют с натяжением до 50% по существующей методике постуральной коррекции, которое направлено на изменение осанки и положения тела [19].
• Двухдневный перерыв между курсами, подобранный по собственным наблюдениям в пилотном исследовании, необходим во избежание раздражения кожных покровов.
Совокупность существенных отличительных признаков является новой и обеспечивает достижение технического результата и выполнение задачи изобретения.
Для подтверждения эффективности заявляемого способа приводим примеры из клинической практики:
Пример 1. Пациентка М.,32 года, офисный работник.
Диагноз: Синдром позвоночной артерии.
До лечения:
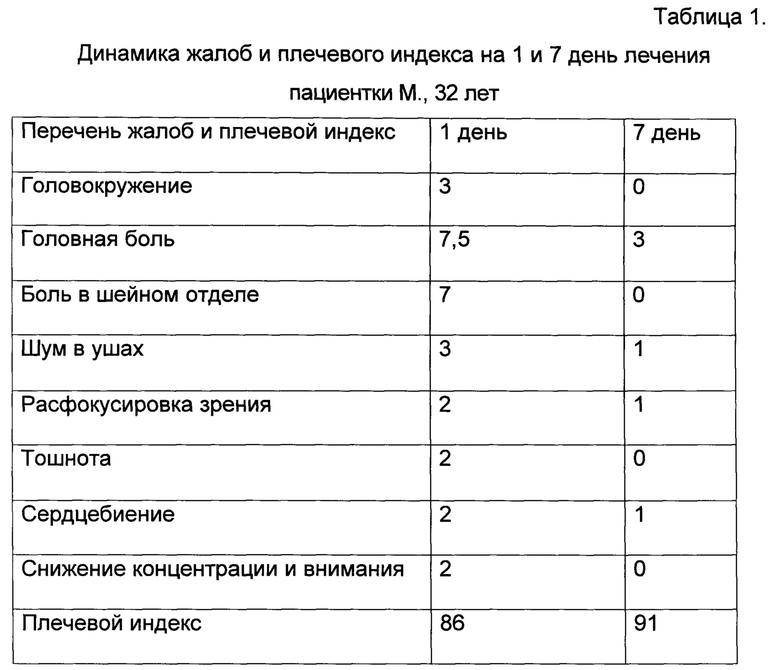
Предъявляла жалобы на головокружение (3б по международной классификации функционирования-МКФ), головную боль (7,5 по визуальной аналоговой шкале боли- ВАШ), боль в шейном отделе (7 по ВАШ), шум в ушах (3б по МКФ), расфокусировку зрения (2б по МКФ), тошноту (2б по МКФ), сердцебиение (2б по МКФ), снижение концентрации и внимания (2б по МКФ), плечевой индекс 86%.
При обследовании:
На МРТ головного мозга без новообразований и очагов глиоза;
на рентгенограммах шейного отдела нестабильность С5-С6, выпрямление физиологического лордоза, нарушение статической функции позвоночника, дегенеративно-дистрофические изменения;
при дуплексном сканировании брахицефальных артерий выявлено: не- прямолинейность хода позвоночных артерий, вертеброгенное влияние на позвоночные артерии при функциональных пробах, повышение тонуса артерий и снижение упруго-эластичных свойств. На фоне медикаментозной терапии, включающей бетагистин, нимесулид, цитиколин, толперизон, было проведено кинезиотейпирование паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня Th12a также на области плечевой дуги в проекции горизонтальной дорзальной порции трапецевидных мышц, начиная от выступающей части перехода шейного и грудного отдела позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% на 5 дней однократным курсом. На 7 день лечения:
Головокружение (0б по МКФ), головная боль (3 по ВАШ), боль в шейном отделе (0 по ВАШ), шум в ушах (1б по МКФ), расфокусировка зрения (1б по МКФ), тошноту (0б по МКФ), сердцебиение (1б по МКФ), снижение концентрации и внимания (0б по МКФ), плечевой индекс 91%.
По данным дуплексного сканирования ПА увеличение показателей линейных скоростей кровотока.
По данным шкалы оценки головокружения (DHI), вестибулярного опросника (VRBQ), краткого опросника оценки качества жизни (SF36), шкалы тревоги Шихана и шкалы Бека (тест на депрессию) отмечается улучшение по всем показателям в том числе и качества жизни и психоэмоционального состояния.
Пример 2. Пациентка В.,33 года, офисный работник.
Диагноз: Синдром позвоночной артерии.
До лечения:
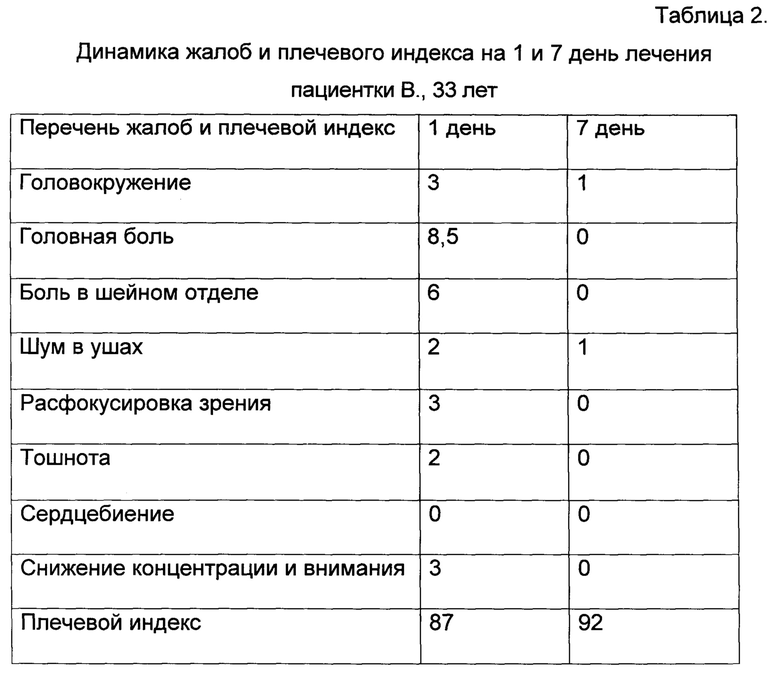
Предъявляла жалобы на головокружение (3б по МКФ), головную боль (8,5 по ВАШ), боль в шейном отделе (6 по ВАШ), шум в ушах (2б по МКФ), расфокусировка зрения (3б по МКФ), тошноту (2б по МКФ), сердцебиение (0б по МКФ), снижение концентрации и внимания (3б по МКФ), плечевой индекс 87%. При обследовании:
На МРТ головного мозга заместительная гидроцефалия, без новообразований и очагов глиоза, на рентгенограммах шейного отдела лестничная нестабильность С2-С6, выпрямление физиологического лордоза, дегенеративно-дистрофические изменения в виде начального спондилеза, спондилоартроза, наличие аномалии Киммерле, при дуплексном сканировании брахицефальных артерий выявлена асимметрия кровотока на 30%, гипоплазия позвоночной артерии справа, непрямолинейность хода позвоночных артерий, вертеброгенное влияние на позвоночные артерии при функциональных пробах, повышение тонуса артерий.
На фоне медикаментозной терапии, включающей диосмин, бетагистин, нимесулид, цитиколин, толперизон, было проведено кинезиотейпирование паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня ТМ2, а также на области плечевой дуги в проекции горизонтальной дорзальной порции трапецевидных мышц, начиная от выступающей части перехода шейного и грудного отдела позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% для постуральной коррекции на 5 дней с двухдневным перерывом между двухкратным курсом.
Головокружение (1б по МКФ), головная боль (0 по ВАШ), боль в шейном отделе (0 по ВАШ), шум в ушах (1б по МКФ), расфокусировка зрения (0б по МКФ), тошноту (0б по МКФ), сердцебиение (0б по МКФ), снижение концентрации и внимания (0б по МКФ), плечевой индекс 92%.
По данным дуплексного сканирования ПА увеличение показателей линейной скорости кровотока.
Аналогичные результаты по данным шкалы оценки головокружения (DHI), вестибулярного опросника (VRBQ), краткого опросника оценки качества жизни (SF36), шкалы тревоги Шихана и шкалы Бека (тест на депрессию) отмечается улучшение по всем показателям в том числе и качества жизни и психоэмоционального состояния.
Пример 3. Пациентка О., 28 лет, учитель.
Диагноз: Синдром позвоночной артерии.
До лечения:
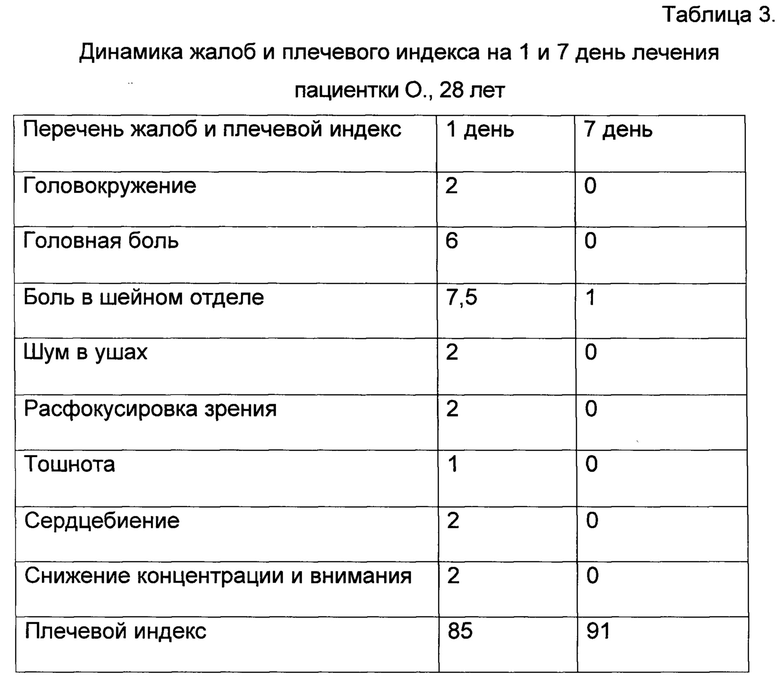
Предъявляла жалобы на головокружение (2б по МКФ), головную боль (6 по ВАШ), боль в шейном отделе (7,5 по ВАШ), шум в ушах (2б по МКФ), расфокусировка зрения (2б по МКФ), тошноту (1б по МКФ), сердцебиение (2б по МКФ), снижение концентрации и внимания (2б по МКФ), плечевой индекс 85%.
При обследовании:
На МРТ головного мозга расширение ликворных пространств, без новообразований и очагов глиоза, на рентгенограммах шейного отдела лестничная нестабильность С4-С6, выпрямление физиологического лордоза, дегенеративно-дистрофические изменения в виде начального спондилоартроза, наличие неполной аномалии Киммерле, при дуплексном сканировании брахицефальных артерий выявлена асимметрия кровотока на 20%, непрямолинейность хода позвоночных артерий, вертеброгенное влияние на позвоночные артерии при функциональных пробах с 30% уменьшением, повышение тонуса артерий. На фоне медикаментозной терапии, включающей диосмин, бетагистин, нимесулид, цитиколин, толперизон, было проведено кинезиотейпирование паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня ТМ2, а также на области плечевой дуги в проекции горизонтальной дорзальной порции трапецевидных мышц, начиная от выступающей части перехода шейного и грудного отдела позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% для постуральной коррекции на 5 дней с двухдневным перерывом между трехкратным курсом.
На 21 день лечения:
Головокружение (0б по МКФ), головная боль (0б по ВАШ), боль в шейном отделе (1б по ВАШ), шум в ушах (0б по МКФ), расфокусировка зрения (0б по МКФ), тошноту (0б по МКФ), сердцебиение (0б по МКФ), снижение концентрации и внимания (0б по МКФ), плечевой индекс 91%.
По данным дуплексного сканирования ПА увеличение показателей линейной скорости кровотока.
Аналогичные результаты по данным шкалы оценки головокружения (DHI), вестибулярного опросника (VRBQ), краткого опросника оценки качества жизни (SF36), шкалы тревоги Шихана и шкалы Бека (тест на депрессию) отмечается улучшение по всем показателям в том числе и качества жизни и психоэмоционального состояния.
Нами обследовано 60 человек. Все наблюдаемые пациенты имели диагноз задний шейный симпатический синдром. Все прошли общее неврологическое и отоневрологическое обследование. Пациенты разделены методом рандомизации на 2 группы. Первая группа получала медикаментозное лечение и ношение ортопедической шейной шины Шанца по 40 мин утром и вечером (гр. Контроль), вторая группа - медикаментозное лечение и кинезиотейпирование (гр. КТ).
Обе группы получали базовое медикаментозное лечение, включающее венотоники, НПВП, препараты, нормализующие кровоток в позвоночных артериях, нейрометаболические препараты, миорелаксанты, спазмолитики, гистаминоподобные, антимигренозные препараты.
Осанку оценивали с помощью определения плечевого индекса (индекса «сутулости») по О.А. Аксеновой. Оценка индекса: до 89,9% -сутулость, от 90 до 100% - нормальная осанка.
Эффективность терапии определяли на основании анализа жалоб пациентов (оценка частоты и выраженности приступов головокружения, головной боли и боли в шейном отделе позвоночника).
Оценку выраженности приступов головокружения проводили с помощью шкалы оценки головокружения ([Dizziness Handicap inventory (DHI)] на 1-й день, 7-й день лечения.
DHI разработана G. Jacobson и C.W. Newman [20] в 1990 г.и широко применяется для объективизации выраженности головокружения в различных клинических исследованиях. Шкала включает 25 вопросов с тремя вариантами ответов на каждый («да», «нет», «иногда»). Ответ на вопрос «да» оценивался в 4 балла, «иногда» - в 2 балла, «нет» - в 0 баллов. Таким образом, сумма баллов по DHI может составлять от 0 (нет головокружения) до 100 (очень выраженное головокружение). Сумма баллов от 1 до 30 - легкое головокружение, от 31 до 60 - умеренное, свыше 60 - выраженное головокружение. DHI имеет три подшкалы: функциональную (по ней оценивают, в какой степени головокружение нарушает повседневную активность больного), эмоциональную (в какой степени головокружение нарушает эмоциональное состояние больного) и физикальную (в какой степени движения головы и тела влияют на головокружение) [20]. В целом эта шкала позволяет количественно оценить влияние вестибулярных заболеваний на физическое и эмоциональное состояние пациента, что особенно важно при динамическом контроле за ходом лечения.
Оценку головной боли и боли в шейном отделе проводили по визуальной аналоговой шкале (ВАШ) на 1-й, 7-й день лечения.
Также проводилось общее неврологическое обследование по стандартной методике и отоневрологическое обследование позиционных проб (Дикса-Холлпайка и МакКлюра-Пагнини, проба Хальмаги, проба с энергичным встряхиванием головы (headshaking), походка (фланговая, тандемная), проба Фукуда, проба Вебера и Ринне, проба Вальсальвы, ортостатическая проба). Для оценки в динамике кровотока использовали дуплексное сканирование брахицефальных артерий с оценкой показателей (Vm; Vps; Vd; RI; PI).
Помимо общего клинического и неврологического обследований, всем больным были проведены: компьютерная или магнитно-резонансная томография головного мозга, рентгенография шейного отдела позвоночника с функциональными пробами.
Для анализа полученных в процессе выполнения работы исходных данных использовалась система STATISTICA for Windows (версия 10 Лиц. BXXR310F964808FA-V). [21].
Массив исходных данных состоял из результатов визуальной аналоговой шкалы (ВАШ), данных шкалы оценки головокружения (DHI), данных дуплексного сканирования линейных скоростей кровотока по позвоночным артериям, данных плечевого индекса для 60 пациентов двух групп: гр. КТ, гр. Контроль.
В соответствии с целями и задачами исследования, а также с учетом особенностей анализируемых переменных мы проводили:
- построение и визуальный анализ графиков и диаграмм разброса данных;
- определение типов распределений данных;
- построение гистограмм разброса данных;
- расчет изменения анализируемых показателей к 7 дню лечения.
- расчет элементарных статистик (средние значения, ошибки средних, среднеквадратические отклонения, размах разброса данных, медианы и квартили) [21].
Оценка сопоставимости групп по полу проводилась с помощью непараметрических методов χ2, критерия Пирсона, критерия Фишера. [22, 23].
Сравнение изучаемых количественных параметров, в т.ч. изменения показателей в динамике. Возраст, характеристики кинезиотейпирования, плечевой индекс, линейные скорости кровотока, данные опросников и шкал в исследуемых группах осуществлялось с использованием критериев Манна-Уитни, Колмогорова-Смирнова, медианного хи-квадрат и модуля ANOVA. [22, 23].
Для оценки изменения показателей к 7 дню, по сравнению с первым, применяли непараметрические критерии Вилкоксона и Знаков.
Для визуализации структуры исходных данных и полученных результатов их анализа мы использовали графические возможности системы Statstica for Windows и модуль построения диаграмм системы Microsoft Office. Количественные показатели в различных исследуемых подгруппах для полноты описания и удобства восприятия и сравнения мы представили в форме «Вох & Whisker Plot» - диаграммы Тьюки, когда на одном поле при различных группировках на основе качественных критериев отражены медиана, квартили, минимум и максимум для конкретного параметра. Критерием статистической значимости получаемых выводов мы считали общепринятую в медицине величину Р<0,05. [22, 23]. Рандомизация проводилась с помощью случайного выбора лечащим врачом одной из групп, согласно которой будет проходить лечение. Результаты оценки выраженности головокружения по шкале оценки головокружения DHI (ШОГ) в 1-ый день лечения и на 7-ой день представлены в табл. 4.
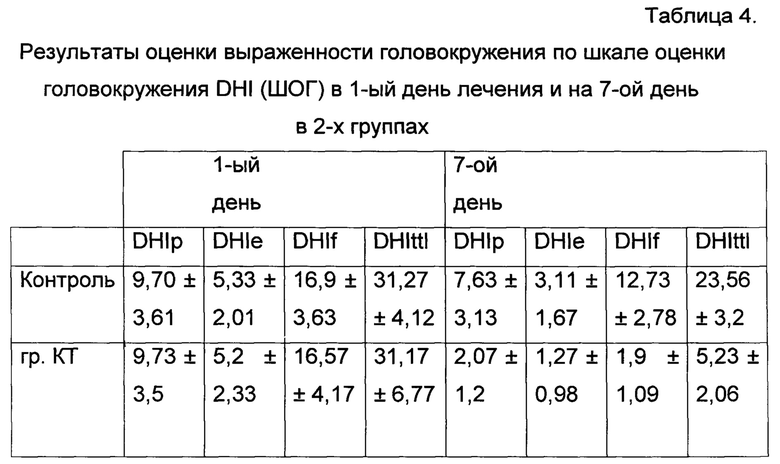
Как видно из табл. 4, средние значения суммы баллов по DHI в группе с кинезиотейпированием значимо уменьшаются на 7-ой день (т.е. разница между суммами баллов ≥10); причем эти изменения статистически достоверны (р<0,05).
Динамика в группе с кинезиотейпированием отмечается и при анализе среднего балла по функциональной, эмоциональной и физикальной подшкалам DHI: показатели 1-ого и 7-го дня значимо различаются и статистически достоверны (р<0,05).
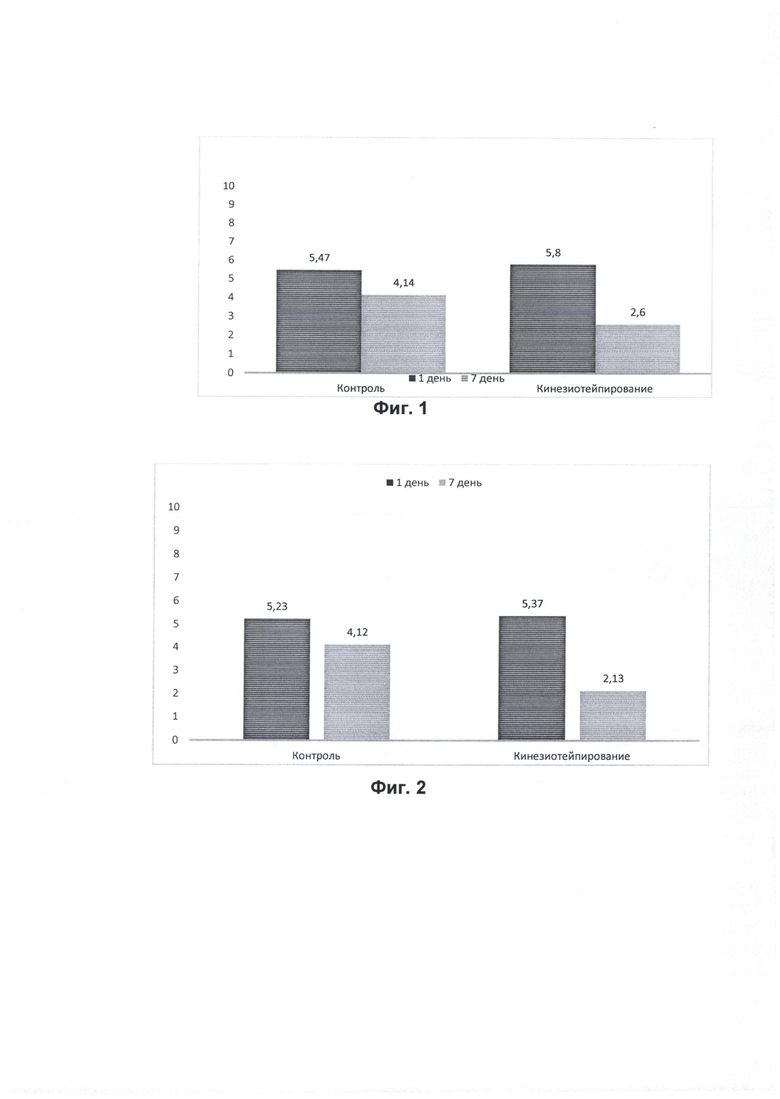
Данные статистического показателя средней по результатам визуальной аналоговой шкалы оценки головной боли представлены на Фиг. 1.
Данные статистического показателя средней со стандартным отклонением визуальной аналоговой шкалы оценки боли в шейном отделе представлены на Фиг. 2.
Из данных Фиг. 1. и Фиг. 2 статистического показателя средней со стандартным отклонением видно значительное уменьшение боли в группе кинезиотейпирования в сравнении со значениями группы контроля на 7-ой день лечения, причем эти изменения статистически достоверны (р<0,05).
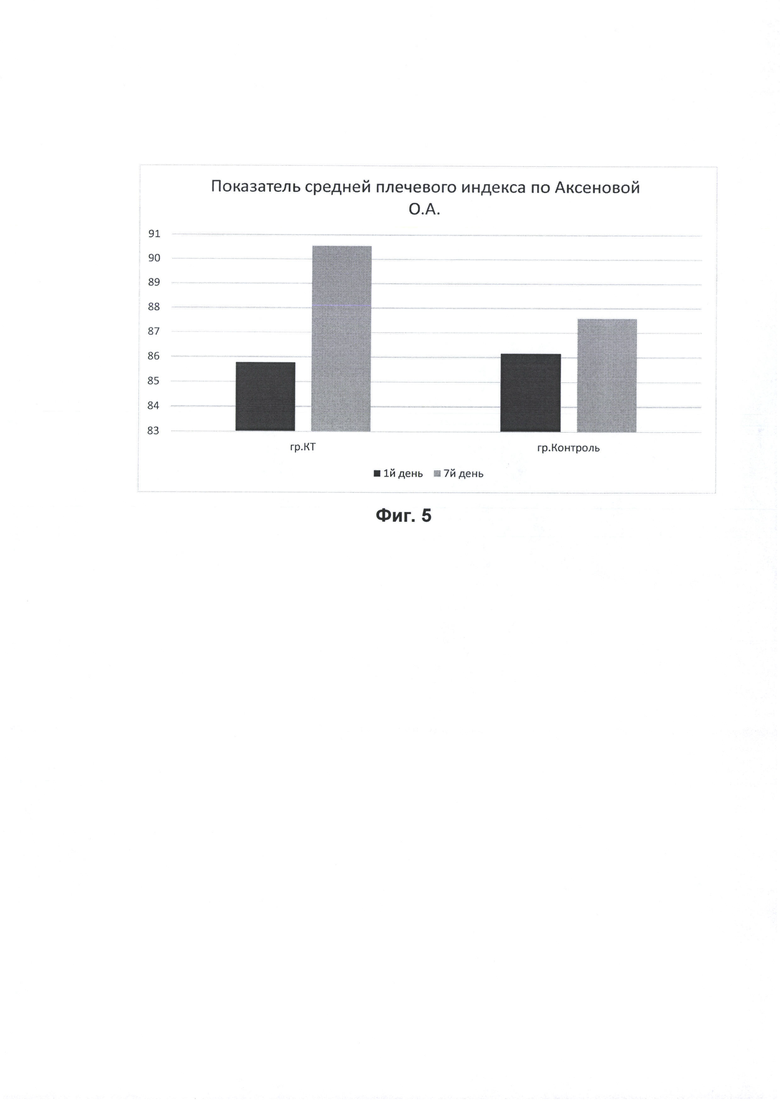
Значение статистического показателя средней со стандартным отклонением плечевого индекса по Аксеновой О.А. в группе кинезиотейпирования на 7-ой день лечения в сравнении с группой контроля отмечается нормализация осанки, что видно из таблицы 5.
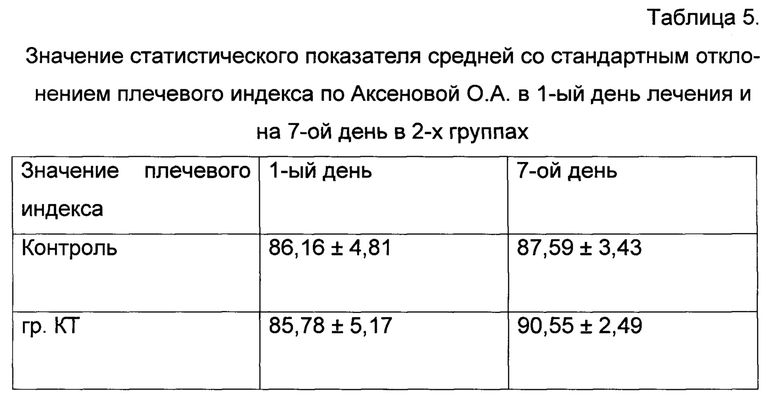
Это дает возможность судить об эффективности кинезиотейпирования для коррекции верхнего перекрестного синдрома, изменения статистически достоверны на 7-ой день лечения (р<0,05).
Значения медианы и размаха минимальных и максимальных значений линейных скоростей кровотока (пульсовой скорости) при ультразвуковом исследовании правой и левой позвоночных артерий на экстракраниальном уровне представлены в таблице 6.
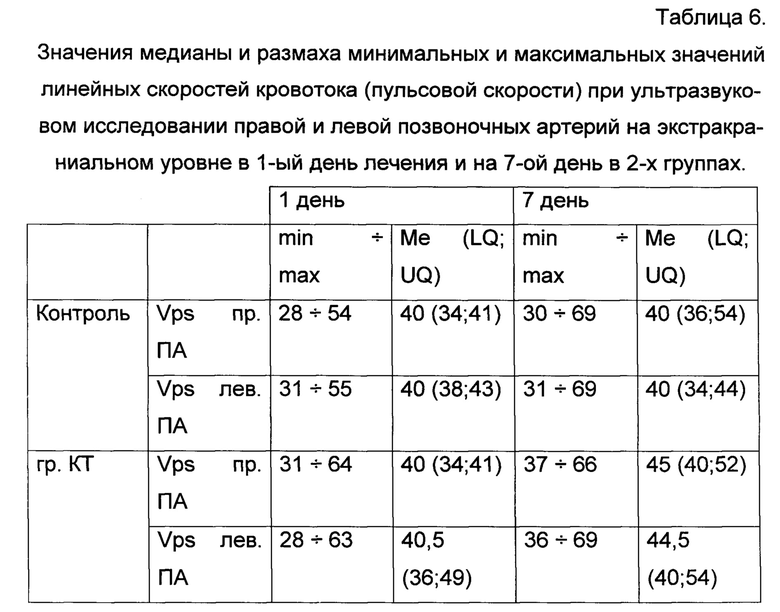
Из таблицы 6 видно, что улучшение линейных скоростей кровотока по правой и левой позвоночным артериям (пульсовой скорости) на экстракраниальном уровне в группе с применением кинезиотейпирования, статистически достоверно слева (р<0,05).
Значения размаха минимальных и максимальных значений и медианы линейных скоростей кровотока (минутной скорости) при ультразвуковом исследовании правой и левой позвоночных артерий на экстракраниальном уровне представлены в таблице 7.
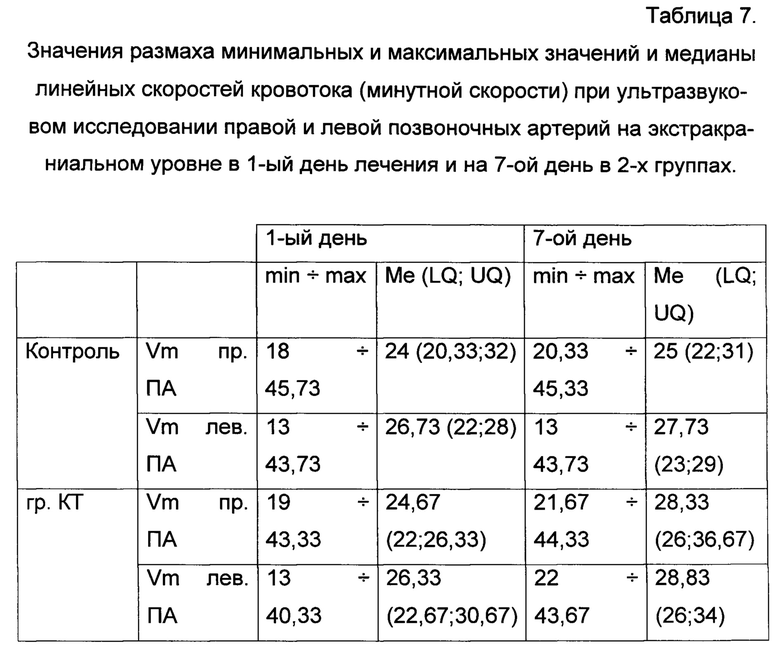
По данным таблицы 7 видно, что увеличение линейных скоростей кровотока (минутной скорости) по позвоночным артериям на экстракраниальном уровне в группе с применением кинезиотейпирования, статистически достоверно слева (р<0,05).
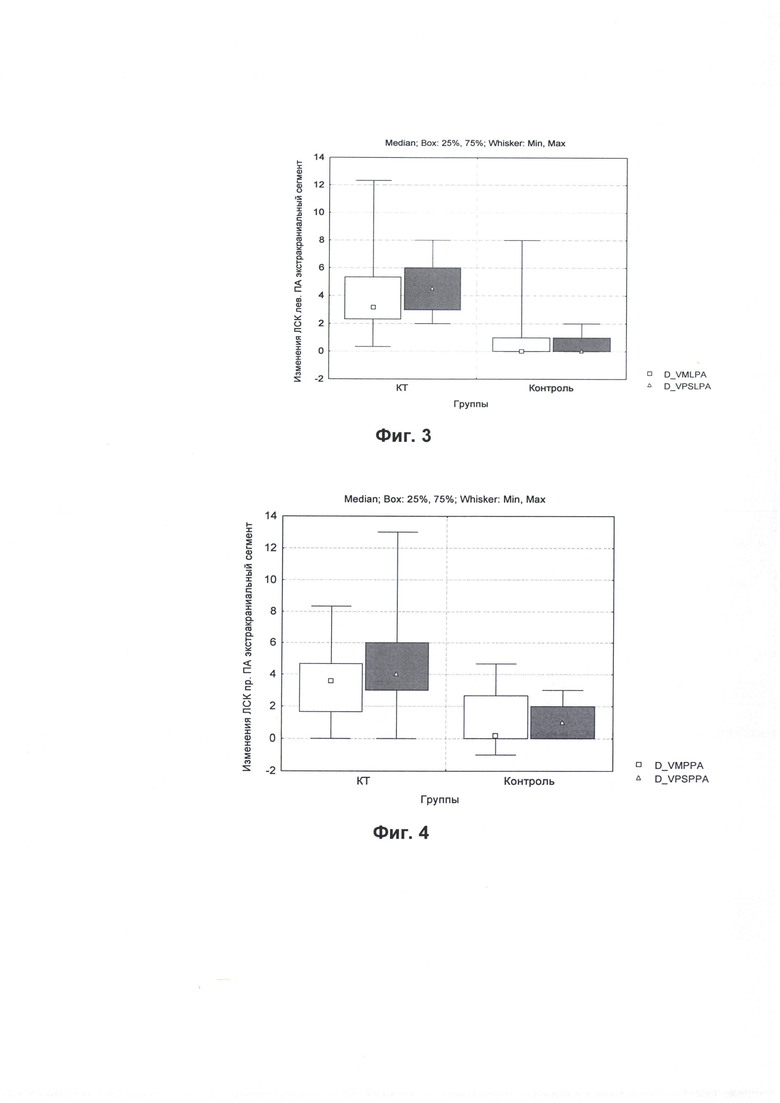
Значение динамики показателей по левой позвоночной артерии экстракраниально, т.е. разность между значениями линейных скоростей кровотока 1-го и 7-го дня представлены на Фиг. 3. Статистически достоверные результаты (р<0,05) улучшение скорости кровотока получены в группе кинезиотейпирования со стороны левой позвоночной артерии, в сравнении с группой контроля, так и по данным значений динамики размаха минимальных и максимальных значений и медианы отмечается статистически значимое (р<0,05) увеличения скоростей кровотока, в сравнении с группой контроля. По данным литературы, возможно это связано с особенностями анатомии канала и структурно-морфометрическими особенностями внутрика-нального отдела позвоночных артерий у человека, что заключается в преобладании диаметра левой позвоночной артерии, а также преобладанием диаметра отверстий поперечных отростков слева. Возможно, это также связано с особенностями строения сосудов и отхождением ЛПА от дуги аорты [24].
Значение динамики показателей по правой позвоночной артерии экстракраниально, т.е. разность между значениями линейных скоростей кровотока 1-го и 7-го дня представлены на Фиг. 4. Статистически достоверного изменения линейных скоростей кровотока по правой позвоночной артерии в сравнении с группой контроля не получено, но по данным значений динамики размаха минимальных и максимальных значений и медианы отмечается статистически значимое (р<0,05) увеличения скоростей кровотока в сравнении с группой контроля.
Значения медианы и размаха минимальных и максимальных значений линейных скоростей кровотока при ультразвуковом исследовании правой и левой позвоночных артерий на интракраниальном уровне представлены в таблице 8.

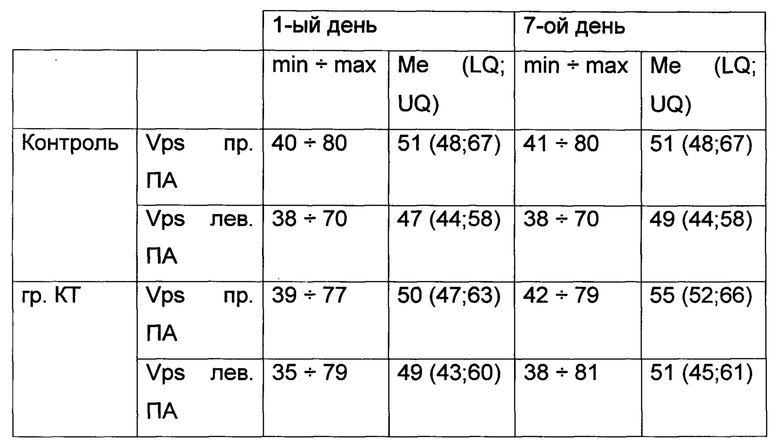
Значения медианы и размаха минимальных и максимальных значений линейных скоростей кровотока при ультразвуковом исследовании правой и левой позвоночных артерий на интракраниальном уровне представлены в таблице 9.
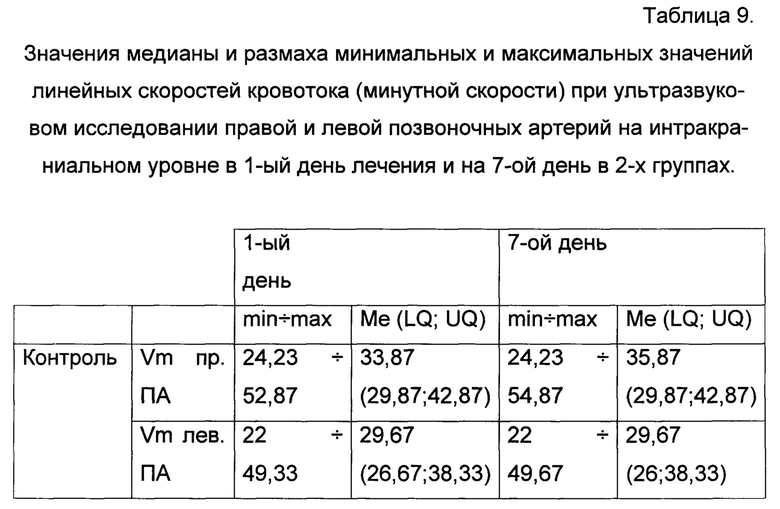

Из данных показателей медианы и размаха минимальных и максимальных значений видно увеличение скорости кровотока интракраниально по позвоночным артериям в группе с использованием кинезиотейпирования на 7-ой день лечения в сравнении с контрольной группой, но статистически значимого улучшение линейных скоростей кровотока на интракраниальном уровне не получено, но по значениям динамики изменений линейных скоростей кровотока в группе кинезиотейпирования наблюдается статистически значимое (р<0,05) увеличение скоростей кровотока в сравнении с группой контроля. Для заднего шейного симпатического синдрома характерны биомеханические нарушения в виде верхнего перекрестного синдрома, проявляющегося снижением плечевого индекса.
На Фиг. 5 представлены показатели средней плечевого индекса по Аксеновой О.А. на 1-ый и 7-ой день, на котором видна динамика изменения плечевого индекса в группе с применением кинезиотейпирования, где наглядно представлены изменение значения в сторону нормализации осанки статистически достоверно (р<0,05) в сравнении с группой контроля.
Таким образом, заявляемый способ лечения больных с задним шейным симпатическим синдромом обеспечивает:
• постоянное воздействие на мышечно-связочный аппарат и уменьшение протракции головы в течение дня;
• коррекцию верхнего перекрестного синдрома (протракции головы), включающей коррекцию положения головы, плечевого пояса, а также коррекцию осанки грудного отдела, характеризуемой по плечевому индексу по О.А. Аксеновой;
• стабилизацию тонуса всех мышц шейного отдела, что снижает его гиперподвижность, что, в свою очередь, снижает риск травматизации связочного аппарата суставов шейного отдела;
• снижение риска растяжения капсул межпозвоночных суставов,
что позволяет:
• повысить эффективность лечения, проявляющуюся в увеличении линейных скоростей кровотока по ПА в экстракраниальном и интракраниальном сегментах, уменьшении клинических проявлений в виде головокружения, головной боли, боли в шейном отделе, верхнего перекрестного синдрома;
• расширить контингент больных за счет больных, отказавшихся от использования ортопедической шейной шины Шанца в связи с нарушением венозного оттока головы, что сопровождалось учащением и/или увеличением головной боли, а также тех больных, которым не всегда возможно подобрать нужный размер ортопедической шейной шины Шанца, так как существуют только 4 размера, а также за счет тех пациентов, которые отказались от использования шины Шанца по эстетическим соображениям, включая ограничение ее применения в условиях работы.
Список литературы:
1. Пантелеева Е.А. Синдром позвоночной артерии и тактика ведения пациентов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012. 112(12). 46-50.
2. Яриков А.В., Перльмуттер О.А., Фраерман А.П., Мухин А.С., Бояршинов А.А., Носков А.И., Отдельное Л.А. Вертеброгенный синдром позвоночной артерии: патогенез, клиническая картина, диагностика и лечение. ЭНИ Забайкальский медицинский вестник. 2019; 4. 181-192.
3. Когнитивные нарушения при цереброваскулярных заболеваниях / Е.И. Гусев, А.Н. Боголепова. - 3-е изд., доп. - М.: МЕДпресс-информ, 2013. - 176 с.
4. Шевцов В.И., Худяев А.Т., Люлин С.В., Корытников М.А. Комплексное лечение больных с вертеброгенным синдромом позвоночной артерии. Гений ортопедии. 2004. 2. 68-73.
5. Захматова Т.В., Щедренок В.В., Себелев К.И., Могучая О.В. Вертеброгенный синдром позвоночной артерии: современные подходы диагностики и лечения. Тюменский медицинский журнал. 2012. 2. 26.
6. Попелянский, Я.Ю. Шейный остеохондроз / Я.Ю. Попелянский. - М.: Медицина, 1966 - 136 с.
7. Li J., Gu Т., Yang Н., Liang L., Jiang D., Wang Z., Yuan W., Wang X. Sympathetic nerve innervation in cervical posterior longitudinal ligament as a potential causative factor in cervical spondylosis with sympathetic symptoms and preliminary evidence. Medical Hypotheses; 2014; 82 (5): 631-635.
8. Nathan P.W., Smith M.C. The location of descending fibres to sympathetic preganglionic vasomotor and sudomotor neurons in man. Journal of neurology, neurosurgery, and psychiatry; 1987; 50 (10): 1253-1262.
9. Миняева O.B., Сафин Ш.М., Новиков А.Ю. Комплесное восстановительное лечение синдрома позвоночной артерии с использованием физиотерапии, акупунктуры и мануальной терапии. // Научное обозрение. Медицинские науки. - 2016. - №1. - С. 30-33
10. Иваничев Г.А. Патогенетические аспекты формирования и проявления классических болевых мышечных синдромов. Мануальная терапия. 2009; 3 (35): 3-12.
11. Kase Kenzo, Wallis Jim. Clinical therapeutic applications of the Kine-siotaping method. Albuquerque. 2003.
12. Kenzo Kase. Illustrated Kinesio Taping -Kin'l-Kai. Tokyo. 2005.
13. Harry Pijnappel. Medical Taping Concept. Netherlands. 2012.
14. Birgit Kumbrink. K-Taping: An illustrated guide- Basic- Techniques- Indications. Berlin. 2012.
15. Lee J., Yoo W., and Gak H. The Immediate Effect of Anterior Pelvic Tilt Taping on Pelvic Inclination. Journal of Physical Therapy Science. 2011:23 (2): 201-203.
16.  Fernandez-de-las-Penas, C, Cleland, J., Huijbregts, P. and Gutierrez-Vega, M. D. R.. Short-Term Effects Of Cervical Kinesio_Taping On Pain And Cervical Range Of_Motion In Patients With Acute_Whiplash Injury: A Randomized_Clinical Trial. Journal of Orthopaedic & Sports Physical Therapy. 2009; 39(7):515-521.
Fernandez-de-las-Penas, C, Cleland, J., Huijbregts, P. and Gutierrez-Vega, M. D. R.. Short-Term Effects Of Cervical Kinesio_Taping On Pain And Cervical Range Of_Motion In Patients With Acute_Whiplash Injury: A Randomized_Clinical Trial. Journal of Orthopaedic & Sports Physical Therapy. 2009; 39(7):515-521.
17. Joscha K., Julian M. What are the level of evidence and the efficacy of medical taping on circulation, muscle function, correction, pain and proprioception? European School of Physiotherapy. 2010; 1-15.
18. Konishi Y. Tactile stimulation with Kinesiology tape alleviates muscle weakness attributable to attenuation of la afferents. Journal of Science and Medicine in Sport. 2013:16 (1):45-48.
19. Биргит Кумбринк. K-Taping. -Основы -Техники -Показания. Иллюстрированное руководство. Второе издание. Академия К- Tapinga. Дортртмунд. Германия. 2016.
20. Jacobson GP, Newman CW. The development of the Dizziness Handicap Inventory. Arch Otolaryngol Head Neck Surg. 1990; 116:424-7.
21. Боровиков В.П., «Популярное введение в современный анализ данных в системе STATISTICAL Технология и методология современного анализа данных. - Москва, «Горячая линия-Телеком», 2013, 288 с.
22. Реброва О.В. Статистический анализ медицинских данных с помощью пакета программ «Статистика». - Москва, Медиа Сфера, 2002. - 380 с.
23. Плавинский С.Л. Введение в биостатистику для медиков. - Москва, Астрель, 2011. - 584 с.
24. Маркелова М.В. Анатомия канала и структурно-морфометрические особенности внутриканального отдела позвоночных артерий у человека. Автореферат. Новосибирск, 2009.
Изобретение относится к медицине, а именно к неврологии и медицинской реабилитации, и может быть использовано для лечения больных с задним шейным симпатическим синдромом путем проведения медикаментозной терапии и коррекции биомеханических нарушений шейного и грудного отделов позвоночника. В качестве коррекции биомеханических нарушений шейного и грудного отделов позвоночника используют кинезиотейпирование. При этом нанесение тейпа проводят паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня Th12. Затем проводят поперечное нанесение тейпа по плечевой дуге в проекции горизонтальной дорзальной порции трапециевидных мышц, начиная от выступающей части перехода шейного и грудного отделов позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% на 5 дней, что составляет один курс лечения. Курсы выполняют 1-3 раза, с двухдневным перерывом между ними. Способ обеспечивает постоянное воздействие на мышечно-связочный аппарат и уменьшение протракции головы в течение дня, коррекцию верхнего перекрестного синдрома, стабилизацию тонуса всех мышц шейного отдела, снижение риска растяжения капсул межпозвоночных суставов за счет кинезиотейпирования с натяжением до 50%. 5 ил., 9 табл., 3 пр.
Способ лечения больных с задним шейным симпатическим синдромом путем проведения медикаментозной терапии и коррекции биомеханических нарушений шейного и грудного отделов позвоночника, отличающийся тем, что в качестве коррекции биомеханических нарушений шейного и грудного отделов позвоночника используют кинезиотейпирование, при этом нанесение тейпа проводят паравертебрально на обе стороны в проекции разгибателей шейного и грудного отделов позвоночника от волосистой части головы до уровня Th12, затем проводят поперечное нанесение тейпа по плечевой дуге в проекции горизонтальной дорзальной порции трапециевидных мышц, начиная от выступающей части перехода шейного и грудного отделов позвоночника в направлении акромиальных точек до верхних частей плеч с натяжением до 50% на 5 дней, что составляет один курс лечения, курсы выполняют 1-3 раза, с двухдневным перерывом между ними.
| Попелянский Я.Ю | |||
| Шейный остеохондроз / Я.Ю | |||
| Попелянский | |||
| - М.: Медицина, 1966 | |||
| Регулятор для ветряного двигателя в ветроэлектрических установках | 1921 |
|
SU136A1 |
| Способ восстановительного лечения поражений в краниовертебральном сочленении позвоночника на уровне сустава С0/С1 | 2019 |
|
RU2728099C1 |
| СПОСОБ ЛЕЧЕНИЯ ШЕЙНОГО ОСТЕОХОНДРОЗА С СОПУТСТВУЮЩИМ СИНДРОМОМ ПОЗВОНОЧНОЙ АРТЕРИИ | 1997 |
|
RU2150929C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДОРСОПАТИИ ПОЗВОНОЧНИКА У ВРАЧЕЙ-СТОМАТОЛОГОВ | 2010 |
|
RU2428148C1 |
| Челнок для вязки сетей | 1929 |
|
SU18880A1 |
| US 20140257155 A1, 11.09.2014 | |||
| AU 2012257803 A1, 19.12.2013 | |||
| Касаткин М.С | |||
| Основы кинезиотейпирования | |||
| Учебное пособие / М.С | |||
| Касаткин, Е.Е | |||
| Ачкасов, О.Б | |||
Авторы
Даты
2021-02-08—Публикация
2020-07-15—Подача