Изобретение относится к медицине.
Описанные ниже под номерами 1-4 средства применяют, в частности, для лечения инвазивной карциномы молочной железы неспецифического типа (http://healthierworld.ru/molochnaya-zheleza/preparaty-dlya-himioterapii-pri-rake-molochnoj -zhelezy.html):
1. антинеопластики - противоопухолевые препараты, механизм работы которых основан на присоединении к ДНК клеток опухоли элементов алкильного ряда, что блокирует их митотическую активность и приводит к гибели злокачественного новообразования. К этой группе относятся такие лекарственные средства как: Циклофосфамид, Мелфалан, Манномустин, Эстрамустин, Бусульфан, которые обладают высокой токсичностью (http://healthierworld.ru/molochnaya-zheleza/preparaty-dlya-himioterapii-pri-rake-molochnoj-zhelezy.html; https://medside.ru/tsiklofosfamid; https://www.rlsnet.ru/mnn_index_id_335.htm), что ограничивает область их применения;
2. антиметаболиты - противоопухолевые цитостатики, обладающие свойствами конкурентного антагонизма по отношению к биохимическим процессам, необходимым для жизнедеятельности злокачественного новообразования, что приводит к гибели опухолевых клеток. К этой группе относятся такие лекарственные средства как: Азатиоприн, Метотрексат, Тегафур, Фопурин, которые также обладают высокой токсичностью и частотой побочных эффектов, в том числе, выраженным иммуносупрессивным действием (https://www.rlsnet.ru/tn_index_id_4126.htm; https://www.rlsnet.ru/mnn_index_id_955.htm), повреждающим действием на хромосомы в соматических клетках и в клетках костного мозга (https://www.rlsnet.ru/mnn_index_id_955.htm), а также канцерогенным действием (https://www.rlsnet.ru/tn_index_id_4126.htm);
3. таксаны - препараты растительного происхождения, обладающие противоопухолевым и цитостатическим действием. Механизм их действия связан с ингибированием клеточного деления за счет повреждения микротубулярной сети в клетках на стадии митоза и в интерфазе. К этой группе относятся такие лекарственные средства как: Доцетаксел, Паклитаксел, Таксол, Таксотер.
Препараты этой группы обладают несколько меньшей токсичностью, чем вышеописанные средства, однако они также имеют множество побочных эффектов (https://www.rlsnet.ru/mnn_index_id_1874.htm; https://www.rlsnet.ru/mnn_index_id_l714.htm);
4. антрациклины - группа лекарственных препаратов, относящаяся к антибиотикам. Механизм их действия связан с ингибированием синтеза нуклеиновых кислот путем встраивания в молекулу ДНК и взаимодействия с РНК-полимеразами. Кроме того, они ингибируют топоизомеразу II, нарушают вторичную спирализацию ДНК (https://www.rlsnet.ru/mnn_index_id_621.htm; https://www.rlsnet.ru/mnn_index_id_99.htm) и способны синтезировать свободно-радикальные соединения, которые повреждают мембраны, белковые и липидные элементы клеток организма (http://healthierworld.ru/molochnaya-zheleza/preparaty-dlya-himioterapii-pri-rake-molochnoj-zhelezy.html).
К антрациклинам относятся следующие медикаменты: Доксорубицин, Даунорубицин, Идарубицин.
Эти препараты оказывают токсическое воздействие на сердце и могут привести к необратимой дилатационной кардиомиопатии (http://healthierworld.ru/molochnaya-zheleza/preparaty-dlya-himioterapii-pri-rake-molochnoj-zhelezy.html). Обладая высокой противоопухолевой и противолейкозной активностью, препараты данной группы отличаются низкой избирательностью действия, что обусловливает их токсический эффект, угнетение кроветворения и иммуносупрессивное действие. Имеются сведения об их канцерогенном действии (https://www.rlsnet.ru/mnn_index_id_99.htm).
Известен фактор дифференцировки, выделенный из культуральной среды клеток линии HL-60 (линия клеток промиелоцитарного лейкоза человека), получение которого описано в статье «Новый фактор дифференцировки из культуральной среды клеток линии HL-60, обработанных ретиноевой кислотой. Выделение и определение первичной структуры» авторов Костанян И.А., Астаповой М.В., Старовойтовой Е.В., Драницыной С.М., Липкина В.М. (Биоорган, химия. 1995. Т. 21. С. 243-248).
Этот фактор в дальнейших работах авторов получил наименование «Human Leukemia Differentiation Factor», или «HLDF».
Данный фактор представляет собой гликозилированный белок с молекулярной массой 8,2 кДа, содержащий 54 аминокислотных остатка (а.о.), который получается при гликозилировании и протеолитическом процессинге, в результате чего от N-конца экспрессированного белка отщепляется 43 аминокислотных остатка при расщеплении связи Q43-А44. HLDF способен индуцировать дифференцировку клеток HL-60 в фенотипически зрелые гранулоциты (Костанян И.А., Астапова М.В., Старовойтова Е.В., Драницына С.М., Липкин В.М. // Биоорган. химия. 1995. Т. 21. С. 243-248).
Данный фактор дифференцировки обнаруживается в организме человека в норме и при патологии (Соснина А.В., Морозов Д.В., Вараксин Н.А., Вонаршенко А.В., Байдакова Л.К., Аутеншлюс А.И., Липкин В.М. Способность фактора дифференцировки HLDF регулировать цитокинпродуцирующую функцию клеток крови при аденокарциномах желудка // ДАН. 2014. Т. 454. №5. С. 603-605).
Показано, что антитела к фактору HLDF являются специфическими маркерами апоптоза и позволяют оценить скорость запрограммированной гибели клеток в ходе нормального менструального цикла и при патологических процессах эндометрия. Отмечается, что антитела к фактору HLDF могут быть использованы в качестве нового иммуногистохимического маркера для дифференциальной диагностики доброкачественных и злокачественных процессов эндометрия (Ковязин В.А., Щелокова Е.Е., Костанян И.А. и др. «Проапоптотический фактор HLDF в нормальном, гиперпластическом и опухолевом эндометрии» /Архив патологии. Том: 69. Номер: 3 Год: 2007. Стр.: 23-26).
Известна работа «Классы и субклассы антител к фактору дифференцировки HLDF и пептидам гапонина, взаимосвязь их уровня с патогистологическими параметрами аденокарцином толстой кишки» авторов Сосниной А.В., Михайловой Е.С., Аутеншлюс А.И. и др. (Иммунология. Том: 33. Номер: 2. Год: 2012. Стр.: 92-94). Авторы установили, что при аденокарциномах толстой кишки уровень антител к фактору дифференцировки HLDF и пептидам гапонина субкласса G2 был более высоким при большем содержании высокодифференцированных клеток в опухоли. Предполагается, что аутоантитела к фактору дифференцировки HLDF и гапонину являются регуляторами их биологических эффектов.
Таким образом, в отношении полноразмерного фактора дифференцировки HLDF известна его способность индуцировать дифференцировку клеток промиелоцитарного лейкоза HL-60 в фенотипически зрелые гранулоциты, т.е. имеются сведения о его влиянии на бластные формы клеток крови, в то время как его способность влиять на эпителиальные клетки, а тем более на опухолевую ткань, и в частности на инвазивную карциному молочной железы неспецифического типа, которая является самой распространенной опухолью молочной железы, из уровня техники не известна. Также не известна способность полноразмерного фактора дифференцировки HLDF снижать относительное содержание низкодифференцированных и повышать относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа.
При изучении фактора HLDF был идентифицирован его фрагмент длиной 6 а.о., а именно: Thr-Gly-Glu-Asn-His-Arg (TGENHR) (авторы назвали его «пептид HLDF-6»), полностью воспроизводящий дифференцирующую активность полноразмерного фактора (Костанян И.А., Астапова М.В., Наволоцкая Е.В., Лепихова Т.Н., Драницына С.М., Телегин Г.Б., Родионов И.Л., Байдакова Л.К., Золотарев Ю.А., Молотковская И.М., Липкин В.М. Биологически активный фрагмент фактора дифференцировки клеток линии HL-60. идентификация и свойства // Биоорганическая химия. 2000. Т. 26. №7. С. 505-511). Данный пептид был получен методом твердофазного пептидного синтеза (патент РФ №2213747). Он обладает свойством индуцировать дифференциацию и ингибировать пролиферацию клеток-мишеней промиелоцитарного лейкоза HL-60 и эритромиелоцитарного лейкоза К-562.
В работе Батеневой А.В., Бабенко О.А., Даниленко Е.Д. и др. «Исследование противоопухолевых свойств липосомальной формы фрагмента фактора дифференцировки HLDF в культуре клеток» (Экспериментальная и клиническая фармакология. Том: 73. Номер: 2. Год: 2010. Стр.: 18-21) на первичной культуре клеток лимфосаркомы мышей показано, что липосомальная форма пептида HLDF-6 обладает способностью ингибировать пролиферацию и усиливать гибель клеток лимфосаркомы штаммов LS и RLS.
На модели карциномы легких Льюис установлено, что шестичленный пептид HLDF-6 обладает антиметастатическим и иммуномодулирующим действием (Сысоева Г.М., Фадина В.А., Даниленко Е.Д.. и др. Противоопухолевое и иммуномодулирующее действие фрагмента фактора дифференцировки клеточной линии HL-60 на мышах с карциномой легких Льюис//Бюллетень экспериментальной биологии и медицины. Том: 147. Номер: 2. Год: 2009. Стр.: 190-193). При этом авторы отмечают, что пептид HLDF-6 не обладал способностью тормозить рост первичного опухолевого узла, но проявлял выраженные антиметастатические свойства. Отмечается наличие у пептида HLDF-6 иммуномодулирующей активности, которой, по мнению авторов, и объясняется антиметастатическое действие препарата.
Таким образом, из литературы известно свойство пептида HLDF-6 ингибировать пролиферативную активность культуры клеток лимфосаркомы и оказывать на них цитотоксическое действие. Однако на модели карциномы Льюиса, то есть на модели солидной опухоли, цитотоксическое действие подтверждено не было, хотя авторами и отмечено антиметастатическое и иммуномодулирующее действие пептида HLDF-6. Источников, которые свидетельствовали бы о действии пептида HLDF-6 на опухолевой процесс в молочной железе, не обнаружено. Тем более отсутствуют сведения о влиянии данного препарата на инвазивную карциному молочной железы неспецифического типа. Также не известна способность пептида HLDF-6 снижать относительное содержание низкодифференцированных и повышать относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа.
Известна нейропротективная и ноотропная активность пептида HLDF-6 (Bogachouk АР, Storozheva ZI, Solovjeva OA, Sherstnev VV, Zolotarev YA, Azev VN, Rodionov IL, Surina EA, Lipkin VM. Comparative study of the neuroprotective and nootropic activities of the carboxylate and amide forms of the HLDF-6 peptide in animal models of Alzheimer's disease // J Psychopharmacol. 2016 Jan; 30(l):78-92. doi: 10.1177/0269881115616393), отмечается возможность потенциального применения HLDF-6 и его амидной формы при нарушениях памяти, связанных с нейродегенеративными заболеваниями (Sewell RD, Gruden MA, Pache DM, Storogeva ZI, Kostanyan IA, Proshin AT, Yurasov VV, Sherstnev VV. Does the human leukaemia differentiation factor fragment HLDF6 improve memory via brain DNA and protein synthesis? //J Psychopharmacol. 2005 Nov; 19(6):602-8; Богачук А.П., Сторожева З.И., Телегин Г.Б., Чернов А.С., Прошин А.Т., Шерстнев В.В., Золотарев Ю.А., Липкин В.М. Специфическая активность амидной формы пептида HLDF-6: изучение на трансгенной модели болезни Альцгеймера // Acta Naturae (русскоязычная версия). 2017. Т. 9. №3 (34). С. 68-74).
Таким образом, из уровня техники не известна способность ни полноразмерного фактора дифференцировки HLDF, ни его укороченной, синтезированной версии - пептида HLDF-6 влиять на опухолевую ткань, и в частности на инвазивную карциному молочной железы неспецифического типа. Также не известна их способность снижать относительное содержание низкодифференцированных клеток не путем их разрушения, а путем повышения их дифференцировки, в результате чего повышается относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа.
Раскрытие изобретения
В качестве средства, снижающего относительное содержание низкодифференцированных и повышающего относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа человека, предлагается применение фактора дифференцировки, получаемого из культуральной среды промиелоцитарной лейкемической линии клеток человека HL-60, обработанных ретиноевой кислотой (Human Leukemia Differentiation Factor, HLDF), имеющего молекулярную массу 8,2 к Да, представляющего собой гликопротеин, белковая часть которого соответствует молекулярной массе 6,2 кДа и имеет следующую аминокислотную последовательность: AGIMASLLKMLSAGPFVGWVSQMIPFSDWPRRWHRLKELLTGENHRCGIFVINK (SEQ ID NO: 1: Ala Gly Ile Met Ala Ser Leu Leu Lys Met Leu Ser Ala Gly Pro Phe Val Gly Trp Val Ser Gln Met Ile Pro Phe Ser Asp Trp Pro Arg Arg Trp His Arg Leu Lys Glu Leu Leu Thr Gly Glu Asn His Arg Cys Gly Ile Phe Val Ile Asn Lys).
Выделение фактора дифференцировки HLDF из культуральной среды линии клеток HL-60 включает адаптацию клеток к росту на бессывороточной среде; обработку их ретиноевой кислотой; отделение культуральной среды от клеток; ее фильтрацию; осаждение путем высаливания сульфатом аммония; ресуспенидрование осажденного материала; разделение его с помощью гель-фильтрации; выделение диализом наиболее активной фракции, которую подвергают ионно-обменной хроматографии; элюируют фракцию, полученную при концентрации NaCl, равной 0.05 М; выделяют ее диализом; лиофильно высушивают.
Более подробно способ получения фактора дифференцировки описан ниже.
Технические результаты предлагаемого изобретения:
1) снижение относительного содержания низкодифференцированных клеток и повышение относительного содержания высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа;
2) снижение относительного содержания низкодифференцированных клеток происходит путем трансформации клеток с повышением их дифференцировки, а не путем их разрушения.
Большинство противоопухолевых средств направлено на уничтожение опухоли путем разрушения клеток, что сопровождается цитотоксическим действием в отношении других клеток организма.
В доступной литературе не найдено описание средств для лечения инвазивной карциномы молочной железы неспецифического типа, которые обладали бы не цитотоксическим действием, а способностью повышать дифференцировку опухолевых клеток.
3) в связи с тем, что механизм действия HLDF связан с трансформацией клеток, он не оказывает цитотоксического действия, что доказывается отсутствием статистически значимого различия между количеством опухолевых клеток, общим количестве митозов, количеством патологических и физиологических митозов при применении HLDF и при отсутствии его применения;
4) HLDF не вызывает усиления дистрофически-дегенеративных изменений, а также явлений апоптоза;
5) в отличие от антрациклинов HLDF не обладает повреждающим действием на мембраны, белковые и липидные элементы клеток организма, т.к., как было указано выше, количество митозов не отличается при применении HLDF и отсутствии его применения, что является показателем того, что биосинтетические процессы в клетках, которые зависят от состояния в том числе и мембран, протекают в обычном для опухоли режиме.
Получение фактора дифференцировки HLDF
Клетки человека промиелоцитарной лейкемической линии HL-60, полученной из крови больного острым лейкозом, адаптируют к росту на бессывороточной среде. Для этого взвесь клеток, содержащую 2×105 клеток/мл, в количестве 20 мл помещают в бессывороточную среду RPMI-1640 (80 мл), в которую дополнительно внесены этаноламин 20 мкМ, аскорбиновая кислота (3 мкг/мл) и цитрат железа 500 мкМ (далее - питательная среда). Клетки культивируют при 37°С в атмосфере увлажненного 5% СО2 и пересаживают каждые 3-4 дня 2×105 клеток/мл в новые емкости, осуществляя 2-3 пассажа.
Полученные адаптированные клетки в концентрации 2×105 клеток/мл в количестве 20 мл помещают во флаконы и добавляют до 100 мл питательной среды RPMI-1640, в которую дополнительно внесены этаноламин 20 мкМ, аскорбиновая кислота (3 мкг/мл) и цитрат железа 500 мкМ. Таким образом готовят 15 флаконов. Сразу после рассева во флаконы с клетками и питательной средой вносят полностью транс-ретиноевую кислоту с конечной концентрацией в среде культивирования 30 нмоль/л.
Через 3-4 суток питательную среду культивирования из всех флаконов (1,5 л) фильтруют через фильтр 0,45 ц, добавляют сульфат аммония до 70% насыщения при 4°С (рН 7,0).
Осажденный материал ресуспендируют в 15 мл 0,1 М трис-HCl, 0,2 М NaCl, рН 7,4. Разделение полученного материала с помощью гель-фильтрации осуществляют в том же буфере на колонке (1×80 см) Toyopearl HW55 (Toyosoda, Япония) со скоростью элюции 3 мл/ч. Получают 5 фракций, обладающих дифференцирующей активностью. Наиболее активную фракцию I (активность - 150 ед. акт./мг) диализуют против раствора аммиака и наносят на колонку с анионообменником Mono Q HR5/5 (FPLC, Pharmacia), уравновешенную 0,01 М этаноламином, рН 9,2. Элюцию осуществляют градиентом концентрации NaCl. Дифференцирующая активность обнаруживается в элюате при концентрации NaCl, равной 0.05 М. Активную фракцию диализуют против раствора аммиака и лиофильно высушивают.В результате получается 0,024 мг активной фракции фактора дифференцировки HLDF.
Обоснование изобретения
Материалом исследования служили образцы опухолей 24 женщин с инвазивной карциномой молочной железы неспецифического типа. Образцы опухоли пациентки объемом 8 мм3 получали методом трепанобиопсии и помещали в 2 флакона, в одном из которых находилась только питательная среда DMEM-F12 в объеме 1 мл, а в другом - питательная среда в таком же объеме с HLDF (предоставленного Институтом биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН) в концентрации 20 мкг/мл (Freeman А.Е., Hoffman R.М. In vivo-like growth of human tumors in vitro // PNAS. - 1986. - Vol. 83. - P. 2694-2698.).
После инкубирования при 37°C в течение 72 ч образцы опухоли извлекали из среды и фиксировали в 10% растворе формалина. Из залитых в парафин объектов делали серийные срезы толщиной 7 мкм, которые окрашивали гематоксилином Гаррисона и эозином. Морфометрический анализ осуществлялся на базе микроскопа Micros МС 300А, цифровой камеры СХ 13с («Baumer Electric GmbH», Германия) и программного обеспечения Image J 1.42g (Национальный институт здоровья, США).
Для каждого пациента оценивалось по 8 микрофотографий (площадь каждой - 95578 мкм2), в результате чего тестируемая площадь составила 764624 мкм2. Определение степени дифференцировки клеток проводилось на основании анализа клеточного и ядерного полиморфизма (Шабалова И.П., Джангирова Т.В., Волченко Н.Н., Пугачев К.К. Цитологический атлас: Диагностика заболеваний молочной железы. - М. - Тверь: ООО «Издательство «Триада», 2005. - 119 с.; Рак молочной железы. Практическое руководство для врачей / [Ю.Ю. Андреева и др.]; под ред. Г.А. Франка, Л.Э. Завалишиной, К.М. Пожарисского. - М.: Практическая медицина, 2014. - 176 с.). Кроме того, на микрофотографиях определялось количество опухолевых клеток, общее количество митозов, из них -количество физиологических и патологических митозов.
Статистическую обработку результатов исследования проводили с использованием программного пакета для статистической обработки SPSS v 17.0 for Windows. Для сравнения зависимых групп использовали критерий Вилкоксона. Различия между значениями сравниваемых параметров расценивали как статистически значимые при р<0,05. Полученные в ходе исследования данные представлены как медиана (Me) и интерквартильный размах (Q1; Q3).
Результаты исследования
При изучении образцов опухолей, культивирование которых осуществлялось без добавления в среду HLDF, было отмечено, что инвазивная карцинома неспецифичного типа характеризовалась типичным строением с формированием гнезд, кластеров и трабекул. В части опухолей выявлялись четкие тубулярные структуры с просветом в центре. Участков некроза опухоли не наблюдалось, подавляющее большинство клеточных элементов было без признаков дегенеративно-дистрофических изменений, апоптотические тельца отсутствовали. Вместе с тем клетки опухоли были довольно вариабельны по строению.
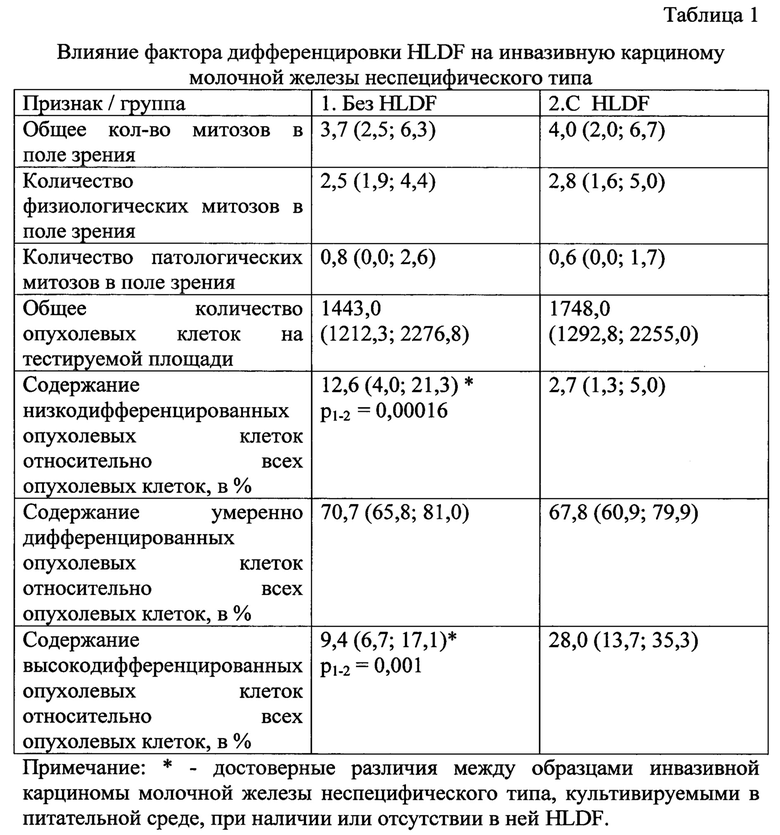
При морфометрическом анализе было выявлено, что низкодифференцированные опухолевые клетки, для которых характерны крупные ядра неправильной формы, в том числе с выростами, неровными контурами, с грубым хроматином, одним или несколькими ядрышками, составляли 12,6% (4,0; 21,3) (таблица 1). Умеренно дифференцированные клетки, для которых характерно умеренное увеличение размеров клеток, умеренный клеточный и ядерный полиморфизм, составляли 70,7% (65,8; 81,0). Высокодифференцированные клетки, имеющие мелкие одноморфные ядра с дисперсным распределением хроматина без ядрышек, составили 9,4% (6,7; 17,1) от общего количества опухолевых клеток.
При изучении образцов опухолей, культивирование которых осуществлялось с добавлением в среду HLDF, было отмечено, что инвазивная карцинома неспецифичного типа характеризовалась типичной картиной, присущей этому гистологическому варианту рака молочной железы. Так же, как и при культивировании без добавления HLDF, участков некроза клеточных элементов не отмечалось, дистрофически-дегенеративные изменения наблюдались лишь у единичных опухолевых клеток, апоптотические тельца отсутствовали. Вместе с тем обращал на себя внимание меньший клеточный и ядерный полиморфизм клеток опухоли, значительно реже выявлялись клеточные элементы, ядра которых имели укрупненные ядрышки.
При морфометрическом анализе было выявлено, что низкодифференцированные опухолевые клетки составили всего 2,7% (1,3; 5,0), что достоверно отличалось от аналогичного показателя образцов, которые культивировались без добавления в среду HLDF (таблица 1). Умереннодифференцированные клетки составляли 67,8% (60,9; 79,9), что статистически значимо не отличалось от их относительного содержания при культивировании без добавления в среду HLDF. Высокодифференцированные клетки составили 28,0% (13,7; 35,3) от общего количества опухолевых клеток, что было достоверно выше, чем при культивировании без добавления в среду фактора дифференцировки.
Обращает на себя внимание тот факт, что общее количество опухолевых клеток на тестируемой площади молочной железы статистически значимо не отличалось в образцах, которые культивировались без добавления и с добавлением HLDF, что свидетельствует о том, что добавление HLDF в среду не вызывает гибель опухолевых клеток, но влияет на соотношение клеток с различной дифференцировкой, приводя к снижению относительного содержания низкодифференцированных и увеличению относительного содержания высокодифференцированных клеток.
Кроме того, общее количество митозов в поле зрения, количество физиологических и патологических митозов достоверно не различались в образцах, которые культивировались без добавления и с добавлением HLDF, что также свидетельствует в пользу того, что изменения относительного содержания низко- и высокодифференцированных клеток связаны не с появлением новой популяции клеток, а с изменением соотношения между клетками с различной дифференцировкой.
Таким образом, фактор дифференцировки HLDF (Human Leukemia Differentiation Factor) вызывает снижение относительного содержания низкодифференцированных клеток и повышение относительного содержания высокодифференцированных клеток инвазивной карциномы молочной железы неспецифического типа.
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное образовательное учреждение высшего образования «Новосибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО НГМУ Минздрава России);
Федеральное государственное бюджетное научное учреждение "Федеральный исследовательский центр фундаментальной и трансляционной медицины" (ФИЦ ФТМ);
Федеральное государственное бюджетное учреждение науки «Институт биоорганической химии им. Академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук» (ИБХ РАН).
<120> Средство, снижающее относительное содержание низкодифференцированных и повышающее относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа
<160>1
<210>1
<211>54
<212>PRT
<213>Homo sapiens
<400>
Ala Gly Ile Met Ala Ser Leu Leu Lys Met Leu Ser Ala Gly Pro Phe Val Gly Trp Val Ser Gin Met Ile Pro Phe Ser Asp Trp Pro Arg Arg Trp His Arg Leu Lys Glu Leu Leu Thr Gly Glu Asn His Arg Cys Gly Ile Phe Val Ile Asn Lys
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, снижающее относительное содержание низкодифференцированных и повышающее относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа | 2022 |
|
RU2786528C1 |
| Композиция для повышения содержания высокодифференцированных клеток в аденокарциноме молочной железы | 2018 |
|
RU2697199C1 |
| АНТИТЕЛО К ФАКТОРУ HLDF, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ПЕПТИД С АНТИГЕННЫМИ И НК-ГИДРОЛИЗУЮЩИМИ СВОЙСТВАМИ И СПОСОБ ДИАГНОСТИКИ АНАПЛАСТИЧЕСКОГО СОСТОЯНИЯ КЛЕТКИ ЧЕЛОВЕКА | 2000 |
|
RU2276672C2 |
| Способ прогнозирования эффективности применения средства для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы и композиция для его осуществления | 2018 |
|
RU2705398C1 |
| Рекомбинантный Fab-scFv на основе нейтрализующего антитела против интерферона бета-1а человека и антитела против рецептора ErbB2 человека | 2019 |
|
RU2748953C1 |
| Способ прогнозирования гематогенного метастазирования при инвазивной карциноме неспецифического типа молочной железы на основе определения различных популяций циркулирующих опухолевых клеток в крови до лечения | 2018 |
|
RU2678202C1 |
| Способ прогнозирования риска опухолевой прогрессии у больных раком молочной железы | 2024 |
|
RU2838618C1 |
| Способ активации цитотоксических Т-лимфоцитов в популяции мононуклеарных клеток крови при помощи мембранных везикул, полученных из генетически модифицированных опухолевых клеток меланомы М14 со сверхэкспрессией интерлейкина 2 | 2022 |
|
RU2790867C1 |
| ПРИМЕНЕНИЕ РЕКОМБИНАНТНОГО АНАЛОГА ВОДОРАСТВОРИМОГО ДОМЕНА БЕЛКА LYNX1 ДЛЯ ТОРМОЖЕНИЯ РОСТА КЛЕТОК КАРЦИНОМ | 2019 |
|
RU2721129C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ ЗЛОКАЧЕСТВЕННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2485517C2 |
Изобретение относится к области биотехнологии, а именно к применению фактора дифференцировки в качестве средства, снижающего относительное содержание низкодифференцированных и повышающего относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа человека. Указанный фактор получен из культуральной среды промиелоцитарной лейкемической линии клеток человека HL-60, обработанных ретиноевой кислотой, имеющего молекулярную массу 8,2 кДа, представляющего собой гликопротеин, белковая часть которого соответствует молекулярной массе 6,2 кДа и имеет следующую аминокислотную последовательность: AGIMASLLKMLSAGPFVGWSQMIPFSDWPRRWHRLKELLTGENHRCGIFVINK. Изобретение позволяет оказывать противоопухолевое действие, не разрушая опухолевые клетки, а трансформируя их; не оказывает цитотоксического действия, в частности не вызывает усиления дистрофически-дегенеративных изменений, явлений апоптоза, повреждения мембран, белковых и липидных элементов клеток организма. 1 з.п. ф-лы, 1 табл.
1. Применение фактора дифференцировки, полученного из культуральной среды промиелоцитарной лейкемической линии клеток человека HL-60, обработанных ретиноевой кислотой, имеющего молекулярную массу 8,2 кДа, представляющего собой гликопротеин, белковая часть которого соответствует молекулярной массе 6,2 кДа и имеет следующую аминокислотную последовательность: AGIMASLLKMLSAGPFVGWSQMIPFSDWPRRWHRLKELLTGENHRCGIFVINK, в качестве средства, снижающего относительное содержание низкодифференцированных и повышающего относительное содержание высокодифференцированных клеток в инвазивной карциноме молочной железы неспецифического типа человека.
2. Применение фактора дифференцировки по п. 1, отличающееся тем, что его получение из культуральной среды линии клеток человека HL-60 включает адаптацию клеток к росту на безсывороточной среде перед обработкой клеток ретиноевой кислотой; отделение культуральной среды от клеток; ее фильтрацию; осаждение путем высаливания сульфатом аммония; ресуспенидрование осажденного материала; разделение его с помощью гель-фильтрации; выделение диализом наиболее активной фракции, которую подвергают ионно-обменной хроматографии; элюируют фракцию, полученную при концентрации NaCl, равной 0.05 М; выделяют ее диализом; лиофильно высушивают.
| VENTER J.C., et al | |||
| "The sequence of the human genome.", Science | |||
| Мяльно-трепальный станок для обработки тресты лубовых растений | 1922 |
|
SU200A1 |
| КЛЕТОЧНАЯ ЛИНИЯ А4 Т-ЛИМФОБЛАСТНОГО ЛЕЙКОЗА ЧЕЛОВЕКА, ИСПОЛЬЗУЕМАЯ ДЛЯ СКРИНИНГА ПРОТИВООПУХОЛЕВЫХ ПРЕПАРАТОВ | 2004 |
|
RU2267532C1 |
| KOSTANYAN I.A., et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Isolation and primary structure", FEBS Lett | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| WO2011079017 A2, 30.06.2011. | |||
Авторы
Даты
2021-02-24—Публикация
2019-12-11—Подача