Изобретение относится к медицине, конкретно к онкологии.
Изобретение может быть использовано для подбора больных раком молочной железы с целью повышения эффективности дифференцировочной терапии для снижения степени злокачественности аденокарциномы молочной железы в дооперационный период.
Одним из подходов в лечении злокачественных новообразований является индукционная и неоадъювантная терапия, которые представляют собой первый этап лечения рака различной этиологии. Известная как основная терапия, или терапия первой линии, индукционная и неоадъювантная терапия назначается с целью уменьшения количества раковых клеток и для подготовки больного к хирургическому лечению. Поскольку уменьшение количества малигнизированных клеток в опухоли может быть достигнуто за счет снижения в ней содержания наиболее злокачественных низкодифференцированных клеток и повышения содержания высокодифференцированных клеток, то к вышеуказанному направлению в лечении злокачественных новообразований можно отнести и дифференцировочную терапию. Этот вид лечения злокачественных новообразований основывается на концепции о возможности инициации дифференцировки опухолевых клеток, их реверсии в нормальный фенотип, что снизит степень злокачественности опухоли в предоперационный период (Kawamata Н., Tachibana М., Fujimori Т., Imai Y. Differentiation-inducingtherapyforsolidtumors // Curr. Pharm. Des. - 2006. - Vol.12. - №3. - P. 379-385).
инкубированной без Композиции, и при величине ИВКСЦ, равной или превышающей 700, прогнозируют повышение относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы данного пациента с помощью Композиции.
Техническими результатами предлагаемого способа являются следующие:
- способ позволяет прогнозировать эффективность/неэффективность ее применения для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы пациента с инвазивным протоковым раком;
- способ позволяет отобрать пациентов с аденокарциномами молочной железы, у которых с вероятностью 1,00 (т.е. у 100% пациентов) можно с помощью данной Композиции повысить относительное содержание высокодифференцированных клеток в опухоли и этим снизить ее злокачественность;
- способ позволяет сделать прогноз в отношении каждого пациента,
- Композиция наряду со свойством стимулировать дифференцировку опухолевых клеток у ряда пациентов с аденокарциномами молочной железы обладает также свойством стимулировать наработку иммунокомпетентными клетками крови данного ряда пациентов цитокинов IL-6, TNF-α и G-CSF в такой определенной мере, что это дает возможность с вероятностью, равной единице, прогнозировать у этих пациентов повышение содержания высокодифференцированных клеток в аденокарциноме молочной железы.
Перечень фигур иллюстративного материала
Фиг. 1. ROC-кривая, полученная при ROC-анализе индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-
CSF иммунокомпетентными клетками крови составила 700 и более. AUC: 1,0 - отличное качество модели.
Фиг. 2. ROC-кривая, полученная при ROC-анализе индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови составила 300-699. AUC: 0,667 - среднее качество модели.
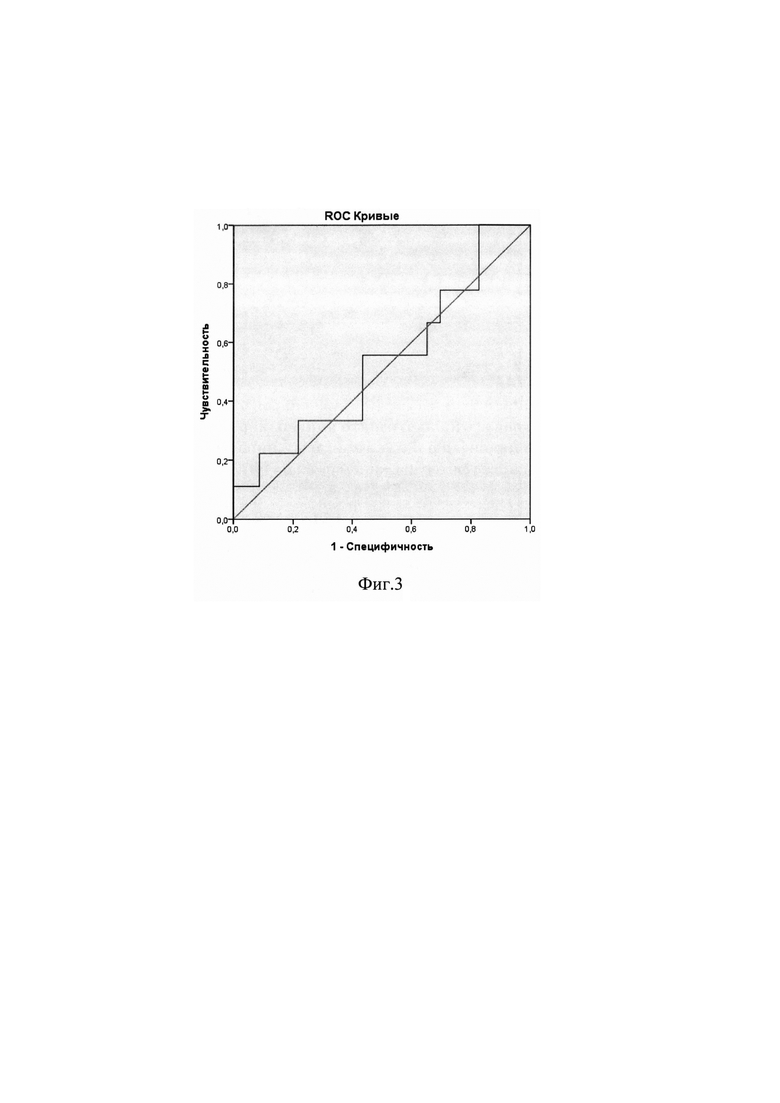
Фиг. 3. ROC-кривая, полученная при ROC-анализе индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови составила 15-299. AUC: 0,536 - неудовлетворительное качество модели.
Способ прогнозирования эффективности применения вышеуказанного средства для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы осуществляют следующим образом.
Цельную кровь, в количестве 1 мл, взятую из вены пациента с инвазивным протоковым раком молочной железы, который гистологически характеризуется как аденокарцинома, помещают в стерильный флакон с 4 мл среды DMEM/F12, содержащей Hepes (15 mM), гепарин (2,5 ЕД/мл), гентамицин (100 мкг/мл).
Аккуратно перемешивают содержимое флакона, затем из него в стерильных условиях забирают 0,980 мл разбавленной крови и помещают ее в стерильный флакон, содержащий 0,020 мл физиологического раствора с Композицией, включающей фитогемагглютинин Р, фитогемагглютинин М, конканавалин А, липополисахарид (Escherichia coli), взятые в соотношении (мас. ч.) 1:1:2:1 соответственно, достигая их эффективных концентраций.
В качестве эффективных концентраций компонентов Композиции в конечном разведении (в растворе с кровью) могут быть использованы, например, следующие: фитогемагглютинин Р - 1,6-2,4 мкг/мл, фитогемагглютинин М - 1,6-2,4 мкг/мл, конканавалин А - 3,2-4,8 мкг/мл, липополисахарид из Escherichia coli - 1,6-2,4 мкг/мл, т.е. 8-12 мкг Композиции в 1 мл при указанном выше соотношении компонентов в Композиции (мас. ч.).
Из того же указанного выше флакона с кровью пациента и питательной средой DMEM/F12, содержащей Hepes, гепарин, гентамицин, снова забирают 0,980 мл разбавленной крови и помещают ее в другой стерильный флакон, содержащий 0,020 мл физиологического раствора.
Содержимое флаконов аккуратно перемешивают и помещают в термостат при 37°С на 24 часа. В течение первого часа инкубации содержимое флаконов аккуратно перемешивают 1 раз.
После инкубации путем центрифугирования при 3000 об/мин в течение 10 минут осаждают клетки крови и отбирают супернатанты из пробы крови, инкубированной с Композицией (продукция цитокинов под влиянием Композиции), и из пробы крови, инкубированной без Композиции (спонтанная продукция цитокинов), в которых с помощью твердофазного иммуноферментного анализа определяют концентрации цитокинов IL-6, TNF-α и G-CSF (в пг/мл).
Индекс влияния Композиции на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови вычисляют по формуле: ИВКСЦ=(AIL-6+ATNF-α+AG-CSF): (БIL-6+БTNF-α+БG-CSF), где AIL-6, ATNF-α, AG-CSF - концентрации (пг/мл) IL-6, TNF-α и G-CSF в пробе с Композицией, БIL-6, БTNF-α, БG-CSF - концентрации IL-6, TNF-α и G-CSF в пробе без Композиции. При величине ИВКСЦ, равной или превышающей 700, прогнозируют повышение относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы данного пациента под влиянием Композиции.
Обоснование изобретения
Изучение влияния Композиции на дифференцировку опухолевых клеток в биоптатах аденокарциномы молочной железы
В качестве объекта для изучения влияния Композиции на дифференцировку опухолевых клеток служили биоптаты опухолей 45 женщин в возрасте от 43 до 75 лет с инвазивным протоковым раком, являющимся по гистологическому типу аденокарциномой II и III степени злокачественности.
Биоптаты были получены методом витальной трепанобиопсии во время предоперационного клинико-лабораторного обследования пациентов.
Биоптаты каждой больной объемом 8 мм3 помещали в 2 стеклянных флакона.
Флакон №1 (тест-контроль) содержал: 1 мл стерильной питательной среды DMEM/F12, Hepes (15 mM), гепарин (2,5 ЕД/мл), гентамицин (100 мкг/мл), L-глютамин (0,6 мг/мл) и биоптат аденокарциномы молочной железы одной больной объемом 8 мм3.
Флакон №2 (тест на стимуляцию дифференцировки опухолевых клеток Композицией) содержал: 1 мл стерильной питательной среды DMEM/F12, Hepes (15 mM), гепарин (2,5 ЕД/мл), гентамицин (100 мкг/мл), L-глютамин (0,6 мг/мл), биоптат аденокарциномы молочной железы той же больной объемом 8 мм3 и Композицию, включающую фитогемагглютинин Р (РНА-Р), фитогемагглютинин М (РНА-М), конканавалин А (COnA), липополисахарид LPS (Lipopolysaccharide Escherichia coli), взятые в соотношении (мас. ч.) 1:1:2:1 соответственно. В описываемом исследовании использовались следующие концентрации компонентов Композиции в конечном разведении: фитогемагглютинин Р - 2 мкг/мл, фитогемагглютинин М - 2 мкг/мл, конканавалин А - 4 мкг/мл, липополисахарид (Lipopolysaccharide from Escherichia coli) - 2 мкг/мл.
После инкубирования при 37°С в течение 72 ч биоптаты аденокарцином молочной железы извлекали из флаконов и фиксировали в
растворе 10% нейтрального формалина для дальнейшего патогистологического исследования.
Патогистологическое исследование проводилось на препаратах аденокарциномы молочной железы, окрашенных по стандартной методике гематоксилином и эозином. В опухолевой ткани подсчитывали относительно содержание (%) клеток различной степени дифференцировки: высокодифференцированных (ВД), умереннодифференцированных (УД) и низкодифференцированных (НД). Для этого с помощью морфометрической сетки с 121 рабочими точками-узлами, вставленной в окуляр микроскопа, при увеличении 20×1,5×10=300х определяли количество точек, попавших на высоко-, умеренно- и низкодифференцированные опухолевые клетки. В каждом препарате подсчитывали клетки в 10 полях зрения и для Каждой категории клеток подсчитывали среднее арифметическое значение, выраженное в процентах (Автандилов Г.Г. Медицинская морфометрия. - М.: Медицина, 1990. - 381 с.).
При оценке принадлежности опухолевых клеток к ВД, УД или НД учитывали степень выраженности клеточного полиморфизма, ядерно-цитоплазматическое соотношение, наличие митозов, в том числе патологических, способность к структурообразованию (формированию желез), сохранение функций клеток (слизеобразование). ВД клетки характеризовались приближенной к нормальным клеткам формой, преобладанием цитоплазмы над ядром, способностью строить железы и продуцировать слизь. НД клетки характеризовались неправильной формой, выраженным полиморфизмом, преобладанием ядра над цитоплазмой, отсутствием способности к формированию структур, диффузным ростом, наличием большого количества митозов, в том числе и патологических. УД клетки занимали промежуточное положение между ВД и НД клетками по выраженности вышеуказанных признаков.
Индекс повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптатах молочной железы для каждого пациента вычисляли по формуле: ИПВД=(ВД:НД)К/(ВД:НД)БК (где (ВД:НД)К - отношение среднего значения (по 10 полям зрения) доли высокодифференцированных клеток (%) к среднему значению доли низкодифференцированных клеток (%) в биоптате аденокарциномы молочной железы после стимуляции Композицией, (ВД:НД)БК - отношение среднего значения доли высокодифференцированных клеток (%) к среднему значению доли низкодифференцированных клеток (%) в биоптате аденокарциномы молочной железы без стимуляции Композицией.
Определение ИПВД у больных с опухолью молочной железы показало, что из 45 пациентов с инвазивным протоковым раком ИПВД с величиной 1,1 и более (вариабельность 1,1-5,0) (ИПВД≥1,1 свидетельствует о стимуляции дифференцировки и повышении относительного содержания высокодифференцированных клеток в биоптате аденокарциномы молочной железы под влиянием Композиции) отмечался у 20 человек (44,4%), а с величиной менее 1,1-25 человек (55,6%).
В группе пациентов с показателем ИПВД 1,1 и более различия между количеством высокодифференцированных опухолевых клеток в биоптатах аденокарциномы молочной железы без стимуляции дифференцировки Композицией и количеством высокодифференцированных опухолевых клеток в биоптатах после стимуляции их Композицией оказались статистически значимы (р=0,004) при оценке с помощью непараметрического критерия Манна-Уитни.
Изучение влияния Композиции на продукцию цитокинов иммунокомпетентными клетками крови пациентов и связи между повышением содержания высокодифференцированных клеток в опухоли и показателями крови
Для того, чтобы разработать способ прогнозирования эффективности применения Композиции для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы
того или иного больного, не используя биоптаты и трепанобиопсию, а по показателям его крови (показателям продукции различных цитокинов иммунокомпетентными клетками крови), параллельно изучению влияния Композиции на дифференцировку опухолевых клеток в биоптатах исследовали кровь вышеуказанных 45 пациентов.
Аналогично тому, как в разделе «Способ…. осуществляют следующим образом» описано определение концентрации цитокинов IL-6, TNF-α и G-CSF в супернатанте пробы крови пациента после инкубации их с Композицией и без нее, определяли концентрации цитокинов IL-2, IL-6, IL-8, IL-10, IL-17, IL-18, IL-1b, IL-1Ra, TNF-α, IFN-γ, G-CSF, GM-CSF, VEGF-A в супернатантах проб крови пациента после инкубации их с Композицией и без нее.
После этого для каждого цитокина вычисляли индекс влияния Композиции (ИВКЦ) на продукцию данного цитокина иммунокомпетентными клетками крови по формуле: ИВКЦ=АЦ: БЦ, где АЦ - концентрация (пг/мл) цитокина в супернатанте пробы крови пациента, инкубированных с Композицией, а БЦ - концентрация (пг/мл) цитокина в супернатанте пробы крови пациента, инкубированных без Композиции.
Из таблицы 1 видно, что с величинами ИПВД опухоли коррелировали величины ИВКЦ крови только трех цитокинов: IL-6, G-CSF и VEGF-A.
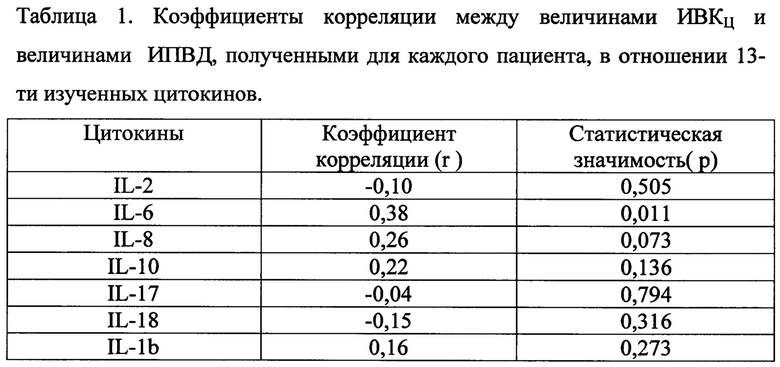
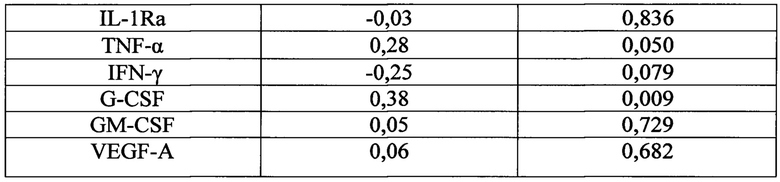
Примечание. ИВКЦ - индекс влияния Композиции на продукцию исследуемого цитокина в пробе крови пациента; ИПВД - индекс повышения содержания высокодифференцированных опухолевых клеток в биоптате молочной железы того же пациента.
При помощи корреляционного анализа было установлено, что индекс влияния Композиции на суммарную продукцию IL-6, TNF-α и G-CSF (ИВКСЦ) иммунокомпектентными клетками крови имеет более значительную корреляционную связь с показателем ИПВД опухоли, чем показатели ИВКЦ каждого отдельного цитокина (IL-6, TNF-α или G-CSF): r=0,42, р=0,003. Суммарный индекс по трем цитокинам ИВКСЦ определяют по формуле: ИВКСЦ=(AIL-6+ATNF-α+AG-CSF): (БIL-6+БTNF-α+БG-CSF), где AIL-6, ATNF-α, AG-CSF - концентрации (пг/мл) IL-6, TNF-α и G-CSF в пробе с Композицией, БIL-6, БTNF-α, БG-CSF - концентрации IL-6, TNF-α и G-CSF в пробе без Композиции.
При сопоставлении величин ИПВД (индекс повышения содержания высокодифференцированных опухолевых клеток в биоптатах опухоли молочной железы) и ИВКСЦ (индекс влияния Композиции на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови), полученных для каждого пациента, оказалось, что у всех пациентов с ИПВД равном или превышающем 1,1, т.е. у всех пациентов, у которых имело место повышение в биоптате опухоли относительного содержания высокодифференцированных клеток под влиянием Композиции, ИВКСЦ был равным или превышал 700 (табл. 2).
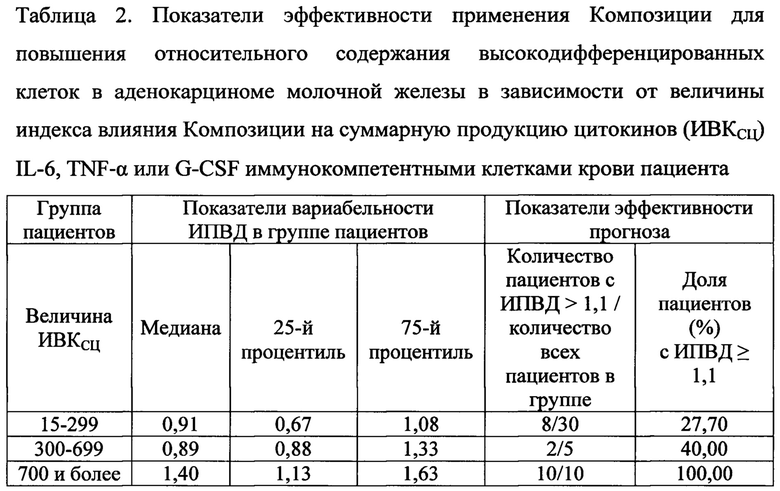
Из таблицы 2 видно, что у всех пациентов (100%), у который ИВКСЦ был равным или превышал 700, наблюдалось повышение относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы, т.е. ИПВД был равным или превышал 1,1.
При этом было установлено, что в группе пациентов с показателем ИПВД 1,1 и более различия между количеством высокодифференцированных опухолевых клеток без стимуляции Композицией и количеством высокодифференцированных опухолевых клеток после стимуляции Композицией были статистически значимы (р=0,004) при оценке с помощью непараметрического критерия Манна-Уитни.
Описанные выше результаты позволили заключить, что у пациента с величиной ИВКСЦ, равной или превышающей 700, будет иметь место повышение дифференцировки опухолевых клеток в аденокарциноме подвлиянием Композиции.
Полученные результаты позволяют перейти от показателя ИПВД (индекса повышения содержания высокодифференцированных опухолевых клеток), полученного при исследовании биоптатов аденокарциномы молочной железы, к показателю ИВКСЦ (индекс влияния Композиции на суммарную продукцию IL-6, TNF-α и G-CSF), полученному малоинвазивным методом (осуществляется только забор 1 мл крови).
Предлагаемый способ даст возможность выделить группу пациентов с аденокарциномой молочной железы, у которых применение Композиции повысит относительное содержание высокодифференцированных опухолевых клеток в аденокарциноме молочной железы, что приведет к снижению степени злокачественности опухоли.
Для получения числового выражения клинической значимости и эффективности предлагаемого способа использовали ROC-анализ с определением показателя AUC (AreaUnderCurve), который рассчитывали при помощи метода трапеций. О качестве способа судили по экспертной шкале для значений AUC, согласно которой значение AUC, равное 0,9-1,0 свидетельствует об отличном качестве модели, 0,8-0,9 - об очень хорошем качестве модели, 0,7-0,8 - о хорошем качестве модели, 0,6-0,7 - среднем качестве модели, 0,5-0,6 - неудовлетворительном качестве.
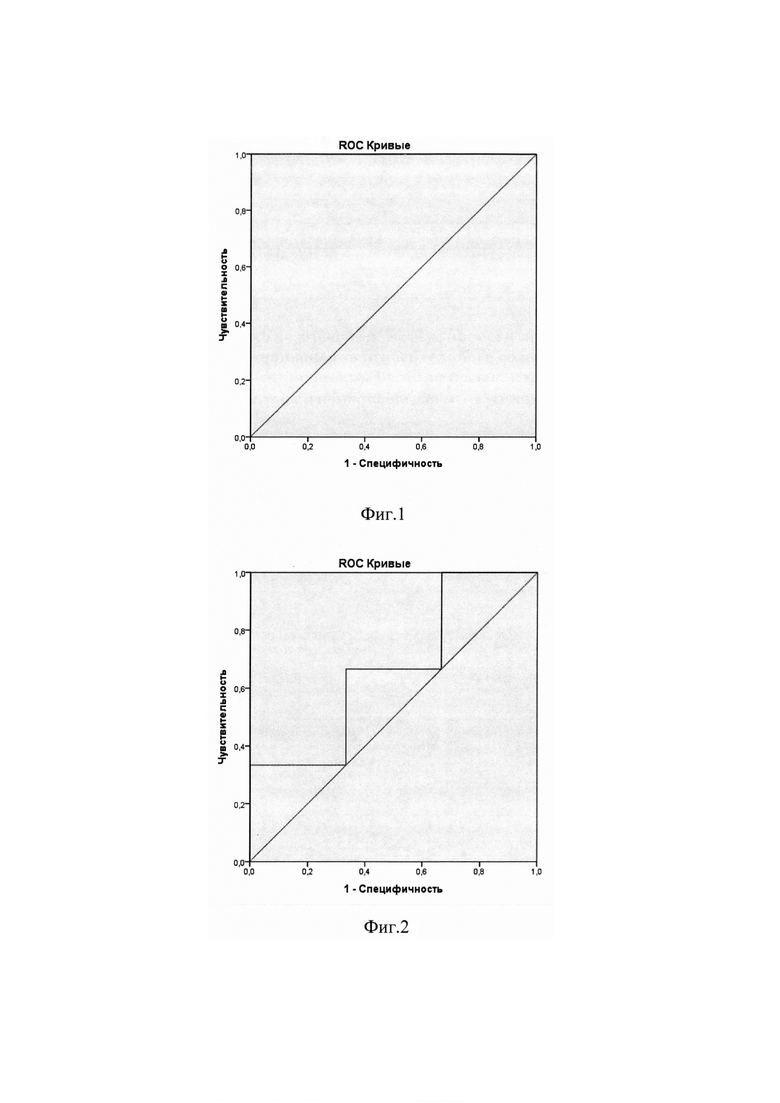
В результате ROC-анализа величин индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови составляла 700 и более, было получено значение AUC равное 1,0 (фиг. 1). Это указывает на отличное качество предложенного способа для оценки эффективности прогнозирования при величине ИВКСЦ у пациента равной 700 и более.
В результате ROC-анализа величин индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния
Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови находилась в пределах 300-699, было получено значение AUC: 0,667 (фиг. 2). Это указывает на среднее качество модели для оценки эффективности прогнозирования, если значения ИВКСЦ будут находиться в интервале 300-699.
В результате ROC-анализа величин индекса повышения содержания высокодифференцированных опухолевых клеток (ИПВД) в биоптате молочной железы в группе пациентов, у которых величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови находилась в пределах 15-299, было получено значение AUC: 0,536 (фиг. 3). Это указывает на неудовлетворительное качество модели для оценки эффективности прогнозирования, если значения ИВКСЦ будут находиться в интервале 15-299.
Таким образом, предлагаемый способ прогнозирования эффективности применения Композиции для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы у пациентов с инвазивным протоковым раком при величине индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови, равном 700 и более, показал отличное качество (AUC=1,0).
Клинические примеры
1. Больная Ш-ва, 75 лет, диагноз - инвазивный протоковый рак молочной железы.
Величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками периферической крови составила 848,1.
Заключение - применение вышеописанной Композиции повысит относительное содержание высокодифференцированных клеток в аденокарциноме молочной железы данной больной.
При исследовании биоптата данной пациентки величина ИПВД составила 5,00. Прогноз оказался правильным.
2. Больная Г-р, 68 лет, диагноз - инвазивный протоковый рак молочной железы.
Величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками периферической крови составила 726,9.
Заключение - применение вышеописанной Композиции повысит относительное содержание высокодифференцированных клеток в аденокарциноме молочной железы данной больной.
При исследовании биоптата данной пациентки величина ИПВД составила 1,63. Прогноз оказался правильным.
3. Больная П-о, 75 лет, диагноз - инвазивный протоковый рак молочной железы.
Величина индекса влияния Композиции (ИВКСЦ) на суммарную продукцию IL-6, TNF-α и G-CSF иммунокомпетентными клетками периферической крови составила 48,2.
Заключение - применение вышеописанной Композиции не повысит относительное содержание высокодифференцированных клеток в аденокарциноме молочной железы данной больной.
При исследовании биоптата данной пациентки величина ИПВД составила 0,78. Прогноз оказался правильным. пациентов повышение содержания высокодифференцированных клеток в аденокарциноме молочной железы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композиция для повышения содержания высокодифференцированных клеток в аденокарциноме молочной железы | 2018 |
|
RU2697199C1 |
| Способ выявления HER2 положительного молекулярного подтипа рака молочной железы | 2024 |
|
RU2839351C1 |
| Способ прогнозирования продолжительности жизни больных с метастатическими формами опухолей | 2023 |
|
RU2821659C1 |
| Способ оценки чувствительности опухоли к иммуноонкологическим препаратам | 2021 |
|
RU2771760C1 |
| Способ иммунотерапии рака молочной железы с помощью антиген-активированных дендритных клеток | 2016 |
|
RU2645464C1 |
| Способ прогнозирования развития метастазов у больных нерезектабельным трижды негативным раком молочной железы | 2023 |
|
RU2802141C1 |
| Способ прогнозирования длительности безрецидивного периода у больных резектабельным трижды негативным раком молочной железы | 2021 |
|
RU2780922C1 |
| Способ определения тактики лечения больных с метастатическими формами и рецидивами трижды негативного рака молочной железы | 2023 |
|
RU2818730C1 |
| Способ выявления предраковых изменений в молочной железе | 2017 |
|
RU2674164C1 |
| Способ иммунодиагностики рака желудка | 2023 |
|
RU2818734C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для прогнозирования эффективности применения средства для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы пациента с инвазивным протоковым раком. Указанным средством для повышения относительного содержания высокодифференцированных клеток является композиция, состоящая из фитогемагглютинина Р, фитогемагглютинина М, конканавалина А, липополисахарида из Escherichia coli, взятых в соотношении (мас. ч.) 1:1:2:1 соответственно (далее - Композиция). При этом определяют концентрации цитокинов IL-6, TNF-α и G-CSF в супернатанте пробы крови данного пациента, инкубированной с Композицией и без нее. После чего вычисляют индекс влияния Композиции (ИВКСЦ) на суммарную продукцию цитокинов IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови по формуле: ИВКСЦ=(AIL-6+ATNF-α+AG-CSF):(БIL-6+БTNF-α+БG-CSF), где AIL-6, ATNF-α, AG-CSF - концентрации (пг/мл) IL-6, TNF-α и G-CSF в супернатанте пробы крови пациента, инкубированной с Композицией, а БIL-6, БTNF-α, БG-CSF - концентрации IL-6, TNF-α и G-CSF в супернатанте пробы крови пациента, инкубированной без Композиции. При величине ИВКСЦ, равной или превышающей 700, прогнозируют повышение относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы данного пациента с помощью Композиции. Использование данного способа позволяет отобрать пациентов, у которых с помощью Композиции возможно повысить относительное содержание высокодифференцированных клеток в опухоли и снизить ее злокачественность. Композиция обладает свойствами стимулировать дифференцировку опухолевых клеток у ряда пациентов и стимулировать наработку иммунокомпетентными клетками крови данного ряда пациентов. 3 пр., 2 табл., 3 ил.
Способ прогнозирования эффективности применения средства для повышения относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы пациента с инвазивным протоковым раком, характеризующийся тем, что указанным средством для повышения относительного содержания высокодифференцированных клеток является композиция, состоящая из фитогемагглютинина Р, фитогемагглютинина М, конканавалина А, липополисахарида из Escherichia coli, взятых в соотношении (мас. ч.) 1:1:2:1 соответственно (далее - Композиция), при этом определяют концентрации цитокинов IL-6, TNF-α и G-CSF в супернатанте пробы крови данного пациента, инкубированной с Композицией и без нее, после чего вычисляют индекс влияния Композиции (ИВКСЦ) на суммарную продукцию цитокинов IL-6, TNF-α и G-CSF иммунокомпетентными клетками крови по формуле: ИВКСЦ=(AIL-6+ATNF-α+AG-CSF):(БIL-6+БTNF-α+БG-CSF), где AIL-6, ATNF-α, AG-CSF - концентрации (пг/мл) IL-6, TNF-α и G-CSF в супернатанте пробы крови пациента, инкубированной с Композицией, а БIL-6, БTNF-α, БG-CSF - концентрации IL-6, TNF-α и G-CSF в супернатанте пробы крови пациента, инкубированной без Композиции, и при величине ИВКСЦ, равной или превышающей 700, прогнозируют повышение относительного содержания высокодифференцированных клеток в аденокарциноме молочной железы данного пациента с помощью Композиции.
| КУНЦ Т.А | |||
| и др | |||
| Cравнительная оценка продукции цитокинов иммунокомпетентными клетками крови и опухоли в различных возрастных группах больных инвазивным протоковым раком молочной железы // Медицинская иммунология | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| - С | |||
| ДРОВОПИЛЬНО-ДРОВОКОЛЬНОЕ УСТРОЙСТВО | 1923 |
|
SU567A1 |
| АРХИПОВ С.А | |||
| и др | |||
| Цитокинпродуцирующий резерв иммунокомпетентных клеток крови и инвазивного протокового рака молочной железы, его взаимосвязь с патогистологическими и иммуногистохимическими параметрами злокачественного новообразования // Медицинская иммунология | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| - С | |||
| Устройство для механических испытаний лубовых волокон | 1922 |
|
SU459A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ НЕОАДЪЮВАНТНОЙ ХИМИОТЕРАПИИ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2469651C2 |
| WO 2011003905 A1, 13.01.2011 | |||
| BACUS S.S | |||
| et al | |||
| ПРИСПОСОБЛЕНИЕ К КОСЕ ДЛЯ КОСЬБЫ ДВУМЯ РУКАМИ (ОКОСЬЕ) | 1921 |
|
SU565A1 |
| Carcinog | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| - P | |||
| Способ приготовления консистентных мазей | 1912 |
|
SU350A1 |
Авторы
Даты
2019-11-07—Публикация
2018-08-17—Подача