Область техники
Эта заявка испрашивает приоритет и преимущество заявки на патент Кореи №10-2017-0079354, поданной в Корейское ведомство по интеллектуальной собственности 22 июня 2017 года, раскрытие которой включено в настоящий документ посредством ссылки.
Настоящее изобретение относится к системе доставки лекарственного средства, имеющей двойную структуру ядро-оболочка, и, в частности, к двойной системе доставки нанолекарства, имеющей внутреннюю структуру ядро-оболочка, содержащую плохо растворимое соединение камптотецина и водорастворимое соединение камптотецина внутри, и оболочку из амфифильного полимера, и к способу ее получения.
Предшествующий уровень техники
Для создания лекарственного средства, являющегося плохо растворимым, которое будет использоваться для инъекции, по существу необходима стадия солюбилизации и для преодоления такой проблемы использовались эмульсии, содержащие поверхностно-активные вещества, микроэмульсии, липосомы, мицеллы, пегилирование или получение пролекарств. 7-Этил-10-гидроксикамптотецин (SN-38), который является одним из лекарств, обладающих наибольшей активностью в качестве противоопухолевого средства на основе камптотецина, поставляется в виде иринотекана в форме пролекарства (торговое наименование: CAMTOSAR®, выпускаемое компанией Новартис), которое, в основном, гидролизуется карбоксилэстеразой II (CESII) in vivo для превращения в SN-38 в активной форме. Однако степень такого превращения составляет всего 2-8% ее отклонения также очень велики, и, таким образом, такое лекарство трудно правильно вводить больным раком, нуждающимся в точном соблюдении дозы, в результате чего его действие и побочные эффекты трудно предсказать.
Другой способ солюбилизации плохо растворимого лекарственного средства заключается в образовании мицелл лекарственного средства, имеющих наноразмерный диаметр частиц. Чтобы обеспечить инъекцию наномицелл для обеспечения стерильности и стабильности, водный раствор наномицелл стерильно фильтруют через фильтр 0,22 мкм, а затем в процессе изготовления превращают в порошок во время лиофильной сушки. В этом процессе, когда лиофилизированный продукт снова растворяют в растворителе для инъекций (физиологическом растворе или т.п.), из-за агломерации мицелл может образовываться большое количество макрочастиц (от 200 нм или более до нескольких десятков мкм). В частности, частицы размером более 5 мкм могут вызывать серьезные побочные эффекты при инъекции в организм человека и, таким образом, строго проверяются с помощью тестов на нерастворимые твердые частицы в Фармакопее США, Европейской фармакопее и Корейской фармакопее. Следовательно, в способе солюбилизации, при котором размеры частиц мало изменяются до и после лиофильной сушки, несмотря на мицеллообразование, частицы демонстрируют однородное распределение, и, в частности, нет частиц размером несколько мкм или более.
Между тем, для приготовления инъекционного препарата важно растворить активный ингредиент в подходящем растворителе, однако камптотецин или SN-38, который является гидрофобным соединением на основе камптотецина, хорошо не растворяется ни в воде, ни в большинстве летучих полярных органических растворителей (метаноле, этаноле, ацетонитриле, этилацетате и т.д.), используемых для приготовления фармацевтических препаратов. Растворители, способные растворять такие гидрофобные соединения на основе камптотецина, ограничены нелетучими растворителями, такими как диметилсульфоксид (ДМСО), диметилформамид, толуол и диоксан. Однако для удаления этих растворителей необходима процедура диализа и, несмотря на диализ, эти растворители трудно полностью удалить, что вызывает токсические проблемы, если они остаются.
Поэтому авторы настоящего изобретения искали и пытались разработать композиции стабильных частиц, в которых: камптотецин и SN-38, которые являются весьма плохо растворимыми противораковыми активными ингредиентами, можно вводить непосредственно в активной форме, а не в форме пролекарства; нет проблем с остаточными растворителями в процессе приготовления; мало изменяется размер частиц до и после сублимационной сушки; и не образуются макроагломерированные частицы размером несколько мкм или более.
Во всем описании приведены ссылки на многие патентные документы и приведены из них цитаты. Раскрытие цитируемых документов и патентных документов полностью включено путем ссылки в настоящее описание, а уровень техники, в которую входит настоящее изобретение, и детали настоящего изобретения поясняются более ясно.
Подробное описание изобретения
Техническая проблема
Аспект настоящего изобретения заключается в предложении частицы, включающей: i) гидрофобное соединение на основе камптотецина; ii) гидрофильное соединение на основе камптотецина; и iii) амфифильный блок-сополимер, состоящий из гидрофобного блока и гидрофильного блока.
Другой аспект настоящего изобретения заключается в предложении фармацевтической композиции для лечения рака, содержащей указанную частицу и фармацевтически приемлемый носитель.
Еще один аспект настоящего изобретения заключается в предложении способа получения частицы, включающего:
(а) формирование внутренней структуры ядро-оболочка, содержащей гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина; и (b) формирование внешней структуры ядро-оболочка, содержащей амфифильный сополимер.
Другие цели и преимущества настоящего изобретения станут более очевидными из следующего подробного описания изобретения, формулы изобретения и графических материалов.
Техническое решение
В соответствии с одним аспектом настоящего изобретения предложены изобретения с 1 по 33, охарактеризованные ниже:
1. Частица, содержащая:
i) гидрофобное соединение на основе камптотецина;
ii) гидрофильное соединение на основе камптотецина; и
iii) амфифильный блок-сополимер, состоящий из гидрофобного блока и гидрофильного блока.
2. Частица по п. 1, в которой гидрофобное соединение на основе камптотецина представляет собой по меньшей мере одно, выбранное из группы, состоящей из 7-этил-10-гидроксикамптотецина (SN-38), камптотецина, 10-гидроксикамптотецина и их фармацевтически приемлемой соли.
3. Частица по п. 1, в которой гидрофильное соединение на основе камптотецина представляет собой по меньшей мере одно, выбранное из иринотекана, топотекана, белотекана, экзатекана, луртотекана, синотекана, рубитекана, 9-нитрокамптотецина, 9-аминокамптотецина, гиматекана, BNP-1530, DB-67, BN-80915, BN-80927, их фармацевтически приемлемой соли, их глюкуронидного метаболита и глюкуронидного метаболита гидрофобного соединения на основе камптотецина.
4. Частица по п. 1, в которой амфифильный блок-сополимер состоит из блоков А-В или А-В-А,
(a) где А представляет собой гидрофильный полимер, который представляет собой монометоксиполиэтиленгликоль, диметоксиполиэтиленгликоль, полиэтиленгликоль, полипропиленгликоль, монометоксиполипропиленгликоль, полиэтиленоксид, полиакриловую кислоту или их полимер; и
(b) где В представляет собой гидрофобный полимер, который представляет собой полимолочную кислоту, полилактид, полигликолевую кислоту, полигликолид, сополимер полимолочной кислоты и гликолевой кислоты, полиминдальную кислоту, поликапролактон, полидиоксан-2-он, полиглутаминовую кислоту, полиаспарагиновую кислоту, полиорнитин, сложный полиортоэфир, их производное или сополимер двух или более соединений, выбранных из них.
5. Частица по п. 4, в которой сред нечисловая молекулярная масса гидрофильного полимера А составляет 500-10000 Да.
6. Частица по п. 4, в которой сред нечисловая молекулярная масса гидрофобного полимера В составляет 500-10000 Да.
7. Частица по п. 1, в которой массовое соотношение гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина составляет от 1:10 до 10:1.
8. Частица по п. 1, в которой массовое соотношение суммы гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина к амфифильному блок-сополимеру составляет от 1:200 до 10:1.
9. Частица по п. 1, в которой среднечисленный размер частицы составляет 10-500 нм.
10. Частица по п. 1, в которой частица имеет двойную структуру ядро-оболочка:
(a) внутреннюю структуру ядро-оболочка, содержащую гидрофильное соединение на основе камптотецина и гидрофобное соединение на основе камптотецина; и
(b) внешнюю структуру ядро-оболочка, содержащую амфифильный блок-сополимер.
11. Частица по п. 1, где частица имеет структуру двухслойной мицеллы.
12. Фармацевтическая композиция для лечения рака, содержащая частицу по любому из п.п. 1-11 и фармацевтически приемлемый носитель.
13. Композиция по п. 12, где рак выбран из группы, состоящей из рака желудка, рака яичника, рака матки, мелкоклеточного рака легкого, немелкоклеточного рака легкого, рака поджелудочной железы, рака молочной железы, рака пищевода, рака полости рта, рака прямой кишки, рака ободочной кишки, рака толстой кишки, рака почки, рака предстательной железы, меланомы, рака печени, рака желчного пузыря и других желчных протоков, рака щитовидной железы, рака мочевого пузыря, рака мозга и центральной нервной системы, рака кости, рака кожи, неходжкинской лимфомы и лимфомы Ходжкина, и рака крови.
14. Композиция по п. 12, где композиция дополнительно содержит различные типы противораковых лекарств.
15. Композиция по п. 12, дополнительно содержащая наполнитель сахарозу, маннит, сорбит, глицерин, трегалозу и полиэтиленгликоль, и наполнитель циклодекстрин.
16. Способ лечения рака, включающий введение субъекту фармацевтической композиции по любому из п.п. 1-15.
17. Способ по п. 16, где субъектом является человек, мышь, крыса, морская свинка, собака, кошка, лошадь, корова, свинья, обезьяна, шимпанзе, павиан или макака-резус.
18. Способ получения частицы, включающий:
(a) формирование внутренней структуры ядро-оболочка, содержащей гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина; и
(b) формирование внешней структуры ядро-оболочка, содержащей амфифильный сополимер.
19. Способ по п. 18, где стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; и
где стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе.
20. Способ по п. 18, где стадия (а) включает смешивание основного водного раствора, в котором растворено гидрофобное соединение камптотецина, и водного раствора, в котором растворено гидрофильное соединение камптотецина; и
где стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе.
21. Способ по п. 20, где водный раствор, в котором растворено гидрофильное соединение камптотецина, представляет собой основный, нейтральный или кислый водный раствор.
22. Способ по п. 20, где стадия (а) включает:
(а1) смешивание основного водного раствора, в котором растворено гидрофобное соединение на основе камптотецина, и основного, нейтрального или кислого водного раствора, в котором растворено гидрофильное соединение на основе камптотецина; и
(а2) снижение рН смешанного водного раствора до 7 или ниже.
23. Способ по п. 18, где стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; и
где стадия (b) включает смешивание смеси гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина с амфифильным блок-сополимером в органическом растворителе.
24. Способ по любому из пп. 18-23, где гидрофобное соединение на основе камптотецина представляет собой по меньшей мере одно, выбранное из группы, состоящей из 7-этил-10-гидроксикамптотецина (SN-38), камптотецина, 10-гидроксикамптотецина и их фармацевтически приемлемой соли.
25. Способ по любому из пп. 18-24, где гидрофильное соединение на основе камптотецина представляет собой по меньшей мере одно, выбранное из иринотекана, топотекана, белотекана, экзатекана, луртотекана, синотекана, рубитекана, 9-нитрокамптотецина, 9-аминокамптотецина, гиматекана, BNP-1530, DB-67, BN-80915, BN-80927, их фармацевтически приемлемой соли, их глюкуронидного метаболита и глюкуронидного метаболита гидрофобного соединения на основе камптотецина.
26. Способ по любому из пп. 18-24, где амфифильный блок-сополимер состоит из блоков А-В или А-В-А,
(a) где А представляет собой гидрофильный полимер, который представляет собой монометоксиполиэтиленгликоль, диметоксиполиэтиленгликоль, полиэтиленгликоль, полипропиленгликоль, монометоксипропиленгликоль, полиэтиленоксид, полиакриловую кислоту или их полимер; и
(b) где В представляет собой гидрофобный полимер, который представляет собой полимолочную кислоту, полилактид, полигликолевую кислоту, полигликолид, сополимер полимолочной кислоты и гликолевой кислоты, полиминдальную кислоту, поликапролактон, полидиоксан-2-он, полиглутаминовую кислоту, полиаспарагиновую кислоту, полиорнитин, сложный полиортоэфир, их производное или сополимер двух или более соединений, выбранных из них.
27. Способ по п. 26, где молекулярная масса гидрофильного полимера А составляет 500-10000 Да.
28. Способ по п. 26, где молекулярная масса гидрофобного полимера В составляет 500-10000 Да.
29. Способ по любому из п.п. 18-24, где массовое соотношение гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина составляет от 1:10 до 10:1.
30. Способ по любому из п.п. 18-24, где массовое соотношение суммы гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина к амфифильному блок-сополимеру составляет от 1:200 до 10:1.
31. Способ по любому из п.п. 18-24, где органический растворитель представляет собой С1-С5 спирт (метанол, этанол, пропанол, бутанол, н-бутанол, изопропанол, 1-пентанол, 2-бутоксиэтанол, изобутиловый спирт и т.п.), алкилацетат, ацетон, ацетонитрил, хлороформ, бензол, толуол, ксилол, ацетон, фторалкан, пентан, гексан, 2,2,4-триметилпентан, декан, цикпогексан, цикпопентан, диизобутилен, 1-пентен, 1-хлорбутан, 1-хлорпентан, диизопропиловый эфир, 2-хлорпропан, 1-хлорпропан, хлорбензол, бензол, диэтиловый эфир, диэтилсульфид, дихлорметан, 1,2-дихлорэтан, анилин, диэтиламин, простой эфир, четыреххлористый углерод, тетрагидрофуран (ТГФ) или смешанный растворитель из них.
32. Способ по п. 21 или 22, где кислый водный раствор включает по меньшей мере одно, выбранное из фармацевтически приемлемых неорганических кислот, включая соляную кислоту, азотную кислоту, серную кислоту и фосфорную кислоту, или органических кислот, включая лимонную кислоту, яблочную кислоту, молочную кислоту, уксусную кислоту и винную кислоту.
33. Способ по п. 21 или 22, где рН кислого водного раствора составляет от 1,0 до 6.
34. Способ по п. 20, где основный раствор включает по меньшей мере одно, выбранное из группы, состоящей из неорганической щелочи, щелочной соли органической кислоты и алкиламина, неорганической щелочи, включая гидроксид натрия, гидроксид калия, дигидрофосфат натрия, дигидрофосфат калия, гидроксид магния, карбонат натрия и гидрокарбонат натрия.
35. Способ по п. 20, где рН основного водного раствора составляет от 8 до 13.
Авторы настоящего изобретения пытались улучшить растворимость и стабильность гидрофобного соединения на основе камптотецина, применение которого ограничено из-за его весьма плохой растворимости, несмотря на его сильную противораковую активность, и в результате авторы настоящего изобретения подтвердили, что смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в водном растворителе или органическом растворителе приводит к получению частицы ядро-оболочка (мицеллы), имеющей структуры ядра и оболочки, образованные из гидрофобных и гидрофильных соединений, соответственно. Кроме того, было подтверждено, что добавление амфифильного блок-сополимера к частице ядро-оболочка образует частицу с двойной структурой ядро-оболочка (двухслойную мицеллу), в которой указанная частица заключена в оболочку из амфифильного блок-сополимера.
Согласно варианту осуществления настоящего изобретения частица с двойной структурой ядро-оболочка, содержащая как гидрофобное соединение на основе камптотецина, так и гидрофильное соединение на основе камптотецина, в настоящем изобретении имеет значительно улучшенную растворимость по сравнению с существующим плохо растворимым камптотецином, даже без введения в форме пролекарства. Следовательно, эффективность лекарственного средства активного камптотецина (SN-38) может проявляться независимо от активности карбоксилэстеразы II (CESII) in vivo. Кроме того, было подтверждено, что частицы согласно настоящему изобретению не вызывают агломерации или осаждения частиц, даже если частицы вновь растворяют в водном растворителе после лиофильной сушки, и, таким образом, частицы имеют лекарственную форму с весьма превосходной стабильностью. Следовательно, настоящее изобретение предлагает композицию частиц со стабильной двойной структурой ядро-оболочка, которая усовершенствована по сравнению с существующей однослойной наномицеллой, для решения проблемы низкой растворимости плохо растворимого лекарственного средства.
В соответствии с одним аспектом настоящего изобретения предложена частица, содержащая: i) гидрофобное соединение на основе камптотецина; ii) гидрофильное соединение на основе камптотецина; и iii) амфифильный блок-сополимер, состоящий из гидрофобного блока и гидрофильного блока.
В данном описании камптотецин представляет собой ингибитор топоизомеразы, обнаруженный в коре и стебле дерева Камптотека (Camptotheca (Дерево счастья)), и проявляет очень хороший противораковый эффект на доклинической стадии, но его нельзя использовать из-за его низкой растворимости. Поэтому исследователи разработали аналоги камптотецина для улучшения растворимости камптотецина. В настоящее время одобрены три типа производных камптотецина: иринотекан, топотекан и белотекан, которые используются в химиотерапии при раке.
Используемый здесь термин «гидрофобность» относится к отторжению молекул воды и агломерации, как к тенденции, проявляющейся в неполярных материалах. Когда гидрофобный материал присутствует в гидрофильной жидкости, гидрофобный материал агломерирует, усиливая гидрофобные связи, как если бы гидрофобный материал боялся воды.
Используемый здесь термин «гидрофильность» относится к свойству растворяться в воде с сильным сродством к воде, как к тенденции, проявляемой в полярных материалах. Например, гидрофильное полимерное соединение или мицелло-коллоидная поверхность поверхностно-активного вещества имеет сильную гидрофильность.
Согласно одному варианту осуществления изобретения гидрофобное соединение на основе камптотецина выбирают из группы, состоящей из 7-этил-10-гидроксикамптотецина (SN-38), камптотецина, 10-гидроксикамптотецина и их фармацевтически приемлемой соли, но не ограничиваются этим.
Согласно другому варианту осуществления настоящего изобретения гидрофильное соединение на основе камптотецина выбирают из иринотекана, топотекана, белотекана, экзатекана, луртотекана, синотекана, рубитекана, 9-нитрокамптотецина, 9-аминокамптотецина, гиматекана, BNP-1530, DB-67, BN -80915, BN-80927, их фармацевтически приемлемых солей, их глюкуронидного метаболита и глюкуронидного метаболита гидрофобного соединения на основе камптотецина, но не ограничиваются этим.
Согласно конкретному варианту осуществления настоящего изобретения гидрофобное соединение на основе камптотецина, которое входит в состав частицы настоящего изобретения, может представлять собой камптотецин, SN-38 или их смесь, а также гидрофильное соединение на основе камптотецина, которое входит в состав частицы настоящего изобретения, может представлять собой гидрохлорид иринотекана, гидрохлорид топотекана и аналог глюкуронида SN-38.
Используемый здесь термин «сополимер» относится к полимеру, полученному из двух или более различных типов мономеров. Например, реакция стиролакрилонитрила в реакционном сосуде приводит к получению сополимера, содержащего оба мономера. Термин «блок-сополимер» относится к сополимеру, имеющему форму, в которой блок одного типа мономеров связан с блоком другого типа мономеров. Случай, когда за блоком материала А следует блок материала В, выражается как -[-АВ-]-. Цепь называется типом АВ, если цепь включает по одной цепи каждого мономера, типом ABA, если блоки А присутствуют на обоих концах блока В, находящегося в центре, и типом ABC, если в главной цепи присутствуют три различных типа блоков. Блок-сополимер, в основном, получают ионной полимеризацией. В отличие от других сополимеров, этот блок-сополимер обладает многими физическими свойствами гомополимера, образованного из двух типов мономеров.
В соответствии с одним вариантом осуществления настоящего изобретения амфифильный блок-сополимер, входящий в состав частицы настоящего изобретения, состоит из блока А-В или блока А-В-А. Здесь А представляет собой гидрофильный полимер, который представляет собой монометоксиполиэтиленгликоль, диметоксиполиэтиленгликоль, полиэтиленгликоль, полипропиленгликоль, монометоксипропиленгликоль, полиэтиленоксид, полиакриловую кислоту или их полимер, но не ограничивается этим. Кроме того, В представляет собой гидрофобный полимер, который представляет собой полимолочную кислоту, полилактид, полигликолевую кислоту, полигликолид, сополимер полимолочной кислоты и гликолевой кислоты, полиминдальную кислоту, поликапролактон, полидиоксан-2-он, полиглутаминовую кислоту, полиаспарагиновую кислоту, полиорнитин, полиортоэфир, их производное или сополимер двух или более соединений, выбранных из них, но не ограничен ими. Специалисту в данной области будет очевидно, что любое соединение, из которого можно получить амфифильный блок-сополимер, пригодный в данной области, может быть использовано без ограничения.
В конкретном варианте осуществления настоящего изобретения амфифильным блок-сополимером является ПЭГ-ПКЛ [поли(этиленгликоль)-b-поли-(карпролактон)]; ПЭГ-ПМК [поли(этиленгликоль)-b-поли(молочная кислота)]; мПЭГ-ПГК [монометоксиполи(этиленгликоль)-b-поли(гликолевая кислота)]; мПЭГ-ПЛГК [монометоксиполи(этиленгликоль)-b-поли(лактид-со-гликолид)]; ПЭГ-ПБЛА [поли(этиленгликоль)-b-поли(β-бензил-L-аспарагиновая кислота)]; n31-p(Glu) [поли(этиленгликоль)-b-поли(глутаминовая кислота)]; ПЭГ-р(Аэр) [поли(этиленгликоль)-b-поли(аспарагиновая кислота)]; и/или ПЭГ-ПМК-ПЭГ [поли(этиленгликоль)-b-поли(молочная кислота)-b-поли(этиленгликоль).
В соответствии с одним вариантом осуществления настоящего изобретения гидрофильный полимер А и гидрофобный полимер В, каждый имеет среднечисловую молекулярную массу 500-10000 Да и, более конкретно, 1000-7000 Да. Когда среднечисловая молекулярная масса гидрофильного полимера А и гидрофобного полимера В составляет менее 500 Да или более 10000 Да, полученные частицы имеют средний размер 200 нм или более и имеют многомодальное распределение, и, таким образом, из них трудно получить наночастицы, предписанные FDACLUA.
Согласно другому варианту осуществления настоящего изобретения массовое соотношение гидрофобного соединения на основе камптотецина к гидрофильному соединению на основе камптотехина, которые входят в состав частицы настоящего изобретения, составляет 1-10:1-10, 1-10:1-5, 1-10:1-3, 1-10:1, 1-5:1-10, 1-3:1-10 или 1:1-10, в частности 1-5:1-5, 1-5:1-3, 1-5:1, 1-3:1-5 или 1:1-5, и более конкретно - 1-3:1-3, 1-3:1 или 1:1-3, но не ограничивается этим.
Согласно одному варианту осуществления настоящего изобретения массовое соотношение (а) суммы гидрофобного соединения на основе камптотецинации и гидрофильного соединения на основе камптотехина к (b) амфифильному блок-сополимеру составляет 1:0,1-200, 1:0,5-200 1:1-200, 1:2-200, 1:5-200, 1:10-200, 1:50-200, 1:100-200, 1:150-200, 1:0,1-100, 1:0,5-100, 1:1-100, 1:2-100, 1:5-100, 1:10-100, 1:20-100, 1:50-100, 1:0,1-50, 1:0,5-50, 1:1-50, 1:5-50, 1:10-50, 1:20-50, 1:0,1-20, 1:0,5-20, 1:1-20, 1:5-20, 1:10-20, 1:0,1-10, 1:0,5-10 или 1:1-10.
Используемый здесь термин «до» или «-» между двумя числовыми значениями означает диапазон числовых значений, включая числовые значения, указанные до и после этого термина.
Между тем, частица согласно настоящему изобретению имеет двойную структуру ядро-оболочка, включающую в себя следующее:
(а) внутреннюю структуру ядро-оболочка, содержащую гидрофильное соединение на основе камптотецина и гидрофобное соединение на основе камптотецина; и (б) внешнюю структуру ядро-оболочка, содержащую амфифильный блок-сополимер.
Кроме того, частица согласно настоящему изобретению имеет структуру двухслойной мицеллы.
Известно, что амфифильный блок-сополимер, в котором гидрофильный блок и гидрофобный блок объединены в определенном соотношении, образует мицеллу путем самосборки в водном растворе. Внутренняя часть мицеллы является гидрофобной, и, таким образом, амфифильный блок-сополимер применяется в качестве системы доставки лекарственного средства для плохо растворимого препарата. Хорошо известно, что двойной блок-сополимер полистирол-полиэтиленоксид (PS-b-PEO) образует сферическую мицеллу, имеющую нерастворимое ядро (PS) и растворимую оболочку (РЕО) в воде.
Как описано выше, частица согласно настоящему изобретению включает (а) гидрофильное соединение на основе камптотецина и гидрофобное соединение на основе камптотецина; и (b) амфифильный блок-сополимер.
Как доказано в примере настоящего изобретения, смешивание гидрофильного соединения на основе камптотецина и гидрофобного соединения на основе камптотецина значительно увеличивает растворимость в водных растворителях и приводит к образованию частиц. Здесь вполне вероятно, что гидрофильное соединение на основе камптотецина служит гидрофильным блоком амфифильного сополимера, а гидрофобное соединение на основе камптотецина служит гидрофобным блоком амфифильного сополимера, образуя структуру ядро-оболочка (мицеллу).
Следовательно, частица согласно настоящему изобретению образует двойную мицеллу (двойную структуру ядро-оболочка), содержащую: однослойную мицеллу внутри и амфифильный блок-сополимер, содержащий однослойную мицеллу внутри, где в однослойной мицелле гидрофильное соединение на основе камптотецина и гидрофобное соединение на основе камптотецина составляют структуру ядро-оболочка. Более конкретно, гидрофобный блок амфифильного блок-сополимера образует нерастворимое ядро в однослойной мицелле, которая является относительно гидрофобной и состоит из соединений на основе камптотецина, а гидрофильный блок образует растворимую оболочку по отношению к внешнему водному растворителю, и, как результат, образуется двойная мицелла с двойной структурой ядро-оболочка.
Согласно варианту осуществления настоящего изобретения частицы с двойной структурой ядро-оболочка спонтанно образуют частицы при диспергировании в водном растворе.
Согласно варианту осуществления настоящего изобретения среднечисленный размер частиц составляет 10-500 нм, 10-400 нм, 10-300 нм или 10-200 нм, а более конкретно - 20-500 нм, 20-400 нм, 20-300 нм или 20-200 нм. Среднечисленный размер частиц согласно настоящему изобретению демонстрирует ограниченное изменение даже до или после лиофилизации частиц. Причина, по-видимому, заключается в том, что, во первых, гидрофобные и гидрофильные соединения на основе камптотецина представляют собой структурированную мицеллу ядро-оболочка, а во-вторых, амфифильный блок-сополимер представляет собой внешнюю оболочку, окружающую мицеллу, так что во время лиофилизации вторая внешняя оболочка служит в качестве криопротектора, препятствующего быстрой кристаллизации, агломерации, разрушению частиц первичной внутренней структуры ядро-оболочка. В результате частицы согласно настоящему изобретению не подвержены агломерации или осаждению, даже когда частицы повторно растворяют в водном растворителе после лиофильной сушки. Следовательно, настоящее изобретение обеспечивает композицию стабильных частиц с двойной структурой ядро-оболочка, которая усовершенствована по сравнению с существующей однослойной наномицеллой, для решения проблемы растворимости весьма плохо растворимого лекарственного средства.
Согласно другому аспекту настоящее изобретение предлагает фармацевтическую композицию для лечения рака, причем эта фармацевтическая композиция содержит вышеописанные частицы и фармацевтически приемлемый носитель.
В варианте осуществления настоящего изобретения рак выбран из группы, состоящей из рака желудка, рака яичника, рака матки, мелкоклеточного рака легкого, немелкоклеточного рака легкого, рака поджелудочной железы, рака молочной железы, рака пищевода, рака полости рта, рака прямой кишки, рака ободочной кишки, рака толстой кишки, рака почки, рака предстательной железы, меланомы, рака печени, рака желчного пузыря и других желчных протоков, рака щитовидной железы, рака мочевого пузыря, рака мозга и центральной нервной системы, рака кости, рака кожи, неходжкинской лимфомы и лимфомы Ходжкина.
Когда частицы согласно настоящему изобретению или содержащую их композицию готовят в виде фармацевтической композиции, фармацевтическая композиция согласно настоящему изобретению может содержать фармацевтически приемлемый носитель. Фармацевтически приемлемый носитель обычно используют во время приготовления, и его примеры могут включать, но не ограничиваются этим, лактозу, декстрозу, сахарозу, сорбит, маннит, крахмал, камедь акации, фосфат кальция, альгинат, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, сироп, метилцеллюлозу, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло. Фармацевтическая композиция согласно настоящему изобретению может дополнительно содержать лубрикант, смачивающий агент, подсластитель, ароматизатор, эмульгатор, суспендирующий агент, консервант и тому подобное, в дополнение к вышеуказанным ингредиентам. Подходящие фармацевтически приемлемые носители и агенты подробно описаны в Remington's Pharmaceutical Sciences (19 издание, 1995).
В конкретном варианте осуществления настоящего изобретения фармацевтическая композиция может дополнительно содержать сахарозу, маннит, сорбит, глицерин, трегалозу, эксципиент на основе полиэтиленгликоля и эксципиент на основе цикподекстрина (альфа-, бета- и гамма-циклодекстрин, гидроксициклодекстрин или производное цикподекстрина). Эксципиент, добавляемый к частицам, которые соответствуют активному ингредиенту настоящей фармацевтической композиции, служит в качестве криопротектора или осморегулятора и его вводят в композицию в процессе лиофилизации, испарения растворителя или тому подобного.
Фармацевтическую композицию согласно настоящему изобретению можно вводить перорально или парентерально, и примеры парентерального введения могут включать внутривенное введение, подкожное введение, внутрикожное введение, внутримышечное введение, интраназальное введение, введение через слизистую оболочку, интрадуральное введение, внутрибрюшинное введение, внутриглазное введение и т.д., в частности, фармацевтическую композицию согласно настоящему изобретению можно вводить внутривенно.
Подходящая доза фармацевтической композиции согласно настоящему изобретению варьируется в зависимости от таких факторов, как способ приготовления, способ введения, возраст пациента, масса тела, пол, тяжесть заболевания и питание, время введения, способ введения, скорость выведения и ответная реакция. Обычные специалисты могут легко определить и назначить дозу, эффективную для желаемого лечения или профилактики. Согласно варианту осуществления настоящего изобретения суточная доза фармацевтической композиции согласно настоящему изобретению составляет 0,001-100 мг/кг.
Фармацевтическая композиция согласно настоящему изобретению может быть приготовлена в виде единичной дозированной формы или в многодозовом контейнере с использованием фармацевтически приемлемого носителя и/или эксципиента в соответствии со способом, который осуществит специалист в области техники, к которой относится настоящее изобретение. Здесь лекарственная форма может представлять собой раствор в масляной или водной среде, суспензию, эмульсию, экстракт, порошок, гранулы, таблетку или капсулу и может дополнительно содержать диспергатор или стабилизатор.
Фармацевтическую композицию согласно настоящему изобретению можно вводить параллельно с известным соединением или фармацевтической композицией, обладающей эффектом лечения рака.
В варианте осуществления настоящего изобретения композиция согласно настоящему изобретению дополнительно содержит другой тип противоракового лекарственного средства. В частности, композиция согласно настоящему изобретению дополнительно содержит плохо растворимое противораковое лекарственное средство, такое как паклитаксел или доцетаксел.
Плохо растворимые противораковые лекарственные средства, представленные паклитакселом и доцетакселом, имеют низкую степень использования из-за плохой растворимости, подобно вышеупомянутому камптотецину, но эти плохо растворимые противораковые лекарственные средства имеют значительно улучшенную растворимость, когда они содержатся в двойных мицеллярных частицах настоящего изобретения. Следовательно, частица согласно настоящему изобретению сама по себе является противораковым лекарственным средством на основе камптотецина и может быть выгодно использована в качестве платформы системы доставки лекарственных средств, в которую можно загрузить плохо растворимые противораковые лекарственные средства или новые потенциальные лекарственные средства с проблемами низкой растворимости для улучшения их растворимости.
Согласно еще одному аспекту настоящее изобретение относится к способу лечения рака, включающему введение субъекту вышеописанной фармацевтической композиции согласно настоящему изобретению.
Используемый здесь термин «введение» или «вводить» относится к непосредственному применению терапевтически эффективного количества композиции согласно настоящему изобретению субъектом (т.е. объектом) с раком, в результате чего такое же количество композиции оказывается в организме субъекта.
Термин «терапевтически эффективное количество» композиции относится к количеству композиции, которое является достаточным для оказания терапевтического или профилактического эффекта у субъекта, которому вводят композицию, и, таким образом, этот термин имеет значение, включающее «профилактически эффективное количество». Используемый здесь термин «субъект» включает, но не ограничивается этим, человека, мышь, крысу, морскую свинку, собаку, кошку, лошадь, корову, свинью, обезьяну, шимпанзе, павиана или макаку-резуса. В частности, субъектом в настоящем изобретении является человек. Поскольку способ лечения рака согласно настоящему изобретению включает стадию введения фармацевтической композиции для лечения рака в соответствии с одним из аспектов настоящего изобретения, перекрывающиеся описания между ними опущены, чтобы избежать чрезмерного усложнения описания.
Согласно еще одному аспекту настоящего изобретения предложен способ получения частицы, включающий:
(a) формирование внутренней структуры ядро-оболочка, содержащей гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина; и
(b) формирование внешней структуры ядро-оболочка, содержащей амфифильный сополимер.
В варианте осуществления настоящего изобретения стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе.
Поскольку гидрофобное соединение на основе камптотецина согласно настоящему изобретению является сильно гидрофобным, требуется особая методика растворения или способ получения. В примере настоящего изобретения, чтобы преодолеть такую плохую растворимость, гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина сначала одновременно растворяют в органическом растворителе, а затем органический растворитель полностью удаляют, используя роторный вакуумный испаритель, таким образом получая смесь соединений на основе камптотецина в форме пленки. Затем в эту смесь добавляют небольшое количество водного растворителя (например, дистиллированной воды) при интенсивном перемешивании с использованием вихревого смесителя или ультразвука, получая тем самым наноразмерный первичный комплекс ядро-оболочка.
Затем амфифильный полимер, предварительно растворенный в водном растворителе (например, в дистиллированной воде), добавляют к первичному комплексу ядро-оболочка с последующим гомогенным и сильным перемешиванием с использованием вихревого смесителя или ультразвука, получая таким образом наноразмерные частицы с двойной структурой ядро-оболочка. Наконец, к ним добавляют криопротектор и изотонический агент для полного растворения в нем, а затем полученный раствор фильтруют через стерильный фильтр 0,22 мкм с последующей лиофильной сушкой. При добавлении к 0,9% раствору хлорида натрия для инъекций, 5% раствору глюкозы для инъекций или к воде для инъекций конечный лиофилизированный материал самоорганизуется с образованием частиц с двойной структурой ядро-оболочка со среднечисленным размером частиц 20-200 нм.
В случае, когда частицы, изготовленные в соответствии с настоящим изобретением, имеют размер частиц 200 нм или менее, неселективного удаления ретикулоэндотелиальной (RES) системы в организме можно избежать, и, таким образом, предпочтительно изготавливать частицы, имеющие однородный размер частиц 200 нм или менее.
В другом варианте осуществления настоящего изобретения стадия (а) включает смешивание основного водного раствора, в котором растворено гидрофобное соединение камптотецина, и водного раствора, в котором растворено гидрофильное соединение камптотецина; стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе.
В этом случае водный раствор, в котором растворено гидрофильное соединение камптотецина, может быть основным, нейтральным или кислым водным раствором.
Первичное внутреннее ядро-оболочка может быть изготовлено следующим способом, помимо способа получения в органическом растворителе. Соединение на основе гидрофобного камптотецина (например камптотецин, SN-38) имеет очень низкую растворимость в кислом или нейтральном водном растворе с рН 7 или менее, но растворимость гидрофобного соединения на основе камптотецина быстро увеличивается в основном водном растворе, поскольку лактоновое кольцо раскрывается с образованием структуры карбоновой кислоты. Следовательно, гидрофобное соединение на основе камптотецина растворяют в основном водном растворе и затем к нему добавляют водный раствор, в котором растворено гидрофильное соединение на основе камптотецина, с понижением рН до 7 или менее, так что гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина образуют мицеллу, кислотность нейтрализуется и лактоновое кольцо замыкается с восстановлением тем самым его первоначальной химической структуры.
В конкретном варианте осуществления настоящего изобретения стадия (а) включает в себя: (а1) смешивание основного водного раствора, в котором растворено гидрофобное соединение на основе камптотецина, и основного, нейтрального или кислого водного раствора, в котором растворено гидрофильное соединение на основе камптотецина; и (а2) снижение рН смешанного водного раствора до 7 или ниже.
В примере настоящего изобретения камптотецин или SN-38 растворяли в основном водном растворе и гидрофильное соединение на основе камптотецина, предварительно растворенное в водном растворе, добавляли к основному водному раствору при сильном перемешивании с использованием ультразвука или вихревого смесителя, затем добавляли кислый водный раствор для доведения рН до 7 или менее, получая тем самым первичные частицы ядро-оболочка. Амфифильный полимер, предварительно растворенный в водном растворителе (например, в дистиллированной воде), добавляли к смеси полученных первичных частиц ядро-оболочка при перемешивании с использованием ультразвука или вихревого смесителя, таким образом получая смесь с двойной структурой ядро-оболочка. К ней дополнительно добавляли криопротектор и изотонизирующий агент для растворения в нем, затем проводили стерильную фильтрацию с использованием фильтра 0,22 мкм и затем лиофилизациию.
В способе получения согласно настоящему изобретению кислый водный раствор содержит фармацевтически приемлемую неорганическую кислоту, такую как соляная кислота, азотная кислота, серная кислота или фосфорная кислота и по меньшей мере одну органическую кислоту, выбранную из группы, состоящей из лимонной кислоты, яблочной кислоты, молочной кислоты, уксусной кислоты и винной кислоты. рН кислого водного раствора составляет 1-6. Кроме того, в способе получения согласно настоящему изобретению основный водный раствор содержит: неорганическую щелочь, включая гидроксид натрия, гидроксид калия, дигидрофосфат натрия, дигидрофосфат калия, гидроксид магния, карбонат натрия и гидрокарбонат натрия, щелочную соль органической кислоты, алкиламин или их смесь. рН основного водного раствора составляет 8-13.
В еще одном варианте осуществления настоящего изобретения стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; стадия (b) включает смешивание смеси гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина с амфифильным блок-сополимером в органическом растворителе.
В настоящем изобретении стадию (а) (формирование внутренней структуры ядро-оболочка) и стадию (b) (формирование внешней структуры ядро-оболочка) можно выполнять за одну стадию.
В примере настоящего изобретения показан способ одновременного изготовления первичных частиц внутренней структуры ядро-оболочка и вторичных частиц внешней структуры ядро-оболочка. Гидрофобный камптотецин (например 10-гидроксикамптотецин или SN-38) вместе с гидрофильным камптотецином (например гидрохлоридом иринотекана) добавляли в органический растворитель и полностью растворяли при перемешивании и добавляли амфифильный блок-сополимер (например, мПЭГ - ПМК), предварительно растворенный в органическом растворителе, при перемешивании. Раствор смеси сушили с помощью роторного вакуумного испарителя и к остаткам добавляли водный растворитель (например дистиллированную воду) с последующей ультразвуковой обработкой в ультразвуковом очистителе в течение 10 минут, в результате чего получали частицы двойных наномицелл.
В способе получения частиц согласно настоящему изобретению определения гидрофобного соединения на основе камптотецина, гидрофильного соединения на основе камптотецина и амфифильного блок-сополимера, из которых состоят частицы, являются такими, как описано выше в отношении частиц настоящего изобретения.
В способе получения согласно настоящему изобретению органический растворитель представляет собой С1-С5 спирт (метанол, этанол, пропанол, бутанол, н-бутанол, изопропанол, 1-пентанол, 2-бутоксиэтанол, изобутиловый спирт и т.д.), алкилацетат, ацетон, ацетонитрил, хлороформ, бензол, толуол, ксилол, ацетон, фторалкан, пентан, гексан, 2,2,4-триметилпентан, декан, цикпогексан, диизобутилен, 1-пентен, 1-хпорбутан 1-хлорпентан, диизопропиловый эфир, 2-хлорпропан, 1-хлорпропан, хлорбензол, бензол, диэтиловый эфир, диэтилсульфид, дихлорметан, 1,2-дихлорэтан, анилин, диэтиламин, простой эфир, четыреххлористый углерод, тетрагидрофуран (ТГФ) или смешанный растворитель из них, но не ограничивается этим.
Полезные эффекты
Частицы с двойной структурой ядро-оболочка, изготовленные в соответствии с настоящим изобретением, не осаждаются в виде кристаллов даже при разбавлении до достаточно низкой концентрации в водном растворе, что приводит к очень стабильным частицам. Частицы согласно настоящему изобретению показывают однородное распределение частиц в растворителе для инъекций до и после лиофилизации. Доля частиц размером 200 нм или более составляет 10% или менее, а частицы размером 500 нм или более отсутствуют. Кроме того, настоящее изобретение показывает превосходные результаты по сравнению с существующими однослойными мицеллами в тестах на эффективность на животных и в фармакокинетических тестах, и не использует поверхностно-активное вещество (Cremophore EL, Pluronic и т.д.), вызывающее гиперчувствительность, и, таким образом, использование частиц настоящего изобретения может обеспечить фармацевтическую композицию или платформу системы доставки лекарственных средств, которые являются безопасными для организма человека.
Краткое описание графических материалов
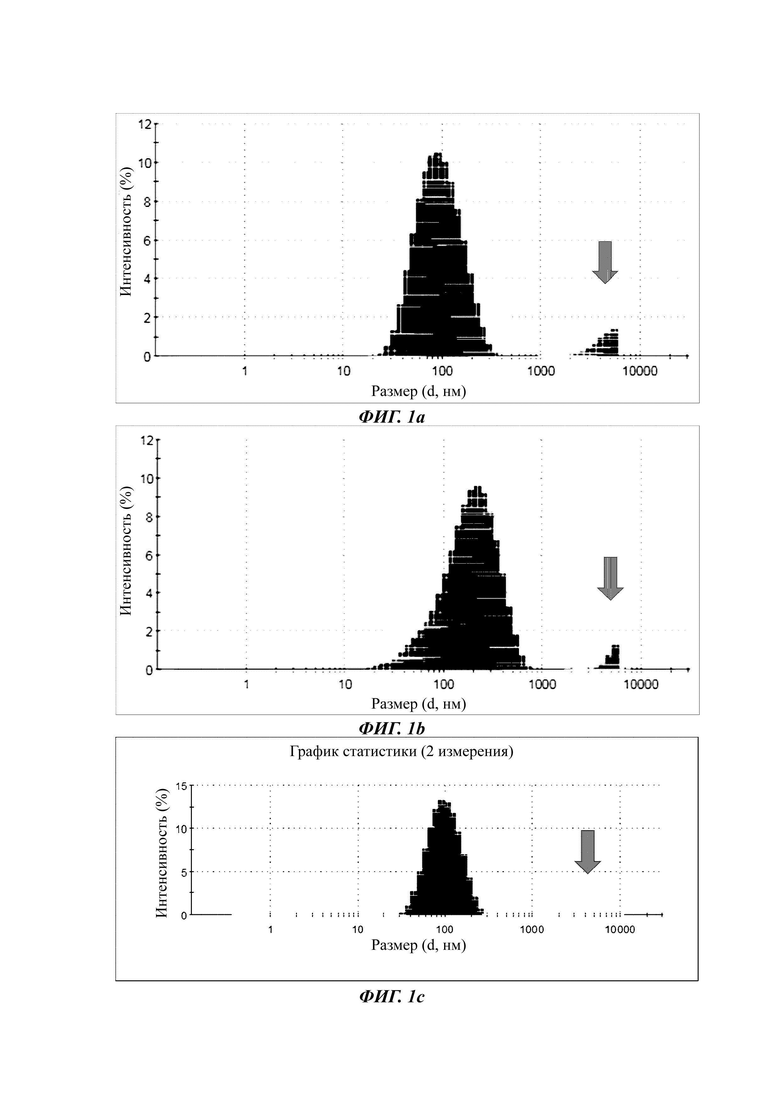
Фиг. 1а и 1b - это графики, показывающие результаты измерения размеров частиц, образовавшихся в водном растворе после лиофилизации, методом динамического рассеяния света (DLS - от англ. dynamic light scattering) в отношении частиц ядро-оболочка (однослойных мицелл), состоящих из SN-38 и иринотекана, в соответствии с примером настоящего изобретения. Фиг. 1с представляет собой график, показывающий результаты измерения размеров частиц, образованных в водном растворе после лиофильной сушки, методом динамического рассеяния света (DLS) в отношении частиц с двойной структурой ядро-оболочка (двухслойная мицелла) в соответствии с примером настоящего изобретения.
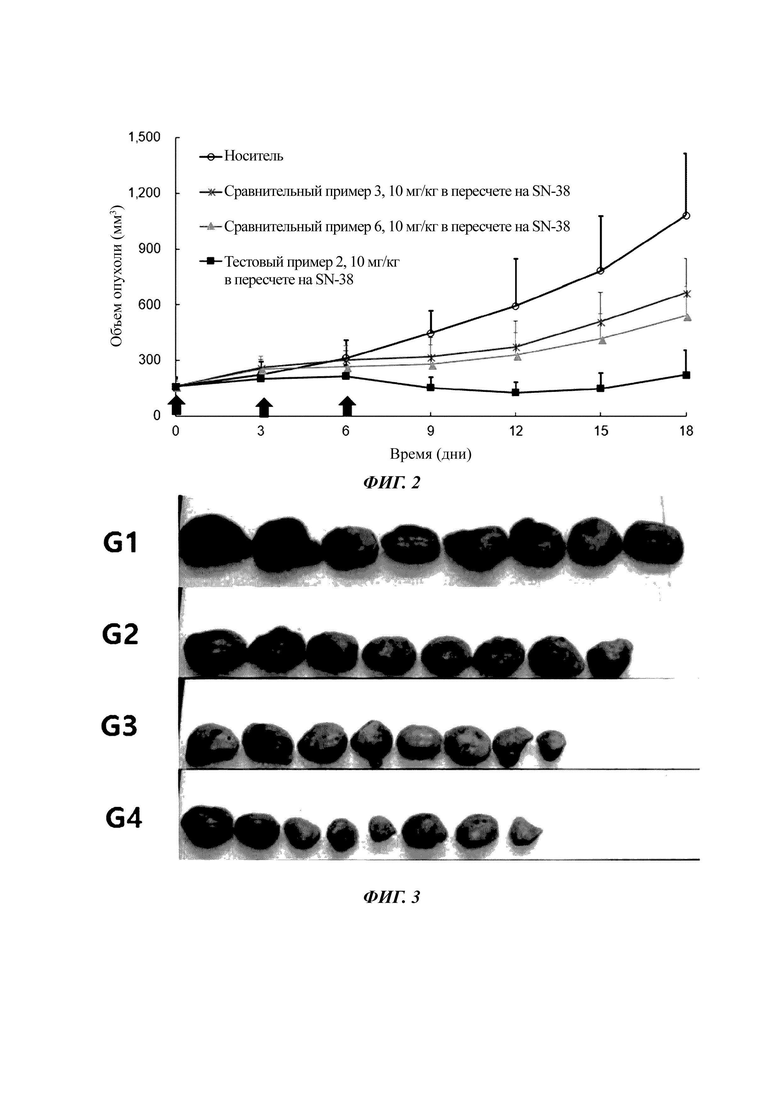
Фиг. 2 и 3 - это график и изображения выделенных опухолей, соответственно, для сравнения ингибирующего действия на опухоль частиц ядро-оболочка (однослойных мицелл) и частиц с двойной структурой ядро-оболочка (двухслойных мицелл) на мышиных моделях колоректального рака в соответствии с примером настоящего изобретения.
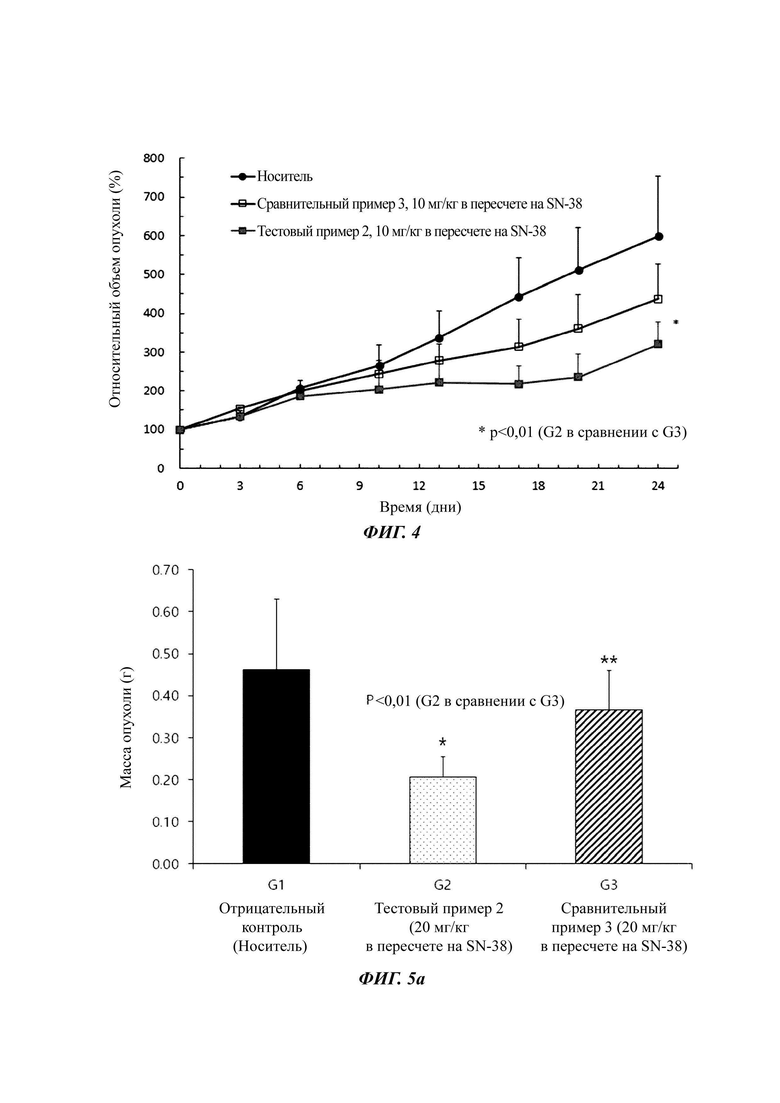
Фиг. 4 представляет собой график для сравнения эффекта ингибирования опухоли между частицами со структурой ядро-оболочка (однослойными мицеллами) и частицами с двойной структурой ядро-оболочка (двухслойными мицеллами) на мышиных моделях рака поджелудочной железы (AsPc-1, ксенотрансплантат) в соответствии с примером настоящего изобретения.
Фиг. 5а и 5b - это график и изображения выделенных опухолей, соответственно, для сравнения ингибирующего действия на опухоль частиц ядро-оболочка (однослойных мицелл) и частиц с двойной структурой ядро-оболочка (двухслойных мицелл) на мышиных моделях рака поджелудочной железы (MiaPaca-2, ортотопические) согласно примеру настоящего изобретения.
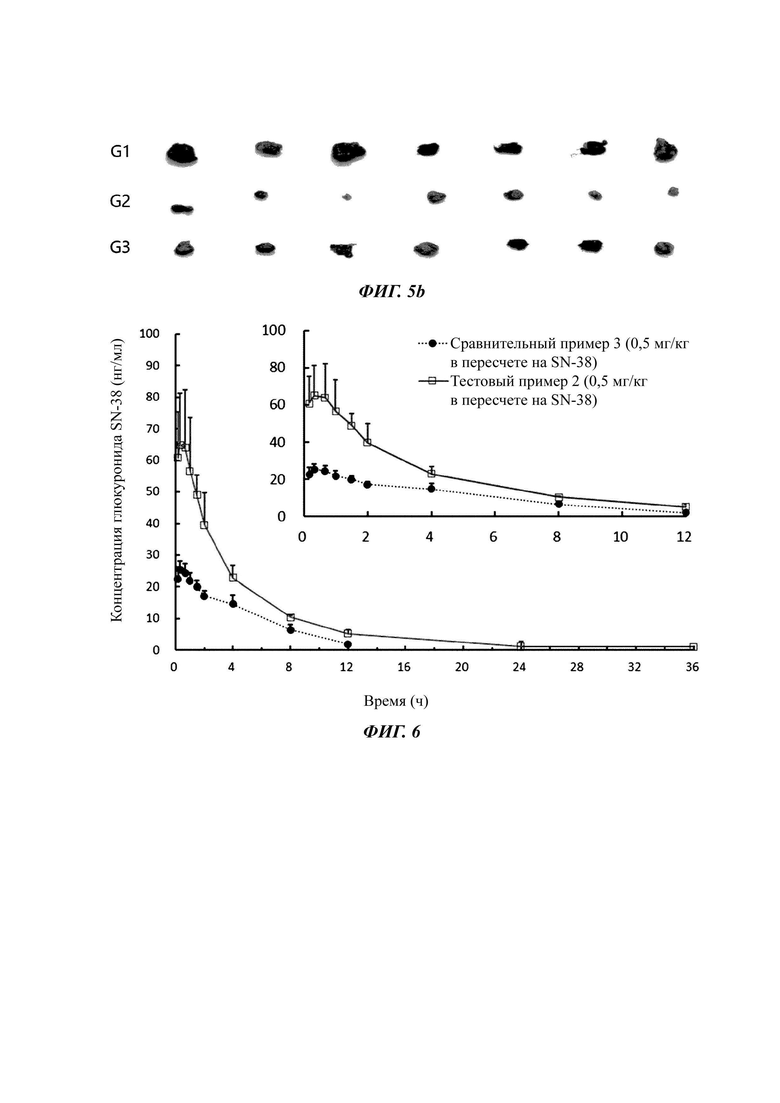
Фиг. 6 представляет собой график, показывающий концентрацию глюкуронида SN-38 в крови для сравнения фармакокинетических характеристик между частицами ядро-оболочка (однослойными мицеллами) и частицами с двойной структурой ядро-оболочка (двухслойными мицеллами) согласно настоящему изобретению.
Варианты осуществления изобретения
Далее настоящее изобретение будет подробно описано со ссылкой на примеры. Эти примеры предназначены только для более конкретной иллюстрации настоящего изобретения и специалистам в данной области техники будет очевидно, что объем настоящего изобретения не ограничивается этими примерами.
ПРИМЕРЫ
Во всем настоящем описании термин «%», используемый для выражения концентрации конкретного материала, если особо не указано иное, относится к (мас./мас.)% для твердого вещества/твердого вещества, (мас./об.)% для твердого вещества/жидкости и (об./об.)% для жидкости/жидкости.
Материалы
Среди соединений, используемых в настоящем изобретении, были использованы гидрофобные и гидрофильные соединения на основе камптотецина, полисахариды, такие как трегалоза, циклодекстрин, полиэтиленгликоль и тому подобное от Sigma-Aldrich, AbCem, Toronto Research Chemical (Канада) или Tocris (США), использованы полимеры от Akina Inc (США), Advanced Polymer Materials (Канада), Shanghai Liang Chemical Co., LTD (Китай), NanoSoft Polymer (США) и Samyang BioPharm (Корея).
Пример 1. Растворимость в различных растворителях, когда гидрофобное соединение камптотецина растворяли отдельно или гидрофобное соединение камптотецина и гидрофильное соединение камптотецина растворяли в смеси
Изменение растворимости в зависимости от растворителя измеряли, когда гидрофобное соединение камптотецина, камптотецин или 7-этил-10-гидроксикамптотецин (SN-38) растворяли отдельно или вместе с гидрофильным соединением на основе камптотецина, иринотеканом (СРТ-11), топотеканом или белотеканом (CKD-602).
1) Растворимость в различных растворителях, когда гидрофобное соединение камптотецина растворяли отдельно
Пересыщенный раствор готовили путем добавления 20 мг гидрофобного соединения камптотецина (камптотецина или SN-38) к 5 мл этанола, ацетонитрила, ацетона, этилацетата, хлороформа, диметилсульфоксида или дистиллированной воды с последующей ультразвуковой обработкой в течение 30 минут. Приготовленный пересыщенный раствор фильтровали через фильтр 0,45 мкм и фильтрат надлежащим образом разбавляли с последующим анализом ВЭЖХ.
2) Растворимость в различных растворителях, когда гидрофобное соединение камптотецина и гидрофильное соединение камптотецина растворяли в смеси
Авторы настоящего изобретения готовили пересыщенный раствор путем добавления 20 мг гидрофильного соединения камптотецина (гидрохлорида иринотекана, гидрохлорида топотекана или белотекана) к 5 мл этанола, ацетонитрила, хлороформа, этилацетата, диметилсульфоксида или дистиллированной воды и затем путем добавления 20 мг гидрофобного соединения камптотецина (SN-38 или камптотецина) с последующей ультразвуковой обработкой в течение 30 минут. Приготовленный пересыщенный раствор фильтровали через фильтр 0,45 мкм и фильтрат надлежащим образом разбавляли с последующим анализом ВЭЖХ.
Условия ВЭЖХ (Agilent 1200 Series, США) были следующими. Колонка представляла собой CapcellPak С8 (5 м, 4,6 мм × 25 см, Shiseido); подвижная фаза представляла собой смешанный растворитель метанол : ацетонитрил : буфер (2,8 г/л дигидрофосфата натрия, 1,8 г/л водного раствора 1-октансульфоната) = 17:24:59 (об./об.); скорость потока составляла 1,5 мл/мин; длина волны измерения - УФ 255 нм; количество впрыскиваемого образца составляло 15 мкл. Результаты теста на растворимость приведены в таблице 1 ниже.
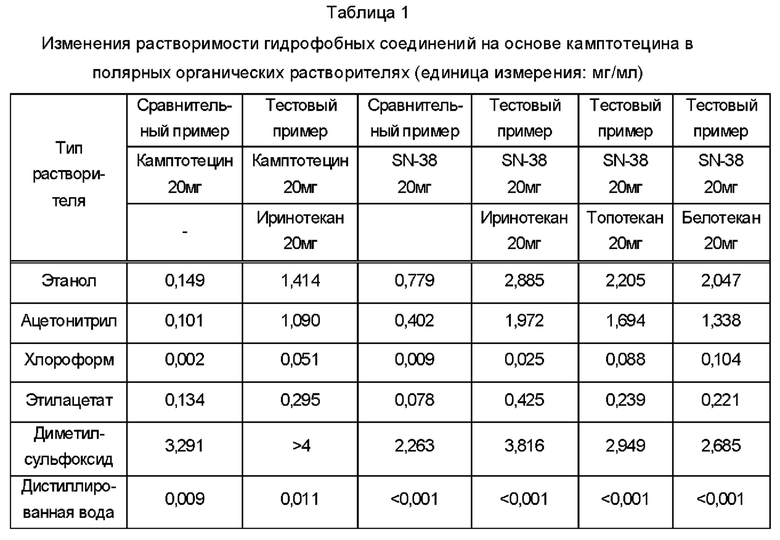
Как показано в приведенной выше Таблице 1, слаборастворимое соединение камптотецин или SN-38 само по себе растворялось с трудом в большинстве растворителей, включая воду, и растворялось в количестве 2,26-3,29 мг/мл только в диметилсульфоксиде (ДМСО) как в нелетучем растворителе. Однако камптотецин или SN-38 при растворении вместе с относительно гидрофильным препаратом, гидрохлоридом иринотекана, гидрохлоридом топотекана или белотеканом, имел растворимость в 15 раз больше, что соответствует подходящему уровню растворимости, необходимому для изготовления лекарств. Таким образом, на основании приведенных выше результатов было подтверждено, что растворимость гидрофобных соединений камптотецина значительно увеличивается при растворении в смеси с гидрофильным соединением камптотецина.
Пример 2: Изготовление первичной структуры ядро-оболочка (однослойных мицелл) и вторичной структуры ядро-оболочка (частиц с двойной структурой ядро-оболочка) из гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе и оценка размера частиц
В данном примере гидрофобное соединение на основе камптотецина, камптотецин или SN-38, и гидрофильное соединение на основе камптотецина, гидрохлорид иринотекана, гидрохлорид топотекана, белотекан или глюкуронид SN-38, или амфифильный полимер (ПЭГ-ПБЛА) растворяли в органическом растворителе для получения первичных частиц ядро-оболочка (однослойных мицелл) и к ним добавляли амфифильный полимер для получения вторичных частиц ядро-оболочка (двухслойных мицелл).
1) Изготовление первичного ядра-оболочки (однослойных мицелл) (сравнительные примеры 1-6)
Первичные частицы ядро-оболочка в виде однослойных мицелл получали с использованием в качестве основного ингредиента гидрофобного камптотецина (камптотецина или SN-38) и водорастворимого камптотецина (гидрохлорида иринотекана, гидрохлорида топотекана или глюкуронида SN-38) в качестве амфифильного соединения для образования мицелл или амфифильного полимера (поли(этиленгликоль)-поли(β-бутиролактон-молочной кислоты), ПЭГ-ПБЛА, как показано в Таблице 2 ниже.
В частности, 20 мг водорастворимого камптотецина (гидрохлорида иринотекана, гидрохлорида топотекана или глюкуронида SN-38) или ПЭГ-ПБЛА добавляли к 20 мг гидрофобного камптотецина и затем добавляли 100 мл органического растворителя (раствор 50:50 смеси этанола и ацетонитрила) до полного растворения с последующей сушкой в роторном вакуумном испарителе. 20 мл дистиллированной воды добавляли к высушенному продукту с последующей ультразвуковой обработкой при 20-30°C в течение 20 минут в ультразвуковом очистителе (UC-20, 20 Гц, 400 Вт, Jeio Tech, Корея), получая таким образом наноразмерные частицы (однослойные мицеллы) в дисперсном состоянии в водном растворе. 600 мг D-трегалозы добавляли к водному раствору, содержащему наноразмерные частицы, тем самым достигая полного растворения, и затем раствор фильтровали через стерильный фильтр 0,22 мкм и фильтрат сушили вымораживанием. Лиофильную сушку проводили в общей сложности в течение 62 часов при температурном цикле -45°C → -20°C → 0°C → 20°C при вакуумном давлении 100 мТорр или ниже и использовали устройство для лиофильной сушки от Operon (Корея). Аликвоту приготовленного лиофилизированного продукта отбирали и снова растворяли в дистиллированной воде для инъекций, а размер частиц измеряли с помощью динамического рассеяния света (DLS) (Zetasizer (ТМ), Malvern, UK).
2) Изготовление частиц с двойной структурой ядро-оболочка (двухслойных мицелл) (Тестовые примеры 1-4)
Для приготовления композиции двухслойных частиц, имеющих двойную структуру ядро-оболочка, авторы настоящего изобретения добавляли по 20 мг гидрофобного камптотецина и гидрофильного камптотецина в 100 мл органического растворителя (смешанный раствор 50:50 из этанола и ацетонитрила) для растворения в нем с последующей сушкой с помощью роторного вакуумного испарителя (Buchi). 200 мл дистиллированной воды добавляли к высушенному продукту с последующей ультразвуковой обработкой при 20-30°C в течение 20 минут в ультразвуковом очистителе, получая таким образом наноразмерные частицы ядро-оболочка (однослойные мицеллы) в диспергированном состоянии в водном растворе. При перемешивании водного раствора, смешанного с частицами ядро-оболочка, медленно добавляли 90 мг амфифильного блок-сополимера метоксиполи(этиленгликоль)-поли(лактида) (мПЭГ-ПМК) (молекулярная масса мПЭГ: молекулярная масса ПМК=2000:1500), предварительно растворенного в 10 мл дистиллированной воды, с последующим перемешиванием при 20-30°C в течение 6 часов, тем самым получая частицы с двойной структурой ядро-оболочка в дисперсном состоянии в водном растворе. 600 мг D-трегалозы в качестве криопротектора добавляли к водному раствору, содержащему частицы с двойной структурой ядро-оболочка, для растворения в нем, и затем смесь фильтровали через стерильный фильтр 0,22 мкм, а затем проводили лиофилизацию тем же способом, что и при изготовлении первичных частиц ядро-оболочка, тем самым получая лиофилизированный продукт в виде белого порошка. Предварительно определенное количество лиофилизированного продукта снова растворяли в воде для инъекций для измерения размера частиц. Кроме того, измеряли средние размеры частиц до и после лиофильной сушки и сравнивали долю частиц с размерами 200 нм или более и форму распределения (одно- или многомодальное распределение).
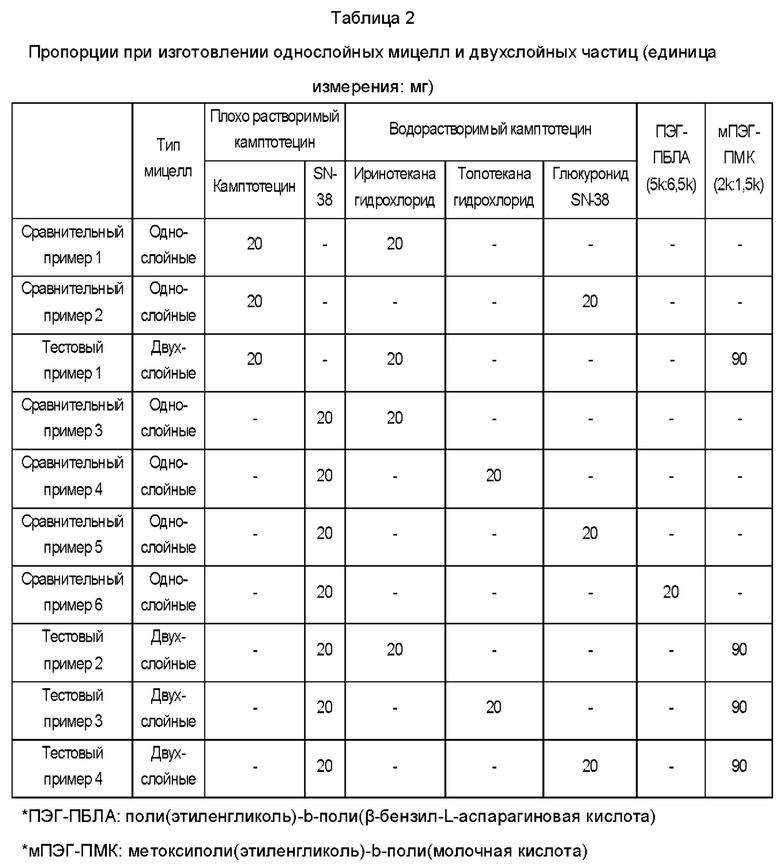

Как показано в таблице 3 выше, что касается среднего размера частиц после лиофильной сушки, первичные частицы ядро-оболочка (однослойные мицеллы), состоящие из плохо растворимого камптотецина и водорастворимого камптотецина, или первичные частицы ядро-оболочка, состоящие из плохо растворимого камптотецина и амфифильного полимера, увеличились примерно в 1,2-1,5 раза, а частицы с двойной структурой ядро-оболочка (двухслойные мицеллы) увеличились только примерно в 1,1 раза.
Что касается первичных частиц ядро-оболочка (однослойных мицелл), то после лиофильной сушки частицы размером 200 нм или более образуются в больших количествах, около 16-40%, и особенно образуются частицы размером в несколько микрометров (мкм) или более, способные влиять на безопасность при введении в организм человека (сравнительные примеры с 1 по 6 в таблице 3 и на фиг. 1а и 1b). В то же время, что касается частиц с двойной структурой ядро-оболочка, были обнаружены частицы размером 200 нм или более в количестве примерно 2,4-3,1% для SN-38 и примерно 4,8% для камптотецина, причем оба значения составляют менее 5%, что показывает очень благоприятные результаты, а частицы размером 500 нм или более не были обнаружены (Тестовые примеры с 1 по 4 в таблице 3 и фиг. 1с).
В конкретном распределении первичные частицы ядро-оболочка (однослойные мицеллы) показали распределение с несколькими пиками (фиг. 1а и 1b), а вторичные частицы ядро-оболочка показали однородное распределение, подтверждая очень стабильную структуру (фиг. 1с). Кроме того, средний размер первичных частиц ядро-оболочка (однослойных мицелл) был меньше, чем у частиц с двойной структурой ядро-оболочка (двухслойных мицелл) примерно на 10 нм до лиофильной сушки, но изменение размера частиц до и после лиофильной сушки было очень велико, в результате чего частицы с двойной структурой ядро-оболочка (двухслойные мицеллы) были очень физически стабильны.
Пример 3: Оценка стабильности первичных частиц ядро-оболочка (однослойных мицелл) и частиц с двойной структурой ядро-оболочка (двухслойных мицелл)
В данном примере сравнивали однослойные мицеллы (сравнительные примеры 1, 3 и 6) и частицы с двойной структурой ядро-оболочка (Тестовые примеры 1 и 2) на предмет изменения размера частиц, где образцы продуктов, изготовленных в соответствии со стандартами испытаний на стабильность лекарственного средства хранили в течение шести месяцев в условиях ускоренного испытания (40°C, относительная влажность 75%). Результаты показаны в таблице 4.
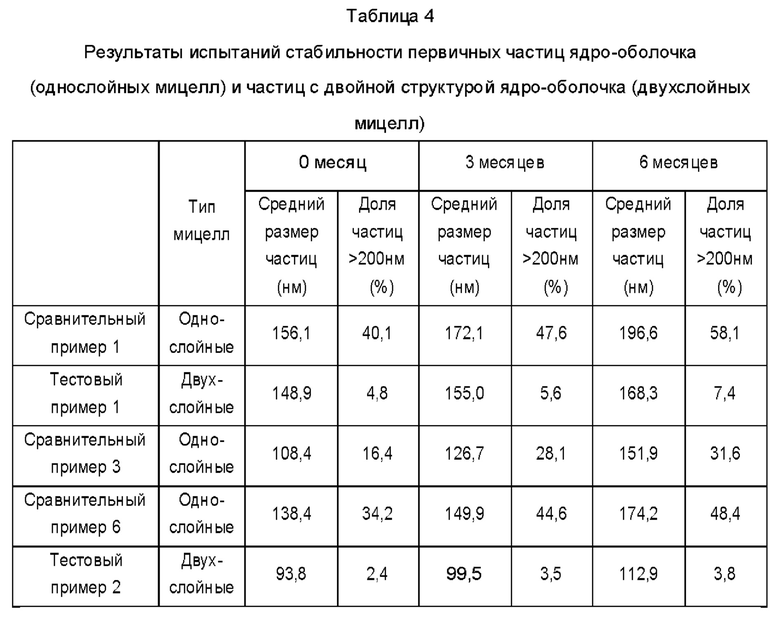
Первичные частицы ядро-оболочка (однослойные мицеллы), содержащие камптотецин или SN-38 в качестве основного ингредиента, и частицы с двойной структурой ядро-оболочка (двухслойные мицеллы) подвергали испытаниям на стабильность. В результате, в случае однослойных мицелл средний размер частиц увеличивался примерно на 50% или более, а доля частиц с размерами 200 нм или более быстро увеличивалась до 58% в условиях ускоренного испытания. В случае двухслойных частиц средний размер частиц увеличивался примерно на 20%, а доля частиц с размерами 200 нм или более ограничивалась в пределах 3,8% для SN-38 и 7,4% для камптотецина. Следовательно, можно видеть, что структура двухслойных частиц согласно настоящему изобретению была значительно улучшена с точки зрения стабильности по сравнению с однослойными мицеллами.
Пример 5. Изготовление частиц с двойной структурой ядро-оболочка в зависимости от типа амфифильного полимера и молекулярной массы амфифильного полимера.
В данном примере частицы с двойной структурой ядро-оболочка изготавливали с использованием различных амфифильных полимеров (блок-сополимеров). Как показано в таблице 5, использовали по 20 мг SN-38 и гидрохлорида иринотекана в качестве гидрофобного и гидрофильного соединений камптотецина, 500 мг трегалозы в качестве криопротектора и по 90 мг каждого из амфифильных полимеров. Способ изготовления осуществляли таким же образом, как и способ изготовления частиц ядро-оболочка в приведенном выше примере 2, и для сравнения конкретных размеров после лиофильной сушки материалы снова растворяли в воде для инъекций.
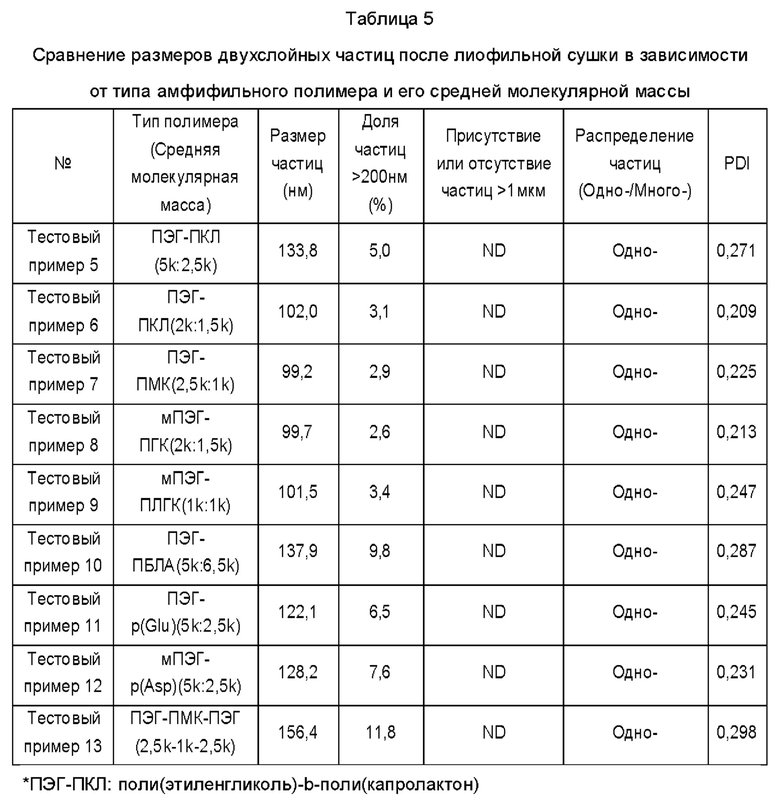

Как показано в Таблице 5 выше, можно видеть, что двухслойные частицы согласно настоящему изобретению могут быть изготовлены с использованием различных амфифильных полимеров (блок-сополимеров) и амфифильных полимеров, имеющих различные средние молекулярные массы, и стабильность частиц была превосходной.
Пример 6: Оценка размера частиц в зависимости от типа криопротектора
В данном примере наблюдали влияние криопротектора при изготовлении первичных частиц ядро-оболочка (однослойных мицелл) и частиц с двойной структурой ядро-оболочка. В качестве гидрофобных соединений камптотецина выбирали 10-гидроксикамптотецин и SN-48; в качестве гидрофильного камптотецина выбирали гидрохлорид иринотекана; и качестве амфифильного полимера использовали мПЭГ-ПМК (2k:1,5k). В качестве криопротектора использовали по 500 мг D-трегалозы, D-маннита, ПЭГ-2000 и гидроксипропил-β-циклодекстрина (HP-b-CD). Частицы с двойной структурой ядро-оболочка изготавливали с использованием композиций, показанных в таблице 6, а способ изготовления выполняли таким же образом, как в примере 2.
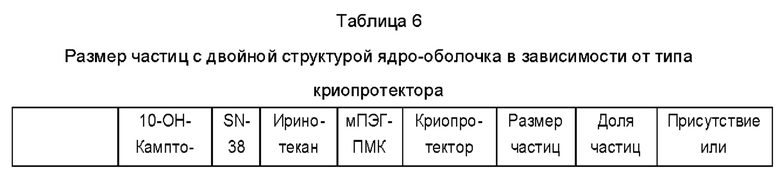
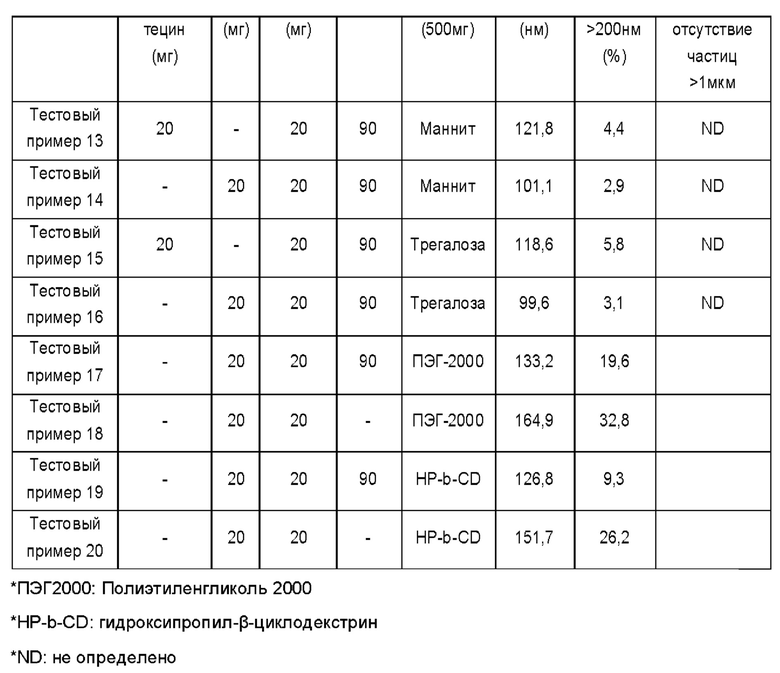
Как показано в Таблице 6, когда в качестве криопротекторов использовали полисахариды маннит и трегалозу, были получены благоприятные результаты с точки зрения размера частиц. При использовании ПЭГ-2000 и HP-b-CD размер частиц был несколько большим, например, были обнаружены частицы размером 1 мкм или более. В Тестовых примерах 18 и 20 для однослойных мицелл были обнаружены относительно крупные частицы размером 200 нм или более и макрочастицы размером 1 мкм или более, когда в качестве криопротекторов использовали полиэтиленгликоль и циклодекстрин.
Пример 7: Изготовление первичных частиц ядро-оболочка и частиц с двойной структурой ядро-оболочка в условиях водорастворимого растворителя
Первичные частицы ядро-оболочка (однослойные мицеллы) можно изготовить в водном растворе, а также в органическом растворителе, как в примере 2. Как показано в таблице 7 ниже, 10 мг SN-38 полностью растворились в 0,1 мл 0,5 М водного раствора гидроксида натрия, полученный раствор переливали и нейтрализовали в водном растворе гидрохлорида иринотекана (1 мг/мл), предварительно растворенного в 15 мл 0,5 мМ водного раствора гидрохлорида, и затем добавляли водный раствор гидрохлорида для доведения рН примерно до 5 с последующей ультразвуковой обработкой, получая таким образом первичные частицы ядро-оболочка (однослойные мицеллы). К ним добавляли 40 мг амфифильного полимера мПЭГ-ПМК с последующим перемешиванием при комнатной температуре в течение 6 часов и дополнительно добавляли 300 мг D-трегалозы для растворения. Раствор смеси фильтровали через стерильный фильтр 0,22 мкм, лиофилизировали и снова растворяли в воде для инъекций, а затем измеряли размер частиц (тестовый пример 21). SN-38 и иринотекан растворяли, используя органический щелочной этаноламин в качестве основного водного раствора или органическую лимонную кислоту в качестве кислого водного раствора, изготавливали двухслойные частицы таким же способом и измеряли размер частиц, соответственно (Тестовые примеры 22 и 23).
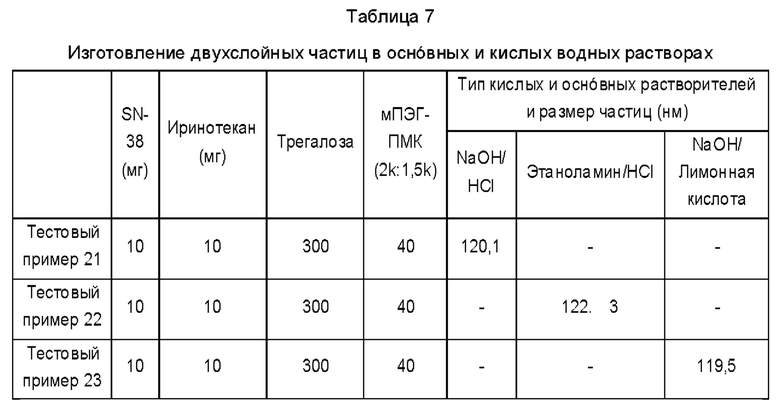
Как показано в Таблице 7, частицы с двойной структурой ядро-оболочка, полученные путем растворения гидрофобного камптотецина и гидрофильного камптотецина в основных и кислых водных растворах, имели размер частиц приблизительно 120 нм и таким образом были успешно изготовлены частицы с двойной структурой ядро-оболочка.
Пример 8: Изготовление частиц с двойной структурой ядро-оболочка путем смешивания
В данном примере показан способ изготовления частиц с двойной структурой ядро-оболочка путем смешивания всего количества гидрофобного камптотецина, гидрофильного камптотецина и амфифильного блок-сополимера за одну стадию. Гидрофобные соединения камптотецина (10-гидроксикамптотецин и SN-38) помещали вместе с 20 мг гидрохлорида иринотекана в 100 мл органического растворителя (раствор смеси 50:50 этанол : ацетонитрил) и полностью растворяли при перемешивании, затем при перемешивании добавляли 90 мг мПЭГ-ПМК (2k:1,5k), растворенный в 10 мл органического растворителя (раствор 50:50 этанол : ацетонитрил).
Смешанный раствор сушили с помощью роторного вакуумного испарителя и к остаткам добавляли 200 мл дистиллированной воды с последующей ультразвуковой обработкой в течение 10 минут в ультразвуковом очистителе, получая таким образом частицы с двойной структурой ядро-оболочка согласно настоящему изобретению. Добавляли 400 мг D-маннита в качестве криопротектора для растворения и этот раствор фильтровали через стерильный фильтр 0,22 мкм, лиофилизировали. Надлежащее количество лиофилизированного продукта снова растворяли в воде для инъекций для измерения размера частиц. Результаты показаны в таблице 8.


Как показано в Таблице 8, частицы с двойной структурой ядро-оболочка, полученные путем смешивания и растворения одновременно гидрофобного камптотецина, гидрофильного камптотецина и амфифильного полимера в органическом растворителе, показали однородное распределение частиц по размеру с размерами приблизительно 120-130 нм, где частицы с размерами 200 нм или более были обнаружены в небольших количествах, 5% или менее, но частицы с размерами 1 мкм или более не были обнаружены, таким образом было подтверждено, что частицы имеют, в целом, благоприятную стабильность.
Пример 9. Сравнение эффекта ингибирования опухоли первичными частицами ядро-оболочка (однослойными мицеллами) и частицами с двойной структурой ядро-оболочка (двухслойными мицеллами) на мышиных моделях опухолей (колоректального рака)
Измеряли противораковый эффект на мышиных моделях колоректального рака композиций однослойных мицелл (сравнительные примеры 3 и 6) и двухслойных частиц (тестовый пример 2) следующим методом.
Предварительно культивированную клеточную линию рака ободочной и прямой кишки (НТ-29) инъецировали в правый бок голых мышей линии Balb/c в количестве 5×106 клеток/0,2 мл и примерно через 7 дней выбирали только опухоли с размером 150-200 мм3. В каждую группу распределяли по девять животных и внутривенно вводили фиктивный препарат (группа без лечения), сравнительный пример (однослойные мицеллы), сравнительный пример 6 (однослойные мицеллы) и тестовый пример 2 (двухслойные частицы), один раз каждые три дня, три раза в общей сложности. Доза составляла 10 мг/кг в пересчете на SN-38. В качестве показателя измерения противоракового эффекта использовали объем опухоли, измеренный каждые три дня после введения тестируемой композиции, который определяли в течение 18 дней. Результаты показаны на фиг. 2 и 3.
В результате измерения эффекта ингибирования опухоли композиции однослойных мицелл (сравнительные примеры 3 и 6) показали эффект ингибирования опухоли примерно 50-60% по сравнению с группой отрицательного контроля, а композиция двухслойных частиц (тестовый пример 2) показала эффект ингибирования опухоли около 80% или более по сравнению с группой отрицательного контроля, что указывает на весьма превосходные эффекты. Эти результаты были обусловлены тем фактом, что мицеллы со стабилизированной структурой и мицеллы со структурой, имеющей размеры до 200 нм или менее, согласно настоящему изобретению эффективно поступали в раковые ткани при стабильном нахождении в организме.
Пример 10: Сравнение эффекта ингибирования опухоли однослойными мицеллами и двухслойными мицеллами на мышиных моделях рака поджелудочной железы (AsPc-1)
Сравнивали эффект ингибирования опухолей на мышиных моделях рака поджелудочной железы композиции однослойных мицелл (сравнительный пример 3) и композиции двухслойных мицелл (тестовый пример 2). Предварительно культивированную клеточную линию рака поджелудочной железы (AsPc-1) инъецировали в правый бок мышей линии BALB/c-nu/nu в количестве 5×106 клеток/0,2 мл и примерно через 10 дней выбирали только опухоли с размером 100-150 мм3. В каждую группу распределяли по десять животных и внутривенно вводили фиктивный препарат (группа без лечения), сравнительный пример 3 и тестовый пример 2, один раз каждые семь дней, три раза в общей сложности. Доза составила 10 мг/кг в пересчете на SN-38. В качестве показателя измерения противоракового эффекта использовали объем опухоли, измеренный каждые три дня после введения тестируемой композиции, который определяли в течение 24 дней. Результаты показаны на фиг. 4.
В результате измерения эффекта ингибирования опухоли композиция однослойных мицелл (сравнительный пример 3) показала эффект ингибирования опухоли примерно 27% по сравнению с группой отрицательного контроля, а композиция двухслойных частиц (тестовый пример 2) показала эффект ингибирования опухоли около 47% или более по сравнению с группой отрицательного контроля, что указывает на весьма превосходные эффекты. Эти результаты аналогичны результатам на моделях с колоректальным раком (Пример 9) и было подтверждено, что композиция двухслойных частиц согласно настоящему изобретению существенно лучше в отношении эффектов ингибирования опухоли по сравнению с однослойными мицеллами.
Пример 11: Сравнительный тест ингибирующего эффекта на опухоль композиций однослойных мицелл и двухслойных частиц на мышиной модели рака поджелудочной железы (MiaPaca-2)
Эффект ингибирования опухоли композицией однослойных мицелл (сравнительный пример 3) сравнивали с эффектом композиции двухслойных частиц (тестовый пример 2) на мышиных моделях с раком поджелудочной железы (ортотопический) на основе SN-38. После разреза 0,7-1 см левого бока самцов мышей линии BALB/c-nu/nu обнажали всю поджелудочную железу и селезенку, а затем вводили предварительно культивированную клеточную линию рака поджелудочной железы (клеточную линию MiaPaca-2) с помощью шприца в количестве 1x107 клеток/0,1 мл. Убеждались, что суспензия опухолевых клеток не вытекает, и органы, подвергшиеся воздействию снаружи, возвращали в исходное положение, а место разреза зашивали хирургической нитью. Примерно через 10 дней после инокуляции линии клеток рака поджелудочной железы группировали животных по массе тела. В каждую группу распределяли по десять животных и вводили фиктивный препарат (группа без лечения), сравнительный пример 3 и тестовый пример 2, один раз каждые семь дней, три раза в общей сложности. Доза составляла 20 мг/кг в пересчете на SN-38. Животных наблюдали в течение 28 дней, а размер и массу опухоли измеряли путем вскрытия на 28 день. Результаты представлены на фиг. 5.
В результате измерения эффекта ингибирования опухоли масса опухоли в группе, не получавшей лечения (группа отрицательного контроля), составляла в среднем 0,46±0,17 г, масса опухоли в группе обработки композицией однослойных мицелл (сравнительный пример 3) составляла 0,37±0,09 г, а масса опухоли в группе обработки композицией двухслойных частиц (тестовый пример 2) составляла 0,21±0,05 г. Следовательно, композиция двухслойных частиц показала ингибирующий эффект на опухоль 55% или более по сравнению с композицией однослойных мицелл и, таким образом, существенно лучший ингибирующий эффект на опухоль.
Пример 12. Фармакокинетический тест на собаках породы бигль.
Фармакокинетические характеристики композиции однослойных мицелл (сравнительный пример 3) сравнивали с характеристиками композиции двухслойных частиц (тестовый пример 2) у собак породы бигль. Самцов биглей весом 7-10 кг разделяли на две группы, по три собаки в каждой группе, в зависимости от веса тела, и внутривенно вводили композицию однослойных мицелл (сравнительный пример 2) и композицию двухслойных частиц (тестовый пример 2) по 0,5 мг/кг в пересчете на SH-38 в течение 10 минут инфузии. Образцы крови отбирали через 0,33, 0,67, 1, 1,5, 2, 4, 8, 12, 24, 36 часов после окончания введения и плазму, полученную центрифугированием крови, предварительно обрабатывали следующим методом для измерения концентрации препарата в плазме. Для предварительной обработки образца к 100 мкл плазмы сначала добавляли 20 мкл S-(+)-камптотецина (500 нг/мл, растворенного в ацетонитриле) в качестве внутреннего стандарта и дополнительно добавляли 500 мкл ацетонитрила с последующим вихревым перемешиванием в течение 30 секунд. После центрифугирования смеси при 12000 об/мин в течение 3 минут, отбирали супернатант и вводили 2 мкл в систему ЖХ-МС/МС (модель API-5000, АВ Sciex). Разделение проводили на колонке Gemini С18 (3 мкм, 2,0×50 мм, Phenomenex, США), подвижная фаза представляла собой 50% раствор ацетонитрила, содержащий 0,1% муравьиной кислоты, и скорость потока составляла 0,25 мл/мин. Условия детектирования МС/МС проводили в режиме положительных ионов, глюкуронид SN-38 детектировали при m/z 569,3 → 393,2 и внутренний стандарт детектировали при m/z 349,2 → 305,2.
Концентрация лекарственного средства в крови после введения показана на фиг. 6, а фармакокинетические параметры для него приведены в таблице 9.

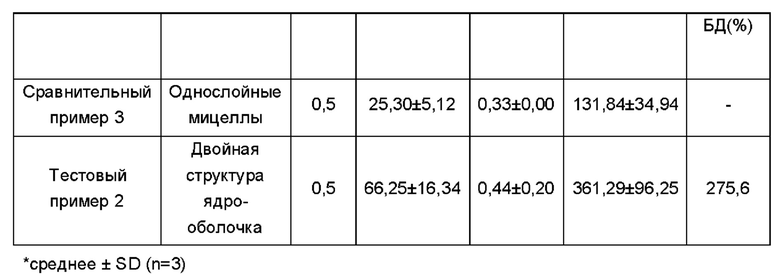
У собак биглей анализировали глюкуронид SN-38, полученный непосредственно из SN-38, солюбилизированный в частицах согласно настоящему изобретению. Результаты подтвердили, что двухслойные частицы согласно настоящему изобретению показали увеличение биодоступности примерно в 2,75 раза по сравнению с однослойными мицеллами. Из приведенных выше результатов было определено, что двухслойные частицы согласно настоящему изобретению максимизируют растворимость плохо растворимого лекарства SN-38 in vivo.
Хотя настоящее изобретение было подробно описано со ссылкой на конкретные признаки, специалистам в данной области техники должно быть очевидно, что это описание предназначено только для предпочтительного варианта осуществления и не ограничивает объем настоящего изобретения.
Настоящее изобретение относится к системе доставки лекарств, имеющей двойную структуру ядро-оболочка, в частности к двойной системе доставки нанолекарства, имеющей внутреннюю структуру ядро-оболочка, содержащую плохо растворимое соединение камптотецина и водорастворимое соединение камптотецина внутри, и амфифильную полимерную оболочку, и к способу ее получения. Частицы с двойной структурой ядро-оболочка, изготовленные в соответствии с настоящим изобретением, образуют очень стабильные частицы и показывают однородное распределение частиц до и после лиофильной сушки. Частицы согласно настоящему изобретению показывают превосходные результаты по сравнению с существующими однослойными мицеллами в тестах на эффективность на животных и в фармакокинетических тестах, и в них не используют поверхностно-активные вещества, вызывающие гиперчувствительность, и, таким образом, применение частиц согласно настоящему изобретению может обеспечить фармацевтическую композицию или платформу системы доставки лекарственного средства, которая безопасна для организма человека. 4 н. и 8 з.п. ф-лы, 6 ил., 9 табл., 12 пр.
1. Частица для доставки лекарственного средства, имеющая структуру двухслойной мицеллы, включающей: (а) внутренную структуру ядро-оболочка, содержащую гидрофобное соединение на основе камптотецина, выбранное из группы, состоящей из 7-этил-10-гидроксикамптотецина (SN-38), камптотецина, 10-гидроксикамптотецина и их фармацевтически приемлемых солей, и гидрофильное соединение на основе камптотецина, выбранное из иринотекана, топотекана, белотекана, их фармацевтически приемлемых солей и глюкуронида SN-38; и (b) внешнюю структуру ядро-оболочка, содержащую амфифильный блок-сополимер, состоящий из блоков A-B или A-B-A, где А представляет собой гидрофильный полимер, который представляет собой монометоксиполиэтиленгликоль, диметоксиполиэтиленгликоль, полиэтиленгликоль, полипропиленгликоль, монометоксиполипропиленгликоль, полиэтиленоксид, полиакриловую кислоту или их полимер; где B представляет собой гидрофобный полимер, который представляет собой полимолочную кислоту, полилактид, полигликолевую кислоту, полигликолид, сополимер полимолочной кислоты и гликолевой кислоты, полиминдальную кислоту, поликапролактон, полидиоксан-2-он, полиглутаминовую кислоту, полиаспарагиновую кислоту, полиорнитин, сложный полиортоэфир, их производное или сополимер двух или более соединений, выбранных из них; и где массовое соотношение гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина составляет от 1:10 до 10:1.
2. Частица по п. 1, в которой среднечисловая молекулярная масса гидрофильного полимера A составляет 500-10000 Да.
3. Частица по п. 1, в которой среднечисловая молекулярная масса гидрофобного полимера B составляет 500-10000 Да.
4. Частица по п. 1, в которой массовое соотношение суммы гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина к амфифильному блок-сополимеру составляет от 1:200 до 10:1.
5. Частица по п. 1, в которой среднечисленный размер частицы составляет 10-500 нм.
6. Фармацевтическая композиция для инъекций при лечении колоректального рака или рака поджелудочной железы, содержащая частицу по любому из пп. 1-5 и фармацевтически приемлемый носитель.
7. Способ лечения колоректального рака или рака поджелудочной железы, включающий введение субъекту фармацевтической композиции по п. 6.
8. Способ получения частицы по п. 1, включающий: (а) формирование внутренней структуры ядро-оболочка, содержащей гидрофобное соединение на основе камптотецина и гидрофильное соединение на основе камптотецина; и (b) формирование внешней структуры ядро-оболочка, содержащей амфифильный сополимер.
9. Способ по п. 8, где стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; и где стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе, где органический растворитель выбран из С1-С5 спирта, алкилацетата, ацетона, ацетонитрила, хлороформа, диметилсульфоксида и их смесей.
10. Способ по п. 8, где стадия (а) включает смешивание основного водного раствора, в котором растворено гидрофобное соединение камптотецина, и водного раствора, в котором растворено гидрофильное соединение камптотецина; и где стадия (b) включает смешивание внутренней структуры ядро-оболочка и амфифильного блок-сополимера в водном растворителе.
11. Способ по п. 8, где стадия (а) включает смешивание гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина в органическом растворителе; и где стадия (b) включает смешивание смеси гидрофобного соединения на основе камптотецина и гидрофильного соединения на основе камптотецина с амфифильным блок-сополимером в органическом растворителе, где органический растворитель выбран из С1-С5 спирта, алкилацетата, ацетона, ацетонитрила, хлороформа, диметилсульфоксида и их смесей.
12. Способ по п. 10, где основный раствор включает по меньшей мере одно, выбранное из группы, состоящей из неорганической щелочи, щелочной соли органической кислоты и алкиламина, при этом неорганическая щелочь включает гидроксид натрия, гидроксид калия, дигидрофосфат натрия, дигидрофосфат калия, гидроксид магния, карбонат натрия и гидрокарбонат натрия.
| CN 102961332 A, 2013.03.13 | |||
| US 2010203150 A1, 2010.08.12 | |||
| US 2012100220 A1, 2012.04.26 | |||
| Opanasopit, P., Yokoyama, M., Watanabe, M., Kawano, K., Maitani, Y., & Okano, T | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Block Copolymer Design for Camptothecin Incorporation into Polymeric Micelles for Passive Tumor Targeting | |||
| Pharmaceutical Research, 21 (11), 2001-2008, найдено онлайн, | |||
Авторы
Даты
2021-03-18—Публикация
2018-06-22—Подача