Данное изобретение касается новых производных пиразин 2-карбоксамида общей формулы (I), применимых в качестве антагонистов метаботропных глутаматных рецепторов:
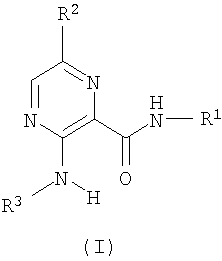
где R1 представляет собой а 5- или 6-членный цикл соответственно формулы (II) или (III):
(II) 






(III) 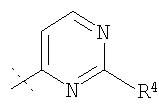



R2 представляет собой Н, C1-С7-алкил, С3-С6-циклоалкил или -(CH2)m-Ra;
R3 представляет собой Н, арил или гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-C1-С7-алкил, -(СО)-Rb, -(CH2)m-Rc, -NH-(CO)-C1-C7- алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, C1-С7-алкил, -O-(CO)-C1-C7-алкил или -(CH2)m-Re;
R5 представляет собой С1-С7-алкил или С1-С7-алкил-С3-С6-циклоалкил; -(CH2)n-O-Rf, С3-С8-алкенил-О-Rf, -(CH2)n-NR9Rh; -C2-С6-алкенил-NRgRh или -(CH2)n-Re;
Ra представляет собой -О-С1-С7-алкил или -ОН;
Rb представляет собой C1-C7-алкил, NH2 или -O-C1-С7-алкил;
Rc представляет собой -ОН, NH2 или NH-(СО)-O-С1-С7-алкил;
Rd представляет собой С1-С7-алкил, -NH2, -NH-С1-С7-алкил или -N-ди(С1-С7-алкил);
Re представляет собой -ОН, -CH2F, -CHF2, -CF3 или -O-(СО)-С1-С7-алкил;
Rf представляет собой C1-С7-алкил, С3-С8-алкенил, С3-С6-циклоалкил, фенил, бензил или -(CO)-R';
Rg, Rh независимо представляют собой Н, С1-С7-алкил, С3-С6-циклоалкил, С3-С8-алкенил, фенил, бензил или -(CO)-R', или Rg и Rh могут также вместе с атомом азота, к которому они присоединены, образовать 5-7-членное гетероциклическое или гетероарильное кольцо, возможно замещенное 1 или 2 группами ОН;
R' представляет собой NH2, -NH-C1-C7-алкил, C1-С7-алкил или С1-С7-алкокси;
m имеет значение от 1 до 4;
n имеет значение от 2 до 6;
а также их фармацевтически приемлемых солей.
Хотя некоторые соединения, полезные в качестве антагонистов метаботропных глутаматных рецепторов группы I, уже были описаны (Bonnefous et al. Dipyridyl amids: potent metabotropic glutamate subtype 5 (mGlu5) receptor antagonists // Bioorganic & Medicinal chemistry Letters, 2005), но не соединения по настоящему изобретению. Кроме того, в общем для соединений формулы (I) утверждалось (Bonnefous et al., см. выше), что когда R1 представляет собой пиридин-3-ил или пиридин-4-ил, соединения являются неактивными. Авторами настоящего изобретения неожиданно было обнаружено, что в протиповоложность этому утверждению 5-положения указанных пиридин-2-иловых соединений на самом деле поддаются замещению атомом фтора и что полученные соединения формулы I, где R1 представляет собой пиридин-4-ил, имеют активность антагонистов рецепторов mGluR5.
Кроме того, неожиданно было обнаружено, что также и другие производные пиразин-2-карбоксамида, иные, чем производные пиридин-2-ила, имеют активность антагонистов рецепторов mGluR5.
В центральной нервной системе (ЦНС) передача сигналов осуществляется путем взимодействия нейромедиатора, высвобождающегося из нейрона, с нейрорецептором.
Было неожиданно обнаружено, что соединения общей формулы I являются антагонистами метаботропных глутаматных рецепторов. Соединения формулы I отличаются ценными терапевтическими свойствами. Они могут быть использованы для лечения или предотвращения заболеваний, опосредованных mGluR5 рецептором.
Глутамат является главным возбуждающим нейромедиатором в мозге и играет уникальную роль в целом ряде процессов в ЦНС. Рецепторы, отвечающие на глутаматные сигналы, делят на две основные группы. Первую основную группу, а именно группу ионотропных рецепторов, образуют лигандзависимые ионные каналы. Метаботропные глутаматные рецепторы (mGluR, от metabotropic glutamate receptors) принадлежат ко второй основной группе и, кроме того, принадлежат семейству рецепторов, связанных с G-белками.
В настоящее время известно восемь разных типов рецепторов семейства mGluR, и некоторые из них еще разделены на подтипы. На основании структурной гомологии, механизмов передачи сигналов и селективности к агонистам эти восемь рецепторов могут быть подразделены на три подгруппы: mGluR1 и mGluR5 принадлежат к группе I, mGluR2 и mGluR3 принадлежат к группе II и mGluR4, mGluR6, mGluR7 и mGluRS принадлежат к группе III.
Лиганды метаботропных глутаматных рецепторов, принадлежащих к первой группе, могут быть использованы для лечения или предотвращения острых и/или хронических неврологических нарушений, таких как психоз, эпилепсия, шизофрения, болезнь Альцгеймера, когнитивные расстройства и нарушения памяти, а также хроническая и острая боль.
Другие состояния, которые можно лечить при этом, представляют собой ограниченную функцию мозга, вызванную операциями шунтирования или трансплантациями, недостаточное мозговое кровоснабжение, травмы спинного мозга, травмы головы, гипоксию, вызванную беременностью, остановку сердца и гипогликемию. Также состояния, которые можно лечить, - это гастроэзофагеальый рефлюкс (GERD, от gastroesophageal reflux disease), синдром ломкой X-хромомсомы (fragile X), ишемия, хорея Хантингтона, боковой амиотрофический склероз (ALS, от amyotrophic lateral sclerosis), слабоумие, вызванное спидом, травмы глаз, ретинопатия, идиопатический паркинсонизм или лекарственный паркинсонизм, а также состояния, которые ведут к глутамат-недостаточным функциям, таким, например, как спазмы мышц, конвульсии, мигрени, недержание мочи, ожирение, никотиновая зависимость, опиатная зависимость, тревога, рвота, дискенезия и депрессии.
Заболевания, которые полностью или частично опосредованы mGluR5, включают в себя, например, острые, травматические и хронические дегенеративные процессы нервной системы, такие как болезнь Альцгеймера, старческое слабоумие, болезнь Паркинсона, хорея Хантингтона, боковой амиотрофический склероз и рассеянный склероз, психиатрические заболевания, такие как шизофрения и тревога, депрессия, боль и наркотическая зависимость (Expert Opin. Ther. Patents (2002), 12, (12)).
Селективные антагонисты mGluR5 особенно пригодны для лечения тревоги и боли.
Данное изобретение относится к соединениям формулы I и их фрамацевтически приемлемым солям, к указанным соединениям как фармацевтически активным субстанциям и к их получению.
Это изобретение также относится к способу получения соединений общей формулы I согласно общим методикам, приведенным здесь для соединений формулы I.
Кроме того, изобретение относится к лекарствам, содержащим одно или более чем одно соединение по данному изобретению и фармацевтически приемлемый эксципиент, для лечения и предотврщения заболеваний, опосредованных mGluR5 рецептором, таких как острые и/или хронические неврологические расстройства, в частности тревога и хроническая или острая боль.
Изобретение также относится к применению соединения по изобретению, а также его фармацевтически приемлемой соли для изготовления лекарства для лечения и предотвращения заболеваний, опосредованных mGluR5 рецептором, как описано выше.
Следующие определения общих терминов, используемых в данном описании, применяются незвисимо от того, встречаются ли эти термины по отдельности или в комбинациях.
«Арил» обозначает одновалентную циклическую ароматическую углеводородную группировку, состоящую из моно-, би- или трициклического ароматического кольца. Предпочтительные арильные группы представляет собой С6-С10-арил. Группа арил может быть возможно замещена, как определено здесь. Примеры арильных группировок включают, но не ограничены ими, возможно замещенные фенил, нафтил, фенантрил, флуоренил, инденил, пенталенил, азуленил, оксидифенил, бифенил, метилендифенил, аминодифенил, дифенилсульфидил, дифенилсульфонил, дифенилизопропилиденил, бензодиоксанил, бензофуранил, бензодиоксилил, бензопиранил, бензоксазинил, бензоксазинонил, бензопиперидинил, бензопиперазинил, бензопирролидинил, бензоморфолинил, метилендиоксифенил, этилендиоксифенил и подобные им, включая их частично гидрогенизированные производные.
«C1-C7 алкил» обозначает группу с прямой или разветвленной углеродной цепью, содежащей от 1 до 7 атомов углерода, например метил, этил, пропил, изо-пропил, изо-бутил, втор-бутил, трет-бутил, пентил, н-гексил, а также те, которые конкретно проиллюстрированы приведенными ниже примерами.
«Галоген» обозначает хлор, йод, фтор и бром.
«Гетероарил» означает моноциклический, бициклический или трициклический радикал из 5-12 кольцевых атомов, предпочтительно 5-9 кольцевых атомов, имеющий по меньшей мере одно ароматическое кольцо, и, кроме того, содержащее один, два или три кольцевых гетероатома, выбранных из N, О или S, причем остальные кольцевые атомы представляют собой С. Гетероарил может быть возможно замещен одним, двумя, тремя или четырьмя заместителями, причем каждый заместитель независмо предсавляет собой гидрокси, циано, алкил, алкокси, тиоалкил, галогено, галогеноалкил, гидроксиалкил, алкоксикарбонил, амино, ацетил, -NHCOOC(СН3)3 или бензил, замещенный галогеном, или для неароматической части цикла кольца также оксо, если иное не указано конкретно. Примеры гетероарильных группировок включают, но не ограничены ими, возможно замещенный имидазолил, возможно замещенный оксазолил, возможно замещенный тиазолил, возможно замещенный пиразинил, возможно замещенный пирролил, возможно замещенный пиридинил, возможно замещенный пиримидинил, возможно замещенный индолил, возможно замещенный изохинолинил, возможно замещенный карбазол-9-ил, возможно замещенный фуранил, возможно замещенный бензофуранил, возможно замещенный бензо[1,2,3]тиадиазолил, возможно замещенный бензо[b]тиофенил, возможно замещенный 9Н-тиоксантенил, возможно замещенный тиено[2,3-с]пиридинил и поодбные или те, которые конкретно проиллюстрированы здесь примерами.
«С3-С6 циклоалкил» обозначает углеродный цикл, содержащий от 3 до 6 атомов углерода в качестве членов цикла, и включает, без ограничения ими, циклопропил, циклобутил, циклопентил, циклогексил, а также те группы, которые конкретно проиллюстрированы примерами, приведенными здесь ниже.
«5-7-членный гетероциклоалкил» обозначает насыщенное циклическое кольцо, содержащее от 1 до 6 атомов углерода в качестве членов цикла, причем остальные члены цикла выбраны из одного или более чем одного О, N или S. Предпочтительные 5-7-членные гетероциклоалкилы представляют собой 5- или 6-членные гетероциклоалкильные группы. Примеры 5-7- или 5- или 6-членных гетероциклоалкильных групп включают (не ограничиваясь ими) возможно замещенные пиперидинил, пиперазинил, гомопиперазинил, азепинил, пирролидинил, пиразолидинил, имидазолинил, имидазолидинил, пиридинил, пиридазинил, пиримидинил, оксазолидинил, изоксазолидинил, морфолинил, тиазолидинил, изотиазолидинил, хинуклидинил, хинолинил, изохинолинил, бензимидазолил, тиадиазолилидинил, бензотиазолидинил, бензоазолилидинил, дигидрофурил, тетрагидрофурил, дигидропиранил, тетрагидропиранил, тиоморфолинил, тиоморфолинилсульфоксид, тиоморфолинилсульфон, дигидрохинолинил, дигидроизохинолинил, тетрагидрохинолинил, тетрагидроизохинолинил, 1-оксо-тиоморфолин, 1,1-диоксотиоморфолин, 1,4-диазепан, 1,4-оксазепан, а также те, которые конкретно проиллюстрированы примерами, приведенными здесь ниже.
Соединения формулы (I) охвытывают следующие соединения формулы (I):

где R1 представляет собой 5- или 6-членный цикл соответственно формулы (II) или (III):
(II) 






(III) 



R2 представляет собой Н, С1-С7-алкил, С3-С6-циклоалкил или -(CH2)m-Ra;
R3 представляет собой арил или гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-C1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF3, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(CO)-С1-С7-алкил или -(CH2)m-Re;
R5 представляет собой С1-С7-алкил или С1-С7-апкил-С3-С6-циклоалкил; -(CH2)n-O-Rf, С3-С8-алкенил-О-Rf, -(CH2)n-NRgRh; -C2-C6-алкенил-NRgRh или -(CH2)n-Re;
Ra представляет собой -O-С1-С7-алкил или -ОН;
Rb представляет собой С1-С7-алкил, NH2 или -О-С1-С7-алкил;
Rc представляет собой -ОН, NH2 или NH-(CO)-O-C1-C7-алкил;
Rd представляет собой С1-С7-алкил, -NH2, -NH-C1-С7-алкил или -N-ди(С1-С7алкил);
Re представляет собой -ОН, -CH2F, -CHF2, -CF3 или -O-(СО)-С1-С7-алкил;
Rf представляет собой С1-С7-алкил, С3-С8-алкенил, С3-С6-циклоалкил, фенил, бензил или -(CO)-R';
Rg, Rh независимо представляют собой Н, С1-С7-алкил, С3-С6-циклоалкил, С3-С8-алкенил, фенил, бензил или -(CO)-R' или Rg и Rh могут также вместе с атомом азота, к которому они присоединены, образовать 5-7-членное гетероциклическое или гетероарильное кольцо, возможно замещенное 1 или 2 группами ОН;
R' представляет собой NH2, -NH-С1-С7-алкил, С1-С7-алкил или С1-С7-алкокси;
m имеет значение от 1 до 4;
n имеет значение от 2 до 6,
а также их фармацевтически приемлемые соли.
Также соединения формулы (I) охватывают следующие соединения формулы (Ia):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ia) по изобретению представляют собой те соединения, где
R2 представляет собой Н или C1-C7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(CO)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например гидрохлорид (1-метил-1Н-пиразол-3-ил)-амида 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ib):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (1b) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(CO)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше, а также их фармацевтически приемлемые соли, например гидрохлорид (2-метил-тиазол-4-ил)-амида 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ic):
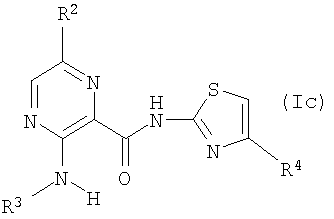
где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ic) по изобретению представляют собой те соединения, где
R2 представляет собой Н или C1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(CO)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например следующие соединения:
3-(3-фторфениламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амид;
3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида дигидрохлорид;
3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амид;
6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида гидрохлорид и
6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амид.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Id):

где R2, R3 и R5 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Id) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -О-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-C1-C7-алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R5 представляет собой С1-С7-алкил или С1-С7-алкил-С3-С6-циклоалкил; -(CH2)n-O-Rf, С3-С8-алкенил-О-Rf, -(CH2)n-NRgRh; -C2-С6-алкенил-NRgRh или -(CH2)n-Re;
Rb, Rc, Rd, Re, Rf, Rg, Rh, m и n являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например следующие соединения:
3-(5-фтор-пиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амид;
6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорид и
6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорид.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ie):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ie) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O2)-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(СН2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено в п.1,
а также их фармацевтически приемлемые соли.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (If):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (If) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-C1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-C1-C7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(CO)- С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ig):
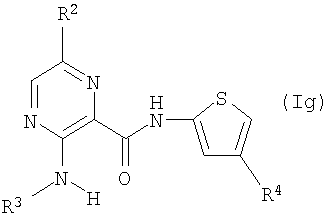
где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ig) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(СО)-Rb, -(CH2)m-Rc, -NH-(CO)- С1-С7-алкил; -O-CH2F, -O-CHF2, -O-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(СН2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ih):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ih) по изобретению представляют собой те соединения, где
R2 представляет собой Н или C1-C7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ii):

где R2, R3 и R4 являются такими, как определено выше. В этом воплощении R4 также может представлять собой Н.
В некоторых воплощениях соединения формулы (Ii) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например следующие соединения:
6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амида гидрохлорид и
6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амид.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ij):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ij) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например следующие соединения:
3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амид;
3-фениламино-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амид и 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амида гидрохлорид.
Далее, соединения, охваченные соединениями формулы (I), представляют собой следующие соединения формулы (Ik):

где R2, R3 и R4 являются такими, как определено выше.
В некоторых воплощениях соединения формулы (Ik) по изобретению представляют собой те соединения, где
R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой Н, фенил или 5- или 6-членный гетероарил, которые возможно замещены следующими заместителями:
CN, Cl, F, Br, CF3, CHF2 или -O-С1-С7-алкил, -(CO)-Rb, -(CH2)m-Rc, -NH-(CO)-С1-С7-алкил; -O-CH2F, -O-CHF2, -О-CF3, -S(O)2-Rd или гетероарил, который возможно замещен С1-С7-алкилом;
R4 представляет собой Н, -ОН, Cl, F, Br, CN, -CHF2, CF3, С1-С7-алкил, -O-(СО)-С1-С7-алкил или -(CH2)m-Re;
Rb, Rc, Rd, Re и m являются такими, как определено выше,
а также их фармацевтически приемлемые соли, например следующие соединения:
3-фениламино-пиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амид и 3-(5-хлор-пиридин-3-иламино)-6-метил-пиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амид.
Данное изобретение также охватывает способы получения соединений по изобретению.
Соединения формулы (I) могут быть получены согласно следующему способу по изобретению, который включает стадии взаимодействия аминозащищенного соединения или соединения со свободной аминогруппой формулы (IVa) или (IV):
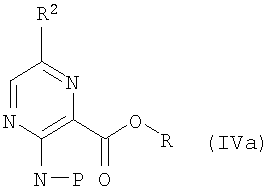

с соединением формулы (VIII):

и затем, при необходимости, снятия защиты с полученного соединения для получения соединения формулы (V):

после чего следует взаимодействие соединения формулы (V) с соединением формулы (IX):

для получения соединения формулы (I), где R1, R2 и R3 являются такими, как определено выше, Х представляет собой галоген, а R представляет собой алкил или аралкил (предпочтительно метил или этил).
Защитная группа может быть, например, карбаматной защитной группой, такой как трет-бутоксикарбонил (-ВОС), или бис-защищенным производным, таким как группа -(ВОС)2.
Соединения формулы (I) также могут быть получены согласно следующему способу по изобретению, который включает стадии взаимодействия соединения формулы (IV):

в реакции диазотирования с нитритом натрия (или нитритом алкила) в присутствии водной минеральной кислоты Н-Х, наконец, в присутствии соли меди (I) CuX с выходом соединения формулы (VI):

после чего следует взаимодействие соединения формулы (VI) с соединением формулы (VIII):

для получения соединения формулы (VII):

после чего следует взаимодействие соединения формулы (VII) с соединеним формулы (X):

для получения соединения формулы (I), где R1, R2 и R3 являются такими, как определено выше, Х представляет собой галоген, а R представляет собой алкил или аралкил (предпочтительно метил или этил).
Этот способ более подробно представлен на схеме I и в общей методике I далее.
Схема 1:
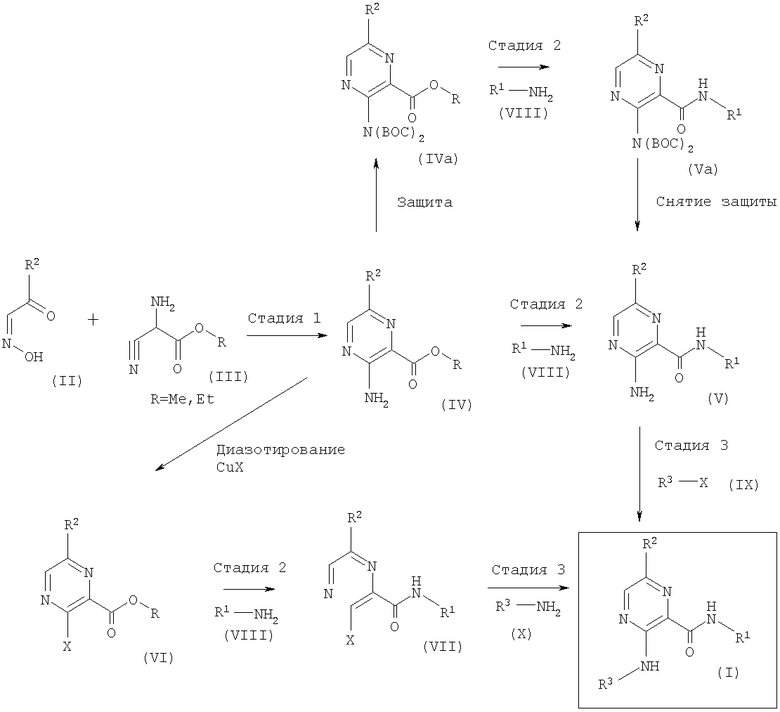
Общая методика I:
Стадия 1
Исходное вещество формулы (IV), где R2 = водород, имеется в продаже. Аналоги, в которых R2 = алкил, могут быть ситезированы путем конденсации соответствующего кетоальдегид-оксима (II) с эфиром амино-циано-уксусной кислоты (III) [J. Med. Chem 1997, 40, 2196-2210] в уксусной кислоте в течение ночи. Соединение формулы (IV) может быть выделено и очищено с помощью традиционных методов.
Стадия 2
К раствору соединения формулы (VIII) в растворителе (например, сухом диоксане) добавляют раствор триметилалюминия в гексане. Затем добавляют соединение формулы (IV), (IVa) или (VI). Соединения формулы (Va), (V) или (VII) могут быть выделены и очищены с помощью традиционных методов.
ВОС-Защита
Соединения формулы (IVa) могут быть получены путем перемешивания соединения формулы (IV) с ди-трет-бутилдикарбонатом и 4-(N,N-диметиламино)пиридином в кипящем дихлорметане с обратным холодильником. Соединение формулы (IVa) может быть выделено и очищено с помощью традиционных методов.
Снятие ВОС-защиты
Соединения формулы (V) могут быть получены путем перемешивания кислого раствора соединения формулы (VII) в подходящем растворителе (например, воде и/или этаноле). Соединение формулы (V) может быть выделено и очищено с помощью традиционных методов.
Стадия 3
Соединение формулы (I) может быть получено либо каталитизируемым сочетанием соединения формулы (V) с соединением формулы (IX), либо сочетанием соединения формулы (VII) с соединением формулы (X) с использованием, например, карбоната цезия, 4,5-бис(дифенилфосфино)-9,9-диметилксантена (Xanthphos) и комплекса три(дибензилиден-ацетон)дипапладия и хлороформа (Pd2(dba)3·CHCl3). Соединение формулы (I) затем может быть выделено и очищено с помощью традиционных методов. В некоторых случаях для соединения формулы (IX), где Х представляет собой атом хлора или фтора и R3 представляет собой гетероциклический остаток, возможно также выполнить стадию сочетания в отсутствие палладиевого катализатора с использованием карбоната цезия в ДМФА. Соединение формулы (I) затем может быть выделено и очищено с помощью традиционных методов.
Общая методика II:

Стадия 1
В качестве альтернативы соединение формулы (X) может быть получено с помощью катализируемого палладием сочетания соединения формулы (IV) с соединением формулы (IX), с использованием, например, карбоната цезия, 4,5-бис(дифенилфосфино)-9,9-диметилксантена (Xanthphos) и комплекса три(дибензилиден-ацетон)дипалладия и хлороформа (Pd2(dba)3·CHCl3). Соединение формулы (X) затем может быть выделено и очищено с помощью традиционных методов.
Стадия 2: ВОС-защита
Соединения формулы (XI) могут быть получены путем перемешивания соединения формулы (X) с ди-трет-бутилдикарбонатом и 4-(N,N-диметиламино)пиридином в кипящем дихлорметане с обратным холодильником. Соединение формулы (XI) может быть выделено и очищено с помощью традиционных методов.
Стадия 3: омыление
Соединения формулы (XII) могут быть получены путем перемешивания соединения формулы (XI) с водным раствором гидроксида лития в течение ночи при комнатной температуре с использованием смеси метанол/ТГФ в качестве сорастворителя. Соединение формулы (XII) может быть выделено и очищено с помощью традиционных методов.
Стадия 4
К раствору соединения формулы (XII), N,N-диизопропиламина и амина формулы (VIII) в растворителе (например, сухом ДМФА) добавляют агент сочетания (например, O-(бензотриазол-1-ил)-1,1,3,3-тетраметилурония тетрафторборат (TBTU)). После перемешивания в течение ночи при комнатной температуре соединение формулы (XIII) может быть выделено и очищено с помощью традиционных методов.
Стадия 5: снятие ВОС-защиты
Соединения формулы (I) могут быть получены путем перемешивания кислого раствора соединения формулы (VIII) в подходящем растворителе (например, воде и/или этаноле). Соединение формулы (I) может быть выделено и очищено с помощью традиционных методов.
Данное изобретение также охватывает лекарство, содержащее одно или более чем одно соединение по изобретению и фармацевтически приемлемые эксципиенты, для лечения и предупреждения заболеваний, опосредованных рецептором mGluR5, таких как острые и/или хронические неврологические нарушения, а также тревога, хроническая или острая боль, недержание мочи и ожирение.
Данное изобретение также охватывает применение соединений по изобретению для изготовления лекарства для лечения или предупреждения вышеуказанных заболеваний.
Фармацевтически приемлемые соли соединений формулы I могут быть легко получены согласно способам, которые известны сами по себе, и принимая во внимание природу соединения, которое собираются получить в солевой форме. Неорганические или органические кислоты, такие как, например, соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота или лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п., пригодны для образования фармацевтически приемлемых солей основного соединения формулы I. Соединения, которые содержат щелочные или щелочно-земельные металлы, например натрий, калий, кальций, магний или подобные, основные амины или основные аминокислоты, подходят для образования фармацевтически приемлемых солей кислотных соединений.
Как было указано выше, соединения формулы (I) и их фармацевтически приемлемые соли являются, как было указано выше, антагонистами метаботропных глутаматных рецепторов и могут быть использованы для лечения или предупреждения заболеваний, опосредованных рецепторами mGluR5, таких как острые и/или хронические неврологические нарушения, когнитивные нарушения и расстройства памяти, а также острая и хроническая боль. Неврологические нарушения, которые можно лечить, представляют собой, например, эпилепсию, шизофрению, тревогу, острые, травматические или хронические дегенеративные процессы в нервной системе, такие как болезнь Альцгеймера, старческое слабоумие, хорея Хантинггона, боковой амиотрофический склероз (ALS), рассеянный склероз, слабоумие, вызванное спидом, травмы глаз, ретинопатия, идиопатический паркинсонизм или лекарственный паркинсонизм, а также состояния, которые ведут к глутамат-недостаточным функциям, таким, например, как спазмы мышц, конвульсии, мигрени, недержание мочи, алкогольная зависимость, никотиновая зависимость, психозы, опиатная зависимость, тревога, рвота, дискенезия и депрессия. Другие состояния, которые можно лечить, представляют собой ограниченную функцию мозга, вызванную операциями шунтирования или трансплантациями, недостаточное мозговое кровоснабжение, травмы спинного мозга, травмы головы, гипоксию, вызванную беременностью, остановку сердца и гипогликемию. И далее: ограниченная функция мозга, ведущая к задержке умственного развития, из-за аномалий во время беременности, замедленное развитие мозга или генетические аномалии, такие как синдром ломкой Х-хромосомы (синдром Fragile-X), болезнь Дауна или заболевания аутического спектра, такие как синдром Каннера, общее расстройство психологического развития (pervasive developmental disorder (PDD)), синдром дефицита внимания (attention deficit disorder (ADD)), также являются возможными показаниями для лечения.
Соединения формулы 1 и их фармацевтически приемлемые соли особенно полезны в качестве аналгетиков. Болевые состояния, которые можно лечить, включают боль при воспалении, например артрит и ревматоидное заболевание, васкулит, невропатическую боль, такую как тройничную или герпетическую невралгию, диабетическую невропатическую боль, каузалгию, гипералгезию, сильную хроническую боль, постоперационную боль и боль, связанную с различными состояниями, таким как рак, стенокардия, почечные или печеночные колики, менструация, мигрень и подагра.
Фармакологическую активность соединений тестировали, используя следующий метод.
Для экспериментов по связыванию кДНК, кодирующей mGlu5a рецептор человека, временно трансфицировали клетки EBNA, используя процедуру, описанную Шлягером и Кристенсеном (Schlaeger, Christensen) [Cytotechnology 15:1-13 (1998)]. Гомогенат клеточных мембран хранили при -80°С до дня проведения эксперимента, когда их оттаивали и ресуспендировали и политронизировали в 15 мМ Tris-HCl, 120 мМ NaCl, 100 мМ KCl, 25 мМ CaCl2, 25 мМ MgCl2, связывающем буфере при рН 7,4 до конечной концентрации для анализа 20 мкг белка на лунку.
Изотермы насыщения определяли добавлением двенадцати концентраций [3H]MPEP (0,04-100 нМ) к этим мембранам (в общем объеме 200 мкл) в течение 1 ч при 4°С. Эксперименты по конкуренции осуществляли с фиксированной концентрацией [3H]МРЕР (2 нМ) и определяли величины ИК50 тестируемых соединений, используя 11 концентраций (0,3-10000 нМ). Инкубирование осуществляли в течение 1 ч при 4°С.
По окончании инкубации мембраны отфильтровывали на юнифильтре (96-луночный белый микропланшет со связанным GF/C фильтром предварительно инкубировали 1 ч в 0,1% PEI в буфере для промывки, Packard BioScience, Meriden, СТ) с харвестером Filtermate 96 (Packard BioScience) и промывали 3 раза холодным 50 мМ Tris-HCl, рН 7,4, буфером. Неспецифическое связывание измеряли в присутствии 10 мкМ МРЕР. Радиоактивность на фильтре подсчитывали (3 мин) на сцинтилляционном счетчике для микропланшетов Packard Top с коррекцией гашения после добавления 45 мкл микросцинта 40 (Canberra Packard S.A., Zürich, Switzerland) и покачивания в течение 20 мин.
Для функционального анализа осуществляли измерения [Са2+]i, как было описано ранее Портером с соавторами (Porter et al.) [Br. J. Pharmacol. 128:13-20 (1999)], на HEK-293 клетках с рекомбинантными рецепторами mGlu5a человека. Эти клетки насыщали красителем с помощью Fluo 4-AM (получен от FLUKA, конечная концентрация 0,2 мкМ). Измерения [Са2+]i осуществляли с использованием флуорометрического ридера для планшетов (FLIPR, Molecular Devices Corporation, La Jolla, CA, USA). Оценку антагониста осуществляли после 5 мин преинкубации с тестируемыми соединениями, за которой следовало добавление субмаксимального количества агониста.
Кривые ингибирования (антагонисты) подгоняли под четырехпараметрическое логистическое уравнение, задавая ИК50 и коэффициент Хилла с использованием программного обеспечения для итеративного нелинейного подбора кривых (Xcel fit).
Для экспериментов по связыванию задавали величины Ki тестируемых соединений. Величины Ki определяются следующей формулой:
Ki=ИК50/[1+L/Kd],
в которой величины ИК50 представляют собой концентрации тестируемых соединений, которые вызывают 50%-ное ингибирование конкурирующего радиолиганда ([3H]MPEP). L представляет собой концентрацию радиолиганда, используемого в экспериментах по связыванию, величина Kd радиолиганда определяется эмпирически для каждой партии приготовленных мембран.
Соединения по настоящему изобретению являются антагонистами рецепторов mGluR5a. Активности соединений формулы I, измеренные в описанном выше анализе, находятся в пределах Ki<4 мкМ и предпочтительно <150 нМ.
Соединения формулы I и их фармацевтически приемлемые соли могут быть использованы в качестве лекарств, например, в форме фрамацевтических препаратов. Фармацевтические препараты могут вводиться перорально, например, в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным также может быть ректальное введение, например, в форме суппозиториев или парентеральное, например, в форме растворов для инъекций.
Соединения формулы I и их фармацевтически приемлемые соли могут быть переработаны с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических препаратов. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. могут быть использованы, например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п.; в зависимости от природы активного вещества, однако, обычно для мягких желатиновых капсул не требуется никаких носителей. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п. Адъюванты, такие как спирты, полиолы, глицерин, растительные масла и т.п., могут быть использованы для водных инъекционных растворов водорастворимых солей соединений формулы I, но, как правило, не являются необходимыми. Подходящими носителями для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, корригенты, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать и другие терапевтически ценные вещества.
Как упоминалось ранее, лекарства, содержащие соединение формулы I или его фармацевтически приемлемые соли и терапевтически инертный эксципиент, также являются предметом данного изобретения, равно как и способ получения таких лекарств, при котором одно или более соединений формулы I или их фармацевтически приемлемых солей и, при желании, одно или более других терапевтически ценных веществ превращают в лекарственную форму вместе с одним или более чем одним терапевтически инертным носителем.
Дозировка может варьировать в широких пределах и, конечно, должна быть подобрана по индувидуальным потребностям в каждом конкретном случае. В общем, эффективная дозировка для перорального или парентерального введения находится в интервале 0,01-20 мг/кг/день, при дозировке 0,1-10 мг/кг/день, являющейся предпочтительной для всех описанных назначений. Суточная дозировка для взрослого человека весом 70 кг соответственно находится в интервале 0,7-1400 мг в день, предпочтительно между 7 и 700 мг в день.
Следующие примеры приводятся для дальнейшего пояснения изобретения, и подразумевается, что они не ограничивают изобретение до конкретных соединений, приведенных в примерах.
Пример 1
3-(Пиридин-3-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амид
Стадия 1: 3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты метиловый эфир
3-Аминопиразин-2-карбоновой кислоты метиловый эфир (0,8 г, 5,2 ммоль) и 3-бромпиридин (1,2 г, 7,8 ммоль) растворяли в 20 мл сухого толуола. Добавляли 4,5-бис(дифенилфосфино)-9,9-диметилксантен (0,6 г, 1,04 ммоль), трет-бутилат натрия (0,75 г, 7,8 ммоль) и комплекс три(дибензилиденацетон)дипалладия и хлороформа (0,54 г, 0,52 ммоль) и реакционную смесь перемешивали при микроволновом облучении в течение 60 минут при 150°С. Реакционную смесь затем выпаривали и очищали флэш-хроматографией на силикагеле (градиент гептан/этилацетат 1:2 -> 0:100). Желаемый продукт получали в виде коричневого твердого вещества (260 мг, 22%), MS: m/e=231,1 (M+H+).
Стадия 2: 3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (3-хлорфенил)-амид
3-Хлоранилин (140 мг, 1,1 ммоль) растворяли в 4 мл диоксана и добавляли 2М раствор триметилалюминия в гептане (0,55 мл, 1,1 ммоль). Раствор перемешивали в течение 1 ч при комнатной температуре и добавляли 3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты метиловый эфир (127 мг, 0.55 ммоль). Реакционную смесь перемешивали в течение 2 ч при 80°С, охлаждали и гасили 0,5 мл воды. Добавляли сульфат натрия, перемешивали в течение 10 минут, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан / этилацетат 1:2 -> 0:100) и желаемый продукт получали в виде желтого твердого вещества (13 мг, 7,2%), MS: m/e=326,2 (M+H+).
Пример 2
3-Фениламинопиразин-2-карбоновой кислоты (3-хлорфенил)-амид
Стадия 1: 3-фениламинопиразин-2-карбоновой кислоты метиловый эфир
Указанное в заголовке соединение, MS: m/e=230,3 (М+H+), выделяли в качестве сопутствующего продукта в примере 1, стадия 1.
Стадия 2: 3-фениламинопиразин-2-карбоновой кислоты (3-хлорфенил)-амид
Указанное в заголовке соединение, MS: m/e=325,1 (M+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-фениламинопиразин-2-карбоновой кислоты метилового эфира и 3-хлоранилина.
Пример 3
3-(5-Фторпиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амид
Стадия 1: 3-ди-(трет-бутоксикарбонил)аминопиразин-2-карбоновой кислоты метиловый эфир
3-Аминопиразин-2-карбоновой кислоты метиловый эфир (2,5 г, 16,3 ммоль), ди-трет-бутилдикарбонат (7,5 г, 34,4 ммоль) и 4-N,N-диметиламино)пиридин (0,1 г, 0,8 ммоль) растворяли в 100 мл дихлорметана и кипятили с обратным холодильником в течение 4 ч. Реакционную смесь охлаждали и экстрагировали насыщенным раствором NaHCO3 и этилацетатом. Органический экстракт сушили сульфатом натрия, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан / этилацетат 90:10 -> 1:1). Желаемое соединение получали в виде белого твердого вещества (4,7 г, 81%), MS: m/e=354,0 (M+H+).
Стадия 2: [3-(1-метил-1Н-пиразол-3-илкарбамоил)-пиразин-2-ил]-карбаминовой кислоты ди-трет-бутиловый эфир
Указанное в заголовке соединение, MS: m/e=219.2 (М+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-ди-(трет-бутоксикарбонил)амино-пиразин-2-карбоновой кислоты метилового эфира и 1-метил-1H-пиразол-3-иламина [Synthesis 1976, с.52].
Стадия 3: 3-аминопиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорид
[3-(1-Метил-1Н-пиразол-3-илкарбамоил)-пиразин-2-ил]-карбаминовой кислоты ди-трет-бутиловый эфир (0,65 г, 1,55 ммоль) растворяли в 10 мл этилацетата и добавляли 8М HCl в этаноле (3,9 мл, 31 ммоль). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре и затем разбавляли 20 мл диизопропилового эфира. Твердый материал отфильтровывали и сушили при 50°С и 15 мбар в течение 1 ч. Желаемое соединение получали в виде желтого твердого вещества (0,37 г, 94%), MS: m/e=219,3 (M+H+).
Стадия 4: 3-(5-фторпиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амид
3-Аминопиразин-2-карбоновой кислоты (1-метил-1 Н-пиразол-3-ил)-амида гидрохлорид (120 мг, 0,47 ммоль), 3,5-дифторпиридин (500 мг, 4,4 ммоль), карбонат цезия (610 мг, 1.89 ммоль) и 1 мл N,N-диметилформамида смешивали и перемешивали при микроволновом облучении в течение 60 минут при 180°С. Реакционную смесь экстрагировали насыщенным раствором NaHCO3 и трижды этилацетатом. Объединенные органические экстракты сушили сульфатом натрия, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан / этилацетат 90:10 -> 30:70). Желаемое соединение получали в виде желтого твердого вещества (24 мг, 16%), MS: m/e=314.0 (M+H+).
Пример 4
3-Фениламинопиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амид
Стадия 1: 3-бром-пиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амид
Указанное в заголовке соединение, MS: m/e=294,9 (M+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-бромпиразин-2-карбоновой кислоты метилового эфира (Пример А) и 2-метил-пиридин-4-иламина (Пример Б).
Стадия 2: 3-фениламинопиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амид
3-Бромпиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амид (130 мг, 0,44 ммоль) и анилин (54 мг, 0,58 ммоль) растворяли в 4 мл сухого диоксана. Добавляли 4,5-бис(дифенилфосфино)-9,9-диметилксантен (51 мг, 0,09 ммоль), карбонат цезия (290 мг, 0,89 ммоль) и комплекс три(дибензилиденацетон)дипалладия и хлороформа (46 мг, 0,044 ммоль), и реакционную смесь перемешивали при микроволновом облучении в течение 50 минут при 150°С. Реакционную смесь затем выпаривали и очищали флэш-хроматографией на силикагеле (гептан/этилацетат 1:1 -> 100% этилацетат). Желаемый продукт получали в виде желтого твердого вещества (47 мг, 35%), MS: m/e=306,2 (M+H+).
Пример 5
3-(5-Хлорпиридин-3-иламино)-6-метилпиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амид
Стадия 1: 3-бром-6-метилпиразин-2-карбоновой кислоты этиловый эфир
Смесь 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В) (2,0 г, 11 ммоль), 4 мл воды и 3,7 мл (33,1 ммоль) 48%-ной бромистоводородной кислоты охлаждали до 5°С. Добавляли по каплям 2,5М раствор NaNO2 в воде (5,3 мл, 13,2 ммоль) при 5°С (выделение N2!). Реакционную смесь перемешивали в течение 1 ч и затем выливали на смесь воды со льдом. Реакционную смесь нейтрализовали Na2CO3 и экстрагировали дважды этилацетатом (200 мл каждый раз). Объединенные органические экстракты сушили сульфатом натрия, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан/этилацетат 90:10 -> 50:50). Желаемое соединение получали в виде бесцветной жидкости (0,53 г, 20%), MS: m/e=245,1 (M+H+).
Стадия 2: 3-бром-6-метилпиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амид
Указанное в заголовке соединение, MS: m/e=307,2 (М+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-бром-6-метилпиразин-2-карбоновой кислоты этилового эфира и 2-метилпиридин-4-иламина (Пример Б).
Стадия: 3-(5-хлорпиридин-3-иламино)-6-метил-пиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амид
Указанное в заголовке соединение, MS: m/e=355,1 (M+H+), готовили в соответствии с общим способом по примеру 4, стадия 2, из 3-бром-6-метилпиразин-2-карбоновой кислоты (2-метилпиридин-4-ил)-амида и 5-хлорпиридин-3-амина.
Пример 6
3-(3-Фторфениламино)-пиразин-2-карбоновой кислоты (4-метилтиазол-2-ил)-амид
Стадия 1: 3-бром-пиразин-2-карбоновой кислоты (4-метилтиазол-2-ил)-амид
Указанное в заголовке соединение, MS: m/e=301,0 (M+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-бромпиразин-2-карбоновой кислоты метилового эфира (Пример А) и 2-амино-4-метилтиазола.
Стадия 2: 3-(3-фторфениламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амид
Указанное в заголовке соединение, MS: m/e=330,1 (M+H+), готовили в соответствии с общим способом по примеру 4, стадия 2, из 3-бромпиразин-2-карбоновой кислоты (4-метилтиазол-2-ил)-амида и 3-фторанилина.
Пример 7
3-(Пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метилтиазол-2-ил)-амида дигидрохлорид
Стадия 1: 3-(трет-бутоксикарбонилпиридин-3-ил-амино)-пиразин-2-карбоновой кислоты метиловый эфир
3-(Пиридин-3-иламино)-пиразин-2-карбоновой кислоты метиловый эфир (Пример 1, стадия 1) (245 мг, 1,06 ммоль), ди-трет-бутилдикарбонат (255 мг, 1,17 ммоль) и 4-(N,N-диметиламино)пиридин (7 мг, 0,05 ммоль) растворяли в 100 мл дихлорметана и кипятили с обратным холодильником в течение 2 ч. Реакционную смесь охлаждали и экстрагировали насыщенным раствором NaHCO3 и этилацетатом. Органический экстракт сушили сульфатом натрия, фильтровали и выпаривали. Желаемое соединение получали в виде коричневого масла (364 мг, >100%), MS: m/e=331,3 (M+H+), которое использовали на следующей стадии без дальнейшей очистки.
Стадия 2: 3-(трет-бутоксикарбонилпиридин-3-иламино)-пиразин-2-карбоновая кислота
3-(трет-Бутоксикарбонилпиридин-3-иламино)-пиразин-2-карбоновой кислоты метиловый эфир (364 мг, 1,1 ммоль) растворяли в 10 мл ТГФ. Добавляли 5 мл метанола, 5 мл воды и гидрат гидроксида лития (139 мг, 3,30 ммоль) и перемешивали в течение ночи при комнатной температуре. Органический растворитель выпаривали и остаток нейтрализовали 2н. раствором HCl. Смесь выпаривали досуха и использовали без дальнейшей очистки на следующей стадии [(405 мг, >100%), MS: m/e=315,2 (М+Н-)].
Стадия 3: [3-(4-метилтиазол-2-илкарбамоил)-пиразин-2-ил]-пиридин-3-ил-карбаминовой кислоты трет-бутиловый эфир
3-(трет-Бутоксикарбонил-пиридин-3-ил-амино)-пиразин-2-карбоновую кислоту (405 мг, 80%, 1,02 ммоль), 2-амино-4-метилтиазол (129 мг, 1,12 ммоль), N,N-диизопропилэтиламин (0,23 мл, 1,33 ммоль) и TBTU (430 мг, 1,33 ммоль) растворяли в 1 мл ДМФА и перемешивали в течение ночи при комнатной температуре. Реакционную смесь гасили водой и экстрагировали дважды этилацетатом. Органические экстракты промывали 2н. раствором NaOH, водой и рассолом, сушили сульфатом натрия, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан/этилацетат 90:10 - > 40:60). Желаемое соединение получали в виде желтой пены (195 мг, 46%), MS: m/e=413,3 (M+H+).
Стадия 4: 3-(Пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида дигидрохлорид
[3-(4-Метил-тиазол-2-илкарбамоил)-пиразин-2-ил]-пиридин-3-ил-карбаминовой кислоты mpem-бутиловый эфир (180 мг, 0,44 ммоль) растворяли в 5 мл этилацетата и добавляли 8М HCl в этаноле (2,2 мл, 17,6 ммоль). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре и затем разбавляли 20 мл диизопропилового эфира. Твердый материал отфильтровывали и сушили при 50°С и 15 мбар в течение 1 ч. Желаемое соединение получали в виде желтого твердого вещества (169 мг, 99%), MS: m/e=313,1 (M+H+).
Пример 8
3-(Пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амид
Стадия 1: 3-(Пиримидин-5-иламино)-пиразин-2-карбоновой кислоты метиловый эфир
Указанное в заголовке соединение, MS: m/e=232,1 (M+H+). готовили в соответствии с общим способом по примеру 4, стадия 2, из 3-аминопиразин-2-карбоновой кислоты метилового эфира и 5-бромпиримидина.
Стадия 2: 3-(Пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-а м ид
Указанное в заголовке соединение, MS: m/e=314,0 (M+H+), готовили в соответствии с общим способом по примеру 1, стадия 2, из 3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты метилового эфира и 2-амино-4-метилтиазола.
Пример 9
6-Метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амида гидрохлорид
Стадия 1: 6-Метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты этиловый эфир
3-Амино-6-метил-пиразин-2-карбоновой кислоты этиловый эфир (Пример В) (800 мг, 4,4 ммоль) и 3-иодпиридин (1,63 г, 8,0 ммоль) растворяли в 17 мл сухого диоксана. Добавляли 4,5-бис(дифенилфосфино)-9,9-диметилксантен (510 мг, 0,88 ммоль), карбонат цезия (2,30 г, 7,0 ммоль) и комплекс три(дибензилиденацетон)дипалладия и хлороформа (460 мг, 0,44 ммоль) и реакционную смесь перемешивали в течение 16 ч при 130°С. Реакционную смесь затем выпаривали и очищали флэш-хроматографией на силикагеле (гептан/этилацетат 9:1 -> гептан/этилацетат 1:2). Желаемый продукт получали в виде желтого масла (455 мг, 40%), MS: m/e=259,2 (M+H+).
Стадия 2: 3-(трет-Бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновой кислоты этиловый эфир
Указанное в заголовке соединение, MS: m/e=359,1 (M+H+), готовили в соответствии с общим способом по примеру 8, стадия 1, из этилового эфира 6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты.
Стадия 3: 3-(трелт-Бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновая кислота
Указанное в заголовке соединение, MS: m/e=329,1 (M+H+), готовили в соответствии с общим способом по примеру 8, стадия 2, из этилового эфира 3-(трет-бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновой кислоты.
Стадия 4: [3-(5-Фтор-пиридин-2-илкарбамоил)-5-метил-пиразин-2-ил]-пиридин-3-ил-карбаминовой кислоты трет-бутиловый эфир
Указанное в заголовке соединение, MS: m/e=425,2 (M+H+), готовили в соответствии с общим способом по примеру 8, стадия 3, из 3-(трет-бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновой кислоты и 2-амино-5-фторпиридина.
Стадия 5: 6-Метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=325,2 (М+H+), готовили в соответствии с общим способом по примеру 8, стадия 4, из [3-(5-фтор-пиридин-2-илкарбамоил)-5-метил-пиразин-2-ил]-пиридин-3-ил-карбаминовой кислоты трет-бутилового эфира.
Пример 10
6-Метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=327,1 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-(трет-бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновой кислоты и 2-амино-4-метилтиазола.
Пример 11
6-Метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=310,3 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-(трет-бутоксикарбонил-пиридин-3-ил-амино)-6-метил-пиразин-2-карбоновой кислоты и 1-метил-1Н-пиразол-3-иламина [Synthesis 1976, с.52].
Пример 12
6-Метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=341,2 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В), 5-бромпиримидина и 3-хлоранилина.
Пример 13
6-Метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амид
Указанное в заголовке соединение, MS: m/e=326,3 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В), 5-бромпиримидина и 2-амино-5-фторпиридина.
Пример 14
6-Метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=311,2 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В), 5-бромпиримидина и 1-метил-1Н-пиразол-3-иламина [Synthesis 1976, с.52].
Пример 15
6-Метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (2-метил-тиазол-4-ил)-амида гидрохлорид
Указанное в заголовке соединение, MS: m/e=328,1 (M+H+), готовили в соответствии с общим способом по примеру 10 из 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В), 5-бромпиримидина и 4-амино-2-метилтиазола (Пример Г).
Пример 16
6-Метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-а м ид
Указанное в заголовке соединение. MS: m/e=328,3 (М+Н+), готовили в соответствии с общим способом по примеру 10 из 3-амино-6-метил-пиразин-2-карбоновой кислоты этилового эфира (Пример В), 5-бромпиримидина и 2-амино-4-метилтиазола.
Синтез промежуточных соединений
Пример А
3-Бром-пиразин-2-карбоновой кислоты метиловый эфир
Указанное в заголовке соединение, MS: m/e=218,9 (М+Н+), готовили из метил 3-аминопиразин-2-карбоксилата по реакции Зандмейера, как описано в литературе.
Пример Б
2-Метил-пиридин-4-иламин
Указанное в заголовке соединение готовили гидрогенизацией N-оксида 4-нитро-2-пиколина, как описано в литературе.
Пример В
3-Амино-6-метил-пиразин-2-карбоновой кислоты этиловый эфир
Стадия 1: 3-Амино-6-метил-4-окси-пиразин-2-карбоновой кислоты этиловый эфир
Амино-циано-уксусной кислоты этиловый эфир (11,2 г, 87,3 ммоль) [J. Med. Chem 1997, 40, 2196-2210] растворяли в 50 мл уксусной кислоты и добавляли по каплям раствор пирувальдегид-1-оксима (10,4 г, 119,4 ммоль) в 50 мл уксусной кислоты при комнатной температуре (экзотермическая! -> охлаждение на ледяной бане). Темно-коричневую смесь перемешивали в течение ночи при комнатной температуре и гасили затем с помощью 100 мл воды. Реакционную смесь выпаривали и экстрагировали дважды водой (100 мл каждый раз) и трижды этилацетатом (200 мл каждый раз). Объединенные органические экстракты сушили сульфатом натрия, фильтровали и выпаривали. Сырой продукт очищали флэш-хроматографией на силикагеле (градиент гептан/этилацетат 90:10 -> 0:100). Желаемое соединение получали в виде желтого твердого вещества (7,1 г, 30%), MS: m/е=198,2 (M+H+).
Стадия 2: 3-Амино-6-метил-пиразин-2-карбоновой кислоты этиловый эфир
3-Амино-6-метил-4-окси-пиразин-2-карбоновой кислоты этиловый эфир (7,1 г, 36 ммоль) растворяли в 350 мл этанола и гидрогенизировали на никеле Ренея в течение 3 ч при комнатной температуре. Реакционную смесь фильтровали и выпаривали. Желаемый сырой продукт получали в виде светло-коричневого твердого вещества и использовали без какой-либо дальнейшей очистки на следующей стадии (6,6 г, 100%), MS: m/e=182,1 (M+H+).
Пример Г
4-Амино-2-метилтиазол
Указанное в заголовке соединение может быть получено в соответствии со способом, описанным в патенте ЕР 321115.
Приготовление Фармацевтических композиций, содержащих соединения по изобретению
Пример I
Таблетки следующего состава готовят традиционным способом:
мг/таблетка
Пример II
Таблетки следующего состава готовят традиционным способом:
мг/таблетка
Пример III
Готовят капсулы следующего состава:
мг/капсула
Активный ингредиент с подходящим размером частиц, кристаллическую лактозу и микрокристаллическую целлюлозу смешивают друг с другом до получения однородной смеси, просеивают и затем примешивают тальк и стеарат магния. Конечной смесью заполняют твердые желатиновые капсулы подходящего размера.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИДИН-2-КАРБОКСАМИДА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR5 | 2006 |
|
RU2411237C2 |
| ПИРИДИН- ИЛИ ПИРИМИДИН-2-КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2427580C2 |
| АЗОТОСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ГЕТЕРОАРИЛОВ | 2011 |
|
RU2559895C2 |
| БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ АЛЛОСТЕРИЧЕСКИХ ИНГИБИТОРОВ SHP2 | 2018 |
|
RU2776846C2 |
| ГЕТЕРОАРИЛЗАМЕЩЕННЫЕ АМИДЫ, СОДЕРЖАЩИЕ НАСЫЩЕННУЮ СВЯЗЫВАЮЩУЮ ГРУППУ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2006 |
|
RU2412181C2 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| ПРОИЗВОДНЫЕ БИПИПЕРИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2296751C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха | 2004 |
|
RU2346944C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2047604C1 |
| ПИРАЗОЛОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2539568C2 |
Данное изобретение относится к новым производным пиразин 2-карбоксамида общей формулы (I), где R1 представляет собой 5- или 6-членный цикл, имеющий формулы, опреденные в п.1 формулы изобретения, R2 представляет собой Н или С1-С7-алкил; R3 представляет собой фенил, пиридинил или пиримидинил, которые возможно замещены следующими заместителями: Cl, F или Br; R4 представляет собой Н, Cl, F, Br, CF3 или С1-С7-алкил; R5 представляет собой С1-С7-алкил, а также к их фармацевтически приемлемым солям. Предложенные соединения являются антагонистами метаботропных глутаматных рецепторов (mGluR5). Объектом изобретения также является лекарственное средство на основе предложенных соединений. 2 н. и 15 з.п. ф-лы.

1. Соединения общей формулы (I)

где R1 представляет собой 5- или 6-членный цикл соответственно формулы (II) или (III)
(II) 



(III) 


R2 представляет собой Н или С1-С7-алкил;
R3 представляет собой фенил, пиридинил или пиримидинил, которые возможно замещены следующими заместителями:
Cl, F или Br;
R4 представляет собой Н, Cl, F, Br, CF3 или С1-С7-алкил;
R5 представляет собой С1-С7-алкил;
а также их фармацевтически приемлемые соли.
2. Соединения формулы (Iа) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
3. Соединение формулы (I) по п.1, представляющее собой 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (1-метил-1H-пиразол-3-ил)-амида гидрохлорид.
4. Соединения формулы (Ib) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
5. Соединение формулы (Ib) по п.4, представляющее собой 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (2-метил-тиазол-4-ил)-амида гидрохлорид.
6. Соединения формулы (Ic) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
7. Соединения формулы (Iс) по п.6, выбранные из группы, состоящей из
3-(3-фтор-фениламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида
3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида дигидрохлорида;
3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида;
6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида гидрохлорида и
6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (4-метил-тиазол-2-ил)-амида.
8. Соединения формулы (Id) по п.1

где R2, R3 и R5 являются такими, как определено в п.1.
9. Соединения формулы (Id) по п.8, выбранные из группы, состоящей из
3-(5-фтор-пиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида;
6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорида и
6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (1-метил-1Н-пиразол-3-ил)-амида гидрохлорида.
10. Соединения формулы (Ii) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
11. Соединение формулы (Ii) по п.10, представляющее собой 6-метил-3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амида гидрохлорид или 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (5-фтор-пиридин-2-ил)-амид.
12. Соединения формулы (Ij) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
13. Соединения формулы (Ij) по п.12, выбранные из группы, состоящей из
3-(пиридин-3-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амида,
3-фениламино-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амид и 6-метил-3-(пиримидин-5-иламино)-пиразин-2-карбоновой кислоты (3-хлор-фенил)-амида гидрохлорида.
14. Соединения формулы (Ik) по п.1

где R2, R3 и R4 являются такими, как определено в п.1.
15. Соединения формулы (Ik) по п.14, выбранные из группы, состоящей из
3-фениламино-пиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амида и 3-(5-хлор-пиридин-3-иламино)-6-метил-пиразин-2-карбоновой кислоты (2-метил-пиридин-4-ил)-амида.
16. Соединение по любому из пп.1-15, а также его фармацевтически приемлемая соль для применения в ингибировании активности метаботропного глутаматного рецептора mGluR5.
17. Лекарственное средство, ингибирующее активность метаботропного глутаматного рецептора mGluR5, содержащее одно или более чем одно из соединений по пп.1-15, и фармацевтически приемлемые эксципиенты.
| FELDER, ERNST ET AL "Synthesis of 4(3H)-pteridinones", Journal of Medicinal Chemistry, 1972, 15(2), p.210-211 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ПРОИЗВОДНЫЕ ПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТАГОНИСТИЧЕСКИМ ДЕЙСТВИЕМ НА MGLU R ЧЕЛОВЕКА | 1998 |
|
RU2203889C2 |
Авторы
Даты
2010-12-27—Публикация
2006-03-02—Подача