Изобретение относится к онкологии и онкорадиологии и касается способа одномоментного пункционного чреспеченочного наружно-внутреннего дренирования желчных протоков с трепан-биопсией опухолей головки поджелудочной железы и дистального отдела холедоха и эндоскопической папиллосфинктеротомии большого дуоденального сосочка у больных механической желтухой злокачественного генеза.
В дожелтушном периоде заболевания протекают скрытно, и диагностировать рак головки поджелудочной железы и дистального отдела холедоха удается редко. Механическая желтуха встречается у 50-95% больных (Ю.И. Патютко, А.Г. Котельников, 2007, В.А. Кубышкин, В.А. Вишневский, 2007). Лечебно-диагностический алгоритм у данной группы больных представляет ряд последовательных действий, одними из звеньев которого являются пункционная трепан-биопсия и билиодуоденальное дренирование. Цитологическая диагностика путем браш-биопсии и пункционной аспирационной биопсии имеет ограничения и не позволяет получить 100% информативность о диагнозе, и не дает ответ по гистологической структуре опухоли.
Существует несколько способов выполнения трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха.
Известна пункционная биопсия под контролем эндоскопического ультразвукового исследования (ЭндоУЗИ). (Солодинина Е.Н., 2016 //Эндоскопическое ультразвуковое исследование в диагностике хирургических заболеваний органов панкреатобилиарной зоны.// Диссертация на соискание ученой степени доктора медицинских наук). Способ выполнения пункции включает несколько этапов. Первым этапом выбирается место пункции с учетом близости объекта к датчику эхоэндоскопа, отсутствия интерпозиции сосудов и протоков между датчиком и образованием. Затем производятся позиционирование аппарата так, чтобы очаговое образование находилось в зоне доступной для проведения пункционной иглы. Размер этой зоны зависит от степени изменения угла выходящей из аппарата иглы, что определяется ее смещением при помощи подъемника. Например, в аппаратах фирмы Fujinon данная зона представляет собой сектор с угловым размером около 25°, располагающийся в центральной части экрана и размеченный на экране двумя пунктирными линиями, точкой на экране показано примерное место выхода иглы в плоскость сканирования. После правильного позиционирования объекта на экране эхоэндоскопа в биопсийный канал проводится пункционная игла и фиксируется в нем специальным винтовым разъемом на рукоятке иглы. Затем освобождается нижний фиксатор на рукоятке иглы и внешняя оболочка иглы проводится к выходу из биопсийного канала, что контролируется ее появлением на ультразвуковом экране или визуально по эндоскопическому изображению, фиксатор затягивается. Следующим этапом рекомендуется установка верхнего фиксатора в положение, определяющее глубину пункции по нанесенной на рукоятке иглы шкале, или установку максимальной глубины пункции (8 см) и выполнение манипуляции, ориентируясь на тактильные ощущения и визуализацию иглы на ультразвуковом мониторе. Это связано с тем, что при пункциях, особенно в положении аппарата на длинной петле, игла пружинит в биопсийном канале и устанавливаемое на основании ультразвуковой визуализации расстояние до объекта не всегда соответствует расстоянию, которое надо пройти кончику иглы для достижения заданной точки. После освобождения верхнего фиксатора стилет иглы подтягивается на 0,5-0,6 мм и производится пункция образования под ультразвуковым контролем. После позиционирования иглы внутри новообразования, стилет сначала полностью проводится в просвет иглы с целью удаления из ее просвета клеток стенки полого органа и неизмененной паренхимы поджелудочной железы, попавших в нее при пункции. Затем стилет извлекается. Вакуумная аспирация специальными шприцами используем только при повторной пункции плотных образований, если первая пункция не позволила получить достаточное количество клеточного материала. Обычно используется однократная пункция с 8-10 возвратно-поступательными движениями иглы внутри образования при одновременном изменении угла пункции с помощью подъемника эндоскопа - так называемая «веерная техника». Затем визуально оценивается на стекле количество и качество полученного материала. Если материала недостаточно, выполняется вторая, а при необходимости и третья пункции.
Недостатком способа является то, что получаемый материал чаще цитологический, а способ получения материала с помощью тонкоигольного биопсийного форцепта под контролем эндосонографии обладает более низкой чувствительностью по сравнению с тонкоигольной аспирационной биопсией и высоким процентом осложнений в виде кровотечения. (Е.Р. Двойникова, К.В. Стегний и др. 2018, Солодинина Е.Н., 2016). Билиодуоденальное дренирование не является этапом биопсии, а его одномоментное выполнение несет в себе дополнительные риски осложнений. В лечебно-диагностические процедуру вовлекается большее количество медицинского персонала, что снижает эффективность работы всего лечебного учреждения. Техническая сложность проведения исследования после резекции желудка, гастрэктомии, значительная оператор-зависимость.
Известен также антеградный способ получения морфологического материала (Кулезнева Ю.М., Чрескожные вмешательства в абдоминальной хирургии, М.: Издательская группа «ГЭОТАР-Медиа», 2016, с. 105-107). Для выполнения этих вмешательств необходимо установить интродьюсер, через который можно провести холангиоскоп, биопсийный щипцы, биопсийную щеточку, внутрипросветный УЗ-датчик.
Стандартный интродьюсер устанавливают на длинном буже, с которого его потом сталкивают после того, как рентгеноконтрастная метка оказалась в просвете протока. Стандартный интродьюсер представляет собой пластиковую трубку со «срезанным» дистальным кончиком, на который нанесена рентгеноконтрастная метка; на проксимальном кончике располагается силиконовый клапан, не позволяющий жидкости вытекать из просвета протока, и боковой канал с краником для введения контрастного вещества. Интродьюсер обеспечивает герметичность транспеченочного канала, исключая возможность подтекания желчи и крови в брюшную полость и уменьшая риск повреждения капсулы печени, а также создает необходимый упор при последующем проведении инструментария через стриктуру. Размер интродьюсера зависит от диаметра проводимого инструментария. Для биопсии достаточно будет выбрать интродьюсер 8-10 Fr, для холангиоскопии - от 14 до 22 Fr. Браш-биопсию с помощью щеточки осуществляют под одновременным контролем холангиоскопии и рентгеноскопии для уменьшения риска перфорации стенки протока и только если у больного перед этим некоторое время функционировал наружно-внутренний дренаж, то есть уже был сформирован канал через область стриктуры. Это позволяет снизить травматичность манипуляции. Получение морфологического материала биопсийными щипцами проводят под рентгеноскопическим контролем с дополнительным визуальным контролм посредством холангиоскопа. Для щипцовой биопсии выполняют частичное бужирование стриктуры, после чего дистальный кончик интродьюсера устанавливают непосредственно в зоне сужения протока. По каналу интродьюсера щипцы проводят в закрытом состоянии. Интродьюсер подтягивают выше стриктуры, щипцы раскрывают и, прижимая их в раскрытом состоянии к стенке протока в области стриктуры, пытаются захватить кусочек ткани под постоянным рентгеноскопическим контролем. Обычно это проще сделать у верхнего края стриктуры. После закрытия щипцов их втягивают обратно в интродьюсер и извлекают. В случае отсутствия материала в щипцах манипуляцию повторяют. Но важно помнить, что это достаточно травматичная процедура, связанная с риском повреждения капсулы печени, перфорации стенки желчного протока и кровотечения из области стриктуры. Поэтому число попыток должно быть не более двух-трех, их необходимо выполнять крайне аккуратно и только под общим обезболиванием. Одним из вариантов может быть соскоб материала с баллона после баллонной дилатации стриктуры.
Недостатком этого способа является то, что данное вмешательство является сложным, в определенной степени травматичным и требует двойного визуального контроля (рентгенологического и холангиоскопического), что в свою очередь влечет за собой необходимость создания небезопасного (в плане кровотечения и желчеистечения) широкого транспеченочного канала, требующего дальнейшем установки чреспеченочного желчного дренажа большого диаметра. Это усилит болевой синдром, обусловленный механическим воздействием на межреберный нерв, так как в большинстве случаев пункционный транспеченочный канал проходит через межреберье и удлиняет время оперативного лечения. Взятие морфологического материала ограничивается только проксимальным отделом стриктуры, что в случае не информативности требует повторные биопсии, увеличивающие риск хирургических осложнений и диссеминации опухоли, и развития не только локального, но и общего инфекционного процесса. В дальнейшем требуется поэтапное удаление желчного дренажа с постепенным уменьшением его диаметра. Все это удлиняет время диагностических и лечебных мероприятий.
Наиболее близким к предлагаемому изобретению является способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха патент на изобретение №2722655. Для выполнения этого вмешательства больному вводят металлический сверхжесткий проводник типа Lunderquist по чрескожному пункционному каналу паренхимы печени через гепатикохоледох в двенадцатиперстную кишку (ДНК). При этом, в ДПК заводят всю мягкую часть проводника и дистальный конец его жесткой части, что позволяет сохранить прямолинейную ось холедоха. По металлическому проводнику, установленному в рабочий канал, устройство для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха заводят в гепатикохоледох, тем самым бужируют пункционный канал печени. Далее дистальный конец максимально заводят сквозь зону опухолевого сужения по истинному просвету холедоха, расширив его, таким образом, чтобы внутреннее отверстие пункционного канала достигло проксимальной части опухолевого стеноза. Направление и глубину пункции выбирают исходя из предоперационного анализа КТ и МРТ. Направление пункции устанавливают вращением устройства вокруг оси проводника. Выполняют трепан-биопсию с помощью биопсийной иглы. Для профилактики гематогенного и имплантационного метастазирования после пункции вводят противоопухолевые препараты в просвет гепатикохоледоха. Выполняют чрескожное чреспеченочное наружно-внутреннее дренирование желчных протоков, обеспечивая сдавление пункционного канала опухоли и препятствуя кровотечению.
Недостатком данного способа является то, что вмешательство заканчивается наружно-внутренним дренированием желчных протоков, что при сохраненной целостности большого дуоденального сосочка несет риски острого панкреатита. (Кабанов М.Ю., патент на изобретение №2712008, дата опубликования 23.01.2020) // Способ выполнения чрескожного чреспеченочного дренирующего вмешательства у больных механической желтухой).
Цель изобретения - создание максимально безопасного способа получения гистологического материала из разных мест опухолей головки поджелудочной железы и дистального отдела холедоха с одномоментным билиодуоденальным дренированием при сохранении его эффективности.
Поставленная цель достигается тем, что больному вводят металлический сверхжесткий проводник [3] типа Lunderquist (Фиг. 1) по чрескожному пункционному каналу паренхимы печени через гепатикохоледох в двенадцатиперстную кишку (ДПК). При этом, в ДПК заводят всю мягкую часть проводника и дистальный конец его жесткой части, что позволяет сохранить прямолинейную ось холедоха. По металлическому проводнику [3], установленному в рабочий канал [2], устройство заводят в гепатикохоледох, тем самым бужируют пункционный канал печени. Далее дистальный конец [7] максимально заводят сквозь зону опухолевого сужения по истинному просвету холедоха, расширив его, таким образом, чтобы внутреннее отверстие пункционного канала [4] достигло проксимальной части опухолевого стеноза. Направление и глубину пункции выбирают исходя из предоперационного анализа КТ и МРТ. Направление пункции устанавливают вращением устройства вокруг оси проводника [3]. Выполняют трепан-биопсию с помощью биопсийной иглы. Дистальный конец [7] устройства, обтурировав истинный просвет холедоха в зоне опухоли, препятствует возможности «соскальзывания» пункционной иглы [5] в просвет холедоха, повышая эффективность пункции. Для профилактики гематогенного и имплантационного метастазирования после пункции вводят противоопухолевые препараты в просвет гепатикохоледоха.
Далее по металлическому проводнику [3], проведенному транспапиллярно в двенадцатиперстную кишку в дистальном направлении заводят наружно-внутренний желчный дренаж. При этом становится легко доступной для визуализации и вмешательства верхняя стенка большого дуоденального сосочка. С помощью видео или фибродуоденоскопа с использованием игольчатого (торцевого) папиллотома выполняют рассечение большого дуоденального сосочка. В большинстве случаев необходимости пересечения сфинктерного аппарата не возникает. Материал, из которого выполнен наружно-внутренний желчный дренаж (полиуретан, полихлорвинил) не является токопроводящим, что исключает риск электрического повреждения тканей на протяжении. Наружно-внутренний дренаж желчных протоков позиционируют под рентгеноскопическим контролем и фиксируют, обеспечивая сдавление пункционного канала опухоли и препятствуя кровотечению.
Для пояснения способа прилагаем фиг.1 и фиг.2.
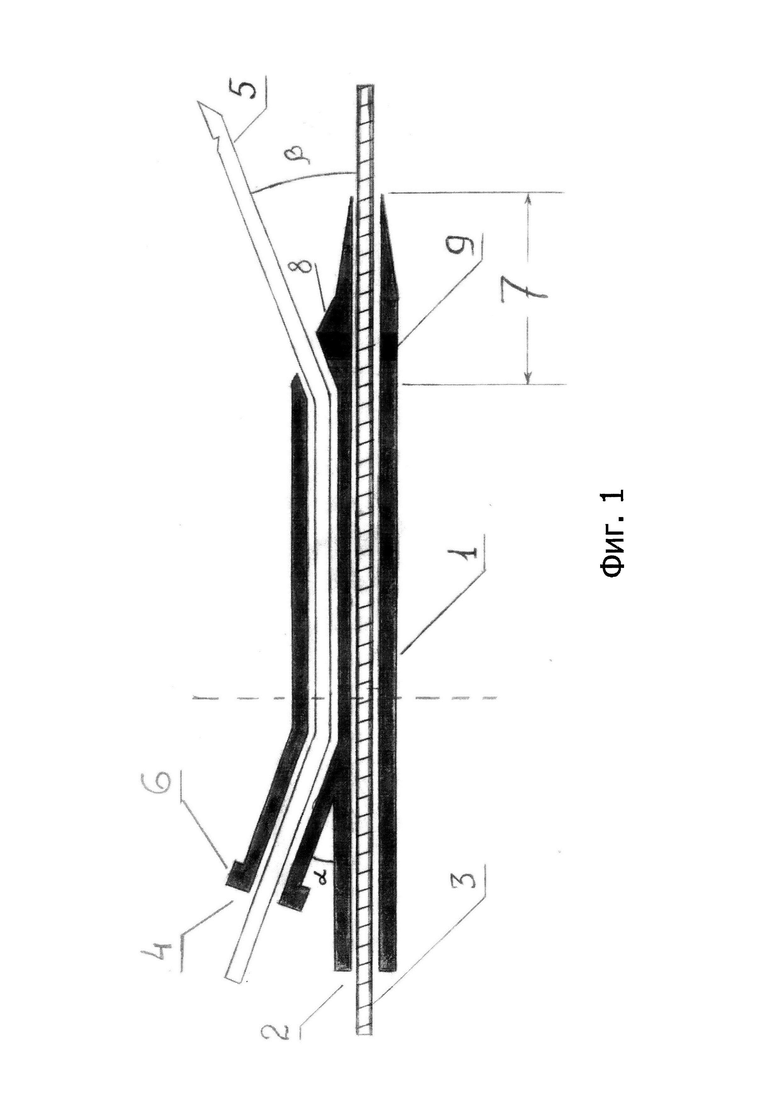
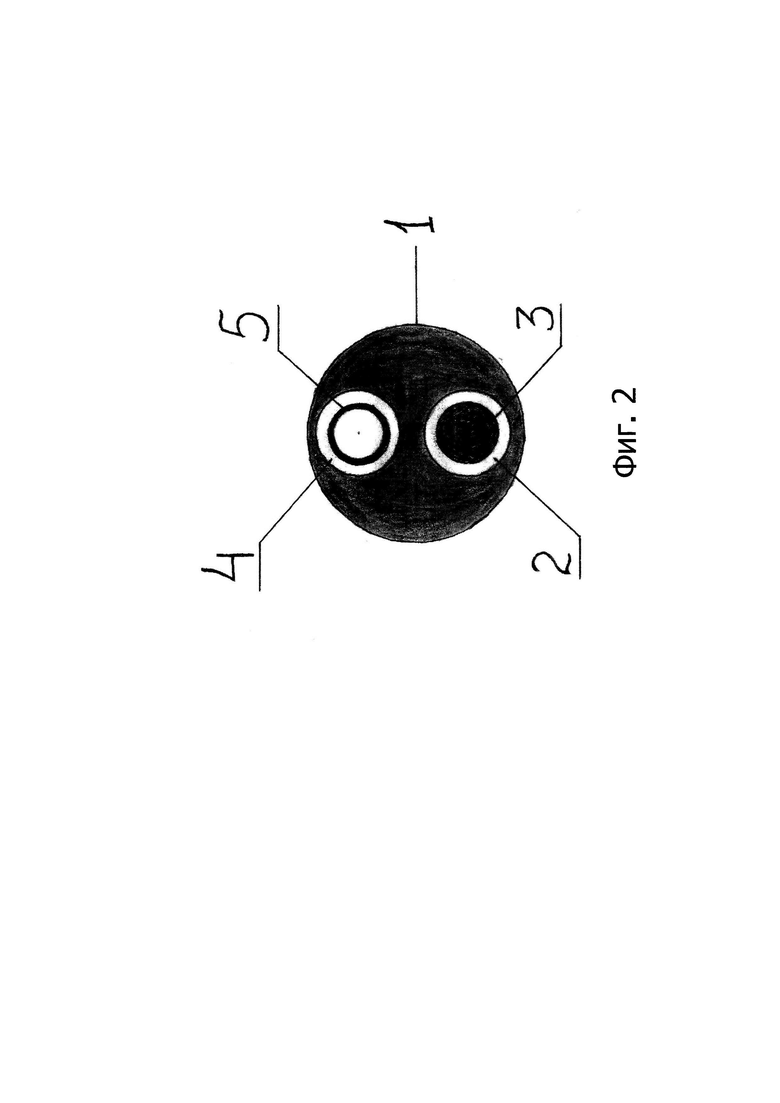
На фиг.1 изображено устройство для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха, состоящее из пластиковой полимерной трубки [1], которая имеет два канала: канал [2] для проведения металлического проводника [3], канал [4] для пункционной иглы [5]. На фиг.2 изображено данное устройство в поперечном сечении в отделе, обозначенном на фиг.1 пунктирной линией. Проксимальные концы каналов [2] и [4] неподвижно зафиксированы относительно друг друга под углом α=20-40°, что обеспечивает удобство работы с устройством. А именно: упрощает доступ к пункционному каналу [4] при заведении пункционной иглы [5]; облегчает вращение устройства вокруг оси проводника [3], тем самым, изменяя направление пункции; контроль положения проксимальных концов [2] и [4] позволяет определять направление пункции. Проксимальный конец пункционного канала [4] имеет коннектор [6] для шприца типа «ЛУЕР/ЛУЕР-ЛОК», что обеспечивает возможность выполнения по ходу оперативного вмешательства холангиографии. Дистальный конец устройства [7] имеет форму усеченного конуса, обеспечивая устройству более легкое прохождение по пункционному транспеченочному каналу с бужирующим эффектом. Между осью внутреннего конца пункционной иглы [5] и осью металлического проводника [3] имеется угол β=5-30°, образуемый за счет выступа [8] в дистальном отделе пункционного канала [4], обеспечивающий безопасное осевое отклонение пункционной иглы при выполнении трепан-биопсии. На уровне внутреннего отверстия пункционного канала [4] расположена рентгеноконтрастная метка [9], которая позволяет контролировать пункционную иглу при повторных ее заведениях с целью взятия биоптатов из разных мест.
Новизна способа заключается в том, что при заборе гистологического материала с помощью игл пункционным транспеченочным холангиостомическим доступом с возможностью выбора глубины и одномоментным бужированием транспеченочного пункционного канала и зоны окклюзии опухолью, сопровождающийся наружно-внутренним дренированием желчных протоков, одномоментно выполняют эндоскопическую папиллосфинктеротомию большого дуоденального сосочка.
Преимущество способа заключается в том, что при сохранении высокой эффективности забора гистологического материала только под рентгенологическим контролем со 100% информативностью при простоте выполнения вмешательства одним хирургом, проводится профилактика острого послеоперационного панкреатита. Одномоментное выполнение чрескожного и эндоскопического этапов операции позволяет ограничиться одним обезболиванием, снизить рентгенологическую нагрузку на пациента и медицинский персонал (эндоскопический этап выполняется только под видеоконтролем), снизить вероятность послеоперационных осложнений, уменьшить сроки стационарного лечения больного.
Пример конкретного выполнения.
Больная К., 1945 года рождения, госпитализирована в хирургическое отделение Клинической больницы СОГМА с диагнозом: Рак дистального отдела холедоха. T2NXM0. Механическая желтуха тяжелой степени. ИБС. ПИКС (неизвестной давности). Гипертоническая болезнь 3 степени, риск 4. ХСН1.
Из обследований: Биохимический анализ крови - Глюкоза - 3,76 ммоль/л; Мочевина - 6,91 ммоль/л; Креатинин - 94,9 мкмоль/л; Общий Билирубин - 432,27 мкмоль/л, АЛТ - 54,85; ACT - 48,02; Общий белок - 89,2 г/л; ПТИ - 62; Фибриноген - 3,1; МНО - 1,58. Анализ крови на гепатиты В и С: отрицательный. КТ органов брюшной полости: Полученные МСКТ более соответствуют признакам рака дистального отдела холедоха. Билиарная гипертензия.
В срочном порядке 17.10.2019 года больной выполнено оперативное вмешательство в объеме: «Чрескожное чреспеченочное наружно-внутреннее дренирование желчных протоков с одномоментной пункционной трепан-биопсией опухоли дистального отдела холедоха и эндоскопической папиллосфинктеротомией большого дуоденального сосочка». Пункционная трепан-биопсия выполнена трансхолангиостомическим доступом с помощью оригинального устройства (патент на изобретение №2722655, заявка на изобретение №2019114525 от 13.05.2019). Послеоперационный период протекал без осложнений.
Цитологическое исследование: в двух полях зрения определяются небольшие скопления клеток овальной и цилиндрической формы с эксцентрично расположенными ядрами. Больше данных за опухолевый процесс.
Патогистологическое заключение: микроскопическая картина холангиоцеллюлярной аденокарциномы.
Патогистологическое заключение (биопсия большого дуоденального сосочка): единичный фокус со строением аденомы с интраэпителиальной неоплазией низкой степени.
Вторым этапом 28.11.2019 года больной выполнено радикальное оперативное лечение в объеме: Гастропанреатодуоденальная резекция.
Патогистологическое заключение:
Холангиоцеллюлярная аденокарцинома G2 холедоха с инвазией в ткань поджелудочной железы, без прорастания в двенадцатиперстную кишку, удаленная в пределах здоровой ткани. Холангиоцеллюлярная аденокарцинома G1 желчного пузыря с инвазией в собственную пластинку слизистой, удаленная в пределах здоровой ткани. В удаленных лимфоузлах опухолевого роста не выявлено.
Послеоперационный период без осложнений.
Заключительный диагноз: Первично-множественный синхронный опухолевый процесс. Рак дистального отдела холедоха T2aN0M0 StII. Рак желчного пузыря T1bN0M0 StI. ИБС. ПИКС (неизвестной давности). Гипертоническая болезнь 3 степени, риск 4. ХСН1.
Простота и безопасность способа делает его экономически более выгодным и безопасным, значительно сокращая сроки стационарного лечения больного.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЙ СПОСОБ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С АНТЕГРАДНОЙ ПАПИЛЛОСФИНКТЕРОТОМИЕЙ И БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2021 |
|
RU2768480C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ МОРФОЛОГИЧЕСКОЙ ВЕРИФИКАЦИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2022 |
|
RU2793842C1 |
| Способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха и устройство для его осуществления | 2019 |
|
RU2722655C1 |
| УСТРОЙСТВО ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2021 |
|
RU2792248C1 |
| ИГЛА ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА | 2020 |
|
RU2771798C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ НЕФУНКЦИОНИРУЮЩЕГО ПЛАСТИКОВОГО БИЛИАРНОГО СТЕНТА ИЗ ЖЕЛЧНЫХ ПРОТОКОВ | 2017 |
|
RU2665622C1 |
| Насадка на автоматическую биопсийную систему | 2020 |
|
RU2753387C1 |
| ПОЛУАВТОМАТИЧЕСКАЯ ИГЛА ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА | 2020 |
|
RU2738627C1 |
| Способ чрескожной чреспеченочной щипковой внутрипротоковой биопсии | 2022 |
|
RU2798679C1 |
| Способ чрескожной чреспеченочной щипцовой внутрипротоковой биопсии | 2018 |
|
RU2701750C1 |
Изобретение относится к медицине, а именно к онкологии и онкорадиологии. Проводят металлический проводник сквозь опухолевый стеноз по истинному просвету холедоха. Осуществляют забор материала для гистологического исследования из разных мест опухолей головки поджелудочной железы и дистального отдела холедоха. Одномоментно выполняют чрескожное пункционное наружно-внутреннее дренирование желчных протоков и эндоскопическую папиллосфинктеротомию большого дуоденального сосочка. Способ позволяет ограничиться одним обезболиванием, снизить рентгенологическую нагрузку на пациента и медицинский персонал, снизить вероятность послеоперационных осложнений, уменьшить сроки стационарного лечения больного. 2 ил., 1 пр.
Комбинированный способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха с билиодуоденальным дренированием, включающий транспеченочный пункционный доступ к желчным протокам, выполняемый под рентгеноскопическим контролем с возможностью выполнения холангиографии, осуществляемый с проведением металлического проводника сквозь опухолевый стеноз по истинному просвету холедоха и забором материала для гистологического исследования из разных мест с одномоментным бужированием транспеченочного пункционного канала и зоны окклюзии опухолью и наружно-внутренним дренированием желчных протоков, отличающийся тем, что одномоментно выполняют чрескожное пункционное наружно-внутреннее дренирование желчных протоков с трепан-биопсией опухолей головки поджелудочной железы и дистального отдела холедоха и эндоскопическую папиллосфинктеротомию большого дуоденального сосочка.
| Способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха и устройство для его осуществления | 2019 |
|
RU2722655C1 |
| СПОСОБ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ ЖЕЛЧНЫХ ПРОТОКОВ | 2015 |
|
RU2579621C1 |
| US 20110213270 A1, 01.09.2011 | |||
| CN 104173077 A, 03.12.2014 | |||
| АЛЕКСЕЙЦЕВ А.В | |||
| Антеградная эндобилиарная щипцовая биопсия под рентгенологическим контролем при диагностике заболеваний органов панкреатодуоденальной зоны, осложненных механической желтухой, диссер.на соиск.уч.ст.к.м.н., Екатеринбург, | |||
Авторы
Даты
2021-05-11—Публикация
2020-08-19—Подача