Изобретение относится к хирургии, онкологии и онкорадиологии и касается способа и устройства пункционной трепан-биопсии опухолей головки поджелудочной железы (ГПЖ) и дистального отдела холедоха (ДОХ) с механической желтухой при одномоментном бужировании пункционного канала печени и области опухолевой стриктуры, позволяющей определить тактику и объем лечения этой тяжелой категории больных.
В дожелтушном периоде заболевания протекают скрытно, и диагностировать рак ГПЖ и ДОХ удается редко. Механическая желтуха встречается у 50-95% больных (Ю.И. Патютко, А.Г. Котельников, 2007, В.А. Кубышкин, В.А. Вишневский, 2007). Лечебно-диагностический алгоритм у данной группы больных представляет ряд последовательных действий, одним из звеньев которого является пункционная трепан-биопсия. Цитологическая диагностика путем браш-биопсии и пункционной аспирационной биопсии имеет ограничения и не позволяет получить 100% информативность о диагнозе, и не дает ответ по гистологической структуре опухоли.
Существует несколько способов выполнения трепан-биопсии опухолей ГПЖ и ДОХ с использованием различных устройств.
Известен чрескожный трансгастральный способ, который предполагает выполнение трепан-биопсии под ультразвуковой навигацией. (Кулезнева Ю.М., Чрескожные вмешательства в абдоминальной хирургии, М.: Издательская группа «ГЭОТАР-Медиа», 2016, с. 23-30). Биопсийная игла, совместимая с многоразовой биопсийной системой или одноразовая полуавтоматическая биопсийная игла под ультразвуковой навигацией в режиме реального времени проводится сквозь переднюю брюшную стенку, переднюю и заднюю стенки желудка и далее в ГПЖ. Если используется полуавтоматическая игла, то она подводится в периферический отдел образования по верхнему контуру. Далее выдвигается внутренняя канюля с «окошком» по направлению к центру патологического очага и нажимается педаль пружинного устройства иглы. С помощью пружинного механизма внутренняя канюля с кусочком ткани мгновенно втягивается в канал основной иглы. После этого игла извлекается. Канюлю снова выдвигается, полученный материал помещается в раствор формалина и направляется на исследование. При пункции с помощью пистолета кончик взведенной иглы подводят к краю патологического образования и нажимают на спусковой механизм. Длину «окошка», т.е. глубину забора ткани (от 10 до 20 мм) выбирают в зависимости от размеров образования. Для получения полноценного гистологического материала целесообразно использовать иглы диаметром не менее 18G (допустимо 16-20G).
Недостатком данного способа является то, что не все опухоли этой локализации, в том числе размером до 2 см, визуализируются при ультразвуковом исследовании (УЗИ). Информативность данного метода составляет от 57 до 98% (Ю.И. Патютко. А.Г. Котельников, 2007). Существует опасность кровотечения из пункционного канала, повреждение органов брюшной полости, острого панкреатита. (Ю.В. Кулезнёва, 2016). Целевое попадание при однократной пункции, особенно для специалиста с небольшим опытом работы затруднено. Данный способ требует в послеоперационном периоде соблюдение постельного режима с оставлением назогастрального зонда.
Биопсийная игла состоит из канюли и стилета с биопсийной камерой («окошко»). В случае с полуавтоматической иглой, она еще дополняется упором для пальцев рук хирурга и плунжером для продвижения стилета и спуска биопсийного механизма. В случае с иглами к автоматической биопсийной системе они дополняются коннектором для шприца ЛУЕР/ЛУЕР-ЛОК, спейсером для установки и контроля, отверстиями втулок, и сантиметровой разметкой. В качестве примера автоматической биопсийной системы используют многоразовое пружинное устройство для толстоигольной биопсии «BARD MAGNUM», которое состоит из корпуса, крышки, регулятора глубины проникновения 15 или 22 мм, пружины, обеспечивающей высокую скорость введения иглы и качественный забор биоптата, стойки салазок опоры для фиксации иглы, предохранителя, исключающего возможность случайного выстрела, индикатора готовности системы и пускового механизма.
Известна также пункционная биопсия под контролем эндоскопического ультразвукового исследования (ЭндоУЗИ). (Солодинина Е.Н., 2016 //Эндоскопическое ультразвуковое исследование в диагностике хирургических заболеваний органов панкреатобилиарной зоны.// Диссертация на соискание ученой степени доктора медицинских наук). Способ выполнения пункции включает несколько этапов. Первым этапом выбирается место пункции с учетом близости объекта к датчику эхоэндоскопа, отсутствия интерпозиции сосудов и протоков между датчиком и образованием. Затем производится позиционирование аппарата так, чтобы очаговое образование находилось в зоне доступной для проведения пункционной иглы. Размер этой зоны зависит от степени изменения угла выходящей из аппарата иглы, что определяется ее смещением при помощи подъемника. Например, в аппаратах фирмы Fujinon данная зона представляет собой сектор с угловым размером около 25°, располагающийся в центральной части экрана и размеченный на экране двумя пунктирными линиями, точкой на экране показано примерное место выхода иглы в плоскость сканирования. После правильного позиционирования объекта на экране эхоэндоскопа в биопсийный канал проводится пункционная игла и фиксируется в нем специальным винтовым разъемом на рукоятке иглы. Затем освобождается нижний фиксатор на рукоятке иглы и внешняя оболочка иглы проводится к выходу из биопсийного канала, что контролируется ее появлением на ультразвуковом экране или визуально по эндоскопическому изображению, фиксатор затягивается. Следующим этапом рекомендуется установка верхнего фиксатора в положение, определяющее глубину пункции по нанесенной на рукоятке иглы шкале, или установку максимальной глубины пункции (8 см) и выполнение манипуляции, ориентируясь на тактильные ощущения и визуализацию иглы на ультразвуковом мониторе. Это связано с тем, что при пункциях, особенно в положении аппарата на длинной петле, игла пружинит в биопсийном канале и устанавливаемое на основании ультразвуковой визуализации расстояние до объекта не всегда соответствует расстоянию, которое надо пройти кончику иглы для достижения заданной точки. После освобождения верхнего фиксатора стилет иглы подтягивается на 0,5-0,6 мм и производится пункция образования под ультразвуковым контролем. После позиционирования иглы внутри новообразования, стилет сначала полностью проводится в просвет иглы с целью удаления из ее просвета клеток стенки полого органа и неизмененной паренхимы поджелудочной железы, попавших в нее при пункции. Затем стилет извлекается. Вакуумная аспирация специальными шприцами используем только при повторной пункции плотных образований, если первая пункция не позволила получить достаточное количество клеточного материала. Обычно используется однократная пункция с 8-10 возвратно-поступательными движениями иглы внутри образования при одновременном изменении угла пункции с помощью подъемника эндоскопа - так называемая «веерная техника». Затем визуально оценивается на стекле количество и качество полученного материала. Если материала недостаточно, выполняется вторая, а при необходимости и третья пункции.
Исследования проводят с использованием видеосистем VP-4400 и VP-4450, с ультразвуковым процессором SU-7000 и SU-8000 и эхоэндоскопом с конвексным датчиком - EG530UT, EG530UT2 (Fujinon, Japan). Электронные эхоэндоскопы этой серии имеют функцию цветового допплеровского картирования и допплеровского сканирования в импульсном режиме, что позволяет четко визуализировать сосуды и оценивать тип кровотока. Ультразвуковые процессоры позволяют выполнять сканирование в широком диапазоне частот: 5, 7,5, 10 и 12 МГц. Пункции производят иглами типа EchoTip ProCore COOK Medical, диаметром 22 или 19G, состоящих из иглы, стилета и рукояти с фиксатором и шкалой глубин.
Недостатком способа является то, что получаемый материал чаще цитологический, а способ получения материала с помощью тонкоигольного биопсийного форцепта под контролем эндосонографии обладает более низкой чувствительностью по сравнению с тонкоигольной аспирационной биопсией и высоким процентом осложнений в виде кровотечения. (Е.Р. Двойникова, К.В. Стегний и др. 2018, Солодинина Е.Н., 2016). В лечебно-диагностические процедуру вовлекается большее количество медицинского персонала, что снижает эффективность работы всего лечебного учреждения. Техническая сложность проведения исследования после резекции желудка, гастрэктомии, значительная оператор-зависимость.
Недостатком устройства является длинный рабочий канал эндоскопа, который позволяет использовать только один тип биопсийных игл (типа EchoTip ProCore) и не применим для автоматических и полуавтоматических биопсийных систем и игл типа «BARD MAGNUM». Пружинящий эффект иглы в биопсийном канале устройства не позволяет использовать шкалу глубин на рукояти иглы и вынуждает руководствоваться только тактильными ощущениями и ультразвуковой визуализацией. (Солодинина Е.Н., 2016). Дороговизна устройства является причиной небольшого количества медицинских учреждений, оснащенных соответствующей аппаратурой (Клинические рекомендации по лечению механической желтухи 2018).
Наиболее близким к предполагаемому изобретению является антеградный способ получения морфологического материала (Кулезнёва Ю.М., Чрескожные вмешательства в абдоминальной хирургии, М.: Издательская группа «ГЭОТАР-Медиа»,2016, с. 105-107). Для выполнения этих вмешательств необходимо установить интродьюсер, через который можно провести холангиоскоп, биопсийный щипцы, биопсийную щеточку, внутрипросветный У3-датчик.
Стандартный интродьюсер представляет собой пластиковую трубку со «срезанным» дистальным кончиком, на который нанесена рентгеноконтрастная метка; на проксимальном кончике располагается силиконовый клапан, не позволяющий жидкости вытекать из просвета протока, и боковой канал с краником для введения контрастного вещества. Интродьюсер устанавливают на длинном буже, с которого его потом сталкивают после того, как рентгеноконтрастная метка оказалась в просвете протока. Интродьюсер обеспечивает герметичность транспеченочного канала, исключая возможность подтекания желчи и крови в брюшную полость и уменьшая риск повреждения капсулы печени, а также создает необходимый упор при последующем проведении инструментария через стриктуру. Размер интродьюсера зависит от диаметра проводимого инструментария. Для биопсии достаточно будет выбрать интродьюсер 8-10 Fr, для холангиоскопии - от 14 до 22 Fr. Браш-биопсию с помощью щеточки осуществляют под одновременным контролем холангиоскопии и рентгеноскопии для уменьшения риска перфорации стенки протока и только если у больного перед этим некоторое время функционировал наружно-внутренний дренаж, то есть уже был сформирован канал через область стриктуры. Это позволяет снизить травматичность манипуляции. Получение морфологического материала биопсийными щипцами проводят под рентгеноскопическим контролем с дополнительным визуальным контролм посредством холангиоскопа. Для щипцовой биопсии выполняют частичное бужирование стриктуры, после чего дистальный кончик интродьюсера устанавливают непосредственно в зоне сужения протока. По каналу интродьюсера щипцы проводят в закрытом состоянии. Интродьюсер подтягивают выше стриктуры, щипцы раскрывают и, прижимая их в раскрытом состоянии к стенке протока в области стриктуры, пытаются захватить кусочек ткани под постоянным рентгеноскопическим контролем. Обычно это проще сделать у верхнего края стриктуры. После закрытия щипцов их втягивают обратно в интродьюсер и извлекают. В случае отсутствия материала в щипцах манипуляцию повторяют. Но важно помнить, что это достаточно травматичная процедура, связанная с риском повреждения капсулы печени, перфорации стенки желчного протока и кровотечения из области стриктуры. Поэтому число попыток должно быть не более двух-трех, их необходимо выполнять крайне аккуратно и только под общим обезболиванием. Одним из вариантов может быть соскоб материала с баллона после баллонной дилатации стриктуры.
Недостатком этого способа является то, что данное вмешательство является сложным, в определенной степени травматичным и требует двойного визуального контроля (рентгенологического и холангиоскопического), что в свою очередь влечет за собой необходимость создания небезопасного (в плане кровотечения и желчеистечения) широкого транспеченочного канала, требующего дальнейшем установки чреспеченочного желчного дренажа большого диаметра. Это усилит болевой синдром, обусловленный механическим воздействием на межреберный нерв, так как в большинстве случаев пункционный транспеченочный канал проходит через межреберье и удлиняет время оперативного лечения. В дальнейшем требуется поэтапное удаление желчного дренажа с постепенным уменьшением его диаметра. Все это удлиняет время диагностических и лечебных мероприятий.
Недостатком устройства является то, что взятие морфологического материала ограничивается только проксимальным отделом стриктуры, что в случае не информативности требует повторные биопсии, увеличивающие риск хирургических осложнений и диссеминации опухоли, и развития не только локального, но и общего инфекционного процесса. Форма устройства не позволяет использовать его в качестве бужа, что требует применения дополнительных бужирующих устройств.
Цель изобретения - создание максимально информативного способа получения гистологического материала из разных мест и глубин опухолей головки поджелудочной железы и дистального отдела холедоха и многофункционального устройства для его осуществления.
Поставленная цель достигается тем, что больному вводят металлический сверхжесткий проводник типа Lunderquist по чрескожному пункционному каналу паренхимы печени через гепатикохоледох в двенадцатиперстную кишку (ДПК). При этом, в ДПК заводят всю мягкую часть проводника и дистальный конец его жесткой части, что позволяет сохранить прямолинейную ось холедоха. По металлическому проводнику, установленному в рабочий канал, устройство заводят в гепатикохоледох, тем самым бужирют пункционный канал печени. Далее дистальный конец максимально заводят сквозь зону опухолевого сужения по истинному просвету холедоха, расширив его, таким образом, чтобы внутреннее отверстие пункционного канала достигло проксимальной части опухолевого стеноза. Направление и глубину пункции выбирают исходя из предоперационного анализа КТ и МРТ. Направление пункции устанавливают вращением устройства вокруг оси проводника. Выполняют трепан-биопсию с помощью биопсийной иглы. Для профилактики гематогенного и имплантационного метастазирования после пункции вводят противоопухолевые препараты в просвет гепатикохоледоха. Выполняют чрескожное чреспеченочное наружно-внутреннее дренирование желчных протоков, обеспечивая сдавление пункционного канала опухоли и препятствуя кровотечению.
Предложенный способ является высоко информативным и эффективным и может быть реализован с помощью технически простого и безопасного устройства для одномоментной трепан-биопсии из разных мест и глубин опухолей ГПЖ и ДОХ.
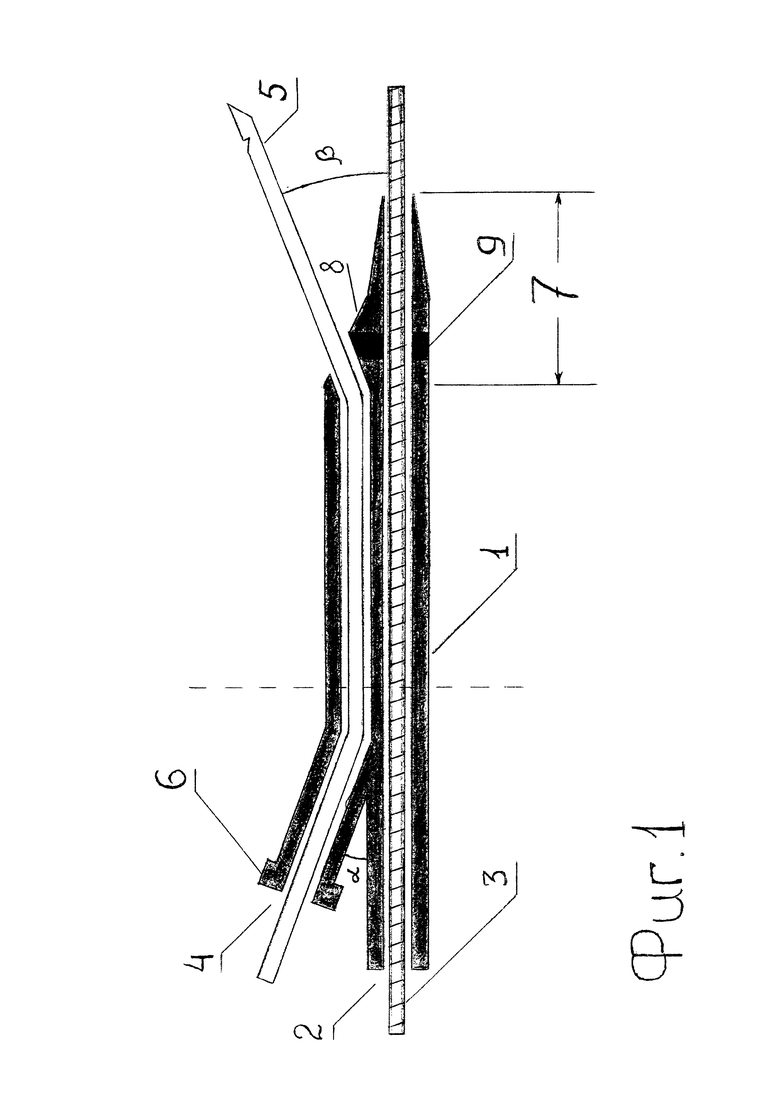
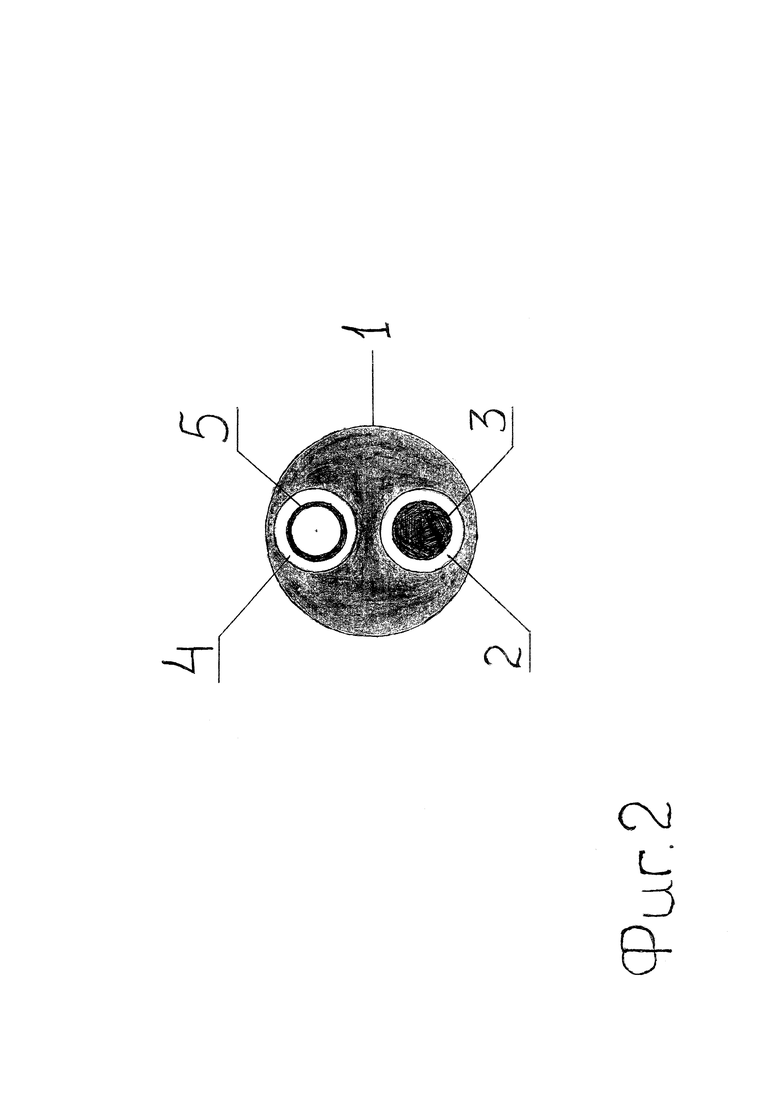
На фиг. 1 изображено универсальное устройство для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха Е.Б. Ревазова, состоящее из пластиковой полимерной трубки 1, которая имеет два канала: канал 2 для проведения металлического проводника 3, канал 4 для пункционной иглы 5. На фиг. 2 изображено данное устройство в поперечном сечении в отделе, обозначенном на фиг. 1 пунктирной линией. Проксимальные концы каналов 2 и 4 неподвижно зафиксированы относительно друг друга под углом α=20-40°, что обеспечивает удобство работы с устройством. А именно: упрощает доступ к пункционному каналу 4 при заведении пункционной иглы 5; облегчает вращение устройства вокруг оси проводника 3, тем самым, изменяя направление пункции; контроль положения проксимальных концов 2 и 4 позволяет определять направление пункции. Проксимальный конец пункционного канала 4 имеет коннектор 6 для шприца типа «ЛУЕР/ЛУЕР-ЛОК», что обеспечивает возможность выполнения по ходу оперативного вмешательства холангиографии. Дистальный конец устройства 7 имеет форму усеченного конуса, обеспечивая устройству более легкое прохождение по пункционному транспеченочному каналу с бужирующим эффектом. Между осью внутреннего конца пункционной иглы 5 и осью металлического проводника 3 имеется угол β=5-30°, образуемый за счет выступа 8 в дистальном отделе пункционного канала 4, обеспечивающий безопасное осевое отклонение пункционной иглы при выполнении трепан-биопсии. На уровне внутреннего отверстия пункционного канала 4 расположена рентгеноконтрастная метка 9, которая позволяет контролировать пункционную иглу при повторных ее заведениях с целью взятия биоптатов из разных мест.
Устройство работает следующим образом. Перед выполнением пункционной биопсии определяют размеры опухоли, отношение ее близлежащим структурам, протяженность окклюзии по данным компьютерной томографии с контрастным усилением и/или магнитно-резонансной томографии. Затем по чрескожному пункционному каналу паренхимы печени через гепатикохоледох в двенадцатиперстную кишку (ДПК) больному вводят металлический сверхжесткий проводник 3 типа Lunderquist. При этом, в ДПК заводят всю мягкую часть проводника и дистальный конец его жесткой части, что позволяет сохранить прямолинейную ось холедоха. По металлическому проводнику 3, установленному в канале 2, устройство заводят в гепатикохоледох, тем самым бужирют пункционный канал печени. Далее дистальный конец 7 максимально заводят сквозь зону сужения по истинному просвету холедоха, расширив его, таким образом, чтобы внутреннее отверстие пункционного канала 4 достигло проксимальной части опухолевого стеноза. Сложение жесткостей проводника и устройства обеспечивают прямолинейную ось в зоне операции. Направление и глубину пункции выбирают исходя из предоперационного анализа КТ и МРТ. Направление пункции устанавливают вращением устройства вокруг оси проводника 3. Трепан-биопсию выполняют с помощью биопсийной иглы типа «BARD» или EchoTip ProCore COOK Medical. Дистальный конец устройства 7, обтурировав истинный просвет холедоха в зоне опухоли, препятствует возможности «соскальзывания» пункционной иглы 5 в просвет холедоха, повышая эффективность пункции. Для профилактики гематогенного и имплантационного метастазирования после пункции по пункционному каналу 4 с помощью шприца типа «ЛУЕР/ЛУЕР-ЛОК», подсоединенному к коннектору 6, вводят противоопухолевые препараты. Затем выполняют чрескожное чреспеченочное наружно-внутреннее дренирование желчных протоков, обеспечивая сдавление пункционного канала опухоли и препятствуя кровотечению.
Новизна способа заключается в том, что забор материала производят с помощью игл транспеченочным холангиостомическим доступом с возможностью выбора глубины; процесс сопровождается одномоментным бужированием транспеченочного пункционного канала и зоны окклюзии опухолью.
Преимущество способа заключается в том, что он позволяет получать материал для гистологического исследования только под рентгенологическим контролем со 100% информативностью при простоте выполнения вмешательства одним хирургом.
Новизна устройства заключается в том, что оно имеет два рабочих канала для пункционной иглы и металлического проводника. Проксимальные концы каналов неподвижно зафиксированы относительно друг друга под углом 20-40°, дистальный конец в форме усеченного конуса, выступ в дистальном отделе пункционного канала, обеспечивающий угол 5-30° между осью внутреннего конца пункционной иглы и осью металлического проводника. Рентгеноконтрастная метка, расположена у внутреннего отверстия пункционного канала.
Дешевизна материала, простота и безопасность способа, возможность работать биопсийными иглами различных типов, возможность выполнения вмешательства одним хирургом, что и на этапе дренирования желчных протоков, делает предлагаемое изобретение универсальным, экономически более выгодным и безопасным, значительно сокращая время операции, необходимое суммарно для декомпрессии желчных протоков и 100% получения гистологического материала с возможностью антибластики.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2021 |
|
RU2792248C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2020 |
|
RU2747591C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ МОРФОЛОГИЧЕСКОЙ ВЕРИФИКАЦИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2022 |
|
RU2793842C1 |
| КОМБИНИРОВАННЫЙ СПОСОБ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА С АНТЕГРАДНОЙ ПАПИЛЛОСФИНКТЕРОТОМИЕЙ И БИЛИОДУОДЕНАЛЬНЫМ ДРЕНИРОВАНИЕМ | 2021 |
|
RU2768480C1 |
| ПОЛУАВТОМАТИЧЕСКАЯ ИГЛА ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА | 2020 |
|
RU2738627C1 |
| ИГЛА ДЛЯ ТРЕПАН-БИОПСИИ ОПУХОЛЕЙ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ДИСТАЛЬНОГО ОТДЕЛА ХОЛЕДОХА | 2020 |
|
RU2771798C2 |
| Насадка на автоматическую биопсийную систему | 2020 |
|
RU2753387C1 |
| Способ чрескожной чреспеченочной щипцовой внутрипротоковой биопсии | 2018 |
|
RU2701750C1 |
| УСТРОЙСТВО ДЛЯ АНТЕГРАДНОЙ БРАШ-БИОПСИИ ЖЕЛЧНЫХ ПРОТОКОВ | 2021 |
|
RU2793415C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ НЕФУНКЦИОНИРУЮЩЕГО ПЛАСТИКОВОГО БИЛИАРНОГО СТЕНТА ИЗ ЖЕЛЧНЫХ ПРОТОКОВ | 2017 |
|
RU2665622C1 |
Изобретение относится к хирургии, а именно к онкологии и онкорадиологии, и может быть использовано для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха. Выполняют транспеченочный пункционный доступ к желчным протокам с забором ткани для гистологического исследования из разных мест, выполняемый под рентгеноскопическим контролем с возможностью выполнения холангиографии. При этом осуществляют проведение металлического проводника сквозь опухолевый стеноз по истинному просвету холедоха. Забор материала производят с одномоментным бужированием транспеченочного пункционного канала и зоны окклюзии опухолью. Устройство для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха включает пластиковую полимерную трубку, коннектор для шприца типа «ЛУЕР/ЛЕУР-ЛОК», рентгеноконтрастную метку. При этом устройство имеет два рабочих канала для пункционной иглы и металлического проводника, проксимальные концы которых неподвижно зафиксированы относительно друг друга под углом 20-40°, дистальный конец в форме усеченного конуса, выступ в дистальном отделе пункционного канала, обеспечивающий угол 5-30° между осью внутреннего конца пункционной иглы и осью металлического проводника, и рентгеноконтрастную метку, расположенную у внутреннего отверстия пункционного канала. Предложенные способ и устройство позволяют получать материал для гистологического исследования только под рентгенологическим контролем со 100% информативностью при простоте выполнения вмешательства. 2 н.п. ф-лы, 2 ил.
1. Способ трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха с использованием устройства по п. 2, включающий транспеченочный пункционный доступ к желчным протокам с забором ткани для гистологического исследования из разных мест, выполняемый под рентгеноскопическим контролем с возможностью выполнения холангиографии, отличающийся тем, что осуществляют проведение металлического проводника сквозь опухолевый стеноз по истинному просвету холедоха, забор материала производят с одномоментным бужированием транспеченочного пункционного канала и зоны окклюзии опухолью.
2. Устройство для трепан-биопсии опухолей головки поджелудочной железы и дистального отдела холедоха, включающее пластиковую полимерную трубку, коннектор для шприца типа «ЛУЕР/ЛЕУР-ЛОК», рентгеноконтрастную метку, отличающееся тем, что устройство имеет два рабочих канала для пункционной иглы и металлического проводника, проксимальные концы которых неподвижно зафиксированы относительно друг друга под углом 20-40°, дистальный конец в форме усеченного конуса, выступ в дистальном отделе пункционного канала, обеспечивающий угол 5-30° между осью внутреннего конца пункционной иглы и осью металлического проводника, и рентгеноконтрастную метку, расположенную у внутреннего отверстия пункционного канала.
| КОВАЛЕНКО Ю.А | |||
| и др | |||
| Новые возможности ранней диагностики воротной холангиокарциномы с помощью катетера направленной биопсии TurboHawk | |||
| Практическая медицина, 2017, N6(107), С | |||
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
| УСТРОЙСТВО ДЛЯ ЭНДОСКОПИЧЕСКОЙ БИОПСИИ ТКАНЕЙ | 2000 |
|
RU2175852C1 |
| СПОСОБ ТРАНСКУТАННОЙ ПУНКЦИИ ОЧАГОВЫХ ОБРАЗОВАНИЙ ПАРЕНХИМАТОЗНЫХ ОРГАНОВ | 2008 |
|
RU2393812C1 |
| ЧРЕСФИСТУЛЬНАЯ ЩИПЦОВАЯ ЭНДОБИЛИАРНАЯ БИОПСИЯ ПОД РЕНТГЕНОЛОГИЧЕСКОЙ ВИЗУАЛИЗАЦИЕЙ | 2012 |
|
RU2533047C2 |
| UA 60870 U, 25.06.2011 | |||
| US 20100240990 А1, 23.09.2010 | |||
| БУРДЮКОВ М.С | |||
| и др | |||
Авторы
Даты
2020-06-02—Публикация
2019-05-13—Подача